Портативный МРТ впервые использовали прямо в отделении интенсивной терапии
Kevin N. Sheth et al. / JAMA Neurology, 2020
Врачи впервые протестировали новый портативный аппарат магнитно-резонансной томографии на пациентах с поражениями головного мозга прямо в отделении интенсивной терапии. Как сообщается в журнале JAMA Neurology, в среднем на одно исследование уходило чуть более 35 минут, а качество полученных изображений было сопоставимо со сканами стандартного аппарата МРТ.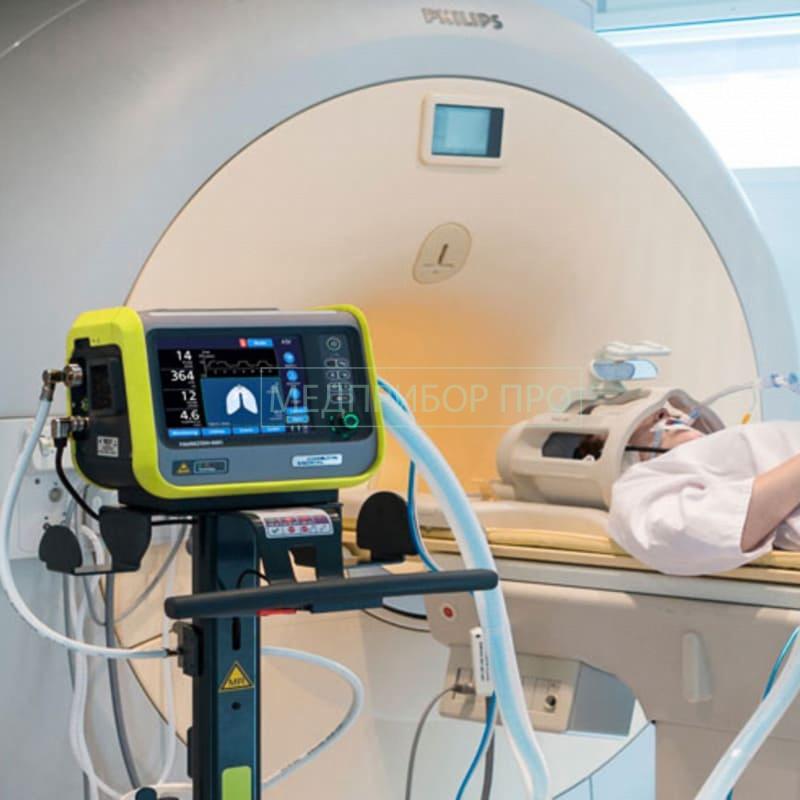
Магнитно-резонансная томография (МРТ) хоть и становится все более рутинной и повседневной практикой, все еще требует участия технических специалистов и жестких мер предосторожности (из-за высокой напряженности магнитного поля) в результате чего создается необходимость транспортировки пациента в отдельные комнаты. Такая ситуация осложняет проведение диагностики у тяжелобольных пациентов, находящихся, например, в отделении интенсивной терапии. Их транспортировка связана со множеством рисков, к тому же актуален и вопрос перемещений пациентов с высоко контагиозными инфекционными заболеваниями.
Последние достижения в разработке МРТ позволили получить данные при низкой напряженности магнитного поля, что допускает использование аппаратов открытого типа. Такие аппараты могут облегчить проведение исследования у маломобильных пациентов, а также они совместимы с близлежащими ферромагнитными материалами, что избавляет от необходимости устанавливать аппарат в специализированных кабинетах.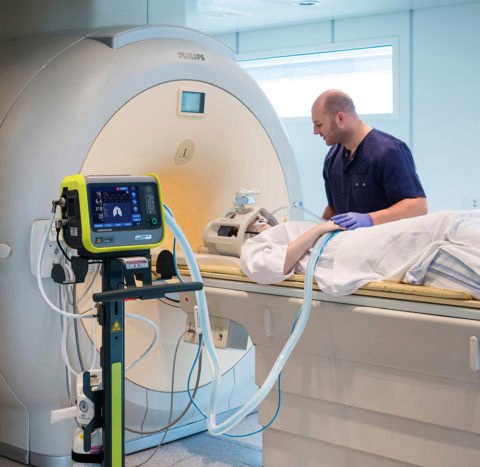
В начале 2020 года компания Hyperfine Research получила разрешение на продажу первого в мире портативного аппарата МРТ, который подключается к обычной электрической сети, а благодаря относительно небольшому размеру его можно поместить в палату интенсивной терапии. Кевин Шет (Kevin N. Sheth) с коллегами из Медицинской школы Йельского университета испытали этот аппарат на 50 пациентах с различными поражениями головного мозга, находившихся в отделении интенсивной терапии.
Портативный аппарат МРТ в палате интенсивной терапии
Kevin N. Sheth et al. / JAMA Neurology, 2020
Исследование проводилось пациентам с ишемическим и геморрагическим инсультами, субарахноидальным кровоизлиянием, черепно-мозговой травмой, опухолью головного мозга и инфекцией COVID-19 с измененным психическим статусом. Обследования проводились в среднем через пять дней (диапазон 0–37 дней) после поступления в отделение интенсивной терапии. 15 пациентам исследование проводилось под наркозом. Чуть больше трети пациентов находились на искусственной вентиляции легких (с эндотрахеальной интубацией или с трахеостомией), а трое пациентов получали непрерывную заместительную почечную терапию.
Обследования проводились в среднем через пять дней (диапазон 0–37 дней) после поступления в отделение интенсивной терапии. 15 пациентам исследование проводилось под наркозом. Чуть больше трети пациентов находились на искусственной вентиляции легких (с эндотрахеальной интубацией или с трахеостомией), а трое пациентов получали непрерывную заместительную почечную терапию.
Все изображения пациентов без COVID-19 от портативного аппарата соответствовали по качеству стандартным МРТ-снимкам (р < 0,001), за исключением одного: на томограмме не визуализировалось диффузное субарахноидальное кровоизлияние.
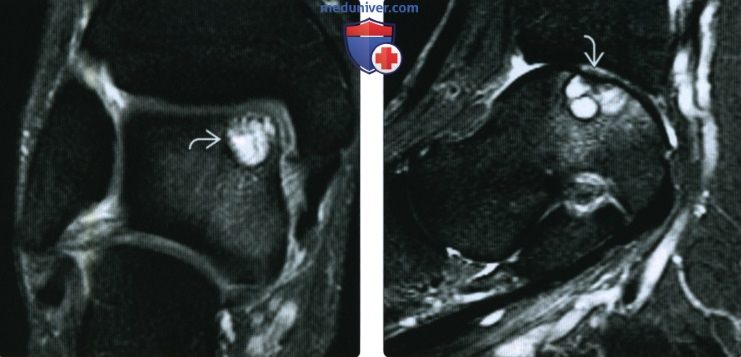
Томограммы, полученные с помощью портативного аппарата МРТ (первые 4 изображения) и стандартного аппарата МРТ (правое изображение), от пациента с кровоизлиянием в левую затылочную область головного мозга
Kevin N. Sheth et al. / JAMA Neurology, 2020
У пациентов с COVID-19 все изображения (внутричерепное кровоизлияние, инсульт, диффузная церебральная гематома, лейкоэнцефалопатия) от портативного МРТ соответствовали стандартным снимкам. При обследованиях врачи не наблюдали никаких нежелательных явлений или осложнений, а все исследование занимало всего 35 минут 40 секунд.
При обследованиях врачи не наблюдали никаких нежелательных явлений или осложнений, а все исследование занимало всего 35 минут 40 секунд.
Основное ограничение этого исследования — небольшое число пациентов. Для подтверждения эффективности метода необходимы дополнительные исследования, в которых результаты диагностики портативным МРТ сравниваются с результатами обычной компьютерной томографии или стандартным МРТ для различных патологий.
Тем не менее, портативность, качество изображения и простота в эксплуатации нового устройства все же позволит быстро и точно диагностировать неврологические нарушения у пациентов в тяжелом состоянии.
Многие современные исследования головного мозга, его работы и его изменений не обходятся без МРТ. С помощью него ученые выяснили, что маленькие дети используют для понимания речи сразу оба полушария головного мозга, а тяжелый физический труд уменьшает размер гиппокампа. Впрочем, МРТ можно сделать не только человеку или животному: в нашей галерее можно посмотреть на томограммы овощей.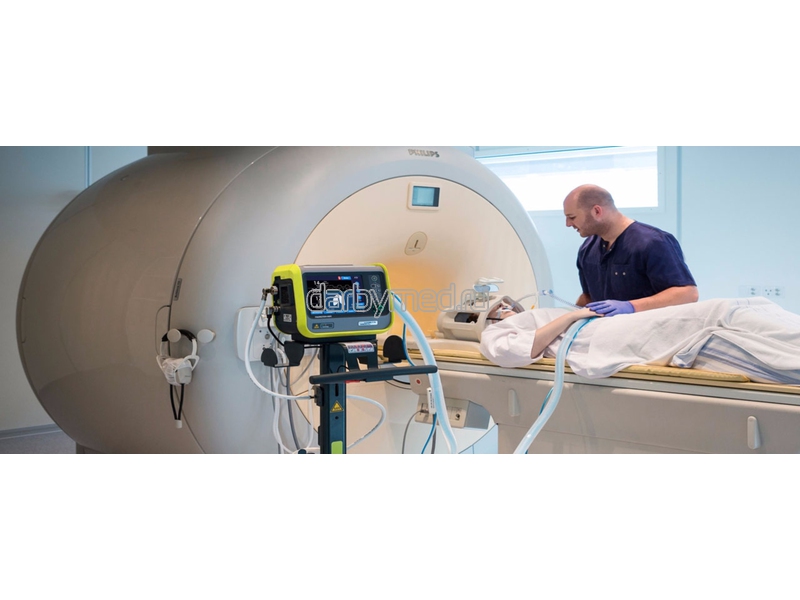
Вячеслав Гоменюк
Аппарат ИВЛ для томографии
LMT Магнитносовместимый неонатальный вентилятор Neo MR
Портативный амагнитный аппарат ИВЛ для новорожденных является принадлежностью инкубаторной системы LMT nomag IC. Данный ИВЛ предназначен для вентиляции легких как во время транспортировки, так и проведения томографии детей. Амагнитный ИВЛ дает возможность обследовать недоношенных и новорожденных детей даже в первые дни жизни и проводить МРТ без применения наркоза или седативных средств. Он обеспечивает вентиляцию легких и поддержание дыхательной функции, если это необходимо ребенку при проведении томографии.
ИВЛ приводится в действие пневматически, что обеспечивает мгновенную вентиляцию легких. Комплексная интегрированная система сигнализации включает визуальные и звуковые сигналы тревоги для высокого давления, постоянного давления, низкого давления / отключения, низкого давления подачи газа и низкого заряда батареи. Имеется возможность использования с ИВЛ Neo MR многоразовых или одноразовых вентиляционных шлангов. Удлиненные шланги с быстроразъемными соединениями для центрального газоснабжения входят в комплектацию вентилятора.
Имеется возможность использования с ИВЛ Neo MR многоразовых или одноразовых вентиляционных шлангов. Удлиненные шланги с быстроразъемными соединениями для центрального газоснабжения входят в комплектацию вентилятора.
Характерные особенности и преимущества использования:
— Легкий портативный аппарат ИВЛ для новорожденных .
— Уникальная вариабельная смешивающая система концентрации газа продлевает время использования кислородного баллона в 3 раза, используя воздушный поток.
— Контроль давления вдоха.
— Независимый регулируемый пневматический сигнал тревоги высокого давления.
— Отдельные функции контроля за временем вдоха и выдоха позволяют легко выбирать оптимальную непрерывную принудительную вентиляцию легких (CMV).
— IMV (перемежающаяся принудительная вентиляция легких) время выдоха.
— PEEP (положительное давление конца выдоха) / CPAP (режим ИВЛ постоянного положительного давления в дыхательных путях) контроль.
— Четыре операционных режима ИВЛ — CMV + РЕЕР; CMV + АКТИВНЫЙ РЕЕР; IMV + CPAP; CPAP.
— Эффективная работа вентилятора Neo MR — пневматические контуры разработаны, чтобы минимизировать потребление газа.
— Всесторонняя интегрированная система сигнализации помогает обнаружить возможные неблагоприятные изменения в вентиляции легких пациента в течение CMV. Включает визуальные и звуковые сигналы тревоги для высокого давления ( при выходе максимального давления вдоха за установленные пределы ), непрерывного давления, низкого давления / разъединения, низкого давления поступления газа и низкого напряжения батареи, плюс многие другие характеристики для обеспечения безопасности.
— Амагнитный аппарат ИВЛ для новорожденных обеспечивает максимальную подвижность для транспортировки в пределах больницы, а также при необходимости в машине скорой помощи.
Комплектация:
В комплектацию ИВЛ входят: 3 амагнитных LMT кислородных баллона с амагнитным редуктором давления кислорода LMT nomag® PR для снабжения ИВЛ кислородом.
Магнитносовместимый регулятор давления LMT nomag® PR
LMT nomag® PR включен в комплектацию аппарата ИВЛ для новорожденных. Кислородный редуктор является магнитнорезонансно совместимым и не дает наводок при проведении МРТ . Присоединяется к кислородным баллонам объемом 5л. LMT nomag® PR постоянно регулирует подачу кислорода как во время транспортировки больных, так и во время проведения МРТ детям. Амагнитный редуктор имеет стандартные входные и выходные отверстия для подсоединения к кислородным баллонам.
LMT nomag® PR регулятор давления может использоваться с ИВЛ без какого-либо риска в магнитно-резонансных средах.
Технические характеристики:
Размеры: 200мм x 50мм x 130мм (Д x Ш x В)
Вес (без шланга): 1,2 кг
Диапазон потока воздуха: 80 л / мин (номинал)
Давление на входе: 200 бар
Давление на выходе: 5 бар ( не регулируется )
Индикатор давления в кислородном баллоне: 0 — 250 бар
Окружающие условия во время работы: 10. ..40°C (-20…70°C во время транспортировки)
..40°C (-20…70°C во время транспортировки)
HAMILTON-MR1
Интеллектуальная вентиляция: от интенсивной терапии до кабинета МРТ
Полнофункциональный реанимационный аппарат ИВЛ – это первый аппарат ИВЛ, который может использоваться в условиях воздействия магнитного поля с индукцией до 50 мТл. Аппарат ИВЛ HAMILTON-MR1 – надежное высокоэффективное устройство, обеспечивающее использование адаптивных режимов вентиляции с поддержкой усовершенствованных стратегий защиты легких. Данный аппарат ИВЛ идеально подходит для реанимационных отделений, подключенные к аппарату ИВЛ пациенты которых транспортируются в кабинет МРТ.
- Данный аппарат ИВЛ классифицируется как приемлемый для МРТ (до 50 мТл) при использовании системы с напряженностью статического магнитного поля 1,5 и 3,0 Тесла.
- Встроенный датчик напряженности магнитного поля TeslaSpy
- Вентиляция легких у взрослых, детей и младенцев
- Время работы от аккумулятора: до 9 часов
- Независимость от баллонов сжатого газа или компрессоров
- Неинвазивная вентиляция легких и встроенный инструмент для выполнения кислородной терапии с высокой скоростью потока
- Расширенные режимы вентиляции, в частности ASV® – адаптивная поддерживающая вентиляция
Универсальный, гибкий, простой в использовании
Возможность транспортировки в пределах медицинского учреждения
Благодаря компактному размеру аппарат ИВЛ HAMILTON-MR1 прост в обращении и идеально подходит для транспортировки пациентов в пределах медицинского учреждения.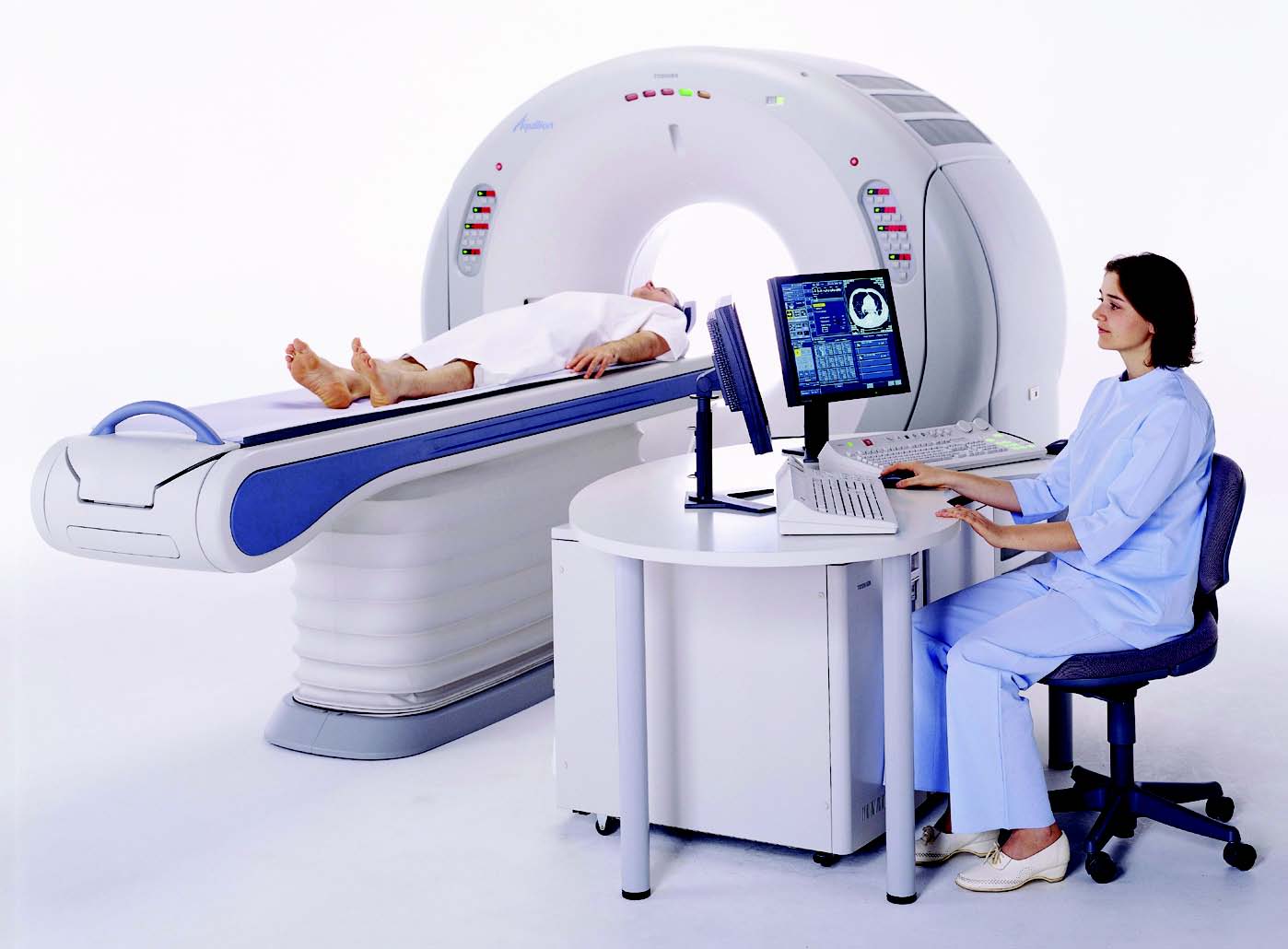 Автоматический тормоз блокирует колеса, как только вы отпускаете ручку тормоза, чтобы предотвратить случайное столкновение тележки аппарата ИВЛ с магнитно-резонансным томографом. По обе стороны тележки расположены крюки для дыхательного контура и кислородного шланга. С помощью дополнительного комплекта с функцией быстрой фиксации и специальной ручкой можно извлечь устройство одним нажатием кнопки и прикрепить его прямо к кушетке.
Автоматический тормоз блокирует колеса, как только вы отпускаете ручку тормоза, чтобы предотвратить случайное столкновение тележки аппарата ИВЛ с магнитно-резонансным томографом. По обе стороны тележки расположены крюки для дыхательного контура и кислородного шланга. С помощью дополнительного комплекта с функцией быстрой фиксации и специальной ручкой можно извлечь устройство одним нажатием кнопки и прикрепить его прямо к кушетке.
В тесном сотрудничестве с пользователями и экспертами в области вентиляции легких наши инженеры разработали интуитивно понятный интерфейс.
В HAMILTON-MR1 и других аппаратах ИВЛ производства компании Hamilton Medical используются одинаковые принципы работы, поэтому, обладая навыками эксплуатации одного устройства, освоить остальные не составит большого труда.
В HAMILTON-MR1 данные мониторинга собираются в системе Ventilation Cockpit и отображаются в виде интуитивно понятных графиков. Это позволяет провести быстрый обзор текущего состояния вентиляции легких пациента и помочь в принятии решений касательно терапии.
Аппарат ИВЛ адаптирован к условиям магнитного резонанса
Аппарат ИВЛ HAMILTON-MR1 обеспечивает непрерывную вентиляцию при транспортировке пациентов из палаты интенсивной терапии в кабинет МРТ и обратно.
Приемлемый для МРТ
- Приемлемый для МРТ до 50 мТл
- Пациента не нужно отключать от аппарата ИВЛ для проведения МРТ
Встроенная плата TeslaSpy обеспечивает еще большую безопасность
- Встроенный датчик напряженности магнитного поля
- Постоянно измеряет уровень напряженности магнитного поля вокруг устройства
Выключатель подачи газовой смеси
- Автоматически переключается между баллоном сжиженного газа и централизованной системой медицинского газоснабжения
- Реагирует немедленно, обеспечивая непрерывную вентиляцию
Кабинет магнитно-резонансной томографии
МРТ
✓ Современный высокопольный томограф EXCELART Vantage AGV с магнитным полем 1,5 Т фирмы Toshiba
✓ Благодаря сочетанию ультракороткого канала (1,4 м) и технологии «Pianissimo» (снижение шума скана), система EXCALART Vantage стала самой благоприятной для адаптации пациентов МРТ-системой в мире.
! Запись закрыта, возобновление работы в 2021 г.
Заведующий отделением: Макогонова Марина Евгеньевна, врач-рентгенолог
Адрес: Политехническая ул., 32
Телефон: 812-775-75-55
Режим работы кабинета МРТ: понедельник — пятница: 09.00-20.0
МРТ в НИИ Фтизиопульмонологии на Политехнической
Магнитно-резонансная томография (МРТ) — неинвазивный метод диагностики для получения изображений внутренних органов без использования рентгеновских лучей. МРТ сканер получает изображения, созданные на основе магнитных полей, генерируемых человеческим телом. МРТ «видит» мягкие ткани (мышцы, нервы, мозг, межпозвоночные диски, связки и т.д.). Во многих случаях только МРТ может получить диагностическое изображение, необходимое для выбора способа лечения.
Пациента помещают в магнитное поле, затем посылается дополнительный электромагнитный сигнал. Атомы водорода, имеющие одинаковую с сигналом частоту, «возбуждаются» и генерируют свой сигнал, который улавливается аппаратом. Разные виды тканей (кости, мышцы, сосуды и т.д.) имеют различное количество атомов водорода и поэтому они генерируют сигнал с различными характеристиками. Томограф распознает эти сигналы, дешифрует их и строит изображение.
Разные виды тканей (кости, мышцы, сосуды и т.д.) имеют различное количество атомов водорода и поэтому они генерируют сигнал с различными характеристиками. Томограф распознает эти сигналы, дешифрует их и строит изображение.
Вред при МРТ обследовании отсутствует.
Стоимость МРТ-исследований:
- МРТ органов
Магнитно-резонансная томография органов брюшной полости (A05.14.001)
Магнитно-резонансная холангиопанкреатография (A05.15.002)
Магнитно-резонансная томография органов малого таза (A05.30.004)
Магнитно-резонансная томография орагнов малого таза с внутривенным контрастированием (A05.30.004.001)
Магнитно-резонансная томография брюшной полости с внутривенным контрастированием (A05.
 30.005.001)
30.005.001)- МРТ позвоночника
Магнитно-резонансная томография позвоночника (один отдел) (A05.03.002)
Магнитно-резонансная томография позвоночника с контрастированием (один отдел) (A05.03.002.001)
Магнитно-резонансная томография позвоночника (два отдела) (A05.03.002.N001)
Магнитно-резонансная томография позвоночника (три отдела) (A05.03.002.N002)
- МРТ головы
Магнитно-резонансная томография преддверно-улиткового органа и мосто-мозжечкового угла (A05.08.003)
Магнитно-резонансная томография головного мозга (A05.23.009)
Магнитно-резонансная томография головного мозга с контрастированием (A05.
 23.009.001)
23.009.001)Магнитно-резонансная томография головного мозга с сосудистой программой (A05.23.009.001.N001)
Магнитно-резонансная томография глазницы (A05.26.008)
Магнитно резонансная томография лицевого отдела черепа с внутривенным контрастированием (A05.30.010.002)
- МРТ суставов
Магнитно-резонансная томография суставов (один сустав) (A05.04.001)
Магнитно-резонансная томография суставов (один сустав) с контрастированием (A05.04.001.001)
- МРТ шеи
Магнитно-резонансная томография шеи (A05.30.008)
Магнитно резонансная томография шеи с внутривенным контрастированием (A05.
 30.008.001)
30.008.001)- МРТ мягких тканей
Магнитно-резонансная томография мягких тканей (A05.01.002)
Магнитно-резонансная томография мягких тканей с контрастированием(A05.01.002.001)
- МРТ костной ткани
Магнитно-резонансная томография костной ткани (одна область)(A05.03.001)
Магнитно-резонансная томография костной ткани с контрастированием (одна область) (A05.03.001.N001)
- МРТ сосудов
Магнитно-резонансная венография (одна область) (A05.12.005)
Магнитно-резонансная ангиография с контрастированием (одна область) (A05.
 12.006)
12.006)- МРТ прочее
Описание и интерпретация магнитно-резонансных томограмм (A06.30.002.002)
Описание и интерпретация дополнительной магнитно-резонансных томограмм (дополнительный CD-диск или пленка) (A06.30.002.002. N001)
Противопоказания к МРТ
Абсолютные:
- Наличие искусственных водителей ритма, проведение искусственной вентиляции легких.
- Наличие больших металлических имплантантов, осколков.
- Наличие металлических скобок, зажимов на кровеносных сосудах.
- Вес больного более 150 кг.
Относительные:
- Клаустрофобия.
- Эпилепсия, шизофрения.
- Беременность.
- Крайне тяжелое состояние больного.

- Невозможность для пациента сохранять неподвижность во время обследования.
- Наличие металлических зубов, танталовых скобок на грудине противопоказанием к исследованию не является, хотя может снижать качество изображения.
Вопрос о проведении исследования в случае наличия искусственного клапана сердца, кавафильтров решается после консультации с рентгенологом.
Не являются противопоказаниями к МРТ:
- любые зубные протезы;
- брэкет-системы;
- внутриматочные контрацептивы;
- импланты (титановые штифты, тазобедренные суставы и т.п.).
Однако, указанные факторы могут искажать изображение, вызывая так называемые «артефакты» при проведении МРТ. Поэтому при наличии металлических конструкций в вашем теле, надо сообщить об этом врачу кабинета МРТ. В каждом конкретном случае он решает, можно ли получить полноценную информацию от МРТ- исследования.
Что нужно учесть, направляясь на МРТ
МРТ исследования головного мозга, позвоночника, суставов не требуют от пациента никакой предварительной подготовки.

МРТ малого таза лучше проводить с наполненным мочевым пузырем. Для уменьшения перистальтики кишечника рекомендуется накануне принять 2 таблетки «Эспумизана» или принять 2-3 таблетки «Но-шпы» за 1 час перед исследованием (если нет противопоказаний к приему этих препаратов).
Направляясь на МРТ, необходимо помнить, что во время исследования вам необходимо будет снять с себя все металлические украшения и аксессуары.
Лучше не пользоваться декоративной косметикой, т.к. некоторые виды косметических средств содержат металлические частицы, и это может отразиться на качестве исследования.
Во время МРТ исследования необходимо не двигаться от 10 до 50 минут, в зависимости от поставленных задач. Поэтому обычно МРТ обследования не проводятся детям до 6 лет и пациентам с выраженными непроизвольными неконтролируемыми движениями.
что показывает, как сделать, степень поражения легких на кт
Подготовка к КТ
КТ без контраста не требует подготовки.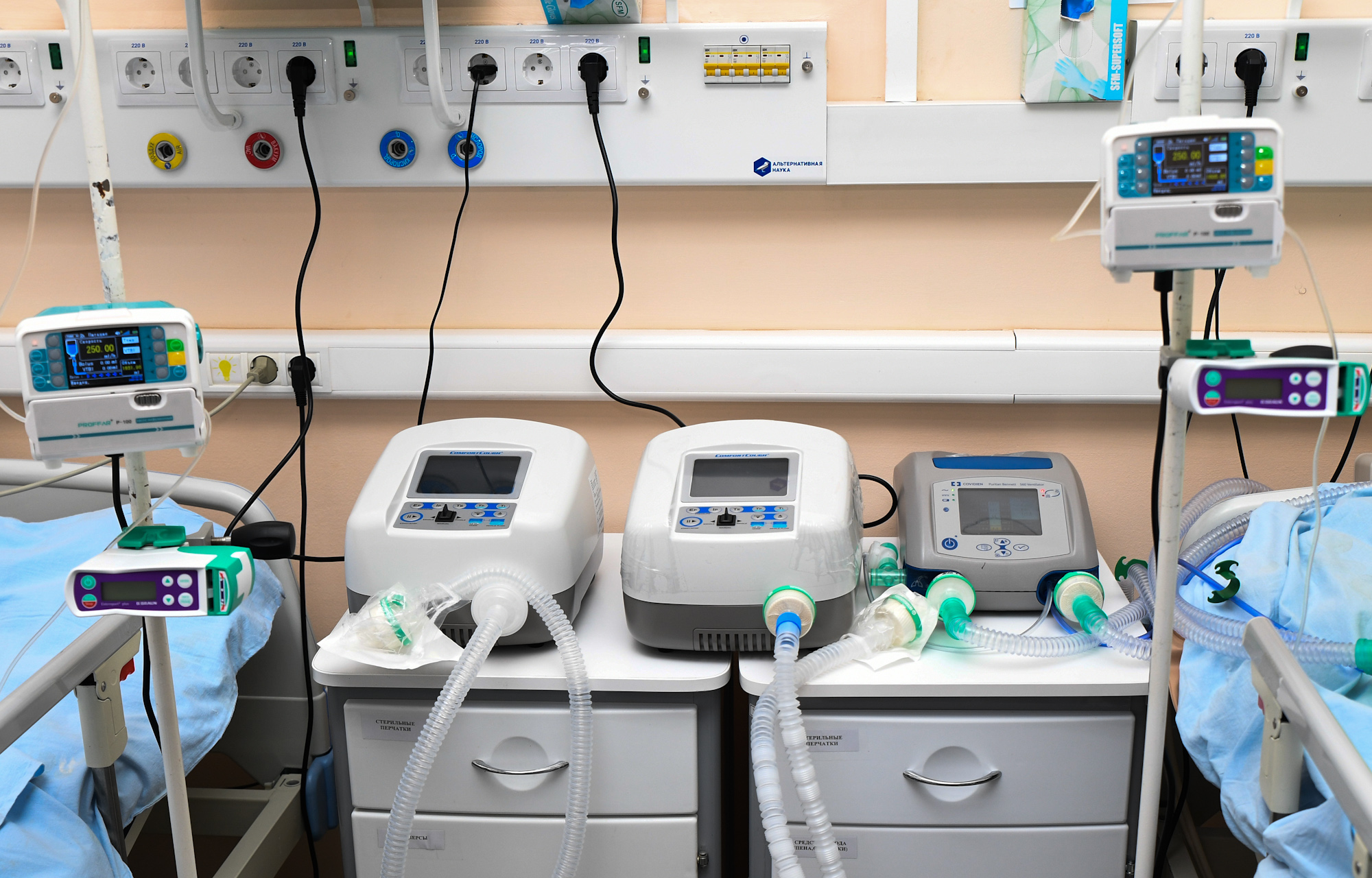 При необходимости контрастного усиления после последнего приема пищи должно пройти не менее 6 часов. Если планируется КТ с контрастом, необходимо сдать анализ на уровень креатинина.
При необходимости контрастного усиления после последнего приема пищи должно пройти не менее 6 часов. Если планируется КТ с контрастом, необходимо сдать анализ на уровень креатинина.
Ваше здоровье – наш главный приоритет
Мы делаем все, чтобы вы получили своевременную
помощь в условиях пандемии COVID-19
Дезинфекция помещений
Дезинфекция по графику
Каждый час выполняем дезинфекцию всех помещений и поверхностей специальными безопасными
дезинфектантами
Безостановочная рециркуляция воздуха
В каждом кабинете мы установили дополнительные бактерицидные рециркуляторы воздуха,
которые работают без остановки
Стерилизация абсолютно всех инструментов клиники
Инструменты подвергаются многоступенчатой стерилизации.
Мы обрабатываем все: даже пишущие ручки
Безопасность пациентов и персонала
Масочный режим всего персонала
Все сотрудники клиники используют одноразовые маски,
которые мы меняем каждые 2 часа.
Контроль за здоровьем сотрудников клиники
Мы ведем учет здоровья каждого сотрудника: измеряем температуру
при входе в клинику, следим за отсутствием симптомов
Бережное отношение к каждому пациенту
Для пациентов клиники мы подготовили индивидуальные средства защиты
на входе клиники
Бесконтактное получение результатов анализов
Результаты анализов пациенты могут получить по электронной почте
Работа в клинике
Обработка процедурного кабинета после каждого пациента
После каждого пациента мы проводим усиленную обработку
кабинетов дезинфицирующим раствором.
Наличие разметки для соблюдения дистанции
Мы разметили зоны возле кабинетов,
чтобы нашим посетителям было проще соблюдать социальную дистанцию
Мы рекомендуем посещать Центр МРТ только по онлайн-записи,
чтобы исключить нежелательные социальные контакты во время пандемии
МРТ в диагностике черепно-мозговой травмы | Новости
Наиболее частыми причинами черепно-мозговой травмы являются дорожно-транспортные происшествия, спортивные травмы, нападения и физическое насилие, подвижные игры и падения.
Для ЧМТ характерна высокая летальность, а также сохранение выраженных неврологических или психических расстройств, в том числе даже после легких или средне-тяжелых травм, что становится причиной нетрудоспособности пострадавших.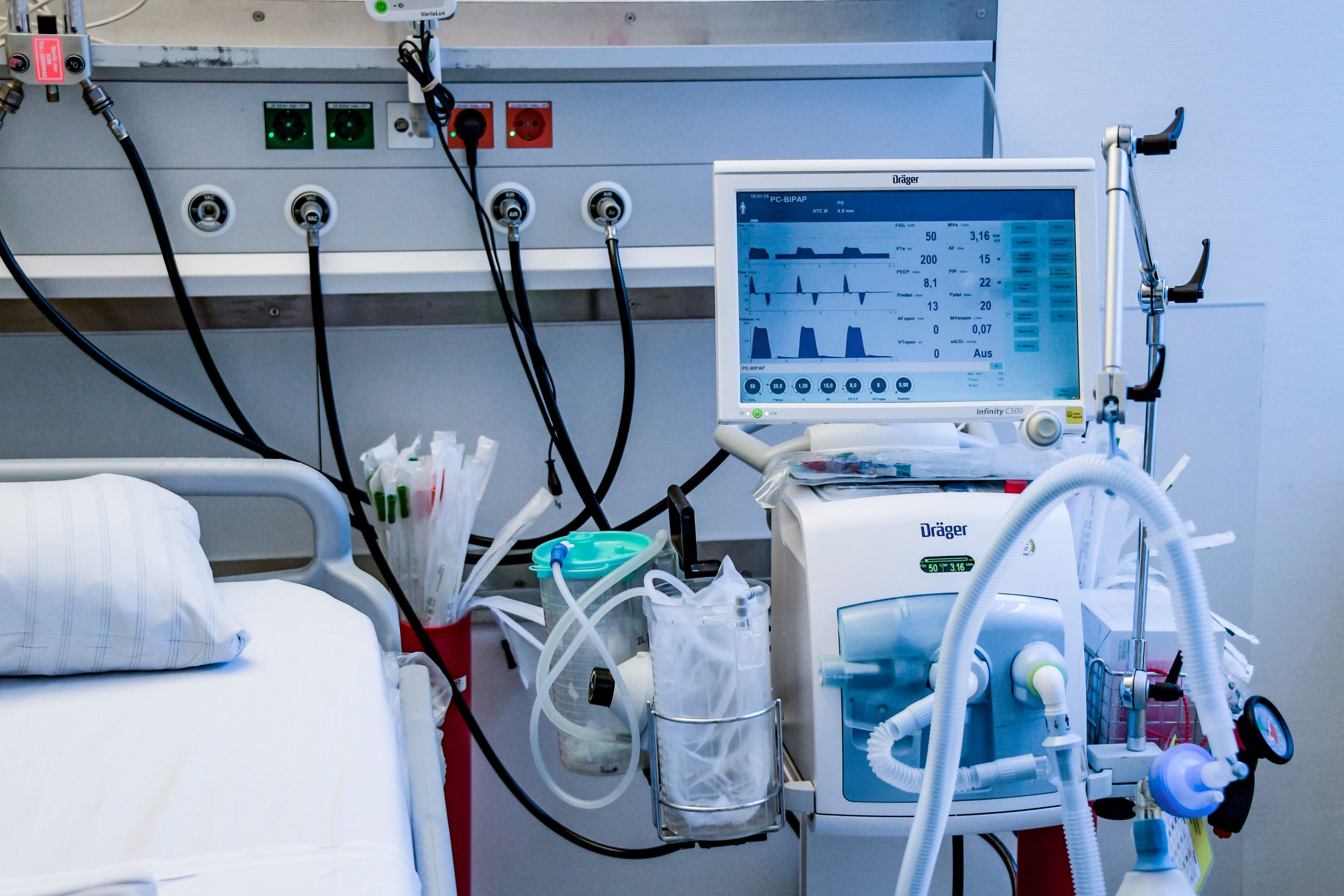
Черепно-мозговые травмы относятся к наиболее распространенным травматическим повреждениям, вызывающим инвалидность и смерть в молодом и среднем возрасте. В общем ряду травм они составляют до 50% всех случаев. Поэтому особенно большое значение имеет правильная диагностика таких повреждений, главными методами которой являются КТ и МРТ головного мозга.
Все черепно-мозговые травмы разделяются на несколько основных типов – сотрясение, сдавление, ушиб головного мозга, кровоизлияние. Особенно серьезными последствиями грозят разрыв внутричерепных кровеносных сосудов и повреждение участков головного мозга. В результате черепно-мозговой травмы может произойти нарушение физико-химических процессов, клеточного питания тканей мозга, утратиться взаимосвязь отдельных участков коры головного мозга и другие осложнения. Для того чтобы по возможности избежать этих осложнений и уменьшить последствия травмы необходима адекватная медикаментозная терапия.
В связи с этим нередко возникает вопрос, какой метод обследования при черепно-мозговой травме лучше – МРТ головного мозга или КТ?
Ответ на этот вопрос неоднозначен. Наиболее часто при симптомах сотрясения, сдавления и ушиба головного мозга, так же как и при инсульте, используется КТ.
Наиболее часто при симптомах сотрясения, сдавления и ушиба головного мозга, так же как и при инсульте, используется КТ.
Это связано не с тем, что этот метод боле информативен, а с тем, что он требует меньше времени. МРТ головного мозга занимает больше времени, чем КТ. Когда счет идет на минуты, это имеет решающее значение. Кроме того, МРТ головного мозга требует неподвижности пациента в течение всего обследования, что не всегда возможно при выраженной симптоматике и неадекватном поведении, связанном с травмой. Однако при поздних симптомах черепно-мозговой травмы и ее осложнениях, врачи нередко делают выбор в пользу МРТ головного мозга. Это связано с тем, что МРТ лучше показывает сосуды, нервные ткани и структуры головного мозга, в то время как КТ лучше показывает костные структуры.
Показаниями МРТ головного мозга после ЧМТ являются такие осложнения как эпилепсия, снижение умственных способностей, ухудшение памяти, личностные изменения, депрессия. Кроме того, этот вид обследования назначается при замедленных реакциях, нарушениях координации движений, ориентации в пространстве, равновесия, снижении концентрации, повышенной утомляемости в сочетании потерей аппетита, головными болями, тошнотой.
Усовершенствование диагностики черепно-мозговой травмы, появление таких высокоточных методов нейровизуализации, как МРТ головного мозга, привело к возможности постановки достоверного диагноза на максимально ранних этапах патологического процесса, своевременности начатого лечения, что способствует снижению летальности и числа осложнений.
МРТ целесообразна для уточнения размеров и расположения кровоизлияний, характера изменения желудочковой системы, перивентрикулярного отека и других реакций мозга на черепно-мозговую травму, для распознавания различных последствий и осложнений.
Противопоказания к применению МРТ связаны в основном с организационными трудностями в обеспечении контроля за состоянием пациента и ИВЛ при грубой клинической декомпенсации. Следует отметить, что созданы специальные аппараты ИВЛ и мониторинга пациентов, находящихся в просвете магнита.
МРТ противопоказана при наличии инородных металлических тел в полости черепа, поскольку существует опасность их смещения под действием магнитного поля и, стало быть, повреждения близлежащих структур головного мозга.
Вероятность положительного прогноза в отношении пострадавшего от черепно мозговой травмы зависит в наибольшей степени от своевременной и точной диагностики. Ранняя диагностика в совокупности с лечением сводят к минимуму негативные последствия черепно мозговой травмы и служат залогом полного восстановления всех жизнеобеспечивающих функций и систем организма.
Наш центр ООО «МРТ Керчь» работает ежедневно, без выходных и перерывов с 8.00 до 20.00. Мы всегда рады помочь Вам! Берегите свое здоровье! Во время диагностируемая патология — залог успешного лечения!
Записаться на диагностику и прием в диагностический медицинский центр ООО «МРТ КЕРЧЬ» с консультативным приемом специалистов по неврологии, терапии, гастроэнтерологии, онкологии Вы можете по телефонам: +7-(978)-924-27-24; +7-(978)-924-27-25.
Ждем Вас по адресу : г. Керчь, ул. Кирова 22, 2 подъезд ( здание СРЗ)
Аппарат ИВЛ HAMILTON-MR1
Полнофункциональный реанимационный аппарат ИВЛ HAMILTON-MR1 обеспечивает непрерывную вентиляцию в отделениях интенсивной терапии, а
также при транспортировке пациентов (например: в кабинет МРТ и
обратно).
Встроенная высокопроизводительная турбина аппарата МРТ ИВЛ HAMILTON-MR1 забирает воздух из атмосферы, что позволяет не зависеть от источников
сжатого воздуха. Это снижает вес и габариты аппарата ИВЛ, что делает
его доступным для транспортировки в пределах медицинского учреждения.
В аппарате ИВЛ HAMILTON-MR1 (как и во всех существующих механических
аппаратах ИВЛ компании Hamilton Medical) предусмотрен дружественный и
понятный интерфейс со специальным режимом интеллектуальной Адаптивной поддерживающей
вентиляции ASV®.
В режиме ASV непрерывно отслеживаются механика внешнего дыхания и дыхательные усилия
пациента, регулируются: частота дыхания, дыхательный объем и время
вдоха для минимизации работы дыхания. Регулировка осуществляется
круглосуточно для каждого дыхательного цикла с момента интубации и
вплоть до экстубации.
В режиме ASV автоматически применяются стратегии защиты легких для предотвращения
осложнений: «АвтоPEEP» и волюмо- или баротравмы.
Режим также предотвращает апноэ, тахипноэ, вентиляцию мертвого
пространства и чрезмерно глубокие вдохи.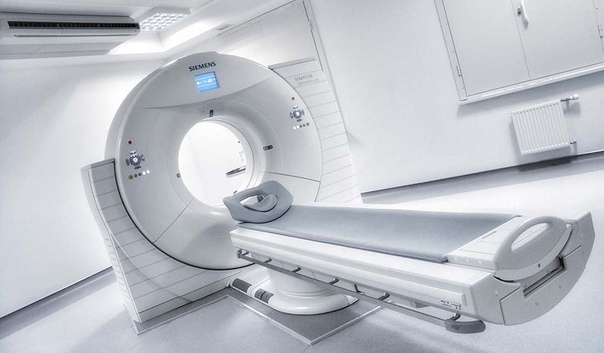 Правила стратегии защиты
Правила стратегии защиты
легких созданы таким образом, чтобы режим ASV стимулировал
спонтанное дыхание пациента.
ASV применяется в реаниматологии с 1998 года и хорошо зарекомендовал себя,
как режим, который позволяет заниматься пациентом, не отвлекаясь на
вентиляцию. Также данный режим сокращает этап отлучения пациента от
ИВЛ.
Для
того чтобы получить консультацию по аппаратам искусственной вентиляции
легких, достаточно позвонить по номеру телефона +7(495)123-39-65 или
заказать обратный звонок. Если Вы уже выбрали и решили купить
современный аппарат ИВЛ, цена и другая информация будет направлена в
письме после запроса информации на сайте. Необходимо лишь указать свое
имя, контактные данные (адрес электронной почты и номер телефона).
Внутрисосудистая лимфома: магнитно-резонансная томография коррелирует с динамикой заболевания в центральной нервной системе
Внутрисосудистая лимфома (ИВЛ) — это неходжкинская лимфома, при которой клон злокачественных лимфоцитов ограничен просветом кровеносных сосудов малого и среднего размера. Несмотря на то, что это системное заболевание, выявлен отчетливый характер поражения органов. Чаще всего поражаются нервная система, кожа и паренхиматозные органы (надпочечники). Изолированное поражение нервной системы является частым явлением и представляет собой самую большую диагностическую проблему, поскольку трудно отличить его от других микроангиопатий, таких как первичный ангиит головного мозга. 1 Повреждение нормальной ткани, вероятно, является результатом ишемии, вызванной окклюзией мелких сосудов. В частности, при отсутствии экстраневральных проявлений ИВЛ заболевание часто ускользает от диагноза, поскольку поражения небольшие и глубоко расположены и, следовательно, подвержены ошибкам выборки или расположены в чувствительных областях, что исключает биопсию.
Несмотря на то, что это системное заболевание, выявлен отчетливый характер поражения органов. Чаще всего поражаются нервная система, кожа и паренхиматозные органы (надпочечники). Изолированное поражение нервной системы является частым явлением и представляет собой самую большую диагностическую проблему, поскольку трудно отличить его от других микроангиопатий, таких как первичный ангиит головного мозга. 1 Повреждение нормальной ткани, вероятно, является результатом ишемии, вызванной окклюзией мелких сосудов. В частности, при отсутствии экстраневральных проявлений ИВЛ заболевание часто ускользает от диагноза, поскольку поражения небольшие и глубоко расположены и, следовательно, подвержены ошибкам выборки или расположены в чувствительных областях, что исключает биопсию.
При отсутствии лечения ИВЛ имеет рецидивно-ремиттирующий или рецидивно-прогрессирующий клинический курс. Чтобы определить рентгенографические корреляты потенциальной диагностической выгоды, мы ретроспективно проанализировали результаты магнитно-резонансной томографии (МРТ) в пяти случаях ИВЛ.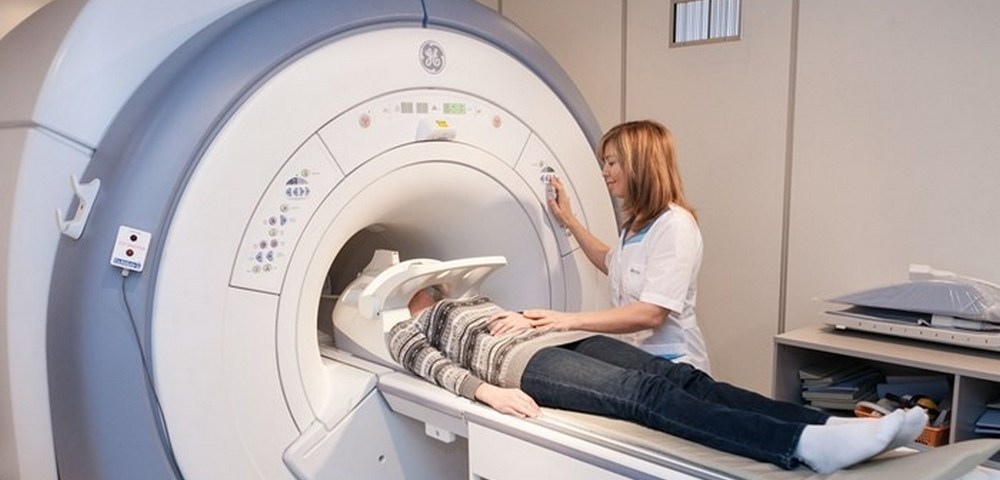 Учитывая известную ишемическую природу поражений ИВЛ, нас особенно интересовали диффузионно-взвешенные последовательности МРТ (DWI). С момента внедрения DWI в повседневную клиническую практику этот вопрос не изучался. Мы также проанализировали снимки МРТ, полученные после начала терапии, чтобы выяснить, существуют ли рентгенографические корреляты ответа на лечение.
Учитывая известную ишемическую природу поражений ИВЛ, нас особенно интересовали диффузионно-взвешенные последовательности МРТ (DWI). С момента внедрения DWI в повседневную клиническую практику этот вопрос не изучался. Мы также проанализировали снимки МРТ, полученные после начала терапии, чтобы выяснить, существуют ли рентгенографические корреляты ответа на лечение.
ПРЕДМЕТЫ И МЕТОДЫ
В период с 1999 по 2002 год мы наблюдали восемь пациентов с ИВЛ в нейроонкологической службе Массачусетской больницы общего профиля и больницы Бригама и женщин.Диагноз был установлен на основании биопсии ткани в трех случаях (рис. 1). У двух пациентов (72M, 79M), у которых не удалось получить биопсию ткани (критическое состояние у одного пациента, поражения спинного мозга и глубоко расположенные небольшие полушарные поражения у другого пациента), анализ спинномозговой жидкости в сочетании с клинической картиной привел к диагноз ИВЛ (см. таблицу 1). Трое пациентов не были включены в это исследование. У двух из этих пациентов мы не смогли установить ни морфологический диагноз, ни проточную цитометрию, ни молекулярный диагноз лимфомы.У третьего пациента неврологические симптомы и рентгенологические аномалии головного мозга полностью отсутствовали.
У двух из этих пациентов мы не смогли установить ни морфологический диагноз, ни проточную цитометрию, ни молекулярный диагноз лимфомы.У третьего пациента неврологические симптомы и рентгенологические аномалии головного мозга полностью отсутствовали.
Стол 1
Рентгенологические данные пациентов, включенных в настоящее исследование
Рисунок 1
Внутрисосудистая лимфома: злокачественные лимфоциты заполняют лептоменингеальную вену (стрелки; окраска H&E) (случай 39F; см. Таблицу 1).
У всех пациентов использовался стандартизированный протокол расширенной магнитно-резонансной нейровизуализации.Помимо анатомических изображений до и после введения гадолиния, DWI предоставила физиологическую информацию. Последовательность построения плоских изображений, взвешенных по диффузионно-взвешенному эхо-сигналу, использовалась для получения данных для создания карт кажущегося коэффициента диффузии (ADC). Шесть изображений с высоким значением b (1000 мм 2 / с) и одно изображение с низким значением b (3 мм 2 / с) были получены для каждого из 23 осевых срезов. Для каждого изображения использовалось 3 возбуждения, чтобы улучшить отношение сигнал / шум.Были использованы следующие параметры: TR = 6 с, TE = 72,9 мс, диффузионное кодирование = 47 мс, матрица 128 × 128, поле зрения 22 × 22, толщина среза 5 мм, интервал 1 мм. Временные точки изображения в этом ретроспективном анализе не были стандартизованы. Часто пациенты проходили несколько МРТ до установления диагноза. После начала химиотерапии МРТ проводилась не реже одного раза в два месяца.
Шесть изображений с высоким значением b (1000 мм 2 / с) и одно изображение с низким значением b (3 мм 2 / с) были получены для каждого из 23 осевых срезов. Для каждого изображения использовалось 3 возбуждения, чтобы улучшить отношение сигнал / шум.Были использованы следующие параметры: TR = 6 с, TE = 72,9 мс, диффузионное кодирование = 47 мс, матрица 128 × 128, поле зрения 22 × 22, толщина среза 5 мм, интервал 1 мм. Временные точки изображения в этом ретроспективном анализе не были стандартизованы. Часто пациенты проходили несколько МРТ до установления диагноза. После начала химиотерапии МРТ проводилась не реже одного раза в два месяца.
Трое пациентов получали химиотерапию метотрексатом (8 г / м 2 ) с двухнедельными интервалами, а один пациент — комбинированную химиотерапию (метотрексат, циклофосфамид, адриамицин, винкристин, преднизон).Один пациент умер до начала терапии.
РЕЗУЛЬТАТЫ
Рентгенографические данные для всех пяти пациентов, включенных в это исследование, сведены в таблицу 1. МРТ выявила множественные поражения, разбросанные по полушариям головного мозга, как наиболее частую рентгенографическую картину ИВЛ, наблюдаемую у всех пациентов. Реже поражались ствол мозга (три пациента) и мозжечок (один пациент). Поражения располагались глубоко в белом веществе полушарий или близко к коре головного мозга (рис. 2А, 3А).У двух пациентов было обнаружено диффузное поражение спинного мозга (рис. 4), у одного из которых также была пояснично-крестцовая радикулопатия. У одного пациента была оптическая нейропатия. При первоначальном проявлении, обычно через несколько дней или недель после начала клинического синдрома, на диффузно-взвешенных изображениях наблюдались гиперинтенсивные поражения, указывающие на ишемию, у трех из четырех пациентов, у которых эти изображения были получены в этот момент времени. У другого пациента DWI показал множественные гиперинтенсивные поражения полушарий через 12 дней после нормальной МРТ (рис. 2B).У четырех пациентов поражения также были идентифицированы как гиперинтенсивные области на последовательностях восстановления с инверсией, ослабленной жидкостью (FLAIR).
МРТ выявила множественные поражения, разбросанные по полушариям головного мозга, как наиболее частую рентгенографическую картину ИВЛ, наблюдаемую у всех пациентов. Реже поражались ствол мозга (три пациента) и мозжечок (один пациент). Поражения располагались глубоко в белом веществе полушарий или близко к коре головного мозга (рис. 2А, 3А).У двух пациентов было обнаружено диффузное поражение спинного мозга (рис. 4), у одного из которых также была пояснично-крестцовая радикулопатия. У одного пациента была оптическая нейропатия. При первоначальном проявлении, обычно через несколько дней или недель после начала клинического синдрома, на диффузно-взвешенных изображениях наблюдались гиперинтенсивные поражения, указывающие на ишемию, у трех из четырех пациентов, у которых эти изображения были получены в этот момент времени. У другого пациента DWI показал множественные гиперинтенсивные поражения полушарий через 12 дней после нормальной МРТ (рис. 2B).У четырех пациентов поражения также были идентифицированы как гиперинтенсивные области на последовательностях восстановления с инверсией, ослабленной жидкостью (FLAIR).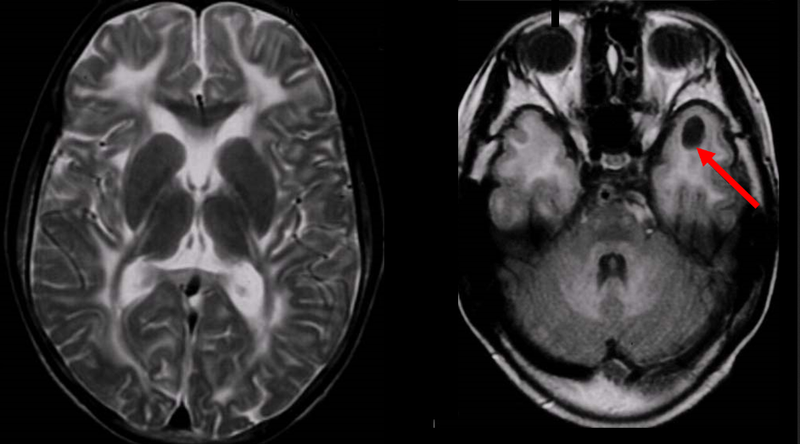 Первоначальное усиление контраста наблюдалось в трех случаях.
Первоначальное усиление контраста наблюдалось в трех случаях.
Рисунок 2
Кейс 60М. (A) Типичный вид острой стадии внутрисосудистой лимфомы. На изображении, взвешенном по диффузии (слева), показаны области коры головного мозга с ограниченной диффузией протонов, разбросанные по обоим полушариям. По крайней мере, поражения левой передней и правой задней лобных частей могут быть идентифицированы на карте кажущегося коэффициента диффузии как гипоинтенсивный сигнал (в центре) и на экспоненциальном изображении как гиперинтенсивный сигнал.Это созвездие соответствует областям острой ишемии. (B) Первый набор диффузно-взвешенных изображений (три верхних изображения) был сделан в начале неврологического синдрома пациента (подострая энцефалопатия). Второй набор взят из исследования, проведенного через 12 дней (три нижних изображения).
Рисунок 3
Корпус 39F. (A) Динамическое развитие и разрешение поражений у пациента с ИВЛ до начала химиотерапии. Показаны изображения, взвешенные по диффузии, из первоначальной презентации (верхний ряд), а также последующих исследований через семь месяцев (средний ряд) и девять месяцев (нижний ряд).Рассеянные точечные гиперинтенсивные области указывают на ограниченную диффузию протонов, соответствующую острой ишемии в различных сосудистых территориях. (B) Эволюция поражений до начала химиотерапии от подострой стадии (слева: последовательность FLAIR, показывающая несколько областей инфаркта, вовлекающих кору и подкорковое белое вещество; посередине: T1 с гадолинием, круговой паттерн усиления) до хронической стадии (справа: T1 без гадолиния, ламинарный некроз, год спустя).
Показаны изображения, взвешенные по диффузии, из первоначальной презентации (верхний ряд), а также последующих исследований через семь месяцев (средний ряд) и девять месяцев (нижний ряд).Рассеянные точечные гиперинтенсивные области указывают на ограниченную диффузию протонов, соответствующую острой ишемии в различных сосудистых территориях. (B) Эволюция поражений до начала химиотерапии от подострой стадии (слева: последовательность FLAIR, показывающая несколько областей инфаркта, вовлекающих кору и подкорковое белое вещество; посередине: T1 с гадолинием, круговой паттерн усиления) до хронической стадии (справа: T1 без гадолиния, ламинарный некроз, год спустя).
Рисунок 4
Корпус 72М.Т2-взвешенные изображения шейного и верхнегрудного отделов позвоночника пациента с внутрисосудистой лимфомой при первичном обращении (слева) и после достижения частичной ремиссии (справа; 13 месяцев химиотерапии высокими дозами метотрексата). Диффузная гиперинтенсивная аномалия сигнала сопровождала клинический синдром прогрессирующего парапареза и нейрогенной дисфункции мочевого пузыря у пациента. Во время второй МРТ аномалии сигнала исчезли, и пациент ходил без посторонней помощи.
Диффузная гиперинтенсивная аномалия сигнала сопровождала клинический синдром прогрессирующего парапареза и нейрогенной дисфункции мочевого пузыря у пациента. Во время второй МРТ аномалии сигнала исчезли, и пациент ходил без посторонней помощи.
Поражения
DWI либо исчезли, либо следовали типичной картине ишемического инсульта мелких сосудов с развитием аномального сигнала FLAIR с последующим усилением гадолинием в подострой стадии и потерей ткани в хронической стадии.Подострая или хроническая фаза ИВЛ сопровождалась удлинением T2 в области поражений, вероятно, представляющих глиоз в результате хронической ишемии и прямого повреждения тканей опухолевыми клетками. Поражения коры в конечном итоге привели к ламинарному некрозу (рис. 3B).
Необработанная ИВЛ имела рецидивирующее прогрессирующее течение (рис. 3А). Каждое обострение происходило по той же схеме, что и описанная выше: возникали новые поражения, первоначально характеризовавшиеся ограниченной диффузией протонов с последующим удлинением T2, усилением и, в конечном итоге, потерей ткани. В какой-то момент наблюдались поражения на разных стадиях развития.
В какой-то момент наблюдались поражения на разных стадиях развития.
Отклонения DWI и FLAIR оказались частично обратимыми, что коррелирует с ответом на химиотерапию (рис. 4).
ОБСУЖДЕНИЕ
Мы задокументировали динамическое развитие и разрешение поражений нервной системы у пяти пациентов с ИВЛ с помощью МРТ.
DWI оказался наиболее чувствительной последовательностью МРТ во время острой фазы ИВЛ. Корреляция со степенью заболевания, оцененная при клиническом обследовании, противоречива.DWI обеспечивает контраст изображения, зависящий от молекулярного движения воды, и оказался наиболее полезным при диагностике острой ишемии. Глубокое ограничение диффузии воды проявляется в течение нескольких минут или часов после ишемии, отражая возможные перемещения воды из внеклеточного во внутриклеточное пространство или изменения натрий / калиевого АТФ-зависимого насосного механизма клеточной мембраны. 2 На диффузно-взвешенных изображениях это приводит к гиперинтенсивному сигналу, а на картах ADC — к гипоинтенсивному сигналу. Изменения T2 при ишемии происходят несколько позже, через 12 часов, а повышение уровня гадолиния — в течение 48 часов. Нормализация ADC происходит в течение одной-четырех недель после ишемического события. 2 Изменения DWI были также замечены нами и другими при образовании лимфомы в паренхиме головного мозга, что, возможно, отражает плотность агрегатов лимфоидной опухоли. 2, 3 Таким образом, изменения DWI могут сопровождать как ишемию, связанную с ИВЛ, так и перемещение опухолевых клеток через стенку сосудов в белое вещество головного мозга.Хотя наши данные свидетельствуют о том, что ишемия представляет собой важный патогенетический механизм ИВЛ, мы наблюдали нормальный DWI у симптомного пациента с ИВЛ, что указывает на существование других механизмов. На хронической стадии заболевания изображения FLAIR служили лучшим маркером степени заболевания. Опять же, корреляция с клинической картиной часто была плохой, а ее прогностическая ценность для исхода была низкой.
Изменения T2 при ишемии происходят несколько позже, через 12 часов, а повышение уровня гадолиния — в течение 48 часов. Нормализация ADC происходит в течение одной-четырех недель после ишемического события. 2 Изменения DWI были также замечены нами и другими при образовании лимфомы в паренхиме головного мозга, что, возможно, отражает плотность агрегатов лимфоидной опухоли. 2, 3 Таким образом, изменения DWI могут сопровождать как ишемию, связанную с ИВЛ, так и перемещение опухолевых клеток через стенку сосудов в белое вещество головного мозга.Хотя наши данные свидетельствуют о том, что ишемия представляет собой важный патогенетический механизм ИВЛ, мы наблюдали нормальный DWI у симптомного пациента с ИВЛ, что указывает на существование других механизмов. На хронической стадии заболевания изображения FLAIR служили лучшим маркером степени заболевания. Опять же, корреляция с клинической картиной часто была плохой, а ее прогностическая ценность для исхода была низкой. У двух наших пациентов были обширные гиперинтенсивные нарушения сигнала Т2, которые, по крайней мере, частично разрешились с помощью химиотерапии.
У двух наших пациентов были обширные гиперинтенсивные нарушения сигнала Т2, которые, по крайней мере, частично разрешились с помощью химиотерапии.
В качестве маркера ответа на терапию повышение уровня гадолиния было менее полезным, чем при паренхиматозной лимфоме ЦНС. Отсутствие очагов, усиливающих контраст, не указывает на полную ремиссию. Мы использовали комбинацию клинических переменных (разрешение неврологических признаков и симптомов или экстраневральных проявлений, таких как кожная сыпь или аутоиммунная гемолитическая анемия), данные DWI (разрешение поражений, отсутствие образования новых поражений) и МР-изображения с усилением гадолиния для руководства химиотерапией.Повторные биопсии экстраневральных участков и анализы спинномозговой жидкости служили маркерами остаточного заболевания в отдельных случаях.
Хотя польза МРТ при ИВЛ с вовлечением нервной системы была отмечена, данные DWI редко приводились в предыдущих отчетах об изменениях нейровизуализации у пациентов с ИВЛ. 4– 6 Наиболее часто регистрируемые результаты МРТ при ИВЛ представляют собой гиперинтенсивные мультифокальные поражения на Т2-взвешенных изображениях. 1, 4, 5, 7, 8, 9, 10, 11, 12, 13, 14, 15, 160004 Подкорковое белое вещество поражается чаще, чем кора, подкорковые ядра или структуры ствола мозга.Мелкие сосуды (артериолы, капилляры, посткапиллярные венулы) поражаются чаще, чем крупные сосуды (виллизиев круг, дуральные синусы; ссылка 13). ИВЛ также может проявляться как единичные или множественные массовые поражения. 12 Увеличение гадолиния зависит от времени МРТ. Менее чем в трети случаев, описанных в литературе, улучшение наблюдалось при первоначальном МРТ. Последующее сканирование выявило улучшение еще на 10%. Поражение твердой мозговой оболочки и / или лептоменингеальное поражение, на что указывает повышение уровня гадолиния, присутствовало у небольшого числа пациентов, 4, 11, 17 , как и очаги кровотечения.
4– 6 Наиболее часто регистрируемые результаты МРТ при ИВЛ представляют собой гиперинтенсивные мультифокальные поражения на Т2-взвешенных изображениях. 1, 4, 5, 7, 8, 9, 10, 11, 12, 13, 14, 15, 160004 Подкорковое белое вещество поражается чаще, чем кора, подкорковые ядра или структуры ствола мозга.Мелкие сосуды (артериолы, капилляры, посткапиллярные венулы) поражаются чаще, чем крупные сосуды (виллизиев круг, дуральные синусы; ссылка 13). ИВЛ также может проявляться как единичные или множественные массовые поражения. 12 Увеличение гадолиния зависит от времени МРТ. Менее чем в трети случаев, описанных в литературе, улучшение наблюдалось при первоначальном МРТ. Последующее сканирование выявило улучшение еще на 10%. Поражение твердой мозговой оболочки и / или лептоменингеальное поражение, на что указывает повышение уровня гадолиния, присутствовало у небольшого числа пациентов, 4, 11, 17 , как и очаги кровотечения. 16 Сообщалось о нескольких случаях с нормальным МРТ головного мозга при первоначальной оценке с неврологическим дефицитом или без него. 16 Бессимптомные поражения МРТ кажутся редкими (наш случай; ссылка 10), но это число, вероятно, занижено, поскольку полные оценки стадии, включая визуализацию всего нейраксиса, широко не выполняются. Поражение спинного мозга является обычным явлением, но чувствительность МРТ низкая. Менее 40% пациентов с подтвержденной аутопсией ИВЛ пуповины имели аномальные МРТ, неизменно гиперинтенсивные поражения Т2. 10, 13, 17 Немногие авторы описали динамическую эволюцию и разрешение повышенных контрастов и гиперинтенсивных Т2 поражений. 4, 5, 10, 16
16 Сообщалось о нескольких случаях с нормальным МРТ головного мозга при первоначальной оценке с неврологическим дефицитом или без него. 16 Бессимптомные поражения МРТ кажутся редкими (наш случай; ссылка 10), но это число, вероятно, занижено, поскольку полные оценки стадии, включая визуализацию всего нейраксиса, широко не выполняются. Поражение спинного мозга является обычным явлением, но чувствительность МРТ низкая. Менее 40% пациентов с подтвержденной аутопсией ИВЛ пуповины имели аномальные МРТ, неизменно гиперинтенсивные поражения Т2. 10, 13, 17 Немногие авторы описали динамическую эволюцию и разрешение повышенных контрастов и гиперинтенсивных Т2 поражений. 4, 5, 10, 16
Дифференциальная диагностика микроангиопатий ИВЛ и ЦНС другой этиологии, например васкулита, остается сложной задачей. 4, 9, 14 ИВЛ и первичный ангиит ЦНС демонстрируют заметное совпадение клинической картины, лабораторных данных и рентгенологических данных.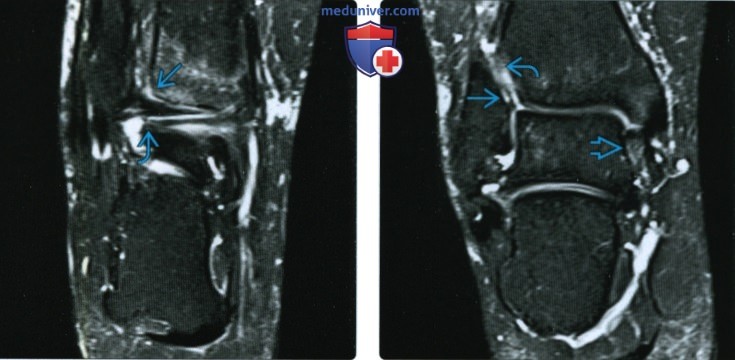 Оба состояния вызывают инфаркты мелких сосудов, разбросанных по глубокому белому веществу полушарий или спинного мозга. 5 Одно только МРТ не может решить эту диагностическую дилемму.
Оба состояния вызывают инфаркты мелких сосудов, разбросанных по глубокому белому веществу полушарий или спинного мозга. 5 Одно только МРТ не может решить эту диагностическую дилемму.
В двух случаях данной серии диагноз лимфома ЦНС был установлен, но гистопатологические признаки внутрисосудистых опухолевых клеток отсутствовали. По оценкам, 40–80% случаев ИВЛ остаются недиагностированными до вскрытия, эти два случая отражают общую клиническую ситуацию. Их динамический паттерн изменений МРТ не отличался от такового у трех пациентов с гистопатологическим диагнозом.Включая их в наше исследование, мы поощряем рассмотрение диагноза ИВЛ на основе клинических данных, рентгенологических данных и лабораторных исследований, даже если серийные биопсии не являются диагностическими или не могут быть выполнены.
Основываясь на нашем опыте и опыте других, рентгенографическую диагностику ИВЛ предлагает:
мультифокальных поражений DWI в сочетании с аномалиями сигнала T2, подтверждающих диагноз ишемии или инфаркта мелких сосудов
Повышение уровня гадолиния, появляющееся вблизи изменений T2 или DWI и сохраняющееся или увеличивающееся в течение недель или месяцев
— динамический образец поражений МРТ с разрешением одних поражений DWI или T2 и новым появлением других.

Эти данные должны привести к биопсии кожи, надпочечников, печени, почек, мозга или других предполагаемых участков поражения. Прогноз для ИВЛ был мрачным, смертность составила более 80%. 1 Однако химиотерапия может вызвать у пациентов длительный ответ. 15, 18 Успешная терапия зависит от ранней диагностики, предшествующей необратимому ишемическому повреждению, и может устранить диффузию, нарушения FLAIR, а также усиление очагов опухоли, сопровождающее как клиническое неврологическое улучшение, так и разрешение лабораторных отклонений.
ССЫЛКИ
- ↵
Стекло J , Hochberg FH, Miller DC. Внутрисосудистый лимфоматоз. Системное заболевание с неврологическими проявлениями. Cancer1993; 71: 3156–64.
- ↵
Schaefer PW , Grant PE, Gonzalez RG. МРТ головного мозга с диффузионно-взвешенной визуализацией.
 Радиология 2000; 217: 331–45.
Радиология 2000; 217: 331–45. - ↵
Moritani T , Shrier DA, Numaguchi Y, et al. Диффузионно-взвешенная эхопланарная МРТ: клиническое применение и подводные камни — иллюстрированное эссе. Clin Imaging 2000; 24: 181–92.
- ↵
Calamia KT , Miller A, Shuster EA, et al. Внутрисосудистый лимфоматоз. Отчет о десяти пациентах с поражением центральной нервной системы и обзор процесса болезни. Adv Exp Med Biol 1999; 455: 249–65.
- ↵
Liow K , Asmar P, Liow M, et al. Внутрисосудистый лимфоматоз: вклад результатов МРТ головного мозга в диагностику. J Neuroimaging 2000; 10: 116–18.
- ↵
De Bruecker Y , Demaerel P, Wilms G, et al. Случай гемипареза, связанного с поражением черепных нервов из-за внутрисосудистого лимфоматоза (2003: 4b).
 Eur Radiol 2003; 13: 1753–5.
Eur Radiol 2003; 13: 1753–5. - ↵
Demirer T , Dail DH, Aboulafia DM.Четыре различных случая внутрисосудистого лимфоматоза и обзор литературы. Рак 1994; 73: 1738–45.
- ↵
Liszka U , Drlicek M, Hitzenberger P, et al. Внутрисосудистый лимфоматоз: клинико-патологическое исследование трех случаев. J Cancer Res Clin Oncol 1994; 120: 164–8.
- ↵
Sienknecht CW , Whetsell WO, Pollock P. Внутрисосудистая злокачественная лимфома («злокачественный ангиоэндотелиоматоз»), имитирующая первичный ангиит центральной нервной системы.J Rheumatol1995; 22: 1769–70.
- ↵
Hashimoto H , Naritomi H, Kazui S, et al. Пресимптомные поражения головного мозга на МРТ у пациента с внутрисосудистым злокачественным лимфоматозом.
 J Neuroimaging 1998; 8: 110–13.
J Neuroimaging 1998; 8: 110–13. - ↵
Williams RL , Meltzer CC, Smirniotopoulos JG, et al. МРТ головного мозга при внутрисосудистом лимфоматозе. AJNR Am J Neuroradiol 1998; 19: 427–31.
- ↵
Massimino M , Giardini R, Cefalo G, et al. Внутрисосудистый лимфоматоз (ИЛ) у ребенка, имитирующий опухоль задней черепной ямки. Журнал Neurooncol 2001; 51: 47–50.
- ↵
Amagasaki K , Yamazaki H, Ohmori K, et al. Злокачественный внутрисосудистый лимфоматоз, связанный со стенозом вен. История болезни. Журнал Neurosurg 1999; 90: 355–8.
- ↵
al Chalabi A , Sivakumaran M, Holton J, et al. Случай внутрисосудистого злокачественного лимфоматоза (ангиотропная лимфома) с повышенными титрами перинуклеарных антинейтрофильных цитоплазматических антител — связь, о которой до сих пор не сообщалось.
 Clin Lab Haematol 1994; 16: 363–9.
Clin Lab Haematol 1994; 16: 363–9. - ↵
DiGiuseppe JA , Nelson WG, Seifter EJ, et al. Внутрисосудистый лимфоматоз: клинико-патологическое исследование 10 случаев и оценка ответа на химиотерапию. Дж. Клин Онкол 1994; 12: 2573–9.
- ↵
Kenez J , Barsi P, Majtenyi K, et al. Может ли внутрисосудистый лимфоматоз имитировать тромбоз синуса? Отчет о болезни с последующим наблюдением через 8 месяцев и летальным исходом. Нейрорадиология 2000; 42: 436–40.
- ↵
Martin-Duverneuil N , Mokhtari K, Behin A, et al. Внутрисосудистый злокачественный лимфоматоз. Нейрорадиология 2002; 44: 749–54.
- ↵
Baehring JM , Longtine J, Hochberg FH. Новый подход к диагностике и лечению внутрисосудистой лимфомы.
 Журнал Neurooncol2003; 61: 237–48.
Журнал Neurooncol2003; 61: 237–48.
Различные модели визуализации ПКНСЛ и ИВЛ: клинический случай | BMC Neurology
Пациент в данном описании случая показал неврологические отклонения, которые не были локализованы как очаговое поражение. Более того, было трудно объяснить эти отклонения с помощью МРТ головного мозга или определить причину при физикальном обследовании. Согласно диагностическим критериям аутоиммунного энцефалита от Lancet Neurology в 2016 году [5], хотя это не было поражением, ограниченным медиальной височной долей в T2WI, наблюдались прогрессирующие неврологические аномалии подострого начала и плеоцитоз спинномозговой жидкости, предполагающие аутоиммунный энцефалит.Иммуномодулирующая терапия была назначена в связи с подозрением на аутоиммунный энцефалит, но без эффекта. Последующая МРТ головного мозга выявила прогрессирующую картину, которая не могла быть объяснена общей сосудистой причиной. Хотя PCNSL была диагностирована с помощью биопсии головного мозга, МРТ головного мозга пациента постоянно показывала уникальное поражение, не типичное для PCNSL.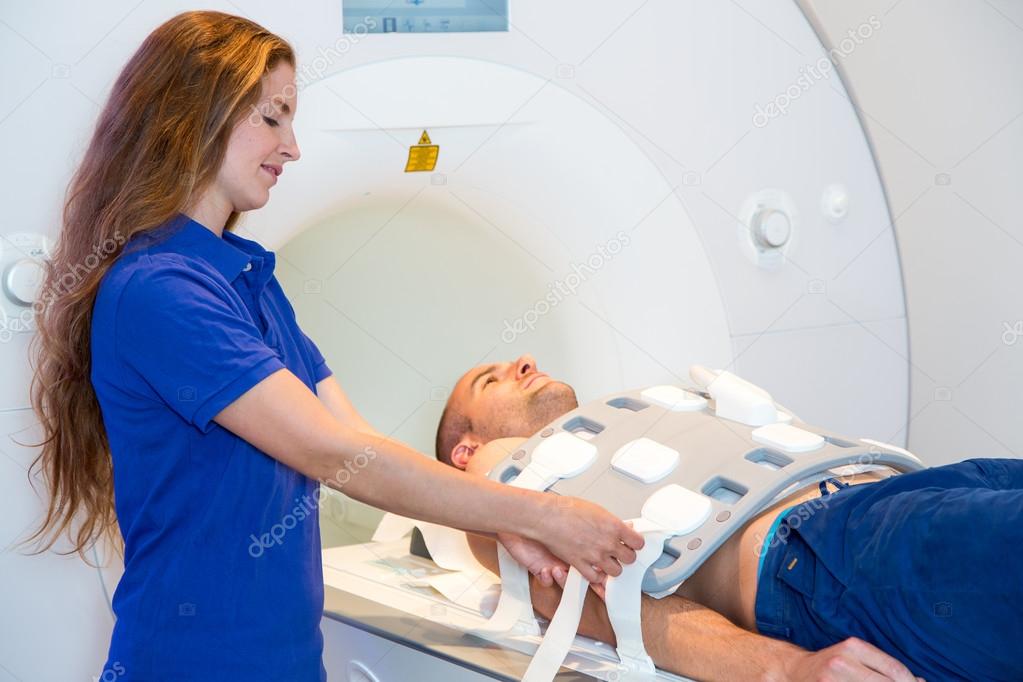 Был частичный ответ на раннюю стероидную терапию; однако симптомы повторились. Вероятность нейровоспалительного заболевания была низкой, поскольку пациент не отвечал на стероиды.Мы диагностировали у пациента ПКНСЛ на основании результатов биопсии и сразу начали химиотерапию.
Был частичный ответ на раннюю стероидную терапию; однако симптомы повторились. Вероятность нейровоспалительного заболевания была низкой, поскольку пациент не отвечал на стероиды.Мы диагностировали у пациента ПКНСЛ на основании результатов биопсии и сразу начали химиотерапию.
ИВЛ, с другой стороны, имеет клинические симптомы, сходные с симптомами других заболеваний, таких как демиелинизирующее заболевание, васкулит, инсульт и церебральная аутосомно-доминантная артериопатия с подкорковыми инфарктами и лейкоэнцефалопатией (CADASIL). Поэтому быстро и точно диагностировать его крайне сложно [6]. Из-за неспецифических клинических симптомов и результатов визуализации более чем у половины пациентов с ИВЛ диагностируется ИВЛ посмертно [7].
PCNSL выявляется на МРТ головного мозга как единичная, однородная, сильно контрастирующая паренхиматозная масса. Более того, отек, наблюдаемый на T2WI, коррелирует с размером повышенного контрастного поражения на T1-взвешенных изображениях. Эти характеристики отражают характеристики PCNSL, такие как гиперцеллюлярность, высокое ядерное / цитоплазматическое соотношение и нарушение гематоэнцефалического барьера. Поражение обычно располагается в центральном полушарии или перивентрикулярном белом веществе головного мозга. Чаще всего возникает в лобной доле.Результаты МРТ головного мозга при ИВЛ представляют собой множественные аномалии на диффузно-взвешенных изображениях (DWI), сопровождаемые аномальным сигналом на T2WI и усилением контрастности, которое предшествует изменениям T2WI или DWI и сохраняется в течение нескольких недель или нескольких месяцев. И различные изменения подкоркового белого вещества или появление нового поражения наблюдаются на T2WI или DWIs [8]. У нашего пациента высокая интенсивность сигнала наблюдалась на T2WI ранней МРТ, но не проявлялась как острый ишемический инсульт на DWI и карте кажущегося коэффициента диффузии (ADC).На последующем изображении на T2WI наблюдались очаги поражения с контрастным усилением и усиленный отек. Более того, на карте DWI и ADC наблюдались острое ишемическое поражение и отек большого размера по сравнению с размером контрастного усиления. В этом случае отек был больше, чем поражение с контрастным усилением, и усиление контраста началось после того, как было обнаружено изменение сигнала на T2WI и DWI.
Поражение обычно располагается в центральном полушарии или перивентрикулярном белом веществе головного мозга. Чаще всего возникает в лобной доле.Результаты МРТ головного мозга при ИВЛ представляют собой множественные аномалии на диффузно-взвешенных изображениях (DWI), сопровождаемые аномальным сигналом на T2WI и усилением контрастности, которое предшествует изменениям T2WI или DWI и сохраняется в течение нескольких недель или нескольких месяцев. И различные изменения подкоркового белого вещества или появление нового поражения наблюдаются на T2WI или DWIs [8]. У нашего пациента высокая интенсивность сигнала наблюдалась на T2WI ранней МРТ, но не проявлялась как острый ишемический инсульт на DWI и карте кажущегося коэффициента диффузии (ADC).На последующем изображении на T2WI наблюдались очаги поражения с контрастным усилением и усиленный отек. Более того, на карте DWI и ADC наблюдались острое ишемическое поражение и отек большого размера по сравнению с размером контрастного усиления. В этом случае отек был больше, чем поражение с контрастным усилением, и усиление контраста началось после того, как было обнаружено изменение сигнала на T2WI и DWI. Эти паттерны отличались от обычных результатов на изображениях PCNSL или IVL.
Эти паттерны отличались от обычных результатов на изображениях PCNSL или IVL.
Кортикостероиды обладают цитотоксическим действием на В-лимфоциты и используются в качестве дополнительного лечения для уменьшения поражения PCNSL [9].Следовательно, они могут повлиять на результаты биопсии. Однако предыдущее исследование показало, что введение кортикостероидов перед биопсией не повлияло на результат [10]. Результаты предполагают, что цитотоксичность кортикостероидов не влияет на диагноз, и введение кортикостероидов не следует откладывать для гистопатологической диагностики. В этом случае перед проведением биопсии вводили кортикостероид, но гистопатологически диагностировать лимфому не составляло труда.Однако радиологический результат отличался от типичного для PCNSL тем, что усиление контраста произошло позже, чем изменения T2WI и DWI. Считается, что разница была вызвана задержкой в усилении контраста, которая могла быть вызвана цитотоксическим эффектом кортикостероида, введенного перед получением изображения с усиленным контрастом, на клетки лимфомы.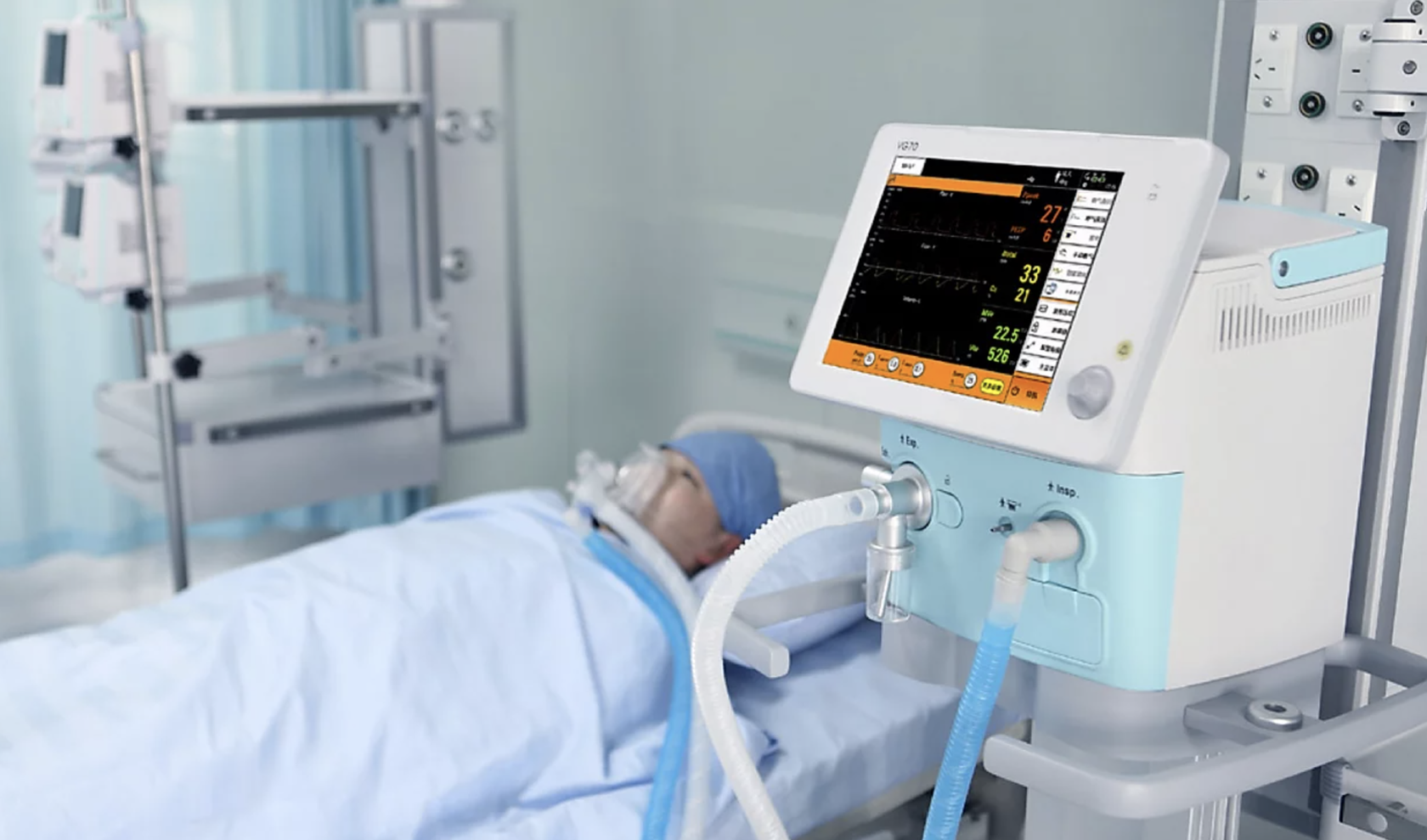 В то же время ожидается, что цитотоксические эффекты могли задержать нарастание отека, и в результате он показал аномальный характер.Более того, хотя клетки лимфомы были в большом количестве в образцах биопсии мозга, возможно, что они не были обнаружены в образцах внутрисосудистой биопсии из-за цитотоксического действия кортикостероида в кровеносных сосудах. Проведение биопсии головного мозга — сложная задача, которая сопряжена с высоким риском осложнений и последствий. С другой стороны, биопсия кожи относительно проста. ИВЛ в основном обнаруживается в коже и центральной нервной системе. Таким образом, биопсия кожи может быть более эффективным методом диагностики даже до введения кортикостероидов [11].
В то же время ожидается, что цитотоксические эффекты могли задержать нарастание отека, и в результате он показал аномальный характер.Более того, хотя клетки лимфомы были в большом количестве в образцах биопсии мозга, возможно, что они не были обнаружены в образцах внутрисосудистой биопсии из-за цитотоксического действия кортикостероида в кровеносных сосудах. Проведение биопсии головного мозга — сложная задача, которая сопряжена с высоким риском осложнений и последствий. С другой стороны, биопсия кожи относительно проста. ИВЛ в основном обнаруживается в коже и центральной нервной системе. Таким образом, биопсия кожи может быть более эффективным методом диагностики даже до введения кортикостероидов [11].
Лечение ИВЛ и ПЦНСЛ аналогично лечению неходжкинской лимфомы. Предыдущее исследование показало, что химиотерапия с использованием режима R-CHOP (ритуксимаб, циклофосфамид, доксорубицин, винкристин и преднизон) значительно улучшила частоту полной ремиссии и окончательную выживаемость пациентов с PCNSL [4]. Как видно из этого случая, хотя PCNSL имеет эффективные методы лечения, прогноз может быть плохим, если диагноз задерживается. Это особенно верно для ИВЛ, которая демонстрирует другие рентгенологические данные и клинические признаки, отличные от PCNSL [11].
Как видно из этого случая, хотя PCNSL имеет эффективные методы лечения, прогноз может быть плохим, если диагноз задерживается. Это особенно верно для ИВЛ, которая демонстрирует другие рентгенологические данные и клинические признаки, отличные от PCNSL [11].
Мы полагаем, что необходимо рассмотреть возможность ПКНСЛ или ИВЛ у пациентов с поражениями DWI, отличными от общего ишемического инсульта и нелокализованной неврологической аномалии, или нетипичных результатов МРТ головного мозга, таких как линейное усиление вдоль артериол без лабораторный результат, указывающий на аутоиммунное заболевание. Поскольку PCNSL и IVL являются излечимыми заболеваниями, это повысит вероятность успешного лечения и лучшего прогноза.
Характеристики внутрисосудистой крупноклеточной В-клеточной лимфомы на МРТ головного мозга
Реферат
РЕЗЮМЕ: ИВЛ характеризуется предрасположенностью к внутрисосудистой пролиферации опухолевых клеток.Предварительная диагностика ИВЛ затруднена из-за ее неспецифических клинических, лабораторных и визуальных проявлений.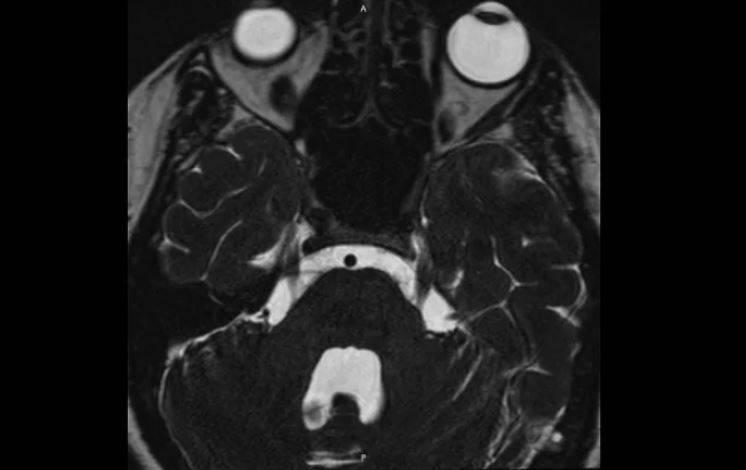 В этом исследовании изучались модели МРТ головного мозга при ИВЛ и их изменения с химиотерапией и без нее. У 9 из 11 обследованных пациентов были обнаружены отклонения от нормы. Мы определяем 5 паттернов аномальных результатов МРТ: 1) инфарктоподобные поражения, 2) неспецифические поражения белого вещества, 3) менингеальное усиление, 4) массоподобные поражения и 5) гиперинтенсивные поражения в мостах на T2WI. У семи пациентов был только один паттерн, в то время как у 2 пациентов было несколько паттернов.Поражения у 7 пролеченных пациентов отреагировали на химиотерапию. Патологические образцы выявили внутрисосудистую инфильтрацию опухолевых клеток с ассоциированными инфарктами, некрозом, застоем, демиелинизацией, васкулитом и экстравазацией опухолевых клеток. Мы пришли к выводу, что модели МРТ могут быть возможными проявлениями доминантной внутрисосудистой инфильтрации опухолевыми клетками с ассоциированной окклюзией или воспалением, в зависимости от уровня пораженных сосудов.
В этом исследовании изучались модели МРТ головного мозга при ИВЛ и их изменения с химиотерапией и без нее. У 9 из 11 обследованных пациентов были обнаружены отклонения от нормы. Мы определяем 5 паттернов аномальных результатов МРТ: 1) инфарктоподобные поражения, 2) неспецифические поражения белого вещества, 3) менингеальное усиление, 4) массоподобные поражения и 5) гиперинтенсивные поражения в мостах на T2WI. У семи пациентов был только один паттерн, в то время как у 2 пациентов было несколько паттернов.Поражения у 7 пролеченных пациентов отреагировали на химиотерапию. Патологические образцы выявили внутрисосудистую инфильтрацию опухолевых клеток с ассоциированными инфарктами, некрозом, застоем, демиелинизацией, васкулитом и экстравазацией опухолевых клеток. Мы пришли к выводу, что модели МРТ могут быть возможными проявлениями доминантной внутрисосудистой инфильтрации опухолевыми клетками с ассоциированной окклюзией или воспалением, в зависимости от уровня пораженных сосудов.
СОКРАЩЕНИЯ:
- ИВЛ
- внутрисосудистая крупноклеточная В-клеточная лимфома
- PRES
- Синдром задней обратимой энцефалопатии
- R-CHOP
- ритуксимаб с циклофосфамидом, винкристином, доксорубицином большого подтипа
4 и экстранизолином 903 IV -клеточная лимфома.
 1 Характеризуется предрасположенностью к внутрисосудистому разрастанию опухолевых клеток в мелких сосудах с предрасположенностью к центральной нервной системе и коже. 2,3 Прижизненная диагностика ИВЛ затруднена из-за различных клинических проявлений и неспецифических лабораторных данных, хотя во многих случаях обнаруживается повышение уровня ЛДГ и растворимого рецептора интерлейкина-2. 4–6 Результаты МРТ головного мозга у пациентов с ИВЛ также разнообразны; эти вариации затрудняют диагностику. 7 После установления правильного диагноза ИВЛ с помощью биопсии ткани полная ремиссия может быть достигнута с помощью химиотерапии с использованием R-CHOP. 8,9 Распознавание и тщательная интерпретация различных результатов МРТ головного мозга может облегчить раннюю диагностику и вмешательство, а также улучшить прогноз этого часто упускаемого из виду заболевания. 10
1 Характеризуется предрасположенностью к внутрисосудистому разрастанию опухолевых клеток в мелких сосудах с предрасположенностью к центральной нервной системе и коже. 2,3 Прижизненная диагностика ИВЛ затруднена из-за различных клинических проявлений и неспецифических лабораторных данных, хотя во многих случаях обнаруживается повышение уровня ЛДГ и растворимого рецептора интерлейкина-2. 4–6 Результаты МРТ головного мозга у пациентов с ИВЛ также разнообразны; эти вариации затрудняют диагностику. 7 После установления правильного диагноза ИВЛ с помощью биопсии ткани полная ремиссия может быть достигнута с помощью химиотерапии с использованием R-CHOP. 8,9 Распознавание и тщательная интерпретация различных результатов МРТ головного мозга может облегчить раннюю диагностику и вмешательство, а также улучшить прогноз этого часто упускаемого из виду заболевания. 10 Корпус серии
Объекты и методы
Институциональный комитет по этике медицинских исследований одобрил это ретроспективное исследование и отказался от информированного согласия.
 Мы ретроспективно проанализировали МРТ головного мозга у 11 последовательных пациентов, которым в период с 1998 по 2009 год был поставлен патологический диагноз ИВЛ. Двум пациентам был поставлен диагноз при патологоанатомическом исследовании, а 9 случаев были диагностированы на основании различных биопсий тканей. Биопсия включала 1 лимфатический узел, 1 легкое и костный мозг, а также 7 случайных биопсий кожи. Трое из 9 пациентов, которым была поставлена биопсия ткани, подверглись вскрытию. Медицинские карты были просмотрены на предмет их симптомов, истории болезни, лабораторных данных и лечения.
Мы ретроспективно проанализировали МРТ головного мозга у 11 последовательных пациентов, которым в период с 1998 по 2009 год был поставлен патологический диагноз ИВЛ. Двум пациентам был поставлен диагноз при патологоанатомическом исследовании, а 9 случаев были диагностированы на основании различных биопсий тканей. Биопсия включала 1 лимфатический узел, 1 легкое и костный мозг, а также 7 случайных биопсий кожи. Трое из 9 пациентов, которым была поставлена биопсия ткани, подверглись вскрытию. Медицинские карты были просмотрены на предмет их симптомов, истории болезни, лабораторных данных и лечения.МРТ выполняли на аппарате 1,5 Тл (Magnetom Vision; Siemens Healthcare, Эрланген, Германия). Осевое T2-взвешенное быстрое спин-эхо-изображение (TR = 4000 мс, TE = 99 мс), корональное T1-взвешенное изображение (TR = 570 мс, TE = 12 мс), осевое восстановление с восстановлением изображения с инверсией с ослаблением жидкости (TR = 9000 мс , TE = 110 мс, TI = 2200 мс), DWI ( b = 1000, TR = 2200 мс, TE = 103,0 мс) и аксиальные, корональные и сагиттальные МРТ изображения после внутривенного введения 0,1 ммоль / кг гадопентетата димеглумина были доступны для всех пациентов.
 Семь из 11 пациентов прошли первоначальную МРТ в течение 1 недели после поступления, а остальные 4 были просканированы в течение 2 месяцев.
Семь из 11 пациентов прошли первоначальную МРТ в течение 1 недели после поступления, а остальные 4 были просканированы в течение 2 месяцев.Три радиолога проанализировали МРТ головного мозга, и результаты были разделены на следующие категории: 1) инфарктоподобные поражения, 2) неспецифические поражения белого вещества, 3) менингеальное усиление, 4) массоподобные поражения или 5) гиперинтенсивные поражения в мостах на T2WI. Критерием инфарктоподобных поражений были гиперинтенсивные участки на T2WI с ограничением диффузии. Неспецифические поражения белого вещества определялись как гиперинтенсивные поражения с плохими краями на T2WI без масс-эффекта или аномального усиления.Критерием менингеального усиления было аномальное усиление вдоль поверхности коры с пиаарахноидальным рисунком, простирающимся на> 1 извилину в> 2 плоскостях на постконтрастных Т1-взвешенных изображениях. Критерием массоподобных поражений служили очаговые области внутри паренхимы с усилением контраста.
Результаты
Характеристики пациентов, симптомы, результаты первичной МРТ головного мозга и изменения в результатах последующих исследований МРТ представлены в интерактивной таблице.
 Пациентами были 4 мужчин и 7 женщин в возрасте от 63 до 84 лет (средний возраст 71,4 года). Симптомами были лихорадка у всех, деменция у 5, одышка у 2, изменения личности у 2 и недомогание у 1 пациента. Пятерым пациентам, включая 3 пролеченных и 2 нелеченых, было проведено патологоанатомическое исследование головного мозга (таблица).
Пациентами были 4 мужчин и 7 женщин в возрасте от 63 до 84 лет (средний возраст 71,4 года). Симптомами были лихорадка у всех, деменция у 5, одышка у 2, изменения личности у 2 и недомогание у 1 пациента. Пятерым пациентам, включая 3 пролеченных и 2 нелеченых, было проведено патологоанатомическое исследование головного мозга (таблица).Таблица
Результаты патологоанатомического исследования головного мозга
МРТ головного мозга была выполнена 11 пациентам до лечения и показала отклонения от нормы у 9 пациентов.У семи пациентов был выявлен один тип поражения, а у 2 пациентов — несколько типов. Двум пациентам не был поставлен диагноз до патологоанатомического обследования, поэтому они не получали лечения ИВЛ. Остальным 7 пациентам с отклонениями от нормы лечили ИВЛ, и все их поражения отреагировали на химиотерапию. Поражения усугубились у 2 нелеченных пациентов.
Инфарто-подобные поражения наблюдались у 2 из 11 пациентов, проявляясь в виде множественных гиперинтенсивных пятен на T2WI с ограничением диффузии в белом веществе, включая перивентрикулярные области, территорию водораздела и мозолистое тело (рис.
 1 A , — B ).У этих пациентов мультифокальные поражения уменьшились в размере и количестве после лечения. Патологоанатомическое исследование выявило множественные инфаркты с закупоркой сосудов опухолевыми клетками, некроз неправильной формы и скопление вокруг закупоренных сосудов (рис. 1 C ). Также часто наблюдались незначительные геморрагические инфаркты. Неспецифические поражения белого вещества наблюдались у 2 из 11 пациентов. Диффузная гиперинтенсивность белого вещества наблюдалась особенно в перивентрикулярных областях (рис. 2 A ).Очаговая гиперинтенсивность белого вещества также наблюдалась в подкорковых областях в случае 3. У этого пациента, у которого не была диагностирована и не лечилась специально по поводу ИВЛ, гиперинтенсивная область постепенно увеличивалась в размерах. Однако у пролеченного пациента повреждения улучшились сразу после начала лечения (рис. 2 B ). Патологоанатомическое исследование выявило диффузную демиелинизацию белого вещества с сосудами, сильно закупоренными опухолевыми клетками в соответствующих областях (рис.
1 A , — B ).У этих пациентов мультифокальные поражения уменьшились в размере и количестве после лечения. Патологоанатомическое исследование выявило множественные инфаркты с закупоркой сосудов опухолевыми клетками, некроз неправильной формы и скопление вокруг закупоренных сосудов (рис. 1 C ). Также часто наблюдались незначительные геморрагические инфаркты. Неспецифические поражения белого вещества наблюдались у 2 из 11 пациентов. Диффузная гиперинтенсивность белого вещества наблюдалась особенно в перивентрикулярных областях (рис. 2 A ).Очаговая гиперинтенсивность белого вещества также наблюдалась в подкорковых областях в случае 3. У этого пациента, у которого не была диагностирована и не лечилась специально по поводу ИВЛ, гиперинтенсивная область постепенно увеличивалась в размерах. Однако у пролеченного пациента повреждения улучшились сразу после начала лечения (рис. 2 B ). Патологоанатомическое исследование выявило диффузную демиелинизацию белого вещества с сосудами, сильно закупоренными опухолевыми клетками в соответствующих областях (рис. 2 C ).
2 C ).Рис 1.
Случай 1.Инфарктоподобное поражение у мужчины 74 лет. A , Axial T2WI показывает гиперинтенсивные пятна в области двустороннего водораздела ( белых стрелок ). B , Соответствующие области показывают ограничение диффузии на DWI ( белые стрелки ). C , Патологический образец показывает некроз неправильной формы ( двойная черная стрелка ) и скопление ( толстые черные стрелки ), окружающие закупоренный сосуд ( наконечник стрелки ) (гематоксилин-эозин, первоначальное увеличение × 25).
Рис 2.
Случай 2. Неспецифическое поражение белого вещества у мужчины 69 лет. A , Axial T2WI показывает диффузную гиперинтенсивность в двусторонних перивентрикулярных областях до лечения ( белые стрелки ). B , T2WI после лечения на 94 день показывает снижение интенсивности аномального сигнала. C , Патологический образец показывает окклюзию сосудов опухолевыми клетками ( черные стрелки ) и диффузную демиелинизацию (D) с признаками инфаркта или без них (Klüver-Barrera, исходное увеличение × 25).

Менингеальное усиление наблюдалось у 2 пациентов (рис. 3 A ). У 1 из 2 пациентов с менингеальным усилением усиление уменьшилось сразу после начала лечения. Окружающих отеков или интрапаренхиматозных поражений не наблюдалось. Патологоанатомическое исследование выявило утолщенные сосудистые стенки и инфильтрацию некротической и субэндотелиальной опухоли с обильными лимфоцитами, окружающими сосудистые стенки (рис. 3 B ). Массовидные поражения наблюдались у 1 пациента с множественными интрапаренхиматозными очаговыми усиленными поражениями и масс-эффектом (рис. 4А).На DWI не было обнаружено никаких отклонений от нормы (рис. 4 B ). После начала химиотерапии наблюдалось постепенное уменьшение усиления контраста и массового эффекта поражений (рис. 4 C ). Патологоанатомическое исследование этого пациента не проводилось. Гиперинтенсивные поражения мостов на T2WI без ограничения диффузии или усиления контраста наблюдались у 5 из 11 пациентов. Этот образец интенсивности сигнала был единственным отклонением от нормы у 4 из 5 пациентов.
 У всех 5 пациентов были обнаружены симметричные гиперинтенсивные области в центральном мосту, за исключением покрышки моста и вентролатерального моста (рис. 5 A ).Гиперинтенсивные области в мосту уменьшились в размере и интенсивности у всех 4 пациентов, прошедших лечение (Рис. 5 B ). В случае 9 последующая МРТ показала уменьшение размера поражения через 3 дня после лечения. Атрофии ствола головного мозга после лечения не наблюдалось ни в одном из этих 4 случаев.
У всех 5 пациентов были обнаружены симметричные гиперинтенсивные области в центральном мосту, за исключением покрышки моста и вентролатерального моста (рис. 5 A ).Гиперинтенсивные области в мосту уменьшились в размере и интенсивности у всех 4 пациентов, прошедших лечение (Рис. 5 B ). В случае 9 последующая МРТ показала уменьшение размера поражения через 3 дня после лечения. Атрофии ствола головного мозга после лечения не наблюдалось ни в одном из этих 4 случаев.Рис 3.
Случай 2. Улучшение менингеальной оболочки у мужчины 69 лет. , корональное T1-взвешенное изображение с усилением гадолинием показывает аномальное усиление менингеальной области вокруг височной доли до лечения ( белые стрелки ). B , Патологический образец показывает утолщение стенок пораженных сосудов с внутрипросветной ( белая стрелка ) и субэндотелиальной ( черные стрелки ) опухолевой инфильтрацией (гематоксилин-эозин, исходное увеличение × 25).

Рис 4.
Случай 4. Массовидное поражение у мужчины 70 лет. , Т1-взвешенное изображение с усилением коронарного гадолиния показывает кольцевидное усиление до лечения ( белая стрелка ). B , Axial DWI не показывает аномальной интенсивности сигнала в поражении. C , Последующее корональное T1-взвешенное изображение с усилением гадолиния показывает регресс усиления после лечения на 121 день.
Рис 5.
Случай 8. Гиперинтенсивное поражение моста на Т2-взвешенном изображении у 63-летней женщины. A , Аксиальный T2WI показывает симметричные гиперинтенсивные поражения в центре моста, за исключением покрышки моста и вентролатерального моста ( белая стрелка ). DWI показал прохождение T2 без ограничения диффузии (не показано). B , T2WI после химиотерапии показывает снижение интенсивности аномального сигнала в мосту на 85 день ( белая стрелка ).
Из всех 11 пациентов ни у одного пациента не было несоответствующего потребления жидкости или других состояний, которые могут предрасполагать к синдрому осмотической демиелинизации.
 У пациентов не было тяжелой гипертонии, судорог, реакции на химиотерапию или других состояний, которые могут привести к PRES.
У пациентов не было тяжелой гипертонии, судорог, реакции на химиотерапию или других состояний, которые могут привести к PRES.Обсуждение
Мы задокументировали результаты МРТ головного мозга у 11 пациентов с ИВЛ и определили 5 паттернов аномальных результатов; 1) инфарктоподобные поражения, 2) неспецифические поражения белого вещества, 3) менингеальное усиление, 4) массоподобные поражения и 5) гиперинтенсивные поражения в мостах на T2WI.
Инфарктоподобные поражения
Инфарктоподобные поражения позволяют предположить, что опухоль поражает преимущественно мелкие артерии. 11 Эта картина наблюдалась у 36% пациентов с ИВЛ, которым проводилась МРТ головного мозга. 7 Хотя инфарктоподобные поражения наблюдались только у 2 пациентов в нашем исследовании (2/11), 4 из 5 патологоанатомических исследований, в том числе у 2 пациентов без инфарктоподобных поражений на МР-томографии, выявили множественные инфаркты и тяжелую окклюзию сосудов опухолевыми клетками.
 .Низкая частота инфарктоподобных поражений может быть объяснена временем проведения МРТ до лечения и стадией заболевания.
.Низкая частота инфарктоподобных поражений может быть объяснена временем проведения МРТ до лечения и стадией заболевания.Неспецифические поражения белого вещества
Сообщалось о плохо определенных неспецифических поражениях белого вещества, особенно в перивентрикулярной области, и наше исследование показало аналогичное распределение. 7,12 У 2 пациентов с этим паттерном интенсивность сигнала снизилась у 1 пациента после начала лечения и увеличилась у другого пациента, который не лечился по поводу ИВЛ.Патологоанатомическое исследование выявило лейкоэнцефалопатию и тяжелую инфильтрацию опухолевых клеток. Мелкие сосуды, сильно закупоренные опухолевыми клетками, наблюдаемые при патологоанатомическом исследовании, встречались гораздо чаще, чем количество очагов инфаркта на МРТ. Обычно опухолевые клетки не связаны и свободны в просвете в ИВЛ, но патогенез этого паттерна был описан как вялый поток в просвете капилляров или микроинфаркт. 12 Мы предполагаем, что эта картина вызвана застоем и хроническим ишемическим изменением из-за серьезной инфильтрации сосудов опухолевыми клетками.

Улучшение менингеальной оболочки
У пациентов с ИВЛ иногда наблюдается усиление менингеальной оболочки, хотя природа находки не установлена. 7 При патологоанатомическом исследовании сообщалось о тромбообразовании, васкулите с инфильтрацией лимфоцитов и фиброзном утолщении внешнего слоя мелких сосудов в сосудах головного мозга. 2,13 Патологоанатомическое исследование случаев в этом исследовании показало тяжелую воспалительную реакцию менингеальных клеток с опухолевыми клетками.Это патологическое открытие предполагает путь инвазии клеток лимфомы во внесосудистую структуру.
Массовые поражения
Интрапаренхиматозные массоподобные поражения, проявляющиеся обширным вазогенным отеком и масс-эффектом, вопреки характерным особенностям инфильтрации опухолевыми клетками преимущественно в просвет сосудов. Реакция на терапию убедительно свидетельствовала о том, что повреждения были вызваны ИВЛ. Массивные поражения были описаны в предыдущих отчетах как представляющие внесосудистое распространение клеток лимфомы с сопутствующим воспалительным изменением сосудистых стенок и окружающей паренхимы с микроинфарктом.
 2,3,7,14,15 Экстравазация лимфомных клеток и утолщение сосудистой стенки с прямой инфильтрацией опухолевых клеток в сосудистые стенки выявлены при патологоанатомическом исследовании. Патологические изменения, лежащие в основе этой модели, могут быть многофакторными.
2,3,7,14,15 Экстравазация лимфомных клеток и утолщение сосудистой стенки с прямой инфильтрацией опухолевых клеток в сосудистые стенки выявлены при патологоанатомическом исследовании. Патологические изменения, лежащие в основе этой модели, могут быть многофакторными.Гиперинтенсивные поражения моста на T2WI
Гиперинтенсивные поражения центральных мостов на T2WI без усиления или ограничения диффузии наблюдались у 5 из 11 пациентов с ИВЛ до лечения. Насколько нам известно, подобная картина у пациентов с ИВЛ ранее не описывалась в англоязычной литературе.Уменьшение поражений на МРТ у 4 пациентов после начала лечения убедительно свидетельствует о том, что эти поражения являются проявлением ИВЛ. Гиперинтенсивные поражения в центральном мосту, за исключением покрышки моста и вентролатеральной области, на T2WI сходны с обнаружениями при синдроме осмолитической демиелинизации моста и PRES в стволе головного мозга или внутричерепной дуральной артериовенозной фистуле с венозным застоем.
 16–20 У пяти пациентов с гиперинтенсивными поражениями центральных мостов на T2WI не было признаков синдрома осмолитической демиелинизации или типичного PRES.Хотя не было коррелирующих патологических свидетельств от пациентов, у которых была эта картина, 2 из 5 патологоанатомических исследований у других пациентов показали инфильтрацию опухолевых клеток в сосуды, включая мост (рис. 6). Мы предполагаем, что окклюзия сосудов в мелких венах и артериях опухолевыми клетками приводит к венозному застою, который может проявляться как гиперинтенсивность в центральных мостах на T2WI.
16–20 У пяти пациентов с гиперинтенсивными поражениями центральных мостов на T2WI не было признаков синдрома осмолитической демиелинизации или типичного PRES.Хотя не было коррелирующих патологических свидетельств от пациентов, у которых была эта картина, 2 из 5 патологоанатомических исследований у других пациентов показали инфильтрацию опухолевых клеток в сосуды, включая мост (рис. 6). Мы предполагаем, что окклюзия сосудов в мелких венах и артериях опухолевыми клетками приводит к венозному застою, который может проявляться как гиперинтенсивность в центральных мостах на T2WI.Рис 6.
Случай 3. Инфильтрация опухолевых клеток в сосуды моста у мужчины 84 лет.Патологический образец показывает инфильтрацию клеток лимфомы в капилляры моста ( черные стрелки, ) (гематоксилин-эозин, исходное увеличение × 50).
Результаты МРТ головного мозга у пациентов с ИВЛ могут быть разными, но, если рассматривать их вместе с патологическими данными, различные результаты МРТ могут быть логически интерпретированы.
 Когда окклюзия возникает в мелких артериях, можно ожидать множественных небольших инфарктов, таких как инфарктоподобные поражения, видимые на МРТ в этом исследовании.Окклюзия капилляров может вызвать аномальную интенсивность диффузного белого вещества. Мы предположили, что гиперинтенсивные поражения в мосту также были результатом окклюзии капилляров в мосту, как это наблюдалось при патологоанатомическом исследовании в случае 3. Когда большое количество лимфомных клеток вызывает внесосудистую массу, можно ожидать массоподобных повреждений. Утолщение менингеальных сосудов при некоторой воспалительной реакции может проявляться как усиление менингеальных сосудов. Внимание к внутрисосудистой природе этой уникальной лимфомы может привести к лучшему распознаванию различных проявлений МРТ и более своевременной диагностике.
Когда окклюзия возникает в мелких артериях, можно ожидать множественных небольших инфарктов, таких как инфарктоподобные поражения, видимые на МРТ в этом исследовании.Окклюзия капилляров может вызвать аномальную интенсивность диффузного белого вещества. Мы предположили, что гиперинтенсивные поражения в мосту также были результатом окклюзии капилляров в мосту, как это наблюдалось при патологоанатомическом исследовании в случае 3. Когда большое количество лимфомных клеток вызывает внесосудистую массу, можно ожидать массоподобных повреждений. Утолщение менингеальных сосудов при некоторой воспалительной реакции может проявляться как усиление менингеальных сосудов. Внимание к внутрисосудистой природе этой уникальной лимфомы может привести к лучшему распознаванию различных проявлений МРТ и более своевременной диагностике.Это исследование имеет несколько ограничений. Число пациентов невелико из-за редкости этой опухоли, а рентгенологическое наблюдение короткое. Патологоанатомическое исследование головного мозга было выполнено в 5 случаях, в том числе в 1 случае, когда исследовались только двусторонние лобные доли.
 В остальных 6 случаях мозговая ткань не бралась. Массивные поражения и гиперинтенсивные поражения в мосту на T2WI не были патологически доказаны в этом исследовании. У пациентов с тяжелыми заболеваниями биопсия головного мозга часто затруднена, и патологоанатомическое исследование может быть единственным способом проанализировать эти закономерности.
В остальных 6 случаях мозговая ткань не бралась. Массивные поражения и гиперинтенсивные поражения в мосту на T2WI не были патологически доказаны в этом исследовании. У пациентов с тяжелыми заболеваниями биопсия головного мозга часто затруднена, и патологоанатомическое исследование может быть единственным способом проанализировать эти закономерности.Выводы
Инфарто-подобные поражения, неспецифические поражения белого вещества, усиление менингеальной оболочки, массоподобные поражения и гиперинтенсивные поражения в мосту на T2WI наблюдались при МРТ у 9 пациентов с ИВЛ. Каждое из описанных поражений подействовало на соответствующую химиотерапию. Важно распознать эти модели МРТ как возможные проявления доминантной внутрисосудистой инфильтрации опухолевыми клетками с различной степенью ассоциированной окклюзии или воспаления, в зависимости от уровня пораженных сосудов.Своевременное распознавание этих паттернов изображений может привести к ранней диагностике ИВЛ с улучшенным прогнозом.

Благодарности
Мы благодарим Десмонда Белла за его помощь.
- Получено 1 марта 2011 г.
- Принято после пересмотра 11 мая 2011 г.
- © 2012 Американский журнал нейрорадиологии
Ответ на «МРТ стенки сосуда высокого разрешения: появление внутрисосудистой лимфомы, имитирующей центральную нервную систему. Васкулит »
в статье« МРТ сосудистой стенки высокого разрешения: внешний вид внутрисосудистой лимфомы, имитирующий васкулит центральной нервной системы », [1] Schaafsma et al.описывают два интересных случая подтвержденной биопсией внутрисосудистой лимфомы (ИВЛ), которая имитировала вид васкулита на МРТ сосудистой стенки (vwMRI) с концентрическим утолщением и увеличением артериальной стенки. Насколько нам известно, это первые зарегистрированные случаи ИВЛ, которым была проведена vwMRI.
 В нашем учреждении мы просканировали более 200 пациентов с vwMRI, в том числе 47-летнюю женщину с подтвержденной биопсией большой B-клеточной IVL. Ее vwMRI показала множественные области развивающегося ишемического инфаркта, паренхиматозного кровоизлияния, отека и лептоменингеального усиления; однако на vwMRI не было обнаружено утолщения или увеличения стенки сосуда, включая правую теменную долю, где у нее был инфаркт с отеком, и место биопсии мозга.Эта биопсия была характерна для ИВЛ с множественными кортикальными сосудами (ответвлениями M4), патологически расширенными, с опухолевыми лимфоцитами, положительными на CD20 по данным иммуногистохимии. Биопсия центральной нервной системы у пациентов с ИВЛ выявила неопластические лимфоциты в крупных и средних артериях, дистальных кортикальных сосудах, лептоменингеальных перфораторах, капиллярах и даже в венах [2–6]. Учитывая эту сосудистую гетерогенность, результаты vwMRI IVL, несомненно, также сильно различаются. Разрешение текущих протоколов vwMRI, 0.
В нашем учреждении мы просканировали более 200 пациентов с vwMRI, в том числе 47-летнюю женщину с подтвержденной биопсией большой B-клеточной IVL. Ее vwMRI показала множественные области развивающегося ишемического инфаркта, паренхиматозного кровоизлияния, отека и лептоменингеального усиления; однако на vwMRI не было обнаружено утолщения или увеличения стенки сосуда, включая правую теменную долю, где у нее был инфаркт с отеком, и место биопсии мозга.Эта биопсия была характерна для ИВЛ с множественными кортикальными сосудами (ответвлениями M4), патологически расширенными, с опухолевыми лимфоцитами, положительными на CD20 по данным иммуногистохимии. Биопсия центральной нервной системы у пациентов с ИВЛ выявила неопластические лимфоциты в крупных и средних артериях, дистальных кортикальных сосудах, лептоменингеальных перфораторах, капиллярах и даже в венах [2–6]. Учитывая эту сосудистую гетерогенность, результаты vwMRI IVL, несомненно, также сильно различаются. Разрешение текущих протоколов vwMRI, 0. Вокселы размером 5–0,7 мм не позволяют надежно оценить дистальные внутричерепные сосуды, что создает возможность ложноотрицательного исследования, как в случае с нашим пациентом. Более того, как отмечают авторы, при васкулите интрамуральная лимфоцитарная инвазия обеспечивает патофизиологический механизм увеличения концентрической стенки сосуда, тогда как при ИВЛ стенка самого сосуда сохраняется. Учитывая эти проблемы, мы предлагаем с осторожностью интерпретировать их результаты в диагностических целях.
Вокселы размером 5–0,7 мм не позволяют надежно оценить дистальные внутричерепные сосуды, что создает возможность ложноотрицательного исследования, как в случае с нашим пациентом. Более того, как отмечают авторы, при васкулите интрамуральная лимфоцитарная инвазия обеспечивает патофизиологический механизм увеличения концентрической стенки сосуда, тогда как при ИВЛ стенка самого сосуда сохраняется. Учитывая эти проблемы, мы предлагаем с осторожностью интерпретировать их результаты в диагностических целях.A. de Havenon и S. McNally заявляют, что у них нет конфликта интересов.
Внутрисосудистая лимфома с прогрессирующим кровотечением в ЦНС и множественными расслоениями
Введение . Внутрисосудистая лимфома (ИВЛ) — это редкое и часто смертельное заболевание, характеризующееся внутрипросветной пролиферацией лимфоматозных клеток внутри кровеносных сосудов. Из-за неоднородной клинической картины и отсутствия чувствительных диагностических протоколов диагноз ИВЛ чаще всего ставится при вскрытии.
 Однако при ранней диагностике и соответствующей химиотерапии прогноз значительно улучшается и возможна полная ремиссия. Чтобы расширить возможные проявления ИВЛ, мы представляем пациента с атипичным проявлением подтвержденной биопсией внутрисосудистой крупноклеточной В-клеточной лимфомы, которая перенесла расслоение как внутричерепных, так и экстракраниальных артерий в дополнение к прогрессирующим внутричерепным кровоизлияниям. История болезни . Женщина 47 лет обратилась с жалобой на односторонние парестезии.У нее развились прогрессирующие мультифокальные инфаркты и кровотечение с расслоением как внутричерепных, так и экстракраниальных артерий, что привело к коме. Биопсия головного мозга показала ИВЛ. Она прошла агрессивную химиотерапию и остается в полной ремиссии с хорошим неврологическим выздоровлением. Заключение . Известно, что ИВЛ оказывает свою патологию на мелкие артерии и капилляры, но не известно, что вызывает расслоение крупных сосудов. Диагноз следует рассматривать в случаях необъяснимого расслоения артерий и прогрессирующих инсультов.
Однако при ранней диагностике и соответствующей химиотерапии прогноз значительно улучшается и возможна полная ремиссия. Чтобы расширить возможные проявления ИВЛ, мы представляем пациента с атипичным проявлением подтвержденной биопсией внутрисосудистой крупноклеточной В-клеточной лимфомы, которая перенесла расслоение как внутричерепных, так и экстракраниальных артерий в дополнение к прогрессирующим внутричерепным кровоизлияниям. История болезни . Женщина 47 лет обратилась с жалобой на односторонние парестезии.У нее развились прогрессирующие мультифокальные инфаркты и кровотечение с расслоением как внутричерепных, так и экстракраниальных артерий, что привело к коме. Биопсия головного мозга показала ИВЛ. Она прошла агрессивную химиотерапию и остается в полной ремиссии с хорошим неврологическим выздоровлением. Заключение . Известно, что ИВЛ оказывает свою патологию на мелкие артерии и капилляры, но не известно, что вызывает расслоение крупных сосудов. Диагноз следует рассматривать в случаях необъяснимого расслоения артерий и прогрессирующих инсультов. Ранняя диагностика с соответствующим лабораторным обследованием и подтверждением ткани биопсией может привести к значительному улучшению результатов.
Ранняя диагностика с соответствующим лабораторным обследованием и подтверждением ткани биопсией может привести к значительному улучшению результатов.1. Введение
Внутрисосудистая лимфома (ИВЛ) признана Всемирной организацией здравоохранения (ВОЗ) чрезвычайно редким подтипом диффузной экстранодальной крупноклеточной неходжкинской лимфомы с предполагаемой ежегодной заболеваемостью 0,5 случая на 1 000 000 [1 ]. ИВЛ приводит к внутрипросветной пролиферации неопластических лимфоидных клеток в мелких и средних сосудах [2].Эти клетки утратили способность к трансваскулярной миграции из-за дефектов в молекулах адгезии [3]. ИВЛ может затрагивать любую систему органов, особенно центральную нервную систему (ЦНС), и ее разнообразные неврологические проявления часто затрудняют диагностику. Пациенты могут иметь подострую энцефалопатию или деменцию, паралич, судороги или мультифокальные цереброваскулярные нарушения в порядке их частоты [1, 4, 5]. Системные симптомы различаются, но чаще всего встречаются лихорадка и поражения кожи, тогда как лимфаденопатия обычно отсутствует [2].

Серологические аномалии включают анемию (63%), высокий уровень лактатдегидрогеназы (ЛДГ) (82%) и уровни бета 2-микроглобулина (86%) [6]. Поражение костного мозга встречается у 32% пациентов, и спинномозговая жидкость (СМЖ) редко содержит злокачественные клетки [6]. Магнитно-резонансная томография (МРТ) неспецифична и может быть нормальной, хотя есть многочисленные сообщения о быстром прогрессировании церебральных инфарктов [5]. Биопсия органа является золотым стандартом диагностики ИВЛ, но часто выполняется слишком поздно, а случаи поражения ЦНС чаще всего диагностируются посмертно (60%) [7].Случайные биопсии кожи могут помочь поставить диагноз раньше, с чувствительностью до 83% даже без результатов исследования кожи [8, 9]. В то время как ИВЛ может иметь мрачный прогноз со средней выживаемостью без лечения всего через несколько месяцев после постановки диагноза, химиотерапия, содержащая ритуксумаб и доксорубицин, улучшила трехлетнюю выживаемость до 60%, которая может быть увеличена при добавлении метотрексата [1, 10].
 При своевременной диагностике и лечении полная ремиссия наблюдается примерно в 42% случаев, хотя недавние данные о выживаемости при адекватном лечении отсутствуют [11].Мы описываем необычное проявление ИВЛ с множественными рассечениями как внутричерепных, так и экстракраниальных кровеносных сосудов и прогрессирующими внутричерепными кровоизлияниями (ICH).
При своевременной диагностике и лечении полная ремиссия наблюдается примерно в 42% случаев, хотя недавние данные о выживаемости при адекватном лечении отсутствуют [11].Мы описываем необычное проявление ИВЛ с множественными рассечениями как внутричерепных, так и экстракраниальных кровеносных сосудов и прогрессирующими внутричерепными кровоизлияниями (ICH).2. История болезни
У 47-летней женщины с задержкой опорожнения желудка в анамнезе появились мигрирующие парестезии, распространяющиеся вверх по правой стороне. Эти эпизоды происходили ежедневно, длились 20 минут и были связаны с головной болью и спутанностью сознания. В течение месяца, предшествовавшего госпитализации, она была госпитализирована в стационар с правосторонними парестезиями, усилением мигрени с зрительной аурой и сонливостью.Первоначальная МРТ головного мозга с контрастным усилением не дала острых симптомов и показала минимальную фоновую неспецифическую гиперинтенсивность восстановления после инверсии (FLAIR) неспецифической T2-взвешенной жидкости в подкорковом белом веществе.

После беспокойства о фокально-двигательном припадке пациент был переведен в нашу больницу. Лимфаденопатии, кожных повреждений или отеков у нее не было. В неврологическом отношении она изначально была сонной, но легко возбуждалась, а после бодрствования оставалась интерактивной и ориентированной, достаточной для участия в Монреальской когнитивной оценке (MOCA).Ее оценка MOCA составляла 22/30 с заметным дефицитом внимания, речи и абстракции — заметное отклонение от ее исходного уровня высокого функционирования. Остаток ее неврологического осмотра был ничем не примечательным. Лабораторная оценка, включая анализ спинномозговой жидкости, не показала результатов (таблица 1).
Sodium605
2 905 3.6 ммоль / л
1
86.9 fL
86.9 fL
MP
9 fL
brit млЗначение Интерпретация Комплексная метаболическая панель Хлорид 108 ммоль / л CO 2 26 ммоль / л BUN 1
10 мг / л
1,24 мг / дл Высокий Глюкоза 103 мг / дл Кальций 9,2 мг / дл Протеин Низкий Альбумин 4.  1 г / дл
1 г / длБилирубин 0,7 мг / дл Щелочная фосфатаза 60 Ед. Ед / л Анионный зазор 8 ммоль / л Общий анализ крови 3,73 k / РБК 4.47 M / µ l HGB 13,3 г / дл HCT 38,9% MCV2 86.9 fL MCHC 34,2 г / дл RDW 14,8% Высокий Тромбоциты 152 k / µ 6 Низкий
Гранулоцит%, # 63,4, 2,4 k / µ l Моноцит%, # 9,1, 0,3 k / µ l % % Эозинофил%, # 3,1, 0,1 k / µ l Базофил%, # 0,4, 0,0 k / µ l Лимфоцит%, # / µ l Оценка паранеопластических аутоантител (CSF) Нейрональное ядерное антитело, тип 1 Отрицательное ядерное Отрицательное
9060 Нейронные ядерные антитела, тип 3 Отрицательные Глиальные ядерные антитела Отрицательные Цитоплазматические антитела клеток Пуркинье, тип 1 N egative Цитоплазматические Ab клеток Пуркинье, Тип 2 Отрицательные Цитоплазматические Ab клеток Пуркинье, Тип Tr Отрицательные 90MP Отрицательный Дополнительные лабораторные тесты LDH a 427 U / L Высокий Высокий TSH 1.  83 мЕд / л
83 мЕд / лCRP 0,1 мг / дл Протромбиновое время 13,7 сек INR 1,1 мм 905ester 2 905 hr a LDH был проанализирован через 45 дней после получения первоначальных результатов испытаний. b Ферритин был проанализирован через 20 месяцев после получения первоначальных результатов испытаний.
МРТ головного мозга была повторена через 13 дней после первоначального сканирования (рис. 1 (a)), показав два новых очага ограниченной диффузии в левом полуавальном центре левого желудочка, согласующиеся с интервальными инфарктами. Также наблюдалось прогрессирование гиперинтенсивности FLAIR в правой передней поясной извилине, а также в нижней правой и задней левой лобных долях с соответствующими областями петехиального кровотечения на Т2-взвешенных изображениях.
 Непрерывные электроэнцефалограммы (ЭЭГ) подтвердили замедление энцефалопатии без эпилептиформных разрядов.Церебральная ангиография показала нерегулярный гофрированный вид шейных сонных артерий, что, как считается, соответствует хронической фиброзно-мышечной дисплазии (рис. 1 (b)). МРТ стенки сосуда с высоким разрешением не показала увеличения артериальной стенки, что свидетельствовало бы о васкулите. Позитронно-эмиссионная томография (ФДГ-ПЭТ) мозга с 18F-фтордезоксиглюкозой (рис. 2) и компьютерная томография (КТ) грудной клетки, брюшной полости и таза не выявили.
Непрерывные электроэнцефалограммы (ЭЭГ) подтвердили замедление энцефалопатии без эпилептиформных разрядов.Церебральная ангиография показала нерегулярный гофрированный вид шейных сонных артерий, что, как считается, соответствует хронической фиброзно-мышечной дисплазии (рис. 1 (b)). МРТ стенки сосуда с высоким разрешением не показала увеличения артериальной стенки, что свидетельствовало бы о васкулите. Позитронно-эмиссионная томография (ФДГ-ПЭТ) мозга с 18F-фтордезоксиглюкозой (рис. 2) и компьютерная томография (КТ) грудной клетки, брюшной полости и таза не выявили.Поскольку обширное обследование до сих пор было отрицательным (CSF OCB, поток, цитология, HSV / VZV, ANA, ANCA, паранеопластическая панель Mayo, VGKC, AQ4, NMDA, токсикологический анализ, ЭЭГ без явного приступа), пациент получил предположительный диагноз «идиопатический энцефалит» и лечение эмпирически проводилось пятидневным испытанием метилпреднизолона внутривенно с последующим постепенным снижением дозы преднизона.
 В течение одного месяца после выписки у нее клиническое улучшение улучшилось, и она вернулась к работе, но постепенно усилились головная боль, рвота, летаргия и эпизодическое опускание лица слева. Повторная МРТ (рис. 3 (а)) показала заметное интервальное прогрессирование с появлением новых областей цитотоксического отека / инфаркта, вазогенного отека и умеренного правого височно-теменного кровоизлияния, вызывающего отек мозга и сдвиг средней линии, с дополнительными петехиальными кровоизлияниями на Т2-взвешенных изображениях. Появился обширный новый сигнал FLAIR и его усиление, совместимое с разрушением гематоэнцефалического барьера.
В течение одного месяца после выписки у нее клиническое улучшение улучшилось, и она вернулась к работе, но постепенно усилились головная боль, рвота, летаргия и эпизодическое опускание лица слева. Повторная МРТ (рис. 3 (а)) показала заметное интервальное прогрессирование с появлением новых областей цитотоксического отека / инфаркта, вазогенного отека и умеренного правого височно-теменного кровоизлияния, вызывающего отек мозга и сдвиг средней линии, с дополнительными петехиальными кровоизлияниями на Т2-взвешенных изображениях. Появился обширный новый сигнал FLAIR и его усиление, совместимое с разрушением гематоэнцефалического барьера.Анализ ЦСЖ продемонстрировал заметное повышение уровня белка (140 мг / дл) без плеоцитоза. Повторная катетерная ангиография показала новое расслоение правой шейной внутренней сонной артерии в дистальной экстракраниальной части, а также прогрессирование нарушений в просвете, указывающих на прогрессирующую васкулопатию (Рисунок 3 (b)). Магнитно-резонансная ангиография (МРА) головы и шеи в тот же день выявила дополнительные двусторонние расслоения позвоночных артерий с вовлечением всей правой позвоночной артерии и левого сегмента V3 / 4, а также новое сужение двусторонних височных артерий.
 Во время начальной катетерной ангиограммы не было инструментов выше уровня общих сонных артерий или начала позвоночных артерий, чтобы объяснить это открытие. В наш дифференциальный диагноз были включены атипичные васкулиты, воспалительная амилоидная ангиопатия, осложненный синдром задней обратимой энцефалопатии (PRES) и синдром обратимой церебральной вазоконстрикции (RCVS) или ИВЛ (таблица 2). Поскольку повышенный уровень ЛДГ в атипичном случае без инфекции может указывать на ИВЛ, мы измерили ЛДГ и обнаружили, что ее уровень повышен до 450 Ед / л (Таблица 1).
Во время начальной катетерной ангиограммы не было инструментов выше уровня общих сонных артерий или начала позвоночных артерий, чтобы объяснить это открытие. В наш дифференциальный диагноз были включены атипичные васкулиты, воспалительная амилоидная ангиопатия, осложненный синдром задней обратимой энцефалопатии (PRES) и синдром обратимой церебральной вазоконстрикции (RCVS) или ИВЛ (таблица 2). Поскольку повышенный уровень ЛДГ в атипичном случае без инфекции может указывать на ИВЛ, мы измерили ЛДГ и обнаружили, что ее уровень повышен до 450 Ед / л (Таблица 1).5
5 905 96 Визуализация, взвешенная по чувствительности
Дифференциальный диагноз Лаборатория / визуализация Нейросаркоидоз Торебрам ACE Церебральный синус ACE 905 96 ANA, ANCA, SSA, SSB, СОЭ, CRP, панель гепатита Синдром обратимой церебральной вазоконстрикции Катетерная ангиограмма и МРТ стенки сосуда высокого разрешения Аутоиммунный и паранеопластический энцефалит, NMGAS1 панель антител, ПЭТ-сканирование с ФДГ головного мозга Злокачественные новообразования или метастазы в ЦНС Цитология ЦСЖ и проточная цитометрия, КТ грудной клетки, брюшной полости, таза.  ПЭТ головного мозга
ПЭТ головного мозгаИнфекционный эндокардит с септическими эмболами СОЭ, СРБ, лактат Энцефалит (инфекционная этиология) ТБ, RPR, ВИЧ, VZV, HSV, EBV, WNV 2 другие Церебральная аутосомно-доминантная артериопатия с подкорковыми инфарктами и лейкоэнцефалопатией (CADASIL) МРТ Медикаментозная васкулопатия Конглав Ангиотропный ангиотензин Мочи на лекарственные препараты Прогрессирующая мультифокальная лейкоэнцефалопатия Антитела к ВИЧ Клиническое течение пациента прогрессировало до комы и отека мозга.Была сделана биопсия височно-теменного мозга справа. Срезы, окрашенные гематоксилином и эозином, показали патологически растянутые мелкие корковые сосуды опухолевыми лимфоцитами.
 Эти клетки были плеоморфными, гиперхроматными, с выраженными ядрышками и редкими митозами (рис. 4 (а)). Они не попали в окружающий нейропиль. Иммуногистохимия показала, что эти злокачественные клетки диффузно положительны в отношении CD20, маркера В-клеток (рис. 4 (b)). Опухолевые клетки также широко помечены для Mindbomb E3 Ubiquitin Protein Ligase 1 (MIB-1), маркера пролиферации.На основании этих данных пациенту был поставлен диагноз ИВЛ. Пациенту срочно была начата химиотерапия ритуксимабом, циклофосфамидом, доксорубицином, винкристином и преднизоном (R-CHOP) вместе с декомпрессивной трепанацией черепа, что привело к обращению комы и освобождению от аппарата ИВЛ через несколько дней. Затем она получила метотрексат, который остановил прогрессирование ее болезни и позволил ей вернуться домой с модифицированной шкалой Рэнкина 1. Пациентка остается в ремиссии сегодня, четыре года спустя.
Эти клетки были плеоморфными, гиперхроматными, с выраженными ядрышками и редкими митозами (рис. 4 (а)). Они не попали в окружающий нейропиль. Иммуногистохимия показала, что эти злокачественные клетки диффузно положительны в отношении CD20, маркера В-клеток (рис. 4 (b)). Опухолевые клетки также широко помечены для Mindbomb E3 Ubiquitin Protein Ligase 1 (MIB-1), маркера пролиферации.На основании этих данных пациенту был поставлен диагноз ИВЛ. Пациенту срочно была начата химиотерапия ритуксимабом, циклофосфамидом, доксорубицином, винкристином и преднизоном (R-CHOP) вместе с декомпрессивной трепанацией черепа, что привело к обращению комы и освобождению от аппарата ИВЛ через несколько дней. Затем она получила метотрексат, который остановил прогрессирование ее болезни и позволил ей вернуться домой с модифицированной шкалой Рэнкина 1. Пациентка остается в ремиссии сегодня, четыре года спустя.3. Обсуждение
ИВЛ с вовлечением ЦНС — агрессивное состояние с плохим прогнозом, поскольку его разнообразные клинические проявления часто не позволяют поставить диагноз.
 Лабораторные инструменты и инструменты визуализации позволяют понять этиологию, но не обладают достаточной чувствительностью и специфичностью. У нашего пациента было необычное проявление множественных расслоений артерий и прогрессирующей ICH. Она прошла обширное обследование по поводу прогрессирующей энцефалопатии, пока ее состояние не впадало в кому, и потребовалась биопсия головного мозга.Патологическое разрастание внутрипросветных лимфоцитов в мелких внутричерепных сосудах объясняет симптомы и результаты визуализации у нашего пациента. Поскольку артериолы, венулы и капилляры застаиваются злокачественными клетками, может возникнуть внутрипаренхиматозное кровоизлияние и инфаркт. Однако образование множественных расслоений крупных артерий в ее клиническом течении остается необъяснимым. Микрососуды являются известным источником интрамуральных гематом при расслоении артерий и внутрибляшечных кровоизлияний, связанных с утечкой сосудов или разрывом стенок сонных и позвоночных артерий [12].
Лабораторные инструменты и инструменты визуализации позволяют понять этиологию, но не обладают достаточной чувствительностью и специфичностью. У нашего пациента было необычное проявление множественных расслоений артерий и прогрессирующей ICH. Она прошла обширное обследование по поводу прогрессирующей энцефалопатии, пока ее состояние не впадало в кому, и потребовалась биопсия головного мозга.Патологическое разрастание внутрипросветных лимфоцитов в мелких внутричерепных сосудах объясняет симптомы и результаты визуализации у нашего пациента. Поскольку артериолы, венулы и капилляры застаиваются злокачественными клетками, может возникнуть внутрипаренхиматозное кровоизлияние и инфаркт. Однако образование множественных расслоений крупных артерий в ее клиническом течении остается необъяснимым. Микрососуды являются известным источником интрамуральных гематом при расслоении артерий и внутрибляшечных кровоизлияний, связанных с утечкой сосудов или разрывом стенок сонных и позвоночных артерий [12]. Неясно, способна ли ИВЛ проникать в эти мелкие сосуды (vasa vasorum) в стенке артерии, вызывая разрыв и расслоение интимы и адвентиции артерии.
Неясно, способна ли ИВЛ проникать в эти мелкие сосуды (vasa vasorum) в стенке артерии, вызывая разрыв и расслоение интимы и адвентиции артерии.Учитывая ограничения отдельного зарегистрированного случая, мы не можем исключить альтернативную этиологию ее расслоения. Возможно, у нее была либо основная фиброзно-мышечная дисплазия (ящур), либо другое состояние, объясняющее ее расслоение, в дополнение к ИВЛ, объясняющим результаты ее мозга. Однако ее ангиографические исследования показали периодическое развитие новых расслоений крупных артерий, связанных с клиническим и рентгенографическим прогрессированием ее ИВЛ.На сегодняшний день в литературе нет сообщений о поддержке ИВЛ с вовлечением крупных артерий, таких как сонные и позвоночные артерии, заболевание, которое, как известно, затрагивает в основном артериолы, венулы и капилляры.
Этот случай подчеркивает необходимость высокого индекса подозрения на ИВЛ на фоне множественных внутричерепных и экстракраниальных расслоений и ICH, а также прогрессирование результатов, несмотря на стандартную медикаментозную терапию.
 Наша пациентка вышла из комы и в настоящее время остается в ремиссии четыре года спустя благодаря точному гистопатологическому диагнозу и своевременному лечению, что резко контрастирует с большинством пациентов, которым диагноз ставится посмертно.При оценке прогрессирующего энцефалита неясной этиологии незамедлительная биопсия головного мозга оказалась необходимой для направления лечения. Однако могут быть причины, по которым биопсия головного мозга может быть отложена или неточна из-за опасений относительно процедурного риска или когда образование опухолевой массы практически отсутствует, что может привести к недиагностическим результатам, которые могут существенно отсрочить начало терапии. . Результаты визуализации, такие как диффузные рассеянные очаги гиперинтенсивности Т2 и диффузного ограничения, петехиальные и паренхиматозные кровоизлияния с расслоением артерий или без него, должны вызвать подозрение на это неуловимое заболевание даже при отсутствии обнаруживаемых массовых поражений.
Наша пациентка вышла из комы и в настоящее время остается в ремиссии четыре года спустя благодаря точному гистопатологическому диагнозу и своевременному лечению, что резко контрастирует с большинством пациентов, которым диагноз ставится посмертно.При оценке прогрессирующего энцефалита неясной этиологии незамедлительная биопсия головного мозга оказалась необходимой для направления лечения. Однако могут быть причины, по которым биопсия головного мозга может быть отложена или неточна из-за опасений относительно процедурного риска или когда образование опухолевой массы практически отсутствует, что может привести к недиагностическим результатам, которые могут существенно отсрочить начало терапии. . Результаты визуализации, такие как диффузные рассеянные очаги гиперинтенсивности Т2 и диффузного ограничения, петехиальные и паренхиматозные кровоизлияния с расслоением артерий или без него, должны вызвать подозрение на это неуловимое заболевание даже при отсутствии обнаруживаемых массовых поражений. Стратегии ранней клинической диагностики могут позволить начать лечение раньше. Эти стратегии позволяют поставить диагноз путем ассимиляции других важных данных, включая сывороточные опухолевые маркеры, ЛДГ (лактатдегидрогеназа) и растворимый IL2R (рецептор интерлейкина-2), а также случайную биопсию кожи и костного мозга с помощью проточной цитометрии [6, 8, 9, 13 , 14]. В частности, поражение ЦНС лимфомы на момент постановки диагноза предвещает худший прогноз, и считается, что у этих пациентов выше частота рецидивов, особенно в ЦНС [15].Было высказано предположение, что положительные результаты биопсии кожи могут быть полезны в случаях без доказанного заболевания ЦНС в качестве фактора риска для последующего рецидива в ЦНС, хотя для подтверждения этого необходимы дальнейшие исследования [15]. Остается потребность в лучшем патофизиологическом понимании этого неуловимого заболевания.
Стратегии ранней клинической диагностики могут позволить начать лечение раньше. Эти стратегии позволяют поставить диагноз путем ассимиляции других важных данных, включая сывороточные опухолевые маркеры, ЛДГ (лактатдегидрогеназа) и растворимый IL2R (рецептор интерлейкина-2), а также случайную биопсию кожи и костного мозга с помощью проточной цитометрии [6, 8, 9, 13 , 14]. В частности, поражение ЦНС лимфомы на момент постановки диагноза предвещает худший прогноз, и считается, что у этих пациентов выше частота рецидивов, особенно в ЦНС [15].Было высказано предположение, что положительные результаты биопсии кожи могут быть полезны в случаях без доказанного заболевания ЦНС в качестве фактора риска для последующего рецидива в ЦНС, хотя для подтверждения этого необходимы дальнейшие исследования [15]. Остается потребность в лучшем патофизиологическом понимании этого неуловимого заболевания.Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Финансирование
Доктора де Хавенона поддерживает NIH-NINDS K23NS105924.
 ДокторMcNally поддерживается грантом развития ученых Американской кардиологической ассоциации 17SDG33460420 и NIH NHLBI 1R01 HL127582-01A1.
ДокторMcNally поддерживается грантом развития ученых Американской кардиологической ассоциации 17SDG33460420 и NIH NHLBI 1R01 HL127582-01A1.Благодарности
Мы смиренно благодарим пациентку за примерную щедрость, мужество и терпение на протяжении всего курса диагностики, лечения и жизни после госпитализации. Мы также хотели бы поблагодарить Стефани Линч за критический обзор рукописи и помощь в публикации.
Диагностика и лечение внутрисосудистого лимфоматоза | Аллергия и клиническая иммунология | JAMA Neurology
Цель
Описать пациента с необычно хорошим исходом редкой лимфомы высокой степени злокачественности, которая часто поражает нервную систему.Дизайн
История болезни.Настройка
Университетская больница.Чемодан
70-летний фармацевт сначала обратился с симптомами менингоэнцефалита, а через 6 месяцев — с острым состоянием спутанности сознания с последующим сложным частичным эпилептическим статусом. Диагностика внутрисосудистого лимфоматоза производилась с помощью обнаружения и биопсии двусторонней опухоли надпочечника.
Диагностика внутрисосудистого лимфоматоза производилась с помощью обнаружения и биопсии двусторонней опухоли надпочечника.Основные итоги и результаты
Полихимиотерапия, состоящая из CHOP (циклофосфамида, доксорубицина гидрохлорида, винкристина сульфата и преднизона), привела к полной ремиссии.В настоящее время продолжительность жизни пациента превышает 2,5 года.Выводы
Возможность внутрисосудистого лимфоматоза следует учитывать у взрослых пациентов с неясным менингоэнцефалитическим синдромом, острым спутанным состоянием, деменцией или другими необъяснимыми неврологическими состояниями с признаками системного заболевания. При внутрисосудистом лимфоматозе, как и при других неходжкинских лимфомах высокой степени злокачественности, стандартным лечением должна быть полихимиотерапия CHOP.ВНУТРИСосудистый лимфоматоз (ИВЛ), или ангиотропная крупноклеточная лимфома, был впервые описан Pfleger и Tappeiner 1 в 1959 году как кожное проявление системного эндотелиоматоза у молодой пациентки.
 Считалось, что пролиферирующие клетки имеют эндотелиальное происхождение, но иммуногистохимические исследования показали, что злокачественные клетки несут иммунофенотип B- или T-клеточного происхождения. 2 , 3 Внутрисосудистый лимфоматоз считается редкой экстранодальной неходжкинской лимфомой высокой степени злокачественности с тропизмом к эндотелию. Сродство опухолевых клеток к эндотелию капилляров можно объяснить рецепторами лимфоцитов к антигенам эндотелиальных мембран. 2 , 4 Заболевание начинается в широком возрастном диапазоне, с предрасположенностью к пациентам седьмого десятилетия жизни.Четкой половой разницы нет. Гистологическая характеристика — разрастание крупных атипичных лимфоидных клеток в просвете капилляров, мелких вен и артерий. 3 Разрастание кровеносных сосудов паренхиматозных органов приводит к тромбозам и вторичным гипоксическим повреждениям. Нервная система и кожа часто поражаются. Также часто наблюдается инфильтрация легких, почек, надпочечников или простаты.
Считалось, что пролиферирующие клетки имеют эндотелиальное происхождение, но иммуногистохимические исследования показали, что злокачественные клетки несут иммунофенотип B- или T-клеточного происхождения. 2 , 3 Внутрисосудистый лимфоматоз считается редкой экстранодальной неходжкинской лимфомой высокой степени злокачественности с тропизмом к эндотелию. Сродство опухолевых клеток к эндотелию капилляров можно объяснить рецепторами лимфоцитов к антигенам эндотелиальных мембран. 2 , 4 Заболевание начинается в широком возрастном диапазоне, с предрасположенностью к пациентам седьмого десятилетия жизни.Четкой половой разницы нет. Гистологическая характеристика — разрастание крупных атипичных лимфоидных клеток в просвете капилляров, мелких вен и артерий. 3 Разрастание кровеносных сосудов паренхиматозных органов приводит к тромбозам и вторичным гипоксическим повреждениям. Нервная система и кожа часто поражаются. Также часто наблюдается инфильтрация легких, почек, надпочечников или простаты. Могут быть вовлечены все органы по отдельности или в комбинации, но печень, селезенка, лимфатические узлы и костный мозг относительно сохранены до поздних стадий заболевания.Обычно циркулирующие клетки лимфомы отсутствуют в крови или спинномозговой жидкости (ЦСЖ). Около двух третей пациентов имеют неврологические признаки, из которых наиболее часто сообщалось о диффузных церебральных признаках, деменции или очаговых церебральных признаках. 5 Некоторые пациенты обращаются к неврологу с миелопатией, периферической невропатией, полирадикулопатией или миопатией. 6 Большинство случаев было диагностировано только при вскрытии из-за вводящих в заблуждение клинических признаков, имитирующих дегенеративную деменцию, васкулит, инсульт, инфекцию или другие новообразования.Диагноз можно установить с помощью биопсии пораженного органа (ов). Применяются различные методы лечения, включая химиотерапию, стероидную и лучевую терапию. Время выживания у большинства пациентов составляет менее 1 года.
Могут быть вовлечены все органы по отдельности или в комбинации, но печень, селезенка, лимфатические узлы и костный мозг относительно сохранены до поздних стадий заболевания.Обычно циркулирующие клетки лимфомы отсутствуют в крови или спинномозговой жидкости (ЦСЖ). Около двух третей пациентов имеют неврологические признаки, из которых наиболее часто сообщалось о диффузных церебральных признаках, деменции или очаговых церебральных признаках. 5 Некоторые пациенты обращаются к неврологу с миелопатией, периферической невропатией, полирадикулопатией или миопатией. 6 Большинство случаев было диагностировано только при вскрытии из-за вводящих в заблуждение клинических признаков, имитирующих дегенеративную деменцию, васкулит, инсульт, инфекцию или другие новообразования.Диагноз можно установить с помощью биопсии пораженного органа (ов). Применяются различные методы лечения, включая химиотерапию, стероидную и лучевую терапию. Время выживания у большинства пациентов составляет менее 1 года. 6 Поскольку ИВЛ часто проявляется неврологическими симптомами и потенциально излечима, диагностика этого состояния важна для неврологов.
6 Поскольку ИВЛ часто проявляется неврологическими симптомами и потенциально излечима, диагностика этого состояния важна для неврологов.70-летний фармацевт был госпитализирован 4 апреля 1996 г. из-за лихорадки, головной боли, рвоты, сонливости и генерализованного припадка, начинавшегося с клонических подергиваний правой верхней конечности.Он перенес ранее операцию аортокоронарного шунтирования. При осмотре скованности шеи или очагового неврологического дефицита не выявлено. Обычные лабораторные исследования показали анемию (уровень гемоглобина 10,1 г / л), а значение С-реактивного белка было повышено с 0,033 до 0,112 г / л. Выполнена люмбальная пункция. Результаты в CSF включали повышенный уровень белка (1,9 г / л) и небольшой плеоцитоз (20,3 × 10 6 клеток) с преобладанием лимфоцитов (0,96 лимфоцитов, 0,02 моноцитов и 0.02 полиморфные ядерные клетки). Результаты цитологического исследования не выявили злокачественных клеток, но свидетельствовали о воспалительном процессе.
 Черепная компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) не выявила аномалий, тогда как электроэнцефалография (ЭЭГ) показала умеренное или тяжелое генерализованное замедление фоновой активности и фокальной дельта-активности над левой лобно-височной и левой теменной областями. Результаты серологических тестов CSF на вирусы, Treponema, видов и Borrelia burgdorferi , а также тестирование полимеразной цепной реакции на Herpes simplex и Mycobacterium tuberculosis были отрицательными.Ацикловир натрия давали до тех пор, пока не стали известны результаты серологической реакции и полимеразной цепной реакции. Пациент выздоровел через несколько дней. Он отказался от дальнейших диагностических процедур и был выписан на курс противоэпилептического лечения. Первым диагнозом был менингоэнцефалит неустановленного происхождения.
Черепная компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) не выявила аномалий, тогда как электроэнцефалография (ЭЭГ) показала умеренное или тяжелое генерализованное замедление фоновой активности и фокальной дельта-активности над левой лобно-височной и левой теменной областями. Результаты серологических тестов CSF на вирусы, Treponema, видов и Borrelia burgdorferi , а также тестирование полимеразной цепной реакции на Herpes simplex и Mycobacterium tuberculosis были отрицательными.Ацикловир натрия давали до тех пор, пока не стали известны результаты серологической реакции и полимеразной цепной реакции. Пациент выздоровел через несколько дней. Он отказался от дальнейших диагностических процедур и был выписан на курс противоэпилептического лечения. Первым диагнозом был менингоэнцефалит неустановленного происхождения.В течение следующих нескольких месяцев его жена наблюдала потерю энергии, дефицит памяти и трудности на работе в аптеке.
 Он заказывал неправильные материалы, дважды оплачивал счета и испытывал трудности с чтением рецептов и вождением автомобиля, но со временем симптомы улучшились.Шесть месяцев спустя, 15 октября 1996 г., он был повторно госпитализирован из-за острой дезориентации, трудностей с поиском слов и неспособности закончить предложения. При осмотре температура 38,2 ° C, артериальное давление 140/80 мм рт. Ст., Пульс 76 / мин. Психологические тесты выявили непостоянную дезориентацию в пространстве, времени и окружении, а также уменьшение размаха пальцев. Его поведение было изменено повышенным драйвом, колеблющейся бдительностью, возбуждением и измененной аффективностью (сначала эйфория, затем раздражительность).Его речь была увеличенной и бессвязной. У него были небольшие трудности с именованием, чтением, письмом и расчетами. Кодирование и поиск списка слов были существенно сокращены. Он показал лишь минимальные отклонения при копировании сложной геометрической фигуры. Психические изменения соответствовали делирию в соответствии с критериями Диагностического и статистического руководства по психическим расстройствам , четвертое издание .
Он заказывал неправильные материалы, дважды оплачивал счета и испытывал трудности с чтением рецептов и вождением автомобиля, но со временем симптомы улучшились.Шесть месяцев спустя, 15 октября 1996 г., он был повторно госпитализирован из-за острой дезориентации, трудностей с поиском слов и неспособности закончить предложения. При осмотре температура 38,2 ° C, артериальное давление 140/80 мм рт. Ст., Пульс 76 / мин. Психологические тесты выявили непостоянную дезориентацию в пространстве, времени и окружении, а также уменьшение размаха пальцев. Его поведение было изменено повышенным драйвом, колеблющейся бдительностью, возбуждением и измененной аффективностью (сначала эйфория, затем раздражительность).Его речь была увеличенной и бессвязной. У него были небольшие трудности с именованием, чтением, письмом и расчетами. Кодирование и поиск списка слов были существенно сокращены. Он показал лишь минимальные отклонения при копировании сложной геометрической фигуры. Психические изменения соответствовали делирию в соответствии с критериями Диагностического и статистического руководства по психическим расстройствам , четвертое издание . 7 При плановых лабораторных исследованиях выявлена анемия (уровень гемоглобина 11.4 г / л), повышенный уровень С-реактивного белка (0,183 г / л) и повышенная скорость оседания (66 мм / ч). ЦСЖ содержала высокий уровень белка (2,7 г / л), но количество клеток было в пределах нормы, и результаты цитологических исследований были нормальными. Моноклонального белка или недостаточности надпочечников обнаружено не было. Анти-Hu, анти-Yo или специфические антинейрональные антитела не присутствовали. Результаты ЭЭГ были аналогичны тем, что были зарегистрированы 6 месяцев назад, показывая умеренную или тяжелую медленноволновую аномалию в обоих полушариях и постоянную дельта-активность в левой лобно-височной и левой теменной областях.МРТ черепа показала небольшую гиперинтенсивную область в левом заднем чечевицеобразном ядре (рис. 1) с минимальным усилением контраста. Не было усиления контраста мозговых оболочек и инфаркта коры. Дифференциальный диагноз клинического синдрома включал паранеопластический (лимбический) энцефалит.
7 При плановых лабораторных исследованиях выявлена анемия (уровень гемоглобина 11.4 г / л), повышенный уровень С-реактивного белка (0,183 г / л) и повышенная скорость оседания (66 мм / ч). ЦСЖ содержала высокий уровень белка (2,7 г / л), но количество клеток было в пределах нормы, и результаты цитологических исследований были нормальными. Моноклонального белка или недостаточности надпочечников обнаружено не было. Анти-Hu, анти-Yo или специфические антинейрональные антитела не присутствовали. Результаты ЭЭГ были аналогичны тем, что были зарегистрированы 6 месяцев назад, показывая умеренную или тяжелую медленноволновую аномалию в обоих полушариях и постоянную дельта-активность в левой лобно-височной и левой теменной областях.МРТ черепа показала небольшую гиперинтенсивную область в левом заднем чечевицеобразном ядре (рис. 1) с минимальным усилением контраста. Не было усиления контраста мозговых оболочек и инфаркта коры. Дифференциальный диагноз клинического синдрома включал паранеопластический (лимбический) энцефалит. Поэтому была проведена компьютерная томография грудной клетки и брюшной полости. Двусторонние опухолевые образования надпочечников размером 7 × 3 × 3 см с правой стороны и 6 × 5 × 3 см с левой стороны были обнаружены в сочетании с множественными лимфатическими узлами в средостении и забрюшинном пространстве, увеличенными до 2 см (рис. 2). .Биопсия правого надпочечника под контролем КТ была отложена из-за развития сложного парциального эпилептического статуса 23 октября, когда у пациента появились ступор, шлепки по губам и эпилептиформные выделения на левой височной стороне, которые разрешились при лечении фенитоином натрия. . Наконец, результаты биопсии показали, что синусоиды надпочечников заполнены некогезивными агрегатами злокачественных лимфоидных клеток (рис. 3) с сильной реакцией на антитела к CD20, специфичные для В-лимфоцитов. Был поставлен диагноз внутрисосудистой лимфомы с поражением как надпочечников, так и головного мозга, а также лимфатических узлов средостения и забрюшинного пространства.
Поэтому была проведена компьютерная томография грудной клетки и брюшной полости. Двусторонние опухолевые образования надпочечников размером 7 × 3 × 3 см с правой стороны и 6 × 5 × 3 см с левой стороны были обнаружены в сочетании с множественными лимфатическими узлами в средостении и забрюшинном пространстве, увеличенными до 2 см (рис. 2). .Биопсия правого надпочечника под контролем КТ была отложена из-за развития сложного парциального эпилептического статуса 23 октября, когда у пациента появились ступор, шлепки по губам и эпилептиформные выделения на левой височной стороне, которые разрешились при лечении фенитоином натрия. . Наконец, результаты биопсии показали, что синусоиды надпочечников заполнены некогезивными агрегатами злокачественных лимфоидных клеток (рис. 3) с сильной реакцией на антитела к CD20, специфичные для В-лимфоцитов. Был поставлен диагноз внутрисосудистой лимфомы с поражением как надпочечников, так и головного мозга, а также лимфатических узлов средостения и забрюшинного пространства. Была начата химиотерапия CHOP (состоящая из циклофосфамида, доксорубицина гидрохлорида, винкристина сульфата и преднизона), последний из 8 курсов был проведен в марте 1997 года. Клинические, лабораторные и визуальные данные улучшились вскоре после первого цикла химиотерапии. Помимо легкой сенсорной полинейропатии, после завершения лечения неврологических отклонений не обнаружено. Несмотря на умеренно повышенные уровни лактатдегидрогеназы и β 2 -микроглобулина, считается, что у пациента наблюдается полная ремиссия в течение 34 месяцев после появления первых симптомов или в течение 28 месяцев после начала химиотерапии.
Была начата химиотерапия CHOP (состоящая из циклофосфамида, доксорубицина гидрохлорида, винкристина сульфата и преднизона), последний из 8 курсов был проведен в марте 1997 года. Клинические, лабораторные и визуальные данные улучшились вскоре после первого цикла химиотерапии. Помимо легкой сенсорной полинейропатии, после завершения лечения неврологических отклонений не обнаружено. Несмотря на умеренно повышенные уровни лактатдегидрогеназы и β 2 -микроглобулина, считается, что у пациента наблюдается полная ремиссия в течение 34 месяцев после появления первых симптомов или в течение 28 месяцев после начала химиотерапии.Рисунок 1.
Осевое Т2-взвешенное магнитно-резонансное изображение, показывающее гиперинтенсивное поражение в задней части левого чечевицеобразного ядра (черная стрелка).
Рисунок 2.
Осевое компьютерное томографическое сканирование верхней части живота, показывающее двусторонние опухоли надпочечников (черные стрелки) и увеличенные ретрокруральные и парааортальные лимфатические узлы (белые стрелки).

Рисунок 3.
Увеличение с большим увеличением показывает капилляр надпочечников, заполненный некогезивным агрегатом злокачественных лимфоидных клеток (окрашивание периодической кислотой – Шиффа, исходное увеличение × 1120).
У пациентов с ИВЛ наблюдается широкий спектр неврологических синдромов, включая деменцию, делирий, судороги, очаговые неврологические симптомы, миелопатию, полирадикулопатию, периферическую невропатию и миопатию. Диагноз обычно не ставится перед вскрытием из-за быстрого прогрессирования и смешанных клинических признаков, имитирующих воспалительный, сосудистый или дегенеративный процесс, который в случае поражения центральной нервной системы предполагает менингоэнцефалит, церебральный васкулит, инсульт или деменцию.У нашего пациента с острым спутанным состоянием и признаками системного заболевания (лихорадка, повышенная скорость оседания, анемия) диагноз был поставлен с учетом возможности паранеопластического синдрома.
 Окончательный диагноз был поставлен при обнаружении двусторонней опухоли надпочечников. Биопсия этого органа представляла собой альтернативу биопсии головного мозга. Нелокализационные результаты нейроповеденческих и ЭЭГ у нашего пациента, вероятно, отражают диффузную инфильтрацию мелких церебральных сосудов, тогда как более очаговые ЭЭГ и ограниченные изменения и изменения МРТ в левом полушарии отражают локальный максимум инфильтративного процесса, ведущего к тромбозу и последующему видимому инфаркту. на МРТ и сложные парциальные припадки.Таким образом, имело место сочетание диффузных (или энцефалопатических) и местных церебральных проявлений. Неясно, было ли улучшение после первоначального проявления в виде менингоэнцефалита результатом спонтанной временной ремиссии лимфомы или восстановления после ишемического события, не видимого на КТ и МРТ. При ИВЛ с неврологическим синдромом исследования спинномозговой жидкости и процедуры визуализации головного мозга обычно дают неспецифические или даже нормальные результаты.
Окончательный диагноз был поставлен при обнаружении двусторонней опухоли надпочечников. Биопсия этого органа представляла собой альтернативу биопсии головного мозга. Нелокализационные результаты нейроповеденческих и ЭЭГ у нашего пациента, вероятно, отражают диффузную инфильтрацию мелких церебральных сосудов, тогда как более очаговые ЭЭГ и ограниченные изменения и изменения МРТ в левом полушарии отражают локальный максимум инфильтративного процесса, ведущего к тромбозу и последующему видимому инфаркту. на МРТ и сложные парциальные припадки.Таким образом, имело место сочетание диффузных (или энцефалопатических) и местных церебральных проявлений. Неясно, было ли улучшение после первоначального проявления в виде менингоэнцефалита результатом спонтанной временной ремиссии лимфомы или восстановления после ишемического события, не видимого на КТ и МРТ. При ИВЛ с неврологическим синдромом исследования спинномозговой жидкости и процедуры визуализации головного мозга обычно дают неспецифические или даже нормальные результаты. Напротив, поиск увеличенных или пораженных инфарктом внутренних органов, как показано в отчете о случае, может иметь важное значение для выявления основного заболевания.Диагноз можно поставить только с помощью биопсии одного из пораженных органов, в основном головного мозга, кожи или легких. 5 Биопсия висцерального органа, когда это имеет смысл, представляет собой альтернативу биопсии головного мозга. Хотя надпочечник был диагностическим органом только у 1 пациента при обследовании 32 пациентов с ИВЛ, 5 он встречается гораздо чаще. В ряде случаев сообщалось о двустороннем увеличении надпочечников, которое может привести к надпочечниковой недостаточности. 4 , 8 -10 Сообщалось, что инфильтрация надпочечников присутствует в 60% случаев вскрытия. 10 Поэтому КТ брюшной полости всегда следует выполнять в клинических условиях, упомянутых выше. Ответ на химиотерапию CHOP у нашего пациента был отличным, что привело к полной ремиссии и бессимптомной выживаемости, которая в настоящее время превышает 32 месяца.
Напротив, поиск увеличенных или пораженных инфарктом внутренних органов, как показано в отчете о случае, может иметь важное значение для выявления основного заболевания.Диагноз можно поставить только с помощью биопсии одного из пораженных органов, в основном головного мозга, кожи или легких. 5 Биопсия висцерального органа, когда это имеет смысл, представляет собой альтернативу биопсии головного мозга. Хотя надпочечник был диагностическим органом только у 1 пациента при обследовании 32 пациентов с ИВЛ, 5 он встречается гораздо чаще. В ряде случаев сообщалось о двустороннем увеличении надпочечников, которое может привести к надпочечниковой недостаточности. 4 , 8 -10 Сообщалось, что инфильтрация надпочечников присутствует в 60% случаев вскрытия. 10 Поэтому КТ брюшной полости всегда следует выполнять в клинических условиях, упомянутых выше. Ответ на химиотерапию CHOP у нашего пациента был отличным, что привело к полной ремиссии и бессимптомной выживаемости, которая в настоящее время превышает 32 месяца. Режимы химиотерапии, направленные на лимфомы средней и высокой степени злокачественности, кажутся наиболее благоприятными. Хотя нет более крупных серий случаев или рандомизированных исследований, природа заболевания (лимфома высокой степени) и, по крайней мере, 1 опрос пациентов в литературе предполагают использование химиотерапии CHOP для пациентов с ИВЛ.Из 23 пациентов, получавших химиотерапию CHOP, 6 (55%) из 11 достигли полной ремиссии. 2 Напротив, ответ на стероидную терапию с лучевой терапией или без нее, вероятно, плохой. Сообщалось о временном, но резком улучшении после плазмафереза у пациента с ИВЛ и антителами к гликопротеинам, ассоциированным с миелином. 11 Спонтанная ремиссия наблюдалась у пациента с рентгенологическими проявлениями церебрального артериита. 12
Режимы химиотерапии, направленные на лимфомы средней и высокой степени злокачественности, кажутся наиболее благоприятными. Хотя нет более крупных серий случаев или рандомизированных исследований, природа заболевания (лимфома высокой степени) и, по крайней мере, 1 опрос пациентов в литературе предполагают использование химиотерапии CHOP для пациентов с ИВЛ.Из 23 пациентов, получавших химиотерапию CHOP, 6 (55%) из 11 достигли полной ремиссии. 2 Напротив, ответ на стероидную терапию с лучевой терапией или без нее, вероятно, плохой. Сообщалось о временном, но резком улучшении после плазмафереза у пациента с ИВЛ и антителами к гликопротеинам, ассоциированным с миелином. 11 Спонтанная ремиссия наблюдалась у пациента с рентгенологическими проявлениями церебрального артериита. 12 Внутрисосудистый лимфоматоз следует учитывать при дифференциальной диагностике необъяснимого менингоэнцефалита, состояния острой спутанности сознания, деменции или синдромов, подобных инсульту.
 Обследования должны включать органы, часто пораженные ИВЛ, такие как почки, надпочечники, печень и легкие. В случае поражения внутренних органов или кожи биопсия пораженного органа может привести к постановке диагноза без биопсии головного мозга. Лечение химиотерапией CHOP, как и при других неходжкинских лимфомах высокой степени, должно быть стандартной терапией.
Обследования должны включать органы, часто пораженные ИВЛ, такие как почки, надпочечники, печень и легкие. В случае поражения внутренних органов или кожи биопсия пораженного органа может привести к постановке диагноза без биопсии головного мозга. Лечение химиотерапией CHOP, как и при других неходжкинских лимфомах высокой степени, должно быть стандартной терапией.Принята к публикации 28 апреля 1999 г.
Представлен в качестве плаката на Седьмом заседании Европейского неврологического общества, Родос, Греция, 15 июня 1997 г.
Отпечатки: Томас П. Бауманн, доктор медицины, отделение неврологии, университетская больница, Frauenklinikstrasse 26, CH-8091 Zurich, Switzerland.
1.Пфлегер
LTappeiner
J Zur Kenntnis der systemisierten Endotheliomatose der cutanen Blutgefässe. Hautarzt. 1959; 10359-363Google Scholar2.Demirer
TDavid
HDAboulafia
DM. Четыре различных случая внутрисосудистого лимфоматоза и обзор литературы. Рак. 1994; 731738-1745Google ScholarCrossref 3. Фитиль
Рак. 1994; 731738-1745Google ScholarCrossref 3. Фитиль
MRStacey
Е.М. Внутрисосудистый лимфоматоз: клинико-патологические особенности и дифференциальный диагноз. Semin Diagn Pathol. 1991; 891-101Google Scholar4.Shanks
Дж. Х. Харрис
MHowat
AJFreemont
AJ Ангиотропная лимфома с эндокринным поражением. Гистопатология. 1997; 31161-166Google ScholarCrossref 5.Liszka
UDrlicek
MHitzenberger
п
и другие.Внутрисосудистый лимфоматоз: клинико-патологическое исследование трех случаев. J Cancer Res Clin Oncol. 1994; 120164-168Google ScholarCrossref 6. Левин
KHLutz
G Ангиотропная крупноклеточная лимфома с поражением периферических нервов и скелетных мышц. Неврология. 1996; 471009-1011Google ScholarCrossref 7.
Американская психиатрическая ассоциация, Диагностическое и статистическое руководство по психическим расстройствам, четвертое издание . Вашингтон, округ Колумбия, Американская психиатрическая ассоциация, 1994;
8.Шейбани
KBattifora
HWinberg
CD
и другие. Еще одно доказательство того, что «злокачественный ангиоэндотелиоматоз» представляет собой ангиотропную крупноклеточную лимфому. N Engl J Med. 1986; 314943–948Google ScholarCrossref 9.Chu
PCosta
Я. Лахманн
MF Ангиотропная крупноклеточная лимфома, проявляющаяся как первичная надпочечниковая недостаточность. Hum Pathol. 1996; 27209-211Google ScholarCrossref 10. Масатаке
SKatsushige
С.М.акото
МТошики
УХироши
T Случай ангиотропной лимфомы, диагностированный при биопсии надпочечников. Clin Neurol. 1992; 32747-751Google Scholar11. Harris
Harris
PCSigman
JDJaeckle
К.А. Внутрисосудистый злокачественный лимфоматоз: уменьшение неврологических симптомов с помощью плазмафереза. Ann Neurol. 1994; 35357-359Google ScholarCrossref 12.LeWitt
PAForno
LSBrant-Zawadzki
M Неопластический ангиоэндотелиоз: случай спонтанного регресса и рентгенологических проявлений церебрального артериита. Неврология. 1983; 3339-44Google ScholarCrossrefВнутрисосудистая лимфома в виде поперечного миелита у пациента с миелодиспластическим синдромом
Резюме: Справочная информация: Внутрисосудистая лимфома (ИВЛ) — редкий подтип В-клеточной лимфомы больших размеров, который часто проявляется неврологическими признаками.Как известно, диагностика ИВЛ является сложной задачей и часто не устанавливается до патологоанатомического исследования.
Описание случая: Здесь мы описываем случай 72-летнего мужчины с миелодиспластическим синдромом (МДС), переходно-клеточной карциномой и ишемической болезнью сердца в анамнезе, который поступил с острым прогрессирующим спастическим парапарезом, локализованным в позвоночнике с помощью МРТ.
 и лабораторные данные, убедительно указывающие на диагноз идиопатический поперечный миелит (TM). После того, как лечение кортикостероидами не дало устойчивого улучшения, обследование на потенциальное скрытое интрамедуллярное злокачественное новообразование спинного мозга привело к случайной биопсии кожи, которая показала лежащую в основе ИВЛ, которая, как было показано, имитирует ТМ.
и лабораторные данные, убедительно указывающие на диагноз идиопатический поперечный миелит (TM). После того, как лечение кортикостероидами не дало устойчивого улучшения, обследование на потенциальное скрытое интрамедуллярное злокачественное новообразование спинного мозга привело к случайной биопсии кожи, которая показала лежащую в основе ИВЛ, которая, как было показано, имитирует ТМ.Обсуждение: МДС обычно прогрессирует до острого миелоидного лейкоза (ОМЛ), но, как известно, не вызывает лимфоидных злокачественных новообразований, несмотря на несколько сообщений об ИВЛ после постановки диагноза МДС. У пациентов с подозрением на ТМ МРТ имеет решающее значение для исключения компрессионной миелопатии, но недостаточна для диагностики ИВЛ, и при подозрении на ИВЛ следует попытаться диагностировать случайную биопсию кожи перед биопсией мозга или позвоночника, даже при отсутствии явных кожных изменений. Ранняя диагностика имеет решающее значение для назначения пациентов на соответствующую химиотерапию, поэтому ИВЛ всегда должна быть в дифференциальной диагностике у пациентов с явным TM, с или без МДС.

Резюме: Здесь мы описываем случай 72-летнего мужчины с внутрисосудистой лимфомой (ИВЛ) позвоночника, которая была замаскирована как поперечный миелит (ТМ) и осложнена существующим диагнозом миелодиспластического синдрома (МДС). ИВЛ следует рассматривать у пациентов с прогрессирующими очаговыми неврологическими симптомами, с или без МДС. При подозрении на ИВЛ сначала следует попытаться поставить диагноз путем случайной биопсии кожи, прежде чем рассматривать возможность проведения биопсии головного или спинного мозга, даже без явных кожных проявлений. Ссылки: 1. Арбер Д.А., Орази А., Хассерджиан Р., Тиле Дж., Боровиц М.Дж., Ле Бо М.М. и др. Пересмотр 2016 г. классификации миелоидных новообразований и острого лейкоза Всемирной организации здравоохранения. Кровь 2016; 127: 2391–405.
2. Валенсия-Санчес С. Поперечный миелит. BMJ Best Practice. Июнь 2020 г. https://bestpractice.bmj.com/topics/en-gb/1061. По состоянию на 8 июля 2020 г.
3. Pawar NH, Loke E, Aw DC.

 30.005.001)
30.005.001)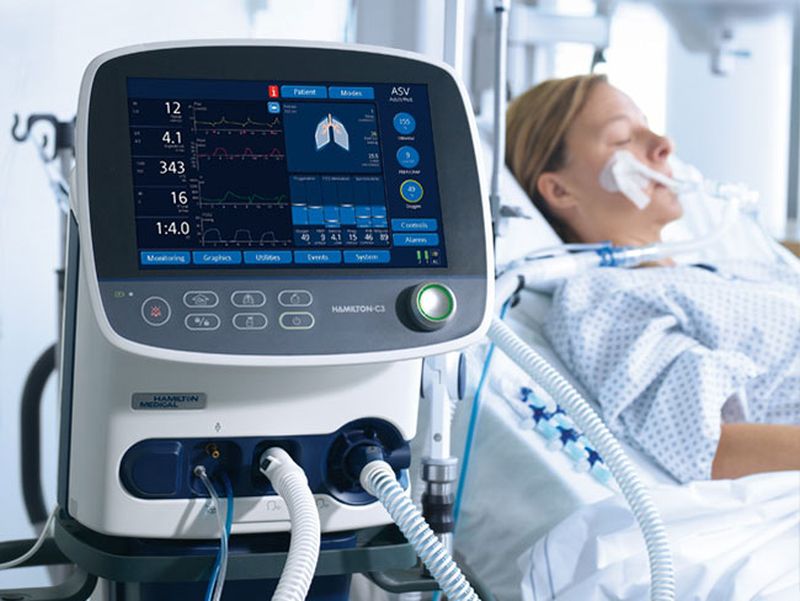 23.009.001)
23.009.001) 30.008.001)
30.008.001)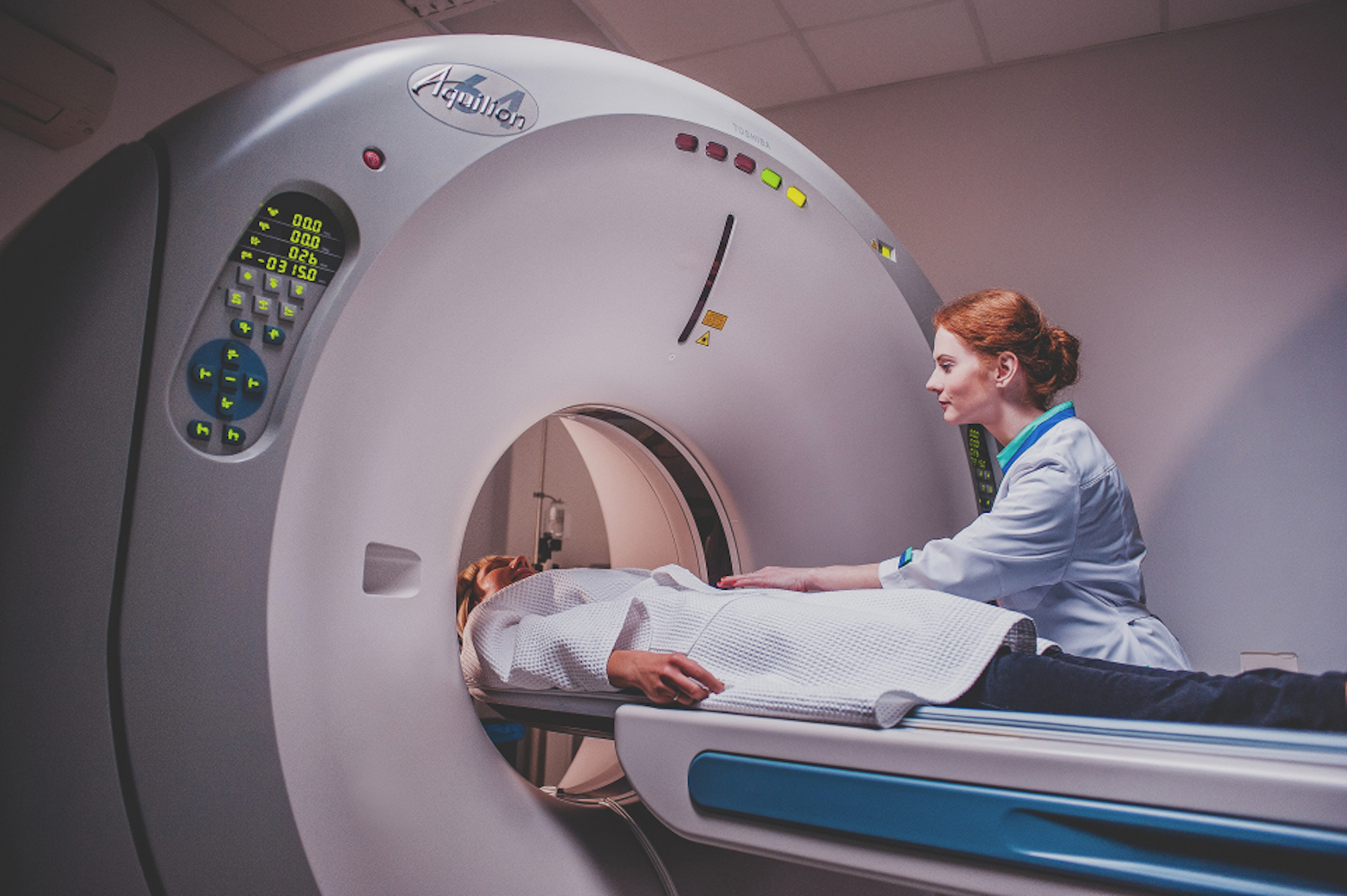 12.006)
12.006)

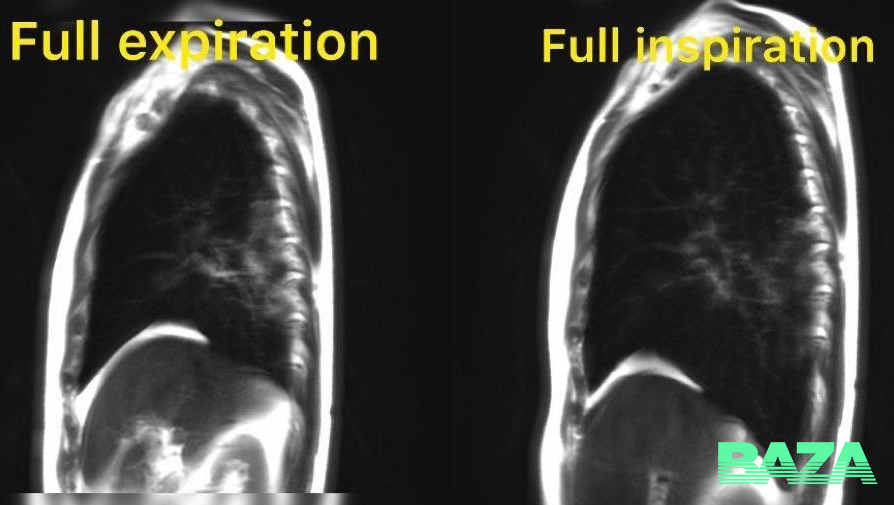
 Радиология 2000; 217: 331–45.
Радиология 2000; 217: 331–45.  Eur Radiol 2003; 13: 1753–5.
Eur Radiol 2003; 13: 1753–5.  J Neuroimaging 1998; 8: 110–13.
J Neuroimaging 1998; 8: 110–13.  Clin Lab Haematol 1994; 16: 363–9.
Clin Lab Haematol 1994; 16: 363–9.  Журнал Neurooncol2003; 61: 237–48.
Журнал Neurooncol2003; 61: 237–48. 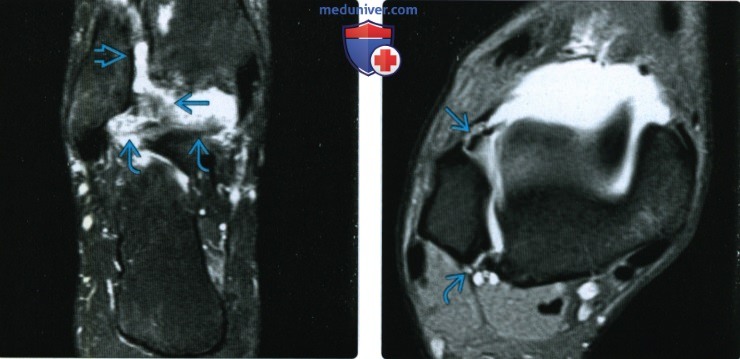 1 Характеризуется предрасположенностью к внутрисосудистому разрастанию опухолевых клеток в мелких сосудах с предрасположенностью к центральной нервной системе и коже. 2,3 Прижизненная диагностика ИВЛ затруднена из-за различных клинических проявлений и неспецифических лабораторных данных, хотя во многих случаях обнаруживается повышение уровня ЛДГ и растворимого рецептора интерлейкина-2. 4–6 Результаты МРТ головного мозга у пациентов с ИВЛ также разнообразны; эти вариации затрудняют диагностику. 7 После установления правильного диагноза ИВЛ с помощью биопсии ткани полная ремиссия может быть достигнута с помощью химиотерапии с использованием R-CHOP. 8,9 Распознавание и тщательная интерпретация различных результатов МРТ головного мозга может облегчить раннюю диагностику и вмешательство, а также улучшить прогноз этого часто упускаемого из виду заболевания. 10
1 Характеризуется предрасположенностью к внутрисосудистому разрастанию опухолевых клеток в мелких сосудах с предрасположенностью к центральной нервной системе и коже. 2,3 Прижизненная диагностика ИВЛ затруднена из-за различных клинических проявлений и неспецифических лабораторных данных, хотя во многих случаях обнаруживается повышение уровня ЛДГ и растворимого рецептора интерлейкина-2. 4–6 Результаты МРТ головного мозга у пациентов с ИВЛ также разнообразны; эти вариации затрудняют диагностику. 7 После установления правильного диагноза ИВЛ с помощью биопсии ткани полная ремиссия может быть достигнута с помощью химиотерапии с использованием R-CHOP. 8,9 Распознавание и тщательная интерпретация различных результатов МРТ головного мозга может облегчить раннюю диагностику и вмешательство, а также улучшить прогноз этого часто упускаемого из виду заболевания. 10  Мы ретроспективно проанализировали МРТ головного мозга у 11 последовательных пациентов, которым в период с 1998 по 2009 год был поставлен патологический диагноз ИВЛ. Двум пациентам был поставлен диагноз при патологоанатомическом исследовании, а 9 случаев были диагностированы на основании различных биопсий тканей. Биопсия включала 1 лимфатический узел, 1 легкое и костный мозг, а также 7 случайных биопсий кожи. Трое из 9 пациентов, которым была поставлена биопсия ткани, подверглись вскрытию. Медицинские карты были просмотрены на предмет их симптомов, истории болезни, лабораторных данных и лечения.
Мы ретроспективно проанализировали МРТ головного мозга у 11 последовательных пациентов, которым в период с 1998 по 2009 год был поставлен патологический диагноз ИВЛ. Двум пациентам был поставлен диагноз при патологоанатомическом исследовании, а 9 случаев были диагностированы на основании различных биопсий тканей. Биопсия включала 1 лимфатический узел, 1 легкое и костный мозг, а также 7 случайных биопсий кожи. Трое из 9 пациентов, которым была поставлена биопсия ткани, подверглись вскрытию. Медицинские карты были просмотрены на предмет их симптомов, истории болезни, лабораторных данных и лечения. Семь из 11 пациентов прошли первоначальную МРТ в течение 1 недели после поступления, а остальные 4 были просканированы в течение 2 месяцев.
Семь из 11 пациентов прошли первоначальную МРТ в течение 1 недели после поступления, а остальные 4 были просканированы в течение 2 месяцев. Пациентами были 4 мужчин и 7 женщин в возрасте от 63 до 84 лет (средний возраст 71,4 года). Симптомами были лихорадка у всех, деменция у 5, одышка у 2, изменения личности у 2 и недомогание у 1 пациента. Пятерым пациентам, включая 3 пролеченных и 2 нелеченых, было проведено патологоанатомическое исследование головного мозга (таблица).
Пациентами были 4 мужчин и 7 женщин в возрасте от 63 до 84 лет (средний возраст 71,4 года). Симптомами были лихорадка у всех, деменция у 5, одышка у 2, изменения личности у 2 и недомогание у 1 пациента. Пятерым пациентам, включая 3 пролеченных и 2 нелеченых, было проведено патологоанатомическое исследование головного мозга (таблица). 1 A , — B ).У этих пациентов мультифокальные поражения уменьшились в размере и количестве после лечения. Патологоанатомическое исследование выявило множественные инфаркты с закупоркой сосудов опухолевыми клетками, некроз неправильной формы и скопление вокруг закупоренных сосудов (рис. 1 C ). Также часто наблюдались незначительные геморрагические инфаркты. Неспецифические поражения белого вещества наблюдались у 2 из 11 пациентов. Диффузная гиперинтенсивность белого вещества наблюдалась особенно в перивентрикулярных областях (рис. 2 A ).Очаговая гиперинтенсивность белого вещества также наблюдалась в подкорковых областях в случае 3. У этого пациента, у которого не была диагностирована и не лечилась специально по поводу ИВЛ, гиперинтенсивная область постепенно увеличивалась в размерах. Однако у пролеченного пациента повреждения улучшились сразу после начала лечения (рис. 2 B ). Патологоанатомическое исследование выявило диффузную демиелинизацию белого вещества с сосудами, сильно закупоренными опухолевыми клетками в соответствующих областях (рис.
1 A , — B ).У этих пациентов мультифокальные поражения уменьшились в размере и количестве после лечения. Патологоанатомическое исследование выявило множественные инфаркты с закупоркой сосудов опухолевыми клетками, некроз неправильной формы и скопление вокруг закупоренных сосудов (рис. 1 C ). Также часто наблюдались незначительные геморрагические инфаркты. Неспецифические поражения белого вещества наблюдались у 2 из 11 пациентов. Диффузная гиперинтенсивность белого вещества наблюдалась особенно в перивентрикулярных областях (рис. 2 A ).Очаговая гиперинтенсивность белого вещества также наблюдалась в подкорковых областях в случае 3. У этого пациента, у которого не была диагностирована и не лечилась специально по поводу ИВЛ, гиперинтенсивная область постепенно увеличивалась в размерах. Однако у пролеченного пациента повреждения улучшились сразу после начала лечения (рис. 2 B ). Патологоанатомическое исследование выявило диффузную демиелинизацию белого вещества с сосудами, сильно закупоренными опухолевыми клетками в соответствующих областях (рис.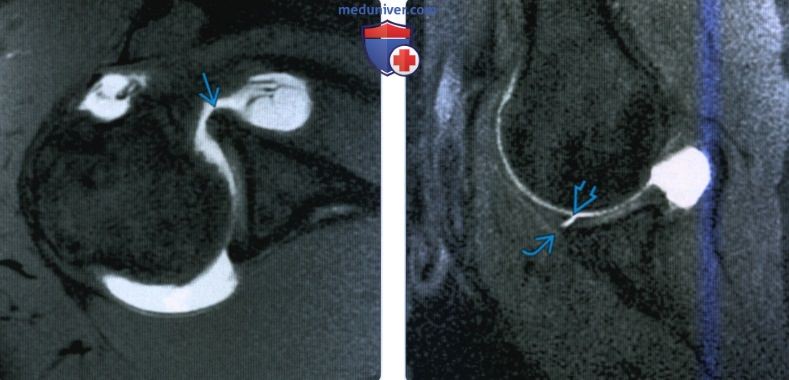 2 C ).
2 C ).
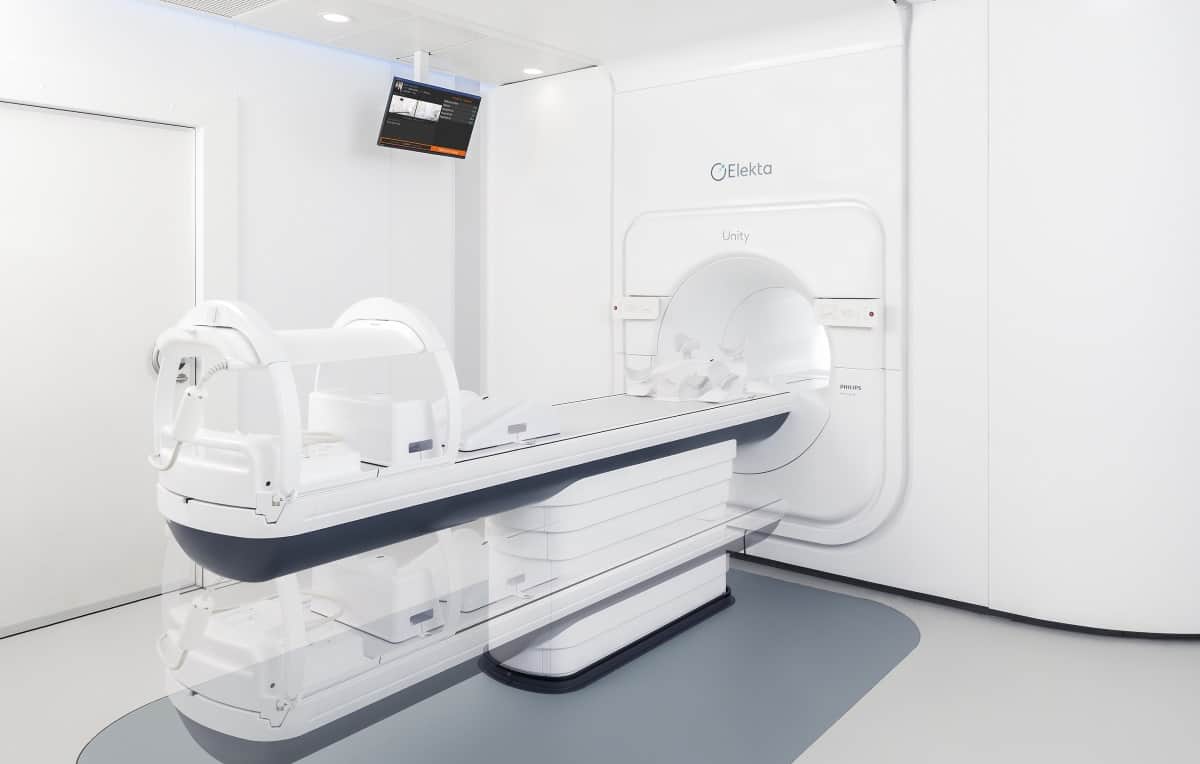 У всех 5 пациентов были обнаружены симметричные гиперинтенсивные области в центральном мосту, за исключением покрышки моста и вентролатерального моста (рис. 5 A ).Гиперинтенсивные области в мосту уменьшились в размере и интенсивности у всех 4 пациентов, прошедших лечение (Рис. 5 B ). В случае 9 последующая МРТ показала уменьшение размера поражения через 3 дня после лечения. Атрофии ствола головного мозга после лечения не наблюдалось ни в одном из этих 4 случаев.
У всех 5 пациентов были обнаружены симметричные гиперинтенсивные области в центральном мосту, за исключением покрышки моста и вентролатерального моста (рис. 5 A ).Гиперинтенсивные области в мосту уменьшились в размере и интенсивности у всех 4 пациентов, прошедших лечение (Рис. 5 B ). В случае 9 последующая МРТ показала уменьшение размера поражения через 3 дня после лечения. Атрофии ствола головного мозга после лечения не наблюдалось ни в одном из этих 4 случаев.
 У пациентов не было тяжелой гипертонии, судорог, реакции на химиотерапию или других состояний, которые могут привести к PRES.
У пациентов не было тяжелой гипертонии, судорог, реакции на химиотерапию или других состояний, которые могут привести к PRES. .Низкая частота инфарктоподобных поражений может быть объяснена временем проведения МРТ до лечения и стадией заболевания.
.Низкая частота инфарктоподобных поражений может быть объяснена временем проведения МРТ до лечения и стадией заболевания.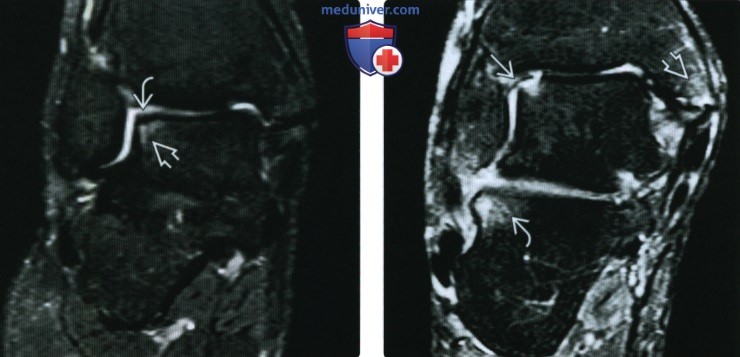
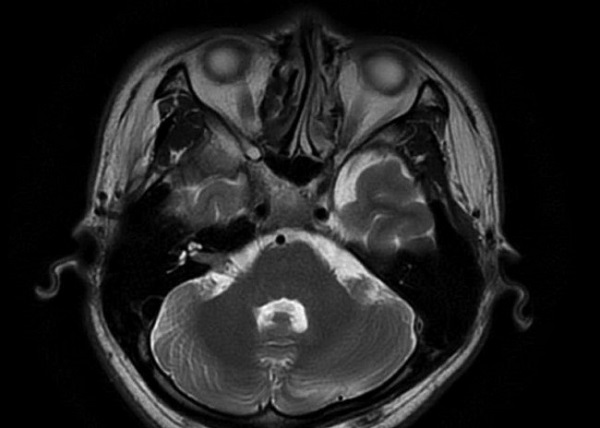 2,3,7,14,15 Экстравазация лимфомных клеток и утолщение сосудистой стенки с прямой инфильтрацией опухолевых клеток в сосудистые стенки выявлены при патологоанатомическом исследовании. Патологические изменения, лежащие в основе этой модели, могут быть многофакторными.
2,3,7,14,15 Экстравазация лимфомных клеток и утолщение сосудистой стенки с прямой инфильтрацией опухолевых клеток в сосудистые стенки выявлены при патологоанатомическом исследовании. Патологические изменения, лежащие в основе этой модели, могут быть многофакторными. Когда окклюзия возникает в мелких артериях, можно ожидать множественных небольших инфарктов, таких как инфарктоподобные поражения, видимые на МРТ в этом исследовании.Окклюзия капилляров может вызвать аномальную интенсивность диффузного белого вещества. Мы предположили, что гиперинтенсивные поражения в мосту также были результатом окклюзии капилляров в мосту, как это наблюдалось при патологоанатомическом исследовании в случае 3. Когда большое количество лимфомных клеток вызывает внесосудистую массу, можно ожидать массоподобных повреждений. Утолщение менингеальных сосудов при некоторой воспалительной реакции может проявляться как усиление менингеальных сосудов. Внимание к внутрисосудистой природе этой уникальной лимфомы может привести к лучшему распознаванию различных проявлений МРТ и более своевременной диагностике.
Когда окклюзия возникает в мелких артериях, можно ожидать множественных небольших инфарктов, таких как инфарктоподобные поражения, видимые на МРТ в этом исследовании.Окклюзия капилляров может вызвать аномальную интенсивность диффузного белого вещества. Мы предположили, что гиперинтенсивные поражения в мосту также были результатом окклюзии капилляров в мосту, как это наблюдалось при патологоанатомическом исследовании в случае 3. Когда большое количество лимфомных клеток вызывает внесосудистую массу, можно ожидать массоподобных повреждений. Утолщение менингеальных сосудов при некоторой воспалительной реакции может проявляться как усиление менингеальных сосудов. Внимание к внутрисосудистой природе этой уникальной лимфомы может привести к лучшему распознаванию различных проявлений МРТ и более своевременной диагностике. В остальных 6 случаях мозговая ткань не бралась. Массивные поражения и гиперинтенсивные поражения в мосту на T2WI не были патологически доказаны в этом исследовании. У пациентов с тяжелыми заболеваниями биопсия головного мозга часто затруднена, и патологоанатомическое исследование может быть единственным способом проанализировать эти закономерности.
В остальных 6 случаях мозговая ткань не бралась. Массивные поражения и гиперинтенсивные поражения в мосту на T2WI не были патологически доказаны в этом исследовании. У пациентов с тяжелыми заболеваниями биопсия головного мозга часто затруднена, и патологоанатомическое исследование может быть единственным способом проанализировать эти закономерности.
 В нашем учреждении мы просканировали более 200 пациентов с vwMRI, в том числе 47-летнюю женщину с подтвержденной биопсией большой B-клеточной IVL. Ее vwMRI показала множественные области развивающегося ишемического инфаркта, паренхиматозного кровоизлияния, отека и лептоменингеального усиления; однако на vwMRI не было обнаружено утолщения или увеличения стенки сосуда, включая правую теменную долю, где у нее был инфаркт с отеком, и место биопсии мозга.Эта биопсия была характерна для ИВЛ с множественными кортикальными сосудами (ответвлениями M4), патологически расширенными, с опухолевыми лимфоцитами, положительными на CD20 по данным иммуногистохимии. Биопсия центральной нервной системы у пациентов с ИВЛ выявила неопластические лимфоциты в крупных и средних артериях, дистальных кортикальных сосудах, лептоменингеальных перфораторах, капиллярах и даже в венах [2–6]. Учитывая эту сосудистую гетерогенность, результаты vwMRI IVL, несомненно, также сильно различаются. Разрешение текущих протоколов vwMRI, 0.
В нашем учреждении мы просканировали более 200 пациентов с vwMRI, в том числе 47-летнюю женщину с подтвержденной биопсией большой B-клеточной IVL. Ее vwMRI показала множественные области развивающегося ишемического инфаркта, паренхиматозного кровоизлияния, отека и лептоменингеального усиления; однако на vwMRI не было обнаружено утолщения или увеличения стенки сосуда, включая правую теменную долю, где у нее был инфаркт с отеком, и место биопсии мозга.Эта биопсия была характерна для ИВЛ с множественными кортикальными сосудами (ответвлениями M4), патологически расширенными, с опухолевыми лимфоцитами, положительными на CD20 по данным иммуногистохимии. Биопсия центральной нервной системы у пациентов с ИВЛ выявила неопластические лимфоциты в крупных и средних артериях, дистальных кортикальных сосудах, лептоменингеальных перфораторах, капиллярах и даже в венах [2–6]. Учитывая эту сосудистую гетерогенность, результаты vwMRI IVL, несомненно, также сильно различаются. Разрешение текущих протоколов vwMRI, 0.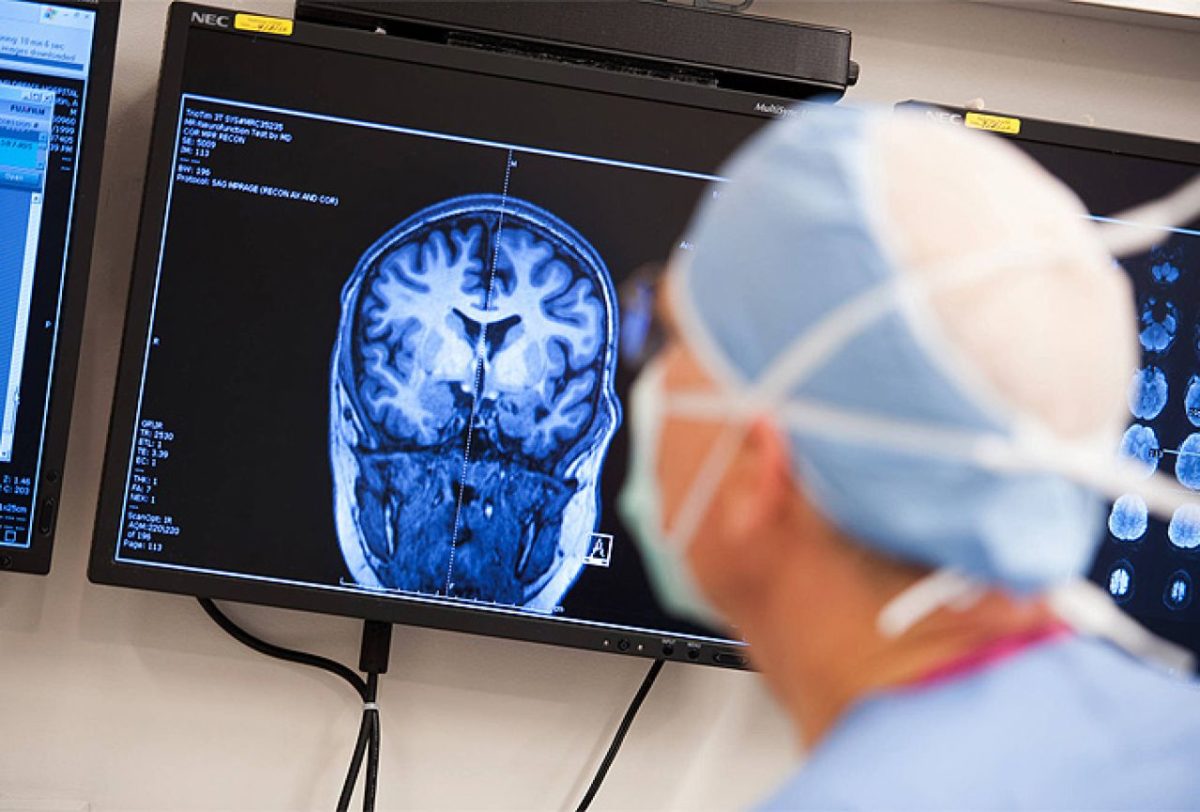 Вокселы размером 5–0,7 мм не позволяют надежно оценить дистальные внутричерепные сосуды, что создает возможность ложноотрицательного исследования, как в случае с нашим пациентом. Более того, как отмечают авторы, при васкулите интрамуральная лимфоцитарная инвазия обеспечивает патофизиологический механизм увеличения концентрической стенки сосуда, тогда как при ИВЛ стенка самого сосуда сохраняется. Учитывая эти проблемы, мы предлагаем с осторожностью интерпретировать их результаты в диагностических целях.
Вокселы размером 5–0,7 мм не позволяют надежно оценить дистальные внутричерепные сосуды, что создает возможность ложноотрицательного исследования, как в случае с нашим пациентом. Более того, как отмечают авторы, при васкулите интрамуральная лимфоцитарная инвазия обеспечивает патофизиологический механизм увеличения концентрической стенки сосуда, тогда как при ИВЛ стенка самого сосуда сохраняется. Учитывая эти проблемы, мы предлагаем с осторожностью интерпретировать их результаты в диагностических целях.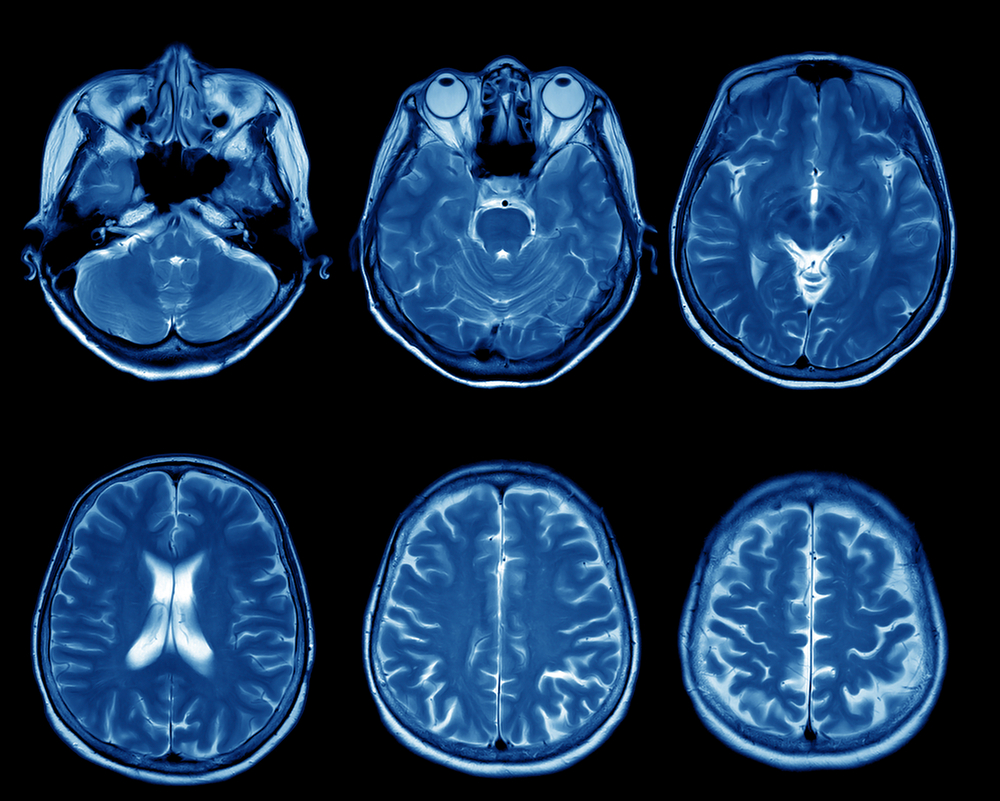 Однако при ранней диагностике и соответствующей химиотерапии прогноз значительно улучшается и возможна полная ремиссия. Чтобы расширить возможные проявления ИВЛ, мы представляем пациента с атипичным проявлением подтвержденной биопсией внутрисосудистой крупноклеточной В-клеточной лимфомы, которая перенесла расслоение как внутричерепных, так и экстракраниальных артерий в дополнение к прогрессирующим внутричерепным кровоизлияниям. История болезни . Женщина 47 лет обратилась с жалобой на односторонние парестезии.У нее развились прогрессирующие мультифокальные инфаркты и кровотечение с расслоением как внутричерепных, так и экстракраниальных артерий, что привело к коме. Биопсия головного мозга показала ИВЛ. Она прошла агрессивную химиотерапию и остается в полной ремиссии с хорошим неврологическим выздоровлением. Заключение . Известно, что ИВЛ оказывает свою патологию на мелкие артерии и капилляры, но не известно, что вызывает расслоение крупных сосудов. Диагноз следует рассматривать в случаях необъяснимого расслоения артерий и прогрессирующих инсультов.
Однако при ранней диагностике и соответствующей химиотерапии прогноз значительно улучшается и возможна полная ремиссия. Чтобы расширить возможные проявления ИВЛ, мы представляем пациента с атипичным проявлением подтвержденной биопсией внутрисосудистой крупноклеточной В-клеточной лимфомы, которая перенесла расслоение как внутричерепных, так и экстракраниальных артерий в дополнение к прогрессирующим внутричерепным кровоизлияниям. История болезни . Женщина 47 лет обратилась с жалобой на односторонние парестезии.У нее развились прогрессирующие мультифокальные инфаркты и кровотечение с расслоением как внутричерепных, так и экстракраниальных артерий, что привело к коме. Биопсия головного мозга показала ИВЛ. Она прошла агрессивную химиотерапию и остается в полной ремиссии с хорошим неврологическим выздоровлением. Заключение . Известно, что ИВЛ оказывает свою патологию на мелкие артерии и капилляры, но не известно, что вызывает расслоение крупных сосудов. Диагноз следует рассматривать в случаях необъяснимого расслоения артерий и прогрессирующих инсультов.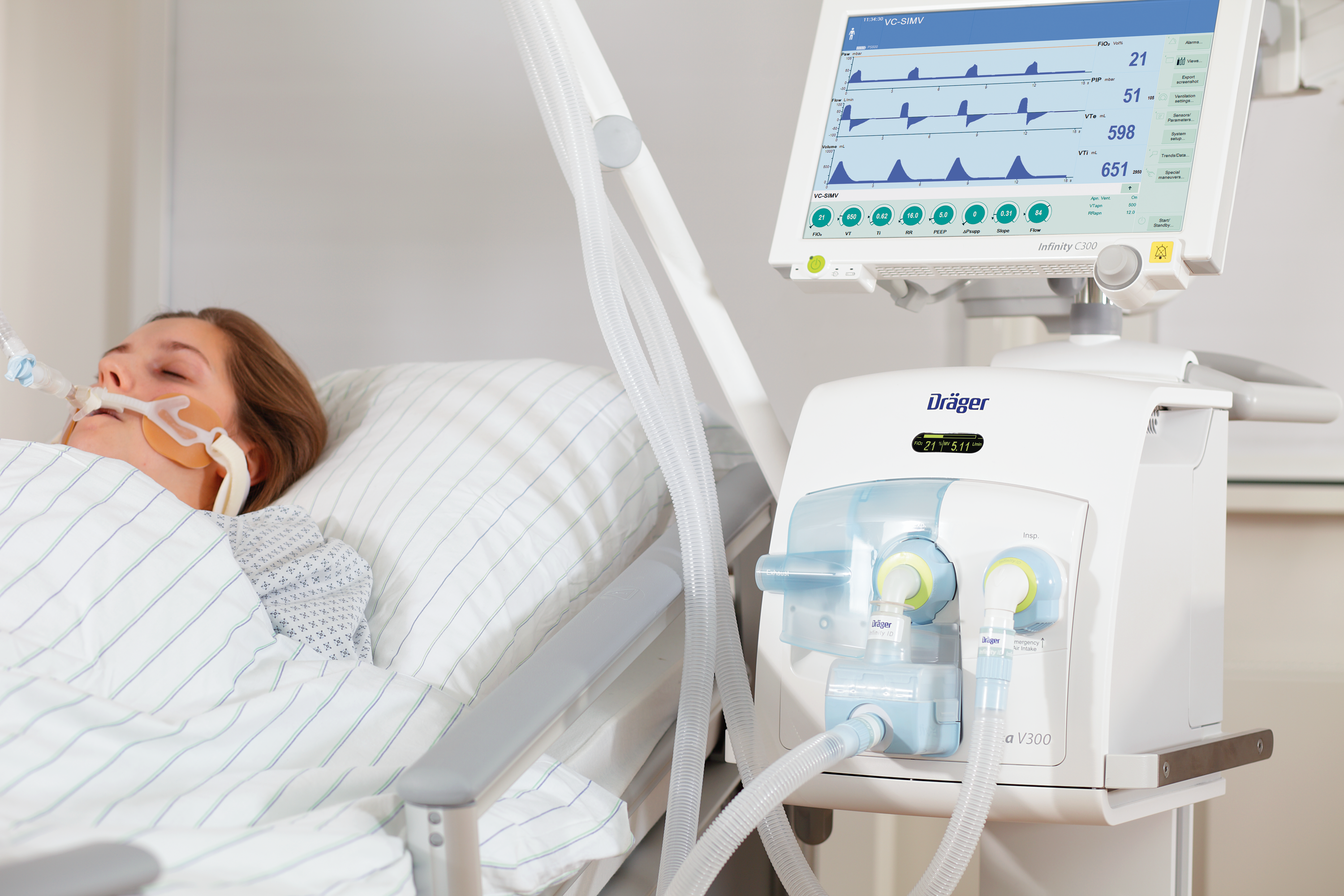 Ранняя диагностика с соответствующим лабораторным обследованием и подтверждением ткани биопсией может привести к значительному улучшению результатов.
Ранняя диагностика с соответствующим лабораторным обследованием и подтверждением ткани биопсией может привести к значительному улучшению результатов.
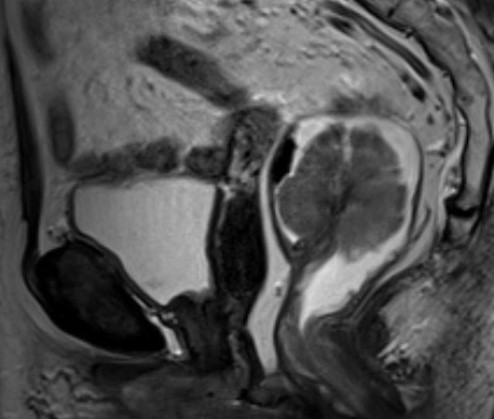 При своевременной диагностике и лечении полная ремиссия наблюдается примерно в 42% случаев, хотя недавние данные о выживаемости при адекватном лечении отсутствуют [11].Мы описываем необычное проявление ИВЛ с множественными рассечениями как внутричерепных, так и экстракраниальных кровеносных сосудов и прогрессирующими внутричерепными кровоизлияниями (ICH).
При своевременной диагностике и лечении полная ремиссия наблюдается примерно в 42% случаев, хотя недавние данные о выживаемости при адекватном лечении отсутствуют [11].Мы описываем необычное проявление ИВЛ с множественными рассечениями как внутричерепных, так и экстракраниальных кровеносных сосудов и прогрессирующими внутричерепными кровоизлияниями (ICH).
 1 г / дл
1 г / дл 83 мЕд / л
83 мЕд / л Непрерывные электроэнцефалограммы (ЭЭГ) подтвердили замедление энцефалопатии без эпилептиформных разрядов.Церебральная ангиография показала нерегулярный гофрированный вид шейных сонных артерий, что, как считается, соответствует хронической фиброзно-мышечной дисплазии (рис. 1 (b)). МРТ стенки сосуда с высоким разрешением не показала увеличения артериальной стенки, что свидетельствовало бы о васкулите. Позитронно-эмиссионная томография (ФДГ-ПЭТ) мозга с 18F-фтордезоксиглюкозой (рис. 2) и компьютерная томография (КТ) грудной клетки, брюшной полости и таза не выявили.
Непрерывные электроэнцефалограммы (ЭЭГ) подтвердили замедление энцефалопатии без эпилептиформных разрядов.Церебральная ангиография показала нерегулярный гофрированный вид шейных сонных артерий, что, как считается, соответствует хронической фиброзно-мышечной дисплазии (рис. 1 (b)). МРТ стенки сосуда с высоким разрешением не показала увеличения артериальной стенки, что свидетельствовало бы о васкулите. Позитронно-эмиссионная томография (ФДГ-ПЭТ) мозга с 18F-фтордезоксиглюкозой (рис. 2) и компьютерная томография (КТ) грудной клетки, брюшной полости и таза не выявили. В течение одного месяца после выписки у нее клиническое улучшение улучшилось, и она вернулась к работе, но постепенно усилились головная боль, рвота, летаргия и эпизодическое опускание лица слева. Повторная МРТ (рис. 3 (а)) показала заметное интервальное прогрессирование с появлением новых областей цитотоксического отека / инфаркта, вазогенного отека и умеренного правого височно-теменного кровоизлияния, вызывающего отек мозга и сдвиг средней линии, с дополнительными петехиальными кровоизлияниями на Т2-взвешенных изображениях. Появился обширный новый сигнал FLAIR и его усиление, совместимое с разрушением гематоэнцефалического барьера.
В течение одного месяца после выписки у нее клиническое улучшение улучшилось, и она вернулась к работе, но постепенно усилились головная боль, рвота, летаргия и эпизодическое опускание лица слева. Повторная МРТ (рис. 3 (а)) показала заметное интервальное прогрессирование с появлением новых областей цитотоксического отека / инфаркта, вазогенного отека и умеренного правого височно-теменного кровоизлияния, вызывающего отек мозга и сдвиг средней линии, с дополнительными петехиальными кровоизлияниями на Т2-взвешенных изображениях. Появился обширный новый сигнал FLAIR и его усиление, совместимое с разрушением гематоэнцефалического барьера.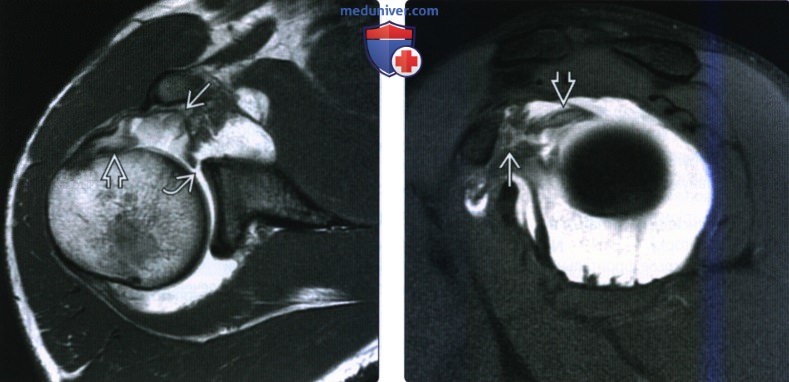 Во время начальной катетерной ангиограммы не было инструментов выше уровня общих сонных артерий или начала позвоночных артерий, чтобы объяснить это открытие. В наш дифференциальный диагноз были включены атипичные васкулиты, воспалительная амилоидная ангиопатия, осложненный синдром задней обратимой энцефалопатии (PRES) и синдром обратимой церебральной вазоконстрикции (RCVS) или ИВЛ (таблица 2). Поскольку повышенный уровень ЛДГ в атипичном случае без инфекции может указывать на ИВЛ, мы измерили ЛДГ и обнаружили, что ее уровень повышен до 450 Ед / л (Таблица 1).
Во время начальной катетерной ангиограммы не было инструментов выше уровня общих сонных артерий или начала позвоночных артерий, чтобы объяснить это открытие. В наш дифференциальный диагноз были включены атипичные васкулиты, воспалительная амилоидная ангиопатия, осложненный синдром задней обратимой энцефалопатии (PRES) и синдром обратимой церебральной вазоконстрикции (RCVS) или ИВЛ (таблица 2). Поскольку повышенный уровень ЛДГ в атипичном случае без инфекции может указывать на ИВЛ, мы измерили ЛДГ и обнаружили, что ее уровень повышен до 450 Ед / л (Таблица 1). ПЭТ головного мозга
ПЭТ головного мозга Эти клетки были плеоморфными, гиперхроматными, с выраженными ядрышками и редкими митозами (рис. 4 (а)). Они не попали в окружающий нейропиль. Иммуногистохимия показала, что эти злокачественные клетки диффузно положительны в отношении CD20, маркера В-клеток (рис. 4 (b)). Опухолевые клетки также широко помечены для Mindbomb E3 Ubiquitin Protein Ligase 1 (MIB-1), маркера пролиферации.На основании этих данных пациенту был поставлен диагноз ИВЛ. Пациенту срочно была начата химиотерапия ритуксимабом, циклофосфамидом, доксорубицином, винкристином и преднизоном (R-CHOP) вместе с декомпрессивной трепанацией черепа, что привело к обращению комы и освобождению от аппарата ИВЛ через несколько дней. Затем она получила метотрексат, который остановил прогрессирование ее болезни и позволил ей вернуться домой с модифицированной шкалой Рэнкина 1. Пациентка остается в ремиссии сегодня, четыре года спустя.
Эти клетки были плеоморфными, гиперхроматными, с выраженными ядрышками и редкими митозами (рис. 4 (а)). Они не попали в окружающий нейропиль. Иммуногистохимия показала, что эти злокачественные клетки диффузно положительны в отношении CD20, маркера В-клеток (рис. 4 (b)). Опухолевые клетки также широко помечены для Mindbomb E3 Ubiquitin Protein Ligase 1 (MIB-1), маркера пролиферации.На основании этих данных пациенту был поставлен диагноз ИВЛ. Пациенту срочно была начата химиотерапия ритуксимабом, циклофосфамидом, доксорубицином, винкристином и преднизоном (R-CHOP) вместе с декомпрессивной трепанацией черепа, что привело к обращению комы и освобождению от аппарата ИВЛ через несколько дней. Затем она получила метотрексат, который остановил прогрессирование ее болезни и позволил ей вернуться домой с модифицированной шкалой Рэнкина 1. Пациентка остается в ремиссии сегодня, четыре года спустя. Лабораторные инструменты и инструменты визуализации позволяют понять этиологию, но не обладают достаточной чувствительностью и специфичностью. У нашего пациента было необычное проявление множественных расслоений артерий и прогрессирующей ICH. Она прошла обширное обследование по поводу прогрессирующей энцефалопатии, пока ее состояние не впадало в кому, и потребовалась биопсия головного мозга.Патологическое разрастание внутрипросветных лимфоцитов в мелких внутричерепных сосудах объясняет симптомы и результаты визуализации у нашего пациента. Поскольку артериолы, венулы и капилляры застаиваются злокачественными клетками, может возникнуть внутрипаренхиматозное кровоизлияние и инфаркт. Однако образование множественных расслоений крупных артерий в ее клиническом течении остается необъяснимым. Микрососуды являются известным источником интрамуральных гематом при расслоении артерий и внутрибляшечных кровоизлияний, связанных с утечкой сосудов или разрывом стенок сонных и позвоночных артерий [12].
Лабораторные инструменты и инструменты визуализации позволяют понять этиологию, но не обладают достаточной чувствительностью и специфичностью. У нашего пациента было необычное проявление множественных расслоений артерий и прогрессирующей ICH. Она прошла обширное обследование по поводу прогрессирующей энцефалопатии, пока ее состояние не впадало в кому, и потребовалась биопсия головного мозга.Патологическое разрастание внутрипросветных лимфоцитов в мелких внутричерепных сосудах объясняет симптомы и результаты визуализации у нашего пациента. Поскольку артериолы, венулы и капилляры застаиваются злокачественными клетками, может возникнуть внутрипаренхиматозное кровоизлияние и инфаркт. Однако образование множественных расслоений крупных артерий в ее клиническом течении остается необъяснимым. Микрососуды являются известным источником интрамуральных гематом при расслоении артерий и внутрибляшечных кровоизлияний, связанных с утечкой сосудов или разрывом стенок сонных и позвоночных артерий [12]. Неясно, способна ли ИВЛ проникать в эти мелкие сосуды (vasa vasorum) в стенке артерии, вызывая разрыв и расслоение интимы и адвентиции артерии.
Неясно, способна ли ИВЛ проникать в эти мелкие сосуды (vasa vasorum) в стенке артерии, вызывая разрыв и расслоение интимы и адвентиции артерии. Наша пациентка вышла из комы и в настоящее время остается в ремиссии четыре года спустя благодаря точному гистопатологическому диагнозу и своевременному лечению, что резко контрастирует с большинством пациентов, которым диагноз ставится посмертно.При оценке прогрессирующего энцефалита неясной этиологии незамедлительная биопсия головного мозга оказалась необходимой для направления лечения. Однако могут быть причины, по которым биопсия головного мозга может быть отложена или неточна из-за опасений относительно процедурного риска или когда образование опухолевой массы практически отсутствует, что может привести к недиагностическим результатам, которые могут существенно отсрочить начало терапии. . Результаты визуализации, такие как диффузные рассеянные очаги гиперинтенсивности Т2 и диффузного ограничения, петехиальные и паренхиматозные кровоизлияния с расслоением артерий или без него, должны вызвать подозрение на это неуловимое заболевание даже при отсутствии обнаруживаемых массовых поражений.
Наша пациентка вышла из комы и в настоящее время остается в ремиссии четыре года спустя благодаря точному гистопатологическому диагнозу и своевременному лечению, что резко контрастирует с большинством пациентов, которым диагноз ставится посмертно.При оценке прогрессирующего энцефалита неясной этиологии незамедлительная биопсия головного мозга оказалась необходимой для направления лечения. Однако могут быть причины, по которым биопсия головного мозга может быть отложена или неточна из-за опасений относительно процедурного риска или когда образование опухолевой массы практически отсутствует, что может привести к недиагностическим результатам, которые могут существенно отсрочить начало терапии. . Результаты визуализации, такие как диффузные рассеянные очаги гиперинтенсивности Т2 и диффузного ограничения, петехиальные и паренхиматозные кровоизлияния с расслоением артерий или без него, должны вызвать подозрение на это неуловимое заболевание даже при отсутствии обнаруживаемых массовых поражений.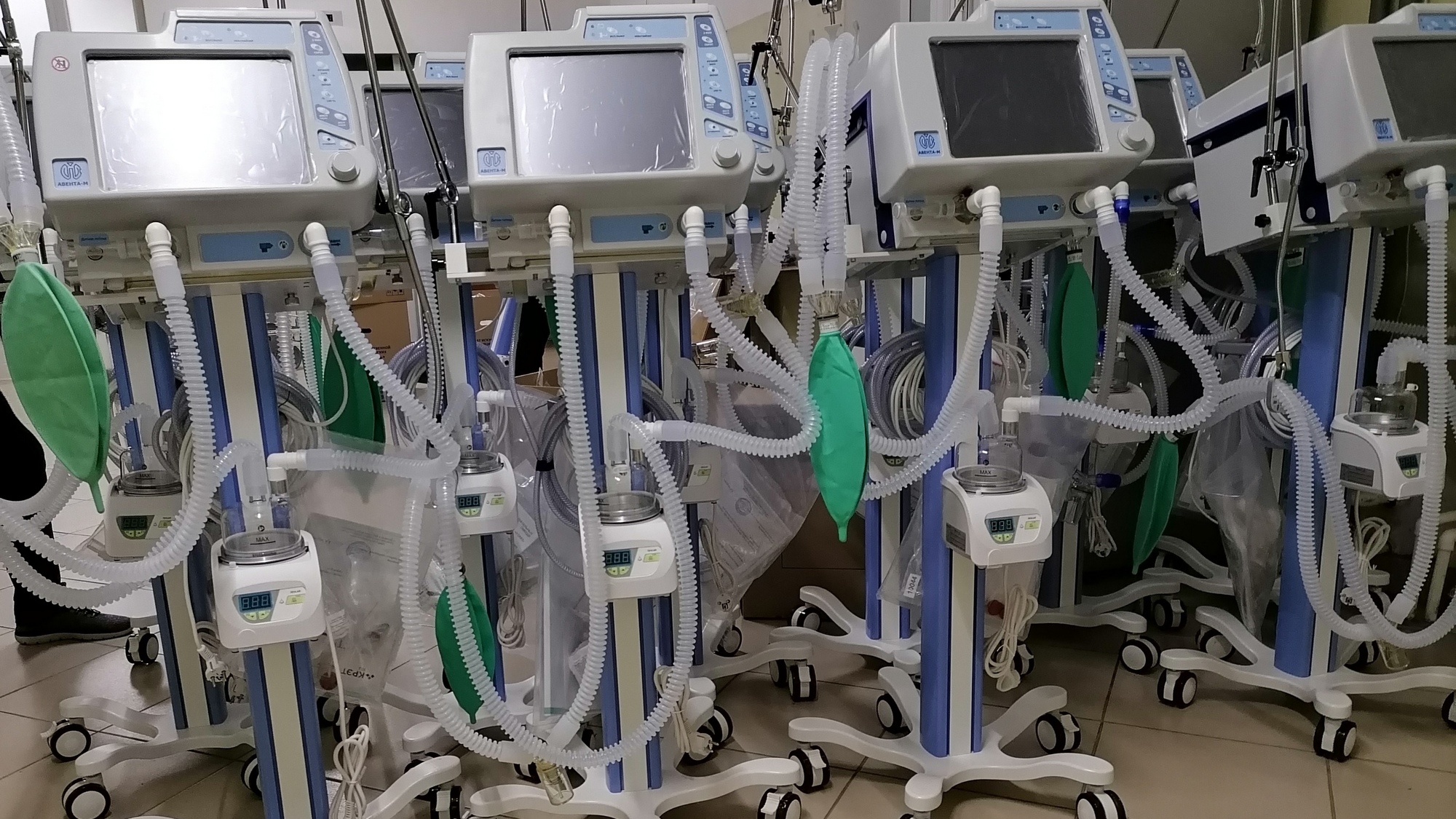 Стратегии ранней клинической диагностики могут позволить начать лечение раньше. Эти стратегии позволяют поставить диагноз путем ассимиляции других важных данных, включая сывороточные опухолевые маркеры, ЛДГ (лактатдегидрогеназа) и растворимый IL2R (рецептор интерлейкина-2), а также случайную биопсию кожи и костного мозга с помощью проточной цитометрии [6, 8, 9, 13 , 14]. В частности, поражение ЦНС лимфомы на момент постановки диагноза предвещает худший прогноз, и считается, что у этих пациентов выше частота рецидивов, особенно в ЦНС [15].Было высказано предположение, что положительные результаты биопсии кожи могут быть полезны в случаях без доказанного заболевания ЦНС в качестве фактора риска для последующего рецидива в ЦНС, хотя для подтверждения этого необходимы дальнейшие исследования [15]. Остается потребность в лучшем патофизиологическом понимании этого неуловимого заболевания.
Стратегии ранней клинической диагностики могут позволить начать лечение раньше. Эти стратегии позволяют поставить диагноз путем ассимиляции других важных данных, включая сывороточные опухолевые маркеры, ЛДГ (лактатдегидрогеназа) и растворимый IL2R (рецептор интерлейкина-2), а также случайную биопсию кожи и костного мозга с помощью проточной цитометрии [6, 8, 9, 13 , 14]. В частности, поражение ЦНС лимфомы на момент постановки диагноза предвещает худший прогноз, и считается, что у этих пациентов выше частота рецидивов, особенно в ЦНС [15].Было высказано предположение, что положительные результаты биопсии кожи могут быть полезны в случаях без доказанного заболевания ЦНС в качестве фактора риска для последующего рецидива в ЦНС, хотя для подтверждения этого необходимы дальнейшие исследования [15]. Остается потребность в лучшем патофизиологическом понимании этого неуловимого заболевания. ДокторMcNally поддерживается грантом развития ученых Американской кардиологической ассоциации 17SDG33460420 и NIH NHLBI 1R01 HL127582-01A1.
ДокторMcNally поддерживается грантом развития ученых Американской кардиологической ассоциации 17SDG33460420 и NIH NHLBI 1R01 HL127582-01A1.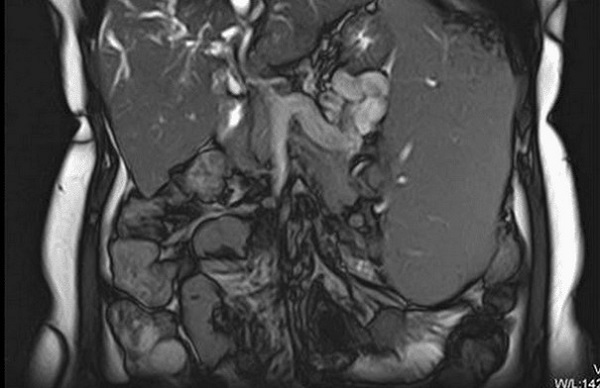 Диагностика внутрисосудистого лимфоматоза производилась с помощью обнаружения и биопсии двусторонней опухоли надпочечника.
Диагностика внутрисосудистого лимфоматоза производилась с помощью обнаружения и биопсии двусторонней опухоли надпочечника. Считалось, что пролиферирующие клетки имеют эндотелиальное происхождение, но иммуногистохимические исследования показали, что злокачественные клетки несут иммунофенотип B- или T-клеточного происхождения. 2 , 3 Внутрисосудистый лимфоматоз считается редкой экстранодальной неходжкинской лимфомой высокой степени злокачественности с тропизмом к эндотелию. Сродство опухолевых клеток к эндотелию капилляров можно объяснить рецепторами лимфоцитов к антигенам эндотелиальных мембран. 2 , 4 Заболевание начинается в широком возрастном диапазоне, с предрасположенностью к пациентам седьмого десятилетия жизни.Четкой половой разницы нет. Гистологическая характеристика — разрастание крупных атипичных лимфоидных клеток в просвете капилляров, мелких вен и артерий. 3 Разрастание кровеносных сосудов паренхиматозных органов приводит к тромбозам и вторичным гипоксическим повреждениям. Нервная система и кожа часто поражаются. Также часто наблюдается инфильтрация легких, почек, надпочечников или простаты.
Считалось, что пролиферирующие клетки имеют эндотелиальное происхождение, но иммуногистохимические исследования показали, что злокачественные клетки несут иммунофенотип B- или T-клеточного происхождения. 2 , 3 Внутрисосудистый лимфоматоз считается редкой экстранодальной неходжкинской лимфомой высокой степени злокачественности с тропизмом к эндотелию. Сродство опухолевых клеток к эндотелию капилляров можно объяснить рецепторами лимфоцитов к антигенам эндотелиальных мембран. 2 , 4 Заболевание начинается в широком возрастном диапазоне, с предрасположенностью к пациентам седьмого десятилетия жизни.Четкой половой разницы нет. Гистологическая характеристика — разрастание крупных атипичных лимфоидных клеток в просвете капилляров, мелких вен и артерий. 3 Разрастание кровеносных сосудов паренхиматозных органов приводит к тромбозам и вторичным гипоксическим повреждениям. Нервная система и кожа часто поражаются. Также часто наблюдается инфильтрация легких, почек, надпочечников или простаты.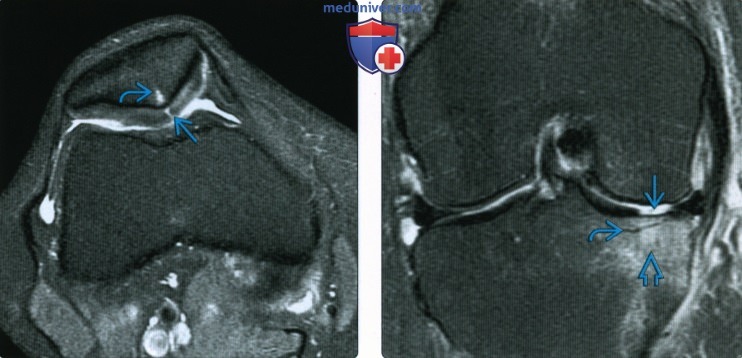 Могут быть вовлечены все органы по отдельности или в комбинации, но печень, селезенка, лимфатические узлы и костный мозг относительно сохранены до поздних стадий заболевания.Обычно циркулирующие клетки лимфомы отсутствуют в крови или спинномозговой жидкости (ЦСЖ). Около двух третей пациентов имеют неврологические признаки, из которых наиболее часто сообщалось о диффузных церебральных признаках, деменции или очаговых церебральных признаках. 5 Некоторые пациенты обращаются к неврологу с миелопатией, периферической невропатией, полирадикулопатией или миопатией. 6 Большинство случаев было диагностировано только при вскрытии из-за вводящих в заблуждение клинических признаков, имитирующих дегенеративную деменцию, васкулит, инсульт, инфекцию или другие новообразования.Диагноз можно установить с помощью биопсии пораженного органа (ов). Применяются различные методы лечения, включая химиотерапию, стероидную и лучевую терапию. Время выживания у большинства пациентов составляет менее 1 года.
Могут быть вовлечены все органы по отдельности или в комбинации, но печень, селезенка, лимфатические узлы и костный мозг относительно сохранены до поздних стадий заболевания.Обычно циркулирующие клетки лимфомы отсутствуют в крови или спинномозговой жидкости (ЦСЖ). Около двух третей пациентов имеют неврологические признаки, из которых наиболее часто сообщалось о диффузных церебральных признаках, деменции или очаговых церебральных признаках. 5 Некоторые пациенты обращаются к неврологу с миелопатией, периферической невропатией, полирадикулопатией или миопатией. 6 Большинство случаев было диагностировано только при вскрытии из-за вводящих в заблуждение клинических признаков, имитирующих дегенеративную деменцию, васкулит, инсульт, инфекцию или другие новообразования.Диагноз можно установить с помощью биопсии пораженного органа (ов). Применяются различные методы лечения, включая химиотерапию, стероидную и лучевую терапию. Время выживания у большинства пациентов составляет менее 1 года.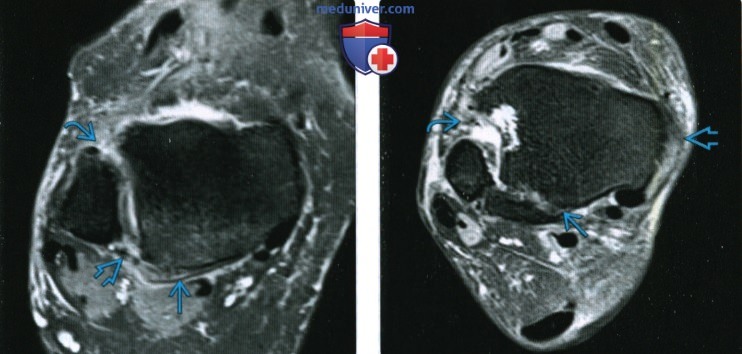 6 Поскольку ИВЛ часто проявляется неврологическими симптомами и потенциально излечима, диагностика этого состояния важна для неврологов.
6 Поскольку ИВЛ часто проявляется неврологическими симптомами и потенциально излечима, диагностика этого состояния важна для неврологов. Черепная компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) не выявила аномалий, тогда как электроэнцефалография (ЭЭГ) показала умеренное или тяжелое генерализованное замедление фоновой активности и фокальной дельта-активности над левой лобно-височной и левой теменной областями. Результаты серологических тестов CSF на вирусы, Treponema, видов и Borrelia burgdorferi , а также тестирование полимеразной цепной реакции на Herpes simplex и Mycobacterium tuberculosis были отрицательными.Ацикловир натрия давали до тех пор, пока не стали известны результаты серологической реакции и полимеразной цепной реакции. Пациент выздоровел через несколько дней. Он отказался от дальнейших диагностических процедур и был выписан на курс противоэпилептического лечения. Первым диагнозом был менингоэнцефалит неустановленного происхождения.
Черепная компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) не выявила аномалий, тогда как электроэнцефалография (ЭЭГ) показала умеренное или тяжелое генерализованное замедление фоновой активности и фокальной дельта-активности над левой лобно-височной и левой теменной областями. Результаты серологических тестов CSF на вирусы, Treponema, видов и Borrelia burgdorferi , а также тестирование полимеразной цепной реакции на Herpes simplex и Mycobacterium tuberculosis были отрицательными.Ацикловир натрия давали до тех пор, пока не стали известны результаты серологической реакции и полимеразной цепной реакции. Пациент выздоровел через несколько дней. Он отказался от дальнейших диагностических процедур и был выписан на курс противоэпилептического лечения. Первым диагнозом был менингоэнцефалит неустановленного происхождения. Он заказывал неправильные материалы, дважды оплачивал счета и испытывал трудности с чтением рецептов и вождением автомобиля, но со временем симптомы улучшились.Шесть месяцев спустя, 15 октября 1996 г., он был повторно госпитализирован из-за острой дезориентации, трудностей с поиском слов и неспособности закончить предложения. При осмотре температура 38,2 ° C, артериальное давление 140/80 мм рт. Ст., Пульс 76 / мин. Психологические тесты выявили непостоянную дезориентацию в пространстве, времени и окружении, а также уменьшение размаха пальцев. Его поведение было изменено повышенным драйвом, колеблющейся бдительностью, возбуждением и измененной аффективностью (сначала эйфория, затем раздражительность).Его речь была увеличенной и бессвязной. У него были небольшие трудности с именованием, чтением, письмом и расчетами. Кодирование и поиск списка слов были существенно сокращены. Он показал лишь минимальные отклонения при копировании сложной геометрической фигуры. Психические изменения соответствовали делирию в соответствии с критериями Диагностического и статистического руководства по психическим расстройствам , четвертое издание .
Он заказывал неправильные материалы, дважды оплачивал счета и испытывал трудности с чтением рецептов и вождением автомобиля, но со временем симптомы улучшились.Шесть месяцев спустя, 15 октября 1996 г., он был повторно госпитализирован из-за острой дезориентации, трудностей с поиском слов и неспособности закончить предложения. При осмотре температура 38,2 ° C, артериальное давление 140/80 мм рт. Ст., Пульс 76 / мин. Психологические тесты выявили непостоянную дезориентацию в пространстве, времени и окружении, а также уменьшение размаха пальцев. Его поведение было изменено повышенным драйвом, колеблющейся бдительностью, возбуждением и измененной аффективностью (сначала эйфория, затем раздражительность).Его речь была увеличенной и бессвязной. У него были небольшие трудности с именованием, чтением, письмом и расчетами. Кодирование и поиск списка слов были существенно сокращены. Он показал лишь минимальные отклонения при копировании сложной геометрической фигуры. Психические изменения соответствовали делирию в соответствии с критериями Диагностического и статистического руководства по психическим расстройствам , четвертое издание . 7 При плановых лабораторных исследованиях выявлена анемия (уровень гемоглобина 11.4 г / л), повышенный уровень С-реактивного белка (0,183 г / л) и повышенная скорость оседания (66 мм / ч). ЦСЖ содержала высокий уровень белка (2,7 г / л), но количество клеток было в пределах нормы, и результаты цитологических исследований были нормальными. Моноклонального белка или недостаточности надпочечников обнаружено не было. Анти-Hu, анти-Yo или специфические антинейрональные антитела не присутствовали. Результаты ЭЭГ были аналогичны тем, что были зарегистрированы 6 месяцев назад, показывая умеренную или тяжелую медленноволновую аномалию в обоих полушариях и постоянную дельта-активность в левой лобно-височной и левой теменной областях.МРТ черепа показала небольшую гиперинтенсивную область в левом заднем чечевицеобразном ядре (рис. 1) с минимальным усилением контраста. Не было усиления контраста мозговых оболочек и инфаркта коры. Дифференциальный диагноз клинического синдрома включал паранеопластический (лимбический) энцефалит.
7 При плановых лабораторных исследованиях выявлена анемия (уровень гемоглобина 11.4 г / л), повышенный уровень С-реактивного белка (0,183 г / л) и повышенная скорость оседания (66 мм / ч). ЦСЖ содержала высокий уровень белка (2,7 г / л), но количество клеток было в пределах нормы, и результаты цитологических исследований были нормальными. Моноклонального белка или недостаточности надпочечников обнаружено не было. Анти-Hu, анти-Yo или специфические антинейрональные антитела не присутствовали. Результаты ЭЭГ были аналогичны тем, что были зарегистрированы 6 месяцев назад, показывая умеренную или тяжелую медленноволновую аномалию в обоих полушариях и постоянную дельта-активность в левой лобно-височной и левой теменной областях.МРТ черепа показала небольшую гиперинтенсивную область в левом заднем чечевицеобразном ядре (рис. 1) с минимальным усилением контраста. Не было усиления контраста мозговых оболочек и инфаркта коры. Дифференциальный диагноз клинического синдрома включал паранеопластический (лимбический) энцефалит. Поэтому была проведена компьютерная томография грудной клетки и брюшной полости. Двусторонние опухолевые образования надпочечников размером 7 × 3 × 3 см с правой стороны и 6 × 5 × 3 см с левой стороны были обнаружены в сочетании с множественными лимфатическими узлами в средостении и забрюшинном пространстве, увеличенными до 2 см (рис. 2). .Биопсия правого надпочечника под контролем КТ была отложена из-за развития сложного парциального эпилептического статуса 23 октября, когда у пациента появились ступор, шлепки по губам и эпилептиформные выделения на левой височной стороне, которые разрешились при лечении фенитоином натрия. . Наконец, результаты биопсии показали, что синусоиды надпочечников заполнены некогезивными агрегатами злокачественных лимфоидных клеток (рис. 3) с сильной реакцией на антитела к CD20, специфичные для В-лимфоцитов. Был поставлен диагноз внутрисосудистой лимфомы с поражением как надпочечников, так и головного мозга, а также лимфатических узлов средостения и забрюшинного пространства.
Поэтому была проведена компьютерная томография грудной клетки и брюшной полости. Двусторонние опухолевые образования надпочечников размером 7 × 3 × 3 см с правой стороны и 6 × 5 × 3 см с левой стороны были обнаружены в сочетании с множественными лимфатическими узлами в средостении и забрюшинном пространстве, увеличенными до 2 см (рис. 2). .Биопсия правого надпочечника под контролем КТ была отложена из-за развития сложного парциального эпилептического статуса 23 октября, когда у пациента появились ступор, шлепки по губам и эпилептиформные выделения на левой височной стороне, которые разрешились при лечении фенитоином натрия. . Наконец, результаты биопсии показали, что синусоиды надпочечников заполнены некогезивными агрегатами злокачественных лимфоидных клеток (рис. 3) с сильной реакцией на антитела к CD20, специфичные для В-лимфоцитов. Был поставлен диагноз внутрисосудистой лимфомы с поражением как надпочечников, так и головного мозга, а также лимфатических узлов средостения и забрюшинного пространства. Была начата химиотерапия CHOP (состоящая из циклофосфамида, доксорубицина гидрохлорида, винкристина сульфата и преднизона), последний из 8 курсов был проведен в марте 1997 года. Клинические, лабораторные и визуальные данные улучшились вскоре после первого цикла химиотерапии. Помимо легкой сенсорной полинейропатии, после завершения лечения неврологических отклонений не обнаружено. Несмотря на умеренно повышенные уровни лактатдегидрогеназы и β 2 -микроглобулина, считается, что у пациента наблюдается полная ремиссия в течение 34 месяцев после появления первых симптомов или в течение 28 месяцев после начала химиотерапии.
Была начата химиотерапия CHOP (состоящая из циклофосфамида, доксорубицина гидрохлорида, винкристина сульфата и преднизона), последний из 8 курсов был проведен в марте 1997 года. Клинические, лабораторные и визуальные данные улучшились вскоре после первого цикла химиотерапии. Помимо легкой сенсорной полинейропатии, после завершения лечения неврологических отклонений не обнаружено. Несмотря на умеренно повышенные уровни лактатдегидрогеназы и β 2 -микроглобулина, считается, что у пациента наблюдается полная ремиссия в течение 34 месяцев после появления первых симптомов или в течение 28 месяцев после начала химиотерапии. Окончательный диагноз был поставлен при обнаружении двусторонней опухоли надпочечников. Биопсия этого органа представляла собой альтернативу биопсии головного мозга. Нелокализационные результаты нейроповеденческих и ЭЭГ у нашего пациента, вероятно, отражают диффузную инфильтрацию мелких церебральных сосудов, тогда как более очаговые ЭЭГ и ограниченные изменения и изменения МРТ в левом полушарии отражают локальный максимум инфильтративного процесса, ведущего к тромбозу и последующему видимому инфаркту. на МРТ и сложные парциальные припадки.Таким образом, имело место сочетание диффузных (или энцефалопатических) и местных церебральных проявлений. Неясно, было ли улучшение после первоначального проявления в виде менингоэнцефалита результатом спонтанной временной ремиссии лимфомы или восстановления после ишемического события, не видимого на КТ и МРТ. При ИВЛ с неврологическим синдромом исследования спинномозговой жидкости и процедуры визуализации головного мозга обычно дают неспецифические или даже нормальные результаты.
Окончательный диагноз был поставлен при обнаружении двусторонней опухоли надпочечников. Биопсия этого органа представляла собой альтернативу биопсии головного мозга. Нелокализационные результаты нейроповеденческих и ЭЭГ у нашего пациента, вероятно, отражают диффузную инфильтрацию мелких церебральных сосудов, тогда как более очаговые ЭЭГ и ограниченные изменения и изменения МРТ в левом полушарии отражают локальный максимум инфильтративного процесса, ведущего к тромбозу и последующему видимому инфаркту. на МРТ и сложные парциальные припадки.Таким образом, имело место сочетание диффузных (или энцефалопатических) и местных церебральных проявлений. Неясно, было ли улучшение после первоначального проявления в виде менингоэнцефалита результатом спонтанной временной ремиссии лимфомы или восстановления после ишемического события, не видимого на КТ и МРТ. При ИВЛ с неврологическим синдромом исследования спинномозговой жидкости и процедуры визуализации головного мозга обычно дают неспецифические или даже нормальные результаты. Напротив, поиск увеличенных или пораженных инфарктом внутренних органов, как показано в отчете о случае, может иметь важное значение для выявления основного заболевания.Диагноз можно поставить только с помощью биопсии одного из пораженных органов, в основном головного мозга, кожи или легких. 5 Биопсия висцерального органа, когда это имеет смысл, представляет собой альтернативу биопсии головного мозга. Хотя надпочечник был диагностическим органом только у 1 пациента при обследовании 32 пациентов с ИВЛ, 5 он встречается гораздо чаще. В ряде случаев сообщалось о двустороннем увеличении надпочечников, которое может привести к надпочечниковой недостаточности. 4 , 8 -10 Сообщалось, что инфильтрация надпочечников присутствует в 60% случаев вскрытия. 10 Поэтому КТ брюшной полости всегда следует выполнять в клинических условиях, упомянутых выше. Ответ на химиотерапию CHOP у нашего пациента был отличным, что привело к полной ремиссии и бессимптомной выживаемости, которая в настоящее время превышает 32 месяца.
Напротив, поиск увеличенных или пораженных инфарктом внутренних органов, как показано в отчете о случае, может иметь важное значение для выявления основного заболевания.Диагноз можно поставить только с помощью биопсии одного из пораженных органов, в основном головного мозга, кожи или легких. 5 Биопсия висцерального органа, когда это имеет смысл, представляет собой альтернативу биопсии головного мозга. Хотя надпочечник был диагностическим органом только у 1 пациента при обследовании 32 пациентов с ИВЛ, 5 он встречается гораздо чаще. В ряде случаев сообщалось о двустороннем увеличении надпочечников, которое может привести к надпочечниковой недостаточности. 4 , 8 -10 Сообщалось, что инфильтрация надпочечников присутствует в 60% случаев вскрытия. 10 Поэтому КТ брюшной полости всегда следует выполнять в клинических условиях, упомянутых выше. Ответ на химиотерапию CHOP у нашего пациента был отличным, что привело к полной ремиссии и бессимптомной выживаемости, которая в настоящее время превышает 32 месяца. Режимы химиотерапии, направленные на лимфомы средней и высокой степени злокачественности, кажутся наиболее благоприятными. Хотя нет более крупных серий случаев или рандомизированных исследований, природа заболевания (лимфома высокой степени) и, по крайней мере, 1 опрос пациентов в литературе предполагают использование химиотерапии CHOP для пациентов с ИВЛ.Из 23 пациентов, получавших химиотерапию CHOP, 6 (55%) из 11 достигли полной ремиссии. 2 Напротив, ответ на стероидную терапию с лучевой терапией или без нее, вероятно, плохой. Сообщалось о временном, но резком улучшении после плазмафереза у пациента с ИВЛ и антителами к гликопротеинам, ассоциированным с миелином. 11 Спонтанная ремиссия наблюдалась у пациента с рентгенологическими проявлениями церебрального артериита. 12
Режимы химиотерапии, направленные на лимфомы средней и высокой степени злокачественности, кажутся наиболее благоприятными. Хотя нет более крупных серий случаев или рандомизированных исследований, природа заболевания (лимфома высокой степени) и, по крайней мере, 1 опрос пациентов в литературе предполагают использование химиотерапии CHOP для пациентов с ИВЛ.Из 23 пациентов, получавших химиотерапию CHOP, 6 (55%) из 11 достигли полной ремиссии. 2 Напротив, ответ на стероидную терапию с лучевой терапией или без нее, вероятно, плохой. Сообщалось о временном, но резком улучшении после плазмафереза у пациента с ИВЛ и антителами к гликопротеинам, ассоциированным с миелином. 11 Спонтанная ремиссия наблюдалась у пациента с рентгенологическими проявлениями церебрального артериита. 12  Обследования должны включать органы, часто пораженные ИВЛ, такие как почки, надпочечники, печень и легкие. В случае поражения внутренних органов или кожи биопсия пораженного органа может привести к постановке диагноза без биопсии головного мозга. Лечение химиотерапией CHOP, как и при других неходжкинских лимфомах высокой степени, должно быть стандартной терапией.
Обследования должны включать органы, часто пораженные ИВЛ, такие как почки, надпочечники, печень и легкие. В случае поражения внутренних органов или кожи биопсия пораженного органа может привести к постановке диагноза без биопсии головного мозга. Лечение химиотерапией CHOP, как и при других неходжкинских лимфомах высокой степени, должно быть стандартной терапией.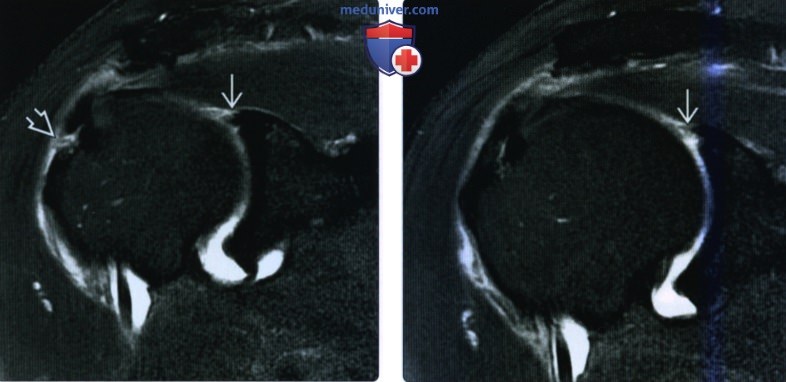 Рак. 1994; 731738-1745Google ScholarCrossref 3. Фитиль
Рак. 1994; 731738-1745Google ScholarCrossref 3. Фитиль
 Harris
Harris и лабораторные данные, убедительно указывающие на диагноз идиопатический поперечный миелит (TM). После того, как лечение кортикостероидами не дало устойчивого улучшения, обследование на потенциальное скрытое интрамедуллярное злокачественное новообразование спинного мозга привело к случайной биопсии кожи, которая показала лежащую в основе ИВЛ, которая, как было показано, имитирует ТМ.
и лабораторные данные, убедительно указывающие на диагноз идиопатический поперечный миелит (TM). После того, как лечение кортикостероидами не дало устойчивого улучшения, обследование на потенциальное скрытое интрамедуллярное злокачественное новообразование спинного мозга привело к случайной биопсии кожи, которая показала лежащую в основе ИВЛ, которая, как было показано, имитирует ТМ.