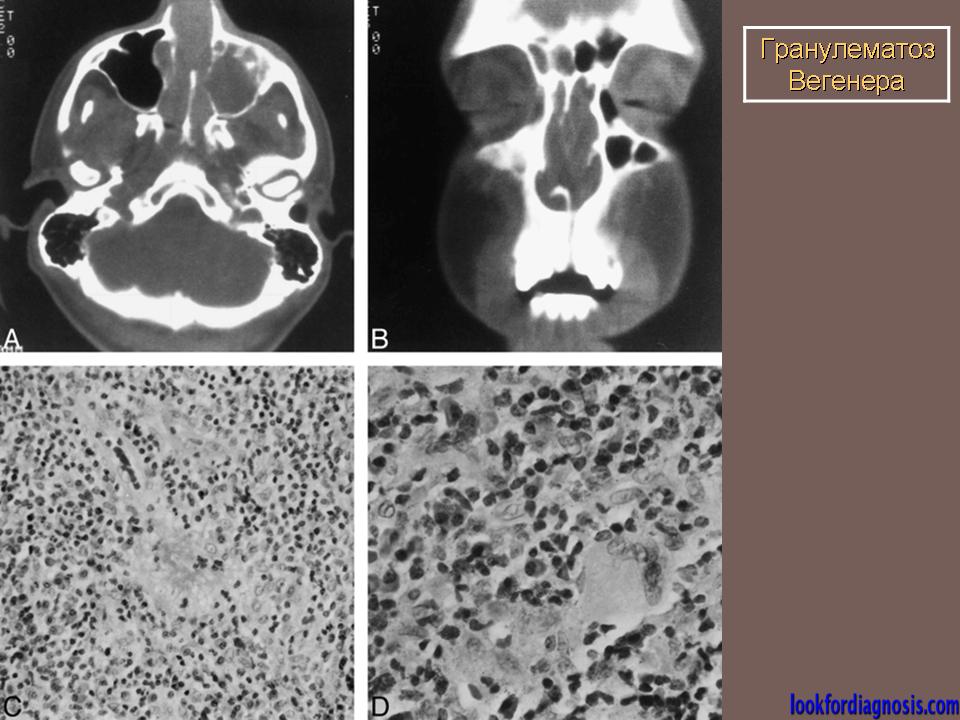
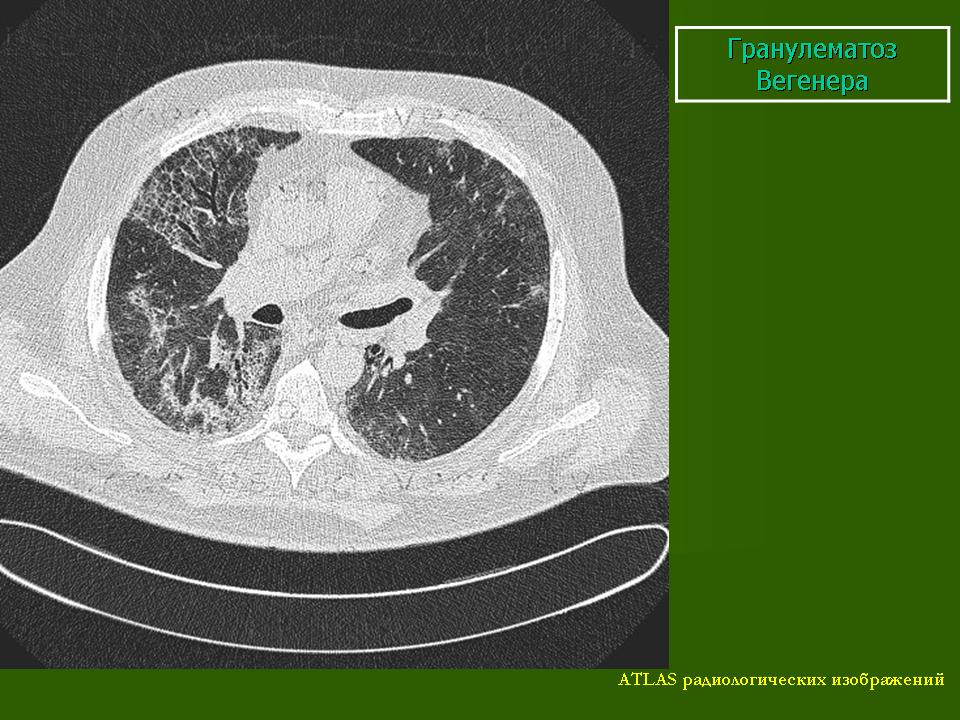
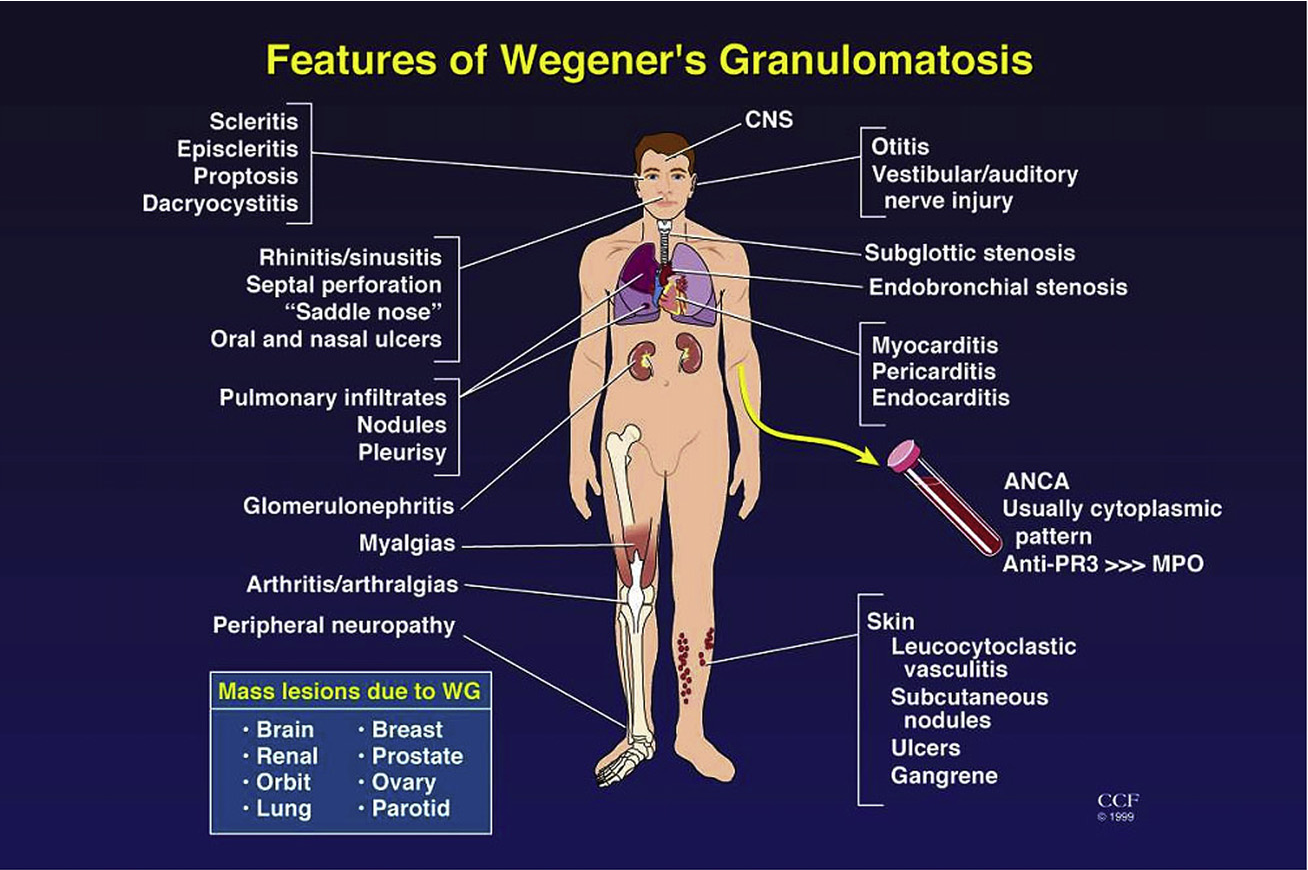
Трудности дифференциальной диагностики абсцедирующей пневмонии и ограниченного варианта гранулематоза Вегенера | Романов
1. Багиров М. А., Токаев Т. К., Зайцева А. С., Токаев К. В., Евдокимов Ю. А., Хоменко В. А. Пневмонэктомия у пациента с осложненным течением гранулематоза Вегенера // Туб. и болезни легких. – 2018. – Т. 96, № 3. – С. 49-54. https://doi.org/10.21292/2075-1230-2018-96-3-49-54.
2. Бекетова Т. В. Европейские (EULAR/ERA-EDTA) рекомендации по диагностике и лечению АНЦА-ассоциированных системных васкулитов-2016 // Научно-практическая ревматология. – 2017. – Т. 55, № 1. – С. 12-16.
3. Гранулематоз Вегенера. Клинические рекомендации МЗ РФ / под ред. А. А. Баранова. – М.: МЗ РФ, 2017. – 73 с.
4. Крутько В. С., Потейко П. И., Ходош Э. М. Гранулематоз Вегенера (распространенность, причина, диагностика, собственные наблюдения) // Новости медицины и фармации. Пульмонология. Аллергология. Антимикробная терапия. – 2015. – № 1 (530). – С. 63-72.
5. Нагноительные заболевания легких. Национальные клинические рекомендации (проект) / под ред. Е. А. Корымасова. http://thoracic.ru/wp-content/uploads/НКР-по-лечению-нагноительных-заболеваний-легких-_ПРОЕКТ_.pdf.
6. Румянцев А. Г. Лечение васкулитов, ассоциированных с антинейтрофильными цитоплазматическими антителами // Вопросы гематологии/онкологии и иммунопатологии в педиатрии. – 2016. – № 2. – С. 6-14. DOI: 10.20953/1726-1708-2016-2-5-13.
7. Greco А., Marinelli C. , Fusconi M. et al. Clinic manifestations in granulomatosis with polyangiitis // Int. J. Immunopathol. Pharmacol. – 2016. – Vol. 29, № 2. – P. 151-159. DOI: 10.1177/0394632015617063.
, Fusconi M. et al. Clinic manifestations in granulomatosis with polyangiitis // Int. J. Immunopathol. Pharmacol. – 2016. – Vol. 29, № 2. – P. 151-159. DOI: 10.1177/0394632015617063.
8. Lutalo, P. M., D’Cruz D. P. Diagnosis and classification of granulomatosis with polyangiitis (aka Wegener’s granulomatosis) // J. Autoimmun. – 2014. – Vol. 48-49. – P. 94-98.
9. Yates M., Watts R. A., Bajema I. M. et al. EULAR/ERA-EDTA recommendations for the management of ANCA-associated vasculitis // Ann. Rheum. Dis. – 2016. – Vol. 75.– P. 1583-1594. doi: 10.1136/annrheumdis-2016-209133 originally published online June 23, 2016.
Лечение гранулематоза Вегенера в Ивано-Франковске
Гранулематоз Вегенера — одна из разновидностей системных васкулитов, редкая патология соединительной ткани, сопровождающееся гранулематозно-некротическими изменениями сосудов. Патология привлекает также органы дыхания, почки, нервная система, органы зрения.
Данная патология может возникнуть в любом возрасте, большинство случаев приходится на 25-55 лет, чаще у мужчин. Гранулематоз Вегенера не является слишком распространенным в мире. В странах Европы частота заболеваемости составляет 5 на 100 000 населения.
ПРИЧИНЫ ПОЯВЛЕНИЯ ГРАНУЛЕМАТОЗА ВЕГЕНЕРА
Причины возникновения гранулематоза Вегенера являются такими же как и при других системных васкулитах. Систематическое проникновение инфекций и вирусов приводят к иммунной дисфункции. Наша иммунная система теряет способность дифференцировать чужеродные клетки от собственных клеток организма. Происходит саморазрушение клеток, тканей, органов. Конечно, не последнюю роль играет наследственная предрасположенность к системным патологий.
ПРИЗНАКИ И СИМПТОМЫ ПАТОЛОГИИ ВЕГЕНЕРА
Классическая картина гранулематоза Вегенера включает следующие симптомы:
- боль в суставах;
- общая слабость, быстрая утомляемость;
- охриплость голоса, кашель;
- симптомы общей интоксикации;
- потеря аппетита;
- головокружение;
- частые носовые кровотечения;
- усиленная потливость ночью;
- онемение рук;
- кровь в моче и др.

Дифференцирующими показателями,которые четко указывают на наличие именно гаранулематоза Вегенера, является поражение верхних дыхательных путей, легких и почек.
Различают 4 стадии развития гранулематоза Вегенера:
- I стадия — риногенный гранулематоз — проявляется стойким поражением верхних дыхательных путей. При этом у пациента диагностируются такие патологии как: гнойно-некротический риносинусит, назофарингит, деформация перегородки носа, ларингит;
- ІІ стадия — легочная — соответственно в процесс патогенеза привлекается некротические-язвенные поражения легких, формируется вторичное воспаление;
- III стадии — генерализованное поражение — непосредственная генерализация патологического процесса, заболевания почек, сосудов, органа зрения и др.;
- ІV стадия — терминальная — развитие дыхательной и почечной недостаточности, что не совместимо с жизнью человека.
Существует также лимитированная форма заболевания, без поражения почек. Однако, такие случаи встречаются в 15-20%. Если в процесс вовлечены почки, тогда сразу же происходят заметные изменения в организме: гематурия (кровь в моче), боли в пояснице, протеинурия (значительное количество белка в моче).
К сожалению, на данный момент летальность вследствие гранулематоза Вегенера является достаточно высокой, что обусловлено поздней диагностикой заболевания и последующим полным разрушением дыхательной системы и почек.
ДИАГНОСТИКА И ЛЕЧЕНИЕ ГРАНУЛЕМАТОЗА ВЕГЕНЕРА
Диагноз «Гранулематоз Вегенера» можно выставить при условии, что замечены 2 из 4 критериев Американского колледжа ревматологов, а именно:
1. Поражение верхних дыхательных путей.
2. Наличие инфильтративных изменений в легких, что доказывает рентгенография органов грудной клетки.
3. Язвы в ротовой полости.
4. Мочевой синдром.
Достоверность диагноза также следует подкрепить лабораторным обследованием: общий анализ крови (с лейкоцитарной формулой), общий анализ мочи, анализ крови на ANCA, биопсия пораженных участков, биохимический анализ крови.
Главной целью лечения гранулематоза Вегенера является достижение полной ремиссии, предупреждения появления осложнений, предотвращение необратимых деструкционных изменений внутренних органов. Проводится активная гормональная иммуносупрессивная терапия (ГКС), лечение циклофосфоамидамы, общеукрепляющая терапия, поддержание нормального функционирования почек.
Помните! Чем быстрее проведена диагностика и начато лечение — тем больший эффект и высокий процент положительных прогнозов! Не теряйте времени — обратитесь к специалистам Оксфорд Медикал, чтобы получить качественную своевременную медицинскую помощь!
Запись по телефону: 777 299
Легочной синдром при гранулематозе с полиангиитом (гранулематозе Вегенера) (лекция)
SOVREMENNAYA PEDIATRIYA.2017.8(88):120-124; doi 10.15574/SP.2017.88.120
Цимбалиста О. Л.
ВГУУ «Ивано-Франковский медицинский университет», Украина
В лекции изложены современные взгляды на факторы риска, патогенез, основные морфологические критерии гранулематоза с полиангиитом (гранулематоза Вегенера). Подробно изложены клиническая манифестация легочного синдрома при данном системном васкулите, основные диагностические критерии и принципы лечения.
Ключевые слова: гранулематоз Вегенера, патология легких, клиника, диагностика, терапия.
Литература
1. Бекетова Т.В. (2012). Грануломатоз с полиангантом, патогенетически связанный с антинейрофильными цитоплазматическими антителами: особенности клинического течения. Научно-практическая ревматология. 50; 6: 19—28. https://doi.org/10.14412/1995-4484-2012-1288
2. Бекетова Т.В. (2014). Современная классификация системных васкулитов. Терапевтический архив. 86; 5: 94—98.
3. Беловол А.Н. Князькова И.И., Шаповалова А.В. (2012). Гранулематоз Вегенера / Гранулематоз с полиангитом. Практическая антология. 1/2: 16—21.
Практическая антология. 1/2: 16—21.
4. Болезни органов дыхания. (2000). Под ред. Н.Р. Палеева. Москва: Медицина: 728.
5. Охотнікова О.М., Поночеєва О.В., Мелліна К.В., Кваченюк О.Г. 2017. Ендотеліальна дисфункція як фактор розвитку, тяжкого перебігу і прогнозу системних васкулітів у дітей. Клінічна імунологія Алергологія Інсектологія. 2: 46—52.
6. Зербіно Д.Д., Зімба О.О. (2013). Грануломатоз Вегенера: ускладнення та причини смерті. Український медичний часопис. 5: 127—130.
7. Штаатц Г., Хоннеф Д., Пирот В., Радков Т. (2010). Лучевая диагностика. Детские болезни. Москва: МЕДпресс-информ.: 400.
8. Насонов Е.Л., Баранов А.А. (1998). Современное представление об этиологии и патогенезе системных васкулитов: роль инфекции и генетической предрасположенности. Часть І. Клиническая медицина. 7: 5—10.
9. Овсяников Д.Ю., Ильницкая А.С., Ахоледиани С.Д. (2015). Легочно-почечный синдром у детей: клинические наблюдения гранулематоза с полианшитом (Венегера) и синдром Гудпасчера. Педиатрия. Журнал им. Г.Н. Сперанского. 94; 4: 43—57.
10. Очерки клинической пульмонологии. (2016). Под ред. В.К. Гаврисюка. Київ: 336.
11. Семенкова Е.Н., Кривошеев О.Г., Новиков П.И., Осипенко В.И. (2001). Поражение легких при гранулематозе Вегенера. Клиническая медицина. 1: 10—13.
12. Пульмонология. Национальное руководство. (2009). Под ред. А.Г. Чучалина. Москва: ГЭОТАР-Медиа: 960.
13. Рациональная диагностика и фармакотерапия заболеваний органов дыхания. (2008). Под ред. Ю.И. Фещенко, Л.Я. Яшиной. Киев: Здоровье: 265.
14. Ревматология. Национальное руководство. (2008). Под ред. Е.Л. Насонова, В.А. Насоновой. Москва: ГЭОТАР-Медиа: 720.
15. Ревматология. Клинические рекомендации. (2011). Под ред. Е.Л. Насонова. Москва: ГЭОТАР-Медиа: 752.
16. Руководство по детской ревматологии. (2011). Под ред. Н.А. Геппе, Н.С. Подчерняевой, Г.А. Лыскиной. Москва: ГЭОТАР-Медиа: 720.
17. Справочник по пульмонологии. (2009). Под ред. Чучалина, М.М. Ильковича. Москва: ГЭОТАР-Медиа: 928.
Справочник по пульмонологии. (2009). Под ред. Чучалина, М.М. Ильковича. Москва: ГЭОТАР-Медиа: 928.
18. Хронические заболевания легких у детей. (2011). Под ред. Н.Н. Розиновой, Ю.Л. Мизерницкого. Москва: Практика: 224с.
19. Polychronopeulos VS, Prakas UBS, Goblin JM et al. (2005). Airway involvement in Wegener’s granulomatosis. Rheumatic Disease Clinics of North America. 33: 755-775. https://doi.org/10.1016/j.rdc.2007.09.004; PMid:18037115
20. Bouros D, Pneumatikos I, Tzouvelekis A. (2008). Pleural involvement in systemic autoimmune disorders. Respiration. 75: 361-371. https://doi.org/10.1159/000119051; PMid:18477860
21. Hansell DM. (2002). Small-vessel diseases of the lung: CT-pathologic correlates. Radiology. 225: 639-653. https://doi.org/10.1148/radiol.2253011490; PMid:12461242
22. Harper SL. (2001). Wegener’s granulomatosis: the relationship between ocular and systemic disease. Rheumatology. 28: 1025-1026.
23. Lane SE, Waffs R, Scoft DG. (2005). Epidemiology of systemic vasculitis. Current Rheumatology Reports. 7: 270-275. https://doi.org/10.1007/s11926-005-0036-5; PMid:16045829
24. Martinez DPM, Sivasothy P. (2009). Vasculitis of the upper and lower airway. Best Practice & Research Clinical Rheumatology. 23: 403-417. https://doi.org/10.1016/j.berh.2009.02.003; PMid:19508947
25. Pesсi A, Manganelli P. (2007). Respiratory system involvement in antineutrophil cytoplasmic-associated systemic vasculitides. Clinical, patholological, radiological and therapeutic considerations. Rheumatology. 8: 25-42. https://doi.org/10.1093/rheumatology/kei217; PMid:16418204
26. Phillip R, Lugman R. (2008). Mortality in systemic vasculitis. Clinical and Experimental Rheumatology. 26: 94-104.
27. Thickett DR, Richter AG, Nathani N et al. (2006). Pulmonary manifestations of anti-neutrophil cytoplasmic antibody (ANCA) — positive vasculitis. Rheumatology. 45: 261-268.
28. Lohrmann C, Uhl ML, Kotter E et al. (2005). Pulmonary manifestations of Wegener granulomatosis: CT findings in 57 patients and a review of the literature. European Journal of Radiology. 53: 471-477. https://doi.org/10.1016/j.ejrad.2004.04.016; PMid:15741022
(2005). Pulmonary manifestations of Wegener granulomatosis: CT findings in 57 patients and a review of the literature. European Journal of Radiology. 53: 471-477. https://doi.org/10.1016/j.ejrad.2004.04.016; PMid:15741022
29. Manganelli P, Fietta P, Garotti M et al. (2006). Respiratory system involvement is systemic vasculitides. Clinical and Experimental Rheumatology. 24(41): 48-59.
30. Savige J. (2000). Antineutrophil cytoplasmic antibodies and associated diseases: a review of the clinical and laboratory features. Kidney International. 57: 846-862. https://doi.org/10.1046/j.1523-1755.2000.057003846.x; PMid:10720938
31. Lee KS, Kirn TS, Fujimoto K et al. (2003). Thoracic manifestation of Wegener’s granulomatosis: CT findings in 30 patients. European Radiology. 13: 43-51. PMid:12541109
32. Frankel SK, Cosgrove GP, Fischer A et al. (2006). Update in the diagnosis and management of pulmonary vasculitis. Chest. 129: 452-465. https://doi.org/10.1378/chest.129.2.452; PMid:16478866
33. Jennette JC. (2013). 2012 revised International Chapel Hill Consensus Conference Nomenclature of Vasculitides. Arthritis & Rheumatology. 65(1): 1-11. https://doi.org/10.1002/art.37715; PMid:23045170
Гранулематоз Вегенера у больного 16 лет | Черняев
1. Баранов А.А. Легочные васкулиты. В кн.: Чучалин А.Г. (ред.). Респираторная медицина. Руководство. М.: ГЭОТАР-Медиа; 2007; т. 2: 108–132.
2. Lie J.T. Wegener’s granulomatosis: histological documentation of common and uncommon manifestations in 216 patients. Vasa 1997; 26 (4): 261–270.
3. Wegener F. On generalized septic vessel diseases. Translation of classic paper. Thorax 1937; 42: 918–919.
4. Liebow A.A. The J.Burns Amberson lecture: pulmonary angiitis and granulomatosis. Am. Rev. Respir. Dis. 1973; 1089: 1–17.
Liebow A.A. The J.Burns Amberson lecture: pulmonary angiitis and granulomatosis. Am. Rev. Respir. Dis. 1973; 1089: 1–17.
5. Tauber E., Wojnarowski C., Horcher E. et al. Necrotizing sarcoid granulomatosis in a 14-year-old female. Eur. Respir. J. 1999; 13: 703–705.
6. de Lange T.E., Simsek S., Kramer M.H., Nanayakkra P.W. A case of cocaine-induced panhypopituitarism with human neutrophil elastase-specific anti- neutrophil cytoplasmic antibodies. Eur. J. Endocrinol. 2009; 160 (3): 499–502.
7. Hewins P., Tervaert J.W., Savage C.O., Kallenberg C.G. Is Wegener’s granulomatosis an autoimmune disease? Curr. Opin. Rheumatol. 2000; 12 (1): 3–10.
8. Yi E.S., Colby T.V. Wegener’s granulomatosis. Semin. Diagn. Pathol. 2001; 18 (1): 34–46.
9. Lamprecht P., Gross W.L. Wegener’s granulomatosis. Herz 2004; 29 (1): 47–56.
10. Jose R.J., Dilworth J.P., Cleverley J. et al. Wegener’s granulomatosis with multiple pulmonary nodules – diagnostic difficulties. J. Roy. Soc. Med. Sh. Rep. 2010; 1: 34–36.
11. Martinez F., Chung J.H., Digumarthy S.R. et al. Common and uncommon manifestations of Wegener granulomatosis at chest CT: radiolodic-pathologic correlation. Radiographics 2012; 32 (1): 51–69.
12. Труфанов Г.Е., Митусова Г.М. Лучевая диагностика заболеваний и повреждений органов грудной полости. В кн.: Труфанов Г.Е., Митусова Г.М. (ред.). Атлас рентгено-компьютерно-томографических изображений: Руководство для врачей. СПб.: ЭЛБИ-СПб.; 2008. 197–256.
СПб.: ЭЛБИ-СПб.; 2008. 197–256.
13. James D.G., Sharma O.M. Respiratory diseases. Rev. Med. Postgrad. Med. J. 1990; 66: 1–15.
14. Wilk A. Clinical and pathophyological significance of antineutrophill cytoplasmic autoantibodies in vasculitis syndromes. Med. Rheumatol. 2009; 19: 590–599.
15. Joerg L., Kerstin A., Niko B. et al. A typical Wegener’s granulomatosis – but not pauci-immune! Minerva Urol. Nefrol. 2012; 64 (2): 149–152.
16. Takala J.H., Kautiainen H., Leirisalo+Repo M. Survival of patients with Wegener’s granulomatosis diagnosed in Finland in 1981–2000. Scand. J. Rheumatol. 2010; 39 (1): 71–76.
17. Hoffman G.S., Kerr G.S., Leavitt K.Wegener’s granulomatosis an analysis of 158 patients. Ann. Intern. Med. 1992; 116: 488–498.
18. Кhan A.M., Elahi F., Hashmi S.R. et al. Wegener’s granulomatosis: a rare, chronic and multisystem disease. Surgeon 2006; 4 (1): 45–52.
19. Battikh R., M’sadek F., Ben Abdelhafidh N. et al. Pneumocystis pneumonia in non HIV patients. Med. Mal. Infect. 2007; 37 (9): 605–608.
20. Lowry L., Cairns T., Thom M., Bain B.J. Case 38: central nervous system lymphoma in a patient previously treated for Wegener’s granulomatosis. Leukemia and Lymphoma 2008; 49 (8): 1610–1611.
запись к врачу — ДокДок СПб
Лоры (отоларингологи) Санкт-Петербурга — последние отзывы
Мария Юрьевна очень хороший доктор и миля женщина. Она мне всё объяснила, показала, проверила и дала рекомендации.
Она мне всё объяснила, показала, проверила и дала рекомендации.
Дильшотбек,
24 февраля 2021
Женщина толковая. Она провела осмотр и взяла анализы.
На модерации,
07 апреля 2021
Доктор выписал лекарства, которые помогли. Мы остались довольны!
Кирилл,
03 апреля 2021
Очень грамотный, хороший и приветливый доктор. Он меня внимательно осмотрел.
Валентин,
02 апреля 2021
Врач быстро нашёл подход к ребенку. Он мне все грамотно и подробно объяснил.
Он мне все грамотно и подробно объяснил.
Анастасия,
02 апреля 2021
Врач хорошо общается с детьми. Она сразу нашла к ребенку подход и назначила лечение, после которого уже есть улучшение.
Елена,
02 апреля 2021
Хороший специалист. Прием длился очень мало времени. Специалист очень резко отвечала на мои вопросы. Это выглядело так, что она хотела побыстрее от меня избавиться. Она посмотрела состояние моих связок. В целом, я получила то, зачем пришла. Я уже не первый раз обращаюсь к врачу.
Людмила,
31 марта 2021
Вежливый доктор. Он посмотрел мои уши, нос и горло, понятно все объяснил и рассказал, что нужно принимать.
Анастасия,
31 марта 2021
Специалист внимательный. Он прописал мне медикаменты и сказал сдать анализы. Я доволен врачом! Спасибо большое!
Максим,
30 марта 2021
Я три раза обращалась в бесплатную поликлинику, и мне не помогли. Доктор доступно мне все объяснила, рассказала и лишнего ничего не прописала. Вежливый врач.
Валерия,
29 марта 2021
Показать 10 отзывов из 2632
Сравнительная оценка методов лучевой диагностики при гранулематозе Вегенера
Сравнительная оценка методов лучевой диагностики
при гранулематозе Вегенера
Крючков И.А, Чехонацкий В.А.
Научный руководитель – к.м.н., доцент Илясова Е.Б.
ГБОУ ВПО Саратовский ГМУ им. В.И. Разумовского Минздрава РФ
Кафедра лучевой диагностики и лучевой терапии
Актуальность. Учитывая трудности диагностики достаточно редкого заболевания — гранулематоза Вегенера (ГВ), актуальным является вопрос об информативности лучевых методов при его выявлении.
Учитывая трудности диагностики достаточно редкого заболевания — гранулематоза Вегенера (ГВ), актуальным является вопрос об информативности лучевых методов при его выявлении.
Цель исследования — сравнение диагностических возможностей рентгенологического исследования (РИ) и компьютерной томографии (КТ) при ГВ.
Материал — морфологически подтвержденный ГВ у 9 пациентов, которые находились на обследовании и лечении в КБ им. С.Р. Миротворцева СГМУ.
Методы исследования: анализ историй болезни, оценка теневой картины РИ и КТ.
Результаты. РИ органов грудной полости у 5 пациентов выявило двухсторонние ограниченные фокусные затемнения, в остальных случаях – односторонние, при КТ двухсторонние инфильтраты выявлены у 8 пациентов. Контуры инфильтратов при РИ у 7 пациентов были четкими, у 2 – нечеткими, при КТ — у всех пациентов четкими. Множественные сухие полости в инфильтратах были выявлении при РИ в 6 случаях, при КТ – у 8 пациентов.
При РГ черепа в подбородочно-носовой проекции, костный отдел перегородки носа был разрушен в 2 случаях, при КТ – в 4, истончение перегородки было у 3 пациентов и «разлохмаченность» контуров – у 2. У всех пациентов при РГ и КТ были признаки двухстороннего гайморита. Разрушение медиальной стенки верхнечелюстной пазухи было выявлено у 4 пациентов при РГ и у 5 – при КТ. Истончение медиальной стенки гайморовой пазухи со снижением интенсивности её рисунка, а также частичное разрушение решётчатого лабиринта, обнаружено только при КТ у 4 пациентов, как и истончение тела клиновидной кости у 3 пациентов.
Выводы. РИ является достаточно информативным при ГВ, однако для уточнения характера и распространенности внутрилегочных и костных изменений, необходима КТ.
Антитела к протеиназе 3 (PR3), IgG
Протеиназа 3 является небольшим белком (29 кДа), локализующимся в азурофильных гранулах нейтрофилов, гранулах моноцитов и цитоплазме эндотелиальных клеток. Это один из основных антигенов антител к цитоплазме нейтрофилов (№№ 970), который в иммунофлюоресцентном тесте индуцирует цитоплазматический тип свечения (цАНЦА, cANCA). Определение антител к протеиназе 3 является высокоспецифичным лабораторным тестом в диагностике гранулематоза с полиангиитом (ранее называемого «гранулематоз Вегенера»), тяжелого заболевания, проявляющегося триадой — гранулематозным поражением верхних дыхательных путей, легких и почек. Часто это заболевание сопровождается полиневритом.
Определение антител к протеиназе 3 является высокоспецифичным лабораторным тестом в диагностике гранулематоза с полиангиитом (ранее называемого «гранулематоз Вегенера»), тяжелого заболевания, проявляющегося триадой — гранулематозным поражением верхних дыхательных путей, легких и почек. Часто это заболевание сопровождается полиневритом.
Высокие титры антител к протеиназе 3 встречаются у 90-95% больных с развернутой картиной активного гранулематозного процесса. Локализованные формы гранулематоза Вегенера, поражающие верхние дыхательные пути, реже сопровождаются образованием аутоантител (50-60%). Редко антитела к протеиназе 3 могут быть обнаружены при других АНЦА-ассоциированных васулитах – микроскопическом полиангиите, синдроме Чарга-Страусс и узелковом полиартериите. Содержание антинейтрофильных антител при гранулематозе Вегенера является клинически значимым и коррелирует с активностью заболевания. Высокий их титр служит основанием для патогенетической иммуносупрессивной терапии.
Для повышения чувствительности серологического обследования пациентов с системными васкулитами действующие международные рекомендации требуют одновременного использования иммунофлюоресцентного теста обнаружения антител к цитоплазме нейтрофилов (см. №№ 970) и выявления антител к основным антигенам АНЦА — протеиназе 3 и антител к миелопероксидазе (см.№ 823).
Предпочтительно выдержать 4 часа после последнего приема пищи, обязательных требований нет.
Интерпретация результатов исследования содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т.д.
Единицы измерения: относительные единицы (отн.ед/мл).
Референсные значения: <20 отн. ед/мл.
ед/мл.
Выявление антител к протеиназе 3 служит одним из основных методов диагностики АНЦА-ассоциированных васкулитов. Отсутствие диагностических титров антител к протеиназе 3 значительно снижает вероятность гранулематоза Вегенера даже при развернутой клинической картине системного васкулита. При лимитированных формах гранулематоза антитела могут отсутствовать более чем у 50% пациентов. В этом случае может быть рекомендовано использовать определение панели антигенов антинейтрофильных антител (см. № 821).
Гранулематоз с полиангиитом (GPA, ранее назывался Wegener’s)
Обзор
Что такое гранулематоз с полиангиитом (GPA, ранее называвшийся синдромом Вегенера)?
Гранулематоз с полиангиитом (GPA, ранее называвшийся болезнью Вегенера) — редкое заболевание неизвестной причины. Это результат воспаления в тканях, называемого гранулематозным воспалением и воспалением кровеносных сосудов («васкулит»), которое может повредить системы органов.Области, наиболее часто поражаемые GPA, включают пазухи, легкие и почки, но может быть поражен любой участок.
Что такое васкулит?
Васкулит — это общий термин, обозначающий воспаление кровеносных сосудов. При воспалении кровеносный сосуд может ослабнуть и растянуться, образуя аневризму, или стать настолько тонким, что разорвется, что приведет к кровотечению в ткани. Васкулит также может вызвать сужение кровеносных сосудов до полного закрытия сосуда.Это может привести к повреждению органов из-за потери кислорода и питательных веществ, поступающих с кровью.
Каковы особенности гранулематоза с полиангиитом (ГПА)?
GPA в первую очередь влияет на верхние дыхательные пути (пазухи, нос, трахею [верхний воздуховод]), легкие и почки. Также может быть поражен любой другой орган в организме.
Симптомы GPA и их тяжесть у разных пациентов различаются. Общие признаки заболевания могут включать:
- Потеря аппетита
- Похудание
- Лихорадка
- Усталость
Большинство пациентов сначала замечают симптомы в дыхательных путях.Симптомы могут включать:
- Постоянный насморк (также называемый ринореей) или образование корок и язв в носу
- Боль в носу или лице
- Носовое кровотечение или необычные выделения из носа, вызванные воспалением носа или пазух
- Кашель, который может включать кровавую мокроту, вызванную воспалением верхних или нижних дыхательных путей (легких)
- Дискомфорт в груди с одышкой или без нее
- Воспаление среднего уха (также называемое средним отитом), боль или потеря слуха
- Изменение голоса, хрипы или одышка, вызванные воспалением трахеи
Другие возможные функции:
- Воспаление глаза и / или давление за глазом, затрудняющее движение глаз, с потерей зрения или без нее
- Боль в суставах (артрит) или боль в мышцах
- Сыпь или кожные язвы
- Воспаление почек (хотя воспаление почек является обычным явлением, обычно оно не связано с такими симптомами, как боль).
Кто страдает гранулематозом с полиангиитом (ГПА)?
GPA может быть у людей любого возраста. Пиковая возрастная группа заболевания — от 40 до 60 лет. Похоже, это одинаково влияет на мужчин и женщин.
Симптомы и причины
Что вызывает гранулематоз при полиангиите (ГПА)?
Причина GPA неизвестна.GPA не является формой рака, не заразен и обычно не возникает в семьях. Данные исследовательских лабораторий убедительно подтверждают идею о том, что иммунная система играет решающую роль в GPA, так что иммунная система вызывает воспаление и повреждение кровеносных сосудов и тканей.
Диагностика и тесты
Как диагностируется гранулематоз с полиангиитом (ГПА)?
GPA имеет симптомы, схожие с рядом других расстройств, что может затруднить диагностику.Однако для наиболее эффективного и успешного лечения критически важна ранняя диагностика.
При подозрении на диагноз ГПД часто выполняется биопсия (образец ткани) пораженного участка, чтобы попытаться подтвердить наличие васкулита. Биопсия рекомендуется только для тех участков органов, в которых обнаружены отклонения от нормы при осмотре, лабораторных исследованиях или визуализации.
Это сочетание симптомов, результатов медицинского осмотра, лабораторных тестов, рентгеновских лучей, а иногда и биопсии (образца) пораженной ткани (кожи, носовых оболочек, пазух, легких, почек или других участков), которые вместе подтверждают диагноз. GPA.После лечения эти факторы также имеют решающее значение при оценке активности заболевания или ремиссии.
Положительный анализ крови на антинейтрофильные цитоплазматические антитела (ANCA) может подтвердить предполагаемый диагноз заболевания. Однако этот анализ крови сам по себе не подтверждает диагноз ГПД и не определяет активность заболевания.
GPA часто поражает легкие. У пациентов с ГПД, у которых нет легочных симптомов (кашель или одышка), визуализирующие тесты (обычные рентгеновские снимки или компьютерная томография) выявляют аномалии легких примерно в одной трети случаев.Поэтому при подозрении на активный ГПД важно выполнять снимки легких, даже если у вас нет никаких симптомов заболевания легких.
Ведение и лечение
Как лечится гранулематоз с полиангиитом (ГПА)?
Поскольку GPA часто представляет собой опасное для жизни заболевание, его лечат различными мощными лекарствами, которые, как было доказано, спасают жизнь. Лекарства, подавляющие иммунную систему, составляют основу лечения ГПД. Степень тяжести заболевания в каждом отдельном случае определяет, какие иммуносупрессивные препараты используются. Существует множество иммуносупрессивных препаратов, которые используются при GPA, каждое из которых имеет индивидуальные побочные эффекты.
Лекарства, подавляющие иммунную систему, составляют основу лечения ГПД. Степень тяжести заболевания в каждом отдельном случае определяет, какие иммуносупрессивные препараты используются. Существует множество иммуносупрессивных препаратов, которые используются при GPA, каждое из которых имеет индивидуальные побочные эффекты.
Людей с ГПД с поражением критических систем органов обычно лечат кортикостероидами в сочетании с другими иммуносупрессивными препаратами, такими как циклофосфамид (Cytoxan®) или ритуксимаб (Rituxan®).У пациентов с менее тяжелым ГПД вначале можно использовать кортикостероиды и метотрексат. Цель лечения — остановить все травмы, возникающие в результате GPA. Если активность болезни можно полностью «отключить», это называется «ремиссией». Как только становится очевидным, что болезнь улучшается, врачи постепенно снижают дозу кортикостероидов и в конечном итоге надеются полностью отменить ее. Когда используется циклофосфамид, его назначают только до момента ремиссии (обычно от 3 до 6 месяцев), после чего его переключают на другой иммунодепрессант, такой как метотрексат, азатиоприн (Imuran®) или микофенолят мофетил (Cellcept®). ) для поддержания ремиссии.Продолжительность лечения поддерживающими иммуносупрессивными препаратами может варьироваться в зависимости от человека. В большинстве случаев его назначают как минимум в течение 2 лет, прежде чем будет рассмотрен вопрос о медленном снижении дозы до прекращения приема.
Все эти лекарства также используются для лечения других заболеваний. Азатиоприн и микофенолят мофетил используются для предотвращения отторжения трансплантата органов. Метотрексат используется для лечения ревматоидного артрита и псориаза. И циклофосфамид, и метотрексат назначаются в высоких дозах для лечения определенных типов рака и поэтому иногда называются «химиотерапией».«При лечении рака эти лекарства работают, убивая или замедляя рост быстро размножающихся раковых клеток. При васкулите эти лекарства вводятся в дозах, которые от 10 до 100 раз ниже, чем те, которые используются для лечения рака, и их основной эффект заключается в том, чтобы влиять на поведение иммунной системы таким образом, что приводит к иммуносупрессии. Ритуксимаб относится к классу лекарств, называемых биологическими агентами, которые нацелены на определенный элемент иммунной системы. Недавние исследования показали, что ритуксимаб был так же эффективен, как циклофосфамид, для лечения тяжелого активного GPA.
Ритуксимаб относится к классу лекарств, называемых биологическими агентами, которые нацелены на определенный элемент иммунной системы. Недавние исследования показали, что ритуксимаб был так же эффективен, как циклофосфамид, для лечения тяжелого активного GPA.
Какие побочные эффекты связаны с лечением гранулематоза с полиангиитом (ГПА)?
Поскольку эти лекарства подавляют иммунную систему, существует повышенный риск развития серьезных инфекций. Каждый иммунодепрессивный препарат также имеет уникальный набор потенциальных побочных эффектов. Мониторинг побочных эффектов, связанных с каждым лекарством, имеет решающее значение для предотвращения или минимизации их возникновения. Кроме того, тот факт, что пациент может изначально переносить лечение, не гарантирует, что переносимость останется неизменной с течением времени.
Независимо от того, какое лекарство используется, постоянный мониторинг лабораторной работы пациента имеет важное значение при лечении этих заболеваний. Метотрексат, азатиоприн и циклофосфамид могут подавлять способность пациента вырабатывать клетки крови. Если пациент проходит регулярные лабораторные исследования, за которыми тщательно наблюдают, это подавление производства клеток будет обнаружено, и доза лекарства может быть скорректирована или отменена в зависимости от степени тяжести. Циклофосфамид также имеет важные побочные эффекты, такие как снижение фертильности у более молодых пациентов, а также повышенный риск развития рака мочевого пузыря.Использование ритуксимаба в редких случаях связано с повышенным риском инфекции головного мозга, которая может быть опасной для жизни.
Перспективы / Прогноз
Каковы перспективы для людей с гранулематозом и полиангиитом (ГПД)?
После достижения ремиссии возможно повторение GPA (часто называемое «рецидивом»). Рецидивы могут быть похожи на те, которые испытывал пациент во время постановки диагноза, или симптомы могут отличаться. Вероятность серьезного рецидива можно свести к минимуму, если незамедлительно сообщать врачу о любых новых симптомах, регулярно осматривать врача и проводить постоянный мониторинг с помощью лабораторных тестов и визуализации. Подход к лечению рецидивов аналогичен лечению недавно диагностированного заболевания.
Рецидивы могут быть похожи на те, которые испытывал пациент во время постановки диагноза, или симптомы могут отличаться. Вероятность серьезного рецидива можно свести к минимуму, если незамедлительно сообщать врачу о любых новых симптомах, регулярно осматривать врача и проводить постоянный мониторинг с помощью лабораторных тестов и визуализации. Подход к лечению рецидивов аналогичен лечению недавно диагностированного заболевания.
GPA — очень серьезное заболевание, лечение которого сопряжено со значительными рисками. Однако лечение может спасти жизнь, если диагноз поставлен своевременно и начато соответствующее лечение.
До признания эффективной терапии в 1970-х годах половина всех пациентов с этим заболеванием умирала в течение 5 месяцев после постановки диагноза. Сегодня более 80% пролеченных пациентов живы по крайней мере восемь лет спустя. Многие люди со средним баллом успеваемости продемонстрировали долгосрочное выживание, когда многие из них могут вести относительно нормальный образ жизни. Если прошлое является прелюдией к будущему, текущие исследования приведут к дальнейшим открытиям и даже лучшему лечению.
Гранулематоз с полиангиитом (GPA, ранее Гранулематоз Вегенера): основы практики, предыстория, этиология
Фаучи А.С., Хейнс Б.С., Кац П., Вольф С.М.Гранулематоз Вегенера: проспективный клинический и терапевтический опыт с 85 пациентами в течение 21 года. Энн Интерн Мед. . Январь 1983 г. 98 (1): 76-85. [Медлайн].
Manganelli P, Fietta P, Carotti M, Pesci A, Salaffi F. Участие дыхательной системы в системном васкулите. Clin Exp Rheumatol . Март-апрель 2006 г. 24: S48-S59. [Медлайн].
Hoffman GS, Kerr GS, Leavitt RY, et al. Гранулематоз Вегенера: анализ 158 пациентов. Энн Интерн Мед. . 1992 15 марта. 116 (6): 488-98. [Медлайн].
116 (6): 488-98. [Медлайн].
Мухтяр С., Гильевин Л., Сид М.К. и др. Рекомендации EULAR по лечению первичного васкулита малых и средних сосудов. Энн Рум Дис . March 2009. 68: 310-317. [Медлайн].
Джейн Д., Расмуссен Н., Андрасси К. и др. Рандомизированное исследование поддерживающей терапии васкулита, связанного с антинейтрофильными цитоплазматическими антителами. N Engl J Med .Июль 2003. 349 (1): 36-44. [Медлайн].
Metzler C, Miehle N, Manger K и др. Повышенная частота рецидивов при пероральном приеме метотрексата по сравнению с лефлуномидом для поддержания ремиссии при гранулематозе Вегенера. Ревматология (Оксфорд) . Июль 2007. 46 (7): 1087-1091. [Медлайн].
Falk RJ, Gross WL, Guillevin L, et al. Гранулематоз с полиангиитом (болезнь Вегенера): альтернативное название гранулематоза Вегенера. Энн Рум Дис .2011. 70: 704. [Медлайн].
Ливитт Р.Ю., Фаучи А.С., Блох Д.А. и др. Критерии классификации гранулематоза Вегенера, принятые в 1990 г. Американским колледжем ревматологии. Rheum артрита . August 1990. 33 (8): 1101-1107. [Медлайн].
Исследовательская группа по исследованию гранулематоза и этанерцепта Вегенера (WGET). Ограниченный гранулематоз Вегенера по сравнению с тяжелым: исходные данные о пациентах в исследовании гранулематоза Вегенера с этанерцептом. Rheum артрита . Август 2003. 48 (8): 2299-2309. [Медлайн].
Финкельман Дж. Д., Ли А. С., Хаммел А. М. и др. ANCA выявляются почти у всех пациентов с активным тяжелым гранулематозом Вегенера. Am J Med . Июль 2007. 120: 643.e9-14. [Медлайн].
[Медлайн].
Boomsma MM, Stegeman CA, van der Leij MJ, et al. Прогнозирование рецидивов гранулематоза Вегенера путем измерения уровней антинейтрофильных цитоплазматических антител: проспективное исследование. Rheum артрита . Сентябрь 2000. 43 (9): 2025-33. [Медлайн].
Финкельман Дж. Д., Меркель П. А., Шредер Д. и др. Антинейтрофильные цитоплазматические антитела к антипротеиназе 3 и активность заболевания при гранулематозе Вегенера. Энн Интерн Мед. . Ноябрь 2007. 147 (9): 611-9. [Медлайн].
Исследовательская группа по исследованию гранулематоза и этанерцепта Вегенера (WGET). Этанерцепт плюс стандартная терапия гранулематоза Вегенера. N Engl J Med .2005 27 января. 352 (4): 351-61. [Медлайн].
Schlieben DJ, Korbet SM, Kimura RE, Schwartz MM, Lewis EJ. Легочно-почечный синдром у новорожденного с плацентарной передачей ANCA. Am J Kidney Dis . 2005 апр. 45 (4): 758-61. [Медлайн].
Stegeman CA, Tervaert JW, Sluiter WJ, Manson WL, de Jong PE, Kallenberg CG. Связь хронического носительства Staphylococcus aureus через нос и более высокой частоты рецидивов гранулематоза Вегенера. Энн Интерн Мед. . Январь 1994. 120 (1): 12-17. [Медлайн].
Stone JH, Merkel PA, Spiera R, Seo P, Langford CA, Hoffman GS и др. Ритуксимаб в сравнении с циклофосфамидом при ANCA-ассоциированном васкулите. N Engl J Med . 15 июля 2010 г. 363 (3): 221-32. [Медлайн].
Jones RB, Tervaert JW, Hauser T. и др. Ритуксимаб в сравнении с циклофосфамидом при ANCA-ассоциированном почечном васкулите. N Engl J Med . Июль 2010. 363 (3): 211-20.[Медлайн].
363 (3): 211-20.[Медлайн].
Kallenberg CGM. Патогенез PR3-ANCA-ассоциированного васкулита. J Аутоиммунный . Февраль-март 2008. 30: 29-36. [Медлайн].
Falk RJ, Terrell RS, Charles LA, Jennett C. Антинейтрофильные цитоплазматические аутоантитела заставляют нейтрофилы дегранулировать и продуцировать кислородные радикалы in vitro. Proc Natl Acad Sci USA . June 1990. 87: 4115-4119.
Kallenberg CGM. Патофизиология ANCA-ассоциированного васкулита мелких сосудов. Curr Rheumatol Rep . Декабрь 2010. 12 (6): 399-405. [Медлайн].
Сяо Х., Херинга П., Лю З. и др. Роль нейтрофилов в индукции гломерулонефрита антителами против миелопероксидазы. Ам Дж. Патол . Июль 2005. 167 (1): 39-45. [Медлайн].
Kallenberg CGM, Heeringa P, Stegeman CA. Механизмы заболевания: патогенез и лечение ANCA-ассоциированного васкулита. Нат Клин Практик Ревматол .Декабрь 2006. 2: 661-670. [Медлайн].
Moosig F, Lamprecht P, Gross WL. Гранулематоз Вегенера: современная точка зрения. Clin Rev Allergy Immunol . Октябрь 2008. 35 (1-2): 19-21. [Медлайн].
Spagnolo P, Richeldi L, DuBois RM. Триггеры окружающей среды и факторы восприимчивости при идиопатических гранулематозных заболеваниях. Semin Respir Crit Care Med . Декабрь 2008. 29: 610-619. [Медлайн].
Carr EJ, Niederer HA, Williams J, et al.Подтверждение генетической ассоциации CTLA4 и PTPN22 с ANCA-ассоциированным васкулитом. BMC Med Genet . Декабрь 2009. 10: 121. [Медлайн].
Heckmann M, Holle JU, Arning L, et al. Локус количественного признака гранулематоза Вегенера на хромосоме 6p21.3, что характеризует генотипирование tagSNP. Энн Рум Дис . Июль 2008. 67 (7): 972-9. [Медлайн].
Pendergraft WF 3rd, Preston GA, Shah RR, et al. Аутоиммунитет запускается cPR-3 (105-201), белком, комплементарным аутоантигенной протеиназе-3 человека. Нат Мед . Январь 2004. 10 (1): 72-9. [Медлайн].
Каин Р., Экснер М., Брандес Р. и др. Молекулярная мимикрия при слабоммунном фокально-некротическом гломерулонефрите. Нат Мед .Октябрь 2008. 14 (10): 1088-96. [Медлайн].
Hogan SL, Cooper GS, Savitz DA, et al. Связь воздействия диоксида кремния с антинейтрофильными цитоплазматическими аутоантителами васкулитом мелких сосудов: популяционное исследование случай-контроль. Clin J Am Soc Nephrol . Март 2007. 2 (2): 290-9. [Медлайн].
Watts RA, Lane SE, Koldingsnes W. et al. Эпидемиология васкулитов в Европе. Энн Рум Дис . Декабрь 2001. 60 (12): 1156-7.[Медлайн].
Lane SE, Watts R, Scott DGI. Эпидемиология системных васкулитов. Curr Rheumatol Rep . Август 2005. 7: 270-275. [Медлайн].
Iudici M, Quartier P, Terrier B, Mouthon L, Guillevin L, Puéchal X. Детский гранулематоз с полиангиитом и микроскопическим полиангиитом: систематический обзор и метаанализ. Орфанет Дж. Редкие Дис. . 2016 22 октября. 11 (1): 141. [Медлайн]. [Полный текст].
11 (1): 141. [Медлайн]. [Полный текст].
Мухтяр С, Флоссманн О, Хельмих Б и др.Результаты исследований васкулита, ассоциированного с антинейтрофильными цитоплазматическими антителами: систематический обзор целевой группы Европейской лиги против ревматизма по системному васкулиту. Энн Рум Дис . Июль 2008. 67: 1004-1010. [Медлайн].
Haroun MK, Stone JH, Nair R, Racusen L, Hellmann DB, Eustace JA. Корреляция процента нормальных клубочков с почечным исходом при гранулематозе Вегенера. Ам Дж. Нефрол . Сентябрь-декабрь 2002. 22 (5-6): 497-503.[Медлайн].
Hauer HA, Bajema IM, Van Houwelingen HC, et al. Детерминанты исхода при ANCA-ассоциированном гломерулонефрите: проспективный клинико-гистопатологический анализ 96 пациентов. Почки Инт . Ноябрь 2002. 62 (5): 1732-1742. [Медлайн].
Renaudineau Y, Le Meur Y. Поражение почек при гранулематозе Вегенера. Клиника Рев Аллерг Иммунол . Октябрь 2008. 35: 22-29. [Медлайн].
Walsh M, Merkel PA, Mahr A, Jayne D.Влияние продолжительности терапии глюкокортикоидами на частоту рецидивов при васкулите, ассоциированном с антинейтрофильными цитоплазматическими антителами: метаанализ. Центр по уходу за артритом (Хобокен) . 2010 августа 62 (8): 1166-73. [Медлайн].
Филипп Р., Лукмани Р. Смертность при системном васкулите: систематический обзор. Clin Exp Rheumatol . Сентябрь-октябрь 2008 г. 26: S94-S104. [Медлайн].
Seo P, Min Y-I, Holbrook JT, et al. Повреждения, вызванные гранулематозом Вегенера, и его лечение: проспективные данные исследования гранулематоза Вегенера с этанерцептом (WGET).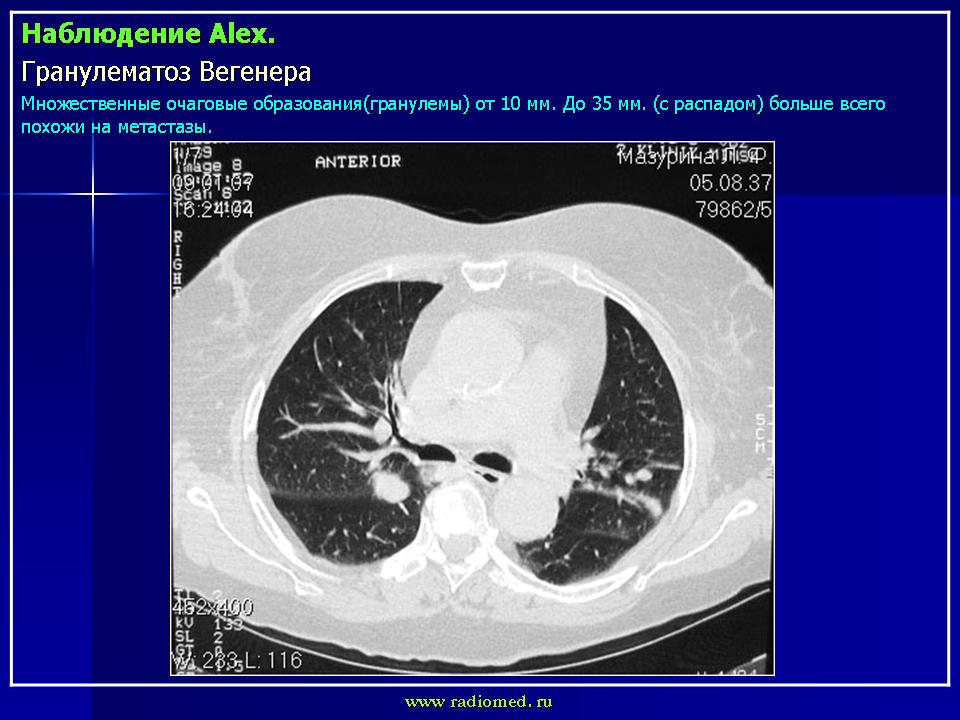 Rheum артрита . July 2005. 52: 2168-2178. [Медлайн].
Rheum артрита . July 2005. 52: 2168-2178. [Медлайн].
Le Guenno G, Mahr A, Pagnoux C, Dhote R, Guillevin L. Частота и предикторы уротоксических побочных эффектов у пациентов с системными некротическими васкулитами, принимающих циклофосфамид. Rheum артрита . 2011 17 февраля [Medline].
Heijl C, Harper L, Flossmann O и др. Заболеваемость злокачественными новообразованиями у пациентов, получавших лечение по поводу васкулита, ассоциированного с антинейтрофильными цитоплазматическими антителами: последующие данные клинических исследований Европейской группы изучения васкулита. Энн Рум Дис . Август 2011. 70 (8): 1415-1421. [Медлайн].
Суппиа Р., судья А., Батра Р. и др. Модель для прогнозирования сердечно-сосудистых событий у пациентов с впервые диагностированным гранулематозом Вегенера и микроскопическим полиангиитом. Центр по уходу за артритом (Хобокен) . 2011 14 января [Medline].
Aviña-Zubieta JA, Mai A., Amiri N, Dehghan N, Ann Tan J, Sayre EC, et al. Риск инфаркта миокарда и инсульта у пациентов с гранулематозом с полиангиитом (Вегенера): популяционное исследование. Ревматический артрит . 2016 ноябрь 68 (11): 2752-2759. [Медлайн].
Литтл М.А., Найтингейл П., Вербург, Калифорния и др. Ранняя смертность при системном васкулите: относительный вклад нежелательных явлений и активного васкулита. Энн Рум Дис . Июнь 2010. 69 (6): 1036-43. [Медлайн].
Wallace ZS, Lu N, Miloslavsky E, Unizony S, Stone JH, Choi HK. Общенациональные тенденции госпитализаций и госпитальной смертности от гранулематоза с полиангиитом. Центр по уходу за артритом (Хобокен) . 2016 г. 7 июля [Medline].
2016 г. 7 июля [Medline].
Holle JU, Gross WL. Неврологические нарушения при гранулематозе Вегенера. Curr Opin Rheumatol . 2011 23 января (1): 7-11. [Медлайн].
Флориан А., Славич М., Блокманс Д., Дымарковский С., Богерт Дж. Поражение сердца при гранулематозе с полиангиитом (гранулематоз Вегенера). Тираж . 2011 27 сентября. 124 (13): e342-4. [Медлайн].
McGeoch L, Carette S, Cuthbertson D, Hoffman GS, Khalidi N, Koening CL, et al.Поражение сердца при гранулематозе с полиангиитом. Дж. Ревматол . 2015 июл.42 (7): 1209-12. [Медлайн].
Hazebroek MR, Kemna MJ, Schalla S, Sanders-van Wijk S, Gerretsen SC, Dennert R, et al. Распространенность и прогностическая значимость поражения сердца при ANCA-ассоциированном васкулите: эозинофильный гранулематоз с полиангиитом и гранулематоз с полиангиитом. Инт Дж. Кардиол . 2015 15 ноября. 199: 170-9. [Медлайн].
Аль-Хаким Д.А., Феделе С., Карлос Р., Портер С.Экстранодальная NK / Т-клеточная лимфома носового типа. Oral Oncol . Январь 2007. 43 (1): 4-14. [Медлайн].
Франкель С.К., Косгроув Г.П., Фишер А. Последние данные по диагностике и лечению легочного васкулита. Сундук . Февраль 2006. 129 (2): 452-65. [Медлайн].
Bossuyt X, Cohen Tervaert JW, Arimura Y, et al. Документ с изложением позиции: Пересмотренный международный консенсус 2017 года по тестированию ANCA при гранулематозе с полиангиитом и микроскопическим полиангиитом. Нат Ревматол . 2017 13 ноября (11): 683-692. [Медлайн].
Rottem M, Fauci AS, Hallahan CW, Kerr GS, Lebovics R, Leavitt RY, et al. Гранулематоз Вегенера у детей и подростков: клиническая картина и исходы. Дж. Педиатр . 1993, январь 122 (1): 26-31. [Медлайн].
Гранулематоз Вегенера у детей и подростков: клиническая картина и исходы. Дж. Педиатр . 1993, январь 122 (1): 26-31. [Медлайн].
Polychronopoulos VS, Prakash UBS, Golbin JM, Edell ES, Specks U. Участие дыхательных путей в гранулематозе Вегенера. Rheum Dis Clin N Am .Ноябрь 2007. 33: 755-775. [Медлайн].
Эрвье Б., Дюран С, Массо А, Понге Т, Хамиду М., Муссини Дж. М.. Использование биопсии мышц для диагностики системных васкулитов. Дж. Ревматол . 2011 Март 38 (3): 470-4. [Медлайн].
Нунокава Т., Йокогава Н., Шимада К., Энацу К., Суги С. Использование мышечной биопсии в диагностике системного васкулита, поражающего сосуды малого и среднего размера: перспективная оценка в Японии. Scand J Rheumatol .2015 8. 1-5 октября. [Медлайн].
DeGroot K, Harper L, Jayne DRW и др. Импульс против ежедневного перорального приема циклофосфамида для индукции ремиссии при васкулите, ассоциированном с антинейтрофильными цитоплазматическими антителами: рандомизированное исследование. Энн Интерн Мед. . Май 2009. 150: 670-680. [Медлайн].
Monach PA, Arnold LM, Merkel PA. Частота и профилактика токсичности циклофосфамида для мочевого пузыря при лечении ревматических заболеваний: обзор, основанный на данных. Rheum артрита . 2010 Январь 62 (1): 9-21. [Медлайн].
Clowse ME, Copland SC, Hsieh TC, Chow SC, Hoffman GS, Merkel PA и др. Резерв яичников снижается пероральной терапией циклофосфамидом при гранулематозе с полиангиитом (Вегенера). Центр по уходу за артритом (Хобокен) . 2011 декабрь 63 (12): 1777-81. [Медлайн].
Specks U, Merkel PA, Seo P, Spiera R, Langford CA, Hoffman GS, et al. Эффективность схем индукции ремиссии при ANCA-ассоциированном васкулите. N Engl J Med . 2013 авг., 1. 369 (5): 417-27. [Медлайн].
Garcia-Valladares I, Espinoza LR. Ритуксимаб превосходит циклофосфамид при ANCA-ассоциированном васкулите по индукции ремиссии и с лучшим профилем безопасности? Curr Rheumatol Rep . Декабрь 2010. 12 (6): 395-8. [Медлайн].
Овен PM, Hellmich B, Voswinkel J, et al. Недостаточная эффективность ритуксимаба при гранулематозе Вегенера с рефрактерными гранулематозными проявлениями. Энн Рум Дис . Июль 2006 г. 65 (7): 853-858. [Медлайн].
Seo P, Specks U, Keogh KA. Эффективность ритуксимаба при ограниченном гранулематозе Вегенера с рефрактерными гранулематозными проявлениями. Дж. Ревматол .Октябрь 2008. 35 (10): 2017-2023. [Медлайн].
Gottenberg JE, Ravaud P, Bardin T, et al. Факторы риска тяжелых инфекций у пациентов с ревматоидным артритом, получавших ритуксимаб в аутоиммунном реестре и регистре ритуксимаба. Rheum артрита . 2010 сентябрь 62 (9): 2625-32. [Медлайн].
Джонс Р. Б., Ферраро А. Дж., Чаудри А. Н. и др. Многоцентровое исследование терапии ритуксимабом рефрактерного антинейтрофильного цитоплазматического васкулита. Rheum артрита . 2009 Июль 60 (7): 2156-68. [Медлайн].
Tesfa D, Ajeganova S, Hägglund H, et al. Поздняя нейтропения после терапии ритуксимабом при ревматических заболеваниях: связь с истощением B-лимфоцитов и инфекциями. Rheum артрита . Август 2011. 63 (8): 2209-2214. [Медлайн].
Поздняя нейтропения после терапии ритуксимабом при ревматических заболеваниях: связь с истощением B-лимфоцитов и инфекциями. Rheum артрита . Август 2011. 63 (8): 2209-2214. [Медлайн].
McGregor JG, Hogan SL, Hu Y, Jennette CE, Falk RJ, Nachman PH. Глюкокортикоиды, частота рецидивов и инфекций при заболевании, связанном с цитоплазматическими антителами нейтрофилов. Clin J Am Soc Nephrol . 2012 Февраль 7 (2): 240-7. [Медлайн]. [Полный текст].
Klemmer PJ, Chalermskulrat W, Reif MS, Hogan SL, Henke DC, Falk RJ. Плазмаферез при диффузном альвеолярном кровотечении у пациентов с васкулитом мелких сосудов. Am J Kidney Dis . Декабрь 2003. 42 (6): 1149-1153. [Медлайн].
Пьюзи CD, Рис AJ, Эванс DJ, Питерс Д.К., Локвуд CM. Плазмообмен при очаговом некротическом гломерулонефрите без антител против GBM. Почки Инт . Октябрь 1991. 40 (4): 757-763. [Медлайн].
Джейн Д. Р., Гаскин Г., Расмуссен Н. и др. Рандомизированное исследование плазмафереза или высоких доз метилпреднизолона в качестве дополнительной терапии тяжелого почечного васкулита. Дж. Ам Соц Нефрол . Июль 2007. 18 (7): 2180-2188. [Медлайн].
Casian A, Jayne D. Плазмообмен в лечении гранулематоза Вегенера, микроскопического полиангиита, синдрома Черга-Стросса и почечно-ограниченного васкулита. Curr Opin Rheumatol . 2011 23 января (1): 12-7. [Медлайн].
DeGroot K, Rasmussen N, Bacon PA, et al. Рандомизированное испытание циклофосфамида по сравнению с метотрексатом для индукции ремиссии при раннем системном васкулите, ассоциированном с цитоплазматическими антителами к антинейтрофилам. Rheum артрита . Август 2005. 52: 2461-2469. [Медлайн].
Август 2005. 52: 2461-2469. [Медлайн].
Rhee EP, Laliberte KA, Niles JL. Ритуксимаб в качестве поддерживающей терапии васкулита, ассоциированного с антинейтрофильными цитоплазматическими антителами. Clin J Am Soc Nephrol . 2010 5 (8): 1394-400. [Медлайн]. [Полный текст].
Sanders JS, Slot MC, Stegeman CA. Поддерживающая терапия васкулита, связанного с антинейтрофильными цитоплазматическими аутоантителами. N Engl J Med . Ноябрь 2003. 349 (21): 2072-2073. [Медлайн].
Slot MC, Tervaert JW, Boomsma MM, Stegeman CA. Положительный титр классических антинейтрофильных цитоплазматических антител (C-ANCA) при переходе на терапию азатиоприном, связанный с рецидивом васкулита, связанного с протеиназой 3. Rheum артрита . April 2004. 51 (2): 269-273. [Медлайн].
Pagnoux C, Mahr A, Hamidou MA, et al. Поддерживающая терапия азатиоприном или метотрексатом при ANCA-ассоциированном васкулите. N Engl J Med . Декабрь 2008. 359: 2790-2803. [Медлайн].
Puéchal X, Pagnoux C, Perrodeau É, Hamidou M, Boffa JJ, et al. Отдаленные результаты исследования WEGENT по поддержанию ремиссии гранулематоза с полиангиитом или микроскопическим полиангиитом. Ревматический артрит . 2015 16 октября [Medline].
Reinhold-Keller E, Fink CO, Herlyn K, Gross WL, De Groot K. Высокая частота рецидивов почек у 71 пациента с гранулематозом Вегенера при поддержании ремиссии низкими дозами метотрексата. Rheum артрита . Июнь 2002. 47 (3): 326-32. [Медлайн].
Langford CA, Talar-Williams C, Barron KS, Sneller MC. Использование циклофосфамидной индукционной схемы поддерживающей терапии метотрексатом для лечения гранулематоза Вегенера: длительное наблюдение и частота рецидивов. Am J Med . April 2003. 114 (6): 463-9. [Медлайн].
Am J Med . April 2003. 114 (6): 463-9. [Медлайн].
Langford CA, Talar-Williams C, Barron KS, Sneller MC. Поэтапный подход к лечению гранулематоза Вегенера: индукция ремиссии глюкокортикоидами и ежедневный переход на метотрексат для поддержания ремиссии. Rheum артрита . Декабрь 1999. 42 (12): 2666-73. [Медлайн].
Снеллер М.С., Хоффман Г.С., Талар-Уильямс К., Керр Г.С., Халлахан К.В., Фаучи А.С.Анализ 42 пациентов с гранулематозом Вегенера, получавших метотрексат и преднизон. Rheum артрита . May 1995. 38 (5): 608-13. [Медлайн].
Guillevin L, et al; Французская группа по изучению васкулита. Сравнение ритуксимаба и азатиоприна при лечении ANCA-ассоциированного васкулита. N Engl J Med . 2014 6 ноября. 371 (19): 1771-80. [Медлайн]. [Полный текст].
Terrier B, et al; Французская группа по изучению васкулита. Долгосрочная эффективность поддерживающих режимов ремиссии ANCA-ассоциированных васкулитов. Энн Рум Дис . 2018 августа 77 (8): 1150-1156. [Медлайн].
Charles P, et al; Французская группа по изучению васкулита. Сравнение индивидуально подобранного и фиксированного режима ритуксимаба для поддержания ремиссии ANCA-ассоциированного васкулита: результаты многоцентрового рандомизированного контролируемого исследования III фазы (MAINRITSAN2). Энн Рум Дис . 2018 Август 77 (8): 1143-1149. [Медлайн].
Stegeman CA, Tervaert JW, de Jong PE, Kallenberg CG.Триметоприм-сульфаметоксазол (ко-тримоксазол) для профилактики рецидивов гранулематоза Вегенера. Голландская исследовательская группа по ко-тримоксазолу Вегенера. N Engl J Med . 1996 июл 4. 335 (1): 16-20.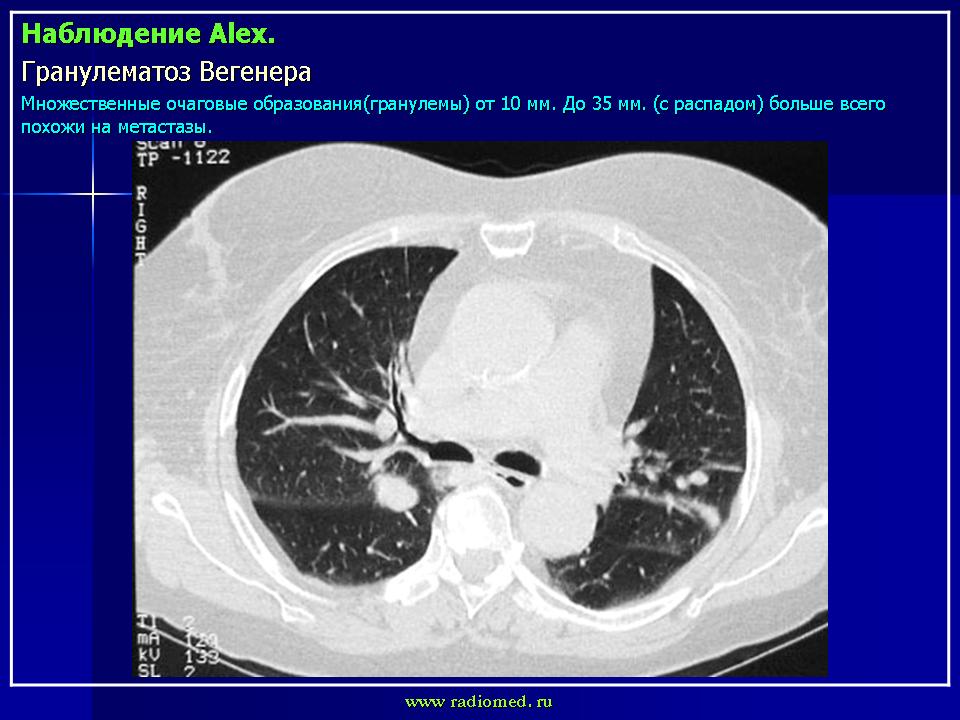 [Медлайн].
[Медлайн].
Bosch X, Guilabert A, Espinosa G, Mirapeix E. Лечение васкулита, связанного с антинейтрофильными цитоплазматическими антителами: систематический обзор. ЯМА . Август 2007. 298: 655-669. [Медлайн].
Martinez V, Cohen P, Pagnoux C, et al.Внутривенные иммуноглобулины при рецидивах системных васкулитов, связанных с антинейтрофильными цитоплазматическими аутоантителами: результаты многоцентрового проспективного открытого исследования 22 пациентов. Rheum артрита . Январь 2008. 58 (1): 308-371. [Медлайн].
Сильва Ф., Спекс Ю., Калра С. и др. Микофенолата мофетил для индукции и поддержания ремиссии при микроскопическом полиангиите с поражением почек от легкой до умеренной степени — проспективное открытое пилотное исследование. Clin J Am Soc Nephrol . Март 2010. 5 (3): 445-53. [Медлайн].
Joy MS, Hogan SL, Jennette JC, Falk RJ, Nachman PH. Пилотное исследование с использованием микофенолятмофетила при рецидивирующем или резистентном ANCA васкулите мелких сосудов. Циферблат нефрола . Декабрь 2005. 20 (12): 2725-2732. [Медлайн].
Коукулаки М, Джейн ДР. Микофенолят мофетил при системном васкулите, ассоциированном с антинейтрофильной цитоплазмой и антителами. Нефрон Клинический Практик .2006. 102 (3-4): c100-7. [Медлайн].
Nowack R, Göbel U, Klooker P, Hergesell O, Andrassy K, van der Woude FJ. Микофенолят мофетил для поддерживающей терапии гранулематоза Вегенера и микроскопического полиангиита: пилотное исследование с участием 11 пациентов с поражением почек. Дж. Ам Соц Нефрол . 1999 Сентябрь 10 (9): 1965-71. [Медлайн].
Stone JH, Uhlfelder ML, Hellmann DB, Crook S, Bedocs NM, Hoffman GS. Этанерцепт в сочетании с традиционным лечением гранулематоза Вегенера: открытое шестимесячное исследование для оценки безопасности. Rheum артрита . May 2001. 44 (5): 1149-1154. [Медлайн].
Бут А, Харпер Л., Хаммад Т., Бэкон П., Гриффит М., Леви Дж. И др. Проспективное исследование блокады TNF-альфа инфликсимабом при системном васкулите, ассоциированном с антинейтрофильными цитоплазматическими антителами. Дж. Ам Соц Нефрол . 2004 15 марта (3): 717-21. [Медлайн].
Ли Р.В., Д’Круз Д.П. Новые методы лечения васкулита, ассоциированного с антинейтрофильными цитоплазматическими антителами. Наркотики . 2008. 68: 747-770. [Медлайн].
Sangle SR, Hughes GR, D’Cruz DP. Инфликсимаб у пациентов с трудно поддающимся лечению системным васкулитом: неблагоприятный исход и значительные побочные эффекты. Энн Рум Дис . April 2007. 66 (4): 564-565. [Медлайн].
Hinze CH, Colbert RA. Истощение В-клеток при гранулематозе Вегенера. Clin Rev Allergy Immunol . Июнь 2008. 34: 372-379. [Медлайн].
Schmitt WH, Birck R, Heinzel PA, et al. Длительное лечение рефрактерного гранулематоза Вегенера с 15-дезоксиспергуалином: открытое исследование с участием семи пациентов. Циферблат нефрола . Июнь 2005. 20 (6): 1083-1092. [Медлайн].
[Медлайн].
Birck R, Warnatz K, Lorenz HM, et al.15-Деоксиспергуалин у пациентов с рефрактерным ANCA-ассоциированным системным васкулитом: открытое шестимесячное исследование для оценки безопасности и эффективности. Дж. Ам Соц Нефрол . Февраль 2003. 14 (2): 440-7. [Медлайн].
Schmitt WH, Hagen EC, Neumann I, et al. Лечение рефрактерного гранулематоза Вегенера антитимоцитарным глобулином (АТГ): открытое исследование с участием 15 пациентов. Почки Инт . Апрель 2004. 65 (4): 1440-1448. [Медлайн].
Уолш М., Чаудри А., Джейн Д.Долгосрочное наблюдение за рецидивирующим / рефрактерным васкулитом, связанным с антителами к цитоплазме нейтрофилов, леченным алемтузумабом (CAMPATH-1H). Энн Рум Дис . Сентябрь 2008 г. 67 (9): 1322-1327. [Медлайн].
Reynolds J, Tam FW, Chandraker A, et al. Блокада CD28-B7 предотвращает развитие экспериментального аутоиммунного гломерулонефрита. Дж. Клин Инвест . March 2000. 105 (5): 643-51. [Медлайн].
Girard C, Charles P, Terrier B, Bussonne G, Cohen P, Pagnoux C, et al.Трахеобронхиальные стенозы при гранулематозе с полиангиитом (Вегенера): отчет о 26 случаях. Медицина (Балтимор) . 2015 август 94 (32): e1088. [Медлайн].
Hoffman GS, Thomas-Golbanov CK, Chan J, Akst LM, Eliachar I. Лечение субгортального стеноза, вызванного гранулематозом Вегенера, кортикостероидами внутри очага поражения и дилатацией. Дж. Ревматол . May 2003. 30 (5): 1017-21. [Медлайн].
Langford CA, Sneller MC, Hallahan CW, et al.Клинические особенности и лечение стеноза подсвязочного канала у пациентов с гранулематозом Вегенера. Rheum артрита . Октябрь 1996. 39 (10): 1754-60. [Медлайн].
Rheum артрита . Октябрь 1996. 39 (10): 1754-60. [Медлайн].
Мартинес Дель Перо М., Джейн Д., Чаудри А., Сивазоти П., Яни П. Долгосрочный исход стеноза дыхательных путей при гранулематозе с полиангиитом (гранулематоз Вегенера): обсервационное исследование. JAMA Otolaryngol Head Neck Surg . 2014 ноябрь 140 (11): 1038-44. [Медлайн].
Ezzat WH, Compton RA, Basa KC, Levi J.Реконструктивные методы седловидной деформации носа при гранулематозе с полиангиитом: систематический обзор. JAMA Otolaryngol Head Neck Surg . 2017 1 мая. 143 (5): 507-512. [Медлайн].
Wallace ZS, Wallwork R, Zhang Y, Lu N, Cortazar F, Niles JL, et al. Повышение выживаемости с трансплантацией почек при терминальной стадии почечной недостаточности из-за гранулематоза с полиангиитом: данные Системы данных по почкам США. Энн Рум Дис . 2018 сен.77 (9): 1333-1338. [Медлайн].
Эспозито Д., Тримпу П., Джульяно Д., Делин М., Рагнарссон О. Дисфункция гипофиза при гранулематозе с полиангиитом. Гипофиз . 2017 20 октября (5): 594-601. [Медлайн]. [Полный текст].
Петерс Дж. Э., Гупта В., Саид ИТ, Оффиа К., Джавад АСМ. Тяжелый локализованный гранулематоз с полиангиитом (гранулематоз Вегенера), проявляющийся обширным параличом черепных нервов и несахарным диабетом: отчет о клиническом случае и обзор литературы. BMC Neurol . 2018 1 мая. 18 (1): 59. [Медлайн]. [Полный текст].
Гранулематоз Вегенера | BW Arthritis & Rheumatology, PA
Гранулематоз Вегенера, также известный как гранулематоз с полиангиитом (ГПА), — редкое заболевание, характеризующееся воспалением кровеносных сосудов. Помимо блокировки кровотока к жизненно важным органам, это состояние вызывает образование гранулем (воспаленных масс) вокруг кровеносных сосудов, разрушая нормальные ткани.
Заболевание может повлиять на уши, нос и носовые пазухи.В наиболее серьезных случаях обычно поражаются почки, легкие и верхние дыхательные пути. Ограниченный приток крови к этим областям может нанести непоправимый ущерб. Хотя это заболевание может быть фатальным, если его не лечить, ранняя диагностика и лечение могут привести к полному выздоровлению.
Причины гранулематоза Вегенера
Хотя причина гранулематоза Вегенера неизвестна, исследования показывают, что это аутоиммунное заболевание вызывается событием, которое приводит к воспалению. Считается, что у некоторых людей это воспаление вызывает ненормальную реакцию иммунной системы.Аномальная реакция иммунной системы приводит к дальнейшему воспалению, сужению кровеносных сосудов и образованию гранулем. Вполне возможно, что первоначальным триггером является инфекция, но до настоящего времени не было связано ни одной конкретной инфекции с этим заболеванием.
Гранулематоз Вегенера обычно проявляется у пациентов в возрасте от 40 до 65 лет, чаще всего у выходцев из Северной Европы. Он редко встречается у детей, но был зарегистрирован у младенцев в возрасте 3 месяцев.
Симптомы гранулематоза Вегенера
Частые приступы синусита, иногда сопровождающиеся лихорадкой, недомоганием и ночным потоотделением, являются частым симптомом гранулематоза Вегенера. Другие симптомы могут включать:
- Хронический насморк
- Кашель
- Охриплость
- Боль в суставах
- Хронические ушные инфекции
- Изменения кожи
- Конъюнктивит
Поскольку эти симптомы также могут быть результатом ряда других медицинских проблем, они могут не привести к своевременной диагностике.Обычно пациенты обращаются за медицинской консультацией по следующим, более серьезным симптомам:
- Носовые кровотечения, воспаленные десны
- Ночные поты
- Кровавый кашель, боль в груди
- Одышка или хрипы
- Кровь в моче
- Сильный отек глаза
Пациенты с болезнью Вегенера могут также страдать от потери аппетита и последующей потери веса.
Диагностика гранулематоза Вегенера
Диагностика гранулематоза Вегенера обычно включает набор тестов.Эти тесты могут включать:
- Анализы крови на определенные белки
- Общий анализ мочи на белок или кровь в моче
- Рентген грудной клетки
- Компьютерная томография грудной клетки или носовых пазух
- Бронхоскопия
Окончательный диагноз гранулематоза Вегенера зависит от результатов биопсии пораженной ткани. Ткань может быть удалена со слизистой оболочки носа, дыхательных путей или легких, кожи или почек. Биопсия проводится для определения наличия васкулита или гранулем.
Лечение гранулематоза Вегенера
При ранней диагностике и лечении пациенты могут вылечиться от гранулематоза Вегенера в течение нескольких месяцев, хотя обычно им требуется поддерживающая терапия на срок до 2 лет или дольше. Необходимо тщательное наблюдение, поскольку примерно у половины всех пациентов заболевание рецидивирует. Лечение гранулематоза Вегенера включает введение:
- Кортикостероиды, такие как преднизон
- Иммунодепрессанты, такие как метотрексат
- Биологические препараты
Другие прописанные лекарства могут использоваться для противодействия побочным эффектам этих основных лекарств, таким как потеря костной массы или инфекции легких.Фолиевая кислота или фолиевая кислота (лейковорин) обычно назначают для борьбы с истощением фолиевой кислоты, связанным с использованием метотрексата.
Осложнения лечения гранулематоза Вегенера
В тяжелых случаях или случаях, обнаруженных на поздних стадиях, это заболевание может лечиться экспериментальными препаратами, такими как внутривенный иммуноглобулин. Если почки повреждены, может потребоваться плазмаферез или даже трансплантация почки.
Дополнительные ресурсы
Произошла ошибка при настройке вашего пользовательского файла cookie
Произошла ошибка при настройке вашего пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности.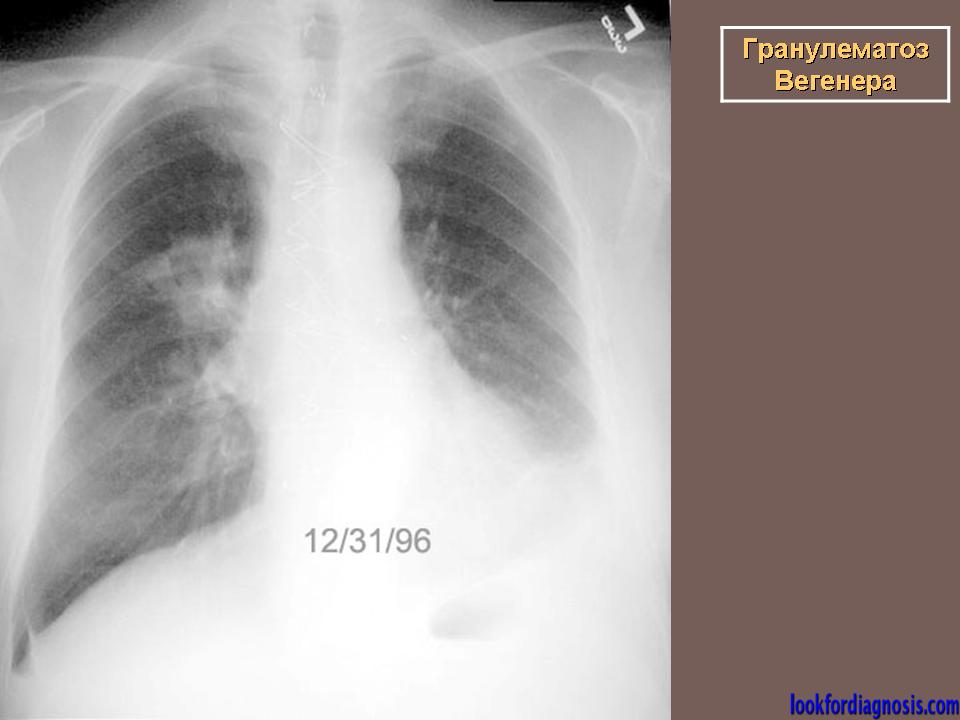 Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г.,
браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере. - Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie
потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт
Например, сайт
не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к
остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Диагностические соображения при синоназальном гранулематозе Вегенера, клинически ошибочно принимаемом за карциному
Мы сообщаем о случае гранулематоза Вегенера, клинически ошибочно принятого за карциному, у 21-летней девушки с язвенной массой носоглотки, связанной с увеличенными латероцервикальными узлами. Поражение было клинически заподозрено как злокачественное на основании клинических и радиологических данных (а именно, компьютерной томографии и позитронно-эмиссионной томографии).Однако множественные биопсии не позволили установить наличие злокачественного новообразования, показав гистологические изменения, указывающие на гранулематоз Вегенера. Определение cANCA в сыворотке подтвердило диагноз гранулематоза Вегенера. Клинические данные и исследования изображений предполагали ошибочный диагноз злокачественного новообразования, тогда как окончательный диагноз гранулематоза Вегенера был установлен только после повторных биопсий, что привело к правильному терапевтическому подходу. Гранулематоз Вегенера должен быть добавлен к списку дифференциальных диагнозов новообразований носоглотки, связанных с увеличенными латероцервикальными узлами или без них.
1. Введение
Гранулематоз Вегенера (WG) — системное аутоиммунное заболевание, гистологически характеризующееся некротическим гранулематозным воспалением с васкулитом. Он принадлежит к группе антинейтрофильных цитоплазматических антител (ANCA-), ассоциированных с васкулитом, которые ответственны за воспаление WG. Диагноз WG обычно основан на распознавании клинической картины и обнаружении ANCA в сыворотке, особенно cANCA anti-PR3 [1, 2].
Синоназальный тракт является наиболее часто поражаемым участком в области головы и шеи, и этот участок может быть единственным пораженным органом WG [3]. Однако диагностика WG может быть сложной задачей, когда пациент обращается в онкологически ориентированное отделение или когда он сталкивается с исследованиями изображений (например, компьютерной томографией и ПЭТ), предполагающими злокачественное заболевание. Эти обстоятельства могут способствовать недиагностированию WG, что приводит к задержке в правильном терапевтическом подходе.
Однако диагностика WG может быть сложной задачей, когда пациент обращается в онкологически ориентированное отделение или когда он сталкивается с исследованиями изображений (например, компьютерной томографией и ПЭТ), предполагающими злокачественное заболевание. Эти обстоятельства могут способствовать недиагностированию WG, что приводит к задержке в правильном терапевтическом подходе.
Что касается гистологии, наличие некротических гранулем, воспалений и васкулитов является отличительной чертой WG. Однако эти патогномоничные черты могут быть упущены патологоанатомами либо на ранней стадии заболевания, либо при столкновении с небольшими фрагментами ткани.
В данном документе мы представляем случай синоназальной WG, клинически и радиологически ошибочно принятой за недифференцированный рак носоглотки.
2. Изучение клинического случая
В нашу больницу поступила 21-летняя девушка с 3-месячным отитом в анамнезе. Клиническая оценка, которая включала назальное фиброскопическое исследование, выявила наличие вегетативной и изъязвленной массы носоглотки, затрагивающей левую евстахиеву трубу, что указывает на злокачественное новообразование (рис. 1).
Наличие увеличенных латероцервикальных узлов подтвердило клиническое подозрение на злокачественное новообразование.Ее первоначальная компьютерная томография показала большую массу в левой стенке носоглотки с признаками, указывающими на новообразование, с локальным распространением в левое околоплотное пространство латерально. Для дальнейшей оценки ей сделали ФДГ ПЭТ / КТ (Gemini GXL; Philips, Голландия). Сканирование всего тела выполняли через 50 минут после внутривенной инъекции 208 МБк (5,6 мКи) 18F-FDG, выявляя фокальную область накопления FDG-6-фосфата в ринофаринксе, вовлекающую левое парафарингеальное пространство (максимальное стандартное значение поглощения:) (Рисунок 2) .
Даже результаты ПЭТ подтвердили клинический диагноз злокачественности. Выполнена биопсия. Гистология была отрицательной на карциному и лимфому на основании морфологических и иммуногистохимических данных (нормальное распределение цитокератинов: CD20, CD3, bcl-2, bcl-6, CD10 и CD5).
Из-за клинических и радиологических подозрений на злокачественную опухоль была выполнена дополнительная биопсия. Гистологическое исследование выявило морфологические иммуногистохимические результаты, идентичные предыдущим, что привело к описательному диагнозу «отсутствие признаков злокачественности».«Началась неспецифическая медикаментозная терапия. Поскольку клинические симптомы не реагировали на терапию, была проведена третья биопсия, показавшая наличие гранулематозного воспаления с разбросанными гигантскими клетками и васкулита, указывающего на болезнь Вегенера (рис. 3).
На основе этих гистологических данных было выполнено определение ANCA в сыворотке, которое показало сильную положительную () cANCA и, таким образом, подтвердило гистологический диагноз WG. Клиническая оценка исключила поражение легких и почек.Пациенты начали терапию ритуксимабом (химерное моноклональное антитело к CD20) и внезапно улучшили клинические симптомы.
3. Обсуждение
WG — это аутоиммунное заболевание, гистологически характеризующееся некротическим гранулематозным воспалением, связанным с васкулитом малых и средних сосудов. WG принадлежит к группе антинейтрофильных цитоплазматических антител (ANCA-), ассоциированных с васкулитом, которые ответственны за воспаление WG. Определение сывороточного ANCA может помочь в диагностике WG, но положительность ANCA не всегда является окончательной для диагностики, а отрицательность для ANCA недостаточна для отклонения диагноза [1, 2].
Хотя легкие и почки обычно вовлекаются в течение WG, могут быть затронуты многие другие органы, включая верхние дыхательные пути [4, 5]. Однако типичные некротические гранулемы и васкулит патологоанатомы могут не заметить либо на ранней стадии заболевания, либо в небольших фрагментах ткани. Следовательно, диагностика может быть сложной задачей, когда типичные гистологические признаки отсутствуют, или когда легкие и почки не вовлечены в заболевание, или даже когда пациент обращается в онкологически ориентированное отделение. Более того, рентгенологические данные (например, компьютерная томография и ПЭТ) могут привести к ошибочному диагнозу из-за совпадения характеристик с другими заболеваниями, включая злокачественные новообразования. Таким образом, необычная клиническая картина вместе с неспецифическими рентгенологическими и гистологическими особенностями может отсрочить постановку правильного диагноза, что приведет к ошибочному терапевтическому подходу с драматическими клиническими последствиями [6].
Более того, рентгенологические данные (например, компьютерная томография и ПЭТ) могут привести к ошибочному диагнозу из-за совпадения характеристик с другими заболеваниями, включая злокачественные новообразования. Таким образом, необычная клиническая картина вместе с неспецифическими рентгенологическими и гистологическими особенностями может отсрочить постановку правильного диагноза, что приведет к ошибочному терапевтическому подходу с драматическими клиническими последствиями [6].
В данном случае подозрения на злокачественные новообразования были сильно подтверждены либо клинической картиной, либо анализом изображений (а именно, компьютерной томографией и ПЭТ / КТ).Карциномы придаточных пазух носа — это высокоагрессивное новообразование, возникающее из полости носа и придаточных пазух носа. Хотя карцинома носовых пазух встречается редко, ее следует заподозрить при обнаружении изъязвленной слизистой оболочки этого тракта даже у молодых пациентов [7]. Клинические проявления обычно включают носовое кровотечение, заложенность носа, выделения из носа с периодическими кровянистыми выделениями и серьезный средний отит, которые могут быть одними из самых ранних симптомов. Другие симптомы включают затрудненное дыхание, шейную лимфаденопатию и поражение черепных нервов [8].Представление пациентами опухоли шеи в виде шейной лимфаденопатии усиливает подозрение на метастатический рак. Принимая во внимание все эти соображения, в нашем случае клиническое подозрение на карциному было предпочтительным клиническим диагнозом.
Более того, даже анализ изображений вместе с ПЭТ-исследованием ориентировал и поддерживал клиническую диагностику злокачественных новообразований. Предварительные исследования показали многообещающие результаты при оценке злокачественных заболеваний головы и шеи с помощью комбинированной ПЭТ / КТ, поскольку ПЭТ с 18F-ФДГ, как сообщается, чувствительна для диагностики и определения стадии нескольких типов злокачественных новообразований [9, 10].Однако накопление 18F-FDG неспецифично для опухолей, а поглощение 18F-FDG при доброкачественных процессах широко известно [11].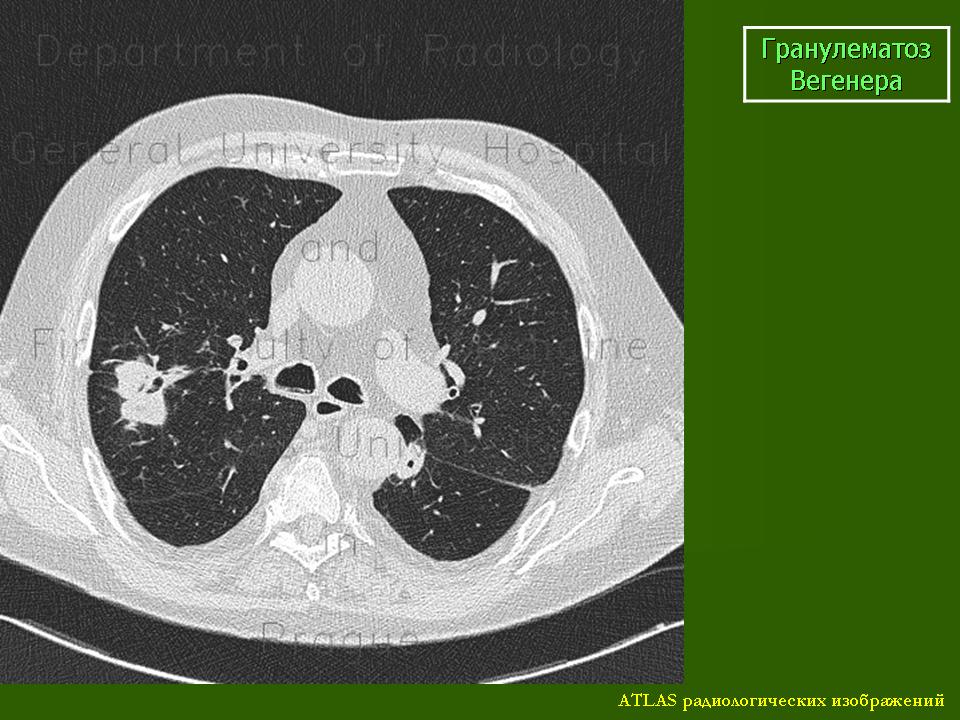 Однако отличить злокачественные новообразования от доброкачественных воспалительных или инфекционных процессов сложно, поскольку и то, и другое может вызвать повышенное поглощение 18F-FDG. Внедорожники были предложены как полезные для дискриминации. Значение обрезания является спорным; хотя общепринято значение 2,5–3,9, между злокачественными и доброкачественными образованиями все еще существует значительное совпадение [12, 13].
Однако отличить злокачественные новообразования от доброкачественных воспалительных или инфекционных процессов сложно, поскольку и то, и другое может вызвать повышенное поглощение 18F-FDG. Внедорожники были предложены как полезные для дискриминации. Значение обрезания является спорным; хотя общепринято значение 2,5–3,9, между злокачественными и доброкачественными образованиями все еще существует значительное совпадение [12, 13].
Хотя клинически это указывает на злокачественное новообразование, точный диагноз основывается на гистологическом подтверждении заболевания.В данном случае две последовательные биопсии дали отрицательный результат на злокачественные новообразования. Следует подчеркнуть, что клинический диагноз, отличный от «злокачественного новообразования», следует заподозрить при последовательном гистологическом диагнозе «отсутствие признаков заболевания» на биоптатах. WG должен быть одним из дифференциальных диагнозов положительных результатов ПЭТ / КТ 18F-FDG при доброкачественных заболеваниях в сочетании с соответствующей клинической базой. Ложноположительные результаты возможны только с 18FDG-PET, потому что может присутствовать инфекционный или воспалительный процесс, вызывающий поглощение, и потому что может происходить физиологическое поглощение такими структурами, как миндалины, слюнные железы и мышцы [14, 15].
Признание WG на ранней стадии имеет первостепенное значение, поскольку, если болезнь не лечить, ее клиническое течение ускоряется. Наш случай подчеркивает, что поражение носовых пазух носа может клинически перекрывать карциному придаточных пазух носа и должно быть включено в список дифференциальных диагнозов масс этой области. С другой стороны, патологи должны учитывать, что WG не может быть гистологически очевидным в небольших биоптатах и что минимальные изменения, включая очаговый некроз или гранулематозное воспаление, могут свидетельствовать о WG.
В заключение, включение WG в список дифференциальных диагнозов синоназальных новообразований может иметь практическое значение для тестирования сывороточного ANCA, чтобы подтвердить или поддержать диагноз WG. Это могло бы иметь более рентабельный эффект при диагностике и лечении необычного, но недостаточно диагностируемого состояния синоназального тракта.
Это могло бы иметь более рентабельный эффект при диагностике и лечении необычного, но недостаточно диагностируемого состояния синоназального тракта.
Гранулематоз Вегенера | Thorax
Гранулематоз Вегенера (WG) — это некротический гранулематозный васкулит, который имеет клиническую предрасположенность к поражению верхних дыхательных путей, легких и почек.Причина WG остается неясной, хотя недавние исследования начали проливать свет на иммунные механизмы, которые могут играть роль в патофизиологии заболевания. Терапевтические вмешательства в РГ были в основном неэффективными до тех пор, пока не было введено комбинированное лечение циклофосфамидом и глюкокортикоидами, которое резко улучшило исход пациентов. Хотя рецидив заболевания и токсичность лекарств остаются проблемой при использовании этого режима, он дал нам возможность для более длительного наблюдения за пациентами, благодаря которым мы получили более глубокое понимание болезни.
Эпидемиология
Распространенность WG в Соединенных Штатах оценивается как минимум три на 100 000 с соотношением мужчин и женщин примерно 1: 1. Большинство пациентов (80–97%) составляют европеоид, в то время как афроамериканцы составляют около 2–8% от большинства когорт. Средний возраст на момент постановки диагноза составляет около 40-55 лет, хотя могут быть затронуты люди любого возраста1. Существуют ли значительные различия в начале заболевания в разные сезоны или в осаждении болезни из-за вдыхания определенных твердых или газообразных материалов или инфекции, остается открытым. предмет разногласий.Недавние исследования не подтвердили идею сезонных колебаний независимо от того, получены ли данные из восприятия пациентом начала заболевания, медицинских записей или национальных обследований при выписке из больницы1.
2
В исследовании случай-контроль, в котором сравнивали пациентов с РГ, здоровых людей из контрольной группы, лиц с идиопатическими воспалительными легочными заболеваниями и различными ревматологическими заболеваниями, оценивалось воздействие твердых частиц окружающей среды и газообразных веществ.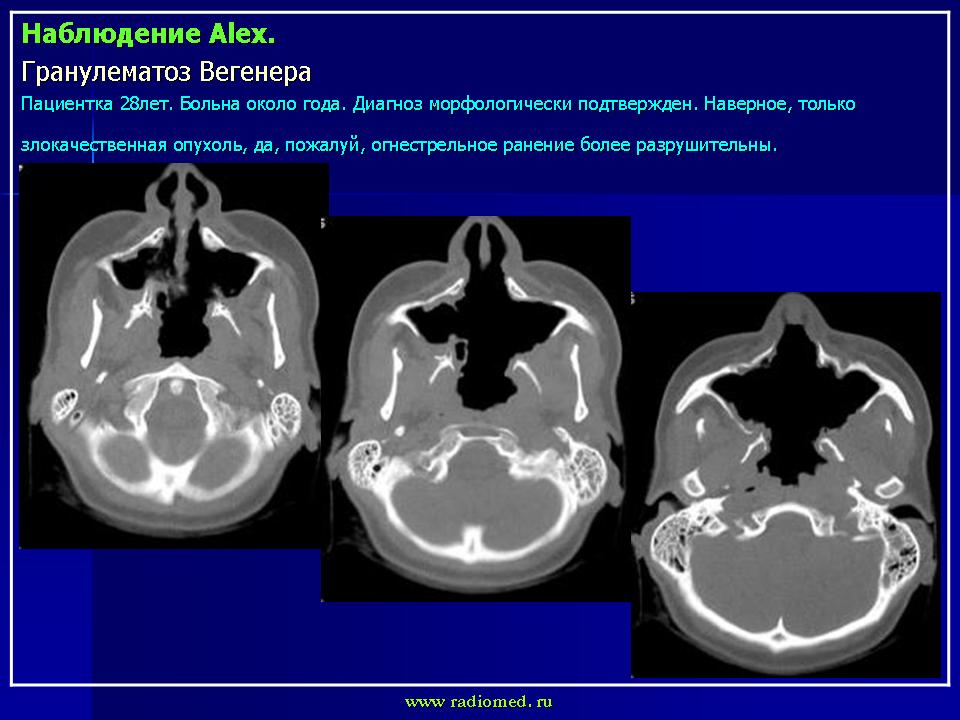 2 Более 75% пациентов во всех группах отметили воздействие окружающей среды. вдыхаемые материалы в течение года до начала заболевания (или даты интервью для здоровых людей из контрольной группы).Отсутствие разительной разницы между пациентами с WG и контрольными субъектами, редкость семейных случаев и отсутствие доминантного генотипа HLA среди пациентов с WG подтверждают представление о том, что приобретенная восприимчивость хозяина играет важную роль в этиологии заболевания.
2 Более 75% пациентов во всех группах отметили воздействие окружающей среды. вдыхаемые материалы в течение года до начала заболевания (или даты интервью для здоровых людей из контрольной группы).Отсутствие разительной разницы между пациентами с WG и контрольными субъектами, редкость семейных случаев и отсутствие доминантного генотипа HLA среди пациентов с WG подтверждают представление о том, что приобретенная восприимчивость хозяина играет важную роль в этиологии заболевания.
Клинические особенности
Более 90% пациентов с ГВ в первую очередь обращаются за медицинской помощью по поводу симптомов верхних и / или нижних дыхательных путей3. Заболевание носовых пазух и носовых пазух характеризуется заложенностью и носовым кровотечением из-за рыхлости слизистой оболочки, изъязвления и утолщения.Перфорация носовой перегородки и / или седловидная деформация могут возникнуть в результате разрушения носового хряща. Подсвязочный стеноз наблюдается примерно у 20% пациентов и может вызвать опасное для жизни нарушение проходимости дыхательных путей. Для выявления этого поражения важен высокий индекс подозрения, поскольку он часто впервые диагностируется при отсутствии других признаков активной WG и имеет неспецифические симптомы, такие как одышка, изменения голоса и кашель. при отоларингологической визуализации внегрудная непроходимость можно предположить по изменениям петли поток-объем (рис. 1).
фигура 1
Петля потока-объема у пациента с гранулематозом Вегенера с подсвязочным отверстием диаметром 2 мм. Уплощение наблюдается как на вдохе, так и на выдохе, что соответствует фиксированной внегрудной обструкции.
В нижних дыхательных путях WG может поражать паренхиму легких, бронхи и, в редких случаях, плевру. Рентгенограммы грудной клетки должны быть получены у всех пациентов с подозрением на ГВ, так как 34% случаев с рентгенологическими аномалиями оказались бессимптомными.3 Хотя двусторонние узелковые инфильтраты являются обычным явлением, можно наблюдать широкий спектр рентгенологических характеристик, включая единичные узелки / инфильтраты, полостное заболевание и диффузное альвеолярное кровотечение (рис. 2). Воспаление и стеноз эндобронхиальных дыхательных путей (рис. 3) обнаруживаются по крайней мере у 15% пациентов с поражением легких.
2). Воспаление и стеноз эндобронхиальных дыхательных путей (рис. 3) обнаруживаются по крайней мере у 15% пациентов с поражением легких.
6 Эндобронхиальное заболевание может проявляться кашлем, хрипом, одышкой, кровохарканьем или симптомами, связанными с коллапсом легких или постобструктивной инфекцией.
фигура 2
Различный спектр рентгенографических аномалий, затрагивающих легочную паренхиму при гранулематозе Вегенера, по данным компьютерной томографии: (A) двусторонние узловые инфильтраты, (B) полостная болезнь, (C) легочное кровотечение.
Рисунок 3
Сужение эндобронхиальных дыхательных путей при гранулематозе Вегенера.
Гломерулонефрит является одним из наиболее серьезных проявлений ВГ, поскольку он может быстро прогрессировать до полной почечной недостаточности при отсутствии симптомов.5 Обнаружение обычно осуществляется по аномальным лабораторным результатам, таким как протеинурия, активный осадок мочи с микроскопической гематурией. цилиндры эритроцитов и потенциально снижение функции почек, о чем свидетельствует повышение сывороточного креатинина или снижение клиренса креатинина.Постоянная бдительность в отношении гломерулонефрита имеет важное значение, поскольку он присутствует при диагностике только у 20% пациентов, но развивается у 80% пациентов в какой-то момент в течение их заболевания.
Хотя классически считается, что WG включает триаду системы органов верхних дыхательных путей, легких и почек, она может поражать практически любой участок (таблица 1). Среди участков, которые имеют значительный потенциал заболеваемости, находятся глаза и нервная система. В WG наблюдался широкий спектр глазных проявлений, которые могут угрожать зрению, воздействуя непосредственно на глаз или участвуя в его смежных структурах.7 Такие проявления включают эписклерит, склерит, конъюнктивит, кератит, увеит, васкулит сетчатки, неврит зрительного нерва и ретроорбитальную псевдоопухоль. Множественный мононеврит наблюдался у 15% пациентов и 8% имели заболевание центральной нервной системы8
Таблица 1
Гранулематоз Вегенера: клинический профиль поражения органов1-150
Диагностика и клиническое использование ANCA
Дифференциальный диагноз WG часто основан на участках поражения органов и часто включает инфекции, новообразования, заболевания соединительной ткани и другие гранулематозные заболевания. Поскольку лекарства, используемые для лечения WG, потенциально токсичны и могут ухудшить эти другие состояния, окончательный диагноз имеет важное значение.
Поскольку лекарства, используемые для лечения WG, потенциально токсичны и могут ухудшить эти другие состояния, окончательный диагноз имеет важное значение.
Диагноз WG обычно ставится на основании гистологической демонстрации васкулита, гранулематозного воспаления и некроза9 в клинически совместимых условиях (рис. 4). Эти гистологические особенности часто неоднородны по распределению, при этом вероятность получения положительного результата биопсии зависит от участка органа и, в частности, от количества полученной ткани.10
11 Решение о том, из какого места следует взять образец биопсии, должно основываться на индивидуальных факторах, включая тяжесть заболевания, инвазивность процедуры, вероятность положительного результата на основе данных из литературы и срочность начала лечения.
Рисунок 4
Паренхима легких, показывающая гистологические признаки гранулематоза Вегенера: некроз, гранулематозное воспаление и васкулит.
Антинейтрофильные цитоплазматические антитела (ANCA) были впервые описаны в 198212, а в 1985 году было обнаружено, что они имеют высокую степень ассоциации с активными WG.13 С момента их описания были обнаружены два основных образца иммунофлуоресцентного окрашивания ANCA — цитоплазматический образец (c-ANCA) и перинуклеарный образец (p-ANCA). c-ANCA обнаружен у 70–90% пациентов с активной WG; его антигеном-мишенью является протеиназа-3, сериновая протеаза массой 29 кДа, обнаруженная в азурофильных гранулах нейтрофилов.14 p-ANCA имеет более широкий диапазон ассоциаций болезни и антигенной специфичности, но наблюдается у 5-10% пациентов с WG, где она обычно направлен против миелопероксидазы, другого компонента нейтрофильных гранул.15
16
Сообщается, что чувствительность ANCA для WG колеблется от 28% до 92% 13.
17-19 Этот широкий спектр частично отражает различные критерии, которые применялись для постановки диагноза WG. Несколько серий продемонстрировали высокую специфичность c-ANCA для WG в диапазоне от 80% до 100%. Такая высокая степень чувствительности и специфичности c-ANCA для WG вызвала интерес к вопросу о том, можно ли его использовать в качестве средства диагностики.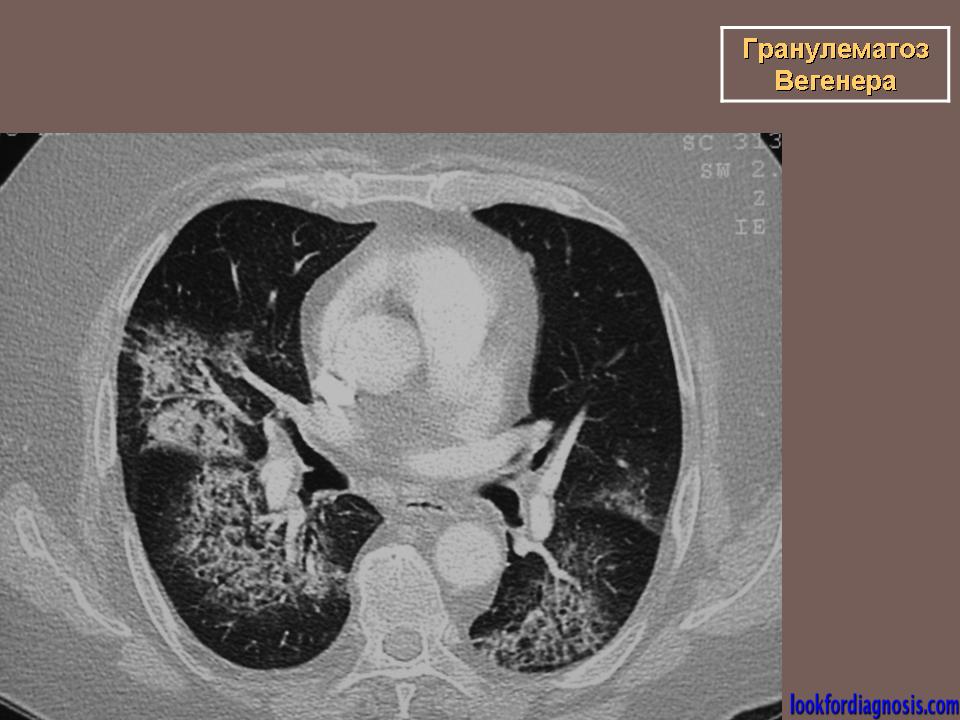 Несмотря на эти результаты, на полезность ANCA в качестве диагностического теста также влияет вероятность заболевания до теста, которая будет низкой в большинстве клинических ситуаций, учитывая необычный характер WG.Сообщалось также о положительных результатах теста ANCA при других заболеваниях, которые являются частью дифференциальной диагностики WG16.
Несмотря на эти результаты, на полезность ANCA в качестве диагностического теста также влияет вероятность заболевания до теста, которая будет низкой в большинстве клинических ситуаций, учитывая необычный характер WG.Сообщалось также о положительных результатах теста ANCA при других заболеваниях, которые являются частью дифференциальной диагностики WG16.
Таким образом, хотя положительный результат теста c-ANCA может быть полезен для предположения о возможности WG, его обычно не следует использовать вместо образца биопсии для постановки диагноза.21
Поскольку титры ANCA будут меняться в течение болезни и, как было установлено, при активном заболевании выше, чем при неактивном, 13
17-19 некоторые авторы сомневаются, можно ли использовать последовательные титры ANCA для прогнозирования рецидива заболевания и принятия решений о лечении.22 Однако в одной серии, в которой пациенты наблюдались серийно в течение 18 месяцев, у 44% пациентов, у которых отмечалось четырехкратное повышение титра ANCA, не наблюдалось последующего увеличения клинической активности заболевания.23 Учитывая возможность того, что обострение заболевания может не произойти, и токсичность лечения может быть значительным, повышение титра ANCA само по себе не должно использоваться как основание для возобновления или увеличения лечения. Однако такой вывод должен побудить к тщательной оценке любых объективных свидетельств активного заболевания и частому наблюдению за пациентом.
Лечение
Необработанная WG исторически имела неблагоприятный исход со средним сроком выживания в пять месяцев.9 Глюкокортикоиды были первым лечением, которое было опробовано в WG, и, хотя они замедляли смертность, среднее время выживания оставалось всего 12,5 месяцев.24 Комбинированное лечение с ежедневным лечением циклофосфамид и глюкокортикоиды стали важным достижением 3.
5 По этой схеме пациенты получали циклофосфамид в дозе 2 мг / кг / день в течение одного года после ремиссии, которая затем снижалась и прекращалась. Наряду с этим был начат прием преднизона в дозе 1 мг / кг / сут. Эта доза продолжалась в течение одного месяца, после чего, если наступало улучшение, ее снижали по графику через день до прекращения приема, что обычно происходило через 6–12 месяцев. Из 133 пациентов, получавших это лечение и наблюдавшихся в течение 6 месяцев — 24 лет (всего 1229 пациенто-лет), у 91% наблюдалось заметное улучшение их заболевания, у 75% была достигнута полная ремиссия, а выживаемость составила 80%. наблюдаемый.3 Этот режим остается наиболее эффективным лечением активной ГВ, и любого пациента с непосредственно угрожающим жизни заболеванием или быстро прогрессирующим гломерулонефритом следует лечить ежедневным циклофосфамидом и глюкокортикоидами, если нет серьезных противопоказаний. Несмотря на преимущества этого лечения, рецидив заболевания был обнаружен у 50% пациентов, а заболеваемость из-за токсичности, связанной с лекарственными препаратами, наблюдалась у 42%. По оценкам Каплана-Мейера, заболеваемость составит 16% через 15 лет после первого воздействия препарата на пациента.25 Другие злокачественные новообразования, которые чаще наблюдаются у пациентов, получавших циклофосфамид, включают миелопролиферативные заболевания и возможное увеличение случаев рака кожи.
Наряду с этим был начат прием преднизона в дозе 1 мг / кг / сут. Эта доза продолжалась в течение одного месяца, после чего, если наступало улучшение, ее снижали по графику через день до прекращения приема, что обычно происходило через 6–12 месяцев. Из 133 пациентов, получавших это лечение и наблюдавшихся в течение 6 месяцев — 24 лет (всего 1229 пациенто-лет), у 91% наблюдалось заметное улучшение их заболевания, у 75% была достигнута полная ремиссия, а выживаемость составила 80%. наблюдаемый.3 Этот режим остается наиболее эффективным лечением активной ГВ, и любого пациента с непосредственно угрожающим жизни заболеванием или быстро прогрессирующим гломерулонефритом следует лечить ежедневным циклофосфамидом и глюкокортикоидами, если нет серьезных противопоказаний. Несмотря на преимущества этого лечения, рецидив заболевания был обнаружен у 50% пациентов, а заболеваемость из-за токсичности, связанной с лекарственными препаратами, наблюдалась у 42%. По оценкам Каплана-Мейера, заболеваемость составит 16% через 15 лет после первого воздействия препарата на пациента.25 Другие злокачественные новообразования, которые чаще наблюдаются у пациентов, получавших циклофосфамид, включают миелопролиферативные заболевания и возможное увеличение случаев рака кожи.
26 Хотя некоторые побочные эффекты циклофосфамида могут быть уменьшены путем периодического приема препарата, проспективные стандартизированные исследования, которые были выполнены на сегодняшний день, предполагают, что прерывистое дозирование связано с более высокой вероятностью рецидива.27-29 По этой причине мы остаемся неизменными. рекомендация о том, что циклофосфамид следует вводить ежедневно для WG.
Использование низких доз метотрексата и глюкокортикоидов изучалось у пациентов, у которых не было непосредственно угрожающего жизни заболевания или у которых развилось токсическое действие, связанное с циклофосфамидом. 30-32 При этом режиме пациенты получали метотрексат 20-25 мг один раз в неделю плюс преднизон, который был назначен. сужается по графику, аналогичному описанному для циклофосфамида. Метотрексат назначали в течение одного года после наступления ремиссии, затем его уменьшили и отменили.Из 42 пациентов, получавших эту схему, 33 (79%) достигли ремиссии с рецидивом, наступившим у 19 (58%) в среднем через 29 месяцев.32 Только три пациента не ответили на лечение, и произошло три смертельных исхода, ни один из которых не был вызван активным заболеванием. васкулит. Pneumocystis carinii пневмония была наиболее часто наблюдаемым тяжелым побочным эффектом, поэтому мы рекомендуем профилактическое лечение триметопримом 160 мг / сульфаметоксазол 800 мг три раза в неделю для всех пациентов с ГГ, у которых нет аллергии на сульфаниламиды и которые получают цитотоксический агент и ежедневно глюкокортикоиды. .Эти данные подтверждают использование метотрексата в качестве приемлемой альтернативы для начального лечения отобранных пациентов, у которых нет немедленного опасного для жизни заболевания или у которых наблюдались значительные побочные эффекты, связанные с циклофосфамидом. Было также обнаружено, что метотрексат успешно поддерживает ремиссию у пациентов, которые были индуцированы циклофосфамидом.33 Хотя время последующего наблюдения в этой серии было слишком коротким, чтобы полностью оценить частоту рецидивов, он предоставляет дополнительные доказательства относительной эффективности и безопасности метотрексата в РГ. .
сужается по графику, аналогичному описанному для циклофосфамида. Метотрексат назначали в течение одного года после наступления ремиссии, затем его уменьшили и отменили.Из 42 пациентов, получавших эту схему, 33 (79%) достигли ремиссии с рецидивом, наступившим у 19 (58%) в среднем через 29 месяцев.32 Только три пациента не ответили на лечение, и произошло три смертельных исхода, ни один из которых не был вызван активным заболеванием. васкулит. Pneumocystis carinii пневмония была наиболее часто наблюдаемым тяжелым побочным эффектом, поэтому мы рекомендуем профилактическое лечение триметопримом 160 мг / сульфаметоксазол 800 мг три раза в неделю для всех пациентов с ГГ, у которых нет аллергии на сульфаниламиды и которые получают цитотоксический агент и ежедневно глюкокортикоиды. .Эти данные подтверждают использование метотрексата в качестве приемлемой альтернативы для начального лечения отобранных пациентов, у которых нет немедленного опасного для жизни заболевания или у которых наблюдались значительные побочные эффекты, связанные с циклофосфамидом. Было также обнаружено, что метотрексат успешно поддерживает ремиссию у пациентов, которые были индуцированы циклофосфамидом.33 Хотя время последующего наблюдения в этой серии было слишком коротким, чтобы полностью оценить частоту рецидивов, он предоставляет дополнительные доказательства относительной эффективности и безопасности метотрексата в РГ. .
Данные о других иммуносупрессивных и цитотоксических средствах ограничены, они поступают из отчетов о случаях заболевания и небольших серий. Такие препараты следует рассматривать только в качестве начального лечения, если есть противопоказания к циклофосфамиду или метотрексату. Было обнаружено, что азатиоприн не эффективен для индукции ремиссии, но может играть полезную роль в поддержании ремиссии у пациентов, у которых развивается токсичность в отношении циклофосфамида.5 Хлорамбуцил и циклоспорин имели переменную эффективность в отчетах от небольшого числа пациентов, но их способность вызывать злокачественные новообразования и нефротоксичность, соответственно, необходимо учитывать. 34 Хотя сообщалось о положительных результатах внутривенного введения иммуноглобулина 35, в одной серии исследований не было обнаружено положительных результатов у пациентов с заболеваниями основных органов36.
34 Хотя сообщалось о положительных результатах внутривенного введения иммуноглобулина 35, в одной серии исследований не было обнаружено положительных результатов у пациентов с заболеваниями основных органов36.
Несколько авторов сообщили о пользе использования триметоприма / сульфаметоксазола при лечении WG, ограниченного верхними и / или нижними дыхательными путями, 37
38, хотя методологические проблемы усложнили интерпретацию этих результатов. У ряда пациентов с подтвержденной биопсией WG, у которых инфекция была исключена, а другие виды лечения не добавлялись или не увеличивались в течение предыдущих трех месяцев, триметоприм / сульфаметоксазол оказал незначительное влияние или не оказал никакого влияния на предотвращение прогрессирования заболевания.3 Триметоприм / сульфаметоксазол можно рассматривать у пациентов с заболеванием, изолированным от верхних дыхательных путей, но он не рекомендуется для лечения заболеваний нижних дыхательных путей и никогда не должен использоваться отдельно при гломерулонефрите. Может ли триметоприм / сульфаметоксазол уменьшить рецидивы заболевания, также было исследовано в исследовании Stegeman et al .
39, в которых пациенты были рандомизированы для приема комбинации препаратов или плацебо, когда их заболевание находилось в стадии ремиссии во время или после лечения глюкокортикоидами и циклофосфамидом.Через 24 месяца у 82% пациентов в группе триметоприма / сульфаметоксазола была ремиссия по сравнению с 60% пациентов, получавших плацебо. Однако при разбивке по типу рецидива только рецидив заболевания верхних дыхательных путей был значительно снижен в группе, получавшей лечение, без разницы в рецидивах основных систем органов. В качестве предостережения, хотя пациенты, принимающие метотрексат, могут безопасно получать триметоприм / сульфаметоксазол три раза в неделю для профилактики пневмонии Pneumocystis , их не следует лечить триметопримом / сульфаметоксазолом два раза в день, поскольку эта комбинация связана с серьезным подавлением костного мозга.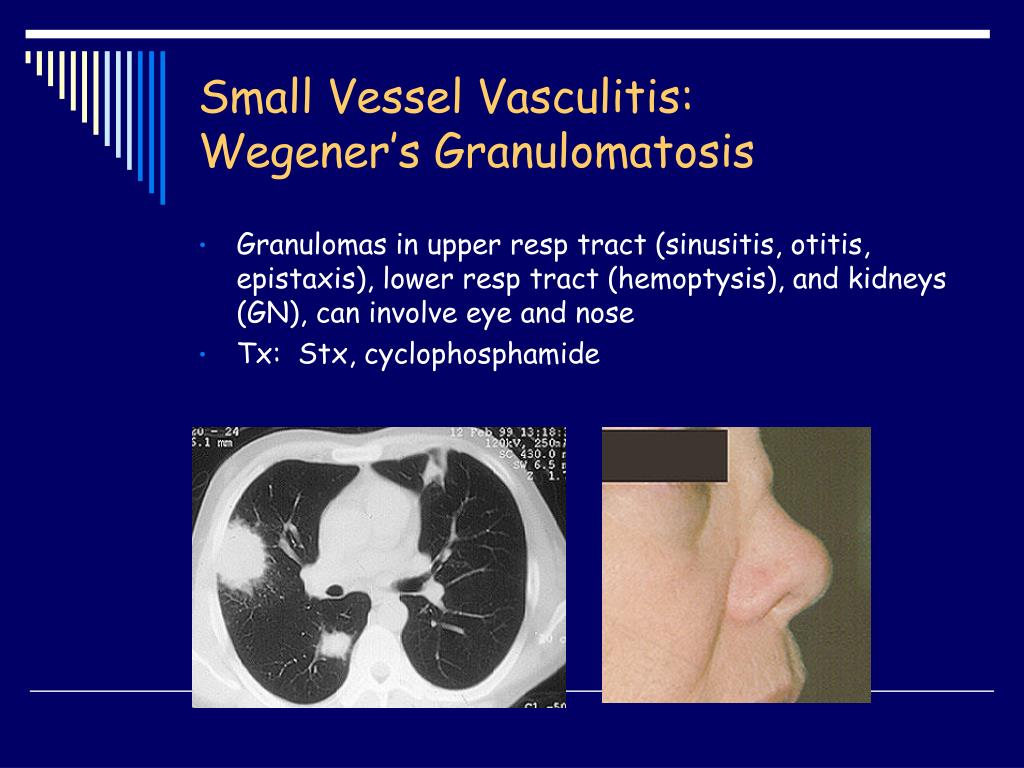 32
32
Хотя наличие заболевания, поражающего основной орган (легкие, почки, нервную систему), требует лечения глюкокортикоидами и цитотоксическими агентами, не все проявления WG могут потребовать системной иммуносупрессивной терапии или ответить на нее. Изолированные симптомы носовых пазух можно лечить поэтапно, начиная с антибиотиков, орошения и назальных стероидов. Если это неэффективно и инфекция отсутствует, можно рассмотреть возможность применения пероральных глюкокортикоидов и / или метотрексата.Пациенты, которых лечат таким образом, должны находиться под пристальным наблюдением для подтверждения активности заболевания в других органах, поскольку такое поражение может протекать бессимптомно и потребовать другого терапевтического подхода.
Подсвязочный стеноз, связанный с WG, часто не проходит медикаментозно. Один из подходов, который оказался эффективным, заключается в сочетании механического расширения трахеи с интратрахеальной инъекцией глюкокортикоида длительного действия.4 Учитывая невосприимчивость этого поражения к медикаментозному лечению, пациенты, которым требуется иммуносупрессивное лечение по поводу других проявлений, должны проходить эту процедуру одновременно. .Тем не менее, при отсутствии активности основных заболеваний органов, субгортальный стеноз, связанный с WG, можно эффективно лечить, используя только этот метод.
Патогенез
Хотя причина WG остается неясной, несколько различных направлений исследований начали исследовать механизмы, которые могут играть роль в заболевании, и определить возможные области для терапевтического вмешательства в будущем.
За последние 15 лет все больше косвенных доказательств подтверждают мнение о том, что ANCA может усиливать иммуно-воспалительные явления, которые способствуют развитию WG и связанного с ним расстройства, микроскопического полиангиита.Хотя большинство пациентов с WG, вырабатывающих ANCA, обладают специфичностью антител к протеиназе-3 (PR-3), 40-42 не все пациенты являются ANCA-положительными.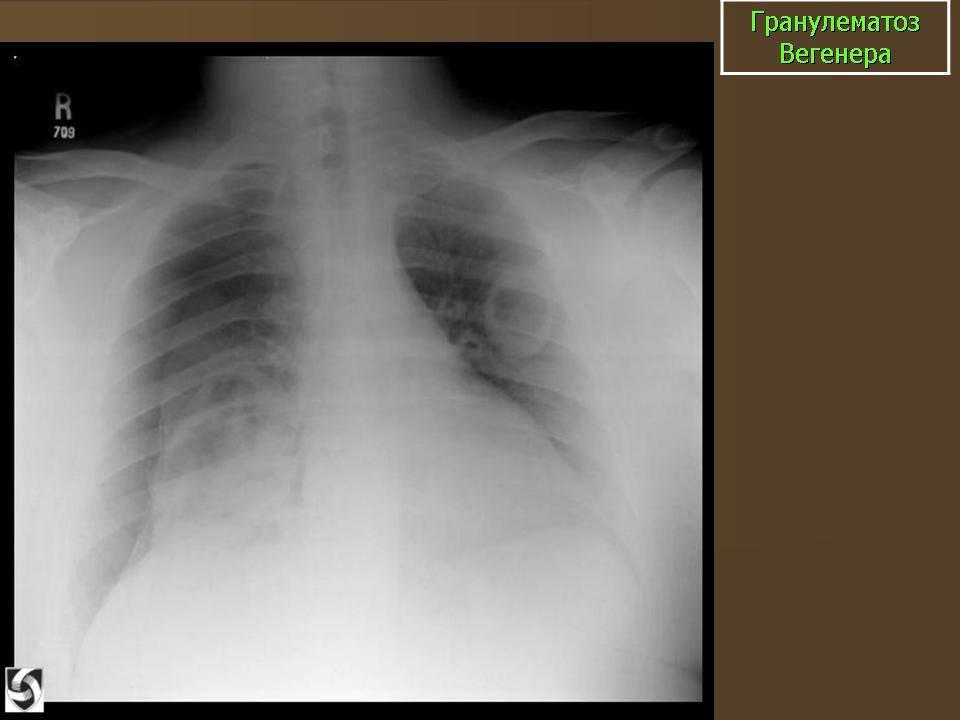 В исследовании Hauschild et al
В исследовании Hauschild et al
Было протестировано 40 более 23 700 образцов сыворотки более чем 13 600 пациентов, из которых 445 имели ГВ. У тех людей, у которых была ограниченная WG без наличия гломерулонефрита, ANCA был положительным в 55%. Однако у пациентов с заболеванием, включающим гломерулонефрит, ANCA присутствовал в 88%. Похоже, что чем тяжелее заболевание, включая наличие гломерулонефрита, тем больше вероятность того, что тест ANCA будет положительным.Важным моментом этого и многих других исследований является то, что ANCA не всегда присутствует у всех пациентов с WG. Попытки идентифицировать иммунные комплексы, содержащие антитела к PR-3 и комплемент в пораженных тканях, как правило, были безрезультатными. Таким образом, за исключением ограничений чувствительности теста, отсутствие ANCA у значительного меньшинства пациентов с активным заболеванием может указывать на то, что, если он играет определенную роль, это не является существенной ролью. Тем не менее, большое количество данных указывает на то, что ANCA, обычно со специфичностью к PR-3, а иногда и к миелопероксидазе (MPO), может способствовать активации и повреждению кровеносных сосудов.
Активированные нейтрофилы экспрессируют множество цитоплазматических антигенов на своей клеточной поверхности, многие из которых являются ферментами.43-45 Связывание антител с отображаемой протеиназой-3, МПО и множеством других цитоплазматических ферментов нейтрофилов усиливает активацию нейтрофилов, дегрануляцию и производство супероксида. Цитоплазматические ферменты нейтрофилов могут также связываться с эндотелиальными клетками, где они могут непосредственно вызывать повреждение, а также усиливать активацию эндотелиальных клеток (46).
47 В исследованиях in vitro связывание анти-PR-3 с эндотелиальными клетками приводит к увеличению выработки эндотелиальными клетками IL-8, чрезвычайно мощного хемотаксического агента нейтрофилов.48 Одновременно с этими событиями эндотелиальные клетки, подвергшиеся воздействию анти-PR-3, также последовательно увеличивают продукцию IL-1α и тканевого фактора, основного инициатора каскада свертывания. 49 Моноцит, как и нейтрофил, также продуцирует PR- 3, и при активации и воздействии анти-PR-3 они также значительно увеличивают продукцию IL-8, дополнительно создавая основу для усиленного хемотаксиса нейтрофилов.50 Если эндотелиальные клетки также были способны продуцировать и экспрессировать PR-3, дальнейшее усиление сосудистого повреждения последует.В то время как некоторые исследователи продемонстрировали продукцию PR-3 эндотелиальными клетками, другие — нет, и противоречивые результаты являются предметом значительных разногласий.51-54 Эффекты ANCA, которые приводят к усилению активации нейтрофилов и эндотелиальных клеток и повреждению, суммированы в рис. 5. Вкратце, эти данные представляют собой убедительные косвенные доказательства, указывающие на роль ANCA в патогенезе WG и микроскопического полиангиита. Хотя эти наблюдения демонстрируют способность ANCA усиливать повреждение сосудов, они не объясняют избирательность органа.Гипотезы, основанные на ANCA, были бы более интригующими, если бы было показано, что исследования, которые включали преимущественно пораженные органы в WG, такие как дыхательные пути и почки, обеспечивали среду, благоприятствующую опосредованному ANCA повреждению.
49 Моноцит, как и нейтрофил, также продуцирует PR- 3, и при активации и воздействии анти-PR-3 они также значительно увеличивают продукцию IL-8, дополнительно создавая основу для усиленного хемотаксиса нейтрофилов.50 Если эндотелиальные клетки также были способны продуцировать и экспрессировать PR-3, дальнейшее усиление сосудистого повреждения последует.В то время как некоторые исследователи продемонстрировали продукцию PR-3 эндотелиальными клетками, другие — нет, и противоречивые результаты являются предметом значительных разногласий.51-54 Эффекты ANCA, которые приводят к усилению активации нейтрофилов и эндотелиальных клеток и повреждению, суммированы в рис. 5. Вкратце, эти данные представляют собой убедительные косвенные доказательства, указывающие на роль ANCA в патогенезе WG и микроскопического полиангиита. Хотя эти наблюдения демонстрируют способность ANCA усиливать повреждение сосудов, они не объясняют избирательность органа.Гипотезы, основанные на ANCA, были бы более интригующими, если бы было показано, что исследования, которые включали преимущественно пораженные органы в WG, такие как дыхательные пути и почки, обеспечивали среду, благоприятствующую опосредованному ANCA повреждению.
Рисунок 5.
(A) При активации нейтрофилы подвергаются дегрануляции и выбросу супероксида. Некоторые цитоплазматические антигены / ферменты могут затем связываться с мембраной нейтрофилов, включая протеиназу-3 (PR-3), белок, увеличивающий бактерицидную проницаемость (BPI), миелопероксидазу (MPO) и лактоферрин (LF).Когда один из этих антигенов связывается подходящим антителом, таким как анти-PR-3, степень активации нейтрофилов и всплеска супероксида увеличивается. (B) После высвобождения белки, такие как PR-3, могут связываться с эндотелиальными клетками (ЭК), где они могут вызывать повреждение и активацию эндотелиальных клеток. Антитела, связанные с PR-3 на эндотелиальной поверхности, могут затем привести к усиленной экспрессии молекул адгезии, увеличению продукции IL-8 и привлечению нейтрофилов, связыванию и дальнейшему повреждению эндотелиальных клеток.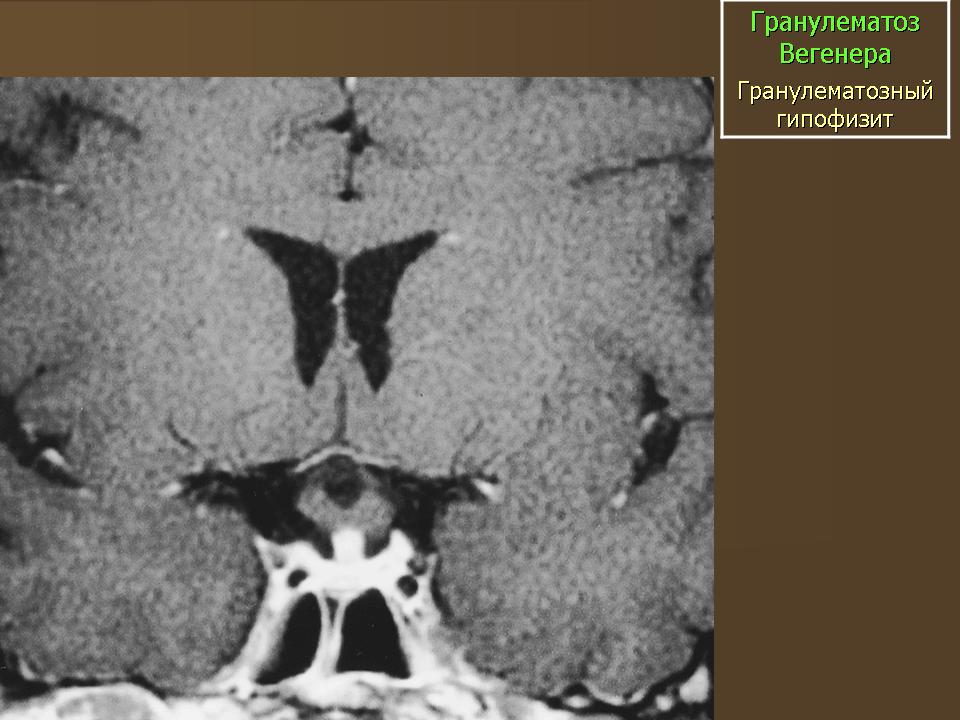 (C) Через эти механизмы могут быть задействованы различные пути, все из которых приводят к повреждению сосудов. В настоящее время эти механизмы неадекватно объясняют преимущественное нацеливание на органы при таких заболеваниях, как WG, когда наибольшая степень повреждения возникает в верхних дыхательных путях, нижних дыхательных путях и почках. Воспроизведено с разрешения Хоффмана и Спекс 42.
(C) Через эти механизмы могут быть задействованы различные пути, все из которых приводят к повреждению сосудов. В настоящее время эти механизмы неадекватно объясняют преимущественное нацеливание на органы при таких заболеваниях, как WG, когда наибольшая степень повреждения возникает в верхних дыхательных путях, нижних дыхательных путях и почках. Воспроизведено с разрешения Хоффмана и Спекс 42.
Потенциальная роль инфекции в инициировании и стимулировании развития РГ остается областью повышенного интереса. Пациенты с WG и другими васкулитами часто имеют клинические признаки, указывающие на инфекционное заболевание.В WG следует особо отметить, что дыхательные пути почти всегда изначально задействованы. В исследованиях бронхоальвеолярного лаважа участвовали пациенты с впервые диагностированным заболеванием и те, у кого возникла реактивация заболевания, а также люди в стадии ремиссии. Даже в тех случаях, когда клинические признаки активного заболевания дыхательных путей отсутствуют, пациенты обычно имеют нейтрофильный альвеолит в начале заболевания и реактивации заболевания.55-57 Было высказано предположение, что стимуляция дыхательных путей, вызывающая нейтрофильный ответ у иммунологически восприимчивого хозяина, может вызвать системные события, которые мы распознаем как WG.На сегодняшний день гистопатологические исследования образцов биопсии дыхательных путей, включая специальные окрашивания для микроорганизмов и культуры на бактерии, микобактерии, грибы, микоплазмы и респираторные вирусы, не смогли выявить возбудителя инфекции. Однако в большинстве попыток использовались обычные лабораторные методы. Более сложные молекулярные методы, включая полимеразную цепную реакцию (ПЦР), позволили идентифицировать инфекционные агенты при других заболеваниях, при которых требования к культивированию были необычайно требовательными, а специальные окрашивания тканей были недостаточно чувствительны.
Дальнейшее изучение инфекционной этиологии следует поощрять по нескольким причинам. Известно, что некоторые инфекции связаны с определенными типами васкулита. Болезнь Марека, ускоренная форма атеросклероза и воспаления сосудов, вызывается вирусом куриного птичьего герпеса. Болезнь может уничтожить целые стада животных, и ее можно предотвратить с помощью иммунизации58. Сообщалось, что у человека васкулит возникает в связи с гепатитом B, гепатитом C, вирусом Эпштейна-Барра, парво-B19 и ВИЧ-инфекциями.Однако у большинства пациентов, страдающих этими инфекциями, развиваются различные клинические проблемы, и только у <1% инфицированных людей развивается васкулит. Это наблюдение предполагает уникальную аномалию хозяина, которая приводит к этой особой форме проявления болезни. Несколько исследований на животных подтвердили эту гипотезу. Например, у множества иммунологически дефектных мышей с нормальным внешним видом разовьется васкулит после инфекций, вызванных гамма-вирусом герпеса. Васкулит у этих животных особенно очевиден на фоне генетической недостаточности гамма-интерферона или рецептора гамма-интерферона.59
60
Известно, что некоторые инфекции связаны с определенными типами васкулита. Болезнь Марека, ускоренная форма атеросклероза и воспаления сосудов, вызывается вирусом куриного птичьего герпеса. Болезнь может уничтожить целые стада животных, и ее можно предотвратить с помощью иммунизации58. Сообщалось, что у человека васкулит возникает в связи с гепатитом B, гепатитом C, вирусом Эпштейна-Барра, парво-B19 и ВИЧ-инфекциями.Однако у большинства пациентов, страдающих этими инфекциями, развиваются различные клинические проблемы, и только у <1% инфицированных людей развивается васкулит. Это наблюдение предполагает уникальную аномалию хозяина, которая приводит к этой особой форме проявления болезни. Несколько исследований на животных подтвердили эту гипотезу. Например, у множества иммунологически дефектных мышей с нормальным внешним видом разовьется васкулит после инфекций, вызванных гамма-вирусом герпеса. Васкулит у этих животных особенно очевиден на фоне генетической недостаточности гамма-интерферона или рецептора гамма-интерферона.59
60
Некоторые полагают, что стойкая инфекция как стимул к васкулиту неприемлема, потому что в большинстве случаев иммуносупрессивная терапия спасает жизнь, и пациенты не умирают от обширной инфекции. Пациенты с гепатитом B или ассоциированным с гепатитом C васкулитом часто значительно улучшаются, однако при иммуносупрессивной терапии у них увеличивается вирусная нагрузка. Подобный сценарий хорошо задокументирован для норок, инфицированных вирусом алеутской болезни. Различные штаммы вирусов вызывают заболевание разной степени тяжести, и, хотя все норки восприимчивы, алеутские норки особенно восприимчивы к инфекции.У инфицированных животных вырабатываются циркулирующие иммунные комплексы, и у них развивается летальная форма васкулита, которую можно предотвратить лечением циклофосфамидом, хотя виремия сохраняется.61
62
Эти животные модели, в которых васкулит и инфекция встречаются вместе, показывают сходство с васкулитом у людей.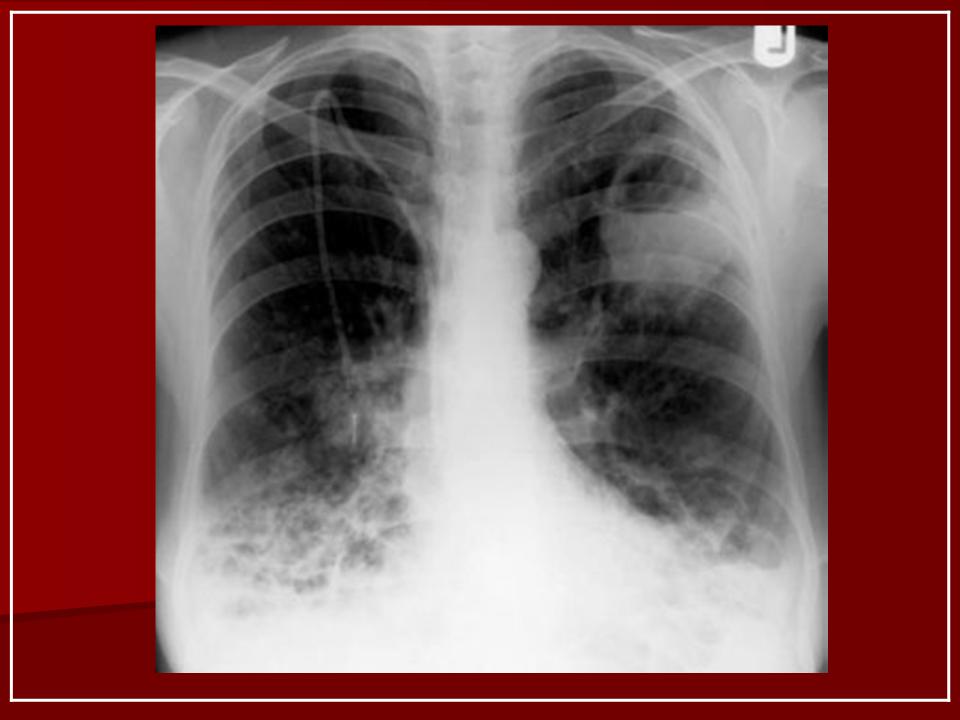 Поражение органов и сосудов обычно неоднородно с многочисленными участками «скиповых поражений». Не все организмы вызывают одинаковую картину васкулита. В модели мышей с инфекцией гамма-вирусом герпеса заболевание возникает в основном в крупных артериях, таких как аорта и ее основные ветви, тогда как в случае болезни алеутской норки поражения обнаруживаются в основном в сосудах малого и среднего размера.Возможно, что уникальные свойства инфекционных агентов, такие как сродство к определенным тканевым субстратам, очаговые свойства тканей, гемодинамические характеристики органа и уникальный иммунный ответ различных участков, могут быть важны для «нацеливания» васкулита на орган. Недавние исследования на человеке показывают, что инфицирование Chlamydia pneumoniae или цитомегаловирусом может усиливать воспалительный компонент атеросклероза. Могут ли эти организмы вызывать усиленный воспалительный ответ у иммунологически дефектного хозяина, аналогично тому, как это происходит у животных? Мы надеемся, что по крайней мере некоторые из идиопатических васкулитов будут иметь инфекционную этиологию и, следовательно, будут иметь потенциал для лечебной терапии.
Поражение органов и сосудов обычно неоднородно с многочисленными участками «скиповых поражений». Не все организмы вызывают одинаковую картину васкулита. В модели мышей с инфекцией гамма-вирусом герпеса заболевание возникает в основном в крупных артериях, таких как аорта и ее основные ветви, тогда как в случае болезни алеутской норки поражения обнаруживаются в основном в сосудах малого и среднего размера.Возможно, что уникальные свойства инфекционных агентов, такие как сродство к определенным тканевым субстратам, очаговые свойства тканей, гемодинамические характеристики органа и уникальный иммунный ответ различных участков, могут быть важны для «нацеливания» васкулита на орган. Недавние исследования на человеке показывают, что инфицирование Chlamydia pneumoniae или цитомегаловирусом может усиливать воспалительный компонент атеросклероза. Могут ли эти организмы вызывать усиленный воспалительный ответ у иммунологически дефектного хозяина, аналогично тому, как это происходит у животных? Мы надеемся, что по крайней мере некоторые из идиопатических васкулитов будут иметь инфекционную этиологию и, следовательно, будут иметь потенциал для лечебной терапии.
Другая область исследований была сосредоточена на попытке понять механизмы, лежащие в основе развития гранулем в WG. Было обнаружено, что при других заболеваниях гранулематозное воспаление является процессом, опосредованным сенсибилизированными CD4 + Т-клетками, которые продуцируют цитокины Th2 (IL-2, IFN-γ, TNF-α). Присутствие аналогичного воспаления в WG поднимает вопрос, могут ли повреждение тканей и васкулит быть опосредованными аберрантным иммунным ответом Th2. Поддержка этого механизма была получена в результате нескольких исследований.Как количественные, так и качественные отклонения в продукции цитокинов были описаны в WG и связанных с ними васкулитных синдромах. Повышенные сывороточные уровни IL-1, IL-2, IL-6 и TNF-α63.
64 и повышенная продукция TNF-α циркулирующими мононуклеарными клетками65 сообщалось у пациентов с WG.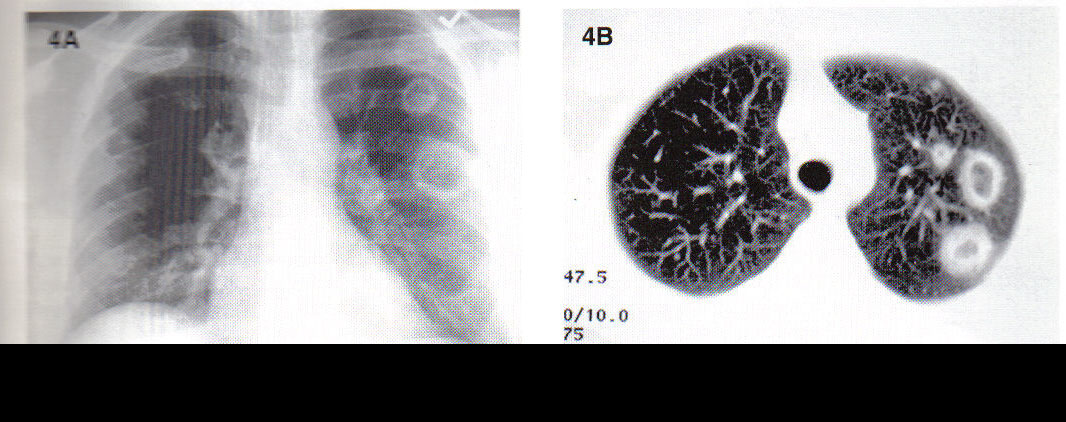 Более поздние исследования были сосредоточены на продукции провоспалительных цитокинов при активных васкулитах in situ. Повышенная продукция IL-1 и TNF-α была обнаружена в почечных клубочках пациентов с WG и активным гломерулонефритом с использованием полимеразной цепной реакции с обратной транскрипцией (RT-PCR), гибридизации in situ и иммуногистохимических методов.66 Используя аналогичный подход, Weyand и его коллеги67 обнаружили мРНК для IL-1, TNF-α, IL-6, IL-2, IFN-γ и TGF-β в срезах височных артерий пациентов с гигантоклеточным артериитом, еще одним гранулематозом. синдром васкулита. В параллельных исследованиях гистологически нормальных височных артерий у пациентов с ревматической полимиалгией была обнаружена мРНК для IL-1, TNF-α, IL-6 и IL-2, но образцы тканей не содержали последовательности IFN-γ, что позволяет предположить, что IFN-γ может быть вовлечен в развитие явного артериита.
Более поздние исследования были сосредоточены на продукции провоспалительных цитокинов при активных васкулитах in situ. Повышенная продукция IL-1 и TNF-α была обнаружена в почечных клубочках пациентов с WG и активным гломерулонефритом с использованием полимеразной цепной реакции с обратной транскрипцией (RT-PCR), гибридизации in situ и иммуногистохимических методов.66 Используя аналогичный подход, Weyand и его коллеги67 обнаружили мРНК для IL-1, TNF-α, IL-6, IL-2, IFN-γ и TGF-β в срезах височных артерий пациентов с гигантоклеточным артериитом, еще одним гранулематозом. синдром васкулита. В параллельных исследованиях гистологически нормальных височных артерий у пациентов с ревматической полимиалгией была обнаружена мРНК для IL-1, TNF-α, IL-6 и IL-2, но образцы тканей не содержали последовательности IFN-γ, что позволяет предположить, что IFN-γ может быть вовлечен в развитие явного артериита.
Недавние данные Ludviksson et al предоставили наиболее убедительные на сегодняшний день доказательства того, что Т-клетки, связанные с гранулематозным воспалением WG, смещены в сторону цитокинового паттерна Th2.68 Исследования лимфоцитов периферической крови у пациентов с активными WG показали, что CD4 + Т-клетки продуцировали в 10–20 раз более высокие уровни IFN-γ и значительно больше TNF-α, чем CD4 + T-клетки из нормального контроля. Напротив, не было разницы в уровне Th3-ассоциированных цитокинов (IL-4, IL-5 или IL-10), продуцируемых Т-клетками пациентов с WG, по сравнению с контрольными субъектами.Обнаружение того, что поражения WG связаны с Т-клетками, смещенными в сторону дифференцировки клеток Th2, подразумевает нарушение регуляции IL-12, первичного индуктора Т-клеток, продуцирующих IFN-γ. Хотя самые высокие уровни продукции IL-12 были получены с моноцитами от пациентов с активным заболеванием, Ludviksson et al наблюдали, что моноциты от пациентов с неактивным заболеванием также производили повышенное количество IL-12,68. Это предполагает увеличение продукции IL-12. не является вторичным эффектом воспалительного процесса, а, скорее, первичным признаком WG.
не является вторичным эффектом воспалительного процесса, а, скорее, первичным признаком WG.
На основании этих наблюдений было выдвинуто предположение, что воздействие на пациентов с WG экологических воздействий (таких как инфекции) и / или аутоантигенов вызывает чрезмерный ответ макрофагов на IL-12, ведущий к несбалансированной продукции цитокинов Th2. Такая аберрантная продукция TNF-α и INF-γ может инициировать и поддерживать гранулематозное воспалительное поражение сосудов, которое характеризует WG. На этот процесс может дополнительно влиять ANCA, который может усиливать активацию нейтрофилов, эндотелиальных клеток и моноцитов.Однако, как отмечалось ранее, поскольку значительная часть пациентов с WG является ANCA-отрицательной, существенная роль ANCA в этом процессе маловероятна. Эти результаты имеют потенциально важное значение для лечения WG. В частности, они предполагают, что подходы, которые подавляют путь Th2 и продукцию IL-12, могут остановить воспаление. Это подтверждается открытием, что добавление экзогенного IL-10 вызывает дозозависимую блокаду продукции INF-γ мононуклеарными клетками периферической крови пациентов с активным WG.68
Выводы
WG — это системный васкулит, который может быть связан со значительной заболеваемостью и смертностью в результате заболевания или его лечения. Многое остается неизвестным о факторах, которые инициируют и поддерживают воспалительный процесс WG, хотя в последние годы были достигнуты значительные успехи. По мере достижения дальнейшего понимания может стать возможным воздействовать на терапевтически важные элементы в патофизиологических механизмах, лежащих в основе WG, тем самым устраняя риски агентов, которые связаны с неселективной иммуносупрессией.Однако до этого времени лечение активного заболевания, угрожающего основным органам, цитотоксическим агентом в сочетании с глюкокортикоидами будет оставаться основным средством борьбы с заболеванием и продления выживаемости пациентов.
Гранулематоз с полиангиитом — AMBOSS
Последнее обновление: 16 октября 2020 г.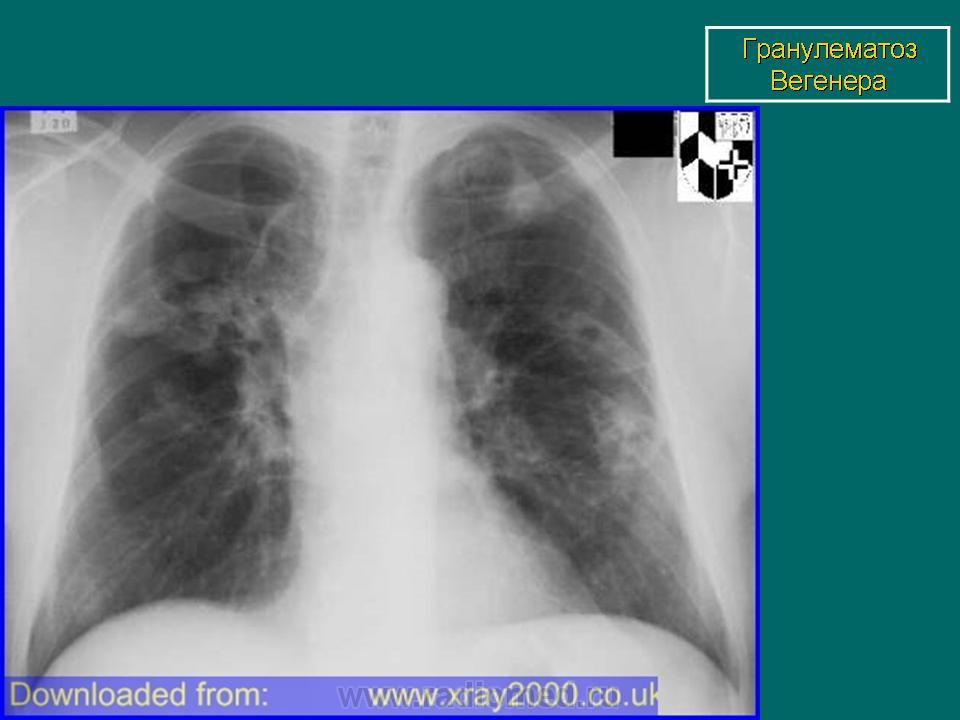
Резюме
Гранулематоз с полиангиитом (GPA, ранее известный как гранулематоз Вегенера) — это системный васкулит, поражающий сосуды малого и среднего размера.Пациенты обычно изначально страдают от ограниченной формы, которая может состоять из конституциональных симптомов и локализованных проявлений, таких как хронический синусит, ринит, средний отит, состояния глаз и / или поражения кожи. На более поздних стадиях могут возникнуть более серьезные проявления, включая легочные осложнения и гломерулонефрит, хотя также могут быть поражены кожа, глаза и сердце. Диагноз ставится на основании лабораторных исследований (положительный результат на PR3-ANCA / c-ANCA), визуализации и биопсии пораженных органов, которые демонстрируют некротическое гранулематозное воспаление.ГПА лечат иммунодепрессантами, обычно состоящими из глюкокортикоидов в сочетании с метотрексатом, циклофосфамидом или ритуксимабом. Рецидивы часты.
Эпидемиология
Эпидемиологические данные относятся к США, если не указано иное.
Этиология
Патофизиология
Клинические особенности
- Конституциональные симптомы: лихорадка; , ночная потливость, похудание, артралгии
- Поражение ЛОР: часто первое клиническое проявление
- Нижние дыхательные пути: потенциально опасны для жизни
- Поражение почек: потенциально опасно для жизни
- Поражения кожи
- Поражение глаз
- Поражение сердца: потенциально опасное для жизни
Проявления со стороны верхних дыхательных путей (i.е., гнойные, иногда кровянистые выделения, хронические инфекции носоглотки, седловидная деформация носа) являются наиболее частыми основными жалобами.
Триада GPA: некротический васкулит мелких артерий, проявления верхних / нижних дыхательных путей и гломерулонефрит.
Диагностика
- Лабораторный анализ
- Визуализация: рентгенография грудной клетки / КТ показывают множественные двусторонние кавитирующие узелковые поражения.

- Патология
- Диагноз должен подтверждаться биопсией пораженной ткани.
- Обычно показана классическая триада:
Для подтверждения диагноза необходима биопсия.
Дифференциальные диагнозы
Перечисленные здесь дифференциальные диагнозы не являются исчерпывающими.
Лечение
Прогноз
- Без адекватного лечения 1-летняя выживаемость составляет. [16]
- 5-летняя выживаемость при адекватном лечении составляет ок. 80%. [17]
Ссылки
Пейс C, Presicce M, Lamacchia F, Ferrari D, Sergiacomi G.Возникновение гранулематоза с полиангиитом, скрытым пороком сердца, у пожилого мужчины. Клинические случаи по радиологии . 2020; 15
(1): с.54-58.
DOI: 10.1016 / j.radcr.2019.09.037. | Открыть в режиме чтения QxMDPanupattanapong S, Stwalley DL, White AJ, Olsen MA, French AR, Hartman ME. Эпидемиология и исходы гранулематоза с полиангиитом у детей и взрослого населения трудоспособного возраста в Соединенных Штатах: анализ большой национальной базы данных заявлений.. Артрит и ревматология (Хобокен, Нью-Джерси) . 2018; 70
(12): с.2067-2076.
DOI: 10.1002 / art.40577. | Открыть в режиме чтения QxMDде Линд ван Вейнгаарден Р.А., ван Рейн Л., Хаген ЕС и др. Гипотезы об этиологии васкулита, ассоциированного с антинейтрофильными цитоплазматическими аутоантителами: причина скрыта, но известен результат .. Clin J Am Soc Nephrol . 2008; 3
(1): с.237-52.
DOI: 10.2215 / CJN.03550807. | Открыть в режиме чтения QxMD- Гранулематоз Вегенера. https://radiopaedia.org/articles/granulomatosis-with-polyangiitis .
Обновлено: 13 апреля 2017 г.
Доступ: 13 апреля 2017 г. Хира Р., Чоудхари К., Бина В.Т., Саймон Р. Клубничный гингивит: диагностический признак гранулематоза десен Вегенера !. Стоматологический исследовательский журнал . 2012; 9
(Приложение 1): стр. S123-6.Сун И.Й., Ким Ю.М., Чо Ю.К., Сон Дж. Х. Роль десневых проявлений в диагностике гранулематоза с полиангиитом (гранулематоз Вегенера).. Журнал пародонта и имплантологии . 2015; 45
(6): с.247-51.
DOI: 10.5051 / jpis.2015.45.6.247. | Открыть в режиме чтения QxMDКасим А., Патель Дж. ANCA-позитивный васкулит (ANCA-позитивный ангит). StatPearls . 2020 г.
.Уолш М., Меркель П.А., Пех К.А. и др. Плазмообмен и глюкокортикоиды при тяжелом ANCA-ассоциированном васкулите .. N Engl J Med . 2020; 382
(7): стр.622-631.
DOI: 10.1056 / NEJMoa1803537. | Открыть в режиме чтения QxMDМилославский Е.М., Найлс Дж. Л., Уоллес З. С. и др. Сокращение продолжительности приема глюкокортикоидов при ANCA-ассоциированном васкулите: пилотное исследование .. Semin Arthritis Rheum . 2018; 48
(2): с.288-292.
DOI: 10.1016 / j.semarthrit.2018.01.013. | Открыть в режиме чтения QxMDЧарльз П., Перродо Э, Самсон М. и др. Долгосрочное использование ритуксимаба для поддержания ремиссии антинейтрофильного цитоплазматического васкулита: рандомизированное исследование.. Ann Intern Med . 2020; 173
(3): с.179-187.
DOI: 10.7326 / M19-3827. | Открыть в режиме чтения QxMDPagnoux C, Mahr A, Hamidou MA, et al. Азатиоприн или метотрексат для лечения ANCA-ассоциированного васкулита. N Engl J Med . 2008; 359
(26): с.2790-803.
DOI: 10.1056 / NEJMoa0802311. | Открыть в режиме чтения QxMDКубаиси Б.