Наркоз с назотрахеальной интубацией
В 90% случаев у переболевших covid выявляют остаточные явления изменения легких. Наиболее распространен фиброз, когда в легких появляется рубцовая ткань и нарушается насыщение крови кислородом. При ковид-инфекции также могут поражаться почки, печень, желудочно-кишечный тракт, сердце.
Распространенные последствия
Поражение легких:
- одышка при физической нагрузке
-
кашель -
повышенная температура тела в пределах 37.0° — 37.5° продолжительное время
Повышенное тромбообразование:
опасное для жизни состояние, в результате образования тромбов может развиваться инсульт, инфаркт миокарда или тромбоэмболия.
Заболевания сердца:
нарушения ритма, воспаление миокарда, проявляющимися тяжестью в области сердца, перебоями в работе сердца.
Заболевание почек:
нарушение выделительной функции, развитие почечной недостаточности.
Расстройство нервной системы:
головная боль, нарушение зрения, рассеянность, снижение памяти, снижение концентрации внимания, нарушение сна, чувство страха, депрессия.
Расстройство желудочно-кишечного тракта:
боли в животе, тяжесть в правом подреберье, тошнота, нарушение пищеварения.
Слабость и боль в мышцах
Мужское бесплодие
Консультация врачом пульмонологом
- Исследование функции внешнего дыхания (ФВД)
-
Лабораторную диагностику -
Пульсоксиметрия
Программа реабилитации после Ковид-19
Программа может корректироваться и дополняться лечащим врачом с учетом состояния пациента и особенности перенесенного заболевания.
Индивидуальный подбор лекарственных препаратов
Дыхательная гимнастика
Позволяет улучшить вентиляцию лёгких и насыщения крови кислородом. Регулярное выполнение упражнений увеличивает объём лёгких.
Регулярное выполнение упражнений увеличивает объём лёгких.
ВЛОК (внутривенное лазерное облучение крови)
Оздоровление организма при помощи действия световой энергии на кровь непосредственно в самих сосудах. Процедура проводится с помощью аппарата — АЛТ «Матрикс-ВЛОК». Сеанс длится 15-20 мин. Помогает улучшить свойства крови, повысить иммунитет, снизить отёчность, снабдить органы кислородом, восстановить обмен веществ.
Ингаляции
Лечение, основанное на вдыхании паров необходимых лекарств через небулайзер в дыхательные пути. Местный эффект от использования ингалятора наступает моментально.
Лечебный массаж
Нормализует работу дыхательной системы. Массирующие движения обеспечивают повышение интенсивности кровоснабжения и проходимости бронхов.
Рефлексотерапия
Лечебный способ воздействия на определённые акупунктурные точки организма при помощи специальных игл. Активизирует и восстанавливает внутренние природные силы организма человека.
Комплексная реабилитация позволит полностью восстановиться
- Уменьшить очаги воспаления в кратчайшие сроки;
-
Улучшить вентиляцию легких; -
Нормализовать поступления кислорода в организм; -
Устранить обструкцию бронхов; -
Предотвратить формирование фиброзной ткани, как основной причины развития дыхательной недостаточности после пневмонии.
Реабилитация необходима абсолютно всем пациентам, перенесшим коронавирусную инфекцию, пневмонию и ОРВИ, для восстановления и сохранения качества жизни!
Программу ведут
Снятие с искусственной вентиляции легких с использованием поддержки давлением или Т-образной трубки для попытки самостоятельного дыхания
Пациентам с тяжелым заболеванием легких, например, с острой дыхательной недостаточностью, может потребоваться инвазивная искусственная вентиляция легких через эндотрахеальную трубку или трахеостому до тех пор, пока их основное заболевание не будет либо вылечено, либо стабилизировано. Однако, как ранняя приостановка, так и задержка в снятии с искусственной вентиляции легких (ИВЛ), может привести к осложнениям, которые могут отсрочить снятие пациентов с ИВЛ и увеличить длительность пребывания в отделении интенсивной терапии (ОИТ) и больнице. Предыдущие исследования и систематические обзоры позволяют предположить, что следует внедрить протокол снятия с ИВЛ для того, чтобы проводить ежедневную оценку пациентов, которые могут быть готовы к снятию с ИВЛ. Способность к спонтанному дыханию можно оценить с помощью теста спонтанного дыхания с использованием Т-образной трубки (Т-образный разветвитель) или с помощью уменьшения давления, создаваемого в дыхательных путях, чтобы обеспечить низкие уровни поддержки давлением (ПД) (от 5 до 10 см Н)2О) После удаления эндотрахеальной трубки (экстубации) пациентов наблюдают и мониторируют в течение 48 часов. Если в течение этого периода не потребуется возобновления вентиляционной поддержки, считается, что снятие с ИВЛ прошло успешно. Для этого Кокрейновского систематического обзора мы провели поиск в базах данных медицинской литературы по июнь 2012 года и включили девять исследований с участием 1208 взрослых пациентов, которые находились на инвазивной искусственной вентиляции в течение, по меньшей мере, 24 часов. В этих испытаниях сравнивали поддержку давлением (ПД) и использование Т-образной трубки (622 пациента рандомизированы на применение ПД и 586 рандомизированы на использование Т-образной трубки). Не было четких доказательств, чтобы подтвердить, что ПД превосходила применение Т-образной трубки в отношении успешности снятия (отлучения) с ИВЛ, необходимости повторной интубации, смертности в ОИТ и других факторов, включая длительность пребывания в отделении долгосрочного отлучения, пневмонию и индекс быстрого поверхностного дыхания. У большего числа пациентов, которые получали ПД, тест спонтанного дыхания был успешным и дыхательная трубка была удалена. В отношении таких исходов, как частота дыхания и дыхательный объем, применение ПД превосходило использование Т-образной трубки в двух испытаниях.
Однако, как ранняя приостановка, так и задержка в снятии с искусственной вентиляции легких (ИВЛ), может привести к осложнениям, которые могут отсрочить снятие пациентов с ИВЛ и увеличить длительность пребывания в отделении интенсивной терапии (ОИТ) и больнице. Предыдущие исследования и систематические обзоры позволяют предположить, что следует внедрить протокол снятия с ИВЛ для того, чтобы проводить ежедневную оценку пациентов, которые могут быть готовы к снятию с ИВЛ. Способность к спонтанному дыханию можно оценить с помощью теста спонтанного дыхания с использованием Т-образной трубки (Т-образный разветвитель) или с помощью уменьшения давления, создаваемого в дыхательных путях, чтобы обеспечить низкие уровни поддержки давлением (ПД) (от 5 до 10 см Н)2О) После удаления эндотрахеальной трубки (экстубации) пациентов наблюдают и мониторируют в течение 48 часов. Если в течение этого периода не потребуется возобновления вентиляционной поддержки, считается, что снятие с ИВЛ прошло успешно. Для этого Кокрейновского систематического обзора мы провели поиск в базах данных медицинской литературы по июнь 2012 года и включили девять исследований с участием 1208 взрослых пациентов, которые находились на инвазивной искусственной вентиляции в течение, по меньшей мере, 24 часов. В этих испытаниях сравнивали поддержку давлением (ПД) и использование Т-образной трубки (622 пациента рандомизированы на применение ПД и 586 рандомизированы на использование Т-образной трубки). Не было четких доказательств, чтобы подтвердить, что ПД превосходила применение Т-образной трубки в отношении успешности снятия (отлучения) с ИВЛ, необходимости повторной интубации, смертности в ОИТ и других факторов, включая длительность пребывания в отделении долгосрочного отлучения, пневмонию и индекс быстрого поверхностного дыхания. У большего числа пациентов, которые получали ПД, тест спонтанного дыхания был успешным и дыхательная трубка была удалена. В отношении таких исходов, как частота дыхания и дыхательный объем, применение ПД превосходило использование Т-образной трубки в двух испытаниях. В трех исследованиях сообщили, что длительность снятия с ИВЛ была короче во время применения ПД, и в одном исследовании, в котором пациентам устанавливали Т-образную трубку, время снятия было короче. Из-за ограничений в дизайне исследований и неточности в оценках эффектов мы оценили качество доказательств как низкое. Мы провели повторный поиск в декабре 2013 года. Мы будем работать с любыми исследованиями, представляющими интерес, при обновлении обзора.
В трех исследованиях сообщили, что длительность снятия с ИВЛ была короче во время применения ПД, и в одном исследовании, в котором пациентам устанавливали Т-образную трубку, время снятия было короче. Из-за ограничений в дизайне исследований и неточности в оценках эффектов мы оценили качество доказательств как низкое. Мы провели повторный поиск в декабре 2013 года. Мы будем работать с любыми исследованиями, представляющими интерес, при обновлении обзора.
Режимы вентиляции в анестезиологической практике Текст научной статьи по специальности «Медицинские технологии»
УДК 616-089.5:612.216.2 А.В. Вабищевич
РЕЖИМЫ ВЕНТИЛЯЦИИ В АНЕСТЕЗИОЛОГИЧЕСКОЙ ПРАКТИКЕ
Российский научный центр хирургии РАМН (Москва)
Ключевые слова: искусственная вентиляция легких, наркозно-дыхательная аппаратура.
В настоящее время анестезиолог может располагать достаточно большим арсеналом наркозно-ды-хательных аппаратов, способных обеспечить различные варианты вентиляции как во время операции, так и в послеоперационном периоде. Создано много модификаций дыхательных контуров, с помощью которых можно осуществлять вентиляционную поддержку сообразно тяжести состояния больного, состояние его респираторной функции. Ведущие фирмы-производители наркозно-дыхательной аппаратуры предлагают большое количество аппаратов, которые различаются по целевому назначению, сложности, эффективности, удобству использования. Достаточно широкий выбор позволяет рационально обеспечить современную операционную аппаратурой той степени сложности, которая могла бы соответствовать уровню анестезиологического обеспечения, сложности и травматичности проводимых операций.
В связи с этим представляется целесообразным рассмотреть основные вопросы, касающиеся возможных вариантов интраоперационной вентиляции, показаний к их использованию, а также определить оборудование, которое необходимо в том или ином клиническом случае.
Дыхательные контуры
Основной задачей наркозной аппаратуры любой степени сложности является обеспечение дыхательной функции организма, т.е. эффективного газообмена в условиях самостоятельного или искусственного дыхания пациента. Дыхательный контур обеспечивает подачу кислорода и анестетиков от наркозного аппарата в дыхательные пути (легкие) больного и выведение из них выдыхаемой смеси. Различают два основных типа дыхательных контуров: с реверсией и без реверсии газовой смеси. Под реверсией понимается полное или частичное повторное вдыхание пациентом той газонаркотической смеси, которая уже была выдохнута [2, 5, 6].
Наиболее простыми являются нереверсивные системы, которые не используют выдыхаемую смесь повторно и работа которых зависит от уровня потока свежего газа. Несколько вариантов подобных систем (Jackson-Rees, Bain) описаны Mapelson и до сих пор
используются в некоторых областях анестезиологии, например в педиатрии. Однако для предотвращения накопления СО2 в контуре требуется поток свежего газа, превышающего минутную вентиляцию минимум в два раза [10]. В зависимости от того, что является резервуаром газов — атмосфера, дыхательный мешок или баллон наркозного аппарата, — контур можно назвать открытым или полуоткрытым. В любом варианте выдыхаемый газ полностью уходит в атмосферу. Аппарат обеспечивает подачу смеси с высоким содержанием кислорода и возможность использования ингаляционных анестетиков. Преимуществом подобных систем является их небольшая масса и легкость в работе. К недостаткам можно отнести избыточный расход кислорода и анестетиков, загрязнение атмосферы операционной, большие потери тепла и влаги [6, 13].
Основными компонентами реверсивной, или циркуляционной системы являются емкости или магистрали доставки свежего газа, однонаправленные клапаны вдоха и выдоха, приводящие и отводящие гофрированные шланги, Y-образный коннектор, клапан сброса, резервуарный мешок и емкость с абсорбентом СО2. Нереверсивные клапаны направляют циркуляцию газового потока только в одном направлении и через абсорбер. Подобная полузакрытая система может стать практически закрытой при условии, что поток свежего газа равен объему газов, потребляемых пациентом (250-300 мл кислорода в минуту плюс поглощение ингаляционных анестетиков). Мертвое пространство в подобной системе составляет лишь объем в эндотрахеальной трубке и соединении с Y-образным коннектором. Очевидно, что на современном наркозном аппарате при необходимости возможно проведение вентиляции и по закрытому, и по полуоткрытому контуру, что весьма важно при адаптации больного к самостоятельному дыханию после искусственной вентиляции легких (ИВЛ) [4, 13].
Нереверсивные клапаны направляют циркуляцию газового потока только в одном направлении и через абсорбер. Подобная полузакрытая система может стать практически закрытой при условии, что поток свежего газа равен объему газов, потребляемых пациентом (250-300 мл кислорода в минуту плюс поглощение ингаляционных анестетиков). Мертвое пространство в подобной системе составляет лишь объем в эндотрахеальной трубке и соединении с Y-образным коннектором. Очевидно, что на современном наркозном аппарате при необходимости возможно проведение вентиляции и по закрытому, и по полуоткрытому контуру, что весьма важно при адаптации больного к самостоятельному дыханию после искусственной вентиляции легких (ИВЛ) [4, 13].
Аппараты ИВЛ
Оставляя за скобками достаточно редко использующиеся ныне аппараты «железные легкие», кирасно-го типа, искусственного смещения диафрагмы, элек-трофренические и т.д., следует отметить, что основным видом наркозных аппаратов стали модели, работающие на принципе вдувания в легкие газовой смеси под положительным давлением. Эти респираторы можно разделить на несколько групп в зависимости от характера переключения с вдоха на выдох. К ним относятся прессоциклические аппараты, в которых фаза вдоха заканчивается при достижении заданного давления в дыхательных путях. Слабым местом подобных аппаратов, как правило, является возможность утечки и снижения дыхательного объема — переключения на выдох может не произойти до достижения заданной величины давления, и респиратор может неопределенно долго находиться в фазе вдоха. Следующим типом являются частотные аппараты,
в которых задана определенная продолжительность вдоха и выдоха. В них дыхательный объем и пиковое давление на вдохе зависят от растяжимости легких. Дыхательный объем будет зависеть от заданной продолжительности вдоха и скорости инспираторного потока. В респираторах с переключением по объему продолжительность фазы вдоха и давление в дыхательных путях колеблются в зависимости от достижения заданного объема (при этом фактором безопасности может служить параллельно существующее ограничение по давлению) [3, 5].
Во время вдоха респираторы генерируют дыхательный объем, подавая поток газа по градиенту давления. Во время всего дыхательного цикла вне зависимости от механических свойств легких в дыхательном контуре сохраняется либо постоянное давление (генераторы постоянного давления), либо постоянная скорость потока (генераторы постоянного потока). Эти генераторы характеризуются непостоянным давлением и потоком на протяжении одного цикла, но характер их изменений постоянно повторяется в каждом цикле.
Подобные аппараты могут работать как от электрического привода, так и от сжатого газа. В качестве движущего газа принято использовать кислород, чтобы при нарушении герметичности меха была исключена опасность гипоксии.
Степень безопасности зависит от оснащенности наркозных аппаратов системами сигнализации и тревоги, реагирующими на разгерметизацию, снижение пикового давления в контуре либо, наоборот, на чрезмерное повышение давления в дыхательных путях, изменение давления в кислородной магистрали.
Режимы вентиляции
Выбор метода и режима вентиляции определяется конкретной клинической ситуацией, характером патологии, видом хирургического вмешательства, планируемой продолжительностью операции, общим состоянием больного и состоянием его дыхательной системы. Различные виды анестезии могут проводиться с сохраненным самостоятельным дыханием, с вентиляционной поддержкой через маску, разнообразные воздуховоды (ларингеальную маску и пр.). Естественными ограничениями применимости самостоятельного дыхания являются седация или внутривенная анестезия, глубина которой вызывает угнетение дыхания и продолжительность операции. В любом случае определяющими становятся фармакологические эффекты анестетиков, гипнотиков, седативных препаратов, которые имеют тенденцию к кумуляции и рано или поздно могут вызвать депрессию самостоятельного дыхания.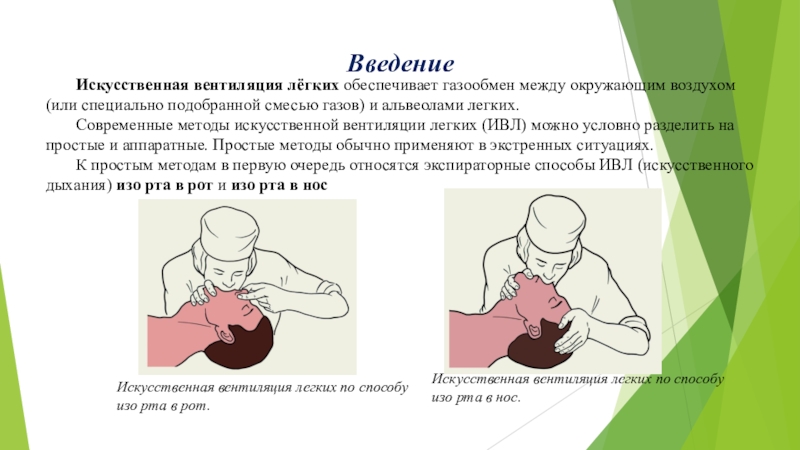 Поэтому даже надежные методы проводниковой анестезии (эпиду-ральная, спинальная, блокады верхних и нижних конечностей) могут потребовать проведения ИВЛ при длительных многочасовых операциях [8, 12].
Поэтому даже надежные методы проводниковой анестезии (эпиду-ральная, спинальная, блокады верхних и нижних конечностей) могут потребовать проведения ИВЛ при длительных многочасовых операциях [8, 12].
В большинстве случаев при неосложненных клинических ситуациях для поддержания адекватного
газообмена достаточно ИВЛ в режиме, близком к физиологическому дыханию, т.е. частота дыханий, дыхательный объем, минутный объем вентиляции, продолжительность вдоха и выдоха подбираются в зависимости от возрастной нормы и веса больного. Большинство плановых и экстренных операций успешно проводятся в условиях ИВЛ с мышечными в режиме нормовентиляции с перемежающимся положительным давлением. В плановой хирургии исходными данными, на которые может ориентироваться анестезиолог, определяющий интраоперационные параметры вентиляции, являются показатели функции внешнего дыхания, обычно определяемые в ходе предоперационного обследования. Данные спирограммы определяют основные легочные объемы и емкости (дыхательный, минутный, резервный, функциональную остаточную емкость, емкость вдоха, жизненную емкость и т.д.). Определяется наличие и характер нарушений дыхательной функции легких (обструктив-ный, рестриктивный, смешанный). Исходя из полученных данных, анестезиолог подбирает начальные параметры вентиляции и уже в процессе анестезии, ориентируясь на данные газоанализатора (сатурация, оксиметрия, капнометрия), вентилометрии и лабораторные экспресс-показатели газообмена по пробам крови, определяет оптимальные параметры вентиляции. Факторами, о которых анестезиологу необходимо помнить даже при самом благоприятном течении операции и анестезии, являются изменение характера (активности, глубины, частоты) дыхания под влиянием анестезии и при переводе больного в горизонтальное положение, увеличение мертвого пространства, перераспределение регионарного легочного кровотока, возможность увеличения внутрилегочного шунта, депрессивное влияние анестезии на функциональную остаточную емкость легких и т. д.
д.
Ряд клинических ситуаций, прежде всего связанных с патологией легких, наличием легочной, легоч-но-сердечной недостаточности, травматическими нарушениями, развитием шока различного генеза, отека легких, может сопровождаться развитием ги-поксемии. В этих случаях может оказаться необходимым повышение внутрилегочного давления, которое позволяет повысить растяжимость легких и нивелировать вентиляционно-перфузионные нарушения, уменьшить фракцию внутрилегочного шунтирования и повысить оксигенацию артериальной крови. Во время операции использование положительного давления в конце выдоха возможно только через герметичную интубационную эндотрахеальную трубку. С помощью лицевой маски трудно добиться необходимой степени герметичности. С другой стороны, под плотно прижатой лицевой маской избыточное давление повышает риск нагнетания газа в желудок и регургитации. В меньшей степени это относится к различным типам ларингеальных маскок, хотя и они не полностью исключают возможность попадания газа в желудок.
При некоторых клинических ситуациях, связанных прежде всего с легочной патологией, возможности традиционной ИВЛ оказываются ограниченными и не всегда могут обеспечить адекватный газообмен. При эндоларингеальных вмешательствах, ларинго-бронхоскопии у больных с бронхоплевральными свищами при необходимости проведения однолегочной вентиляции целесообразным оказывается использование методов высокочастотной вентиляции легких [11]. Наиболее распространенными являются методы струйной высокочастотной вентиляции: чрескатетер-ная и инжекционная. В настоящее время существуют различные методики с использованием специальных эндотрахеальных трубок, в которых есть каналы для высокочастотной ИВЛ, специальные катетеры для чрескожной чрестрахеальной струйной высокочастотной вентиляции. Метод имеет свою нишу в клинической анестезиологии, хотя, несомненно, требует определенного опыта использования, ограничен по продолжительности использования и должен применяться в негерметичном контуре.
Внедрение современных высокотехнологичных наркозных аппаратов позволило широко применять весьма перспективный метод низкопоточной анестезии. В соответствии с общепринятой классификацией, основанной на величине объемной скорости суммарного потока свежих газов, подаваемых из газовой магистрали, баллонов или иных резервуаров в наркозный аппарат, принято различать следующие контуры: высокопоточный — больше 6 л/мин., среднепоточный — более 3 л/мин., низкопоточный (low-flow) — более 1 л/мин., минимальный (minimal-flow) — 0,4-1 л/мин., закрытый контур — поток свежего газа равен его поглощению больным [14]. Конструкция современных наркозных аппаратов и испарителей ингаляционных анестетиков обеспечивает поддержание постоянной фармакологически активной концентрации анестетика в дыхательном контуре, альвеолярном объеме при снижении подачи свежего газа до минимально возможной объемной скорости (0,3-0,5 л/мин.). Естественным стремлением анестезиолога является снижение расхода препаратов во время анестезии и поиск методов, которые могли бы обеспечить подобный подход. Использование современных ингаляционных анестетиков в низкопоточном контуре наркозного аппарата позволяет существенно снизить расход ингаляционного анестетика, надежно обеспечивая адекватную анестезию, поддержание ИВЛ и газообмена [2, 9, 13].
Режимы вспомогательного дыхания — вспомогательно-принудительная ИВЛ (Assist-Control Ventilation), перемежающаяся принудительная ИВЛ (Intermittent Mandatory Ventilation — IMV) интра-операционно могут использоваться на заключительных этапах анестезии при адаптации пациента к самостоятельному дыханию. В режиме вспомогательно-принудительной ИВЛ датчик давления в дыхательном контуре позволяет использовать попытку
самостоятельного вдоха для запуска поддерживающего движения аппарата на вдох. Настроенный на минимальную фиксированную частоту дыхания при заданной величине разряжения, аппарат ИВЛ запускает функцию вдоха при каждой попытке самостоятельного дыхания. Режим перемежающейся принудительной ИВЛ предусматривает возможность самостоятельного дыхания. Основным физиологическим преимуществом этого режима вентиляции является снижение среднего давления в дыхательных путях. Помимо возможности самостоятельно дышать через аппарат ИВЛ, на нем можно установить определенное количество принудительных вдохов. Этим задается минимально гарантированный дыхательный объем. При высокой заданной частоте аппаратных вдохов (10-12 в мин.) наркозный аппарат обеспечит практически весь минутный объем дыхания. При малой частоте заданных вдохов (2-4 в мин.) аппарат осуществляет минимум респираторной поддержки. При синхронизированной перемежающейся принудительной ИВЛ (SIMV) аппаратный вдох по возможности совпадает с началом самостоятельного вдоха. Использование этих методов позволяет надежно и безопасно пройти период восстановления самостоятельного дыхания [1, 13].
Режим перемежающейся принудительной ИВЛ предусматривает возможность самостоятельного дыхания. Основным физиологическим преимуществом этого режима вентиляции является снижение среднего давления в дыхательных путях. Помимо возможности самостоятельно дышать через аппарат ИВЛ, на нем можно установить определенное количество принудительных вдохов. Этим задается минимально гарантированный дыхательный объем. При высокой заданной частоте аппаратных вдохов (10-12 в мин.) наркозный аппарат обеспечит практически весь минутный объем дыхания. При малой частоте заданных вдохов (2-4 в мин.) аппарат осуществляет минимум респираторной поддержки. При синхронизированной перемежающейся принудительной ИВЛ (SIMV) аппаратный вдох по возможности совпадает с началом самостоятельного вдоха. Использование этих методов позволяет надежно и безопасно пройти период восстановления самостоятельного дыхания [1, 13].
Большинство современных наркозно-дыхатель-ных аппаратов, как правило, имеют ограниченные возможности использования указанных выше режимов вентиляции. Как уже было сказано, во время анестезии, даже весьма продолжительной, наибольшее применение получил метод принудительной объемной ИВЛ. Определенное место занимают методы высокочастотной вентиляции, методы раздельной и однолегочной вентиляции легких, ряд операций можно выполнять в условиях проводниковой анестезии с сохраненным самостоятельным дыханием. Более сложные респираторы с расширенными возможностями проведения ИВЛ с поддерживающим давлением (Pressure Support), с управлением по давлению (Pressure Control) и т.д. используются в отделениях реанимации и интенсивной терапии при лечении тяжелых нарушений системы дыхания.
В заключение следует отметить важность и необходимость наличия постоянного информативного мониторинга при проведении ИВЛ. Минимально необходимая информация может быть обеспечена при наличии данных пульсооксиметрии, электрокардиографии, газометрии в дыхательном контуре на вдохе и выдохе (О2, СО2, ингаляционные анестетики).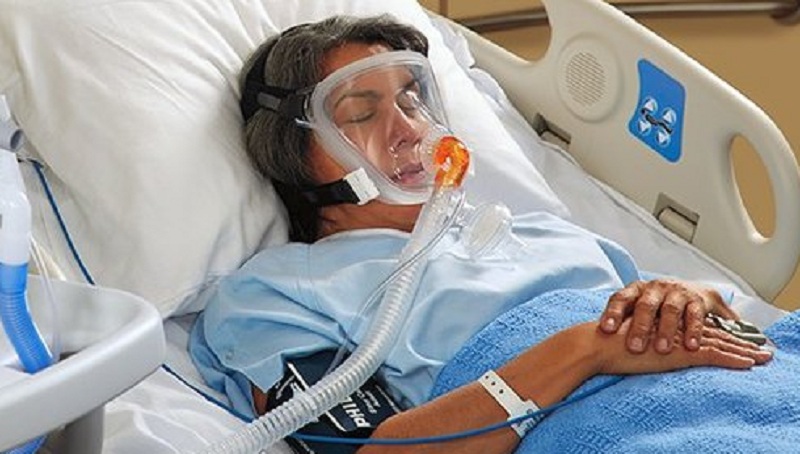 Периодически должен осуществляться контроль окси-генации крови (артерия, вена). Безопасность пациента может быть гарантирована только при наличии тщательного мониторинга давления в дыхательных путях (пикового, плато, среднего). При этом можно выявить нарушения герметичности дыхательного контура, неправильное положение, обтурацию эндо-трахеальной трубки и другие проблемы, связанные с вентиляцией пациента.
Периодически должен осуществляться контроль окси-генации крови (артерия, вена). Безопасность пациента может быть гарантирована только при наличии тщательного мониторинга давления в дыхательных путях (пикового, плато, среднего). При этом можно выявить нарушения герметичности дыхательного контура, неправильное положение, обтурацию эндо-трахеальной трубки и другие проблемы, связанные с вентиляцией пациента.
Литература
1. Андроге Г.Д., Тобин М.Д. Дыхательная недостаточность. — М.: Медицина, 2003.
2. Бараш П., Куллен Б., Стэлтинг Р. Клиническая анестезиология. — М. : Медицинская литература, 2004.
3. Бунятян А.А. Руководство по анестезиологии. — М.: Медицина, 1994.
4. Бунятян А.А., Вабищевич А.В., Светлов В.А., Козлов С.П. // Итоги. Результаты научных исследований по программной тематике — М. : РНЦХ РАМН. — 1998. — С. 93-106.
5. Бунятян А.А., Рябов Г.А., Маневич А.З. Анестезиология и реаниматология. — М.: Медицина, 1977.
6. Вабищевич А.В., Кожевников В.А., Титов В.А. и др. // Анестезиология и реаниматология. — 2000. — № 5. — С. 11-13.
7. Габа Д.М., Фиш К.Дж, Хауард С.К. Критические ситуации в анестезиологии. — М. : Медицина, 2000.
8. Зильбер А.П. Респираторная медицина. — Изд-во Петрозаводского гос. ун-та, 1996.
9. Зильбер А.П. ИВЛ при острой дыхательной недостаточности. — М.: Медицина, 1978.
10. Зильбер А.П., Шурыгин И.А. Высокочастотная вентиляция легких. — Изд-во Петрозаводского гос. унта, 1993.
УДК 576.311.336:519.2
А.В. Юркевич, Г.И. Оскольский, Ю.Ю. Первов
МОРФОЛОГИЧЕСКИЕ И МОЛЕКУЛЯРНО-ГЕНЕТИЧЕСКИЕ АСПЕКТЫ ЯДРЫШКОВОГО ОРГАНИЗАТОРА РИБОСОМ
Дальневосточный государственный медицинский университет (г. Хабаровск)
Ключевые слова: морфометрия, новые подходы.
Описательный характер морфологических исследований не во всех случаях бывает достаточен для углубленного анализа явлений, обобщений изучаемых процессов, оценки наблюдаемых изменений. В этой связи традиционные методы регистрации морфологических изменений, оставаясь базовыми, должны дополняться количественным анализом. Выявление ведущих диагностических признаков, меняющейся их величины и частоты их проявления и динамического характера связей между ними — основная задача количественной патологической морфологии [1]. Объектом морфометрических исследований в морфологии обычно являются клетки, ядра, ядрышки, клеточные органеллы. Нередко объектом морфометрического исследования становятся нервные волокна, кровеносные капилляры [3].
Успех морфометрического исследования во многом определяется наличием соответствующей изме-
11. Кассиль В.Л., Лескин Г.С., Хаппий Х.Х. Высокочастотная вентиляция легких. — М. : Биоарт, 1993.
12. Клиническая анестезиология: Справочник / пер. с англ. под ред. В.А. Гологорского, В.В. Яснецова. — М. : ГЭОТАР-МЕД, 2001.
13. Морган Д.Э., Мэгид С.М. Клиническая анестезиология. — М. : Бином, 2000.
14. Эрдман В. // Актуальные проблемы анестезиологии и реаниматологии. — Архангельск-Тромсе, 1995. — С. 108-113.
— Архангельск-Тромсе, 1995. — С. 108-113.
Поступила в редакцию 28.12.04.
MODES OF VENTILATION IN ANAESTHESIOLOGICAL PRACTICE A.V. Vabichtchevich
Russian Research Center of Surgery RAMS (Moscow) Summary — Intraoperating support of ventilation is carried out in various modes — at the kept independent breath, with the help of artificial ventilation easy (IPPV) and various variants of auxiliary ventilation. The basic method of carrying out of ventilation is compulsory volumetric ventilation with positive pressure with a high, small and low stream gas mixes. There are rather useful methods of high-frequency ventilation at carrying out of complex lungs operations. Modern requirements to safety of anesthesia and adequate ventilating support demand constant informative monitoring.
Pacific Medical Journal, 2005, No. 1, p. 82-85.
рительной аппаратуры. Долгое время на вооружении морфологов были в основном разнообразные окулярные вставки, изготовленные промышленным или кустарным способами, окулярмикрометры. Новый этап в медицинской морфометрии начался с появлением доступных компьютерных анализаторов изображений. Первое их поколение появилось в 1965 г. В 80-х годах ХХ века появилось третье поколение систем: IBAS (1982), «Ситико» (1984), «Роботрон» (1986), «Интеграл» (1987), «Макс-1000» (1990), «Ме-кос» (1996) [2, 4, 15].
Анализ изображения различных микроскопических объектов с помощью компьютерных программ положил начало компьютерной морфометрии, позволяющей проводить количественный анализ морфологии клеток и тканей с применением многомерной статистики, теории вероятности и информатики. В настоящее время одним из наиболее перспективных направлений в морфометрическом анализе является многопараметрическое описание объектов, выделение с помощью процедур факторного анализа главных компонент и математическое моделирование на основе дискриминантного анализа [1].
Используя указанные подходы, С.А. Степанову и др. [5] удалось с высокой достоверностью объективно дифференцировать ряд вариантов тиреоидной патологии с иммунными нарушениями. В.М. Погорелову и др. [4] с точностью порядка 60% удалось дифференцировать различные морфотипы ядер при неход-жкинских лимфомах. В.И. Цыганкову и др. [7] на основе процедур дискриминантного анализа удалось
Искусственная вентиляция легких при анестезии кошек и собак
Введение
Применение искусственной вентиляции, в анестезиологической практике кошек и собак, несколько отличается от таковой в гуманной медицине, методы поддержания дыхания используются значительно реже. При анестезии мелких домашних животных предпочтение отдается общей анестезии на спонтанном дыхании, но для использования искусственной вентиляции существуют четкие показания. Анестезисту приходится проводить вспомогательную или управляемую вентиляцию легких в течение всего периода анестезии, и он должен быть знаком с ее основами.
Цель искусственной (вспомогательной и управляемой) вентиляции – оптимизация обмена газов в легких (оксигенация крови) и обеспечение адекватного дыхания, без индукции повреждения легких и нарушения функции сердечнососудистой системы. В идеале, целью вентиляции явялется поддержание уровня углекислоты (PaCO2) крови между 35 и 50 мм рт.ст., и уровня кислорода (PaO2) более 80 мм рт.ст.
Вспомогательная вентиляция – обеспечение пациента под анестезией повышенным объемом дыхательной смеси на фоне сохраненного спонтанного дыхания животного. Управляемая (контролируемая) вентиляция – обеспечение пациента под анестезией повышенным объемом дыхательной смеси в отсутствии спонтанного дыхания животного. Любая процедура, при которой анестезист обеспечивает или контролирует доставку кислороды и анестетического газа к пациенту, именуется как вентиляция с положительным давлением (ВПД). Это может достигаться манипуляциями с дыхательным мешком (bagging) или использованием вентилятора, при этом, целью является получение пациентом адекватного количества кислорода, и обеспечение возможности выдоха адекватного количества углекислоты. Обычными показаниями к ИВЛ является неадекватность собственных дыхательных попыток для достижения цели.
Это может достигаться манипуляциями с дыхательным мешком (bagging) или использованием вентилятора, при этом, целью является получение пациентом адекватного количества кислорода, и обеспечение возможности выдоха адекватного количества углекислоты. Обычными показаниями к ИВЛ является неадекватность собственных дыхательных попыток для достижения цели.
Вентиляция у бодрствующих животных
Для лучшего понимания сути вентиляции с положительным давлением (ВПД), необходимо понимание механики нормального дыхания и вероятных причин его нарушения при анестезии. Процесс дыхания – физическое движение дыхательной смеси по воздухоносным путям до альвеол и обратно, при этом происходит поступление кислорода в кровь (оксигенация) и выделение из крови углекислоты. Дыхание или вентиляция состоит из двух частей: вдох (активная фаза) и выдох (пассивная фаза). Дыхание зависит от синхронного движения дыхательных мышц, регуляция которых осуществляется дыхательным центром, расположенным в продолговатом мозгу. Работу дыхательного центра определяет уровень углекислоты артериальной крови (PaСО2), при повышении уровня выше порога возбуждения (порядка 40 мм рт.ст.), дыхательный центр генерирует нервные импульсы, которые стимулируют межреберные и диафрагмальные мышцы, что сопровождается расширением грудной клетки.
Движения мышц на фазе вдоха создают отрицательное давление (легочной вакуум) внутри грудной полости, легкие расправляются и засасывают в себя дыхательную смесь (до уровня альвеол). При достижении легкими адекватного объема нервные импульсы посылают обратную связь в дыхательный центр, сигнализируя о необходимости остановки активной фазы дыхания (вдоха). Межреберные мышцы и диафрагма расслабляются, внешнее давление способствуют свободному спадению грудной клетки и легких (выдох). Сам выдох пассивен, что означает отсутствие активного движения мышц (исключение принудительный выдох в период повышенной активности). В период выдоха уровень углекислоты вновь начинает расти, и, после короткой паузы, дыхательный центр инициирует следующий вдох.
Далее приводятся средние физиологические параметры, которые характеризуют нормальное дыхание. В норме, фаза выдоха примерно в два раза длиннее фазы вдоха (соотношение 1:2). Дыхательный объем (ДО) определяет количество входящего в газа легкие за одного дыхание, в норме составляет 10-15 мл/кг, во многом зависит от глубины дыхания животного. Число дыхательных движений (ЧДД) – количество дыхательных циклов за одну минуту, у собак составляет 10-30 дыханий в минуту (подвержено сильным вариациям в зависимости от возбуждения), у кошек составляет 20-40 дыханий в минуту. Минутный объем дыхания (МОД) – количество воздуха движущегося через легкие за одну минуту, данный показатель может высчитываться по формуле – ДО х ЧДД.
Вентиляция у животных в анестезии
Вентиляция у животных при общей анестезии значительно отличается от вентиляции в сознании, основные различия включают следующее два фактора:
• Угнетение дыхательного центра препаратами для наркоза. Транквилизаторы и общие анестетики обычно снижают активность дыхательного центра, отмечается замедленный ответ на повышение уровня углекислоты в крови (повышение порога возбуждения). Обычно, это означает снижение числа дыхательных движения, не смотря на значительное повышение уровня CO2. Посему, ЧДД в наркозе у животных в норме составляет 8-20 в минуту, тогда как в сознании у тех же животных число дыханий в минуту будет составлять 15-30.
• Миорелаксация дыхательных мышц (межреберных, диафрагмальных) на фоне воздействия препаратов для наркоза. Воздействия анестетических препаратов на дыхательные мышцы ведет к снижению объема их движений и снижению дыхательного объема (соответственно и минутного объема дыхания).
Угнетение дыхательного центра и миорелаксация дыхательных мышц у животного в наркозе может вести к следующим потенциальным проблемам:
• Гиперкапния. У животного в наркозе обычно отмечается некоторый рост уровня углекислоты артериальной крови (PaCO2), по причине снижения и минутного объема дыхания (МОД) и неполной элиминации. Рост углекислоты в крови сопровождается соединением его с водой и формированием ионов бикарбоната (HCO3-) и водорода (H+), данные ионы снижают рН циркулирующей крови, ведя к дыхательному ацидозу. У здоровых бодрствующих животных составляет рН составляет 7.38–7.42, при анестезии – рН может упасть до 7.20.
Рост углекислоты в крови сопровождается соединением его с водой и формированием ионов бикарбоната (HCO3-) и водорода (H+), данные ионы снижают рН циркулирующей крови, ведя к дыхательному ацидозу. У здоровых бодрствующих животных составляет рН составляет 7.38–7.42, при анестезии – рН может упасть до 7.20.
• Гипоксемия. При дыхании комнатным воздухом, на фоне общей анестезии, уровень кислорода может значительно снижаться в результате снижения МОД. При использовании кислорода данный феномен отмечается значительно реже.
• Формирование ателектазов. Снижение ДО в анестезии, ведет к неполному расправлению легких при вдохе и частичному спадению альвеол (особенно в нижних отделах).
Существуют некоторая группа риска, т.е. те животные и ситуации, в которых повышен риск развития в наркозе гиперкапнии, гипоксемии и ателектазов, данные осложнения чаще отмечаются в следующих ситуациях:
• Повышение длительности анестезии (более 90 минут).
• Ожирение.
• Применение в наркозе нейромышечных блокаторов (миорелаксантов).
• Предшествующие заболевания легких (пр. пневмония, различные виды отека легких).
• Предшествующая травма головы.
• Хирургические процедуры с вовлечением грудной клетки или диафрагмы. Такие животные могут иметь предшествующие сердечнососудистые или легочные заболевание и подвержены значительному риску сердечнососудистого коллапса при традиционной анестезии без ИВЛ.
При подсоединении пациента к дыхательному контуру, он получает чистый кислород и проблема с гипоксемией развивается только при поражении паренхимы легких или выраженном угнетении дыхательного центра. Для предотвращения развития ателектазов, в период анестезии применяются манипуляции с дыхательным мешком (примерно 1 раз в 5 минут). Уровень углекислоты в артериальной крови во время анестезии обычно поддерживается чуть выше физиологического уровня, при его превышении – используются различные методы искусственной вентиляции легких (вспомогательная или контролируемая).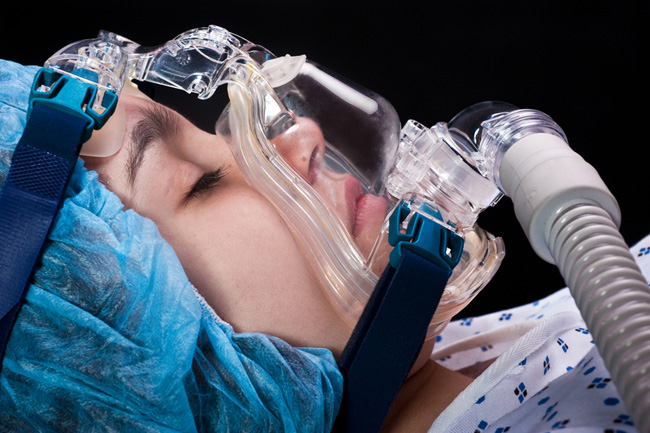
Типы контролируемой вентиляции
При анестезии пациента существуют два основных типа контролируемой вентиляции – мануальный и механический, как бы то ни было, пациент должен быть интубирован и подсоединен к дыхательному контуру. Далее приводятся некоторые характеристики того и другого типа вентиляции.
1. Мануальная вентиляция – осуществляется у пациента, присоединенного к дыхательному контуру, посредством сдавливания резервуарного (дыхательного) мешка. Общий термин, используемый для определении мануальной вентиляции животного под наркозом – баггинг (bagging). При данном типе вентиляции с положительным давлением, легкие наполняются дыхательной смесью под давлением, когда анестезист сжимает руками дыхательный мешок на фоне прикрытого (закрытого) клапана сброса. Выдох при этом пассивный, происходит под действием атмосферного давления, на фоне снижения давления в дыхательному контуре (устранение мануального сдавливания мешка). В рутинной практике баггинг чаще применяется для предотвращения формирования ателектазов – манипуляции с мешком проводятся один раз в 2-10 минут. Часть пациентов требуют искусственной вентиляции весь период анестезии, при этом, манипуляции с мешком определяются как перемежающаяся принудительная вентиляция.
2. Механическая вентиляция – искусственная вентиляция легких у пациента в анестезии, осуществляемая посредством специального аппарата (вентилятора). По сути, механическая вентиляция отличается от мануальной, лишь использованием специального прибора, который встраивается вместо мешка в дыхательный контур. Как и при ручной вентиляции, выдох при использовании аппарата ИВЛ — пассивный. Вентиляторы практически не применяют для периодической вентиляции, чаще используют для перемежающейся принудительной вентиляции.
Мануальная вентиляция
Существуют различные схемы мануальной вентиляции, в общем и целом, она всегда подстраивается под конкретные нужды пациента. Манипуляции с мешком могут применяться в виде баггинга для предотвращения формирования ателектазов, сразу после интубации, для облегчения ввода в общую анестезию, и в качестве коррекции различных видов депрессии дыхания.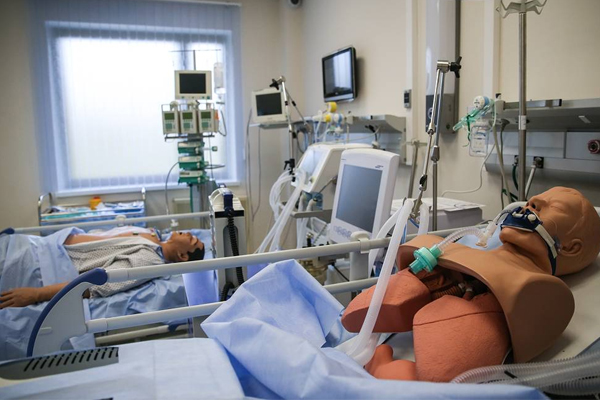
При ИВЛ дыхательным мешком клапан сброса частично или полностью перекрывается, компрессия резервуарного мешка ведет к созданию давления в легких пациента и вдоху. Выдох пассивен, наступает в момент расправления дыхательного мешка (ослабление давления руки). Компрессия мешка занимает 1-1.5 секунды (активный вдох), грудная клетка должна расправляться на тот же уровень, как у бодрствующего пациента. Создание избыточного давления (превышающего 20 см. водного столба) и увеличение продолжительности вдоха способны повредить легкие и нарушить венозный возврат крови к сердцу.
При вводе животного в наркоз, непосредственно после интубации и подключения дыхательного контура, часто отмечается апноэ различной степени выраженности. В таких случаях манипуляция с дыхательным мешком помогает пережить период гипоксемии, провести насыщение крови ингаляционным анестетиком и плавно перейти на спонтанное дыхание пациента (облегчает вход в наркоз).
У части пациентов, при общей анестезии, отмечается умеренная дыхательная депрессия, при этом развивается гипоксемия и гиперкапния на фоне снижения либо дыхательного объема (поверхностное дыхание), либо числа дыхательных движений (менее 6 дыханий в минуту). В данном случае незаменима вспомогательная вентиляция посредством периодической компрессии мешка (подстройка под дыхание пациента), иногда, лучшим выбором является переход на перемежающуюся принудительную вентиляцию (мануальную или механическую).
У пациентов на фоне исходных заболеваний (пр. заболевания сердечно-легочной системы, диафрагмальная грыжа, острое расширение и заворот желудка) ожидаемо тяжелое угнетение дыхания при общей анестезии, и предпочтение отдается анестезии не на спонтанном дыхании, а используя различные методы принудительной вентиляции легких, в ряде случаев, допустимо использование мануальных способов вентиляции (не механических). Ниже приводится схема проведения перемежающейся принудительной вентиляции легких кошек и собак.
Блок. Проведение перемежающейся принудительной вентиляции (ППВ).
Проведение перемежающейся принудительной вентиляции (ППВ).
Основными показаниями к ППВ являются предшествующие заболевания (сердечно-легочные патологии, диафрагмальная грыжа, ОРЖ и пр.), низкий дыхательным объем и снижение числа дыхательных движений (менее 6 дыханий в минуту).
1. Перемежающаяся принудительная вентиляция начинается сразу после интубации и подключения к дыхательному контуру.
2. Дыхательный объем должен несколько превышать обычный (10-15 мл/кг), первоначальная частота дыхательных движений составляет 8-20 в минуту (в зависимости от массы пациенты). Остановка спонтанного дыхания на фоне данной вентиляции отмечается в течение 1 минуты после снижения уровня углекислоты в крови.
3. Сохранение попыток спонтанного дыхания после 5-10 минут принудительной вентиляции может служить показанием для использования миорелаксантов (нейромышечных блокаторов), для устранения сопротивления пациента.
4. При достижении контроля (синхронизации пациента) адекватная частота вентиляции составляет 6-12 движений в минуту.
5. Рекомендуемое пиковое давление у МДЖ составляет 15-20 см водного столба, вмешательства на открытой грудной клетке могут потребовать повышения данного давления.
6. Время вдоха должно составлять 1-1.5 секунды, время выдоха 2-3 секунды (как минимум). Соотношение вдох:выдох сохраняется на уровне 1:2.
7. Клапан сброса во время мануальной вентиляции закрыт или частично закрыт, но должен открываться после каждые 2-3 вдоха. Анестезист должен позволять снижаться до нуля давления в период выдоха, так, чтобы нормализовалась сердечнососудистая функция (улучшение венозного возврата и повышение ударного объема).
8. При окончании хирургической процедуры ток анестетика прекращается (установка испарителя на ноль), вентиляция продолжается чистым кислородом. При использовании миорелаксантов, они должны быть реверсированы (при возможности).
9. Для «отлучения» животного от вентилятора число дыханий сокращается до 2-3 в минуту, до появления признаков спонтанного дыхания. При появлении самостоятельного дыхания вентиляция может перейти на вспомогательную, посредством сжимания резервуарного мешка при каждом вдохе. В конце концов, животное обретает способность поддерживать нормальный ДО и ЧДД, и вспомогательная вентиляция прекращается. Согревание гипотермичных пациентов, стимуляция сжатием подушечек пальцев, нежное потирание грудной клетки и живота, или скручиванием уха – могут помочь пациенту быстрее восстановить спонтанное дыхание.
При появлении самостоятельного дыхания вентиляция может перейти на вспомогательную, посредством сжимания резервуарного мешка при каждом вдохе. В конце концов, животное обретает способность поддерживать нормальный ДО и ЧДД, и вспомогательная вентиляция прекращается. Согревание гипотермичных пациентов, стимуляция сжатием подушечек пальцев, нежное потирание грудной клетки и живота, или скручиванием уха – могут помочь пациенту быстрее восстановить спонтанное дыхание.
При проведении вспомогательной и контролируемой вентиляции лучшим методом мониторинга ее эффективности является пульсоксиметрия и капнография.
Механическая вентиляция
Механическая вентиляция – проведение искусственной вентиляции легких посредством специализированного аппарата (вентилятора). Вентилятор, также именуемый как аппарат искусственной вентиляции легких (ИВЛ) – специализированный прибор, который при анестезии встраивается в дыхательный контур, и выполняет функцию дыхательного мешка при перемежающейся принудительной вентиляции легких. По сути, механическая вентиляция сходна с перемежающейся положительной вентиляции проводимой дыхательным мешком, однако, вместо мешка, движения газовой смеси по дыхательному контуру определяет аппарат искусственной вентиляции. Проведение механической вентиляции показано в тех случаях, когда манипуляции с дыхательным мешком (баггинг) затруднительны для анестезиста (высокая длительность) и для более точного дозирования ИВЛ при прямых показаниях к принудительной вентиляции.
Как при ручной вентиляции, механическая вентиляция особенно показана для пациентов с компромиссом дыхательной системы. У обычных пациентов анестезию лучше проводить на спонтанной вентиляции с периодическим баггингом (каждые 5 минут). Механическая вентиляция особенно полезна у животных при торакостомиии или других длительных операциях, когда ручная перемежающаяся принудительная вентиляция затруднительна для анестезиста.
При анестезии мелких домашних животных, могут использоваться различные вентиляторы, которые несколько отличаются по дизайну, но основой их является дыхательные меха, движения в которых контролируются прибором. Вентилятор обычно присоединяется к порту дыхательного мешка. Движения мехов могут осуществляться посредством сжатого газа или специальным мотором, объем и частоту дыхания задает электроника.
Вентилятор обычно присоединяется к порту дыхательного мешка. Движения мехов могут осуществляться посредством сжатого газа или специальным мотором, объем и частоту дыхания задает электроника.
При проведении ИВЛ, существует три основных параметра вдоха – объем, пиковое давление и время. Исходя из этого, существует три основных типа вентиляторов – с ограничением по объему, давлению и времени:
1. Вентилятор с ограничением по давлению (pressure-cycled ventilators) – вдох животного проводится до момента установленного пикового давления, затем происходит остановка, не смотря на продолжительность и доставленный объем.
2. Вентилятор с ограничением по объему(volume-cycled ventilators) – в момент вдоха животному доставляется точный дыхательный объем, который вводится вне зависимости давления необходимое в достижение данного объема.
3. Вентилятор с ограничением по времени (time-cycled ventilators) – доставка газовой смеси и сам вдох дозируются во времени.
В практике анестезии мелких домашних животных, чаще используются аппараты искусственной вентиляции легких с ограничением по объему, вентиляторы с ограничением по давлению используются чуть реже, и вентиляторы с ограничением по времени – практически не используются.
Основными параметрами, которые устанавливает анестезист на аппарате искусственной вентиляции легких, являются дыхательный объем (ДО), частота дыхательных движений (ЧДД), пиковое давление и соотношение длительности вдоха к длительности выдоха. В каждом конкретном случае, установки могут подыгрываться исходя из нужд пациента. Дыхательный объем обычно составляет 10-15 мл/кг, число дыхательных движений – 6-12 дыханий в минуту, время вдоха = 1–1.5 секунды, длительность выдоха = 2-6 секунд (при соотношении вдоха/выдоха 1:2–1:4), пиковое давление составляет 12-20 см водного столба.
Мониторинг механической вентиляции, в первую очередь осуществляется наблюдениями за движениями грудной клетки, лучшие результаты достигаются при оценке сатурации крови кислородом (пульсоксиметрия) и уровня углекислоты в конце выдоха (капнометрия).
Риски контролируемой вентиляции.
Контролируемая вентиляция (как мануальная так и механическая) не безопасное мероприятие, и, потенциально может нанести вред здоровью животного. Ниже представлены основные риски проведения ИВЛ в анестезии:
• Механическая травма легких (обычно альвеол) при создании избыточного давления, может сопровождаться развитием пневоторакса или пневмомедистинума.
• Снижение венозного возврата (следовательно сердечного выброса) при избытке положительного давления на протяжении дыхательного цикла.
• Значительное снижение уровня углекислоты в крови (гипокапния) при избыточной вентиляции ведет к респираторному алкалозу, который при тяжелом течении способен вызывать сужение сосудов мозга (вазоконстрикция) и снижение тока крови в головном мозгу.
• Передозировка ингаляционного анестетика. Принудительная вентиляции более эффективно в доставке анестетического газа, что может вести к передозировке (пр. гипотензия, повышение депрессии ЦНС). В таких случаях, следует проводить более тесный мониторинг стадий и уровня анестезии и, при необходимости, снижать установки испарителя анестетика.
Как заключение, контролируемая вентиляция легких при анестезии животных способна повысить операционные риски, и требует от анестезиста более тесного мониторинга состояние пациента.
Миорелаксанты (нейромышечные блокаторы)
Миорелаксанты или нейромышечные блокаторы первично воздействуют на нейромышечное соединение, что сопровождается расслаблением (параличом) мышц. Термин нейромышечные блокаторы несколько неуклюж, но более описателен для данного класса препаратов, он определяет, что данные лекарства воздействует первично на нейромышечное соединение. Термин миорелаксанты более общий, он описывает любое лекарство, вызывающе расслабление мышц, в данную группу также могут попасть миорелаксанты центрального действия (пример альфа2-адернагонисты, бензодиазепины). В России для данной группы препаратов более принят термин «миорелаксанты», и, поэтому, дальше будет использоваться именно он.
Миорелаксанты (также именуемые как нейромышечные блокаторы) широко используются в гуманной анестезиологии, в практике мелких домашних животных имеют ограниченное применение. При анестезии кошек и собак отдается большее предпочтение ингаляционному наркозу, при сохраненном спонтанном дыхании животного, нежели чем управляемой вентиляции. Несмотря на это, у кошек и собак существуют некоторые абсолютные и относительные показания к использованию миорелаксантов, ниже чуть подробнее о них:
• Применение миорелаксантов у пациентов требующих механической вентиляции легких предотвращает спонтанные дыхательные движения, что облегчает контроль и проведении вентиляции. Использование миорелаксантов особенно полезно при торакальных и диафрагмальных операциях.
• Использование миорелаксантов при ортопедических вмешательствах дает отличное расслабление мышц, что может быть показано у некоторых групп пациентов.
• Миорелаксанты широко применяются при офтальмологических операциях, на фоне их воздействия прекращаются движения глаз и отмечается их удержание в центральной, нежели чем в вентральной, позиции, что значительно облегчает хирургические манипуляции.
• Миорелаксанты при кесаревом сечении позволяют облегчить манипуляции с беременной маткой, при том, что они не проникают через плацентарный барьер.
• Миорелаксанты могут оказать пользу при трудной интубации (пр. животные с ларингоспазмом), поскольку они позволяют быстро контролировать дыхательные пути без кашля.
• Иногда, миорелаксанты используются в схемах сбалансированной анестезии, при которой различные препараты используются для обеспечения трех основных компонентов общей анестезии – бессознательного состояния, миорелаксации и общей анальгезии. Вместо применения высоких доз одного препарата (пр. пропофол для индукции общей анестезии) сбалансированные техники включают низкие дозы нескольких препаратов. Основная цель сбалансированной анестезии – минимизировать сердечнососудистые, дыхательные и другие побочные эффекты.
При использовании миорелаксантов у животных всегда следует помнить об этической стороне вопроса. Суть в том, что их введение без должной седации негуманно, пациенты находятся в полном сознании, сохраняют нормальную чувствительность к болевым стимулам но, не способны движением или как то по другому противостоять.
Основные побочные эффекты использования миорелаксантов связаны с потерей мышечной активности, животные не способны поддерживать собственное дыхание и защищать роговицу посредством моргания. Для предотвращения этих факторов, всегда используется контролируемая вентиляция легких и защита глаз различными лубрикантами. Также, животные при воздействии миорелаксантов склонны к развитию гипотермии, по причине снижения теплопродукции в мышцах, анестезист должен уделять особое внимание мониторингу температуры тела животного в анестезии.
Основная точка приложения мышечных релаксантов – блокада импульса от моторных (двигательных) нейронов к мышечным синапсам, место действия – нейромышечное соединение, где нейронами высвобождается ацетилхолин в непосредственной близости к мышечной концевой пластинке. Нейромышечные блокаторы подразделяются на две большие группы – деполяризующие и недеполяризующие миорелаксанты, обе группы воздействуют на ацетилхолиновые рецепторы, но несколько различными способами.
Деполяризирующие миорелаксанты (пр. сукцинилхолин) вызывают одну волну активности на нейромышечное соединение, с последующей рефрактерностью к дальнейшей нервной стимуляции мыщц. Животные, получающие данные препараты, проявляют спонтанные подергивания мышц с последующим их параличом. Сукцинилхолин имеет быстрое время наступления действия (20 секунд), но короткую продолжительность эффекта, полезен для быстрой интубации. Потенциальные побочные эффекты сукцинилхолина включают гиперкалиемию и аритмию.
Недеполяризующие миорелаксанты (пр. галламин, панкурониум, и др) блокируют рецепторы концевой пластики. Их классификация предполагает, что они не вызывают начальной волны активности на нейромышечное соединение, и не отмечаются спонтанные мышечные движения. Потенциальные побочные эффекты данных препаратов включают высвобождение гистамина, гипотензию или гипертензию, тахикардию и желудочковые аритмии.
Совместное использование миорелаксантов с ингаляционными анестетиками увеличивает силу их действия. Животные, получающие недавнее лечение органофосфатными инсектицидами, также проявляют повышенную чувствительность к воздействию миорелаксантов. Некоторые другие препараты, включая кортикостероиды, барбитураты, фуросемид, другие диуретики, противоопухолевые препараты, адреналин, тетрациклин и аминогликозиты – по различному могут влиять на силу действия мышечных релаксантов.
Миорелаксанты обычно вводятся путем медленной внутривенной инъекции, дозы варьируют в зависимости от вида животного и выбранного протокола. У большинства препаратов время наступления действия составляет 2 минуты, и длительность действия составляет 10-30 минут (сильно варьирует в зависимости от конкретного препарата). При необходимости более длительного действия применяется повторное введение. В качестве альтернативы, некоторые препараты вводятся посредством постоянной инфузии.
Несмотря на используемые препараты, поражаются только поперечно полосатые (скелетные) мышцы, бессознательные мышцы не затрагиваются (миокард, гладкие мышцы кишечника и мочевого пузыря). Скелетные мышцы поражаются в предсказуемом порядке: первыми парализуются мышцы лица и шеи, затем отмечается паралич хвоста, конечностей и живота. Межреберные мышцы и диафрагма поражаются последними.
При использовании миорелаксантов возникают некоторые трудности при оценке глубины анестезии, так как происходит угнетение нормального рефлекторного ответа и отсутствие тонуса челюсти. Число сердечных сокращений (ЧСС) и артериальное давление (АД) могут дать некоторое понятие о глубине анестезии. Развитии саливации или лакримации обычно означает не достаточную глубину анестезии.
Действие недеполяризующих препаратов при окончании анестезии должно обращаться (реверсироваться) антихолинэстеразными препаратами (не смотря на побочные эффекты), деполяризующие релаксанты не подлежат реверсии. Реверсия недеполяризующих миорелаксантов проводится не взирая на вероятные побочные эффекты используемых препаратов, чаще применяется эдрофоний, неостигмин и пиридостигмин (в Европе доступен «sugammadex»). При этом, животное должно находиться в состоянии легкой анестезии. После наступления действия реверсивных препаратов, у животного отмечаются признаки возвращения мышечного тонуса – вращения глаз, появление активного рефлекса век и общее повышение мышечного тонуса. Иногда, эффект реверсивных агентов исчерпывается на фоне не полной элиминации миорелаксантов, в данном случае может потребоваться более длительная дыхательная поддержка и повторные дозы реверсивных препаратов.
Реверсивные агенты могут иметь нежелательные побочные эффекты, такие как брадикардия и повышение бронхиальной и слюнной секреции, и должны быть использованы только после премедикации атропином или гликопиролатом. Эдрофоний и sugammadex имеют меньше побочных эффектов по сравнению с неостигмином.
Валерий Шубин, ветеринарный врач, г. Балаково
Онкология
ГУЗ РКОД МЗ РТ г. Казань
Реферат. Представлены результаты ретроспективного анализа влияния сроков экстубации на частоту дыхательных осложнений и выявления факторов, влияющих на сроки экстубации больных после хирургического лечения опухолей грудного и абдоминального отдела пищевода, выполненные в РКОД МЗ РТ г. Казани. Больные были разделены на две группы в зависимости от сроков экстубации: в 1-й группе — ранней экстубации (РЭ) — 42 (35,6%) пациента были экстубированы в течение 4 часов после операции и во 2-й группе — поздней экстубации (ПЭ) — 76 (64,4%) пациентов были экстубированы свыше 4 часов после окончания операции. При сравнительном анализе была выявлена безопасность ранней экстубации больных после операции на пищеводе, уменьшение частоты послеоперационных дыхательных осложнений, в частности пневмоний, и послеоперационной летальности в группе ранней экстубации. Возраст, наличие предоперационной лучевой терапии и сопутствующей дыхательной патологии, применение одно-легочной вентиляции не повлияли на сроки экстубации. Лишь использование интраоперационной грудной эпиду-ральной анестезии местными анестетиками способствовало ранней экстубации.
Ключевые слова: ранняя экстубация, хирургия пищевода, эпидуральная анестезия.
Несмотря на существенные достижения в технике хирургических вмешательств, совершенствование методов анестезиологического пособия и послеоперационного ведения больных, высокая частота послеоперационных осложнений и летальности остаются одной из важных проблем в хирургии больных раком пищевода. Частота послеоперационных осложнений после операций по поводу рака пищевода достигает 60-75%, а летальность 8-15%. Послеоперационные легочные осложнения встречаются от 20 до 40% случаев и являются наиболее частотой причиной послеоперационной летальности больных [2; 9; 18; 20].
Респираторные осложнения у данных больных могут быть связаны с особенностями хирургического вмешательства, с агрессивными факторами анестезиологического пособия и искусственной вентиляции легких (ИВЛ) [1; 3; 5; 11; 21; 27].
Исторически сложилось, что после эзофагэктомии необходимо проведение продленной ИВЛ в связи с тяжестью операционного вмешательства и побочными эффектами высоких доз наркотических анальгетиков и ингаляционных анестетиков. Учитывая, что современные мнения о необходимости и влиянии ранней экстубации на послеоперационные результаты в хирургии пищевода порой диаметрально противоположны [6; 8; 15; 17; 22; 25], нами проведён ретроспективный анализ по данным нашей клиники в период с января 2008 по декабрь 2009 года.
Цель исследования
Изучить частоту послеоперационных осложнений и летальность в хирургии злокачественных образований пищевода в зависимости от сроков экстубации и выявить факторы, влияющие на сроки экстубации.
Материал и методы
В зависимости от сроков экстубации больные разделены на две группы: 1-я группа (n = 42) — больные, переведённые на самостоятельное дыхание и экстубиро-ванные до 4 часов после окончания операции (ранняя экстубация — РЭ), 2-я группа (n=76) — больные, переведённые на самостоятельное дыхание и экстубированные более 4 часов после окончания операции (поздняя экстубация — ПЭ).
В первой группе (РЭ) было 10 женщин и 32 мужчины, соотношение — 1:3,2; во второй группе (ПЭ) -19 женщин и 57 мужчин, соотношение — 1:3.
Медиана возрастного распределения больных составила: в первой группе (РЭ) 60,5 лет (диапазон 38-80 лет), во второй группе (ПЭ) 61 год (диапазон 46-81 год). Каждый пятый пациент в обеих группах был старше 70 лет.
Каждому второму больному в обеих группах проводилась предоперационная дистанционная лучевая терапия (ДЛТ), и каждый второй больной имел длительный анамнез курения (таблица 1). Каждый третий больной страдал ишемической болезнью сердца (ИБС) с нарушением ритма. У каждого пятого больного выявлена хроническая обструктивная болезнь легких (ХОБЛ).
Вводный наркоз проводился пропофолом или ке-тамином. Общая анестезия поддерживалась севофлю-раном с/или без закиси азота. Миорелаксация поддерживалась ардуаном. ИВЛ проводилась аппаратами «Дрегер» (Германия), моделями «Примус» и «Фабиус», в послеоперационном периоде «Evita4» и «Savina».
В условиях операционной по срединной линии производилась пункция и катетеризация эпидурального пространства на уровне Th5-Th8. Интраоперационная ГЭА местными анестетиками (0,5-0,75% ропивакаин «Астра Зенека», Швеция; 2% лидокаин «Биосинтез», Россия) в качестве компонента анестезии не была проведена в 30,5% случаев (36 из 118 больных), и интра-операционная анальгезия осуществлялась традиционным внутривенным введением наркотических анальгетиков. Всем пациентам в послеоперационном периоде проводилась мультимодальная анальгезия с использованием местных анестетиков (0,2% ропивакаин «Астра Зенека», Швеция), наркотических и нестероидных противовоспалительных анальгетиков.
Интраоперационно проводился контроль глубины анестезии BIS-монитором «А-2000ХР» (США). Гемодина-мический, газовый мониторинг в интраоперационном и послеоперационном периоде осуществлялся аппаратами «Дрегер» (Германия).
Хирургическое вмешательство трансхиатальным доступом с анастомозом на шее было произведено в половине случаев, при трансторакальном и видеоторако-скопическом доступе внутриплевральный анастомоз был наложен почти в каждом пятом случае (11 из 58 человек). Распределение больных по доступу в исследуемых группах представлено в таблице 2.
Перевод на самостоятельное дыхание и экстубация были выполнены врачом отделения анестезиологии и реаниматологии при достижении необходимых критериев (таблица 3).
Статистический анализ проведен методом вариационной статистики с применением критерия Стьюдента. Различия считались достоверными при р<0,05.
Результаты и их обсуждение
Длительность оперативного вмешательства, количество пациентов и длительность однолегочной вентиляции, использование ГЭА местными анестетиками, объём интраоперационно перелитой жидкости в исследуемых группах представлены в таблице 4.
После окончания операции в 31% случаев (13 из 42 больных) первой группы (РЭ) были переведены в палату отделения анестезиологии и реаниматологии (ОАиР) при восстановленном самостоятельном дыхании, а в 69% случаев (29 из 42 больных) на ИВЛ с длительностью 104,1 мин. ± 35,3 мин. Всем 76 больным второй группы (ПЭ) после окончания операции ИВЛ проводилась в течение 287,4 мин. ± 202,5 мин. (р<0,01).
В первой группе (РЭ) пациенты после восстановления самостоятельного дыхания были экстубированы через 96,2 мин. ± 28,6 мин. Пациенты первой группы (13 из 42 больных), доставленные в палату ОАиР на самостоятельном дыхании, были экстубированы через 101,5 мин. ± 28,8 мин., а пациенты первой группы (29 из 42 больных), доставленные в палату ОАиР на ИВЛ, после восстановления самостоятельного дыхания были экстубированы через 93,8 мин. ± 28,7 мин. Во второй группе (ПЭ) больные после перевода на самостоятельное дыхание были экстубированы через 181,2 мин. ± 112,7 мин. (р<0,01).
Таким образом, время от окончания операции до экс-тубации в первой группе (РЭ) составило 171,6 мин. ± 63,6 мин., а во второй группе (ПЭ) — 483,3мин. ± 266,7 мин. (р<0,01) (рис. 1).
Различные послеоперационные осложнения развились в 35,6% случаев (42 из 118 больных), а летальность составила 9,3% (11 из 118 больных).
В первой группе (РЭ) послеоперационные осложнения развились в 21,4% случаев, а во второй группе (ПЭ) -в 43,4% случаев (р<0,01). Летальность в первой группе (РЭ) составила 2,4%, тогда как во второй группе (ПЭ) -13,2% (р<0,01). Сочетанные осложнения возникли у 4 из 9 (44,4%) и 22 из 33 (66,7%) больных в каждой группе соответственно. В структуре послеоперационных осложнений в обеих группах преобладали дыхательные и гнойно-септические осложнения, связанные с несостоятельностью анастомоза или трансплантата (таблица 5).
Из числа дыхательных осложнений наибольшую часть составили послеоперационные пневмонии, которые развились в 20,3% случаев, ОРДС развился в 2,5% случаев. Несостоятельность эзофагогастроанастомоза развилась в 12,7% случаев. Сердечные осложнения в основном выражались нарушениями ритма сердечных сокращений, возникших в 6,8% случаев, и зачастую развивались на фоне дыхательных нарушений.
Частота послеоперационных пневмоний, нарушение ритма сердечных сокращений, несостоятельность эзофагогастроанастомоза и летальность в исследуемых группах представлена на рисунке 2.
Также следует обратить внимание на следующий факт: у пациентов с двухлегочной ИВЛ послеоперационные пневмонии развились в 11,7% случаев (7 из 60 больных), а с однолегочной ИВЛ — в 29,3% случаев (17 из 58 больных) (р<0,05) (рис. 3). Большая травма-тичность, длительность хирургического вмешательства, влияние однолегочной вентиляции, усугубляющиеся непосредственным механическим повреждением легкого и органов средостения, денервацией бифуркации трахеи и бронхов при удалении лимфатических коллекторов, приводили к включению внелегочных механизмов развития дыхательных недостаточностей и пневмоний у пациентов после трансторакального доступа. Однако частота развития послеоперационных пневмоний после анестезиологического пособия с однолегочной вентиляцией легкого у больных в первой группе (РЭ) ниже, чем у больных второй группы (ПЭ), даже с традиционной двухлегочной вентиляцией, прооперированных транс-хиатальным способом 10,5% (2 из 19 больных) против 18,9% (7 из 37 больных) соответственно (р=0,81).
Возраст (р=0,12), предоперационная ДЛТ (р=0,23), курение (р=0,20), влияние однолегочной вентиляции (р=0,61) не отразились на сроках экстубации. Лишь использование ГЭА в качестве компонента анестезии позволило рано выполнить экстубацию в 47,6% случаев (39 из 82 больных), тогда как у больных без ГЭА в качестве компонента анестезии ранняя экстубация была возможна лишь в 8,3% случаев (3 из 36 больных) (р<0,01).
Основной задачей анестезиолога является защита пациента от пагубных последствий неконтролируемой симпатоадреналовой реакции на хирургический стресс, а к периоду пробуждения пациентов анестезиологи зачастую подходят пассивно, считая его чем-то вторичным [1]. Однако, по данным литературы [12; 28; 29], затянувшееся пробуждение и отсроченная экстубация приводят к более частым респираторным осложнениям и увеличению длительности послеоперационного пребывания больных в палатах интенсивной терапии, с удорожанием лечения в торакоабдоминальной хирургии.
В патофизиологической основе повышения риска развития послеоперационных респираторных осложнений при продленной искусственной вентиляции легких лежит нефизиологичность ИВЛ, связанная с созданием положительного давления в дыхательных путях, альвеолах и плевральных полостях, приводящая к баротравмам, волюмотравмам, ателектотравмам, биотравмам альвеол и бронхиол, так называемым респираторно-ассоциированным повреждениям, а также неблагоприятным влиянием ИВЛ на дренажную функцию трахео-бронхиального дерева, которая усугубляется действием анестезиологических препаратов и влиянием однолегоч-ной вентиляции [4; 7; 11; 16; 24; 26].
В настоящее время в ряде зарубежных публикаций показана безопасность ранней экстубации после операций на пищеводе [19; 23; 30]. Авторы публикаций не отмечают повышения частоты послеоперационных осложнений при ранней экстубации больных. Лишь в одном рандомизированном исследовании показано статистически недостоверное повышение частоты послеоперационной летальности в группе ранней экстубации [10]. В отечественной литературе мы не нашли исследований по вопросам применения ранней экстубации после хирургического лечения больных раком пищевода.
Полученные данные нашего ретроспективного анализа не противоречат данным авторов, которые показали уменьшение послеоперационных дыхательных осложнений у рано экстубированных пациентов [12; 13; 14; 15]. В то же время при анализе факторов, влияющих на сроки экстубации, выявлено, что лишь использование ГЭА как компонента анестезии способствовало ранней экстубации больных раком пищевода, что совпадало с мнениями зарубежных коллег [15; 19; 30].
Энтузиазм анестезиологов, стремящихся к ранней экстубации больных после высокотравматических операций, должен быть основан на выборе адекватной анестезии в интраоперационном периоде как важного фактора, влияющего на сроки экстубации и частоту развития послеоперационных дыхательных осложнений.
Учитывая, что исследование носит ретроспективный характер, эти предварительно полученные данные заслуживают дальнейшего изучения в рандомизированных клинических испытаниях.
Выводы
1. Исторически сложившаяся парадигма о необходимости продленной ИВЛ после высокотравматичных операций в послеоперационном периоде может быть подвергнута сомнению. Применение ранней экстуба-ции после хирургических вмешательств у больных раком пищевода не связано с повышением частоты послеоперационных дыхательных осложнений и после операционной летальности.
2. Применение интраоперационной ГЭА местными анестетиками способствует более раннему переводу больных на самостоятельное дыхание и ранней экс-тубации.
3. Применение однолегочной вентиляции сопряжено с повышением частоты послеоперационных пневмоний. Ранняя экстубация больных с однолегочной вентиляцией в хирургии пищевода способствует снижению риска развития послеоперационных пневмоний по сравнению с двухлегочной вентиляцией, но поздно экстубированных больных.
Литература
1. Горобец Е.С. Принципы анестезии при абдоминальных онкологических операциях / Е.С. Горобец // Вестник интенсивной терапии. -2008. — № 2. — С.1-25.
2. Давыдов М.И. Рак пищевода / М.И. Давыдов, И.С. Стилиди. — 3-е изд., испр. и доп. — М., Издательская группа РОНЦ, Практическая медицина, 2007. — 392 с.: ил.
3. Кассиль В.Л. Влияние высокочастотной вентиляции легких на гемодинамику и функциональное состояние миокарда у больных раком пищевода с острой дыхательной недостаточностью в послеоперационном периоде/ В.Л. Кассиль, О.Г. Мазурина, В.Е. Соловьев, Э.Г. Карамян // Анестезиология и реаниматология. — 1992. — № 4. — С.32-36.
4. Кассиль В.Л. Искусственная и вспомогательная вентиляция легких / В.Л. Кассиль, М.А. Выжигина, Г.С. Лескин. — М.: Медицина, 2004. — 480 с.
5. Мазурина О.Г. Особенности развития дыхательной недостаточности в раннем послеоперационном периоде после операций по поводу рака пищевода и кардии / О.Г. Мазурина, В.Е. Соловьёв, Э.Г. Карамян, [и др.] // Анестезиология и реаниматология. — 1991. — № 5. — С. 17-21.
6. Мирошников Б. М. Хирургия рака пищевода. / Б. М. Мирошников, К. М. Лебединский. — СПб.: Фолиант, 2002. — 304 с.
7. Можаев Г.А. Влияние искусственной вентиляции лёгких на муко-цилиарный аппарат и местный иммунитет дыхательной системы во время общей анестезии / А.Г. Можаев, В.В. Носов // Анестезиология и реаниматология. — 1985. — № 4. — С. 52-55.
8. Стамов В.И. Анестезия при радикальных операциях по поводу рака пищевода / В.И. Стамов, М.Д. Чернов // Анестезиология и реаниматология. — 2002. — № 5. — С. 49-54.
9. Atkins B.Z. Reducing hospital morbidity and mortality following esophagectomy /B.Z. Atkins, A.S. Shah, K.A., Hutcheson [et al.] // Ann. Thorac. Surg. — 2004. — Vol. 78, № 4. — Р. 1170-1176.
10. Bartels H. Early extubation vs. late extubation after esophagus resection: a randomized, prospective study [Article in German] / H. Bartels, H.J. Stein, J.R. Siewert // Langenbecks Arch Chir. Suppl. Kongressbd. — 1998.- № 115. — Р. 1074-1076.
11. Baudouin S. V. Lung injury after thoracotomy / S. V. Baudouin // Br. J. Anaesth. — 2003. — Vol.91, № 1. — Р. 132-142.
12. Brodner G. A. Мultimodal approach to control postoperative pathophysiology and rehabilitation in patients undergoing abdominothoracic esophagectomy. / G. Brodner, E. Pogatzki, H. Van Aken [et al.] //Anesth. &Analg. — 1998. — Vol. 86, Р. 228-234.
13. Buise M. Pulmonary morbidity following esophagectomy is decreased after introduction of a multimodal anesthetic regimen./ M. Buise , J. Van Bommel, M. Mehra // Acta Anaesthesiol. Belg. — 2008. — Vol. 59, № 4. — Р 257-261.
14. Caldwell M.T. Timing of extubation after oesophagectomy. / M.T. Caldwell, P.G. Murphy, R. Page, [et al.] // Br. J. Surg. — 1993. — Vol. 80, № 12. — Р. 1537-1539.
15. Chandrashekar M.V. Immediate extubation and epidural analgesia allow safe management in a high-dependency unit after two-stage oesophagectomy. Results of eight years of experience in a specialized upper gastrointestinal unit in a district general hospital. / M.V. Chandrashekar, M. Irving, J. Wayman [et al.] // Br. J. Anaesth. — 2003. — Vol. 90, №4. — Р. 474-479.
16. De Conno E. Anesthetic-induced improvement of the inflammatory response to one-lung ventilation / E. De Conno, M.P. Steurer, M. Wittlinger [et al.] // Anesthesiology. — 2009. — Vol. 110, № 6. — Р. 1316-1326.
17. Forshaw M.J. Postoperative ventilation in the recovery area / M.J. Forshaw, A.Z. Khan, A.R. Davies // Ann. R.Coll. Surg. Engl. — 2007. -Vol. 89, № 4. — р. 449; author reply 449-450.
18. Goan Y.G. An audit of surgical outcomes of esophageal squamous cell carcinoma. / Y.G Goan ., H.C Chang, H.K Hsu, Y.P Chou // Eur. J. Cardiothorac. Surg. — 2007. — Vol. 31, № 3. — Р. 536-544.
19. Lanuti M. Feasibility and outcomes of an early extubation policy after esophagectomy./ Lanuti M., de Delva P.E., Maher A. [et al.] // Ann. Thorac. Surg. — 2006. — Vol. 82, № 6. — Р. 2037-2041.
20. McCulloch P. Mortality and morbidity in gastro-oesophageal cancer surgery: initial results of ASCOT multicentre prospective cohort study / P. McCulloch J. Ward P. P Tekkis and for the ASCOT group of surgeons// Br.Med.J. — 2003. — Vol. 22, № 327. — Р. 1192-1197.
21. Ricard J-D. Ventilator-induced lung injury /J-D. Ricard, D. Dreyfuss, G. Saumon // Europ.Respir.J. — 2003. — Vol. 22, № 42. — Р. 2-9
22. Robertson S.A. Ventilatory and intensive care requirements following oesophageal resection / S.A. Robertson, R.J. Skipworth, D.L. Clarke // Ann. R. Coll. Surg. Engl. — 2006. — Vol. 88, № 4. — Р 354-357.
23. Rocker M. Early extubation after two-stage oesophagectomy / M. Rocker, T. J. Havard, A. Wagle [et al.] // Br. J. Anaesth. — 2003. — Vol. 91, № 5. — Р 760.
24. Schilling T. The Pulmonary Immune Effects of Mechanical Ventilation in Patients Undergoing Thoracic Surgery/ T. Schilling , A. Kozian, C. Huth [et al.] // Anes. & Analg. — 2005. — Vol. 101, № 4. — Р. 957-965.
25. Shah M. Oesophagectomy and elective postoperative ventilation. / M. Shah, А. Pearce // Br. J. Anaesth. — 2004. — Vol. 92, № 6. — Р. 907-908; author reply 908.
26. Slutsky A.S. Lung Injury Caused by Mechanical Ventilation / A.S. Slutsky // Chest. — 1999. — Vol. 116, — suppl 1 Р. 9-15.
27. Tandon S. Peri-operative risk factors for acute lung injury after elective oesophagectomy / S.Tandon, A. Batchelor, R. Bullock [et al.] // Br. J. Anaesth. — 2001. — Vol. 86, № 5. — Р. 633-638.
28. Von Dossow V. Thoracic Epidural Anesthesia Combined with General Anesthesia: The Preferred Anesthetic Technique for Thoracic Surgery / V. Von Dossow, M. Welte, U. Zaune [et al.] // Anes. & Analg. — 2001. — Vol. 92, № 4. -Р. 848-854.
29. Zehr K.J. Standardized clinical pathways for major thoracic cases reduces hospital costs/ K.J. Zehr, P.B. Dawson, S.C. Yang, R.F. Heitmiller// Ann. Thorac. Surg. — 1998. — Vol. 66. — Р. 914-919.
30. Yap F.H. Early extubation after transthoracic oesophagectomy/ F.H. Yaр, J.Y. Lau , G.M. Joynt [et al.] // Hong Kong Med. J. — 2003. — Vol. 9, № 2. — Р. 98-102.
Учебная программа
Учебная программа
Учебная программа последипломного профессионального обучения в клинической ординатуре по специальности «Анестезиология и реаниматология» № 14.00.37.
Теоретические основы анестезиологии и реаниматологии
Физиология
Дыхание: функция легких, функциональные процессы в легких
Легочные объемы
- определения, методики измерения, нормальные объемы и временные константы
- спирометрия, статистические и динамические объемы, мертвое пространствво, вымывание азота, разведение гелия, плетизмография тела, потребление кислорода, выделение СО2, тест с нагрузкой
Легочная механика
- податливость (комплайнс), градиент плеврального давления, кривые соотношения поток/объем и их трактовка, сурфактант
- легочная резистентность, принципы измерения газовых потоков
- методика измерения
- работа дыхания
- регуляция тонуса дыхательных путей
Вентиляция кровоток
- нарушения вентиляции
- нарушение кровотока в легких, зоны, гипоксическая легочная вазоконстрикция
- измерение соотношения V/Q, объяснение А аО2, а АСО2, Vd/Vt, Qs/Qt, сканирование легких
Диффузия
- определение: газовые законы
- диффузионная легочная емкость, измерение
- оксигенация при апное, диффузионная гипоксия
Газообменная функция крови
- Транспорт О2, физическая растворимость, насыщение, в О2, кривая диссоциации, эффект Бора, нормальный кислотно-щелочный баланс и его компенсаторные сдвиги
Регуляция вентиляции легких
- дыхательный центр
- центральные и периферические хеморецепторы, проприоцептивные рецепторы, дыхательные мышцы и рефлексы, иннервация легких
- СО2 и О2 кривые
Сердечно-сосудистая система
Сердечный цикл
- контроль сердечного ритма
- синхронность давления, кровотока, ЭКГ, шумов, действия клапанов сердца
- импульс распространения
- нормальная ЭКГ
- электрофизиология
Функция желудков сердца
- закон Франка Старлинга, преднагрузка, постнагрузка, давления в полостях сердца в различные фазы сокращения
- сила, вязкость, длина, скорость укорочения
- сократимость миокарда, возможности и ограничения измерения
- сердечный выброс
- утилизация О2 миокардом.
Венозный возраст
- венозный тонус, контролирующие факторы
- мышечные сокращения, внутригрудное давление, положение тела
- объем крови
Кровяное давление
- систолическое, диастолическое, среднее, перфузионное
- внутрисердечное, легочное, венозное
- общее сосудистое сопротивление
Микроциркуляция
- капиллярная диффузия, осмотическое давление
- контроль пре и посткапиллярных сфинктеров
- реология, вязкость крови
Регионарная перфузия
- церебральная
- коронарная
- легочная
- почечная
- бассейна кишечника и печени
- мышц и кожных покровов
Регуляция циркуляции и объема крови
- центральная: вазомоторный центр, питуитарно-почечная система
- периферическая: рецепторы и рефлексы
- гормональный контроль
Центральная и периферическая нервная система:
Мозг
- кора мозга: функциональная организация
- электроэнцефалограмма
- величина волн, частота и амплитуда, истинные и обработанные волны
- сон, судорожная ЭЭГ, О2 и СО2 , смерть мозга
- глубина анестезии, специфический эффект анестетиков
- соматосенсорный, слуховой и зрительный вызванные ответы
Спинной мозг
- основы функциональной организации, ствол мозга, активирующая ретикулярная cистема
- спинальные рефлексы
- проводящие пути
- вызванные потенциалы
Цереброспинальная жидкость
- образование, объем, состав, поток и давление
- гематоэнцефалический барьер
- объем мозга, податливость (комплайнс)
- влияние на состав крови и кислотно-щелочной баланс
Нейромышечная и синаптическая передача
- морфология, рецепторы
- мембранный потенциал, механизм
- потенциал действия, характеристики, перемещение (потоков) ионов
- синапс, передатчики, прекурсоры, ионы, конечные эффекты, трансмиссионные характеристики
Сокращения скелетных мышц, деполяризация, роль кальция, актин, миозин, энергетические запасы и их реализация.
Механизмы боли
- центральные регуляторы
- рецепция боли
- трансмиссия, рецепторы, афферентные волокна, спинальные клетки и тракты
Автономная нервная система
- симпатическая: рецепторы, передатчики, ответные реакции и конечный эффект
- парасимпатическая система: рецепторы, передатчики, ответные реакции и конечный эффект
- ганглионарная трансмиссия
- рефлексы: восходящие и нисходящие столбы (пути)
Функции печени:
Двойное кровоснабжение.
- Метаболические функции
- Экскреторные функции
- Механизмы метаболизма лекарственных средств и их экскреция
- Тесты оценки функционального состояния печени
Функция почек:
- Кровоток, клубочковая фильтрация, канальцевая реасорбция и секреция
- Тесты оценки функции почек
- регуляция внеклеточной жидкости: ренин, ангиотензин, альдостерон
- Регуляция осмолярности: АДГ
- Регуляция кислотно-щелочного баланса
- Экскреция фармакологических средств почками
Функция эндокринных желез (гипофиз, щитовидная железа, паращитовидные железы, надпочечники, поджелудочная железа).
- Температурная регуляция:
- Температура в организме: центральная и периферическая
- Терморегулирующие центры, концепция термобаланса
- Термопродукция и поддержание постоянства температуры
- Термопотери: механизмы
- Методики измерения температуры: регионарная t и градиенты
- Специфика терморегуляции у детей
Фармакология
Основные положения
- Фармакокинетика, соединение с белками, коэффициент распределения, ионизации, тканевое потребление
- Элиминация, биотрансформация, конечное действие
Анестетики-газы и жидкости (испаряющиеся)
- Физические свойства
- Механизмы действия
- Эффекты на ЦНС
- Эффекты на циркуляцию
- Эффекты на дыхание
- Эффекты на нейромышечную проводимость
- Эффекты на функцию почек
- Эффекты на функцию печени
- Биотрансформация, токсичность
- Минимальная альвеолярная концентрация
Анестетики интравенозные (опиоиды и неопиоидные анестетики)
- Механизм действия
- Фармакокинетика и фармакодинамика
- Метаболизма и экскреция
- Эффект на циркуляцию
- Эффект на другие органы
- Побочные эффекты
Анестетики местные
- Принцип действия
- Биотрансформация и экскреция
- Сравнительная оценка препаратов и химических групп
- Пролонгированность эффекта
- Токсичность, аллергия, профилактика
Мышечные релаксанты (деполяризующие, недеполяризующие)
- Механизм действия
- Побочные эффекты, не связанные с релаксацией
- Побочные эффекты, связанные с ненормальным действием релаксантов
- Биотрансформация и экскреция
- Пролонгированный эффект, конечное действие
- Антагонисты
- Совместимость с другими лекарственными средствами, антибиотиками
Отдельные группы препаратов:
Влияющие на симпатическую нервную систему:
- передатчики и типы рецепторов
- эффекты на органы мишени, метаболические эффекты
- агонисты: альфа и бета блокаторы, антигипертензивные средства, ганглиоблокаторы, периферические вазодилятаторы
Влияющие на парасимпатическую нервную систему:
- передатчики
- мускариноподобный эффект
- никотиноподобный эффект
- агонисты: холинергические и антихолинестеразные препараты
Сердечные средства.
- Дигиталис: действие и токсичность
- Кардиотонические средства
- Антиаритмические средства
- Антиангинальные препараты
- Вазодилятаторы
- Электролиты: влияние на сердце
Препараты, влияющие на ЦНС (общее действие, сравнительная оценка препаратов; эффект на циркуляцию, дыхание, побочные эффекты).
Пре и постанестетическая медикация:
- опиаты
- антагонисты опиатов, агонист антагонист
- барбитураты
- транквилизаторы: фенотиазины, бутирофеноны, бензодиазепины
- антидепрессанты ингибиторы МАО, трициклические соединения, амфетамины, антипаркинсонические средства
- этиловый спирт
- гипнотики барбитуровые и небарбитуровые
- аналептики; доксапрам, физостигмин, антагонисты бензодиазепинов
- антиэметики, фенотиазины, бутирофеноны, антихолинэргические средства
- антигистаминные средства: механизм действия
- злоупотребление лекарствами и наркомания, толерантность и зависимость
Диуретики (осмотические, др. механизма действия)
- механизм действия
- сравнительная оценка различных средств
- побочные эффекты
- эффект на электролитный баланс и КЩС
- ультрафильтрация
Совместимость препаратов
- белковое связывание
- влияние pH
- энзимная индукция и ингибиция
- кровоток печени
Фармакогенетика
- злокачественная гипертермия (включая терапию)
- дефицит псевдохолинэстеразы
Реакции на препараты (анафилактоидные, анафилактические, токсикоаллергические).
Анатомия
Топографическая анатомия ориентиры
- Шея: участки для трахеотомии, крикоидная мембрана, наружная и внутренняя яремные вены, грудной лимфатический проток, сонная и позвоночная артерии
- Грудная клетка: доли легких, область сердца, места аускультации
- Живот: величина печени
- Таз: вертебральный уровень, топография
- Конечности: взаиморасположение костей, нервы и артерии
Рентгенологическая анатомия грудной клетки.
- контуры сердца, размеры отдельных камер сердца, их увеличение
- средостение, анатомия долей
- структура костей
Респираторная система.
- Нос
- Глотка: отделы глотки, иннервация
- Гортань: иннервация мышц, кровоснабжение хрящей, голосовые связки, их позиция при параличе, различия у взрослых и детей
- Трахея: структура на шее и в грудной клетке
- Легкие: их отделы, бронхоскопическая анатомия, бронхиальная и легочная циркуляция, микроскопическая анатомия
- Дыхательная мускулатура, вспомогательные мышцы
Сердечно сосудистая система.
- Нормальная анатомия сердца и магистральных сосудов
- Проводящая система сердца, иннервация, коронарное кровообращение
- Кровоснабжение других органов
Нервная система
Мозг:
- большие ядра и мосты
- дыхательный центр
- кровоснабжение мозга, Вилизиев круг, венозный дренаж
- Спинной мозг
- вариации вертебральной конфигурации
- спинальные нервы (уровень выхода, покровы, нарушения чувствительности)
- кровоснабжение
- Оболочки мозга, эпидуральное и субарахноидальное пространства.
Автономная нервная система - симпатическая: локализация ганглиев
- парасимпатическая: локализация ганглиев
- черепно-мозговые нервы: глаз, слюнных желез, гортани
- крестцовые нервы: иннервация тазовых органов
- пути реализации вагальных рефлексов
- каротидные и аортальные тельца, каротидный синус
Регионарная анестезия, блокада основных нервных стволов
- Автономных: звездчатый, поясничный, солнечное сплетение
- Голова и шея: шейный
- Конечности: плечевое сплетение, локтевой, лучевой и седалищные нервы, бедренный, латеральный кожный бедренный нерв, запирательный нерв
- Позвоночный столб: интеркостальные нервы, паравертебральные соматические нервы
- Спинной мозг: эпидуральная, каудальная и спинальная блокада
Биохимия
Нормальный метаболизм
Карбонгидраты
- аэробный и анаэробный процессы, энзимы, метаболиты
- взаимоотношения между гормонами: инсулин, гормон роста, глюкокортикоиды, глюкагон, адреналин
- проявление стресса
Белки
- функция, гормоны, антитела
- RN DN, генетические изменения
- циклическая АМР, функция
- специфический органный метаболизм (мозг, сердце)
Регуляция кислотно-щелочного баланса:
- буферные системы
- эффекты нарушения баланса электролитов
- органная перфузия
Водный и электролитный баланс:
- нарушения и регуляция
- водные пространства
Физика
Механика
- Измерение давления газов и жидкостей
- Переходники, регуляторы (редукторы, медицинские газовые баллоны)
Скорость потока
- Упругость, плотность, ламинарный и турбулентный потоки
- Флоуметры: ротаметр, электромагнитный, ультразвуковой, пневмотахограмма
Свойства жидкостей, газов и паров
- Диффузия газов
- Коэффициенты растворимости
- Относительная и абсолютная влажность
- Критическая температура, критическое давление
Газовые законы. Испарители
- Давление паров и расчеты концентрации анестетиков
- Типы испарителей
Поступления и изменения ингаляционных анестетиков
- Кривые поступления и элиминации: эффекты вентиляции, циркуляции, системы циркуляции
- Эффект концентрации
- Вторичные эффекты газов
- Закись азота и закрытые пространства
Типы наркозных аппаратов. Физика дыхательных систем
- Принципы: сопротивление, турбулентный поток, механические мертвое пространство, вспомогательное дыхание, растворимость, потери, газовые смеси, влажность, подогрев
- Составные части: коннекторы, адапторы, маска, эндотрахеальная трубка, дыхателный мешок, выпускной клапан, дыхательные шланги, клапаны
- Классификация: основная: инсуффляция, спонтанное дыхание, закрытый, открытый, полуоткрытый, полузакрытый контуры
- Специфическая: Т-образные системы: Аэра, Джексон Риз, Бена, Меплесона
- Абсорберы: принципы, канистра, эффективность
- Системы дыхания: для взрослых, детей, характеристики
- Системы оксигенации: FiO2
- Системы эвакуации (сброса) газов
Методы мониторинга
- Сосудистые давления: артериальное, центральное венозное давление, давление в легочной артерии, левом предсердии, конечно диастолическое давление в левом желудочке
- Функци сердца: тоны сердца, ЭКГ, эхокардиография, кардиокимография, сердечный выброс
- Функции мозга: ЭЭГ, вызванные потенциалы, мониторинг функции мозга
- Нейромышечная функция: нервные стимуляторы
- Вентиляция: респирометры, сила вдоха
- Концентрация газов: О2, СО2, анестетиков газообразных и паров
- Температура
- Кислород: оксиметрия, чрезкожное О2
Отдельные детали
- Газы крови: электроды для измерения рН, РО2, РСО2, калибровка, температурная коррекция, ошибки
- Концентрация газов: инфракрасная абсорбция, парамагнитный эффект, масс спектрометрия, газовая хроматография, азометр, капнография
- Сердечный выброс: метод Фика, разведения краски, термодилюции
- датчики давления (типы)
- Доплер, осциллометрия
- подогреватели крови
- Эхокардиография
Дыхательные аппараты
- Классификация
- Принципы действия: вспомогательное дыхание, конторальные узлы, ограничивающие давление, избыточный объем, FiO2 контроль, мониторы: давления, содержания кислорода, апное, соотношения вдох/выдох, бактериальные фильтры, дыхание с положительным давлением на выдохе, высокочастотная вентиляция, микробиология, осложнения, адаптация детей с дыхательным аппаратом
- Увлажнители, распылители
- Системы опасности: в операционной, электрическая, в наркозном аппарате, в дыхательных аппаратах, подача О2.Дефибрилляторы: внутренний, наружный, имплантируемый, напряжение и сила тока, синхронизация, размеры электродов и их позиция.
Водители ритма сердца (пейсмейкеры)
- Временные, постоянные (эпикардиальные, эндокардиальные), чрескожные
- Типы: с фиксированным ритмом, синхронизированным, для проведения возбуждения ритма желудочка, предсердия, при предсердножелудочковой блокаде
- Стандартная номенклатура
- Причины неэффективной работы (эффект ожога, наводка)
Опасности взрывов и возгорания при использовании электроприборов
- Причины возгораний: статическое электричество, нарушение правил обращения с кислородным баллоном
- Предупреждение: заземление, изоляция проводов
- Опасности высокого и низкого напряжения тока
Математика
- Логарифмы, графики простых зависимостей, экспотенциальная функция, диаграммы
- Статистика: модель и популяция, вероятность, среднеарифметическая величина, стандартные отклонения и ошибка, Т-тест, Х, корреляция, достоверность
- Компьютер: данные расчетные, данные, характеризующие процессы, данные анализа, применение в анестезиологии
Учебная программа циклов профессиональной подготовки специалистов анестезиологов-реаниматологов.
Содержание:
Модуль 1. Избранные вопросы интраоперационного мониторинга.
- Применение компьютеризированной анестезиологической карты
- Безопасность — основной принцип современной анестезиологии.
- Комплексный мониторинг газообмена в анестезиологии и ИТ
- Осложнения мониторинга
- Оценка транспорта кислорода.
- Мониторинг малого круга кровообращения, функции правого и левого сердца. Новейшие технологии.
- Инвазивный мониторинг кровообращения.
- Современные методы оценки нейро-мышечного блока во время операции и анестезии.
- Пластиковое оборудование для целей интраоперационного мониторинга.
- Неинвазивный мониторинг.
- Персональный компьютер-помощник анестезиолога.
- ЭЭГ-компьютерный мониторинг функции мозга.
- Телемониторинг в практике анестезиолога-реаниматолога. Дистационное обучение.
- Мониторинг кровообращения. Физиологический профиль МХ-04. Формулы для расчета. Типичные ошибки.
- Комплекс мониторного контроля ЭКГ для отделений интенсивной терапии и реанимации.
- Дифференцированный подход к использованию методов оценки производительности сердца у больных в отделениях интенсивной терапии и реанимации.
- Мониторинг респираторной поддержки у больных в отделениях реанимации и интенсивной терапии.
- Достижения и перспективы компьютерной диагностики в интенсивной терапии.
- Оценка кардиореспираторной системы отделения реанимации и интенсивной терапии.
- Мониторинг функции дыхания в интенсивной терапии.
- Компьютерная система поддержания блока нервно-мышечной проводимости.
- Современные компьютерные технологии и прогнозирование внезапной смерти.
- Методы определения внесосудистой жидкости в легких; клиническая трактовка.
- Методология научных исследований в анестезиологии. Юридические и деонтологические аспекты научных исследований во время операции и анестезии.
Модуль 2. Патофизиология хирургического стресса.
- Патофизиология и механизмы гипер — и гипокарбии.
- Патофизиология открытой грудной клетки, искусственной вентиляции легких, искусственной однолегочной вентиляции.
- Физиология и патофизиология дыхания, острая дыхательная недостаточность.
- Физиология и патофизиология кровообращения, острая сердечно-сосудистая недостаточность.
- Клиническая патобиохимия.
- Травматический шок: патогенез, клиника, лечение.
- Инфекционно-токсический шок.
- Респираторный дистресс-синдром, патогенез, клиника, лечение.
- Синдром полиорганной недостаточности.
- Синдром дессиминированного внутрисосудистого свертывания.
- Бронхиальное кровообращение и лимфообращение в легких.
- Нереспираторные функции легких.
Модуль 3. Клиническая фармакология в анестезиологии и интенсивной терапии.
- Фармакодинамика и фармакокинетика в анестезиологии.
- Фармакодинамика и фармакокинетика миорелаксантов.
- Новые опиоиды в анестезиологии.
- Применение альфаадренопозитивных препаратов в анестезиологии и ИТ у больных с сопутствующими заболеваниями легких.
- Наркотические анальгетики в анестезиологии.
- Неопиоидные анальгетики.
- Вазодилятаторы в интенсивной терапии критических состояний.
- Фармакодинамика и фармакокинетика ингаляционных анестетиков.
- Фармакодинамика и фармакокинетика местных анестетиков, и их клиническая трактовка.
- Фармакодинамика и фармакокинетика внутривенных анестетиков. Target control anaesthesia.
- Принципы составления многокомпонентных методов анестезии.
- Современная антибиотикотерапия в анестезии, реанимации и интенсивной терапии: патофизиология. обоснование, принципы, методы.
Модуль 4. Избранные вопросы анестезии в специализированных разделах хирургии.
4.1 Кардио — и торакальная хирургия.
- Регуляция инотропной функции сердца.
- Внутривенная анестезия в кардиохирургии.
- Внутрилегочное шунтирование и методы его коррекции.
- Особенности анестезии при операциях на сердце.
- Анестезиологическое обеспечение больных при операциях на аорте и ее ветвях.
- Методы защиты головного и спинного мозга в хирургии аорты и ее ветвей.
- Анестезиологические проблемы у больных с сопутствующей сердечно-сосудистой патологией.
- Артериальная гипертензия-классификация, возможности коррекции с учетом типа гемодинамики. Значение миокардиальной недостаточности в периоперационном периоде.
- Нарушение газообмена и кровообращения при ТЭЛА, лечение, ИТ.
- Анестезия в эндоскопии и вентиляционное обеспечение бронхологических исследований.
- Диагностика и лечение малого сердечного выброса.
- Сердечно-легочная реанимация.
- Особенности анестезии у больных с ишемической болезнью.
- Факторы кислородотранспортной функции системы кровообращения после операций на сердце.
- Современные аспекты искусственного кровообращения.
- Защита миокарда от ишемических и реперфузионных повреждений.
- Холодовая и кровяная кордиоплегия.
- Особенности анестезии и факторы риска при радикальной коррекции тетрады Фалло.
- Периоперационный инфаркт миокарда (клиника, диагностика, лечение)
- Острая послеоперационная дыхательная недостаточность.
- Клинические аспекты использования электрокардиостимуляции у кардиологических больных.
- Современные аспекты анестезиологического обеспечения в торакальной хирургии: обоснование, принципы, методики.
- Традиционные и специальные методы ИВЛ в торакальной хирургии: методики; гемодинамические, газообменные и метаболические эффекты.
- Особенности анестезиологического обеспечения при больших операциях на трахее и бронхах.
- Интубация трахеи и бронхов в торакальной хирургии.
- ВЧ ИВЛ: механизмы газообмена, аэродинамика, биомеханика.
- Высокочастотная ИВЛ: методы, режимы, аппаратура, оптимизация газообмена, легочного и системного кровообращения.
- Искусственная однолегочная вентиляция: проблемы и решения.
- Респираторная ВЧ-терапия МЭЛхА.
- Некоторые специальные приемы в анестезиологическом обеспечении операций на легких, трахее, бронхах и органах средостения.
- Фармакотерапия синдрома низкого сердечного выброса.
- Ведение послеоперационного периода в кардиохирургии.
- Ведение послеоперационного периода в общей и торакальной хирургии.
- ВЧ ИВЛ терапия микроэмболии легочной артерии (МЭЛА).
- Операционная патофизиология кровообращения. Влияние анестетиков на кровообращение, влияние искусственной вентиляции легких, операционный стресс и его предупреждение. Оценка операционных сдвигов центральной и периферической гемодинамики. Методы изучения и контроля кровообращения в операционной.
- Вопросы клинической фармакологии. Гипотензивные и вазоактивные препараты — ганглиоблокаторы, блокаторы кальциевых канальцев, сердечные гликозиды, антиаритмические препараты.
- Общие принципы инфузионной терапии. Характеристика инфузионных препаратов. Критерии выбора и построения различных инфузионных программ. При операциях на брахиоцефальных сосудах, почечных, аорте и ее ветвях. Методы контроля адекватности инфузионной терапии.
- Общие принципы предоперационной подготовки больных с заболеваниями сердечно-сосудистой системы.
- Гемодинамические эффекты гипер- и гипокарбии.
4.2 В других областях хирургии.
- Анестезия в ИТ и акушерстве.
- Особенности анестезии при гестозах.
- Новые технологии в педиатрической анестезии.
- Амбулаторная анестезия.
- Анестезия в трудных условиях.
- Проблемы нейроанестезии.
- Анестезия в экстренной хирургии.
Модуль 5. Избранные вопросы современной анестезиологической и морфо-функциональной защиты в хирургии.
- Проблема премедикации. Индивидуальная премедикация.
- Тотальная внутривенная анестезия. Современное состояние и перспектива.
- Аллергические и анафилактоидные реакции в анестезиологии.
- Цитогенетические эффекты ингаляционных анестетиков и способы их профилактики.
- Ингаляционная анестезия. Период поддержания. Клиническая фармакология, Критерии адекватности.
- Тотальная внутривенная анестезия. Период поддержания, Клиническая фармакология, критерии адекватности.
- Водно-электролитный баланс, его влияние на эффективность газообмена и коррекция во время операции, анестезии. Принципы построения программ инфузионной терапии.
- Гипертензия во время операции и способы ее коррекции.
- Инфузионная терапия. Принципы построения инфузионных программ.
- Поддержание теплового гомеостаза и его значение в комплексе мероприятий анестезиологической защиты.
- Операционно-анестезиологический риск, выбор метода и техники анестезии.
- Эпидемиологические аспекты анестезиологии и реаниматологии.
- Отсроченная предоперационная подготовка.
- Вводный наркоз.
- Анестезия и ИТ у больных с сахарным диабетом.
- Астматический статус, Современные аспекты ИТ.
- Парэнтеральное питание.
- Селективная деконтаминация желудочно-кишечного тракта.
- Неклостридиальная инфекция в ИТ и анестезиологии.
- Гиповолемический шок.
- Сердечно-легочная реанимация.
- Метаболизм глюкозы во время анестезии. Анестезия и диабет.
- Проблемы массивных гемотрансфузий.
- Диагностика и коррекция нарушений кислотно-основного состояния у хирургических больных.
- Экстрокорпоральная детоксикация в комплексной терапии критических состояний.
- Коррекция нарушений гемодинамики при сепсисе.
Модуль 6. Избранные вопросы регионарных методик анестезии.
- Современные пути развития регионарной анестезии.
- Регионарная анестезия у пациентов с сопутствующей патологией.
- Эпидуральная и спинально-эпидуральная анестезия при операциях на органах брюшной и грудной полости.
- Осложнения регионарной анестезии.
- Продленные методы регионарной анестезии.
- Сбалансированная анестезия на основе регионарных блокад.
- Общая анестезия и варианты вентиляционной поддержки при длительных операциях с микрохирургической техникой.
- Эпидуральная анестезия в акушерстве.
- Комплексный мониторинг газообмена в анестезиологии и ИТ.
- Контролируемая пациентом анальгезия.
Модуль 7. Избранные вопросы респираторной терапии.
- Ларингеальная маска — новый подход к респираторной поддержке во время операции.
- Традиционные и специальные методы ИВЛ в торакальной хирургии: методики; гемодинамические, газообменные и метаболические эффекты. Выбор интубационных трубок. Возможные ошибки, опасности и осложнения
- Интубация трахеи и бронхов в торакальной хирургии.
- Высокочастотная ИВЛ: методы, режимы, аппаратура, оптимизация газообмена, легочного и системного кровообращения.
- Искусственная однолегочная вентиляция: проблемы и решения.
- Патофизиология открытой грудной клетки и искусственной вентиляции легких.
- Респираторная ВЧ-терапия МЭЛхА.
- ВЧ ИВЛ: механизмы газообмена, аэродинамика, биомеханика.
- Нарушение газообмена и кровообращения при ТЭЛА, лечение, ИТ. ВЧ ИВЛ терапия микроэмболии легочной артерии (МЭЛА).
- Методы определения внесосудистой жидкости в легких; клиническая трактовка.
- Миорелаксанты и восстановление спонтанного дыхания после операции, анестезии и ИВЛ.
- Астматический статус, Современные аспекты ИТ.
- Вентиляционное обеспечение бронхологических исследований.
- Масочные методы респираторной поддержки.
- Респираторная поддержка у больных в отделениях реанимации и интенсивной терапии.
- Оценка кардиореспираторной системы отделения реанимации и интенсивной терапии.
- Мониторинг функции дыхания в интенсивной терапии.
- Комплексный мониторинг газообмена в анестезиологии и ИТ. Оценка транспорта кислорода.
Модуль 8. Достижения современной анестезиологии и реаниматологии (интенсивной терапии).
- Организационные и юридические основы службы анестезиологии. Этические и деонтологические аспекты.
- Современные фармакологические средства для общей и местной анестезии. Фармакодинамика и фармакокинетика.
- Современные принципы защиты больного в период воздействия хирургического стресса.
- Наркозно-дыхательная и контрольно-диагностическая аппаратура.
- Мониторинг в современной операционной.
- Анестезия у больных с хирургической патологией сердца и сосудов.
- Анестезия и искусственная вентиляция легких в торакальной хирургии.
- Анестезия при инструментальных методах диагностики и лечения.
- Особенности анестезиологического обеспечения длительных операций в восстановительно-пластической хирургии.
- Лечение хронического болевого синдрома.
- Регионарные методы анестезии, эпидуральная и спинальная анестезия.
- Дезинфекция и стерилизация наркозно-диагностической аппаратуры.
- Иммунные реакции при анестезии.
- Основы социальной гигиены.
- Клиническая физиология и биохимия
- Анестезия и интенсивная терапия в травматологии и ортопедии.
- Анестезия и интенсивная терапия при операциях у больных с сопутствующими заболеваниями.
- Реанимация и интенсивная терапия при сердечно-сосудистой недостаточности.
- Реанимация и интенсивная терапия при острых заболеваниях печени, желудочно-кишечного тракта, поджелудочной железы и почек
Модуль 9. Нарушение гомеостаза и их коррекция во время операции и анестезии.
- Гипоксия
- Балланс жидкости в организме и его коррекция
- Синдром иммунного дефицита (AIDS)
- Осложнение инвазивного мониторинга
- Кислородный гомеостаз в условиях анестезии и интенсивной терапии.
- Диагностика, профилактика и коррекция нарушений кислородного гомеостаза
- Контроль гумморального гомеостаза во время операции и анестезии. Лабораторные методы экспресс-диагностики.
- Анестезиологические проблемы, связанные с нарушением функций ферментов.
Модуль 10. Анестезия у больных с сопутствующими заболеваниями.
- Анестезия у больных с заболеваниями крови.
- Анестезия и интенсивная терапия у больных с ожирением.
- Анестезия и интенсивная терапия у больных с заболеваниями печени.
- Токсемия беременных.
- Анестезия и диабет
- Злокачественная гипертермия.
Модуль 11. Анестезия и интенсивная терапия при реконструктивных операциях на органах грудной и брюшной полости.
- Основные принципы анестезиологического обеспечения операции на сердце и магистральных сосудах.
- Анестезиологические проблемы современной торакальной хирургии.
- Основные аспекты анестезиологического пособия при реконструктивных операциях на пищеводе, желудке, печени, желчных путях.
- Актуальные вопросы анестезии при реконструктивных операциях, выполняемых с микрохирургической техникой.
- Анестезиологическое обеспечение диагностических эндоскопических процедур в амбулаторной практике.
- Принципы анестезии при пересадке органов.
- ГБО в реконструктивной хирургии.
- Интраоперационный компьютерный мониторинг жизненно-важных функций организма и безопасность в анестезиологии.
Жизнь после операции коррекции приобретенного порока сердца
Итак, пациенту успешно проведена операция. Что дальше? Из операционной пациент переводится в отделение реанимации, где находится под пристальным наблюдением бригады реаниматологов в течение 24-48 часов. В ближайшие после операции, 2-3 часа пациент просыпается от наркоза, его отключают от аппарата искусственной вентиляции легких и он может разговаривать. На следующее утро пациент уже может сидеть на кровати и самостоятельно принимать пищу. На 2-е сутки после операции (прошедшей без осложнений), пациентов уже переводят в общую палату отделения, где за ними продолжает наблюдение медицинский персонала, оперировавший хирург. Проводятся ежедневные перевязки и, параллельно, подбор лекарственной терапии.
Примерно, на 9 сутки снимаются послеоперационные швы и пациенты переводятся на следующий этап лечения в кардиологическое отделение городской больницы либо в профильный кардиологический санаторий «Сосновая горка».
Единственным неудобством для пациентов с механическими клапанами является пожизненный приём ВАРФАРИНА под контролем МНО или ПТИ. Но следует знать, что современный механический клапан, при правильном подборе и постоянном приёме антикоагулянтов, прослужит Вам долгую жизнь.
Но ВАРФАРИН необходимо принимать ВСЕГДА! И какой бы механический клапан Вы бы не имплантировали, весь труд хирурга пойдёт на смарку, если Вы не будете соблюдать правильный приём антикоагулянтов.
Также важна профилактика инфекционного эндокардита у больных с искусственными клапанами сердца. При стоматологических процедурах (требующих манипуляций в гингивальной и периапикальной зонах зуба или перфорации слизистой ротовой полости, включая работу с корнем и снятие зубного камня) следует принять:
1) амоксициллин 2 г внутрь за 1 час до процедуры, или
2) ампициллин 2 г в/м или в/в за 30 мин до процедуры или
3) клиндамицин(линкамицин) 600 мг в/м за 1 час до процедуры при аллергии на пенициллин или ампициллин.
Помните, у Вас была открытая операция на сердце и, чтобы правильно срослась грудина, важно первые 4–6 недель:
- не водить машину самостоятельно;
- ездить на заднем сиденье;
- ограничить подъемы тяжестей руками и вставать с сиденья, опираясь на ноги (!). То есть, вставать «ногами»;
- не поднимать на руки детей и животных;
- не подвешивать грузы на ремне, расположенном на талии;
- обуваясь, необходимо держать ногу на плоскости выше или «пересекать» голеностопным суставом уровень противоположного бедра, а не наклоняться всем корпусом тела вниз к ноге;
- не открывать туго закрытые крышки, тяжелые створки окон или дверей;
- рекомендуется принимать душ, сидя боком, используя специальный стульчик, что позволит минимизировать воздействие на грудную клетку.
- при совершении каких-либо действий необходимо выполнять их двумя руками, а также исключать действия, которые требуют отведение рук за спину.
В последующие 8–12 недель следует ограничить следующие действия:
- не поднимать тяжести более 5 кг;
- быть осторожным при изменении положения тела,избегая подъема тяжести; пользоваться в этих случаях ногами;
- не вращать верхней частью тела, не протирать, не чистить поверхности;
- избегать подметания пола, плавания, езды на велосипеде;
- избегать занятия энергичными видами спорта/деятельности (гольф, теннис, плавание и т.д.) в течение 3 мес.;
- прежде чем возобновить данные виды деятельности, необходима консультация врача;
- при ощущении щелчка, хлопка, треска, скрипа в грудине – немедленно обратиться к хирургу.
Во всем остальном обычном, ежедневном поведении, можете не нарушать сложившихся привычек. Естественно, если эти привычки – не вредные.
Механическая вентиляция
Что такое механический вентилятор?
Механический вентилятор — это аппарат, который помогает пациенту дышать (вентилировать), когда он переносит операцию или не может дышать самостоятельно из-за тяжелого заболевания. Пациент подключен к аппарату искусственной вентиляции легких с помощью полой трубки (искусственного дыхательного пути), которая проходит у него во рту и спускается в основной дыхательный путь или трахею. Они остаются на аппарате ИВЛ до тех пор, пока не станут достаточно хорошо, чтобы дышать самостоятельно.
Почему мы используем механические вентиляторы?
Механический вентилятор используется для уменьшения работы дыхания до тех пор, пока состояние пациента не улучшится настолько, что он больше не понадобится. Аппарат обеспечивает поступление в организм достаточного количества кислорода и удаление углекислого газа. Это необходимо, когда определенные заболевания препятствуют нормальному дыханию.
Каковы преимущества механической вентиляции легких?
Основные преимущества механической вентиляции:
- Пациенту не нужно так много работать, чтобы дышать — его дыхательные мышцы отдыхают.
- Пациенту нужно время на восстановление в надежде, что дыхание снова станет нормальным.
- Помогает пациенту получать достаточное количество кислорода и выводит углекислый газ.
- Сохраняет стабильные дыхательные пути и предотвращает травмы от аспирации.
Важно отметить, что искусственная вентиляция легких не излечивает пациента. Скорее, это дает пациенту шанс быть стабильным, пока лекарства и лечение помогают ему выздороветь.
Каковы риски механической вентиляции легких?
Основной риск искусственной вентиляции легких — это инфекция, поскольку искусственный дыхательный путь (дыхательная трубка) может позволить микробам проникнуть в легкие.Этот риск заражения увеличивается по мере необходимости более длительной механической вентиляции и достигает максимума примерно через две недели. Другой риск — повреждение легких, вызванное либо чрезмерным раздувом, либо повторяющимся открытием и схлопыванием небольших воздушных мешочков (Ialveoli) легких. Иногда пациентов невозможно отлучить от аппарата ИВЛ, и им может потребоваться длительная поддержка. Когда это происходит, трубка удаляется изо рта и заменяется на более мелкие дыхательные пути в шее. Это называется трахеостомией. Использование аппарата ИВЛ может продлить процесс смерти, если считается, что выздоровление пациента маловероятно.
Какие процедуры могут помочь пациенту с искусственным дыханием, подключенным к аппарату искусственной вентиляции легких?
- Отсасывание: Это процедура, при которой катетер (тонкая полая трубка) вставляется в дыхательную трубку, чтобы помочь удалить выделения (слизь). Эта процедура может вызвать у пациента кашель или рвоту, и на нее может быть неудобно смотреть. Кроме того, во время всасывания в выделениях может появиться кровавый оттенок. Важно понимать, что это жизненно важная процедура для очистки дыхательных путей от выделений.
- Лекарства в аэрозольной форме (спреи): Пациенту могут потребоваться лекарства, которые вводятся через дыхательную трубку. Эти лекарства могут быть нацелены на дыхательные пути или легкие и могут быть более эффективными при доставке таким образом.
- Бронхоскопия : В этой процедуре врач вводит небольшой светильник с камерой в дыхательные пути пациента через дыхательную трубку. Это очень эффективный инструмент для проверки дыхательных путей в легких. Иногда врач берет образцы слизи или ткани, чтобы направлять терапию пациента.
Как долго пациент остается подключенным к аппарату искусственной вентиляции легких?
Основное назначение аппарата ИВЛ — дать пациенту время на выздоровление. Обычно, как только пациент может самостоятельно дышать, его отключают от аппарата искусственной вентиляции легких.
Лица, осуществляющие уход, проведут серию тестов, чтобы проверить способность пациента дышать самостоятельно. Когда причина проблемы с дыханием устранена и становится очевидным, что пациент может эффективно дышать самостоятельно, их снимают с аппарата ИВЛ.
Кто ухаживает за пациентом на аппарате искусственной вентиляции легких?
- Врач: Врач, как правило, анестезиолог, пульмонолог или реаниматолог (терапевт). Эти врачи прошли специальную подготовку в области искусственной вентиляции легких и занимаются искусственной вентиляцией легких и ежедневно заботятся о таких пациентах.
- Практикующая медсестра: Практикующая медсестра помогает врачу оценивать состояние пациента и составлять заказы на терапию.Практикующие медсестры в отделениях интенсивной терапии проходят специальную подготовку по уходу за пациентами, подключенными к аппаратам искусственной вентиляции легких.
- Дипломированная медсестра: Дипломированные медсестры, ухаживающие за пациентами на ИВЛ, прошли специальную подготовку по уходу за этими пациентами.
- Респираторный терапевт: Респираторный терапевт обучен оценке, лечению и уходу за пациентами с респираторными (дыхательными) заболеваниями и пациентами с искусственными дыхательными путями, подключенными к аппаратам искусственной вентиляции легких.
- Сотрудник по уходу за пациентом: Сотрудник по уходу за пациентом обучен уходу за пациентами в условиях интенсивной терапии.
Практика интраоперационной ИВЛ у пациентов торакальной хирургии и ее связь с послеоперационными легочными осложнениями: результаты многоцентрового проспективного наблюдательного исследования | BMC Anesthesiology
Weiser TG, Regenbogen SE, Thompson KD, Haynes AB, Lipsitz SR, Berry WR, Gawande AA.Оценка глобального объема хирургических операций: стратегия моделирования на основе имеющихся данных. Ланцет. 2008. 372 (9633): 139–44.
Артикул
Google Scholar
Бейнбридж Д., Мартин Дж., Аранго М., Ченг Д., Доказательное исследование периоперационных клинических исходов G. Периоперационная и связанная с анестезией смертность в развитых и развивающихся странах: систематический обзор и метаанализ. Ланцет. 2012. 380 (9847): 1075–81.
Артикул
Google Scholar
Следователи LV. Эпидемиология, практика вентиляции и исходы для пациентов с повышенным риском послеоперационных легочных осложнений: LAS VEGAS — обсервационное исследование в 29 странах. Eur J Anaesthesiol. 2017; 34 (8): 492–507.
Артикул
Google Scholar
Сентурк М. Новые концепции управления однокомпонентной вентиляцией легких. Curr Opin Anaesthesiol. 2006; 19 (1): 1–4.
Артикул
Google Scholar
Severgnini P, Selmo G, Lanza C, Chiesa A, Frigerio A, Bacuzzi A, Dionigi G, Novario R, Gregoretti C, de Abreu MG, et al. Защитная механическая вентиляция легких во время общей анестезии при открытых операциях на брюшной полости улучшает послеоперационную функцию легких. Анестезиология. 2013. 118 (6): 1307–21.
CAS
Статья
Google Scholar
Hemmes SN, Serpa Neto A, Schultz MJ. Интраоперационные вентиляционные стратегии для предотвращения послеоперационных легочных осложнений: метаанализ.Curr Opin Anaesthesiol. 2013. 26 (2): 126–33.
Артикул
Google Scholar
Сеть исследователей PROVE для сети клинических испытаний Европейского общества анестезиологов; Сабрин Н. Т. Хеммес, Марсело Гама де Абреу, Пелози П., Шульц М.Дж. Сравнение высокого и низкого положительного давления в конце выдоха во время общей анестезии при открытой абдоминальной хирургии (исследование PROVHILO): многоцентровое рандомизированное контролируемое исследование. Ланцет. 2014. 384 (9942): 495–503.
Янг К.С., Харрис Е.М., Ваккиано С., Боднар С., Букови Б., Эллиотт Р.Р.Д., Мильярез Дж., Рагейн С., Третуэи Б., Вудворд А. и др. Защитная вентиляция легких для хирургического пациента: согласованные рекомендации международных экспертов. Br J Anaesth. 2019; 123 (6): 898–913.
Артикул
Google Scholar
Hemmes SN, de Abreu MG, Pelosi P, Schultz MJ. Сеть клинических исследований ESA 2012: LAS VEGAS — местная оценка вентиляции легких во время общей анестезии при хирургии и ее влияние на послеоперационные легочные осложнения: проспективное, наблюдательное, международное, многоцентровое когортное исследование.Eur J Anaesthesiol. 2013. 30 (5): 205–7.
Артикул
Google Scholar
Арозулла А.М., Дейли Дж., Хендерсон В.Г., Хури С.Ф. Многофакторный индекс риска для прогнозирования послеоперационной дыхательной недостаточности у мужчин после обширных некардиальных операций. Программа повышения качества хирургической помощи Национальной администрации ветеранов. Ann Surg. 2000. 232 (2): 242–53.
CAS
Статья
Google Scholar
Арозулла А.М., Хури С.Ф., Хендерсон В.Г., Дейли Дж., Участники Национального исследования по улучшению качества хирургии ветеранов П. Разработка и проверка многофакторного индекса риска для прогнозирования послеоперационной пневмонии после серьезной некардиальной хирургии. Ann Intern Med. 2001. 135 (10): 847–57.
CAS
Статья
Google Scholar
Канет Дж., Галларт Л., Гомар С., Палузи Дж., Валлес Дж., Кастильо Дж., Сабате С., Мазо В., Брионес З., Санчис Дж. И др.Прогнозирование послеоперационных легочных осложнений в популяционной хирургической когорте. Анестезиология. 2010. 113 (6): 1338–50.
Артикул
Google Scholar
Smetana GW. Предоперационная оценка легких: выявление и снижение риска легочных осложнений. Cleve Clin J Med. 2006; 73 (Приложение 1): S36–41.
Артикул
Google Scholar
Гулднер А., Поцелуй Т., Серпа Нето А., Хеммес С.Н., Канет Дж., Спит П.М., Рокко П.Р., Шульц М.Дж., Пелоси П., Гама де Абреу М.Интраоперационная защитная механическая вентиляция для профилактики послеоперационных легочных осложнений: всесторонний обзор роли дыхательного объема, положительного давления в конце выдоха и маневров по рекрутменту легких. Анестезиология. 2015; 123 (3): 692–713.
Артикул
Google Scholar
Серпа Нето А., Хеммес С. Н., Барбас С. С., Бейдерлинден М., Биль М., Биннекаде Дж. М., Канет Дж., Фернандес-Бустаманте А., Футье Е., Гаджич О. и др.Защитная вентиляция в сравнении с традиционной вентиляцией в хирургии: систематический обзор и индивидуальные данные пациента. Метаанализ. Анестезиология. 2015; 123 (1): 66–78.
Артикул
Google Scholar
Futier E, Marret E, Jaber S. Периоперационная вентиляция с положительным давлением: комплексный подход к улучшению лечения легких. Анестезиология. 2014. 121 (2): 400–8.
Артикул
Google Scholar
Слуцкий А.С., Раньери ВМ. Повреждение легких, вызванное искусственной вентиляцией легких. N Engl J Med. 2013. 369 (22): 2126–36.
CAS
Статья
Google Scholar
Поцелуй Т., Виттенштейн Дж., Беккер К., Бирр К., Циннелла Дж., Коэн Е., Эль-Тахан М.Р., Фалькао Л.Ф., Грегоретти С., Гранелл М. и др. Защитная вентиляция с высоким или низким положительным давлением в конце выдоха во время вентиляции одного легкого для торакальной хирургии (PROTHOR): протокол исследования для рандомизированного контролируемого исследования.Испытания. 2019; 20 (1): 213.
CAS
Статья
Google Scholar
Маррет Э., Чинотти Р., Берард Л., Пириу В., Джобард Дж., Барруканд Б., Раду Д., Джабер С., Боннет Ф, PPVsg. Защитная вентиляция во время анестезии снижает количество серьезных послеоперационных осложнений после операции по поводу рака легкого: двойное слепое рандомизированное контролируемое исследование. Eur J Anaesthesiol. 2018; 35 (10): 727–35.
Артикул
Google Scholar
Лозер Дж., Слингер П. Повреждение легкого после вентиляции одного легкого: обзор патофизиологических механизмов, влияющих на вентилируемое и спавшееся легкое. Anesth Analg. 2015; 121 (2): 302–18.
Артикул
Google Scholar
фон Эльм Э., Альтман Д.Г., Эггер М., Покок С.Дж., Гоцше П.К., Ванденбрук Дж. П., Инициатива С. Утверждение об усилении отчетности по обсервационным исследованиям в эпидемиологии (STROBE): руководство по составлению отчетов о наблюдательных исследованиях.Int J Surg. 2014; 12 (12): 1495–9.
Артикул
Google Scholar
Бендиксен Х. Х., Хедли-Уайт Дж., Лейвер МБ. Нарушение оксигенации у хирургических больных во время общей анестезии с контролируемой вентиляцией. Понятие об ателектазе. N Engl J Med. 1963; 269: 991–6.
CAS
Статья
Google Scholar
Бенумоф Дж. Традиционное и дифференциальное ведение легких при однолегочной вентиляции.В кн .: Анестезия при торакальной хирургии. Филадельфия: Сондерс, Вирджиния; 1995. стр. 799.
Стропальщик П. Периоперационная травма легкого. Лучшая практика Res Clin Anaesthesiol. 2008. 22 (1): 177–91.
Артикул
Google Scholar
Futier E, Constantin JM, Paugam-Burtz C, Pascal J, Eurin M, Neuschwander A, Marret E, Beaussier M, Gutton C., Lefrant JY, et al. Испытание интраоперационной вентиляции с низким дыхательным объемом в абдоминальной хирургии.N Engl J Med. 2013. 369 (5): 428–37.
CAS
Статья
Google Scholar
Blank RS, Colquhoun DA, Durieux ME, Kozower BD, McMurry TL, Bender SP, Naik BI. Управление односторонней вентиляцией легких: влияние дыхательного объема на осложнения после торакальной хирургии. Анестезиология. 2016; 124 (6): 1286–95.
Артикул
Google Scholar
Колкухун Д.А., Наик Б.И., Дюрье М.Э., Шанкс А.М., Хетерпал С.П., Бендер С.П., Бланк Р.С., следователи М.Управление вариациями вентиляции одним легким и тенденции в клинической практике: отчет группы многоцентровых периоперационных результатов. Anesth Analg. 2018; 126 (2): 495–502.
Артикул
Google Scholar
Бланк РС, Леш РЭ. Вентиляция с низким дыхательным объемом у хирургического пациента: не особенно низкая и, возможно, не особенно защитная. Anesth Analg. 2019; 128 (4): 831–3.
Артикул
Google Scholar
Ball L, Hemmes SNT, Serpa Neto A, Bluth T, Canet J, Hiesmayr M, Hollmann MW, Mills GH, Vidal Melo MF, Putensen C и др. Параметры интраоперационной вентиляции и их связи с послеоперационными легочными осложнениями у пациентов с ожирением. Br J Anaesth. 2018; 121 (4): 899–908.
CAS
Статья
Google Scholar
Baudouin SV. Травма легкого после торакотомии. Br J Anaesth. 2003. 91 (1): 132–42.
CAS
Статья
Google Scholar
Цао С., Луи Б.Е., Мелфи Ф, Веронези Дж., Раззак Р., Романо Дж., Новеллис П., Ранганат Н.К., Парк Б.Дж. Влияние легочной функции на легочные осложнения после роботизированной торакоскопической лобэктомии. Eur J Cardiothorac Surg. 2020; 57 (2): 338–342.
Им И, Пак Х.Й., Шин С., Шин Ш, Ли Х, Ан Дж. Х., Сон И, Чо Дж. Х., Ким Х. К., Зо Джи и др. Распространенность и факторы риска легочных осложнений после радикальной резекции у здоровых пожилых пациентов с раком легкого на ранней стадии.Respir Res. 2019; 20 (1): 136.
Артикул
Google Scholar
Серпа Нето А., Хеммес С. Н., Барбас С. С., Бейдерлинден М., Фернандес-Бустаманте А., Футье Е., Холлманн М. В., Джабер С., Козиан А., Ликер М. и др. Заболеваемость и смертность, связанные с послеоперационным повреждением легких, у пациентов, перенесших абдоминальные или торакальные операции: систематический обзор и метаанализ. Ланцет Респир Мед. 2014. 2 (12): 1007–15.
Артикул
Google Scholar
Комитет по написанию PCGotPVNftCTNotESoA, Bluth T, Serpa Neto A, Schultz MJ, Pelosi P, Gama de Abreu M. Влияние интраоперационного высокого положительного давления в конце выдоха (PEEP) с маневрами набора по сравнению с низким PEEP на послеоперационные легочные осложнения у пациентов с ожирением : Рандомизированное клиническое испытание. ДЖАМА. 2019; 321 (23): 2292–305.
Артикул
Google Scholar
Пелоси П., Рокко П.Р., Гама де Абреу М. Закройте легкие и держите их в покое, чтобы минимизировать повреждение легких, вызванное вентилятором.Crit Care. 2018; 22 (1): 72.
Артикул
Google Scholar
% PDF-1.4
%
232 0 объект
>
эндобдж
xref
232 84
0000000016 00000 н.
0000002611 00000 н.
0000002770 00000 н.
0000004128 00000 н.
0000004163 00000 п.
0000004316 00000 н.
0000004466 00000 н.
0000004719 00000 н.
0000005247 00000 н.
0000005756 00000 н.
0000005998 00000 н.
0000006259 00000 н.
0000006309 00000 н.
0000006359 00000 н.
0000006473 00000 н.
0000006823 00000 н.
0000022323 00000 п.
0000022463 00000 п.
0000023069 00000 п.
0000023316 00000 п.
0000023428 00000 п.
0000023455 00000 п.
0000023954 00000 п.
0000024540 00000 п.
0000024567 00000 п.
0000024698 00000 п.
0000025012 00000 п.
0000040405 00000 п.
0000040773 00000 п.
0000053553 00000 п.
0000065347 00000 п.
0000079939 00000 н.
0000096704 00000 п.
0000111226 00000 н.
0000125913 00000 н.
0000126096 00000 н.
0000126343 00000 п.
0000139415 00000 н.
0000142251 00000 н.
0000142337 00000 н.
0000150195 00000 н.
0000150265 00000 н.
0000150633 00000 н.
0000164072 00000 н.
0000164333 00000 н.
0000173660 00000 н.
0000173764 00000 н.
0000173833 00000 н.
0000173903 00000 н.
0000173981 00000 н.
0000174147 00000 н.
0000174264 00000 н.
0000175448 00000 н.
0000175745 00000 н.
0000176101 00000 н.
0000185225 00000 н.
0000185264 00000 н.
0000186316 00000 н.
0000186355 00000 н.
0000186601 00000 н.
0000186949 00000 н.
0000187290 00000 н.
0000187436 00000 н.
0000187585 00000 н.
0000187979 00000 н.
0000188372 00000 н.
0000188493 00000 н.
0000188642 00000 н.
0000188848 00000 н.
0000189054 00000 н.
0000189270 00000 н.
0000189849 00000 н.
00001 00000 н.
0000191009 00000 н.
0000192184 00000 н.
0000192390 00000 н.
0000192599 00000 н.
0000192808 00000 н.
0000193023 00000 н.
0000193236 00000 н.
0000193444 00000 н.
0000193655 00000 н.
0000002432 00000 н.
0000001976 00000 н.
трейлер
] / Назад 289945 / XRefStm 2432 >>
startxref
0
%% EOF
315 0 объект
> поток
hb«b`b`c` Ab,? F
Механическая вентиляция в отделении интенсивной терапии
Механическая вентиляция легких — одно из наиболее распространенных вмешательств, проводимых в отделении интенсивной терапии.Более половины пациентов в отделении интенсивной терапии вентилируются в первые 24 часа после поступления в отделение интенсивной терапии; состоит из лиц с острой дыхательной недостаточностью, нарушением функции легких, затрудненным дыханием или неспособностью защитить свои дыхательные пути. Основная функция легких — добавлять кислород и удалять CO2 из крови, проходящей через капиллярное русло легких. Легкие поражены миллионом альвеол (гроздей винограда), цепляющихся друг за друга и попадающих в бронхиолярное дерево через приточную сеть дыхательных путей, в конечном итоге попадающих в главные бронхи и трахею.Существует несколько режимов поддержки искусственной вентиляции легких, которые обеспечивают подачу воздуха пациенту в зависимости от давления, потока и объема. Хотя ИВЛ спасает жизнь, она может быть связана с опасными для жизни осложнениями, включая утечку воздуха и пневмонию.
Многие состояния предрасполагают пациентов к острому повреждению легких. Общей чертой острого повреждения легких является активация лейкоцитов (нейтрофилов) и воспаление легких. Причины острой дыхательной недостаточности могут быть внелегочными, такими как внутрибрюшный сепсис, панкреатит или внутричерепная гипертензия; или причина может быть внутрилегочной, такой как пневмония, ушиб легкого или аспирация.Когда человеку больше не нужна механическая вентиляция, его можно отлучить от аппарата ИВЛ. Все кандидаты на отлучение должны иметь адекватную оксигенацию, адекватную элиминацию углекислого газа, адекватную силу и резерв дыхательных мышц, а также способность защищать свои дыхательные пути. После выполнения этих условий ряд легко получаемых прикроватных параметров можно использовать для прогнозирования вероятности снятия пациента с опоры аппарата ИВЛ. Параметры включают минутную вентиляцию, спирометрию, соотношение PA02 / FI02 и индекс быстрого поверхностного дыхания.Неинвазивная вентиляция (CPAP или BIPAP) относится к использованию техник искусственной вентиляции легких, которые не обходят верхние дыхательные пути. Это может оказаться очень полезным для пациентов с отеком легких из-за сердечной недостаточности, пациентов с ослабленным иммунитетом, после аспирации или обострения хронической обструктивной болезни легких. Неинвазивная вентиляция также может служить мостом между экстубацией и спонтанной вентиляцией, когда пациент дышит самостоятельно. Измерения адекватности дыхания включают использование газов артериальной крови, пульсоксиметрию и измерение CO2 в конце выдоха.
Фактов:
790 257 госпитализаций с применением ИВЛ в 2005 г., что составляет 2,7 эпизода ИВЛ на 1000 населения; оценочные национальные расходы составили 27 миллиардов, что составляет 12% всех затрат на больницу.
Острое повреждение легких и синдром острого респираторного дистресса оценивались в 86,2 / 100,000 и 64,0 / 100,000 человеко-лет соответственно.
В 2004 году общий уровень смертности 49 688 пациентов из 349 отделений интенсивной терапии составил 31%, в то время как госпитальная летальность составила 37%.
В когортном исследовании с использованием записей о выписке из больниц за 2005 год из шести штатов (Массачусетс, Мэриленд, Нью-Джерси, Нью-Йорк, Техас и Вашингтон) наблюдались следующие статистические данные:
-Больничная летальность пациентов, находящихся на ИВЛ, составила 34,5%, и только 30,8% пациентов были выписаны из больницы домой.
— 44,6% имели хотя бы одно серьезное сопутствующее заболевание; наиболее частыми сопутствующими заболеваниями были диабет (13,2%) и легочные заболевания (13,2%).2%)
-Ежедневные дополнительные затраты на ИВЛ для пациентов ОИТ оцениваются от 600 до 1500 долларов в день
— Средняя продолжительность пребывания составила 14,1 +/- 16,9 дней, что составляет 7,1% больничных дней
-Средние затраты на больницу составили 34 257 долларов (+/- 40 559 долларов) с более низкими средними затратами в сельских и небольших больницах.
Прекращение ИВЛ продолжает оставаться одним из самых сложных событий в управлении интенсивной терапией, и значительная часть времени, проводимого на аппарате ИВЛ (40%), посвящается отлучению от груди..
Как преждевременная, так и отсроченная экстубация связаны с неблагоприятными исходами. Время экстубации имеет решающее значение. Время и метод отлучения варьируются среди врачей.
Веб-сайтов:
http://www.thoracic.org/clinical/critical-care/patient-information/index.php от Американского торакального общества — здесь есть отличная информация, хотя навигация немного неудобна.
http://www.thoracic.org/clinical/critical-care/patient-information/icu-devices-and-procedures/mechanical-ventilator.php
Раздел по отлучению от вентиляционного отверстия:
http://www.thoracic.org/clinical/critical-care/patient-information/icu-devices-and-procedures/weaning-from-mechanical-ventilation.php
Секция на аппарате ИВЛ
http://www.nhlbi.nih.gov/health/dci/Diseases/vent/vent_what.html
От Национального института сердца, легких и крови — о механических вентиляторах
http://www.nlm.nih.gov/medlineplus/criticalcare.html
От MedlinePlus — множество хороших ссылок и PDF-файлов
Статей:
Эпидемиология искусственной вентиляции легких в США.H Wunsch, W. Linde-Zwirble, D Angus, M Hartman, E. Milbrandt, J Kahn. Crit Care Med 2010; 38: 1947-1953
Механическая вентиляция: эпидемиологические исследования современной практики. Э. Голигер, Н. Фергюсон. Curr Opin Crit Care 15: 44-51
Эпидемиологические исследования современной практики. Э. Голигер, Н. Фергюсон. Curr Opin Crit Care. 2009, 15: 44-51
Эпидемиология ИВЛ: анализ базы данных SAPS 3. П. Метниц, Б. Метниц, Р. Морено, П. Бауэр, Л. Дель Сорбо, С. Хоерманн, С. Афонсу де Карвалью, В. Раньери.Intensive Care Med 2009 35: 816-825
Автор: Орландо Киртон, доктор медицины (2011)
% PDF-1.4
%
431 0 объект
>
endobj xref
431 102
0000000044 00000 н.
0000003099 00000 н.
0000003342 00000 п.
0000003402 00000 п.
0000003935 00000 н.
0000004036 00000 н.
0000004204 00000 н.
0000004263 00000 н.
0000004431 00000 н.
0000004490 00000 н.
0000004656 00000 н.
0000004715 00000 н.
0000004883 00000 н.
0000004942 00000 н.
0000005110 00000 н.
0000005169 00000 н.
0000005337 00000 н.
0000005396 00000 н.
0000005564 00000 н.
0000005732 00000 н.
0000005791 00000 н.
0000005959 00000 н.
0000006018 00000 н.
0000006186 00000 п.
0000006246 00000 н.
0000006393 00000 п.
0000006422 00000 н.
0000006595 00000 н.
0000006867 00000 н.
0000007333 00000 п.
0000007409 00000 н.
0000007718 00000 н.
0000008112 00000 н.
0000008471 00000 п.
0000008744 00000 н.
0000010226 00000 п.
0000010433 00000 п.
0000010748 00000 п.
0000011022 00000 п.
0000011642 00000 п.
0000012454 00000 п.
0000013145 00000 п.
0000013418 00000 п.
0000021197 00000 п.
0000021303 00000 п.
0000021731 00000 п.
0000022159 00000 п.
0000022435 00000 п.
0000025750 00000 п.
0000025872 00000 п.
0000025996 00000 н.
0000026035 00000 п.
0000028689 00000 п.
0000029464 00000 н.
0000030183 00000 п.
0000030873 00000 п.
0000031604 00000 п.
0000032302 00000 п.
0000033038 00000 п.
0000033455 00000 п.
0000033735 00000 п.
0000033826 00000 п.
0000033972 00000 п.
0000034058 00000 п.
0000034163 00000 п.
0000034223 00000 п.
0000034368 00000 п.
0000034454 00000 п.
0000034546 00000 п.
0000034606 00000 п.
0000034698 00000 п.
0000034758 00000 п.
0000034887 00000 п.
0000034947 00000 п.
0000035065 00000 п.
0000035125 00000 п.
0000035234 00000 п.
0000035294 00000 п.
0000035398 00000 п.
0000035459 00000 п.
0000035571 00000 п.
0000035632 00000 п.
0000035718 00000 п.
0000035779 00000 п.
0000035839 00000 п.
0000035899 00000 н.
0000036007 00000 п.
0000036068 00000 п.
0000036201 00000 п.
0000036285 00000 п.
0000036382 00000 п.
0000036443 00000 п.
0000036533 00000 п.
0000036594 00000 п.
0000036655 00000 п.
0000036716 00000 п.
0000036814 00000 п.
0000036875 00000 п.
0000036959 00000 п.
0000037019 00000 п.
0000037079 00000 п.
0000002396 00000 н.
трейлер
] / Назад 725177 / Размер 533 / Корень 432 0 R
>>
startxref
0
%% EOF
532 0 объект
>
транслировать
xc«b`f`g`ad @
Механическая вентиляция и ЭКМО — Бригам и женская больница
Механическая вентиляция легких — это процедура жизнеобеспечения, которая помогает людям дышать, когда они не могут дышать самостоятельно.В зависимости от состояния здоровья пациента вентилятор, также называемый респиратором или дыхательным аппаратом, может поддерживать или полностью контролировать дыхание в течение короткого или длительного периода времени. При традиционной искусственной вентиляции легких пациент подключается к аппарату ИВЛ через трубку во рту (эндотрахеальная трубка) или в шее (трахеостомическая трубка). Неинвазивная вентиляция легких — это новый метод лечения, проводимый через маску. Искусственная вентиляция легких может потребоваться при различных состояниях, включая сепсис, пневмонию и сердечную недостаточность.
Экстракорпоральная мембранная оксигенация (ЭКМО) — это усовершенствованный тип механического жизнеобеспечения, который удаляет кровь из организма, насыщает кислородом и удаляет из нее углекислый газ, а затем возвращает кровь в организм, позволяя поврежденным легким или сердцу пациента восстановиться . Существует два вида ЭКМО: веноартериальная, поддерживающая сердце и легкие; и венозный, который поддерживает оксигенацию только легких. ЭКМО также служит мостом для пациентов с тяжелой сердечной и дыхательной недостаточностью до и после операции, включая трансплантацию легких.
Почему выбирают Бригам и женскую больницу?
Сертифицированные пульмонологи, врачи реанимации и торакальные хирурги в Центре легких Бригама и женской больницы (BWH) возглавляют многопрофильную команду специалистов по ИВЛ и ЭКМО, а также кардиохирургов и анестезиологов. Вместе с респираторными терапевтами и медсестрами они заботятся о людях с очень сложными респираторными заболеваниями в наших современных стационарных отделениях интенсивной терапии.Наш совместный подход позволяет врачам справляться с самыми сложными случаями с использованием ряда традиционных технологий и минимально инвазивных методов. Мы стремимся улучшить функцию легких и помочь пациентам снова дышать самостоятельно, чтобы они могли восстановить независимость.
Прочтите эту статью о пациенте с трансплантацией легкого в BWH, который прошел курс лечения ЭКМО.
Как мне записаться на прием?
Позвоните в Центр лечения легких по телефону 1-844-BWH-LUNG (1-844-294-5864), чтобы записаться на прием к специалисту по интенсивной терапии или записаться на прием через Интернет.
Я врач. Как мне направить пациента?
Врачи могут позвонить по телефону 1-844-BWH-LUNG (1-844-294-5864), чтобы направить пациента, или могут сделать онлайн-направление.
Кто ваши специалисты по ИВЛ и ЭКМО?
Где вы находитесь?
Позвоните в Центр лечения легких по телефону 1-844-BWH-LUNG (1-844-294-5864), чтобы записаться на прием к специалисту по интенсивной терапии или записаться на прием через Интернет.
Вентиляция с низким дыхательным объемом в операционной — где мы сейчас?
Искусственная вентиляция легких с высоким дыхательным объемом (TV) (10-15 мл / кг) исторически поощрялась для анестезированных пациентов в операционных, особенно при абдоминальных и торакальных процедурах.Эта практика была основана на исследовании, опубликованном в журнале New England Journal of Medicine в 1963 году. Оно проводилось с участием 18 пациентов, перенесших лапаротомию, и показало, что более высокое TV привело к меньшему ателектазу, меньшему ацидозу и улучшению оксигенации по сравнению с более низким TV. 1 Однако за последние два десятилетия лабораторные и клинические исследования связали более высокое TV, особенно с более высоким давлением накачивания, с большей степенью повреждения легких. Действительно, концепция защитной вентиляции легких была популяризирована в эпохальном сетевом исследовании острого респираторного дистресс-синдрома (ARDS), опубликованном в 2000 году, которое показало, что более низкий TV (6-8 мл / кг) улучшает выживаемость у находящихся на ИВЛ пациентов с ОРДС в критическом состоянии. 2 Это открытие вызвало категорические изменения в дыхательной практике у тяжелобольных пациентов с повреждением легких и подняло вопросы о пользе низкой ТВ-вентиляции для пациентов с неповрежденными легкими.
За последние несколько лет все больше исследований связывают улучшение послеоперационных исходов с интраоперационной низкой ТВ-вентиляцией. 3 Несмотря на растущее количество доказательств, медленное внедрение защиты легких в операционных произошло. Поскольку выбор более низкого ТВ прост в реализации и не требует дополнительных затрат, не следует ли рассматривать использование низких телевизоров в качестве метода вентиляции легких пациентов во время операции? В этой статье представлен краткий обзор физиологического обоснования и клинических данных в поддержку низкой ТВ-вентиляции в операционной с целью информирования и практического руководства для клиницистов.
Защитная вентиляция легких — физиологическое обоснование
Механическая вентиляция легких может вызвать повреждение легких (известное как повреждение легких, вызванное вентилятором (VILI)) с помощью ряда различных механизмов, включая повторяющееся чрезмерное растяжение аэрированного легкого (волютравма), циклическое вовлечение и прекращение рекрутирования легочных единиц (ателектравма) , и применение высоких давлений плато (баротравма). 4 Вредные эффекты механической вентиляции, по-видимому, опосредованы локализованным воспалением и системным высвобождением воспалительных цитокинов (биотравма).Биотравма не только способствует повреждению легких, но также может способствовать системному повреждению из-за распространения этих медиаторов воспаления в системный кровоток, вызывая дисфункцию удаленных органов. 5
Общая анестезия влияет на функцию легких в первую очередь за счет потери мышечного тонуса, что способствует развитию ателектаза легких. Развитие ателектаза очень распространено и встречается более чем у 90% субъектов, подвергающихся общей анестезии, особенно когда оно сопровождается нервно-мышечной блокадой. 6 Ателектаз легкого может также способствовать развитию VILI за счет чрезмерного растяжения не спавшихся единиц легкого и циклического открытия и закрытия соседних складывающихся единиц легкого.
В исследованиях VILI на животных часто использовался подход с множественными ударами, при котором повреждение легких сначала было вызвано предшествующим инсультом (например, системным воспалением или сепсисом), а затем усиливалось вредным воздействием большого ТВ. 7,8 Однако исследования также продемонстрировали, что вентиляция только с высоким TV — без предшествующего инсульта — также может вызвать ВИЛИ. 9 Особо следует отметить, что большинство животных моделей VILI использовали относительно короткие периоды вентиляции, напоминающие клинические условия операционной.
Эти данные свидетельствуют о том, что стратегии вентиляции с использованием высоких дыхательных объемов во время операции могут быть вредными. Кроме того, можно предположить, что потенциальные вредные эффекты механической вентиляции можно свести к минимуму за счет использования более низких телевизоров, вызывающих меньшее растяжение легких, в сочетании с положительным давлением в конце выдоха (PEEP) или маневров набора для поддержания объема легких.
Клинические данные по защитной вентиляции легких
Ряд небольших клинических исследований интраоперационной вентиляции показал, что вентиляция с низким ТВ может улучшить легочную механику и оксигенацию, 10,11 уменьшить местную продукцию медиаторов воспаления, 12 и сократить продолжительность послеоперационной вентиляции. 13 Объединенный метаанализ 8 из этих исследований также показал, что стратегии интраоперационной вентиляции с низким TV были связаны со снижением частоты послеоперационных легочных осложнений. 14 Три недавних рандомизированных контролируемых исследования (РКИ) с участием пациентов, перенесших различные операции, предоставили дополнительные доказательства преимуществ (включая улучшение послеоперационной легочной функции и снижение легочных осложнений) интраоперационной вентиляции с низким TV (прогнозируемый 6-7 мл / кг). масса тела (PBW)). 15,16,17 Важно подчеркнуть, что во всех трех испытаниях защитная вентиляция легких состояла из набора мер: с различиями в размере телевизоров, уровнях PEEP и использовании маневров набора; поэтому невозможно установить, какая защитная мера принесла наибольшую пользу.Однако недавний метаанализ данных отдельных пациентов, который включал данные этих трех испытаний, показал, что польза от защиты легких лучше всего объясняется снижением TV, а не более высокими уровнями PEEP. 3
Хотя важно признать, что использование низкого TV без PEEP способствует формированию ателектаза, оптимальное значение PEEP для интраоперационной защиты легких остается неясным. В одном недавно опубликованном многоцентровом РКИ с низким TV (8 мл / кг) у пациентов без ожирения, подвергшихся абдоминальной хирургии, сравнивалась интраоперационная вентиляция с низким уровнем PEEP (0-2 см H 2 O) и высоким уровнем PEEP (12 см H 2 О). 18 Не было различий в частоте послеоперационных легочных осложнений между группами. 18 Однако использование более высоких уровней PEEP было связано с интраоперационной гипотензией и большей потребностью в вазоактивных препаратах. Несмотря на эти данные, другие группы пациентов могут получить пользу от более высоких уровней ПДКВ, например, страдающим ожирением или перенесшим лапароскопическую абдоминальную операцию с инсуффляцией газа, которая может усилить ателектаз. Тем не менее, оптимальная комбинация PEEP и TV, а также дополнительные преимущества маневров вербовки неизвестны.
Текущая практика и движение вперед
Низкая ТВ-вентиляция все чаще используется в операционных, как было показано в недавнем отчете о практике интраоперационной вентиляции в 5 крупных университетских больницах США. 19 В этом исследовании почти 60% случаев использовали средний дыхательный объем <8 мл на кг PBW в 2013 году по сравнению с менее чем 25% случаев в 2005 году. Телевизионная вентиляция может принести клиническую пользу некоторым пациентам, поэтому важно учитывать, есть ли какой-либо потенциальный вред, связанный с широким распространением этой практики.Утверждалось, что для некоторых пациентов вентиляция с низким дыхательным объемом может способствовать ателектазу, усиливать дисинхронизацию пациента и аппарата ИВЛ и увеличивать усилия пациента во время спонтанной вентиляции, что может вызвать усталость и повреждение легких. 20 Таким образом, каждый из этих пагубных эффектов может компенсировать потенциальные положительные эффекты низкого ТВ. Поскольку уменьшение нагрузки на легкие во время механической вентиляции является механистическим объяснением положительного воздействия более низких телевизоров, выбор защитной вентиляции легких, вероятно, должен быть индивидуальным.При использовании вентиляции с низким ТВ, клиницисты должны учитывать тип и продолжительность процедуры, существовавшую ранее податливость легких и наличие легочного заболевания, а также последствия для легочного стресса, если пациенту разрешено дышать спонтанно или ему будет назначена контролируемая вентиляция.
В дальнейшем ряд вопросов, касающихся специфики интраоперационной защитной вентиляции легких, остается без ответа, включая оптимальные уровни давления при вождении, преимущества легких
маневров набора и выбора оптимального уровня PEEP.К счастью, в настоящее время проводится ряд рандомизированных контрольных испытаний, чтобы лучше охарактеризовать методы защиты легких в специализированных группах населения. 21-23 Результаты этих испытаний могут еще больше повысить безопасность интраоперационной вентиляции. Пока эта информация не будет доступна, существующие данные свидетельствуют о том, что контролируемая вентиляция с использованием низких дыхательных объемов вместе с использованием низких и средних уровней ПДКВ является безопасной практикой и, вероятно, полезна для большинства пациентов во время операции.
Список литературы
- Bendixen HH, Хедли-Уайт Дж., Лейвер МБ. Нарушение оксигенации у хирургических больных во время общей анестезии с контролируемой вентиляцией. Понятие об ателектазе. N Engl J Med 1963; 269: 991–6.
- Клиническая сеть по поводу острого респираторного дистресс-синдрома. Вентиляция с меньшими дыхательными объемами по сравнению с традиционными дыхательными объемами при остром повреждении легких и остром респираторном дистресс-синдроме. N Engl J Med 2000; 342: 1301–8.
- Серпа Нето А, Хеммес СНТ, Барбас CSV и др. Защитная вентиляция в сравнении с традиционной вентиляцией в хирургии: систематический обзор и метаанализ индивидуальных данных пациента. Анестезиология 2015; 123: 66–78.
- Слуцкий А.С., Раньери ВМ. Повреждение легких, вызванное искусственной вентиляцией легких. N Engl J Med 2013, 369: 2126–2136.
- Hegeman MA, Henmus MP, Heijnen CJ, et al. Активация эндотелия, вызванная вентилятором, и воспаление в легких и дистальных органах. Crit Care 2009; 13: R182.
- Дугган М, Кавана Б.П. Легочный ателектаз: патогенное периоперационное заболевание. Анестезиология 2005; 102: 838–854.
- Слуцкий А.С., Тремблай Л.Н. Множественная системная органная недостаточность. Способствует ли механическая вентиляция? Am J Respir Crit Care Med 1998; 157: 1721–5.
- Tremblay L, Valenza F, Ribeiro SP, Li J, Slutsky AS. Повреждающие дыхательные стратегии увеличивают экспрессию цитокинов и м-РНК c-fos в изолированной модели легкого крысы. J Clin Invest 1997; 99: 944–52.
- Silva PL, Negrini D, Rocco PR. Механизмы вентиляции легких в здоровых легких. Best Practices Clin Anaesthesiol 2015; 29: 301–13.
- Чейни М.А., Николов М.П., Блейкман Б.П., Бахос М. Защитная вентиляция ослабляет послеоперационную легочную дисфункцию у пациентов, перенесших сердечно-легочное шунтирование. J Cardiothorac Vasc Anesth 2000; 14: 514–8.
- Michelet P, D’Journo XB, Roch A, et al. Защитная вентиляция влияет на системное воспаление после эзофагэктомии: рандомизированное контролируемое исследование. Анестезиология 2006; 105: 911–9.
- Zupancich E, Paparella D, Turani F и др. Механическая вентиляция влияет на медиаторы воспаления у пациентов, перенесших искусственное кровообращение при кардиохирургических вмешательствах: рандомизированное клиническое исследование. J Thorac Cardiovasc Surg 2005; 130: 378–83.
- Сундар С., Новак В., Джервис К. и др. Влияние вентиляции с низким дыхательным объемом на время экстубации у кардиохирургических пациентов. Анестезиология 2011; 114: 1102–1110.
- Hemmes SN, Serpa Neto A, Schultz MJ. Интраоперационные вентиляционные стратегии для предотвращения послеоперационных легочных осложнений: метаанализ. Curr Opin Anaesthesiol 2013; 26: 126–33.
- Severgnini P, Selmo G, Lanza C и др. Защитная механическая вентиляция легких во время общей анестезии при открытых операциях на брюшной полости улучшает послеоперационную функцию легких. Анестезиология 2013; 118: 1307–21.
- Futier E, Constantin JM, Paugam-Burtz C, et al.Испытание интраоперационной вентиляции с низким дыхательным объемом в абдоминальной хирургии. N Engl J Med 2013; 369: 428–37.
- Ge Y, Yuan L, Jiang X, Wang X, Xu R, Ma W. Влияние механической вентиляции легких с защитой легких на респираторную функцию у пожилых людей, перенесших артродез. Чжун Нан Да Сюэ Сюэ Бао И Сюэ Бань 2013; 38: 81–5.
- PROVE Сетевые исследователи для сети клинических испытаний Европейского общества анестезиологов, Hemmes SN, Gama de Abreu M, Pelosi P, Schultz MJ.Сравнение высокого и низкого положительного давления в конце выдоха во время общей анестезии при открытой абдоминальной хирургии (исследование PROVHILO): многоцентровое рандомизированное контролируемое исследование. Ланцет 2014; 384: 495–503.
- Wanderer JP, Ehrenfeld JM, Epstein RH, et al. Временные тенденции и текущие модели практики интраоперационной вентиляции в академических медицинских центрах США: ретроспективное исследование. BMC Anesthesio l 2015; 15:40.
- Gattinoni L. Контрпункт: Является ли механическая вентиляция легких с низким дыхательным объемом предпочтительной для всех пациентов на ИВЛ? Нет. Сундук 2011; 140: 11–3.
- Технический университет Дрездена. Защитная вентиляция с более высоким ПДКВ по сравнению с более низким во время общей анестезии при хирургических вмешательствах у пациентов с ожирением (PROBESE). Доступно по адресу: http://clinicaltrials.gov/show/NCT02148692 Последнее обращение 01.04.2016.
- Assistance Publique — Hôpitaux de Paris. Легочная хирургия и защитная механическая вентиляция (VPP). Доступно по адресу: http://clinicaltrials.gov/show/NCT00805077 Последнее обращение 01.04.2016.
- Fundación para la Investigación del Hospital Clínico de Valencia.Индивидуальная периоперационная стратегия открытой вентиляции легких (iPROVE). Доступно по адресу http://clinicaltrials.gov/show/NCT02158923 Последнее обращение 01.
