Лимфогранулематоз (ходжкинская лимфома) | Фонд «Подари жизнь»
Суть болезни
Лимфогранулематоз (ЛГМ, болезнь Ходжкина, лимфома Ходжкина) – заболевание лимфатической системы, особый тип лимфомы, то есть злокачественного заболевания, где опухолевая ткань возникает из лимфоцитов. Для ЛГМ характерно прежде всего опухолевое поражение лимфатических узлов с постепенным распространением заболевания от одной группы лимфоузлов к другой. Могут поражаться также другие органы, прежде всего селезенка, а также печень, легкие, кишечник, костный мозг и т.п.
Отличительной чертой ЛГМ по сравнению с другими лимфомами является присутствие в пораженных болезнью лимфоузлах особого типа клеток, называемых клетками Березовского-Штернберга-Рид. Это гигантские клетки, возникшие из B-лимфоцитов.
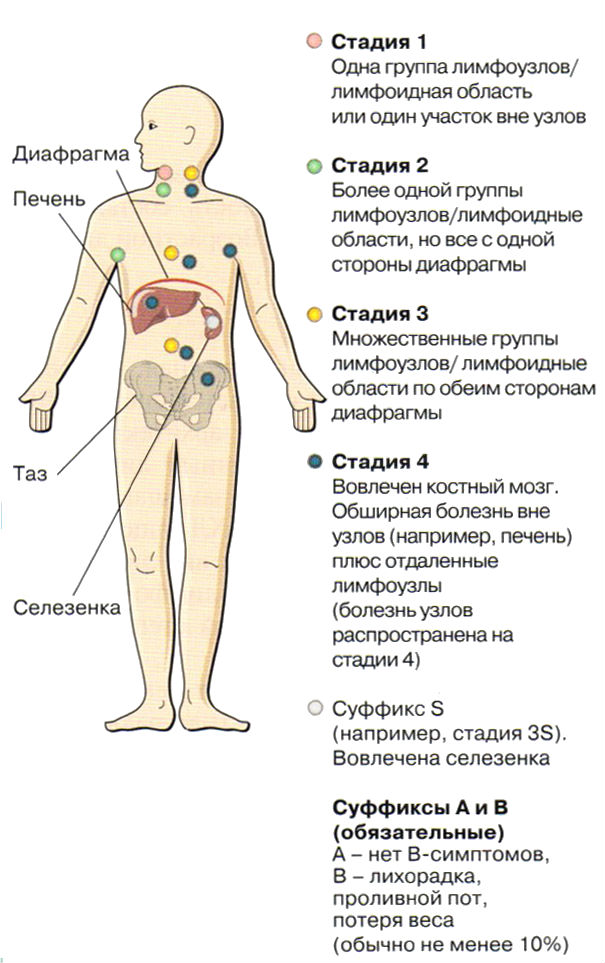
В зависимости от распространенности процесса различают четыре стадии ЛГМ.
- Стадия I – вовлечены лимфоузлы только одной области или один орган вне лимфоузлов.

- Стадия II – вовлечены лимфоузлы в двух или более областях с одной стороны диафрагмы или одна группа лимфоузлов и один орган также с одной стороны диафрагмы.
- Стадия III – вовлечены лимфоузлы с обеих сторон диафрагмы; возможно также поражение селезенки и других органов вне лимфоузлов.
- Стадия IV – наблюдается распространенное поражение одного или более внутренних органов – таких как печень, костный мозг, легкие, кишечник; оно может сопровождаться или не сопровождаться поражением лимфоузлов.
В обозначении стадии заболевания могут использоваться также дополнительные символы: А (системные клинические симптомы отсутствуют), В (присутствуют), E (вовлечены не только лимфоузлы, но и другие органы), S (вовлечена селезенка).
Различают несколько гистологических вариантов ЛГМ: с нодулярным склерозом (40-50% всех случаев ЛГМ), смешанноклеточный (около 30% всех случаев ЛГМ), с лимфоидным преобладанием и с истощением лимфоидной ткани (редкие варианты).
Частота встречаемости, факторы риска
ЛГМ имеет два возрастных пика заболеваемости: один в молодом возрасте (15-35 лет), второй в пожилом. ЛГМ встречается в среднем с частотой около 1 случая на 25 тысяч населения в год, при этом дети и подростки составляют около 10-15% заболевших, а у детей дошкольного возраста болезнь встречается редко. Мужчины болеют несколько чаще женщин.
Факторы, влияющие на риск заболевания ЛГМ, постоянно изучаются. Могут играть роль как генетическая предрасположенность, так и некоторые вирусные инфекции. Так, считается, что риск развития ЛГМ повышен у людей, инфицированных вирусом Эпштейна-Барр (широко распространенным вирусом из группы герпетических вирусов). Риск развития ЛГМ увеличивается при иммунодефицитных состояниях, включая СПИД.
Признаки и симптомы
При ЛГМ наблюдается безболезненное увеличение лимфатических узлов – чаще всего шейных и надключичных, лимфоузлов грудной полости (области средостения), порой подмышечных, паховых и лимфоузлов брюшной полости. Это самый характерный симптом болезни. Взрослые больные иногда отмечают, что увеличенные лимфоузлы становятся болезненными после приема алкоголя.
Это самый характерный симптом болезни. Взрослые больные иногда отмечают, что увеличенные лимфоузлы становятся болезненными после приема алкоголя.
Важными симптомами являются ночная потливость, повышение температуры и снижение веса. Наличие этих «системных» симптомов отражается буквой «В» в обозначении стадии болезни и играет роль в оценке активности опухоли. Среди других возможных симптомов можно назвать утомляемость, увеличение печени и/или селезенки, боли в спине, кожный зуд. Из-за увеличенных лимфоузлов грудной полости могут возникнуть затрудненное дыхание, кашель.
По мере развития опухолевого процесса самочувствие больного ухудшается. На поздних стадиях развития болезни может наблюдаться желтуха, если опухоль распространилась в печень и перекрывает желчные протоки. Могут возникать отеки лица, шеи и рук (так называемый синдром сдавления верхней полой вены), отеки ног.
Диагностика
Чтобы отличить ЛГМ от других онкологических и неонкологических заболеваний, необходимо провести исследование опухоли – увеличенного лимфатического узла или очага в других тканях тела. Для этого производят его хирургическое удаление или биопсию с микроскопическим и иммуногистохимическим исследованием образца. Обнаружение клеток Березовского-Штернберга-Рид (крупных клеток особого вида, специфичных для ЛГМ) и их предшественников (клеток Ходжкина) является важным признаком ЛГМ; эти опухолевые клетки окружены другими клетками – лимфоцитами, эозинофилами и др.
Для этого производят его хирургическое удаление или биопсию с микроскопическим и иммуногистохимическим исследованием образца. Обнаружение клеток Березовского-Штернберга-Рид (крупных клеток особого вида, специфичных для ЛГМ) и их предшественников (клеток Ходжкина) является важным признаком ЛГМ; эти опухолевые клетки окружены другими клетками – лимфоцитами, эозинофилами и др.
Для обнаружения конкретных пораженных опухолью участков – лимфатических узлов и/или внутренних органов – используют различные методы визуализации: рентгенографию, ультразвуковое исследование (УЗИ), компьютерную томографию (КТ) и позитронно-эмиссионную томографию (ПЭТ). Именно ПЭТ считается самым эффективным тестом для определения стадии ЛГМ и оценки ответа на лечение. Возможны и другие исследования.
Производится костномозговая пункция и/или трепанобиопсия с последующим исследованием образца костного мозга, чтобы понять, поражен ли болезнью этот орган.
Лечение
Лечение ЛГМ основано на сочетании химиотерапии и облучения. Выбор конкретной терапии зависит от варианта болезни, возраста пациента, стадии (локальное или распространенное поражение организма), сопутствующих заболеваний и других факторов.
Выбор конкретной терапии зависит от варианта болезни, возраста пациента, стадии (локальное или распространенное поражение организма), сопутствующих заболеваний и других факторов.
В химиотерапии ЛГМ у детей и подростков в России успешно используют протоколы, предложенные немецкими онкогематологами. Эти протоколы позволяют получить высокий процент излечения с минимальными побочными эффектами, что очень важно при этой болезни. Также могут применяться курсы ABVD (адриабластин, блеомицин, винбластин, дакарбазин), BEACOPP (блеомицин, этопозид, адриамицин, циклофосфамид, винкристин, прокарбазин, преднизон) и другие химиотерапевтические курсы, количество которых определяют в зависимости от стадии болезни.
За химиотерапией следует лучевая терапия. Дозу облучения определяет врач-онкогематолог в зависимости от стадии заболевания, используемого протокола и облучаемого органа.
При оценке предпочтительности различных протоколов следует учитывать не только их эффективность в лечении основного заболевания, но также токсичность и повышение вероятности возникновения новых (вторичных) онкозаболеваний после терапии. Больные, излечившиеся от ЛГМ, и врачи, их наблюдающие, должны помнить о риске развития вторичных опухолей и о необходимости регулярных осмотров.
Больные, излечившиеся от ЛГМ, и врачи, их наблюдающие, должны помнить о риске развития вторичных опухолей и о необходимости регулярных осмотров.
В сложных случаях (устойчивость болезни к терапии, рецидивы) может применяться высокодозная терапия с аутологичной трансплантацией костного мозга. Аллогенная трансплантация используется лишь в редких случаях.
В последние годы у больных ходжкинской лимфомой появились новые шансы. В случае отсутствия ответа на стандартную терапию или рецидива болезни могут использоваться схемы химиотерапии с новейшим препаратом «Адцетрис» (брентуксимаб ведотин) или иммунотерапии с препаратом «Опдиво» (ниволумаб).
Прогноз
ЛГМ относится к числу тех опухолевых заболеваний, которые наиболее эффективно излечиваются на современном уровне развития медицины. Среди молодых пациентов выздоравливают около 90% больных. У пожилых пациентов выживаемость хуже, но в среднем прогноз все равно достаточно хороший. Даже в случае рецидива можно излечивать около половины пациентов.
Прогноз, разумеется, зависит также от стадии заболевания: среди пациентов, у которых болезнь была диагностирована на стадиях I-II, доля излечивающихся превышает 90%, тогда как при обнаружении ЛГМ на стадии IV эта доля снижается до 65-70%.
После пятилетней ремиссии болезнь, как правило, считается излеченной. Однако и после излечения от ЛГМ необходима пожизненная онкологическая настороженность, так как вторичные опухоли иногда развиваются даже через 10-20 лет после окончания лечения. Могут возникнуть и другие отдаленные последствия – например, кардиомиопатия (поражение миокарда) как следствие химиотерапии. Благодаря разработке новых протоколов вероятность побочных эффектов уменьшается, однако полностью исключить их нельзя.
Лимфогранулематоз
Лимфогранулематоз (лимфома Ходжкина, болезнь Ходжкина) — это онкологическое заболевание лимфатической системы, при котором в лимфоидной ткани при микроскопическом исследовании находят клетки Березовского-Штернберга-Рида. Название эти клетки получили в память об ученых, принимавших участие в их открытии и изучении. Лимфогранулематоз часто встречается у детей позднего подросткового возраста и также имеет пики заболеваемости в 20 и 50 лет. Впервые заболевание было описано английским врачом Т.
Название эти клетки получили в память об ученых, принимавших участие в их открытии и изучении. Лимфогранулематоз часто встречается у детей позднего подросткового возраста и также имеет пики заболеваемости в 20 и 50 лет. Впервые заболевание было описано английским врачом Т.
Ходжкиным в 1832 году.
Существует 5 видов лимфогранулематоза. Правильный диагноз можно поставить только после исследования ткани лимфатического узла, получаемой при биопсии.
Варианты лимфогранулематоза:
- Вариант нодулярного склероза (наиболее распространенный — 75%)
- Смешанно-клеточный вариант
- Вариант с лимфоидным истощением (наименее распространенный — менее 5%)
- Вариант с большим количеством лимфоцитов
- Нодулярный вариант с преобладанием лимфоцитов
ЛИМФОГРАНУЛЕМАТОЗ — СТАДИИ ЗАБОЛЕВАНИЯ
В зависимости от степени распространенности заболевания выделяют 4 стадии лимфогранулематоза:
I стадия — опухоль находится в лимфатических узлах одной области или в одном органе за пределами лимфатических узлов (IE)
II стадия — поражение лимфатических узлов в двух и более областях по одну сторону диафрагмы или органа и лимфатических узлов по одну сторону диафрагмы (IIE)
III стадия — поражение лимфатических узлов по обе стороны диафрагмы (III), которое может также сопровождаться поражением селезенки (IIIS). При сочетании поражения лимфатических узлов по обе стороны диафрагмы с локализованным поражением внелимфатического органа или участка определяется стадия IIIE, а если в дополнение к этому поражена еще и селезенка — то стадия IIISE. Стадию III также подразделяют на III(1) и III(2). В первом случае опухолевый процесс локализован в верхней части брюшной полости, а при стадии III(2) он также поражает лимфатические узлы, расположенные в тазу и вдоль аорты.
При сочетании поражения лимфатических узлов по обе стороны диафрагмы с локализованным поражением внелимфатического органа или участка определяется стадия IIIE, а если в дополнение к этому поражена еще и селезенка — то стадия IIISE. Стадию III также подразделяют на III(1) и III(2). В первом случае опухолевый процесс локализован в верхней части брюшной полости, а при стадии III(2) он также поражает лимфатические узлы, расположенные в тазу и вдоль аорты.
IV стадия — заболевание распространяется помимо лимфатических узлов на внутренние органы: печень, почки, кишку, костный мозг и др. с их диффузным поражением Буква Е означает то, что опухоль распространяется на органы и ткани, расположенные рядом с пораженными группами крупных лимфатических узлов, а S — поражение селезенки. В диагнозе заболевания отражают отсутствие или наличие таких симптомов как лихорадка, проливные поты и потеря массы тела. Если эти симптомы наблюдаются, то в диагнозе будет фигурировать буква Б (или латинская В), если эти симптомы отсутствуют, то будет указана буква А.
вернуться к списку заболеваний
Лимфогранулематоз — ПроМедицина Уфа
Лимфогранулематоз или болезнь Ходжкина — это опухолевое заболевание лимфатической системы. Для лимфогранулематоза специфично увеличение различных групп лимфатических узлов, чаще нижнечелюстных, надключичных, медиастинальных.
Средний показатель заболеваемости лимфогранулематозом составляет 2,2 случая на 100 тысяч населения. Среди заболевших чаще встречаются молодые люди в возрасте 20-30 лет. Второй пик заболеваемости приходится на возраст старше 60 лет. У мужчин болезнь Ходжкина развивается в 2 раза чаще, чем у женщин.
Причины
Причины лимфогранулематоза до сих пор не выяснены. В числе основных рассматриваются вирусная, наследственная и иммунная версии происхождения болезни.
В пораженных лимфоузлах определяются опухолевые клетки Ходжкина и Рид-Березовского-Штернберга, что является отличительной особенностью данного заболевания. И поэтому некоторые специалисты склоняются к вирусной этимологии заболевания.
На наследственную версию указывает то, лимфогранулематоз встречается в три раза чаще в семьях, где уже были зарегистрированы такие больные.
Также не исключено, что провоцирующими лимфогранулематоз факторами является влияние токсических веществ, ионизирующего излучения, лекарственных препаратов. Это указывает на иммунное происхождение заболевания.
Симптомы
Симптомы лимфогранулематоза весьма разнообразны. Начинаясь в лимфатических узлах, болезненный процесс может распространяться практически на все органы, в этом случае появляются различные проявления интоксикации: слабость, вялость, сонливость, головные боли. Преимущественное поражение того или иного органа или системы и определяет картину заболевания.
Первым проявлением лимфогранулематоза обычно становится увеличение лимфатических узлов. Этот процесс, как правило, не сопровождается нарушением самочувствия больного. Увеличенные лимфатические узлы в редких случаях болезненны. Постепенно, иногда быстро увеличиваясь, они сливаются в крупные образования.
У части больных заболевание начинается с увеличения лимфатических узлов средостения. Это увеличение может проявиться в поздние сроки, когда размеры образования значительны, кашлем, одышкой, реже — болями за грудиной.
В единичных случаях болезнь начинается с изолированного поражения околоаортальных лимфатических узлов. Больной жалуется на боли в области поясницы, возникающие, в основном, ночью.
Иногда заболевание начинается остро. Больной испытывает лихорадку, ночное потение, быстро худеет. Обычно в этих случаях незначительное увеличение лимфатических узлов появляется позднее.
Иногда лимфогранулематоз поражает легочную ткань. Поражения легких обычно не сопровождаются внешними проявлениями. Довольно часто при лимфогранулематозе обнаруживается скопление жидкости в плевральных полостях. Как правило, это заметно при рентгенологическом исследовании.
Наиболее частыми проявлениями увеличения лимфоузлов при лимфогранулематозе могут быть: кашель, одышка, нарушение глотания, отеки, нарушение пищеварения, поражение нервной системы, поражение почек.
Диагностика
Кроме тщательного исследования симптомов заболевания, врач может назначить ряд дополнительных лабораторных и инструментальных исследований, позволяющих подтвердить или опровергнуть диагноз.
В диагностике лимфогранулематоза применяются: общий и биохимический анализы крови, инструментальные методы обследования, пункция костного мозга, гистологическое исследование лимфатических узлов, иммунофенотипирование лимфоцитов.
Лечение
На начальных стадиях заболевания используется метод лучевой терапии. При более поздних стадиях лимфогранулематоза, применяется химиотерапия. Достаточно часто данные методы используют совместно.
При значительном распространении болезни в организме, доля химиотерапии возрастает. В крайних случаях используются большие дозы химиотерапии и трансплантация костного мозга в организм больного.
Выбор метода лечения определяется стадией процесса. Для исключения поражения внутренних органов и лимфатических узлов вводят рентгеноконтрастное вещество в лимфатические сосуды конечностей, нередко прибегают к диагностической лапаротомии с биопсией печени и забрюшинных лимфатических узлов. Селезенку удаляют как важный очаг болезни.
Селезенку удаляют как важный очаг болезни.
Лимфогранулематоз у детей лечится с помощью комплексной терапии: совмещённое применение лучевого лечения и разнообразных схем полихимиотерапии.
После достижения ремиссии больной должен оставаться под наблюдением врача, так как важно вовремя диагностировать возможность рецидивов.
Современное лечение лимфомы Ходжкина (лимфогранулематоза) | Демина Е.А.
Российский онкологический научный центр им. Н.Н. Блохина РАМН
К концу ХХ века 10–летняя безрецидивная выживаемость больных лимфомой Ходжкина, по данным крупных исследовательских центров, при ранних стадиях достигла 90%: EORTC (Европейская организация по исследованию и лечению рака), 1993 г. – 92%, Stanford, 1997 г. – 93%, Harvard, 1999 г. – 96%, РОНЦ, 1988 г. – 89%. При распространенных стадиях 5–летняя выживаемость при этом заболевании, по данным NCI (Национальный раковый институт, США), 1999 г. достигает 60% [1,5]. В течение двух последних десятилетий прошлого века проводились многочисленные клинические исследования – велся целенаправленный поиск наилучшей комбинации химиотерапии и оптимального сочетания лучевой и химиотерапии при лечении больных лимфомой Ходжкина (название употребляется в соответствии с классификацией лимфом, принятой ВОЗ в 2001 г. ). Анализ этих исследований позволил предложить новую комбинацию факторов риска и иное разделение больных по прогностическим группам при выборе программы лечения. Появились и новая стратегия лечения, и новые терапевтические программы.
). Анализ этих исследований позволил предложить новую комбинацию факторов риска и иное разделение больных по прогностическим группам при выборе программы лечения. Появились и новая стратегия лечения, и новые терапевтические программы.
С конца 70–х годов в зарубежной литературе вместо терминов «локализованные» и «генерализованные» стадии стали использоваться термины «early» – ранние и «advanced» – распространенные (продвинутые) стадии в значении местно–распространенный/диссеминированный процесс (аналогично терминологии при солидных опухолях). Обоснованием для этих терминов стал анализ результатов радикальной лучевой терапии лимфомы Ходжкина, при котором было показано, что эффективность лечения зависит от общей массы опухоли: при поражении только одной анатомической зоны лимфатических коллекторов 10–летняя безрецидивная выживаемость достигала 80%, в то время как при поражении 4 и более зон – лишь 23% [5]. Кроме того, 10–летняя безрецидивная выживаемость больных с I–II стадиями и массивным поражением средостения оказалась такой же низкой (56%), как у больных с распространенными стадиями (62%) [5]. С онкологической точки зрения этот факт легко объясняется тем, что эффективность лечения всех опухолей, и лимфомы Ходжкина в том числе, зависит от общей массы опухоли. При IIIА стадии с небольшими числом, малыми размерами лимфатических узлов и двумя зонами поражения общая масса опухоли меньше, чем при I или II стадиях с массивным поражением средостения.
С онкологической точки зрения этот факт легко объясняется тем, что эффективность лечения всех опухолей, и лимфомы Ходжкина в том числе, зависит от общей массы опухоли. При IIIА стадии с небольшими числом, малыми размерами лимфатических узлов и двумя зонами поражения общая масса опухоли меньше, чем при I или II стадиях с массивным поражением средостения.
В конце 70–х годов на смену радикальной лучевой терапии при I–III А стадиях лимфомы Ходжкина приходит комбинированное химио–лучевое лечение. К этому времени по результатам радикальной лучевой терапии определены прогностические факторы для I–II стадий лимфомы Ходжкина [6,9]. Набор прогностических факторов несколько варьировал у различных исследовательских групп, но в целом к неблагоприятным прогностическим факторам для I и II стадий были отнесены следующие факторы: возраст старше 40 (или 50) лет, поражение 3 и более лимфатических областей (или 4 и более), СОЭ выше 30 мм/час при наличии симптомов интоксикации и выше 50 мм/час при их отсутствии, гистологические варианты смешанноклеточный и лимфоидное истощение, а также массивное (медиастинально–торокальный индекс (МТИ) более 0,33) поражение медиастинальных лимфатических узлов. Эти прогностические факторы разделяли только больных с I и II стадиями лимфомы Ходжкина на две группы, нуждающиеся в различном объеме лечения.
Эти прогностические факторы разделяли только больных с I и II стадиями лимфомы Ходжкина на две группы, нуждающиеся в различном объеме лечения.
В связи с тем, что понятие «поражение 3 и более лимфатических областей» неоднозначно трактовалось разными исследователями, на V международном симпозиуме по лимфогранулематозу в сентябре 2001 года было обращено особое внимание на различие терминов «area» – область и «region» – зона. Было уточнено, что термином «зона» (region) обозначаются анатомические зоны, по которым устанавливается стадия заболевания в соответствии с классификацией, принятой в Ann–Arbor. Термин «область» (area) – более широкое понятие, область может включать в себя одну или более зон. Так, в одну область были включены шейные, над– и подключичные лимфатические узлы с одной стороны. Также в одну область объединены медиастинальные лимфатические узлы и лимфатические узлы корней легких; одной областью считаются лимфатические узлы «верхнего этажа» брюшной полости (ворота печени, ворота селезенки и корень брыжейки) и одной областью – лимфатические узлы «нижнего этажа» брюшной полости (парааортальные и мезентериальные).
Во второй половине 90–х годов EORTC и Германской группой по изучению лимфомы Ходжкина (GHDG) был проведен многофакторный анализ прогностических факторов. В исследование было включено более 14000 больных [5]. Этот анализ показал, что для всех больных лимфомой Ходжкина при использовании химиотерапии и комбинированного лечения, кроме стадии заболевания и симптомов интоксикации, прогностически значимыми являются только следующие факторы:
1. Массивное поражение средостения (МТИ >0,33).
2. Массивное поражение селезенки (наличие 5 и более очагов или увеличение органа с его диффузной инфильтрацией).
3. Экстранодальное поражение в пределах стадии, обозначаемой символом «Е».
4. Поражение трех или более областей лимфоузлов.
5. Увеличение СОЭ>30 мм/час при стадии Б и >50 мм/час при стадии А [2,3,5].
Эти факторы в совокупности со стадией заболевания и симптомами интоксикации позволили исследователям из GHDG разделить больных лимфомой Ходжкина на прогностические группы. В соответствии с объемом опухолевой массы были выделены три прогностические группы – с благоприятным, промежуточным и неблагоприятным прогнозом (табл. 1), и тем самым выбор программы лечения был поставлен в прямую зависимость от объема опухолевой массы.
В соответствии с объемом опухолевой массы были выделены три прогностические группы – с благоприятным, промежуточным и неблагоприятным прогнозом (табл. 1), и тем самым выбор программы лечения был поставлен в прямую зависимость от объема опухолевой массы.
Адекватные дозы лучевой терапии на каждое лучевое поле для лимфомы Ходжкина были разработаны H. Kaplan в 60–х годах. Именно он показал, что при дозе облучения в 30 Гр риск рецидива в облученном поле составляет всего 11%, а в интервале доз от 35 до 40 Гр снижается лишь до 4,4%, но 100–процентная эффективность все равно не достигается при дальнейшем повышении дозы облучения. Еще трижды, в середине 70–х годов Fletcher G.H. и Shukovsky L.G., в начале 90–х годов Brincker H. и Bentzen S.M. и в конце 90–х годов M.Loeffler с соавторами проводили анализ эффективности различных доз лучевой терапии для больных с лимфомой Ходжкина [2,3,5,6]. Все три исследования на большом клиническом материале подтвердили выводы, сделанные H. Kaplan, о достижении максимальной тумороцидной дозы в интервале между 30 и 40 Гр и нецелесообразности превышения дозы локального облучения выше 40 Гр, в том числе и на большие опухолевые массы. Brincker H. и Bentzen S.M. при анализе всех опубликованных исследований с 1960 по 1990 гг. показали, что при проведении только радикальной лучевой терапии 95% контроль за лимфомой Ходжкина достигается для лимфатических узлов размером менее 6,0 см при дозе 26,5 Гр, а для лимфатических узлов более 6,0 см при дозе 32,5 Гр [6]. Эти данные были подтверждены клиническим исследованием M.Loeffler с соавторами (1997 г.), которое показало, что при использовании 20 Гр, 30 Гр и 40 Гр на зоны исходно пораженных лимфатических узлов (на большие массивы доза облучения всегда достигала 40 Гр) в рамках комбинированной химио–лучевой терапии не выявлено различия в результатах лечения: 4–летняя выживаемость, свободная от неудач лечения, составила 86%, 80% и 90% соответственно, а общая выживаемость – 93%, 94% и 88% (р=0,5) [5].
Kaplan, о достижении максимальной тумороцидной дозы в интервале между 30 и 40 Гр и нецелесообразности превышения дозы локального облучения выше 40 Гр, в том числе и на большие опухолевые массы. Brincker H. и Bentzen S.M. при анализе всех опубликованных исследований с 1960 по 1990 гг. показали, что при проведении только радикальной лучевой терапии 95% контроль за лимфомой Ходжкина достигается для лимфатических узлов размером менее 6,0 см при дозе 26,5 Гр, а для лимфатических узлов более 6,0 см при дозе 32,5 Гр [6]. Эти данные были подтверждены клиническим исследованием M.Loeffler с соавторами (1997 г.), которое показало, что при использовании 20 Гр, 30 Гр и 40 Гр на зоны исходно пораженных лимфатических узлов (на большие массивы доза облучения всегда достигала 40 Гр) в рамках комбинированной химио–лучевой терапии не выявлено различия в результатах лечения: 4–летняя выживаемость, свободная от неудач лечения, составила 86%, 80% и 90% соответственно, а общая выживаемость – 93%, 94% и 88% (р=0,5) [5].
До настоящего времени при лечении первичных больных лимфомой Ходжкина использовались две основные схемы полихимиотерапии – схема МОРР (и ее аналоги) и схема ABVD. Длительный, 30–летний спор о преимуществе одной из схем был решен в последнее десятилетие в пользу программы ABVD. В конце 80–х – начале 90–х годов три крупные исследовательские группы опубликовали результаты больших рандомизированных исследований. Эти исследования показали статистически значимое преимущество комбинированных программ, в которых использовалась полихимиотерапия по схеме ABVD, по сравнению с программами со схемой МОРР. В исследовании EORTC (1997 г.) при одинаковой 10–летней общей выживаемости (больные с I–II стадиями лимфомы Ходжкина и неблагоприятным прогнозом, 6 циклов полихимиотерапии и лучевая терапия) риск неудачи лечения к 10 годам составил 24% для больных, получавших химиотерапию МОРР, и 12% для больных, получавших химиотерапию ABVD (p<0,01). В исследовании Миланской группы (1987 г. ) выявилось преимущество схемы ABVD перед схемой МОРР как по непосредственным результатам (частота полных ремиссий 92% и 82% соответственно, p<0,02), так и по отдаленным – семилетняя выживаемость до прогрессирования составила 63% и 91% (p<0,02), а общая выживаемость – 68% и 77% (p<0,003) соответственно. В исследовании CALGB (Cancer and Leukemia group B, 1992 г.) также выявилось преимущество в 7–летней общей выживаемости (77% против 68%, p<0,02) и 7–летней выживаемости, свободной от неудач лечения (81% против 63%, p<0,03) [5]. В прошедшем году GHSH также подтвердила преимущество программы ABVD перед программой МОРР. Поэтому на V международном симпозиуме по лимфоме Ходжкина в сентябре 2001 года в Кельне схема ABVD (адриамицин 25 мг/м2, блеомицин 10 мг/м2, винбластин 6 мг/м2, дакарбазин 375 мг/м2, все препараты вводятся в 1 и 15–й дни с интервалом в 2 недели) была признана приоритетной для первичных больных с лимфомой Ходжкина.
) выявилось преимущество схемы ABVD перед схемой МОРР как по непосредственным результатам (частота полных ремиссий 92% и 82% соответственно, p<0,02), так и по отдаленным – семилетняя выживаемость до прогрессирования составила 63% и 91% (p<0,02), а общая выживаемость – 68% и 77% (p<0,003) соответственно. В исследовании CALGB (Cancer and Leukemia group B, 1992 г.) также выявилось преимущество в 7–летней общей выживаемости (77% против 68%, p<0,02) и 7–летней выживаемости, свободной от неудач лечения (81% против 63%, p<0,03) [5]. В прошедшем году GHSH также подтвердила преимущество программы ABVD перед программой МОРР. Поэтому на V международном симпозиуме по лимфоме Ходжкина в сентябре 2001 года в Кельне схема ABVD (адриамицин 25 мг/м2, блеомицин 10 мг/м2, винбластин 6 мг/м2, дакарбазин 375 мг/м2, все препараты вводятся в 1 и 15–й дни с интервалом в 2 недели) была признана приоритетной для первичных больных с лимфомой Ходжкина.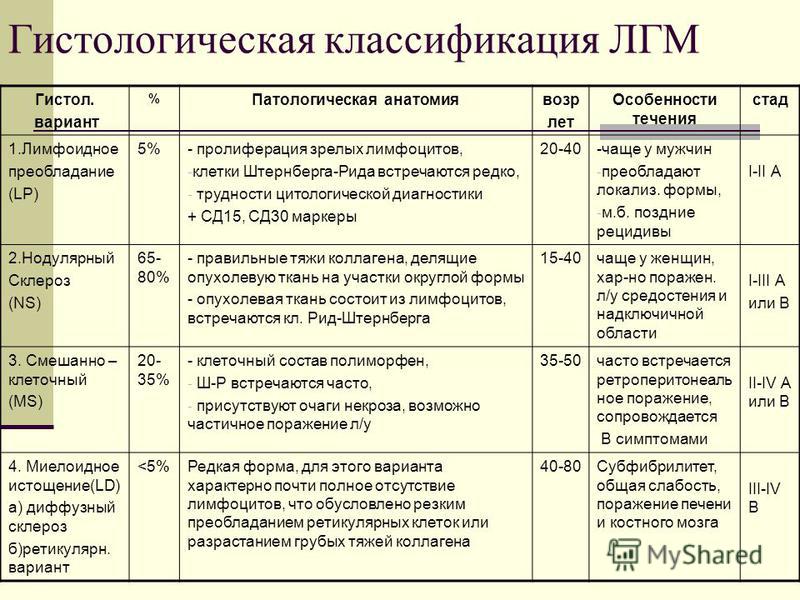
В последние десятилетия комбинированное химио–лучевое лечение прочно заняло лидирующее положение в лечении всех первичных больных лимфомой Ходжкина.
Для первичных больных лимфомой Ходжкина основной идеологией терапии стало положение: «Объем лечения соответствует объему поражения». Разделение больных на три прогностические группы облегчает выбор адекватной программы лечения.
Лечение больных с благоприятным прогнозом
Эта группа больных малочисленна и требует небольшого объема лечения. Во всех исследованиях длительная (10–летняя и более) выживаемость в этой группе достигает 96–100%. За последние два десятилетия в этой группе больных несколькими крупными рандомизированными исследованиями было доказано преимущество комбинированной терапии. В исследовании EORTC 6–летняя выживаемость, свободная от неудач лечения, составила в группе комбинированного лечения 90%, в то время как в группе, получавшей радикальную лучевую терапию, лишь 81% – p<0,019 [5]. В рандомизированном исследовании GHSH проведено сравнение комбинированной терапии, состоящей из 2 курсов по схеме ABVD и последующего облучения расширенными полями с лечением по радикальной лучевой программе. Получены аналогичные результаты: 2–летняя свободная от неудач лечения выживаемость составила 96% и 87% соответственно – p<0,05 [5]. Аналогичные результаты опубликовала Манчестерская группа (111 больных): 3–летняя выживаемость до прогрессирования в группе комбинированного химио–лучевого лечения 91% по сравнению с 73% в группе, получавшей только лучевую терапию расширенными полями. Программа Манчестерской группы интересна тем, что она очень короткая, состоит из 4 недель полихимиотерапии по схеме VAPEC–B (винкристин 1,4 мг/м2 1–й и 8–й дни, адрибластин 35 мг/м2 1–й и 15–й дни, преднизолон 50 мг внутрь с 1–го по 28 день ежедневно, этопозид 100 мг/м2 в/в с 15–го по 19 день ежедневно, блеомицин 10 мг/м2 1–й и 8–й дни). После двухнедельного интервала следует лучевая терапия на зоны исходного поражения.
В рандомизированном исследовании GHSH проведено сравнение комбинированной терапии, состоящей из 2 курсов по схеме ABVD и последующего облучения расширенными полями с лечением по радикальной лучевой программе. Получены аналогичные результаты: 2–летняя свободная от неудач лечения выживаемость составила 96% и 87% соответственно – p<0,05 [5]. Аналогичные результаты опубликовала Манчестерская группа (111 больных): 3–летняя выживаемость до прогрессирования в группе комбинированного химио–лучевого лечения 91% по сравнению с 73% в группе, получавшей только лучевую терапию расширенными полями. Программа Манчестерской группы интересна тем, что она очень короткая, состоит из 4 недель полихимиотерапии по схеме VAPEC–B (винкристин 1,4 мг/м2 1–й и 8–й дни, адрибластин 35 мг/м2 1–й и 15–й дни, преднизолон 50 мг внутрь с 1–го по 28 день ежедневно, этопозид 100 мг/м2 в/в с 15–го по 19 день ежедневно, блеомицин 10 мг/м2 1–й и 8–й дни). После двухнедельного интервала следует лучевая терапия на зоны исходного поражения. Вся программа выполняется за 10 недель [5]. В 1978–88 гг. в РОНЦ им. Н.Н. Блохина РАМН также проводилось рандомизированное исследование по лечению этой группы больных (85 человек). Сравнивалась комбинированная терапия (4 цикла CVPP + облучение зон исходного поражения) и радикальная лучевая терапия. Шестилетняя выживаемость, свободная от неудач лечения, составила 88% и 63% соответственно – p<0,01 при одинаковой общей выживаемости.
Вся программа выполняется за 10 недель [5]. В 1978–88 гг. в РОНЦ им. Н.Н. Блохина РАМН также проводилось рандомизированное исследование по лечению этой группы больных (85 человек). Сравнивалась комбинированная терапия (4 цикла CVPP + облучение зон исходного поражения) и радикальная лучевая терапия. Шестилетняя выживаемость, свободная от неудач лечения, составила 88% и 63% соответственно – p<0,01 при одинаковой общей выживаемости.
Лечение больных промежуточной прогностической группы
Эта группа больных лимфомой Ходжкина наиболее многочисленна, и принципиальное преимущество комбинированной терапии для этой группы больных было доказано еще к началу 90–х годов. В рандомизированном исследовании EORTC (1977–1982 гг.) 15–летняя общая выживаемость оказалась одинаковой – 69%, но риск рецидива на этот срок в группе больных, получавших радикальную лучевую терапию, составил 35% по сравнению с 16% в группе комбинированного лечения – p<0,001. Преимущество комбинированной терапии было выявлено и при сравнении ее с полихимиотерапией. Опубликованные A.Preti с соавторами результаты рандомизированного исследования (104 больных) показали преимущество комбинированной терапии как по 7–летней общей выживаемости (84% против 66% p<0,01), так и по безрецидивной выживаемости (75% против 34% – p<0,001) [5]. Такие же результаты были получены при аналогичном рандомизированном исследовании в РОНЦ. Шестилетняя общая выживаемость в группах больных с промежуточным прогнозом, получавших полихимиотерапию (6 циклов по схеме CVPP), радикальную лучевую терапию и комбинированное лечение (6 циклов CVPP + облучение лимфатических коллекторов выше диафрагмы) составила 88%, 77% и 94% соответственно (p<0,01), а безрецидивная выживаемость 46%, 60% и 87% соответственно (p<0,01). Однако в терапии этой группы до последнего времени оставался открытым вопрос об объеме лучевой терапии – надо ли облучать только зоны исходного поражения или необходимо использовать широкопольное облучение на все лимфатические коллекторы выше диафрагмы. Два крупных рандомизированных исследования показали нецелесообразность широкопольного облучения в рамках комбинированной терапии.
Опубликованные A.Preti с соавторами результаты рандомизированного исследования (104 больных) показали преимущество комбинированной терапии как по 7–летней общей выживаемости (84% против 66% p<0,01), так и по безрецидивной выживаемости (75% против 34% – p<0,001) [5]. Такие же результаты были получены при аналогичном рандомизированном исследовании в РОНЦ. Шестилетняя общая выживаемость в группах больных с промежуточным прогнозом, получавших полихимиотерапию (6 циклов по схеме CVPP), радикальную лучевую терапию и комбинированное лечение (6 циклов CVPP + облучение лимфатических коллекторов выше диафрагмы) составила 88%, 77% и 94% соответственно (p<0,01), а безрецидивная выживаемость 46%, 60% и 87% соответственно (p<0,01). Однако в терапии этой группы до последнего времени оставался открытым вопрос об объеме лучевой терапии – надо ли облучать только зоны исходного поражения или необходимо использовать широкопольное облучение на все лимфатические коллекторы выше диафрагмы. Два крупных рандомизированных исследования показали нецелесообразность широкопольного облучения в рамках комбинированной терапии. Французская кооперированная группа (1985 г., 218 больных) не выявила различия в 6–летнем безрецидивном течении при облучении только зон исходного поражения по сравнению с методикой расширенных полей (87% против 93% – р=0,15) в рамках комбинированного химио–лучевого лечения [8]. Аналогичные данные были представлены Ruffer J–U. (GSHG) на V международном симпозиуме по лимфоме Ходжкина в сентябре 2001 года в Кельне. Рандомизировано 1068 больных, частота полных ремиссий оказалась одинаковой (97% и 98%), а 2–летняя выживаемость, свободная от неудач лечения, достигла 92% и 94%, при одинаковой общей выживаемости (97%) в обеих группах [7]. В РОНЦ до 1989 г. эта группа больных получала комбинированное лечение: 6 циклов CVPP и облучение всех лимфатических коллекторов выше диафрагмы в дозе 36 Гр, а с 1990 г. по 2000 г. объем облучения был сокращен до зон исходного поражения в той же дозе. Медиана наблюдения составила 80 мес и 43 мес соответственно, частота полных ремиссий – 93% и 98%. Шестилетняя общая выживаемость достигла 94% и 97%, а выживаемость, свободная от неудач лечения – 81% и 81% соответственно.
Французская кооперированная группа (1985 г., 218 больных) не выявила различия в 6–летнем безрецидивном течении при облучении только зон исходного поражения по сравнению с методикой расширенных полей (87% против 93% – р=0,15) в рамках комбинированного химио–лучевого лечения [8]. Аналогичные данные были представлены Ruffer J–U. (GSHG) на V международном симпозиуме по лимфоме Ходжкина в сентябре 2001 года в Кельне. Рандомизировано 1068 больных, частота полных ремиссий оказалась одинаковой (97% и 98%), а 2–летняя выживаемость, свободная от неудач лечения, достигла 92% и 94%, при одинаковой общей выживаемости (97%) в обеих группах [7]. В РОНЦ до 1989 г. эта группа больных получала комбинированное лечение: 6 циклов CVPP и облучение всех лимфатических коллекторов выше диафрагмы в дозе 36 Гр, а с 1990 г. по 2000 г. объем облучения был сокращен до зон исходного поражения в той же дозе. Медиана наблюдения составила 80 мес и 43 мес соответственно, частота полных ремиссий – 93% и 98%. Шестилетняя общая выживаемость достигла 94% и 97%, а выживаемость, свободная от неудач лечения – 81% и 81% соответственно. Как видно из всех этих исследований, для больных с лимфомой Ходжкина сокращение объема лучевой терапии в рамках комбинированного химио–лучевого лечения до облучения только зон исходного поражения не снижает ни непосредственных, ни отдаленных результатов лечения.
Как видно из всех этих исследований, для больных с лимфомой Ходжкина сокращение объема лучевой терапии в рамках комбинированного химио–лучевого лечения до облучения только зон исходного поражения не снижает ни непосредственных, ни отдаленных результатов лечения.
Лечение больных неблагоприятной прогностической группы
Для лечения этой группы больных всегда использовалась полихимиотерапия. Непосредственная эффективность лечения достигала 60–80% полных ремиссий, но 5–летняя выживаемость редко превышала 60%, а выживаемость, свободная от неудач лечения, достигла лишь 40% [2,3,5]. В начале 80–х годов две группы исследователей (из Ванкувера и из Милана) предложили объединить в одной программе обе схемы полихимиотерапии первой линии (MOPP и ABVD) для повышения эффективности терапии. В 80–х – начале 90–х годов 9 крупных исследовательских групп провели многоцентровые рандомизированные исследования, пытаясь доказать преимущество 7–8–компонентной полихимиотерапии перед 4–компонентной. Только в 3 из 9 исследований было показано незначительное преимущество многокомпонентной химиотерапии перед 4–компонентной по безрецидивной выживаемости, однако остальные 6 исследований не выявили никаких различий [4,5].
Только в 3 из 9 исследований было показано незначительное преимущество многокомпонентной химиотерапии перед 4–компонентной по безрецидивной выживаемости, однако остальные 6 исследований не выявили никаких различий [4,5].
В начале 90–х годов две группы исследователей – из Стэнфорда и из Германии (GHSG) – независимо друг от друга предложили новую концепцию для лечения этих больных. Проанализировав предшествовавшие программы лечения в большой группе больных (более 700 человек в группе GHSG), эти исследователи предложили иные принципы интенсификации лечения. Кроме объединения в одной схеме основных препаратов первой линии и эскалации доз, был сокращен интервал между циклами химиотерапии, чем достигалась более высокая еженедельная дозная нагрузка в течение всей программы лечения. Широкое внедрение в лечебную практику гранулоцитарных и макрофагальных колониестимулирующих факторов (граноцит, нейпоген, лейкомакс) позволило проводить всю программу лечения в оптимальном режиме без удлинения интервалов.
Стэнфордская группа предложила программу Stanford V, а GHSG – схемы ВЕАСОРР–базовый и ВЕАСОРР–эскалированный с добавлением лучевой терапии в дозе 30–36 Гр на зоны исходно больших массивов и/или остаточные опухолевые массы. Программа Stanford V состоит из 12–недельной беспрерывной полихимиотерапии и последующей лучевой терапии у больных, не достигших полной ремиссии. Лечение получили 126 больных и при 4,5–летней медиане наблюдения прогнозируемая 8–летняя общая выживаемость составила 96%, а выживаемость, свободная от неудач лечения – 89% [5]. GHSG предложила программу, состоящую из 8 циклов полихимиотерапии ВЕАСОРР базового или эскалированного уровня с последующим облучением. Эта исследовательская группа представила наиболее убедительные доказательства преимущества нового принципа лечения в рандомизированном многоцентровом исследовании. Было проведено сравнение 8 циклов ВЕАСОРР базового (циклофосфамид 650 мг/м2 в 1–й день, адрибластин 25 мг/м2 в 1–й день, вепезид 100 мг/м2 1–3–й дни, прокарбазин 100 мг/м2 1–7 дни, преднизолон 40 мг/м2 1–8 дни, блеомицин 10 мг/м2 в 8–й день и винкристин 1,4 мг/м2 в 8–й день, курс возобновляется на 21–й день) и эскалированного (по дозам адрибластина, вепезида и циклофосфамида) уровней, со стандартной полихимиотерапией СОРР/ABVD (4 двойных цикла). Облучение зон исходно больших массивов и/или остаточных опухолевых масс проводилось во всех трех сравниваемых программах. Всего в исследование было включено 689 больных. Частота полных ремиссий составила 83%, 88% и 95% в группах больных, получавших полихимиотерапию СОРР/ABVD, ВЕАСОРР–базовый и ВЕАСОРР–эскалированный. Статистически значимо больше было больных с прогрессированием заболевания в группе, получавшей СОРР/ABVD – 13% по сравнению с 9% и 2% соответственно в группах, получавших ВЕАСОРР–базовый и ВЕАСОРР–эскалированный, что и обеспечило лучшую 2–летнюю выживаемость, свободную от неудач лечения в группах, получавших ВЕАСОРР: 72%, 81%, 89% соответственно, р<0,05. Общая выживаемость также имела тенденцию к повышению в группах больных, лечившихся по программе ВЕАСОРР – 89%, 94%, 96% соответственно, однако различия статистически незначимы. Смертность в процессе лечения от осложнений терапии была одинаковой – 3%, 1% и 2%, но в группе получавших ВЕАСОРР–эскалированный было больше миелоидных лейкозов (4 больных), в то время, как в группах, получавших СОРР/ABVD и ВЕАСОРР–базовый – неходжкинских лимфом – 4 и 5 соответственно.
Облучение зон исходно больших массивов и/или остаточных опухолевых масс проводилось во всех трех сравниваемых программах. Всего в исследование было включено 689 больных. Частота полных ремиссий составила 83%, 88% и 95% в группах больных, получавших полихимиотерапию СОРР/ABVD, ВЕАСОРР–базовый и ВЕАСОРР–эскалированный. Статистически значимо больше было больных с прогрессированием заболевания в группе, получавшей СОРР/ABVD – 13% по сравнению с 9% и 2% соответственно в группах, получавших ВЕАСОРР–базовый и ВЕАСОРР–эскалированный, что и обеспечило лучшую 2–летнюю выживаемость, свободную от неудач лечения в группах, получавших ВЕАСОРР: 72%, 81%, 89% соответственно, р<0,05. Общая выживаемость также имела тенденцию к повышению в группах больных, лечившихся по программе ВЕАСОРР – 89%, 94%, 96% соответственно, однако различия статистически незначимы. Смертность в процессе лечения от осложнений терапии была одинаковой – 3%, 1% и 2%, но в группе получавших ВЕАСОРР–эскалированный было больше миелоидных лейкозов (4 больных), в то время, как в группах, получавших СОРР/ABVD и ВЕАСОРР–базовый – неходжкинских лимфом – 4 и 5 соответственно.
В РОНЦ с декабря 1998 г. проводится лечение по программе ВЕАСОРР–базовый 67 больных. К январю 2002 г. закончили лечение, после чего прослежены в течение 3 месяцев и оценены 25 больных. Общее число циклов полихимиотерапии составило 192, но в стационаре проведено лишь 40 циклов – 20% от общего числа циклов, что свидетельствует о хорошей переносимости программы. Медиана наблюдения составила 17 месяцев. Острый миелоидный лейкоз М4 развился в полной ремиссии лимфомы Ходжкина у 1 больной. Частота полных ремиссий достигла 88%, выживаемость, свободная от неудач лечения на медиану наблюдения – 75%, а общая выживаемость – 83%.
Заключение
Таким образом, прошедшее столетие показало возможность излечения большинства больных лимфомой Ходжкина, а на рубеже столетий были сформулированы новые концепции лечения этих больных. Ушли в прошлое радикальная лучевая терапия и широкопольное облучение. Лучевая терапия стала применяться для всех больных только в сочетании с химиотерапией, исключительно на зоны поражения и в дозах не выше 30–40 Гр. Четко определилась тенденция к дальнейшему снижению суммарных очаговых доз облучения.
Четко определилась тенденция к дальнейшему снижению суммарных очаговых доз облучения.
Основным лечебным принципом стало соответствие объема терапии объему опухолевой массы. Разделение больных на прогностические группы в соответствии с объемом опухолевой массы позволило более адекватно выбирать программу лечения. Так, для благоприятной прогностической группы с минимальным объемом поражения показан минимальный объем лечения – 2–4 цикла химиотерапии + облучение только исходно пораженных лимфатических коллекторов; для промежуточной прогностической группы – 4–6 циклов полихимиотерапии + облучение только исходно пораженных зон; для неблагоприятной прогностической группы с большим объемом опухоли максимальный объем лечения – 8 циклов полихимиотерапии + облучение зон исходно больших массивов и/или зон с остаточными лимфатическими узлами.
Литература:
1. Клиническая онкогематология.// Ред. Волкова М.А. // Москва, Медицина, 2001.
2. Bailliere’s Clinical Haematology. International Practice and Research. Hodgkin’s Disease. // Guest editor V. Diehl. – 1996.
Bailliere’s Clinical Haematology. International Practice and Research. Hodgkin’s Disease. // Guest editor V. Diehl. – 1996.
3. Cancer. Principles & Practice of Oncology. 4th Edition. // Ed. by V.T.DeVita, S. Hellman, S.A. Rosenberg // Philadelphia. – 1993. – V 2. – Р. 1819–1858.
4. Diehl V., Franklin J., Hansenclever D. et al. // Ann. of Oncol. – 1998. – V 9. (Suppl 5). – P. 68 – 71.
5. Hodgkin’s disease. // Ed. by Mauch P.V., Armitage J.O., Diehl V. et al // Philadelphia. – 1999.
6. Brincker H., Bentzen S.M.//Radiotherapy & Oncology, 30 (1994), 227–230.
7. Ruffer J–U., Sieber M., Pfistner B., et al.// Leukemia & Lymphoma –2001. – V 42 (Suppl. 2). – Abstr. P–095.– P.54
8. Zittoun R., Audebert A., Hoerni B. Et al.// J. Clin/ Oncol. – 1985. – V 3. – P. 203–214.
.
Болезнь Ходжкина › Болезни › ДокторПитер.ру
Болезнь Ходжкина (лимфогранулематоз) – это злокачественное заболевание, поражающее лимфатическую систему. Заболевание может возникнуть в любом органе, имеющем лимфоидную ткань (лимфатические узлы, селезенка, вилочковая железа, аденоиды, миндалины).
Заболевание может возникнуть в любом органе, имеющем лимфоидную ткань (лимфатические узлы, селезенка, вилочковая железа, аденоиды, миндалины).
Признаки
Болезнь начинается с увеличения лимфатических узлов. Обычно сначала увеличиваются паховые, шейно-надключичные и подмышечные узлы. Однако в 15-20 % случаев в первую очередь увеличиваются лимфатические узлы брюшной и грудной полости. При этом пациентов также беспокоит кашель, боль в груди, одышка, ощущение тяжести в животе и потеря аппетита. Иногда лимфоузлы увеличиваются до таких огромных размеров, что сдавливают желудок и смещают почки.
Также для лимфогранулематоза характерно повышение температуры, озноб, потливость. Температура тела скачет то вверх, то вниз. Повышение температуры сопровождается ознобом, а ее снижение – обильным потоотделением. Аппетит у пациента снижается. Пациент теряет вес, у него развивается кахексия (истощение). Примерно треть страдающих болезнью Ходжкина беспокоит кожный зуд, причем интенсивность его может быть различной – от умеренного до изнуряющего.
Описание
Предполагается, что лимфогранулематоз был известен уже в 1666 году. По крайней мере, именно в это время в трудах Malpighi встречается описание заболевания, похожего на то, что сейчас известно как болезнь Ходжкина.
Однако названо это заболевание по имени Томаса Ходжкина, который в 1832 году сообщил о семи пациентах с общими симптомами – увеличением лимфатических узлов, увеличением селезенки, кахексией. Все семь пациентов умерли. А Ходжкин предложил выделить эти случаи в самостоятельное заболевание. Через 23 года С. Уилкс внимательно изучил исследования Ходжкина, добавил к ним собственные наблюдения еще за 11 пациентами и назвал заболевание болезнью Ходжкина. Значительный вклад в изучение лимфогранулематоза также сделали С.Я. Березовский (1890), Штернберг (1899) и Рид (1902). Они описали опухолевые клетки, которые обнаруживаются при этом заболевании в лимфатических узлах. В России эти клетки называют клетками Березовского-Штернберга, а за рубежом – клетками Штернберга-Рида. Некоторые специалисты называют их клетками Березовского-Штернберга-Рида.
Некоторые специалисты называют их клетками Березовского-Штернберга-Рида.
Лимфогранулематозом можно заболеть в любом возрасте, однако чаще он развивается у молодых мужчин в возрасте 16-30 лет, либо у пожилых мужчин старше 50 лет. У детей до года это заболевание не встречается, у детей до 5 лет оно выявляется крайне редко. Частота заболеваемости примерно 3 человека на 1 млн населения в год. Частота заболеваемости среди детей в России – 1,9 на 100 тыс населения.
Что именно вызывает это заболевание, неизвестно. Однако есть гипотеза, что причина – вирусы. Считается, что спровоцировать начало этого заболевания могут:
Известно также, что если один из близнецов страдает лимфогранулематозом, то у второго повышается риск развития этого заболевания.
Болезнь Ходжкина может протекать молниеносно, от 4 до 6 месяцев, либо медленно, до 20 лет.
В течение болезни выделяют четыре стадии:
-
При лимфогранулематозе первой стадии поражены лимфатические узлы одной области (I), или поражен один какой-либо орган или его участок (Ie).
-
Вторая стадия характеризуется поражением лимфатических узлов двух или нескольких областей по одну сторону диафрагмы (II) выше или ниже ее. Также возможно локализованное поражение внелимфатического органа или его участка и лимфатических узлов одной или нескольких областей по одну сторону диафрагмы (IIe). -
При третьей стадии заболевания поражены лимфатические узлы по обе стороны диафрагмы (III), при этом может быть поражена селезенка (IIIs) или какой-то внелимфатический орган или его участок (IIIe). Возможно также поражение и того, и другого (IIIse). -
Четвертая стадия болезни Ходжкина характеризуется диффузным или диссеминированным поражением одного или нескольких внелимфатических органов или тканей, сопровождающимся или не сопровождающимся поражением лимфатических узлов.
При этом каждая стадия подразделяется на категории, которые обозначаются буквами. Категория «а» означает отсутствие у пациента симптомов заболевания.
Категория «а» означает отсутствие у пациента симптомов заболевания.
Категория «в» означает, что у пациента есть как минимум один из нижеследующих симптомов:
-
необъяснимая потеря массы тела более 10 % от первоначальной за последние полгода; -
необъяснимая лихорадка с температурой более 38°С; -
обильное потоотделение.
Категория «е» присваивается, если опухоль распространена на органы и ткани, расположенные рядом с пораженными группами лимфатических узлов.
Если рядом со стадией есть буква «s», значит, у пациента поражена селезенка.
Буква «x» означает, что образование достигло большого размера.
Также выделяют четыре гистологических типа болезни Ходжкина.
При лимфогистоцитарном типе (15 % всех случаев лимфогранулематоза) в биоптате преобладают зрелые лимфоциты, клеток Березовского-Штернберга-Рида мало. Этот тип болезни с низкой злокачественностью, обнаруживается он на ранних стадиях. Пациенты чаще всего мужчины моложе 35 лет.
Пациенты чаще всего мужчины моложе 35 лет.
Нодулярный склероз – это наиболее частый тип болезни Ходжкина, примерно 40-45 % всех случаев. Чаще им страдают молодые женщины. Поражаются обычно лимфатические узлы средостения. В биоптате обнаруживаются не только клетки Березовского-Штернберга-Рида, но и лакунарные клетки – большие, со множеством ядер и с пенистой цитоплазмой. Прогноз при этом заболевании, как правило, хороший.
В 30 % случаев болезни Ходжкина бывает смешанноклеточный тип. Им часто страдают пожилые люди, дети, а также ВИЧ-инфицированные. Это заболевание чаще развивается у мужчин. Заболевание обычно обнаруживается на II-III стадии. В биоптате много клеток Березовского-Штернберга-Рида.
Самый редкий тип – протекающий с подавлением лимфоидной ткани. Это менее 5 % случаев болезни Ходжкина. Страдают им в основном пожилые пациенты. В биоптате преобладают клетки Березовского-Штернберга-Рида и почти нет лимфоцитов.
Диагностика
Для диагностики этого заболевания требуется консультация онколога и гематолога. Обязательно делают биопсию лимфатических узлов, так как основной диагностический признак заболевания – наличие клеток Березовского-Штернберга-Рида в биоптате.
Также проводят ультразвуковое исследование органов брюшной полости, компьютерную или магнитно-резонансную томографию органов грудной клетки. Делают и биопсию костного мозга.
Дифференцировать болезнь Ходжкина нужно с бактериальными и вирусными инфекциями и неходжкинскими лимфомами.
Лечение
При отсутствии лечения в течение 10 лет выживает менее 10 % пациентов. Наиболее эффективное лечение – лучевая терапия и противоопухолевые средства. Лучевая терапия используется у пациентов с I и IIА стадиями заболевания, на IIВ и IIIА этот метод сочетается с медикаментозным лечением. На IIIВ и IV стадиях лимфогранулематоза применяют обычно только медикаментозную терапию противоопухолевыми препаратами.
При поражении костного мозга проводят его аутотрансплантацию. Правда, такое поражение встречается довольно редко.
Окончательно излеченными считаются те, у кого полная ремиссия продолжается более 5 лет.
Профилактика
Эффективной профилактики болезни Ходжкина не существует, так как неизвестна точная причина этого заболевания.
© Доктор Питер
ABC-медицина
Термин «лимфома» объединяет группу гематологических заболеваний лимфатической ткани, которые характеризуются увеличением лимфатических узлов и/или поражением внутренних органов, где происходит бесконтрольное скопление «опухолевых» лимфоцитов. В результате неограниченного деления таких клеток происходит нарушение в работе различных систем организма. Все лимфомы подразделяются на 2 группы: лимфома Ходжкина (лимфогранулематоз) и неходжкинские лимфомы.
Причины
В настоящее время точно не установлено, почему возникают лимфомы. Однако было определено несколько факторов, которые повышают риск развития данных заболеваний. Среди причин можно отметить снижение иммунитета, наличие ВИЧ-инфекции, вируса Эпштейна-Барра, вируса гепатита В или С, Т-лимфоцитарного вируса 1 типа. При это стоит сказать, что лимфома не является вирусным заболеванием, то есть исключена ее передача от человека к человеку.
Однако было определено несколько факторов, которые повышают риск развития данных заболеваний. Среди причин можно отметить снижение иммунитета, наличие ВИЧ-инфекции, вируса Эпштейна-Барра, вируса гепатита В или С, Т-лимфоцитарного вируса 1 типа. При это стоит сказать, что лимфома не является вирусным заболеванием, то есть исключена ее передача от человека к человеку.
В группе риска также находятся люди, работающие на производствах, связанных с воздействием различных химических веществ (например, на фармацевтических предприятиях). Существует и генетическая предрасположенность – вероятность возникновения лимфомы повышается, если этим заболеванием страдают ближайшие родственники.
Симптомы
Симптомы лимфомы зависят от того, к какому виду она относится – крупноклеточная, фолликулярная и пр. Например, при лимфоме кожи возникает кожный зуд разной степени, который может появиться еще до поражения лимфатических узлов. При этом зуд распространен по всему телу с локализацией в области грудного отдела, головы, ладоней и стоп.
В большинстве случаев первым и основным симптомом лимфомы любого вида является существенное увеличение размеров лимфатических узлов на шее, в паху и подмышечных впадинах. В отличие от поражения инфекционными заболеваниями, при лимфоме воспаленные узлы не болезненны, с течением времени они не уменьшаются в размерах (даже при приеме антибиотиков). К другим признакам заболевания можно отнести:
- повышение температуры тела;
- слабость;
- повышенную потливость;
- потерю веса;
- нарушение пищеварения;
- затруднение дыхания;
- ощущение давления в области шеи и/или лица;
- распирающие боли в нижней части спины.
Поставить точный диагноз и определить, на какой стадии находится лимфома, может только врач по результатам обследования и анализов пациента.
Лечение
Для лечения лимфомы применяются облучение и полихимиотерапия (и их комбинация), то есть методы, которые используются и при других различных онкологических заболеваниях. Курс терапии определяется врачом в каждом конкретном случае с учетом вида и стадии заболевания, а также индивидуальных особенностей организма пациента.
Курс терапии определяется врачом в каждом конкретном случае с учетом вида и стадии заболевания, а также индивидуальных особенностей организма пациента.
Для записи на прием к специалистам клиники «АВС-Медицина» позвоните по телефону +7 (495) 223-38-83 или заполните заявку на сайте.
Городская клиническая больница №31 — Пациентам в помощь. Гематологические заболевания. Введение. Часть I. Лимфомы (страница 11)
Страница 11 из 33
Хронический лимфоцитарный лейкоз\лимфома из малых лимфоцитов
Хронический лимфоцитарный лейкоз\лимфома из малых лимфоцитов относится к классу индолентных, или вялотекущих, медленных лимфом. При этом заболевании изменяется состав крови, а также иногда увеличиваются лимфатические узлы и селезенка. У больного могут появляться и такие признаки болезни, которые называются «В-симптомы»: поднимается температура, он быстро худеет и может сильно потеть вечером и ночью. В связи с тем, что болезнетворные клетки поселяются в костном мозге и вытесняют нормальные, то в крови снижается количество гемоглобина и тромбоцитов и одновременно повышается количество лейкоцитов. Когда гемоглобина меньше нормы, больной быстро слабеет. Когда мало тромбоцитов, начинается кровоточивость, то есть без причины возникают мелкие и крупные «синяки» на коже и во рту, появляется кровь при чистке зубов, менструальные кровотечения у женщин длятся дольше.
В связи с тем, что болезнетворные клетки поселяются в костном мозге и вытесняют нормальные, то в крови снижается количество гемоглобина и тромбоцитов и одновременно повышается количество лейкоцитов. Когда гемоглобина меньше нормы, больной быстро слабеет. Когда мало тромбоцитов, начинается кровоточивость, то есть без причины возникают мелкие и крупные «синяки» на коже и во рту, появляется кровь при чистке зубов, менструальные кровотечения у женщин длятся дольше.
Болезнь часто проявляется своими осложнениями, поскольку даже на самой ранней стадии она может вызвать другие нарушения иммунитета: аутоиммунные осложнения, холодовой агглютинационный синдром, криоглобулинемию, артриты и так далее.
Диагноз
Хронический лимфоцитарный лейкоз всегда сопровождается повышением количества лимфоцитов крови, поэтому часто для установления диагноза достаточно провести проточную цитометрию крови. Эта болезнь способна перерождаться в более агрессивную диффузную В-клеточную крупноклеточную лимфому, и значит, если увеличены лимфатические узлы, необходимо сделать биопсию увеличенного узла для морфологического и иммуногистохимического исследования. Только после такого комплексного исследования можно быть уверенным в диагнозе и провести эффективное лечение.
Только после такого комплексного исследования можно быть уверенным в диагнозе и провести эффективное лечение.
Чтобы точно узнать, есть ли увеличенные лимфатические узлы или одиночные образования (опухоли) и каково их количество в тех частях тела, которые нельзя увидеть простым глазом или прощупать руками, необходимо сделать компьютерную томографию грудной клетки, брюшной полости, малого таза. Стадию болезни устанавливают по системе предложенной Rai и Binet, которая показывает, увеличены ли селезенка и лимфоузлы, изменен ли состав крови.
Если заболевание проявляется только увеличением лимфатических узлов, то врачи называют данное состояние «лимфомой из малых лимфоцитов». Если же у пациента в крови повышены лейкоциты, снижены гемоглобин и тромбоциты, то ставят диагноз «хронический лимфоцитарный лейкоз». Когда врач-морфолог выдает заключение по результатам исследования лимфатического узла, то диагноз иногда пишет через косую черту, тем более что прогноз и лечение у этих заболеваний одинаковые. Более точный диагноз ставит лечащий врач на основании всей полноты анализов пациента.
Более точный диагноз ставит лечащий врач на основании всей полноты анализов пациента.
Лечение
В тех случаях, когда болезнь протекает медленно и бессимптомно, то есть не имеет выраженных и беспокоящих признаков, лечение можно отложить. Пациенты сдают время от времени контрольные анализы крови и наблюдаются амбулаторно. Только тогда, когда появляются тревожные признаки болезни, врач-гематолог решает начать лечение.
Показания к началу лечения:
- Уменьшение количества клеток крови (тромбоцитов, эритроцитов).
- Аутоиммунные осложнения.
- Увеличение лимфатических узлов, селезенки, печени, которое сопровождается болью или другими жалобами.
- Появление В-симптомов или сильной слабости.
- Быстрое увеличение количества опухолевых клеток крови
Лечение хронического лимфоцитарного лейкоза небольшим, но достаточным введением в организм больного лекарств, включая ритуксимаб, имеет хороший, стойкий эффект. Применение современных схем лечения позволяют успешно лечить более 95% пациентов.
Применение современных схем лечения позволяют успешно лечить более 95% пациентов.
стадий лимфомы Ходжкина | Стадии болезни Ходжкина
После того, как кому-то поставят диагноз лимфома Ходжкина (ЛХ), врачи попытаются выяснить, распространилась ли она, и если да, то как далеко. Этот процесс называется staging . Стадия рака описывает, сколько рака находится в организме. Это помогает определить, насколько серьезен рак и как лучше его лечить. Врачи также используют стадию рака, когда говорят о статистике выживаемости.
HL обычно начинается в лимфатических узлах.Если он распространяется, то обычно на другой набор соседних лимфатических узлов. Он также может проникать (прорастать) в близлежащие органы. В редких случаях HL начинается в органе, отличном от лимфатических узлов, например в легком.
Сцена основана на:
- Ваша история болезни
- Если у вас есть определенные симптомы (называемые симптомами B)
- Физический осмотр
- Биопсии
- Визуализирующие обследования, которые обычно включают рентген грудной клетки, компьютерную томографию грудной клетки / брюшной полости / таза и ПЭТ-сканирование.

- Аспирация и биопсия костного мозга (иногда, но не всегда)
Эти обследования, тесты и биопсии обсуждаются в разделе «Тесты на лимфому Ходжкина».
В целом, результаты визуализационных тестов, таких как ПЭТ и КТ, являются наиболее важными при определении стадии лимфомы.
Классификация Лугано
Система стадирования — это способ для команды специалистов по лечению рака оценить степень распространения рака. Для лимфомы Ходжкина используется классификация Лугано , основанная на более старой системе Ann Arbor . Он состоит из 4 этапов, обозначенных I, II, III и IV.
Для ограниченной стадии (I или II) HL, которая затрагивает орган вне лимфатической системы, к стадии добавляется буква E (например, стадия IE или IIE).
Этап I: Любое из следующих условий означает, что HL является этапом I:
- HL обнаруживается только в 1 области лимфатических узлов или лимфоидном органе, таком как тимус (I).

- Рак обнаруживается только в 1 части 1 органа вне лимфатической системы (IE).
Стадия II: Любое из следующих условий означает, что HL является стадией II:
- HL обнаруживается в 2 или более областях лимфатических узлов на одной стороне (выше или ниже) диафрагмы, которая представляет собой тонкую мышцу под легкими, разделяющую грудную клетку и брюшную полость (II).
- Рак распространяется локально из области одного лимфатического узла в соседний орган (IIE).
Стадия III: Любое из следующих условий означает, что HL является стадией III:
- HL обнаруживается в областях лимфатических узлов с обеих сторон (выше и ниже) диафрагмы (III).
- HL находится в лимфатических узлах над диафрагмой и в селезенке.
Стадия IV: HL широко распространился по крайней мере в один орган за пределами лимфатической системы, такой как печень, костный мозг или легкие.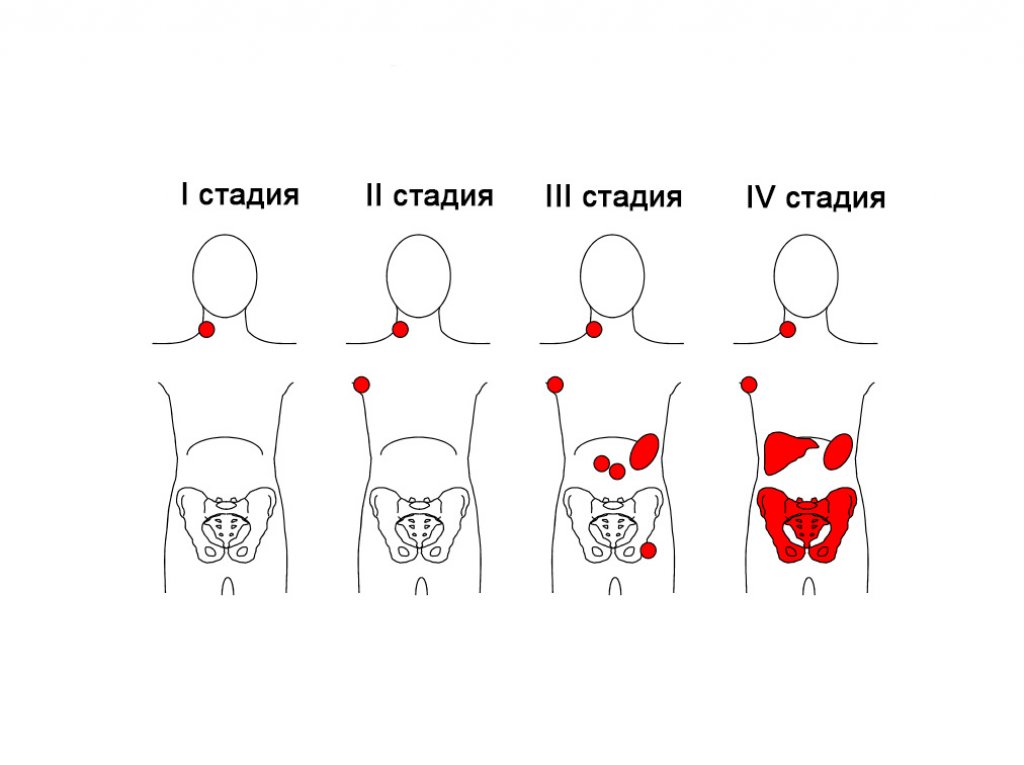
Другие модификаторы также могут быть использованы для описания стадии лимфомы Ходжкина:
Объемная болезнь
Этот термин используется для описания опухолей в грудной клетке, ширина которых составляет не менее tum ширины грудной клетки, или опухолей в других областях, которые имеют диаметр не менее 10 сантиметров (около 4 дюймов). Обычно это обозначается добавлением буквы X к сцене. Это особенно важно при лимфомах II стадии, потому что объемное заболевание может потребовать более интенсивного лечения.
A vs.B
Каждому этапу также может быть присвоена буква (A или B). B добавляется (например, стадия IIIB), если у человека наблюдается любой из этих симптомов B :
- Потеря более 10% массы тела за предыдущие 6 месяцев (без диеты)
- Необъяснимая лихорадка не менее 38 ° C (100,4 ° F)
- Обливание ночного пота
Если у человека наблюдаются какие-либо симптомы B, это обычно означает, что лимфома прогрессирует, и часто рекомендуется более интенсивное лечение. Если симптомы B отсутствуют, к стадии добавляется буква A.
Если симптомы B отсутствуют, к стадии добавляется буква A.
Резистентная или рецидивирующая лимфома Ходжкина
Устойчивый или рецидивирующий HL не является частью официальной системы стадирования, но врачи или медсестры могут использовать эти термины для описания того, что происходит с лимфомой в некоторых случаях.
- Термины устойчивый или прогрессирующий болезнь используются, когда лимфома не проходит или прогрессирует (растет) во время лечения.
- Рецидив или рецидив заболевания означает, что HL прошел после лечения, но теперь вернулся. Если лимфома возвращается, она может быть в том же месте, где она возникла, или в другой части тела. Это может произойти вскоре после лечения или спустя годы.
Этапы | Лимфома Ходжкина | Исследования рака Великобритании
Стадии лимфомы Ходжкина говорят о количестве и местах в организме, пораженных лимфомой. Знание стадии лимфомы Ходжкина поможет вашему врачу решить, какое лечение вам нужно.
Знание стадии лимфомы Ходжкина поможет вашему врачу решить, какое лечение вам нужно.
Классификация Лугано используется для определения стадии лимфомы. Всего 4 этапа. Или они могут быть упрощены до ограниченной или продвинутой стадии.
Как врачи разрабатывают вашу стадию
Врачи проверяют, находится ли лимфома с одной стороны или с обеих сторон диафрагмы. И находится ли он внутри или вне лимфатической системы. Они измерит размер лимфомы. Они делают это, проводя различные тесты, такие как компьютерная томография или ПЭТ.Они также проверит, есть ли у вас какие-либо симптомы.
Диафрагма
Диафрагма (произносится как диафрам) — это большая дыхательная мышца, отделяющая грудную клетку от области живота (брюшной полости).
Врачи используют диафрагму как направляющую, потому что она находится примерно на полпути вниз по телу.
Внутри или вне лимфатической системы
Врачи проверяют, поражена ли лимфома:
- узлы и органы лимфатической системы — они называются лимфатическими участками
- участками вне лимфатических узлов — называются экстранодальными (или экстралимфатическими) участками
Лимфатические участки включают группу лимфатических узлов или орган лимфатической системы , например вилочковая железа или селезенка.
Экстранодальные участки включают легкие, печень, кровь, костный мозг, почки, головной и спинной мозг.
Ваш врач может использовать букву E после номера стадии, если у вас лимфома вне лимфатической системы. Ваш врач или медсестра могут объяснить, что это означает в вашей ситуации.
Б симптомы
Ваш врач добавит букву B к вашей стадии (например, стадии 1B), если у вас есть какие-либо из следующих симптомов:
- сильное потоотделение ночью
- высокие температуры, которые приходят и уходят, часто ночью
- необъяснимая потеря веса, более одной десятой (10%) массы вашего тела за последние 6 месяцев
Если у вас нет любой из этих симптомов ваш врач добавит букву A к вашей стадии (например, стадия 2A).
Людям с симптомами группы В может потребоваться больше лечения, чем тем, у кого они отсутствуют.
Объемная болезнь
Это означает:
- лимфатический узел размером 10 см или более
- лимфома в центре груди (средостение), которое составляет не менее трети ширины груди
Стадия 1
Это означает, что у вас есть один из следующих:
- лимфома в одном лимфатическом узле или одной группе лимфатических узлов, или в органе лимфатической системы (например, тимус)
- лимфома в экстранодальном участке (1E)
Ниже приведен пример лимфомы 1 стадии.
Лечение лимфомы Ходжкина 1 стадии обычно состоит из 2–4 курсов химиотерапии. Вы также можете пройти лучевую терапию.
Вы также можете пройти лучевую терапию.
2 этап
Это означает один из следующих:
- ваша лимфома находится в двух или более группах лимфатических узлов
- ваша лимфома находится на экстранодальном участке и одной или нескольких группах лимфатических узлов (2E)
В обоих случаях 2 участка лимфомы находятся на одной стороне диафрагмы.
Ниже приведен пример этапа 2.
Лечение лимфомы Ходжкина 2 стадии обычно состоит из 2–4 курсов химиотерапии. Вы также можете пройти лучевую терапию.
Стадия 3
Это означает, что у вас лимфома с обеих сторон диафрагмы.
Одним из примеров является то, что лимфома находится в лимфатических узлах с обеих сторон диафрагмы. Другой пример (см. Ниже) — лимфома находится в лимфатических узлах над диафрагмой, а также лимфома в селезенке.
Лечение лимфомы Ходжкина 3 стадии, как правило, состоит из 6-8 курсов химиотерапии. Как часть этого, вам могут быть назначены стероиды. И вы также можете пройти лучевую терапию.
Как часть этого, вам могут быть назначены стероиды. И вы также можете пройти лучевую терапию.
4 этап
Этап 4 означает одно из следующего:
- ваша лимфома находится в экстранодальном участке и поражены лимфатические узлы
- ваша лимфома находится в нескольких экстранодальных участках, например в печени, костях или легких
Ниже приведен пример лимфомы 4 стадии.
Лечение лимфомы Ходжкина 4 стадии обычно включает от 6 до 8 курсов химиотерапии.Как часть этого, вам могут быть назначены стероиды. И вы также можете пройти лучевую терапию.
Эти этапы упрощены
Ваш врач может описать вашу лимфому как ограниченную (раннюю) или запущенную стадию.
Ограниченная сцена
Ограниченная стадия обычно означает, что у вас лимфома Ходжкина стадии 1 или 2А.
Продвинутый уровень
Продвинутая стадия означает, что у вас лимфома Ходжкина стадии 2B, 3 или 4. У некоторых людей с объемной лимфомой 2 стадии может быть запущенное заболевание, в зависимости от их обстоятельств.
Рецидивирующая лимфома Ходжкина
Лимфома Ходжкина, которая вернулась после лечения, называется рецидивирующей болезнью.
Ваши врачи не поставят это так же, как когда вам впервые поставили диагноз. Но вы все равно можете пройти дополнительное лечение, и это часто срабатывает. Ваше лечение может включать пересадку стволовых клеток.
Лимфома Ходжкина — AMBOSS
Резюме
Лимфома Ходжкина (HL) — это злокачественная лимфома, которая обычно имеет B-клеточное происхождение. Заболеваемость HL имеет бимодальное возрастное распределение с пиками в 3 -е -е и 6 -е –8 -е десятилетия жизни. ВОЗ классифицирует HL на два типа: классический HL (CHL) и HL с преобладанием узловых лимфоцитов (NLPHL). ХЛС делится на четыре подтипа: узловой склероз (наиболее распространенный), смешанная клеточность, лимфоцитарный дефицит и ХЛ с высоким содержанием лимфоцитов. Факторы риска развития HL включают в себя инфекционный мононуклеоз, вызванный вирусом Эпштейна-Барра (EBV), и иммунодефицит (например, ВИЧ-инфекцию) в анамнезе. HL обычно проявляется безболезненной шейной лимфаденопатией, лихорадкой, ночным потоотделением и непроизвольной потерей веса.Лихорадка Пель-Эбштейна (циклическая лихорадка с периодами как высокой, так и нормальной температуры) и вызванная алкоголем боль в пораженных лимфатических узлах встречаются реже, но специфичны для HL. Подозрительные лимфатические узлы иссекаются, и окончательный диагноз ставится с помощью гистологического анализа, который характерно выявляет патогномоничные клетки Рида-Штернберга (злокачественные В-клетки). Модифицированная классификация Анн-Арбора (система стадирования по Котсуолду) используется для определения стадии HL на основании как локализации лимфомы относительно диафрагмы, так и наличия системных симптомов.
ВОЗ классифицирует HL на два типа: классический HL (CHL) и HL с преобладанием узловых лимфоцитов (NLPHL). ХЛС делится на четыре подтипа: узловой склероз (наиболее распространенный), смешанная клеточность, лимфоцитарный дефицит и ХЛ с высоким содержанием лимфоцитов. Факторы риска развития HL включают в себя инфекционный мононуклеоз, вызванный вирусом Эпштейна-Барра (EBV), и иммунодефицит (например, ВИЧ-инфекцию) в анамнезе. HL обычно проявляется безболезненной шейной лимфаденопатией, лихорадкой, ночным потоотделением и непроизвольной потерей веса.Лихорадка Пель-Эбштейна (циклическая лихорадка с периодами как высокой, так и нормальной температуры) и вызванная алкоголем боль в пораженных лимфатических узлах встречаются реже, но специфичны для HL. Подозрительные лимфатические узлы иссекаются, и окончательный диагноз ставится с помощью гистологического анализа, который характерно выявляет патогномоничные клетки Рида-Штернберга (злокачественные В-клетки). Модифицированная классификация Анн-Арбора (система стадирования по Котсуолду) используется для определения стадии HL на основании как локализации лимфомы относительно диафрагмы, так и наличия системных симптомов. Лечение обычно начинается с лечебной целью. На ранних стадиях лечение обычно ограничивается лучевой терапией и химиотерапией. На более поздних стадиях, когда местное облучение часто оказывается безуспешным или нецелесообразным из-за распространения опухоли, основным методом лечения является полихимиотерапия.
Лечение обычно начинается с лечебной целью. На ранних стадиях лечение обычно ограничивается лучевой терапией и химиотерапией. На более поздних стадиях, когда местное облучение часто оказывается безуспешным или нецелесообразным из-за распространения опухоли, основным методом лечения является полихимиотерапия.
Эпидемиология
- Заболеваемость
- 2–3 / 100 000 в год [1]
- Различия подтипа в зависимости от возраста (см. «Патология» ниже)
- Молодые люди: узловой склероз HL
- Пожилые люди: смешанная клеточность HL
- Возраст: бимодальное распределение [2]
- 1 st пик: 25–30 лет
- 2 nd пик: 50–70 лет
- Пол: ♂> ♀ [2]
- Преобладание мужчин, особенно в педиатрических случаях
- Исключение: ♀ = ♂ при узловой склерозирующей HL (наиболее распространенный тип)
Эпидемиологические данные относятся к США, если не указано иное.
Этиология
Точные причины неизвестны, но с HL связано несколько факторов риска. [3] [4]
Клинические особенности
- Безболезненная лимфаденопатия
- Симптомы B [5]
- Лихорадка Пель-Эбштейна: перемежающаяся лихорадка с периодами высокой температуры в течение 1-2 недель, за которыми следуют периоды афебрилитета в течение 1-2 недель. Относительно редко, но очень специфично для HL.
- Боль, вызванная алкоголем: Боль в пораженных лимфатических узлах после приема алкоголя.Относительно редко, но очень специфично для HL.
- Зуд (очаговый или генерализованный)
Этапы
| Cotswolds модифицированная система Анн-Арбор (на основе исходной ступенчатой системы Анн-Арбора) [6] [7] | |
|---|---|
| Этап | Описание | области 1 лимфатического узла (I N ) или 1 экстранодального (I E ) очага |
| II | Ограничено одной стороной диафрагмы: вовлечение ≥ 2 (II N ) областей лимфатических узлов или экстранодальные очаги (II E ) |
| III | С обеих сторон диафрагмы: поражение ≥ 2 (III N ) участков лимфатических узлов или экстранодальных очагов (III E ) |
| Распространяется на один или несколько экстралимфатических органов независимо от поражения лимфатических узлов | |
Дополнительные модификаторы
| |
Стадия зависит от количества пораженных узлов, наличия или отсутствия симптомов B, а также наличия или отсутствия заболевания на обеих сторонах диафрагмы.
Диагностика
Диагностика HL в первую очередь основана на истории болезни и клинических особенностях (симптомы B, локализация поражения лимфатических узлов) и подтверждается биопсией лимфатических узлов.
Анализы крови
Клетки Рида-Штернберга являются двухъядерными с положительными CD15 / CD30. Чтобы вспомнить маркеры клеток, помните, что 2 x 15 = 30.
Imaging
Патология
| Гистологическая классификация лимфомы Ходжкина (ВОЗ) | ||||
|---|---|---|---|---|
| Классификация | Подтип | Характеристики | Прогноз | Патология |
| ||||
| Классический HL со смешанной клеточностью (MCHL) |
|
| ||
| Классическая HL с высоким содержанием лимфоцитов (LRHL) |
| |||
| Лимфоцитарно-истощенный классический HL (LDHL) |
| |||
| Лимфома Ходжкина с преобладанием лимфоцитов (5%) | HL с преобладанием узловых лимфоцитов (NLPHL) |
| ||
Дифференциальные диагнозы
Дифференциальная диагностика лимфаденопатии
Исследование лимфатических узлов может дать важные диагностические ключи. Генерализованная лимфаденопатия обычно является признаком системного заболевания, такого как ВИЧ, микобактериальная инфекция (например, туберкулез), инфекционный мононуклеоз, системная красная волчанка или сывороточная болезнь. Признаки злокачественного новообразования включают быстрый рост, безболезненность, твердость / грубость и фиксацию на подлежащих или окружающих тканях. Однако чаще всего видимой причины или патологии нет.
Генерализованная лимфаденопатия обычно является признаком системного заболевания, такого как ВИЧ, микобактериальная инфекция (например, туберкулез), инфекционный мононуклеоз, системная красная волчанка или сывороточная болезнь. Признаки злокачественного новообразования включают быстрый рост, безболезненность, твердость / грубость и фиксацию на подлежащих или окружающих тканях. Однако чаще всего видимой причины или патологии нет.
| Характеристика | Нормальная | Инфекция | Злокачественная опухоль |
|---|---|---|---|
| Размер | |||
| Консистенция 1 | |||
| Нежный / безболезненный | |||
| Фиксация |
357 |
Дифференциальный диагноз B-симптомов
Перечисленные здесь дифференциальные диагнозы не являются исчерпывающими.
Лечение
- Ранняя стадия (I и II): комбинация химиотерапии и лучевой терапии
- Продвинутая стадия (III и IV и часто II с объемным заболеванием): комбинированная химиотерапия с лучевой терапией в отдельных случаях
- Обычно рассматриваются три возможных подхода к лечению:
- ABVD
- Стэнфорд V: доксорубицин, винбластин, мехлорэтамин, винкристин, блеомицин, этопозид, преднизон
- BEACOPP: блеомицин, этопозид, адриамицин (доксорубицин), циклофосфамид, онковин (винкристин), прокарбазин, преднизон
- Обычно рассматриваются три возможных подхода к лечению:
- Первичная рефрактерная или рецидивирующая болезнь: испытание альтернативной химиотерапии или рассмотрение возможности высокодозной химиотерапии и трансплантации аутологичных стволовых клеток
Независимо от стадии, лечение обычно начинается с лечебной целью.
Прогноз
- Хороший прогноз
- Прогноз во многом определяется стадией заболевания (т.е. на более низкой стадии прогноз лучше).

- ∼ 10–20% пациентов разовьются вторичные злокачественные новообразования (особенно рак легких; связанные с лучевой терапией и химиотерапией) [9]
- Неблагоприятные факторы для лимфомы Ходжкина (актуальны при выборе схемы лечения)
- Международная прогностическая шкала (IPS): оценка прогноза у пациентов с запущенным заболеванием (за каждый присутствующий фактор пациент получает один балл)
- Факторы IPS
- Категории IPS: На основе рассчитанного IPS пациентов можно разделить на следующие категории:
- Хороший прогноз (IPS 0–1)
- Хороший прогноз (IPS 2–3)
- Плохой прогноз (IPS 4–7)
Лимфома Ходжкина — Диагноз — NHS
Если вы обратитесь к своему терапевту, потому что вас беспокоят симптомы лимфомы Ходжкина, он спросит о вашем здоровье и проведет простой медицинский осмотр.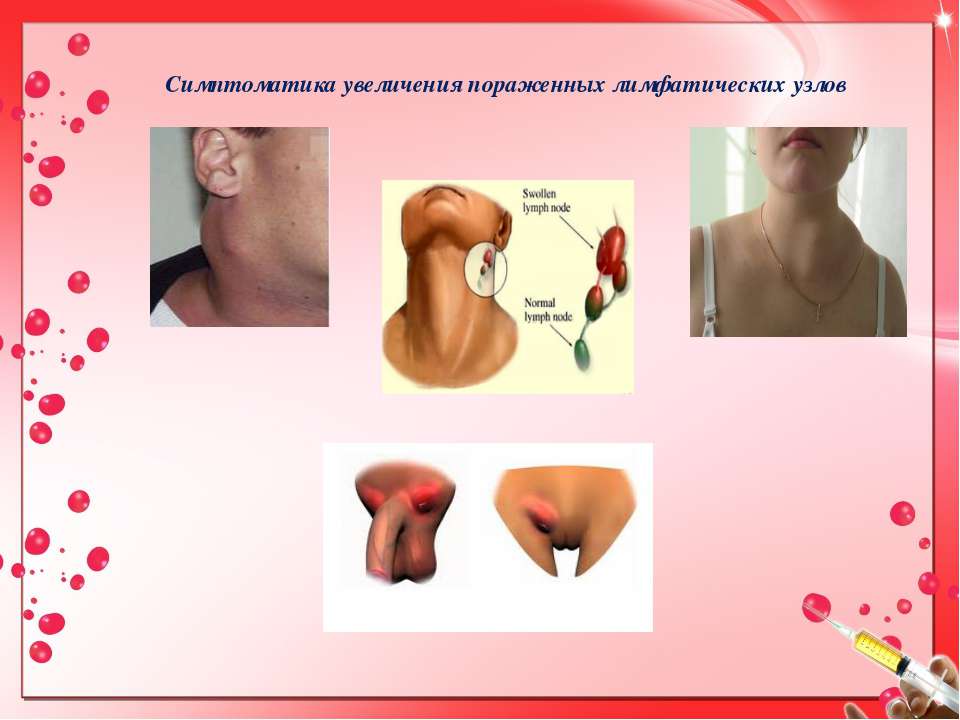
При необходимости ваш терапевт направит вас в больницу для проведения дополнительных анализов.
В 2015 году Национальный институт здравоохранения и повышения квалификации (NICE) опубликовал рекомендации, которые помогают врачам общей практики распознавать признаки и симптомы лимфомы Ходжкина и быстрее направлять людей на нужные тесты.
Чтобы узнать, следует ли направлять вас на дополнительные анализы при подозрении на лимфому Ходжкина, прочтите руководство NICE 2015 по подозрению на рак: признание и направление.
Если вас направят в больницу, обычно проводят биопсию, поскольку это единственный способ подтвердить диагноз лимфомы Ходжкина.
Биопсия
Биопсия включает удаление части или всего пораженного лимфатического узла, который затем исследуется в лаборатории.
Биопсия — это небольшие операции, которые часто можно провести под местной анестезией (при обезболивании пораженной области). В некоторых случаях пораженный лимфатический узел труднодоступен, и может потребоваться общая анестезия (когда вы спите).
В некоторых случаях пораженный лимфатический узел труднодоступен, и может потребоваться общая анестезия (когда вы спите).
Патологоанатом (специалист по изучению пораженных тканей) проверяет образец ткани на наличие раковых клеток.Если они обнаруживают раковые клетки, они также могут точно определить, какой у вас тип лимфомы Ходжкина, что является важным фактором при планировании лечения.
Дальнейшие испытания
Если биопсия подтверждает диагноз лимфомы Ходжкина, потребуется дальнейшее исследование, чтобы проверить, насколько далеко распространилась лимфома. Это позволяет врачу диагностировать стадию вашей лимфомы.
Дополнительные тесты могут включать:
- анализы крови — образцы крови будут браться во время диагностики и лечения для проверки вашего общего состояния здоровья, уровней красных и белых клеток и тромбоцитов в крови, а также того, насколько хорошо работают такие органы, как печень и почки.

- образец костного мозга — может быть проведена еще одна биопсия, чтобы увидеть, распространился ли рак на ваш костный мозг; для этого используется длинная игла для удаления образца костного мозга из таза, и это можно сделать с использованием местного анестетика
- Рентген грудной клетки — с его помощью можно проверить, распространился ли рак на грудную клетку или легкие
- компьютерная томография (КТ) — это сканирование требует серии рентгеновских снимков, которые создают трехмерное изображение внутренней части тела для проверки распространения рака.
- Магнитно-резонансная томография (МРТ) — в этом сканировании используются сильные магнитные поля для создания детального изображения участков вашего тела и проверки распространения рака.
- сканирование позитронно-эмиссионной томографии (ПЭТ) — это сканирование измеряет активность клеток в различных частях тела и может проверить распространение рака и эффективность лечения; обычно его проводят одновременно с компьютерной томографией, чтобы точно показать, как работают ткани различных участков тела
Стадии лимфомы Ходжкина
Когда тестирование будет завершено, можно будет определить стадию лимфомы. «Стадия» означает оценку рака по степени его распространения.
«Стадия» означает оценку рака по степени его распространения.
Основные стадии лимфомы Ходжкина:
- стадия 1 — рак ограничен 1 группой лимфатических узлов, таких как шея или паховые узлы, расположенные выше или ниже диафрагмы (мышечный лист под легкими)
- стадия 2 — поражены 2 или более группы лимфатических узлов, выше или ниже диафрагмы
- 3 стадия — рак распространился на группы лимфатических узлов выше и ниже диафрагмы
- стадия 4 — рак распространился по лимфатической системе и теперь присутствует в органах или костном мозге
Медицинские работники также добавляют буквы «A» или «B» к вашей стадии, чтобы указать, есть ли у вас определенные симптомы.
«А» ставится после вашего этапа, если у вас нет дополнительных симптомов, кроме увеличения лимфатических узлов. «B» ставится после стадии, если у вас есть дополнительные симптомы потери веса, лихорадки или ночного потоотделения.
Прочтите о том, как бороться с раком и о своих эмоциях.
Последняя проверка страницы: 20 сентября 2018 г.
Срок следующей проверки: 20 сентября 2021 г.
Лимфома Ходжкина: основы практики, предпосылки, патофизиология
Swerdlow SH, Campo E, Harris NL, Jaffe ES, Pileri SA, Stein H, Thiele J, Vardiman JW, eds. Классификация опухолей Всемирной организации здравоохранения: патология и генетика опухолей гемопоэтических и лимфоидных тканей . 4-е изд. Лион, Франция: IARC Press; 2008.
Swerdlow SH, Campo E, Pileri SA, Harris NL, Stein H, Siebert R, et al. Пересмотр 2016 г. классификации лимфоидных новообразований Всемирной организации здравоохранения. Кровь . 2016 19 мая. 127 (20): 2375-90. [Медлайн]. [Полный текст].
Хентрих М., Маретта Л. , Чоу К.Ю. и др.Высокоактивная антиретровирусная терапия (ВААРТ) улучшает выживаемость при ВИЧ-ассоциированной болезни Ходжкина: результаты многоцентрового исследования. Энн Онкол . 2006 июн.17 (6): 914-9. [Медлайн]. [Полный текст].
, Чоу К.Ю. и др.Высокоактивная антиретровирусная терапия (ВААРТ) улучшает выживаемость при ВИЧ-ассоциированной болезни Ходжкина: результаты многоцентрового исследования. Энн Онкол . 2006 июн.17 (6): 914-9. [Медлайн]. [Полный текст].
[Руководство] NCCN Руководство по клинической практике в онкологии: лимфома Ходжкина. Национальная всеобъемлющая онкологическая сеть. Доступно на http://www.nccn.org/professionals/physician_gls/pdf/hodgkins.pdf. Версия 2.2020 — 17 апреля 2020 г .; Дата обращения: 5 июня 2020 г.
[Рекомендации] Эйхенауэр Д.А., Алеман БМП, Андре М., Федерико М., Хатчингс М., Иллидж Т. и др.Лимфома Ходжкина: Руководство ESMO по клинической практике для диагностики, лечения и последующего наблюдения. Энн Онкол . 2018 23 мая. 25 Suppl 3: iii70-5. [Медлайн]. [Полный текст].
Cheson BD, Pfistner B, Juweid ME, et al. Пересмотренные критерии ответа на злокачественную лимфому. Дж Клин Онкол . 2007 10 февраля. 25 (5): 579-86. [Медлайн]. [Полный текст].
Пересмотренные критерии ответа на злокачественную лимфому. Дж Клин Онкол . 2007 10 февраля. 25 (5): 579-86. [Медлайн]. [Полный текст].
Schmitz N, Pfistner B, Sextro M и др. Агрессивная традиционная химиотерапия по сравнению с высокодозной химиотерапией с трансплантацией аутологичных гемопоэтических стволовых клеток при рецидиве химиочувствительной болезни Ходжкина: рандомизированное исследование. Ланцет . 2002 15 июня. 359 (9323): 2065-71. [Медлайн].
Томас Р.К., Ре Д., Вольф Дж., Диль В. Часть I: Лимфома Ходжкина — молекулярная биология клеток Ходжкина и Рида-Штернберга. Ланцет Онкол . 2004 5 (1): 11-8. [Медлайн].
Re D, Kuppers R, Diehl V. Молекулярный патогенез лимфомы Ходжкина. Дж Клин Онкол . 2005, 10 сентября, 23 (26): 6379-86. [Медлайн].
Hjalgrim H, Smedby KE, Rostgaard K и др. Инфекционный мононуклеоз, социальная среда в детстве и риск лимфомы Ходжкина. Cancer Res . 2007 г. 1. 67 (5): 2382-8. [Медлайн].
Стаал С.П., Амбиндер Р., Бешорнер В.Е., Хейворд Г.С., Манн Р. Обзор ДНК вируса Эпштейна-Барра в лимфоидной ткани. Частое обнаружение при болезни Ходжкина. Ам Дж. Клин Патол . 1989, январь, 91 (1): 1-5. [Медлайн].
Hjalgrim H, Askling J, Rostgaard K, Hamilton-Dutoit S, Frisch M, Zhang JS, et al. Характеристика лимфомы Ходжкина после инфекционного мононуклеоза. N Engl J Med . 2 октября 2003 г. 349 (14): 1324-32. [Медлайн].
Pallesen G, Hamilton-Dutoit SJ, Rowe M, Young LS. Экспрессия продуктов латентных генов вируса Эпштейна-Барра в опухолевых клетках болезни Ходжкина. Ланцет . 1991, 9 февраля. 337 (8737): 320-2. [Медлайн].
Голдин Л. Р., Пфайфер Р. М., Гридли Г., Гейл М. Х., Ли Х, Меллемкьяер Л. и др. Семейная агрегация лимфомы Ходжкина и родственных опухолей. Рак .2004 г. 1. 100 (9): 1902-8. [Медлайн].
Harty LC, Lin AY, Goldstein AM, Jaffe ES, Carrington M, Tucker MA и др. Гены HLA-DR, HLA-DQ и TAP при семейной болезни Ходжкина. Кровь . 2002 15 января. 99 (2): 690-3. [Медлайн].
99 (2): 690-3. [Медлайн].
Mack TM, Cozen W, Shibata DK, Weiss LM, Nathwani BN, Hernandez AM, et al. Конкордантность болезни Ходжкина у однояйцевых близнецов, предполагающая генетическую предрасположенность к молодой взрослой форме болезни. N Engl J Med . 1995 16 февраля. 332 (7): 413-8. [Медлайн].
Mueller NE, Лимфома Грюффермана С. Ходжкина. Schottenfeld D, Fraumeni JF Jr, ред. Эпидемиология и профилактика рака . Нью-Йорк, Нью-Йорк: издательство Оксфордского университета; 2006. 872-97.
Enciso-Mora V, Broderick P, Ma Y, Jarrett RF, Hjalgrim H, Hemminki K, et al. Полногеномное ассоциативное исследование лимфомы Ходжкина идентифицирует новые локусы восприимчивости в 2p16.1 (REL), 8q24.21 и 10п14 (GATA3). Нат Генет . 2010 декабрь 42 (12): 1126-30. [Медлайн].
Национальный институт рака. Информационные бюллетени SEER stat: лимфома Ходжкина. Доступно на http: //www.seer.cancer.gov / statfacts / html / hodg.html. Дата обращения: 5 июня 2020 г.
Сигель Р.Л., Миллер К.Д., Джемаль А. Статистика рака, 2020. CA Cancer J Clin . 2020 января 70 (1): 7-30. [Медлайн]. [Полный текст].
Sant M, Allemani C, Tereanu C, De Angelis R, Capocaccia R, Visser O и др. Заболеваемость гематологическими злокачественными новообразованиями в Европе по морфологическим подтипам: результаты проекта HAEMACARE. Кровь . 11 ноября 2010 г. 116 (19): 3724-34. [Медлайн].
11 ноября 2010 г. 116 (19): 3724-34. [Медлайн].
Correa P, O’Conor GT. Эпидемиологические закономерности болезни Ходжкина. Инт Дж. Рак . 1971 15 сентября. 8 (2): 192-201. [Медлайн].
Cancer Research UK. Лимфома Ходжкина — статистика заболеваемости в Великобритании. Доступно по адресу http://www.cancerresearchuk.org/cancer-info/cancerstats/types/hodgkinslymphoma/incidence/#O Total. Дата обращения: 5 июня 2020 г.
Лимфома — Ходжкина: Статистика. Cancer.Net. Доступно на https: // www.Cancer.net/cancer-types/lymphoma-hodgkin/statistics. Январь 2020; Дата обращения: 5 июня 2020 г.
Das P, Ng A, Constine LS, Hodgson DC, Mendenhall NP, Morris DE, et al. Критерии соответствия ACR при лимфоме Ходжкина: благоприятный прогноз I и II стадии. Дж. Ам Колл Радиол . 2008 5 (10): 1054-66. [Медлайн]. [Полный текст].
Ам Колл Радиол . 2008 5 (10): 1054-66. [Медлайн]. [Полный текст].
Das P, Ng A, Constine LS, Advani R, Flowers C., Friedberg J, et al. Критерии соответствия ACR (R) для лимфомы Ходжкина — неблагоприятная клиническая стадия I и II. Дж. Ам Колл Радиол . 2011 Май. 8 (5): 302-8. [Медлайн]. [Полный текст].
Hasenclever D, Diehl V. Прогностическая оценка прогрессирующей болезни Ходжкина. Международный проект «Прогностические факторы» по продвинутой болезни Ходжкина. N Engl J Med . 1998 19 ноября. 339 (21): 1506-14. [Медлайн]. [Полный текст].
Steidl C, Lee T., Shah SP, Farinha P, Han G, Nayar T. и др. Макрофаги, связанные с опухолью, и выживаемость при классической лимфоме Ходжкина. N Engl J Med . 2010 г. 11 марта. 362 (10): 875-85. [Медлайн]. [Полный текст].
Swerdlow SH, Campo E, Harris NL, et al, eds. Классификация опухолей гемопоэтических и лимфоидных тканей ВОЗ .4-е изд. Лион, Франция: IARC Press; 2008.
Менард Ф., Бессон С., Ринс П. и др. Гемофагоцитарный синдром, связанный с лимфомой Ходжкина: заболевание, сильно коррелированное с вирусом Эпштейна-Барра. Клин Инфекция Дис . 2008 15 августа. 47 (4): 531-4. [Медлайн].
Juweid ME, Stroobants S, Hoekstra OS, Mottaghy FM, Dietlein M, Guermazi A, et al. Использование позитронно-эмиссионной томографии для оценки реакции лимфомы: консенсус Подкомитета по визуализации Международного проекта гармонизации лимфомы. Дж Клин Онкол . 2007 10 февраля. 25 (5): 571-8. [Медлайн].
Дж Клин Онкол . 2007 10 февраля. 25 (5): 571-8. [Медлайн].
Juweid ME, Stroobants S, Hoekstra OS и др. Использование позитронно-эмиссионной томографии для оценки реакции лимфомы: консенсус Подкомитета по визуализации Международного проекта гармонизации лимфомы. Дж Клин Онкол . 2007 10 февраля. 25 (5): 571-8. [Медлайн]. [Полный текст].
Vassilakopoulos TP, Angelopoulou MK, Constantinou N, Karmiris T., Repoussis P, Roussou P, et al.Разработка и проверка правила клинического прогноза поражения костного мозга у пациентов с лимфомой Ходжкина. Кровь . 2005 г. 1. 105 (5): 1875-80. [Медлайн].
Cosset JM, Henry-Amar M, Meerwaldt JH, Carde P, Noordijk EM, Thomas J, et al. Испытания EORTC для болезни Ходжкина ограниченной стадии. Кооперативная группа EORTC Lymphoma Cooperative Group. евро J Рак . 1992. 28A (11): 1847-50. [Медлайн].
1992. 28A (11): 1847-50. [Медлайн].
Engert A, Plütschow A, Eich HT, Lohri A, Dörken B, Borchmann P и др.Снижение интенсивности лечения у пациентов с лимфомой Ходжкина на ранней стадии. N Engl J Med . 12 августа 2010 г. 363 (7): 640-52. [Медлайн].
ДеВита В.Т. Младший. Избирательный анамнез терапии болезни Ходжкина. Br J Haematol . 2003 сентябрь 122 (5): 718-27. [Медлайн].
Коннорс Дж. Современные методы лечения: лимфома Ходжкина. Дж Клин Онкол . 2005 10 сентября. 23 (26): 6400-8. [Медлайн].
Адвани Р., Маеда Л., Лавори П. и др.Влияние позитивной позитронно-эмиссионной томографии на прогнозирование отсутствия прогрессирования после химиотерапии в Стэнфорде V при болезни Ходжкина. Дж Клин Онкол . 2007, 1. 25 (25): 3902-7. [Медлайн]. [Полный текст].
25 (25): 3902-7. [Медлайн]. [Полный текст].
Галламини А., Хатчингс М., Ригаччи Л. и др. Ранняя промежуточная 2- [18F] фтор-2-дезокси-D-глюкоза позитронно-эмиссионная томография прогностически превосходит международную прогностическую шкалу лимфомы Ходжкина на поздней стадии: отчет совместного итальянско-датского исследования. Дж Клин Онкол . 2007 20 августа. 25 (24): 3746-52. [Медлайн]. [Полный текст].
Джонсон П., Федерико М., Кирквуд А., Фосса А., Беркан Л., Карелла А. и др. Адаптированное лечение с помощью промежуточного ПЭТ-КТ при прогрессирующей лимфоме Ходжкина. N Engl J Med . 2016, 23 июня. 374 (25): 2419-29. [Медлайн]. [Полный текст].
Левин Дж. М., Вайнер М, Келли К. М.. Регулярное использование ПЭТ-сканирований после завершения лечения детской болезни Ходжкина приводит к высокому уровню ложноположительных результатов. J Педиатр Hematol Oncol . 2006 28 ноября (11): 711-4. [Медлайн].
J Педиатр Hematol Oncol . 2006 28 ноября (11): 711-4. [Медлайн].
Wilder RB, Ng A, Constine LS, et al, для Экспертной группы по радиационной онкологии — лимфома Ходжкина. Критерии соответствия ACR (R) Лимфома Ходжкина — стадии III и IV [онлайн-публикация] . Рестон, штат Вирджиния: Американский колледж радиологии; 2010. [Полный текст].
Koeck J, Abo-Madyan Y, Lohr F, Stieler F, Kriz J, Mueller RP и др. Лучевая терапия ранней средостенной лимфомы Ходжкина по данным Немецкой исследовательской группы Ходжкина (GHSG): роль лучевой терапии с модуляцией интенсивности и лучевой терапии пораженных узлов. Int J Radiat Oncol Biol Phys . 2012 May 1. 83 (1): 268-76. [Медлайн].
Specht L, Yahalom J, Illidge T, Berthelsen AK, Constine LS, Eich HT, et al. Современная лучевая терапия лимфомы Ходжкина: полевые и дозовые рекомендации Международной группы радиационной онкологии лимфомы (ILROG). Int J Radiat Oncol Biol Phys . 2014 15 июля. 89 (4): 854-62. [Медлайн].
Int J Radiat Oncol Biol Phys . 2014 15 июля. 89 (4): 854-62. [Медлайн].
Noordijk EM, Carde P, Dupouy N, Hagenbeek A, Krol AD, Kluin-Nelemans JC, et al.Комбинированная терапия лимфомы Ходжкина I или II клинической стадии: долгосрочные результаты рандомизированных контролируемых исследований Европейской организации по исследованию и лечению рака. H7. Дж Клин Онкол . 1. 24 июля 2006 г. (19): 3128-35. [Медлайн].
Энгерт А., Шиллер П., Йостинг А., Херрманн Р. и др. Лучевая терапия с вовлеченным полем одинаково эффективна и менее токсична по сравнению с лучевой терапией с расширенным полем после четырех курсов химиотерапии у пациентов с ранней стадией неблагоприятной лимфомы Ходжкина… J Clin Oncol . 1 октября 2003 г. 21 (19): 3601-8. [Медлайн].
Аракелян Н., Джейс Дж. П., Делвейл В. , Бриер Дж., Молес-Моро М. П., Сенекал Д. и др. Сниженные по сравнению с полными дозами облучения после 3 циклов комбинированного приема доксорубицина, блеомицина, винбластина и дакарбазина на ранних стадиях лимфомы Ходжкина: результаты рандомизированного исследования. Рак . 2010 сен 1. 116 (17): 4054-62. [Медлайн].
, Бриер Дж., Молес-Моро М. П., Сенекал Д. и др. Сниженные по сравнению с полными дозами облучения после 3 циклов комбинированного приема доксорубицина, блеомицина, винбластина и дакарбазина на ранних стадиях лимфомы Ходжкина: результаты рандомизированного исследования. Рак . 2010 сен 1. 116 (17): 4054-62. [Медлайн].
Канеллос Г.П., Андерсон Дж. Р., Проперт К. Дж. И др.Химиотерапия прогрессирующей болезни Ходжкина с использованием MOPP, ABVD или MOPP, чередующихся с ABVD. N Engl J Med . 1992, 19 ноября. 327 (21): 1478-84. [Медлайн].
Connors JM, et al; Эшелон-1 исследовательская группа. Брентуксимаб Ведотин с химиотерапией при лимфоме Ходжкина стадии III или IV. N Engl J Med . 2018 25 января. 378 (4): 331-344. [Медлайн]. [Полный текст].
Хорнинг С.Дж., Хоппе Р.Т., Бреслин С. и др. Stanford V и лучевая терапия для локально распространенной и распространенной болезни Ходжкина: зрелые результаты проспективного клинического исследования. Дж Клин Онкол . 2002 1 февраля. 20 (3): 630-7. [Медлайн]. [Полный текст].
Stanford V и лучевая терапия для локально распространенной и распространенной болезни Ходжкина: зрелые результаты проспективного клинического исследования. Дж Клин Онкол . 2002 1 февраля. 20 (3): 630-7. [Медлайн]. [Полный текст].
Адвани Р.Х., Хонг Ф., Фишер Р.И., Бартлетт Н.Л., Робинсон К.С., Гаскойн Р.Д. и др. Рандомизированное исследование фазы III, сравнивающее лучевую терапию ABVD Plus со схемой Стэнфордского V у пациентов с локально распространенной и объемной лимфомой Ходжкина средостения I или II стадии: анализ субпопуляции североамериканского межгруппового исследования E2496. Дж Клин Онкол . 2015, 10 июня. 33 (17): 1936-42. [Медлайн].
Diehl V, Franklin J, Pfreundschuh M, et al.Стандартная и повышенная химиотерапия BEACOPP по сравнению с COPP-ABVD при запущенной болезни Ходжкина. N Engl J Med . 12 июня 2003 г. 348 (24): 2386-95. [Медлайн]. [Полный текст].
[Медлайн]. [Полный текст].
Вивиани С., Зинзани П.Л., Рамбальди А. и др. ABVD по сравнению с BEACOPP при лимфоме Ходжкина, когда планируется применение высоких доз. N Engl J Med . 2011 г., 21 июля. 365 (3): 203-12. [Медлайн].
Bauer K, Skoetz N, Monsef I, Engert A, Brillant C. Сравнение химиотерапии, включающей усиление BEACOPP, с химиотерапией, включая ABVD, для пациентов с ранней неблагоприятной или продвинутой стадией лимфомы Ходжкина. Кокрановская база данных Syst Rev . 2011 10 августа. CD007941. [Медлайн].
Mounier N, Brice P, Bologna S, Briere J, Gaillard I., Heczko M, et al. ABVD (8 циклов) по сравнению с BEACOPP (4 усиленных цикла ≥ 4 исходных): окончательные результаты при лимфоме Ходжкина низкого риска стадии III-IV (IPS 0-2) рандомизированного исследования LYSA h44. Энн Онкол . 2014 25 августа (8): 1622-8. [Медлайн].
2014 25 августа (8): 1622-8. [Медлайн].
Carde P, Karrasch M, Fortpied C, Brice P, Khaled H, Casasnovas O и др.Восемь циклов ABVD по сравнению с четырьмя циклами BEACOPPescalated плюс четыре цикла BEACOPPbaseline на стадиях с III по IV, международная прогностическая оценка ≥ 3, лимфома Ходжкина с высоким риском: первые результаты межгруппового исследования фазы III EORTC 20012. Дж Клин Онкол . 2016 25 апреля. [Medline].
Эдвардс-Беннет С.М., Джекс Л.М., Московиц С.Х. и др. Стэнфордская программа V для локально обширной и прогрессирующей лимфомы Ходжкина: опыт Мемориального онкологического центра Слоуна-Кеттеринга. Энн Онкол . 2010 21 марта (3): 574-81. [Медлайн].
Gayoso J, Balsalobre P, Pascual MJ, Castilla-Llorente C, López-Corral L, Kwon M, et al. Схемы кондиционирования с пониженной интенсивностью на основе бусульфана для гаплоидентичной трансплантации при рецидивирующей / рефрактерной лимфоме Ходжкина: многоцентровый опыт Испании. Пересадка костного мозга . 2016 9 мая. [Medline].
Пересадка костного мозга . 2016 9 мая. [Medline].
Moskowitz CH, Nademanee A, Masszi T., Agura E, Holowiecki J, Abidi MH, et al.Брентуксимаб ведотин в качестве консолидирующей терапии после трансплантации аутологичных стволовых клеток у пациентов с лимфомой Ходжкина с риском рецидива или прогрессирования (AETHERA): рандомизированное двойное слепое плацебо-контролируемое исследование фазы 3. Ланцет . 2015 9 мая. 385 (9980): 1853-62. [Медлайн].
Ferme C, Eghbali H, Meerwaldt JH и др. Химиотерапия плюс лучевая терапия при ранней стадии болезни Ходжкина. N Engl J Med . 2007 8 ноября. 357 (19): 1916-27.[Медлайн]. [Полный текст].
Энгерт А., Франклин Дж., Эйх Х.Т. и др. Два цикла доксорубицина, блеомицина, винбластина и дакарбазина плюс лучевая терапия расширенного поля превосходит только лучевую терапию при ранней благоприятной лимфоме Ходжкина: окончательные результаты исследования GHSG HD7. Дж Клин Онкол . 2007 10 августа. 25 (23): 3495-502. [Медлайн]. [Полный текст].
Дж Клин Онкол . 2007 10 августа. 25 (23): 3495-502. [Медлайн]. [Полный текст].
Herbst C, Rehan FA, Brillant C, Bohlius J, Skoetz N, Schulz H, et al. Комбинированное лечение улучшает контроль опухоли и общую выживаемость у пациентов с лимфомой Ходжкина на ранней стадии: систематический обзор. Haematologica . 2010 Март 95 (3): 494-500. [Медлайн]. [Полный текст].
Meyer RM, Gospodarowicz MK, Connors JM, Pearcey RG, Wells WA, Winter JN, et al. Только ABVD по сравнению с лучевой терапией при лимфоме Ходжкина ограниченной стадии. N Engl J Med . 2012 г. 2 февраля. 366 (5): 399-408. [Медлайн].
Hutchings M, Mikhaeel NG, Fields PA, Nunan T, Timothy AR. Прогностическая ценность промежуточной ФДГ-ПЭТ после двух или трех курсов химиотерапии при лимфоме Ходжкина. Энн Онкол . 2005 июл. 16 (7): 1160-8. [Медлайн].
16 (7): 1160-8. [Медлайн].
Hutchings M, Loft A, Hansen M, Pedersen LM, Buhl T, Jurlander J и др. ФДГ-ПЭТ после двух курсов химиотерапии прогнозирует неэффективность лечения и выживаемость без прогрессирования при лимфоме Ходжкина. Кровь . 2006 1 января. 107 (1): 52-9. [Медлайн].
Advani RH, Хорнинг SJ. Лечение ранней стадии болезни Ходжкина. Семин Гематол . 1999 июл.36 (3): 270-81. [Медлайн].
фон Тресков Б., Плутшоу А., Фукс М., Климм Б., Маркова Дж., Лори А. и др. Повышение дозы при ранней неблагоприятной лимфоме Ходжкина: окончательный анализ исследования German Hodgkin Study Group HD14. Дж Клин Онкол . 2012 20 марта. 30 (9): 907-13. [Медлайн].
Armitage JO. Лимфома Ходжкина на ранней стадии. N Engl J Med . 12 августа 2010 г. 363 (7): 653-62. [Медлайн].
12 августа 2010 г. 363 (7): 653-62. [Медлайн].
Дагган Д. Б., Петрони Г. Р., Джонсон Дж. Л., Глик Дж. Х., Фишер Р. И., Коннорс Дж. М. и др.Рандомизированное сравнение ABVD и гибрида MOPP / ABV для лечения запущенной болезни Ходжкина: отчет межгруппового исследования. Дж Клин Онкол . 2003 15 февраля. 21 (4): 607-14. [Медлайн].
Johnson PW, Radford JA, Cullen MH, Sydes MR, Walewski J, Jack AS и др. Сравнение ABVD и чередующихся или гибридных схем с несколькими лекарствами для лечения прогрессирующей лимфомы Ходжкина: результаты исследования LY09 группы лимфомы Соединенного Королевства (ISRCTN97144519). Дж Клин Онкол .2005 20 декабря. 23 (36): 9208-18. [Медлайн].
Boleti E, Mead GM. ABVD при лимфоме Ходжкина: полная химиотерапия без снижения дозы или факторов роста. Энн Онкол . 2007 февраля 18 (2): 376-80. [Медлайн].
2007 февраля 18 (2): 376-80. [Медлайн].
Веджвуд А., Юнес А. Профилактическое использование филграстима с режимами химиотерапии ABVD и BEACOPP для лимфомы Ходжкина. Клин Лимфома Миелома . 2007 декабря 8 Приложение 2: S63-6. [Медлайн].
Saxman SB, Николс CR, Einhorn LH.Легочная токсичность у пациентов с поздней стадией опухолей половых клеток, получающих блеомицин с фактором, стимулирующим колонии гранулоцитов, и без него. Сундук . 1997 г., 111 (3): 657-60. [Медлайн].
Федерико М., Луминари С., Яннитто Э., Полимено Г., Марчеселли Л., Монтанини А. и др. ABVD в сравнении с BEACOPP в сравнении с CEC для начального лечения пациентов с прогрессирующей лимфомой Ходжкина: результаты исследования HD2000 Gruppo Italiano per lo Studio dei Linfomi. Дж Клин Онкол . 2009 10 февраля. 27 (5): 805-11. [Медлайн].
[Медлайн].
Энгерт А., Хаверкамп Х, Кобе С., Маркова Дж., Реннер С., Хо А. и др. Химиотерапия пониженной интенсивности и лучевая терапия под контролем ПЭТ у пациентов с продвинутой стадией лимфомы Ходжкина (исследование HD15): рандомизированное открытое исследование не меньшей эффективности, фаза 3. Ланцет . 2012 г. 12 мая. 379 (9828): 1791-9. [Медлайн].
Хорнинг С.Дж., Хоппе Р.Т., Адвани Р. и др. Эффективность и отдаленные эффекты химиотерапии и лучевой терапии Stanford V при нелеченой болезни Ходжкина: зрелые данные для пациентов на ранней и поздней стадиях [аннотация 308]. Кровь . 2004. 104: 92a.
Гордон Л.И., Хонг Ф., Фишер Р.И. и др. Рандомизированное исследование III фазы ABVD по сравнению со Стэнфордским V / — лучевой терапией при локально обширной и продвинутой стадии лимфомы Ходжкина . .. Кровь (Тезисы ежегодного собрания ASH) . 2010. 116 (21): 185; (E2496) [аннотация 415].
.. Кровь (Тезисы ежегодного собрания ASH) . 2010. 116 (21): 185; (E2496) [аннотация 415].
Хоппе РТ. Болезнь Ходжкина — роль лучевой терапии при запущенном заболевании. Энн Онкол . 1996. 7 Suppl 4: 99-103.[Медлайн].
Loeffler M, Brosteanu O, Hasenclever D, Sextro M, Assouline D, Bartolucci AA, et al. Мета-анализ испытаний химиотерапии и комбинированного лечения болезни Ходжкина. Международная база данных по исследованию болезни Ходжкина. Дж Клин Онкол . 1998 марта 16 (3): 818-29. [Медлайн].
Aleman BM, Raemaekers JM, Tomisic R, Baaijens MH, Bortolus R, Lybeert ML, et al. Лучевая терапия с участием поля для пациентов с частичной ремиссией после химиотерапии прогрессирующей лимфомы Ходжкина. Int J Radiat Oncol Biol Phys . 2007 г. 1. 67 (1): 19-30. [Медлайн].
Портлок CS. Болезнь Ходжкина с преобладанием узловых лимфоцитов. Cancer Treat Res . 2006. 131: 353-62. [Медлайн].
Schulz H, Rehwald U, Morschhauser F, et al. Ритуксимаб при рецидивной лимфоме Ходжкина с преобладанием лимфоцитов: долгосрочные результаты исследования фазы 2, проведенного Немецкой исследовательской группой по лимфоме Ходжкина (GHSG). Кровь . 2008 г., 1. 111 (1): 109-11. [Медлайн]. [Полный текст].
Eichenauer DA, Fuchs M, Pluetschow A, et al. Фаза 2 исследования ритуксимаба при впервые выявленной лимфоме Ходжкина с преобладанием узловых лимфоцитов стадии IA: отчет Немецкой исследовательской группы Hodgkin. Кровь . 2011 20 октября. 118 (16): 4363-5. [Медлайн].
Фаза 2 исследования ритуксимаба при впервые выявленной лимфоме Ходжкина с преобладанием узловых лимфоцитов стадии IA: отчет Немецкой исследовательской группы Hodgkin. Кровь . 2011 20 октября. 118 (16): 4363-5. [Медлайн].
Savage KJ, Skinnider B, Al-Mansour M, Sehn LH, Gascoyne RD, Connors JM. Лечение лимфомы Ходжкина на ограниченной стадии с преобладанием узловых лимфоцитов аналогично классической лимфоме Ходжкина с ABVD может улучшить исход. Кровь . 2011 27 октября, 118 (17): 4585-90. [Медлайн].
Лавуа Дж. К., Коннорс Дж. М., Филлипс Г. Л. и др. Высокодозная химиотерапия и трансплантация аутологичных стволовых клеток при первичной рефрактерной или рецидивирующей лимфоме Ходжкина: долгосрочный результат у первых 100 пациентов, пролеченных в Ванкувере. Кровь . 2005 15 августа. 106 (4): 1473-8. [Медлайн]. [Полный текст].
Przepiorka D, van Besien K, Khouri I, et al. Кармустин, этопозид, цитарабин и мелфалан как препаративная схема аллогенной трансплантации при злокачественной лимфоме высокого риска. Энн Онкол . 1999 Май. 10 (5): 527-32. [Медлайн]. [Полный текст].
Андерлини П., Салиба Р., Ачолону С. и др. Флударабин-мелфалан как препаративный режим для кондиционирующей аллогенной трансплантации стволовых клеток пониженной интенсивности при рецидивирующей и рефрактерной лимфоме Ходжкина: обновленный опыт онкологического центра им. М.Д. Андерсона. Haematologica . 2008 Февраль 93 (2): 257-64. [Медлайн]. [Полный текст].
Юнес А., Гопал А. К., Смит С. Е., Анселл С. М., Розенблатт Д. Д., Сэвидж К. Дж. И др. Результаты основного исследования фазы II брентуксимаб ведотина у пациентов с рецидивирующей или рефрактерной лимфомой Ходжкина. Дж Клин Онкол . 2012 20 июня. 30 (18): 2183-9. [Медлайн]. [Полный текст].
Анселл С.М., Лесохин А.М., Боррелло И., Халвани А., Скотт Е.С., Гутьеррес М. и др.Блокада PD-1 ниволумабом при рецидивирующей или рефрактерной лимфоме Ходжкина. N Engl J Med . 2015 22 января. 372 (4): 311-9. [Медлайн]. [Полный текст].
Ansell S, et al. Ниволумаб у пациентов (пациенты) с рецидивирующей или рефрактерной классической лимфомой Ходжкина (R / R cHL): клинические результаты расширенного наблюдения за исследованием фазы 1 (CA209-039). Кровь . 2015. 126 (23): [Полный текст].
Кровь . 2015. 126 (23): [Полный текст].
Чен Р., Зинзани П.Л., Фанале М.А., Арман П., Джонсон Н.А., Брайс П. и др.Исследование фазы II эффективности и безопасности пембролизумаба при рецидивирующей / рефрактерной классической лимфоме Ходжкина. Дж Клин Онкол . 2017 г. 1. 35 (19): 2125-2132. [Медлайн]. [Полный текст].
Bowser AD. Пембролизумаб пролонгированный ВБП по сравнению с брентуксимабом ведотином при R / R лимфоме Ходжкина. Медицинские новости Medscape. Доступно на https://www.medscape.com/viewarticle/931483. 1 июня 2020 г .; Дата обращения: 5 июня 2020 г.
Алеман Б.М., ван ден Белт-Дусебаут А.В., Де Брюин М.Л. и др.Поздняя кардиотоксичность после лечения лимфомы Ходжкина. Кровь . 1 марта 2007 г. 109 (5): 1878-86. [Медлайн]. [Полный текст].
Heidenreich PA, Schnittger I, Strauss HW, et al. Скрининг на ишемическую болезнь сердца после облучения средостения на болезнь Ходжкина. Дж Клин Онкол . 2007 г., 1. 25 (1): 43-9. [Медлайн]. [Полный текст].
Milano MT, Li H, Constine LS, Travis LB. Выживаемость после второго первичного рака легких: популяционное исследование 187 пациентов с лимфомой Ходжкина. Рак . 2011 15 декабря. 117 (24): 5538-47. [Медлайн].
Swerdlow AJ, Хиггинс CD, Смит П. и др. Второй риск рака после химиотерапии лимфомы Ходжкина: совместное британское когортное исследование. Дж Клин Онкол .2011 г., 1 ноября. 29 (31): 4096-104. [Медлайн].
Дж Клин Онкол .2011 г., 1 ноября. 29 (31): 4096-104. [Медлайн].
Барбаро П.М., Джонстон К., Далла-Поцца Л., Кон Р.Дж., Ван Я.А., Маршалл Г.М. и др. Снижение частоты повторных солидных опухолей у лиц, переживших лимфому Ходжкина в детстве, лечившихся без лучевой терапии. Энн Онкол . 2011 22 декабря (12): 2569-74. [Медлайн].
Берингер К., Брейер К., Рейнеке Т. и др. Вторичная аменорея после лимфомы Ходжкина зависит от возраста на момент лечения, стадии заболевания, режима химиотерапии и использования оральных контрацептивов во время терапии: отчет Немецкой группы исследования лимфомы Ходжкина. Дж Клин Онкол . 2005 20 октября. 23 (30): 7555-64. [Медлайн].
Sieniawski M, Reineke T, Josting A, et al. Оценка мужской фертильности у пациентов с лимфомой Ходжкина, проходящих лечение в клинических испытаниях Немецкой исследовательской группы Ходжкина (GHSG).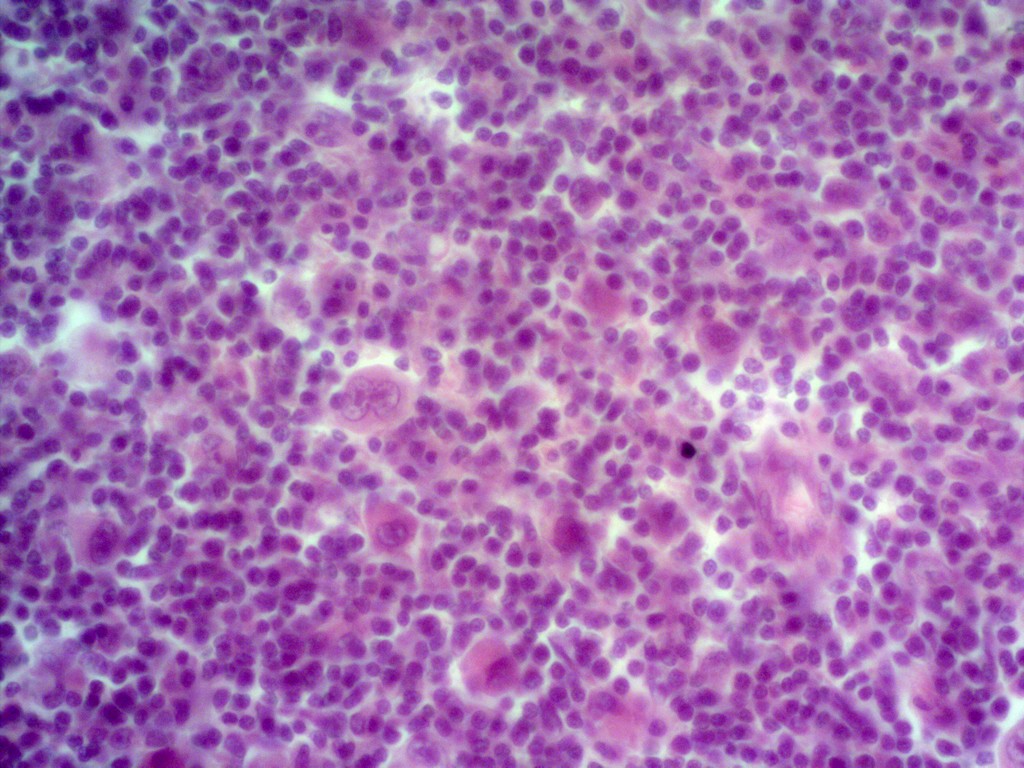 Энн Онкол . 2008 19 октября (10): 1795-801. [Медлайн].
Энн Онкол . 2008 19 октября (10): 1795-801. [Медлайн].
Kornblith AB, Herndon JE 2nd, Zuckerman E, et al. Сравнение психосоциальной адаптации продвинутой стадии болезни Ходжкина и выживших после острой лейкемии.Рак и лейкемия Группа B. Ann Oncol . 1998 марта, 9 (3): 297-306. [Медлайн].
Loge JH, Abrahamsen AF, Ekeberg, Kaasa S. Усталость и психические расстройства среди выживших после болезни Ходжкина. J Устранение болевых симптомов . 2000 февраля 19 (2): 91-9. [Медлайн].
Нг А., Константин Л.С., Адвани Р., Дас П., Флауэрс С., Фридберг Дж. И др. Критерии соответствия ACR: наблюдение лимфомы Ходжкина. Curr Probl Cancer .2010 май-июнь. 34 (3): 211-27. [Медлайн]. [Полный текст].
Андре М., Босли А. BEACOPP увеличил по сравнению с ABVD при прогрессирующей лимфоме Ходжкина. Ланцет Онкол . 2013 12 августа [Medline].
Ланцет Онкол . 2013 12 августа [Medline].
Moskowitz AJ, Schöder H, Yahalom J, McCall SJ, Fox SY и др. Адаптированная к ПЭТ последовательная терапия спасения с применением брентуксимаб ведотина с последующим усилением ифосамида, карбоплатина и этопозида для пациентов с рецидивирующей и рефрактерной лимфомой Ходжкина: нерандомизированное открытое одноцентровое исследование фазы 2. Ланцет Онкол . 2015 16 марта (3): 284-92. [Медлайн].
Гарсия-Санс Р., Суреда А., Алонсо-Альварес С., Гонсалес А. П., Родригес А. и др. Оценка схемы лечения брентуксимабом ведотином плюс ESHAP (BRESHAP) у пациентов с рефрактерной или рецидивирующей лимфомой Ходжкина: предварительные результаты исследования фазы I-II в Испанской группе лимфомы и трансплантации костного мозга (GELTAMO). Кровь . 2015. [Полный текст].
LaCasce AS, Bociek RG, Sawas A, Caimi P, Agura E, Matous J, et al. Брентуксимаб ведотин плюс бендамустин: высокоактивный режим первой помощи при рецидивирующей или рефрактерной лимфоме Ходжкина. Кровь . 2018 5 июля.132 (1): 40-48. [Медлайн]. [Полный текст].
Эррера А.Ф., Московиц А.Дж., Бартлетт Н.Л., Восе Дж.М., Рамчандрен Р., Фельдман Т.А. и др. Промежуточные результаты применения брентуксимаб ведотина в комбинации с ниволумабом у пациентов с рецидивирующей или рефрактерной лимфомой Ходжкина. Кровь . 2018 15 марта. 131 (11): 1183-1194. [Медлайн]. [Полный текст].
131 (11): 1183-1194. [Медлайн]. [Полный текст].
Рамчандрен Р., Фанале М., Руэда А. и др. Ниволумаб при недавно диагностированной поздней стадии классической лимфомы Ходжкина (cHL): результаты исследования фазы 2 Checkmate 205. Кровь . 2017. 130 (Приложение 1): 651. [Полный текст].
Wang CM, Wu ZQ, Wang Y, Guo YL, Dai HR, Wang XH и др. Аутологичные Т-клетки, экспрессирующие рецепторы химерного антигена CD30 для рецидивирующей или рефрактерной лимфомы Ходжкина: открытое испытание фазы I. Clin Cancer Res . 2017 г. 1. 23 (5): 1156-1166. [Медлайн]. [Полный текст].
Листер Т.А., Кроутер Д., Сатклифф С.Б., Глатштейн Э., Канеллос Г.П., Янг Р.К. и др. Отчет комитета, созванного для обсуждения оценки и определения стадий пациентов с болезнью Ходжкина: заседание Котсуолдса. Дж Клин Онкол . 1989 г., 7 (11): 1630-6. [Медлайн].
1989 г., 7 (11): 1630-6. [Медлайн].
[Рекомендации] Cheson BD, Fisher RI, Barrington SF, et al. Рекомендации по первоначальной оценке, стадированию и оценке ответа на лимфому Ходжкина и неходжкинскую лимфому: классификация Лугано. Дж Клин Онкол . 2014 20 сентября. 32 (27): 3059-68. [Медлайн]. [Полный текст].
Knipe H, Pfleger R, et al. Пятибалльная шкала Довиля. Радиопедия. Доступно на https: // radiopaedia.org / articles / deauville — пятибалльная шкала. Дата обращения: 3 августа 2020 г.
[Рекомендации] Hoppe RT, Advani RH, Ai WZ, et al. Лимфома Ходжкина, Версия 2.2020, Руководство NCCN по клинической практике в онкологии. J Natl Compr Canc Netw . 2020 июня 18 (6): 755-781. [Медлайн]. [Полный текст].
Федерико М., Беллей М. , Брис П., Бругиателли М., Наглер А., Гиссельбрехт С. и др. Терапия высокими дозами и трансплантация аутологичных стволовых клеток по сравнению с традиционной терапией для пациентов с прогрессирующей лимфомой Ходжкина, отвечающих на терапию первой линии. Дж Клин Онкол . 15 июня 2003 г., 21 (12): 2320-5. [Медлайн].
, Брис П., Бругиателли М., Наглер А., Гиссельбрехт С. и др. Терапия высокими дозами и трансплантация аутологичных стволовых клеток по сравнению с традиционной терапией для пациентов с прогрессирующей лимфомой Ходжкина, отвечающих на терапию первой линии. Дж Клин Онкол . 15 июня 2003 г., 21 (12): 2320-5. [Медлайн].
Connors JM, et al; Эшелон-1 исследовательская группа. Брентуксимаб Ведотин с химиотерапией при лимфоме Ходжкина стадии III или IV. N Engl J Med . 2018 25 января. 378 (4): 331-344. [Медлайн]. [Полный текст].
Canioni D, Deau-Fischer B, Taupin P, et al. Прогностическое значение новых иммуногистохимических маркеров при рефрактерной классической лимфоме Ходжкина: исследование 59 случаев. PLoS Один . 2009 22 июля, 4 (7): e6341. [Медлайн]. [Полный текст].
Chang ET, Canchola AJ, Cockburn M и др. Ультрафиолетовое излучение взрослого населения, чувствительность к солнцу, диетический витамин D и риск лимфоидных злокачественных новообразований в исследовании учителей Калифорнии. Кровь . 2011 г. 11 августа. 118 (6): 1591-9. [Медлайн]. [Полный текст].
Ультрафиолетовое излучение взрослого населения, чувствительность к солнцу, диетический витамин D и риск лимфоидных злокачественных новообразований в исследовании учителей Калифорнии. Кровь . 2011 г. 11 августа. 118 (6): 1591-9. [Медлайн]. [Полный текст].
Eich HT, Diehl V, Gorgen H и др. Интенсивная химиотерапия и лучевая терапия с пониженной дозой у пациентов с ранней неблагоприятной лимфомой Ходжкина: окончательный анализ исследования German Hodgkin Study Group HD11. Дж Клин Онкол . 2010 сен 20. 28 (27): 4199-206. [Медлайн].
Симптомы лимфогранулематоза
Содержание
Лимфогранулематоз — это патологическое гранулематозно-неопластическое поражение лимфатической системы, также называемое лимфомой Ходжкина. Лимфогранулематоз был впервые описан в 1832 году врачом Томасом Ходжкином, который объяснил несколько моментов в течении болезни. Вначале обычно увеличиваются лимфатические узлы и селезенка, затем появляется лихорадка и кахексия, которые впоследствии приводят пациентов к летальному исходу.
 А в 1875 году Кутарев провел первые гистологические исследования лимфатического узла, который был удален еще при жизни больного.
А в 1875 году Кутарев провел первые гистологические исследования лимфатического узла, который был удален еще при жизни больного.
В 1890 году русский ученый Березовский описал гистологическую картину болезни Ходжкина. Они определили патогномоничные гигантские клетки, характерные для этого заболевания. В 1897–1898 годах уже венскими патологами была описана полиморфно-клеточная гранулема с гигантскими многоядерными клетками, которые впоследствии стали известны как клетки Березовского-Рида-Штернберга.
Необходимость изучения болезни Ходжкина объясняется поражением больных с раннего возраста (чаще всего от 15 до 40 лет). Также для этого заболевания характерно волнообразное течение. Первый ток приходится на двадцатилетний возраст, а второй — на 60 лет.
Лимфогранулематоз занимает десятое место среди онкологических патологий, при котором наибольший процент поражений встречается у мужчин, чем у женщин.
Причины лимфогранулематоза
До недавнего времени лимфогранулематоз считался заболеванием инфекционного происхождения. Считалось, что его возбудителем может быть туберкулезная палочка. Реже эту роль назначают стрептококку, кишечной палочке, бледной спирохете и дифтерийной палочке. Были также предположения о вирусной этиологии болезни Ходжкина, но это также не подтвердилось.
Считалось, что его возбудителем может быть туберкулезная палочка. Реже эту роль назначают стрептококку, кишечной палочке, бледной спирохете и дифтерийной палочке. Были также предположения о вирусной этиологии болезни Ходжкина, но это также не подтвердилось.
В настоящее время установлено, что опухолевое новообразование (гематосаркома и лейкемия) считается определенной патологией кроветворной системы, а злокачественные клетки Березовского-Штернберга вызывают развитие лимфогранулематоза.
Кроме того, до конца не изучены некоторые жизненные факторы, которые могут способствовать возникновению болезни. К ним относятся образ жизни, вредные привычки, пищевые привычки и профессиональные вредности. Некоторые исследования предоставляют данные о возможном риске болезни Ходжкина у людей, перенесших инфекционный мононуклеоз или кожные заболевания, работающих в швейной или деревообрабатывающей промышленности, в сельском хозяйстве, а также среди химиков и врачей.
Сообщалось о случаях болезни Ходжкина у нескольких членов одной семьи или в одной команде.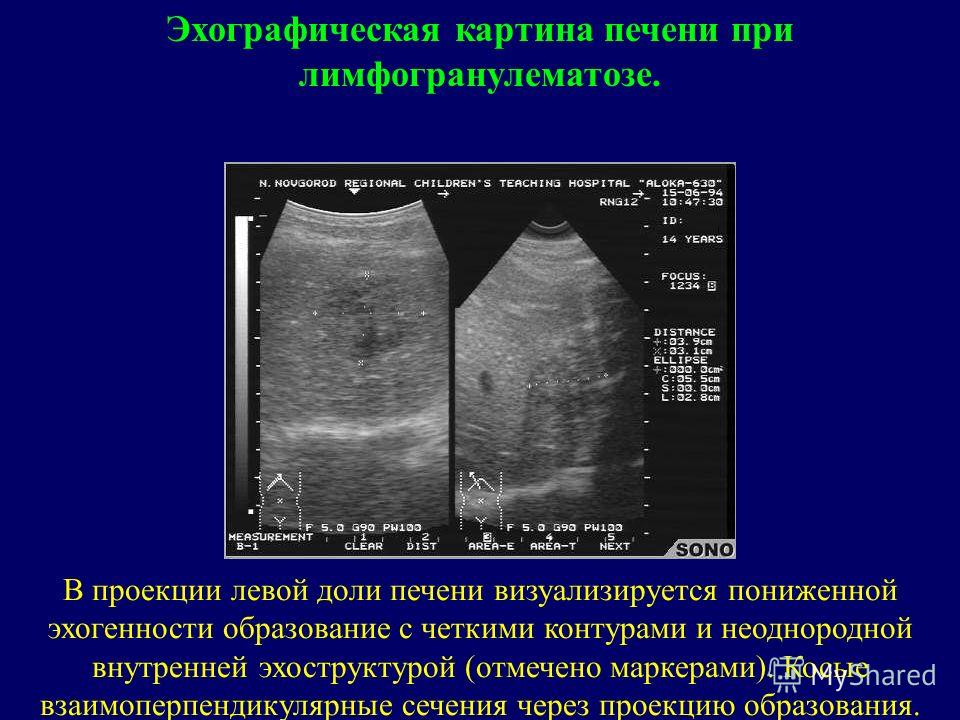 Это говорит о существовании роли слабовирулентной инфекции вирусной этиологии и генетической предрасположенности организма, однако окончательных доказательств пока нет. Таким образом, определенные и точные причины болезни Ходжкина до сих пор не найдены.
Это говорит о существовании роли слабовирулентной инфекции вирусной этиологии и генетической предрасположенности организма, однако окончательных доказательств пока нет. Таким образом, определенные и точные причины болезни Ходжкина до сих пор не найдены.
Симптомы лимфогранулематоза
Клиническая картина болезни Ходжкина характеризуется двумя типами: естественной и хронической.
При естественном течении болезни Ходжкина происходит чередование процессов обострения и ремиссии, но иногда болезнь приобретает быстрое, острое начало с сильным подъемом температуры, сильным потоотделением и распространением опухоли на различные внутренние органы.Без оказания медицинской помощи такие пациенты могут умереть в течение нескольких недель от начала патологического процесса или в ближайшие месяцы.
Но чаще всего у 90% лимфогранулематоз хронический, с периодическими обострениями, в результате которых патологический процесс перемещается на новые лимфатические узлы, ткани и органы.
На течение болезни Ходжкина отрицательно влияют несколько факторов, например солнечное излучение, беременность и физиотерапия.
Клинические симптомы болезни характеризуются местными и общими признаками.При диагностике патологии большое значение могут иметь общие проявления. Среди них увеличение различных групп лимфатических узлов и появление патологических образований в тканях и внутренних органах. В первую очередь поражаются периферические лимфатические узлы, для которых характерно увеличение в размерах без особой причины или может совпадать с простудой. Такие лимфатические узлы при пальпации имеют неровную округлую или овальную форму с упругой консистенцией. Как правило, они не связаны между собой и с соседними тканями, подвижны и безболезненны.Кожа без изменений, легко собирается в складку, свищ не появляется.
В 80% случаев лимфогранулематоз поражает лимфатические узлы, расположенные в области шеи. Его окружность увеличивается, контуры приобретают неровности, а иногда и визуально заметные выпячивания лимфатических узлов, если поражены они во множественном числе. На момент обращения к врачу почти у 25% пациентов одновременно пальпировали шейные лимфатические узлы и значительно увеличились надключичные.
На момент обращения к врачу почти у 25% пациентов одновременно пальпировали шейные лимфатические узлы и значительно увеличились надключичные.
Очень редко диагностируется первичный лимфогранулематоз подмышечных и паховых лимфатических узлов.Намного чаще происходит одновременное поражение этих лимфатических узлов с шейными лимфатическими узлами или средостением. Иногда заболевание может начаться с воспаления затылочных, поднижнечелюстных и околоушных лимфатических узлов.
У 20% больных лимфогранулематоз поражает лимфатические узлы средостения. Диагностика этого периода заболевания возможна при выборочном рентгенологическом исследовании легких. Но клиническая картина в течение длительного периода не проявляет никаких симптомов, а при значительном увеличении лимфоузлов пациенты жалуются на затрудненное дыхание, одышку, боли в груди и кашель.
Перкуссией определить малый размер лимфатических узлов невозможно. Но увеличенные конгломераты притупляют перкуторный звук, а дыхание ослабляется на больших и малых участках грудной клетки. На более поздних стадиях заболевания, после сдавления лимфоузлов в грудном протоке или при присоединении инфекции второй степени, образуется плеврит. Иногда у пациентов развивается синдром сдавления средостения или ателектаз легкого.
На более поздних стадиях заболевания, после сдавления лимфоузлов в грудном протоке или при присоединении инфекции второй степени, образуется плеврит. Иногда у пациентов развивается синдром сдавления средостения или ателектаз легкого.
В редких случаях можно встретить поражение забрюшинных лимфатических узлов или подвздошных узлов при первичной форме лимфомы Ходжкина.Такое поражение протекает без видимых клинических симптомов. Только при множественных поражениях появляются боли постоянного или периодического характера в поясничной области, животе и нижних конечностях; вздутие живота и расстройство стула.
При значительном увеличении лимфатических узлов в подвздошной области наблюдается нарушение лимфодренажа от конечностей, что является следствием отека дистальных отделов стопы и голени.
Лимфогранулематоз поражает также внутренние органы.Второе место после лимфоузлов очага поражения занимает селезенка. Однако клинические симптомы никак себя не проявляют. При пальпации селезенка практически в норме и не достигает больших размеров, поэтому ее сложно прощупать и можно только при множественных и крупных поражениях органа.
Гораздо реже встречается лимфогранулематоз других органов с первичными проявлениями болезни. Но в основном этот патологический процесс протекает в сочетании с поражением лимфатических узлов и проявляется в виде боли и симптомов, связанных с нарушением функции этих органов.
При поражении лимфогранулематозом костей больные жалуются на боли разной интенсивности и припухлость со стороны пораженного очага.
Иногда заболевание распространяется на кожу. В этом случае возникают небольшие инфильтраты и язвы округлой формы, приобретающие темно-красный цвет или изменения в виде сыпи, крапивницы, экземы, связанные с нарушением иммунитета пациентов.
Почти у 50% больных отмечаются симптомы интоксикации, при которых повышается температура тела, появляется потливость ночью, возникает кожный зуд и резкое похудание.Многие пациенты жалуются на общую слабость, боли в суставах, мышцах и костях, а также на головную боль.
Существует три основных клинических симптома, ухудшающих прогноз лимфогранулематоза. Во-первых, это потеря веса без особой причины за полгода до десяти процентов. Во-вторых, это обильные ночные поты. И, в-третьих, необъяснимый подъем температуры тела выше 39? C в течение трех дней.
Во-первых, это потеря веса без особой причины за полгода до десяти процентов. Во-вторых, это обильные ночные поты. И, в-третьих, необъяснимый подъем температуры тела выше 39? C в течение трех дней.
Проявление генерализованного кожного зуда также является признаком интоксикации.
Лимфогранулематоз поражает костный мозг без специфических особенностей и диагностируется в 5% случаев, а при вскрытии — в 30% случаев.
Стадия лимфогранулематоза
Лимфогранулематоз обычно поражает лимфатические узлы, гораздо реже патологический процесс распространяется на селезенку, печень, легкие и другие органы. Поэтому проявления болезни Ходжкина подразделяются на лимфатические и экстралимфатические.
Когда «лимфатический» поражает лимфатические узлы, селезенку, тимус, лимфоидное глоточное кольцо, аппендикс и пейеровы бляшки.Все остальные поражения являются экстралимфатическими проявлениями болезни.
На сегодняшний день самая распространенная классификация болезни Ходжкина, предложенная в 1966 году Лукасемом. Различают четыре гистологических типа лимфогранулематоза: лимфогистиоцитарный, узлово-склеротический, смешано-клеточный и ретикулярный.
Различают четыре гистологических типа лимфогранулематоза: лимфогистиоцитарный, узлово-склеротический, смешано-клеточный и ретикулярный.
Считается, что болезнь Ходжкина развивается единично. В первую очередь поражается один участок лимфоидной ткани в лимфатическом узле, а затем злокачественные клетки распространяются по лимфатической системе в новые очаги, где они инфицируют новые лимфатические узлы.Поэтому именно этим лимфогранулематоз отличается от других патологических образований, поскольку может поражать лимфоидную ткань на удаленных от основного очага злокачественного образования участках. В то время она затрудняла развитие подразделения болезни Ходжкина на стадии, которая была окончательно принята по международной классификации в 1971 году. Она рассматривает четыре стадии болезни.
На первой или локальной стадии лимфомы Ходжкина поражается одна зона лимфатических узлов или одна дополнительная лимфатическая ткань, а может быть, и орган.
На второй или региональной стадии лимфогранулематоза поражаются две зоны лимфатических узлов, а иногда и больше, локализованные на одной стороне диафрагмы. Но разные зоны лимфатических узлов могут быть вовлечены в патологический процесс одновременно с поражением одной экстралимфатической ткани, органа, расположенного с одной стороны от диафрагмы.
Но разные зоны лимфатических узлов могут быть вовлечены в патологический процесс одновременно с поражением одной экстралимфатической ткани, органа, расположенного с одной стороны от диафрагмы.
На третьей или генерализованной стадии лимфогранулематоза зоны лимфатических узлов поражаются в единственном или множественном числе с двух сторон диафрагмы.Этот процесс может включать пораженную селезенку, одну дополнительную лимфатическую ткань или орган.
На четвертой или диссеминированной стадии лимфогранулематоза одна или несколько экстралимфатических тканей или органов поражаются диффузно, с одновременным поражением лимфатических узлов или без него.
Кроме того, при наличии у пациента симптомов интоксикации к стадии добавляется индекс — «Б», а при отсутствии — «А». Также известно, что прогноз болезни Ходжкина ухудшается, когда эти симптомы объединяются в стадии патологического процесса.
Лимфогранулематоз у детей
Эта злокачественная патология встречается у детей в соотношении 1: 100 000. И это намного ниже, чем у взрослых. Лимфогранулематоз также не поражает детей до первого года жизни. Основной пик заболевания приходится на дошкольный возраст. Причем до десяти лет эта возрастная группа среди мальчиков по заболеваемости преобладает над девочками. И уже с 15–16 лет соотношение полов выравнивается.
И это намного ниже, чем у взрослых. Лимфогранулематоз также не поражает детей до первого года жизни. Основной пик заболевания приходится на дошкольный возраст. Причем до десяти лет эта возрастная группа среди мальчиков по заболеваемости преобладает над девочками. И уже с 15–16 лет соотношение полов выравнивается.
Детский лимфогранулематоз характеризуется злокачественными изменениями лимфоидной ткани и распространением лимфогранулемы на лимфатические узлы и соматические органы.Как правило, лимфогранулематоз переходит с одного пораженного участка на другой.
У детей в основном диагностируется шейная лимфаденопатия, которая характеризуется различными воспалительными процессами в носовой полости и ротоглотке. Как правило, к этим изменениям присоединяются поражения верхних шейных и подчелюстных лимфатических узлов. Но уже при поражении надключичной и нижней шейки возникает подозрение на болезнь Ходжкина. Иногда (20% случаев) в патологический процесс вовлекаются подмышечные лимфатические узлы, а менее 5% — паховые.
Если поражено большое количество лимфатических узлов средостения, то поражаются легочная ткань, плевра и перикард, грудная клетка с возможным развитием компрессионного синдрома. В это время лицо ребенка становится одутловатым с признаками цианоза, развивается кашель и одышка при незначительных физических нагрузках, а также тахикардия.
При редком поражении поддиафрагмальных лимфатических узлов дети особых жалоб не предъявляют. Затем в патологический процесс включается селезенка, в редких случаях — печень.У ребенка повышенная температура тела, слабость, ночная потливость, снижение аппетита, он становится постоянно сонливым и апатичным. В анализе крови возможно повышение СОЭ. При лимфогранулематозе четвертой стадии (диссеминированном) определяется уменьшение количества эритроцитов и тромбоцитов в крови. Поэтому при этих проявлениях обязательна биопсия.
Также отмечены определенные признаки активности патологического процесса. К ним относятся: повышенный уровень гаптоглобина, присутствие повышенного количества церулоплазмина, фибриногена и лактатдегидрогеназы.
При поражении лимфогранулематозом внутригрудных лимфатических узлов у ребенка появляется кашель, начинающийся кашлем и переходящий в судороги. Ребенок постоянно жалуется на боли в груди или в области сердца, усиливающиеся очередным приступом кашля.
У детей с болезнью Ходжкина парааортальные лимфатические узлы располагаются рядом с сосудами в области ворот печени, почек и селезенки. При поражении забрюшинных лимфатических узлов в сочетании с селезенкой дети жалуются на появление периодических болей в животе разной интенсивности.
Лимфогранулематоз изменяет практически все ткани и органы в организме больных детей. Экстранодальные поражения включают легочную ткань, кости, плевру и печень. Гораздо реже лимфогранулематоз изменяет костный мозг.
Для диагностики этого злокачественного новообразования у детей в США в 1971 году были проведены определенные виды обследований, которые необходимы для правильного определения стадии болезни Ходжкина и выбора лечения. Прежде всего, при сборе анамнеза ребенка особое внимание уделяется всем симптомам.Затем при необходимости сделайте биопсию и осмотрите пораженные участки. После этого назначают лабораторные анализы для определения биохимических показателей. Обязательное исследование — это рентген грудной клетки в разных проекциях, как прямой, так и боковой, а также компьютерная томография. В случаях, когда есть подозрения на патологические изменения костного мозга, назначают трепанобиопсию, проводят сканирование поражений костей, почек, печени.
Лечение лимфогранулематоза
К основным методам лечения патологического процесса в лимфатической системе относятся медикаментозный метод, лучевая терапия и их сочетание.
Однако в последние несколько десятилетий хирургическое удаление пораженных лимфатических узлов остается одним из методов лечения болезни Ходжкина. Но уже в девятнадцатом веке было обнаружено, что хирургические вмешательства приводят к распространению патологического процесса. Поэтому лечение болезни Ходжкина ограничивалось общеукрепляющими средствами.
Первое облучение лимфатических узлов было произведено в 1901 году двум больным лимфогранулематозом. А в 1906 году этот метод лечения появился в России.Но только с 1940-х годов химиотерапия была добавлена к лучевой терапии. Первым химиотерапевтическим препаратом был Мустарген, относящийся к группе хлорэтиламинозов. С 1947 года Ларионов использует свой аналог — эмбихин. Однако до шестидесятых годов прошлого века химиотерапия нерегулярно применялась для лечения болезни Ходжкина. Это, как правило, выглядело паллиативно и носило исследовательский характер. Облучение оставалось основой лечения болезни, но с начала 1960 года был предложен новейший курс медикаментозной терапии — это MORR.
При радикальном лучевом лечении как самостоятельной терапии общая доза на пораженные очаги составляет 40 Гр за четыре-шесть недель, а для профилактических зон — 30-50 Гр за три-четыре недели. Этот метод лечения назначают пациентам в I А — II А патологической стадии болезни Ходжкина с благоприятным прогнозом.
В последние годы все большее распространение получают комбинированные программы терапии. Пациенты с благоприятным прогнозом болезни Ходжкина проходят лечение по специальной программе: два курса полихимиотерапии по любой из схем первого ряда, воздействие на пораженные участки в дозе 36 Гр, два цикла медикаментозной терапии. в соответствии с выбранной схемой, которая применялась до воздействия.
Комбинированная терапия относится к методу, который считается выбором пациентов I, II (I E — II E) стадий болезни Ходжкина с неблагоприятным прогнозом. Терапия в этом случае начинается с полихимиотерапии. По объему такое лечение всегда намного больше, чем при благоприятном прогнозе. Здесь программа применяется в трех курсах полихимиотерапии из любой схемы первой линии, лучевой терапии пораженных участков (36 Гр), трех консолидирующих курсах химиотерапии.
Для лечения третьей стадии (А) болезни Ходжкина в основном используется химиолучевая комбинированная терапия.Таким пациентам с благоприятным прогнозом назначают четыре курса полихимиотерапии первой линии с последующим облучением пораженных участков (30–40 Гр). А пациентам с неблагоприятным прогнозом — 6–8 курсов химиотерапии по схемам первого ряда, облучение 30 Гр (при абсолютной ремиссии) и 40 Гр (при остаточных опухолевых процессах). Пациентам третьей (Б) — четвертой стадии с генерализацией процесса применяется циклическая химиотерапия.
Схемы первой линии включают: MORR, MVPP, CVPP, COPP, LVPP, ABVD.
Схема MORP включает внутривенное введение таких препаратов, как Embiquina и Oncovina; внутрь — Прокарбазин и Преднизолон с перерывом в две недели.
Схема MVPP, аналогичная MORR, только Онковин был заменен на Винбластин с перерывом между курсами в четыре недели.
Схема
CVPP: прокарбизин и преднизолон вводятся перорально в течение двух недель; в 1-й и 8-й дни внутривенно: Винбластин и Циклофосфамид с двухнедельным интервалом.
Схема COPP идентична CVPP, только Винбластин заменяется Винкристином, с перерывом между курсами в две недели.
Схема LVPP, аналогичная CVPP, но с заменой циклофосфамида на хлорбутин с первого по четырнадцатый день для приема внутрь и с перерывом между циклами в три или четыре недели.
Схема ABVD включает внутривенное введение в первый и четырнадцатый день таких препаратов: DTIK в дозе 375 мг / м2, блеомицин в дозе 10 мг / м2, винбластин в дозе 6 мг / м2 и адриамицин в дозе 25 мг / м2 с интервалами между циклами в две недели. .
При использовании только циклической химиотерапии для пациентов на любой стадии болезни Ходжкина лечение проводят до достижения полной ремиссии. Затем нужно сделать еще два контрольных курса. Абсолютного излечения у пациентов с генерализованными стадиями лимфогранулематоза невозможно добиться до четвертого курса полихимиотерапии. Следовательно, необходимо провести минимальный курс всей программы в шесть циклов.
Для лечения поздних рецидивов патологических процессов, возникших после двух лет полного выздоровления, в лечении применяют те же методы, что и при первой диагностике заболевания.
Ранние рецидивы (до двух лет), не достигшие полной ремиссии, вызывают большие трудности в лечении. Больным первой и второй стадиями болезни Ходжкина с благоприятным прогнозом по краевым рецидивам, появившимся через 5 месяцев после облучения, проводится курс лучевой терапии в дозе 40 Гр. Все остальные пациенты меняют химиотерапию.
При лечении ранних форм рецидивов генерализованного характера после химиолучевой терапии для пациентов с первичной резистентностью и пациентов с продолжающимися рецидивами назначают схемы второй линии или высокие дозы химиотерапии (схема третьей линии).
Схемы второй линии включают:
B-CAVe, который включает препараты, которые вводятся внутривенно в первый день, представляет собой винбластин в дозе 6 мг / м2 и доксорубицин в дозе 60 мг / м2 и блеомицин, также внутривенно в дозе 5 мг / м2 в первый, двадцать восьмой и восьмой дни. тридцать пять и ломустин 100 мг / м2 перорально. Курс повторяют на сорок второй день.
КЭП: внутривенно капельно вводят с первого по пятый день этопозид 100 мг / м2; перорально, в первый день, CCNU в дозе 80 мг / м2 и преднизон в дозе 60 мг / м2, с первого по пятый день.С повторением курса на 28 день.
ПЕСС: все препараты принимают внутрь — в первый день CCNU 100 мг / м2, этопозид 200 мг / м2 с первого по третий день, Лакерон 20 мг / м2 с первого по пятый и Преднизолон 40 мг / м2 с первого по пятый. с первого по седьмой день Перерыв — три недели.
ABVD: препараты назначают только внутривенно. Это на 1-й и 14-й дни блеомицина в дозе 10 мг / м2 и доксорубицина в дозе 25 мг / м2; с первого по пятый день — имидазол-карбоксамид в дозе 175 мг / м2.Перерыв — четыре, шесть недель.
MOPP / ABV: Онковин и Мустарген вводят внутривенно в 1-й день, а Винбластин, Адриамицин и Блеомицин — в 8-й день; Натулан и Преднизолон находятся внутри. С перерывом между курсами три недели.
Высокодозная химиотерапия — это схема BEAM, которая включает внутривенное введение таких препаратов, как кармустин, этопозид, цитозар, мелфалан на шестой день и трансплантацию стволовых клеток на седьмой день.
Пациентам с третьей стадией болезни Ходжкина спленэктомия назначается при тяжелых симптомах спленомегалии и плохом кроветворении, что препятствует лечению цитостатиками после неудачи химиолучевой терапии.
После выбранного и проведенного лечения состояние пациента подвергается определенной оценке. Есть несколько критериев оценки результатов лечения больных лимфогранулематозом. Проводится физикальным обследованием, рентгенологическим и ультразвуковым исследованиями после третьего и шестого курсов терапии.
Основные критерии включают полную или частичную ремиссию, стабилизацию или прогрессирование. При полной ремиссии полностью исчезают все клинические симптомы болезни Ходжкина, в том числе лабораторные признаки опухолевого процесса с периодом четыре недели.Для частичной ремиссии характерно уменьшение патологического новообразования почти на 50%. Стабилизация говорит об уменьшении опухоли также вдвое, при отсутствии и появлении новых злокачественных образований на 25%. По мере прогрессирования заболевания появляются новые очаги поражения и увеличивается размер опухоли.
Прогноз лимфогранулематоза
Общая пятилетняя безрецидивная выживаемость больных лимфогранулематозом локальной формы с наддиафрагмальной локализацией опухоли и комплексным лечением составляет 90%.Для третьей стадии болезни типа А — выживаемость 80%, для этой же стадии типа В — 60%, а для четвертой — около 45%.
Похожие сообщения
Лимфома Ходжкина | Справочная статья по радиологии
Лимфома Ходжкина или Болезнь Ходжкина ( HD ) является разновидностью лимфомы и составляет ~ 1% всех раковых заболеваний. Болезнь Ходжкина распространяется непрерывно и предсказуемо по лимфатическим путям и излечима примерно в 90% случаев, в зависимости от ее стадии и подтипа.
Существует бимодальное распределение по возрасту пораженных пациентов, с пиками у молодых людей (15-34 года) и пожилых пациентов (> 55 лет).
Типичное проявление — безболезненная лимфаденопатия. Могут присутствовать системные симптомы (симптомы B), такие как ночная потливость и потеря веса.
Необычным проявлением, описанным при болезни Ходжкина, является боль в пораженных органах после употребления алкоголя.
Заболевание характеризуется наличием клеток Рида-Штернберга (которые считаются разновидностью В-клеток).Однако эти клетки занимают очень небольшую часть (<5%) от общей популяции клеток пораженного лимфатического узла. Еще одна особенность - непрерывное распространение. ВЭБ-инфекция присутствует у 40-80% в зависимости от подтипа 4 .
Подтипы
Существует пять признанных гистологических подтипов, разделенных на две группы: классические и неклассические.
Классический
Положительный результат на CD15 / CD30 и отрицательный на CD20 / CD45 / EMA:
- узловой склерозирование: ≈70%
- смешанная клеточность: ≈25%
- с высоким содержанием лимфоцитов: 5%
- Истощение лимфоцитов: <5%
Неклассический
Положительный результат на CD 19, 20, 22, 79a / EMA и отрицательный на CD15 / CD30:
- с преобладанием узловых лимфоцитов (узловая парагранулема)
Классификация
Для классификации лимфом см. Классификацию ВОЗ новообразования лимфоидных тканей.
Местоположение
Узловая болезнь
Болезнь Ходжкина обычно почти полностью поражает лимфатические узлы. Обычно он начинается в верхней части тела (шея, подмышки, грудь).
Экстранодальная болезнь Ходжкина, хотя и нечасто, может быть обнаружена в любой системе органов либо как первичное проявление, либо как распространение системного заболевания. Это различие важно, поскольку диссеминированное заболевание имеет худший прогноз. Экстранодальное заболевание может возникать через инвазию в соседние ткани или через гематогенное распространение.
Органоспецифическое поражение:
Стадия
В отличие от других типов лимфомы болезнь Ходжкина обычно характеризуется систематическим характером узлового распространения, поэтому важна точная стадия.
См. Основную статью: стадия лимфомы Ходжкина.
Лечение и прогноз
Прогноз зависит от стадии, а также от нескольких других факторов, таких как возраст, серологические маркеры (СОЭ), наличие симптомов B и гистологический подтип опухоли:
- с преобладанием узловых лимфоцитов: лучший прогноз
- Лимфоциты истощены: прогноз хуже
Лечение зависит от стадии заболевания:
- стадия IIa и ниже: локализованная лучевая терапия
- стадия IIb и выше: химиотерапия +/- лучевая терапия на участки большой опухоли
.





 g., ВИЧ-инфицированные)
g., ВИЧ-инфицированные)
