Почечная остеодистрофия — причины, симптомы, диагностика и лечение
Почечная остеодистрофия – это изменение морфологии костей у пациентов с хроническим заболеванием почек, вызванное нарушением минерально-костного обмена. Симптомы включают патологические переломы, костные боли, деформацию скелета. Диагностика основана на данных биопсии, рентгенографии, денситометрии, КТ и МРТ, маркерах костного обмена. Лечение подразумевает коррекцию кальций-фосфорного обмена: назначают метаболиты витамина Д, фосфат-связывающие средства. При отсутствии эффекта возможно выполнение паратиреоидэктомии, в исключительных случаях производят трансплантацию почки.
Общие сведения
Термин почечная остеодистрофия используется с 1943 года, когда была выявлена связь между костными изменениями и ХПН. В 2006 году предложено название МКН-ХБП (минерально-костные нарушения, связанные с хронической болезнью почек), патологию стали рассматривать как прогрессирующее осложнение почечной недостаточности.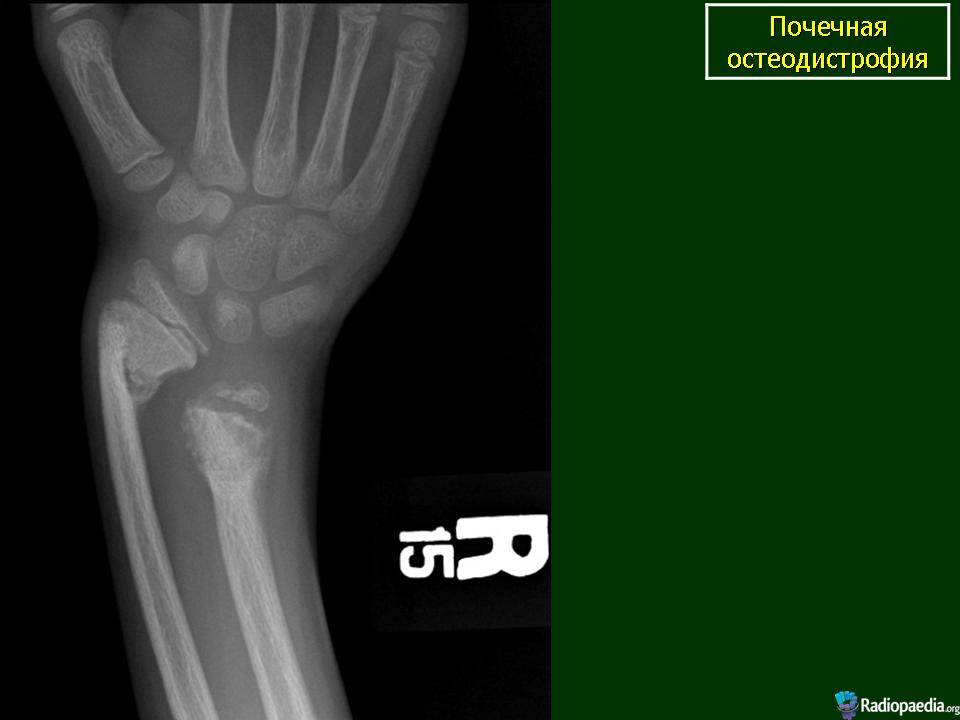 Нарушение присутствует у большинства пациентов с ХБП при снижении скорости клубочковой фильтрации ниже 50%, у 90-100% больных (взрослых и детей) с терминальной стадией ХПН, находящихся на заместительной терапии. Риск переломов по сравнению с общепопуляционным повышается в 4-5 раз. У пациентов старше 60 лет метаболическую остеопатию регистрируют в 3 раза чаще.
Нарушение присутствует у большинства пациентов с ХБП при снижении скорости клубочковой фильтрации ниже 50%, у 90-100% больных (взрослых и детей) с терминальной стадией ХПН, находящихся на заместительной терапии. Риск переломов по сравнению с общепопуляционным повышается в 4-5 раз. У пациентов старше 60 лет метаболическую остеопатию регистрируют в 3 раза чаще.
Почечная остеодистрофия
Причины
В норме костная ткань постоянно ремоделируется, а почки поддерживают нормальный уровень фосфора и кальция в крови. При гипокальциемии любого генеза паращитовидные железы выделяют гормон, который провоцирует вымывание минерала из костей, что приводит к их деминерализации. Почечная остеодистрофия – один из признаков хронической почечной недостаточности, которая является исходом многих урологических и нефрологических патологий. Поэтому заболевания, вызывающие ХПН, одновременно считают триггерами нарушения костного метаболизма:
- Врожденные и наследственные болезни.
 Поликистоз почек, синдром Альпорта и врожденная гипоплазия часто осложняются почечной недостаточностью с развитием метаболической остеопатии. Для этих патологий типичен отягощенный семейный анамнез. Частота встречаемости 0,5-3%. В большинстве наблюдений клинические проявления остеодистрофии присутствуют с детства (почечный рахит).
Поликистоз почек, синдром Альпорта и врожденная гипоплазия часто осложняются почечной недостаточностью с развитием метаболической остеопатии. Для этих патологий типичен отягощенный семейный анамнез. Частота встречаемости 0,5-3%. В большинстве наблюдений клинические проявления остеодистрофии присутствуют с детства (почечный рахит). - Гломерулярные патологии. Включают первичные гломерулонефриты, вторичную гломерулярную болезнь почек, характерную для системной красной волчанки, диабетической нефропатии и геморрагических васкулитов. Сахарный диабет является одной из наиболее частых причин утраты функциональной способности почек, на его долю приходится 44%, на гломерулярную патологию – 8% случаев.
- Сосудистые заболевания. Атеросклероз и системный склероз с поражением почек нарушают кровоснабжение, вызывают ишемию тканей, следствием чего становится прогрессирующая гибель нефронов. Гипертоническая болезнь, осложненная нефропатией, в 30% случаев приводит к ХПН и метаболической болезни костной ткани.
 Остеодистрофия сочетается с серьезными осложнениями со стороны сердечно-сосудистой системы, сопряженными с высокой летальностью.
Остеодистрофия сочетается с серьезными осложнениями со стороны сердечно-сосудистой системы, сопряженными с высокой летальностью. - Тубулоинтерстициальные болезни. Тубулоинтерстициальный нефрит, который прогрессирует до ХПН с нарушениями метаболизма костей, может носить идиопатический, лекарственный или иммунологический характер. Мочеполовой туберкулез, шистосомоз, нефрокальциноз также проявляются постепенной утратой функциональных структур почки. Применение противовирусных лекарств для лечения гепатита В, ВИЧ-инфекции связано с дисфункцией канальцев и гипофосфатемической остеомаляцией.
- Состояния, сопровождающиеся обструкцией. Мочекаменная болезнь, гиперплазия предстательной железы, опухоли малого таза и забрюшинный фиброз характеризуются нарушением адекватной уродинамики. Застой мочи способствует размножению бактериальной микрофлоры, развитию рецидивирующего вторичного пиелонефрита с гидронефротической трансформацией чашечно-лоханочной системы.
 При двустороннем поражении присоединяется ХБП, запускающая процессы остеодистрофии.
При двустороннем поражении присоединяется ХБП, запускающая процессы остеодистрофии.
К утяжеляющим факторам относят неправильное питание, приводящее к гиповитаминозу витамина D, состояние постменопаузы, сопровождающееся нарушением минерального обмена, вредные привычки. К ренальной остеопатии предрасполагает пожилой возраст, неадекватный прием кальцитриола. У больных, принимающих антациды по поводу язв ЖКТ или получающих заместительную почечную терапию, в организме накапливается алюминий. Это является дополнительной причиной остеомаляции на фоне ингибирования активности остеобластов.
Патогенез
Почечная остеодистрофия описывается как результат гиперпаратиреоза, вторичной гиперфосфатемии с гипокальциемией, провоцируемых снижением экскреции фосфатов поврежденными почками. Наиболее важной причиной снижения уровня кальцитриола при ХПН является высокий уровень фактора роста фибробластов 23 (FGF23, фосфатонин), который вырабатывается остеоцитами и остеокластами в ответ на гиперфосфатемию.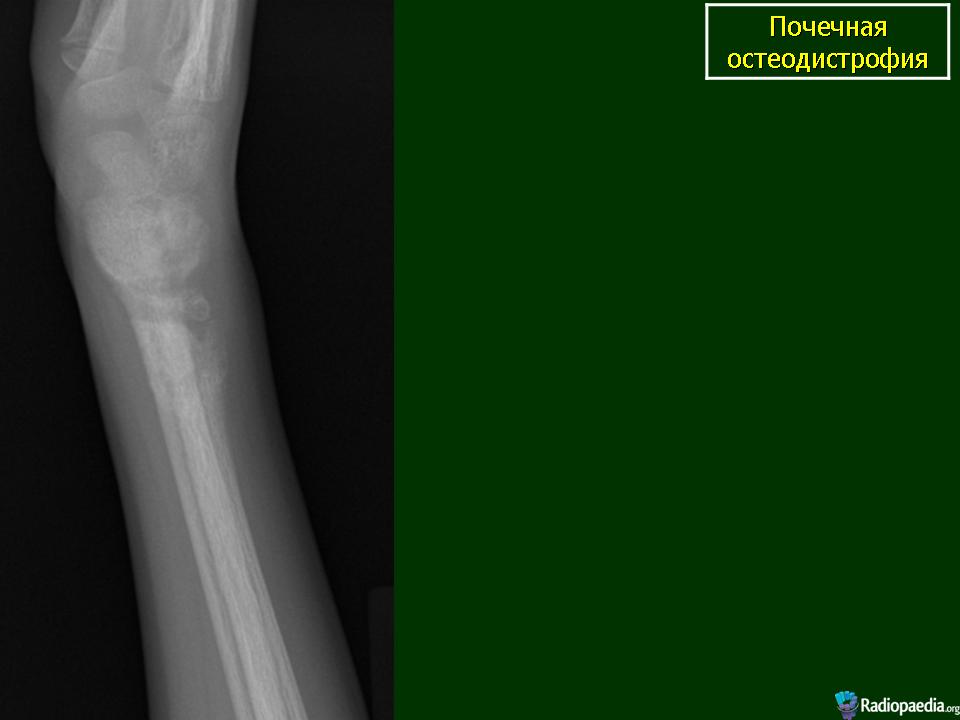 Соединение способствует уменьшению реабсорбции фосфора в проксимальных канальцах нефрона, блокирует активность 1-альфа-гидроксилазы.
Соединение способствует уменьшению реабсорбции фосфора в проксимальных канальцах нефрона, блокирует активность 1-альфа-гидроксилазы.
1-альфа-гидроксилаза влияет на трансформацию 25(OH)D в 1,25(OH)2D и уменьшение всасывания витамина D стенками кишечника. Этот компенсаторный механизм поддерживает уровень фосфатов в норме при их усиленной экскреции с мочой. Поскольку большое количество FGF23 необходимо для поддержания нормального уровня сывороточного фосфора, синтез кальцитриола подавляется, что провоцирует снижение абсорбции Са, гипокальциемию. Этому же способствует деструкция проксимальных канальцев (место образования кальцитриола), ацидоз на фоне уремии, снижение запасов субстанций для выработки активного гормона.
Гипокальциемия поддерживается еще одним компенсаторным механизмом – усилением секреции паратиреоидного гормона. Его чрезмерная выработка увеличивает скорость резорбции, приводит к изменениям структуры скелета за счет вторичного гиперпаратиреоза.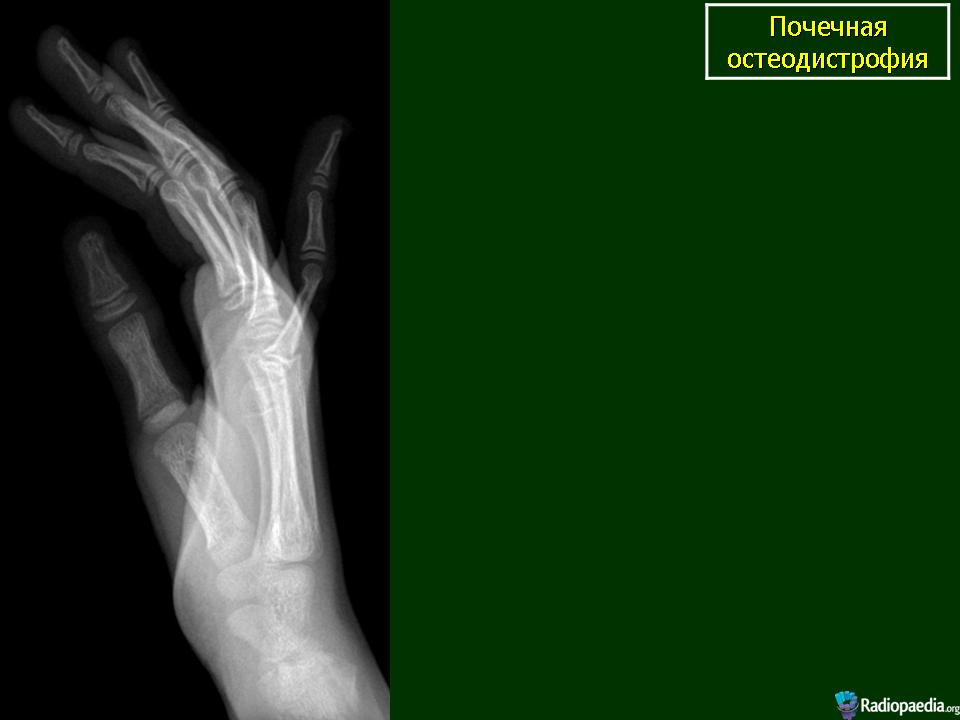 Прогрессирование ренальной дисфункции с гиперфосфатемией стимулирует гиперплазию паращитовидных желез, гиперсекрецию паратиреоидных гормонов, что постепенно ведет к развитию аденомы. Усиленный обмен и ремоделирование кости заканчиваются нарушением ее архитектоники, минерализации, утратой прочности.
Прогрессирование ренальной дисфункции с гиперфосфатемией стимулирует гиперплазию паращитовидных желез, гиперсекрецию паратиреоидных гормонов, что постепенно ведет к развитию аденомы. Усиленный обмен и ремоделирование кости заканчиваются нарушением ее архитектоники, минерализации, утратой прочности.
Классификация
В основе систематизации патологии лежит оценка результатов гистологического исследования биоптатов костной ткани. Выделяют три основополагающих процесса, обозначаемых английской аббревиатурой TMV: интенсивность метаболизма (низкий, нормальный, высокий), минерализацию кости (нормальная, нарушенная), объем (низкий, в норме, высокий). Классификация была предложена экспертами в 2009 году, основана на корреляции между активностью обменных процессов костной ткани, морфологическими изменениями и содержанием в крови интактного паратиреоидного гормона. Почечная остеодистрофия, связанная с ХБП, может протекать:
- С увеличением процессов метаболизма.
 Клинические проявления включают фиброзный остеит, вторичный гиперпаратиреоз. Другое название – гиперпаратиреоидная болезнь костей.
Клинические проявления включают фиброзный остеит, вторичный гиперпаратиреоз. Другое название – гиперпаратиреоидная болезнь костей. - Со снижением обменных процессов. Группа включает адинамическую болезнь скелета, остеомаляцию (деминерализация костного вещества, не сопровождающаяся выраженным изменением белкового синтеза в матриксе и приводящая к размягчению кости).
- В комбинированном варианте. Комбинированная форма сочетает умеренный вторичный гиперпаратиреоз (ВГПТ) и остеомаляцию.
К наиболее распространенным формам почечной остеопатии относят фиброзный остеит и смешанную остеодистрофию (высокий метаболизм), умеренный ВГПТ (нормальный костный метаболизм), адинамическую костную болезнь и остеомаляцию, для которой характерен низкий уровень обмена. Фиброзный остеит считается классическим проявлением ВГПТ и уремии, встречается в 40%. Остеомаляция и сочетанная форма обнаруживаются менее чем в 10% биоптатов.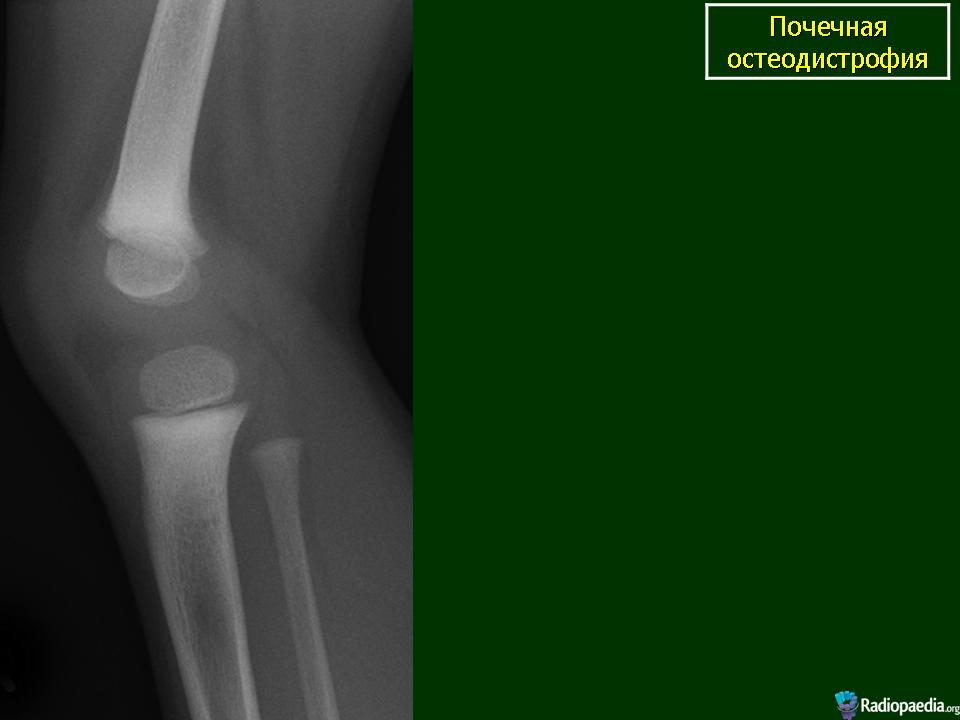 На долю адинамической болезни, по разным источникам, приходится от 15-60%.
На долю адинамической болезни, по разным источникам, приходится от 15-60%.
Симптомы почечной остеодистрофии
Патология включает признаки вторичного гиперпаратиреоза, рахита, остеомаляции и остеопороза. Рахит с остеомаляцией встречаются у детей, вторичный гиперпаратиреоз с остеомаляцией – у взрослых. Клиника вариативна, зависит от формы ренальной остеодистрофии. Заболевание долгое время протекает бессимптомно. В последующем пациенты предъявляют жалобы на суставные боли, усиливающиеся при движении, костную ломоту. При накоплении кальция в хрящах отмечается ограничение объема движений из-за утраты эластичности суставных поверхностей, появляется утиная (переваливающаяся) походка.
Кальцификация стенки поверхностных сосудов вызывает кальцифилаксию, что проявляется очагами некроза на коже. Процесс сопровождается кожным зудом, который может быть временным или постоянным. Кальций отвечает за нервно-мышечную передачу, ее нарушение проявляется мышечной слабостью, которая постепенно прогрессирует, распространяясь на верхние конечности. Со стороны нервной системы обнаруживается апатия, постоянная сонливость, ухудшение памяти. Сердечно-сосудистые проявления представлены загрудинной болью, одышкой, тахикардией.
Со стороны нервной системы обнаруживается апатия, постоянная сонливость, ухудшение памяти. Сердечно-сосудистые проявления представлены загрудинной болью, одышкой, тахикардией.
Осложнения
К осложнениям относят переломы и деформации костей, разрывы сухожилий. Со стороны сердца регистрируют очаговые изменения миокарда, клиника напоминает инфаркт. Острый гиперкальциемический криз – неотложное состояние, которое требует немедленной госпитализации и развивается при достижении уровня Са выше 3,5 нмоль/л. Для него характерны резкая слабость, изменение сознания, абдоминальные боли, сопровождаемые неукротимой рвотой. ЭКГ фиксирует нарушение ритма, блокады.
Как осложнения рассматривают кальцификации сосудов, приводящие к атеросклерозу, гипертонии, застойной сердечной недостаточности. Отложение кальцинатов в легких может стать причиной дыхательной недостаточности. Почечная остеодистрофия с низким метаболизмом часто сопровождается тяжелой анемией, устойчивой к лечению эритропоэтином. При этом страдает общее самочувствие, значительно ухудшается качество жизни. У детей вследствие нарушенного минерального обмена развивается карликовость, О-образные и Х-образные деформации нижних конечностей.
При этом страдает общее самочувствие, значительно ухудшается качество жизни. У детей вследствие нарушенного минерального обмена развивается карликовость, О-образные и Х-образные деформации нижних конечностей.
Диагностика
Диагноз устанавливают на основании жалоб, данных физикального осмотра, оценки результатов лабораторных и инструментальных исследований. Наиболее информативна биопсия костной ткани, но вмешательство рекомендовано не всем пациентам из-за инвазивности. Процедуру осуществляют в специализированных клиниках для исключения адинамической формы патологии, в спорных ситуациях или при решении вопроса о целесообразности операции. К инструментальным и лабораторным способам диагностики остеодистрофии на фоне болезни почек относят:
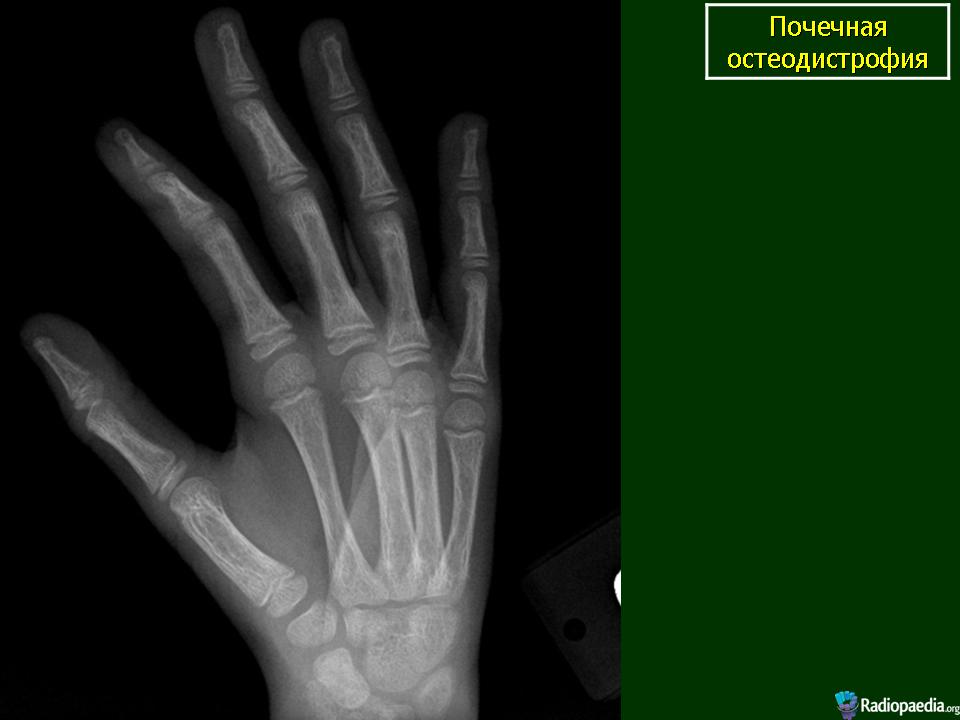
- Рентгенографию. Первичный способ визуализации, используемый для оценки состояния костной ткани у пациентов, страдающих нефрологическими и урологическими заболеваниями. Рентгенограммы визуализируют переломы, специфические изменения скелета при остеодистрофиях.
 Из-за лучевой нагрузки методика имеет ограничения по количеству исследований, особенно в детском возрасте.
Из-за лучевой нагрузки методика имеет ограничения по количеству исследований, особенно в детском возрасте. - Денситометрию. Обычно выполняют двухэнергетическую рентгеновскую абсорбциометрию в поясничном отделе позвоночника, проксимальном отделе бедренной кости и дистальном отделе предплечья. Исследование показывает изменения, типичные для остеопении и остеопороза, позволяет спрогнозировать риск переломов. Процедуру повторяют в динамике для оценки плотности костей на фоне проводимой терапии. Показаниями к денситометрии также являются ХПН, планируемый гемодиализ или трансплантация.
- МРТ и КТ. Назначаются при недостаточной информативности других методик. Компьютерная томография обеспечивает высококачественную визуализацию патологических изменений скелета, которые не выявляются при выполнении обычной рентгенографии. МРТ дает возможность оценить состояние прилегающих тканей: сухожилий, связок, хрящей.
- Лабораторные анализы.
 Оценка костного метаболизма позволяет судить о степени ремоделирования ткани. Уровень Са обычно низкий, сывороточный Р выше нормы (зависит от стадии ХБП). Щелочная фосфатаза повышена из-за остеобластической активности. Лучшим неинвазивным вариантом диагностики подтипов почечной остеодистрофии является определение уровня ПТГ для оценки костного метаболизма.
Оценка костного метаболизма позволяет судить о степени ремоделирования ткани. Уровень Са обычно низкий, сывороточный Р выше нормы (зависит от стадии ХБП). Щелочная фосфатаза повышена из-за остеобластической активности. Лучшим неинвазивным вариантом диагностики подтипов почечной остеодистрофии является определение уровня ПТГ для оценки костного метаболизма.
Дифференциальную диагностику проводят с миеломной болезнью, остеопорозом внепочечной этиологии, резорбтивной остеомаляцией на фоне дефицита витамина D. Основным критерием является сохранность почечной функции, мочевина и креатинин, как правило, не превышают нормы или снижены незначительно. Причиной остеомаляции иногда служит идиопатическая гиперкальциурия, не связанная с ацидозом. Ученые предполагают, что усиленная потеря Са происходит из-за сопутствующего пиелонефрита с аномальным строением канальцев.
Лечение почечной остеодистрофии
Заместительная терапия без других методик не может устранить нарушения фосфорно-кальциевого обмена и предотвратить костную патологию при терминальной уремии. Поддержка электролитного баланса включает назначение препаратов, которые способствуют обеспечению максимально близкого к норме уровня сывороточного кальция, фосфора, подавляют активность паратиреоидных желез. Адекватное лечение ренальной остеодистрофии во многом определяет качество жизни больных.
Поддержка электролитного баланса включает назначение препаратов, которые способствуют обеспечению максимально близкого к норме уровня сывороточного кальция, фосфора, подавляют активность паратиреоидных желез. Адекватное лечение ренальной остеодистрофии во многом определяет качество жизни больных.
Огромное значение имеет диета, поскольку именно с пищей поступает большинство минералов. Гиперфосфатемию предупреждают ограничением продуктов, содержащих большое количество белка (мясо, молоко, яйца). Концентрацию кальция важно поддерживать на верхней границе нормы, для этого в рацион включают темно-зеленые овощи, тофу, цитрусовые, по показаниям дополнительно вводят кальциевые добавки. Соотношение Са и Р должно составлять 1:1. Врач постоянно контролирует электролиты крови, гормональный профиль, корректируют схему терапии.
Медикаментозное лечение
Выбор того или иного препарата производится с учетом формы остеодистрофии, стадии хронической болезни почек, тяжести вторичного гиперпаратиреоза. При подборе учитывают побочные эффекты от приема медикаментов, выявляющиеся у пациента. К основным группам лекарственных средств относят:
При подборе учитывают побочные эффекты от приема медикаментов, выявляющиеся у пациента. К основным группам лекарственных средств относят:
- Фосфатбиндеры (связыватели фосфора). Кальция карбонат и кальция ацетат назначаются с начальных стадий ХПН, препятствует всасыванию фосфата в ЖКТ. Их прием особенно актуален при гемодиализе. При неэффективности пересматривают подход к ЗПТ: увеличивают площадь поверхности диализирующей мембраны, продолжительность процедуры, количество сеансов. Используемые ранее препараты на основе гидроокиси алюминия сейчас утратили актуальность из-за риска накопления соединения и связанных с этим осложнений. Их лучшей альтернативой является севеламер.
- Средства с витамином Д. Кальцитриол и альфакальцидол способствуют снижению активности паратиреоидных желез. При ЗПТ их применяют для профилактики и лечения вторичного гиперпаратиреоза. Персистирующая гипокальциемия с нормальными показателями фосфорного обмена корректируется путем назначения витамина D, который усиливает всасывание Са.
 На фоне приема уменьшается болевой синдром, усиливается минерализация костной ткани, особенно при фиброзно-кистозном остите.
На фоне приема уменьшается болевой синдром, усиливается минерализация костной ткани, особенно при фиброзно-кистозном остите. - Бисфосфонаты. Опыт использования медикаментов этой группы недостаточен, есть данные, что препараты предотвращали костную деминерализацию после пересадки почки. ЗПТ и прием метаболитов витамина Д для коррекции вторичного гиперпаратиреоза иногда осложняется стойкой гиперкальциемией. Бисфосфонаты в таких случаях способствовали нормализации состояния, хорошо выводились из организма с помощью гемодиализа.
Хирургическое лечение
Удаление ткани паратиреоидных желез показано, если ПТГ превышает 800 пг/мл в течение 3 месяцев, несмотря на консервативную терапию и принятые меры: отмену витамина Д, отказ от использования диализирующего раствора с высоким содержанием Са, соблюдение диеты. Возвратная гиперкальциемия, появление ишемических некрозов, изнуряющий кожный зуд также требуют хирургического лечения. Вмешательство обосновано перед трансплантацией почки, поскольку послеоперационный период сопровождается гиперкальциемией. Наиболее часто выполняют субтотальную паратиреоидэктомию.
Вмешательство обосновано перед трансплантацией почки, поскольку послеоперационный период сопровождается гиперкальциемией. Наиболее часто выполняют субтотальную паратиреоидэктомию.
Прогноз и профилактика
При своевременной терапии почечная остеодистрофия поддается коррекции. Тяжесть состояния определяется стадией почечной недостаточности; после трансплантации почки прогноз для жизни более оптимистичен. Значительное улучшение самочувствия наблюдается при субтотальной резекции паращитовидных желез – минерализация усиливается через 3-6 месяцев после операции, в течение 10 дней купируется костно-суставной болевой синдром, увеличивается мышечная сила.
Профилактика подразумевает выявление гиперпаратиреоидных состояний, отказ от курения и злоупотребления алкоголем, правильное питание. Превентивные меры для пациентов на ЗПТ включают прием витамина Д после каждого сеанса гемодиализа. При первых симптомах неблагополучия со стороны органов мочевыделения важно сразу обратиться к урологу или нефрологу, что позволит диагностировать патологию на ранней стадии.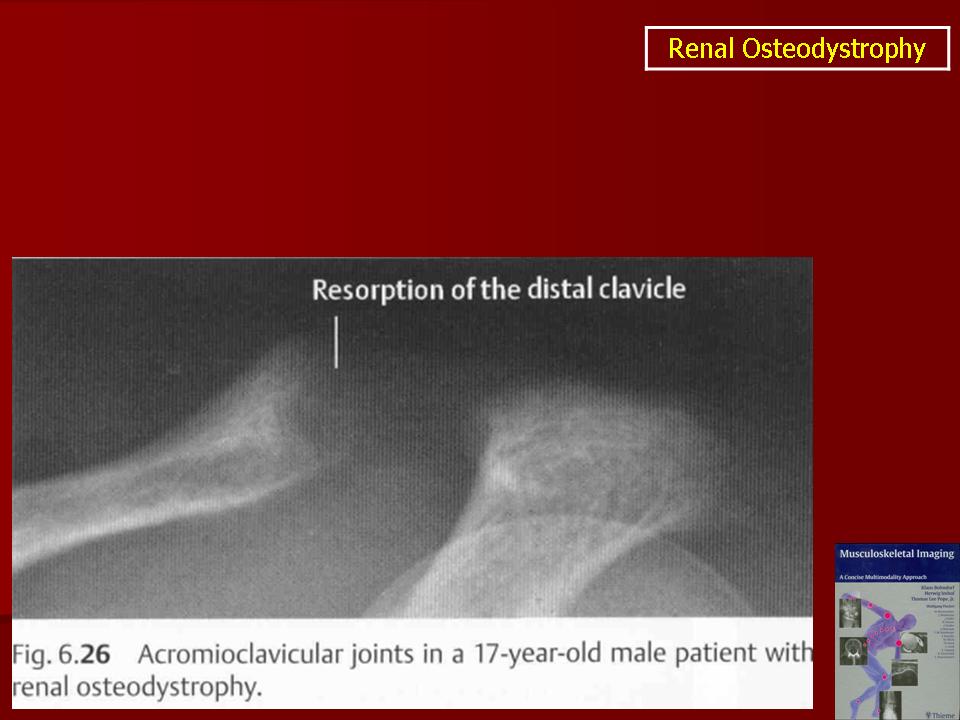 Адекватное лечение помогает предотвратить или максимально отсрочить развитие почечной недостаточности, а следовательно – и остеодистрофии.
Адекватное лечение помогает предотвратить или максимально отсрочить развитие почечной недостаточности, а следовательно – и остеодистрофии.
Почечная остеодистрофия
Термин «почечная остеодистрофия» означает нарушение роста и процесса формирования костей скелета у детей с хронической почечной недостаточностью вследствие изменения минерального обмена и обмена веществ в кости. Характерны нарушение всасывания кальция, гиперфункция паращитовидных желез, обызвествление сосудов кожи и внутренних органов и нарушение образования в почках биологически активного витамина D. Почечная остеодистрофия развивается при поражении почечных канальцев и нормальной клубочковой фильтрации. По мере прогрессирования процесса происходит гибель нефронов с развитием функциональной недостаточности клубочков и уремии.
Состояние, ранее называвшееся почечным рахитом или почечной карликовостью вследствие резкого замедления роста, имеет рентгенологическую картину, сходную с таковой при рахите.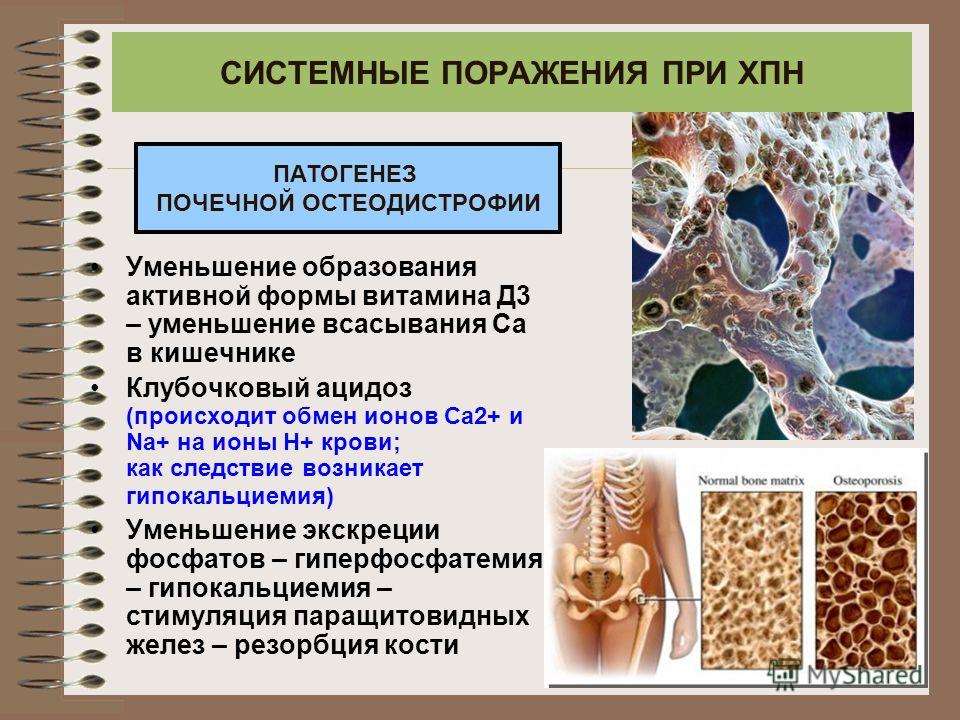 Эти изменения вначале относили за счет нарушения минерализации в результате дефицита витамина D. Однако результаты проведенных в последнее время исследований иммунофизиологии паращитовидных желез и гистологических исследований костей свидетельствуют о том. что вторичный гиперпаратиреоз также имеет большое значение в различии клинической и рентгенологической картины при уремической остеодистрофии. Є внедрением в клиническую практику гемодиализа и пересадки почек основным осложнением хронической почечной недостаточности у детей стала почечная остеодистрофия.
Эти изменения вначале относили за счет нарушения минерализации в результате дефицита витамина D. Однако результаты проведенных в последнее время исследований иммунофизиологии паращитовидных желез и гистологических исследований костей свидетельствуют о том. что вторичный гиперпаратиреоз также имеет большое значение в различии клинической и рентгенологической картины при уремической остеодистрофии. Є внедрением в клиническую практику гемодиализа и пересадки почек основным осложнением хронической почечной недостаточности у детей стала почечная остеодистрофия.
Патогенез. Патогенез заболевания сложен. Костные изменения резистентны к терапии витамином D в физиологических дозах, как правило, достаточных для коррекции простого авитаминоза. Подобная резистентность приводит к нарушению всасывания кальция и фосфора и нарушению минерализации костей. Резистентность к витамину D можно объяснить тем фактом, что почки представляют собой конечный пункт синтеза его основных метаболитов.
По мере снижения клубочковой фильтрации развивается вторичный гиперпаратиреоз. Повышение уровня фосфатов в крови приводит к гипокальциемии и высвобождению паратгормона. При определенном критическом почечном пороге, т. е. при снижении скорости клубочковой фильтрации приблизительно до 20-30% от нормы, фосфатурическая почечная реакция на повышение уровня паратгормона утрачивается, и при тенденции к нормализации содержания кальция в крови развивается компенсаторный гиперпаратиреоз. Рентгенологические и гистологические изменения указывают на опосредованную остеокластами резорбцию кости. Кроме того, происходит эндостальный фиброз, повышается обмен в костной ткани с замещением правильной пластинчатой ее структуры дезорганизованной и структурно непрочной костной тканью. Хронический метаболический ацидоз, увеличивая резорбцию кальция и нарушая превращение витамина D в биологически активную форму, вероятно, способствует изменениям костной ткани.
Повышение уровня фосфатов в крови приводит к гипокальциемии и высвобождению паратгормона. При определенном критическом почечном пороге, т. е. при снижении скорости клубочковой фильтрации приблизительно до 20-30% от нормы, фосфатурическая почечная реакция на повышение уровня паратгормона утрачивается, и при тенденции к нормализации содержания кальция в крови развивается компенсаторный гиперпаратиреоз. Рентгенологические и гистологические изменения указывают на опосредованную остеокластами резорбцию кости. Кроме того, происходит эндостальный фиброз, повышается обмен в костной ткани с замещением правильной пластинчатой ее структуры дезорганизованной и структурно непрочной костной тканью. Хронический метаболический ацидоз, увеличивая резорбцию кальция и нарушая превращение витамина D в биологически активную форму, вероятно, способствует изменениям костной ткани.
Патологоанатомическая картина довольно разнообразна. При биопсии костных трабекул обнаруживают остеомаляцию, явления фиброзного остита или наиболее распространенную смешанную форму. Нарушение процесса минерализации можно подтвердить назначением больному до биопсии тетрациклина; этот флюоресцирующий антибиотик задерживается в участках минерализации.
Нарушение процесса минерализации можно подтвердить назначением больному до биопсии тетрациклина; этот флюоресцирующий антибиотик задерживается в участках минерализации.
Изменения эпифизарной ростковой пластинки на рентгенограмме иногда сходны с таковыми при алиментарном рахите, но в большинстве случаев значительно отличаются; гистологически это скорее фиброзный остит, чем рахит. Кажущееся увеличение ростковой пластинки в продольном направлении обусловлено образованием полосы метафизарного фиброза с дис пластическими трабекулами. Недостаточная минерализация приводит к нарушению формирования костей с длительным сохранением хряща, увеличению диаметра эпифизов и изменению контура метафизов.
Клиническая картина. Чем раньше у детей развивается хроническая почечная недостаточность, тем длительнее ее течение и тем чаще и тяжелее протекает остеодистрофия. У детей с врожденным заболеванием почек, в основном до 5летнего возраста, интервал между началом заболевания и конечной стадией почечной недостаточности более длительный, чем при позднее развивающихся гломерулонефритах..jpg) При врожденной нефропатии процесс в костной ткани протекает значительно быстрее, поскольку развивается в период ее максимального роста и перестройки.
При врожденной нефропатии процесс в костной ткани протекает значительно быстрее, поскольку развивается в период ее максимального роста и перестройки.
К ранним симптомам почечной остеодистрофии относится замедление роста в результате метаболического ацидоза, недостаточно калорийного питания, гормональных нарушений и нарушений минерального обмена в сочетании с хронической почечной недостаточностью. Отставание роста иногда происходит без ретгенологических изменений скелета. При прогрессировании заболевания развиваются мышечная слабость, боли в костях, деформации костей, смещение эпифизов и переломы в области метафизов метастатическое обызвествление и зуд. Особенно заметны у маленьких детей варусное искривление коленного сустава, выступающие лобные кости и патологические изменения зубов. Тетанус встречается редко вследствие сочетанного защитного эффекта метаболического ацидоза и гиперпаратиреоза.
Результаты лабораторных исследований. У больных возможна незначительная гипокальциемия, но за счет повышения уровня фосфора в крови произведение сахар обычно остается увеличенным. Повышение активности щелочной фосфатазы, отражающее усиленную перестройку костной ткани, не относится к характерным признакам ни у детей, ни у взрослых.
Повышение активности щелочной фосфатазы, отражающее усиленную перестройку костной ткани, не относится к характерным признакам ни у детей, ни у взрослых.
Субпериостальные эрозии средних и дистальных фаланг, обнаруживаемые на рентгенограмме костей, считают довольна ранним и специфическим признаком фиброзного остеита. Они. локализуются и в дистальной части ключицы и на внутренней поверхности дистальных отделов бедренной и проксимальных отделов большеберцовой костей. Ранние диагностически ценные данные можно получить при чрескожной биопсии кости. Л все же к наиболее ранним признакам даже при таком выраженном снижении скорости клубочковой фильтрации, как 40-50 мл/ относится повышение в крови уровня гіаратгормона. Степень его повышения коррелирует с рентгенологическими и гистологическими признаками фиброзного остеита; но между выраженностью гистологических изменений при остеомаляции и биохимическими изменениями в крови, рентгенологическими признаками рахита, остеопении или утолщении трабекул такой четкой корреляции не выявлено.
Лечение
При почечной остеодистрофии эффекта достигают с помощью:
1) коррекции гиперфосфатемии;
2) приема достаточного количества кальция;
3) применения витамина D.
Лечение следует начинать возможно раньше, поскольку замедление роста у детей раннего возраста имеет большое значение для окончательного роста. Вопрос о том, следует ли начинать его до появления рентгенологических или биохимических изменений, остается открытым.
С целью коррекции гиперфосфатемии внутрь назначают препараты, связывающие фосфаты. Гель гидрата окиси алюминия или его углекислую соль применяют в начальной дозе 20- 30 мг/, затем ее регулируют, поддерживая уровень фосфора в крови между 40-50 мг/л. Дозу увеличивают при одновременном введении витамина D. Необходимо обеспечить поступление в организм кальция в дозе 1 — 1,5 г/сут; его назначают в форме углекислой соли вследствие наибольшего содержания в нем элементарного кальция. Ацидоз тщательно корригируют с помощью гидрокарбоната натрия.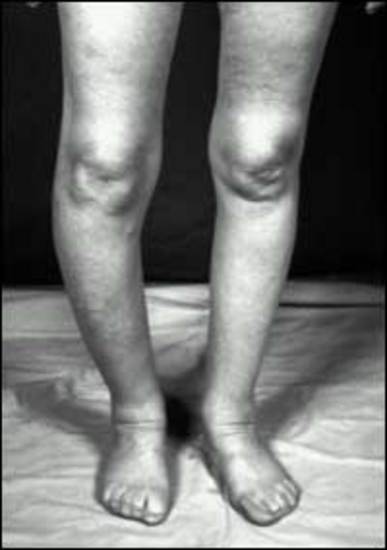 Начальная доза его составляет обычно 1-2 мэкв/.
Начальная доза его составляет обычно 1-2 мэкв/.
Для лечения больных с уремической остеодистрофией используют некоторые формы витамина D. Большие дозы его способствуют уменьшению изменений в костях и частично воздействуют на течение гиперпаратиреоза. Начальная доза составляет 5000-10 000 ЕД/сут, в некоторых случаях ее увеличивают до 100 000-200 000 ЕД/сут. Терапевтический диапазон препарата мал; из-за большого периода его полужизни у больных с хронической почечной недостаточностью часто развивается длительно сохраняющаяся гиперкальциемия. В последние годы вместо витамина D предпочитают применять дигидротахистерол вследствие его более короткого периода полужизни. Кроме того, с теоретической точки зрения преимущество заключается в том, что для его активации требуется лишь гидроксилирование в печени в 25м положении, без гидроксилирования в 1м положении в почках. Начальная доза составляет 0,1-0,2 мг/сут. При любом методе лечения оптимально подобранной дозой считается нормализующая уровень кальция в крови и способствующая исчезновению рентгенологических изменений.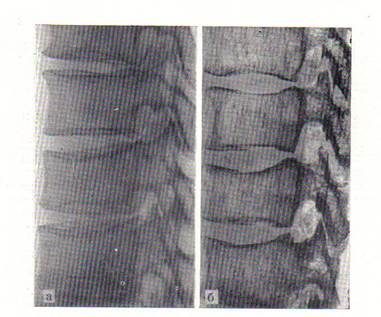 После достижения этих результатов ее уменьшают. Во время лечения проводят тщательный контроль за уровнем кальция и фосфора в крови. Эффективным при остеодистрофии оказывается 1,25[ОН]2С)з и 25[OH]D3; эти препараты, проходящие в настоящее время клинические испытания, представляются перспективными.
После достижения этих результатов ее уменьшают. Во время лечения проводят тщательный контроль за уровнем кальция и фосфора в крови. Эффективным при остеодистрофии оказывается 1,25[ОН]2С)з и 25[OH]D3; эти препараты, проходящие в настоящее время клинические испытания, представляются перспективными.
Гемодиализ корригирует клинические проявления со стороны костей, но может вызвать обострение процесса; эффект предсказать нельзя. Недиагностированная или некорригированная гиперкальциемия может ускорить развитие почечной недостаточности или способствует метастатическому обызвествлению барабанных перепонок, роговицы, конъюнктивальной оболочки, кожи и сосудов. При развитии гиперкальциемии применение витамина D следует прекратить до нормализации уровня кальция, затем его введение возобновляют, но в меньших дозах.
Удаление паращитовидных желез показано лишь у тщательно отобранных больных с тяжело протекающим вторичным гиперпаратиреозом, устойчивым к проводимому лечению. Показаниями к операции служат выраженные боли в костях, нарушение умственного развития, изнуряющий зуд, переломы, хроническая гиперкальциемия и реже метастатические обызвествления. Операцию выполняют лишь при выраженном повышении в крови уровня паратгормона.
Операцию выполняют лишь при выраженном повышении в крови уровня паратгормона.
Почечная остеодистрофия у детей > Архив — Клинические протоколы МЗ РК
Диагностические критерии
Жалобы и анамнез: субфебрилитет, частые инфекции, боли в ногах, искривление ног, отставание в физическом развитии, нарушение прорезывания зубов, жажду, слабость, недомогание (В).
Физикальное обследование: отставание в физическом развитии, искривление ног по варусному типу, утиная походка.
Лабораторные исследования: выраженная гипофосфатемия, фосфатурия, повышение ЩФ, реже гипокальциемия, аминоацидурия, снижение концентрационной функции почек, анемия (В), при тубулярном ацидозе – метаболический ацидоз, камни в почках.
Инструментальные исследования:
1. УЗИ почек: при первичной остеодистрофии – нормальные размеры почек, при вторичной – уменьшенные.
2. Рентгенография трубчатых костей: рахитоподобные изменения в метаэпифизарной зоне с блюдцеобразным ее расширением, остеопороз.
3. Рентгенография органов брюшной полости: камни в почках и мочевых путях.
Показания для консультации специалистов: ЛОР-врача, стоматолога, гинеколога — для санации инфекции носоглотки, полости рта и наружных половых органов; окулиста — для оценки изменений микрососудов; ортопеда — для решения вопроса оперативной коррекции деформаций костей; уролога — при мочекаменной болезни.
Минимум обследования при направлении в стационар:
1. ОАМ.
2. ОАК.
3. Проба Зимницкого.
4. Креатинин, общий белок, трансаминазы, тимоловая проба и билирубин крови.
5. УЗИ почек.
Перечень основных диагностических мероприятий:
1. УЗИ почек.
2. Допплерография сосудов почек.
3. Измерение АД, учет диуреза.
4. ЭКГ.
5. ОАК, ОАМ, гематокрит.
6. Определение калия, натрия, кальция, магния, фосфора.
7. Определение общего белка, белковых фракций.
8. Определение холестерина, АЛТ, АСТ, билирубина.
9. ИФА на гепатиты.
10. ИФА на паратгормон.
11. Исследование кислотно-основного состояния.
12. Бак посев мочи.
13. Определение щелочной фосфатазы.
14. Определение креатинина, мочевины.
15. Определение глюкозы.
16. Рентгенография и денситометрия трубчатых костей.
Перечень дополнительных диагностических мероприятий:
1. Определение группы крови и резус-фактор.
2. Коагулограмма 1 (протромбиновое время, фибриноген, тромбиновое время, АЧТВ, фибринолитическая активность плазмы).
3. Определение ферритина.
4..jpg) Рентгенограмма грудной клетки.
Рентгенограмма грудной клетки.
Почечная остеодистрофия — лекарства и препараты для лечения заболеваний
В данном разделе собрана информация о лекарственных препаратах, их свойствах и способах применения, побочных действиях и противопоказаниях. На данный момент существует огромное количество медицинских препаратов, но не все они одинаково эффективны.
Каждое лекарство имеет свое фармакологическое действие. Правильное определение нужных лекарств — основной шаг для успешного лечения заболеваний. Для того, чтобы избежать нежелательных последствий перед использованием тех или других лекарств проконсультируйтесь с врачем и прочитайте инструкцию по применению. Обратите особое внимание на взадимодействие с другими лекарствами, а также на условия использования при беременности.
Каждый лекарственный препарат подробно описан нашими специалистами в данном разделе медицинского портала EUROLAB. Для просмотра лекарств укажите интересующие Вас характеристики.Также Вы можете искать нужный Вам препарат по алфавиту.
Поиск препарата
Перечень препаратов для лечения заболеваний категории «Почечная остеодистрофия»
Препараты по назначению(заболевания)
- Этальфа (Раствор для внутривенного введения)
Если Вас интересуют еще какие-нибудь лекарственные средства и препараты, категории “Почечная остеодистрофия” их описания и инструкции по применению, синонимы и аналоги, информация о составе и форме выпуска, показания к применению и побочные эффекты, способы применения, дозировки и противопоказания, примечания о лечении лекарством детей, новорожденных и беременных, цена и отзывы о медикаментах или же у Вас есть какие-либо другие вопросы и предложения – напишите нам, мы обязательно постараемся Вам помочь.
Костные осложнения при заболеваниях почек
Одна из причин заключается в том, что точный диагноз основывается на данных биопсии костной ткани, но, к сожалению, ее выполняют редко, за исключением специальных центров. Морфологические изменения костной ткани, встречаемые при почечной недостаточности, известны как «почечная остеодистрофия». Синдром имеет значение из-за увеличения распространенности почечной остеодистрофии, включения пациентов в программы по диализу с последующим увеличением продолжительности жизни пациентов с хронической почечной недостаточностью, а также вследствие ассоциации почечной недостаточности с повышенной заболеваемостью и преждевременной смертностью. Последнее связано с сосудистыми изменениями, включая эктопические кальцификации. Принят более широкий термин — «минеральное и костное заболевание, связанное с хронической почечной недостаточностью». Этот термин охватывает многие аспекты данного осложнения хронической почечной недостаточности.
Почечную остеодистрофию можно классифицировать по типу костного ремоделирования: низкое, нормальное или высокое; по степени минерализации: нормальная или сниженная; по величине костного объема: низкий, нормальный или высокий. Кроме клеточного компонента, кость состоит из большого количества органического вещества (остеоида) и неорганического матрикса (минерального). Ежегодно происходит оборот около 15% костной ткани. Остеоид, синтезируемый остеобластами, представлен главным образом коллагеном I типа с протеогликанами и другими белками, представленными в относительно небольших количествах, включая фибронектин и остеонектин. Неорганический компонент состоит в основном из кристаллов гидроксиапатита. Кроме количества минерализованной костной ткани (которая определяет МПКТ) и ненарушенной микроструктуры кости, необходим правильный баланс между органическими и неорганическими компонентами для обеспечения нормальных механических свойств (прочность, способность амортизировать удар и способность к деформации). ПТГ и концентрация активного витамина D (1,25-дигидрокси-витамин D3; кальцитриол) служат самыми важными показателями структуры костной ткани и метаболизма кальция. ПТГ поддерживает содержание кальция в плазме путем повышения абсорбции в кишечнике, повышения реабсорбции почками и мобилизации кальция из костной ткани. Избыток ПТГ приводит к повышению ремоделирования костной ткани. Это касается и губчатых, и трубчатых костей. Более 98% активного витамина D3 синтезируется в эпителии проксимальных канальцев почек, и синтез этот снижен у пациентов с почечной недостаточностью. Синтез в норме повышается под действием ПТГ, существует обратная отрицательная связь, посредством которой витамин D3 снижает секрецию ПТГ. Ключевыми показателями, оцениваемыми при биопсии костной ткани, служат объем костной ткани, костное ремоделирование (с использованием двойного связывания с тетрациклином), минерализация остеоидной ткани и отложение металлов (особенно алюминия). Это способствует диагностике некоторых форм заболеваний костей, вызванных почечной недостаточностью.
Заболевание с высокой интенсивностью обмена костной ткани (фиброзно-кистозный остеит)
Оно характеризуется избыточным количеством ПТГ и повышенной активностью остеобластов и остеокластов. Равновесие может быть нарушено в сторону или чрезмерного образования кости, или избыточного распада. Первая ситуация приводит к чрезмерной выработке остеоида и перитрабекулярному фиброзу, которые могут нарушить образование костного мозга. Чрезмерный распад костной ткани может привести к характерному кистозному изменению. Повышенная пористость губчатой кости способствует повышенному риску возникновения переломов. Заболевание обычно носит бессимптомный характер, показатели рутинного биохимического анализа крови в пределах нормы, за исключением повышенной концентрации ПТГ. Увеличение содержания витамина D (активной фракции, действующей на рецепторы витамина D) и кальция (действующего через рецепторы, чувствительные к кальцию) служит мощным стимулом снижения секреции ПТГ. Обе реакции угнетаются при вторичном гиперпаратиреозе, и секреция ПТГ неадекватно высокая. Триггером данного повышения ПТГ, вероятно, служат низкие концентрации кальцитриола. Высокие концентрации фосфатов приводят к связыванию кальция, затем к снижению концентрации ионизированного кальция и соответственно повышению секреции ПТГ. Кроме этого, фосфат может прямо повышать секрецию ПТГ и угнетать 1α-гидроксилазу почек.
Нарушенная минерализация (остеомаляция)
Это прямое следствие субоптимального содержания витамина D, хотя она обычно не носит тяжелый характер, требующий постановки клинического диагноза остеомаляции. В прошлом основным фактором риска было воздействие алюминия, и поскольку сейчас это не так распространено, чистая остеомаляция становится менее характерной для хронической почечной недостаточности.
Смешанная почечная остеодистрофия
Симптомы избытка ПТГ сочетаются с нарушенной минерализацией, обусловленной относительной недостаточностью витамина D.
Адинамическая болезнь кости (состояние низкого оборота костной ткани)
Это противоположная сторона состояния, наблюдаемого при избытке ПТГ, и особенно она характерна для пациентов пожилого возраста и лиц с сахарным диабетом. По данным анализа биопсийных образцов, она встречается с частотой до 50%. Адинамическая болезнь кости больше всего характерна в тех случаях, где существует избыточная терапия препаратами кальция и витамина D, после паратиреоидэктомии или при алюминиевой интоксикации. Адинамическая болезнь кости представлена снижением объема остеоида и очень небольшими признаками активности остеобластов или остеокластов, а также отсутствием связывания с тетрациклином. Данное заболевание ассоциировано с повышенным риском возникновения переломов, костной боли и эктопической кальцификации. При адинамической болезни костей минерализация костной ткани нормальная.
Обследование должно включать определение сывороточного ПТГ, кальция (откорректированного по концентрации альбумина или ионизированного), фосфата, ЩФ и бикарбонатов плазмы, а также визуализацию очагов кальцификации в мягких тканях. В то время как точный диагноз почечной остеодистрофии требует проведения биопсии кости, широкое применение данного метода ограничено вследствие его инвазивности, необходимости длительной подготовки пациента с применением двойной тетрациклиновой метки и возможности интерпретации лишь в специализированных центрах. ПТГ — единственный наиболее приемлемый биомаркер, его концентрация повышена при усилении костного ремоделирования. Место маркеров костного ремоделирования в диагностике не установлено, хотя они могут помочь в мониторинге эффектов проводимого лечения. Маркеры образования костной ткани включают остеопротегерин, общую и специфичную для костной ткани ЩФ, остеокальцин и проколлаген I типа с карбоксиконцевым пептидом. К маркерам резорбции костной ткани относят пиридинолин и деоксипиридинолин, тартрат-резистентную кислую фосфатазу (TRAP) и проколлаген I типа с перекрестно связанным карбоксиконцевым пептидом.
Определение МПКТ полностью не коррелирует с риском переломов. Дистальный отдел лучевой кости служит предпочитаемым местом определения МПКТ при хронической почечной недостаточности. Проблема заключается в том, что низкая МПКТ не обязательно указывает на остеопороз и, следовательно, на необходимость антирезорбтивной терапии. Биопсия кости показана, когда биохимические проявления трудно интерпретировать, когда манифестирует перелом или костная боль и когда они не могут быть объяснены при помощи неинвазивных методов, при возможности алюминиевой интоксикации и в случаях, когда имеется выраженная и прогрессирующая кальцификация сосудов. Гистоморфометрия кости использует показатели ремоделирования, минерализации и объема для классификации почечной остеодистрофии (классификация TMV). Биопсию обычно берут из гребня подвздошной кости. Применение двух курсов тетрациклина в течение 4 нед до проведения биопсии позволит оценить образование костной ткани и степень минерализации.
В целом метаболические аномалии, приводящие к нарушению морфологии кости и кальцификации сосудов, не встречаются до тех пор, пока СКФ не снизится ниже 60 мл/минх1,73 м2. Однако эти костные и сосудистые изменения наблюдаются у детей и молодых взрослых при более легком снижении СКФ (<90 мл/минх1,73 м2). Следует проявлять осторожность в диагностике чистого остеопороза у пациента с почечной недостаточностью. При рутинном скрининге кальцификацию сосудов лучше всего выявлять с помощью простой рентгенограммы брюшной полости в боковой проекции, определяя кальцификацию аорты. КТ дает более точную информацию; описаны количественные методы в исследовательских целях, но рутинное применение КТ в настоящее время неоправдано.
Высокие концентрации фосфатов можно снизить с помощью эффективной почечной заместительной терапии (диализ или трансплантат), хотя ответ на диализ часто неполный. Следует ограничить поступление фосфатов с пищей. Многим пациентам необходимо лечение препаратами, связывающими фосфаты. Употребление до еды препарата алюкап (алюминия гидроксидр) очень эффективно, но при длительном применении существует риск токсических эффектов на костную ткань и головной мозг. Препараты кальцикью, тайтралакр и фосс-Экс (кальция ацетат) — кальцийсодержащие фосфатсвязывающие лекарственные средства, которые принимают за 15 мин до еды. Севеламер стали применять недавно, это фосфатсвязывающий препарат, не содержащий ни алюминия, ни кальция. Необходимо провести адекватное лечение витамином D. Поскольку существует проблема образования в почках активного 1,25-дигидрокси-витамина D3, обычно требуется применение активного аналога витамина D, например альфакальцидола. Цинакалцет — агонист кальция, действующий на кальций-чувствительный рецептор в клетках паращитовидных желез, приводит к снижению секреции ПТГ. Препарат относительно дорогой, но эффективный. Хирургическое удаление паращитовидных желез показано пациентам с очень высокими значениями ПТГ.
Результаты последних исследований
Получены новые данные, что у многих пациентов могут быть скрытые незначительные аномалии при ранней стадии нарушения функции почек, и эти аномалии играют роль в прогнозе. Левин (Levin) и соавт. изучили 1814 пациентов с различной степенью нарушения функции почек. Субоптимальные значения витамина D (<22 пг/мл) были у 13% пациентов с установленной СКФ >80 мл/мин и у более 60% с СКФ <30 мл/мин. Высокая концентрация ПТГ была характерна даже для пациентов с легкой почечной недостаточностью (СКФ >80 мл/мин).
У пациентов с заболеванием почек кальцификация сосудов приводит к структурным изменениям в сосудистой стенке и усиленному атерогенезу. Однако пациенты с бессимптомным гиперпаратиреозом могут иметь незначительные нарушения функции сосудов, которые способствуют развитию макрососудистых состояний. Эти нарушения включают инсулинорезистентность, активацию эндотелия и повышение ригидности артерии. У пациентов с бессимптомным течением заболевания изменения толерантности к глюкозе быстро не прогрессируют. Фалло (Fallo) и соавт. показали повышение концентраций растворимого Е-селектина и фактора VIII фон Виллебранда у пациентов с гиперпаратиреозом. Эти показатели предоставляют данные об активации эндотелия и могут помочь оценить сердечно-сосудистый риск до и после лечения гиперпаратиреоза.
Нарушения минерального обмена способствуют развитию инсулинорезистентности и сахарного диабета II типа. С другой стороны, лечение сахарного диабета может повлиять на состояние костной ткани и минерального обмена. Тиазолидиндионы (росиглитазон и пиоглитазон) широко используют при лечении сахарного диабета II типа. В костной ткани эти препараты усиливают адипогенез и снижают дифференцировку остеобластов. Именно поэтому вызывает беспокойство, что они могут предрасполагать к развитию остеопороза. Недавно полученные данные свидетельствуют, что применение глитазоновых препаратов может снизить МПКТ. Необходимо определить, обусловливает ли это повышенный риск переломов.
Термин «почечная остеодистрофия» имеет ограниченное применение в рутинной клинической практике, поскольку это состояние можно диагностировать и классифицировать только по результатам биопсии костной ткани. В настоящее время маркеры костного ремоделирования не могут специфически диагностировать костные осложнения хронической почечной недостаточности. Кальцификация сосудов служит важным маркером риска у пациентов с заболеванием почек и представляет часть метаболического нарушения, которое также приводит к поражению костей. Биохимические изменения метаболизма кальция, фосфата, витамина D и ПТГ появляются, когда установленная СКФ падает ниже 40 мл/мин, но незначительные изменения могут наблюдаться при почечной недостаточности легкой степени. У вышеуказанного пациента необходимо оценить содержание кальция и витамина D. Наличие почечной недостаточности означает, что терапия бисфосфонатами ему не показана без более детального определения основного статуса костной ткани. Добавление витамина D может снизить уровни ПТГ и, таким образом, костное ремоделирование. Низкая МПКТ в данном случае подтверждает сниженный минеральный состав костей, но может отражать недостаточность витамина D и повышение синтеза ПТГ, а не просто первичный остеопороз.
Дистрофия почек: причины, патогенез и клиника
Терминоэлемент «дистрофия» является производным двух терминов и в переводе означает нарушение обмена. Оно затрагивает большое количество органов. Особенно это касается тех из них, которые играют важную роль в обмене веществ. Не даром дистрофия почек может служить маркером многих подобных заболеваний.
Краткая анатомо-физиологическая характеристика почек
Почки являются парными органам. Внешне они напоминают форму плода бобовых. Расположены с обеих сторон от позвоночника, в области 11−12 грудных и 1−2 поясничных позвонков. Средний размер органа не превышает 12 см в длину и 3−5 см в толщину. Их вогнутые поверхности обращены к позвоночному столбу, соответственно, выпуклые — от него.
Каждая почка состоит из нескольких слоев плотной ткани.
- Соединительнотканная капсула. Она покрывает практически весь орган. В области синуса (расположен практически по центру стороны, обращенной к позвоночнику) она переходит в оболочку мочеточника. Там же в почку входят два крупных сосуда. Это почечные вена и артерия.
- Корковое вещество находиться непосредственно под капсулой. Сразу под ним залегает мозговое вещество. Оно содержит нефроны. От мозгового вещества, по направлению к синусу отходят отростки. Здесь находятся кровеносные и лимфатические сосуды. На разрезе цвет коркового, мозгового веществ и отростков одинаков. Поэтому их считают единой анатомической структурой.
- Практически в центре органа, между отростками залегают так называемые почечные пирамиды. Названы так за свою трапециевидную форму. Основание направлено к корковому веществу, а верхушка — в сторону синуса.
- Почечные чашечки. Полости в которые переходят пирамиды. Они открываются в лоханку, из которой, в свою очередь, выходит мочеточник.
Основное функционирование почек можно представить следующим образом. Почечная артерия после «входа» в орган начинает ветвиться на несколько ветвей. Они проходят в ткани отростков и проникают в мозговое вещество. Здесь они еще делятся на более мелкие сосуды до размеров артериол, которые идут в нефрон. Там за счет еще более мелкого ветвления они образуют сосудистый клубок. Благодаря плотному его окружению специальными клетками (подоцитами) здесь происходит первичная фильтрация крови. Дальше в венулы походят только клетки крови, часть плазмы и некоторые белки.
Все остальное, а это шлаки, электролиты, углеводы, липиды и некоторые протеины задерживаются фильтрами подоцитов и вместе с частью плазмы попадают в канальцы нефрона. Это называется первичной мочой. Она скапливается в чашечке Боумена-Шумлянского, которая полукругом окружает сосудистый клубочек. Ее основание — это начало почечного канальца. По нему первичная моча попадает в каналец, который достаточно длинный, что идет из мозгового вещества в пирамиды. Здесь он делает петлю и «поднимается» в мозговое вещество.
На всем пути он густо окутан венозными сосудами, идущими из выносящего сосуда. Это необходимо для реабсорбции (обратного всасывания) белков, липидов, углеводов, некоторых электролитов и воды. В результате чего из канальцев в почечную чашечку попадают только шлаки, электролиты и часть воды. Это называется вторичной мочой. Она идет в лоханку, откуда выводится по мочеточнику.
Это важно! У человека в норме образуется до 180 литров первичной мочи в день. Из этого количества реабсорбируется около 90−95%. Таким образом, ежесуточный объем вторичной мочи не превышает 2-х литров. Можно только представить какое количество органических молекул проходит через почки. Данное обстоятельство дает наглядное объяснение, почему нарушение обмена веществ часто сказывается на почках.
Механизмы и причины дистрофии
Общим для всех видов дистрофий является начальный этап развития. Он заключается в следующем:
- Нарушение обмена группы молекул.
- Избыточное накопление данных молекул в клетках органа.
Дальнейший механизм различается в зависимости от конкретного вида дистрофии. Но об это будет сказано ниже. Что касается причин развития дистрофий, они разделяются на две большие группы.
- Врожденные дистрофии. Обусловлены генетическими и/или врожденными дефектами на любом этапе метаболизма вещества: от синтеза, до распада. Для почек, из врожденных дистрофий больше всего характеристика нарушения белкового и жирового обменов.
- Приобретенные дистрофии возникают в результате нарушения любого этапа метаболизма вещества под действием внешних причин. Наиболее вероятными причинами считаются вирусные инфекции, хронические бактериальные инфекции, облучение, хронические интоксикации, а также некоторые заболевания. К ним относят сахарный диабет, некоторые новообразования, травмы.
Виды дистрофии
Это важно! Все дистрофии почек могут разделятся в зависимости от причин появления и конкретного вещества. В первом случае данные заболевания делятся на врожденные и приобретенные дистрофии. Но более правильным с точки зрения практической медицины считается разделение дистрофий по видам веществ.
Согласно вышеописанному положению дистрофии делятся на три категории:
- Диспротеинозы. Это дистрофии вызванные нарушением обмена белков. Они могут быть как врожденными, так и приобретенными. Для почек характерны следующие виды:
- Зернистая дистрофия. Она развивается в результате внутриклеточного отека и выхода белка в цитоплазму. Но так как белок является не растворимым веществом, то в цитоплазме он образует своеобразные «зерна». Поэтому зернистая дистрофия почек и получила свое название.
- Гиалиново-капельная дистрофия. Является результатом дальнейшего развития первого вида. Здесь, белковые молекулы в результате значительного накопления начинает соединятся в своеобразные «капли» хрящеподобной консистенции и цвета. По своей структуре эти белковые образования напоминают гиалин — основной белковый «строительный материал» хрящей. Это обстоятельство объясняет почему гиалиново капельная дистрофия почек получила такое название.
- Роговая дистрофия. Развивается при избыточном накоплении кератина. Этот бело в норме характерен только для эпителиальных клеток. Но в случае постоянного воздействия на не эпителиальную клетку повреждающего фактора из фибрилл цитоплазмы начинается «сборка» молекул кератина.
- Гидропическая дистрофия. Особый вид белковых дистрофий. Она возникает при чрезмерном увеличении водяных вакуолей клетки. Чаще всего в клетке встречается одна гигантская вакуоль, содержащая прозрачную жидкость. При этом остальных органелл практически нет. В том числе отсутствует ядро, которое разрушается этой вакуолью. Основная причина дистрофии — вирусная инфекция. Для структур почек данный вид более всего характерен для канальцев. Однако гидропическая дистрофия эпителия канальцев почки здесь обусловлена не столько вирусной инфекций, но хроническим воспалением вообще.
- Жировые дистрофии или липидозы. Встречаются несколько реже. Причем, они часто носят приобретенный характер, чем белковые. Для которых в одинаковой степени характерен тот и другой варианты. И одним из главных факторов жировой дистрофии считается ишемия — недостаток кислорода. Об этом хорошо свидетельствует тот факт, что жировая дистрофия почек часто наблюдается при хронических инфекциях и интоксикации некоторыми неорганическими веществами: мышьяк, висмут, ртуть, а также хроническом алкоголизме.
- Углеводные дистрофии менее характерны для почек. Это во многом связано с тем, что почки играют малую роль в обмене углеводов. Однако при некоторых заболеваниях углеводная дистрофия почек может встречаться достаточно часто. В ее основе лежит отложение молекул углеводов при их избытке. Самым ярким примером данного вида дистрофии является сахарный диабет.
Почечная остеодистрофия | патология | Britannica
Почечная остеодистрофия , также называемая почечный рахит , хроническое, вероятно наследственное заболевание, характеризующееся дисфункцией почек, минеральной потерей костной массы и деформациями типа рахита, кальцификациями в аномальных местах и гиперактивностью паращитовидных желез. Потеря кальция и задержка фосфора происходят из-за неправильной работы почек; это вызывает перепроизводство паратгормона, что приводит к деминерализации хорошо сформированных костей и неспособности кальцифицировать вновь развивающуюся кость.Костные аномалии развиваются медленнее, чем почечная недостаточность; если последнее тяжелое, смерть может наступить в детстве до того, как станут очевидными аномалии скелета. Если почечная недостаточность не тотальная, это может вызвать карликовость и частые переломы у детей; у взрослых наблюдается постепенное размягчение и искривление костей. Вторичный гиперпаратиреоз, тип почечной остеодистрофии, может быть приобретенным заболеванием, обнаруживаемым у лиц с хронической почечной недостаточностью. Хотя влияние приобретенного заболевания на метаболизм костей более ограничено, чем влияние наследственной почечной остеодистрофии, из-за его начала в позднем возрасте оно вызывает аналогичные изменения в метаболизме кальция и фосфора и деминерализации костей с течением времени.
Британская викторина
Болезни, расстройства и многое другое: медицинская викторина
Какое состояние вызвано отложением солей мочевой кислоты? Как еще называют переломную лихорадку? Узнайте, что вы знаете о болезнях, расстройствах и многом другом.
Лечение остеодистрофии почек зависит от состояния химического баланса пациента.Трансплантация почки была успешной в некоторых случаях, связанных с тяжелой дисфункцией почек, а удаление неисправных паращитовидных желез иногда эффективно для контроля симптомов.
почечная остеодистрофия — это … Что такое почечная остеодистрофия?
Почечная остеодистрофия — Инфобокс Название заболевания = Почечная остеодистрофия Заголовок = ЗаболеванияDB = ICD10 = ICD10 | N | 25 | 0 | n | 25 ICD9 = ICD9 | 588.0 ICDO = OMIM = MedlinePlus = eMedopic Radio = 500 D012080 Почечная остеодистрофия — это патология костей,…… Wikipedia
Почечная остеодистрофия — Комбинация заболеваний костей, обычно вызываемых хронической почечной недостаточностью (заболевание почек).Также может возникать из-за нарушения функции почек при рождении (врожденное). При отказе почек смерть неминуема, если не будет проведен диализ.…… Медицинский словарь
почечная остеодистрофия — ▪ патология, также называемая хроническим почечным рахитом, вероятно наследственное заболевание, характеризующееся дисфункцией почек, минеральной потерей костной массы и деформациями типа рахита, кальцификациями в аномальных местах и гиперактивностью околощитовидных желез… Универсальный
Остеодистрофия — Классификация и внешние ресурсы МКБ 10 Q78.9 МКБ 9 756,50… Википедия
почечный рахит — n ПОЧЕЧНАЯ ОСТЕОДИСТРОФИЯ * * * рахит, встречающийся у детей и вторичный по отношению к почечной дисфункции, связанной с гиперфосфатемией; этот термин также используется более свободно как синоним почечной остеодистрофии… Медицинский словарь
Почечная недостаточность — Классификация и внешние ресурсы МКБ 10 N17 N19 МКБ 9… Википедия
остеодистрофия — дефект костного образования.SYN: остеодистрофия. [osteo + G. dys, сложный, несовершенный, + trophe, питание] Наследственная Олбрайт o. наследственная форма гиперпаратиреоза, связанная с внематочной… Медицинский словарь
остеодистрофия — н. любое генерализованное заболевание костей, возникшее в результате нарушения обмена веществ. При почечной остеодистрофии хроническая почечная недостаточность приводит к диффузным изменениям костей в результате остеомаляции, вторичного гиперпаратиреоза (чрезмерная секреция паращитовидных желез…… Новый медиаакальный словарь
почечная карликовость — карликовость в результате хронической почечной недостаточности, например, почечной остеодистрофии… Медицинский словарь
Остеодистрофия почек — Нарушение роста костей, вызванное хронической почечной недостаточностью (заболевание почек).Также… Медицинский словарь
остеодистрофия — существительное нарушение развития костей; обычно связано с заболеванием почек или нарушениями обмена кальция и фосфора • Гиперонимы: ↑ дистрофия… Полезный английский словарь
ПОЧЕЧНАЯ ОСТЕОДИСТРОФИЯ
ПОЧЕЧНАЯ ОСТЕОДИСТРОФИЯ
ПОЧЕЧНАЯ ОСТЕОДИСТРОФИЯ
Брайан Дж. МакГинли, доктор медицины, ординатор отделения ортопедической хирургии
С.Джей Кумар, доктор медицины, лечащий врач ортопедической хирургии
21 сентября 1995
ПРЕДСТАВЛЕНИЕ КЛИНИЧЕСКОГО ДЕЛА
ОРТОПЕДИЧЕСКОЕ ОТДЕЛЕНИЕ
ИНСТИТУТ АЛЬФРЕДА И. ДЮПОНА
УИЛМИНГТОН, Делавэр
История болезни:
Дж. Г. — 14 3/12 лет. мальчик, который пожаловался на боль в
правая нога в течение 9 месяцев и возникшая контрактура правого колена
за этот период.В анамнезе нет серьезных травм. Родился 3 недели
недоношенный с двусторонней гипоплазией почек и судорожным расстройством. Три
трансплантация почек не удалась, и в настоящее время он получает перитонеальный диализ
четыре раза в день. Задержка роста и задержки в развитии в детстве
включают низкий рост, стояние в 16 месяцев и ходьбу в 2 года. Он
перенес перелом правой голени и малоберцовой кости за 6 лет до обращения
после минимальной травмы.
ФИЗИЧЕСКИЙ ОБСЛЕДОВАНИЕ: 5 футов 4 дюйма. Плохой зубной камень, правое колено сгибается на 15 градусов.
контрактура, болезненный диск правого бедра и колена.
РАДИОГРАФИЧЕСКАЯ ОЦЕНКА: Остеопения, субкортикальная резорбция,
прозрачные метафизарные полосы,
расширение метафиза и «позвоночник рюггер-джерси».
ЛЕКАРСТВО: Карбонат кальция и ацетат кальция
ПАТОФИЗИОЛОГИЯ:
Хроническая почечная недостаточность часто приводит к вторичному гиперпаратиреозу.Стимулом к повышению уровня ПТГ является гипокальциемия, ацидоз, снижение уровня витамина 1,25 (ОН).
D и гиперфосфатемия.
КЛИНИЧЕСКИЕ НАХОДКИ:
Задержка роста и деформации костей, включая искривление нижних конечностей
в амбулаторных. Рахитические четки и выступающее расширенное нижнее лицо из-за
к разрастанию нижней челюсти и верхней челюсти. Боль в костях с переломом или без него.
Внематочные кальцификации конъюнктивы и кожи.Соскальзывание бедренной кости
также может возникать эпифиз.
РАДИОГРАФИЯ:
Ранний — Остеопения
Истончение коры и трабекул дает рентгеновский снимок «матового стекла»
Череп из соли и перца
Утолщение и истирание метафиза, без образования чашечек
Поздняя оссификация эпифизов
Epiphyseal Slips — дошкольный возраст: проксимальный и дистальный бедренный и дистальный
большеберцовая
Дети старшего возраста: проксимальный отдел бедра и дистальный отдел предплечья
Поздний — вторичный гиперпаратиреоз
Поднадкостничная кортикальная резорбция — Дистальная фаланга, конец ключицы,
седалищная кость, лобковая кость, SI суставы, метафизарно-диафизарный переход длинных костей
Lucent метафизарные полосы — изменения зоны роста — лучший индикатор
степени тяжести вторичного гиперпаратиреоза
Искривление длинных костей
Rugger Jersey spine — Остеосклероз замыкательных пластинок позвоночника.
кузова
Коричневая опухоль (редко) — ребро или челюсть
Амилоидоз — Множественные кисты костей: пястные кости, бедро, запястье, проксимальная плечевая кость,
лобковые ветви и проксимальный отдел голени.
ЛАБОРАТОРИИ:
- Мочевина повышенная
- Фосфат повышенный
- Щелочная фосфатаза повышенная
- Повышенный PTH
- Пониженное содержание кальция
- Пониженный pH
ЛЕЧЕНИЕ:
ЗАДАЧИ:
- Поддерживайте нормальный уровень кальция и фосфата, избегайте экстраскелетных
кальцификации и избегайте накопления алюминия или железа.
ПЛАН:
- Уменьшить количество фосфатов в рационе (нл. С 1000-1800 мг / день до 400-800 мг / день)
- Фосфатные связующие — соединения алюминия (избегать длительного использования), кальций
Карбонатные (гиперкальциемия, диарея, метаболический алкалоз) побочные эффекты уменьшились
с 4-14г / сут.
- Витамин D 100000-200000 МЕ / день — Следите за уровнем кальция и рентгеном
для нормализации 50 000 I.Ед. 3 раза в неделю.
- Кальцитриол (1,25 (OH) Vit D) эффективен при уменьшении боли в костях, заживлении
и сила мышц
- Снижение щелочной фосфатазы и ПТГ. Избегайте гиперкальциемии. Доза 0,25-1,5 мкг / сут.
Поддерживайте уровень кальция на уровне 10,5-11.
ЛЕЧЕНИЕ:
- При интоксикации алюминием требуется дефероксамин 0,5–1 г в неделю в течение 4–10 месяцев.
Следить за инфицированием Rhizopus или Yersinia
- Бикарбонат натрия и бикарбонат кальция для коррекции ацидоза.
- Гиперпаратиреоидэктомия при гиперкальциемии> 11,5, экстраскелетные кальцификации,
скелетные боли и кожный зуд. Необходимо исключить другие причины.
- Отложить хирургическое вмешательство до завершения лечения
- Пиннинг SCFE предпочтительнее консервативного лечения.
существует противоречие
- Гормон роста
ПРОГНОЗ:
Улучшение прогноза при диализе и трансплантации привело к длительному
жизнь у этих пациентов.Лечение остеодистрофии агрессивными фармакологическими средствами.
вмешательство может привести к более нормальному росту и активности.
ССЫЛКИ:
- Тачджян МО: Почечная остеодистрофия. В детской ортопедии. 2-е издание.
Эд. Тачджян, штат Миссури, Филадельфия: W.B. Компания Saunders.1990
- Goodman WG et al. Почечная остеодистрофия у взрослых и детей. В Primer
по метаболическим заболеваниям костей и нарушениям минерального обмена.2-й
издание. Эд. Favus MJ. Нью-Йорк: Raven Press. 1993.
- Kaplan FS et al. Почечная остеодистрофия. В ортопедической фундаментальной науке.
Эд. Саймон СР. Американская академия хирургов-ортопедов. 1994 г.
- Hruska KA, Teitelbaum SL. Почечная остеодистрофия: обзорная статья. N Eng.
J of Med.

 Поликистоз почек, синдром Альпорта и врожденная гипоплазия часто осложняются почечной недостаточностью с развитием метаболической остеопатии. Для этих патологий типичен отягощенный семейный анамнез. Частота встречаемости 0,5-3%. В большинстве наблюдений клинические проявления остеодистрофии присутствуют с детства (почечный рахит).
Поликистоз почек, синдром Альпорта и врожденная гипоплазия часто осложняются почечной недостаточностью с развитием метаболической остеопатии. Для этих патологий типичен отягощенный семейный анамнез. Частота встречаемости 0,5-3%. В большинстве наблюдений клинические проявления остеодистрофии присутствуют с детства (почечный рахит).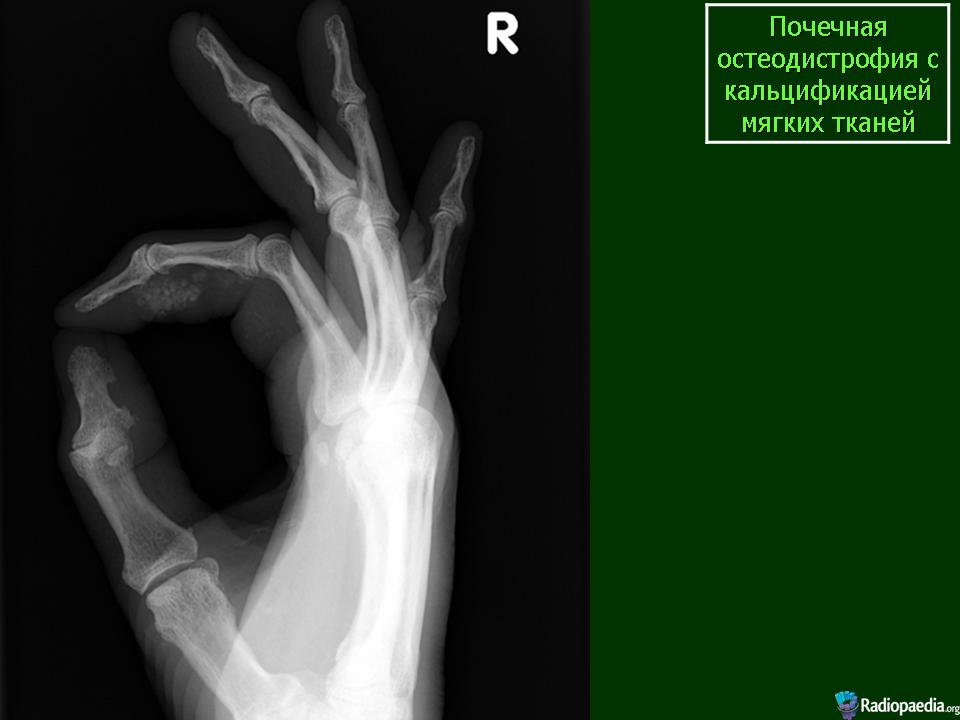 Остеодистрофия сочетается с серьезными осложнениями со стороны сердечно-сосудистой системы, сопряженными с высокой летальностью.
Остеодистрофия сочетается с серьезными осложнениями со стороны сердечно-сосудистой системы, сопряженными с высокой летальностью.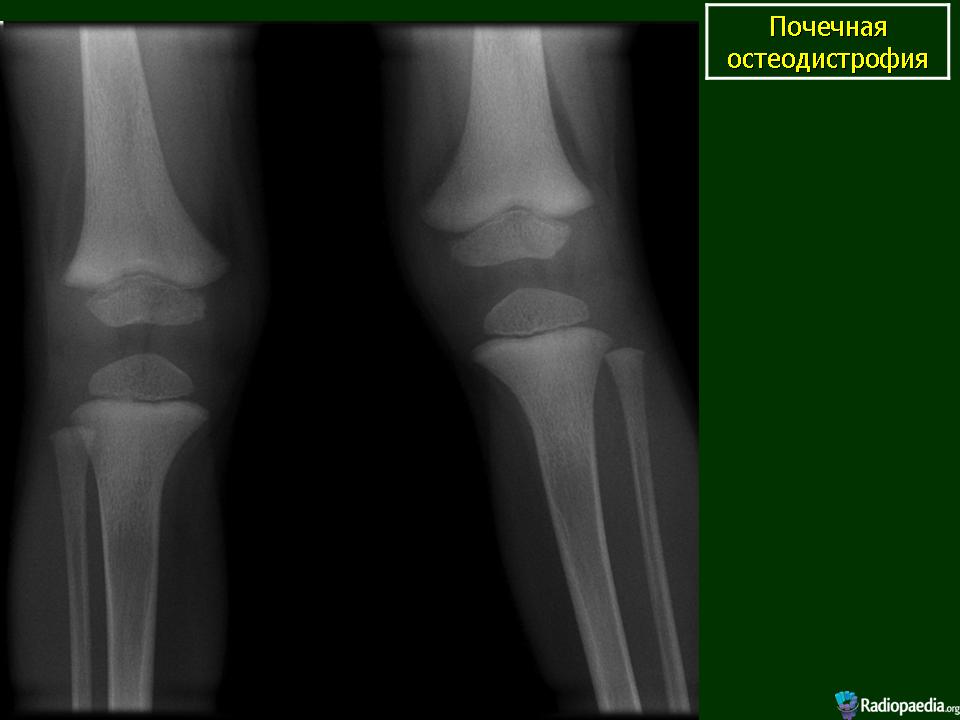 При двустороннем поражении присоединяется ХБП, запускающая процессы остеодистрофии.
При двустороннем поражении присоединяется ХБП, запускающая процессы остеодистрофии.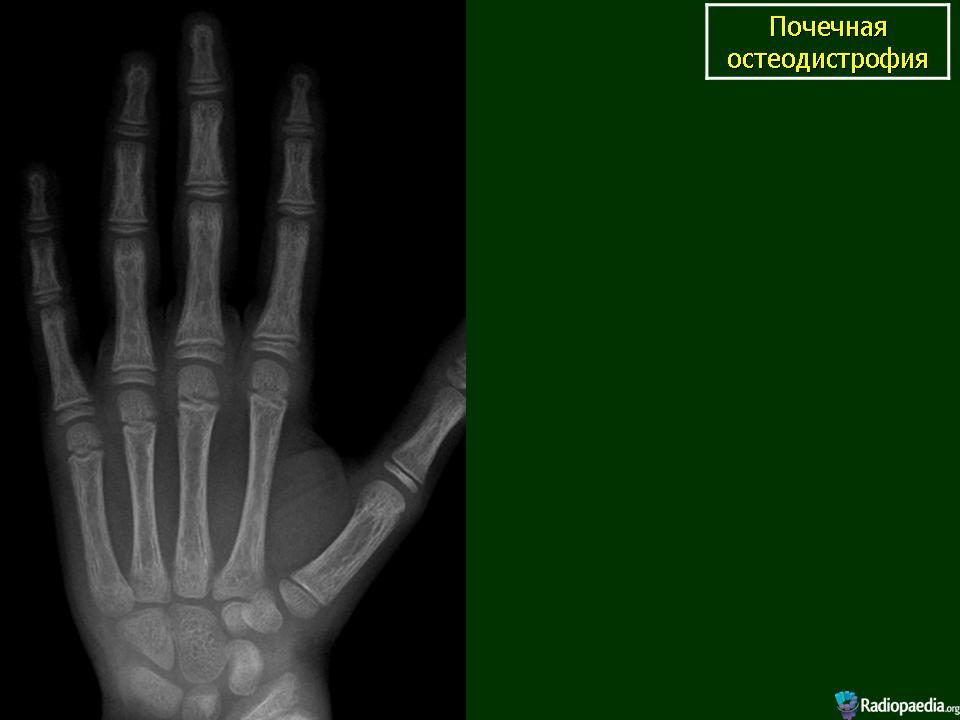 Клинические проявления включают фиброзный остеит, вторичный гиперпаратиреоз. Другое название – гиперпаратиреоидная болезнь костей.
Клинические проявления включают фиброзный остеит, вторичный гиперпаратиреоз. Другое название – гиперпаратиреоидная болезнь костей. Из-за лучевой нагрузки методика имеет ограничения по количеству исследований, особенно в детском возрасте.
Из-за лучевой нагрузки методика имеет ограничения по количеству исследований, особенно в детском возрасте. Оценка костного метаболизма позволяет судить о степени ремоделирования ткани. Уровень Са обычно низкий, сывороточный Р выше нормы (зависит от стадии ХБП). Щелочная фосфатаза повышена из-за остеобластической активности. Лучшим неинвазивным вариантом диагностики подтипов почечной остеодистрофии является определение уровня ПТГ для оценки костного метаболизма.
Оценка костного метаболизма позволяет судить о степени ремоделирования ткани. Уровень Са обычно низкий, сывороточный Р выше нормы (зависит от стадии ХБП). Щелочная фосфатаза повышена из-за остеобластической активности. Лучшим неинвазивным вариантом диагностики подтипов почечной остеодистрофии является определение уровня ПТГ для оценки костного метаболизма.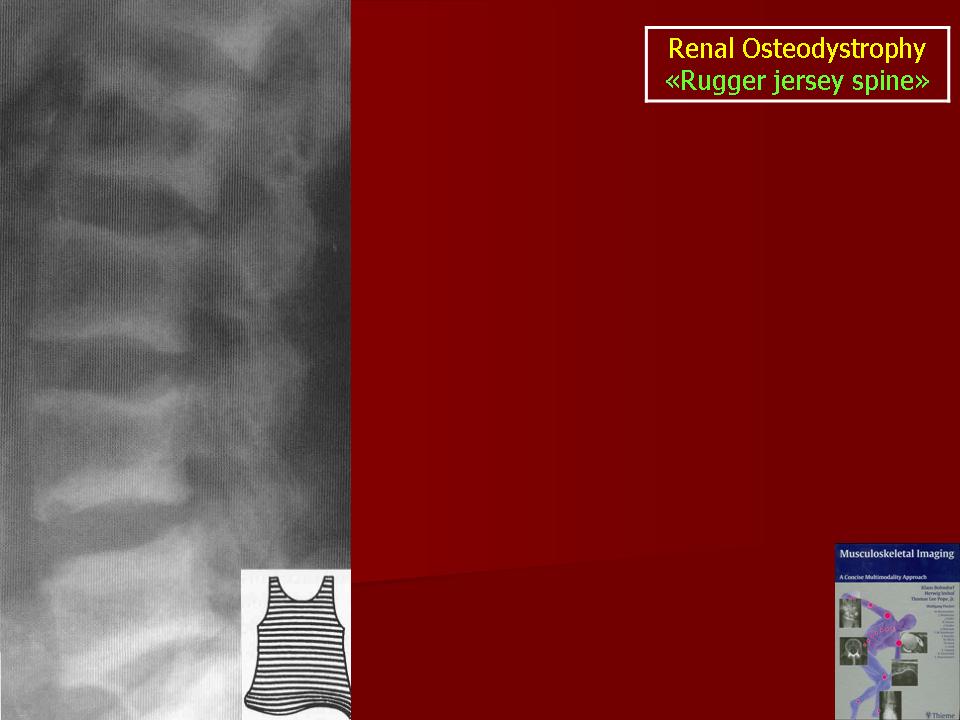 На фоне приема уменьшается болевой синдром, усиливается минерализация костной ткани, особенно при фиброзно-кистозном остите.
На фоне приема уменьшается болевой синдром, усиливается минерализация костной ткани, особенно при фиброзно-кистозном остите.