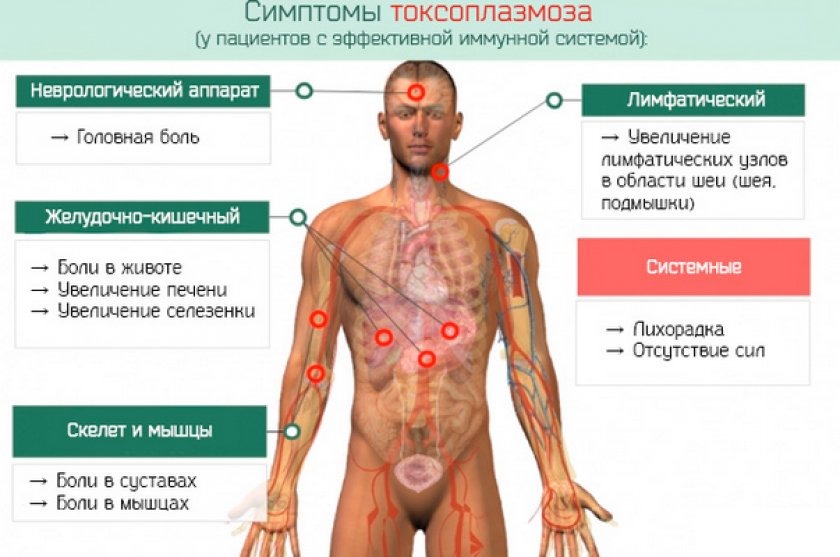
Симптомы токсоплазмоза у человека, признаки и диагностика поражения
Токсоплазмоз — паразитарное заболевание, вызванное простейшими. В организм человека возбудитель попадает из каловых масс кошек, после употребления плохо обработанного мяса, при переливании инфицированной крови, а также вертикальным способом — от матери к ребенку внутриутробно.
Патология довольно редко протекает в острой форме или имеет значительное влияние на состояние здоровья человека — большинство пациентов даже не догадываются об инфекции. Но существует обстоятельство, когда токсоплазмоз крайне опасен — это беременность. Заражение во время вынашивания ребенка очень опасно — возбудитель способен стать причиной необратимых изменений в организме ребенка, вызвать его гибель еще до рождения.
Что такое токсоплазмоз? Характеристика заболевания
Токсоплазмоз вызывает одноклеточный простейший организм со сложным жизненным циклом. Человек чаще всего заражается паразитами после контакта с инфицированными кошками или их калом (питомцы заражаются после поедания грызунов). Попав в человеческое тело, токсоплазмы разносятся по сосудам или оседают в тканях органов, мышцах. Их скопление вызывает разрушение клеток тела, образование полостей (цист, псевдоцист, кальцинатов).
Попав в человеческое тело, токсоплазмы разносятся по сосудам или оседают в тканях органов, мышцах. Их скопление вызывает разрушение клеток тела, образование полостей (цист, псевдоцист, кальцинатов).
Токсоплазмоз классифицируют в зависимости от способа заражения:
- Приобретенный — инфицирование происходит после рождения. Чаще всего протекает незаметно, без выраженной симптоматики, не приносит дискомфорта (хронический тип). Реже встречается острая форма — отличается заметными симптомами.
- Врожденный — внутриутробное инфицирование плода. Заражение может стать причиной недоразвитости плода, уродств, инвалидности или смерти.
Паразиты могут локализоваться в разных частях человеческого организма.
В зависимости от зоны их жизнедеятельности выделяют типы болезни:
- Кардиологический — поражение сердечной мышцы, сопровождается соответствующей симптоматикой: слабость, боли в грудине, одышка.
- Лимфонодулярный — поражение лимфатических узлов (их увеличение и болезненность при пальпации).

- Офтальмологический — нарушения зрительной функции, поражение глаз при токсоплазмозе.
- Менингоэнцефалический — нарушения нервной системы. Самый заметный признак — систематические головные боли.
- Генерализованный — с одновременным поражением нескольких систем органов.
Заболевание имеет разные симптомы, зависящие от локации паразитов, и поэтому заподозрить его очень сложно. При хроническом протекании носитель может без дискомфорта жить, не догадываясь о болезни.
Причины и развитие токсоплазмоза
Существуют пути передачи токсоплазмоза:
- При контакте с кошкой — простейшие в большом количестве содержатся в фекалиях животных, могут переноситься на шерсть, продукты питания, предметы мебели.
- При поедании недостаточно хорошо обработанного зараженного мяса.
- При переливании крови от донора, инфицированного токсоплазмами.
- При пересадке зараженных внутренних органов.
- Внутриутробная инвазия — плод инфицируется от болеющей матери.

Патология протекает незаметно у людей со сформированным иммунитетом, а в случае ослабленной защиты организма, инфекция может дать знать о себе ярко выраженными симптомами. Дефекты иммунитета могут быть вызваны такими серьезными болезнями, как СПИД, онкологические образования. Также активно проявляется болезнь у детей, при внутриутробной инвазии или приеме лекарств, подавляющих работу иммунной системы.
При попадании простейших в организм человека, они переносятся по сосудам в мышечные ткани и органы тела или же оседают в определенной локации. Скапливаясь, они разрушают клетки, образуют цисты, псевдоцисты и кальцинаты (умершие паразиты в твердой оболочке, образующейся после контакта с солями кальция).
Чем опасен токсоплазмоз? Иммунитет к болезни
Для здорового взрослого человека токсоплазмы не опасны. Инвазия остается незамеченной, не наносит повреждений, которые отобразились бы на самочувствии заболевшего или функционировании внутренних органов.
Опасность существует лишь в случаях:
- При беременности — внутриутробное заражение наиболее опасно — плод может получить увечья еще до рождения или погибнуть.
- При тяжелых патологиях, угнетающих иммунитет — у больных СПИДом, пациентов с онкологическими опухолями, а также перенесших агрессивное лечение препаратами, подавляющими естественную защиту организма.
При опасном протекании токсоплазмоза, возбудитель может вызвать необратимые изменения в организме или даже стать причиной инвалидности, летального исхода.
Опасность токсоплазмоза может выражаться в изменениях в организме:
- Паралич отдельных участков тела.
- Кома.
- Частичная потеря чувствительности.
- Спонтанный выкидыш, замирание плода.
- Слепота.
- Глухота.
- Воспалительные процессы в сердце, легких с последующей остановкой их работы (что становится причиной смерти пациента).
При внутриутробном заражении ребенок часто погибает в короткие сроки после рождения или же имеет патологии, существенно влияющие на его развитие и жизнедеятельность.
При перенесении токсоплазмоза формируется стойкий иммунитет на всю жизнь и в дальнейшем можно не бояться этой болезни даже при стремительном снижении иммунитета или при беременности.
Общие симптомы токсоплазмоза
Признаки заболевания очень обширны и зависят от степени развития патологии, ее локации в организме человека.
К общим симптомам токсоплазмоза относят:
- Головная боль.
- Повышение температуры тела (от 37 до 39 C).
- Кожные симптомы токсоплазмоза: высыпания аллергического характера (крапивница).
- Увеличение лимфатических узлов, их болезненность при пальпации.
- Боли в мышечных тканях и суставах.
- Увеличение селезенки и печени (заметно при пальпации).
- Желтушность кожных покровов, глазного яблока.
- Нарушения зрения (частичная или полная слепота, двоение изображения, вспышки).
- Хроническая усталость, вялость, сонливость.
Подобную симптоматику часто путают с простудой, гриппом или ОРВИ.
Острая форма: симптомы
Острая стадия токсоплазмоза также чаще всего похожа на ОРВИ.
Самые характерные симптомы:
- Повышение температуры.
- Увеличение лимфатических узлов (шейных и затылочных).
- Частые головные боли.
- Боль в мышцах и суставах.
- Общая слабость, потливость, быстрая утомляемость, сонливость.
Признаки острого токсоплазмоза исчезают через 5-7 дней. Если иммунная система исправно функционирует, болезнь больше не дает о себе знать. При наличии угнетающих факторов, токсоплазмы поражают тело локально, вызывают воспалительные процессы в органах, нарушая их работу.
Симптомы хронической формы
Хроническая форма имеет смазанную симптоматику, и заподозрить болезнь по ощутимым признакам тяжело.
Токсоплазмоз имеет те же признаки, что и любая вяло протекающая форма инфекции:
- Головная боль.
- Субфебрильная температура тела (37-37,5 C).
- Увеличенные лимфатические узлы.

- Слабость, хроническая утомляемость.
- Снижение работоспособности, концентрации внимания.
Хроническая форма проявляется через 5-7 дней после попадания простейших в тело человека из-за контакта с кошачьими фекалиями или через 2-3 недели после поедания недостаточно обработанного зараженного мяса.
Точная диагностика Токсоплазмоза
Исследования на выявление паразитов проводится в таких случаях:
- При наличии у пациента ВИЧ и других состояний, связанных с угнетением иммунной системы.
- При планировании беременности и у женщин в положении с целью определения группы риска к первичному инфицированию.
- При лимфаденопатии в период вынашивание ребенка (если до беременности исследования не проводились).
- При подозрении на внутриутробное заражение ребенка.
- При лихорадке, лимфаденопатии, гепатоспленомегалии неясной этиологии.
При наличии таких показаний к диагностике, врач назначает ряд анализов, направленных на выявление простейших и антител к ним в организме пациента. Комплекс исследований включает в себя опрос пациента (наличие симптомов, когда впервые возникли, не появились ли новые питомцы или не сменились ли недавно предпочтения в еде) и лабораторные анализы.
Комплекс исследований включает в себя опрос пациента (наличие симптомов, когда впервые возникли, не появились ли новые питомцы или не сменились ли недавно предпочтения в еде) и лабораторные анализы.
Для диагностики токсоплазмоза применяют такие лабораторные исследования:
- Биохимический анализ крови — выявит нарушения работы печени.
- Общий анализ крови — покажет развитие воспалительного процесса в теле пациента.
- Бактериальный посев — токсоплазмы активно растут в благоприятной среде — именно в такие условия помещают образец материала.
- Иммуноферментное исследование антител к возбудителю (чаще всего назначается на этапе планирования беременности) — при выявлении антител к токсоплазмам назначают дополнительные анализы, чтобы подтвердить подозрение на инфекцию.
- Полимеразная цепная реакция (ПЦР) — точный анализ, позволяющий выявить гены простейшего возбудителя.
- Проба с токсоплазмином — подкожно вводятся ослабленные паразиты, и фиксируется реакция на пробу: покраснение свидетельствует об инвазии, отсутствие изменений — соответственно об отсутствии инфекции в организме.

Анализы (помимо общего и биохимического исследования крови) информативны и позволяют точно диагностировать патологию и назначить лечение, если это требуется.
Токсоплазмоз при беременности — в чем опасность?
Токсоплазма — это внутриклеточный паразит, чрезвычайно распространенный повсеместно (в некоторых районах уровень зараженности достигает 90%). Несмотря на такую распространенность, опасность этих паразитов преувеличена — для человека со сформировавшимся иммунитетом эти простейшие безвредны. Но в случае первичного инфицирования во время беременности (вероятность мала и едва достигает 1%) возникает опасность для ребенка — внутриутробное заражение чревато инвалидностью, уродствами, замиранием плода до рождения, самопроизвольным выкидышем или смертью в короткие сроки после появления на свет. Несмотря на такие серьезные последствия вплоть до летального исхода, токсоплазмоз у матери далеко не всегда передается малышу и угрожает его жизни.
Сроки вынашивания и период заражения паразитами крайне важны в ситуации с токсоплазмозом. При инфицировании матери в 1-ом триместре вероятность передачи паразитов ребенку достигает всего 17%. В 3-ем — возрастает до 65%.
При инфицировании матери в 1-ом триместре вероятность передачи паразитов ребенку достигает всего 17%. В 3-ем — возрастает до 65%.
При этом важна тяжесть поражений, которую может вызвать токсоплазма: на сроках формирования внутренних органов плода (первый триместр) поражения будут самыми серьезными и часто несовместимыми с жизнью. При заражении сформировавшегося эмбриона в 3-м триместре урон будет незначительным и меньше повлияет на состояние здоровья малыша в дальнейшем.
При выявлении паразитоза у матери на ранних сроках вынашивания, врач может посоветовать прерывание беременности после проведения ряда анализов. Важно, чтобы для диагностики применялось сразу несколько методов и исследования проводились в динамике — только тогда можно предпринимать дальнейшие действия по поводу ведения беременности или аборта.
Если результаты диагностики свидетельствуют об инфицировании матери до 24 недели беременности, то гинеколог рекомендует прерывание. При отказе от аборта назначается лечение.
Важно! Токсоплазма опасна для плода только в случае инфицирования женщины не более чем за 3 месяца до беременности или после зачатия.
Как определить время попадания инфекции в тело будущей матери?
Период заражения можно узнать, изучив результаты анализов на иммуноглобулины IgM и IgG:
- IgM +, IgG -. Самая неблагоприятная картина во время вынашивания плода — это означает, что первичное инфицирование случилось совсем недавно и опасно для ребенка.
- IgM +, IgG +. Спорный результат, свидетельствующий о том, что токсоплазма паразитирует в теле менее года. В этом случае врач назначает еще одно исследование, по истечению 3-х недель. Увеличение IgG по сравнению с первым анализом свидетельствует об острой стадии токсоплазмоза.
- IgM -, IgG +. Такой результат получает подавляющее большинство женщин, он означает, что токсоплазма в организме не представляет опасности, так как инфицирование было более чем год назад и не представляет никакой опасности.
- IgM -, IgG -. Отсутствие обоих иммуноглобулинов — хороший показатель, означающий, что пациент никогда не стыкался с этим видом паразитов. Но в то же время ситуация требует предельной осторожности — важно не контактировать с кошками и соблюдать правила гигиены особенно тщательно до конца срока.
Даже при выявлении острой стадии токсоплазмоза последствия для ребенка не всегда обязательны или опасны — возможно, ребенок избежит инфекции. Чтобы убедиться в этом, доктор рекомендует провести анализ околоплодных вод: путем прокалывания плодного пузыря через переднюю брюшную стенку, осуществляется забор материала для изучения. Такой метод будет информативен не ранее, чем через 30 суток после инфицирования женщины.
В качестве вспомогательного способа подтверждения или опровержения передачи токсоплазмы малышу используют и ультразвуковое исследование плода (УЗИ). Метод позволяет выяснить размеры печени, и селезенки ребенка (при поражении паразитами органы будут увеличены), увидеть изменение головного мозга, кальцинаты в черепной коробке или плаценте.
Симптомы токсоплазмоза при беременности не отличаются от протекания болезни в обычный период жизни.
Важно! Если до зачатия ребенка в вашем доме жила кошка, то токсоплазмоз не страшен вашему будущему ребенку. Хозяева этих питомцев стыкаются с паразитами в обязательном порядке и при отсутствии патологий иммунитета, вырабатывают защиту к простейшим.
К каким докторам следует обращаться, если у Вас токсоплазмоз?
Лечением токсоплазмоза занимается инфекционист. Но с подозрением на такой диагноз к нему попадают чаще всего по направлению от терапевта, офтальмолога, невролога, гинеколога (при планировании беременности).
Важно! Лечение проводится только в случае острого протекания болезни на фоне сбоев в работе иммунной системы или при беременности. Хронический токсоплазмоз не представляет опасности для женщины и ее будущего ребенка.
Токсоплазмоз нельзя назвать опасным заболеванием для человечества. Для того чтобы встреча с этими паразитами прошла безболезненно, следует ответственно подходить к планированию беременности и уделить внимание формированию иммунитета.
Источник статьи: https://immunitet1.ru/
Симптомы хронического токсоплазмоза у человека и методы лечения
- Тифоподобный – протекает без серьёзных нарушений нервной системы. Сопровождается миалгией, головной болью, упадком сил. Прогноз такой формы болезни благоприятный.
- Смешанный – объединяет симптоматику энцефалитической и тифоподобной форм острого токсоплазмоза. Чаще всего встречается именно такой хронический токсоплазмоз.
Острый приобретённый токсоплазмоз переносится больным очень тяжело, а без наличия должного лечения может привести к летальному исходу.
После стихания симптомов заболевание переходит в хроническую или латентную формы.
Характеристика хронического приобретённого токсоплазмоза
Токсоплазмоз может сразу перейти в хроническую форму, минуя острую, в случае если человек обладает сильным иммунитетом и организм может сопротивляться паразиту. Хронический приобретённый токсоплазмоз характеризуется постепенным вялотекущим течением болезни. Возможны периоды обострений. Сначала у больного появляется субфебрильная температура тела (37,0⁰C -37,2⁰C), которая держится довольно длительное время. Происходит воспаление шейных, паховых, ключичных и подмышечных лимфоузлов. Изначально они мягкие, при пальпации достаточно болезненные, через время уменьшаются в размерах, уплотняются. Человека могут тревожить боли в мышцах и суставах, а также головные боли. У больного наблюдается значительная потеря веса. Достаточно ярко выражены симптомы хронической интоксикации организма:
- обострение других хронических болезней;
- вялость и раздражительность;
- быстрая утомляемость;
- нарушения работы желудочно-кишечного тракта;
- повышенная потливость;
- озноб;
- неприятный запах изо рта;
- высыпания на коже;
- обострение аллергических реакций;
- нарушения сна;
- ухудшения состояния кожи и волос.
На фоне всех этих симптомов развиваются нарушения нервной системы, сопровождающиеся признаками эмоциональной неустойчивости даже судорожных припадков. Нередки вегетососудистые расстройства, а также поражения глаз. Часто больной страдает от нарушения работы желез внутренней секреции, а именно надпочечников и щитовидной железы. У женщин возможны сбои менструального цикла, привычное невынашивание беременности, ау мужчин- урологические нарушения, эректильная дисфункция.
Наши читатели пишут
Тема:
Во всех бедах виноваты паразиты!
От кого:
Елены В.
Последние несколько лет чувствовала себя очень плохо. Постоянная усталость, бессонница, какая-то апатия, лень, частые головные боли. С пищеварением тоже были проблемы, утром неприятный запах изо рта.
А вот и моя история
Все это начало скапливаться и я поняла, что двигаюсь в каком-то не том направлении. Стала вести здоровый образ жизни, правильно питаться, но на мое самочувствие это не повлияло. Врачи тоже ничего толком сказать не могли. Вроде как все в норме, но я то чувствую что, мой организм не здоров.
Потом я пошла в одну дорогую клинику и сдала все анализы, так вот в одном из анализов у меня обнаружили паразитов. Это были не обычные глисты, а какой-то определенный вид, которым, по словам врачей, заражен практически каждый, в большей или меньшей степени. Вывести из организма их практически невозможно. Я пропила курс противопаразитных лекарств, которые назначили мне в той клиники, но результата почти не было.
Через пару недель я наткнулась на одну статью в интернете. Эта статья буквально изменила мою жизнь. Сделала все, как там написано и уже через несколько дней, я почувствовала, значительные улучшения в своем организме. Стала высыпаться намного быстрее, появилась та энергия, которая была в молодости. Голова больше не болит, появилась ясность в сознании, мозг стал работать намного лучше. Пищеварение наладилось, несмотря на то, что питаюсь я сейчас как попало. Сдала анализы и убедилась в том, что больше во мне никто не живет!
Кто хочет почистить свой организм от паразитов, причем неважно, какие виды этих тварей в вас живут – прочитайте эту статью, уверена на 100% вам поможет!
Перейти к статье>>>
Если больной жалуется на боли в мышцах, то при пальпации можно обнаружить небольшие уплотнения. Это цисты – места скопления паразитов. Внутри этих новообразований появляются кальцинаты, которые можно обнаружить также, при рентгенографии. Кальцинаты являются известковыми капсулами с омертвевшей тканью внутри. Иногда такие капсулы у больного токсоплазмозом обнаруживаются в тканях лёгких, головного мозга, печени.
Симптоматика хронического токсоплазмоза очень схожа с проявлениями других заболеваний. Довольно часто у больных находят признаки хламидиоза, гепатита, герпеса, онкологических заболеваний. Из-за проблем в постановке правильного диагноза, очень начать лечение болезни на ранних сроках. По этой же причине женщин планирующим беременность, направляют на анализ на токсоплазмоз. Даже во время хронической форме болезни может произойти внутриутробное заражение плода, что грозит необратимыми последствиями.
Многие люди, заражённые токсоплазмой, могут и не догадываться о своей болезни и носить паразитов в своём теле долгие годы. Известен результат может быть только после анализа крови на этого возбудителя. Хроническое течение болезни может принимать волнообразный характер, что означает периодическую смену клинически выраженных и стёртых форм. Часто токсоплазмоз переходит в латентную форму.
Латентный приобретённый токсоплазмоз
Хронический приобретённый токсоплазмоз способен переходить в латентную форму. Такое течение болезни характеризуется полным отсутствием симптомов болезни как таковых. И даже тщательное обследование не даёт никаких результатов. У латентного приобретённого токсоплазмоза различают две формы:
- Первично – латентную, которая развивается срезу же после заражения человека. Больной может и не догадываться о наличии паразитов в своём теле, так как симптоматика токсоплазмоза отсутствует.
- Вторично – латентную, которая наступает после угасания симптомов токсоплазмоза и может иметь внезапные вспышки обострения.
Отсутствие симптомов, вовсе не означает отсутствие токсоплазмы в организме человека. Снижение защитных функций организма, на фоне беременности или болезни, может привести к проявлению симптомов токсоплазмоза.
Латентный приобретённый токсоплазмоз можно отнести к тем болезням, которые случаются единожды и не требуют лечения, так как протекают бессимптомно и не вызывают дискомфорта у больного.
Врождённый токсоплазмоз
Как упоминалось ранее, токсоплазмоз очень опасен во время беременности. В первую очередь имеется угроза не матери, а плоду. Клинические проявления заболевания зависят от срока беременности, на котором произошло инфицирование возбудителем. Чем раньше произошло заражение матери, тем выше вероятность заражения плода и тем тяжелее форма токсоплазмоза.
Острая форма врождённого токсоплазмоза часто приводит к летальному исходу в первые недели жизни ребёнка. Также возможен переход болезни в неактивную форму, оставляя за собой нарушения нервной системы: гидроцефалию, микрофтальмию, хориоретинит, судороги, паралич глазных мышц и другие грубые пороки развития.
Клинические признаки врождённого токсоплазмоза у ребёнка могут быть заметны сразу после рождения или же обнаружиться спустя некоторое время. К общим симптомам можно отнести: повышение температуры тела, снижение аппетита, появление сыпи, проявлению судорог.
В 75-80% врождённый токсоплазмоз протекает в латентной форме, что может привести к его обострению в период полового созревания. Латентное течение болезни может привести к ожирению, а также к гипогенитализму у мальчиков и преждевременному половому созреванию у девочек.
Женщинам, планирующим беременность необходимо пройти анализ на токсоплазму до зачатия ребёнка, ведь от этого будет зависеть жизнь и здоровье малыша. Не стоит пренебрегать этим, ведь последствия могут быть очень печальными
Диагностика токсоплазмоза
В виду того, что токсоплазмоз обладает неспецифическими симптомами, которые легко спутать с проявлениями многих других болезней, диагноз устанавливают на основе клинических данных и результатов обследований. Также во внимание берутся и другие факторы, такие как: контакт с кошками, употребление в пищу немытых овощей и фруктов или мяса, не прошедшего достаточную термическую обработку.
Диагностика токсоплазмоза проводится несколькими способами, которые отличаются друг от друга:
- Паразитологический метод заключается в обнаружение токсоплазмы в тканях или жидкостях организма. Такой способ эффективен лишь для того, чтоб узнать есть ли в организме возбудитель, но не даёт сведений о том, когда произошло заражение, что очень важно во время лечения.
- Серологические методы (РСК,РНГА, ИФА) и аллергическая внутрикожная проба с токсоплазмином имеют более точные результаты, так как принцип их заключается в обнаружении специфических антител в крови потенциального больного. В зависимости от наличия тех или иных иммуноглобулинов становится понятно, когда именно произошло заражение. Анализ ИФА назначается женщинам, только планирующим беременность, так как давно перенесённая болезнь, не несёт опасности для плода, а впервые проникшая в организм беременной женщины токсоплазма может стать источником многих проблем.
- Полимерно-цепная реакция является не основным, а скорее дополнительным методом диагностики, так как имеет специфические требования к оборудованию, и как следствие высокую стоимость самого анализа. Из-за высокой чувствительности оборудования с помощью ПЦР можно обнаружить даже незначительную концентрацию паразита в организме.
Лечение токсоплазмоза
Врачи относят хронический токсоплазмоз к заболеваниям, которые невозможно вылечить, ведь возбудитель образует скопления, окруженные плотной оболочкой, не позволяющей воздействовать на него химиотерапевтическим препаратам. При этом антитела, выработанные иммунной системой больного человека, остаются на всю жизнь.
Хоть вылечить токсоплазмоз не реально, но можно максимально снизить риск осложнений связанных с этим заболеванием. Лечение назначается специалистом, только в том случае, если диагноз на 100% подтверждён. Так как заболевание имеет симптоматику схожую со многими другими болезнями, то без проведения полной диагностики больного, лечение не назначается.
Для лечения острой формы токсоплазмоза успешно используются антибиотики группы макролидов, а также Пириметамин и Сульфадимезин в сочетании с десенсибилизирующей терапией, витаминами. Также большое значение имеет вакцинотерапия токсоплазмином.
Помимо этого больному назначают курс различных противомикробных, противовирусных и противогрибковых препаратов. Лечение длительное и разделяется на несколько курсов. Химиотерапия довольно эффективна при острой форме токсоплазмоза, но абсолютно бессмысленна в хронической его форме.
Лечение хронического токсоплазмоза сводится к переводу болезни в латентную (бессимптомную) форму.Особое внимание уделяется иммунной системе и повышению её сопротивляемости паразитам. В основном лечение хронического токсоплазмоза назначается в периоды его обострения, но существуют ситуации, в которых нет возможности ожидать следующего обострения болезни. К этим причинам можно отнести беременность, угрозу потери зрения, а также развитие бесплодия.
Профилактика токсоплазмоза
Так как носителем токсоплазмоза являются домашние кошки, то профилактику болезни стоит начинать именно с них. Особенно это касается бездомных животных. Принося нового питомца в дом необходимо позаботиться о посещении с ним ветеринарного врача. Так как животное может быть источником заражения не только токсоплазмой, но и другими паразитами, людям со сниженным в связи с различными заболеваниями иммунитетом необходимо позаботиться о профилактике.
Но даже если вы не имеете контакта с кошками, то не стоит забывать о неспецифических путях заражения токсоплазмой, а именно, через немытые овощи и фрукты, а также мясо, не прошедшее достаточную термическую обработку.
Как и любое другое заболевание, токсоплазмоз гораздо проще предотвратить, чем лечить его. Важно придерживаться элементарных правил гигиены, и своевременно обращаться к врачу, при наличии симптомов болезни.
Токсоплазмоз у человека-что это такое, симптомы, как лечить
Что такое токсоплазмоз, почему он возникает у человека и животных, как эту болезнь выявить, лечить, а лучше – предупредить?
Токсоплазмоз – заболевание, которое вызывается микроскопическими паразитами – токсоплазмами. По статистике ВОЗ носителями токсоплазмы являются почти 50% населения нашей планеты (в США и России – 20-35%, а в странах с влажным и жарким климатом – до 95% жителей).
Если иммунная система организма работает нормально, заражение токсоплазмозом не вызывает развития заболевания. Если же в отлаженном механизме защиты организма от внешних и внутренних угроз происходит сбой, токсоплазмы активизируются, поражая лимфатическую и нервную систему, скелетную мускулатуру и сердечную мышцу, орган зрения и головной мозг. Особенно опасен токсоплазмоз при беременности, вызывая тяжелое поражение нервной системы и внутренних органов плода, частую его гибель до или сразу после рождения.
Вот уже на протяжении более 50 лет ученые изучают связь инфицирования человека токсоплазмами с возникновением психических расстройств – появлением раздражительности, вспышек агрессии, снижении настроения, склонности к самоубийствам, увеличения риска развития шизофрении.
Как происходит заражение токсоплазмозом?
- Основной источник заражения – кошки, 50-60% которых являются носителями токсоплазмоза. Выделяются токсоплазмы из организма кошки с калом, а во время периодического «умывания» животного – разносятся по всей шерсти и затем очень быстро попадают в окружающее пространство, сохраняясь на предметах окружающей обстановки, на улице в земле и воде месяцами. Человек заражается обычно при контакте с кошкой и уборке ее экскрементов. Если руки будут недостаточно вымыты, токсоплазма попадает в организм человека во время приема пищи. Возможен водной, бытовой и воздушный путь передачи инфекции. Подсчитано, что в местности, где обитает много кошек, в каждой щепотке земли содержится несколько сотен яиц (ооцист) токсоплазмы, а каждая кошка за свою жизнь «производит» около одного миллиарда цист паразитов.
- Передача инфекции от матери к плоду (внутриутробное заражение)
- Изредка можно заразиться токсоплазмозом при употреблении в пищу сырого или недостаточно прожаренного (проваренного) мяса – свинины, баранины, оленины.
- При наличии микроповреждений кожи заражение может произойти и при обработке сырого мяса (приготовление пищи, работа по разделке туш…)
Признаки токсоплазмоза
При нормальном иммунитете в большинстве случаев токсоплазмоз у человека не возникает. Если же заболевание возникает, то чаще оно протекает скрыто, без каких-либо явных симптомов неблагополучия (может наблюдаться небольшое повышение температуры, слабость, повышенная утомляемость). Выявить хронический токсоплазмоз в этих случаях можно только с помощью лабораторных анализов (серологические реакции, кожные аллергические пробы).
При выраженном снижении защитных сил организма (СПИД и другие иммунодефициты) часто встречается острое течение болезни. При этом повышается температура до 38-40°C, появляется выраженная головная боль, головокружение, может быть рвота, судороги и другие признаки поражения нервной системы. Как правило при остром токсоплазмозе увеличиваются лимфатические узлы (чаще шейные), а также печень и селезенка, нарушается зрение, поражается сердце.
Влияние токсоплазмоза на психику
Уже на протяжении 50 лет проводятся исследования, подтверждающие негативное влияние токсоплазмоза на нервную систему человека, его психические функции. Так установлено, что инфицирование токсоплазмой повышает уровень агрессии, делает человека более раздражительным, меняет его настроение, повышает вероятность совершения необдуманных поступков, увеличивает вероятность суицида.
Есть данные о том, что инфицированность токсоплазмами намного чаще встречается при шизофрении и других психических расстройствах, проявляющихся бредом, галлюцинациями и нарушениями поведения.
Принципы лечения и профилактики токсоплазмоза
При нормальном иммунитете, как уже говорилось, заболевание, как правило, не возникает или протекает в легкой форме и заканчивается выздоровлением без использования каких-либо лекарственных средств.
При снижении защитных сил организма назначаются медикаменты, оказывающие специфическое противопаразитарное действие на возбудителя токсоплазмоза. Обычно используются такие средства, как хлоридин, бисептол, а также антибиотики-макролиды (азитромицин, рокситромицин, спирамицин). Лечение проводится в течение 1-3 недель.
В качестве профилактических мероприятий необходимо отметить, прежде всего, борьбу с токсоплазмозом домашних животных путем их обследования и полноценного лечения. Не стоит кормить животных сырым мясом.
Что касается самих людей, то важно соблюдать простые меры личной и общественной гигиены (тщательно мыть руки перед каждым приемом пищи, поддерживать чистоту в помещениях и по возможности – на улице возле дома). Особый контроль необходим за беременными как в плане недопущения заражения (минимизация контактов с животными, соблюдение личной гигиены), так и для своевременной диагностики заболевания (проведение необходимых анализов) и его лечения.
Токсоплазмоз [LifeBio.wiki]
Токсоплазмоз является паразитарным заболеванием, вызываемым Toxoplasma gondii. Токсоплазмоз обычно не вызывает явных симптомов у взрослых. Иногда у людей может наблюдаться легкая, похожая на грипп болезнь в виде мышечных болей и болезненных лимфатических узлов в течение нескольких недель или месяцев. У небольшого числа людей могут возникнуть проблемы со зрением. У людей со слабой иммунной системой могут возникнуть серьезные симптомы, такие как судороги и плохая координация. При заражении во время беременности, у ребенка может возникнуть заболевание, известное как врожденный токсоплазмоз.
Токсоплазмоз обычно распространяется при употреблении в пищу плохо приготовленной пищи, которая содержит цисты; а также при контакте с инфицированными кошачьими экскрементами; и от матери к ребенку во время беременности, если мать заражается. 1) Редко болезнь может передаваться при переливании крови. Болезнь не передается от человека к человеку. Паразит, как известно, размножается половым путем только в семействе кошек. Тем не менее, он может заразить большинство видов теплокровных животных, включая людей. Диагноз обычно ставится на основе анализа крови на антитела или амниотической жидкости на ДНК паразита.
Профилактика заключается в правильном приготовлении пищи. Беременным женщинам также рекомендуется не чистить ящики для кошачьих туалетов или носить перчатки во время и мыть руки после этого. 2) Лечение здоровых людей обычно не требуется. Во время беременности, для лечения могут быть использованы спирамицин или пириметамин / сульфадиазин и фолиновая кислота.
До половины людей в мире инфицированы токсоплазмозом, но не имеют симптомов. В Соединенных Штатах токсоплазмозом страдают около 11% людей, в то время как в некоторых регионах мира это количество достигает более 60%. В год фиксируется около 200000 случаев врожденного токсоплазмоза. Чарльз Николь и Луи Мансо впервые описали токсоплазму в 1908 году. В 1941 году была подтверждена передача токсоплазмоза во время беременности от матери ребенку. 3)
Признаки и симптомы
Острый токсоплазмоз
Острый токсоплазмоз у здоровых взрослых часто протекает бессимптомно. 4) Тем не менее, симптомы могут проявляться и часто напоминают грипп: опухшие лимфатические узлы, головные боли, лихорадка и усталость или мышечные боли и боли, которые длятся в течение месяца или более. У человека с полностью функционирующей иммунной системой редко возникают тяжелые симптомы в результате инфекции. Люди с ослабленной иммунной системой могут испытывать головную боль, спутанность сознания, плохую координацию, судороги, проблемы с легкими, которые могут напоминать туберкулез или пневмонию Pneumocystis jiroveci (распространенную оппортунистическую инфекцию, которая встречается у людей со СПИДом), или помутнение зрения, вызванное тяжелым воспалением сетчатки (глазной токсоплазмоз). У маленьких детей и людей с ослабленным иммунитетом, например, людей с ВИЧ / СПИДом, у людей, проходящих определенные виды химиотерапии, или недавно прошедших трансплантацию органа, может развиться тяжелый токсоплазмоз. Он может привести к повреждению головного мозга (энцефалит) или глаз (некротический ретинохоридит). Младенцы, инфицированные через передачу плаценты, могут родиться с любой из этих проблем или с пороками носа, хотя эти осложнения у новорожденных редки. Токсоплазматические трофозоиты, вызывающие острый токсоплазмоз, называются тахизоитами и обычно обнаруживаются в жидкостях организма.
Набухшие лимфатические узлы обычно находятся в области шеи или под подбородком, за которыми следуют подмышки и пах. Отек может возникать в разное время после первоначальной инфекции, сохраняться и рецидивировать в течение разного времени независимо от противопаразитарного лечения. Обычно отечность встречается у взрослых в отдельных местах, но у детей чаще встречается несколько участков опухания. Увеличенные лимфатические узлы в 60% случаев рассасываются в течение 1-2 месяцев. Однако, четверти пострадавших требуется 2–4 месяца, чтобы вернуться к нормальной жизни, а 8% — 4–6 месяцев. Значительное число пострадавших (6%) возвращаются в нормальное состояние намного позже.
Латентный токсоплазмоз
Из-за бессимптомной природы заболевания, жертвы легко заражаются T. gondii и развивают токсоплазмоз, не зная об этом. Хотя в течение первых нескольких недель после заражения иногда появляются легкие симптомы, напоминающие грипп, инфекция T. gondii не вызывает выраженных симптомов у здоровых людей. У большинства не страдающих иммунодефицитом людей инфекция переходит в латентную фазу, во время которой присутствуют только брадиозоиты (в тканевых кистах), эти тканевые кисты и даже поражения могут возникать в сетчатке, альвеолярной оболочке легких (где острая инфекция может имитировать инфекцию Pneumocystis jirovecii), сердце, скелетных мышцах и центральной нервной системе (ЦНС), включая головной мозг. 5) Кисты образуются в ЦНС (тканях мозга) при заражении T. gondii и сохраняются в течение всей жизни хозяина. У большинства младенцев, инфицированных в утробе матери, симптомы при рождении отсутствуют, но могут развиться в более позднем возрасте.
В обзорах серологических исследований было установлено, что 30–50% населения мира подвергались и могут быть хронически инфицированы скрытым токсоплазмозом, хотя уровни заражения в разных странах отличаются 6). Это латентное состояние инфекции в последнее время ассоциируется с многочисленными бременами болезней, изменениями нервной системы и тонкими гендерно-зависимыми изменениями поведения у иммунокомпетентных людей.
Кожный токсоплазмоз
В редких случаях кожные поражения могут возникать при приобретенной форме заболевания, включая полиформные эритемные поражения, розеолы, узлы, похожие на пруриго, крапивницу и макулопапулезные поражения. У новорожденных могут наблюдаться точечные пятна, синяки. Диагноз кожного токсоплазмоза основывается на тахизоитной форме T. gondii, обнаруженной в эпидермисе. Кожный токсоплазмоз обнаруживается на всех уровнях эпидермиса, имеет размер около 6 на 2 мкм и имеет форму дуги, причем ядро составляет одну треть его размера. Его можно определить с помощью электронной микроскопии или окрашивания ткани Гимзы, где цитоплазма имеет синий цвет, ядро – красный.
Причина
Паразитология
В своем жизненном цикле, T. gondii принимает несколько форм. Тахизоиты ответственны за острую инфекцию; они быстро делятся и распространяются по тканям организма. Тахизоиты также известны как «тахизойские мерозоиты», описательный термин, который более точно передает паразитологическую природу этой стадии. После пролиферации, тахизоиты превращаются в брадиозоиты, которые находятся внутри латентных кист внутриклеточной ткани, которые образуются главным образом в мышцах и мозге. Образование кист частично вызвано давлением со стороны иммунной системы хозяина. 7) Брадизоиты (также называемые «брадиозойскими мерозоитами») не реагируют на антибиотики. После образования, брадизоиты могут оставаться в тканях на протяжении всей жизни хозяина. У здорового хозяина, если некоторые брадиозоиты превращаются обратно в активные тахизоиты, иммунная система быстро уничтожает их. Однако, у людей с ослабленным иммунитетом или у плодов, у которых отсутствует развитая иммунная система, тахизоиты могут разрастаться и вызывать значительные неврологические повреждения.
Выживание паразита зависит от баланса между выживанием хозяина и распространением паразита. T. gondii достигает этого баланса, манипулируя иммунным ответом хозяина, снижая иммунный ответ хозяина и усиливая репродуктивное преимущество паразита. Как только паразит заражает нормальную клетку хозяина, он противостоит повреждениям, вызванным иммунной системой хозяина, и меняет иммунные процессы в организме хозяина.
При проникновении в клетку-хозяина, паразит образует мембрану паразитофорного вакуоля (ПВ) из мембраны клетки-хозяина. 8) ПВ инкапсулирует паразита и является устойчивой к активности эндолизосомной системы и может контролировать митохондрии и эндоплазматический ретикулум хозяина.
При первом проникновении в клетку, паразит высвобождает белки ROP из луковицы органеллы роптрия. Эти белки транслоцируются в ядро и на поверхность ПВ-мембраны, где они могут активировать STAT-пути для модуляции экспрессии цитокинов на уровне транскрипции, связывать и инактивировать разрушающие ПВ-мембрану белки IRG, помимо других возможных эффектов. Кроме того, некоторые штаммы T. gondii могут секретировать белок, известный как GRA15, активируя путь NF-κB, который активирует провоспалительный цитокин IL-12 в раннем иммунном ответе, что может привести к латентной фазе развития паразита. Способность паразита секретировать эти белки зависит от его генотипа и влияет на его вирулентность.
Паразит также влияет на антиапоптотический механизм, позволяя инфицированным клеткам-хозяевам сохраняться и размножаться. Одним из методов устойчивости к апоптозу является разрушение эффекторных про-апоптозных белков, таких как BAX и BAK. Чтобы разрушить эти белки, T. gondii вызывает конформационные изменения белков, которые препятствуют транспортировке белков в различные клеточные отделы, где они инициируют события апоптоза. T. gondii, однако, не вызывает подавления эффекторных белков проапоптоза.
T. gondii также обладает способностью инициировать аутофагию клеток хозяина. 9) Это приводит к уменьшению количества здоровых, неинфицированных клеток и, следовательно, меньшему количеству клеток-хозяев, чтобы атаковать зараженные клетки. Исследования Wang et al. показывают, что инфицированные клетки приводят к более высоким уровням аутофагосом в нормальных и инфицированных клетках. Их исследования показывают, что T. gondii вызывает аутофагию клеток хозяина, используя кальций-зависимый путь. Другое исследование предполагает, что паразит может напрямую влиять на высвобождение кальция из запасов кальция, которые важны для сигнальных процессов клеток.
Механизмы, описанные выше, позволяют T. gondii сохраняться в хозяине. Некоторыми ограничивающими факторами для токсоплазмы является то, что ее влияние на клетки-хозяева сильнее в слабой иммунной системе и зависит от количества, поэтому большое количество T. gondii на клетку-хозяина вызывает более серьезный эффект. Влияние на хозяина также зависит от силы иммунной системы хозяина. У иммунокомпетентных людей обычно нет серьезных симптомов или вообще никаких симптомов, в то время как летальный исход или тяжелые осложнения могут наблюдаться у людей со слабым иммунитетом. 10)
Поскольку паразит может изменять иммунный ответ хозяина, он также может оказывать положительное или отрицательное влияние на иммунный ответ на другие патогенные угрозы. Это включает, но не ограничивается ответами на инфекции, вызываемые Helicobacter felis, Leishmania major или другими паразитами, такими как Nippostrongylus brasiliensis.
Передача
Токсоплазмоз обычно передается через рот при случайном употреблении ооцист Toxoplasma gondii или тканевых цист. Также может иметь место врожденная передача от матери к плоду. Передача может также происходить во время процесса трансплантации твердого органа или трансплантации гематогенных стволовых клеток.
Пероральная передача может происходить через:
Проглатывание сырого или частично приготовленного мяса, особенно свинины, баранины или оленины, содержащего цист токсоплазмы: распространенность инфекции в странах, где традиционно употребляется недоваренное мясо, связана с этим методом передачи. Тканевые цисты могут также проглатываться во время контакта рук со ртом после обработки недоваренного мяса или от использования ножей, посуды или разделочных досок, загрязненных сырым мясом.
Проглатывание немытых фруктов или овощей, которые были в контакте с загрязненной почвой, содержащей зараженные экскременты кошек.
Проглатывание кошачьих экскрементов, содержащих ооцисты: это может происходить при контакте рук со ртом после работы в саду, чистки кошачьего туалета, контакта с детскими песочницами; паразит может выживать в окружающей среде в течение нескольких месяцев.
Попадание в организм неочищенной, нефильтрованной воды путем непосредственного потребления или использования воды для приготовления пищи.
Питье непастеризованного молока и молочных продуктов, особенно козьего молока.
Попадание в организм сырых морепродуктов.
Кошки выделяют возбудителя в своих экскрементах в течение нескольких недель после заражения болезнью, обычно путем употребления в пищу зараженного промежуточного хозяина, который может включать млекопитающих (например, грызунов) или птиц. Выделение ооцист обычно начинается с третьего дня после поедания инфицированных промежуточных хозяев и может продолжаться неделями. Ооцисты не являются инфекционными при выведении из организма. Примерно через день ооциста подвергается процессу, называемому споруляцией, и становится потенциально патогенной. Помимо кошек, птицы и млекопитающие, включая людей, также являются промежуточным хозяином паразита и участвуют в процессе передачи. Однако, патогенность зависит от возраста и видов, вовлеченных в инфекцию, и способа передачи T. gondii. 11)
Токсоплазмоз также может передаваться при трансплантации цельных органов. Токсоплазма-серонегативные реципиенты, которые получают органы от недавно инфицированных токсоплазма-серопозитивных доноров, подвергаются риску заражения. Реципиенты органов, у которых имеется латентный токсоплазмоз, подвергаются риску возобновления заболевания в их организма из-за иммуносупрессии, возникающей во время трансплантации цельного органа. Реципиенты трансплантатов гематогенных стволовых клеток могут подвергаться более высокому риску инфекции из-за более длительных периодов иммуносупрессии.
Трансплантация сердца и легких обеспечивает самый высокий риск инфицирования токсоплазмозом из-за поперечно-полосатой мышцы, составляющей сердце, которая может содержать цисты, и риски для других органов и тканей варьируются в широких пределах. Риск передачи может быть снижен путем скрининга доноров и реципиентов до процедуры пересадки и предоставления лечения.
Меры предосторожности при беременности
Врожденный токсоплазмоз является специфической формой токсоплазмоза, при которой нерожденный плод заражается через плаценту. Врожденный токсоплазмоз связан со смертью и выкидышем, а у младенцев – с неврологическим дефицитом, нейрокогнитивным дефицитом и хориоретинитом. Положительный титр антител указывает на предшествующее воздействие и иммунитет и в значительной степени обеспечивает безопасность нерожденного плода. Простой анализ крови во время первого дородового визита к врачу может определить, была ли женщина ранее подвергнута воздействию токсоплазмы, и, следовательно, подвергается ли она риску. Если женщина впервые подвергается воздействию T. gondii во время беременности, плод подвергается особому риску.
Существует не так много доказательств влияния информирования женщин до беременности на профилактику врожденного токсоплазмоза. Тем не менее, предполагается эффективность информирования родителей до рождения ребенка, поскольку это может способствовать улучшению питания, личной гигиены и гигиены домашних животных. Необходимы дополнительные исследования, чтобы выяснить, может ли дородовое обучение снизить врожденный токсоплазмоз. 12)
Для беременных женщин с отрицательным титром антител, что указывает на отсутствие предшествующего воздействия T. gondii, рекомендуется проводить серологическое тестирование ежемесячно, так как лечение во время беременности для женщин, впервые подвергшихся воздействию T. gondii, значительно снижает риск передачи паразита плоду. Так как иммунная система ребенка не развивается полностью в течение первого года жизни, а эластичные цисты, которые образуются по всему телу, очень трудно уничтожить антипротозойными препаратами, инфекция может быть очень серьезной у детей.
Несмотря на эти риски, в большинстве стран беременные женщины не проходят регулярный скрининг на токсоплазмоз по причинам экономической эффективности и большого количества ложноположительных результатов; Португалия, Франция, Австрия, Уругвай, и Италия являются заметными исключениями, и некоторые региональные программы скрининга действуют в Германии, Швейцарии и Бельгии. 13) Поскольку инвазивное пренатальное тестирование сопряжено с определенным риском для плода (предотвращено 18,5 случаев потери беременности на случай токсоплазмоза), предпочтительным является постнатальный или неонатальный скрининг. Исключением являются случаи, когда отмечаются аномалии развития плода, и в этом случае можно проводить скрининг.
Беременным женщинам следует избегать употребления сырого мяса, сырого молока (особенно козьего молока) и не рекомендуется употреблять сырое или недоваренное мясо независимо от его типа. 14) Из-за очевидной связи между токсоплазмой и кошками, также часто рекомендуется избегать контакта с фекалиями кошек и воздерживаться от садоводства (фекалии кошек часто встречаются в садовой почве) или, по крайней мере, носить перчатки при таком контакте. Большинство кошек не выделяют ооцист активно, поскольку они заражаются в течение первых шести месяцев своей жизни. Однако эти ооцисты погружаются в почву, спорулируют её и остаются заразными в течение периодов от нескольких месяцев до более года. Многочисленные исследования показали, что жизнь в семье с кошкой не является значительным фактором риска инфекции T. gondii, хотя жизнь с несколькими котятами имеет некоторую корелляцию.
В 2006 году, чешская исследовательская группа обнаружила, что женщины с высоким уровнем антител к токсоплазмозу значительно чаще рожают мальчиков, чем девочек. В большинстве групп рождаемость составляет около 51% мальчиков, но у женщин, инфицированных T. gondii, вероятность рождения мальчика составляет до 72%. 15)
Диагноз
Диагноз токсоплазмоза у людей ставится биологическим, серологическим, гистологическим или молекулярным методами или с помощью некоторой комбинации вышеуказанных методов. Токсоплазмоз трудно отличить от первичной лимфомы центральной нервной системы. Он имитирует некоторые другие инфекционные заболевания, поэтому его клинические признаки неспецифичны и не достаточно характерны для определенного диагноза. В результате, диагноз ставится путем испытания терапии (пириметамин, сульфадиазин и фолиновая кислота (USAN: лейковорин)), если лекарственные средства не оказывают клинического эффекта и не улучшают повторную визуализацию.
T. gondii также может быть обнаружен в крови, амниотической жидкости или спинномозговой жидкости с помощью полимеразной цепной реакции. 16) T. gondii может существовать в хозяине как неактивная киста, которую, вероятно, трудно обнаружить.
Серологическое тестирование может обнаружить антитела к T. gondii в сыворотке крови с использованием таких методов, как тест красителя Сабина-Фельдмана (DT), анализ непрямой гемагглютинации, анализ непрямого флуоресцентного антитела (IFA), тест прямой агглютинации, тест латексной агглютинации (LAT), иммуноферментный анализ (ELISA) и тест на иммуносорбентную агглютинацию (IAAT).
Наиболее часто используемые тесты для измерения антител IgG – это DT, ELISA, IFA и модифицированный тест на прямую агглютинацию. Антитела IgG обычно появляются в течение недели или двух после заражения, достигают пика в течение одного-двух месяцев, а затем снижаются с различной скоростью. Антитела к токсоплазме IgG обычно сохраняются в течение всей жизни и поэтому могут присутствовать в кровотоке в результате текущей или предыдущей инфекции. 17)
В некоторой степени, острые токсоплазмозные инфекции можно дифференцировать от хронических инфекций, используя тест на авидность IgG, который является вариацией теста ELISA. В первом ответе на инфекцию, токсоплазменный IgG имеет низкое сродство к антигену токсоплазмы; в последующие недели и месяцы, сродство IgG к антигену увеличивается. На основании теста на авидность IgG, если IgG у инфицированного человека имеет высокую аффинность, это означает, что заражение началось за три-пять месяцев до тестирования. Это особенно полезно при врожденной инфекции, когда состояние беременности и гестационный возраст во время инфекции определяют лечение.
В отличие от IgG, антитела IgM могут использоваться для выявления острой, но, как правило, не хронической инфекции. Антитела IgM появляются быстрее после заражения, чем антитела IgG, и исчезают быстрее, чем антитела IgG после восстановления. В большинстве случаев, специфичные к T. gondii антитела IgM могут быть впервые обнаружены приблизительно через неделю после приобретения первичной инфекции и уменьшаться в течение одного-шести месяцев; 25% инфицированных в течение семи месяцев оказывают отрицательный результат на специфический для T. gondii IgM. Однако, IgM может быть обнаружен через месяцы или годы после заражения, во время хронической фазы, и возможны ложноположительные результаты при острой инфекции. Наиболее часто используемыми тестами для измерения антител IgM являются двойной IgM-ELISA, тест IFA и анализ иммуносорбентной агглютинации (IgM-ISAGA). Коммерческие тестовые наборы часто имеют низкую специфичность, а полученные результаты часто неверно интерпретируются.
Врожденный токсоплазмоз
Рекомендации по диагностике врожденного токсоплазмоза включают в себя: пренатальную диагностику, основанную на исследовании амниотической жидкости и ультразвуковых исследованиях; неонатальную диагностику, основанную на молекулярном тестировании плаценты и пуповинной крови и сравнительных серологических тестах матери и ребенка, и клиническое обследование при рождении; и раннюю детскую диагностику, основанную на неврологических и офтальмологических исследованиях и серологическом обследовании в течение первого года жизни. Во время беременности рекомендуется серологическое тестирование с интервалом в три недели.
Хотя диагностика токсоплазмоза в значительной степени зависит от серологического выявления специфического анти-токсоплазменного иммуноглобулина, серологическое тестирование имеет ограничения. Например, оно может не обнаружить активную фазу инфекции T. gondii, потому что специфический антитоксоплазменный IgG или IgM может не продуцироваться в течение нескольких недель после заражения. В результате, у беременной женщины может быть отрицательный результат во время активной фазы инфекции T. gondii, приводящий к необнаруженному и поэтому необработанному врожденному токсоплазмозу. 18) Кроме того, тест может не выявлять инфекции T. gondii у пациентов с ослабленным иммунитетом, поскольку титры специфических антител против токсоплазмы IgG или IgM могут не повышаться у пациентов этого типа.
Многие методы PCR были разработаны для диагностики токсоплазмоза с использованием клинических образцов, которые включают амниотическую жидкость, кровь, спинномозговую жидкость и биопсию ткани. Наиболее чувствительным методом на основе PCR является гнездовая PCR с последующей гибридизацией продуктов PCR. Основным недостатком этих методов является то, что они отнимают много времени и не дают количественных данных.
PCR в реальном времени полезна для обнаружения патогенов, экспрессии и регуляции генов, а также аллельной дискриминации. Этот метод PCR использует 5′-нуклеазную активность ДНК-полимеразы Taq для расщепления нерасширенного флуоресцентно-меченного зонда гибридизации во время фазы расширения PCR. Второй флуоресцентный краситель, например 6-карбокси-тетраметил-родамин, гасит флуоресценцию интактного зонда. Нуклеазное расщепление гибридизационного зонда во время PCR высвобождает эффект гашения, приводящий к увеличению флуоресценции, пропорциональной количеству продукта PCR, который может контролироваться детектором последовательности.
Токсоплазмоз нельзя обнаружить с помощью иммуноокрашивания. Лимфатические узлы, пораженные токсоплазмой, имеют характерные изменения, включая плохо разграниченные реактивные зародышевые центры, кластеры моноцитоидных В-клеток и рассеянные эпителиоидные гистиоциты.
Классическая триада врожденного токсоплазмоза включает: хориоретинит, гидроцефалию и внутричерепной атеросклероз. Другие последствия включают нейросенсорную глухоту, судороги и умственную отсталость.
Лечение
Лечение часто рекомендуется только людям с серьезными проблемами со здоровьем, таким как люди с ВИЧ, чей уровень CD4 составляет менее 200 клеток / мм3, потому что заболевание является наиболее серьезным при слабой иммунной системе. Триметоприм / сульфаметоксазол является препаратом выбора для предотвращения токсоплазмоза, но не для лечения активного заболевания. Исследование 2012 года показывает новый многообещающий способ лечения активной и скрытой формы этого заболевания с использованием двух эндохиноподобных хинолонов. 19)
Острый токсоплазмоз
Лекарства, назначаемые при остром токсоплазмозе, включают:
Пириметамин – противомалярийный препарат
Сульфадиазин – антибиотик, используемый в сочетании с пириметамином для лечения токсоплазмоза
Комбинированная терапия обычно проводится с добавками фолиевой кислоты, чтобы снизить частоту тромбоцитопении.
Комбинированная терапия наиболее полезна в условиях ВИЧ.
Клиндамицин
Спирамицин – антибиотик, который чаще всего используется беременными женщинами для предотвращения заражения их детей.
(другие антибиотики, такие как миноциклин, нашли некоторое применение в качестве терапии спасения).
При инфицировании во время беременности, спирамицин рекомендуется в первом и раннем втором триместрах, а пириметамин / сульфадиазин и лейковорин – в конце второго и третьего триместров.
Латентная фаза
У людей со скрытым токсоплазмозом, цисты невосприимчивы к этим методам лечения, так как антибиотики не достигают брадизоитов в достаточной концентрации.
Лекарственные препараты, назначаемые при скрытом токсоплазмозе:
Атоваквон – антибиотик, который использовался для уничтожения цист токсоплазмы у больных СПИДом
Клиндамицин – антибиотик, который в комбинации с атоваквоном, по-видимому, оптимально убивает цисты у мышей
Врожденный токсоплазмоз
Когда у беременной женщины диагностируется острый токсоплазмоз, можно использовать амниоцентез, чтобы определить, инфицирован ли плод. Когда у беременной женщины развивается острый токсоплазмоз, тахизоиты имеют приблизительно 30%-ную вероятность проникновения в ткань плаценты и оттуда – проникновения и заражения плода. По мере того, как гестационный возраст во время заражения увеличивается, вероятность заражения плода также увеличивается.
Если паразит еще не достиг плода, спирамицин может помочь предотвратить передачу в плаценту. Если плод был заражен, беременную женщину после первого триместра можно лечить пириметамином и сульфадиазином, фолиевой кислотой. Лечение начинают после первого триместра, потому что пириметамин обладает антифолатным эффектом, а недостаток фолиевой кислоты может помешать формированию мозга плода и вызвать тромбоцитопению. Инфекция на более ранних сроках беременности коррелирует с худшими исходами для плода и новорожденного, особенно когда инфекция не лечится.
Эпидемиология
Инфекции T. gondii встречается во всем мире, хотя уровни заражения значительно различаются в зависимости от страны. Что касается женщин детородного возраста, опрос, проведенный в 99 исследованиях в 44 странах, показал, что районы наибольшей распространенности находятся в Латинской Америке (около 50–80%), частях Восточной и Центральной Европы (около 20–60%), на Ближнем Востоке (около 30–50%), части Юго-Восточной Азии (около 20–60%) и части Африки (около 20–55%).
В Соединенных Штатах, данные Национального обследования здоровья и питания (NHANES) с 1999 по 2004 год показали, что 9,0% людей в возрасте от 12 до 49 лет, родившихся в США, были серопозитивными по отношению к антителам IgG против T. gondii, по сравнению с 14,1% по измерию NHANES в 1988–1994 годах. 20) В опросе 1999–2004 годов 7,7% родившихся в США и 28,1% женщин 15–44 лет, родившихся за рубежом, были серопозитивными по T. gondii. Тенденция к снижению серопревалентности наблюдалась в многочисленных исследованиях в США и многих европейских странах. Toxoplasma gondii считается второй по значимости причиной смерти, связанной с пищевыми продуктами, и четвертой по значимости причиной госпитализации, связанной с пищевыми продуктами, в Соединенных Штатах 21).
Протистом, ответственным за токсоплазмоз, является T. gondii. Существует три основных типа T. gondii, ответственных за паттерны токсоплазмоза во всем мире – типы I, II и III. Эти три типа T. gondii оказывают различное влияние на некоторых хозяев, в основном, на мышей и людей, из-за их различий в генотипах.
Тип I: вирулентный у мышей и людей, наблюдается у больных СПИДом.
Тип II: не вирулентный у мышей, вирулентный у людей (в основном, в Европе и Северной Америке), наблюдаемый у пациентов со СПИДом.
Тип III: не вирулентен у мышей, вирулентен, главным образом, у животных, но наблюдается в меньшей степени у людей.
Современные методы серотипирования могут только отделить тип I или III от паразитов типа II.
Поскольку паразит представляет особую угрозу для плода, когда заражение происходит во время беременности, большая часть глобальных эпидемиологических данных, касающихся T. gondii, поступает из тестов на серопозитивность у женщин детородного возраста. Тесты на серопозитивность определяют наличие антител против T. gondii в крови, поэтому, хотя серопозитивность гарантирует, что человек подвергся воздействию паразита, это не обязательно гарантирует хроническую степень инфицирования. 22)
История
Toxoplasma gondii была впервые описана в 1908 году Николь и Мансо в Тунисе и независимо Сплендором в Бразилии. Splendore сообщил о вирусе в кролике, в то время как Nicolle и Manceaux идентифицировали его у североафриканского грызуна гунди (Ctenodactylus gundi). В 1909 году Николь и Мансо обнаружили вирус у лейшмании. Nicolle и Manceaux тогда назвали его Toxoplasma gondii из-за изогнутой формы его инфекционной стадии (греческий корень «toxon» = лук).
Первый зарегистрированный случай врожденного токсоплазмоза был описан в 1923 году, но он не был идентифицирован как вызванный T. gondii. Янко (1923) подробно описал результаты вскрытия 11-месячного мальчика, который поступил в больницу с гидроцефалией. У мальчика наблюдались классические признаки токсоплазмоза, включая хориоретинит (воспаление сосудистой оболочки и сетчатки глаза). Гистология выявила ряд «спороцитов», хотя Янко не идентифицировал их как T. gondii.
Лишь в 1937 году первый подробный научный анализ T. gondii был проведен с использованием методов, ранее разработанных для анализа вирусов. В 1937 г. Сабин и Олицкий проанализировали T. gondii на лабораторных обезьянах и мышах. Сабин и Олицкий показали, что T. gondii был облигатным внутриклеточным паразитом и что мыши, которых кормили зараженной T. gondii тканью, также заразились инфекцией. Так, Сабин и Олицкий продемонстрировали T. gondii как возбудителя, передаваемого между животными.
T. gondii был впервые описан как человеческий патоген в 1939 году в детской больнице в Нью-Йорке. 23) Вольф, Коуэн и Пейдж идентифицировали инфекцию T. gondii у новорожденной девочки, рожденной доношенной с помощью кесарева сечения. Через три дня у ребенка развились судороги и хориоретинит на обоих глазах. Затем у ребенка развился энцефаломиелит, и он умер в возрасте одного месяца. Вольф, Коуэн и Пейдж изолировали T. gondii от поражений мозговой ткани. Внутричерепная инъекция образцов головного и спинного мозга мышам, кроликам и крысам вызывала энцефалит у животных. Вольф, Коуэн и Пейдж рассмотрели дополнительные случаи и пришли к выводу, что T. gondii производил узнаваемые симптомы, и они могли передаваться от матери к ребенку.
Первый взрослый случай токсоплазмоза был зарегистрирован в 1940 году без неврологических признаков. Пинкертон и Вайнман сообщили о наличии токсоплазмы у 22-летнего мужчины из Перу, который умер от последующей бактериальной инфекции и лихорадки.
В 1948 году Сабин и Фельдман создали серологический тест с красителем, основанный на способности антител пациента изменять окрашивание токсоплазмы. Тест красителя Сабина Фельдмана в настоящее время является золотым стандартом для выявления инфекции токсоплазмой.
Передача токсоплазмы при употреблении в пищу сырого или недоваренного мяса была продемонстрирована Desmonts et al. в 1965 году в Париже. Десмонтс заметил, что терапевтическое потребление сырой говядины или конины в туберкулезной больнице было связано с увеличением количества токсоплазмозных антител на 50% в год. Это означает, что больше T. gondii передавалось через сырое мясо.
В 1974 году Desmonts и Couvreur показали, что инфекция в течение первых двух триместров связана с наибольшим вредом для плода, что передача зависит от того, когда матери были заражены во время беременности, что матери с антителами до беременности не передавали инфекцию плоду, и что спирамицин понизил передачу вируса плоду.
Токсоплазма привлекла больше внимания в 1970-х годах с ростом иммуносупрессивного лечения после трансплантации органов или костного мозга и эпидемией СПИДа 1980-х годов. Пациенты с пониженной функцией иммунной системы гораздо более подвержены заболеваниям.
Общество и культура
Синдром безумной кошатницы
Синдром безумной кошатницы – термин, введенный информационными организациями для описания научных результатов, которые связывают паразита Toxoplasma gondii с некоторыми психическими расстройствами и поведенческими проблемами. 24) Хотя исследователи обнаружили, что владение кошкой не сильно увеличивает риск инфекции T. gondii у беременных женщин, предполагаемая корреляция между владением кошкой в детстве и последующим развитием шизофрении предполагает, что необходимы дальнейшие исследования, чтобы определить фактор риска для детей. Термин «синдром сумасшедшей кошатницы» опирается как на стереотип, так и на популярный культурный ориентир. Этот термин появился в результате увеличения сообщений о связи токсоплазмоза и кошек. Кошатница – это культурный стереотип женщины, часто старой девы, которая навязчиво подбирает и заводит кошек. Ярослав Флегр (биолог) является сторонником теории, что токсоплазмоз влияет на поведение человека. 25)
Известные случаи
У теннисиста Артура Эша возникли неврологические проблемы из-за токсоплазмоза (и позже было установлено, что он ВИЧ-положительный).
Актер Мерритт Бутрик был ВИЧ-инфицированным и умер от токсоплазмоза в результате его уже ослабленной иммунной системы.
Педро Самора, ведущий реалити-шоу и активист по ВИЧ / СПИДу, был диагностирован токсоплазмозом в результате ослабления его иммунной системы ВИЧ .
Принц Франсуа, граф Клермон, претендующий на престол Франции, имел врожденный токсоплазмоз.
Актриса Лесли Эш заболела токсоплазмозом на втором месяце беременности.
Британский бегун на средние дистанции Себастьян Коу заболел токсоплазмозом в 1983 году, вероятно, из-за контакта с кошкой во время тренировки в Италии.
Теннисистка Мартина Навратилова страдала токсоплазмозом во время Открытого чемпионата США 1982 года.
Другие животные
Toxoplasma gondii поражает практически всех теплокровных животных; эти тахизоиты были обнаружены у птицы 26)
Хотя T. gondii обладает способностью заражать практически всех теплокровных животных, восприимчивость и скорость заражения сильно различаются у разных родов и видов животных. Уровни инфицирования в популяциях одного и того же вида также могут широко варьироваться из-за различий в расположении, рационе питания и других факторах.
Хотя заражение T. gondii было отмечено у нескольких видов азиатских приматов, серопревалентность антител к T. gondii была впервые обнаружена у макак-токе (Macaca sinica), обитающих только на острове Шри-Ланка.
Австралийские сумчатые особенно подвержены токсоплазмозу. Токсоплазмоз смертельно опасен для валлаби, коал, вомбатов, падемелонов и маленьких дасюрид, а тасманийский бандикут обычно умирает в течение примерно 3 недель после заражения.
По оценкам, 23% диких свиней в мире являются серопозитивными для T. gondii. 27) Серопревалентность варьируется по всему земному шару с самой высокой серопревалентностью в Северной Америке (32%) и Европе (26%) и самой низкой – в Азии (13%) и Южной Америке (5%). Географические регионы, расположенные в более высоких широтах, и регионы, где наблюдается более теплый и влажный климат, связаны с повышенной серопревалентностью T. gondii среди дикого кабана. Дикий кабан, зараженный T. gondii, представляет потенциальный риск для здоровья людей, потребляющих мясо.
Животноводство
Среди домашнего скота, свиньи, овцы и козы имеют самые высокие показатели хронической инфекции T. gondii. Распространенность T. gondii среди мясных видов животных широко варьируется как внутри стран, так и между странами 28), и было показано, что на уровни заражения существенное влияние оказывают различные методы ведения сельского хозяйства. Например, животные, содержащиеся на открытом воздухе или в условиях свободного пространства, подвержены большему риску заражения, чем животные, выращенные в помещении или в коммерческих условиях содержания.
В Соединенных Штатах был измерен процент свиней, содержащих в организме жизнеспособных паразитов (с помощью биоанализа на мышах или кошках) до 92,7% и до 0% в зависимости от фермы или стада. Обследования серопревалентности (антитела к T. gondii в крови) встречаются чаще, и такие измерения свидетельствуют о высокой относительной серопревалентности у свиней во всем мире. Наряду со свиньями, овцы и козы являются одними из наиболее часто инфицированных животных, имеющих эпидемиологическое значение для заражения людей. Было установлено, что распространенность жизнеспособных T. gondii в тканях овец (с помощью биоанализа) достигает 78% в Соединенных Штатах, а обследование коз, предназначенных для потребления в Соединенных Штатах в 2011 году, показало, что серопревалентность составляет 53,4%. 29)
Из-за отсутствия контакта с окружающей средой, цыплята, выращиваемые в крупномасштабных закрытых помещениях, обычно не заражаются T. gondii. Куры, находящиеся на свободном выгуле или выращенные на заднем дворе, гораздо чаще заражаются. Обследование цыплят свободного выгула в США показало, что распространенность заражения составляет 17–100% в зависимости от фермы. Поскольку куриное мясо, как правило, тщательно готовят перед употреблением, домашняя птица, как правило, не считается существенным фактором риска заражения человека T. gondii.
Хотя крупный рогатый скот и буйволы могут быть заражены T. gondii, паразит, как правило, уничтожается или уменьшается до неопределяемого уровня в течение нескольких недель после воздействия. Цисты редко присутствуют в мясе буйвола или говядине, и считается, что мясо этих животных имеет низкий риск.
Лошади считаются устойчивыми к хронической инфекции T. gondii. Тем не менее, жизнеспособные клетки были выделены из американских лошадей, убитых на экспорт, и тяжелый токсоплазмоз человека во Франции был эпидемиологически связан с потреблением конского мяса.
Домашние кошки
В 1942 году первый случай кошачьего токсоплазмоза был диагностирован и зарегистрирован у домашней кошки в Мидлтауне, штат Нью-Йорк. 30) Исследователи смогли выделить ооцисты из фекалий кошек, и было также отмечено, что ооцисты могут быть инфекционными в окружающей среде до 12 месяцев.
По оценкам, серопревалентность T. gondii у домашних кошек во всем мире составляет около 30–40%. В Соединенных Штатах не было сделано официальной национальной оценки, но местные опросы показали, что уровни варьировались от 16% до 80%. Опрос 2012 года по 445 чистокровным домашним кошкам и 45 приютам в Финляндии выявил общую серопревалентность 48,4%. В 2010 году исследование диких кошек из Гизы, Египет, показало общую серопревалентность 97,4%. Другое исследование из Колумбии показало, что серопревалентность составляет 89,3%, тогда как в китайском исследовании серопревалентность составляет 2,1%. 31)
Уровень заражения T. gondii у домашних кошек широко варьируется в зависимости от рациона и образа жизни кошки. Дикие кошки, которые охотятся за своей едой, чаще заражаются токсоплазмозом, чем домашние кошки. Распространенность T. gondii в популяциях кошек зависит от наличия инфицированных птиц и мелких млекопитающих.
Большинство зараженных кошек будут распространять ооцист только один раз в жизни, в течение периода от одной до двух недель. Хотя этот период выделения довольно преходящий, одна кошка может выделять миллионы ооцист, причем каждая ооциста способна распространяться и выживать в течение нескольких месяцев. Приблизительно 1% кошек в любой момент времени активно выбрасывают ооцисты.
Трудно контролировать популяцию кошек с инфицированными ооцистами из-за отсутствия эффективной вакцины. В большинстве случаев, это остается проблемой, доступные ныне программы имеют сомнительную эффективность. 32)
Грызуны
Было показано, что заражение T. gondii изменяет поведение мышей и крыс таким образом, что, как считается, увеличивает вероятность того, что грызун окажется съеденным кошкой. Инфицированные грызуны демонстрируют снижение врожденного отвращения к запахам кошек; в то время как неинфицированные мыши и крысы, как правило, избегают областей, помеченных мочой кошки или запахом тела кошки, это отвращение уменьшается или устраняется у инфицированных животных. 33) Более того, некоторые данные свидетельствуют о том, что эта потеря отвращения может быть специфической для запахов кошачьих: при выборе между двумя запахами хищника (кошки или норки) инфицированные грызуны проявляют значительно более сильное предпочтение запахам кошки, чем неинфицированные.
У грызунов изменения в поведении, вызванные T. gondii, происходят посредством эпигенетического ремоделирования в нейронах, связанного с наблюдаемым поведением, например, оно модифицирует эпигенетическое метилирование для индуцирования гипометилирования генов, связанных с аргинин-вазопрессином в медиальной миндалине, для значительного уменьшения отвращения к хищнику. 34) Подобные эпигенетически-индуцированные поведенческие изменения также наблюдались в мышиной модели зависимости, где изменения в экспрессии гистон-модифицирующих ферментов посредством нокаута гена или ингибирования фермента в специфических нейронах вызывали изменения в поведении, связанном с наркотиками. Широко распространенное гистон-лизиновое ацетилирование в корковых астроцитах, по-видимому, является еще одним эпигенетическим механизмом, используемым Т. gondii.
Грызуны, инфицированные T. gondii, демонстрируют ряд поведенческих изменений, помимо измененных реакций на запахи кошек. Крысы, зараженные паразитом, проявляют повышенный уровень активности и пониженное неофобное поведение (меньше боятся нового). Точно так же, у зараженных мышей наблюдаются изменения в моделях локомоции и исследовательского поведения во время экспериментальных испытаний. Эти модели включают в себя перемещение на большие расстояния, движение на более высоких скоростях, ускорение в течение более длительных периодов времени и уменьшение времени неподвижности при размещении на новом участке. Также было показано, что инфицированные грызуны испытывают меньшую тревогу, используя традиционные модели, такие как возвышенные лабиринты, открытое поле и тесты социального взаимодействия. 35)
Морские млекопитающие
Калифорнийский университет в Дэвисе, изучавший выдр Мертвого моря, собранных с 1998 по 2004 год, обнаружил, что токсоплазмоз стал причиной смерти 13% животных. Близость к стоку пресной воды в океан была основным фактором риска. Проглатывание ооцист из фекалий считается наиболее вероятным конечным источником заражения. 36) Поверхностные стоки, содержащие экскременты диких кошек и отходы домашних кошек, спущенных в унитаз, являются возможными источниками ооцист. Эти же источники могли также привести к заражению токсоплазмозом находящейся под угрозой исчезновения гавайского тюленя-монаха. Заражение паразитом привело к гибели, по меньшей мере, четырех гавайских тюленей-монахов. Заражение гавайских тюленей-монахов Т. gondii было впервые отмечено в 2004 году. 37) Распространение паразита угрожает этому ластоногому. Паразиты были обнаружены у дельфинов и китов. Исследователи Блэк и Мэсси считают, что анчоусовые, которые путешествуют из устьев рек в открытый океан, могут способствовать распространению болезни.
Гигантская панда
Сообщалось, что причиной смерти гигантской панды в зоопарке в Китае, которая умерла в 2014 году от острого гастроэнтерита и респираторных заболеваний, была T. gondii. Несмотря на кажущуюся анекдотичность, в этом отчете подчеркивается, что все виды теплокровных, вероятно, инфицированы T. gondii, включая исчезающие виды, такие как гигантская панда.
Исследования
Хроническая инфекция T. gondii традиционно считается бессимптомной у людей с нормальной иммунной функцией. 38) Некоторые данные свидетельствуют о том, что скрытая инфекция может незаметно влиять на ряд человеческих поведений и тенденций, а инфекция может изменить восприимчивость или интенсивность ряда психических или неврологических расстройств.
В большинстве текущих исследований, в которых были обнаружены положительные корреляции между титрами антител к T. gondii и определенными поведенческими признаками или неврологическими расстройствами, тесты серопозитивности T. gondii проводятся после появления изученного заболевания или поведенческого признака; то есть, часто неясно, увеличивает ли заражение паразитом шансы иметь определенную черту или расстройство, или же наличие определенной черты или расстройства увеличивает шансы заразиться паразитом. Группы людей с определенными поведенческими особенностями или неврологическими расстройствами могут иметь определенные поведенческие тенденции, которые увеличивают вероятность воздействия и заражения T. gondii; в результате трудно подтвердить причинно-следственную связь между инфекциями T. gondii и связанными с ней неврологическими расстройствами или поведенческими особенностями.
Психическое здоровье
Некоторые данные связывают T. gondii с шизофренией. Два метаанализа 2012 года показали, что уровень антител к T. gondii у людей с шизофренией был в 2,7 раза выше, чем в контрольной группе. 39) Поэтому позитивность антител к T. gondii считалась промежуточным фактором риска по сравнению с другими известными факторами риска. Отмеченные предостережения включают в себя то, что тесты на антитела не выявляют токсоплазмоз напрямую, у большинства людей с шизофренией нет антител к токсоплазмозу, и может существовать систематическая ошибка публикации. В большинстве этих исследований проверялись люди, уже диагностированные шизофренией на антитела к T. gondii, ассоциации между T. gondii и шизофренией были обнаружены до появления симптомов шизофрении. Исследования, пытавшиеся объяснить половые различия при возникновении шизофрении, показали, что это можно объяснить вторым пиком заболеваемости инфекцией T. gondii в возрасте от 25 до 30 лет, наблюдаемым только у женщин. Хотя механизм, поддерживающий связь между шизофренией и инфекцией T. gondii, неясен, в исследованиях была предпринята попытка определить молекулярный механизм для объяснения корреляции. 40) Антипсихотические препараты, используемые при шизофрении, по-видимому, ингибируют репликацию тахизоитов T. gondii в клеточной культуре. При условии, что на самом деле существует причинно-следственная связь между T. gondii и шизофренией, исследования еще не определили, почему у некоторых людей со скрытым токсоплазмозом развивается шизофрения, а у других нет, однако некоторые правдоподобные объяснения включают различную генетическую восприимчивость, различия в паразитных штаммах и различия в пути заражения T. gondii.
Также были обнаружены корреляции между титрами антител к T. gondii и ОКР, самоубийствам у людей с расстройствами настроения, включая биполярное расстройство. Было показано, что положительные титры антител к T. gondii не коррелируют с клинической депрессией или дистимией. Хотя между T. gondii и многими психологическими расстройствами существует корреляция, основной механизм неясен. Исследование, проведенное в 2016 году, показало, что «было мало доказательств того, что T. gondii был связан с повышенным риском психических расстройств, плохим контролем импульсов, аберрациями личности или нейрокогнитивными нарушениями» 41).
Неврологические расстройства
Скрытая инфекция была связана с болезнью Паркинсона и болезнью Альцгеймера. 42)
Существует отрицательная связь между инфекцией паразита T. gondii и рассеянным склерозом; исследователи пришли к выводу, что инфекция токсоплазмоза может быть защитным фактором.
Дорожно-транспортные происшествия
Скрытая инфекция T. gondii у людей была связана с более высоким риском автомобильных аварий, возможно, из-за ухудшения психомоторных характеристик или усиления уровня рискованности в личностном профиле.
Изменение климата
Сообщается, что изменение климата влияет на возникновение, выживание, распространение и передачу T. gondii. T. gondii был обнаружен в канадской Арктике, месте, которое когда-то было слишком холодным для его выживания. Более высокие температуры увеличивают время выживания T. gondii. Изменения в популяциях птиц, грызунов и насекомых, а также в характере миграции могут повлиять на распространение T. gondii из-за их роли в качестве резервуара и переносчика вируса. Предполагается также, что урбанизация и естественное ухудшение окружающей среды влияют на передачу T. gondii и повышают риск заражения.
:Tags
Список использованной литературы:
1)
«Parasites – Toxoplasmosis (Toxoplasma infection) Epidemiology & Risk Factors». March 26, 2015. Archived from the original on 23 August 2015. Retrieved 22 August 2015.
2)
«Parasites – Toxoplasmosis (Toxoplasma infection) Biology». March 17, 2015. Archived from the original on 28 August 2015. Retrieved 22 August 2015.
3)
«Parasites – Toxoplasmosis (Toxoplasma infection) Prevention & Control». January 10, 2013. Archived from the original on 22 August 2015. Retrieved 22 August 2015.
4)
Dupont CD, Christian DA, Hunter CA (2012). «Immune response and immunopathology during toxoplasmosis». Seminars in Immunopathology. 34 (6): 793–813. doi:10.1007/s00281-012-0339-3. PMC 3498595. PMID 22955326
5)
Dubey JP, Hodgin EC, Hamir AN (2006). «Acute fatal toxoplasmosis in squirrels (Sciurus carolensis) with bradyzoites in visceral tissues». The Journal of Parasitology. 92 (3): 658–9. doi:10.1645/GE-749R.1. PMID 16884019
6)
Parlog A, Schlüter D, Dunay IR (March 2015). «Toxoplasma gondii-induced neuronal alterations». Parasite Immunology. 37 (3): 159–170. doi:10.1111/pim.12157. hdl:10033/346575. PMID 25376390. The zoonotic pathogen Toxoplasma gondii infects over 30% of the human population. The intracellular parasite can persist lifelong in the CNS within neurons modifying their function and structure, thus leading to specific behavioural changes of the host. … Furthermore, investigations of the human population have correlated Toxoplasma seropositivity with changes in neurological functions; however, the complex underlying mechanisms of the subtle behavioural alteration are still not fully understood. The parasites are able to induce direct modifications in the infected cells, for example by altering dopamine metabolism, by functionally silencing neurons as well as by hindering apoptosis.
7)
Markus, MB (1987). «Terms for coccidian merozoites». Annals of Tropical Medicine and Parasitology. 81 (4): 463. doi:10.1080/00034983.1987.11812147. PMID 3446034
8)
Miller CM; Boulter NR; Ikin RJ; Smith NC (January 2009). «The immunobiology of the innate response to Toxoplasma gondii». International Journal for Parasitology. 39 (1): 23–39. doi:10.1016/j.ijpara.2008.08.002. PMID 18775432
9)
Hippe D, Weber A, Zhou L, Chang DC, Häcker G, Lüder CG (2009). «Toxoplasma gondii infection confers resistance against BimS-induced apoptosis by preventing the activation and mitochondrial targeting of pro-apoptotic Bax». Journal of Cell Science. 122 (Pt 19): 3511–21. doi:10.1242/jcs.050963. PMID 19737817
10)
Wang Y, Weiss LM, Orlofsky A (2009). «Host cell autophagy is induced by Toxoplasma gondii and contributes to parasite growth». The Journal of Biological Chemistry. 284 (3): 1694–701. doi:10.1074/jbc.M807890200. PMC 2615531. PMID 19028680
11)
Assadi-Rad, A.M.; New, John C.; Patton, Sharon (April 1995). «Risk factors associated with transmission of Toxoplasma gondii to sows kept in different management systems in Tennessee». Veterinary Parasitology. 57 (4): 289–297. doi:10.1016/0304-4017(94)00677-5
12)
Di Mario, S; Basevi, V; Gagliotti, C; Spettoli, D; Gori, G; D’Amico, R; Magrini, N (23 October 2015). «Prenatal education for congenital toxoplasmosis». Cochrane Database of Systematic Reviews. 10 (10): CD006171. doi:10.1002/14651858.CD006171.pub4. PMID 26493047.
13)
De Paschale M, Agrappi C, Clerici P, Mirri P, Manco MT, Cavallari S, Viganò EF (2008). «Seroprevalence and incidence of Toxoplasma gondii infection in the Legnano area of Italy». Clinical Microbiology and Infection. 14 (2): 186–9. doi:10.1111/j.1469-0691.2007.01883.x. PMID 18034857.
14)
Kapperud, Georg; Jenum, Pal A.; Stray-Pedersen, Babill; Melby, Kjetil K.; Eskild, Anne; Eng, Jan (1996). «Risk factors for Toxoplasma gondii infection in pregnancy. Results of a prospective case-control study in Norway». American Journal of Epidemiology. 144 (4): 405–412. doi:10.1093/oxfordjournals.aje.a008942. PMID 8712198
15)
Ian Sample, science correspondent (2006-10-12). «Pregnant women infected by cat parasite more likely to give birth to boys, say researchers | Science». The Guardian. London. Archived from the original on 2014-02-19. Retrieved 2013-02-14.
16)
Switaj K, Master A, Skrzypczak M, Zaborowski P (2005). «Recent trends in molecular diagnostics for Toxoplasma gondii infections». Clinical Microbiology and Infection. 11 (3): 170–6. doi:10.1111/j.1469-0691.2004.01073.x. PMID 15715713.
17)
Jones JL, Parise ME, Fiore AE (2014). «Neglected parasitic infections in the United States: toxoplasmosis». American Journal of Tropical Medicine and Hygiene. 90 (5): 794–9. doi:10.4269/ajtmh.13-0722. PMC 4015566. PMID 24808246
18)
Lin MH, Chen TC, Kuo TT, Tseng CC, Tseng CP (2000). «Real-time PCR for quantitative detection of Toxoplasma gondii». Journal of Clinical Microbiology. 38 (11): 4121–5. PMC 87551. PMID 11060078.
19)
Doggett JS, Nilsen A, Forquer I, Wegmann KW, Jones-Brando L, Yolken RH, Bordón C, Charman SA, Katneni K, Schultz T, Burrows JN, Hinrichs DJ, Meunier B, Carruthers VB, Riscoe MK (2012). «Endochin-like quinolones are highly efficacious against acute and latent experimental toxoplasmosis». Proceedings of the National Academy of Sciences of the United States of America. 109 (39): 15936–41. Bibcode:2012PNAS..10915936D. doi:10.1073/pnas.1208069109. PMC 3465437. PMID 23019377.
20)
Jones JL, Kruszon-Moran D, Sanders-Lewis K, Wilson M (September 2007). «Toxoplasma gondii infection in the United States, 1999 2004, decline from the prior decade». American Journal of Tropical Medicine and Hygiene. 77 (3): 405–10. PMID 17827351
21)
Scallan, Elaine; Hoekstra, Robert; Angulo, Frederick; Tauxe, Robert; Widdowson, Marc-Alain; Roy, Sharon; Jones, Jeffery; Griffin, Patricia (January 2011). «Foodborne Illness Acquired in the United States — Major Pathogens». Emerging Infectious Diseases. 17 (1): 7–15. doi:10.3201/eid1701.P11101. PMC 3375761. PMID 21192848.
22)
Dubey JP, Frenkel JK (May 1998). «Toxoplasmosis of rats: a review, with considerations of their value as an animal model and their possible role in epidemiology». Veterinary Parasitology. 77 (1): 1–32. doi:10.1016/S0304-4017(97)00227-6. PMID 9652380.
23)
Tucker, Abigail (2016). The Lion In the Living Room: How House Cats Tamed Us And Took Over the World. Simon & Schuster. p. 108. ISBN 978-1-4767-3823-9.
24)
Fox, Stuart (2010-03-09). «Gold Nanoparticles and Lasers Kill the Brain Parasite That Causes «Crazy Cat Lady» Syndrome». Popsci. Archived from the original on 2010-03-12.
25)
Flegr Jaroslav (2007). «Effects of Toxoplasma on human behavior». Schizophrenia Bulletin. 33 (3): 757–760. doi:10.1093/schbul/sbl074. PMC 2526142. PMID 17218612. Archived from the original on 2015-02-19.
26)
Rigoulet, Jacques; Hennache, Alain; Lagourette, Pierre; George, Catherine; Longeart, Loïc; Le Net, Jean-Loïc; Dubey, Jitender P. (2014). «Toxoplasmosis in a bar-shouldered dove (Geopelia humeralis) from the Zoo of Clères, France». Parasite. 21: 62. doi:10.1051/parasite/2014062. ISSN 1776-1042. PMC 4236686. PMID 25407506.
27)
Riahi, Mohammad; Fakhri, Yadollah; Hanifehpour, Hooman; Valizadeh, Soghra; Gholizadeh, Majid; Hosseini-Pouya, Rokhsane; Gamble, H.Ray (September 2017). «The global seroprevalence of Toxoplasma gondii among wild boars: A systematic review and meta-analysis». Veterinary Parasitology. 244: 12–20. doi:10.1016/j.vetpar.2017.07.013. PMID 28917302.
28)
Tenter AM, Heckeroth AR, Weiss LM (November 2000). «Toxoplasma gondii: from animals to humans». International Journal for Parasitology. 30 (12–13): 1217–58. doi:10.1016/S0020-7519(00)00124-7. PMC 3109627. PMID 11113252.
29)
Dubey JP, Rajendran C, Ferreira LR, Martins J, Kwok OC, Hill DE, Villena I, Zhou H, Su C, Jones JL (July 2011). «High prevalence and genotypes of Toxoplasma gondii isolated from goats, from a retail meat store, destined for human consumption in the USA». International Journal for Parasitology. 41 (8): 827–33. doi:10.1016/j.ijpara.2011.03.006. PMID 21515278
30)
Dubey, Jitender P. (2008-12-01). «The history of Toxoplasma gondii–the first 100 years». The Journal of Eukaryotic Microbiology. 55 (6): 467–475. doi:10.1111/j.1550-7408.2008.00345.x. ISSN 1550-7408. PMID 19120791
31)
Dubey, JP (2010). Toxoplasmosis of Animals and Humans. ISBN 978-1-4200-9236-3.
32)
Andersen, Mark C.; Martin, Brent J.; Roemer, Gary W. (2004-12-15). «Use of matrix population models to estimate the efficacy of euthanasia versus trap-neuter-return for management of free-roaming cats». Journal of the American Veterinary Medical Association. 225 (12): 1871–1876. doi:10.2460/javma.2004.225.1871. ISSN 0003-1488. PMID 15643836.
33)
Vyas A, Kim SK, Giacomini N, Boothroyd JC, Sapolsky RM (Apr 10, 2007). «Behavioral changes induced by Toxoplasma infection of rodents are highly specific to aversion of cat odors». Proceedings of the National Academy of Sciences of the United States of America. 104 (15): 6442–7. Bibcode:2007PNAS..104.6442V. doi:10.1073/pnas.0608310104. PMC 1851063. PMID 17404235.
34)
Flegr J, Markoš A (December 2014). «Masterpiece of epigenetic engineering – how Toxoplasma gondii reprogrammes host brains to change fear to sexual attraction». Molecular Ecology. 23 (24): 5934–5936. doi:10.1111/mec.13006. PMID 25532868.
35)
Gonzalez LE, Rojnik B, Urrea F, Urdaneta H, Petrosino P, Colasante C, Pino S, Hernandez L (Feb 12, 2007). «Toxoplasma gondii infection lower anxiety as measured in the plus-maze and social interaction tests in rats: A behavioral analysis». Behavioural Brain Research. 177 (1): 70–9. doi:10.1016/j.bbr.2006.11.012. PMID 17169442.
36)
«Treating Disease in the Developing World». Talk of the Nation Science Friday. National Public Radio. December 16, 2005. Archived from the original on April 27, 2006.
37)
Honnold, SP; Braun, R; Scott, DP; Sreekumar, C; Dubey, JP (June 2005). «Toxoplasmosis in a Hawaiian monk seal (Monachus schauinslandi)» (Submitted manuscript). Journal of Parasitology. 91 (3): 695–7. doi:10.1645/GE-469R. PMID 16108571.
38)
Fuglewicz, AJ; Piotrowski, P; Stodolak, A (September 2017). «Relationship between toxoplasmosis and schizophrenia: A review». Advances in Clinical and Experimental Medicine. 26 (6): 1031–1036. PMID 29068607
39)
Torrey EF, Bartko JJ, Yolken RH (2012). «Toxoplasmosis gondii and other risk factors for schizophrenia: An update». Schizophrenia Bulletin. 38 (3): 642–647. doi:10.1093/schbul/sbs043. PMC 3329973. PMID 22446566. Archived from the original on 2015-09-04.
40)
Flegr J (2013). «How and why toxoplasma makes us crazy». Trends in Parasitology. 29 (4): 156–163. doi:10.1016/j.pt.2013.01.007. PMID 23433494.
41)
Sugden, Karen; Moffitt, Terrie E.; Pinto, Lauriane; Poulton, Richie; Williams, Benjamin S.; Caspi, Avshalom; Tanowitz, Herbert B. (17 February 2016). «Is Toxoplasma Gondii Infection Related to Brain and Behavior Impairments in Humans? Evidence from a Population-Representative Birth Cohort». PLOS ONE. 11 (2): e0148435. Bibcode:2016PLoSO..1148435S. doi:10.1371/journal.pone.0148435. PMC 4757034. PMID 26886853
42)
Yan, Chao; Liang, Li-Jun; Zheng, Kui-Yang; Zhu, Xing-Quan (2016). «Impact of environmental factors on the emergence, transmission and distribution of Toxoplasma gondii». Parasites & Vectors. 9 (137): 137. doi:10.1186/s13071-016-1432-6. PMC 4785633. PMID 26965989.
токсоплазмоз.txt · Последние изменения: 2019/08/10 10:04 — nataly
Что такое токсоплазмоз? Симптомы, причины, диагностика и лечение
Людям со здоровой иммунной системой обычно не требуется лечение, но сочетание антибиотиков и противомалярийных препаратов может помочь с симптомами.
Лекарства, которые обычно используются для инфицированных здоровых (небеременных) взрослых, включают пириметамин и сульфадиазин, а также фолиновую кислоту (лейковорин), по данным Mayo Clinic. (5)
Людей с ослабленной иммунной системой, например, людей, живущих с ВИЧ, также можно лечить этими препаратами до тех пор, пока их состояние не улучшится, хотя некоторым потребуется пожизненное лечение в более низкой дозе или альтернативными препаратами, сообщает CDC.(6)
В этих ситуациях также могут использоваться другие комбинации лекарств, такие как пириметамин плюс клиндамицин.
Беременных женщин в первом или начале второго триместра обычно лечат спирамицином, а у женщин в конце второго или третьего триместра — пириметамином и сульфадиазином плюс лейковорин.
Новорожденных обычно лечат пириметамином и сульфадиазином плюс лейковорин в течение первого года жизни. Это общие рекомендации, которые могут быть адаптированы к конкретным потребностям и факторам риска каждого пациента.(5)
Профилактика токсоплазмоза
Чтобы предотвратить заражение токсоплазмозом через пищевые продукты, CDC рекомендует следующие рекомендации:
Используйте пищевой термометр, чтобы гарантировать, что мясо и птица приготовлены при безопасной температуре.
Согласно Министерству сельского хозяйства США (USDA), целые куски мяса должны быть приготовлены при внутренней температуре не менее 145 градусов по Фаренгейту; фарш должен быть приготовлен как минимум до 160 градусов по Фаренгейту; и птица должна быть приготовлена как минимум до 165 градусов по Фаренгейту.
Очистите или тщательно вымойте фрукты и овощи перед употреблением.
Тщательно мойте разделочные доски, посуду, посуду и поверхности, контактировавшие с сырым мясом или птицей, морепродуктами и немытыми продуктами.
Не употребляйте непастеризованное козье молоко.
Избегайте употребления сырых или недоваренных устриц, мидий и моллюсков.
Чтобы предотвратить заражение кошек, владельцы кошек должны ежедневно менять туалетный лоток, избегать кормления своего питомца сырым или недоваренным мясом и держать кошку в помещении, чтобы снизить риск заражения.Беременным женщинам не следует чистить туалетный лоток, если это возможно, или, если никто другой не может, надеть одноразовые перчатки и после этого вымыть руки.
Всем следует избегать употребления неочищенной воды и носить перчатки во время работы в саду или при контакте с почвой или песком. Не забудьте после этого всегда мыть руки, так как в этих местах может быть заражение кошачьими фекалиями. (7)
7 странных фактов о паразите, контролирующем разум, Toxoplasma Gondii
Может ли паразит контролировать ваш разум?
Киста ткани Toxoplasma gondii.(Изображение предоставлено CDC)
Одноклеточный паразит, Toxoplasma gondii, , возможно, наиболее известен своей связью с кошками. Паразит может перемещаться от кошачьего хозяина к человеку, чаще всего через контакт с кошачьими фекалиями. И хотя паразит обычно вызывает только легкую инфекцию (у людей могут быть симптомы гриппа), у людей с ослабленной иммунной системой инфекции могут вызывать серьезные проблемы, от судорог до серьезных проблем с легкими.
Но инфекция T. gondii может также иметь совершенно странные эффекты.На протяжении многих лет паразит не только удивлял и ставил исследователей в тупик, но и позволил по-новому взглянуть на то, как работает человеческое поведение.
Вот семь странных фактов о T. gondii .
Было показано, что T. gondii увеличивает бесстрашие у крыс.
Крысы водятся по всему миру. (Изображение предоставлено: Alkestida | shutterstock)
Крысы, зараженные паразитом, похоже, утратили свой типичный страх перед кошками, а точнее, страх кошачьей мочи.Исследование 2011 года, проведенное в PLOS ONE, показало, что инфицированные крысы начинают чувствовать своего рода «сексуальное влечение» к запаху кошачьей мочи, а не к своей обычной защитной реакции на запах.
Это может быть связано с тем, что инфекция T. gondii изменяет нейронную активность в определенных областях мозга, говорят исследователи. Они писали, что паразит «подавляет врожденную реакцию страха», так что крысы больше не избегают запаха кошачьей мочи. Вместо этого влюбленные крысы тянутся к нему — и к своей смерти.
T. gondii может перепрыгивать почти между всеми теплокровными животными.
(Изображение предоставлено: Arrleyd80 / Shutterstock.com)
Кошки и крысы — не единственные животные, которые могут являться переносчиками паразита. T. gondii — исключительный паразит в том смысле, что он может перепрыгивать практически с любого теплокровного существа на другое. По оценкам Центров по контролю и профилактике заболеваний, хотя примерно 6 из 10 инфекционных заболеваний человека являются зоонозными (что означает, что они могут передаваться от животных к человеку), по данным Центров по контролю и профилактике заболеваний, вряд ли какие-либо из них разделяют широкую универсальность организмов-хозяев T. gondii .
Ученые точно не установили, почему это так, но некоторые исследования, такие как исследование 2011 года, опубликованное в Proceedings of the National Academy of Sciences, показывают, что по крайней мере часть ответа может быть найдена в белках паразита: когда определенный тип белка удаляется, паразит больше не является вирулентным. Исследователи предполагают, что это происходит потому, что эти белки разрушают ключевые белки в клетке хозяина, которые являются ключевыми для иммунного ответа хозяина. [10 смертельных болезней, распространенных среди разных видов]
Другие предполагают, что T.gondii мог способствовать другим типам психических заболеваний, даже самоубийству.
Паразиты Toxoplasma gondii, растущие в образце ткани мозга. (Изображение предоставлено CDC / Jonathan W.M. Gold. M.D.)
Шизофрения — не единственное психологическое расстройство, которое, возможно, связано с T. gondii. Исследование 2011 года, проведенное на мышах и опубликованное в журнале PLOS ONE, показало, что паразит может вызывать выброс из инфицированных клеток мозга высоких уровней нейромедиатора дофамина.
Повышение уровня дофамина может сыграть роль в некоторых расстройствах настроения, таких как биполярное заболевание, которое, согласно исследованию, было связано с нарушениями дофамина.Другое исследование, проведенное на людях, предполагает, что Toxoplasma может быть связано с импульсивностью и даже самоубийством.
Паразит не был бы первым патогеном, который изменит мозг и поведение людей. Вирус бешенства, смертельно опасный для людей, уже давно показал разрушительные неврологические эффекты.
Некоторые исследования показывают, что T. gondii связан с шизофренией.
Выздоровление человека после серьезного стрессового события может частично зависеть от его самооценки, как показало новое исследование.(Изображение предоставлено: изображение мозга через Shutterstock)
Одним из самых пугающих — и самых противоречивых — возможных эффектов Toxoplasma является его воздействие на разум. Если женщина заразилась паразитом во время беременности, ее плод может подвергаться риску развития шизофрении и других психических расстройств, согласно исследованию, проведенному в 2006 году среди жителей Дании и опубликованному в журнале Biological Psychiatry.
И это еще не все. В исследовании 2014 года, опубликованном в The Journal of Nervous and Mental Disease, было обнаружено антител Toxoplasma у пациентов с шизофренией, что предоставило дополнительные доказательства потенциальной связи между паразитом и психическим заболеванием.
T. gondii неизлечим.
(Изображение предоставлено: Monkey Business Images / Shutterstock.com)
Нет доступных лекарств для лечения T. gondii. Кроме бдительности, чтобы попытаться предотвратить заражение, делать больше нечего.
В исследовании 2005 года, опубликованном в Американском журнале акушерства и гинекологии, медицинские работники рекомендовали беременным женщинам и женщинам, желающим забеременеть, пройти обследование на T. gondii . Авторы также предложили, чтобы женщины понимали факторы риска заражения, такие как контакт с кошками (и особенно туалетными лотками и фекалиями), употребление неправильно приготовленного мяса и употребление неочищенной воды.
До половины мира могут быть заражены.
(Изображение предоставлено: Савченко Людмила / Shutterstock.com)
Исследователи, похоже, не могут прийти к единому мнению о том, насколько широко распространен T. gondii , отчасти потому, что многие случаи могут остаться незамеченными. Исследование 2002 года, опубликованное в журнале Clinical Microbiology and Infection, показало, что от 16 до 40 процентов людей во всем мире инфицированы, но в некоторых регионах, например, в некоторых частях Центральной Америки, Южной Америки и континентальной Европы, показатели составляют от 50 до 80 процентов.
Исследование 2011 года, опубликованное в Journal of Global Infectious Diseases, дало гораздо более высокую оценку числа инфицированных: около 6 миллиардов человек во всем мире, или более 80 процентов мира.
По оценкам Центров по контролю и профилактике заболеваний, около 60 миллионов человек в Соединенных Штатах — или почти 20 процентов — инфицированы. Простой анализ крови может определить, есть ли у вас антитела T. gondii , которые указывают на заражение паразитом. [7 абсолютно ужасных инфекций головы]
Чаще всего Т.gondii не имеет симптомов.
Toxoplasma gondii присутствует в жидкостях организма мышей. (Изображение предоставлено CDC / д-р Л.Л. Мур, младший)
Хотя T. gondii может вызывать симптомы гриппа в легких случаях, исследование 2014 года, опубликованное в Американском журнале тропической медицины и гигиены, показало, что в подавляющем большинстве случаев люди испытывают только легкие симптомы или совсем не испытывают никаких симптомов. Авторы писали, что, возможно, именно поэтому исследователи в значительной степени пренебрегают паразитом.
Паразит наиболее опасен для людей с уже существующими заболеваниями, такими как болезни, которые способствуют подавлению иммунной системы.Но большинство людей, инфицированных T. gondii , никогда даже не узнают, что у них он есть.
Первоначально опубликовано на Live Science.
Симптомы, диагностика, лечение и причины токсоплазмоза
Токсоплазмоз: введение
Токсоплазмоз:
Токсоплазмоз
это инфекция, вызванная одноклеточным паразитом по имени Toxoplasma
gondii . Встречается по всему миру. Более 60 … подробнее о токсоплазмозе.
Токсоплазмоз: Инфекция, часто передающаяся от кошек и их фекалий.Более подробная информация о симптомах,
причины и методы лечения токсоплазмоза доступны ниже.
Симптомы токсоплазмоза
См. Полный список из 33
симптомы токсоплазмоза
Средства для лечения токсоплазмоза
Подробнее о лечении токсоплазмоза
Домашняя диагностика
Домашнее медицинское обследование, связанное с токсоплазмозом:
Токсоплазмоз поставлен неверно?
Токсоплазмоз: истории болезни пациентов
Токсоплазмоз: количество смертей
Узнайте больше о Смерти и Токсоплазмозе.
Виды токсоплазмоза
Подробнее о Типах токсоплазмоза
Токсоплазмоз: осложнения
Обзор возможных медицинских осложнений, связанных с токсоплазмозом:
- Осложнения беременных, впервые инфицированных токсоплазмозом:
- Осложнения токсоплазмоза у плода или новорожденного:
- дополнительные сложности … »
Причины токсоплазмоза
Подробнее о причинах токсоплазмоза.
Дополнительная информация о причинах токсоплазмоза:
Заболевания, связанные с токсоплазмозом
Изучите причины этих заболеваний, которые похожи на токсоплазмоз или связаны с ним:
Ошибочный диагноз и токсоплазмоз
Антибиотики часто вызывают диарею : использование антибиотиков весьма вероятно
вызвать диарею у пациентов.
Причина в том, что антибиотики убивают не только «плохие» бактерии,
но также может убить «хорошие» бактерии в кишечнике….прочитайте больше »
Синусит ставится перед диагнозом : Есть тенденция ставить диагноз синусит,
когда состояние действительно является безобидным осложнением другой инфекции,
например, простуда …. читать дальше »
Коклюш часто не диагностируется : Хотя большинство детей в западном мире
иммунизированные против коклюша (также называемого «коклюш»), эта защита носит
примерно через 15 лет.
Таким образом, любой подросток или взрослый … читать дальше »
Подробнее о неправильном диагнозе и токсоплазмозе
Токсоплазмоз: врачи и специалисты-исследователи
Врачи и специалисты в области научных исследований:
Другие услуги врача, терапевта и специалиста по исследованию:
Токсоплазмоз: Анимация
Больше анимации и видео о токсоплазмозе
Прогноз токсоплазмоза
Прогноз токсоплазмоза:
Потому что Toxoplasma
инфекции обычно не вызывают симптомов или вызывают только легкие симптомы, и ваш
иммунная система не дает паразитам, оставшимся в вашем организме, вызывать
дальнейшие симптомы, большинству людей не нужно беспокоиться об этом.(Источник: отрывок из Toxoplasmosis: DPD)
Подробнее о прогнозе токсоплазмоза
Исследования токсоплазмоза
Посетите наши исследовательские страницы, чтобы узнать о текущих исследованиях методов лечения токсоплазмоза.
Клинические испытания токсоплазмоза
На веб-сайте ClinicalTrials.gov, расположенном в США, приводится информация о федеральных
и частные клинические испытания с участием людей-добровольцев.
Некоторые из клинических испытаний, перечисленных в ClinicalTrials.gov для токсоплазмоза включают:
Посмотреть полный список из 12
Клинические испытания токсоплазмоза
Профилактика токсоплазмоза
Информация о профилактике токсоплазмоза собрана из различных источников данных.
и может быть неточным или неполным.
Ни один из этих методов не гарантирует предотвращения токсоплазмоза.
- Избегайте кошек
- Избегайте кошачьих фекалий
- Избегайте попадания на почву или садовые участки, которые могут быть загрязнены кошачьими фекалиями
- Избегайте детских песочниц
- Тест на иммунитет к токсоплазмозу
- еще предупреждений… »
Подробнее о профилактике токсоплазмоза
Статистика токсоплазмоза
Токсоплазмоз: общие темы по теме
Типы токсоплазмоза
Доски сообщений о токсоплазмозе
Связанные форумы и медицинские истории:
Пользовательские интерактивные форумы
Прочтите о другом опыте, задайте вопрос о токсоплазмозе или ответьте на чей-нибудь вопрос на наших досках сообщений:
Выдержки из статьи о токсоплазмозе
Токсоплазмоз
это инфекция, вызванная одноклеточным паразитом по имени Toxoplasma
gondii .Встречается по всему миру. Более 60 миллионов человек
в США, вероятно, инфицированы Toxoplasma
паразит, но у очень немногих есть симптомы, потому что иммунная система обычно
не дает паразиту вызвать болезнь. (Источник: отрывок из Toxoplasmosis: DPD)
Определения токсоплазмоза:
Род простейших, паразитирующих на птицах и млекопитающих. T. gondii — один из наиболее распространенных инфекционных патогенных паразитов животных человека.- (Источник — База данных болезней)
Инфекция, вызванная паразитами, переданная человеку от зараженных кошек; заражение беременной женщиной может привести к серьезным повреждениям плода.
— (Источник — WordNet 2.1)
Токсоплазмоз внесен в список «редких заболеваний» Управлением
Редкие заболевания (ORD) Национального института здоровья
(НАЦИОНАЛЬНЫЕ ИНСТИТУТЫ ЗДРАВООХРАНЕНИЯ США). Это означает, что токсоплазмоз или подтип токсоплазмоза,
затрагивает менее 200 000 человек среди населения США.
Источник — Национальные институты здравоохранения (NIH).
Ophanet, консорциум европейских партнеров,
в настоящее время определяет состояние, которое встречается редко, когда оно затрагивает 1 человека из 2000.Они перечисляют Токсоплазмоз как «редкое заболевание».
Источник — Orphanet
Содержимое для токсоплазмоза:
Опросы пользователей и форумы
»Следующая страница: Что такое токсоплазмоз?
Медицинские инструменты и изделия:
Инструменты и услуги:
Медицинские изделия:
Форумы и доски сообщений
- Задайте или ответьте на вопрос по телефону
Infogalactic: ядро планетарных знаний
Токсоплазмоз — это паразитарное заболевание, вызываемое Toxoplasma gondii . [1] Инфекции токсоплазмоза обычно не вызывают симптомов у взрослых людей. [2] Иногда может быть несколько недель или месяцев легких гриппоподобных заболеваний, таких как мышечные боли и болезненные лимфатические узлы. [3] У небольшого числа людей могут развиться проблемы со зрением. У людей со слабой иммунной системой могут возникнуть серьезные симптомы, такие как судороги и нарушение координации. При заражении во время беременности у ребенка может развиться состояние, известное как врожденный токсоплазмоз. [3]
Токсоплазмоз обычно передается при употреблении плохо приготовленной пищи, содержащей цисты, контакте с инфицированными кошачьими фекалиями и от матери к ребенку во время беременности, если мать инфицирована.В редких случаях заболевание может передаваться при переливании крови. Иным образом между людьми это не распространяется. [1] Известно, что паразиты размножаются половым путем только в семействе кошачьих. Однако он может заразить большинство видов теплокровных животных, включая человека. [4] Диагностика обычно проводится путем анализа крови на антитела или путем анализа околоплодных вод на ДНК паразита. [5]
Профилактика заключается в правильном приготовлении и приготовлении пищи. Беременным женщинам также рекомендуется не чистить кошачьи туалеты. [6] Обычно в лечении здоровых людей не требуется. Во время беременности для лечения могут использоваться спирамицин или пириметамин / сульфадиазин и фолиевая кислота. [7]
До половины населения мира инфицированы токсоплазмозом, но не имеют никаких симптомов. [8] В Соединенных Штатах Америки этим заболеванием подвержено около 23% [9] , а в некоторых регионах мира этот показатель достигает 95%. [1] Ежегодно происходит около 200 000 случаев врожденного токсоплазмоза. [10] Шарль Николь и Луи Мансо впервые описали этот организм в 1908 году. В 1941 году была подтверждена передача во время беременности от матери ребенку. [11]
Признаки и симптомы
Заражение имеет три стадии:
Острый токсоплазмоз
Острый токсоплазмоз у здоровых взрослых часто протекает бессимптомно. [12] [13] Однако симптомы могут проявляться и часто похожи на грипп: увеличение лимфатических узлов, головные боли, лихорадка и усталость, [14] или боли в мышцах и боли, которые длятся в течение месяца или более .В редких случаях после заражения у человека с полностью функционирующей иммунной системой развиваются серьезные симптомы. Люди с ослабленной иммунной системой могут испытывать головную боль, спутанность сознания, плохую координацию, судороги, проблемы с легкими, которые могут напоминать туберкулез или пневмонию Pneumocystis jiroveci (распространенная оппортунистическая инфекция, которая встречается у людей со СПИДом), или помутнение зрения, вызванное тяжелым воспалением сетчатка (глазной токсоплазмоз) [14] Маленькие дети и люди с ослабленным иммунитетом, например, люди с ВИЧ / СПИДом, принимающие определенные виды химиотерапии или недавно перенесшие трансплантацию органов, могут развить тяжелый токсоплазмоз.Это может вызвать повреждение мозга (энцефалит) или глаз (некротический ретинохориоидит). [15] Младенцы, инфицированные через плаценту, могут родиться с любой из этих проблем или с пороками развития носа, хотя эти осложнения у новорожденных встречаются редко. Токсоплазматические трофозоиты, вызывающие острый токсоплазмоз, называются тахизоитами и обычно обнаруживаются в жидкостях организма.
Увеличенные лимфатические узлы обычно находятся на шее или под подбородком, за ними следуют подмышки и пах.Отек может возникать в разное время после первоначальной инфекции, сохраняться и повторяться разное время независимо от лечения противопаразитарными средствами. [16] У взрослых он обычно обнаруживается на отдельных участках, но у детей чаще встречается несколько участков. Увеличенные лимфатические узлы рассасываются в течение одного-двух месяцев в 60% случаев. Однако четверти пострадавших требуется от двух до четырех месяцев, чтобы вернуться в нормальное состояние, а у 8% — от четырех до шести месяцев. Значительное количество (6%) возвращается к норме гораздо позже. [17]
Латентный токсоплазмоз
Из-за бессимптомной природы [12] [13] хозяин может легко заразиться Toxoplasma gondii и заболеть токсоплазмозом, не зная об этом. Хотя легкие, похожие на грипп симптомы иногда возникают в течение первых нескольких недель после заражения, заражение T. gondii не вызывает легко наблюдаемых симптомов у здоровых взрослых людей. [8] [18] У большинства иммунокомпетентных людей инфекция переходит в латентную фазу, во время которой присутствуют только брадизоиты (тканевые кисты); [19] эти тканевые кисты и даже поражения могут возникать в сетчатке, альвеолярной выстилке легких (где инфекция может имитировать инфекцию Pneumocystis jirovecii ), сердце, скелетных мышцах и центральной нервной системе (ЦНС), включая мозг. [20] Кисты образуются в ЦНС (ткани мозга) при инфицировании T. gondii и сохраняются в течение всей жизни хозяина. [21] У большинства младенцев, инфицированных еще в утробе матери, симптомы отсутствуют при рождении, но симптомы могут развиться в более позднем возрасте. [22]
Обзоры серологических исследований показали, что 30–50% населения мира подвергалось воздействию латентного токсоплазмоза и может быть хронически инфицировано им, хотя уровни инфицирования значительно различаются от страны к стране. [8] [23] [24] Это латентное состояние инфекции недавно было связано с многочисленными болезнями, [8] нейронными изменениями, [21] [23] и тонким полом -зависимые поведенческие изменения у иммунокомпетентных людей. [25] [26]
Кожный токсоплазмоз
В редких случаях поражения кожи могут возникать в приобретенных формах заболевания, включая многоформные высыпания, похожие на розеолу и эритему, узелки, похожие на пруриго, крапивницу и пятнисто-папулезные поражения.У новорожденных могут быть точечные пятна, экхимозы или поражения, напоминающие черничный кекс. Диагностика кожного токсоплазмоза основывается на тахизоитной форме T. gondii , обнаруженной в эпидермисе. [27] Он обнаружен на всех уровнях эпидермиса, имеет размер около 6 мкм на 2 мкм, имеет дугообразную форму, а ядро составляет одну треть его размера. Его можно идентифицировать с помощью электронной микроскопии или окрашивания ткани по Гимзе, где цитоплазма показывает синий цвет, а ядро - красное.