Самарская городская клиническая больница №8 Новости
Реакция Манту, Диаскин-тест, квантифероновый тест, Т-спот, ПЦР, а может флюорография?
Туберкулёз в России распространён настолько, что к сорока годам 70-90% жителей нашей страны инфицированы им. Это не значит, что они больны: после инфицирования иммунитет большинства людей справляется с бактерией. Вероятность заболеть составляет в среднем 8% в первые два года после инфицирования, затем постепенно снижается, и формируется приобретенный клеточный иммунитет. Поэтому так важно проходить регулярные проверки на туберкулёз и проверять своих детей.
Зачем нужна прививка БЦЖ?
ВОЗ рекомендует массовую вакцинацию новорожденных против туберкулёза во всех странах, где эта болезнь распространена. Поэтому на 3-5 день после рождения, еще в роддоме, всем новорожденным бесплатно делают прививку БЦЖ. Но эта вакцина не защищает от инфицирования туберкулёзом. Её задача несколько иная. Если не привитый ребенок младше 2 лет будет инфицирован туберкулёзом, у него крайне высока вероятность развития туберкулезного менингита и генерализованных форм туберкулеза, которые очень быстро приводят к смерти. БЦЖ достаточно надёжно защищает ребенка именно от этих форм. Она также защищает детей от легочной формы туберкулеза, но уже менее эффективно.
БЦЖ достаточно надёжно защищает ребенка именно от этих форм. Она также защищает детей от легочной формы туберкулеза, но уже менее эффективно.
Какие ещё прививки нужны детям до 2-х лет?
Проба Манту
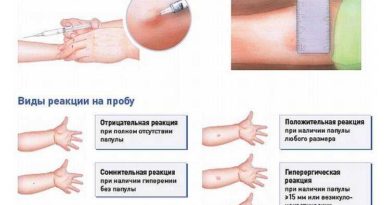
Проба Манту ежегодно проводится всем детям до 7 лет. Это не прививка (!), а иммунологический тест, показывающий, есть ли в организме возбудитель туберкулеза. При этом внутрикожно вводится туберкулин — специфический белок, содержащий антигены человеческого и бычьего туберкулеза. Через 72 часа измеряется размер папулы. На результат реакции Манту может повлиять посещение сауны, долгое принятие ванны, бассейн и расчёсывание места введения пробы. Временный контакт с водой никак не влияет на результаты пробы Манту, поэтому мнение о том, что Манту нельзя мочить — миф.
Диаскинтест тест
Также является кожной пробой. Но если в Манту используются антигены как человеческого, так и бычьего туберкулеза, то в диаскинтесте — только антигены туберкулеза человека. Диаскинтест гораздо более специфичен: реакция на него возникает, только если в организме есть активные бактерии туберкулеза. Проще говоря — если проба Манту положительная, это ещё ничего не значит: эта проба часто дает и ложноположительные реакции. А вот после диаскинтеста появилась реакция — это более серьёзный показатель.
Диаскинтест гораздо более специфичен: реакция на него возникает, только если в организме есть активные бактерии туберкулеза. Проще говоря — если проба Манту положительная, это ещё ничего не значит: эта проба часто дает и ложноположительные реакции. А вот после диаскинтеста появилась реакция — это более серьёзный показатель.
Точность Манту составляет 50-70%, диаскинтеста — 90%.
Квантифероновый тест
Квантифероновый тест — один из новых методов диагностики туберкулёза по анализу крови. Он основан на определении в крови гамма-интерферона, который вырабатывают клетки в ответ на внедрение туберкулезной палочки. В отличие от Манту и диаскинтеста, квантифероновый тест не требует введения в организм никаких антигенов и бактерий. Кровь для исследования берут из вены. Результат готов через несколько дней, и его точность намного выше, чем у кожных проб. Тест будет положительным, только если человек действительно болен.
T.SPOT.TB («ти-спот»)
Этот метод диагностики туберкулеза по крови аналогичен квантифероновому тесту. Отличие в том, что квантифероновый тест определяет в крови гамма-интерферон, вырабатываемый в ответ на внедрение туберкулезной палочки, а Т-СПОТ определяет сами Т-клетки, которые вырабатывают гамма-интерферон на присутствие микобактерии туберкулеза. Оба теста одинаково чувствительны и информативны (до 97%), они чувствительнее диаскинтеста и намного чувствительнее реакции Манту. «Ти-спот» практически исключает ложноположительные и ложноотрицательные реакции, в то время как квантифероновый тест все-таки может давать ложноположительную реакцию, если во время сдачи крови было заболевание ОРВИ.
Отличие в том, что квантифероновый тест определяет в крови гамма-интерферон, вырабатываемый в ответ на внедрение туберкулезной палочки, а Т-СПОТ определяет сами Т-клетки, которые вырабатывают гамма-интерферон на присутствие микобактерии туберкулеза. Оба теста одинаково чувствительны и информативны (до 97%), они чувствительнее диаскинтеста и намного чувствительнее реакции Манту. «Ти-спот» практически исключает ложноположительные и ложноотрицательные реакции, в то время как квантифероновый тест все-таки может давать ложноположительную реакцию, если во время сдачи крови было заболевание ОРВИ.
Флюорография
Всем взрослым с 15 лет в России рекомендуется раз в год проходить флюорографию. Детям с 15 до 17 лет разрешено выполнять Флюрографию, но это не отменяет постановку Диаскинтеста. Справку со свежим снимком требуют везде — даже при посещении ребенка в больнице. Флюорография — это скорее «коллективный барьер» на пути туберкулеза, чем метод выбора для индивидуальной проверки. Флюрография выявляет только легочные формы туберкулеза.
Флюрография выявляет только легочные формы туберкулеза.
Памятка для родителей по вакцинопрофилактике
Предупредить! Защитить! Привить!
Вакционопрофилактика – система мероприятий, осуществляемых в целях предупреждения, ограничения распространения и ликвидации инфекционных болезней путём проведения профилактических прививок.
Одним из важнейших мероприятий, предпринимаемых для сохранения и укрепления здоровья детей, является организация и проведение профилактических прививок.
Защиту организма от возбудителей инфекционных заболеваний осуществляет иммунная система. Она способна защитить ребенка от постоянно окружающих нас микроорганизмов (кишечной палочки, стрептококков и других), но не всегда в силах справиться с возбудителями дифтерии, вирусного гепатита «А», «В», столбняка, коклюша, кори и других инфекционных заболеваний. Прививки, полученные в детстве, в большинстве случаев, создают основу иммунитета против отдельных инфекций на всю жизнь.
Рекомендации перед вакцинацией и после
Перед прививкой ребенка нужно оберегать от контактов с больными. При наличии пищевой аллергии необходимо строго соблюдать диету, не вводить в рацион новые продукты. Такой же тактики нужно придерживаться в течение 5-7 дней после прививки.
После прививки у некоторых детей может наблюдаться постпрививочная реакция, такая как: повышение температуры, покраснение или уплотнение в месте введения вакцины. Это закономерная реакция, которая говорит о начале формирования защиты от инфекции. Как правило, такая реакция носит кратковременный характер (1-3 дня).
При повышении температуры до 380 не требуется никакого лечения, температура выше 380, необходимо использовать жаропонижающие средства, назначение сделает врач-педиатр, в соответствии с возрастом вашего ребенка.
В случае покраснения и уплотнения в месте введения вакцины, необходимо поставить в известность медработника, проводившего прививку. Для детей, у которых наблюдалась постпрививочная реакция, рекомендуются подготовительные мероприятия, которые назначит врач перед следующей прививкой.
Для детей, у которых наблюдалась постпрививочная реакция, рекомендуются подготовительные мероприятия, которые назначит врач перед следующей прививкой.
Каждый человек имеет право сделать свой выбор – прививаться или нет, но родители должны знать, что отказываясь от прививок, они лишают своих детей прав на здоровье. Кроме того, если в детском учреждении карантин по какой-то инфекции, а у вашего ребёнка отсутствует прививка, то его могут не принять в детский коллектив.
Родители! Отказываясь от прививок, Вы не только лишаете защиты своего ребенка, но и подвергаете опасности других детей, а также способствуете распространению инфекционных заболеваний в обществе.
Важно подчеркнуть, что современная медицина не имеет пока более эффективного средства профилактики инфекционных заболеваний, чем вакцинация.
Календарь профилактических прививок детям
Возраст | Название прививки | Вид вакцинации |
12 часов | вирусный гепатит В (ВГВ) | первая вакцинация |
3-5 суток | туберкулез (БЦЖ) | вакцинация |
1 мес. | ВГВ | вторая вакцинация |
3 мес. | полиомиелит | первая вакцинация |
4 мес. | АКДС, полиомиелит | вторая вакцинация |
5 мес. | АКДС, ВГВ, полиомиелит [или инактивированная полиомиелитная вакцина (ИПВ)] | третья вакцинация |
1 год | корь, краснуха, эпидемический паротит | первая вакцинация |
2 года | полиомиелит | вторая ревакцинация |
6 лет | корь, краснуха, эпидемический паротит дифтерия, столбняк | ревакцинация |
7 лет | полиомиелит туберкулез (БЦЖ) | третья ревакцинация ревакцинация |
13 лет | ВГВ (если ранее не прививался) | трехкратная вакцинация |
14 лет | туберкулез (БЦЖ) | ревакцинация |
Каждый год до 15 лет ребенку проводится туберкулинодиагностика (проба Манту)
Вакцинация защищает здоровье человека на каждом этапе его жизни
Пять причин сделать прививку:
- Предупредить ненужные страдания, связанные с заболеванием.

- Предупредить развитие осложненных форм болезни.
- Предупредить негативное влияние на планы семьи.
- Наличие широкого спектра вакцин с высоким профилем безопасности и профилактической эффективности.
Возможность индивидуализации иммунизации: применение разных схем и методов вакцинации для создания достаточного иммунитета у каждого прививаемого человека
Иммунизация – метод создания искусственного иммунитета у людей и животных.
Почему нельзя мочить Манту?
Почти все мы помним из детства туберкулиновую пробу (или реакцию Манту) — тест, который позволяет выявить в организме туберкулёзную инфекцию. Про него до сих пор слагают легенды, основная из которых: Манту нельзя мочить. The Village спросил у будущего педиатра, правда ли это и если да, то по какой причине.
Надежда Потимко
студентка 6-го курса Педиатрического университета
Пробу Манту делают всем детям и подросткам. Вакцинированным БЦЖ (это прививка против туберкулёза) первую пробу Манту выполняют в двенадцатимесячном возрасте. Детям, не вакцинированным БЦЖ, пробу проводят с шестимесячного возраста раз в полгода до получения прививки, а в дальнейшем — раз в год. Пропускать пробы крайне нежелательно.
Детям, не вакцинированным БЦЖ, пробу проводят с шестимесячного возраста раз в полгода до получения прививки, а в дальнейшем — раз в год. Пропускать пробы крайне нежелательно.
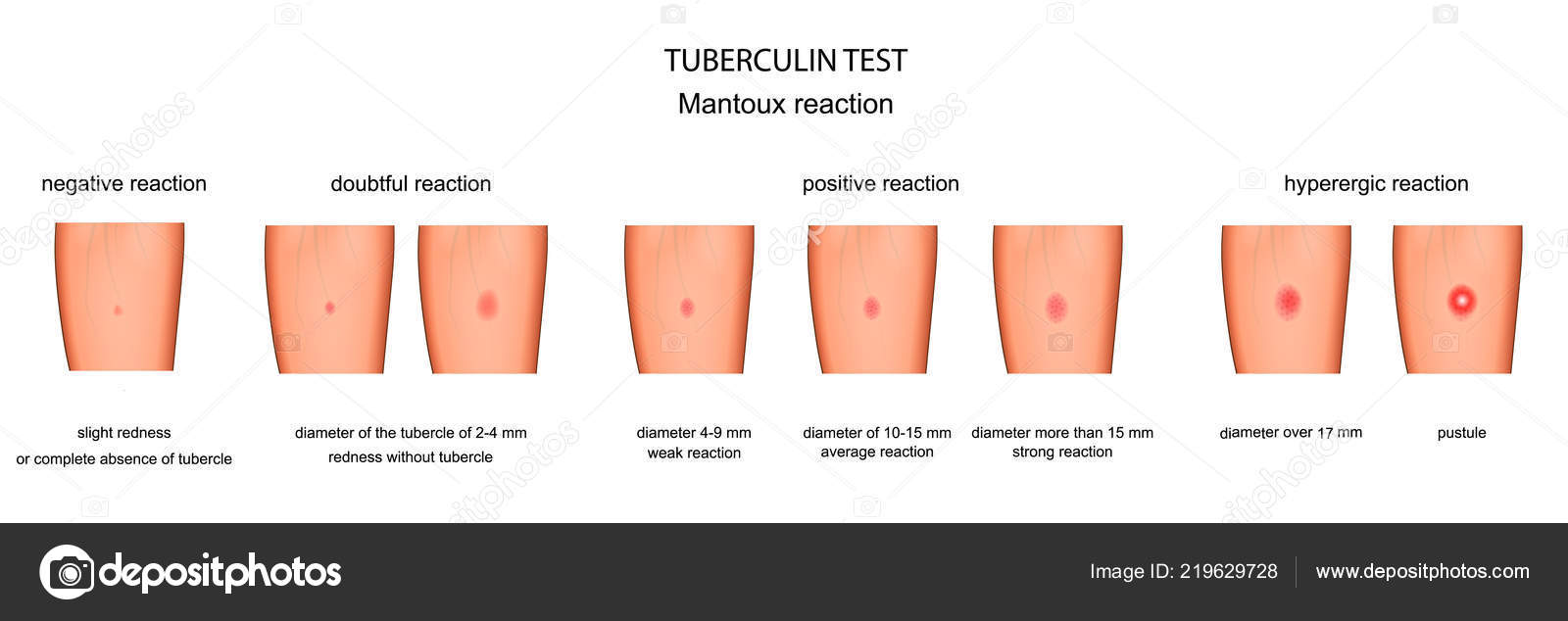
Результат пробы оценивают через 72 часа, измеряя размер папулы, которая развивается на месте введения препарата.
Можно ли мочить Манту? На самом деле мыться в течение этих трёх дней, конечно, можно, но осторожно — руки лучше не касаться. Можно защитить платком или полотенцем, но не полиэтиленом или пластырем: под недышащим материалом кожа сопреет, размокнет. Попадание воды — раздражение, которое вызовет усиление реакции, и её могут счесть положительной. Тогда потребуются дополнительные пробы. То есть брызги при усердном мытье рук не опасны, а вот посещение бассейна, сауны или бани стоит отложить. И совершенно точно нельзя Манту греть, тереть, чесать или покрывать йодной сеткой.
В остальном реакция на пробу Манту может быть положительной, если человек действительно инфицирован или уже болен, а также если его иммунный ответ чем-то усилен — например, инфекционным или соматическим заболеванием или аллергией.
Взрослым пробу Манту не делают: массовым методом диагностики является ежегодная флюорография. Вообще туберкулёз коварен бессимптомностью начала и тяжестью течения, так что не защищаться от него прививками и отказываться от своевременной диагностики опасно для жизни.
Иллюстрация: Настя Яровая
(PDF) Гигантская реакция Манту
www.ijmm.org
79Январь-март 2009
профессиональные контакты и неконтактные. Бугорок
1984; 65: 191-4.
Агарвал П. Туберкулиновая кожная проба. В: Sharma SK, Mohan A, 2.
редакторы. Туберкулез. 1
ул
изд. Нью-Дели: Jaypee Brothers
Medical Publishers (P) Ltd; 2006. с. 117-32.
Waters MF, Stanford JL. Гигантские реакции на туберкулин у 3.
больных лепроматозной лепрой.Int J Lepr Other Mycobact Dis
1985; 53: 546-53.
R Avasthi, * SC Chaudhary, D Mohanty
Медицинский факультет, Медицинский колледж университета
Больница наук и Гуру Тег Бахадур, Дели, Индия
* Автор для переписки (электронная почта: rediffmail. Получено: 18.06.08 Принято: 6.07.08 Сравнение традиционного метода культивирования крови в бульоне и ручного лизиса Метод центрифугирования для обнаружения фунгемии Уважаемый редактор, Фунгемия связана с высокая заболеваемость и смертность балла.Были внедрены различные методы диагностики фунгемии , такие как обычная бульонная культуральная среда, слепых или макроскопических субкультур, вентилируемая и аэрированная двухфазная культуральная среда , культуральная среда с перемешиванием лизиса-фильтрацией, радиометрические и нерадиометрические методы , центрифугирование лизиса метод и т. Д. [1] Из них разумной альтернативой представляется метод лизиса-центрифугирования , который сочетает в себе двойное преимущество : повышенный выход и короткое время обнаружения по сравнению к традиционной системе гемокультуры . [2] Центрифугирование лизиса коммерчески доступно в виде изолирующей системы , оно также может быть выполнено вручную [3] , для которого доступны ограниченные исследования. направлено на оценку техники центрифугирования с ручным лизисом для выявления фунгемии . Девяносто шесть пациентов были обследованы в больнице общего профиля третичного уровня в Мумбаи с октября 2004 г. по февраля 2006 г.Пациенты с факторами риска, такими как длительный прием антибиотиков широкого спектра действия, длительная госпитализация, введение центральных и периферических линий, респираторная вентиляция, наличие мочевого катетера, использование цитотоксических препаратов, недоношенность и низкие роды веса были включены в исследование . У каждого пациента были собраны образцы крови и обработано двумя способами; обычный посев крови и ручное центрифугирование лизиса (MLC).Традиционный метод был выполнен путем посева крови в культуру крови бутылок, содержащих бульон для инфузии сердца мозга. Бутылки инкубировали при 37 0 ° C и периодически встряхивали. делали субкультуры на скошенных срезах Sabouraud Dextrose Agar (SDA). [1,4] Методика MLC была , следуя описанию Bianchi et al. [3] Образцы крови собирали в автоклавированную центрифужную пробирку, содержащую изотонический физиологический раствор с 5% сапонином и 0.4% натриевая соль полианэтолсульфоновой кислоты. Содержимое перемешивали встряхиванием. Выдержав пробирок при комнатной температуре в течение 1 часа, центрифугировали при 3000 об / мин в течение 30 минут. Супернатант удаляли и осадок инокулировали на SDA и кровяной агар для инфузии сердца мозга (BHIA) в дупликации с соблюдением асептических мер предосторожности. Один набор SDA и BHIA инкубировали при комнатной температуре, а другой набор — две культуральные среды при 37 0 ° C в течение 6 недель.Рост грибов определяли стандартными микологическими методами. [5] Все грибковые изоляты принадлежали Candida spp. Кандидемия была диагностирована путем выделения Candida spp. по крайней мере из двух образцов культуры крови или одного образца культуры крови с подтверждающими клиническими признаками. Статистический анализ был выполнен с использованием критерия хи-квадрат в статистическом программном обеспечении Minitab 14. Для проверки статистической значимости урожайности Candida и времени , необходимого для его роста с помощью обоих методов, был проведен критерий хи-квадрат . и были получены точные P-значения (P ≤ 0.01 считалось значительным). Из 96 обследованных пациентов 32 (33,3%) имели фунгемию. C. albicans был выделен у 17 (53,1%), C. parapsilosis — у , — у шести (18,8%), C. tropicalis — у пяти (15,6%) и C. glabrata — — у четырех (12,5%) пациентов. одним или обоими методами. Из 32 образца с положительной культурой 17 (53,1%) изолятов выросли с помощью обоих методов, 12 (37,5%) выросли с помощью MLC, а три (9. Следовательно, 20 (62,5%) были положительными при использовании стандартного метода , тогда как 29 (90,62%) были положительными при использовании MLC. Таким образом, было обнаружено, что центрифугирование с лизисом вручную превосходит метод по сравнению с обычным методом в том, что выход Candida был больше при использовании прежнего метода (значение P 0,008). Время, необходимое для обнаружения грибкового патогена к , оба метода также были соблюдены. Максимальное количество изолятов выросло за первую неделю при использовании обоих методов, всего из 18 (90%) выросло за первую неделю обычным методом и 28 (96.5%) методом MLC. Было замечено, что только два (10%) изолята были выделены в течение 48 часов с помощью обычного метода, в то время как девять (31%) изолятов были выделены методом MLC в течение 48 часов (таблица 1). Время, необходимое для роста Candida с помощью MLC, меньше , хотя эта разница не была обнаружена статистически значимой (значение P 0,083). оказался лучшим методом для восстановления C.albicans из крови в данном исследовании. Одиннадцать (64,7%) изолятов C. albicans выросли обычным способом, а 17 (100%) изолятов — методом MLC. Было обнаружено, что разница составляет Соответствие Через 24 часа после получения стандартной кожной пробы 5-единиц очищенного протеинового производного туберкулина (PPD) 22-летний афроамериканец представил со слегка розовым приподнятым твердым налетом на месте инъекции ( A ).Его предыдущие результаты теста PPD были отрицательными. Он отрицал какие-либо конституциональные симптомы и высыпания. В остальном он был здоров, не принимал никаких лекарств и не имел ВИЧ. Бляшка имела диаметр 20 мм и гранулематозный вид с резкими границами, которые не изменились после 48 часов наблюдения. Ударная биопсия поражения показала выраженный спонгиотический дерматит с внутриэпидермальной и субэпидермальной везикуляцией и разбросанными эозинофилами, что соответствует гиперчувствительности туберкулинового типа. Во время теста PPD (Манту) туберкулиновый антиген вводится внутрикожно. Положительный ответ, который обозначается уплотнением, образованием пузырей или гиперчувствительностью, представляет собой реакцию гиперчувствительности IV типа (замедленного типа). 1 Реакции типа IV вовлекают сенсибилизированные Т-лимфоциты, которые рекрутируются в участок PPD, где высвобождаются цитокины, такие как интерферон гамма и фактор некроза опухоли. Последующее уплотнение возникает в результате расширения сосудов, отека, отложения фибрина и привлечения других воспалительных клеток. Согласно вкладышу в упаковку, атипичные реакции, такие как волдыри, гранулемы и местный некроз, после теста PPD очень редки. 2 Из более чем 5000 туберкулиновых кожных тестов, которые мы провели за последние 5 лет, был только 1 случай образования волдырей на участке PPD ( B ) и 1 гиперчувствительная реакция повышенной чувствительности (см. фото A ) . Тем не менее, местный некроз был зарегистрирован у 2,5% пациентов с положительным ответом. Новый анализ на основе сыворотки — QuantiFERON-TB — оказался эффективным инструментом скрининга на латентную инфекцию Mycobacterium tuberculosis .Анализ может различать ответы, вызванные нетуберкулезными микобактериями; интерпретация результатов гораздо более объективна, чем кожная проба. 4 Ключевой момент: неосложненное уплотнение типично для обычного положительного ответа. Могут возникать местный некроз, образование пузырей и преувеличенные реакции, которые также считаются положительными реакциями. Мнения или утверждения, содержащиеся в данном документе, являются частной точкой зрения авторов и не должны рассматриваться как официальные или отражающие точку зрения Министерства армии или Министерства обороны. Ссылки: 1. Американское торакальное общество. Стандарты диагностики и классификация туберкулеза у взрослых и детей. Am J Respir Crit Care Med. 2000; 161: 1376-1395. Цели . Оценить корреляцию между продолжительностью лечения преднизоном и метотрексатом (MTX) и дозировкой с диаметром уплотнения TST-реакции у пациентов с ревматоидным артритом (RA). Метод . Мы ретроспективно проанализировали последовательные случаи пациентов с РА, которые были кандидатами на терапию TNF-i. Поскольку ежегодно регистрируется почти 8 миллионов новых случаев туберкулеза (ТБ), заболеваемость и смертность от ТБ остаются серьезными проблемами в мире. Хотя иммунный ответ человека очень эффективен при контроле начальной инфекции Mycobacterium tuberculosis [1], у некоторых людей не могут быть уничтожены все жизнеспособные организмы, что приводит к латентной туберкулезной инфекции (ЛТИ).Люди с ЛТИ бессимптомны, но они являются носителями микроорганизмов Mycobacterium, которые могут реактивироваться и вызывать заболевание при определенных обстоятельствах, связанных с известными факторами риска. Принято считать, что пациенты с системными воспалительными заболеваниями восприимчивы к инфекции ТБ из-за подавления их иммунной системы, которое может быть вызвано стероидным лечением или лечением противоревматическими препаратами, модифицирующими заболевание (DMARD), или наличием самого заболевания. Примерно 10 лет назад туберкулиновая кожная проба (ТКП) была единственным доступным тестом для выявления ЛТИ. Однако его точность среди определенных групп пациентов сомнительна.Согласно руководящим принципам Центров по контролю и профилактике заболеваний уплотнение ≥ 5 мм классифицируется как положительное в следующих группах: пациенты с ВИЧ-инфекцией, пациенты, недавно имевшие тесный контакт с людьми, инфицированными ТБ, пациенты, перенесшие трансплантацию органов или получают иммуносупрессивную терапию (например, TNF-1, метотрексат, преднизон и циклоспорин), и пациенты, у которых рентгенограммы грудной клетки показывают фиброзные изменения, соответствующие перенесенному ТБ [4]. Несколько факторов были упомянуты как факторы, влияющие на результаты кожного теста TST. Интерпретация результатов теста затруднена у пациентов, получивших вакцину Bacille Chalmette-Guerin или подвергшихся воздействию нетуберкулезных микобактерий. У пациентов с ревматическим заболеванием, иммунный ответ которых нарушен, ТКП также может быть неверно истолкована. Действительно, среди пациентов с ревматическим заболеванием эффективность теста страдает от низкой положительной и отрицательной прогностической ценности [4, 5]. Целью исследования было оценить корреляцию между продолжительностью и дозировкой лечения преднизоном и метотрексатом (МТ) с размером реакции ТКП у пациентов с РА. Поскольку основной целью этого исследования было сравнение распределений результатов TST, оценки результатов на «положительные» или «отрицательные» не проводились. Это ретроспективное исследование было проведено в отделении ревматологии в сотрудничестве с отделением пульмонологии Медицинского центра Барзилай, Израиль.ТКП выполняли по методу Манту путем инъекции 5 туберкулиновых единиц (ТЕ) очищенного производного белка во внутреннюю поверхность предплечья и последующего измерения максимального размера уплотнения через 72 часа, как рекомендовано [6]. Исследование проводилось в едином центре, и все измерения TST проводились одним высококвалифицированным наблюдателем. Анергия была исключена повторением TST в течение двух недель для всех субъектов, у которых исходный результат TST был 0 мм. Мы сравнили результаты среднего размера реакции TST между следующими группами: пациенты с РА, которые проходили лечение преднизоном во время TST, пациенты с РА, не принимавшие преднизон в анамнезе, и здоровые люди. Наша выборка исследования включала 43 (средний возраст 57,7 ± 13,1 года, 86% женщин) пациентов с РА, получавших лечение преднизоном, 22 (средний возраст 59,9 ± 10,8 лет, 73% женщины) пациентов, не получавших преднизон, и 195 (средний возраст 51,5 ± 10,9 года, 67% женщины) здоровые субъекты (HS). (7) 9000 мы не обнаружили существенной разницы средние значения TST между тремя группами. У пациентов с РА, получавших лечение преднизоном, средний размер TST составлял 5,3 мм ± 6,6 мм; в группе пациентов с РА без лечения преднизоном средний размер TST составлял 7,8 мм ± 6,2 мм; а в группе HS средний размер TST составил 7.6 мм ± 7,0 мм, p = 0,149 (таблица 2 и рисунок 1). ) Не было обнаружено корреляции между размером TST и преднизоном [среднее значение uy = 5,2 ± 5,6, (r = 0,229, p = 0,140)] и между размером TST и метотрексатом uy у пациентов, получавших терапию преднизоном [среднее uy = 14. Точный диагноз ЛТИ у пациентов до начала лечения TNF-i и последующего профилактического противотуберкулезного лечения имеет решающее значение для предотвращения реактивации ТБ. Принятая в настоящее время стратегия скрининга, основанная на ТКП, рентгенографии грудной клетки и данных, собранных с помощью опросника стратификации риска, значительно снизила скорость реактивации ТБ при терапии TNF-i [7].Несмотря на этот успех, правильный подход к диагностике ЛТИ все еще обсуждается. Основная проблема связана с интерпретацией результатов ТКП у пациентов с воспалительным артритом [8]. У пациентов с РА, получающих лечение иммунодепрессантами, неправильная интерпретация может привести к ложноотрицательным результатам тестов, что может нанести серьезный вред пациентам. Чтобы избежать ложноотрицательных результатов среди пациентов, рекомендуемый размер уплотнения составляет 5 мм. Результаты нашего исследования, в котором не было обнаружено ослабления результатов TST среди пациентов с РА по сравнению с пациентами с HS, контрастировали с результатами предыдущих исследований, которые показали ослабленный ответ [9, 10], но согласуются с результатами нескольких других исследования [3, 11, 12].Наблюдаемые расхождения, вероятно, связаны с различиями между некоторыми особенностями стран, в которых проводились исследования. Например, хотя в развивающихся странах реакция TST может быть ослаблена в результате плохих социально-экономических условий и статуса дополнительных заболеваний, в развитых странах эти эффекты уменьшены или отсутствуют. Снижение порогового значения для положительной реакции TST до 5 мм среди пациентов с РА, получающих иммуносупрессивные препараты, может привести к выявлению большего числа случаев ЛТИ.Хотя это увеличение будет происходить за счет соответствующего увеличения доли ложноположительных результатов, снижение порогового значения оправдано, если ослабляющее действие иммуносупрессивных препаратов на реакцию размера TST убедительно доказано. Известно, что высокие дозы преднизона (более 15 мг / сут) оказывают ослабляющее действие на размер TST, о чем согласны все исследования. Однако эффективность длительного лечения пациентов с РА низкими дозами преднизона (менее 10 мг) окончательно не определена [10, 11, 13]. В нашем исследовании использование низких доз преднизона не было связано с уменьшением размера уплотнения TST у пациентов с РА по сравнению с пациентами с HS, даже если лечение продолжалось в течение нескольких лет. Точно так же метотрексат не влиял на результаты ТКП, как в предыдущем исследовании [11]. Следовательно, учитывая результаты нашего исследования вместе с результатами предыдущих работ, снижение порогового значения размера уплотнения для реакции TST у пациентов с РА может быть оправдано в местах с высокой распространенностью инфекции ТБ.В других местах, где распространенность инфекции ТБ невысока, такое снижение может привести лишь к ограниченному сокращению ложноотрицательных результатов. Кроме того, это также может привести к увеличению ложноположительных результатов TST и, как следствие, к предоставлению ненужного лечения. У нашего исследования есть несколько ограничений. Во-первых, небольшое количество испытуемых (n = 260) может снизить шансы на получение статистически значимых результатов. Во-вторых, мы не анализировали корреляцию между результатами ТКП и активностью заболевания, и мы не могли предоставить статус БЦЖ для участников исследования.Однако, поскольку участники нашего исследования могли получать вакцинацию БЦЖ только в раннем детстве, средний возраст участников предполагает, что их предыдущая вакцинация не должна влиять на ТКП, поскольку защита от вакцинации БЦЖ со временем снижается и обычно длится до 10 лет [14]. В-третьих, хотя тест TST является субъективным и могут возникать вариации внутри наблюдателя, золотой стандарт диагностики латентного туберкулеза был недоступен для нас, поскольку тест QuantiFERON или тест Golden T-Spot обычно не выполняются в нашей стране.Наконец, средний возраст нашей группы пациентов в исследовании был значительно выше, чем у здоровых контролей, сценарий, который может привести к меньшему диаметру TST в группе пациентов по сравнению со здоровым контролем. В заключение, представленные здесь данные свидетельствуют о том, что соблюдение принятых основанных на ТКП рекомендаций по диагностике ЛТИ, основанных на пороговом значении размера реакции ТКП, равном 5 мм, может привести к переоценке величины эффекта в виде чрезмерно большого числа положительных результатов, которые, в свою очередь, приводят к гипердиагностике ЛТИ.Наши данные наводят на мысль о пересмотре алгоритмов, используемых для тестирования на ЛТИ, особенно для неэндемичных популяций. Фактически, для таких популяций может быть оправдана замена традиционного TST новыми диагностическими инструментами, такими как анализ QuantiFERON. Для проверки наших результатов необходимы более масштабные исследования. Данные, использованные для подтверждения результатов этого исследования, включены в статью. Ольга Рейтблат, Цахи Т.Лерман, Орнит Коэн и Татьяна Рейтблат заявляют, что у них нет конфликта интересов в отношении публикации этой статьи. com )
com ) Настоящее исследование
Настоящее исследование На 3-й, 5-й и 7-й день
На 3-й, 5-й и 7-й день
 4%) обычным способом.
4%) обычным способом. Метод MLC
Метод MLC Ответы на атипичные кожные туберкулиновые пробы
 3
3 Ссылки:
2. Производное очищенного белка туберкулина (Манту) Tubersol ® Диагностический антиген. Авентис Пастер, Свифтвотер, Пенсильвания. Доступно по адресу: www.vaccineshoppe.com/US_PDF/752-21_4611.pdf. Проверено 5 июля 2007 г.
Производное очищенного белка туберкулина (Манту) Tubersol ® Диагностический антиген. Авентис Пастер, Свифтвотер, Пенсильвания. Доступно по адресу: www.vaccineshoppe.com/US_PDF/752-21_4611.pdf. Проверено 5 июля 2007 г.
3. Фолль М. Уменьшение чрезмерных реакций после туберкулиновой кожной пробы (метод Менделя-Манту) [на немецком языке]. Gesundheitswesen. 2002; 64: 544-547.
4. Mazurek GH, LoBue PA, Daley CL, et al. Сравнение гамма-анализа цельной крови с туберкулиновым кожным тестом для выявления латентной инфекции Mycobacterium tuberculosis . JAMA. 2001; 286: 1740-1747. Влияние преднизона на реакцию туберкулиновой кожной пробы у пациентов с ревматоидным артритом
 Были записаны измерения TST, дозы преднизона и метотрексата и продолжительность лечения. Контрольную группу случайным образом выбирали из здоровых испытуемых. Мы сравнили размер реакции TST между следующими тремя группами: пациенты с РА, получавшие текущее лечение преднизоном, пациенты, ранее не получавшие преднизон, и здоровые люди. Результатов . В нашу выборку вошли 43 пациента с РА, получавших преднизон, 22 пациента, ранее не получавших преднизон, и 195 здоровых субъектов.Не было значимой разницы в средних значениях TST между группами (5,3 ± 6,6, 7,8 ± 6,2 и 7,6 ± 7,0, соответственно, p = 0,149). Не было отмечено корреляции между размером TST и преднизоном uy (r = 0,229, p = 0,140) или метотрексатом uy у пациентов с и без терапии преднизоном (r = 0,219, p = 0,158; и r = -0,293, p = 0,186, соответственно) . Выводы . Наши результаты показывают, что терапия преднизоном не может влиять на размер реакции TST у пациентов с РА. Кроме того, реакция TST у пациентов с РА может быть такой же, как у здоровых людей.
Были записаны измерения TST, дозы преднизона и метотрексата и продолжительность лечения. Контрольную группу случайным образом выбирали из здоровых испытуемых. Мы сравнили размер реакции TST между следующими тремя группами: пациенты с РА, получавшие текущее лечение преднизоном, пациенты, ранее не получавшие преднизон, и здоровые люди. Результатов . В нашу выборку вошли 43 пациента с РА, получавших преднизон, 22 пациента, ранее не получавших преднизон, и 195 здоровых субъектов.Не было значимой разницы в средних значениях TST между группами (5,3 ± 6,6, 7,8 ± 6,2 и 7,6 ± 7,0, соответственно, p = 0,149). Не было отмечено корреляции между размером TST и преднизоном uy (r = 0,229, p = 0,140) или метотрексатом uy у пациентов с и без терапии преднизоном (r = 0,219, p = 0,158; и r = -0,293, p = 0,186, соответственно) . Выводы . Наши результаты показывают, что терапия преднизоном не может влиять на размер реакции TST у пациентов с РА. Кроме того, реакция TST у пациентов с РА может быть такой же, как у здоровых людей. Поэтому мы предлагаем пересмотреть критерий реакции ТКП 5 мм для определения латентной инфекции ТБ в нашей популяции.
Поэтому мы предлагаем пересмотреть критерий реакции ТКП 5 мм для определения латентной инфекции ТБ в нашей популяции. 1. Введение
 Пациенты с ревматоидным артритом (РА) имели повышенную заболеваемость туберкулезом в нескольких исследованиях, в том числе в крупном наблюдательном когортном исследовании из Японии, в котором сообщалось о 3.В 2 раза повышен риск ТБ у больных РА, получавших стандартную терапию БПВП [2]. Хотя введение ингибиторов фактора некроза опухоли альфа (TNF-i) для лечения РА представляет собой значительный прогресс в этой области, терапия связана с увеличением заболеваемости активным туберкулезом среди населения пациентов с РА [3]. .
Пациенты с ревматоидным артритом (РА) имели повышенную заболеваемость туберкулезом в нескольких исследованиях, в том числе в крупном наблюдательном когортном исследовании из Японии, в котором сообщалось о 3.В 2 раза повышен риск ТБ у больных РА, получавших стандартную терапию БПВП [2]. Хотя введение ингибиторов фактора некроза опухоли альфа (TNF-i) для лечения РА представляет собой значительный прогресс в этой области, терапия связана с увеличением заболеваемости активным туберкулезом среди населения пациентов с РА [3]. .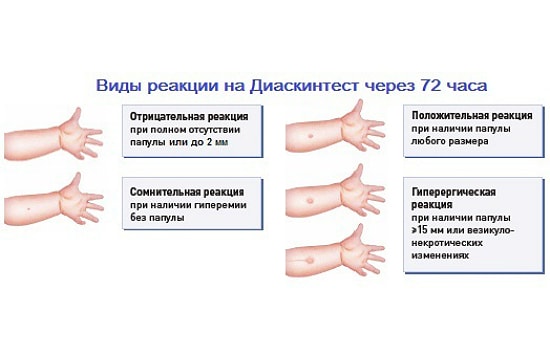 Хотя это руководство относит пациентов с РА, получающих лечение иммунодепрессантами, к группе пациентов с высоким риском развития активного ТБ, оно не определяет ни дозу, ни продолжительность иммуносупрессивного лечения, и в нем упоминается только лечение высокими дозами для лечения пациенты, принимающие стероиды.
Хотя это руководство относит пациентов с РА, получающих лечение иммунодепрессантами, к группе пациентов с высоким риском развития активного ТБ, оно не определяет ни дозу, ни продолжительность иммуносупрессивного лечения, и в нем упоминается только лечение высокими дозами для лечения пациенты, принимающие стероиды. В этом отношении величина реакции TST сравнивалась у пациентов с РА, получавших и не принимавших преднизон. Кроме того, сравнивали размер реакции TST между здоровыми субъектами (HS) и пациентами с РА, которые лечились иммуносупрессивными препаратами.
В этом отношении величина реакции TST сравнивалась у пациентов с РА, получавших и не принимавших преднизон. Кроме того, сравнивали размер реакции TST между здоровыми субъектами (HS) и пациентами с РА, которые лечились иммуносупрессивными препаратами. 2. Пациенты и методы
 Второй результат был признан окончательным.Информация для социально-демографических анкет и анкет для скрининга на туберкулез была получена из медицинских карт, и были записаны текущая история болезни и лечение. Общие критерии исключения: активный туберкулез, наличие активного туберкулеза в анамнезе и недавний иммигрант (менее 5 лет в Израиле). Кроме того, были ретроспективно рассмотрены последовательные случаи пациентов с РА, которые были кандидатами на терапию TNF-i. Были записаны измерения TST, дозы преднизона и метотрексата и продолжительность лечения. Активный туберкулез (ТБ) был исключен на основании рентгенологического исследования грудной клетки и анамнеза пациента.Контрольная группа была случайным образом выбрана из здоровых людей, прошедших ТКП в пульмонологической клинике нашего учреждения.
Второй результат был признан окончательным.Информация для социально-демографических анкет и анкет для скрининга на туберкулез была получена из медицинских карт, и были записаны текущая история болезни и лечение. Общие критерии исключения: активный туберкулез, наличие активного туберкулеза в анамнезе и недавний иммигрант (менее 5 лет в Израиле). Кроме того, были ретроспективно рассмотрены последовательные случаи пациентов с РА, которые были кандидатами на терапию TNF-i. Были записаны измерения TST, дозы преднизона и метотрексата и продолжительность лечения. Активный туберкулез (ТБ) был исключен на основании рентгенологического исследования грудной клетки и анамнеза пациента.Контрольная группа была случайным образом выбрана из здоровых людей, прошедших ТКП в пульмонологической клинике нашего учреждения. Следующий субанализ был проведен для включения лечения метотрексатом среди пациентов с РА. Для сравнения различий между группами использовали односторонний дисперсионный анализ.Мы ввели оценку за единицу-год ( u-y ) лечения с учетом средней дозы лекарства и количества лет, в течение которых лекарство принималось. Затем мы рассчитали u-y баллов для преднизона и метотрексата, разделив дозировку лекарства на его минимальную единицу (5 мг / день и 2,5 мг / неделю, соответственно), а затем умножив результат на количество лет лечения. Корреляция между этими баллами и размером реакции TST оценивалась с использованием коэффициента корреляции Пирсона (r).Значения p <0,05 считались значимыми.
Следующий субанализ был проведен для включения лечения метотрексатом среди пациентов с РА. Для сравнения различий между группами использовали односторонний дисперсионный анализ.Мы ввели оценку за единицу-год ( u-y ) лечения с учетом средней дозы лекарства и количества лет, в течение которых лекарство принималось. Затем мы рассчитали u-y баллов для преднизона и метотрексата, разделив дозировку лекарства на его минимальную единицу (5 мг / день и 2,5 мг / неделю, соответственно), а затем умножив результат на количество лет лечения. Корреляция между этими баллами и размером реакции TST оценивалась с использованием коэффициента корреляции Пирсона (r).Значения p <0,05 считались значимыми. 3. Результаты
 Средний возраст между группами пациентов с РА и группой HS значительно различается, и, следовательно, значительно более высокая частота системной гипертензии была обнаружена в группах с RA.По другим заболеваниям между группами не было различий. Исходные характеристики пациентов с РА и ГС показаны в Таблице 1.
Средний возраст между группами пациентов с РА и группой HS значительно различается, и, следовательно, значительно более высокая частота системной гипертензии была обнаружена в группах с RA.По другим заболеваниям между группами не было различий. Исходные характеристики пациентов с РА и ГС показаны в Таблице 1. Переменная Пациенты с РА (n = 654) Контроль (n = 195) Значение P Возраст (лет) 58.4 ± 12,3 51,5 ± 10,9 <0,001 Женский ( ) 53 (82) 131 (67) 0,028 Системная гипертензия ( ) 38 (59) 64 (33) <0,001 Сахарный диабет (15323 ) 9034 9034 (11) 0.  383
383 Сердечно-сосудистые заболевания ( ) 3 (5) 16 (8) 0,420 Хроническая болезнь легких ( ) 9033 1433 0,372 Хроническая почечная недостаточность ( ) 3 (5) 9 (5) 0,999 Болезнь печени ( ) 2) 9 (5) 0.459 История злокачественных новообразований ( ) 2 (3) 5 (3) 0,999 
Размер TST (мм) РА с терапией преднизоном (n = 43) РА с терапией преднизоном (n = 43) Элементы управления (n = 195) Значение P Среднее ± SD 5.3 ± 6,6 7,8 ± 6,2 7,6 ± 7,0 0,149 Медиана 3,0 4,5 7,0 Диапазон 9034 0, 9034 0 ] 0, 27]  4 ± 28,2 (r = 0,219, p = 0,158)] или без терапии преднизоном [среднее u-y = 30,7 ± 32,4 (r = -0,293, p = 0,186)] (рис. 2).
4 ± 28,2 (r = 0,219, p = 0,158)] или без терапии преднизоном [среднее u-y = 30,7 ± 32,4 (r = -0,293, p = 0,186)] (рис. 2). 4. Обсуждение
Доступность данных
Конфликт интересов