Синовит: Виды,Симптомы,Лечение | Doc.ua
Виды
Синовит может носить инфекционный или неинфекционный характер. Инфекционный синовит, причины которого кроются в инфекциях, может появиться из-за проникновения в полость синовиальной оболочки крови или лимфы возбудителя, к примеру, из другого инфекционного очага воспаления в организме. Он может быть осложнением гнойно-воспалительного процесса, например, сифилиса, туберкулеза и т.д. Кроме того, он может развиваться, если в полость синовиальной оболочки проникла травма.
Неинфекционные синовиты разделяются на следующие подвиды:
- травматические, которые возникают как результат травмы связки или сустава. Часто встречаются у спортсменов и у больных гемофилией;
- аллергический – встречается реже, может являться осложнением перенесенных инфекционных заболеваний;
- возникающий на фоне эндокринных изменений, например, у диабетиков;
- нейрогенный, который возникает в результате сильного стресса или неврологических заболеваний.
Симптомы
При синовите поражается один сустав или связка, множественный характер заболевание носит только изредка. При такой болезни, как синовит, симптомы могут быть общими для различных форм заболевания.
Общие признаки синовита для всех типов таковы:
- отеки и сглаживание контуров суставов;
- болевые ощущения при нагрузке, снижение уровня движения в пораженной зоне;
- повышение температуры тела – общей или в пораженном участке;
- слабость, плохое самочувствие.
Некоторые из указанных симптомов могут быть проявляться сильнее иных, однако при инфекционных синовитах все признаки выражены больше, чем при неинфекционных.
Симптомы инфекционной формы: инфекционный синовит почти всегда начинается остро, резко повышается температура тела, появляется боль и чувство распирания в суставах. Через несколько часов сустав отекает, появляются симптомы: интоксикация, головная боль, слабость, беспокойство, изредка возможна рвота.
Признаки неинфекционной формы: симптомы неинфекционных форм развиваются медленнее с существенной вариацией, которая может зависеть от причины заболевания. Первый симптом – это ощущение дискомфорта в зоне пораженного сустава и боль при нагрузке на него. Заболевание развивается на протяжении нескольких дней. Постепенно проявляется отечность, деформация сустава, нарастание боли. Если болезнь протекает легко, то симптомы могут исчезнуть сами, а после заболевание может пройти само.
Диагностика
Чтобы диагноз был подтвержден, проводится пункция, которая заключается в обезболивании сустава и прокалывании его иглой с целью забора синовиальной жидкости на диагностичекое исследования. Почти всегда такое действие дает возможность правильно определить тактику лечения и построить прогноз. Однако, специалист может назначить и другие, дополнительные методы исследования, например, УЗИ суставов, рентген сустава или же исследования крови, которые способны отличить синовит от иных заболеваний опорно-двигательного аппарата.
Лечение
Диагностику и лечение заболевания должен проводить врач-хирург. Цель лечения – не только устранить заболевание, которое стало причиной синовита, но и не допустить, чтобы развился хронический синовит. Продолжительность лечения и его особенности определяются причинами и характером течения болезни, общим состоянием здоровья человека и точно поставленным диагнозом.
Если болезнь проходит легко, то можно туго забинтовать сустав для его обездвиживания, пока организм самостоятельно не устранит процесс воспаления. При более серьезных случаях должна быть проведена пункция, которая устраняет лишнюю жидкость, а также назначены антибиотики или противовоспалительные аппараты для введения внутрь.
Смесь препаратов, которые будут вводиться внутрь сустава, должна зависеть от результата проведенного исследования суставной жидкости и анализа возможных аллергических реакций:
- при наличии бактерий определяют их чувствительность и добавляют в состав смеси антибиотики, разведенные в растворе обезболивающего;
- если бактериальный компонент выявлен не был, то используются так называемые «коктейли» против воспаления, которые включают в себя противовоспалительные препараты, обезболивающие и некоторые витамины и их комплексы.
 Такие смеси отличаются высокой эффективностью и сильным противовоспалительным и восстанавливающим действием.
Такие смеси отличаются высокой эффективностью и сильным противовоспалительным и восстанавливающим действием.
После проведения процедур на область поражения врач назначает УВЧ или электрофорез. Если такое лечение не приносит результатов, что бывает в крайних случаях, то проводится операция, направленная на полное или частичное удаление синовиальной оболочки.
Успешность лечения, как и его длительность, прямо зависят от сроков постановки диагноза и времени начала лечения.
Если при наличии такой проблемы, как синовит, лечение было произведено грамотно и своевременно, то почти всегда наблюдается полное выздоровление и сохранение функций сустава. Сам процесс лечения болезни продолжается 4–8 дней, после него следует фаза восстановления и профилактики, которая занимает 1–2 недели.
Осложнения
При синовите возможны следующие осложнения:
- артрит;
- снижение объема движения в результате изменений поверхностей суставов или синовиальной оболочки;
- распространение процесса на другие участки связочного аппарата;
- самым серьезным и опасным осложнением является сепсис, который может нести угрозу для жизни. Сепсис представляет собой появление возбудителя в крови, который может развиться у людей со слабым иммунитетом или при долгом отсутствии лечения.
Профилактика
Суть профилактики синовита заключается в вовремя оказанном лечении воспалительных болезней, которые могут его спровоцировать. Очень важно соблюдать меры предосторожности при занятиях спортом, не допускать падения и травм, правильно питаться, чтобы укрепить связочный аппарат и предотвратить синовит суставов или связок.
Поиск препаратов в аптеках можно совершить онлайн в нашем каталоге со всей информацией о медикаментах. Также, есть возможность забронировать нужные препараты.
Диагностика и лечение синовита коленного сустава | | Infopro54
Врачи сети клиник «Здравствуй» помогут вылечить это заболевание. Но в первую очередь они установят причины его развития и на основе поставленного диагноза подберут эффективную терапию.
Но в первую очередь они установят причины его развития и на основе поставленного диагноза подберут эффективную терапию.
Виды синовита и особенности протекания заболевания
Суставная полость заполняется экссудатом, в результате чего сочленение сильно увеличивается в размерах.
Окружая суставы со связками, синовиальная оболочка, гарантирует им защиту, синтезирует смазку, уменьшающую трение в процессе движения.
В большинстве случаев заболевание начинает прогрессировать в крупных суставах. Проверить суставы, и пройти курс лечения позвоночника можно в специализированной клинике.
Синовит классифицируют на инфекционный и неинфекционный.
Первая разновидность развивается при попадании в синовиальную оболочку с кровью возбудителя, к примеру, из другого очага инфекции в организме. Зачастую синовит являет собой осложнение гнойных и воспалительных процессов.
Неинфекционная разновидность данного заболевания может быть вызвана:
- травмами;
- аллергией;
- патологиями эндокринной системы;
- нейрогенными факторами.
Травматическими синовитами чаще всего страдают спортсмены.
Аллергические возникают на фоне пневмонии, бронхита.
Нарушение метаболизма – еще одна возможная причина синовита.
К нейрогенным факторам относят сильный стресс либо осложнения неврологического характера.
Обычно синовит поражает один сустав или связку, множественная патология встречается редко.
Специалисты сети клиник «Здравствуй» сумет установить истинную причину синовита коленного сустава.
Симптомы синовитов
К главным симптомам синовита относят:
- боль при физических нагрузках;
- увеличение температуры тела;
- общее недомогание;
- снижение подвижности в зоне поражения;
- изменение суставных контуров.
Некоторые из этих признаков могут быть более выраженными по сравнению с другими. При инфекционных синовитах симптоматика всегда более явная и проявляется она внезапно, с резким увеличением температуры тела. В суставе возникает боль и чувство распирания, он быстро отекает. Помимо этого, появляются признаки интоксикации – бледнеют кожные покровы, начинает болеть голова.
В суставе возникает боль и чувство распирания, он быстро отекает. Помимо этого, появляются признаки интоксикации – бледнеют кожные покровы, начинает болеть голова.
Развитие неинфекционных синовитов более медленное. Симптомы зависят от причины появления заболевания. Обычно первым признаком становится дискомфорт в пораженной зоне, боль при нагрузке.
Патология развивается за несколько дней, постепенно появляются отеки, боль нарастает, а суставы деформируются.
При легких формах протекания заболевания симптомы в условиях отсутствия нагрузок могут исчезать, в редких случаях возможно самопроизвольное выздоровление.
Диагностика
Чтобы подтвердить диагноз, пациенту делают пункцию: обезболивают и прокалывают тонкой иголкой суставную полость, выполняя последующий забор синовиальной жидкости. Ее подвергают микроскопическому и цитологическому исследованию, чтобы установить причину патологии. Если во взятом на анализ материале обнаруживается возбудитель, определяют его восприимчивость к лекарственным препаратам.
Результаты пункции дают возможность выработать правильную тактику терапии.
Синовит является менее распространенной патологией опорно-двигательного аппарата по сравнению с артритом и остеоартрозом, но они обладают схожей клинической картиной. По этой причине врач может посчитать необходимым проведение дополнительного обследования, например, рентгенографии сустава и ультразвука. Это даст возможность отличить синовит от других патологий.
Терапия синовита коленного сустава
Терапию и диагностику синовита осуществляет врач-хирург. При выявлении этого заболевания важно не допустить его перехода в хроническую форму.
Особенность терапии и продолжительность зависят от тяжести недуга и индивидуального состояния здоровья.
При легкой форме врач может просто забинтовать сустав, чтобы лишить его подвижности до того момента, пока организм самостоятельно не справится с воспалительным процессом.
Если ситуация серьезная, назначают пункцию, чтобы удалить лишнюю жидкость и ввести внутрь лекарства, снимающие воспаление.:max_bytes(150000):strip_icc()/synovial_joint-5b6efd4c46e0fb00253e4c5e.jpg)
Препараты для введения в суставную полость подбирают исходя из результата анализа суставной жидкости, с учетом возможной аллергии.
При обнаружении в ходе исследования бактерий, устанавливают их чувствительность и включают в состав лекарств антибиотики.
Правильно подобранная смесь препаратов позволяет справиться с воспалением и добиться полного излечения с сохранением подвижности сустава.
Источник изображения: pixabay.com
Вопрос от: Светлана — Клиника Здоровье 365 г. Екатеринбург
Вопрос Ревматологу
Вопрос от Светлана
Вопрос: Здравствуйте!
Мне 26 лет. С сентября этого года у меня без всяких внешних причин стали происходить периодически щелчки в коленях (не в обоих сразу, а по очереди), но это было редко, 1раз в 2 недели, преимущественно во время спуска/подъема по лестнице, и потом после щелчка колено болело некоторое время. При приседаниях раздается очень хорошо слышимый хруст. Меня это беспокоило, но особого внимания не обратила. А в ноябре выдались выходные, во время которых пришлось довольно мого ходить, и у меня заболели кости от стопы до колена, затем боль прошла через несколько дней. Я сходила на узи коленного сустава и голеностопа — на левой ноге узи не показало никаких изменений — все в номре, все отлично, а на правой ноге выявили — в полости коленного сустава незначительное количество избыточной жидкости и утолщение синовиальной оболочки, в остальном все в номре и без особенностей; правый голеностопный сустав — в полости незначительное количество выпота, синовиальная оболочка утолщена. Все остальное так же без изменений. Заключение УЗИ — эхографическая картина синовита правого коленного сустава и голеностопного сустава.
Но боли меня волновали и бывали чаще всего и сильней в левой ноге. Переломов у меня никогда никаких не было. Из инфекционных заболеваний недавно был уреаплазмоз в высокой степени, я его лечила, но контрольных анализов еще не делала. Больше никаких серьезных заболевай не было. Только ОРЗ, ОРВИ, один раз лет в 12 ангина без осложнений, и хронический букет болезней ЖКТ (колит, панкреатит, холицистит, гастродуоденит, дисбактериох и т.д.) с самого детства, если не с рождения; все болезни ЖКТ были введены лет в 13 в стойкую ремиссию, никогда больше они меня не беспокоили, и не было даже единичных приступов. Родилась с врожденной дисплазией ног, но мне все вылечили – упражнениями и спец.ремешками. Ревматолог, к которому я обратилась с данными УЗИ, сказала, что скорей всего у меня реактивный артрит, для подтверждения отправила на анализы крови — ОАК, антихламидии A, G, M, АСЛ-О, С-реактивный белок, СОЭ (по Вестергрену). Результаты УЗИ у нее не вызвали никаких вопросов, по ее словам такое иногда бывает, и это нормально, и никакого синовита у меня нет. Предварительное лечение прописала — ЛФК, Доросан-спрей 3 раза в день, свечи Моксалин 15мг 6 дн. Я все это сделала, колени больше не отщелкивали, но появилось ощущение увеличившейся хрупкости костей. В последний прием появились результат анализов крови — антихламидии в пределах референсных значений, отрицательны (т.е. хламидиоза у меня нет), остальные показатели (АСЛ-О, С-реакт.белок, гематокрит, гемоглобин, эритроциты, MCV, MCH, MCHC, лейкоциты, палочкоядерные нейтроф., нейтрофилы сегментояд., нейтрофилы общ.число, лимфоциты, моноциты, эозинофилы, базофилы, СОЭ по Вестергрену) в пределах референсных значений — в норме. Кроме тромбоцитов — референсные значения 150-400 тыс/мкл, а по моим анализам у меня их 138 тыс/мкл. Врач сказала, что это все таки реактивный артрит, отчего появился — ну может быть из-за плоскостопия (оно у меня тоже есть с детства), лечение — ЛФК и препарат Дона — 30 дней по 1 порошку, периодичность лечения 1 раз в полгода. Доросан-спрей применять только во время возникновения сильной боли и только на коленный сустав. И все. А ночью после приема врача, у меня начала ныть левая нога — и по ощущениям, это не мышца, а кость.
Больше никаких серьезных заболевай не было. Только ОРЗ, ОРВИ, один раз лет в 12 ангина без осложнений, и хронический букет болезней ЖКТ (колит, панкреатит, холицистит, гастродуоденит, дисбактериох и т.д.) с самого детства, если не с рождения; все болезни ЖКТ были введены лет в 13 в стойкую ремиссию, никогда больше они меня не беспокоили, и не было даже единичных приступов. Родилась с врожденной дисплазией ног, но мне все вылечили – упражнениями и спец.ремешками. Ревматолог, к которому я обратилась с данными УЗИ, сказала, что скорей всего у меня реактивный артрит, для подтверждения отправила на анализы крови — ОАК, антихламидии A, G, M, АСЛ-О, С-реактивный белок, СОЭ (по Вестергрену). Результаты УЗИ у нее не вызвали никаких вопросов, по ее словам такое иногда бывает, и это нормально, и никакого синовита у меня нет. Предварительное лечение прописала — ЛФК, Доросан-спрей 3 раза в день, свечи Моксалин 15мг 6 дн. Я все это сделала, колени больше не отщелкивали, но появилось ощущение увеличившейся хрупкости костей. В последний прием появились результат анализов крови — антихламидии в пределах референсных значений, отрицательны (т.е. хламидиоза у меня нет), остальные показатели (АСЛ-О, С-реакт.белок, гематокрит, гемоглобин, эритроциты, MCV, MCH, MCHC, лейкоциты, палочкоядерные нейтроф., нейтрофилы сегментояд., нейтрофилы общ.число, лимфоциты, моноциты, эозинофилы, базофилы, СОЭ по Вестергрену) в пределах референсных значений — в норме. Кроме тромбоцитов — референсные значения 150-400 тыс/мкл, а по моим анализам у меня их 138 тыс/мкл. Врач сказала, что это все таки реактивный артрит, отчего появился — ну может быть из-за плоскостопия (оно у меня тоже есть с детства), лечение — ЛФК и препарат Дона — 30 дней по 1 порошку, периодичность лечения 1 раз в полгода. Доросан-спрей применять только во время возникновения сильной боли и только на коленный сустав. И все. А ночью после приема врача, у меня начала ныть левая нога — и по ощущениям, это не мышца, а кость.
Подскажите, пожалуйста, правильно ли мне поставили диагноз, правильное ли назначили лечение? Может ли решить проблему прием только одного этого препарата Дона?
Спасибо
Ответ:
Здравствуйте, Светлана.
По Вашему описанию Вам действительно поставили правильный диагноз — реактивный (т.е. вторичный) артрит. Причиной может быть, как уреаплазмоз, который дает мощный реактивный артрит, так и плоскостопие, на фоне которого страдают все вышерасположенные суставы. Кровь на ИППП (хламидии и уреалазма и др.) не самый надежный метод диагностики. Для подтверждения диагноза необходим ПЦР соскоб на ИППП. При положительном результате показано повторное лечение (санация у гинеколога). При отрицательном результате рекомендую продолжить лечение назначенное ревматологом, добавив к нему препараты кальция, курсом 2-3 месяца 2 раза в год.
С уважением, зав. поликлиническим отделением, Рудник В.Б.
Назад
Самолечение при боли в суставах – вред!
Фото: GLOBAL LOOK PRESS
С ТОЧКИ ЗРЕНИЯ СУСТАВА
Сустав – сложное образование. В него входят как минимум 2 кости, покрытые хрящом, к области сустава прикрепляются сухожилия, рядом с ним проходят нервы и кровеносные сосуды. Изнутри сустав покрывает синовиальная оболочка, в которой находится синовиальная жидкость. И всё это может воспаляться, травмироваться, болеть.
Основные причины боли в суставах условно можно выделить 2: воспаление и механическое повреждение.
Воспаление суставов и боль связаны с синовиальной оболочки. Это выстилка сустава, которая защищает хрящ и вырабатывает «синовиальную жидкость», которая заполняет сустав и обеспечивает его нетравматичное движение. Синовиальная оболочка богата сосудами и нервами, именно здесь зарождается боль.
Воспаляется синовиальная оболочка чаще всего от аутоиммунного поражения – когда иммунная система «путает» её клетки с инфекцией. Инфекций, вызывающих такой артрит, более 30 – это и кишечные, и дыхательные, и урогенитальные патогены. Подобный механизм и при большой группе РЕВМАТИЧЕСКИХ ЗАБОЛЕВАНИЙ. Например, ревматоидный артрит. При этом воспаление суставов – только один из симптомов. Также поражаются кожа, сердце, почки и другие органы.
Еще одна причина – остеоартроз. Это возрастное заболевание, при котором хрящ деградирует, а суставная поверхность разрастается, повреждая синовиальную оболочку. Присоединяется воспаление и появляется боль. Разрастания кости называются «остеофитами» — их иногда можно обнаружить.
Вы всё еще считаете возможным самостоятельно лечить боль в суставах?
С ТОЧКИ ЗРЕНИЯ ЛЕКАРСТВА
Лекарства бывают правильными и неправильными.
Неправильные – это БАДы и так называемые народные средства. Эффективность этих препаратов не доказана, а вред не изучен. Классический пример – чаи для похудания, многие из которых основаны на мочегонном эффекте. Во-первых, удаление из организма жидкости похуданием не является (это просто обезвоживание), во-вторых, любой мочегонный препарат чреват потерей солей, аритмиями, повреждением почек и другими проблемами.
Самое главное свойство правильных лекарств – это показания к приему препарата. И они должны быть ориентированы не на симптом, а на конкретное заболевание. При этом для разных заболеваний – разные дозы и длительность приема. Например, при хламидийном реактивном артрите надо лечить, конечно же, в первую очередь инфекцию – противомикробными средствами.
С ТОЧКИ ЗРЕНИЯ ВРАЧА
Многие пациенты длительно ведут борьбу с болезнью самостоятельно. Пробуют до 5 средств, применяют прогревания в тех случаях, когда это противопоказано. Используют противовоспалительные средства в неправильных дозах и слишком долго, обеспечивая повреждение печени, почек, слизистой желудка.
Иногда такой пациент приходит к врачу уже с запущенным заболеванием и осложнениями проводившегося лечения. Подобрать лечение врач может только на основании обследования – это и рентгенологическое исследование суставов, и лабораторное исследование воспаления.
В федеральной лаборатории «Гемотест» централизованная технологическая база площадью 3 500 квадратных метров включает 5 аналитических лабораторий.
Пример такого обследования – в лаборатории федерального масштаба «Гемотест». Здесь Вы можете пройти обследование на патологию суставов в любом из 185 городов Российской Федерации, где есть отделения лаборатории (подробнее на сайте). Всего в «Гемотест» выполняется более 3 000 лабораторных анализов по всем медицинским специальностям. Из них более 60 – для диагностики заболеваний суставов. Пример скрининга – комплексное исследование СУСТАВЫ, которое включает общий анализ крови и СОЭ, белки воспаления и мочевую кислоту.
Здесь Вы можете пройти обследование на патологию суставов в любом из 185 городов Российской Федерации, где есть отделения лаборатории (подробнее на сайте). Всего в «Гемотест» выполняется более 3 000 лабораторных анализов по всем медицинским специальностям. Из них более 60 – для диагностики заболеваний суставов. Пример скрининга – комплексное исследование СУСТАВЫ, которое включает общий анализ крови и СОЭ, белки воспаления и мочевую кислоту.
Также в отделе молекулярно-генетических исследований выполняются исследования на инфекционные причины воспаления суставов и выявляется генетическая предрасположенность к аутоиммунным заболеваниям.
Для выявления самой частой причины аутоиммунного поражения суставов создано комплексное исследование РЕВМАТОИДНЫЙ АРТРИТ.
С ТОЧКИ ЗРЕНИЯ ПАЦИЕНТА
Медицина – неточная наука. Здесь недостаточно знать какой-то факт. Необходимо знать в теории и практике все аспекты проблемы. Иначе можно жестоко ошибиться.
Пример. Молодой мужчина со значительным избыточным весом похудел на 20 килограммов за достаточно короткий срок – 3 месяца. В конце победного периода борьбы с ожирением у него разболелись суставы. Это вызвало недоумение у пациента и его родственников – «такой большой вес суставы носили и ничего, а тут вдруг разболелись». Причину не могли понять. А для врача она банальная и понятна уже из разговора – подагра. При этом заболевании резкое снижение веса с разрушением белка приводит к существенному повышению мочевой кислоты в крови. Кристаллы мочевой кислоты выпадают на синовиальной оболочке сустава, вызывая её воспаление и очень «злую» жестокую боль. При выполнении биохимического анализа крови у такого пациента будет выявляться повышенный уровень МОЧЕВОЙ КИСЛОТЫ.
Таким образом, проблема воспаления суставов – сложная и требует визита к врачу. Самостоятельно Вы просто можете даже не знать о возможных причинах болезни. Затягивать и заниматься самолечением не стоит – это только ударит по карману и здоровью. Необходимо пройти обследование и грамотно решить вопрос с лечением.
Необходимо пройти обследование и грамотно решить вопрос с лечением.
Будьте здоровы!
Реклама
Пигментный виллонодулярный синовит коленного сустава. Клинический случай.
Дата публикации: 05.07.2018
Пигментный виллонодулярный синовит является идиопатическим пролиферативным заболеванием синовиальной оболочки. Из-за отсутствия типичной специфической клинической картины нередки случаи неправильной и несвоевременной диагностики. При отсутствии лечения данное заболевание может привести к тяжёлым дегенеративным изменениям и остеоартрозу. Для правильной диагностики необходима настороженность в отношении пигментного виллонодулярного синовита. Вследствие редкости данного заболевания (1,8 случая на 1 миллион) не существует «стандартного» лечения, при этом хирургическое удаление патологически изменённых тканей считается предпочтительным. В послеоперационном периоде во многих случаях требуется лучевая терапия.
Пациентка П., 59 лет, обратилась с жалобами на периодическую боль без чёткой локализации в правом коленном суставе, возникающую при увеличении коленного сустава в размере. Боль беспокоила пациенту в течение последних 6 месяцев. Амбулаторно по поводу «рецидивирующего синовита» назначали нестероидные противовоспалительные препараты и физиотерапевтическое лечение, выполнялись многократные пункции коленного сустава, после которых наступало непродолжительное облегчение. При пункции получали жидкость бурого цвета.
Пациентке в КМЦ выполнена операция – артроскопия правого коленного сустава, биопсия синовиальной оболочки, парциальная синовэктомия. Удаление синовиальной оболочки, после забора материала для гистологического исследования, проводили при помощи шейвера/синовиального резектора. (рисунок 1 и 2). После операции пациентка консультирована онкологами КМЦ, направлена на лучевую терапию.
Артроскопическая картина коленного сустава пациентки с виллонодулярным синовитом. Слева – гипертрофированная синовиальная оболочка в межмыщелковом пространстве. Справа – межмыщелковое пространство после резекции гипертрофированной синовиальной оболочки.
Справа – межмыщелковое пространство после резекции гипертрофированной синовиальной оболочки.
Артроскопическая картина коленного сустава пациентки с виллонодулярным синовитом. Слева – гипертрофированная синовиальная оболочка в межмыщелковом пространстве. Справа – межмыщелковое пространство после резекции гипертрофированной синовиальной оболочки.
Артроскопическая картина коленного сустава пациентки с виллонодулярным синовитом. Слева – гипертрофированная синовиальная оболочка в верхнем завороте. Справа – верхний заворот после резекции гипертрофированной синовиальной оболочки.
Артроскопическая картина коленного сустава пациентки с виллонодулярным синовитом. Слева – гипертрофированная синовиальная оболочка в верхнем завороте. Справа – верхний заворот после резекции гипертрофированной синовиальной оболочки.
Другие новости
Синовиальная саркома
Одна из самых частых (9—13%) из злокачественных опухолей мягких тканей. Развивается у людей любого возраста (редко у лиц старше 50 лет) из синовиальных оболочек суставов, сухожильных влагалищ, слизистых сумок и фасций, но чаще всего из синовий крупных суставов нижних и верхних конечностей. Может, однако, возникнуть и в любой другой локализации. Чаще всего поражает коленный и голеностопный суставы — 45%. На суставы приходится 40% случаев, на слизистые сумки 40% и на сухожильные влагалища 20%.
Макроскопически образование часто представлено опухолевым узлом от мягко-эластической (при наличии в опухоли кистозных полостей) до плотной консистенции (при отложении в опухоли солей кальция). Нередки случаи с выраженным инфильтративным ростом, при котором опухоль не выявляет четких границ с окружающими мягкими тканями. Синовиальная саркома довольно часто распространяется на кость и разрушает ее. На разрезе ткань опухоли белого или бело-розового цвета с участками некроза, кровоизлияний, иногда с кистозными полостями и слизистым содержимым, напоминающим синовиальную жидкость.
Морфологически различают два типа синовиальных сарком: волокнистую (напоминающую фибросаркому) и целлюлярную (железистоподобную). Последняя форма имеет тенденцию к образованию папилломатозных выростов, проникающих в кистозные полости. Выделяют также 2 типа опухоли — монофазная и бифазная, последняя имеет лучший прогноз.
Синовиальная саркома — одна из наиболее злокачественных опухолей мягких тканей. Выявлению опухоли могут предшествовать боли, которые отличают синовиальную саркому от большинства других опухолей мягких тканей. В опухоли могут образовываться кистозные полости, и тогда она эластична, или в ней откладываются соли кальция, и тогда опухоль становится плотной. В правильной постановке диагноза помогает локализация опухоли вблизи суставов или костей конечностей.
При рентгенологическом исследовании могут быть обнаружены кальцинаты на фоне мягкотканного образования, деструкция близлежащих тканей. Синовиальная саркома способна к лимфогенному метастазированию.
Рецидивы возникают в 26,4% случаев, при неоадъювантном подходе к лечению — 9,1%, метастсзы 36,7% и 25% соответственно, общая 5-летняя выживаемость составляет 65,1% после комплексного лечения.
Лечение ревматоидного артрита, запись на прием в Нижнем Новгороде
Аутоиммунное заболевание: природа этого заболевания, не смотря на множество провоцирующих факторов (генетика, окружающая среда, инфекции) связана со сбоем в работе иммунной системы. Иммунные комплексы, «оседающие» главным образом на оболочках суставов, (инфекционные антигены + защитные антитела организма человека) запускают целый каскад воспалительных реакций. Происходит превращение нормальной (защитной) воспалительной реакции в хроническую, направленную уже против собственных клеток. Такой сбой/дефект иммунитета в результате и приводит к РА.
Воспалительное и прогрессирующее заболевание: в основе клиники ревматоидного артрита всегда лежит воспаление. Пораженный сустав изначально воспаляется, а уже затем вследствие прогрессирующего течения заболевания в нем происходят эрозивно-деструктивные изменения, он склонен к деформации и даже (при отсутствии лечения) к анкилозированию – патологической (полной) неподвижности.
Причины развития ревматоидного артрита: генетическая предрасположенность или факторы окружающей среды?
На сегодняшний день досконально причины данного заболевания неизвестны. Описаны факторы, которые могут спровоцировать или повысить риск развития патологии. Ревматоидный артрит считается мультифакториальным заболевания, говоря проще, многофакторным.
Генетика. Генетическая предрасположенность имеет место быть, и она доказана научными исследованиями и экспериментами: выделены гены, связанные с развитием ревматоидного артрита. Это значит, что риск заболеть РА связан с наследственной склонностью к аутоиммунным реакциям.
Инфекционные агенты. Весомую роль в развитии ревматоидного артрита, как и всех ревматических заболеваний, играют инфекционные факторы. Бактерии, вирусы и простейшие – это гипотетические триггеры (пусковые механизмы) развития аутоиммунных реакций, приводящих к ревматоидному артриту. Вирусы: герпеса, цитомегаловирус, респираторно-синцитиальный вирус, Эпштейна-Барр, гепатита В и С, кори, паротита, парвовирус, вирус Коксаки и др. Бактерии: боррелия (инфекция боррелиоз), иерсиния (иерсиниоз, псевдотуберкулез), сальмонелла (сальмонеллез), стрептококковая инфекция. Простейшие микроорганизмы: микоплазмы, хламидии.
Факторы внешней среды и самого организма. Пусковыми факторами могут быть переохлаждение, стресс, интоксикация, курение, заболевания эндокринной системы, тяжелый физический труд.
Функция синовиума в суставе
Синовиальная оболочка, также называемая синовиальной оболочкой, — это мягкая ткань, выстилающая пространство диартродиальных суставов, влагалищ сухожилий и сумок. Синовиальная оболочка выстилает всю внутреннюю поверхность сустава, за исключением тех мест, где сустав выстлан хрящом. Синовиальная оболочка имеет внешний слой (субинтиму) и внутренний слой (интима). Клетки интимы называются синовиоцитами. Существует два типа синовиоцитов: тип A (происходящий из макрофагов) и тип B (происходящий из фибробластов). Субинтима состоит из внутрисуставных (внутри сустава) сосудов, таких как кровеносные и лимфатические сосуды, а также нервов. Под слоем синовиоцитов находится либо жировая ткань, либо фиброзная ткань. В синовиальной оболочке вырабатывается синовиальная жидкость — вещество, которое смазывает и питает хрящи и кости внутри суставной капсулы.
Субинтима состоит из внутрисуставных (внутри сустава) сосудов, таких как кровеносные и лимфатические сосуды, а также нервов. Под слоем синовиоцитов находится либо жировая ткань, либо фиброзная ткань. В синовиальной оболочке вырабатывается синовиальная жидкость — вещество, которое смазывает и питает хрящи и кости внутри суставной капсулы.
Питер Дазли / Getty Images
Синовиум при ревматоидном артрите
Как и многие другие ревматические заболевания, ревматоидный артрит является аутоиммунным заболеванием.При аутоиммунном заболевании или состоянии иммунная система человека, которая обычно помогает защитить организм от инфекций и болезней, атакует собственные ткани сустава по неизвестным причинам. При ревматоидном артрите клетки иммунной системы перемещаются в синовиальную оболочку и вызывают воспаление (синовит). Воспалительный процесс характеризуется разрастанием синовиальных клеток, повышенной васкуляризацией и инфильтрацией ткани воспалительными клетками, включая лимфоциты, плазматические клетки и активированные макрофаги.Это проявляется в виде типичных симптомов ревматоидного артрита — тепла, покраснения, отека и боли.
По мере прогрессирования ревматоидного артрита воспаленная синовиальная оболочка проникает в хрящ и кость сустава и разрушает их. Окружающие мышцы, связки и сухожилия, которые поддерживают и стабилизируют сустав, становятся слабыми и не могут нормально работать. Эти эффекты приводят к боли в суставах и повреждению суставов, которые обычно наблюдаются у людей с ревматоидным артритом. Понимание того, что происходит с синовиальной оболочкой при ревматоидном артрите, поможет вам понять симптомы и тяжесть заболевания.
Лечение целевого воспаленного синовиума — скоро ли?
Исследователи были заинтересованы в разработке тканеспецифичных методов лечения ревматоидного артрита. Возможные лекарственные препараты могут воздействовать на синовиальную оболочку с повышенной эффективностью и снижением системной токсичности. Если исследование этого процесса увенчается успехом, агенты визуализации могут быть доставлены непосредственно в синовиальную оболочку, что позволит оценить активный синовит в нескольких суставах. Хотя в этой области были достигнуты успехи, специфический синовиальный рецептор еще предстоит открыть.Взаимодействие с другими людьми
Если исследование этого процесса увенчается успехом, агенты визуализации могут быть доставлены непосредственно в синовиальную оболочку, что позволит оценить активный синовит в нескольких суставах. Хотя в этой области были достигнуты успехи, специфический синовиальный рецептор еще предстоит открыть.Взаимодействие с другими людьми
Synovium — обзор | Темы ScienceDirect
Синовиальная оболочка
Синовиальная оболочка представляет собой тонкий слой соединительной ткани, выстилающий синовиальную сумку, поверхность сустава и оболочки сухожилий. В синовиальной оболочке содержатся два основных типа клеток: синовиоциты типа A и синовиоциты типа B. Для сравнения, синовиоциты типа A — это макрофаги с фагоцитарной функцией, а синовиоциты типа B — это фибробластоподобные клетки, которые функционируют для образования синовиальной жидкости. В 2001 году Де Бари и его коллеги представили первые доказательства МСК, выделенных из синовиальной оболочки взрослых. 95 Из этого исследования синовиальную оболочку коленных суставов взрослого человека обрабатывали ферментативно, чтобы высвободить популяцию стволовых клеток, которая была выращена в культуре, а затем индуцирована для дифференцировки в клоны хондроцитов, остеоцитов, адипоцитов и миоцитов. 95 Другим ключевым выводом этого исследования является то, что возраст донора, прохождение клеток и криоконсервация не повлияли существенно на мультилинейный потенциал стволовых клеток, происходящих из синовиальной оболочки. 95 При тщательном наблюдении синовиальные МСК имеют фенотип, аналогичный синовиоцитам типа B. 96 Подобно поверхностным маркерам для других источников МСК, синовиальные МСК положительны в отношении поверхностных маркеров CD44, CD90 и CD105. Однако, в отличие от других источников МСК, синовиальные МСК имеют более высокую экспрессию CD44, рецептора гиалуронана, который может экспрессировать уридиндифосфоглюкозодегидрогеназу, которая является жизненно важным ферментом, участвующим в синтезе гиалуронана. 96 По сравнению с другими источниками МСК стволовые клетки синовиального происхождения обладают более высоким потенциалом роста с более высокой эффективностью образования колоний, кратным увеличением и кинетикой роста. 65 В частности, анализы хондрогенеза in vitro показали большую продукцию хондроцитов синовиальными клетками, чем другие участки стволовых клеток. 65
96 По сравнению с другими источниками МСК стволовые клетки синовиального происхождения обладают более высоким потенциалом роста с более высокой эффективностью образования колоний, кратным увеличением и кинетикой роста. 65 В частности, анализы хондрогенеза in vitro показали большую продукцию хондроцитов синовиальными клетками, чем другие участки стволовых клеток. 65
Учитывая эти характеристики in vitro, стволовые клетки синовиального происхождения были дополнительно исследованы на животных моделях. На модели кролика Кога и его коллеги трансплантировали недифференцированные МСК синовиальной оболочки в дефекты суставного хряща полной толщины взрослых кроликов. 97 В результате этой локальной трансплантации ранее недифференцированные синовиальные МСК трансформировались в терминально дифференцированные хондроциты.В зависимости от местного микроокружения синовиальные МСК дифференцировались в разные клетки в зависимости от положения внутри дефекта хряща. В этих условиях синовиальные МСК дифференцировались в остеоциты в более глубокой зоне дефектов хряща и в хондроциты в поверхностной зоне дефектов хряща. 97 Аналогичным образом синовиальные МСК, трансплантированные в дефекты суставного хряща полной толщины на модели свиньи, привели к регенерации хряща уже через 3 месяца после процедуры, что было тщательно изучено с помощью артроскопического, гистологического и МРТ анализов. 98 Точно так же на модели дефекта кости у кроликов было обнаружено, что синовиальные МСК с гидроксиапатитом ускоряют остеоиндукцию. 99 МСК синовиального происхождения, в то же время, также продемонстрировали способность окончательно дифференцироваться вниз по клону миоцитов. De Bari et al. Имплантировали взрослому человеку МСК, происходящие из синовиальной мембраны, в мышиную модель, что внесло вклад в регенерацию скелетных мышц и устойчивое функционирование сателлитных клеток. 100 Не менее важно, что заживление сухожилия до кости было оценено Джу и его коллегами на модели трансплантата ахиллова сухожилия крысы.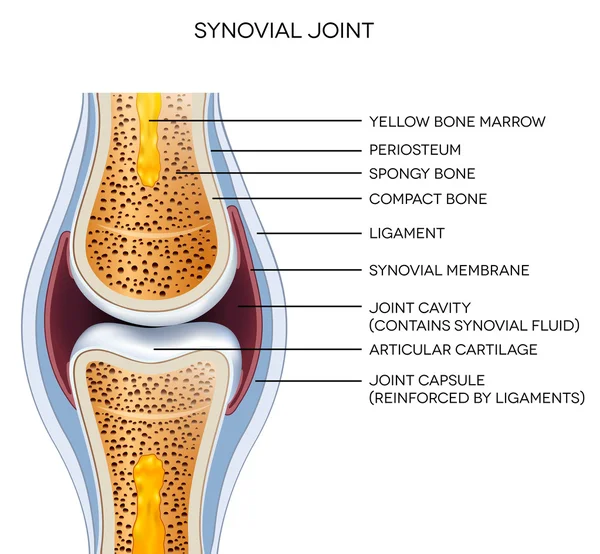 101 Как продемонстрировали Ju et al., Синовиальные МСК, имплантированные в костные туннели, ускоряли раннее ремоделирование сухожилия до заживления кости. 101 В клиническом исследовании Sekiya et al. Трансплантировали МСК синовиального происхождения пациентам с единичным симптоматическим поражением хряща мыщелка бедренной кости, что привело к значительному улучшению показателей МРТ, гистологических показателей и показателей Лисхольма. 102 В совокупности исследования MSC, происходящих из синовиальной оболочки, показывают некоторые многообещающие результаты на животных, которые ожидают более столь же многообещающих результатов, которые будут продемонстрированы на людях.
101 Как продемонстрировали Ju et al., Синовиальные МСК, имплантированные в костные туннели, ускоряли раннее ремоделирование сухожилия до заживления кости. 101 В клиническом исследовании Sekiya et al. Трансплантировали МСК синовиального происхождения пациентам с единичным симптоматическим поражением хряща мыщелка бедренной кости, что привело к значительному улучшению показателей МРТ, гистологических показателей и показателей Лисхольма. 102 В совокупности исследования MSC, происходящих из синовиальной оболочки, показывают некоторые многообещающие результаты на животных, которые ожидают более столь же многообещающих результатов, которые будут продемонстрированы на людях.
Синовиальная мембрана — обзор
Синовиальная мембрана и синовиальная жидкость
Синовиальная мембрана, или синовиальная оболочка, выстилает полость сустава и состоит из двух слоев: интимы и субинтима. Слой интимы в значительной степени отвечает за содержание синовиальной жидкости, обычно имеет толщину от одного до четырех слоев клеток и не имеет базальной мембраны. Отсутствие базальной мембраны имеет отношение к роли, которую синовиальная оболочка играет в определении содержания синовиальной жидкости в суставе, и будет рассмотрено более подробно позже.Субинтимальный слой состоит из фиброзной, ареолярной и жировой тканей. В субинтимальной ткани присутствует очень хорошее кровоснабжение, а также иннервация, исходящая как от периферических, так и от мышечных нервных ветвей (рис. 78-2). 2,3 Фактически, используя артроскоп крупным планом и сфокусировавшись непосредственно на нормальной синовиальной мембране, можно увидеть отдельные эритроциты, проходящие через капиллярную сеть ворсинок. При общем и артроскопическом осмотре синовиальная оболочка имеет плоские участки, смешанные с участками рыхлых скоплений ворсинок.Эти области ворсинок часто описываются как «похожие на водоросли» при артроскопическом осмотре в жидкой среде. Считается, что два вида синовиальной оболочки связаны с биомеханическими характеристиками области сустава, поскольку они остаются относительно неизменными на протяжении всей жизни здоровых суставов.
Считается, что два вида синовиальной оболочки связаны с биомеханическими характеристиками области сустава, поскольку они остаются относительно неизменными на протяжении всей жизни здоровых суставов.
Клеточная популяция интимного слоя основана на двух основных функциях: фагоцитоз, и секреция белка . Эти типы клеток исторически классифицируются как синовиоциты типа A или B на основании ультраструктуры и иммуногистологических характеристик.Клетки, участвующие в фагоцитозе или пиноцитозе, называются синовиоцитами типа А, тогда как те, которые отвечают за секрецию белка, называются синовиоцитами типа B. 4 Совсем недавно появилось описание ячеек типа C, и считается, что эти ячейки представляют собой тип ячейки между типом A и B. Поскольку ячейки типа A и B продемонстрировали функции, назначенные другому типу ячеек, и потому что было показано, что синовиоциты динамичны, вполне вероятно, что клетки типа C представляют синовиоциты при переходе от типа A к типу B или наоборот. 5,6
Когда основное внимание уделяется функции интимы синовиоцитов, важность его роли как в здоровье, так и в заболевании сустава становится очевидной. Одна из функций — фагоцитоз — механизм, посредством которого нежелательные частицы могут выводиться из сустава. Однако центральная роль синовиоцитов заключается в секреции белков, которые вносят вклад как в анаболический, так и в катаболический метаболизм сустава в целом. Как и многие другие метаболические процессы, при наличии сдержек и противовесов эти метаболические процессы являются частью нормального обмена, но когда происходит нерегулируемая или аберрантная регуляция, эти же процессы могут привести к развитию болезни.Синовиоциты отвечают за секрецию разнообразного набора белков, которые вносят вклад в собственно синовиальную мембрану, а также за состав синовиальной жидкости, и они включают гиалуронан, коллаген, лубрицин, матриксные металлопротеиназы (про-ММП). , интерлейкины и эйкозаноиды (например, простагландин E 2 ). 7,8 Размах этих белков в патофизиологии сустава подчеркивает важность этой ткани.
7,8 Размах этих белков в патофизиологии сустава подчеркивает важность этой ткани.
Другая важная роль синовиальной оболочки — регулировать состав синовиальной жидкости. Синовиальную жидкость часто называют ультрафильтратом плазмы. Этот термин подразумевает более пассивный процесс, но на самом деле он очень динамичен и взаимосвязан со многими факторами, включая молекулы, составляющие синовиальную жидкость (например, размер и концентрацию гиалуроновой кислоты), степень воспаления и лимфатический дренаж. Компоненты плазмы, такие как глюкоза, кислород, диоксид углерода и белки, обычно размером менее 10 кДа, пропускаются через эндотелий субинтимы и вносят вклад в состав синовиальной жидкости, тогда как большие молекулы исключаются.Стандартные методы цитологического исследования, а также уровни нормального и болезненного состояния компонентов будут сообщены позже. Большинство лабораторий считают нормальным уровень менее 500 клеток на децилитр синовиальной жидкости.
Молекулы, такие как гиалуронан и лубрицин, вносятся в синовиальную жидкость непосредственно синовиоцитами. Считается, что эти молекулы важны для стерического исключения (то есть стерического препятствия: процесса разделения молекул по размеру) более крупных молекул из синовиальной полости, регулируя, таким образом, состав синовиальной жидкости (рис. 78-3), а также граничные смазки стыковых поверхностей.Регулирование размера и концентрации гиалуронана в синовиальной жидкости неизвестно, но эти два фактора действительно влияют на функциональные свойства, приписываемые молекуле. Для определения как концентрации, так и молекулярной массы (или размера) гиалуронана использовались различные методы. Разнообразие методов позволило получить широкий диапазон нормальных значений от 0,33 до 1,5 мг / мл и несколько тысяч килодальтон соответственно. 7,9 Период полувыведения эндогенного гиалуронана оценивался путем инъекции радиоактивно меченного гиалуронана в сустав и отслеживания его деградации и клиренса. Похоже, что большая часть экзогенного гиалуронана выводится в течение 48 часов через синовиальную оболочку и лимфатические сосуды, причем деградация происходит как в синовиальной оболочке, так и в печени. 7
Похоже, что большая часть экзогенного гиалуронана выводится в течение 48 часов через синовиальную оболочку и лимфатические сосуды, причем деградация происходит как в синовиальной оболочке, так и в печени. 7
Что такое синовит и как он влияет на артрит? — CreakyJoints
Синовит — это медицинский термин, обозначающий воспаление синовиальной оболочки, мембраны, выстилающей ваши суставы. В здоровых суставах толщина этой защитной ткани составляет всего несколько клеток. Его работа — производить жидкость, которая смазывает и питает сустав.
Когда оболочка раздражена или воспалена, она становится толще и набухает из-за избытка синовиальной жидкости. Воспаленная синовиальная оболочка может в конечном итоге проникнуть в хрящ и кость сустава и разрушить их.
Что такое синовит?
Основным симптомом синовита является боль в суставах, сопровождающаяся теплом, припухлостью и скованностью, которые усиливаются по утрам. Вы можете ощущать симптомы синовита в разных суставах в разное время.
Иногда, однако, ваш сустав болит сильнее, чем кажется, по данным Больницы специальной хирургии — другими словами, при синовите может не быть явного отека или признаков травмы, вызывающих боль в суставах.
Кто болеет синовитом?
Синовит возникает при воспалительном артрите, — говорит Винисиус Домингес, доктор медицины, доцент медицины Университета штата Флорида и медицинский советник CreakyJoints. Это распространено при ревматоидном артрите (РА), но также встречается при псориатическом артрите, волчанке и подагре. Однако, по словам доктора Домингеса, синовит обычно не сопровождается остеоартритом. Эта изнашиваемая форма артрита практически не вызывает синовиального воспаления.
При РА ваша иммунная система по ошибке атакует здоровую синовиальную оболочку.«Когда у вас РА, один из способов определить, является ли заболевание активным или неактивным, — это наличие синовита», — объясняет д-р Домингес. «Синовит — это активный воспалительный артрит».
То же самое и с подагрой. Хотя эта форма артрита является хронической, симптомы, такие как боль в суставах, воспаление и покраснение, приходят и уходят. По словам доктора Домингеса, во время приступа подагры у вас может быть синовит подагры, но он не будет длиться вечно. Как только приступ будет вылечен, синовит снова исчезнет.
Однако воспалительный артрит — не единственная причина синовита.Травма или травма сустава могут вызвать временное реактивное воспаление подкладки.
Как диагностируют синовит?
Врачи изучают ваш анамнез и исследуют сустав на предмет тепла, нежности при прикосновении, опухоли или утолщения сустава, который кажется «губчатым». При синовите более глубокого сустава, например бедра, вам может потребоваться МРТ или другой визуализирующий тест, чтобы подтвердить диагноз синовита.
Если в анамнезе есть травма сустава, воспаление будет локальным в поврежденном суставе.При воспалительном артрите синовит может проявляться в одном или нескольких суставах. По словам доктора Домингеса, ваш врач может дифференцировать это на основе истории болезни.
Как лечится синовит?
Лечение зависит от причины: нестероидные противовоспалительные препараты (НПВП), отпускаемые без рецепта, такие как ибупрофен, могут помочь уменьшить боль и отек синовита, вызванного воспалительным артритом или поврежденным суставом. Прием модифицирующих болезнь лекарств или биопрепаратов для лечения воспалительного артрита поможет уменьшить воспаление и синовит.При подагре ваш врач порекомендует лекарства для снижения уровня мочевой кислоты. В некоторых случаях ваш врач может предложить инъекции стероидов в сустав.
Если эти методы лечения не снимают симптомов и синовит не проходит, вам может потребоваться синовэктомия — процедура, при которой удаляется большая часть синовиальной оболочки.
Продолжайте читать
Синовит при остеоартрите: современное понимание с терапевтическими последствиями | Исследования и терапия артрита
Отдел UNDoEaSAP.Перспективы мирового населения: обзор 2015 г., основные выводы и предварительные таблицы. 2016 г. https://esa.un.org/unpd/wpp/.
Томас Э., Пит Дж., Крофт П. Определение и картирование человека с остеоартритом для популяционных исследований и общественного здравоохранения. Ревматология (Оксфорд). 2014; 53 (2): 338–45.
Артикул
Google Scholar
Гольденберг Д.Л., Иган М.С., Коэн А.С.. Воспалительный синовит при дегенеративном заболевании суставов.J Rheumatol. 1982; 9 (2): 204–9.
CAS
PubMed
Google Scholar
Беренбаум Ф. Остеоартроз как воспалительное заболевание (остеоартроз — это не остеоартроз!). Хрящевой артроз. 2013. 21 (1): 16–21.
CAS
Статья
PubMed
Google Scholar
Селлэм Дж., Беренбаум Ф. Роль синовита в патофизиологии и клинических симптомах остеоартрита.Nat Rev Rheumatol. 2010. 6 (11): 625–35.
CAS
Статья
PubMed
Google Scholar
Scanzello CR, Goldring SR. Роль синовита в патогенезе остеоартроза. Кость. 2012. 51 (2): 249–57.
CAS
Статья
PubMed
PubMed Central
Google Scholar
Smith MD. Нормальная синовиальная оболочка. Откройте Rheumatol J. 2011; 5: 100–6.
Артикул
PubMed
PubMed Central
Google Scholar
Prieto-Potin I, Largo R, Roman-Blas JA, et al. Характеристика многоядерных гигантских клеток в синовиальной оболочке и субхондральной кости при остеоартрите коленного сустава и ревматоидном артрите. BMC Musculoskelet Disord. 2015; 16: 226.
Артикул
PubMed
PubMed Central
Google Scholar
Klein-Wieringa IR, de Lange-Brokaar BJ, Yusuf E, et al. Воспалительные клетки у пациентов с конечной стадией остеоартроза коленного сустава: сравнение синовиальной оболочки и подколеночной жировой подушечки.J Rheumatol. 2016; 43 (4): 771–8.
Артикул
PubMed
Google Scholar
Deligne C, Casulli S, Pigenet A, et al. Дифференциальная экспрессия интерлейкина-17 и интерлейкина-22 в воспаленной и невоспаленной синовиальной оболочке пациентов с остеоартритом. Хрящевой артроз. 2015; 23 (11): 1843–52.
CAS
Статья
PubMed
Google Scholar
de Lange-Brokaar BJ, Ioan-Facsinay A, van Osch GJ, et al.Синовиальное воспаление, иммунные клетки и их цитокины при остеоартрите: обзор. Хрящевой артроз. 2012; 20 (12): 1484–99.
Артикул
PubMed
Google Scholar
Соколово Ю., Лепус СМ. Роль воспаления в патогенезе остеоартроза: последние данные и интерпретации. Ther Adv Musculoskelet Dis. 2013. 5 (2): 77–94.
CAS
Статья
PubMed
PubMed Central
Google Scholar
Золотое кольцо МБ. Хондрогенез, дифференцировка хондроцитов и метаболизм суставного хряща при здоровье и остеоартрите. Ther Adv Musculoskelet Dis. 2012. 4 (4): 269–85.
CAS
Статья
PubMed
PubMed Central
Google Scholar
Пончел Ф., Бурска А.Н., Хенсор Э.М. и др. Изменение состава иммунных клеток периферической крови при остеоартрозе. Хрящевой артроз. 2015; 23 (11): 1870–8.
CAS
Статья
PubMed
PubMed Central
Google Scholar
Siebuhr AS, Bay-Jensen AC, Jordan JM и др. Остеоартрит, вызванный воспалением (или синовитом): возможность персонализировать прогноз и лечение? Scand J Rheumatol. 2016; 45 (2): 87–98.
CAS
Статья
PubMed
Google Scholar
Войдасевич П., Понятовский Л.А., Шукевич Д. Роль воспалительных и противовоспалительных цитокинов в патогенезе остеоартрита. Медиаторы Inflamm. 2014; 2014: 561459.
Артикул
PubMed
PubMed Central
Google Scholar
Гамильтон Дж. А., Кук А. Д., Так П. П.. Терапия антиколониестимулирующими факторами воспалительных и аутоиммунных заболеваний. Nat Rev Drug Discov. 2017; 16 (1): 53–70.
CAS
Статья
Google Scholar
Pustjens MF, Mastbergen SC, Steen-Louws C, et al. Синеркин IL4-10 вызывает прямое и непрямое структурное восстановление хряща при остеоартрите.Хрящевой артроз. 2016; 24: S532.
Артикул
Google Scholar
Guermazi A, Roemer FW, Haugen IK, et al. Полуколичественная оценка патологии суставов при остеоартрозе на основе МРТ. Nat Rev Rheumatol. 2013. 9 (4): 236–51.
Артикул
PubMed
Google Scholar
Перл А.Д., Сканцелло С.Р., Джордж С. и др. Повышенные уровни высокочувствительного С-реактивного белка связаны с местными воспалительными явлениями у пациентов с остеоартритом.Хрящевой артроз. 2007. 15 (5): 516–23.
CAS
Статья
PubMed
Google Scholar
de Lange-Brokaar BJ, Ioan-Facsinay A, Yusuf E, et al. Степень синовита на МРТ методом комплексной полуколичественной оценки всего коленного сустава коррелирует с гистологическими и макроскопическими особенностями воспаления синовиальной ткани при остеоартрозе коленного сустава. Хрящевой артроз. 2014. 22 (10): 1606–13.
Артикул
PubMed
Google Scholar
Loeuille D, Sauliere N, Champigneulle J, et al. Сравнение неусиленных и усиленных последовательностей при оценке выпота и синовита при ОА коленного сустава: ассоциации с клиническими, макроскопическими и микроскопическими особенностями. Хрящевой артроз. 2011; 19 (12): 1433–1433.
CAS
Статья
PubMed
Google Scholar
Neogi T, Guermazi A, Roemer F, et al. Связь воспаления суставов с болевой сенсибилизацией при остеоартрите коленного сустава: многоцентровое исследование остеоартрита.Arthritis Rheumatol. 2016; 68 (3): 654–61.
Артикул
PubMed
Google Scholar
Гермази А., Хаяши Д., Ремер Ф. В. и др. Синовит при остеоартрозе коленного сустава, оцениваемый с помощью магнитно-резонансной томографии (МРТ) с контрастным усилением, связан с рентгенологическим тибиофеморальным остеоартритом и широко распространенным повреждением хряща, обнаруженным с помощью МРТ: исследование MOST. J Rheumatol. 2014; 41 (3): 501–8.
Артикул
PubMed
Google Scholar
Бейкер К., Грейнджер А., Ниу Дж. И др. Связь синовита с болью в коленях с помощью МРТ с контрастным усилением. Ann Rheum Dis. 2010. 69 (10): 1779–83.
CAS
Статья
PubMed
Google Scholar
Хауген И.К., Бойесен П., Слатковски-Кристенсен Б. и др. Связь между синовитом, определенным с помощью МРТ, поражениями костного мозга и структурными особенностями, а также измерениями боли и физических функций при остеоартрите кисти. Ann Rheum Dis. 2012. 71 (6): 899–904.
Артикул
PubMed
Google Scholar
Сарманова А., Холл М, Моисей Дж. И др. Синовиальные изменения, обнаруженные с помощью ультразвука у людей с остеоартритом коленного сустава — метаанализ обсервационных исследований. Хрящевой артроз. 2016; 24 (8): 1376–83.
CAS
Статья
PubMed
PubMed Central
Google Scholar
Д’Агостино М.А., Конаган П., Ле Барс М. и др.Отчет EULAR об использовании ультразвукового исследования при болезненном остеоартрите коленного сустава. Часть 1: распространенность воспаления при остеоартрозе. Ann Rheum Dis. 2005. 64 (12): 1703–1709.
Артикул
PubMed
PubMed Central
Google Scholar
Матиссен А., Слатковски-Кристенсен Б., Квиен Т.К. и др. Воспаление, обнаруженное при ультразвуковом исследовании, позволяет прогнозировать рентгенологическое прогрессирование остеоартрита кисти через 5 лет. Ann Rheum Dis. 2016; 75 (5): 825–30.
Артикул
PubMed
Google Scholar
Kortekaas MC, Kwok WY, Reijnierse M, et al. Боль в руке. Остеоартроз связан с воспалением: значение ультразвука. Ann Rheum Dis. 2010. 69 (7): 1367–9.
Артикул
PubMed
Google Scholar
Roze RH, Bierma-Zeinstra SM, Agricola R, et al. Различия в характеристиках МРТ между двумя разными субпопуляциями остеоартрита: данные Osteoarthritis Initiative.Хрящевой артроз. 2016; 24 (5): 822–6.
CAS
Статья
PubMed
Google Scholar
Kortekaas MC, Kwok WY, Reijnierse M, et al. При эрозивном остеоартрите кисти на УЗИ обнаруживается больше воспалительных признаков, чем при остеоартрите остальных рук. Ann Rheum Dis. 2013. 72 (6): 930–4.
Артикул
PubMed
Google Scholar
de Lange-Brokaar BJ, Ioan-Facsinay A, Yusuf E, et al.Связь боли при остеоартрозе коленного сустава с различными паттернами синовита. Arthritis Rheumatol. 2015; 67 (3): 733–40.
Артикул
PubMed
Google Scholar
Wang X, Jin X, Han W, et al. Поперечные и продольные ассоциации между выпотным синовитом в коленном суставе и болью в коленях у пожилых людей. J Rheumatol. 2016; 43 (1): 121–30.
Артикул
PubMed
Google Scholar
Юсуф Э., Кортекаас М.С., Ватт I и др. Объясняют ли аномалии коленного сустава, визуализированные на МРТ, боль в коленях при остеоартрите коленного сустава? Систематический обзор. Ann Rheum Dis. 2011; 70 (1): 60–7.
Артикул
PubMed
Google Scholar
Риис Р.Г., Гудбергсен Х., Хенриксен М. и др. Синовит, оцененный с помощью статической и динамической магнитно-резонансной томографии с контрастным усилением, и его связь с болью при остеоартрите коленного сустава: поперечное исследование.Eur J Radiol. 2016. 85 (6): 1099–108.
Артикул
PubMed
Google Scholar
Hill CL, Hunter DJ, Niu J, et al. Синовит, обнаруженный на магнитно-резонансной томографии, и его связь с болью и потерей хряща при остеоартрите коленного сустава. Ann Rheum Dis. 2007. 66 (12): 1599–603.
Артикул
PubMed
PubMed Central
Google Scholar
Zhang Y, Nevitt M, Niu J, et al.Колебания боли в коленях и изменения поражений костного мозга, излияния и синовита на магнитно-резонансной томографии. Ревматоидный артрит. 2011; 63 (3): 691–9.
Артикул
PubMed
Google Scholar
de Lange-Brokaar BJ, Ioan-Facsinay A, Yusuf E, et al. Эволюция синовита при остеоартрозе коленных суставов и его связь с клиническими особенностями. Хрящевой артроз. 2016; 24 (11): 1867–74.
Артикул
PubMed
Google Scholar
Хауген И.К., Слатковски Кристенсен Б., Бойесен П. и др. Увеличение синовита и поражения костного мозга связано с болезненностью суставов при остеоартрите рук. Ann Rheum Dis. 2016; 75 (4): 702–8.
CAS
Статья
PubMed
Google Scholar
Фелсон Д.Т., Ниу Дж., Неоги Т. и др. Синовит и риск остеоартроза коленного сустава: исследование MOST. Хрящевой артроз. 2016; 24 (3): 458–64.
CAS
Статья
PubMed
Google Scholar
Roemer FW, Guermazi A, Felson DT, et al. Наличие суставного выпота и синовита, обнаруженного на МРТ, увеличивает риск потери хрящевой ткани в коленях без остеоартрита через 30 месяцев наблюдения: исследование MOST. Ann Rheum Dis. 2011; 70 (10): 1804–1809.
Артикул
PubMed
PubMed Central
Google Scholar
Atukorala I, Kwoh CK, Guermazi A, et al. Синовит при остеоартрозе коленного сустава: предвестник болезни? Ann Rheum Dis. 2016; 75 (2): 390–5.
CAS
Статья
PubMed
Google Scholar
Roemer FW, Kwoh CK, Hannon MJ и др. Что на первом месте? Поражение нескольких тканей, приводящее к рентгенологическому остеоартриту: анализ траектории на основе магнитно-резонансной томографии в течение четырех лет в рамках инициативы по остеоартриту. Arthritis Rheumatol. 2015; 67 (8): 2085–96.
Артикул
PubMed
PubMed Central
Google Scholar
Конаган П.Г., Д’Агостино М.А., Ле Барс М. и др. Клинические и ультразвуковые предикторы замены суставов при остеоартрите коленного сустава: результаты большого трехлетнего проспективного исследования EULAR. Ann Rheum Dis. 2010. 69 (4): 644–7.
CAS
Статья
PubMed
Google Scholar
Collins JE, Losina E, Nevitt MC, et al. Полуколичественные визуализирующие биомаркеры прогрессирования остеоартрита коленного сустава: данные Консорциума биомаркеров FNIH OA.Arthritis Rheumatol. 2016; 68 (10): 2422–31.
CAS
Статья
PubMed
Google Scholar
Kortekaas MC, Kwok WY, Reijnierse M, et al. Ультразвуковые признаки воспаления показывают независимую связь с прогрессированием структурных повреждений после более чем 2-летнего наблюдения у пациентов с остеоартритом кисти. Ann Rheum Dis. 2015; 74 (9): 1720–4.
Артикул
PubMed
Google Scholar
Хауген И.К., Слатковски-Кристенсен Б., Бойесен П. и др. Результаты МРТ позволяют прогнозировать рентгенологическое прогрессирование и развитие эрозий при остеоартрите кисти. Ann Rheum Dis. 2016; 75 (1): 117–23.
Артикул
PubMed
Google Scholar
Дамман В., Лю Р., Блум Дж. Л. и др. Поражения костного мозга и синовит на МРТ ассоциируются с рентгенологическим прогрессированием после 2 лет лечения остеоартрита кисти. Ann Rheum Dis. 2017; 76 (1): 214–17.
CAS
Статья
PubMed
Google Scholar
О’Нил Т.В., Паркс М.Дж., Марикар Н. и др. Объем синовиальной ткани: цель лечения остеоартрита коленного сустава (ОА). Ann Rheum Dis. 2016; 75 (1): 84–90.
Артикул
PubMed
Google Scholar
Gait AD, Hodgson R, Parkes MJ, et al. Синовиальный объем в сравнении с измерениями синовиальной оболочки с помощью МРТ с динамическим контрастированием как меры ответа при остеоартрите.Хрящевой артроз. 2016; 24 (8): 1392–8.
CAS
Статья
PubMed
PubMed Central
Google Scholar
Уэнам С.Ю., Баламуди С., Грейнджер А.Дж. и др. Реакция на новые, динамические, контрастные магнитно-резонансные измерения общего синовита коленного сустава после введения внутрисуставных кортикостероидов при болезненном остеоартрите. Хрящевой артроз. 2014. 22 (10): 1614–8.
CAS
Статья
PubMed
Google Scholar
Чжан В., Нуки Дж., Московиц Р.В. и др. Рекомендации OARSI по лечению остеоартрита тазобедренного и коленного суставов: часть III: изменения в доказательствах после систематического кумулятивного обновления исследований, опубликованных до января 2009 г. Остеоартроз Хрящ. 2010. 18 (4): 476–99.
CAS
Статья
PubMed
Google Scholar
Робинсон П., Кинан А.М., Конаган П.Г. Клиническая эффективность и доза-реакция внутрисуставной инъекции кортикостероидов под визуальным контролем при остеоартрите тазобедренного сустава.Ревматология (Оксфорд). 2007. 46 (2): 285–91.
CAS
Статья
Google Scholar
Уэнам С.Ю., Хенсор Э.М., Грейнджер А.Дж. и др. Рандомизированное двойное слепое плацебо-контролируемое исследование низких доз перорального преднизолона для лечения болезненного остеоартрита рук. Ревматология (Оксфорд). 2012. 51 (12): 2286–94.
CAS
Статья
Google Scholar
Кин Х.И., Уэйкфилд Р.Дж., Хенсор Э.М. и др.Реакция симптомов и синовита на внутримышечный метилпреднизолон при остеоартрите руки: ультразвуковое исследование. Ревматология (Оксфорд). 2010. 49 (6): 1093–100.
Артикул
Google Scholar
Конаган П.Г., Коэн С., Джордан Дж и др. Устойчивые и выраженные анальгетические преимущества у людей с остеоартритом коленного сустава при использовании FX006, внутрисуставного препарата триамцинолона ацетонида с пролонгированным высвобождением: результаты двойного слепого рандомизированного исследования с параллельными группами с определением дозХрящевой артроз. 2016; 24: S49–50.
Артикул
Google Scholar
Венхэм С.Ю., Грейнджер А.Дж., Хенсор Э.М. и др. Метотрексат для снятия боли при остеоартрите коленного сустава: открытое исследование. Ревматология (Оксфорд). 2013; 52 (5): 888–92.
CAS
Статья
Google Scholar
Уэнам С.Ю., Макдермотт М., Конаган П.Г. Биологические методы лечения остеоартроза.Curr Pharm Des. 2015; 21 (17): 2206–15.
CAS
Статья
PubMed
Google Scholar
Клоппенбург М., Рамонда Р., Квок В.-Й и др. OP0095 Рандомизированное плацебо-контролируемое исследование для оценки клинической эффективности и структурно-модифицирующих свойств подкожного этанерцепта (ETN) у пациентов с эрозивно-воспалительным остеоартритом кисти (OA). Ann Rheum Dis. 2016; 75 Дополнение 2: 90–1.
Артикул
Google Scholar
Ларссон С., Энглунд М., Струглиц А. и др. Интерлейкин-6 и фактор некроза опухоли альфа в синовиальной жидкости связаны с прогрессированием рентгенологического остеоартрита коленного сустава у пациентов, перенесших ранее менискэктомию. Хрящевой артроз. 2015; 23 (11): 1906–14.
CAS
Статья
PubMed
Google Scholar
Хаяши Д., Ремер Ф.В., Катур А. и др. Визуализация синовита при остеоартрозе: текущее состояние и перспективы.Semin Arthritis Rheum. 2011. 41 (2): 116–30.
Артикул
PubMed
Google Scholar
Вклад костного мозга в синовиальную гиперплазию в результате повреждения суставной поверхности | Исследования и терапия артрита
Животные
Эксперименты на животных были одобрены Министерством внутренних дел Великобритании и проводились в соответствии с Законом Великобритании о животных (научные процедуры) 1986 года и Кодексом правил Министерства внутренних дел Великобритании. Мыши C57BL / 6 дикого типа были приобретены в Charles River Laboratories (Эдинбург, Великобритания).Мышей C57BL / 6-Tg14 (act-EGFP) OsbY01 (далее Act-eGFP ), которые повсеместно экспрессируют усиленный GFP [16], были выведены в нашем животноводческом учреждении (первоначально получено от профессора Окабе, Genome Information Research. Center, Университет Осаки, Осака, Япония).
Трансплантация костного мозга
Трансплантация костного мозга выполнялась, как описано ранее [17]. Мыши (самки в возрасте от 7 до 9 недель) получали облучение всего тела двумя дозами по 5 Гр с интервалом в 3 часа. Донорские клетки выделяли путем промывания клеток костного мозга из бедренной, большеберцовой и тазовой костей PBS с добавлением 2% фетальной телячьей сыворотки (FCS).Всего 5 × 10 6 донорских клеток на мышь были доставлены через 24 часа после облучения путем инъекции в хвостовую вену. Химеризм определяли в образце периферической крови, взятой из хвостовой вены через 3 недели после трансплантации, с использованием проточной цитометрии.
Повреждение суставной поверхности
Процедура повреждения суставной поверхности была выполнена, как описано ранее [15]. Вкратце, через 3-4 недели после трансплантации костного мозга мышей анестезировали и подвергали хирургическому вмешательству под диссекционным микроскопом.Был сделан разрез, чтобы открыть кожу в области коленного сустава, а затем разрез по медиальной стороне связки надколенника и через четырехглавую мышцу, чтобы помочь вывиху надколенника. Канавка надколенника была обнажена, и царапина на всю толщину хряща по длине канавки была сделана с использованием иглы 25-го размера. Затем переместили коленную чашечку и зашили суставную капсулу и кожу. Контралатеральное колено служило неповрежденным внутренним контролем. Ложнооперированные коленные суставы были подвергнуты артротомии, но повреждений хряща не было.
Введение аналога нуклеозида
Введение аналога нуклеозида выполняли, как описано ранее [4]. Вкратце, 4-недельные мыши получали йоддезоксиуридин (IdU; Sigma-Aldrich, Дорсет, Великобритания) в питьевой воде (1 мг / мл) в течение 3 недель с последующим 5-недельным периодом вымывания. Сразу после повреждения поверхности сустава мышам вводили хлордезоксиуридин (CldU; Sigma-Aldrich) подкожно (10 мг / мл), а затем вводили CldU с питьевой водой (1 мг / мл) в течение 7 дней.
Выделение клеток костного мозга
Клетки костного мозга выделяли, как описано ранее [18]. Вкратце, конечности мышей рассекали и мышцы удаляли с помощью скальпеля. Затем кости разрезали ножницами на мелкие фрагменты, трижды промывали буфером HBSS + (сбалансированный солевой раствор Хэнка [HBSS] с добавлением 2% FCS, 10 мМ HEPES и 1% пенициллина [10 000 Ед / мл] / стрептомицина [10 мг / мл]) и инкубировали в предварительно нагретой среде DMEM с добавлением 0,2% коллагеназы типа I (Sigma-Aldrich), 10 мМ HEPES и 1% пенициллина (10000 Ед / мл) / стрептомицина (10 мг / мл) в течение 1 часа в воде. баню встряхивают при 140 об / мин.Образцы встряхивали каждые 10 минут, чтобы способствовать диссоциации клеток. После инкубации с коллагеназой супернатант собирали через фильтр с размером пор 70 мкм, а кости дополнительно измельчали в ступке пестиком примерно с 50 нажатиями. Раздробленные костные фрагменты несколько раз промывали буфером HBSS + до прозрачности, и все собранные клетки осаждали. После лизирования эритроцитов с использованием буфера BD Pharm Lyse (BD Biosciences, Оксфорд, Великобритания) клетки промывали и подсчитывали жизнеспособные клетки с использованием исключения трипанового синего.
Анализ
CFU-F
Клетки костного мозга высевали при 2,5 × 10 4 клеток / см 2 и поддерживали в базальной среде MesenCult MSC с добавлением стимулирующих добавок MesenCult (STEMCELL Technologies, Ванкувер, Британская Колумбия, Канада) в соответствии с с инструкциями производителя в течение 2 недель, после чего подсчитывали количество КОЕ-F. Кластеры из ≥32 клеток считались колониями. Тридцать две клетки были выбраны, потому что это представляет собой популяцию клеток, полученную по крайней мере из пяти удвоений популяции одной клетки, тем самым не считая транзитно-амплифицирующих клеток [19].Флуоресценцию GFP регистрировали с помощью микроскопа EVOS FL (Life Technologies, Карлсбад, Калифорния, США).
Проточная цитометрия
Мононуклеарные клетки периферической крови окрашивали антителом CD45-перидин-хлорофилл-протеиновый комплекс (PerCP) -цианин 5.5 (Cy5.5) (клон 30-F11; eBioscience, Сан-Диего, Калифорния, США). Свежевыделенные клетки костного мозга совместно окрашивали CD45-фикоэритрином (клон 30-F11; BD Biosciences), CD140a-аллофикоцианином (клон APA5; BD Biosciences) и антигеном 1 стволовых клеток (Sca-1) -PerCP-Cy5.5 (клон D7; eBioscience) в течение 30 минут при 4 ° C. Клетки анализировали с использованием проточного цитометра BD LSR II (BD Biosciences). Мертвые клетки исключались из анализа на основании окрашивания красителем жизнеспособности eFluor 780 (65-0865; eBioscience).
Гистология
Коленные суставы фиксировали в 4% параформальдегиде без метанола (TAAB Laboratories Equipment, Aldermaston, UK) в течение 24 часов при 4 ° C, а затем декальцинировали в 10% этилендиаминтетрауксусной кислоте (EDTA) (VWR International, Lutterworth, UK). ) в PBS в течение 2 недель.Затем образцы либо заливали парафином и разрезали на срезы размером 5 мкм с использованием стандартного микротома (Leica RM2125 RT; Leica Biosystems, Милтон-Кейнс, Великобритания), либо для прямой визуализации GFP под флуоресцентным микроскопом, инкубировали последовательно в 15% и 30% сахароза в PBS, встроенная в OCT соединения (VWR International) над жидким азотом и разрезают на 8-мкм срезы с помощью криостата (Leica CM1850 UV; Leica Biosystems). Окрашивание гематоксилином и эозином (H&E) проводили согласно стандартным протоколам.
Иммунофлуоресцентное окрашивание
Иммунофлуоресцентное окрашивание парафиновых срезов проводили, как описано ранее [4], с некоторыми изменениями. Извлечение антигена осуществлялось либо (1) на основе ферментов путем инкубации со свиным пепсином от 1 до 3 мг / мл (Sigma-Aldrich) в течение 45 минут при 37 ° C, либо (2) при нагревании в растворе на основе ЭДТА ( pH 9; Vector Laboratories, Burlingame, CA, USA) или цитратный буферный раствор (pH 6; Vector Laboratories) в течение 30 минут в пароварке. Автофлуоресценцию гасили инкубацией в 1% растворе Sudan Black B (Sigma-Aldrich) (в 70% этаноле) в течение 20 минут при комнатной температуре, а неспецифическое связывание блокировали 1% бычьим сывороточным альбумином (Sigma-Aldrich) в течение 1 часа. часЗатем срезы инкубировали с первичными антителами (перечисленными в подразделе непосредственно ниже) в течение ночи при 4 ° C в увлажненной камере с последующей инкубацией с вторичными антителами, конъюгированными с Alexa Fluor 488 или Alexa Fluor 594 (Life Technologies), в течение 1 часа в комнате. температура в темноте. Ядра контрастировали 4 ‘, 6-диамидино-2-фенилиндолом (DAPI, Life Technologies).
Антитела
Использовали следующие первичные антитела: анти-GFP (поликлональные антитела цыплят; Abcam, Кембридж, Великобритания), анти-GFP (моноклональные антитела кролика; Abcam), анти-бромдезоксиуридин (моноклональные антитела крысы, клон ICR1, перекрестный -реагирует с CldU, но не с IdU; Abcam), анти-IdU (мышиное моноклональное антитело, клон 32D8.D9; Abcam), фактор фон Виллебранда (анти-vWF) (кроличьи поликлональные антитела; Дако, Эли, Великобритания), рецептор фактора роста антитромбоцитов α (анти-Pdgfrα) (кроличьи поликлональные антитела; Abcam) и анти-CD16. / CD32 (козье моноклональное антитело; R&D Systems, Миннеаполис, Миннесота, США).
Визуализация и подсчет клеток
Изображения криосрезов и залитых парафином срезов получали с помощью конфокального микроскопа Zeiss LSM 710 (Carl Zeiss Microscopy, Йена, Германия) для флуоресцентного анализа или микроскопа Zeiss Imager Axioskop 40 (Carl Zeiss Microscopy) оснащен камерой ProgRes C14 (Jenoptik, Йена, Германия) для срезов, окрашенных H и E.Обработку изображений и ручной подсчет клеток выполняли с использованием программного обеспечения ZEN 2010 (Carl Zeiss Microscopy) или ImageJ (Национальные институты здравоохранения, Бетесда, Мэриленд, США). Для каждого условия были проанализированы три секции на коленный сустав, по крайней мере, от трех мышей. Подсчитывали минимум 200 клеток из каждого коленного сустава мыши. Чтобы избежать мешающего влияния медиальной парапателлярной артротомии на поврежденные коленные суставы, количественную оценку проводили в латеральном отделе колена.
Статистика
Данные анализировали с помощью программного обеспечения IBM SPSS (IBM, Армонк, Нью-Йорк, США) и Prism (GraphPad Software, Ла-Холла, Калифорния, США).Статистическая значимость определялась с использованием либо тестов t для двухгрупповых сравнений, либо двухфакторного дисперсионного анализа и апостериорного критерия Бонферрони для многогрупповых сравнений, при этом p <0,05 считалось значимым.
% PDF-1.4
%
176 0 объект
>
эндобдж
xref
176 102
0000000016 00000 н.
0000003336 00000 н.
0000003457 00000 н.
0000004152 00000 н.
0000004290 00000 н.
0000004610 00000 н.
0000004731 00000 н.
0000004932 00000 н.
0000005451 00000 п.
0000005655 00000 н.
0000005767 00000 н.
0000005931 00000 н.
0000006026 00000 н.
0000006140 00000 н.
0000006484 00000 н.
0000006511 00000 н.
0000006836 00000 н.
0000010985 00000 п.
0000014888 00000 п.
0000018844 00000 п.
0000022771 00000 п.
0000023295 00000 п.
0000023699 00000 п.
0000024309 00000 п.
0000024535 00000 п.
0000024773 00000 п.
0000025440 00000 п.
0000025609 00000 п.
0000026254 00000 п.
0000026778 00000 п.
0000027125 00000 п.
0000027492 00000 п.
0000027865 00000 н.
0000031831 00000 п.
0000032049 00000 п.
0000032177 00000 п.
0000032498 00000 п.
0000032859 00000 п.
0000036131 00000 п.
0000036245 00000 п.
0000036272 00000 н.
0000036583 00000 п.
0000036814 00000 п.
0000036841 00000 п.
0000037150 00000 п.
0000037292 00000 п.
0000037425 00000 п.
0000037822 00000 п.
0000038311 00000 п.
0000038448 00000 н.
0000038587 00000 п.
0000039181 00000 п.
0000042164 00000 п.
0000042441 00000 п.
0000045335 00000 п.
0000049828 00000 п.
0000049909 00000 н.
0000050910 00000 п.
0000050980 00000 п.
0000051173 00000 п.
0000051441 00000 п.
0000061627 00000 н.
0000064863 00000 п.
0000064944 00000 п.
0000065014 00000 п.
0000067324 00000 п.
0000067501 00000 п.
0000070862 00000 п.
0000070943 00000 п.
0000073614 00000 п.
0000073887 00000 п.
0000073957 00000 п.
0000074131 00000 п.
0000075911 00000 п.
0000078993 00000 п.
0000079255 00000 п.
0000079325 00000 п.
0000079439 00000 п.
0000091312 00000 п.

 Такие смеси отличаются высокой эффективностью и сильным противовоспалительным и восстанавливающим действием.
Такие смеси отличаются высокой эффективностью и сильным противовоспалительным и восстанавливающим действием.