Тромбоз брюшной аорты | Ведущие доктора | Лучшие клиники | Отзывы
Тромбоз брюшной аорты – это фактическая закупорка сосудов, которая ведет к сильнейшим болям и другим опасным симптомам.
Лечение тромбоза брюшной аорты в клиниках Германии, Израиля, Австрии, США, Финляндии и Швейцарии направлено на скорейшее устранение закупорки при помощи современных хирургических методов, позволяющих в щадящем для пациента режиме устранить проблему и сохранить ему не только здоровье, но и жизнь.
Преимущества лечения тромбоза брюшной аорты за границей
Лечение тромбоза брюшной аорты за рубежом проводится, как правило, при помощи удаления расширенного сосуда и замещения его синтезированным сосудом или индивидуально разработанным протезом. Преимуществами лечения в рекомендованных нами клиниках является строго индивидуальный подход к каждому пациенту и выбор наиболее эффективного варианта лечения, что гарантирует отсутствие проявлений различных осложнений.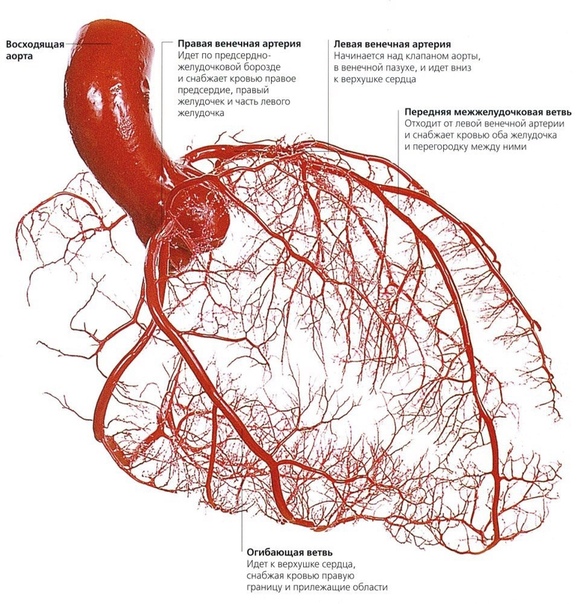 Операции по удалению тромбоза брюшной аорты проводятся при использовании общей анестезии. Послеоперационный период проходит в комфортнейших условиях и под присмотром специалистов четко контролирующих процесс выздоровления.
Операции по удалению тромбоза брюшной аорты проводятся при использовании общей анестезии. Послеоперационный период проходит в комфортнейших условиях и под присмотром специалистов четко контролирующих процесс выздоровления.
Диагностика тромбоза брюшной аорты за границей
Пациенты рекомендуемых нами медицинских центров получают возможность пройти диагностику на самом высоком уровне. Такой диагноз как тромбоз брюшной аорты устанавливается при помощи МРТ, рентгенконтрастной ангиографии, ультразвукового допплерографиеского сканирования и спиральной компьютерной томографии.
Организация лечения тромбоза брюшной аорты за границей
Компания «Пациент Менеджмент» является идеальной платформой для организации плодотворного и комфортного лечения тромбоза брюшной аорты за границей.
Нашим преимуществом является то, что у нас работают исключительно высококвалифицированные консультанты, которые помогут Вам получить ответы на все вопросы, а также предложат идеальные варианты конкретных медицинских учреждений и врачей.
Мы занимаемся всеми вопросами планирования и организации лечения в клиниках Германии, Израиля, Австрии, США, Финляндии и Швейцарии, которые являются основными странами, куда так активно стремятся многие русскоговорящие медицинские туристы.
Обращайтесь к нам, и мы приложим все усилия для достижения ожидаемого положительного результата – полного излечения или, как минимум, восстановления здоровья настолько насколько это вообще возможно.
Тромбоз и эмболия артерий: лечение в Киеве
Описание болезни
В практике сосудистого хирурга часто приходится сталкиваться с подобными ситуациями, как острые сосудистые заболевания, тромбозы и эмболии артерий – внезапная закупорка магистральных сосудов. Мгновенное прекращение доставки крови к органу запускает целый каскад патолофизиологических реакций, приводящих в итоге к гибели органа, а порой и организма.
Артериальным тромбозом называется образование тромба на измененной стенке артерии с постепенным его ростом и закупоркой (окклюзией) просвета сосуда.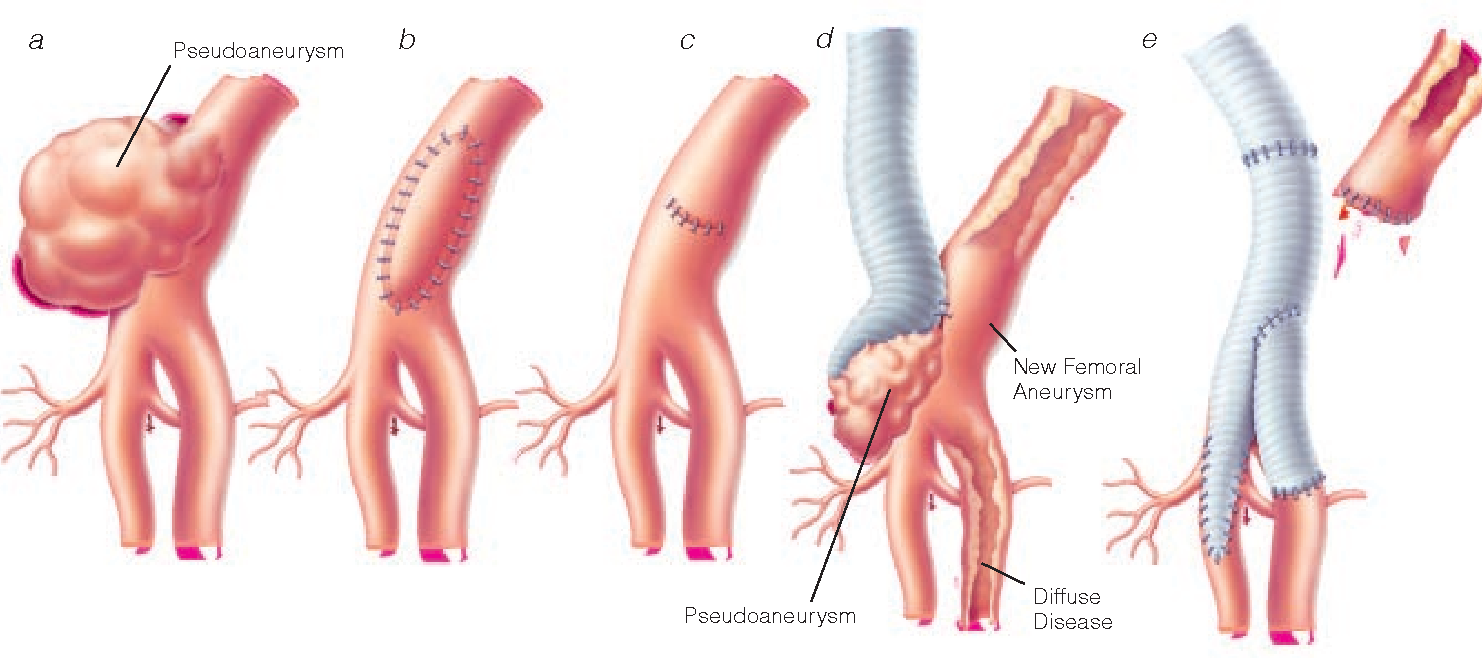 Основной причиной тромбоза является облитерирующий атеросклероз. Изменение сосудистой стенки ведет к завихрению крови, агрегацией (склеиванию) тромбоцитов и образованию тромбов. Эмболия это иммиграция тромба из другого органа (сердца или аорты) в другой, неизмененный сосуд с острой его окклюзией и продолженным ростом тромба. Наиболее часто эмболии случаются при болезнях сердца (инфаркт миокарда, мерцательная аритмия, инфекционное поражение сердечных клапанов) и при патологическом расширении крупных сосудов – аневризмах. Процесс эмболии напоминает рулетку, когда невозможно предсказать, куда полетит тромб. При попадании его в мозговые сосуды развивается инсульт, в кишечник – его омертвение, а если тромб попадает в руку или ногу, развивается их гангрена.
Основной причиной тромбоза является облитерирующий атеросклероз. Изменение сосудистой стенки ведет к завихрению крови, агрегацией (склеиванию) тромбоцитов и образованию тромбов. Эмболия это иммиграция тромба из другого органа (сердца или аорты) в другой, неизмененный сосуд с острой его окклюзией и продолженным ростом тромба. Наиболее часто эмболии случаются при болезнях сердца (инфаркт миокарда, мерцательная аритмия, инфекционное поражение сердечных клапанов) и при патологическом расширении крупных сосудов – аневризмах. Процесс эмболии напоминает рулетку, когда невозможно предсказать, куда полетит тромб. При попадании его в мозговые сосуды развивается инсульт, в кишечник – его омертвение, а если тромб попадает в руку или ногу, развивается их гангрена.
Развитие болезни
При тромбозе или эмболии, нормальное кровоснабжение в бассейне закупоренного сосуда внезапно прекращается и развивается патологическое состояние называемое острой ишемией. При ишемии кислородный голод приводит к прекращению функционирования, а в последующем, и гибели тканей пораженного органа. Выключение функции начинается с нервной ткани – самой высокоспециализированной. При этом вначале происходит ее раздражение, что приводит к сильной боли, затем прекращается проведение нервного импульса – исчезает чувствительность, конечность “деревенеет”. В итоге развивается вялый паралич мышц – активные движения прекращаются.
Выключение функции начинается с нервной ткани – самой высокоспециализированной. При этом вначале происходит ее раздражение, что приводит к сильной боли, затем прекращается проведение нервного импульса – исчезает чувствительность, конечность “деревенеет”. В итоге развивается вялый паралич мышц – активные движения прекращаются.
После гибели нервной ткани наступает черед мышечной ткани. Этот процесс сопровождается окоченением отдельных мышц и их групп с развитием тугоподвижности суставов, а в последующем и невозможности согнуть конечность ни в одном суставе. Подобное состояние называется мышечной контрактурой. Наиболее жизнеспособной оказывается кожа. Нередко приходилось наблюдать полную гибель мышц, тогда как кожа внешне оставалась не измененной. Полная мышечная контрактура свидетельствует о гибели конечности и необходимости срочной ее ампутации с целью спасения жизни, так как всасывание продуктов мышечного распада приводит к необратимому отравлению организма с нарушением функции всех жизненно-важных органов.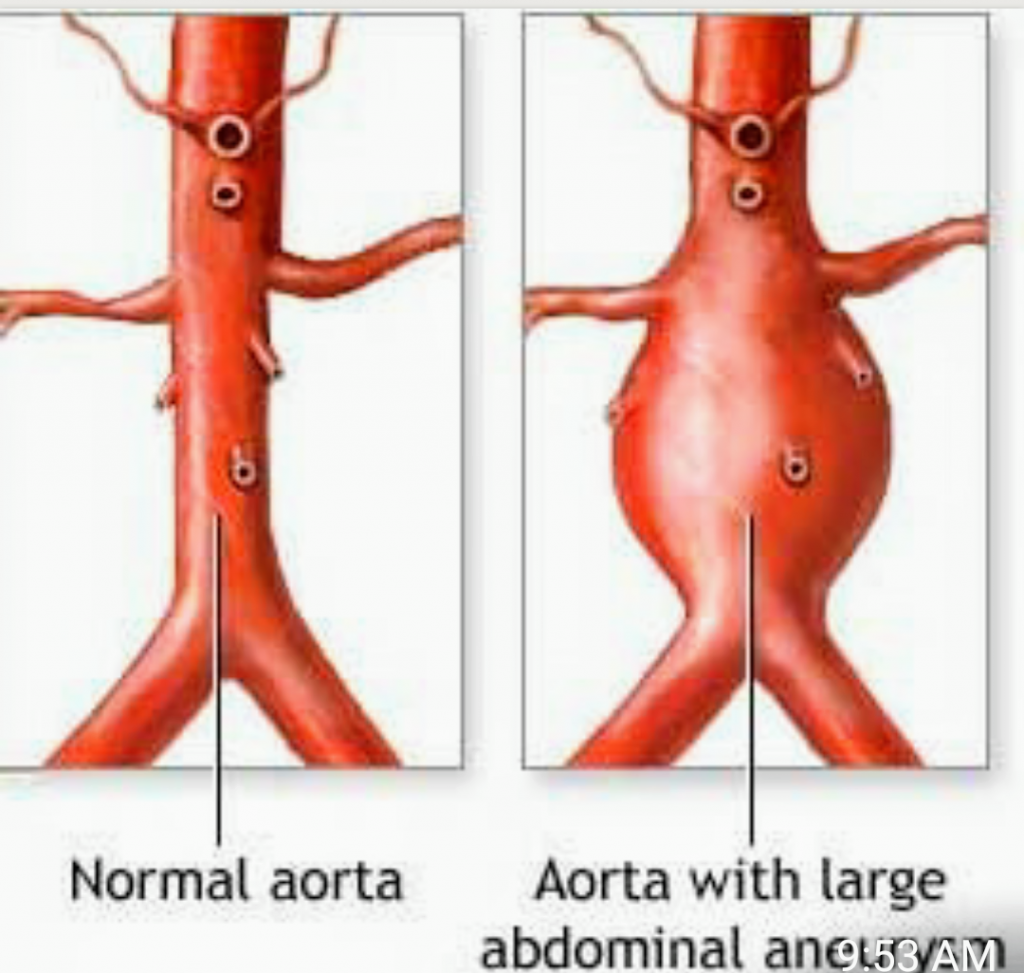
Процесс развития острой ишемии достаточно быстрый, но на определенных этапах обратимый. Если орган или конечность утратили свою функцию, но еще не погибли, то восстановление кровообращения дает шанс полного их восстановления.
В целом при тромбозах есть 2-5 дней для спасения конечности. При эмболиях нарушение кровоснабжения наступает мгновенно, что приводит к резкому спазму, внезапно опустевших сосудов и полному прекращению кровоснабжения конечности. Если принять обезболивающие препараты и спазмолитики, то спазм может уменьшиться, а кровообращение в конечности улучшится. Однако, так или иначе, доставка кислорода резко уменьшается, что запускает процесс острой ишемии. При эмболиях лучшие результаты лечения при восстановлении кровотока до 6 часов, от начала заболевания. До 12 часов можно спасти только 60% конечностей, после 24 часов лишь 20 %.
Как проявляется ишемия?
Боль – универсальная сигнальная реакция, при ишемии особенно выражена в самом начале болезни. При эмболии боль сильнее и напоминает удар хлыстом, нередко бывает очень сильной. При тромбозах болевые ощущения менее выражены и нередко характеризуются фразами “нога затекла, онемела”. Постепенно болевые ощущения могут затихать, что создает ложное ощущение улучшения, однако оно связано с гибелью нервных окончаний. Второй основной признак – изменение окраски кожных покровов и резкое снижение температуры конечности. Она становится “ледяной” на ощупь. При эмболии чаще вначале кожа резко бледнеет, затем по мере уменьшения боли начинает синеть, становится “мраморной”.
При тромбозах болевые ощущения менее выражены и нередко характеризуются фразами “нога затекла, онемела”. Постепенно болевые ощущения могут затихать, что создает ложное ощущение улучшения, однако оно связано с гибелью нервных окончаний. Второй основной признак – изменение окраски кожных покровов и резкое снижение температуры конечности. Она становится “ледяной” на ощупь. При эмболии чаще вначале кожа резко бледнеет, затем по мере уменьшения боли начинает синеть, становится “мраморной”.
При тромбозах “бледная” стадия чаще отсутствует. Следующим этапом исчезает чувствительность. При этом сохраняется чувство тупой боли, но покалывание иглой, прикосновение горячим и холодным не ощущается. Вслед за исчезновением чувствительности исчезают и движения. Пораженная конечность не воспринимается, как своя, но пассивные движения еще возможны. Этот этап является последним, когда еще можно восстановить функцию конечности. В дальнейшем развивается отек мышц, частичная и полная мышечная контрактура.
Что делать?
Тромбэмболэктомия с подколенной артерии и ее трифуркации с помощью катетера ФогартиТромбэмболэктомия с помощью катетера Фогарти
Ответ простой – срочно обращаться к сосудистому хирургу. От времени зависит все. В самом начале необходимо принять обезболивающие препараты, спазмолитики (но-шпа, папаверин). Ни в коем случае нельзя согревать больную конечность. В стационаре при эмболии в ближайшие часы сделают экстренную операцию по извлечению тромбов (эмболэктомию). При тромбозе можно несколько дней дообследоваться, установить точный диагноз, провести предоперационную подготовку. Операции при тромбозах технически сложней, так как необходимо восстановить проходимость сосудов, измененных атеросклерозом сосудов. Могут потребоваться операции шунтирования или протезирования закупоренного участка. При своевременно сделанной операции результаты очень неплохие. При эмболиях удается спасти конечность в 90% случаев, при тромбозах 75-85%.
Главное в лечении острых сосудистых заболеваний, как и в медицине в целом – предупреждение их развития.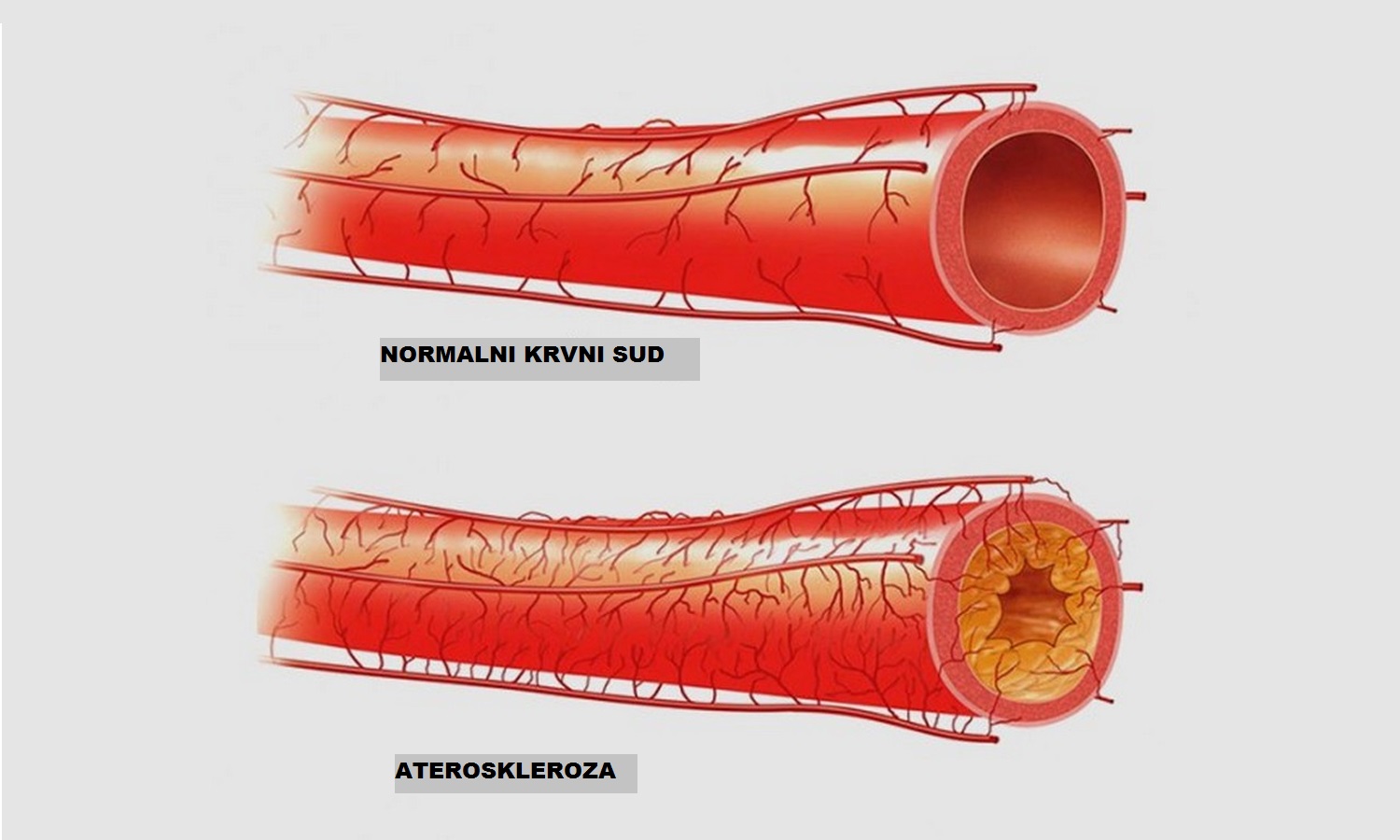 Проявления облитерирующего атеросклероза сосудов нижних конечностей требуют профилактического назначения специальных сосудистых препаратов, снижения тромбогенного потенциала крови, при необходимости плановую хирургическую операцию на сосудах.
Проявления облитерирующего атеросклероза сосудов нижних конечностей требуют профилактического назначения специальных сосудистых препаратов, снижения тромбогенного потенциала крови, при необходимости плановую хирургическую операцию на сосудах.
Для предупреждения эмболии необходимо устранять болезни, приводящие к образованию тромбов. В этом вопросе лучше всех поможет кардиолог. Если фактор риска невозможно устранить, то подбирается дозировка специального антитромботического препарата, который принимается пожизненно.
Помните, что любые, впервые возникшие, боли или неприятные ощущения в конечностях должны стать поводом к обращению за консультацией сосудистому хирургу.
Методики лечения
Аневризма брюшной аорты: лечение, симптомы, причины, профилактика | Болезни артерий
Что такое аорта
Аорта — самый большой сосуд в организме человека, который уносит кровь от сердца к органам и конечностям. Верхний отдел аорты проходит внутри грудной клетки, этот отдел называется грудной аортой.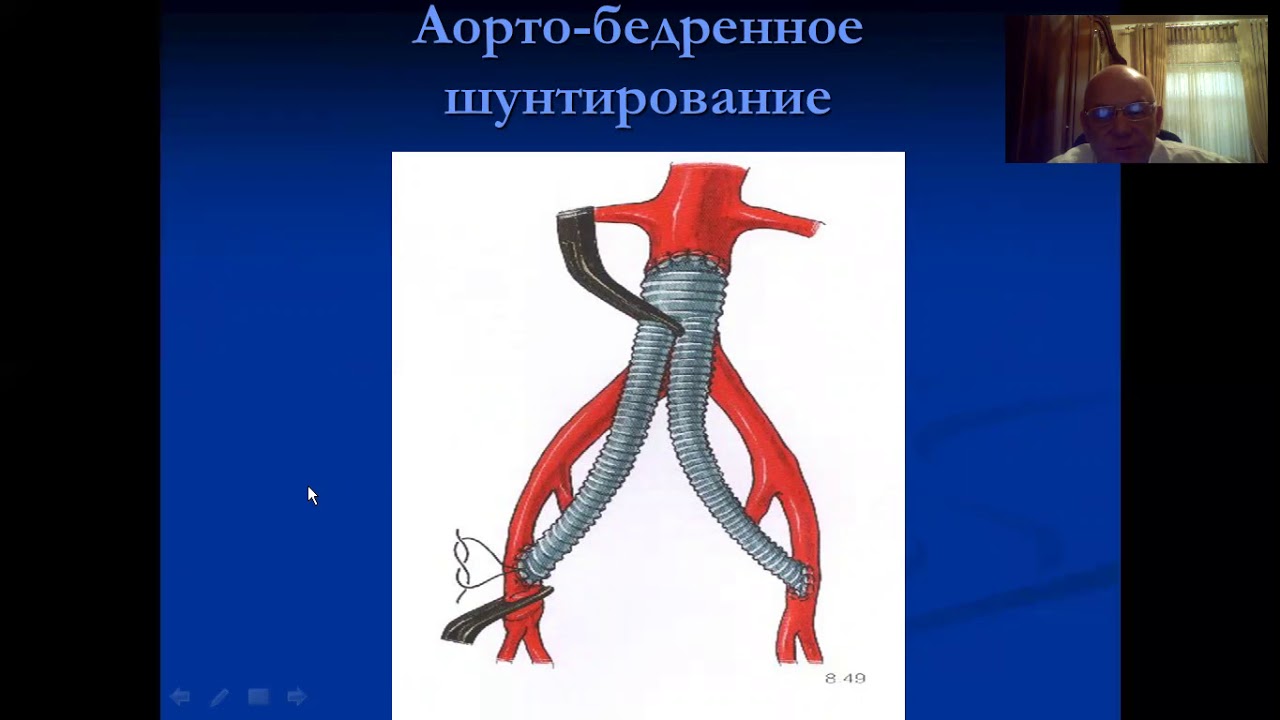 Нижняя часть находится в брюшной полости и называется брюшной аортой. Она доставляет кровь к нижней части тела. В нижней части живота брюшная аорта делится на два крупных сосуда — подвздошные артерии, которые несут кровь к нижним конечностям.
Нижняя часть находится в брюшной полости и называется брюшной аортой. Она доставляет кровь к нижней части тела. В нижней части живота брюшная аорта делится на два крупных сосуда — подвздошные артерии, которые несут кровь к нижним конечностям.
Стенка аорты состоит из трех слоев: внутренний (интима), средний (медиа), наружный (адвентиция).
Аневризма аорты брюшной полости
Аневризма брюшной аорты — это хроническое дегенеративное заболевание с угрожающими жизни осложнениями. Под аневризмой брюшной аорты понимают увеличение её диаметра более чем на 50% в сравнении с нормой или локальное выбухание её стенки. Под давлением крови, текущей через этот сосуд, расширение или выбухание аорты может прогрессировать. Диаметр нормальной аорты в брюшном отделе приблизительно равен 2 см. Однако в месте аневризмы аорта может быть расширена до 7 см. и более.
Чем опасна аневризма аорты
Аневризма аорты представляет большой риск для здоровья, так как она может разорваться. Разорванная аневризма может вызвать массивное внутреннее кровотечение, которое, в свою очередь, приводит к шоку или смертельному исходу.
Разорванная аневризма может вызвать массивное внутреннее кровотечение, которое, в свою очередь, приводит к шоку или смертельному исходу.
Аневризма аорты брюшной полости может вызывать и другие серьезные проблемы для здоровья. В мешке аневризмы часто формируются сгустки крови (тромбы) или происходит отрыв частей аневризмы, которые с током крови продвигаются по ветвям аорты к внутренним органам и конечностям. Если один из кровеносных сосудов становится блокированным, это может вызывать выраженную боль и приводить к гибели органа или потери нижней конечности. К счастью, если диагностировать аневризму аорты на ранних стадиях, то лечение может быть своевременным, безопасным и эффективным.
Виды аневризм аорты
Выделяют «истинную» и «ложную» аневризмы аорты. Истинная аневризма развивается вследствие постепенного ослабления всех слоев стенки аорты. Ложная аневризма, как правило, является результатом травмы. Она формируется из соединительной ткани, окружающей аорту. Полость ложной аневризмы заполняется кровью через возникшую в стенке аорты трещину. Сами стенки аорты в формировании аневризмы не участвуют.
Сами стенки аорты в формировании аневризмы не участвуют.
В зависимости от формы выделяют:
- мешотчатую аневризму — расширение полости аорты только с одной стороны;
- веретенообразную (фузиформную) аневризму — расширение полости аневризмы со всех сторон;
- смешанную аневризму — сочетание мешотчатой и веретенообразной форм.
Причины и факторы риска развития аневризмы брюшной аорты
Причины развития аневризм брюшной аорты весьма разнообразны. Самой частой причиной развития аневризмы является атеросклероз. На долю атеросклеротических аневризм приходится 96% от общего числа всех аневризм. Помимо этого заболевание может быть как врожденными (фибромускулярная дисплазия, кистозный медионекроз Эрдгейма, синдром Марфана и др.), так и приобретенным (воспалительные и невоспалительные). Воспаление аорты возникает при внедрении различных микроорганизмов (сифилис, туберкулез, сальмонеллёз и пр.) или как результат аллергическо-воспалительного процесса (неспецифический аортоартериит). Невоспалительные аневризмы наиболее часто развиваются при атеросклеротическом поражении аорты. Реже являются результатом травмы её стенки.
Невоспалительные аневризмы наиболее часто развиваются при атеросклеротическом поражении аорты. Реже являются результатом травмы её стенки.
Факторы риска развития аневризмы
- Артериальная гипертензия;
- Курение;
- Наличие аневризм у других членов семьи. Что свидетельствует о роли наследственного фактора в развитии этого заболевания;
- Пол: мужчины в возрасте старше 60 лет (у женщин аневризмы брюшного отдела аорты возникают реже).
Симптомы и признаки аневризмы брюшной аорты
У большинства пациентов аневризмы брюшной аорты протекают без каких-либо проявлений и являются случайной находкой при обследованиях и операциях по другому поводу.
При развитии признаков аневризмы пациент испытывает один или несколько указанных ниже симптомов:
- Ощущение пульсации в животе, подобной сердцебиению, неприятное ощущение тяжести или распирания.
- Тупая, ноющая боль в животе, в области пупка, чаще слева.
Важное значение имеют косвенные признаки аневризмы брюшной аорты:
- Абдоминальный синдром.
 Проявляется появлением отрыжки, рвоты, неустойчивого стула или запоров, отсутствием аппетита и похуданием;
Проявляется появлением отрыжки, рвоты, неустойчивого стула или запоров, отсутствием аппетита и похуданием; - Ишиорадикулярный синдром. Проявляется болями в пояснице, нарушениями чувствительности и расстройствами движений в нижних конечностях;
- Синдром хронической ишемии нижних конечностей. Проявляется в появлении боли в мышцах нижних конечностей при ходьбе, иногда в покое, похолодания кожи нижних конечностей;
- Урологический синдром. Проявляется болями и тяжести в пояснице, нарушением мочеиспускания, появлением крови в моче.
Предвестниками разрыва может быть усиление болей в животе.
При разрыве аневризмы, пациент внезапно ощущает усиление или появлении боли в животе, иногда «отдающую» в поясницу, паховую область и промежность, а также выраженную слабость, головокружение. Это симптомы массивного внутреннего кровотечения. Развитие такой ситуации опасно для жизни! Пациенту нужна экстренная медицинская помощь!
Диагностика аневризм брюшной аорты
Наиболее часто аневризмы брюшной аорты выявляют при ультразвуковом исследовании органов брюшной полости.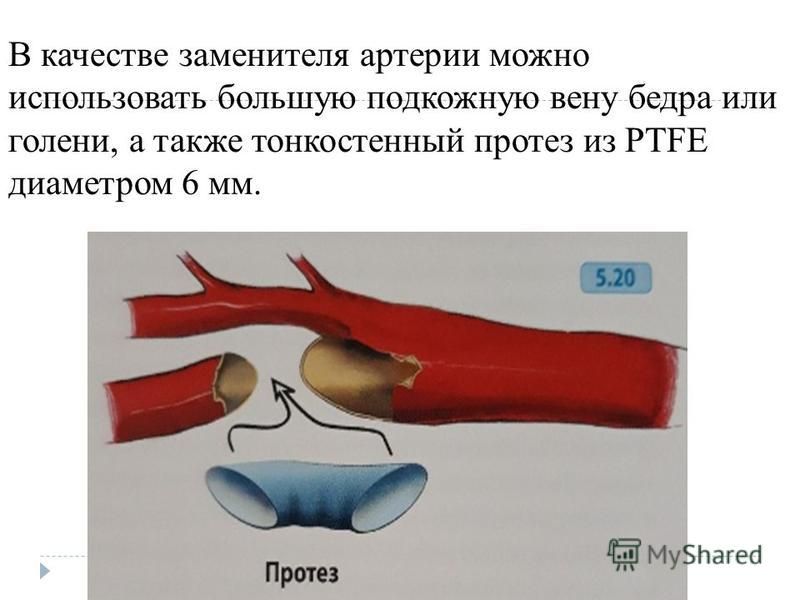 Как правило, обнаружение аневризмы является случайной находкой. Если врач подозревает у пациента аневризму аорты для уточнения диагноза используются современные методы диагностики.
Как правило, обнаружение аневризмы является случайной находкой. Если врач подозревает у пациента аневризму аорты для уточнения диагноза используются современные методы диагностики.
Методы диагностики аневризмы брюшной аорты
При необходимости исследуется брюшной и грудной отдел аорты.
Методы лечения аневризмы аорты
Существует несколько методик лечения аневризмы аорты. Важно знать преимущества и недостатки каждой из этих методик. Подходы к лечению аневризм брюшного отдела аорты:
Наблюдение за пациентом в динамике
При размере аневризмы менее 4,5 см. в диаметре пациенту рекомендовано наблюдение сосудистого хирурга, т. к. риск операции превышает риск разрыва аневризмы аорты. Таким пациентам должны проводится повторные ультразвуковые исследования и/или компьютерная томография не реже 1 раза в 6 месяцев.
При диаметре аневризмы более 5 см. хирургическое вмешательство становится предпочтительным, так как с увеличением размеров аневризмы повышается риск разрыва аневризмы.
Если размер аневризмы увеличивается более чем на 1 см. в год, риск разрыва возрастает и хирургическое лечение также становиться предпочтительным.
Открытое хирургическое вмешательство: резекция аневризмы и протезирование аорты
Хирургическое лечение направлено на профилактику жизнеугрожающих осложнений. Риск хирургического вмешательства связан с возможными осложнениями, которые включают инфаркт, инсульт, потерю конечности, острую ишемию кишечника, сексуальную дисфункцию у мужчин, эмболизацию, инфекцию протеза и почечную недостаточность.
Операция выполняется под общим наркозом. Суть операции в удалении аневризматического расширения и замещение его синтетическим протезом. Средний показатель смертности при открытых вмешательствах составляет 3-5 %. Однако, может быть выше при вовлечении в аневризму почечных и/или подвздошных артерий, а также в силу имеющейся у пациента сопутствующей патологии. Наблюдение в послеоперационном периоде осуществляется один раз в год. Отдаленные результаты лечения хорошие.
Отдаленные результаты лечения хорошие.
Эндоваскулярное протезирование аневризма аорты: установка стент-графта
Эндопротезирование аневризмы аорты является современной альтернативой открытому вмешательству. Операция выполняется под спинальной или местной анестезией через небольшие разрезы/проколы в паховых областях. Через вышеуказанные доступы в бедренную артерию под контролем рентгена вводятся катетеры. По которым, в дальнейшем, будет подводится эндопротез к аневризматическому расширению. Эндопротез или стент-графт брюшной аорты представляет собой сетчатый каркас, выполненный из специального сплава и обернутый синтетическим материалом. Последним этапом операции является установка стент-графта в место аневризматического расширения аорты.
В конечном счете аневризма «выключается» из кровотока и риск ее разрыва становится маловероятным. После эндопротезирования аорты пациент наблюдается в стационаре 2-4 дня и выписывается.
Эта методика позволяет снизить частоту ранних осложнений, сократить сроки пребывания пациентов в стационаре и уменьшить показатель смертности до 1-2%. Наблюдение в послеоперационном периоде осуществляется каждые 4-6 месяцев с использованием ультразвуковых методик, КТ-ангиографии, рентгенконтратной ангиографии. Эндоваскулярный метод лечения, безусловно, менее травматичный. Ежегодно, только в США, проводится около 40 000 подобных операций.
Наблюдение в послеоперационном периоде осуществляется каждые 4-6 месяцев с использованием ультразвуковых методик, КТ-ангиографии, рентгенконтратной ангиографии. Эндоваскулярный метод лечения, безусловно, менее травматичный. Ежегодно, только в США, проводится около 40 000 подобных операций.
Таким образом, выбор методики лечения аневризмы брюшного аорты основывается на индивидуальных особенностях пациента.
Эндоваскулярное лечение острого тромбоза тибиоперонеального ствола. Клинический случай | Чигидинова
1. Cheng B., Li J.Y., Li X.C. MiR-323b-5p acts as a novel diagnostic biomarker for critical limb ischemia in type 2 diabetic patients. Sci Reports. 2018;8(1):15080. DOI: 10.1038/s41598-018-33310-4
2. Peripheral Arterial Diseases (Diagnosis and Treatment of). 2017 ESC Clinical Practice Guidelines. Eur Heart J. 2018;39(9):763–816. DOI: 10.1093/eurheartj/ehx095
Eur Heart J. 2018;39(9):763–816. DOI: 10.1093/eurheartj/ehx095
3. Митичкин А.Е., Папоян С.А., Щеголев А.А., Квицаридзе Б.А., Мутаев М.М., Сазонов М.Ю. и др. Сочетанные эндоваскулярные и реконструктивные операции при многоэтажных поражениях артерий нижних конечностей. Анналы хирургии. 2016;21(3):187– 92. DOI: 10.18821/1560-9502-2016-21-3-187-192
4. Morley R.L., Sharma A., Horsch A.D., Hinchliffe R.J. Peripheral artery disease. BMJ. 2018;360:j5842. DOI: 10.1136/bmj.j5842
5. Li J., Yang X., Wang X., Jia X., Wang Z., Deng A., et al. Siglec-5 is a novel marker of critical limb ischemia in patients with diabetes. Sci Reports. 2017;7:11272. DOI: 10.1038/s41598-017-11820-x
6..jpg) Reinecke H., Unrath M., Freisinger E., Bunzemeier H., Meyborg M., Lüders F., et al. Peripheral arterial disease and critical limb ischaemia: still poor outcomes and lack of guideline adherence. Eur Heart J. 2015;36(15):932–38. DOI: 10.1093/eurheartj/ehv006
Reinecke H., Unrath M., Freisinger E., Bunzemeier H., Meyborg M., Lüders F., et al. Peripheral arterial disease and critical limb ischaemia: still poor outcomes and lack of guideline adherence. Eur Heart J. 2015;36(15):932–38. DOI: 10.1093/eurheartj/ehv006
7. Rosenfield K. Jaff M.R., White C.J., Rocha-Singh K., Mena-Hurtado C., Metzger D.C., et al. Trial of a paclitaxel-coated balloon for femoropopliteal artery disease. N Engl J Med. 2015;373(2):145–53. DOI: 10.1056/ NEJMoa1406235
8. Tepe G., Laird J., Schneider P., Brodmann M., Krishnan P., Micari A., et al. Drug-coated balloon versus standard percutaneous transluminal angioplasty for the treatment of superficial femoral and popliteal peripheral artery disease: 12-month results from the IN.PACT SFA randomized trial. Circulation. 2015;131(5):495–502. DOI: 10. 1161/ CIRCULATIONAHA.114.011004
1161/ CIRCULATIONAHA.114.011004
9. Singh S., Armstrong E.J., Sherif W., Alvandi B., Westin G.G., Singh G.D., et al. Association of elevated fasting glucose with lower patency and increased major adverse limb events among patients with diabetes undergoing infrapopliteal balloon angioplasty. Vasc Med. 2014;19(4):307–14. DOI: 10.1177/1358863X14538330
10. Dominguez A. 3rd, Bahadorani J., Reeves R., Mahmud E., Patel M. Endovascular therapy for critical limb ischemia. Expert Rev Cardiovasc Ther. 2015;13(4):429–44. DOI: 10.1586/14779072.2015.1019472
11. Popplewell M.A., Davies H., Jarrett H., Bate G., Grant M., Patel S., et al. Bypass versus angio plasty in severe ischaemia of the leg — 2 (BASIL-2) trial: study protocol for a randomised controlled trial. Trials 2016;17:11. DOI: 10.1186/s13063-015-1114-2
12. Teraa M., Conte M.S., Moll F.L., Verhaar M.C. Critical limb ischemia: current trends and future directions. J Am Heart Assoc. 2016;5(2):e002938. DOI: 10.1161/JAHA.115.002938
13. Moazzami K., Moazzami B., Roohi A. Local intramuscular transplantation of autologous mononuclear cells for critical lower limb ischaemia. Cochrane Database Syst Rev. 2014;12:CD008347. DOI: 10.1002/14651858.CD008347.pub2
14. Peeters Weem S.M., Teraa M., de Borst G.J., Verhaar M.C., Moll F.L. Bone marrow derived cell therapy in critical limb ischemia: a metaanalysis of randomized placebo controlled trials. Eur J Vasc Endovasc Surg. 2015;50(6):775–83. DOI: 10.1016/j.ejvs.2015.08.018
15. Кавтеладзе З.А., Даниленко С.Ю., Петренко П.Н., Брутян Г.А., Желтов Н.Ю., Эртман В.Г., и др. Возможности эндоваскулярной хирургии при повторных вмешательствах на магистральных артериях нижних конечностей. Эндоваскулярная хирургия. 2015;2(4):45–51.
16. Бояринцев В.В., Закарян Н.В., Шелеско А.А., Панков А.С., Давтян А.Г. Современные возможности рентгенoэндоваскулярной хирургии в экстренной и неотложной практике. Кремлевская медицина. Клинический вестник. 2016;(2):9–11.
Дуплексное сканирование брюшной аорты | Здравница
Аорта – это самый большой сосуд (артерия) в нашем организме. По аорте кровь идет из сердца ко всем органам и тканям. Выходя из сердца, аорта проходит через грудную клетку, где она носит название грудного отдела. В брюшной полости аорта называется брюшной аортой. Через этот отдел аорты поступает кровь к нижней части тела, органам брюшной полости. В нижнем отделе живота аорта делится на две ветви – подвздошные артерии, которые участвуют в кровоснабжении нижних конечностей.
Аневризма (от лат. aneuryno — расширяю) — расширение сосуда или выбухание его стенки кнаружи, возникающее вследствие разнообразных поражений, понижающих прочность и эластичность сосудистой стенки. Давление крови, текущей через брюшную аорту приводит к её выпиранию, как воздушный шар. Аневризмы аорты наносят большой риск для здоровья, так как они могут разорваться. Разрыв аневризмы может вызвать внутреннее кровотечение, которое может привести к смерти. Также при данном заболевании могут сформироваться тромбы которые могут оторваться и с током крови попасть в более мелкие сосуды и привести к тромбозу (закупорке) артерии. Нередко аневризма брюшной аорты протекает бессимптомно.
Наиболее частые признаки аневризмы это:
• боли в животе — наиболее постоянный симптом, локализуются обычно в околопупочной области или в левой половине живота, могут быть постоянными, ноющими или носить приступообразный характер, иногда иррадиируют в поясничную или паховую область.
• чувство усиленной пульсации в животе, ощущение тяжести и распирания в над пупком, вздутие живота.
• в редких случаях, боль в ногах, побледнение нижней конечности
• при разрыве аневризмы можете внезапно почувствовать интенсивную слабость, головокружение, или боль, и потеря сознания. Это — опасная для жизни ситуация, и Вы должны немедленно госпитализироваться.
Причины развития аневризм весьма разнообразны.Основной причиной их развития является атеросклероз и такие факторы риска как артериальная гипертензия.
Кроме этого факторами риска являются:
• Мужской пол старше 60 лет.
• Наличие непосредственного родственника, который имел АБА.
• Наличие высокого кровяного давления.
• Курение.
• Высокий уровень холестерина.
• Сахарный диабет.
Риск развития аневризмы увеличивается с возрастом.
Дуплексное сканирование брюшной аорты и ее ветвей объединяет допплерометрическое и традиционное ультразвуковое сканирование, позволяющие в реальном режиме оценить эхоструктуру стенок сосудов и исследовать внутрипросветный кровоток. Дуплексное сканирование позволяет выявить аневризматические расширения и расслоения грудной или брюшной аорты; аномалии, тромбозы, сдавление, атеросклеротические и др. поражения ветвей аорты; определять локализацию патологии, протяженность и степень нарушения кровотока. Дуплексное сканирование брюшной аорты и ее ветвей требует подготовки, направленной на уменьшение метеоризма в кишечнике: за 2-3 дня до диагностики исключить из рациона молочные продукты, черный хлеб, сырые овощи и фрукты. В эти дни можно принимать таблетки, уменьшающие газообразование (например, Эспумизан по 2-3 капсулы 4 раза в день, активированный уголь по 2 таблетки или другие сорбенты). Перед процедурой не принимать слабительные препараты, не ставить клизмы и не кушать не меньше 8 часов (лучше проводить исследование с утра после голодания во время ночного сна).
Ответить
Эндоваскулярное лечение острой ишемии нижних конечностей
Острая ишемия нижних конечностей развивается вследствие окклюзии артерии тромбом или эмболом, что приводит к резкому снижению притока крови к тканям и, как следствие, к развитию гангрены конечности. Острая ишемия является наиболее частой причиной ампутации конечности, приводящей к инвалидизации, и в тяжёлых случаях, смерти пациента.
Заболеваемость острой ишемией конечности составляет 14 пациентов на 100 тыс. населения, ежегодно достигая 16 % от всех сосудистых заболеваний. Несмотря на совершенствование методов диагностики и хирургического лечения, сохраняется высокая 30 дневная летальность (до 15 % после классической тромбэктомии) и большой процент инвалидизации (10-30%) пациентов. Каждому четвёртому пациенту после классической тромбэктомии в раннем послеоперационном периоде выполняется высокая ампутация конечности.
В настоящее время самыми частыми причинами острой ишемии нижних конечностей являются тромбоз и эмболия артерии. Тромбоз – острая окклюзия артерии на фоне атеросклеротического поражения сосудистой стенки. Патогенетическими факторами, приводящими к возникновению тромбоза, являются три основные причины: повреждение сосудистой стенки, гиперкоагуляция и изменение кровотока в зоне стеноза.
Эмболия – острая окклюзия сосуда вследствие миграции эмбола в целевой сосуд. Выявляют две основные причины эмболии: кардиальные и некардиальные.
Кардиальные: миграция тромбов из полостей сердца при фибрилляции предсердий, аневризме левого желудочка, инфаркте миокарда, с поверхности искусственных клапанов сердца, вегетаций при бактериальном эндокардите. Некардиальные: миграция пристеночных тромбов или атеросклеротического детрита из проксимально расположенных отделов сосудистой системы, например, из аневризмы брюшного отдела аорты.
Для оценки тяжести и выраженности клинических проявлений и степени повреждения тканей, принята классификация острой ишемии конечности, предложенная Затевахиным И.И. и соавт. в 2002 году.
| Степень ишемии | Характер ишемии | Клинические признаки | Прогноз |
| I | Не угрожающая | Онемение, парестезии, боль | Угрозы для конечности нет |
| II (А-Б-В) | Угрожающая | Парез, паралич, субфасциальный отек | Угроза гибели конечности в кратчайшие сроки. Необходима срочная реваскуляризация |
| III (А-Б) | Необратимая | Дистальная или тотальная контрактура, некротические дефекты, гангрена конечности | Конечность нежизнеспособна, угроза для жизни. Необходима ампутация |
Всем пациентам с острой ишемией конечности и сохраненной жизнеспособностью тканей, в сроки до 14 дней с начала заболевания показано выполнение экстренной операции!
В настоящее время, единственным эффективным методом лечения острой ишемии конечности является выполнение хирургического вмешательства – эмболтромбэктомии из магистральных артерий.
Хирургические вмешательства разделяются на два вида: открытая классическая эмболтромбэктомия и малоинвазивная эндоваскулярная катетерная эмболтромбэктомия.
Для принятия решения о виде оперативного вмешательства определяется характер и патогенез окклюзии артерии: эмболия или тромбоз на фоне атеросклеротического или диабетического поражения магистральных артерий, оценивается степень ишемического повреждения тканей конечности.
Пациентам с эмболическим характером окклюзии выполняется открытая классическая эмболтромбэктомия, эффективно устраняющая причину ишемии. Пациентам с тромбозом магистральных артерий, для проведения дифференциального диагноза между тромбозом и артериальной эмболией, выполняются неинвазивные методы визуализации или ангиография. Наиболее частой причиной тромбоза артерий является изменение сосудистой стенки атеросклеротической бляшкой со значительным стенозированием просвета. Классическая тромбэктомия не позволяет эффективно удалить тромб и устранить стеноз артерии. Эндоваскулярная катетерная тромбэктомия, одновременно с удалением тромботических масс, позволяет выполнить баллонную ангиопластику и стентирование атеросклеротически стенозированной артерии, эффективно восстанавливая кровоснабжение конечности.
У пожилых пациентов с тяжелой сопутствующей патологией, эндоваскулярная катетерная тромбэктомия является единственным методом хирургического лечения. Преимуществами эндоваскулярного метода лечения являются: низкая травматичность, быстрое достижение реперфузии конечности, одномоментное лечение сопутствующих стено-окклюзирующих поражений целевой артерий, низкий уровень осложнений.
Эндоваскулярная катетерная тромбэктомия состоит из двух этапов.
1.Диагностическая ангиография — выполняется под местным обезболиванием через пункцию лучевой артерии. Под контролем рентгеновского излучения диагностический катетер проводится в инфраренальный отдел аорты. С помощью автоматического инъектора по катетеру в сосуд вводится контрастное средство и выполняются серии динамических полипроекционных ангиограмм. По результатам ангиографии принимается решение о тактике оперативного вмешательства.
Операция – эндоваскулярная катетерная тромбэктомия выполняется через пункцию общей бедренной артерии. К месту тромботической окклюзии подводится катетер с большим внутренним просветом и производится контролируемая аспирация и экстракция тромба с одновременным его фрагментированием. После успешной аспирации выполняется контрольная ангиография. При выявлении в просвете артерии стеноза или диссекции (надрыв внутренней стенки сосуда) препятствующих току крови, операция завершается баллонной ангиопластикой или стентированием. Имплантация стента в сосуд создает каркас, который расширяет просвет артерии, устраняет пролабирование атеросклеротической бляшки и препятствет распространению диссекции интимы.
Полностью восстановленный просвет артерии после эндоваскулярной катетерной тромбэктомии и стентирования пораженного участка артерии
Эндоваскулярная катетерная тромбэктомия, дополненная баллонной ангиопластикой и стентированием артерий, является новым и высокоэффективным методом хирургического лечения острой артериальной ишемии конечности. Использование визуального контроля эффективности проводимой операции и одновременное устранение причины тромбоза, позволяет получить хорошие непосредственные и отдалённые результаты операции, предотвращая развитие повторного тромбоза артерий.
ГБУЗ «ТОКБ им. В.Д. Бабенко» является единственным медицинским учреждением области, где с 2018 года начато выполнение эндоваскулярных операций при острой ишемии конечности. За 6 месяцев текущего года в отделении рентгенэндоваскулярных методов диагностики и лечения выполнено 6 катетерных эндоваскулярных тромбэктомий из артерий нижних конечностей. Средний возраст пациентов составил 69 лет. У 4-х пациентов тромбэктомия была дополнена стентированием артерии. Осложнений при проведении операций и в послеоперационном периоде не было. Во всех случаях операция завершилась успешно и удалось сохранить конечность пациентам.
Вопрос врачу: как избежать тромбоза
Что можно сделать, чтобы снизить риск тромбообразования? Какую роль в возникновении тромбозов играет наследственность? Какое обследование нужно пройти, чтобы проверить состояние своих сосудов? Какие методы исследования используются сегодня? Всем ли в определенном возрасте нужны антикоагулянты?
На эти и другие вопросы пациентов отвечает сердечно-сосудистый хирург НМИЦ хирургии им. А.В. Вишневского, кандидат медицинских наук, доцент Заурбек Ахсарбекович Адырхаев.
– Какую роль в возникновении тромбозов играет наследственность?
– С точки зрения наследственности есть несколько факторов, которые могут предопределять повышенные риски тромбозов. Первый из них – генетические мутации, которых существует не менее 12. При артериальных тромбозах это еще врожденная гиперхолестеринемия и гипергомоцистеинемия. Эти и другие наследственные факторы, которые cпособны на уровне реологии крови предопределять повышенную предрасположенность к тромбообразованию – как венозному, так и артериальному – могут быть выявлены с помощью лабораторной диагностики.
– Артериальные тромбозы и атеросклеротические бляшки – это явления одного ряда?
– Бляшки могут повышать риски артериального тромбоза – сужать просвет сосуда и тем самым способствовать изменению спектра кровотока в этой области. Либо они фрагментируются – и тогда их кусочки могут отрываться, закрывая просвет сосуда или затрудняя локально ток крови в нем, что приводит к снижению скорости кровотока и образованию тромбов в этой области.
– В чем отличия тромба от бляшки? У них разная структура?
– Бляшка – более плотное образование, тромб же представляет собой сгусток крови. Свежий тромб – багрово-красного цвета, мягкий, по структуре чем-то напоминающий слизня.
– Почему у одних он образуется, а у других нет? Каков механизм такого загустения крови?
– Все сосудистые врачи знают правила «триады Вирхова» (Рудольф Вирхов – немецкий патолог, пионер в патофизиологии тромбоза). Чтобы процесс формирования тромба был запущен, обязательно должны иметь место три фактора: замедление кровотока, повреждение эндотелия (внутренней выстилки сосуда) и коагулопатия (повышенная свертываемость крови). Только при наличии этих трех факторов возможно образование тромба. Одного фактора недостаточно, но если он присутствует, как правило, к нему присоединяются другие и рано или поздно начинают себя проявлять. Проще говоря, если у пациента есть наследственная коагулопатия, он уже находится в группе риска. Он может отправиться в долгий 8-часовой перелет, уснуть в самолете и не проснуться, потому что к его коагулопатии присоединится такой фактор, как снижение скорости кровотока.
– В каких случаях она снижается?
– При длительных статических нагрузках – если человек долго стоит, или сидит, или едет в машине, летит в самолете… Словом, нахождение в неподвижном состоянии способствует образованию венозного тромбоза. В группе риска также пациенты, которые имеют какую-то сопутствующую патологию – онкозаболевания, гинекологические заболевания, требующие приема гормональных препаратов. Кстати, оральные контрацептивы также повышают эти риски.
Артериальные тромбозы очень редко случаются без наличия системного атеросклероза. Другим фактором риска их возникновения, безусловно, является нарушение сердечного ритма. Если у пациента даже с невыраженным атеросклерозом есть мерцательная аритмия, то на ее фоне образовываются тромбы в сердце, которые могут мигрировать и закрывать сосуды, в том числе магистральные – вплоть до аорты и подвздошных артерий, вызывая острую ишемию сосудов ног.
– В каких частях тела обычно образуются тромбы?
– При венозных тромбозах самая частая локализация – глубокие вены ног. Опасность заключается в том, что тромб быстро поднимается с нижних конечностей в бедренные подвздошные вены. Это несет в себе колоссальные риски тромбоэмболии легочной артерии – то, что в народе часто называют «тромб оторвался». Это самое грозное осложнение венозных тромбозов, и, конечно, если оно вовремя не диагностировано, то несет в себе реальную угрозу для жизни пациента.
При артериальных тромбозах самое распространенное осложнение – эмболия в бифуркацию аорты, когда закрываются подвздошные артерии, а также эмболия в артерии ног. Чаще всего страдают артерии голени и поверхностные бедренные артерии, хотя могут и другие. Здесь уже речь идет о спасении конечности, потому что, как правило, у таких больных возникает острая ишемия, которая требует экстренного оперативного вмешательства с целью восстановления кровотока в ноге. И если это не будет сделано в ближайшие часы, пациент может потерять ногу.
– А если тромбоз есть, но он бессимптомный, что должно побудить человека отправиться к врачу?
– Тут нам тоже придется разделить тромбозы венозные и артериальные. В первом случае это, как правило, ощущение напряжения в нижней конечности, иногда уже визуально оцениваемый ее отек, боль и покраснение по ходу вен, которые просвечиваются на ноге. Вот эти моменты должны, конечно, насторожить, особенно если это случается после тех эпизодов, о которых мы говорили, – приема гормональных препаратов, беременности у женщин в 3-м триместре, длительных переездов, сидячей работы… Если человек ощущает напряжение, отек и боль в конечности, а также покраснение и гиперемию по ходу вены, конечно, он должен обратиться к врачу.
Если тромбоз локализуется только в венах голени, зачастую для пациента это даже может пройти незамеченным, и мы узнаем об этом потом – когда он обследуется по каким-то другим причинам. Делая ультразвук, мы видим, что вены изменены, и даже если тромбов нет, есть признаки того, что пациент тромбоз перенес.
Что касается артериального тромбоза, то его сложно не заметить. Если кровоток в каком-то сегменте конечности прекращается внезапно, пациент так или иначе это почувствует. Безусловно, это острая боль, похолодание конечности. Чем больше по времени длится ишемия, тем больше неврологических осложнений присоединяется – в виде онемения ноги, ограничения движения в голеностопном, в коленном суставе. На более поздних стадиях, конечно, появляется отек.
Самая тяжелая стадия – формирование так называемой контрактуры в коленном и голеностопном суставах, когда пациент уже не может двигать ногой самостоятельно из-за сильного болевого синдрома в результате спазмирования мышц. Меняется цвет ноги, она становится сначала бледной, потом появляется мраморная окраска. Тяжелые эпизоды острой ишемии сопровождаются такими опасными осложнениями, как флегмона стопы и т.д.
Если этот процесс развивается быстро, он может привести к влажной гангрене, когда пациенту уже помочь невозможно. Поэтому так важно не пропустить первые симптомы – резкую боль, которая приобретает постоянный характер, похолодание ноги, изменение цвета кожных покровов. И, безусловно, пытаться лечиться домашними средствами не следует, нужно срочно обращаться к врачу.
– Чем отличается доплерография сосудов ног от УЗИ, и в каких случаях делается это исследование?
– Доплерографическое исследование показывает в основном скоростные характеристики кровотока, она не направлена на то, чтобы определить состояние внутренней выстилки сосуда, визуализировать бляшки или тромбы, которые там гнездятся. Это сегодня уже не информативно, и в своей рутинной практике мы переходим на цветовое дуплексное сканирование. Оно позволяет получить полные данные как о скоростных характеристиках кровотока, так и о состоянии сосуда в целом: толщине его стенки, степени воспаления, если оно есть, наличии или отсутствии атеросклеротических бляшек, насколько они сужают просвет сосуда, есть в нем тромбы или нет, насколько они распространяются, сколько сантиметров сосуда занимают, как плотно фиксированы к стенке (что тоже очень важно).
– Мы говорим про ноги, но ведь бывают тромбы и в сосудах головы. Или это отдельная история?
– Такой тромбоз ведет к грозному осложнению – инсульту. Сегодня в Москве, да и по всей России, открыто огромное количество сосудистых центров, которые призваны бороться с острыми коронарными синдромами и острыми инсультами. Тромбоз выливается в так называемый инсульт в ходу, то есть у пациента присутствует вся клиника инсульта (немеет часть тела, рука или нога, нарушается речь и т.д.). Если к такому пациенту вовремя приедет скорая помощь, она доставит его в один из сосудистых центров, где будет предпринята попытка либо системного или локального тромболизиса (растворения тромбов), либо механической тромбоэкстракции, когда с помощью специальных устройств этот тромб из артерии извлекается.
Сейчас для этого все возможности есть, и довольно успешно с этими состояниями справляются. Главное – сделать все вовремя, попасть в так называемое терапевтическое окно (от 6 до 12 часов).
– Существует мнение, что после определенного возраста всем нужно принимать кроворазжижающие препараты, и все будет в порядке.
– Начнем с того, что может человек сделать сам, чтобы максимально себя обезопасить. Первое и основное – это активный образ жизни. Нужны аэробные нагрузки. Я говорю своим пациентам: вы должны гулять 30-60 минут в день, причем не прогулочным шагом, а ускоряясь до 3-4 км в час. Занимайтесь скандинавской ходьбой, плавайте, делайте то, что вам больше нравится, но обязательно двигайтесь! И на воздухе вы должны проводить не менее получаса-часа в день, причем проводить активно. Безусловно, надо отказаться от курения – это доказанный факт риска атеросклероза и любых осложнений атеротромбоза.
Третье – конечно, питание. Сейчас самая популярная диета, которая звучит во всех рекомендациях, – средиземноморская. Она доступна, и придерживаться ее легко и приятно. Принципы очень просты: ограничение потребления животных жиров и красного мяса (до 1-2 раз в неделю), преобладание растительных жиров и рыбы, основа рациона – растительная пища и растительные белки.
И еще важный момент. Для того чтобы снизить риск тромбообразования, нужно соблюдать адекватный режим гидратации организма. Человек должен потреблять необходимое количество жидкости в день, и это никак не меньше литра-полутора (с супом, киселем, водой, чаем, — необязательно пить только чистую воду). Потребляя жидкость, вы добиваетесь разжижения крови физиологическим путем. Если человек регулярно не добирает жидкости и в его кровеносном русле недостаточное ее количество, естественно, кровь будет сгущаться, и концентрация красных кровяных телец на 1 мл крови будет возрастать. В этой ситуации он может, например, сходить в баню и вернуться оттуда с венозным или артериальным тромбозом. Потея, человек теряет до нескольких литров жидкости, а значит, такое же количество должен восполнить.
Теперь по поводу препаратов. Я считаю, что без рекомендации врача ничего никому принимать не следует. Терапевты амбулаторного звена сейчас весьма образованы в области профилактики и возможных осложнений сердечно-сосудистых заболеваний, поэтому каждый человек должен наблюдаться в поликлинике, проходить диспансеризацию, которая возрождается в нашей стране, и при наличии проблем — состоять на учете у кардиолога или терапевта, который в соответствии с показаниями будет назначать терапию. А пить препарат, который на слуху или который соседке прописали — нельзя.
Раньше для снижения рисков инфарктов и инсультов всем подряд назначали аспирин – так вот сейчас стали появляться исследования, которые говорят о сомнительной пользе бесконтрольного и поголовного назначения аспирина. 40 процентов людей вообще толерантны к этому препарату, то есть, принимая аспирин, они не получают того эффекта, ради которого его пьют. И никто, кто назначает этот аспирин, не отслеживает ожидаемый эффект. Зато негативное воздействие на желудок есть у всех и уже давно доказано.
– Но ведь появились новые поколения антиагрегантов.
– Они тоже не показаны всем, поскольку настолько сильно разжижают кровь, что влекут за собой риск кровотечения. Да, кому-то они нужны, особенно после 50 лет, но их должны назначать врачи по показаниям. Каждый должен заниматься своим делом. Врач – лечить, а пациент – будучи ответственным за свое здоровье – по максимуму стараться вести здоровый образ жизни и своевременно и периодически обращаться докторам.
– Вы говорили о здоровом образе жизни. А если, скажем, тромб уже есть или формируется, разве фитнес не может спровоцировать его движение?
– Если в возрасте 50 лет вы впервые в своей жизни решили заняться фитнесом, безусловно, сначала вы должны обследоваться. Перед началом занятий необходимо пройти элементарное фитнес-тестирование. Это совсем не то, когда рассказывают, как и какой тренажер работает, вас должен проконсультировать врач, который определит вашу толерантность к физической нагрузке, сделает тесты под контролем ЭКГ и других приборов.
– Смоделируем такую ситуацию. Человек знает, что в его роду были инсульты и случаи тромбов. И он хочет максимально себя обезопасить. Какие обследования ему сделать, чтобы проверить состояние сосудов?
– Во-первых, общий и биохимический анализ крови, на липидный профиль – узнать индекс атерогенности (соотношение липопротеидов высокой и низкой плотности).
Нужно сдать коагулограмму – посмотреть показатели свертываемости крови, сделать ЭКГ, измерить лодыжечно-плечевой индекс, отражающий состояние кровообращения в нижних конечностях. Если этот индекс снижен, можно говорить о системном атеросклерозе. Надо определить в крови уровень гомоцистеина (повышенный его показатель тоже может говорить об атеросклеротических осложнениях), а также сделать ультразвук сонных артерий.
Я бы еще не упускал из виду ультразвук брюшной полости, на котором можно посмотреть, нет ли аневризмы аорты, которая часто бывает первым манифестирующим заболеванием у пациента с атеросклерозом. И, безусловно, если проводить более углубленное обследование, потребуется эхокардиография, позволяющая увидеть, нормально ли функционирует сердечная мышца.
Головной мозг, сердце и нижние конечности – вот точки риска атеросклероза и образования тромбов для человека, который знает свою наследственную предрасположенность к этим заболеваниям. И перечисленные исследования – тот минимум, который позволит ему составить первичную картину.
– И после этого жить спокойно?
– Не совсем так. Человек, который сделал все эти исследования, должен потом прийти к врачу. Даже если показатели в пределах нормы, это может быть верхняя граница нормы, что уже свидетельствует о каких-то изменениях. Только врач может определить риски. А если изменения в сосудах выявлены, раз в год надо обследования повторять.
Более того, я всем рекомендую следить за сахаром крови, потому что сахарный диабет тоже является одним из факторов риска и ухудшает прогноз у больных с атеросклерозом. Что касается венозного тромбоза, здесь следует обратить внимание, не отекают ли у вас ноги к концу рабочего дня, не чувствуется ли дискомфорт после длительных переездов и перелетов, не бывает ли трудно надеть сапоги или туфли. В этом случае нужно делать ультразвук вен и опять же обращаться к врачу.
Главное – не заниматься самолечением, это никогда не будет эффективно. Берегите свои сосуды и здоровье в целом!
Полная версия интервью опубликована в №5/20 журнала «Будь здоров».
Отчет о случае бессимптомного тромбоза аорты, случайно обнаруженного с помощью компьютерной томографии у практически здорового человека, перенесшего онкологические операции в анамнезе | Thrombosis Journal
75-летнему японцу, у которого в анамнезе не было тромбозов или тромбоэмболий, 2 года назад была проведена резекция правой верхней доли легкого по поводу аденокарциномы локализованной аденокарциномы без отдаленных метастазов. Химиотерапия и лучевая терапия не проводились. После операции каждые 6 месяцев проводилась контрольная КТ, а через 1 год операции выполнялась фтордезоксиглюкозо-позитронно-эмиссионная томография (ФДГ-ПЭТ) для проверки рецидива рака легких, и результаты показали отсутствие рецидивов или отдаленных результатов. метастазы и отсутствие аномалий грудной аорты или неожиданного тромба на стенке (рис.1а). Однако через 1,5 года после первичной операции случайно был обнаружен тромб аорты в нисходящей дуге аорты (рис. 1б). В то время пациент был явно здоров, с температурой тела 36,2 ° C, артериальным давлением 122/68 мм рт.ст., частотой сердечных сокращений 76 ударов в минуту и периферическим кислородным насыщением 96% в воздухе помещения. Лабораторные данные показали несколько повышенный уровень D-димера, снижение активности протеина C в плазме, а также нормальную функцию печени и липидный профиль (таблица 1). Волчаночный антикоагулянт или антикардиолипиновые антитела не были обнаружены, и пациент бросил курить в 60-летнем возрасте (индекс Бринкмана 800).Хотя причина и значение снижения активности протеина C не были полностью поняты, мы начали антикоагулянтную терапию тромбоза аорты с использованием варфарина. Последующая компьютерная томография показала, что тромб аорты постепенно регрессировал и был полностью устранен через 6 месяцев антикоагулянтной терапии без серьезных осложнений (рис. 1c). Затем антикоагулянтная терапия была прекращена без рецидива тромба аорты, и активность протеина С в плазме восстановилась в пределах нормы (72%).
Фиг.1
Компьютерная томография (КТ) грудной клетки с контрастным усилением, проведенная через 1 год после операции по поводу рака легких ( a ) КТ грудной клетки с контрастным усилением через 1,5 года после операции по поводу рака легких. Случайно был обнаружен тромб аорты в дистальной части дуги аорты ( b ) КТ грудной клетки с контрастированием через 2 года после операции по поводу рака легкого. Тромб в дистальном отделе дуги аорты исчез после 6 месяцев антикоагулянтной терапии без симптомов дистальной эмболии ( c ) Стрелки указывают на тромбоз
Таблица 1 Характеристики корпуса
Тромбоз аорты — редкое заболевание, которое может вызывать дистальную эмболию, но также может быть случайно обнаружено в бессимптомных случаях [1, 2].Хотя часто наблюдается тромб на стенке аорты, связанный с аномальным заболеванием аорты, таким как аневризма аорты и расслоение аорты, тромб в очевидно здоровой аорте встречается очень редко, поскольку кровоток в аорте слишком быстрый для свертывания и образования растущего тромба. [1, 2]. Известно, что триада Вирхова для тромбообразования, включающая гиперкоагуляцию, застой кровотока и повреждение сосудистой стенки, играет важную роль в формировании тромба, однако эта концепция обычно применяется для тромбоза вен и / или мелких артерий [6].С другой стороны, хорошо известна тромбоэмболия, осложненная фибрилляцией предсердий, но аритмия не может быть этиологией местного тромба аорты. Таким образом, подробный механизм этиологии тромбоза аорты до конца не изучен [1, 2].
В настоящем отчете мы описываем случай тромбоза аорты, который наблюдался у практически здорового мужчины в послеоперационном состоянии после операции по поводу рака легкого со сниженной активностью протеина C. Хотя хорошо известно, что наследственная недостаточность протеина С связана с рецидивирующим тромбозом [8, 9], у этого пациента и его семьи не было эпизодов тромбоза.Более того, активность протеина C восстанавливалась в пределах нормы после прекращения антикоагулянтной терапии. Дефицит протеина C часто наблюдается в острой фазе тромбоза и у пациентов, проходящих антикоагулянтную терапию, поскольку протеин C и протеин S представляют собой витамин K-зависимые гликопротеины, которые в таких условиях массово теряются [8, 9]. Таким образом, вклад дефицита протеина C в развитие тромбоза аорты, хотя и возможен, неясен. Настоящий случай контрастирует с несколькими недавними сообщениями о тромбозе аорты, которые были связаны со злокачественными заболеваниями, гематологическими нарушениями и тромбозами, связанными с химиотерапией, особенно в отношении химиотерапии на основе цисплатина [4, 5].Фактически, фон нашего ранее описанного случая тромбоза аорты включал злокачественную лимфому и связанную с ней химиотерапию [6].
Терапевтическая стратегия тромбоза аорты противоречива, однако основная стратегия — консервативная фармакотерапия [1–3]. Нет никаких окончательных данных относительно выбора антитромботической терапии или подходящей продолжительности такого лечения в случае тромбоза аорты. Поэтому мы выбрали терапию варфарином на 6 месяцев в соответствии со стандартной терапией при венозном тромбозе.После прекращения терапии варфарином рецидив тромбоза аорты не подтверждался более 6 месяцев. Другой стратегией является хирургическое лечение, которое особенно полезно для симптоматических случаев дистальной тромбоэмболии, иногда также может выбираться комбинированная терапия [1–3]. Мы выбрали консервативную фармакотерапию, поскольку признаки дистальной тромбоэмболии не были очевидны. Однако в последнее время техника лечения аортальным стент-графтом была значительно улучшена, что позволяет выбрать альтернативный метод лечения тромбоза аорты, особенно в экстренных случаях или в неблагоприятных условиях [10].
Артериальный тромбоз — NHS
Артериальный тромбоз — это сгусток крови в артерии, который может быть очень серьезным, поскольку может препятствовать попаданию крови в важные органы.
Артерии — это кровеносные сосуды, по которым кровь идет от сердца к остальным частям тела и сердечной мышце.
Симптомы и риски артериального тромбоза
Сгусток крови обычно не имеет никаких симптомов, пока он не блокирует приток крови к части тела.
Это может вызвать несколько серьезных проблем, в том числе:
- сердечный приступ, когда приток крови к сердечной мышце внезапно блокируется, вызывая боль в груди, одышку и головокружение
- инсульт, при котором прекращается приток крови к мозгу; основные симптомы — отвисание лица с одной стороны, слабость с одной стороны тела и невнятная речь
- транзиторная ишемическая атака (ТИА) или «мини-инсульт», когда приток крови к мозгу временно блокируется, вызывая кратковременные симптомы инсульта.
- критическая ишемия конечности (осложнение заболевания периферических артерий), когда кровоток в конечности блокируется, вызывая болезненность, обесцвечивание (бледное или синее) и холод
Все эти состояния требуют неотложной медицинской помощи.Немедленно обратитесь за медицинской помощью, позвонив по номеру 999, если вы или кто-либо из ваших опекунов испытываете эти симптомы.
Причины тромбоза артерий
Артериальный тромбоз обычно поражает людей, артерии которых забиты жировыми отложениями. Это называется атеросклерозом.
Эти отложения вызывают со временем затвердевание и сужение артерий и повышают риск образования тромбов.
Следующее может увеличить риск развития атеросклероза:
Иногда артериальный тромбоз может быть вызван состоянием, повышающим вероятность свертывания крови, например фибрилляцией предсердий или антифосфолипидным синдромом.
Снизьте риск артериального тромбоза
Невозможно полностью предотвратить образование тромбов, но вы можете снизить риск, снизив риск атеросклероза.
Главное, что вы можете сделать:
Если у вас высокий риск образования тромба, ваш врач может также порекомендовать принимать такие лекарства, как:
Лечение артериального тромбоза
Если у вас разовьется артериальный тромбоз, возможно, потребуется лечение лекарствами или хирургическое вмешательство.
Лечебные процедуры включают:
- Инъекции лекарства, называемого тромболитиком, которое растворяет некоторые тромбы
- операция по удалению тромба (эмболэктомия)
- операция по расширению пораженной артерии — например, ангиопластика (при которой внутри артерии помещается полая трубка, чтобы удерживать ее открытой)
- операция по отведению крови вокруг заблокированной артерии — например, шунтирование коронарной артерии (где кровеносный сосуд, взятый из другой части тела, используется для обхода закупорки в артерии, которая снабжает сердечную мышцу)
Другие виды сгустков крови
Помимо артериального тромбоза, существует несколько других типов тромбов, в том числе:
- венозная тромбоэмболия (ВТЭ) — тромб в вене
- ТГВ (тромбоз глубоких вен) — сгусток крови в одной из глубоких вен тела, обычно в ноге
- эмболия — кровоток в артерии блокируется инородным телом; это может быть сгусток крови или что-то еще, например, пузырь воздуха
- тромбоэмболия легочной артерии — сгусток крови в легочной артерии, по которому кровь транспортируется от сердца к легким
Последняя проверка страницы: 9 января 2020 г.
Срок следующего рассмотрения: 9 января 2023 г.
Лечение, лечение и исход первичного тромба аорты
Предпосылки .Первичный тромб аорты — редкое явление, о котором нечасто сообщается в литературе. Здесь мы обсуждаем представление и ведение пациента с первичным тромбом грудной стенки. Краткое изложение дела . 46-летняя женщина, в анамнезе которой была табачная зависимость, обратилась с жалобой на субфебрильную лихорадку и внезапное начало сильной боли в правом верхнем квадранте живота с сопутствующими тошнотой и рвотой. Компьютерная томография (КТ) выявила внутрипросветный полиповидный дефект наполнения, возникающий из-за выступа перешейка аорты в проксимальную нисходящую аорту, и результаты, соответствующие инфаркту селезенки и правой почки.Инфекционное, аутоиммунное, гематологическое и онкологическое обследования — все безрезультатно. Пациент начал принимать гепарин, а затем перешел на апиксабан 5 мг два раза в день и 81 мг аспирина в день. Ее также проконсультировали относительно отказа от курения. Контрольная КТ через два месяца показала разрешение тромба. В дальнейшем у пациента не было тромбоэмболических осложнений. Обсуждение . Мы представляем уникальный случай первичного тромба аорты. Насколько нам известно, это первый зарегистрированный случай, успешно управляемый с помощью NOAC.Этот диагноз является диагнозом исключения, и его необходимо пройти тщательное обследование. Наша цель — повысить осведомленность об этом состоянии и об успешном лечении апиксабаном пациентов из группы низкого риска.
1. Предпосылки
Тромбы на стенке аорты встречаются редко и обычно связаны с тяжелым атеросклерозом или наличием аневризмы. Еще более редким явлением является образование первичного тромба аорты без инфекционных, неопластических, травматических, аутоиммунных или гиперкоагуляционных триггеров, ответственных за образование тромба.На сегодняшний день нет единого мнения о лечении этого состояния; однако варианты включают антикоагулянты, тромболитики, хирургическое вмешательство на аорте и тромбоаспирацию. Здесь мы описываем редкий случай первичного тромба аорты с системной эмболизацией нижних конечностей, почек и селезенки. Это один из первых случаев в литературе, описывающих эффективное лечение этого состояния с помощью перорального антикоагулянта прямого действия.
2. Введение
Тромбы в грудном отделе аорты чаще всего связаны с тяжелым атеросклерозом или аневризмой аорты [1, 2].Первичный тромб аорты при отсутствии аневризмы, атеросклерозе средней и тяжелой степени, гиперкоагуляции, злокачественных новообразованиях, инфекциях или аутоиммунных состояниях встречается чрезвычайно редко [2–4]. Лечение первичного тромба аорты в настоящее время недостаточно определено [5, 6]. Здесь мы описываем редкий случай тромба грудного отдела аорты с периферической эмболизацией, проявляющийся в виде боли в животе и боли в нижних конечностях. Это один из первых случаев в литературе, описывающих использование пероральных антикоагулянтов прямого действия при лечении первичных тромбов аорты.Мы стремимся повысить осведомленность об этом состоянии и обобщить патофизиологию, а также существующие варианты лечения, доступные нам.
3. Описание корпуса
3.1. Презентация и первоначальная оценка
46-летняя женщина, в анамнезе которой болела табачная зависимость, обратилась с жалобой на субфебрильную лихорадку и внезапное начало сильной боли в правом верхнем квадранте живота с сопутствующими тошнотой и рвотой. Компьютерная томография (КТ), выполненная в отделении неотложной помощи, выявила внутрипросветный полиповидный дефект наполнения, возникающий из перешейка аорты, выступающего в проксимальный нисходящий отдел аорты, и результаты, соответствующие инфарктам селезенки и правой почки (Рисунки 1 (a) -1 (c) )).Учитывая лихорадку, возникло опасение по поводу сепсиса, поэтому ей начали принимать антибиотики широкого спектра действия. Гепарин также вызывает кардиоэмболические явления неясной этиологии; однако позже его прекратили, чтобы предотвратить геморрагическую трансформацию имеющихся инфарктов. Пациент был госпитализирован для дальнейшего обследования.
3.2. Стационарное обследование
Трансторакальная эхокардиограмма не показала результатов, позволяющих предположить клапанный или сердечный источник эмбола (рис. 2). Было проведено контрастное исследование с взбалтыванием пузырьков физиологического раствора без признаков внутрисердечного шунтирования (рис. 3).Затем была выполнена чреспищеводная эхокардиограмма, которая выявила большую эхогенную подвижную массу, прикрепленную к стенке нисходящей грудной аорты (рисунки 4 (a) и 4 (b)). Двусторонняя артериальная допплерография нижних конечностей выявила тяжелую подколенно-большеберцовую артериальную болезнь левой нижней конечности (рис. 5).
Исследование других органических причин было обширным. Инфекционное обследование было отрицательным и включало тестирование на бактериальную инфекцию, грибковую инфекцию, ВИЧ, антитела к Bartonella henselae, антитела к Coxiella burnetii, антитела к лептоспирам, сифилис, антиген галактоманнана aspergillus и антиген гистоплазмы.Обследование гиперкоагуляции также было ничем не примечательным и включало DRVVT-скрининг на антикоагулянт волчанки, антикардиолипиновые антитела (× 2), скрининг на уровень гомоцистеина, пароксизмальную ночную гемоглобинурию, активность белков C и S, антитромбиновые мутации, а также определение лейденского генотипа фактора V и протромбина. Аутоиммунное обследование также было неустойчивым и включало тестирование на антинуклеарные антитела, антинейтрофильные цитоплазматические антитела, антитела против двухцепочечной ДНК, ревматоидный фактор, циклический цитруллинированный пептид, антитело Сджогрена, антитела к миелопероксидазе, аутоантитела к протеиназе 3, уровни комплемента и антитела Смита. .Учитывая, что нет острой угрозы ишемии конечности или органа, в значительной степени отрицательное обследование и нет простого механизма для удаления тромба аорты, мы решили управлять пациентом с медицинской точки зрения с тщательным амбулаторным наблюдением. Ей начали принимать гепарин в стационаре, который был переведен на апиксабан 5 мг два раза в день и 81 мг аспирина в день. Это было сделано в первую очередь из-за того, что пациент предпочитает избегать частых проверок МНО. Сертифицированный гематолог согласился использовать апиксабан с ежемесячным амбулаторным наблюдением, чтобы обеспечить соблюдение пациентом режима лечения и клиническое улучшение.Пациента также проконсультировали относительно отказа от курения. Катетерная или хирургическая тромбоэмболэктомия могла бы рассматриваться, если бы у пациента развивалась острая ишемия конечностей или угрожающий орган.
3.3. Контрольное наблюдение через месяц
Через месяц пациентка была осмотрена в клинике, и у него не было симптомов боли в груди, спине или животе. Она отрицала значительную боль в покое или при нагрузке и не обнаружила длительно незаживающих ран ни на одной из ее нижних конечностей. Она отметила, что до отдыха могла пройти примерно четверть мили без симптомов.Она сообщила о приверженности ее ежедневному приему аспирина и дважды в день Eliquis. В это время была проведена повторная компьютерная томография брюшной полости и таза, которая показала полное исчезновение дефекта наполнения перешейка аорты и проксимального отдела нисходящей аорты. КТ не обнаружила пустот. Селезенка демонстрировала дольчатый верхний край с потерей объема, а правая почка демонстрировала дольчатый вид правого нижнего полюса, совместимого с рубцами от предыдущего инфаркта (рис. 6).Пациентке было приказано продолжить антитромботический режим и последующее наблюдение через один месяц.
3.4. Двухмесячное наблюдение
В это время у пациента больше не было никаких симптомов боли, отека или хромоты. Она сообщила, что может возобновить свою повседневную деятельность без ограничений. Результаты КТА были обсуждены с пациенткой во время ее двухмесячного наблюдения, и ей было рекомендовано продолжать активность в соответствии с переносимостью. В это время, учитывая разрешение образования после антикоагуляции, было сочтено, что это, скорее всего, тромб аорты.Что касается продолжительности терапии, мы сочли, что это, вероятно, было неспровоцировано, и, учитывая, что это было артериальное, мы решили продолжить антикоагулянтную терапию еще как минимум 12 месяцев до дальнейшей гематологической оценки.
4. Обсуждение
Артериальный тромб — редкое клиническое явление, особенно при отсутствии аневризмы или тяжелого атеросклероза. Частота эмболических событий выше у подвижных тромбов на ножке по сравнению с тромбами, которые являются слоистыми и неподвижными (73% против 12% риска эмболизации, соответственно) [7].Наиболее частое проявление включает последствия, связанные с тромбоэмболическими явлениями, наблюдаемыми у нашего пациента [2]. Эти осложнения серьезны; поэтому раннее выявление и устранение их причин являются обязательными для оказания помощи пациентам.
Тромбы аорты обычно вторичны по отношению к аневризматическому заболеванию, расслоению или тяжелому атеросклерозу [5]. Следует всегда исследовать альтернативные патологии, которые могут предрасполагать к риску артериального тромбоза, чтобы предотвратить будущие тромбы и их последствия.Возможные причины включают травмы, злокачественные новообразования, состояния гиперкоагуляции (лейденская мутация фактора V, полицитемия, дефицит антитромбина III, дефицит протеина C и / или S и т. Д.) И аутоиммунные нарушения [2, 8–10]. Другие факторы риска, включая наличие микроскопического атеросклеротического заболевания (трудно исключить клинически), курение и использование оральных контрацептивов, также следует учитывать у пациентов, если это необходимо.
Дистальная эмболизация тромба вызывает симптомы, характерные для пораженного органа.Тромбоэмболический посев в почечную сосудистую сеть может привести к острому повреждению и недостаточности почек в зависимости от почечного образования дистальнее заблокированной артерии [11]. Осложнения посева в селезенку включают, помимо прочего, боль в левом верхнем квадранте, анемию, лейкоцитоз, псевдокисту селезенки, абсцесс или кровоизлияние [12]. Любой из четырех основных типов острой ишемии брыжейки (острая тромбоэмболическая окклюзия верхней брыжеечной артерии, тромбоз брыжеечной артерии, тромбоз брыжеечной артерии и неокклюзионная мезентериальная ишемия) являются потенциальными осложнениями посева тромба в сосудистую сеть толстой кишки и могут привести к значительной смертности и смертности. [13].Посев эмболов на нижние конечности может привести к острой ишемии конечностей, частота ампутации которой составляет 13-15%, а смертность — 9-12% [14].
Исследования и варианты лечения в соответствии с рекомендациями в настоящее время ограничены, и не было никаких проспективных испытаний, посвященных терапевтическим стратегиям. Варианты лечения включают антикоагулянтную терапию, хирургическое вмешательство на аорте, тромболитическую терапию и тромбоаспирацию [1, 15, 16]. Наиболее распространенный подход к начальному ведению — антикоагулянтная терапия [2, 5].У пациентов с рецидивом эмболизации дистальной артерии или сохранением тромба может быть рассмотрено хирургическое вмешательство на аорте [5, 17, 18]. Было опубликовано несколько исследований, предполагающих, что агрессивное лечение с помощью хирургического вмешательства на аорте может привести к меньшему количеству рецидивов дистальной эмболизации и осложнений, включая ампутацию дистального отдела конечности, особенно в восходящей аорте или дуге аорты [1, 2, 5, 19]. В отношении нашей пациентки, учитывая ее резко отрицательную оценку и отсутствие факторов риска, мы выбрали лечение апиксабаном и аспирином.Кроме того, возникла серьезная озабоченность по поводу дистальной эмболизации, учитывая ее расположение и подвижность. Насколько нам известно, мы сообщаем об одном из первых случаев успешного лечения не зависящим от витамина К пероральным антикоагулянтом.
Уникальность нашего пациента в том, что очень обширное обследование не помогло определить этиологию образования артериального тромба. Наши рабочие диагнозы были обширными и включали эндокардит, парадоксальную эмболию, новообразование сердца и все возможные причины аортита.После исключения источников инфекции посредством обширной оценки и аутоиммунных состояний, которые могли привести к аортиту, мы решили эмпирически лечить пациента апиксабаном и низкими дозами аспирина. К счастью, тромб у нашей пациентки разрешился, и через два месяца наблюдения у нее не было никаких остаточных симптомов.
5. Заключение
Первичный тромб аорты — редкое явление, ранее описанное в литературе. Это диагноз исключения, и инфекционные, злокачественные, гиперкоагуляционные и аутоиммунные причины должны быть исключены.Что касается лечения, некоторые исследования рекомендуют агрессивное лечение для предотвращения риска рецидива тромба и артериальной эмболии, в то время как другие рекомендуют более консервативное, менее инвазивное медицинское лечение; тем не менее, в настоящее время нет консенсуса экспертов или руководящих принципов в отношении прямой терапии или ее продолжительности. Учитывая отсутствие стандартизированных руководств в настоящее время, мы рекомендуем индивидуальный подход к пациенту, который учитывает ожидаемую приверженность к лечению и последующее наблюдение, факторы риска, результаты лабораторных исследований и риск дальнейшей эмболизации.Мы предполагаем, что у пациентов из группы низкого риска использование прямых ингибиторов фактора Ха для пероральной антикоагуляции может быть приемлемой альтернативой кумадину.
Конфликт интересов
Все авторы заявляют об отсутствии конфликта интересов.
Дополнительные материалы
Изображения, полученные с помощью чреспищеводной эхокардиограммы большой массы (тромба), прикрепленной к стенке нисходящей грудной аорты. (Дополнительные материалы)
Тромбоз предположительно нормальной грудной аорты и артериальная эмболия
ВВЕДЕНИЕ
Этиологическая диагностика артериальных эмболий — сложная задача.Тем не менее, источник эмболии может быть идентифицирован у 90-95% пациентов с помощью неинвазивных методов визуализации.1,2 Около 85% эмболий периферических артерий происходят из сердца2. Чреспищеводная эхокардиография (ЧЭЭ) очень полезна в этом состоянии, потому что она позволяет провести тщательное обследование как сердца, так и грудной аорты1. В настоящее время аорта вызывает все больший интерес как потенциальный источник эмболий; было подсчитано, что 5% эмболий происходят из аорты1. Тромбы в основном исходят из брюшной аорты и прикрепляются к аневризмам или артериосклеротическим поражениям, хотя они также были обнаружены в очевидно здоровых сегментах сосудов.Присутствие тромбов в грудной аорте встречается гораздо реже, особенно при отсутствии сопутствующей аневризмы или атеросклеротического заболевания.3,4 Оптимальное лечение для этих пациентов не определено.
Целью настоящего исследования является описание клинических характеристик и эволюции 3 пациентов с эмболией периферических артерий, у которых был зарегистрирован тромбоз грудной аорты.
МЕТОДЫ
В период с сентября 2002 г. по июль 2006 г. тромбы грудной аорты были обнаружены у 3 пациентов, поступивших в нашу больницу по поводу артериальной эмболии.Методы визуализации, использованные у этих пациентов, включали TEE, компьютерную томографию (CT) и / или магнитно-резонансную томографию (MR). У всех пациентов была макроскопически нормальная аорта (без артериосклероза и аневризм).
РЕЗУЛЬТАТЫ
Характеристики исследуемых пациентов описаны ниже и представлены в таблице 1.
Случай 1
54-летний мужчина с гипертонией и дислипидемией обратился в отделение неотложной помощи по поводу внезапной боли в правой части. рука, которая показала отсутствие плечевого пульса.ЧВЭ была проведена для исключения острого заболевания аорты. Образование было обнаружено в нисходящей аорте, непосредственно дистальнее левой подключичной артерии, и было интерпретировано как лоскут от расслоения. Впоследствии артериография дополнительно зафиксировала дефект наполнения восходящей аорты на расстоянии 3 см от плоскости аортального клапана. Пациенту был поставлен диагноз расслоение аорты типа А, и ему была сделана операция. В послеоперационном периоде перенес обширный инсульт и умер. Исследование хирургического образца выявило тромб, прикрепленный к небольшой атеросклеротической бляшке в восходящей аорте.Рассечения не было.
Случай 2
Женщина 47 лет, страдающая гипертонией, обратилась за консультацией по поводу боли в эпигастральной области и левом подреберье. КТ органов брюшной полости и таза выявила массивный инфаркт селезенки (рис. 1). Трансторакальная эхокардиография (ТТЭ) была нормальной, посев крови был отрицательным. TEE показал большую, очень подвижную массу, закрепленную в перешейке аорты (Рисунок 1). Аорта в норме. Было начато внутривенное введение гепарина, но образование аорты сохранялось при последующих исследованиях.Таким образом, было показано хирургическое вмешательство и было удалено 2 новообразования (рис. 2). Гистологическое исследование подтвердило их тромботическую природу. Тест на гиперкоагуляцию был нормальным.
Рис. 1. Визуальные исследования (пациент 2). A: компьютерная томография брюшной полости, аксиальный вид, показывает большую плотную область в селезенке (массивный инфаркт селезенки) (*). B: магнитно-резонансная томография, сагиттальный вид восходящей аорты, дуги аорты и проксимальной части нисходящей грудной аорты; В просвете аорты наблюдаются 2 изображения высокой плотности (стрелки), соответствующие тромбам аорты.C: чреспищеводная эхокардиография, вид по длинной оси нисходящей грудной аорты дистальнее левой подключичной артерии; наблюдается плотное пальцевидное изображение, соответствующее самому дистальному тромбу. D: чреспищеводная эхокардиография, вид в разрезе нисходящей грудной аорты дистальнее начала левой подключичной артерии, на которой также очевиден тромб.
Рисунок 2. Хирургический образец. A: макроскопическое изображение неправильной, неоднородной, пальцевидной массы; точка привязки находится в крайнем правом углу.B: поперечные срезы на нескольких уровнях тромба, на которых видна его неоднородная природа.
Случай 3
Мужчина 52 лет, курильщик с гиперхолестеринемией и гипертонией, обратился в отделение неотложной помощи с болью в правой подвздошной ямке, рвотой и диареей. КТ брюшной полости показала признаки илеита, инфаркта левой почки и массивного инфаркта селезенки. Культуры крови были отрицательными. Результаты TTE и TEE исключили сердечное происхождение. TEE обнаружил образование на ножке, закрепленное в перешейке аорты.Стенка аорты имела нормальный вид. Пациенту была начата антикоагулянтная терапия гепарином и назначена операция. На МРТ-исследовании, проведенном перед операцией, было замечено исчезновение тромба. Тест на тромбофилию был отрицательным.
ОБСУЖДЕНИЕ
Мы представляем 3 пациентов с артериальной эмболией и тромбозом грудной аорты с явно нормальной стенкой. Сообщалось о нескольких сериях пациентов с тромбами грудной аорты (Таблица 2) .1-7 Наши пациенты имеют некоторые важные особенности с описанными случаями, но также имеют некоторые особенности.
Наиболее частой клинической картиной является эмболия конечностей с определенной предрасположенностью к левой руке7. Эта клиническая картина наблюдалась у пациента 1 настоящего исследования, хотя пораженной конечностью была правая рука. У других пациентов была висцеральная эмболия. Это необычная локализация, которая наблюдалась только у 5 пациентов из числа включенных в вышеупомянутую серию. Иногда наблюдаются множественные эмболии (10% пациентов на момент клинической картины в самой большой серии6).В нашей серии у пациента 3 было несколько эмболий, и все они были локализованы во внутренних органах.
Наиболее частым местом расположения тромбов грудной аорты является область перешейка аорты и его часть дистальнее дуги аорты, на стороне, противоположной истоку подключичной артерии.7 У всех наших пациентов были тромбы в этой области и у пациентов. 1 и 2 было обнаружено более одного тромба. У пациента 1 один из тромбов находился в восходящей аорте, что является наиболее необычным местом.
Патофизиология тромбов аорты недостаточно изучена. Они чаще встречаются у пациентов пожилого возраста и у пациентов с несколькими сердечно-сосудистыми факторами риска и тяжелым атеросклерозом аорты, 1,6 хотя они также были описаны в очевидно нормальных аортах и у пациентов с ограниченным артериосклерозом в том месте, где тромб прикрепляется к судно. Средний возраст наших пациентов составлял 51 год, и, за исключением третьего случая, у них был низкий профиль сердечно-сосудистого риска.В некоторых сериях 4 тромбоза аорты сопровождалось хроническим воспалительным заболеванием, которое отсутствовало у наших пациентов. Тест на гиперкоагуляцию был отрицательным у всех 3 пациентов, что часто обнаруживается в других опубликованных сериях.2,6,7
Дифференциальный диагноз тромбов аорты должен быть установлен с другими новообразованиями аорты, такими как опухоли.8 Для постановки точного диагноза необходимы гистологические и иммуногистохимические исследования. исследований, но МРТ является наиболее полезным визуализирующим тестом для дифференциальной диагностики.8 Дифференциальный диагноз с расслоением аорты также важен из-за терапевтических последствий.ЧВЭ может быть лучше, чем другие методы визуализации, применяемые для этой цели, в частности CT.9
Наиболее широко используемый метод диагностики тромбоза аорты в описанных сериях — это ЧЭЭ. Этот тест имеет высокую диагностическую точность и позволяет оценить размер, морфологию и место закрепления тромба, а также характеристики стенки аорты. Хотя нет исследований, сравнивающих различные методы визуализации при диагностике тромбоза аорты, вполне вероятно, что они имеют такую же диагностическую точность, как и при других заболеваниях грудной аорты.
Существует общее мнение, что эти пациенты должны получать антикоагулянтную терапию.1,2,4-7 Хирургическое лечение (тромбэктомия) применяется в отдельных случаях рецидивирующей эмболии или стойкого тромба, несмотря на надлежащую антикоагулянтную терапию. Как и у нашего третьего пациента, полное рассасывание тромба было описано после антикоагулянтной терапии.2,7 Некоторые авторы рекомендуют TEE за 24 часа до операции для подтверждения стойкого тромба.7 Все наши пациенты, за исключением пациента 1 (в у которого изначально предполагалось расслоение) получали антикоагулянтную терапию гепарином натрия.Пациенту 2 тромбэктомия была выполнена после неэффективности антикоагулянтной терапии.
Прогноз этих пациентов в основном определяется последствиями эмболии. В нашей серии 1 пациент умер из-за массивной церебральной эмболии. Клиническое развитие двух других пациентов было благоприятным, и не было никаких доказательств рецидива при последующем наблюдении.
У пациентов с артериальной эмболией рекомендуется исследовать грудную аорту как возможный источник в дополнение к типичным эмболическим очагам, даже у пациентов без классических сердечно-сосудистых факторов риска.
Для переписки: д-р И. Вилакоста.
Instituto Cardiovascular. Больница Университарио Сан-Карлос.
Проф. Мартин Лагос, серийный номер. 28040. Мадрид. España.
E-mail: [email protected]
Поступила 8 марта 2007 г.
Принята к публикации 19 июля 2007 г.
Разрешение тромба аорты при антикоагулянтной терапии | Европейский журнал кардио-торакальной хирургии
Аннотация
У 50-летней женщины, поступившей из-за инфаркта почки, с помощью чреспищеводной эхокардиографии и магнитно-резонансной томографии был обнаружен плавающий высокоподвижный тромб длиной 10 см и диаметром 15–20 мм в нисходящей аорте.Она была плохим кандидатом на операцию из-за обструктивного заболевания легких и ожирения. При внутривенной гепаринизации со значениями теста протромбинового времени от 80 до 100 с с последующей пероральной антикоагуляцией с международными нормализованными значениями отношения от 3,0 до 4,0 тромб разрешился через 10 недель, и в течение следующих 30 месяцев рецидивов не наблюдалось.
1 Введение
Существует неопределенность в отношении лечения тромбов аорты. Варианты лечения включают хирургическое удаление путем аортотомии с эндартерэктомией, тромбэктомии или баллонной эмболэктомии, тромболизиса или антикоагуляции [1–10].Мы представляем случай, когда большой, очень подвижный тромб в нисходящей аорте рассосался во время терапии гепарином и фенпрокумоном.
2 История болезни
50-летняя женщина с ожирением и хронической обструктивной болезнью легких была госпитализирована из-за внезапной боли в пояснице с псевдорадикулярным облучением обеих ног и живота. При поступлении уже исчезли боли в ногах и пальпировался весь дистальный пульс нижних конечностей.
Восемь лет назад она перенесла хирургическую транспозицию подключичной каротической артерии после эмболии левой верхней конечности из-за стеноза левой подключичной артерии.Проведенная в то время ангиография атеросклероза не показала. С тех пор пациентка получала пероральную антикоагулянтную терапию фенпрокумоном. У нее была низкая комплаентность, и при тестировании ее терапевтом значения международного нормализованного отношения (МНО) были только между 1,2 и 1,6. Из-за хронической обструктивной болезни легких она лечилась пероральными глюкокортикоидами в течение последних 3 лет. За исключением курения, у нее не было факторов риска сосудистых заболеваний. Фактические симптомы были объяснены — только клинически — подозрением на эмболию нижних конечностей и инфарктом левой почки, подтвержденным компьютерной томографией.Антикардиолипиновые антитела, антитромбин III, протеин C, протеин S, фибриноген, количество тромбоцитов, оценка на васкулит и серологические тесты на сифилис были нормальными. При чреспищеводной эхокардиографии (ЧЭ) в нисходящей аорте выявляется плавающий высокоподвижный тромб длиной 10 см и диаметром 15–20 мм. На стенке аорты не было атеромы. Ни TEE, ни компьютерная томография, ни магнитно-резонансная томография (МРТ) не выявили кальцификации или утолщения стенки аорты. МРТ сердца выявила единственное место прикрепления тромба в культе левой подключичной артерии (рис.1)
. Из-за ожирения и заболеваний легких риск операции считался слишком высоким. Тромболизис был отклонен из-за размера тромба и опасений, что он может повторно эмболизировать. Таким образом, пациенту была проведена внутривенная гепаринизация в течение 3 недель со значениями теста протромбинового времени (PTT) от 80 до 100 с (исходное значение PTT 23,7 с) с последующей пероральной антикоагуляцией со значениями INR от 3,0 до 4,0. Других клинически очевидных эмболических событий не произошло. Поскольку ЧЭЭ, проведенная через 4 недели, показала регресс тромба до длины 4 см, она была выписана из больницы.МРТ сердца еще через 6 недель показала полное рассасывание тромба аорты. Только в культе подключичной артерии был виден небольшой тромб (рис. 1). После увольнения пациентка улучшила комплаентность, и стало возможным достичь и поддерживать ее значения МНО между 3,0 и 4,0. В течение последующего периода наблюдения продолжительностью 30 месяцев не было никаких событий, указывающих на эмболию, а также не было выявлено повторения тромбообразования при эхокардиографическом и магнитно-резонансном исследованиях.
Рис.1
МРТ-изображение восходящей аорты, дуги аорты и нисходящей аорты, показывающее большой тромб, берущий свое начало в культе левой подключичной артерии и расширяющийся без дальнейшего введения на 10 см в нисходящую аорту (слева). Через 10 недель тромб аорты полностью рассосался (справа). Только внутри культи артерии виден небольшой тромб.
Рис. 1
МРТ-изображение восходящей аорты, дуги аорты и нисходящей аорты, показывающее большой тромб, берущий свое начало в культе левой подключичной артерии и распространяющийся без дальнейшего введения на 10 см в нисходящую аорту (слева).Через 10 недель тромб аорты полностью рассосался (справа). Только внутри культи артерии виден небольшой тромб.
3 Обсуждение
Тромбы аорты, происходящие из атеромы, являются источником эмболии, особенно у пациентов старше 70 лет, поэтому рекомендуется антикоагулянтная терапия [5,6]. В редких случаях тромбы могут происходить из стенки аорты без атеромы, как в представленном случае [7–10]. Здесь культя левой подключичной артерии, скорее всего, служила очагом для образования тромба.Хроническое лечение глюкокортикоидами могло способствовать гиперкоагуляции, как и в других зарегистрированных случаях [8,10]. Кроме того, недостаточная антикоагуляция могла способствовать развитию тромба.
Идеальное лечение подвижных тромбов аорты без атероматоза не определено. Хирургическое удаление путем аортотомии с эндартерэктомией, тромбэктомия или баллонная эмболэктомия и тромболизис являются предлагаемыми методами лечения [1–3,7–10]. Хирургическая и тромболитическая терапия сопряжены с рисками.Антикоагулянтная терапия может, по крайней мере, избежать хирургического риска, но предполагает риск повторной, потенциально опасной для жизни эмболизации [8,9]. Разрешение небольших подвижных тромбов аорты размером 0,5–3 см при антикоагулянтной терапии было документально подтверждено с помощью TEE и компьютерной томографии [2,8,9]. Еще в двух случаях с большими тромбами аорты размером 10 см и 15 см антикоагулянтная терапия была проведена без эмболических событий [4]. Было ли в нашем случае разрешение тромба связано с антикоагулянтной терапией, безмолвной повторной эмболизацией или спонтанным фибринолизом, нельзя было окончательно решить, но мы предполагаем, что антикоагулянтная терапия позволила эндогенной фибринолитической системе растворить тромб.Внутривенная гепаринизация у нашего пациента потребовала длительной госпитализации на 4 недели. Только после того периода, когда TEE показал значительное уменьшение размера тромба, переход на пероральные антикоагулянты и увольнение пациента сочли оправданным.
Поскольку большие подвижные тромбы аорты без атероматоза аорты рассасываются во время сильной и хорошо контролируемой антикоагулянтной терапии, этот случай может дать толчок к использованию антикоагулянтной терапии в аналогичных ситуациях. Однако антикоагулянтную терапию у пациента с подвижными тромбами аорты следует проводить только в больницах, оборудованных сосудистой хирургией.Следует проявлять особую осторожность, чтобы поддерживать уровень антикоагуляции в целевом диапазоне, внимательно наблюдать за пациентом на предмет возможных эмболических событий и госпитализировать пациента до тех пор, пока не будет задокументировано значительное уменьшение размера тромба.
Список литературы
[1],,,,.
Рецидивирующая системная эмболизация, вызванная тромбами аорты
,
Ann Thorac Surg
,
1994
, vol.
57
(стр.
466
—
468
) [2],,,,
для Filiale Echocardiographie de la Sociéte Francaise de Cardiologie
.
Подвижные тромбозы дуги аорты без остатков аорты. Чреспищеводная эхокардиографическая находка, связанная с необъяснимой артериальной эмболией
,
Circulation
,
1997
, vol.
96
(стр.
288
—
294
) [3],,,,,.
Успешный тромболизис тромба дуги аорты у пациента после эмболии брыжейки
,
N Engl J Med
,
1992
, vol.
327
(стр.
500
—
501
) [4],,,.
Массивный тромб аорты, обнаруженный при чреспищеводной эхокардиографии как причина периферической эмболии у молодых пациентов
,
Am Heart J
,
1996
, vol.
132
(стр.
882
—
883
) [5],,,,,.
Распространенность изъязвленных бляшек на дуге аорты у пациентов с инсультом
,
N Engl J Med
,
1992
, vol.
326
(стр.
221
—
225
) [6],,,.
Подвижная атерома аорты и системные эмболы: эффективность антикоагуляции и влияние морфологии бляшек на повторный инсульт
,
J Am Coll Cardiol
,
1998
, vol.
31
(стр.
124
—
128
) [7],,,,.
Инфаркт селезенки, вызванный большим тромбом грудной аорты
,
Ann Vasc Surg
,
1998
, vol.
12
(стр.
609
—
611
) [8],,,,.
Первичный тромб на стенке аорты: проявление и лечение
,
Ann Vasc Surg
,
1999
, vol.
13
(стр.
52
—
59
) [9],,,,,,.
Trombo en aorta torÁcica como causa de Embolismo Periférico Diagnosticado por ecocardiografía transesofÁgica
,
Rev Esp Cardiol
,
1997
, vol.
50
(стр.
62
—
64
) [10],,,,.
Рецидивирующая эмболия, вызванная плавающим тромбом в грудной аорте
,
Ann Vasc Surg
,
1998
, vol.
12
(стр.
609
—
611
)
© 2001 Издано Elsevier Science B.V.
Elsevier Science B.V.
Тромбоз брюшной аорты как начальное проявление инфекции COVID-19: отчет о болезни
Тромбоз брюшной аорты как начальное проявление инфекции COVID-19: отчет о клиническом случае
Уильям Закари Вебстер, Отделение внутренней медицины, Медицинский факультет Университета Южной Каролины, Колумбия, Южная Каролина, США
Амрит Срау, Карла Круз Морел, Отделение легочной и реанимации, Университет Южной Каролины Школа медицины-Prisma Health, Колумбия, SC 29203, США
Вклад авторов : Вебстер WZ написал оригинальную рукопись с исчерпывающим обзором литературы по теме; Круз Морел К. редактировал первоначальный отчет и участвовал в обзоре литературы; Sraow A также участвовал в редактировании отчета.
Заявление об информированном согласии : Все авторы получили информированное согласие на публикацию данной рукописи. Кроме того, от пациента было получено информированное согласие на публикацию этой рукописи при том понимании, что вся идентифицирующая информация была опущена.
Заявление о конфликте интересов : Нет никаких конфликтов интересов со стороны других авторов этой рукописи, включая доктора. Уильям Вебстер, Амрит Срау и Карла Круз-Морель.
Контрольный список CARE (2016) выписка : Авторы прочитали Контрольный список CARE (2016), и рукопись была подготовлена и отредактирована в соответствии с Контрольным списком CARE (2016).
Открытый доступ : Эта статья представляет собой статью с открытым доступом, которая была выбрана штатным редактором и полностью прорецензирована внешними рецензентами. Он распространяется в соответствии с лицензией Creative Commons Attribution NonCommercial (CC BY-NC 4.0), которая разрешает другим распространять, ремикшировать, адаптировать, использовать эту работу в некоммерческих целях и лицензировать свои производные работы на других условиях, при условии, что оригинал работа правильно процитирована и используется в некоммерческих целях.См .: http://creativecommons.org/licenses/by-nc/4.0/
Автор, ответственный за переписку : Уильям Закари Вебстер, доктор медицины, доктор внутренних болезней, Медицинская школа Университета Южной Каролины, 5 Richland Medical Park Доктор, Колумбия, SC 29203, США. [email protected]
Получено: 7 июля 2020 г.
Началась экспертная оценка : 9 июля 2020 г.
Первое решение : 21 июля 2020 г.
Доработано: 2 августа 2020 г.
Принято: 1 сентября 2020 г.
Статья в прессе : 1 сентября 2020 г.
Опубликована онлайн: 18 сентября 2020 г.
Тромб аорты у пациентов с тяжелой формой COVID-19: обзор трех случаев
Коронавирус 2 тяжелого острого респираторного синдрома (SARS-CoV-2) — это незнакомый респираторный вирус, который появился в Ухане, Китай в декабре 2019 года и быстро распространился по всему миру [1 ].
Клинический спектр коронавирусной болезни 2019 (COVID-19) охватывает от бессимптомной инфекции до легкого или тяжелого поражения дыхательных путей с потенциальной дыхательной недостаточностью и даже летальным исходом [2]. Недавно сообщалось о вторичном поражении многих других органов с тромбоэмболическими осложнениями, включая центральную и периферическую нервную систему [3], а также сердечную [4, 5] или сосудистую системы [6,7,8,9].
Тромботические артериальные события (APE или церебральный инсульт) ранее были связаны с другими вирусными инфекциями, особенно среди пациентов с ВИЧ, но об острых аортальных событиях не сообщалось [10].
COVID-19 может предрасполагать как к венозным, так и к артериальным тромботическим явлениям, особенно у тяжелых пациентов. Недавно сообщалось о повышении частоты острой тромбоэмболии легких (ОЛЭ) у пациентов с COVID-19 [11]. Эти сосудистые события могут быть связаны с несколькими факторами, включая гипервоспалительные процессы, гипоксию, диффузную внутрисосудистую коагуляцию [12] и иммобилизацию. Используются разные протоколы приема антикоагулянтов не только между учреждениями, но и между странами, поскольку для пациентов с COVID-19 не было достигнуто реального консенсуса по антикоагулянтам [13].
В нашей больнице мы разработали специальный протокол скрининга, чтобы исключить APE у пациентов с COVID-19 со значительным увеличением D-димера, даже при улучшении клинических и аналитических параметров. Мы представляем трех пациентов с подтвержденным COVID-19 с флотирующими тромбами аорты. Двое из них прошли скрининг APE, а другой — расширенное исследование острого ишемического инсульта. Основные аналитические и клинические профили описаны в Таблице 1.
Таблица 1 Основные характеристики пациентов с тромбом аорты
Случай 1
В наше отделение неотложной помощи поступил 78-летний мужчина с дислипидемией с 4-дневной лихорадкой и отсутствием болезни. другие симптомы.Клиническое обследование было нормальным, за исключением температуры 37,2 ºC. Лабораторные тесты показали лимфопению, повышение фибриногена, ЛДГ и D-димера. Рентген грудной клетки (CXR) показал многодолевые интерстициальные помутнения в правом легком. При поступлении мы начали лечение пиперациллин-тазобактамом, азитромицином, гидроксихлорохином, метилпреднизолоном и эноксапарином в дозе 60 мг в сутки. Спустя 48 часов у пациента продолжалась стойкая лихорадка и повышение потребности в кислороде. Рентгенография показала быстрое прогрессирование помутнения и было обнаружено значительное увеличение количества острых реагентов, таких как ферритин и ИЛ-6, поэтому однократная доза тоцилизумаба в дозе 600 мг была введена в соответствии с протоколами больницы (критерии тяжести).На 5-й день после госпитализации (9 дней от появления симптомов) у пациента в следующие 72 часа наблюдалось явное улучшение со снижением показателей С-реактивного белка (СРБ) и ферритина. Несмотря на первоначальное снижение, D-димер значительно увеличился до 3570 мкг / л. Была проведена КТ-ангиография, показавшая множественные сегментарные тромбоэмболии легочной артерии, многодолевую пневмонию и три плавающих тромба в дуге аорты и нисходящей аорте (рис. 1). Низкомолекулярный гепарин (LWMH) начинали с дозы антикоагулянта.Мы не диагностировали коагулопатии или кровотечений. Состояние пациента ухудшилось до тяжелой дыхательной недостаточности, и он умер на 18-й день от поступления в больницу.
Рис. 1
КТ-ангиография легочных артерий. Аксиальные и сагиттальные MinIP-реконструкции. Случайное обнаружение трех плавающих тромбов: один сразу после бифуркации левой подключичной артерии (12,2 мм) и два в нисходящей аорте сразу после артериальной связки (8,7 мм и 10,2 мм)
Случай два
76-летний мужчина Мужчина с гипертонией, дислипидемией и сахарным диабетом поступил в отделение неотложной помощи с лихорадкой, астенией и болями в пояснице в течение последних 2 недель.По прибытии у него была высокая температура, 120 ударов в минуту, базальная сатурация кислорода 87% и 22 вдоха в минуту. Лабораторные тесты показали лимфопению и повышение фибриногена, D-димера, ЛДГ, креатинина и СРБ. Рентгенография выявила однодолевые помутнения в нижней левой доле. При поступлении мы начали лечение азитромицином, гидроксихлорохином, цефтриаксоном, метилпреднизолоном и эноксапарином по 40 мг в сутки. Девяносто шесть часов спустя у пациента продолжалась лихорадка, одышка и тахипноэ, которым требовался высокий поток кислорода для увеличения сатурации кислорода до 92%.Значения CRP, D-димера, ферритина и IL-6 прогрессивно увеличивались. Рентгенография показала ухудшение с появлением многодолевых и двусторонних помутнений, поэтому мы увеличили дозу НМГ до 60 мг в день и вводили разовую дозу тоцилизумаба без клинического улучшения. На 11-й день от поступления (26-й день от появления симптомов) у пациента произошел резкий эпизод потери силы в правом теле с падением на землю. Обследование показало глобальную афазию, окуло-головное отклонение влево и правую фациобрахиокруральную гемиплегию.Неулучшенная КТ головного мозга (УЛКТ) не показала признаков острого кровоизлияния, масс-эффекта или сдвига средней линии. Мы начали лечение ацетилсалициловой кислотой внутривенно и снизили дозу низкомолекулярного гепарина до 40 мг в день, но неврологического улучшения не наблюдалось. Через 48 часов была проведена новая УЛКТ, которая показала признаки, совместимые с полным ишемическим инсультом левой средней мозговой артерии с признаком гиперплотности сосудов в левой внутричерепной внутренней сонной артерии (рис. 2а). Мы выполнили ангио-КТ церебральных артерий и сонных артерий в качестве дополнительного исследования ишемического инсульта.Он показал полную окклюзию левой внутренней сонной артерии, кстати, два внутрипросветных тромба по 8 мм каждый были идентифицированы в восходящей аорте. Мы не рассматривали фибринолиз или эмболэктомию в течение нескольких часов развития симптомов. Мы увеличили дозу НМГ до доз антикоагулянтов, и пациент был выписан в центр временного пребывания для завершения реабилитации. Мы намеревались продолжить лечение антикоагулянтами в течение как минимум 3 месяцев после события и принять решение на специализированной консультации после переоценки заднего отдела с новой клинической, аналитической и визуализационной информацией, если только не появится серьезное нежелательное явление или новые научные доказательства, которые позволят установить другое лечение.
Рис. 2
КТ головного мозга без улучшения, показывающая гиперплотную внутричерепную левую внутреннюю сонную артерию в ее каменистом сегменте. b и c КТ-ангиография церебральных артерий (протокол от дуги к вершине). Осевая (B) и корональная (C) реконструкция MIP, показывающая полный дефект наполнения после петрозумного сегмента левой сонной артерии и отсутствие левой средней мозговой артерии. d КТ-ангиография церебральных артерий (протокол от дуги к вершине).Реконструкция MIP, показывающая левую общую сонную артерию (красная стрелка) и внутреннюю сонную артерию (красная стрелка) с выступающим луковицей сонной артерии и кальцинированными атеросклеротическими бляшками без признаков сужения просвета или утолщения стенки. e КТ-ангиография сонных и церебральных артерий MIP-реконструкция. Случайное обнаружение двух плавающих тромбов размером около 10 мм в восходящей аорте, непосредственно перед началом правой брахиоцефальной артерии
Случай 3
64-летний мужчина, бывший курильщик, с гипертонией и тяжелым синдромом обструктивного апноэ во сне синдром, обратился в отделение неотложной помощи из-за сухого кашля, одышки и высокой температуры в течение последних 4 дней.Клиническое обследование было нормальным, за исключением температуры 37,3 ºC. Лабораторные тесты показали повышение фибриногена, D-димера и CRP. Рентгенография показала однодолевые интерстициальные помутнения в правой верхней доле. Мы начали лечение гидроксихлорохином и азитромицином, через 48 часов пациентку выписали. Во время амбулаторного наблюдения у пациента была рентгенография с обширным помутнением легких, лимфопенией и значительным повышением уровня СРБ, поэтому он был повторно госпитализирован с добавлением к предыдущему лечению метилпреднизолона и однократной дозы 600 мг тоцилизумаба (4-й день с начала лечения). первое посещение отделения неотложной помощи).Все лабораторные маркеры воспаления улучшились, но D-димер резко увеличился до 4640 мкг / л, поэтому через 7 дней после поступления (11-й день от появления симптомов) была проведена КТ для поиска APE, показавшая плавающий тромб посередине. сегмент нисходящей грудной аорты (рис. 3). Мы начали принимать НМГ в дозе антикоагулянта.

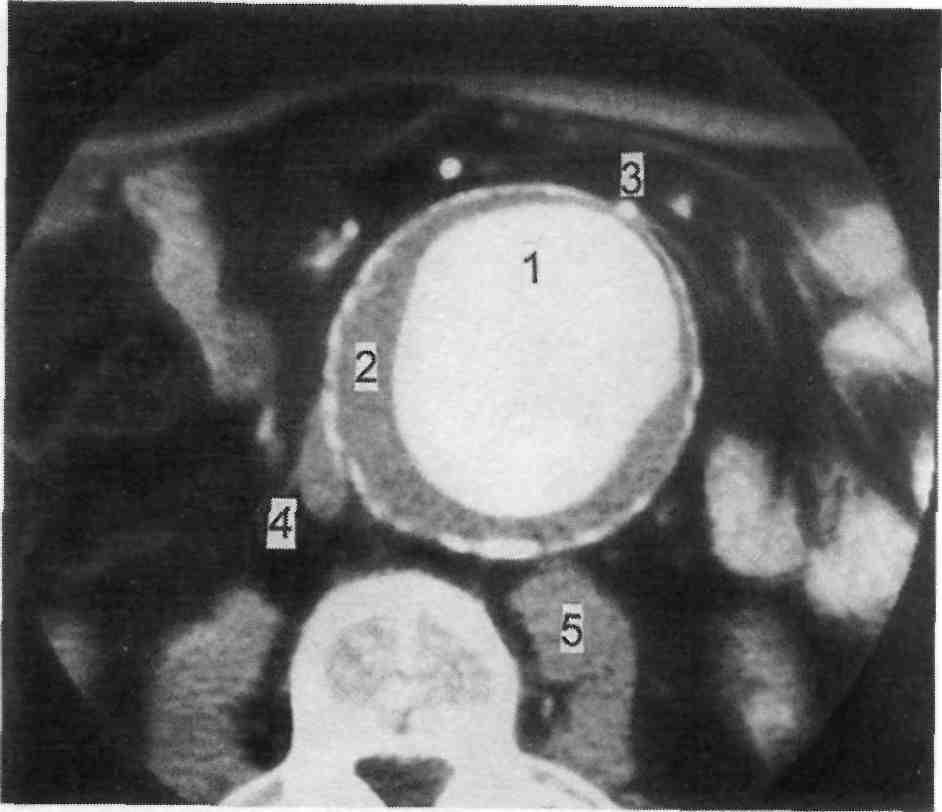 Проявляется появлением отрыжки, рвоты, неустойчивого стула или запоров, отсутствием аппетита и похуданием;
Проявляется появлением отрыжки, рвоты, неустойчивого стула или запоров, отсутствием аппетита и похуданием;