Что такое менингококковая инфекция у детей — Пинская центральная поликлиника
Менингококковая инфекция — острое инфекционное заболевание, возбудителем которого являются бактерии — менингококкки. Она является одной из самых тяжелых инфекций детского возраста.
Менингококковой инфекцией болеет только человек. Источником инфекции является больной или носитель менингококка. Наиболее опасны носители, так как они могут заражать окружающих, а сами при этом не болеют.
Передается инфекция воздушно-капельным путем (при чихании, разговоре, кашле, поцелуе).Заболевание регистрируется в течении года, но наибольшая активизация заболеваемости — в зимне — весенний период.
Инкубационный период заболевания длится в среднем 5-7 дней. Чаще болеют дети до трехлетнего возраста.
Микроб неустойчив во внешней среде: погибает при нагревании до 50 градусов в течение 5 минут, при кипячении — за 30 секунд, в непроветриваемом помещении — через 20 минут, прямой солнечный свет убивает менингококков за 2-8 часов, под действием ультрафиолетовых лучей -мгновенно.
Симптомы менингококковой инфекции у детей:
Менингококковая инфекция может проявляться различными симптомами:
1) резко повышается температура до высоких цифр;
2) появляется рвота, не связанная с приемом пищи или лекарств, иногда болезнь начинается именно с рвоты;
3) появляется сильная, порой нестерпимая головная боль, боль в мышцах и суставах;
4) появляется сыпь (к концу первых суток) в виде звездочек неправильной формы и различной величины, розового, красного или пурпурного цвета, имеющая тенденцию к слиянию на наружных поверхностях бедер, голеней, плеч, ягодицах, несколько реже – на туловище.
Менингококкцемия (менингококковая бактериемия, менингококковый сепсис) — клиническая форма менингококковой инфекции, при которой, кроме кожи, могут поражаться различные органы (надпочечники, почки, легкие, селезенка, глаза, суставы).
Менингококкцемия имеет острое начало, иногда внезапное, температура тела быстро повышается до высоких отметок. Ребенка знобит, наблюдается сильная головная боль, рвота. Поскольку груднички не могут рассказать о головной боли, этот симптом у них проявляется пронзительным криком и плачем.
В более тяжелых случаях возможна потеря сознания, у детей раннего возраста — судороги. Симптомы нарастают на протяжении 1-2 суток. В конце первого или в начале второго дня заболевания проявляется геморрагическая сыпь на всем теле, но наибольшее ее количество сосредоточено на ягодицах и ногах. На местах обширных поражений некрозы в последующем отторгаются и образуются дефекты и рубцы. Может быть поражение суставов в виде синовитов или артритов. Обычно находят изменения мелких суставов пальцев рук, ног, реже крупных суставов. От детей могут поступать жалобы на боль в суставах, иногда визуально заметно их припухание, гиперемия кожи над суставами.
Менингококкцемия бывает таких форм: легкая, среднетяжелая и тяжелая. Самой тяжелой формой признана молниеносная. В таких случаях болезнь начинается резко, температура тела повышается, появляется обильная геморрагическая сыпь, элементы которой быстро сливаются, становясь похожими на трупные пятна. Кожа ребенка бледная и холодная на ощупь, черты лица заостряются. Артериальное давление сильно снижается, наблюдается тахикардия, нитевидный пульс, выраженная одышка. Менингиальные симптомы непостоянны. Может появиться острое набухание и отек мозга, что проявляется такими симптомами как резкая головная боль, судороги, потери сознания, психомоторное возбуждение, повторная рвота. Если не проведена своевременная терапия, летальный исход наступает спустя 12-24 часа после начала заболевания.
Менингококковый менингит – еще одна форма заболевания, которая начинается остро, с сильно повышенной температуры и сильного озноба.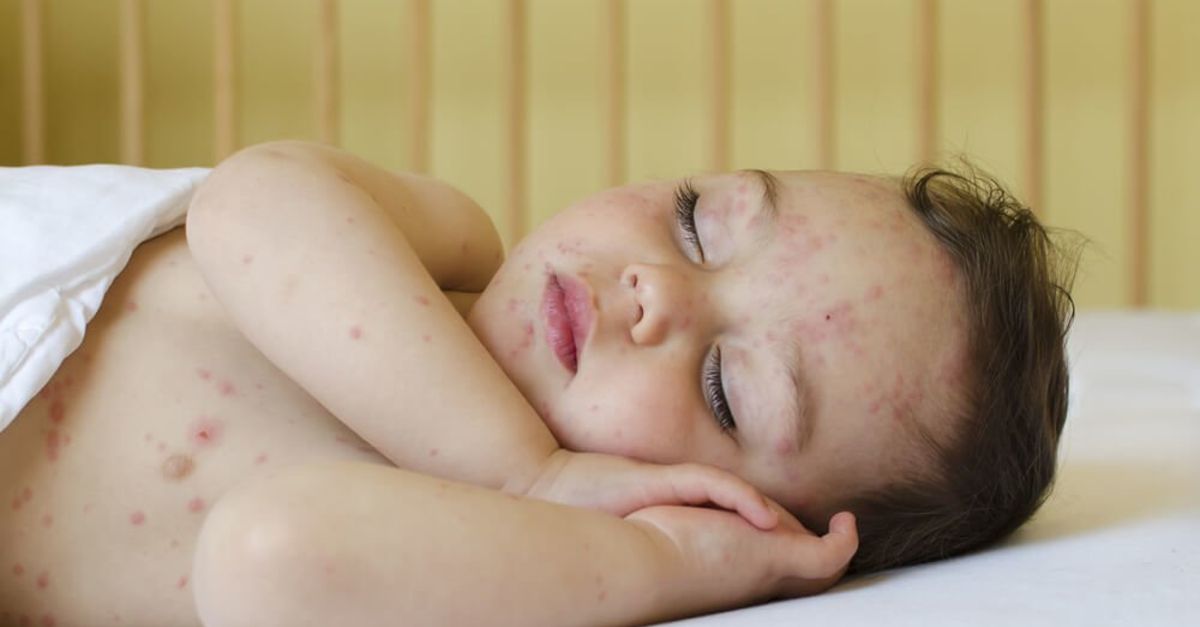 Проявляются такие симптомы как головная боль, не имеющая четкого расположения, беспокойство, расстройства сна, вскрикивания. Возбуждение у некоторых детей может сменяться заторможенностью, безразличием к окружающему.Могут возникать боли по позвоночнику. От прикосновений болевые ощущения усиливаются.
Проявляются такие симптомы как головная боль, не имеющая четкого расположения, беспокойство, расстройства сна, вскрикивания. Возбуждение у некоторых детей может сменяться заторможенностью, безразличием к окружающему.Могут возникать боли по позвоночнику. От прикосновений болевые ощущения усиливаются.
Гиперестезия – один из характерных и наиболее проявляющихся симптомов гнойного менингита. Важным симптомом является рвота, которая не связана с приемами пищи, и начинающаяся с первого дня заболевания.
Менингококковый менингоэнцефалит – форма менингококковой инфекции, которая случается в основном у детей раннего возраста. С первых суток заболевания наблюдается симптоматика: нарушение сознания, двигательное возбуждение, судороги. Есть вероятность монопарезов, бульбарных параличей, мозжечковой атаксии, глазодвигательных расстройств. Болезнь имеет тяжелое течение, нередко заканчивается летальным исходом.
Профилактика менингококковой инфекции у детей:
В случае появления острых симптомов: повышения температуры тела до 40 градусов, сильной головной боли необходимо срочно вызывать «скорую помощь» и быстро доставить больного в больницу. Несвоевременное обращение к врачу и поздно начатое лечение может стоить больному жизни. Чем раньше оказана медицинская помощь, тем быстрее наступит и эффективнее результаты выздоровления.
Следует как можно раньше изолировать больного, выделить ему индивидуальную посуду и средства личной гигиены, обеспечит больному абсолютный покой и хороший уход. Если случаи заболевания выявлены в коллективе, туда в течение 10 дней не принимают новых людей и не переводят детей из группы в группу или из класса в класс. Для профилактики важны общие гигиенические мероприятия: разукрупнение детских коллективов, обработка предметов обихода хлорсодержащими растворами, частое проветривание помещений, влажная уборка, кипячение игрушек, посуды, ультрафиолетовое облучение помещений и т. д.
д.
Помните! Что при малейших подобных симптомах заболевания надо быстро вызвать врача.
Соблюдение всех мер профилактики менингококковой инфекции позволит сохранить здоровье вам и вашим детям.
Филиал «Детская поликлиника»
УЗ «Пинская детская больница»
Зав. 2-ым педиатрическим отделением
Луниченко Нина Семеновна
Защита ребенка от менингококковой инфекции
Менингококковый менингит – острое инфекционное заболевание. Инфекция передается воздушно-капельным путем и на начальной стадии часто имеет симптомы схожие с обычной острой респираторной инфекцией.
Риск заболеть менингитом выше у подростков и маленьких детей, поскольку их организм не способен эффективно вырабатывать иммунитет против инфекции. Согласно данным федерального сайта Национальной ассоциации специалистов по контролю инфекций, в нашей стране заболеваемость составляет в среднем 5 человек на 100 тысяч населения в год, что является довольно высоким показателем по сравнению с развитыми странами.
Чем опасен менингококк?
Менингококковая инфекция, так же как пневмококковая и гемофильная, очень коварна. Этот микроорганизм может бессимптомно находиться в носоглотке, не доставлять носителю особых неудобств и никак не проявляться.
Особенность данного заболевания состоит в стремительном развитии симптомов и в течение нескольких часов может привести к серьезным последствиям.
Характер протекания заболевания.
Инфекция протекает в нескольких формах, одна из которых назофарингит, когда заболевание проявляется в виде насморка. К сожалению, чаще заболевание носит тяжелый характер и проявляется в виде менингита (воспаление оболочек головного и спинного мозга).
Новая вакцина защитит детей.
Эпидемиологи России и специалисты по иммунопрофилактике давно ждали данную вакцину, поскольку, во-первых, она отличается очень высоким качеством, а во-вторых, с ее помощью появилась возможность защитить от менингококка маленьких детей. По данным Роспотребнадзора, максимальная заболеваемость наблюдается именно у детей в возрасте 1-5 лет.
По данным Роспотребнадзора, максимальная заболеваемость наблюдается именно у детей в возрасте 1-5 лет.
В прошлом году в нашей стране была зарегистрирована первая в мире четырехвалентная конъюгированная менингококковая вакцина «Менактра» (Sanofi, США), которая формирует у детей высокий и длительный иммунитет против четырех разновидностей менингококков.
Применение препарата возможно у детей уже с 9 месяцев (в тот период, когда чаще всего происходит заражение, и заболевание носит наиболее сложный характер).
Применение вакцины «Менактра» вызывает выработку специфических антител, что защищает ребенка от развития опасных для жизни генерализованных форм инфекций (менингококковый менингит, менингококковый сепсис).
Высокая эффективность и безопасность вакцины «Менактра» доказана в ходе международных научных исследований и подтверждена опытом клинического применения в течение 10 лет.
Вакцинация против менингококковой инфекции давно используется в странах Европы и США и включена в их Национальные календари.
Предлагаем Вам защитить Вашего ребенка и заранее сделать прививку от менингококковой инфекции.
Получить более подробную информацию, а также записаться на прием к педиатру и вакцинацию Вы можете по телефонам 37-00-45, 37-00-29.
С НАМИ ВАШ РЕБЕНОК БУДЕТ ЗДОРОВ!
Менингококковая инфекция у детей :: АЦМД
Формат написания статей для сайта клиники подразумевает описания клинического случая из практики врача. Попробую… Но случай не с благоприятной концовкой.
Начиная работать участковым педиатром, в очередной раз пришла на первичный патронаж к новорожденному ребенку. Собирая анамнез жизни малыша, мама мне рассказала, что настоящие беременность и роды – вторые, а первый ребенок умер в возрасте 2-х месяцев от перенесенного менингита. Естественно, я спросила, где новорожденный мог заразиться такой тяжелой инфекцией? Со слов матери, после рождения малыша, в гости с поздравлениями приходило большое количество родственников, как потом выяснилось, кто то из них и оказался носителем менингококка.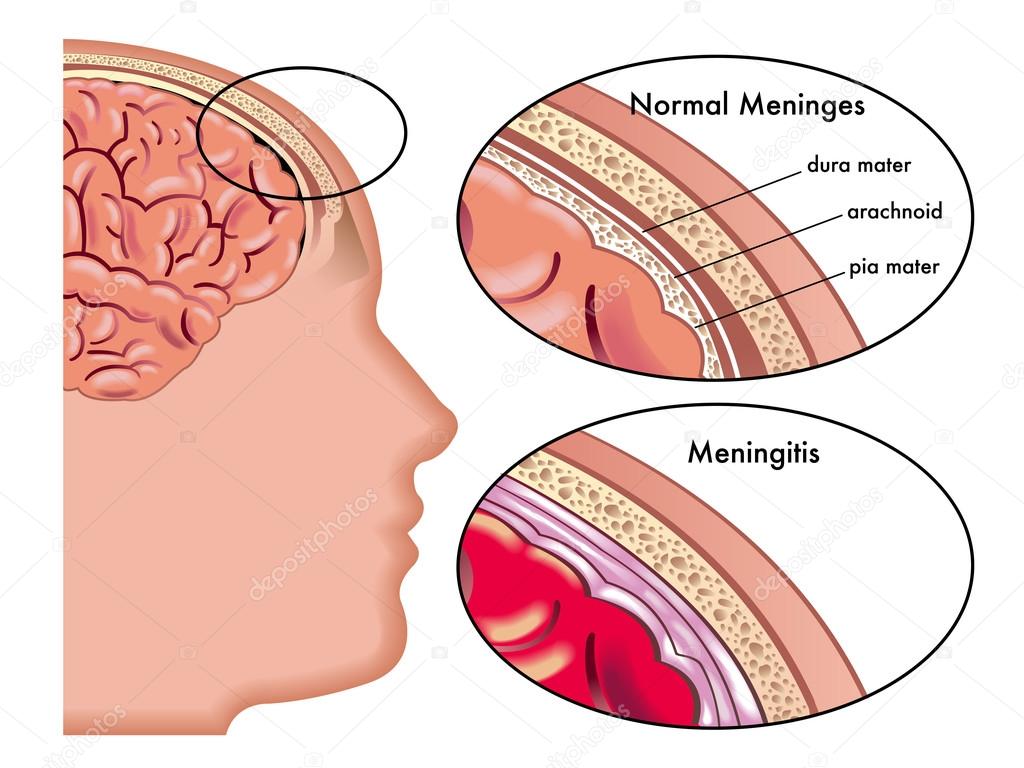 Печальная история, в которой вроде никто и не виноват.
Печальная история, в которой вроде никто и не виноват.
Основные признаки менингококковой инфекции у детей
Дорогие наши родители, в данной статье обратим Ваше внимание на основные признаки менингококковой инфекции у детей, так как в последние пару лет участились случаи ее возникновения.
Менингококковая инфекция – заболевание с острым началом, разнообразными симптомами, тяжестью протекания (от назофарингита до менингита и менингоэнцефалита с вовлечением других органов и систем). Вызывает данный недуг бактерия менингококк, которая имеет в себе эндотоксин, что, в свою очередь, является сильным сосудистым ядом при воздействии которого повышается проницаемость сосудов и происходит спазм капилляров. Болеют этим заболеванием только люди и передается оно воздушно-капельным путем. Заразиться можно, контактируя тесно с больными или бактерионосителями. Индекс контагиозности (заразности, восприимчивости) не высокий, до 10-15%. Обратите внимание, наибольший процент заболеваемости приходится на детей до 5 лет. Смертность зависит от тяжести протекания, возраста больного, формы болезни, наличия осложнений, своевременности диагностики и начатого лечения.
Рассмотрим, как же проявляется данная страшная инфекция?
Клиническая картина зависит от формы, в которой она протекает:
Локальная – назофарингит (с инкубационным периодом (от момента заражения до первых симптомов болезни) 2-4-6 дней): острое начало с температурой до 38 градусов. Данная форма никак не отличается от течения любого другого ОРВИ, что и может затруднять диагностику. Она наиболее благоприятна, выздоровление уже на 5-7 день болезни.
Генерализованные – более тяжёлые, и могут приводить к летальному исходу (менингококкцемия, менингит или их сочетания).
Редкие формы – эндокардит, пневмония, иридоциклит, что так же вызваны менингококком.
Менингококкцемия – форма, при которой в патологический процесс вовлекается главным образом кожа, но могут и другие органы. Характеризируется острым началом, высокой температурой, сильной головной болью (у детей-грудничков пронзительный крик), рвотой, ознобом, потерей сознания, судорогами. На второй день болезни появляется характерная геморрагическая сыпь на коже, больше ноги и ягодицы, но на других участках тела тоже встречается. Нередко вовлекаются суставы (полиартриты), функция которых после болезни полностью восстанавливается. Наиболее опасна молниеносная форма менингококкцемии.
Характеризируется острым началом, высокой температурой, сильной головной болью (у детей-грудничков пронзительный крик), рвотой, ознобом, потерей сознания, судорогами. На второй день болезни появляется характерная геморрагическая сыпь на коже, больше ноги и ягодицы, но на других участках тела тоже встречается. Нередко вовлекаются суставы (полиартриты), функция которых после болезни полностью восстанавливается. Наиболее опасна молниеносная форма менингококкцемии.
Менингококковый менингит – начало острое, с повышение температуры тела до 39-40 градусов, с резкой сильной головной болью, беспокойством, раздражительностью. Любое прикосновение к ребенку носит резкое усиление болевых ощущений. Одними из проностически важных симптомов являются спонтанная рвота и клонико-тонические судороги, появление со 2-3 дня болезни менингококковых симптомов.
Менингококковый менингоэнцефалит – чаще у детей раннего возраста. По симптомах больше проявляется неврологическая симптоматика: возбуждение, судороги, параличи.
Течение болезни длительное, с длительным восстановительным периодом (от 4 недель до 3-х месяцев), с волнообразным течением. Окончательная диагностика менингококковой инфекции проводится с помощью люмбальной пункции. Принимаются во внимание результаты анализа спинно-мозговой жидкости, а также показатели крови.
К общим профилактическим мерам относятся гигиена рук, носа, тела, игрушек, посуды, белья, частое проветривание помещений, раннее и своевременное выявление и изоляция больных и носителей. В учебных учреждениях на 10 дней накладывается карантин, проводят посев из носа на менингококк всех контактных 2 раза в течении 3-7 дней, обязательно подается экстренное извещение в СЭС. Само лечение проводится только в стационаре инфекционного специализированного отделения.
Дорогие родители! Если у Вашего малыша Вы обнаружили хотя бы один из вышеперечисленных симптомов, не занимайтесь самолечением, а в кратчайшие сроки обращайтесь за квалифицированной помощью!
Здоровья и благополучия Вам и Вашим деткам!
Профилактика менингококковой инфекции
Менингококковая инфекция, в быту известна как менингит — инфекционное (заразное) заболевание.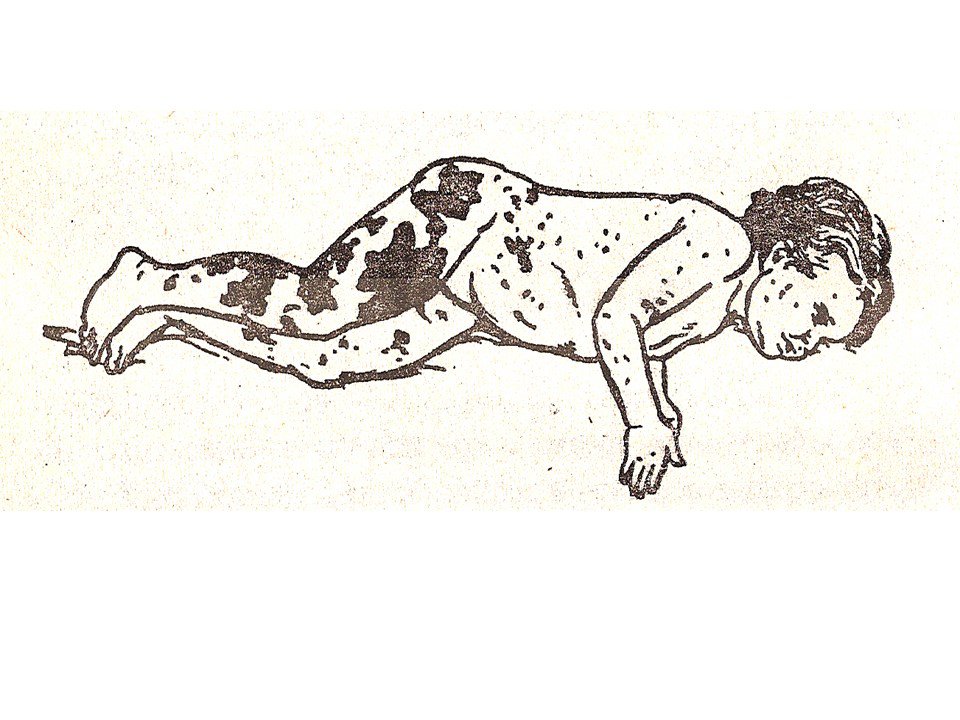 Проявляется в виде острого
Проявляется в виде острого
заболевания менингита (воспаление мозговых оболочек) или менингококкового сепсиса (заражение крови), а иногда назофарингита
(воспаление слизистой носа и глотки). Первые признаки болезни ничем не отличаются от обычной простуды: насморк, кашель. Затем
появляются три главных симптома: высокая температура тела до 38-40 градусов, внезапные приступы рвоты и сильная головная боль.
У грудных детей появляется резкий плач. Появляется и характерная для таких больных поза: они лежат, запрокинув голову назад,
ноги поджаты к животу. При попытке наклонить голову к груди отмечается сопротивление, напряжение мышц шеи и затылка. Если
иммунная система ослаблена, микроб проникает в кровь и на коже конечностей, ягодицах, боковых поверхностях туловища появляется
сыпь не правильной звёздчатой формы пурпурно-красного цвета, не исчезающая при надавливании. Развивается тяжёлая форма, зачастую
молниеносно протекающая- менингококкового сепсиса с поражением почек и надпочечников, возникновением отёка головного мозга,
инфекционно-токсического шока и смертельным исходом.
Кто является источником инфекции?
Источником инфекции может быть больной человек и носители менингококка. Наиболее опасны носители (внешне здоровые люди,
имеющие микробы в организме), поскольку на одного заболевшего приходится 1800 носителей. Опасность носителей менингококковой
инфекции объясняется тем, что они сами не болеют, но могут заражать окружающих. Менингококковая инфекция встречается повсеместно,
во всех странах мира. Чаще болеют дети в возрасте 1-2 лет, у которых недостаточный иммунитет, среди взрослых — молодые люди
до 30 лет. Заболеваемость повышается в зимне-весенний период, чему способствует скученность людей в общественных местах, транспорте,
Заболеваемость повышается в зимне-весенний период, чему способствует скученность людей в общественных местах, транспорте,
недостаточное нахождение на свежем воздухе.
Как передаётся заболевание?
Путь передачи инфекции — воздушно-капельный (при кашле, чихании, разговоре). Возбудитель – менингококк крайне неустойчив
во внешней среде, быстро погибает при охлаждении и высыхании, при кипячении – за 30 секунд. Микроб проникает через слизистые
оболочки верхних дыхательных путей в организм здорового человека при длительном и тесном общении с источником инфекции (рядом
спят, принимают пищу, учатся, воспитываются). От момента заражения до начала заболевания проходит от одного до десяти дней.
Больной заразен для окружающих с первых дней болезни. Восприимчивость к заболеванию высокая. Менингиты сопровождаются воспалением
оболочек головного и спинного мозга, могут вызываться вирусами (серозные) и бактериями (гнойные). Конечно же, более опасными
являются бактериальные менингиты, смертность от которых достигает 40%, даже при своевременно начатом лечении.
Каковы могут быть последствия?
После перенесенного заболевания может развиться осложнение – глухота, у маленьких детей – глухонемота, в редких
случаях – параличи. Не занимайтесь самолечением, немедленно вызывайте врача на дом или скорую медицинскую помощь, чем
раньше будет оказана квалифицированная медицинская помощь, тем быстрее и эффективнее будут результаты выздоровления.
Меры неспецифической профилактики.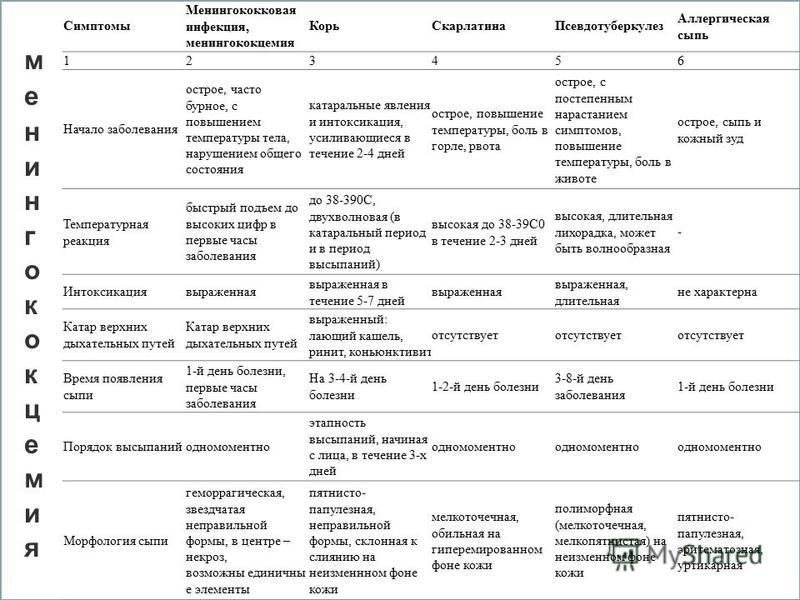
·избегайте переохлаждений,
·ограничьте поездки с ребенком в общественном транспорте,
·не посещайте с ребенком зрелищные мероприятия, магазины, парикмахерские и друге места массового нахождения людей,
·больше гуляйте с ребенком на открытом воздухе,
·праздничные мероприятия, связанные с рождением ребёнка, лучше проводите вне квартиры, где он находится,
·принятие водных процедур, соблюдение режима дня – повышают сопротивляемость организма.
·в случае простудных проявлений у взрослых, необходимо пользоваться марлевыми (одноразовыми масками).
·в помещении, где находился больной (очаге) необходимо проведение ежедневной, влажной уборки, частое проветривание;
·в детских учреждениях необходимо обеззараживание воздуха бактерицидными лампами,
·недопустимо скученность детей в спальных помещениях.
·все лица, общавшиеся с больным в семье, коллективе в течение 10 дней должны подвергаться медицинскому наблюдению,
обследованию на носительство менингококков.
Существует ли вакцина против менингококковой инфекции?
Согласно национальному календарю профилактических прививок вакцинация против менингококковой инфекции проводится
по эпидемическим показаниям.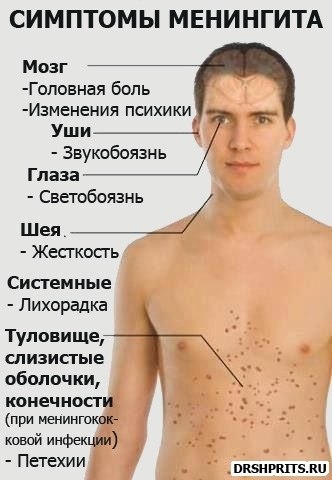
Вакцинируются дети, подростки, взрослые в очагах менингококковой инфекции, вызванной менингококками серогрупп А или С.
Вакцинация проводится в эндемичных регионах, а также в случае эпидемии, вызванной менингококками серогрупп А или С.
Самолечение недопустимо!
Менингококковая инфекция
Дата публикации: .
Менингококковая инфекция — острое инфекционное заболевание, вызываемое менингококком, протекающее с разнообразными клиническими проявлениями: от бессимптомного носительства и назофарингита до генерализованных форм (гнойного менингита, менингоэнцефалита и менингококцемии с поражением различных органов и систем).
Бактерия N. meningitidis передается от человека человеку через капли выделений из дыхательных путей или горла носителя. Курение, а также тесный и продолжительный контакт, такой как поцелуй, чихание или кашель в сторону другого человека или проживание в непосредственной близости с инфицированным человеком-носителем, способствует распространению болезни. Массовые мероприятия также облегчают передачу бактерии.
В группу риска входят дети до 5 лет. Особенность инфекции в том, что по причине наличия у менингококка защитной капсулы маленькие дети (1-5 лет) неспособны эффективно вырабатывать иммунитет против природной инфекции.
Заболеваемость менингококковой инфекцией регистрируется на протяжении всего года, но большинство случаев приходятся на период сезонного подъема — с февраля по апрель.
Обычно инкубационный период длится 4 дня, но может варьировать от 2 до 10 дней.
При попадании менингококка к здоровому человеку возможно три варианта развития событий:
Первый: менингококк живет на слизистой (максимально до 6 недель) и потом исчезает. Человек был и остается здоровым, только распространяет бактерию дальше. Это называется носительство. Так реагирует большинство детей и практически все здоровые взрослые.
Человек был и остается здоровым, только распространяет бактерию дальше. Это называется носительство. Так реагирует большинство детей и практически все здоровые взрослые.
Второй: после заражения в месте внедрения бактерии развивается местная воспалительная реакция – менингококковый назофарингит (воспаление носа и глотки). Клиника — как у обычной простуды. Температура, кашель, насморк, красное горло. Заподозрить в этом случае менингококковую инфекцию можно только тогда, когда в районе о подъеме заболеваемости данной инфекцией всем известно. В остальных случаях это будет расценено, как обычное ОРВИ и, как обычное ОРВИ, благополучно и без лечения пройдет самостоятельно за 5-7 дней.
Третий: в 1% случаев, когда организм ослаблен, менингококк прорывает защиту слизистых и попадет в кровь, разносится с её током по всему организму. Так развиваются генерализованные формы менингококковой инфекции: менингит, менингококцемия, менингоэнцефалит, смешанные формы. Это чрезвычайная ситуация. Бактерию легко уничтожить, она хорошо поддается антибиотикам, но вот справиться с последствиями ее пребывания в организме бывает сложно. До сих пор, даже при своевременно начатом лечении, до 10% детей с тяжелыми формами менингококковой инфекции погибают.
Менингит начинается, как правило, остро, с резкого озноба и повышения температуры тела до 38-40°С.
Заболевание также характеризуется:
- выраженной общей слабостью
- болями в глазных яблоках, особенно при движении
- головной болью в лобно-височных, реже — затылочных областях. Головная боль быстро нарастает, становится разлитой, мучительной, давящего или распирающего характера.
- исчезновением аппетита
- тошнотой, рвотой, не приносящая облегчения.
- повышенной чувствительностью ко всем видам внешних раздражителей (например, светобоязнью),
- вялостью, заторможенностью, нарушением сна.

- при тяжелых формах менингита характерны нарушения сознания.
Через 12-14 ч от начала болезни появляются объективные симптомы раздражения мозговых оболочек (невозможно наклонить голову вперед; в положении лежа при приближении подбородка к груди непроизвольно сгибаются ноги).
У новорожденных детей и детей до 2х лет жизни обычно менингит не сопровождается типичными симптомами. В этой возрастной группе менингит чаще проявляется следующими симптомами:
- высокая лихорадка
- постоянный монотонный плач
- чрезмерная сонливость, или напротив — чрезмерная раздражительность
- пассивность или медлительность
- отказ от еды
- выбухание родничков на голове
- скованность в теле ребенка, особенно в области шеи.
Одна из тяжелейших форм менингококковой инфекции –менингококцемия. Ключевым симптомом этой формы является геморрагическая сыпь: в виде мелких синячков; начинается с маленьких розовых пятен или синих пятен звездчатой формы и быстро увеличивается в количестве и диаметре, становясь багрового цвета. Чаще всего сыпь возникает на ягодицах, ногах, руках.
Это крайне опасное заболевание, угрожающее жизни человека. Если вдруг когда-нибудь на фоне высокой температуры Вы обнаружите такую сыпь, особенно если новые элементы сыпи будут появляться один за одним за считанные минуты — СРОЧНО вызывайте скорую помощь.
Профилактика
1.Вакцинация (вакцина от менингококковой инфекции не входит в Национальный календарь профилактических прививок и может вводиться по желанию родителей и при проживании/выезде в регионы, где отмечаются вспышки менингококковой инфекции)
2.Химиопрофилактика (незамедлительное профилактическое назначение антибиотиков лицам, находившимся в тесном контакте с больным, снижает риск передачи инфекции).
3.Неспецифическая профилактика (тщательно мойте руки; не используйте общие напитки, продукты питания, соломки, столовые приборы, бальзамы для губ или зубные щетки; поддерживайте вашу иммунную систему с помощью разумного труда, достаточного отдыха, регулярных физических тренировок и соблюдая здоровую диету с большим количеством свежих фруктов, овощей и цельных злаков; больше гуляйте на открытом воздухе, избегайте поездок в общественном транспорте, длительно не находитесь в помещениях, где имеется большое скопление людей).
Подготовила: врач-инфекционист Некрасова Е.С.
Профилактика менингококковой инфекциии | ГАУЗ ТО «Городская поликлиника №3»
Менингококковая инфекция, в быту известна как менингит — инфекционное (заразное) заболевание. Проявляется в виде острого заболевания менингита (воспаление мозговых оболочек) или менингококкового сепсиса (заражение крови), а иногда назофарингита (воспаление слизистой носа и глотки).
Для заболевания характерно:
- легкость распространения заболевания, в основном воздушно-капельным путем — при кашле, чихании, разговоре, при достаточно тесном и продолжительном общении;
- первичная симптоматика менингококковой инфекции нередко схожа с проявлениями других острых респираторных инфекций (ОРИ), что порой затрудняет диагностику заболевания;
- опасностью заболевания в том, что оно может развиваться в считанные часы и даже минуты, так называемые «молниеносные» формы заболевания, и спасти больного удается не всегда.
Инкубационный период продолжается от 2 до 10 суток.
Заболевание начинается внезапно. Например, ребенок ложится спать совершенно здоровым, а ночью он неожиданно становится неспокойным, ощущает мышечную слабость; если с ребенком возможен словесный контакт, то он будет жаловаться на сильную головную боль, которая не снимается обычными обезболивающими средствами. В течение часа обычно поднимается температура до 39-40°С, через 5-6 часов возникает рвота, не приносящая облегчения больному. Но самый грозный симптом, на который обязательно надо обратить внимание, — появление сыпи
Меры неспецифической профилактики.
- избегайте переохлаждений,
- ограничьте поездки с ребенком в общественном транспорте,
- не посещайте с ребенком зрелищные мероприятия, магазины, парикмахерские и друге места массового нахождения людей,
- больше гуляйте с ребенком на открытом воздухе,
- принятие водных процедур, соблюдение режима дня – повышают сопротивляемость организма.

- в случае простудных проявлений у взрослых, необходимо пользоваться одноразовыми масками.
- в помещении, где находился больной (очаге) необходимо проведение ежедневной, влажной уборки, частое проветривание;
- в детских учреждениях необходимо обеззараживание воздуха бактерицидными лампами,
- недопустимо скученность детей в спальных помещениях.
- все лица, общавшиеся с больным в семье, коллективе в течение 10 дней должны подвергаться медицинскому наблюдению, обследованию на носительство менингококков.
Специфическая профилактика:
Согласно национальному календарю профилактических прививок вакцинация против менингококковой инфекции проводится по эпидемическим показаниям.
Вакцинация осуществляется полисахаридными вакцинами: Менинго А+С (Санофи Авентис), Манцевакс (ГлаксоСмитКляйн)
Вакцинируются дети с 9 месячного возраста, подростки, взрослые (до 55 лет) в очагах менингококковой инфекции, вызванной менингококками серогрупп А или С.
Схема вакцинации: от 9 до 23 месяцев – 2 введения с интервалом не менее 3 месяцев, с 2 до 55 лет – 1 введение.
Менингококковая инфекция у детей | Официальный сайт Санаторно-курортный комплекс ДиЛУЧ
Главная → Менингококковая инфекция у детей
Менингококковая инфекция – это одно из самых опасных заболеваний, которому могут оказаться подвержены дети. Ее симптом очень разнообразны, могут быть как местными, так и распространенными по всему организму малыша. Каждый из них по-своему неприятен. Но самый опасный вариант протекания болезни – это полное отсутствие тревожных признаков.
Процесс развития патологии очень стремителен. Тяжелейшее поражение организма происходит за считанные дни, и во многих случаях может привести к летальному исходу. Согласно статистике, более 85% заболевших – это дети, большая часть из которых не достигла даже двухлетнего возраста.
В чем причины возникновения менингококковой инфекции у детей? Как проявляет себя эта страшная болезнь? Каковы ее основные симптомы? И как проводится диагностика инфекции у детей?
Причины инфекции у детей
Возбудителем менингококка является штамм, переносчиком которого становится либо болеющий человек, либо простой носитель. Что интересно, по статистике, на одного заболевшего человека приходится около трех тысяч носителей. Эти люди полностью здоровы, но легко могут передать штамм будущему больному.
Как правило, инфекцию переносят взрослые, а вот подвергаются болезни дети. Заражение происходит воздушно-капельным путем при тесном контакте, от 50 см и ближе. Менингококк крайне неустойчив во внешней среде, он погибает в течении получаса.
Как и у многих других острых вирусных заболеваний, пик этой инфекции приходится на межсезонье. Наибольшее число случаев заболевания фиксируется с февраля п апрель. Это могут быть как локальные случаи болезни, так и вспышки эпидемии.
Микроб подобного вида очень быстро мутирует и приспосабливается, поэтому вспышки болезни регистрируются с точной периодичность раз в 8-10 лет.
Как проявляется менингококковая инфекция у детей
Менингококк обычно отличает достаточно коротким инкубационным периодом, который, в среднем, составляет лишь от 3 до 10 дней. Инфекция может принимать одну из трех форм проявления:
- Локальная. Человек является переносчиком инфекции без ярко выраженных симптомов либо страдает назофарингитом менингококкового характера.
- Общая. Симптомами заболевания становятся такие опаснейшие явления, как менингит (воспаление оболочек головного мозга), сепсис, менингоэнцефалит.
- Смешанная форма. Сочетание нескольких форм проявления инфекции.
Симптомы менингококковой инфекции у детей
В зависимости от формы протекания заболевания, менингококк может проявлять себя совершенно по-разному.
|
Проявление менингококковой инфекции
|
Симптомы
|
|
Назофарингит
|
Повышение температуры тела; слабость, апатия и недомогание; заложенность носа; потеря аппетита и нарушения сна; болевые ощущения при глотании.
|
|
Менингит
|
Резкое ухудшение самочувствия и скачок температуры тела до 40 градусов; позывы рвоты, которые невозможно остановить; дрожь и светобоязнь; повышенная чувствительность всего тела; невозможность коснуться подбородком грудной клетки и наклонить голову; периодические судороги и сильная головная боль; учащенное дыхание и сердцебиение; расстройства сознания и обострение реакции на раздражители.
|
|
Менингококцемия
|
Непрекращающаяся тревожность и позывы к рвоте; резкий скачок температуры тела до критических показателей; сыпь на коже, напоминающая звездочки синего цвета; боль при движениях в суставах; падение артериального давления; носовые и кишечные кровотечения; отсутствие мочеиспускания.
|
Своевременная точная диагностика и правильно подобранное лечение могут гарантировать достаточно позитивный прогноз заболевания. Но основная проблема заключается в том, что даже обращение к врачу спустя сутки от появления первых признаков болезни, считается поздним обращением. При нем могут возникнуть крайне негативные последствия и осложнения патологии вплоть до летального исхода. Наиболее распространенное осложнение – это нарушения работы слухового нерва и заражения бактериального характера, которые плохо заживают.
Диагностика менингококковой инфекции у детей
Диагностика менингококковой инфекции состоит из нескольких этапов. Первый из них – первичный осмотр и беседа с лечащим врачом. Обычно, в ходе этого осмотра врач выясняет основную информацию:
- Осматривает ребенка на предмет сыпи, измеряет температуру тела и давление
- Составляет анамнез заболевания
- Выясняет, имелся ли у заболевшего контакт с носителем инфекции
- Проверяет наличие специфических симптомов
Уже после этого назначаются аппаратные и лабораторные исследования:
- Общий анализ крови и мазок на определение менингококка
- Анализ спинномозговой жидкости
- Проба на чувствительность к антибиотикам
- Бактериальный посев и мазок из носовой полости
При необходимости назначаются дополнительные консультации специалиста невролога или инфекциониста.
Менингококковая инфекция в детском возрасте:
эпидемиология, клиника и профилактика
J Prev Med Hyg. 2015 Авг; 56 (3): E121 – E124.
Детское отделение интенсивной терапии, Отделение патофизиологии и трансплантации, Миланский университет, Фонд IRCCS Ca ‘Granda, Ospedale Maggiore Policlinico, Милан, Италия
Автор, отвечающий за переписку. Отделение патофизиологии и трансплантации, Миланский университет, Fondazione IRCCS Ca ‘Granda Ospedale Maggiore Policlinico, via Commenda 9, 20122 Милан, Италия — Электронная почта: [email protected]
Поступила в редакцию 16 июля 2015 г .; Принято 28 августа 2015 г.
© Авторские права Pacini Editore SPA, Пиза, Италия Это статья в открытом доступе, распространяемая в соответствии с условиями некоммерческой лицензии Creative Commons Attribution без производных, которая разрешает некоммерческое использование, распространение и воспроизведение в любых цифровых средний, при условии, что оригинальная работа правильно процитирована и никоим образом не изменена. Подробнее см. Http://creativecommons.org/licenses/by-nc-nd/3.0 / Эта статья цитируется другими статьями в PMC.
Резюме
Инвазивная менингококковая инфекция (IMD) представляет собой проблему общественного здравоохранения и является основной причиной заболеваемости и смертности во всем мире. IMD может протекать как эндемическое заболевание со спорадическими случаями или как эпидемии со вспышками. Штаммы менингита Neisseria делятся на 13 серогрупп, но только пять (A, B, C, W-135 и Y) ответственны за большинство IMD во всем мире. Все возрастные группы подвержены риску IMD, но особенно уязвимы младенцы и подростки.Наиболее частыми клиническими проявлениями IMD являются менингит и сепсис, хотя в некоторых случаях присутствуют обе клинические картины. Клиническая картина может различаться в зависимости от возраста; У маленьких детей клинические проявления могут быть более коварными, и диагностика может быть более сложной по сравнению с детьми старшего возраста или подростками.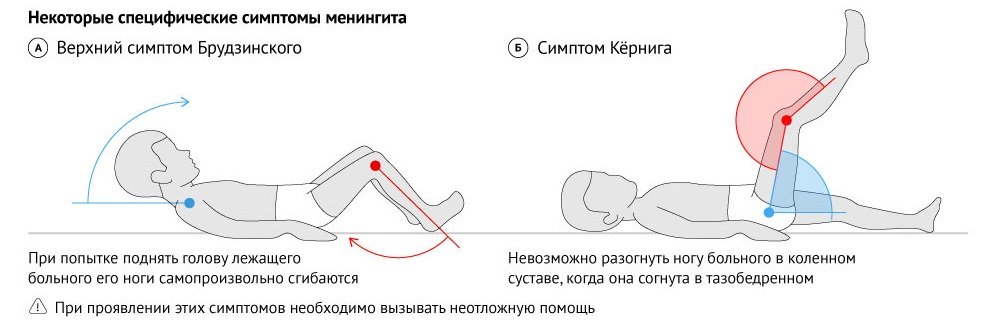 Смерть наступает в 6-10% случаев, а от последствий — в 4,3-11,2% случаев. Раннее выявление детей с менингококковой инфекцией важно для начала системной антибактериальной терапии, хотя вакцинация остается лучшей стратегией борьбы с менингококковой инфекцией.Недавно во всем мире были внедрены различные менингококковые вакцины, что привело к снижению общего бремени болезни. Целью следующих нескольких лет должно быть увеличение охвата вакцинацией против менингококковых заболеваний, продолжение мониторинга IMD и разработка уникальной вакцины, способной охватить все основные штаммы менингококка.
Смерть наступает в 6-10% случаев, а от последствий — в 4,3-11,2% случаев. Раннее выявление детей с менингококковой инфекцией важно для начала системной антибактериальной терапии, хотя вакцинация остается лучшей стратегией борьбы с менингококковой инфекцией.Недавно во всем мире были внедрены различные менингококковые вакцины, что привело к снижению общего бремени болезни. Целью следующих нескольких лет должно быть увеличение охвата вакцинацией против менингококковых заболеваний, продолжение мониторинга IMD и разработка уникальной вакцины, способной охватить все основные штаммы менингококка.
Ключевые слова: Дети, Инвазивная менингококковая инфекция, Менингококковая инфекция, Детский возраст, Neisseria meningitidis
Введение
Neisseria meningitidis — анаэробный грамотрицательный диплококк, вызывающий инвазивное менингококковое заболевание (IMDD). проблема общественного здравоохранения и ведущая причина заболеваемости и смертности во всем мире [1, 2].В глобальном масштабе заболеваемость IMD составляет 500 000 случаев ежегодно, хотя заболеваемость колеблется от <1 на 100 000 в год в Северной Америке и Европе до 10–1 000 на 100 000 в год в «поясе менингита» в Африке к югу от Сахары [3, 4]. Смерть наступает в 6-10% случаев, а от последствий - в 4,3-11,2% случаев [5].
Менингококковое носительство, которое представляет собой первый этап передачи болезни, меняется в зависимости от возраста и условий. Известно, что N. meningitidis колонизирует носоглотку у 5-10% бессимптомных взрослых людей.Недавнее исследование показало, что распространенность носительства увеличивается в детстве с 4,5% у младенцев до пика в 23,7% у 19-летних, а затем снижается до 7,8% у 50-летних [6]. В этом обзоре обобщены новые данные о менингококковой инфекции у детей и возможностях ее профилактики.
Эпидемиология
Штаммы N. meningitidis делятся на 13 серогрупп на основе иммунохимии их капсульных полисахаридов; однако только пять серогрупп (A, B, C, W-135, Y и X) ответственны за большинство случаев IMD в
мир [4]. IMD может протекать как эндемическое заболевание со спорадическими случаями или как эпидемии со вспышками. Все возрастные группы подвержены риску IMD, но младенцы и подростки особенно уязвимы из-за исчезновения материнских антител в раннем возрасте и высокой скорости колонизации носоглотки [2, 3]. Некоторые учреждения, такие как школы, общежития университетов и казармы, подвержены высокому риску передачи N. meningitidis . Более того, низкий социально-экономический статус, принадлежность к меньшинствам, иммунодефицит и аспления предрасполагают людей к менингококковой инфекции [2, 3].
IMD может протекать как эндемическое заболевание со спорадическими случаями или как эпидемии со вспышками. Все возрастные группы подвержены риску IMD, но младенцы и подростки особенно уязвимы из-за исчезновения материнских антител в раннем возрасте и высокой скорости колонизации носоглотки [2, 3]. Некоторые учреждения, такие как школы, общежития университетов и казармы, подвержены высокому риску передачи N. meningitidis . Более того, низкий социально-экономический статус, принадлежность к меньшинствам, иммунодефицит и аспления предрасполагают людей к менингококковой инфекции [2, 3].
Серогруппы, вызывающие IMD, различаются географически, в основном, из-за различий в иммунитете населения и факторов окружающей среды. Менингококк серогруппы A (MenA) встречается в Африке и некоторых районах Азии, тогда как серогруппы B (MenB), C (MenC) и Y (MenY) преобладают на других континентах, включая Европу и Северную Америку [2, 4]. В 13 странах, входящих в африканский «пояс менингита», MenA был ответственен за большинство случаев в 2007–2009 годах, в то время как менингококк серогруппы W135 (MenW135) преобладал в 2010 и 2011 годах [4].Хотя MenC редко встречается в Африке, в 2013 и 2014 годах были зарегистрированы две вспышки, вызванные новым штаммом MenC, в Нигерии и Кебби, соответственно [7]. Более того, в 2006-2010 гг. Вспышки MenX были описаны в Нигере, Того, Кении, Уганде и Буркина-Фасо [8]. В Европе MenB является основной причиной IMD, за ним следуют MenC и MenY [4]. В странах с установленными программами вакцинации MenC заболеваемость MenC значительно снизилась [2, 4]. По сравнению с США, IMD, вызванный MenY, в Европе встречается редко.Однако в последние годы сообщалось о росте этой серогруппы, особенно в странах Северной Европы [9].
Клинические проявления и последствия
Наиболее частыми клиническими проявлениями менингококковой инфекции являются менингит и сепсис, хотя в некоторых случаях присутствуют обе клинические картины [3, 10–12]. Однако признаки и симптомы в начале заболевания, такие как насморк и боль в горле, могут напоминать симптомы распространенных респираторных вирусных инфекций [11].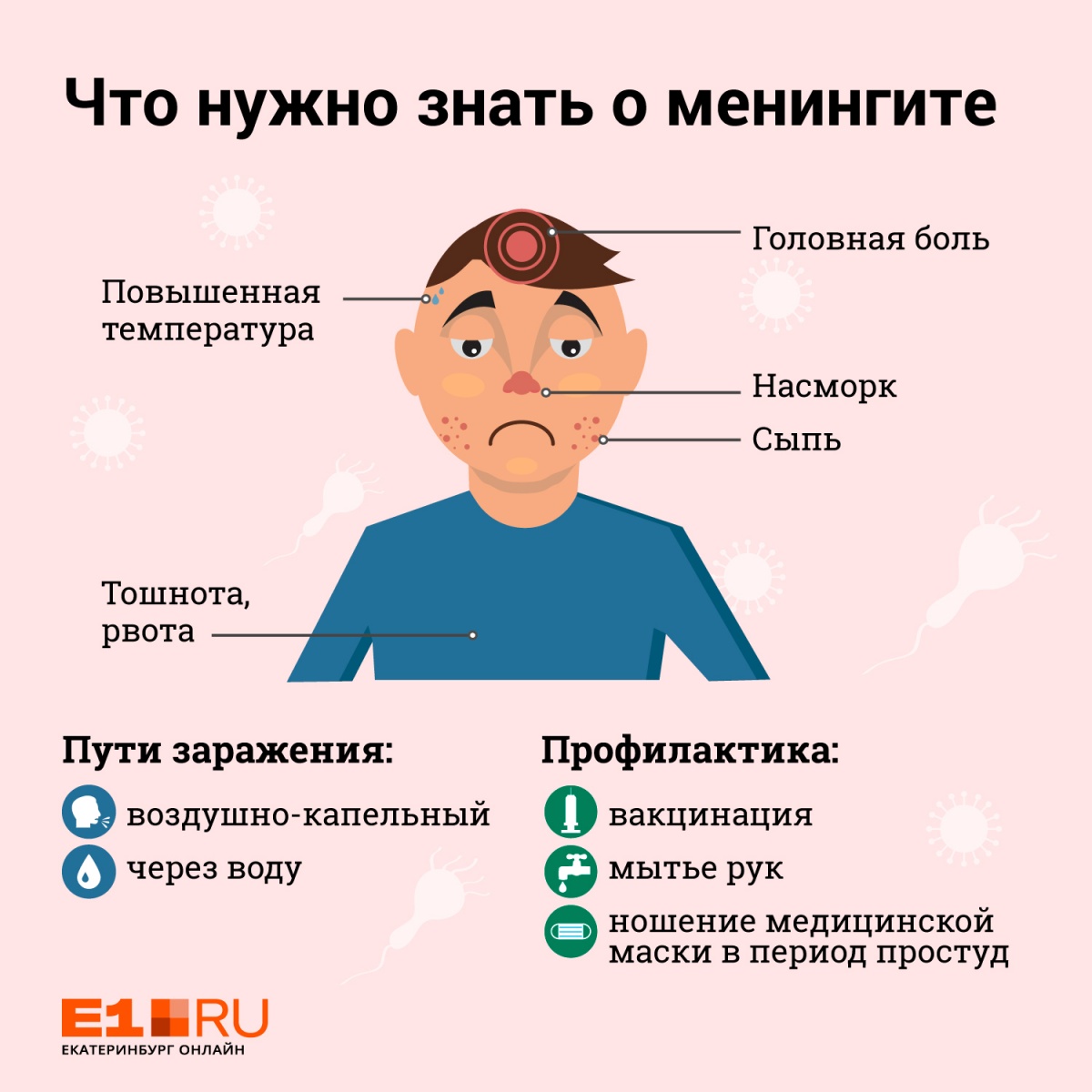 Инкубационный период колеблется от 1 до 14 дней, хотя обычно длится менее 2 дней [11].
Инкубационный период колеблется от 1 до 14 дней, хотя обычно длится менее 2 дней [11].
Клиническая картина может различаться в зависимости от возраста, и детям нередко изначально ставят неправильный диагноз. У маленьких детей клинические проявления могут быть более коварными с неспецифическими признаками; таким образом, диагностика может быть более сложной, чем у детей старшего возраста или подростков. Раздражительность и вялость — общие черты в этом возрасте. В некоторых случаях приступы с очаговым началом могут возникать в начале заболевания.Кроме того, скованность шеи у детей младше 2 лет встречается редко [3, 10–12]. Выдувание переднего родничка может наблюдаться у детей младше 18 месяцев. В целом у младенцев болезнь прогрессирует быстрее, чем у детей старшего возраста [12]. Как и у взрослых, у детей старшего возраста наиболее частыми симптомами являются лихорадка, тошнота, рвота, светобоязнь, головная боль, возбуждение, снижение уровня сознания и скованность шеи. Однако судороги и очаговые неврологические признаки встречаются реже [3, 10–12].Септический шок чаще встречается у детей и быстро прогрессирует с полиорганной недостаточностью и смертью в течение 24 часов [3, 10–12]. Часто неспецифические симптомы, такие как лихорадка, сонливость, тошнота и рвота, раздражительность и плохое питание, появляются в течение 4-6 часов от начала заболевания [3, 10-12]. Одним из наиболее частых симптомов, связанных с сепсисом, является быстро прогрессирующая геморрагическая сыпь, которая обычно начинается на нижних конечностях, хотя могут быть поражены слизистые оболочки и склеры [3, 10–12].Поражения кожи включают пятна, макулопапулы, крапивницу, петехии, пурпуру и экхимозы. Пурпурная сыпь может прогрессировать до молниеносной пурпуры, кожного проявления диссеминированного внутрисосудистого свертывания крови. Эти случаи часто связаны с септическим шоком и некрозом кожи, ишемией или инфарктом пальцев или конечностей, которые обычно требуют ампутации [3, 10–12]. У детей и подростков были выявлены три клинических признака раннего сепсиса: боль в ногах, холодные руки и ноги и ненормальный цвет кожи. Эти особенности могут указывать на нарушение жизненно важных функций [11]. Некоторые авторы сообщали о хронической менингококкемии, которая состояла из повторяющихся приступов лихорадки, артралгии и / или артрита, связанных с сыпью и головной болью [3, 11].
Эти особенности могут указывать на нарушение жизненно важных функций [11]. Некоторые авторы сообщали о хронической менингококкемии, которая состояла из повторяющихся приступов лихорадки, артралгии и / или артрита, связанных с сыпью и головной болью [3, 11].
IMD — это опасное для жизни заболевание с очень высоким уровнем тяжелых последствий среди выживших. В недавней статье Sadargani et al. оценили результаты IMD у 868 субъектов (52% взрослых и 48% детей) в Канаде в период с 2002 по 2011 год. Смертность у детей была ниже, чем у взрослых, но 21% детей (особенно в возрасте до 5 лет) имели по крайней мере одно осложнение по сравнению с 15% взрослых.Наибольшая частота осложнений наблюдалась у детей с септическим шоком без менингита, а наиболее частыми последствиями были потеря слуха, глухота, судороги, ампутация и рубцевание кожи [13]. В исследовании, в котором оценивались исходы IMD у 181 ребенка в возрасте до 15 лет, летальность составила 11,6%, а у 33% пациентов было зарегистрировано как минимум одно долгосрочное осложнение: трудности в учебе (22,6%), слух нарушениями (7%), неврологическими (12,2%), поведенческими (14,8%) и моторными (10.4%) дефицит [14].
Продолжительность заболевания до поступления и наличие судорог, очаговых неврологических нарушений, пониженного уровня сознания и низкого уровня глюкозы в спинномозговой жидкости могут быть связаны с высоким риском осложнений [11]. Ван и др. продемонстрировали, что последствия имели место у всех детей младше 1 года с IMD и недоношенными в анамнезе [15].
Лечение
Ввиду серьезности менингококковой инфекции, включая высокую летальность и возможность возникновения осложнений, ранняя клиническая и лабораторная диагностика очень важна.Люмбальная пункция должна выполняться во всех подозреваемых случаях с клиническими признаками и симптомами IMD. В большинстве случаев спинномозговая жидкость (ЦСЖ) выявляет высокое давление открытия, плеоцитоз, высокий уровень белка и низкий уровень глюкозы [10]. N. meningitidis следует обнаруживать в спинномозговой жидкости или крови с помощью окрашивания по Граму, стандартной культуры и / или полимеразной цепной реакции (ПЦР) [10, 11]. Эти обследования необходимо проводить очень быстро, чтобы избежать задержек в назначении терапии. Иногда стандартные посевы могут давать ложноотрицательные результаты из-за предварительного приема пероральных антибиотиков, что снижает чувствительность исследования.В этих случаях может быть полезна ПЦР [10]. Люмбальная пункция может быть опасна для пациентов с затяжными припадками, пациентов с ослабленным иммунитетом, при наличии признаков объемных поражений и у пациентов с тяжелым нарушением сознания и шоком [10].
N. meningitidis следует обнаруживать в спинномозговой жидкости или крови с помощью окрашивания по Граму, стандартной культуры и / или полимеразной цепной реакции (ПЦР) [10, 11]. Эти обследования необходимо проводить очень быстро, чтобы избежать задержек в назначении терапии. Иногда стандартные посевы могут давать ложноотрицательные результаты из-за предварительного приема пероральных антибиотиков, что снижает чувствительность исследования.В этих случаях может быть полезна ПЦР [10]. Люмбальная пункция может быть опасна для пациентов с затяжными припадками, пациентов с ослабленным иммунитетом, при наличии признаков объемных поражений и у пациентов с тяжелым нарушением сознания и шоком [10].
Своевременное и адекватное внутривенное лечение антибиотиками необходимо для остановки распространения и уничтожения N. meningitidis . Местная резистентность к антибиотикам должна определять выбор антибиотика. В большинстве случаев цефалоспорин третьего поколения (например, цефалоспорин третьего поколения) внутривенно вводится внутривенно.г., 100 мг / кг / день цефтриаксона, вводимого внутривенно. в одной суточной дозе или 100 мг / кг / сут цефотаксим, вводимый внутривенно. разделенные на три дневные дозы) следует использовать в качестве лечения первого выбора. Если эти антибиотики недоступны, следует начать внутривенное введение пенициллина [10, 11]. Если возможно, результат чувствительности к антибиотикам может служить ориентиром для продолжения антибактериальной терапии. Рекомендуемая продолжительность лечения составляет 7-10 дней, хотя недавние исследования показали, что стерилизация спинномозговой жидкости может происходить в течение 3-4 дней [10, 11].
Профилактика показана и рекомендуется только для близких контактов с индексным случаем (т. Е. Субъектов, которые оставались с индексным случаем более 4 часов в течение 7 предыдущих дней). В этих случаях пероральный рифампицин или ципрофлоксацин являются препаратами выбора в зависимости от возраста [11].
Менингококковые вакцины
Вакцинация остается лучшей стратегией предотвращения менингококковой инфекции из-за высокой смертности и серьезных последствий, которые могут возникнуть в результате инфекции, несмотря на своевременное лечение антибиотиками.Недавно во всем мире были внедрены новые менингококковые вакцины, что привело к снижению общего бремени болезни.
С момента внедрения конъюгированной вакцины против менингококка серогруппы C заболеваемость MenC значительно снизилась [16]. Коммерчески доступные моновалентные конъюгированные вакцины включают Menjugate (MCC-CRM197), Meningitec (MCC-CRM197) и NeisVac (MCC-TT). Также были получены четырехвалентные вакцины, содержащие менингококковые серогруппы ACWY, конъюгированные с различными белками.На рынке представлены продукты Menactra (ACWY-DT), лицензированные для детей в возрасте от 2 до 55 лет, Menveo (ACWYCRM197), лицензированные в Европе и США для детей в возрасте ≥ 2 лет, и Nimenrix (ACWY-TT), лицензированные в Европе для младенцев. Возраст ≥12 месяцев. Эти конъюгированные вакцины оказались безопасными и эффективными для защиты людей от менингита; более того, эти вакцины продемонстрировали коллективный иммунитет, прервав передачу носительства [17-19]. Четырехвалентные полисахаридные вакцины Menomune и Mencevax также оказались безопасными и вызывают бактерицидные антитела у детей старшего возраста и взрослых; однако они не используются в программах плановой вакцинации из-за их низкой иммуногенности у маленьких детей, краткосрочной защиты и неспособности вызвать коллективный иммунитет [16, 18].К сожалению, четырехвалентные менингококковые вакцины ACYW (конъюгированные или полисахаридные) не получили широкого распространения в развивающихся странах из-за высокой стоимости. Эффективная и безопасная конъюгированная вакцина против MenA (MenAfrivac), впервые лицензированная в Индии в 2009 году, была введена в африканский «пояс менингита» в 2010 году для субъектов в возрасте 1-29 лет; эта вакцина внедряется в этих регионах с целью защиты всего населения, подвергающегося риску, к 2016 году [18].
Учитывая высокий уровень заболеваемости MenB в развитых странах, производство вакцины, эффективной против этого серотипа, было приоритетной задачей.Однако вакцины против MenB было сложно производить. Поскольку внешняя полисахаридная капсула MenB напоминает молекулы адгезии на поверхности нервных клеток, конъюгированные вакцины не защищают от болезни MenB и, более того, могут вызывать аутоиммунный ответ [5, 20]. Первая вакцина, показавшая частичную эффективность против болезни MenB, была произведена на Кубе, в Новой Зеландии и Норвегии, но она была штаммоспецифичной и поэтому использовалась только для борьбы с эпидемиями [5]. По этим причинам эту вакцину нельзя считать эффективной против различных штаммов MenB, вызывающих эпидемии во всем мире.После нескольких попыток с использованием обратной вакцинологии была получена многокомпонентная вакцина MenB (4CMenB, Bexsero), охватывающая различные штаммы [5, 21]. 4CMenB состоит из четырех компонентов: первый компонент представляет собой белок, связывающий фактор H (fHbp), слитый с белком GNA 2091, второй — адгезию A Neisseria (NadA), третий — белок, связывающий гепарин Neisseria (NHba), слитый с белком GNA 2091. GNA 1030, а четвертым компонентом был OMV NZ98 / 254, который имеет несколько антигенных компонентов (основной компонент — PorA).Три антигена fHbp, NadA и NHba вызывают сывороточные бактерицидные антитела, в то время как два антигена GNA 2091 и GNA 1030 улучшают иммуногенность основных антигенов при слиянии с ними [5, 20]. В январе 2013 года 4CMenB был лицензирован в Европейском Союзе, а затем в Австралии и Канаде для использования у пациентов старше 2 месяцев [5, 20]. Учитывая низкую частоту IMD, довольно сложно оценить влияние любой менингококковой вакцины с помощью рандомизированных контролируемых клинических исследований.Хотя серологические методы можно использовать для оценки защиты других менингококковых вакцин, эти методы нельзя было использовать для 4CMenB из-за большого количества генетически различных штаммов MenB, вызывающих IMD. Чтобы преодолеть эту проблему, производитель вакцины использовал новый метод, называемый системой типирования менингококкового антигена (MATS), который использует уникальный вакцинный антиген-специфический ELISA, способный обнаруживать качественные и количественные различия в антигенах fHbp, NHba и NadA; затем результаты объединяются с информацией о типировании PorA [5].Результаты анализа 1052 штаммов MenB, выделенных из разных стран Европы, показали, что 4CMenB может защищать от 68% -88% штаммов MenB [5]. Двухвалентная рекомбинантная вакцина fHbp (также известная как LP2086; Trumenba) разрабатывалась с 2006 г. и в настоящее время одобрена Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США для использования у детей в возрасте от 10 до 25 лет [26]. Эта вакцина оказалась безопасной в исследовании фазы 3 примерно с 5600 здоровыми людьми в возрасте от 10 до 25 лет и была иммуногенной и безопасной при совместном применении с обычными менингококковыми инфекциями A, C, Y и W, а также с вакциной против столбняка, дифтерии и коклюша (Tdap). вакцины в фазе 2 исследования у более чем 2600 здоровых людей в возрасте от 10 до 12 лет [26].Исследования этой вакцины продолжаются в Европе, и ожидается, что в 2017 году будет получено одобрение Европейского агентства по лекарственным средствам.
Чтобы преодолеть эту проблему, производитель вакцины использовал новый метод, называемый системой типирования менингококкового антигена (MATS), который использует уникальный вакцинный антиген-специфический ELISA, способный обнаруживать качественные и количественные различия в антигенах fHbp, NHba и NadA; затем результаты объединяются с информацией о типировании PorA [5].Результаты анализа 1052 штаммов MenB, выделенных из разных стран Европы, показали, что 4CMenB может защищать от 68% -88% штаммов MenB [5]. Двухвалентная рекомбинантная вакцина fHbp (также известная как LP2086; Trumenba) разрабатывалась с 2006 г. и в настоящее время одобрена Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США для использования у детей в возрасте от 10 до 25 лет [26]. Эта вакцина оказалась безопасной в исследовании фазы 3 примерно с 5600 здоровыми людьми в возрасте от 10 до 25 лет и была иммуногенной и безопасной при совместном применении с обычными менингококковыми инфекциями A, C, Y и W, а также с вакциной против столбняка, дифтерии и коклюша (Tdap). вакцины в фазе 2 исследования у более чем 2600 здоровых людей в возрасте от 10 до 12 лет [26].Исследования этой вакцины продолжаются в Европе, и ожидается, что в 2017 году будет получено одобрение Европейского агентства по лекарственным средствам.
В будущем для оптимальных профилактических стратегий потребуется уникальная вакцина против MenA, B, C, W и Y. Недавняя фаза 2 В исследовании оценивали иммуногенность, безопасность и реактогенность у здоровых подростков исследуемой композиции менингококковой вакцины ABCWY, состоящей из рекомбинантных белков (rMenB) и компонентов OMV лицензированной вакцины серогруппы B в сочетании с компонентами лицензированной четырехвалентной конъюгированной менингококковой вакцины (MenACWY-CRM). ) [23].Авторы показали, что исследуемый состав MenABCWY, содержащий компоненты OMV, вызывал высокий ответ против всех штаммов с приемлемым профилем безопасности [23].
В связи с появлением MenX в Африке в последние десятилетия чрезвычайно важно разработать новую вакцину, эффективную против этого серотипа. В настоящее время нет лицензированной вакцины, но интересные данные были получены в недавнем исследовании, проведенном на мышах, в котором оценивалась иммуногенность везикул внешней мембраны MenX (XOMV) или полисахарида MenX (X-PS) в сочетании с бивалентной вакциной AW-OMV ранее. продемонстрировали иммуногенность у мышей [24].Авторы продемонстрировали, что высокий ответ антител индуцировался после двух доз X-OMV отдельно или в сочетании с AW-OMV. Напротив, X-PS не был иммуногенным сам по себе, но был иммуногенным в сочетании с AW-OMV.
В настоящее время нет лицензированной вакцины, но интересные данные были получены в недавнем исследовании, проведенном на мышах, в котором оценивалась иммуногенность везикул внешней мембраны MenX (XOMV) или полисахарида MenX (X-PS) в сочетании с бивалентной вакциной AW-OMV ранее. продемонстрировали иммуногенность у мышей [24].Авторы продемонстрировали, что высокий ответ антител индуцировался после двух доз X-OMV отдельно или в сочетании с AW-OMV. Напротив, X-PS не был иммуногенным сам по себе, но был иммуногенным в сочетании с AW-OMV.
Выводы
IMD представляет собой серьезную и опасную для жизни проблему для мирового сообщества. Раннее выявление детей с менингококковой инфекцией обязательно, чтобы немедленно начать системную антибактериальную терапию и избежать смерти или долгосрочных последствий.Вакцинация представляет собой лучшую стратегию предотвращения менингококковой инфекции. В последнее время внедрение новых конъюгированных вакцин, эффективных для детей раннего возраста, значительно снизило заболеваемость IMD во многих странах. Более того, доступность новых вакцин против MenB позволит еще больше расширить профилактические возможности против IMD. Целью следующих нескольких лет должно быть увеличение охвата вакцинацией против менингококковых заболеваний, продолжение мониторинга IMD и разработка уникальной вакцины, способной охватить все основные штаммы менингококка.
Ссылки
1. Хатами А., Поллард А.Дж. Эпидемиология менингококка
болезнь и влияние вакцин. Экспертные ревакцины. 2010. 9: 285–298. [PubMed] [Google Scholar] 3. Двилов Р., Фанелла С. Инвазивная менингококковая инфекция в 21 -м веке — обновление для клиницистов. Curr Neurol Neurosci
Отчет 2015; 15: 2–9. [PubMed] [Google Scholar] 4. Гальперин С.А., Беттингер Дж. А., Гринвуд Б. и др. Изменение
и динамическая эпидемиология менингококковой инфекции. Вакцина. 2012; 30: B26 – B36.[PubMed] [Google Scholar] 5. Эспозито С., Принципи Н. Профиль вакцины 4CMenB: четырехкомпонентный
Вакцина против Neisseria meningitidis серогруппы B. Эксперт Ред.
Эксперт Ред.
Вакцина. 2014; 13: 193–202. [PubMed] [Google Scholar] 6. Кристенсен Х., Мэй М., Хикман М. и др. Менингококковое носительство
по возрасту: систематический обзор и метаанализ. Ланцет. 2010. 10: 853–861. [PubMed] [Google Scholar] 7. Функ А., Уадиале К., Камау С. и др. Последовательные вспышки из-за
новый штамм Neisseria Meningitidis серогруппы C в Северной
Нигерия, 2013-2014 гг.Вспышки токов PLOS. 2014; 6 [Бесплатная статья PMC] [PubMed] [Google Scholar] 8. Се О, Поллард А.Дж., Мюллер Дж. И др. Появление серогруппы X
менингококковая инфекция в Африке: необходимость вакцины. Вакцина. 2013; 31: 2852–2861. [PubMed] [Google Scholar] 9. Торёс Б., Тулин Хедберг С., Якобссон С. и др. Наблюдение
инвазивной Neisseria meningitidis с обновлением серогруппы Y,
Швеция с 2010 по 2012 год. Euro Surveill. 2014; 19 pii 20940. [PubMed] [Google Scholar] 10. Бранко Р., Таскер Р. Менингококковый менингит.Варианты лечения Curr
Neurol. 2010; 12: 464–474. [PubMed] [Google Scholar] 11. Sabatini C, Bosis S, Semino M, Senatore L, Principi N, Esposito S. Клинические проявления менингококковой инфекции в детстве. J Prev Med Hyg. 2012; 53: 116–119. [PubMed] [Google Scholar] 12. Дасс Хазарика Р., Дека Н.М., Хирием А.Б. и др. Инвазивный менингококковый
инфекция: анализ 110 случаев оказания третичной медицинской помощи
центр в Северо-Восточной Индии. Индийский J Pediatr. 2013; 80: 359–364. [Бесплатная статья PMC] [PubMed] [Google Scholar] 13. Садарангани М., Шайфеле Д.В., Гальперин С.А. и др.Следователи
Канадской программы мониторинга иммунизации, ACTive
(ВЛИЯНИЕ)
, следователь. Исходы инвазивного менингококкового заболевания
у взрослых и детей в Канаде в период с 2002 по 2011 год:
проспективное когортное исследование. Clin Infect Dis. 2015; 60: e27 – e35. [PubMed] [Google Scholar] 14. Штейн-Замир Ч., Соколов И., Абрамсон Н и др. Клинические особенности
и отдаленные последствия инвазивного менингококкового заболевания
у детей. Pediatr Infect Dis J. 2014; 33: 777–779. [PubMed] [Google Scholar] 15. Ван Б., Кларк М., Томас Н. и др.Клиническая нагрузка и
Ван Б., Кларк М., Томас Н. и др.Клиническая нагрузка и
предикторы последствий инвазивного менингококкового заболевания
у австралийских детей. Pediatr Infect Dis J. 2014; 33: 316–318. [PubMed] [Google Scholar] 16. Заимствование Р., Абад Р., Троттер С. и др. Эффективность менингококковой инфекции
программы вакцинации серогруппы C. Вакцина. 2013; 31: 4477–4486. [PubMed] [Google Scholar] 17. Прочтите RC, Baxter D, Chadwick DR, et al. Эффект четырехвалентного
менингококковый гликонъюгат ACWY или менингококк серогруппы B
вакцина против менингококкового носительства: слепой наблюдатель,
3 фаза рандомизированного клинического исследования.Ланцет. 2014; 384: 2123–2131. [PubMed] [Google Scholar] 18. Хедари CP, Хинкарлы RW, Дбайбо GS. Менигококковые серогруппы
Конъюгированная вакцина против столбнячного анатоксина A, C, W-135 и Y: a
новая конъюгированная вакцина против инвазивной менингококковой инфекции. Устойчивость к заражению лекарствами. 2014; 7: 85–99. [Бесплатная статья PMC] [PubMed] [Google Scholar] 19. Ли Х.Дж., Чунг М.Х., Ким В.Дж. и др. Иммуногенность и безопасность
новой четырехвалентной конъюгированной менингококковой вакцины
(MenACWY-CRM) у здоровых корейских подростков и взрослых. Int J Infect Dis.2014; 28: 204–210. [PubMed] [Google Scholar] 21. Макнамара Л.А., Шумате А.М., Йонсен П. и др. Первое использование
менингококковая вакцина серогруппы B в США в ответ на
университетская вспышка. Педиатрия. 2015; 135: 798–804. [Бесплатная статья PMC] [PubMed] [Google Scholar] 23. Saez-Llorens X, Aguilera Vaca DC, Abarca K и др. Иммногенность
и безопасность исследуемых вакцинных составов
против манингококков серогрупп A, B, C, W и Y у здоровых
подростки. Hum Vaccin Immunother. 2015; 13 [Epub перед
печать] [Бесплатная статья PMC] [PubMed] [Google Scholar] 24.Тунхейм Г., Нэсс Л. М., Асеведо Р. и др. Доклиническая иммуногенность
исследование трехвалентных менингококковых вакцин AWX-OMV
для пояса африканского менингита. Вакцина. 2014; 32: 6631–6638. [PubMed] [Google Scholar]
Бактериальный менингит у детей | Бостонская детская больница
Что такое менингит?
Менингит — это инфекция, вызывающая воспаление трех тонких слоев ткани, известных как мозговые оболочки, которые покрывают головной и спинной мозг. Менингит может быть вызван вирусом или бактериями.
Менингит может быть вызван вирусом или бактериями.
В целом бактериальный менингит опаснее вирусного менингита. Бактериальный менингит может вызвать необратимые повреждения, включая потерю слуха, умственную отсталость или даже смерть. Приблизительно 3000 человек в США, или каждый 100000 человек, ежегодно заболевают бактериальным менингитом.
Типичное лечение включает госпитализацию и прием антибиотиков.
В чем разница между бактериальным менингитом и вирусным менингитом?
Симптомы:
- Вирусный менингит — лихорадка, головная боль, ригидность шеи, чувствительность к свету, сонливость, спутанность сознания.
- Бактериальный менингит — высокая температура, сильная головная боль, ригидность шеи, чувствительность к свету, сонливость, спутанность сознания. Также могут возникнуть сыпь, тошнота, рвота и боль в горле.
Эффекты:
- Вирусный менингит — временные симптомы гриппа, головная боль и ригидность шеи.
- Бактериальный менингит — возможность поражения головного мозга различной степени, включая потерю слуха и умственную отсталость. Может быть смертельным, если вовремя не лечить.
Уровень серьезности:
- Вирусный менингит — проходит сам по себе обычно в течение трех-десяти дней.
- Бактериальный менингит — опасный для жизни. Немедленно требуется медицинская помощь.
Лечение:
- Вирусный менингит — Постельный режим, Тайленол.
- Бактериальный менингит — Госпитализация и антибиотики.
Насколько распространен бактериальный менингит?
Приблизительно 3000 человек в Соединенных Штатах — или один из 100000 — заболевают бактериальным менингитом каждый год, большинство из них младенцы, дети, студенты колледжей и пожилые люди.Заболеваемость бактериальным менингитом обычно достигает пика зимой или ранней весной. Люди, у которых проявляются симптомы в летнее время, чаще болеют вирусным менингитом, чем бактериальным менингитом.
Люди, у которых проявляются симптомы в летнее время, чаще болеют вирусным менингитом, чем бактериальным менингитом.
Профилактика бактериального менингита
Самая распространенная причина бактериального менингита у детей, Haemophilus influenzae b (Hib), была почти устранена благодаря вакцине, разработанной в Бостонской детской больнице в 1990 году.
- До этого примерно у 10 000 детей ежегодно диагностировали менингит, и 5 процентов из них не выживали.
- Иммунизация Hib теперь является обычной вакцинацией детей, которая предотвращает сотни смертей в год.
Заболеваемость другой основной причиной бактериального менингита — бактериями пневмококка — также резко снизилась благодаря широкому использованию пневмококковой вакцины Prevnar.
Менингококковая вакцина, особенно против менингококковых бактерий, рекомендуется для учащихся, поступающих в общежитие средней школы или колледжа. Он действует от трех до пяти лет, однако защищает не от всех штаммов менингококковых бактерий.
Как мы лечим бактериальный менингит
В связи с быстрым и тяжелым течением бактериального менингита Boston Children’s призывает всех родителей немедленно обратиться за лечением, если вы подозреваете бактериальный менингит. После госпитализации врачи выяснят конкретную причину менингита у вашего ребенка и назначат соответствующее лечение. Конечная цель быстрого лечения — убедиться, что ваш ребенок выздоравливает без каких-либо необратимых повреждений.
Каковы признаки и симптомы менингококкового менингита у детей раннего возраста?
Автор
Франсиско де Ассис Акино Гондим, доктор медицинских наук, магистр, FAAN Профессор адъюнто неврологии и клинических навыков, кафедра внутренней медицины, Федеральный университет Сеара, Бразилия
Франсиско де Ассис Акино Гондим, доктор медицинских наук, магистр наук, FAAN является членом следующих медицинских обществ: Американской академии неврологии, Американской ассоциации нейромышечной и электродиагностической медицины, Международного общества паркинсона и двигательных расстройств
Раскрытие информации: служить (d) в качестве директора, должностного лица, партнера, сотрудника, советника, консультанта или Доверенное лицо: Консультант Pfizer, PTC Therapeutics и Alnylam
Выступать (d) в качестве докладчика или члена бюро докладчиков для: Speaker for Shire, PTC Therapeutics и BSL Beringer
Получил гранты на поездки от: Aché, Biogen, Genzyme, Ipsen, Novartis, Baxter, Teva, Pfizer.
Соавтор (ы)
Маниш К Сингх, доктор медицины Доцент кафедры неврологии, преподавательский факультет программы резидентуры по лечению боли и неврологии, Университетская больница Ганемана, Медицинский колледж Дрекселя; Медицинский директор, неврология и лечение боли, Институт нейробиологии Джерси
Маниш К Сингх, доктор медицины, является членом следующих медицинских обществ: Американской академии неврологии, Американской академии медицины боли, Американского общества головной боли, Американской ассоциации врачей индийского происхождения , Американская медицинская ассоциация, Американское общество региональной анестезии и медицины боли
Раскрытие информации: не раскрывать.
Специальная редакционная коллегия
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: Получил зарплату от Medscape за работу. для: Medscape.
Флориан П. Томас, доктор медицинских наук, магистр медицины, магистр медицины Председатель Института неврологии и Департамент неврологии, директор Национального центра рассеянного склероза РС и Центра передового опыта Фонда наследственной невропатии Медицинского центра Университета Хакенсак; Председатель-основатель и профессор кафедры неврологии Медицинской школы Хакенсак-Меридиан Университета Сетон-Холл; Почетный профессор кафедры неврологии Медицинской школы университета Сент-Луиса; Главный редактор, Journal of Spinal Cord Medicine
Флориан П. Томас, доктор медицинских наук, магистр наук, магистр медицины, является членом следующих медицинских обществ: Академия специалистов по травмам спинного мозга, Американская академия неврологии, Американская неврологическая ассоциация, Консорциум Центров рассеянного склероза, Национальное общество рассеянного склероза, Sigma Xi
Раскрытие информации: нечего раскрывать.
Главный редактор
Ниранджан Н Сингх, MBBS, MD, DM, FAHS, FAANEM Адъюнкт-профессор неврологии, Медицинский факультет Университета Миссури-Колумбия; Медицинский директор программы по лечению инсульта Святой Марии, Институт неврологии SSM, SSM Health
Ниранджан Н. Сингх, MBBS, MD, DM, FAHS, FAANEM является членом следующих медицинских обществ: Американской академии неврологии, Американской ассоциации нервно-мышечной и электродиагностической медицины. , Американское общество головной боли
Раскрытие информации: нечего раскрывать.
Дополнительные участники
Norman C Reynolds, Jr, MD Невролог, Медицинский центр по делам ветеранов Милуоки; Клинический профессор, Медицинский колледж Висконсина
Норман С. Рейнольдс-младший, доктор медицины является членом следующих медицинских обществ: Американской академии неврологии, Ассоциации военных хирургов США, Международного общества паркинсона и двигательных расстройств, Сигма Си, Общества Neuroscience
Раскрытие: нечего раскрывать.
Благодарности
Авторы и редакторы Medscape Reference выражают признательность предыдущему автору Сидни Е. Кроулу, доктору медицины, за вклад в разработку и написание исходной статьи.
Менингококцемия Артикул
.
Непрерывное образование
Neisseria meningitidis (менингококк) — важная бактериальная инфекция, проявляющаяся в виде менингита или сепсиса, или, чаще, их комбинации.Бессимптомная колонизация глотки — это начальный этап инфицирования человека, который является естественным резервуаром. Из носоглотки кокк достигает мозговых оболочек, перемещаясь через слизистую носоглотки и периневральную оболочку обонятельного нерва через решетчатую пластинку решетчатой кости. Распространение кровотока на мозговые оболочки вызывает менингит. У некоторых детей преобладающим признаком является сердечно-сосудистый коллапс, приводящий к септическому шоку. В этом упражнении рассматриваются проявления, оценка и лечение менингококкемии и подчеркивается роль межпрофессиональной группы в ведении пациентов с этой инфекцией.
Распространение кровотока на мозговые оболочки вызывает менингит. У некоторых детей преобладающим признаком является сердечно-сосудистый коллапс, приводящий к септическому шоку. В этом упражнении рассматриваются проявления, оценка и лечение менингококкемии и подчеркивается роль межпрофессиональной группы в ведении пациентов с этой инфекцией.
Целей:
- Определите этиологию менингококкемии.
- Опишите состояние пациента с менингококкемией.
- Обобщите доступные варианты лечения и ведения менингококкемии.
- Обрисовать в общих чертах некоторые стратегии межпрофессиональной команды для улучшения координации оказания помощи и коммуникации, чтобы продвинуть лечение менингококкемии и улучшить результаты лечения пациентов.
Введение
Одним из наиболее серьезных и опасных для жизни инфекционных заболеваний в детском возрасте является бактериемия, следствием которой является септический шок, при котором вследствие эндотоксемии возникает недостаточная перфузия тканей. Neisseria meningitidis ( Meningococcus ) — важная бактериальная инфекция, проявляющаяся в виде менингита или сепсиса, или, чаще, их комбинации. Бессимптомная колонизация глотки — это начальная стадия инфекции, естественными резервуарами которой являются люди.Из носоглотки кокк достигает мозговых оболочек, перемещаясь через слизистую носоглотки и периневральную оболочку обонятельного нерва через решетчатую пластинку решетчатой кости. Распространение кровотока на мозговые оболочки вызывает менингит. У некоторых детей преобладающим признаком является сердечно-сосудистый коллапс, приводящий к септическому шоку.
Передача происходит воздушно-капельным путем и требует тесного прямого контакта. Дети младше 5 лет не обладают адекватным иммунитетом против полисахаридных антигенов N. meningitidis . Факторы риска инфекционных заболеваний в детских учреждениях включают иммунологическую восприимчивость, недостаточную осведомленность и соблюдение правил гигиены, естественную склонность к близости, частый оральный контакт с объектами в окружающей среде.
meningitidis . Факторы риска инфекционных заболеваний в детских учреждениях включают иммунологическую восприимчивость, недостаточную осведомленность и соблюдение правил гигиены, естественную склонность к близости, частый оральный контакт с объектами в окружающей среде.
Инвазивная менингококковая инфекция встречается в 2 возрастных группах: младенцы, уязвимые из-за исчезновения в раннем возрасте материнских антител, и подростки с высокой скоростью колонизации носоглотки. [1] [2]
Этиология
Н.meningitidis — грамотрицательный кокк попарно с приплюснутыми соседними сторонами. Он неподвижен, аэробен и факультативно анаэробен. Он производит каталазу и является оксидазоположительным. Он производит кислоту из глюкозы и мальтозы. Свежие изоляты требуют обогащенной среды, такой как кровь или шоколадный агар. Инкубация в увлажненной среде с 10% двуокиси углерода (CO2) ускоряет рост.
Факторы вирулентности включают полисахаридную капсулу, которая увеличивает инвазивность, подавляя фагоцитоз и увеличивая выживаемость организма во время инвазии кровотока и центральной нервной системы (ЦНС).Пили опосредуют прикрепление, колонизацию и вторжение организмов в клетки слизистой оболочки носоглотки. Антигенная вариация пилей по кассетному механизму позволяет бактерии избежать иммунной системы хозяина.
Внешние мембранные белки
Пориновые белки могут внедряться в мембраны клеток-мишеней, а фаголизосомы могут вызывать апоптоз. Белок OPC участвует в прилипании к слизистой оболочке и инвазии эндотелиальных клеток. Протеаза IgA1 гидролизует молекулы IgA1 в шарнирных областях.Фермент инактивирует IgA1 на поверхности слизистой оболочки, обеспечивая начальное прикрепление и последующую инвазию. Патогенные Neisseria выживают и размножаются благодаря своей способности извлекать железо из железосвязывающих белков с высоким сродством. N. meningitidis может приобретать устойчивость к пенициллину от комменсальных видов Neisseria в носоглотке через фрагменты ДНК путем трансформации. Meningococcus также демонстрирует изменение фазы поверхностных антигенов, таким образом избегая иммунного ответа хозяина.
Meningococcus также демонстрирует изменение фазы поверхностных антигенов, таким образом избегая иммунного ответа хозяина.
Капсульные полисахариды являются антигенными и составляют основу серогрупп. Двенадцать серогрупп — это A, B, C, H, I, K, L, X, Y, Z, W-135 и 29F. Серогруппы A, B, C, W-135, X и Y являются наиболее частыми причинами инвазивных заболеваний во всем мире.
Эпидемиология
США
Инвазивные инфекции, вызываемые N. meningitidis , регистрируются через Национальную систему надзора, подлежащую уведомлению в Соединенных Штатах.Количество случаев, о которых было сообщено в Центры по контролю и профилактике заболеваний (CDC) в 2013 и 2014 годах, составило 556 и 564, соответственно. Это самые низкие показатели в США.
В 2014 г. общая заболеваемость инвазивным менингококком в США составила 0,14 на 100 000 населения. Из зарегистрированных случаев 25% случаев были бактериемией с летальным исходом 20%. Распределение серогрупп составляло 26% серогруппы B, 36% серогруппы C, 9% серогруппы Y и 28% других серогрупп.В Соединенных Штатах серогруппа B ответственна за 65% младенческих заболеваний, а серогруппы C и Y ответственны за подростковые заболевания. Среди непривитых вспышки вызваны серогруппой C.
Пик менингококковой инфекции в США приходится на период с ноября по март. Постепенное увеличение защитных антител против менингококков наблюдается между 2 и 12 годами. Пассивный внутриутробный перенос антител IgG происходит у новорожденных, если у матери есть антитела против менингококков.
Международный
В развивающихся странах уровень заболеваемости инвазивным менингококком составляет от 10 до 25 случаев на 100 000 жителей в год. Самый высокий уровень от 10 до 1000 на 100000 в год наблюдается в поясе в Африке к югу от Сахары, называемом поясом менингита, с повторяющимися эпидемиями группы A. Смерть наступает в 6-10% случаев, а осложнения — в 4,3-11,2. % случаев. [3] Группа A преобладала с 2007 по 2009 год, в то время как серогруппа W135 преобладала с 2010 по 2011 год.[4] В 2013 и 2014 годах в Нигерии и Кебби произошли 2 вспышки менингококка серогруппы C, штамма, относительно редкого в Африке. [5]
% случаев. [3] Группа A преобладала с 2007 по 2009 год, в то время как серогруппа W135 преобладала с 2010 по 2011 год.[4] В 2013 и 2014 годах в Нигерии и Кебби произошли 2 вспышки менингококка серогруппы C, штамма, относительно редкого в Африке. [5]
Международные вспышки инфекции N. meningitidis произошли в 1987 и 2000 годах в связи с паломничеством хаджа в Мекку. Вспышка 1987 г. была вызвана серогруппой А, а вспышка 2000 г. — серогруппой W-135. Серогруппа W появилась в других регионах, включая Южную Америку и Англию. В европейских странах число инвазивных заболеваний серогруппы C снизилось, а серогруппа B вызывает от 60% до 72% случаев инвазивных заболеваний.В Азии крупные эпидемии, вызванные серогруппой А, исторически происходили в Китае, Индии, Непале и России. Совсем недавно серогруппы B и C стали причиной в этой области. [6]
Сообщается о повышении серогруппы Y в странах Северной Европы. [7]
Патофизиология
Основной причиной сердечно-сосудистого коллапса при сепсисе является недостаточность периферического кровообращения. Дисфункция сердца из-за недостаточности миокарда играет важную роль в развитии менингококковой инфекции.Более высокие концентрации эндотоксина (LOS) были связаны с шоком, почечной недостаточностью и респираторным дистрессом. Высокие концентрации IL-6 и IL-8 наблюдаются у пациентов с менингококковым шоком.
TNF и IL-1 активируют эндотелиальные клетки, увеличивая их проницаемость и адгезию для лейкоцитов. Избыточное производство оксида азота снижает артериальное давление из-за расширения сосудов. Это также ухудшает сократительную способность сердца.
Ретракция эндотелиальных клеток при взаимодействии с бактериальными эндотелиальными клетками приводит к потере целостности, вызывая капиллярные кровоизлияния и образование тромбов в пурпурных поражениях.Когда большое количество бактерий колонизирует кровеносные сосуды и приводит к соответствующей передаче сигналов, это является причиной обширных пурпурных поражений и тяжести шока у Purpura fulminans [8]
.
Гистопатология
Гистология кожных поражений показывает эндотелиальный некроз капилляров и мелких вен дермы и подкожной клетчатки. Наблюдаются нейтрофильная инфильтрация и окклюзия сосудов лейкоцитами, тромбоцитами, фибриновыми тромбами и кровоизлияния.Менингококки видны в эндотелии и тромбах.
История и физика
Спектр заболевания, вызываемого N. meningitidis , варьируется от бессимптомного носительства до смерти от молниеносной менингококкемии. Менингококковый менингит и сепсис — частые синдромы, о которых сообщается, хотя в некоторых случаях присутствуют обе клинические картины. [9] [10] [11]
Признаки и симптомы менингококкемии включают раннюю инфекцию верхних дыхательных путей с ринитом, фарингитом, тонзиллитом и ларингитом.У пациентов наблюдается лихорадка с головной болью, рвотой и вялостью. Как правило, у пациентов с менингококкемией наблюдается лихорадка и геморрагическая сыпь, за которыми следуют признаки тяжелой недостаточности кровообращения. Пурпура и шок часто развиваются в течение нескольких часов. Кожные проявления — от диффузных пятнистостей до обширных пурпурных поражений. Петехии или пурпура наблюдаются у 50-60% пациентов. У 20-30% детей может не быть сыпи при предъявлении.
Хроническая менингококкемия определяется как менингококковая септицемия с лихорадкой в течение как минимум недели до начала терапии антибиотиками и без менингеальных симптомов.При хронической менингококкемии бактерии никогда не обнаруживаются при биопсии или посеве кожных повреждений. Исследователи предполагают, что изменения кожи и артрит могут быть результатом комплексов антиген-антитело. Диагноз устанавливают путем идентификации организма в посеве крови. Выздоровление происходит быстро после лечения антибиотиками.
Ряд исследователей подчеркнули миокардиальные проявления, связанные с менингококковым менингитом, включая сердечную недостаточность с отеком легких и высокое центральное венозное давление, сопровождающее признаки плохой периферической перфузии. Лечение миокардиальной недостаточности может улучшить ситуацию. Повышенный уровень интерлейкина 6 может быть медиатором депрессии миокарда при септическом шоке, вызванном менингококковой инфекцией. [12]
Лечение миокардиальной недостаточности может улучшить ситуацию. Повышенный уровень интерлейкина 6 может быть медиатором депрессии миокарда при септическом шоке, вызванном менингококковой инфекцией. [12]
Оценка
Диагноз должен быть поставлен клинически, и лечение антибиотиками широкого спектра действия должно быть начато в ожидании идентификации микроорганизмов.
Микробиологический диагноз
- Контроль общественного здравоохранения
- Чувствительность к антибиотикам
- Для исключения других организмов
Пятно по Граму
Цереброспинальная жидкость (ЦСЖ) при менингите показывает грамотрицательные внутриклеточные и внеклеточные диплококки.
- Поражения кожи при менингококкемии: аспирационная игла и соскоб окрашиваются по Граму
- Бледный слой крови Окраска по Граму
Культура
- CSF инокулируют на шоколадный агар и инкубируют в 3–5% CO2
- Образцы слизистой оболочки инокулируют в селективную среду — шоколадный агар Тайера-Мартина, к которому добавлены ванкомицин, колистин и нистатин для подавления комменсалов.
- Посев крови: положительный результат от 40% до 75% до начала лечения.Посевы спинномозговой жидкости положительны у 90% нелеченных пациентов с менингитом
- Объединение результатов посевов крови и ЦСЖ с окрашиванием ЦСЖ по Граму позволяет выявить 94% антигена менингита.
Обнаружение антигена
- Менингококковый антиген в спинномозговой жидкости (сыворотка и моча имеют перекрестные реакции): латексная агглютинация; Низкая чувствительность и специфичность для капсульного типа B
- ПЦР позволяет обнаружить менингококковую ДНК в спинномозговой жидкости, плазме и сыворотке.Чувствительность и специфичность выше 90%. Он более чувствителен, чем посев крови.
 Диагноз можно поставить за 4-8 часов. Предыдущая терапия антибиотиками меньше влияет на ПЦР-анализы.
Диагноз можно поставить за 4-8 часов. Предыдущая терапия антибиотиками меньше влияет на ПЦР-анализы.
Анализ
Визуализация
- Если пациент находится в коме, компьютерная томография (КТ) головного мозга помогает исключить внутричерепное кровоизлияние.
Гематологические и метаболические аномалии
При менингококковом менингите повышаются показатели ЦСЖ, лейкоцитов, лейкоцитов периферической крови и С-реактивного белка, прокальцитонина и СОЭ.ЦСЖ имеет повышенный уровень белка, низкий уровень глюкозы и грамотрицательные бактерии , диплококк .
- При менингококковой сепсисе в тяжелых случаях наблюдаются метаболические нарушения, такие как гипогликемия, гипокалиемия, гипокальциемия, гипомагниемия, гипофосфатемия и метаболический ацидоз. Также наблюдаются анемия, коагулопатия, снижение уровня протеина C, фибриногена, протромбина и факторов свертывания (V, VII и X).
Лечение / менеджмент
Противомикробные препараты
Для начальной терапии используются цефалоспорин-цефтриаксон третьего поколения или цефотаксим.
Продолжающееся заболевание:
- Цефтриаксон (80 мг / кг в день в 1-2 приема внутривенно [в / в])
- Цефотаксим (200 мг / кг в сутки в 3-4 приема внутривенно)
- Пенициллин G (50 мг / кг каждые 4-6 часов в / в)
- Хлорамфеникол (100 мг / кг / день в 4 приема, перорально или внутривенно)
- Меропенем для людей с тяжелой аллергией
Рекомендуемая продолжительность лечения как при менингите, так и при менингококкемии составляет 7 дней.
Дополнительные и экспериментальные методы лечения
Кортикостероидная терапия: Замещающие дозы (25 мг / м3 гидрокортизона 4 раза) ежедневно полезны для детей с рефрактерным шоком, связанным с нарушением реакции надпочечников.
- Рекомбинантный бактерицидный белок, увеличивающий проницаемость (rBPI), связывается с эндотоксином и блокирует воспалительный каскад.
 У детей, получавших rBPI, было меньше ампутаций и переливаний продуктов крови, а также улучшились функциональные результаты.
У детей, получавших rBPI, было меньше ампутаций и переливаний продуктов крови, а также улучшились функциональные результаты. - Другими дополнительными методами лечения сепсиса являются плазмаферез, экстракорпоральная мембранная оксигенация (ЭКМО), фибринолиз и антимедиаторная терапия.
Управление неотложной помощью
- После защиты дыхательных путей приоритетами у детей с менингококковой инфекцией являются:
- Коррекция сердечно-сосудистого шока и
- Контроль повышенного внутричерепного давления
- Агрессивная жидкостная реанимация 0.9% раствор NaCl в объеме 20 мл / кг в течение 5–10 минут имеет значение и повторяется до тех пор, пока шок не пройдет. Инотропная поддержка необходима для поддержания перфузии тканей.
- В качестве альтернативы можно использовать раствор человеческого альбумина.
- Анемия, коагулопатия находится под наблюдением и коррекцией.
- В случаях повышенного внутричерепного давления необходимо обеспечить адекватную церебральную перфузию путем коррекции шока и оказания нейроинтенсивной терапии.
Дифференциальная диагностика
Инфекционный
- Пятнистая лихорадка Скалистых гор
- Эрлихиоз
- Стрептококковая пневмония
- Гемофильная инфекция типа B
- Стрептококк группы А
- Золотистый стафилококк
- Грамотрицательный бактериальный сепсис с DIC
- Инфекционный эндокардит
- Гонококцемия
- Крысиная лихорадка
- Сыпной тиф
- Вторичный сифилис
Не Инфекционные
- Пурпура Геноха-Шонлейна
- Острый геморрагический отек у младенцев
- Нарушения тромбоцитов (идиопатическая тромбоцитопеническая пурпура)
- Коллагеновая болезнь сосудов
- Неопластические процессы
Прогноз
- Балльные системы предназначены для прогнозирования прогноза менингококковой инфекции.Большинство прогностических систем оценки сходятся во мнении, что молниеносная пурпура и шок — плохие прогностические признаки.
- Прогностическая шкала менингококковой сепсиса Глазго (GMSPS) оценивает 7 ключевых пунктов: гипотензию, разницу в температуре ядра кожи, кома, острое ухудшение состояния, отсутствие менингизма, прогрессирующая пурпура и дефицит оснований.
- В детской больнице Лос-Анджелеса 5 признаков коррелировали с плохим прогнозом: шок или судороги, гипотермия, общее количество лейкоцитов менее 5000 / мм, количество тромбоцитов менее 100000 / мм и развитие Purpura fulminans .
- Общая смертность от инвазивной менингококковой инфекции в США составляет от 7% до 19%.
- Ретроспективный популяционный анализ смертности от менингококковой инфекции в США с 1990 по 2002 год выявил 3335 случаев смерти от менингококков.
Осложнения
- Последствиями менингококкемии являются некроз кожи (ишемический инфаркт кожи и мягких тканей), потеря слуха, глухота, судороги, ампутация и рубцевание кожи.Нарушение перфузии органов из-за гиповолемии, сужения сосудов и миокардиальной недостаточности приводит к преренальной недостаточности, проявляющейся в виде олигурии, анурии или острого некроза канальцев.
- Иммунологические или реактивные осложнения, такие как артрит, кожный васкулит, ирит и перикардит, вызваны отложением иммунных комплексов с полисахаридным антигеном, IgG и C3, что приводит к острому воспалению.
Жемчуг и другие выпуски
Профилактика / Профилактика
Профилактика вакцин
Моновалентные капсульные конъюгированные менингококковые вакцины группы C (MenC) используются в Европе, Австралии и Канаде для плановой иммунизации младенцев и детей ясельного возраста.Они очень эффективны, хотя рекомендуется их ревакцинация в подростковом возрасте.
Четырехвалентные конъюгированные вакцины против менингококков A, C, Y, W (Men ACYW) используются для иммунизации подростков в Северной Америке. Он используется в качестве вакцины для групп высокого риска и путешественников во многих странах. Он также заменяет Men C в качестве вспомогательного средства для подростков за пределами Соединенных Штатов.
Бустерные дозы Men ACYW рекомендуются в Соединенных Штатах для детей из групп высокого риска и лиц, иммунизированных в возрасте до 15 лет.Капсульные вакцины везикул наружных мембран группы B (OMV) используются для вспышек заболеваний с участием единичных клонов.
Две капсульные вакцины группы B (Men B-4C, 2 дозы и Men B-FHbp, 3 дозы) лицензированы для людей старше 10 лет. В США он рекомендован пациентам из группы риска и при вспышках заболеваний и может назначаться в возрасте от 16 до 23 лет по усмотрению врача.
Химиопрофилактика для контактов с больными менингококковой болезнью
Доза антибиотика
Рифампицин: 10 мг / кг на дозу; Перорально каждые 12 часов, 4 дозы (для младенцев младше 1 месяца, 5 мг / кг на дозу)
Цефтриаксон: однократная инъекция 125 мг для младше 15 лет и 250 мг для старше 15 лет *
Ципрофлоксацин : 20 мг / кг (макс. 500 мг) старше 1 месяца *
* Данные Комитета по инфекционным заболеваниям Американской академии педиатрии.Красная книга 2015 Отчет Комитета по инфекционным болезням, 30-е издание. Элк Гроув, Иллинойс, Американская академия педиатрии, 2015 г.
Улучшение результатов команды здравоохранения
Менингококкемия — это серьезная опасная для жизни инфекция, с которой лучше всего справляется многопрофильная бригада, в которую входят медсестры интенсивной терапии. Лечение следует начинать даже при низком уровне подозрений на инфекцию; даже задержка на несколько часов может оказаться фатальной.Фармацевт должен информировать пациентов о пользе менингококковой вакцины, особенно для пожилых людей, поскольку она может спасти жизнь.
Перспективы пациентов с менингококкемией ограничены; к сожалению, большинство пациентов умирают, несмотря на адекватное лечение.
Клиническая картина менингококцемии: анамнез, физикальное обследование
Эль Башир Х, Лаунди М., Буй Р. Диагностика и лечение бактериального менингита. Арка Дис Детский .2003 июл.88 (7): 615-20. [Медлайн]. [Полный текст].
[Директива] Campsall PA, Laupland KB, Niven DJ. Тяжелая менингококковая инфекция: обзор эпидемиологии, диагностики и лечения. Клиника интенсивной терапии . 2013 июл.29 (3): 393-409. [Медлайн].
Welch SB, Nadel S. Лечение менингококковой инфекции. Арка Дис Детский . 2003 июл.88 (7): 608-14. [Медлайн]. [Полный текст].
Wang X, Theodore MJ, Mair R, Trujillo-Lopez E., du Plessis M, Wolter N, et al.Клиническая проверка мультиплексных ПЦР в реальном времени для выявления возбудителей бактериального менингита. Дж. Клин Микробиол . 2012 Март 50 (3): 702-8. [Медлайн].
[Рекомендации] Крам-Цианфлон Н. Профилактика и борьба с менингококковой инфекцией: рекомендации по применению менингококковых вакцин у педиатрических пациентов. Инфекция Дис Тер . 2016. 116 (2): 89-112. [Медлайн].
[Рекомендации] Профилактика менингококковой инфекции и борьба с ней. MMWR Рекомендуемая Репутация . 2013 22 марта. 62: 1-22. [Медлайн].
Хорино Т., Като Т., Сато Ф., Сакамото М., Накадзава И., Йошида М. и др. Менингококцемия без менингита в Японии. Медицинский работник . 2008. 47 (17): 1543-7. [Медлайн].
Поллард А.Дж., Надел С., Нинис Н., Фауст С.Н., Левин М. Экстренное ведение менингококковой инфекции: восемь лет спустя. Арка Дис Детский . 2007 апр. 92 (4): 283-6. [Медлайн]. [Полный текст].
Zughaier SM.Капсульные полисахариды Neisseria meningitidis вызывают воспалительные реакции через TLR2 и TLR4-MD-2. Дж Лейкок Биол . 2011 Март 89 (3): 469-80. [Медлайн]. [Полный текст].
Coureuil M, Join-Lambert O, Lécuyer H, Bourdoulous S, Marullo S, Nassif X. Патогенез менингококкемии. Колд Спринг Харб Перспект Мед . 1 июня 2013 г. 3 (6): [Medline].
Brandtzaeg P, van Deuren M. Классификация и патогенез менингококковых инфекций. Методы Мол Биол . 2012. 799: 21-35. [Медлайн].
Brozna JP. Реакция Шварцмана. Семенной тромб Hemost . 1990 Октябрь 16 (4): 326-32. [Медлайн].
Livorsi DJ, Stenehjem E, Stephens DS. Факторы вирулентности грамотрицательных бактерий при сепсисе с акцентом на Neisseria meningitidis. Contrib Microbiol . 2011. 17: 31-47. [Медлайн].
Plant L, Sundqvist J, Zughaier S, Lovkvist L, Stephens DS, Jonsson AB.Структура липоолигосахаридов способствует множеству стадий вирулентности Neisseria meningitidis. Заражение иммунной . 2006 Февраль 74 (2): 1360-7. [Медлайн]. [Полный текст].
Sanders MS, van Well GT, Ouburg S, Morré SA, van Furth AM. Полиморфизм Toll-подобного рецептора 9 связан с переменными тяжести в когорте выживших после менингококкового менингита. BMC Инфекция Дис . 2012 11 мая, 12:12. [Медлайн].
Патан Н., Фауст С. Н., Левин М.Патофизиология менингококкового менингита и сепсиса. Арка Дис Детский . 2003 июл.88 (7): 601-7. [Медлайн]. [Полный текст].
Faust SN, Levin M, Harrison OB, Goldin RD, Lockhart MS, Kondaveeti S, et al. Дисфункция активации эндотелиального протеина С при тяжелом менингококковом сепсисе. N Engl J Med . 2001, 9 августа. 345 (6): 408-16. [Медлайн].
Pathan N, Hemingway CA, Alizadeh AA, Stephens AC, Boldrick JC, Oragui EE, et al.Роль интерлейкина 6 в дисфункции миокарда при менингококковом септическом шоке. Ланцет . 2004 17 января. 363 (9404): 203-9. [Медлайн].
Pathan N, Williams EJ, Oragui EE, Stephens AC, Levin M. Изменения оси рецептора интерлейкина-6 / растворимого интерлейкина-6 при менингококковом септическом шоке. Crit Care Med . 2005 августа 33 (8): 1839-44. [Медлайн].
Bergounioux J, Coureuil M, Belli E, Ly M, Cambillau M, Goudin N, et al.Экспериментальные доказательства бактериальной колонизации коронарного русла человека и ткани миокарда во время менингококкемии. Заражение иммунной . 1 августа 2016 г. [Medline].
MacLennan J, Kafatos G, Neal K, Andrews N, Cameron JC, Roberts R, et al. Социальное поведение и менингококковое носительство у британских подростков. Emerg Infect Dis . 2006 июн. 12 (6): 950-7. [Медлайн]. [Полный текст].
Фабер Дж., Хеннингер Н., Финн А., Зенц В., Зепп Ф, Кнуф М.Вариант toll-подобного рецептора 4 связан с летальным исходом у детей с инвазивным менингококковым заболеванием. Акта Педиатр . 2009 Март 98 (3): 548-52. [Медлайн].
Jansen AG, Sanders EA, VAN DER Ende A, VAN Loon AM, Hoes AW, Hak E. Инвазивное пневмококковое и менингококковое заболевание: связь с вирусом гриппа и активностью респираторно-синцитиального вируса ?. Эпидемиол. Инфекция . 2008 ноябрь 136 (11): 1448-54. [Медлайн]. [Полный текст].
Fijen CA, Kuijper EJ, te Bulte MT, Daha MR, Dankert J.Оценка дефицита комплемента у пациентов с менингококковой инфекцией в Нидерландах. Клин Инфекция Дис . 1999, 28 января (1): 98-105. [Медлайн].
MacNeil JR, Blain AE, Wang X, Cohn AC. Текущая эпидемиология и тенденции развития менингококковой инфекции — США, 1996-2015 гг. Клин Инфекция Дис . 2018 г. 3 апреля. 66 (8): 1276-1281. [Медлайн].
Бактериальный менингит. CDC. Доступно на http://www.cdc.gov/meningitis/bacterial.html. 2015; Доступ: май 2015 г.
[Рекомендации] Cohn AC, MacNeil JR, Clark TA, Ortega-Sanchez IR, Briere EZ, Meissner HC, et al. Профилактика менингококковой инфекции и борьба с ней: рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Рекомендуемая Репутация . 2013 22 марта. 62 (RR-2): 1-28. [Медлайн].
Ортега-Санчес И.Р., Мельцер М.И., Шепард С., Зелл Э., Мессонье М.Л., Билуха О. и др. Экономика кампании догоняющей вакцинации подростков против менингококковой инфекции в США. Клин Инфекция Дис . 2008 г. 1. 46 (1): 1-13. [Медлайн].
Кэти К., Левин М, Фауст С.Н. Применение лекарств при остром менингококковом заболевании. Arch Dis Детское обучение, изд. . 2008 Октябрь 93 (5): 151-8. [Медлайн].
Mbaeyi SA, Джозеф SJ, Blain A, Wang X, Hariri S, MacNeil JR. Менингококковая инфекция среди молодых людей студенческого возраста: 2014-2016 гг. Педиатрия . 143 (1) января 2019 г .: [Medline].
Аткинсон Б., Ганди А., Балмер П.История вспышек менингококковой инфекции в США: значение для вакцинации и профилактики заболеваний. Фармакотерапия . 2016 августа 36 (8): 880-92. [Медлайн].
Marshall GS, Dempsey AF, Srivastava A, Isturiz RE. Студенты колледжей США подвергаются повышенному риску менингококковой инфекции серогруппы B. J Детский инфекционный Dis Soc . 2019 11 мая. [Medline].
Soeters HM, Whaley M, Alexander-Scott N, Kanadanian KV, MacNeil JR, Martin SW, et al.Оценка менингококкового носительства в ответ на вспышку менингококковой инфекции серогруппы B и кампанию массовой вакцинации в колледже Род-Айленда, 2015-2016 гг. Клин Инфекция Дис . 2017 15 апреля. 64 (8): 1115-1122. [Медлайн].
Хосе Франсиско Сантос Н., Вивиан Матос Ф., Кэролайн Алвес Ф., Марта Сильва М.С., Лейла Карвалью С. Распространенность носительства Neisseria meningitidis в Америке в 21 веке: систематический обзор. Браз Дж. Инфекция Дис .22 июля 2019 г. [Medline].
Tappero JW, Reporter R, Wenger JD, Ward BA, Reeves MW, Missbach TS, et al. Менингококковая инфекция в округе Лос-Анджелес, Калифорния, и среди мужчин в окружных тюрьмах. N Engl J Med . 1996, 19 сентября. 335 (12): 833-40. [Медлайн].
Brundage JF, Ryan MA, Feighner BH, Erdtmann FJ. Менингококковая инфекция среди военнослужащих США в связи с рутинным использованием вакцин с различными компонентами, специфичными для серогрупп, 1964–1998 гг. Клин Инфекция Дис . 2002 декабрь 1. 35 (11): 1376-81. [Медлайн].
Саймон М.С., Вайс Д., Гулик РМ. Инвазивная менингококковая инфекция у мужчин, практикующих секс с мужчинами. Энн Интерн Мед. 2013 20 августа. 159 (4): 300-1. [Медлайн].
Bozio CH, Blain A, MacNeil J, Retchless A, Weil LM, Wang X и др. Эпиднадзор за менингококковой инфекцией среди МСМ — США, 2015-2016 гг. MMWR Morb Mortal Wkly Rep .2018, 28 сентября. 67 (38): 1060-1063. [Медлайн].
Миллер Л., Аракаки Л., Рамаутар А., Бодач С., Браунштейн С.Л., Кеннеди Дж. И др. Повышенный риск инвазивной менингококковой инфекции среди людей с ВИЧ. Энн Интерн Мед. 2014 7 января. 160 (1): 30-7. [Медлайн].
Сейвар Дж. Дж., Джонсон Д., Попович Т., Миллер Дж. М., Даунс Ф., Сомсел П. и др. Оценка риска лабораторного менингококкового заболевания. Дж. Клин Микробиол . 2005 сен.43 (9): 4811-4. [Медлайн].
Rosenstein NE, Perkins BA, Stephens DS, Lefkowitz L, Cartter ML, Danila R, et al. Изменяющаяся эпидемиология менингококковой инфекции в США, 1992–1996 гг. Дж. Заразить Дис . 1999 декабрь 180 (6): 1894-901. [Медлайн].
Центры по контролю и профилактике заболеваний (CDC). Уведомление для медицинских работников: выявление и сообщение о менингококковой инфекции серогруппы B, связанной со вспышками, в Принстонском университете и Калифорнийском университете в Санта-Барбаре.Доступно по адресу http://emergency.cdc.gov/han/han00357.asp. 27 ноября 2013 г .;
Уайлдер-Смит А. Менингококковое носительство W135 в связи с паломничеством в хадж 2001 г .: опыт Сингапура. Int J Антимикробные агенты . 2003 21 февраля (2): 112-5. [Медлайн].
Wilder-Smith A, Barkham TM, Earnest A, Paton NI. Приобретение менингококкового носителя W135 у паломников хаджа и передача его домашним контактам: проспективное исследование. BMJ . 2002, 17 августа. 325 (7360): 365-6. [Медлайн]. [Полный текст].
Wilder-Smith A, Chow A, Goh KT. Возникновение и исчезновение менингококковой инфекции W135. Эпидемиол. Инфекция . 2010 июль 138 (7): 976-8. [Медлайн].
Hart CA, Cuevas LE. Менингококковая инфекция в Африке. Энн Троп Мед Паразитол . 1997 Октябрь 91 (7): 777-85. [Медлайн].
Vyse A, Wolter JM, Chen J, Ng T, Soriano-Gabarro M.Менингококковая инфекция в Азии: недооцененное бремя общественного здравоохранения. Эпидемиол. Инфекция . 2011 15.1-19 апреля. [Медлайн]. [Полный текст].
Ladhani SN, Giuliani MM, Biolchi A, Pizza M, Beebeejaun K, Lucidarme J, et al. Эффективность менингококковой вакцины B против эндемического гипервирулентного штамма Neisseria meningitidis W, Англия. Emerg Infect Dis . 2016 22 февраля (2): 309-11. [Медлайн].
Инвазивная менингококковая инфекция в Англии: ежегодные лабораторно подтвержденные отчеты за эпидемиологический период с 2017 по 2018 год.Общественное здравоохранение Англии. Доступно по адресу https://assets.publishing.service.gov.uk/government/uploads/system/uploads/attachment_data/file/751821/hpr3818_IMD.pdf. 26 октября 2018 г .; Дата обращения: 13 августа 2019 г.
Шарип А., Сорвильо Ф., Ределингс М.Д., Маскола Л., Мудрый М., Нгуен Д.М. Популяционный анализ смертности от менингококковой инфекции в США: 1990-2002 гг. Педиатр Инфекция Дис. J . 2006 25 марта (3): 191-4. [Медлайн].
Christensen H, May M, Bowen L, Hickman M, Trotter CL.Менингококковое носительство по возрасту: систематический обзор и метаанализ. Ланцет Инфекция Дис . 2010 декабрь 10 (12): 853-61. [Медлайн].
Моура А.С., Паблос-Мендес А., Лейтон М., Вайс Д. Эпидемиология менингококковой инфекции, Нью-Йорк, 1989–2000. Emerg Infect Dis . 2003 марта 9 (3): 355-61. [Медлайн]. [Полный текст].
Kaplan SL, Schutze GE, Leake JA, Barson WJ, Halasa NB, Byington CL, et al. Многоцентровое наблюдение за инвазивными менингококковыми инфекциями у детей. Педиатрия . 2006 Октябрь 118 (4): e979-84. [Медлайн].
Дартон Т., Гивер М., Нейлор С., Джек Д.Л., Качмарски Э.Б., Заем Р. и др. Тяжесть менингококковой инфекции, связанная с бактериальной нагрузкой в геноме. Клин Инфекция Дис . 2009 г. 1. 48 (5): 587-94. [Медлайн].
Bouneb R, Mellouli M, Regaieg H, Majdoub S, Chouchène I, Boussarsar M. Менингококцемия, осложненная миокардитом, у 16-летнего молодого человека: описание случая. Пан Афр Мед J . 2018. 29: 149. [Медлайн].
Gawalkar AA, Tale S, Chhabria BA, Bhalla A. Миокардит и молниеносная пурпура при менингококкемии. QJM . 2017 г. 1. 110 (11): 755-756. [Медлайн].
Зейдан А., Тарик С., Фальтас Б., Урбан М., МакГроди К. Случай первичного менингококкового перикардита, вызванного Neisseria meningitidis серотипа Y, с быстрой эволюцией в тампонаду сердца. Дж. Интерн. Мед. Наук . 2008 сен.23 (9): 1532-5. [Медлайн]. [Полный текст].
Vienne P, Ducos-Galand M, Guiyoule A, Pires R, Giorgini D, Taha MK и др. Роль отдельных штаммов Neisseria meningitidis при менингококковом артрите, перикардите и пневмонии. Клин Инфекция Дис . 2003 15 декабря. 37 (12): 1639-42. [Медлайн].
Вонг Дж. С., Балакришнан В. Эндогенный эндофтальмит Neisseria meningitidis: клинический случай и обзор литературы. J Педиатр, офтальмол, косоглазие .1999 май-июнь. 36 (3): 145-52. [Медлайн].
Гарсия Н.С., Каштелу Дж.С., Рамос В., Резенде Г.С., Перейра FE. Частота миокардита при смертельной менингококковой инфекции у детей: наблюдения за 31 случаем, изученным при вскрытии. Rev Soc Бюстгальтеры Med Trop . 1999 сентябрь-октябрь. 32 (5): 517-22. [Медлайн].
Борг Дж., Кристи Д., Коэн П. Г., Буй Р., Винер Р. М.. Исходы менингококковой инфекции в подростковом возрасте: проспективное когортное исследование. Педиатрия . 2009 Март 123 (3): e502-9. [Медлайн].
Buysse CM, Raat H, Hazelzet JA, Hulst JM, Cransberg K, Hop WC, et al. Долгосрочный статус здоровья детей, переживших менингококковый септический шок. Арх Педиатр Адолеск Мед . 2008 ноябрь 162 (11): 1036-41. [Медлайн].
Buysse CM, Oranje AP, Zuidema E, Hazelzet JA, Hop WC, Diepstraten AF, et al. Долговременное рубцевание кожи и ортопедические последствия у лиц, переживших менингококковый септический шок. Арка Дис Детский . 2009 Май. 94 (5): 381-6. [Медлайн].
Стивенс Д.С., Гринвуд Б., Брандцег П. Эпидемический менингит, менингококкемия и Neisseria meningitidis. Ланцет . 30 июня 2007 г., 369 (9580): 2196-210. [Медлайн].
Feldman HA. Менингококковые инфекции. Расширенный медицинский центр . 1972. 18: 117-40. [Медлайн].
Thimmesch M, Bodart E, Gavage P, Misson JP, Frère J. [Два отчета о случаях менингококкемии.Обзор литературы по хронической менингококкемии. Арх. Педиатр . 23 июня 2016 г. (6): 595-8. [Медлайн].
Feldman HA. Менингококковые инфекции. Расширенный медицинский центр . 1972. 18: 117-40. [Медлайн].
Durand ML, Calderwood SB, Weber DJ, Miller SI, Southwick FS, Caviness VS Jr, et al. Острый бактериальный менингит у взрослых. Обзор 493 серий. N Engl J Med . 1993, 7 января. 328 (1): 21-8. [Медлайн].
Parmentier L, Garzoni C, Antille C, Kaiser L, Ninet B, Borradori L.Ценность нового анализа Neisseria meningitidis — специфической полимеразной цепной реакции в образцах биопсии кожи в качестве диагностического инструмента при хронической менингококкемии. Арка Дерматол . 2008 июнь 144 (6): 770-3. [Медлайн].
Periappuram M, Тейлор MR, Кин CT. Быстрое обнаружение менингококков из петехий при острой менингококковой инфекции. J Заражение . 1995 31 ноября (3): 201-3. [Медлайн].
Arend SM, Lavrijsen AP, Kuijken I, van der Plas RN, Kuijper EJ.Проспективное контролируемое исследование диагностической ценности биопсии кожи у пациентов с предполагаемой менингококковой инфекцией. Eur J Clin Microbiol Infect Dis . 2006 25 октября (10): 643-9. [Медлайн].
Долан Томас Дж., Хэтчер С.П., Саттерфилд Д.А., Теодор М.Дж., Бах М.С., Линскотт К.Б. и др. ПЦР в реальном времени на основе sodC для обнаружения Neisseria meningitidis. PLoS Один . 2011 5 мая. 6 (5): e19361. [Медлайн]. [Полный текст].
Guarner J, Greer PW, Whitney A, Shieh WJ, Fischer M, White EH, et al.Патогенез и диагностика менингококковой инфекции человека с использованием иммуногистохимического анализа и ПЦР. Ам Дж. Клин Патол . 2004 ноябрь 122 (5): 754-64. [Медлайн].
Фернандес-Родригес А., Алькала Б., Альварес-Лафуэнте Р. Обнаружение Neisseria meningitidis в фиксированных формалином тканях после внезапной смерти в режиме реального времени с помощью полимеразной цепной реакции. Диагностика микробиологических инфекций . 2008 апр. 60 (4): 339-46. [Медлайн].
Bryant PA, Li HY, Zaia A, Griffith J, Hogg G, Curtis N, et al.Проспективное исследование высокочувствительной, специфической и клинически полезной ПЦР в реальном времени для диагностики менингококковой инфекции у детей. Дж. Клин Микробиол . 2004 июл.42 (7): 2919-25. [Медлайн]. [Полный текст].
de Filippis I, do Nascimento CR, Clementino MB, Sereno AB, Rebelo C, Souza NN, et al. Быстрое обнаружение Neisseria meningitidis в спинномозговой жидкости с помощью одностадийной полимеразной цепной реакции гена nspA. Диагностика микробиологических инфекций .2005 Февраль 51 (2): 85-90. [Медлайн].
Линь Х.В., Инь Дж. Х., Ло Дж. П., Ван Й. Х., Ли Си, Лу Дж. Дж. Использование универсального анализа полимеразной цепной реакции и расщепления эндонуклеазами для быстрого обнаружения Neisseria meningitides. Дж. Микробиол Иммунол Инфекция . 2004 Декабрь 37 (6): 371-4. [Медлайн].
Ричардсон, округ Колумбия, Луи Л., Луи М., Симор А.Е. Оценка экспресс-анализа ПЦР для диагностики менингококкового менингита. Дж. Клин Микробиол .2003 г., 41 (8): 3851-3. [Медлайн]. [Полный текст].
Агентство по охране здоровья. Руководство по ведению общественного здравоохранения при менингококковой инфекции в Великобритании. [Полный текст].
van de Beek D, Cabellos C, Dzupova O, Esposito S, Klein M, Kloek AT, et al. Рекомендации ESCMID: диагностика и лечение острого бактериального менингита. Клин Микробиол Инфекция . 2016 май. 22 Приложение 3: С37-62. [Медлайн].
Sprung CL, Annane D, Keh D, Moreno R, Singer M, Freivogel K, et al.Гидрокортизонотерапия у больных септическим шоком. N Engl J Med . 2008, 10 января. 358 (2): 111-24. [Медлайн].
Яешке Р., Ангус, округ Колумбия. Жизнь в условиях неопределенности в отделении интенсивной терапии: следует ли лечить пациентов с сепсисом стероидами ?. ЯМА . 2009 г. 10 июня. 301 (22): 2388-90. [Медлайн].
Tuncer AM, Gur I, Ertem U, et al. Цефтриаксон один раз в день при менингококкемии и менингококковом менингите. Педиатр Инфекция Дис. J .1988 7 октября (10): 711-3. [Медлайн].
Hart CA, Cuevas LE. Менингококковая инфекция в Африке. Энн Троп Мед Паразитол . 1997 Октябрь 91 (7): 777-85. [Медлайн].
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов. Цефтриаксон (продается как роцефин), информация . 2008: [Полный текст].
Рош. Важное разъяснение предписывающей информации. Противопоказания. http://www.rocheusa.com. Доступно по адресу http: // www.gene.com/gene/products/information/rocephin. Доступ: 28 июня 2012 г.
Агентство по регулированию лекарственных средств и изделий медицинского назначения. цефтриаксон; несовместимость с растворами, содержащими кальций . 2008: [Полный текст].
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов. Цефтриаксон (продается как роцефин) Информация. http://www.fda.gov. Доступно по адресу http://www.fda.gov/Cder/drug/infopage/ceftriaxone/default.htm. Доступ: апрель 2009 г.
Eliakim-Raz N, Lador A, Leibovici-Weissman Y, Elbaz M, Paul M, Leibovici L.Эффективность и безопасность левомицетина: возрождение старых антибиотиков? Систематический обзор и метаанализ рандомизированных контролируемых исследований. J Антимикробный препарат Chemother . 2015 Апрель 70 (4): 979-96. [Медлайн].
Brouwer MC, McIntyre P, de Gans J, Prasad K, van de Beek D. Кортикостероиды при остром бактериальном менингите. Кокрановская база данных Syst Rev . 2010 8 сентября. CD004405. [Медлайн].
Herrera R, Hobar PC, Гинзбург CM.Хирургическое вмешательство при осложнениях молниеносной пурпуры, вызванной менингококковой инфекцией. Педиатр Инфекция Дис. J . 1994 13 августа (8): 734-7. [Медлайн].
Besner GE, Klamar JE. Искусственная кожа Integra в качестве полезного дополнения при лечении молниеносной пурпуры. J Средство от ожогов Rehabil . 1998 июл-авг. 19 (4): 324-9. [Медлайн].
Файбис С., Видмер Р., Сапир С., Перец Б., Шапира Дж. Менингококковая септицемия и стоматологические осложнения: обзор литературы и два отчета о случаях. Инт Дж. Педиатр Дент . 2005 г., май. 15 (3): 213-9. [Медлайн].
Aaberge IS, Oster P, Helland OS, Kristoffersen AC, Ypma E, Høiby EA, et al. Комбинированное введение менингококковой вакцины везикул наружных мембран серогруппы B и конъюгированной вакцины серогруппы C, показанное для профилактики менингококкового заболевания, является безопасным и иммуногенным. Клин Диаг Лаборатория Иммунол . 2005 г., май. 12 (5): 599-605. [Медлайн]. [Полный текст].
Bethell D, Pollard AJ.Менингококковые вакцины. Вакцины Эксперт Рев . 2002 Июнь 1 (1): 75-84. [Медлайн].
Поллард А.Дж. Глобальная эпидемиология менингококковой инфекции и эффективность вакцин. Педиатр Инфекция Дис. J . 2004 г., 23 декабря (12 доп.): S274-9. [Медлайн].
Браун Т. ACIP обновляет рекомендации по вакцине против менингококка B. Medscape. Доступно на http://www.medscape.com/viewarticle/880617. 25 мая 2017 г .; Доступ: 1 июня 2017 г.
[Рекомендации] Паттон М.Э., Стивенс Д., Мур К., Макнил Дж. Р.Обновленные рекомендации по применению менингококковой вакцины MenB-FHbp серогруппы B — Консультативный комитет по практике иммунизации, 2016 г. MMWR Morb Mortal Wkly Rep . 2017 г. 19 мая. 66 (19): 509-513. [Медлайн].
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Первая вакцина, одобренная FDA для предотвращения менингококковой инфекции серогруппы B. Доступно по адресу http://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm420998.htm. 29 октября 2014 г .;
[Руководство] Комитет по инфекционным заболеваниям Американской академии педиатрии.Обновленные рекомендации по применению менингококковых вакцин. Педиатрия . 2014 Август 134 (2): 400-3. [Медлайн].
Такер МЭ. Новая менингококковая вакцина рекомендована для младенцев из группы высокого риска. Медицинские новости Medscape. 24 января 2013 г. Доступно по адресу http://www.medscape.com/viewarticle/778124. Доступ: 5 февраля 2013 г.
Менингококковая вакцинация младенцев: Рекомендации и обоснование Консультативного комитета по практике иммунизации (ACIP). MMWR Morb Mortal Wkly Rep . 2013 25 января. 62: 52-4. [Медлайн].
Brown T. ACIP OKs вакцина против менингита (Menveo) для младенцев из группы высокого риска. Медицинские новости Medscape. Доступно на http://www.medscape.com/viewarticle/813066. Доступ: 28 октября 2013 г.
Харрисон Л. Х., Шатт К. А., Арнольд К. Э., Стерн Э. Дж., Пондо Т., Кильбаух Дж. А. и др. Менингококковое носительство среди старшеклассников Джорджии и Мэриленда. Дж. Заразить Дис . 2015 июн 1.211 (11): 1761-8. [Медлайн].
Basta NE, Mahmoud AA, Wolfson J, Ploss A, Heller BL, Hanna S, et al. Иммуногенность вакцины против менингококка B во время университетской вспышки. N Engl J Med . 2016 21 июля. 375 (3): 220-8. [Медлайн].
Обновление: синдром Гийена-Барре среди реципиентов конъюгированной менингококковой вакцины Menactra — США, июнь 2005 г. — сентябрь 2006 г. MMWR Morb Mortal Wkly Rep . 2006 20 октября. 55 (41): 1120-4.[Медлайн].
[Руководство] Обновленные рекомендации по использованию конъюгированных менингококковых вакцин — Консультативный комитет по практике иммунизации (ACIP), 2010. MMWR Morb Mortal Wkly Rep . 2011 28 января. 60 (3): 72-6. [Медлайн].
Fraser A, Gafter-Gvili A, Paul M, Leibovici L. Профилактическое использование антибиотиков для профилактики менингококковых инфекций: систематический обзор и метаанализ рандомизированных исследований. Eur J Clin Microbiol Infect Dis .2005 24 марта (3): 172-81. [Медлайн].
Дэвисон К.Л., Рамзи Мэн. Эпидемиология острого менингита у детей в Англии и Уэльсе. Арка Дис Детский . 2003 августа 88 (8): 662-4. [Медлайн]. [Полный текст].
Агентство по охране здоровья. Инвазивные менингококковые инфекции, Англия и Уэльс, лабораторные отчеты: 51-52 недели / 2007 г. . [Полный текст].
Батиста Р.С., Гомес А.П., Дутра Газинео Дж.Л., Бальбино Мигель П.С., Сантана Л.А., Оливейра Л. и др.Менингококковая инфекция, клинический и эпидемиологический обзор. Азиатский Пак Джей Троп Мед . 2017 10 ноября (11): 1019-1029. [Медлайн].
Jarva H, Ram S, Vogel U, Blom AM, Meri S. Связывание ингибитора комплемента C4bp с Neisseria meningitidis серогруппы B. Дж. Иммунол . 2005 15 мая. 174 (10): 6299-307. [Медлайн].
Нкоси Дж., Такрар А., Кумар К., Ахмади Р., Фанг Т., Литвин М. и др. Менингококковый миоперикардит серотипа Y. Диагностика микробиологических инфекций . 2009 Февраль 63 (2): 223-7. [Медлайн].
Aiuto LT, Barone SR, Cohen PS, Boxer RA. Рекомбинантный тканевый активатор плазминогена восстанавливает перфузию у молниеносной менингококковой пурпуры. Crit Care Med . 1997 июн.25 (6): 1079-82. [Медлайн].
Derkx B, Wittes J, McCloskey R. Рандомизированное плацебо-контролируемое исследование HA-1A, человеческого моноклонального антитела к эндотоксину, у детей с менингококковым септическим шоком.Европейская группа исследования педиатрического менингококкового септического шока. Клин Инфекция Дис . 1999, 28 апреля (4): 770-7. [Медлайн].
Ривард Г.Е., Дэвид М., Фаррелл С., Шварц ХП. Лечение молниеносной пурпуры при менингококкемии концентратом протеина С. J Педиатр . 1995 апр. 126 (4): 646-52. [Медлайн].
de Kleijn ED, de Groot R, Hack CE, Mulder PG, Engl W., Moritz B, et al. Активация протеина C после инфузии концентрата протеина C у детей с тяжелым менингококковым сепсисом и молниеносной пурпурой: рандомизированное двойное слепое плацебо-контролируемое исследование по подбору доз. Crit Care Med . 31 июня 2003 г. (6): 1839-47. [Медлайн].
Надел С., Гольдштейн Б., Уильямс М.Д., Далтон Х., Петерс М., Масиас В.Л. и др. Дротрекогин альфа (активированный) у детей с тяжелым сепсисом: многоцентровое рандомизированное контролируемое исследование III фазы. Ланцет . 2007 10 марта. 369 (9564): 836-43. [Медлайн].
Левин М., Квинт П.А., Гольдштейн Б., Бартон П., Брэдли Дж. С., Шеми С. Д. и др. Рекомбинантный бактерицидный белок, повышающий проницаемость (rBPI21), в качестве дополнительного лечения детей с тяжелым менингококковым сепсисом: рандомизированное исследование.rBPI21 Группа изучения менингококкового сепсиса. Ланцет . 2000 16 сентября. 356 (9234): 961-7. [Медлайн].
Винсент Дж. Л., Абрахам Э., Аннан Д., Бернар Дж., Риверс Э., Ван ден Берге Г. Снижение смертности при сепсисе: новые направления. Центр внимания . 2002 г., 6, приложение 3: S1-18. [Медлайн]. [Полный текст].
Day KM, Haub N, Betts H, Inwald DP. Гипергликемия связана с заболеваемостью менингококковым сепсисом у детей в критическом состоянии. Медицинский центр для педиатров . 2008 9 ноября (6): 636-40. [Медлайн].
Лицензирование конъюгированной менингококковой вакцины для детей в возрасте от 2 до 10 лет и обновленное руководство по бустерной дозе для подростков и других лиц с повышенным риском менингококковой инфекции — Консультативный комитет по практике иммунизации (ACIP), 2011. MMWR Morb Mortal Wkly Rep . 2011 5 августа. 60 (30): 1018-9. [Медлайн].
Лицензирование конъюгированной менингококковой вакцины (Menveo) и руководство по применению — Консультативный комитет по практике иммунизации (ACIP), 2010 г. MMWR Morb Mortal Wkly Rep . 2010 марта 12, 59 (9): 273. [Медлайн].
Вакцины против Haemophilus influenzae типа b (Hib) и менингококковой серогруппы C (MenC) для детей — Информационный бюллетень. Доступно по адресу http://www.dh.gov.uk/en/Publicationsandstatistics/Publications/PublicationsPolicyAndGuidance/DH_106052. Дата обращения: 07.08.2011.
Обновленные рекомендации по использованию конъюгированных менингококковых вакцин — Консультативный комитет по практике иммунизации (ACIP), 2010 г. MMWR Morb Mortal Wkly Rep . 2011 28 января. 60 (3): 72-6. [Медлайн].
Endler G, Marculescu R., Starkl P, et al. Полиморфизмы в кластере генов интерлейкина-1 у детей и молодых людей с системной менингококкемией. Clin Chem . 2006 Март 52 (3): 511-4. [Медлайн].
Пресс-релиз FDA. FDA одобряет первую вакцину для предотвращения менингококковой инфекции у младенцев и детей ясельного возраста. 22 апреля 2011 г. Доступно по адресу http: // www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm252392.htm. Доступ: 27 апреля 2011 г.
Миллер Л., Аракаки Л., Рамаутар А. и др. Повышенный риск инвазивной менингококковой инфекции среди людей с ВИЧ. Энн Интерн Мед. 2013 29 октября. [Medline].
Razminia M, Salem Y, Elbzour M, Teves D, Deshmukh H, Khosla S. Важность ранней диагностики и терапии острого менингококкового миокардита: клинический случай с обзором литературы. Am J Ther . 2005 май-июнь. 12 (3): 269-71. [Медлайн].
[Рекомендации] Рекомендация Консультативного комитета по практике иммунизации (ACIP) по использованию четырехвалентной менингококковой конъюгированной вакцины (MenACWY-D) среди детей в возрасте от 9 до 23 месяцев с повышенным риском инвазивной менингококковой инфекции. MMWR Morb Mortal Wkly Rep . 2011, 14 октября. 60 (40): 1391-2. [Медлайн].
Вакнин Ю. Риск менингококковой инфекции у людей с ВИЧ в 10 раз выше. Медицинские новости Medscape . 30 октября 2013 г. [Полный текст].
Менингококцемия — обзор | Темы ScienceDirect
Поддерживающая терапия
Менингококкемия часто осложняется сосудистым коллапсом и шоком. Нередки случаи мультисистемной органной недостаточности. Менингококковый ЛПС является мощным токсином и запускает каскад событий, характеризующихся высвобождением множества провоспалительных цитокинов. 105 Girardin и соавторы 106 продемонстрировали, что сывороточные концентрации фактора некроза опухоли-α (TNF-α), интерлейкина-1 (IL-1) и интерферона-γ (INF-γ) коррелируют с тяжестью менингококкемии. у детей.Waage и соавторы 105, 107–109 тщательно изучали эту проблему во время недавних эпидемий в Норвегии. Ясно, что высокие сывороточные концентрации IL-6 и IL-1 связаны с летальным исходом у детей. IL-1 был обнаружен исключительно у пациентов с высокими концентрациями IL-6, TNF-α и LPS и быстро летальным исходом. Обширная активация комплемента также происходит при молниеносной менингококкемии. Продукты активации комплемента в сочетании с другими медиаторами могут способствовать мультисистемной органной недостаточности и смерти в тяжелых случаях.Несмотря на эти новые знания, дополнительная терапия специфическими поликлональными или моноклональными антителами к провоспалительным цитокинам остается исследовательской на момент написания этой статьи и имеет недоказанную пользу при молниеносной менингококкемии. 110 Несмотря на предположение, что синдром Уотерхауса-Фридериксена частично опосредован кровоизлиянием в надпочечники, использование кортикостероидов остается спорным. Хотя кортикостероиды могут быть полезными при некоторых формах бактериального менингита, высокие дозы связаны с худшим исходом при сепсисе и септическом шоке.При подозрении на инвазивную менингококковую инфекцию лучше избегать кортикостероидов. 111 Кроме того, не рекомендуется рутинное использование гепарина в терапии ДВС-синдрома. Некоторые специалисты рекомендуют гепарин, если у пациента активно кровотечение; Польза этого подхода остается недоказанной и может быть вредной. 9, 112, 113 Однако введение гепарина, по-видимому, уменьшило осложнения некроза пальцев и конечностей, ужасного осложнения, у небольшой неконтролируемой группы пациентов с молниеносной пурпурой 114 и заслуживает дальнейшего оценка.Другие серьезные опасные для жизни процессы, такие как почечная недостаточность; системный ацидоз; острый респираторный дистресс-синдром; менингококковая пневмония; нозокомиальная пневмония из-за аспирации; и неврологические осложнения, включая кому, несахарный диабет и повышенное внутричерепное давление, могут потребоваться в острой фазе. Очевидно, что к этим проблемам лучше всего подойти в условиях отделения интенсивной терапии. 4, 9, 98–100 Во время эпидемий такие осложнения могут легко перегрузить ресурсы общественного здравоохранения в условиях ограниченных ресурсов.Перикардит может незаметно развиться в фазе выздоровления. Менингококки обычно не обнаруживаются в перикардиальной жидкости, и тампонада сердца встречается редко. 52
Несмотря на агрессивную поддерживающую терапию и назначение соответствующих противомикробных препаратов, исход для пациентов с фульминантной менингококкемией часто оказывается неблагоприятным. Методика, заслуживающая дальнейшего изучения, — это плазмаферез. Этот метод был опробован, хотя и в крайне ограниченном масштабе, у отчаянно больных пациентов и может привести к быстрому снижению сывороточных концентраций TNF-α и повышению показателей смертности и заболеваемости. 115 Хотя контролируемые клинические испытания не проводились, результаты у тяжелобольных пациентов, изученных в этих испытаниях, намного лучше, чем ожидалось, по сравнению с историческим контролем. Веновенозная диафильтрация или экстракорпоральная мембранная оксигенация также использовались, по-видимому, с некоторым успехом, при менингококкемии, 116, 117 , но эти методы также остаются экспериментальными в настоящее время. Однако введение N-концевого фрагмента рекомбинантного белка, увеличивающего бактерицидную проницаемость (rBPI21), улучшает функциональный исход детей с менингококкемией, но исследование было недостаточно масштабным, чтобы выявить положительный эффект в отношении смертности. 118
Менингококкемия приводит к глубокому снижению концентрации сывороточного протеина С. Введение рекомбинантного протеина C может ограничить степень некроза тканей (и снизить смертность), 119 , но необходимы дополнительные данные. Этот метод дорогостоящий, что исключает возможность его использования во многих областях.
Оценены прогностические показатели исходов от менингококкемии. Одна система, разработанная Корнелиссом и его коллегами, основанная на сывороточных концентрациях калия, тромбоцитов и С-реактивного белка, а также на избытке оснований, предсказывает выживание или смерть у 86% пациентов. 120
Наконец, менингококкемия связана с сверхнормальными концентрациями в плазме ингибитора активатора плазминогена (PAI-1). Дети с функциональным полиморфизмом делеции / вставки (46–56) в промоторной области PAI-1 вырабатывают более высокие концентрации и подвергаются повышенному риску коагулопатии и смерти от менингококкемии. 121
Менингококковая пневмония: обзор | Пневмония
Пневмония, вызванная Neisseria meningitidis (менингококк), впервые была описана Якобицем в 1907 году у пациентов с пневмонией, у которых N.meningitidis был выделен из образцов мокроты [1]. Первыми случаями были солдаты, делящие бараки, которые, вероятно, были инфицированы от одного индексного пациента [2]. Интересно, что даже много лет назад Якобиц признал, что здоровые люди могут содержать N. meningitidis в своих ротоглотках, так что выделение микроорганизма не может обеспечить окончательный клинический диагноз менингококковой пневмонии [1, 2]. Во время пандемии гриппа 1918–1919 гг. Было описано большое количество случаев менингококковой пневмонии у пациентов, перенесших первичную вирусную инфекцию [3].С момента описания этих первоначальных случаев в нескольких исследованиях, сериях случаев, а также во множестве сообщений о случаях были описаны случаи менингококковой пневмонии, встречающейся преимущественно у подростков, взрослых и пожилых людей [2]. Совсем недавно Фоссен и его коллеги, изучив литературу, смогли выявить 344 случая, зарегистрированных в Северной и Южной Америке, Европе, Австралии и Азии в период с 1906 по 2015 год [2]. Эти авторы также отметили, что при обзоре национальных обследований заболеваемости инвазивной менингококковой инфекцией (IMD) пневмония была отмечена как наиболее частое неврологическое заболевание органов, встречающееся в 66 из 364 случаев (17% случаев).В этом контексте пневмония, связанная с менингококковой инфекцией, может быть первичной, если она возникает сама по себе без признаков ранее существовавшего менингита или менингококкемии [4], но также может возникать в связи или как осложнение обоих этих состояний и / или при других проявлениях менингококковой инфекции. Опубликованные в литературе случаи менингококковой пневмонии включают как первичные, так и ассоциированные пневмонии. Однако не все авторы описывают случаи отдельно, поэтому часто бывает трудно отличить истинные первичные инфекции в литературе.
Neisseria meningitidis
Микроорганизм
N. meningitidis (менингококк) представляет собой грамотрицательный аэробный диплококк. Он имеет типичную форму фасоли или почек и является облигатным патогеном человека [5,6,7]. Микроорганизм часто колонизирует ротоглотку или носоглотку даже у здоровых людей, но может также колонизировать другие части тела [7]. Микроорганизм хорошо растет на шоколаде и кровяном агаре при температуре от 35 до 37 ° C в атмосфере 5–10% углекислого газа [8, 9], а подтверждение наличия этого микроорганизма в клинических образцах проводится по результатам серии углеводных ферментаций [8].Микроорганизм обладает рядом факторов вирулентности (см. Ниже), включая полисахаридную капсулу. Хотя эта капсула важна для защиты микроорганизмов от комплемент-опосредованного фагоцитоза и лизиса, она также позволяет дифференцировать 13 серогрупп микроорганизма, из которых серогруппы A, B, C, W, X и Y в значительной степени ответственны за заболевания человека. [5,6,7].
Эпидемиология менингококковой инфекции
Хотя менингококковая инфекция широко распространена во всем мире, эпидемиология этого состояния варьируется в разных географических регионах, эволюционировала и изменялась с течением времени [10,11,12,13,14].Заболевание может возникать в виде спорадических случаев, вспышек или крупных эпидемий [11]. Эпидемии с большим числом инфицированных пациентов периодически возникают в регионе Африки к югу от Сахары (часто называемом «поясом менингита») с периодичностью от пяти до 10 лет [5,6,7]. Однако в таких странах, как Бразилия, он, как правило, носит эндемический характер с периодическими эпидемиями [7]. В развитом мире инфекция, как правило, носит эндемический характер и несколько ограничена [5,6,7], хотя в таких странах, как Соединенные Штаты (США), наблюдалось увеличение вспышек, а также изменение серогрупп. часто вызывает инфекцию [5, 14].
Распределение различных серогрупп варьируется как во времени, так и географически, что может объяснять различные клинические проявления инфекции в регионах и хронологически [7, 11]. Важно отметить, что знание распределения серотипов в различных регионах необходимо для разработки программ вакцинации [5]. В зависимости от сезона инфекции чаще встречаются зимой или ранней весной. Эндемические инфекции возникают в основном у детей в возрасте до 10 лет, тогда как во время эпидемических инфекций инфицируется широкий возрастной диапазон пациентов [7].В целом инфекция чаще встречается у мужчин, но у пациентов старше 50 лет чаще встречается у женщин [7]. Что касается передачи, развитие IMD связано с недавним приобретением патогенного штамма восприимчивым человеком, чаще всего в результате тесного физического контакта [8].
Факторы риска менингококковой инфекции
Факторы риска пациента
Возраст является важным фактором риска менингококковой пневмонии, которая возникает в основном у пожилых людей старше 50 лет и является наиболее частым проявлением IMD у лиц старше 65 лет. , в отличие от менингококкового менингита, который встречается преимущественно у детей и подростков [2, 15].Однако более свежие данные свидетельствуют о том, что возрастное распределение менингококковой пневмонии является бимодальным и возникает в возрасте до 30 лет и после 60 лет [2]. Хотя все серогруппы менингококка могут вызывать пневмонию, менее распространенные серогруппы патогена участвуют чаще, как обсуждается ниже [2, 8].
К другим факторам риска IMD относятся курение, дефицит иммуноглобулина и комплемента, аспления, дефицит маннозосвязывающего лектина и другие генетические аномалии [2, 16, 17] и, возможно, инфекция, вызванная вирусом иммунодефицита человека (ВИЧ) [15, 18, 19] .Дополнительные факторы риска включают тесный контакт с пациентами, у которых есть менингококковая инфекция, людьми, живущими в непосредственной близости (например, призывниками [как упоминалось выше], студентами университетов и людьми, совершающими хадж), а также предшествующий грипп и другие респираторные вирусные и бактериальные инфекции. в том числе вызванные Haemophilus influenzae и Streptococcus pneumoniae [16, 17, 19, 20]. Уинстед в своей серии случаев менингококковой пневмонии, собранных за 25-летний период, отметил сопутствующую вирусную инфекцию, а также лежащую в основе лимфому, множественную миелому, астму, хроническую обструктивную болезнь легких (ХОБЛ), инсулинозависимый сахарный диабет и другие формы заболевания. сахарный диабет, системная красная волчанка, ВИЧ-инфекция, серповидноклеточная анемия, ишемическая болезнь сердца / пациенты с шунтированием коронарной артерии и цирроз печени среди его пациентов [19].Эти факторы риска приведены в таблице 1.
Таблица 1 Возможные факторы риска инвазивного менингококкового заболевания и / или менингококковой пневмонии
Конкретные серогруппы менингококка
Исследования показали, что частота серогруппы Y, которая ранее была относительно редкой в Европе, остается высокой или увеличивается в некоторых регионах страны. на континенте [21], причем ряд исследований и клинических случаев указали на связь серогруппы Y с менингококковой пневмонией [22,23,24,25,26].В Англии и Уэльсе в период с 2007 по 2009 год было выявлено все большее число лабораторно подтвержденных случаев IMD, вызванных серогруппой Y, при этом было обнаружено, что клональный тип cc174 связан с неменингеальным заболеванием, особенно пневмонией, у пожилых (> 65 лет) [22]. Среди инфицированных серогруппой Y средний возраст начала заболевания был самым высоким у пациентов с пневмонией (86,1 года [IQR 69,9–90,0] по сравнению с 42,8 [IQR 14,4–71,7]; p <0,0001). Люди с пневмонией чаще имели сопутствующие заболевания (13/19 [68%] по сравнению с 12/46 [26%]; p = 0.001), тогда как летальность была значительно выше от пневмонии, чем от менингита (9/19 [47%] против 2/22 [9%]), сепсиса (1/17 [6%]) или других состояний (без смертельных исходов). . После поправки на возраст было установлено, что основные заболевания и пневмония (OR 7,0; 95% ДИ 1,4–36,4; p = 0,020) были независимо связаны со смертью. Инфекции, вызванные серогруппой Y, также значительно увеличились в Швеции в период с 1995 по 2012 год: в одном ретроспективном обсервационном исследовании 175 пациентов было документально подтверждено наличие пневмонии у 34 (19%) пациентов, либо отдельно, либо в связи с другим очагом инфекции [26].В этом исследовании самая высокая смертность была для случаев бактериемии с неизвестным фокусом (13%), тогда как смертность для случаев пневмонии составила 9%.
Ряд исследований и клинических случаев из США также подтвердили важность серогруппы Y как причины менингококковой пневмонии, либо самой по себе, либо связанной с другими формами менингококковой инфекции [27,28,29]. Дополнительные исследования в армии США [30,31,32] и Финляндии [33] также подтвердили, что серогруппа Y является причиной менингококковой пневмонии.В одной серии из 12 случаев первичной менингококковой пневмонии, зарегистрированных в США, инфекция серогруппы Y была зарегистрирована в двух случаях, что подтверждено радиологическими данными о пневмонии и выделением микроорганизма при посеве крови [30]. В другом таком исследовании менингококковая инфекция серогруппы Y возникла у 88 новобранцев ВВС США, 68 из которых страдали первичной бактериальной пневмонией, что гораздо чаще, чем менингококкемия или менингит [31]. Все случаи в конечном итоге хорошо отреагировали на терапию антибиотиками.В финском исследовании молниеносный случай менингококковой пневмонии, осложненный сепсисом, перикардитом и плевральным выпотом, побудил исследовать распределение серогрупп менингококка в посевах из носоглотки среди новобранцев из того же отделения [33]. В исследовании документально подтверждено, что 14 из 31 (46%) культивированных изолятов относятся к серогруппе Y, почти полностью выделены от лиц, вакцинированных против серогрупп A и C. также отметили, что серогруппа W-135 связана с пневмонией, особенно у пожилых пациентов [34,35,36,37,38,39,40,41].Последнее исследование, общенациональное ретроспективное исследование, в котором анализировались эпидемиологические данные 115 пациентов с лабораторно подтвержденным менингококковым заболеванием, показало, что на серогруппу W-135 приходилось 26% всех случаев и что большинство пациентов (76,7%) были старше 20 лет. лет [41]. Не было обнаружено различий в представленных характеристиках, кроме более высокой распространенности пневмонии у пациентов с инфекцией W-135 (23,8% против 1,5%; OR 20,6; 95% ДИ 2,3–189,0; p = 0,003) [41]. Наконец, в отчете о клиническом случае из США описан 16-летний студент с клиническими признаками и рентгенологическими данными, совместимыми с пневмонией, который при посеве мокроты выявил менингококк серогруппы B [42].
Патогенез
Колонизация ротоглотки Neisseria meningitidis
Как указано Laver et al., Neisseria meningitidis «является одним из немногих потенциальных патогенов, которые могут незаметно колонизировать ротоглотку, представляющую ее носоглотку. биологическая ниша »[43]. По оценкам, частота колонизации ротоглотки этим исключительно человеческим патогеном составляет около 10–35% и 5,9% взрослых и детей, соответственно [44]. Как упоминалось выше, уровень колонизации значительно увеличивается как при активном курении сигарет, так и при воздействии побочного табачного дыма [45,46,47], вероятно, как следствие опосредованного дымом подавления врожденных и адаптивных иммунных механизмов дыхательных путей [48] , 49].Сигаретный дым также напрямую влияет на респираторные патогены, что приводит к усилению механизмов бактериальной вирулентности, в частности к увеличению образования биопленок [50,51,52].
Наиболее важные факторы вирулентности менингококка в отношении колонизации носоглотки включают протеазу иммуноглобулина A1 (IgA1) и антифагоцитарную полисахаридную капсулу, а также ряд связывающих эпителий бактериальных адгезинов. Протеаза IgA1, которая наиболее важна для людей, ранее подвергавшихся воздействию, представляет собой сайт-специфичную сериновую протеазу.Он расщепляет молекулу антитела в шарнирной области, разделяя области Fab и Fc, предотвращая изгнание патогена за счет мукоцилиарного клиренса, способствуя прикреплению к респираторному эпителию [53]. Также было высказано предположение, что менингококковая протеаза IgA1 может иметь более широкую, чем предполагалось ранее, субстратную специфичность, включая другие иммунно-ассоциированные белки, такие как рецептор фактора некроза опухоли типа II [54] и ассоциированный с лизосомами мембранный белок человека [55].
Несмотря на свою главную роль в противодействии фагоцитозу, полисахаридная капсула менингококка отталкивает слизь, что также препятствует мукоцилиарному клиренсу [56].Капсульные полисахариды четырех из шести основных серогрупп, связанных с инвазивным заболеванием, в частности серогрупп B, C, W и Y, состоят из производных сиаловой кислоты. Капсулы других инвазивных групп, серогрупп A и X, состоят из повторяющихся единиц O-ацетилированного (α1 → 6) -связанного N-ацетил-D-маннозамин-1-фосфата [57] и (α-1 → 4 ) N -ацетилглюкозамин-1-фосфат [58] соответственно. Сиаловые кислоты также присутствуют в гликоконъюгатах клеточной поверхности эукариотических клеток и защищают не только клетки-хозяева, но и те менингококковые серогруппы с капсулами, содержащими сиаловую кислоту, от атаки альтернативного пути комплемента через связывание основного регуляторного белкового фактора H ( fH), что достигается за счет ингибирования C3-конвертазы и инактивации C3b [59].
Следующий этап колонизации носоглотки менингококком включает прикрепление возбудителя к респираторному эпителию, процесс, который требует уменьшения размера капсулы, чтобы обнажить лежащие в основе белковые адгезины. Первоначальный контакт между патогеном и эпителием опосредуется пилями IV типа; это сложные структуры, состоящие из более чем двадцати белков, которые вносят вклад в формирование полностью функционального адгезина, при этом компоненты PilE и PilV играют важную роль в адгезии [60, 61].Однако идентичность рецептора эпителиальных клеток, на который нацелены пилусы Типа IV, остается неуловимой. Возможным соперником, идентифицированным в эндотелиальных клетках головного мозга, является CD147 (также известный как EMMPRIN или индуктор металлопротеиназы внеклеточного матрикса) [62]. Хотя он также экспрессируется на эпителиальных клетках, участие CD147 в прикреплении менингококка к респираторному эпителию, опосредованному ворсинками IV типа, остается неопределенным.
Тип IV, опосредованное пилисными эпителиями, обеспечивает последующее более прочное связывание, опосредованное менингококковыми белками помутнения, Opa и Opc [60].Opa нацелена на рецептор клеточной адгезии карциноэмбрионального антигена (CEACAM) на эпителии, в основном на рецептор CEACAM1 [63], в то время как Opc, как сообщается, связывается с активированным витронектином на эндотелиальных клетках [64], также присутствующим на эпителии. Различные минорные адгезины, такие как NadA (Neisseria adhesin A), также вносят вклад в прикрепление эпителия, и они были подробно описаны в другом месте [60].
Достигнув потенциально враждебной среды носоглотки, менингококк использует несколько стратегий для обеспечения устойчивости.Как показали экспериментальные системы, это, во-первых, инфицирование эпителиальных клеток патогеном и внутриклеточная выживаемость, что требует восстановления инкапсулированного фенотипа [65]. Во-вторых, менингококк также сохраняется в носоглотке за счет заключения в биопленку [66]. В этих условиях внеклеточная дезоксирибонуклеиновая кислота (ДНК) представляет собой главный структурный компонент менингококковых биопленок, способствуя связыванию поверхностных белков и других внеклеточных полимеров с образованием эффективных многоклеточных биопленок [66].
Транслокация менингококка в нижние дыхательные пути
Несмотря на распространение в легкие через кровоток или от человека к человеку при вдыхании загрязненных аэрозольных капель, микроаспирация менингококков, заключенных в биопленку, находящихся в носоглотке, является наиболее вероятным механизмом. транслокации менингококка в нижние дыхательные пути [2]. В этом последнем контексте следует отметить, что недавняя инфекция вирусом гриппа, в частности, а также предшествующий фарингит, были связаны с развитием менингококковой пневмонии [67, 68, 69].
Учитывая кажущуюся меньшую вирулентность менингококка по сравнению с таковой у продуцирующих экзотоксин бактериальных респираторных патогенов, таких как Streptococcus pneumoniae, Staphylococcus aureus и Pseudomonas aeruginosa , менингококку может потребоваться триггер для достижения полной патогенности. В этом контексте вирус гриппа является особенно эффективным партнером в отношении облегчения развития менингококковой пневмонии. Это было убедительно продемонстрировано на мышиной модели экспериментальной инфекции, в которой было обнаружено, что первоначальная инфекция вирусом гриппа A предрасполагает к последующему развитию менингококковой бактериемии [70].Механизмы, с помощью которых предшествующая вирусная инфекция гриппа может вызвать развитие менингококковой пневмонии, включают следующее: i) угнетение мукоцилиарного эскалатора [71]; ii) в случае штаммов менингококка, принадлежащих к группе капсульных полисахаридов, содержащих сиаловую кислоту, вирусная нейраминидаза опосредует расщепление капсульной сиаловой кислоты, обнажая лежащие в основе бактериальные адгезины, способствуя адгезии к респираторному эпителию [61]; и iii) связанные с вирусной инфекцией повышенные уровни легочного интерферона-γ [70], которые вызывают подавление экспрессии поглотителя альвеолярных макрофагов класса A, MARCO (рецептор макрофагов с коллагеновой структурой) [72], опсонина, который активно связывает неопсонизированные Н.meningitidis через взаимодействие с неидентифицированными белковыми лигандами [73].
Попав в нижние дыхательные пути, менингококк использует ряд факторов вирулентности, которые позволяют патогену подавлять или отвлекать легочную защиту хозяина, что приводит к развитию тяжелой инфекции.
Механизмы вирулентности менингококка
Несмотря на полисахаридную капсулу и протеазу IgA1, менингококк обладает рядом дополнительных факторов вирулентности, которые обеспечивают выживание и распространение патогена в нижних дыхательных путях.Они включают:
Фактор H-связывающий белок (fHbp), поверхностный липопротеин массой 27 кДа, давно признанный ключевым фактором вирулентности менингококка, экспрессируется большинством вирулентных штаммов патогена [74]. Что касается его роли в бактериальной вирулентности, fHbp связывает главный регулятор альтернативного пути активации комплемента, fH, с бактериальной поверхностью, тем самым обеспечивая защиту от опосредованного комплементом опсонофагоцитоза и уничтожения бактерий [74].Кроме того, Porin A, один из двух менингококковых поринов, которые играют решающую роль в ионном обмене, также, как сообщается, ослабляет активацию классического пути комплемента посредством взаимодействия с C4b-связывающим белком [75];
Липоолигосахаридный эндотоксин (ЛОС) также является ключевым фактором вирулентности менингококка. Он расположен на внешней мембране менингококка и состоит из гидрофобного липидного компонента А, связанного с внешним гидрофильным олигосахаридом.Как и другие бактериальные эндотоксины, LOS обладает мощной провоспалительной активностью, опосредованной, прежде всего, посредством взаимодействия с комплексом Toll-подобного рецептора 4 / MD2 на клетках врожденной иммунной системы, что приводит к инициации MyD88-зависимого сигнального каскада и, как следствие, продукции спектр воспалительных цитокинов / хемокинов [76, 77]. Несмотря на потенциальную защиту, интенсивность LOS-активируемой воспалительной реакции, вероятно, приведет к повреждению легких, а также к дисфункции легочных адаптивных иммунных механизмов.Кроме того, высвобождение LOS, содержащегося во внеклеточных везикулах [78], может отвлекать иммунные механизмы, нацеленные на менингококки, одновременно усиливая вредные воспалительные реакции. Более того, связывание спонтанно высвобождаемых везикул наружной мембраны менингококка, как сообщается, предотвращает захват интактных организмов внеклеточными ловушками нейтрофилов in vitro [79];
Изменение размера капсулы также является стратегией, используемой менингококком для уклонения от адаптивных иммунных механизмов.В этом контексте следует отметить, что капсульные полисахариды серогрупп A, B, C, W и Y препятствуют активации классического пути комплемента, предотвращая отложение C4b после активации комплемента антикапсулярным полисахаридом IgG и Антитела IgM, а также через антагонизм связывания антител IgM, направленных против LOS [80]. Кроме того, слабая иммуногенность капсульного полисахарида менингококка серогруппы B также способствует вирулентности этой серогруппы патогена.
События, связанные с колонизацией ротоглотки и инвазией менингококка в нижние дыхательные пути, суммированы на рис. 1.
Рис. 1
Возможные стадии патогенеза менингококковой пневмонии
Клиническая картина
В то время как менингококковый менингит является наиболее частым проявлением менингококковой инфекции, первичная пневмония встречается примерно у 5-10% пациентов с менингококковой болезнью [6, 7].Клинические проявления менингококковой пневмонии неотличимы от пневмонии, вызванной другими инфекционными патогенами, и хотя такие симптомы, как лихорадка, озноб и плевритная боль в груди, встречаются более чем в 50% случаев, продуктивный кашель и одышка встречаются реже [2 ]. Сыпь может возникнуть у пациентов с пневмонией и ассоциированным сепсисом, но менингококкемия — редкое сопровождение пневмонии [2]. Ни лабораторные данные, ни рентгенологические особенности не позволяют дифференцировать пневмонию от других причин [2].
Серия случаев — IMD
В течение многих лет сообщалось о ряде серий случаев, описывающих либо менингококковое заболевание, из которого у некоторых пациентов была пневмония [15, 81, 82], либо, в частности, менингококковая пневмония [19, 83]. Стивенс и его коллеги провели проспективное популяционное наблюдение за взрослыми пациентами в Атланте, США, в период с 1 декабря 1988 г. по 30 ноября 1993 г., в ходе которого из обычно стерильных участков было выделено N. meningitidis [15]. В целом 14 из 44 взрослых (32%) имели пневмонию, синусит или трахеобронхит как вероятный источник бактериемии, при этом пневмония встречалась в 10/44 (23%) случаях.Семь из 10 случаев пневмонии были в возрасте > 50 лет, в то время как в группе 18–24 лет не было пневмонии. Серогруппы Y, W-135 и B были наиболее частыми причинами пневмонии, как описано в другом месте. Другое исследование IMD было проведено в округе Даллас, США, в период с 1992 по 1997 год [81]. Всего выявлен 151 пациент. Пожилые пациенты (> 50 лет) чаще болели пневмонией (32% против 4%; p = 0,0001) и реже болели менингитом (p = 0.0001) по сравнению с более молодыми пациентами. Среди пациентов с пневмонией наблюдалась тенденция к увеличению числа инфекций, вызванных серогруппой Y. Кроме того, Хазарика и его коллеги сообщили о вспышке IMD у детей в Индии в период с января 2008 г. по июнь 2009 г. [82]. Пневмония возникла в 6,4% случаев.
Серия случаев — менингококковая пневмония
Путч и его коллеги изучали госпитализированных пациентов с пневмонией в Кливленде, США, в течение двух периодов времени в 1968 году, взяв мокроту или аспират трахеи, которые были культивированы для оптимизации выделения N.meningitidis, , а также сыворотки острой и выздоравливающей крови [83]. Для определения уровня носительства патогена были получены посевы из горла и сыворотки у бессимптомных амбулаторных пациентов и посевы мокроты у госпитализированных пациентов без острой респираторной инфекции. Ставки носителей составляли 7 и 13% в начальный и второй периоды соответственно. В целом у 47 пациентов со средним возрастом 46 лет была острая пневмония с менингококком, выделенным из посева мокроты в 14 (30%) случаях. Кроме того, менингококк был выделен из посевов мокроты в семи из 23 случаев (30%) респираторной инфекции, отличной от пневмонии, но не у кого-либо из пациентов без респираторной инфекции.Преобладающей серогруппой у пациентов с пневмонией и без нее была серогруппа B. Винстед и его коллеги проанализировали 58 случаев менингококковой пневмонии всех возрастов, 50 из которых ранее были описаны в литературе, с добавлением восьми новых случаев [19]. Средний возраст составлял 57,5 года, и 27 (52,9%) были мужчинами. В целом, 29 случаев имели предшествующие сопутствующие заболевания (5 имели другие недавние или сопутствующие инфекции, 4 пациента имели сахарный диабет и 4 ХОБЛ, 3 пациента получали кортикостероиды [2 с астмой и 1 с системной красной волчанкой], 3 пациента имели миелому или лимфому и 2 случая имели ВИЧ-инфекцию).Были и другие, менее распространенные сопутствующие заболевания. Лихорадка, озноб и связанная с ними плевритная боль в груди наблюдались в> 50% случаев, тогда как продуктивный кашель и одышка встречались реже. Были отмечены различные рентгенологические данные, включая плевральный выпот у шести пациентов (13,3%). Наиболее частой изолированной серогруппой была Y (44%), за которой следовала W135 (19,2%). Использовались различные методы лечения антибиотиками. Осложнения включали септический шок у двух пациентов, в то время как абсцесс легкого, экссудативный плевральный выпот, остановка дыхания, перикардит и лекарственная нейтропения наблюдались у каждого пациента.Средний возраст пяти (8,62%) умерших пациентов был почти на 20 лет больше, чем у выживших.
Отчеты о случаях — менингококковая пневмония
Множество историй болезни пациентов всех возрастов с менингококковой пневмонией было опубликовано за годы из различных регионов мира, включая США [4, 20, 42, 84,85,86 , 87,88], Европа [24, 89,90,91,92,93,94,95,96,97], Великобритания [98, 99], Россия [100], Япония [101,102,103], Тайвань [ 104], Австралии [105], Южной Америки [106, 107] и Оман [69].Характеристики пациентов с менингококковой пневмонией были аналогичны характеристикам, описанным в других разделах этого обзора.
Другие респираторные синдромы
Менингококковые инфекции также описаны как вызывающие респираторные симптомы или состояния, отличные от внебольничной пневмонии. В одном тематическом исследовании описан пациент с менингококкемией, который первоначально проявлялся как неспецифический «гриппоподобный» синдром, а затем значительно ухудшился [108]. Фактически, проявление симптомов со стороны верхних дыхательных путей, таких как насморк и фарингит, вместе с лихорадкой и другими симптомами, является частым ранним проявлением менингита, особенно у детей, за которым впоследствии следуют классические признаки менингита или сепсиса [6]. .В одном исследовании, проведенном в крупной районной больнице общего профиля в Нидерландах, сообщалось о 46 изолятах N. meningitidis , культивируемых из респираторных секретов 44 пациентов, из которых у одного была пневмония, у 19 — острые респираторные инфекции, а у 18 — острые гнойные обострения хронического бронхита [ 109]. В остальных случаях, у всех была гнойная мокрота, наблюдались различные симптомы. N. meningitidis также был выделен в других исследованиях у пациентов с острым и хроническим бронхитом [110, 111] или другими типами не связанных с пневмонией инфекций нижних дыхательных путей [112].Более того, N. meningitidis также зарегистрировано как причина внутрибольничной пневмонии [113,114,115,116].
Среди респираторных осложнений, отмеченных у пациентов с менингококковой пневмонией, кавитационная легочная инфекция [117], плевральный выпот [118, 119] и эмпиема [120, 121], последний случай вызван резистентным к пенициллину N .meningitidis.
Лабораторная диагностика
Традиционные методы микробиологического посева, основанные на выделении менингококка из слюны или стерильных биологических жидкостей, обычно крови или плевральной жидкости, остаются краеугольным камнем лабораторной диагностики IMD [122].Однако очень вероятно, что менингококковая пневмония не диагностируется по нескольким причинам: i) пневмония часто клинически неотличима от других пневмоний, таких как пневмококковая пневмония; ii) мокрота недостоверна для диагностики, поскольку трудно отличить бессимптомных носителей ротоглотки от случаев пневмонии, вызванной менингококком; и iii) посевы крови относительно нечувствительны [2]. В последнем контексте частота положительных результатов посева крови при постановке диагноза менингококковой пневмонии варьируется от 6 до 79.3% [19, 31]. В случае подтверждения и доступности методы микробиологического культивирования могут быть подкреплены подходами на основе ПЦР, включая мультиплексную полимеразную цепную реакцию (ПЦР) для одновременного выявления менингококковой, пневмококковой инфекции и инфекции Haemophilus influenzae [122]. Также доступны тесты латексной агглютинации для обнаружения капсульных полисахаридов, специфичных для менингококковой группы, в моче и спинномозговой жидкости, но не в крови. Однако они имеют ограниченное диагностическое применение из-за высокой частоты ложноположительных результатов, а также из-за неспособности выявить менингококковую инфекцию серогруппы B, которая распространена во многих странах [122].
Лечение менингококковой пневмонии
До 1991 г. пенициллин был препаратом выбора для лечения менингококковых инфекций [2]. Однако с появлением в 1991 г. штаммов, устойчивых к пенициллину [123], в условиях высокой смертности, связанной с IMD, рекомендация по эмпирическому лечению была изменена на цефалоспорин третьего поколения [2]. Хотя это обычно не делается, но если обнаруживается чувствительность микроорганизмов к пенициллину, может быть рассмотрена терапия IMD высокими дозами пенициллина.Что касается изолятов менингококков с пониженной восприимчивостью к пенициллину, а также с развивающейся устойчивостью к другим антибиотикам, они были обнаружены в Испании, Европе, Южной Африке, США, Канаде и Бразилии [123,124,125,126,127,128,129,130,131], причем в последнем исследовании также сообщается об устойчивости к антибиотикам. менингококк на ципрофлоксацин. Альтернативные варианты лекарств включают меропенем (недоступность цефалоспорина третьего поколения), хлорамфеникол (при тяжелой аллергии на бета-лактам), азтреонам (если хлорамфеникол недоступен в случае тяжелой аллергии на бета-лактам) или фторхинолон, такой как моксифлоксацин (в настоящее время ограничено в США из-за учета устойчивости менингококков к фторхинолонам и отсутствия контролируемых исследований IMD) [7].
Хотя оптимальный режим лечения менингококковой пневмонии per se не определен, он, вероятно, аналогичен таковому для IMD [2]. Фактически, было отмечено, что в большинстве случаев менингококковая пневмония получали пенициллин до 1991 г., а в большинстве случаев — цефалоспорин после этой даты [19].
Кортикостероиды использовались в качестве дополнительной терапии у пациентов с менингитом, но их польза, по-видимому, очевидна при пневмококковом, а не менингококковом менингите.Соответственно, эти агенты обычно не рекомендуются в клинических условиях менингококковой инфекции [2, 132]. Хотя появляются новые данные о пользе дополнительной терапии кортикостероидами у пациентов с тяжелой внебольничной пневмонией, сообщений о возможной пользе кортикостероидов при тяжелой менингококковой пневмонии нет [2].
Профилактика
Химиопрофилактика
Химиопрофилактика для устранения носоглотки рекомендуется при тесном контакте с больными менингококковой инфекцией, у которых риск заражения значительно повышен (в 400-800 раз выше, чем в общей популяции) [17 ].Используемые антибиотики включают рифампицин, цефтриаксон, азитромицин и фторхинолоны, хотя опасения по поводу устойчивости к антибиотикам окружают использование рифампицина и фторхинолонов [5, 7, 17]. Как указано в другом месте, были описаны внутрибольничные случаи менингококковой пневмонии, некоторые из которых, по-видимому, развились после контакта с пациентами с менингококковой пневмонией [114, 115]. В то время как рекомендации по профилактике основаны на исследованиях контактов со случаями менингита, эпидемиология менингококковой инфекции предполагает, что аналогичные преимущества можно увидеть и при химиопрофилактике в условиях контакта с больными менингококковой пневмонией [8].
Иммунизация
Профилактика тяжелой менингококковой инфекции в значительной степени основана на иммунопрофилактике менингококкового менингита. Как и в случае профилактики инвазивного пневмококкового заболевания, существуют два типа полисахаридных вакцин на основе менингококковых капсул. Во-первых, вакцины, которые состоят исключительно из капсульных полисахаридов, полученных из четырех основных вызывающих заболевание серогрупп менингококка, в частности A, C, Y и W-135, и, во-вторых, конъюгированные вакцины, в которых капсульные полисахариды химически связаны с подходящий иммуногенный белок-носитель, обычно дифтерийный анатоксин CRM197 [133].По данным Всемирной организации здравоохранения (ВОЗ), менингококковые полисахаридные вакцины бывают двухвалентными (серогруппы A и C), трехвалентными (серогруппы A, C и W-135) или четырехвалентными (A, C, Y, W-135) [133] . Однако, как и пневмококковые полисахаридные вакцины, очищенные капсульные полисахаридные вакцины, очищенные от менингококков, также слабо иммуногенны, неэффективны для очень молодых особей и не способствуют защите стада. Действительно, Санофи-Пастер недавно объявила о прекращении производства Menomune®, четырехвалентной полисахаридной вакцины, одобренной в 1981 г. Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) США для профилактики инвазивного менингококкового заболевания (серогруппы A, C, Y и W). -135) у лиц из группы высокого риска в возрасте от 2 лет и старше.
В настоящее время существует два основных типа менингококковой четырехвалентной конъюгированной вакцины. Это Menactra® и Menveo®, лицензированные в США в 2005 и 2010 годах соответственно. Оба содержат очищенные менингококковые полисахариды (A, C, Y и W-135), конъюгированные с CRM197. Аналогичная вакцина, Nimenrix®, содержащая те же капсульные полисахариды, конъюгированные с анатоксином столбняка в качестве белкового носителя, доступна за пределами США. По сравнению с вакцинами, содержащими только очищенные полисахариды, конъюгированные вакцины обладают повышенной иммуногенностью, подходят для использования у очень маленьких детей, предотвращают носительство и вызывают защиту стада [133].Однако недостаточный охват против серотипа B остается ограничением для этих вакцин.
Для решения этой проблемы были разработаны две новые капсульные вакцины на основе белка, не содержащие полисахаридов, специально нацеленные на серогруппу B N. meningitidis. Это Trumenba® (MenB-FHbp), лицензированный для использования в США в 2014 году, и Bexsero® (4CMenB), лицензированный в США, Канаде, Европе и Австралии, странах и регионах, в которых инвазивное заболевание вызвано N. meningitidis серогруппы . B остается серьезной проблемой.Trumenba®, производимый Wyeth Pharmaceuticals Inc., в первую очередь рекомендуется для иммунизации лиц из группы риска в возрасте ≥10–25 лет и состоит из двух рекомбинантных вариантов менингококкового поверхностного белка, fHBp [134, 135]. Bexsero®, производимая GlaxoSmithKline plc, представляет собой более сложную вакцину, которая состоит из трех рекомбинантных менингококковых белков серогруппы B в сочетании с везикулами внешней мембраны, полученными из штамма NZ98 / 254 группы B [136]. Из составляющих белков два из них, а именно.fHbp и гепарин-связывающий белок Neisseria (NHBA) представляют собой рекомбинантные слитые белки, а третий — интактный рекомбинантный белок адгезин, NadA. Везикулы, полученные из штамма NZ98 / 254, обогащены четвертым иммуногенным белком, PorA [136]. Как и Trumenba®, Bexsero® также рекомендуется для защиты лиц «группы риска» в возрасте ≥10–25 лет и продемонстрировал защитную эффективность в диапазоне примерно 64–78% у подростков и младенцев, будучи представленным в стране. программы иммунизации Соединенного Королевства и Ирландии [137 138 139 140].
Что касается новых потенциальных антигенов-кандидатов в вакцины, протеаза IgA1 менингококка, которая имеет ограниченное количество общих эпитопов с эпитопами своего пневмококкового аналога, показала многообещающую способность обеспечивать перекрестную защиту от обоих бактериальных патогенов при доклинической оценке. [141].
В таблице 2 описаны типы и области применения менингококковых вакцин.
Таблица 2 Типы и применение менингококковых вакцин
Смертность
Менингококковая пневмония имеет более высокий уровень летальности, чем менингококковый менингит (16% и 9–14% соответственно), с возрастом (самый высокий у пациентов старше 65 лет) возраста), конкретных серогрупп (выше среди штаммов серогруппы W, чем у штаммов серогруппы B) и основного заболевания, которые являются важными факторами риска, как и другие инфекции нижних дыхательных путей [2].



 Диагноз можно поставить за 4-8 часов. Предыдущая терапия антибиотиками меньше влияет на ПЦР-анализы.
Диагноз можно поставить за 4-8 часов. Предыдущая терапия антибиотиками меньше влияет на ПЦР-анализы. У детей, получавших rBPI, было меньше ампутаций и переливаний продуктов крови, а также улучшились функциональные результаты.
У детей, получавших rBPI, было меньше ампутаций и переливаний продуктов крови, а также улучшились функциональные результаты.