Бактериологическая диагностика анаэробной инфекции
Бактериологическая диагностика анаэробной инфекции
Анаэробные микроорганизмы, являясь представителями нормальной микрофлоры, в то же время они имеют потенциальные способности для развития инфекционного процесса практически в любом органе. Вследствие разных причин, например, при длительной терапии иммунодепрессантами, антибиотиками, а также в результате травмы, хирургического вмешательства, эти микроорганизмы попадают в кровяное русло, брюшную полость, различные органы и ткани и становятся причиной тяжелых гнойно-воспалительных процессов, сопровождающихся высокой смертностью, особенно при анаэробном сепсисе.
Важную роль анаэробы играют при развитии осложнений после хирургических вмешательств. В амбулаторной практике анаэробные инфекции с большой частотой встречаются у стоматологических, гинекологических больных, у женщин с отягощенным акушерским анамнезом.
Анаэробы являются участниками гнойно- воспалительных процессов, возникающих во всех отделах генитального тракта женщин. Их выделяют как единственного возбудителя или в составе ассоциации с аэробами при таких распространенных заболеваниях, как вагинит, вагиноз, послеродовый эндометрит. Установлена этиологическая роль анаэробов при возникновении воспалительных заболеваний придатков матки и околоматочного пространства, которые часто являются следствием абортов, инструментальных диагностических мероприятий, применения внутриматочных спиралей, хирургических вмешательств. Анаэробы также играют важную роль при возникновении пародонтоза — воспалительного процесса в тканях, прилегающих к зубам. По данным ВОЗ, около 95% взрослого населения планеты и 80% детей имеют признаки пародонтоза. Воспалительный процесс в тканях десны изначально возникает из-за массивных микробных скоплений и выделяемых ими ферментов и токсинов.
Бактериологическая диагностика при подозрении на анаэробную инфекцию весьма актуальна поскольку позволяет назначить наиболее эффективное лечение.
Принципы забора материала на исследование.
Материал для исследования следует брать по возможности до начала химиотерапии и лучше во время вскрытия или дренирования гнойного очага.
Особенно актуально проведение бактериологического анализа при неэффективности антимикробной терапии и при неблагоприятном течении заболевания и возникновении осложнений.
Отбор проб клинического материала при подозрении на анаэробную инфекцию и транспортировка этих образцов в бактериологическую лабораторию имеет ряд трудностей, связанных с необходимостью избежать агрессивного действия кислорода воздуха на строгие анаэробы.
Так как анаэробы являются представителями нормальной микрофлоры человека, материал для исследования следует брать с соблюдением правил асептики и строго с места локализации очага, чтобы исключить загрязнение посторонней микрофлорой.
Оптимальным способом получения проб материала является его аспирация с помощью шприца. Материал, забранный в шприц, должен быть доставлен в лабораторию для исследования в максимально короткий срок. Транспортные среды позволяют сохранить жизнеспособность анаэробных бактерий в течение достаточно продолжительного срока, указанного в инструкции.
Материал, забранный в шприц, должен быть доставлен в лабораторию для исследования в максимально короткий срок. Транспортные среды позволяют сохранить жизнеспособность анаэробных бактерий в течение достаточно продолжительного срока, указанного в инструкции.
Методы исследования.
Исследование клинического материала на анаэробы включает в себя все этапы культурального исследования, принятого в бактериологии, в том числе: выделение анаэробных микроорганизмов на искусственных питательных средах, изучение их свойств и идентификацию. Однако, учитывая физиологические особенности этой обширной группы микроорганизмов и их высокие питательные потребности, культивирование этих микробных патогенов представляется сложным и недоступным для большинства бактериологических лабораторий.
В лаборатории клинической микробиологии ГБУЗ НО «КДЦ» проводятся исследования на анаэробную инфекцию с использованием специального оборудования , импортных питательных сред и тест-систем для идентификации изучаемых микроорганизмов до рода и вида.
причины, симптомы, диагностика, лечение, профилактика
Представляет собой инфекционный процесс, возникающий при инфицировании спорообразующей или неспорообразующей флорой в благоприятных условиях для ее жизнедеятельности.
Причины
Анаэробная инфекция является естественной микрофлорой для слизистых оболочек, кожи, пищеварительного тракта, мочеполовых органов и по своим токсическим свойствам считается условно-патогенной. Эти микроорганизмы только в благоприятных условиях становится причиной возникновения эндогенной анаэробной инфекции.
В естественной среде эндогенные анаэробная инфекция содержится в почве, разлагающихся органических останках и способна вызывать патологические процессы при проникновении в рану из окружающей среды.
Степень патогенности инфекции зависит от количества приникших микроорганизмов в рану и биологических особенностей микроорганизма. Основная роль в развитии недуга отводится свойствам ферментов, которые вырабатывает микроорганизмы, эндо- и экзотоксинам и неспецифическим факторам метаболизма. Ферменты могут повышать вирулентность анаэробов, а также вызывать деструкцию мышечной и соединительной тканей. Иногда эндо- и экзотоксины могут вызывать повреждение эндотелия сосудов, внутрисосудистый гемолиз и тромбоз. Некоторые микроорганизмы вырабатывают токсины, которые способны вызывать повреждение почек, нервных волокон и сердечной мышцы.
Ферменты могут повышать вирулентность анаэробов, а также вызывать деструкцию мышечной и соединительной тканей. Иногда эндо- и экзотоксины могут вызывать повреждение эндотелия сосудов, внутрисосудистый гемолиз и тромбоз. Некоторые микроорганизмы вырабатывают токсины, которые способны вызывать повреждение почек, нервных волокон и сердечной мышцы.
Благоприятными условиями для развития анаэробной инфекции считается их проникновение в рану с дальнейшим проникновением ее в кровеносное русло, а также снижением окислительно-восстановительных способностей тканей. Проникновение анаэробной инфекции в полость нары может происходить при оперативном вмешательстве, инвазивных манипуляциях, прободении внутренних органов, ожогах, укусах животных, синдроме длительного сдавления, нарушении целостности кожи и слизистых, вызванных травмами.
Симптомы
Вене зависимости от локализации и типа возбудителя при анаэробной инфекции у пациентов отмечается резкая манифестация заболевания и типичное сочетание системных и местных симптомов. После инфицирования симптомы заболевания появляются у пациента на третий день или раньше.
После инфицирования симптомы заболевания появляются у пациента на третий день или раньше.
Практически у всех больных возникают признаки тяжелой интоксикации, и резко ухудшается состояние, еще до появления местных проявлений. У таких больных быстро нарастают симптомы лихорадки, возникает озноб, повышение температуры, также может отмечаться появление тошноты, слабости и головных болей. Иногда может отмечаться понижение артериального давления, учащение сердечного ритма, гемолитическая анемия, акроцианоз, желтушность кожи и склер.
В области проникновения инфекции возникает прогрессирующая распирающая боль, крапивница, эмфизема и газообразующие процессы, сопровождающиеся выделением резкого неприятного запаха, обусловленного выделением из раны метана, водорода и азота. Из раны может выделяться гнойно-кровянистый либо слизнево-гнойный секрет, который имеет неоднородный окрас и содержит в незначительном количестве вкрапления жира и газовых пузырьков.
Диагностика
При выявлении данной патологии особое значение имеет клиническая симптоматика, позволяющая заподозрить у больного наличие этого типа инфекции.
В связи с тем, что заболевание, вызванное анаэробной инфекцией, отличаются быстрым течением рекомендовано проведение экспресс-диагностики основанной на изучении отделяемого с окраской мазка по Грамму и проведении газожидкостной хроматографии. Таким больным назначается проведение общего и биохимического анализа крови, а также рентгенографическое исследование, позволяющее выявить скопление газа в пораженных тканях или полостях.
Лечение
Лечение анаэробной инфекции основано на полном удалении некротизированных тканей, проведении массивной антибактериальной и дезинтоксикационной терапии. Во многом эффективность терапии зависит от своевременности оказания хирургической помощи. После иссечения поврежденных тканей проводят промывание и дренирование гнойной полости либо тканей. В случае тяжелой деструкции тканей может потребоваться проведение ампутации конечности.
Профилактика
Профилактика анаэробной инфекции основана на предупреждении проникновения инфекции в рану, а также проведении качественной первичной хирургической обработке раневой поверхности.
Анаэробная инфекция: причины, симптомы и диагностика
Анаэробная инфекция – это токсическая раневая инфекция. Вызывает тяжелое состояние, при котором анаэробные микроорганизмы поражают мышечную и соединительную ткань с образованием гнилостного экссудата и газообразующих процессов.
Появляются быстро отмирающие ткани, некроз прогрессирует. Анаэробная инфекция относится к условно-патогенным микроорганизмам. Представляет собой большую опасность для жизни пациента. При несвоевременно оказанной медицинской помощи процент летального исхода высокий.
Причины заболевания
Размножение анаэробной инфекции происходит бесконтрольно. Благоприятной почвой для этого размножения выступают негативные экзогенные и эндогенные факторы. Нормальная микрофлора человека нарушается, развивается иммунодефицит, что приводит к различным заболеваниям.
Это может быть:
- Длительный прием антибактериальных или противовирусных препаратов;
- Инфицирование плода в утробе матери;
- Злоупотребление иммунодепрессантами;
- Загрязнение ран землей;
- Проникновение инфекции во время операций.

К сопутствующим заболеваниям, во время которых может развиться анаэробная инфекция, относятся сахарный диабет, опухоли и др.
Патогенные микроорганизмы могут находиться в виде спор в земле, на одежде человека, его коже.
Симптомы
Заболевание возникает внезапно с преобладанием симптомов общей интоксикации организма.
Наблюдается:
- Почернение раны;
- Лихорадка и сильный озноб;
- Спутанность сознания, головокружение;
- Развитие гипотонии и тахикардии;
- Диспепсия;
- Сильная жажда;
- Землистого оттенка покровы лица;
- Учащенное дыхание;
- Неровный пульс.
Вначале заболевания происходит заторможенность и апатия, которые сменяются нервозностью и возбуждением. Также заметно посинение вокруг носогубного треугольника.
Местные симптомы выражены отеком тканей вокруг раны, нестерпимой болью, гнойно-некротическим воспалением. В ранах при пальпации прощупывается наличие газа.
Такое воспаление нарастает быстро, прогрессирует. Если не принять срочные меры, произойдет быстрое отмирание тканей. В этом кроется главная опасность воздействия анаэробной инфекции, которую еще называют газовой гангреной.
Методы диагностики
В зависимости от состояния больного и тяжести заболевания назначается:
Важна дифференциация от рожистого воспаления, пневмоперитонеума, эритемы.
Лечение и осложнения
В лечении важна радикальная хирургическая обработка пораженного участка с широким рассечением его для удаления отмерших тканей. Проводится декомпрессия окружающих тканей, обязательное дренирование. Полости ран подлежат регулярному частому промыванию антисептическими растворами, специальной обработке.
Зачастую приходится проводить повторную некрэктомию. Если деструкция пораженного участка слишком большая и глубокая, проводится ампутация.
Главные составляющие в лечении:
- Интенсивная инфузионная терапия;
- Лечение антибиотиками широкого спектра действия;
- Гипербарическая оксигенация;
- Плазмаферез;
- Экстракорпоральная гемокоррекция;
- Введение противогангренозной сыворотки;
- Дезинтоксикация организма.

Также применяется физиотерапевтическое лечение. В основном это лазер и/или ультразвук, озонотерапия.
Лечение обязательно должно быть комплексным.
Профилактика
Именно полноценная первичная обработка раневой поверхности служит хорошей профилактикой против анаэробной или другой инфекции. Такая обработка должна проводиться в наиболее короткие сроки, лучше сразу после получения ранения.
Такие действия временно подавляют развитие болезнетворных микроорганизмов, развитие инфекционного процесса уменьшается.
Клиника, диагностика и лечение неклостридиальной анаэробной инфекции желчевыводящих путей в военных лечебных учреждениях
12 и 0 7 3
ВОЕННО-МЕДИЦИНСКАЯ ОРДЕНА ЛЕНИНА КРАСНОЗНАМЕННАЯ АКАДЕМИЯ ИМЕНИ С. М. КИРОВА
На правах рукописи
ДЖАЛАШЕВ
Яков Хачехпарович
КЛИНИКА, ДИАГНОСТИКА И ЛЕЧЕНИЕ НЕКЛОСТРИДИАЛЬ»НОЙ АНАЭРОБНОЙ ИНФЕКЦИИ ЖЕЛЧЕВЫВОДЯЩИХ ПУТЕЙ В ВОЕННЫХ ЛЕЧЕБНЫХ УЧРЕЖДЕНИЯХ
14. 00.27 — хирургия 03.00.07 — микробиология
00.27 — хирургия 03.00.07 — микробиология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени кандидата медицинских наук
САНКТ-ПЕТЕРБУРГ — 1992
Работа выполнена на кафедре хирургии Военно-медицинского факультета при Центральном институте усовершенствования врачей.
Научные р у к о в о д и т е л и: доктор медицинских наук профессор Э. А. Нечаев; доктор медицинских наук доцент В. И. Кочеровец.
О ф и ц и а л ь и ы е оппоненты: доктор медицинских «аук профессор П, Н. Зубарев; доктор медицинских наук В. Н. Чеботкевич.
Ведущая организация — Научный центр хирургии Российской ЛЛ1Н.
Защита диссертация состоится 1992 года
в часов на заседании специализированного совета Д 106.03.04 Во-
енно-медицинской ордена Ленина Краснознаменной академии имени С. М. Кирова (191175, Санкт-Петербург, К-175, ул. Лебедева, 6).
С диссертацией можно ознакомиться в фундаментальной библиотеке ВМсдА имени С. М. Кирова. *
М. Кирова. *
Автореферат разослан 1992 года.
Ученый секретарь специализированного совета доктор медицинских наук профессор Грицанов А. И,
ОЩЛЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы. Воспалительные заболевания хелчо-выводящих путей относятся к числу наиболее распрос ■•раненных среди хирургической патологии органов бровной полости. Возрастающее значение этих заболеваний на современной этапе развития хирургии обусловлено увеличением количества больных покилого и старческого возраста с многочисленными сопутствующими патологическими процессами, выраяешшми явлениями интоксикации» и летальными исходами, гнойно-септическими осложнениями бактериальной природы /Гостищев В.К. и соавт., 1988, Гринов М.В.,
1988, Буянов B.U. и соавт,, 1990, Королев Б.А., Пиковский
Д.Л., 1990, Савельев B.C., Гелъфавд Б.Р., 1990, Kelghley к „д. в. ‘1970, I’/oJoch У., 1982, Lycidßkis Ii. J., 1983, iVunro R., Sorrel T.C., 1986, Heisa П. et al., 1988/.
Усовершенствовала техники анаэробного культивирования позволило установить, что в возникновении и течении гнойно-воспалительных процессов желчевыводяпр« путей наряду с апроб-ной микрофлорой и клостридиями принимают участие неспорообра-зугоцие анаэробные бактерии /Петровский.Б.В. и соавт., 1984, Арикьянц М.С. и соавт., 1986, 1987, Минасян Л.А., Оганесян С.С., 1988, Земсков B.C. и соавт., 1989, Колесов А.П. и соавт.,
1989, П eisen М. L., Juete3en Т., 1975, Ь’пв1П111* IV„!., Rosenblatt J.К., 1977, Shinadu K. et al., 1977, 1?S1, Pitt H.A. et al., 1982, Sakacushi Y. et al., 1983, Gitgen-Cerru A. ot al.,
1986, Brooi: i,, 1669/. Однако целенаправленные исследования отечественных авторов, посвященные клииико-микробиологической диагностике и лечению неклостридиальной анаэробной инфекции гелчевыводшцих путей, представлены только несколькими работами /Шервашидзе Г.Г., 1986, Арикьянц И.С. и соавт., 1987, Дхо-робеков А. Д., 1988/.. …
Для большинства специалистов военных лечебных учреждений многие организационные и специальные вопросы данной проблемы остаются неизученными /Нечаев Э. А. и соавт., 1991/. Анализ ее состояния в военных лечебных учреждениях’показал, что:
А. и соавт., 1991/. Анализ ее состояния в военных лечебных учреждениях’показал, что:
— не всегда на должном методическом уровне проводится этиологическая диагностика и экспресс-диагностика неклостриди-альной анаэробной инфекции гепатобилиарной систем; ,
— отсутствуют обобщенные данные .об этнологической роли
неспорообразующих анаэробов у больных о различными формами воспалительных заболеваний билиарного тракта}
> — военные хирурги на располагают практическими критериями клинической диагностики неклостридиальной анаэробной инфекции желчевыводягцих путей и не используют их в повседневной работе;
— нэ изучен характер расстройств иммунного статуса у больных о гнойно-воспалительными заболеваниями желчевыводящих путей анапробноЯ этиологии из числа военнослужащих;
— схемы этиотропной антибактериальной терапии гнойных хирургически* инфекций желчевыводящих путей применяются без учета анаэробного компонента микрофлоры желчи;
— окончательно не решены вопросы тактики антибактериальной профилактики послеоперационных инфекционных осложнений при хирургическом лечении больных с деструктивным холециститом.
Все это определяет актуальность избранной темы и свидетельствует о необходимости проведения настоящего исследования.
Цели и задачи исследования. Целью работы явилось изучение роли неспорообразущих анаэробов в этиологии гнойно-воспалитель-М1х заболеваний желчевыводящих путей, выявление особенностей их клинического течения, разработка и оценка эффективности методов этиологической диагностики, экспресс-диагностики и этио-тропной антибактериальной терапии в военных лечебных учреждениях
Для достижения цели поставлены следующие задачи:
1. Установить роль неклостридиальных анаэробов в этиологической структуре воспалительных заболеваний хелчевг/водяцих путей и их гнойных осложнений,
2. Выявить клинические признаки и изучить особенности течения неклостридиальной анаэробной инфекции при воспалительной патологии билиарной системы.
3. Оценить информативность методов лабораторной экспресс-диагностики анаэробной инфекции органов гепатобилиарной системы в условиях практической работы хирургических отделений военных лечебных учреждений. их путей и гнойно-септическими осложнениями;
их путей и гнойно-септическими осложнениями;
— определена эффективность экспресс-диагностики неклостридиальной анаэробной инфекции методами экстренной бактериоскопии и парофаэной газовой хроматографии;
— установлен характер нарушений иммунитета у большее с анаэробным гнойным холангитом и деструктивным холециститом, выявлена зависимость этих расстройств с развитием послеоперационных инфекционных осложнений;
— предложены и апробированы схемы этиотропной антибактериальной терапии с воздействием на аэробные и аназробные возбудители гноЛно-воспалительных процессов яе лч о вшзодящих путей;
— обосновано использование целевых сочетаний антибактериальных препаратов в комплексе мер по предупреждению послеоперационных инфекционных осложнений в хирургии деструктивного холецистита.
Практическая ценность работы. Разработана и внедрена в клиническую практику система этиологической диагностики неклостридиальной анаэробной инфекции при воспалительных заболеваниях желчевыводящих путей и гнойных осложнениях.
В процессе выполнения работы доказана необходимость применения в военных лечебных учреждениях информативных, общедоступных и относительно простых экспресс-методов обнаружения неспо-рообразущих анаэробов: световой микроскопии и парофазной газовой хроматографии.
Установлено, что ориентировочная диагностика неклостридиальной анаэробной инфекции желчевнводящих путей может быть проведена по клиническим данным до получения результатов бактериологического анализа.
Ha основании бактериологических данных о лекарственной чувствительности микроорганизмов определены оптимальные варианты антибактериальной терапии при гнойной холангите и осложненном холецистите.
Разработан г Активный метод комбинированной антибактериальной профилактики послеоперационных инфекционных осложнений, позволивший практически в 2 раза снизить частоту раневой инфекции при хирургическом лечении деструктивного холецистита.
Результаты исследования позволили своевременно верифицировать этиологию инфекции желчевыводящих путай и обоснованно проводить в полном объема этиотропную терапия, что привело к существенному улучшению результатов лечения, сокращению сроков нетрудоспособности и пребывания больных в стационаре.
Основное положения, выносимые на защиту;
1. Участие неспорообразующих анаэробов в гнойно-воспалительных процессах желчевыводящих путей утяжеляет клиническое течение.
2. Неклостридиальная анаэробная инфекция желчевыводящих ггтей сопровождается развитием вторичного имыунодефицитного состояния. Выраженная степень иммунодефицита с преимущественный угнетением Т-клеточиого звена иммунитета является фактором риска возникновения послеоперационных гнойных осложнений.
3. Экспресс-диагностика неклостридиальной анаэробной инфекции органов гепатобилиарной системы с помощью экстренной бактериоскопии и парофазной газовой хроматографии вместе с клинической информацией позволяют в течение 20 ыин — 2 ч с точностью до 97-9Й< поставить правильный этиологический диагноз.
4. Включение в схемы антибактериальной терапии и профилактики анаэробоцидных препаратов улучшает результаты лечения больных с гнойно-воспалительными заболеваниями желчевыводящих путей и снижает количество послеоперационных нагноений ран при хирургическом лечении деструктивного холецистита.
Апробация работы и публикации. Материалы диссертации доложены на УП Всероссийском съезде хирургов «Актуальные вопросы абдоминальной хирургии» /Ленинград, 1989/, Всесоюзных конференциях «Проблемы клинической микробиологии в неинфекционной клинике» /Винница, 1983/, «Актуальные проблемы нозокомиальиых ин-
фекциЯ и лекарственной устойчивости микроорганизмов» /Минск, 1986/, «Актуальные проблемы химиотерапии бактериальное инфекций» /Москва, 1991/, Республиканском симпозиуме «Новые катоды диагностики и лечения гнойных хирургических заболепаний» /Андижан, 1983/, Республиканской конференции «Сепсис» /Тбилиси, 1984/, научной конференции «Иеоостридиальная анаяробная инфекция» /Ленинград, 1982/, XI научной конкуренции молол« ученых и специалистов акадеши /Ленинград, 1990/, научно-методической конференции, посвященной 10-летию кафедры хирургии ШедЗ при’ЦИУВ «Актуальные вопросы последипломной подготовки военных врачей /методология и клиника/» /Москва, 1990/, научно-методической конференции «Острый перитонит /вопроси диагностики, лечения и профилактики/» /Москва, 1991/.
. По теме диссертации опубликовано 20 печатных работ, в той числе 4 в центральных хирургических ;курналах и внедрено 10 рационализаторских предложешй.
Реализация работы. Комплекс разработанных приемов этиологической диагностики неклостридиалыюй анаэробной инфекции, тактика антибактериальной терапии и схет антибиотикопрофилак-гики применяются в практической работе при обследовании и лечении больных с гнойно-воспэлительнмш! заболеваниями органов гепатобилиарной систем в отделениях неотложной и абдошшальной хирургии ГШГ им.К.Н.Бурденко, ЦЕКГ км. А. А.Вишневского, ЦШГ, хирургических отделениях клиник ЕМГХ и общей хирургии ВДедА им. С.Н.Кирова. Основные положения диссертации используются при проведении занятий на кафедрах микробиологии ВМедА им. С.М.Кирова и хирургии К’ед’З при ЦИУВ.
Объем и структура диссертащш. Диссертационная работа состоит из введения, обзора литературы, главы с изложением рснов-ных сведений об «использованных методиках и характере обследованных больных, трех глав собственных исследований, заключения, выводов, практических рекомендаций и приложения. Материалы диссертации изложены на 147 страницах машинописного текста, иллюстрированы 40 рисунками и 13 таблицами. Список литературы содержит 99 работ отечественных и 191 зарубежных авторов.
Материалы диссертации изложены на 147 страницах машинописного текста, иллюстрированы 40 рисунками и 13 таблицами. Список литературы содержит 99 работ отечественных и 191 зарубежных авторов.
СОДЕРЖАНИЕ РАБОТЫ Материал и метода исследования. В основу настоящей работы
£ •/’ / ‘г
положены результаты обследования и лечения 252 больных с воспалительными заболеваниями келчевыводящих путей, находившихся н& стационарном лечении в клиниках К.1ГХ и общей хирургии ВМедА ии.С,М.Кирова, а также отделении неотложной хирургии ГВКГ им. Н.Н.Гурдонко. Под наблюдением было 126 больных с острым каль-кулозшм холециститом, 80 больных с хроническим калькулезныи холециститом и 46 больных с гнойным холангитом различной этиологии. Среди обследованных 157 /62,ЗХ/ были мужчины и 95 /37.7/-7 — женщины.Преобладание лиц мужского пола обусловлено контингентом больных военных лечебных учреждений. Значительная часть пациентов относилась к старшей возрастной группе, пред-ставлешюй офицерами в отставке. sac 12а» фирмы «Toshiba» /Япония/ в реальном масштабе времени, компьютерную томографию на аппарате «Somatom-2 » /ЗРГ/.
sac 12а» фирмы «Toshiba» /Япония/ в реальном масштабе времени, компьютерную томографию на аппарате «Somatom-2 » /ЗРГ/.
Биохимические исследования проводились общепринятыми методами и в процессе лечения на аппарате «тесЬпАсоп » /СШЛ/. Для характеристики эндогетюй интоксикации, динамики воспалительного процесса использовали подсчет лейкоцитарного индекса интоксикации /ЛШ/ по Я.Я.Кальф-Калифу /1941/ и опродолошю в плазме крови содержания молекул средней массы /ЖМ/ методом прямой спектрофотометрии надосадочной кидкости по Н.И.Габри-8лян /1981/.
Бактериологические исследования выполнены на кафедре микробиологии ВМедА им. С.М.Кирова и в бактериологической лаборатории ГШГ им.Н.Н.Бурденко. Материалом для исследования служили пузырная желчь и желчь гепатикохоледоха, содержимое пара-везикальных и холангиогеиных абсцессов, перптопеалышП вшот, гнойное раневое отдаляемое. Выделение и идентификацию из диагностического материала неспорообразукзщих анаоробов осуществляли с использованием строгой анаэробной техшки в соответствии с методическими рокомендацшми «Минздрава /Кочоровоц В. по1п1 *вг а!. /1965/;
по1п1 *вг а!. /1965/;
— фагоцитарной активности лейкоцитов /ФАЛ/ о рассчетоы показателя завершенности фагоцитоза /ГШ/ и фагоцитарного индекса /ФИ/ по методу В.Н.Бермана и Е.Н.Славской /1958/;
— теста восстановления нитросинего тетразолия /НСТ-теста/ по методике ь°.!!.ригк ег п1. /1968/;
— содержания лизоцима в сыворотке крови и Сд-фракции комплемента — методом нммунодифГузии в агар с использованием моноспецифических сывороток /ЧСЗР/;
— бактерицидной активности сыворотки крови /ЕАСК/ — по методике Е.Ф.Чериушенко и Л.С.Когосовой /1978/;
— циркулирующих иммунных комплексов /ЦИК/ в сыворотке крови по методике У.Навкоув ег а1. /1977/,
Гистологические исследования тканей стенки желчного пузыря и биоптатов печени проводили с•окрашиванием препаратов гематоксилин- эозином, азуром-П-эозином и по Граму-Вейгерту, Грам-принадлежность бактерий в тканях исследовали с помощью гисто-бактериоскопии тканевых срезов, окрашенных по Граму в модификации к. Вгоуш, н.норрв /1978/. 1!икрофотографированиа гистологических срезов производили на пленку «Микраг-300» и фотопластинки «Микрат» фотоаппаратами «Зениг-ИА» и «мооп «.
Вгоуш, н.норрв /1978/. 1!икрофотографированиа гистологических срезов производили на пленку «Микраг-300» и фотопластинки «Микрат» фотоаппаратами «Зениг-ИА» и «мооп «.
Математическая обработка результатов исследования произведена методом вариационной статистики с помощью программируемого микрокалькулятора ЕККЛ «Электроника БЗ-34». Оценка ста-
тистической значимости показателей и достоверности сравниваемых выборок производилась по критерию Стыодента при уровне значимости не ниже р<0,05.
РЕЗУЛЬТАТУ ИССЛЕДОВАНИЯ
В результате проведанных бактериологических исследований установлено, что из 252 обследованных с воспалительными заболеваниями желчевыводацих путей у 173 /63,3?«/ имелось бактериальное инфицирование желчи. При анализе бактериологических находок выявлены следующие варианты бактериохолии: аэробный, аэробно-анаэробный и сугубо анаэробный. Из них преобладающим был аэробный вариант, который диагностирован у 106 /42,1%/ больных. Ассоциации аэробов и анаэробов обнаружены в 62 /24,6*/, тогда как сугубо анаэробная бактериохолия — только в 5 /2Н/ наблюдениях.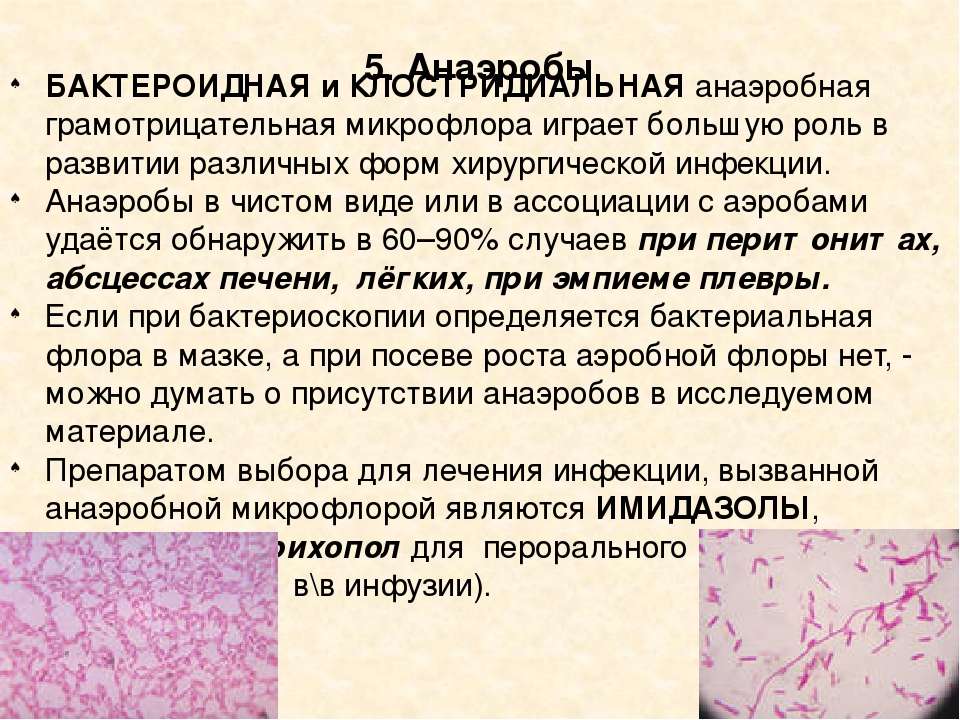 ей системе протекал с участием возбудителей неклостридиальной анаэробной инфекции.
ей системе протекал с участием возбудителей неклостридиальной анаэробной инфекции.
Частота обнаружения неклостридиалышх анаэробов в зависимости от характера воспалительного процесса имела значимые различия. Наиболее часто /5-1,3%/ эти микроорганизмы находили при гнойном холангита, реже /27%; р«: 0,05/ — при остром калькулез-ном холецистите и крайне редко /5%; рс0,001/ — при хроническом калькулезном холилстите. Вместе с том, у Сольных с неклостридиальной анаэробной инфекцией отмечена общая, независящая от вида билиарной патологии закономерность — полимикробкый характер инфекционного процесса. ¡Сак правило в желчи присутствовали 2-3 микроорганизма в примерном соотношении 1-2 аэробов к I анаэробу. Роль неклостридиальных анаэробов как самостоятельного этиологического »актора при бактериальных инфекциях желче-выводящих путей была невелика /0,8-4,356/.
Следует отметить, что этиологические особенности бактериохолии касались не столько видового состава микрофлоры и характера доминирующих представителей, сколько соотношения аэробного и анаэробного компонентов микрофлоры яелчи. Так, у больных с
Так, у больных с
3 Цм, 5 {ь
гнойным холангитоы бактериохолия носила преимущественно смешанный аэробно-анаэробный характер /53,5$/. При остром каль-куяезном холецистите имелось некоторое преобладание аэробного варианта инфекции /5895/ над аэробно-анаэробным /40,95«/. Микрофлора желчи у больных с хроническим калькулезным холециститом в большинстве случаев /88,W была представлена аэробами.
При остром кальнулезном холецистите этиологическая роль неклостридиапьных анаэробов отчетливо возрастала с увеличением продолжительности сроков от начала заболевания. Среди госпитализированных в 1-е сутки болезни их участие в инфекционном процессе выявлено у 12, Dí больных, а в последующие дни — у 44,Ш /р< 0,001/. Частота обнаружения аэробной микрофлоры в эти сроки не имела значимых различий. Судя по приведенным цифрам на ранних этапах развития острого холецистита этиологическим агентом бактериохолии являются аэробы и только в последующем по мере прогрессировав!« воспалительных и деструктивных изменений присоединяется анаэробная микрофлора. По данным количественных бактериологических исследований степень бактериального обсеменения желчи составила 5,7+1, Ibg КОЕ/мл, ткани желчного пузыря — 5,4+0,8lg КОЕ/г, причем, более выраженные степени количественного содержания микробов отмечались у больных с гангренозным холециститом. При гангренозном поражении желчного пузыря анаэробы обнаруживались почти в 3 раза чаще, чем при флегмонозном /62,и Zl,&% соответственно; р с 0,001/, что отражает общую патогенетическую взаимосвязь анаэробной инфекции с деструктивными процессами.
По данным количественных бактериологических исследований степень бактериального обсеменения желчи составила 5,7+1, Ibg КОЕ/мл, ткани желчного пузыря — 5,4+0,8lg КОЕ/г, причем, более выраженные степени количественного содержания микробов отмечались у больных с гангренозным холециститом. При гангренозном поражении желчного пузыря анаэробы обнаруживались почти в 3 раза чаще, чем при флегмонозном /62,и Zl,&% соответственно; р с 0,001/, что отражает общую патогенетическую взаимосвязь анаэробной инфекции с деструктивными процессами.
Применение в военных лечебных учреждениях методологии строгой анаэробной техники значительно расширило возможности этиологической диагностики бактериальной инфекции желчевыводя-щих путей. Новый методический подход обеспечил верификацию более полного видового состава микрофлоры желчи не только за счет выявления неидонтифицированных ранее неспорообразующих анаэробов, но и благодаря повышению инициального роста в ана-еростатах факультативных анаэробов и микроаэрофильных стрептококков. Менее информативными оказались посевы при культивировании в условиях аэробиоза по стандартной методике.
Менее информативными оказались посевы при культивировании в условиях аэробиоза по стандартной методике.
Б процессе микробиологических исследований желчи выделено 310 штаммов микроорганизмов, из которых 228 /73,6%/ — аэробы
и факультативные анаэробы и 82 /26,4%/ — облигатные анаэробы и: микроаэрофилышв стрептококки. В средне« на каядый положительный посев приходилось 1,8 штамма, в том число 1,3 штамма аэробов и 0,5 шташа анаэробов. Среди аэробной микрофлоры жол-чи доминировали грамотрицательные колиформгыэ палочки /табл.2/.
Таблица 2
Микро-флора желчи при воспалительных заболеваниях желчевыводяцих путей
Аэробы
Количество штаммов
абс. %
Анаэробы
Количество штаммов
абс. #
Е. сои
Enterobacter зр. Klebsiella ар. Proteus вр, Citrobacter sp.
Pseudo»or.o3 aeruginosa
Acinetoliocter ap. Alcaligeno cp. Serratia яр. Arizona cp. Недифференцированные грагютрицатель-ные палочки Bacillus sp. 0,8 0,4+0,4
0,8 0,4+0,4
5 2,2+1,0
6 2,6+1,1
25 II, 0+2,1
4 1,8+0,9
7 3,1+1,1
3 1,3+0,8
6 2,6+1,1
2 0,8+0,6
B. frogilia
Ii, nelar.ino£enicuo
Uicteroidc3 sp.
Punobacteriurn вр.
Veillonella cp.
I’eptococcuo op.
Peptostrepto-coccua op.
Clontridiun porfringena Lactobacillus cp. Actino~yccn sp. .’iif idobucteriutn sp, I.utocteriun lenlum
Iropicriibacte-riun sp,
;;t rep toccccus tnaorobius
.Streptococcus ¡aicroaeropfcilus
23 28,1+5,0
I 1,2+1,2
8 9,8+3,3
2 2,4+1,7
2 2,4+1,7
II 13,4+3,8
15 I8,3±4,3
4 4,9+2,4
2 2,4+1,7
2 2,4+1,7
, 3 3,7+2,1
I 1,2+1,2
I •1,2+1,2
I 1,2+1,2
6 7,3+2,9
Всего
Э*
228 100 Всего
BZ 100
Чшце других встречались кишечная палочка /34,254/, протеи /9,6*/ и энторобактери /9,25»/. /, диоксидин /78,Все изученные штаммы бактероидов и некоторые грашто-локительные кокки были чувствительны к левомицетину, клиндами-цину и метронидазолу. Антибиотикорезистентные штаммы чаще отмечались у болышх с длительным анамнезом и предшествующей антибактериальной терапией.
/, диоксидин /78,Все изученные штаммы бактероидов и некоторые грашто-локительные кокки были чувствительны к левомицетину, клиндами-цину и метронидазолу. Антибиотикорезистентные штаммы чаще отмечались у болышх с длительным анамнезом и предшествующей антибактериальной терапией.
При бактериологическом исследовании содержимого холангио-гешшх гнойников у 7 больных выявлена этиологическая роль не-спорообразующих анаэробов. В 4 случаях обнаружены аэробно-анаэробные ассоциации, в 3 — причиной нагноения являлись монокультуры и.хгаьШв . Наряду с этим, послеоперационные гнойные осложнения ран у 9 больных оказались вызванными представителями, неклостридиальной анаэробной микрофлоры в ассоциациях с другими микроорганизмами. По своим видовым характеристикам выделенные возбудители в 78% случаев били идентичны микроорганизмам, обна-
ружегошм в пузырной желчи, что подтверждает роль бактерий жел-чевыводящей системы в этиологии раневой инфекции.
Имеющиеся в лечебной практике бактериологические методы исследования на анаэробы позволяют получить окончательный ответ только ретроспективно, когда его клиническая значимость утрачивает силу. .
.
Иммунологический статус при документированной неклостриди-альной анаэробной инфекции изучен у 22 больных о деструктивным холециститом и у 18 больных с гнойным холангитом. Полученные данные позволили определить состояние противомикробной защиты, на фоне которого развивалась неклострвдиальная анаэробная инфекция и понять причины частых послеоперационных инфекционных осложнений. В целом, нарушения иммунореактивности у этих больных характеризовались подавлением клеточного и отсутствием до-
статочной защитной реакции со стороны гуморального иммунитета. Угнетение иммунной системы перед операцией проявлялось общей лимфопенией, снижением по сравнению с контрольными цифрами абсолютного и относительного количества Т-клеток при некотором повышении относительного содержания «активных» Т-лимфоцитов, снижением пролиферативного ответа в РБТЛ на ФГА, снижением содержания В-клеток, диспропорцией основных классов сывороточных иммуноглобуллинов, подавлением фагоцитоза, снижением БАСК, уровня Сд-фракции комплемента и лизоцима в сыворотке крови, ростом содержания ЦЖ /табл. 3/. Указанные изменения свидетельствовали о наличии вторичного иммунодефицитного состояния. При этом степень угнетения иммунологических реакций коррелировала с тяжестью гнойного заболевания, выраженностью патологического процесса в билиарной системе, глубиной эндогенной интоксикации и метаболических нарушений. Особенно выраженное падение показателей клеточного и гуморального иммунитета, неспецифггческях гуморальных факторов резистентности отмечалось у больных с анаэробным гнойно-септическим ходангитом, септические шоком и деструктивным холециститом, осложненным разлитым перитонитом.
3/. Указанные изменения свидетельствовали о наличии вторичного иммунодефицитного состояния. При этом степень угнетения иммунологических реакций коррелировала с тяжестью гнойного заболевания, выраженностью патологического процесса в билиарной системе, глубиной эндогенной интоксикации и метаболических нарушений. Особенно выраженное падение показателей клеточного и гуморального иммунитета, неспецифггческях гуморальных факторов резистентности отмечалось у больных с анаэробным гнойно-септическим ходангитом, септические шоком и деструктивным холециститом, осложненным разлитым перитонитом.
Как выяснилось, достоверно более глубокие нарушения клеточных и гуморальных защитных реакций перед операцией /значительное угнетение Т-клеточного звена иммунитета, снижение функциональной активности в РЕТЛ на ФГА, уменьшение ЕАСК, сывороточных 1е в и 1с А / отмечались в подгруппе больных, у которых в послеоперационном периоде развились гнойно-воспалительные осложнения. Поскольку дооперациониая иммунодепрессия способствует отягощенному течению послеоперационного периода, то степень угнетения иммунитета можно рассматривать как дополнительный критерий тяжести патологического процесса, а снижение Т-клеток — как прогностический фактор риска послеоперационных инфекционных осложнений. 2,3 51+2,б3« . 43+1,3
2,3 51+2,б3« . 43+1,3
ФАЛ,?« 52,4+1, б3™* 48,6+2,33®* 65,3+2,2
иг /■ зд+о.г3™* 2,0+0,1ХУХ .6.7+0,3
П335,# 62,5+1,в*** 57,4+1, б*** 71,3+1,7
Примечание: различия достоверны по сравнению с контрольной группой — х р < 0,05, ** р < 0,01, гар< 0,001
операции в связи с иммунодепрессивным эффектом операционной травмы происходило дальнейшее угнетение большинства клеточных и гуморальных факторов иммунитета. Подобные изменения носили транзиторный характер и соответствовали сравнительно тяжелому состоянию больных. По мере клинического выздоровления /7-9 сутки после операции/ изученные иммунологические показатели восстанавливались до уровня дооперационных значений или приближались к ним, но нормализации ни по одному из них еще не происходило. У лиц с неблагоприятным течением заболевания отмечалась более выраженная иммунодепрессия и соответственно напряженнее и длительнее протекали восстановительные процессы. Выявленные изменения количественных и функциональных показателей ишунореактивности позволили повысить точность диагностики дисбалансов иммунной системы для полноценной коррекции вторичного иммунодефицита. / больных,.у которых в желчи обнаружены анаэробы, превышал 60 лет. Число сопутствующих заболеваний у них было достоверно выше, чем у больных с бактериохолией иной -этиологии или абактериальным воспалением желчного пузыря. Такие больные поступали в стационар преимущественно /81,15»/ позже» 24 часов от начала заболсвания.В связи с этим у 97,3% госпитализированных имелись осложненные форш острого холецистита с преобладанием в структуре осложнений гнойных и гнойно-некротических процессов, а оперативные вмешательства производились несвоевременно в условиях запущенного гнойного заболевания.
/ больных,.у которых в желчи обнаружены анаэробы, превышал 60 лет. Число сопутствующих заболеваний у них было достоверно выше, чем у больных с бактериохолией иной -этиологии или абактериальным воспалением желчного пузыря. Такие больные поступали в стационар преимущественно /81,15»/ позже» 24 часов от начала заболсвания.В связи с этим у 97,3% госпитализированных имелись осложненные форш острого холецистита с преобладанием в структуре осложнений гнойных и гнойно-некротических процессов, а оперативные вмешательства производились несвоевременно в условиях запущенного гнойного заболевания.
При развитии неклостридиальной анаэробной,инфекции деструктивный холецистит характеризовался тяжелым клиническим течением. Заболевание почти всегда имело острое начало, сопровождалось выраженными клиническими и. клинико-лабораторными признаками активности воспалительного процесса и обменными нарушениями. При этом быстро ухудшалось общое состояние, несмотря на интенсивную консервативную терапию прогрессировали воспалительно-деструктивный процесс в желчном пузыре и интоксикационный синдром, рано появлялись признаки печеночной и печеночно-почеч-
— I? -
ной недостаточности. Характерным признаком неклостридиальной анаэробной инфекции являлось наличие в желчевыводящих путях буро-зеленоватого или коричневатого цвета гнойной желчи с гнилостным запахом, а также ихорозный запах содержимого паравези-кальных и холангиогенных гнойников, воспалительного эксудата брюшной полости.
Характерным признаком неклостридиальной анаэробной инфекции являлось наличие в желчевыводящих путях буро-зеленоватого или коричневатого цвета гнойной желчи с гнилостным запахом, а также ихорозный запах содержимого паравези-кальных и холангиогенных гнойников, воспалительного эксудата брюшной полости.
Сопоставление микробиологических находок с клиническими данными показало, что обнаружение в очагах гнойного воспаления билиарной системы ассоциаций е,со11 и в, fragiiia, как правило, коррелировало с тяжелой клиничесной картиной заболевания. Послеоперационный период у этих больных чаще осложнялся гнойно-воспалительными процессами, которые являлись основными причинами летальных исходов. Данные литературы и собственные клинические наблюдения свидетельствуют о тон, что в связи с высоким темпом воспалительно-деструктивных изменений в желчном пузыре, неуклонным нарастанием интоксикации и метаболических нарушений оперативные вмешательства при анаэробном деструктивном холецистите необходимо производить как можно раньше, предпочтительнее в 1-е сутки госпитализации, до развития гнойно-септических осложнений. ая бактериохо-лия и внутрипротоковая гелчная гкпертензия. Поэтому главным принципом лечения анаэробного гнойного холангита следует считать раннюю декомпрессию желчных протоков в сочетании с рациональной антибактериальной терапией, полноценной и своевременной коррекцией нарупений метаболизма.
ая бактериохо-лия и внутрипротоковая гелчная гкпертензия. Поэтому главным принципом лечения анаэробного гнойного холангита следует считать раннюю декомпрессию желчных протоков в сочетании с рациональной антибактериальной терапией, полноценной и своевременной коррекцией нарупений метаболизма.
Антибактериальную терапию гнойно-воспалительных заболеваний желчевыводящих путей начинали эмпирически на основании изучения клинической картины заболевания и данных лабораторной экспресс-диагностики. В дальнейшем с учетом антибиотикограммы корректировали лечение, подбирая наиболее эффективные препараты. Эгиотропность антибиотикотерапии достигалась применением комбинаций антибактериальных препаратов, активных по отношению к аэробным и анаэробным возбудителям билиарной инфекции. В процессе слепой и направленной терапии у 78 больных с деструктивным холециститом и гнойным холангитом использовали следующиев комбинации препаратов:
I/ гентамицин /160-320 мг/сут в/м/ + ампициллин /1,5 г/сут в/м/ + трихопол /1,5 г/сут внутрь/ или метрогил /100 мл/500 мг/ 1-2 раза в сутки в/в/;
2/ пенициллин /18-20 тыс Ед/сут в/в/ + клиндамицин /9001200 мг/сут в/м или в/в/ + трихопол /1,5 г/сут внутрь/ или мет-рогил /100мл /500 мг/ 1-2 раза в сутки в/в/;
3/ цефоперазон /1,0-2,0 г в/м или в/в/ + трихопол /1,5 г/сут внутрь/ или метрогил /100 мл /500 мг/ 1-2 раза в сутки в/в/. Оценка клинической эффективности указанных сочетаний показала, что разработанные схемы комбинированной антибактериальной терапии способствовали улучшению состояния больных, -нормализации ‘ показателей инфекционно-воспалительного процесса и функционального состояния печени в более ранние сроки, чем у больных контрольной группы, которым проводилась антибиотикотерапия без уче-
Оценка клинической эффективности указанных сочетаний показала, что разработанные схемы комбинированной антибактериальной терапии способствовали улучшению состояния больных, -нормализации ‘ показателей инфекционно-воспалительного процесса и функционального состояния печени в более ранние сроки, чем у больных контрольной группы, которым проводилась антибиотикотерапия без уче-
та анаэробного компоненте микрофлоры желчи. Применение комбинированной антибактериальной терапии наряду с фракционным чрес-дренажным промыванием желчевыводящих путей 1% раствором диокси-дина, 0,5% раствором хлоргексидина биглюконата, интраоперационной санацией ложа желчного пузыря и орошением подпеченочного пространства антисептиками через дренажи в правом подреберье после операции позволило в 4 раза снизить летальность /р<0,05/, в 2 раза — количество послеоперационных инфекционных осложнений /р<0,05/, на 7,1 дней сократить продолжительность лечения больных в стационара /р<0,01/.
В результате анализа полученных в работе данных выработана тактика антибактериальной профилактики послеоперационных инфекционных осложнений при хирургическом лечении деструктивного холецистита. В этих целях в схемы профилактики включали анаэро-боцидный препарат — метронидазол /гентамицин + метронидазол, ампициллин + метронидазол, цефоперазон + метронидазол/. Введение препаратов совпадало с премедикацией, поэтому оперативное вмешательство проводилось на фоне предельных концентраций антибактериальных препаратов в крови, тканях и пузырной желчи. После операции антибиотикопрофилактику продолжали в течение 3 суток внутримышечно или внутривенно в общетерапевтических дозировках о интервалом 6-12 часов. Метронидазол применяли в таблетках по 0,5 г 3 раза в день, в виде ректальных свечей по 3-5 г в день ийи внутривенно по 100 мл /500 мг/ 1-2 раза в день. Осуществленный комплекс профилактических мероприятий с целенаправленным превентивным воздействием на неклостридиальную анаэробную микрофлору обеспечил снижение частоты нагноений операционных ран с 15,2% до 5,8% /р< 0,05/и сокращение пребывания больных в стационаре на 2,4 дня /р<0,05/. Таким образом, комбинированная антибактериальная профилактика при хирургическом лечении деструктивного холецистита значительно эффективнее по сравнению с традиционной антибиотикопрофилакгикой пенициллина-ми и аминогликозидами.
В этих целях в схемы профилактики включали анаэро-боцидный препарат — метронидазол /гентамицин + метронидазол, ампициллин + метронидазол, цефоперазон + метронидазол/. Введение препаратов совпадало с премедикацией, поэтому оперативное вмешательство проводилось на фоне предельных концентраций антибактериальных препаратов в крови, тканях и пузырной желчи. После операции антибиотикопрофилактику продолжали в течение 3 суток внутримышечно или внутривенно в общетерапевтических дозировках о интервалом 6-12 часов. Метронидазол применяли в таблетках по 0,5 г 3 раза в день, в виде ректальных свечей по 3-5 г в день ийи внутривенно по 100 мл /500 мг/ 1-2 раза в день. Осуществленный комплекс профилактических мероприятий с целенаправленным превентивным воздействием на неклостридиальную анаэробную микрофлору обеспечил снижение частоты нагноений операционных ран с 15,2% до 5,8% /р< 0,05/и сокращение пребывания больных в стационаре на 2,4 дня /р<0,05/. Таким образом, комбинированная антибактериальная профилактика при хирургическом лечении деструктивного холецистита значительно эффективнее по сравнению с традиционной антибиотикопрофилакгикой пенициллина-ми и аминогликозидами.
о
вывода
I. Разработанная система этиологической диагностики не-клостридиальной анаэробной инфекции позволила установить, что в развитии гнойно-воспалительных заболеваний желчевыводящих путей у 25% хирургических больных имеют значение неспорообра-
зущие анаэробы /бактероиды, особенно В.ГгосШв , анаэробные кокки и др./. Эти микроорганизмы выделяются преимущественно /92,1%/ в ассоциациях с аэробной и факультативно-анаэробной микрофлорой и редко /7,9%/ — в монокультуре. Наиболее часто /54,Ъ%/ неклостридиальная анаэробная инфекция наблюдается при гнойном холангите.
2. Экспресс-диагностика неклостридиальной анаэробной инфекции с помощью экстренной бактериоскопии и парофазной газовой хроматографии позволяет в ранние сроки достоверно идентифицировать характер микрофлоры гнойных очагов гепатобилиарной системы и целенаправленно проводить этиотропную терапию.
3. При гнойно-воспалительных заболеваниях желчевыводящих путей анаэробной этиологии отмечается угнетение клеточного иммунитета, неспецифической резистентности в основном за счет Т-клеточного звена и фагоцитарной активности лейкоцитов. В 1-3 сутки после операции нарушения клеточных и гуморальных защитных реакций углубляются, к 7-9 суткам имеют тенденцию к нормализации. Устранение иммунодефицита отчетливо проявляется в период клинического улучшения состояния больных.
В 1-3 сутки после операции нарушения клеточных и гуморальных защитных реакций углубляются, к 7-9 суткам имеют тенденцию к нормализации. Устранение иммунодефицита отчетливо проявляется в период клинического улучшения состояния больных.
4. Факторами риска развития неклостридиальной анаэробной инфекции при воспалительной патологии желчевыводящих путей являются пожилой и старческий возраст, сопутствующие хронические заболевания /распространенный атеросклероз, гипертоническая болезнь с расстройством кровообращения, сахарный диабет/, длительность и частота рецидивов инфекционно-воспалительного процесса, стриктуры билиодигестивных анастомозов, неэффективная антибактериальная терапия аминогликозидами.
5. Для клинической картины хирургических заболеваний желчевыводящих путей, протекающих с участием неспорообразующих анаэробов, характерны бурное, подчас септическое начало, высокий темп прогрессировать воспалительных и деструктивных процессов, выраженная гнойная интоксикация, наличие в желчевыво-дящих путях коричневатого или,буро-зеленого цвета желчи с неприятным гнилостным запахом.
6. Возникновение и течение неклостридиальной анаэробной инфекции желчевыводящих путей сопровождается частыми гнойно-септическими осложнениями, которые являются основными причинами летальных исходов у больных с деструктивным холециститом
и гнойным холангитом. Особая тяжесть и неблагоприятное течение заболевания отмечаются при участии в воспалительном процессе бшшарной системы ассоциаций Е.соИ и в.ггае±Х1а,
?. Послеоперационные инфекционные осложнения у больных с кеклостридиальной анаэробной инфекцией желчевыводящих путей развиваются при наличии до операции вьгралешшх нарушений Т-сис-темы иммунитета, гипоиммуногдобулинемии, депрессии фагоцитарной активности лейкоцитов и недостаточности бактерицидной активности сыворотки крови. Данные иммунологические показатели наряду с клинико-микробиолопическими критериями позволяют прогнозировать осложненное течение послеоперационного периода.
8. Комплексная антибактериальная терапия, активная по отношению к аэробам и анаэробам /гентамицин + ампициллин + три-хопол, пенициллин + клиндамицин +- ампициллин, цефоперазон + метронидазол/ способствует быстрой ликвидации гнойно-воспалительного процесса в желчевыводящих путях, снижению летальности и улучшению результатов этиотропного лечения.
9. Применение предложенных схем комбинированной антибактериальной профилактики /гентамицин + метронидазол, ампициллин + метронидазол, цефоперазон + метронидазол/ при хирургическом лечении деструктивного холецистита приводит практически к двухкратному снижению частоты рановой инфекции и сокращению продолжительности лечения больных в стационаре в среднем на 2,4 дня. . ‘
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
Для повышения эффективности этиологической диагностики гнойно-воспалительных заболеваний органов гепатобилиарной системы в военных лечебных учреждениях целесообразно проводить микробиологические исследования с помощью строгой анаэробной техники, позволяющей установить присутствие в диагностическом материале не только неспорообразующих анаэробов, но и всей микрофлоры патологического процесса, включая факультативно-анаэ-робныз, микроаэрофильше и аэробные микроорганизмы, «
Для ускоренной диагностики гнойно-воспалительных заболеваний желчевыводящих путей, протекакщх о участием неспорообра-зующих анаэробов рекомендуется в качестве экспресс-методов использовать экстренную бактериоскопию и парофазнуа газовую хроматограф:«).
— 22 -
Знание факторов риска, патогенетических особенностей и характерных клинических проявлений позволяет в большинстве случаев осуществить предварительную диагностику неклостридиальной анаэробной инфекции при деструктивном холецистите и гнойном хо-лангитв,
В связи с прогрессирующим течением, быстрым развитием необратимых воспалительно-деструктивных изменений хирургические и инструментальные вмешательства у больных с анаэробным деструктивным холециститом следует выполнять в первые сутки госпитализации до развития гнойно-септических осложнений.
Зтиотропная терапия хирургических гнойных инфекций желче-выводящих путей должна предусматривать применение комбинаций антибактериальных препаратов, обеспечивающих воздействие на весь спектр аэробных и анаэробных возбудителей. Системную антибактериальную терапию необходимо сочетать с подведением антисептиков и антибиотиков непосредственно в очаг инфекции путем интрахоледохеальных чресдренажных лаважей при гнойном холангите, чресдренажного орошения подпеченочного пространства при деструктивном холецистите,
В комплекс профилактики послеоперационных инфекционных осложнений при хирургическом лечении деструктивного холецистита необходимо включать комбинации антибактериальных препаратов, что позволит снизить частоту раневой инфекции в послеоперационном периоде и сократить продолжительность лечения больных в хирургических стационарах воешшх лечебных учреждений.
■ СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
1. К вопросу о микрофлоре желчи при хроническом кальку-лезном холецистите // Неклостридиальная анаэробная инфекция. -Л.: Воен.-мед.акад., 1982. — С.51-52 /соавт. В.И.Кочеровец , В.А.Тарасов/. •»■■
2. Этиология бактобилий при калькулезном холецистите // Тез.докл.Всесоюз.науч-практ.конф. «Проблемы клинической микробиологии в неинфекционной клинике». — М., 1983. — С.61-62 /соавт. В.И.Кочеровец/.
3. Микробиологическая диагностика хирургических гнойных инфекций желчных путей // Тез.докл.Всесоюз.конф. «Новые методы диагностики я лечения гнойных хирургических заболеваний». -
— 23 -
Андижан, 1983. — C.I29-I3I /соавт. В.И.Кочеровец/.
4. Септический холангит // Тез.докл.Республ.конф. «Сепсис1*. — Тбилиси, 1984. — С.243-245 /соавт. В.А.Тарасов, С.В.Оболенский/.
5. Неклостридиальная анаэробная инфекция при заболеваниях печени и желчевыводящих путей // Вестник хирургии. — 1984. -
— 1984. -
Р 4. — С,133-138 /соавт. В.И.Кочеровец, A.B.Столбовой/.
6. Калькулезный холецистит, осложненный ненлостридиальной анаэробной инфекцией // Хирургия. — 1984. — .1? 7. — C.I35-I36 /соавт. В.И .Кочеровец, О.А.Ленцнер/.
7. Применение метронидазола в комплексном лечении гнойного холангита // Тез.докл.итоговой конф.воен.-науч.о-ва слушателей. -Л.: Воен.-мед. акад., 1985. — С.92.
8. Кликико-микробиологическая характеристика неклостри-диальной анаэробной инфекции в хирургии желчных путей // Там яе, С.93.
9. Опыт работы анаэробной диагностической лаборатории // Тез.докл.Всесоюз,конф. «Актуальные проблемы нозокомиальннх инфекций и лекарственной устойчивости микроорганизмов». -Минск, 1986. — С.126-127 /соавт. В.И.Кочеровец, А.В.Столбовой,
A.B.Кочетков, И.А.Борисов, Е.Ф.Кира, М.В.Рогачев, А.С.Гук/.
10. Клиника и диагностика послеоперационных нагноений ран, вызванных неспорообразующими анаэробами после оперативных вмешательств на желчных путях // Тез. докл.науч.-метод.конф . «Актуальные вопросы профессиональной подготовки медицинской службы Балтийского флота. — Калининград, 1986. — С.18-19 /соавт. В.И.Кочеровец, А.Г.Мирошниченко/.
докл.науч.-метод.конф . «Актуальные вопросы профессиональной подготовки медицинской службы Балтийского флота. — Калининград, 1986. — С.18-19 /соавт. В.И.Кочеровец, А.Г.Мирошниченко/.
11. Клинико-микробиологическая диагностика неклостриди-альной анаэробной инфекции при хирургических заболеваниях желчных путей и абсцессе печени // Вестник хирургии. — 1986. -Р.8, — С.27-30 /соавт. В.И.Кочеровец, В.А.Тарасов/.
12. Этиологические аспекты хирургического лечения гнойных холангитов // Тез.УП Воеросс. съезда хирургов «Актуальные вопросы абдоминальной хирургии», — Л., 1989. — С.246-24,5′ /соавт.
B.А.Панов, В.И.Кочеровец, С.А.Мартемьянов, И.В.Берлев/.
13. Клинико-иммунологичесиив параллели при осложненном остром холецистите, обусловленном ненлостридиальной анаэробной инфекцией // Тез.докл.науч-метод.конф., посвященной 10-летию кафедры хирургии Воен.-мед. факультета при ЦИУВ «Актуальные
вопросы последипломной подготовки военных врачей /методология и клиника/». — М., 1990. — С.70-71.
— М., 1990. — С.70-71.
14. Значение ЛИИ в оценке тяжести эндотоксикоза у больных острым осложненным холециститом и неклостридиальной анаэробной инфекцией желчных путей // Там же, С.174 / соавт. В.А.Панов/.
15. Парофазная хроматография как метод экспресс-диагностики неклостридиальной анаэробной инфекции в хирургии гнойно-воспалительных заболеваний желчных путей // Матер.науч.конф. молодых ученых академии. — Л.: Воен.-мед.акад., 1990. — С.39 /соавт. Г.И.Заболотнова/.
16. Кдинико-иммунологичесхая характеристика и современная лабораторная диагностика анаэробного деструктивного холецистита, осложненного местным и разлитым перитонитом // Тез.докл. науч.-метод.конф, «Острый перитонит /вопросы диагностики, лечо-нмя и профилактики/». — !>!., 1991. — С.56-57.
17. Этиологические особенности неклостридиальной анаэробной инфекции при калькулезном холецистите // Тез.докл.Всесоюз. конф. «Актуальные проблемы химиотерапии бактериальных инфекций». — М., 1991. — С.176-178 /соавт. А.М.Половой/.
— С.176-178 /соавт. А.М.Половой/.
18. Применение ыетронидазола в комплексной антибактериальной профилактике послеоперационных инфекционных осложнений при хирургическом лечении деструктивного холецистита // Tau Ее,
С.633-635 /соавт. В.А.Тарасов/. °
19. Клинихо-микробиологические проблемы острого гнойного оботруктивного холангита в хирургии внепеченочных желчных протоков // Вестник хирургии. — 1991. — Р 5. — С.35-36 /соавт. В.А.Панов, В.И.Кочеровец/.
20. Этиологическая диагностика неклостридиальной анаэробной инфекции органов гепатобилиарной системы в военных лечебных учреждениях // Воен.-мед. журн. — 1991. — № 4. — С.38-43 /соавт. Э.А.Нечаев, В.И.Кочеровец, В.А.Тарасов, А.М.Половой/.
Анаэробная инфекция — словарь ветеринарных терминов — ВЦ Зоовет
инфекционный процесс, вызываемый анаэробами. Характеризуется быстро возникающим и прогрессирующим некрозом тканей с образованием в них газов и отсутствием выраженных воспалительных явлений, тяжелой интоксикацией.
Это одна из самых тяжело протекающих инфекций, которая приводит к развитию выраженной эндогенной интоксикации с поражением жизненно важных органов и систем и сохраняет высокий процент летальности. Анаэробы делятся на 2 вида: спорообразующие анаэробы, или клостридии, и неспорообразующие, или неклостридиальные, анаэробы.
Выделяют также эндогенные и экзогенные анаэробные микроорганизмы. Эндогенные анаэробы являются составной частью нормальной микрофлоры организма и обнаруживаются главным образом в кишечнике, органах мочеполовой системы. Их можно также выявить на поверхности кожи, слизистых оболочек, в отделяемом из дыхательных путей. Экзогенные анаэробы обнаруживаются в почве, разлагающихся органических соединениях, на одежде человека.
Развитие анаэробной инфекции может быть молниеносным (до 1 суток с момента травмы или операции), острым (в пределах 3 — 4 суток) и подострым (более 4 суток).
Возможность возникновения анаэробной инфекции зависит от количества анаэробов в ране, морфологических особенностей и вирулентности возбудителя, влияния сопутствующих микроорганизмов и др. Реализация патогенных свойств анаэробов возможна при соответствующем состоянии организма и лишь при наличии участков тканей, лишенных кровоснабжения, хронической интоксикации организма, сопровождающейся снижением его защитных сил, и др.
Реализация патогенных свойств анаэробов возможна при соответствующем состоянии организма и лишь при наличии участков тканей, лишенных кровоснабжения, хронической интоксикации организма, сопровождающейся снижением его защитных сил, и др.
Основой лечения анаэробной инфекции является оперативное вмешательство: широкое рассечение очага поражения и иссечение некротизированных тканей с обработкой антисептиками и адекватным дренированием.
Ведущая роль в лечении после операции принадлежит антибактериальной терапии, в основе которой лежит использование антибиотиков, обычно широкого спектра действия: полусинтетических пенициллинов, цефалоспоринов, аминогликозидов и др., а также препаратов, избирательно действующих на анаэробы (клиндамицин, метронидазол и др.).
В тяжелых случаях, как правило, назначают максимальные суточные дозы препаратов. Кроме того, применяют антисептические средства, избирательно действующие на анаэробы: диоксидин, димексид и др.
Широко используются инфузионная терапия (введение препаратов крови, плазмы, кровезаменителей, растворов аминокислот и др.), современные методы детоксикации иммуностимуляторы, антикоагулянты и др.
Профилактика анаэробной инфекции состоит в своевременной и адекватной хирургической обработке ран, тщательном соблюдении асептики и антисептики при плановых оперативных вмешательствах, рациональном использовании антибиотиков.
Лечение при анаэробной инфекции
Лечение при анаэробной инфекции должно быть комплексным, с учетом биологических особенностей анаэробных микробов, их ассоциаций, патогенеза и форм проявления болезни. Оно должно включать прежде всего хирургические и специфические лечебные мероприятия в сочетании с осмо-оксигено и патогенетической терапией. Главное при этом состоит в том, чтобы все лечебные меры были применены возможно раньше, по возможности до клинического проявления инфекции либо в самом начале ее.
Хирургическое лечение имеет большое профилактическое и лечебное значение, а в ряде случаев оказывается ведущим. При свежих глубоких ранах с большой зоной повреждения мышечной ткани, с почвенно-навозным загрязнением совершенно необходима хирургическая обработка (см. ниже). Животных с признаками анаэробной инфекции изолируют и проводят лечебные процедуры в отдельном помещении, не связанном со стационаром, перевязочной или общим манежем, где ведется прием больных животных. Резиновую обувь, перчатки, хирургическое белье, инструментарий тщательно моют и стерилизуют. Помещения и оборудование, где обрабатывают и содержат животных, подвергают дезинфекции. Перевязочный материал, веревки, загрязненные экссудатом, сжигают. Газовый абсцесс вскрывают широким разрезом, иссекают мертвые ткани, ликвидируют ниши, карманы и применяют горячие (40°) гипертонические растворы средних солей с перекисью водорода, калием перманганатом либо с хлорамином.
Газовую флегмону, газовые отеки, зону газовой гангрены рассекают широким (лампасным) одним или несколькими разрезами в пределах отека, до границы признаков кровоточивости, мертвые ткани иссекают. Зашитые раны с признаками развивающейся анаэробной инфекции (отеки с крипитацией, выделение газа и пр.) немедленно вскрывают, производят дополнительные рассечения, делают контрапертуры, иссекают мертвые ткани до появления кровотечения. До, во время и непосредственно после иссечения раны длительно орошают (до 20 мин) указанными выше растворами. В них целесообразно добавлять скипидара от 2 до 10%. Промытые раны рыхло дренируют с Sol.
Вместо дренирования рану можно обильно припудривать сложными пудрами с антибиотиками (Acidi borici 6,0, Iodoformii 2,0, Penicillini 500 000 (1 000 000) ЕД. Наружное, для депонирования раны) либо другими подобными порошками (см. Справочник по ветеринарной хирургии. М., Колос, 1977).
Большого внимания заслуживают внутримышечные инъекции антибиотиков и оксигенотерапия. Кислород через иглу нагнетают из кислородной подушки в пограничные здоровые ткани и непосредственно в зону анаэробного очага.
Не специфическое лечение заключается в использовании средств и методов охранительной терапии (новокаинантибиотиковые блокады, внутрисосудистые инъекции), дезинтоксикации и выведении токсинов (инъекции 40%-кого гексаметилентетрамина с дозой кофеина, 10% раствора кальция хлорида с 20%-ным раствором глюкозы, переливание совместимой крови либо 10% реополиглюкина, а также насыщение организма поливитаминами).
Специфическое лечение и профилактика сводятся к применению смеси моновалентных противогангренозных сывороток. С профилактической целью сыворотку вводят внутримышечно (табл. 2) или подкожно в зоне здоровых тканей, где не нарушено кровообращение, чтобы лучше происходило всасывание. Во избежание анафилаксического шока вначале вводят в вену 2- 5 мл сыворотки. Затем через 1-2 ч при отсутствии признаков шока вводят не менее 5 профилактических доз противогангренозных сывороток, разведенных в 3-5 раз стерильным изотоническим раствором натрия хлорида. Такое же количество смеси сывороток инъецируют внутримышечно в зоне и вокруг поражения, на границе отека. Таким образом, в организме больного животного создается депо готовых антител, способствующих выздоровлению. При появлении шоковых признаков введение сыворотки прекращают и внутривенно инъецируют крупным животным 50-100 мл 10%-ного раствора кальция хлорида, а под кожу вводят эфедрин и камфору.
Похожий материал по теме: |
описание болезни, симптомы, диагностика, лечение
Справочная информация о болезни Анаэробная инфекция (Газовая гангрена, Злокачественный отек, Газовая флегмона) (собаки): описание, симптомы, признаки, диагностика, лечение домашних животных
Вид животного:
Собаки
Описание болезни:
Инфекционный процесс, вызываемый анаэробами. Характеризуется быстро возникающим и прогрессирующим некрозом тканей с образованием в них газов и отсутствием выраженных воспалительных явлений, тяжелой интоксикацией.
Характеризуется быстро возникающим и прогрессирующим некрозом тканей с образованием в них газов и отсутствием выраженных воспалительных явлений, тяжелой интоксикацией.
Причины развития болезни
Предрасполагают: кровопотеря, переутомление, гиповитаминозы, недостаточное питание, длительное применение жгута, отсутствие неподвижности травмированного органа, наличие в ране гноеродных микробов.
Симптомы болезни
Может появиться в глубоких колотых, ушибленно-рваных, размозженных ранах с карманами и углублениями, при открытых раздробленных переломах.
Диагностика болезни
Диагностика на основании клинических признаков.
Лечение болезни
Раны такого характера обрабатываются только врачом (за исключением первой помощи)! Основой лечения анаэробной инфекции является оперативное вмешательство: широкое рассечение очага поражения и иссечение некротизированных тканей с обработкой антисептиками и адекватным дренированием.
Ведущая роль в лечении после операции принадлежит антибактериальной терапии (назначают антибиотики широкого спектра действия: полусинтетические пенициллины, цефалоспориноы, аминогликозиды и др., а также препаратов, избирательно действующих на анаэробы (клиндамицин, метронидазол и др.). )
В тяжелых случаях, назначают максимальные суточные дозы препаратов и применяют антисептические средства, избирательно действующие на анаэробы: диоксидин, димексид и др. Широко используются инфузионная терапия (введение препаратов крови, плазмы, кровезаменителей, растворов аминокислот и др.), современные методы детоксикации иммуностимуляторы, антикоагулянты и др. Профилактика анаэробной инфекции состоит в своевременной и адекватной хирургической обработке ран, тщательном соблюдении асептики и антисептики при плановых оперативных вмешательствах, рациональном использовании антибиотиков.
Болезни по видам животных
Нужны деньги до зарплаты?
более 30 сервисов
Кредиты онлайн на карту за 15 минут
до 180 дней
макс срок
до 20 000 грн.
макс сумма
Забавное видео
Этот малыш еще ходит в садик, но в баскетбол играет как настоящий профи!
Метронидазол по-прежнему является препаратом выбора для лечения анаэробных инфекций | Клинические инфекционные болезни
Аннотация
Метронидазол используется для лечения инфекций более 45 лет и до сих пор успешно применяется для лечения трихомониаза, амебиаза и лямблиоза. Анаэробные бактериальные инфекции, вызываемые видами Bacteroides , фузобактериями и клостридиями, благоприятно реагируют на терапию метронидазолом.Также сообщалось о хороших клинических результатах в лечении вагиноза, вызванного Gardnerella vaginalis . Показатели устойчивости к метронидазолу, как правило, остаются низкими; однако в нескольких исследованиях сообщалось о снижении восприимчивости среди видов Bacteroides , а также о различных механизмах устойчивости. Были описаны устойчивые к метронидазолу штаммы Helicobacter pylori , но комбинированная терапия (например, метронидазол, амоксициллин или кларитромицин плюс омепразол) все еще рекомендуется для искоренения этого патогена у пациентов с гастродуоденальной язвой.Метронидазол считается экономически эффективным лекарством из-за его низкой стоимости, хорошей активности против патогенных анаэробных бактерий, благоприятных фармакокинетических и фармакодинамических свойств и незначительных побочных эффектов.
Анаэробные бактериальные инфекции, вызываемые видами Bacteroides , фузобактериями и клостридиями, благоприятно реагируют на терапию метронидазолом.Также сообщалось о хороших клинических результатах в лечении вагиноза, вызванного Gardnerella vaginalis . Показатели устойчивости к метронидазолу, как правило, остаются низкими; однако в нескольких исследованиях сообщалось о снижении восприимчивости среди видов Bacteroides , а также о различных механизмах устойчивости. Были описаны устойчивые к метронидазолу штаммы Helicobacter pylori , но комбинированная терапия (например, метронидазол, амоксициллин или кларитромицин плюс омепразол) все еще рекомендуется для искоренения этого патогена у пациентов с гастродуоденальной язвой.Метронидазол считается экономически эффективным лекарством из-за его низкой стоимости, хорошей активности против патогенных анаэробных бактерий, благоприятных фармакокинетических и фармакодинамических свойств и незначительных побочных эффектов. Метронидазол по-прежнему является стандартным критерием терапии анаэробных инфекций, как это было описано Талли и его коллегами 35 лет назад.
Метронидазол по-прежнему является стандартным критерием терапии анаэробных инфекций, как это было описано Талли и его коллегами 35 лет назад.
Метронидазол — противомикробное средство, которое используется в клинической медицине более 45 лет. Первоначально он был показан для лечения инфекции, вызванной Trichomonas vaginalis , а затем было показано, что он эффективен против других протозойных инфекций, таких как амебиаз и лямблиоз.Насколько нам известно, первый отчет о влиянии метронидазола на лечение анаэробных инфекций был опубликован в 1962 году Shinn [1]. В этом исследовании острый язвенный гингивит успешно лечился с помощью терапии метронидазолом. Однако значительные успехи были сделаны Талли и др. [2, 3] в больнице для ветеранов Уодсворта в Лос-Анджелесе 10 лет спустя; Талли и его коллеги показали, что метронидазол полезен при лечении системных анаэробных инфекций, в том числе вызванных Bacteroides fragilis. Позже метронидазол был введен для лечения инфекции Clostridium difficile и до сих пор рекомендуется в качестве альтернативы ванкомицину для лечения этой инфекции. Схемы лечения для уничтожения Helicobacter pylori по-прежнему включают метронидазол в сочетании с другими агентами. Метронидазол также показан для лечения бактериального вагиноза, вызванного Gardnerella vaginalis. Несмотря на 45 лет широкого применения, метронидазол остается стандартным критерием для лечения и профилактики анаэробных инфекций (рис. 1).
Схемы лечения для уничтожения Helicobacter pylori по-прежнему включают метронидазол в сочетании с другими агентами. Метронидазол также показан для лечения бактериального вагиноза, вызванного Gardnerella vaginalis. Несмотря на 45 лет широкого применения, метронидазол остается стандартным критерием для лечения и профилактики анаэробных инфекций (рис. 1).
Рисунок 1
Фрэнсис П. Талли (справа) и Карл Эрик Норд (слева) обсуждают использование метронидазола для профилактики и лечения анаэробных инфекций в Медицинской школе Университета Гифу в Гифу, Япония, в 1985 году. Фотография : Профессор Казуэ Уэно, Гифу, Япония.
Рисунок 1
Фрэнсис П. Талли (справа) и Карл Эрик Норд (слева) обсуждают использование метронидазола для профилактики и лечения анаэробных инфекций в Медицинской школе Университета Гифу в Гифу, Япония, в 1985 году.Фотография: профессор Казуэ Уэно, Гифу, Япония.
Терапевтическое использование метронидазола при анаэробных инфекциях
Метронидазол высокоактивен в отношении грамотрицательных анаэробных бактерий, таких как B. fragilis , и грамположительных анаэробных бактерий, таких как C. difficile. Фармакокинетические и фармакодинамические свойства препарата благоприятны, он доступен в форме пероральных, внутривенных, вагинальных и местных форм. После перорального приема метронидазол хорошо всасывается, а его пиковые концентрации в плазме крови возникают через 1-2 часа после приема.Метронидазол является основным компонентом плазмы, но также присутствует меньшее количество активных метаболитов. Связывание с белками низкое; <20% циркулирующего метронидазола связывается с белками плазмы. Как исходное соединение, так и метаболит обладают бактерицидной активностью in vitro против большинства штаммов анаэробных бактерий, за исключением C. difficile , а также трихомонацидной активностью in vitro. Концентрации метронидазола в спинномозговой жидкости и слюне аналогичны таковым в плазме.Бактерицидные концентрации метронидазола также были обнаружены в гное от абсцессов печени. Основным путем выведения метронидазола и его метаболитов является моча, при этом экскреция с калом составляет незначительную часть.
fragilis , и грамположительных анаэробных бактерий, таких как C. difficile. Фармакокинетические и фармакодинамические свойства препарата благоприятны, он доступен в форме пероральных, внутривенных, вагинальных и местных форм. После перорального приема метронидазол хорошо всасывается, а его пиковые концентрации в плазме крови возникают через 1-2 часа после приема.Метронидазол является основным компонентом плазмы, но также присутствует меньшее количество активных метаболитов. Связывание с белками низкое; <20% циркулирующего метронидазола связывается с белками плазмы. Как исходное соединение, так и метаболит обладают бактерицидной активностью in vitro против большинства штаммов анаэробных бактерий, за исключением C. difficile , а также трихомонацидной активностью in vitro. Концентрации метронидазола в спинномозговой жидкости и слюне аналогичны таковым в плазме.Бактерицидные концентрации метронидазола также были обнаружены в гное от абсцессов печени. Основным путем выведения метронидазола и его метаболитов является моча, при этом экскреция с калом составляет незначительную часть. Метронидазол метаболизируется в печени, и одновременный прием препаратов, которые увеличивают или снижают активность микросомальных ферментов печени, может привести к изменению концентрации в плазме. Метронидазол усиливает антикоагулянтный эффект варфарина и других пероральных антикоагулянтов кумарина, что приводит к увеличению протромбинового времени.Метронидазол у некоторых пациентов может влиять на метаболизм алкоголя, что приводит к непереносимости.
Метронидазол метаболизируется в печени, и одновременный прием препаратов, которые увеличивают или снижают активность микросомальных ферментов печени, может привести к изменению концентрации в плазме. Метронидазол усиливает антикоагулянтный эффект варфарина и других пероральных антикоагулянтов кумарина, что приводит к увеличению протромбинового времени.Метронидазол у некоторых пациентов может влиять на метаболизм алкоголя, что приводит к непереносимости.
Профиль безопасности метронидазола хорошо известен, и побочные эффекты считаются в основном от легкой до умеренной степени тяжести. Наиболее частые побочные реакции возникают со стороны желудочно-кишечного тракта. Сообщалось о редких серьезных побочных реакциях, включая судорожные припадки и периферическую невропатию, характеризующиеся в основном онемением или парестезией конечностей, у пациентов, получавших длительное лечение метронидазолом.
В терапевтической обзорной статье, опубликованной более 10 лет назад Freeman et al [4], обобщены клинические данные по терапевтическому применению метронидазола при анаэробных инфекциях. Исследования, опубликованные в 1998–2008 годах, подтверждают эти клинические отчеты.
Исследования, опубликованные в 1998–2008 годах, подтверждают эти клинические отчеты.
Метронидазол в клинической практике
Метронидазол эффективен для лечения анаэробных инфекций, таких как внутрибрюшные инфекции, гинекологические инфекции, сепсис, эндокардит, инфекции костей и суставов, инфекции центральной нервной системы, инфекции дыхательных путей, инфекции кожи и структур кожи, а также инфекции полости рта и зубов. инфекции.Метронидазол также используется в качестве профилактики перед абдоминальными и гинекологическими хирургическими вмешательствами, чтобы снизить риск послеоперационной анаэробной инфекции. Для лечения смешанной аэробной и анаэробной инфекции метронидазол следует использовать в сочетании с другими антибактериальными средствами, которые подходят для лечения аэробной инфекции, поскольку он неэффективен против аэробных бактерий (Таблица 1). Метронидазол также дает хорошие клинические результаты, когда он используется для лечения лямблиоза, трихомониаза и амебиаза, и рекомендуется для лечения пациентов с бактериальным вагинозом или неспецифическим вагинитом, вызванным G. vaginalis.
vaginalis.
Таблица 1
Клиническое применение метронидазола
Таблица 1
Клиническое применение метронидазола
В соответствии с международными рекомендациями, метронидазол также является компонентом комбинированных схем лечения (например, в комбинации с омепразолом, кларитромицином и амоксициллином) для лечения инфекций H. pylori , таких как гастродуоденальные язвы. Кроме того, лечение метронидазолом рассматривается для пациентов с болезнью Крона, которая не реагирует на сульфасалазин.Местно применяемый метронидазол эффективен для лечения розацеа от умеренной до тяжелой. Кроме того, гель с метронидазолом используется в стоматологии для лечения периодонтита у пациентов, у которых механическая обработка раны неэффективна или невозможна.
Лечение метронидазолом C. difficile . В течение последних нескольких лет сообщалось о растущем числе клинических неудач лечения метронидазолом инфекции C. difficile [5].Причины меньшей эффективности метронидазола по сравнению с ванкомицином не очевидны. Большинство штаммов C. difficile все еще чувствительны к метронидазолу. Считается, что фармакокинетические и фармакодинамические свойства метронидазола являются причиной клинических неудач. Для пациентов с тяжелой инфекцией C. difficile в Северной Америке рекомендуется терапия ванкомицином, но она дает различные клинические ответы [6]. Таким образом, новые агенты исследуются по этому показанию.Было продемонстрировано, что из противомикробных препаратов фидоксамицин, рамопланин и рифаксимин проявляют активность в отношении C. difficile [7]. Другой подход заключался в разработке вещества, связывающего токсины, толевамера; однако исследования фазы 3 показали, что он уступает терапии ванкомицином. Моноклональные антитела и вакцина C.difficile также проходят фазу 2 испытаний. Пробиотики, такие как Lactobacillus rhamnosus GG и Saccharomyces boulardii , не дали положительных клинических результатов.
difficile [5].Причины меньшей эффективности метронидазола по сравнению с ванкомицином не очевидны. Большинство штаммов C. difficile все еще чувствительны к метронидазолу. Считается, что фармакокинетические и фармакодинамические свойства метронидазола являются причиной клинических неудач. Для пациентов с тяжелой инфекцией C. difficile в Северной Америке рекомендуется терапия ванкомицином, но она дает различные клинические ответы [6]. Таким образом, новые агенты исследуются по этому показанию.Было продемонстрировано, что из противомикробных препаратов фидоксамицин, рамопланин и рифаксимин проявляют активность в отношении C. difficile [7]. Другой подход заключался в разработке вещества, связывающего токсины, толевамера; однако исследования фазы 3 показали, что он уступает терапии ванкомицином. Моноклональные антитела и вакцина C.difficile также проходят фазу 2 испытаний. Пробиотики, такие как Lactobacillus rhamnosus GG и Saccharomyces boulardii , не дали положительных клинических результатов. Лечение пациентов с множественными рецидивами инфекции C. difficile оказалось самой сложной задачей. Одним из новых подходов может быть использование метронидазола в различных комбинациях с этими новыми противомикробными средствами, связывающими токсины, иммуномодуляторами, нетоксигенными штаммами C. difficile и / или пробиотиками. Рекомендуются клинические испытания терапевтических комбинаций этих агентов.
Лечение пациентов с множественными рецидивами инфекции C. difficile оказалось самой сложной задачей. Одним из новых подходов может быть использование метронидазола в различных комбинациях с этими новыми противомикробными средствами, связывающими токсины, иммуномодуляторами, нетоксигенными штаммами C. difficile и / или пробиотиками. Рекомендуются клинические испытания терапевтических комбинаций этих агентов.
Метронидазол для лечения интраабдоминальных инфекций . Осложненные и серьезные внутрибрюшные инфекции часто встречаются в клинической медицине, и их лечение требует передовых больничных ресурсов.За последние 10 лет лечение интраабдоминальных инфекций значительно улучшилось. Правильное использование противомикробных средств обязательно. Новое руководство по диагностике и лечению осложненных внутрибрюшных инфекций у взрослых и детей было написано Американским обществом инфекционных болезней, Обществом хирургических инфекций и Обществом педиатрических инфекционных болезней, и в настоящее время они пересматриваются (Соломкин Дж. С., личное сообщение ) (Таблица 2). В данном руководстве инфекции разделяются на 2 категории: инфекции, приобретенные в сообществе, и инфекции, связанные с оказанием медицинской помощи.При умеренных внебольничных инфекциях у взрослых рекомендуется использовать метронидазол в сочетании с цефазолином, цефуроксимом, цефтриаксоном или хинолоном. Метронидазол вместе с цефтазидином или цефепимом или монотерапия карбапенемами и пиперациллин-тазобактамом рекомендуется для лечения тяжелой внебольничной внутрибрюшной инфекции. Детям рекомендуется метронидазол в сочетании с цефуроксимом или цефтриаксоном. Альтернативным средством является цефокситин. Пероральный метронидазол в комбинации с пероральными цефалоспоринами второго или третьего поколения также может быть эффективным.Связанные с оказанием медицинской помощи внутрибрюшные инфекции часто вызываются более устойчивыми к лекарствам микроорганизмами, такими как Staphylococcus aureus , энтерококки, Pseudomonas aeruginosa, Acinetobacter baumanni, виды Klebsiella , виды Enterobacter , виды и Proteus Candida видов.
С., личное сообщение ) (Таблица 2). В данном руководстве инфекции разделяются на 2 категории: инфекции, приобретенные в сообществе, и инфекции, связанные с оказанием медицинской помощи.При умеренных внебольничных инфекциях у взрослых рекомендуется использовать метронидазол в сочетании с цефазолином, цефуроксимом, цефтриаксоном или хинолоном. Метронидазол вместе с цефтазидином или цефепимом или монотерапия карбапенемами и пиперациллин-тазобактамом рекомендуется для лечения тяжелой внебольничной внутрибрюшной инфекции. Детям рекомендуется метронидазол в сочетании с цефуроксимом или цефтриаксоном. Альтернативным средством является цефокситин. Пероральный метронидазол в комбинации с пероральными цефалоспоринами второго или третьего поколения также может быть эффективным.Связанные с оказанием медицинской помощи внутрибрюшные инфекции часто вызываются более устойчивыми к лекарствам микроорганизмами, такими как Staphylococcus aureus , энтерококки, Pseudomonas aeruginosa, Acinetobacter baumanni, виды Klebsiella , виды Enterobacter , виды и Proteus Candida видов. Для этих инфекций рекомендуется комбинированное лекарственное лечение, основанное на типах восприимчивости микроорганизмов.
Для этих инфекций рекомендуется комбинированное лекарственное лечение, основанное на типах восприимчивости микроорганизмов.
Выздоравливающих пациентов с осложненными внутрибрюшными инфекциями часто можно лечить пероральными противомикробными препаратами.Для взрослых может быть эффективным метронидазол в сочетании с фторхинолоном или триметоприм-сульфаметоксазолом. Детям можно назначать метронидазол перорально в сочетании с пероральными цефалоспоринами второго или третьего поколения.
Благоприятная эффективность метронидазола для лечения интраабдоминальных инфекций была недавно показана Matthaiou et al [8] в метаанализе, сравнивающем лечение метронидазолом и ципрофлоксацином с лечением β-лактамными антибиотиками широкого спектра действия.Авторы обнаружили, что для пациентов с интраабдоминальными инфекциями лечение метронидазолом и ципрофлоксацином было связано с большим успехом, чем лечение β-лактамными агентами. Недавно Wang et al [9] показали, что 1 г метронидазола, вводимый внутривенно один раз в день для лечения тяжелых внутрибрюшных и тазовых инфекций, имеет фармакокинетические и фармакоэкономические преимущества по сравнению с лечением, назначаемым каждые 6-8 часов.
Механизмы действия и устойчивость к метронидазолу
Метронидазол активен в отношении множества простейших и бактерий.Он проникает в клетку в виде пролекарства путем пассивной диффузии и активируется либо в цитоплазме бактерий, либо в специфических органеллах простейших, в то время как лекарственно-устойчивые клетки испытывают недостаток в активации лекарства. Молекула метронидазола превращается в короткоживущий свободный нитрозо-радикал за счет внутриклеточного восстановления, которое включает перенос электрона на нитрогруппу лекарственного средства. Эта форма препарата цитотоксична и может взаимодействовать с молекулой ДНК. Фактический механизм действия еще полностью не выяснен, но включает ингибирование синтеза ДНК и повреждение ДНК в результате окисления, вызывая одноцепочечные и двухцепочечные разрывы, которые приводят к деградации ДНК и гибели клеток.Активированная восстановленная молекула метронидазола неспецифически связывается с бактериальной ДНК, инактивируя ДНК и ферменты организма и приводя к высокому уровню разрыва ДНК с немедленным действием препарата, но без лизиса клеток [10, 11]. В аэробных клетках отсутствуют белки-переносчики электронов с достаточным отрицательным окислительно-восстановительным потенциалом; следовательно, препарат активен только против бактерий с анаэробным метаболизмом, хотя препарат эффективен против некоторых микроаэрофилов, таких как H. pylori. Кроме того, повторное окисление может происходить в присутствии молекулярного кислорода и может превращать соединение обратно в его исходную неактивную форму [12].Доноры электронов, участвующие в процессе восстановления, различаются в зависимости от организма. В анаэробных бактериях акцепторы электронов флаводоксин и ферредоксин, которые получают электроны от комплекса пируват-ферредоксин оксиредуктаза, играют важную роль, хотя другие ферменты и компоненты переноса электронов также могут участвовать в этом процессе. Каждый из этих акцепторов имеет потенциал восстановления ниже, чем у молекулы метронидазола, и тем самым будет отдавать свои электроны лекарству [12]. В г.pylori , в чувствительность к метронидазолу, по-видимому, вовлечен отдельный механизм, который включает стадию переноса 2-х электронов при восстановлении соединения с использованием нечувствительной к кислороду нитроредуктазы (rdxA).
В аэробных клетках отсутствуют белки-переносчики электронов с достаточным отрицательным окислительно-восстановительным потенциалом; следовательно, препарат активен только против бактерий с анаэробным метаболизмом, хотя препарат эффективен против некоторых микроаэрофилов, таких как H. pylori. Кроме того, повторное окисление может происходить в присутствии молекулярного кислорода и может превращать соединение обратно в его исходную неактивную форму [12].Доноры электронов, участвующие в процессе восстановления, различаются в зависимости от организма. В анаэробных бактериях акцепторы электронов флаводоксин и ферредоксин, которые получают электроны от комплекса пируват-ферредоксин оксиредуктаза, играют важную роль, хотя другие ферменты и компоненты переноса электронов также могут участвовать в этом процессе. Каждый из этих акцепторов имеет потенциал восстановления ниже, чем у молекулы метронидазола, и тем самым будет отдавать свои электроны лекарству [12]. В г.pylori , в чувствительность к метронидазолу, по-видимому, вовлечен отдельный механизм, который включает стадию переноса 2-х электронов при восстановлении соединения с использованием нечувствительной к кислороду нитроредуктазы (rdxA). Клоны, устойчивые к метронидазолу, обычно мутируют в гене rdxA [10, 13].
Клоны, устойчивые к метронидазолу, обычно мутируют в гене rdxA [10, 13].
Было предложено несколько механизмов устойчивости анаэробных бактерий к метронидазолу. Эти механизмы различаются у разных организмов, но основной причиной устойчивости является снижение поглощения лекарственного средства или изменение эффективности восстановления (таблица 3).Эти 2 механизма действуют вместе; снижение активности нитроредуктазы приводит к снижению поглощения препарата. Другие механизмы включают активный отток, инактивацию препарата и усиление репарации повреждений ДНК [10]. Гены специфической устойчивости (nim) , придающие устойчивость к нитроимидазолам, были выделены у разных родов грамположительных и грамотрицательных анаэробных бактерий, в том числе у видов Bacteroides [14, 15]. Было показано, что перенос этих генов придает устойчивость к метронидазолу у реципиентов, инфицированных чувствительным вирусом [16].Гены nim кодируют альтернативную редуктазу, которая может превращать нитроимидазол в нетоксичное производное, тем самым предотвращая токсический эффект, вызывающий разрушение ДНК [12, 17]. К настоящему времени обнаружено 7 членов генов — от ним A до ним G, хотя обнаружение новых вариантов указывает на существование еще большего разнообразия этих генов в анаэробном сообществе, чем первоначально ожидалось. Исследования распространенности ним генов зафиксировали чрезмерную представленность ним A среди анаэробов [15].Гены nim обычно обнаруживаются на низкокопийных плазмидах, но также локализуются на бактериальной хромосоме и, как было показано, могут передаваться посредством процесса конъюгирования. Специфические регуляторные элементы, известные как инсерционные последовательности, часто связаны с генами nim . Элементы инсерционной последовательности подвижны и, как полагают, участвуют в пластичности геномов прокариот. Им была приписана роль в экспрессии нескольких генов устойчивости у видов Bacteroides , в том числе для метронидазола, эритромицин-клиндамицина, цефокситина и карбапенемов.Эти элементы можно найти на бактериальной хромосоме, на плазмидах и во множестве копий [18].
К настоящему времени обнаружено 7 членов генов — от ним A до ним G, хотя обнаружение новых вариантов указывает на существование еще большего разнообразия этих генов в анаэробном сообществе, чем первоначально ожидалось. Исследования распространенности ним генов зафиксировали чрезмерную представленность ним A среди анаэробов [15].Гены nim обычно обнаруживаются на низкокопийных плазмидах, но также локализуются на бактериальной хромосоме и, как было показано, могут передаваться посредством процесса конъюгирования. Специфические регуляторные элементы, известные как инсерционные последовательности, часто связаны с генами nim . Элементы инсерционной последовательности подвижны и, как полагают, участвуют в пластичности геномов прокариот. Им была приписана роль в экспрессии нескольких генов устойчивости у видов Bacteroides , в том числе для метронидазола, эритромицин-клиндамицина, цефокситина и карбапенемов.Эти элементы можно найти на бактериальной хромосоме, на плазмидах и во множестве копий [18].
Таблица 3
Предлагаемые механизмы устойчивости к метронидазолу у анаэробных бактерий
Таблица 3
Предлагаемые механизмы устойчивости к метронидазолу у анаэробных бактерий
Присутствие генов ним не всегда связано с устойчивостью, а их фактическое влияние Клинически значимая резистентность к метронидазолу еще не ясна. nim — Отрицательные штаммы, проявляющие высокий уровень устойчивости, выделяются время от времени, что указывает на важность дополнительных механизмов устойчивости. Тем не менее, наличие nim генов значительно увеличивает риск снижения чувствительности к метронидазолу [15]. Среди> 1500 исследованных клинических штаммов в исследовании Löfmark et al [15], 2 различные популяции с точки зрения восприимчивости могут быть выделены в соответствии с распределением минимальной ингибирующей концентрации (МИК) для штаммов nim -положительных и nim -отрицательных штаммов. [15].Таким образом, был выявлен значительный относительный риск резистентности к метронидазолу (МИК, ≥32 мг / л; согласно определению Института клинических и лабораторных стандартов) среди ним -положительных штаммов (отношение шансов 26; 95% доверительный интервал 4,6–2) 147), тогда как риск снижения чувствительности (МПК, ≥8 мг / л) был даже выше среди нимей -положительных штаммов (отношение шансов, 53; 95% доверительный интервал, 19–147). Эта последняя точка разрыва отделяет нормальную популяцию восприимчивых изолятов от изолятов, экспрессирующих детерминанты устойчивости, и также считается европейской точкой разрыва для устойчивости к метронидазолу [19].
Эта последняя точка разрыва отделяет нормальную популяцию восприимчивых изолятов от изолятов, экспрессирующих детерминанты устойчивости, и также считается европейской точкой разрыва для устойчивости к метронидазолу [19].
Другие механизмы, которые могут способствовать развитию устойчивости у видов Bacteroides , включают откачивающие насосы. О какой-либо системе оттока у видов Bacteroides существует мало или совсем нет данных, но избыточная экспрессия насосов оттока часто участвует в множественной лекарственной устойчивости у других видов и к другим антибиотикам. Pumbwe et al [20, 21] предполагают, что избыточная экспрессия оттока играет роль в устойчивости к метронидазолу и может вызывать устойчивость к фторхинолонам от низкой до средней и высокую устойчивость к β-лактамам у клинических штаммов Bacteroides .Этот механизм может играть важную роль в увеличении числа изолированных клинических штаммов с множественной лекарственной устойчивостью, в которых отсутствует какой-либо из известных nim генов. Требуются дополнительные исследования. Изменение систем репарации ДНК, играющих роль в устойчивости к метронидазолу у H. pylori , является еще одним не полностью изученным механизмом у штаммов Bacteroides . Избыточная экспрессия ферментов, участвующих в процессе, коррелирует со снижением чувствительности к антибиотикам.Сильный кандидат — белок recA; мутанты, дефицитные по его экспрессии, чувствительны к кислородному стрессу и действию метронидазола. Другие гены семейства rec также были предложены для участия в репарации ДНК, хотя они не были так хорошо изучены [22].
Требуются дополнительные исследования. Изменение систем репарации ДНК, играющих роль в устойчивости к метронидазолу у H. pylori , является еще одним не полностью изученным механизмом у штаммов Bacteroides . Избыточная экспрессия ферментов, участвующих в процессе, коррелирует со снижением чувствительности к антибиотикам.Сильный кандидат — белок recA; мутанты, дефицитные по его экспрессии, чувствительны к кислородному стрессу и действию метронидазола. Другие гены семейства rec также были предложены для участия в репарации ДНК, хотя они не были так хорошо изучены [22].
Механизм индуцибельной устойчивости к метронидазолу — еще одна особенность препарата метронидазол, которая может иметь клинические последствия. Обратимая и необратимая резистентность высокого уровня была индуцирована у чувствительных клинических штаммов Bacteroides с использованием субингибирующих концентраций метронидазола [15, 23].Субингибирующие концентрации метронидазола могут влиять на клеточные свойства членов группы B. fragilis , что влияет на их взаимодействие с защитой хозяина [24]. В анализе in vitro было показано, что устойчивость к метронидазолу связана с превосходной активностью интернализации H. pylori , обеспечивая защиту от лечения антибиотиками [25].
fragilis , что влияет на их взаимодействие с защитой хозяина [24]. В анализе in vitro было показано, что устойчивость к метронидазолу связана с превосходной активностью интернализации H. pylori , обеспечивая защиту от лечения антибиотиками [25].
Метронидазол и нормальная микрофлора
Было показано, что изменения в бактериальном составе и разрастание дрожжей, а также отбор устойчивых штаммов связаны с приемом метронидазола в сочетании с другими агентами, такими как амоксициллин и кларитромицин [26].Воздействие метронидазола на нормальную микрофлору варьируется в зависимости от пораженного участка тела. Концентрации метронидазола, превышающие значения МПК анаэробов, обнаруживаются во время лечения в жидкостях организма, таких как слюна, что может объяснять уменьшение количества анаэробных бактерий ротоглотки после комбинированного лечения метронидазолом и кларитромицином [27]. В исследовании Adamsson и др. [27] также было зарегистрировано подавление анаэробной флоры кишечника, вероятно, в результате введения кларитромицина.Концентрация активного метронидазола в кале при приеме невысока, так как средство хорошо всасывается и выводится преимущественно за счет метаболизма печени; однако высокие концентрации были измерены в ткани толстой кишки [28]. После перорального приема одного метронидазола в нормальной микрофлоре кишечника наблюдались лишь незначительные изменения. Известная клиническая эффективность перорального приема метронидазола при лечении диареи и колита, вызванных C. difficile , объясняется высоким уровнем в плазме крови в сочетании с повышенным проникновением метронидазола через поврежденную слизистую оболочку толстой кишки у инфицированных пациентов [26].Считается, что большая часть метронидазола, поражающего C. difficile , попадает в кишечник путем диффузии из сыворотки крови в слизистую оболочку кишечника.
[27] также было зарегистрировано подавление анаэробной флоры кишечника, вероятно, в результате введения кларитромицина.Концентрация активного метронидазола в кале при приеме невысока, так как средство хорошо всасывается и выводится преимущественно за счет метаболизма печени; однако высокие концентрации были измерены в ткани толстой кишки [28]. После перорального приема одного метронидазола в нормальной микрофлоре кишечника наблюдались лишь незначительные изменения. Известная клиническая эффективность перорального приема метронидазола при лечении диареи и колита, вызванных C. difficile , объясняется высоким уровнем в плазме крови в сочетании с повышенным проникновением метронидазола через поврежденную слизистую оболочку толстой кишки у инфицированных пациентов [26].Считается, что большая часть метронидазола, поражающего C. difficile , попадает в кишечник путем диффузии из сыворотки крови в слизистую оболочку кишечника.
Нормальная микрофлора служит резервуаром детерминант устойчивости к антибиотикам, где может происходить некоторое распространение устойчивости [29, 30]. Практически все гены у видов Bacteroides , кодирующие устойчивость к антибиотикам, включая метронидазол, были обнаружены на трансмиссивных элементах [18, 31]. Эта возможность передачи может способствовать распространению сопротивления; до сих пор устойчивость к метронидазолу оставалась низкой.
Практически все гены у видов Bacteroides , кодирующие устойчивость к антибиотикам, включая метронидазол, были обнаружены на трансмиссивных элементах [18, 31]. Эта возможность передачи может способствовать распространению сопротивления; до сих пор устойчивость к метронидазолу оставалась низкой.
Уровни устойчивости к метронидазолу
Устойчивость к анаэробным патогенам в целом остается низкой; однако паттерны восприимчивости анаэробных бактерий претерпевают изменения, и в последние годы сообщалось о снижении чувствительности in vitro к различным противомикробным препаратам. Эти данные получены преимущественно из международных и национальных исследований; индивидуальные обследования в больницах на чувствительность к анаэробным бактериям остаются редкостью (таблица 4).Практика во многих лабораториях определения облигатных анаэробов по чувствительности к метронидазолу является фактором, который способствует вероятной недооценке истинных показателей устойчивости. Предполагается, что наросты вокруг дисков являются факультативными анаэробами с естественно сниженной восприимчивостью, и эти штаммы не исследовались в дальнейшем [46]. Следовательно, лечение анаэробных инфекций, как правило, является эмпирическим и основано на опубликованных отчетах о показателях восприимчивости, что подчеркивает важность справочных лабораторий, предоставляющих достоверную и обновленную информацию [47].У анаэробов наблюдается общее снижение восприимчивости к метронидазолу. Большинство неспорообразующих грамположительных анаэробных бактерий, включая изоляты видов Actinomyces, Bifidobacterium, Eubacterium, Lactobacillus и Propionibacterium , по своей природе обладают пониженной чувствительностью к метронидазолу. Сообщалось о резистентности к метронидазолу у видов Sutterella [48]. Чувствительность по-прежнему очень высока у видов Fusobacterium, Prevotella и Porphymonas ; грамположительные анаэробные кокки; и все видов Bacteroides [34].
Предполагается, что наросты вокруг дисков являются факультативными анаэробами с естественно сниженной восприимчивостью, и эти штаммы не исследовались в дальнейшем [46]. Следовательно, лечение анаэробных инфекций, как правило, является эмпирическим и основано на опубликованных отчетах о показателях восприимчивости, что подчеркивает важность справочных лабораторий, предоставляющих достоверную и обновленную информацию [47].У анаэробов наблюдается общее снижение восприимчивости к метронидазолу. Большинство неспорообразующих грамположительных анаэробных бактерий, включая изоляты видов Actinomyces, Bifidobacterium, Eubacterium, Lactobacillus и Propionibacterium , по своей природе обладают пониженной чувствительностью к метронидазолу. Сообщалось о резистентности к метронидазолу у видов Sutterella [48]. Чувствительность по-прежнему очень высока у видов Fusobacterium, Prevotella и Porphymonas ; грамположительные анаэробные кокки; и все видов Bacteroides [34].
Таблица 4
Избранные опубликованные данные о распределении минимальных ингибирующих концентраций (МИК) метронидазола среди клинических изолятов Bacteroides fragilis
Таблица 4
Избранные опубликованные данные о распределении минимальных ингибирующих концентраций (МИК) для метронида Клинические изоляты Bacteroides fragilis
Бактерии, принадлежащие к группе B. fragilis , являются клинически наиболее часто встречающимися анаэробными патогенами.Метронидазол был препаратом выбора для лечения инфекции Bacteroides и остается надежным для этого применения [49]. Первый устойчивый к метронидазолу штамм Bacteroides был зарегистрирован в 1978 г. [50]. Резистентность к метронидазолу среди этой группы обычно ниже 1%, но в 1998 г. в Соединенном Королевстве были зарегистрированы уровни до 7,5% [46]. По сравнению с уровнем резистентности к метронидазолу, составлявшим 1,9% в 1995 г. и 3,8% в 1997 г., показатель 7,5% мог представлять возможное повышение устойчивости у B. fragilis , который был достигнут при МИК ≥32 мг / л, но он также мог отражать систематическую ошибку отбора материала, отправленного в референс-лабораторию. Истинную заболеваемость оценить сложно. Штаммы, устойчивые к метронидазолу с низким уровнем активности, могут быть упущены из виду, потому что порог в 32 мг / л, установленный Институтом клинических и лабораторных стандартов, намного выше порогового уровня в 4 мг / л для штаммов, изолированных в сообществе. Тем не менее, устойчивость B. fragilis к метронидазолу является низкой, согласно принятым контрольным точкам и международным данным.Пониженная восприимчивость к метронидазолу при МПК 4–16 мг / л встречается чаще (до 4,5%), что указывает на наличие механизмов резистентности [32, 33]. Несмотря на низкий уровень устойчивости к метронидазолу, сообщалось о неудачах лечения, связанных с устойчивостью к метронидазолу, и были идентифицированы штаммы с множественной лекарственной устойчивостью [51, 52]. Во многих случаях инфекция не может быть связана с одним патогеном из-за отсутствия идентификации и тестирования на чувствительность анаэробов, а также из-за полимикробной природы анаэробных инфекций, которые также часто устраняются с помощью дренажа или хирургического вмешательства.
fragilis , который был достигнут при МИК ≥32 мг / л, но он также мог отражать систематическую ошибку отбора материала, отправленного в референс-лабораторию. Истинную заболеваемость оценить сложно. Штаммы, устойчивые к метронидазолу с низким уровнем активности, могут быть упущены из виду, потому что порог в 32 мг / л, установленный Институтом клинических и лабораторных стандартов, намного выше порогового уровня в 4 мг / л для штаммов, изолированных в сообществе. Тем не менее, устойчивость B. fragilis к метронидазолу является низкой, согласно принятым контрольным точкам и международным данным.Пониженная восприимчивость к метронидазолу при МПК 4–16 мг / л встречается чаще (до 4,5%), что указывает на наличие механизмов резистентности [32, 33]. Несмотря на низкий уровень устойчивости к метронидазолу, сообщалось о неудачах лечения, связанных с устойчивостью к метронидазолу, и были идентифицированы штаммы с множественной лекарственной устойчивостью [51, 52]. Во многих случаях инфекция не может быть связана с одним патогеном из-за отсутствия идентификации и тестирования на чувствительность анаэробов, а также из-за полимикробной природы анаэробных инфекций, которые также часто устраняются с помощью дренажа или хирургического вмешательства. Результаты ретроспективных и проспективных исследований коррелировали клиническую неудачу с устойчивостью к антибиотикам у анаэробных бактерий [47, 53].
Результаты ретроспективных и проспективных исследований коррелировали клиническую неудачу с устойчивостью к антибиотикам у анаэробных бактерий [47, 53].
Не сообщалось о значительной клинической устойчивости к метронидазолу или ванкомицину у штаммов C. difficile . Были выделены некоторые устойчивые к метронидазолу штаммы C. difficile ; однако они редко выделяются среди токсигенных бактерий. В исследовании Wong et al [54], который сообщил о первом хорошо задокументированном случае резистентности к метронидазолу C.difficile у пациента с диареей, ассоциированной с C. difficile , среди 100 штаммов обнаружен 1 токсигенно-устойчивый изолят [55]. В отчете Анаэробного референс-центра лабораторной службы общественного здравоохранения Соединенного Королевства ни один клинический изолят из более чем 10 000 протестированных штаммов не был устойчивым, тогда как был обнаружен только один устойчивый нетоксигенный штамм (экологического происхождения) [56]. Неудачи лечения не являются редкостью, но еще не были однозначно связаны с лекарственно-устойчивыми штаммами.В 10-летнем проспективном исследовании изолятов от пациентов, перенесших неэффективность лечения, все изоляты имели МПК <1 мг / л; таким образом, пониженная восприимчивость инфицированных штаммов C. difficile не считалась причиной неудач [55].
Неудачи лечения не являются редкостью, но еще не были однозначно связаны с лекарственно-устойчивыми штаммами.В 10-летнем проспективном исследовании изолятов от пациентов, перенесших неэффективность лечения, все изоляты имели МПК <1 мг / л; таким образом, пониженная восприимчивость инфицированных штаммов C. difficile не считалась причиной неудач [55].
Метронидазол широко используется в качестве терапевтического средства против инфекции H. pylori в кишечнике человека и является одним из немногих антибиотиков — в первую очередь как часть комбинированной схемы лечения — которые эффективны в устранении микроорганизма.Антибиотикотерапия является обычной для этого состояния, но частота неудач достигает 20% при тройной комбинированной терапии, в которой метронидазол является краеугольным камнем [57]. Резистентность к метронидазолу считается основным фактором неэффективности лечения. Высокая частота использования метронидазола может вызвать устойчивость не только у H. pylori , но также у видов Bacteroides и других кишечных анаэробов. Благодаря хорошо известной безопасности и эффективности в клинической практике, метронидазол по-прежнему остается краеугольным камнем в лечении анаэробных инфекций во всем мире.
pylori , но также у видов Bacteroides и других кишечных анаэробов. Благодаря хорошо известной безопасности и эффективности в клинической практике, метронидазол по-прежнему остается краеугольным камнем в лечении анаэробных инфекций во всем мире.
Благодарности
Возможный конфликт интересов . Все авторы: без конфликтов.
Финансовая поддержка . Шведский исследовательский совет (348-2006-6862).
Дополнение к спонсорству . Эта статья является частью приложения, озаглавленного «Симпозиум в честь памяти Фрэнсиса П. Талли, доктора медицины, состоявшийся в Медицинском центре Тафтса и Медицинской школе Университета Тафтса, 11 июня 2007 г.», спонсором которого был Медицинский центр Тафтса, неограниченный грант от Cubist Pharmaceuticals.
Список литературы
1.
Метронидазол при остром язвенном гингивите
,
Ланцет
,
1962
, т.
279
(стр.
1191
—
0
) 2,,.
Метронидазол в сравнении с анаэробами: данные in vitro и первоначальные клинические наблюдения
,
Calif Med
,
1972
, vol.
117
(стр.
22
—
6
) 3,,.
Лечение анаэробных инфекций метронидазолом
,
Противомикробные препараты Chemother
,
1975
, т.
7
(стр.
672
—
5
) 4,,.
Метронидазол: терапевтический обзор и обновление
,
Drugs
,
1997
, vol.
54
(стр.
679
—
708
) 5.
Клиническое ведение болезни, ассоциированной с Clostridium difficile
,
Clin Infect Dis
,
2007
, vol.
45
Дополнение 2
(стр.
122
—
8
) 6,,,.
Сравнение ванкомицина и метронидазола для лечения диареи, ассоциированной с Clostridium difficile , стратифицированной по тяжести заболевания
,
Clin Infect Dis
,
2007
, vol.
45
(стр.
302
—
7
) 7,,.
Лечение инфекции Clostridium difficile
,
Clin Infect Dis
,
2008
, т.
46
Дополнение 1
(стр.
32
—
42
) 8,,,.
Ципрофлоксацин / метронидазол в сравнении с лечением интраабдоминальных инфекций на основе бета-лактама: метаанализ сравнительных исследований
,
Int J Antimicrob Agents
,
2006
, vol.
28
(стр.
159
—
65
) 9,,,,,.
Однократное введение метронидазола в сравнении с многократным ежедневным приемом при серьезных интраабдоминальных / тазовых инфекциях и инфекциях диабетической стопы
,
J Chemother
,
2007
, vol.
19
(стр.
410
—
6
) 10,.
Молекулярные основы устойчивости к метронидазолу патогенных бактерий и простейших
,
Drug Resist Updat
,
1999
, vol.
2
(стр.
289
—
94
) 11,,,,,.
Хромосомный разрыв в группе B. fragilis , вызванный лечением метронидазолом
,
Anaerobe
,
2000
, vol.
6
(стр.
149
—
53
) 12.
Генетика устойчивости к 5-нитроимидазолу у Bacteroides видов
,
Anaerobe
,
1996
, т.
2
(стр.
59
—
69
) 13,.
Мутационный анализ устойчивости к метронидазолу у Helicobacter pylori
,
Противомикробные агенты Chemother
,
2005
, vol.
49
(стр.
1236
—
7
) 14,,.
Гены устойчивости к нитроимидазолу ( ним B) в анаэробных грамположительных кокках (ранее Peptostreptococcus spp.)
,
J Antimicrob Chemother
,
2004
, vol.
54
(стр.
240
—
2
) 15,,,.
Индуцируемые гены устойчивости к метронидазолу и гены nim в клинических изолятах группы Bacteroides fragilis
,
Противомикробные агенты Chemother
,
2005
, vol.
49
(стр.
1253
—
6
) 16,,,.
Переносимая устойчивость к 5-нитроимидазолу в группе Bacteroides fragilis
,
Плазмида
,
1989
, т.
21
(стр.
151
—
4
) 17,,,,,.
Структурная основа устойчивости к 5-нитроимидазольным антибиотикам: кристаллическая структура NimA из Deinococcus radiodurans
,
J Biol Chem
,
2004
, vol.
279
(стр.
55840
—
9
) 18,,.
Роль конъюгативных транспозонов Bacteroides в распространении генов устойчивости к антибиотикам
,
Cell Mol Life Sci
,
2002
, vol.
59
(стр.
2044
—
54
) 19
Европейский комитет по тестированию чувствительности к противомикробным препаратам
20,,,.
BmeRABC5 — это система множественного оттока лекарств, которая может придавать устойчивость к метронидазолу у Bacteroides fragilis
,
Microb Drug Resist
,
2007
, vol.
13
(стр.
96
—
101
) 21,,.
Сверхэкспрессия эффлюксного насоса у мутантов Bacteroides fragilis с множественной антибиотикорезистентностью
,
Antimicrob Agents Chemother
,
2006
, vol.
50
(стр.
3150
—
3
) 22,,, et al.
Mycobacterium bovis BCG rec Делеционный мутант демонстрирует повышенную чувствительность к ДНК-повреждающим агентам, но выживаемость дикого типа в модели инфекции мыши
,
Infect Immun
,
2001
, vol.
69
(стр.
3562
—
8
) 23,.
Устойчивость к метронидазолу у Bacteroides spp. несущих генов и отбор медленнорастущих мутантов, устойчивых к метронидазолу
,
J Antimicrob Chemother
,
2004
, vol.
54
(стр.
109
—
16
) 24« и др.
Повышенная патогенность чувствительных штаммов группы Bacteroides fragilis , подвергнутых воздействию низких доз метронидазола
,
Microbes Infect
,
2003
, vol.
5
(стр.
19
—
26
) 25,,,,,.
Ассоциация устойчивости к антибиотикам и более высокой активности интернализации у устойчивых изолятов Helicobacter pylori
,
J Antimicrob Chemother
,
2006
, vol.
57
(стр.
466
—
71
) 26,,.
Влияние противомикробных препаратов на экологический баланс микрофлоры человека
,
Lancet Infect Dis
,
2001
, т.
1
(стр.
101
—
14
) 27,,,,.
Сравнительные эффекты омепразола, амоксициллина и метронидазола по сравнению с омепразолом, кларитромицином и метронидазолом на микрофлору полости рта, желудка и кишечника у пациентов, инфицированных Helicobacter pylori
,
J Antimicrob Chemother 1999
,
J Antimicrob Chemother.
44
(стр.
629
—
40
) 28,,,.
Сравнительная фармакокинетика метронидазола и тинидазола и их проникновение в ткани
,
Scand J Gastroenterol
,
1985
, vol.
20
(стр.
945
—
50
) 29,,,.
Свидетельства широкого переноса гена устойчивости среди Bacteroides spp. и среди Bacteroides и других родов в толстой кишке человека
,
Appl Environ Microbiol
,
2001
, vol.
67
(стр.
561
—
8
) 30,,.
Кишечные бактерии человека как резервуары для генов устойчивости к антибиотикам
,
Trends Microbiol
,
2004
, vol.
12
(стр.
412
—
6
) 31.
Роль конъюгативных транспозонов в распространении устойчивости к антибиотикам между бактериями, обитающими в желудочно-кишечном тракте
,
Cell Mol Life Sci
,
2002
, vol.
59
(стр.
2071
—
82
) 32,.
Чувствительность к противомикробным препаратам изолятов группы Bacteroides fragilis в Европе
,
Clin Microbiol Infect
,
2003
, т.
9
(стр.
475
—
88
) 33« и др.
Национальное исследование чувствительности Bacteroides fragilis группы : отчет и анализ тенденций в Соединенных Штатах с 1997 по 2004 год
,
Антимикробные агенты Chemother
,
2007
, vol.
51
(стр.
1649
—
55
) 34,,,,,.
Многоцентровое исследование изменяющейся чувствительности к антимикробным препаратам in vitro клинических изолятов группы Bacteroides fragilis , Prevotella, Fusobacterium, Porphyromonas и Peptostreptococcus , видов
,
30004 Antimicrob.
45
(стр.
1238
—
43
) 35« и др.
Чувствительность группы Bacteroides fragilis в США в 1981 г.
,
Противомикробные агенты Chemother
,
1983
, т.
23
(стр.
536
—
40
) 36,,,.
Группа Bacteroides fragilis : тенденции устойчивости
,
Curr Microbiol
,
2006
, vol.
52
(стр.
153
—
7
) 37,,,,,.
Пониженная восприимчивость к нитроимидазолам среди видов Bacteroides в Бразилии
,
Curr Microbiol
,
2006
, vol.
52
(стр.
27
—
32
) 38« и др.
Третье бельгийское многоцентровое исследование чувствительности анаэробных бактерий к антибиотикам
,
J Antimicrob Chemother
,
2007
, vol.
59
(стр.
132
—
9
) 39« и др.
Устойчивость анаэробных грамотрицательных бактерий к антибиотикам: уроки французского многоцентрового исследования
,
Anaerobe
,
2003
, vol.
9
(стр.
105
—
11
) 40,.
Чувствительность группы Bacteroides fragilis к новым хинолонам и другим стандартным антианаэробным агентам
,
J Antimicrob Chemother
,
2001
, vol.
48
(стр.
127
—
30
) 41,,,.
Чувствительность к антибиотикам изолятов анаэробных бактерий в культуре крови в больнице норвежского университета
,
APMIS
,
2007
, vol.
115
(стр.
956
—
61
) 42,,.
Чувствительность к антибиотикам in vitro и молекулярный анализ анаэробных бактерий, выделенных в Кейптауне, Южная Африка
,
J Antimicrob Chemother
,
1998
, vol.
42
(стр.
245
—
8
) 43,,,,.
Антимикробная чувствительность анаэробных бактерий в Новой Зеландии: 1999–2003 гг.
,
J Antimicrob Chemother
,
2006
, vol.
57
(стр.
992
—
8
) 44,,,.
Антимикробная чувствительность штаммов Bacteroides fragilis и Bacteroides thetaiotaomicron , выделенных из клинических образцов и кишечной микробиоты человека
,
Anaerobe
,
2004
, vol.
10
(стр.
255
—
9
) 45,,,,.
Многоцентровое исследование in vitro активности семи антимикробных препаратов, включая эртапенем, против недавно выделенных грамотрицательных анаэробных бактерий в Греции
,
Clin Microbiol Infect
,
2005
, vol.
11
(стр.
820
—
4
) 46,,.
Устойчивость к метронидазолу среди клинических изолятов, принадлежащих к группе Bacteroides fragilis : время для беспокойства?
,
J Antimicrob Chemother
,
1999
, т.
44
(стр.
580
—
1
) 47.
Анаэробы: устойчивость к антибиотикам, клиническое значение и роль тестирования на чувствительность
,
Anaerobe
,
2006
, vol.
12
(стр.
115
—
21
) 48,,,,,. ,
Wadsworth-KTL anaerobic bacteriology manua
,
2002
6-е изд.
Belmont, CA
Star Publishing
49,,.
Устойчивость к противомикробным препаратам и лечение анаэробных инфекций
,
Expert Rev Anti Infect Ther
,
2007
, vol.
5
(стр.
685
—
701
) 50,,,.
Bacteroides fragilis , резистентный к метронидазолу после длительной терапии
,
Ланцет
,
1978
, т.
1
(стр.
214
—
0
) 51,,,,.
Bacteroides видов с высокой устойчивостью к метронидазолу: возникающая клиническая проблема?
,
Clin Microbiol Infect
,
1999
, т.
5
(стр.
166
—
9
) 52,,,,.
Анаэробный сепсис, вызванный множественной лекарственной устойчивостью Bacteroides fragilis: микробиологическое излечение и клинический ответ на терапию линезолидом
,
Clin Infect Dis
,
2005
, vol.
40
(стр.
e67
—
8
) 53« и др.
Устойчивость к противомикробным препаратам и клинические исходы бактериемии Bacteroides : результаты многоцентрового проспективного наблюдательного исследования
,
Clin Infect Dis
,
2000
, vol.
30
(стр.
870
—
6
) 54,,,.
Тестирование чувствительности Clostridium difficile к метронидазолу и ванкомицину методом дисковой диффузии и Etest
,
Diagn Microbiol Infect Dis
,
1999
, vol.
34
(стр.
1
—
6
) 55,,.
Устойчивость к метронидазолу у Clostridium difficile
,
Clin Infect Dis
,
2000
, т.
31
(стр.
625
—
6
) 56,,,,.
Эпиднадзор за устойчивостью к метронидазолу и ванкомицину у генетически разных и эпидемических изолятов в Великобритании Clostridium difficile в большой клинической больнице
,
J Antimicrob Chemother
,
2005
, vol.
56
(стр.
988
—
9
) 57,.
Обзорная статья: лечение рефрактерной инфекции Helicobacter pylori
,
Aliment Pharmacol Ther
,
2003
, vol.
17
(стр.
1333
—
43
)
Рисунки и таблицы
Таблица 2
Противомикробные агенты для внутрибрюшных инфекций, рекомендованные Американским обществом инфекционных болезней, Обществом хирургических инфекций и Обществом детских инфекционных болезней
Таблица 2
Противомикробные агенты, рекомендуемые для внутрибрюшных инфекций Американским обществом инфекционистов, Обществом хирургических инфекций и Обществом педиатрических инфекционных болезней
© 2009 Американского общества инфекционистов.
анаэробных инфекций — HealthyChildren.org
Некоторые инфекции вызываются бактериями, которые не могут выжить или размножаться в присутствии кислорода. Эти бактерии, называемые анаэробами, обычно обитают в желудочно-кишечном тракте, где количество кислорода ограничено. По определению, термин анаэробный означает «жизнь без воздуха».
Вот краткое описание анаэробных инфекций, иногда поражающих детей.
Актиномикоз (опухоль челюсти) чаще всего вызывается разновидностью бактерий, называемых Actinomyces. Эта инфекция обычно возникает на лице и шее, иногда после стоматологической инфекции или такой процедуры, как удаление зуба или хирургическая операция на ротовой полости, или после травмы лица. Это может также повлиять на другие части тела, включая живот, где это может быть связано с перфорацией кишечника или травмой в этой области. При наличии этих инфекций могут образовываться абсцессы (скопления гноя). Актиномикоз редко развивается у младенцев и детей.
Актиномикоз редко развивается у младенцев и детей.
Лабораторные тесты могут подтвердить присутствие бактерий Actinomyces .Когда актиномикоз диагностирован, ваш врач может лечить его внутривенными антибиотиками (например, пенициллин, ампициллин) в течение 4-6 недель, а затем принимать высокие дозы антибиотиков внутрь в течение месяцев.
Bacteroides и Prevotella инфекции. Бактериальные организмы видов под названием Bacteroides и Prevotella являются анаэробными. Это обычные организмы во рту, желудочно-кишечном тракте и женских половых путях. Они могут вызывать инфекции в различных частях тела у детей и взрослых любого возраста.Наиболее распространены зубные инфекции, воспаление слизистой оболочки брюшной полости (перитонит) и абсцессы в брюшной полости, матке или трубах. В других частях тела эти бактерии были связаны с такими состояниями, как хронические инфекции уха, глубокие инфекции кожи и абсцессы легких.
Культуры могут быть собраны и отправлены в лабораторию для идентификации и подтверждения организмов, ответственных за инфекцию, с определением того, какие виды присутствуют: Bacteroides или Prevotella .Эти инфекции лечат антибиотиками, такими как клиндамицин или метронидазол. В большинстве случаев бактерии устойчивы к пенициллиновым препаратам. Если образовался абсцесс, возможно, потребуется его дренировать с помощью иглы или хирургическим путем.
Информация, содержащаяся на этом веб-сайте, не должна использоваться вместо медицинской помощи и рекомендаций вашего педиатра. Ваш педиатр может порекомендовать различные варианты лечения в зависимости от индивидуальных фактов и обстоятельств.
Bacteroides Infection Medication: Antibiotics, Other
Brook I. Местная микробная флора человека. Хирургические инфекционные болезни . 3-е изд. Норуолк, Коннектикут: Appleton & Lange; 1995. 37.
.
Jousime-Somers H, Summanen P, Citron DM. Бельмонт, Калифорния, Wadsworth-KTL Руководство по анаэробной бактериологии . 6-е изд. Star Publishing; 2002.
Brook I, Wexler HM, Goldstein EJ.Антианаэробные противомикробные препараты: анализ спектра и чувствительности. Clin Microbiol Ред. . 2013 июл.26 (3): 526-46. [Медлайн].
Брук I. Увеличение роста аэробных и факультативных бактерий при смешанных инфекциях, вызываемых видами Bacteroides. Инфекционный иммунитет . 1985 Декабрь 50 (3): 929-31. [Медлайн].
Goldstein EJC, Citron DM, Tyrrell KL. In vitro активность эравациклина и противомикробных препаратов сравнения против 143 недавних штаммов видов Bacteroides и Parabacteroides. Анаэроб . 2018 Август 52: 122-124. [Медлайн].
Merino VR, Nakano V, Liu C, Song Y, Finegold SM, Avila-Campos MJ. Количественное определение подтипов энтеротоксигенных Bacteroides fragilis, выделенных у детей с диареей и без нее. Дж. Клин Микробиол . 2011 Январь 49 (1): 416-8. [Медлайн].
Брук И. Микробиология и лечение абдоминальных инфекций. Dig Dis Sci . 2008 г., 53 (10): 2585-91. [Медлайн].
Finegold SM. Анаэробные бактерии в болезнях человека . Орландо, Флорида: Academic Press; 1977.
Брук I. Роль анаэробных бактерий в бактериемии. Анаэроб . 2010 июн. 16 (3): 183-9. [Медлайн].
Брук I. Роль бактерий, продуцирующих бета-лактамазы, в смешанных инфекциях. BMC Infect Dis . 2009 14 декабря 9: 202. [Медлайн]. [Полный текст].
Nord CE.Роль анаэробных бактерий в повторяющихся эпизодах синусита и тонзиллита. Clin Infect Dis . 1995 июн.20 (6): 1512-24. [Медлайн].
Брук И. Анаэробные бактерии в верхних дыхательных путях, инфекциях головы и шеи: микробиология и лечение. Анаэроб . 2012 Апрель 18 (2): 214-20. [Медлайн].
Брук И. Микробиология синуситов. Proc Am Thorac Soc . 2011 марта 8 (1): 90-100. [Медлайн].
Брук И.Пенициллиновая недостаточность в лечении стрептококкового фаринго-тонзиллита. Curr Infect Dis Rep . 2013 июн.15 (3): 232-5. [Медлайн].
Bartlett JG. Насколько важны анаэробные бактерии при аспирационной пневмонии: когда их лечить и какова оптимальная терапия. Инфекция Dis Clin North Am . 2013 27 марта (1): 149-55. [Медлайн].
Мазуски Ю.Е., Соломкин Ю.С. Внутрибрюшные инфекции. Surg Clin North Am .2009 Апрель 89 (2): 421-37, ix. [Медлайн].
Митчелл С., Прабху М. Воспалительное заболевание тазовых органов: современные концепции патогенеза, диагностики и лечения. Инфекция Dis Clin North Am . 2013 27 декабря (4): 793-809. [Медлайн].
Thomas N, Brook I. Инфекции, связанные с укусами животных: микробиология и лечение. Expert Rev Anti Infect Ther . 2011 Февраля 9 (2): 215-26. [Медлайн].
Brook I, Frazier EH.Клинико-микробиологические особенности некротического фасциита. Дж. Клин Микробиол . 1995 Сентябрь 33 (9): 2382-7. [Медлайн].
Брук I. Микробиология и лечение суставных и костных инфекций, вызванных анаэробными бактериями. Дж. Ортоп Ски . 2008 марта 13 (2): 160-9. [Медлайн].
Dorsher CW, Rosenblatt JE, Wilson WR, Ilstrup DM. Анаэробная бактериемия: скорость снижения за 15-летний период. Ред. Заразить Dis . 1991 июль-август.13 (4): 633-6. [Медлайн].
Lassmann B, Gustafson DR, Wood CM, Rosenblatt JE. Повторное появление анаэробной бактериемии. Clin Infect Dis . 2007 г., 1. 44 (7): 895-900. [Медлайн].
Феннер Л., Видмер А.Ф., Штрауб С., Фрей Р. Снижается ли частота анаэробной бактериемии? Анализ 114000 посевов крови за десятилетний период. Дж. Клин Микробиол . 2008 июл. 46 (7): 2432-4. [Медлайн].
Брук И.Роль анаэробных бактерий в бактериемии. Анаэроб . 2010 июн. 16 (3): 183-9. [Медлайн].
Джонсон-Бак А., Ли Дж., Тевари М., Уолтер Н.Г. Руководство по обнаружению нуклеиновых кислот с помощью кинетического снятия отпечатков пальцев. Методы . 2019 15 января 153: 3-12. [Медлайн].
Снидман Д.Р., Якобус Н.В., Макдермотт Л.А., Голан Й., Голдштейн Э.Дж., Харрелл Л. Обновленная информация об устойчивости группы Bacteroides fragilis и родственных видов с особым вниманием к карбапенемам 2006-2009 гг. Анаэроб . 2011 17 августа (4): 147-51. [Медлайн].
Goto T, Tanaka K, Minh Tran C, Watanabe K. Полная последовательность pBFUK1, мобилизуемой плазмиды, несущей карбапенемазу, из Bacteroides fragilis, и распределение pBFUK1-подобных плазмид среди клинических изолятов B. fragilis, устойчивых к карбапенемам. J Antibiot (Токио) . 2013 апр. 66 (4): 239-42. [Медлайн].
Hecht DW. Анаэробы: устойчивость к антибиотикам, клиническое значение и роль тестирования на чувствительность. Анаэроб . 2006 июн. 12 (3): 115-21. [Медлайн].
Шервуд Дж. Э., Фрейзер С., Цитрон Д. М., Векслер Х., Блейкли Дж., Джоблинг К. Множественные лекарственно-устойчивые бактерии Bacteroides fragilis, полученные из крови и тяжелых ран ног, вызванных самодельным взрывным устройством (СВУ) в Афганистане. Анаэроб . 2011 17 августа (4): 152-5. [Медлайн].
Центры по контролю и профилактике заболеваний (CDC). Bacteroides fragilis с множественной лекарственной устойчивостью — Сиэтл, Вашингтон, 2013 г. MMWR Morb Mortal Wkly Rep . 2013 30 августа. 62 (34): 694-6. [Медлайн].
Mastrantonio P, Cardines R, Spigaglia P. Олигонуклеотидные зонды для обнаружения цефалоспориназ среди штаммов Bacteroides. Противомикробные агенты Chemother . 1996 Апрель 40 (4): 1014-6. [Медлайн].
Снайдман Д.Р., Якобус Н.В., Макдермотт Л.А., Гольдштейн Е.Дж., Харрелл Л., Дженкинс С.Г. и др. Динамика устойчивости к противомикробным препаратам среди видов Bacteroides и Parabacteroides в Соединенных Штатах в 2010-2012 гг. По сравнению с 2008-2009 гг. Анаэроб . 2017 Февраль 43: 21–26. [Медлайн].
Лю CY, Huang YT, Liao CH, Yen LC, Lin HY, Hsueh PR. Тенденции к росту устойчивости к противомикробным препаратам среди клинически важных анаэробов и изолятов Bacteroides fragilis, вызывающих нозокомиальные инфекции: возникающая устойчивость к карбапенемам. Противомикробные агенты Chemother . 2008 Сентябрь 52 (9): 3161-8. [Медлайн].
Goldstein EJ, Citron DM, Merriam CV. Активность линезолида по сравнению с активностью выбранных макролидов и других агентов против аэробных и анаэробных патогенов, выделенных при инфекциях укусов мягких тканей у людей. Противомикробные агенты Chemother . 1999 июн. 43 (6): 1469-74. [Медлайн].
Sanai Y, Persson GR, Starr JR, Luis HS, Bernardo M, Leitao J. Наличие и устойчивость к антибиотикам Porphyromonas gingivalis, Prevotella intermedia и Prevotella nigrescens у детей. Дж Клин Периодонтол . 2002, 29 октября (10): 929-34. [Медлайн].
Niestępski S, Harnisz M, Korzeniewska E, Aguilera-Arreola MG, Contreras-Rodríguez A, Filipkowska Z, et al.Возникновение устойчивости к противомикробным препаратам у экологических штаммов группы Bacteroides fragilis. Окружающая среда Инт . 2019 Март 124: 408-419. [Медлайн].
Kierzkowska M, Majewska A, Szymanek-Majchrzak K, Sawicka-Grzelak A, Mlynarczyk A, Mlynarczyk G. Эффект клиндамицина против изолятов Bacteroides и Parabacteroides in vitro в Польше. J Glob Antimicrob Resist . 2018 июн.13: 49-52. [Медлайн].
Олдридж К.Е., Эшкрафт Д., Камбре К., Пирсон К.Л., Дженкинс С.Г., Розенблатт Дж.Многоцентровое исследование изменения чувствительности к противомикробным препаратам in vitro клинических изолятов группы Bacteroides fragilis, Prevotella, Fusobacterium, Porphyromonas и Peptostreptococcus. Противомикробные агенты Chemother . 2001 апр. 45 (4): 1238-43. [Медлайн].
Hansen KCM, Schwensen SAF, Henriksen DP, Justesen US, Sydenham TV. Устойчивость к противомикробным препаратам в группе Bacteroides fragilis в образцах фекалий пациентов, получающих антибиотики широкого спектра действия. Анаэроб . 2017 Октябрь 47: 79-85. [Медлайн].
Nord CE, Oprica C. Устойчивость к антибиотикам у Propionibacterium acnes. Микробиологические и клинические аспекты. Анаэроб . 2006 окт-дек. 12 (5-6): 207-10. [Медлайн].
Goldstein EJ, Citron DM, Warren YA, Tyrrell KL, Merriam CV, Fernandez H. Активность моксифлоксацина in vitro против 923 анаэробов, выделенных при внутрибрюшных инфекциях человека. Противомикробные агенты Chemother .2006 январь 50 (1): 148-55. [Медлайн].
Gao Q, Wu S, Xu T, Zhao X, Huang H, Hu F. Появление устойчивости к карбапенемам у Bacteroides fragilis в Китае. Int J Антимикробные агенты . 2019 июн. 53 (6): 859-863. [Медлайн].
Брук I. Антимикробное лечение анаэробных инфекций. Expert Opin Pharmacother . 2011 12 августа (11): 1691-707. [Медлайн].
Брук I. Анаэробные инфекции. Диагностика и лечение. Informa Healthcare USA, Inc . 4-е изд. Нью-Йорк, Нью-Йорк: 2007.
Ву М., МакНалти Н.П., Родионов Д.А., Хорошкин М.С., Гриффин Н.В., Ченг Дж. И др. Генетические детерминанты приспособленности in vivo и реакции на диету у нескольких кишечных бактерий человека. Наука . 2015 Октябрь 2. 350 (6256): aac5992. [Медлайн].
противомикробных препаратов, используемых при лечении анаэробных инфекций у детей
Beard, CM .; Noller, K.L .; О’Фаллон, М.; Курляндия, Л. и Доккрти, М.Б .: Отсутствие доказательств рака из-за использования метронидазола. Медицинский журнал Новой Англии 301: 519–522 (1979).
PubMed
Статья
CAS
Google ученый
Berlatzky, Y .; Рубин, С.З .; Michel, J .; Сакс, Т. и Шиллер, М .: Использование клиндамицина и гентамицина в хирургии детских колоний. Журнал детской хирургии 11: 943–946 (1976).
PubMed
Статья
CAS
Google ученый
Берман, Б.W .; Кинг, Ф. Х. младший, Рубенштейн, Д. С. и Лонг, С. С.: Менингит Bactcroides fragilis у новорожденного, успешно пролеченного метронидазолом. Журнал педиатрии 93: 793–795 (1979).
Google ученый
Брук, И.: Карбенициллин в лечении аспирационной пневмонии у детей. Текущие терапевтические исследования 23: 136–147 (1978).
Google ученый
Брук, И.: Клиндамицин в лечении аспирационной пневмонии у детей. Противомикробные агенты и химиотерапия 15: 342–345 (1979a).
PubMed
Статья
CAS
Google ученый
Брук, И .: Бактериология и лечение хронического среднего отита у детей. Ларингоскоп 89: 1129–1134 (1979b).
PubMed
CAS
Google ученый
Брук, И.: Анаэробные изоляты в лечении хронического рецидивирующего суперального отита с помощью одного карбенициллина и в сочетании с гентамицином.Инфекция 5: 247–251 (1979c).
Артикул
Google ученый
Brook, I .; Calhoun, L. и Yocum, P .: Бета-лактамаз-продуцирующие изоляты видов Bacteroides от детей. Антимикробные агенты и химиотерапия 18: 164–166 (1980).
PubMed
Статья
CAS
Google ученый
Брук, И.: Активность моксалактама (LY-P27935) против анаэробных микроорганизмов in vitro.Журнал антимикробной химиотерапии 6: 676–679 (1980).
PubMed
Статья
CAS
Google ученый
Brook, I .; Gillmore, J .; Coolbaugh, J.C. и Walker, R.I .: In vitro защита бета-гемолитических стрептококков группы A с помощью Bacteroides. Журнал антимикробной химиотерапии (в печати 1983 г.).
Google ученый
Брук, И .: Бактериология внутричерепного абсцесса у детей.Журнал нейрохирургии 54: 484–488 (1981).
PubMed
Статья
CAS
Google ученый
Брук, И.: Лечение анаэробных инфекций у детей метронидазолом. Фармакология развития и терапия 6: 187–198 (1983).
PubMed
CAS
Google ученый
Brook, I .; Coolbaugh, J.C. и Walker, R.I .: синергизм in vitro и in vivo между аминогликозидом и пенициллином против группы Bacteroides melaninogenicus .№ аннотации 653. Труды 22-й Международной конференции по противомикробным препаратам и химиотерапии, Флорида, 1982.
Bryan, L.E .; Кованд, С. и Ван Ден Эльзен, Х.М.: Механизм устойчивости к аминогликозидным антибиотикам у анаэробных бактерий: Clostridium perfringens и Bacteroides fragilis. Противомикробные агенты и химиотерапия 15: 7–13 (1979).
PubMed
Статья
CAS
Google ученый
Брайант Р.E .; Рашад, А.Л .; Mazza, J.A. и Hammond, D.: β- активность лактамаска в гное человека. Журнал инфекционных болезней 142: 594–601 (1980).
PubMed
Статья
CAS
Google ученый
Busch, D.F .; Jureshi, L.A .; Саттер, В. и Finegold, S.M .: Восприимчивость анаэробов дыхательных путей к пероральным пенициллинам и цефалоспоринам. Антимикробные агенты и химиотерапия 10: 713–720 (1976).
PubMed
Статья
CAS
Google ученый
Буш, Д.F .; Саттер, В. и Finegold, S.M .: Активность комбинаций противомикробных агентов против Bacteroides fragilis . Journal of Infectious Diseases 133: 321–328 (1976).
PubMed
Статья
CAS
Google ученый
Chow, A.W .; Монтгомери, Дж. З. и Гузе, Л.Б .: Парентеральная терапия клиндамицином при тяжелых анаэробных инфекциях. Архивы внутренней медицины 134: 78–82 (1974).
PubMed
Статья
CAS
Google ученый
Чоу, А.W .; Паттен, В. и Гузе, Л.Б .: Чувствительность анаэробных бактерий к метронидазолу: относительная устойчивость неспорообразующих грамположительных бацилл. Журнал инфекционных болезней 131: 182–185 (1975).
PubMed
Статья
CAS
Google ученый
Cohen, S.M .; Entruk, E .; Фон Эш, AM; Crovetti, A.J. и Брайан, Г.Т .: Канцерогенность 5-нитрофуранов, 5-нитромидазолов, 4-нитробензолов и родственных соединений. Журнал Национального института рака 51: 403–417 (1973).
PubMed
CAS
Google ученый
де Лувуа, Дж. И Херли, Р .: Инактивация пенициллина гнойным экссудатом. Британский медицинский журнал 1: 998–1000 (1977).
PubMed
Статья
Google ученый
Fass, R.J .; Ротили, К.А. и Прайор, Р.Б .: Взаимодействие клиндамицина и гентамицина in vitro. Противомикробные агенты и химиотерапия 6: 582–587 (1974).
PubMed
Статья
CAS
Google ученый
Finegold, S.M .; Харада, Н. и Миллер, Л.Г .: Активность линкомицина против анаэробов и влияние на нормальную фекальную флору человека. Противомикробные агенты и химиотерапия 6: 659–667 (1966).
Google ученый
Finegold, S.M .; Bartlett, J.G .; Чоу, A.W .; Флора, Д.Дж .; Грогач, С.Л .; Harder, E.J. и Талли Ф.П .: Управление анаэробными инфекциями. Анналы внутренней медицины 83: 375–389 (1975).
PubMed
CAS
Google ученый
Fiedelman, W. и Webb, CD .: Клиническая оценка карбенициллина при лечении инфекции, вызванной анаэробными бактериями. Текущие терапевтические исследования 18: 441–451 (1975).
PubMed
CAS
Google ученый
Finegold, S.М .: Анаэробные бактерии в болезнях человека (Academic Press, Нью-Йорк, 1977).
Google ученый
George, W.L .; Саттер, В.Л .; Goldstein, E.J.C .; Людсиг, С. и Finegold, S.M .: Этиология колита, связанного с антимикробными агентами. Ланцет 1: 802 (1978).
PubMed
Статья
CAS
Google ученый
Горбач С.Л. и Бартлетт Дж. Г .: Анаэробные инфекции.Медицинский журнал Новой Англии 290: 1177–1184, 1237–1245, 1289–1294 (1974).
PubMed
Статья
CAS
Google ученый
Горбач С.Л. и Thadepalli, H .: Клиндамицин в лечении чистых и смешанных анаэробных инфекций. Архивы внутренней медицины 134: 87–92 (1974).
PubMed
Статья
CAS
Google ученый
Hackman, A.S. и Уилкинс, Т.D .: Защита Fusobactcrium necrophorum от пенициллина с помощью Bacteroides fragilis in vivo. Антимикробные агенты и химиотерапия 7: 698–703 (1975).
PubMed
Статья
CAS
Google ученый
Хакман А. и Уилкинс Т.Д .: Влияние продукции пенициллиназы штаммами Bacteroides melaninogenicus и Bacteroides oralis на пенициллиновую терапию экспериментальной смешанной анаэробной инфекции у мышей. Архивы оральной биологии 21: 385–389 (1976).
PubMed
Статья
CAS
Google ученый
Hescltine, P.N.R .; Busch, D.F .; Meyer, R.D. и Finegold, S.M .: Cefoxitin: Клиническая оценка у 38 пациентов. Антимикробные агенты и химиотерапия 11: 427–434 (1977).
Артикул
Google ученый
Ingham, H.R .; Селкон, Дж. Б. и Роксби, С. М.: Бактериологическое исследование отогенных церебральных абсцессов: химиотерапевтическая роль метронидазола.Британский медицинский журнал 2: 991–994 (1977).
PubMed
Статья
CAS
Google ученый
Kagnoff, M.F .; Армстронг Д. и Блевинс А .: Бактериемия бактерий. Опыт работы в стационаре по поводу опухолевых заболеваний. Рак 29: 245–251 (1972).
PubMed
Статья
CAS
Google ученый
Laufer, J .; Mignon, H. и Videau, D.: L’association metronidazole-spiramycine: Concentrations et syntergie in situ comparecs aux CMI de la flore buccale.Revue de Stomatologie et de Chirurgie Maxillofaciale 74: 387–392 (1974).
CAS
Google ученый
Лоу, Б.Дж. и Маркс, М.И.: Отличный исход менингита Bacteroides у новорожденного, получавшего метронидазол. Педиатрия 66: 463–465 (1980).
PubMed
CAS
Google ученый
Ли, округ Колумбия: инфекции Bacteroides. Ланцет 2: 1081–1082 (1973).
PubMed
Статья
CAS
Google ученый
Льюис, П.; Goldstein, J.C .; Sutter, L. и Finegold, S.M .: терапия анаэробных инфекций эритромицином; в Current Chemotherapy, стр. 653–655 (Американское общество микробиологии, Вашингтон, округ Колумбия, 1978).
Google ученый
Масуда, Г. и Томиока, С .: Возможная активность бета-лактамаз, обнаруживаемая в инфекционных клинических образцах. Журнал антибиотиков (Токио) 30: 1093–1097 (1977).
Артикул
CAS
Google ученый
О’Грейди, Л.Р. и Ральф, E.D .: Анаэробный менингит и бактериемия, вызываемые видами Fusobacterium. Американский журнал болезней детей 130: 871–873 (1976).
PubMed
Google ученый
O’Keefe, J.P .; Tally, F.P .; Барза М. и Горбач С.Л .: Инактивация пенициллина G во время экспериментального заражения Bacteroides fragilis. Journal of Infectious Diseases 137: 437–442 (1978).
PubMed
Статья
Google ученый
Пинкус, Г.; Вето, Г. и Брауде, А .: Bacteroides pcnicillinase. Журнал бактериологии 96: 1437–1438 (1968).
PubMed
CAS
Google ученый
Rahal, J.J .: Комбинации антибиотиков: клиническое значение синергизма и антагонизма. Медицина 57: 179–195 (1978).
PubMed
Статья
Google ученый
Ralph, E.D. и Кирби У. М.: Уникальное бактерицидное действие метронидазола против Bacteroides fragilis и Clostridium perfringens .Антимикробные агенты и химиотерапия 8: 409–414 (1975).
PubMed
Статья
CAS
Google ученый
Randolph, M.F. и Моррис, К.Е .: колит, связанный с клиндамицином, у детей. Перспективное исследование и отрицательный отчет. Клиническая педиатрия 26: 722–725 (1977).
Артикул
Google ученый
Рединг, К. и Коул, М .: Клавулановая кислота: бета-лактамаза, ингибирующая бета-лактам из Streptomyces clavuligerus.Противомикробные агенты и химиотерапия 11: 852–857 (1977).
PubMed
Статья
CAS
Google ученый
Rodriguez, W .; Ross, S .; Хан, В .; Маккей Д. и Московиц П .: Клиндамицин в лечении остеомиелита у детей. Отчет о 29 случаях. Американский журнал болезней детей 131: 1088–1093 (1977).
PubMed
CAS
Google ученый
Rom, S.; Флинн, Д. и Ноун, П .: Анаэробные инфекции у новорожденных. Раннее обнаружение методом газожидкостной хроматографии и ответ на метронидазол. Архивы болезней детства 52: 740 (1977).
PubMed
Статья
CAS
Google ученый
Roy, I .; Бах В. и Тадепалли А. Активность тикарциллина in vitro против анаэробных бактерий по сравнению с карбенициллином и пенициллином. Антимикробные агенты и химиотерапия 11: 258–261 (1977).
PubMed
Статья
CAS
Google ученый
Рустиа, М. и Шубик, П .: Экспериментальная индукция опухолей молочной железы гемпатом и других опухолей метронидазолом у небредных крыс Sas: WRC (WT) BR. Журнал Национального института рака 63: 863–867 (1979).
PubMed
CAS
Google ученый
Shoemaker, E.H. и Йоу, Э.М.: Клиническая оценка эритромицина.Архивы внутренней медицины 93: 397–406 (1954).
PubMed
Статья
CAS
Google ученый
Саттер, В.Л. и Finegold, S.M .: Восприимчивость анаэробных бактерий к карбенициллину, цефокситину и родственным лекарствам. Журнал инфекционных болезней 131: 417–422 (1975).
PubMed
Статья
CAS
Google ученый
Саттер, В.Л. и Finegold, S.М .: Восприимчивость анаэробных бактерий к 23 антимикробным препаратам. Антимикробные агенты и химиотерапия 10: 736–752 (1976).
PubMed
Статья
CAS
Google ученый
Tacking, R .: Бактерии, продуцирующие пенциллиназу, при смешанных инфекциях у кроликов, получавших пенициллин. Acta Pathologica et Microbiologica Scandinavica 35: 445–454 (1954).
PubMed
Статья
CAS
Google ученый
Талли, Ф.П.; Jacobus, N.V .; Бартлетт, Дж. и Горбач, С.Л .: Активность пенициллинов против анаэробов in vitro. Противомикробные агенты и химиотерапия 7: 413–414 (1975).
PubMed
Статья
CAS
Google ученый
Tally, P .; Саттер, Л. и Файнголд, С. М.: Лечение анаэробных инфекций метронидазолом. Противомикробные агенты и химиотерапия 7: 672–675 (1975).
PubMed
Статья
CAS
Google ученый
Талли, Ф.П .: Факторы, влияющие на антимикробные препараты при анаэробном абсцессе. Журнал антимикробной химиотерапии 4: 299–302 (1978).
PubMed
Статья
CAS
Google ученый
Tedesco, F.J .; Бартон, Р.В. и Альперс, Д.Х .: Колит, связанный с клиндамицином: проспективное исследование. Анналы внутренней медицины 81: 429 (1974).
PubMed
CAS
Google ученый
Тадепалли, Х.и Хуанг Дж. Т .: Лечение анаэробных инфекций: сравнение карбенициллина с клиндамицином и гентамицином. Текущие терапевтические исследования 22: 549–555 (1977).
Google ученый
Уилан, J.P.F. и Хейл, Дж. Х .: Бактерицидная активность метронидазола против Bacteroides fragilis. Журнал клинической патологии 26: 393–395 (1973).
PubMed
Статья
CAS
Google ученый
Вуст, Дж.и Уилкинс, Т.Д .: Влияние клавулановой кислоты на анаэробные бактерии, устойчивые к бета-лактамным антибиотикам. Противомикробные агенты и химиотерапия 13: 130–133 (1978).
PubMed
Статья
CAS
Google ученый
Анаэробные инфекции Артикул
Введение
Анаэробные бактерии являются частью нормальной микрофлоры кожи и слизистых оболочек человека. Место анаэробной инфекции обычно является местом нормальной колонизации.Спектр инфекций варьируется от местных абсцессов до опасных для жизни инфекций. Анаэробные бактерии отличаются от аэробных бактерий потребностью в кислороде. Кислород токсичен для анаэробов, что можно объяснить отсутствием в анаэробах ферментов каталазы, супероксиддисмутазы и пероксидазы. Анаэробы являются привередливыми организмами, и их трудно выращивать, если не используются надлежащие методы сбора и культивирования. Диагноз требует клинического подозрения и правильной микробиологической идентификации.[1] [2]
В зависимости от потребности в кислороде бактерии можно разделить на следующие группы:
Облигатные аэробы , которым нужен кислород в качестве конечного акцептора электронов и не имеют других источников энергии, таких как ферментация.
Обязательные анаэробы , которые получают энергию в процессе ферментации и используют органические соединения в качестве конечных акцепторов электронов.
Факультативные анаэробы могут расти в присутствии или в отсутствие кислорода.
Облигатные анаэробы можно далее подразделить на 2 типа в зависимости от процентного содержания кислорода, который может оказаться токсичным. Строгие облигатные анаэробы , которые не выживут, если в окружающей среде содержится более половины процента кислорода, в то время как умеренные облигатные анаэробы все еще могут расти в среде с содержанием кислорода от 2 до 8 процентов.
Этиология
Общие очаги анаэробных инфекций включают полости рта, брюшной полости и таза; однако анаэробы могут вызывать инфекции других областей, таких как голова, шея и кожа.Клинически значимые анаэробы, связанные с инфекциями человека, следующие:
грамположительные
грамположительные, спорообразующие b acilli
Clostridium : это споровые анаэробы, ответственные за некоторые из более серьезных человеческих инфекций. На их долю приходится около 10% всех анаэробных инфекций. Важными представителями этого семейства являются Clostridium difficile , вызывающие C.difficile . Clostridium perfringens , вызывающая газовую гангрену или инфекции мягких тканей. Clostridium septicum , который также вызывает газовую гангрену.
грамположительные, n спорообразующие бациллы
Actinomyces: Они колонизируют желудочно-кишечный тракт (ЖКТ) человека, и инфекции возникают в результате разрыва кожно-слизистого барьера. 3 наиболее распространенных анатомических участка, пораженных Actinomyces , — это шейно-лицевой, грудной и абдоминальный отделы.
Propionibacterium : Этот вид является частью нормальной флоры кожи и слизистых оболочек. Наиболее значительным членом этого семейства является Propionibacterium acne , который играет роль в патогенезе вульгарных угрей.
Bifidobacterium : это нормальная флора кишечного тракта. Обычно он не патогенный; однако зарегистрированы педиатрические инфекции в виде хронического среднего отита, абсцессов брюшной полости и перитонита.
Lactobacillus: Эти организмы также обычно встречаются в желудочно-кишечном тракте и могут быть выделены из многих пищевых продуктов. Они обладают низким патогенным потенциалом; однако описаны случаи абсцессов брюшной полости, аспирационной пневмонии и бактериемии, особенно у новорожденных.
Peptococcus и Peptostreptococcus : Эти анаэробы являются частью ротовой полости, желудочно-кишечного тракта, верхних дыхательных путей и мочеполовых путей, а также кожи.Они могут быть патогенными и вызывать многочисленные инфекции, такие как хронический средний отит, хронический синусит, аспирационная пневмония, воспалительные заболевания органов малого таза, включая абсцессы яичников и трубок.
Другие члены включают Eubacterium, Bifidobacterium, Arcanobacterium, и микроаэрофильные Streptococcus ( Streptococcus anginosus, Streptococcus mediate).
Грамотрицательные
Bacteroides: Это наиболее часто обнаруживаемые анаэробные патогены из клинических образцов. Они являются частью кишечной микрофлоры человека и нормальной микрофлоры женских половых органов. Эти организмы чаще всего являются причиной внутрибрюшных инфекций, особенно абсцессов. Большинство этих абсцессов представляют собой смешанные инфекции. Они также могут вызывать экстраабдоминальные инфекции, такие как аспирационная пневмония, абсцессы головного мозга и другие.
Fusobacterium : Один из видов этой группы анаэробов, Fusobacterium necrophorum, , является частой причиной перитонзиллярных абсцессов, связанных с осложнением тромбоза внутренней яремной вены, известного как синдром Лемьера.
Campylobacter: Является одной из наиболее частых причин острого гастроэнтерита.
Prevotella: Это нормальная флора ротовой полости и кишечного тракта человека. У детей они часто связаны с инфекциями головы и шеи, такими как перитонзиллярные абсцессы, заглоточные абсцессы, а также перинеальные или перианальные инфекции, такие как пилонидальный абсцесс.
Veillonella: Иногда ассоциируется с абсцессами брюшной полости и аспирационной пневмонией у детей.
Эпидемиология
Анаэробы являются частью местной или местной флоры, особенно ротовой полости, кишечника человека и женских половых путей. Колонизация анаэробами зависит от возраста, расположения органа и факторов окружающей среды. Например, у младенцев, находящихся на исключительно грудном вскармливании, кишечная флора преимущественно представлена Bifidobacterium , с небольшим количеством видов Bacteroides и Enterococcus . С другой стороны, младенцы, которых кормят коровьим молоком, имеют кишечную флору, аналогичную флоре кишечника взрослых, которая содержит грамотрицательные анаэробы и факультативные бациллы.[3] [4] [5]
Анаэробы являются частью местной флоры, которая сопротивляется колонизации и вторжению со стороны некоренной флоры. Тем не менее, инфекции от анаэробов действительно возникают и обычно возникают в результате нарушения кожно-слизистого барьера или иммуносупрессии. Анаэробные инфекции органов включают, но не ограничиваются ими, абсцессы головного мозга, стоматологические инфекции, аспирационную пневмонию, абсцессы легких, инфекции укусов (животных / человека), абсцессы брюшной полости и некротические инфекции мягких тканей.
Патофизиология
Патогенез анаэробных инфекций включает разрушение поверхности слизистой оболочки и проникновение анаэробных бактерий с проникновением в глубокие ткани.Механизмы проникновения включают местную травму, операцию, перфорацию внутренних органов (например, аппендицит), некроз тканей и нарушение очистки стерильного участка (хронический синусит, пневмония). Место и степень заражения зависят от факторов вирулентности организма и иммунитета хозяина.
Факторами вирулентности, способствующими анаэробным инфекциям, являются факторы адгезии (фимбрии и лектин), факторы инвазии (фосфолипаза С, липополисахариды и протеазы), факторы, участвующие в деструкции тканей (фибринолиз, ацетилглюкозаминидаза и выработка коллагеназы), устойчивость капсулы к фагоцитозу, и другие.У хозяина с ослабленным иммунитетом наблюдаются серьезные инфекции.
При участии в абсцессе анаэробы обычно являются частью полимикробной инфекции. Экспериментальные модели на крысах со смешанными инфекциями показали, что рост анаэробов, а также анаэробов усиливается при полимикробных инфекциях.
История и физика
Большинство анаэробных инфекций у детей носят локальный характер, и инфекции кровотока составляют менее 2% случаев.Подход к анаэробным инфекциям включает определение предрасполагающих факторов. Это следующие данные:
- Инфекция участка органа, заразная участку с местной колонизацией (ротовая полость, кишечник)
- Непроходимость: например, инородное тело в носу, непроходимость аппендикса, непроходимость кишечника
- Перфорация: полых внутренних органов, например, перфорация кишечника.
- Неспособность хозяина очищать выделения, например, дети с церебральным параличом предрасположены к аспирационной пневмонии.
- Укусы животных и людей с проникающими травмами ротовой полости анаэробами
Другие важные признаки анаэробной инфекции включают наличие состояния, предрасполагающего человека к анаэробной инфекции, например, некроз тканей, выделения с неприятным запахом, инфекция, приводящая к тромбофлебиту, отсутствие улучшения при подозрении на анаэробную активность антибиотиками.
Клиницисты должны получить анаэробную культуру при подозрении на анаэробную инфекцию.
Общие инфекции в области органов при анаэробных и аэробных инфекциях
Инфекции головы и шеи: Анаэробы обычно вызывают стоматологические инфекции, такие как зубные абсцессы, гингивит и пародонтит. Обычно присутствуют результаты осмотра: кариес или плохой прикус. Анаэробы также вовлечены вместе с другими аэробами в гнойные инфекции заглоточного абсцесса, перитонзиллярного абсцесса, шейного лимфаденита, глубоких абсцессов шеи и паротита.Анаэроб, связанный с Fusobacterium, связан с осложнением перитонзиллярного абсцесса, известным как синдром Лемьера. Синдром Лемьера вызывается септическим тромбофлебитом яремной вены и метастатическими эмболами в легкие и печень.
Анаэробы также вызываются хроническим средним отитом и хроническим синуситом наряду с другими аэробами, такими как Staphylococcus aureus и Pseudomonas.
Инфекции центральной нервной системы (ЦНС): Анаэробы обычно выделяются в культурах из абсцессов головного мозга, которые возникают в результате осложнения синусита, среднего отита, стоматологических инфекций.Обычно выделяют 3 анаэроба: Fusobacterium , Prevotella и Bacteroides . Эти же микроорганизмы встречаются и при эпидуральных инфекциях.
Внутрибрюшные инфекции: Повреждение стенки кишечника, видимое на перфорированном отростке, дает кишечным анаэробам доступ в брюшную полость. В течение нескольких дней или недель это приводит к формированию абсцессов брюшной полости. Абсцессы брюшной полости почти всегда представляют собой смешанные инфекции, содержащие как аэробы, так и анаэробы.Наиболее частым анаэробом, вызывающим абдоминальные инфекции, является Bacteroides fragilis, за которым следуют видов Lactobacillus и Clostridium .
Анаэробы также являются частой причиной абсцессов печени. Обычными ассоциированными анаэробами являются виды Bacteroides и Fusobacterium .
Воспалительные заболевания органов малого таза: Все анаэробы участвуют в воспалительных заболеваниях органов малого таза (ВЗОМТ). Сексуально активным женщинам с признаками и симптомами, совместимыми с воспалительными заболеваниями органов малого таза, показана эмпирическая антимикробная терапия против анаэробов и анаэробов.Обычными анаэробами, участвующими в ВЗОМТ, являются Prevotella , Porphyromonas, Clostridium .
Легочные инфекции наблюдаются у детей, которые не могут контролировать секрецию верхних дыхательных путей или не имеют нормального кашлевого рефлекса, например, у детей с церебральным параличом и трахеопищеводными мальформациями. Аспирация приводит к пневмонии, которая при отсутствии лечения может перерасти в абсцесс. Преобладающие патогены, участвующие в аспирационной пневмонии, являются частью ротоглоточной флоры и включают Peptostreptococcus, Prevotella, Bacteroides fragilis и Fusobacterium.
Инфекции кожи и мягких тканей: Анаэробы могут вызвать периректальный абсцесс или лицевой абсцесс у детей. Bacteroides fragilis и Clostridium обычно участвуют в периректальных инфекциях, а Prevotella , Porphyromonas и Fusobacterium участвуют в оральных инфекциях.
Оценка
Выявление серьезных анаэробных инфекций
Своевременное выявление важно для начала эмпирической терапии.Опасные для жизни инфекции, такие как столбняк, газовая гангрена или детский ботулизм, вызываются спорообразующими анаэробами, Clostridium tetanus , Clostridium perfringens, или Clostridium botulism соответственно [6] [7].
История травмы, например проникающая травма ногтя или наличие омертвевшей ткани, должна требовать обследования на столбняк у иммунизированного ребенка.
Газовая гангрена вызывается Clostridium perfringens или Clostridium septicum .Это неотложная медицинская помощь, требующая хирургической обработки раны в дополнение к антибактериальной терапии пенициллином, содержащим антибиотик в сочетании с клиндамицином.
Ботулизм проявляется как нисходящий паралич, особенно у младенцев. Часты случаи употребления поврежденных консервов, использования меда, проживания или путешествия в эндемичные регионы (высокое количество клостридиальных спор). Результаты физикального обследования относятся к младенцу без лихорадки с острым началом трудностей с кормлением и поражением бульбара (отсутствие рвотного рефлекса).В отношении подозреваемых случаев экспертиза предоставляется Министерством здравоохранения Калифорнии (www.infantilebotulism.org). Стул следует отправить для проверки на наличие спор Clostridium botulism . Основой лечения является поддерживающая терапия с применением иммуноглобулина против ботулизма или без него (BabyBIG).
У подростка с болью в горле, болью в шее и тахикардией, непропорциональной лихорадке, следует учитывать синдром Лемьера. Для выявления тромбофлебита внутренних яремных вен необходимо выполнить ультразвуковое исследование шеи, а для выявления септических эмболов — сделать рентген грудной клетки.
Местные инфекции, включая абсцессы
Абсцессы, ограниченные ЦНС, областью головы и шеи. Область живота можно диагностировать с помощью соответствующей анаэробной культуры. Образец следует собирать в стерильном месте, желательно в обход нормальной микрофлоры, с помощью пункционной аспирации или хирургического исследования. Аспират ткани или жидкости предпочтительнее мазка. После сбора образец следует отправить в анаэробную транспортную среду, и он должен быть инокулирован в бескислородной среде.
Лечение / менеджмент
Шаг 1
Лечение анаэробной инфекции зависит от места инфицирования, хозяина, а также наличия или отсутствия абсцесса. Как правило, абсцесс всегда следует осушать , а посевы направлять на аэробную и анаэробную культуру. Кроме того, хирургическая обработка некротической ткани при клостридийно-некротическом фасциите имеет решающее значение в лечении. [8] [9] [10]
Шаг 2
После получения необходимых культур ребенку следует назначить эмпирические антибиотики с активностью против анаэробов.Ниже приведены варианты выбора:
Метронидазол : Обладает отличной активностью против грамотрицательных веществ, таких как Bacteroides fragilis . Его активность против грамположительных результатов хорошая, хотя и менее надежная. Метронидазол имеет отличную биодоступность (100%) и хорошо проникает в ткани, включая центральную нервную систему и брюшную полость. Метронидазол вызывает металлический привкус во рту, который часто называют причиной прекращения приема.
Клиндамицин активен против многих анаэробов.Устойчивость клиндамицина к Bacteroides fragilis возрастает, и он менее надежен по сравнению с метронидазолом, ингибитором пенициллина / бета-лактамазы или карбапенемом. Клиндамицин, вводимый внутривенно или перорально, хорошо проникает в ткани, включая абсцессы, кости и суставы. Клиндамицин, однако, не попадает в центральную нервную систему.
Комбинация ингибиторов пенициллина / бета-лактамазы : Пенициллин сам по себе активен против анаэробов, которые не продуцируют бета-лактамазы, таких как Clostridium perfringens .Однако большинство грамотрицательных анаэробов действительно продуцируют бета-лактамазу и комбинированные пенициллины, такие как пероральный амоксициллин / клавуланат или внутривенный (IV) / внутримышечный (IM) ампициллин / сульбактам, тикарциллин / клавуланат и пиперациллин / тазобактам.
Цефалоспорин второго поколения: Что касается цефалоспоринов, то цефалоспорины второго поколения цефокситин, цефотетан и цефметазол более активны в отношении Bacteroides fragilis. Однако, учитывая возрастающую резистентность, они не рекомендуются в качестве эмпирического лечения.Обычно используется в хирургической профилактике.
Карбапенемы : Обладают отличной активностью против анаэробов, а также аэробов, вовлеченных в интраабдоминальные и другие органы, такие как ЦНС. Меропенем немного более активен, чем имипенем, в отношении грамотрицательных бактерий.
Хинолоны : Хорошо всасываются при пероральном приеме и проникают в ткани. Однако сопротивление возрастает, и их следует применять только детям с аллергией на бета-лактам. Хинолоны, обладающие активностью против анаэробов, включают левофлоксацин и моксифлоксацин.
Дифференциальная диагностика
- Ботулизм можно спутать с другими неврологическими состояниями, такими как синдром Гийена-Барре, и инфекционными причинами паралича, такими как энтеровирусная инфекция или паралич или парез, вызванный вирусом Западного Нила.
- Аэробные абсцессы из Escherichia coli , Pseudomonas, такие как абсцесс мозга, абсцессы головы и шеи, инфекции легких и внутрибрюшные инфекции.
Жемчуг и другие выпуски
- Рассмотрите возможность анаэробной инфекции, если место подозрения на инфекцию находится рядом с нормальной местной анаэробной флорой, такой как рот, кишечник или женские половые пути.
- Определение предрасположенности, такой как непроходимость, перфорация, травма, неспособность хозяина очищать секреты, снижение притока крови к ткани, например некроз ткани.
- Признаки анаэробной инфекции включают выделения с неприятным запахом, а инфекция не реагирует на антибиотики без какой-либо анаэробной активности.
- Следует предпринять попытку отправить анаэробные культуры, что предполагает надлежащий сбор, быструю транспортировку и использование надлежащих методов культивирования. Тканевый или гнойный материал предпочтительнее посылать мазки.
- Метронидазол обладает анаэробной активностью широкого спектра действия с наименьшей резистентностью. Другие анаэробные антибиотики включают клиндамицин, комбинацию ингибиторов пенициллина бета-лактамазы, цефалоспорины второго поколения, карбапенемы и хинолоны.
Улучшение результатов команды здравоохранения
Анаэробные инфекции распространены как в амбулаторных, так и в стационарных условиях. Поскольку эти инфекции могут поражать различные органы и проявляться по-разному, с ними лучше всего справляется группа специалистов. Для поставщиков первичной медико-санитарной помощи, практикующих медсестер и других медицинских работников важно проконсультироваться со специалистом по инфекционным заболеваниям, когда они сталкиваются с инфекцией, которая не поддается лечению обычными антибиотиками или имеет странное проявление.Фармацевт должен пересмотреть выбор лекарств, взаимодействия с ними и соблюдение пациентом режима лечения, а также сообщить о проблемах команде. Медсестры должны помогать в координации ухода, способствовать общению между членами межпрофессиональной команды и помогать в обучении пациентов и их семей. При необходимости следует привлекать медсестер, прошедших специальную подготовку, включая медико-хирургические и инфекционные службы.
При неправильном диагнозе анаэробные инфекции приводят к высокой смертности. [11] [12] [13]
Прогноз зависит от типа анаэробной инфекции.
- В нашу эпоху вакцинации от столбняка и поддерживающей терапии столбняк не виден в развитых странах мира. У любого ребенка с чистой проникающей ранкой должна быть проведена вакцинация от столбняка, а в случае зараженной раны следует рассмотреть возможность использования противостолбнячной вакцины и столбнячных иммуноглобулинов на основе последней вакцины против столбняка.
- Любую загрязненную рану следует очистить и удалить инородное тело.
- Хорошая гигиена полости рта и полости рта предотвращает анаэробные инфекции.
- При операциях на брюшной полости, требующих проникновения полых внутренних органов, следует рассмотреть возможность применения антибиотиков с анаэробной активностью, таких как цефокситин.
Если рана инфицирована анаэробными бактериями, существуют ли специальные повязки, которые нельзя использовать?
Сестринская практика часто включает в себя выполнение процедур, по поводу которых возникают споры или сомнения. В практическом вопросе мы просим экспертов определить, как медсестры должны подходить к этим ситуациям
Q.Если рана инфицирована анаэробными бактериями, существуют ли специальные повязки, которые нельзя использовать?
A. Несмотря на опасения, что окклюзионные повязки могут стимулировать анаэробный рост, создавая обедненную кислородом среду, нет никаких доказательств, подтверждающих это.
Анаэробы
Облигатные анаэробные и микроаэрофильные бактерии живут в бескислородной среде (Таблица 1). Это привело к дебатам о безопасности использования окклюзионных повязок, особенно гидроколлоидов, для инфицированных ран (Finnie, 2002; Jones and Gill, 1998).
Классифицирующая инфекция
В ранах всегда присутствуют бактерии, но большинство из них не инфицированы. Рана инфицируется, когда «микробы размножаются до такой степени, что поражаются ткани хозяина и заживление ран задерживается» (Cooper, 2005).
Чтобы идентифицировать возбудителя болезни, необходимо взять микробиологический образец в соответствии со стандартными операционными процедурами (Health Protection Agency, 2006). Основная цель взятия проб — определить чувствительность возбудителя к антибиотикам.Когда подозревается или известно, что анаэробы являются возбудителем раневой инфекции, антибиотиком выбора обычно является метронидазол.
Образец гноя / экссудата предпочтительнее мазка из раны, потому что он обычно дает более надежные результаты (HPA, 2006). В мазке из раны следует использовать транспортную среду Amies с углем (HPA, 2006). Предпочтительна быстрая доставка в лабораторию (1-2 часа), но, если это невозможно, хранения при комнатной температуре достаточно для поддержания роста как аэробных, так и анаэробных бактерий (Bowler et al, 2001).В культуре анаэробов потребуется инкубационный период 2-7 дней, в зависимости от микроба. При запросе расследования важно предоставить информацию, относящуюся к образцу (таблица 2). Если есть подозрение на анаэробы, об этом следует упомянуть, поэтому укажите «включить анаэробы».
Анаэробы могут составлять 22–62% микробной популяции в ране (Bowler et al, 2001). Следовательно, есть основания подозревать анаэробное присутствие при наличии признаков раневой инфекции.
Выбор заправки
Окклюзионные повязки вызвали споры об их безопасном использовании, поскольку они создают гипоксическую среду, которая стимулирует размножение анаэробов (Marshall et al, 1990). Недавних исследований этого не проводилось, возможно, потому что присутствие анаэробных бактерий под этими повязками не увеличивает вероятность развития инфекции и не задерживает заживление (Mousa, 1997; Gilchrist and Reed, 1989). Возможно, слегка кислая среда под этими повязками враждебна бактериям, но это зависит от продуктов (Thomas and Loveless, 1997).
Выбор повязки зависит от многих факторов, в том числе от практичности и типа раны. Гидроколлоид не обладает способностью абсорбировать высокий уровень экссудата, поэтому требуется более частая смена повязки, без которой могут возникнуть такие осложнения, как мацерация вокруг раны. Это исключило бы использование повязки этого типа, а не присутствие анаэробов. То же самое можно сказать и о гидрогелевых повязках с высоким содержанием воды.
Заключение
Выбор повязки требует множества соображений, слишком много для обсуждения здесь.Если на ране наблюдаются признаки клинической инфекции, анаэробной или нет, выбор повязки, вероятно, будет зависеть от лечения симптомов, места раны и образа жизни пациента. Гидроколлоиды и гидрогели следует использовать с осторожностью не потому, что они могут усилить инфекцию, а потому, что они могут быть неподходящими для условий ран. л
Хайди Гай, бакалавр наук, штат Род-Айленд, , преподаватель жизнеспособности тканей, Восточный и Северный Хартфордширский фонд здравоохранения / Университет Хартфордшира
| Таблица 1.классификация бактерий | |
КЛАССИФИКАЦИЯ
| ОПИСАНИЕ
|
Облигатные аэробы
| Невозможно выжить без кислорода
|
Факультативные анаэробы
| Аэробный, но может быть анаэробным; предпочитаю аэробные условия
|
Микроаэрофильные бактерии
| Может переносить небольшое количество кислорода
|
Облигатные анаэробы
| Неспособен выжить в кислороде, но может прожить несколько дней в воздухе (Bowler et al, 2001 )
|
| Источник: Gladwin and Trattler (2008) | |
Таблица 2.Информация о образце
- Место раны
- Заболевания, например диабет 2 типа
- Глубокая полость
- Подрыв
- Malodour
- Кишечник или «грязная» хирургия
- Ишемия под раной
- Гангрена или омертвевшая ткань
Bowler PG et al. (2001) Микробиология ран и связанные подходы к лечению ран. Обзоры клинической микробиологии ; 14: 2, 244-269.
Cooper R (2005) Понимание раневой инфекции. В: Определение критериев заражения. Позиционный документ Европейской ассоциации лечения ран. Лондон: MEP.
Finnie A (2002) Гидроколлоиды в лечении ран: за и против. Британский журнал медсестер по месту жительства; 7: 7, 338-345.
Gilchrist B, Reed C (1989) Бактериология хронических венозных язв, леченных окклюзионными гидроколлоидными повязками. Британский журнал дерматологии; 121: 3, 337-344.
Gladwin M, Trattler B (2008) Клиническая микробиология стала до смешного простой. Майами: Медмастер.
Агентство по охране здоровья (2006) Исследование кожи, поверхностных и нехирургических мазков из ран. BSOP11 выпуск 4.1.
Джонс В., Гилл Д. (1998) Гидроколлоидные повязки и поражения стопы при диабете. Диабетическая стопа; 1: 4, 127-134.
Marshall DA et al. (1990) Окклюзионные повязки: влияет ли тип повязки на рост распространенных бактериальных патогенов? Archives of Surgery; 125: 9, 1136–1139.
Mousa HA (1997) Аэробные, анаэробные и грибковые ожоговые раневые инфекции. Журнал госпитальной инфекции; 37: 317-323.
Thomas S, Loveless P (1997) Сравнительное исследование свойств двенадцати гидроколлоидных повязок.
анаэробных инфекций | Encyclopedia.com
Определение
Анаэробная инфекция — это инфекция, вызываемая бактериями (называемыми анаэробами), которые не могут расти в присутствии кислорода.Анаэробные бактерии могут заразить глубоких ран, глубоких тканей и внутренние органы, где мало кислорода. Эти инфекции характеризуются образованием абсцесса , гноем с неприятным запахом и разрушением тканей.
Описание
Анаэробный означает «жизнь без воздуха». Анаэробные бактерии растут в местах, где полностью или почти полностью отсутствует кислород. Обычно они находятся во рту, желудочно-кишечном тракте, влагалище и на коже. Обычно известные болезни, вызываемые анаэробными бактериями, включают газовую гангрену , столбняк, и ботулизм. Почти все стоматологические инфекции вызываются анаэробными бактериями.
Анаэробные бактерии могут вызвать инфекцию, если нормальный барьер (например, кожа, десны или стенка кишечника) поврежден в результате операции, травмы или болезни. Обычно иммунная система убивает любые вторгшиеся бактерии, но иногда бактерии могут расти и вызывать инфекцию. Участки тела с разрушением тканей (некрозом) или плохим кровоснабжением содержат мало кислорода и способствуют росту анаэробных бактерий. Состояние с низким содержанием кислорода может быть следствием болезни кровеносных сосудов, шока , травмы и хирургического вмешательства.
Анаэробные бактерии могут вызвать инфекцию практически в любом месте тела. Например:
- Рот, голова и шея. Инфекции могут возникать в корневых каналах, деснах (гингивит), челюсти, миндалинах, горле, пазухах и ушах.
- Легкое. Анаэробные бактерии могут вызывать пневмонии, абсцессов легких, инфицирование слизистой оболочки легкого ( эмпиемы, ) и расширение легочных бронхов ( бронхоэктазы, ).
- Интраабдоминальный. Анаэробные инфекции в брюшной полости включают образование абсцесса, перитонита, и аппендицита.
- Женские половые пути. Анаэробные бактерии могут вызывать абсцессы таза, воспалительные заболевания тазовых органов, воспаления слизистой оболочки матки (эндометрит) и инфекции тазовых органов после аборта, родов, и хирургических вмешательств.
- Кожа и мягкие ткани. Анаэробные бактерии являются частыми причинами диабетических кожных язв, гангрены, деструктивной инфекции глубоких слоев кожи и тканей (некротический фасцит) и инфекций укушенных ран.
- Центральная нервная система.Анаэробные бактерии могут вызывать абсцессы головного и спинного мозга.
- Кровоток. Анаэробные бактерии могут быть обнаружены в кровотоке больных пациентов (состояние, называемое бактериемией).
КЛЮЧЕВЫЕ ТЕРМИНЫ
Абсцесс — Шишка, заполненная гноем, возникшая в результате инфекции.
Анаэробный — Жизнь и рост без кислорода.
Некроз— Гибель и разрушение тканей в результате инфекции или болезни.
Причины и симптомы
Люди, перенесшие шок, травмы или хирургические операции, а также люди с заболеваниями кровеносных сосудов или опухолями, подвергаются повышенному риску заражения анаэробными бактериями.Существует множество различных видов анаэробных бактерий, которые могут вызвать инфекцию. Действительно, большинство анаэробных инфекций — это «смешанные инфекции», что означает, что растет смесь разных бактерий. Наиболее частыми возбудителями инфекций являются анаэробные бактерии видов Bacteroides fragilis, Peptostreptococcus и Clostridium .
Признаки и симптомы анаэробной инфекции могут различаться в зависимости от локализации инфекции. Как правило, анаэробные инфекции приводят к разрушению тканей, абсцессу, из которого вытекает зловонный гной, и, возможно, к лихорадке . Симптомы специфических инфекций следующие:
- Инфекции зубов и десен. Опухшие, болезненные кровоточащие десны, неприятный запах изо рта, и боль. При тяжелых инфекциях могут образовываться мокнущие язвы.
- Инфекция горла. сильнейшая ангина, неприятный запах изо рта, неприятный привкус во рту, жар и ощущение удушья.
- Инфекция легких. Боль в груди, кашель, затрудненное дыхание, жар, неприятный запах мокроты и потеря веса.
- Интраабдоминальная инфекция.Боль, жар и, возможно, после операции выделения из раны с неприятным запахом.
- Тазовая инфекция. Зловонный гной или кровь, вытекающая из матки, общая или локализованная тазовая боль, жар и озноб.
- Инфекция кожи и мягких тканей. Инфицированные раны красные, болезненные, опухшие, из них может выделяться гной с неприятным запахом. Кожная инфекция вызывает локальный отек, боль, покраснение и, возможно, болезненную открытую язву (язву), из которой вытекает гной с неприятным запахом. Тяжелые кожные инфекции могут вызвать обширное разрушение тканей (некроз).
- Кровоток. Инвазия кровотока вызывает высокую температуру (до 105 ° F [40,6 ° C]), озноб, общее недомогание и может быть смертельным.
Диагноз
Диагноз анаэробной инфекции основывается в первую очередь на симптомах, истории болезни пациента и местонахождении инфекции. Зловонная инфекция или выделения из абсцесса являются признаком анаэробной инфекции. Этот неприятный запах создается анаэробными бактериями и встречается у одной трети или половины пациентов на поздних стадиях инфицирования.Другие ключи к анаэробной инфекции включают некроз тканей и газообразование в месте инфекции. Образец из инфицированного места может быть получен с помощью тампона или иглы и шприца, чтобы определить, какие бактерии вызывают инфекцию. Поскольку эти бактерии легко уничтожаются кислородом, они редко растут в лабораторных культурах образцов тканей или гноя.
Недавний анамнез пациента помогает диагностировать анаэробную инфекцию. Пациенты, перенесшие или недавно перенесшие операцию, стоматологию, опухоли, заболевание кровеносных сосудов или травмы, подвержены этой инфекции.Отсутствие улучшения после лечения антибиотиками , которые не способны убить анаэробы, является еще одним признаком того, что инфекция вызвана анаэробами. Местоположение и тип инфекции также помогают в диагностике.
Диагностические тесты могут включать анализы крови для определения наличия бактерий в кровотоке и рентгеновские снимки для выявления внутренних инфекций.
Лечение
При серьезных инфекциях может потребоваться госпитализация для лечения. При анаэробных инфекциях необходимо немедленное лечение антибиотиками.Лабораторные исследования могут выявить бактерии, вызывающие инфекцию, а также какой антибиотик подействует лучше всего. Не все антибиотики действуют против всех анаэробных бактерий, но почти все анаэробы убиваются хлорамфениколом (хлоромицетин), метронидазолом (флагил или протостат) и имипенемом (примаксин). Другие антибиотики, которые можно использовать, включают клиндамицин (Клеоцин) или цефокситин (Мефоксин).
Хирургическое удаление или дренирование абсцесса требуется почти всегда. Это может включать дренаж с помощью иглы и шприца для удаления гноя из кожного абсцесса (так называемая «аспирация»).Перед процедурой аспирации эту область обезболивают. Также некоторые внутренние абсцессы можно дренировать с помощью этой процедуры с помощью ультразвука (устройство, которое использует звуковые волны для визуализации внутренних органов). Этот вид дренирования абсцесса можно провести в кабинете врача.
Прогноз
Полное выздоровление должно быть достигнуто с помощью соответствующей хирургии и лечения антибиотиками. Нелеченные или неконтролируемые инфекции могут вызвать серьезное разрушение тканей и костей, для восстановления которого потребуется пластических операций .Серьезные инфекции могут быть опасными для жизни.
Профилактика
Хотя анаэробные инфекции могут возникнуть у любого человека, соблюдение правил гигиены и общее состояние здоровья могут помочь предотвратить инфекции.
Ресурсы
КНИГИ
Фаучи, Энтони С. и др., Редакторы. Принципы внутренней медицины Харрисона . Нью-Йорк: McGraw-Hill, 1997.
Gale Encyclopedia of Medicine, 3-е изд. Роуленд, Белинда,
.



 В таком случае создаются неблагоприятные условия для возбудителей, предупреждаются нервнодистрофические и гангренозные процессы и не подавляются защитные силы организма.
В таком случае создаются неблагоприятные условия для возбудителей, предупреждаются нервнодистрофические и гангренозные процессы и не подавляются защитные силы организма. Перед началом операции осуществляют новокаинантибиотиковую инфильтрацию по периферии зоны отека.
Перед началом операции осуществляют новокаинантибиотиковую инфильтрацию по периферии зоны отека. natrii chloridi 20%; Hydrogenii peroxydati 3% aa 100,0, Ol.Terebenthini 10,0.
natrii chloridi 20%; Hydrogenii peroxydati 3% aa 100,0, Ol.Terebenthini 10,0.