Развитие и лечение синдрома Корсакова
Синдром Корсакова был определен Victor et al. (1971) как патологическое психическое состояние, характеризующееся нарушениями памяти и обучаемости, более значительными по сравнению с поражением других когнитивных функций на фоне повышенной восприимчивости и раздражительности пациента. Синдром Корсакова обычно развивается вслед за энцефалопатией Вернике в результате несвоевременно поставленного диагноза и лечения недостаточными дозами тиамина. A.D. Thomson et al. в статье «The Evolution and Treatment of Korsakoff’s Syndrome», опубликованной в журнале Neuropsychology Review (2012; 22: 81-92), проанализировали механизмы развития синдрома Вернике – Корсакова, а также эффективность тиамина в лечении данного состояния.
Энцефалопатия Вернике
Энцефалопатия Вернике – острое нейропсихиатрическое состояние, вызванное недостатком тиамина (витамина B1) в головном мозге. Данное заболевание часто встречается у лиц, злоупотребляющих алкоголем. Причинами дефицита тиамина могут быть недостаточное поступление его с пищей, сниженная усвояемость и недостаточный уровень его превращения в активный метаболит. В процесс могут быть вовлечены один или несколько из перечисленных факторов. При своевременном назначении адекватных доз парентерального тиамина энцефалопатия Вернике является обратимой. Недиагностированная или неправильно леченая энцефалопатия Вернике обычно переходит в хроническую форму – синдром Корсакова. Из этого следует, что при данном синдроме необходимо проводить своевременную диагностику энцефалопатии Вернике, соответствующее лечение и профилактику.
Причинами дефицита тиамина могут быть недостаточное поступление его с пищей, сниженная усвояемость и недостаточный уровень его превращения в активный метаболит. В процесс могут быть вовлечены один или несколько из перечисленных факторов. При своевременном назначении адекватных доз парентерального тиамина энцефалопатия Вернике является обратимой. Недиагностированная или неправильно леченая энцефалопатия Вернике обычно переходит в хроническую форму – синдром Корсакова. Из этого следует, что при данном синдроме необходимо проводить своевременную диагностику энцефалопатии Вернике, соответствующее лечение и профилактику.
В случае если причиной энцефалопатии является изолированный дефицит тиамина (например, у военнопленных, при чрезмерной рвоте у беременных или при раке желудка), терапия небольшими дозами тиамина перорально/подкожно обычно является эффективной, и заболевание в очень редких случаях переходит в синдром Корсакова. Если же энцефалопатия Вернике развивается у лиц, злоупотребляющих алкоголем, ситуация усложняется, поскольку считается, что алкоголь компрометирует систему транспорта тиамина и нарушает его утилизацию. В связи с этим лица, злоупотребляющие алкоголем, нуждаются в более высоких дозах тиамина и парентеральном его введении. К сожалению, синдром Корсакова является частым исходом у таких пациентов, и причины этого обсуждаются далее.
В связи с этим лица, злоупотребляющие алкоголем, нуждаются в более высоких дозах тиамина и парентеральном его введении. К сожалению, синдром Корсакова является частым исходом у таких пациентов, и причины этого обсуждаются далее.
Поражение головного мозга, связанное с алкоголем
Длительное употребление алкоголя приводит к когнитивным нарушениям, и эти эффекты широко описаны в литературе как «алкогольная деменция», «деменция алкоголиков», «алкоголь-индуцированная деменция», «связанные с приемом алкоголя когнитивные нарушения», «алкогольное поражение головного мозга». У лиц, злоупотребляющих алкоголем в анамнезе и страдающих синдромом Вернике – Корсакова, признаки поражения головного мозга являются результатом одновременно дефицита тиамина и алкогольной интоксикации. В дополнение к этому сочетание эффектов дефицита тиамина и алкогольной интоксикации может приводить к тяжелым и необратимым нарушениям. Из этого следует, что синдром Вернике – Корсакова может быть более гетерогенным состоянием, чем это предполагалось ранее, и больные, демонстрирующие ряд неврологических расстройств, нуждаются в комплексном подходе к терапии (Zahr et al. , 2011).
, 2011).
Согласно имеющимся данным, приблизительно у 10% больных деменцией патология является «алкоголь-индуцированной», и эта цифра выше в регионах с низкими социально-экономическими показателями (Lishman, 1990; MacRae, Cox, 2003). Точную распространенность алкогольного поражения головного мозга оценить нелегко, поскольку это «скрытый» и изолированный контингент пациентов, неопределенной численности, часто недообследованных, нередко без определенного места жительства или проживающих в приютах и общежитиях, без финансовых ресурсов и доступа к квалифицированной медицинской помощи. В связи с тем, что лица с алкогольным поражением головного мозга зачастую более молодые, чем больные другими видами деменции, их потребности отличаются, а лечение и реабилитация имеют свои особенности. Первый контакт таких пациентов с врачом в основном происходит уже при госпитализации в стационар, и медперсонал палаты неотложной медицинской помощи должен обратить внимание на ряд проявлений, которых может быть множество.
Данные аутопсии больных, у которых проводилось патоморфологическое исследование зон головного мозга, ассоциированные с развитием синдрома Вернике – Корсакова, продемонстрировали характерные для этого синдрома нейропатологические изменения у 1,5% общей популяции и у 12,5% алкоголезависимых (Harper, 2006; Harper et al., 1988, 2003). При вовлечении в процесс тиамин-зависимого поражения мозжечка эта цифра возрастает до 35% (Torvik et al., 1982).
В недавнем исследовании, проведенном в Великобритании, врачи выявили признаки мальнутриции (недостаточности питания) почти у каждого третьего госпитализированного пациента, и причины этой недостаточности были в основном социальными (Russell, Elia, 2009). Мальнутриция, встречавшаяся среди всех возрастных групп и диагностических категорий, была, однако, более распространенной у пациентов в возрасте старше 65 лет. У данной группы больных сопутствующими часто являются гастроинтестинальная и неврологическая патология, что усложняет диагностический поиск и последующее лечение.
Таким образом, профилактика синдрома Корсакова и алкогольное поражение головного мозга – серьезные проблемы общественного здравоохранения как в развитых, так и в развивающихся странах.
Интоксикация, абстиненция и дефицит тиамина у лиц, употребляющих алкоголь
Алкоголь – неспецифическое вещество, взаимодействующее с рядом нейротрансмиттерных путей, в том числе с системами g-аминомасляной кислоты (ГАМК) и глутамата, что лежит в основе развития толерантности и зависимости (Marshall et al., 2010). ГАМК является одним из основных медиаторов торможения в ЦНС, а глутамат – ключевым медиатором возбуждения. Алкоголь активирует тормозные ГАМК-рецепторы и является антагонистом для рецепторов глутамата (N-метил-D-аспарагиновая кислота [NMDA]), а хроническое злоупотребление алкоголем приводит к адаптации этих нейромедиаторных систем с компенсаторным снижением функции ГАМК и повышением таковой глутамата. Когда зависимый от алкоголя человек внезапно прекращает пить, нарушается баланс этих систем с возникновением признаков и симптомов отмены алкоголя. В тяжелых случаях у пациента развивается алкогольный абстинентный синдром с судорогами или алкогольным делирием. Во время отмены алкоголя повышается уровень кортизола, что свидетельствует о наличии стресса (Mendelson, Stein, 1966; Keedwell et al., 2001).
В тяжелых случаях у пациента развивается алкогольный абстинентный синдром с судорогами или алкогольным делирием. Во время отмены алкоголя повышается уровень кортизола, что свидетельствует о наличии стресса (Mendelson, Stein, 1966; Keedwell et al., 2001).
Чередование периодов запоя и отмены может привести к глутамат-индуцированной возбудимости и стойкому повреждению нейронов (Brust, 2010). Повышенная необходимость в тиамине, вероятнее всего, возникает в головном мозге употребляющего алкоголь человека по причине увеличения потребности в метаболизме алкоголя, которая в свою очередь может возрасти во время абстиненции. Дефицит тиамина также вызывает избыточное высвобождение глутамата, таким образом, в сочетании с алкоголь-индуцированным расстройством регуляции рецепторов глутамата это увеличивает вероятность нейроинтоксикации. Не случайно, что при изучении историй болезни, описывающих энцефалопатию Вернике, становится очевидным, что она в основном возникает во время периода внезапной, непредвиденной и непролеченой алкогольной абстиненции.
Если дефицит тиамина появляется во время алкогольной абстиненции, быстро его устранить путем назначения только тиамина в пероральной или парентеральной формах маловероятно. По причине дефицита других питательных веществ и нарушения клеточного гомеостаза необходимы также постоянная отмена алкоголя и сбалансированное питание (Thomson, 2000; Thomson et al., 2002). Неизвестно, насколько долго сохраняется это состояние, и его продолжительность, возможно, варьирует у разных пациентов. Нормальная концентрация тиамина дифосфата в крови не является гарантией того, что требуемое количество тиамина достигло ферментных систем клеток головного мозга. Таким образом, целесообразно проведение дальнейших исследований с целью оптимизации лечения энцефалопатии Вернике и профилактики синдрома Корсакова.
Влияние алкоголя на концентрацию тиамина
Существуют две экспериментальные животные модели дефицита тиамина: лекарственно-индуцированный, вызванный антагонистами тиамина, такими как пиритиамин и окситиамин, а также недостаточное поступление его с пищей. Эксперименты на животных не полностью отражают процессы, происходящие в человеческом теле, однако они дают нам представление о патогенезе чистого дефицита тиамина в группах с/без использования алкоголя. Недостаток тиамина в рационе макак резус, даже после одного периода тиаминового голодания, ассоциировался с развитием нарушений в отдельных структурах головного мозга (нижние бугорки и медиальные вестибулярные ядра), тогда как другие структуры были более устойчивыми (Witt, Goldman-Rakic, 1983). Повреждение базальных ганглиев скорее было связано с длительными, чем с частыми эпизодами тиаминового голодания. Сосцевидные тела и дорсомедиальное ядро таламуса оставались интактными, что, возможно, указывает на то, что повреждение этих структур происходит на более поздних стадиях дефицита тиамина (Witt, Goldman-Rakic, 1983). Несмотря на отсутствие дегенерации нейронов в сосцевидных телах и дорсомедиальном ядре таламуса, у обезьян отмечались признаки нарушения памяти, аналогичные таковым у пациентов с синдромом Вернике – Корсакова (Witt, Goldman-Rakic, 1983).
Эксперименты на животных не полностью отражают процессы, происходящие в человеческом теле, однако они дают нам представление о патогенезе чистого дефицита тиамина в группах с/без использования алкоголя. Недостаток тиамина в рационе макак резус, даже после одного периода тиаминового голодания, ассоциировался с развитием нарушений в отдельных структурах головного мозга (нижние бугорки и медиальные вестибулярные ядра), тогда как другие структуры были более устойчивыми (Witt, Goldman-Rakic, 1983). Повреждение базальных ганглиев скорее было связано с длительными, чем с частыми эпизодами тиаминового голодания. Сосцевидные тела и дорсомедиальное ядро таламуса оставались интактными, что, возможно, указывает на то, что повреждение этих структур происходит на более поздних стадиях дефицита тиамина (Witt, Goldman-Rakic, 1983). Несмотря на отсутствие дегенерации нейронов в сосцевидных телах и дорсомедиальном ядре таламуса, у обезьян отмечались признаки нарушения памяти, аналогичные таковым у пациентов с синдромом Вернике – Корсакова (Witt, Goldman-Rakic, 1983).
В условиях недостатка тиамина нарушения, вызванные алкоголем, становятся более тяжелыми, а повторные эпизоды его дефицита вызывают интегральное поражение головного мозга (Crowe, El-Hadj, 2002; Price et al., 1993; Ciccia, Langlais, 2000).
Из полученных результатов можно сделать вывод, что пациенты, злоупотребляющие алкоголем, нуждаются в профилактическом назначении оральных или парентеральных (при нарушении всасывания) форм тиамина с нейропротекторной целью в периоды прохождения антиалкогольной реабилитации, детоксикации или при любом их обращении к врачу. Оценку способности абсорбировать пероральный тиамин можно провести путем выявления адекватного увеличения уровня циркулирующего тиамина дифосфата, однако этот метод недоступен для рутинной практики. Если этого недостаточно, и пациенты остаются в группе риска, рекомендуется назначение 250 мг тиамина гидрохлорида внутримышечно один раз в день в течение 5 дней (Thomson et al., 2002; Thomson, Marshall, 2006). Эта дозировка тиамина не оценивалась в контролируемых исследованиях, и на сегодняшний день не установлена нижняя граница уровня тиамина дифосфата, при котором у пациентов не будут наблюдаться нарушения в ЦНС (Thomson et al. , 2009).
, 2009).
В экспериментальных моделях на животных, основанных на отдельных предположительных механизмах дефицита тиамина, не представляется возможным отразить взаимодействие этого дефицита и других витаминодефицитов, имеющее место у лиц с различной степенью алкогольной зависимости, интоксикации и абстиненции, поскольку эти состояния тяжело воспроизвести у животных.
Вполне вероятно, что причиной синдрома Корсакова является не только недостаток тиамина. Отсутствие терапевтического ответа на тиамин отчасти может быть обусловлено необратимым повреждением клеток, вызванным предшествующим дефицитом тиамина, но его причинами также могут быть недостаточное количество других питательных веществ и нейротоксичность алкоголя.
| Патофизиология энцефалопатии Вернике Генетическая предрасположенность |
Факторы, влияющие на транспорт тиамина у лиц с алкогольной зависимостью
Генетическая предрасположенность
Существует мнение, что некоторые люди имеют генетическую предрасположенность к развитию энцефалопатии Вернике. Генетические нарушения транспорта тиамина у алкоголиков могут проявляться только при условии употребления достаточного количества алкоголя, уменьшая таким образом доступность тиамина и вызывая нарушение в системах его транспорта и накопления. Недавно были обнаружены два гена, ответственные за клеточный транспорт тиамина: THTR1 – переносчик с низкой аффинностью и THTR2 – с высокой. Также исследователи выявили изменения в некоторых генах у пациентов с энцефалопатией Вернике, которые потенциально могли нарушить экспрессию генов (Guerrini et al., 2005, 2009).
Генетические нарушения транспорта тиамина у алкоголиков могут проявляться только при условии употребления достаточного количества алкоголя, уменьшая таким образом доступность тиамина и вызывая нарушение в системах его транспорта и накопления. Недавно были обнаружены два гена, ответственные за клеточный транспорт тиамина: THTR1 – переносчик с низкой аффинностью и THTR2 – с высокой. Также исследователи выявили изменения в некоторых генах у пациентов с энцефалопатией Вернике, которые потенциально могли нарушить экспрессию генов (Guerrini et al., 2005, 2009).
Согласно Subramanian et al. (2010), хроническое употребление алкоголя у крыс, находящихся на диете Lieber – De Carli (жидкая диета, содержащая полноценное количество питательных веществ и этанол), ассоциировалось с уменьшением опосредованного переноса тиамина через мембрану щеточной каемки и базолатеральную мембрану в почках, а также с угнетением экспрессии переносчиков тиамина THTR1 и THTR2 путем блокады транскрипции их генов (Lieber, De Carli, 1989). Кроме того, существенно снижалась экспрессия тиаминфосфокиназы – фермента, превращающего тиамин в коэнзим. Помимо этого было обнаружено, что хроническое употребление алкоголя уменьшало всасывание тиамина в кишечнике, сопровождалось снижением транскрипции и экспрессии генов переносчиков тиамина (Subramanya et al., 2010), подтверждая наблюдения, сделанные в 1960-е гг. (Thomson, 1966; Thomson et al., 1970; Thomson, Leevy, 1972).
Кроме того, существенно снижалась экспрессия тиаминфосфокиназы – фермента, превращающего тиамин в коэнзим. Помимо этого было обнаружено, что хроническое употребление алкоголя уменьшало всасывание тиамина в кишечнике, сопровождалось снижением транскрипции и экспрессии генов переносчиков тиамина (Subramanya et al., 2010), подтверждая наблюдения, сделанные в 1960-е гг. (Thomson, 1966; Thomson et al., 1970; Thomson, Leevy, 1972).
Недостаточное поступление тиамина
Лица, страдающие алкогольной зависимостью, обычно не уделяют должного внимания своему питанию. Очень часто происходит потеря питательных веществ по причине рвоты, диареи и стеатореи. Общие запасы тиамина в организме невелики, около 30 мг (дневная норма, составляющая 1-2 мг, увеличивается при метаболизме алкоголя), и при недостаточном поступлении они истощаются за несколько недель, даже если при этом не нарушено всасывание в ЖКТ.
Нарушение всасывание тиамина
В 1960-е гг. было продемонстрировано, как алкоголь может влиять на всасывание тиамина в организме человека, что требует активного транспорта. Недостаточное питание является дополнительным фактором, усугубляющим мальабсорбцию (Thomson, 1966; Thomson et al., 1968, 1970; Thomson, Leevy, 1972). Алкогольное поражение печени нарушает образование запасов тиамина и его фосфорилирование. Когда мальабсорбция, возникшая по причине приема алкоголя и недостаточного питания, становится значительной, лечения только пероральными формами тиамина недостаточно (Thomson, 2000; Thomson, Marshall, 2006).
Недостаточное питание является дополнительным фактором, усугубляющим мальабсорбцию (Thomson, 1966; Thomson et al., 1968, 1970; Thomson, Leevy, 1972). Алкогольное поражение печени нарушает образование запасов тиамина и его фосфорилирование. Когда мальабсорбция, возникшая по причине приема алкоголя и недостаточного питания, становится значительной, лечения только пероральными формами тиамина недостаточно (Thomson, 2000; Thomson, Marshall, 2006).
Нарушение транспорта тиамина
Поражение, вызванное дефицитом тиамина и метаболизмом алкоголя, вероятно, нарушает нормальный транспорт тиамина в различных органах, в том числе перенос его через гематоэнцефалический барьер, а также вызывает повреждение апоферментных систем, которым затем требуется больше тиамина для нормальной работы (Pratt et al., 1985: Heap et al., 2002). Нарастающие изменения становятся причиной того, что лечение пероральными формами тиамина неэффективно, поскольку не обеспечивает достаточной его концентрации в крови для прохождения через гематоэнцефалический барьер (Thomson et al. , 2002). Это существенно отличается от энцефалопатии Вернике, вызванной только дефицитом тиамина, поскольку у таких пациентов не нарушен транспорт тиамина и имеет место терапевтический ответ даже на небольшие дозы препарата.
, 2002). Это существенно отличается от энцефалопатии Вернике, вызванной только дефицитом тиамина, поскольку у таких пациентов не нарушен транспорт тиамина и имеет место терапевтический ответ даже на небольшие дозы препарата.
Дефицит других питательных веществ
В дополнение к эффектам этанола на кишечный транспорт тиамина, дефицит других питательных веществ у пациентов, злоупотребляющих алкоголем, может также влиять на всасывание. Дефицит фолиевой кислоты ассоциируется с уменьшением содержания тиамина в крови и печени крыс, что дает возможность предположить сопутствующее нарушение всасывания тиамина. Thomson et al. (1972) обнаружили менее эффективное всасывание тиамина у крыс с дефицитом фолиевой кислоты и таким образом подтвердили, что фолиевая кислота играет важную роль в интеграции систем активного транспорта (Howard et al., 1974). Дефицит витаминов B6 и B12 у крыс может привести к нарушению образования запасов тиамина (Nishino, Itokawa, 1977). Кроме того, кинетика тиаминового транспорта может видоизменяться под влиянием самого тиамина (Hoyumpa et al. , 1976).
, 1976).
Эти открытия подчеркивают необходимость заместительной терапии всех недостающих питательных веществ у данного контингента пациентов. Ограниченное количество исследований при участии людей свидетельствует о том, что при физиологических уровнях поступления тиамина, даже при условии его дополнительного перорального приема, всасывание зависит от систем активного транспорта, на которые могут значительно влиять вышеописанные факторы (Thomson, Leevy, 1972).
В отличие от всасывания тиамина дисульфида, которое происходит путем диффузии, для водорастворимых соединений, таких как тиамина гидрохлорид, этот факт не был доказан (Thomson et al., 1971, 1983; Baker et al., 1974).
Данный механизм может также оказывать воздействие на транспорт тиамина внутрь нейрона. Нарушение транспорта фолиевой кислоты иногда является одним из механизмов, приводящих к когнитивным расстройствам, поскольку фолиевая кислота – стимулятор нейрогенеза, а имеющиеся данные указывают на то, что этот процесс нарушен в гиппокампе в предпатологической стадии синдрома Вернике – Корсакова. Печеночная энцефалопатия и гипогликемия также могут способствовать развитию данной патологии. Acker et al. (1982) продемонстрировали, что изменения топографии головного мозга у лиц, хронически употребляющих алкоголь, становятся более выраженными при усугублении печеночной патологии. Успешные профилактика и лечение синдрома Корсакова зависят от эффективной заместительной терапии всех недостающих питательных веществ и попыток предотвратить или устранить нейроинтоксикацию. Недавние протеомные исследования продемонстрировали значительное снижение активности тиамин-зависимого фермента транскетолазы у зависимых от алкоголя лиц с циррозом печени по сравнению с контрольной группой или алкоголезависимыми без цирроза (Matsumoto, 2009).
Печеночная энцефалопатия и гипогликемия также могут способствовать развитию данной патологии. Acker et al. (1982) продемонстрировали, что изменения топографии головного мозга у лиц, хронически употребляющих алкоголь, становятся более выраженными при усугублении печеночной патологии. Успешные профилактика и лечение синдрома Корсакова зависят от эффективной заместительной терапии всех недостающих питательных веществ и попыток предотвратить или устранить нейроинтоксикацию. Недавние протеомные исследования продемонстрировали значительное снижение активности тиамин-зависимого фермента транскетолазы у зависимых от алкоголя лиц с циррозом печени по сравнению с контрольной группой или алкоголезависимыми без цирроза (Matsumoto, 2009).
Эффекты пониженного содержания тиамина в крови
В многочисленных исследованиях, проводимых в разных странах, был обнаружен сниженный уровень тиамина в крови у алкоголезависимых пациентов (Leevy и соавт., 1965; Thomson et al., 1987; Cook et al., 1998; Mancinelli et al. , 2003; Brust, 2010). Тиамина дифосфат также является кофактором для ряда тиамин-зависимых ферментов. Дефицит тиамина приводит к снижению активности этих ферментов, а это в свою очередь – к нарушению митохондриальной активности, расстройствам кислородного метаболизма, снижению энергетического статуса и, в итоге, к гибели отдельных нейронов.
, 2003; Brust, 2010). Тиамина дифосфат также является кофактором для ряда тиамин-зависимых ферментов. Дефицит тиамина приводит к снижению активности этих ферментов, а это в свою очередь – к нарушению митохондриальной активности, расстройствам кислородного метаболизма, снижению энергетического статуса и, в итоге, к гибели отдельных нейронов.
Генетика
Ключевая роль тиамина в метаболизме глюкозы и энергии обусловливает его необходимость для ЦНС.
Так, 80% тиамина в головном мозге находится в виде тиамина дифосфата, кофактора для трех тиамин-зависимых ферментов, играющих важную роль в метаболизме клеток головного мозга – a-кетоглутаратдегидрогеназного комплекса, транскетолазы и пируватдегидрогеназы. Butterworth et al. продемонстрировали значительное снижение активности тиамин-зависимых ферментов: пируватдегидрогеназного комплекса, a-кетоглутаратдегидрогеназы и транскетолазы в образцах аутопсии червя мозжечка у пациентов со злоупотреблением алкоголем в анамнезе и диагнозом синдром Вернике-Корсакова, подтвержденным клинически и патоморфологически (Butterworth et al. , 1993).
, 1993).
Некоторые авторы отмечают важную роль переносчиков тиамина в патогенезе заболеваний, вызванных дефицитом тиамина. Тиамин не синтезируется организмом человека, а поступает из экзогенных источников путем всасывания в кишечнике. Клеточный транспорт тиамина опосредован специфическими белками-переносчиками, недавно описанными как переносчик тиамина 1 (THTR1) и переносчик тиамина 2 (THTR2), кодируемыми соответственно SLC19A2- и SLC19A3-генами (Guerrini et al., 2009). Исследования показали усиленную экспрессию переносчиков тиамина в тканях кишечника, плаценты, почек и мозга (Guerrini et al., 2005).
Концепция нарушения функции одного из переносчиков тиамина имеет особое значение при выборе стратеги лечения как энцефалопатии Вернике так и синдрома Корсакова.
Синдром Вернике – Корсакова может быть очень сложным, многофакторным заболеванием, в патогенезе которого важное место занимает взаимодействие нескольких генов и окружающей среды. Однако вполне возможно «мегафенное» действие (резко меняющее фенотип) генов, ответственных за предрасположенность к развитию синдрома Вернике – Корсакова. Гены переносчиков тиамина вполне могут оказывать такой эффект.
Гены переносчиков тиамина вполне могут оказывать такой эффект.
Особенности дозирования тиамина для лечения энцефалопатии Вернике
Головной мозг весит около 1,5 кг, что составляет всего 2% от массы тела, но получает 15% от сердечного выброса и использует 20% от общего кислорода, поступающего в организм. В состоянии покоя все его энергетические потребности обеспечиваются глюкозой. Около половины тиамина, содержащегося в мозге (главным образом в форме тиамина дифосфата), вовлечено в процесс окисления пирувата и от него зависит почти все потребление мозгом кислорода (McIlwain, Bachelard, 1971).
Постоянное поступление тиамина в головной мозг необходимо для синтетических и обменных процессов. При нормальной концентрации тиамина в плазме он поглощается нервной тканью почти исключительно путем процесса, опосредованного высокоаффинным переносчиком. Поглощение тиамина происходит со скоростью 0,3 мкг/ч/г ткани, что немногим отличается от скорости обмена тиамина в головном мозге (0,3-0,5 мкг/ч/г ткани (Greenwood et al. , 1980; Greenwood, Pratt, 1982; Rindi et al., 1980). Этого достаточно лишь для обеспечения потребностей мозга, что делает его очень уязвимым для любого снижения уровня тиамина в крови. Может происходить и пассивная диффузия, требующая, однако, высоких концентраций тиамина, которых невозможно достичь путем перорального приема у ослабленных пациентов, употребляющих алкоголь (Thomson et al., 2002). При поражении апоферментных систем возрастает потребность в тиамине и вероятность развития энцефалопатии Вернике или синдрома Корсакова (Pratt et al., 1985; Heap et al., 2002). Также есть предположение, что при генетических аномалиях системы транспорта или повреждении ферментных комплексов внутри нейрона так называемый «нормальный» уровень тиамина в крови не является достаточным. Этим можно хотя бы отчасти объяснить, почему пациенты с алкоголизмом и энцефалопатией Вернике нуждаются в высоких дозах парентерального тиамина.
, 1980; Greenwood, Pratt, 1982; Rindi et al., 1980). Этого достаточно лишь для обеспечения потребностей мозга, что делает его очень уязвимым для любого снижения уровня тиамина в крови. Может происходить и пассивная диффузия, требующая, однако, высоких концентраций тиамина, которых невозможно достичь путем перорального приема у ослабленных пациентов, употребляющих алкоголь (Thomson et al., 2002). При поражении апоферментных систем возрастает потребность в тиамине и вероятность развития энцефалопатии Вернике или синдрома Корсакова (Pratt et al., 1985; Heap et al., 2002). Также есть предположение, что при генетических аномалиях системы транспорта или повреждении ферментных комплексов внутри нейрона так называемый «нормальный» уровень тиамина в крови не является достаточным. Этим можно хотя бы отчасти объяснить, почему пациенты с алкоголизмом и энцефалопатией Вернике нуждаются в высоких дозах парентерального тиамина.
Современное лечение энцефалопатии Вернике
В случае если энцефалопатия Вернике вызвана исключительно недостатком тиамина, адекватного терапевтического ответа можно достичь путем назначения небольших пероральных и парентеральных доз (De Wardener, Lennox, 1947). Для лечения пациентов с энцефалопатией Вернике, связанной со злоупотреблением алкоголем, необходимы значительно более высокие дозы парентерального тиамина (до 1 г в течение первых 24 часов), так как в этих случаях предполагается нарушение систем его транспорта.
Для лечения пациентов с энцефалопатией Вернике, связанной со злоупотреблением алкоголем, необходимы значительно более высокие дозы парентерального тиамина (до 1 г в течение первых 24 часов), так как в этих случаях предполагается нарушение систем его транспорта.
Парентеральный тиамин в дозировке 100-250 мг не всегда предотвращает летальный исход, и длительное наблюдение за пациентами с данным состоянием позволяет выявить у них синдром Корсакова в 56-84% случаев (Victor et al., 1971; Wood et al., 1986; Thomson et al., 2008). Такой результат не обязательно связан с необратимыми изменениями в головном мозге, имеющими место на момент начала лечения. В других исследованиях показано, что эти дозы являются субоптимальными и не могут удовлетворить потребность в тиамине, уменьшить клинические проявления или предотвратить смертельный исход (Cook et al., 1998). Описаны случаи, когда была потребность ввести до 1 г тиамина в течение первых часов для получения терапевтического ответа (Cook et al. , 1998; Nakada, Knight, 1984; Lindberg, Oyler, 1990).
, 1998; Nakada, Knight, 1984; Lindberg, Oyler, 1990).
Дозы тиамина, рекомендуемые Британским национальным формуляром и Королевской коллегией врачей в Лондоне и разрешенные для использования в Великобритании Агентством по регулированию лекарственных средств с 1994 г., также соответствуют доказательно обоснованным принципам, опубликованным Британской ассоциацией психофармакологии, Европейской федерацией неврологических обществ, а также руководству Национального института здоровья и клинического совершенствования (Lingford-Hughes et al., 2004; Galvin et al., 2010; NICE 2011).
| Клиническая оценка пациентов с риском дефицита тиамина (Thomson et al., 2009) Ранние признаки и симптомы дефицита тиамина Потеря аппетита Поздние признаки и симптомы Классическая триада: глазодвигательные нарушения, мозжечковая дисфункция (атаксия) и спутанность сознания Критерии для определения энцефалопатии Вернике: 2 из нижеследующих (Caine et al. Неполноценное питание |
Определение риска развития энцефалопатии Вернике
Pitel et al. (2011) использовали критерии, разработанные Caine et al. (1997), для определения индивидуального риска развития энцефалопатии Вернике у 56 пациентов с алкогольной абстиненцией. Контрольную группу составили 38 здоровых добровольцев. В основной группе 15 пациентов (27%) не соответствовали ни одному критерию, 32 (57%) – одному, и 9 (16%) – 2 и более. Так, у алкоголезависимых пациентов, которые не отвечали ни одному критерию, показатели были такими же, как и в контрольной группе. Легкие и средней степени тяжести нарушения были выявлены у больных, соответствовавших одному критерию, тяжелые – двум и более. Уровень тиамина дифосфата определялся у 28 пациентов из основной группы и у 22 – из группы контроля. Несмотря на то, что существенных отличий между уровнями тиамина дифосфата в обеих группах не наблюдалось, они избирательно соответствовали степени нарушения памяти у пациентов, употреблявших алкоголь. Анализируя данные, можно сделать вывод, что критерии Caine et al. могут успешно применяться для определения риска развития энцефалопатии Вернике у алкоголезависимых пациентов, диагноз у которых был впоследствии подтвержден патоморфологически (Pitel et al., 2011).
Анализируя данные, можно сделать вывод, что критерии Caine et al. могут успешно применяться для определения риска развития энцефалопатии Вернике у алкоголезависимых пациентов, диагноз у которых был впоследствии подтвержден патоморфологически (Pitel et al., 2011).
Сделанные открытия указывают на необходимость поддерживать нормальный уровень тиамина в крови и вероятность ухудшения памяти у лиц с нарушенным транспортом тиамина. Это должно найти отражение в клинической практике в виде профилактических мероприятий, которые могут быть применимы к алкоголезависимым пациентам при обращении за любой медицинской помощью, а не только при лечении энцефалопатии Вернике.
Необходимость определения оптимальной дозы парентерального тиамина для профилактики и терапии энцефалопатии Вернике также подчеркивалась в двух обзорах (Day et al., 2008; Sechi, Serra, 2007). Galvin et al. (2010) сравнивали клинические признаки заболевания у пациентов, употреблявших и не употреблявших алкоголь, для его определения использовав критерии Caine et al. , а также МРТ-исследование. Неполноценное питание и рвота чаще наблюдались в группах не употреблявших алкоголь, тогда как глазодвигательные и мозжечковые нарушения, классическая триада и измененное сознание – у алкоголезависимых. Следует предположить, что энцефалопатия Вернике, возникшая вследствие нарушенной диеты, чаще расценивается как «остро возникший синдром». В то же время у лиц, страдающих алкоголизмом, этот синдром протекает скрыто, субклинически, на его проявления часто не обращают внимания или по ошибке принимают за последствия приема алкоголя, и таким образом пациенты не получают своевременного лечения.
, а также МРТ-исследование. Неполноценное питание и рвота чаще наблюдались в группах не употреблявших алкоголь, тогда как глазодвигательные и мозжечковые нарушения, классическая триада и измененное сознание – у алкоголезависимых. Следует предположить, что энцефалопатия Вернике, возникшая вследствие нарушенной диеты, чаще расценивается как «остро возникший синдром». В то же время у лиц, страдающих алкоголизмом, этот синдром протекает скрыто, субклинически, на его проявления часто не обращают внимания или по ошибке принимают за последствия приема алкоголя, и таким образом пациенты не получают своевременного лечения.
Изменения в головном мозге могут быть необратимыми еще до начала терапии, однако определить это наверняка можно только пройдя полный курс лечения установленной оптимальной дозой тиамина. Величина дозы для конкретного пациента на сегодняшний день неизвестна. Предпочтение отдается комбинированным препаратам, содержащим ряд питательных веществ.
Вполне вероятно, что терапевтический ответ на применение тиамина может изменяться под влиянием алкоголь-индуцированной нейроинтоксикации. Молодые пациенты, даже находясь в более тяжелом состоянии, могут реагировать быстрее на заместительную терапию тиамином, тогда как у лиц пожилого возраста, давно употребляющих алкоголь, с многочисленными субклиническими эпизодами энцефалопатии Вернике в анамнезе, прогноз менее благоприятный.
Молодые пациенты, даже находясь в более тяжелом состоянии, могут реагировать быстрее на заместительную терапию тиамином, тогда как у лиц пожилого возраста, давно употребляющих алкоголь, с многочисленными субклиническими эпизодами энцефалопатии Вернике в анамнезе, прогноз менее благоприятный.
| Неотложная терапия энцефалопатии Вернике Тиамин в дозе 500 мг три раза в день 23 дня и 250 мг/сут следующие 35 дней: в/в капельно, в течение 30 минут, в 50100 мл изотонического раствора натрия хлорида |
Клинические аспекты синдрома Корсакова
Синдром Корсакова характеризуется глубокой антероградной и ретроградной амнезией, дезориентацией в пространстве и времени и отсутствием понимания происходящего.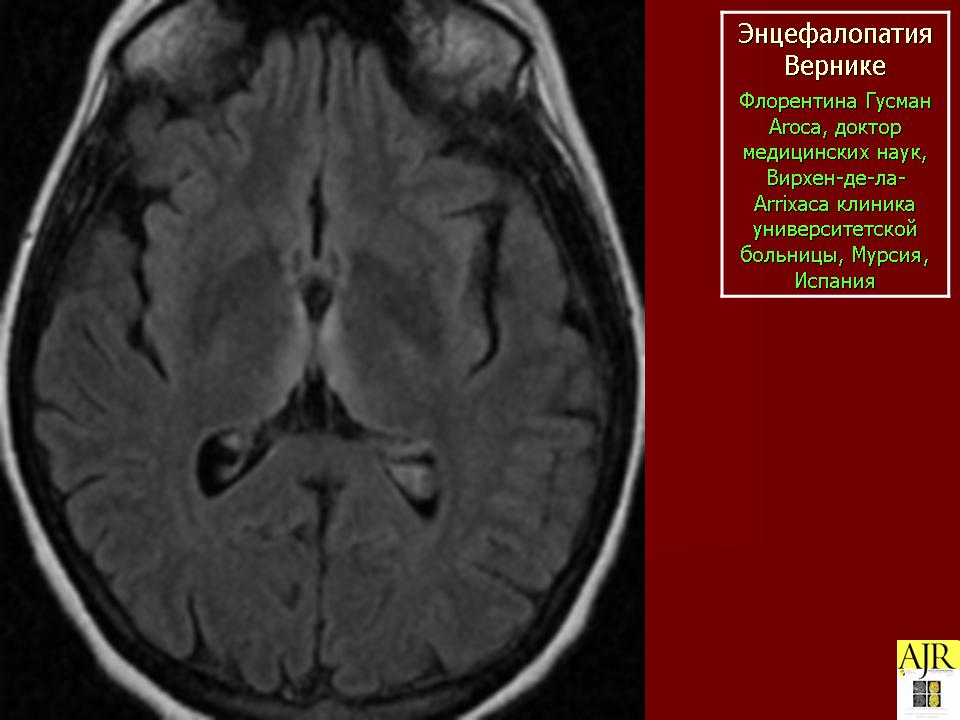 Также могут возникать периферическая нейропатия, нистагм и атаксия. Последние два признака характерны также для ранних проявлений энцефалопатии Вернике. К типичным признакам и симптомам относятся также конфабуляции, тревога и апатия.
Также могут возникать периферическая нейропатия, нистагм и атаксия. Последние два признака характерны также для ранних проявлений энцефалопатии Вернике. К типичным признакам и симптомам относятся также конфабуляции, тревога и апатия.
Пациенты с синдром Корсакова плохо выполняют тесты на проверку лобных функций, особенно исполнительных (Kopelman, 1989). Помимо этого были продемонстрированы нарушения пространственно-временной ориентации (Kopelman, 1989). IQ чаще всего не страдает, как и оперативная память (Jacobson, Lishman, 1987). Процедурная и семантическая память также могут быть сохранены.
При клинической оценке больных с синдромом Корсакова необходимо обратить внимание на сбор анамнеза и физикальное обследование (Kopelman et al., 2009). Анамнез, собранный у семьи и друзей, может предоставить сведения о жизни пациента до госпитализации, длительности его злоупотребления алкоголем, осложнениях и видимом ухудшении состояния. При физикальном обследовании часто можно выявить периферическую нейропатию и мозжечковую атаксию.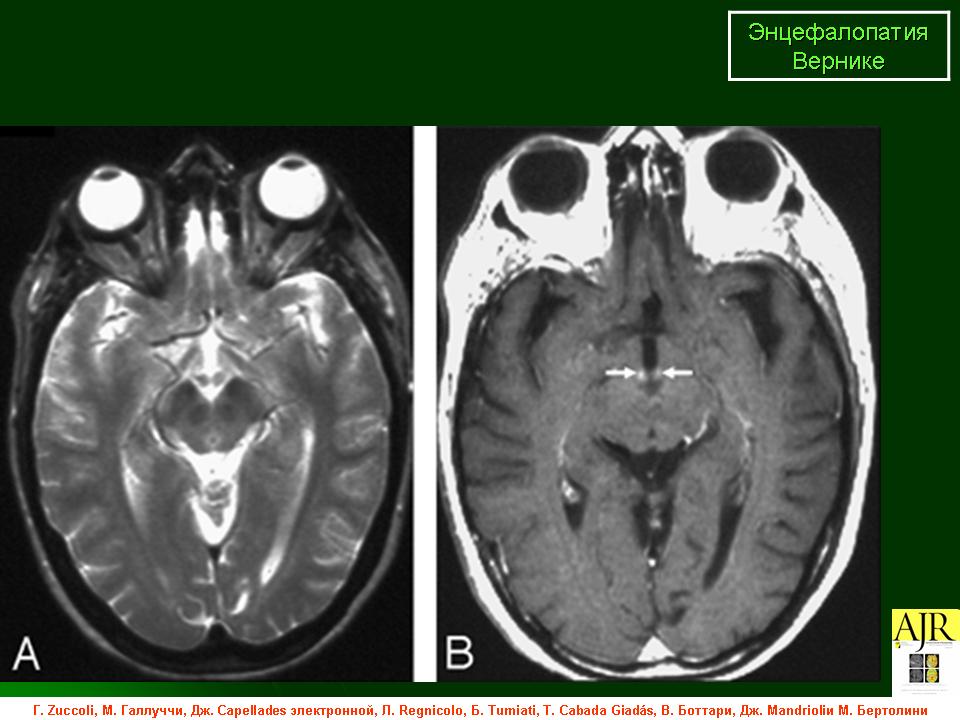 Оценка когнитивных функций должна проводиться только спустя 4 недели после отмены алкоголя.
Оценка когнитивных функций должна проводиться только спустя 4 недели после отмены алкоголя.
Оказание помощи пациентам с синдромом Корсакова
Пациентам с синдром Корсакова и алкогольным поражением головного мозга необходима комплексная поддержка, хорошо интегрированная медицинская, социальная помощь и уход.
Наряду с рекомендациями по применению тиамина, целесообразно рассмотреть комплексную программу лечения и обеспечить условия для полной алкогольной реабилитации, а также дальнейшее наблюдение специалистами с целью мониторинга улучшения когнитивных функций, психического и физического благополучия (Leenane, 1986).
Таким пациентам, а также их родственникам и опекунам необходимо обеспечить всестороннюю комплексную поддержку с учетом их когнитивных и поведенческих особенностей.
Выводы
Синдром Корсакова возникает по причине вовремя не поставленного диагноза энцефалопатии Вернике или ее лечения недостаточными дозами тиамина. Иногда у пациентов до начала лечения уже есть стойкое необратимое или полуобратимое поражение головного мозга, и это может ограничивать терапевтический ответ. Из этого следует, что необходимо выявлять пациентов, находящихся в группе риска и проводить терапию надлежащими дозами парентерального тиамина. Своевременное вмешательство имеет решающее значение, прежде чем под влиянием изменений, происходящих в мозге, потребность в тиамине увеличится до уровня, который организм больного не в состоянии обеспечить.
Из этого следует, что необходимо выявлять пациентов, находящихся в группе риска и проводить терапию надлежащими дозами парентерального тиамина. Своевременное вмешательство имеет решающее значение, прежде чем под влиянием изменений, происходящих в мозге, потребность в тиамине увеличится до уровня, который организм больного не в состоянии обеспечить.
Было выдвинуто предположение о том, что существует разница между синдромом Вернике – Корсакова, обусловленным пищевым дефицитом тиамина, и данным синдромом, связанным с дефицитом тиамина на фоне приема алкоголя. Доказательства опираются на тот факт, что синдром Корсакова редко возникает в первом случае, но часто встречается у больных алкоголизмом. Тот факт, что для лечения энцефалопатии Вернике у алкоголезависимых лиц необходимы большие дозы тиамина, также подтверждает различные механизмы возникновения.
Эти две причины энцефалопатии Вернике имеют определенные отличия. Биохимические механизмы заболевания, вызванного недостаточным поступлением тиамина с пищей, относительно простые. В отличие от этого, дефицит тиамина, сочетающийся со злоупотреблением алкоголем (зависимостью), вызывает значительные изменения в головном мозге и во всем организме больного. В такой ситуации необходимо увеличить дозы парентерального тиамина. Однако заместительная терапия тиамином не окажет быстрого действия на стойкие, глубокие нарушения, которые, вероятно, появились задолго до начала терапии. Именно поэтому так важно понимать связь между возникающими биохимическими изменениями и нарушением всасывания витаминов, чтобы предотвратить его до развития энцефалопатии Вернике, а также определить его роль в повреждении головного мозга, связанном с синдромом Корсакова.
В отличие от этого, дефицит тиамина, сочетающийся со злоупотреблением алкоголем (зависимостью), вызывает значительные изменения в головном мозге и во всем организме больного. В такой ситуации необходимо увеличить дозы парентерального тиамина. Однако заместительная терапия тиамином не окажет быстрого действия на стойкие, глубокие нарушения, которые, вероятно, появились задолго до начала терапии. Именно поэтому так важно понимать связь между возникающими биохимическими изменениями и нарушением всасывания витаминов, чтобы предотвратить его до развития энцефалопатии Вернике, а также определить его роль в повреждении головного мозга, связанном с синдромом Корсакова.
Следует принимать во внимание, что нормальный уровень тиамиа дифосфата или активность транскетолазы в эритроцитах не гарантируют достаточного количества тиамина дифосфата или тиамина трифосфата в клетках головного мозга по причине возможного нарушения транспорта внутрь нейрона. Более того, определение активности одного фермента не означает, что все ферментные системы работают нормально. Потребность в тиамине в некоторой мере определяется алкоголь-индуцированным повреждением апоферментов и нарушением работы переносчиков тиамина.
Потребность в тиамине в некоторой мере определяется алкоголь-индуцированным повреждением апоферментов и нарушением работы переносчиков тиамина.
Несмотря на лечение тиамином, синдром Корсакова может развиваться у многих лиц с энцефалопатией Вернике, употребляющих алкоголь. Одной из возможных причин этого может быть тот факт, что тиамин часто назначается перорально и не абсорбируется организмом пациента в количествах, позволяющих создать в крови концентрацию тиамина, достаточную для прохождения его через гематоэнцефалический барьер и обеспечения необходимого количества в клетках мозга. Некоторые люди находятся в группе повышенного риска по причине генетической предрасположенности. Это означает, что их потребность в тиамине повышена, и концентрация его в плазме крови для прохождения в клетки головного мозга тоже должна быть больше. Иногда причиной могу быть стойкие необратимые изменения в ЦНС, произошедшие до начала лечения.
Терапевтический ответ на парентеральное применение тиамина у различных пациентов может быть разным: некоторым достаточно невысоких доз тиамина, другим же необходимо ввести не менее 1 г парентерально в течение первых 24 часов. К сожалению, нет официальных контролируемых плацебо исследований с различными дозировками тиамина, которыми можно бы было руководствоваться при назначении лечения, равно как и по подбору дозы для каждого конкретного пациента. Дефицит других питательных веществ, например фолиевой кислоты и магния, отчасти ограничивает терапевтический ответ на тиамин, и потребуется время для восстановления после повреждения, вызванного сочетанными эффектами дефицита тиамина и алкоголя. Таким образом, целесообразным является применение стабильных высоких доз парентерального тиамина наряду с обеспечением всеми другими питательными веществами, необходимыми для работы головного мозга, и длительное наблюдение за состоянием пациента. Для оптимизации терапии также необходимы полный отказ от приема алкоголя и коррекция диеты.
К сожалению, нет официальных контролируемых плацебо исследований с различными дозировками тиамина, которыми можно бы было руководствоваться при назначении лечения, равно как и по подбору дозы для каждого конкретного пациента. Дефицит других питательных веществ, например фолиевой кислоты и магния, отчасти ограничивает терапевтический ответ на тиамин, и потребуется время для восстановления после повреждения, вызванного сочетанными эффектами дефицита тиамина и алкоголя. Таким образом, целесообразным является применение стабильных высоких доз парентерального тиамина наряду с обеспечением всеми другими питательными веществами, необходимыми для работы головного мозга, и длительное наблюдение за состоянием пациента. Для оптимизации терапии также необходимы полный отказ от приема алкоголя и коррекция диеты.
Выявление, раннее вмешательство и соответствующее лечение с применением тиамина, отказ от приема алкоголя и комплексная всесторонняя реабилитация – все это необходимо для удовлетворения потребностей этого изолированного и стигматизированного контингента пациентов.
Подготовила Лариса Калашник
Энцефалопатия Вернике — Медичний центр «Ліко-Мед»
Дата публикации
3 октября 2018
Что такое?
Энцефалопатия Вернике является серьезным заболеванием мозга, которое вызывается длительным дефицитом тиамина (витамина В1). Такая патология чаще всего развивается у алкоголиков, в редких случаях – у лиц, проходящих химиотерапевтическое лечение, с хронической рвотой, расстройством пищевого поведения, прошедших лечение методом бариатрической хирургии. Энцефалопатия Вернике может вызывать спутанность сознания, нарушение мышечной координации, проблемы со зрением. Подобное состояние часто сопровождается другой хронической патологией ‑ синдромом Корсакова (корсаковским синдромом), для которого характерна потеря памяти. Когда эти две патологии развиваются одновременно, говорят об одной болезни ‑ синдроме Вернике-Корсакова.
Чего ожидать?
Энцефалопатия Вернике приводит к повреждению таламуса и гипоталамуса ‑ областей головного мозга. Процесс повреждения мозга можно замедлить или обратить вспять, если провести лечение на ранней стадии. Энцефалопатия Вернике обычно приводит к другому состоянию, называемому синдромом Корсакова, при котором наблюдаются хронические проблемы с памятью. У некоторых больных память может быть восстановлена при своевременном лечении. Отсутствие лечения ухудшает состояние больного и чревато летальным исходом. Энцефалопатия Вернике и синдром Корсакова лечатся приемом тиамина (витамина B1). Некоторые пациенты нуждаются в стационарном лечении.
Процесс повреждения мозга можно замедлить или обратить вспять, если провести лечение на ранней стадии. Энцефалопатия Вернике обычно приводит к другому состоянию, называемому синдромом Корсакова, при котором наблюдаются хронические проблемы с памятью. У некоторых больных память может быть восстановлена при своевременном лечении. Отсутствие лечения ухудшает состояние больного и чревато летальным исходом. Энцефалопатия Вернике и синдром Корсакова лечатся приемом тиамина (витамина B1). Некоторые пациенты нуждаются в стационарном лечении.
Распространенность
От энцефалопатии Вернике страдает от 1% до 3% людей.
Лечение
Лечение энцефалопатии Вернике включает прием тиамина и отказ от употребления алкоголя.
Когда обращаться к врачу?
При наличии симптомов энцефалопатии Вернике или отсутствии улучшения на фоне проводимого лечения требуется срочная медицинская помощь.
О чем спросить врача?
- Являются ли наблюдаемые симптомы следствием энцефалопатии Вернике или имеются другие причины?
- Какое лечение необходимо?
- Требуется ли госпитализация?
- Приведет ли лечение к улучшению состояния?
- Уменьшатся ли проблемы с памятью?
- Есть ли необходимость в консультации психотерапевта?
Постановка диагноза
При диагностике энцефалопатии Вернике врач ознакамливается с историей болезни и проводит физикальный осмотр. Также может понадобиться проведение анализов крови и мочи, КТ или МРТ мозга.
Также может понадобиться проведение анализов крови и мочи, КТ или МРТ мозга.
Факторы риска
- Злоупотребление алкоголем.
- Расстройства пищевого поведения.
- Прохождение химиотерапевтического лечения.
- ВИЧ.
- Хирургическое вмешательство с целью снижения веса.
МРТ Центр в Санкт-Петербурге — Эцефалопатия Вернике
Энцефалопатия Вернике — говоря научным языком: острый верхний геморрагический полиоэнцефалит Гайе-Вернике. Если дать этому недугу более простое определение, то это болезнь, поражающая головной мозг человека. Вообще то данный недуг не есть редкостью в современном обществе, а все, потому что основной причиной его возникновения есть не что иное, как хроническая алкогольная зависимость. То есть человек в большинстве случаев сам не способен осознать свой недуг, даже если его мучают страшные головные боли. Очень часто этот недуг сопровождается частыми и обильными носовыми кровотечениями, повышенным давлением, общей слабостью и так далее.
Причины заболевания
Не смотря на то что основной причиной самой болезни есть острый авитаминоз, а именно недостаток в организме витамина В1, спровоцировать ее могут сразу три фактора:
Хронический алкоголизм — алкоголь в непомерных дозах да еще при недостатке нормального питания и так оказывает разрушительное влияние на основные участки головного мозга, а если к нему еще и присоединить острый авитаминоз это уже реальный шанс оказаться в группе риска,
СПИД — кроме иммунодефицита, СПИД влечет за собой и поражение некоторых участков мозга,
Истощение — несбалансированное а попросту говоря скудное питание, так или иначе, вызывает авитаминоз,
Опухоли — злокачественные новообразования на любой части головного мозга,
Гемодиализ — одна из форм лечения при острой почечной недостаточности.
Главная угроза заболевания в том, что зачастую, симптомы не имеют «букетных» проявлений, и не воспринимаются серьезно. Но если вовремя не диагностировать болезнь, а это можно сделать, только проведя полное и тщательное исследование, в том числе сделав МРТ головного мозга, больной может резко впасть в кому которая в большинстве случаев имеет летальный исход.
Симптомы заболевания
Симптоматика в принципе идентична к большинству симптомов любой из болезней мозга. Основными симптомами принято считать:
- Яркую потерю ориентации в пространстве (хроническую, в трезвом состоянии и при приеме алкоголя),
- Полная апатия к радостным или горестным событиям в жизни больного,
- Излишняя агрессия,
- Стойкость к боли,
- Двусторонний паралич наружной прямой мышцы глаза,
- Излишняя, просто таки ненормальная возбудимость,
- Странности в поведении, которые ранее не наблюдались и т.д.
Но четко определить, что все эти симптомы есть проявлением именно болезни Энцефалопатия Вернике, сможет только МРТ головного мозга.
ФГБНУ НЦПЗ. ‹‹Экзогенные психические расстройства››
Энцефалопатия Гайе — Вернике. Заболевают преимущественно мужчины от 30 до 50 лет, изредка старше. Описаны случаи заболевания и во втором десятилетии жизни [Дягилева В. П., 1971]. Психоз начинается с делирия со скудными, отрывочными однообразными и статичными зрительными галлюцинациями и иллюзиями. Преобладает тревожный аффект. Двигательное возбуждение проявляется в основном стереотипными действиями, как при обыденных или профессиональных занятиях, и в ограниченном пространстве, часто в пределах постели. Возможны периодические кратковременные состояния обездвиженности с напряжением мышц. Больные однообразно выкрикивают отдельные слова, невнятно бормочут. Временами бывает «молчаливое» возбуждение. Речевой контакт обычно невозможен. Речевая бессвязность обусловливает сходство начальных делириозных картин с аменцией. Это сходство усиливается при появлении мусситирующего делирия. Спустя несколько дней клиническая картина изменяется. Днем возникает оглушение сознания, или сомнолентность, при утяжелении состояния развивается сопор — псевдоэнцефалитический синдром [Enkin M., 1957]. В наиболее тяжелых случаях сопор переходит в кому. Значительно реже появлению симптомов оглушения предшествует апатический ступор [Ларичева Г.
П., 1971]. Психоз начинается с делирия со скудными, отрывочными однообразными и статичными зрительными галлюцинациями и иллюзиями. Преобладает тревожный аффект. Двигательное возбуждение проявляется в основном стереотипными действиями, как при обыденных или профессиональных занятиях, и в ограниченном пространстве, часто в пределах постели. Возможны периодические кратковременные состояния обездвиженности с напряжением мышц. Больные однообразно выкрикивают отдельные слова, невнятно бормочут. Временами бывает «молчаливое» возбуждение. Речевой контакт обычно невозможен. Речевая бессвязность обусловливает сходство начальных делириозных картин с аменцией. Это сходство усиливается при появлении мусситирующего делирия. Спустя несколько дней клиническая картина изменяется. Днем возникает оглушение сознания, или сомнолентность, при утяжелении состояния развивается сопор — псевдоэнцефалитический синдром [Enkin M., 1957]. В наиболее тяжелых случаях сопор переходит в кому. Значительно реже появлению симптомов оглушения предшествует апатический ступор [Ларичева Г. И., 1969]. Психопатологические симптомы всегда сочетаются с неврологическими и соматическими нарушениями [Демичев А. П., 1970]. Ухудшению психического состояния неизменно сопутствует утяжеление соматоневрологических расстройств. Наиболее отчетливо выражены разнообразные неврологические расстройства. Их проявления могут быстро меняться. Часто возникают фибриллярные подергивания мускулатуры губ и других мышц лица. Постоянны сложные гиперкинезы, в которых перемежаются дрожание, подергивания, хореиформные, атетоидные и другие движения. Возможны приступы торсионного спазма. Интенсивность и распространенность гиперкинезов, как и их проявления, различны. Также изменчивы и нарушения мышечного тонуса в форме гипер- или гипотонии.
И., 1969]. Психопатологические симптомы всегда сочетаются с неврологическими и соматическими нарушениями [Демичев А. П., 1970]. Ухудшению психического состояния неизменно сопутствует утяжеление соматоневрологических расстройств. Наиболее отчетливо выражены разнообразные неврологические расстройства. Их проявления могут быстро меняться. Часто возникают фибриллярные подергивания мускулатуры губ и других мышц лица. Постоянны сложные гиперкинезы, в которых перемежаются дрожание, подергивания, хореиформные, атетоидные и другие движения. Возможны приступы торсионного спазма. Интенсивность и распространенность гиперкинезов, как и их проявления, различны. Также изменчивы и нарушения мышечного тонуса в форме гипер- или гипотонии.
Мышечная гипертония может развиваться резкими приступами. Ее интенсивность бывает столь значительной, что позволяет говорить о децеребрационной ригидности. Характерна так называемая оппозиционная гипертония — нарастание сопротивления при энергичных попытках изменить положение конечностей. Гипертония мышц нижних конечностей иногда сочетается с гипотонией мышц рук. Постоянны симптомы орального автоматизма: хоботковый рефлекс, спонтанное вытягивание губ и хватательные рефлексы. В развернутой, а иногда и в терминальной стадии болезни всегда присутствует атаксия.
Гипертония мышц нижних конечностей иногда сочетается с гипотонией мышц рук. Постоянны симптомы орального автоматизма: хоботковый рефлекс, спонтанное вытягивание губ и хватательные рефлексы. В развернутой, а иногда и в терминальной стадии болезни всегда присутствует атаксия.
Развиваются нистагм, птоз, диплопия, страбизм, неподвижный взгляд, зрачковые расстройства — так называемый симптом Гуддена: миоз, анизокория, ослабление реакции на свет вплоть до ее полного исчезновения и нарушение конвергенции. Наиболее ранний и постоянный симптом — нистагм, чаще крупноразмашистый, горизонтальный, которым глазодвигательные нарушения могут ограничиться [Демичев А. П., 1970; Wardner H., Lennox В., 1947]. Как правило, наблюдаются гиперпатия и полиневриты, сопровождаемые легкими парезами и пирамидными знаками. Из менингеальных симптомов чаще всего наблюдается ригидность мышц затылка. При спинномозговой пункции лежа отмечается (хотя и не всегда) несколько повышенное давление цереброспинальной жидкости (до 200—400 мм вод. ст., реже выше). В последней может быть повышено содержание белка при нормальном цитозе.
ст., реже выше). В последней может быть повышено содержание белка при нормальном цитозе.
При пневмоэнцефалографии обнаруживают явления гидроцефалии, в частности расширение боковых желудочков. Возможны трофические нарушения: больные физически истощены, выглядят старше своих лет. Лицо одутловатое или сальное. Язык подергивается, малинового цвета, сосочки с краев сглажены. Гипертермия постоянна, повышение температуры тела до 40—41 °С — прогностически неблагоприятный признак. Кожа сухая, с шелушением или, напротив, влажная, с обильным, в виде капель росы потоотделением. Конечности отечны. Легко образуются обширные некротические пролежни. Постоянны тахикардия и аритмия. АД по мере утяжеления психоза снижается, легко возникают коллаптоидные состояния. Дыхание учащено. Печень может быть увеличенной и болезненной. Нередко отмечается частый жидкий стул. В крови — лейкоцитоз.
Через 3—10 дней после развития манифестных симптомов болезни психические и соматовегетативные расстройства могут на некоторое время значительно редуцироваться. Эти «светлые промежутки» продолжаются от одного до нескольких дней. Повторные ухудшения, которых может быть несколько, обычно менее тяжелы и менее продолжительны, чем предыдущие.
Эти «светлые промежутки» продолжаются от одного до нескольких дней. Повторные ухудшения, которых может быть несколько, обычно менее тяжелы и менее продолжительны, чем предыдущие.
Самым ранним признаком выздоровления служит нормализация сна, вначале лишь во вторую половину, а далее в течение всей ночи. У женщин с началом улучшения состояния могут появиться симптомы конфабуляторной спутанности, свидетельствующие о возможности последующего развития корсаковского синдрома. Смерть чаще наступает в середине или к концу 2-й недели от начала психоза. Нередко летальному исходу способствуют присоединяющиеся интеркуррентные заболевания, в первую очередь пневмонии. Психоз, не приводящий к смерти, обычно длится 3—6 нед и более. Обычным исходом энцефалопатии Гайе — Вернике является психоорганический синдром различной глубины, продолжительности и структуры, а также корсаковский синдром (чаще у женщин) и симптомы псевдопаралича (у мужчин).
Митигированная острая энцефалопатия впервые описана С. С. Корсаковым (1887). В продромальном периоде, продолжающемся 1—2 мес, преобладает астения с выраженной раздражительностью, гиперестезией, пониженным настроением, нарушениями сна, диспепсическими расстройствами. Неврологические симптомы преимущественно имеют форму невритов. Манифестные расстройства проявляются нетяжелой делириозной симптоматикой ночью, а днем наблюдается либо легкая сонливость, либо тревожно-дисфорическая депрессия с ипохондрией. Всегда можно выявить отчетливое нарушение запоминания. Вегетативно-неврологические расстройства постоянны, но мало выражены. Острый психоз сменяется астенией, иногда в сочетании с депрессией. Продолжительность болезненных расстройств от нескольких недель до 2—3 мес. Явления астении исчезают раньше, чем нарушения памяти.
С. Корсаковым (1887). В продромальном периоде, продолжающемся 1—2 мес, преобладает астения с выраженной раздражительностью, гиперестезией, пониженным настроением, нарушениями сна, диспепсическими расстройствами. Неврологические симптомы преимущественно имеют форму невритов. Манифестные расстройства проявляются нетяжелой делириозной симптоматикой ночью, а днем наблюдается либо легкая сонливость, либо тревожно-дисфорическая депрессия с ипохондрией. Всегда можно выявить отчетливое нарушение запоминания. Вегетативно-неврологические расстройства постоянны, но мало выражены. Острый психоз сменяется астенией, иногда в сочетании с депрессией. Продолжительность болезненных расстройств от нескольких недель до 2—3 мес. Явления астении исчезают раньше, чем нарушения памяти.
Энцефалопатия со сверхострым «молниеносным» течением. Считается, что заболевают только мужчины. В продроме, длящемся 2—3 нед, преобладает адинамическая астения с выраженными вегетативно-неврологическими расстройствами, интенсивность которых резко усиливается при развитии инициальных симптомов психоза. Психоз с самого начала проявляется профессиональным или мусситирующим делирием. Температура тела повышается до 40—41 °С. Через 1 или несколько дней развивается тяжелое оглушение вплоть до комы. Смерть наступает чаще всего на 3—6-й день болезни. При своевременно начатом лечении возможно выздоровление с развитием преходящего или затяжного псевдопаралитического синдрома.
Психоз с самого начала проявляется профессиональным или мусситирующим делирием. Температура тела повышается до 40—41 °С. Через 1 или несколько дней развивается тяжелое оглушение вплоть до комы. Смерть наступает чаще всего на 3—6-й день болезни. При своевременно начатом лечении возможно выздоровление с развитием преходящего или затяжного псевдопаралитического синдрома.
РЕДКИЙ КЛИНИЧЕСКИЙ СЛУЧАЙ ЭНЦЕФАЛОПАТИИ ГАЙЕ – ВЕРНИКЕ У БЕРЕМЕННОЙ: ВОПРОСЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ | Смертина
1. Сиволап Ю. П., Дамулин И. В. Синдром Вернике – Корсакова /Неврология, нейропсихиатрия, психосоматика. 2014. № 4. С. 76–80.
2. Netravathi M., Sinha S., Taly A. B., Bindu P. S, Bharath R. D. Hyperemesisgravidarum-induced Wernickes encephalopathy: Serial clinical, electrophysiological and MR imaging observations // J Neurol Sci. 2009. No. 284 (1–2). Р. 214–216.
No. 284 (1–2). Р. 214–216.
3. Schabelman E., Kuo D. Glucose Before Thiamine for Wernicke Encephalopathy: a Literature Review // J Emerg Med. 2012. No. 42 (4). Р. 488–494.
4. Barron S., Lewis B., Wellmann K. et al. Polyamine Modulation of NMDARs as a Mechanism to Reduce Effects of Alcohol Dependence // Recent Pat CNS Drug Discov. 2012. No. 7 (2). Р. 129–144.
5. Wills T. A., Klug J. R., Silberman Y. et al. GluN2B Subunit Deletion Reveals Key Role in Acute and Chronic Ethanol Sensitivity of Glutamate Synapses in Bed Nucleus of the Stria Terminalis // Proc Natl Acad Sci USA. 2012. No. 109 (5). Р. 278–287.
6. Kopelman M. D., Thomson A. D., Guerrini I., Marshall E. J. The Korsakoff Syndrome: Clinical Aspects, Psychology and Treatment // Alcohol Alcohol. 2009. No. 44 (2). Р. 148–154.
2009. No. 44 (2). Р. 148–154.
7. Дудорова Е. Ю., Дамулин И. В., Хатьков И. Е. Неврологические
8. осложнения, вызванные дефицитом витаминов после бариартрических операций // Терапевт. архив. 2015. № 12. С. 117–121.
9. Galvin R., Bråthen G., Ivashynka A. et al. EFNS Guidelines for Diagnosis, Therapy and Prevention of Wernicke Encephalopathy // Eur J Neurol. 2010. No. 17 (12). Р. 1408–1418.
10. Сиволап Ю. П., Дамулин И. В. Энцефалопатия Вернике и корсаковский психоз: клинико-патогенетические соотношения, диагностика и лечение // Журн. неврологии и психиатрии. 2013. № 6. Вып. 2. С. 20–26.
11. Scalzo S. J., Bowden S. C., Ambrose M. I., Whelan G., Cook M. J.
J., Bowden S. C., Ambrose M. I., Whelan G., Cook M. J.
12. Wernicke Korsakoff Syndrome not Related to Alcohol Use: a Systematic Review // J Neurol Neurosurg Psychiatry. 2015. No. 86 (12). Р. 1362–1368.
13. Latt N., Dore G. Thiamine in the Treatment of Wernicke Encephalopathy in Patients with Alcohol Use Disorders // J Intern Med. 2014. No. 44 (9). Р. 911–915
14. Semple D., Smyth R. Oxford Handbook of Psychiatry. Oxford : Oxford University Press, 2013. 1057 p.
15. Meier S., Daeppen J. B. Prevalence, Prophylaxis and Treatment of
16. Wernicke Encephalopathy. Thiamine, How Much and How Do We Give it? // Rev Med Suiss.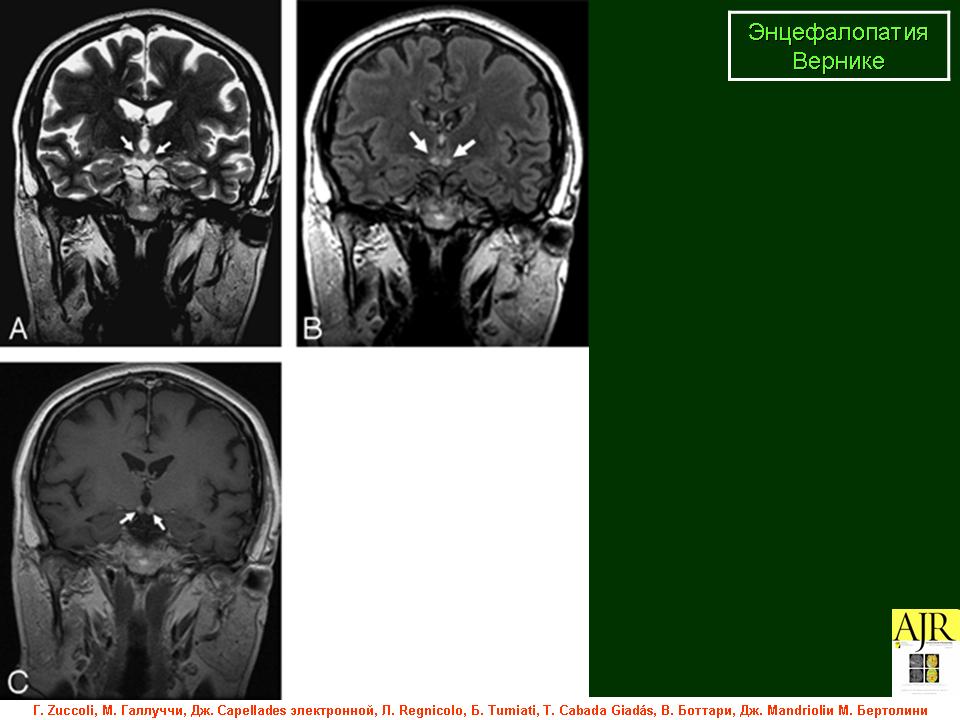 2005. No. 1 (26). Р. 1740–1744.
2005. No. 1 (26). Р. 1740–1744.
17. Sechi G., Serra A. Wernickes Encephalopathy: New Clinical Settings and Recent Advances in Diagnosis and Management // Lancet
18. Neurol. 2007. No. 6. Р. 442–455.
19. Zara G., Codemo V., Palmieri A., Schiff S., Cagnin A., Citton V. et al. Neurological Complications in Hyperemesis Gravidarum // Neurol Set. 2012. No. 33 (1). Р. 133–135.
Синдром Вернике-Корсакова
Синдром Вернике-Корсакова (СВК) — это заболевание, включающее в себя острую и хроническую стадии нейродегенеративного процесса, которое возникает в результате дефицита тиамина и развивается, как правило, у лиц с тяжелыми формами алкоголизма. «Как правило», потому что крайне редко это состояние развивается вне связи с употреблением алкоголя. Острую стадию процесса называют энцефалопатией Гайе-Вернике, хроническую, резидуальную — корсаковским психозом, или синдромом Корсакова [2].
Острую стадию процесса называют энцефалопатией Гайе-Вернике, хроническую, резидуальную — корсаковским психозом, или синдромом Корсакова [2].
Классическим проявлением острой энцефалопатии Вернике является тетрада симптомов: офтальмоплегия, атаксия, нистагм, помрачение сознания [2]. Следует отметить, что полная тетрада обнаруживается лишь 20 % случаев, с этими связаны сложности при диагностике этого состояния. При неполном выздоровлении острая стадия энцефалопатии сменяется хронической, при этом наблюдаются необратимые изменения структур головного мозга, отвечающих за процесс консолидации памяти [1, 2]. Таким образом, больной с трудом запоминает только что поступившую в мозг информацию (фиксационная амнезия), при этом наблюдается относительная сохранность иных психических функций [1, 2].
Разбирая данный синдром, стоит в отдельности рассмотреть энцефалопатию Вернике и корсаковский психоз.
Энцефалопатия Вернике (ЭВ) — это острое мозговое расстройство, которое проявляется тяжелыми неврологическими и психическими нарушениями, в половине случаев заканчивающееся летально. Впервые данная патология была описана Карлом Вернике в 1881 году, как «острый верхний геморрагический полиоэнцефалит» («polyoencephalitis haemorrhagica superior acuta») [2,3].
Впервые данная патология была описана Карлом Вернике в 1881 году, как «острый верхний геморрагический полиоэнцефалит» («polyoencephalitis haemorrhagica superior acuta») [2,3].
В основе патогенеза лежит развитие нейродегенеративных изменений в результате дефицита витамина В1 [2]. В основе причин может лежать как недоедание, так и недостаточное усвоение, однако в конечно итоге происходит нарушение превращения тиамина в тиаминпирофосфат (ТПФ), который является активной частью ТПФ-зависимых ферментов, таких как: альфа-кетоглутаратдегидрогеназа, транскетолаза, пируватдегидрогеназа [4,2]. Данные ферменты катализируют биохимические реакции, которые обеспечивают нормальный метаболизм нервной ткани. Нарушается преодоление тиамином гематоэнцефалического барьера, нарушается клеточный транспорт, что ведет к недостатку витамина B1 в мозге, что в свою очередь приводит к понижению активности ТПФ-зависимых ферментов, а те ведут к лактат-ацидозу, за ним следует нарушение митохондриальных функций, как следствие угнетение тканевого дыхания, что в свою очередь снижает энергетическое обеспечение нейронов и нейроглии. Чаще всего в процесс вовлекаются медиодорсальные ядра зрительного бугра, гипоталамуса, мамиллярных тел и покрышки среднего мозга, с характерной прижизненной симптоматикой. Смерть чаще всего возникает в результате кровоизлияния в мозг [2, 3].
Чаще всего в процесс вовлекаются медиодорсальные ядра зрительного бугра, гипоталамуса, мамиллярных тел и покрышки среднего мозга, с характерной прижизненной симптоматикой. Смерть чаще всего возникает в результате кровоизлияния в мозг [2, 3].
Энцефалопатии Вернике присуща следующая тетрада: офтальмоплегия, нистагм, атаксия, помрачение сознания. Хотя иногда констатируются и отек дисков зрительных нервов и кровоизлияния в сетчатку. При ЭВ снижается температура тела, возникает тахикардия, нарастает слабость. Одним из показателей состояния пациента является степень нарушения сознания. В ряде случаев ЭВ следует за непродолжительным периодом тяжелого алкогольного делирия, в этом случае наблюдается постепенное снижение интенсивности психомоторного возбуждения и нарастание отрешенности, переход делирия в мусситирующую (бормочущую) форму или же аментивноподобное возбуждение, ограниченное пределами постели. По мере дальнейшего ухудшения состояния начинает снижаться уровень сознания с формированием сопора и комы.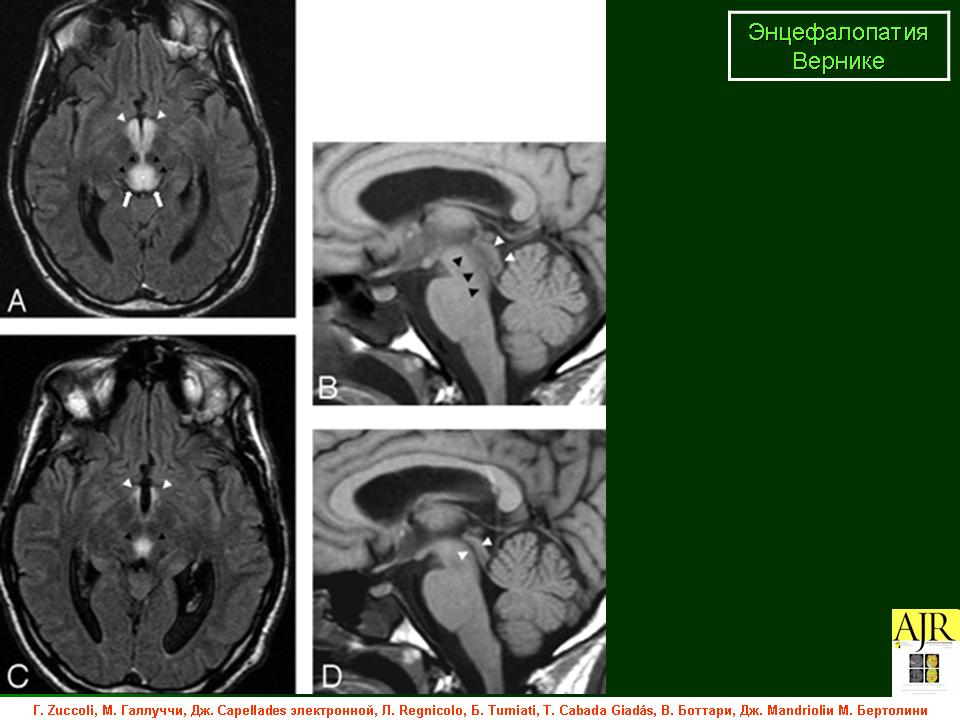 Пациенты, как правило, имеют сниженную массу тела, иногда страдают от обезвоживания [4, 5].
Пациенты, как правило, имеют сниженную массу тела, иногда страдают от обезвоживания [4, 5].
.
Рисунок 1 | Роль тиамина в метаболизме глюкозы
Корсаковский психоз
Различие в патогенезе между корсаковским психозом и энцефалопатией Вернике заключается в степени обратимости изменений. Так, в первом случае изменения необратимы, в то время как во втором случае изменения характеризуются биохимическими сдвигами, что теоретически подразумевает под собой возможность корректировки при своевременном лечении ударными дозами тиамина. При синдроме Корсакова происходит нарушение проводимости мамиллярно-таламических путей, в результате чего нарушается консолидация памяти. Повреждаются мамиллярные тела и ядра зрительного бугра [2].
Ведущим симптомом является амнезия, в первую очередь — фиксационная, определяющая особый тип дезориентировки таких пациентов. Лишенный возможности фиксировать новую информацию, пациент с корсаковским психозом неспособен запомнить текущую дату, место, в котором находится, и расположение палат, имя соседа по палате или лечащего врача, однако при этом часто может по косвенным признакам опознать, что находится в больнице, а за окном — весна. Фиксационной амнезии также сопутствует и (антеро)ретроградная, которая, однако, не определяет тяжесть состояния пациента. Изредка амнезия сопровождается конфабуляциями — ложными воспоминаниями, которыми пациент заполняет пробелы в своей памяти. Также нельзя не отметить, что у больных развивается нижний вялый парапарез и параплегии в результате полиневропатии.
Фиксационной амнезии также сопутствует и (антеро)ретроградная, которая, однако, не определяет тяжесть состояния пациента. Изредка амнезия сопровождается конфабуляциями — ложными воспоминаниями, которыми пациент заполняет пробелы в своей памяти. Также нельзя не отметить, что у больных развивается нижний вялый парапарез и параплегии в результате полиневропатии.
Важным является упомянуть описание корсаковского психоза, составленного самим С. С. Корсаковым: «От одного больного приходилось слышать почти постоянно следующее: “я залежался сегодня, сейчас встану — только вот сию минуту ноги как-то свело — как только они разойдутся, я и встану”. У него была длительная контрактура в коленях, но он, не помня о ее существовании, считал, что это только дело данной минуты. Этот же больной категорически утверждал, что у него никаких болей в ногах нет, а между тем у него были очень сильные стреляющие боли: когда стрельнет, он закричит, а потом сейчас же на вопрос ответит, что у него решительно никаких болей нет. … Этот же больной, читая газету, мог десять раз подряд прочесть одну и ту же строчку как нечто совершенно новое; бывало так, что случайно глаза его остановятся на чем-нибудь интересном, и он прочтет эту строчку вслух своей матери и рассмеется; но в это время он, конечно, на несколько секунд оторвет глаза от того места, которое читал, а потом, когда его глаза опять нападут на это место, хотя бы сейчас же, он снова с теми же словами: “послушай, мама” — читает это место, и таким образом может повторяться много раз…» [2].
… Этот же больной, читая газету, мог десять раз подряд прочесть одну и ту же строчку как нечто совершенно новое; бывало так, что случайно глаза его остановятся на чем-нибудь интересном, и он прочтет эту строчку вслух своей матери и рассмеется; но в это время он, конечно, на несколько секунд оторвет глаза от того места, которое читал, а потом, когда его глаза опять нападут на это место, хотя бы сейчас же, он снова с теми же словами: “послушай, мама” — читает это место, и таким образом может повторяться много раз…» [2].
Диагностика заболевания происходит на основании результатов МРТ, клинической картины, анамнеза и данных лабораторной диагностики.
.
Рисунок 2 | МРТ головного мозга
1 — гиперинтенсивный сигнал не только от периакведуктального серого вещества и маммилярных тел, но и белого вещества среднего мозга.
2, 3 — гиперинтенсивный сигнал от отдельных участков серого вещества коры головного мозга.
4 — участок центральной демиелинизации в области среднего мозга и верхней части варолиева моста.
5 — накопление контраста в оболочках мозга и отдельных участках коры [4].
Так, при МРТ головного мозга может выявляться поражение определенных участков серого вещества, в данном случае поражено серое вещество покрышки среднего мозга. Почти всегда при синдроме Вернике-Корсакова выявляется поражение мамиллярных тел, данный снимок не является исключением. На изображении также видно поражение гиппокампа и гипоталамуса с незначительным накоплением контраста в этих областях, также характерное для СВК.
Лечение острой энцефалопатии Вернике заключается в неотложном — в течение 48–72 часов с момента появления неврологической симптоматики, — введении больших доз тиамина (витамина B1) [1,2].
Рекомендуется внутривенное введение тиамина, так как прием таблетированных форм не позволяет создать высокую концентрацию действующего вещества в крови в короткое время, обеспечить проникновение через гематоэнцефалический барьер и поступление в мозг в достаточном количестве [3,2].
Схема лечения включает в себя внутривенное введение тиамина от 200 до 500 мг 3 раза в сутки в течении 7 дней. С 8 дня внутривенное введение тиамина заменяется на пероральное с уменьшением дозы до 200 мг в сутки в течении 2 недель, затем 100 мг в сутки в течении еще 2 недель [2].
Рекомендуемая продолжительность введения тиамина при энцефалопатии Вернике составляет 2–3 мес, а при корсаковском психозе она достигает 2 лет [2].
Часто данное заболевание сопровождается полиневропатией. Лечение включает в себя альфа-липоевую кислоту (АЛК; син. тиоктовая кислота). АЛК по биохимической активности близко к витамину группы В. Одним из биологических эффектов является взаимодействие с ТПФ-зависимыми ферментами, в том числе пируватдегидрогеназой, которая катализирует биохимические реакции в центральных и периферических нервных образованиях. АЛК также оказывает антиоксидантное действие, подавляя окислительные реакции в митохондриях, тем самым предупреждая их повреждение и, как следствие, угнетение энергетических процессов. Стоит упомянуть, что вещество взаимодействует с витаминами группы С и Е, тем самым стимулируя их способность к обезвреживанию свободных радикалов (СР) [3,2].
Стоит упомянуть, что вещество взаимодействует с витаминами группы С и Е, тем самым стимулируя их способность к обезвреживанию свободных радикалов (СР) [3,2].
При лечении пациентов с энцефалопатией Вернике необходимо избегать обезвоживания и дефицита электролитов, в частности калия и магния. Коррекция водно-электролитного баланса осуществляется с помощью инфузии плазмозамещающих растворов. Также во время лечения СВК необходимо избегать введения больших доз глюкозы пациентам с хроническим алкоголизмом и с алкогольным делирием, так как это усиливает дефицит витамина В1, как следствие увеличивая риск развития энцефалопатии либо утяжеление ее течения [2].
Источники:
- Latt N, Dore G. Thiamine in the treatment of Wernicke encephalopathy in patients with alcohol use disorders. J Intern Med. 2014;44(9):911-5.
- И.В. Дамулин Синдром Вернике-Корсакова / И.В. Дамулин, С.Ю Петрович // Клиническая медицина. Обзор литературы по неврологии, нейропсихологии.
 — 2014 — С.76-80
— 2014 — С.76-80 - Meier S, Daeppen JB. Prevalence, prophylaxis and treatment of Wernicke encephalopa-thy. Thiamine, how much and how do we give it? Rev Med Suisse. 2005;1(26):1740-4.
- С. В. Котов Синдром Вернике-Корсакова / А. И. Лобаков, С. В. Котов, Е. В. Исакова Г. А. Сташук Т. В. Волченкова // Журнал неврологии и психиатрии им. С.С. Корсакова. — 2016 116(7), — С .4-11
- Schabelman E, Kuo D. Glucose before thiamine for Wernicke encephalopathy: a literature review. J Emerg Med. 2012;42(4):488-494.
симптомы, причины, лечение и диагностика
Заболевание, при котором у человека наблюдается снижение словесно-логического мышления и проявляются другие расстройства восприятия речи, получило название сенсорная афазия. В отличие от других форм, сенсорная считается легкой, пациент способен воспринимать отдельные слова и короткие фразы на не во всех случаях. Человек с расстройством такого плана слышит, но не так как надо, слова звучат, будто на другом языке.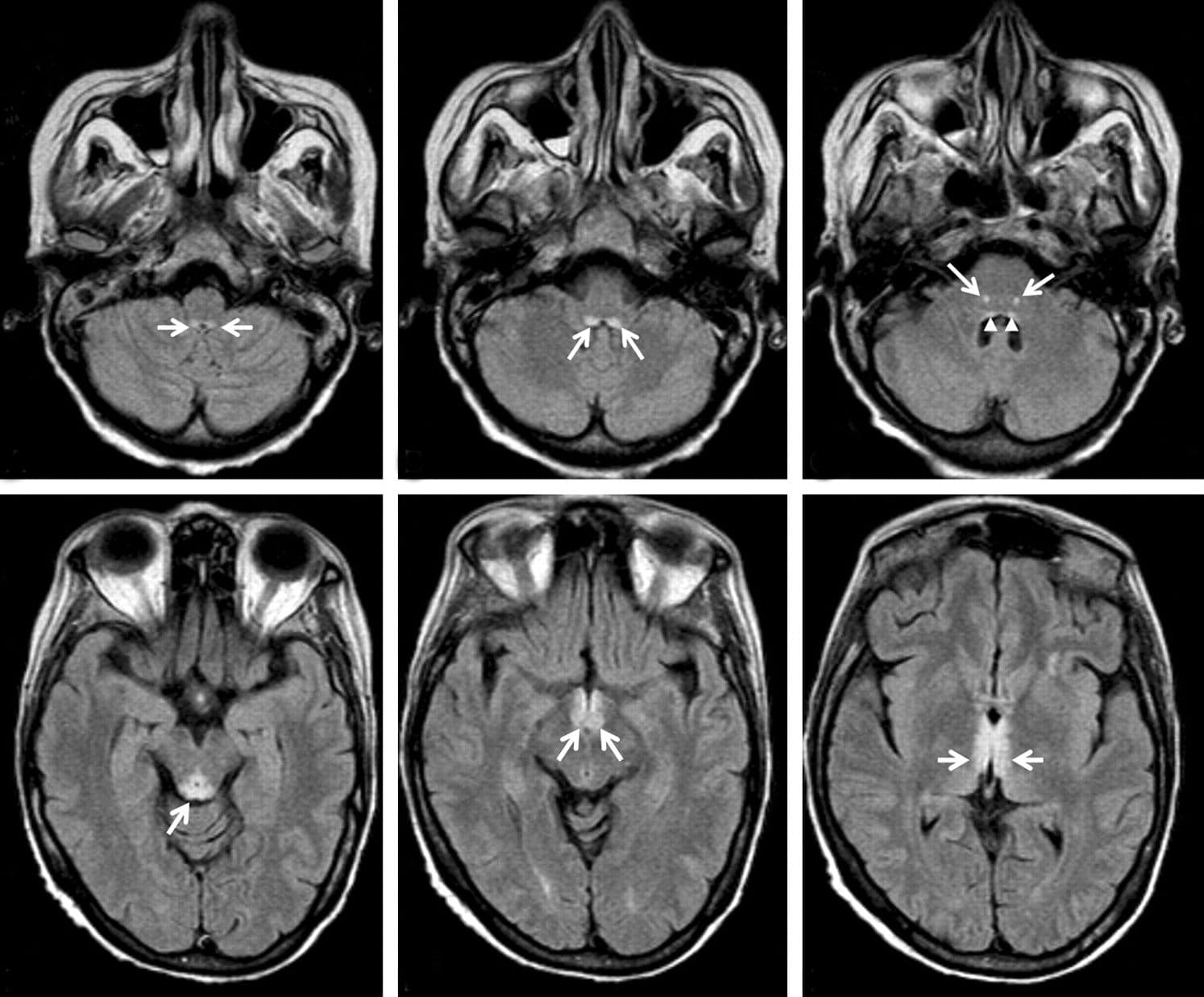 На этом фоне усиливается тревога, не исключена дезориентация в пространстве.
На этом фоне усиливается тревога, не исключена дезориентация в пространстве.
Информация о заболевании
Сенсорная афазия – речевое расстройство, имеющее общие симптомы и схожее течение с алалией. Различие в том, что последняя, проявляется только у детей, а афазию диагностируют у взрослых пациентов, перенесших инсульт и другие поражения головного мозга. При этом расстройстве человек не воспринимает обращенную к нему речь.
Сенсорная афазия проявляется, если у человека происходит поражение головного мозга в области височных долей. При этом само заболевание насчитывает 3 подвида:
- корковая. Тяжелое расстройство, сопровождающееся поражением центра Вернике, отвечающего за восприятие и обработку звуков. Расстройство полное, человек не понимает и не произносит звуки;
- транскортикальная сенсорная афазия или акустико гностическая сенсорная афазия. В процессе этого заболевания нарушается проведение нервного импульса между центрами Вернике и Брока, находящимися в лобной доле мозга.
 При этом сохраняется способность к восприятию простых речевых конструкций;
При этом сохраняется способность к восприятию простых речевых конструкций; - субкортикальная. Поражение сопровождается искажением трансляции импульсов от центров, воспринимающих звуковую информацию, выступающих процессорами преобразования.
Симптомы сенсорной афазии:
- отсутствие способности воспринимать речь при сохранном слухе;
- нарушения речи различного уровня, ее полное отсутствие;
- тревожность, сопровождаемая агрессией, связанная с непониманием происходящего;
- повышенная двигательная активность, пациенты не находят себе место;
- судороги;
- нарушения сознания;
- ухудшение зрения.
Сенсорная афазия возникает при таких заболеваниях, способных ее спровоцировать:
- менингит;
- инсульт;
- энцефалит;
- печеночная энцефалопатия;
- цереброваскулярная недостаточность;
- транзиторные ишемические атаки;
- травмы головного мозга;
- эпилептический синдром;
- опухолевые процессы.

Специфические методы профилактики – отсутствуют. Достаточно периодически посещать врача невролога, чтобы минимизировать риск развития инсульта и суметь предупредить сосудистые изменения головного мозга.
В 60% при инсульте головного мозга состояние пациента можно улучшить. В ряде случаев, при незначительных нарушениях, слаженной работе пациента, его родственников, логопеда и дефектолога, удается добиться полного и устойчивого восстановления.
Общие сведения о лечении
Вылечить рекуррентную сенсорную афазию и восстановить способность человека воспринимать речь других и участвовать в диалоге возможно. Для этого при появлении первых признаков расстройства стоит обратиться к профильным специалистам: неврологу, логопеду, дефектологу. Проблему устраняют консервативно и оперативным способом, в ходе нейрохирургической операции.
На начальном этапе диагностики сенсорной афазии, специалисты оценивают тяжесть состояния пациента в ходе беседы, обращают внимание на определенные аспекты:
- осознает ли человек ситуацию при беседе;
- как ориентируется в ситуации;
- может ли выразить свое мнение, рассказать о размышления;
- есть ли речевые автоматизмы.

В качестве основного метода диагностики используется МРТ. Это исследование позволяет четко визуализировать состояние нервных тканей. После первичного обследования проводится визуализация отдельных участков мозга, височных долей. Для оценки кровотока проводят сканирование сосудов шеи и головного мозга, это позволяет оценить тяжесть патологии.
Терапия стационарная. На ранних этапах воздействие заключается в первичной помощи и адаптации, устранение симптомов и борьбу с причиной. После восстановления возможности воспринимать звуки проводятся реабилитационные мероприятия.
Для терапии применяют средства ноотропного действия, антигипоксические препараты. Использования медикаментов достаточно, если случаи незапущенные. При аневризмах и опухолях, восстановить способность воспринимать речь не получится без оперативного вмешательства.
Распространенные вопросы
Какой шанс на полное восстановление функций после инсульта?
Вероятность полного восстановления речи после инсульта присутствует, но точный прогноз можно сделать после осмотра пациента и оценки его состояния. Лучших результатов можно достичь, если пациент молодой. В зрелом и пожилом возрасте. Восстановление проходит сложнее и не всегда дает результаты.
Лучших результатов можно достичь, если пациент молодой. В зрелом и пожилом возрасте. Восстановление проходит сложнее и не всегда дает результаты.
Нужен ли пациенту логопед?
Восстановлением речи у взрослых пациентов занимается логопед, но обращаться к нему можно только после консультации с неврологом. Важно убедиться, что организм способен воспринимать нагрузку и готов к обучению.
Сколько длится лечение?
Установить точные сроки восстановления при нарушениях неврогенного происхождения невозможно. Крайне важно то, насколько быстро организм отреагирует на назначенные медикаменты. Многое зависит от тяжести состояния самого пациента, его возраста и того, сколько времени прошло после травматического воздействия или приступа.
Какие последствия афазии для человека?
По мнению психиатров, таким людям очень тяжело находиться в обществе. Из-за подобного непонимания сильно страдает нервная система, потому главная задача медиков – ликвидировать проблему и вернуть пациента к нормальной жизни. Если восстановление невозможно, показана консультация психиатра для коррекции агрессии и других расстройств.
Из-за подобного непонимания сильно страдает нервная система, потому главная задача медиков – ликвидировать проблему и вернуть пациента к нормальной жизни. Если восстановление невозможно, показана консультация психиатра для коррекции агрессии и других расстройств.
Что должны делать родственники?
Логопедические занятия помогают восстановить речь, но лучших результатов можно добиться, если заниматься с человеком ежедневно, проходя несколько уроков. Делать это может сам пациент (при легком поражении), в тяжелых случаях занятия должны контролировать родственники.
Энцефалопатия Вернике — проект EMCrit
Вы здесь: Домашняя страница / IBCC / Энцефалопатия Вернике
, Джош Фаркас
СОДЕРЖАНИЕ
патофизиология
(к оглавлению)
биохимия
- Тиамин является кофактором многочисленных ферментативных реакций, участвующих в энергетическом обмене, как показано ниже.
 Дефицит тиамина имеет следующие последствия:
Дефицит тиамина имеет следующие последствия:- (1) Накопление лактата
- (2) Избыточное производство глутамата, которое может привести к чрезмерной возбуждающей нейротрансмиссии в головном мозге
- Это может вызвать вазогенный и цитотоксический отек.
Фармакология тиамина
- Суточная потребность в тиамине ~ 1-2 мг. Тиамин всасывается в тощей кишке и сохраняется в печени. Абсорбция относительно неэффективная ; например, одно исследование здоровых добровольцев показало, что всасывается только 5% пероральной дозы 50 мг. (30146080) Однако недавнее исследование предполагает, что это можно преодолеть с помощью очень высоких доз перорального тиамина, как показано на рисунке ниже.(22305197)
- Общие запасы тиамина в организме составляют ~ 30 мг (но потенциально ниже при заболеваниях печени).
- Недостаточное потребление тиамина может вызвать дефицит у здоровых человек в течение ~ 2-4 недель.
 (32551830) В контексте острого или хронического заболевания дефицит может возникнуть быстрее.
(32551830) В контексте острого или хронического заболевания дефицит может возникнуть быстрее.
признаки и симптомы
(вернуться к содержанию)
Признаки и симптомы обычно недостоверны при диагностике.Классическая триада энцефалопатии, офтальмоплегии и атаксии присутствует только в ~ 15% случаев. Среди неалкогольных пациентов с энцефалопатией Вернике триада встречается еще реже. (31171116)
# 1 = энцефалопатия
- Делирий — наиболее стойкая клиническая характеристика.
- Это может прогрессировать до комы.
- Изолированная энцефалопатия без глазных или мозжечковых признаков может чаще встречаться при неалкогольной энцефалопатии Вернике.(323)
# 2 = офтальмоплегия
- Горизонтальный нистагм — наиболее частая находка (хотя может встречаться как горизонтальный, так и вертикальный нистагм).

- Параличи черепных нервов могут включать:
- Отводящий нерв (CN6) — обычно двусторонний.
- Паралич сопряженного взгляда.
- Они могут прогрессировать до полной офтальмоплегии.
# 3 = атаксия
- Ноги поражены больше, чем руки (поскольку атаксия возникает из-за вестибулярной дисфункции в сочетании с дисфункцией мозжечка).
- В первую очередь влияет на походку (руки и речь обычно не затрагиваются).
другие потенциальные ключи к разгадке энцефалопатии Вернике
- Гипотермия (из-за поражения гипоталамуса).
- Гипотония.

Другие клинические признаки недостаточности тиамина
- Периферическая невропатия («сухой бери-бери»)
- Может вызывать боль , парестезии, слабость и / или потерю чувствительности.
- Сердечная недостаточность с высоким выбросом («мокрый бери-бери»)
- Боль в животе, рвота и лактоацидоз («желудочно-кишечный бери-бери»)
Факторы риска
(вернуться к содержанию)
🔑 Алкоголизм является причиной только ~ 50% энцефалопатии Вернике.Другие случаи могут возникать из-за множества факторов, часто многофакторным образом. Факторы, предрасполагающие к энцефалопатии Вернике, можно разделить примерно на четыре группы:
# 1/4: снижение потребления тиамина
- Недоедание, например, из-за:
- Расстройство, связанное с употреблением психоактивных веществ, алкоголизм
- Деменция, бедность
- Шизофрения
- Нервная анорексия
- Кахексия (например, связанная со СПИДом, злокачественными новообразованиями)
- Модные диеты
- Гиперемезис
- Hyperemesis gravidarum
- Синдром каннабиноидной гиперемезии
- Полное парентеральное питание без тиамина
# 2/4: снижение всасывания в желудочно-кишечном тракте
- Болезнь Крона
- Язвенная болезнь, хронический гастрит
- Хроническая диарея
- Желудочно-кишечная хирургия (особенно бариатрическая хирургия)
# 3/4: пониженная способность печени накапливать тиамин
- Цирроз любой этиологии
- Алкоголизм
# 4/4: повышенное использование или удаление тиамина
- Большое количество углеводов (особенно синдром возобновления питания)
- Гиперметаболические состояния (например,г.
 , сепсис, системное воспаление, гипертиреоз)
, сепсис, системное воспаление, гипертиреоз) - Некоторые быстрорастущие злокачественные новообразования
- Гемодиализ или перитонеальный диализ
- Диурез (особенно у пациентов с сердечной недостаточностью, принимающих хронические диуретики)
- Метронидазол может действовать как антагонист тиамина. (323)
эпидемиология
(вернуться к содержанию)
Энцефалопатия Вернике может быть более распространенной, чем принято считать
- ~ 1% распространенности среди населения в целом.
- ~ 12,5% распространенности среди людей с алкоголизмом.
- ~ 8% распространенность среди пациентов, перенесших бариатрическую операцию. (30364782)
Дефицит тиамина как ятрогенное осложнение госпитализации
- Причинные факторы:
- Существовавшая ранее неадекватность запасов тиамина.
- Неадекватное питание (например, длительное время с НКО).

- Гиперметаболические состояния (например, инфекция, воспаление).
- Повышенная экскреция с мочой (e.g., диурез или диализ).
- Распространенность дефицита тиамина среди тяжелобольных пациентов может быть высокой, при этом в некоторых статьях сообщается о ~ 20%. (30146080)
- Энцефалопатия Вернике может первоначально проявиться в пределах больницы после госпитализации по поводу другого заболевания. Это будет чрезвычайно сложно диагностировать, так как это будет связано с многофакторным делирием (ранее называвшимся «психозом в отделении интенсивной терапии»).
- Дефицит тиамина также может способствовать развитию невропатии в отделении интенсивной терапии или желудочно-кишечной дисфункции у некоторых пациентов.(30146080) Одно рандомизированное контролируемое исследование, в котором изучалась эффективность тиамина при септическом шоке, не выявило положительного эффекта в целом, но привело к снижению смертности в подгруппе пациентов с дефицитом тиамина.
 (26771781)
(26771781)
лабораторные исследования
(вернуться к содержанию)
Уровень тиаминдифосфата цельной крови
- Уровень тиамина дифосфата в цельной крови в значительной степени отражает уровень тиамина в эритроцитах. Это может быть более точным, чем измерение тиамина сыворотки или плазмы , так как тиамин цельной крови является более точным отражением внутриклеточных запасов тиамина.
- Обычно считается, что нормальное значение составляет 70-180 нМ / л, хотя универсально определенного порогового значения не существует. (30151974)
- Уровни тиаминдифосфата в цельной крови, по-видимому, превосходят другие тесты на уровни тиамина. (25564426) Однако его чувствительность и специфичность остаются неясными.
изображение
(назад к содержанию)
КТ
- Компьютерная томография обычно не выявляет энцефалопатию Вернике.
 Основная роль — исключить альтернативной этиологии.
Основная роль — исключить альтернативной этиологии. - CT может показать сниженное ослабление в периакведуктальном сером веществе и медиальной части таламуса. (323) Также может быть усиление контраста.
МРТ
- МРТ имеет чувствительность ~ 50% со специфичностью ~ 90%. (323) Однако МРТ может нормализоваться в течение нескольких дней после начала приема тиамина.
- Распространение отклонений:
- Симметричный
- Типичное расположение: паравентрикулярные области таламуса, гипоталамуса, маммиллярные тела, периакведуктальная область и дно четвертого желудочка.(323)
- Дополнительные аномалии могут быть замечены в скорлупе, хвостатом теле, звездочке мозолистого тела, спинном мозговом веществе, мосте, красном ядре, черной субстанции среднего мозга, ядре черепного нерва, черве, зубчатом ядре, паравермической области мозжечка, своде и прецентральная и постцентральная извилины.
 (323)
(323)
- Выводы:
- Повышенный сигнал T2 и сигналы восстановления инверсии с ослаблением жидкости (T2 / FLARE).
- Пониженный сигнал T1.
- Нарушение диффузии.
- Повышение контрастности может быть результатом нарушения гематоэнцефалического барьера.
- Примечание: аномалии мозолистого тела должны вызывать беспокойство по поводу болезни Маркиафава-Бигнами (из-за алкоголизма и дефицита витаминов).
дифференциальная диагностика и обеспечение диагностики
(вернуться к содержанию)
Дифференциальный диагноз будет зависеть от состояния пациента, поэтому он может немного отличаться.Однако некоторые общие соображения могут включать:
- Отмена алкоголя
- Синдром возобновления питания (который может включать энцефалопатию Вернике плюс наложенных электролитных аномалий)
- Печеночная энцефалопатия
- Гидроцефалия нормального давления
- Ишемический инсульт в задней части кровообращения
- Септический шок (недостаточность тиамина, вызывающая энцефалопатию Вернике, плюс сердечная недостаточность с высоким выбросом и лактоацидоз)
обеспечение диагноза энцефалопатии Вернике
- Не существует диагностических критериев, которые были бы чувствительными и специфичными.
 Следовательно, требуется клиническая оценка.
Следовательно, требуется клиническая оценка. - Следует начать эмпирический прием тиамина. Пока идет диагностический процесс (до постановки окончательного диагноза).
- Следует обратить внимание на следующие компоненты:
- (1) Факторы риска дефицита тиамина.
- (2) Исключение альтернативных диагностических возможностей.
- (3) Нейровизуализация (особенно МРТ) иногда может оказать сильную поддержку.
- (4) Клинический ответ на внутривенное введение тиамина (в некоторых случаях офтальмоплегия может исчезнуть в течение нескольких часов после начала терапии).
- (5) Уровни тиамина в цельной крови (это может быть полезно для ретроспективной постановки диагноза).
- Следует предпринять попытки достичь диагностической достоверности, поскольку энцефалопатия Вернике требует продолжительного курса внутривенного введения тиамина.
профилактика
(вернуться к содержанию)
общепринятые подходы к профилактике энцефалопатии Вернике
- Добавки тиамина — разумное вмешательство для пациентов из группы риска (например,г.
 , больные алкоголизмом или недоеданием). Подробнее о факторах риска дефицита тиамина выше.
, больные алкоголизмом или недоеданием). Подробнее о факторах риска дефицита тиамина выше. - Для этой цели часто используется 100 мг тиамина внутривенно / внутримышечно (при отсутствии доказательств высокого уровня).
- Пероральный тиамин, вероятно, также подходит для этой цели (с преимуществами, касающимися меньшей стоимости и простоты применения). Одно небольшое исследование показало, что в популяции пациентов с алкоголизмом прием 250 мг тиамина внутримышечно через три дня генерировал аналогичные уровни тиамина по сравнению с режимом приема 50 мг перорально пять раз в день.(3358822) Это говорит о том, что пероральный прием ~ 200 мг два раза в день может быть достаточным для предотвращения дефицита у пациентов из группы риска.
- В клинической практике пациентов из группы риска часто лечат тиамином внутривенно в течение нескольких дней, а затем полностью прекращают прием тиамина. Вместо того, чтобы полностью прекращать прием тиамина, было бы разумнее перейти от внутривенного введения тиамина к пероральному добавлению высоких доз, который можно было бы продолжать на протяжении всего курса лечения пациента в стационаре.

- Однако пероральный прием тиамина не может быть жизнеспособной стратегией для пациентов с нарушением всасывания тиамина в желудочно-кишечном тракте.
- В клинической практике пациентов из группы риска часто лечат тиамином внутривенно в течение нескольких дней, а затем полностью прекращают прием тиамина. Вместо того, чтобы полностью прекращать прием тиамина, было бы разумнее перейти от внутривенного введения тиамина к пероральному добавлению высоких доз, который можно было бы продолжать на протяжении всего курса лечения пациента в стационаре.
Может ли более агрессивная профилактика быть полезной среди тяжелобольных?
- Почти все тяжелобольные пациенты будут иметь по крайней мере один фактор риска дефицита тиамина (например, снижение потребления пищи, диурез, системное воспаление, диализ). Следовательно, дефицит тиамина очень распространен среди пациентов в критическом состоянии (как описано выше).
- Пероральное введение тиамина, вероятно, эффективно, безопасно и дешево (стоит примерно ~ 10 долларов на пациента в течение всего пребывания в ОИТ).
- ОИТ очень дорого обходится, по оценкам, один эпизод делирия ОИТ может стоить ~ 17 000 долларов. (30179988)
- Это говорит о том, что если частота энцефалопатии Вернике выше, чем один из ~ 1700 пациентов (0,05%), то рутинное введение тиамина может быть клинически полезным.
 и позволяют сократить расходы. Имеющиеся данные показывают, что частота энцефалопатии Вернике значительно превышает 0.05%, что может сделать профилактику логичным вмешательством. (24666443)
и позволяют сократить расходы. Имеющиеся данные показывают, что частота энцефалопатии Вернике значительно превышает 0.05%, что может сделать профилактику логичным вмешательством. (24666443)
Делирий
обработка
(вернуться к содержанию)
тиамин
- Если есть сомнения относительно диагноза, следует начать эмпирическое лечение.
- Внутривенный тиамин полностью безопасен.
- Отсутствие терапии может привести к хронической неврологической травме.
- В идеале тиамин следует вводить одновременно или до приема углеводов (например,g., пища или декстроза внутривенно).
- Обычно требуется парентеральный тиамин, поскольку пероральное всасывание неэффективно. (28680171) Если внутривенный тиамин недоступен , то можно попытаться использовать очень высокие дозы перорального тиамина для преодоления низкой биодоступности (например, возможно, 500-1500 мг перорально каждые 8 часов) .
 (22305197)
(22305197) - Нет ни четко определенного режима дозирования, ни доказательств высокого качества. В статьях часто рекомендуется следующее: (32551830)
- i) 500 мг внутривенно 3 раза в сутки в течение 2-3 дней, затем
- ii) 200-500 мг внутривенно ежедневно в течение ~ 5 дней или до исчезновения клинического улучшения, затем
- iii) пероральный тиамин (e.г, 100-500 мг перорально 3 раза в день)
- Офтальмопарез может улучшиться в течение нескольких часов после внутривенного введения тиамина.
магний
- Обоснование обеспечения необходимого уровня магния:
- Магний является кофактором активности тиамина и способствует поглощению тиамина клетками.
- Заболевания, приводящие к дефициту тиамина, часто также вызывают дефицит магния (особенно алкоголизм).
- Проверьте и агрессивно восполните запасы магния (подробнее об этом здесь).
прогноз
(вернуться к содержанию)
- Глазные аномалии обычно начинают улучшаться в течение примерно одного дня.

- Атаксия и спутанность сознания обычно проходят в течение недели. Путаница обычно проходит в течение месяца.
- Хронический психоз Корсакова (отмеченный конфабуляцией) может возникать у пациентов с отсроченным лечением.
сводка
(вернуться к содержанию)
подкаст
(назад к содержанию)
Следуйте за нами в iTunes
вопросы и обсуждения
(вернуться к содержанию)
Чтобы эта страница оставалась небольшой и быстрой, вопросы и обсуждение этого сообщения можно найти на другой странице. здесь .
- Неспособность рассмотреть энцефалопатию Вернике у пациентов с атипичными факторами риска (например, пациенты интенсивной терапии, hyperemesis gravidarum, хроническое использование диуретиков при сердечной недостаточности).
- Недостаточная доза и продолжительность приема тиамина для пациентов с энцефалопатией Вернике.
 Одного или двух дней внутривенного введения тиамина недостаточно!
Одного или двух дней внутривенного введения тиамина недостаточно! - Неправильно исключен диагноз энцефалопатии Вернике, поскольку у пациентов отсутствует классическая триада симптомов (спутанность сознания, атаксия, офтальмоплегия).Фактически, очень редко у пациентов с энцефалопатией Вернике обнаруживаются все эти компоненты.
- Неадекватное использование тиаминовой профилактики энцефалопатии Вернике среди критически больных пациентов из группы риска. Пероральный тиамин, вероятно, подходит для этой цели, поэтому затраты на профилактику незначительны.
Далее:
5-минутное резюме Анны Пикенс (EM in 5)
ссылки
- 03358822 Бейнс М., Блай Дж. Г., Мэдден Дж. С..Уровни тиамина в тканях госпитализированных алкоголиков до и после приема пероральных или парентеральных витаминов.
 Алкоголь Алкоголь. 1988; 23 (1): 49-52 [PubMed]
Алкоголь Алкоголь. 1988; 23 (1): 49-52 [PubMed] - 22305197 Smithline HA, Donnino M, Greenblatt DJ. Фармакокинетика высоких доз перорального гидрохлорида тиамина у здоровых людей. BMC Clin Pharmacol. 2012 4 февраля; 12: 4. DOI: 10.1186 / 1472-6904-12-4 [PubMed]
- 24666443 Блэкмор К., Уэллет Дж. Ф., Нивен Д., Киркпатрик А. В., Болл К. Г.. Профилактика делирия у пациентов с травмами: даем ли мы шанс профилактике тиамином? Может J Surg.2014 Апрель; 57 (2): 78-81. DOI: 10.1503 / cjs.020112 [PubMed]
- 25564426 Франк LL. Тиамин в клинической практике. JPEN J Parenter Enteral Nutr. 2015 июл; 39 (5): 503-20. DOI: 10.1177 / 0148607114565245 [PubMed]
- 25985980 Валлийский А., Роджерс П., Клифт Ф. Неалкогольная энцефалопатия Вернике. CJEM. 2016 июл; 18 (4): 309-12. DOI: 10.1017 / cem.2015.27 [PubMed]
- 26771781 Доннино М.
 В., Андерсен Л.В., Чейз М., Берг К.М., Тидсвелл М., Гиберсон Т., Вулф Р., Московиц А., Смитлайн Н., Нго Л., Кокки Миннесота; Научно-исследовательская группа Центра реанимации.Рандомизированное, двойное слепое, плацебо-контролируемое исследование тиамина как метаболического реанимационного средства при септическом шоке: пилотное исследование. Crit Care Med. 2016 Февраль; 44 (2): 360-7. DOI: 10.1097 / CCM.0000000000001572 [PubMed]
В., Андерсен Л.В., Чейз М., Берг К.М., Тидсвелл М., Гиберсон Т., Вулф Р., Московиц А., Смитлайн Н., Нго Л., Кокки Миннесота; Научно-исследовательская группа Центра реанимации.Рандомизированное, двойное слепое, плацебо-контролируемое исследование тиамина как метаболического реанимационного средства при септическом шоке: пилотное исследование. Crit Care Med. 2016 Февраль; 44 (2): 360-7. DOI: 10.1097 / CCM.0000000000001572 [PubMed] - 26869612 Infante MT, Fancellu R, Murialdo A, Barletta L, Castellan L, Serrati C. Проблемы диагностики и лечения энцефалопатии Вернике: отчет о 2 случаях. Nutr Clin Pract. 2016 Апрель; 31 (2): 186-90. DOI: 10.1177 / 0884533615621753 [PubMed]
- 28680171 Алим Ю., Бейтс Д., Ланжевен А., Верри Д., Дерш-Миллс Д., Герман Р. Дж., Минц М., Гош С.Практика назначения тиамина взрослым пациентам, поступающим в терапевтическую службу. Может J Hosp Pharm. 2017 май-июнь; 70 (3): 179-187.
 DOI: 10.4212 / cjhp.v70i3.1657 [PubMed]
DOI: 10.4212 / cjhp.v70i3.1657 [PubMed] - 30146080 Attaluri P, Castillo A, Edriss H, Nugent K. Дефицит тиамина: важное значение для тяжелобольных пациентов. Am J Med Sci. Октябрь 2018; 356 (4): 382-390. DOI: 10.1016 / j.amjms.2018.06.015 [PubMed]
- 30151974 Whitfield KC, Bourassa MW, Adamolekun B, Bergeron G, Bettendorff L, Brown KH, Cox L, Fattal-Valevski A, Fischer PR, Frank EL, Hiffler L, Hlaing LM, Jefferds ME, Kapner S, Kounnavong , Mousavi MPS, Roth DE, Tsaloglou MN, Wieringa F, Combs GF Jr.Расстройства, связанные с недостаточностью тиамина: диагностика, распространенность и дорожная карта для глобальных программ борьбы. Ann N Y Acad Sci. Октябрь 2018; 1430 (1): 3-43. DOI: 10.1111 / nyas.13919 [PubMed]
- 30179988 Василевскис Е.Е., Чандрасекхар Р., Хольц С.Х., Грейвс Дж., Сперофф Т., Жирар Т.Д., Патель М.Б., Хьюз К.Г., Цао А., Пандхарипанд П.
 П., Эли Е.В. Стоимость делирия и комы в отделении интенсивной терапии у пациента отделения интенсивной терапии. Med Care. Октябрь 2018; 56 (10): 890-897. DOI: 10.1097 / MLR.0000000000000975 [PubMed]
П., Эли Е.В. Стоимость делирия и комы в отделении интенсивной терапии у пациента отделения интенсивной терапии. Med Care. Октябрь 2018; 56 (10): 890-897. DOI: 10.1097 / MLR.0000000000000975 [PubMed] - 30364782 Patel S, Topiwala K, Hudson L.Энцефалопатия Вернике. Cureus. 2018 22 августа; 10 (8): e3187. DOI: 10.7759 / cureus.3187 [PubMed]
- 31171116 Синха С., Катария А, Колла Б.П., Тусиус Н., Лукьянова Л.Л. Энцефалопатия Вернике-Клинические жемчужины. Mayo Clin Proc. 2019 июн; 94 (6): 1065-1072. DOI: 10.1016 / j.mayocp.2019.02.018 [PubMed]
- 32041699 Фудзикава Т., Согабе Ю. Энцефалопатия Вернике. CMAJ. 2020 10 февраля; 192 (6): E143. DOI: 10.1503 / cmaj.1 [PubMed]
- 32551830 Конке S, Мик CL.Не ищите, не находите: диагностическая проблема энцефалопатии Вернике. Энн Клин Биохим. 2020 июл 13: 4563220939604.
 DOI: 10.1177 / 0004563220939604 [PubMed]
DOI: 10.1177 / 0004563220939604 [PubMed] - 323 Ota Y, Capizzano AA, Moritani T, Naganawa S, Kurokawa R, Srinivasan A. Всесторонний обзор энцефалопатии Вернике: патофизиология, клинические симптомы и результаты визуализации. Jpn J Radiol. 2020 Сен; 38 (9): 809-820. DOI: 10.1007 / s11604-020-00989-3 [PubMed]
Интернет-книга интенсивной терапии — это онлайн-учебник, написанный Джошем Фаркасом (@PulmCrit), доцентом кафедры легочной медицины и реанимации Университета Вермонта.
Синдром Вернике-Корсакова | Family Caregiver Alliance
Определение
Синдром Вернике-Корсакова (WKS) — неврологическое заболевание. Энцефалопатия Вернике и психоз Корсакова — это, соответственно, острая и хроническая фазы одного и того же заболевания.
WKS вызван дефицитом тиамина витамина B. Тиамин играет роль в метаболизме глюкозы для выработки энергии для мозга. Отсутствие тиамина приводит к недостаточному снабжению энергией головного мозга, особенно гипоталамуса , который регулирует температуру тела, рост и аппетит, а также играет роль в эмоциональной реакции. Гипоталамус также контролирует функции гипофиза, включая метаболизм и гормоны, а также маммиллярных тел, где нервные пути соединяют различные части мозга, участвующие в функциях памяти. Заболевание обычно связано с хроническим алкоголизмом, но может быть связано с недоеданием или другими состояниями, вызывающими дефицит питательных веществ.
Гипоталамус также контролирует функции гипофиза, включая метаболизм и гормоны, а также маммиллярных тел, где нервные пути соединяют различные части мозга, участвующие в функциях памяти. Заболевание обычно связано с хроническим алкоголизмом, но может быть связано с недоеданием или другими состояниями, вызывающими дефицит питательных веществ.
Обзор
WKS имеет относительно низкую распространенность (от 0,4% до 2,8% зарегистрированных вскрытий).Однако вполне вероятно, что о болезни не сообщают и не диагностируют. По оценкам, 25% случаев WKS были пропущены, если мозг пострадавших людей не исследовался под микроскопом. Другое исследование показало, что только 20% клинических диагнозов WKS были поставлены правильно при жизни по сравнению с результатами вскрытия. Более того, WKS, по-видимому, является лишь одним отдельным заболеванием, вызывающим деменцию, связанную с алкоголем. На основании клинических исследований было обнаружено, что от 22% до 29% людей с деменцией сильно пьющие или алкоголики, а от 9% до 23% пожилых алкоголиков, получающих лечение от алкоголизма, также страдают деменцией./79_2.jpg)
По оценкам, от 1,1 до 2,3 миллиона пожилых американцев имеют проблемы с алкоголем. Медицинские исследователи все еще не могут найти более полного определения связи между злоупотреблением алкоголем и симптомами деменции.
Симптомы
Симптомы WKS могут быть длительными или постоянными, и их следует отличать от острых проявлений употребления алкоголя или периода алкогольной «отмены». Заболевание характеризуется спутанностью сознания, амнезией (постоянным провалом в памяти) и нарушением кратковременной памяти.По оценкам, 80% людей с WKS по-прежнему страдают хроническим расстройством памяти. Люди часто кажутся апатичными и невнимательными, а некоторые могут испытывать возбуждение. Кроме того, WKS имеет тенденцию ухудшать способность человека изучать новую информацию или задачи. Люди с WKS, как известно, «конфабулируют» (придумывают или изобретают информацию, чтобы компенсировать плохую память). Другие симптомы включают атаксию (слабость в конечностях или нарушение мышечной координации, неустойчивую походку), медленную ходьбу, быстрые, похожие на тремор движения глаз и паралич глазных мышц.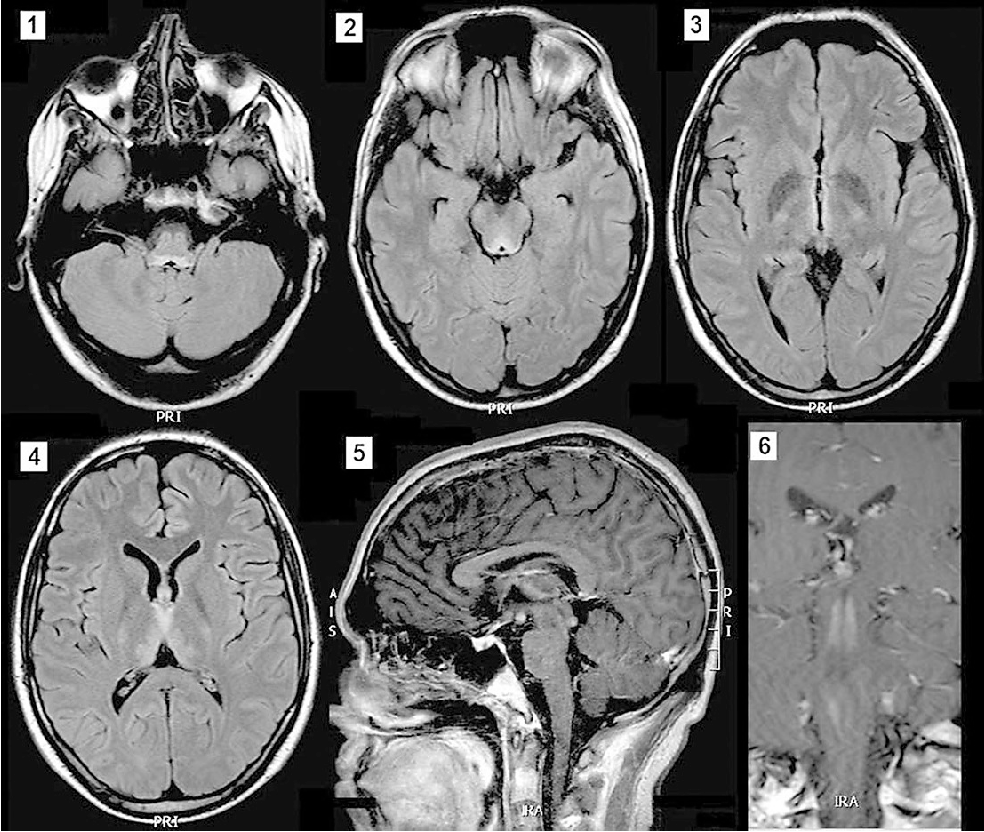 Может быть снижена мелкая моторика (например, движения рук или пальцев), а также может пострадать обоняние. На поздних стадиях может наступить кома. Хотя заболевание можно вылечить, если его поймают на достаточно ранней стадии, уровень смертности от WKS относительно высок, от 10% до 20%.
Может быть снижена мелкая моторика (например, движения рук или пальцев), а также может пострадать обоняние. На поздних стадиях может наступить кома. Хотя заболевание можно вылечить, если его поймают на достаточно ранней стадии, уровень смертности от WKS относительно высок, от 10% до 20%.
Диагностика
WKS часто упускают из виду как диагноз. В острой фазе физикальное обследование может выявить изменения кожи и красный «мясистый» язык. Кроме того, следует провести анализ крови, электролитов и функциональные пробы печени.Даже в хронической фазе МРТ может показать сморщенные маммиллярные тела и другие изменения в головном мозге. КТ показала увеличенные желудочки и диэнцефальные поражения.
Важно, чтобы полная история болезни включала информацию о ежедневных привычках питья человека, как в настоящем, так и в прошлом. Следует проконсультироваться с семьей, друзьями и прошлыми медицинскими записями, чтобы получить максимально полную информацию об анамнезе человека, употреблявшего алкоголь. Предлагаемые критерии для диагностики деменции, связанной с алкоголем (не строго WKS), предполагают, что диагноз ставится по крайней мере через 60 дней после последнего воздействия алкоголя и что «значительный» алкогольный анамнез будет включать в среднем 35 порций алкоголя в неделю для мужчин (28 для женщин) не менее пяти лет.Как правило, период значительного употребления алкоголя должен быть в пределах трех лет от начала деменции.
Предлагаемые критерии для диагностики деменции, связанной с алкоголем (не строго WKS), предполагают, что диагноз ставится по крайней мере через 60 дней после последнего воздействия алкоголя и что «значительный» алкогольный анамнез будет включать в среднем 35 порций алкоголя в неделю для мужчин (28 для женщин) не менее пяти лет.Как правило, период значительного употребления алкоголя должен быть в пределах трех лет от начала деменции.
Недавние медицинские исследования также показывают, что генетический маркер APOE4 является важным предиктором глобального интеллектуального дефицита у людей с WKS. Люди с генотипом APOE могут испытывать определенное взаимодействие с тяжелым употреблением алкоголя, которое может предрасполагать их к WKS. Обеспокоенность по поводу наследственной предрасположенности к WKS следует обсудить с генетическим консультантом.
При подозрении на WKS, не связанный с алкоголем, врач может исследовать нервную анорексию, гипермезис беременных, тяжелое недоедание и другие нарушения или хирургические процедуры, которые ухудшают всасывание тиамина в кишечнике.
Лечение
При раннем выявлении WKS можно предотвратить и вылечить. Лечение состоит из заместительной терапии тиамином, иногда вместе с другими витаминами. Дозировки могут отличаться, и врач должен внимательно их контролировать. Если потребление алкоголя прекратится и лечение будет назначено должным образом, люди с ранней стадией WKS могут ожидать заметного выздоровления и могут быть способны выполнять простые повторяющиеся задачи.
Однако спутанность сознания может исчезнуть через некоторое время, и даже неполное восстановление памяти может занять до года.На более поздних стадиях, если повреждение головного мозга необратимо, люди, вероятно, будут иметь длительные проблемы с памятью и походкой (например, нарушение координации мышц и онемение или слабость в конечностях).
Проблемы семейства
Уход за членом семьи с WKS или алкогольной деменцией представляет собой множество проблем для членов семьи. Устойчивые симптомы деменции и других неврологических проблем представляют собой тяжелые условия даже в самых лучших условиях.Причудливое или сбивающее с толку поведение может быть истолковано семьей как продолжение «запойного» пьянства, даже если человек бросил пить.
Устойчивые симптомы деменции и других неврологических проблем представляют собой тяжелые условия даже в самых лучших условиях.Причудливое или сбивающее с толку поведение может быть истолковано семьей как продолжение «запойного» пьянства, даже если человек бросил пить.
Лица, злоупотребляющие алкоголем, часто изолируются от своих семей и близких. Напряженные отношения — обычное дело в семьях алкоголиков. Как человек, осуществляющий уход, вы можете обижаться на заботу о родителе или супруге, которые на протяжении всей жизни злоупотребляли алкоголем. Кроме того, может быть трудно убедить человека с ограниченными возможностями бросить пить, так как большинство людей, страдающих WKS, длительное время были алкоголиками.Обсудите с врачом или психиатром эффективные стратегии предотвращения употребления алкоголя любимым человеком. Как ни странно, люди с WKS могут быть довольно апатичными и редко требуют алкоголь, но, скорее всего, примут его, если им предложат.
Семьям следует заручиться помощью и поддержкой специалистов в области психического здоровья или социальных работников, имеющих опыт работы с алкоголизмом. Семейные встречи или группы поддержки также могут быть полезны для объединения дополнительных членов семьи, чтобы помочь человеку из WKS.Куратор или семейный консультант могут помочь семье разобраться в проблемах и организовать соответствующие услуги поддержки. В тяжелых случаях или когда семья не может обеспечить надлежащий уход, можно обратиться за помощью в интернат. Для сбитого с толку пациента с WKS следует рассмотреть вопрос о домах престарелых, которые предоставляют особую помощь при деменции.
Семейные встречи или группы поддержки также могут быть полезны для объединения дополнительных членов семьи, чтобы помочь человеку из WKS.Куратор или семейный консультант могут помочь семье разобраться в проблемах и организовать соответствующие услуги поддержки. В тяжелых случаях или когда семья не может обеспечить надлежащий уход, можно обратиться за помощью в интернат. Для сбитого с толку пациента с WKS следует рассмотреть вопрос о домах престарелых, которые предоставляют особую помощь при деменции.
Исследования показывают, что алкоголизм часто передается по наследству. Наличие дополнительных членов семьи, являющихся алкоголиками, увеличивает бремя ухода. Некоторые исследования показали, что человек, чей родитель в анамнезе был алкоголизмом, может иметь наследственную предрасположенность к алкогольной зависимости и связанным с алкоголем неврологическим проблемам (периферическим невропатиям).Такие данные свидетельствуют о том, что людям в семьях алкоголиков необходимо принимать особые меры предосторожности, чтобы избегать чрезмерного употребления алкоголя, чтобы снизить собственный риск возникновения связанных с алкоголем проблем со здоровьем.
Уход за человеком с помощью WKS
Важно следить за тем, чтобы пострадавший продолжал воздерживаться от употребления алкоголя и чтобы он придерживался сбалансированной диеты с адекватным потреблением тиамина. Однако даже если человек перестанет пить и восполнит запасы тиамина, симптомы болезни (например,g., проблемное поведение, возбуждение, отсутствие координации, дефицит обучения) могут продолжаться. У абстинентного (т. Е. Трезвого) пациента с WKS эти симптомы следует рассматривать как часть заболевания, вызванного необратимым повреждением мозга и нервной системы.
Семейные опекуны должны принимать меры предосторожности для обеспечения безопасности человека с WKS, а также других членов семьи. Не следует оставлять сбитого с толку или дезориентированного человека одного. Необходимо наблюдение, чтобы человек не ушел из дома, не оставил включенной плиту или проточную воду.
Кратковременные проблемы с памятью означают, что сбитый с толку человек может повторять один и тот же вопрос снова и снова. Чтобы справиться с частым повторением, часто требуется метод проб и ошибок и сочетание стратегий. Во-первых, проявите терпение и отвечайте спокойно. Смущенный человек поймет ваше настроение и может еще больше расстроиться, если ваш голос будет громким или злым. Кроме того, разместите в доме напоминания, чтобы помочь человеку чувствовать себя в большей безопасности. Маркируйте внутренние двери и ящики словами или картинками.Делайте заметки (например, ужин в 18:00 ). Еще одна стратегия — отвлечь человека другой темой или делом (например, короткой прогулкой, воспоминаниями по старой фотографии и т. Д.).
Чтобы справиться с частым повторением, часто требуется метод проб и ошибок и сочетание стратегий. Во-первых, проявите терпение и отвечайте спокойно. Смущенный человек поймет ваше настроение и может еще больше расстроиться, если ваш голос будет громким или злым. Кроме того, разместите в доме напоминания, чтобы помочь человеку чувствовать себя в большей безопасности. Маркируйте внутренние двери и ящики словами или картинками.Делайте заметки (например, ужин в 18:00 ). Еще одна стратегия — отвлечь человека другой темой или делом (например, короткой прогулкой, воспоминаниями по старой фотографии и т. Д.).
Если человек продолжает волноваться, симптомы следует обсудить с врачом, неврологом или психиатром. Могут быть доступны лекарства, которые помогают контролировать вспышки или беспокойство.
Не менее важно, чтобы лицо, осуществляющее уход, получало некоторую поддержку и свободное время от постоянных требований по уходу.Удостоверьтесь, что у вас есть время, чтобы заняться своими собственными потребностями, включая хорошее питание, достаточный сон и регулярные медицинские осмотры. Может потребоваться работник по уходу на дому, друг или член семьи, чтобы периодически предоставлять временную помощь, чтобы помочь вашему близкому и снять стресс с вас, члена семьи, осуществляющего уход.
Может потребоваться работник по уходу на дому, друг или член семьи, чтобы периодически предоставлять временную помощь, чтобы помочь вашему близкому и снять стресс с вас, члена семьи, осуществляющего уход.
Ресурсы
Альянс семейных опекунов
Национальный центр опеки
(415) 434-3388 | (800) 445-8106
Веб-сайт: www.caregiver.org
Эл. почта: [адрес электронной почты защищен]
FCA CareJourney: www.caregiver.org/carejourney
Навигатор по семейному уходу: www.caregiver.org/family-care-navigator
Family Caregiver Alliance (FCA) стремится улучшить качество жизни лиц, осуществляющих уход, посредством образования, услуг, исследований и защиты. Через свой Национальный центр по уходу FCA предлагает информацию по текущим социальным вопросам, вопросам государственной политики и ухода, а также оказывает помощь в разработке государственных и частных программ для лиц, осуществляющих уход. Для жителей большей части района залива Сан-Франциско FCA предоставляет услуги прямой семейной поддержки лицам, осуществляющим уход за больными с болезнью Альцгеймера, инсультом, БАС, травмой головы, болезнью Паркинсона и другими изнурительными заболеваниями мозга, поражающими взрослых.
Для жителей большей части района залива Сан-Франциско FCA предоставляет услуги прямой семейной поддержки лицам, осуществляющим уход за больными с болезнью Альцгеймера, инсультом, БАС, травмой головы, болезнью Паркинсона и другими изнурительными заболеваниями мозга, поражающими взрослых.
Прочие организации и ссылки
Национальная организация по редким заболеваниям
www.rarediseases.org
Национальный институт злоупотребления алкоголем и алкоголизма
www.niaaa.nih.gov
Американская ассоциация брака и Семейная терапия
www.aamft.org
National Eldercare Locator
www.eldercare.acl.gov
Этот информационный бюллетень был подготовлен Family Caregiver и проверен Питером Мартином, доктором медицины, Медицинский факультет Университета Вандербильта. © 1998 Альянс семейных опекунов. Все права защищены.
Алкогольная деменция: что такое синдром Вернике-Корсакова?
Синдром Вернике-Корсакова (также называемый алкогольной деменцией) — это набор неврологических состояний, возникающих в результате дефицита тиамина (витамина B1).Когда кто-то испытывает дефицит тиамина, его мозг менее способен перерабатывать сахар в энергию, которую мозг может использовать для функционирования. Это, в свою очередь, может привести к развитию симптомов деменции, включая спутанность сознания и потерю памяти. Синдром Вернике-Корсакова может значительно повлиять на продолжительность жизни и требует немедленного лечения.
Крит из Studio OMG / Getty Images
Синдром Вернике-Корсакова состоит из двух отдельных состояний: сначала развивается энцефалопатия Вернике, а затем синдром Корсакова, который часто проявляется в виде стихания симптомов энцефалопатии Вернике.
Синдром Вернике-Корсакова также может называться психозом Корсакова, энцефалопатией Вернике, алкогольной энцефалопатией, энцефалопатией — алкогольной, алкогольной деменцией, деменцией Вернике и болезнью Вернике. Неофициально некоторые люди также называют это состояние синдромом «мокрого мозга».
Неофициально некоторые люди также называют это состояние синдромом «мокрого мозга».
Симптомы энцефалопатии Вернике
Симптомы энцефалопатии Вернике включают внезапный эпизод снижения умственных способностей, спутанность сознания, тремор ног, шатание, снижение мышечной координации, изменения зрения и глаз (включая опущение век, двоение в глазах и ненормальные движения глаз вперед и назад) и другие симптомы отмены алкоголя.Симптомы энцефалопатии Вернике часто классифицируются как триада из глазных (глаз), мозжечковых (баланс и контроль тела) и симптомов спутанности сознания.
Энцефалопатия Вернике — это состояние, которое требует немедленной медицинской помощи и при соответствующем лечении может быть обратимым.
Симптомы синдрома Корсакова
Симптомы синдрома Корсакова включают потерю памяти (включая способность восстанавливать старые воспоминания и способность формировать новые), галлюцинации и конфабуляцию (придумывание историй).Синдром Корсакова обычно является хроническим заболеванием, которое обычно, но не всегда, следует за эпизодом энцефалопатии Вернике. Взаимодействие с другими людьми
Взаимодействие с другими людьми
Распространенность
Трудно сказать, насколько распространен синдром Вернике-Корсакова, поскольку исследования показывают, что он значительно недооценен. В одном исследовании, опубликованном в 2009 году, этот показатель составляет около 1-2 процентов от общей численности населения и 12-14 процентов среди злоупотребляющих алкоголем. Однако его диагноз часто упускается из виду, о чем свидетельствует более высокая степень выявления расстройства при вскрытии мозга, чем при диагностировании при жизни.Взаимодействие с другими людьми
Причины
Наиболее частым риском синдрома Вермике-Корсакова является злоупотребление алкоголем, но он также может быть вызван СПИДом, раком, хроническими инфекциями, диализом почек, анорексией и неспособностью организма усваивать питательные вещества из пищи. Интересно, что риск также увеличивается после бариатрической операции по поводу ожирения. Взаимодействие с другими людьми
Некоторые случаи энцефалопатии Вернике также могут быть вызваны экстремальной диетой, которая не позволяет организму получать питательные вещества, необходимые для поддержания здорового функционирования.
Диагностика
Чтобы диагностировать энцефалопатию Вернике, необходимо проверить уровень тиамина в крови человека. Тиамин также известен как витамин B1.
Единого теста на синдром Вернике-Корсакова не существует. Вместо этого он диагностируется путем исключения других состояний. Оценка может включать когнитивные оценки, анализы крови и неврологические обследования для оценки движения глаз, силы мышц и координации. МРТ также можно использовать для выявления поражений в головном мозге, которые могут развиться в результате заболевания.Взаимодействие с другими людьми
Некоторые случаи неалкогольной энцефалопатии Вернике были упущены из-за наличия других заболеваний, таких как тяжелое биполярное расстройство или шизофрения, вызвавшие расстройства пищевого поведения. Тестирование на тиаминовые расстройства при острой спутанности сознания и дезориентации имеет решающее значение для выявления и надлежащего лечения.
Лечение
Энцефалопатия Вернике требует немедленного лечения, которое обычно состоит из высоких доз тиамина, вводимых внутривенно. Некоторые исследования показывают, что, когда энцефалопатия Вермике возникает из-за злоупотребления алкоголем, человеку может потребоваться более высокая дозировка тиамина, чем при ее развитии по другим причинам.
Некоторые исследования показывают, что, когда энцефалопатия Вермике возникает из-за злоупотребления алкоголем, человеку может потребоваться более высокая дозировка тиамина, чем при ее развитии по другим причинам.
Текущее лечение синдрома Вернике-Корсакова включает воздержание от алкоголя, адекватное питание и витаминные добавки.
Прогноз
Прогноз синдрома Вернике-Корсакова разнообразен. По оценкам Ассоциации Альцгеймера, при соответствующем лечении примерно 25% людей полностью выздоровеют, около половины улучшится, но не восстановят полноценное функционирование, и около 25% останутся примерно такими же.Взаимодействие с другими людьми
Любое улучшение функционирования обычно происходит в течение первых двух лет после появления симптомов. Продолжительность жизни может оставаться нормальной, если человек не употребляет алкоголь.
Согласно Руководствам Merck, около 10-20% людей с нелеченной энцефалопатией Вернике не выживают. Однако при лечении прогноз синдрома Вернике-Корсакова намного лучше, чем при болезни Альцгеймера и других типах деменции, снижение которых носит хронический и прогрессирующий характер, несмотря на попытки лечения. Взаимодействие с другими людьми
Взаимодействие с другими людьми
Слово Verywell
Синдром Вернике-Корсакова — это набор состояний, которые могут вызывать симптомы спутанности сознания, потери памяти и дезориентации, а также физические признаки, такие как мышечная слабость и проблемы с движением глаз. Хотя поначалу вы можете не решаться обратиться за помощью к себе или любимому человеку, важно помнить, что быстрое лечение, помимо отказа от употребления алкоголя, может позволить вам восстановить большую часть функций, которые нарушаются при развитии этого синдрома.
границ | Случай хронической энцефалопатии Вернике: нейропсихологическое исследование
Введение
Энцефалопатия Вернике (WE) — это острый психоневрологический синдром, возникающий в результате дефицита витамина B1 (тиамина) (1). Синдром характеризуется спутанностью сознания, нарушением внимания, бессвязностью, нарушением движений глаз и атаксией, хотя часто присутствует только одна или две характеристики (2–4). В промышленно развитых странах большинство пациентов с WE имеют хронический алкоголизм и пренебрежение собой (5).МЫ требует немедленного лечения тиамином внутривенно или внутримышечно. Когда пациенты с WE получают своевременное лечение парентеральной заместительной тиаминовой терапией, это спасательная мера, которая также может предотвратить развитие хронического повреждения головного мозга (6). Если WE не лечить или неправильно лечить либо низкими дозами тиамина, либо пероральной заместительной терапией тиамином, это может привести к опасной для жизни ситуации с уровнем смертности до 20% пациентов (4). У пациентов, которые выживают при таком отсутствии лечения, развиваются различные степени повреждения головного мозга, хотя точное течение болезни не совсем понятно (7).Прогрессирование в хорошо известную форму хронической амнезии, синдром Корсакова (СК), не редкость [Ref. (8), см. Рисунок 1]. Обычно СК следует за WE, когда острая спутанность сознания проходит в течение одной-двух недель.
В промышленно развитых странах большинство пациентов с WE имеют хронический алкоголизм и пренебрежение собой (5).МЫ требует немедленного лечения тиамином внутривенно или внутримышечно. Когда пациенты с WE получают своевременное лечение парентеральной заместительной тиаминовой терапией, это спасательная мера, которая также может предотвратить развитие хронического повреждения головного мозга (6). Если WE не лечить или неправильно лечить либо низкими дозами тиамина, либо пероральной заместительной терапией тиамином, это может привести к опасной для жизни ситуации с уровнем смертности до 20% пациентов (4). У пациентов, которые выживают при таком отсутствии лечения, развиваются различные степени повреждения головного мозга, хотя точное течение болезни не совсем понятно (7).Прогрессирование в хорошо известную форму хронической амнезии, синдром Корсакова (СК), не редкость [Ref. (8), см. Рисунок 1]. Обычно СК следует за WE, когда острая спутанность сознания проходит в течение одной-двух недель. Основные характеристики этого улучшения включают способность концентрироваться в течение более длительного времени, меньшую непоследовательность в поведении и ясное сознание в течение дня, несмотря на тяжелую амнезию (8–10).
Основные характеристики этого улучшения включают способность концентрироваться в течение более длительного времени, меньшую непоследовательность в поведении и ясное сознание в течение дня, несмотря на тяжелую амнезию (8–10).
Рис. 1. Эволюция энцефалопатии Вернике, предложенная Harper et al.(3) и Day et al. (11) . См. Kopelman et al. (8) для обзора.
Описания случаев НЭ, при которых симптомы быстро не улучшаются, немногочисленны и часто ограничиваются острой ситуацией. Примеры таких случаев описаны во время Второй мировой войны после голодания военнопленных (12). Описания когнитивных последствий длительной спутанности сознания после WE в настоящее время в литературе отсутствуют. Однако такое нейропсихиатрическое описание тяжелых случаев МЭ имеет решающее значение, поскольку дает представление о серьезности синдрома.Несмотря на текущие стандарты оказания неотложной помощи в промышленно развитых странах, подавляющее большинство пациентов с НЭ не получают должного лечения, что приводит к тому, что пациенты длительное время сохраняют замешательство (13-15)..jpg) Здесь мы представляем тематическое исследование, которое иллюстрирует когнитивные и поведенческие характеристики, включая признаки замешательства, пациента, который был госпитализирован в нашу клинику с нелеченным WE. Нейропсихологическое обследование выявило поразительные когнитивные нарушения, в отличие от СК. Важно отметить, что первоначальные когнитивные и нейропсихиатрические проблемы не разрешились вовремя, что дает пример пациента с острым WE, который перешел в хронический.
Здесь мы представляем тематическое исследование, которое иллюстрирует когнитивные и поведенческие характеристики, включая признаки замешательства, пациента, который был госпитализирован в нашу клинику с нелеченным WE. Нейропсихологическое обследование выявило поразительные когнитивные нарушения, в отличие от СК. Важно отметить, что первоначальные когнитивные и нейропсихиатрические проблемы не разрешились вовремя, что дает пример пациента с острым WE, который перешел в хронический.
Отчет о болезни
Биографическая история
По словам членов семьи, до возникновения неврологических проблем пациент функционировал независимо. Сын пациентки навещал ее несколько раз в неделю. В своем доме она могла вести домашнее хозяйство, несмотря на злоупотребление алкоголем. Количество алкоголя, которое она потребляла, варьировалось от одной до трех бутылок вина каждый день. Она развелась за 12 месяцев до постановки диагноза WE. За 6 месяцев до госпитализации пациентка работала на мультиварке в больнице. Последний месяц она плохо ела и употребляла алкоголь в течение дня. Он сказал, что пациентка не хочет есть, но все же рассказала о вещах, которые она хотела бы предпринять для борьбы с алкоголизмом. За день до того, как ее нашли, у нее был телефонный звонок с сыном. Сын сообщил, что телефонный звонок включал регулярный обмен информацией без какого-либо заметного обмена информацией.
Последний месяц она плохо ела и употребляла алкоголь в течение дня. Он сказал, что пациентка не хочет есть, но все же рассказала о вещах, которые она хотела бы предпринять для борьбы с алкоголизмом. За день до того, как ее нашли, у нее был телефонный звонок с сыном. Сын сообщил, что телефонный звонок включал регулярный обмен информацией без какого-либо заметного обмена информацией.
История болезни
Наша пациентка — женщина 54 лет с 7-летним анамнезом злоупотребления алкоголем.Пациент не имел психиатрического анамнеза. Ее нашли в своем доме на полу в гостиной. Согласно сообщениям ее сына, который нашел ее, она не могла двигать ногами, показывала странные движения глаз, у нее были зрительные галлюцинации еды, лежащей вокруг нее, она говорила ерунду и страдала недержанием мочи. После посещения ее дома терапевтом ее сыну сказали дать матери отдохнуть. Спустя 5 дней и без видимых изменений в ее ситуации, посещающий ее психиатр направил ее в больницу, где ей поставили диагноз WE, и она прошла курс перорального лечения тиамином. Впоследствии пациентка была помещена в отделение наркологического центра, где пробыла почти 8 месяцев. Здесь ее поведение было описано как бессвязное и запутанное. Она показала принуждение к регулярному посещению туалета и часто просить медперсонал о сигаретах. После пребывания в наркологическом центре ее направили в нашу клинику для пациентов с СК.
Впоследствии пациентка была помещена в отделение наркологического центра, где пробыла почти 8 месяцев. Здесь ее поведение было описано как бессвязное и запутанное. Она показала принуждение к регулярному посещению туалета и часто просить медперсонал о сигаретах. После пребывания в наркологическом центре ее направили в нашу клинику для пациентов с СК.
Методы
Через четыре месяца после того, как ее нашли, в наркологическом центре было проведено нейропсихологическое обследование (Т1).Через шестнадцать месяцев после первой оценки когнитивные функции были повторно оценены (Т2). Результаты первой и второй нейропсихологической оценки отображены в таблице 1. Референсная группа хронического саркома Капоши отображается в последнем столбце. Результаты для контрольной группы были взяты из групповых исследований пациентов с хроническим СК, как показано в таблице 1. Первая нейропсихологическая оценка состояла из шкалы интеллекта взрослых Векслера-III (16), стандартных прогрессивных матриц Равена (17), беглости слов. Животные и профессии (18), Размах цифр вперед и назад (16), Комплексная задача Рея по фигуре (19), Шкала памяти Векслера-R, Визуальная интеграция Хупера (20), Струп (21), Задача создания следов (22) и Ключевое задание по поиску поведенческой оценки дизисполнительного синдрома.Вторая нейропсихологическая оценка состояла из краткого исследования психического состояния, задания когнитивного скрининга (23), беглости слов животных, прямого и обратного диапазона цифр, задания следа, теста зрительной ассоциации (24), задания на сложную фигуру Рей и лобно-височного теста. Шкала оценки деменции (25). Первый автор проинформировал пациентку о ее желании участвовать. Письменное информированное согласие было получено от законного представителя. Процедура выполнялась в соответствии с руководящими принципами Хельсинкской декларации и руководящими принципами набора некомпетентных пациентов [см.Ref. (26)].
Животные и профессии (18), Размах цифр вперед и назад (16), Комплексная задача Рея по фигуре (19), Шкала памяти Векслера-R, Визуальная интеграция Хупера (20), Струп (21), Задача создания следов (22) и Ключевое задание по поиску поведенческой оценки дизисполнительного синдрома.Вторая нейропсихологическая оценка состояла из краткого исследования психического состояния, задания когнитивного скрининга (23), беглости слов животных, прямого и обратного диапазона цифр, задания следа, теста зрительной ассоциации (24), задания на сложную фигуру Рей и лобно-височного теста. Шкала оценки деменции (25). Первый автор проинформировал пациентку о ее желании участвовать. Письменное информированное согласие было получено от законного представителя. Процедура выполнялась в соответствии с руководящими принципами Хельсинкской декларации и руководящими принципами набора некомпетентных пациентов [см.Ref. (26)].
Таблица 1 . Результаты теста нейропсихологической оценки через 4 и 16 месяцев после поступления в стационар в нашем случае и контрольной группе СК .
Результаты
Наблюдения и нейропсихологическая оценка на T1
Качественные наблюдения за T1 показали последовательную картину поразительных нарушений. Сообщалось о психическом замешательстве с предпочтением продолжать просить сигареты, повышенной отвлекаемостью и дезорганизацией поведения.Пациент часто уходил во время разговора. Ее поведение выглядело сильно дезорганизованным. Когда она сидела за компьютером, выполняя пасьянс, она энергично двигала ногами вверх и вниз, возможно, как симптом поздней стадии МЭ (4). Более того, она заходила в свою комнату, раздевалась, лежала в постели всего пару минут. После этого она одевалась сама, просила медперсонал принести сигареты, курила и входила в свою комнату, чтобы раздеться, лежала в постели всего пару минут и снова одевалась.Во время обеда и ужина она заходила в комнату, съедала один кусочек и немедленно выходила из комнаты. По ночам она просила у персонала поесть. Согласно отчетам медперсонала, в течение дня она не проявляла ни положительных, ни отрицательных эмоций.
В левом столбце таблицы 1 показаны результаты тестов по нейропсихологической оценке через 4 месяца после поступления в больницу. Первоначально (T1) ее результативность при нейропсихологической оценке соответствовала профилю когнитивного ухудшения, показывая снижение производительности тестов на внимание, ориентацию, интеллект, беглость слов, рабочую память, долговременную память, конструкцию и исполнительное функционирование. по сравнению со здоровыми участниками.Важно отметить, что на когнитивный профиль серьезно повлияли расстройства внимания, соответствующие острой WE. Нейропсихологические показатели варьировали от умеренных до тяжелых, за исключением перцептивных способностей. Контрольные группы пациентов с СК имели нарушения ориентации, долговременной памяти и управляющих функций. При выполнении заданий, предназначенных для индексации ориентации, беглости слов, рабочей памяти, зрительного строения и интеллекта, результативность пациента была более чем на 1 SD ниже среднего балла в контрольных группах KS. Это говорит о том, что как природа, так и степень когнитивных расстройств в тематическом исследовании были чрезвычайно серьезными.
Это говорит о том, что как природа, так и степень когнитивных расстройств в тематическом исследовании были чрезвычайно серьезными.
Наблюдения и нейропсихологическая оценка T2
Качественные наблюдения за спутанным поведением продолжались во время ее пребывания в нашей клинике Корсаков, без каких-либо признаков улучшения или ухудшения с течением времени. Пациентка выглядела настолько отвлекающей, если члены команды могли ее мотивировать. Она часто раздевалась и поправлялась в своей комнате.
В правом столбце Таблицы 1 показаны результаты тестов по нейропсихологической оценке через 16 месяцев после поступления в больницу. Паттерн когнитивного функционирования соответствовал паттерну наблюдаемой когнитивной дисфункции в момент T1. Пациент продемонстрировал схожую производительность в когнитивных задачах: снижение производительности тестов на ориентацию, интеллект, беглость слов, рабочую память, долговременную память, построение, внимание и исполнительное функционирование по сравнению со здоровыми участниками. Проблемы с вниманием были столь же разительны, как и на Т1. Когнитивный паттерн был стабильным по сравнению с T1, тогда как улучшения в случае KS следует ожидать на основании доступной литературы (см. Рисунок 1).
Проблемы с вниманием были столь же разительны, как и на Т1. Когнитивный паттерн был стабильным по сравнению с T1, тогда как улучшения в случае KS следует ожидать на основании доступной литературы (см. Рисунок 1).
Обсуждение
Пациент, представленный в данном отчете, показал отчетливую хроническую картину когнитивных и психоневрологических нарушений в течение тяжелой НЭ. Признаки замешательства и непоследовательного поведения были очевидны и не исчезли вовремя. Когнитивные нарушения внимания, долговременной памяти, рабочей памяти, зрительной конструкции и беглости слов стали очевидными как через 4, так и через 16 месяцев после поступления в больницу.Важно отметить, что дефицит внимания серьезно повлиял на когнитивный профиль по обоим нейропсихологическим оценкам. По сравнению с контрольной группой с KS, у пациента был более широкий спектр тяжелых когнитивных нарушений. Пациентка могла действовать независимо до того момента, когда у нее развился МЭ. Когнитивные и нейропсихиатрические проблемы соответствовали острым симптомам НЭ и не улучшились в течение ее пребывания в клинике, что позволяет предположить, что НЭ у нее перешло в хроническую форму.
Энцефалопатия Вернике — это опасное для жизни состояние, возникающее после острого дефицита тиамина (5).В то время как большое количество исследований WE было посвящено успешному лечению WE в острой фазе, описания случаев, когда спутанность сознания не проходит быстро, в настоящее время отсутствуют. Это поразительно, учитывая, что в клинической практике МЭ не получают должного лечения, и пациенты по-прежнему попадают в больницы общего профиля или психиатрические больницы с длительными состояниями спутанности сознания (13–15). Более того, WE является потенциально смертельным исходом примерно у 20% пациентов (8). Настоящее тематическое исследование предполагает, что МЫ могут привести не только к опасной для жизни острой ситуации, но и к хронической форме МЭ, включая хроническое состояние растерянности и дезорганизованного поведения.Тяжесть психоневрологических симптомов заставляет пациента нуждаться в пожизненной помощи.
Возможным объяснением того, почему у пациента в данном исследовании развилась тяжелая хроническая картина когнитивных проблем, может быть поздняя госпитализация и неадекватное лечение заместительной тиаминовой терапией. Хотя пациентка была обнаружена лежащей на полу с обильными симптомами неврологического заболевания (например, странные движения глаз, зрительные галлюцинации, недержание мочи), ее не госпитализировали в первые 5 дней и в течение этого периода не лечили.Поскольку тяжелые когнитивные расстройства являются следствием нелеченного или недостаточно леченного дефицита тиамина, пациент должен был немедленно получить заместительную терапию тиамином (7). В данном случае диагноз WE был поставлен в больнице, после чего был начат пероральный прием тиамина. Этот момент времени приема добавок тиамина считается очень поздней компенсацией дефицита тиамина (13). Более того, оральная заместительная терапия менее эффективна, чем парентеральная заместительная терапия (4).
Хотя пациентка была обнаружена лежащей на полу с обильными симптомами неврологического заболевания (например, странные движения глаз, зрительные галлюцинации, недержание мочи), ее не госпитализировали в первые 5 дней и в течение этого периода не лечили.Поскольку тяжелые когнитивные расстройства являются следствием нелеченного или недостаточно леченного дефицита тиамина, пациент должен был немедленно получить заместительную терапию тиамином (7). В данном случае диагноз WE был поставлен в больнице, после чего был начат пероральный прием тиамина. Этот момент времени приема добавок тиамина считается очень поздней компенсацией дефицита тиамина (13). Более того, оральная заместительная терапия менее эффективна, чем парентеральная заместительная терапия (4).
Учитывая, что прогноз WE, как известно, зависит от скорости компенсации дефицита тиамина (14) и серьезных хронических когнитивных нарушений, связанных с хроническим WE, наблюдаемых в настоящем исследовании, наши результаты показывают, что для того, чтобы Избегайте тяжелых хронических психоневрологических симптомов. Современные стандарты лечения предполагают, что парентерально (внутривенно или внутримышечно тиамин следует вводить от 200 до 500 мг три раза в день до исчезновения симптомов острой НЭ (32).Чтобы предотвратить тяжелые и хронические когнитивные расстройства, врачи должны иметь высокий индекс подозрения на WE и соответственно вводить парентеральный тиамин (7).
Современные стандарты лечения предполагают, что парентерально (внутривенно или внутримышечно тиамин следует вводить от 200 до 500 мг три раза в день до исчезновения симптомов острой НЭ (32).Чтобы предотвратить тяжелые и хронические когнитивные расстройства, врачи должны иметь высокий индекс подозрения на WE и соответственно вводить парентеральный тиамин (7).
Хотя в нашем исследовании пациент имел историю злоупотребления алкоголем, нейрокогнитивные симптомы имели острое начало, как сообщается в WE, что делает алкогольную деменцию неправдоподобным объяснением серьезных острых когнитивных проблем (33). Более того, когнитивные проблемы оставались стабильными в течение 16 месяцев, в отличие от прогрессирующей деменции.В отличие от СК, у пациентки были хронические проблемы с функцией внимания, рабочей памяти, зрительной конструкцией и функцией беглости слов.
В заключение, текущее тематическое исследование иллюстрирует когнитивные и поведенческие характеристики пациента, который был госпитализирован в нашу клинику с нелеченным WE. Наше описание представляет собой первое сообщение о пациенте с длительным состоянием замешательства после WE, предполагающее, что WE может стать хроническим в случае поздней заместительной терапии тиамином.
Наше описание представляет собой первое сообщение о пациенте с длительным состоянием замешательства после WE, предполагающее, что WE может стать хроническим в случае поздней заместительной терапии тиамином.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Благодарности
Мы благодарим пациентку и ее семью за их желание участвовать. Таня К. В. Ниджбоер была поддержана грантом NWO № 451-10-013.
Список литературы
1. Манзо Л., Локателли С., Кандура С.М., Коста Л.Г.Нейротоксичность питания и алкоголя. Нейротоксикология (1994) 15 : 555–65.
2. Вернике К. Lehrbuch der gehirnkrankheiten fur aerzte und studirende . Кассель Теодор Фишер (1881) 2 : 229–42.
3. Харпер К.Г., Джайлс М., Финлей-Джонс Р. Клинические признаки комплекса Вернике-Корсакова: ретроспективный анализ 131 случая, диагностированного при вскрытии. J Neurol Neurosurg Psychiatry (1986) 49 : 341–5.DOI: 10.1136 / jnnp.49.4.341
Харпер К.Г., Джайлс М., Финлей-Джонс Р. Клинические признаки комплекса Вернике-Корсакова: ретроспективный анализ 131 случая, диагностированного при вскрытии. J Neurol Neurosurg Psychiatry (1986) 49 : 341–5.DOI: 10.1136 / jnnp.49.4.341
Pubmed Аннотация | Pubmed Полный текст | CrossRef Полный текст
5. Копельман М.Д. Расстройства памяти. Мозг (2002) 125 : 2152–90. DOI: 10.1093 / мозг / awf229
CrossRef Полный текст
11. День Е, Бентам П., Каллаган Р., Курувилла Т., Джордж С. Тиамин для синдрома Вернике-Корсакова у людей, подверженных риску злоупотребления алкоголем. Кокрановская база данных Syst Rev (2004) (1): CD004033.
12. De Wardener HE, Леннокс Б. Церебральный бери-бери (энцефалопатия Вернике): обзор 52 случаев в сингапурском госпитале для военнопленных. Ланцет (1947) 1 : 11–7. DOI: 10.1016 / S0140-6736 (47) 91272-5
DOI: 10.1016 / S0140-6736 (47) 91272-5
CrossRef Полный текст
14. Изенберг-Грзеда Э, Чабон Б., Николсон С.Е. Назначение тиамина больным с расстройствами, связанными с употреблением алкоголя: насколько хорошо мы себя чувствуем? J Addict Med (2014) 8 : 1–5.DOI: 10.1097 / 01.ADM.0000435320.72857.c8
Pubmed Аннотация | Pubmed Полный текст | CrossRef Полный текст
15. Oudman E, Wijnia JW. Рекомендации BNF по лечению энцефалопатии Вернике: потерялись в переводе? Алкоголь Спирт (2014) 49 : 118. DOI: 10.1093 / alcalc / agt179
CrossRef Полный текст
16. Uterwijk J. Техническое руководство WAIS-III (на голландском языке) .Лиссе: Swets & Zeitlinger (2000).
17. Рэйвен Дж., Рэйвен Дж. С., Суд JH. Общий обзор . Оксфорд: Издательство Оксфордского университета (1995).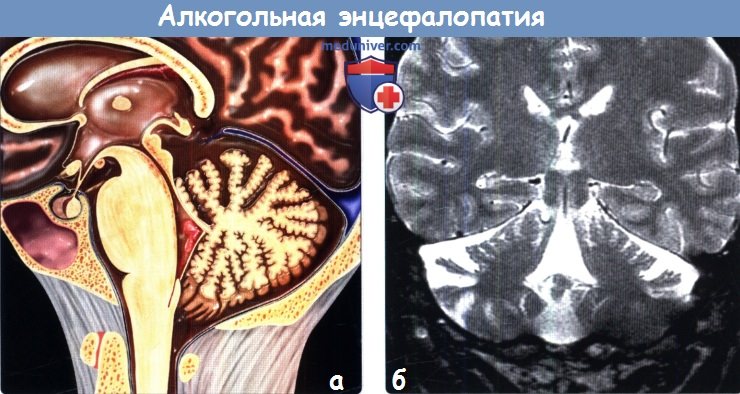
18. Малдер Дж. Л., Деккер PH, Деккер Р. Тест на беглость слов (на голландском языке) . Лейден: PITS BV (2006).
19. Мейерс Дж. Э., Мейерс КР. Rey Комплексное испытание фигуры и распознавания (RCFT). Профессиональное руководство . Лутц: Ресурсы психологической оценки, Inc.(1995).
20. Уокер Р.Г. Пересмотренный тест зрительной организации гупера как мера повреждения мозга. J Clin Psychol (1956) 12 : 387–88. DOI: 10.1002 / 1097-4679 (195610) 12: 4 <387 :: AID-JCLP2270120421> 3.0.CO; 2-J
CrossRef Полный текст
21. Hammes JGW. De Stroop Color Word Test Manual (на голландском языке) . Лисс: Swets en Zeitlinger (1971).
23.де Грааф А., Дилман Б.Г. Руководство по тесту когнитивного скрининга (на голландском языке) . Лиссе: Swets & Zeitlinger (1991).
24. Lindeboom J, Schmand B, Tulner L, Walstra G, Jonker C. Тест визуальной ассоциации для выявления ранней деменции типа Альцгеймера. J Neurol Neurosurg Psychiatry (2002) 73 : 126–33. DOI: 10.1136 / jnnp.73.2.126
Lindeboom J, Schmand B, Tulner L, Walstra G, Jonker C. Тест визуальной ассоциации для выявления ранней деменции типа Альцгеймера. J Neurol Neurosurg Psychiatry (2002) 73 : 126–33. DOI: 10.1136 / jnnp.73.2.126
Pubmed Аннотация | Pubmed Полный текст | CrossRef Полный текст
25.Mioshi E, Hsieh S, Savage S, Hornberger M, Hodges JR. Клиническая стадия и прогрессирование лобно-височной деменции. Неврология (2010) 74 : 1591–7. DOI: 10.1212 / WNL.0b013e3181e04070
Pubmed Аннотация | Pubmed Полный текст | CrossRef Полный текст
26. Meulenbroek O, Vernooij-Dassen M, Kessels RPC, Graff MJL, Sjögren MJC, Schalk BWM и др. Информированное согласие в исследовании деменции. Законодательство, теоретические концепции и способы оценки способности давать согласие. Eur Geriatr Med (2010) 1 : 58–63. DOI: 10.1016 / j.eurger.2010.01.009
CrossRef Полный текст
27. Вестер AJ, Westhoff J, Kessels RPC, Egger JIM. Монреальский когнитивный тест (MoCa) как мера тяжести амнезии у пациентов с когнитивными нарушениями, связанными с алкоголем, и синдромом Корсакова. Clin Neuropsychiatry (2013) 10 : 134–41.
Вестер AJ, Westhoff J, Kessels RPC, Egger JIM. Монреальский когнитивный тест (MoCa) как мера тяжести амнезии у пациентов с когнитивными нарушениями, связанными с алкоголем, и синдромом Корсакова. Clin Neuropsychiatry (2013) 10 : 134–41.
28.Oudman E, Nijboer TCW, Postma A, Wijnia JW, Kerklaan S, Lindsen K и др. Освоение инструментальной повседневной деятельности у пациентов с синдромом Корсакова: сравнение метода проб и ошибок и безошибочного обучения. Neuropsychol Rehabil (2013) 23 : 888–913. DOI: 10.1080 / 09602011.2013.835738
Pubmed Аннотация | Pubmed Полный текст | CrossRef Полный текст
29. Kessels RPC, Kortrijk HE, Wester AJ, Nys GS.Конфабуляционное поведение и ложные воспоминания при синдроме Корсакова: роль исходной памяти и исполнительных функций. Psychiatry Clin Neurosci (2008) 62 : 220–5. DOI: 10.1111 / j.1440-1819.2008.01758.x
Pubmed Аннотация | Pubmed Полный текст | CrossRef Полный текст
30. Fujiwara E, Brand M, Borsutzky S, Steingass H-P, Markowitsch HJ. Когнитивные способности пациентов с алкогольным синдромом Корсакова после детоксикации остаются стабильными в течение двух лет. J Clin Exp Neuropsychol (2008) 30 : 576–87. DOI: 10.1080 / 138033
Fujiwara E, Brand M, Borsutzky S, Steingass H-P, Markowitsch HJ. Когнитивные способности пациентов с алкогольным синдромом Корсакова после детоксикации остаются стабильными в течение двух лет. J Clin Exp Neuropsychol (2008) 30 : 576–87. DOI: 10.1080 / 138033
557271
Pubmed Аннотация | Pubmed Полный текст | CrossRef Полный текст
31. Уэлч Л.В., Каннингем А.Т., Эккардт М.Дж., Мартин П.Р. Нарушения скорости мелкой моторики при алкогольном синдроме Корсакова. Alcohol Clin Exp Res (1997) 21 : 134–9. DOI: 10.1097 / 00000374-199702000-00020
Pubmed Аннотация | Pubmed Полный текст | CrossRef Полный текст
32.Томсон А.Д., Кук СН, Туке Р., Генри Дж. Отчет Королевского колледжа врачей об алкоголе: руководство по лечению энцефалопатии Вернике в отделении неотложной помощи. Алкоголь Спирт (2002) 37 : 513–21. DOI: 10.1093 / alcalc / 37.6.513
Pubmed Аннотация | Pubmed Полный текст | CrossRef Полный текст
33. Oslin D, Atkinson RM, Smith DM, Hendrie H. Алкогольная деменция: предлагаемые клинические критерии. Int J Geriatr Psychiatry (1998) 13 : 203–12. DOI: 10.1002 / (SICI) 1099-1166 (199804) 13: 4 <203 :: AID-GPS734> 3.0.CO; 2-B
Oslin D, Atkinson RM, Smith DM, Hendrie H. Алкогольная деменция: предлагаемые клинические критерии. Int J Geriatr Psychiatry (1998) 13 : 203–12. DOI: 10.1002 / (SICI) 1099-1166 (199804) 13: 4 <203 :: AID-GPS734> 3.0.CO; 2-B
Pubmed Аннотация | Pubmed Полный текст | CrossRef Полный текст
Что вам нужно знать
Синдром Вернике-Корсакова (WKS), поражающий 1-2 процента населения, представляет собой неврологическое заболевание, которое представляет собой комбинацию энцефалопатии Вернике и синдрома Корсакова. WKS часто называют алкогольным слабоумием или алкогольным слабоумием, и он в первую очередь вызван недостатком тиамина.Хотя это заболевание головного мозга обычно поддается лечению, при диагностировании и лечении на ранних стадиях последствия WKS могут быть очень серьезными и привести к необратимой деменции.
В Центре болезни Альцгеймера и слабоумия на Лонг-Айленде (LIAD) мы помогаем семьям, страдающим от всех форм деменции, включая WKS. Мы предлагаем ряд поддерживающих решений как для людей с диагнозом, так и для тех, кто за ними ухаживает. Давайте подробнее рассмотрим это условие, а также то, как LIAD Center предлагает поддержку.
Что такое синдром Вернике-Корсакова?
Как мы ранее упоминали, WKS на самом деле состоит из двух различных состояний, которые часто встречаются вместе:
- Энцефалопатия Вернике
- Синдром Корсакова
Синдром Корсакова имеет тенденцию развиваться по мере исчезновения симптомов, связанных с Вернике. Болезнь Вернике вызывает повреждение нижних отделов мозга, называемых гипоталамусом и таламусом. С другой стороны, психоз Корсакова вызван необратимым повреждением частей мозга, связанных с памятью.
Хотя условия разные, оба они вызваны повреждением головного мозга в результате дефицита витамина B1 или тиамина. Этот дефицит относительно часто встречается у людей, страдающих алкогольным расстройством, а также у тех, чей организм не может должным образом усваивать пищевые питательные вещества.
Какие симптомы связаны с Вернике-Корсаковым?
WKS часто характеризуется симптомами слабоумия, наиболее заметным из которых обычно является спутанность сознания. Специфические симптомы, связанные с энцефалопатией Вернике, включают:
- Снижение остроты зрения и спутанность сознания, которая может привести к коме и смерти
- Аномальные движения глаз и другие изменения зрения, такие как опущенное веко и двоение в глазах.
- Снижение координации мышц, которое может привести к тремору ног
- Алкогольная абстиненция
Симптомы синдрома Корсакова могут включать:
- Проблемы с формированием или сохранением новых воспоминаний
- Рассказывание выдуманных историй (конфабуляция)
- Галлюцинации
Факторы риска и причины WKS
Диета и образ жизни — два основных фактора риска, связанных с WKS. Кроме того, основными факторами риска развития WKS являются хроническое злоупотребление алкоголем и недоедание.При хроническом злоупотреблении алкоголем организм может препятствовать правильному усвоению витамина B1, что способствует этому заболеванию мозга. Другие факторы риска, связанные с WKS, включают:
- Недоедание
- Расстройства иммунной системы, которые могут повлиять на всасывание витамина B1, например СПИД
- Регулярный диализ почек, который также снижает абсорбцию тиамина
Причины WKS
Несомненно, число Одной из причин синдрома Вернике-Корсакова является алкоголизм.Эта связь может быть объяснена тем, что люди, страдающие алкоголизмом, обычно придерживаются худшего рациона. Менее распространенные причины Вернике-Корсакова включают состояния, ограничивающие усвоение пищи, такие как:
- Рак толстой кишки, вызывающий дискомфорт при приеме пищи
- Рак желудка, который может ограничивать всасывание пищи
- Операция обходного желудочного анастомоза, которая может затруднить соблюдение питания потребности из-за меньшего размера порции пищи
- Расстройства пищевого поведения.
Как поставить диагноз
Слишком часто WKS ошибочно принимают за болезнь Альцгеймера или другой тип деменции. Это может замедлить процесс получения надлежащего лечения. Диагностика обычно включает тщательное физическое обследование и изучение истории болезни. Ваш любимый человек также может быть обследован на предмет алкоголизма. Если есть подозрение на недостаточное питание, для подтверждения могут быть проведены тесты на питание. Существует два основных теста такого рода:
- Тест сывороточного альбумина: Этот тест измеряет уровни белка в крови, связанные с дефицитом питательных веществ, а также проблемами с печенью и почками, которые могут повлиять на усвоение пищи.
- Тест на витамин B1 в сыворотке: Цель этого теста — проверить уровень B1 в крови. Это делается путем анализа активности ферментов — низкие уровни указывают на дефицит B1.
Поскольку диагностика WKS часто выполняется путем исключения, можно также провести дополнительное тестирование. Некоторые из них могут включать компьютерную томографию или МРТ для выявления изменений или аномалий головного мозга. Электрокардиограмма может быть проведена до и после приема витамина B1, чтобы увидеть, есть ли связь.
Как обращаются с WKS?
Если симптомы тяжелые, начальное лечение WKS может включать госпитализацию. В этом случае B1 можно вводить внутривенно или перорально. Также часто рекомендуется сбалансированная диета для увеличения абсорбции B1 и восстановления нормального уровня. В некоторых случаях вашему любимому человеку может потребоваться отдельное лечение от алкоголизма.
Что касается прогнозов, своевременное лечение может обратить вспять неврологические симптомы, связанные с WKS.Однако реакция на лечение также будет зависеть от таких факторов, как время, когда заболевание было впервые диагностировано, и насколько далеко оно было в то время. Если не лечить, WKS может вызвать необратимое повреждение мозга.
В любом случае наиболее эффективным способом предотвращения WKS является сбалансированная диета, включающая продукты, богатые витамином B1. Варианты включают нежирную свинину, цельнозерновой хлеб, горох, яркие фрукты и зеленые листовые овощи. Кроме того, призовите своих близких избегать чрезмерного употребления алкоголя и побудите их получить доступ к лечению, которое им необходимо при злоупотреблении алкоголем; и будьте активны в отношении любых заметных изменений умственных способностей.
Связаться с Центром деменции на Лонг-Айленде
Если у вас есть близкий человек, страдающий синдромом Вернике-Корсакова, Центр болезни Альцгеймера и слабоумия на Лонг-Айленде предлагает широкий спектр услуг по поддержке.
Свяжитесь с нами сегодня, чтобы узнать больше о том, как мы можем помочь, позвонив по телефону (516) 767-6856 или посетив наш веб-сайт www.lidementia.org.
Почему врачи должны быть более бдительными при диагностике и лечении энцефалопатии Вернике
Аномальные движения глаз.Нетвердая походка. Бред. Более века врачи использовали эту триаду симптомов для диагностики энцефалопатии Вернике (также называемой синдромом Вернике-Корсакова), неврологического состояния, вызванного дефицитом витаминов группы B, таких как тиамин.
Те, кто страдает алкогольными расстройствами или недоедают, подвергаются наибольшему риску развития этого состояния, говорит Карин Нойфельд , клинический директор психиатрии в Медицинском центре Джона Хопкинса Бэйвью, которая недавно прочитала лекцию Grand Rounds на эту тему.Но сегодня врачи должны думать не только о триаде, но и подозревать болезнь Вернике у любого пациента из группы риска, имеющего один или несколько симптомов. По ее словам, быстрое лечение высокими дозами тиамина может обратить симптомы вспять: «Если на фоне алкоголизма есть делирий, заподозрите синдром Вернике-Корсакова». Презентация может включать широкий спектр симптомов, включая потерю слуха; затруднение глотания; утомляемость и апатия; нарушения памяти и настроения, такие как амнезия, раздражительность или психоз; нарушения возбуждения, включая апноэ во сне и сонливость; полинейропатия; переохлаждение; гипергидроз и лактоацидоз.
«Вероятно, можно с уверенностью сказать, что мы упускаем случаи, которые наблюдаются в условиях неотложной больницы и за ее пределами», — говорит Нойфельд. «Отчасти это связано с признанием. Но также может быть, что мы наблюдаем больше случаев болезни Вернике из-за того, что все больше людей подвергаются хирургическим процедурам для похудания. Все, что снижает усвоение питательных веществ, подвергает вас большему риску ». Один из сотрудников Нойфельда видел пациентку, у которой местный невролог диагностировал деменцию Альцгеймера, но на самом деле у нее была болезнь Вернике.С лечением все изменилось. Нойфельд отмечает, что ей сделали резекцию кишечника и она много пила.
«Что действительно круто в болезни Вернике, так это то, что если у вас есть глазные патологии, эти глазные признаки исчезнут в течение нескольких часов или суток после введения высоких доз тиамина», — говорит она. Проблемы с походкой исчезают в течение нескольких дней или недель, и даже проблемы с памятью исчезают со временем, хотя обычно это происходит в течение недель или месяцев. «Многие пациенты Вернике, не получающие лечения, попадают в дома престарелых, поэтому крайне важно, чтобы мы более агрессивно подходили к лечению.”
Мозгу необходим постоянный поток тиамина для эффективной работы, говорит Нойфельд, но тело может хранить только 30 миллиграммов за один раз. Хотя в США нет установленного протокола для инфузий тиамина, текущее мнение, основанное на протоколах Соединенного Королевства, состоит в том, чтобы вводить три дозы по 500 миллиграммов внутривенно в течение двух-трех дней, говорит Нойфельд, а затем 100 миллиграммов перорально три раза в день для оставшаяся часть пребывания пациента в больнице или во время амбулаторного лечения до исчезновения симптомов.
Медицинский консьерж
Johns Hopkins предлагает бесплатную помощь в записи на прием и в планировании поездки. Запросить бесплатную помощь:
Все поля обязательны *
Синдром Вернике-Корсакова — Фонд детской неврологии
Описание
Энцефалопатия Вернике — дегенеративное заболевание головного мозга, вызванное недостатком тиамина (витамина B1).Это может быть результатом злоупотребления алкоголем, недостатка питания, продолжительной рвоты, расстройств пищевого поведения или последствий химиотерапии. Дефицит B1 вызывает повреждение таламуса и гипоталамуса головного мозга. Симптомы включают спутанность сознания, проблемы со зрением, кому, переохлаждение, низкое кровяное давление и нарушение координации мышц (атаксия). Синдром Корсакова (также называемый амнезическим синдромом Корсакова) — это нарушение памяти, которое возникает в результате дефицита витамина B1 и связано с алкоголизмом. Синдром Корсакова повреждает нервные клетки и поддерживающие клетки головного и спинного мозга, а также часть мозга, отвечающую за память.Симптомы включают амнезию, тремор, кому, дезориентацию и проблемы со зрением. Основными особенностями расстройства являются проблемы с получением новой информации или установлением новых воспоминаний, а также с восстановлением предыдущих воспоминаний. Хотя болезни Вернике и Корсакова являются родственными расстройствами, некоторые ученые полагают, что это разные стадии одного и того же расстройства, которое называется синдромом Вернике-Корсакова. Энцефалопатия Вернике представляет собой «острую» фазу расстройства, а амнестический синдром Корсакова представляет собой расстройство, прогрессирующее до «хронической» или длительной стадии.
Лечение
Лечение включает замену тиамина и обеспечение правильного питания и гидратации. В некоторых случаях также рекомендуется медикаментозная терапия. Прекращение употребления алкоголя может предотвратить дальнейшее повреждение нервов и головного мозга. У людей с энцефалопатией Вернике очень важно начать заместительную терапию тиамином до начала восполнения питательных веществ.
Прогноз
Большинство симптомов энцефалопатии Вернике можно обратить вспять, если выявлять и лечить быстро и полностью.Прекращение употребления алкоголя может предотвратить дальнейшее повреждение нервов и головного мозга. Однако улучшение функции памяти происходит медленно и, как правило, не полностью. Без лечения эти расстройства могут привести к инвалидности и угрозе для жизни.
Исследования
Национальный институт неврологических расстройств и инсульта поддерживает исследования по неврологическим расстройствам, таким как энцефалопатия Вернике, амнезический синдром Корсакова и синдром Вернике-Корсакова, чтобы расширить наше понимание функциональных изменений заболеваний и способов их лечения.

 , 1997)
, 1997) — 2014 — С.76-80
— 2014 — С.76-80 При этом сохраняется способность к восприятию простых речевых конструкций;
При этом сохраняется способность к восприятию простых речевых конструкций;

 Дефицит тиамина имеет следующие последствия:
Дефицит тиамина имеет следующие последствия: (32551830) В контексте острого или хронического заболевания дефицит может возникнуть быстрее.
(32551830) В контексте острого или хронического заболевания дефицит может возникнуть быстрее.

 , сепсис, системное воспаление, гипертиреоз)
, сепсис, системное воспаление, гипертиреоз)
 (26771781)
(26771781) Основная роль — исключить альтернативной этиологии.
Основная роль — исключить альтернативной этиологии. (323)
(323) Следовательно, требуется клиническая оценка.
Следовательно, требуется клиническая оценка. , больные алкоголизмом или недоеданием). Подробнее о факторах риска дефицита тиамина выше.
, больные алкоголизмом или недоеданием). Подробнее о факторах риска дефицита тиамина выше.
 и позволяют сократить расходы. Имеющиеся данные показывают, что частота энцефалопатии Вернике значительно превышает 0.05%, что может сделать профилактику логичным вмешательством. (24666443)
и позволяют сократить расходы. Имеющиеся данные показывают, что частота энцефалопатии Вернике значительно превышает 0.05%, что может сделать профилактику логичным вмешательством. (24666443) (22305197)
(22305197)
 Одного или двух дней внутривенного введения тиамина недостаточно!
Одного или двух дней внутривенного введения тиамина недостаточно! Алкоголь Алкоголь. 1988; 23 (1): 49-52 [PubMed]
Алкоголь Алкоголь. 1988; 23 (1): 49-52 [PubMed] В., Андерсен Л.В., Чейз М., Берг К.М., Тидсвелл М., Гиберсон Т., Вулф Р., Московиц А., Смитлайн Н., Нго Л., Кокки Миннесота; Научно-исследовательская группа Центра реанимации.Рандомизированное, двойное слепое, плацебо-контролируемое исследование тиамина как метаболического реанимационного средства при септическом шоке: пилотное исследование. Crit Care Med. 2016 Февраль; 44 (2): 360-7. DOI: 10.1097 / CCM.0000000000001572 [PubMed]
В., Андерсен Л.В., Чейз М., Берг К.М., Тидсвелл М., Гиберсон Т., Вулф Р., Московиц А., Смитлайн Н., Нго Л., Кокки Миннесота; Научно-исследовательская группа Центра реанимации.Рандомизированное, двойное слепое, плацебо-контролируемое исследование тиамина как метаболического реанимационного средства при септическом шоке: пилотное исследование. Crit Care Med. 2016 Февраль; 44 (2): 360-7. DOI: 10.1097 / CCM.0000000000001572 [PubMed] DOI: 10.4212 / cjhp.v70i3.1657 [PubMed]
DOI: 10.4212 / cjhp.v70i3.1657 [PubMed] П., Эли Е.В. Стоимость делирия и комы в отделении интенсивной терапии у пациента отделения интенсивной терапии. Med Care. Октябрь 2018; 56 (10): 890-897. DOI: 10.1097 / MLR.0000000000000975 [PubMed]
П., Эли Е.В. Стоимость делирия и комы в отделении интенсивной терапии у пациента отделения интенсивной терапии. Med Care. Октябрь 2018; 56 (10): 890-897. DOI: 10.1097 / MLR.0000000000000975 [PubMed] DOI: 10.1177 / 0004563220939604 [PubMed]
DOI: 10.1177 / 0004563220939604 [PubMed]