Эпителиопатия роговицы
Рецидивирующая эрозия роговицы — это заболевание, связанное с самым наружным слоем клеток роговицы, называемым эпителием. Оно связано со слабостью прикрепления эпителия к подлежащему слою роговицы — боуменовой оболочке, что приводит к его легкому слущиванию. Боль и дискомфорт часто довольно интенсивны, схожие с таковыми при попадании инородного тела в глаз. Наиболее часто рецидивирующая эрозия роговицы развивается после травмы роговицы или как осложнение дистрофии роговицы.
Утром, при открытии глаз пациенты часто испытывают резкую боль, размытое зрение, слезотечение и светобоязнь. Это происходит потому, что веки при открытии глаз сдирают слабо прикрепленный эпителий с боуменовой оболочки. Как следует из названия заболевания, через некоторое время после заживления образуются новые эрозии. Рецидивирующая эрозия роговицы может поражать один или оба глаза в зависимости от вызвавшей ее причины.
Признаки (симптомы)
-
Сильная боль в глазу (особенно при подъеме утром) -
Низкое зрение -
Чувство инородного тела -
Сухость и раздражение -
Слезотечение -
Покраснение глаза -
Светобоязнь
Диагностика
Используя щелевую лампу, доктор исследует роговицу под большим увеличением. Красящий раствор флюоресцина используется для прокрашивания эрозии и более четкого определения ее расположения, глубины и протяженности.
Красящий раствор флюоресцина используется для прокрашивания эрозии и более четкого определения ее расположения, глубины и протяженности.
Лечение
Солевые растворы в каплях назначаются как первый этап лечения. Эти препараты помогают более крепкому прикреплению эпителия к боуменовой оболочке. Искусственная слеза и питательные гели и мази используется для лучшего, соответственно, смачивания и питания роговицы.
При частых рецидивах и неэффективном лечении улучшение может быть получено фототерапевтической кератэктомией (ФТК). Эта операция схожа с фоторефракционной кератэктомией (ФРК), выполняемой при близорукости, астигматизме и дальнозоркости , и выполняется с помощью эксимерного лазера для удаления эпителия роговицы и воздействия на боуменову оболочку для стимуляции нормального заживления.
Контактные линзы: правила пользования — Latvijas Amerikas acu centrs
Каждый из нас желает видеть окружающий мир четко и в мелких деталях, наслаждаясь качеством жизни, которое нам предоставляет хорошее зрение.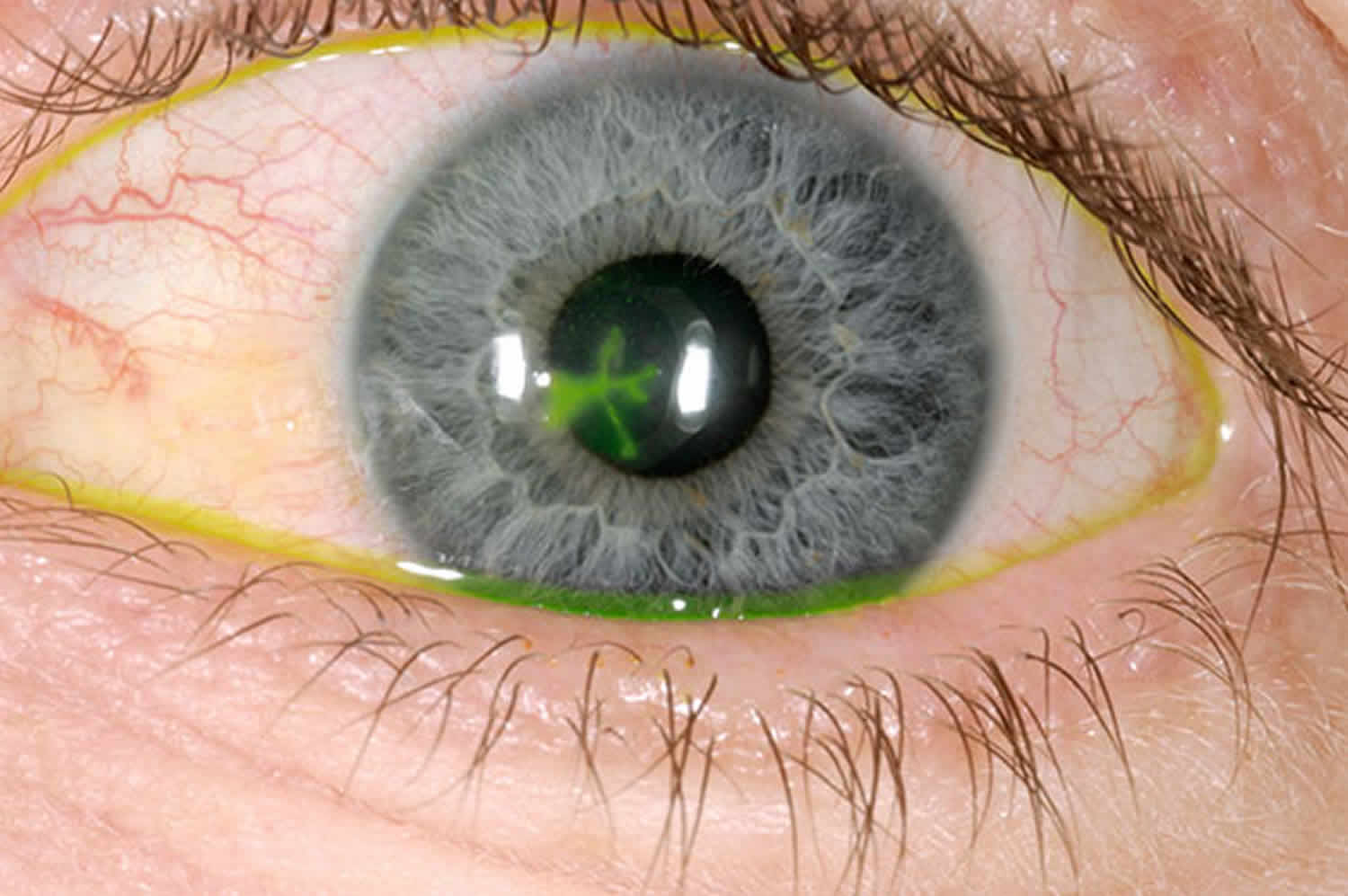 Зачастую, для того чтобы это обеспечить, выбор падает на контактные линзы. Прообраз современных контактных линз ведет свое начало с 16-го века, когда Леонардо да Винчи нарисовал свою идею о способе коррекции плохого зрения. Первые контактные линзы были сделаны гораздо позже — только через 300 лет. Они были сделаны из стекла, которое не было удобным и безопасным материалом.
Зачастую, для того чтобы это обеспечить, выбор падает на контактные линзы. Прообраз современных контактных линз ведет свое начало с 16-го века, когда Леонардо да Винчи нарисовал свою идею о способе коррекции плохого зрения. Первые контактные линзы были сделаны гораздо позже — только через 300 лет. Они были сделаны из стекла, которое не было удобным и безопасным материалом.
В настоящее время более 125 миллионов человек во всем мире не могут представить свою жизнь без контактных линз. Для того, чтобы контактные линзы были безопасны для ношения, необходимо понимать и соблюдать правила их использования.
1-ое правило – Правильный уход, хранение, установка, снятие контактных линз – в зависимости от типа контактных линз эти правила могут различаться, но при первой покупке контактных линз клиенту всегда разъясняются основные принципы их использования. После извлечения контактных линз из упаковки их всегда следует хранить только в контейнере для контактных линз, к тому же учитывая пространство, предусмотренное для каждой линзы.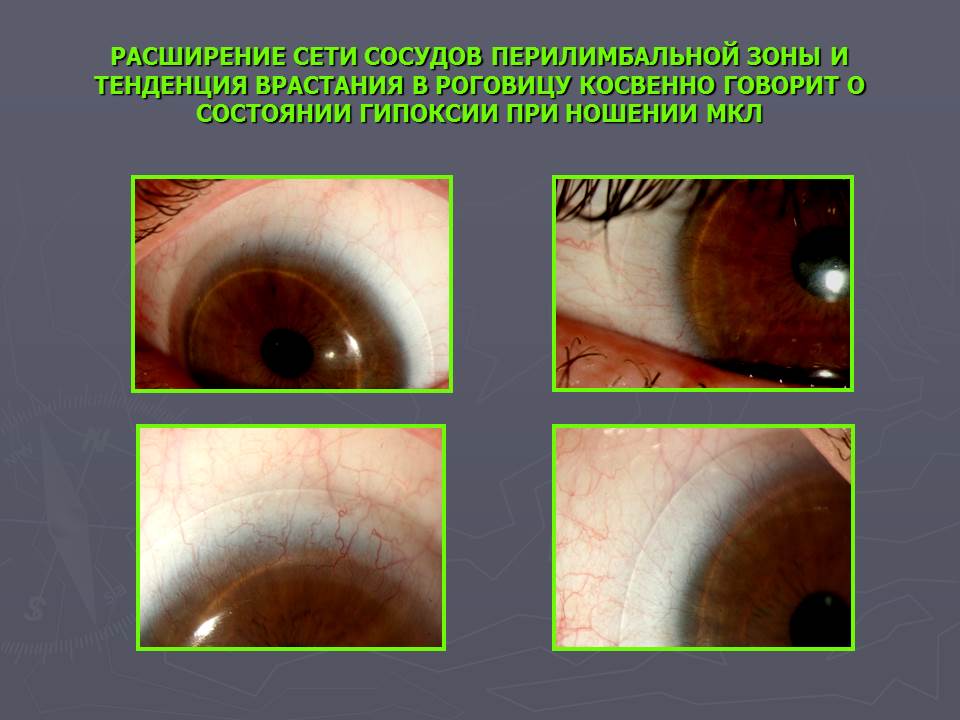 После каждого использования контактные линзы должны быть механически очищены и промыты дезинфицирующим средством для контактных линз, а затем помещены в контейнер до следующего раза использования. Контейнер для хранения контактных линз всегда следует очищать и промывать дезинфицирующим средством для контактных линз. Контейнерный раствор следует регулярно менять. Цель дезинфицирующего средства для контактных линз — снизить до минимума концентрацию микробов в линзе. Обязательно соблюдайте правила использования как контактных линз, так и дезинфицирующего средства, например, их нельзя оставлять на солнце. Солнце и тепло создают благоприятные условия для размножения бактерий, тем самым увеличивая риск попадания инфекции в глаза. При чистке, установке и снятии контактных линз следует соблюдать правила личной гигиены — тщательно мыть руки перед любыми манипуляциями с контактными линзами. Целью этих правил является снижение риска развития инфекции глаз.
После каждого использования контактные линзы должны быть механически очищены и промыты дезинфицирующим средством для контактных линз, а затем помещены в контейнер до следующего раза использования. Контейнер для хранения контактных линз всегда следует очищать и промывать дезинфицирующим средством для контактных линз. Контейнерный раствор следует регулярно менять. Цель дезинфицирующего средства для контактных линз — снизить до минимума концентрацию микробов в линзе. Обязательно соблюдайте правила использования как контактных линз, так и дезинфицирующего средства, например, их нельзя оставлять на солнце. Солнце и тепло создают благоприятные условия для размножения бактерий, тем самым увеличивая риск попадания инфекции в глаза. При чистке, установке и снятии контактных линз следует соблюдать правила личной гигиены — тщательно мыть руки перед любыми манипуляциями с контактными линзами. Целью этих правил является снижение риска развития инфекции глаз.
2-ое правило – правильное ношение контактных линз. Следует соблюдать режим использования контактных линз. Каждая контактная линза в зависимости от материала и толщины (определяется диоптрией) имеет свою воздухопроницаемость. И наоборот, если контактные линзы носят дольше, чем предписано, снабжение роговицы кислородом снижается, и возникает отек роговицы (помутнение зрения, которое также можно не заметить), что в случае длительного воздействия приводит к неоваскуляризации роговицы или к росту новообразованных кровеносных сосудов на периферии роговицы. Вот почему нельзя спать, не снимая контактные линзы, потому что во сне естественным образом без контактных линз, снабжение роговицы кислородом уже снижено. Необходимо соблюдать режим использования контактных линз. При помещении контактной линзы в глаз, она воспринимается как посторонний объект, когда из слез к ней прилипают белки, она становится биосовместимой с человеческим глазом, но чем дольше продолжительность ношения контактных линз, тем больше образуется этих отложений (включая жиры, пыль и др.
Следует соблюдать режим использования контактных линз. Каждая контактная линза в зависимости от материала и толщины (определяется диоптрией) имеет свою воздухопроницаемость. И наоборот, если контактные линзы носят дольше, чем предписано, снабжение роговицы кислородом снижается, и возникает отек роговицы (помутнение зрения, которое также можно не заметить), что в случае длительного воздействия приводит к неоваскуляризации роговицы или к росту новообразованных кровеносных сосудов на периферии роговицы. Вот почему нельзя спать, не снимая контактные линзы, потому что во сне естественным образом без контактных линз, снабжение роговицы кислородом уже снижено. Необходимо соблюдать режим использования контактных линз. При помещении контактной линзы в глаз, она воспринимается как посторонний объект, когда из слез к ней прилипают белки, она становится биосовместимой с человеческим глазом, но чем дольше продолжительность ношения контактных линз, тем больше образуется этих отложений (включая жиры, пыль и др.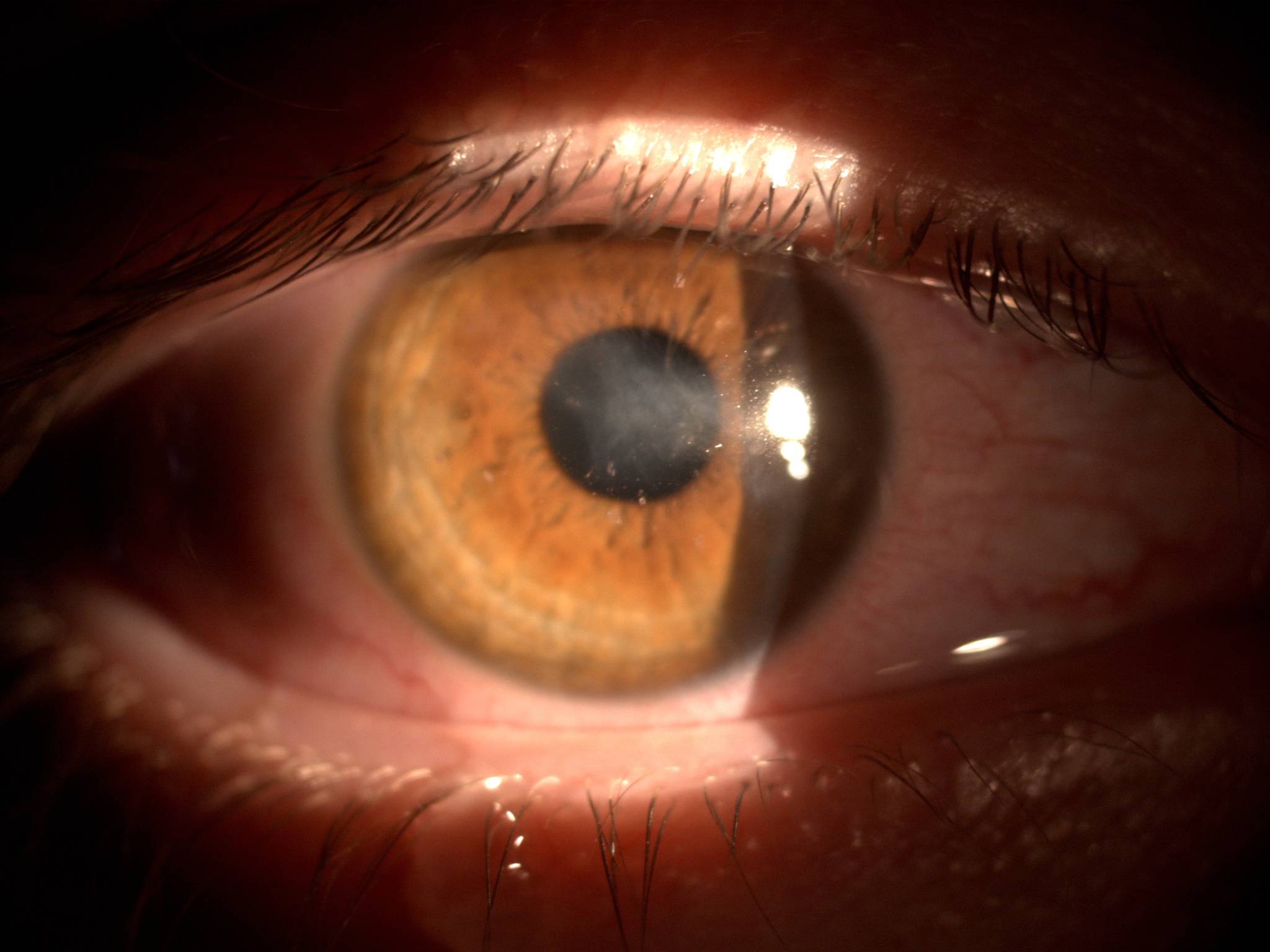 ), что приводит к снижению воздухопроницаемости контактных линз (снижается снабжение роговицы кислородом), линза поглощает меньше влаги и снижается прозрачность (помутнение зрения). Со временем белки на линзе денатурируют (разлагаются), и линза снова воспринимается как инородное тело — она начинает мешать и вызывать дискомфорт.
), что приводит к снижению воздухопроницаемости контактных линз (снижается снабжение роговицы кислородом), линза поглощает меньше влаги и снижается прозрачность (помутнение зрения). Со временем белки на линзе денатурируют (разлагаются), и линза снова воспринимается как инородное тело — она начинает мешать и вызывать дискомфорт.
3-е правило – уход за глазами. КЛ предусмотрены для здоровых глаз. Подача кислорода к роговице (около 21% в течение дня) обеспечивает слезная пленка, в то время как КЛ распределяет слезную пленку и нарушает ее нормальную структуру, она становится тоньше, быстро высыхает, в то время как сухая поверхность роговицы и линза создают дискомфорт, а сухая мягкая КЛ уменьшает подачу воздуха к роговице, потому что поры в ней заблокированы вышеупомянутыми белками. Следовательно, следует своевременно позаботиться об увлажнении глаза, используя искусственные слезы несколько раз в день (если КЛ находится в глазу, используйте искусственные слезы, которые предназначены для использования непосредственно во время ношения КЛ, чтобы избежать образования отложений на КЛ, после снятия КЛ рекомендуется использовать эпителизирующий гель или мазь, которые заживляют микротравмы роговицы, которые образуются при установке и удалении КЛ из глаза). Поэтому, пользователи КЛ входят в группу риска синдрома сухого глаза, конечно, если к тому же существуют усиливающие риск обстоятельства или заболевания, которые способствуют развитию синдрома сухого глаза (сухой воздух в помещении, кондиционеры, работа с компьютером, заболевания щитовидной железы и др.), образование синдрома сухого глаза неизбежно, поэтому важно его увлажнять. Ярко выраженный синдром сухого глаза и ношение КЛ может привести к эпителиопатии роговицы или к небольшим дефектам эпителия роговицы, которые окрашены специальным красящим флуоресцином. В таких случаях обычно проявляются симптомы синдрома сухого глаза и может также возникнуть слезоточивость, что иногда зависит от индивидуальной чувствительности пациента. В таких случаях следует прекратить использование КЛ, чтобы избежать инфекции. Таким образом, пользователи КЛ с выраженными симптомами синдрома сухого глаза (ощущение присутствия инородного тела, как будто песок в глазах, дискомфорт, слезоточивость на солнце, при сильном ветре, усиленное моргание и покраснение глаз) должны обратиться к врачу.
Поэтому, пользователи КЛ входят в группу риска синдрома сухого глаза, конечно, если к тому же существуют усиливающие риск обстоятельства или заболевания, которые способствуют развитию синдрома сухого глаза (сухой воздух в помещении, кондиционеры, работа с компьютером, заболевания щитовидной железы и др.), образование синдрома сухого глаза неизбежно, поэтому важно его увлажнять. Ярко выраженный синдром сухого глаза и ношение КЛ может привести к эпителиопатии роговицы или к небольшим дефектам эпителия роговицы, которые окрашены специальным красящим флуоресцином. В таких случаях обычно проявляются симптомы синдрома сухого глаза и может также возникнуть слезоточивость, что иногда зависит от индивидуальной чувствительности пациента. В таких случаях следует прекратить использование КЛ, чтобы избежать инфекции. Таким образом, пользователи КЛ с выраженными симптомами синдрома сухого глаза (ощущение присутствия инородного тела, как будто песок в глазах, дискомфорт, слезоточивость на солнце, при сильном ветре, усиленное моргание и покраснение глаз) должны обратиться к врачу.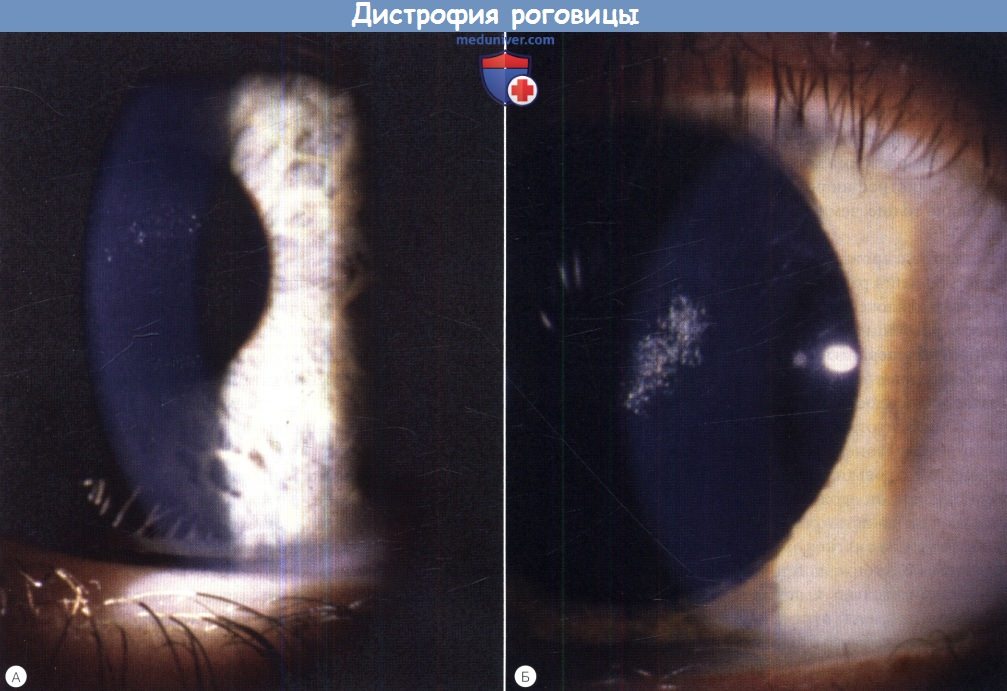
Нельзя ложиться спать, не сняв КЛ, потому что во время сна в результате давления века КЛ прижимается ближе к роговице и часто прилипает к ней, в таких случаях состояние роговицы ухудшается еще больше (она становится очень сухой, возникает эпителиопатия или в особо тяжелых случаях кератит или воспаление роговицы). Также основное правило использования ночных линз (в результате использования специальных КЛ в ночное время меняется изгиб роговицы, и использование средств для коррекции зрения в течение дня не требуется) — это здоровые глаза с хорошей слезной пленкой. При скольжении век по краям КЛ (когда глаза моргают), конъюнктива век воспаляется и вызывает хроническое раздражение и воспаление конъюнктивы век, которое выражается в виде гиперемии век (покраснение), фолликулярной реакции (неровная поверхность слизистой оболочки), что может вызвать чувство дискомфорта. По этим причинам следует избегать длительного ношения КЛ и чаще давать возможность глазам отдохнуть от КЛ, например, по выходным, если вы являетесь постоянным пользователем КЛ.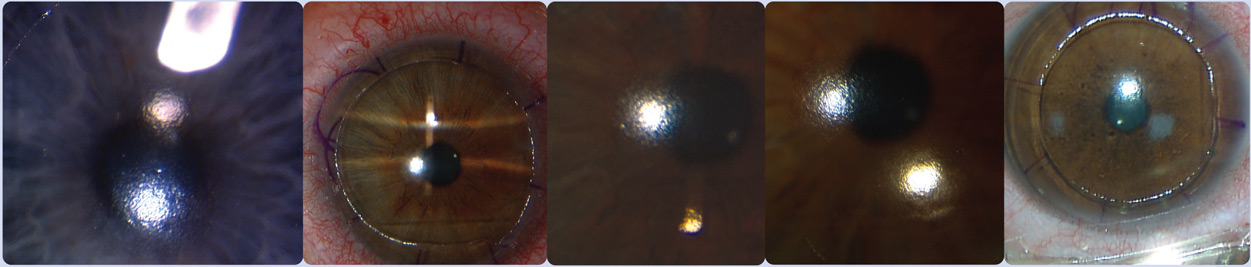 В случае обострения неприятных симптомов всегда следует обратиться к глазному врачу, контроль у глазного врача пользователь КЛ должен проходить 1-2 раза в год.
В случае обострения неприятных симптомов всегда следует обратиться к глазному врачу, контроль у глазного врача пользователь КЛ должен проходить 1-2 раза в год.
4-ое правило – не снимая КЛ, категорически запрещено: купаться (в бассейне, озере, реке, море, океане). В водоемах живет множество опасных микроорганизмов (напр., pseudomona aeruginosa, acanthaomeba), которые проникают в глаза, за контактную линзу, и обычно там задерживаются потому, что из-за КЛ при моргании глаза слезная пленка полностью не восстанавливается, и если в результате снятия КЛ появляются небольшие микротравмы, то это место и время, благоприятное для развития инфекции. Занятия спортом на пляже. Во-первых, когда песчинки попадают в глаз и за контактную линзу, они вызывают эрозию роговицы (дефект верхнего слоя роговицы или эпителия), во-вторых, в песке много микроорганизмов, в том числе грибков, которые очень опасны в случае развития глазной инфекции. Также нежелательно выполнять работы по уборке в подвалах, туалетах и других местах, где потенциально может присутствовать грибок и другие опасные микроорганизмы.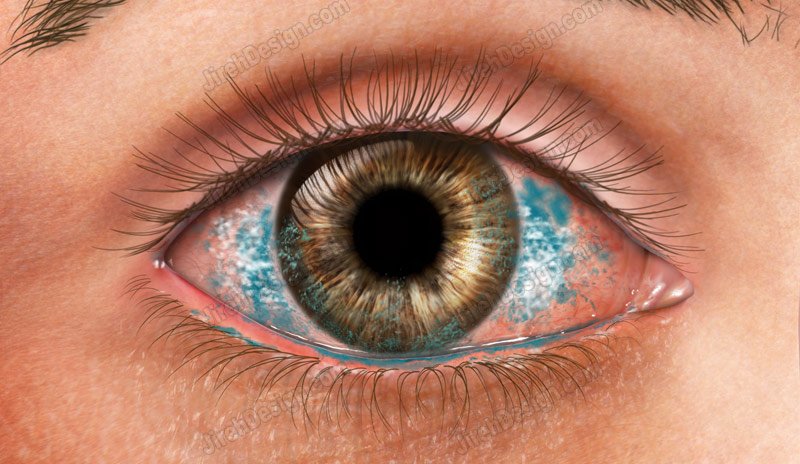
Если в глазу имеется бактериальная инфекция, это очень неприятно (глаз покалывает, болит, слезится, зрение размыто, могут быть покраснения и выделения из глаз), но обычно относительно легко поддается лечению с антибактериальными препаратами. Если в глазу развивается грибковая инфекция, состояние глаза относительно спокойное (зуд, слезы, но часто меньше покраснений и не болят). Грибковый кератит трудно поддается лечению. Зачастую возникают сложности биомикроскопически дифференцировать бактериальный кератит от грибкового кератита, и в этих случаях помогает исследование бактериологического образца, который взят из конъюнктивального мешка или роговицы. Если вовремя не лечить кератит, в роговице может развиться более глубокий дефект роговицы, даже язва роговицы.
В случае подозрения на анамнестический и биомикроскопический грибковый кератит немедленно начинают эмпирическую противогрибковую терапию локально в каплях и / или внутривенно, в более тяжелых случаях требуется стационарное лечение. В тяжелых случаях при развитии инфекции могут быть применены интрастромальные инфильтрации противогрибковых медикаментов (в более глубоких слоях роговицы) или прием лекарств, терапевтическая кератопластика или вырезание поврежденного фрагмента роговицы и замена донорской роговицей, и если процесс зашел слишком далеко, и не помогает ни один из вышеперечисленных вариантов, можно использовать более обширное хирургическое вмешательство.
В тяжелых случаях при развитии инфекции могут быть применены интрастромальные инфильтрации противогрибковых медикаментов (в более глубоких слоях роговицы) или прием лекарств, терапевтическая кератопластика или вырезание поврежденного фрагмента роговицы и замена донорской роговицей, и если процесс зашел слишком далеко, и не помогает ни один из вышеперечисленных вариантов, можно использовать более обширное хирургическое вмешательство.
Ношение контактные линзы строго запрещено, если глаза воспалены.
В некоторых случаях заболеваний глаз под наблюдением врача КЛ используются в терапевтических целях.
Будьте осторожны!
Роговица и ее изменение при сахарном диабете | Бикбов
Сахарный диабет (СД) – самое распространенное эндокринное заболевание населения экономически развитых стран [1, 2]. В 2014 г. в мире было зарегистрировано более 387 млн больных СД. В России на 2015 г. было зарегистрировано более 4 млн пациентов с СД, и это число постоянно увеличивается. По данным И.И. Дедова с соавт. (2016), среди взрослого населения России почти у 20% наблюдается предиабет, еще более чем 2 млн человек не подозревают о своем диагнозе [1].
По данным И.И. Дедова с соавт. (2016), среди взрослого населения России почти у 20% наблюдается предиабет, еще более чем 2 млн человек не подозревают о своем диагнозе [1].
Нарушение углеводного обмена приводит к патологическим изменениям практически во всех органах и тканях, поэтому СД является одной из приоритетных медико-социальных проблем [3]. Гипергликемия – основная причина, запускающая биохимические, гемодинамические и структурные изменения в сосудах, нервах и органах. Ежегодно растет число больных с СД, нуждающихся в квалифицированной помощи офтальмологов. Из-за особой функциональной важности зрительного анализатора часто именно глазные проявления этого заболевания в первую очередь приводят к инвалидизации больных [4]. Как показывает практика, специалисты многих городских и районных поликлиник оказываются неподготовленными к работе с пациентами этого профиля.
До 20% слепых потеряли зрение из-за диабетического поражения глаз. Около 70% пациентов с СД имеют осложнения со стороны роговицы – диабетическую кератопатию (ДК) [5].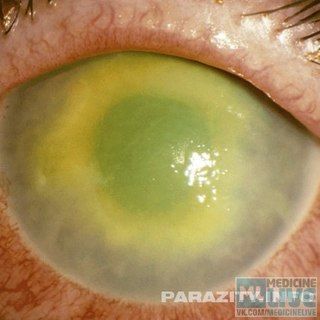 Учитывая тонкую архитектонику роговицы, диагностика ДК, особенно на ранних стадиях заболевания, не всегда представляется возможной. Тем не менее нарушение обменных процессов в организме при СД касается и этой важной оптической структуры глаза. Исследователи, описывая изменения глаз при диабете, чаще заостряют внимание на распространенном позднем осложнении – диабетической ретинопатии, упуская изменения роговицы. В литературе имеется немного данных о синдроме сухого глаза (ССГ) среди больных с СД, несмотря на то, что проблема очевидна и актуальна, учитывая то, что количество таких пациентов ежегодно увеличивается [6, 7].
Учитывая тонкую архитектонику роговицы, диагностика ДК, особенно на ранних стадиях заболевания, не всегда представляется возможной. Тем не менее нарушение обменных процессов в организме при СД касается и этой важной оптической структуры глаза. Исследователи, описывая изменения глаз при диабете, чаще заостряют внимание на распространенном позднем осложнении – диабетической ретинопатии, упуская изменения роговицы. В литературе имеется немного данных о синдроме сухого глаза (ССГ) среди больных с СД, несмотря на то, что проблема очевидна и актуальна, учитывая то, что количество таких пациентов ежегодно увеличивается [6, 7].
Диабетическая полинейропатия (ДПН) является наиболее распространенным осложнением СД, при которой происходит необратимая дисфункция нервов. Повреждение нервных волокон, в том числе и в роговице, может предшествовать развитию других осложнений СД и в ряде случаев быть первым клиническим признаком нарушения углеводного обмена. Крайне важно как можно раньше обнаружить изменение нервных волокон роговицы (НВР) для определения своевременной диагностики и выработки тактики лечения. Уместно, прежде всего, остановиться на анатомии роговицы.
Уместно, прежде всего, остановиться на анатомии роговицы.
Анатомия роговицы
Роговица – основная часть глазной поверхности («Ocular Surface»), которая также включает эпителий конъюнктивы, слезную пленку, веки и их железы, слезопродуцирующие и слезоотводящие органы. При СД могут возникнуть заболевания глазной поверхности – сложные по своей природе и многогранные по своим проявлениям [7].
Роговица имеет толщину 520–550 мкм и наибольшую преломляющую силу из всех внутриглазных структур (около 40,0 дптр). В норме она прозрачная, не имеет кровеносных сосудов [8, 9, 10]. Роговица содержит более 7000 чувствительных нервных окончаний на 1 мм2, тогда как кожа – около 2000 на 1 мм2 [11, 12]. Для обеспечения достаточного питания эпителиального слоя на 2,1 млн базальных клеток роговицы приходится до 1,4 млн нервных окончаний. Обильная иннервация роговицы представлена трофическими, чувствительными и вегетативными нервными волокнами [8]. Высокая чувствительность роговицы обеспечивается системой длинных цилиарных нервов (от глазничной ветви тройничного нерва), образующих перелимбальные нервные сплетения. Входя в роговицу, нервные волокна теряют миелиновую оболочку и становятся невидимыми, образуя суббазальное нервное сплетение между базальным эпителием и боуменовой мембраной. Нервы роговицы выглядят как тонкие ветвящиеся белые линии, идущие от лимба до передних и средних слоев стромы. При этом ход нервных волокон ориентирован параллельно коллагеновым фибриллам стромы [11].
Входя в роговицу, нервные волокна теряют миелиновую оболочку и становятся невидимыми, образуя суббазальное нервное сплетение между базальным эпителием и боуменовой мембраной. Нервы роговицы выглядят как тонкие ветвящиеся белые линии, идущие от лимба до передних и средних слоев стромы. При этом ход нервных волокон ориентирован параллельно коллагеновым фибриллам стромы [11].
Особенности анатомического строения позволяют использовать роговицу для оценки изменений периферической нервной системы, возникающих при СД [13–16].
Методы диагностики cостояния роговицы при СД
Комплексное исследование роговицы необходимо для своевременной диагностики и мониторинга ее заболеваний, динамического наблюдения за состоянием глаза при проведении кераторефракционных и интраокулярных операций [17].
Общеизвестны патоморфологические методы исследований: пункционная биопсия кожи, биопсия нервов и определение плотности эпидермальных нервных волокон в биоптатах кожи, которые могут быть использованы на доклинической стадии полинейропатии.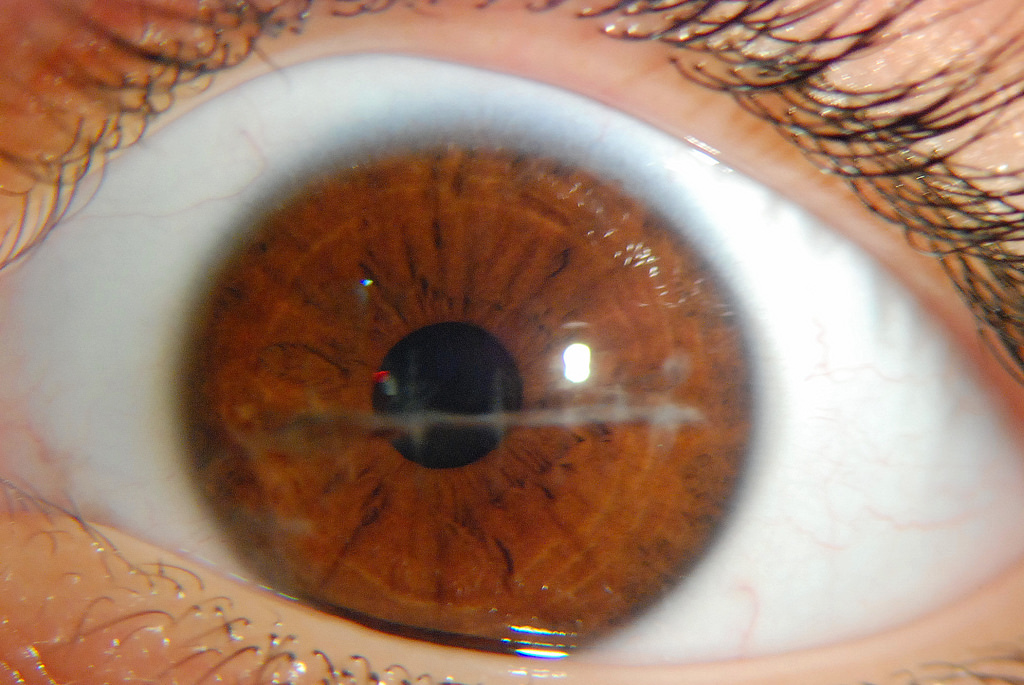 Лазерная допплеровская флюорометрия оценивает микроциркуляторное русло кожи: скорость кровотока и базальную температуру. Однако эти методы инвазивны и сопряжены с риском развития инфекционных осложнений. Кроме того, необходимость проведения данного исследования в патоморфологической лаборатории удлиняет период диагностики [18, 19].
Лазерная допплеровская флюорометрия оценивает микроциркуляторное русло кожи: скорость кровотока и базальную температуру. Однако эти методы инвазивны и сопряжены с риском развития инфекционных осложнений. Кроме того, необходимость проведения данного исследования в патоморфологической лаборатории удлиняет период диагностики [18, 19].
Для оценки архитектоники роговицы применяют биомикроскопию, зеркальную микроскопию эндотелия. Тонкой диагностике роговицы в последние годы способствовало появление новых диагностических методов: конфокальной микроскопии роговицы (КМР), оптической когерентной томографии, ультразвуковой биомикроскопии [20].
МР – неинвазивный прижизненный метод ее исследования при послойном сканировании используется в офтальмологии с 80-х гг. прошлого века и позволяет оценить на микроструктурном уровне состояние всех слоев оболочки [21, 22]. Этим методом на клеточном уровне выявляют различные виды эпителиопатии, нервные волокна и сплетения, микрострии, явление гомогенизации стромы, зоны с нарушением прозрачности и рубцевания, что можно использовать для диагностики ДПН [23, 24]. Предложены оценочные показатели нервов: расположение и ветвление, толщина, ширина, извитость, плотность и рефлективность [20, 25–27].
Предложены оценочные показатели нервов: расположение и ветвление, толщина, ширина, извитость, плотность и рефлективность [20, 25–27].
Оптическая когерентная томография, основанная на отражательной способности биологических структур, дает возможность провести качественные микроструктурные исследования, позволяющие оценить динамику развития и локализацию изменений в слоях роговицы при СД [28].
Измерение толщины роговицы и ее структур осуществляется с помощью современных ультразвуковых сканирующих кератопахиметров (Pentacam, Германия) [20].
Вошедший в офтальмологическую практику метод ультразвуковой биомикроскопии позволяет бесконтактно с высокой разрешающей способностью визуализировать структуры переднего сегмента глаза [29].
Клинико-морфологические изменения роговицы при СД
Вовлечение роговицы в патологический процесс обычно встречается на фоне уже выявленных симптомов СД. Bikbova G. и соавт. (2016) подробно описали патофизиологическую роль различных факторов, включая накопление в эндотелии продуктов гликирования, снижение активности аденозин-трифосфатазы и др.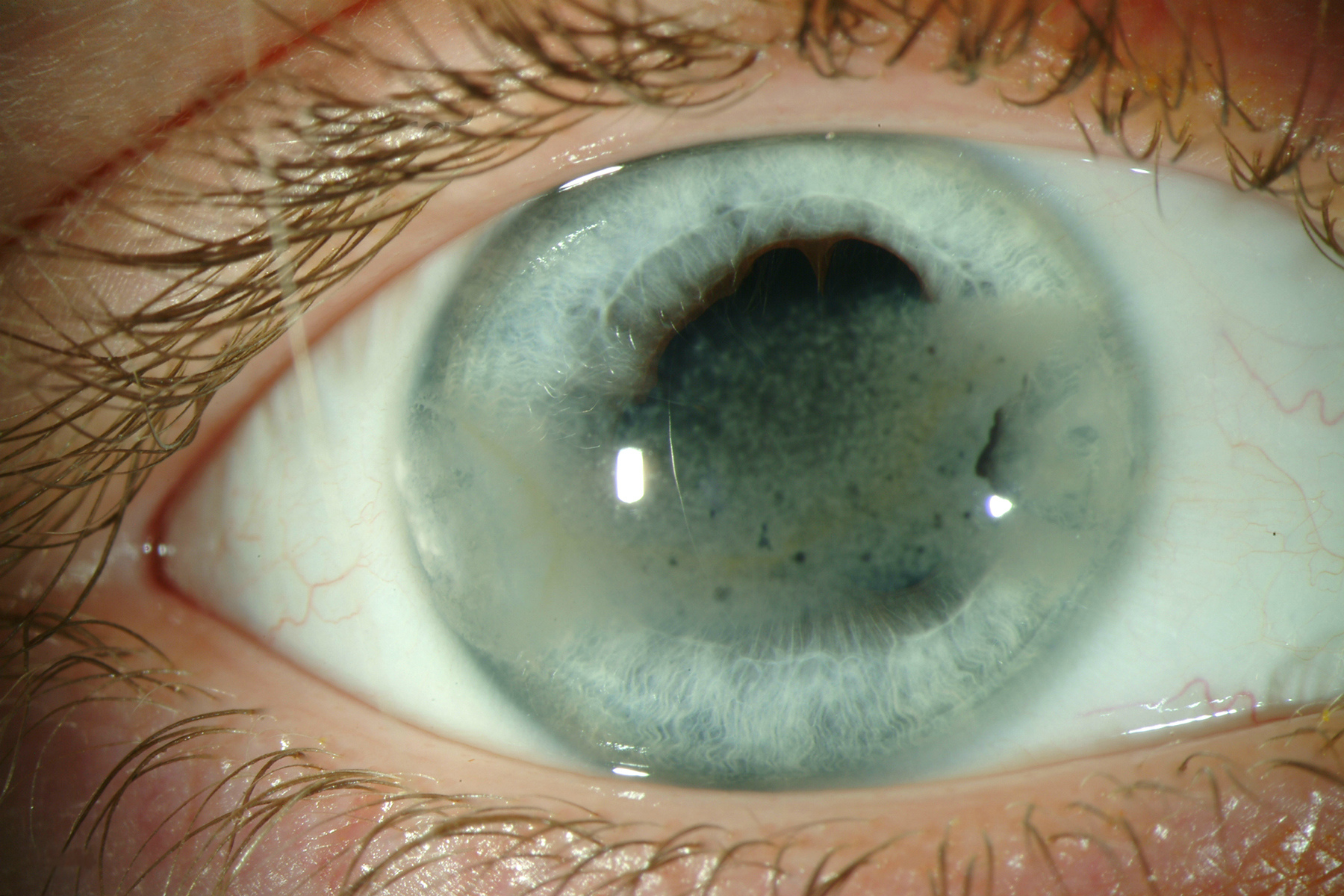 , в возникновении корнеальной кератопатии и эндотелиальной дисфункции роговицы при диабете [30]. При диабете страдают структурные слои роговицы: слезная пленка, передний и задний эпителий, строма, боуменовая и десцеметовая мембраны, обеспечивающие качество зрения. Глазные изменения при СД вторичны и возникают на основе прогрессирования основного заболевания [13, 25, 26].
, в возникновении корнеальной кератопатии и эндотелиальной дисфункции роговицы при диабете [30]. При диабете страдают структурные слои роговицы: слезная пленка, передний и задний эпителий, строма, боуменовая и десцеметовая мембраны, обеспечивающие качество зрения. Глазные изменения при СД вторичны и возникают на основе прогрессирования основного заболевания [13, 25, 26].
Эпителий роговицы при СД
Клинические изменения эпителия роговицы при диабете не специфичны, характеризуются субъективным дискомфортом различной степени выраженности при отсутствии заметных объективных проявлений и часто зависят от тяжести заболевания [5, 26].
При диабете нарушается качественное прикрепление эпителия к подлежащей базальной мембране. Поверхностные микродефекты имеют тенденцию к рецидивированию, в результате чего возникают эрозии. Последние являются причиной болевого синдрома, однако в связи с высокой скоростью регенерации эпителия в большинстве случаев этот период относительно непродолжительный. Заживление эпителиальных дефектов происходит неравномерно, они, как правило, приобретают неправильную конфигурацию. При глубоком разрушении стромы появляются десцеметоцеле или язвы роговицы, сопровождающиеся перфорацией [31]. Отличительной чертой последних являются отсутствие воспалительной реакции и превалирование расстройства обменных процессов, характерных для диабета [32]. Анамнез, продолжительность и динамическое наблюдение за пациентами с СД являются основными факторами для диагностики.
Заживление эпителиальных дефектов происходит неравномерно, они, как правило, приобретают неправильную конфигурацию. При глубоком разрушении стромы появляются десцеметоцеле или язвы роговицы, сопровождающиеся перфорацией [31]. Отличительной чертой последних являются отсутствие воспалительной реакции и превалирование расстройства обменных процессов, характерных для диабета [32]. Анамнез, продолжительность и динамическое наблюдение за пациентами с СД являются основными факторами для диагностики.
В литературе недостаточно описаны начальные признаки ДК и нейропатии, динамика репаративных процессов. Не определены нормативные значения этих показателей. При СД в 5,4 раза увеличивается проницаемость эпителия роговицы для водных и солевых растворов по сравнению с нормой. При нарушении эпителиального слоя роговицы больные жалуются на чувство инородного тела за веками, светобоязнь, блефароспазм, плохую переносимость глазами ветра, пыли, кондиционированного воздуха и дыма, ухудшение зрительной работоспособности, колебания остроты зрения.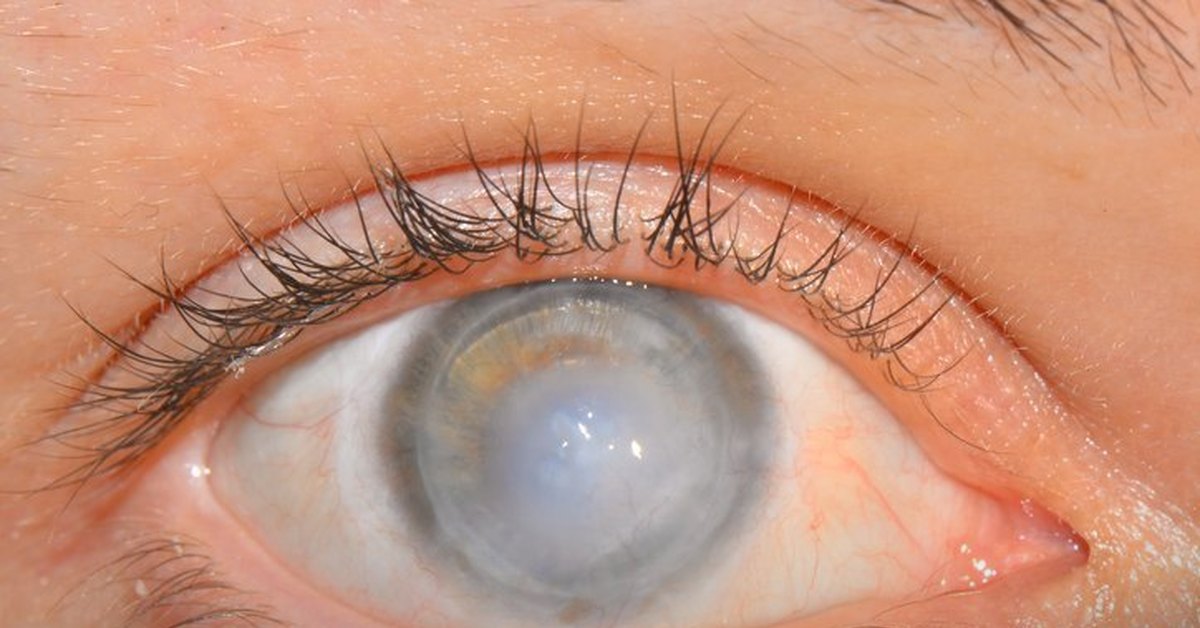 Эти жалобы не строго патогномоничны для СД, так как могут появляться у больных с хроническими конъюнктивитами и ССГ [33].
Эти жалобы не строго патогномоничны для СД, так как могут появляться у больных с хроническими конъюнктивитами и ССГ [33].
Ранние диабетические изменения переднего сегмента глаза при обоих типах СД включают конъюнктивальные микроангиопатии и микроаневризмы, нарушение эпителиального слоя роговицы, появление точечных кератопатий, рецидивирующих эрозий, изменение десцеметовой оболочки, пигментные депозиты на эндотелии.
Нервные волокна роговицы при СД
Согласно современным представлениям, немиелинизированные нервные волокна поражаются значительно раньше, чем окруженные миелином [27]. В настоящее время большое внимание уделяется состоянию нервов роговицы для поддержания нормального состояния глазной поверхности при СД для раннего выявления ДПН [11, 34–36]. В этом помогает метод конфокальной микроскопии роговицы. Для оценки плотности эпителиальных НВР в разных секторах роговицы с учетом возраста и пола Jiucheng He et al. (2010) разработали метод картирования, который создает полную картину архитектоники нервов роговицы человека.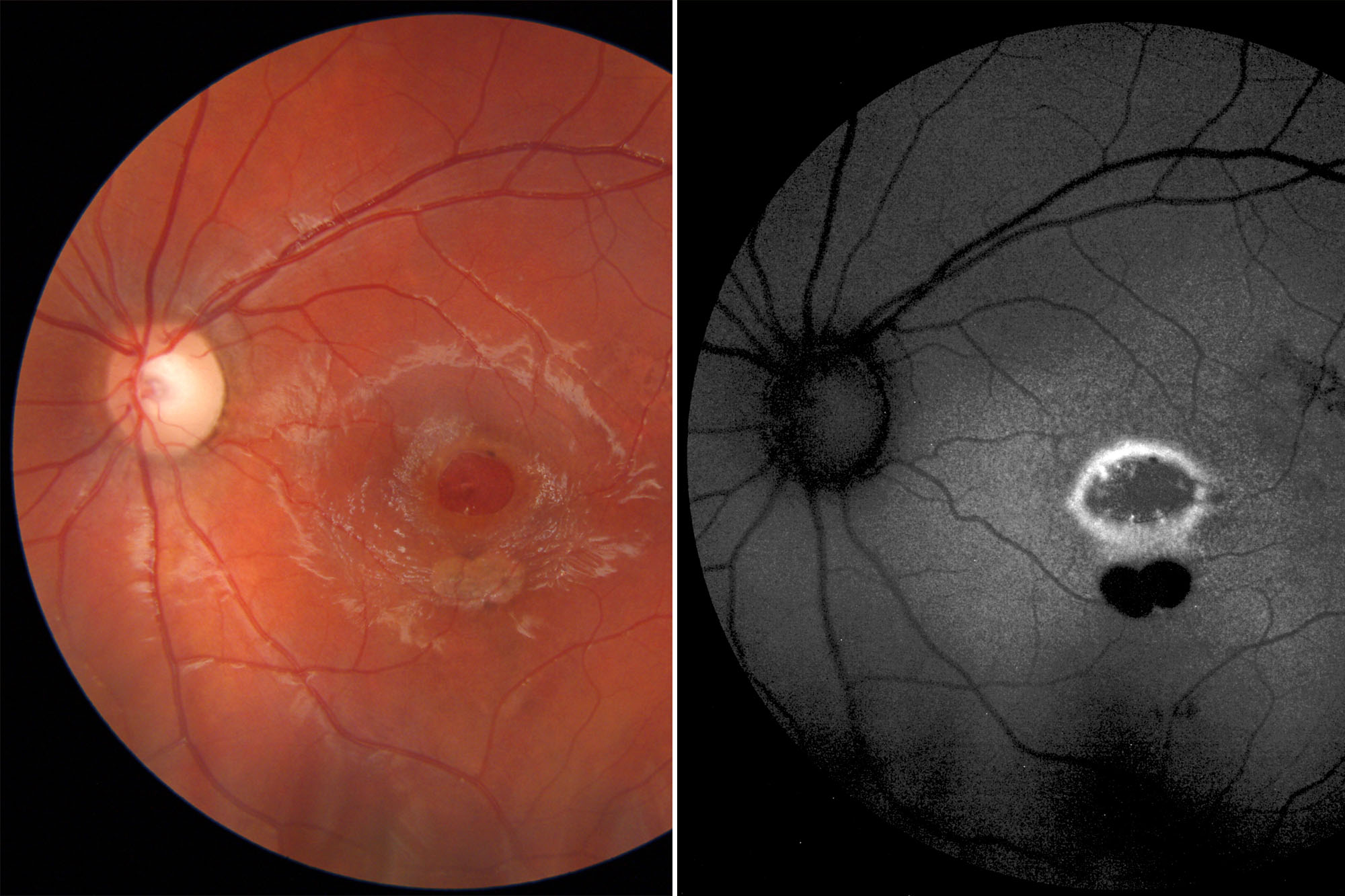 Авторами изучены 28 свежих роговиц человека 14 доноров различного возраста. Установлено, что плотность НВР выше в центре роговицы по сравнению с периферией и снижается по мере старения, главным образом после 70 лет, нет разницы в плотности нервных волокон между четырьмя квадрантами роговицы, а также мужчинами и женщинами [12].
Авторами изучены 28 свежих роговиц человека 14 доноров различного возраста. Установлено, что плотность НВР выше в центре роговицы по сравнению с периферией и снижается по мере старения, главным образом после 70 лет, нет разницы в плотности нервных волокон между четырьмя квадрантами роговицы, а также мужчинами и женщинами [12].
Используя КМР, ряд авторов обнаружили при диабете значительное уменьшение числа длинных нервных волокон в суббазальном нервном сплетении, плотность которых прогрессивно снижается по мере прогрессирования заболевания. В связи с этим снижается и чувствительность роговицы, развиваются кератопатии вплоть до язвенных дефектов не только роговицы, но и нижних конечностей [5, 19].
С.Э. Аветисов с соавт. (2015) изучали возрастные изменения НВР при СД 1 и 2 типов [37]. Исследования проводили у 37 пациентов (74 глаза) с СД 1 типа и 51 пациента (102 глаза) с СД 2 типа. На основании оригинального метода морфометрического анализа авторы выявили, что при СД имеет место повышение степени извитости и уменьшение анизотропии направленности НВР. Полученные результаты согласуются с другими исследованиями и подтверждают принципиальную возможность использования показателей состояния НВР в качестве критерия диагностики и мониторинга ДПН [25, 26, 35].
Полученные результаты согласуются с другими исследованиями и подтверждают принципиальную возможность использования показателей состояния НВР в качестве критерия диагностики и мониторинга ДПН [25, 26, 35].
Выявление поражения периферической нервной системы при нарушении углеводного обмена еще на доклинической стадии очень важно. Уже доказано, что у больных диабетом нарушение функции периферических нервов ведет к дистальной ДПН, развитию «диабетической стопы» – серьезного осложнения СД, приводящего к ампутации нижней конечности [16, 18, 27, 38]. При этом поражаются сосуды, питающие нервные волокна, ветви и сплетения, нарушаются метаболические процессы [4, 30].
Метод КМР выявляет ранние неврологические нарушения при диабете [20, 21]. Выявлена корреляция между плотностью НВР и интраэпидермальных нервных волокон. Поэтому при первых признаках нарушения углеводного обмена целесообразно выполнение КМР [36].
Quattrini C. et al. (2007) проводили сравнительную оценку показателей КМР, пункционной биопсии кожи, нейрофизиологического обследования 54 пациентов с диабетом и 15 здоровых добровольцев. Было выявлено значительное снижение плотности нервных волокон и их ветвей, которое коррелировало со снижением плотности интраэпидермальных нервных волокон в коже, что может служить тестом для выявления ранних неврологических нарушений при диабете [26].
Было выявлено значительное снижение плотности нервных волокон и их ветвей, которое коррелировало со снижением плотности интраэпидермальных нервных волокон в коже, что может служить тестом для выявления ранних неврологических нарушений при диабете [26].
КМР является надежным неинвазивным морфологическим методом, выявляющим признаки раннего повреждения нервов и их ветвей, а роговица может служить суррогатной оболочкой для оценки динамики ДПН и эффективности лечения [27].
Плотность клеток стромы роговицы при СД
Quadrado M. (2006) методом конфокальной микроскопии определял плотность клеток роговицы во всех слоях с помощью аутофлюоресценции у 15 больных СД и 15 здоровых лиц [39]. В обеих группах плотность клеток в среднем слое стромы была ниже, чем в передней и задней (Р<0,02), в базальном слое при СД – значительно ниже, чем у здоровых лиц. Другие исследователи показали, что у пациентов с СД 2 типа и хорошим гликемическим контролем не выявлено изменений плотности клеток роговицы и ее морфологической структуры [40]. При росте показателя гипергликемии в базальной мембране роговицы накапливаются токсичные продукты обмена, которые ведут к гибели клеток, их дисфункции, повреждению боуменовой мембраны, появлению отека и помутнений в роговице, замедлению заживления ран и расстройству зрения.
При росте показателя гипергликемии в базальной мембране роговицы накапливаются токсичные продукты обмена, которые ведут к гибели клеток, их дисфункции, повреждению боуменовой мембраны, появлению отека и помутнений в роговице, замедлению заживления ран и расстройству зрения.
Эндотелий роговицы при СД
Общеизвестно, что эндотелий роговицы представляет собой слой плоских гексагональных клеток и является одним из наиболее важных структурных компонентов, обеспечивающих нормальную толщину и прозрачность роговицы [9]. Увеличение толщины роговицы при СД связано с нарушением основной функции эндотелиальных клеток – регуляции содержания воды за счет повышения проницаемости в строму солей и метаболитов и снижения ее осмотического давления. Установлено повышение толщины роговицы в центре на 20–27 мкм по сравнению с нормой, что может быть использовано в качестве диагностического теста при диабете.
Leelawongtawun W. и соавт. (2015) не выявили разницы в плотности эндотелиальных клеток больных СД и здоровых лиц, однако при прогрессировании болезни отмечали изменение формы клеток с последующим развитием полимегатизма [41]. По данным других авторов, происходит снижение плотности эндотелиальных клеток, полимегатизм и плеоморфизм, при том, что процент клеток достоверно не отличается от нормы [42]. Другие исследователи наблюдали при СД 1 типа выраженную аутофлюоресценцию роговицы, полимегатизм, полиморфизм, тогда как при СД 2 типа не было достоверных изменений клеток по сравнению с контролем [43]. Отсутствие специфических изменений клеток эндотелия при СД 1 и 2 типа усложняет дифференциальную диагностику между ними.
По данным других авторов, происходит снижение плотности эндотелиальных клеток, полимегатизм и плеоморфизм, при том, что процент клеток достоверно не отличается от нормы [42]. Другие исследователи наблюдали при СД 1 типа выраженную аутофлюоресценцию роговицы, полимегатизм, полиморфизм, тогда как при СД 2 типа не было достоверных изменений клеток по сравнению с контролем [43]. Отсутствие специфических изменений клеток эндотелия при СД 1 и 2 типа усложняет дифференциальную диагностику между ними.
Отягощающее влияние СД на течение других процессов в глазу
В настоящее время ССГ является одним из самых распространенных заболеваний, в связи с чем большую актуальность приобретает проблема коррекции нарушений слезопродукции, восстановление составляющих компонентов слезной пленки и нормальной структуры глазной поверхности [6].
Достаточно подробно Т.Н. Сафронова и А.С. Патеюк (2015) описали систему глазной поверхности, главная задача которой – обеспечение и поддержание нормальной физиологии, увлажненности и гладкости рефракционной поверхности роговицы, ее гомеостаза.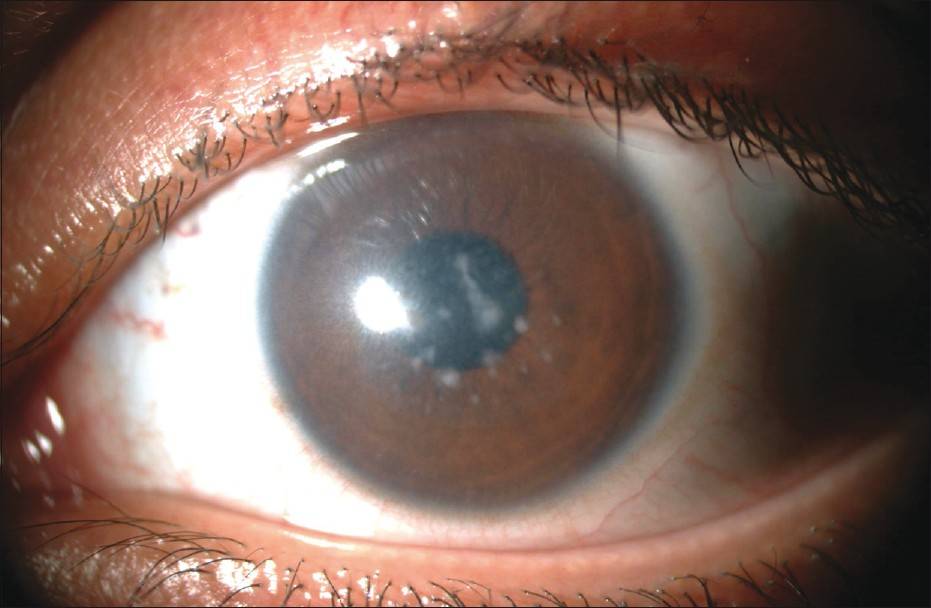 Дефицит гормонов отражается на гомеостазе последней, сохранности роговицы (чувствительность, толщина, кривизна) и стабильности слезной пленки [7]. Нарушение состава и свойств слезной пленки (рН, осмолярности, объема, вязкости) ведет к повреждению эпителия глазной поверхности – развитию ССГ, что имеет место при СД [7, 33]. По мере прогрессирования СД отмечаются увеличение толщины роговицы и нарушение ее чувствительности, дефицит слезопродукции, развитие ССГ, которые возрастают у лиц старше 50 лет. Все это является результатом нарушения метаболизма и прогрессирования диабетической нейропатии.
Дефицит гормонов отражается на гомеостазе последней, сохранности роговицы (чувствительность, толщина, кривизна) и стабильности слезной пленки [7]. Нарушение состава и свойств слезной пленки (рН, осмолярности, объема, вязкости) ведет к повреждению эпителия глазной поверхности – развитию ССГ, что имеет место при СД [7, 33]. По мере прогрессирования СД отмечаются увеличение толщины роговицы и нарушение ее чувствительности, дефицит слезопродукции, развитие ССГ, которые возрастают у лиц старше 50 лет. Все это является результатом нарушения метаболизма и прогрессирования диабетической нейропатии.
M. Manaviat с соавт. (2008) проводили клинические исследования передней поверхности глаза 199 больных СД и выявили ССГ у 54,3%. Высокую распространенность последнего авторы объяснили частотой нейротрофических поражений роговицы и влиянием окружающей среды, включая климатические особенности региона. Присоединение симптомов «сухого глаза» может привести к тяжелым осложнениям, в том числе язве роговицы.
Известно, что СД влияет на метаболические процессы, физиологические, морфологические и клинические изменения роговицы человека [30]. Гистологические исследования показывают изменения во всех слоях последней. Ряд исследователей оценили возможности биологического окислительного «склеивания» роговичного коллагена под воздействием энзимов, тепла или излучения определенной длины волны и повышения резистентности стромального коллагена у больных СД. Механизм индукции «склеивания» коллагена при диабете включает каскад биохимических окислительных реакций, отражающих неферментативное гликирование белков. Феномен повышения диаметра коллагена был продемонстрирован методом сканирующей электронной микроскопии [44]. Диабетические изменения на фоне длительной гипергликемии являются мультифункциональными, при этом ускоряются обменные реакции (процесс гликирования – реакция между белками и глюкозой) [30]. Генерация гетерогенных химических субстанций, общеизвестных как конечные продукты гликирования, вызывает кросслинкинг коллагеновых волокон в дополнение к другим матриксным компонентам: эластину и протеогликанам роговицы. Goldich и соавт. (2009) исследовали биомеханические параметры роговиц 40 пациентов с диабетом и 40 здоровых добровольцев. Было установлено, что при диабете увеличиваются показатели корнеального гистерезиса, фактора резистентности роговицы и ее толщины в центре при отсутствии достоверной разницы внутриглазвного давления в обеих группах. Эту точку зрения поддерживают другие исследователи [45, 46].
Goldich и соавт. (2009) исследовали биомеханические параметры роговиц 40 пациентов с диабетом и 40 здоровых добровольцев. Было установлено, что при диабете увеличиваются показатели корнеального гистерезиса, фактора резистентности роговицы и ее толщины в центре при отсутствии достоверной разницы внутриглазвного давления в обеих группах. Эту точку зрения поддерживают другие исследователи [45, 46].
Интересны исследования M. Naderan и соавт. (2014), которые изучали развитие кератэктазий у больных диабетом. Сравнивали степень прогрессирования эктазии в двух группах по 1383 пациентов в каждой с кератоконусом и без него [47]. Установили, что распространенность кератоконуса у больных СД была ниже и составляла 0,8% по сравнению с контролем (2,2%). По мнению авторов, отмечается «защитный эффект диабета» против возникновения кератоконуса. Результаты изучения показали, что при диабете имеет место естественный кросслинкинг роговицы, который способствует получению значимого биомеханического эффекта, в связи с чем предупреждается или замедляется процесс развития кератэктазии.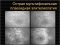 По мере прогрессирования основного заболевания снижается риск возникновения последней, тем не менее, эта связь до конца не ясна. Seiler Т. и соавт. (2000) поддерживают эту точку зрения, однако их данные находятся в противоречии с исследованиями I.C. Kuo (2006), который не нашел связи двух заболеваний [48, 49].
По мере прогрессирования основного заболевания снижается риск возникновения последней, тем не менее, эта связь до конца не ясна. Seiler Т. и соавт. (2000) поддерживают эту точку зрения, однако их данные находятся в противоречии с исследованиями I.C. Kuo (2006), который не нашел связи двух заболеваний [48, 49].
Сахарный диабет – фон, на котором полостные операции глаза чаще сопровождаются осложнениями, на что указывают многие авторы. Так, Б.Э. Малюгин, А.О. Марцинкевич (2016) представили данные о частоте развития экссудативно-воспалительных реакций переднего отдела глаза, в том числе и роговицы, после факоэмульсификации катаракт у больных с СД [17]. Другие авторы показали, что при диабете после лазерных кераторефракционных операций увеличивается риск развития дефектов эпителия и эрозий роговицы, ее отеков, и пути их предупреждения [50, 51]. При проведении хирургических вмешательств на сетчатке и стекловидном теле у пациентов с СД отмечаются осложнения со стороны роговицы в виде отека, стойких дефектов эпителия [52, 53, 54].
Заключение
Многие аспекты возникновения и прогноза нарушений роговицы при СД остаются спорными и окончательно не изученными. Полное представление о состоянии роговицы при СД складывается на основании исследования клинических, инструментальных и морфологических признаков. Тщательный офтальмологический осмотр пациента нужно начинать с роговицы, используя современные ультразвуковые и лазерные методы диагностики. Проведение неинвазивного метода диагностики – КМР позволяет выявить ранние проявления корнеальной нейропатии и ДПН. Дискутабельными являются вопросы своевременной диагностики и истинного прогноза течения полинейропатии при СД с учетом определения роли изменений нервных волокон суррогатной роговицы. Полостные операции глаз у больных СД могут сопровождаться развитием корнеальных осложнений. Актуален дальнейший поиск прижизненных прогностических факторов, позволяющих выделить больных с высоким риском корнеальной и ДПН при СД.
Дополнительная информация
Финансирование работы
Исследование проведено в рамках научно-исследовательской работы при поддержке ГБУ «Уфимский НИИ глазных болезней Академии наук Республики Башкортостан»
Конфликт интересов
Авторы сообщают об отсутствии конфликта интересов, связанных с публикацией настоящей статьи. .
.
Участие авторов
Бикбов М.М. – концепция обзора, сбор и анализ материала, написание текста рукописи; Суркова В.К. – написание и редактирование текста рукописи.
1. Дедов И.И., Шестакова М.В., Галстян Г.Р. Распространенность сахарного диабета 2 типа у взрослого населения России (исследование NATION) // Сахарный диабет. – 2016. – Т. 19. – №2 – C. 104-112. [Dedov II, Shestakova MV, Galstyan GR. The prevalence of type 2 diabetes mellitus in the adult population of Russia (NATION study). Diabetes mellitus. 2016;19(2):104-112. (In Russ).] doi: 10.14341/DM2004116-17
2. Дедов И.И., Омельяновский В.В., Шестакова М.В., и др. Cахарный диабет как экономическая проблема в Российской Федерации // Сахарный диабет. – 2016. – Т. 19. – №1 – C. 30-43. [Dedov II, Omelyanovskiy VV, Shestakova MV, Avksentieva MV, Ignatieva VI. Diabetes mellitus as an economic problem in Russian Federation. Diabetes mellitus. 2016;19(1):30-43. (In Russ).]. doi: 10. 14341/DM 7784
[Dedov II, Omelyanovskiy VV, Shestakova MV, Avksentieva MV, Ignatieva VI. Diabetes mellitus as an economic problem in Russian Federation. Diabetes mellitus. 2016;19(1):30-43. (In Russ).]. doi: 10. 14341/DM 7784
3. Сахарный диабет и нарушения углеводного обмена. Эндокринология по Вильямсу / Под ред. Дедова И.И., Мельниченко Г.А. – Рид Элсивер; 2010. [Diabetes mellitus and disorders of carbohydrate metabolism. Endocrinology for Williams / Ed by Dedov II, Mel’nichenko GA. Rid Elsiver; 2010. (In Russ).]
4. Балашевич Л.И., Бржевский В.В., Измайлов А.С., и др. Глазные проявления диабета. – М.: Медицина; 2004. [Balashevich LI, Brzhevskii VV, Izmailov AS, et al. Glaznye proyavleniya diabeta. Moscow: Medicina; 2004. (In Russ).]
5. Lockwood A, Hope-Ross M, Chell P. Neurotrophic keratopathy and diabetes mellitus. Eye (Lond). 2006;20(7):837-839. doi: 10.1038/sj.eye.6702053
Lockwood A, Hope-Ross M, Chell P. Neurotrophic keratopathy and diabetes mellitus. Eye (Lond). 2006;20(7):837-839. doi: 10.1038/sj.eye.6702053
6. Sweeney DF, Millar TJ, Raju SR. Tear film stability: a review. Exp Eye Res. 2013;117:28-38. doi: 10.1016/j.exer.2013.08.010
7. Сафонова Т.Н., Патеюк А.С. Система глазной поверхности. // Вестник офтальмологии. 2015. – Т. 131. – №1. – С.96 – 102. [Safonova TN, Pateyuk LS. Ocular surface system integrity. Vestnik oftal’mologii. 2015;131(1):96-102. (In Russ)]. doi: 10.17116/oftalma2015131196-102
8. Marfurt CF, Cox J, Deek S, Dvorscak L. Anatomy of the human corneal innervation. Exp Eye Res. 2010;90(4):478-492. doi: 10.1016/j.exer.2009.12.010
9. Вит В.В. Строение зрительной системы человека. – Одесса: Астропринт; 2010. [Vit VV. The structure of the human visual system. Odessa: Astroprint; 2010. (In Russ).]
Вит В.В. Строение зрительной системы человека. – Одесса: Астропринт; 2010. [Vit VV. The structure of the human visual system. Odessa: Astroprint; 2010. (In Russ).]
10. Krachmer J., Mannis M., Holland E. Eds. Cornea fundamentals, diagnosis, and management. 3 rd ed. Mosby Elsevier. St. Louis; 2011.
11. Al-Aqaba MA, Fares U, Suleman H, et al. Architecture and distribution of human corneal nerves. Br J Ophthalmol. 2010;94(6):784-789. doi: 10.1136/bjo.2009.173799
12. He J, Bazan NG, Bazan HE. Mapping the entire human corneal nerve architecture. Exp Eye Res. 2010;91(4):513-523. doi: 10.1016/j.exer.2010.07.007
13. DeMill DL, Hussain M, Pop-Busui R, Shtein RM. Ocular surface disease in patients with diabetic peripheral neuropathy. Br J Ophthalmol. 2015. pii: bjophthalmol-2015-307369. doi: 10.1136/bjophthalmol-2015-307369
Ocular surface disease in patients with diabetic peripheral neuropathy. Br J Ophthalmol. 2015. pii: bjophthalmol-2015-307369. doi: 10.1136/bjophthalmol-2015-307369
14. Edwards K, Pritchard N, Gosschalk K, et al. Wide-Field Assessment of the Human Corneal Subbasal Nerve Plexus in Diabetic Neuropathy Using a Novel Mapping Technique. Cornea. 2012;31(9):1078-1082. doi: 10.1097/ICO.0b013e318245c012
15. Nitoda E, Kallinikos P, Pallikaris A, et al. Correlation of diabetic retinopathy and corneal neuropathy using confocal microscopy. Curr Eye Res. 2012;37(10):898-906. doi: 10.3109/02713683.2012.683507
16. Tavakoli M, Ferdousi M, Petropoulos IN, et al. Normative values for corneal nerve morphology assessed using corneal confocal microscopy: a multinational normative data set. Diabetes Care. 2015;38(5):838-843. doi: 10.2337/dc14-2311
Diabetes Care. 2015;38(5):838-843. doi: 10.2337/dc14-2311
17. Малюгин Б.Э., Марцинкевич А.О. Современные подходы к профилактике послеоперационных воспалительных осложнений в хирургии катаракты у больных с сахарным диабетом. // Офтальмохирургия. – 2016. – Т. 1. – С.85-90. [Malyugin BE, Martsinkevich AO. Modern approaches to the prevention of post-cataract surgery inflammation in diabetic patients. Oftal’mohirurgija. 2016;1:85-90. (In Russ)].
18. Lauria G, Hsieh ST, Johansson O, et al. European Federation of Neurological Societies/Peripheral Nerve Society Guideline on the use of skin biopsy in the diagnosis of small fiber neuropathy. Report of a joint task force of the European Federation of Neurological Societies and the Peripheral Nerve Society. Eur J Neurol. 2010;17(7):903-912, e944-909. doi: 10.1111/j.1468-1331. 2010.03023.x
2010.03023.x
19. Tesfaye S, Boulton AJ, Dyck PJ, et al. Diabetic neuropathies: update on definitions, diagnostic criteria, estimation of severity, and treatments. Diabetes Care. 2010;33(10):2285-2293. doi: 10.2337/dc10-1303
20. Аветисов С.Э., Егорова Г.Б., Кобзева М.В., и др. Клиническое значение современных методов исследования роговицы. // Вестник офтальмологии. – 2013 – №5. – С.22-31. [Avetisov SE, Egorova GB, Kobzeva MV, et al. The clinical significance of contemporary research methods cornea. Vestnik oftal’mologii. 2013;(5):22-31. (In Russ)]
21. Tavakoli M, Hossain P, Malik RA. Clinical applications of corneal confocal microscopy. Clinical ophthalmology (Auckland, N.Z.). 2008;2(2):435-445.
22. Petropoulos IN, Manzoor T, Morgan P, et al. Repeatability of In Vivo Corneal Confocal Microscopy to Quantify Corneal Nerve Morphology. Cornea. 2013;32(5):e83-e89. doi: 10.1097/ICO.0b013e3182749419
Petropoulos IN, Manzoor T, Morgan P, et al. Repeatability of In Vivo Corneal Confocal Microscopy to Quantify Corneal Nerve Morphology. Cornea. 2013;32(5):e83-e89. doi: 10.1097/ICO.0b013e3182749419
23. Dabbah MA, Graham J, Petropoulos IN, et al. Automatic analysis of diabetic peripheral neuropathy using multi-scale quantitative morphology of nerve fibres in corneal confocal microscopy imaging. Med Image Anal. 2011;15(5):738-747. doi: 10.1016/j.media.2011.05.016
24. Егорова Г.Б., Рогова А.Я., Митичкина Т.С. Диагностические возможности конфокальной микроскопии первичных эктазий роговицы. // Вестник офтальмологии. – 2012 – №6 – С.25-29. [Egorova GB, Rogova AYa, Mitichkina TS. The diagnostic capabilities of confocal microscopy of primary corneal ectasia. Vestnik oftal’mologii. 2012;(6):25-29. (In Russ)].
25. Malik RA, Kallinikos P, Abbott CA, et al. Corneal confocal microscopy: a non-invasive surrogate of nerve fibre damage and repair in diabetic patients. Diabetologia. 2003;46(5):683-688. doi: 10.1007/s00125-003-1086-8
Malik RA, Kallinikos P, Abbott CA, et al. Corneal confocal microscopy: a non-invasive surrogate of nerve fibre damage and repair in diabetic patients. Diabetologia. 2003;46(5):683-688. doi: 10.1007/s00125-003-1086-8
26. Quattrini C, Tavakoli M, Jeziorska M, et al. Surrogate markers of small fiber damage in human diabetic neuropathy. Diabetes. 2007;56(8):2148-2154. doi: 10.2337/db07-0285
27. Артемова Е.В., Галстян Г.Р., Атарщиков Д.С., и др. Конфокальная микроскопия роговицы – новый неинвазивный метод диагностики начальных проявлений повреждения периферической нервной системы при сахарном диабете. // Проблемы эндокринологии. – 2015 – Т. 61. – №2 – С.32-38. [Artemova EV, Galstyan GR, Atarshchikov DS, et al. Confocal retinal microscopy – the new non-invasive method for diagnostics of the early manifestations of the lesions in the peripheral nervous system associated with diabetes mellitus. Problems of Endocrinology. 2015;61(2):32-38. (In Russ)] doi: 10.14341/probl201561232-38.
Problems of Endocrinology. 2015;61(2):32-38. (In Russ)] doi: 10.14341/probl201561232-38.
28. Huang D, Li Y, Radhakrishnan S. Optical coherence tomography of the anterior segment of the eye. Ophthalmology Clinics of North America. 2004;17(1):1-6. doi: 10.1016/s0896-1549(03)00103-2
29. Тахчиди Х.П., Егорова Э.В., Узунян Д.Г. Ультразвуковая биомикроскопия в диагностике патологии переднего сегмента глаза. – М.: Издательский центр «Микрохирургия глаза»; 2007. [Takhchidi KhP, Egorova EV, Uzunyan DG. Ultrasound biomicroscopy in the diagnosis of diseases of anterior segment of the eye. Moscow: Izdatel’skii tsentr «Mikrokhirurgiya glaza»; 2007. (In Russ)].
30. Bikbova G, Oshitari T, Tawada A, Yamamoto S. Corneal Changes in Diabetes Mellitus.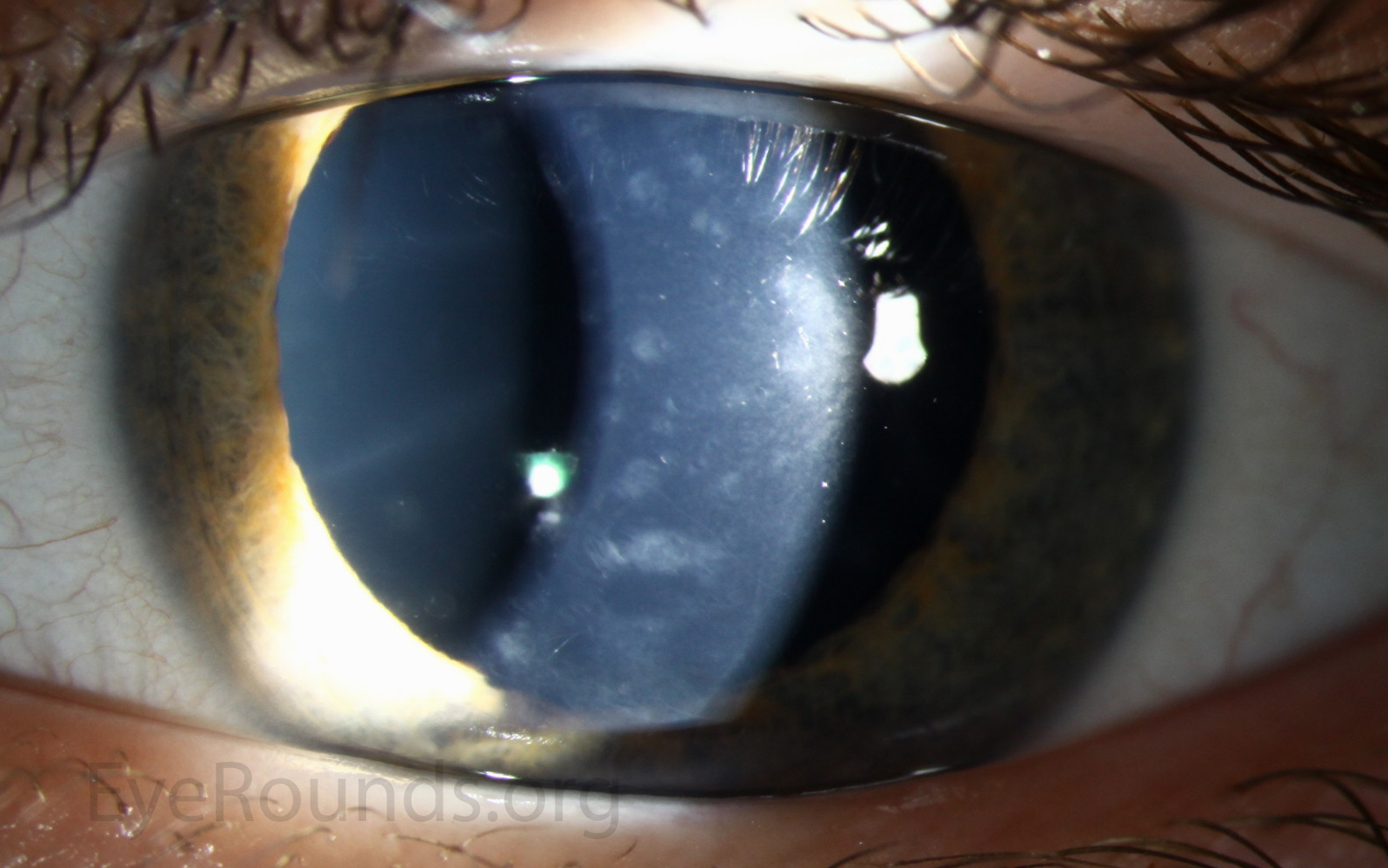 Current Diabetes Reviews. 2012;8(4):294-302. doi: 10.2174/157339912800840479
Current Diabetes Reviews. 2012;8(4):294-302. doi: 10.2174/157339912800840479
31. Inoue K, Kato S, Ohara C, et al. Ocular and Systemic Factors Relevant to Diabetic Keratoepitheliopathy. Cornea. 2001;20(8):798-801. doi: 10.1097/00003226-200111000-00004
32. Nakahara M, Miyata K, Otani S, et al. A randomised, placebo controlled clinical trial of the aldose reductase inhibitor CT-112 as management of corneal epithelial disorders in diabetic patients. Br J Ophthalmol. 2005;89(3):266-268. doi: 10.1136/bjo.2004.049841
33. Бржеский В.В. Синдром «сухого глаза». Офтальмология. Национальное руководство / Под редакцией С.Э. Аветисова, Е.А. Егорова, Л.К. Мошетовой, В.В. Нероева, Х.П. Тахчиди. М.: ГЭОТАР-Медиа; 2008. [Brzheskii VV. The syndrome of «dry eye».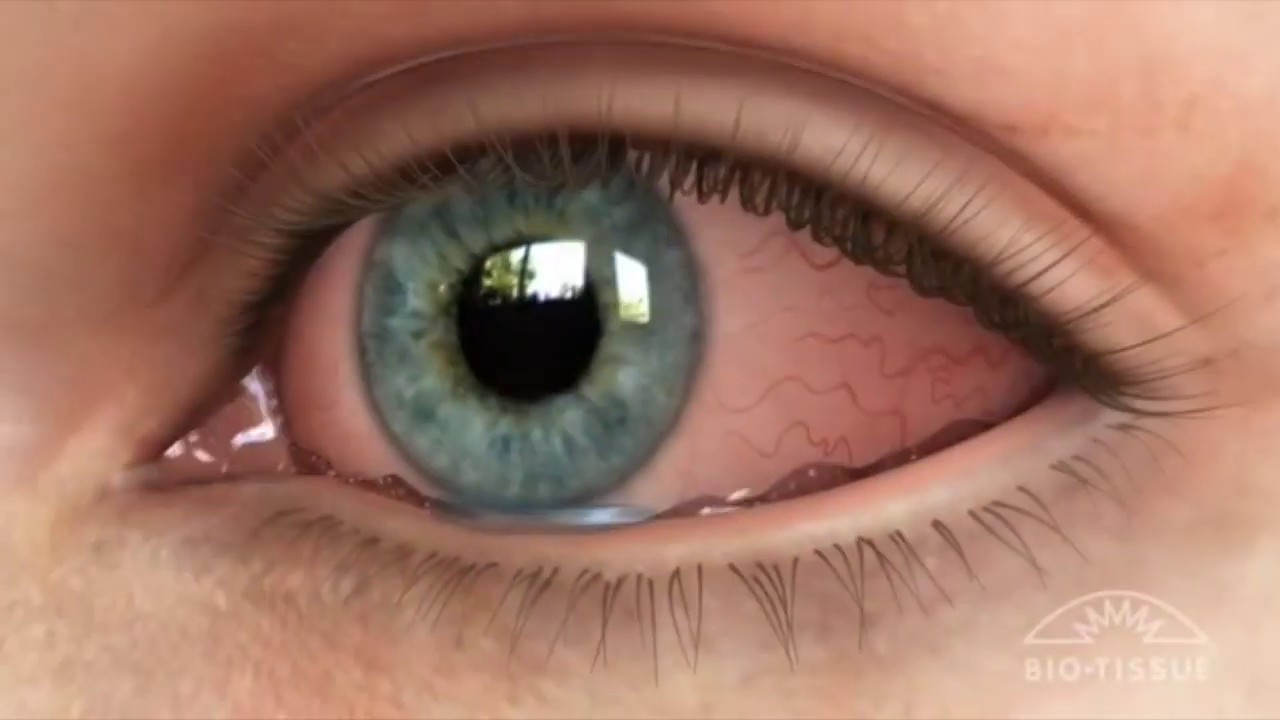 Ophthalmology. National leadership / Edited by SE Avetisov, EA Egorov, LK Mosheta, VV Neroev, KhP Takhchidi. Moscow: GEOTAR-Media; 2008. (In Russ).]
Ophthalmology. National leadership / Edited by SE Avetisov, EA Egorov, LK Mosheta, VV Neroev, KhP Takhchidi. Moscow: GEOTAR-Media; 2008. (In Russ).]
34. Petropoulos IN, Manzoor T, Morgan P, et al. Repeatability of in vivo corneal confocal microscopy to quantify corneal nerve morphology. Cornea. 2013;32(5):e83-89. doi: 10.1097/ICO.0b013e3182749419
35. Dehghani C, Pritchard N, Edwards K, et al. Fully automated, semiautomated, and manual morphometric analysis of corneal subbasal nerve plexus in individuals with and without diabetes. Cornea. 2014;33(7):696-702. doi: 10.1097/ICO.0000000000000152
36. Сурнина З.В. Возможности световой и лазерной биомикроскопии роговицы в ранней диагностике диабетической полинейропатии. // Вестник офтальмологии. – 2015. – Т. 131. – №1 – С.104-108. [Surnina ZV. Opportunities for confocal and laser biomicroscopy of corneal nerves in diabetic polyneuropathy. Vestnik oftal’mologii. 2015;131(1):104-108. (In Russ).] doi: 10.17116/oftalma20151311104-108
– 2015. – Т. 131. – №1 – С.104-108. [Surnina ZV. Opportunities for confocal and laser biomicroscopy of corneal nerves in diabetic polyneuropathy. Vestnik oftal’mologii. 2015;131(1):104-108. (In Russ).] doi: 10.17116/oftalma20151311104-108
37. Аветисов С.Э., Новиков И.А., Махотин С.С., Сурнина З.В. Новый принцип морфометрического исследования нервных волокон роговицы на основе конфокальной биомикроскопии при сахарном диабете. // Вестник офтальмологии. – 2015 – №4. – С.5-14. [Avetisov SE, Novikov IA, Makhotin SS, Surnina ZV. New approach to corneal nerve fibers morphometry in diabetes mellitus on the basis of confocal biomicroscopy. Vestnik oftal’mologii. 2015;131(4):5-14. (In Russ)] doi: 10.17116/oftalma201513145-14
38. Edwards K, Pritchard N, Vagenas D, et al. Standardizing corneal nerve fibre length for nerve tortuosity increases its association with measures of diabetic neuropathy. Diabet Med. 2014;31(10):1205-1209. doi: 10.1111/dme.12466
Diabet Med. 2014;31(10):1205-1209. doi: 10.1111/dme.12466
39. Quadrado MJ, Popper M, Morgado AM, et al. Diabetes and corneal cell densities in humans by in vivo confocal microscopy. Cornea. 2006;25(7):761-768. doi: 10.1097/01.ico.0000224635.49439.d1
40. Efron N, Lee G, Lim RN, et al. Development and validation of the QUT corneal nerve grading scale. Cornea. 2014;33(4):376-381. doi: 10.1097/ICO.0000000000000084
41. Leelawongtawun W, Suphachearaphan W, Kampitak K, Leelawongtawun R. A comparative study of corneal endothelial structure between diabetes and non-diabetes. J Med Assos Thai. 2015;98(5):484-488.
42. Shenoy R, Khandekar R, Bialasiewicz A, Al Muniri A. Corneal endothelium in patients with diabetes mellitus: a historical cohort study. Eur J Ophthalmol. 2009;19(3):369. doi: 10.5301/EJO.2009.4277
Corneal endothelium in patients with diabetes mellitus: a historical cohort study. Eur J Ophthalmol. 2009;19(3):369. doi: 10.5301/EJO.2009.4277
43. Larsson L-I. Structure and Function of the Corneal Endothelium in Diabetes Mellitus Type I and Type II. Archives of Ophthalmology. 1996;114(1):9. doi: 10.1001/archopht.1996.01100130007001
44. Wollensak G, Wilsch M, Spoerl E, Seiler T. Collagen Fiber Diameter in the Rabbit Cornea After Collagen Crosslinking by Riboflavin/UVA. Cornea. 2004;23(5):503-507. doi: 10.1097/01.ico.0000105827.85025.7f
45. Бикбов М.М., Суркова В.К., Зайнуллина Н.Б., и др. Морфологические изменения роговицы после лечения кератоконуса методом кросслинкинга роговичного коллагена. // Катарактальная и рефракционная хирургия.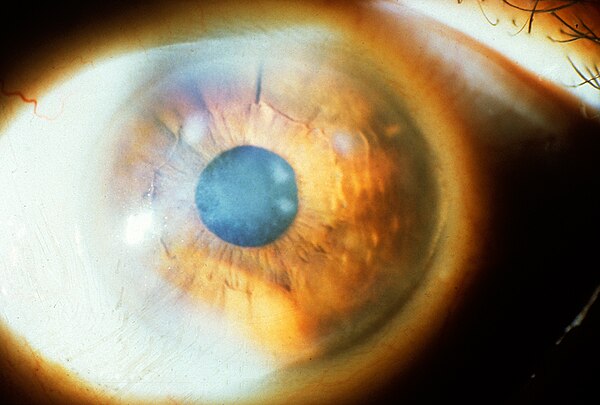 – 2014. – Т. 14. – №3 – С.18-22. [Bikbov M, Bikbova G, Surkova V, et al. Morphological changes in cornea after corneal collagen cross-linking as keratoconus treatment. Cataractal and Refractive Surgery. 2014;14(3):18-22. (In Russ)]
– 2014. – Т. 14. – №3 – С.18-22. [Bikbov M, Bikbova G, Surkova V, et al. Morphological changes in cornea after corneal collagen cross-linking as keratoconus treatment. Cataractal and Refractive Surgery. 2014;14(3):18-22. (In Russ)]
46. Бикбов М.М., Бикбова Г.М. Эктазия роговицы. – М.: Офтальмология; 2011. [Bikbov MM, Bikbova GM. Corneal ectasia. Moscow: Oftal’mologija; 2011. (In Russ)].
47. Naderan M, Naderan M, Rezagholizadeh F, et al. Association between diabetes and keratoconus: a case-control study. Cornea. 2014;33(12):1271-1273. doi: 10.1097/ICO.0000000000000282
48. Seiler T, Huhle S, Spoerl E, Kunath H. Manifest diabetes and keratoconus: A retrospective case-control study. Graefe’s Archive for Clinical and Experimental Ophthalmology. 2000;238(10):822-825. doi: 10.1007/s004179900111
2000;238(10):822-825. doi: 10.1007/s004179900111
49. Kuo IC, Broman A, Pirouzmanesh A, Melia M. Is there an association between diabetes and keratoconus? Ophthalmology. 2006;113(2):184-190. doi: 10.1016/j.ophtha.2005.10.009
50. Halkiadakis I, Belfair N, Gimbel HV. Laser in situ keratomileusis in patients with diabetes. J Cataract Refract Surg. 2005;31(10):1895-1898. doi: 10.1016/j.jcrs.2005.03.075
51. Simpson RG, Moshirfar M, Edmonds JN, Christiansen SM. Laser in-situ keratomileusis in patients with diabetes mellitus: a review of the literature. Clin Ophthalmol. 2012;6:1665-1674. doi: 10.2147/OPTH.S36382
52. Балашевич Л.И., Измайлов А. С. Диабетическая офтальмопатия. – СПб.: Изд. «Человек»; 2012. [Balashevich LI, Izmailov AS. Diabetic ophthalmopathy. Saint-Petersburg.: Izd. «Chelovek»; 2012. (In Russ).]
С. Диабетическая офтальмопатия. – СПб.: Изд. «Человек»; 2012. [Balashevich LI, Izmailov AS. Diabetic ophthalmopathy. Saint-Petersburg.: Izd. «Chelovek»; 2012. (In Russ).]
53. Pinarci EY, Bayar SA, Sizmaz S, et al. Anterior segment complications after phacovitrectomy in diabetic and nondiabetic patients. Eur J Ophthalmol. 2013;23(2):223-229. doi: 10.5301/ejo.5000203
54. Chen H-F, Yeung L, Yang K-J, Sun C-C. Persistent corneal epithelial defect after pars plana vitrectomy. Retina. 2016;36(1):148-155.
Ночные линзы — ортокератология в офтальмологической клинике «Мой взгляд»
ОК-терапия, или ортокератология — особая процедура, позволяющая без оперативного вмешательства вернуть зрение пациенту. Ее суть заключается в следующем: человек на ночь надевает специальные жесткие линзы, которые не препятствуют газообмену. Они не причиняют человеку дискомфорт.
Ее суть заключается в следующем: человек на ночь надевает специальные жесткие линзы, которые не препятствуют газообмену. Они не причиняют человеку дискомфорт.
Сущность методики ортокератологии
Использование ночных линз позволяет изменить форму роговицы, делая ее более плоской. Уплощение оболочки позволяет убрать рефракционные нарушения структур глаза. В частности, под давлением линзы клетки роговицы перераспределяются таким образом, что начинают преломлять световые лучи слабее. Это позволяет изображению фокусироваться на сетчатке.
Современные ортокератологические линзы предназначены для использования во время сна. Восьми часов вполне достаточно, чтобы вернуть остроту и четкость зрительного восприятия на сутки, при этом в обычных контактных линзах или очках необходимости нет.
Терапия с применением ночных линз дает кратковременный эффект, поскольку роговица без постоянного воздействия корректирующих линз полностью восстанавливает форму в течение нескольких дней. Методика не позволяет навсегда избавиться от проблем со зрением.
Методика не позволяет навсегда избавиться от проблем со зрением.
Для каждого пациента подбор ночных линз проводится в индивидуальном порядке, с учетом его физиологических особенностей и степени близорукости, поэтому их нельзя приобрести в салонах оптики или других точках продаж.
В клинике «Мой взгляд» подбор данных линз проводит специалист с высокой профессиональной квалификацией. В своей работе ортокератолог использует японский кератотопограф СТ-1000. Процедура включает детальный анализ роговицы и ее компонентов. Результатом обследования является полная карта структур. Кроме того, при подборе ночных линз пациент может рассчитывать на консультацию специалиста, готовые к ношению линзы и годовое диспансерное наблюдение.
Рекомендуемый возраст
-
Дети. Использование ночных линз разрешено с 6-летнего возраста. -
Взрослые. В данном случае никаких ограничений по возрасту пациента нет.
В данном случае никаких ограничений по возрасту пациента нет.
Несмотря на это, при работе с лицами старше 40 лет учитываются нарушения аккомодации, обусловленные возрастными особенностями, степень слезопродукции и некоторые другие факторы.
Показания к применению
Использование методики ортокератологии целесообразно в следующих случаях:
-
Возникновение синдрома сухого глаза, то есть недостаточное слезопроизводство при использовании обычных контактных линз. -
Миопия, в том числе прогрессирующая. -
Ситуация, когда ношение очков или линз невозможно ввиду профессиональной деятельности пациента или его активного образа жизни (активные занятия спортом, работа в запыленных помещениях, постоянный контакт в аэрозолями и т. д.) -
Когда лазерная коррекция каким-то причинам не показана.
Противопоказания
Ношение ночных линз противопоказано при:
-
Отсутствии одного глаза. -
Воспалениях переднего отрезка в стадии обострения. -
Воспалениях век в любой стадии, в том числе и хроническом проявлении. -
Выраженном ксерозе, то есть недостатке выработки слезы. -
Пониженной чувствительности роговицы. -
Выраженном лагофтальме. -
Наличии мутных пятен или рубцов различной этиологии на роговице. -
Выраженном нистагме, не позволяющем провести процедуру подбора -
Эпителиопатии роговицы. -
Пеллюцидной краевой дегенерации. -
Кератоконусе или кератоглобусе.
-
После проведения коррекции зрения по методу Lasik.
Исманкулов «Глазные болезни». Глава 10. Патология роговой оболочки
Исманкулов «Глазные болезни». Глава 10. Патология роговой оболочки
- Аномалии роговой оболочки
- Экзогенные кератиты
- Эндогенные кератиты
- Дистрофии роговой оболочки
- Опухоли роговой оболочки
ПАТОЛОГИЯ РОГОВОЙ ОБОЛОЧКИ
Ранее описано, что роговая оболочка обладает следующими свойствами: определенной величиной, сферичностью, зеркальностью, блеском, прозрачностью, а также чувствительностью. Если изменяются эти ее свойства, то возникают сочетания диагностических признаков, характеризующих различные заболевания роговицы. Изменения в роговице могут быть врожденными и приобретенными. Врожденными изменениями являются аномалии размеров роговицы: микрокорнеа (microcornea), если горизонтальный размер менее 11 мм, мегалокорнеа (megalocornea), если горизонтальный размер более 12 см.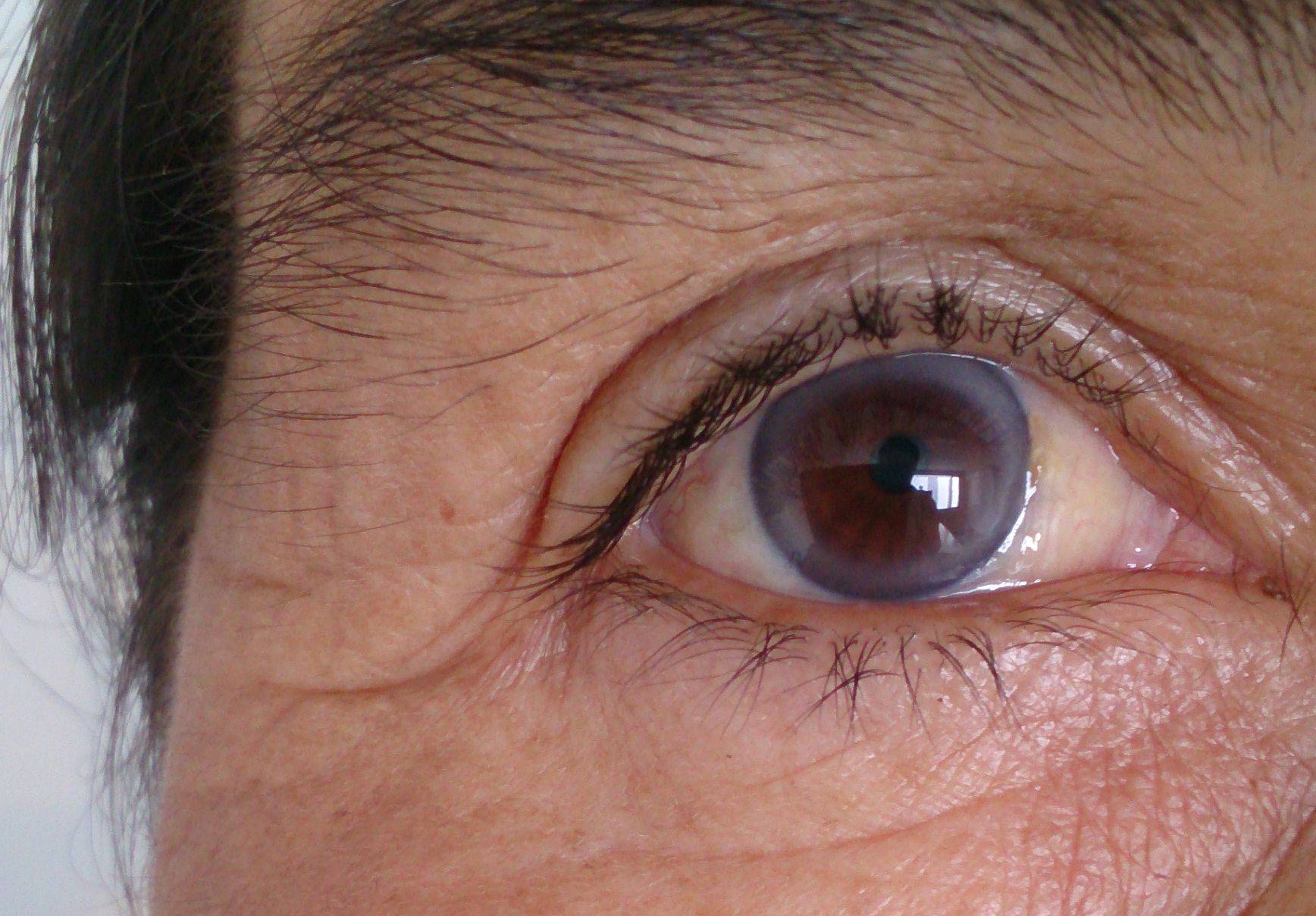 Нормальные размеры роговицы определяются измерением миллиметровой линейкой ее горизонтального (11-12 мм) и вертикального меридиана (10-11 мм).
Нормальные размеры роговицы определяются измерением миллиметровой линейкой ее горизонтального (11-12 мм) и вертикального меридиана (10-11 мм).
<< ОГЛАВЛЕНИЕ
У новорожденного горизонтальный размер роговицы 9 мм. Аномалии формы и кривизны роговицы: кератоконус (keratoconus), кератоглобус (keratoglobus), уплощение роговицы (applanatio corneae), кератоторус, вертикально-овальная роговица.
Могут быть также врожденные помутнения роговицы, которые встречаются в качестве аномалий развития или последствий внутриутробных воспалений и семейно-наследственные дистрофии роговицы.
Кератоконус (см. рис. 14), как врожденная аномалия, нередко сочетается с другими аномалиями развития глаз и разных органов. Кератоконус может быть и приобретенным. Чаще развивается в возрасте 15-20 лет, медленно прогрессирует, зрение падает постепенно. У вершины конуса десцеметова оболочка может разрываться и тогда вследствие проникновения влаги в ее ткань, мутнеет строма роговой оболочки (острый кератоконус).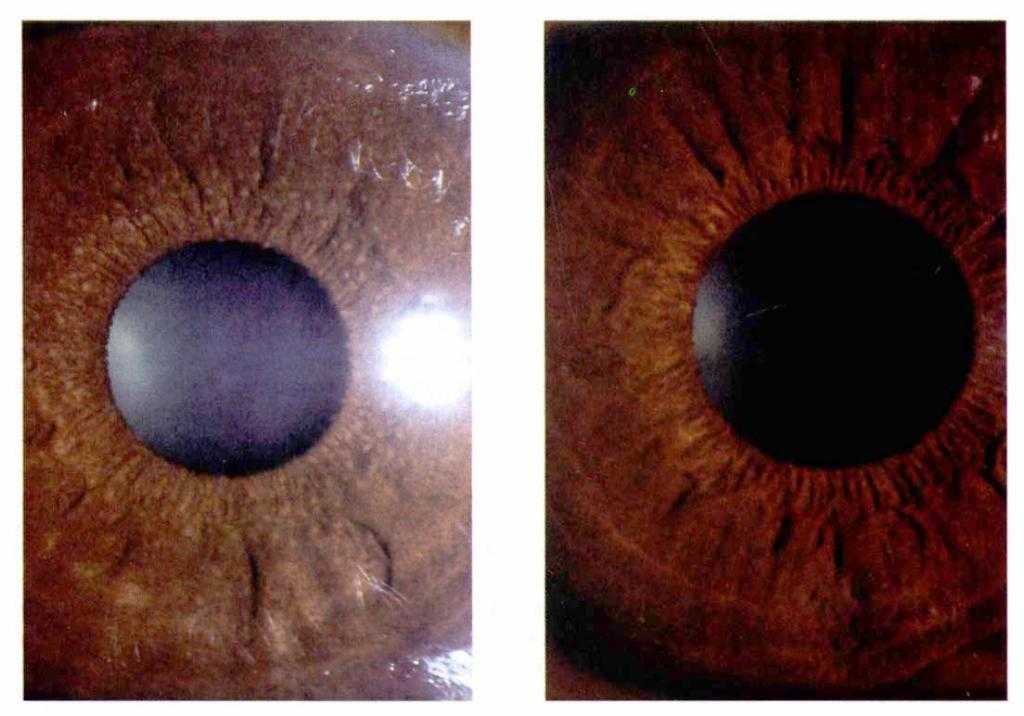
Диагноз кератоконуса ставится на основании биомикроскопии, офтальмометрии, рефрактометрии, кератометрии и кератотопографии. При кератоконусе выявляется выраженный астигматизм, чаще неправильный. Толщина роговицы в центре уменьшается, оптическая сила роговицы достигает 56-62 дптр. Этиопатогенез кератоконуса пока недостаточно выяснен. Корригируется контактными линзами, лечится пересадкой роговицы.
Кератоглобус отличается от кератоконуса шаровидной формой выпячивания роговицы, истонченной приблизительно на 1/3 толщины. Растягиваются периферические отделы роговицы. Чаще имеется близорукость и астигматизм с понижением зрения. Возникает в детском возрасте и медленно прогрессирует. Иногда сочетается с общей патологией (синдромом синих склер, тугоухостью, ломкостью костей). Заболевание, как правило, двустороннее. Наибольший эффект коррекции дают контактные линзы.
Плоская роговица встречается редко, может быть изолированной и в сочетании с другими аномалиями развития глаза (микрокорнеа, микрофтальм и др. ).
).
Мегалокорнеа бывает врожденной аномалией. Если горизонтальный размер роговицы новорожденного большее на 1 мм, то следует говорить о макрокорнеа. Мегалокорнеа бывает при детской глаукоме – гидрофтальм (hydrophthalmus congenitus), а также может возникнуть вследствие растяжения роговой оболочки при других заболеваниях глаза.
Микрокорнеа характеризуется уменьшением горизонтального диаметра роговицы и составляет меньше 10 мм. Это касается взрослых людей. Если у ребенка горизонтальный размер меньше на 1 мм по сравнению с возрастной нормой, то говорят о микрокорнеа. Иногда сочетается с другими аномалиями развития глаза (микрофтальм и др.). Радиус кривизны роговицы обычно уменьшен, рефракция может быть эмметропической, гиперметропической и редко миопической. Острота зрения нормальная или несколько понижена. Микрокорнеа, как и макрокорнеа осложняется глаукомой.
Микрофтальм может быть также следствием атрофия глазного яблока, в результате воспалительных заболеваний. Отсутствие роговицы может быть только при криптофтальме.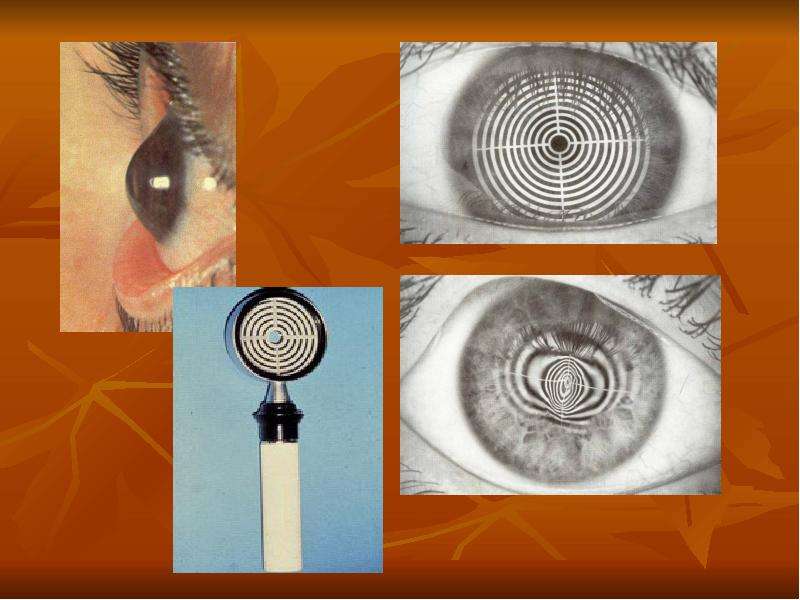
Врожденные помутнения роговицы встречаются редко. В связи с ростом роговицы, помутнения могут иногда почти полностью исчезать. Стабильные и выраженные помутнения с 3-х летнего возраста подлежат оперативному лечению.
ВОСПАЛИТЕЛЬНЫЕ ЗАБОЛЕВАНИЯ РОГОВИЦЫ
В патологии роговицы основное место занимают воспалительные процессы — кератиты и их последствия. Субъективными симптомами кератитов являются: светобоязнь, слезотечение, блефароспазм, боль, ощущение постороннего и снижение зрения. Объективные признаки — это нарушение прозрачности, зеркальности роговицы. К числу объективных симптомов относятся также перикорнеальная инъекция, врастание поверхностных и глубоких сосудов, расстройство чувствительности.
Общая симптоматология кератитов у детей такая же, как и у взрослых, за исключением некоторых форм кератитов, которые отличаются своеобразными особенностями клиники и течения процесса. О них будет указано при рассмотрении этих форм у взрослых.
Нарушение прозрачности выражается появлением в роговице помутнений, имеющих белый, серый или серовато-желтый цвет.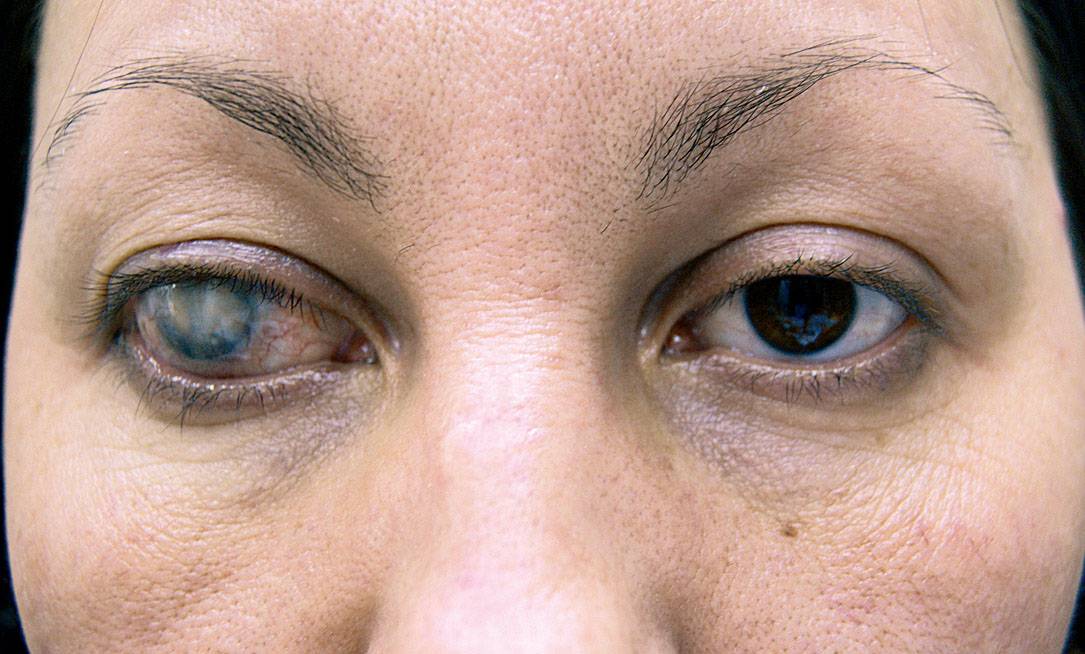 Помутнения могут быть воспалительного, дегенеративного происхождения или представляют последствия перенесенного воспаления роговицы. При старых помутнениях поверхность роговицы бывает блестящей, зеркальной, при свежей — становится тусклой, матовой, шероховатой, с образованием дефектов вещества. В отличие от дегенеративных помутнений, при которых инъекция встречается редко, при свежих помутнениях воспалительного характера имеется перикорнеальная инъекция различной интенсивности — от слабо розового венчика вокруг роговицы до темно-фиолетовой мрачной окраски, широким поясом охватывающего роговицу. В ряде случаев перикорнеальная инъекция может сочетаться с гиперемией конъюнктивы глазного яблока и тогда она определяется как смешанная инъекция глазного яблока. Анатомической основой помутнений при кератитах является инфильтрат, т.е. скопление в ткани роговицы клеток, проникающих сюда из краевой петлистой сети. Для диагностики имеет значение локализация инфильтрата, который может находиться в различных слоях роговой оболочки, а также его характер (диффузный или состоит из отдельных точек, черточек, узелков).
Помутнения могут быть воспалительного, дегенеративного происхождения или представляют последствия перенесенного воспаления роговицы. При старых помутнениях поверхность роговицы бывает блестящей, зеркальной, при свежей — становится тусклой, матовой, шероховатой, с образованием дефектов вещества. В отличие от дегенеративных помутнений, при которых инъекция встречается редко, при свежих помутнениях воспалительного характера имеется перикорнеальная инъекция различной интенсивности — от слабо розового венчика вокруг роговицы до темно-фиолетовой мрачной окраски, широким поясом охватывающего роговицу. В ряде случаев перикорнеальная инъекция может сочетаться с гиперемией конъюнктивы глазного яблока и тогда она определяется как смешанная инъекция глазного яблока. Анатомической основой помутнений при кератитах является инфильтрат, т.е. скопление в ткани роговицы клеток, проникающих сюда из краевой петлистой сети. Для диагностики имеет значение локализация инфильтрата, который может находиться в различных слоях роговой оболочки, а также его характер (диффузный или состоит из отдельных точек, черточек, узелков).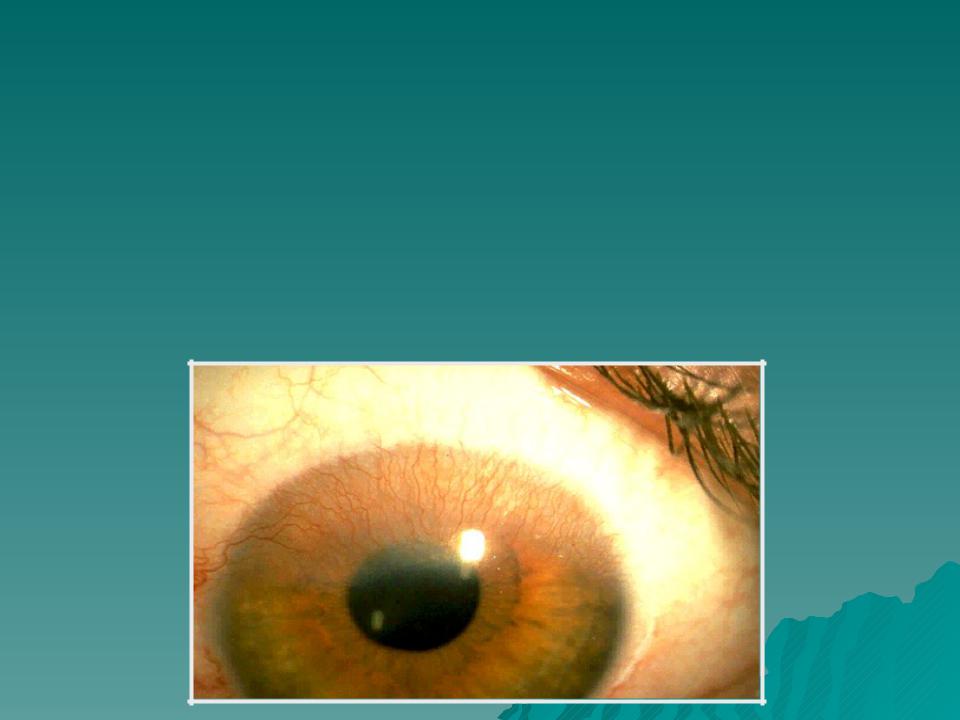 Цвет инфильтрата зависит от клеточного состава. Если лейкоцитов мало, он серый, если много — желтый. В процессе развития воспаления и увеличения количества лейкоцитов может происходить изменение его цвета. Края инфильтрата обычно стушеваны за счет перифокального отека роговицы. Инфильтрат может находиться в различных участках роговицы — как на периферии ее, так и в центральной зоне. Очень часто вслед за образованием инфильтрата, а иногда в периоде регрессии происходит прорастание сосудов в роговицу из конъюнктивальных, эписклеральных или склеральных сосудов. (Известно, что в нормальной роговице сосудов нет.) Соответственно в роговице различают поверхностные и глубокие сосуды. Поверхностные сосуды идут с конъюнктивы на роговицу через лимб в ее поверхностных слоях, свободно извиваясь и древовидно ветвясь, часто анастомозируя друг с другом. Они имеют ярко-красный цвет. Глубокие сосуды в лимбе не видны, а видны только в роговице. Они кажутся тусклыми, серовато-красными, идут прямолинейно, не анастомозируют друг с другом и часто имеют вид щеточек, метелочек или щетинок.
Цвет инфильтрата зависит от клеточного состава. Если лейкоцитов мало, он серый, если много — желтый. В процессе развития воспаления и увеличения количества лейкоцитов может происходить изменение его цвета. Края инфильтрата обычно стушеваны за счет перифокального отека роговицы. Инфильтрат может находиться в различных участках роговицы — как на периферии ее, так и в центральной зоне. Очень часто вслед за образованием инфильтрата, а иногда в периоде регрессии происходит прорастание сосудов в роговицу из конъюнктивальных, эписклеральных или склеральных сосудов. (Известно, что в нормальной роговице сосудов нет.) Соответственно в роговице различают поверхностные и глубокие сосуды. Поверхностные сосуды идут с конъюнктивы на роговицу через лимб в ее поверхностных слоях, свободно извиваясь и древовидно ветвясь, часто анастомозируя друг с другом. Они имеют ярко-красный цвет. Глубокие сосуды в лимбе не видны, а видны только в роговице. Они кажутся тусклыми, серовато-красными, идут прямолинейно, не анастомозируют друг с другом и часто имеют вид щеточек, метелочек или щетинок. Врастание сосудов в роговицу — это проявление компенсаторных и восстановительных процессов, свойственных организму.
Врастание сосудов в роговицу — это проявление компенсаторных и восстановительных процессов, свойственных организму.
Клетки стенок новообразованных сосудов и клетки роговицы являются тем материалом, которым заполняются дефекты ткани. Но эти восстановительные участки состоят из соединительной рубцовой ткани, которая оптически не прозрачна. Сосуды, которые вросли в роговицу остаются на всю жизнь. Они запустевают и видны только с помощью щелевой лампы в виде сероватых нитей.
Значительная часть кератитов сопровождается снижением чувствительности роговой оболочки, нередко и на втором глазу, а это говорит о том, что процесс не является чисто местным. Снижение чувствительности бывает чаще при нейрогенных кератитах. Потеря блеска зависит от нарушения целостности эпителия. Эпителий в области инфильтрации разрушается и эрозируется. В этом можно убедиться, если закапать 1% раствор флюоресцеина, который окрашивает эрозированную поверхность в зеленовато-желтоватый цвет. Сферичность изменяется в соответствии с массивностью и локализацией инфильтрации и отека ткани роговицы.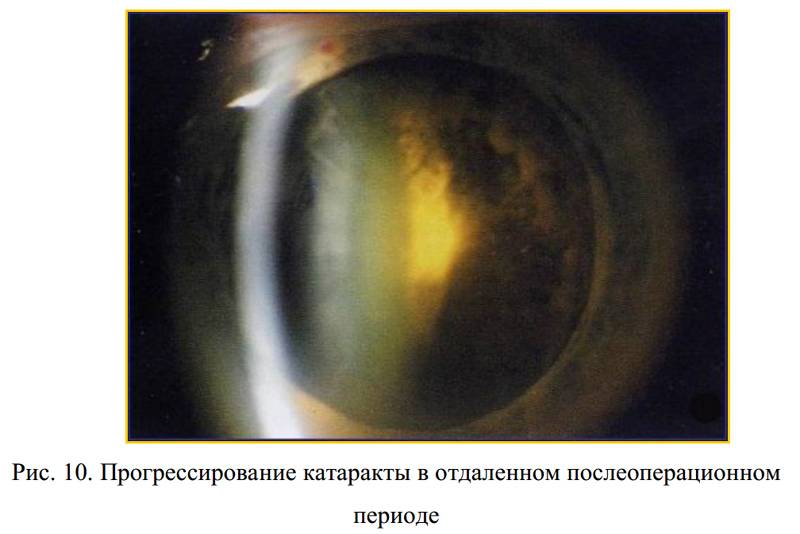 Судьба инфильтрата может быть различна. Небольшие поверхностные инфильтраты могут полностью рассосаться без последствий или оставить после себя чуть заметные помутнения (облачко). Более глубоко расположенные инфильтраты организуются и в результате остаются стойкие, поверхностные или глубокие помутнения — пятно, лейкома. Если помутнение расположено в центре, то значительно снижается острота зрения. Инфильтрат может изъязвиться и даже закончиться прободением роговицы. В отверстие может выпасть радужка, которая затем срастается с краями отверстия и образуется бельмо сращенное с радужкой. Может развиться эндофтальмит и панофтальмит.
Судьба инфильтрата может быть различна. Небольшие поверхностные инфильтраты могут полностью рассосаться без последствий или оставить после себя чуть заметные помутнения (облачко). Более глубоко расположенные инфильтраты организуются и в результате остаются стойкие, поверхностные или глубокие помутнения — пятно, лейкома. Если помутнение расположено в центре, то значительно снижается острота зрения. Инфильтрат может изъязвиться и даже закончиться прободением роговицы. В отверстие может выпасть радужка, которая затем срастается с краями отверстия и образуется бельмо сращенное с радужкой. Может развиться эндофтальмит и панофтальмит.
Симптоматика кератитов зависит от причины, путей распространения заболевания, локализации поражения, состояния оболочек глаза и общего состояния организма. Сходная клиническая картина и симптоматика кератитов различного происхождения создают трудности для выяснения этиологии процесса. Поэтому до настоящего времени нет такой классификации, которая бы удовлетворяла врачей в практической работе.
Наиболее принятой классификацией является следующая:
- Экзогенные кератиты
- Кератиты, обусловленные механической, химической или физической травмой.
- Инфекционные кератиты бактериального и вирусного происхождения.
- Кератиты, обусловленные заболеваниями конъюнктивы, век, мейбомиевых желез.
- Грибковые кератиты.
- Паразитарные (акантамебы)
- Эндогенные кератиты
- Туберкулезные: гематогенные и аллергические.
- Сифилитические.
- Бруцеллезные.
- Лепрозные.
- При малярии.
- Герпетические кератиты.
- Нейропаралитические.
- Кератиты при общих инфекционных заболеваниях.
- Авитаминозные.
- Кератиты невыясненной этиологии.
- Прочие.
ЭКЗОГЕННЫЕ КЕРАТИТЫ
Инфекционные кератиты бактериального происхождения
Ползучая язва до эры сульфаниламидов и антибиотиков протекала очень тяжело, часто оканчивалась слепотой. Ползучая язва роговицы вызывается чаще пневмококком, реже стафилококком и стрептококком, синегнойной палочкой, которые внедряются в ткань роговицы через дефект в ее поверхности. Пневмококки и другая флора находятся в конъюнктивальной полости при конъюнктивите, а также как сапрофит во флоре конъюнктивального мешка здоровых людей. В 50% случаев диплококк находится в слезном мешке при хроническом его воспалении (дакриоцистит). Внедрившийся в роговицу, чаще пневмококк, благодаря своим мощным протеолитическим свойствам вызывает довольно быстро бурный воспалительно-некротический процесс. При типичном течении ползучей язвы роговицы в первые сутки появляется инфильтрат, имеющий желтовато-гнойный оттенок. Гнойная инфильтрация находится ближе к какой-либо одной стороне дефекта, в эту сторону и начинает распространяться инфильтрат. Распространение идет как по поверхности, так и в глубину. Заболевание сопровождается сильными режущими болями, слезотечением, светобоязнью, блефароспазмом, выраженной смешанной инъекцией глазного яблока и хемозом конъюнктивы.
Ползучая язва роговицы вызывается чаще пневмококком, реже стафилококком и стрептококком, синегнойной палочкой, которые внедряются в ткань роговицы через дефект в ее поверхности. Пневмококки и другая флора находятся в конъюнктивальной полости при конъюнктивите, а также как сапрофит во флоре конъюнктивального мешка здоровых людей. В 50% случаев диплококк находится в слезном мешке при хроническом его воспалении (дакриоцистит). Внедрившийся в роговицу, чаще пневмококк, благодаря своим мощным протеолитическим свойствам вызывает довольно быстро бурный воспалительно-некротический процесс. При типичном течении ползучей язвы роговицы в первые сутки появляется инфильтрат, имеющий желтовато-гнойный оттенок. Гнойная инфильтрация находится ближе к какой-либо одной стороне дефекта, в эту сторону и начинает распространяться инфильтрат. Распространение идет как по поверхности, так и в глубину. Заболевание сопровождается сильными режущими болями, слезотечением, светобоязнью, блефароспазмом, выраженной смешанной инъекцией глазного яблока и хемозом конъюнктивы.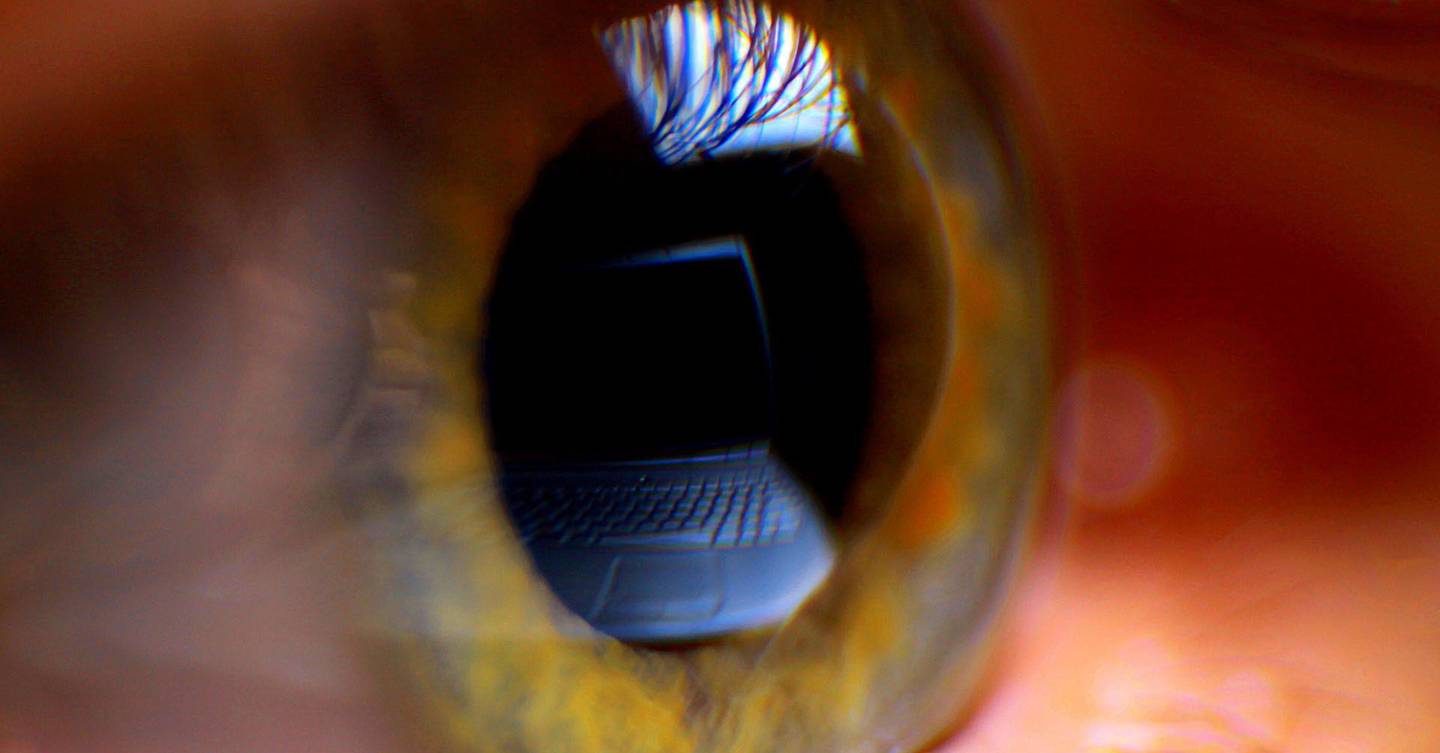 В следующие дни инфильтрат заметно продвигается в прозрачную часть роговицы, изъязвляется. Прогрессирующий край язвы — подрытый, регрессивный — покатый. Регрессивный край быстро покрывается эпителием и очищается. Постепенно очищается вся язва, эпителий покрывает дно язвы, образуя фасетку в роговице. Затем ткань роговицы в месте язвы заменяется соединительной тканью, которая нарушает прозрачность роговицы. При проникновении язвы вглубь роговицы основное препятствие встречается со стороны десцеметовой оболочки, которая оказывается наиболее устойчивой к разъедающему действию пневмококка, чем другой флоры. Здесь дальнейшее прогрессирование язвенного процесса может остановиться. Десцеметова оболочка под влиянием внутриглазного давления в виде прозрачного пузырька – десцеметоцеле (грыжа — descemetoсele) выпячивается в отверстие, образованное язвой. В случае прободения роговицы, может образоваться сращенное бельмо роговицы, панофтальмит, атрофия глазного яблока с необратимой слепотой. В передней камере гной (hypopyon), состоящий из фибрина и лейкоцитов.
В следующие дни инфильтрат заметно продвигается в прозрачную часть роговицы, изъязвляется. Прогрессирующий край язвы — подрытый, регрессивный — покатый. Регрессивный край быстро покрывается эпителием и очищается. Постепенно очищается вся язва, эпителий покрывает дно язвы, образуя фасетку в роговице. Затем ткань роговицы в месте язвы заменяется соединительной тканью, которая нарушает прозрачность роговицы. При проникновении язвы вглубь роговицы основное препятствие встречается со стороны десцеметовой оболочки, которая оказывается наиболее устойчивой к разъедающему действию пневмококка, чем другой флоры. Здесь дальнейшее прогрессирование язвенного процесса может остановиться. Десцеметова оболочка под влиянием внутриглазного давления в виде прозрачного пузырька – десцеметоцеле (грыжа — descemetoсele) выпячивается в отверстие, образованное язвой. В случае прободения роговицы, может образоваться сращенное бельмо роговицы, панофтальмит, атрофия глазного яблока с необратимой слепотой. В передней камере гной (hypopyon), состоящий из фибрина и лейкоцитов.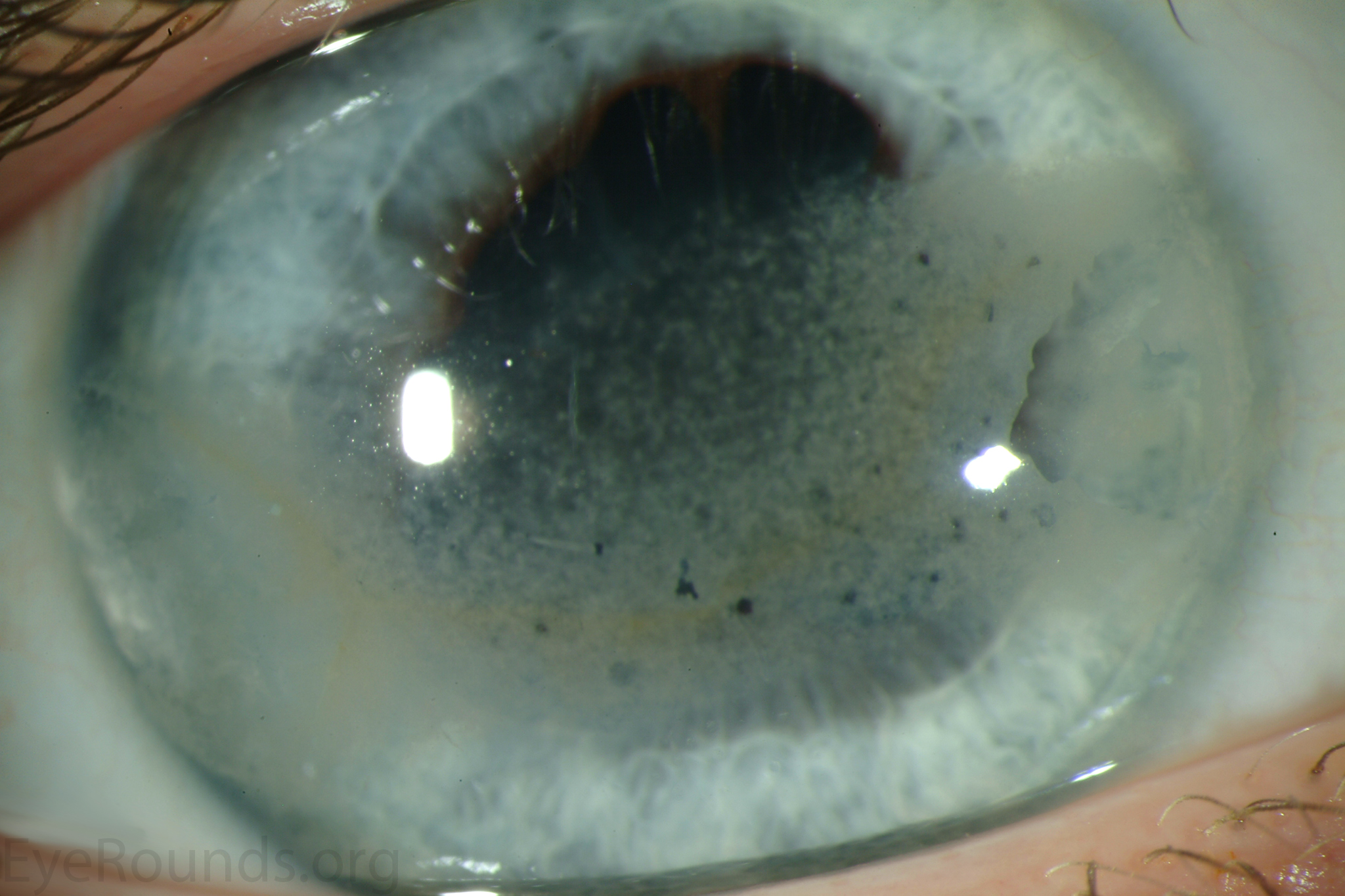 До прободения язвы гной стерильный, т.к. возникает под действием токсинов.
До прободения язвы гной стерильный, т.к. возникает под действием токсинов.
Бактериальные язвы могут вызываться синегнойной палочкой. Инфильтрат имеет желто-зеленый цвет, образованная язва быстро расплавляет роговицу, уже на 2-3-й день болезни происходит перфорация, эндофтальмит и гибель глаза. Язва роговицы – наиболее тяжелое осложнение при использовании мягких контактных линз длительного ношения, с контактными линзами связан большой процент бактериальных кератитов.
Разъедающая язва Мурена, описанная в 1876 году — хроническая прогрессирующая краевая язва иммунного генеза. Чаще встречается у пожилых людей, у 25 % больных она бывает двусторонней. Образование краевой язвы сопровождается поверхностной инфильтрацией роговой оболочки у ее края. Неглубокие дефекты сливаясь, принимают форму полнолуния. Край язвы резко подрыт. Язва прогрессирует в течение нескольких месяцев, сопровождается сильными болями. Нередко сопутствует хронический циклит. Периферические кератиты имеют иммунный генез и обычно возникают при системных заболеваниях (гранулематоз Вегенера, узелковый периартериит, ревматоидный артрит и др. ) или возникают как токсико-аллергические реакции на лекарственные препараты или стафилококковую инфекцию конъюнктивы и краев век.
) или возникают как токсико-аллергические реакции на лекарственные препараты или стафилококковую инфекцию конъюнктивы и краев век.
Гранулематоз Вегенера – это хронический неспецифический воспалительный процесс, сопровождающийся образованием некротических гранулем. Причиной дальнейших симптомов является некротическое гранулематозное воспаление кровеносных сосудов, начиная от верхних дыхательных путей, далее поражаются мягкие ткани и кости. Иногда эти гранулемы напоминают специфические гранулемы при сифилисе, туберкулезе, саркоидозе Бека.
Грибковые кератиты вызывают лучистые, плесневые и дрожжевые грибы после даже незначительных повреждений роговицы. Могут переходить с кожных покровов. Грибы проникают в глубокие слои роговицы. Субъективные симптомы выражены слабо. Воспалительный очаг в роговице имеет белую или желтоватую окраску, четкие границы, как бы состоит из крупинок. Очаг окружен ограниченным валиком инфильтрации. Неоваскуляризация отсутствует. При ползучих язвах грибковой этиологии имеется гипопион. Течение заболевания длительное. Возможна перфорация роговицы с образованием грубого бельма. Диагноз подтверждается микроскопическим исследованием соскоба.
Течение заболевания длительное. Возможна перфорация роговицы с образованием грубого бельма. Диагноз подтверждается микроскопическим исследованием соскоба.
Принципы лечения язв роговицы различного происхождения предложил Ю.Ф.Майчук (1999 – 2003). Лечение с использованием лекарственных препаратов, успешно вошедших в практику в последние годы включает специфическую и патогенетическую фармакотерапию.
Тяжелая герпетическая язва. Противовирусная терапия – Зовиракс, 3 % глазная мазь, 5 раз в сутки или Локферон 8 000 МЕ/мл, инстилляции 8 раз в сутки. Можно сочетать оба препарата, сокращая число закапываний. Валтрекс, таблетки 500 мг, 2 раза в сутки, или Зовиракс, таблетки 200 мг, 5 раз в сутки. Метаболическая терапия – глазные капли Витасик, Тауфон, Витайодурол, Слеза натуральная, Корнерегель или Солкосерил 2 раза в сутки. Антиаллергическая, противовоспалительная – капли Лекролин и Наклоф 2 раза в сутки.
Иммуномодулирующая и системная терапия показана при затяжном тяжелом течении или при частых рецидивах (Лекопид, Такривин).
Гипотензивная, в случае вторичной глаукомы или глазной гипертензии – тимолол, трусопт 2 раза в сутки.
Общеукрепляющая, антиоксидантная терапия – тауфон в/м или гистохром парабульбарно.
Язва роговицы, вызванная синегнойной палочкой. Антибактериальная терапия местно: Окацин, Тобрамицин, Гентамицин + Полимиксин. Глазные капли Окацин или Флоксал закапывать 6 раз в сутки, или сочетание двух антибиотиков Окацина или Флоксала с Тобромицином. Парабульбарно: тобромицин (гентамицин), Цефотоксим. Системно: Ципрофлоксацин в таблетках или Гентамицин (Тобромицин), Цефтазидин в инъекциях.
Антиаллергическая – глазные капли Лекролин или Сперсаллерг 2 раза в сутки. Глазная мазь – Пренацид или Гидрокортизон на веки при явлениях блефарита. Парабульбарно: инъекции Гистохрома (10 дней) или Дексаметазона 2-3 дня (при выраженном раздражении). Внутрь – Кларитин по 1 таб. в сутки 5-7 дней.
Метаболическая – глазные капли Витасик, Вита-йодурол, Тауфон, Слеза натуральная, Лакрисифи.
Язва роговицы вызванная стафилококком, стрептококком, пневмококком. Антибактериальная. Местно: Окацин, Витабакт, Сульфацил-натрия, Флоксал, Тетрациклин, Гентамицин, Эритромицин 4-6 раз в сутки. Парабульбарно: Тобрамицин, Гентамицин, Амикацин, Цефазолин. Системно: Таваник, Максаквин, Эритромицин, Доксициклин, Цефазолин. Антиаллергическая, противовоспалительная – капли Лекролин и Наклоф 2 раза в сутки. Метаболическая – глазные капли Витасик, Вита-йодурол, Карнозин, Тауфон 2 раза в сутки.
Язва роговицы грибковая. Противогрибковая терапия. Местно: суспензия кетаконазола, капли флуконазола, мазь миконазола 4 раза в сутки. Промывание конъюнктивального мешка раствором борной кислоты.
Внутрь: низорал 200 мг, 2 раза в сутки, итраконазол 100 мг, 2 раза в сутки, дифлокан 50 мг, 1 раз в сутки.
Антиаллергическая, противовоспалительная: глазные капли Сперсаллерг (при сильном раздражении) или Лекролин (при умеренном раздражении), Наклоф. Парабульбарно: дексаметазон 0,3 мл 1 раз в первый день (при тяжелом течении).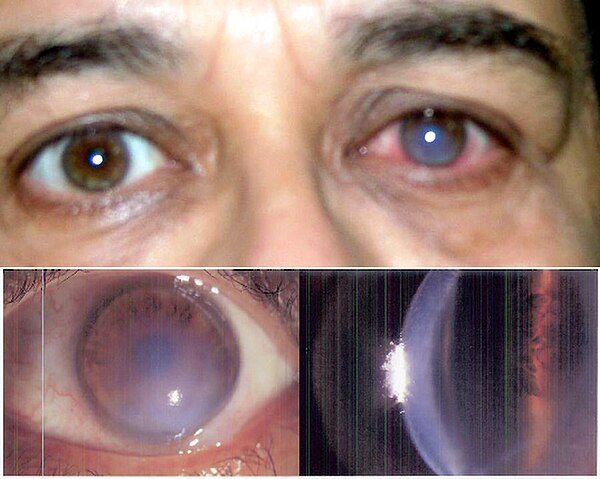
Метаболическая – глазные капли Витасик, Вита-йодурол, Карнозин, Тауфон 2 раза в сутки.
Гипотензивная – тимолол, трусопт 2 раза в сутки (по показаниям).
Язва роговицы акантамебная (кератит акантамебный). Антипаразитарная терапия. Местно: Окацин, Неомицин, Кетаконазол, Хлороксидин в виде глазных капель. Внутрь: Кетокеназол, Низорал 200 мг, 2 раза в сутки, итраконазол 100 мг, 2 раза в сутки.
Антиаллергическая, противовоспалительная: глазные капли Наклоф, Лекролин,. Парабульбарно: дексаметазон 0,3 мл 1 раз в день, 1-2 дня.
Метаболическая –Витасик, Вита-йодурол, Тауфон 2 раза в сутки.
Гипотензивная – глазные капли тимолол, трусопт 2 раза в сутки (по показаниям).
Язва роговицы, вызванная гонококком. Антибактериальная терапия. Местно: промывание раствором борной кислоты. Инстилляции Окацина, Пенициллина 6-8 раз в сутки. Системно: Таваник по 1 таб. 2 раза в сутки или пенициллин внутримышечно. Антиаллергическая, противовоспалительная: Сперсаллерг или Наклоф 2 раза в сутки. Кларитин по 1 таб. в сутки. Метаболическая – глазные капли Витасик, Вита-йодурол, Карнозин, Тауфон 2 раза в сутки.
Кларитин по 1 таб. в сутки. Метаболическая – глазные капли Витасик, Вита-йодурол, Карнозин, Тауфон 2 раза в сутки.
Рецидивирующая эрозия роговицы. Метаболическая – глазные капли Витасик, Вита-йодурол, Карнозин, Тауфон, Цитохром инстилляции 4-5 раз в сутки. Глазной гель Корнерегель, Солкосерил 2 раза в день. Антиаллергическая Глазные капли Лекролин или Сперсаллерг 1-2 раза в сутки. При сильных болях – глазной гель Актовегин, Слеза натуральная, Видисик гель, на ночь. При лабораторном подтверждении герпевирусной инфекции – антигерпетическое лечение – глазная мазь Зовиракс 3-4 раза в сутки. Глазные капли интерферона – локферон, 4-6 раз в сутки.
При бактериальной инфекции – глазные капли Витабакт, Окацин, Тетрациклин 3 раза в сутки. При упорных рецидивах – эксимер-лазерная фототерапевтическая кератэктомия. Метаболическая терапия – глазные капли Витасик, Вита-йодурол, Карнозин, Тауфон 2 раза в сутки. Антиаллергическая, противовоспалительная: Лекролин, Сперсаллерг или Наклоф 2 раза в сутки.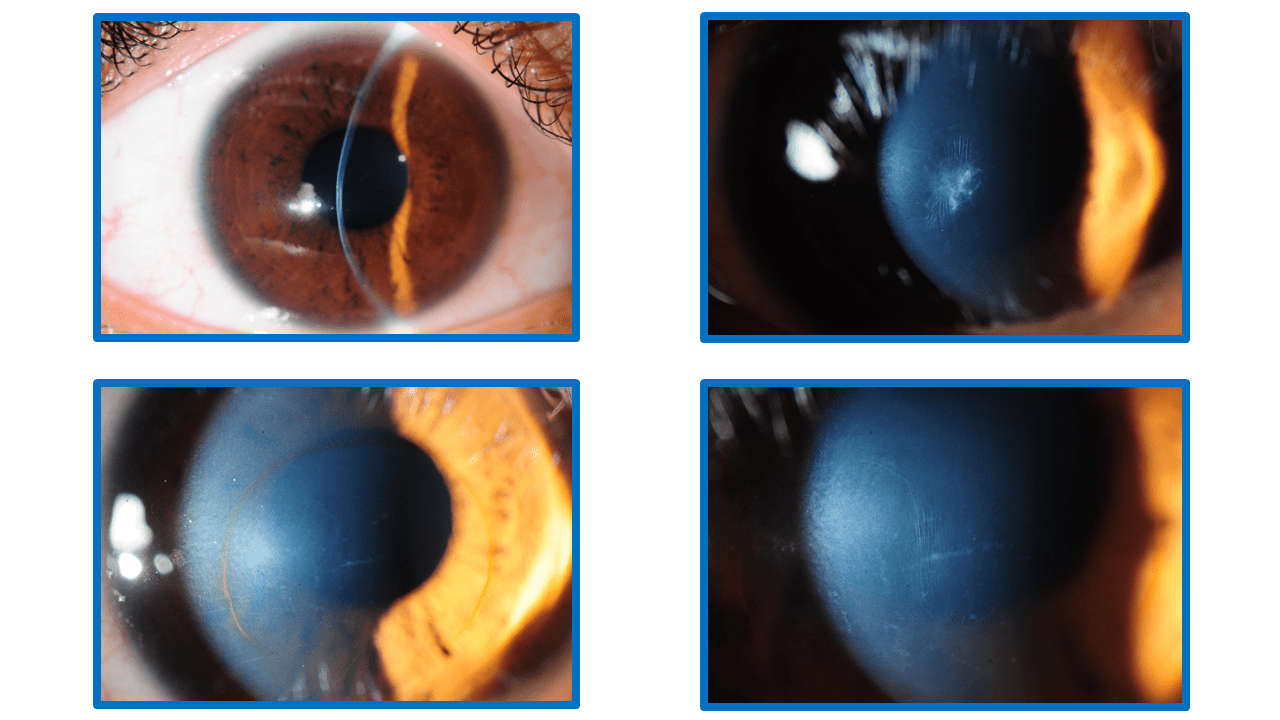 При бурном течении парабульбарно дексаметазон 0,3 мл в первый день, внутрь — Кларитин по 1 таб. в сутки, 3 дня.
При бурном течении парабульбарно дексаметазон 0,3 мл в первый день, внутрь — Кларитин по 1 таб. в сутки, 3 дня.
Герпетические заболевания роговицы . Возбудителем является вирус простого герпеса – ВПГ-1, выделяемый из слизистой полости рта, носоглотки, глаз, кожи и ВПГ-2 или генитальный тип, выделяемый, главным образом, со слизистых генитальных органов. В настоящее время выделено 8 типов герпевирусов у человека. Герпес 1 и 2 типа – возбудители герпетической инфекции. Герпес 3 типа , или герпес варицелла зостер – возбудитель ветряной оспы и опоясывающего лишая. Герпес 4 типа – вирус Эпштейна-Барр, возбудитель инфекционного мононуклеоза. Герпес 5 типа – возбудитель цитомегаловирусной инфекции.
Вирус простого герпеса относится к ДНК-содержащим вирусам. Постоянным хозяином вируса является человек. Заражение может произойти во время родов, когда вирус попадает из зараженных половых путей матери в верхние дыхательные пути и конъюнктиву новорожденных. Позднее при поцелуе, при кормлении с ложки, побывавшей во рту матери, через игрушки, предметы обихода..jpg) Путь передачи может быть и воздушно-капельный.
Путь передачи может быть и воздушно-капельный.
При проникновении в организм возбудитель через кожный покров и слизистые оболочки проникает в лимфатические узлы, кровь, а затем в различные органы и ткани, и наконец, в нервные ганглии. Здесь первоначальный штамм остается на всю жизнь, а персистирующие в ганглиях вибрионы и вызывают рецидивы заболевания. Поражаются преимущественно клетки эпителиального происхождения. Может быть врожденная и приобретенная герпетическая инфекция. Приобретенная может быть первичной и рецидивирующей. Наиболее частой формой первичной герпетической инфекции является острый герпетический стоматит. Наиболее частой формой рецидивирующей герпетической инфекции является поражение кожи и слизистых.
Офтальмогерпес – это распространенная тяжелая форма рецидивирующей герпетической инфекции.
Генитальный герпес чаще вызывается ВПГ-2, он может быть первичным и рецидивирующим. Поражение ЦНС может быть проявлением, как первичной, так и рецидивирующей инфекции, как ВПГ-1, так и ВПГ-2 и развивается в виде серозного менингита, энцефалита, менингоэнцефалита. Генерализованная форма герпетической инфекции встречается, как правило, у новорожденных и лиц с тяжелым нарушением иммунной системы.
Генерализованная форма герпетической инфекции встречается, как правило, у новорожденных и лиц с тяжелым нарушением иммунной системы.
Герпетическая инфекция относится, как и аденовирусная, к инфекциям, которые долго, иногда всю жизнь могут оставаться латентными (в коже, слизистых, слюнных и слезных железах, в тканях глаза, в нервных ганглиях тройничного и пояснично-крестцового нерва, в эритроцитах и лейкоцитах). Факторами, провоцирующими герпес, являются лихорадочные заболевания, микротравмы роговицы, переохлаждения и перегревания, отрицательные аффекты. У детей – детские инфекции, профилактические прививки. Рецидивы заболевания связывают с хроническими заболеваниями носоглотки и полости рта, а также с туберкулезными и аллергическими состояниями.
Герпетические кератиты бывают первичные и послепервичные. Первичные герпетические кератиты выявляются в 25 % случаев герпетических кератитов у детей. Инфицирование происходит в возрасте от 5-6 месяцев до 5 лет (Е.И.Сидоренко, 2002).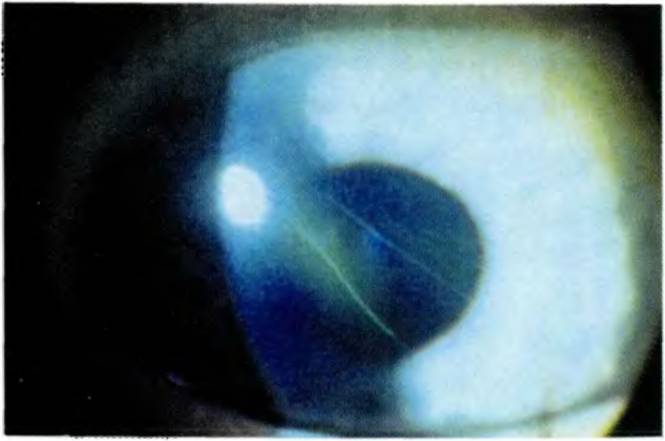 Одновременно с заболеваниями роговицы бывают пузырьковые высыпания на губах, крыльях носа, веках и других местах, как кожи, так и слизистых оболочек. Заболевание начинается с корнеального синдрома, затем появляются сероватые очаги помутнений в роговице и образуются пузырьки (везикулы). Это – мелкие, полупрозрачные пузырьки, которые довольно быстро лопаются и образуются язвочки. Регенерирует эпителий очень медленно, чувствительность роговицы резко снижается. Но, как правило, везикулярные инфильтраты сливаются, переходя в древовидный кератит или метагерпетический кератит с иридоциклитом. Заболевание протекает длительно и тяжело с частыми рецидивами и обострениями.
Одновременно с заболеваниями роговицы бывают пузырьковые высыпания на губах, крыльях носа, веках и других местах, как кожи, так и слизистых оболочек. Заболевание начинается с корнеального синдрома, затем появляются сероватые очаги помутнений в роговице и образуются пузырьки (везикулы). Это – мелкие, полупрозрачные пузырьки, которые довольно быстро лопаются и образуются язвочки. Регенерирует эпителий очень медленно, чувствительность роговицы резко снижается. Но, как правило, везикулярные инфильтраты сливаются, переходя в древовидный кератит или метагерпетический кератит с иридоциклитом. Заболевание протекает длительно и тяжело с частыми рецидивами и обострениями.
Послепервичные герпетические кератиты бывают у детей старше трех лет, а у взрослых чаще в возрасте 20-40 лет и появляются на фоне общего ослабления организма, снижения его сопротивляемости, преимущественно зимой и осенью. Ремиссии более продолжительные.
Чаще встречаются древовидный, метагерпетический и стромальный. Как правило, заболевает один глаз и лишь иногда – два. Мелкие пузырьки и поверхностные инфильтраты, соединяясь между собой, образуют различные фигуры в виде небольших веточек. Форма их разная, но характерным являются утолщения по ходу помутнений. Древовидный кератит сопровождается, кроме свойственной кератитам симптоматики, неврологическими болями по ходу первой и второй ветви тройничного нерва. После слущивания эпителия воспалительный очаг превращается в поверхностную язву, окруженную мутным, приподнятым эпителием. Течение длительное. Древовидный кератит может распространяться на глубокие слои стромы, трансформируясь в дисковидный или в диффузный интерстициальный кератит. Нередко древовидный кератит переходит в кератоувеит, при котором инфильтраты располагаются глубоко в строме роговицы. Затем образуется большой очаг изъязвления, который местами рубцуется, местами появляются эпителиальные вздутия, пузырьки. Отек, то уменьшается, то усиливается. При иридоциклите, кроме преципитатов может появиться гипопион.
Как правило, заболевает один глаз и лишь иногда – два. Мелкие пузырьки и поверхностные инфильтраты, соединяясь между собой, образуют различные фигуры в виде небольших веточек. Форма их разная, но характерным являются утолщения по ходу помутнений. Древовидный кератит сопровождается, кроме свойственной кератитам симптоматики, неврологическими болями по ходу первой и второй ветви тройничного нерва. После слущивания эпителия воспалительный очаг превращается в поверхностную язву, окруженную мутным, приподнятым эпителием. Течение длительное. Древовидный кератит может распространяться на глубокие слои стромы, трансформируясь в дисковидный или в диффузный интерстициальный кератит. Нередко древовидный кератит переходит в кератоувеит, при котором инфильтраты располагаются глубоко в строме роговицы. Затем образуется большой очаг изъязвления, который местами рубцуется, местами появляются эпителиальные вздутия, пузырьки. Отек, то уменьшается, то усиливается. При иридоциклите, кроме преципитатов может появиться гипопион. Процесс длится месяцами.
Процесс длится месяцами.
Дисковидный кератит в типичных случаях начинается с отека эпителия в центральной или парацентральной зоне роговицы, затем он распространяется на строму, которая утолщается и формируется круглый очаг в толще стромы, серовато-белого цвета, нередко с белым пятнышком в центре (некроз). Соответственно диску на задней поверхности роговицы преципитаты. Часто бывает серозный иридоциклит. Инфильтрат замещается соединительной тканью, зрение резко снижается. Дисковидный кератит может перейти в глубокий интерстициальный кератит, осложниться воспалением увеального тракта, вторичной гипертензией.
Кератиты вызываемые вирусом варицелла зостер – это воспаление роговицы в двух несходных клинических формах, у детей в период острой инфекции ветряной оспы или кератит герпес у взрослых, перенесших в детстве ветряную оспу. В организм человека вирус опоясывающего герпеса находятся в клетках межпозвоночных ганглиев или ганглиев черепных нервов, где он пребывает в латентном состоянии. Переход этого вируса из латентного состояния в активное клинически проявляется общими инфекционными симптомами, такими как головная боль, общая слабость, субфебрильная температура, озноб, парестезии. Отмечается болезненность и припухание регионарных лимфатических узлов и такое состояние диагностируют как грипп, ОРВИ, аденовирусная инфекция и др. через 2-3 дня появляются односторонние высыпания в зоне иннервации первой ветви тройничного нерва. Следующие 2-3 недели на месте везикул появляются коричневые корочки, которые затем отпадают. При поражении первой ветви тройничного нерва отмечаются выраженные боли в области глазного яблока, орбиты. Наблюдается отек век, гиперемия конъюнктивы, инъекция сосудов склеры, нарушения чувствительности, развиваются явления ганглионеврита. Спустя неделю на коже лба и волосистой части головы появляются герпетические высыпания – пузырьки, заполненные мутной жидкостью, через несколько дней они лопаются и покрываются корочками, которые постепенно отпадают. Через 7 недель развивается альтернирующий синдром в виде контрлатеральной гемиплегии, вследствие прямой инвазии вирусов в кровеносные сосуды и развитием церебрального гранулематозного некротического ангиита.
Переход этого вируса из латентного состояния в активное клинически проявляется общими инфекционными симптомами, такими как головная боль, общая слабость, субфебрильная температура, озноб, парестезии. Отмечается болезненность и припухание регионарных лимфатических узлов и такое состояние диагностируют как грипп, ОРВИ, аденовирусная инфекция и др. через 2-3 дня появляются односторонние высыпания в зоне иннервации первой ветви тройничного нерва. Следующие 2-3 недели на месте везикул появляются коричневые корочки, которые затем отпадают. При поражении первой ветви тройничного нерва отмечаются выраженные боли в области глазного яблока, орбиты. Наблюдается отек век, гиперемия конъюнктивы, инъекция сосудов склеры, нарушения чувствительности, развиваются явления ганглионеврита. Спустя неделю на коже лба и волосистой части головы появляются герпетические высыпания – пузырьки, заполненные мутной жидкостью, через несколько дней они лопаются и покрываются корочками, которые постепенно отпадают. Через 7 недель развивается альтернирующий синдром в виде контрлатеральной гемиплегии, вследствие прямой инвазии вирусов в кровеносные сосуды и развитием церебрального гранулематозного некротического ангиита. Этому способствует также склонность к повышенному тромбообразованию у больных опоясывающим герпесом.
Этому способствует также склонность к повышенному тромбообразованию у больных опоясывающим герпесом.
Ю.Ф.Майчук (2003) приводит следующую частоту клинических проявлений глазного герпеса зостера. Везикулярная сыпь на верхних веках (95 %) сопровождается сильным отеком, а в 12 % — выраженным птозом. Резко выраженное раздражение конъюнктивы возникает в 30 %, а в 4 5 сопровождается фолликулярной реакцией. Эпителиальный кератит выявлен у 14 % больных, реже дисковидный (3 %), наиболее часто стромальный кератит с изъязвлением – у 60 % больных. Повышение внутриглазного давления обнаруживается часто , в 77 % случаев. Следует иметь в виду, что в течение 10 дней от начала воспалений больной опоясывающим герпесом является источником заражения ветряной оспой. Отдаленные последствия – помутнение роговицы, вторичная глаукома, хронический или рецидивирующий увеит, снижение чувствительности роговицы. Глазной зостер часто сопровождается тяжелой длительной невралгией.
Диагностика герпетического кератита. вирусологическая, серологическая – реакция нейтрализации вируса сывороткой больного и РСК, внутрикожные пробы – реакция на антиген вируса герпеса, цитологические методы диагностики, которые являются наиболее простыми методами.
вирусологическая, серологическая – реакция нейтрализации вируса сывороткой больного и РСК, внутрикожные пробы – реакция на антиген вируса герпеса, цитологические методы диагностики, которые являются наиболее простыми методами.
Лечение: должно быть направлено на борьбу с вирусом герпеса, с воспалительной реакцией, на усиление сопротивляемости организма, стимуляцию регенераторной способности роговицы. Первым препаратом селективного противовирусного действия был диоксуридин (0,1 % офтан-иду), который и сегодня остается в офтальмологической практике для лечения герпетических конъюнктивитов и поверхностных кератитов. Затем в практику вошли отечественные противовирусные препараты: оксолиновая мазь 0,25 – 0,5 %, теброфеновая мазь 0,5-1,0 %, 3-4 раза в день, 0,5-1,0 % флореналь в виде капель, мази и глазных лекарственных пленок, 0,05 % бонафтоновая мазь 3 раза в день, при вирусемии бонафтон дают внутрь по 50 мг 4 раза в день.
Наиболее эффективным и менее токсичным является ацикловир (зовиракс), который избирательно действует на вирусы простого герпеса 1 и 2, вирус варицелла зостер, Эпштейна-Бара и цитомегаловирус. Кроме 3 % мази ацикловир применяется внутривенно по 250 мг три раза в сутки, в течение 7-10 дней. И в таблетках по 0,2, 5 раз в день в течение 5-ти дней. Сходным действием обладает фамцикловир, его дают по 250 мг 3 раза в сутки в течение 7 дней. При герпес зостер лечение кератитов имеет свои особенности. Необходимы высокие дозы противовирусных средств в 2-3 раза превышающие при герпетическом кератите, вызванном вирусом простого герпеса. Применяют дополнительное системное и местное лечение в связи со значительными кожными поражениями. Валтрекс – ацикловир второго поколения применяют 2 раза в день в таблетках по 500 мг, в течение 5 дней. При острых кожных проявлениях ацикловир (зовиракс) назначают внутрь по 600-800 мг 5 раз в день или Валтрекс по 1,0 2-3 раза в день, 7-10 дней. Внутривенно в связи с интоксикацией назначают капельно дезинтоксикационные препараты – гемодез, 5 % раствор глюкозы.
Кроме 3 % мази ацикловир применяется внутривенно по 250 мг три раза в сутки, в течение 7-10 дней. И в таблетках по 0,2, 5 раз в день в течение 5-ти дней. Сходным действием обладает фамцикловир, его дают по 250 мг 3 раза в сутки в течение 7 дней. При герпес зостер лечение кератитов имеет свои особенности. Необходимы высокие дозы противовирусных средств в 2-3 раза превышающие при герпетическом кератите, вызванном вирусом простого герпеса. Применяют дополнительное системное и местное лечение в связи со значительными кожными поражениями. Валтрекс – ацикловир второго поколения применяют 2 раза в день в таблетках по 500 мг, в течение 5 дней. При острых кожных проявлениях ацикловир (зовиракс) назначают внутрь по 600-800 мг 5 раз в день или Валтрекс по 1,0 2-3 раза в день, 7-10 дней. Внутривенно в связи с интоксикацией назначают капельно дезинтоксикационные препараты – гемодез, 5 % раствор глюкозы.
Пораженную кожу век и лица смазывают подсушивающими и антисептическими растворами – бриллиантового зеленого, 10 % метиленового синего или жидкости Кастелани.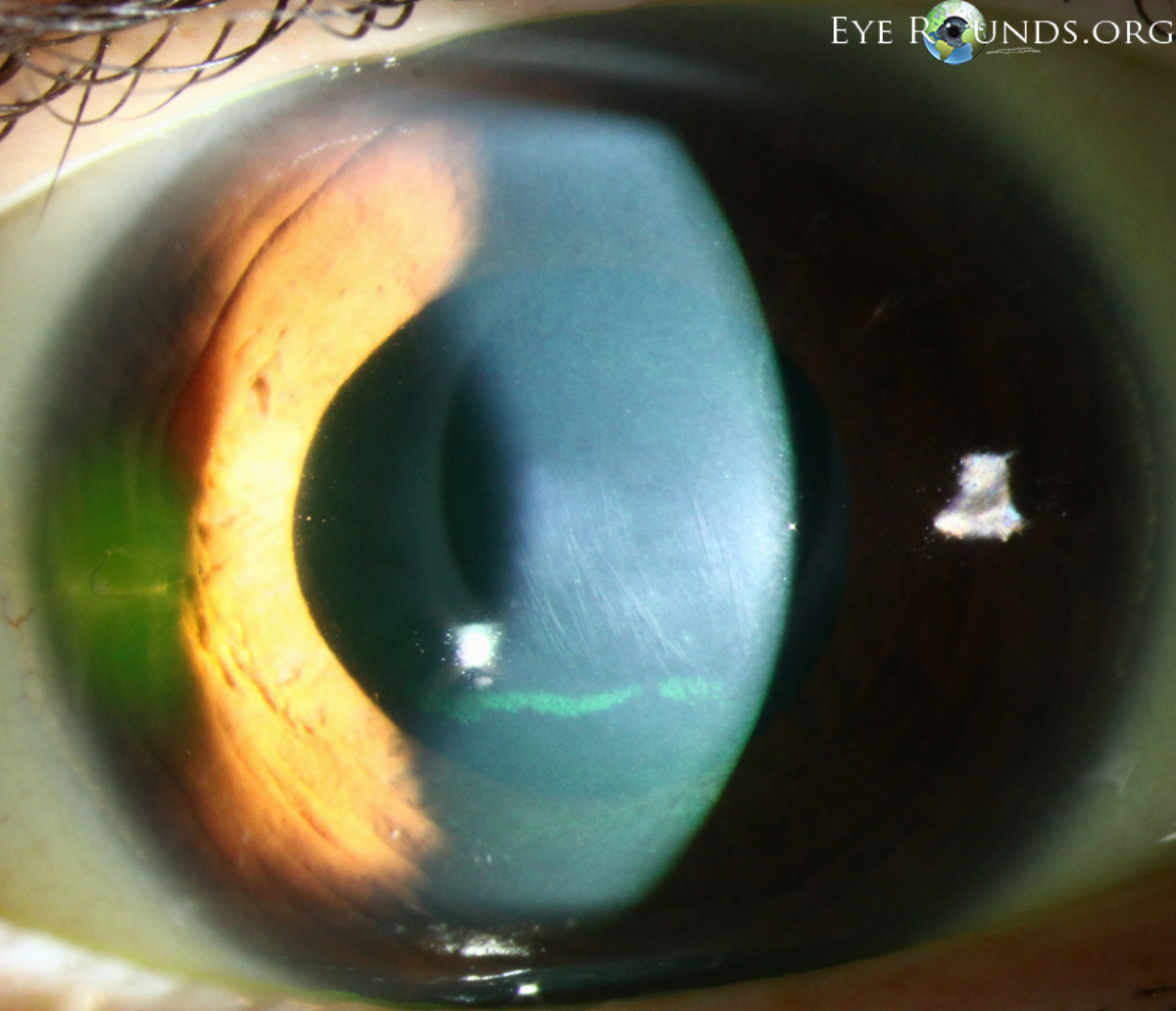
Местно рекомендуют наклоф 0,1 %, тауфон 4 %, витасик, корнерегель, солкосерил 2 % гель или актовегин. Важным препаратом является интерферон, лактоферон и интерфероногены. Из последних лучшим является полудан, который применяется в виде капель 100 МЕ в 0,5 мл дистиллированной воды, субконъюнктивально или парабульбарно в той же концентрации, на курс № 5-10. Для улучшения метаболических процессов назначают внутримышечно тималин ежедневно в течение 5-20 дней, внутримышечно вмтамины группы В (В1, В6, В12) и аскорбиновою кислоту. Применяются иммуностимуляторы и иммуномодуляторы. Левамизол по 150 мг ежедневно 3 дня подряд в неделю, в течение 1 месяца. Через 3-6 месяцев повторный курс. Детям по 20-50 мг в сутки в 2-3 приема по 3 дня в неделю в течение 4-5 недель. В качестве иммунокорректора применяют также нуклеиновую кислоту или нуклеиновокислый натрий в дозе от 0,4 до 1,0 грамма в сутки в 3-5 приемов ежедневно, 10-30 дней. Применяют Т-активин подкожно 2 раза в день из расчета 1-2 мкг/кг в течение 1-2 недель, неспецифический гамма-глобулин (противокоревой, противогриппозный) в виде инстилляций, подконъюнктивальных инъекций по 0,3 1 раз в два-три дня.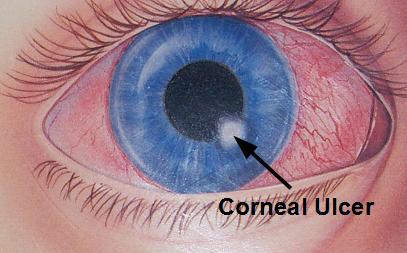 Всего № 5. Для борьбы с вторичной инфекцией и ее предупреждением инстилляции 30 5 раствора сульфацила натрия, глазных капель: окацин, флоксал, а также антибиотики в виде мазей (1 % тетерациклиновая, флоксал, эритромициновая). Для профилактики и лечения иридоциклита применяются мидриатики (1 % мидриацил, 1 % атропин, 1 % гомотропин).
Всего № 5. Для борьбы с вторичной инфекцией и ее предупреждением инстилляции 30 5 раствора сульфацила натрия, глазных капель: окацин, флоксал, а также антибиотики в виде мазей (1 % тетерациклиновая, флоксал, эритромициновая). Для профилактики и лечения иридоциклита применяются мидриатики (1 % мидриацил, 1 % атропин, 1 % гомотропин).
Для терапии различных форм герпетического кератита применяются пчелиный яд, мед, рентгеновские лучи Букки, вета-терапия, диатермия, диадинамические токи, магнитофорез и электрофорез с различными лекарственными веществами, стимуляция гелий-неоновым лазером. После стихания острых процессов применяются кортикостероиды в малых дозах.
В случае повышения ВГД – диакарб по 0,125-0,25 2 раза в день, глицероаскорбат 50 % р-р по 1,0 грамму на 1 кг веса, глазные капли тимолол, трусопт. При болях – анальгетики и периорбитальные новокаиновые блокады. Довольно удовлетворительный результат получается при соскабливании и тушировании герпетической эрозии 5 % йодной настойкой или 20 % сернокислым цинком, раствором эфира, перекиси водорода, а затем назначаются дезинфицирующие капли и мази.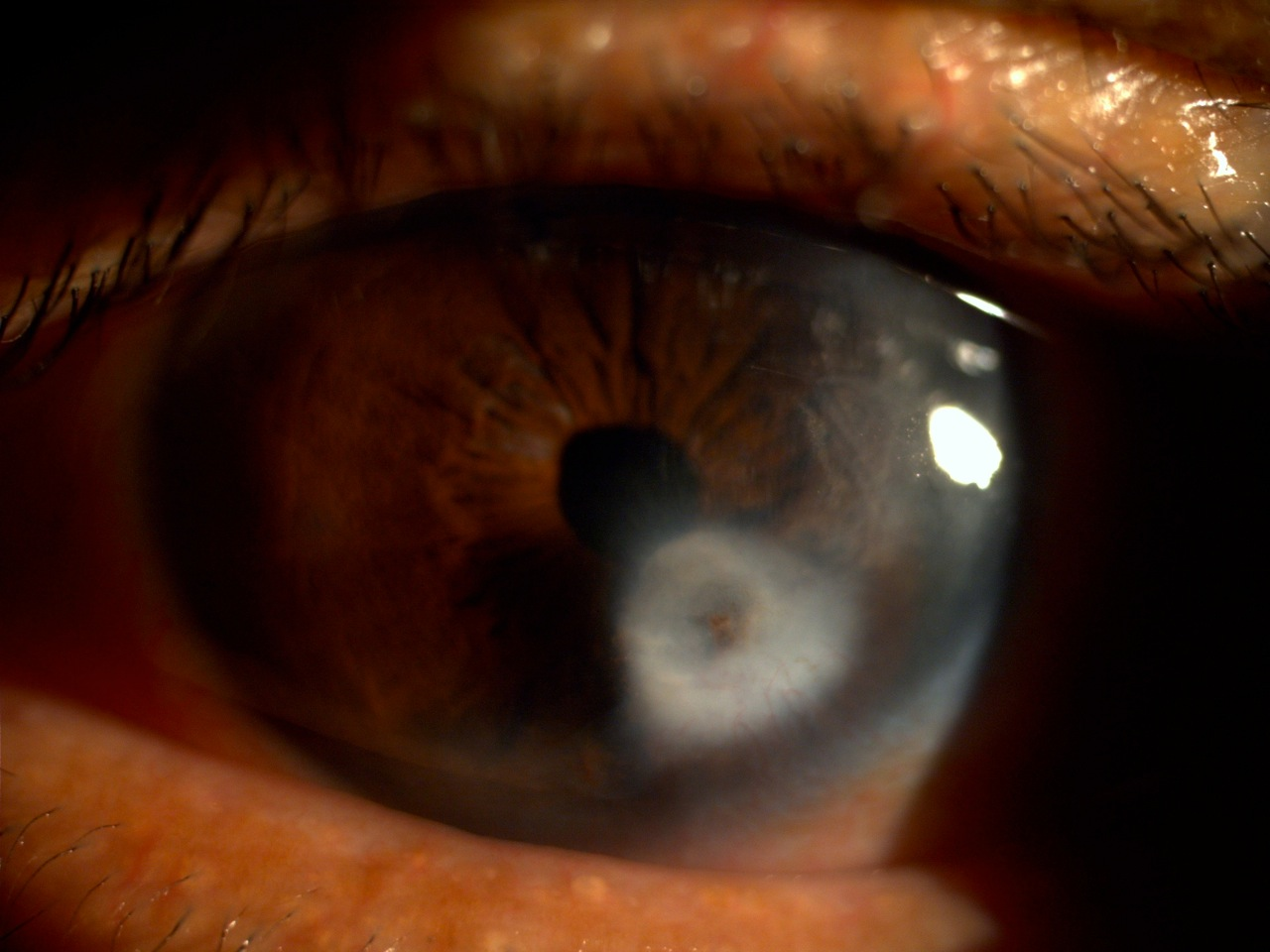 Теперь соскабливание можно делать с помощью эксимер-лазера. О лечении герпетических язв было уже ранее сказано. При отсутствии эффекта от медиваментозной терапии и при угрозе перфорации роговицы показана послойная или сквозная кератопластика. При пересадке роговицы возможны рецидивы буллезной кератопатии, которую А.А.Каспаров и др. (2000) связывают с отеком трансплантата с ободка собственной роговицы, где сохраняется популяция патологически измененных клеток. Поэтому предложено после иссечения бельма нанесение криоаппликаций на ободок собственной роговицы со стороны эндотелия.
Теперь соскабливание можно делать с помощью эксимер-лазера. О лечении герпетических язв было уже ранее сказано. При отсутствии эффекта от медиваментозной терапии и при угрозе перфорации роговицы показана послойная или сквозная кератопластика. При пересадке роговицы возможны рецидивы буллезной кератопатии, которую А.А.Каспаров и др. (2000) связывают с отеком трансплантата с ободка собственной роговицы, где сохраняется популяция патологически измененных клеток. Поэтому предложено после иссечения бельма нанесение криоаппликаций на ободок собственной роговицы со стороны эндотелия.
После лечения проводится диспансеризация с реабилитационной терапией и противорецидивным лечением. Противорецидивное лечение начинают через 3-4-недели после полного исчезновения клинических признаков воспаления – иммунокоррекция Т-активином по 50 мг через день № 9 каждые 3-6 месяцев, или левамизолом по 150 мг 1 раз в неделю в течение 2-3 месяцев. Курс можно повторят 2 раза в год. Иногда применяют вакцинотерапию при частых обострениях офтальмогерпеса.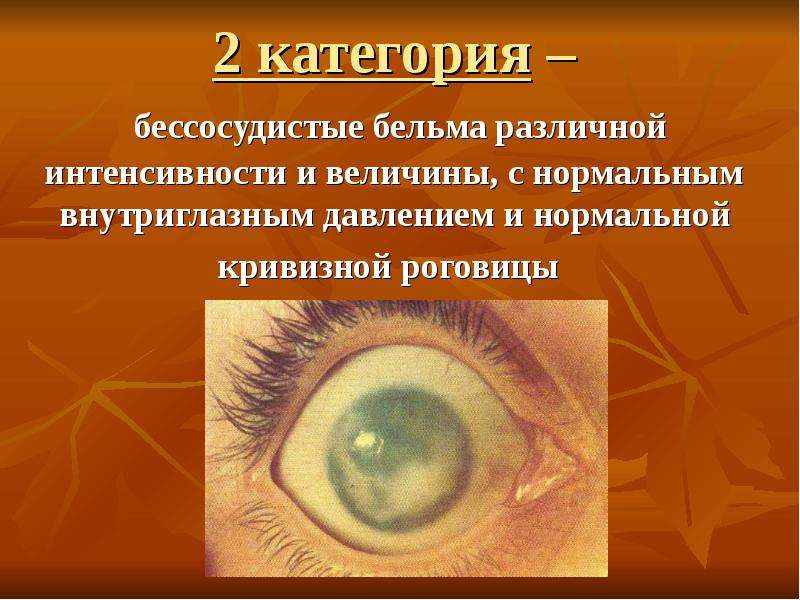 Вакцина вводится внутрикожно по 0,2 мл через 2 дня, № 5.
Вакцина вводится внутрикожно по 0,2 мл через 2 дня, № 5.
Нейропаралитический кератит (keratitis neuroparalytica) является типичным представителем нейрогенных заболеваний. Болезнь развивается при параличе первой ветви тройничного нерва, в результате операций или инъекций алкоголя в область узла Гассера, при давлении на нерв опухолью, костными отломками после травм, а также в исходе воспалительных процессов. Причиной нейропаралитического кератита нередко являются перенесенные инфекционные болезни (грипп и др.). Иногда кератит развивается быстро, через один-два дня после повреждения тройничного нерва, а иногда спустя несколько месяцев. Болезнь начинается с легкой перикорнеальной инъекции, которая в дальнейшем не усиливается и даже может совсем исчезнуть. В эпителии роговицы появляется множество очень мелких серых слегка приподнятых точек. В типичных случаях процесс в роговице возникает в центре, где эпителий отторгается и образуется его дефект. Образовавшаяся язва протекает очень вяло, не причиняет никаких субъективных ощущений, явления раздражения, светобоязнь, слезотечение отсутствуют.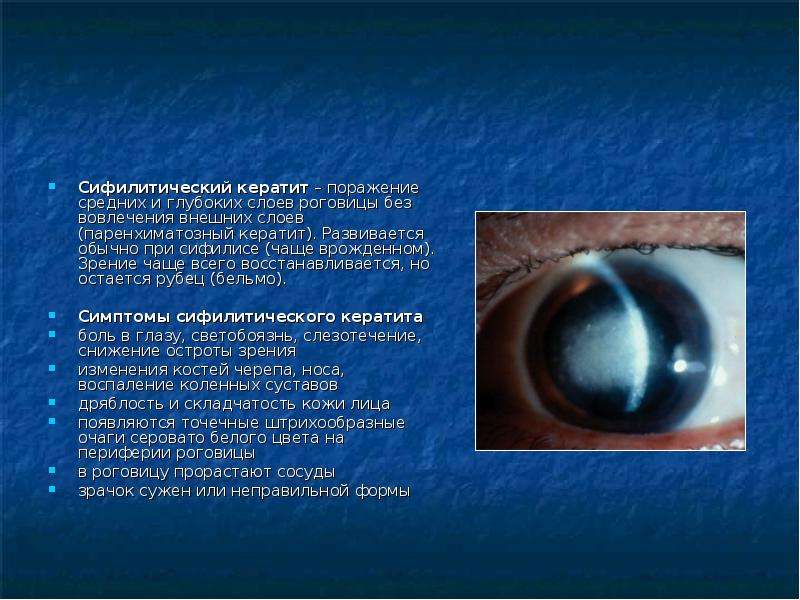 Чувствительность роговицы совершенно потеряна. Язва то подживает, то снова увеличивается. Течение очень длительное, иногда до года. Если не присоединится вторичная инфекция, язва подживает, оставляя различной степени помутнения, а если присоединится, то язва может стать гнойной с последующим тяжелым исходом. В основе патологического состояния лежит нарушение нейротрофических процессов, обусловливающих нормальную трофику роговицы.
Чувствительность роговицы совершенно потеряна. Язва то подживает, то снова увеличивается. Течение очень длительное, иногда до года. Если не присоединится вторичная инфекция, язва подживает, оставляя различной степени помутнения, а если присоединится, то язва может стать гнойной с последующим тяжелым исходом. В основе патологического состояния лежит нарушение нейротрофических процессов, обусловливающих нормальную трофику роговицы.
Лечение. Для улучшения трофики роговицы рекомендуются курсы перивазальной блокады новокаином, диатермия на область шейных симпатических узлов. В глаз цитраль 0,01% 3 раза в день, рибофлавин 0,02%, тиаминовая мазь 0,5%, инсулиновая мазь (40 ЕД на 10,0 мазевой основы). Для предупреждения вторичной инфекции применяют капли, мази из антибиотиков широкого спектра действия и сульфаниламидов. (1% тетрациклиновая мазь, 30% раствор альбуцида и антибиотики в виде капель – окацин, флоксал). Для улучшения трофики назначают АТФ по 1 мл внутримышечно (N 30), нерабол по 1 т 3 раза в день в течение месяца.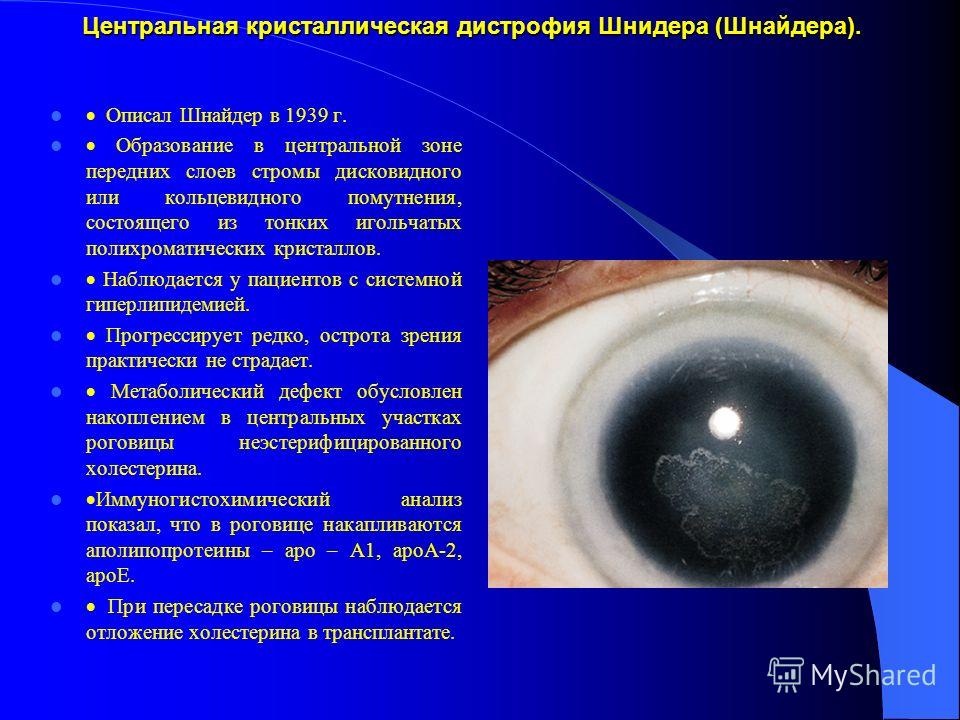 При болях — анальгетические средства. Для искусственной охраны роговицы от внешних воздействий (механических частиц в воздухе, химических веществ, дыма, высыхания и т.д.) рекомендуют ношение герметических очков, наподобие таковых у мотоциклистов. В исключительно тяжелых случаях производят тарзоррафию.
При болях — анальгетические средства. Для искусственной охраны роговицы от внешних воздействий (механических частиц в воздухе, химических веществ, дыма, высыхания и т.д.) рекомендуют ношение герметических очков, наподобие таковых у мотоциклистов. В исключительно тяжелых случаях производят тарзоррафию.
КЕРАТИТ ПРИ НЕСМЫКАНИИ ГЛАЗНОЙ ЩЕЛИ
(keratitis e lagophthalmo)
Этот кератит возникает при паралитическом и рубцовом лагофтальме — «заячьем глазе», который может быть при парезах и параличе лицевого нерва различного происхождения, после операций на лице, в области околоушной слюнной железы, на сосцевидном отростке и т.д., при резком экзофтальме на почве базедовой болезни, опухоли орбиты, злокачественном экзофтальме, при периоститах костей орбиты и т.д. В связи с отсутствием мигательного рефлекса и отсутствия увлажнения, играющего важную роль в нормальном обмене роговицы, последняя высыхает, перерождается. Поверхность роговицы становится матовой. Погибший эпителиальный покров отторгается, появляются эрозии роговицы, а затем ее помутнения, преимущественно в нижней части, непокрытой веками. Вследствие дальнейшего распространения некротического процесса на паренхиму роговицы эрозия может превратиться в вяло текущую, торпидную язву с горизонтальной границей соответственно краю верхнего века. Язва может захватить всю толщу роговицы. При присоединении вторичной инфекции возможно образование гнойной язвы с частичным или полным разрушением роговой оболочки, с последующим панофтальмитом и слепотой.
Погибший эпителиальный покров отторгается, появляются эрозии роговицы, а затем ее помутнения, преимущественно в нижней части, непокрытой веками. Вследствие дальнейшего распространения некротического процесса на паренхиму роговицы эрозия может превратиться в вяло текущую, торпидную язву с горизонтальной границей соответственно краю верхнего века. Язва может захватить всю толщу роговицы. При присоединении вторичной инфекции возможно образование гнойной язвы с частичным или полным разрушением роговой оболочки, с последующим панофтальмитом и слепотой.
Лечение должно быть направлено на устранение лагофтальма, предупреждение высыхания роговицы, улучшение ее трофики и борьбу с вторичной инфекцией. Несколько раз в день в конъюнктивальный мешок закапывают рыбий жир, вазелиновое, облепиховое масло, витамины (цитраль — 0,01% 3 раза в день, рибофлавин с аскорбиновой кислотой и глюкозой), 1% раствор хинина гидрохлорида, искусственную слезу, закладывают 0,5% тиаминовую мазь, применяют корнерегель.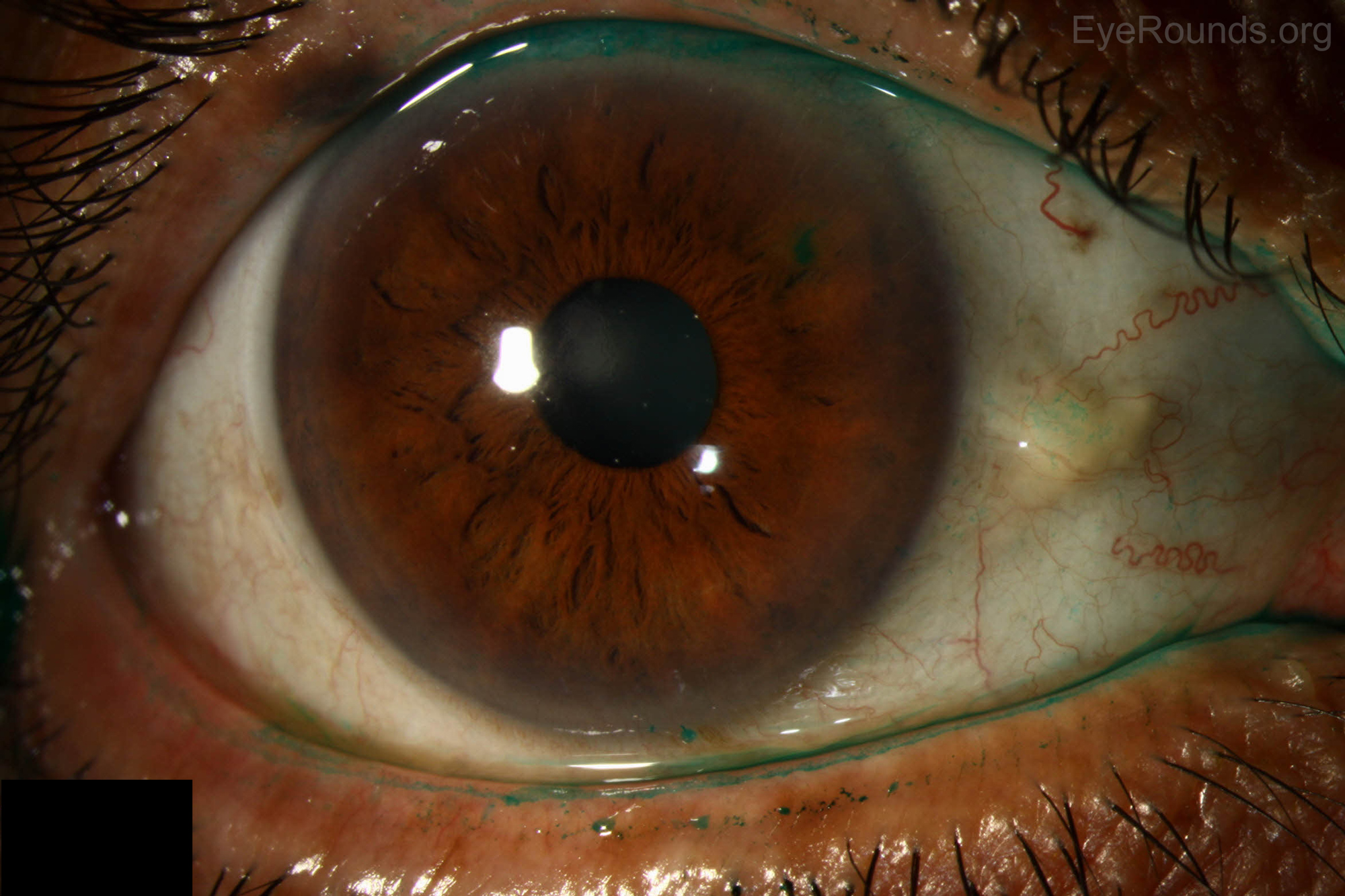 Для предупреждения вторичной инфекции рекомендуются инстилляция 30% раствора сульфацила натрия, 0,25% раствор левомицетина 4 раза в день, применение на ночь 1% тетрациклиновой или другой из антибиотиков или сульфаниламидов мази и накладывание на глаз повязки проводится по правилам лечения кератитов. При неустранимом лагофтальме и кератите, не поддающемся медикаментозному лечению, прибегают к тарзорафии.
Для предупреждения вторичной инфекции рекомендуются инстилляция 30% раствора сульфацила натрия, 0,25% раствор левомицетина 4 раза в день, применение на ночь 1% тетрациклиновой или другой из антибиотиков или сульфаниламидов мази и накладывание на глаз повязки проводится по правилам лечения кератитов. При неустранимом лагофтальме и кератите, не поддающемся медикаментозному лечению, прибегают к тарзорафии.
ПАРЕНХИМАТОЗНЫЙ КЕРАТИТ
(при врожденном сифилисе)
Паренхиматозный кератит является самым частым и самым типичным поражением глаз при позднем врожденном сифилисе. Эта форма врожденного сифилиса проявляется обычно в возрасте от 5 до 20 лет, редко в возрасте 1-5 лет, в единичных случаях встречается у грудных детей. У девочек кератит встречается чаще.
Характерна для паренхиматозного кератита триада Гетчинсона: кератит, гетчинсоновские зубы, тугоухость. Полная триада в настоящее время встречается редко. Реже всего отмечается тугоухость.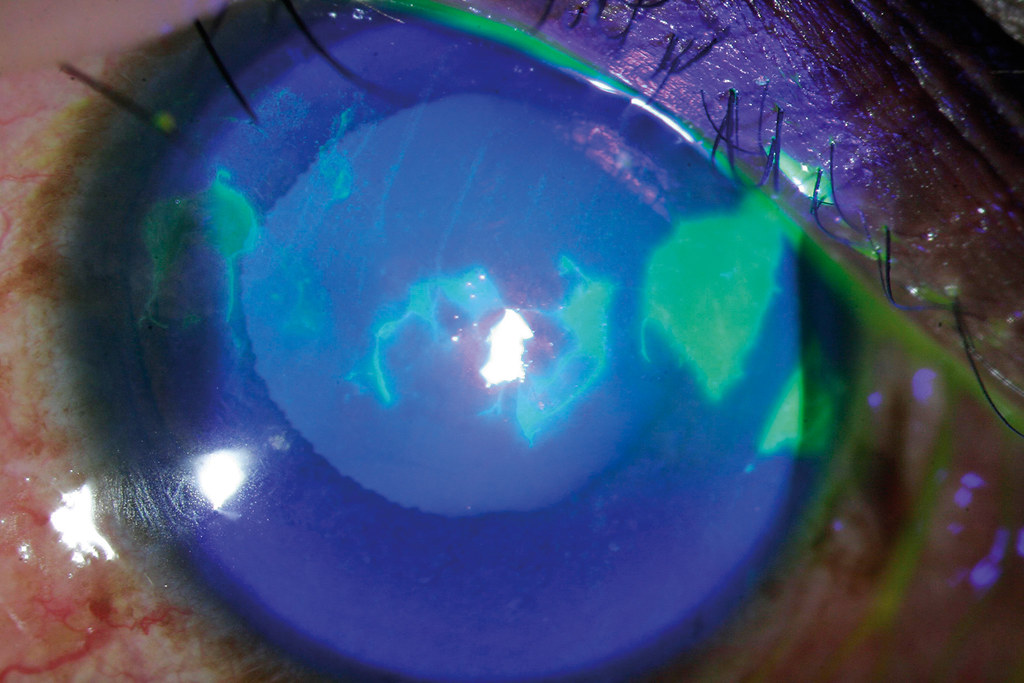 Гетчинсоновские зубы и другие их дистрофии встречаются при паренхиматозном кератите также у 1/3-1/4 всех больных. С различной частотой сочетаются с паренхиматозным кератитом не глазные проявления позднего врожденного сифилиса, разнообразные поражения системы костей в форме олимпийского лба, гипертрофических периоститов, гуммозных разрушений костей, в частности носовой перегородки с деформацией носа, перфорацией твердого неба, типичные периостальные наросты на передних поверхностях большеберцовых костей (саблевидные голени), поражение суставов, в особенности коленных, изъязвившиеся гуммы кожных покровов, слизистых оболочек и др. Почти у половины больных при паренхиматозном кератите наблюдаются заболевания центральной нервной системы. Паренхиматозный кератит в большинстве случаев двусторонний. Развитие типичного диффузного паренхиматозного кератита начинается с появления умеренной гиперемии глаза, светобоязни, слезотечения и помутнения роговицы, чаще сверху, вблизи участка набухшего лимба.
Гетчинсоновские зубы и другие их дистрофии встречаются при паренхиматозном кератите также у 1/3-1/4 всех больных. С различной частотой сочетаются с паренхиматозным кератитом не глазные проявления позднего врожденного сифилиса, разнообразные поражения системы костей в форме олимпийского лба, гипертрофических периоститов, гуммозных разрушений костей, в частности носовой перегородки с деформацией носа, перфорацией твердого неба, типичные периостальные наросты на передних поверхностях большеберцовых костей (саблевидные голени), поражение суставов, в особенности коленных, изъязвившиеся гуммы кожных покровов, слизистых оболочек и др. Почти у половины больных при паренхиматозном кератите наблюдаются заболевания центральной нервной системы. Паренхиматозный кератит в большинстве случаев двусторонний. Развитие типичного диффузного паренхиматозного кератита начинается с появления умеренной гиперемии глаза, светобоязни, слезотечения и помутнения роговицы, чаще сверху, вблизи участка набухшего лимба. Биомикроскопическое исследование показывает, что эти помутнения состоят из мелких инфильтратов в форме точек и штрихов, расположенных в глубоких и средних слоях роговицы. Поверхность роговицы над помутнением делается шероховатой. Чувствительность понижается. Постепенно все явления нарастают, увеличивается инъекция, помутнение распространяется все дальше и дальше, и наконец, вся роговица становится мутной и тусклой, как часовое стекло, приобретая иногда фарфорово-белый оттенок. Одновременно с появлением помутнений в роговице появляются сосуды, которые идут в ее глубоких слоях и сохраняют черты глубоких сосудов. В течение периода нарастания явлений имеется сильная светобоязнь, слезотечение, часто самопроизвольные боли, а также боли при пальпации в области цилиарного тела. Если возможно рассмотреть радужную оболочку, то видно, что зрачок сужен или неправильной формы, радужка гиперемирована. На задней поверхности роговицы видны преципитаты, имеются также складки десцеметовой оболочки. На высоте процесса зрение падает до 0,01 или до светоощущения.
Биомикроскопическое исследование показывает, что эти помутнения состоят из мелких инфильтратов в форме точек и штрихов, расположенных в глубоких и средних слоях роговицы. Поверхность роговицы над помутнением делается шероховатой. Чувствительность понижается. Постепенно все явления нарастают, увеличивается инъекция, помутнение распространяется все дальше и дальше, и наконец, вся роговица становится мутной и тусклой, как часовое стекло, приобретая иногда фарфорово-белый оттенок. Одновременно с появлением помутнений в роговице появляются сосуды, которые идут в ее глубоких слоях и сохраняют черты глубоких сосудов. В течение периода нарастания явлений имеется сильная светобоязнь, слезотечение, часто самопроизвольные боли, а также боли при пальпации в области цилиарного тела. Если возможно рассмотреть радужную оболочку, то видно, что зрачок сужен или неправильной формы, радужка гиперемирована. На задней поверхности роговицы видны преципитаты, имеются также складки десцеметовой оболочки. На высоте процесса зрение падает до 0,01 или до светоощущения.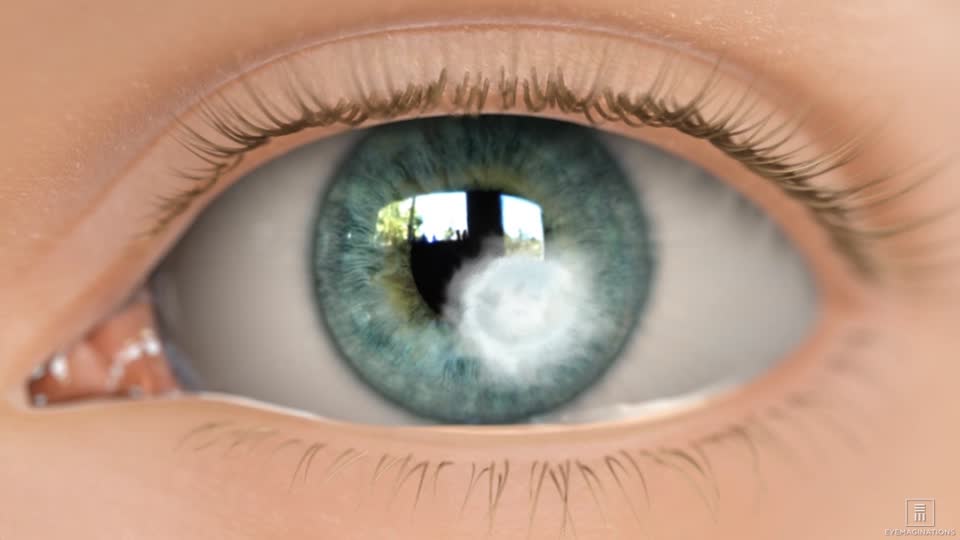
Период нарастания явлений длится 6-8 недель, а затем они постепенно стихают, уменьшается раздражение глаза и инъекция, ослабевают субъективные ощущения. Одновременно с периферии начинается просветление роговицы, которое распространяется к ее центру. Центр дольше всего остается мутным, просветляясь в последнюю очередь. Процесс рассасывания идет очень медленно и пока роговица просветлеет проходит несколько месяцев (до года и более). В нетяжелых случаях роговица кажется совершенно прозрачной, и только с помощью щелевой лампы видны остатки помутнений и запустевшие сосуды, которые остаются навсегда. В 70% случаях зрение в той или иной мере восстанавливается, однако в ряде случаев, когда на роговице остаются стойкие помутнения, острота зрения снижается значительно. Может быть отклонение от описанного типичного течения паренхиматозного кератита, когда воспалительная инфильтрация роговицы начинается с центра, а не с периферии и разрешение процесса тоже происходит с центра. Бывают случаи, когда развивается очень мало сосудов или они совсем отсутствуют.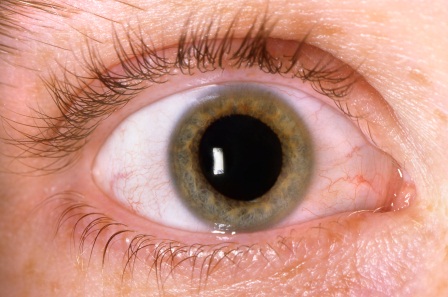 В этих случаях рассасывание помутнений идет особенно медленно. В единичных случаях паренхиматозный кератит может сопровождаться изъязвлением роговицы с тяжелым течением. Почти в половине всех случаев паренхиматозный кератит осложняется иритом, иногда с обильными жирными преципитатами и мощными задними синехиями. Внутриглазное давление в большинстве случаев понижено, но нередко оно повышается и иногда даже значительно. Все это надо учитывать при лечении. Довольно часто при паренхиматозном кератите отмечается хориоретинит, который развивается независимо от него и может быть как при врожденном, так и при приобретенном сифилисе. Иногда при приобретенном сифилисе может развиться гумма хориоидеи. В стекловидном теле помутнения. Редко наблюдается поражение зрительного нерва и параличи глазных мышц. Они являются обычно симптомами поражения центральной нервной системы. Могут наблюдаться рецидивы паренхиматозного кератита. Приобретенный сифилитический кератит, как правило, протекает более легко и быстро.
В этих случаях рассасывание помутнений идет особенно медленно. В единичных случаях паренхиматозный кератит может сопровождаться изъязвлением роговицы с тяжелым течением. Почти в половине всех случаев паренхиматозный кератит осложняется иритом, иногда с обильными жирными преципитатами и мощными задними синехиями. Внутриглазное давление в большинстве случаев понижено, но нередко оно повышается и иногда даже значительно. Все это надо учитывать при лечении. Довольно часто при паренхиматозном кератите отмечается хориоретинит, который развивается независимо от него и может быть как при врожденном, так и при приобретенном сифилисе. Иногда при приобретенном сифилисе может развиться гумма хориоидеи. В стекловидном теле помутнения. Редко наблюдается поражение зрительного нерва и параличи глазных мышц. Они являются обычно симптомами поражения центральной нервной системы. Могут наблюдаться рецидивы паренхиматозного кератита. Приобретенный сифилитический кератит, как правило, протекает более легко и быстро.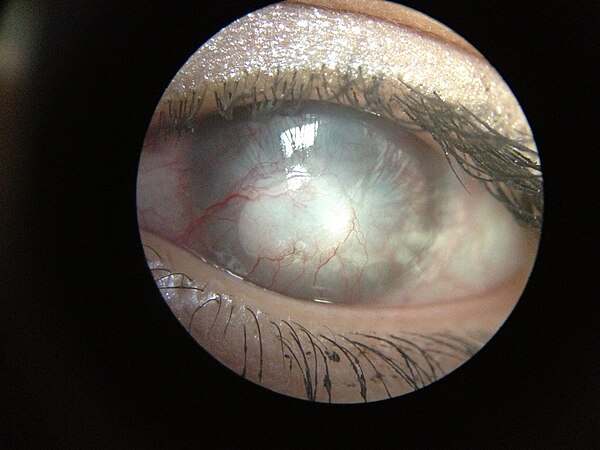 В отличие от врожденного поражается только один глаз. Патогенез не может до сих пор считаться вполне выясненным. Большинство рассматривает это заболевание как аллергический процесс. Внутриутробно или в самом раннем детстве спирохеты, находящиеся в прозрачной роговице сенсибилизирует ее ткань продуктами их распада. Если в более позднем возрасте спирохетный аллерген попадает в ткань сенсибилизированной роговицы, то возникает аллергический процесс по типу реакции аллерген-антитело.
В отличие от врожденного поражается только один глаз. Патогенез не может до сих пор считаться вполне выясненным. Большинство рассматривает это заболевание как аллергический процесс. Внутриутробно или в самом раннем детстве спирохеты, находящиеся в прозрачной роговице сенсибилизирует ее ткань продуктами их распада. Если в более позднем возрасте спирохетный аллерген попадает в ткань сенсибилизированной роговицы, то возникает аллергический процесс по типу реакции аллерген-антитело.
Провоцирующими факторами возникновения паренхиматозного кератита являются травмы глаза, расстройства деятельности желез внутренней секреции, общие заболевания, нарушение питания и т.д. Диагноз устанавливают на основании типичной клинической картины, признаков врожденного сифилиса, серологических положительных проб, при исследовании крови и спинномозговой жидкости, а также данных семейного анамнеза (частые произвольные выкидыши, мертворожденность, недоношенность плодов, высокая смертность детей раннего возраста, разные явления сифилиса у других детей в семье).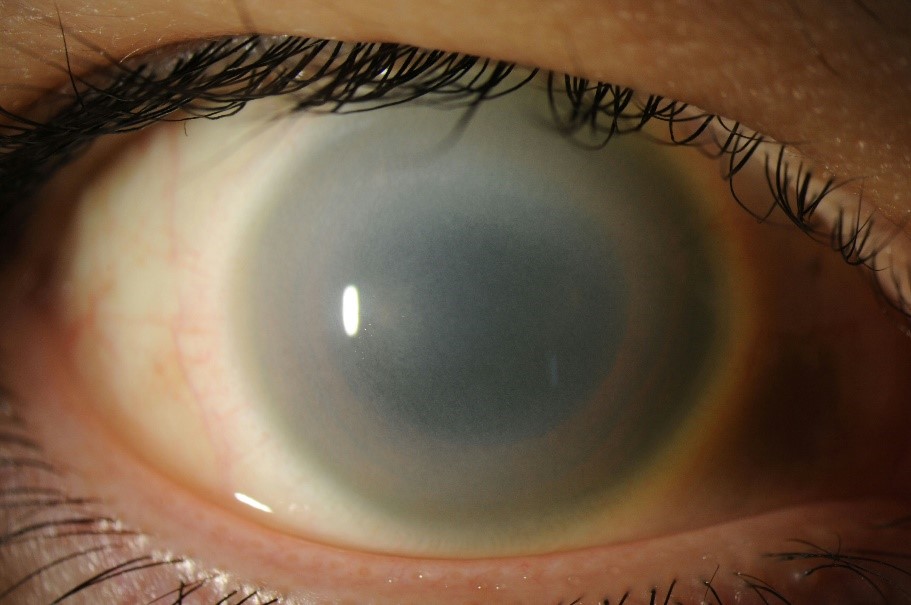
Лечение сифилитического кератита осуществляется в венерологическом диспансере, под наблюдением окулиста. Местное лечение направлено на рассасывание инфильтратов и уменьшение явлений ирита и иридоциклита. Назначают 1 % раствор сульфата атропина в виде капель, в случае, если зрачок не расширяется, то добавляют 0,1 % раствор адреналина и закладывают за веки в виде «фитилька». Субконъюнктивально – дексаметазон 0,4 % р-р., у детей применяют 1 % желтую ртутную мазь 2 раза в день, рекомендуются пиявки на висок, на веки сухое тепло. Для рассасывания помутнений рекомендуют раствор или мазь этилморфина в возрастающих концентрациях (от 1 до 8 %), 3 % раствор иодида калия 3-4 раза в день, 0,1 % раствор лидазы 4=5 раз в день, фонофорез с лидазой, внутрь йодистые препараты. Если в течение 1-1,5 лет не удается добиться рассасывания помутнений — сквозная кератопластика.
ТУБЕРКУЛЕЗНЫЕ КЕРАТИТЫ
Туберкулезные кератиты возникают как гематогенные бактериальные метастазы или аллергические кератиты.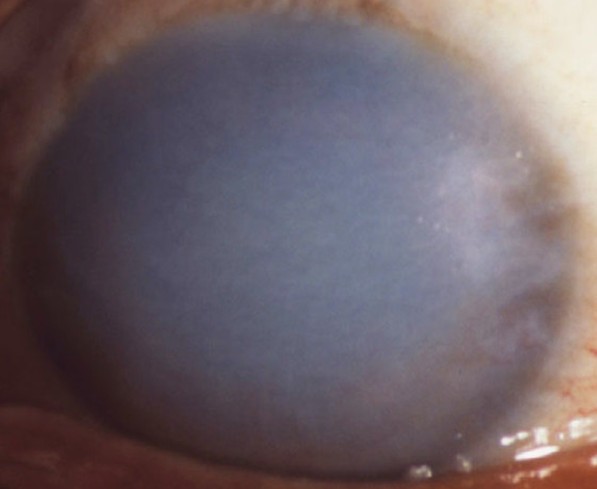
Гематогенные туберкулезные кератиты встречаются в нескольких формах:
- Глубокий диффузный кератит характеризуется диффузным помутнением роговицы, в которой выделяются отдельные желтоватые очажки. Через 2-4 месяца от начала заболевания в роговицу врастают глубокие и поверхностные сосуды. Течение очень медленное с улучшениями и обострениями, часто сопровождающиеся иридоциклитом. Как правило, остаются стойкие рубцовые помутнения, часто значительно снижающие зрение.
- Глубокий ограниченный кератит возникает большей частью у больных, перенесших в детстве фликтенулезный кератит. Ограниченные инфильтраты располагаются в задних слоях роговой оболочки. Васкуляризация роговицы умеренная. Кератит часто сопровождается появлением преципитатов, образованием складок десцеметовой оболочки, реакцией радужки. Инфильтраты могут частично рассосаться, а могут изъязвиться с последующим исходом в бельмо.
- Склерозирующий кератит. Клиническая картина склерозирующего кератита имеет свои особенности.
 Он может развиться в тесной связи с глубоким склеритом. Очаги из склеры распространяются в глубокие слои роговицы, иногда наоборот, инфильтраты имеют форму треугольника с вершиной, направленных к центру зрачка. Иногда они появляются в нескольких местах роговой оболочки. Сосуды прорастают через 6-7 недель как глубокие, так и поверхностные, но их бывает очень мало. Часто присоединяется иридоциклит. Явления раздражения могут быть очень сильными и умеренными. Постепенно явления раздражения стихают, помутнения у вершины и по краю постепенно несколько рассасываются, но основания помутнения организуются в соединительную ткань, имеющую интенсивное синевато-белое помутнение, по цвету напоминающее склеру. Получается впечатление, что ткань склеры в этом участке заменила собой ткань роговицы. В тяжелых случаях большая часть роговицы может стать непрозрачной. Процесс тянется месяцами и годами, часто рецидивирует. Этиологический диагноз кератитов устанавливается по клинической картине, изменениях в легких или бронхопульмональных лимфатических узлах, температурной кривой, по положительным туберкулиновым реакциям и т.
Он может развиться в тесной связи с глубоким склеритом. Очаги из склеры распространяются в глубокие слои роговицы, иногда наоборот, инфильтраты имеют форму треугольника с вершиной, направленных к центру зрачка. Иногда они появляются в нескольких местах роговой оболочки. Сосуды прорастают через 6-7 недель как глубокие, так и поверхностные, но их бывает очень мало. Часто присоединяется иридоциклит. Явления раздражения могут быть очень сильными и умеренными. Постепенно явления раздражения стихают, помутнения у вершины и по краю постепенно несколько рассасываются, но основания помутнения организуются в соединительную ткань, имеющую интенсивное синевато-белое помутнение, по цвету напоминающее склеру. Получается впечатление, что ткань склеры в этом участке заменила собой ткань роговицы. В тяжелых случаях большая часть роговицы может стать непрозрачной. Процесс тянется месяцами и годами, часто рецидивирует. Этиологический диагноз кератитов устанавливается по клинической картине, изменениях в легких или бронхопульмональных лимфатических узлах, температурной кривой, по положительным туберкулиновым реакциям и т. д. Дифференцируют с люэтическим паренхиматозным кератитом, при котором сосуды только глубокие, обычно поражается оба глаза, всегда положительная реакция Вассермана. При нейрогенных кератитах понижена чувствительность роговицы, не развиваются кровеносные сосуды.
д. Дифференцируют с люэтическим паренхиматозным кератитом, при котором сосуды только глубокие, обычно поражается оба глаза, всегда положительная реакция Вассермана. При нейрогенных кератитах понижена чувствительность роговицы, не развиваются кровеносные сосуды.
Лечение туберкулезных кератитов является процессом длительным и зависит от характера заболевания, вирулентности возбудителя, состояния иммунитета, сроков и характера лечения, активности внеглазных туберкулезных очагов. Проводят туберкулостатическую терапию в сочетании с десенсебилизирующей, симптоматической и общеукрепляющей.
Химиотерапия – применяется длительное непрерывное комбинированное лечение антибактериальными препаратами сос меной антибактериальных средств на различных этапах. Наиболее эффективными являются противотуберкулезные препараты первого ряда: изониазид, феназид, рифампицин, рифабутин, пиразинамид, этамбутол. В резервную группу противотуберкулезных препаратов второго ряда включают: циклосерин, этионамид и протионамид парааминосалициловая кислота (ПАСК), тиоацетазол, капреомицин, канамицин, амикацин, хинолоновые антибиотики. Изониазид (тубазид) — суточная доза 0,6-0,9 г. Местно: под конъюнктиву 3 % раствор (0,3-0,5 мл), ретробульбарно 3 % (0,5 мл), парабульбарно 3 % (0,5-1,0 мл), электрофорез с 3 % раствором. Рифампицин – суточная доза 25 мкг/кг на один прием. Одновременно назначают десенсебилизирующие средства (хлористый кальций в/в 10 % р-р, глюконата кальция в/м 10 % р-р, димедрол, супрастин, тавегил, фенкарол, кларитин). Применяют стимулятор иммунитета левамизол по 150 мг 3 дня, перерыв 10 дней (4 курса), обменный плазмафорез 4-5 раз, витаминотерапия.
Изониазид (тубазид) — суточная доза 0,6-0,9 г. Местно: под конъюнктиву 3 % раствор (0,3-0,5 мл), ретробульбарно 3 % (0,5 мл), парабульбарно 3 % (0,5-1,0 мл), электрофорез с 3 % раствором. Рифампицин – суточная доза 25 мкг/кг на один прием. Одновременно назначают десенсебилизирующие средства (хлористый кальций в/в 10 % р-р, глюконата кальция в/м 10 % р-р, димедрол, супрастин, тавегил, фенкарол, кларитин). Применяют стимулятор иммунитета левамизол по 150 мг 3 дня, перерыв 10 дней (4 курса), обменный плазмафорез 4-5 раз, витаминотерапия.
Для расширения зрачка инстилляции 1 % раствора атропина 2-3 раза в день.
При присоединении бактериальной инфекции применяют инстилляции 30 % раствора сульфацила натрия, глазные капли окацин, флоксал, 1 % тетрациклиновая мазь. Довольно рано рекомендуется рассасывающая терапия 1-8 % р-р этилморфина гидрохлорида в виде инстилляций или мази, электрофорез с 3 % р-ром калия йодида, лидазы.
Туберкулезно-аллергические кератиты
В большинстве случаев бывает у детей 2-3 лет, реже подростков, но могут наблюдаться и у взрослых. Заболевание протекает остро и сопровождается светобоязнью, слезотечением, блефароспазмом, перикорнеальной инъекцией.
Фликтенулезный кератит характеризуется появлением фликтен – сероватых полупрозрачных узелков, состоящих из лимфоцитов, эпителиоидных и гигантских клеток. Они могут быть мелкими множественными и единичными (солитарными). Располагаются фликтены в поверхностных слоях роговицы, но могут захватывать и другие слои. Развитие фликтен сопровождается новообразованием поверхностных сосудов. Фликтены могут рассосаться без изъязвления, а могут распадаться, превращаясь во фликтенулезные язвы, исходом которых может быть и перфорация, сращенное бельмо или частичная стафилома. При некротической форме возможно расплавление роговицы.
Одной из форм туберкулезно-аллергического кератита может быть пучочковый кератит, или странствующая фликтена. Развивается из краевого инфильтрата, в периферический край которого врастают сосуды, а сам инфильтрат медленно распространяется по роговице, пока головка инфильтрата не достигнет противоположной части лимба. Участки лежащие позади инфильтрата очищаются и заполняются пучком сосудов. Не бывает ни глубокого изъязвления, ни перфорации роговицы, но остаются стойкие помутнения в виде полосы.
Еще одной формой является паннозный фликтенулезный кератит. Характерен тем, что васкуляризация роговицы выражена очень интенсивно, иногда вся роговица имеет красноватую окраску. Вследствие отека роговицы она выглядит диффузно мутной. Часто обостряется и рецидивирует. Остаются стойкие помутнения. Туберкулезная этиология фликтенулезных кератитов доказана. Отвергнута бациллярная теория и всеми признан аллергический характер заболевания.
Лечение: основным критерием при этих формах является характер внеглазного туберкулезного процесса. Проводят активную противотуберкулезную, противовоспалительную и десенсебилизирующую терапию. Общее лечение как при метастатических туберкулезных кератитах.
Местно применяют 0,1 % раствор дексаметазона или 0,3 % р-р преднизолона, 2 % р-р амидопирина, р-р стрептомицин-хлоркальциевого комплекса (50 000 ЕД стрептомицина в 1 мл дистиллированной воды). Физиотерапевтические процедуры проводят в виде электрофореза стрептомицина ежедневно, на курс 20 процедур. Далее электрофорез кальция чередуют с электрофорезом гидрокортзона. При наслоении бактериальной инфекции применяют антибактериальные средства (р-р 30 % альбуцида, капли фуциталмик, окацин). Используют витаминные капли (цитраль, рибофлавин с аскорбиновой кислотой) и 1% раствор хинина гидрохлорида 4 раза в сутки. У детей 1 % желтая ртутная мазь. После стихания воспалительного процесса рассасывающая терапия (3 % р-р иодида калия, 0,1 % р-р лидазы. Диета с ограничением углеводо и солей. Необходимы витамины группы А, В, С. если в процесс вовлечена радужная оболочка и цилиарное тело – мидриатики.
Акантамебные поражения роговицы. Первые сообщения об акантамебном кератите появились в литературе в 1974 г. Подробно об этом заболевании пишет в обзоре литературе Э.С.Аветисов с соавт. Акантамебы – мелкие, свободно живущие простейшие, рода Acanthomoeba, семейства Acanthomoebbidae, обитающие в почве или в различных водоемах, пресной, солоноватой, колодезной, минеральной, хлорированной воде бассейнов, горячей воде бань, сточных водах и их осадках, экскрементах человека и животных, пыли, установках кондиционирования воздуха. Из 22 видов акантамеб 8 известны как возбудители оппортунистических инфекций у человека, в том числе энцефалита, а также поражения легких, кожи и других органов. Развитие акантомебного инфекционного процесса происходит при контакте тканей с возбудителем. Микротравмы роговицы и контакт с загрязненной водой являются факторами риска, в 85 % заболевание связывали с ношением контактных линз. Акантомебный склерокератит описан после пересадки роговой оболочки и экстракции катаракты. Процесс прогрессирует медленно. Имеется перикорнеальная инъекция, точечные субэпителиальные инфильтраты, которые могут сливаться образуя фигуру веточки дерева, поэтому иногда ставят ошибочный диагноз – герпетический кератит. Процесс прогрессирует постепенно, как в глубину, так и по поверхности, формируются кольцевидные инфильтраты, появление которых является патогномоничным признаком. Процесс может закончиться перфорацией или десцеметоцеле, может осложниться склерозом, а также повышением внутриглазного давления. Для ранней диагностики важными являются сильные болевые ощущения, стромальные кольцевидные инфильтраты, анамнез.
В медленном течении акантомебного кератита Ю.Ф.Майчук выделяет 4 стадии. 1).Явления поверхностного кератита на фоне ограниченного отека эпителия. 2).Усиление инфильтрации роговицы, формирование точечных очагов. 3).Картина стромального кольцевидного кератита. 4).Формирование язвенного кератита с угрозой перфорации роговицы на фоне гипопиона и иридоциклита.
Свободноживущие принадлежащие к роду Acanthomоeba, могут быть причиной гранулематозного амебного энцефалита. Причиной поздней диагностики акантомебного кератита является незнание клинической картины болезни, которая имеет часто атипичное течение, имеет длительный латентный период. Заболевание на ранних стадиях трактуется как герпетический или микотический кератит. Диагноз основывается на положительных результатах лабораторных исследований (культуральные методы, химические реакции и прямое микроскопирование).
В работах Д.Ю.Майчука (2003) было показано, что современным и высокоинформативным диагностическим методом является прижизненная конфокальная микроскопия роговицы. Во всех случаях кератитов, не поддающихся традиционной терапии, но сопровождающихся инфильтрацией стромы роговицы (особенно у пациентов носящих контактные линзы или пользовавшихся загрязненной водой) должно возникнуть подозрение на акантомебный кератит.
Лечение представляет большие трудности. Ю.Ф.Майчук (2000) считает, что оптимальным терапевтическим алгоритмом при акантомебном кератите является местное применение тобромицина или окацина в сочетании с хлоргексидином или эмульсией кетоконазола, в сочетании с пероральным приемом кетоконазола (низорала) по 200 мг 2 раза в день, или гентаконазола по 100 мг 2 раза в день, или дифлюкана по 50 мг 1 раз в день.
Синдром «сухого глаза» (ССГ) бывает не только как самостоятельное заболевание, как синдром Съёгрена, а может быть следствием перенесенных острых инфекционных глазных заболеваний, таких как аденовирусный конъюнктивит и эпидемический кератоконъюнктивит, бактериальный блефароконъюнктивит, демодекозный блефароконъюнктивит, а также при заболеваниях, вызванных гормональными изменениями, эндокринопатиями, гиповитаминозом А, в результате аллергических факторов, при аутоиммунных заболеваниях, вредных экологических воздействиях. Основной причиной развития заболевания является нарушение стабильности прероговичной слезной пленки. Толщина слезной пленки не превышает 10 мкм.
Большинство исследователей признает трехслойное строение слезной пленки. Наружный слой – липидный – тончайший (0,03-0,05 мкм), предохраняет пленку от высыхания. Изнутри пленка представлена слоем муцина (0,02-0,05 мкм), который сглаживает все микронеровности эпителиальной поверхности, обеспечивая зеркальный блеск, а липидный слой придает гладкость внешней поверхности слезной пленки.
Основной причиной заболевания, особенно у людей до 45 лет, являются транзиторные нарушения стабильности слезной пленки, связанные с систематическим воздействием на орган зрения кондиционированного воздуха, электромагнитных излучений, действием офисной аппаратуры. Влияют лазерные рефракционные операции, дым, смог, косметические средства, иногда контактные линзы. В более старшем возрасте важной причиной нарушения слезной пленки является дисфункция бокаловидных клеток конъюнктивы при климаксе, синдроме Съёгрена и систематическая инстилляция глазных капель, (чаще бета-адреноблокаторов). В любом возрасте имеет значение общее состояние здоровья, психологические, производственные и генетические факторы.
Жалоб у больных довольно много – покраснение глаз, ощущение инородного тела, чувство жжения, слезотечение, зуд, утомление глаз, боль при инстилляции в конъюнктивальную полость глазных капель, ухудшение зрительной работоспособности к вечеру, плохая переносимость ветра, кондиционированного воздуха, дыма ощущение «сухости» в глазу и др. При объективном осмотре обращается внимание на состояние век (выворот, заворот, выворот слезной точки, дефекты век, рубцы, наличие блефарита), состояние слезного мениска (высота в норме около 0,2 мм), состояние конъюнктивы (образование конъюнктивальных складок, параллельных краю век, лейкоплакия, симблефарон). Состояние роговицы (микроэрозии, рубцы, васкуляризация, дистрофии, чувствительность), состояние слезной пленки (образование пены, нити). Далее приводится тест Ширмера, при котором в норме за 5 минут смачивается более 15 мм полоски. И время разрыва слезной пленки (менее 10 секунд). Время разрыва слезной пленки (проба Норе), определяется следующим образом обследуемого просят посмотреть вниз и оттянув верхнее веко, орошают область лимба в меридиане 12 часов одной каплей 0,1 или 0,2 флюоресцеина. Врач включает секундомер и через окуляры щелевой лампы наблюдает за окрашенной поверхностью роговицы до появления разрыва в слезной пленке в виде черной дыры или щели. Измерения проводят три раза и рассчитывают средний результат. Время разрушения слезной пленки: более 10 секунд – норма, 5-10 секунд – ниже нормы, менее 5 секунд – резкое снижение. Обращается внимание на конъюнктивальные складки, параллельные заднему краю века, которые обычно видны во всех четырех квадрантах. Пациент смотрит прямо перед собой и несколько раз моргает. Врач осматривает 4 квадранта на предмет наличия или отсутствия конъюнктивальных складок с помощью щелевой лампы. Высота складки сравнивается с высотой слезного мениска.
При синдроме «сухого глаза» выделяют следующие клинические формы роговичных поражений и их лечение (Ю.Ф.Майчук, 1997-2002): эпителиопатия, эрозия роговицы, нитчатый кератит, язва роговицы, ксерофтальмия. При эпителиопатии – светобоязнь, пенистое отделяемое в конъюнктивальном мешке, гиперемия и разрыхленность конъюнктивы, тусклая и шероховатая роговица, мелкоточечная эпителиопатия. Проба Ширмера – в среднем 10,4 мм за 5 минут. Рекомендуется 4 % тауфон на полиглюкине, по 1 капле 2-3 раза в день в течение 3-х недель. Витасик по 1 кап 3 раза в течение 2-3 недель, искусственная слеза 2-3 раза в день в течение 4-х недель.
Рецидивирующая эрозия – 4 % тауфон по 1 капле 3-4 раза в день, после стихания острого процесса 2 раза в день, витасик по 1 капле 2-4 раза в день в течение 3-х дней, затем 2 раза в день 2-3 недели. Искусственную слезу с первого дня по 1 кап 3-4 раза в день или офтагель 2-3 раза в день.
Нитчатый кератит – сухой кератоконъюнктивит – при нем отмечается светобоязнь, блефароспазм, гиперемия конъюнктивы век, в конъюнктивальном мешке обилие белого нитчатого отделяемого, на ресницах корочки бело-желтого цвета, сосуды конъюнктивы глазного яблока застойны, расширены, роговица тусклая, поверхность неровная. При снятии нитей (десквамированного эпителия) обнажаются эрозии. Секреция слезы 1,2 мм за 5 минут. Рекомендуется 4 % тауфон на полиглюкине, по 1 капле 3 раза в день в течение 4-х недель. Витасик по 1 кап 4 раза в течение 3 недель, искусственная слеза 5-6 раз в день, офтагель 2-3 раза в день.
Язва роговицы – светобоязнь, блефароспазм, отек и гиперемия кожи век, конъюнктива век и глазного яблока сухая, сморщенная, сосуды расширены, застойны, лимб расширен. Эпителий роговицы тусклый, неровный, эрозированный, точечные инфильтраты и язвы. Проба Ширмера 0-1 мм за 5 минут. Схема лечения: 4 % тауфон на полиглюкине, по 1 капле 6-8 раза в день, длительно. Витасик по 1 кап 4 раза в день, чаще в сочетании с тауфоном, в течение 1 месяца, вита-йодурол 3 раза в день, корнерегель 2 раза в день, искусственная слеза по 1 кап. 4-6 раз в день. При вторичной инфекции – противоинфекционное лечение, назначают 1-2 раза в день видисик, корнерегель, в виде 5 % геля.
Поражение глаз при синдроме Съегрена. В 1933 году шведский офтальмолог Съегрен дал клиническое и гистологическое описание болезни. Клиническими симптомами является поражение слезных и слюнных желез, верхних отделов дыхательных путей и желудочно-кишечного тракта на фоне деформирующего полиартрита. Течение болезни хроническое.
Субъективно со стороны глаз — ощущению рези, сухости, зуда, жжения, ощущения песка в глазах, светобоязнь, затуманивание, отсутствие слез при смехе, плаче, снижение остроты зрения, боли в глазу. При объективном осмотре — светобоязнь, разрыхленность и гиперемия конъюнктивы, тягучее отделяемое в конъюнктивальном мешке в виде тонких эластичных нитей (слущенный эпителий и слизь). Роговая оболочка становится менее прозрачной, имеет матовый вид, истыкана. После удаления нитей, сначала подвижных, а затем неподвижных, остаются эрозии, окрашивающиеся флюоресцеином. Далее врастают сосуды и усиливается помутнение. Проба Шримера — от 0 до 3-5 мм. Затем появляется ксеростомия. Слюна становится вязкой, сухой, отмечается резко выраженная сиалопения. Сухой становится красная кайма губ. Развивается гастрит, колит, гиперпигментация кожи, выпадают волосы, деформирующий полиартрит различной выраженности. Всегда поражаются оба глаза, чаще у женщин после 40 лет. Этиология и патогенез до конца не выяснены, относят к коллагенозам.
Синдром Шарлена. Описал чилийский офтальмолог в 1931 году – невралгия назо-цилиарного нерва с поражением роговицы. Это – наиболее крупная ветка первой ветви тройничного нерва, конечной ветвью которой является надлобный нерв. Назо-цилиарный нерв посылает ветку к цилиарному узлу, от которого идут к глазу короткие цилиарные нервы. От ствола назо-цилиарного нерва отходят длинные цилиарные нервы, которые вместе с короткими образуют нервное сплетение в области цилиарного тела и вокруг роговой оболочки. Ветви от этого сплетения проникают в роговицу в качестве чувствительных и трофических нервов (боль, слезотечение, секреция слизистой носовой полости) и трофические расстройства (высыпания на коже и роговице). Обычно внезапно наступают приступы острых болей в глазу, вокруг глаза, в соответствующей половине головы и лица, блефароспазм, слезотечение. Боль, жжение в слизистой носа и в зонах с повышенной чувствительностью (над ноздрей и в области верхне-внутреннего угла глазницы). На коже носа могут быть пузырьки типа герпеса. Со стороны глаз поверхностный язвенный или нейротрофический кератит, ирит, иридоциклит. Приступ длится 10-60 минут. Иногда неделями больные ночи проводят сидя. Надо тщательно обследоваться для выявления причин заболевания.
ДИСТРОФИИ РОГОВОЙ ОБОЛОЧКИ
Дистрофические процессы в роговой оболочке делятся на первичные и вторичные. Первичные дистрофии бывают, как правило, врожденные и связаны с нарушением обмена. Так как изменения при первичной дистрофии первоначально возникают в том или ином слое роговицы, то различают дистрофии эпителия, боуменовой мембраны, стромы, эндотелия. Среди них особое место занимают первичные стромальные дистрофии, которые проявляются в детском или юношеском возрасте, имеют ареактивное прогрессирующее течение. Процесс двусторонний.
Типичными семейно-наследственными дегенерациями роговой оболочки являются: гранулярная дистрофия Гренува, пятнистая дистрофия Фера, решетчатая дистрофия, описанная Диммером. Последняя наиболее частая клиническая форма, составляющая до 43 % от общего числа больных с первичной стромальной дистрофией (Ю.Ф.Майчук, 1993).
Вторичные дистрофии (правильнее – дегенерации) роговицы проявляются односторонним поражением и зависят от местного патологического процесса в глазу. Могут возникнуть после оперативных вмешательств, после травм, ожогов конъюнктивы и склеры, после перенесенных заболеваний, таких как кератит, иридоциклит, увеит. Часто дистрофия встречается в детском возрасте при ревматоидном артрите и глаукоме. К вторичным дистрофиям относят также веретено Крукенберга (пигментация роговицы), кольцо Кайзера-Флейшера, буллезную дистрофию, жировую, гиалиновую, известковую.
Лечение семейно-наследственных дистрофий. Симптоматическое (витаминные капли, мази, тауфон, эмоксипин, ретинол, актовегин, вита-йодурол, корнерегель). Однако, эффект небольшой, поэтому проводят послойную или сквозную пересадку роговицы.
Лечение вторичных дистрофий. Патогенетическое и этиологическое (нейротрофические и рассасывающие препараты — витаминные капли, 0,05% тиаминовая мазь, 3% раствор калия йодида или натрия йодида). Ферменты (0,1% раствор лидазы и др.), биогенные стимуляторы, аутогемотерапия, физиотерапия и др. Применяют также кортикостероиды. По показаниям кератопластика или кератопротезирование.
ИСХОДЫ КЕРАТИТОВ
При всяком заболевании роговой оболочки образуется инфильтрат, который или проходит бесследно или оставляет стойкие той или иной величины и интенсивности помутнения. Полностью рассасывается инфильтрат, образовавшийся в самых поверхностных слоях роговицы. Инфильтрат же, расположенный в строме роговицы может резорбироваться, как это бывает при паренхиматозных сифилитических кератитах или оставить помутнение. В зависимости от интенсивности помутнения различают облачко (nubecula corneae), пятно роговицы (macula corneae) и бельмо (leucoma).
Бельмо — это интенсивный белый рубец роговицы. Если он занимает всю роговицу, то она представляется несколько уплощенной (aplanatio corneae) или наоборот, поверхность лейкомы может быть выпячена (leucoma eсtaticum). Если язвенный процесс в роговой оболочке сопровождался прободением роговицы, а в прободное отверстие выпала радужная оболочка и здесь зарубцевалась, то образуется лейкома, спаянная с радужкой (leucoma corneae adhaerens). Плоская, спаянная с радужкой лейкома под влиянием внутриглазного давления может растягиваться и выпячиваться, образуя так называемые стафиломы (staphyloma). Тонкая выпяченная стенка стафиломы легко доступна различным механическим повреждениям, которые могут открыть ворота для инфекции и привести к серьезному заболеванию, вплоть до панофтальмита. Бельмо роговицы сращенное с радужкой, а особенно со стафиломой часто, кроме значительного, а иногда и полного снижения зрения приводят к вторичной глаукоме.
Лечение — для рассасывания свежих помутнений роговой оболочки применяют капли дионина в возрастающей концентрации (1-6%), у детей 1% желтую ртутную мазь, 0,5% преднизолоновую мазь, 2-3 раза в день 1% раствор лидазы. Физиотерапевтическое лечение (электрофорез с экстрактом алоэ, аскорбиновой кислотой, кортизоном), тканевую терапию (подкожные инъекции и имплантации экстракта плаценты, взвеси плаценты и др. Надо отметить, что перечисленное лечение оказывает значительно лучший эффект у маленьких детей и значительно худший у взрослых. Небольшое поверхностно расположенное помутнение в центральном отделе роговицы может быть удалено с помощью ножа или эксимерного лазера (кератэктомия). Если образовалось стойкое бельмо, применяют хирургические способы лечения — пересадку роговой оболочки. Главной целью операции пересадки роговой оболочки является оптическая, т.е. восстановление утраченного зрения. В некоторых случаях кератопластика проводится с лечебной целью, т.е. иссечение некротической ткани для спасения глаза как органа. Как подготовительный этап оптической кератопластики, проводится мелиоративная пересадка роговой оболочки. Также с тектонической целью производят операции при фистулах и других дефектах роговицы.
Косметическую кератопластику производят на слепых глазах. Рефракционную кератопластику выполняют на здоровых глазах с целью изменения оптики глаза (когда больной не хочет носить очки и контактные линзы). Если помутнение не захватывает глубокие слои роговицы, проводится послойная кератопластика. Лечебная послойная кератопластика может быть произведена и в центре и на периферии роговицы, в пределах зоны ее поражения.
Сквозную кератопластику чаще всего проводят с лечебной целью. Она может быть субтотальной (диаметр роговицы более 5 мм), частичной (трансплантат 2-4 мм) и тотальной (диаметр пересаженной роговицы равен диаметру роговицы реципиента). При неэффективности кератопластики проводится кератопротезирование.
ОПУХОЛИ РОГОВОЙ ОБОЛОЧКИ.
К ним относятся дермоиды, которые чаще располагаются вблизи нижненаружного или наружного лимба, имеет беловато-желтый цвет и рано распространяются на роговицу, иногда прорастая до ее глубоких слоев. Поверхность дермоида на роговице гладкая, блестящая, белого цвета.
Папиллома ороговевающая, располагается вблизи лимба в виде серовато-белого образования, с шероховатой поверхностью. При распространении на роговицу она имеет вид полупрозрачного образования с сероватым оттенком. Ороговевающая папиллома подлежит лазерэксцизии, так как описаны случаи ее озлакачествления.
Может быть эпителиома Боуэна, которая так же как и предыдущие новообразования распространяется на роговицу с конъюнктивы.
Лечение хирургическое или комбинированное. Обрабатывают опухоль раствором митомицина с 0,04% за 2-3 дня до операции, затем производится иссечение опухоли и обработка операционной раны раствором митомицина на операционном столе, а затем еще 2-3 дня. Может быть также эффективной короткодистанционная рентгенотерапия. Первичный приобретенный меланоз конъюнктивы, достигая зону лимба, может распространятся на роговицу.
Лечение – широкая лазеркоагуляция или электроэксцизия опухоли с предварительными аппликациями 0,04 %раствора митомицина С. Неплохие результаты дает криодеструкция, но при небольшом распространении опухоли. Это новообразование в 2/3 процентах случаев подвергается озлакачествлению.
Роговица может страдать при чешуйчато-клеточном раке конъюнктивы, который растет медленно, но инвазируется в глубжележащие ткани и может разрушать роговицу. Склеру и прорастать в полость глаза. При небольших опухолях лимба и роговицы эффект дает инстилляция мономицина С, по специальной схеме, в течение 2-х недель. Можно комбинировать локальное иссечение опухоли с криодеструкцией (А.Ф.Бровкина, 2002).
В роговицу из конъюнктивы может прорасти злокачественная опухоль – меланома. Лечение опухоли надо начинать как можно раньше (см. раздел новообразования конъюнктивы).
Вопросы:
- Какие важные для обменных процессов вещества сосредоточены в эпителии роговицы?
- Назовите источники питания роговицы.
- Для чего необходима слезная пленка, и что она собой представляет?
- Назовите основные субъективные симптомы кератитов.
- Факторы необходимые для возникновения язвы роговицы.
- Лекарственные средства, применяемые для лечения герпетических кератитов.
- Опишите клиническую картину кератитa при Herpes Zoster.
- Какие отдаленные последствия глазного зостера.
- Причины нейропаралитического кератита.
- Назовите причины лагофтальма и лечение кератитов возникающих при них.
- Виды и лечение диффузного паренхиматозного кератита при позднем врожденном сифилисе.
- Какое и где проводится лечение при кератите на почве сифилиса?
- Отличие диффузного паренхиматозного туберкулезного кератита от сифилитического.
- Виды туберкулезно-аллергических заболеваний роговицы и их лечение.
- Особенности течения грибкового кератита.
- Что является важным для ранней диагностики акантамебного поражения роговицы?
- Назовите местное лечение акантамебного кератита.
- Назовите причины синдрома «сухого глаза».
- Назовите виды типичных семейно-наследственных дегенераций роговой оболочки.
- Когда могут возникнуть вторичные дегенерации роговицы?
- Какие хирургические методы лечения применяются при бельмах роговицы у взрослых и детей?
- Назовите доброкачественные опухоли роговицы и дайте им характеристику.
- Изменения при синдроме Съёгрена со стороны глаз, слизистой полости рта и других органов.
Профилактика и лечение поражений роговицы при эндокринной офтальмопатии
На правах рукописи
Исманлова Диляра Султанмуратовна
ПРОФИЛАКТИКА И ЛЕЧЕНИЕ ПОРАЖЕНИЙ РОГОВИЦЫ ПРИ ЭНДОКРИННОЙ ОФТАЛЬМОПАТИИ
14.01.07 — глазные болезни АВТОРЕФЕРАТ
диссертации на соискание ученой степени кандидата медицинских наук
Москва 2010 г
003493573
Работа выполнена на кафедре глазных болезней ММА им. Учреждении Российской академии медицинских исследовательском институте глазных болезней РАМН
И.М. Сеченова и в наук Научно-
Научный руководитель:
Доктор медицинских наук, профессор Груша Ярослав Олегович
Официальные оппоненты:
Доктор медицинских наук, профессор Фролов Михаил Александрович
Доктор медицинских наук Маложен Сергей Андреевич
Ведущая организация:
ФГУ МНТК «Микрохирургия глаза» им. академика С.Н. Федорова
Защита состоится м^/^ГС^ 2010 г. в 14.00 на заседании
диссертационного совета Д. 001. 040. 01 при Учреждении Российской академии медицинских наук Научно-исследовательском институте глазных болезней РАМН по адресу: 119021, Москва, ул. Россолимо, д. 11 А, Б.
С диссертацией можно ознакомиться в библиотеке НИИ глазных болезней РАМН
Автореферат диссертации разослан «// » февраля 2010 г
Ученый секретарь диссертационного совета, доктор медицинских наук
Макашова Надежда Васильевна
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ Актуальность исследований
Эндокринная офтальмопатия (ЭОП) — прогрессирующее заболевание мягких тканей орбиты и глаза, в основе которого лежит иммуномедиаторное воспаление экстраокулярных мышц и орбитальной клетчатки (А.Ф. Бровкина, 2006). ЭОП развивается у 50-70% больных с болезнью Грейвса-Базедова (Wiersinga W.M., Bartalena L, 2002).
Одним из наиболее тяжелых, приводящих к значительному снижению зрения, осложнений ЭОП является поражение роговицы. Прогрессирование стромальных дефектов нередко осложняется гнойным расплавлением роговицы. При неудаче устранения лагофтальма, уменьшения объема мягких тканей орбиты и снижения внутриорбитального давления возможна перфорация роговицы, что по данным Ogura J.H. (1978) у 1,8% больных приводит к развитию панофтальмита.
Подобное течение ЭОП отмечается редко, в связи с чем в литературе встречаются лишь описания отдельных клинических случаев и нет четких рекомендаций по лечению этой категории пациентов (Heinz С, Eckstein А et. al, 2004). В связи с тяжелыми последствиями вовлечения роговицы в патологический процесс профилактика этого состояния приобретает особенную актуальность, однако данные о факторах риска поражения роговицы при ЭОП различны и немногочислены (Бровкина А.Ф., Пантелеева О.Г., 2003; Eckstein А.К., Finkenrath А. et. al., 2004). Кроме того, тяжелое соматическое состояние этих пациентов иногда не позволяет проводить весь комплекс хирургических мероприятий, включая декомпрессию орбиты, направленных на адекватную защиту роговицы. В связи с чем поиск новых неинвазивных методов остается важной задачей в лечении таких пациентов.
Иногда роговица вовлекается в патологический процесс при незначительных изменениях положения глазного яблока и век, или, наоборот, при выраженном экзофтальме и лагофтальме может длительно оставаться •.
интактной. В связи с этим большой интерес представляет изучение влияния внутренних защитных факторов роговицы на процессы ее эпителизации. Одним из таких факторов является семейство антимикробных пептидов дефенсинов, синтезирующихся в эпителиальных клетках конъюнктивы и роговицы (Schroder J-M, Raida М. et al., 1999; Chaly YV, Paleolog E.M. et. al., 2000). р-дефенсин-2 (HBD-2) в норме не вырабатывается, его синтез стимулируется антигенами бактерий, а также при нарушении целостности эпителия роговицы. Получены первые результаты указывающие на роль этого белка при инфекционных заболеваниях роговицы и при синдроме «сухого глаза», однако исследований, посвященных его роли в защите роговицы при ЭОП, не проводили.
Целью данной работы было определение факторов риска поражения роговицы, разработка мер профилактики и оценка эффективности лечения тяжелой кератопатии при ЭОП. Задачи исследования:
1. На основании комплексного обследования пациентов с ЭОП выявить факторы риска поражения роговицы при этом заболевании.
2. Изучить связь экспрессии гена Р-дефенсина-2 и возникновения кератопатии у больных с ЭОП.
3. Выявить морфологические изменения конъюнктивы, лежащие в основе ее прокрашивания витальными красителями у больных с ЭОП.
4. Выявить морфологические изменения роговицы у пациентов с тяжелым поражением роговицы при ЭОП.
5. Разработать малоинвазивную методику временной коррекции лагофтальма при ЭОП.
6. Оценить эффективность комбинированного лечения пациентов с тяжелыми поражениями роговицы при ЭОП.
Научная новизна и практическая значимость работы У 46 пациентов с ЭОП (92 глаза) при помощи различных диагностических методов произведена оценка состояния роговицы и
конъюнктивы, в результате чего выявлены факторы риска, а также прогностически значимые параметры поражения роговицы при ЭОП. Впервые изучена связь экспрессии гена НВО-2 и выраженности кератопатии при ЭОП. Впервые выявлены морфологические характеристики конъюнктивы, окрашиваемой витальными красителями, и дисков роговицы, полученных интраоперационно при сквозной и послойной кератопластике у пациентов с тяжелыми поражениями роговицы при ЭОП. Произведена оценка эффективности комбинированного лечения при тяжелых поражениях роговицы при ЭОП. Впервые при этой патологии изучена возможность применения инъекционного геля на основе гиалуроновой кислоты для уменьшения величины глазной щели и коррекции лагофтальма.
Виедреиие результатов работы в практику
Разработанные диагностические методики, способы профилактики и лечения применены на кафедре глазных болезней ММ А им. И.М. Сеченова и в клинике НИИ глазных болезней РАМН.
Основные положения, выносимые на защиту
1. Выявлены факторы риска и прогностически значимые параметры поражения роговицы при эндокринной офтальмопатии (ЭОП).
2. Одним из факторов, приводящих к тяжелому поражению роговицы при ЭОП, является снижение экспрессии гена (3-дефенсина-2.
3. Специфических для ЭОП изменений при морфологическом исследовании бульбарной конъюнктивы и удаленных дисков роговицы не выявлено.
4. Временную коррекцию лагофтальма у больных с ЭОП возможно осуществить путем введения под кожу верхнего века геля на основе гиалуроновой кислоты.
5. У пациентов с тяжелыми поражениями роговицы эффективным является комбинированное лечение, заключающееся в
5
Апробация работы
Предварительные результаты исследования доложены на V конференции молодых ученых России с международным участием «Фундаментальные науки и прогресс клинической медицины» (Москва,
2008), на 17 конгрессе Европейского общества офтальмологов (Амстердам,
2009), на конференции молодых ученых «Актуальные вопросы офтальмологии» (Москва, 2009), на заседании кафедры глазных болезней ММА им. И.М. Сеченова (Москва, 2010) и на заседании проблемной комиссии «Микрохирургия и реконструктивная офтальмохирургия» НИИ глазных болезней РАМН 08.02.2010.
Объем и структура диссертации
Диссертация изложена на _ страницах машинописного текста и
состоит из введения, 3 глав, заключения, выводов, практических рекомендаций и списка литературы, включающего 4 отечественных и 135 иностранных источников. Диссертация иллюстрирована 9 таблицами и 26 рисунками.
СОДЕРЖАНИЕ РАБОТЫ
Характеристика клинического материала и методов исследования
В исследование было включено 46 пациентов (92 глаза) с диагнозом ЭОП, проходивших обследование и лечение в НИИ ГБ РАМН.
Все больные прошли обследование у эндокринолога, которое включало: определение уровня тиреоидных гормонов, тиреотропного гормона (ТТГ), антител к тиреопероксидазе (ТПО) и рецепторам ТТГ. У 26 пациентов был установлен диагноз диффузный токсический зоб, у 8 пациентов — узловой токсический зоб, у 7 пациентов — узловой эутиреоидный зоб, у 5 человек -аутоиммунный тиреоидит. 18 пациентов на момент первого осмотра получали
медикаментозное тиреостатическое лечение (по схеме «блокируй-замещай»), 10 пациентов находились в стадии ремиссии тиреотоксикоза после медикаментозного лечения, 11 пациентов получали заместительную гормональную терапию по поводу гипотиреоза в исходе аутоиммунного тиреоидита (5 человек) или после хирургического лечения (6 человек), остальные 7 пациентов не имели нарушений гормонального статуса в анамнезе. У всех пациентов, вошедших в исследование, уровень тиреоидных гормонов был в пределах нормы на момент начала лечения.
Обследование пациентов включало в себя стандартное офтальмологическое (наружный осмотр, визометрия, тонометрия, компьютерная периметрия, биомикроскопия, офтальмоскопия), а также дополнительные методы: экзофтальмометрия, орбитометрия, биометрические измерения (PF, MRDi, MRD2, MLD|, MLD2, величина лагофтальма), тест Ширмера I, окраска витальными красителями, определение чувствительности роговицы. Морфологическое исследование включало в себя импрессионную цитологию и исследование полутонких срезов конъюнктивы (совместно с заведующим отделом лабораторной и морфологической диагностики, консервации ткани и клеточных технологий НИИ ГБ РАМН A.A. Федоровым). Из лучевых методов диагностики использовали ультразвуковое исследование (УЗИ) и/или компьютерную томографию (KT) или магнитно-резонансную томографию орбит.
Экзофтальмометрию проводили при помощи экзофтальмометра Hertel. Степень смещения глазного яблока до и после костной декомпрессии орбиты оценивали орбитомегром Naugle, поскольку при использованной нами технике сформированный дефект латерального края орбиты не позволяет корректно выполнить экзофтальмометрию по Hertel.
Часть биометрических измерений оценивались при помощи разработанного нами инструмента (положительное решение на получение патента РФ №2008.150.568 от 14.01.10).
Для окраски поверхности глаза использовали следующие витальные красители: флюоресцеин натрия (FNa) для выявления эпителиопатии роговицы, бенгальский розовый и лиссаминовый зеленый для исследования состояния конъюнктивы. Для оценки степени повреждения глазной поверхности использовали шкалу Национального Института Глаза (National Eye Institute Workshop grading system, NEI, США). Степень кератопатии определяли по площади и интенсивности окрашивания роговицы флюоресцеином: роговицу делили на 5 сегментов (верхний, нижний, латеральный, медиальный и центральный), в каждом из которых оценивали степень окраски по 3-х балльной шкале в зависимости от интенсивности окрашивания, где 0 баллов — отсутствие окрашивания, 1 балл — слабое окрашивание, 2 балла — умеренное, 3 балла — выраженное. Степень поражения конъюнктивы определяли при окрашивании ее поверхности бенгальским розовым и/или лиссаминовым зеленым: для этого бульбарную конъюнктиву условно делили на 6 участков, в каждом из которых независимо оценивали интенсивность окрашивания по трехбалльной шкале (аналогично оценке окрашивания роговицы). Максимальное количество баллов для роговицы составляло 15, а для конъюнктивы — 18, при этом значения более 3 баллов считали патологическими.
Чувствительность роговицы определяли при помощи ворсинки ваты в четырех квадрантах и оценивали по следующей шкале: 3 балла — нормальная чувствительность, 2 балла — сниженная чувствительность (роговичный рефлекс сохранен), 1 балл — сильно сниженная чувствительность (роговичный рефлекс отсутствует, однако пациент чувствует прикосновение), 0 баллов -полное отсутствие чувствительности.
Импрессионное цитологическое исследование проводили следующим образом: стандартных размеров полоску миллипорового фильтра с легким давлением прикладывали в течение 5 сек к интересующему участку бульбарной конъюнктивы, после чего отпечаток сразу переносили на обезжиренное предметное стекло. Полученный отпечаток фиксировали
метиловым спиртом в течение 3-2 минут и окрашивали по методу Гимза. Исследование и фоторегистрацию цитологических препаратов проводили на «Фотомикроскопе-Ш» (фирмы «Opton», Германия) при увеличении х160.
Для исследования структуры зоны конъюнктивы, прокрашенной лиссаминовым зеленым, применяли метод полутонких срезов. Забор материала производили после фоторегистрации результатов окрашивания витальными красителями для точной локализации места взятия образца тканей. Полутонкие срезы готовили на ультратоме «NOVA» (LKB, Швеция), окрашивали толуидиновым синим и полихромным красителем (метиленовый синий — фуксин). Светооптическое исследование полутонких срезов и их микрофотографирование проводили на «Фотомикроскопе -111».
Экспрессию гена HBD-2 клетками конъюнктивы выявляли при помощи ПЦР в режиме реального времени (к.м.н. Ганковская O.A.). Забор конъюнктивы производили в операционной или процедурном кабинете под местной анестезией.
Активность ЭОП оценивали по шкале клинической активности CAS (Clinical Activity Score), при этом наличие каждого из признаков оценивали в 1 балл, при сумме баллов более 3 орбитальный процесс считали активным.
Проводимое лечение зависело от стадии, активности и степени компенсации ЭОП. Пульс-терапию по схеме акад. А.Ф. Бровкиной метилпреднизолоном проводили всем пациентам в активную фазу орбитального воспалительного процесса при тяжелом поражении роговицы и при оптической нейропатии. В случае активизации процесса при снижении дозы глюкокортикоидов дополнительно местно вводили пролонгированные формы глюкокортикоидов (дипроспан, целестон).
При недостаточной эффективности пульс-терапии пациентам проводили курс дистанционной у-терапии (ДГТ) на базе ГКБ № 31 (проф. Гарбузов М.И.), в суммарной дозе 15-20 Гр за 10 сеансов.
Местное симптоматическое лечение было направлено на профилактику и лечение экспозиционных изменений роговицы. При отсутствии признаков
поражения роговицы пациентам назначали препараты искусственной слезы. При легкой кератопатии (точечное локальное окрашивание эпителия роговицы) к слезозаменителям добавляли корнеопротекторы (корнерегель), мазь витАпос и тетрациклиновую мазь на ночь. Кроме того, при лагофтальме применяли подклеивание век пластырем на время сна, окклюзию нижних слезных точек. При обширных дефектах эпителия и/или дефектах стромы роговицы к выше перечисленным препаратам добавляли антибактериальные препараты широкого спектра действия. В некоторых случаях для защиты роговицы при выраженном лагофтальме и кератопатии использовали лечебные мягкие контактные линзы.
По показаниям проводили хирургическое лечение: внутреннюю и/или костно-внутреннююю декомпрессию орбиты, тарзорафии, отсечение сухожилия верхней тарзальной мышцы, блефаротомию, пластику нижнего века мукопериостальным лоскутом, биопокрытие роговицы (амнионом или аутоконъюнктивой или аутослизистой с губы или корнеосклеральным лоскутом), кератопластику (сквозную или послойную).
Внутреннюю декомпрессию орбиты проводили через транскутанный или трансконъюнктивальный доступ, удаляли жир височно-носового и верхне-носового квадрантов экстра- и интракональной клетчатки орбиты. Костно-внутреннюю декомпрессию орбиты проводили по методике P.A. Голдберга (1995г). Одной пациентке эндоназальная декомпрессия медиальной стенки орбиты была проведена в клинике JIOP-болезней ММ А им. И.М. Сеченова (проф. A.C. Лопатин, к.м.н. П.А. Кочетков).
Кровавую тарзорафию выполняли для уменьшения лагофтальма и сужения глазной щели. При этом веки расщепляли на переднюю и заднюю пластинки, отсекали частично или полностью сухожилие мышцы, поднимающей верхнее веко, и затем послойно накладывали швы. В случаях выраженного экзофтальма использовали замковую тарзорафию. Во всех случаях операцию заканчивали наложением дополнительных швов на
силиконовых или специально разработанных прокладках (положительное решение на выдачу патента РФ №2008128006 от 9.06.09).
В некоторых случаях для лучшей иммобилизации век после тарзорафии в мышцу, поднимающую верхнее веко, вводили ботулогоксин типа А (БТА).
С целью устранения ретракции использовали отсечение сухожилия верхней тарзальной мышцы или полнослойную блефаротомию, на нижнее веко пересаживали мукопериостальный лоскут.
При лечении пациентов с выраженным синдромом «сухого глаза» производили окклюзию нижних слезных точек следующими способами: использование окклюдеров (временная окклюзия), радиохирургическая коагуляция слезной точки и окклюзия трансплантатом слизистой.
Кроме хирургических методов коррекции ретракции век и лагофтальма использовали инъекции геля на основе стабилизированной гиалуроновой кислоты (Restylane) (положительное решение на выдачу патента РФ№2009104805 от 19.01.10). Гиалуроновую кислоту вводили в верхнее веко кпереди от сухожилия леватора и/или внутрь и/или под претарзальную часть круговой мышцы глаза и/или подкожно.
Пациентам с тяжелыми, длительно не заживающими дефектам стромы роговицы производили следующие хирургические вмешательства: биопокрытие силиковысушенным амнионом, аутоконъюнктивой, корнеосклеральным лоскутом или аллосклерой, сквозную или послойную кератопластику (проф. A.A. Каспаров, д.м.н. С.А. Маложен, к.м.н. C.B. Труфанов). Наиболее частой операцией на роговице было покрытие амнионом. Для этого вмешательства использовали высушенную на силикагеле амниотическую оболочку. Операцию проводили следующим образом: округлый амниотический лоскут расправляли на поверхности роговицы и фиксировали его паралимбалыю к эписклере узловыми или П-образными швами, покрывая зону дефекта роговицы.
Для статистической обработки использовали программный комплекс Epi Info 5.0 (совместно с проф. Герасимовым А.Н.). Связь числовых
показателей исследовали при помощи непараметрических критериев Колмогорова-Смирнова и Манна-Уитни. Для анализа факторов риска использовали корреляционный анализ, для прогнозирования -многофакторный регрессионный анализ. Сравнение данных до и после лечения проводили с использованием критерия Уилкоксоиа. Результаты собственных исследований
В исследование включено 46 пациентов (92 глаза) с диагнозом ЭОП, проходивших обследование и лечение в НИИ ГБ РАМН. В исследование вошли 31 женщина и 15 мужчин, возраст от 18 до 76 лет (в среднем 50,3 ±1,4 лет). Активность ЭОП по клинической шкале CAS — 5,7±0,3 баллов. Сроки наблюдения от 6 до 37 мес (в среднем 13,5 ±10,8 мес). Результаты, полученные при анализе клинических данных, приведены в сводной таблице 1.
Табл. 1. Результаты анализа клинических данных.
Min Мах M m а
Возраст, гг 18 76 50,283 1,393 13,360
Длительность, ЭОП мес 2 130 23,626 3,330 31,771
CAS, баллы 0 10 5,685 0,308 2,957
Острота зрения 0 1 0,822 0,034 0,322
Экзофтальм, мм 15 28 20,924 0,305 2,922
Лагофтальм, мм 0 9 2,120 0,215 2,064
PF, мм 8 18 12,522 0,288 2,761
MLDi, мм 0 4 0,783 0,096 0,915
MLD?, мм 0 6 1,417 0,155 1,469
Чувствительность роговицы, баллы 0 12 6,587 0,347 3,329
Окрашивание лиссаминовым зеленым, баллы 0 16 4,565 0,440 4,217
Окрашивание FNa, баллы 0 15 5,207 0,615 5,896
Тест Ширмера I, мм 0 30 11,522 0,796 7,637
Больные различались по стадии заболевания: при первом посещении у 33 (71,7%) пациентов была активная стадия орбитального воспаления
12
различной степени выраженности, а у 13 пациентов (28,3%) был фиброз. Длительность ЭОП в среднем составила 23,6 мес (от 2 до 130мес).
Активность ЭОП определялась согласно клинической шкале активности CAS. У 22 больных (47,8%) заболевание находилось в активной фазе, при этом степень активности для левого и правого глаза достоверно не различалась. Из 46 пациентов у 33 значение CAS на левом и правом глазу совпадало, у 7 — отличалось на единицу, у 4 — на 2 единицы и по одному — на 3 и 4 единицы, что говорит о практически одинаковой вовлеченности обеих орбит в патологический процесс.
Острота зрения в среднем составила 0,822±0,034, при этом при активной стадии средняя острота зрения составила 0,893±0,031, а в стадии фиброза — 0,642±0,08. Эта разница статистически достоверна (р<0,05). Кроме того, была выявлена достоверная обратная корреляционная связь остроты зрения и степени активности ЭОП (р = 0,031).
Выстояние глазного яблока по данным экзофтальмометрии в среднем составило 20,9 ± 0,3 мм. Была выявлена достоверная отрицательная связь экзофтальма с остротой зрения (р<0,001).
Величина лагофтальма в среднем составила 2,1 ±0,2 мм. Была выявлена достоверная положительная корреляционная связь лагофтальма с активностью заболевания и степенью экзофтальма и отрицательная — с остротой зрения (во всех случаях р<0,001).
Ширина глазной щели в среднем составила 12,5±2,8 мм. Достоверная корреляционная связь этого параметра была выявлена со степенью активности ЭОП, остротой зрения, данными экзофтальмометрии и величиной лагофтальма.
Оценку выраженности поражения роговицы производили по интенсивности и площади окрашивания роговицы флюоресцеином. В зависимости от степени окрашивания роговицы были выделены 3 группы. В 1-й группе (54 глаза) при биомикроскопии и окрашивании флюоресцеином признаки поражения роговицы отсутствовали, среднее значение степени
окрашивания роговицы составило 0,87±1,06 балла. Во 2-ю группу вошли 18 глаз с эпителиопатией различной степени выраженности, в среднем 7,33±2,28 балла. В 3-ю группу вошли 20 глаз с язвенными дефектами стромы роговицы, различными по площади и глубине поражения, наличие которых оценивалось в 15 баллов.
Были выявлены положительные корреляционные связи выраженности окрашивания роговицы с возрастом, активностью заболевания, данными экзофтальмометрии, лагофтальмом, РБ, М1ШЬ МЯ02, ретракцией нижнего века и окраской лиссаминовым зеленым; достоверные отрицательные связи были выявлены с остротой зрения и чувствительностью (табл. 2.).
Табл. 2. Результаты корреляционного анализа окрашивания роговицы флюоресцеином с другими показателями.
Коэффициент корреляции,г Р
Возраст 0,385 <0,001
Длительность 0,202 0,060
CAS 0,314 0,003
Острота зрения -0,737 <0,001
ЭОМ 0,490 <0.001
Лагофтальм 0,499 <0,001
PF 0,336 0,001
MRD, 0,212 0,048
MRD, 0,314 0,003
MLD, 0,140 0,195
mld2 0,598 <0,001
Чувствительность роговицы -0,630 <0,001
Окраска лиссаминовым зеленым 0,907 <0,001
Тест Ширмера -0,164 0,128
При проведении многофакторного регрессионного анализа были определены следующие факторы, позволяющие прогнозировать вероятность поражения роговицы при ЭОП (оценивали по окрашиванию роговицы флюоресцеином >3 баллов): возраст пациента, активность ЭОП, степень
окрашивания конъюнктивы лиссаминовым зеленым, величина глазной щели и ретракции верхнего века. Был получен следующий прогноз: прогноз неблагоприятного варианта = -0,4991 + 0,0748 * степень окраски лиссаминовым зеленым + 0,004><возраст + 0,0206хвеличину глазной щели + 0,0145 х CAS+0,0214 х MLD!. Интерпретация полученного значения представлена в таблице 3.
Табл. 3 Соотношение величины полученного прогноза и вероятности поражения роговицы при ЭОП.
Доля поражения роговицы
менее 0,1 0,0%
0.1 — 0,2 12,5%
0,2 — 0,3 20,0%
0.3 — 0,4 25,0%
0,4 — 0,5 40,0%
0,5 и более 100,0%
Импрессионное цитологическое и гистологическое исследование зоны прокрашивания бульбарной конъюнктивы лиссаминовым зеленым провели 15 пациентам, у которых отмечалось окрашивание. При импрессионном цитологическом исследовании конъюнктивы были выявлены следующие изменения: выраженная дистрофия с клеточным полиморфизмом, уменьшение количества или полное исчезновение бокаловидных клеток, снижение регенераторной способности, повышенная десквамация поверхностного слоя клеток, а также признаки кератинизации эпителия с локальной лейкоцитарной инфильтрацией. Эти данные характеризуют изменения конъюнктивы, типичные для ССГ, и не являются специфичными для пациентов с ЭОП.
Гистологическое исследование полутонких срезов конъюнктивы выявило следующие морфологические особенности: неравномерную толщину эпителия с точечными эрозиями, отсутствие бокаловидных клеток, дистрофические изменения (вакуолизация цитоплазмы, зерна кератогиалина в
цитоплазме), расширение лимфатических сосудов, наличие тучных клеток в непосредственной близости от конъюнктивальных кровеносных сосудов.
При гистологическом исследовании дисков роговиц, удаленных при операциях послойной и сквозной кератопластики у пациентов с тяжелым поражением роговицы при ЭОП, отмечено утолщение и ороговение эпителия, окружающего язвенную поверхность, врастание фиброваскулярной ткани в субэпителиальное пространство с признаками кровоизлияния и расплавления гомогенизированной стромы.
Для выявления экспрессии гена HBD-2 клетками конъюнктивального эпителия у 10 пациентов (10 глаз) без кератопатии и 7 пациентов (10 глаз) с тяжелым поражением роговицы методом ПЦР исследовали образец бульбарной конъюнктивы. У больных без патологии роговицы средний показатель экспрессии гена составил 8,19±0,31, а у больных второй группы -7,4±0,33, разница была статистически достоверна (р=0,01). Таким образом, у пациентов с тяжелыми поражениями роговицы отмечается снижение экспрессии гена HBD-2.
Тактика лечения пациентов зависела от активности и степени компенсации орбитального воспалительного процесса, вовлечения роговицы и зрительного нерва. Пульс-терапия метиллреднизолоном была проведена 21 пациентам. Основными показаниями для внутривенного введения высоких доз глюкокортикоидов были высокая активность заболевания (7 и более баллов по CAS), тяжелое поражение роговицы, оптическая нейропатия. Все пациенты удовлетворительно перенесли лечение высокими дозами глюкокортикоидов, в ряде случаев наблюдались следующие осложнения: у 6 пациентов отмечалось преходящее повышение уровня глюкозы в крови после внутривенного переливания (у 1 пациентки потребовалось дополнительное подкожное введение инсулина для нормализации этого показателя), спустя некоторое время после начала приема глюкокортикоидов у 7 пациентов развился умеренно выраженный синдром Кушинга, однако после отмены стероидов внешний вид пациентов возвращался к исходному уровню. Других
побочных реакций и осложнений в сроки наблюдения (от 2 до 130 мес) нами отмечено не было.
7 пациентам был проведен курс ДГТ (суммарная доза облучения 20 Гр на обе орбиты). Из осложнений этого вида лечения в одном случае отмечалась преходящая аллопеция височной области.
Местное симптоматическое лечение проводили всем пациентам трех групп. Больным 1-й группы без признаков поражения роговицы (54 глаза) назначали препараты искусственной слезы. При значениях теста Ширмера менее 6 мм в нижние слезные точки устанавливали окклюдеры (8 глаз). В течение всего периода наблюдений ухудшения состояния роговицы отмечено не было, разница среднего значения степени окрашивания роговицы флюоресцеином до и после лечения была статистически не достоверна. 4 пациентам была проведена пульс-терапия метилпреднизолоном по поводу оптической нейропатии.
При незначительно выраженной кератопатии (18 глаз) у пациентов 2-й группы помимо слезозаместиггельной терапии пациенты применяли корнеопротекторы (корнерегель), мазь на основе витамина А (витАпос) и тетрациклиновую мазь 1-3 раза в день. Ретробульбарные инъекции пролонгированных форм глюкокортикоидов (дипроспан, целестон) выполнили 7 пациентам (7 глаз), 4 из них после пульс-терапии. Пульс-терапия метилпреднизолоном была проведена 9 пациентам, ДГТ — 2 пациентам. При значениях теста Ширмера 5 и менее в нижние слезные точки устанавливали окклюдеры (7 глаз).
Хирургическое лечение в этой группе больных включало костно-жировую декомпрессию орбиты (2 глаза), коррекцию ретракции верхнего века (1 блефаротомия, 4 отсечения сухожилия верхней тарзальной мышцы), частичную тарзорафию (2 глаза). Кроме того, для коррекции лагофтальма у 4 пациентов (6 глаз) использовали введение геля на основе гиалуроновой кислоты в верхнее веко. В результате лечения у всех пациентов было отмечено улучшение состояния роговицы, степень окрашивания
флюоресцеином в среднем составила 1,6±1,1 баллов. Разница этого показателя до и после лечения была статистически достоверна (р<0,01).
15 пациентам 3-й группы (20 глаз) с тяжелым поражением роговицы проводили комбинированное патогенетически ориентированное и хирургическое лечение. 12 больным проводили пульс-терапию метилпреднизолоном и 5 — ДГТ. В 8 случаях установили окклюдер, в 4 случаях нижняя слезная точка была коагулирована, в 1 — закрыта трансплантатом слизистой.
Оперативное лечение включало в себя следующие методики: 11 декомпрессий орбиты (5 внутренних и 6 костно-внутрениих), 13 тарзорафий (4 полные, 9 частичных), 1 блефаротомию, 3 пластики нижнего века мукопериостальным лоскутом и 6 операций на верхней тарзальной мышце. На роговице было выполнено 14 хирургических вмешательств: 3 биопокрытия амнионом, 4 — аутоконъюнктивой, 1 — корнеосклеральным лоскутом, 3 — аллосклерой, 2 сквозные и 1 послойная кератопластика. 5 пациентам проводили повторные операции на роговице, во всех этих случаях это было связано с лизисом биопокрытия или отторжением трансплантата, причем подобные осложнения отмечались, если одновременно не была произведена тарзорафия. Во время повторных вмешательств обязательно производили частичную или полную тарзорафию, что позволило избежать лизиса биопокрытия.
Эффективность лечения оценивали по нескольким параметрам: острота зрения, состояние роговицы, выстояние глазного яблока, величина лагофтальма, ширина глазной щели, ретракция верхнего и нижнего век. В результате было показано, что по всем этим параметрам после лечения отмечалась выраженная положительная динамика (табл. 4), во всех случаях разница была статистически достоверна.
Таблица 4. Средние значения биометрических показателей до и после комбинированного лечения (М±т).
Острота зрения Экзофтальм, мм Лагофта-льм, мм PF, мм MLDi, мм MLDj, мм Окраска FNa, баллы
До 0,43*0,33 23,25*1,95 4,1*1,63 14,48*1,73 1,23*0,95 2,75*1,03 13,5*2,4
лечения
После 0,69*0,31 20,43*2,13 0,53*0,61 9,36*2,39 0,17*0,28 0,78*0,78 2,25*1,68
лечения
Р <0.02 <0.02 <0.02 <0.02 <0.02 <0.02 <0.01
Кроме хирургических методов коррекции лагофтальма для этих целей была изучена возможность применения препарата на основе гиалуроновой кислоты. Всего 7 пациентам (10 глаз) в верхнее веко был введен гель, средний объем составил 0,25 мл (от 0,2 до 0,4 мл), при этом у 2 пациентов эта манипуляция была выполнена после операций для коррекции остаточного лагофтальма, а у остальных эта методика была единственным вмешательством с целью уменьшения ширины глазной щели и величины несмыкания глазной щели. У всех пациентов применяли препарат Ле81у1апе (<3-Мес1, Швеция), регистрационное удостоверение ФСМ2006/1113. Препарат представляет собой стабилизированную гиалуроновую кислоту неживотного происхождения, в состав входят гиалуроновая кислота 20мг/мд, натрия хлорид 0,9% 9мг, вода для инъекций до 1мл; количество частиц 100000 в 1 мл. Оценка основных биометрических параметров век и состояния роговицы проводилась до введения препарата, через 1 неделю, 1,2, 4 и 6 месяцев после инъекции. Средний срок наблюдения после инъекции составил 11,2 месяца (от 6 до 24 мес.). Уменьшение величины лагофтальма, сужение ширины глазной щели, а также значительное улучшение состояния роговицы было отмечено у всех пациентов. По нашим данным положительный эффект после инъекции был наиболее выраженным в течение 4 мес и сохранялся до 6 мес.
Во время и после введения геля серьезных осложнений отмечено не было. В ранние сроки пациенты жаловались на отечность, неровность контура века/век, болезненность и гиперемию в месте инъекции. У 5 пациентов были незначительные постинъекционные подкожные геморрагии.
У большинства пациентов инъекция не привела к появлению значимого птоза верхнего века. При выполнении инъекций каких-либо технических сложностей не возникло. Однако отмечались некоторые недостатки метода, такие как появление подкожного валика в месте инъекции, что может повлиять на косметический эффект (особенно при одностороннем применении или одномоментном введении значительного объема препарата).
ВЫВОДЫ
1. При комплексном обследовании 46 больных (92 глаза) выявлены следующие модифицируемые факторы риска поражения роговицы при ЭОП: активность воспалительного процесса в орбите, величина экзофтальма, лагофтальма и глазной щели, ретракция нижнего века, увеличение степени окрашивания конъюнктивы витальными красителями и уменьшение чувствительности роговицы. Коррекция указанных факторов риска позволила осуществить профилактику поражений роговицы при ЭОП.
2. Впервые выявлено, что снижение экспрессии гена р-дефенсина-2, наряду с другими факторами риска, может приводить к поражению роговицы при ЭОП.
3. Согласно полученным данным морфологического исследования, прокрашивание бульбарной конъюнктивы витальными красителями обусловлено точечными эрозиями эпителия и повышенной десквамацией поверхностных клеток. Выявленные изменения не являются специфичными для ЭОП.
4. Морфологические изменения при тяжелом поражении роговицы не являются специфичными для ЭОП и представлены периферическим изъязвлением с утолщением и кератинизацией окружающего язву эпителия, субэпителиальной фиброваскулярной пролиферацией.
5. Введение в верхнее веко препарата на основе гиалуроновой кислоты позволило проводить временную коррекцию лагофтальма и уменьшить ширину глазной щели при ЭОП.
6. Комбинированное лечение, заключающееся в выполнении реконструктивных операций на веках, орбите и роговице в сочетании с комплексом патогенетически ориентированной терапии орбитального воспаления (глюкокортикоиды, дистанционная у-терапия), позволило добиться органосохранного эффекта и улучшения состояния роговицы у 15 пациентов (20 глаз) с тяжелым поражением роговицы при ЭОП.
Практические рекомендации
1. Для определения вероятности поражения роговицы при ЭОП можно использовать следующие прогностические факторы: возраст пациента, активность заболевания, ширина глазной щели, величина ретракции верхнего века и степень окрашивания конъюнктивы витальными красителями.
2. Лечение больных с дефектами стромы роговицы при ЭОП должно быть комбинированным и включать биопокрытия роговицы, операции на орбите и веках. При высокой активности орбитального воспалительного процесса необходимо одновременное системное применение глюкокортикоидов.
3. Покрытие роговицы амниотической мембраной целесообразно сочетать с проведением одномоментной частичной или полной тарзорафией, что значительно снижает риск ухудшения состояния роговицы, лизиса и травматизации биопокрытия при мигательных движениях.
4. В качестве временного способа коррекции лагофтальма и уменьшения ширины глазной щели при ЭОП возможно введение в верхнее веко геля на основе гиалуроновой кислоты как в качестве самостоятельной процедуры, так и в качестве одного из этапов комбинированного лечения. Это особенно актуально у пациентов с тяжелым соматическим статусом или при отказе пациента от оперативного вмешательства.
Список работ, опубликованных по теме диссертации
1. К вопросу о тактике лечения тяжелых поражений роговицы при эндокринной офтальмопатии// Материалы научно-практической конференции «современные методы диагностики и лечения заболеваний роговицы и склеры». — Москва. — 2007. — т.2 — с. 2125 (в соавт. с Грушей Я.О., Каспаровым A.A., Стоюхиной A.C.).
2. Комбинированное хирургическое лечение язвы роговицы при эндокринной офтальмопатии// Вестник офтальмологии. — 2008. -Т. 124 (№6) — С. 57-59 (в соавт. с Грушей Я.О.,Каспаровым A.A., Киселевой Т.Н., Федоровым A.A., Филимоновым Г.П., Зайцевым A.B., Полуниной A.A.).
3. Комплексное лечение декомпенсированного отечного экзофтальма// Вестник офтальмологии. — 2009. — 3 — 46-50 (в соавт. с Грушей Я.О., Каспаровым A.A., Стоюхиной A.C., Мерзляковой О.Ю.).
4. Исмаилова Д.С. Диагностика и лечение патологии роговицы при эндокринной офтальмопатии// Сборник тезисов конференции молодых ученых «Актуальные вопросы офтальмологии». -Москва. — 2009. — с. 267-269.
5. Синдром «сухого глаза» и тяжелые поражения роговицы у больных с эндокринной офтальмопатией// Врач. — 2009. — №3 -с.72-76. (в соавт. с Сафоновой Т.Н., Грушей Я.О., Федоровым A.A.).
6. Treatment of severe corneal exposure keratopathy associated with thyroid eye disease// The 17th congress of the European society of ophthalmology. — Amsterdam — 2009. — p. 125. (coauthors Grusha Y.O., Kasparov A.A.).
7. Компрессионная пластина для сведения биологических тканей лигатурой и фиксации лигатурных швов.// Положительное решение №2008128006 от 09.06.2009 на выдачу патента РФ (в соавт. с Грушей Я.О., Агафоновой Е.И., Игнатьевой Ю.Ф., Поповым П.М.).
8. Устройство для измерения величины лагофтальма и глазной щели.// Положительное решение №2008150568 от 14.01.2010 на выдачу патента РФ (в соавт. с Грушей Я.О., Игнатьевой Ю.Ф.)
9. Способ уменьшения величины глазной щели.// Положительное решение №2009104805 от 19.01.2010 на выдачу патента РФ (в соавт. с Грушей Я.О., Игнатьевой Ю.Ф., Агафоновой Е.И.).
Ю.Первый опыт применения препарата стабилизированной гиалуроновой кислоты для коррекции лагофтальма// Вестник офтальмологии. — 2010. — 1 — 39-42 (в соавт. с Грушей Я.О., Иванченко Ю.Ф., Агафоновой Е.И.).
Список сокращений
БТА — ботулотоксин типа А ДГТ — дистанционная у-терапия КТ — компьютерная томография ПЦР — полимеразная цепная реакция ССГ — синдром сухого глаза ТПО — тиреопероксидаза ТТГ — тиреотропный гормон УЗИ — ультразвуковое исследование ЭОП — эндокринная офтальмопатия
CAS — шкала клинической активности (Clinical Activity Score) FNa — флюоресцеин натрия HBD-2 — р-дефенсин-2
MLDi — расстояние от верхнего лимба до края верхнего века MLD2 — расстояние от нижнего лимба до края нижнего века MRD) — расстояние от рефлекса роговицы до края верхнего века MRD2 — расстояние от рефлекса роговицы до края нижнего века PF — ширина глазной щели M — среднее арифметическое
m — статистическая ошибка среднего (среднеквадратичное отклонение среднего по группе) о — среднеквадратичное отклонение
Подписано в печать 25 февраля 2010 г.
Формат 60×90/16
Объём 1,0 п.л.
Тираж 100 экз.
Заказ №270210282
Оттиражировано на ризографе в ООО «УниверПринт» ИНН/КПП 7728572912X772801001
Адрес: 119333, г. Москва, Университетский проспект, д. 6, кор
Тел.740-76-47,989-15-83.
http://www.imiverprint.ru
Осложнения и последствия ношения контактных линз
Серьезные осложнения и последствия ношения контактных линз, которые могут возникнуть в результате использования контактных линз, можно разделить на следующие основные группы:
- – Последствия гипоксического изменения роговицы в период ношения линз
- – Воспалительные, инфекционные осложнения во время ношения линз
- – Аллергические осложнения при ношении линз
- – Последствия ношения связанные с неправильным подбором размера линз
Последствия гипоксического повреждения роговицы при ношения линз
Гипоксические изменения возникают только при ношении гидрогелевых контактных линз, у которых коэффициент пропускания кислорода Dk/t менее 100, при несоблюдении режима ношения линз, ношении линз круглые сутки, более 8-10 часов в день. Гипоксия проявляется покраснением глаз после а также во время ношения линз.
Дело в том, что роговая оболочка (роговица глаза) на поверхность которой одевается контактная линза, не имеет собственных сосудов, она прозрачная, блестящая, влажная для того, чтобы обеспечить беспрепятственное прохождение световых лучей внутрь глаза. Поверхность роговицы состоит из уникального эпителия, способного к быстрой регенерации, что помогает быстро восстановить поверхность роговицы при повреждении поверхностного эпителия.
Гипоксия при плотной посадке линз
Питание роговица получает из сосудов лимбальной зоны. Лимбальная зона – это сосудистое кольцо, которое находится на границе склеры и роговицы. Именно поэтому важно, чтобы край контактной линзы не передавливал эту область, что бывает при плотной посадке контактной линзы. Контактная линза с плотной посадкой может вызвать гипоксические повреждения роговицы глаз даже в том случае, если ее коэффициент пропускания кислорода будет более 100. Правильность посадки контактной линзы может оценить только врач офтальмолог.
Еще один источник питания для роговицы – это слеза. Слезная пленка постоянно омывает роговицу, на которой находится контактная линза, и доставляет необходимые для ее жизнедеятельности питательные вещества и кислород.
Гипоксия глаз во время сна в линзах
Кроме вышеперечисленного, роговица получает кислород из воздуха. Поэтому даже без контактной линзы во время сна, при закрытых веках роговица испытывает состояние физиологической гипоксии. Но благодаря хорошим компенсаторным возможностям поверхностного эпителия роговицы, микроповреждения, возникающие в результате физиологической гипоксии быстро восстанавливаются.
Но если на время сна не снимать контактные линзы, то гипоксические повреждения роговицы глаз будут намного больше, компенсаторных возможностей поверхностного эпителия может не хватить и это приведет к осложнениям связанным с не правильным ношением контактных линз.
Что происходит с поверхностью роговицы при дневном ношении гидрогелевых контактных линз? Если контактная линза подобрана правильно, имеет хорошую посадку, не давит на лимбальную зону, но имеет коэффициент пропускания кислорода Dk/t ниже 100, то вследствии ограничения поступления кислорода к роговице даже при дневном режиме ношения линз, рано или поздно возникают гипоксические повреждения роговицы.
Последствия гипоксии роговицы
На первом этапе при ограничении объема необходимого кислорода, возникает эпителиопатия роговицы. Увидеть эпителиопатию роговицы можно при осмотре в щелевой лампе, после окрашивания роговицы специальным красителем.
Видимые проявления гипоксии роговицы – это появление прорастающих в прозрачную роговицу сосудов из лимбальной зоны.
На следующим этапе гипоксии появляются эрозии роговицы и как правило присоединяется инфекция, так как недостаточное количество кислорода является хорошей средой для размножения бактерий.
На этом этапе, как правило, обращаются к врачу, так как ношение контактных линз становится уже не возможным.
После проведенного лечения для предотвращения повторного возникновения эрозии, рекомендовано ношение только силикон-гидрогелевых линз с высоким показателем Dk/t, например Air Optix Night and Day или контактных линз Biofinity, разрешается только дневной режим ношения линз.
Воспалительные осложнения, инфекционные осложнения во время ношения линз
Воспалительные осложнения могут возникнуть при ношении любых контактных линз плановой замены как из гидрогелевого, так и из силикон-гидрогелевого материала, кроме однодневных линз.
Однодневные контактные линзы в этом отношении самые безопасные, даже в случае проникновения внутрь линзы возбудителя, нет условий для его дальнейшего развития. Однодневные линзы рассчитаны только на один день ношения, вечером их снимают и выбрасывают. На следующий день одевают новую, чистую пару линз.
Контактные линзы плановой замены – на две недели, на месяц, на три месяца, на полгода, в случае проникновения возбудителя бактерии или вируса внутрь линзы, создают благоприятные условия для их размножения -оптимальная влажность и температура тела. Это приводит к инфицированию линз и развитию вирусных, бактериальных или смешанных вирусно-бактериальных кератитов и конъюнктивитов с возможными серьезными осложнениями.
Инфицирование линз происходит следующими путями:
– в случае несоблюдения правил ухода за линзами. Контейнер для линз может стать источником заражения линз, если он не меняется раз в месяц. Бактерии или грибы могут размножатся на стенках контейнера и инфицировать линзы. Раствор для ухода за линзами должен меняться каждый день, при повторном использовании раствора не очищается полностью.
– в случае ношения контактных линз во время простудных заболеваний, вирус, который находится в слезе проникает в контактную линзу и размножаясь там вызывает инфицирование конъюнктивы и роговицы.
– через воду, плавание в водоемах или бассейне в линзах плановой замены, бактерии присутствующие в воде могут попасть в линзу. Особенно опасна в этом отношении бактерия акантамеба. Этот вид микроорганизмов живет в воде и проникая в линзу во время купания вызывает тяжелый акантамебный кератит, который плохо поддается лечению медикаментами. Последствия акантамебного кератита печальные – это прободение роговицы в результате ее расплавления.
Пока единственным методом лечения акантамебного кератита считается пересадка донорской роговицы.
Ограничения на ношение линз во время лечения
Во время лечения всех других вирусных или бактериальных кератитов и конъюнктивитов запрещено ношение контактных линз до полного излечивания всех симптомов. После выздоровления рекомендовано начинать ношение контактных линз с однодневных линз. Для профилактики воспалительных осложнений рекомендуется во время простудных заболеваний не пользоваться контактными линзами, а носить очки.
Во время плавания в бассейне, для купания в открытых водоемах, особенно во время поездки на море пользоваться только однодневными контактными линзами. Соблюдайте правила ухода за контактными линзами, не перенашивайте линзы, каждый день наливайте в контейнер с линзами чистый раствор, предназначенный для ухода за ними, регулярно не реже одного раза в месяц меняйте контейнер для линз на новый.
Аллергические осложнения при ношении линз
Аллергические конъюнктивиты возникают при ношении контактных линз плановой замены у людей предрасположенных к аллергическим реакциям, у аллергиков. Контактная линза обладает способностью накапливать в себе вещества, которые могут быть аллергенами и в случае предрасположенности к аллергии, эти вещества могут привести к сенсибилизации и развитию аллергического конъюнктивита.
Для профилактики аллергического конъюнктивита рекомендуется носить однодневные контактные линзы или постоянно или на время действия известного аллергена, например во время цветения растений, пыльца которых является причиной обострения аллергической реакции.
Последствия связанные с неправильным подбором размера линз
Как подобрать размер контактных линз вам может посоветовать только врач офтальмолог, во время подбора линз врач всегда оценивает посадку контактных линз на роговице. В норме линза должна полностью покрывать зону лимба, смещаться на 1,5 -2 мм при моргании, при пуш-ап тесте легко смещаться и возвращаться в исходное положение – это правильная, безопасная посадка линз. При свободной посадке контактная линза слишком подвижна, децентрируется.
При плотной посадке линза смещается менее 1,5-2 мм или вообще не подвижна. При такой посадке нарушаются обменные процессы в роговице за счет гипоксии. Края линзы пережимают сосуды лимбальной зоны, не достаточный обмен слезы в пространстве между линзой и роговицей приводит к развитию осложнений.
Врач-офтальмолог Наталья Гусакова
Дина Р
02.04.18
Здравствуйте, ношу линзы уже 18 лет. Последние годы носила Oasys(2-недельные). 1,5 года назад впервые купила очки и решила надевать их хотя бы 1 раз в неделю. Из-за этого или нет, но через пару месяцев вдруг начались внезапные проблемы типа сухости и слезотечения и во время ношения линз и во время ношения очков. Причем может 10 мин дискомфорт, потом норм. Или 3 дня покраснение (без гноя и т.п.), снова норм. Врачи говорят, что глаза привыкли к увлажняющему компоненту, встроенному в эти линзы, тип надо менять линзы. Уже год пробую новые линзы. Биофинити однозначно не нравятся — сохнут на глазах, вечером прямо отдираю. Каплями пользуюсь. Понравились Bausch+Lomb Ultra, но судя по всему в них так же используется доп увлажнение — технология MoistureSeal…
Вопросы: 1. действительно ли линзы типа Oasys вызывают привыкание или это маркетинг? (упорно продают Биофинити) 2. существуют ли очковые линзы, которые не искажают?
Наталья Гусакова
16.01.17
Дина, здравствуйте! Последствия от ношения цветных линз точно такие же как и при ношении обычных, прозрачных линз.
Дина
14.01.17
Здравствуйте Наталья. Подскажите, последствия ношения цветных линз будут такими же как при ношении контактных линз, или у них есть свои особенности?
Когда сухой глаз нарушает целостность роговицы
Болезнь сухого глаза (DED) поражает все части функциональной единицы слезной железы, включая роговицу, конъюнктиву, мейбомиевые железы, слезные железы и взаимосвязанную иннервацию. Как клиницисты, мы склонны выявлять сухость глаз, выслушивая жалобы пациентов на симптомы, связанные с DED, и внимательно исследуя роговицу. Это не ошибочный подход, учитывая, что роговица имеет решающее значение для зрения и часто является первой структурой, нарушенной DED.
В этой статье подробно рассматривается влияние DED на роговицу, в том числе то, что мы знаем о патофизиологии заболевания, исходном инсульте и методах его развития.
| У этого пациента наблюдается диффузная точечная эпителиопатия и сниженная барьерная функция, связанная с сухим глазом. |
Основы роговицы
Роговица человека представляет собой бессосудистую структуру, состоящую из нескольких отдельных слоев. 1 Самый внешний слой, эпителий роговицы, состоит из трех слоистых слоев клеток: базального эпителия, крыловых клеток и апикальных клеток. 1
Базальный эпителий . Он контактирует с подлежащей базальной мембраной и прикрепляет эпителиальный комплекс к структурной части роговицы. 1
Ячейки крыла . Они находятся в средней части эпителия и представляют восходящую миграцию части базального эпителия в промежуточном состоянии к апикальным клеткам. 1
Апикальные клетки . Это самые внешние клетки, которые находятся в непосредственном контакте со слезной пленкой. 1 Апикальные клетки содержат микровиллы и микроворсинки, которые доходят до слезной пленки на 0,5 мкм и покрыты плотным гликокаликсом. Состоящий из нескольких трансмембранных муцинов, которые образуют мукоадгезивный комплекс, гликокаликс прикрепляет слезную пленку к апикальному эпителию и защищает от бактерий. 1
Роговица получает питательные вещества и кислород из двух разных областей.Периферическая роговица получает питание от лимбальной области, которая содержит сосудистые петли конъюнктивы. Центральная передняя часть роговицы, а именно эпителий роговицы, получает большую часть кислорода и питательных веществ из слезной пленки.
Поверхность эпителия образована нишами стволовых клеток в лимбе, которые производят временные амплифицирующие клетки. 1 Они мигрируют через мембрану Боумена к центральной роговице, дальше от лимба и кровоснабжения. Во время нормального клеточного обновления временные потомки амплифицирующих клеток будут мигрировать через роговицу и дифференцироваться в базальные клетки, а затем в крылатые и апикальные эпителиальные клетки.
Роговица, являясь наиболее иннервируемой тканью в организме с рецепторами, насчитывающими примерно 6000 сенсорных терминалов на квадратный миллиметр, предназначена для отслеживания изменений в окружающей среде, в том числе для защитной слезной пленки, и обеспечения обратной связи. 2,3 Большинство этих рецепторов роговицы являются механорецепторами, которые обнаруживают прикосновение или боль; но примерно от 10% до 15% реагируют на изменения температуры и осмолярности, что может помочь обнаружить испарение и предоставить средства для регулирования базальной секреции. 4
| Окрашивание роговицы показывает значительную потерю эпителиального барьера при сильном синдроме сухого глаза с потерей мукоадгезивного слоя и плохой смачиваемостью слезной пленки. Щелкните изображение, чтобы увеличить. |
Healthy Tear Film
В здоровом глазу слезная пленка стабильна и обеспечивает достаточную преломляющую поверхность для хорошего зрения. Он поддерживает глазную поверхность, обеспечивая кислород и питательные вещества, и защищает ее от осушающей среды, такой как ветер, а также от токсинов, микробов и твердых частиц.
Здоровая слезная пленка состоит из множества составных частей. Имеет сложный набор и сбалансированное количество электролитов. 5 От нейтрального до слабокислого. 5 Слезная пленка содержит лизоцим и лакритин в качестве защитных медиаторов, а также сотни белков и протеолитических ферментов, которые поддерживают нормальную клеточную функцию эпителия роговицы и обеспечивают защитный барьер для окружающей среды. 5
Несколько желез на поверхности глаза и вокруг нее образуют составные части слезной пленки, в первую очередь слезные и добавочные железы, мейбомиевые железы и бокаловидные клетки конъюнктивы.
Несмотря на все свои важные функции, слезная пленка в здоровом глазу чрезвычайно тонкая, в среднем от 2 до 5,5 мкм по роговице. 6
| У этого пациента нарушение конъюнктивального эпителия распространяется на роговицу в виде макропунктатных эрозий, вызванных сухим глазом. |
Гомеостаз
Вся эта система предназначена для мониторинга окружающей среды и поддержания гомеостаза путем компенсации изменений температуры и влажности и защиты открытых тканей от бактерий и других нарушителей.
Нормальный глаз поддерживает свою гомеостатическую среду с помощью этого мониторинга и компенсирующих действий. Например, способность слезной функциональной единицы компенсировать и регулировать производство и объем слезы является отличительной чертой системы здоровой глазной поверхности. Слезы — это компенсаторный рефлекторный механизм, предназначенный для увеличения или восстановления объема, восстановления осмотического баланса или выведения токсинов или раздражителей.
При «сухом глазу» пациенты страдают потерей гомеостаза, и механизмы, обычно предназначенные для защиты глаза, такие как включение хронической воспалительной реакции, могут противодействовать ему и приводить к прогрессированию ДЭД.Возвращаясь к примеру слезотечения, пациенты с умеренным синдромом сухого глаза часто испытывают слезотечение как реакцию на стресс (например, при чтении или пребывании на холоде и сквозняке). Напротив, у более тяжелых пациентов с синдромом сухого глаза, особенно с диагнозом аутоиммунных состояний, таких как синдром Шегрена, могут быть повреждены железы и нейросенсорные системы из-за хронического воспаления, что не позволяет глазной системе компенсировать стресс-факторы повышенной потребности в испарении. 7
Тестирование DEDНесколько тестов могут помочь вам количественно оценить серьезность сухого глаза, включая окрашивание роговицы и конъюнктивы жизненно важным красителем, а также тестирование в месте оказания медицинской помощи на наличие или степень воспалительного процесса участие.Окрашивание роговицы и конъюнктивы, пожалуй, один из наиболее доступных и легко поддающихся количественной оценке методов оценки повреждения глазной поверхности. Степень тяжести поражения роговицы является ключевым признаком при определении степени тяжести DED. Существует несколько систем оценки, помогающих классифицировать синдром сухого глаза, например, Оксфордская схема, система Ван Бьистервельда и рекомендации NEI / Industry Workshop. 19 Инстилляция флуоресцеина натрия — полезный диагностический инструмент для определения степени повреждения глазной поверхности.Окрашивание флуоресцеином будет присутствовать в клетках с дефектными плотными контактами или нарушенным гликокаликсом. 20 Помните, умеренное фоновое поглощение флуоресцеинового красителя считается нормальным, поэтому существует более слабая корреляция между тяжестью заболевания и поглощением пятен при легких формах сухого глаза. 21 Лиссаминовый зеленый, еще один жизненно важный краситель, хорошо переносимый пациентами, будет поглощаться эпителиальными клетками с поврежденной клеточной мембраной и обеспечивает средство оценки как роговицы, так и конъюнктивы. Несмотря на то, что существует ряд вариантов тестирования для обеспечения систематических средств оценки наличия окрашивания на роговице, ни один конкретный метод, похоже, не имеет более высокой точности или лучшей корреляции с серьезностью заболевания, поэтому метод тестирования полностью зависит от клинициста. . |
Воздействие на роговицу
Потеря гомеостаза имеет множество последствий для роговицы, включая жалобы на зрение, повышенный риск инфекции, кератита и микроэрозий и, конечно же, воспаления.
Расплывчатое зрение . Поскольку роговица зависит от функции самой тонкой части слезной пленки, нечеткое и непостоянное зрение может быть одним из первых ключей к диагностике сухого глаза. Пятилетнее проспективное многоцентровое исследование Progression of Ocular Findings Study (PROOF) показывает, что одно из основных различий между людьми с легкой степенью DED и людьми без сухого глаза заключается в том, как они воспринимают качество своего зрения. В обеих группах исходная острота зрения с максимальной коррекцией зрения (BCVA) составляла 20/20.Тем не менее, 58,5% из тех, у кого был второй уровень сухости глаз, как это определено руководящими принципами Международной целевой группы, выразили умеренное, серьезное или очень серьезное недовольство своим зрением, по сравнению только с 13,7% в контрольной группе. 8,9
Воспаление . Гиперосмолярность слезной пленки — один из ключевых механизмов, управляющих воспалением и прогрессированием ДЭД. Кроме того, в основе гиперосмолярности может лежать испарительное напряжение.
Исследования осмолярности показывают, что разница в уровнях осмолярности между менисками слезы и прекорнеальной слезной пленкой, вероятно, существует, причем прекорнеальная слезная пленка имеет более высокую осмолярность. 10 У пациентов с синдромом сухого глаза эта разница может быть еще больше. Математические модели осмолярности в прекорнеальной слезной пленке показывают быстрое увеличение из-за испарения и уменьшения времени разрушения слезы. Это может повысить осмолярность прекорнеальной слезной пленки до уровней, которые являются довольно высокими (например, 1900 мОсм / мл) по сравнению с нормальным (например, 300 мОсм), особенно там, где слезная пленка отделяется или разрушается. 11 Напротив, самые высокие значения в слезном мениске составляют значительно ниже 500 мОсм.
На клеточном уровне повышенная осмолярность вызывает воспаление посредством передачи сигналов клетками. Рецепторы клеточных мембран, такие как toll-подобные рецепторы (TLR), инициируют внутренние процессы передачи сигналов в клетке, в первую очередь за счет активации NF-kB и митоген-активируемой протеинкиназы (MAPK). 12 Эти два цитоплазматических сигнальных пути активируют транскрипцию цитокинов (в первую очередь IL-1) и матриксных металлопротеиназ (MMP). ММП представляют собой субстрат-специфические протеолитические ферменты, которые регулируют отложение внеклеточного матрикса, а также его деградацию. 12
Кератит . В периоды высокого испарительного стресса увеличение осмолярности слезной пленки вызывает воспаление, которое начинается в апикальных клетках роговицы. Повышенная осмолярность слезной пленки изменяет нормальный внутренний / внешний осмотический градиент, перемещая воду и внутреннее ионное содержание клеток во внеклеточное пространство. Это приводит к потере объема клеток, что приводит к образованию промежутков между соседними эпителиальными клетками, что приводит к появлению «тонкого» поверхностного точечного кератита (SPK) и усиленному проникновению флуоресцеина в более глубокие слои эпителия роговицы, а затем в переднюю строму. .
Недавние измерения SPK-поражений, наблюдаемых у пациентов с синдромом сухого глаза, показывают, что средний диаметр меньше диаметра здоровой эпителиальной клетки. Скорее всего, это «сдутые» или сморщенные клетки, которые находятся в процессе апоптоза и впитали краситель. 2
При более запущенных формах состояния хроническая эпителиальная недостаточность может также привести к усилению регуляции муцина и формированию нитевидного кератита, при котором слизистые спайки цепляются за участки с хронической нерегулярностью или нарушением эпителия.
| Точечная эпителиальная кератопатия этого пациента затрагивает центральную роговицу в случае синдрома сухого глаза Шегрена. Щелкните изображение, чтобы увеличить. |
Инфекции . Сухой глаз постоянно является одним из трех основных факторов риска бактериального кератита. 13,14 Целостность роговицы необходима как врожденная защита от бактерий. Хронические разрывы поверхности роговицы в сочетании с уменьшением содержания лизоцима и лактоферрина, которые обеспечивают вторую защиту от бактерий, предрасполагают сухой глаз к более высокому риску инфицирования роговицы.Это становится еще более важным для тех, кто носит контактные линзы, которые подвергаются воздействию бактериальных биопленок, а также матриц контактных линз, которые со временем могут быть загрязнены и заселены рядом бактерий, грибков и паразитов.
На клеточном уровне активация лимфоцитов, рекрутирование и инфильтрация тканей Т-лимфоцитами — все признаки DED — могут в конечном итоге снизить устойчивость к инфекции. Активация и рекрутирование Th2 / Th27 через сигнальный путь ядерного фактора каппа-бета (Nf-KB) является важной частью механизма, который управляет преобразованием острого ответа в хроническое воспаление и, по-видимому, играет ключевую роль в прогрессировании заболевания. 15,16 Инфильтрация слезной железы приводит к повреждению и дисфункции секреторных ацинусов. В конечном итоге это меняет состав слезной пленки.
Снижение молекул эпителиального барьера роговицы . Хотя в организме человека существует по крайней мере 30 известных ММП, ММР-3 и -9 кажутся особенно важными для поддержания эпителиального барьера роговицы. Например, повышенный уровень ММР-9 коррелирует с повышенным окрашиванием роговицы у пациентов с синдромом сухого глаза, но также повышается при инфекции роговицы, рецидивирующей эрозии и других патологиях, при которых нарушен эпителиальный барьер роговицы. 17 MMP-9 обычно находится на поверхности глаза в небольших количествах, ниже 41 нг / мл в здоровой роговице. Уровни выше 41 нг / мл связаны с нарушением эпителия. MMP-9 влияет на соединения между эпителиальными клетками, разрушая молекулу окклюдина, критического компонента плотных контактов.
По мере увеличения концентрации провоспалительных молекул количество соединений, поддерживающих эпителий роговицы, может уменьшаться. Молекула индуктора металлопротеиназы внеклеточного матрикса (EMMPRIN), рецептор эпителиальных клеток роговицы типа 1, который может играть важную роль в поддержании эпителиального барьера роговицы, увеличивается пропорционально уровням MMP-9. 18 Исследования показывают обратную зависимость между количеством EMMPRIN и окклюдином в роговице. Поскольку окклюдин имеет решающее значение для поддержания плотных контактов между соседними эпителиальными клетками, общий барьер роговицы нарушается.
Базальная секреция, неврологические изменения и симптомы . При воспалении повреждение ноцицепторов роговицы и связанных с ними неврологических путей может снизить базальную секрецию слезы, а также способствовать морфологическим изменениям в структуре нервов, которые могут привести к болевым ощущениям или, наоборот, к гипестезии и нейротрофии, несмотря на обострение болезни. 4,7
Механическая десквамация эпителия . В нормальном глазу слезная пленка обеспечивает амортизацию и смазку, помогая векам перемещаться по поверхности глаза с минимальным трением. Однако при сухом глазу уменьшается как объем, так и содержание слезной пленки, подвергая гликокаликс и апикальный эпителий воздействию сил трения моргания. Это приводит к усилению десквамации эпителия по сравнению с нормальными глазами.
Болезнь сухого глаза имеет ряд негативных последствий для глазной системы, начиная с нарушения гомеостатических механизмов, предназначенных для защиты здоровья глазной поверхности.Мы можем использовать роговицу в качестве окна для оценки степени тяжести ДЭД, и как только эти системы нарушены, воспалительное поражение тканей роговицы и конъюнктивы затрудняет возвращение к исходной гомеостатической функции. Нарушаются процессы, которые направляют заживление ран роговицы и образование плотных стыков. Продолжающееся повреждение роговичного барьера и нарушение целостности роговицы приводит к появлению пониженной смачиваемости из-за разрушения или потери гликокаликса, точечной кератопатии, микроэрозий, развития нитей и повышенного риска инфекции.
Выявляя проблемы на раннем этапе, мы можем сделать задачу восстановления гомеостаза глазной поверхности и предотвращения прогрессирования заболевания менее сложной.
Доктор Хаусвирт — доцент кафедры офтальмологии Медицинской школы Университета Колорадо в Денвере, штат Колорадо.
Острая микрокистозная эпителиопатия роговицы после ежедневного ношения мягких контактных линз | JAMA Офтальмология
Мы описываем 4 пациентов, у которых развилась острая двусторонняя микрокистозная эпителиопатия роговицы с заметным снижением остроты зрения после ежедневного ношения мягких контактных линз.Кисты исчезли в течение 4 недель с полным восстановлением зрения, хотя у 1 пациента развилось центральное уплощение роговицы. Исследование биоптата эпителия от 1 пациента дало отрицательный результат на Acanthamoeba . Однако апоптоз был продемонстрирован окрашиванием с помощью анализа TUNEL (TdT-опосредованное мечение dUTP по никому концу). Мы считаем, что это явление является следствием острой гипоксии роговицы.
Эпителиальные микрокисты — это небольшие (от 15 до 50 мкм) включения, ранее описанные как отсроченная реакция на длительное ношение контактных линз. 1 Реже наблюдаются после ежедневного ношения мягких или жестких контактных линз. У пациентов, пользующихся мягкими линзами длительного ношения, микрокисты обычно развиваются через 4-8 недель. Количество развивающихся кист зависит от проницаемости линз для кислорода и продолжительности ношения, и они исчезают через несколько месяцев после прекращения ношения линз. Обычно они возникают в небольшом количестве в центре или на средней периферии роговицы и редко вызывают симптомы. Напротив, мы описываем 4 пациентов, которые ежедневно носили мягкие контактные линзы, у которых развилось резкое ухудшение зрения, связанное с крупной микрокистозной эпителиопатией.Обсуждаются клинические особенности и возможное происхождение этого состояния.
Были идентифицированы четыре пациента, которые ежедневно носили мягкие контактные линзы и у которых была острая двусторонняя микрокистозная эпителиопатия роговицы (таблица 1). При первом осмотре всем посоветовали не носить контактные линзы; затем им дали местный антибиотик (0,5% хлорамфеникол 4 раза в день в течение 1 недели) и обследовали до полного исчезновения микроцист.Первому пациенту была выполнена биопсия эпителия, чтобы исключить кератит Acanthamoeba как причину; Часть биопсийного образца инкубировали на непищевом агаре, засеянном убитой Escherichia coli , а оставшуюся часть исследовали с использованием кроличьих моноклональных антител против Acanthamoeba . Также был проведен тест TUNEL (TdT-опосредованное мечение ник-конца dUTP) (Gibco BRL, Пейсли, Соединенное Королевство), который идентифицирует умирающие (апоптотические) клетки путем мечения фрагментированной ДНК.
Характеристики пациентов с острой микрокистозной эпителиопатией роговицы от повседневного ношения мягких контактных линз
Двое пациентов носили линзы постоянно, а двое — только для общественных мероприятий. Все пациенты отрицали предыдущие проблемы с линзами, ношение на ночь или злоупотребление контактными линзами. Все носили линзы за день до появления симптомов и после пробуждения отметили заметное ухудшение зрения с легким дискомфортом от инородного тела.
Первые осмотры проводились через 1-3 дня после появления симптомов. Зрение ухудшилось на всех глазах и еще больше ухудшилось у 2 пациентов, несмотря на прекращение ношения контактных линз (таблица 1). У всех была умеренная гиперемия конъюнктивы, небольшой хемоз, но не было переднего увеита. У 2 пациентов микрокисты простирались до лимба, но у 2, которые были замечены позже, было периферическое кольцо нормального эпителия диаметром примерно 2 мм (рис. 1). Наблюдалось только рассеянное точечное поглощение флуоресцеина эпителием.Толщина центральной роговицы была нормальной, стромальных полос не было, и после разрешения все пациенты имели нормальную структуру эндотелиальных клеток без признаков заболевания базальной мембраны эпителия. Неоваскуляризация периферической роговицы отсутствовала.
Рис. 1.
Слева, клиническая фотография случая 1, сделанная утром в день появления симптомов. Обратите внимание на большое количество кист, которые почти сливаются в эпителий. Справа: клиническая фотография случая 2, сделанная через 3 дня после появления симптомов.Периферическая роговица (нижняя часть фотографии) без кист.
Разрешение микроцист увеличивалось в центре, и все глаза были свободны от кист в течение 4 недель. У пациента 3 на одном глазу образовалась эпителиальная эрозия диаметром 2 мм, которая зажила без дальнейших симптомов. У пациента 1 развилось двустороннее слабое субэпителиальное помутнение, которое исчезло через 4 недели. У этой пациентки были показания кератометрии в 1988 г. (7,55 мм при 180 / 7,60 при 090 OD; 7,60 мм при 180 / 7,75 при 090 OS), когда ей впервые были установлены линзы Permaflex (Wesley Jesson, PBH Ltd, Саутгемптон, Соединенное Королевство) ( 8.70: 14.40: −9.50 OD, 8.70: 14.40: −8.50 OS), которые она носила без происшествий в течение 5 лет. Через четыре недели после того, как мы увидели ее, ее миопия уменьшилась с -9,50 / -0,75 на 015 OD; От -8,75 / -1,25 при 180 OS до -5,25 / -1,00 при 050 OD; −3,75 / −1,00 при 145 OS, и эта рефракция стабильна в течение 24 месяцев. Показания кератометрии не изменились, но видеокератоскопия показала апикальное уплощение роговицы примерно на 4 диоптрии.
Все пациенты впоследствии вернулись к ношению контактных линз.Пациент 1 перешел на ежедневное ношение жестких газопроницаемых контактных линз после 9 месяцев без линз, в то время как остальные вернулись к ежедневному ношению мягких контактных линз с рекомендацией, чтобы время ежедневного ношения не превышало 8 часов. После минимального периода наблюдения в течение 20 месяцев рецидива симптомов не наблюдалось.
Результаты исследования биоптата роговичного эпителия были отрицательными для Acanthamoeba . Гистологическое исследование показало поверхностные кисты, содержащие сморщенные эпителиальные клетки с небольшими конденсированными ядрами или фрагментами ядерного материала, часто с темной гомогенной эозинофильной цитоплазмой (рис. 2).Анализ TUNEL показал, что некоторые из этих клеток имели ядра с расщепленной ДНК (рис. 2, вставка).
Рис. 2.
Микрофотография биоптата, взятого из эпителия роговицы из пациента 1, который сложен таким образом, что его поверхностная поверхность вогнута. Обратите внимание на микроцисты, содержащие сморщенные эпителиальные клетки с конденсированным ядерным материалом (гематоксилин-эозин, исходное увеличение × 60). Вставка, одиночная TUNEL (TdT-опосредованная мечение ник-конца dUTP) положительная по анализу клетка (исходное увеличение × 75).
Считается, что образование микрокист роговичного эпителия после длительного ношения контактных линз является результатом хронической гипоксии, которая приводит к гибели клеток и накоплению мусора в межклеточных карманах. 1 Повышенная метаболическая активность после прекращения ношения линз может привести к увеличению количества микроцист, которые затем очищаются от эпителия кпереди. 1 Сопутствующие аномалии, такие как слабые осевые инфильтраты стромы, встречаются редко. 2
Мы предполагаем, что острая микрокистозная эпителиопатия роговицы также является ответом на гипоксию. Причина внезапного начала болезни после периода беспроблемного ношения линз неясна, а механизм уплощения апикальной части роговицы у одного пациента не выяснен. Недавнее исследование выделения эпителиальных клеток роговицы показало, что некоторые поверхностные клетки обычно имеют фрагментированную ДНК и что гибель клеток, как определено с помощью анализа жизнеспособности кальцеина-этидия, является нормальным признаком обновления эпителиальных клеток роговицы. 3 Гипоксия — признанная причина апоптоза, 4 , и вполне возможно, что преждевременная гибель клеток под эпителиальной поверхностью способствовала образованию микроцист у наших пациентов.
Рассмотрены другие причины эпителиальной микрокистозной кератопатии. 5 Однако ни у одного из наших пациентов не было признаков ассоциированной дистрофии роговицы или эндотелиальной недостаточности, инфекции, хирургического вмешательства или ссадины в анамнезе, а также ассоциированных внешних заболеваний глаз.Ни один химический компонент систем ухода за контактными линзами не был общим для всех случаев, хотя нельзя исключить неспецифический токсический побочный эффект как возможный механизм. Результаты культивирования и иммуногистохимии для Acanthamoeba , еще одной причины эпителиопатии у пользователей контактных линз, также были отрицательными. Поэтому мы считаем, что гипоксия является наиболее вероятной причиной и что это явление может быть шагом на пути к индуцированному контактными линзами эпителиальному некрозу.
Кроличье моноклональное антитело против Acanthamoeba было подарком Саймона Килвингтона, доктора философии, Лаборатория общественного здравоохранения, Бат, Англия.
Автор, ответственный за переписку: Стивен Дж. Тафт, доктор медицины, FRCOphth, глазная больница Мурфилдс, Лондон, EC1V 2PD, Англия (электронная почта: [email protected]).
1.Холден
BASweeney
Д.Ф. Значение микрокистозного ответа: обзор. Optom Vis Sci. 1991; 68703-707Google ScholarCrossref 2.Kenyon
EPolse
KASeger
РГ Влияние режима ношения на осложнения длительного ношения. Офтальмология. 1986; 93231-236Google ScholarCrossref 3.Ren
HWilson
G Апоптоз эпителия роговицы. Invest Ophthalmol Vis Sci. 1996; 371017-1025Google Scholar4.Shimizu
SEguchi
YKamiike
W
и другие. Индукция апоптоза, а также некроза посредством гипоксии и преимущественное предотвращение апоптоза с помощью Bcl-2 и Bcl-XL. Cancer Res. 1996; 562161-2166Google Scholar 5.Bron
AJTripathi
RC Кистозные поражения эпителия роговицы, I: клинические аспекты. Br J Ophthalmol. 1973; 57361-375 Google ScholarCrossref
Эпителиопатия роговицы сухого глаза вызывает гиперестезию при механической стимуляции воздушной струей
Резюме
Цель
Оценить чувствительность роговицы в различных группах: здоровые люди, пациенты с синдромом сухого глаза и пациенты с сухим глазом и без него после лазерного кератомилеза in situ (LASIK ) с использованием модифицированного газового эстезиометра Belmonte.
Дизайн
Ретроспективное клиническое исследование случай-контроль.
Методы
Мы обследовали 20 здоровых субъектов, 20 пациентов с синдромом сухого глаза, 20 пациентов с синдромом сухого глаза после LASIK и шесть пациентов с синдромом сухого глаза после LASIK. Ощущение роговицы измеряли с помощью модифицированного газового эстезиометра Belmonte, который использует два разных стимула для оценки механических и полимодальных рецепторов на поверхности роговицы. Механорецепторы оценивали по 2-секундным импульсным воздушным струям переменной интенсивности. Полимодальные рецепторы измеряли путем стимуляции роговицы 2-секундными импульсными воздушными струями с различной концентрацией CO 2 , газа, который превращается в угольную кислоту при контакте с поверхностью роговицы.Основным критерием результата было определение чувствительности роговицы.
Результаты
Среднее значение ± стандартное отклонение (± SD) возраста было одинаковым во всех группах. Средний механический порог составил 61,50 ± 20,07 мл / мин в нормальной группе (n = 20), 34,60 ± 21,09 мл / мин в сухой группе (n = 20, P <0,05 по сравнению с нормой), 99,50 ± 47,40 мл. / мин в группе пост-LASIK (n = 20, P <0,01 по сравнению с нормой) и 50,00 ± 15,49 мл / мин у пациентов с сухим кератитом после LASIK (n = 06, P <.05 по сравнению с пост-LASIK). Процент CO 2 , вызывающий дискомфорт, был одинаковым во всех группах ( P > 0,05). Никаких половых различий отмечено не было ( P, > 0,05). Обнаружена значимая обратная корреляция между порогом механической стимуляции и степенью окрашивания роговицы флуоресцеином.
Выводы
Модифицированный бесконтактный эстезиометр Belmonte представляет собой сложный прибор, который может оценивать различные типы сенсорных рецепторов роговицы.Пациенты с синдромом сухого глаза были сверхчувствительны к воздушной струе этого инструмента, и это, по-видимому, связано с изменением барьерной функции эпителия роговицы. Глубокая гипестезия наблюдалась после LASIK и, как и у пациентов с синдромом сухого глаза, после LASIK были сенсибилизированы. Эти результаты позволяют по-новому взглянуть на гиперчувствительность к стрессам окружающей среды, особенно к сквознякам, которые испытывают пациенты с синдромом сухого глаза.
Рекомендуемые статьиЦитирующие статьи (0)
Полный текст
Copyright © 2004 Elsevier Inc.Все права защищены.
Рекомендуемые статьи
Ссылки на статьи
АТИПИЧНАЯ ЭПИТЕЛИОПАТИЯ РОГОВИЦЫ, НАЛИЧИЕ НА HERPES ZOSTER OPHTHALMICUS
Абстрактные
Предпосылки: вирус опоясывающего герпеса может быть физически и визуально изнурительным заболеванием. Чем раньше вы обнаружите признаки и симптомы, тем раньше можно будет начать лечение.Снижение вероятности рубцевания роговицы и постгерпетической невралгии имеет первостепенное значение в лечении заболевания. Этот плакат иллюстрирует атипичную эпителиопатию роговицы и последующий стромальный кератит вместе с офтальмологическими признаками и симптомами и вариантами лечения с уникальной точки зрения пациента, который также является автором. ОКТ роговицы используется при лечении кератита.
ОПИСАНИЕ СЛУЧАЯ (И): Здоровый окулист мужского пола 45 лет обратился с ощущением инородного тела и перемежающейся острой колющей болью в глазу слева, сопровождающейся болью при боковом движении.BVA составляла 20/20 в каждом глазу. Конъюнктивальной или склеральной инъекции не было. Множественные крошечные беловатые эпителиальные бляшки, которые не были псевдодендритами, были отмечены на средне-периферической роговице, которая была минимально окрашена бенгальским розовым. Кондиционер был глубоким и тихим. На 2-й день появилась болезненность левой височной части головы. Был поставлен диагноз «опоясывающий лишай», и было начато лечение валацикловиром 1000 мг три раза в сутки и местным преднизолона ацетатом 1% четыре раза в сутки вместе с 5% гоматропином один раз в сутки. На 7-й день на левом лбу появились два небольших эритематозных пятна, но они так и не появились.От боли была назначена титрованная доза перорального габапентина 300 мг 3 раза в сутки и ибупрофена. Эпителиопатия разрешилась через 8 недель, стромальный кератит развился через 14 дней и продолжается через 18 месяцев. Невралгия разрешилась примерно через 12 недель.
ВЫВОДЫ: Офтальмологический герпес опоясывающий лишай может быть разрушительным заболеванием, и связанный с ним кератит значительно увеличивает вероятность рубцевания роговицы. Оптометристы должны знать о ранних, типичных и атипичных признаках и симптомах, чтобы можно было целесообразно начать надлежащее лечение, что снижает вероятность постгерпетической невралгии и заболеваний глаз.
Moran CORE | Развитие волнообразной эпителиопатии
Развитие волнообразной эпителиопатии
На главную / Наружные болезни и роговица / Клинический подход к заболеваниям глазной поверхности
Название : Развитие волнообразной эпителиопатии: подтип частичной недостаточности лимбальных стволовых клеток
Автор (и): Уильям Б. Вест младший
Фотограф : Фотографии любезно предоставлены Dr.Маджид Моширфар
Дата : 03.09.20
Изображения :
Ключевые слова / Основные темы: Развитие волнообразной эпителиопатии, частичный дефицит лимбальных стволовых клеток, дефицит лимбальных стволовых клеток, эпителиопатия
ОСНОВНАЯ категория:
Наружные болезни и роговица> Клинический подход к заболеваниям глазной поверхности> Дефицит лимбальных стволовых клеток> Развитие волнообразной эпителиопатии
Диагноз : Развитие волнообразной эпителиопатии
Описание изображения :
Прогрессирующая волнообразная эпителиопатия (AWE) — это форма нарушения глазной поверхности, которая была впервые описана D’Aversa et.al. в 1997 году. Он характеризуется четко выраженным эпителиальным бляшкой с шероховатой волнообразной формой и точечным рисунком при окрашивании флуоресцеином. Также может присутствовать субэпителиальная помутнение. Бляшка возникает от лимба роговицы, чаще всего вверху, и расширяется к зрительной оси. Пациенты поступают с историей прогрессирующей потери зрения в течение нескольких месяцев, а также с раздражением глаз и ощущением инородного тела.
Хотя точная патофизиология плохо изучена, предполагается, что AWE является подтипом частичной недостаточности лимбальных стволовых клеток (PLSCD).Лимбальные стволовые клетки являются предшественниками эпителия роговицы и находятся в лимбе. Эпителиальные клетки мигрируют от лимба к центру роговицы, образуя поверхность роговицы. При дефиците лимбальных стволовых клеток некоторые или все лимбальные стволовые клетки становятся дисфункциональными и не могут производить нормальный эпителий. Этот процесс чаще всего приводит к разрушению эпителиального слоя, вызывая поверхностное воспаление, которое, в свою очередь, вызывает неоваскуляризацию или конъюнктивальную инвазию роговицы.
Напротив, при AWE поверхность эпителия становится ненормальной, но не разрушается, и конъюнктивализация обычно не происходит. AWE был связан с историей глазных травм, хирургических вмешательств или химического или токсического воздействия на глазную поверхность.
Хотя потенциальный дифференциальный диагноз этого расстройства широк, вероятные соображения включают:
- Врастание эпителия
- Болезнь сухого глаза
- Диффузный пластинчатый кератит (DLK)
- Центральная токсическая кератопатия (CTK)
- Дефицит лимбальных стволовых клеток (LSCD)
- Плоская неоплазия поверхности глаза
- Интраэпителиальная неоплазия конъюнктивы
- Герпетический кератит
Первоначальное лечение этого заболевания включает консервативные меры для уменьшения воспаления и максимального заживления.Эти методы лечения включают искусственные слезы, пероральный доксициклин или местные кортикостероиды. Может использоваться поверхностная кератэктомия, которая обычно обеспечивает временное рассасывание бляшки; однако налет почти всегда рецидивирует. Добавление местного нитрата серебра, нанесенного с помощью ватного тампона на пораженный участок после санации роговицы, по-видимому, обеспечивает стабильное выздоровление. Простая трансплантация лимбальных стволовых клеток может быть выполнена для регенерации лимба роговицы, если нитрат серебра не дал результата. Обычно это выполняется путем сбора лимбальных стволовых клеток из здорового глаза (если болезнь не двусторонняя).Интерферон альфа-2b, местный или пероральный циклоспорин, пробки слезных точек, склеральные линзы, витамин А, аутологичная сыворотка крови, капли амниотической мембраны и фторметолон могут быть полезны при лечении AWE, поскольку они успешно использовались при лечении других разновидностей PLSCD. Эффективность местных кортикостероидов не доказана.
На этом видео показан левый глаз 36-летнего мужчины с шестимесячной историей потери зрения и ощущения инородного тела после LASIK.Перед операцией у него в анамнезе было хроническое покраснение и раздражение левого глаза перед операцией, а также возможное химическое повреждение этого глаза в детстве. Видно, что классическая волнообразная бляшка продвигается от лимба как снизу, так и вверх.
Заключение:
Прогрессирующая волнообразная эпителиопатия — это тип частичной недостаточности лимбальных стволовых клеток, образующий характерную волнистую эпителиальную бляшку, которая расширяется от лимба к зрительной оси. Это связано с повреждением лимбальных стволовых клеток и лечится поверхностной кератэктомией и трансплантацией нитрата серебра или лимбальных стволовых клеток.После лечения прогноз обычно отличный.
Ссылки :
- D’Aversa G, Luchs JL, Fox MJ, Rosenbaum PS, Udell IJ. Прогрессирующая волнообразная эпителиопатия: клинические особенности и лечение. Офтальмология [Интернет]. Американская академия офтальмологии, Inc; 1997. 104 (6): 962–969. Доступно по ссылке: http://dx.doi.org/10.1016/S0161-6420(97)30199-7 PMID: 9186437
- Россен Дж., Амрам А., Милани Б. и др. Дефицит лимбальных стволовых клеток, вызванный контактными линзами. Ocul Surf.2016; 14 (4): 419-434. DOI: 10.1016 / j.jtos.2016.06.003
- Ким Б.Ю., Риаз К.М., Бахтиари П. и др. Обратимое с медицинской точки зрения заболевание лимбальных стволовых клеток: клинические особенности и стратегии лечения. Офтальмология. 2014; 121 (10): 2053-2058. DOI: 10.1016 / j.ophtha.2014.04.025
- Moshirfar M, Hastings JP. Односторонняя прогрессирующая эпителиопатия после LASIK [Интернет]. Журнал катаракты и рефракционной хирургии. Липпинкотт Уильямс и Уилкинс; 2020 [цитируется 25 августа 2020 г.]. п. 646–651. Доступно по адресу: https: // pubmed.ncbi.nlm.nih.gov/32271301/ PMID: 32271301
- Tan JCK, Tat LT, Coroneo MT. Лечение частичной недостаточности лимбальных стволовых клеток местным интерфероном α-2b и ретиноевой кислотой. Br J Ophthalmol. 2016; 100 (7): 944-948. DOI: 10.1136 / bjophthalmol-2015-307411
- Маджид Моширфар, доктор медицины, Уильям Б. Уэст-младший, Ясмин К. Ронкильо. Развитие волнообразной эпителиопатии. Statpearls. 2020. https://pubmed.ncbi.nlm.nih.gov/32119296/
- Уильям Б. Уэст младший, Ясмин К. Ронкильо, Маджид Моширфар, доктор медицины.Развитие волнообразной эпителиопатии. Эйевики. 2020.
- https://eyewiki.aao.org/Advancing_Wavelike_Epitheliopathy#:~:text=Advancing%20Wavelike%20Epitheliopathy%20is%20an,the%20center%20of%20the%20cornea.
Допуск факультета: Griffin Jardine, MD
Нижний колонтитул :
- Заявление об авторских правах: Copyright William B. West Jr., © 2020. Для получения дополнительной информации о правах на эту коллекцию посетите: URL-адрес страницы с информацией об авторских правах на Moran CORE
- Идентификатор: Moran_CORE_29777
.
Раскрытие информации (финансовое или иное): Не подлежит раскрытию.
Whorl Whorl, Twists and Twirls
Эпителиопатии роговицы трудно поддаются лечению, поскольку они возникают в результате множества различных причин, которые часто трудно устранить. Часто картина пораженной роговицы может помочь в постановке диагноза, хотя некоторые нетипичные проявления могут сбивать с толку. Симптомы эпителиопатии роговицы могут включать песчанистость, жжение, сухость, слезотечение, светобоязнь и нечеткое зрение. Терапевтические варианты включают лубриканты, рестазис (циклоспорин, аллерган), местные стероиды, окклюзию слезных точек, контактные линзы, тарзоррафию и трансплантацию лимбальных стволовых клеток.
Склеральные линзы, все более популярный вариант лечения, могут принести пользу пациентам с хронической эпителиопатией роговицы и связанными с ней симптомами, поддерживая контакт резервуара с жидкостью с поверхностью роговицы и обеспечивая превосходную оптику газопроницаемых линз для коррекции зрения. В колонке этого месяца рассказывается о случае, когда необычный тип эпителиопатии роговицы не поддается лечению другими вариантами лечения, но значительно выигрывает от склеральных линз GP.
Пример использования
37-летний темнокожий мужчина был направлен специалистом по роговице для установки контактных линз.Ранее он обращался к нескольким офтальмологам по поводу симптомов светобоязни, нечеткости зрения и хронического раздражения. В ходе этих посещений у него был диагностирован синдром сухого глаза, и его лечили лубрикантами, рестазисом, окклюзией точечных каналов и местными стероидами. Все эти методы лечения принесли лишь минимальное улучшение; он все еще страдал и продолжал носить солнцезащитные очки в помещении и две пары солнцезащитных очков на улице. Его зрение ухудшилось до такой степени, что он чувствовал себя небезопасным за рулем.
| 1а.Склеральные линзы подходят к внешнему диаметру. |
Специалист по роговице диагностировал у него эпителиопатию роговицы; однако в настоящее время конкретная этиология не установлена. Перед любым хирургическим вмешательством ему было рекомендовано рассмотреть возможность использования склеральных линз.
При осмотре острота зрения без коррекции составляла 20/60 O.U. Рефракция не улучшила его зрение. Обследование с помощью щелевой лампы выявило 2+ бульбарных инъекций в конъюнктиву и лимб и от 2 до 3+ витков окрашивания роговицы.В наиболее плотных областях окрашивания наблюдались небольшие повышенные концентрации эпителия. В конъюнктиву век также вводили 2+ О.Е., но все остальные внутренние и внешние признаки были нормальными.
После обсуждения возможных вариантов пациент согласился на пробу склеральных линз. На каждый глаз поместили линзу, и он мог сообщить о некотором немедленном улучшении его зрительного комфорта. При чрезмерном преломлении он мог видеть почти 20/20 в каждом глазу. Ему подобрали и заказали следующие линзы Jupiter из материала Boston XO со стандартными периферийными кривыми: 46.Базовая кривая 00 мм, мощность -1,75D и внешний диаметр 15,6 мм; Базовая кривая 46,00 мм, мощность -2,00D и внешний диаметр 15,6 мм.
Анализ
Причина такого выбора линз была двоякой. Во-первых, из-за его хронической светобоязни и чувствительных глаз было бы трудно использовать линзы большего диаметра. Дизайн Юпитера по существу нормальной формы роговицы обеспечит хороший резервуар слезы в центре, где находится основная часть эпителиопатии.
| 1б. Склеральные линзы подходят O.S. |
Во-вторых, посадка линзы обеспечивала полный свод роговицы и хорошее центрирование (, рисунки 1a и 1b, ). Острота зрения через линзы составляла 20/20 на каждый глаз. Пациент по-прежнему сообщил о некоторой степени светочувствительности, но чувство раздражения уменьшилось, и он в целом был доволен комфортом и взволнован своим зрением.Он мог работать в помещении без солнцезащитных очков и на улице всего с одной парой. Он продолжает носить линзы постоянно.
Завитковидная эпителиопатия роговицы может наблюдаться у пациентов с некоторыми специфическими системными заболеваниями, такими как пигментное недержание мочи, кератоконус с ношением линз GP, дефицит лимбальных стволовых клеток или постпроникающая кератопластика. 1-3 В зависимости от тяжести эпителиального заболевания могут быть эффективны различные методы лечения. Однако во многих случаях зрение можно восстановить, улучшить здоровье эпителия и облегчить симптомы, просто используя склеральные линзы GP. 4
1. Selvadurai D, Salomão DR, Baratz KH. Аномалии роговицы у incontinentia pigmenti: гистопатологические и конфокальные корреляции. Роговица. 2008 августа; 27 (7): 833-6.
2. Somodi S, Hahnel C, Slowik C, et al. Конфокальная микроскопия in vivo и конфокальная лазерно-сканирующая флуоресцентная микроскопия при кератоконусе. Ger J Ophthalmol. 1996 ноя; 5 (6): 518-25.
3. Озбек З., Рабер ИМ. Успешное лечение аниридных заболеваний глазной поверхности при длительном ношении перевязочных контактных линз.Роговица. 2006 Февраль; 25 (2): 245-7.
4. Rosenthal P, Croteau A. Вентилируемые газом газопроницаемые склеральные контактные линзы — эффективный вариант для лечения тяжелых заболеваний глазной поверхности и многих заболеваний роговицы, которые в противном случае потребовали бы проникающей кератопластики. Линзы для контакта с глазами. 2005 Май; 31 (3): 130-4.
Конфокальная микроскопия in vivo и оптическая когерентная томография переднего сегмента, анализ микрокистозного кератита
Цель . Описать результаты конфокальной микроскопии in vivo (IVCM) и оптической когерентной томографии переднего сегмента (AS-OCT) в случае двусторонней острой микрокистозной эпителиопатии после ежедневного ношения мягких контактных линз. Методы . IVCM и AS-OCT использовались при лечении двусторонней эпителиопатии у пациента 23 лет в острой стадии заболевания и при выздоровлении через 4 дня лечения. Изображения были проанализированы и сопоставлены. Результатов . На AS-OCT правого глаза была выявлена общая гиперрефлективность и увеличение толщины центрального эпителия роговицы до 150 мкм мкм с многочисленными гипорефлективными маленькими овальными кистами, которые полностью разрешились на 4-й день после диагностики и лечения.Сканирование AS-OCT левого глаза выявило овальный гиперрефлективный материал в эпителии роговицы. ВЖК обоих глаз выявила многочисленные микроцисты разного размера, заполненные гиперрефлективным материалом, в основном в поверхностных эпителиальных слоях. Эпителиальные клетки показали полиморфизм с нарушением цитоархитектуры. В базальных эпителиальных клетках и передней строме наблюдались воспалительные изменения. Строма и эндотелий задней части роговицы имели нормальную морфологию. Выводы .Микрокистозный кератит проявился как локализованное микрокистозное воспаление эпителия на AS-OCT, что было подтверждено IVCM. И IVCM, и AS-OCT являются полезными диагностическими инструментами в случае кистозного воспаления эпителия роговицы.
1. Введение
Кератит — это заболевание, характеризующееся возникновением воспалительной инфильтрации в одном или нескольких слоях роговицы, таких как эпителий, слой Боумена, строма роговицы и эндотелий с десцеметовой мембраной. В большинстве случаев кератит считается острым офтальмологическим заболеванием и требует неотложного лечения [1].
Есть два основных типа кератита: инфекционный и неинфекционный. Инфекционный кератит включает бактериальные, вирусные, грибковые и протозойные воспаления. Неинфекционный кератит включает множество заболеваний, вызванных аномальной иммунологической реакцией или нарушением физиологических процессов на поверхности глаза [2].
Дифференциальная диагностика кератита представляет собой серьезную проблему из-за частого появления схожих клинических симптомов как при инфекционных, так и неинфекционных воспалениях.Неспецифическая умеренная или сильная боль, снижение остроты зрения, светобоязнь и раздражение поверхности глаз являются субъективными симптомами, о которых сообщают пациенты с кератитом. Диагноз в основном основывается на клиническом опыте врача, а также на результатах микробиологического анализа. Было показано, что положительная прогностическая ценность клинического опыта врача очень различается в зависимости от этиологии инфекции. Частота положительных посевов в случаях инфекционного кератита широко варьировала от 40 до 70% из-за множества ограничивающих факторов [3–5].По этим причинам задержки в диагностике и лечении являются обычным явлением, и существует острая необходимость в использовании новых надежных методов диагностики кератита. Как оптическая когерентная томография, так и конфокальная микроскопия являются неинвазивными методами визуализации, которые, как уже было доказано, помогают в дифференциальной диагностике, особенно в случаях атипичного или сложного инфекционного кератита [6–9].
Основные факторы риска, которые следует учитывать при диагностике воспаления роговицы, включают использование контактных линз, повреждение роговицы с разрывом эпителия, вирусные заболевания и некоторые системные заболевания, такие как аутоиммунные заболевания.
До 80% воспалений роговицы обнаруживаются у тех, кто носит контактные линзы [10]. Распространенность воспалений роговицы у людей, носящих контактные линзы, относительно постоянна в последние годы и начинается с 2–4 случаев на 10 000 пользователей в год у тех, кто носит мягкие контактные линзы, и достигает до 20 случаев на 10 000 пользователей в год у тех, кто носит контактные линзы в ночное время [11 ].
Микрокистозный кератит — один из подтипов кератита, характеризующийся появлением мелких (диаметром от 15 до 50 мкм), неправильных и полупрозрачных включений в эпителии роговицы.
Причины возникновения микрокист до конца не изучены. Возможными считаются хроническая гипоксия, воспалительные механизмы и механическое давление на поверхность роговицы.
Микрокистозный кератит относительно распространен среди людей, носящих контактные линзы. Требуется дифференциальная диагностика с другими инфекционными и асептическими воспалениями [12].
2. История болезни
Пациентка 28 лет была госпитализирована в глазное отделение в связи с внезапной значительной двусторонней потерей остроты зрения.Пациент не сообщал о боли или светобоязни. Затуманенное и нечеткое зрение пациентка обнаружила утром после пробуждения.
В анамнезе выявлен двусторонний конъюнктивит, возникший около месяца назад и полностью исчезнувший в течение недели после лечения тобрамицином местного действия. Кроме того, около пяти лет пациент носит корректирующие контактные линзы (–3,0 Dsph. На оба глаза). Пациент использовал мягкие контактные линзы для одноразового и ежедневного ношения, содержащие 31% нелфилкона А и 69% воды.При поступлении BCVA составляло RE 0, 6 и LE 0, 4. Внутриглазное давление было RE 14 мм рт. Ст. И LE 12 мм рт. Ст.
Обследование с помощью щелевой лампы показало многочисленные мелкие включения в поверхностной и центральной части роговицы без эрозии роговицы и без помутнения роговицы. Менее выраженные изменения были обнаружены в периферической части роговицы. Между глазами наблюдалась асимметрия аномалий роговицы, при этом правый глаз выявлял более серьезные и выраженные изменения роговицы. Окрашивание флуоресцеином было отрицательным в обоих глазах.При осмотре признаков острого воспаления не обнаружено. Остальные структуры глаза были нормальными (рисунки 1 (а) и 1 (б)).
Оптическая когерентная томография переднего сегмента глаза (DRI Triton, Topcon, Токио, Япония) выявила изменения разной степени выраженности между глазами. Обе роговицы были отечными с увеличением толщины центральной роговицы до 611 мкм мкм правого глаза и 538 мкм мкм левого глаза. Увеличение толщины роговицы было связано с отеком эпителия, главным образом в центральной части роговицы, что было продемонстрировано на карте роговицы.Толщина периферического эпителия обоих глаз составляла от 54 до 71 мкм мкм. На АС-ОКТ правого глаза выявлена общая гиперрефлективность и увеличение толщины центрального эпителия роговицы до 150 мкм мкм с многочисленными гипорефлективными мелкими овальными кистами. Гипорефлективные кисты располагались в пределах 2 мм от центральной части роговицы. Сканирование AS-OCT левого глаза выявило несколько овальных гиперрефлективных материалов в центральном эпителии роговицы. Отражательная способность эпителия роговицы была нормальной, а увеличение центральной толщины составило до 90 мкм мкм, что значительно менее серьезно по сравнению с правым глазом (рис. 2).
Конфокальная микроскопия in vivo (HRT 3, Heidelberg Engineering GmbH, Германия) обоих глаз показала аналогичные морфологические изменения, но интенсивность также была значительно выше в правом глазу. Были обнаружены многочисленные микроцисты размером от 8 мкм мкм до 38 мкм мкм. Большинство маленьких микроцист были заполнены гомогенным материалом с высокой отражающей способностью, но более крупные кисты были заполнены гетерогенным гипорефлексивным и гиперотражающим материалом. Эпителиальные клетки показали полиморфизм с нарушением цитоархитектуры и нарушением слоистой структуры эпителия.В базальных эпителиальных клетках и передней строме наблюдались воспалительные изменения. В центре базальных эпителиальных клеток наблюдались ярко отражающие и круглые структуры, повышенная плотность клеток Лангерганса и активированные кератоциты в передней строме. Роговичные нервы в слое Боумена присутствовали, но видимость слоя была нарушена оптическими тенями от кист, гиперрефлективными структурами в центре базальных клеток и повышенной плотностью клеток Лангерганса. Строма и эндотелий задней части роговицы имели нормальную морфологию (рис. 3).
Пациенту также был проведен базовый лабораторный анализ, включая морфологию с микроскопическим мазком, С-реактивный белок, белок Бенс-Джонса в моче и протеинограмму. Все результаты были нормальными.
Острый микрокистозный кератит диагностирован на основании исследования с помощью щелевой лампы и результатов AS-OCT и IVCM.
Пациенту вводили местно 0,1% дексаметазон в оба глаза 7 раз в день вместе с глазными каплями без консервантов.
После четырех дней лечения наблюдалась значительная ремиссия симптомов.При контрольном посещении на четвертый день лечения BCVA составлял RE 1,0 и LE 1,0. Были выполнены исследования с помощью щелевой лампы, а также ОКТ и IVCM.
ОКТ-исследование показало полную ремиссию симптомов, и толщина центральной роговицы и центрального эпителия вернулась к норме и составила RE 552 мкм м, 54 мкм мкм и 547 мкм мкм и 56 мкм мкм. , соответственно. Также не было нарушения отражательной способности эпителия. Исследование IVCM не показало кист в поверхностных слоях эпителия, но все еще были признаки активации воспаления базальных эпителиальных клеток и передней стромы роговицы, но их интенсивность была минимальной по сравнению с анализом, выполненным при постановке диагноза.
Пациенту было рекомендовано использовать дексаметазон для местного применения один раз в день для обоих глаз в сопровождении искусственной слезы. При следующих визитах рецидивов не было.
3. Обсуждение
Насколько нам известно, это первый отчет в литературе, описывающий использование оптической когерентной томографии переднего сегмента глаза и конфокальной микроскопии при остром микрокистозном кератите.
Микроцисты эпителия роговицы были впервые описаны в 1970-х годах у пациентов, носивших гидрогелевые контактные линзы.В зависимости от исследования, частота микрокист в эпителии роговицы составляла 4 процента в первые дни ношения линз и увеличивалась до 30% после 3 месяцев ношения линз. В некоторых публикациях сообщается о 100-процентной частоте кист у пациентов, которые носили контактные линзы в течение шести месяцев и превышали утвержденный период ежедневного использования. Их появление коррелировало со временем ношения контактных линз и их проницаемостью для кислорода (Dk / L). Возможные причины включали замедленную реакцию эпителия на хроническую гипоксию роговицы и хроническое механическое сжатие эпителия.Острота зрения не ухудшалась из-за появления микрокист. Время, необходимое для исчезновения кист с момента прекращения ношения линз, составило около 3 месяцев [12].
Микрокистозный кератит — неспецифическое воспаление. Возможными причинами могут быть гипоксия роговицы из-за использования контактных линз, воспаление протозойной этиологии и дистрофия роговицы, такая как дистрофия Мессмана, дистрофия Когана, буллезная кератопатия и синдром рецидивирующей эрозии роговицы [13].
Для исключения протозойного кератита была проведена конфокальная микроскопия — чувствительный тест, исключающий ранние стадии этого воспаления [14].Его специфичность зависит от типа конфокальной структуры, видимой при исследовании, и достигает 94% в случае кист и трофозоитов, в то время как гораздо более низкая специфичность 50% достигается, когда видны структуры с морфологией «светлого пятна» [15]. В нашем случае ни одной из структур, характерных для простейшего воспалительного процесса, в ИВКМ не обнаружено. Признаков дистрофии или повреждения эндотелия роговицы также не обнаружено. Мы также исключили инфекционный анамнез или воздействие химических веществ, а также рецидивирующие эрозии роговицы.
Неравномерное увеличение толщины центрального эпителия роговицы было характерной чертой, наблюдаемой при ОКТ. В норме средняя толщина эпителия роговицы в популяции составляет 53,4 ± 4,6 мкм м [16]. Нишино и др. выполнили оптическую когерентную томографию и конфокальную микроскопию in vivo у пациентов с генетически подтвержденной дистрофией Мессмана (MECD: мутация в гене KRT12), что также должно быть принято во внимание при дифференциальной диагностике нашего пациента. В случае MECD увеличение толщины эпителия роговицы до 64.8 мкм м. Толщина эпителия роговицы оставалась постоянной. Однако в нашем случае толщина эпителия роговицы была больше и достигала 100 мкм. Кроме того, наибольшая толщина эпителия имела место в центральной части роговицы, в то время как периферический эпителий оставался нормальным. Эпителиальный отек способствовал увеличению CCT примерно до 611 микрон, в то время как Nishino et al. отметили снижение CCT примерно до 499 микрон, несмотря на отек эпителия. В случае дистрофии Мессмана исследование IVCM подчеркивает меньшее накопление гиперотражающего материала в слое эпителиальных клеток, изменения морфологии субэпителиальных нервов, атрофию мембраны Боумена и наблюдаемые изменения в строме роговицы (точечные и игольчатые гиперрефлективные отложения).Изменения IVCM при кистозной кератопатии влияют только на эпителиальный слой. Многочисленные тонкие эндотелиальные кисты, аккуратно окрашенные флуоресцеином, демонстрируют сходные признаки дистрофии Мессмана и микрокистозного кератита. [17].
Гиперотражающие точки, ограниченные эпителиальными слоями роговицы, также были обнаружены в AS-OCT Thanathanee et al. у всех пациентов с микроспоридиальным кератоконъюнктивитом. Во всех случаях не было расширения в стромальный слой. Более того, почти во всех случаях поражения были немного приподняты над эпителиальной поверхностью (12/13).Первые два результата аналогичны наблюдениям, видимым в ОКТ у нашего пациента. Однако в нашем случае гиперрефлективные эпителиальные поражения не возвышались над поверхностью роговицы. Еще одно различие между нашим случаем и микроспоридной инфекцией — это красный глаз, обнаруженный при исследовании с помощью щелевой лампы, который был представлен в цитируемой статье [18].
При микрокистозном кератите снижается острота зрения. В литературе описаны случаи большого ухудшения ОА (1/60) до незначительного снижения (6/12).Обращает на себя внимание симметрия изменений [19]. Однако у нашего пациента острота зрения при поступлении на правый и левый глаз значительно различалась. Механизм этого явления остается невыясненным. Время износа линз, тип, производитель и тип жидкости для хранения были одинаковыми.
Истончение центральной роговицы — возможный исход микрокистозного кератита [19]. В нашем случае осложнения не возникло, и ЧМТ после выздоровления составила 552 и 547 мкм соответственно для правого и левого глаза.
После исключения других причин воспаления мы полагаем, что основной причиной острого кистозного ответа у нашего пациента была гипоксия эпителиальных клеток роговицы. Эта потенциальная причина была также упомянута Tuft et al. в статье, описывающей подобные случаи [19].
Также неизвестны причины, по которым, несмотря на многолетний бессимптомный анамнез ношения контактных линз, у нашего пациента наступила острая фаза заболевания. Возможно, что воспалительные механизмы участвуют в высвобождении механизмов острой гипоксии.Эпителий роговицы постоянно обновляется новыми клетками, продуцируемыми митозом в базальной мембране эпителия и смыванием мертвых клеток с поверхности роговицы слезной пленкой. Нормальный эпителий состоит в основном из живых клеток, а небольшая часть из них — мертвые клетки. Морфологически они не отличаются от живых клеток, но их можно очень просто удалить, поскольку они не образуют постоянных связей с соседними клетками [20]. Гипоксия — хорошо изученный фактор, вызывающий преждевременный апоптоз и некроз клеток [21].Следовательно, возможно, что образование микроцист вызвано преждевременным индуцированным апоптозом эпителиальных клеток роговицы, которым не удалось мигрировать на ее поверхность. Накопление продуктов апоптоза в межклеточных пространствах эпителия, по-видимому, подтверждается исследованием IVCM, показывающим гиперотражающий материал в эпителиальных пространствах, а также отек некоторых клеток.
В заключение, как оптическая когерентная томография переднего сегмента глаза, так и конфокальная микроскопия in vivo являются широко используемыми инструментами в дифференциальной диагностике микрокистозного кератита.ОКТ позволила оценить динамику изменения толщины роговицы, а также оценить морфологию эпителия и стромы роговицы. Обследование определило разницу между центральным и периферическим эпителием. Анализ с помощью конфокальной микроскопии выявил изменения клеточной структуры, в основном эпителий, демонстрирующий полиморфизм наряду с нарушением цитоархитектуры и большую кисту, заполненную гетерогенным гипорефлексивным и гиперрефлективным материалом.

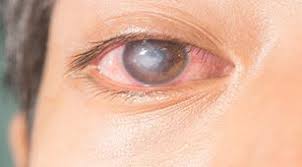 В данном случае никаких ограничений по возрасту пациента нет.
В данном случае никаких ограничений по возрасту пациента нет.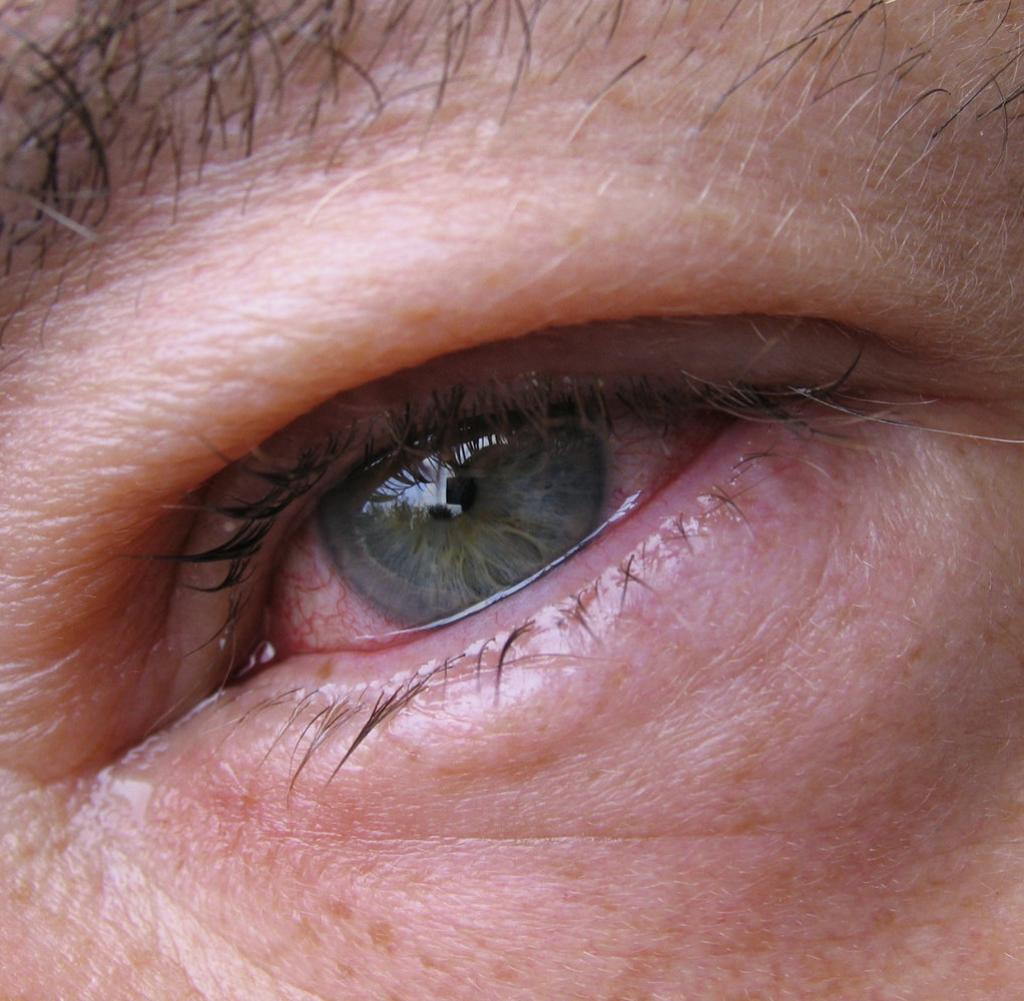
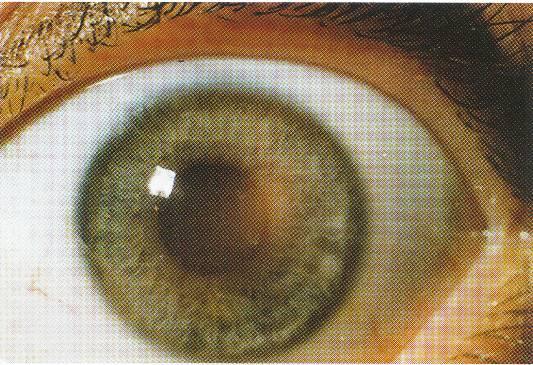
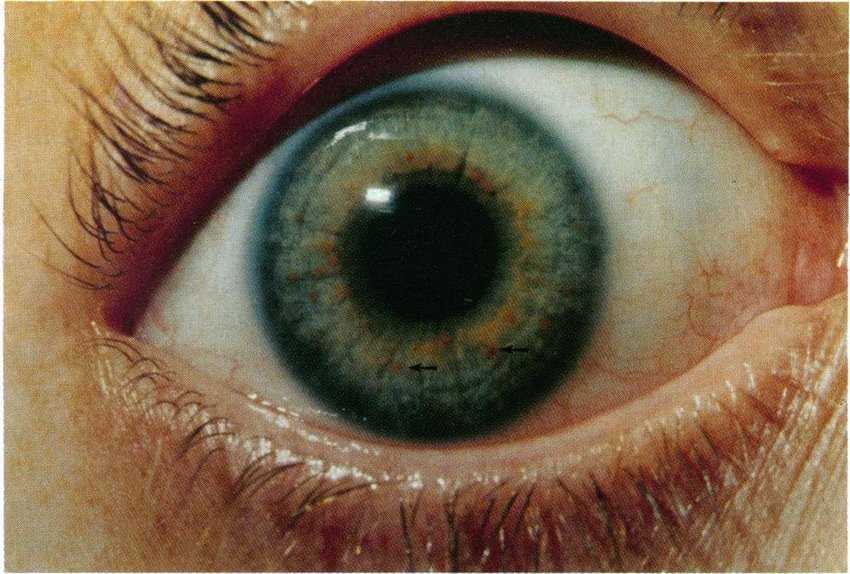 Он может развиться в тесной связи с глубоким склеритом. Очаги из склеры распространяются в глубокие слои роговицы, иногда наоборот, инфильтраты имеют форму треугольника с вершиной, направленных к центру зрачка. Иногда они появляются в нескольких местах роговой оболочки. Сосуды прорастают через 6-7 недель как глубокие, так и поверхностные, но их бывает очень мало. Часто присоединяется иридоциклит. Явления раздражения могут быть очень сильными и умеренными. Постепенно явления раздражения стихают, помутнения у вершины и по краю постепенно несколько рассасываются, но основания помутнения организуются в соединительную ткань, имеющую интенсивное синевато-белое помутнение, по цвету напоминающее склеру. Получается впечатление, что ткань склеры в этом участке заменила собой ткань роговицы. В тяжелых случаях большая часть роговицы может стать непрозрачной. Процесс тянется месяцами и годами, часто рецидивирует. Этиологический диагноз кератитов устанавливается по клинической картине, изменениях в легких или бронхопульмональных лимфатических узлах, температурной кривой, по положительным туберкулиновым реакциям и т.
Он может развиться в тесной связи с глубоким склеритом. Очаги из склеры распространяются в глубокие слои роговицы, иногда наоборот, инфильтраты имеют форму треугольника с вершиной, направленных к центру зрачка. Иногда они появляются в нескольких местах роговой оболочки. Сосуды прорастают через 6-7 недель как глубокие, так и поверхностные, но их бывает очень мало. Часто присоединяется иридоциклит. Явления раздражения могут быть очень сильными и умеренными. Постепенно явления раздражения стихают, помутнения у вершины и по краю постепенно несколько рассасываются, но основания помутнения организуются в соединительную ткань, имеющую интенсивное синевато-белое помутнение, по цвету напоминающее склеру. Получается впечатление, что ткань склеры в этом участке заменила собой ткань роговицы. В тяжелых случаях большая часть роговицы может стать непрозрачной. Процесс тянется месяцами и годами, часто рецидивирует. Этиологический диагноз кератитов устанавливается по клинической картине, изменениях в легких или бронхопульмональных лимфатических узлах, температурной кривой, по положительным туберкулиновым реакциям и т. д. Дифференцируют с люэтическим паренхиматозным кератитом, при котором сосуды только глубокие, обычно поражается оба глаза, всегда положительная реакция Вассермана. При нейрогенных кератитах понижена чувствительность роговицы, не развиваются кровеносные сосуды.
д. Дифференцируют с люэтическим паренхиматозным кератитом, при котором сосуды только глубокие, обычно поражается оба глаза, всегда положительная реакция Вассермана. При нейрогенных кератитах понижена чувствительность роговицы, не развиваются кровеносные сосуды.