Локальные постинъекционные осложнения или медикаментозноеятрогенное заболевание
31
27. Urakov A., Urakova N., Kasatkin A. Safe injections of antimicrobial drugs // Journal of Infection Prevention. —2013. V 14. — Р. 1—9.
28. Urakova N. A. Decrease of the temperature of the head of the fetus during birth as a symptom of Hypoxia // Thermolgy International. — 2013. 23 (2). — P 74-75.
29. Urakov A.L., Kasatkin A.A., Urakova N.A., Ammer K. Infrared Thermographic Investigation of Fingers and Palms During and After Application of Cuff Occlusion Test In Patients With Hemorrhagic Shock // Thermology International. — 2014. 24 (1). — P. 5-10.
© Н.А. Уракова, А.Л. Ураков, 2014
УДК 615.011:616-003.214-003.2-002. 4:615.256.55
4:615.256.55
Н.А. Уракова, А.Л. Ураков
ЛОКАЛЬНЫЕ ПОСТИНЪЕКЦИОННЫЕ ОСЛОЖНЕНИЯ ИЛИ МЕДИКАМЕНТОЗНОЕ ЯТРОГЕННОЕ ЗАБОЛЕВАНИЕ — ИНЪЕКЦИОННАЯ БОЛЕЗНЬ
Кафедра общей и клинической фармакологии (зав. кафедрой — проф. А.Л. Ураков)
ГБОУ ВПО «Ижевская государственная медицинская академия» МЗ РФ
Показано, что растворы для инъекции, в состав которых входят спирты, кетоны, альдегиды, кислоты и/или соли щелочных и тяжелых металлов в концентрациях, обеспечивающих местное денатурирующее действие, вызывают ожог тканей в месте инъекции. При этом лекарственные средства, содержащие спирты, кетоны, альдегиды и кислоты вызывают химическую денатурацию белков, а соли щелочных металлов обезвоживают клетки вплоть до их гибели. Причем, первая группа средств вызывает некротическое действие практически немедленно, а вторая — только через несколько минут локального взаимодействия. Описываются этиология, патогенез, варианты течения этих постинъекционных осложнений, которые предлагается объединить в новое заболевание — «инъекционная болезнь».
Описываются этиология, патогенез, варианты течения этих постинъекционных осложнений, которые предлагается объединить в новое заболевание — «инъекционная болезнь».
Ключевые слова: инъекции, инъекционная болезнь, постинъекционные осложнения, кровоподтеки, гематомы, инфильтраты, некрозы, абсцессы, флегмоны.
LOCAL AFTER INJECTION COMPLICATIONS OR INJECTION DISEASE N.A. Urakova, A.L. Urakov
It is shown that the solutions for injections, which include alcohols, ketones, aldehydes, acid and/or salts of alkali and heavy metals concentrations in providing local anti-natural action, cause burn tissues in the place of injection. The medicines containing alcohols, ketones, aldehydes and acids cause chemical denaturation of proteins, salts of alkaline metals dehydrated cells until their death. Moreover, the first group of causes necrotic action almost immediately, and the second — only after a few minutes of local interaction.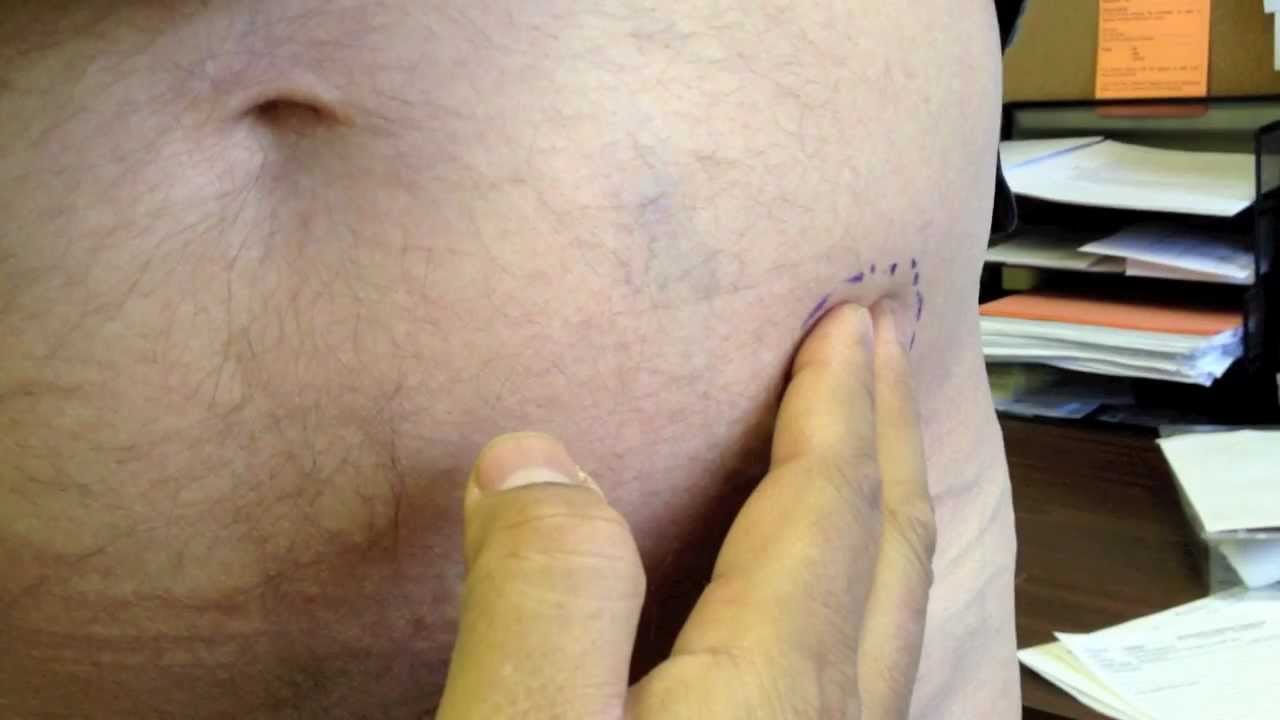 It is established local after injection tissue irritation can cause the blood that’s shed abroad inside the tissue bleeding. Describes the etiology, pathogenesis, and variants of these possible complications, which proposed to merge into a new disease — «injection disease».
It is established local after injection tissue irritation can cause the blood that’s shed abroad inside the tissue bleeding. Describes the etiology, pathogenesis, and variants of these possible complications, which proposed to merge into a new disease — «injection disease».
Key words: injection, injection disease, post-injection complications, bruising, hematoma, infiltration, necrosis, abscesses, cellulitis.
В каждой клинике мира сегодня практически каждый пациент ежедневно получает инъекции различных лекарственных средств [8, 9]. При этом в местах инъекций всегда появляются кровоизлияния, гематомы, кровоподтеки и воспалительные инфильтраты [7, 10]. Реже в этих местах появляются гнойные абсцессы, флегмоны и открытые гнойные раны [9], которые традиционно относят к осложнениям инъекций, возникающим из-за нарушений правил асептики и техники инъекций [1, 2]. Однако в последние годы было установлено, что некрозы и абсцессы при инъекциях возникают не из-за нарушений правил асептики и технологий прокалывания, а из-за физико-химической агрессивности лекарств, которые при инъекциях в кожу и в клетчаточные ткани могут оказывать прижигающее действие [3, 4, 5, 6, 8, 9, 11].
В связи с тем, что локальные постинъекционные повреждения мягких тканей все чаще требуют судебной фармакологической экспертизы, нами предложено относить их к медикаментозной ятрогенной болезни в виде нового самостоятельного заболевания — инъекционная болезнь [7, 9].
При исследовании пациентов нескольких клиник показано, что у них до госпитализации места предполагаемых инъекций в области ягодиц, бедер и рук здоровы практически в 99% случаев, а к концу госпитального лечения — выглядят больными у 100% пациентов. Причем, в последний день госпитального лечения кожа в области ягодиц и бедер у каждого из них имеет множественные локальные воспаления округлой формы, локализованные
вокруг мест проколов. Указанные воспаления имеют характер колото-инфильтративных повреждений различных степеней тяжести и сроков давности. Помимо этого, у каждого третьего пациента дополнительно к указанным повреждениям в местах инъекций имеются кровоподтеки.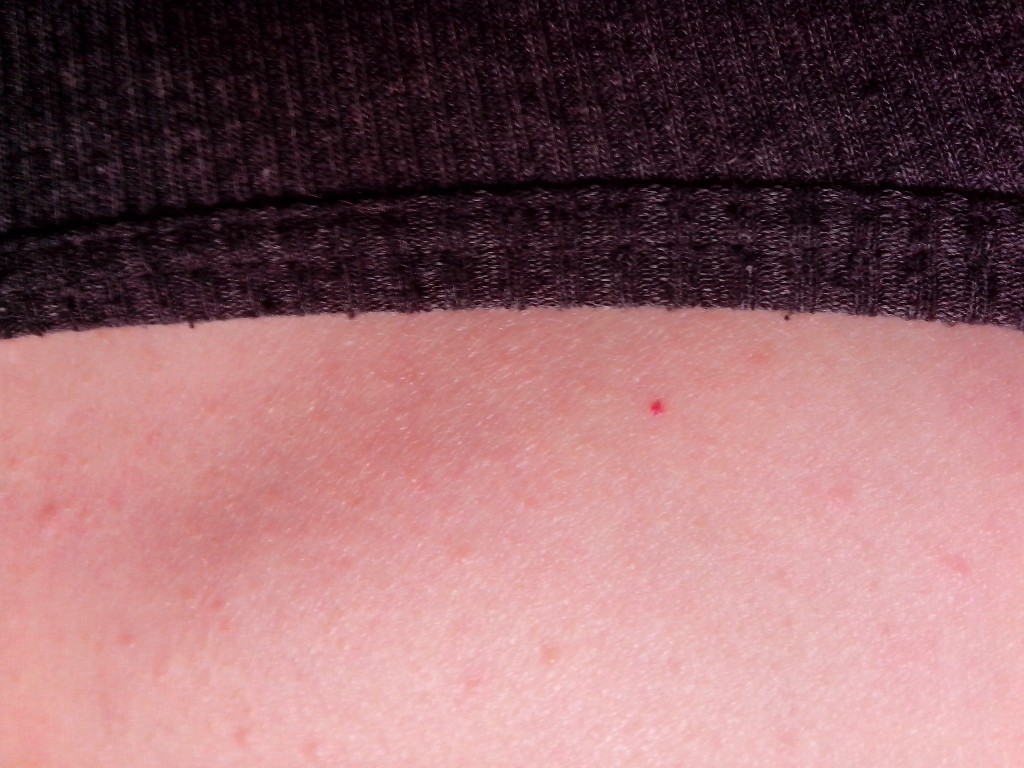
Исследования на поросятах показали, что локальные повреждения мягких тканей в местах инъекций возникают как от их прокалываний инъекционными иглами, так и от медикаментозных инфильтраций. При этом самой уязвимой к инъекционной болезни является клетчаточная ткань.
Выяснено, что характер инъекционной болезни зависит от лекарственных средств. По локальной агрессивности все препараты можно разделить на 3 группы: сильные, умеренные и слабые.
В группу сильных агрессоров, способных вызвать не только выраженное воспаление, но и некроз, а также абсцесс, входят спирты, кетоны, альдегиды, кислоты, щелочи, кальция хлорид и натрия хлорид. Установлено, что инъекции в кожу или под кожу этилового спирта, ацетона, уксусной кислоты, нашатырного спирта, скипидара или керосина, либо насыщенных растворов кальция хлорида или натрия хлорида тут же вызывают физико-химический ожог кожи и подкожно-жировой клетчатки. Данное локальное повреждение сопровождается формированием очага выраженной гиперемии, гипертермии, болезненности и отечности, а кожа в нем через несколько минут приобретает темно-вишневую окраску. Через сутки в этом очаге возникает некроз тканей, а затем — абсцесс и/или открытая гнойная рана. Важно подчеркнуть, что эти некрозы
Данное локальное повреждение сопровождается формированием очага выраженной гиперемии, гипертермии, болезненности и отечности, а кожа в нем через несколько минут приобретает темно-вишневую окраску. Через сутки в этом очаге возникает некроз тканей, а затем — абсцесс и/или открытая гнойная рана. Важно подчеркнуть, что эти некрозы
32
и гнойные абсцессы вызывают, прежде всего, именно антисептики, дезинфицирующие и прижигающие средства.
В группу умеренных агрессоров, вызывающих умеренное местное раздражение тканей и локальное воспаленных инфильтратов, входят ненасыщенные водные растворы солей щелочных и тяжелых металлов. Эту группу представляют гипертонические растворы солей натрия, калия, кальция, магния, железа и других металлов. Растворы этих веществ в концентрации более 10% оказывают раздражающее и денатурирующее действие. Но оно возникает не вмиг, а только через несколько минут после непрерывного взаимодействия с тканями. Причем, повышение их концентрации в растворах выше указанного уровня повышает их местное раздражающее действие, которое при определенных условиях взаимодействия может трансформироваться в прижигающее действие, напоминающее собой некротическое действие препаратов первой группы.
Причем, повышение их концентрации в растворах выше указанного уровня повышает их местное раздражающее действие, которое при определенных условиях взаимодействия может трансформироваться в прижигающее действие, напоминающее собой некротическое действие препаратов первой группы.
Дело в том, что повышение концентрации солей в растворах повышает их гиперосмотическую активность, которая у большинства веществ при достижении ими концентрации более 10% способна стать причиной денатурирующего действия и физико-химического ожога. В связи с этим гиперосмотические (гипертонические) растворы 20% пирацетама, 20% натрия оксибутирата, 24% кордиамина, 25% сернокислой магнезии, 50% метамизола натрия (анальгина), 60 и 76% урографина и других растворов лекарственных средств с аналогичной концентрацией вызывают обезвоживание клеток, поэтому через несколько минут взаимодействия с ними могут погубить их.
Установлено, что из всех растворов для инъекций, имеющих показатель концентрации 10%, самыми гиперосмотическими являются растворы солей натрия и кальция. Так, растворы натрия оксибутирата, натрия тиопентала, натрия гексобарбитала, натрия метамизола, натрия тиосульфата, натрия кофеина-бензоата, натрия сульфацила, натрия гидрокарбоната, натрия цитрата, натрия бензилпенициллина и натрия цефазолина в концентрации 10% имеют осмотическую активность соответственно 1650±10, 1700±11, 1300±9, 800±5, 930±5,840±5, 810±5, 1900±10, 900±5, 570±5, 540±5 (Р>95, n=5) мОсмоль/л воды, а растворы кальция хлорида, кальция глюконата, магния сульфата, глюкозы, маннита, эуфиллина, урографина, пирацетама и лидокаина гидрохлорида в концентрации 10% имеют осмотическую активность соответственно 1300±7, 1200±8 580±5, 600±3, 720±5, 620±5, 540±5, 670±6 (Р>95, n=5) мОсмоль/л воды.
Так, растворы натрия оксибутирата, натрия тиопентала, натрия гексобарбитала, натрия метамизола, натрия тиосульфата, натрия кофеина-бензоата, натрия сульфацила, натрия гидрокарбоната, натрия цитрата, натрия бензилпенициллина и натрия цефазолина в концентрации 10% имеют осмотическую активность соответственно 1650±10, 1700±11, 1300±9, 800±5, 930±5,840±5, 810±5, 1900±10, 900±5, 570±5, 540±5 (Р>95, n=5) мОсмоль/л воды, а растворы кальция хлорида, кальция глюконата, магния сульфата, глюкозы, маннита, эуфиллина, урографина, пирацетама и лидокаина гидрохлорида в концентрации 10% имеют осмотическую активность соответственно 1300±7, 1200±8 580±5, 600±3, 720±5, 620±5, 540±5, 670±6 (Р>95, n=5) мОсмоль/л воды.
Показано, что подкожные инъекции водных растворов 10% кальция хлорид, 10% кальция глюконата, 10% натрия хлорида или 10% натрия оксибутирата, либо растворов 20% натрия сульфацила, 20% натрия оксибутирата, 20% глюкозы, 20% пирацетама, либо растворов 25% магния сернокислого, 50% натрия метамизола, 60 или 76% урографина приводят к образованию медикаментозных инфильтратов, которые не рассасываются и не уменьшаются в первые минуты после инъекции, а увеличиваются в размерах. При этом в коже на месте инъекции уже через несколько секунд развивается очаг гиперемии, гипертермии, болезненности и отечности. Через 5-10 минут кожа над ним становится ярко-красной, после этого еще через 2,5±0,5 минуты кожа в этом участке становится темно-синюшно-багровой, а сам участок кожи приобретает форму круга с четкими границами и узкой ярко красной каемкой по наружной окружности. На следующие сутки в рамках этого синюшно-багрового участка кожи развивается некроз.
При этом в коже на месте инъекции уже через несколько секунд развивается очаг гиперемии, гипертермии, болезненности и отечности. Через 5-10 минут кожа над ним становится ярко-красной, после этого еще через 2,5±0,5 минуты кожа в этом участке становится темно-синюшно-багровой, а сам участок кожи приобретает форму круга с четкими границами и узкой ярко красной каемкой по наружной окружности. На следующие сутки в рамках этого синюшно-багрового участка кожи развивается некроз.
Кроме этого выяснено, что растворы 10% кальция хлорида и 10% кальция глюконата оказывают в местах
инъекций денатурирующее действие на кожу и клетчатку не только за счет гиперосмотической активности и дегидратирующего действия, но и за счет специфического необратимого повреждения митохондрий и разобщения в них дыхания и окислительного фосфорилирования, при котором энергия окисления субстратов цикла Кребса выделяется в виде тепла.
Установлено, что чрезмерно выраженная местная физиологическая активность катионов калия также способна вызывать некроз кожи и клетчатки в местах инъекций. В частности, раствор 4% калия хлорида и растворы иных солей калия аналогичной концентрации модулирует потенциал действия для клеток гладкомышечных образования сосудистых стенок и вызывает спазм кровеносных сосудов. Более того, в гладких мышцах стенок кровеносных сосудов развивается гиперкалиевая контрактура, которая полностью перекрывает их внутренний просвет и прекращает движение крови в них. Это вызывает ишемию, а затем некроз подкожно-жировой клетчатки в местах инъекций раствора 4% калия хлорида, а также иных солей калия (в частности, калия бензилпенициллина).
В группу слабых местно раздражающих средств, подкожные инъекции которых вызывают формирование обратимых локальных воспалений мягких тканей в местах инъекций, входят водные растворы всех остальных лекарственных средств. Дело в том, что даже вода для инъекции и изотонические растворы 0,9% натрия хлорида вызывают при инъекциях локальное постинъекционное воспаление, которое чаще всего носит кратковременный и обратимый характер. Кроме этого, болезнь кожи, подкожно-жировой клетчатки и других проколотых тканей в месте инъекции любого лекарства вызывает их прокалывание инъекционными иглами, кровоизлияние и кровавое имбибирование.
Дело в том, что даже вода для инъекции и изотонические растворы 0,9% натрия хлорида вызывают при инъекциях локальное постинъекционное воспаление, которое чаще всего носит кратковременный и обратимый характер. Кроме этого, болезнь кожи, подкожно-жировой клетчатки и других проколотых тканей в месте инъекции любого лекарства вызывает их прокалывание инъекционными иглами, кровоизлияние и кровавое имбибирование.
Установлено, что независимо от денатурирующего действия лекарств многократные проколы кожи, подкожно-жировой клетчатки, скелетной мышцы и/или вены ведут к появлению множества изолированных локальных воспалений кожи, каждое из которых на протяжении 3-4х дней после инъекции имеет розовато-красный цвет, а в последующие дни последовательно меняет свою окраску подобно изменению цвета кровоподтеку кожи, который при аналогичной давности превращается в синяк, и начинает «цвести». Поэтому в первые 4-5 дней ежедневных многократных инъекций кожа в выбранном месте инъекций имеет пятна одной окраски (розово-красного цвета), а в последующие дни — разной окраски (помимо пятен розовато-красного цвета, появляются пятна синего и желто-зеленого цветов). Иными словами, через несколько дней ежедневных инъекций кожа в местах инъекций приобретает разноцветную пятнистость. Указанная разноцветная пятнистость кожи сохраняется в последующем не менее недели.
Иными словами, через несколько дней ежедневных инъекций кожа в местах инъекций приобретает разноцветную пятнистость. Указанная разноцветная пятнистость кожи сохраняется в последующем не менее недели.
Показано, что при высокой безопасности введенных лекарств и при соблюдении техники инъекций инъекционная болезнь проявляется локальным асептическим мини-воспалением кожи и подкожно-жировой клетчатки, развивающимся вокруг мест их проколов. При этой легкой форме течения болезни воспаление имеет легкое течение и обратимый характер, поэтому проходит самостоятельно в среднем за неделю и параллельно с этим завершается рубцеванием ранок.
Следовательно, любая инъекция любого лекарственного средства вызывает характерное колото-инфильтративное повреждение кожи и подкожно-жировой клетчатки в месте прокола и медикаментозной инфильтрации тканей, которые «заболевают» как от проколов их инъек-
33
торами, так и от инфильтраций растворами лекарственных средств. Поскольку заболевание вызывают инъекции, оно было названо «Инъекционной болезнью».
Поскольку заболевание вызывают инъекции, оно было названо «Инъекционной болезнью».
Результаты наших клинических исследований показывают, что при низкой безопасности введенных лекарств и выполненных инъекций инъекционная болезнь развивается бурно, сохраняет локальный характер и протекает в двух вариантах: в виде кровавого либо в виде медикаментозного повреждения тканей.
При кровавом варианте болезнь проявляется массивным и ярким окрашиванием кожи вследствие ее кровавого имбибирования, а при медикаментозном варианте болезнь проявляется локальным воспалением клетчаточных и/или мышечных тканей вследствие их внутритканевого химического ожога. Причем, кровавый вариант болезни протекает без некроза и абсцессов, а медикаментозный вариант течет с некрозом тканей, нередко осложняется их инфицированием, нагноением и формированием гнойного абсцесса, появление которого требует госпитализации пациентки в гнойное отделение для хирургического лечения. Профилактика кровавой формы инъекционной болезни сводится к предотвращению внутритканевого кровотечения в раневом канале. Остановить кровотечение позволяет, например, гипертермическая «сварка» крови.
Профилактика кровавой формы инъекционной болезни сводится к предотвращению внутритканевого кровотечения в раневом канале. Остановить кровотечение позволяет, например, гипертермическая «сварка» крови.
При медикаментозном варианте течения инъекционной болезни кожа на месте «плохой» внутривенной инъекции, выполненной в области локтевой ямки, «плохой» внутримышечной инъекции, выполненной в области верхнего наружного квадранта ягодичной мышцы при введении растворов анальгетических, спазмолитических, анестезирующих, антигистаминных и химиотерапевтических средств, а также на месте «плохой» подкожной инъекции, выполненной в области верхней наружной поверхности плеча при введении витаминных и противовирусных препаратов, имеет следы выраженного воспаления. Воспаленный участок кожи имеет существенные размеры: как правило от 3 до 7 см в диаметре.
При этом само медикаментозное воспаление инфильтрированных тканей находится под кожей, носит необратимый и деструктивный характер, развивается очень интенсивно и бурно, как нарыв, поэтому проявляется отечностью, локальной гиперемией, гипертермией и
болезненностью. Деструктивное медикаментозно-воспалительное повреждение тканей чаще всего вызывает их некроз, который нередко инфицируется и трансформируется в абсцесс. Указанный вариант течения инъекционной болезни требует локального лечения аналогично лечению банального карбункула или травматического абсцесса. Как правило, необходимо хирургическое лечение. Завершается процесс воспаления рубцеванием.
Деструктивное медикаментозно-воспалительное повреждение тканей чаще всего вызывает их некроз, который нередко инфицируется и трансформируется в абсцесс. Указанный вариант течения инъекционной болезни требует локального лечения аналогично лечению банального карбункула или травматического абсцесса. Как правило, необходимо хирургическое лечение. Завершается процесс воспаления рубцеванием.
Профилактика медикаментозной формы инъекционной болезни сводится к предотвращению внутритканевого физико-химического ожога. Исключить ожог позволяет, например, разведение растворов лекарственных средств водой для инъекции или раствором 0,25% новокаина до уровня их изотонической активности.
Таким образом, инъекции лекарств вызывают инъекционно-медикаментозное ятрогенное заболевание кожи и других тканей, которое имеет характер локального воспаления. Оно может быть обратимым и необратимым, а также кровавым и бескровным. Диагностическим симптомом инъекционно-медикаментозной болезни является характерная цветная пятнистость кожи. При легком течении болезни кожа имеет мелкую пятнистость. Причем, по мере увеличения срока давности произведенных инъекций цветная пятнистость меняет свою окраску и размерность подобно «цветению» банального кровоподтека или синяка. При умеренном течении «кровавой» формы болезни кожа имеет 1-2 крупных «цветных» пятна, то есть имеет крупную пятнистость. При тяжелом течении медикаментозной формы инъекционной болезни кожа над местом инъекции приобретает темно-вишневое окрашивание уже через 5-10 минут после инъекции.
Диагностическим симптомом инъекционно-медикаментозной болезни является характерная цветная пятнистость кожи. При легком течении болезни кожа имеет мелкую пятнистость. Причем, по мере увеличения срока давности произведенных инъекций цветная пятнистость меняет свою окраску и размерность подобно «цветению» банального кровоподтека или синяка. При умеренном течении «кровавой» формы болезни кожа имеет 1-2 крупных «цветных» пятна, то есть имеет крупную пятнистость. При тяжелом течении медикаментозной формы инъекционной болезни кожа над местом инъекции приобретает темно-вишневое окрашивание уже через 5-10 минут после инъекции.
Причиной «инъекционной болезни» кожи и подкожно-жировой клетчатки является одно- или многократное колото-инфильтративное специфическое и стандартизированное, но неведомое врачам колото-инфильтративное травмирование кожи, подкожно-жировой клетчатки и других тканей, вызванное, с одной стороны, специфической механической агрессивностью стандартных инъекто-ров, обусловленное их особыми размерами и формами, а, с другой стороны, чрезмерно высокой фармацевтической агрессивностью качественных растворов лекарственных средств, способных оказывать местное раздражающее и прижигающее действие.
Литература:
1. Стручков В.И., Гостищев В.К., Стручков Ю.В. Руководство по гнойной хирургии. -М.: Медицина. — 1984. — 512 с.
2. Ураков А.Л., Стрелкова Т.Н., Корепанова М.В., Уракова Н.А. Возможная роль качества лекарств в клинико-фармацевтической оценке степени безопасности инфузионной терапии./Нижегородский медицинский журнал. — 2004. — № 1. — С. 42 — 44.
3. Ураков А.Л., Уракова Н.А., Михайлова Н.А. и др. Местная постинъекционная агрессивность растворов лекарственных средств
в инфильтрированных тканях и способы ее устранения/Медицинский альманах. — 2007. — № 1. — С. 95 — 97.
4. Ураков А.Л., Уракова Т.В. Уракова Т.В., Касаткин А.А. Мониторинг инфракрасного излучения в области инъекции как способ оценки степени локальной агрессивности лекарств и инъекторов/Медицинский альманах. — 2009. — № 3. — С.133 — 136.
— 2009. — № 3. — С.133 — 136.
5. Ураков А.Л., Уракова Н.А., Уракова Т.В. и др. Использование тепловизора для оценки постинъекционной и постинфузионной локальной токсичности растворов лекарственных средств//Проблемы экспертизы в медицине. — 2009. — № 1. — С. 27- 29.
6. Ураков А.Л., Уракова Н.А., Козлова Т.С. Локальная токсичность лекарств как показатель их вероятной агрессивности при мест-
ном применении/Вестник Уральской медицинской академической науки. — 2011. — № 1 (33). — С.105 — 108.
7. Ураков А.Л., Уракова Н.А. Постинъекционные кровоподтеки, инфильтраты, некрозы и абсцессы могут вызывать лекарства из-за отсутствия контроля их физико-химической агрессивности// Современные проблемы науки и образования. [Электронный ресурс] — 2012. — № 5;- С. 5 — ; URL: www.science-education. ru/105-6812. (дата обращения; 17.05.2012).
ru/105-6812. (дата обращения; 17.05.2012).
8. Ураков А.Л. Кровь как объект экспертизы внутривенного введения лекарств// Проблемы экспертизы в медицине. — 2013. — № 3.
— С. 22 — 26.
9. Уракова Н.А., Ураков А.Л. Инъекционная болезнь кожи // Современные проблемы науки и образования. [Электронный ресурс]
— 2013. — № 1. С. 19 — 23; URL: http://www.science-education.ru/107-8171 (дата обращения: 22.01.2013).
10. UrakovA.L., Urakova N.A. Thermography of the skin as a method of increasing local injection safety// Thermology International. — 2013.
— V. 23. — N 2. — P 70 -72.
11. Urakov A., Urakova N., Kasatkin A., Chernova L. Physical-сhemical aggressiveness of solutions of medicines as a factor in the rheology of the blood inside veins and catheters// Journal of Chemistry and Chemical Engineering. — 2014. — V. 8, N.01. — P. 61 — 65.
Physical-сhemical aggressiveness of solutions of medicines as a factor in the rheology of the blood inside veins and catheters// Journal of Chemistry and Chemical Engineering. — 2014. — V. 8, N.01. — P. 61 — 65.
Инфильтрат – Справочник заболеваний | МЦОЗ
Инфильтрат — это скопление в тканях организма клеточных элементов, несвойственных для этой области, а также крови и лимфы. Его формирование сопровождается увеличением ткани в объеме, она уплотняется, меняет цвет, в очаге ощущается болезненность.
Лечение и прогноз этого состояния зависят от вида и причины его возникновения:
- Воспалительный инфильтрат.
- Причиной его развития становятся травмы и распространение инфекции. Инфильтраты бывают внутримышечными, подкожными, также они образуются в грудной и брюшной полости.
- Воспалительный инфильтрат представляет собой выпот клеток крови в ткани. При присоединении инфекции он становится гнойным.
 Помимо нагноения с образованием флегмоны и абсцесса инфильтрат может рассасываться, склерозироваться или заживать с образованием рубца.
Помимо нагноения с образованием флегмоны и абсцесса инфильтрат может рассасываться, склерозироваться или заживать с образованием рубца. - Опухолевый инфильтрат.
- Развивается при инвазивном росте новообразования, когда клетки опухоли прорастают в здоровые ткани, постепенно разрушая ее.
В медицине выделяется еще несколько разновидностей этого состояния.
Легочный
Представляет собой скопление различных клеток в легочной ткани. При этом ткань уплотняется, увеличивается в объеме, а работа органов дыхания затрудняется. Причина образования инфильтрата легкого — проникновение инфекции и паразитов (аскаридоз), развитие опухоли, аллергический процесс.
Для определения патологии решающую роль играет рентгенологическое обследование. Также назначаются анализы крови для определения природы болезни и возможных возбудителей.
Лечение зависит от причины патологии. Терапию назначает врач-пульмонолог.
Послеооперационный
Инфильтрат после операции — это осложнение, возникшее в результате хирургического вмешательства. Причина развития патологии — инфицирование и травматизация тканей.
Причина развития патологии — инфицирование и травматизация тканей.
Также возникновению инфильтратов способствует нарушение кровообращения в области вмешательства и сниженная сопротивляемость инфекциям в послеоперационном периоде.
Патология развивается постепенно. Она обнаруживается на первой или второй неделе после операции. У человека поднимается температура, появляются боли в области брюшной полости, возникает задержка стула. В области вмешательства врач определяет болезненное уплотнение.
Инфильтрат опасен остановкой затягивания послеоперационной раны и ее нагноением, поэтому сразу при его обнаружении хирург назначает антибиотикотерапию.
Постинъекционный
Патология развивается на месте подкожных или внутримышечных уколов. Чаще всего инфильтрат возникает после инъекций в ягодичную мышцу: появляется болезненность, при пальпации обнаруживается уплотнение. Кожа краснеет, температура поднимается до субфебрильных цифр.
Причиной развития становится нарушение правил постановки уколов (тупые иглы, быстрое введение препарата, частые инъекции в одну и ту же область, несоблюдение правил асептики).
Для лечения инфильтрата используются местные средства (йодная сетка), методы физиотерапии (электрофорез), УВЧ и антибиотикотерапия.
Аппендикулярный инфильтрат
Это осложнение острого аппендицита, которое проявляется в виде спаянных между собой тканей аппендикса с органами, расположенными поблизости (слепая кишка, тонкая кишка, сальник).
Образование формируется на 2–5 день от начала болезни. После формирования инфильтрата острую боль в правой подвздошной области сменяет тупая и ноющая. В крови также определяется воспаление (повышенное СОЭ, лейкоцитоз). Температура поднимается до субфебрильных цифр. Со временем уплотнение может нагноиться или рассосаться. Образование лечится консервативным путем: врач назначает антибиотики, физиотерапевтические процедуры. Через 2 месяца проводится плановая аппендэктомия.
«Шишки» от уколов: как избежать их появления?
Постинъекционный инфильтрат («шишка») может стать причиной абсцесса, поэтому следует избегать его возникновение. «Шишка» и ее осложнение – абсцесс – появляются вследствие нарушения техники введения медикаментов или нарушения санитарно-гигиенических норм. Плохо обработанная поверхность в месте инъекции, руки медсестры процедурного кабинета, расходные материалы (шприц, вата) – все это может стать причиной возникновения инфильтрата («шишки»). Медики предупреждают о том, что самолечение может быть опасно, так как человек, не владеющий техникой, может нарушить правила введение инъекций, что впоследствии вызовет постинъекционный инфильтрат и его осложнения. Иногда «шишки» возникают и в том случае, когда процедура выполнены правильно. Причиной могут стать:
«Шишка» и ее осложнение – абсцесс – появляются вследствие нарушения техники введения медикаментов или нарушения санитарно-гигиенических норм. Плохо обработанная поверхность в месте инъекции, руки медсестры процедурного кабинета, расходные материалы (шприц, вата) – все это может стать причиной возникновения инфильтрата («шишки»). Медики предупреждают о том, что самолечение может быть опасно, так как человек, не владеющий техникой, может нарушить правила введение инъекций, что впоследствии вызовет постинъекционный инфильтрат и его осложнения. Иногда «шишки» возникают и в том случае, когда процедура выполнены правильно. Причиной могут стать:
Ослабленный иммунитет.
Аутоиммунные заболевания.
Ожирение (из-за большого слоя подкожной клетчатки возникает инфильтрат).
Кожная аллергия (при наличии гнойничков на коже).
Расчесывание того места, куда была сделана инъекция.
Как распознать инфильтрат?
На месте укола появилась припухлость, кожа на месте инфильтрата может быть покрасневшей и горячей, при прикасании возможны болевые ощущения. Возможно значительное повышение температуры тела. На данном этапе необходимо сделать все, чтобы избежать воспалительного процесса и абсцесса.
Возможно значительное повышение температуры тела. На данном этапе необходимо сделать все, чтобы избежать воспалительного процесса и абсцесса.
Основная ошибка, которую часто допускают люди, решившие бороться с «шишками» самостоятельно – это прогревание, которое недопустимо, если в пораженном месте уже начался абсцесс. Поэтому важна консультация врача – отличить инфильтрат от абсцесса очень сложно. Инфильтрат лечат йодными сетками, физиотерапией и, как было сказано выше, прогреванием. Разумнее всего в случае появления «шишки» обратится к терапевту, который точно определит состояние пораженного участка и назначит адекватное лечение. В нашем медицинском центре принимает врач-терапевт Оспанова К., а также работает процедурный кабинет, где квалифицированные медсестры выполнят процедуры, назначенные врачами нашего или других медицинских центров. Записаться к терапевту или в процедурный кабинет можно прямо сейчас.
Клинико-фармакологическая коррекция динамики постинъекционных подкожно-жировых инфильтратов при инъекциях болеутоляющих средств, назначаемых в детской хирургии
На правах рукописи
оозоео 1~?з
Гасников Константин Владимирович
КШШИКО-ФАРМАКОЛОГИЧЕСКАЯ КОРРЕКЦИЯ ДИНАМИКИ ПОСТИНЪЕКЦИОННЫХ ПОДКОЖНО-ЖИРОВЫХ ИНФИЛЬТРАТОВ ПРИ ИНЪЕКЦИЯХ БОЛЕУТОЛЯЮЩИХ СРЕДСТВ, НАЗНАЧАЕМЫХ В ДЕТСКОЙ ХИРУРГИИ
14 00 25 — фармакология, клиническая фармакология 14 00 35 — детская хирургия
АВТОРЕФЕРАТ
диссертации на соискание ученой степени кандидата медицинских наук
2 4 МАЙ 2007
Уфа-2007
003060173
Работа выполнена на кафедре общей и клинической фармакологии ГОУ В1Ю «Ижевская государственная медицинская академия Федерального агентства по здравоохранению и социальному развитию»
Научные руководители.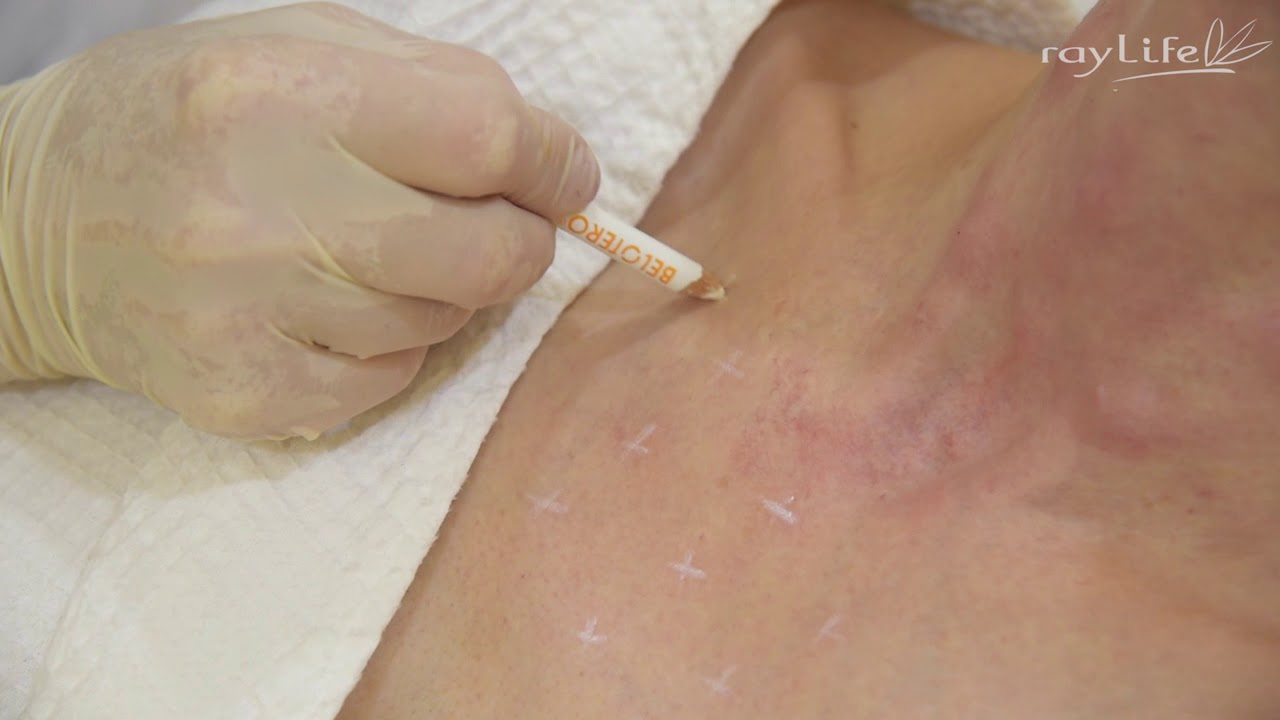 — доктор медицинских наук, профессор
— доктор медицинских наук, профессор
Александр Ливиевич Ураков
— доктор медицинских наук, профессор Николай Сергеевич Стрелков
Официальные оппоненты: — доктор медицинских наук, профессор
Валеева Лилия Анваровна
— доктор медицинских наук, профессор Мамлеев Игорь Айратович
Ведущая организация: Государственное учреждение
«Научно-исследовательский институт фармакологии им. В.В. Закусова РАМН»
Защита диссертации состоится «__» _____ 2007 г
в _ часов на заседании диссертационного совета Д 208 006 03 при
Государственном образовательном учреждении высшего профессионального образования «Башкирский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию», по адресу 450000, Республика Башкортостан, г Уфа, ул Ленина, 3
С диссертацией можно ознакомиться в библиотеке Государственного образовательного учреждения высшего профессионального образования «Башкирский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию» (г Уфа, Центр, ул Ленина, 3)
Автореферат разослан «_»_2007 г
Ученый секретарь диссертационного совета доктор медицинских наук, профессор
Г.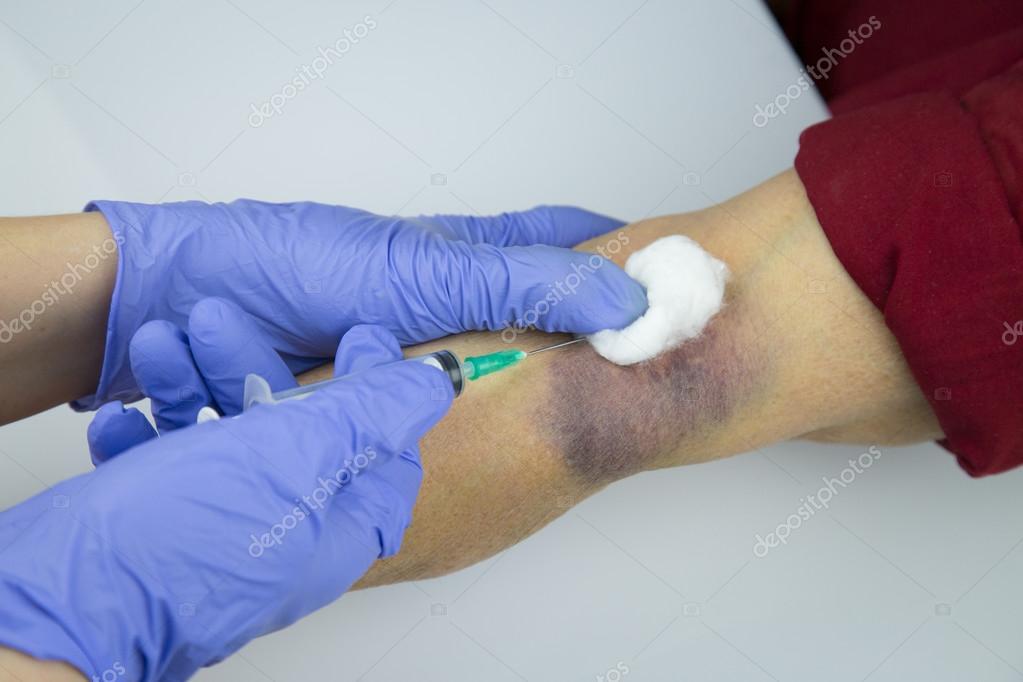 Х. Мирсаева
Х. Мирсаева
Общая характеристика работы
Актуальность проблемы. Выяснение причин возникновения и разработка способов предотвращения постинъекционных некрозов и абсцессов, возникающих в детской хирургической практике после внутривенных, внутримышечных и подкожных инъекций растворов болеутоляющих лекарственных средств, является одной из актуальных задач современного здравоохранения, поскольку для детей пока не создано лекарств, обладающих абсолютной постинъекционной безопасностью (Харкевич ДА, 1999, 2000, Фассахов РС, 2005, Лент Ричард, 2005) Показано, что возникновение постинъекционных инфильтратов и абсцессов зависит не только от соблюдения мер асептики, состояния и реактивности тканей, но и от некоторых физико-химических показателей качества лекарств (Стрелков НС и соавт, 2006, Ураков АЛ и соавт, 2006) В частности, выраженную агрессивную роль может играть чрезмерно кислая или чрезмерно щелочная среда лекарственного средства, а также его чрезмерно высокая осмотическая активность (Ураков А Л и соавт, 2000 — 2006) Однако, роль этих физико-химических показателей качества болеутоляющих лекарственных средств в формировании постинъекционных инфильтратов и абсцессов у детей остается недостаточно изученной
Широкое клиническое применение с целью болеутоления при лечении хирургических болезней детского возраста находят в настоящее время такие нестероидные противовоспалительные средства, как анальгин и диклофенак натрия Известно, что в некоторых случаях инъекции растворов этих средств в мягкие ткани способны вызвать образование постинъекционных инфильтратов и абсцессов, однако механизм их формирования и роль физико-химических факторов взаимодействия в динамике постинъекционпых медикаментозных инфильтратов остается недостаточно изученной (Машковский М Д, 2000, Михайлов И Б , 2004)
В связи с этим, выяснение роли физико-химических показателей качества растворов нестероидных противовоспалительных лекарственных средств в формировании постинъекционных инфильтратов с целью выяснения путей предотвращения постинъекционных осложнений у взрослых и детей представляется актуальным и практически важным
Цель работы. Целью работы является выявление физико-химических факторов агрессивности растворов лекарственных средств и разработка способов предотвращения постинъекционных некрозов Задачи работы:
Целью работы является выявление физико-химических факторов агрессивности растворов лекарственных средств и разработка способов предотвращения постинъекционных некрозов Задачи работы:
1 Изучить диапазон значений физико-химических показателей качества инъекционных растворов НПВС, наиболее часто применяемых в детской хирургии
2 Исследовать динамику постинъекционных инфильтратов ПЖК, вызванных инъекциями растворов НПВС с учетом их физико-химических показателей качества
3 Разработать способ экспресс-оценки степени постинъекционной безопасности растворов лекарственных средств
4 Разработать способ предотвращения пост инъекционного некроза тканей
Научная новизна результатов Показано, что качество применяемых в детской хирургической практике растворов болеутоляющих лекарственных средств не соответствует физико-химическому состоянию мягких тканей, в которые производятся инъекции Причем, диапазон физико-химических показателей качества растворов лекарственных средств, предназначенных для внутримышечных инъекций, не отличается от диапазона физико-химических показателей качества растворов, предназначенных для внутривенных и подкожных инъекций, а выбор и назначение лекарств производится врачами-детскими хирургами без учета фнзжо-химических показателей качества препаратов разных серий и производителей
В экспериментальных исследованиях на двухмесячных поросятах, в исследованиях с порциями крови доноров и сырого яичного бежа in vitro установлены закономерности местного некротизиругощего действия лекарственных средств с учетом физико-химических и биологических показателей их качества, наличия денатурирующего действия на белки Показано, что инъекции под кожу и в мышцу, введение в сырой яичный белок или в плазму крови препаратов диклофенака натрия, произведенного AGIO (серия DZ-789), в составе которого отсутствуют органические растворители, не вызывает постшгьекционный некроз тканей и не денатурирует белок В то же время, препараты диклофенака, произведенные фирмами Сотекс (Россия), AGIO (Индия) и Hemofarm (Сербия и Черногория), в составе которых присутствует 24% бензилового и изопропилового спиртов, вызывает образование постинъекционного некроза и немедленное помутнение сырого яичного белка из-за денатурирующего действия
Установлено, что глюконат кальция способен устранять физико-химическую агрессивность препаратов диклофенака за счет химической реакции катионов кальция с диклофенаком натрия и его растворителем прогашенгликолем с образованием кальциевых солей Это лишает препараты диклофенака денатурирующей активности и способно предотвратить развитие постинъекционного некроза при инъекциях в мягкие ткани
Разработан способ предотвращения постинъекционого некроза тканей, вызываемого ошибочным введением препаратов диклофенака в подкожно-жировую клетчатку Способ основан на своевременном обкалывании медикаментозного инфильтрата раствором глюконата кальция
Разработан «пробирочный» способ экспресс-оценки степени постинъекционной безопасности лекарственных средств, основанный на выявлении кольца помутнения сырого яичного белка в пробирке на границе сред после наслаивания на белок исследуемого препарата
Научно-практическая ценность работы и реализация результатов исследования Тема диссертации является составной частью плана научно-исследовательской работы кафедры хирургических болезней детского возраста и кафедры общей и клинической фармакологии ГОУ ВПО «Ижевская государственная медицинская академия Федерального агентства по здравоохранению и социальному развитию» с 11 мая 2004 года
Выявление закономерностей местного раздражающего и денатурирующего действия лекарственных средств с определенной осмотичностью и денатурирующей активностью позволило оценить практическую значимость физико-химических показателей качества лекарств, применяемых в виде внутримышечных и подкожных инъекций, и предложить сырой яичный белок в роли индикатора для выявления денатурирующей активности средств и экспресс-оценки степени постинъекционной безопасности лекарств Обнаружена способность раствора 10% глюконата кальция выступать в роли антидота в отношении препаратов диклофенака, содержащих в качестве растворителя пропиленгликоль
Внедрение в практику.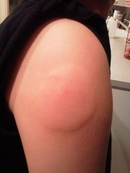 Результаты исследований внедрены в процесс обучения студентов и врачей на кафедре хирургических болезней детского возраста и на кафедре общей и клинической фармакологии Ижевской государственной медицинской академии, используются в практической деятельности врачами ГУЗ «Республиканская детская клиническая больница УР», а также легли в основу заявки на изобретение «Способ экспресс-оценки степени постинъекционной безопасности лекарственных средств» (Заявка на выдачу патента РФ №2006140932 (044705) и заявки на изобретение «Способ предотвращения постинъекционного некроза» (Заявка на выдачу патента РФ №2006140915(044688)
Результаты исследований внедрены в процесс обучения студентов и врачей на кафедре хирургических болезней детского возраста и на кафедре общей и клинической фармакологии Ижевской государственной медицинской академии, используются в практической деятельности врачами ГУЗ «Республиканская детская клиническая больница УР», а также легли в основу заявки на изобретение «Способ экспресс-оценки степени постинъекционной безопасности лекарственных средств» (Заявка на выдачу патента РФ №2006140932 (044705) и заявки на изобретение «Способ предотвращения постинъекционного некроза» (Заявка на выдачу патента РФ №2006140915(044688)
Основные положения, выносимые на защиту:
1 Вода для инъекций, растворы 0,25%, 0,5%, 1% и 2% новокаина являются гипоосмотичными, а растворы 2,5% диклофенака натрия, 5% и 10% натрия хлорида, 10% кальция глюконата, 10% хлорида кальция, 50% метамизола натрия являются гиперосмотичными, поэтому при подкожных инъекциях они вызывают раздражение ПЖК и способствуют возникновению реактивного воспаления
2 Перечень входящих ингредиентов и физико-химические показатели качества растворов 2,5% диклофенака натрия, произведенных разными производителями, разные Помимо диклофенака натрия в состав препарата могут входить бензиловый спирт, маннит, пропиленгликоль, натрия гидросульфит, натрия гидроксид, натрия метабисульфит, соляная кислота,
натрия сульфит безводный, повышающие постинъекционную агрессивность препаратов
3 Растворы диклофенака натрия, произведенные разными производителями, имеют различную степень постинъекционной безопасности Раствор 2,5% диклофенака натрия, произведенный фирмой AGIO го серии DZ-789, не образует кольцо помутнения в пробирке с сырым яичным белком и не вызывает постинъекционный некроз при подкожных и внутримышечных инъекциях Раствор 2,5% диклофенака натрия, произведенный Сотекс (Россия), Hemofarm (Сербия и Черногория) и AGIO (Индия), образует кольцо помутнения в пробирке с сырым яичным белком и вызывает постинъекционный некроз при подкожных инъекциях, поскольку содержит в своем составе 24% многоатомных спиртов, обладающих денатурирующим и некротизирующим действием
Апробация работы.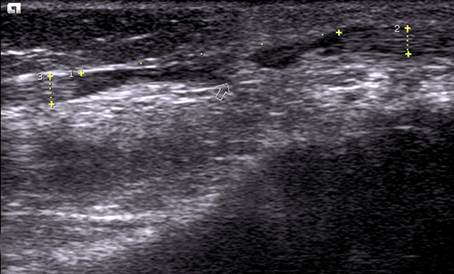
Результаты работы и основные положения диссертации доложены на 5-м конгрессе молодых ученых и специалистов «Науки о человеке» (Томск, 20 -21 мая 2004 г ), на V Российском национальном конгрессе «Человек и лекарство» (Москва 21-25 апреля 1998 г), на 2-м Съезде РНОФ (Москва, 21-25 апреля 2003 г), на 4-й международной конференции «Биологические основы индивидуальной чувствительности к психотропным средствам» (Москва, 13-16 марта2006 г)
Публикации.
По теме диссертации опубликовано 10 работ, подано 2 заявки на выдачу патентов РФ на изобретения
Структура и объем работы.
Диссертация изложена на 176 страницах машинописного текста, иллюстрирована 25 рисунками, 4 фотографиями и 23 таблицами, включает в себя обзор литературы, материалы и методы исследования, результаты собственных исследований, обсуждение полученных результатов, заключение, выводы, практические рекомендации и список использованной литературы, представленный 267 источником, в том числе 127 зарубежными
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Проведен ретроспективный анализ качества клинического применения растворов лекарственных средств в детской хирургии на основании анализа врачебных назначений по картам 100 стационарных больных хирургических и ортопедо-травматологических отделений ГУЗ «Республиканская детская клиническая больница УР», поступивших на лечение в 2002 — 2006 годах Оценивалось количество назначенных лекарственных средств каждому пациенту на день и на весь курс лечения, количество растворов лекарственных препаратов, назначенных при этом в инъекциях детям разных возрастных
групп (до 1 месяца, от 1 месяца до 1 года, от 1 года до 3 лет, от 3 лет до 10 лет, от 10 до 15 лет), частота и количество назначений лекарственных средств в определенных лекарственных формах, предназначенных для инъекционного введения, и фабричная готовность для их назначения детям разных возрастных групп Анализировалась технология инъекционного введения растворов лекарственных средств, наличие указаний врача по изменению объема и способа инъекций
Визуальную оценку постинъекционного инфильтрата производили ad oculus в экспериментах на 20 двухмесячных поросятах массой 5 — 7 кг, с помощью методов пальпации и с помощью УЗИ при применении соответствующих датчиков (Стрелкова Т Н, 2004) Одновременно с двух сторон (в правую и левую части тела) производили инъекционное введение изучаемого препарата и раствора 0,9% натрия хлорида Затем осуществляли непосредственное измерение с помощью линейки диаметра кожной папулы над подкожным инфильтратом и наблюдение за изменением цвета кожи над ним на протяжении 60 минут после подкожных инъекций в области передней брюшной стенки поросят Фиксировали интервал времени между инъекцией и возникновением гиперемии, отека, повышения температуры (симптомов воспаления) Оценивали динамику изменения окраски кожи, продолжительность, обратимость или необратимость воспалительного процесса, высоту, диаметр и глубину зоны воспалительного поражения, последовательность и время протекания стадий воспаления и регенерации Регистрировали развитие септического или асептического постиньекционного абсцесса В общей сумме поставлено 820 опытов
Эксперименты проведены в условиях лицензированного вивария ГОУ ВПО «Ижевская государственная медицинская академия МзиСР РФ» на бодрствующих двухмесячных поросятах обоего пола породы ландрас массой от 5 до 7 кг Инъекции растворов лекарственных средств производили в дневное время суток одноразовыми шприцами «Шприц двухдетальный 0,7×38 мм типа Луер 5Б мл/ml» производства «TYUMEN-MEDICO» (партия К133) в строгом соответствии с общепринятыми технологиями при соблюдении условий асептики и антисептики
В работе использованы готовые для инъекций растворы лекарственных средств разных производителей и серий, отвечающие своим качеством требованиям соответствующих фармакопейных статей и снабженные сертификатами качества и паспортами лекарственных средств установленного образца
Осмотичность растворов лекарственных средств определена с помощью прибора OSMOMAT-030 RS производства фирмы ANSELMA Industries (Австрия), работающего на криоскопическом принципе
Для измерения величины рН растворов лекарственных средств использован потенциометрический метод Измерения производили с
помощью универсального ионометра ЭВ-74, как электрод сравнения использован хлорсеребряный электрод заводского изготовления по общепринятой методике
В исследованиях использована кровь 20 пациентов, находящихся на лечении в реанимационном отделении 2 юродской клинической больницы, при утреннем заборе крови из пальца, по добровольному информированному согласию граждан
Изучение морфологических особенностей состояния форменных элементов крови осуществлено цитологически с помощью микроскопа «JIOMO МИКМЕД-2» при 1000-кратном иммерсионном увеличении по мазкам крови, приготовляемым по стандартной методике (Петров AB и соавт, 1979, Селиванова КФ, 1985, Ашджанян НА и соавт, 1998), до и после смешивания порции крови с порцией раствора лекарственного средства в соотношении 1 1 (Садилова П Ю , 2002) При этом применена стандартная технология приготовления мазка крови Исследованию подвергнуты всего 40 мазков крови
Для статистической обработки данных была использована программа BIOSTAT V 4 03 (©1998 McGravv Hill, перевод на русский язык ©1998 «Практика»), предназначенная для статистической обработки медицинских исследований, а также t — критерии Стьюдента (Лучкевич В С и соавт , 1996) Статистическую обработку данных выполняли с помощью персонального компьютера типа IBM PC марки LG LW65-P797, серийный номер 512KIDE202770, с использованием программы «Microsoft® Excel» (©Корпорация Майкрософт (Microsoft Corporation), 1985-1999)
Вычисляли среднюю арифметическую (М), ошибку средней арифметической (т), а также коэффициент достоверности (±), коэффициент корреляции (г) Степень различия показателей определяли в каждой серии по отношению к исходным показателям в контроле Достоверной считали разницу показателей при Р<0,05
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
В результате ретроспективного исследования врачебных назначений, сделанных врачами-детскими хирургами в историях болезней пациентов детского возраста, были обнаружены назначения нескольких десятков лекарственных средств для инъекций Причем, препараты для инъекционного введения были назначены всем без исключения пациентам Общий перечень назначенных лекарственных средств составил 98 наименований При этом пациентам разных возрастных групп врачи назначали практически одни и те же лекарства В историях болезни, листах врачебных назначений и картах интенсивной терапии отсутствуют указания на производителей лекарственных средств и номеров серий В связи с этим на основании информации, указанной в листах врачебных назначений, невозможно сделать заключение о том,
лекарства каких именно производителей вводились в организм того или иного ребенка и какие физико-химические показатели качества имело каждое лекарственное средство
Затем нами был проведен анализ указаний на особенности технологии выполнения инъекций тех или иных лекарственных препаратов тому или иному ребенку с учетом возраста и массы тела Ни в одной истории болезни не было указано, каким шприцом, с помощью какой иглы, в какую часть тела и на какую глубину следует осуществлять инъекционное введение того или иного раствора лекарственного средства Все лекарственные средства назначались в инъекциях ежедневно и многократно, но в медицинских документах отсутствует информация о наблюдениях за динамикой постинъекционного инфильтрата мягких тканей в первые минуты и часы после инъекции, не отражено ежедневное состояние места инъекции Кроме этого, в эпикризе отсутствует информация о состоянии мягких тканей, выбранных для инъекций
В то же время, проведенный нами анонимный опрос медицинского персонала этих отделений свидетельствует о том, что постинъекционные инфильтраты мышц и клетчатки иногда возникают, но из-за боязни наказания эти факты не отражаются в документах Медицинские сестры указывают, что чаще всего возникают инфильтраты глубоких тканей верхненаружного квадранта ягодичной мышцы у тех детей, которым врач назначает сразу по 3-4 препарата для внутримышечных инъекций 3 раза в день или 6 раз в сутки При этом медицинские сестры указывают на то, что при необходимости одновременных инъекций нескольких лекарств они производят внутримышечные инъекции в одну из ягодиц, а последующие инъекции производят в ту ягодицу, которая, по мнению ребенка, меньше болит В тех случаях, когда из-за многократных и частых инъекций пациент ощущает боль в обеих ягодицах, инъекции производят в любую из них Медицинские сестры указывают, что порой при пальпации ягодичной мышцы отмечается наличие в глубине мягких тканей твердого уплотнения Однако, последующие инъекции не отменяются, лишь для уменьшения чувства боли медицинские сестры по своему усмотрению разводят препарат раствором 0,25% новокаина в 2-3 раза
Тем не менее, никакого анализа подобных осложнений не проводится Отсутствуют и практические рекомендации по предотвращению постинъекционных осложнений
Далее исследована осмотическая активность лекарственных средств местноанестезирующего действия При этом были получены результаты, свидетельствующие о том, что осмотичность большинства растворов лекарственных средств для инъекций отличается от уровня 280-300 мОсм/л воды (Таблица 1)
Таблица 1
Осмотическая активность растворов некоторых местноанестезирующих лекарственных средств (мОсм/л воды)
№№ ri/n Название, производитель, серия Концентрация Величина осмотич-ности в мОсм/л
1 Раствор новокаина 0,25% — 100 мл, Аптека № 131 (Ижевск), серия №300505 0,25% 18±0,6*
2 Раствор новокаина 0,25% — 200 мл, Аптека № 169 (Ижевск), серия №230505 0,25% 17,4±0,5*
3 Раствор новокаина 0,5% — 100 мл, Аптека № 131 (Ижевск), серия №300505 0,5% 33,5±1,1*
4 Раствор новокаина 0,5% — 100 мл, Аптека № 137 (Ижевск), серия №150505 0,5% 33,0±0,7*
5 Раствор новокаина 0,5% — 5 мл, «Биохимик» (Саранск), серия №61005 0,5% 27,0±0,2*
6 Раствор новокаина 1% — 5 мл, «Биохимик» (Саранск), серия №150605 1% 78,6±1,6*
7 Раствор новокаина 2% — 5 мл, «Ай-Си-Эн Октябрь», серия №190605 2% 130±2,9*
8 Раствор лидокаина гидрохлорида 2% — 2 мл, ОАО «Мосхимфармпрепараты» им Семашко, серия №100705 2% 333±9,2*
9 Раствор лидокаина гидрохлорида 10% — 2 мл, ОАО«Мосхимфармпрепараты» им Семашко, серия №200705 10% 663±7,7*
10 Раствор лидокаина гидрохлорида 10% — 2 мл, «Эгис АО» (Венгрия), серия №250605 10% 796±9,5*
Примечание * — достоверно при Р<0,05 (п=5) по сравнению с осмотичностью раствора 0,9% натрия хлорида
Как следует из приведенных результатов, осмотичность растворов находится в прямой зависимости от величины концентрации растворенных лекарственных средств, поэтому осмотичность растворов тем выше, чем более высока в нем концентрация местного анестетика
Исследование кислотности препаратов показало, что они имеют величину рН ниже 7,0 Причем, раствор в ампулах оказался более кислым, чем во флаконах (Таблица 2)
Таблица 2
Величина рН раствора 0,9% натрия хлорида, воды для инъекций и
местных анестетиков разных производителей и серий
№№ п/п Препарат Производитель и серия Величина РН
1 Р-р 0,9% натрия хлорида д/ин, 200 мл ОАО «Биохимик» (Саранск) Серия №3500704 6,44±0,07*
2 Р-р 0,9% натрия хлорида д/ин, 200 мл Аптека №131 (Ижевск) Серия №310504 6,71±0,05*
3 Р-р 0,9% натрия хлорида д/ин, 400 мл ОАО «Биохимик» (Саранск) Серия №2700604 6,83±0,07*
4 Р-р 0,9% натрия хлорида д/ин, 400 мл ОАО «Биосинтез» (Пенза) Серия №110104 7,25±0,07*
5 Р-р 0,9% натрия хлорида д/ин, 400 мл Аптека №137 г (Ижевск) Серия №30 06 04 7,10±0,03*
6 Р-р 0,9% натрия хлорида д/ин, 10 мл АО «Галичфарм» (Украина) Серия №300604 5,34±0,05*
7 Р-р 0,9% натрия хлорида д/ин , 10 мл «Белмедпрепараты» (Беларусь) Серия №101405 6,48±0,0 5*
8 Р-р 0,9% натрия хлорида д/ин, 10 мл «Белмедпрепараты» (Беларусь) Серия №101004 5,83±0,04*
9 Р-р 0,9% натрия хлорида д/ин, 10 мл «Эндокрининяй препаратай» АО (Литва) Серия №150605 6,15±0,05*
10 Вода для инъекций в амп 2 мл ГП «Львовдиалвкт» (Украина) Серия №30104 6,85±0,07*
11 Вода для инъекций в амп 2 мл ГП «Львовдиалект» (Украина) Серия №1151205 5,22±0,05*
12 Р-р новокаина 0,5% 5 мл «Биохимик» (Саранск) Серия №941003 4,00± 0,03*
13 Р-р новокаина 0,5% 5 мл ОАО «Биосинтез» (Пенза) Серия №48102000 4,35±0,04*
14 Р-р1 новокаина 0,5% 5 мл д/ин Борисовский з-д мед препаратов (Беларусь) Серия №180803 4,12±0,03*
15 Р-р новокаина 0,5% 5 мл «Вирион» (Россия) Серия №560603 3,97±0,03*
16 Р-р новокаина 0,5% 5 мл ОАО «Дальхимфарм» Хабаровск Серия №210101 4,25±0,04*
17 Р-р новокаина 0,5% 5 мл «Новосибхимфарм» (Россия) Серия №30703 3,87±0,03*
18 Р-р лидокаина гидрохлорида 2% 2 мл д/ин ОПХФП «Биостимулятор» (Россия) 901201 5,81±0,06*
19 Р-р лидокаина гидрохлорида 2 % 2 мл д/ин «МХФП им Семашко» (Россия) 120403 5,31±0,05*
20 Р-р лидокаина гидрохлорида 2 % 2 мл д/ин «ICN Полифарм» 230403 5,85±0,06*
21 Р-р лидокаина гидрохлорида 2 % 2 мл д/ин ЗАО «Верофарм» 1500803 5,44±0,05*
Примечание *- достоверно при Р<0,05, п=5
Анализ полученных данных позволяет заявить, что все растворы изученных нами лекарственных средств обладают закисляющими свойствами, поскольку имеют рН ниже 7,4, но кислотнос1Ь препаратов не обусловлена величиной их концентрации
Таким образом, вода для инъекций, растворы 0,25%, 0,5%, 1 и 2% новокаина являются гипоосмотичными и кислыми, растворы 2 и 10% лидокаина гидрохлорида — гиперосмотичными и тоже кислыми, а растворы 0,9% натрия хлорида у некоторых производителей и в некоторых сериях не обладают изоосмотичностью и имеют рН ниже изоуровня крови человека
Проведенное нами в хирургическом отделении ГУЗ «РДКБ УР» измерение температурных режимов лекарственных препаратов позволило показать, что растворы лекарственных средств, вводимые пациентам в виде внутримышечных инъекций, вводятся с температурой ниже температуры тела человека, поскольку имеют комнатную температуру В зимнее время года она составляет 19-20°С, а в летнее — 23-24°С
Далее, нами исследована осмотическая активность нестероидных противовоспалительных средств, произведенных для инъекций Полученные результаты свидетельствуют о том, что дииапазоны осмотической и кислотной активности их растворов существенно отличаются от уровней осмотичности и щелочности нормальной крови и плазмы человека Более того, оказалось, что показатель осмотичности растворов для инъекций не включен в список контролируемых показателей качества, поэтому препараты разных серий и разных производителей имеют различную осмотическую активность, и все они обладают чрезмерно высокой гиперосмотичностью
Например, раствор 50% натрия метамизола (анальгина), произведенный фирмой АО «Санитас» (Литва) (серия №1900010), имеет осмотичносгь 3330 ± 12 мОсм/л (Р<0,05, п=5), раствор 2,5% ортофена объемом 3 мл, произведенный фирмой «Брынцалов А» (серия № 77 09 2000), имеет показатель осмотической активности 4168 ± 5 мОсм/л (Р<0,05, п=5), этот же препарат в ампулах по 3 мл, выпущенный фирмой Индус Фарма ПвтЛтд, (серия № D-801), имеет осмотическую активность 3952 ± 8 мОсм/л воды (Р<0,05, п=5), раствор 2,5% диклофенака натрия, произведенный фирмами AGIO (Индия), Hemofarm (Сербия и Черногория) и Сотекс (Россия) имеет осмотичность соответственно 3695 ± 9, 4023 ± 10 и 3994 ± 7 мОсм/л воды (Р<0,05, п=5)
Далее, было проведено исследование значений рН тех же растворов лекарственных средств Выявленные значения рН оказались в диапазоне от 5,7±0,04 (раствор 50% анальгина АО «Санитас» (Литва)) до 8,48±0,07 (диклофенак, раствор для инъекций, 25 мг/мл, 3 мл Hemofarm (Сербия и Черногория) Таким образом, растворы нестероидпых противовоспалительных средств не обладают изощелочностыо, то есть не имеют величину рН 7,4 (Таблица 3)
Таблица 3
Осмотичность (мОсм/л воды) и pH растворов некоторых нестероидных противовоспалительных лекарственных средств
№№ п/п Название, производитель, серия Величина осмотично-сги в мОсм/л рн
1 50% раствор анальгина 2 мл, АО «Санитас» (Литва) серия №1900010 3330±12* 5,7±0,04*
2 Раствор 2,5% ортофена 3 мл, «Биохимик», серия № 80405 4168 ± 5* б,2±0,05*
3 Диклофенак, 75 мг/3 мл, Индус Фарма ПвтЛтд, серия №D-801 3952 ± 8* 6,65±0,05*
4 Диклоген, раствор для инъекций, 75 мг, Змл, AGIO (Индия), серия D6-5042 3695 ±9* 8,23+0,07*
5 Диклофенак, раствор дня инъекций, 25 мг/мл, 3 мл, Hemofarm (Сербия и Черногория), серия 1171205 4023 ± 10* 8,48±0,07*
6 Диклофенак раствор для инъекций, 25мг/мл, Змл, Сотекс (Россия), серия 310905 3994 ±7* 8,3±0,06*
Примечание *- достоверно при Р<0,05 (п=5)
Помимо этого оказалось, что температурный режим растворов НПВС при инъекции в мягкие ткани отличается от температуры тела ребенка летом температура растворов составляет 22-23″С, а зимой — 19-21°С
Таким образом, растворы нестероидных противовоспалительных средств, изготовленные различными производителями, имеют осмотичность, кислотность и температурный режим, отличающиеся от соответствующих показателей нормальной крови и плазмы здорового ребенка
Далее исследована осмотическая активность растворов 10% хлорида кальция и 10% глюконата кальция, произведенных различными производителями Полученные данные свидетельствуют о том, что все растворы препаратов кальция являются гиперосмотичными по отношению к изоуровню крови Например, раствор 10% кальция хлорида, произведенный НПО «Микроген», обладает осмотической активностью 1293 ± 7 мОсм/л воды, а раствор 10% кальция глюконата, выпущенный ЗАО «Верофарм» имеет осмотичность 1199 ± 12 мОсм/л воды(Р<0,05, п=5)
В следующей серии экспериментов нами исследована кислотность растворов этих лекарственных средств Все исследованные растворы оказались кислыми Раствор 10% кальция хлорида в ампулах по 10 мл, произведенный НПО «Микроген» (серия № 151204), имеет рН 5,7±0,05 (Р<0,05, п=5), а раствор 10% кальция хлорида в ампулах по 10 мл, произведенный ЗАО «Верофарм» (серия № 241104) имеет рН 6,2±0,04 (Р<0,05, п=5)
Таким образом, растворы кальция хлорида 10% и кальция глюконата 10% различных производителей по отношению к внутренней среде организма человека являются гиперосмотичными и закисляющими
Затем нами исследована динамика рассасывания постинъекционных медикаментозных инфильтратов, созданных путем инъекции в подкожно-жировую клетчатку живота поросят растворов местных анестетиков различной концентрации, а также воды для инъекций и раствора 0,9% натрия хлорида, обладающих определенными физико-химическими показателями качества
В первой серии опытов нами была изучена динамика рассасывания постинъекционного медикаментозного инфильтрата под кожей живота поросят после введения разных объемов 0,9% раствора натрия хлорида в условиях нормо-, гипер- и гипотермии Для этого место инъекции либо охлаждали, прикладывая пузырь с тающим льдом, либо нагревали с помощью грелки с теплой водой при температуре 60°С, либо оставляли в исходном состоянии Результат эксперимента оценивался как визуально, так и с помощью УЗИ места инъекции
Показано, что продолжительность рассасывания постинъекционного инфильтрата термо- и объемозависима При этом, увеличение объема вводимого препарата и создание в области инъекции относительно низкой температуры приводят к увеличению продолжительности рассасывания постинъекционного инфильтрата (Рис 1)
30 25
20 -
15
10 5 О
0,1мл 0,5 мл 1,0 мл 2,0 мл
И Нормотермия □ Локальная гипотермия ЕЗ Локальная гипертермия
Рисунок 1 Продолжительность рассасывания постинъекционных инфильтратов после подкожного введения в области живота поросят разных объемов 0,9% раствора натрия хлорида в условиях локальной нормо-, гипо-, и гипертермии
Во второй серии экспериментов нами изучены особенности рассасывания постинъекционного медикаментозного инфильтрата, образованного инъекцией под кожу живота поросят 1 мл раствора 0,9% натрия хлорида (контрольная группа), 1 мл воды для инъекций, 1 мл раствора 0,25%, 0,5%, 1% или 2% новокаина, либо 1 мл раствора 2%, или 10% лидокаина гидрохлорида При этом визуальная оценка состояния кожи и ПЖК дополнена ультразвуковым исследованием
Полученные результаты показывают, что первоначальные размеры постинъекционных инфильтратов после инъекции 1 мл растворов указанных лекарственных средств соизмеримы друг с другом Дальнейшая динамика размеров медикаментозных инфильтратов была разной
Динамика рассасывания инфильтрата, образованного инъекцией 1 мл раствора 0,9% натрия хлорида, была принята нами за эталон безопасного рассасывания Наиболее близким к этому эталону рассасывания оказалось рассасывание инфильтрата, образованного инъекцией раствора 2% лидокаина гидрохлорида Наибольшие отличия в динамике рассасывания постинъекционного инфильтрата от таковой в контрольной группе нами выявлены при инъекциях 10% раствора лидокаина гидрохлорида и воды для инъекций
В частности, в первые 30 минут после инъекции размер инфильтрата увеличивается, а не уменьшается, достигая максимального значения на 17 ± 0,6 минуте с момента инъекции Кроме этого, такой постинъекционный инфильтрат не исчезает даже в течение часа после инъекции (Рис 2)
Диаметр папулы, см 1,4 и
1 мин 5 мин 10 мин 15 мин 20 мин 30 мин 45 мин 60 мин
Время, мин
1 0,9%р-р натрия хлорида 3 ■»»■»&ю»явода для инъекций
2 —-О — 10%р-р лидокаина гидрохлорида 4 * А — 2%р-р лидокаина гидрохлорида
Рисунок 2 Динамика изменения диаметра (см) постинъекционной папулы при подкожном инъекционном введении 0,1 мл воды для инъекции, растворов 0,9% натрия хлорида, 2% или 10% растворов лидокаина гидрохлорида
Оценивая динамику рассасывания постииъекционных инфильтратов, возникших после инъекций растворов 0,25%, 0,5%, 1% и 2% новокаина, отметим, что таковая не достигает, но приближается к динамике рассасывания постинъекционного инфильтрата, обусловленного введением изотонического раствора 0 9% натрия хлорида, по мере увеличения концентрации новокаина в растворе (Рис 3)
Выявленная нами ранее осмотическая активность указанных лекарственных средств подтверждает предположение о том, что скорость рассасывания постинъекционного медикаментозного инфильтрата осмозависима следующим образом чем ближе осмотичность лекарственного препарата к изоуровню, тем быстрее рассасывается инфильтрат, обусловленный его инъекционным введением Так, быстрее прочих в исследуемой группе рассасывался инфильтрат после введения под кожу живота поросенка раствора 2% лидокаина гидрохлорида, имеющего осмотичность, близкую к изоуровню нормальной крови (333 ± 2,4 мОсмоль/л воды) Инфильтраты, возникшие после инъекций раствора 10% лидокаина гидрохлорида и воды для инъекций рассасывались дольше прочих — более 60 минут и 38,8±02 минут соответственно (Р < 0,05, п = 5)
См
0,8
1 мин 5 мин 10 мин 15 мин 20 мин 30 мин 45 мин
Рисунок 3 Динамика изменения диаметра (см) постинъекционной папулы при подкожном инъекционном введении 0,1 мл раствора 0,25% новокаина (1), 0,5% новокаина (2), 1% новокаина (3), 2% новокаина (4), 0,9% натрия хлорида (5)
Анализ установленных ранее величин рН исследованных нами лекарственных препаратов не позволяет обоснованно утверждать, что динамика рассасывания инфильтратов после инъекций этих лекарств кислотозависима В частности, рассасывание инфильтратов, образованных инъекцией под кожу поросят растворов 2% и 10% лидокаина гидрохлорида, имеющих сопоставимые величины рН, достоверно отличается друг от друга
Существенных различий в разрешении постинъекционного инфильтрата после инъекции под кожу живота поросенка растворов диклофенака натрия различных производителей не отмечается Так, спустя 1 минуту после введения под кожу препарата «Диклофенак, раствор для инъекций, 25 мг/мл, 3 мл», произведенного НешоГагт (Сербия и Черногория) (серии 1171205), площадь постинъекционного инфильтрата составила 3,92±0,09 см2, и по истечении часа с начала опыта уменьшилась до 2,2±0,01 см2 Сходная динамика наблюдалась и у всех остальных растворов диклофенака натрия различных производителей (Рис 4)
Площадь, сч2
1 мин 5 мин 10 мин 15 мин 20 мин 30 мин 45 мин 60 мин
Время, мин
Рисунок 4 Динамика изменения площади постинъекционного инфильтрата после введения растворов диклофенака натрия различных производителей 1 Диклофенак (НешоГагт), 2 Диклофенак (Сотекс), 3 Диклоген (АОЮ), 4 Диклофенак (Индус Фарма)
Как следует из приведенных данных, для каждого из четырех представленных препаратов выраженность признаков воспаления была достаточно большой Признаки воспаления были наиболее выражены после инъекции препарата диклофенака натрия «Диклоген, раствор для инъекций,
75 мг, Змл», произведенного фирмой AGIO (Индия) Наименее опасным с точки зрения проявления неблагоприятного местного действия оказался раствор «Диклофенак, раствор для инъекций, 25 мг/мл, 3 мл», произведенный фирмой Hemofarm (Сербия и Черногория) Все без исключения растворы при подкожном введении вызывали бурную воспалительную реакцию вплоть до формирования некроза
Исследование динамики постинъекционного инфильтрата в ПЖК поросят после подкожной инъекции 1 мл раствора 50% метамизола натрия, произведенного разными производителями, показывают, что процессы рассасывания не имеют достоверных отличий (Рисунок 5)
Рисунок 5 Динамика изменения площади постинъекционного инфильтрата после подкожной инъекции 1 мл раствора 50% натрия метамизола различных производителей 1 — Berlin-Chemie AG (Германия), 2 — Alkaloid (Македония), 3 — Dee-Pharma (Индия)
Далее, нами была изучена динамика возникновения и разрешения постинъекционного инфильтрата, возникающего при введении различных объемов растворов 10% хлорида кальция и 10% глюконата кальция Показано, что подкожное введение растворов 10% хлорида кальция и 10% глюконата кальция во всех случаях вызывает постинъекционное неспецифическое воспаление в месте подкожно-жирового медикаментозного инфильтрата, причем оно возникает вне зависимости от объема введенного раствора Так,
введение 0,1 мл раствора 10% хлорида кальция приводит к формированию обратимого постинъекционного воспаления, которое разрешается полным исчезновением признаков воспалительной реакции к концу первого часа после введения, и не вызывает постинъекционного некроза ПЖК по истечении суток а, введение раствора 10% хлорида кальция в объеме, превышающем 0,1 мл, во всех случаях приводит к образованию постинъекционного воспаления и постинъекционного некроза через 24 часа после введения
Обнаружено, что после инъекции под кожу живота поросенка 0,1 и 0,2 мл раствора 10% глюконата возникает обратимое постинъекционное воспаление, полностью проходящее через 60 минут Введение раствора 10% глюконата кальция в объеме, большем, чем 0,2 мл, образует стойкий инфильтрат, который через сутки трансформируется в некроз
Изучив закономерности местного действия лекарственных средств для инъекций, мы пришли к предположению о том, что лекарственные средства, предназначенные для инъекционного введения (выпускаемые производителями преимущественно в виде растворов для инъекций), могут вызывать нежелательные постинъекционные последствия, прежде всего в ПЖК В частности причиной этому может быть физико-химическое состояние лекарств Так, лекарственные средства могут быть чрезмерно кислыми или чрезмерно щелочными, либо чрезмерно гиперосмотичными Кроме этого они могут обладать денатурирующим действием за счет наличия спиртов или альдегидов
В качестве способа биологической оценки степени безопасности лекарственных средств для биологической ткани нами предложена оценка морфологического состояния эритроцитов через 1-3 минуты взаимодействия порции крови с соизмеримой порцией исследуемого лекарственного средства Для проверки данного предположения нами проведена серия опытов m vitro с донорской кровыо и растворами лекарственных средств
Порция крови взаимодействовала в соотношении 1 1 и при температуре 24°С с порцией растворов следующих качественных лекарственных средств раствор 0,9% натрия хлорида, раствор 50% метамизола натрия, раствор 10% кальция хлорида, раствор 10% кальция глюконата, раствор 2,5% диклогена (AGIO), раствор 2,5% диклофенака натрия (Сотекс, Россия), раствор 2,5% диклофенака натрия (Hemofarm, Сербия и Черногория)
В роли контроля выступало каждый раз морфологическое состояние эритроцитов крови до взаимодействия с лекарством Красные кровяные тельца имели дисковидную форму и их диаметр был равен 7,2±1,3 мк (Р<0,05, п=30), что соответствовало физиологической норме
В результате проведенных исследований установлено, что через 3 минуты взаимодействия равных объемов крови и растворов лекарственных средств эритроциты остались неизмененными только в растворе 0,9% натрия
хлорида В растворах остальных лекарственных средств эритроциты оказались измененными
Через 1 минуту после взаимодействия крови с указанными лекарственными средствами значительные изменения в состоянии эритроцитов крови выявлены после введения ее к раствору 50% анальгина В этом случае выявлен анизоцитоз большей части эритроцитов 88±7,9% (Р<0,05, п=30)), диаметр которых оказался равен 4,2±0,7 мк (Р<0,05, п=30), те уменьшился по сравнению с контрольным в 1,5 раза Изменение формы красных кровяных клеток (пойкилоцитоз) выражалось в появление эхиноцитов — 67±4,8% (Р<0,05, п=30) клеток Одной минуты взаимодействия этого лекарственного средства с кровью оказалось достаточно, чтобы значительная часть эритроцитов изменила свою форму и размер
После 3-х минутного взаимодействия порции крови с анальгином процент анизоцитов повышается до 95±8,1% (Р<0,05, п=30), при этом диаметр эритроцитов уменьшается до 2,8±0,3 мк (Р<0,05, п=30), а количество эхиноцитов достигает 93±8,0% (Р<0,05, п=30)
В дальнейшем были проведены исследования, посвященные изучению взаимодействия порции крови с порцией раствора 2,5% диклогена (AGIO), раствора 2,5% дикпофенака натрия (Сотекс, Россия), раствора 2,5% диклофенака натрия (Hemofarm, Сербия и Черногория) в соотношении 1 1 и при температуре 24°С Однако было установлено, что при смешивании порции крови с любым из вышеперечисленных растворов лекарственных средств, происходило выпадение хлопьев на лабораторных стеклах и разделение фракций крови на белую и красные порции В ряде случаев происходило сворачивание крови на стекле, в связи с чем окрашивание мазков представлялось технически не выполнимым
Таким образом, все исследованные нами лекарственные средства способны вызывать морфологические изменения форменных элементов крови в виде изменения формы и размеров эритроцитов, возникающее уже при 1-х минутном взаимодействии порции крови с любым лекарственным средством, и усиливающиеся при увеличение продолжительности их взаимодействия Выявление этих изменений, а также выявление способности препаратов свертывать кровь может быть использовано в качестве биологического способа оценки постинъекционной безопасности Однако, как показывают полученные результаты, более безопасным и более дешевым способом экспресс-оценки степени агрессивности лекарств может является оценка состояния сырого яичного белка в пробирке после наслаивания на белок исследуемого средства
На основании теоретических, лабораторных и экспериментальных исследований разработаны изобретения «Способ экспресс-оценки степени безопасности лекарственных средств для инъекций» и «Способ биологической оценки степени постинъекционной безопасности лекарственных средств»
Суть первого из них в том, что предварительно определяют период постинъекционного рассасывания в избранной ткани аналогичного объема раствора 0,9% натрия хлорида, затем готовый для инъекции раствор лекарственного средства наслаивают на поверхность свеже приготовленного сырого яичного белка в прозрачной пробирке и на протяжении периода времени постиньекционного рассасывания медикаментозного инфильтрата в избранной ткани визуально в проходящем свете наблюдают за прозрачностью белка на границе сред, а при появлении ободка помутнения белесоватого цвета судят о низкой постинъекционной безопасности лекарственного средства
Суть второго изобретения заключается в том, что исследуемый препарат вводят инъекционно под кожу живота поросенка в объеме, достаточном для создания эффекта «лимонной корочки», засекают время, определяют динамику постинъекционного воспаления кожи и подкожно-жировой клетчатки и при приобретении им необратимого характера и возникновении некротических изменений судят о низкой постинъекционной безопасности препарата и возможности провоцирования им постиньекционного некроза
ВЫВОДЫ
1 Растворы местных анестетиков и нестероидных противовоспалительных средств в процессе инъекции в мягкие ткани имеют температуру в пределах 19-24°С (те являются холодными), величину рН ниже 7,0 (т е являются кислыми) и величину осмотической активности ниже, либо выше 280-300 мОсм/л воды
2 При подкожных и внутримышечных инъекциях растворы лекарственных средств вводятся без учета их температурного режима, осмотической и кислотной активности Состояние постинъекционного медикаментозного инфильтрата не контролируется, а динамика его не учитывается при повторных инъекциях
3 Вода для инъекций, растворы 0,25%, 0,5%, 1% новокаина, 1% и 2% лидокаина гидрохлорида, 0,9% натрия хлорида имеют осмотичность в пределах 0-280 мОсм/л воды, имеют рН ниже 7,0, по не денатурируют сырой яичный белок Подкожные инъекции этих средств вызывают кратковременное обратимое воспаление подкожно-жировой клетчатки
4 Растворы 10% натрия хлорида, 10% кальция глюконата, 10% кальция хлорида, 50% метамизола натрия являются кислыми, поскольку их рН ниже 7,0, пшеросмотичными, поскольку превышают изоосмотический уровень более, чем в 5-10 раз, не денатурируют сырой яичный белок Подкожные инъекции этих средств вызывают постинъекционное воспаление, переходящее в некроз
5 Препараты дикпофенака натрия разных производителей имеют разные составы и разную постинъекционную безопасность Некоторые из них могут
содержать до 24% спиртов и альдегидов, поэтому способны оказывать денатурирующее действие и вызывать постинъекционные некрозы
6 Физико-химическое взаимодействие глюконата кальция с препаратами диклофенака лишает их денатурирующей активности и предотвращает развитие постиньекционного некроза при инъекциях в мягкие ткани Поэтому глюконат кальция может быть использован в роли антидота препаратов диклофенака при ошибочном введении их в подкожно-жировую клетчатку
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1 Для предотвращения постинъекционного некроза при ошибочном введении препаратов диклофенака в подкожно-жировую клетчатку медикаментозный инфильтрат следует обколоть раствором 10% кальция глюконата в объеме 1/3 от введенного объема препарата диклофенака
2 Выявление кольца помутнения прозрачного сырого яичного белка в пробирке в первые несколько минут после наслаивания на него исследуемого препарата свидетельствует о наличии у препарата денатурирующей активности и низкой его постинъекционной безопасности
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ
1 Ураков А Л Место фармакотепловых и фармакохолодовых воздействий в фармакотерапии ряда неотложных патологических состояний / Ураков А Л , Гасников К В , Дионесова Л. С , Галин С В , Бендерская Е Ю // Тезисы докладов 5 Российского национального конгресса «Человек и лекарство» (21-25 апреля 1998 г Москва) М — 1998 — С 222
С , Галин С В , Бендерская Е Ю // Тезисы докладов 5 Российского национального конгресса «Человек и лекарство» (21-25 апреля 1998 г Москва) М — 1998 — С 222
2 Гасников К В О проблемах информационного обеспечения контроля за движением фальсифицированных лекарственных средств в регионе / Гасников К В, Губина С В // Труды ижевской государственной медицинской академии — Том ХЫ — Ижевск Экспертиза — 2003 -С 51-52
3 Гасников К В Роль физико-технических обстоятельств взаимодействия растворов местных анестетиков с тканями при инфильтрационной анестезии / Гасников К В / Сборник статей по материалам 5-го конгресса молодых ученых и специалистов «Науки о человеке» — (Томск 20-21 мая 2004) — Томск -2004 — С 169
4 Тихомирова М Ю Клинические гидродинамические особенности взаимодействия растворов 0,9% натрия хлорида и 0,25% новокаина с биологическими жидкостями на примере ликвора / Тихомирова М Ю, Любимова Н Е, Гасников К В // Состояние и перспективы развития последипломного образования специалистов здравоохранения Сборник статей — Ижевск-2004 — С 310-311
5 Ураков А Л Морфологическая характеристика постиньекционного медикаментозного инфильтрата тканей / Ураков А Л, Садилова П Ю,
Ватулин В В, Уракова H А, Гасяиков К В // Морфологические ведомости — Москва — Берлин — № 3-4 — 2004 — С 64
6 Ураков A JI Физико-химическое состояние ликвора при введении в пего растворов антибиотиков, анисептиков, глюкокортикоидов и местных анестетиков // Ураков A JI, Тихомирова M Ю , Гасников К В / Сборник статей «Состояние и перспективы развития последипломного образования специалистов здравоохранения» Ижевск ООО Мединформсервис -Ижевск, 2004 — С 302-304
7 Гасников К В Семилетний опыт работы с комплексом задач «Формализованная история болезни» / Гасников К В // Сборник статей «Состояние и перспективы развития последипломного образования специалистов здравоохранения» Ижевск ООО Мединформсервис -Ижевск, 2004 — С 247-249
8 Ураков A JI Патологическая роль физико-химических факторов взаимодействия лекарств с соединительной тканью при инъекциях / Ураков А Л , Христофорова О В , Стрелкова Т H , Гасников К В // Тематический научный сборник «Физиология и патология соединительной ткани», посвященный 70-летию со дня основания кафедры биохимии Ижевск Экспертиза — 2004 — С -185-188
9 Гасников К В Роль физико-технических обстоятельств взаимодействия растворов местных анестетиков с тканями при инфильтрационной анестезии / Гасников К В // Сборник статей «Влияние социально-экономических преобразований на здоровье и здравоохранение» Ижевск ООО Мединформсервис -Ижевск — 2005-С 359
10 Ураков АЛ Способ биологической оценки степени постинъекционной безопасности лекарственных средств / Ураков А Л, Стрелков H С, Садилова П Ю , Уракова H А , Гасников К В // Проблемы экспертизы в медицине — № 4 [24] -2006 — Т 6 — С 67-69
Подписано в печать 17 04 2007 Тираж 100 экз Заказ №9-2007 Формат 60×90/16
Отпечатано на предприятии ООО «Мединформсервис» 426076, Удмуртская Республика, г Ижевск, ул Свободы, 139 С оригинал-макета Заказчика
Администрация города БрянкиЛуганской Народной Республики
Постинъекционный абсцесс – это одна из разновидностей абсцессов, возникающая после какого-либо инъекционного введения препаратов. Такой абсцесс после укола, будь то внутримышечная или внутривенная инъекция, проявляется развитием болезненного воспалительного элемента с гнойным содержимым. Основное количество постинъекционных абсцессов возникают при проведении инъекций самостоятельно, в домашних условиях.
Такой абсцесс после укола, будь то внутримышечная или внутривенная инъекция, проявляется развитием болезненного воспалительного элемента с гнойным содержимым. Основное количество постинъекционных абсцессов возникают при проведении инъекций самостоятельно, в домашних условиях.
Причины постинъекционного абсцесса
Главной причиной образования постинъекционного абсцесса, считается игнорирование правил дезинфекции при проведении инъекции. Так, бактерии могут проникнуть в кожу пациента посредством немытых рук, через нестерильные шприцы или вводимый раствор, с плохо обработанных кожных покровов человека, которому проводится процедура. Известны и другие факторы риска, которые могут привести к появлению абсцесса после укола:
•Неправильное введение медикаментозных растворов.
•Продолжительные курсы инъекций, выполняемых на одном и том же участке тела.
•Малый мышечный слой на фоне увеличенной жировой прослойки.
•Повреждение сосуда во время инъекции, когда происходит внутритканевое кровоизлияние с последующим формированием абсцесса после укола.
•Несоблюдение пациентом правил гигиены.
•Дерматиты и другие болезни кожных покровов, особенно в тех местах, где стандартно делают инъекции.
•Сильно ослабленный иммунитет, аутоиммунные патологии, аллергические заболевания.
•Постоянный постельный режим, в результате чего кровь слабо циркулирует.
Сроки возникновения абсцесса: от 2-х дней и более. Чаще всего встречаются постинъекционные абсцессы ягодицы, бедра, реже — на локтевом сгибе, в подлопаточной области и предплечье.
Симптомы развития постинъекционного абсцесса:
•появление болезненного уплотнения в области инъекций;
•боли, вначале несильные и беспокоящие при пальпации и движении, а затем постоянные, интенсивные, пульсирующие;
•припухлость, покраснение кожи над участком уплотнения, а впоследствии – ее синюшность;
•повышение температуры тела;
•общая слабость, потливость.
Если такое случилось, то обращение к врачу должно быть не просто обязательным, но и немедленным: правильно выполненная инъекция не должна иметь описанной выше реакции.
При любом варианте абсцесса после укола проводится немедленное хирургическое вскрытие воспаленного очага. Только при хирургическом вмешательстве возможно полностью удалить гнойную капсулу и залечить рану до полного очищения. После операции вскрытия абсцесса назначается антибактериальное лечение.
Осложнения и последствия постинъекционных абсцессов
Если гнойный процесс не лечить, либо лечить неправильно, то количество гноя в капсуле может достичь такого уровня, когда её стенки не выдерживают и прорываются. Гнойное содержимое попадает в близкорасположенные ткани: образуется обширное флегмонозное воспаление, которое со временем может осложниться появлением свищей и перфораций.
В запущенных ситуациях может развиваться септическое поражение – генерализованное инфекционное заболевание, вызванное попаданием бактерий из локализованного очага в общий кровоток. Другое общепринятое название сепсиса – это заражение крови, считающееся тяжелой патологией. Также попадание патогенной флоры в систему кровообращения может обернуться развитием остеомиелита, при котором наблюдаются гнойно-некротические процессы в костной ткани, костном мозге и рядом расположенных мягких тканях.
Профилактика
В качестве профилактических мер следует использовать такие правила:
•для проведения инъекций следует использовать только одноразовые шприцы и иглы;
•при частых инъекциях необходимо менять место введения препаратов;
•нельзя вводить инъекционный раствор, предназначенный для внутривенного или подкожного вливания, для внутримышечной инъекции;
•нельзя вводить препарат, который заведомо не стерилен, либо негоден, либо содержит посторонние примеси или осадок;
•непосредственно перед введением препарата следует провести обеззараживание кожи в месте инъекции 700 спиртом;
•во время проведения инъекции нельзя прикасаться к игле пальцами, даже если они обработаны дезинфицирующей жидкостью;
•после введения лекарства, необходимо спиртовым ватным тампоном помассировать место укола, для лучшего распространения и всасывания лекарства в мышечную систему организма;
•после проведения инъекции, следить за местом укола несколько дней. Если вокруг него образовалось уплотнение, это свидетельствует о начале воспалительного процесса;
•нельзя проводить инъекцию, если накануне на этом месте образовалось внутритканевое кровоизлияние;
•нельзя смешивать в одном шприце несколько препаратов, если нет уверенности в том, что они являются фармакологически и химически совместимыми;
•внутримышечное и подкожное введение препаратов не должно быть резким, чтобы лекарство могло постепенно распределиться в тканях.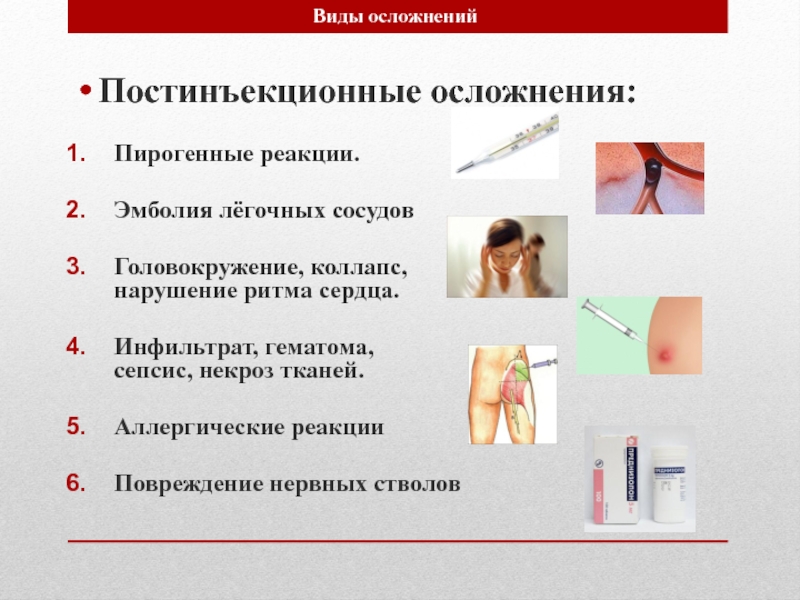
Не занимайтесь самолечением! Инъекции следует проводить в асептических условиях, со строгим соблюдением всех правил дезинфекции и гигиены.
Инфильтрат. Словарь терминов лучевой диагностики
Главная
глоссарий
Инфильтрат
Инфильтрат — это межклеточное скопление жидкости с примесями клеточных компонентов, лимфы, крови, приводящее к увеличению объема и уплотнению ткани на данном участке (по аналогии с губкой, пропитанной жидкостью).
Инфильтратам предшествует воспаление инфекционной природы или опухолевый процесс. В первом случае причиной могут быть вирусы, бактерии, грибки, поражающие органы и ткани. Если к воспалительному очагу присоединяется инфекция, возможно нагноение с последующим образованием абсцесса, флегмоны, рубца (в процессе заживления).
Опухолевые инфильтраты возникают при инвазивном росте новообразования, когда клетки новообразования начинают разрушать и замещать здоровые ткани. На КТ инфильтраты визуализируются как локальные уплотнения, имеющие более светлый цвет по сравнению с окружающими тканями.
На КТ инфильтраты визуализируются как локальные уплотнения, имеющие более светлый цвет по сравнению с окружающими тканями.
Легочный инфильтрат — скопление жидкости (экссудата) в легочной паренхиме. В норме альвеолярные пузырьки заполнены воздухом, благодаря этому человек может дышать. Участки легких с инфильтратами теряют функциональные свойства и отекают, в этой связи врачи говорят о поражении легких (например, при пневмонии). Причиной легочного инфильтрата может быть бактериальная, грибковая или вирусная инфекция, паразитическое заболевание, аллергия, развитие опухоли.
Послеоперационный инфильтрат — осложнение хирургического вмешательства, которое возникает из-за инфекции на травмированном участке. «Спусковым механизмом» может быть ослабленный иммунитет пациента, который не может сопротивляться инфекциям в послеоперационном периоде. Неглубокий послеоперационный инфильтрат может проявляться как пальпируемое уплотнение, покраснение и нагноение кожи.
Постинъекционный инфильтрат — осложнение после подкожных или внутримышечных инъекций, спровоцированное нарушением правил асептики и медицинской техники проведения уколов. Проявляется болью, покраснением кожи, повышенной температурой.
Аппендикулярный инфильтрат — воспаление, вызванное сращением аппендикса со слепой, тонкой кишкой или сальником. Наблюдается при аппендиците на 2-4 день заболевания. Вызывает острую боль, повышение температуры тела, нагноение.
Что делать, если у ребенка припухло бедро после прививки
16/10/2020
Ребенку сделали прививку от дифтерии, столбняка и коклюша в бедро. Вдруг через некоторое время появилась припухлость в месте укола. Конечно же, любые отклонения от нормы вызывают беспокойство, и вы идете к врачу. Врач успокаивает и говорит, что это пройдет, это такая реакция на прививку АКДС. Она возможна и описана в инструкции как допустимая постпрививочная реакция. Вы успокаиваетесь и ждете какое-то время, но что-то лучше не становится и как-то покраснело, затвердело то место на бедре, куда была введена прививка. Беспокойство побуждает вас пойти к хирургу.
Она возможна и описана в инструкции как допустимая постпрививочная реакция. Вы успокаиваетесь и ждете какое-то время, но что-то лучше не становится и как-то покраснело, затвердело то место на бедре, куда была введена прививка. Беспокойство побуждает вас пойти к хирургу.
Давайте поговорим о постпрививочном и постинъекционном инфильтрате. Что же думают практические врачи на эту тему?
Педиатры порой встречаются с местной реакцией на прививку именно на бедре, потому что прививки малышам от дифтерии, коклюша и столбняка делают именно в наружную поверхность бедра. На бедре после прививки у некоторых детей появляется припухлость, и размер этой припухлости может быть различным — от нескольких сантиметров до отека большей части боковой поверхности бедра. При этом малыш нормально себя ведет и место припухлости не болит.
Через какое-то время отечность проходит бесследно, или может сохраняться небольшое уплотнение в месте укола, которое ощущается как шишечка при прощупывании. Но и эта шишечка через какое-то время исчезнет. Вот именно такой сценарий благоприятен. Такая реакция происходит за счет местного иммунного ответа тканей на вакцину. Это постпрививочный небактериальный инфильтрат. Он не требует лечения — ни общего, ни местного.
Вот именно такой сценарий благоприятен. Такая реакция происходит за счет местного иммунного ответа тканей на вакцину. Это постпрививочный небактериальный инфильтрат. Он не требует лечения — ни общего, ни местного.
Но вот другой вариант развития событий. Отек и затвердевание тканей в месте укола нарастают, и нет тенденции к их исчезновению даже спустя 7—10 дней. Здесь есть опасения, что безобидный постпрививочный инфильтрат может перейти в постинъекционный инфильтрат, который проходит несколько стадий развития — от катаральной до гнойной. В таких случаях надо вместе с врачом держать ситуацию под контролем. Здесь помогает ультразвуковое исследование мягких тканей и врачебное наблюдение в динамике. Только визуальный осмотр и данные УЗИ мягких тканей в помощь врачу помогут выбрать тактику лечения. Выбор стоит между консервативным лечением мазями или хирургическим лечением. Выжидательная тактика врача оправдана в том случае, если у ребенка нет болезненности и выделений в месте инъекции.
Лечение инфильтрации и экстравазации
Что такое периферийное устройство для внутривенных вливаний?
Периферический внутривенный катетер — это катетер (очень тонкая гибкая трубка), который вводится в небольшую вену на коже черепа, кисти, руки, ноги или ступни. Это делается для того, чтобы жидкости или лекарства попадали прямо в кровоток. IV фиксируется лентой или повязкой.
Что такое инфильтрация или экстравазация?
Иногда жидкость или лекарство просачиваются в ткани вокруг вены.Разница между инфильтрацией и экстравазией заключается в типе вытекшего лекарства или жидкости.
- Инфильтрация — если жидкость не содержит пузырьков (не раздражает ткани), это называется инфильтрацией.
- Экстравазация — если жидкость представляет собой везикант (жидкость, которая раздражает ткани), это называется экстравазацией. Повреждение тканей из-за этих жидкостей может быть замечено или не замечено во время утечки, и для его развития могут потребоваться недели или месяцы.

Как это происходит?
- Катетеры могут со временем забиваться
- Катетеры могут неожиданно выйти
- Внутривенные жидкости могут вытекать из вены или артерии из-за раздражения
Каковы признаки инфильтрации / экстравазации?
- Покраснение вокруг узла
- Отек, отечность или твердая кожа вокруг пораженного участка
- Побледнение (более светлая кожа вокруг IV участка)
- Боль или нежность вокруг узла
- IV не работает
- Охлаждение температуры кожи вокруг места внутривенного вливания или на коже черепа, кисти, руки, ноги или ступни рядом с местом
Что происходит после инфильтрации / экстравазации?
- Будет проведена экспертиза участка
- В зависимости от степени тяжести можно проконсультироваться с дополнительными членами медицинской бригады (например, с фармацевтом или медсестрой, специализирующейся на уходе за кожей) для обсуждения вариантов лечения.

- IV будет удален
- Сайт будет проверяться ежечасно, пока не вернется к исходному состоянию
Как лечится?
Некоторые возможные методы лечения:
- Максимально приподнимите участок, чтобы уменьшить отек.
- Применяйте теплый или холодный компресс (в зависимости от жидкости) на 30 минут каждые 2-3 часа, чтобы уменьшить отек и дискомфорт.
- Лекарство — Если рекомендовано, лекарство от экстравазации вводится в течение 24 часов для достижения наилучшего эффекта.
Самым распространенным лекарством является гиалуронидаза (Wydase®), которое вводится в небольших количествах непосредственно под кожу.
Что я могу сделать, чтобы предотвратить инфильтрацию / экстравазацию?
- Сообщите медицинским работникам вашего ребенка, если у вашего ребенка в прошлом было несколько попыток поставить капельницу.
- Если повязка для внутривенного вливания ослабла, сообщите об этом медсестре, чтобы ее можно было заменить или укрепить соответствующим образом.

- Будьте осторожны при перемещении ребенка, чтобы не дать ему ударить, потянуть или сдвинуть капельницу.
- Не позволяйте ребенку натягивать капельницу. Используйте отвлечение, чтобы отвлечь ребенка от этого. Спросите у Child Life, чем может заниматься ваш ребенок.
- Если иммобилайзер или мягкая стяжка необходимы для защиты места внутривенного вливания, оставьте его включенным.
- Не допускайте попадания постельных принадлежностей в место внутривенного вливания.
- Если вас беспокоит, что капельница не работает или выглядит иначе, сообщите об этом медсестре.
Что еще мне нужно знать?
В зависимости от тяжести инфильтрации / экстравазации вам может быть рекомендовано контролировать пораженный участок после выписки.
Позвоните в свою клинику, если состояние пораженного участка ухудшается, например:
- Повышенный отек
- Вздутие
- Открытие кожи
Немедленно обратитесь в отделение неотложной помощи, если у вашего ребенка есть одно из следующего:
- Температура выше 101.
 5 ° F
5 ° F - Рука, рука, нога или ступня рядом с удаленным местом внутривенного введения меняют цвет (сине-фиолетовый).
- Рука, рука, нога или ступня рядом с удаленным местом внутривенного вливания меняют температуру (становится холодно).
- Рука, рука, нога или ступня рядом с удаленным местом внутривенного вливания опухает и становится твердой, и пальцы рук и ног не могут двигаться.
Дополнительные ресурсы
Группа практиков по уходу за детской стомой — это группа медсестер, которые могут помочь с проникновением и экстравазией.Они доступны в рабочее время для последующих амбулаторных посещений. Назначения можно записать по телефону 651-220-6530.
Вопросы?
Эта информация не относится к вашему ребенку, но дает общую информацию. Если у вас есть вопросы, позвоните своему врачу или в клинику.
Последний отзыв 7/2019
Вернуться к началу
Инфильтрация малых суставов: альтернативное лечение боли в руках и ногах — | Центр обезболивания
- Escrito por Pain Relief
- Категория: Блог
- Creado: 03 Abril 2019
- Visto: 3260
Инфильтрация малых суставов: альтернативное лечение боли в руках и ногах
- Инъекции в суставы, сумки, оболочки сухожилий и мягкие ткани человеческого тела — полезная диагностическая и терапевтическая процедура.

- Эти инъекции наиболее полезны в случаях повреждения суставов или тканей и воспалений.
- Боль в суставах может быть просто болезненной (артралгия) или воспаленной (артрит)
- Существует более 100 различных типов артрита
Боль в мелких суставах может повлиять на любой сустав, особенно если пациент страдает воспалительными состояниями, такими как ревматоидный артрит, или любыми другими широко известными заболеваниями соединительной ткани.Артрит — это воспаление суставов. Это может повлиять на один или несколько суставов. Существует более 100 различных типов артритов с разными причинами и методами лечения. Двумя наиболее распространенными типами являются остеоартрит (ОА) и ревматоидный артрит (РА).
Обширный практический опыт подтверждает эффективность инъекций в суставы и мягкие ткани для решения многих распространенных проблем. Большинство воспалительных состояний можно вылечить с помощью инфильтрации изображений под рентгеноскопическим контролем.
Большинство воспалительных состояний можно вылечить с помощью инфильтрации изображений под рентгеноскопическим контролем.
Когда воспаление поражает руку или пальцы, пациент может жаловаться на следующее:
* Воспаление мелких суставов обычно сопровождается теплом, отеком (вызванным внутрисуставной жидкостью или инфузией) и редко — эритемой. Боль может возникать при движении или в покое.
* Краска пальцами в основном на мизинцах пальцев, боль в руке, отечность и скованность.
* Мелкие суставы кисти и пальцев могут быть теплыми и нежными на ощупь
* Покраснение кожи вокруг сустава
* Диапазон движений может быть уменьшен
* Суставы пальцев или суставы рук могут быть деформированы .
* Усталость
* Симптомы канала запястья, такие как онемение, покалывание и жжение в руках.
* Боль при пробуждении или по утрам с ригидностью, которая сохраняется в течение длительного времени. Многие люди с артритом замечают, что их симптомы усиливаются утром
Как диагностируется артрит?
- Физикальное обследование необходимо при любой оценке боли в небольших суставах.

- Ваш врач обычно проверяет кожу вокруг суставов, теплые или красные суставы и ограниченный диапазон эмоций суставов.
- При необходимости врач может направить вас к специалисту.
- Анализ крови проводится для оценки элементов, связанных с воспалением, вместе с исследованием общей жидкости, что помогает в определении вашего артрита.
- Анализы крови проверяют наличие определенных типов антител, таких как ревматоидный фактор (RF), антинуклеарные антитела (ANA).
- Визуализирующие исследования являются частью начальной оценки и обычно включают рентген, МРТ, компьютерную томографию.
Показания к диагностическим и терапевтическим инъекциям
- Состояние мягких тканей
- Бурсит
- Тендинит или тендиноз
- Триггерные точки
- Ганглиозные кисты
- Невромы
- Захват суставов
- Поражение суставов состояния
- Вытекание неизвестного происхождения или подозрение на инфекцию (только диагностическое)
- Кристаллоидные артропатии
- Синовит
- Воспалительный артрит
- Продвинутый остеоартрит
Эти инъекции наиболее полезны в случаях повреждения и воспаления суставов или тканей.
Анамнез боли, местной и направленной, даст важные ключи к пониманию основной патологии.
Показания к аспирации и инъекции суставов или мягких тканей делятся на две категории: диагностические и терапевтические. Обычным диагностическим показанием для введения иглы в сустав является аспирация синовиальной жидкости для оценки. Оценка синовиальной жидкости позволяет дифференцировать различные этиологии заболеваний суставов, включая инфекции, воспаления и травмы. Второе диагностическое показание включает инъекцию местного анестетика для подтверждения предполагаемого диагноза путем облегчения симптомов пораженной части тела.
Терапевтические показания для аспирации и инъекции суставов или мягких тканей включают уменьшение подвижности и боли, а также инъекции лекарств в качестве терапевтического дополнения к другим формам лечения. Следует соблюдать осторожность при удалении жидкости для снятия боли из-за возможности занести инфекцию и вызвать дальнейшее или новое кровотечение в сустав. Кроме того, во многих случаях может произойти раннее повторное накопление жидкости.
Кроме того, во многих случаях может произойти раннее повторное накопление жидкости.
Терапевтические инъекции кортикостероидов всегда следует рассматривать как адъювантную терапию.Неправильное или неизбирательное применение кортикостероидов может иметь плохой исход. Эти инъекции никогда не должны выполняться без диагностического определения и конкретного плана лечения. Врачи должны сопротивляться внешнему давлению для быстрого возвращения спортсменов к занятиям спортом с помощью инъекций в суставы или мягких тканей.
Возможные осложнения
Использование
процедур для суставов и мягких тканей может привести к ряду потенциальных осложнений.Местное заражение всегда возможно, но этого можно избежать, соблюдая соответствующую технику. Инъекции в суставы всегда следует выполнять с использованием стерильной процедуры
для предотвращения септического артрита. Местные реакции в месте инъекции могут включать отек, болезненность и тепло, которые могут развиваться через несколько часов после инъекции и могут длиться до двух дней.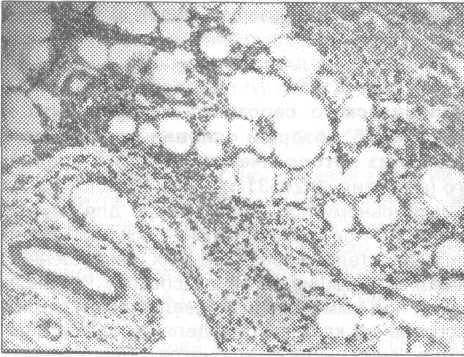 Обострение стероидов после инъекции, которое считается индуцированным кристаллами синовитом, вызванным консервантами в суспензии для инъекций, может возникнуть в течение первых 24–36 часов после инъекции
Обострение стероидов после инъекции, которое считается индуцированным кристаллами синовитом, вызванным консервантами в суспензии для инъекций, может возникнуть в течение первых 24–36 часов после инъекции
.Этот
является самоограничивающимся и реагирует на прикладывание пакетов со льдом не более чем с 15-минутными интервалами.
Атрофия мягких тканей (жира) и местная депигментация возможны при любой инъекции стероидов в мягкие ткани, особенно в поверхностные участки (например, латеральный надмыщелок). Околосуставные кальцификаты описаны в литературе, но встречаются редко. Разрыва сухожилия можно избежать, если не вводить инъекцию непосредственно в само сухожилие.
Возможны системные эффекты (особенно после инъекции триамцинолона ацетонида [Аристокорта] или инъекции в вену или артерию), и пациенты всегда должны находиться под пристальным наблюдением реакции.Сообщалось об изменении вкуса в течение одного-двух дней после инъекции стероидов. Возможна гипергликемия у больных сахарным диабетом.
Чтобы избежать прямого повреждения иглой суставного хряща или местных нервов, следует обращать внимание на анатомические ориентиры и глубину инъекции.
Инструкции и уход после инъекции
На место инъекции следует наложить липкую повязку. Чтобы свести к минимуму боль и воспаление после выхода из офиса, пациенту следует посоветовать прикладывать лед к месту инъекции (не более чем на 15 минут за раз, один или два раза в час), и могут быть приняты нестероидные противовоспалительные используется, особенно в течение первых 24-48 часов.Пораженный участок должен находиться в покое от физических нагрузок в течение нескольких дней после инъекции из-за небольшой вероятности локальных разрывов тканей вследствие временно высоких концентраций стероида. Этот риск уменьшается по мере того, как стероид рассеивается. Пациентов следует научить искать признаки инфекции, включая эритему, тепло или припухлость в месте инъекции, или системные признаки, включая лихорадку и озноб. Пациент должен содержать в чистоте место инъекции и может принимать ванну.
Пациент должен содержать в чистоте место инъекции и может принимать ванну.
Заключение
Обширный практический опыт подтверждает эффективность инъекций в суставы и мягкие ткани для решения многих распространенных проблем.
Эти инъекции наиболее полезны при повреждениях и воспалениях суставов или тканей. История боли, местной и направленной, даст важные ключи к разгадке основной патологии. Медицинский осмотр чрезвычайно помогает в установлении диагноза. Знание анатомии области инъекции имеет важное значение. Инъекции в суставы, сумки, оболочки сухожилий и мягкие ткани человеческого тела — полезная диагностическая и терапевтическая процедура.
https: // www.youtube.com/watch?v=RdpaPYpQlTA
Хроническая боль в брюшной стенке и инфильтрация кожных нервов брюшной полости под контролем УЗИ: серия клинических случаев | Медицина боли
Абстрактные
Справочная информация..jpg) Хроническая боль в брюшной стенке встречается примерно у 10–30% пациентов с хронической болью в животе. Ущемление кожных нервов брюшной полости на боковой границе прямой мышцы живота считается причиной боли в брюшной стенке.Мы сообщаем о нашем опыте лечения таких пациентов с использованием инфильтрации кожных нервов брюшной полости под контролем УЗИ.
Хроническая боль в брюшной стенке встречается примерно у 10–30% пациентов с хронической болью в животе. Ущемление кожных нервов брюшной полости на боковой границе прямой мышцы живота считается причиной боли в брюшной стенке.Мы сообщаем о нашем опыте лечения таких пациентов с использованием инфильтрации кожных нервов брюшной полости под контролем УЗИ.
Методы. Мы провели ретроспективный аудит инфильтрации кожных нервов живота, проведенный в период с сентября 2008 г. по август 2009 г. в нашем центре. Все пациенты получили инъекции местного анестетика и стероидов под контролем УЗИ. Реакция на инфильтрацию оценивалась при телефонном разговоре после процедуры, а также в клинике последующего наблюдения.Краткая инвентаризация боли (BPI) и оценка боли по числовой шкале были сопоставлены по двум точкам: первичная амбулаторная клиника и последующая клиника в течение 5 месяцев после инъекции.
Результаты. Девять пациентов получили инъекции кожных нервов живота под контролем УЗИ за рассматриваемый период. Шесть пациентов сообщили об уменьшении боли на 50% или более (ответившие), а три пациента — нет. Показатели боли и BPI показали тенденцию к снижению у респондентов. Средняя продолжительность наблюдения составила 12 недель.
Шесть пациентов сообщили об уменьшении боли на 50% или более (ответившие), а три пациента — нет. Показатели боли и BPI показали тенденцию к снижению у респондентов. Средняя продолжительность наблюдения составила 12 недель.
Заключение. Ультразвук можно надежно использовать для инфильтрации кожных нервов живота. Это повысит безопасность, а также диагностическую полезность процедуры.
Введение
Хроническая боль в брюшной стенке встречается примерно у 10–30% пациентов с хронической болью в животе [1,2]. В литературе обсуждались различные причины, такие как миофасциальная боль, грудная радикулопатия, поражения брюшной стенки, включая защемление нерва, и отраженная боль, вторичная по причине конвергенции нервов из брюшных или грудных внутренних органов.Из них хорошо известна синдром защемления кожного нерва живота (АКНЕ). Эпплгейт отчетливо объяснил это в 1972 г. ущемлением кожной ветви торакоабдоминальных межреберных нервов у латеральной границы прямой мышцы живота [3]. Carnett в 1926 году описал это клиническое состояние как межреберную невралгию [4]. Предварительно это состояние диагностируется по локализации боли в животе при пальпации и положительному результату теста Карнетта (усиление или отсутствие уменьшения боли при сокращении мышц живота при пальпации).Облегчение боли инъекцией 1-2 мл местного анестетика в точке максимальной болезненности, депонированной в передней фасции прямой мышцы живота, считается подтверждением диагноза [5]. Эти инъекции обычно проводятся вслепую с переменным успехом. Ультразвук идеально подходит для повышения точности этих инъекций. Мы сообщаем о нашем опыте инфильтрации передней кожной ветви торакоабдоминальных межреберных нервов с использованием ультразвукового контроля.
Carnett в 1926 году описал это клиническое состояние как межреберную невралгию [4]. Предварительно это состояние диагностируется по локализации боли в животе при пальпации и положительному результату теста Карнетта (усиление или отсутствие уменьшения боли при сокращении мышц живота при пальпации).Облегчение боли инъекцией 1-2 мл местного анестетика в точке максимальной болезненности, депонированной в передней фасции прямой мышцы живота, считается подтверждением диагноза [5]. Эти инъекции обычно проводятся вслепую с переменным успехом. Ультразвук идеально подходит для повышения точности этих инъекций. Мы сообщаем о нашем опыте инфильтрации передней кожной ветви торакоабдоминальных межреберных нервов с использованием ультразвукового контроля.
Анатомия и патофизиология
Торакоабдоминальные (Т8–12) межреберные нервы проходят в плоскости мышц между внутренней косой и поперечной мышцами живота, достигая латеральной границы прямой мышцы живота, где они поворачиваются на 90 градусов, чтобы войти в канал прямой мышцы живота. Нерв и его сосуды образуют отдельный пучок и пересекают канал прямой мышцы живота, продолжая действовать как передние кожные нервы брюшной полости (рис. 1). Таких каналов по пять с каждой стороны латеральной границы прямой мышцы живота [6]. Нервы, выходящие из этих отверстий, можно увидеть при ультразвуковом исследовании (рис. 2).
Нерв и его сосуды образуют отдельный пучок и пересекают канал прямой мышцы живота, продолжая действовать как передние кожные нервы брюшной полости (рис. 1). Таких каналов по пять с каждой стороны латеральной границы прямой мышцы живота [6]. Нервы, выходящие из этих отверстий, можно увидеть при ультразвуковом исследовании (рис. 2).
Рисунок 1
Схематическое изображение кожного нерва живота в канале прямой мышцы живота.
Рисунок 1
Схематическое изображение кожного нерва живота в канале прямой мышцы живота.
Рисунок 2
Ультрасонографическое изображение кожного нерва брюшной полости в пределах прямой мышцы.
Рисунок 2
Ультрасонографическое изображение кожного нерва брюшной полости в пределах прямой мышцы.
Копелл и Томпсон постулировали, что защемление периферического нерва происходит на анатомических участках, где нерв меняет направление, чтобы войти в фиброзный или костно-фиброзный туннель, или где нерв проходит по фиброзной или мышечной связке. В этих местах наиболее вероятно возникновение механически вызванного раздражения, вызывающего защемление [7].Эпплгейт предположил, что ишемия нерва может быть вызвана локальным сдавлением нерва на уровне кольца из-за наложения мягкого пучка на твердое кольцо [8]. Сокращение мышц на этих участках может вызвать дополнительное повреждение за счет прямого сжатия, хотя также вероятно натяжение нерва из-за мышечной активности.
В этих местах наиболее вероятно возникновение механически вызванного раздражения, вызывающего защемление [7].Эпплгейт предположил, что ишемия нерва может быть вызвана локальным сдавлением нерва на уровне кольца из-за наложения мягкого пучка на твердое кольцо [8]. Сокращение мышц на этих участках может вызвать дополнительное повреждение за счет прямого сжатия, хотя также вероятно натяжение нерва из-за мышечной активности.
Техническое описание
Пациента помещают в положение лежа на спине и просят сократить прямую мышцу, подняв голову или обе ноги вместе.Мы определили и отметили точку максимальной чувствительности на латеральной границе прямой мышцы живота. Использовали высокочастотный (10–15 МГц) 38-миллиметровый широкополосный линейный преобразователь системы MicroMaxx от SonoSite® Inc. (Ботелл, Вашингтон, США) ультразвуковой сканер.
Мы расположили датчик по средней линии, чтобы получить вид по короткой оси (анатомическое поперечное положение), чтобы визуализировать медиальную границу прямой мышцы и белую линию. Прямая мышца может быть идентифицирована как гипоэхогенная область, содержащаяся в гиперэхогенной фасции прямой мышцы живота.Глубина сканирования регулируется таким образом, чтобы просматривалась вся прямая мышца. Датчик перемещается в боковом направлении, чтобы получить вид на боковой конец прямой мышцы и полулунную линию. И белая линия, и полулунная выглядят как гиперэхогенные полосы. Примерно на 0,5–1,0 см медиальнее полулунной линии брюшной кожный нерв можно увидеть как «гиперэхогенную точку» в мышечной массе. Обычно это соответствует максимальной точке нежности, отмеченной ранее. Для оптимального обзора нерва может потребоваться цефало-каудальное движение и наклон датчика.При соблюдении правил асептики 22G 1,5 дюйма. длинная спинномозговая игла BD (Becton, Dickinson and Co., Франклин-Лейкс, Нью-Джерси, США) продвигается по продольной оси датчика к целевой области. Это позволяет визуализировать ход иглы. Для выявления распространения раствора вокруг нерва проводится пробная инъекция 0,5 мл.
Прямая мышца может быть идентифицирована как гипоэхогенная область, содержащаяся в гиперэхогенной фасции прямой мышцы живота.Глубина сканирования регулируется таким образом, чтобы просматривалась вся прямая мышца. Датчик перемещается в боковом направлении, чтобы получить вид на боковой конец прямой мышцы и полулунную линию. И белая линия, и полулунная выглядят как гиперэхогенные полосы. Примерно на 0,5–1,0 см медиальнее полулунной линии брюшной кожный нерв можно увидеть как «гиперэхогенную точку» в мышечной массе. Обычно это соответствует максимальной точке нежности, отмеченной ранее. Для оптимального обзора нерва может потребоваться цефало-каудальное движение и наклон датчика.При соблюдении правил асептики 22G 1,5 дюйма. длинная спинномозговая игла BD (Becton, Dickinson and Co., Франклин-Лейкс, Нью-Джерси, США) продвигается по продольной оси датчика к целевой области. Это позволяет визуализировать ход иглы. Для выявления распространения раствора вокруг нерва проводится пробная инъекция 0,5 мл. При необходимости игла регулируется более тонко, чтобы оптимизировать распространение раствора. Мы использовали объемы до 3 мл, чтобы обеспечить равномерное вертикальное распределение инъекционной жидкости в мышечной массе.Вводимый раствор должен выглядеть как увеличивающаяся гипоэхогенная область (рис. 3).
При необходимости игла регулируется более тонко, чтобы оптимизировать распространение раствора. Мы использовали объемы до 3 мл, чтобы обеспечить равномерное вертикальное распределение инъекционной жидкости в мышечной массе.Вводимый раствор должен выглядеть как увеличивающаяся гипоэхогенная область (рис. 3).
Рисунок 3
Ультрасонографический снимок хода иглы и распространения инъекционной жидкости вокруг кожного нерва живота.
Рис. 3
Ультрасонографический снимок хода иглы и распределения инъекционной жидкости вокруг кожного нерва живота.
Методы
Мы провели ретроспективный аудит последовательных инъекций кожных нервов живота, выполненных в период с сентября 2008 года по август 2009 года в нашем центре.Эти пациенты были первоначально осмотрены в клинике хронической боли, где предварительный диагноз АКНЕ был поставлен после положительного знака Карнетта и соответствующей точки максимальной чувствительности кожных нервов живота. Пациенты были включены в список пациентов с инфильтрацией кожных нервов живота под контролем УЗИ. Пациенты заполнили краткую шкалу оценки боли (BPI) при посещении клиники и прошли двухнедельный телефонный осмотр после процедуры в рамках нашей повседневной практики.
Пациенты были включены в список пациентов с инфильтрацией кожных нервов живота под контролем УЗИ. Пациенты заполнили краткую шкалу оценки боли (BPI) при посещении клиники и прошли двухнедельный телефонный осмотр после процедуры в рамках нашей повседневной практики.
Ответ на инъекцию и общее впечатление пациента о шкале изменений были получены из телефонных обзоров клиник.Оценки боли (11-балльная числовая рейтинговая шкала) и баллы вмешательства были сопоставлены с диаграммами BPI в двух временных точках: первоначальный амбулаторный визит в клинику и последующий визит в клинику в течение 5 месяцев после инъекции. Процентное облегчение, о котором сообщили пациенты, было зарегистрировано при телефонном разговоре после процедуры и в клинике последующего наблюдения. Один пациент получил более одной инъекции в разные моменты времени. В этом случае оценка боли регистрируется после последней инъекции.
Результаты
В течение годичного периода аудита девяти пациентам были выполнены инъекции кожных нервов живота под контролем УЗИ. В таблице 1 приведены характеристики пациента, а также место, сторона и количество инъекций. Шесть пациентов сообщили об уменьшении боли на 50% или более и, таким образом, ответили на лечение, а три пациента сообщили об уменьшении боли (не ответили). Одному из респондентов потребовалось две инъекции для достижения более чем 50% облегчения боли в телефонной клинике. Средний процент облегчения боли составил 60% при телефонном разговоре после процедуры. Из шести респондентов у четырех пациентов наблюдалось постоянное уменьшение боли на 50% или более, у одного наблюдалось постоянное облегчение боли на 20%, а другой был потерян для последующего наблюдения.Средняя продолжительность наблюдения составила 12 недель (от 11 до 20 недель). Хотя показатели боли и BPI показали тенденцию к снижению в клинике последующего наблюдения, статистической разницы до и после лечения не было. Результаты телефонного разговора и последующих действий также сведены в таблицу (Таблицы 2 и 3).
В таблице 1 приведены характеристики пациента, а также место, сторона и количество инъекций. Шесть пациентов сообщили об уменьшении боли на 50% или более и, таким образом, ответили на лечение, а три пациента сообщили об уменьшении боли (не ответили). Одному из респондентов потребовалось две инъекции для достижения более чем 50% облегчения боли в телефонной клинике. Средний процент облегчения боли составил 60% при телефонном разговоре после процедуры. Из шести респондентов у четырех пациентов наблюдалось постоянное уменьшение боли на 50% или более, у одного наблюдалось постоянное облегчение боли на 20%, а другой был потерян для последующего наблюдения.Средняя продолжительность наблюдения составила 12 недель (от 11 до 20 недель). Хотя показатели боли и BPI показали тенденцию к снижению в клинике последующего наблюдения, статистической разницы до и после лечения не было. Результаты телефонного разговора и последующих действий также сведены в таблицу (Таблицы 2 и 3).
Таблица 1
Сведения о пациенте и инъекции
| Случай | Пол | Возраст | Продолжительность симптомов (лет) | Сторона | Участок | Количество инъекций | Введенный объем | |||||||||||||
| 1 | Внутренний | 52 | 5 | Правый | T8 и T9 | 2 | 3 | 0. 5% l-бупивакаин и триамцинолон 40 мг 5% l-бупивакаин и триамцинолон 40 мг | ||||||||||||
| 2 | Женский | 34 | 2 | правый | T8 и T11 | 1 | 4 | 0,5% l-bupamivacaine | ||||||||||||
| 3 | Мужской | 73 | 1 | Правый | T11 | 1 | 2 | 0,5% l-бупивакаин и триамцинолон 40 мг | 904 | |||||||||||
| 904 | Левый | T9 | 1 | 2 | 0.5% л-бупивакаин и триамцинолон 40 мг | |||||||||||||||
| 5 | Женский | 54 | 1 | Правый | T8, 9, 10 | 1 | 9 | 9 | 0,5% l277 | 6 | Женский | 45 | 4 | Левый | T11 | 1 | 3 | 0,5% l-бупивакаин и триамцинолон 40 мг | ||
| 7 4410 | Мужской Правый | T10 | 1 | 3 | 0. 5% l-бупивакаин и триамцинолон 40 мг 5% l-бупивакаин и триамцинолон 40 мг | |||||||||||||||
| 8 | Женский | 23 | 4 | Левый | T8 и T9 | 1 | 3 | 0,5% l-bupamivacaine | 0,5% l-буп | |||||||||||
| 9 | Женский | 80 | 1 | Левый | T11 | 1 | 3 | 0,5% l-бупивакаин и триамцинолон 40 мг Возраст |
Таблица для инъекций6 | Случай | Пол | Возраст | Продолжительность симптомов (лет) | Сторона | Участок | Количество инъекций | Введенный объем | Введенный наркотик | Женщина 5 | Правый | T8 и T9 | 2 | 3 | 0. 5% l-бупивакаин и триамцинолон 40 мг 5% l-бупивакаин и триамцинолон 40 мг |
| 2 | Женский | 34 | 2 | правый | T8 и T11 | 1 | 4 | 0,5% l-bupamivacaine | ||||||||||||
| 3 | Мужской | 73 | 1 | Правый | T11 | 1 | 2 | 0,5% l-бупивакаин и триамцинолон 40 мг | 904 | |||||||||||
| 904 | Левый | T9 | 1 | 2 | 0.5% л-бупивакаин и триамцинолон 40 мг | |||||||||||||||
| 5 | Женский | 54 | 1 | Правый | T8, 9, 10 | 1 | 9 | 9 | 0,5% l277 | 6 | Женский | 45 | 4 | Левый | T11 | 1 | 3 | 0,5% l-бупивакаин и триамцинолон 40 мг | ||
| 7 4410 | Мужской Правый | T10 | 1 | 3 | 0. 5% l-бупивакаин и триамцинолон 40 мг 5% l-бупивакаин и триамцинолон 40 мг | |||||||||||||||
| 8 | Женский | 23 | 4 | Левый | T8 и T9 | 1 | 3 | 0,5% l-bupamivacaine | 0,5% l-буп | |||||||||||
| 9 | Женский | 80 | 1 | Левый | T11 | 1 | 3 | 0,5% l-бупивакаин и триамцинолон 40 мг Возраст |
Таблица 2 Показатели боли (NRS) и BPI, ответ на инъекции и продолжительность продолжающегося обезболивания
Таблица 2 Показатели боли (NRS) и BPI, реакция на инъекции и продолжительность текущего обезболивания
Таблица 3 Оценка боли и BPI респондентов и не ответивших
Таблица 3 Показатели боли и BPI респондентов и не ответивших
Обсуждение Мы провели поиск в базе данных Pubmed® и в Google Scholar, используя термины: «Ультразвук, передний кожный нерв и кожный нерв живота. Поскольку АКНЕ представляет собой синдром защемления периферического нерва, он в основном диагностируется после реакции на инфильтрацию местного анестетика [8]. Мы не знаем о пользе исследований нервной проводимости в этом состоянии. Мы предлагаем использовать блокаду кожного нерва брюшной полости под контролем УЗИ в качестве точного диагностического инструмента с потенциальной терапевтической эффективностью.Ультразвуковой контроль помогает определить местонахождение нерва и распределить инъекционный раствор вокруг него. Это приводит к гидродиссекции, в результате чего высвобождается любой захват. В нашей серии случаев мы отметили, что глубина нерва от кожи может составлять всего 0,75 см. Возможность визуализировать курс иглы и распространение инъекционного раствора обеспечивает безопасность процедуры. Хотя большие объемы могут снизить специфичность, мы выбрали объемы от 2 мл до 3 мл, чтобы оптимизировать распространение инъекционного раствора в вертикальном канале прямой мышцы живота.Мы добавили стероиды в наш инъекционный препарат из-за их мембраностабилизирующих свойств, пытаясь продлить облегчение боли. Из девяти наших пациентов пятеро получили облегчение боли с помощью одной инъекции, а двое — нет, что подразумевает диагностический характер этой процедуры. У остальных двух пациентов после первой инъекции было отмечено только 20% облегчение боли; один пациент предпочел пройти повторную инъекцию и впоследствии достиг 80% облегчения боли, в то время как другой не хотел дальнейшей интервенционной терапии. Хотя это мог быть случай АКНЕ, мы не включили в список респондентов, поскольку в клинике телефонного обзора пороговым значением было 50% обезболивания.Такой частичный ответ можно объяснить неадекватным распределением инъекционной жидкости в вертикальном канале прямой мышцы живота в первый раз. Местные инъекции могут быть терапевтическими. Куан и др. сообщают, что 95% пациентов испытывают облегчение боли после одной или двух инъекций [9]. Макгрэди и Маркс использовали стимулятор периферического нерва для локализации нерва и использовали 1 мл 6% фенола для лечения. Они сообщили, что 59% их пациентов с диагнозом АКНЕ получили полное облегчение боли, а у 36% было несколько симптомов, но не требовалось дальнейшего лечения [10].В нашей серии исследований две трети пациентов с абдоминальной болью и положительным симптомом Карнетта достигли эффективного обезболивания в течение средней продолжительности 12 недель после инъекции местного анестетика и стероидов под контролем УЗИ. Мы действительно повторили инфильтрацию стероидами между 6–8 месяцами начальной терапии для всех пациентов с АКНЭС, чтобы сохранить контроль над болью. Только один из них был потерян для дальнейшего изучения. Ни у одного из них в нашей практике не было второго повтора. Различные статьи, в том числе редакционная статья в The Lancet , подчеркивают увеличение расходов на здравоохранение из-за недостаточной осведомленности врачей об этом состоянии [1,11,12]. В заключение, ультразвук можно надежно использовать для инфильтрации кожных нервов брюшной полости. Это повысит безопасность, а также диагностическую полезность процедуры. БлагодарностиМы благодарим г-на Бена Мэйсона, графического дизайнера, Департамент медицинской иллюстрации, Университет Абердина, за его вклад в создание рисунков. Список литературы1 . Хроническая боль в брюшной стенке: проблема, о которой часто забывают.Практический подход к диагностике и лечению . Am J Gastroenterol 2002 ; 97 ( 4 ): 824 — 30 ,2 . Является ли болезненность брюшной стенки полезным признаком при диагностике неспецифической боли в животе? Ann R Coll Surg Engl 1988 ; 70 : 233 — 4 ,3 . Синдром защемления кожного нерва живота . Хирургия 1972 ; 71 ( 1 ): 118 — 24 .4 . Межреберная невралгия как причина боли и болезненности в животе . Surg Gynecol Obstet 1926 ; 42 : 625 — 32 ,5 . Хроническая боль в брюшной стенке — диагностическая проблема для хирурга . Am J Surg 2009 ; 198 : 129 — 34 ,6 . Микроанатомия структур, способствующих синдрому защемления кожного нерва живота . J Am Board Fam Pract 1997 ; 10 ( 5 ): 329 — 32 ,7 . Периферические невропатии . Малабар, Флорида : Роберт Э. Крейгер Паблишинг ; 1976 : 1 — 7 , 85 — 8 ,8 . Синдром защемления кожного абдоминального нерва (АКНЕ): часто игнорируемая причина боли . Пермь J 2002 ; 6 ( 3 ): 20 — 7 .9 et al. Эффективность лечения боли в брюшной стенке путем местной инъекции . Тайвань J Obstet Gynecol 2006 ; 45 : 239 — 43 .10 . Лечение синдрома ущемления брюшного нерва с помощью нервного стимулятора . Ann R Coll Surg Engl 1988 ; 70 : 120 — 22 .11 Тест на болезненность брюшной стенки: может ли Carnett сократить расходы? Ланцет 1991 ; 337 : 1134 .12 . Хроническая боль в брюшной стенке. . Dig Dis Sci 1994 ; 39 : 1935 — 41 . Wiley Periodicals, Inc. Реакция в месте инъекции — Управление побочными эффектами Chemocare.com Обсуждаемые здесь реакции в месте инъекции — это местные кожные реакции, возникающие при Лекарства, вызывающие реакции в месте инъекции: Лекарства, которые могут вызвать реакцию в месте инъекции, делятся на 2 типа: Раздражители вызывают кратковременное и ограниченное раздражение вены:
Везиканты вызывают реакцию в месте инъекции, которую часто называют химическим веществом.
Управление симптомами: Предотвращение экстравазации — ключ к лечению этих типов инъекций. Медсестра или врач, делающие такие инъекции химиотерапии, должны быть осторожны. Может быть рекомендовано устройство для центрального венозного доступа, например:
Что можно сделать, чтобы предотвратить реакцию в месте инъекции:
Лечение или лекарственные препараты для лечения реакции в месте инъекции:
Когда обращаться к врачу или поставщику медицинских услуг:
Примечание: Мы настоятельно рекомендуем вам поговорить со своим врачом. Chemocare.com предназначен для предоставления самой последней информации о химиотерапии пациентам и их семьям, опекунам и друзьям. Для получения информации о программе наставничества «Четвертый ангел» посетите сайт www.4thangel.org . послеоперационных обезболивающих эффектов местной инфильтрации раны с помощью кеторолака после паховой герниоррафии — полный текст Дизайн исследования представляет собой проспективное рандомизированное двойное слепое контролируемое исследование пациентов, перенесших плановую одностороннюю паховую грыжу в больнице Раматибоди в течение этого периода. 1 июля 2018 г. — 30 июня 2020 г. Первичным результатом является изучение эффективности инъекций кеторолака для снятия боли после операции по поводу герниоррафии, а вторичным результатом является изучение побочных эффектов и осложнений после инъекции кеторолака: анафилактический шок, аномальное кровотечение из хирургической раны, желудочно-кишечное кровотечение и острое повреждение почек. После одобрения этическим комитетом пациенты, которым назначена плановая односторонняя паховая грыжи под общей анестезией и которые соответствуют критериям включения, будут набраны для этого исследования после получения информированного согласия хирургических ординаторов или хирургического персонала амбулаторного отделения (OPD). Пациенты, соответствующие критериям исключения, будут исключены. Во время предоперационного визита пациенты познакомятся с концепцией визуальной аналоговой шкалы (ВАШ), которая варьируется от 0 = отсутствие боли до 10 = сильная боль. После проведения общей анестезии в операционной, пациент будет случайным образом выбран в одну из двух частей диаграммы этого отчета (соотношение 1: 1) путем рисования запечатанного непрозрачного конверта одним из ответственных хирургических ординаторов или лечащим хирургом. Все пациенты будут подвергнуты герниоррафии с помощью техники Lichtenstein-Free Repair. После того, как оболочка брюшной полости будет закрыта препаратом Викрил № 0, пациенты из группы кеторолака получат местную инфильтрацию в слое оболочки брюшной полости кеторолаком 30 мг в 10 мл физиологического раствора. Подготовлен стандартный план послеоперационного обезболивания. Все пациенты будут получать одну таблетку парацетамола перорально по 500 мг каждые 6 часов, если лечащий врач разрешает послеоперационный пероральный прием. Пациентам с оценкой по ВАШ> 3 назначают парентеральные опиоиды (морфин). Медсестрам-волонтерам, ухаживающим за пациентами в предоперационном и послеоперационном периоде, выдаются стандартные протоколы оценки боли.Все исследователи боли и пациенты не осведомлены о назначении лечения на протяжении всего процесса оценки боли. После операции медсестра стационарного отделения будет записывать оценку боли пациентов через 4,8 и 12 часов после операции, используя оценку по ВАШ, и записывать результаты в форму записи данных исследования, прикрепленную к карте медицинских карт каждого пациента. Также записываются дополнительные данные об использовании морфина. Все побочные эффекты и осложнения после инъекции кеторолака, такие как анафилактический шок, аномальное кровотечение из хирургической раны, желудочно-кишечное кровотечение и острое повреждение почек, будут регистрироваться и лечиться лечащим врачом-резидентом или консультантом.Все данные собираются главным исследователем из карты пациента и формы записи данных. Данные выражены как среднее ± стандартное отклонение. Параметрические данные сравниваются между группами. Статистическая значимость установлена на уровне p <0,05. Наднадкостничные инъекции (местная инфильтрация) | Местная анестезия в детской стоматологии | Курс непрерывного образования Наднадкостничная инъекция (широко известная как местная инфильтрация) показана всякий раз, когда стоматологические процедуры ограничиваются определенной областью верхней или нижней челюсти.Концевые окончания нервов, иннервирующих область, анестезируются. Показаниями являются анестезия пульпы всех зубов верхней челюсти (постоянных и первичных), передних зубов нижней челюсти (первичных и постоянных) и первичных моляров нижней челюсти, когда лечение ограничено одним или двумя зубами. Местная инфильтрация моляров нижней челюсти В ряде исследований сообщалось об эффективности инъекции раствора местного анестетика в слизисто-буккальную складку между корнями основных моляров нижней челюсти. Q23.При сравнении эффективности инфильтрации нижней челюсти с анестезией с блокадой нижней челюсти, было принято общее мнение, что эти две техники были одинаково эффективны для восстановительных процедур, но блокада нижней челюсти была более эффективной для пульпотомии и экстракции, чем инфильтрация нижней челюсти. Местная инфильтрация резцов нижней челюсти Показания к инфильтрации резцов нижней челюсти:
Если планируется лечение квадранта с вовлечением передних и передних зубов, необходима инфильтрация нижней челюсти для анестезии терминальных концов нижних альвеолярных нервов, которые пересекают среднюю линию от контралатерального квадранта. Синдром грушевидной мышцы | Анестезиология | Американское общество анестезиологовСиндром PIRIFORMIS — редкая и часто не диагностируемая причина боли в ягодицах и ногах. Лечение синдрома грушевидной мышцы включает инъекцию в грушевидную мышцу местного анестетика и стероида 7–9 или ботулотоксина. 10 Некоторые исследователи также вводят разбавленный местный анестетик и стероид в область седалищного нерва. 7,8 В то время как старые техники инъекций применялись вслепую, 1,2 новые методы включали использование электромиографии мышц 9 или компьютерной томографии (КТ) 10 для выявления грушевидной мышцы и использование нервного стимулятора для определения седалищного нерва.7,8 Более широкому применению этих методов препятствует недостаточная доступность электромиографии мышц и КТ в большинстве клиник по лечению боли. В этой статье мы представляем результаты наших анатомических диссекций, которые имеют отношение к этиологии синдрома грушевидной мышцы и технике инъекции в грушевидную мышцу. Мы ретроспективно проанализировали карты 19 пациентов, которым вводили инъекцию в период с октября 2001 г. по сентябрь 2002 г. Первые три пациента получили инъекции до нашего исследования трупов, тогда как остальные пациенты получили инъекции после проведения исследования.Мы отметили место введения иглы с точки зрения расстояния (латерального и каудального) от нижней границы КПС, глубины введения иглы, при которой возникает двигательный ответ стопы, интенсивности стимула, необходимого для стимуляции седалищного нерва. Мы выбрали нижнюю границу КПС в качестве ориентира из-за ее анатомического отношения к грушевидной мышце и седалищного нерва и простоты визуализации при рентгеноскопии. Нижняя граница КПС хорошо знакома специалистам по обезболиванию, потому что это наиболее частое место инъекции у пациентов с дисфункцией КПС. Грушевидная мышца расположена в большом седалищном отверстии между крестцом, КПС и бедренной костью.Нижний край КПС расположен примерно на уровне S3 позвонка или между S2 и S3 позвонками, 11 а седалищный нерв находится ниже грушевидной мышцы. Таким образом, доступ к седалищному нерву и грушевидной мышце можно получить, введя иглу в большое седалищное отверстие, латерально и каудально до нижней границы КПС. Перед исследованием трупа мы произвольно выбрали участок на 1 см латеральнее и на 1 см каудальнее нижней границы КПС в качестве точки введения иглы.Смещали иглу в сторону, если седалищный нерв не располагался на глубине 13 см. После нашего исследования на трупе, которое показало более латеральное расположение седалищного нерва по отношению к КПС, мы вставили иглу на 2 см латеральнее и на 1 см каудальнее КПС. Пациент находится в наклонном положении, область ягодиц подготовлена и задрапирована, КПС определяется при рентгеноскопии. После инфильтрации местного анестетика вводится 15-сантиметровая изолированная игла, подключенная к нервному стимулятору, и продвигается вперед до тех пор, пока не будет вызвана двигательная реакция стопы (рис.1). Вызванный ответ стопы при интенсивности нервного стимулятора 0,2–0,6 мА указывает на близость кончика иглы к седалищному нерву. Допускается любая двигательная реакция (, например, , инверсия стопы, эверсия, тыльное сгибание или подошвенное сгибание). Рис. 1. Задний вид крестца, подвздошной кости и большого вертела бедренной кости, показывающий ход грушевидной мышцы, седалищного нерва и место инъекции ( X ). Рис. 1. Задний вид крестца, подвздошной кости и большого вертела бедренной кости, показывающий ход грушевидной мышцы, седалищного нерва и место инъекции ( X ).
Рис. 2. Флюороскопический вид иглы в грушевидной мышце, очерченной введенным рентгеноконтрастным красителем. Игла вводится на 1,5 ± 0,8 см латеральнее и на 1,2 ± 0,6 см каудально до нижней границы крестцово-подвздошного сустава. Рис. 2. Флюороскопический вид иглы в грушевидной мышце, очерченной введенным рентгеноконтрастным красителем. Игла вводится на 1,5 ± 0,8 см латеральнее и на 1,2 ± 0,6 см каудально до нижней границы крестцово-подвздошного сустава.
Мы отметили реакцию пациентов на инъекцию, любые связанные с ней диагнозы и предыдущее лечение, полученное до инъекции. Показанием для инъекции грушевидной / перисцитарной мышц было наличие признаков и симптомов синдрома грушевидной мышцы и неполное облегчение от предыдущего лечения.У пациентов была боль в ягодицах, которая распространялась на бедро или на ипсилатеральную заднюю часть бедра и ногу и имела положительные симптомы Ласега, Фрейберга и Пейса. Грушевидная мышца берет начало от передней поверхности S2 – S4 крестцовых позвонков, ягодичной поверхности подвздошной кости у задней поверхности подвздошной ости и капсулы КПС.4,5 Он проходит латерально через большое седалищное отверстие, становится сухожильным и прикрепляется к грушевидной ямке на медиальной стороне большого вертела бедренной кости. Ягодичные нервы, ягодичные сосуды, седалищный нерв и задний кожный нерв бедра проходят ниже грушевидной мышцы. Ветви спинномозговых нервов L5, S1 и S2 иннервируют грушевидную мышцу. Существует шесть возможных анатомических соотношений между седалищным нервом и грушевидной мышцей 1,16,17: (1) седалищный нерв проходит ниже грушевидной мышцы; (2) разделенный нерв проходит через мышцу и под ней; (3) разделенный нерв проходит через мышцу и над ней; (4) разделенный нерв проходит выше и ниже мышцы; (5) неразделенный нерв проходит через грушевидную мышцу; или (6) над мышцей проходит неразделенный нерв. Аномалии седалищного нерва и грушевидной мышцы могут вызывать ишиас. Синдром грушевидной мышцы, термин, впервые введенный Робинсоном 13, затрагивает 5–6% пациентов, направленных для лечения боли в спине и ногах. 1,15 Это вызвано травмой таза или ягодиц, 1,21 гипертрофией грушевидной мышцы, 5,8,9 анатомическими аномалиями грушевидной мышцы или седалищного нерва, 5,6 разницей в длине ног (разница минимум 0,5 дюйма длины ног), 4 или миозит грушевидной мышцы. Боль в ягодицах и радикулит, изначально вызванные травмой, могут привести к воспалению и спазму мышцы.15 Воспалительные вещества, такие как простагландин, гистамин, брадикинин и серотонин, выделяются из воспаленной мышцы и могут раздражать седалищный нерв, вызывая цикл боли-спазма-воспаления-раздражения. 23,24 Воспаленная, спастическая или растянутая грушевидная мышца может сдавливать седалищный нерв между мышцей и тазом, 6,13 при этом сжатие происходит между сухожильной частью мышцы и костным тазом. 6 У пациентов, у которых грушевидная мышца расположена кпереди от седалищного нерва, компрессия нерва происходит между верхним краем грушевидной мышцы и верхним краем большого седалищного отверстия. Дифференциальный диагноз синдрома грушевидной мышцы включает причины боли в пояснице и ишиаса.Обычно ошибочно принимаемый за грыжу межпозвоночного диска, у пациента с синдромом грушевидной мышцы обычно нет неврологических нарушений. 15 При дифференциальной диагностике синдрома следует учитывать стеноз позвоночного канала, фасеточный синдром, дисфункцию КПС, вертельный бурсит, синдром миофасциальной боли, опухоль таза, эндометриоз и состояния, раздражающие седалищный нерв. Эти условия часто можно устранить, собрав полную историю болезни и проведя тщательное физическое обследование. Parziale 1 перечислил шесть основных признаков синдрома: (1) история травмы крестцово-подвздошной и ягодичной области; (2) боль в области КПС, большой седалищной вырезки и грушевидной мышцы, распространяющаяся вниз по ноге и вызывающая затруднения при ходьбе; (3) острое обострение боли при наклоне или поднятии тяжести и умеренное облегчение при вытяжении; (4) пальпируемое образование колбасной формы над грушевидной мышцей, болезненное при пальпации; (5) положительный знак Ласега 13; и (6) возможная атрофия ягодичных мышц. При физикальном обследовании может быть обнаружен наклон таза и неровности лопаток 4 или болезненность в ягодицах от медиального края большого седалищного отверстия до большого вертела. 1 В ягодицах может ощущаться веретенообразная масса, а при ректальном и тазовом исследованиях может быть болезненность грушевидной мышцы. 1,2 Боль усиливается при сгибании, приведении и внутреннем вращении бедра. Симптом Ласега — боль при произвольном сгибании, приведении и внутреннем вращении бедра.13,24 Признак Фрейберга, или боль при вынужденном внутреннем вращении вытянутого бедра, 14 возникает из-за растяжения грушевидной мышцы и давления на седалищный нерв в крестцово-остистой связке. Признаком темпа является боль и слабость при отведении бедра с сопротивлением, когда пациент сидит (, т.е. , когда бедро согнуто). 15,20 Эти признаки лучше понять, если понять, что функция грушевидной мышцы заключается во внешнем вращении тазобедренного сустава, когда бедро разгибается в тазобедренном суставе и отводит согнутое бедро. Хотя когда-то считалось, что диагноз синдрома грушевидной мышцы является исключительно клиническим, 19,20 последних отчетов показывают диагностическую ценность электромиографии, КТ и магнитно-резонансной томографии.Электромиография может обнаруживать миопатические и нейропатические изменения, включая задержку H-рефлекса с пораженной ногой в согнутом, приведенном и внутренне повернутом положении по сравнению с тем же H-рефлексом в нормальном анатомическом положении. 26A 3-SD удлинение H-рефлекса недавно было рекомендовано в качестве физиологического критерия синдрома грушевидной мышцы. Это открытие предполагает захват нерва абдуктором бедра и внешним вращающим устройством, , то есть , грушевидной мышцей, под которой он проходит. Лечение синдрома грушевидной мышцы включает физиотерапию в сочетании с использованием противовоспалительных препаратов, анальгетиков и миорелаксантов для уменьшения воспаления, спазма и боли. 1,2,28 Необходимо исправить аномальную биомеханику, вызванную осанкой, наклонным тазом и неравномерностью длины ног.1 Физическая терапия включает в себя растяжение грушевидной мышцы со сгибанием, приведением и внутренним вращением бедра 1,2, за которым следует давление, прикладываемое к мышце. Было обнаружено, что ультразвуковое лечение уменьшает боль. 4,29 Когда симптомы уменьшаются, к режиму добавляется укрепление отводящих мышц бедра. Также рекомендуется использовать спрей с водяным охлаждением для растягивания мягких тканей. Пациенты, не отвечающие на консервативную терапию, являются кандидатами на инъекции местного анестетика и / или стероидов.Предыдущие авторы предполагали, что инъекция должна производиться в очаге боли и раздражительности глубоко в брюшной части мышцы 15, либо в медиальном аспекте мышцы 1,2, либо в латеральном аспекте 31, где происходит сильное сжатие седалищного нерва. 6 Инъекции стероидов каудаля и местных анестетиков также оказались эффективными. При каудальных инъекциях введенный раствор диффундирует по рукавам нервных корешков и проксимальной части седалищного нерва, блокируя нервы, которые иннервируют грушевидную мышцу.32 Хирургическое вмешательство может быть рассмотрено в упорных случаях или при документально подтвержденной анатомической аномалии грушевидной мышцы, которая может быть истончена, разделена или удалена. Старые методы инъекции грушевидной мышцы применялись вслепую, 1, 2, 15, тогда как новые методы включают идентификацию грушевидной мышцы с помощью электромиографии 9 или с использованием компьютерной томографии.10Fishman et al. 9 использовал рентгеноскопическое наблюдение и электромиографию для определения грушевидной мышцы. В их методике пациент находится в положении лежа, и ожидаемое положение грушевидной мышцы определяется с использованием большого вертела бедренной кости и латеральной границы крестца и КПС в качестве ориентиров. Размещение иглы в грушевидной мышце подтверждается электромиографией мышц и введением контрастного вещества. Авторы не смогли измерить глубину иглы, необходимую для достижения грушевидной мышцы, и не описали реакцию своих пациентов на инъекцию. Новый метод определяет положение мышцы с помощью КТ и вводит иглу с помощью КТ. 10 Местный анестетик (2 мл 0,5% бупивакаина) вводится в мышцу с последующей инъекцией 100 ЕД ботулинического токсина типа А. Однако более широкое применение этого метода ограничивается отсутствием оборудования компьютерной томографии в большинстве центров лечения боли. Мы вводим стероид в грушевидную мышцу и область возле седалищного нерва. Инъекция в грушевидную мышцу уменьшает отек и / или спазм мышцы. Мы также вводим стероид и разбавитель рядом с седалищным нервом, независимо от того, есть ли признаки защемления седалищного нерва, потому что в случае синдрома грушевидной мышцы, вероятно, есть некоторое воспаление нерва. Наш успех в локализации седалищного нерва до исследования на трупе, когда мы вводили иглу на 1 см латеральнее КПС, вероятно, был связан с широким диаметром седалищного нерва. Разница в расстояниях между нашим трупом и клиническими исследованиями может быть связана с углом наклона С-образной дуги рентгеноскопии по отношению к анатомическим структурам и неточными измерениями при рентгеноскопии ( i. Интересно отметить, что некоторые из наших пациентов получали облегчение на срок до 3 месяцев даже после инъекций местных анестетиков и стероидов. Относительно длительное облегчение, наблюдаемое у некоторых наших пациентов и пациентов в исследовании Ханании и Китаина, может быть связано с одновременной перисциатической инъекцией стероида. Однако наши клинические результаты являются ретроспективными данными, и более убедительные результаты могут быть получены из проспективных рандомизированных исследований, сравнивающих инъекции грушевидной мышцы / перисцита при консервативном лечении ( i. Ботулинический токсин можно использовать, если пациент реагирует на инъекции стероидов и местных анестетиков. Токсин блокирует высвобождение ацетилхолина в нервно-мышечном соединении 37 и использовался при лечении очаговых дистоний, таких как блефароспазм, спастическая кривошея, спастическая дисфония или гемифациальный спазм. 37,38 Инъекция ботулинического токсина приводит к длительному расслаблению мышцы, и восстановление мышцы зависит от нервно-мышечного разрастания и реиннервации мышцы, что занимает от нескольких недель до месяцев.Инъекции ботулина применялись при лечении миофасциального болевого синдрома 38,39 и синдрома грушевидной мышцы. Использовали дозы 100 мышиного токсина ботулотоксина типа A (ботокс) 10 в 4 мл бупивакаина и 5 000–10 000 единиц ботулотоксина типа B. Сообщенные осложнения инъекции ботулотоксина включают плечевую плексопатию, полирадикулоневрит, 41 и местный псориазиформный дерматит. 42 Следует избегать инъекции в седалищный нерв, если токсин будет использоваться в инъекциях грушевидной мышцы. Рандомизированное исследование сравнивало ботулинический токсин типа А с метилпреднизолоном у пациентов с «миофасциальной грушевидной болью». 10 В этом исследовании инъекция грушевидной мышцы проводилась под контролем КТ и не сопровождалась перисциатической инъекцией. Через 30 дней после инъекции у пациентов в обеих группах наблюдалось заметное снижение оценки боли без существенной разницы между двумя группами. Однако пациенты, которым вводили инъекцию ботулина, имели значительно более низкие показатели боли через 60 дней после инъекции.10 Таким образом, мы обсудили причины синдрома грушевидной мышцы, включая анатомические аномалии грушевидной мышцы и седалищного нерва. Из нашего исследования трупа и из предыдущих исследований анатомии кажется, что анатомические причины синдрома грушевидной мышцы встречаются редко. Мы изучили литературу о синдроме грушевидной мышцы, его признаках, симптомах и методах лечения. Исходя из нашего первоначального клинического опыта, мы пришли к выводу, что синдром чистой грушевидной мышцы встречается редко и обычно сосуществует с другими причинами боли в спине, ягодицах и радикулите.Диагноз синдрома грушевидной мышцы ставится после тщательного медицинского обследования и исключения других причин ишиаса. Наконец, мы представили методику инъекции в грушевидную мышцу и около седалищного нерва под контролем рентгеноскопии и нервного стимулятора. Мы надеемся, что более широкое применение нашей техники приведет к лучшему лечению пациентов с синдромом грушевидной мышцы и приведет к контролируемым исследованиям эффективности инъекционных техник при этом синдроме. . | |||||||||||

 Помимо нагноения с образованием флегмоны и абсцесса инфильтрат может рассасываться, склерозироваться или заживать с образованием рубца.
Помимо нагноения с образованием флегмоны и абсцесса инфильтрат может рассасываться, склерозироваться или заживать с образованием рубца.

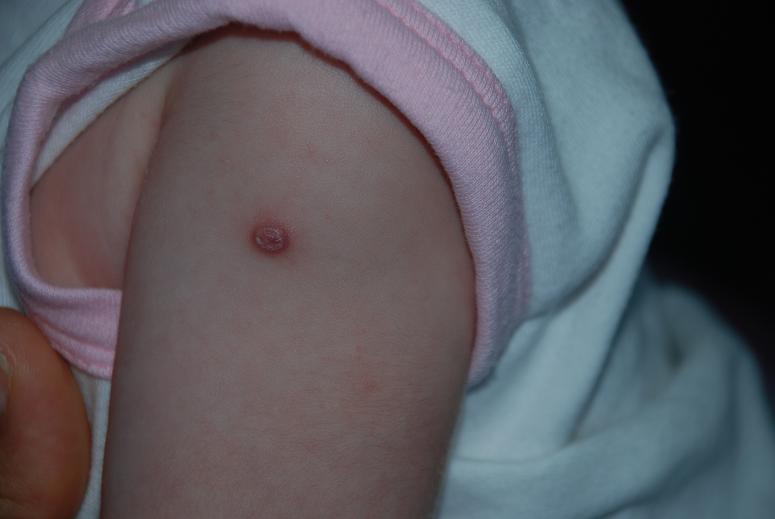
 5 ° F
5 ° F

 5% л-бупивакаин и триамцинолон 40 мг
5% л-бупивакаин и триамцинолон 40 мг «Мы не обнаружили каких-либо предыдущих историй болезни / серий у взрослых. Следовательно, мы считаем, что это первая серия случаев, в которой сообщается об успешном использовании инфильтрации кожных нервов брюшной полости под контролем УЗИ.
«Мы не обнаружили каких-либо предыдущих историй болезни / серий у взрослых. Следовательно, мы считаем, что это первая серия случаев, в которой сообщается об успешном использовании инфильтрации кожных нервов брюшной полости под контролем УЗИ.
 Стоимость госпитализации и диагностических процедур варьируется от 1296 до 6727 долларов на пациента до постановки диагноза [1,12]. Srinivasan et al. отмечают, что вероятность пропуска заболевания внутренних органов составляет менее 7% при строгом соблюдении диагностических критериев [12]. Это можно улучшить только с помощью ультразвукового контроля. Ультразвуковой контроль придает точность и безопасность для установления диагноза. Это следует учитывать у пациентов с болью в брюшной стенке перед тем, как подвергнуться различным инвазивным процедурам, таким как лапароскопия.
Стоимость госпитализации и диагностических процедур варьируется от 1296 до 6727 долларов на пациента до постановки диагноза [1,12]. Srinivasan et al. отмечают, что вероятность пропуска заболевания внутренних органов составляет менее 7% при строгом соблюдении диагностических критериев [12]. Это можно улучшить только с помощью ультразвукового контроля. Ультразвуковой контроль придает точность и безопасность для установления диагноза. Это следует учитывать у пациентов с болью в брюшной стенке перед тем, как подвергнуться различным инвазивным процедурам, таким как лапароскопия.
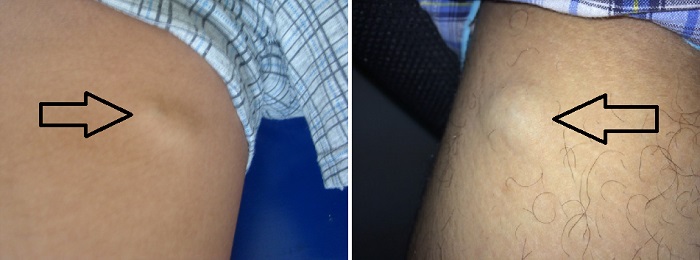 Диагностическая достоверность и стоимость
Диагностическая достоверность и стоимость

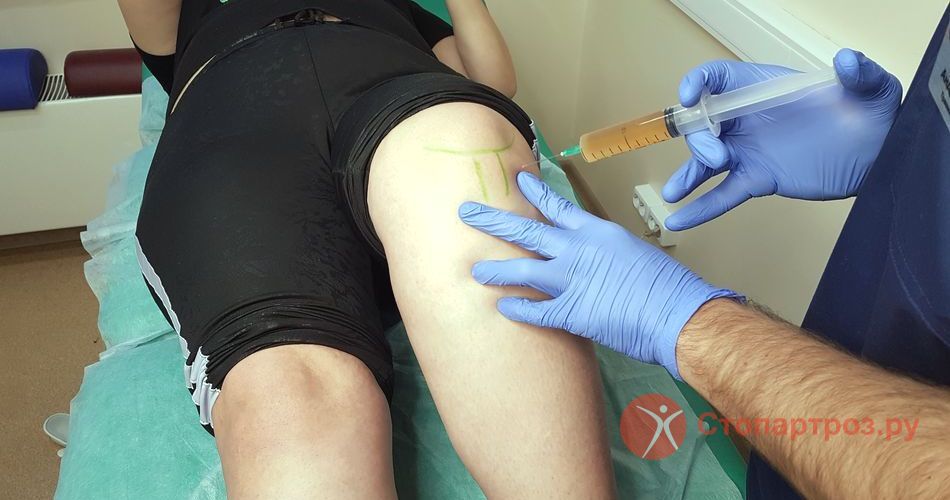


 Этот катетер можно установить в
Этот катетер можно установить в
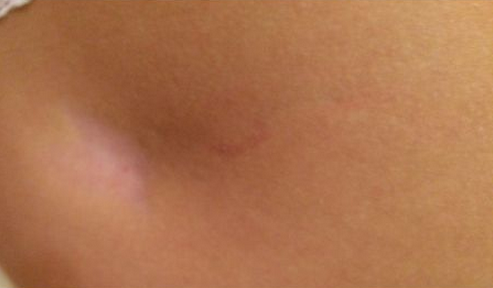


 и пациенты из контрольной группы получат местную инфильтрацию 0,5% бупивакаином 10 мл. И тогда закрытие кожи будет выполнено нейлоном 3-0.
и пациенты из контрольной группы получат местную инфильтрацию 0,5% бупивакаином 10 мл. И тогда закрытие кожи будет выполнено нейлоном 3-0.
 Он также обеспечивает анестезию мягких тканей в качестве дополнения к регионарной блокаде. Противопоказаниями являются инфекция или острое воспаление в области инъекции и в местах, где плотная кость покрывает вершины зубов, т.е.е., постоянные первые моляры у детей. Он не рекомендуется для больших площадей из-за необходимости введения нескольких игл и необходимости введения больших общих объемов местного анестетика, что может привести к токсичности.
Он также обеспечивает анестезию мягких тканей в качестве дополнения к регионарной блокаде. Противопоказаниями являются инфекция или острое воспаление в области инъекции и в местах, где плотная кость покрывает вершины зубов, т.е.е., постоянные первые моляры у детей. Он не рекомендуется для больших площадей из-за необходимости введения нескольких игл и необходимости введения больших общих объемов местного анестетика, что может привести к токсичности. Инфильтрацию нижней челюсти следует рассматривать в ситуациях, когда нужно выполнить двусторонние восстановительные процедуры без анестезии языка. Двусторонняя анестезия языка неудобна как для детей, так и для взрослых.
Инфильтрацию нижней челюсти следует рассматривать в ситуациях, когда нужно выполнить двусторонние восстановительные процедуры без анестезии языка. Двусторонняя анестезия языка неудобна как для детей, так и для взрослых. 1–4 Это может быть вызвано анатомическими аномалиями грушевидной мышцы и седалищного нерва, что приводит к раздражению седалищного нерва грушевидной мышцей.Действительно, описаны случаи синдрома, вторичного по отношению к аномалиям грушевидной мышцы. 5,6
1–4 Это может быть вызвано анатомическими аномалиями грушевидной мышцы и седалищного нерва, что приводит к раздражению седалищного нерва грушевидной мышцей.Действительно, описаны случаи синдрома, вторичного по отношению к аномалиям грушевидной мышцы. 5,6 Мы описываем нашу технику инъекции седалищного нерва и грушевидной мышцы под контролем рентгеноскопии и нервным стимулятором на основе наших анатомических данных.В нашей технике инъекции используются ориентиры и оборудование, знакомые анестезиологу и обеспечивающие правильное размещение. Мы представляем наши первоначальные клинические результаты, а также рассматриваем этиологию, клинические проявления и лечение синдрома грушевидной мышцы.
Мы описываем нашу технику инъекции седалищного нерва и грушевидной мышцы под контролем рентгеноскопии и нервным стимулятором на основе наших анатомических данных.В нашей технике инъекции используются ориентиры и оборудование, знакомые анестезиологу и обеспечивающие правильное размещение. Мы представляем наши первоначальные клинические результаты, а также рассматриваем этиологию, клинические проявления и лечение синдрома грушевидной мышцы. , и вызванный ответ стопы. Экспертный совет Северо-Западного университета одобрил исследование, которое включало нашу технику инъекции и клиническую реакцию пациентов. Письменное информированное согласие на процедуру было получено от каждого пациента.
, и вызванный ответ стопы. Экспертный совет Северо-Западного университета одобрил исследование, которое включало нашу технику инъекции и клиническую реакцию пациентов. Письменное информированное согласие на процедуру было получено от каждого пациента.
 12 Игла отводится на 3–5 мм, пока не исчезнет вызванная двигательная реакция, и рядом с седалищным нервом вводится стероид (40–60 мг метилпреднизолона или 40 мг триамцинолона) в 5–6 мл физиологического раствора. Затем иглу отводят еще на 3–8 мм, чтобы поместить кончик иглы в брюшко грушевидной мышцы.Йогексол (2–4 мл) вводится для очертания грушевидной мышцы (рис. 2), затем стероид (40 метилпреднизолон или 40 мг триамцинолона) в 7–10 мл 1% лидокаина. После процедуры пациента переводят в палату для восстановления на 1 час или до исчезновения онемения ног, в зависимости от того, какой период дольше.
12 Игла отводится на 3–5 мм, пока не исчезнет вызванная двигательная реакция, и рядом с седалищным нервом вводится стероид (40–60 мг метилпреднизолона или 40 мг триамцинолона) в 5–6 мл физиологического раствора. Затем иглу отводят еще на 3–8 мм, чтобы поместить кончик иглы в брюшко грушевидной мышцы.Йогексол (2–4 мл) вводится для очертания грушевидной мышцы (рис. 2), затем стероид (40 метилпреднизолон или 40 мг триамцинолона) в 7–10 мл 1% лидокаина. После процедуры пациента переводят в палату для восстановления на 1 час или до исчезновения онемения ног, в зависимости от того, какой период дольше.
 13–15 Критериями реакции на инъекцию были уменьшение боли в ягодицах и ногах, повышение активности и улучшение симптомов Ласега, Фрейберга и Пейса.
13–15 Критериями реакции на инъекцию были уменьшение боли в ягодицах и ногах, повышение активности и улучшение симптомов Ласега, Фрейберга и Пейса.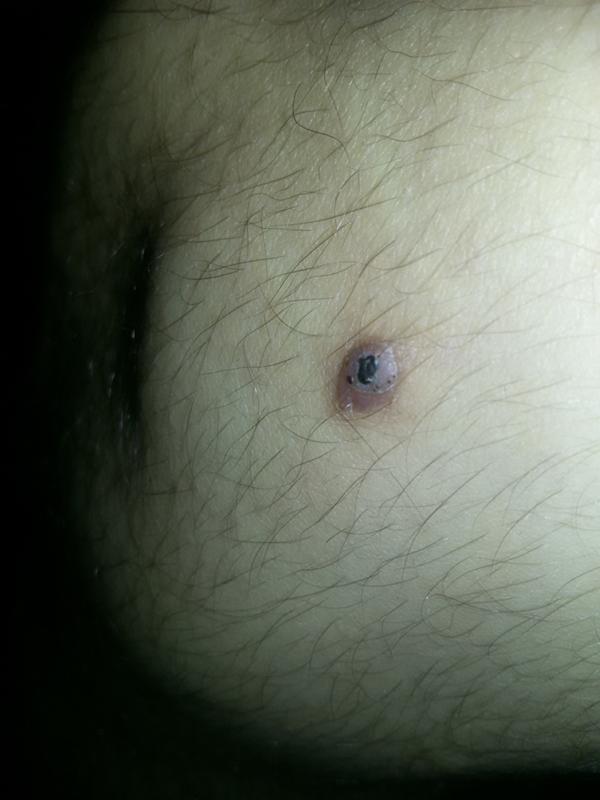 В одном из клинических случаев описан пациент, у которого ишиас уменьшился после хирургического разреза нижней головки двудольной грушевидной мышцы. 5 У другого пациента была фасциальная сужающая повязка вокруг седалищного нерва и грушевидная мышца, лежащая перед нервом. Боль в бедрах и ягодицах, а также ишиас уменьшились после резекции фиброзной ленты и разреза грушевидной мышцы для восстановления нормального взаимодействия нерва и мышцы. Предыдущие авторы предлагали захват седалищного нерва грушевидной мышцей и рекомендовали хирургическое высвобождение мышцы и ее фасции в качестве лечения пациентов с синдромом грушевидной мышцы.18–20
В одном из клинических случаев описан пациент, у которого ишиас уменьшился после хирургического разреза нижней головки двудольной грушевидной мышцы. 5 У другого пациента была фасциальная сужающая повязка вокруг седалищного нерва и грушевидная мышца, лежащая перед нервом. Боль в бедрах и ягодицах, а также ишиас уменьшились после резекции фиброзной ленты и разреза грушевидной мышцы для восстановления нормального взаимодействия нерва и мышцы. Предыдущие авторы предлагали захват седалищного нерва грушевидной мышцей и рекомендовали хирургическое высвобождение мышцы и ее фасции в качестве лечения пациентов с синдромом грушевидной мышцы.18–20 22 Некоторые исследователи считают синдром грушевидной мышцы одной из форм миофасциального болевого синдрома. 10 Травма в анамнезе обычно возникает примерно в 50% случаев синдрома. 15 Травма обычно не является драматической и может возникнуть за несколько месяцев до появления первых симптомов. Это также может быть следствием операции по замене тазобедренного сустава. 20
22 Некоторые исследователи считают синдром грушевидной мышцы одной из форм миофасциального болевого синдрома. 10 Травма в анамнезе обычно возникает примерно в 50% случаев синдрома. 15 Травма обычно не является драматической и может возникнуть за несколько месяцев до появления первых симптомов. Это также может быть следствием операции по замене тазобедренного сустава. 20 6 Пациенты с защемлением седалищного нерва могут иметь неврологический дефицит и отклонения в результатах электродиагностики. 5 Ишиас после ламинэктомии может быть результатом поражения нервных корешков рубцовой тканью, что приводит к «укорочению» седалищного нерва, что делает его склонным к повторному напряжению и травмам грушевидной мышцей. 18
6 Пациенты с защемлением седалищного нерва могут иметь неврологический дефицит и отклонения в результатах электродиагностики. 5 Ишиас после ламинэктомии может быть результатом поражения нервных корешков рубцовой тканью, что приводит к «укорочению» седалищного нерва, что делает его склонным к повторному напряжению и травмам грушевидной мышцей. 18 1 Диагноз синдрома грушевидной мышцы обычно ставится после исключения этих возможностей.Изолированное поражение грушевидной мышцы встречается редко и обычно возникает в результате травм мягких тканей в результате вращательных и / или сгибательных движений бедра и туловища. 2 У наших пациентов выявлено сопутствующее наличие синдрома с другими причинами боли в спине и ногах (таблица 1). Тщательное медицинское обследование обычно позволяет определить активную причину боли пациента, чтобы можно было назначить соответствующее лечение.
1 Диагноз синдрома грушевидной мышцы обычно ставится после исключения этих возможностей.Изолированное поражение грушевидной мышцы встречается редко и обычно возникает в результате травм мягких тканей в результате вращательных и / или сгибательных движений бедра и туловища. 2 У наших пациентов выявлено сопутствующее наличие синдрома с другими причинами боли в спине и ногах (таблица 1). Тщательное медицинское обследование обычно позволяет определить активную причину боли пациента, чтобы можно было назначить соответствующее лечение. Пациент с синдромом грушевидной мышцы обычно сообщает о боли в ягодицах с облучением ипсилатеральной ноги или без него 1; Боль в ягодицах обычно распространяется от крестца к большому вертлугу. 1,2,5 В то время как Холлин 4 подчеркнул редкое возникновение боли в пояснице, Парциале 1 отметил разную степень паралюмбальной боли. Если грушевидная мышца раздражает седалищный нерв, у пациента может появиться боль в ягодицах, иррадирующая в ипсилатеральную ногу. 9 Боль может распространяться в заднюю часть бедра вниз до колена, если поражен задний кожный нерв бедра.2,4 Боль обычно усиливается при длительном сидении (, например, , вождение или езда на велосипеде) или при вставании из сидячего положения. 1,2 Боль возникает при дефекации из-за близости грушевидной мышцы к боковой стенке таза и усиливается после сидения на твердой поверхности с кошельком в заднем кармане. У пациента также может быть диспареуния. 1 В анамнезе может быть хромота, когда пациент волочит голень на пораженной стороне 20, и пациент может сообщить о онемении стопы.
Пациент с синдромом грушевидной мышцы обычно сообщает о боли в ягодицах с облучением ипсилатеральной ноги или без него 1; Боль в ягодицах обычно распространяется от крестца к большому вертлугу. 1,2,5 В то время как Холлин 4 подчеркнул редкое возникновение боли в пояснице, Парциале 1 отметил разную степень паралюмбальной боли. Если грушевидная мышца раздражает седалищный нерв, у пациента может появиться боль в ягодицах, иррадирующая в ипсилатеральную ногу. 9 Боль может распространяться в заднюю часть бедра вниз до колена, если поражен задний кожный нерв бедра.2,4 Боль обычно усиливается при длительном сидении (, например, , вождение или езда на велосипеде) или при вставании из сидячего положения. 1,2 Боль возникает при дефекации из-за близости грушевидной мышцы к боковой стенке таза и усиливается после сидения на твердой поверхности с кошельком в заднем кармане. У пациента также может быть диспареуния. 1 В анамнезе может быть хромота, когда пациент волочит голень на пораженной стороне 20, и пациент может сообщить о онемении стопы. 4
4 2,25 Неврологические симптомы обычно отрицательные. 1Хотя результаты теста на прямой ноге могут быть нормальными, при его раздражении может наблюдаться ограничение и боль во время тестирования, а также онемение в областях, снабжаемых седалищным нервом.
2,25 Неврологические симптомы обычно отрицательные. 1Хотя результаты теста на прямой ноге могут быть нормальными, при его раздражении может наблюдаться ограничение и боль во время тестирования, а также онемение в областях, снабжаемых седалищным нервом. КТ мягких тканей таза может показать аномальное поглощение грушевидной мышцей 27 или увеличенной мышцей 24, тогда как магнитно-резонансная томография подтверждает увеличенную грушевидную мышцу, но с нормальной интенсивностью. 24
КТ мягких тканей таза может показать аномальное поглощение грушевидной мышцей 27 или увеличенной мышцей 24, тогда как магнитно-резонансная томография подтверждает увеличенную грушевидную мышцу, но с нормальной интенсивностью. 24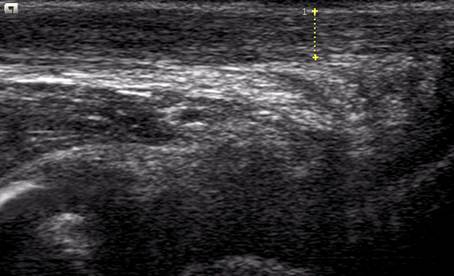 30
30 1,2,19,33,34 Мышцы внутренней запирательной мышцы, gemelli и quadratus femoris могут компенсировать потерю функции piriformis, потому что эти мышцы имеют общие прикрепления с мышцей piriformis. 1,13
1,2,19,33,34 Мышцы внутренней запирательной мышцы, gemelli и quadratus femoris могут компенсировать потерю функции piriformis, потому что эти мышцы имеют общие прикрепления с мышцей piriformis. 1,13 Несмотря на успех в идентификации грушевидной мышцы, их метод использует электромиографию мышц, которая недоступна в большинстве центров по лечению боли. Похоже, что в месте введения иглы Fishman et al. 9 находится сбоку от места установки. Их метод не позволяет определить местонахождение седалищного нерва, если игла не введена медиальнее, потому что седалищный нерв находится ближе к КПС, чем большой вертел бедренной кости (рис. 1). Следует отметить, что Fishman et al. 9 предназначался для введения стероида только в грушевидную мышцу и не планировал делать инъекцию рядом с седалищным нервом.
Несмотря на успех в идентификации грушевидной мышцы, их метод использует электромиографию мышц, которая недоступна в большинстве центров по лечению боли. Похоже, что в месте введения иглы Fishman et al. 9 находится сбоку от места установки. Их метод не позволяет определить местонахождение седалищного нерва, если игла не введена медиальнее, потому что седалищный нерв находится ближе к КПС, чем большой вертел бедренной кости (рис. 1). Следует отметить, что Fishman et al. 9 предназначался для введения стероида только в грушевидную мышцу и не планировал делать инъекцию рядом с седалищным нервом. Еще одна новая техника — перискиатическая инъекция, которую использовали Ханания и Китаин. 7,8 В этой технике пациент находится в боковом или полупроничном положении, при этом независимые бедро и колено согнуты, а зависимая конечность выпрямлена. После обнаружения седалищного нерва с помощью нервного стимулятора вводится 40 мг метилпреднизолона в 5–10 мл разбавленного местного анестетика, а игла извлекается на несколько сантиметров. Авторы описали шесть пациентов, которые ранее не реагировали или частично отвечали на инъекции в слепую грушевидную мышцу или эпидуральные инъекции стероидов.Используя эту технику инъекции, их пациенты чувствовали облегчение боли на срок до 18 месяцев.
Еще одна новая техника — перискиатическая инъекция, которую использовали Ханания и Китаин. 7,8 В этой технике пациент находится в боковом или полупроничном положении, при этом независимые бедро и колено согнуты, а зависимая конечность выпрямлена. После обнаружения седалищного нерва с помощью нервного стимулятора вводится 40 мг метилпреднизолона в 5–10 мл разбавленного местного анестетика, а игла извлекается на несколько сантиметров. Авторы описали шесть пациентов, которые ранее не реагировали или частично отвечали на инъекции в слепую грушевидную мышцу или эпидуральные инъекции стероидов.Используя эту технику инъекции, их пациенты чувствовали облегчение боли на срок до 18 месяцев. Стероиды обладают противовоспалительным действием, и было показано, что местное применение метилпреднизолона специфически блокирует передачу ноцицептивных волокон. 35,36 Мы не используем местный или очень разбавленный местный анестетик для перискиатической инъекции, чтобы минимизировать моторную блокаду, и используем местный анестетик, а не физиологический раствор для инъекции грушевидной мышцы, чтобы расслабить грушевидную мышцу и разорвать цикл боли и спазмов. Рекомендуется вводить местный анестетик в брюшко мышцы, чтобы избежать попадания местного анестетика в седалищный нерв, что приведет к сенсорной и моторной блокаде ноги и ступни; это особенно важно при инъекции ботулотоксина.
Стероиды обладают противовоспалительным действием, и было показано, что местное применение метилпреднизолона специфически блокирует передачу ноцицептивных волокон. 35,36 Мы не используем местный или очень разбавленный местный анестетик для перискиатической инъекции, чтобы минимизировать моторную блокаду, и используем местный анестетик, а не физиологический раствор для инъекции грушевидной мышцы, чтобы расслабить грушевидную мышцу и разорвать цикл боли и спазмов. Рекомендуется вводить местный анестетик в брюшко мышцы, чтобы избежать попадания местного анестетика в седалищный нерв, что приведет к сенсорной и моторной блокаде ноги и ступни; это особенно важно при инъекции ботулотоксина. е. , размер 1 см на рентгеновской пленке — это не совсем 1 см анатомически). В нашем исследовании на трупах мы измерили расстояние от КПС до середины седалищного нерва, тогда как в нашем клиническом исследовании мы могли стимулировать край седалищного нерва. Каудальное расположение иглы по отношению к нижней границе КПС зависит от расположения иглы в большой седалищной вырезке. Каудальное расположение 0,5–1,5 см является идеальным, потому что более каудальное прикрепление может определить местонахождение седалищного нерва, но может пропустить грушевидную мышцу.
е. , размер 1 см на рентгеновской пленке — это не совсем 1 см анатомически). В нашем исследовании на трупах мы измерили расстояние от КПС до середины седалищного нерва, тогда как в нашем клиническом исследовании мы могли стимулировать край седалищного нерва. Каудальное расположение иглы по отношению к нижней границе КПС зависит от расположения иглы в большой седалищной вырезке. Каудальное расположение 0,5–1,5 см является идеальным, потому что более каудальное прикрепление может определить местонахождение седалищного нерва, но может пропустить грушевидную мышцу. е. , физиотерапия или инъекция ботулотоксина).
е. , физиотерапия или инъекция ботулотоксина).