ДИФТЕРИЙНЫЕ МИОКАРДИТЫ: взаимосвязь нарушений регионарной сократимости левого желудочка и проводимости | #02-03/99
У больных дифтерийными миокардитами довольно часто встречаются различные нарушения проводимости. Наиболее клинически и прогностически неблагоприятными считаются бифасцикулярная блокада и полная AV-блокада, которые требуют постановки больному временного электрокардиостимулятора (ВЭКС) [5, 8], хотя часто эта мера оказывается неэффективной. Тяжесть нарушений проводимости часто соответствует тяжести течения дифтерийных миокардитов. Однако не всегда при тяжелых формах миокардитов, даже заканчивающихся летальным исходом, наблюдаются серьезные нарушения проводимости. Показателем тяжести поражения миокарда при дифтерийных миокардитах [1] являются нарушения регионарной сократимости левого желудочка (ЛЖ), выявляемые при двухмерном эхокардиографическом исследовании.
В исследование были включены 64 больных дифтерийными миокардитами (27 мужчин, 37 женщин, средний возраст 42,6±14,2 лет). Диагноз дифтерийного миокардита формировался на основании критериев Нью-йоркской ассоциации сердца (1980). Тяжесть течения миокардита определялась исходя из принятых клинико-инструментальных критериев [2, 3, 4]. В зависимости от тяжести течения миокардита были выделены три группы больных: первая группа с легким течением (33 больных), вторая со среднетяжелым течением (18 больных), третья с тяжелым течением (13 больных).
Всем больным наряду с общеклиническими методами обследования проводились в динамике (каждые 5-7 дней) электрокардиография (ЭКГ) в 12 стандартных отведениях и двухмерная эхокардиография (ЭхоКГ) в стандартных позициях: парастернальной позиции длинной оси ЛЖ и короткой оси на уровне митрального клапана, папиллярных мышц, верхушки, а также в апикальных позициях двух- и четырехкамерного сердца. Использовалось деление миокарда ЛЖ на 16
Дифтерийный токсин имеет тропность не только к миокарду, но и к нервной системе.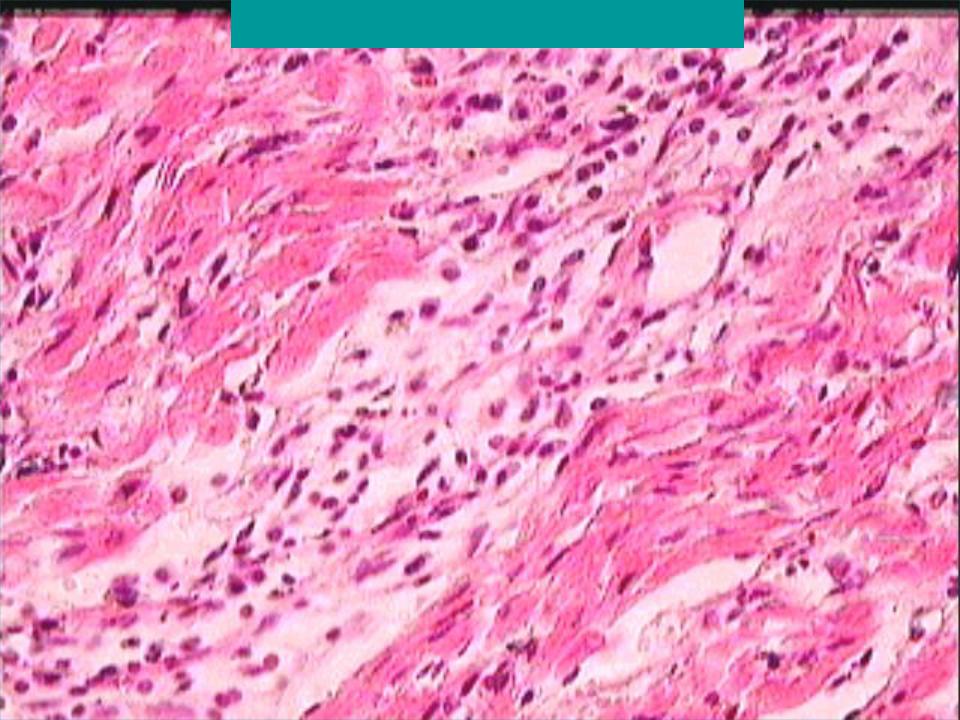 Поэтому он способен поражать проводящую систему сердца, вызывая блокады на различных уровнях Поэтому он способен поражать проводящую систему сердца, вызывая блокады на различных уровнях |
сегментов, рекомендованное Американской ассоциацией эхокардиографии. Анализ нарушений регионарной сократимости миокарда ЛЖ проводился по унифицированной семибалльной шкале: 1 – нормокинезия, 2 – гипокинезия, 3 – акинезия, 4 – дискинезия, 5 – аневризма, 6 – акинезия с рубцом, 7 – дискинезия с рубцом. Суммарные нарушения регионарной сократимости оценивались с помощью индекса асинергии (ИА) ЛЖ, равного частному от деления суммы значений сократимости 16 сегментов на их количество. Статистическая обработка проводилась с помощью стандартных методов вариационной статистики с использованием критерия Стьюдента.
| Рисунок 1. Преходящая блокада правой ножки пучка Гиса |
Наибольший интерес представляла группа больных с тяжелым течением миокардита, в которой у 77% больных отмечались нарушения проводимости. В этой группе были выделены две подгруппы: А – трое больных с нарушениями проводимости, при которых требовалась постановка ВЭКС (полная AV-блокада, бифасцикулярная блокада), и Б – десять больных с нарушениями проводимости, при которых не было необходимости в постановке ВЭКС (преходящая AV-блокада I степени, неполная или полная блокада одной ножки пучка Гиса или одной ветви левой ножки пучка Гиса, замедление внутрижелудочковой проводимости) (рисунок 1). В подгруппе А отмечался один летальный исход, несмотря на постановку ВЭКС. В подгруппе Б было три летальных исхода от прогрессирующей сердечно-сосудистой недостаточности.
| Рисунок 2. AV-блокада I степени |
В обеих подгруппах при ЭхоКГ-исследовании отмечались выраженные нарушения регионарной сократимости ЛЖ. Однако изучение локализации асинергичных сегментов показало, что в подгруппе А преимущественно были поражены передне-перегородочные, передние сегменты. У этих больных отмечались также инфарктоподобные изменения на ЭКГ (зубцы QS) в передних грудных отведениях. В подгруппе Б наиболее выражены были изменения нижних, задних или боковых сегментов (рисунок 2). У одного больного из подгруппы Б с летальным исходом миокардита отмечалась акинезия нижних и задних сегментов с формированием зубцов QS во II, III, aVF-отведениях, в то время как из нарушений проводимости наблюдалось всего лишь замедление внутрижелудочковой проводимости. ИА ЛЖ в обеих подгруппах был более 1,5, что свидетельствовало о поражении большого количества сегментов и тяжести этого поражения.
У этих больных отмечались также инфарктоподобные изменения на ЭКГ (зубцы QS) в передних грудных отведениях. В подгруппе Б наиболее выражены были изменения нижних, задних или боковых сегментов (рисунок 2). У одного больного из подгруппы Б с летальным исходом миокардита отмечалась акинезия нижних и задних сегментов с формированием зубцов QS во II, III, aVF-отведениях, в то время как из нарушений проводимости наблюдалось всего лишь замедление внутрижелудочковой проводимости. ИА ЛЖ в обеих подгруппах был более 1,5, что свидетельствовало о поражении большого количества сегментов и тяжести этого поражения.
В группе больных со среднетяжелым течением миокардита только у двух больных (11%) отмечались нарушения проводимости: у одного больного с гипокинезией задне-перегородочного, нижнего сегментов развилась полная блокада правой ножки пучка Гиса, у второго больного с гипокинезией заднего и нижнего сегмента неполная блокада передней ветви левой ножки пучка Гиса. У остальных больных этой группы хотя и отмечалась гипокинезия различных сегментов ЛЖ, в том числе передних и передне-перегородочных, тем не менее нарушений проводимости не было. Однако гипокинез у больных без нарушений проводимости отмечался всего лишь в двух-четырех сегментах и ИА ЛЖ был от 1,25 до 1,38.
| V1 | |
| V2 | |
| V3 | |
| V4 | |
| V5 | |
| V6 | |
| Рисунок 3. Полная AV-блокада; поставлен ВЭКС | |
В группе с легким течением миокардита только у трех больных (9%) наблюдалась преходящая AV-блокада I степени и у одного больного — нарушения ВЖП (3%). Нарушений регионарной сократимости у них не наблюдалось (ИА ЛЖ был равен 1).
Известно, что дифтерийный токсин имеет тропность как к миокарду, так и к нервной системе [7]. Тропностью к нервной системе, в частности к проводящей системе сердца, и объясняются в литературе нарушения внутрисердечной проводимости, наблюдаемые при дифтерийных миокардитах [6]. Результаты нашего исследования демонстрируют, что в развитии нарушений проводимости не менее значимы поражения сократительного миокарда в тех участках, которые окружают проводящую систему сердца. Большое значение в появлении тех или иных нарушений проводимости имеет площадь поражения миокарда, то есть количество и степень выраженности поражения сегментов ЛЖ. При ИА ЛЖ более 1,5 у большинства больных наблюдаются нарушения проводимости. При ИА ЛЖ от 1,25 до 1,38 нарушения проводимости отмечаются только у 11% больных. При легких миокардитах, отсутствии нарушений регионарной сократимости ЛЖ у 6% больных отмечалась преходящая AV-блокада.
Тропностью к нервной системе, в частности к проводящей системе сердца, и объясняются в литературе нарушения внутрисердечной проводимости, наблюдаемые при дифтерийных миокардитах [6]. Результаты нашего исследования демонстрируют, что в развитии нарушений проводимости не менее значимы поражения сократительного миокарда в тех участках, которые окружают проводящую систему сердца. Большое значение в появлении тех или иных нарушений проводимости имеет площадь поражения миокарда, то есть количество и степень выраженности поражения сегментов ЛЖ. При ИА ЛЖ более 1,5 у большинства больных наблюдаются нарушения проводимости. При ИА ЛЖ от 1,25 до 1,38 нарушения проводимости отмечаются только у 11% больных. При легких миокардитах, отсутствии нарушений регионарной сократимости ЛЖ у 6% больных отмечалась преходящая AV-блокада.
При большой площади поражения миокарда (ИА ЛЖ 1,5) локализация участков поражения обусловливает появление тех или иных нарушений проводимости. Поражение сегментов в области передней стенки, межжелудочковой перегородки приводит к развитию неблагоприятных в клиническом и прогностическом плане нарушений проводимости, таких как полная AV-блокада, бифасцикулярная блокада. Частая неэффективность постановки ВЭКС в этих случаях также доказывает отсутствие изолированного поражения проводящей системы сердца и наличие тяжелого поражения всего миокарда, в том числе и сократительных кардиомиоцитов. При локализации поражения миокарда только в области, окружающей проводящую систему сердца, вероятность эффективности ВЭКС значительно возрастает. При преимущественном поражении сегментов в области задней, нижней, боковой стенок ЛЖ и ИА ЛЖ более 1,5 нарушения проводимости возникают, но они не являются прогностически неблагоприятными.
| В возникновении нарушений проводимости значение имеет не только патология проводящей системы сердца, но и кардиомиоцитов, а также площадь поражения миокарда |
Итак, можно выделить группу больных с тяжелым течением миокардита (ИА ЛЖ 1,5) и преимущественным поражением небольшой площади миокарда; т. е. при небольшом количестве асинергичных участков нарушений проводимости передне-перегородочных сегментов ЛЖ эту группу можно рассматривать как прогностически неблагоприятную в плане развития полной AV-блокады. У таких больных развитие AV-блокады I степени необходимо расценивать как опасный признак, так как возможен очень быстрый переход к полной AV-блокаде.
е. при небольшом количестве асинергичных участков нарушений проводимости передне-перегородочных сегментов ЛЖ эту группу можно рассматривать как прогностически неблагоприятную в плане развития полной AV-блокады. У таких больных развитие AV-блокады I степени необходимо расценивать как опасный признак, так как возможен очень быстрый переход к полной AV-блокаде.
При небольшом количестве асинергичных сегментов нарушений проводимости чаще всего не бывает, и только у 11% таких больных развивались изолированная полная или неполная блокада ветвей или ножек пучка Гиса. Локализация пораженных участков не влияет на появление нарушений проводимости, по всей видимости из-за небольшой площади поражения миокарда.
Таким образом, полученные данные демонстрируют существование связи между тяжестью, локализацией нарушений регионарной сократимости ЛЖ и появлением нарушений проводимости, а также позволяют выявлять прогностически неблагоприятную в плане развития полной AV-блокады группу больных для возможно более ранней постановки ВЭКС и повышения выживаемости в этой группе больных.
Литература
1. Голиков А. П., Ющук Н. Д., Газарян Г. А. и др. Нарушения регионарной сократимости левого желудочка при дифтерийных миокардитах. Сб. науч. раб. (ММСИ 75 лет). М., 1997. 61-62.
2. Турьянов М. Х., Беляева Н. М., Царегородцев А. Д. и др. // Дифтерия. М., 1996. C. 254.
3. Фаворова Л. А., Астафьева Н. В., Корженкова М. П. и др. // Дифтерия. М., 1988. C. 208.
4. Шульдяков А. А., Зайцева И. А., Цека Ю. С. и др. Дифтерийные миокардиты: клинико-лабораторные критерии тяжести. Сб. науч. тр. Махачкала, 1996. C. 78-80.
5. Arauljo J. A. R., Campelo A. L. P., Maia C. M. S. et al. Myocardite difterica de tipo maligno. // Arq. Bras. Card. 1990. 54 (2): 117-120.
6. Bethel D. B., Dulng N. M., Loan H. Th. et al. Prognostic valule of electrocardiographic monitoring of patients with severe diphtheria // Clin.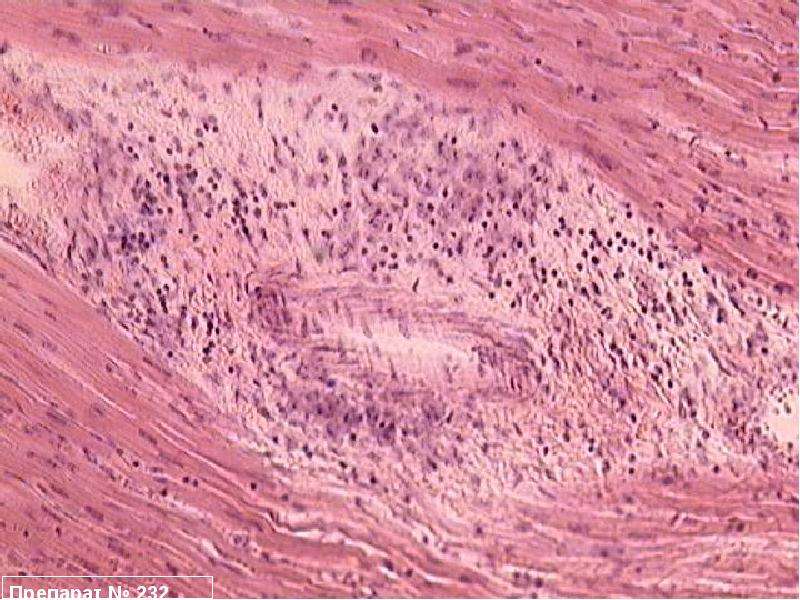 Infect. Dis. 1995. 20: 1259-1265.
Infect. Dis. 1995. 20: 1259-1265.
7. Collier R. J. Diphtheria toxin: mode of action and strulctulre // Bacteriol. Rev. 1975. 39: 54-59.
8. Stockins B. A., Lanas F. T., Saavedra J. G. et al. Prognosis in patients with diphtheric myocarditis and bradyarrhythmias: assesment of resullts of ventricullar pacing // Br. Heart. J. 1994. 72: 190-191.
Электрокардиографческие изменения у больных острым дифтерийным миокардитом Текст научной статьи по специальности «Клиническая медицина»
PSEUDOTUBERCULOSIS IN HUMAN
G.P. Somov,1 Isaak Salmover,2 V.P. Maliy 3
Institute of epidemiology and microbiology SD RAMN, Vladivostok,1 Jerusalem,2 Kharkov medical academy of postgraduate educatione3
SUMMARY
The pseudotuberculous infection contamination is widespread everywhere, clinic is characterized by a considerable polymorphism. More often disease shows representative (94,3 %) flow with a lesion of different organs and systems. The pseudotuberculosis called by serovar III of Y. pseudotuberculosis, flows past rougherly as contrasted to by forms called by serovar I of the agent.
KEYWORDS: pseudotuberculosis, clinic, classification, diagnostic
УДК 616.1
ЭЛЕКТРОКАРДИОГРАФЧЕСКИЕ ИЗМЕНЕНИЯ У БОЛЬНЫХ ОСТРЫМ ДИФТЕРИЙНЫМ МИОКАРДИТОМ
Н.Ф. Шустваль, В.П. Малый, А.К. Полукчи, Д.Э. Рыспаева, В.М.Дмитренко
Харьковская медицинская академия последипломного образования
РЕЗЮМЕ
У 146 больных дифтерийным миокардитом изучены в динамике электрокардиографические изменения. Наиболее часто при этом выявлялись синусовая брадикардия у 48,7%, синусовая тахикардия у 32,3%, предсердная экстрасистолия у 23,5%, желудочковая экстрасистолия у 38,7%, предсердная пароксизмальная тахикардия у 9%, желудочковая пароксизмальная тахикардия у 5%, атриовентрикулярная блокада I степени — у 19%,II степени — у 8,5%, III степени — у 5,4%, блокада правой ножки пучка Гиса — у 13,2%, левой ножки — у 22,6% больных. Блокада левой ножки пучка Гиса сопровождалась кардиомегалией со значительными нарушениями гемодинамики. Электрокардиографическое исследование является достаточно информативным методом в диагностике осложнений со стороны сердечной мышцы у больных дифтерией.
Наиболее часто при этом выявлялись синусовая брадикардия у 48,7%, синусовая тахикардия у 32,3%, предсердная экстрасистолия у 23,5%, желудочковая экстрасистолия у 38,7%, предсердная пароксизмальная тахикардия у 9%, желудочковая пароксизмальная тахикардия у 5%, атриовентрикулярная блокада I степени — у 19%,II степени — у 8,5%, III степени — у 5,4%, блокада правой ножки пучка Гиса — у 13,2%, левой ножки — у 22,6% больных. Блокада левой ножки пучка Гиса сопровождалась кардиомегалией со значительными нарушениями гемодинамики. Электрокардиографическое исследование является достаточно информативным методом в диагностике осложнений со стороны сердечной мышцы у больных дифтерией.
КЛЮЧЕВЫЕ СЛОВА: дифтерийный миокардит, диагностика, электрокардиография
Изучение закономерностей течения значительно распространившейся в последние годы дифтерийной инфекции показало, что она нередко сопровождается тяжелыми осложнениями со стороны сердечно-сосудистой системы, в частности миокардита, который заметно ухудшает течение и прогноз дифтерии [1, 2, 3]. Тяжелые сердечно-сосудистые нарушения, приводящие к смерти больного, связаны с токсическим поражением сердечной мышцы и развитием в ней воспалительных и дегенеративных изменений [1,6], которые могут оказывать существенное влияние на динамику процессов деполяризации и реполяризации миокарда. Учитывая значимость и актуальность возникшей проблемы, а также принимая во внимание, что закономерности изменений сердечно-сосудистой системы при дифтерии у взрослых из-за редкости заболевания в предыдущие годы детально не анализировались, представлялось целесообразным провести комплексное изучение клинико-электрокардиографических изменений у больных острым дифтерийным миокардитом в зависимости от степени тяжести заболевания.
В исследование были включены 146 больных дифтерийным миокардитом (66 мужчин и 80 женщин, в возрасте от 16 до 69
лет). Диагноз дифтерийного миокардита формировался на основании критериев Нью-йоркской ассоциации сердца (1980). Тяжесть течения миокардита определялась исходя из принятых клинико-инструментальных критериев [5]. В зависимости от тяжести течения миокардита были выделены три группы больных: первая группа с легким течением (37 больных), вторая со среднетяжелым течением (49 больных), третья с тяжелым течением (60 больных).
Диагноз дифтерийного миокардита формировался на основании критериев Нью-йоркской ассоциации сердца (1980). Тяжесть течения миокардита определялась исходя из принятых клинико-инструментальных критериев [5]. В зависимости от тяжести течения миокардита были выделены три группы больных: первая группа с легким течением (37 больных), вторая со среднетяжелым течением (49 больных), третья с тяжелым течением (60 больных).
Всем больным наряду с общеклиническими методами обследования регистрировали в динамике электрокардиограммы (ЭКГ) в 12-ти стандартных отведениях. У обследованных детально анализировались жалобы, данные анамнеза, объективного и электрокардиографического исследования, а также клинико-биохимические показатели крови.
Ведущими симптомами дифтерийного миокардита были:
а) сердечная недостаточность;
б) сосудистая недостаточность;
в) нарушения ритма и проводимости;
г) болевой (коронарный) синдром;
д) псевдоклапанные проявления;
е) малосимптомный вариант;
ж) смешанный вариант.
В связи с тем, что дифтерийный миокардит может протекать с минимальными клиническими проявлениями большое значение в его выявлении имеют инструментальные методы исследования, главным образом электрокардиография. Это относится в первую очередь к миокардитам со стертой клинической картиной (бессимптомный и малосимптомный варианты). Изменения электрической активности сердца могут быть кратковременными или более стойкими. При этом даже существенные изменения ЭКГ могут иметь тенденцию к спонтанному восстановлению, особенно в начальный период заболевания. Нередко изменения ЭКГ, прослеженные в динамике, являются единственным достоверным признаком поражения миокарда.
Нередко изменения ЭКГ, прослеженные в динамике, являются единственным достоверным признаком поражения миокарда.
С миокардитом могут быть связаны изменения процессов деполяризации, реполяризации предсердий и желудочков, различные расстройства ритма и проводимости. Изменения в миокарде диффузного характера регистрируются у 64% больных, очаговоподобные — у 16%. Необходимо иметь в виду, что в ряде наблюдений, даже при диффузных или обширных миокардитах, данные ЭКГ могут быть в норме или незначительно изменены.
При анализе ЭКГ установлено, что наиболее рано претерпевает изменения зубец Т в виде его уплощения и трансформацией в двухфазный или отрицательный. Сегмент 8Т у 38% больных оставался на изолинии, у 52,8% больных смещался ниже изолинии на 1,5-3 мм, у 9,7% был дугообразно смещен кверху от изолинии на 1,5-2 мм и переходил в отрицательный, заостренный или двухфазный зубец Т. При миоперикардитах наблюдалось конкордантное смещение сегмента 8-Т в I, II и III стандартных, АУЬ, АУТ, VI-6 отведениях.
Комплекс (}Н.8 при миокардитах с легким и среднетяжелым течением меняется мало. У больных с тяжелым миокардитом отмечается снижение вольтажа комплекса (}Н.8, уши-рение, зазубривание или расщепление его зубцов, формирование комплекса ()-8, блокад ножек пучка Гиса.
Нарушение ритма сердца наблюдались часто, причем нередко имело место сложное нарушение ритма и проводимости. Стойкая синусовая тахикардия выявлена у 32,3% больных, синусовая брадикардия — у 48,7%. В 6 случаях наблюдалась миграция источника автоматизма по предсердиям. Предсердная экстрасистолия зарегистрирована у 23,5% больных, желудочковая экстрасистолия — у 38,7%; нередко экстрасистолы имели характер Я на Т, у некоторых больных они
были политопными или групповыми, алло-ритмия по типу бигеминии и тригеминии. Мерцательная аритмия определена у 18% обследованных, трепетание предсердий — у 5%. Пароксизмы предсердной тахикардии наблюдались у 9% больных, пароксизмы желудочковой тахикардии — у 5%.
Мерцательная аритмия определена у 18% обследованных, трепетание предсердий — у 5%. Пароксизмы предсердной тахикардии наблюдались у 9% больных, пароксизмы желудочковой тахикардии — у 5%.
Атриовентрикулярная блокада I степени выявлена у 19% больных, II степени — у 8,5%, III степени — у 5,4%. Блокада правой ножки пучка Гиса была у 13,2%, левой ножки — у 22,6% больных. Блокада левой ножки пучка Гиса сопровождалась, как правило, кардиомегалией со значительными проявлениями недостаточности кровообращения.
Отмечено более легкое клиническое течение дифтерийного миокардита у больных с наджелудочковыми экстрасистолами, в то время как желудочковые, особенно политоп-ные, экстрасистолы чаще выявлялись у больных с кардиомегалией и сопровождались выраженной сердечной недостаточностью.
Мерцание и трепетание предсердий возникают главным образом у лиц страдавших ранее заболеваниями сердца (пороки сердца, алкогольная, диабетическая, атеросклеротическая миокардиопатии, гипертоническое сердце и др.).
Миокардиты могут вызывать стойкие отклонения на ЭКГ в течение 2-4, иногда 612 месяцев; изменения, обусловленные пос-тмиокардитическим кардиосклерозом, необратимы.
Для интерпритации электрокардиографических изменений у больных дифтерией следует иметь в виду, что они могут быть связаны с рядом причин, обусловленных инфекционным процессом, а не миокардитом как таковым — нервными влияниями, биохимическими отклонениями (ацидоз, алкалоз, электролитные нарушения), фармакологическим действием лекарств. Изменения ЭКГ при миокардитах неспецифичны и не всегда являются неоспоримым доказательством диагноза, поэтому их необходимо интерпретировать с учетом клинико-биохимических, бактериологических и иммунологических данных.
В заключение важно отметить, что для легкой формы дифтерийного миокардита характерны очаговые поражения миокарда, малая выраженность клинических проявлений, нормальные границы сердца, отсутствие недостаточности кровообращения, благоприятное течение, преходящие электрокардиографические изменения, которые сохраняются до 1-1,5 месяца.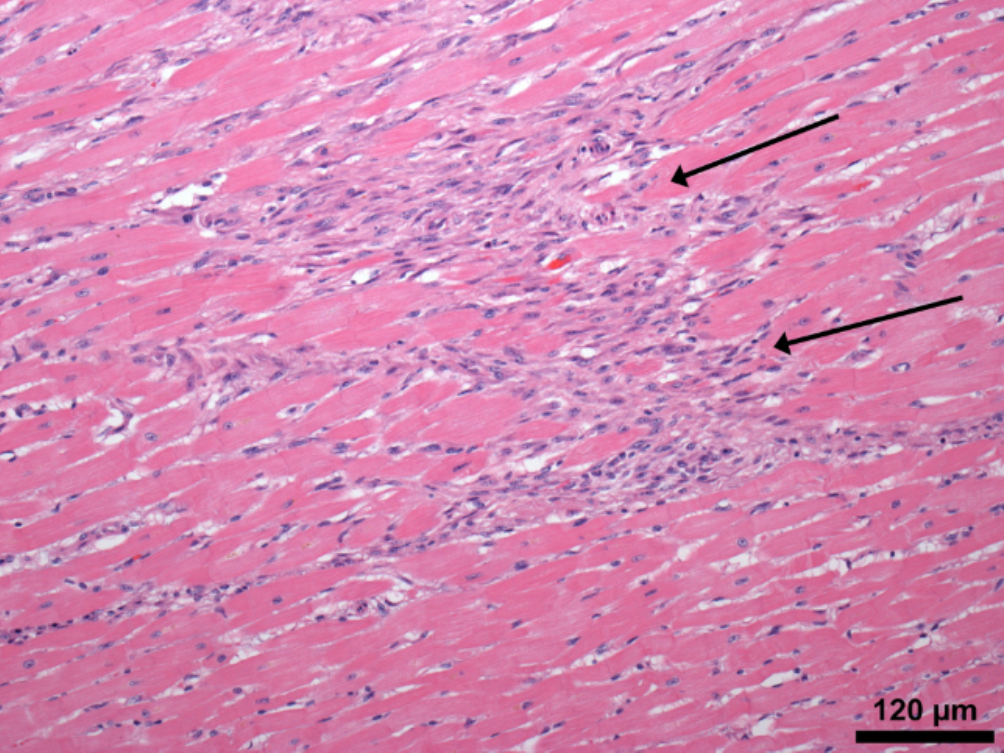
Среднетяжелая форма миокардита про-
является кардиомегалией, отсутствием застойной недостаточности кровообращения, выраженностью клинических данных, по данным ЭКГ многоочаговым характером поражения миокарда с нарушениями автоматизма, возбудимости и проводимости сердца. ЭКГ изменения сохраняются в течение 1,5-3 месяцев, а в некоторых случаях и более продолжительное время.
Для тяжелой формы миокардита характерны тяжелое течение, кардиомегалия,
ЛИТЕРАТУРА
1. Амосова Е.Н., Ткаченко Л.А., Дуда АК.//Украинский кардиологический журнал 1997. №4. С. 48-52.
2. Аникин В.О.//Кардиология. 1998. №8. С. 50-52.
3. Возианова Ж.И., Дуда А.К., Амосова Е.Н.//Врачебное дело. 1999. №4. С. 22-27.
4. Турьянов М.X., Беляева Н.М., Царегородцев А.Д. Дифтерия. -М.: 1996. 252 с.
5. Шульдяков А.А., Зайцев И.А., Цена Ю.С. Сб. научных трудов. Махачкала. 1996. С. 78-80.
6. ЮщукН.Д., Филиппов П.Г. // Тер. арх. 1997. №11. С.10-14.
У ХВОРИХ ГОСТРИМ
Н.Ф. Шустваль, В.П. Малий, О.К. Полукчі, Д.Э. Риспаєва, В.М. Дмітренко
Харківська медична академія післядипломної освіти
РЕЗЮМЕ
У 146 хворих дифтерійним міокардитом вивчені в динаміки електрокардиографчні зміни. Найбільше часто при цьому виявлялися синусовая брадикардія в 48,7%, синусовая тахікардія в 32,3%, предсердная зкстрасистолія в 23,5%, желудочковая зкстрасистолія в 38,7%, предсердна пароксиз-мальна тахікардія в 9%, желудочкова пароксизмальна тахікардія в 5%, атриовентрикулярна блокада І ступеня — у 19%, II ступеня — у 8,5%, III ступеня — у 5,4%, блокада правої ніжки пучка Гиса — у 13,2%, лівої ніжки — у 22,6% хворих. Блокада лівої ніжки пучка Гиса супроводжувалася кардиомегалией зі значними порушеннями гемодинамики. Електрокардиографическое дослідження є досить інформативним методом у діагностиці ускладнень з боку серцевого м’яза в хворих дифтерією.
Блокада лівої ніжки пучка Гиса супроводжувалася кардиомегалией зі значними порушеннями гемодинамики. Електрокардиографическое дослідження є досить інформативним методом у діагностиці ускладнень з боку серцевого м’яза в хворих дифтерією.
КЛЮЧОВІ СЛОВА: дифтерійний міокардит, діагностика, електрокардіографія
ELECTROCARDIOGRAPHY CHANGES IN PATIENTS WITH ACUTE DIPHTHERIC MYOCARDITIS
N.F. Shystval, V.P. Maliy, A.K. Polykchi, D.E. Ryspaeva, V.M. Dmitrenko
Kharkov Medical Academy of Postgraduate Education
SUMMARY
Electrocardiography changes in dynamics in 146 patients with diphtheritic myocarditis have been studied. The most often pathology was: sinus bradycardia for 48,7 %, sinus tachycardia for 32,3 %, atrial extra-systolia for 23,5 %, ventricular extrasystolia for 38,7 %, atrial Bouveret’s disease for 9 %, ventricular Bou-veret’s disease for 5 %, atrioventricular blockage I degree — for 19 %, II degree — for 8,5 %, III degree — for 5,4 %, blockage of a dextral leg of a ventriculonector — for 13,2 %, left-hand leg — for 22,6 %. The blockage of the left-hand leg of a ventriculonector was accompanied by a cardiomegaly with considerable violations of hemodynamics. Electrocardiography investigation is a quite informative method in diagnostic of complications on the part of a cardiac muscle in patients with diphtheria.
KEYWORDS: diphtheric myocarditis, diagnostic, electrocardiography
ЕЛЕКТРОКАРДЮГРАФІЧИИ ЗМІНИ ДИФТЕРІЙНИМ МІОКАРДИТОМ
выраженность всех клинических проявлений, прогрессирующая недостаточность кровообращения, по данным ЭКГ диффузное поражение миокарда с нарушениями автоматизма, возбудимости и проводимости сердца. Электрокардиографические изменения сохраняются от 3-6 до 12 месяцев.
Электрокардиографические изменения сохраняются от 3-6 до 12 месяцев.
Электрокардиографическое исследование является достаточно информативным методом в диагностике осложнений со стороны сердечной мышцы у больных дифтерией.
УДК 616.1
Профилактика заболевания дифтерией
Дифтерия — острое инфекционное заболевание, протекающее с интоксикацией, развитием
воспалительного процесса, сопровождающегося образованием фибринозной пленки в месте внедрения возбудителя.
Возбудитель заболевания — дифтерийная палочка, которая хорошо сохраняется в окружающей среде. Так,
в воде и молоке она жизнеспособна 7 дней; на игрушках, белье, книгах, посуде — нескольких недель. Все дезинфицирующие средства
(перекись водорода, хлорамин и т.п.) в обычных концентрациях убивают дифтерийную палочку; под действием прямых солнечных лучей
она погибает через несколько часов.
Источником инфекции является больной человек
или носитель бактерии дифтерии. Ведущий путь передачи дифтерии — воздушно – капельный (при вдыхании бактерий от больного
или носителя дифтерии), реже – бытовой путь (через предметы, игрушки и т.д.).
Инкубационный (скрытый) период заболевания
составляет от 2 до 10 дней.
Проявления дифтерии различны. Непродолжительная
лихорадка, с подъемом температуры от 38 до 40С, слабость, головные боли, снижение аппетита, артериальная гипотензия. Изменения
ротоглотки в виде налётов белого цвета, при попытке снятия налёта обнажается эрозивная поверхность. Дифтерия ротоглотки проявляется
болью в горле, при токсических формах развивается отёк шеи и верхней половины грудной клетки, выраженная бледность кожи. При
При
дифтерии дыхательных путей: грубый лающий кашель, одышка. При дифтерии носа: затруднение носового дыхания, кровянистое отделяемое
из носовых ходов.
Боль в горле при глотании — ранний симптом дифтерии ротоглотки. В зеве
обнаруживается неяркое покраснение, отечность миндалин и небных дужек, на которых формируются белые или серовато-белые плотные
пленчатые налеты с перламутровым блеском.
Характерные симптомы заболевания:
бледность кожи, грубый “лающий” кашель, хриплость голоса и затрудненное дыхание. Охриплость усиливается вплоть
до полной потери голоса, развивается расстройство дыхания — оно становится слышным на расстоянии, возникают приступы удушья,
ребенок синеет, мечется в кровати, быстро слабеет. При несвоевременном оказании медицинской помощи может наступить смерть.
Клиническая картина дифтерии у взрослых в настоящее время отличается значительным увеличением
числа тяжелых, токсических форм, которые характеризуются теми же симптомами, что и у детей. Иногда единственным симптомом
поражения гортани является осиплость голоса. Осложнения у взрослых могут развиться при любой форме дифтерии. Наиболее частым
осложнением является миокардит (поражение миокарда — сердечной мышцы).
Любые формы дифтерии требуют строгой изоляции
больного и лечения только в условиях больницы.
Самой эффективной мерой профилактики дифтерии является иммунизация.
Вакцинация
детей против дифтерии:
I | II | III |
3 месяца | 4,5 | 6 месяцев |
Первая ревакцинация — 18 месяцев
Вторая ревакцинация
— 7 лет
Третья ревакцинация — 14 лет
Прививка против дифтерии проводится
одновременно с вакцинацией против коклюша и столбняка АКДС –вакциной (Адсорбированная коклюшно –дифтерийно –
столбнячная вакцина), которая состоит из взвеси убитых коклюшных микробов и очищенных дифтерийного и столбнячного анатоксинов,
адсорбированных (очищенных) на гидроксиде алюминия.
АКДС — комбинированные вакцины против дифтерии, столбняка
и коклюша.
АДС — вакцины против дифтерии и столбняка применяющиеся при наличии тех
или иных противопоказаний к АКДС-вакцинам, включая перенесенный коклюш.
АДС-М —
вакцины для профилактики дифтерии и столбняка у детей старше 6 лет и взрослых, со сниженным содержанием дифтерийного компонента.
АД-М
— моновакцина для профилактики дифтерии.
Все компоненты АКДС-вакцин способны формировать иммунитет практически
у 100% привитых.
АКДС вводятся внутримышечно, детям до 18 месяцев — в передне-наружную
поверхность бедра, детям старше 18 месяцев — в дельтовидную мышцу (верхняя треть плеча). Введение вакцины в ягодичную
мышц не желательно, поскольку ягодицы грудного ребенка имеют большую прослойку жировой ткани и препарат может попасть в жировую
клетчатку.
Анатоксины (АДС, АДС-М и АД-М) детям дошкольного возраста вводят так же, как
АКДС вакцину, а школьникам препарат можно вводить еще и подкожно в подлопаточную область.
Вакцинация взрослых.
Плановой иммунизации подлежат лица в возрасте 25 лет и старше, не получившие ревакцинации в
течение последних 10 лет. Повторные ревакцинации против дифтерии осуществляют каждые 10 лет.
Если взрослые лица ранее не были привиты против дифтерии, не болели дифтерией и не были носителями токсигенных коринебактерий
дифтерии, то они должны получить полный курс прививок (2 вакцинации с интервалом 45 дней и через 6 — 9 месяцев — ревакцинацию).
Последующие ревакцинации им также проводят каждые 10 лет.
Взрослым, привитым или не привитым,
переболевшим дифтерией в легкой форме, или носителям токсигенных коринебактерий дополнительную прививку против дифтерии не
делают. Ревакцинацию им следует провести через 10 лет после заболевания или выявленного носительства.
Ревакцинацию им следует провести через 10 лет после заболевания или выявленного носительства.
Взрослым, перенесшим токсические формы дифтерии, независимо от полученных ранее прививок прививку против дифтерии
проводят не ранее чем через 6 месяцев после перенесенного заболевания двукратно с интервалом 45 дней. Последующие ревакцинации
делают каждые 10 лет.
При проведении противоэпидемических мероприятий в очаге дифтерии
прививкам подлежат контактировавшие лица, не привитые или не имеющие защитного уровня дифтерийного антитоксина по результатам
серологического обследования, а также лица, у которых с момента последней прививки против дифтерии прошло 10 лет и более.
Вакцина поставляется в лечебно-профилактические учреждения города Ижевска за счет федерального
бюджета и для населения является бесплатной.
Диагностика дифтерийной инфекции
Дифтерия (дифтерийная инфекция) — острое инфекционное, бактериальное заболевание. Возбудителем является палочковидная бактерия вида Corynebacterium, которую еще называют дифтерийная палочка или бацилла Лёффлера по имени первооткрывателя.
Болезнь передается воздушно-капельным и контактно-бытовым путем. Преимущественно поражает ротоглотку, чуть реже нос, верхние дыхательные пути. Может затрагивать глаза, кожу и половые органы. В России проводится вакцинация от дифтерии начиная с 3-х месячного возраста, поэтому случаи заболевания достаточно редки. Согласно данным ВОЗ в мире получают три рекомендуемые дозы 86% детей, в результате чего формируется стойкий пожизненный иммунитет.
Причины
Источником болезни является инфицированный человек: больной или носитель патогенного штамма. Возбудитель выделяется из организма в период выздоровления достаточно долго: от 15 дней до 3 месяцев. Путь передачи ― аэрозольный, чаще заражение происходит воздушно-капельным путем, реже контактно-бытовым или воздушно-пылевым путем. Палочка может оставаться активной на использованной больным посуде, полотенцах. Способна размножаться в продуктах питания: готовых блюдах, мясе, молоке, сыре.
Путь передачи ― аэрозольный, чаще заражение происходит воздушно-капельным путем, реже контактно-бытовым или воздушно-пылевым путем. Палочка может оставаться активной на использованной больным посуде, полотенцах. Способна размножаться в продуктах питания: готовых блюдах, мясе, молоке, сыре.
Бактерия обладает устойчивостью ко внешней среде, сохраняет жизнеспособность на протяжении 2 месяцев. На гладких поверхностях долго не задерживается, ее можно обнаружить на мягких игрушках, одежде, постельном белье, коврах, изделиях из шерсти. Дифтерийная палочка переносит холод, но погибает при температуре +60 С в течение 10 минут. Для нее также губительно ультрафиолетовое излучение (UV-лампы и прямые солнечные лучи), дезинфицирующие средства содержащие лизол или хлор.
Классификация
Дифтерию разделяют на локализованную и распространенную формы.
По вариантам течение делят на 4 формы:
Дифтерия ротоглотки, которая подразделяется на:
-
Локализованную, характеризующуюся катаральным, островчатым и плёночным воспалением небных миндалин. -
Распространенную, отличимую по наличию налета не только на миндалинах, но и на других слизистых ротоглотки. -
Субтоксическую, гипертоксическую и токсическую с 1 по 3 степени. -
Дифтерийный круп гортани, форма имеющая несколько вариантов течения: -
Локализованный (затронута только гортань). -
Распространенная, при котором поражена также трахея. -
Нисходящий, затрагивающий также и бронхи. -
Дифтерия, локализующаяся на других органах (участках тела): дифтерия носа, глаз, кожных покровов, половых органов.
-
Комбинированная форма заболевания, при которой затронуто несколько органов в не перечисленных выше комбинация.
В международной классификации болезней дифтерия имеет код A36.0 и несколько форм, исходя из локализации: дифтерия глотки, носоглотки, гортани, кожи, другая и неуточненная.
Симптомы дифтерии
К классической симптоматике, идентичной для большинства форм дифтерии, относятся:
-
повышение температуры; -
выраженная слабость; -
не сильный болевой синдром в горле; -
затрудненное глотание; -
плотно спаянный налет на миндалинах, чаще серо-белого цвета; -
отек шеи и слизистых, увеличение небных миндалин и шейных лимфоузлов.
При некоторых формах заболевания симптомы могут отличаться. В 75% случаев диагностируют локализованную форму. В 90% случаев диагностируют дифтерию носоглотки. Начало острое с умеренной интоксикацией организма, сопровождается повышением температуры тела до +39 С. Лихорадка, длится не более 3 дней. Затем, появляется налет, который уплотняется, приобретает блеск. Любые попытки удалить его вызывают кровотечение.
Дифтерия ротоглотки
Локализованная форма выражается в появлении фибринозных (чаще) или рыхлых (реже) на небных миндалинах. Носоглотка воспаляется, лимфоузлы неравномерно увеличиваются. Воспаления могут быть двусторонними и односторонними. Температура, как правило, не повышается, интоксикация слабо выражена. Болевые ощущения незначительные.
Локализованная дифтерия ротоглотки одна из самых легких форм. При своевременном лечении не прогрессирует, быстро заканчивается выздоровлением. Если болезнь сопровождалась температурой, она проходит на 2 — 3 сутки, налет на миндалинах сходит через неделю.
Если болезнь сопровождалась температурой, она проходит на 2 — 3 сутки, налет на миндалинах сходит через неделю.
Распространенная форма встречается редко, отличается наличием налета не только на миндалинах, а также окружающих слизистых. Болевой синдром, интоксикация, увеличение лимфоузлов более сильные. Возникает боль в горле и области шеи, больному трудно глотать. Температура повышенная. Из основных симптомов:
-
Багровый цвет миндалин. -
Налет на миндалинах, язычке и небных дужках. -
Болезненная отечность подкожной клетчатки над лимфоузлами. Воспаление часто одностороннее.
Токсическая форма чаще диагностируется у взрослых. Для нее характерно бурное начало с повышением температуры до высоких значений. Среди основных симптомов:
-
Тахикардия. -
Цианоз губ. -
Артериальная гипотензия. -
Интенсивная боль в горле, шее, животе.
На фоне интоксикации и высокой температуры возможны тошнота, рвота, бредовые состояния, возбуждение.
Наиболее тяжело протекает гипертоксическая форма дифтерийной инфекции. Она развивается на фоне ослабленного иммунитета, у лиц с хроническими болезнями. Например, алкоголизм, цирроз, СПИД, сахарный диабет. Заболевание опасно высокой вероятностью развития геморрагического синдрома с надпочечниковой недостаточностью. Без своевременной медицинской помощи человек может умереть в течение 1 — 2 дней.
Дифтерийный круп
-
Локализованная форма. Патологические процессы органичны слизистой гортани. -
Распространенная форма. Инфицированы гортань и трахея.
Инфицированы гортань и трахея.
-
Нисходящая форма. Помимо гортани и трахеи, затронуты также бронхи.
Заболевание чаще отмечают у детей и младенцев. В последние годы возрастает число инфицированных среди взрослых. Иногда круп сопровождает дифтерию ротоглотки, в особо тяжелых формах патологические процессы могут проходить от ротовой полости до бронх. При этом, интоксикация слабо выражена, может возникнуть тошнота, повышение температуры. Инфекционный процесс сопровождается отечностью слизистых, воспалением дыхательных путей и голосовых складок гортани.
Заболевание проходит тремя последовательными стадиям:
-
Дисфоническая ― осиплость голоса, «лающий» кашель, дыхание шумное, кожные покровы бледны. Продолжительность стадии от 1 до 7 дней. -
Стенотическая стадия (стеноз гортани) ― сужение просвета приводящее к затрудненному дыханию. -
Асфиксическая ― сужение гортани достигает пика, иногда вовсе перекрывается, приводя к непроходимости дыхательных путей. До наступления этой стадии больной должен проходить лечение в стационаре. В противном случае гипоксия приведет к нарушению работы мозга, человек может умереть от удушья.
Дифтерия носа
Выражается в наличие фибринозного или пленчатого налета на слизистой. Выделения серозно-гнойные, дыхание через нос затруднено. Кожные покровы вокруг ноздрей раздражены. Температура тела повышается редко, признаки интоксикации отсутствуют. Часто дифтерия носа сопровождает поражения ротовой полости.
Дифтерия глаз
Конъюнктивит, часто односторонний, характеризуется умеренными серозными выделениями. Воспаление конъюнктивы сопровождается отечностью век. Интоксикация слабо выражена, температура не поднимается.
Токсическая дифтерия глаз отличается сильной отечностью век, выраженными гнойными выделениями, острым началом. Почти всегда затрагивает оба глаза. Отмечается общая интоксикация организма, лихорадка.
Другие формы дифтерии
Сюда входят дифтерийные инфекции уха, кожи, половых органов. Диагностируются редко, связаны со способом заражения. Могут сопровождать дифтерию ротоглотки или носа. Пораженные участки отечны, ближайшие лимфоузлы воспалены. Наблюдаются фибринозные налеты, гнойные выделения.
Кожные инфекции развиваются в местах повреждения: царапины, раны. Дифтерия половых органов вызывает поражения крайней плоти у мужчин, слизистой влагалища у женщин. Могут быть поражены ближайшие ткани и слизистые. Мочеиспускание при воспаленной уретре вызывает боль, бывают гнойные выделения. Общее состояния больных удовлетворительное, без симптомов интоксикации и повышенной температуры. В отличие от других форм, заболевание может протекать медленно и долго.
Бессимптомное носительство
У лиц, ранее перенесших дифтерию, можно наблюдать бессимптомное носительство. Переход заболевания в эту стадию отмечают у людей с хроническими болезнями, в частности с хроническими воспалениями носоглотки. Сроки носительства индивидуальны.
Диагностика дифтерии
Нередко клинический диагноз дифтерии ставят без проведения лабораторных анализов исходя из наличия серых пленок на слизистой горла. Это может иметь место в небольших населенных пунктах, при не сильном течении болезни у относительно здоровых взрослых. При обследовании детей, людей с хроническими заболеваниями, при неясной клинике рекомендовано проведение лабораторного исследования.
Наиболее часто выполняют следующие лабораторные тесты:
-
бактериологический анализ мазка; -
серологический анализ; -
ПЦР-анализ; -
клинический анализ крови; -
анализ на антитела.
Диагностика дифтерийного крупа осуществляется путем осмотра гортани через ларингоскоп. При развитии неврологических патологий требуется наблюдение невролога. При наличие признаков дифтерийного миокардита ― кардиолога, проведение УЗИ сердца и ЭКГ.
Краткое описание лабораторных исследований на дифтерию
Бактериологический анализ мазка является основным для постановки диагноза. Для исследования берут биоматериал, помещают его в питательную среду. Он находится в лаборатории 5 – 7 дней, за это время можно обнаружить не только развитие дифтерийной палочки, но и наличие у нее токсигенных свойств. Если выявлен токсигенный штамм, необходимо обследовать всех контактировавших с больным.
Дополнительно может быть проведена ПЦР-диагностика. Она не является обязательной для постановки диагноза. Забор материала происходит по аналогичной схеме. ПЦР позволяет выявить патоген и определить токсичен ли он.
Анализы на антитела (РПГА или ИФА) используются для постановки диагноза. Они занимают меньше времени, чем бактериологический анализ мазка, от 2 до 5 дней. Позволяют оценить уровень иммунитета (степень защищенность организма от инфекции). Поэтому эти анализы назначают людям, перед приемом на работу в лечебные учреждения и другие структуры, входящие в зону риска. Для исследования необходима венозная кровь.
Вне зависимости от метода диагностики РПГА или ИФА, результаты анализов расшифровывают одинаково. Маркер уровня равен 1:10 или 0,01 МЕ/мл. Если полученное значение ниже, значит шанс заболеть высок, необходима вакцинация.
Клинический анализ крови является вспомогательным методом, поскольку позволяет выявить лишь наличие бактериального воспаления. Результат нельзя использовать для дифференциальной диагностики, невозможно отличить дифтерию от ангины. Для проведения КАО используют венозную кровь.
После выявления возбудителя или при подозрении на дифтерию клиницист обязан в течение 24 часов уведомить органы здравоохранения. Это необходимо для организации ведения дозы антитоксической противодифтерийной сыворотки (АПДС) инфицированному, а также для проведения эпидрасследования и выявления круга контактных лиц. На это мероприятие службе здравоохранения отводится 48 часов.
Лечение
Дифтерию лечат врачи-инфекционисты, при осложненном течении заболевания могут привлекаться другие специалисты. Больных госпитализируют в инфекционные отделения клинических больниц. Амбулаторное лечение недопустимо, даже для бессимптомных носителей.
Терапия основывается на введении противодифтерийной антитоксической сыворотки. Среди дополнительных медикаментов:
-
При развитии вторичной инфекции назначают прием антибиотиков. -
При токсических формах дифтерии назначают глюкозу, кокарбоксилазу, глюкокортикоидные препараты. При необходимости может быть назначен плазмаферез (фильтрация плазмы крови) для очищения от токсических веществ. -
При угрозе асфиксии осуществляется интубация трахеи (введение эндотрахеальной трубки). При обтурации пленками, нарушающими непроходимость верхних дыхательных путей проводят трахеостомию (создание соустья полости в трахеи хирургическим путем).
Осложнения
Дифтерия несет серьезную опасность своими осложнениями, как во время заболевания, так и после выздоровления. Чаще всего течение болезни осложняется токсическим нефрозом (острое поражение почек), недостаточностью надпочечников, инфекционно-токсическим шоком, приводящим к коме. Нередки воспаления миокардита и стволов нервной системы. Среди серьезных осложнений паралич дыхательных путей, он может привести к асфиксии.
Самая частая причина смерти ― миокардит, как правило, наступает в конце первой, начале второй недели с момента заражения. Поражение нервной системы может произойти как в период болезни, так и через несколько месяцев после выздоровления. Также наблюдаются ранние и поздние периферические параличи. Это приводит к следующим последствиям: гнусавость голоса, поперхивание во время приема пищи, вываливание ее через нос, паралич мимической мускулатуры лица, косоглазие, птоз, невозможность различать вблизи мелкие предметы.
Прогноз и профилактика
Наиболее благоприятен прогноз при локализованных, легких и средних формах. Но, при условии своевременно оказанного лечения с использованием АПДС. Наиболее опасны и менее благоприятны токсические формы заболевания, позднее начало лечения и развитие осложнений.
Профилактика дифтерии заключается в своевременной вакцинации. Первая прививка ставится детям в возрасте 3-х месяцев, последующие в срок 9 — 12 месяцев, затем 7 лет, 12 лет и подросткам в 16-летнем возрасте. Пройти вакцинацию могут и взрослые. Иммунитет после прививки и перенесенного заболевания сохраняется на протяжении 10 лет. Массовая вакцинация населения позволила снизить смертность от дифтерии до < 5%. Ранее она достигала 60%.
Преимущества АО «СЗДЦМ»
Сдать анализы на дифтерию и другие бактериальные инфекции можно в одном из подразделений Северо-Западного центра доказательной медицины. Здесь для вас созданы все условия:
-
Доброжелательные сотрудники и отсутствие очередей. -
Квалифицированные лаборанты и точное, современное оборудование. -
Быстрая готовность результатов и несколько способов их получения.
Лабораторные терминалы и медицинские центры имеют удобное расположение для проезда на общественном транспорте и личном авто. Пройти исследование можно в Санкт-Петербурге и других городах ЛО, Великом Новгороде и Новгородское области, Калининграде и Пскове.
Вакцинация против дифтерии и столбняка
Вакцинация против дифтерии и столбняка
Согласно федеральных законов «О санитарно-эпидемиологическом благополучии населения» №52-ФЗ от 1999г. и «О качестве и безопасности пищевых продуктов» №29-ФЗ от 2000г. работники предприятий по производству пищевых продуктов, общественного питания и продовольственной торговли проходят обязательную вакцинацию против дифтерии (1 раз в 10 лет), брюшного тифа (1 раз в 3 года), кори (в возрасте до 35 лет) и гепатита А (1 раз в 10 лет), работники непищевых предприятий проходят обязательную вакцинацию против дифтерии и столбняка -1 раз в 10 лет.
Дифтерия
Дифтерия – инфекция, вызываемая дифтерийной палочкой. При дифтерии может возникать тяжелая ангина и выраженная интоксикация, иногда развивается поражение гортани (круп) с затруднением дыхания. Заболевание может осложняться поражением сердца, почек, нервной системы. Дифтерией болеют в любом возрасте, заражение происходит от больных и бактерионосителей воздушно-капельным путем, а так же через предметы, загрязненные капельками слюны и слизи из носоглотки.
Инфекция передается воздушно-капельным путем от больных и внешне здоровых носителей. Возможно заражение дифтерией через предметы, не исключается передача через продукты питания.
Во время эпидемии первой половины 90-х годов на территории стран СНГ, возникшей по причине низкого охвата прививками, дифтерией заболело около 120 тыс. человек, погибло около 6 тыс. человек. Начиная с 2002 года в России вновь отмечается рост заболеваемости, сопровождающийся увеличением доли тяжелых токсических форм до 25% и смещением заболеваемости на взрослых, что также вызвано снижением охвата ревакцинациями взрослого населения. По данным 2003 года лишь около 50% взрослых имеют иммунитет к этой инфекции.
Профилактика осуществляется с помощью вакцинации. Эффективность современных вакцин составляет 95-100%. Всемирной организацией здравоохранения вакцинация рекомендована для всех без исключения стран мира.
Осложнениями дифтерии могут быть: миокардит, полиневрит, параличи, снижение зрения, поражение почек.
Заболеваемость дифтерией в России в 2001 году составила 0.57 на 100 тысяч населения, что превышает таковую в большинстве экономически развитых государств.
Столбняк
Столбняк вызывается токсином столбнячной палочки, которая проникает в организм через кожные раны при травмах. Очень тяжелое, часто смертельное заболевание, проявляющееся в поражении нервной системы. Столбнячная палочка находится в основном в земле, куда попадает с испражнениями животных. От человека к человеку заболевание не передается.
Источником инфекции являются травоядные животные, у которых столбнячная палочка является частью микрофлоры кишечника; микроб сохраняется в почве длительное время в виде спор. Путь заражения человека — через загрязненные (обычно, почвой) раны кожи и слизистых оболочек.
Симптомы столбняка вызываются действием на нервную систему токсина, вырабатываемого бактерией. Они сначала выражаются в местных, а в последствии и генерализованных спазмах (тонических судорогах) мышц. Несмотря на экстренную реанимацию даже в развитых странах смертность достигает 25%. В развивающихся странах она достигает 80%. После перенесенного заболевания иммунитет у человека не формируется. Смерть, как правило, наступает в результате спазма дыхательной мускулатуры и паралича сердечной мышцы.
Заболеваемость столбняком в России составляет около 0.03 на 100 тысяч населения, а столбняк новорожденных не регистрируется. Этих результатов удалось достичь только благодаря массовой вакцинации. Целесообразность ее обусловлена повсеместным распространением возбудителей и тяжестью заболевания.
За подробной информацией Вы можете обратиться:
Гаврилюк Александр – тел. (812) 380-33-34 доб.78949, Email: [email protected]
Сингатуллов Ренат – тел. (812) 380-33-34 доб.78946, Email: [email protected]
Дифтерии и столняка |
Вакцинация против дифтерии
Дифтерия – это опасное инфекционное заболевание, которое вызывается микроорганизмом рода коринебактерии (бацилла Лёффлера).
Заболевание передается преимущественно воздушно-капельным путем и поражает органы дыхательной системы, кожу, глаза, нервную и даже половую систему. Повышение температуры, боль в горле, слабость, отек тканей шеи, увеличение многих групп лимфоузлов и появление налета на миндалинах в виде пленок – далеко не все прелести дифтерии.
Столбняк – патология крайне тяжело поддается терапии, вакцинация считается оптимальным методом для борьбы с ней. Когда делают прививку от столбняка? С 14-16 лет вакцинация против болезни каждые 10 лет. Ограничений по возрасту нет, что связано с ростом продолжительности жизни и широким распространением болезни. При нарушении графика иммунизации или при возникновении экстренной ситуации могут делать внеочередную прививку от столбняка.
Делать прививку от дифтерии и столбняка взрослым? – да, ведь заболевание опасно своими осложнениями.
- Развиваются заболевания нервной системы, чаще в виде параличей дыхательных путей, конечностей, мышц шеи и голосовых связок.
- Воспаление мышцы сердца или миокардит.
- Может наступить смертельный исход вследствие паралича дыхательной мускулатуры.
За последние десятилетия количество случаев заболеваемости дифтерией удалось значительно снизить благодаря вакцинации. Единичные случаи дифтерии чаще встречаются в коллективах, где есть не привитые.
Осложнения при отсутствии вакцинации от столбняка
- Наличие долго незаживающих ран, гнойные нарывы на коже
- Появление ран на кожном покрове или слизистой оболочке в результате обморожений, травм, сильных ожогов
- Укус животного
- Грядущая операция (если ранее прививку АКДС и АДС-м не делали)
График вакцинации от дифтерии для взрослых
В случае, если человек получил все прививки в положенное время – то вакцину вводят начиная с 14-16-летнего возраста каждые 10 лет однократно.
Если человек пропустил вакцинацию более 10 лет, то иммунизация против дифтерии и столбняка проводится по схеме 0-1-6, то есть интервал между первой и второй вакцинацией 30-45 дней, ревакцинация через 6 месяцев от первой прививки, далее через каждые 10 лет проводится однократная ревакцинация.
Все данные о необходимых прививках содержаться в прививочной карте в медицинской книжке. Их составляет и ведет участковая служба в поликлинике. Вызывает на прием и вакцинацию чаще всего участковая медсестра.
Вакцинация против дифтерии и столбняка входят в обязательные прививки согласно национальному календарю профилактических прививок. Приказу МЗ РФ от 21.03.2014г. “Об утверждении национального календаря профилактических прививок и профилактических прививок по эпидемическим показаниям”.
Дифтерия
Дифтерия — инфекционное заболевание, вызываемое бактерией Corynebacterium diphtheriae (бацилла Лёффлера). Чаще всего поражает ротоглотку, но нередко затрагивает гортань, бронхи, кожу и другие органы. Инфекция передаётся воздушно-капельным путём. Возможен контактно-бытовой путь передачи, особенно в жарких странах, где часты кожные формы дифтерии. Тяжесть болезни обусловлена крайне ядовитым токсином, который выделяет дифтерийная палочка. Встречаются и доброкачественные формы, например дифтерия носа, которая протекает без выраженной интоксикации.
Если дифтерия поражает ротоглотку, то помимо тяжёлой интоксикации, возможно развитие крупа — закупорки дыхательных путей дифтерийной плёнкой и отёком, особенно у детей.
Возбудитель
Дифтерийная палочка — грамположительные палочковидные бактерии рода Corynebacterium. Впервые возбудитель был обнаружен на срезах плёнок, полученных из ротоглотки больных в 1883 г. Эдвином Клебсом. Через год Фридрихом Лёффлером была выделена чистая культура. Дифтерийный токсин получили Э. Ру и А. Иерсен. Анатоксин обнаружил Рамон Гастон в 1923 г. и предложил использовать его для активной иммунизации.
Corynebacterium diphtheriae — крупные, прямые, слегка изогнутые полиморфные палочковидные бактерии. На полюсах клеток локализуются метахроматические зёрна волютина, придавая клеткам характерную форму «булавы». Зёрна волютина окрашиваются метиленовым синим по Нейссеру. На микропрепаратах располагаются одиночно, или, вследствие особенностей деления клеток, располагаются в форме латинской буквы V или Y. Спор и капсул не образуют.
Источники инфицирования
Дифтерия является антропонозом, то есть резервуаром болезни выступают люди. Заражение здорового человека может произойти от:
- Больного дифтерией. Чем более выражена тяжесть, тем больше бактерий выделяет больной.
- Здорового носителя бактерии.
Пути передачи
- Воздушно-капельный (при кашле, чихании)
- Контактно-бытовой (через предметы, с которыми соприкасался больной)
- Пищевой — через заражённые продукты (молоко, сыр и пр.)
Классификация
По локализации различают локализованную и распространённую формы дифтерии.
По формам и вариантам течения различают:
- Дифтерия ротоглотки:
- локализованная — с катаральным, островчатым и плёночным воспалением;
- распространённая — с налётами за пределами ротоглотки;
- субтоксическая, токсическая (I, II и III степени), гипертоксическая.
- Дифтерийный круп:
- локализованный — дифтерия гортани;
- распространённый — дифтерия гортани и трахеи;
- нисходящий — дифтерия гортани, трахеи, бронхов.
- Дифтерия других локализаций: носа, глаз, кожи, половых органов.
- Комбинированные формы дифтерии с одновременным поражением нескольких органов.
Клиническая картина
Грязно-белая плёнка на мягком нёбе, классический признак дифтерии.
Заболевание сопровождается следующими симптомами:
- Повышение температуры;
- Бледность кожных покровов;
- Выраженная слабость;
- Отёк мягких тканей шеи;
- Лёгкая боль в горле, затруднение глотания;
- Увеличение нёбных миндалин;
- Гиперемия и отёк слизистой глотки;
- Плёнчатый налёт (может быть любого цвета, но чаще всего бывает серо-белым), покрывающий нёбные миндалины и иногда распространяющийся на нёбные дужки, мягкое нёбо, боковые стенки глотки, гортань;
- Увеличение шейных лимфоузлов.
Дифтерия ротоглотки
Самой частой формой дифтерии (90—95 % всех случаев) является дифтерия ротоглотки. При локализованной форме налёты только на миндалинах. Интоксикация слабо выражена, температура до 38—39°С, головная боль, недомогание, незначительные боли при глотании. Наиболее типична плёнчатая (сплошная) форма дифтерии, при которой плёнка с очерченными краями покрывает всю миндалину, трудно снимается шпателем; при попытке её снятия, поверхность миндалины кровоточит; плёнка плотная; лимфатические узлы малоболезненны, подвижны. При островчатой форме налёты имеют вид островков различной величины, расположены чаще вне лакун, на внутренней стороне миндалин, края налётов неровные.
Распространённая дифтерия
При распространённой форме дифтерии, налёты распространяются за пределы миндалин на нёбные дужки и язычок. Интоксикация более выражена: отмечаются вялость, боль в горле. Регионарные лимфатические узлы увеличены до крупного боба, чувствительны, но отёка шейной клетчатки нет.
Токсическая дифтерия
При токсической, одной из самых тяжёлых форм дифтерии, заболевание начинается бурно, с первых часов температура повышается до 40°С, выражены вялость, сонливость, сильная слабость, головная боль и боль в горле, иногда боль в шее и в животе. Появляются гиперемия и отечность зева, налёты, вначале нежные желеобразные в виде паутинообразной сетки. Ко 2—3-му дню налёты становятся толстыми, грязно-серого цвета, полностью покрывают миндалины, дужки, язычок, мягкое и твёрдое нёбо.
Дыхание через нос затруднено, сукровичные выделения из носа, иногда плёнки на его слизистой; голос становится сдавленным с гнусавым оттенком. Изо рта периодически появляется сладковато-приторный запах. Увеличиваются все группы шейных лимфатических узлов, которые образуют конгломерат, эластичный и болезненный, с отёком шеи (видно при осмотре больного). Цвет кожных покровов не изменён, надавливание безболезненное, не оставляет ямок. При токсической дифтерии I степени отёк шейной клетчатки достигает середины шеи; при токсической дифтерии II степени — отёк до ключицы; при III степени — отёк клетчатки ниже ключицы.
Гипертоксическая и геморрагическая формы
Наиболее тяжёлыми являются гипертоксические и геморрагические формы дифтерии.
При гипертоксической форме резко выражены симптомы интоксикации. Наблюдаются гипертермия, бессознательное состояние, коллапс, судороги. В зеве обширные налёты и отёк. Течение болезни стремительное. Летальный исход наступает на 2—3-й день болезни при нарастании сердечно-сосудистой недостаточности.
Геморрагическая форма дифтерии отличается множественной геморрагической сыпью с обширными кровоизлияниями, кровотечением из носа, дёсен, желудочно-кишечного тракта. В ротоглотке дифтерические налёты пропитаны кровью.
Развитие этих тяжёлых форм наблюдается при запоздалой диагностике и позднем введении противодифтерийной сыворотки. Без её применения выздоровление наступает лишь при локализованной форме дифтерии, но в этом случае, как правило, развиваются типичные осложнения: миокардит, периферические параличи. При раннем введении сыворотки симптомы интоксикации исчезают быстро, налёты в зеве отторгаются к 6—8-му дню.
Дифтерия других локализаций
Кроме зева, дифтерия может поражать слизистые оболочки носа, глаз, половых органов, а также раневые поверхности. Токсигенные Corynebacterium diphtheriae выделяют токсин, который вызывает отёк и некроз слизистых, поражает миокард, периферические нервы (особенно часто — языкоглоточный и блуждающий с развитием паралича мягкого нёба), почки.
Лечение.
Лечение дифтерии проводится только в условиях стационара (в больнице). Госпитализация обязательна для всех больных, а также больных с подозрением на дифтерию и бактерионосителей.
Главным в лечении всех форм дифтерии (кроме бактерионосительства) является введение антитоксической противодифтерийной сыворотки (ПДС), которая подавляет дифтерийный токсин. Антибиотики не оказывают существенного действия на возбудителя дифтерии.
Осложнения
Осложнения дифтерии связаны с повреждением нервных и других клеток крайне ядовитым дифтерийным токсином.
Миокардиты, нарушения работы нервной системы, которые обычно проявляются в виде параличей. Чаще всего дифтерия осложняется параличами мягкого нёба, голосовых связок, мышц шеи, дыхательных путей и конечностей. Из-за паралича дыхательных путей может наступить асфиксия (при крупе), провоцирующая летальный исход.
Иммунитет
После перенесённого заболевания формируется нестойкий иммунитет, и приблизительно через 10-11 лет человек может заболеть вновь. Повторное заболевание носит нетяжёлый характер и переносится легче.
Профилактика
Основное значение в борьбе с дифтерией имеет активная плановая вакцинация населения вакцинами, содержащими адсорбированный дифтерийный анатоксин (АКДС-вакцина, АКДС-анатоксин, АДС—М-анатоксин), которая проводится в соответствии с календарём профилактических прививок; это позволяет создать длительный и напряжённый антитоксический иммунитет.
Большую роль в предупреждении распространения инфекции играют раннее выявление больных дифтерией, в том числе лёгкими и стёртыми формами, путём активного наблюдения и раннего бактериологического обследования больных ангиной, паратонзиллярным абсцессом, острым паратонзиллярным абсцессом; выявление носителей токсигенных штаммов коринебактерий дифтерии в очагах инфекции и при обследовании коллективов риска.
Больные и носители токсигенных коринебактерий подлежат изоляции и лечению (санации) в условиях стационара.
Дифтерия | Nature Reviews Disease Primers
Wagner, K. S. et al. Дифтерия в Соединенном Королевстве, 1986–2008 гг .: возрастающая роль Corynebacterium ulcerans . Epidemiol. Заразить. 138 , 1519–1530 (2010).
CAS
PubMed
Статья
Google Scholar
Индумати В. А., Шиха Р. и Сурьяпракаш Д. Р. Дифтерийное заболевание у полностью иммунизированного ребенка, вызываемое Corynebacterium pseudodiphtheriticum . Indian J. Med. Microbiol. 32 , 443–445 (2014).
CAS
PubMed
Статья
Google Scholar
Pimenta, F. P. et al. ПЦР на ген dtxR: приложение для диагностики нетоксигенных и токсигенных Corynebacterium diphtheriae . Мол. Клетка. Зонды 22 , 189–192 (2008).
CAS
PubMed
Статья
Google Scholar
Bolt, F. et al. Мультилокусное типирование последовательностей выявляет доказательства рекомбинации и двух различных линий Corynebacterium diphtheriae . J. Clin. Microbiol. 48 , 4177–4185 (2010).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Всемирная организация здравоохранения. Вакцина против дифтерии: позиционный документ ВОЗ — август 2017 г. Wkly Epidemiol. Рек. 92 , 417–435 (2017). В этом всеобъемлющем документе с изложением позиции обобщается важная и полезная информация о дифтерии и вакцинах .
Google Scholar
Эфстратиу А. и Джордж Р. С. Микробиология и эпидемиология дифтерии. Rev. Med. Microbiol. 7 , 31 (1996). В данной статье представлены подробности выделения и идентификации Corynebacterium diphtheriae и других видов с точки зрения эпидемиологии инфекции.
Артикул
Google Scholar
Lodeiro-Colatosti, A. et al. Вспышка дифтерии в общинах индейцев, Вонкен, Венесуэла, 2016–2017 гг. Emerg. Заразить. Дис. 24 , 1340–1344 (2018).
PubMed
PubMed Central
Статья
Google Scholar
Page, K. R. et al. Кризис общественного здравоохранения Венесуэлы: чрезвычайная ситуация в регионе. Ланцет 393 , 1254–1260 (2019). Вместе со ссылками 9 и 33 в этом отчете описываются вспышки дифтерии и меры, принятые для борьбы с ее распространением .
PubMed
Статья
Google Scholar
Dureab, F. et al. Вспышка дифтерии в Йемене: влияние конфликта на хрупкую систему здравоохранения. конфл. Здравоохранение 13 , 19 (2019 г.).
PubMed
PubMed Central
Статья
Google Scholar
Bergamini, M. et al. Свидетельства увеличения носительства Corynebacterium spp. у здоровых лиц с низкими титрами антител против дифтерийного анатоксина. Epidemiol. Заразить. 125 , 105–112 (2000).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Шарма, Н. К., Банаваликер, Дж. Н., Ранджан, Р. и Кумар, Р. Бактериологические и эпидемиологические характеристики случаев дифтерии в Дели и его окрестностях — ретроспективное исследование. Indian J. Med. Res. 126 , 545–552 (2007).
CAS
PubMed
Google Scholar
Wagner, K. S. et al. Дифтерия в постэпидемическом периоде, Европа, 2000–2009 гг. Emerg. Заразить. Дис. 18 , 217–225 (2012).
PubMed
PubMed Central
Статья
Google Scholar
Rengganis, I. Вакцинация взрослых от дифтерии. Acta Med. Индонезия 50 , 268–272 (2018).
Google Scholar
van Wijhe, M. et al. Количественная оценка воздействия программ массовой вакцинации на зарегистрированные случаи в Нидерландах. Epidemiol. Заразить. 146 , 716–722 (2018).
PubMed
Статья
Google Scholar
Лови-Тун, Ю. Г., Холл, К. К., Чанг, А.Б., Андерсон, Дж. И О’Грэйди, К.-А. F. Своевременность иммунизации группы детей из числа городских аборигенов и жителей островов Торресова пролива. BMC Public Health 16 , 1159 (2016).
PubMed
PubMed Central
Статья
Google Scholar
Basak, M. Структура и тенденции заболеваемости в инфекционном отделении Медицинского колледжа и больницы Северной Бенгалии. J. Clin. Диаг. Res. 9 , LC01 – LC04 (2015).
PubMed
PubMed Central
Google Scholar
Сайкия, Л., Нат, Р., Сайкия, Н. Дж., Чоудхури, Г. и Саркар, М. Вспышка дифтерии в Ассаме, Индия. Юго-Восточная Азия J. Trop. Med. Общественное здравоохранение 41 , 647–652 (2010).
PubMed
Google Scholar
Хури-Булос Н. и др. Изменяющаяся эпидемиология дифтерии в Иордании. Бык. Всемирный орган здравоохранения. 66 , 65–68 (1988).
CAS
PubMed
PubMed Central
Google Scholar
Larsson, P., Brinkhoff, B. & Larsson, L. Corynebacterium diphtheriae в среде носителей и пациентов. J. Hosp. Заразить. 10 , 282–286 (1987).
CAS
PubMed
Статья
PubMed Central
Google Scholar
Hallander, H.O., Haeggman, S. & Löfdahl, S. Эпидемиологическое типирование Corynebacterium diphtheriae , выделенных в Швеции в 1984–1986 гг. Сканд. J. Infect. Дис. 20 , 173–176 (1988).
CAS
PubMed
Статья
Google Scholar
Витек, К. Дифтерия в бывшем Советском Союзе: возрождение пандемического заболевания. Emerg. Заразить. Дис. 4 , 539–550 (1998).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Центры по контролю и профилактике заболеваний (CDC). Вспышка дифтерии — провинция Сарабури, Таиланд, 1994 г. MMWR Morb. Смертный. Wkly. Реп. 45 , 271–273 (1996).
Google Scholar
Эфстратиу, А. Отчет: первое международное совещание Европейской лабораторной рабочей группы по дифтерии. PHLS Microbiol. Копать землю. 12 , 83–92 (1995).
Google Scholar
Эфстратиу, А. и Рур, К. Европейская лабораторная рабочая группа по дифтерии: глобальная микробиологическая сеть. J. Infect. Дис. 181 , S146 – S151 (2000).
PubMed
Статья
Google Scholar
Neal, S. & Efstratiou, A., от имени DIPNET.ДИПНЕТ — создание специализированной сети эпиднадзора за дифтерией в Европе. евро Surveill. 12 , E9 – E10 (2007).
CAS
PubMed
Статья
Google Scholar
Кембабанова Г. и др. Эпидемическое расследование дифтерии, Республика Казахстан, 1990–1996 гг. J. Infect. Дис. 181 , S94 – S97 (2000).
PubMed
Статья
Google Scholar
Skogen, V. et al. Иммунитет к дифтерии у детей в северной Норвегии и северо-западе России. Вакцина 19 , 197–203 (2000).
CAS
PubMed
Статья
Google Scholar
Маркина С.С., Максимова Н.М., Лазикова Г.Ф. Заболеваемость дифтерией в современной России. Ж. Микробиол. Эпидемиол. Иммунобиол. 1 , 31–37 (2005).
Google Scholar
Besa, N.C. et al. Вспышка дифтерии с высокой смертностью на северо-востоке Нигерии. Epidemiol. Заразить. 142 , 797–802 (2013).
PubMed
PubMed Central
Статья
CAS
Google Scholar
Мурхекар, М. Эпидемиология дифтерии в Индии, 1996–2016: значение для профилактики и борьбы. г. J. Tropical Med. Hyg. 97 , 313–318 (2017).
Артикул
Google Scholar
Matsuyama, R. et al. Анализ неопределенности и чувствительности основного репродуктивного числа дифтерии: тематическое исследование лагеря беженцев рохинджа в Бангладеш, ноябрь – декабрь 2017 г. PeerJ 6 , e4583 (2018).
PubMed
PubMed Central
Статья
Google Scholar
Reynolds, G.E. et al. Действия общественного здравоохранения после вспышки токсигенной кожной дифтерии в центре переселения беженцев в Окленде. Commun. Дис. Intell. Q. Rep. 40 , E475 – E481 (2016).
PubMed
Google Scholar
Рахман, М. Р. и Ислам, К. Массовая вспышка дифтерии среди беженцев рохинджа: извлеченные уроки. J. Travel Med. 26 , 1–3 (2019).
Артикул
Google Scholar
Jablonka, A. et al. Иммунитет против столбняка и дифтерии у беженцев в Европе в 2015 г. Инфекции 45 , 157–164 (2016).
Артикул
CAS
Google Scholar
Exavier, M.-M. и другие. Дифтерия у детей на севере Гаити. J. Trop. Педиатр. 65 , 183–187 (2018).
Артикул
Google Scholar
Raad, I. I., Chaftari, A.-M., Dib, R. W., Graviss, E. A. & Hachem, R. Новые вспышки, связанные с конфликтами и сбоями систем здравоохранения на Ближнем Востоке. Заражение. Контроль. Hosp. Эпидемиол. 39 , 1230–1236 (2018).
PubMed
Статья
Google Scholar
Удгаонкар, США, Дхармадхикари, К. А., Кулкарни, Р. Д., Кулкарни, В. А. и Павар, С. Г. Изучение переносчиков дифтерии в Мирадже. Indian Pediatr. 26 , 435–439 (1989).
CAS
PubMed
Google Scholar
Björkholm, B., Olling, S., Larsson, P. & Hagberg, L. Вспышка дифтерии среди шведских алкоголиков. Инфекции 15 , 354–358 (1987).
Артикул
Google Scholar
Кауфманн Д., Отт П. и Збинден Р. Ларингофарингит, вызванный Corynebacterium ulcerans . Инфекции 30 , 168–170 (2002).
CAS
Статья
Google Scholar
van Dam, A. P. et al. Случай дифтерии в Нидерландах из-за инфекции Corynebacterium ulcerans . Нед. Tijdschr. Geneeskd 147 , 403–406 (2003).
PubMed
Google Scholar
Pers, C. Инфекция, вызванная « Corynebacterium ulcerans », продуцирующим дифтерийный токсин. Acta Pathol. Microbiol. Сканд. Сер. В 95Б , 361–362 (2009).
Google Scholar
Джефкотт, А. Э., Гиллеспи, Э. Х., Давенпорт, К., Эмерсон, Дж. У. и Морони, П. Дж. Нетоксигенный Corynebacterium diphtheriæ в школе-интернате. Ланцет 305 , 1025–1026 (1975).
Артикул
Google Scholar
Уилсон, А. П. Р. Возвращение Corynebacterium diphtheriae: рост нетоксигенных штаммов. J. Hosp. Заразить. 30 , 306–312 (1995). В данной статье представлен метаанализ клинической важности нетоксигенных C. diphtheriae .
PubMed
Статья
Google Scholar
Гублер, Дж., Хубер-Шнайдер, К., Грюнер, Э. и Альтвегг, М. Вспышка нетоксигенной инфекции Corynebacterium diphtheriae : единственный бактериальный клон, вызывающий инвазивную инфекцию среди потребителей наркотиков в Швейцарии. Clin. Заразить. Дис. 27 , 1295–1298 (1998).
CAS
PubMed
Статья
Google Scholar
Ричер М. и др. Нетоксигенный Corynebacterium diphtheriae : новый патоген в Англии и Уэльсе? Emerg. Заразить. Дис. 6 , 640–645 (2000).
CAS
PubMed
PubMed Central
Google Scholar
Усонис, В.и другие. Дифтерия в Литве, 1986–1996 гг. J. Infect. Дис. 181 , S55 – S59 (2000).
PubMed
Статья
Google Scholar
Zasada, AA, Baczewska-Rej, M. & Wardak, S. Рост числа нетоксигенных Corynebacterium diphtheriae инфекций в Польше — молекулярная эпидемиология и антимикробная чувствительность штаммов, выделенных во время прошлых вспышек и циркулирующих в настоящее время в Польше. Внутр. J. Infect. Дис. 14 , e907 – e912 (2010).
CAS
PubMed
Статья
Google Scholar
Канунго, Р., Виджаялакшми, Н., Налини, П. и Бхаттачарья, С. Дифтерия, вызванная нетоксигенными Corynebacterium diphtheriae : отчет о двух случаях. Indian J. Med. Microbiol. 20 , 50–52 (2002).
CAS
PubMed
Google Scholar
Засада А.А., Залеска М., Подласин Р. Б. и Сеферинска И. Первый случай сепсиса, вызванного нетоксигенной Corynebacterium diphtheriae в Польше: отчет о болезни. Ann. Clin. Microbiol. Противомикробный. 4 , 8 (2005).
PubMed
PubMed Central
Статья
Google Scholar
Romney, M. G. et al. Появление инвазивного клона нетоксигенной Corynebacterium diphtheriae среди городской бедноты Ванкувера, Канада. J. Clin. Microbiol. 44 , 1625–1629 (2006).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Засада А.А. Нетоксигенный высокопатогенный клон Corynebacterium diphtheriae , Польша, 2004–2012 гг. Emerg. Заразить. Дис. 19 , 1870–1872 (2013).
PubMed
PubMed Central
Статья
Google Scholar
Мэй, М. Л. А., Макдугалл, Р. Дж. И Робсон, Дж. М. Corynebacterium diphtheriae и вернувшийся тропический путешественник. J. Travel. Med. 21 , 39–44 (2014).
PubMed
Статья
Google Scholar
Сангал В. и Хоскиссон П. А. Эволюция, эпидемиология и разнообразие Corynebacterium diphtheriae : новые взгляды на старого врага. Заражение. Genet. Evolut. 43 , 364–370 (2016).
Артикул
Google Scholar
Grimont, P. A. D. et al. Международная номенклатура риботипов Corynebacterium diphtheriae . Res. Microbiol. 155 , 162–166 (2004). В этой статье описывается база данных риботипов для C. diphtheriae с названиями и размерами фрагментов ДНК каждого риботипа .
CAS
PubMed
Статья
Google Scholar
Мокроусов, И. в Molecular Typing in Bacterial Infections (eds de Filippis, I. & McKee, M. L.) 283–300 (Humana Press, 2012).
Сет-Смит, Х. М. и Эгли, А. Секвенирование всего генома для надзора за дифтерией в условиях низкой заболеваемости. Фронт. Общественное здравоохранение 7 , 235 (2019).
PubMed
PubMed Central
Статья
Google Scholar
Засада, А.A., Jagielski, M., Rzeczkowska, M. & Januszkiewicz, A. Использование MLVA для генотипирования Corynebacterium diphtheriae — предварительные исследования. Med. Dosw. Микробиол. 63 , 209–218 (2011).
CAS
PubMed
Google Scholar
Мокроусов И., Лимещенко Е., Вязовая А., Нарвская О. Сполиготипирование Corynebacterium diphtheriae на основе комбинированного использования двух локусов CRISPR. Biotechnol. J. 2 , 901–906 (2007).
CAS
PubMed
Статья
Google Scholar
Сангал В., Финеран П. К. и Хоскиссон П. А. Новые конфигурации систем CRISPR – Cas типа I и II в Corynebacterium diphtheriae . Микробиология 159 , 2118–2126 (2013).
CAS
PubMed
Статья
Google Scholar
Revez, J. et al. Исследование использования полногеномного секвенирования для эпиднадзора за инфекционными заболеваниями: быстрое расширение национальных возможностей Европы, 2015–2016 гг. Фронт. Общественное здравоохранение 5 , 347 (2017).
PubMed
PubMed Central
Статья
Google Scholar
Coyle, M. B. et al. Молекулярная эпидемиология трех биотипов Corynebacterium diphtheriae во время вспышки болезни в Сиэтле, 1972–1982 гг. J. Infect. Дис. 159 , 670–679 (1989).
CAS
PubMed
Статья
Google Scholar
Popovic, T. et al. Молекулярная эпидемиология дифтерии в России, 1985–1994 гг. J. Infect. Дис. 174 , 1064–1072 (1996).
CAS
PubMed
Статья
Google Scholar
Nakao, H. et al. Неоднородность гена токсина дифтерии, tox, и его регуляторного элемента, dtxR , у штаммов Corynebacterium diphtheriae , вызывающих эпидемическую дифтерию в России и Украине. J. Clin. Microbiol. 34 , 1711–1716 (1996).
CAS
PubMed
PubMed Central
Google Scholar
Комбарова С.И. и др. Генетическая структура штаммов Corynebacterium diphtheriae , выделенных в России во время эпидемий различной интенсивности. Ж. Микробиол. Эпидемиол. Иммунобиол. 3 , 3–8 (2001).
Google Scholar
von Hunolstein, C. et al. Молекулярная эпидемиология и характеристика штаммов Corynebacterium diphtheriae и Corynebacterium ulcerans , выделенных в Италии в 1990-е годы. J. Med. Microbiol. 52 , 181–188 (2003).
Артикул
CAS
Google Scholar
Popovic, T. et al. Молекулярная эпидемиология дифтерии. J. Infect. Дис. 181 (Доп.1), S168 – S177 (2000). В этой обзорной статье описывается молекулярный подтип C. diphtheriae со значительным генетическим разнообразием и стабильностью гена, кодирующего дифтерийный токсин, в эпидемических клонах .
CAS
PubMed
Статья
Google Scholar
Колодкина В.В. и др. Молекулярная эпидемиология штаммов C. diphtheriae в разные фазы эпидемии дифтерии в Беларуси. BMC Infect. Дис. 6 , 129 (2006).
PubMed
PubMed Central
Статья
CAS
Google Scholar
Hong, K.-W. и другие. Сравнительный геномный и филогенетический анализ токсигенного клинического изолята Corynebacterium diphtheriae штамм B-D-16-78 из Малайзии. Infect., Genet. Evolut. 54 , 263–270 (2017).
CAS
Статья
Google Scholar
Grosse-Kock, S. et al. Геномный анализ эндемичных клонов токсигенных и нетоксигенных Corynebacterium diphtheriae в Беларуси во время и после крупной эпидемии 1990-х годов. BMC Genomics 18 , 873 (2017).
PubMed
PubMed Central
Статья
CAS
Google Scholar
Benamrouche, N. et al. Микробиологическая и молекулярная характеристика Corynebacterium diphtheriae , выделенного в Алжире в период с 1992 по 2015 год. Clin. Microbiol. Заразить. 22 , 1005.e1–1005.e7 (2016).
CAS
Статья
Google Scholar
Paveenkittiporn, W., Sripakdee, S., Koobkratok, O., Sangkitporn, S. & Kerdsin, A. Молекулярная эпидемиология и чувствительность к противомикробным препаратам Corynebacterium diphtheriae в Таиланде, 2012 г. . Genet. Evol. 75 , 104007 (2019).
CAS
PubMed
Статья
Google Scholar
Both, L. et al. Молекулярно-эпидемиологический обзор токсигенных дифтерийных инфекций в Англии в период с 2007 по 2013 год. J. Clin. Microbiol. 53 , 567–572 (2015).
CAS
PubMed
PubMed Central
Статья
Google Scholar
du Plessis, M. et al. Молекулярная характеристика изолятов вспышки Corynebacterium diphtheriae , Южная Африка, март – июнь 2015 г. Emerg.Заразить. Дис. 23 , 1308–1315 (2017).
PubMed
PubMed Central
Статья
Google Scholar
Mohd Khalid, M. K. N. et al. Молекулярная характеристика изолятов Corynebacterium diphtheriae в Малайзии в период с 1981 по 2016 год. J. Med. Microbiol. 68 , 105–110 (2019).
PubMed
Статья
CAS
Google Scholar
Meinel, D. M. et al. Расследование вспышки токсигенной Corynebacterium diphtheriae раневой инфекции у беженцев из Северо-Восточной Африки и Сирии в Швейцарии и Германии с помощью полногеномного секвенирования. Clin. Microbiol. Заразить. 22 , 1003.e1–1003.e8 (2016).
CAS
Статья
Google Scholar
Дангель А., Бергер А., Конрад Р., Бишофф Х. и Синг А. Географически разнообразные кластеры нетоксигенной инфекции Corynebacterium diphtheriae , Германия, 2016–2017 гг. Emerg. Заразить. Дис. 24 , 1239–1245 (2018).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Timms, VJ, Nguyen, T., Crighton, T., Yuen, M. & Sintchenko, V. Сравнение всего генома изолятов Corynebacterium diphtheriae из Австралии выявляет различия в пангеномах респираторных и кожные деформации. BMC Genomics 19 , 869 (2018).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Dangel, A., Berger, A., Konrad, R. & Sing, A. Филогения факторов патогенности, связанных с дифтерией, на основе NGS в различных Corynebacterium spp. подразумевает видоспецифичную передачу вирулентности. BMC Microbiol. 19 , 28 (2019). Это геномное исследование обнаружило существование различных генетических фонов DT-опосредованной патогенности у нескольких видов Corynebacterium и показало, что эволюция tox путей передачи способствует появлению патогенных штаммов. .
PubMed
PubMed Central
Статья
Google Scholar
Hardy, B. L. et al. Corynebacterium pseudodiphtheriticum использует компоненты вирулентности Staphylococcus aureus в новой стратегии полимикробной защиты. мБио 10 , e02491-18 (2019).
PubMed
PubMed Central
Статья
Google Scholar
Рэмси, М. М., Фрейре, М. О., Габрильска, Р. А., Рамбо, К. П. и Лемон, К. П. Staphylococcus aureus смещается в сторону комменсализма в ответ на видов Corynebacterium . Фронт. Microbiol. 7 , 1230 (2016).
PubMed
PubMed Central
Статья
Google Scholar
Chen, S. T. & Puthucheary, S. D. Некоторые эпидемиологические аспекты дифтерии в Малайзии. Троп. Геогр. Med. 28 , 211–215 (1976).
CAS
PubMed
Google Scholar
Czajka, U., Wiatrzyk, A., Mosiej, E., Formińska, K. & Zasada, AA Изменения профилей MLST и биотипов изолятов Corynebacterium diphtheriae от периода вспышки дифтерии до периода инвазивные инфекции, вызванные нетоксигенными штаммами, в Польше (1950–2016 гг.). BMC Infect. Дис. 18 , 121 (2018).
PubMed
PubMed Central
Статья
CAS
Google Scholar
Kang, H.J. et al. Медленно формирующаяся изопептидная связь в структуре основного пилина SpaD из Corynebacterium diphtheriae имеет значение для сборки пилуса. Acta Crystallogr. Разд. D Biol. Кристаллогр. 70 , 1190–1201 (2014).
CAS
Статья
Google Scholar
Mandlik, A., Swierczynski, A., Das, A. & Ton-That, H. Corynebacterium diphtheriae использует специфические минорные пилины для нацеливания на эпителиальные клетки глотки человека. Мол. Microbiol. 64 , 111–124 (2007).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Морейра, Л. О., Маттос-Гуаральди, А. Л. и Андраде, А. Ф. Б. Новый липоарабиноманнаноподобный липогликан (CdiLAM) способствует прикреплению Corynebacterium diphtheriae к эпителиальным клеткам. Arch. Microbiol. 190 , 521–530 (2008).
CAS
PubMed
Статья
Google Scholar
Ott, L. et al. Corynebacterium diphtheriae протеин, связанный с инвазией (DIP1281), участвует в организации клеточной поверхности, адгезии и интернализации в эпителиальных клетках. BMC Microbiol. 10 , 2 (2010).
PubMed
PubMed Central
Статья
CAS
Google Scholar
Колодкина В., Денисевич Т., Титов Л. Идентификация гена Corynebacterium diphtheriae , участвующего в прикреплении к эпителиальным клеткам. Заражение. Genet. Evolut. 11 , 518–521 (2011).
CAS
Статья
Google Scholar
Moreira, Ld. O. et al. Влияние ограничения железа на адгезию и углеводы клеточной поверхности штаммов Corynebacterium diphtheriae . заявл.Environ. Microbiol. 69 , 5907–5913 (2003).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Sabbadini, P. S. et al. Corynebacterium diphtheriae 67-72p гемагглютинин, характеризуемый как белок DIP0733, способствует инвазии и индукции апоптоза в клетках HEp-2. Microb. Возбудитель. 52 , 165–176 (2012).
CAS
Статья
Google Scholar
Antunes, C.A. et al. Характеристика DIP0733, многофункционального фактора вирулентности Corynebacterium diphtheriae . Микробиология 161 , 639–647 (2015).
CAS
PubMed
Статья
Google Scholar
Peixoto, R. S. et al. Инвазия эндотелиальных клеток и артритогенный потенциал эндокардита Corynebacterium diphtheriae . Микробиология 160 , 537–546 (2014).
CAS
PubMed
Статья
Google Scholar
Trost, E. et al. Сравнительный анализ двух полных геномов Corynebacterium ulcerans и определение факторов вирулентности кандидатов. BMC Genomics 12 , 383 (2011).
PubMed
PubMed Central
Статья
Google Scholar
Meinel, D. M. et al. Секвенирование нового поколения девяти изолятов Corynebacterium ulcerans выявляет зоонозную передачу и новый предполагаемый остров патогенности, кодирующий дифтерийный токсин. Genome Med. 6 , 113 (2014).
PubMed
PubMed Central
Статья
CAS
Google Scholar
Sangal, V. et al. Дифтеритоподобное заболевание, вызванное токсигенным штаммом Corynebacterium ulcerans . Emerg. Заразить. Дис. 20 , 1257–1258 (2014).
PubMed
PubMed Central
Статья
Google Scholar
Subedi, R. et al. Геномный анализ выявил две различные линии штаммов Corynebacterium ulcerans . Новые микробы. Новый зараз. 25 , 7–13 (2018).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Weerasekera, D. et al. С-концевой домен спиральной спирали Corynebacterium diphtheriae DIP0733 имеет решающее значение для взаимодействия с эпителиальными клетками и патогенности в модельных системах беспозвоночных животных. BMC Microbiol. 18 , 106 (2018).
PubMed
PubMed Central
Статья
CAS
Google Scholar
Santos, L. Sdos et al. Corynebacterium diphtheriae предполагаемый белок устойчивости к теллуриту (CDCE8392_0813) способствует внутриклеточному выживанию в эпителиальных клетках человека и летальности Caenorhabditis elegans . Memórias Inst. Освальдо Круз 110 , 662–668 (2015).
Артикул
CAS
Google Scholar
Холборн, К. П., Шон, К. К. и Ачарья, К. Р. Семейство токсинов-убийц. Изучение механизма ADP-рибозилирования токсинов. FEBS J. 273 , 4579–4593 (2006). В этом обзоре представлен обзор физиологии и особенностей бактериальных ADP-рибозилирующих токсинов со ссылкой на их структурные мотивы, которые дифференцируют различные классы токсинов и их функции .
CAS
PubMed
Статья
Google Scholar
Фримен В. Дж. Исследования вирулентности инфицированных бактериофагом штаммов Corynebacterium diphtheriae . J. Bacteriol. 61 , 675–688 (1951).
CAS
PubMed
PubMed Central
Google Scholar
Laird, W. & Groman, N. Карта профага преобразования коринебактериофага β. J. Virol. 19 , 208–219 (1976).
CAS
PubMed
PubMed Central
Google Scholar
Ratti, G., Covacci, A. & Rappuoli, R. Ген тРНК Arg 2 Corynebacterium diphtheriae представляет собой сайт хромосомной интеграции токсиногенных бактериофагов. Мол. Microbiol. 25 , 1179–1181 (1997).
CAS
PubMed
Статья
Google Scholar
Де Зойса, А., Эфстратиу, А. и Хоуки, П. М. Молекулярная характеристика генов-репрессоров дифтерийного токсина (dtxR), присутствующих в нетоксигенных штаммах Corynebacterium diphtheriae , выделенных в Соединенном Королевстве. J. Clin. Microbiol. 43 , 223–228 (2005).
PubMed
PubMed Central
Статья
CAS
Google Scholar
Сангал В. и Хоскиссон П. А. в Corynebacterium Diphtheriae и родственных токсигенных видах (изд.Бурковский А.) 67–81 (Springer, 2014).
Pohl, E., Holmes, RK & Hol, WGJ Движение ДНК-связывающего домена относительно ядра репрессора дифтерийного токсина (DtxR), обнаруженное в кристаллических структурах Apo- и Holo-DtxR . J. Biol. Chem. 273 , 22420–22427 (1998).
CAS
PubMed
Статья
Google Scholar
Холмс, Р. К. Биология и молекулярная эпидемиология дифтерийного токсина и гена токсина. J. Infect. Дис. 181 , S156 – S167 (2000).
CAS
PubMed
Статья
Google Scholar
Канкл, К. А. и Шмитт, М. П. Анализ DtxR-регулируемого кластера генов транспорта железа и биосинтеза сидерофоров в Corynebacterium diphtheriae . J. Bacteriol. 187 , 422–433 (2005).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Ван З., Шмитт М. П. и Холмс Р. К. Характеристика мутаций, инактивирующих ген репрессора дифтерийного токсина (dtxR). Заражение. Иммун. 62 , 1600–1608 (1994).
CAS
PubMed
PubMed Central
Google Scholar
Kunkle, C. A. & Schmitt, M. P. Анализ регулона Corynebacterium diphtheriae DtxR: идентификация предполагаемой системы синтеза и транспорта сидерофоров, аналогичной системе синтеза и поглощения иерсиниабактина, кодируемой островами высокой патогенности Yersinia. J. Bacteriol. 185 , 6826–6840 (2003).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Yellaboina, S., Ranjan, S., Chakhaiyar, P., Hasnain, SE & Ranjan, A. Прогнозирование регулона DtxR: идентификация сайтов связывания и оперонов, контролируемых репрессором дифтерийного токсина в Corynebacterium diphtheriae . BMC Microbiol. 4 , 38 (2004).
PubMed
PubMed Central
Статья
CAS
Google Scholar
Wittchen, M. et al. Секвенирование транскриптома человеческого патогена Corynebacterium diphtheriae NCTC 13129 обеспечивает детальное понимание его транскрипционного ландшафта и DtxR-опосредованной регуляции транскрипции. BMC Genomics 19 , 82 (2018).
PubMed
PubMed Central
Статья
CAS
Google Scholar
Орам Д. М., Авдалович А. и Холмс Р. К. Создание и характеристика мутаций вставки транспозона в Corynebacterium diphtheriae , которые влияют на экспрессию репрессора дифтерийного токсина (DtxR). J. Bacteriol. 184 , 5723–5732 (2002).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Накао, Х., Мазурова, И.К., Глушкевич, Т., Попович, Т.Анализ гетерогенности гена токсина Corynebacterium diphtheriae , tox, и его регуляторного элемента, dtxR, методом прямого секвенирования. Res. Microbiol. 148 , 45–54 (1997).
CAS
PubMed
Статья
Google Scholar
Колодкина В.Л., Титов Л.П., Шарапа Т.Н., Дрожжина О.Н. Сайты точечных мутаций в промоторе / операторе tox и гене репрессора дифтерийного токсина (DtxR), связанные с уровнем продукции токсина штаммами Corynebacterium diphtheriae изолирован в Беларуси. Мол. Genet. Microbiol. Virol. 22 , 24–33 (2007).
Артикул
Google Scholar
Хэдфилд, Т. Л., Макэвой, П., Полоцкий, Ю., Цинзерлинг, В. А., Яковлев, А. А. Патология дифтерии. J. Infect. Дис. 181 , S116 – S120 (2000). В этой статье представлена подробная информация о патологии дифтерии, которая также включает распространение токсина, вызывающего поражения в отдаленных органах .
PubMed
Статья
Google Scholar
Fratelli, F. et al. Альтернативный метод очистки и детоксикации дифтерийного токсина. Toxicon 57 , 1093–1100 (2011).
CAS
PubMed
Статья
Google Scholar
Мишима, К. Региональное распределение мРНК и белка гепарин-связывающего эпидермального фактора роста-подобного фактора роста в переднем мозге взрослых крыс. Neurosci. Lett. 213 , 153–156 (1996).
CAS
PubMed
Статья
Google Scholar
Nanba, D. & Higashiyama, S. Двойная внутриклеточная передача сигналов путем протеолитического расщепления заякоренного в мембране гепарин-связывающего EGF-подобного фактора роста. Cytokine Growth Factor Rev. 15 , 13–19 (2004).
CAS
PubMed
Статья
Google Scholar
Ивамото, Р. и Мекада, Э. Передача сигналов ErbB и HB-EGF в развитии и функционировании сердца. Cell Struct. Funct. 31 , 1–14 (2006).
CAS
PubMed
Статья
Google Scholar
Collier, R. J. Токсин дифтерии: механизм действия и структура. Бактериол. Ред. 39 , 54–85 (1975).
CAS
PubMed
PubMed Central
Google Scholar
Burch, G. E., Sun, S.-C., Sohal, R. S., Chu, K.-C. & Colcolough, H.L. Дифтерийный миокардит. г. J. Cardiol. 21 , 261–268 (1968).
CAS
PubMed
Статья
Google Scholar
Jayashree, M., Shruthi, N. & Singhi, S. Предикторы исхода у пациентов с дифтерией, получающих интенсивную терапию. Indian Pediatr. 43 , 155–160 (2006).
CAS
PubMed
PubMed Central
Google Scholar
Стокинс, Б. А., Ланас, Ф. Т., Сааведра, Дж. Г. и Опазо, Дж. А. Прогноз у пациентов с дифтерийным миокардитом и брадиаритмией: оценка результатов стимуляции желудочков. Сердце 72 , 190–191 (1994).
CAS
Статья
Google Scholar
Алексеев В.И., Кабоев О.К., Семенова Е.В., Щербакова О.Г., Филатов М.В. Иммунологическое сходство дифтерийного токсина и рецептора EGF. Цитология 52 , 364–370 (2010).
PubMed
Google Scholar
Канвал, С. К., Ядав, Д., Чхапола, В. и Кумар, В. Постдифтеритическая невропатия: клиническое исследование в педиатрическом отделении интенсивной терапии в развивающейся стране. Троп. Докт. 42 , 195–197 (2012).
PubMed
Статья
Google Scholar
Имс, Р. А., Якобсон, С. Г. и Макдональд, В. И. Патологические изменения перекреста зрительных нервов у кошек после местной инъекции дифтерийного токсина. J. Neurol. Sci. 32 , 381–393 (1977).
CAS
PubMed
Статья
Google Scholar
Macgregor, R.R. in Mandell, Douglas, and Bennett’s Principles and Practice of Infectious Diseases 7 edn (eds Mandell G. L., Bennett, J.Э. и Долин Р.) 2687–2693 (Черчилль Ливингстон, 2010).
Bertuccini, L., Baldassarri, L. & von Hunolstein, C. Интернализация нетоксигенных Corynebacterium diphtheriae культивированными клетками респираторного эпителия человека. Microb. Патог. 37 , 111–118 (2004).
CAS
PubMed
Статья
Google Scholar
Sabbadini, P. S. et al. Фибриноген связывается с нетоксигенными и токсигенными штаммами Corynebacterium diphtheriae . Memórias Inst. Освальдо Круз 105 , 706–711 (2010).
CAS
Статья
Google Scholar
Giannini, G., Rappuoli, R. & Ratti, G. Аминокислотная последовательность двух нетоксичных мутантов дифтерийного токсина: CRM45 и CRM197. Nucleic Acids Res. 12 , 4063–4069 (1984).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Чианциотто, Н. П. и Громан, Н. Б. Характеристика бактериофагов из токсикогенных изолятов Corynebacterium diphtheriae , содержащих токсин. Microb. Патог. 22 , 343–351 (1997).
CAS
PubMed
Статья
Google Scholar
Мельников В.Г. и др. Corynebacterium diphtheriae нетоксигенный штамм, несущий ген дифтерийного токсина. Ж.Микробиол. Эпидемиол. Иммунобиол. 1 , 3–7 (2004).
Google Scholar
Trost, E. et al. Пангеномное исследование Corynebacterium diphtheriae , которое дает представление о геномном разнообразии патогенных изолятов от случаев классической дифтерии, эндокардита и пневмонии. J. Bacteriol. 194 , 3199–3215 (2012).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Dinu, S., Damian, M., Badell, E., Dragomirescu, C.C. & Guiso, N. Новые типы репрессоров дифтерийного токсина, представленные в румынской коллекции из изолятов Corynebacterium diphtheriae . J. Basic Microbiol. 54 , 1136–1139 (2013).
PubMed
Статья
CAS
Google Scholar
Закихани К., Нил С. и Эфстратиу А. Возникновение и молекулярная характеристика нетоксигенного tox , несущего ген Corynebacterium diphtheriae биовар-митит в Соединенном Королевстве, 2003–2012 гг. Евронаблюдение 19 , 20819 (2014).
PubMed
Статья
Google Scholar
Фарфур, Э., Баделл, Э., Дину, С., Гийо, С. и Гизо, Н. Микробиологические изменения и разнообразие автохтонных нетоксигенных Corynebacterium diphtheriae , выделенных во Франции. Clin. Microbiol. Заразить. 19 , 980–987 (2013).
CAS
PubMed
Статья
Google Scholar
Patey, O. et al. Клиническое и молекулярное исследование системных инфекций Corynebacterium diphtheriae во Франции. Группа изучения Корин. J. Clin. Microbiol. 35 , 441–445 (1997).
CAS
PubMed
PubMed Central
Google Scholar
Маттос-Гуаральди, А. Л., Дуарте Формига, Л. С. и Перейра, Г. А. Компоненты клеточной поверхности и адгезия в Corynebacterium diphtheriae . Микробы Заражают. 2 , 1507–1512 (2000).
CAS
PubMed
Статья
Google Scholar
Dias, A.A. et al. Corynebacterium ulcerans дифтерия: новый зооноз в Бразилии и во всем мире. Rev. Saude Publ. 45 , 1176–1191 (2011).
Артикул
Google Scholar
Вагнер, Дж.и другие. Инфекция кожи, вызванная Corynebacterium ulcerans и имитирующая классическую кожную дифтерию. Clin. Заразить. Дис. 33 , 1598–1600 (2001).
CAS
PubMed
Статья
Google Scholar
Berger, A. et al. Два случая кожной дифтерии, связанные с профессиональным контактом со свиньями в Германии. Зоонозы общественного здравоохранения 60 , 539–542 (2012).
PubMed
Статья
CAS
Google Scholar
Sekizuka, T. et al. Corynebacterium ulcerans 0102 несет ген, кодирующий дифтерийный токсин, на профаге, отличном от профага C. diphtheriae NCTC 13129. BMC Microbiol. 12 , 72 (2012).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Sing, A., Hogardt, M., Bierschenk, S. & Heesemann, J. Обнаружение различий в нуклеотидных и аминокислотных последовательностях дифтерийного токсина из Corynebacterium diphtheriae и Corynebacterium ulcerans , вызывающих экстраглоточные инфекции. J. Clin. Microbiol. 41 , 4848–4851 (2003).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Синг, А., Berger, A., Schneider-Brachert, W., Holzmann, T. и Reischl, U. Быстрое обнаружение и молекулярная дифференциация токсигенных штаммов Corynebacterium diphtheriae и Corynebacterium ulcerans с помощью LightCycler PCR. J. Clin. Microbiol. 49 , 2485–2489 (2011).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Thouvenin, M., Beilouny, B., Badell, E.& Guiso, N. Corynebacterium ulcerans легочная инфекция. Ann. Биол. Clin. 74 , 117–120 (2016).
Google Scholar
Simpson-Lourêdo, L. et al. Выявление и потенциал вирулентности фосфолипазы D-отрицательной Corynebacterium ulcerans в случае сочетания дифтерии и инфекционного мононуклеоза. Антони ван Левенгук 112 , 1055–1065 (2019).
PubMed
Статья
CAS
Google Scholar
Пил, М. М., Палмер, Г. Г., Стакпул, А. М. и Керр, Т. Г. Лимфаденит человека, вызванный Corynebacterium pseudotuberculosis : отчет о десяти случаях из Австралии и обзор. Clin. Заразить. Дис. 24 , 185–191 (1997).
CAS
PubMed
Статья
Google Scholar
Maximescu, P., Oprişan, A., Pop, A. и Potorac, E. Дальнейшие исследования видов Corynebacterium, способных продуцировать дифтерийный токсин ( C. diphtheriae , C. ulcerans , C. ovis ). J. Gen. Microbiol. 82 , 49–56 (1974).
CAS
PubMed
Статья
Google Scholar
Краева Л.А., Манина Ж. Н., Ценева, Г. Я. & Радченко, А.Г. Этиологическая роль Corynebacterium non diphtheriae у больных с различной патологией. Ж. Микробиол. Эпидемиол. Иммунобиол. 5 , 3–7 (2007).
Google Scholar
Trost, E. et al. Полная последовательность генома Corynebacterium pseudotuberculosis FRC41, выделенная от 12-летней девочки с некротическим лимфаденитом, раскрывает понимание генетических регуляторных сетей, способствующих вирулентности. BMC Genomics 11 , 728 (2010).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Всемирная организация здравоохранения. Оперативный протокол клинического ведения дифтерии. Бангладеш, Кокс-Базар (версия от 10 декабря 2017 г.). ВОЗ https://www.who.int/health-cluster/resources/publications/WHO-operational-protocols-diphtheria.pdf?ua=1 (2017).
Quick, M. L. et al. Факторы риска дифтерии: проспективное исследование методом случай-контроль в Республике Грузия, 1995–1996 гг. J. Infect. Дис. 181 , S121 – S129 (2000).
PubMed
Статья
Google Scholar
Mattos-Guaraldi, A. L. et al. Сопутствующая дифтерия и инфекционный мононуклеоз: трудности ведения, исследования и борьбы с дифтерией в развивающихся странах. J. Med. Microbiol. 60 , 1685–1688 (2011).
CAS
PubMed
Статья
Google Scholar
Маколи Дж. Х., Фернли Дж., Лоуренс А. и Болл Дж. А. Дифтерийная полинейропатия. J. Neurol. Нейрохирургия.Психиатрия 67 , 825–826 (1999).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Pleasure, D. E., Feldmann, B. & Prockop, D. J. Токсин дифтерии подавляет синтез миелиновых протеолипидов и основных белков периферическими нервами in vitro. J. Neurochem. 20 , 81–90 (1973).
CAS
PubMed
Статья
Google Scholar
Пирадов М.А., Пирогов В.Н., Попова Л.М., Авдунина И.А. Дифтерийная полинейропатия. Arch. Neurol. 58 , 1438 (2001).
CAS
PubMed
Статья
Google Scholar
Cléange, A., Meyrignac, C., Roualdes, B., Degos, J.-D. И Герарди, Р. К. Дифтерийная невропатия. Мышечный нерв 18 , 1460–1463 (1995).
Артикул
Google Scholar
Маникьямба Д., Сатьявани А. и Дипа П. Дифтерийная полинейропатия после возобновления дифтерии. J. Pediatr. Neurosci. 10 , 331 (2015). Вместе со ссылкой 222 этот отчет описывает важность полинейропатии как одного из самых тяжелых осложнений дифтерии из-за распространения токсина .
CAS
PubMed
PubMed Central
Статья
Google Scholar
Euzeby, J.P. Список названий прокариот, стоящих в номенклатуре — род Corynebacterium . LPSN http://www.bacterio.net/corynebacterium.html (2013).
Титов Л. и др. Генотипические и фенотипические характеристики штаммов Corynebacterium diphtheriae , выделенных от больных в Беларуси в период эпидемии. J. Clin. Microbiol. 41 , 1285–1288 (2003).
PubMed
PubMed Central
Статья
Google Scholar
Schoenemann, W. Идентификация Corynebacterium diphtheriae методом иммунофлуоресценции [немецкий]. Zentralbl. Бактериол. Ориг. А 240 , 258–264 (1978).
CAS
PubMed
PubMed Central
Google Scholar
Андроулла А., Кристофер Мейпл П. А. и Всемирная организация здравоохранения. Руководство по лабораторной диагностике дифтерии (ВОЗ, 1994).
Конрад Р.и другие. Матричная лазерная десорбционная / ионизационная времяпролетная масс-спектрометрия (MALDI-TOF) как инструмент для быстрой диагностики потенциально токсигенных видов Corynebacterium в лабораторном управлении бактериями, ассоциированными с дифтерией. Евронаблюдение 15 , 19699 (2010).
PubMed
Статья
PubMed Central
Google Scholar
Colman, G., Weaver, E. & Efstratiou, A.Скрининговые тесты на патогенные коринебактерии. J. Clin. Патол. 45 , 46–48 (1992).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Энглер, К. Х., Глушкевич, Т., Мазурова, И. К., Джордж, Р. К., Эфстратиу, А. Модифицированный тест Элек для обнаружения токсигенных коринебактерий в диагностической лаборатории. J. Clin. Microbiol. 35 , 495–498 (1997).
CAS
PubMed
PubMed Central
Google Scholar
Skogen, V. et al. Обнаружение антитоксина дифтерии четырьмя различными методами. Clin. Microbiol. Заразить. 5 , 628–633 (1999).
CAS
PubMed
Статья
Google Scholar
Хамис А., Рауль Д. и Ла Скола Б. Сравнение секвенирования генов rpoB и 16S рРНК для молекулярной идентификации 168 клинических изолятов Corynebacterium . J. Clin. Microbiol. 43 , 1934–1936 (2005).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Mancini, F. et al. Идентификация и молекулярная дискриминация токсигенных и нетоксигенных штаммов дифтерии Corynebacterium с помощью комбинированных анализов полимеразной цепной реакции в реальном времени. Диагн. Microbiol. Заразить. Дис. 73 , 111–120 (2012).
CAS
PubMed
Статья
Google Scholar
Де Зойса, А., Эфстратиу, А., Манн, Г., Харрисон, Т. Г. и Фрай, Н. К. Разработка, проверка и внедрение квадруплексного ПЦР-анализа в реальном времени для идентификации потенциально токсигенных коринебактерий. J. Med. Microbiol. 65 , 1521–1527 (2016).
PubMed
Статья
CAS
Google Scholar
Паллен, М. Дж., Хей, А. Дж., Пакки, Л. Х. и Эфстратиу, А. Полимеразная цепная реакция для скрининга клинических изолятов коринебактерий на продукцию дифтерийного токсина. J. Clin. Патол. 47 , 353–356 (1994).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Мазурова, И. К., Комбарова, С. И., Ярова, Л. М., Григорян, Г. К., Дельвиг, А. А. Реакция коагглютинации для обнаружения дифтерийного токсина. Ж. Микробиол. Эпидемиол. Иммунобиол. 3 , 68–71 (1989).
Google Scholar
Джалгаонкар, С. В. и Саоджи, А. М. Коагглютинация для быстрого тестирования токсинов, продуцирующих Corynebacterium diphtheriae . Indian J. Med. Res. 97 , 35–36 (1993).
CAS
PubMed
Google Scholar
Тома К., Сисават Л. и Иванага М. Анализ обратной пассивной латексной агглютинации для обнаружения токсигенных Corynebacterium diphtheriae . J. Clin. Microbiol. 35 , 3147–3149 (1997).
CAS
PubMed
PubMed Central
Google Scholar
Brenner, N. et al. Валидация моноплексных анализов, выявляющих антитела против токсинов Corynebacterium diphtheriae и Clostridium tetani , вируса краснухи и парвовируса B19 для включения в Multiplex Serology. Методы 158 , 44–53 (2019).
CAS
PubMed
Статья
Google Scholar
Энглер, К. Х. и Эфстратиу, А. Экспресс-иммуноферментный анализ для определения токсигенности среди клинических изолятов коринебактерий. J. Clin. Microbiol. 38 , 1385–1389 (2000).
CAS
PubMed
PubMed Central
Google Scholar
Kristiansen, M., Aggerbeck, H. & Heron, I. Улучшенный ELISA для определения антитоксиновых антител против дифтерии и / или столбняка в сыворотках. APMIS 105 , 843–853 (1997).
CAS
PubMed
Статья
Google Scholar
Томпсон, Н. Л. и Эллнер, П. Д. Быстрое определение токсигенности Corynebacterium diphtheriae с помощью контриммуноэлектрофореза. J. Clin. Microbiol. 7 , 493–494 (1978).
CAS
PubMed
PubMed Central
Google Scholar
Йемул, В. Л. и Сенгупта, С. Р. Противодействующий иммуноэлектрофорез для быстрого тестирования токсинов, продуцирующих Corynebacterium diphtheriae . Indian J. Med. Res. 72 , 187–190 (1980).
CAS
PubMed
Google Scholar
Диаконеску А. Противоиммуноэлектрофорез для выявления токсиногенеза у Corynebacterium diphtheriae . Arch. Рум. Патол. Exp. Microbiol. 42 , 207–212 (1983).
CAS
PubMed
Google Scholar
Aggerbeck, H., Nørgaard-Pedersen, B. & Heron, I. Одновременное количественное определение дифтерийных и столбнячных антител двойным антигеном, флуоресцентный иммуноанализ с временным разрешением. J. Immunol. Методы 190 , 171–183 (1996).
CAS
PubMed
Статья
Google Scholar
Любран, М. М. Бактериальные токсины. Ann. Clin. Лаборатория. Sci. 18 , 58–71 (1988).
CAS
PubMed
Google Scholar
Лаккиредди, Д. Р., Кондур, А. К., Чедиак, Э. Дж., Наир, К. К. и Хан, И. А. Высвобождение сердечного тропонина I при неишемическом обратимом повреждении миокарда в результате острого дифтериального миокардита. Внутр. J. Cardiol. 98 , 351–354 (2005).
PubMed
Статья
Google Scholar
Лумио, Дж. Т., Граундстрем, К. В. Э., Мельник, О. Б., Хухтала, Х. и Рахманова, А. Г. Электрокардиографические аномалии у пациентов с дифтерией: проспективное исследование. г. J. Med. 116 , 78–83 (2004). Эта статья предоставляет исчерпывающую информацию о поражении сердца при респираторной дифтерии, особенно у пожилых пациентов .
PubMed
Статья
Google Scholar
Самдани С., Джайн А., Мина В. и Мина С. Б. Сердечные осложнения при дифтерии и предикторы исходов. Внутр. J. Pediatr. Оториноларингол. 104 , 76–78 (2018).
PubMed
Статья
Google Scholar
Lehnert, F. et al. Corynebacterium diphtheriae Эндокардит, осложненный септическим артритом и абсцессом головного мозга. Arch. Mal. Coeur Vaiss 88 , 899–901 (1995).
CAS
PubMed
Google Scholar
Krassas, A., Sakellaridis, T., Argyriou, M. & Charitos, C. Пиоперикард с последующим констриктивным перикардитом, вызванным Corynebacterium diphtheriae . Взаимодействовать. Кардиоваск. Грудной. Surg. 14 , 875–877 (2012).
PubMed
PubMed Central
Статья
Google Scholar
Ли, Х. (ред.) Радиология инфекционных заболеваний: Том 2 (Springer, 2015).
Баба М., Гиллиатт Р. У., Хардинг А. Э. и Рейнерс К. Демиелинизация после дифтерийного токсина при атрофии аксонов. J. Neurol. Sci. 64 , 199–211 (1984).
CAS
PubMed
Статья
Google Scholar
Ложникова С.М., Пирогов В.Н., Пирадов М.А., Сахарова А.В., Людковская И.Г. Дифтерийная полинейропатия: клинико-морфологическое исследование. Арх. Патол. 59 , 11–17 (1997).
CAS
PubMed
Google Scholar
Гиббельс, Э., Бергер, М., Хербольшаймер, М., Корн, А. и Штаммлер, А. Endplatten und intramuskulären Gef ääen. Acta Neuropathol. 55 , 307–318 (1981).
CAS
PubMed
Статья
Google Scholar
Холтхаус, Д. Дж., Пауэр, Б., Кермод, А. и Голледж, К. Нетоксигенный Corynebacterium diphtheriae : два случая и обзор литературы. J. Infect. 37 , 62–66 (1998).
CAS
PubMed
Статья
Google Scholar
Ледбеттер М.К., Кэннон А.Б. и Коста А.Ф. Электрокардиограмма при дифтерийном миокардите. г. Heart J. 68 , 599–611 (1964).
CAS
PubMed
Статья
Google Scholar
Хавалдар П. В., Санкпал М. Н. и Додданнавар Р. П. Дифтерийный миокардит: клинико-лабораторные параметры прогноза и летального исхода. Ann. Троп. Педиатр. 20 , 209–215 (2016).
Всемирная организация здравоохранения. Вакцина против дифтерии: позиционный документ ВОЗ, август 2017 г. — рекомендации. Vaccine 36 , 199–201 (2018).
CAS
PubMed
Статья
Google Scholar
Центры по контролю и профилактике заболеваний (CDC). Обновленные рекомендации по использованию столбнячного анатоксина, восстановленного дифтерийного анатоксина и бесклеточной коклюшной вакцины (Tdap) у взрослых в возрасте 65 лет и старше — Консультативный комитет по практике иммунизации (ACIP), 2012. MMWR Morb. Смертный. Wkly Rep. 61 , 468–470 (2012).
PubMed
Google Scholar
Моро, П.Л., Юэ, X., Льюис, П., Хабер, П. и Бродер, К. Неблагоприятные события после применения столбнячного анатоксина, сниженного количества дифтерийного анатоксина и бесклеточной коклюшной вакцины (Tdap) взрослым в возрасте 65 лет. лиц в возрасте и старше, зарегистрированные в Системе сообщений о побочных эффектах вакцин (VAERS), 2005–2010 гг. Vaccine 29 , 9404–9408 (2011).
PubMed
Статья
Google Scholar
ВандерЭнде, К., Гачич-Добо, М., Диалло, М.С., Конклин, Л.М. и Уоллес, А.С. Глобальный охват плановой вакцинацией — 2017. MMWR Morbid. Смертный. Wkly Rep. 67 , 1261–1264 (2018).
Артикул
Google Scholar
Blumberg, L.H. et al. Предотвратимая трагедия дифтерии в 21 веке. Внутр. J. Infect. Дис. 71 , 122–123 (2018).
CAS
PubMed
Статья
Google Scholar
Тивари, Т. С. П. и Уортон, М. в Plotkin’s Vaccines 261–275.e7 (Elsevier, 2018).
Кларк А. и Сандерсон К. Сроки вакцинации детей в 45 странах с низким и средним уровнем доходов: анализ данных обследования. Ланцет 373 , 1543–1549 (2009).
PubMed
Статья
Google Scholar
Главное бухгалтерское управление США. Глобальное здоровье: факторы, способствующие низкому уровню вакцинации в развивающихся странах. ГАО / НСИАД-00-4 (ГАО, 1999).
Ананд С. и Бернигхаузен Т. Медицинские работники и охват вакцинацией в развивающихся странах: эконометрический анализ. Ланцет 369 , 1277–1285 (2007).
PubMed
Статья
Google Scholar
Гош, А. и Лакшминараян, Р. Детерминанты со стороны спроса и предложения невакцинации от дифтерии, коклюша и столбняка в сельских районах Индии. Вакцина 35 , 1087–1093 (2017).
PubMed
PubMed Central
Статья
Google Scholar
Глобальный альянс по вакцинам и иммунизации. Вакцина 5-в-1 теперь во всех 73 беднейших странах (ГАВИ, 2014).
Мальхаме, М.и другие. Формирование рынков на благо глобального здоровья — 15-летняя история и уроки, извлеченные из рынка пятивалентных вакцин. Vaccine X 2 , 100033 (2019).
PubMed
PubMed Central
Статья
Google Scholar
Grasse, M., Meryk, A., Schirmer, M., Grubeck-Loebenstein, B. & Weinberger, B. Бустерная вакцинация против столбняка и дифтерии: недостаточная защита от дифтерии у молодых и пожилых людей. Immun. Старение 13 , 26 (2016).
PubMed
PubMed Central
Статья
CAS
Google Scholar
Гальперин С.А. и др. Рандомизированное контролируемое исследование безопасности и иммуногенности ревакцинации против столбняка, дифтерии и бесклеточной коклюшной вакцины (Tdap) у взрослых через 10 лет после введения предыдущей дозы. J. Pediatr. Заразить. Дис. Soc. 8 , 105–114 (2018).
Артикул
Google Scholar
Хассельхорн, Х.-М., Нюблинг, М., Тиллер, Ф. В. и Хофманн, Ф. Факторы, влияющие на иммунитет против дифтерии у взрослых. Vaccine 16 , 70–75 (1998).
CAS
PubMed
Статья
Google Scholar
Dittmann, S. et al. Успешная борьба с эпидемией дифтерии в государствах бывшего Союза Советских Социалистических Республик: извлеченные уроки. J. Infect. Дис. 181 , S10 – S22 (2000).
PubMed
Статья
Google Scholar
Марловиц С. Распространенность дифтерийного иммунитета среди взрослых травмированных в Австрии. Вакцина 19 , 1061–1067 (2000).
CAS
PubMed
Статья
Google Scholar
Völzke, H. et al. Восприимчивость к дифтерии у взрослых: распространенность и связь с гендерными и социальными переменными. Clin. Microbiol. Заразить. 12 , 961–967 (2006).
PubMed
Статья
Google Scholar
Рекомендации Консультативного комитета по практике иммунизации (ACIP). Дифтерия, столбняк и коклюш: рекомендации по применению вакцины и другим профилактическим мерам. MMWR Morb. Смертный. Wkly Rep. 40 , 1–28 (1991).
Google Scholar
Наир, Р. Р. и Джозеф, Т. П. Назотрахеальная интубация при дифтерии. J. Pediatr. Surg. 10 , 201–202 (1975).
CAS
PubMed
Статья
Google Scholar
Both, L., White, J., Mandal, S. & Efstratiou, A. Доступ к дифтерийному антитоксину для терапии и диагностики. Евронаблюдение 19 , 20830 (2014).
PubMed
Статья
Google Scholar
Общественное здравоохранение Англии. Руководство по применению антитоксина против дифтерии. Номер шлюза 2018350 (PHE, 2018).
Миллер, Л. В., Бикхэм, С., Джонс, В. Л., Хизер, К. Д. и Моррис, Р. Х. Носители дифтерии и эффект терапии эритромицином. Антимикробный. Агенты Chemother. 6 , 166–169 (1974).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Challoner, D. R. & Prols, H.G. Окисление свободных жирных кислот и уровни карнитина в дифтерийном миокарде морской свинки. J. Clin. Вкладывать деньги. 51 , 2071–2076 (1972).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Dung, N. M. et al. Лечение тяжелого дифтерийного миокардита путем временной установки кардиостимулятора. Clin. Заразить. Дис. 35 , 1425–1429 (2002).
PubMed
Статья
Google Scholar
Хавальдар П.В. Кардиопротекторный эффект карнитина при молниеносной дифтерии. J. Trop. Педиатр. 43 , 187–188 (1997).
CAS
PubMed
Статья
Google Scholar
Рамос, А. С. М. Ф., Элиас, П. Р. П., Барруканд, Л. и Сильва, Дж. А. Ф. Д. Защитный эффект карнитина при дифтерийном миокардите человека. Педиатр. Res. 18 , 815–819 (1984).
CAS
PubMed
Статья
Google Scholar
Рамос, А.С., Барруканд, Л., Элиас, П.Р., Пиментел, А.М. и Пирес, В.Р. Добавки карнитина при дифтерии. Indian Pediatr. 29 , 1501–1505 (1992).
CAS
PubMed
Google Scholar
Джерри Дж.Л. и Гриноу, В. Б. Дифтероидный эндокардит. Отчет о девяти случаях и обзор литературы. Johns Hopkins Med. J. 139 , 61–68 (1976).
CAS
PubMed
Google Scholar
Логина И. и Донахи М. Дифтерийная полинейропатия: клиническое исследование и сравнение с синдромом Гийена – Барре. J. Neurol. Нейрохирургия. Психиатрия 67 , 433–438 (1999).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Чагина И.А. и др. Чувствительность штаммов Corynebacterium diphtheriae к антибактериальным препаратам. Ж. Микробиол. Эпидемиол. Иммунобиол. 4 , 8–13 (2014).
Google Scholar
Tiwari, T. S. P. et al. Расследование 2 случаев дифтерийного заболевания, вызванного токсигенными Corynebacterium ulcerans . Clin. Заразить. Дис. 46 , 395–401 (2008).
PubMed
Статья
Google Scholar
Фитцджеральд, Р. П., Россер, А. Дж. И Перера, Д. Н. Нетоксигенная резистентная к пенициллину кожная инфекция C. diphtheriae : отчет о болезни и обзор литературы. J. Infect. Общественное здравоохранение 8 , 98–100 (2015).
PubMed
Статья
Google Scholar
Gomes, D.L. R. et al. Субмик пенициллина и эритромицина усиливают образование биопленок и повышают гидрофобность штаммов Corynebacterium diphtheriae . J. Med. Microbiol. 62 , 754–760 (2013).
CAS
PubMed
Статья
Google Scholar
Виттхауэр К., Глостер А. Т., Мейер А. Х., Гудвин Р. Д. и Либ Р. Коморбидность инфекционных заболеваний и тревожных расстройств у взрослых и ее связь с качеством жизни: исследование сообщества. Фронт. Общественное здравоохранение 2 , 80 (2014).
PubMed
PubMed Central
Статья
Google Scholar
Кадирова Р., Картоглу Х. У. и Штребель П. М. Клинические характеристики и ведение 676 госпитализированных больных дифтерией, Кыргызская Республика, 1995. J. Infect. Дис. 181 (Дополнение 1), S110 – S115 (2000).
PubMed
Статья
Google Scholar
Расмуссен, В., Бреммельгаард, А., Корнер, Б., Хаунсё, С. и Расмуссен, Е. Острый Corynebacterium эндокардит, вызывающий разрушение аортального клапана. Успешное лечение антибиотиками и заменой клапана. Сканд. J. Infect. Дис. 11 , 89–92 (1979).
CAS
PubMed
Статья
Google Scholar
Прасад, П. Л. и Рай, П. Л. Проспективное исследование дифтерии при неврологических осложнениях. J. Pediatr. Neurosci. 13 , 313–316 (2018).
PubMed
PubMed Central
Статья
Google Scholar
Pleasure, D. & Messing, A. in Peripheral Neuropathy 4th edn Ch. 95 (ред. Дайк, П. Дж. И Томас, П. К.) 2147–2151 (У. Б. Сондерс, 2005).
Нат, Л., Каур, П. и Трипати, С. Оценка универсальной программы иммунизации и проблемы охвата детей-мигрантов в Харидваре, Уттаракханд, Индия. Indian J. Commun. Med. 40 , 239 (2015).
Артикул
Google Scholar
Всемирная организация здравоохранения. Стандарты эпиднадзора за болезнями, предупреждаемыми с помощью вакцин — дифтерия (ВОЗ, 2018).
Cerdeno-Tarraga, A. M. et al. Полная последовательность генома и анализ Corynebacterium diphtheriae NCTC13129. Nucleic Acids Res. 31 , 6516–6523 (2003).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Всемирная организация здравоохранения. Глобальный план действий по вакцинам. Отчеты о выполнении региональных планов действий в отношении вакцин за 2016 г. http://www.who.int/immunization/sage/meetings/2016/october/3_Regional_vaccine_action_plans_2016_progress_reports.pdf (ВОЗ, 2016).
Альбертсен, Н., Фенкер, И. М., Ноасен, Х. Э. и Педерсен, М. Л. Уровень иммунизации детей в Нууке. Внутр. J. Циркумполярное здравоохранение 77 , 1426948 (2018).
PubMed
PubMed Central
Статья
Google Scholar
Lin, X. et al. Снижение титров вакцинных антител после воздействия нескольких металлов и металлоидов у детей дошкольного возраста, подвергшихся воздействию электронных отходов. Environ. Загрязнение. 220 , 354–363 (2017).
CAS
PubMed
Статья
Google Scholar
Rahman, M. M. et al. Одновременное введение витамина А при плановой иммунизации усиливает ответ антител на вакцину против дифтерии у детей младше шести месяцев. J. Nutr. 129 , 2192–2195 (1999).
CAS
PubMed
Статья
Google Scholar
Вайнбергер, Б. Вакцины для пожилых людей: использование в настоящее время и проблемы будущего. Imun. Старение 15 , 3 (2018).
Артикул
CAS
Google Scholar
Коле, А., Кар, С., Рой, Р. и Чанда, Д. Исходы респираторной дифтерии в специализированной инфекционной больнице. Indian J. Med. Sci. 64 , 373 (2010).
CAS
PubMed
Статья
Google Scholar
Wagner, K. S. et al. Обзор международных проблем, связанных с доступностью и спросом на дифтерийный антитоксин для терапевтического использования. Vaccine 28 , 14–20 (2009).
CAS
PubMed
Статья
PubMed Central
Google Scholar
Сгурис, Дж. Т., Волк, В. К., Анджела, Ф., Портвуд, Л. и Готтсхолл, Р. Ю. Исследования дифтерийного иммуноглобулина, полученного из устаревшей крови человека. Vox Sanguinis 16 , 491–495 (1969).
CAS
PubMed
Статья
PubMed Central
Google Scholar
Севиньи, Л. М. и др. Идентификация человеческого моноклонального антитела для замены антитоксина дифтерии лошадей для лечения дифтерийной интоксикации. Заражение. Иммун. 81 , 3992–4000 (2013).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Yoshimori, T. et al. Моноклональные антитела против фрагмента А дифтерийного токсина Exp. Cell Res. 151 , 344–353 (1984).
CAS
PubMed
Статья
Google Scholar
Цукер Д. Р., Мерфи Дж. Р. и Паппенгеймер А. М. Анализ моноклональных антител к дифтерийному токсину-II. Подавление активности АДФ-рибозилтрансферазы. Мол. Иммунол. 21 , 795–800 (1984).
CAS
PubMed
Статья
Google Scholar
Cha, J.-H. Рецепторный антидот от дифтерии. Заражение. Иммун. 70 , 2344–2350 (2002).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Smith, HL, Cheslock, P., Leney, M., Barton, B. & Molrine, DC Эффективность человеческого моноклонального антитела к дифтерийному токсину относительно дифтерийного антитоксина лошади в модели интоксикации морской свинки . Вирулентность 7 , 660–668 (2016).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Саенс, Дж. Б., Доггетт, Т. А. и Хаслам, Д. Б. Идентификация и характеристика малых молекул, которые ингибируют внутриклеточный транспорт токсина. Заражение. Иммун. 75 , 4552–4561 (2007).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Schnell, L. et al. Семикарбазон EGA подавляет поглощение токсина дифтерии клетками человека и защищает клетки от интоксикации. Токсины 8 , E221 (2016).
PubMed
Статья
CAS
PubMed Central
Google Scholar
Soriano, F., Zapardiel, J. & Nieto, E. Антимикробная чувствительность видов Corynebacterium и других неспорообразующих грамположительных бацилл к 18 антимикробным агентам. Антимикробный. Агенты Chemother. 39 , 208–214 (1995).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Camello, T., Mattos-Guaraldi, A., Duarte, F. и Marques, E. Nondiphtherial Corynebacterium видов, выделенных из клинических образцов пациентов в университетской больнице, Рио-де-Жанейро, Бразилия. Braz. J. Microbiol. 34 , 39–44 (2003).
CAS
Статья
Google Scholar
Чандра, Р. Дифтероиды — важные внутрибольничные патогены. J. Clin. Диаг. Res. 10 , DC28 – DC31 (2016).
Google Scholar
Fricchione, M. J. et al. Нетоксигенный пенициллин и устойчивый к цефалоспоринам Corynebacterium diphtheriae эндокардит у ребенка: описание случая и обзор литературы. J. Детская инфекция. Дис. Soc. 3 , 251–254 (2013).
PubMed
Статья
Google Scholar
Neemuchwala, A.и другие. Структура чувствительности к антибиотикам in vitro не дифтерийных изолятов Corynebacterium в Онтарио, Канада, с 2011 по 2016 годы. Antimicrob. Агенты Chemother . 62 , (2018).
Рокхилл, Р. К., Сумармо, Хадипутранто, Х., Сирегар, С. П. и Муслихун, Б. Устойчивость к тетрациклину Corynebacterium diphtheriae , выделенных от больных дифтерией в Джакарте, Индонезия. Антимикробный. Агенты Chemother. 21 , 842–843 (1982).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Kneen, R. et al. Пенициллин против эритромицина в лечении дифтерии. Clin. Заразить. Дис. 27 , 845–850 (1998).
CAS
PubMed
Статья
Google Scholar
Бурковский А. Роль кориномиколовой кислоты во взаимодействии Corynebacterium – хозяин. Антони ван Левенгук 111 , 717–725 (2018).
CAS
PubMed
Статья
Google Scholar
Ekwueme, D. U. et al. Экономическая оценка использования вакцины против дифтерии, столбняка и бесклеточного коклюша или вакцины против дифтерии, столбняка и цельноклеточного коклюша в США, 1997 г. Arch. Педиатр. Adolesc. Med. 154 , 797 (2000).
CAS
PubMed
Статья
Google Scholar
Центры по контролю и профилактике заболеваний. Программа «Вакцины для детей» (VFC). Текущий прайс-лист на вакцины CDC (CDC, 2019).
Menzies, N.A. et al. Детерминанты стоимости плановой иммунизации младенцев: мета-регрессионный анализ шести страновых исследований. BMC Med. 15 , 178 (2017).
PubMed
PubMed Central
Статья
Google Scholar
Бишай, Д., McQuestion, M., Chaudhry, R. & Wigton, A. Затраты на расширение масштабов вакцинации в беднейших странах мира. Health Aff. 25 , 348–356 (2006).
Артикул
Google Scholar
Д’Сильва, П. Р. и Лала, А. К. Организация дифтерийного токсина в мембранах: исследование с гидрофобным фотомаркированием. J. Biol. Chem. 275 , 11771–11777 (2000).
PubMed
Статья
Google Scholar
Ван Несс, Б.Г., Ховард, Дж. Б. и Бодли, Дж. У. АДФ-рибозилирование фактора удлинения 2 дифтерийным токсином. Выделение и свойства новой рибозиламинокислоты и продуктов ее гидролиза. J. Biol. Chem. 255 , 10717–10720 (1980).
PubMed
Google Scholar
Honjo, T., Nishizuka, Y. & Hayaishi, O. Зависимое от дифтерии токсин-зависимое аденозиндифосфат-рибозилирование аминоацилтрансферазы II и ингибирование синтеза белка. J. Biol. Chem. 243 , 3553–3555 (1968).
CAS
PubMed
Google Scholar
Саймон, Н. К., Акториз, К. и Барбьери, Дж. Т. Новые бактериальные АДФ-рибозилирующие токсины: структура и функция. Nat. Rev. Microbiol. 12 , 599–611 (2014).
CAS
PubMed
PubMed Central
Статья
Google Scholar
Информационный бюллетень о дифтерии
Дифтерия — это острое заболевание, вызываемое токсин-продуцирующими штаммами бактерий Corynebacterium diphtheriae (в некоторых случаях также Corynebacterium ulcerans), которые, как известно, колонизируют слизистые оболочки.После инфицирования после обычно короткого инкубационного периода (2–5 дней) высвобождение цитотоксина может вызвать характерные поражения на пораженных слизистых оболочках (миндалинах, глотке, гортани, носу) или в ранах. Может последовать обструкция дыхательных путей. После всасывания токсин достигает других органов и может вызвать миокардит, паралитические симптомы и нефрит. У невакцинированных лиц, особенно если надлежащее лечение откладывается, смерть может наступить в 10% клинических случаев, несмотря на антибиотики и использование антисывороток. Дифтерия передается в основном путем прямой проекции (распространение капель).Это можно предотвратить с помощью вакцинации.
Информационный бюллетень
Дифтерия — это заболевание, вызываемое бактериями Corynebacterium diphtheriae и Corynebacterium ulcerans. Он может вызывать респираторные симптомы или не респираторные формы, которые влияют на другие части тела, включая кожу.
Симптомы
У людей, инфицированных бактериями дифтерии, могут развиваться симптомы или они могут не проявляться, но они являются переносчиками бактерий и способны заразить других. У большинства людей с дифтерией в первые несколько дней болезни наблюдается инфекция дыхательных путей с болью в горле и субфебрильной температурой.В легких случаях заболевания симптомы не развиваются. Однако, если заболевание более серьезное, образуется плотная оболочка, которая может быть локальной, например, только на миндалинах или глотке, или может покрывать широкую область дыхательных путей пациента. В более тяжелых случаях может развиться опухшая «шея быка». В тропических регионах дифтерия может вызывать кожные симптомы, поражающие кожу. На коже появляются язвы, покрытые серой пленкой, которая не заживает.
Осложнения
Дифтерия может вызывать выброс токсинов в систему кровообращения и ткани, что может вызвать обширное повреждение органов.Могут развиться сердечные осложнения и неврологические осложнения, например паралич. Самая частая причина смерти — удушье при аспирации мембраны.
Способы заразиться дифтерией
Дифтерия передается при контакте с каплями из дыхательных путей инфицированного человека, особенно при кашле или чихании. Если заболевание носит кожный характер, оно может распространяться при контакте с ранами или поражениями инфицированного человека. Люди, которые не лечили дифтерию, могут быть заразными до четырех недель, а люди, являющиеся носителями бактерий, могут быть заразными дольше.Путешествие, тесный контакт с крупным рогатым скотом и употребление сырых молочных продуктов — все это потенциальные факторы риска заражения.
Люди из группы наибольшего риска
Дифтерия очень редко встречается в большинстве европейских стран. Кожная форма болезни встречается в основном в тропических регионах и часто у бедных жителей городских районов и алкоголиков. Люди, которые были в тесном контакте с кем-то, инфицированным дифтерией, должны пройти тестирование на болезнь и находиться под наблюдением в течение семи дней, чтобы увидеть, проявляются ли у них признаки и симптомы.Те, кто живет в одном доме с больным дифтерией, могут пройти профилактический курс антибиотиков. Диагноз «Дифтерия» может быть подтвержден лабораторными исследованиями мазков из горла и носа пациента и анализами крови.
Лечение
Дифтерию можно лечить антитоксинами и антибиотиками.
Как избежать дифтерии
Имеется эффективная вакцина против дифтерии, а массовая иммунизация привела к сокращению числа случаев заболевания в Европе.
Примечание. Информация, содержащаяся в этом информационном бюллетене, предназначена для общей информации и не должна использоваться вместо индивидуального опыта и суждений специалистов здравоохранения.
Миокардит — Harvard Health
Что это?
Миокардит — это воспаление сердечной мышцы, которое снижает способность сердца нормально перекачивать кровь. Это может быть вызвано:
- Инфекция — Многие инфекции были связаны с миокардитом.Некоторые из наиболее вероятных микробов включают:
- Вирусные инфекции — Частая причина миокардита. Миокардит может вызывать множество различных вирусов. Примеры включают аденовирус, вирус Коксаки, вирус Эпштейна-Барра, ВИЧ, ветряную оспу и вирус герпеса человека 6. Часто у человека нет предшествующих симптомов простуды, кашля, заложенности носа или сыпи, и он узнает об инфекции только при сердечной недостаточности. имеет место.
- Бактерии — В редких случаях миокардит является осложнением эндокардита, инфекции сердечных клапанов и внутренней оболочки полостей сердца, вызванной бактериями.У некоторых людей с дифтерией токсин (яд), вырабатываемый бактериями C. diphtheriae, вызывает форму миокардита, которая приводит к дряблой, растянутой сердечной мышце. Поскольку дряблое увеличенное сердце не может эффективно перекачивать кровь, в течение первой недели болезни может развиться тяжелая сердечная недостаточность.
- Болезнь Шагаса — Эта инфекция, вызываемая простейшими Trypanosoma cruzi, передается при укусе насекомого. В Соединенных Штатах миокардит, вызванный болезнью Шагаса, наиболее распространен среди путешественников или иммигрантов из Центральной и Южной Америки.Примерно у одной трети людей с болезнью Шагаса форма хронического (длительного) миокардита развивается через много лет после первого заражения. Этот хронический миокардит приводит к значительному разрушению сердечной мышцы с прогрессирующей сердечной недостаточностью.
- Миокардит Лайма — Болезнь Лайма, инфекция, вызываемая клещевой бактерией Borrelia burgdorferi, может вызывать миокардит или другие проблемы с сердцем.
- Токсичные вещества и некоторые лекарства — Миокардит также может быть вызван:
- Чрезмерное употребление алкоголя
- Радиация,
- Химические вещества (углеводороды и мышьяк)
- Некоторые лекарственные средства, такие как препараты доксорубицина (адриамицина), I
- Воспалительные заболевания — сюда входят системная красная волчанка (СКВ или волчанка) и другие аутоиммунные заболевания и саркоидоз.
Другой тип миокардита — перинатальная кардиомиопатия. По необъяснимым причинам у некоторых женщин на самой последней стадии беременности или вскоре после рождения ребенка наблюдается нарушение функции сердечной мышцы. Это необычное состояние.
Чтобы продолжить чтение этой статьи, вы должны войти в систему .
Подпишитесь на Harvard Health Online, чтобы получать немедленный доступ к новостям в области здравоохранения и информации Гарвардской медицинской школы.
- Исследовать состояние здоровья
- Проверьте свои симптомы
- Подготовка к визиту к врачу или обследованию
- Найдите лучшие методы лечения и процедуры для вас
- Изучите возможности для лучшего питания и физических упражнений
Новые подписки на Harvard Health Online временно недоступны. Нажмите кнопку ниже, чтобы узнать о других наших предложениях по подписке.
Подробнее »
Дифтерия: предпосылки, патофизиология, эпидемиология
Автор
Брюс М Ло, доктор медицины, магистр делового администрирования, CPE, RDMS, FACEP, FAAEM, FACHE Начальник отделения неотложной медицины, больница общего профиля Сентара Норфолк; Врач-врач центра трансфера Sentara; Профессор и помощник директора программы, Основной академический факультет, Департамент неотложной медицины, Медицинская школа Восточной Вирджинии; Член правления Американской академии экстренной медицины
Брюс М Ло, доктор медицины, магистр делового администрирования, CPE, RDMS, FACEP, FAAEM, FACHE является членом следующих медицинских обществ: Американской академии экстренной медицины, Американской ассоциации руководителей врачей, Американского колледжа врачей скорой помощи, Американский колледж руководителей здравоохранения, Американский институт ультразвука в медицине, Ассоциация медсестер скорой помощи, Медицинское общество Вирджинии, Норфолкская медицинская академия, Общество академической неотложной медицины
Раскрытие: Ничего не разглашать.
Специальная редакционная коллегия
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: Получил зарплату от Medscape за работу. для: Medscape.
Барри Дж. Шеридан, DO Главный воин в переходных службах, Армейский медицинский центр Брук
Барри Дж. Шеридан, DO является членом следующих медицинских обществ: Американская академия экстренной медицины
Раскрытие: Ничего не разглашать.
Главный редактор
Джетер (Джей) Притчард Тейлор, III, доктор медицины Доцент кафедры хирургии Медицинской школы Университета Южной Каролины; Лечащий врач, клинический инструктор, специалист по комплаенсу, отделение неотложной медицины, больница Palmetto Richland
Джетер (Джей) Притчард Тейлор, III, доктор медицинских наук, является членом следующих медицинских обществ: Американской академии неотложной медицины, Американского колледжа врачей неотложной помощи, Американская медицинская ассоциация, Колумбийское медицинское общество, Общество академической неотложной медицины, Колледж врачей неотложной помощи Южной Каролины, Медицинская ассоциация Южной Каролины
Раскрытие информации: Служить (d) в качестве директора, должностного лица, партнера, сотрудника, советника, консультанта или попечителя для: Наемный подрядчик — главный редактор Medscape.
Дополнительные участники
Стивен Конрад, доктор медицины, доктор медицинских наук Заведующий отделением неотложной медицины; Руководитель многопрофильной службы интенсивной терапии, профессор кафедры неотложной помощи и внутренней медицины, Центр медицинских наук Университета штата Луизиана
Стивен Конрад, доктор медицинских наук, является членом следующих медицинских обществ: Американского колледжа грудных врачей, Американского колледжа критических врачей. Медицинская медицина, Американский колледж врачей неотложной помощи, Американский колледж врачей, Международное общество трансплантации сердца и легких, Медицинское общество штата Луизиана, Шоковое общество, Общество академической неотложной медицины, Общество неотложной медицинской помощи
Раскрытие: нечего раскрывать.
Благодарности
Allysia M Guy, MD Штатный врач, Отделение неотложной медицины, Медицинский центр Нижнего штата Нью-Йорка
Раскрытие: Ничего не раскрывать.
Лоренцо Паладино, доктор медицины Доцент кафедры неотложной медицины Научного центра здоровья SUNY в Бруклине; Консультант, помощник директора по исследованиям, отделение неотложной медицины, госпитальный центр округа Кингс
Лоренцо Паладино, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha
Раскрытие: Ничего не нужно раскрывать.
Автор: Эльзбета Пилат, MD Штатный врач, Отделение неотложной медицины, Государственный университет Нью-Йорка, Нижний штат Нью-Йорк, Госпитальный центр округа Кингс
Раскрытие: Ничего не нужно раскрывать.
Марк А. Сильверберг, доктор медицины, MMB, FACEP Доцент, заместитель директора резидентуры, Департамент неотложной медицины, Медицинский колледж Нижнего штата Нью-Йорка; Персонал-консультант, Отделение неотложной медицины, Университетская больница Статен-Айленда, Больница округа Кингс, Университетская больница, Медицинский центр в Нижнем штате Нью-Йорка
Марк А. Сильверберг, доктор медицинских наук, MMB, FACEP является членом следующих медицинских обществ: Американского колледжа врачей скорой помощи, Американской медицинской ассоциации, Совета директоров резидентур по неотложной медицине и Общества академической неотложной медицины
Раскрытие: Ничего не нужно раскрывать.
Малини К Сингх, MD Штатный врач, Отделение неотложной медицины, Медицинский центр Якоби / Монтефиоре
Раскрытие: Ничего не нужно раскрывать.
Дифтерия
Дифтерия
Дифтерия
- Является острым заразным заболеванием
- Дифтерия — результат местных и системных эффектов дифтерии.
токсин. - Характеризуется образованием мембран в горле.
- Инфекция может вызвать болезнь или состояние носительства
- Дифтерия была заболеванием детей
Corynebacterium diphtheriae
- Люди — единственный резервуар инфекции
- Аэробный, булавовидный, грамположительный, неподвижный, неинкапсулированный, плеоморфный
палочка с концевым вздутием - При окрашивании часто встречается кластерами, каждая из которых образует острые углы.
другие и напоминают китайские буквы.
Уязвимые хозяева
- Дети, не вакцинированные от C. diphtheria.
- С ослабленным иммунитетом
- Плохо
иммунизированные взрослые
Доступ к людям
- Респираторные капель
- Выделения из носоглотки
- Прямой контакт с кожной инфекцией
- Фомитес
. Организмы могут выжить в пыли и одежде до 6 месяцев.
Патогенные механизмы
Заболевание вызывается экзотоксином, подавляющим синтез белка
эукариотические клетки
Токсин содержит токсичную субъединицу A (активный токсин) и рецептор
связывающая субъединица B.Субъединица B (фрагмент) способствует транслокации
Субъединица от фагосомы до цитозоля с последующим разделением,
обеспечение полной активности субъединицы А в отношении удлинения целевого белка
фактор-2.EF-2 переносит полипептидил-переносящую РНК от акцептора к донору
сайты на рибосоме клетки-хозяина.Субъединица A катализирует перенос аденин-рибозы
фосфат от НАД до EF-2 (рибозилирование АДФ), инактивирующий EF-2 и
выключая синтез белка, токсин C. diphtheria способен подавлять
синтез белков всех эукариотических клеток.Фрагмент А обладает ферментативной активностью
Фрагмент B прикрепляется к клеточным рецепторам и предоставляет
фрагмент А вход в клетку, где он подавляет синтез белка.Экзотоксин i всасывается в кровоток и
распределены, приводя к системным осложнениям, включая демиелинизирующие
невриты и миокардиты.Токсин дифтерии также вызывает локальное разрушение
сайт образования мембраны .
Ген токсина
Ген токсина дифтерии находится в геноме
бактериофаг.Штаммы C. diphtheria должны содержать бактериофаг
(бета-фаг), приобретенный путем трансдукции от других штаммов C. diphtheria, в
чтобы выразить токсин.После трансдукции фаг необходимо лизогенизировать.
Экспрессия токсина (ген лисы) регулируется
кодируемый хромосомами репрессорный белок (DtxR) при ограничении содержания железа.
H ПВО Умани
- Похоже, у нас нет никакой защиты от токсина.Защита есть
обеспечивается только вакцинацией. - С организмами борются?
Клинические проявления
Инкубационный период 2-5 суток
Дифтерия — результат местных и системных эффектов дифтерии.
токсин.
Летальность в нелеченых случаях составляет 10-50%.
Диагностика
Первоначальный диагноз клинический
Нет экспресс-теста
Окраска горла по Граму бесполезна
Организм можно культивировать для подтверждения диагноза.Пропущенный
на обычных культурах. Сообщите в лабораторию о возможном диагнозе.Производство токсинов культивируемых штаммов может осуществляться
иммунодиффузия.Сыворотка на антитела к дифтерийному токсину
Другие полезные оценки
ЭКГ и сердечные ферменты для выявления миокардита
CXR: гиперинфляция, подсвязочное сужение
Терапевтическая стратегия
Строгая изоляция
С.diphtheriae антитоксин дается незамедлительно для нейтрализации
токсин.Обратитесь в CDC за антитоксином и инструкциями по применению.
Не ждать
для подтверждения культуры.Антитела, вырабатываемые против токсина в естественных
инфекционное заболевание.Обработайте токсином, чтобы нейтрализовать свободный токсин перед этим.
связывается с клетками.
Сам организм можно лечить пенициллином ,
цефалоспорины и эритромицин.Сообщить в отдел здравоохранения
Клиническая дифтерия не дает иммунитета, следовательно,
активную иммунизацию дифтерийным анатоксином следует проводить во время
выздоровление.Бронходилататоры при необходимости.
Следите за респираторной обструкцией и примите необходимые
шаги.Следите за миокардитом и чесоткой соответствующим образом
Профилактика
- Своевременная вакцинация
- Дифтерия: иммунизация анатоксином вызывает
ответ антител, предотвращающий заражение дифтерией. - Вакцинация анатоксином = токсин, обработанный формалином
- Дифтерия: иммунизация анатоксином вызывает
- Бустерная доза столбняка-дифтерии каждые 10 лет до взрослого возраста
- Надзор в сообществах, где дифтерия была эндемичной
- Закрыть контакты
- Следует выявить и лечить пероральным эритромицином для
7-10 дней - Обеспечить активной иммунизации
- Следует выявить и лечить пероральным эритромицином для
Прочие виды
Corynebacterium ulcerans:
- Кожная дифтерия
- Обычно вызывается токсическими штаммами.
- Вырабатывает естественный иммунитет
- Может вызывать эпидемии у плохо иммунизированных групп населения.
(PDF) Прогностическое значение электрокардиографических изменений при дифтерийном миокардите: перекрестное исследование
K. Rapolu et al.
1. Введение
Заболеваемость дифтерией в развитых странах неуклонно снижалась после эффективной программы иммунизации
с 1920-х годов.Однако возрождение наблюдалось в основном из-за ослабления иммунитета у взрослых. В
развивающихся странах это заболевание все еще носит эндемический характер и является причиной высокой смертности [1] [2].
Corynebacterium diphtheria продуцирует экзотоксины, которые вызывают фрагментацию ДНК и цитолиз, ингибируя активность фактора элонгации-2
в синтезе белка в дополнение к повреждению проводящей ткани [3] [4]. В миокарде
также наблюдается гиалиновая дегенерация и некроз.Это приводит к развитию миокардита у больных дифтерией
. Миокардит может развиваться примерно у 10–25% пациентов с респираторной дифтерией и считается наиболее серьезным осложнением с высокой зарегистрированной летальностью [5] [6]. Риск развития сердечной токсичности
пропорционален степени тяжести местной инфекции. Дифтерийный миокардит часто проявляется аритмиями
, которые при неправильном лечении могут вызвать внезапную смерть.Пациенты с поражением сердца могут быть асимптотическими (изменения электрокардиограммы (ЭКГ) и / или повышенные сердечные ферменты) или симптоматическими (признаки сердечной недостаточности
) [7].
В Индии дифтерия все еще остается эндемической и связана с молниеносными осложнениями и смертностью [8]. Ряд факторов, таких как недостаточный охват вакцинацией, плохой социально-экономический статус, несвоевременная отчетность и отложенное введение ad-
или недоступность дифтерийного антитоксина, дополнительно способствуют высокой смертности [9].Несмотря на то, что в Индии распространенность этого заболевания была выше
, мы обнаружили нехватку литературы, посвященной заболеваемости, клиническому профилю
, а также клиническим исходам миокардита у пациентов с диагнозом дифтерийный миокардит.
Итак, мы планируем исследование с учетом клинического профиля, клинических исходов, а также статуса иммунизации пациентов с диагнозом дифтерийный миокардит в Индии.
2. Методология
2.1. Дизайн исследования и популяция пациентов
Это было проспективное одноцентровое обсервационное исследование. В общей сложности 33 случая с клинически подтвержденным агнозом дифтерийного миокардита диагнозом дифтерийный миокардит диагнозом
были переведены из «Института тропических и инфекционных болезней сэра Рональда Росса», Хайдарабад, Индия, с августа 2011 г. по декабрь 2012 г. в департамент кардиология, больница общего профиля Османии
, Хайдарабад, Индия, для дальнейшего лечения были включены в исследование. Протокол исследования был одобрен комитетом по этике института
.Письменное информированное согласие было получено от всех пациентов или от
родителей пациента.
Критерии включения: в исследование были включены все пациенты, госпитализированные с клинически подтвержденным диагнозом дифтерия.
миокардит.
Критерии исключения: (1) Пациенты со структурным пороком сердца; (2) пациенты с фоновым анамнезом сахарного диабета,
артериальной гипертензии, болезни сердца; и (3) пациенты с предыдущими изменениями ЭКГ были исключены из этого исследования.
Подробный анамнез и отчеты клинического обследования были собраны с использованием заранее определенной формы истории болезни
. Информация об иммунизации была получена от родителей или сопровождающего пациента. За каждым пациентом внимательно наблюдали
на предмет развития одышки, сердцебиения и дискомфорта в груди, а также гипотензии
. ЭКГ-12 отведения и 2-мерная эхокардиография были сделаны во время поступления и повторены как и
при необходимости.Всем пациентам, у которых развилась полная блокада сердца, был установлен временный кардиостимулятор. Пациент
находился под наблюдением до выписки из стационара.
Мы приняли ранее опубликованные критерии аномальной ЭКГ у пациентов с дифтеритическим миокардитом, как
: аритмия, аномальные зубцы Q, аномалии реполяризации, подъем сегмента ST (подъем> 1 мм в
, по крайней мере, два грудных отведения или одно отведение от конечности. ), Инверсия зубца T (кроме отведений V1 и aVR) изоэлектрические зубцы T и интервал QTc
(> 0.39 с для мужчин и> 0,41 с для женщин), артериовентрикулярная блокада, блокада ножки пучка Гиса и полная блокада сердца
.
2.2. Статистический анализ
Статистический анализ выполняли с использованием статистического пакета для социальных наук (SPSS; Чикаго, Иллинойс, США) pro-
грамм, версия 15. Непрерывные данные выражены как среднее значение + стандартное отклонение.
3. Результаты
За исследуемый период обследовано 33 пациента с дифтерийным миокардитом.Демографические и
Хронология | История вакцин
Дифтерия: детская чума
Когда-то дифтерия была основной причиной болезней и смерти детей. В 1921 году в Соединенных Штатах было зарегистрировано 206 000 случаев дифтерии, в результате которых погибло 15 520 человек. Смертность от дифтерии колеблется от примерно 20% для лиц в возрасте до пяти лет и старше 40 лет до 5–10% для лиц в возрасте 5–40 лет. Смертность, вероятно, была выше до 20 -го века.Дифтерия была третьей по значимости причиной смерти детей в Англии и Уэльсе в 1930-х годах. [1]
С момента внедрения эффективной иммунизации, начиная с 1920-х годов, заболеваемость дифтерией резко упала в Соединенных Штатах и других странах, где вакцинация проводится повсеместно. В период с 2004 по 2008 год случаев дифтерии в США не регистрировалось. Однако болезнь продолжает играть важную роль во всем мире. В 2007 г. было зарегистрировано 4 190 случаев дифтерии, что, вероятно, является заниженной оценкой фактического числа случаев. [2]
Передача и симптомы
Дифтерия передается от человека к человеку, как правило, воздушно-капельным путем. Инфекция вызывается бактериями под названием Corynebacterium diphtheriae. Инфицированный человек, если его не лечить антибиотиками, заразен в течение двух-трех недель. Симптомы включают боль в горле, потерю аппетита и жар. Однако наиболее заметной особенностью дифтерийной инфекции является образование плотного серого вещества, называемого псевдомембраной, над тканями носа, миндалинами, гортань и / или глоткой.
Псевдомембрана образуется из продуктов жизнедеятельности и белков, вызванных токсином, выделяемым бактериями. Псевдомембрана прилипает к тканям и может затруднять дыхание. Сам токсин может попасть в сердце, мышцы, почки и печень, где он может временно или навсегда повредить эти органы.


 Инфицированы гортань и трахея.
Инфицированы гортань и трахея.