Атеросклероз: лекарства с грядки
Лекарствами с грядки традиционно называют овощи. Собственно, овощи изначально и использовали, как лекарства. Первые «аптекарские огороды», как их называли, появились в Европе еще в 15 веке. В таких огородах выращивалась полезные для здоровья растительные продукты. Постепенно. с появлением изобилия овощей, они стали доступными и распространенными продуктами питания. Причем, в последние десятилетия роль овощей в питании только возрастает, особенно в диетических рекомендациях по профилактике и лечению сердечно-сосудистых заболеваний.
Полезное действие овощей, фруктов, ягод на организм:
- Снижение общей калорийности рациона, за счет своей низкой калорийности, поэтому являются основой различных разгрузочных диет.
- Большое содержание балластных веществ (пектина, клетчатки) способствует выведению из организма излишков холестерина.
- Различные токсические вещества: многие синтетические препараты, в т.ч. лекарственные средства, вредные вещества, накапливающиеся после курения и приема алкоголя, обезвреживаются на фоне приема плодоовощной продукции.
- В свежем виде являются богатым источником витаминов С, Р, В, РР, каротина.
- Много солей калия в овощах улучшает работу сердца, и способствуют выделению излишнего количества воды из организма.
- За счет содержания в овощах в большом количестве тартроновой кислоты, некоторые стадии биохимических превращений углеводов в жировые отложения в организме блокируются.
- Богатый состав разнообразных минеральных солей и органических кислот в растительных продуктах питания позволяет разнообразить естественным образом вкусовые ощущения. Это обстоятельство помогает ограничить применение обыкновенной поваренной соли и усилителей вкуса в виде уксуса и других искусственных веществ, не полезных для здоровья.

- Растительный белок, содержащийся в некоторых растениях в значительном количестве, служит основой вегетарианских блюд.
- Вышеуказанные полезные свойства принесет ежедневный прием взрослыми людьми овощей и фруктов в пределах от одного до трех килограмм, преимущественно в свежем виде.
Предостережения при употреблении растительной пищи:
1) Не допускайте длительного хранения свежих овощей и зелени.
2) Исключите попадание прямых солнечных лучей, во избежание разрушения витаминов группы В.
3) Исключите из приема фрукты и овощи с высоким гликемическим индексом (большим содержанием сахара и крахмала), если имеется избыточный вес, ожирение и сахарный диабет.
4) Применяйте наиболее щадящие виды кулинарной обработки пищи: запекание, тушение, отваривание, сушка, квашение. Такие виды, как жарение и маринование, сведите к минимальному. Жарение – самый нежелательный способ, т.к. происходит поглощение большого количества жиров и масел, высокая температурная обработка способствует образованию трансгенного жира, одного из главных виновников формирования атеросклеротических бляшек в артериях, нарушающих нормальное кровоснабжение. Маринование разрушает витамины, частое поступление уксуса приводит к нарушению работы органов пищеварения.
5) Помните, что тепловая обработка не должна быть продолжительной, т.к. разрушаются полезные для организма вещества.
6) Употребляйте только свежеприготовленную еду.
7) Не увлекайтесь монодиетами продолжительное время. Для получения полноценного набора витаминных и минеральных веществ необходимо разнообразие, ежедневное употребление не менее пяти видов разнообразных овощей и фруктов.
8) Знайте, что длительное употребление только растительной пищи (вегетарианство) не восполняет полноценный набор аминокислот для синтеза белков, а значит, ослабляет многие функции организма: иммунную, половую, восстановительную, регуляторную, постепенно снижает умственную и физическую работоспособность;
9) Советуйтесь со своим лечащим врачом по употреблению овощей и фруктов, с учетом индивидуальных особенностей организма и наличия заболеваний.
О популярных растениях с наших огородов
Картофель – способствует лечению артериальной гипертонии. Ученые из Института исследования пищи (Великобритания) обнаружили в картошке какоамины – редкие вещества, которые помогают при повышенном артериальном давлении. Ранее считалось, что какоамины содержаться лишь в травах, используемых в китайской медицине. При избыточном весе применять не более 2-3 картофелин среднего размера в день. При болях в сердце, нарушениях ритма и склонности к отекам очень хорошо использовать картошку в запеченном с кожурой виде для восполнения запасов калия в организме.
Огурец – еще один из лидеров по содержанию калия, способствует нормализации водно-минерального состава организма, а значит нормализации давления, снятию отеков. И размер огурца в этом случае тоже имеет значение: оптимально, если он будет длиной 5-7 см и выращен на открытом грунте.
Морковь – накапливает в себе в период созревания богатый и полезный минеральный состав: кремний, кобальт, медь, магний, железо, что способствует при их ежедневном употреблении лечению анемии, проведению иммунокоррекции, укреплению связок, костей и суставов.
Капуста– один из самых доступных овощей для круглогодичного использования в свежем виде, способствует снятию воспалительных изменений желудочно-кишечного тракта, за счет имеющегося редкого витамина U. Есть данные, что этот витамин эффективен и для лечения тяжелых видов гриппа, например, птичьего. Капуста – хороший источник цинка, магния, калия. Данные минералы играют роль в проведении нервных импульсов, в т.ч. в сердечной мышце. Это способствует профилактике нарушений ритма сердца.
Кабачок – главная его привлекательность в низкой калорийности: на 100 гр. приходится всего 27 ккалорий, поэтому он с успехом может использоваться в разгрузочных диетах. Это легкоусвояемый овощ. Содержащийся в нем фосфор, кальций, калий укрепляет зубы и кости, способствует успокоению и расслаблению, снижению артериального давления.
приходится всего 27 ккалорий, поэтому он с успехом может использоваться в разгрузочных диетах. Это легкоусвояемый овощ. Содержащийся в нем фосфор, кальций, калий укрепляет зубы и кости, способствует успокоению и расслаблению, снижению артериального давления.
Свекла– лидер из овощей по содержанию йода, марганца, магния, молибдена. Эти минералы незаменимы в регуляции работы сердца, мозга, щитовидной железы. Большое количество органических кислот в свекле обладают свойством «растворения» кровеносных сгустков и тромбов в сосудистом русле. Один из простых рецептов для полноценного применения полезных свойств свеклы: ½ стакана натертой сырой свеклы смешать с ½ стакана цветочного меда, применять по 1 столовой ложке 3 раза в день за 30 мин. до еды 3 месяца.
Фасоль, бобы, горох – значительное содержание растительного белка, около 80%, делает их основой вегетарианской диеты. Не забывайте, что растительный белок не имеет всех необходимых организму аминокислот. Малое количество жира и большой состав витаминов группы В – незаменимы в диетах при заболеваниях сердца с повышенным уровнем холестерина в крови.
Чеснок – давнее средство для «чистки» сосудов от атеросклероза, а также противовирусное и антимикробное природное «лекарство». Но надо помнить, что он не может быть полноценной заменой современным лекарствам! Чеснок только вспомогательное средство. Для полноценного самочувствия употребляйте по 1 дольке чеснока ежедневно. При изобильном урожае – измельчите очищенные дольки и высушите для дальнейшего употребления в качестве сухой приправы. Попробуйте сделать чесночное масло: растолочь чеснок в кашицу, сложить в стеклянную банку, смешать с небольшим количеством подсолнечного масла, масло долить столько, чтобы оно закрывало кашицу. Хранить такое масло в холодильнике и употреблять по 1 чайной ложке 3 раза в день за 30 мин. до еды 1 мес., 3-4 курса в год.
до еды 1 мес., 3-4 курса в год.
Лук – активное антибактериальное средство, «лук от семи недуг» — говорят в народе, применяется в любой кухне мира. Кстати, как удалить запах лука после еды? Для этого можно выпить стакан молока или пожевать зелень (укроп, петрушку), или цедру цитрусовых. В отличие от чеснока, в репчатом луке содержится сера, которая препятствует свертыванию крови, т.е. образованию внутрисосудистых тромбов. Благодаря различным соединениям серы в луке происходит снижение уровня холестерина в крови, улучшение функции клеточной мембраны в эритроцитах. Соединения серы способствуют восстановлению и укреплению памяти на фоне атеросклероза сосудов мозга.
Помидоры – как и другие овощи красного цвета, улучшают кровь. По содержанию железа, кроветворного элемента, помидоры в несколько раз превосходят мясо курицы и молоко. В этом плане наиболее полезны ягоды (а по определению ботаников помидорные плоды является ягодой!) насыщенного красного цвета. Свежие помидоры и томатный сок необходимо употреблять для профилактики полиавитаминозов. В помидорах содержится много калия, который выводит из организма соль и излишнюю воду. Выявленные в помидорах биологически активные вещества – ситостерин, холин и тритерпеновые сапонины – это лечебные вещества, снижающие уровень холестерина, спасающие от атеросклероза. Этот факт обрадует людей, желающих привести холестерин в норму.
Приятного аппетита и отличного здоровья!
Информацию подготовила: Шабардина С.В.,
зав. кабинетом медицинской профилактики,
врач по гигиеническому воспитанию
Средства для лечения атеросклероза (снижающие холестерин)【Интернет-Аптека】
Эффективные лекарства от атеросклероза
Атеросклероз – настоящий бич современности. Уровень смертности по причине различных сердечно-сосудистых патологий зашкаливает. При чем в зону риска попадают не только мужчины и женщины, которым за 50. Молодые люди возрасте 20-30 лет, пренебрегающие правилами правильного питания – тоже потенциальные жертвы атеросклероза.
Уровень смертности по причине различных сердечно-сосудистых патологий зашкаливает. При чем в зону риска попадают не только мужчины и женщины, которым за 50. Молодые люди возрасте 20-30 лет, пренебрегающие правилами правильного питания – тоже потенциальные жертвы атеросклероза.
В чем опасность атеросклероза?
Атеросклероз поражает сосуды. Питание, которое перенасыщено жирами животного происхождения – один из главных факторов, приводящих к болезни. Но среди причин атеросклероза можно также назвать:
• наследственность;
• психоэмоциональные перенапряжения;
• постоянное пребывание в состоянии стресса;
• «сидячую» работу.
Когда человек здоров, кровь свободно циркулирует по венам, артериям и мелким сосудам, питая органы и ткани. Если же кровеносная система перенасыщена холестерином, образуются атеросклеротические бляшки. В дальнейшем могут образовываться тромбы, которые отрываясь от стенок сосудов разносятся с кровью по всему организму.
Если диаметр тромба равен просвету сосуда, происходит закупоривание и, как следствие, кровоснабжение нарушается.
Какие лекарства эффективны при атеросклерозе?
Бороться с болезнью гораздо сложнее, чем ее предотвратить. Поэтому стоит прислушаться к советам диетологов и изменить свой рацион. Найдите время для двигательной активности, заведите привычку начинать день с утренней пробежки.
Предупредить инсульт помогут таблетки от атеросклероза сосудов головного мозга.
Если артерии и вены перекрыты на 3/4, то пациенты уже начинают ощущать первые недомогания. В зависимости от того, какие сосуды повреждены больше, могут возникать:
• головокружения;
• обмороки;
• мигрени;
• коликоподобные боли в брюшинном пространстве;
• гипертонические кризы;
• болевые ощущения в области голеней пр.
В «Аптеке гормональных препаратов» представлен широкий ассортимент медпрепаратов, которые дают хороший профилактический и лечебный эффект. Здесь можно купить без наценок таблетки от атеросклероза сосудов, БАДы ведущих производителей из Великобритании, Германии, Македонии, Индии.
Здесь можно купить без наценок таблетки от атеросклероза сосудов, БАДы ведущих производителей из Великобритании, Германии, Македонии, Индии.
Как сделать заказ?
Совершать покупки в «Аптеке гормональных препаратов» просто. Воспользуйтесь фильтром, чтобы указать вид препарата, действующее вещество, форму выпуска. При необходимости можете воспользоваться консультацией опытных менеджеров. Вам помогут подобрать лекарство и оформить заказ. Есть доставка по Киеву и в пригороде.
Атеросклероз сосудов: лечение, симптомы, причины, профилактика | Болезни артерий
Cосуды подверженные атеросклерозу
При атеросклерозе поражаются крупные магистральные артерии — аорта и её ветви. Среди отделов аорты больше всего подвержена атеросклерозу брюшная аорта. Клинически значимый атеросклероз дуги аорты и грудного отдела аорты встречается значительно реже.
Из периферических артерий и непосредственно ветвей аорты следует выделить:
- коронарные (венечные) сосуды,
- питающие сердце,
- брахиоцефальные артерии (БЦА),
- подключичные артерии,
- общие и внутренние сонные артерии (ВСА),
- позвоночные артерии,
- артерии конечностей,
- почечные артерии,
- чревный ствол,
- мезентериальные артерии.
При поражении нескольких артериальных бассейнов говорят о генерализованном (распространенном) атеросклерозе. Наиболее часто атеросклероз поражает коронарный, брахиоцефальный бассейны, а также сосуды, кровоснабжающие нижние конечности.
Чем опасен атеросклероз
Атеросклеротические или, как их ещё называют, холестериновые бляшки, постепенно суживают просвет артерий и делают их менее эластичными. Это создаёт препятствие для нормального тока крови и приводит к недостаточности кровоснабжения питающего органа.
Сужение просвета сосуда атеросклеротической бляшкой называется стенозом, а полная закупорка просвета — окклюзией. Симптомы заболевания начинают проявляться при определенной степени стеноза артерии, в таком случае можно говорить о стенозирующем атеросклерозе сосудов. Так, например, если сужаются артерии сердца, то кровоток к сердечной мышце (миокарду) уменьшается. Это может вызвать появление болей за грудиной и одышки, что в итоге может привести к инфаркту. Частицы атеросклеротической бляшки могут отрываться от стенок артерий и переноситься с кровью до более узких сосудов, полностью блокируя их просвет.
Так, например, если сужаются артерии сердца, то кровоток к сердечной мышце (миокарду) уменьшается. Это может вызвать появление болей за грудиной и одышки, что в итоге может привести к инфаркту. Частицы атеросклеротической бляшки могут отрываться от стенок артерий и переноситься с кровью до более узких сосудов, полностью блокируя их просвет.
Кроме того, опасность атеросклероза заключается в том, что частицы атеросклеротической бляшки могут отрываться от стенок артерий и переноситься с кровью до более узких сосудов, блокируя их просвет. В области атеросклеротических бляшек могут образовываться тромбы, частично или полностью блокируя просвет артерии. В подобных случаях происходит острое нарушение кровоснабжения питающего органа, что может привести к опасным, нередко жизнеугрожающим осложнениям. Описанные механизмы нередко являются причиной инсульта, инфаркта миокарда, тромбоза и облитерирующего атеросклероза сосудов нижних конечностей.
Клиническая картина или симптомы атеросклероза
Симптомы атеросклероза зависят от органа, который питают пораженные атеросклеротическими бляшками сосуды. Так, при поражении коронарных артерий страдает сердечная мышца (миокард), развивается ишемическая болезнь сердца (ИБС). Появляются признаки стенокардии — боли за грудиной и одышка при физической нагрузке или в покое.
Из числа сосудов, питающих головной мозг, наиболее часто атеросклерозом поражается внутренние сонные и позвоночные артерии. При этом пациентов могут беспокоить головокружения, нарушение памяти и зрения, эпизоды потери чувствительности или движений в области лица и в конечностях, нарушения речи. При длительном существовании атеросклеротической бляшки в просвете сонной артерии возможно возникновение изъязвлений на её поверхности, а также тромбов, которые могут уноситься с током крови в сосуды головного мозга, вызывая такие клинические проявления как парез/паралич, внезапную потерю чувствительность в конечностях или в области лица, а также временную слепоту.
При поражении сосудов ног появляются симптомы перемежающей хромоты — боли в икроножных (реже — в ягодичных и бедренных) мышцах, возникающие при ходьбе. При прогрессировании облитерирующего атеросклероза сосудов нижних конечностей в конечном итоге возникают трофические язвы и гангрена конечности. При атеросклерозе подвздошных артерий также может иметь место нарушение потенции (эректильная дисфункция).
Причины возникновения атеросклероза
Причины атеросклероза остаются до конца не изученными. Считается, что начальные стадии атеросклероза возникают уже в молодом возрасте, однако обычно он достигает своей клинической значимости у лиц старшей возрастной группы (старше 50 лет). Выделяют факторы риска атеросклероза, воздействие на которые может существенно замедлить его прогрессирование, снизить выраженность его проявлений и предотвратить возникновение осложнений.
Факторы риска атеросклероза
- Высокое артериальное давление,
- Высокий уровень холестерина в крови — липопротеинов низкой плотности (ЛПНП),
- Диета с высоким содержанием животных жиров,
- Курение,
- Ожирение,
- Отягощённая наследственность,
- Сахарный диабет.
Холестерин и атеросклероз
Важен регулярный контроль анализа крови на так называемый «плохой» холестерин, откладывающийся в стенке артерий и вызывающий появление и рост атеросклеротических бляшек. При повышенном значении холестерина липопротеинов низкой плотности необходимо проконсультироваться у терапевта, кардиолога или сосудистого хирурга. При отсутствии противопоказаний рекомендован прием статинов — медикаментозных препаратов, снижающих уровень «плохого» холестерина в крови.
Профилактика атеросклероза сосудов
Лучшее лечение атеросклероза — его профилактика. Она является необходимой с целью предотвращения возникновения первых признаков и симптомов заболевания, что позволит побороть атеросклероз уже на начальных стадиях. Профилактика заключается в первую очередь в диете: не злоупотреблять жирной пищей, а также обязательном отказе от курения. В случае наличия гипертонической болезни (гипертонии) необходимо поддерживать нормальные значения артериального давления с осуществлением его контроля, а также приема медикаментозных препаратов, предварительно проконсультировавшись у терапевта или кардиолога. При наличии сахарного диабета показано поддержание нормального уровня глюкозы в крови посредством приема сахароснижающих препаратов, назначенных эндокринологом, ежедневный контроль уровня глюкозы в крови, регулярное наблюдение у эндокринолога.
В случае наличия гипертонической болезни (гипертонии) необходимо поддерживать нормальные значения артериального давления с осуществлением его контроля, а также приема медикаментозных препаратов, предварительно проконсультировавшись у терапевта или кардиолога. При наличии сахарного диабета показано поддержание нормального уровня глюкозы в крови посредством приема сахароснижающих препаратов, назначенных эндокринологом, ежедневный контроль уровня глюкозы в крови, регулярное наблюдение у эндокринолога.
Какой врач лечит атеросклероз сосудов?
При подозрении на атеросклероз, необходим осмотр врача-специалиста:
- Ангионевролога — при атеросклерозе сосудов головного мозга;
- Кардиолога — при атеросклерозе сосудов сердца;
- Сосудистого хирурга — при признаках заболеваний артерий рук или ног, шеи, грудной клетки и брюшной полости.
Показаться специалисту (сосудистому хирургу) необходимо в случае, если у вас имеется один или несколько факторов риска атеросклероза, а также присутствуют жалобы, характерные для заболеваний артерий. Особенно важно обратиться за квалифицированной помощью при начальных проявлениях болезни, когда возможно предотвратить развитие тяжёлых осложнений атеросклероза.
Перед тем, как назначить инструментальные методы диагностики врач должен оценить жалобы пациента. Собрать информацию о перенесённых заболеваниях и проведённом в прошлом лечении. Объективный осмотр даёт детальную информацию о тяжести и распространённости заболевания.
В ряде случаев диагноз атеросклероза может быть исключён на этапе первичного осмотра. В случае выявления атеросклероза сосудов той или иной локализации, врач может назначить дополнительное обследование.
Лабораторно-инструментальные исследования, которые могут быть использованы для диагностики атеросклероза:
Как лечить атеросклероз сосудов: медикаментозное лечение атеросклероза
Бороться с атеросклерозом сосудов можно консервативным и оперативным способом. Консервативное лечение атеросклероза применяется при не выраженных и нестенозирующих формах атеросклероза. Оно включает в себя борьбу с факторами риска атеросклероза, а также прием лекарственных препаратов из числа статинов (Симвастатин, Аторвастатин, Розувастатин и др.) и антиагрегантов (ацетилсалициловая кислота, клопидогрель и др.), препятствующих дальнейшему росту атеросклеротических бляшек и образованию тромбов на их поверхности. Медикаментозные препараты назначаются на постоянный или длительный прием.
Оно включает в себя борьбу с факторами риска атеросклероза, а также прием лекарственных препаратов из числа статинов (Симвастатин, Аторвастатин, Розувастатин и др.) и антиагрегантов (ацетилсалициловая кислота, клопидогрель и др.), препятствующих дальнейшему росту атеросклеротических бляшек и образованию тромбов на их поверхности. Медикаментозные препараты назначаются на постоянный или длительный прием.
Обратим ли атеросклероз сосудов?
На данный момент препаратов, позволяющих избавиться от атеросклероза и очистить сосуды от атеросклеротических бляшек не существует.
Атеросклероз – это необратимое заболевание, и полностью вылечить его невозможно. При запущенных формах атеросклероза нередко применяется оперативное лечение. Современные хирургические методы позволяют выполнить операцию эффективно, малотравматичным способом и без серьезных последствий для организма, восстановить просвет пораженного атеросклерозом сосуда и возобновить достаточный приток крови к органу.
Лечение атеросклероза сосудов нижних конечностей
Причины возникновения атеросклероза сосудов нижних конечностей
Атеросклероз — достаточно распространенное заболевание, которое начинает затрагивать человека после 40 лет. Но после 65 процесс развития облитерирующего атеросклероза проходит гораздо быстрее. От сужения сосудов ног в большей степени страдают мужчины – их почти 80 % от всех заболевших.
Так как атеросклероз – это системное заболевание, облитерирующий атеросклероз часто является только частью проблемы. Сосуды сердца, головного мозга, почек также подвергаются разрушительному воздействию этого заболевания.
Факторами, влияющими на развитие заболевания, считаются:
- курение
- стрессы
- лишний вес
- малоподвижный образ жизни
- высокий уровень холестерина
- генетическая предрасположенность
Одним из главных негативных факторов развития атеросклероза нижних конечностей является курение. Никотин и смолы влияют на увеличение количества сердечных сокращений, способствуют развитию бляшек. Из-за курения сосуды становятся более грубыми, теряют свою эластичность и истончаются.
Никотин и смолы влияют на увеличение количества сердечных сокращений, способствуют развитию бляшек. Из-за курения сосуды становятся более грубыми, теряют свою эластичность и истончаются.
Курение также является причиной повышения артериального давления. Атеросклероз сосудов конечностей у курящих людей возникает в два раза чаще, чем у некурящих.
Лишний вес также связан с развитием заболевания – неправильное питание и избыток жировой ткани негативно влияют на сосуды и сердце. К тому же лишний вес, который приводит к серьезной нагрузке на ноги, увеличивает шансы на развитие именно облитерирующего атеросклероза.
Малоподвижный образ жизни, который ведут многие люди, тоже влияет на процесс сужения сосудов. Сидячая работа и отсутствие адекватных физических нагрузок часто приводят к развитию заболевания.
Чтобы избежать этого, необходимо заниматься физкультурой. Это позволит не только улучшить кровоснабжение, но и держать себя в форме.
Стрессовые ситуации, различные волнения не оказывают прямого влияния на возникновение облитерирующего атеросклероза, но являются провоцирующими факторами.
Часто при нервных срывах и стрессах люди «заедают» или «запивают» свои проблемы. Алкоголь, жирная пища, курение – все это приводит к развитию не только атеросклероза, но и к целому букету других, не менее серьезных заболеваний.
Наследственные заболевания – гипертония, ишемическая болезнь сердца, сахарный диабет – имеют не последнее значение в развитии атеросклероза. Если ваши близкие родственники страдали от этих болезней, и особенно отягощенных атеросклерозом, вероятность развития атеросклероза резко увеличивается.
Имеющаяся неблагоприятная наследственность должна держать вас настороже – необходимо очень внимательно следить за своим здоровьем, вести здоровый образ жизни, правильно питаться, заниматься спортом. Исключая дополнительные негативные факторы, вы можете избежать развития атеросклероза.
Препараты для улучшения мозгового кровообращения
Заказать препараты для улучшения мозгового кровообращения
Препараты для улучшения мозгового кровообращения используют при разных заболеваниях. Жители Москвы, Санкт-Петербурга, Московской и Ленинградской областей
Жители Москвы, Санкт-Петербурга, Московской и Ленинградской областей
могут заказать их в каталоге 366.ru, а получить и оплатить в ближайшей аптеке «36,6». Их более 1200, и выбрать подходящую по местоположению довольно
просто. На сайте представлен широкий выбор лекарственных средств.
Поиск по названию, назначению, действующему веществу, бренду и сортировка по алфавиту, стоимости или скидке позволяет каждому клиенту найти
необходимое лекарство или аналог по оптимальной для него цене.
Сеть соблюдает все требования законодательства в сфере фармацевтики, большое внимание уделяется сертификации, условиям хранения и
транспортировки медикаментов и сопутствующих товаров. Есть программа лояльности для владельцев карт «Клуб 36,6».
Показания
Сосудистые препараты для улучшения кровообращения служат для укрепления сосудов и расширения их просветов, за счет чего увеличивается
приток кислорода в периферические отделы головного мозга.
Список симптомов, при которых назначают эти лекарства:
- при головокружениях,
- некоторых видах головных болей,
- ухудшении памяти,
- бессоннице,
- при нарушении умственной деятельности,
- расстройствах психики и двигательной активности.
В составе комплексной терапии их используют для:
- нормализации давления при гипертонии и атеросклерозе,
- улучшения кровотока при шейном остеохондрозе,
- восстановления функций после черепно-мозговых травм и инсультов.
Растительные ангиопротекторные средства могут назначаться в течение длительного периода, в том числе для пожилых пациентов [i].
Противопоказания
Назначать самостоятельно подобные препараты нельзя, поскольку только специалист может учесть все факторы и правильно подобрать комплекс лекарств.
К числу противопоказаний относятся:
- Гиперчувствительность к компонентам препарата;
- Декомпенсированная сердечная недостаточность;
- Задержка жидкости в организме;
- Нарушения функции печени и почек.

Некоторые лекарства при определенных условиях могут использоваться при лечении детей и подростков, а также беременных и кормящих женщин.
Формы выпуска
В какой форме выпуска назначают тот или иной лекарственный препарат, зависит от тяжести состояния, возраста пациента и др.
Капсулы и таблетки для улучшения мозгового кровообращения и памяти могут использоваться как при стационарном или амбулаторном лечении, так и в домашних условиях.
Для более интенсивного лечения применяют порошки для приготовления раствора, флаконы и ампулы для внутривенного или внутримышечного введения.
Страны изготовители
Лекарственные средства для улучшения мозгового кровообращения изготавливают практически во всех странах с развитым фармацевтическим производством.
На сайте вы можете выбрать как препараты российских производителей, так и импортированные из:
- Австрии,
- Беларуси,
- Венгрии,
- Германии,
- Индии.
ПЕРЕД ПРИМЕНЕНИЕМ ПРЕПАРАТОВ НЕОБХОДИМО ОЗНАКОМИТЬСЯ С ИНСТРУКЦИЕЙ ПО ПРИМЕНЕНИЮ ИЛИ ПРОКОНСУЛЬТИРОВАТЬСЯ СО СПЕЦИАЛИСТОМ.
Список литературы:
- [i] Е.А.Катунина, Гинкго билоба: итоги полувекового опыта применения, Полимодальность эффектов гинкго билоба: экспериментальные и клинические
исследования, Неврология и ревматология выпуск 02 (2013) Доступ по ссылке https://www.bilobil.net/ru/pomos-mozgu/angioprotektornye-sredstva/
Как победить атеросклероз
: 8 Ноя 2012 , Недаром помнит вся Россия , том 46,
№4
В России, как и в большинстве экономически развитых стран мира, каждый второй человек умирает от сердечно-сосудистых заболеваний атеросклеротического происхождения и их осложнений, таких как острый инфаркт миокарда. Особенно тревожит тот факт, что в нашей стране смертность от этих заболеваний продолжает расти, в то время как в странах Западной Европы, США, Канаде, Японии и Австралии такую ситуацию удалось переломить.
Особенно тревожит тот факт, что в нашей стране смертность от этих заболеваний продолжает расти, в то время как в странах Западной Европы, США, Канаде, Японии и Австралии такую ситуацию удалось переломить.
Сегодня важнейшим фактором предупреждения развития атеросклероза является эффективная медикаментозная терапия. Одной из важнейших причин появления атеросклероза считается нарушение обмена холестерина, свыше 70 % которого образуется непосредственно в самом организме, а не поступает из пищевых продуктов. Поэтому сегодня лидерами рынка являются гиполипидемические препараты, воздействующие на этапы синтеза и метаболизм такого эндогенного холестерина.
Сегодня перед фармацевтической индустрией стоят задачи не только разработки новых лекарств, но и создания дешевых и эффективных технологий синтеза уже хорошо зарекомендовавших себя препаратов, таких как статины или глитазары. В рамках этого подхода в Институте органической химии им. Н.Н. Ворожцова СО РАН уже разработан способ так называемого «древовидного» синтеза ключевого терапевтически активного фрагмента статинов из доступной яблочной кислоты
Атеросклероз – известное и широко распространенное хроническое заболевание кровеносной системы, которое характеризуется патологическими изменениями в стенках кровеносных сосудов. Как следствие, в ткани и органы поступает недостаточное количество кислорода, что порождает условия для развития стенокардии, инфаркта миокарда и инсульта.
Причины развития атеросклероза до сих пор являются предметом дискуссий и интенсивных исследований. Специалисты обычно оперируют термином «фактор риска». Удельный вес всех этих факторов, среди которых высокое содержание холестерина в крови, гипертония, курение, ожирение, гиподинамия, наследственность и т. д., разный. При этом важно понимать, что само понятие «фактор риска» является статистическим и обнаруженные связи не всегда имеют причинно-следственный характер.
Действительно, хотя значимым фактором риска является избыточный вес, далеко не каждый человек с таким весом может заболеть атеросклерозом, равно как и недостаточная масса тела не может служить гарантией хорошего здоровья.
В этой связи нельзя не упомянуть и так называемый «французский парадокс» – относительно низкий уровень сердечно-сосудистых и онкологических заболеваний у жителей Франции по сравнению с населением соседних несредиземноморских стран, который наблюдается на фоне высококалорийного питания с обилием жиров, широкого распространения табакокурения и сравнительно малоподвижного образа жизни. На возможных причинах этого феномена остановимся ниже, сейчас же стоит отметить, что с точки зрения статистики методичное исключение факторов риска у больных атеросклерозом все же приводит к снижению смертности от этого заболевания. Этот вывод подтверждается и результатами кампаний за здоровый образ жизни, который подразумевает уменьшение табакокурения, борьбу с избыточным весом, здоровое питание и высокую физическую активность, которые успешно проводятся в экономичеcки развитых странах.
На снижении относительного уровня смертности от атеросклероза и его осложнений в этих странах сказывается, безусловно, и множество других факторов, таких как своевременная медицинская помощь в экстренных ситуациях, а также предупреждение осложнений с помощью хирургических методов. Но все же наиболее важным фактором является, по-видимому, эффективное медикаментозное предупреждение развития атеросклероза. Поэтому исследования, направленные на поиск новых классов противоатеросклеротических препаратов, ведутся непрерывно во всем мире.
Его ахиллесова пята
Как в любой затяжной битве, разработчики новых лекарственных средств выбирают наиболее уязвимые места противника. Есть такие «мишени» и у атеросклероза.
Поскольку одной из важнейших причин появления атеросклероза считается нарушение обмена холестерина (в частности, его повышенный уровень в крови), прежде всего представляется логичным блокировать этапы холестеринового синтеза. Дело в том, что более 70 % холестерина, содержащегося в человеческом организме, образуется непосредственно в нем самом, а не поступает из пищевых продуктов.
Дело в том, что более 70 % холестерина, содержащегося в человеческом организме, образуется непосредственно в нем самом, а не поступает из пищевых продуктов.
ХОЛЕСТЕРИН – СВОЙ И ЧУЖОЙ
Атеросклероз – хроническое заболевание, при котором в стенках кровеносных сосудов формируются так называемые атеросклеротические бляшки, сужающие их просвет. В результате к тканям и органам поступает недостаточно кислорода – возникает ишемия.
На ранних этапах заболевания бляшки содержат большое количество липидов. Стенка капсулы такой бляшки легко может быть повреждена, что весьма опасно, так как выход липидов в кровь провоцирует образование тромба. На более поздних стадиях заболевания бляшка содержит меньшее количество липидов и большее – соединительной ткани, а еще позднее происходит отложение солей кальция и обызвествление стенки сосуда. Поздние стадии атеросклероза характеризуются серьезным сужением просвета сосудов и обеспечивают условия для стабильной стенокардии напряжения.
Один из виновников образования атеросклеротических бляшек – холестерин, природный липофильный (жирорастворимый) спирт, который является важным компонентом клеточных мембран.
Вопреки широко распространенному мнению, более 70 % холестерина, содержащегося в нашем организме, поступает не из съеденной пищи, а имеет эндогенное происхождение, т. е. образуется непосредственно в самом организме. Холестерин является также предшественником желчных кислот, стероидных гормонов и липопротеидных комплексов, необходимых для нормального функционирования организма
Имеется довольно большой класс подобных гиполипидемических препаратов, в основном это статины, которые на сегодня являются лидерами противоатеросклеротического рынка. Статины ингибируют в организме одну из первых и, что важно, необратимую стадию синтеза холестерина, блокируя фермент ГМГ-КоА-редуктазу. Начало классу этих фармацевтических препаратов дали соединения компактин и мевинолин, обнаруженные около 40 лет назад в плесневых грибах рода Penicillium. Грибы используют эти вещества в борьбе с бактериями в качестве эффективных антибиотиков, что и неудивительно: фермент связывается со статинами в десять тысяч раз прочнее, чем с самой молекулой-субстратом!
Грибы используют эти вещества в борьбе с бактериями в качестве эффективных антибиотиков, что и неудивительно: фермент связывается со статинами в десять тысяч раз прочнее, чем с самой молекулой-субстратом!
В комплексе со статинами часто используют также препарат эзетимиб, который предотвращает всасывание холестерина в кишечнике.
Другим, более изощренным и тонким подходом к решению проблемы развития атеросклероза является регулирование обмена веществ в организме путем влияния на работу генов, контролирующих такие важнейшие физиологические показатели, как энергетический метаболизм, сосудистый гомеостаз, воспалительные процессы, метаболизм и транспортные системы липидов и липопротеидов. Если статиновый метод лечения атеросклероза можно образно сравнить со штурмом укрепленной крепости, то воздействие на генном уровне – это создание препятствий ее строителям.
В стадии разработки находится еще одна группа препаратов, работающих как ингибиторы белка, который переносит эфиры холестерина и регулирует его баланс между разными классами липопротеинов. Эти вещества, особенно в комбинации с другими средствами, способны понижать уровень холестерина, препятствуя его возвращению в «круговорот» веществ в организме.
Назначить пожизненно
Точно установлено, что медикаментозное снижение в крови уровня жиров, особенно холестерина, приводит к снижению риска развития атеросклероза и его осложнений. Однако использование таких противоферментных препаратов, как статины, – палка о двух концах. Благодаря системе обратных связей организм, реагируя на падение уровня холестерина, начинает усиленно нарабатывать «выключаемые» ферменты. В результате интенсивность синтеза холестерина может восстановиться.
Решение этой проблемы, казалось бы, очевидно – нужно увеличить терапевтическую дозу лекарства. Однако статины, как и многие другие препараты, обладают определенной токсичностью и могут оказывать нежелательные побочные эффекты. Например, некоторые из них в высоких дозах могут вызывать поражение мышечной ткани (рабдомиолиз).
Например, некоторые из них в высоких дозах могут вызывать поражение мышечной ткани (рабдомиолиз).
Кроме того, существует такое понятие, как эффект отмены. При прекращении приема статинов усиленная наработка ферментов может привести к резкому скачку концентрации холестерина в крови, поэтому их принимают в прямом смысле пожизненно.
С другой стороны, статины обладают не только нежелательными побочными, но и одновременно дополнительными лечебными эффектами. Так, выраженное противовоспалительное действие статинов в свое время вызвало даже появление статей с броским заголовком: «Статины – новый аспирин?». Кроме того, были обнаружены также противоопухолевый и антиостеопорозный эффекты статинов.
Победа – за природой
Исследователи продолжают поиски более эффективных и безопасных природных веществ со статиноподобной структурой, а также пытаются синтезировать новые соединения с нужными свойствами.
Однако на этом пути они встречаются с немалыми трудностями. Во-первых, оказалось, что синтез лактонового фрагмента, который определяет терапевтическое действие соединения, – технически непростая задача. Во-вторых, хотя было получено довольно много чисто синтетических препаратов для лечения гиперлипидемии (флувастатин, аторвастатин, церивастатин), они не превосходят по терапевтическим свойствам широко известные компактин и мевинолин, которые сегодня получают биотехнологическим способом.
Поэтому до сих пор мевинолин под названием ловастатин продолжает применяться в медицинской практике, а лидером фармакологического рынка является препарат инеджи – комбинация ближайшего аналога мевинолина симвастатина с эзетимибом. Рекорды же по эффективности побило природное соединение FR901512, недавно выделенное из тех же плесневых грибов (Inoue and Nakada, 2007).
Тем не менее процесс поиска и создания новых синтетических статиновых препаратов не останавливается. Сейчас разрабатываются препараты, принципиально отличающиеся от природных: в липофильной части молекул этих соединений содержатся полярные фрагменты, которые при взаимодействии с ферментом меняют его конформацию (форму). Этот новый тип взаимодействия в конечном итоге позволяет достигать большего эффекта ингибирования синтеза холестерина.
Сейчас разрабатываются препараты, принципиально отличающиеся от природных: в липофильной части молекул этих соединений содержатся полярные фрагменты, которые при взаимодействии с ферментом меняют его конформацию (форму). Этот новый тип взаимодействия в конечном итоге позволяет достигать большего эффекта ингибирования синтеза холестерина.
Повлиять на конформацию фермента и обеспечить лучшее закрепление статина в его активном центре можно с помощью и других методов. Подобный эффект достигается, например, при использовании комплекса симвастатина и аторвастатина с глицирризиновой кислотой, которую получают из корней солодки голой (Толстиков и др., 2006; 2008).
По двойной мишени
К вышеупомянутому новому классу антисклеротических препаратов, действующих на генном уровне, относятся вещества, активирующие так называемые PPAR – особые клеточные белки-рецепторы. PPAR относятся к транскрипционным факторам: они «включают» работу определенных генов, стимулируя наработку соответствующих белков, участвующих в регуляции важнейших физиологических процессов, в том числе метаболизма липопротеинов.
Существуют три формы этих белков-рецепторов – α, β и γ, причем каждая из них активируется своим специфическим соединением (агонистом) – например, жирными кислотами либо простагландинами, участвующими в противовоспалительном ответе. Каждая форма регулирует различные, хотя и частично пересекающиеся каскады биохимических процессов. Например, «активаторы» PPARα влияют на обмен липопротеинов и применяются для лечения нарушения обмена липидов; активаторы PPARγ, участвующие в обмене глюкозы, – для лечения диабета 2 типа.
Давно известно, что больные атеросклерозом часто заболевают диабетом и имеют проблемы с обменом липидов и углеводов в целом. Поэтому в последнее время огромный интерес вызывает создание препаратов на основе двойных (α и γ)(глитазаров – тезаглитазара, рагаглитазара) и даже тройных агонистов этих рецепторов.
Исследования показали, что даже небольшие изменения в химической структуре соединений-агонистов PPAR драматически влияют на их способность селективно связываться с мишенью, а значит, и фармакологические свойства таких веществ могут сильнейшим образом различаться – ведь таким способом мы вмешиваемся в очень тонкие процессы регуляции метаболизма.
В целом этот класс антиатеросклеротических веществ выглядит очень перспективным, поскольку они работают в существенно меньших дозах, чем статины: ведь для посыла сигнала через относительно малочисленные рецепторы требуется существенно меньше молекул, чем для ингибирования большого числа молекул фермента. Отсюда и значительно меньшая токсическая нагрузка на организм: в десятки-сотни раз меньше, чем для статинов, и в тысячи раз – чем для обычных гипогликемических препаратов.
Древовидный синтез
Сегодня перед фармацевтической индустрией стоят задачи не только разработки новых лекарств, но и создания дешевых и эффективных технологий синтеза уже хорошо зарекомендовавших себя препаратов, таких как статины или глитазары.
Классической химической технологией является последовательный синтез соединения. Например, статины синтезируют, начиная с липофильной части, последовательно наращивая молекулы исходного субстрата. Затем на липофильном остове формируется лактоновый фрагмент и лишь на последних этапах синтеза – конечное соединение нужной пространственной конфигурации.
Такая длинная цепочка синтеза весьма затратна, к тому же на каждой стадии высока цена ошибки. Поэтому сегодня предпочтение следует отдать конвергентной (древовидной) схеме синтеза, когда конечную молекулу собирают из отдельно синтезированных фрагментов. Это позволяет существенно уменьшить число стадий синтеза и, соответственно, увеличить выход конечной продукции, учитывая, что на каждой стадии синтеза выход промежуточного продукта всегда меньше 100 %, а зависимость выхода конечного продукта от числа стадий носит степенной характер.
Очевидно, в случае статинов, синтез которых зачастую насчитывает более двадцати стадий, даже частичное введение конвергентного подхода может кратно увеличить выход. Наступление на эту проблему идет широким фронтом, при этом используются как чисто химические подходы, так и биотехнологические, а также всевозможные их комбинации.
В рамках такого подхода в Институте органической химии им. Н. Н. Ворожцова СО РАН уже разработан способ синтеза ключевого лактонового фрагмента статинов из доступной яблочной кислоты (Трошков, Фоменко, Салахутдинов, 2008). Особо отметим, что при этом удалось полностью решить задачу получения вещества определенной пространственной структуры – это необходимо, чтобы конечной продукт имел необходимую терапевтическую активность.
Сегодня все новые и новые соединения проверяются на способность к снижению уровня холестерина, причем не только синтетические, но и всевозможные природные.
В результате были открыты гиполипидемические свойства берберина (алкалоида, добываемого преимущественно из корней барбариса), а также многочисленных природных фенольных соединений, включая флавоноиды, которые являются незаменимыми компонентами пищи человека и других млекопитающих.
Многие источники этих биологически активных соединений входят в наш обычный пищевой рацион, например, зеленый чай, многие ягоды и грибы, вино и т. д. Именно потреблению красного вина, в котором содержится фенольное стильбеновое соединение ресвератрол, приписывался вышеупомянутый «французский парадокс». Однако детальные исследования на лабораторных животных показали, что терапевтически значимая ежедневная доза ресвератрола содержится не в стакане или даже литре, а в десятках литров вина (Baur and Sinclair, 2006)!
Поэтому поиски причин такого многообещающего феномена продолжаются, равно как и поиски новых гиполипидемических препаратов, без которых трудно представить себе жизнь современного человечества.
Литература
Лифшиц Г. И. Тихий убийца атеросклероз. От теории – к практике // НАУКА из первых рук, 2007. № 3 (15). С. 52—61.
Толстиков Г. А. и др. Патенты РФ № 2308947 от 26.02.2006 «Лекарственное средство с гиполипидемическим эффектом „Симваглизин“» и № 2396079 от 03.12.2008 «Лекарственное средство с гиполипидемическим эффектом „Аторваглизин“».
Трошков В. В., Фоменко В. В., Салахутдинов Н. Ф. Патент РФ № 2384577 от 12.05.2008 «Способ получения 2-(оксиран-2-ил)-этанола» .
Gregory S. et al. PPARs and Lipid Ligands in Inflammation and Metabolism // Chem. Rev. 2011. 111. P. 6321—6340.
: 8 Ноя 2012 , Недаром помнит вся Россия , том 46,
№4
Атеросклероз: лекарства, используемые при лечении
Атеросклероз — хроническое заболевание артерий эластического и мышечно-эластического типа, возникающее вследствие нарушения липидного обмена и сопровождающееся отложением холестерина и некоторых фракций липопротеидов в интиме сосудов.
Общие сведения
Неправильное, нерациональное питание, малоподвижность, стрессовые ситуации — все это приводит к возникновению атеросклероза. Атеросклероз — это заболевание, которое поражает магистральные (крупные) сосуды. При этом происходит отложение холестерина в стенке сосуда, в результате чего возникает атеросклеротическая бляшка, суживающая просвет сосуда. Это приводит к тому, что значительно падает кровоток по пораженному сосуду, причем степень снижения кровотока, как правило, пропорциональна степени стеноза (сужения) сосуда.
Атеросклероз приобретает хроническое течение и является самой частой причиной потери трудоспособности и преждевременной смерти. Чаще поражает людей в 40-45 лет и в 3-4 раза чаще мужчин.
Чаще поражает людей в 40-45 лет и в 3-4 раза чаще мужчин.
Причины атеросклероза
Несомненно, большое значение имеют так называемые факторы риска развития атеросклероза. Некоторые из них неустранимы: возраст, принадлежность к мужскому полу, отягощенная по атеросклерозу семейная наследственность. Другие вполне устранимы: артериальная гипертензия, алиментарное ожирение, курение . Третьи устранимы частично (потенциально): сахарный диабет, различные виды нарушений обмена веществ. К факторам риска относят также недостаточную физическую активность, избыточные эмоциональные перенапряжения и личностные особенности человека, нерациональное питание (склонность к перееданию, предпочтение пище, богатой животными жирами и др.).
Симптомы
Эти изменения чаще локализируются в аорте, сердечных, мозговых, почечных артериях и артериях конечностей, чаще нижних. Картина болезни и жалобы больного зависят от поражения тех или иных артерий.
Так атеросклероз коронарных артерий (сосудов сердца) очень часто проявляется в форме стенокардии, инфаркта. В основе патологического процесса, т.е. заболевания, лежит нарушение соответствия между потребностью сердца в кровоснабжении и его реальным осуществлением. Это несоответствие может возникнуть при сохраняющемся на определенном уровне кровоснабжении миокарда, но резко возросшей потребности в нем (стенокардия напряжения или покоя) или при сниженном кровоснабжении (инфаркт миокарда).
Нередко тяжелые формы атеросклероза аорты могут протекать бессимптомно. У больного могут возникать давящие или жгучие боли за грудиной, отдающие в обе руки, шею, спину, верхнюю часть живота. Но в отличие от стенокардии эти боли держатся длительно, то усиливаясь, то ослабевая.
При поражении почечных сосудов наступает тяжелая артериальная гипертония. Атеросклероз артерий головного мозга проявляется снижением работоспособности (особенно умственной), снижением памяти, активного внимания, быстрой утомляемостью. Со временем появляется головокружение, бессонница, больные становятся суетливыми, навязчивыми, придирчивыми. У них снижается интеллект. Осложнением атеросклероза мозговых артерий является нарушение мозгового кровообращения кровоизлияния (инсульт), тромбозы.
У них снижается интеллект. Осложнением атеросклероза мозговых артерий является нарушение мозгового кровообращения кровоизлияния (инсульт), тромбозы.
Атеросклероз артерий конечностей, чаще нижних, проявляется в икроножных мышцах при ходьбе («перемежающаяся хромота»). Появляются зябкость и похолодание конечностей.
Таким образом, атеросклероз приводит к развитию большинства современных «болезней цивилизации».
Что можете сделать вы при атеросклерозе
Атеросклероз медленно текущее заболевание. Очень сложно поймать начало заболевания, а осложнения заболевания угрожают жизни больного. Поэтому нужно наблюдаться у Вашего доктора, периодически контролируя уровень липидов и холестерина в крови, особенно если у Вас имеются предрасполагающие факторы риска.
Что может сделать врач
Врачебная тактика лечения направлена на устранение нервных и психических нагрузок и нормализацию обменных процессов.
Традиционно назначают медикаментозные препараты, снижающие уровень липидов в крови, улучшающих трофику и оксигенацию тканей, улучшающих реологию крови, повышающих эластичность сосудистой стенки. Подбирают рациональное питание, коррегируют режим труда и отдыха, включают систематические занятия лечебной гимнастикой.
При наличии атеросклеротических бляшек, угрожающих нормальному кровоснабжению органов применяются хирургические методы лечения реконструктивные сосудистые операции.
Профилактические меры при атеросклерозе
Профилактика атеросклероза, как практически любого заболевания, основана на исключении факторов его развития. Таким образом, чтобы не допустить появление атеросклероза, следует избегать жирных продуктов, вредных привычек (злоупотребления алкоголем, курения), дефицита двигательной активности и, как следствия, избыточной массы тела, систематических перепадов давления (особенно повышения давления), стрессовых ситуаций.
Внимание! Карта симптомов предназначена исключительно для образовательных целей. Не занимайтесь самолечением; по всем вопросам, касающимся определения заболевания и способов его лечения, обращайтесь к врачу. Наш сайт не несет ответственности за последствия, вызванные использованием размещенной на портале информации.
Не занимайтесь самолечением; по всем вопросам, касающимся определения заболевания и способов его лечения, обращайтесь к врачу. Наш сайт не несет ответственности за последствия, вызванные использованием размещенной на портале информации.
Механизмы берберина для лечения атеросклероза на основе сетевой фармакологии
Атеросклероз — распространенное метаболическое заболевание, характеризующееся нарушением липидного обмена. Процессы атеросклероза включают эндотелиальную дисфункцию, образование нового эндотелиального слоя, липидный осадок, образование пенистых клеток, образование бляшек и взрыв бляшек. Из-за побочных эффектов препаратов первого ряда необходимо срочно открывать новые препараты для лечения атеросклероза. Берберин — один из самых многообещающих натуральных продуктов, полученных из традиционной китайской медицины.Однако панорамный механизм действия берберина против атеросклероза до сих пор не изучен. В этом исследовании мы использовали сетевую фармакологию для изучения взаимодействия между берберином и атеросклерозом. Мы определили потенциальные цели, связанные с берберином и атеросклерозом, из нескольких баз данных. В общей сложности была выявлена 31 и 331 предполагаемая мишень для лечения берберина и атеросклероза соответственно. Затем мы построили мишени для берберина и атеросклероза с данными PPI. Целевая сеть Berberine с данными PPI имела 3204 узла и 79437 ребер.Сеть мишеней атеросклероза с данными PPI имела 5451 узел и 130891 край. Кроме того, мы объединили две сети PPI и получили базовую сеть PPI из объединенной сети PPI. В базовой сети PPI было 132 узла и 3339 ребер. Наконец, мы выполнили функциональный анализ обогащения, включая анализ путей GO и KEGG в базе данных Дэвида. Анализ ГО показал, что биологические процессы коррелировали с переходом G1 / S цикла митотических клеток. Анализ пути KEGG показал, что пути, напрямую связанные с берберином против атеросклероза, представляют собой клеточный цикл, убиквитин-опосредованный протеолиз, сигнальный путь MAPK и сигнальный путь PI3K-Akt. После объединения результатов в контексте с доступными методами лечения атеросклероза мы пришли к выводу, что берберин ингибирует воспаление и пролиферацию клеток при лечении атеросклероза. Наше исследование предоставило вескую теоретическую основу для будущих исследований.
После объединения результатов в контексте с доступными методами лечения атеросклероза мы пришли к выводу, что берберин ингибирует воспаление и пролиферацию клеток при лечении атеросклероза. Наше исследование предоставило вескую теоретическую основу для будущих исследований.
1. Введение
Атеросклероз — распространенное хроническое заболевание, при котором в артериях накапливаются бляшки [1]. Зубной налет состоит из холестерина, кальция, жира и других веществ, находящихся в кровотоке [2]. Высокое кровяное давление, курение, аномальный уровень холестерина и ожирение считаются факторами риска атеросклероза.Почти все люди могут страдать атеросклерозом в возрасте старше 65 лет. Предыдущие исследования показали, что несколько сердечно-сосудистых и цереброваскулярных заболеваний, таких как ишемическая болезнь сердца, инфаркт головного мозга, кровоизлияние в мозг, были связаны с атеросклерозом [3, 4]. Итак, атеросклероз — один из важнейших факторов, ведущих к инвалидности и смерти. Этот беспорядок приводит к тяжелому экономическому и социальному бремени общества в мире [5]. Образование зубного налета — это медленный процесс в течение нескольких лет со сложным клеточным и молекулярным механизмом [6].На ранней стадии циркулирующие в крови моноциты прикрепляются к эндотелию и мигрируют в субэндотелиальное пространство [7]. Макрофаги будут активированы, и частицы окисленных липопротеинов откладываются под эндотелиальными клетками. Позже возникает каскад воспалительной реакции в результате повреждения эндотелия. Повышенная продукция провоспалительных медиаторов, включая интерфероны (IFN), интерлейкины (IL), трансформирующие факторы роста (TGF) и факторы некроза опухоли (TNF), участвуют в инициации и развитии атеросклероза [8].Доступные методы лечения атеросклероза включают статины, хирургическое вмешательство и другие лекарства. Однако у этих методов есть много побочных эффектов [9]. Поэтому очень важно открывать новые лекарства от атеросклероза.
Берберин — биологически активный ингредиент, обнаруженный во многих растениях, таких как китайская золотая нить, желтокорень, европейский барбарис, древесная куркума и феллодендрон [10]. На рисунке 1 показана химическая структура берберина.
На рисунке 1 показана химическая структура берберина.
Традиционная китайская медицина учитывает, что берберин обладает прекрасными эффектами, включая устранение сырости, удаление тепла, детоксикацию и очистку от огня.Кроме того, берберин является основным ингредиентом многих известных отваров китайской медицины. Знаменитые отвары Gegen-Huangqin-Huanglian отвар ( Coptidis rhizome , Scutellariae radix , Puerariae lobatae radix , Glycyrrhizae radix ) и отвар Huanglian-Jie-Du , корневище корневища , корневище 13 Gardeniae fructus , Phellodendri cortex ) содержат берберин [11, 12]. Предыдущие исследования показали, что берберин полезен при лечении многих заболеваний.Lin et al. обнаружили, что берберин эффективен в подавлении пролиферации клеток и стимулировании апоптоза клеток рака груди [13]. Jin et al. показали, что берберин ингибирует остеосаркому, подавляя сигнальную ось caspase-1 / IL-1 β [14]. Ma et al. резюмировал, что берберин облегчает сахарный диабет, борясь с воспалением и окислительным стрессом [15]. За исключением рака и метаболических заболеваний, берберин также оказывает терапевтическое действие при атеросклерозе [16]. Берберин оказывает защитное действие против атеросклероза, регулируя различные проатерогенные клеточные и молекулярные механизмы.Эндотелиальные функции, миграция гладкомышечных клеток сосудов, образование пены из макрофагов и активация тромбоцитов могут быть вовлечены в защитные эффекты берберина против атеросклероза. Однако молекулярные мишени и механизмы действия берберина при атеросклерозе до конца не изучены.
Сетевая фармакология — развивающаяся область, основанная на системной фармакологии для исследования взаимодействия между лекарствами и заболеваниями [17]. В сетевой фармакологии сеть лекарств-мишеней важна для понимания механизма действия лекарств.Мишени болезни могут быть применены в области дизайна лекарств, открытия лекарств и обнаружения биомаркеров [18]. Сложные заболевания, такие как сердечно-сосудистые заболевания и рак, не связаны с мутацией одной молекулы или дисфункцией сигнального пути. Обычно они вызваны целой регуляцией сетевой дисфункции. Сетевая фармакология может привести к прогрессу методологии и теории в разработке лекарств.
Сложные заболевания, такие как сердечно-сосудистые заболевания и рак, не связаны с мутацией одной молекулы или дисфункцией сигнального пути. Обычно они вызваны целой регуляцией сетевой дисфункции. Сетевая фармакология может привести к прогрессу методологии и теории в разработке лекарств.
В настоящем исследовании мы изучили механизм лечения атеросклероза берберином с помощью сетевой фармакологии.Мы определили потенциальные цели, связанные с берберином и атеросклерозом. Затем мы построили сети белок-белкового взаимодействия (PPI) мишеней берберина и мишеней атеросклероза. Позже мы объединили две сети PPI и проанализировали топологические особенности сети, чтобы получить базовую сеть PPI. Наконец, мы выполнили анализ функционального обогащения, включая онтологию генов (GO) и анализ сигнальных путей Киотской энциклопедии генов и геномов (KEGG), чтобы охарактеризовать биологические процессы и пути.Результаты этого исследования предоставили всесторонний и содержательный анализ применения берберина в лечении атеросклероза. Это исследование также предоставило новый механизм действия берберина против атеросклероза.
2. Методы
2.1. Скрининг потенциальных целей для берберина
Были проведены две базы данных для определения потенциальных целей, связанных с берберином. Эти две базы данных включали базу данных по фармакологии систем традиционной китайской медицины (TCMSP) и базу данных STITCH. База данных TCMSP (http: // lsp.nwu.edu.cn/tcmsp.php) — уникальная системная фармакологическая база данных традиционных китайских лекарств, описывающая взаимосвязь между лекарствами, мишенями и заболеваниями. База данных STITCH (http://stitch.embl.de/) — полезный инструмент для обнаружения сетей взаимодействия химических веществ и белков.
2.2. Скрининг потенциальных целей для AS
Четыре базы данных были применены для определения потенциальных целей, связанных с атеросклерозом. Четыре базы данных включали базу данных терапевтических целей (TTD), базу данных DrugBank, базу данных генетических ассоциаций (GAD) и онлайн-менделевское наследование у человека (OMIM). TTD (https://db.idrblab.org/ttd/) — это полезная база данных, содержащая данные об исследовании терапевтических белков и нуклеиновых кислот-мишеней, нацеленных на заболевание. База данных DrugBank (https://www.drugbank.ca/) — это мощная и всеобъемлющая база данных биоинформатики, содержащая информацию о лекарствах и заболеваниях. База данных GAD (https://geneticassociationdb.nih.gov/) — это полезная база данных генетических и белковых ассоциаций данных сложных расстройств и заболеваний. OMIM (https://www.omim.org/) — это авторитетная, своевременная и полная база данных о генах человека и генетических заболеваниях.
TTD (https://db.idrblab.org/ttd/) — это полезная база данных, содержащая данные об исследовании терапевтических белков и нуклеиновых кислот-мишеней, нацеленных на заболевание. База данных DrugBank (https://www.drugbank.ca/) — это мощная и всеобъемлющая база данных биоинформатики, содержащая информацию о лекарствах и заболеваниях. База данных GAD (https://geneticassociationdb.nih.gov/) — это полезная база данных генетических и белковых ассоциаций данных сложных расстройств и заболеваний. OMIM (https://www.omim.org/) — это авторитетная, своевременная и полная база данных о генах человека и генетических заболеваниях.
2.3. Построение сетей PPI
В этом исследовании мы получили данные PPI из плагина Cytoscape BisoGenet. Шесть баз данных PPI в плагине Cytoscape BisoGenet включают базу данных взаимодействующих белков (DIP), биологический общий репозиторий для наборов данных взаимодействия (BioGRID), справочную базу данных белков человека (HPRD), базу данных молекулярных взаимодействий IntAct (IntAct), Molecular INTeraction База данных (MINT) и База данных сети биомолекулярного взаимодействия (BIND).Сеть PPI, прогнозирующая мишени для берберина, была визуализирована и построена с помощью программного обеспечения Cytoscape (версия 3.7.1, Бостон, Массачусетс, США). Кроме того, сеть PPI, прогнозирующая цели атеросклероза, также была визуализирована и построена с помощью программного обеспечения Cytoscape. После получения двух сетей PPI мы объединили эти две сети для получения основной сети PPI. Позже были проанализированы топологические особенности базовой сети PPI.
2.4. Анализ топологических характеристик сети
Шесть параметров использовались для анализа топологических свойств каждого узла в сети взаимодействия.Шесть параметров включали центральность степени (DC), центральность промежуточности (BC), центральность близости (CC), центральность по собственному вектору (EC), локальную среднюю связность (LAC) и центральность сети (NC). Для проведения анализа был использован плагин cytoNCA в программном обеспечении Cytoscape. Вычислительные уравнения и определения этих параметров указывают на топологическую важность узлов в базовой сети PPI.
Вычислительные уравнения и определения этих параметров указывают на топологическую важность узлов в базовой сети PPI.
2.5. Функциональный анализ обогащения
База данных для аннотаций, визуализации и комплексного обнаружения (Дэвид) использовалась для выполнения анализов путей GO и KEGG в этом исследовании.Анализ GO является полезным инструментом биоинформатики для характеристики молекулярной функции (MF), клеточных компонентов (CC) и биологического процесса (BP) генов. Анализ пути KEGG — это набор баз данных, описывающих биологические пути, геномы, лекарства и заболевания. Платформа OmicShare (https://www.omicshare.com/) использовалась для визуализации пузырьковой диаграммы.
3. Результаты
3.1. Возможные цели берберина
Всего 31 предполагаемая цель берберина была идентифицирована с помощью баз данных TCMSP и STITCH.Предполагаемые цели включали ADRB2, CALM1, HSP90AA1, KCNh3 и так далее. Подробная информация о потенциальных мишенях для берберина представлена на Рисунке 2 и в дополнительной таблице 1.
3.2. Возможные цели атеросклероза
Всего с помощью баз данных TTD, DrugBank, GAD, OMIM была идентифицирована 331 предполагаемая цель атеросклероза. Предполагаемые цели включали ABCA1, ANKRD1, CNR2, ICAM1 и так далее. Подробная информация о потенциальных мишенях атеросклероза представлена на Рисунке 3 и в дополнительной таблице 2.
3.3. PPI Network Construction
PPI сети использовались для понимания функций различных мишеней при берберине и атеросклерозе. В этом исследовании мы построили целевую сеть берберина с данными PPI (рисунок 4). Результаты показали, что сеть PPI, нацеленная на берберин, имела 3204 узла и 79437 ребер.
Кроме того, мы построили сеть мишеней атеросклероза с данными PPI (рис. 5). Результаты показали, что сеть PPI, нацеленная на атеросклероз, имела 5451 узел и 130891 край.
Кроме того, мы использовали функцию слияния сети, чтобы построить новую сеть PPI, чтобы раскрыть фармакологический механизм действия берберина против атеросклероза. Объединенная сеть PPI была построена в программе Cytoscape. Результаты показали, что объединенная сеть PPI имеет 2393 узла и 67362 ребра (рисунок 6).
Объединенная сеть PPI была построена в программе Cytoscape. Результаты показали, что объединенная сеть PPI имеет 2393 узла и 67362 ребра (рисунок 6).
3.4. Анализ топологических характеристик сети
Чтобы получить базовую сеть PPI из объединенной сети PPI, мы провели шесть параметров для анализа топологических свойств объединенной сети PPI.Шесть параметров содержали DC, BC, CC, EC, LAC и NC. Параметры были перечислены следующим образом: DC> 71, BC> 0,00074, CC> 0,4829, EC> 0,0301, NC> 30,53, LAC> 20,34. На рисунке 7 показана основная сеть PPI.
В базовой сети PPI было 132 узла и 3339 ребер. Узлы в основной сети PPI включали нейротрофический рецептор тирозинкиназы 1 (NTRK1), рецептор эстрогена 1 (ESR1), опухолевый белок p53 (TP53), cullin 3 (CUL3), белок теплового шока 90 (HSP90), белок-предшественник амилоида бета ( APP), компонент 2 поддерживающего комплекса минихромосом (MCM2), фибронектин 1 (FN1), убиквитин C (UBC) и т. Д.
3.5. Функциональный анализ обогащения
Дэвид был использован для выполнения анализа путей GO и KEGG в этом исследовании. GO анализ потенциальных мишеней для берберина против атеросклероза был проведен, чтобы обнаружить биологический процесс в базе данных Дэвида. Результаты показали, что биологические процессы коррелируют с регуляцией транскрипции с промотора РНК-полимеразы II, негативной регуляцией апоптотического процесса, регуляцией ДНК-темплатной транскрипции, переходом G1 / S митотического клеточного цикла, ответом на повреждение ДНК, убиквитинизацией белка. , связанная с транскрипцией эксцизионная репарация нуклеотидов, эксцизионная репарация нуклеотидов (рис. 8).Гены-мишени каждого биологического процесса были перечислены в дополнительной таблице 3.
Кроме того, мы провели анализ пути KEGG для исследования биологических путей берберина против атеросклероза. 10 основных сигнальных путей были перечислены следующим образом: клеточный цикл, убиквитин-опосредованный протеолиз, сигнальный путь MAPK, сигнальный путь PI3K-Akt, сигнальный путь эстрогена, соединение адгезивов, сплайсосома, сигнальный путь HIF-1, сигнальный путь NOD-подобных рецепторов и Сигнальный путь бегемота (рис. 9).Гены-мишени каждого пути перечислены в дополнительной таблице 4.
9).Гены-мишени каждого пути перечислены в дополнительной таблице 4.
4. Обсуждение
Атеросклероз — распространенное метаболическое заболевание, характеризующееся нарушением липидного обмена. Это многофакторное патологическое заболевание, изменяющее морфологию и функцию стенок артерий [19, 20]. Статины — это гиполипидемические препараты первой линии для лечения атеросклероза [21]. Статины также вызывают множество побочных эффектов у некоторых групп населения [22]. За исключением статинов, другие препараты, регулирующие липиды, также имеют некоторые побочные эффекты.Итак, важно открывать новые методы лечения атеросклероза.
Как представитель традиционной медицины, берберин широко используется в азиатских странах, таких как Китай, Корея и Япония, благодаря клиническим характеристикам и характеристикам безопасности [23]. Предыдущие исследования продемонстрировали терапевтический потенциал берберина в подавлении атеросклероза in vivo . Введение берберина значительно уменьшило площадь атеросклеротической бляшки у мышей ApoE — / — [24]. У мышей ApoE — / — , получавших гомоцистеин-тиолактон (HTL), берберин способствовал стабильности бляшек в артерии, подавляя окислительный стресс [25].Однако механизм действия берберина против атеросклероза до сих пор не изучен. Сетевая фармакология — это новая область исследования взаимодействия между лекарствами и болезнями. Он может дать полную картину лекарственного механизма борьбы с болезнью. В этом исследовании мы построили целевые сети берберина и атеросклероза с данными PPI. Затем мы объединили две сети PPI и проанализировали топологические свойства объединенной сети PPI, чтобы получить базовую сеть PPI. Кроме того, мы провели анализ функционального обогащения, включая анализ путей GO и KEGG, чтобы прояснить множественные механизмы действия берберина против атеросклероза.
Современные методы лечения атеросклероза направлены на контроль факторов риска и поддержание перфузии в пораженных артериях. Доступные лекарства от атеросклероза включают лекарства от холестерина, антиагреганты и другие лекарства [26]. Статины для лечения холестерина и аспирин, являющийся антиагрегантом, широко используются в качестве общепринятых средств лечения атеросклероза. Доступные методы лечения атеросклероза обладают плейотропными аспектами механизмов борьбы с атеросклерозом.Согласно нашим результатам в этом исследовании, берберин может обладать аналогичным механизмом действия с предыдущими препаратами против атеросклероза.
Доступные лекарства от атеросклероза включают лекарства от холестерина, антиагреганты и другие лекарства [26]. Статины для лечения холестерина и аспирин, являющийся антиагрегантом, широко используются в качестве общепринятых средств лечения атеросклероза. Доступные методы лечения атеросклероза обладают плейотропными аспектами механизмов борьбы с атеросклерозом.Согласно нашим результатам в этом исследовании, берберин может обладать аналогичным механизмом действия с предыдущими препаратами против атеросклероза.
Во-первых, доступные лечебные статины и аспирин уменьшают воспалительный статус атеросклероза. Атеросклероз — хроническое воспалительное заболевание, и воспаление играет решающую роль в патогенезе атеросклероза [27]. При воспалительной реакции кровеносных сосудов воспалительные клетки проникают в эндотелий сосудов и высвобождают медиаторы воспаления, обостряя атеросклероз [28].Несколько воспалительных сигнальных путей, включая сигнальный путь MAPK, сигнальный путь PI3K-Akt и опосредованный убиквитином протеолиз, вовлечены в воспалительный ответ на различные внутриклеточные и внеклеточные стимулы [29, 30]. Доступные лечебные статины и аспирин благотворно влияют на атерогенез и предотвращают прогрессирование атеросклероза [31]. Было обнаружено, что статины регулируют внутриклеточные воспалительные пути. Экспрессия воспалительных цитокинов, включая TNF- α , IL-6 и IFN- γ , продуцируемых SMC и макрофагами, может подавляться статинами [32].Помимо воспалительных цитокинов, статины ингибируют экспрессию хемокинов, таких как хемоаттрактантный белок-1 моноцитов (MCP-1), чтобы уменьшить инфильтрацию воспалительных клеток. С-реактивный белок (СРБ), биомаркер воспаления, может снижаться после лечения статинами. Предыдущие исследования также показали, что длительное введение аспирина снижает атеросклеротическое повреждение аорты и воспаление сосудов [33]. Сосудистые воспалительные признаки, включая активность TNF- α , MCP-1 и NF- κ B, подавлялись лечением аспирином. Эндотелиальная функция при воспалении может быть защищена аспирином. В нашем исследовании мы обнаружили, что положительные эффекты берберина при атеросклерозе объясняются их противовоспалительными свойствами. Анализ KEGG в нашем исследовании показал, что сигнальные пути берберина против атеросклероза связаны с убиквитин-опосредованным протеолизом, сигнальным путем MAPK и сигнальным путем PI3K-Akt. Эти воспалительные процессы участвуют в различных стадиях атеросклероза.Система убиквитин-протеасома может регулировать многие биологические клеточные процессы, такие как воспаление и окислительный стресс [34]. Дисфункция убиквитин-протеасомной системы играет решающую роль в прогрессировании бляшки и тенденции к ее разрыву. Анализ GO также обнаружил, что убиквитинирование белков, участвующее в убиквитин-зависимом катаболическом процессе белков, коррелирует с эффектами берберина против атеросклероза. Воспалительный сигнальный путь MAPK играет важную роль в патогенезе образования пенистых клеток при атеросклерозе [35].Образование пенистых клеток зависело от активации компонентов воспалительных путей MAPK, таких как JNK2 и p38 α MAPK. Сигнальный путь PI3K-Akt может регулировать воспалительные процессы атеросклероза, включая состав клеток и формирование окончательного фиброзного колпачка [30]. Ингибирование сигнального пути PI3K-Akt может повышать стабильность атеросклеротических бляшек. Подобно противовоспалительным эффектам доступных методов лечения, мы пришли к выводу, что берберин обладает противовоспалительным действием, ингибируя сигнальные пути при лечении атеросклероза.
Эндотелиальная функция при воспалении может быть защищена аспирином. В нашем исследовании мы обнаружили, что положительные эффекты берберина при атеросклерозе объясняются их противовоспалительными свойствами. Анализ KEGG в нашем исследовании показал, что сигнальные пути берберина против атеросклероза связаны с убиквитин-опосредованным протеолизом, сигнальным путем MAPK и сигнальным путем PI3K-Akt. Эти воспалительные процессы участвуют в различных стадиях атеросклероза.Система убиквитин-протеасома может регулировать многие биологические клеточные процессы, такие как воспаление и окислительный стресс [34]. Дисфункция убиквитин-протеасомной системы играет решающую роль в прогрессировании бляшки и тенденции к ее разрыву. Анализ GO также обнаружил, что убиквитинирование белков, участвующее в убиквитин-зависимом катаболическом процессе белков, коррелирует с эффектами берберина против атеросклероза. Воспалительный сигнальный путь MAPK играет важную роль в патогенезе образования пенистых клеток при атеросклерозе [35].Образование пенистых клеток зависело от активации компонентов воспалительных путей MAPK, таких как JNK2 и p38 α MAPK. Сигнальный путь PI3K-Akt может регулировать воспалительные процессы атеросклероза, включая состав клеток и формирование окончательного фиброзного колпачка [30]. Ингибирование сигнального пути PI3K-Akt может повышать стабильность атеросклеротических бляшек. Подобно противовоспалительным эффектам доступных методов лечения, мы пришли к выводу, что берберин обладает противовоспалительным действием, ингибируя сигнальные пути при лечении атеросклероза.
За исключением подавления воспаления, доступные методы лечения, такие как статины, подавляют пролиферацию клеток при лечении атеросклероза [36]. Разрастание гладкомышечных клеток артерий (ГМК) способствует формированию фиброзной капсулы бляшки и продукции воспалительных цитокинов. Подавление пролиферации SMC статинами замедляет прогрессирование бляшек [37]. В нашем исследовании мы обнаружили, что клеточный цикл участвует в механизме действия берберина против атеросклероза в анализе KEGG. Кроме того, анализ GO показал, что переход G1 / S цикла митотических клеток коррелировал с биологическим действием берберина против атеросклероза. G1 / S-переход митотического клеточного цикла принимает участие в механизме клеточного цикла [38]. Итак, мы пришли к выводу, что берберин может подавлять пролиферацию SMC, влияя на клеточный цикл.
Кроме того, анализ GO показал, что переход G1 / S цикла митотических клеток коррелировал с биологическим действием берберина против атеросклероза. G1 / S-переход митотического клеточного цикла принимает участие в механизме клеточного цикла [38]. Итак, мы пришли к выводу, что берберин может подавлять пролиферацию SMC, влияя на клеточный цикл.
В совокупности доступные методы лечения, такие как аспирин и статины, борются с атеросклерозом, подавляя воспаление и пролиферацию клеток. Объединив результаты в контексте с доступными методами лечения атеросклероза, мы пришли к выводу, что берберин подавляет воспаление и пролиферацию клеток при лечении атеросклероза.Воспалительные пути, включая опосредованный убиквитином протеолиз, сигнальный путь MAPK и сигнальный путь PI3K-Akt, могут быть подавлены берберином. Аберрантную пролиферацию клеток можно ослабить за счет барберинга, регулируя клеточный цикл. G1 / S-переход митотического клеточного цикла может быть вовлечен в механизм регуляции клеточного цикла берберином.
5. Заключение
В заключение, мультицелевые и многокомпонентные эффекты берберина против атеросклероза были четко разъяснены сетевой фармакологией.Мы определили потенциальные цели, связанные с берберином и атеросклерозом, с помощью нескольких баз данных. Затем мы объединили две сети PPI и получили базовую сеть PPI из объединенной сети PPI. Наконец, мы провели анализ функционального обогащения, включая анализ путей GO и KEGG, чтобы прояснить множественные механизмы действия берберина против атеросклероза. Пути, напрямую связанные с берберином против атеросклероза, включают клеточный цикл, протеолиз, опосредованный убиквитином, сигнальный путь MAPK и сигнальный путь PI3K-Akt.Объединив результаты в контексте с доступными методами лечения атеросклероза, мы пришли к выводу, что берберин может подавлять воспаление и пролиферацию клеток при лечении атеросклероза.
Сокращения
| APP: | Белок-предшественник бета-амилоида | |||||
| BC: | Центральность промежуточности | |||||
| BIND: | Сеть биомолекулярных взаимодействий | Общая база данных биомолекулярного взаимодействия | ||||
| BP: | Биологический процесс | |||||
| CC: | Центральность близости | |||||
| CRP: | C-реактивный белок | |||||
| CUL143 | База данных для аннотаций, визуализации и интегрированного открытия | |||||
| DC: | Степень центральности | |||||
| DIP: | База данных взаимодействующих белков | |||||
| EC: | Центральность собственного вектора; ESR1, рецептор эстрогена 1 | |||||
| FN1: | Фибронектин 1 | |||||
| GAD: | База данных генетической ассоциации; GO, Gene Ontology | |||||
| HIF-1: | Фактор 1, индуцируемый гипоксией | |||||
| HPRD: | Справочная база данных белков человека | |||||
| HSP90: | IC142 Белок теплового шока 90 | |||||
| Молекула межклеточной адгезии 1 | ||||||
| IFNs: | Интерфероны | |||||
| IL: | Интерлейкины | |||||
| iNOS: | Intucible | |||||
| KEGG: | Киотская энциклопедия генов и геномов | |||||
| LAC: | средняя локальная связность | |||||
| MAPK: | Mitogen-Activated Proteinkinase | MCM2-активируемый протеинкиназа | MCM-протеинкиназа | |||
| MCP-1: | Хемоаттрактант прот. in-1 in-1 | |||||
| MF: | Молекулярная функция | |||||
| MINT: | База данных Molecular INTeraction | |||||
| MMP: | матричная металлопротеиназа | NCF централизация сети κB: | Ядерный фактор каппа B | |||
| NO: | Оксид азота | |||||
| NTRK1: | Нейротрофический рецептор тирозинкиназы 1 | |||||
| 142 INdelian | Окисленный липопротеин низкой плотности | |||||
| АФК: | Активные формы кислорода | |||||
| PI3K: | Фосфоинозитид-3-киназа | |||||
| PPI14143 | Взаимодействие с белками: | Взаимодействие с белками мышечные клетки | ||||
| TCMSP: | Традиционный китайский Фармакология медицинских систем | |||||
| TGFs: | Трансформирующие факторы роста | |||||
| TNFs: | Факторы некроза опухоли | |||||
| TP53: | Терапевтический белок p14143 | Терапевтический белок p14143 | UBC: | Убиквитин C | ||
| VSMCs: | Клетки гладких мышц сосудов |
Доступность данных
Данные, использованные для подтверждения результатов этого исследования, включены в статью.
Конфликт интересов
Все авторы заявляют об отсутствии конфликта интересов.
Благодарности
Это исследование было поддержано Национальным фондом естественных наук Китая (грант № 81603600).
Дополнительные материалы
Дополнительная таблица 1: потенциальные мишени берберина. Дополнительная таблица 2: потенциальные мишени атеросклероза. Дополнительная таблица 3: гены-мишени каждого биологического процесса. Дополнительная таблица 4: гены-мишени каждого пути. (Дополнительные материалы)
Холестерин и образование артериальных бляшек
ИСТОЧНИКИ:
Американская кардиологическая ассоциация: «Атеросклероз», «Холестерин», «Общие сердечно-сосудистые заболевания», «Что такое атеросклероз?» «Холестерин ЛПНП и ЛПВП: что плохо, а что хорошо?» «Лекарства, снижающие уровень холестерина», «Фитохимические препараты и сердечно-сосудистые заболевания», «Влияние нормального, предгипертензивного и гипертонического уровней артериального давления на прогрессирование коронарного атеросклероза», «Антиагреганты», «Антикоагулянты», «Антикоагулянты», «Вопросы» и ответы о терапии статинами. «
«
Тираж :« Высокая распространенность коронарного атеросклероза у бессимптомных подростков и молодых людей: данные внутрисосудистого ультразвукового исследования ».
Медицинский журнал Новой Англии : «Последние тенденции в острой ишемической болезни сердца — смертность, заболеваемость, медицинское обслуживание и факторы риска», «Исследование сердца в Хельсинки: исследование первичной профилактики гемфиброзила у мужчин среднего возраста с Дислипидемия »,« Сравнение варфарина и аспирина для профилактики рецидивирующего ишемического инсульта.»
Американский колледж кардиологов:« Заявление о защите интересов ».
CDC.gov.
Американский журнал клинического питания : «Эффекты пищевых волокон по снижению холестерина: метаанализ».
Экспертный обзор сердечно-сосудистой терапии : «Биомаркеры, атеросклероз и сердечно-сосудистые события».
Ричард Штайн, доктор медицины, национальный представитель Американской кардиологической ассоциации; профессор медицины и директор программы кардиологии городского сообщества Медицинской школы Нью-Йоркского университета, Нью-Йорк.
Пресс-релиз, FDA.
Тираж : «Ингибиторы вазопептидазы: новая концепция лечения сердечно-сосудистых заболеваний?» «Благоприятные плейотропные эффекты статинов на сердечно-сосудистую систему», «Влияние правастатина и липидов плазмы на клинические события в исследовании коронарной профилактики на западе Шотландии (WOSCOPS)».
Ланцет : «Влияние длительной терапии фенофибратом на сердечно-сосудистые события у 9795 человек с сахарным диабетом 2 типа (исследование FIELD): рандомизированное контролируемое исследование.»
Природа Клиническая практика: эндокринология и метаболизм :« Мера для меры — сахар или жиры? Сочетание риска сердечно-сосудистых заболеваний и диабета с помощью терапии ниацином ».
BMJ : «Совместный метаанализ рандомизированных исследований антитромбоцитарной терапии для предотвращения смерти, инфаркта миокарда и инсульта у пациентов с высоким риском».
АстраЗенека.
Гипергомоцистеинемия, функция сосудов и атеросклероз: действие витаминов
Мадд Ш., Леви Х. Л., Сковби Ф. Нарушения трансульфурации. В: Scriver CR, Beaudet AL, Sly WS, Valle D, eds. Метаболические основы наследственного заболевания , 6-е изд. Нью-Йорк: Макгроу-Хилл, 1989: 693–734.
Google Scholar
МакКалли К.С. Сосудистая патология гомоцистеинемии: значение для патогенеза артериосклероза. AmJ Pathol 1969; 56: 111–128.
Google Scholar
Rosenblatt DS. Наследственные нарушения транспорта и обмена фолиевой кислоты. В: Scriver CR, Beaudet AL, Sly WS, Valle D, eds. Метаболические основы наследственного заболевания , 6-е изд. Нью-Йорк: Макгроу-Хилл, 1989: 2049–2064.
Google Scholar
Stampfer MJ, Malinow MR, Willett MC, et al. Проспективное исследование гомоцистеина плазмы и риска инфаркта миокарда у американских врачей. JAMA 1992; 268: 877–881.
Google Scholar
Жак П.Ф., Розенберг И.Х., Роджерс Г. и др. Концентрация общего гомоцистеина в сыворотке крови у подростков и взрослых американцев: результаты третьего национального обследования здоровья и питания. Am J Clin Nutr 1999; 69: 482–489.
Google Scholar
Канг С.С., Пассен Э.Л., Рагги Н., Вонг П.В.К., Сора Дж. Термолабильный дефект метилентетрагидрофолатредуктазы при ишемической болезни сердца. Тираж 1993; 88: 1463–1469.
Google Scholar
Розен Р. Генетическая предрасположенность к гипергомоцистеинемии: дефицит метилентетрагидрофолатредуктазы (MTHFR). Thromb Haemost 1997; 78: 523–526.
Google Scholar
Морита Х., Курихара Х., Цубаки С. и др. Полиморфизм гена метилентетрагидрофолатредуктазы и ишемический инсульт у японцев. Arterioscler Thromb Vasc Biol 1998; 18: 1465–1469.
Google Scholar
Brattstrom L, Wilcken DE, Ohrvik J, Brudin L. Обычная мутация гена метилентетрагидрофолатредуктазы приводит к гипергомоцистеинемии, но не к сосудистым заболеваниям: результат метаанализа. Тираж 1998; 98: 2520–2526.
Google Scholar
Фолсом А.Р., Ньето Ф.Дж., Макговерн П.Г. и др.Проспективное исследование заболеваемости ишемической болезнью сердца в отношении общего гомоцистеина натощак, связанных генетических полиморфизмов и витаминов группы B: исследование риска атеросклероза в сообществах (ARIC). Тираж 1998; 98: 204–210.
Google Scholar
Верхофф Б.Дж., Трип доктор медицины, Принс М.Х., Кастелейн Дж.Дж., Рейтсма PH. Влияние распространенной мутации метилентетрагидрофолатредуктазы на уровни гомоцистеина, фолиевой кислоты, витамина B12 и на риск преждевременного атеросклероза. Атеросклероз 1998; 141: 161–166.
Google Scholar
Селхуб Дж., Жак П.Ф., Уилсон П.Ф., Раш Д., Розенберг И.Х. Витаминный статус и потребление как основные детерминанты гомоцистеинемии у пожилого населения. JAMA 1993; 270: 2693–2698.
Google Scholar
Naurath HJ, Joosten E, Riezler R, Stabler SP, Allen RH, Lindenbaum J.Эффекты витамина B 12 , фолиевой кислоты и добавок витамина B6 у пожилых людей с нормальной концентрацией витаминов в сыворотке. Lancet 1995; 346: 85–89.
Google Scholar
Nygard O, Refsum H, Ueland PM, Vollset SE. Основные факторы, определяющие образ жизни в распределении общего гомоцистеина в плазме: исследование гомоцистеина hordaland. AmJ Clin Nutr 1998; 67: 263–270.
AmJ Clin Nutr 1998; 67: 263–270.
Google Scholar
Guttormsen AB, Schneede J, Fiskerstrand T, Ueland PM, Refsum HM. Концентрации гомоцистеина и других аминотиоловых соединений в плазме связаны с потреблением пищи у здоровых людей. J Nutr 1994; 124: 1934–1941.
Google Scholar
Фрайер Р. Х., Уилсон Б. Д., Габлер Д. Б., Фицджеральд Л. А., Роджерс Г. М.. Гомоцистеин, фактор риска преждевременного сосудистого заболевания и тромбоза, индуцирует активность тканевого фактора в эндотелиальных клетках. Артериосклер тромб 1993; 13: 1327–1333.
Google Scholar
Роджерс GM, Кейн WH. Активация эндогенного фактора V индуцированным гомоцистеином активатором эндотелиальных клеток сосудов. J Clin Invest 1986; 77: 1909–1916.
Google Scholar
Ленц С.Р., Сэдлер Дж. Э. Ингибирование поверхностной экспрессии тромбомодулина и активации протеина С тромбогенным агентом гомоцистеином. J Clin Invest 1991; 88: 1906–1914.
Google Scholar
Graeber JE, Slott JH, Ulane RE, Schulman JD, Stuart MJ. Влияние гомоцистеина и гомоцистина на метаболизм тромбоцитов и сосудов арахидоновой кислоты. Pediatr Res 1982; 16: 490–493.
Google Scholar
Харпель П.К., Чанг В.Т., Борт В. Гомоцистеин и другие сульфгидильные соединения усиливают связывание липопротеина (а) с фибрином: потенциальная биохимическая связь между тромбозом, атерогенезом и метаболизмом сульфгидрильных соединений. Proc Natl Acad Sci USA 1992; 89: 10193–10197.
Google Scholar
Хаджар К.А., Маури Л., Яковина А.Т. и др. Связывание тканевого активатора плазминогена с хвостовым доменом аннексина II. Прямая модуляция гомоцистеином. J Biol Chem 1998; 273: 9987–9993.
Прямая модуляция гомоцистеином. J Biol Chem 1998; 273: 9987–9993.
Google Scholar
Durand P, Lussier-Cacan S, Blache D. Острая гипергомоцистеинемия, вызванная метиониновой нагрузкой, усиливает агрегацию тромбоцитов, биосинтез тромбоксана и активность тканевого фактора макрофагов у крыс. FASEBJ 1997; 11: 1157–1168.
Google Scholar
Wall RT, Harlan JM, Harker LA, Striker GE. Гомоцистеин-индуцированное повреждение эндотелиальных клеток in vivo : модель для исследования повреждения сосудов. Thromb Res 1980; 18: 113–121.
Google Scholar
Де Гроот П.Г., Виллемс С., Берс GHJ и др. Дисфункция эндотелиальных клеток при гомоцистинурии. Eur J Clin Invest 1983; 13: 405–410.
Google Scholar
Ван Х., Йошизуми М., Лай К. и др. Подавление роста и метилирования p21ras в эндотелиальных клетках сосудов гомоцистеином, но не цистеином. J Biol Chem 1997; 272: 25380–25385.
Google Scholar
Dudman NPB, Temple SE, Guo XW, Fu WY, Perry MA. Гомоцистеин усиливает нейтрофильно-эндотелиальные взаимодействия как в культивируемых клетках человека, так и в клетках крыс in vivo . Circ Res 1999; 84: 409–416.
Google Scholar
Stamler JS, Osborne JA, Jaraki O, et al. Неблагоприятные сосудистые эффекты гомоцистеина модулируются релаксирующим фактором эндотелия и родственными оксидами азота. J Clin Invest 1993; 91: 308–318.
Google Scholar
McCully KS, Ragsdale BD. Производство атеросклероза гомоцистеинемией. Am J Pathol 1970; 61: 1–11.
Google Scholar

Харкер Л.А., Росс Р., Слихтер С.Дж., Скотт С.Р. Гомоцистеин-индуцированный артериосклероз: роль повреждения эндотелиальных клеток и ответ тромбоцитов в его генезе. J Clin Invest 1976; 58: 731–741.
Google Scholar
Hladovec J. Экспериментальная гомоцистеинемия, эндотелиальные поражения и тромбозы. Кровеносные сосуды 1979; 18: 11–20.
Google Scholar
Rolland PH, Friggi A, Barlatier A, et al. Повреждение сосудов мини-свиньи, вызванное гипергомоцистеинемией. Комбинация каптоприла и гидрохлоротиазида предотвращает эластические изменения. Тираж , 1995; 91: 1161–1174.
Google Scholar
Ленц С.Р., Соби К.Г., Пигорс Д.Д. и др. Сосудистая дисфункция у обезьян с гипергомоцистной (е) инемией, вызванной диетой. J Clin Invest 1996; 98: 24–29.
Google Scholar
Ленц С.Р., Малинов М.Р., Пигорс Д.Д., Бхопаткар-Тередесай МБ, Фарачи FM, Хейстад Д.Д. Последствия гипергомоцистной (е) инемии на функцию сосудов у атеросклеротических обезьян. Arterioscler Thromb Vasc Biol 1997; 17: 2930–2934.
Google Scholar
Celermajer DS, Sorensen K, Ryalls M, et al.Нарушение функции эндотелия возникает в системных артериях детей с гомозиготной гомоцистинурией, но не у их гетерозиготных родителей. J Am Coll Cardiol 1993; 22: 854–858.
Google Scholar
Takawol A, Omland T, Gerhard M, Wu JT, Creager MA. Гипергомоцистная (е) инемия связана с нарушением эндотелий-зависимой вазодилатации у людей. Circulation 1997; 95: 1119–1121.
Google Scholar
Иззо М.Р., Фельдман М.Д., Ву С.К. и др. Снижение уровня гомоцистеина в плазме улучшает вазореактивность плечевой артерии у пациентов с ишемической болезнью сердца. Тираж 1995; 92 (Приложение I): I-708 (Реферат).
Снижение уровня гомоцистеина в плазме улучшает вазореактивность плечевой артерии у пациентов с ишемической болезнью сердца. Тираж 1995; 92 (Приложение I): I-708 (Реферат).
Google Scholar
Kanani PM, Sinkey CA, Browning RL, Alleman M, Knapp HR, Haynes WG. Роль оксидантного стресса в эндотелиальной дисфункции, вызванной экспериментальной гипергомоцистной (е) инемией у людей. Тираж 1999 г .; (под давлением).
Беллами М.Ф., Макдауэлл И.Ф., Рэмси М.В. и др. Гипергомоцистеинемия после пероральной нагрузки метионином резко ухудшает эндотелиальную функцию у здоровых взрослых. Тираж 1998; 98: 1848–1852.
Google Scholar
Чемберс Дж. К., МакГрегор А., Жан-Мари Дж., Кунер Дж. С.. Острая гипергомоцистеинемия и эндотелиальная дисфункция. Lancet 1998; 351: 36–37.
Google Scholar
Haynes WG, Sinkey CA, Kanani P. Острая нагрузка метионином вызывает эндотелиальную дисфункцию у людей. J Invest Med 1997; 45: 210A.
Google Scholar
Усуи М., Мацуока Х., Миядзаки Х., Уэда С., Окуда С., Имаидзуми Т. Эндотелиальная дисфункция из-за острой гипергомоцистной (е) инемии: Восстановление с помощью фолиевой кислоты. Clin Sci 1999; 96: 235–239.
Google Scholar
Starkebaum G, Harlan JM. Повреждение эндотелиальных клеток из-за катализируемого медью образования пероксида водорода из гомоцистеина. Дж. Клин Инвест 1993; 77: 1370–1376.
Google Scholar
Heinecke JW, Rosen H, Suzuki LA, Chait A. Роль серосодержащих аминокислот в производстве супероксида и модификации липопротеинов низкой плотности артериальными гладкомышечными клетками. J Biol Chem 1987; 262: 10098-10103.
J Biol Chem 1987; 262: 10098-10103.
Google Scholar
Эмсли AM, Джереми JY, Gomes GN, Angelini GD, Plane F. Исследование ингибирующих эффектов гомоцистеина и меди на опосредованное оксидом азота расслабление изолированной аорты крысы. Brit J Pharmacol 1999; 126: 1034–1040.
Google Scholar
Апчерч Г. Р., младший, Уэлч Г. Н., Фабиан А. Дж. И др. Гомоцист (е )ин снижает биодоступность оксида азота по механизму с участием глутатионпероксидазы. J Biol Chem 1997; 272: 17012–17017.
Google Scholar
Хултберг Б., Андерссон А., Исакссон А. Повреждающие клетки эффекты низких количеств гомоцистеина и ионов меди в культурах линий клеток человека вызваны окислительным стрессом. Токсикология 1997; 123: 33–40.
Google Scholar
Brown JC, Rosenquist TH, Monaghan DT. Активация ERK2 гомоцистеином в клетках гладких мышц сосудов. Biochem Biophys Res Comm 1998; 251: 669–676.
Google Scholar
Тан Л., Мамотт С.Д., Ван Бокксмер Ф.М., Тейлор Р.Р. Влияние гомоцистеина на синтез ДНК в культивируемых гладких мышцах сосудов человека. Атеросклероз 1998; 136: 169–173.
Google Scholar
Далтон М.Л., Гадсон П.Ф., младший, Ренн Р.В., Розенквист Т.Х. Каскад сигналов гомоцистеина: производство фосфолипидов, активация протеинкиназы C и индукция c-fos и c-myb в гладкомышечных клетках. FASEB J 1997; 11: 703–711.
Google Scholar
Southern FN, Cruz N, Fink LM, et al. Гипергомоцистеинемия увеличивает гиперплазию интимы на модели каротидной эндартерэктомии у крыс. J Vasc Surg 1998; 28: 909–918.
Google Scholar
Шарпио П., Бескон А., Ожье Т. и др. Гипергомоцистеинемия вызывает эластолиз в артериях мини-свиней: структурные последствия, специфичность артериального участка и эффект каптоприлгидрохлоротиазида. Matrix Biol 1998; 17: 559–574.
Google Scholar
Sutton-Tyrrell K, Bostom A, Selhub J, Zeigler-Johnson C. Высокие уровни гомоцистеина независимо связаны с изолированной систолической гипертензией у пожилых людей. Circulation 1997; 96: 1745–1749.
Google Scholar
Фиорина П., Ланфредини М., Монтанари А. и др. Гомоцистеин и фолиевая кислота в плазме связаны с артериальным давлением при сахарном диабете 2 типа. Am J Hypertens 1998; 11: 1100–1107.
Google Scholar
Boushey CJ, Beresford SAA, Omenn GS, Molutsky AG. Количественная оценка гомоцистеина плазмы как фактора риска сосудистых заболеваний. JAMA 1995; 274: 1049–1057.
Google Scholar
Graham IM, Daly LE, Refsum HM, et al. Гомоцистеин плазмы как фактор риска сосудистых заболеваний.Европейский проект согласованных действий. JAMA 1997; 277: 1775–1781.
Google Scholar
Montalescot G, Ankri A, Chadefaux-Vekemans B, et al. Гомоцистеин плазмы и степень атеросклероза у пациентов с ишемической болезнью сердца. Int J Cardiol 1997; 60: 295–300.
Google Scholar
Боты М.Л., Лаунер Л.Дж., Линдеманс Дж. И др.Гомоцистеин и краткосрочный риск инфаркта миокарда и инсульта у пожилых людей: исследование TheRotterdam. Arch InternMed 1999; 159: 38–44.
Google Scholar

Ридкер П.М., Бьюринг Дж. Э., Мэнсон Дж. Э., Хеннекенс СН. Проспективное исследование общего гомоцистеина и риска сердечно-сосудистых событий в будущем среди практически здоровых женщин. Тираж 1998; 19 (Приложение): I – 810 (Аннотация).
Google Scholar
Nygard O, Nordrehaug JE, Refsum H, Ueland PM, Farstad M, Vollset SE. Уровни гомоцистеина в плазме и смертность у пациентов с ишемической болезнью сердца. N Engl J Med 1997; 337: 230–236.
Google Scholar
Meleady R, Lindgren A, Boers GHJ, et al. Гомоцистеин плазмы как прогностический фактор риска сосудистых заболеваний. Eur Heart J 1998; 19 (Дополнение): 8 (Аннотация).
Google Scholar
Stehouwer CD, Weijenberg MP, van den Berg M, Jakobs C, Feskens EJ, Kromhout D. Гомоцистеин в сыворотке и риск ишемической болезни сердца и цереброваскулярных заболеваний у пожилых мужчин: 10-летнее наблюдение. Arterioscler Thromb Vasc Biol 1998; 18: 1895–1901.
Google Scholar
Cheng SW, Ting AC, Wong J. Общий гомоцистеин плазмы натощак и атеросклеротическое заболевание периферических сосудов. Ann Vasc Surg 1997; 11: 217–223.
Google Scholar
Тейлор Л.М., младший, Монета Г.Л., Секстон Г.Дж., Шафф Р.А., Портер Дж. М.. Проспективное слепое исследование взаимосвязи между гомоцистеином плазмы и прогрессированием симптоматического заболевания периферических артерий. J Vasc Surg 1999; 29: 8–19.
Google Scholar
Ray JG. Метаанализ гипергомоцистеинемии как фактора риска венозной тромбоэмболии. Arch Intern Med 1998; 158: 2101–2106.
Google Scholar

Петри М., Рубенофф Р., Даллал Г.Е., Надо М.Р., Селхуб Дж., Розенберг И.Х. Гомоцистеин в плазме как фактор риска атеротромботических явлений при системной красной волчанке. Lancet 1996; 348: 1120–1124.
Google Scholar
Ридкер П.М., Хеннекенс С.Х., Селхуб Дж., Милетич Дж. П., Малинов М.Р., Штампфер М.Дж.Взаимосвязь гипергомоцистной (е) инемии, фактора V Лейдена и риска венозной тромбоэмболии в будущем. Тираж 1997; 95: 1777–1782.
Google Scholar
Bostom AG, Shemin D, Verhoef P, et al. Повышенный уровень общего гомоцистеина в плазме натощак и исходы сердечно-сосудистых заболеваний у пациентов на поддерживающем диализе: проспективное исследование. Arterioscler Thromb Vasc Biol 1997; 17: 2554–2558.
Google Scholar
Moustapha A, Naso A, Nahlawi M и др. Проспективное исследование гипергомоцистеинемии как неблагоприятного сердечно-сосудистого фактора риска при терминальной стадии почечной недостаточности. Circulation 1998; 97: 138–141.
Google Scholar
Петерсон Дж. К., Спенс Дж. Д.. Витамины и прогрессирование атеросклероза при гипергомоцистной (е) иемии. Ланцет 1998; 351: 263.
Google Scholar
Дейли Л., Меледи Р., Грэм И. Гомоцистеин натощак или пост-метиониновой нагрузки: что следует измерять в отношении сосудистого риска? Ir J Med Sci 1995; 164 (Приложение 15): 6 (Аннотация).
Google Scholar
van den Berg M, Stehouwer CDA, Bierdrager E, Rauwerda JA. Гомоцистеин плазмы и тяжесть атеросклероза у молодых пациентов с атеросклеротическим заболеванием нижних конечностей. Артериосклер тромб Vasc Biol 1996; 16: 165–171.
Google Scholar
van der Griend R, Haas FJ, Duran M, Biesma DH, Meuwissen OJ, Banga JD. Нагрузочный тест на метионин необходим для выявления гипергомоцистеинемии. J Lab Clin Med 1998; 132: 67–72.
Google Scholar
Сотрудничество исследователей по снижению уровня гомоцистеина. Снижение уровня гомоцистеина в крови с помощью добавок на основе фолиевой кислоты: метаанализ рандомизированных исследований. BMJ 1998; 316: 894–898.
Google Scholar
Bostom AG, Gohh RY, Beaulieu AJ, et al. Лечение гипергомоцистеинемии у реципиентов почечного трансплантата. Рандомизированное плацебо-контролируемое исследование. Ann Intern Med 1997; 127: 1089–1092.
Google Scholar
Malinow MR, Duell PB, Hess DL, et al. Снижение уровней гомоцист (е) ина в плазме с помощью хлопьев для завтрака, обогащенных фолиевой кислотой, у пациентов с ишемической болезнью сердца. N Engl J Med 1998; 338: 1009–1015.
Google Scholar
Jacques PF, Selhub J, Bostom AG, Wilson PWF, Rosenberg IH. Влияние обогащения фолиевой кислотой на концентрацию фолиевой кислоты и гомоцистеина в плазме. N Engl J Med 1999; 340: 1449–1454.
Google Scholar
Атеросклероз и остеопороз. Общие цели для воздействия сердечно-сосудистых и антиостеопоротических препаратов (Часть II).Влияние антиостеопоротических препаратов на состояние сосудистой стенки | Скрипникова
1. Фрит Дж. К., Мёнкконен Дж., Блэкберн Г. и др. Клодронат и инкапсулированный в липосомы клодронат метаболизируются до нетоксичного аналога АТФ, аденозин-5 ‘- (бета, гамма-дихлорметилен) трифосфат в клетках млекопитающих in vitro. J Bone Miner Res. 1997; 12 (9): 1358-67. DOI: 10.1359 / jbmr.1997.12.9.1358.
J Bone Miner Res. 1997; 12 (9): 1358-67. DOI: 10.1359 / jbmr.1997.12.9.1358.
2. Осако М.К., Накагами Х., Койбути Н. и др. Эстроген подавляет кальцификацию сосудов через сосудистую систему RANKL: общий механизм остеопороза и кальцификации сосудов. Circ Res. 2010; 107 (4): 466-75. DOI: 10.1161 / circresaha.110.216846.
3. Ридли А.Дж., Холл А. Небольшой GTP-связывающий белок, который регулирует сборку фокальных спаек и актиновых стрессовых волокон в ответ на факторы роста. Клетка. 1992; 70 (3): 389-99.
4.Канис Дж. А., Бурлет Н., Купер К. и др. Европейское руководство по диагностике и лечению остеопороза у женщин в постменопаузе. Osteoporos Int. 2019; 30 (1): 3-44. DOI: 10.1007 / s00198-018-4704-5.
5. ван Бик Э., Питерман Э., Коэн Л. и др. Фарнезилпирофосфатсинтаза является молекулярной мишенью азотсодержащих бисфосфонатов. Biochem Biophys Res Commun. 1999; 264 (1): 108-11. DOI: 10.1006 / bbrc.1999.1499.
6.Фрит Дж. К., Мёнкконен Дж., Блэкберн Г. и др. Клодронат и инкапсулированный в липосомы клодронат метаболизируются до нетоксичного аналога АТФ, аденозин-5 ‘- (бета, гамма-дихлорметилен) трифосфат в клетках млекопитающих in vitro. J Bone Miner Res. 1997; 12 (9): 1358-67. DOI: 10.1359 / jbmr.1997.12.9.1358.
7. Бевилаква М., Домингес Л.Дж., Розини С., Барбагалло М. Бисфосфонаты и атеросклероз: почему? Волчанка. 2005; 14 (9): 773-9. DOI: 10.1191 / 0961203305lu2219oa.
8.Ридли А.Дж., Холл А. Небольшой GTP-связывающий белок, который регулирует сборку фокальных спаек и актиновых стрессовых волокон в ответ на факторы роста. Клетка. 1992; 70 (3): 389-99.
9. Даненберг H.D., Golomb G., Groothuis A., et al. Липосомальный алендронат подавляет системный врожденный иммунитет и снижает гиперплазию неоинтимы внутри стента у кроликов. Тираж. 2003; 108 (22): 2798-804. DOI: 10.1161 / 01.CIR.0000097002.69209.CD.
Тираж. 2003; 108 (22): 2798-804. DOI: 10.1161 / 01.CIR.0000097002.69209.CD.
10.ван Бик Э., Питерман Э., Коэн Л. и др. Фарнезилпирофосфатсинтаза является молекулярной мишенью азотсодержащих бисфосфонатов. Biochem Biophys Res Commun. 1999; 264 (1): 108-11. DOI: 10.1006 / bbrc.1999.1499.
11. Wu L., Zhu L., Shi W.H., et al. Золедронат подавляет пролиферацию, адгезию и миграцию гладкомышечных клеток сосудов. Eur J Pharmacol. 2009; 602 (1): 124-31. DOI: 10.1016 / j.ejphar.2008.10.043.
12.Бевилаква М., Домингес Л.Дж., Розини С., Барбагалло М. Бисфосфонаты и атеросклероз: почему? Волчанка. 2005; 14 (9): 773-9. DOI: 10.1191 / 0961203305lu2219oa.
13. Zhao Z., Shen W., Zhu H., et al. Золедронат подавляет пролиферацию и активацию фибробластов посредством нацеливания на сигнальный путь TGF-β. Drug Des Devel Ther. 2018; 12: 3021-31. DOI: 10.2147 / DDDT.S168897.
14. Даненберг Х.Д., Голомб Г., Гротуис А., и другие. Липосомальный алендронат подавляет системный врожденный иммунитет и снижает гиперплазию неоинтимы внутри стента у кроликов. Тираж. 2003; 108 (22): 2798-804. DOI: 10.1161 / 01.CIR.0000097002.69209.CD.
15. Изутани Х., Миягава С., Ширакура Р. и др. Делеция реципиентного макрофага снижает тяжесть коронарного артериосклероза трансплантата в модели трансплантации крыс. Transplant Proc. 1997; 29: 861-2.
16.Ву Л., Чжу Л., Ши В.Х. и др. Золедронат подавляет пролиферацию, адгезию и миграцию гладкомышечных клеток сосудов. Eur J Pharmacol. 2009; 602 (1): 124-31. DOI: 10.1016 / j.ejphar.2008.10.043.
17. Майерс Д.Т., Карвелис К.С. Случайное обнаружение кальцинированного диализного трансплантата на сканировании кости Tc-99m MDP. Clin Nucl Med. 1998; 23 (3): 173-4.
Clin Nucl Med. 1998; 23 (3): 173-4.
18. Чжао З., Шен В., Чжу Х. и др. Золедронат подавляет пролиферацию и активацию фибробластов посредством нацеливания на сигнальный путь TGF-β.Drug Des Devel Ther. 2018; 12: 3021-31. DOI: 10.2147 / DDDT.S168897.
19. Ylitalo R., Kalliovalkama J., Wu X., et al. Накопление бисфосфонатов в артериях человека и их влияние на функцию артерий человека и крысы in vitro. Pharmacol Toxicol. 1998; 83: 125-31.
20. Изутани Х., Миягава С., Ширакура Р. и др. Делеция реципиентного макрофага снижает тяжесть коронарного артериосклероза трансплантата в модели трансплантации крыс.Transplant Proc. 1997; 29: 861-2.
21. Кошияма Х., Накамура Ю., Танака С. и др. Уменьшение толщины интима-медиа сонной артерии после 1 года терапии этидронатом по поводу остеопении, связанной с диабетом 2 типа. J Clin Endocrinol Metab. 2000; 85: 2793-6. DOI: 10.1210 / jcem.85.8.6748.
22. Майерс Д.Т., Карвелис К.С. Случайное обнаружение кальцинированного диализного трансплантата на сканировании кости Tc-99m MDP. Clin Nucl Med. 1998; 23 (3): 173-4.
23. Celiloglu M., AydinY., Balci P., et al. Влияние алендроната натрия на толщину интима-медиа сонной артерии и липидный профиль у женщин с постменопаузальным остеопорозом. Менопауза. 2009; 16 (4): 689-93. DOI: 10.1097 / gme.0b013e318194cafd.
24. Ylitalo R., Kalliovalkama J., Wu X., et al. Накопление бисфосфонатов в артериях человека и их влияние на функцию артерий человека и крысы in vitro.Pharmacol Toxicol. 1998; 83: 125-31.
25. Делибаси Т., Эмрал Р., Эрдоган М.Ф. и др. Влияние терапии алендронатом натрия на толщину интимы средней сонной артерии у женщин в постменопаузе с остеопорозом. Adv Ther. 2007; 24 (2): 319-25. DOI: 10.1007 / BF02849900.
Adv Ther. 2007; 24 (2): 319-25. DOI: 10.1007 / BF02849900.
26. Кошияма Х., Накамура Ю., Танака С. и др. Уменьшение толщины интима-медиа сонной артерии после 1 года терапии этидронатом по поводу остеопении, связанной с диабетом 2 типа.J Clin Endocrinol Metab. 2000; 85: 2793-6. DOI: 10.1210 / jcem.85.8.6748.
27. Gonnelli S., Caffarelli C., Tanzilli L., et al. Эффекты внутривенного введения золедроната и ибандроната на толщину интима-медиа сонных артерий, липиды и FGF-23 у женщин с остеопорозом в постменопаузе. Кость. 2014; 61: 27-32. DOI: 10.1016 / j.bone.2013.12.017.
28. Celiloglu M., AydinY., Balci P., et al. Влияние алендроната натрия на толщину интима-медиа сонной артерии и липидный профиль у женщин с постменопаузальным остеопорозом.Менопауза. 2009; 16 (4): 689-93. DOI: 10.1097 / gme.0b013e318194cafd.
29. Лакиш А., Сернес Р., Боаз М. и др. Влияние длительного лечения ризедронатом на комплаентность артерий у пациентов с остеопорозом и факторами риска сердечно-сосудистых заболеваний. Кость. 2008; 43 (2): 279-283. DOI: 10.1016 / j.bone.2008.03.030.
30. Делибаси Т., Эмрал Р., Эрдоган М.Ф. и др. Влияние терапии алендронатом натрия на толщину интимы средней сонной артерии у женщин в постменопаузе с остеопорозом.Adv Ther. 2007; 24 (2): 319-25. DOI: 10.1007 / BF02849900.
31. Ариёси Т., Эйши К., Сакамото И. и др. Влияние этидроновой кислоты на кальцификацию артерий у диализных пациентов. Clin Drug Investigation. 2006; 26 (4): 215-222. DOI: 10.2165 / 00044011-200626040-00006.
32. Gonnelli S., Caffarelli C., Tanzilli L., et al. Эффекты внутривенного введения золедроната и ибандроната на толщину интима-медиа сонных артерий, липиды и FGF-23 у женщин с остеопорозом в постменопаузе. Кость. 2014; 61: 27-32. DOI: 10.1016 / j.bone.2013.12.017.
Кость. 2014; 61: 27-32. DOI: 10.1016 / j.bone.2013.12.017.
33. Хашиба Х., Айзава С., Тамура К., Кого Х. Подавление прогрессирования кальцификации аорты лечением этидронатом у гемодиализных пациентов: долгосрочные эффекты. Ther Apher Dial. 2006; 10 (1): 59-64. DOI: 10.1111 / j.1744-9987.2006.00345.x.
34. Лакиш А., Сернес Р., Боаз М. и др. Влияние длительного лечения ризедронатом на комплаентность артерий у пациентов с остеопорозом и факторами риска сердечно-сосудистых заболеваний.Кость. 2008; 43 (2): 279-283. DOI: 10.1016 / j.bone.2008.03.030.
35. Окамото М., Яманака С., Йошимото В., Шигемацу Т. Алендронат как эффективное средство лечения потери костной массы и кальцификации сосудов у реципиентов почечного трансплантата. J. Трансплантация. 2014; 2014: 269613. DOI: 10.1155 / 2014/269613.
36. Ариёси Т., Эйши К., Сакамото И. и др. Влияние этидроновой кислоты на кальцификацию артерий у диализных пациентов.Clin Drug Investigation. 2006; 26 (4): 215-222. DOI: 10.2165 / 00044011-200626040-00006.
37. Торрегроса Дж. В., Фустер Д., Джентил М. А. и др. Открытое испытание: эффект еженедельного приема ризедроната сразу после трансплантации у реципиентов почек. Трансплантация. 2010; 89 (12): 1476-81. DOI: 10.1155 / 2014/269613.
38. Хашиба Х., Айзава С., Тамура К., Кого Х. Подавление прогрессирования кальцификации аорты лечением этидронатом у гемодиализных пациентов: долгосрочные эффекты.Ther Apher Dial. 2006; 10 (1): 59-64. DOI: 10.1111 / j.1744-9987.2006.00345.x.
39. Hill J.A., Goldin J.G., Gjertson D., et al. Прогрессирование кальцификации коронарных артерий у пациентов, принимающих алендронат по поводу остеопороза. Acad Radiol. 2002; 9 (10): 1148-52.
40. Окамото М., Яманака С., Йошимото В., Шигемацу Т. Алендронат как эффективное средство лечения потери костной массы и кальцификации сосудов у реципиентов почечного трансплантата.J. Трансплантация. 2014; 2014: 269613. DOI: 10.1155 / 2014/269613.
Окамото М., Яманака С., Йошимото В., Шигемацу Т. Алендронат как эффективное средство лечения потери костной массы и кальцификации сосудов у реципиентов почечного трансплантата.J. Трансплантация. 2014; 2014: 269613. DOI: 10.1155 / 2014/269613.
41. Танко Л. Б., Цинь Г., Александерсен П. и др. Эффективные дозы ибандроната не влияют на 3-летнее прогрессирование кальцификации аорты у пожилых женщин с остеопорозом. Osteoporos Int. 2005; 16: 184-90. DOI: 10.1007 / s00198-004-1662-x.
42. Торрегроса Дж. В., Фустер Д., Джентил М. А. и др. Открытое испытание: эффект еженедельного приема ризедроната сразу после трансплантации у реципиентов почек.Трансплантация. 2010; 89 (12): 1476-81. DOI: 10.1155 / 2014/269613.
43. Эльмариа С., Делани Дж. А., О’Брайен К. Д. и др. Использование бисфосфонатов и распространенность кальцификации клапанов и сосудов у женщин. MESA (мультиэтническое исследование атеросклероза). J Am Coll Cardiol. 2010; 56 (21): 1752-9. DOI: 10.1016 / j.jacc.2010.05.050.
44. Hill J.A., Goldin J.G., Gjertson D., et al. Прогрессирование кальцификации коронарных артерий у пациентов, принимающих алендронат по поводу остеопороза.Acad Radiol. 2002; 9 (10): 1148-52.
45. Моэн М.Д., Ким С.Дж. Деносумаб: обзор его использования в лечении постменопаузального остеопороза. Наркотики старения. 2011; 28 (1): 63-82. DOI: 10.2165 / 11203300-000000000-00000.
46. Танко Л.Б., Цинь Г., Александерсен П. и др. Эффективные дозы ибандроната не влияют на 3-летнее прогрессирование кальцификации аорты у пожилых женщин с остеопорозом. Osteoporos Int. 2005; 16: 184-90.DOI: 10.1007 / s00198-004-1662-x.
47. Каммингс С.Р., Сан Мартин Дж., МакКлунг М.Р. и др. СВОБОДА Испытание. Деносумаб для профилактики переломов у женщин в постменопаузе с остеопорозом N Engl J Med.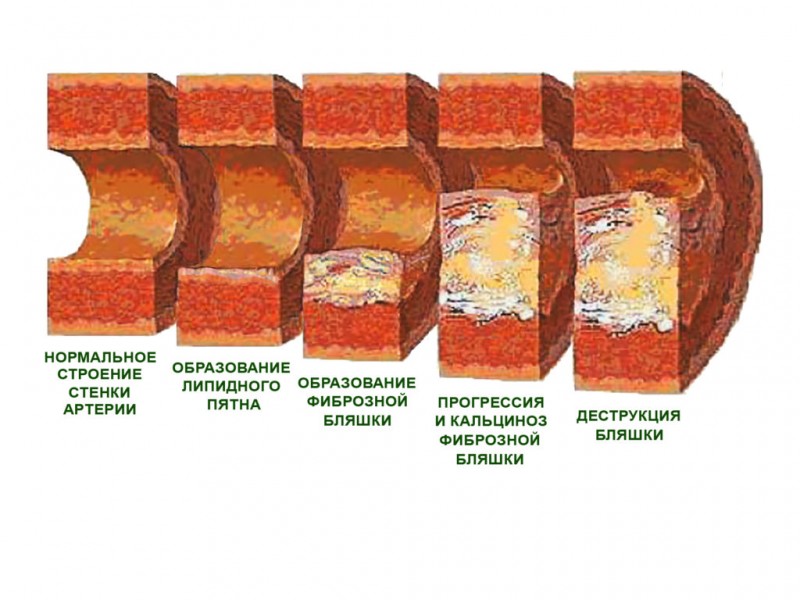 2009; 20; 361 (8): 756-65. DOI: 10.1056 / NEJMoa0809493.
2009; 20; 361 (8): 756-65. DOI: 10.1056 / NEJMoa0809493.
48. Элмариа С., Делани Дж. А., О’Брайен К. Д. и др. Использование бисфосфонатов и распространенность кальцификации клапанов и сосудов у женщин. MESA (мультиэтническое исследование атеросклероза).J Am Coll Cardiol. 2010; 56 (21): 1752-9. DOI: 10.1016 / j.jacc.2010.05.050.
49. Lerman D.A, Prasad S.1., Alotti N. Деносумаб может быть потенциальным ингибитором кальцификации межклеточных клеток клапана in vitro. Int J Cardiovasc Res. 2016; 5 (1). DOI: 10.4172 / 2324-8602.1000249.
50. Моэн М.Д., Ким С.Дж. Деносумаб: обзор его использования в лечении постменопаузального остеопороза. Наркотики старения. 2011; 28 (1): 63-82.DOI: 10.2165 / 11203300-000000000-00000.
51. Helas S., Goettsch C., Schoppet M., et al. Ингибирование активатора рецептора лиганда NF-kappaB деносумабом снижает отложение кальция в сосудах у мышей. Am J Pathol. 2009; 175 (2): 473-8. DOI: 10.2353 / ajpath.2009.080957.
52. Каммингс С.Р., Сан Мартин Дж., МакКлунг М.Р. и др. СВОБОДА Испытание. Деносумаб для профилактики переломов у женщин в постменопаузе с остеопорозом N Engl J Med.2009; 20; 361 (8): 756-65. DOI: 10.1056 / NEJMoa0809493.
53. Самельсон Э.Дж., Миллер П.Д., Кристиансен К. и др. Ингибирование RANKL деносумабом не влияет на 3-летнее прогрессирование кальцификации аорты или частоту неблагоприятных сердечно-сосудистых событий у женщин в постменопаузе с остеопорозом и высоким сердечно-сосудистым риском. J Bone Miner Res. 2014; 29 (2): 450-7. DOI: 10.1002 / jbmr.2043.
54. Лерман Д.А., Прасад С.1., Alotti N. Деносумаб может быть потенциальным ингибитором кальцификации клапанных интерстициальных клеток in vitro. Int J Cardiovasc Res. 2016; 5 (1). DOI: 10.4172 / 2324-8602.1000249.
2016; 5 (1). DOI: 10.4172 / 2324-8602.1000249.
55. Эдинбургский университет. Исследование Изучение влияния препаратов, используемых для лечения остеопороза, на прогрессирование кальцифицирующего стеноза аорты. SALTIERE II. 2014 г. [цитируется 27 мая 2019 г.]. Доступно по адресу: http://clinicaltrials.gov/ct2/show/NOTO2132026.
56.Helas S., Goettsch C., Schoppet M., et al. Ингибирование активатора рецептора лиганда NF-kappaB деносумабом снижает отложение кальция в сосудах у мышей. Am J Pathol. 2009; 175 (2): 473-8. DOI: 10.2353 / ajpath.2009.080957.
57. Guo J., Liu M., Yang D. Подавление передачи сигналов Wnt с помощью Dkk1 ослабляет PTH-опосредованный ответ стромальных клеток и образование новой кости. Cell Metab. 2010; 11 (2): 161-71. DOI: 10.1016 / j.cmet. 2009.12.007.
58.Самельсон Э.Дж., Миллер П.Д., Кристиансен К. и др. Ингибирование RANKL деносумабом не влияет на 3-летнее прогрессирование кальцификации аорты или частоту неблагоприятных сердечно-сосудистых событий у женщин в постменопаузе с остеопорозом и высоким сердечно-сосудистым риском. J Bone Miner Res. 2014; 29 (2): 450-7. DOI: 10.1002 / jbmr.2043.
59. Роблинг А.Г., Кедлая Р., Эллис С.Н. и др. Анаболические и катаболические режимы паратироидного гормона человека 1-34 вызывают специфическое для костей и оболочки ослабление скелетных эффектов у мышей с дефицитом SOST.Эндокринология. 2011; 152 (8): 2963-75. DOI: 10.1210 / en.2011-0049.
60. Эдинбургский университет. Исследование Изучение влияния препаратов, используемых для лечения остеопороза, на прогрессирование кальцифицирующего стеноза аорты. SALTIERE II. 2014 г. [цитируется 27 мая 2019 г.]. Доступно по адресу: http://clinicaltrials.gov/ct2/show/NOTO2132026.
61. Ри Й., Аллен М.Р., Кондон К. и др. Передача сигналов рецептора ПТГ в остеоцитах регулирует формирование надкостницы и интракортикальное ремоделирование.J Bone Miner Res. 2011; 26 (5): 1035-46. DOI: 10.1002 / jbmr.304.
62. Guo J., Liu M., Yang D. Подавление передачи сигналов Wnt с помощью Dkk1 ослабляет PTH-опосредованный ответ стромальных клеток и образование новой кости. Cell Metab. 2010; 11 (2): 161-71. DOI: 10.1016 / j.cmet. 2009.12.007.
63. McClung M.R., Martin J.S., Miller P.D., et al. Противоположные эффекты ремоделирования костей терипаратида и алендроната в увеличении костной массы. Arch Intern Med, 2005; 165Z: 1762-8.DOI: 10.1001 / archinte.165.15.1762.
64. Роблинг А.Г., Кедлая Р., Эллис С.Н. и др. Анаболические и катаболические режимы паратироидного гормона человека 1-34 вызывают специфическое для костей и оболочки ослабление скелетных эффектов у мышей с дефицитом SOST. Эндокринология. 2011; 152 (8): 2963-75. DOI: 10.1210 / en.2011-0049.
65. Сааг К.Г., Шейн Э., Бунен С. и др. Терипаратид или алендронат при остеопорозе, индуцированном глюкокортикоидами.Engl J Med. 2007; 357: 2028-39 DOI: 10.1056 / NEJMoa07140.
66. Ри Й., Аллен М.Р., Кондон К. и др. Передача сигналов рецептора ПТГ в остеоцитах регулирует формирование надкостницы и интракортикальное ремоделирование. J Bone Miner Res. 2011; 26 (5): 1035-46. DOI: 10.1002 / jbmr.304.
67. Shao J.S., Cheng S.L., Charlton-Kachigian N. Терипаратид [паратироидный гормон человека (1-34)] ингибирует остеогенную кальцификацию сосудов у мышей с диабетом с дефицитом рецепторов липопротеинов низкой плотности.J Biol Chem. 2003; 278: 50195-202. DOI: 10.1074 / jbc.M308825200.
68. McClung M.R., Martin J.S., Miller P.D., et al. Противоположные эффекты ремоделирования костей терипаратида и алендроната в увеличении костной массы. Arch Intern Med, 2005; 165Z: 1762-8. DOI: 10.1001 / archinte.165.15.1762.
69. Celer O., Akalın A., Oztunali C., Влияние лечения терипаратидом на эндотелиальную функцию, метаболизм глюкозы и маркеры воспаления у пациентов с постменопаузальным остеопорозом.J Clin Endocrinol. 2016; 85 (4): 556-60. DOI: 10.1111 / cen.13139.
70. Сааг К.Г., Шейн Э., Бунен С. и др. Терипаратид или алендронат при остеопорозе, индуцированном глюкокортикоидами. Engl J Med. 2007; 357: 2028-39 DOI: 10.1056 / NEJMoa07140.
71. Йода М., Иманиши Ю., Нагата Ю. и др. Терапия терипаратидом снижает уровень фосфатов в сыворотке и толщину внутренней оболочки сонной артерии у пациентов с остеопорозом. Calcif Tissue Int.2015л; 97 (1): 32-9. DOI: 10.1007 / s00223-015-0007-4.
72. Shao J.S., Cheng S.L., Charlton-Kachigian N. Терипаратид [паратироидный гормон человека (1-34)] ингибирует остеогенную кальцификацию сосудов у мышей с диабетом с дефицитом рецепторов липопротеинов низкой плотности. J Biol Chem. 2003; 278: 50195-202. DOI: 10.1074 / jbc.M308825200.
73. Passeri E., Mazzaccaro D., Sansoni V., et al. Влияние 12-месячного лечения золедронатом или терипаратидом на толщину интима-медиа сонной артерии у женщин с постменопаузальным остеопорозом: пилотное исследование.Int J Immunopathol Pharmacol. 2019; 33: 2058738418822439. DOI: 10.1177 / 2058738418822439.
74. Celer O., Akalın A., Oztunali C., Влияние лечения терипаратидом на функцию эндотелия, метаболизм глюкозы и маркеры воспаления у пациентов с постменопаузальным остеопорозом. J Clin Endocrinol. 2016; 85 (4): 556-60. DOI: 10.1111 / cen.13139.
75. Cheng X.W., Kikuchi R., Ishii H., et al. Циркулирующий катепсин К как потенциальный новый биомаркер ишемической болезни сердца.Атеросклероз. 2013; 228 (1): 211-6. DOI: 10.1016 / j. Атеросклероз. 2013.01.004.
76. Йода М., Иманиши Ю., Нагата Ю. и др. Терапия терипаратидом снижает уровень фосфатов в сыворотке и толщину внутренней оболочки сонной артерии у пациентов с остеопорозом. Calcif Tissue Int. 2015л; 97 (1): 32-9. DOI: 10.1007 / s00223-015-0007-4.
77. Чжао Х., Цинь Х., Ван С. и др. Повышенные уровни катепсина К в атеросклеротических бляшках человека связаны с нестабильностью бляшек.Exp Ther Med. 2017; 14 (4): 3471-6. DOI: 10.3892 / etm.2017.4935.
78. Passeri E., Mazzaccaro D., Sansoni V., et al. Влияние 12-месячного лечения золедронатом или терипаратидом на толщину интима-медиа сонной артерии у женщин с постменопаузальным остеопорозом: пилотное исследование. Int J Immunopathol Pharmacol. 2019; 33: 2058738418822439. DOI: 10.1177 / 2058738418822439.
79. Li X., Li Y., Jin J., et al. Повышенный уровень катепсина К в сыворотке у пациентов с ишемической болезнью сердца.Йонсей Мед Дж. 2014; 55 (4): 912-9. DOI: 10.3349 / ymj.2014.55.4.912.
80. Cheng X.W., Kikuchi R., Ishii H., et al. Циркулирующий катепсин К как потенциальный новый биомаркер ишемической болезни сердца. Атеросклероз. 2013; 228 (1): 211-6. DOI: 10.1016 / j. Атеросклероз. 2013.01.004.
81. Самохин А.О., Вонг А., Сафтиг П., Бромм Д. Роль катепсина К в структурных изменениях брахиоцефальной артерии при прогрессировании атеросклероза у мышей с дефицитом апоЕ.Атеросклероз. 2008; 200 (1): 58-68. DOI: 10.1016 / j.atherosclerosis.2007.12.047.
82. Чжао Х., Цинь Х., Ван С. и др. Повышенные уровни катепсина К в атеросклеротических бляшках человека связаны с нестабильностью бляшек. Exp Ther Med. 2017; 14 (4): 3471-6. DOI: 10.3892 / etm.2017.4935.
83. Wu H., Du Q., Dai Q., Ge J., Cheng X. Катепсины цистеиновой протеазы при атеросклеротических сердечно-сосудистых заболеваниях. J Atheroscler Thromb.2018; 25 (2): 111-23. DOI: 10.5551 / jat.RV17016.
84. Li X., Li Y., Jin J., et al. Повышенный уровень катепсина К в сыворотке у пациентов с ишемической болезнью сердца. Йонсей Мед Дж. 2014; 55 (4): 912-9. DOI: 10.3349 / ymj.2014.55.4.912.
85. Строуп Г., Кумар С., Джером С. Лечение мощным ингибитором катепсина К сохраняет массу кортикальной и трабекулярной кости у обезьян, подвергшихся овариэктомии. Calcified Tissue International. 2009; 85 (4): 344-55.DOI: 10.1007 / s00223-009-9279-x.
86. Самохин А.О., Вонг А., Сафтиг П., Бромм Д. Роль катепсина К в структурных изменениях брахиоцефальной артерии при прогрессировании атеросклероза у мышей с дефицитом апоЕ. Атеросклероз. 2008; 200 (1): 58-68. DOI: 10.1016 / j.atherosclerosis.2007.12.047.
87. Джером К., Миссбах М., Гамсе Р. Баликатиб, ингибитор катепсина К, стимулирует образование надкостницы у обезьян.Osteoporos Int. 2011; 22: 3001-11. DOI: 10.1007 / s00198-011-1529-x.
88. Wu H., Du Q., Dai Q., Ge J., Cheng X. Катепсины цистеиновой протеазы при атеросклеротических сердечно-сосудистых заболеваниях. J Atheroscler Thromb. 2018; 25 (2): 111-23. DOI: 10.5551 / jat.RV17016.
89. Масарачиа П., Пеннипакер Б., Пикарски М. и др. Оданакатиб снижает метаболизм и увеличивает костную массу в поясничном отделе позвоночника у скелетно зрелых овариэктомированных макак-резусов.J Bone Miner Res. 2011; 27: 509-23. DOI: 10.1002 / jbmr.1475.
90. Строуп Г., Кумар С., Джером С. Лечение мощным ингибитором катепсина К сохраняет массу кортикальной и трабекулярной кости у обезьян, подвергшихся овариэктомии. Calcified Tissue International. 2009; 85 (4): 344-55. DOI: 10.1007 / s00223-009-9279-x.
91. Подгорский И. Будущее антикатепсина К: двойная терапия заболеваний скелета и атеросклероза? Future Med Chem.2009; 1: 21-34.
92. Джером К., Миссбах М., Гамсе Р. Баликатиб, ингибитор катепсина К, стимулирует образование надкостницы у обезьян. Osteoporos Int. 2011; 22: 3001-11. DOI: 10.1007 / s00198-011-1529-x.
93. Zerbini C.A., McClung M.R. Odanacatib у женщин в постменопаузе с низкой минеральной плотностью костей: обзор текущих клинических данных. Ther Adv Musculoskelet Dis. 2013; 5 (4): 199-209. DOI: 10.1177 / 1759720X134
94. Масарачиа П., Пеннипакер Б., Пикарски М. и др. Оданакатиб снижает метаболизм и увеличивает костную массу в поясничном отделе позвоночника у скелетно зрелых овариэктомированных макак-резусов. J Bone Miner Res. 2011; 27: 509-23. DOI: 10.1002 / jbmr.1475.
95. Накамура Т., Шираки М., Фукунага М. и др. Влияние ингибитора катепсина К оданакатиба, вводимого один раз в неделю, на минеральную плотность костей у японских пациентов с остеопорозом — двойное слепое рандомизированное исследование по подбору доз.Osteoporos Int. 2014; 25 (1): 367-76. DOI: 10.1007 / s00198-013-2398-2.
96. Подгорский И. Будущее антикатепсина К: двойная терапия заболеваний скелета и атеросклероза? Future Med Chem. 2009; 1: 21-34.
97. Langdahl B., Binkley N., Bone H., et al. Odanacatib в лечении женщин в постменопаузе с низкой минеральной плотностью костей: пять лет непрерывной терапии в исследовании фазы 2. J Bone Miner Res. 2012; 27 (11): 2251-8.DOI: 10.1002 / jbmr.1695.
98. Zerbini C.A., McClung M.R. Odanacatib у женщин в постменопаузе с низкой минеральной плотностью костей: обзор текущих клинических данных. Ther Adv Musculoskelet Dis. 2013; 5 (4): 199-209. DOI: 10.1177 / 1759720X134
99. Bone H.G., Dempster D.W., Eisman J.A., et al. Odanacatib для лечения постменопаузального остеопороза: история развития, дизайн и характеристики участников LOFT, долгосрочного исследования перелома Odanacatib.Osteoporos Int. 2015; 26 (2): 699-712. DOI: 10.1007 / s00198-014-2944-6.
100. Накамура Т., Шираки М., Фукунага М. и др. Влияние ингибитора катепсина К оданакатиба, вводимого один раз в неделю, на минеральную плотность костей у японских пациентов с остеопорозом — двойное слепое рандомизированное исследование по подбору доз. Osteoporos Int. 2014; 25 (1): 367-76. DOI: 10.1007 / s00198-013-2398-2.
101. Эттингер Б., Блэк Д.М., Митлак Б.H. et al. Снижение риска перелома позвонков у женщин в постменопаузе с остеопорозом, получавших ралоксифен: результаты трехлетнего рандомизированного клинического исследования. Множественные результаты исследователей оценки ралоксифена (БОЛЬШЕ). ДЖАМА. 1999; 282: 637-45.
102. Langdahl B., Binkley N., Bone H., et al. Odanacatib в лечении женщин в постменопаузе с низкой минеральной плотностью костей: пять лет непрерывной терапии в исследовании фазы 2. J Bone Miner Res. 2012; 27 (11): 2251-8.DOI: 10.1002 / jbmr.1695.
103. Канис Дж. А., Йоханссон Х., Оден А., Мак Клоски Е. В. Базедоксифен уменьшает количество позвоночных и клинических переломов у женщин в постменопаузе из группы высокого риска, оцененного с помощью FRAX. Кость. 2009; 44 (6): 1049-54. DOI: 10.1016 / j.bone.2009.02.014.
104. Bone H.G., Dempster D.W., Eisman J.A., et al. Odanacatib для лечения постменопаузального остеопороза: история развития, дизайн и характеристики участников LOFT, долгосрочного исследования перелома Odanacatib.Osteoporos Int. 2015; 26 (2): 699-712. DOI: 10.1007 / s00198-014-2944-6.
105. Кларксон Т.Б., Этун К.Ф., Чен Х. и др. Влияние одного базедоксифена и конъюгированных конских эстрогенов на атеросклероз коронарных и периферических артерий у обезьян в постменопаузе. Менопауза. 2013; 20 (3): 274-81. DOI: 10.1097 / GME.0b013e318271e59b.
106. Ettinger B., Black D.M., Mitlak B.H. и другие. Снижение риска перелома позвонков у женщин в постменопаузе с остеопорозом, получавших ралоксифен: результаты трехлетнего рандомизированного клинического исследования.Множественные результаты исследователей оценки ралоксифена (БОЛЬШЕ). ДЖАМА. 1999; 282: 637-45.
107. Комм Б.С., Томпсон Дж. Р., Миркин С. Сердечно-сосудистая безопасность конъюгированных эстрогенов плюс базедоксифен: метаанализ исследований SMART. Климактерический. 2015; 18 (4): 503-11. DOI: 10.3109 / 13697137.2014.992011.
108. Канис Дж. А., Йоханссон Х., Оден А., Мак Клоски Е. В. Базедоксифен уменьшает количество позвоночных и клинических переломов у женщин в постменопаузе из группы высокого риска, оцененного с помощью FRAX.Кость. 2009; 44 (6): 1049-54. DOI: 10.1016 / j.bone.2009.02.014.
109. Кларксон Т.Б., Этун К.Ф., Чен Х. и др. Влияние одного базедоксифена и конъюгированных конских эстрогенов на атеросклероз коронарных и периферических артерий у обезьян в постменопаузе. Менопауза. 2013; 20 (3): 274-81. DOI: 10.1097 / GME.0b013e318271e59b.
110. Комм Б.С., Томпсон Дж. Р., Миркин С. Сердечно-сосудистая безопасность конъюгированных эстрогенов плюс базедоксифен: метаанализ исследований SMART.Климактерический. 2015; 18 (4): 503-11. DOI: 10.3109 / 13697137.2014.992011.
Церебральный атеросклероз — обзор
Сосудистая деменция
VaD — это заболевание хронической ишемии головного мозга, вызванное церебральным атеросклерозом, заболеванием мелких сосудов (SVD) и церебральной амилоидной ангиопатией (CAA) (Grinberg and Thal, 2010; Thal, 2010; Thal al., 2012; Jellinger, 2013; Khan et al., 2016). Атеросклероз приводит к инфарктам средних / крупных сосудов и характеризуется скоплением холестерина / липидов в стенке сосуда, что приводит к кальцинированным бляшкам, локальному разрыву и тромбозу (Stary, 2000; Jellinger, 2013).СВД приводит к лакунарным инфарктам и поражениям белого вещества и характеризуется артериосклерозом, артериолосклерозом и липогиалинозом сначала в базальных ганглиях, а затем вместе в глубоком белом веществе и лептоменингеальных артериях головного мозга и мозжечка (Thal et al., 2003; Grinberg). и Thal, 2010; Jellinger, 2013). Кортикальные сосуды обычно сохраняются, а ствол мозга поражается только на поздних стадиях SVD (Thal et al., 2003).
Церебральная амилоидная ангиопатия связана с отложениями Aβ в стенках лептоменингеальных и церебральных сосудов (Revesz et al., 2009; Гринберг и Тал, 2010; Аттемс и др., 2011; Еллингер, 2013). В семейных формах CAA другие белки, наряду с Aβ, откладываются в стенках сосудов (Revesz et al., 2009; Grinberg, Thal, 2010; Attems et al., 2011; Jellinger, 2013). В обоих случаях эти отложения белка приводят к разрыву стенки сосуда, микрокровоизлиянию, закупорке капилляров, нарушениям кровотока и микроинфарктам (Thal et al., 2009; Grinberg and Thal, 2010; Okamoto et al., 2012; Jellinger, 2013). CAA начинается в неокортексе, за ним следуют аллокортекс / лимбическая система и мозжечок, и, наконец, базальные ганглии, таламус и ствол мозга (Thal et al., 2003; Гринберг и Тал, 2010; Attems et al., 2011). Было охарактеризовано несколько вариантов VaD, преимущественно по локализации ишемии и вовлеченных сосудов. Наиболее распространенными формами VaD являются мультиинфарктный (большой и SVD), стратегический инфаркт / очаг (единичные инфаркты в стратегических регионах, например, гиппокампе), подкорковый ишемический / инфаркт (SVD; лакунарные инфаркты и поражения белого вещества) и постинсультный инсульт. . Семейные формы VaD, например церебральная аутосомно-доминантная артериопатия с подкорковыми инфарктами и лейкоэнцефалопатией (CADISIL), встречаются редко (Roh and Lee, 2014).Возникающие в результате признаки и симптомы VaD зависят от локализации и тяжести ишемии (Alzheimer’s Association, 2014).
Фермент PCSK6 играет ключевую роль в сосудистых заболеваниях, согласно исследованиям
Новое исследование продемонстрировало, что фермент пропротеин, конвертирующий субтилизин / кексин 6, вызывает структурное и функциональное ремоделирование при сосудистых заболеваниях, что может стать новой терапевтической мишенью.
Исследования показали, что фермент пропротеин, преобразующий субтилизин / кексин 6 (PCSK6), ремоделирует стенки кровеносных сосудов и регулирует функцию гладкомышечных клеток, что приводит к образованию нестабильных атеросклеротических бляшек при сосудистых заболеваниях.По словам исследователей, этот фермент может стать возможной мишенью для новых терапевтических средств против сосудистых заболеваний.
… исследователи надеются, что успех лекарств против PCSK9 — родственного фермента — может повлиять на разработку лекарств, нацеленных на PCSK6 »
В новом исследовании исследователи из группы сосудистой хирургии Каролинского института, Швеция, работали над своим предыдущим исследованием, которое показало, что PCSK6 был одной из наиболее концентрированных молекул в атеросклеротических бляшках у пациентов с нестабильным атеросклерозом сонной артерии.В своей последней работе группа изучила важность PCSK6 при сосудистых заболеваниях человека и обнаружила, что он изменяет поведение гладких мышц и структуру стенок сосудов при различных сосудистых заболеваниях. Нестабильный атеросклероз — это образование бляшки на стенке артерии. либо увеличение размера сосудистой ткани, вызывающее закупорку, либо истончение и разрушение стенки. Эти бляшки могут разорваться при разрушении или разрушении; такие разрывы являются основной причиной инфаркта миокарда, а также могут вызывать инсульты.До этого исследования подробные знания о молекулярных процессах, которые делают атеросклеротические бляшки нестабильными, были минимальными.
В исследовании использовались несколько больших групп пациентов, насчитывающих более 5000 пациентов по всему миру, экспериментальные исследования клеточных культур и эксперименты на животных для проведения генетического анализа. Повышенная экспрессия PCSK6 была обнаружена в нескольких когортах людей, сравнивающих атеросклеротические поражения со здоровыми артериями. Мыши с подавленной экспрессией PCSK6 показали нарушение регуляции гладкомышечных клеток и отсутствие ремоделирования стенок кровеносных сосудов.Более того, подавление PCSK6 в клетках гладких мышц человека in vitro привело к снижению способности к сокращению.
Таким образом, команда пришла к выводу, что PCSK6 может стать будущей молекулой-мишенью для разработки методов лечения сосудистых заболеваний.
Исследователи надеются, что успех лекарств против PCSK9 — родственного фермента — нацеленных на лечение высокого холестерина в крови и сердечно-сосудистых заболеваний, может повлиять на разработку лекарств, нацеленных на PCSK6.
Исследование было опубликовано в журнале « Circulation Research ».
Системы доставки наночастиц для лечения атеросклероза
Краткая статья — Архив промышленной биотехнологии (2019) Том 3, Выпуск 1
Системы доставки лекарств в виде наночастиц для лечения атеросклероза
Майкл Нго, Бханутежа Мадху, Яшвант Патхак
Фармацевтический колледж Танежа, Университет Южной Флориды
Аннотация
Нанотехнологии находятся на переднем крае медицинских технологий.Он имеет огромное количество применений в науках о здоровье, и с его помощью постоянно делаются новые открытия. Атеросклероз, болезнь, которая поражала человечество еще в Древнем Египте, теперь рассматривается вместе с нанотехнологиями для разработки новых способов доставки лекарств для лечения этого сердечного заболевания. Цель данной исследовательской статьи — пролить свет на последние разработки в области нанотехнологий путем анализа недавних реальных приложений для лечения атеросклероза.
Традиционные методы лечения, включая лекарства, изменение образа жизни и даже инвазивные операции. Из трех методов два были идентифицированы как имеющие осложнения. Пероральные препараты и хирургические процедуры доказали свою эффективность в лечении атеросклероза, но оба могут вызвать непреднамеренное повреждение тканей среди других проблем. Нанотехнологии можно использовать для точной доставки лекарств и даже помощи на клеточном уровне, улучшая реакцию лейкоцитов на образование бляшек.Исследования показали многообещающие результаты при использовании нанотехнологий. Использование липосом, разработанных с помощью нанотехнологий, помогло увеличить растворимость статинов, что помогло увеличить абсорбцию и биодоступность. Когда лекарство помещалось внутрь развитой липосомы, оно защищалось до тех пор, пока не достигло целевого участка. Биохимические свойства липосом помогли исследователям прикрепить биомолекулы, такие как антитела, к липосомам, чтобы помочь в нацеливании, а также в направлении и привлечении макрофагов к интересующим областям, таким как участки бляшек.Еще одна нанотехнология, которая продолжает развиваться для медицинского применения, — это углеродные нанотрубки. Эти нанотрубки можно легко выращивать, и они успешно использовались для доставки лекарств и даже создания наноструктур, способствующих росту и регенерации тканей. Нанотехнологии обладают огромным потенциалом для медицины, и применительно к сердечному заболеванию атеросклерозу нанотехнология смогла успешно доказать свою полезность.
Ключевые слова: Углеродное волокно, углеродные нанотрубки, доставка лекарств, микродвигатели, атеросклероз, ЛПНП, липосомы, липосомная доставка лекарств
Введение
1.1 Что такое атеросклероз?
Атеросклероз — широко распространенное заболевание, поражающее жизнь многих людей в Соединенных Штатах. 18 миллионов американцев в возрасте 20 лет и старше страдают сердечными заболеваниями (4). Около 650 000 американцев умирают от болезней сердца каждый год, что составляет до 25% ежегодных смертей в Соединенных Штатах (4). Эти статистические данные вызывают тревогу и с каждым годом продолжают увеличиваться. Чтобы это число не увеличивалось, необходимо обсудить, что такое атеросклероз и причина этого заболевания.
В нормальном состоянии коронарные артерии имеют гладкую внутреннюю поверхность, которая позволяет крови беспрепятственно проходить через них. Однако на стенке коронарной артерии начинает накапливаться ЛПНП или «плохой» холестерин (4). Чтобы бороться с этим, иммунная система организма отправляет белые кровяные тельца для очистки от отложений ЛПНП на стенке артерии (4). Со временем комбинация белых кровяных телец, очищающих и соединяющихся с ЛПНП, в конечном итоге формирует бляшки. Этот налет ограничивает кровоток, что в конечном итоге вызывает атеросклероз.
1,2 Традиционные методы лечения атеросклероза
Современные методы лечения атеросклероза включают использование лекарств в качестве средства защиты. Статины могут использоваться для снижения уровня холестерина ЛПНП для большинства людей (9). Исследования показали, что прием статинов в течение года вызывает снижение уровня ЛПНП на 60%, повышение уровня ЛПВП или хорошего холестерина и снижение уровня триацилглицеридов (9). Еще одна группа препаратов, потенциально способных уменьшить атеросклероз, — это фибраты.Фибраты — это препараты, которые снижают уровень триацилглицеридов, молекул жира, которые способствуют образованию бляшек при атеросклерозе (9). Многие другие препараты могут использоваться для лечения атеросклероза, включая ниацин, препараты для снижения артериального давления и препараты, уменьшающие образование тромбов (9).
Эти препараты доказали свою эффективность при лечении атеросклероза, но у них есть недостатки. Одна из проблем с лекарствами — это неспецифическое нацеливание. Из-за неспецифического нацеливания лекарства могут накапливаться в здоровых тканях (14).Кроме того, попадая в кровоток, лекарство проявляет биологическую активность до того, как достигнет целевого участка (14). Эффективность лекарственного средства можно повысить, если его защитить перед доставкой в определенное место.
Другие виды лечения атеросклероза включают хирургические операции. При атеросклерозе используются три основных типа хирургических вмешательств: чрескожное коронарное вмешательство, аортокоронарное шунтирование и каротидная эндартерэктомия. Чрескожное коронарное вмешательство используется для открытия заблокированных или суженных коронарных артерий, улучшения кровотока к сердцу и облегчения боли в груди (5).После операции используется стент или трубка с мелкой сеткой, чтобы артерии оставались открытыми (5). Каротидная эндартерэктомия похожа на чрескожное коронарное вмешательство, но более специфична, поскольку лечение проводится только на шее. В результате этой процедуры восстанавливается приток крови к мозгу, что может предотвратить инсульт (5). Аортокоронарное шунтирование — это метод, при котором вместо удаления бляшки узкую артерию перенаправляют на другую коронарную артерию (5). Методика перенаправления узкой артерии — это трансплантация.Как и два других метода, аортокоронарное шунтирование улучшает приток крови к сердцу, снимает боль в груди и может предотвратить сердечный приступ.
Как и в случае с лекарствами, у этих методов атеросклеротической хирургии есть недостатки. Во-первых, не доказано, что стентирование помогает людям жить дольше (22). Аортокоронарное шунтирование, или АКШ, является лучшим методом лечения с точки зрения продления жизни пациента со многими проблемными закупорками (22). Однако АКШ — это процесс, на выполнение которого требуется время, что делает его не таким полезным, как стентирование, в ситуации неотложной помощи.Однако основная проблема возникает после хирургических вмешательств. Пациенту по-прежнему необходимо принимать лекарства после процедуры, чтобы предотвратить будущие случаи атеросклероза (22). Хирургия может решить проблемы, вызванные накоплением зубного налета, но ничего не может сделать для его предотвращения. Другими словами, эти типы операций предназначены для лечения проблемы, а не для ее предотвращения.
1.3 Последствия нанотехнологий
Определение нанотехнологии относится к изучению материалов при масштабах длины менее 100 нм (24).Для сравнения: эритроцит человека имеет средний диаметр 7 микрометров или 7000 нанометров (18). Нанотехнология имеет огромное значение для лечения атеросклероза из-за ее невероятно малых размеров. Его можно использовать для удаления бляшек, обнаружения или доставки лекарств. Когда нанотехнология защищает лекарство и доставляет его непосредственно к месту образования бляшки, это предотвращает накопление лекарства в областях здоровых тканей и предотвращает разложение лекарства до того, как оно достигнет целевого места (14).Это позволяет лекарству увеличивать его биологическую активность, что приводит к повышению эффективности лекарственного лечения (14). Кроме того, способность обнаруживать и отправлять лекарства в определенное место позволяет нанотехнологиям объединять терапевтические и диагностические методы в один агент (14). Еще одна потенциальная особенность нанотехнологии заключается в том, что ее можно использовать для помощи иммунной системе в борьбе с зубным налетом. В этой статье будет подробно рассмотрено текущее развитие нанотехнологий для лечения атеросклероза и возможные будущие тенденции.
Основной корпус
1.1 Введение в липосомы
Как обсуждалось во введении, преимуществом использования наночастиц для лечения атеросклероза является доставка лекарств. Но насколько эффективны нанотехнологии в повышении эффективности существующих лекарств? Давайте посмотрим на статины в качестве примера. Статины — это группа препаратов, которые действуют путем ингибирования 3-гидрокси-3-метилглутарил-кофермента А-редуктазы (2). Это делает статины идеальным решением для снижения количества ЛПНП в организме и предотвращения атеросклероза.Однако у статинов есть некоторые ограничения, которые делают их менее эффективным в лечении. Некоторые из его ограничений включают плохую растворимость в воде, низкое пероральное всасывание и ограниченную биодоступность при пероральном введении (2). В этой статье объясняется, что новая нанотехнология позволяет статинам иметь повышенную растворимость, абсорбцию и биодоступность (2). Это также позволяет контролировать высвобождение препарата в пораженные участки.
Одной из технологий, которые могут совершить этот подвиг, являются липосомы.Липосомы представляют собой пузырьки сферической формы, содержащие один или два фосфолипидных бислоя (23). Эта структура очень похожа на те, что находятся в клеточной мембране. Это дает липосомам возможность путешествовать по всему телу через кровоток и в то же время защищать то, что внутри них. Лекарство, такое как статин, можно инкапсулировать внутри липосомы, чтобы защитить ее от окружающей среды организма, прежде чем она достигнет целевого участка. Точно так же, как клеточные мембраны имеют разные белки и сахар, покрытые по всей своей поверхности, липосомы могут иметь разные рецепторы на внешнем липидном слое.Процесс, называемый пегилированием, может прикреплять полиэтиленгликоль к поверхности липосом, увеличивая время, в течение которого липосомы находятся в кровотоке, и шанс нацеливания на бляшки (1).
1.2 Присоединение антител к липосомам
Помимо присоединения полиэтиленгликоля, исследователям также удалось присоединить антитела к липосомам. Когда бляшка начинает накапливаться в артериях, эндотелий повреждается. Это, в свою очередь, заставляет его высвобождать определенные молекулы, которые могут помочь липосомам в его нацеливании (1).Эндотелий экспрессирует множество молекул клеточной адгезии, включая VCAM1, молекулу внутриклеточной адгезии 1, E-селектин, P-селектин, интегрин альфа V бета 3 и JAMS (1). Показано, что JAMS или соединительные адгезионные молекулы являются многообещающими, поскольку они помогают направлять воспалительные клетки к атеросклеротическому участку (1). Антитела против этих молекул могут быть прикреплены к липосомам и отправлены к участку бляшки. Липосомы не только смогут доставлять лекарства в целевой участок, но и посылать сигналы иммунной системе для дальнейшего уменьшения бляшек.Было исследовано, что липосомы с анти-VCAM-1, прикрепленными к поверхности, успешно накапливаются в месте поражения (1). Другое исследование показало, что липосомы с анти-ICAM-1 прочно связываются с эндотелиальными клетками (1). Ученые также обнаружили, что прикрепление антител против эселектина к липосомной поверхности заставляет липосомы накапливаться на эндотелиальных клетках, где были расположены атеросклеротические поражения (1).
Другой потенциальной мишенью, которую могут использовать липосомы, является рецептор ЛПНП-1 или LOX-1 (1).Причина в том, что этот рецептор вызывает активацию эндотелия после высвобождения воспалительных цитокинов из-за окислительного стресса (1). Когда это происходит, окисленные ЛПНП или плохой холестерин могут связываться с рецептором и, таким образом, в конечном итоге создавать бляшки в артерии. Ученые протестировали версию липосом, на поверхности которой было антитело против LOX-1, на мышах с дефицитом рецепторов ЛПНП (1). Результат этого исследования показал, что липосомы, вводимые внутривенно, успешно воздействуют на рецепторы LOX-1 у мышей.
1.3 Использование фосфатидилсерина для помощи макрофагам в нацеливании на бляшки
Помимо прикрепления антител к липосомам для запуска иммунного ответа, липосомы можно использовать для помощи макрофагам в нацеливании на бляшки. Молекула, известная как фосфатидилсерин (ФС), была обнаружена исследователями на поверхности апоптотических клеток и служит аттрактантом для макрофагов (1). Это означает, что если синтетическая версия фосфатидилсерина может быть изготовлена и внедрена на поверхность липосом, это приведет к усилению реакции макрофагов на участки бляшек.Ученые проверили надежность липосом, идущих к атеросклеротическим бляшкам, на кроликах с наследственной гиперлипидемией Ватанабе (1). Исследователи протестировали липосомы, используя метод in vitro и инкапсулируя In-нитрилотриуксусную кислоту в липосомы (1). In-нитрилотриуксусная кислота использовалась учеными для обнаружения липосом в теле кролика с помощью однофотонной эмиссионной компьютерной томографии или ОФЭКТ (1). Через 48 часов исследователи выполнили процедуру ОФЭКТ и обнаружили, что атеросклеротические области легко идентифицировать.Сообщалось, что размер липосом, которые использовались в этом эксперименте, составлял менее 100 нм, поскольку эти липосомы были предназначены для поглощения макрофагами, достигающими участка бляшки (1).
1.4 Транспортировка стволовых клеток с использованием липосом
Как обсуждалось во введении, общие методы восстановления атеросклеротического повреждения включают стентирование и АКШ. Однако проблема с этими хирургическими процедурами заключается в том, что они являются скорее реакционными, чем профилактическими. Предыдущие разделы показали, что липосомы очень надежны с точки зрения точного определения местоположения артериальных бляшек.Способ помочь восстановить зубной налет — это включение стволовых клеток. Преимущества использования стволовых клеток огромны, поскольку они могут дифференцироваться в клетки гладких мышц неоинтимы или эндотелиальные клетки, которые могут выполнять восстановление функции сосудов (1). Однако прямая инъекция стволовых клеток в место поражения привела к неутешительным терапевтическим результатам (1). При использовании прямой инъекции для применения стволовых клеток неточность и задержка процедуры лечения не отличаются от АКШ или стентирования.Во-первых, врачу необходимо знать, где располагается атеросклеротическая бляшка. Обычно это происходит, когда налет уже стал проблемой для пациента. Во-вторых, прямой впрыск может происходить не непосредственно в том месте, где находится зубной налет. Третья и последняя проблема заключается в том, что даже если зубной налет может быть решен в этой конкретной области, это не поможет решить проблему зубного налета, расположенного в другой области тела.
Оказывается, липосомы также можно превратить в носителей стволовых клеток.Как обсуждалось в предыдущем разделе, липосомы очень точно определяют, где расположены артериальные бляшки. Это решает текущую проблему прямого введения стволовых клеток в место поражения. Липосомы могут не только нести лекарства и антитела для уменьшения зубного налета, они также могут нести стволовые клетки для восстановления повреждений, вызванных зубным налетом. Кроме того, липосомы также могут обнаруживать и восстанавливать бляшки в областях, которые врачи не могут обнаружить.
Для этого липосомы должны включать два антитела, CD34 и ICAM-1.CD34 — это антиген, который будет использоваться на поверхности стволовых клеток, а ICAM-1 будет использоваться для навигации по зонам бляшек (1). Когда липосомы, содержащие стволовые клетки, достигают места бляшки, стволовые клетки высвобождаются с помощью техники сонопорации. Этот метод сонопорации включает непрерывную ультразвуковую волну с низкой амплитудой 1 МГц, которая разбивает пузырьки газа, зажатые между липидными бислоями липосомы (1). Это приведет к разрыву липосомы и позволит стволовым клеткам прикрепиться к поврежденной эндотелиальной стенке для выполнения ремонта.
2.1 Введение в углеродные нанотрубки
Нанотрубки из углерода находятся на переднем крае медицинских технологий. Углеродные нанотрубки, обычно созданные из углеводородных производных, таких как нефть и даже переработанный пластик, производятся и используются с 1960 года. Первое применение было в авиационных двигателях, но по мере развития технологии углеродное волокно стало применяться в медицинских технологиях. . Углеродные нанотрубки были идеальным механизмом для восстановления, роста и структурной поддержки тканей, от протезирования до доставки лекарств.
Углеродные нанотрубки относительно тонкие. Они растут по форме типа бакибола толщиной в один атом углерода. Их можно выращивать в лаборатории и, при необходимости, стерилизовать для медицинских целей. По словам Джона Майерса, углеродные нанотрубки меньше углеродных волокон, потому что они сделаны из углерода на молекулярном уровне и имеют толщину менее двух нанометров (7). Это делает углеродные нанотрубки идеальными для доставки лекарств и тканевой терапии.
2.2 Применение углеродных нанотрубок
В недавнем исследовании, проведенном в 2017 году, исследователи обнаружили, что углеродные нанотрубки могут помочь в терапии сердечно-сосудистых тканей.При использовании в качестве «улучшающих матрицу добавок к хитозану, коллагену, полилактиду и т. Д.» нанотрубки привели к тому, что было описано как «механически усиленный каркас для роста мягких тканей и конструкций ткани скелетных мышц (8)». Это революционное открытие находится в разработке с 2012 года и началось с выращивания кардиомиоцитов на структурах, называемых каркасами из углеродных наноматериалов. Когда исходные структуры роста, в основном желатин, были усилены углеродными наноструктурами, исследователи обнаружили новые преимущества, такие как усиленный рост клеток и свойства растущей ткани кардиомиоцитов.
Доставка лекарств — одно из важнейших применений углеродных нанотрубок. Доказано, что углеродные нанотрубки помогают лечить и диагностировать атеросклероз и создаются путем сворачивания листов графена. Лекарства и терапевтические средства прикрепляются либо к внешней, либо к внутренней части пробирки, а затем высвобождаются в целевой участок (13). В одном исследовании углеродные нанотрубки использовались для доставки лекарства, которое стимулирует макрофаги в атеросклеротической бляшке. Было замечено, что стимулированные макрофаги нацелены на мертвые и умирающие клетки, ответственные за атеросклероз, и разрушают их (21).Нанотрубки были настолько эффективны, что при проведении тестов на мышах было замечено, что макрофаги нацелены только на мертвые и умирающие клетки, оставляя только здоровые клетки.
Углеродные нанотрубки могут помочь в визуализации сердечно-сосудистой ткани. В исследовании, проведенном учеными, было успешно визуализировано сердце трупа мыши. Использование углеродных нанотрубок уменьшило необходимое количество излучения источника рентгеновского излучения. Это означает, что использование углеродных нанотрубок для визуализации сердечно-сосудистой ткани оказалось более безопасным и эффективным, чем использование без углеродных нанотрубок (11).Согласно исследованию, опубликованному в Журнале Американской кардиологической ассоциации, углеродные нанотрубки оказались успешными в другом типе визуализации, называемом флуоресцентной визуализацией, и использовались в процедуре лечения рака, называемой фототермической абляцией. Автор Хисанори Косуге утверждает, что «углеродные нанотрубки являются многообещающими« тераностическими »агентами при воспалении сосудов и атеросклерозе (15)».
В обширном обзоре доставки лекарств с помощью углеродных нанотрубок был сделан вывод, что одностенные углеродные нанотрубки вызвали большой интерес в области медицинских исследований из-за их небольшого размера, стабильной структуры и неполярной природы.(17). Структура нанотрубок доказала свою эффективность при переносе лекарств через клеточные мембраны и при переносе больших доз лекарств.
2.3 Недостатки углеродных нанотрубок
Существуют потенциальные опасности использования углеродных нанотрубок для доставки лекарств и терапии. При вдыхании нанотрубки могут напрямую транспортироваться кровотоком в удаленные органы. Это опасно, поскольку доставка лекарств с использованием однослойных и многослойных углеродных нанотрубок потенциально может вызвать доставку лекарств в неправильную область, вызывая фатальные побочные эффекты.Сами нанотрубки также могут быть токсичными для сердечно-сосудистой ткани, на которую они не должны влиять. Побочные эффекты как однослойных, так и многостенных нанотрубок напрямую не изучаются, поэтому их необходимо учитывать перед использованием при лечении сердечно-сосудистых заболеваний у людей. Исследование воздействия многостенных углеродных нанотрубок на пупочную ткань человека показало отрицательные признаки. Эти негативные признаки включают снижение выживаемости клеток, повреждение ДНК и увеличение количества активных форм кислорода. Еще одна возникшая проблема — отрицательные результаты лечения атеросклероза.Исследование показало, что использование многостенных нанотрубок требует дополнительных исследований при лечении атеросклероза, поскольку отрицательные результаты более чем вероятны (12).
Заключение
Липосомы могут решить множество проблем, вызванных атеросклерозом. Компоненты липосомы относительно просты и состоят из сферического липидного бислоя. Этот липидный бислой очень похож на те, что находятся в клеточных мембранах, что позволяет липосомам хорошо переноситься по телу человека.Липосомы также могут служить в качестве носителя для лекарств, уменьшающих образование зубного налета, и стволовых клеток, способствующих восстановлению. Он также может содержать антитела, включенные в липидный бислой, что обеспечивает точную навигацию и обнаружение бляшек. Все эти причины делают липосомы очень многообещающей разработкой нанотехнологий для обнаружения и лечения атеросклероза.
Углеродные нанотрубки стали удивительным прорывом в области медицины, от протезов из углеродных волокон до трубок для транспортировки лекарств в форме кресла.Фуллерены или углеродные нанотрубки очень помогли в экспериментальной терапии рака, а теперь и атеросклероза. Исследования углеродных нанотрубок показали многообещающие результаты и доказали, что они эффективно доставляют лекарства подопытным мышам. Когда препараты, устраняющие атеросклероз, были прикреплены и отправлены испытуемым, лекарство было эффективным в стимуляции макрофагов организма, которые, в свою очередь, начали устранять накопление атеросклеротических бляшек и мертвые клетки.
Нацеливание и лечение пораженных тканей и удаление закупорки бляшек были прямой проблемой для исследований наночастиц при лечении атеросклероза.Нанотехнологические исследования доказали огромную полезность частиц в кардиоторакальном применении. От доставки лекарств до усиления иммунного ответа — нанотехнологии дали медицинским работникам и пациентам новую надежду на будущее.
Тенденции будущего
Металлические наночастицы и углеродные нанотрубки — две очень футуристические технологии, которые разрабатываются для использования в самом ближайшем будущем. Обнаруживаются и тестируются новые молекулярные структуры для прикрепления частиц и трубок.Эти структуры, которые в настоящее время проходят испытания, гораздо менее токсичны и более биосовместимы. У них также есть возможность точно нацелить все, на что нужно нацеливаться (6). Большинство исследований и разработок в области наноматериалов было направлено на лечение рака, поскольку это серьезный насущный вопрос. Однако исследования с использованием нанотрубок доказали свою эффективность не только в отношении рака. Лечение атеросклероза — одна из таких развивающихся областей, в которой нанотрубки добились большого успеха. Углеродные нанотрубки обычно использовались в их одностенном состоянии для доставки лекарств, но были синтезированы новые многостенные нанотрубки, которые показали себя многообещающими в этой области.Единственная проблема заключается в том, что недостаточно испытаний и исследований побочных эффектов как углеродных нанотрубок, так и металлических наночастиц. К сожалению, небольшое количество исследований позволило понять вредные эффекты при неправильном использовании. Еще одна развивающаяся область наноматериалов в медицине — вакцины. Наноматериал на основе полимера показал себя многообещающим в области доставки лекарств, и, согласно исследованию, наночастицы с низкой цитотоксичностью могут защищать антигены разлагающей среды в нашем организме, что приводит к более высокой эффективности поглощения (16).
Углеродные нанотрубки недавно стали известны из-за их потенциала в качестве наномоторов в доставке лекарств и для транспортировки молекул ферментов в организме (10). Текущие исследования экспериментируют с различными комбинациями лекарств и трубок, чтобы увидеть, какая комбинация является наиболее эффективной и наименее разрушительной. Наномоторы могут использоваться в сочетании с другими нанотехнологиями, такими как наночастицы, чтобы иметь возможность управлять с помощью магнетизма, чтобы транспортировать и перемещать материалы туда, куда они должны попасть в теле (25).
Еще одно разрабатываемое применение наночастиц золота — лучевая терапия. Еще одно приложение для лечения рака, наночастицы золота применялись с традиционной лучевой терапией, которая потенциально может повысить вероятность того, что терапия будет направлена и разрушит больную ткань, а не здоровую ткань (20).
Несмотря на то, что липосомы многообещают с точки зрения уменьшения образования атеросклеротических бляшек, их практическое применение имеет ряд недостатков.Кровоток в артериях имеет тенденцию прикладывать напряжение сдвига к эндотелиальной стенке (1). Когда это происходит, наночастицы могут быть смыты с целевого участка. Кроме того, сдвигающее действие кровотока сокращает время взаимодействия между целевой бляшкой и частицами. В настоящее время ученые работают над липосомными составами, которые будут надежно высвобождать свой груз или полезную нагрузку в месте налета, несмотря на повышенное напряжение сдвига, вызванное аномальным кровотоком (1).
Было показано, что использование стволовых клеток для лечения атеросклеротических бляшек является эффективным лечением в сочетании с липосомами. Стволовые клетки можно извлекать из детей или взрослых. Но с возрастом количество стволовых клеток в разных тканях может уменьшаться в 100–10 000 раз (19). Другая проблема заключается в том, что более старые стволовые клетки подвергаются генетической мутации, которая снижает их эффективность в восстановлении вашего тела (19). На данный момент ученые предлагают использовать остатки плаценты и пуповины после рождения ребенка в качестве ресурса стволовых клеток (19).Плацента и пуповина — богатые ресурсы стволовых клеток, которые не подверглись генетическим изменениям. Многие ученые и компании заинтересованы в этом потенциальном предложении, особенно когда ожидается, что к этому году индустрия стволовых клеток вырастет до 170 миллиардов долларов (19).
Список литературы
- «Новый подход к диагностике и лечению атеросклероза: эра липосом». Эльзевье, https://www.sciencedirect.com/science/article/pii/S1359644619303496. Проверено 18 апреля.2020.
- «Применение нанотехнологий для улучшения терапевтических свойств статинов». Эльзевье, https://www.sciencedirect.com/science/article/pii/S1359644618303246. По состоянию на 16 апреля 2020 г.
- «Применение нанотехнологий к атеросклерозу, тромбозу и биологии сосудов». Атеросклероз, тромбоз и сосудистая биология, https://www.ahajournals.org/doi/full/10.1161/01.atv.0000201069.47550.8b. Доступ 3, 2020.
- «Атеросклероз и ишемическая болезнь сердца.”WebMD, https://www.webmd.com/heart-discount / atherosclerosis-and-coronary-artery-болезнь. По состоянию на 10 апреля 2020 г.
- «Атеросклероз». Сосудистая и эндоваскулярная хирургия, https://vascularsurgery.ucsf.edu/conditions—procedures/atherosclerosis.aspx. Доступ 15 апреля 2020 г.
- «Технология биомиметических наночастиц для обнаружения и лечения сердечно-сосудистых заболеваний». Наноразмерные горизонты, https://pubs.rsc.org/en/content/articlelanding/2020/nh/c9nh00291j#! DivAbstract. Доступ 3 апреля 2020 г.
- «Углеродное волокно и углеродные нанотрубки». Салем Пресс, http://eds.a.ebscohost.com.ezproxy.lib.usf.edu/eds/detail/detail?vid=1&sid=76353062- 0f8e-4c51-92b6-f87f36c65d% 40sdc-v- sessmgr03 & bdata = JnNpdzLU9ZpW % 3d # AN = 89474598 & db = ers По состоянию на 18 апреля 2020 г.
- «Каркасы, усиленные углеродным наноматериалом, для создания конструкций сердечной ткани: новый рубеж в инженерии сердечной ткани», Химический факультет и Институт нанотехнологий Ватерлоо, https: // www-sciencedirectcom.ezproxy.lib.usf.edu/science/article/pii/S0008622317304980. По состоянию на 18 апреля 2020 г.
- «Лекарства для лечения атеросклероза». WebMD, https://www.webmd.com/cholesterol- management / medications-to-treatment-atherosclerosis. По состоянию на 11 апреля 2020 г.
- «Изучение конфигурации заряда кресельной однослойной углеродной нанотрубки для доставки лекарств» Материалы сегодня https: // www-sciencedirect- com.ezproxy.lib.usf.edu/science/article/pii/S2214785320306416. Принята 19 апреля 2020 г.
- «Внутренняя томографическая визуализация сердца мыши в микро-КТ из углеродных нанотрубок» Журнал рентгеновской науки и технологий http: // eds.a.ebscohost.com.ezproxy.lib.usf.edu/eds/detail/detail?vid=0&sid=b032c363- e7c6-4177-bdd3-a795a6078670% 40sdc-v- sessmgr03 & bdata =% adc-v- sessmgr03 & bdata =% a3dGU9Zpdbd = 1100x1dx6dx06dx6db = 1 Проверено 19 апреля 2020 г.
- «Внутривенное введение многослойных углеродных нанотрубок влияет на формирование атеросклероза у крыс Sprague-Dawley», журнал по гигиене труда https://www.jstage.jst.go.jp/article/joh/54/5/54_12-0019 -OA / _html / -char / ru. По состоянию на 19 апреля 2020 г.
- «Система доставки лекарств, опосредованная наночастицами, при атеросклеротическом сердечно-сосудистом заболевании» Кардиологический журнал https: // www.sciencedirect.com/science/article/pii/S08717300928 По состоянию на 19 апреля 2020 г.
- «Нанотехнологии для приложений доставки лекарств». AzoNano, https://www.azonano.com/article.aspx?ArticleID=4668. По состоянию на 14 апреля 2020 г.
- Журнал Американской кардиологической ассоциации «Визуализация в ближнем инфракрасном диапазоне и фототермическая абляция воспаления сосудов с использованием одностенных углеродных нанотрубок» https://www.ahajournals.org/doi/10.1161/JAHA.112.002568 Доступ 19 апреля 2020 г.
- «Наноматериалы на основе полимеров и применение в вакцинах и лекарствах» Полимеры https: // www.mdpi.com/2073-4360/10/1/31/htm По состоянию на 19 апреля 2020 г.
- «Прогнозирование доставки лекарственного средства доксорубицина с помощью однослойной углеродной нанотрубки через клеточную мембрану в отсутствие и в присутствии молекул никотина: исследование с помощью моделирования динамики молекул https: // www-tandfonline- com.ezproxy.lib.usf.edu/doi/pdf /10.1080/073.2019.1611474 Доступ 19 апреля 2020 г.
- «Изменение размера красных кровяных телец (эритроцитов)». LabCE, https://www.labce.com/spg579126_red_blood_cell_rbc_size_variation.aspx. По состоянию на 16 апреля 2020 г.
- «Стволовые клетки способны навсегда изменить здоровье и медицину». SingularityHub, https://singularityhub.com/2017/01/17/stem-cells-are-poised-to-change-health-and- Medicine-forever /. По состоянию на 19 апреля 2020 г.
- «Нацеленная лучевая терапия с наночастицами золота: текущее состояние и перспективы на будущее». Медицина будущего https://www.futuremedicine.com/doi/abs/10.2217/nnm.14.55 Доступ 19 апреля 2020 г.
- «Нацеленность на ядро атеросклероза» Американская ассоциация содействия развитию науки https: // science.sciencemag.org/content/367/6480/865.2 По состоянию на 19 апреля 2020 г.
- «Лечение атеросклероза на поздних стадиях». WebMD, https://www.webmd.com/cholesterol- management / treatment-for-advanced-atherosclerosis. Доступ 15 апреля 2020 г.
- «Что такое липосома?» Новости медицинских наук о жизни, https://www.news-medical.net/life- Sciences / What-is-a-Liposome.aspx. Доступ 17 апреля 2020 г.
- «Что такое нанотехнологии?» Nanowerk, https://www.nanowerk.com/nanotechnology/introduction/introduction_to_nanotechnolog y_1.php. По состоянию на 14 апреля 2020 г.