Дифференциальная диагностика и лечение сахарного диабета на фоне болезни Иценко-Кушинга | Дзеранова
Введение
Эндогенный гиперкортицизм – клинический синдром, развивающийся в результате воздействия на организм большого количества глюкокортикоидов. Чаще избыточная секреция этих гормонов надпочечниками обусловлена гиперпродукцией АКТГ передней долей гипофиза (болезнь Иценко-Кушинга). Однако заболевание может развиваться вследствие первичного поражения надпочечников (кортикостерома, гиперплазия коры надпочечников – синдром Иценко-Кушинга), наличия АКТГ- или кортиколиберинпродуцирующей нейроэндокринной опухоли. Иногда клинически схожие симптомы проявляются при особых физиологических и патологических состояниях организма (псевдокушингоидный синдром), таких как беременность, заболевания печени, алкоголизм, метаболический синдром, декомпенсированный сахарный диабет, что требует проведения тщательной дифференциальной диагностики [1].
Болезнь Иценко-Кушинга – довольно редкое, но тяжелое по течению заболевание, сопровождающееся развитием метаболических, кардиоваскулярных, когнитивных и психологических нарушений [2, 3]. Сахарный диабет (СД) – одно из наиболее часто встречающихся осложнений гиперкортицизма (от 20 до 50% пациентов), нарушение толерантности к глюкозе встречается практически у 70% пациентов. Основными причинами возникновения гипергликемии являются активация под действием глюкокортикоидов ключевых ферментов глюконеогенеза в печени и усиление инсулинорезистентности вследствие нарушения передачи сигнального пути рецептора инсулина, активации липолиза и протеолиза. Возраст, генетическая предрасположенность и образ жизни также играют значительную роль в развитии нарушений углеводного обмена у пациентов с гиперкортизолемией [4].
Сахарный диабет (СД) – одно из наиболее часто встречающихся осложнений гиперкортицизма (от 20 до 50% пациентов), нарушение толерантности к глюкозе встречается практически у 70% пациентов. Основными причинами возникновения гипергликемии являются активация под действием глюкокортикоидов ключевых ферментов глюконеогенеза в печени и усиление инсулинорезистентности вследствие нарушения передачи сигнального пути рецептора инсулина, активации липолиза и протеолиза. Возраст, генетическая предрасположенность и образ жизни также играют значительную роль в развитии нарушений углеводного обмена у пациентов с гиперкортизолемией [4].
Оптимальным видом лечения болезни Иценко-Кушинга является нейрохирургическая операция (трансназальная аденомэктомия) [5]. Тем не менее, осложнения гиперкортизолемии, особенно длительной, могут не получить обратного развития после достижения ремиссии основного заболевания [6, 7].
Представляем клинический случай пациентки с тяжелым СД на фоне торпидного течения болезни Иценко-Кушинга в течение 11 лет.
Описание клинического случая
Пациентка М., 56 лет поступила в отделение нейроэндокринологии и остеопатий ФГБУ «Эндо кри но ло гический научный центр» Минздрава России в сентябре 2016 г. с жалобами на нестабильные цифры гликемии, максимально до 18–20 ммоль/л, покалывание, онемение и сильную слабость верхних и нижних конечностей, боли в поясничной области при физической нагрузке, снижение остроты зрения, частое повышение АД до 170/100 мм рт. ст., увеличение массы тела на 8–10 кг за последние 6 мес, несмотря на регулярную активную физическую нагрузку.
Из анамнеза известно, что в 2004 г. при наличии гипергликемии натощак и выраженных отеков нижних конечностей диагностирован СД 2 типа, назначена сахароснижающая терапия препаратами гликлазида и метформина. Наследственный анамнез отягощен по (у матери и бабушки по линии матери).
В мае 2005 г. при обследовании в ЭНЦ у пациентки было выявлено нарушение ритма секреции АКТГ и кортизола в сочетании с отрицательным результатом малой и положительным результатом большой дексаметазоновых проб. По результатам МРТ головного мозга обнаружена микроаденома гипофиза размерами 6×9×8 мм, по данным МСКТ брюшной полости – признаки узелковой гиперплазии правого надпочечника. Была диагностирована болезнь Иценко-Кушинга средней степени тяжести, назначена терапия блокаторами стероидогенеза (кетоконазол) с рекомендацией проведения трансназальной аденомэктомии через 6 мес после стабилизации показателей углеводного обмена.
По результатам МРТ головного мозга обнаружена микроаденома гипофиза размерами 6×9×8 мм, по данным МСКТ брюшной полости – признаки узелковой гиперплазии правого надпочечника. Была диагностирована болезнь Иценко-Кушинга средней степени тяжести, назначена терапия блокаторами стероидогенеза (кетоконазол) с рекомендацией проведения трансназальной аденомэктомии через 6 мес после стабилизации показателей углеводного обмена.
При повторной госпитализации в ЭНЦ в октябре 2005 г. после комплексного обследования на фоне отмены приема кетоконазола убедительных данных за гормональную активность аденомы гипофиза не получено. По решению врачебного консилиума, с учетом периодического повышения уровня АКТГ в анамнезе, был назначен каберголин (Достинекс) 0,25 мг 2 раза в неделю в течение 6 мес с последующим контролем гормонального статуса. Через полгода терапия каберголином самостоятельно прекращена пациенткой. Со слов больной, самочувствие оставалось удовлетворительным. С 2008 по 2014 гг. была отменена и сахароснижающая терапии, наблюдение у специалистов не проводилось.
В 2014 г. в связи с резким ухудшением общего состояния, появлением трофических язв на коже нижних конечностей, выраженных отеков нижних конечностей, повышением уровня АД и значительной гипергликемией был возобновлен прием метформина и глибенкламида. В феврале 2016 г. к лечению добавлена инсулинотерапия препаратом гларгина (Лантус). По предоставленным медицинским данным на протяжении последних нескольких лет периодически регистрируется повышенный уровень АКТГ при концентрации кортизола крови и суточной мочи в пределах референсных значений. По данным рентгеновской денситометрии клинически значимого снижения минеральной плотности кости не выявлено.
При объективном осмотре (см. рис.1) в сентябре 2016 г. отмечалось гиперстеническое телосложение, вес 98 кг, рост 165 см, ИМТ 36,0 кг/м2. Кожные покровы чистые, умеренной влажности, на коже живота – широкие стрии белого цвета. Подкожная жировая клетчатка была распределена по абдоминальному типу, с избыточным отложением в области груди и живота. Климактерический горбик отсутствовал. Кожа стоп сухая, на правой конечности в пяточной области определяется участок гиперемии и гиперкератоза, на медиальной поверхности голени участки гиперпигментации. Отмечено умеренное ограничение подвижности в суставах нижних конечностей, в области голеней и стоп – плотные отеки. Щитовидная железа не увеличена. ЧСС 100 уд. в минуту АД 160/110 мм рт. ст. Тоны сердца приглушены, акцент 2 тона над аортой. Дыхание везикулярное, хрипы не выслушиваются. Живот при поверхностной пальпации мягкий, безболезненный, печень и селезенка не определялись. Симптом поколачивания по пояснице отрицательный с двух сторон.
Климактерический горбик отсутствовал. Кожа стоп сухая, на правой конечности в пяточной области определяется участок гиперемии и гиперкератоза, на медиальной поверхности голени участки гиперпигментации. Отмечено умеренное ограничение подвижности в суставах нижних конечностей, в области голеней и стоп – плотные отеки. Щитовидная железа не увеличена. ЧСС 100 уд. в минуту АД 160/110 мм рт. ст. Тоны сердца приглушены, акцент 2 тона над аортой. Дыхание везикулярное, хрипы не выслушиваются. Живот при поверхностной пальпации мягкий, безболезненный, печень и селезенка не определялись. Симптом поколачивания по пояснице отрицательный с двух сторон.
Рис. 1. Внешний вид пациентки до оперативного лечения.
В ходе обследования были выявлены лабораторные признаки эндогенного АКТГ-зависимого гиперкортицизма (табл. 1). По результатам МРТ головного мозга – картина эндоселлярной макроаденомы гипофиза размерами 7×12×9 мм (рис. 2).
Таблица 1. Данные гормонального исследования до оперативного лечения
Показатели | Значения | Единицы измерения | Референсные значения |
Кортизол (слюна, вечер) | 18,55 | нмоль/л | 0,5–9,4 |
Кортизол (кровь, вечер) | 730,4 | нмоль/л | 46–270 |
АКТГ (вечер) | 82,45 | пг/мл | 0–30 |
Кортизол св. | 1502,08 | нмоль/сут | 60–413 |
Рис. 2. Данные МР-исследования головного мозга до оперативного лечения.
Помимо этого, у пациентки была выявлена гиперхолестеринемия до 6,0 ммоль/л, гипергликемия натощак до 8,6 ммоль/л, после еды до 14,4 ммоль/л. Уровень гликированного гемоглобина 9,1%. Проводилась трехкомпонентная гипотензивная терапия (БКК + бета-блокаторы + ингибиторы АПФ), интенсифицированная инсулинотерапия препаратами ультракороткого и пролонгированного действия в сочетании с приемом метформина, произведена коррекция питания.
В октябре 2016 г. выполнено трансназальное удаление эндо-инфраселлярной аденомы гипофиза. По данным гистологического исследования операционного материала, обнаружены фрагменты аденомы гипофиза из базофильных клеток. Ранний послеоперационный период протекал без осложнений, признаков надпочечниковой недостаточности выявлено не было (на 1-е сутки после операции уровень АКТГ утром 58,7 пг/мл, кортизол крови утром 1013 нмоль/л, на 4-е сутки – АКТГ утром 55,3 пг/мл, кортизол крови утром 267 нмоль/л). При лабораторном исследовании на 5-е сутки после оперативного вмешательства выявлено повышение уровня АКТГ вечером до 44,5 пг/мл, уровни кортизола крови вечером 121,8 нмоль/л, вечерней слюны 3,5 нмоль/л. Уровни гликемии сохранялись повышенными натощак до 10 ммоль/л, после еды до 14,9 ммоль/л на интенсифицированной инсулинотерапии. Полученные данные свидетельствовали об отсутствии гипокортицизма, являющегося несомненным показателем радикально проведенного лечения.
При лабораторном исследовании на 5-е сутки после оперативного вмешательства выявлено повышение уровня АКТГ вечером до 44,5 пг/мл, уровни кортизола крови вечером 121,8 нмоль/л, вечерней слюны 3,5 нмоль/л. Уровни гликемии сохранялись повышенными натощак до 10 ммоль/л, после еды до 14,9 ммоль/л на интенсифицированной инсулинотерапии. Полученные данные свидетельствовали об отсутствии гипокортицизма, являющегося несомненным показателем радикально проведенного лечения.
Тем не менее, на 7–8-е сутки после трансназальной аденомэктомии при контрольном обследовании выявлены клинические и лабораторные признаки вторичной надпочечниковой недостаточности (табл. 2). АД стабилизировано в пределах 110–130/70–80 мм рт. ст. на фоне полной отмены гипотензивной терапии.
Таблица 2. Динамика гормональных показателей после трансназальной аденомэктомии
Показатели | Референсные значения | До операции | 1-е сутки | 4-е сутки | 5-е сутки | 6-е сутки | 7-е сутки |
АКТГ, утро (пг/мл) | 7–66 | 58,72 | 55,3 | ||||
АКТГ, вечер (пг/мл) | 0–30 | 82,45 | 44,45 | ||||
Кортизол крови, утро (нмоль/л) | 123–626 | 1013 | 267 | 28,92 | |||
Кортизол крови, вечер (нмоль/л) | 46–270 | 730,4 | 121,8 | ||||
Кортизол слюны, вечер (нмоль/л) | 0,5–9,4 | 18,55 | 3,53 | ||||
Кортизол св, сут, мочи (нмоль/сут) | 60–413 | 1502,08 | 30 |
Пациентка была выписана в удовлетворительном состоянии с рекомендациями о динамическом наблюдении и обследовании через 6 мес, назначена заместительная терапия препаратом гидрокортизона ацетата (Кортеф) в дозе 25 мг/сут, интенсифицированная инсулинотерапия препаратами ультракороткого и пролонгированного действия в сочетании с метформином.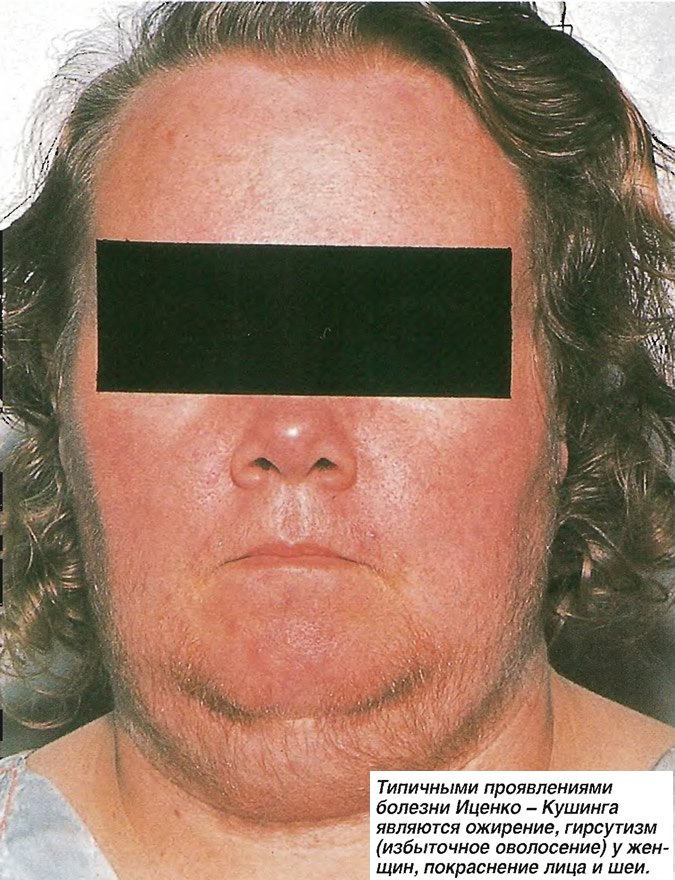
В апреле 2017 г. пациентка была госпитализирована в ФГБУ ЭНЦ Минздрава России для исключения рецидива заболевания и оценки эффективности проводимой терапии. Сохранялись жалобы на слабость в проксимальных мышцах нижних конечностей, парестезии пальцев верхних и нижних конечностей. Объективно отмечена положительная динамика массы тела (вес 95 кг, рост 165 см, ИМТ 34,9 кг/м2). Подкожно жировая клетчатка была развита избыточно, однако распределена относительно равномерно, матронизм отсутствует, периферических отеков нет (рис. 3). При поступлении обращало на себя внимание повышение АД до 160/110 мм рт. ст., несмотря на самостоятельное возобновление антигипертензивной терапии эналаприлом 20 мг/сут. Показатели гликемии на фоне комбинированного лечения метформином и препаратами инсулина ультракороткого и пролонгированного действия в пределах 6,0–10,0 ммоль/л.
Рис. 3. Внешний вид пациентки через 6 месяцев после оперативного лечения.
По результатам проведенного гормонального обследования данных за рецидив эндогенного гиперкортицизма не получено (уровень кортизола крови утром на фоне приема 25 мг/сут гидрокортизона ацетата 163,5 нмоль/л). Достоверных признаков наличия аденомы гипофиза согласно МР-картине не выявлено (рис 4).
Достоверных признаков наличия аденомы гипофиза согласно МР-картине не выявлено (рис 4).
Рис. 4. Данные МР-исследования головного мозга через 6 месяцев после оперативного лечения.
Однако показатели липидного обмена находились выше целевых значений (общий холестерин 5,12 ммоль/л, ЛПНП 3,0 ммоль/л). По данным рентгенологических методов исследования выявлен остеопороз грудного и пояснично-крестцового отделов позвоночника, максимальное снижение минеральной плотности кости -2,5 SD по Т-критерию в L1, артроз суставов нижних конечностей.
В связи с наличием артериальной гипертензии, гипергликемии была проведена коррекция глюкокортикоидной терапии: доза гидрокортизона ацетата (Кортеф) уменьшена до 15 мг/сут. При попытке полной отмены приема препарата было отмечено ухудшение общего самочувствия больной в виде общей слабости и утомляемости, получены неудовлетворительные показатели свободного кортизола суточной мочи (58 нмоль/сут), в связи с чем принято решение о необходимости постоянной заместительной терапии в скорректированной дозе.
Принимая во внимание высокие показатели АД пациентки, была возобновлена трехкомпонентная антигипертензивная терапия (БКК + бета-блокаторы + ингибиторы АПФ), инициирован прием статинов. При достижении стабильных уровней гликемии на фоне соблюдения принципов диетического питания был произведен переход на пероральную сахароснижающую терапию с использованием метформина в дозе 2000 мг/сут, ингибитора ДПП-4 (саксаглиптин) и ингибитора натрий-глюкозного ко-транспортера 2 типа (дапаглифлозин) в сочетании с введением инсулина пролонгированного действия – гларгина (Лантус). На фоне лечения достигнуты целевые значения АД (130–140/70–80 мм рт. ст.) и глюкозы крови (5,0–8,0 ммоль/л).
Обсуждение
Представленный клинический случай иллюстрирует вялотекущий, «тлеющий» гиперкортицизм с длительным периодом (до нескольких лет) относительно удовлетворительного самочувствия пациентки. Сложность распознавания подобного состояния была обусловлена наличием декомпенсированного СД с множественными осложнениями (непролиферативная ретинопатия, диабетическая нефропатия, диабетическая дистальная периферическая полинейропатия, периферическая ангиопатия нижних конечностей), что потребовало проведения дифференциальной диагностики с псевдокушингоидным синдромом. Нарушение углеводного обмена могло иметь как вторичный вследствие гиперкортицизма, так и первичный характер, когда болезнь Иценко-Кушинга внесла вклад в усиление тяжести ранее развившегося диабета. Разграничение органического и функционального гиперкортицизма представляет собой непростую задачу и крайне необходимо, так как раннее выявление и правильно выбранная тактика лечения позволяют предотвратить развитие тяжелых осложнений этих эндокринных заболеваний.
Нарушение углеводного обмена могло иметь как вторичный вследствие гиперкортицизма, так и первичный характер, когда болезнь Иценко-Кушинга внесла вклад в усиление тяжести ранее развившегося диабета. Разграничение органического и функционального гиперкортицизма представляет собой непростую задачу и крайне необходимо, так как раннее выявление и правильно выбранная тактика лечения позволяют предотвратить развитие тяжелых осложнений этих эндокринных заболеваний.
В приведенном примере составляющие метаболического синдрома (артериальная гипертензия, дислипидемия, ожирение, сахарный диабет) не получили обратного развития после устранения гиперкортизолемии. Несмотря на недостаточность функции надпочечников в послеоперационном периоде ни показатели гликемии, ни уровень АД не достигли целевых значений, что потребовало модификации проводимой терапии. Это согласуется с данными зарубежных исследований, по результатам которых только 0,9% прооперированных пациентов с болезнью Иценко-Кушинга и ассоциированным с ней диабетом достигли значительного улучшения контроля гликемии, снижения массы тела и уровня АД [8].
Как известно, больные СД имеют высокий риск развития сердечно-сосудистых осложнений. Сопутствующая артериальная гипертензия дополнительно увеличивает вероятность неблагоприятных кардиоваскулярных событий в несколько раз.
В последнее время активно разрабатываются лекарственные препараты, не только эффективно снижающие уровень глюкозы крови, но и обладающие прямым протективным действием на органы-мишени. Одними из них являются ингибиторы дипептидилпептидазы 4 (иДПП-4). Основной механизм действия глиптинов заключается в препятствии быстрой деградации инкретиновых гормонов, таких как глюкагоноподобный пептид 1 (ГПП-1) и гастроинтестинальный пептид (ГИП), а также других цитокинов, хемокинов, нейропептидов, ростовых факторов, участвующих в различных патофизиологических процессах. Повышение плазменной концентрации ГПП-1 способствует секреции инсулина бета-клетками поджелудочной железы и подавляет выделение глюкагона альфа-клетками, дополнительными эффектами являются замедление опорожнения желудка, усиление чувства насыщения. Посредством влияния через различные сигнальные пути иДПП-4 оказывают цитопротективное действие на печень, почки, сердце, нервную систему, сетчатку глаза. Недавние разработки продемонстрировали возможность использования иДПП-4 в лечении сопутствующей сердечно-сосудистой патологии при СД. Так, in vitro и в преклинических исследованиях показано, что глиптины способствуют регенерации эндотелия в поврежденных сосудах, коррекции дислипидемии, препятствуют развитию атеросклероза [9, 10].
Посредством влияния через различные сигнальные пути иДПП-4 оказывают цитопротективное действие на печень, почки, сердце, нервную систему, сетчатку глаза. Недавние разработки продемонстрировали возможность использования иДПП-4 в лечении сопутствующей сердечно-сосудистой патологии при СД. Так, in vitro и в преклинических исследованиях показано, что глиптины способствуют регенерации эндотелия в поврежденных сосудах, коррекции дислипидемии, препятствуют развитию атеросклероза [9, 10].
Другая недавно одобренная группа лекарственных средств – ингибиторы натрий-глюкозного ко-транс пор тера 2 типа. Наличие кардио-, вазопротективных и гипотензивных эффектов в дополнение к выраженному гипогликемическому действию делает их препаратами выбора у значительного числа пациентов. Блокируя реабсорбцию глюкозы в проксимальных почечных канальцах, они приводят к дефициту калорий, снижению веса, уменьшению абдоминальной и общей подкожно-жировой клетчатки, кровяного давления и риска сердечно-сосудистых осложнений [11]. Таким образом, не случайно саксаглиптин и дапаглифлозин составили основу терапии данной пациентки. Комбинация препаратов с метформином в максимальной дозировке, способствующим снижению инсулинорезистентности, дает надежду на отмену инсулинотерапии и повышение качества жизни больной.
Таким образом, не случайно саксаглиптин и дапаглифлозин составили основу терапии данной пациентки. Комбинация препаратов с метформином в максимальной дозировке, способствующим снижению инсулинорезистентности, дает надежду на отмену инсулинотерапии и повышение качества жизни больной.
Заключение
Болезнь Иценко-Кушинга и СД 2 типа порой имеют схожую клиническую картину, что затрудняет своевременную диагностику эндогенного гиперкортицизма. Наличие нарушений углеводного обмена, особенно в сочетании с другими проявлениями данного нейроэндокринного заболевания, такими как диспластическое ожирение, плохо контролируемая артериальная гипертензия и др., диктует необходимость исключения его вторичного характера. В свою очередь, достижение удовлетворительного послеоперационного результата в отношении кортикотропиномы не всегда приводит к регрессу сформировавшихся осложнений. Отсутствие нормализации показателей гликемии, липидного обмена, артериального давления ставит пациентов в группу высокого риска по развитию сердечно-сосудистых осложнений в дальнейшем и диктует необходимость тщательного динамического контроля специалистами. Для достижения компенсации СД у коморбидных больных стоит рассмотреть терапию препаратами нового поколения (ингибиторы дипептидилпептидазы-4, ингибиторы натрий-глюкозного ко-транспортера 2 типа), при необходимости в сочетании с другими лекарственными средствами.
Для достижения компенсации СД у коморбидных больных стоит рассмотреть терапию препаратами нового поколения (ингибиторы дипептидилпептидазы-4, ингибиторы натрий-глюкозного ко-транспортера 2 типа), при необходимости в сочетании с другими лекарственными средствами.
1. Мельниченко Г.А., Дедов И.И., Белая Ж.Е., и др. Болезнь Иценко-Кушинга: клиника, диагностика, дифференциальная диагностика, методы лечения. Федеральные клинические рекомендации //Проблемы эндокринологии. – 2015. – Т. 61. – № 2. – С. 55-77. [Melnichenko GA, Dedov II, Belaya ZE, et al. Cushing’s disease: the clinical features, diagnostics, differential diagnostics, and methods of treatment. Problems of Endocrinology. 2015;61(2):55-77.] doi: 10.14341/probl201561255-77.
2. Александров А.А., Марова Е.И., Бельченко Л.В., Жимирикина М. Л. Гиперкортицизм: заболеваемость, смертность и факторы риска развития сердечно-сосудистых заболеваний // Врач. — 2007. — № 5. – с.14-16. [Aleksandrov AA, Marova EI, Bel’chenko LV, Zhimirikina ML. Giperkortitsizm: zabolevaemost’, smertnost’ i faktory riska razvitiya serdechno-sosudistykh zabolevaniy. Vrach. 2007;(5):14-16.]
Л. Гиперкортицизм: заболеваемость, смертность и факторы риска развития сердечно-сосудистых заболеваний // Врач. — 2007. — № 5. – с.14-16. [Aleksandrov AA, Marova EI, Bel’chenko LV, Zhimirikina ML. Giperkortitsizm: zabolevaemost’, smertnost’ i faktory riska razvitiya serdechno-sosudistykh zabolevaniy. Vrach. 2007;(5):14-16.]
3. Arnaldi G, Mancini T, Polenta B, Boscaro M. Cardiovascular Risk In Cushing’s Syndrome. Pituitary. 2005;7(4):253-256. doi: 10.1007/s11102-005-1172-7.
4. Sharma ST, Nieman LK, Feelders RA. Comorbidities in Cushing’s disease. Pituitary. 2015;18(2):188-194. doi: 10.1007/s11102-015-0645-6.
5. Lonser RR, Nieman L, Oldfield EH. Cushing’s disease: pathobiology, diagnosis, and management. Journal of Neurosurgery. 2017;126(2):404-417. doi: 10.3171/2016.1.jns152119.
2017;126(2):404-417. doi: 10.3171/2016.1.jns152119.
6. Giordano C, Guarnotta V, Pivonello R, et al. Is diabetes in Cushing’s syndrome only a consequence of hypercortisolism? European Journal of Endocrinology. 2013;170(2):311-319. doi: 10.1530/eje-13-0754.
7. Clayton RN, Raskauskiene D, Reulen RC, Jones PW. Mortality and Morbidity in Cushing’s Disease over 50 Years in Stoke-on-Trent, UK: Audit and Meta-Analysis of Literature. The Journal of Clinical Endocrinology & Metabolism. 2011;96(3):632-642. doi: 10.1210/jc.2010-1942.
8. Steffensen C, Pereira AM, Dekkers OM, Jørgensen JOL. DIAGNOSIS OF ENDOCRINE DISEASE: Prevalence of hypercortisolism in type 2 diabetes patients: a systematic review and meta-analysis. European Journal of Endocrinology. 2016;175(6):R247-R253. doi: 10.1530/eje-16-0434.
2016;175(6):R247-R253. doi: 10.1530/eje-16-0434.
9. Bae EJ. DPP-4 inhibitors in diabetic complications: role of DPP-4 beyond glucose control. Archives of Pharmacal Research. 2016;39(8):1114-1128. doi: 10.1007/s12272-016-0813-x.
10. Remm F, Franz W-M, Brenner C. Gliptins and their target dipeptidyl peptidase 4: implications for the treatment of vascular disease. European Heart Journal – Cardiovascular Pharmacotherapy. 2016;2(3):185-193. doi: 10.1093/ehjcvp/pvv044.
11. Chrysant SG. Promising cardiovascular and blood pressure effects of the SGLT2 inhibitors: a new class of antidiabetic drugs. Drugs of Today. 2017;53(3):191. doi: 10.1358/dot.2017.53.3.2555985.
Синдром Кушинга (гиперкортицизм) — справочник болезней — ЗдоровьеИнфо
Лечение синдрома Кушинга направлено на снижение уровня кортизола в организме. Наиболее оптимальный способ лечения определяется причиной развития синдрома. Существуют следующие виды лечения:
Наиболее оптимальный способ лечения определяется причиной развития синдрома. Существуют следующие виды лечения:
- Постепенное снижение дозы кортикостероидов. Если причиной развития синдрома Кушинга является длительный пример кортикостероидов, то врач может рекомендовать вам постепенно уменьшать дозу препаратов до уровня, который позволяющего продолжать эффективное лечение того состояния, по поводу которого его принимали (астма, артрит и т.д.). Для лечения многих заболеваний успешно применяются препараты нестероидной природы, что позволяет уменьшить дозировку стероидов или отказаться от их применения.
Не уменьшайте дозировку стероидов и не прекращайте их прием самостоятельно. Делайте это только под контролем врача.
Резкое прекращение приема препаратов приводит к развитию дефицита уровня кортизола. Постепенная отмена стероидов в течение длительного времени позволяет организму наладить нормальную выработку собственного кортизола.
- Хирургическое лечение.
 Если причиной развития синдрома Кушинга является опухоль, врач рекомендует ее полное удаление. Опухолями питуитарной железы обычно занимаются нейрохирурги. Они проводят трансназальное удаление опухоли. Опухоли надпочечников, легких и поджелудочной железы удаляют хирурги. Проводятся полостные операции, реже используются малоинвазивные хирургические техники, предполагающие небольшие разрезы.
Если причиной развития синдрома Кушинга является опухоль, врач рекомендует ее полное удаление. Опухолями питуитарной железы обычно занимаются нейрохирурги. Они проводят трансназальное удаление опухоли. Опухоли надпочечников, легких и поджелудочной железы удаляют хирурги. Проводятся полостные операции, реже используются малоинвазивные хирургические техники, предполагающие небольшие разрезы.
После операции вам потребуется заместительная терапия препаратами кортизола, чтобы дать возможность организму скорректировать выработку этого гормона. В большинстве случаев, восстанавливается нормальная выработка кортизола наподчечниками, и под контролем врача возможна постепенная отмена заместительной терапии.
Однако этот процесс может занять год или больше. В ряде случаев, у больных синдромом Кушинга не происходит восстановления нормальной функции надпочечников и требуется пожизненное проведение заместительной гормональной терапии.
- Лучевая терапия.
 Если в ходе операции опухоль не была полностью удалена, врач может назначить вам курс лучевой терапии. Кроме того, лучевая терапия проводится тем больным, у кого есть противопоказания к операции.
Если в ходе операции опухоль не была полностью удалена, врач может назначить вам курс лучевой терапии. Кроме того, лучевая терапия проводится тем больным, у кого есть противопоказания к операции.
Лучевая терапия может проводиться в течение шести недель небольшими дозами излучения, или может быть выполнена с помощью гамма-ножа (стереотаксическая хирургия). В последнем случае, она проводится как монотерапия. Значительная доза излучения направляется на область опухоли, а прилежащие здоровые ткани защищаются от облучения.
- Лекарственные препараты. Лекарственные препараты могут быть назначены для регуляции выработки кортизола в том случае, когда хирургическое лечение и лучевая терапия оказались неэффективны. При тяжелом течение синдрома Кушинга медикаментозное лечение назначается до операции для уменьшения выраженности симптомов и снижения риска хирургического вмешательства.
Лекарственные препараты, которые позволяют контролировать избыточную продукцию кортизола надпочечниками включают кетоконазол (Низорал), митотан (Лизодрен) и метирапон (Метопирон).
Мифепристон (Корлим) показан больным с синдромом Кушинга, у которых есть сахарный диабет 2 типа или нарушение толерантности к глюкозе. Мифепристон не снижает выработку кортизола, но блокирует его действие на ткани.
Побочными эффектами этих препаратов могут быть слабость, тошнота, рвота, головные боли, мышечные боли, повышение артериального давления, снижение уровня калия и отеки. В ряде случаев, развиваются более тяжелые побочные эффекты, например, неврологические осложнения или токсический гепатит.
Новый препарат для лечения синдрома Кушинга — пазиреотид (Сигнифор) снижает выработку АКТГ при опухолях гипофиза. Инъекции этого препарата выполняются дважды в неделю. Он применяется, когда оперативное лечение невозможно или не принесло ожидаемого результата.
Побочные эффекты возникают редко, могут включать диарею, тошноту, повышение уровня сахара крови, головную боль, боль в животе и слабость.
В ряде случаев, из-за наличия опухоли или проводимого лечения развивается дефицит других гормонов питуитарной железы или надпочечников. Тогда врач назначает гормональную заместительную терапию.
Тогда врач назначает гормональную заместительную терапию.
Если ни один из перечисленных выше методов лечение не принес результата, врач может рекомендовать двустороннее удаление надпочечников (билатеральную адреналэктомию). Эта операция устранит избыток кортизола, но после нее требуется пожизненная гормональная заместительная терапия.
Синдром Кушинга у собак и кошек — симптомы, диагностика, лечение
Содержание
- Кортизол
- Симтомы синдрома Кушинга у собак и кошек
- Диагностика
- Лечение синдрома Кушинга у кошек и собак
Это эндокринная патология, связанная с повышенной выработкой кортизола надпочечниками. Данное заболевание является достаточно редким для кошек и широко распространенным у собак. Причиной болезни могут быть как сами надпочечники (15% случаев) – вследствие возникшей в них доброкачественной или злокачественной опухоли, а также гипофиз (до 85% случаев) – который по определенному механизму, опять же чаще из-за доброкачественной опухоли в нем (микро- или макроаденомы) , заставляет надпочечники вырабатывать повышенное количество кортизола. Возможен и ятрогенный гиперадренокортицизм, вызванный длительным применением препаратов, которые по своей структуре близки к кортизолу (т.е. кортикостероидными гормонами).
Возможен и ятрогенный гиперадренокортицизм, вызванный длительным применением препаратов, которые по своей структуре близки к кортизолу (т.е. кортикостероидными гормонами).
Заболевание характерно для животных среднего и старшего возраста. Однако гипофизарный гиперадренокортицизм встречается, хотя и редко, и у молодых животных.
Кортизол
Кортизол это стрессовый гормон и изменения, которые происходят в организме при его постоянной повышенной выработке, достаточно многогранны. Заболевание зачастую развивается очень медленно, и симптомы могут быть слабо выраженными на начальной стадии.
Симтомы синдрома Кушинга у собак и кошек
К наиболее частым клиническим признакам у собак относят повышенную жажду и мочеиспускание, повышенный аппетит. Нередко владелец отмечает мышечную слабость и повышенную утомляемость своего питомца на прогулках, отвисший живот. Характерно двустороннее симметричное прорежение или выпадение шерсти, зуд при этом обычно отсутствует, иногда наблюдается отсутствие роста шерсти после стрижки, изменение цвета кожи (гиперпигментация), у самок могут прекратиться течки.
У кошек симптомы несколько отличаются. Один из наиболее распространенных признаков – это плохо контролируемый сахарный диабет с тяжелой инсулинорезистентностью. И в связи с этим основные жалобы — на повышенные жажду/ мочеиспускание /аппетит. Могут быть сонливость, отвисший живот, мышечная слабость, отсутствие роста шерсти после стрижки, или незначительное выпадение шерсти. Достаточно характерный признак – это истончение и разрывы кожи («ломкая» кожа).
Диагностика
Для того чтобы выявить животных, у которых гиперадренокортицизм можно исключить – используется такой анализ как определение соотношения кортизол/креатинин в утренней моче. Для дальнейшей диагностики заболевания недостаточно простого определения кортизола в сыворотке крови, т.к. данный гормон может быть как повышен по причине стресса или других патологических состояний организма, так и понижен в силу ряда причин. Поэтому необходимо проведения определенных тестов (малая и/или большая дексаметазоновая проба, стимулирующая проба с АКТГ). При необходимости и/или сомнительных результатах проб – проводятся сразу всем возможные тесты или они повторяются через какое-то время.
При необходимости и/или сомнительных результатах проб – проводятся сразу всем возможные тесты или они повторяются через какое-то время.
Необходимо попытаться выяснить где локализована причина заболевания – это надпочечники или гипофиз — и определить возможно ли ее устранить. Для дифференциальной диагностики гипофизарного и надпочечникового гиперадренокортицизма используется большая дексаметазоновая проба, узи, рентгенография, МРТ гипофиза и надпочечников. Если причина в опухоли надпочечника – то показана операция (адреналэктомия). Если животное не операбельно или речь идет о гипофизарном гиперадренокортицизме – то проводится консервативное лечение препаратами, блокирующими синтез кортизола или разрушающими кору надпочечников.
Лечение синдрома Кушинга у кошек и собак
К сожалению, до сих пор препараты для консервативного лечения синдрома Кушинга у собак и кошек остаются не доступными в России, и владельцы вынуждены привозить их самостоятельно из-за рубежа или заказывать на иностранных сайтах.
ветеринарным врачом-эндокринологом «МЕДВЕТ»
© 2014 СВЦ «МЕДВЕТ»
Ятрогенный гиперадренокортицизм, или чем опасны гормоны
Сегодня сложно найти врача, который не использовал бы в своей практике глюкокортикоиды. А значит, и сталкиваться с нежелательными эффектами их применения приходится не редко. Одним из таких эффектов является развитие так называемого «ятрогенного Синдрома Кушинга» или «ятрогенного гиперадренокортицизма». Если разграничить эти понятия, то мы получим следующие определения:
- Гиперадренокортицизм – это состояние, обусловленное хронически высокой концентрацией кортизола в крови;
- Синдром Кушинга – это совокупность клинических и химических нарушений, вызванных воздействием избыточного количества глюкокортикоидов.
Ятрогенная природа этих состояний обуславливается экзогенным поступлением в организм глюкокортикоидов в ходе лечения. Обычно лечению глюкокортикоидами подвергаются животные с тяжелыми заболеваниями, для которых эти препараты являются единственным средством спасения. В таких случаях, применять их приходится не только интенсивно, но и долго, иногда месяцами и годами. Поэтому не удивительно, что помимо лечебного действия, фармакологический эффект гормональных препаратов будет включать и отклонения в организме, связанные с хронической гиперкортизолемией. Поэтому проявление Синдрома Кушинга – естественный и неизбежный спутник лечения.
Обычно лечению глюкокортикоидами подвергаются животные с тяжелыми заболеваниями, для которых эти препараты являются единственным средством спасения. В таких случаях, применять их приходится не только интенсивно, но и долго, иногда месяцами и годами. Поэтому не удивительно, что помимо лечебного действия, фармакологический эффект гормональных препаратов будет включать и отклонения в организме, связанные с хронической гиперкортизолемией. Поэтому проявление Синдрома Кушинга – естественный и неизбежный спутник лечения.
При приеме глюкокортикоидов их концентрация в крови растет, воздействуя на гипоталамус, и убеждая его снизить выработку кортикотропин-рилизинг-гормона (КРГ). В свою очередь, низкий уровень КРГ снижает выработку аденокортикотропного гормона (АКТГ) в гипофизе, из-за чего кора надпочечников входит в состояние функционального покоя. Если этот процесс растягивается во времени, то кора надпочечников атрофируется за ненадобностью. Таким образом, состояние гиперадренокортицизма при отмене препарата переходит в состояние гипоадренокортицизма.
Глюкокортикоиды – это стероидные гормоны, продуцируемые корой надпочечников. К ним относятся кортизол, кортизон и кортикостерон. Наиболее активным у большинства видов животных является кортизол. Исходным материалом для химического синтеза глюкокортикоидов являются холевая кислота, получаемая из тканей крупного рогатого скота, или стероидные соединения, вырабатываемые из растений семейства лилиевых или диоскорейных.
Эффекты глюкокортикоидов согласуются с клиническими признаками ятрогенного гиперадренокортицизма. Основные из них:
- Усиление катаболизма и торможение биосинтеза белков. Как следствие, развивается атрофия мышечной ткани.
- Стимуляция продукции глюкозы, усиление интенсивности глюконеогенеза с развитием гипергликемии и гиперинсулинемии.
- Стимуляция липолиза. В результате растет уровень триглицеридов в крови, и происходит нарушение перераспределения жировой ткани.
- Подавление активности фибробластов.
 Происходит истончение кожи, ухудшается заживление ран.
Происходит истончение кожи, ухудшается заживление ран. - Уменьшение всасывания кальция в кишечнике и усиление его экскреции с мочой. Соответственно, стимулируется резорбция костной ткани.
- Усиление действия катехоламинов. Тем самым стимулируется работа сердца и сосудистый тонус.
- Торможение секреции вазопрессина с развитием таких симптомов как полиурия и полидипсия.
- Снижение концентрации общего тироксина.
- Снижение продукции гонадотропинов. В результате снижается концентрация тестостерона и развивается атрофия семенников у самцов.
- Задержка роста у щенков и котят из-за снижения секреции гормона роста.
Вероятность развития симптомов ятрогенного гиперадренокортицизма зависит от дозы, активности применяемого препарата и продолжительности терапии. Считается, что первые признаки проявляются в среднем через 1-2 недели лечения. Однако, некоторые эффекты, например, полиурия и полидипсия, могут развиться и при однократном применении препарата.
По продолжительности действия глюкокортикоиды делят на препараты короткого, среднего и длительного действия. Чаще всего ятрогенный гиперадренокортицизм развивается после многократных инъекций препаратов длительного действия. Также они отличаются по их глюкокортикоидной и минералкортикоидной активности. Так, активность Преднизолона в 4 раза сильнее, чем у кортизола, а его минералкортикоидная активность немного ниже. Дексаметазон в 30 раз сильнее кортизола и в 7 раз сильнее Преднизолона и не обладает значимой минералкортикоидной активностью. Способы дозирования препаратов весьма вариабельны и зависят от заболевания и индивидуальной чувствительности организма животного.
Поставить диагноз «ятрогенный гиперадренокортицизм» не трудно, так как его эффект следует ожидать при интенсивном лечении глюкокортикоидами. Клинически мы обычно видим такие классические признаки, как полиурия, полидипсия, полифагия, увеличение объема живота, ухудшение качества шерсти, кожные поражения, быстрая утомляемость, отсутствие течек и атрофия семенников. В запущенных случаях также могут развиться кальцификаты, стероидный гепатит, почечная недостаточность с соответствующей симптоматикой.
В запущенных случаях также могут развиться кальцификаты, стероидный гепатит, почечная недостаточность с соответствующей симптоматикой.
Изменения картины крови происходят уже через несколько часов после введения глюкокортикоидов. С другой стороны, у некоторых животных, хронически принимающих стероиды, биохимические изменения могут и не наблюдаться. Из характерных изменений клинического анализа крови выделяют стрессовую лейкограмму, эритроцитоз, тромбоцитоз. В биохимическом анализе мы можем увидеть повышение концентрации глюкозы, холестерина, печеночных трансаминаз. В моче наблюдаются снижение плотности и признаки воспаления, как следствие иммуносупрессии.
Для диагностики гиперадренокортицизма существует ряд специфических тестов, однако в случае с ятрогенной его формой, большинство из них бесполезны. Тогда золотым стандартом является провокационная проба с АКТГ. При подтверждении диагноза мы получаем низкую базальную концентрацию кортизола, а ответ на стимуляцию АКТГ слабый или отсутствует. Таким образом, клинически мы видим классические признаки гиперадренокортицизма, а результаты теста с АКТГ согласуются с гипоадренокортицизмом. Связано это с атрофией коры надпочечников, механизм развития которой рассмотрен выше.
Таким образом, клинически мы видим классические признаки гиперадренокортицизма, а результаты теста с АКТГ согласуются с гипоадренокортицизмом. Связано это с атрофией коры надпочечников, механизм развития которой рассмотрен выше.
При развитии нежелательных эффектов от применения глюкокортикоидов чаще всего достаточно отменить терапию. Тогда состояние постепенно нормализуется и симптомы гиперадренокортицизма сходят на нет. Однако, существуют нюансы, препятствующие отмене препарата. Во-первых, в случае резкого прекращения приема глюкокортикоидов может развиться синдром отмены. Клинически мы увидим симптомы основного заболевания, а затем, и признаки гипоадренокортицизма: рвота, анорексия, апатия. Во-вторых, существует ряд патологий, требующих постоянной дачи глюкокортикоидов, и при отмене препарата возвращаются симптомы основного заболевания, с которым мы боролись.
Для того, чтобы избежать развития синдрома отмены следует отменять препарат постепенно. Разные авторы расходятся во мнении о минимальном курсе применения стероидов, не требующих постепенного снижения дозы. Так, указывают курсы от 1 до 21 дня. В любом случае, принимаемое решение должно основываться на интенсивности наблюдаемых симптомов и исходной дозировке препарата. Снижение дозы до отмены может занимать от нескольких недель до месяца, а возможно и дольше. Предпочтительно снижать не только дозировку, но и кратность применения глюкокортикоидов до 1 раза в 2-3 дня. Не следует снижать дозу более, чем на ¼ в неделю. Также важно учитывать, что в период сильного стресса (предстоящая операция, например) доза должна быть повышена. Количество глюкокортикоидов на последних этапах снижения дозы должно быть несколько ниже физиологической, чтобы постепенно стимулировать работу коры надпочечников.
Так, указывают курсы от 1 до 21 дня. В любом случае, принимаемое решение должно основываться на интенсивности наблюдаемых симптомов и исходной дозировке препарата. Снижение дозы до отмены может занимать от нескольких недель до месяца, а возможно и дольше. Предпочтительно снижать не только дозировку, но и кратность применения глюкокортикоидов до 1 раза в 2-3 дня. Не следует снижать дозу более, чем на ¼ в неделю. Также важно учитывать, что в период сильного стресса (предстоящая операция, например) доза должна быть повышена. Количество глюкокортикоидов на последних этапах снижения дозы должно быть несколько ниже физиологической, чтобы постепенно стимулировать работу коры надпочечников.
В случае возвращения симптомов основного заболевания при отмене глюкокортикоидов существует вариант замены их на другой иммуносупрессивный препарат негормональной природы, например, на Циклоспорин.
При невозможности прекращения лечения глюкокортикоидами задача врача – минимизировать ущерб от их применения. Необходимо регулярно осматривать животное, измерять давление, проводить анализы крови, а при необходимости – рентгенологическое и ультразвуковое исследования. По мере выявления отклонений стараемся их скорректировать. Например, используем инсулиновую терапию при гипергликемии, нормализуем уровень электролитов в крови. При усиленном катаболизме белков и у щенков с задержкой роста целесообразно введение диеты богатой белком. Также в литературе рассматривается возможность применения анаболических стероидов.
Необходимо регулярно осматривать животное, измерять давление, проводить анализы крови, а при необходимости – рентгенологическое и ультразвуковое исследования. По мере выявления отклонений стараемся их скорректировать. Например, используем инсулиновую терапию при гипергликемии, нормализуем уровень электролитов в крови. При усиленном катаболизме белков и у щенков с задержкой роста целесообразно введение диеты богатой белком. Также в литературе рассматривается возможность применения анаболических стероидов.
Ятрогенный гиперадренокортицимзм, по сути, лечению не подлежит. Часто приходится мириться с неблагоприятными эффектами применения глюкокортикоидов, когда от их использования зависит жизнь и самочувствие животного. Поэтому необходимо не только помнить о них, но и информировать владельца животного о том, чего следует ожидать в ходе лечения.
Список использованной литературы:
1. Avrom Caplan, Nicole Fett, Misha Rosenbach etc. Prevention and management of glucocorticoid-induced side effects: A comprehensive review. I Am Acad Dermatol, Volume 76, Nummber 1, January 2017
I Am Acad Dermatol, Volume 76, Nummber 1, January 2017
2. Edward C. Feldman, Richard W. Nelson, Claudia E. Reusch, J. Catharine R. Scott-Moncrieff. Canin and Feline Endjcrinology, Edition 4. 2015
3. Ian M. Adcock, Sharon Mumby. Handbook of Experimental Pharmacology. Glucocorticoids, 2016
4. Mark E.Peterson. Diagnosis of Hiperadrenocorticism in Dogs, 2007
5. Peter J. Barnes. Handbook of Experimental Pharmacology. Glucocorticosteroids, 2016
Макашова А.М.
что это за болезнь и как её лечить
Синдром Иценко-Кушинга – это эндокринное нарушение, при котором в организме длительное время вырабатывается повышенное количество гормона под названием кортизол. Чаще это нарушение называют синдромом Кушинга в честь американского нейрохирурга, который впервые описал это заболевание. В странах постсоветского пространства это нарушение называют синдромом Иценко-Кушинга в честь невропатолога Николая Иценко. В данном материале будут рассмотрены причины, симптомы и методы лечения этой серьёзной болезни.
В странах постсоветского пространства это нарушение называют синдромом Иценко-Кушинга в честь невропатолога Николая Иценко. В данном материале будут рассмотрены причины, симптомы и методы лечения этой серьёзной болезни.
Кортизол – это гормон, выполняющий жизненно важные задачи в нашем организме, включая:
- Помощь в поддержании кровяного давления и сердечно-сосудистой функции,
- Смягчение реакции иммунной системы на воспалительный процесс в организме,
- Поддержание нормального уровня сахара в крови,
- Регуляция метаболизма белков, жиров и углеводов.
Кортизол вырабатывается в коре надпочечников, поэтому чрезмерное его производство также называют гиперкортицизмом (cortex – кора).
У большинства этот синдром развивается после приема глюкокортикоидов – стероидных гормонов, которые химически схожи с естественно продуцируемым кортизолом. Один из таких препаратов – преднизон, который назначают при астме, ревматоидном артрите, волчанке и других воспалительных заболеваниях. Глюкокортикоиды также используются для подавления иммунной реакции после пересадки органов – чтобы организм не отторгал новых органов или тканей.
Глюкокортикоиды также используются для подавления иммунной реакции после пересадки органов – чтобы организм не отторгал новых органов или тканей.
У остальных людей синдром Кушинга развивается по причине нарушения регуляторного механизма, который отвечает за выработку и поддержание «здорового» уровня кортизола. При нормальных условиях процесс производства кортизола следует точной цепочке событий. Сначала гипоталамус посылает кортикотропин-рилизинг-гормон (КРГ) в гипофиз. В свою очередь, КРГ даёт гипофизу сигнал к выработке адренокортикотропина (АКТГ), который стимулирует надпочечники. После того как АКТГ достигает надпочечников, они высвобождают кортизол в кровоток.
Когда концентрация кортизола в крови находится в норме, гипоталамус и гипофиз выделяют меньше кортикотропин-рилизинг-гормона и адренокортикотропина. За счёт этого механизма гарантируется, что количество кортизола сбалансировано и соответствует потребностям организма. Если же с надпочечниками или регуляторным механизмом что-то пойдет не так, процесс выработки кортизола может выйти из-под контроля.
Какие же факторы способны нарушить этот процесс и привести к синдрому Кушинга? Рассмотрим их ниже:
- Аденома (опухоль) гипофиза. Это доброкачественное образование синтезирует избыточное количество гормона АКТГ, который стимулирует надпочечники вырабатывать кортизол. По данным Министерства здравоохранения США, в 70 % случаев виновата именно аденома гипофиза. В этом случае нарушение называют не синдромом, а болезнью Иценко-Кушинга. Чаще от этой формы заболевания страдают женщины.
- АКТГ-эктопированный синдром. В редких случаях опухоли (чаще злокачественные), которые образуются в легких, поджелудочной железе, щитовидке или вилочковой железе, вырабатывают большое количество адренокортикотропного гормона. Это нарушение известно как АКТГ-эктопированный синдром. В большей половине случаев этот синдром вызывается опухолями легких, при этом мужчины страдают в 3 раза чаще, чем женщины.
- Первичное заболевание надпочечников.
 У некоторых людей причиной синдрома Иценко-Кушинга является нарушение функции надпочечников. Наиболее распространенная патология – доброкачественная опухоль коры надпочечников, или аденома. У женщин она встречается в 4-5 раз чаще, чем у мужчин. Средний возраст, в котором аденома образуется чаще всего – 40 лет.
У некоторых людей причиной синдрома Иценко-Кушинга является нарушение функции надпочечников. Наиболее распространенная патология – доброкачественная опухоль коры надпочечников, или аденома. У женщин она встречается в 4-5 раз чаще, чем у мужчин. Средний возраст, в котором аденома образуется чаще всего – 40 лет. - Адренокортикальные карциномы. Злокачественные опухоли надпочечников встречаются очень редко, но также способны вызывать гиперкортицизм. Иногда к синдрому приводит доброкачественное узловое расширение в обоих надпочечниках. Адренокортикальные карциномы являются наименее распространенными причинами развития синдрома.
- Наследственный синдром. Очень редко люди наследуют тенденцию к образованию опухолей на одном или нескольких эндокринных органах. Эти опухоли могут вырабатывать кортизол в больших количествах.
Синдром Кушинга: симптомы
Признаки этого нарушения проявляются по-разному, но у большинства наблюдается ожирение в верхней части тела, округление лица и скопление жира вокруг шеи. Руки и ноги у больных остаются сравнительно худыми. У детей, как правило, наблюдается ожирение и замедленный темп роста.
Руки и ноги у больных остаются сравнительно худыми. У детей, как правило, наблюдается ожирение и замедленный темп роста.
Другие симптомы гиперкортицизма проявляются на коже и костях. Кожа становится тонкой и хрупкой, на ней легко образуются синяки и ушибы, которые медленно заживают. На животе, бедрах, ягодицах, руках и груди могут появиться розовые или фиолетовые растяжки.
Кости так же становятся слабыми. Такие обычные действия, как сгибание туловища, поднимание предметов или подъем со стула могут приводить к болям в спине, а также переломам рёбер или позвоночника.
У женщин синдром Кушинга обычно приводит к избыточному росту волос на лице, шее, молочной железе, животе и бедрах. Менструальные циклы могут потерять привычную регулярность или прекратиться вовсе. У мужчин может развиваться бесплодие, а также потеря интереса к сексу, а иногда – эректильная дисфункция.
Среди остальных симптомов гиперкортицизма:
- Сильная усталость,
- Ослабленные мышцы,
- Высокое кровяное давление,
- Повышение уровня глюкозы в крови,
- Ощущение жажды и частое мочеиспускание,
- Раздражительность, тревожность и депрессия,
- Образование «жирного» горба в верхней части трапециевидной мышцы.

Лечение синдрома Кушинга
Диагностика этого нарушения является не только сложным, но и достаточно длительным процессом. Сложность заключается в том, что многие признаки этой болезни схожи с несколькими другими нарушениями.
Из-за того что синдром Иценко-Кушинга является очень серьёзным заболеванием, важно не только исключить другие нарушения (к примеру, гипертонию или гипотиреоз), но и определить конкретную причину гиперкортицизма. Для этого пациенту назначают несколько диагностических тестов и процедур, включая:
- анализы крови,
- анализ мочи,
- исследование слюны,
- компьютерную томографию гипофиза и надпочечников, а также другие исследования.
Выбор тактики лечения гиперкортицизма зависит от первопричины заболевания. Лечение может включать лучевую терапию, химиотерапию, операцию или приём препаратов, которые препятствуют выработке кортизола.
Снижение дозировки глюкокортикоидов
Если причина скрывается в приеме глюкокортикоидных препаратов, эндокринолог на время уменьшит их дозировку. Во многих случаях эти препараты можно полностью заменить на некортикостероидные средства. Нельзя резко снижать дозировку или полностью отказываться от глюкокортикоидов без консультации с эндокринологом. Это может привести к дефициту кортизола в организме.
Во многих случаях эти препараты можно полностью заменить на некортикостероидные средства. Нельзя резко снижать дозировку или полностью отказываться от глюкокортикоидов без консультации с эндокринологом. Это может привести к дефициту кортизола в организме.
Операция
Если причина синдрома Иценко-Кушинга скрывается в опухоли, рекомендуется хирургическое вмешательство. Опухоли гипофиза обычно удаляются нейрохирургом, который может выполнить эту процедуру через нос. Если опухоль образовалась в надпочечниках, легких или поджелудочной железе, её удаляют с помощью традиционного хирургического метода. В некоторых случаях удаление новообразования выполняется с помощью лапароскопической операции.
Лучевая терапия
Если хирург не может полностью удалить опухоль на гипофизе, кроме операции пациент проходит лучевую терапию. Иногда её проходят больные, которым не подходит хирургическое вмешательство.
Лекарства
Медикаментозное лечение синдрома Кушинга направлено на снижение выработки кортизола и блокирование его отрицательного воздействия на организм.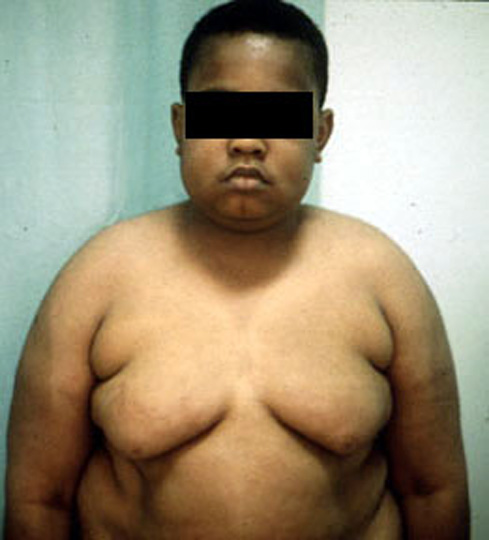 Как правило, препараты принимаются до или после операции, а также после лучевой терапии. Иногда эти лекарства назначают пациентам, которые не хотят или не могут ложиться на операцию.
Как правило, препараты принимаются до или после операции, а также после лучевой терапии. Иногда эти лекарства назначают пациентам, которые не хотят или не могут ложиться на операцию.
Если ни один из терапевтических методов не принёс результата, рекомендуется удаление обоих надпочечников (двусторонняя адреналэктомия). Эта процедура позволит забыть о проблеме избыточной выработки кортизола. После двусторонней адреналэктомии больному придется до конца жизни принимать препарат, который будет заменять кортизол.
Несмотря на то что синдром Иценко-Кушинга является редким заболеванием, при появлении симптомов необходимо как можно раньше обратиться к эндокринологу.
Источники:
- Cushing’s Syndrome, The National Institute of Diabetes and Digestive and Kidney Diseases, Health Information Center,
- Cushing syndrome, Mayo Clinic,
- Cushing’s syndrome, NHS.
Актуальность и перспективные направления изучения проблемы субклинического синдрома Кушинга.
 | Кузнецов
| Кузнецов
1. Terzolo M, Stigliano A, Chiodini I, et al. AME Position Statement on adrenal incidentaloma. Eur J Endocrinol. 2011;164(6):851-870. doi: 10.1530/eje-10-1147.
2. Young WF. The Incidentally discovered adrenal mass. N Engl J Med. 2007;356(6):601-610. doi: 10.1056/NEJMcp065470.
3. Mantero F, Arnaldi G. Management approaches to adrenal incidentalomas. Endocrinol Metab Clin North Am. 2000;29(1):107-125. doi: 10.1016/s0889-8529(05)70119-5.
4. Funder JW, Carey RM, Fardella C, et al. Case detection, diagnosis, and treatment of patients with primary aldosteronism: An Endocrine Society Clinical Practice Guideline. J Clin Endocr Metab.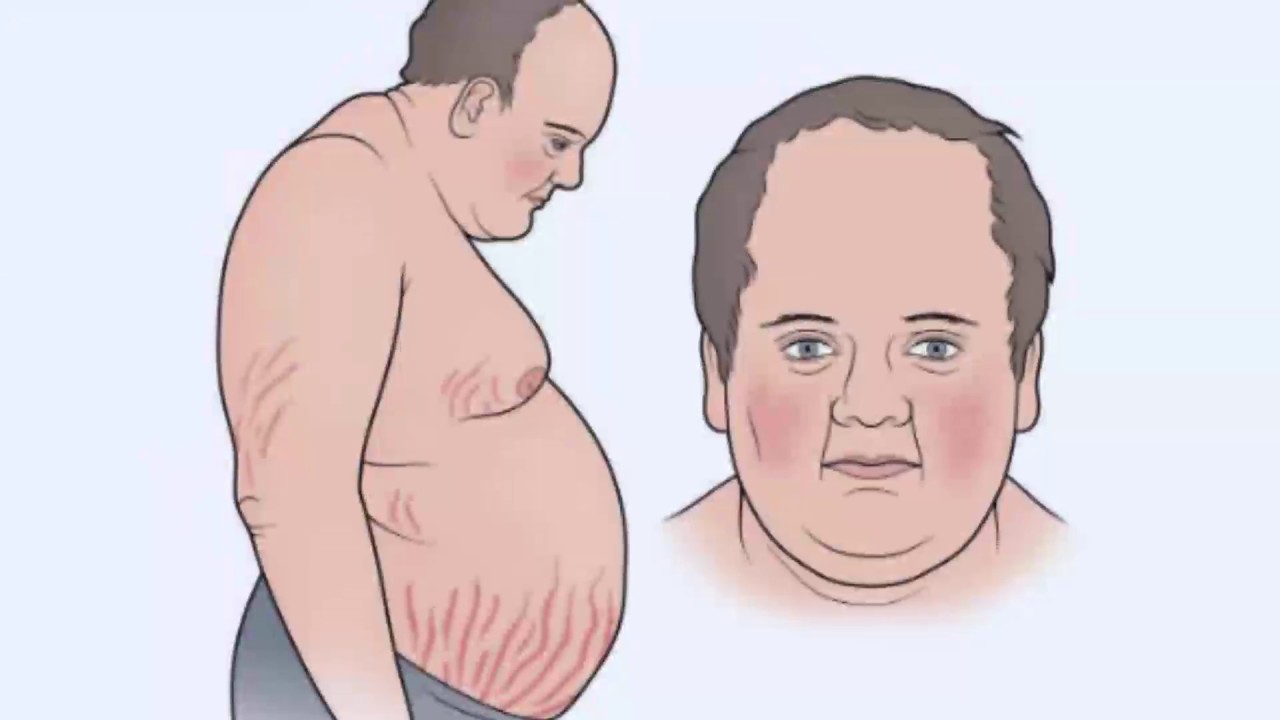 2008;93(9):3266-3281. doi: 10.1210/jc.2008-0104.
2008;93(9):3266-3281. doi: 10.1210/jc.2008-0104.
5. Terzolo M, Bovio S, Pia A, et al. Subclinical Cushing's syndrome. Arq Bras Endocrinol Metabol. 2007;51(8):1272-1279.
6. Reincke M. Subclinical Cushing's syndrome. Endocrinol Metab Clin North Am. 2000;29(1):43-56. doi: 10.1016/s0889-8529(05)70115-8.
7. Beierwaltes WH, Sturman MF, Ryo U, Ice RD. Imaging functional nodules of the adrenal glands with 131-I-19-iodocholesterol. J Nucl Med. 1974;15(4):246-251.
8. Nieman LK. Approach to the patient with an adrenal incidentaloma. J Clin Endocrinol Metab. 2010;95(9):4106-4113. doi: 10.1210/jc.2010-0457.
9. Terzolo M. Adrenal incidentaloma: A new cause of the metabolic syndrome? J Clin Endocrinol Metab. 2002;87(3): 998-1003. doi: 10.1210/jcem.87.3.8277.
Terzolo M. Adrenal incidentaloma: A new cause of the metabolic syndrome? J Clin Endocrinol Metab. 2002;87(3): 998-1003. doi: 10.1210/jcem.87.3.8277.
10. Chiodini I, Morelli V, Salcuni AS, et al. Beneficial metabolic effects of prompt surgical treatment in patients with an adrenal incidentaloma causing biochemical hypercortisolism. J Clin Endocr Metab. 2010;95(6):2736-2745. doi: 10.1210/jc.2009-2387.
11. Chiodini I, Morelli V, Masserini B, et al. Bone mineral density, prevalence of vertebral fractures, and bone quality in patients with adrenal incidentalomas with and without subclinical hypercortisolism: An Italian Multicenter Study. J Clin Endocrinol Metab. 2009;94(9):3207-3214. doi: 10.1210/jc.2009-0468.
12. Toniato A, Merante-Boschin I, Opocher G, et al.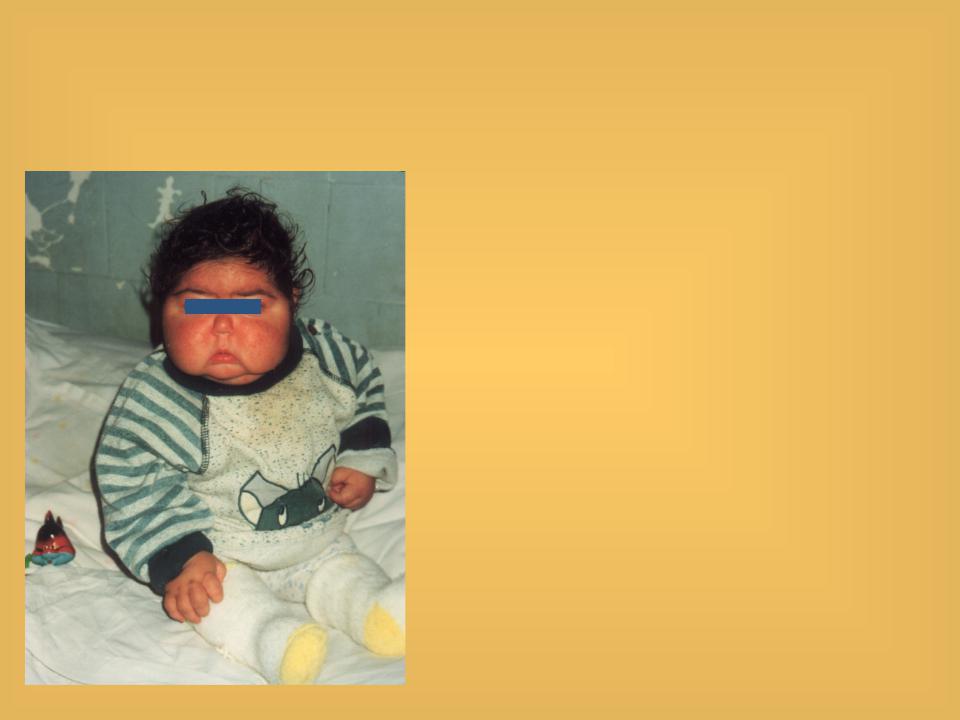 Surgical versus conservative management for subclinical Cushing syndrome in adrenal incidentalomas: a prospective randomized study. Ann Surg. 2009;249(3):388-391. doi: 10.1097/SLA.0b013e31819a47d2.
Surgical versus conservative management for subclinical Cushing syndrome in adrenal incidentalomas: a prospective randomized study. Ann Surg. 2009;249(3):388-391. doi: 10.1097/SLA.0b013e31819a47d2.
13. Emral R, Uysal AR, Asik M, et al. Prevalence of subclinical Cushing's syndrome in 70 patients with adrenal incidentaloma: Clinical, biochemical and surgical outcomes. Endocr J. 2003;50(4):399-408. doi: 10.1507/endocrj.50.399.
14. Mansmann G, Lau J, Balk E, et al. The clinically inapparent adrenal mass: Update in diagnosis and management. Endocr Rev. 2004;25(2):309-340. doi: 10.1210/er.2002-0031.
15. Starker LF, Kunstman JW, Carling T. Subclinical Cushing syndrome. Surg Clin North Am. 2014;94(3):657-668. doi: 10.1016/j. suc.2014.02.008.
suc.2014.02.008.
16. Reimondo G, Allasino B, Bovio S, et al. Pros and cons of dexamethasone suppression test for screening of subclinical Cushing's syndrome in patients with adrenal incidentalomas. J Endocrinol Invest. 2011;34(1):e1-5. doi: 10.3275/7167.
17. Grumbach MM, Biller BM, Braunstein GD, et al. Management of the clinically inapparent adrenal mass (“incidentaloma“). Ann Intern Med. 2003;138(5):424-429.
18. Zeiger MA, Thompson GB, Duh QY, et al. American Association of Clinical Endocrinologists and American Association of Endocrine Surgeons Medical Guidelines for the Management of Adrenal Incidentalomas: executive summary of recommendations. Endocr Pract. 2009;15(5):450-453. doi: 10.4158/EP.15.5.450.
19. Read GF, Walker RF, Wilson DW, Griffiths K. Steroid analysis in saliva for the assessment of endocrine function. Ann N Y Acad Sci. 1990;595(1 Steroid Forma):260-274.
Read GF, Walker RF, Wilson DW, Griffiths K. Steroid analysis in saliva for the assessment of endocrine function. Ann N Y Acad Sci. 1990;595(1 Steroid Forma):260-274.
20. doi: 10.1111/j.1749-6632.1990.tb34300.x.
21. Garde AH, Hansen ÅM. Longterm stability of salivary cortisol. Scand J Clin Lab Invest. 2009;65(5):433-436. doi: 10.1080/00365510510025773.
22. Nunes M-L, Vattaut S, Corcuff J-B, et al. Late-night salivary cortisol for diagnosis of overt and subclinical Cushing’s syndrome in hospitalized and ambulatory patients. J Clin Endocr Metab. 2009;94(2):456-462. doi: 10.1210/jc.2008-1542.
23. Mengden T, Hubmann P, Muller J, et al. Urinary free cortisol versus 17-hydroxycorticosteroids a comparative study of their diagnostic value in Cushing's syndrome. The Clinical Investigator. 1992;70(7). doi: 10.1007/bf00184788.
The Clinical Investigator. 1992;70(7). doi: 10.1007/bf00184788.
24. Carroll BJ, Curtis GC, Davies BM, et al. Urinary free cortisol excretion in depression. Psychol Med. 1976;6(1):43-50.
25. Duclos M, Corcuff JB, Etcheverry N, et al. Abdominal obesity increases overnight cortisol excretion. J Endocrinol Invest. 1999;22(6):465-471. doi: 10.1007/BF03343591.
26. Mericq MV. High fluid intake increases urine free cortisol excretion in normal subjects. J Clin Endocrinol Metab. 1998;83(2):682-684. doi: 10.1210/jcem.83.2.4555.
27. Kidambi S, Raff H, Findling JW. Limitations of nocturnal salivary cortisol and urine free cortisol in the diagnosis of mild Cushing's syndrome. Eur J Endocrinol. 2007;157(6): 725-731. doi: 10.1530/eje-07-0424.
Eur J Endocrinol. 2007;157(6): 725-731. doi: 10.1530/eje-07-0424.
28. Eller-Vainicher C, Morelli V, Salcuni AS, et al. Accuracy of several parameters of hypothalamic-pituitary-adrenal axis activity in predicting before surgery the metabolic effects of the removal of an adrenal incidentaloma. Eur J Endocrinol. 2010;163(6):925-935. doi: 10.1530/eje-10-0602.
29. Valli N, Catargi B, Ronci N, et al. Biochemical screening for subclinical cortisol-secreting adenomas amongst adrenal incidentalomas. Eur J Endocrinol. 2001;144(4):401-408.
30. Tanabe A, Naruse M, Nishikawa T, et al. Autonomy of cortisol secretion in clinically silent adrenal incidentaloma. Horm Metab Res. 2001;33(7):444-450. doi: 10.1055/s-2001-16234.
31. Shiwa T, Oki K, Yamane K, et al. Significantly high level of late-night free cortisol to creatinine ratio in urine specimen in patients with subclinical Cushing's syndrome. Clin Endocrinol (Oxf). 2013;79(5):617-622. doi: 10.1111/cen.12197.
Shiwa T, Oki K, Yamane K, et al. Significantly high level of late-night free cortisol to creatinine ratio in urine specimen in patients with subclinical Cushing's syndrome. Clin Endocrinol (Oxf). 2013;79(5):617-622. doi: 10.1111/cen.12197.
32. Terzolo M, Bovio S, Reimondo G, et al. Subclinical Cushing's syndrome in adrenal incidentalomas. Endocrinol Metab Clin North Am. 2005;34(2):423-439, x. doi: 10.1016/j.ecl.2005.01.008.
33. Masserini B, Morelli V, Bergamaschi S, et al. The limited role of midnight salivary cortisol levels in the diagnosis of subclinical hypercortisolism in patients with adrenal incidentaloma. Eur J Endocrinol. 2009;160(1):87-92. doi: 10.1530/EJE-08-0485.
34. Chiodini I. Clinical review: Diagnosis and treatment of subclinical hypercortisolism. J Clin Endocrinol Metab. 2011;96(5):1223-1236. doi: 10.1210/jc.2010-2722.
J Clin Endocrinol Metab. 2011;96(5):1223-1236. doi: 10.1210/jc.2010-2722.
35. Tsagarakis S, Vassiliadi D, Thalassinos N. Endogenous subclinical hypercortisolism: Diagnostic uncertainties and clinical implications. J Endocrinol Invest. 2006;29(5):471-482. doi: 10.1007/BF03344133.
36. Osella G, Terzolo M, Borretta G, et al. Endocrine evaluation of incidentally discovered adrenal masses (incidentalomas). J Clin Endocrinol Metab. 1994;79(6):1532-1539. doi: 10.1210/jcem.79.6.7989452.
37. Di Dalmazi G, Kisker C, Calebiro D, et al. Novel somatic mutations in the catalytic subunit of the protein kinase A as a cause of adrenal Cushing's syndrome: a European multicentric study. J Clin Endocrinol Metab.2014;99(10):E2093-2100. doi: 10.1210/jc.2014-2152.
doi: 10.1210/jc.2014-2152.
38. Beuschlein F, Fassnacht M, Assie G, et al. Constitutive activation of PKA catalytic subunit in adrenal Cushing's syndrome. N Engl J Med. 2014;370(11):1019-1028.
39. doi: 10.1056/NEJMoa1310359.
40. Cao Y, He M, Gao Z, et al. Activating hotspot L205R mutation in PRKACA and adrenal Cushing's syndrome. Science. 2014;344(6186):913-917. doi: 10.1126/science.1249480.
41. Thiel A, Reis AC, Haase M, et al. PRKACA mutations in cortisol-producing adenomas and adrenal hyperplasia: a single-center study of 60 cases. Eur J Endocrinol. 2015;172(6): 677-685. doi: 10.1530/EJE-14-1113.
42. Sato Y, Maekawa S, Ishii R, et al. Recurrent somatic mutations underlie corticotropin-independent Cushing's syndrome. Science. 2014;344(6186):917-920. doi: 10.1126/science.1252328.
Sato Y, Maekawa S, Ishii R, et al. Recurrent somatic mutations underlie corticotropin-independent Cushing's syndrome. Science. 2014;344(6186):917-920. doi: 10.1126/science.1252328.
43. Goh G, Scholl UI, Healy JM, et al. Recurrent activating mutation in PRKACA in cortisol-producing adrenal tumors. Nat Genet. 2014;46(6):613-617. doi: 10.1038/ng.2956.
44. Cao C, Yang X, Li L, et al. Increased expression of CYP17 and CYP11B1 in subclinical Cushing's syndrome due to adrenal adenomas. Int J Urol. 2011;18(10):691-696. doi: 10.1111/j.1442-2042.2011.02836.x.
45. Mitsuhiro K, Masashi D, Takashi Y. Epigenetic controls of CYP11B2 and CYP11B1 gene in subclinical Cushing syndrome associated with overproduction of aldosterone. Endocr. Soc. 96th Annu. Meet. Expo, 2014.
Endocr. Soc. 96th Annu. Meet. Expo, 2014.
46. Streuli C. Extracellular matrix remodelling and cellular differentiation. Curr Opin Cell Biol. 1999;11(5):634-640. doi: 10.1016/S0955-0674(99)00026-5.
47. Crickard K, Ill CR, Jaffe RB. Control of proliferation of human fetal adrenal cells in vitro. J Clin Endocrinol Metab. 1981;53(4):790-796. doi: 10.1210/jcem-53-4-790.
48. Chamoux E, Narcy A, Lehoux JG, Gallo-Payet N. Fibronectin, laminin, and collagen IV interact with ACTH and angiotensin II to dictate specific cell behavior and secretion in human fetal adrenal cells in culture. Endocr Res.2002;28(4):637-640. doi: 10.1081/ERC-120016978.
49. Andrews RC, Walker BR. Glucocorticoids and insulin resistance: old hormones, new targets. Clin Sci (Lond). 1999;96(5):513-523. doi: 10.1042/CS19980388.
Andrews RC, Walker BR. Glucocorticoids and insulin resistance: old hormones, new targets. Clin Sci (Lond). 1999;96(5):513-523. doi: 10.1042/CS19980388.
50. van Raalte DH, Ouwens DM, Diamant M. Novel insights into glucocorticoid-mediated diabetogenic effects: towards expansion of therapeutic options? Eur J Clin Invest. 2009;39(2):81-93. doi: 10.1111/j.1365-2362.2008.02067.x.
51. Rossi R, Tauchmanova L, Luciano A, et al. Subclinical Cushing's syndrome in patients with adrenal incidentaloma: clinical and biochemical features. J Clin Endocrinol Metab. 2000;85(4):1440-1448. doi: 10.1210/jcem.85.4.6515.
52. Tauchmanova L, Rossi R, Biondi B, et al. Patients with subclinical Cushing's syndrome due to adrenal adenoma have increased cardiovascular risk. J Clin Endocrinol Metab. 2002;87(11):4872-4878. doi: 10.1210/jc.2001-011766.
J Clin Endocrinol Metab. 2002;87(11):4872-4878. doi: 10.1210/jc.2001-011766.
53. Morelli V, Masserini B, Salcuni AS, et al. Subclinical hypercortisolism: correlation between biochemical diagnostic criteria and clinical aspects. Clin Endocrinol (Oxf). 2010;73(2): 161-166. doi: 10.1111/j.1365-2265.2010.03794.x.
54. Mantero F, Terzolo M, Arnaldi G, et al. A survey on adrenal incidentaloma in Italy. Study Group on Adrenal Tumors of the Italian Society of Endocrinology. J Clin Endocrinol Metab. 2000;85(2):637-644. doi: 10.1210/jcem.85.2.6372.
55. Bernini GP, Moretti A, Oriandini C, et al. Long-term morphological and hormonal follow-up in a single unit on 115 patients with adrenal incidentalomas. Br J Cancer. 2005;92(6): 1104-1109. doi: 10.1038/sj.bjc.6602459.
doi: 10.1038/sj.bjc.6602459.
56. Terzolo M, Bovio S, Pia A, et al. Midnight serum cortisol as a marker of increased cardiovascular risk in patients with a clinically inapparent adrenal adenoma. Eur J Endocrinol. 2005;153(2):307-315. doi: 10.1530/eje.1.01959.
57. Sereg M, Szappanos A, Toke J, et al. Atherosclerotic risk factors and complications in patients with non-functioning adrenal adenomas treated with or without adrenalectomy: a long-term follow-up study. Eur J Endocrinol. 2009; 160(4):647-655. doi: 10.1530/EJE-08-0707.
58. Vassilatou E, Vryonidou A, Michalopoulou S, et al. Hormonal activity of adrenal incidentalomas: results from a long-term follow-up study. Clin Endocrinol (Oxf). 2009;70(5):674-679. doi: 10.1111/j. 1365-2265.2008.03492.x.
1365-2265.2008.03492.x.
59. Giordano R, Marinazzo E, Berardelli R, et al. Long-term morphological, hormonal, and clinical follow-up in a single unit on 118 patients with adrenal incidentalomas. Eur J Endocrinol. 2010;162(4):779-785. doi: 10.1530/EJE-09-0957.
60. Comlekci A, Yener S, Ertilav S, et al. Adrenal incidentaloma, clinical, metabolic, follow-up aspects: single centre experience. Endocrine. 2010;37(1):40-46. doi: 10.1007/s12020-009-9260-5.
61. Giordano R, Guaraldi F, Berardelli R, et al. Glucose metabolism in patients with subclinical Cushing's syndrome. Endocrine. 2012;41(3):415-423. doi: 10.1007/s12020-012-9628-9.
62. Di Dalmazi G, Vicennati V, Garelli S, et al. Cardiovascular events and mortality in patients with adrenal incidentalomas that are either non-secreting or associated with intermediate phenotype or subclinical Cushing's syndrome: a 15-year retrospective study. The Lancet Diabetes & Endocrinology. 2014;2(5):396-405. doi: 10.1016/s2213-8587(13)70211-0.
Di Dalmazi G, Vicennati V, Garelli S, et al. Cardiovascular events and mortality in patients with adrenal incidentalomas that are either non-secreting or associated with intermediate phenotype or subclinical Cushing's syndrome: a 15-year retrospective study. The Lancet Diabetes & Endocrinology. 2014;2(5):396-405. doi: 10.1016/s2213-8587(13)70211-0.
63. Di Dalmazi G, Vicennati V, Rinaldi E, et al. Progressively increased patterns of subclinical cortisol hypersecretion in adrenal incidentalomas differently predict major metabolic and cardiovascular outcomes: a large cross-sectional study.Eur J Endocrinol. 2012;166(4):669-677. doi: 10.1530/eje-11-1039.
64. Morelli V, Eller-Vainicher C, Salcuni AS, et al. Risk of new vertebral fractures in patients with adrenal incidentaloma with and without subclinical hypercortisolism: A multicenter longitudinal study. J Bone Miner Res. 2011;26(8):1816-1821. doi: 10.1002/jbmr.398.
J Bone Miner Res. 2011;26(8):1816-1821. doi: 10.1002/jbmr.398.
65. Chiodini I. Bone loss rate in adrenal incidentalomas: A longitudinal study. J Clin Endocrinol Metab. 2001;86(11): 5337-5341. doi: 10.1210/jcem.86.11.8022.
66. Eller-Vainicher C, Morelli V, Ulivieri FM, et al. Bone quality, as measured by trabecular bone score in patients with adrenal incidentalomas with and without subclinical hypercortisolism. J Bone Miner Res. 2012;27(10):2223-2230.doi: 10.1002/jbmr.1648.
67. Lane NE, Yao W. Glucocorticoid-induced bone fragility. Ann N Y Acad Sci. 2010;1192(1):81-83. doi: 10.1111/j.1749-6632.2009.05228.x.
68. Midorikawa S, Sanada H, Hashimoto S, et al. The improvement of insulin resistance in patients with adrenal incidentaloma by surgical resection. Clin Endocrinol (Oxf). 2001;54(6):797-804. doi: 10.1046/j.1365-2265.2001.01274.x.
The improvement of insulin resistance in patients with adrenal incidentaloma by surgical resection. Clin Endocrinol (Oxf). 2001;54(6):797-804. doi: 10.1046/j.1365-2265.2001.01274.x.
69. Mitchell IC, Auchus RJ, Juneja K, et al. “Subclinical Cushing’s syndrome” is not subclinical: improvement after adrenalectomy in 9 patients. Surgery. 2007;142(6):900-905.e901. doi: 10.1016/j.surg.2007.10.001.
70. Bernini G, Moretti A, Iacconi P, et al. Anthropometric, haemodynamic, humoral and hormonal evaluation in patients with incidental adrenocortical adenomas before and after surgery. Eur J Endocrinol. 2003;148(2):213-219. doi: 10.1530/eje.0.1480213.
71. Calebiro D, Di Dalmazi G, Bathon K, et al. cAMP signaling in cortisol-producing adrenal adenoma. Eur J Endocrinol. 2015;173(4):M99-M106. doi: 10.1530/eje-15-0353.
Eur J Endocrinol. 2015;173(4):M99-M106. doi: 10.1530/eje-15-0353.
Синдром Кушинга у собак: причины, симптомы, лечение, прогноз
Содержание статьи
Собачий организм является уникальной системой, в котором происходит множество биохимических процессов, определяющих уровень физического и интеллектуального развития пса.
От правильного функционирования органов внутренней секреции зависит состояние гормонального фона, который, в свою очередь, обеспечивает хорошее состояние здоровья собаки, ее психоэмоциональное развитие и отвечает за продолжительность жизни животного. Но, к сожалению, сбой в работе эндокринной системы вашего питомца может стать причиной такого сложного заболевания, как синдром Кушинга у собак.
Что представляет собой синдром?
Это заболевание, нередко встречающееся у животных старше семи лет, однако иногда заболеть могут и молодые собаки.
Для того чтобы в организме собаки правильно работала система свертываемости крови, было в норме артериальное давление, и он мог справляться с воспалениями, надпочечники животного вырабатывают гормон кортизол. Из-за того, что в критических ситуациях при волнении, испуге кровь собаки выбрасывается большое количество этого вещества, его еще называют гормоном стресса.
Из-за того, что в критических ситуациях при волнении, испуге кровь собаки выбрасывается большое количество этого вещества, его еще называют гормоном стресса.
Но надпочечники не могут «распоряжаться» кортизолом самостоятельно — команду на выработку гормона им дает гипофиз, регулирующий его концентрацию в организме. Если гипофиз перестает контролировать уровень кортизола, то увеличение содержания его в крови становится причиной проявления синдрома Кушинга у собак.
Ветеринары подразделяют данную патологию на:
- болезнь Кушинга появляется в результате поражения гипофиза аденомой;
- вызывается появлением аденомы или карциномы надпочечников у собак;
- ятрогенный гиперадренокортицизм — возникает в результате длительного приема гормональных препаратов.
Таким образом, мы видим, что причинами болезни являются проблемы с надпочечниками или гипофизом у собаки.
Некоторые породы имеют особую предрасположенность к возникновению данного синдрома, поэтому владельцам терьеров, биглей, боксеров, овчарок нужно тщательно следить за самочувствием своих питомцев и периодически делать анализы, выявляющие данную патологию.
Симптомы
Синдром Кушинга у собак имеет довольно яркие проявления, сталкиваясь с которыми, ветеринары могут заподозрить наличие этого заболевания у вашего питомца. От внимания хозяев собаки тоже не укроются такие характерные признаки, как:
- патологическая жажда;
- очень частое мочеиспускание, при котором пес не может дотерпеть до прогулки и писается дома;
- чрезмерный аппетит;
- апатия и слабость;
- ослабление мышц живота и провисание его;
- выпадение шерсти, не сопровождающееся зудом;
- нарушение координации и поведения собаки.
Так как болезнь Кушинга является системным заболеванием, то есть затрагивающим практически все органы и системы, то оно сопровождается еще множеством различных симптомов и вызывает различные осложнения. К осложнениям болезни относятся: сахарный диабет, остеопороз, артериальная гипертензия, расстройства репродуктивных органов.
Диагностика
Если заболевание находится уже в поздней стадии, то внешние признаки будут видны невооруженным глазом. Основными способами диагностики синдрома Кушинга является:
Основными способами диагностики синдрома Кушинга является:
- клинический анализ крови;
- определение биохимических показателей крови;
- анализ мочи с определением белка;
- тесты с введением дексаметазона и адренокортикотропного гормона.
Для того чтобы выявить новообразования на надпочечниках собаки проводят УЗИ органов брюшной полости. Если есть подозрение на опухоль гипофиза, то желательно сделать животному КТ или МРТ, чтобы подтвердить или опровергнуть эти опасения.
Лечение
В зависимости от того, поражение какого органа стало причиной синдрома Кушинга, лечение этой болезни может быть консервативным или оперативным.
Если выявленная опухоль надпочечника, то возможно проведение хирургического вмешательства, в процессе которого удаляется надпочечник. При обнаружении проблем с обоими надпочечниками, удалению подвергаются оба органа, и для коррекции гормонального фона собаки ей назначается пожизненный прием лекарств.
При новообразованиях гипофиза рекомендовано лечение с помощью препаратов, подавляющих производство кортизола. Но этот вариант доступен для ограниченного количества собак из-за дороговизны лечения.
Стандартная лекарственная терапия проводится с помощью проверенных на практике препаратов:
- Гормональное средство «Митотан» снижает уровень кортизола. Первоначальная доза его составляет 50 мкг лекарства на один килограмм веса животного. Прием этого количества лекарства можно разделить на 2-3 раза в сутки. Через две недели делается контрольный анализ крови и если ветеринар отмечает снижение кортизола до нормальных показателей, то препарат дают собаке один раз в неделю в той же дозе.
- Другим популярным в ветеринарной практике способом является лечение «Кетоконазолом». Этот препарат особенно показан тем собакам, у которых болезнь спровоцировала возникновение грибка кожи. При лечении происходит поэтапное увеличение дозы: 1 неделя — 10 мкг на 1 килограмм веса (за 2 приема в сутки), 2 неделя — 20 мкг/1 кг, 3 неделя — 30 мкг/1 кг.

При правильно поставленном диагнозе и грамотно подобранном лечении хозяин почти сразу замечает эффект от терапии — собака перестает «пить тазиками», а общее состояние ее улучшается. Если же на фоне лечения состояние питомца ухудшается, то, скорее всего, это вызвано осложнениями заболевания.
Ветеринар для контроля лечения и поиска причин ухудшений назначает повторные анализы и инструментальные исследования.
При ятрогенном виде синдрома необходимо прекращение гормональной терапии. Но проводить отмену нужно постепенно, осторожно снижая дозу лекарства и контролируя состояние собаки с помощью проведения анализов.
Прогноз жизни животного
Как мы уже отмечали, синдром Кушинга у собак — это сложное и коварное заболевание, которое оказывает негативное влияние на все системы организма животного. Оно нарушает функционирование этих систем, снижает сопротивляемость собаки к бактериальным и паразитарным инфекциям.
Отсюда можно сделать вывод, что прогноз жизни для собаки с этим синдромом будет не очень оптимистичным — даже при своевременно начатом лечении она сможет прожить около трех лет.
Не стоит отчаиваться, если вашему питомцу поставлен этот тяжелый диагноз, потому что забота, правильное лечение и хороший уход продлят жизнь собаки еще на несколько лет и подарят вам радость общения с ней.
Интересные темы
Синдром Кушинга — Уход в клинике Мэйо
Лечение синдрома Кушинга в клинике Мэйо
Ваша бригада по уходу в клинике Мэйо
Синдром Кушинга может одновременно влиять на многие различные системы вашего тела, требуя от врачей, обладающих знаниями из многих дисциплин. Врачи клиники Майо, занимающиеся лечением гормональных заболеваний (эндокринологи), работают с нейрохирургами, эндокринными хирургами, радиологами, патологами, онкологами-радиологами и другими специалистами, чтобы предоставить вам наилучший уход с учетом ваших потребностей.
Расширенная диагностика и лечение
Исследователи клиники Майо внесли большой вклад в диагностику и лечение синдрома Кушинга, включая новые методы МРТ для локализации малых опухолей гипофиза, забор образцов каменистой пазухи, эндоскопическую трансназальную хирургию гипофиза, лапароскопическую адреналэктомию и стереотаксическую радиохирургию.
Опыт и рейтинги
Опыт
Ежегодно врачи клиники Мэйо лечат около 500 человек с синдромом Кушинга.
Диапазон вариантов лечения
Новейшие методы лечения, некоторые из которых были разработаны в клинике Мэйо, доступны людям, получающим лечение от синдрома Кушинга в клинике Мэйо. К ним относятся новые методы MRI для локализации небольших опухолей гипофиза, эндоскопическая трансназальная хирургия гипофиза, стереотаксическая радиохирургия и минимально инвазивная операция по удалению надпочечников (лапароскопическая адреналэктомия).
Руководитель исследований
Отделение эндокринологии, диабета, метаболизма и питания клиники Мэйо занимается проблемами гипофиза и надпочечников и поддерживает большую базу данных людей с синдромом Кушинга в надежде предоставить специалистам полезную информацию для более точной оценки и лечения синдрома Кушинга.
Клиника Мэйо в Рочестере, штат Миннесота, занимает первое место по диабету и эндокринологии в рейтинге лучших больниц U.S. News & World Report. Клиника Mayo в Фениксе / Скоттсдейле, штат Аризона, и клиника Mayo в Джексонвилле, штат Флорида, вошли в число лучших больниц для лечения диабета и эндокринологии по версии U.S. News & World Report. Клиника Мэйо также входит в число лучших детских больниц по диабету и эндокринологии.
Расположение, поездки и проживание
Mayo Clinic имеет крупные кампусы в Фениксе и Скоттсдейле, штат Аризона; Джексонвилл, Флорида; и Рочестер, Миннесота.Система здравоохранения клиники Мэйо имеет десятки отделений в нескольких штатах.
Для получения дополнительной информации о посещении клиники Мэйо выберите свое местоположение ниже:
Расходы и страхование
Клиника Мэйо работает с сотнями страховых компаний и является поставщиком услуг внутри сети для миллионов людей.
В большинстве случаев клиника Мэйо не требует направления к врачу. Некоторые страховщики требуют направления или могут иметь дополнительные требования для определенного медицинского обслуживания.Приоритет всех посещений определяется медицинской потребностью.
Узнайте больше о приемах в клинику Мэйо.
Пожалуйста, свяжитесь со своей страховой компанией, чтобы подтвердить медицинское страхование и получить необходимое разрешение до вашего визита. Часто номер службы поддержки вашего страховщика напечатан на обратной стороне вашей страховой карты.
Дополнительная информация о выставлении счетов и страховании:
Клиника Майо в Аризоне, Флориде и Миннесоте
Система здравоохранения клиники Мэйо
Синдром Кушинга: признаки, причины и лечение
Синдром Кушинга или гиперкортизолизм возникает из-за аномально высокого уровня гормона кортизола.Это может произойти по разным причинам.
В большинстве случаев лечение помогает контролировать уровень кортизола.
Наиболее частыми симптомами этого состояния являются:
Помимо перечисленных выше общих симптомов, есть и другие симптомы, которые иногда могут наблюдаться у людей с синдромом Кушинга.
Сюда могут входить:
У детей
У детей тоже может быть синдром Кушинга, хотя он развивается у них реже, чем у взрослых.Согласно исследованию 2019 года, около 10 процентов новых случаев синдрома Кушинга ежегодно возникают у детей.
Помимо вышеперечисленных симптомов, дети с синдромом Кушинга также могут иметь:
У женщин
Синдром Кушинга чаще встречается у женщин, чем у мужчин. По данным Национального института здоровья (NIH), синдром Кушинга заболевает в три раза больше женщин, чем мужчин.
У женщин с синдромом Кушинга могут появиться лишние волосы на лице и теле.
Чаще всего это происходит на:
- лице и шее
- груди
- животе
- бедрах
Кроме того, женщины с синдромом Кушинга также могут испытывать нерегулярные менструации. В некоторых случаях менструация вообще отсутствует. Отсутствие лечения синдрома Кушинга у женщин может затруднить беременность.
В некоторых случаях менструация вообще отсутствует. Отсутствие лечения синдрома Кушинга у женщин может затруднить беременность.
У мужчин
Как и в случае с женщинами и детьми, мужчины с синдромом Кушинга также могут испытывать некоторые дополнительные симптомы.
Мужчины с синдромом Кушинга могут иметь:
Синдром Кушинга вызван избытком гормона кортизола. Ваши надпочечники вырабатывают кортизол.
Он помогает выполнять ряд функций вашего организма, в том числе:
Ваше тело может вырабатывать высокий уровень кортизола по разным причинам, в том числе:
Кортикостероиды
Наиболее частой причиной синдрома Кушинга является прием кортикостероидных препаратов. , например, преднизон, в высоких дозах в течение длительного периода.Медицинские работники могут назначать их для лечения воспалительных заболеваний, таких как волчанка, или для предотвращения отторжения пересаженного органа.
Высокие дозы инъекционных стероидов для лечения боли в спине также могут вызывать синдром Кушинга. Однако более низких доз стероидов в форме ингалянтов, таких как те, которые используются при астме, или кремов, например, прописанных при экземе, обычно недостаточно, чтобы вызвать состояние.
Однако более низких доз стероидов в форме ингалянтов, таких как те, которые используются при астме, или кремов, например, прописанных при экземе, обычно недостаточно, чтобы вызвать состояние.
Опухоли
Некоторые виды опухолей также могут приводить к повышению выработки кортизола.
Вот некоторые из них:
Болезнь Кушинга
Если синдром Кушинга вызван гипофизом, вырабатывающим АКТГ, который, в свою очередь, превращается в кортизол, это называется болезнью Кушинга.
Как и синдром Кушинга, болезнь Кушинга поражает больше женщин, чем мужчин.
Общая цель лечения синдрома Кушинга — снизить уровень кортизола в организме. Этого можно добиться несколькими способами. Лечение, которое вы получите, будет зависеть от причины вашего заболевания.
Ваш лечащий врач может прописать лекарство для контроля уровня кортизола. Некоторые лекарства снижают выработку кортизола в надпочечниках или снижают выработку АКТГ в гипофизе. Другие лекарства блокируют действие кортизола на ваши ткани.
Примеры включают:
- кетоконазол (Низорал)
- митотан (Лизодрен)
- метирапон (Метопирон)
- пасиреотид (Сигнифор)
- мифепристон (Корлым, Мифепрекс)
0 у лиц с диабетом 982 типа или непереносимостью глюкозы 982 Если вы принимаете кортикостероиды, может потребоваться изменение лекарства или дозировки.Не пытайтесь самостоятельно изменить дозировку. Делать это следует под тщательным медицинским наблюдением.
Опухоли могут быть злокачественными, что означает злокачественные, или доброкачественными, что означает доброкачественные.
Если ваше состояние вызвано опухолью, ваш лечащий врач может захотеть удалить опухоль хирургическим путем. Если опухоль не может быть удалена, ваш лечащий врач может также порекомендовать лучевую терапию или химиотерапию.
Синдром Кушинга бывает особенно сложно диагностировать. Это связано с тем, что многие симптомы, такие как увеличение веса или усталость, могут иметь другие причины.
 Кроме того, сам синдром Кушинга может иметь множество различных причин.
Кроме того, сам синдром Кушинга может иметь множество различных причин.Ваш лечащий врач изучит вашу историю болезни. Они зададут вопросы о симптомах, любых состояниях вашего здоровья и лекарствах, которые вам могут прописать.
Они также проведут медицинский осмотр, на котором будут искать такие признаки, как буйволиный горб, растяжки и синяки.
Затем они могут заказать лабораторные тесты, в том числе:
- 24-часовой тест на свободный кортизол в моче: Для этого теста вам будет предложено собрать мочу в течение 24-часового периода.Затем будут проверены уровни кортизола.
- Измерение кортизола в слюне: У людей без синдрома Кушинга уровень кортизола падает вечером. Этот тест измеряет уровень кортизола в образце слюны, который был собран поздно ночью, чтобы увидеть, не слишком ли высокий уровень кортизола.
- Тест на подавление низких доз дексаметазона: Для этого теста вам дадут дозу дексаметазона поздно вечером.
 Утром ваша кровь будет проверена на уровень кортизола.Обычно дексаметазон вызывает снижение уровня кортизола. Если у вас синдром Кушинга, этого не произойдет.
Утром ваша кровь будет проверена на уровень кортизола.Обычно дексаметазон вызывает снижение уровня кортизола. Если у вас синдром Кушинга, этого не произойдет.
Диагностика причины синдрома Кушинга
После того, как вам поставили диагноз синдрома Кушинга, ваш лечащий врач все равно должен определить причину избыточного производства кортизола.
Тесты, помогающие определить причину, могут включать:
- Тест на адренокортикотропиновый гормон (АКТГ) в крови: Измеряются уровни АКТГ в крови.Низкий уровень АДТГ и высокий уровень кортизола могут указывать на наличие опухоли надпочечников.
- Тест на стимуляцию высвобождающего гормона кортикотропина (CRH): В этом тесте делается укол CRH. Это повысит уровень АКТГ и кортизола у людей с опухолями гипофиза.
- Тест подавления с высокой дозой дексаметазона: Это то же самое, что и тест с низкой дозой, за исключением того, что используется более высокая доза дексаметазона.
 Если уровень кортизола падает, возможно, у вас опухоль гипофиза.В противном случае у вас может быть внематочная опухоль.
Если уровень кортизола падает, возможно, у вас опухоль гипофиза.В противном случае у вас может быть внематочная опухоль. - Взятие пробы каменной пазухи: Кровь берется из вены рядом с гипофизом, а также из вены, расположенной далеко от гипофиза. Дан снимок CRH. Высокий уровень АКТГ в крови возле гипофиза может указывать на опухоль гипофиза. Сходные уровни в обоих образцах указывают на внематочную опухоль.
- Визуализирующие исследования: Сюда могут входить такие вещи, как компьютерная томография и МРТ. Они используются для визуализации надпочечников и гипофиза в поисках опухолей.
Хотя изменения в диете не излечивают ваше состояние, они могут помочь предотвратить еще больший рост уровня кортизола или предотвратить некоторые осложнения.
Вот несколько советов по питанию для людей с синдромом Кушинга:
- Следите за потреблением калорий. Отслеживать количество потребляемых калорий важно, поскольку увеличение веса является одним из основных симптомов синдрома Кушинга.

- Старайтесь избегать употребления алкоголя. Согласно исследованию 2007 года, потребление алкоголя связано с повышением уровня кортизола, особенно у сильно пьющих.
- Следите за уровнем сахара в крови. Синдром Кушинга может привести к повышению уровня глюкозы в крови, поэтому старайтесь не есть продукты, которые могут вызвать повышение уровня сахара в крови. Примеры продуктов, на которых стоит сосредоточиться, включают овощи, фрукты, цельнозерновые продукты и рыбу.
- Уменьшите потребление натрия. Синдром Кушинга также связан с высоким кровяным давлением (гипертонией). Из-за этого постарайтесь ограничить потребление натрия. Вот несколько простых способов сделать это: не добавлять соль в пищу и внимательно читать этикетки продуктов, чтобы проверить содержание натрия.
- Убедитесь, что вы получаете достаточно кальция и витамина D. Синдром Кушинга может ослабить ваши кости, что сделает вас склонными к переломам.
 И кальций, и витамин D могут помочь укрепить ваши кости.
И кальций, и витамин D могут помочь укрепить ваши кости.
Основным фактором риска развития синдрома Кушинга является длительный прием высоких доз кортикостероидов. Если ваш лечащий врач прописал кортикостероиды для лечения какого-либо заболевания, спросите его о дозировке и о том, как долго вы будете их принимать.
Другие факторы риска могут включать:
Некоторые случаи синдрома Кушинга связаны с образованием опухоли.Хотя может быть генетическая предрасположенность к развитию эндокринных опухолей (семейный синдром Кушинга), предотвратить образование опухолей невозможно.
Если у вас синдром Кушинга, важно правильно лечить его. Если вы не лечитесь от него, синдром Кушинга может привести к множеству потенциально серьезных осложнений для здоровья.
Сюда могут входить:
Чем раньше вы начнете лечение, тем лучше ожидаемый результат. Важно отметить, что ваше индивидуальное мировоззрение зависит от конкретной причины и лечения, которое вы получаете.

Для улучшения симптомов может потребоваться некоторое время. Обязательно спросите своего врача о рекомендациях по здоровому питанию, записывайтесь на прием к врачу и постепенно повышайте уровень активности.
Группы поддержки могут помочь вам справиться с синдромом Кушинга. Ваша местная больница или поставщик медицинских услуг может предоставить вам информацию о группах, которые встречаются в вашем районе.
Синдром Кушинга: признаки, причины и лечение
Синдром Кушинга или гиперкортизолизм возникает из-за аномально высокого уровня гормона кортизола.Это может произойти по разным причинам.
В большинстве случаев лечение помогает контролировать уровень кортизола.
Наиболее частыми симптомами этого состояния являются:
Помимо перечисленных выше общих симптомов, есть и другие симптомы, которые иногда могут наблюдаться у людей с синдромом Кушинга.
Сюда могут входить:
У детей
У детей тоже может быть синдром Кушинга, хотя он развивается у них реже, чем у взрослых.
 Согласно исследованию 2019 года, около 10 процентов новых случаев синдрома Кушинга ежегодно возникают у детей.
Согласно исследованию 2019 года, около 10 процентов новых случаев синдрома Кушинга ежегодно возникают у детей.Помимо вышеперечисленных симптомов, дети с синдромом Кушинга также могут иметь:
У женщин
Синдром Кушинга чаще встречается у женщин, чем у мужчин. По данным Национального института здоровья (NIH), синдром Кушинга заболевает в три раза больше женщин, чем мужчин.
У женщин с синдромом Кушинга могут появиться лишние волосы на лице и теле.
Чаще всего это происходит на:
- лице и шее
- груди
- животе
- бедрах
Кроме того, женщины с синдромом Кушинга также могут испытывать нерегулярные менструации. В некоторых случаях менструация вообще отсутствует. Отсутствие лечения синдрома Кушинга у женщин может затруднить беременность.
У мужчин
Как и в случае с женщинами и детьми, мужчины с синдромом Кушинга также могут испытывать некоторые дополнительные симптомы.
Мужчины с синдромом Кушинга могут иметь:
Синдром Кушинга вызван избытком гормона кортизола.
 Ваши надпочечники вырабатывают кортизол.
Ваши надпочечники вырабатывают кортизол.Он помогает выполнять ряд функций вашего организма, в том числе:
Ваше тело может вырабатывать высокий уровень кортизола по разным причинам, в том числе:
Кортикостероиды
Наиболее частой причиной синдрома Кушинга является прием кортикостероидных препаратов. , например, преднизон, в высоких дозах в течение длительного периода.Медицинские работники могут назначать их для лечения воспалительных заболеваний, таких как волчанка, или для предотвращения отторжения пересаженного органа.
Высокие дозы инъекционных стероидов для лечения боли в спине также могут вызывать синдром Кушинга. Однако более низких доз стероидов в форме ингалянтов, таких как те, которые используются при астме, или кремов, например, прописанных при экземе, обычно недостаточно, чтобы вызвать состояние.
Опухоли
Некоторые виды опухолей также могут приводить к повышению выработки кортизола.
Вот некоторые из них:
Болезнь Кушинга
Если синдром Кушинга вызван гипофизом, вырабатывающим АКТГ, который, в свою очередь, превращается в кортизол, это называется болезнью Кушинга.

Как и синдром Кушинга, болезнь Кушинга поражает больше женщин, чем мужчин.
Общая цель лечения синдрома Кушинга — снизить уровень кортизола в организме. Этого можно добиться несколькими способами. Лечение, которое вы получите, будет зависеть от причины вашего заболевания.
Ваш лечащий врач может прописать лекарство для контроля уровня кортизола. Некоторые лекарства снижают выработку кортизола в надпочечниках или снижают выработку АКТГ в гипофизе. Другие лекарства блокируют действие кортизола на ваши ткани.
Примеры включают:
- кетоконазол (Низорал)
- митотан (Лизодрен)
- метирапон (Метопирон)
- пасиреотид (Сигнифор)
- мифепристон (Корлым, Мифепрекс)
0 у лиц с диабетом 982 типа или непереносимостью глюкозы 982 Если вы принимаете кортикостероиды, может потребоваться изменение лекарства или дозировки.Не пытайтесь самостоятельно изменить дозировку. Делать это следует под тщательным медицинским наблюдением.

Опухоли могут быть злокачественными, что означает злокачественные, или доброкачественными, что означает доброкачественные.
Если ваше состояние вызвано опухолью, ваш лечащий врач может захотеть удалить опухоль хирургическим путем. Если опухоль не может быть удалена, ваш лечащий врач может также порекомендовать лучевую терапию или химиотерапию.
Синдром Кушинга бывает особенно сложно диагностировать. Это связано с тем, что многие симптомы, такие как увеличение веса или усталость, могут иметь другие причины.Кроме того, сам синдром Кушинга может иметь множество различных причин.
Ваш лечащий врач изучит вашу историю болезни. Они зададут вопросы о симптомах, любых состояниях вашего здоровья и лекарствах, которые вам могут прописать.
Они также проведут медицинский осмотр, на котором будут искать такие признаки, как буйволиный горб, растяжки и синяки.
Затем они могут заказать лабораторные тесты, в том числе:
- 24-часовой тест на свободный кортизол в моче: Для этого теста вам будет предложено собрать мочу в течение 24-часового периода.
 Затем будут проверены уровни кортизола.
Затем будут проверены уровни кортизола. - Измерение кортизола в слюне: У людей без синдрома Кушинга уровень кортизола падает вечером. Этот тест измеряет уровень кортизола в образце слюны, который был собран поздно ночью, чтобы увидеть, не слишком ли высокий уровень кортизола.
- Тест на подавление низких доз дексаметазона: Для этого теста вам дадут дозу дексаметазона поздно вечером. Утром ваша кровь будет проверена на уровень кортизола.Обычно дексаметазон вызывает снижение уровня кортизола. Если у вас синдром Кушинга, этого не произойдет.
Диагностика причины синдрома Кушинга
После того, как вам поставили диагноз синдрома Кушинга, ваш лечащий врач все равно должен определить причину избыточного производства кортизола.
Тесты, помогающие определить причину, могут включать:
- Тест на адренокортикотропиновый гормон (АКТГ) в крови: Измеряются уровни АКТГ в крови.Низкий уровень АДТГ и высокий уровень кортизола могут указывать на наличие опухоли надпочечников.

- Тест на стимуляцию высвобождающего гормона кортикотропина (CRH): В этом тесте делается укол CRH. Это повысит уровень АКТГ и кортизола у людей с опухолями гипофиза.
- Тест подавления с высокой дозой дексаметазона: Это то же самое, что и тест с низкой дозой, за исключением того, что используется более высокая доза дексаметазона. Если уровень кортизола падает, возможно, у вас опухоль гипофиза.В противном случае у вас может быть внематочная опухоль.
- Взятие пробы каменной пазухи: Кровь берется из вены рядом с гипофизом, а также из вены, расположенной далеко от гипофиза. Дан снимок CRH. Высокий уровень АКТГ в крови возле гипофиза может указывать на опухоль гипофиза. Сходные уровни в обоих образцах указывают на внематочную опухоль.
- Визуализирующие исследования: Сюда могут входить такие вещи, как компьютерная томография и МРТ. Они используются для визуализации надпочечников и гипофиза в поисках опухолей.

Хотя изменения в диете не излечивают ваше состояние, они могут помочь предотвратить еще больший рост уровня кортизола или предотвратить некоторые осложнения.
Вот несколько советов по питанию для людей с синдромом Кушинга:
- Следите за потреблением калорий. Отслеживать количество потребляемых калорий важно, поскольку увеличение веса является одним из основных симптомов синдрома Кушинга.
- Старайтесь избегать употребления алкоголя. Согласно исследованию 2007 года, потребление алкоголя связано с повышением уровня кортизола, особенно у сильно пьющих.
- Следите за уровнем сахара в крови. Синдром Кушинга может привести к повышению уровня глюкозы в крови, поэтому старайтесь не есть продукты, которые могут вызвать повышение уровня сахара в крови. Примеры продуктов, на которых стоит сосредоточиться, включают овощи, фрукты, цельнозерновые продукты и рыбу.
- Уменьшите потребление натрия.
 Синдром Кушинга также связан с высоким кровяным давлением (гипертонией). Из-за этого постарайтесь ограничить потребление натрия. Вот несколько простых способов сделать это: не добавлять соль в пищу и внимательно читать этикетки продуктов, чтобы проверить содержание натрия.
Синдром Кушинга также связан с высоким кровяным давлением (гипертонией). Из-за этого постарайтесь ограничить потребление натрия. Вот несколько простых способов сделать это: не добавлять соль в пищу и внимательно читать этикетки продуктов, чтобы проверить содержание натрия. - Убедитесь, что вы получаете достаточно кальция и витамина D. Синдром Кушинга может ослабить ваши кости, что сделает вас склонными к переломам. И кальций, и витамин D могут помочь укрепить ваши кости.
Основным фактором риска развития синдрома Кушинга является длительный прием высоких доз кортикостероидов. Если ваш лечащий врач прописал кортикостероиды для лечения какого-либо заболевания, спросите его о дозировке и о том, как долго вы будете их принимать.
Другие факторы риска могут включать:
Некоторые случаи синдрома Кушинга связаны с образованием опухоли.Хотя может быть генетическая предрасположенность к развитию эндокринных опухолей (семейный синдром Кушинга), предотвратить образование опухолей невозможно.

Если у вас синдром Кушинга, важно правильно лечить его. Если вы не лечитесь от него, синдром Кушинга может привести к множеству потенциально серьезных осложнений для здоровья.
Сюда могут входить:
Чем раньше вы начнете лечение, тем лучше ожидаемый результат. Важно отметить, что ваше индивидуальное мировоззрение зависит от конкретной причины и лечения, которое вы получаете.
Для улучшения симптомов может потребоваться некоторое время. Обязательно спросите своего врача о рекомендациях по здоровому питанию, записывайтесь на прием к врачу и постепенно повышайте уровень активности.
Группы поддержки могут помочь вам справиться с синдромом Кушинга. Ваша местная больница или поставщик медицинских услуг может предоставить вам информацию о группах, которые встречаются в вашем районе.
Синдром Кушинга: признаки, причины и лечение
Синдром Кушинга или гиперкортизолизм возникает из-за аномально высокого уровня гормона кортизола.Это может произойти по разным причинам.

В большинстве случаев лечение помогает контролировать уровень кортизола.
Наиболее частыми симптомами этого состояния являются:
Помимо перечисленных выше общих симптомов, есть и другие симптомы, которые иногда могут наблюдаться у людей с синдромом Кушинга.
Сюда могут входить:
У детей
У детей тоже может быть синдром Кушинга, хотя он развивается у них реже, чем у взрослых.Согласно исследованию 2019 года, около 10 процентов новых случаев синдрома Кушинга ежегодно возникают у детей.
Помимо вышеперечисленных симптомов, дети с синдромом Кушинга также могут иметь:
У женщин
Синдром Кушинга чаще встречается у женщин, чем у мужчин. По данным Национального института здоровья (NIH), синдром Кушинга заболевает в три раза больше женщин, чем мужчин.
У женщин с синдромом Кушинга могут появиться лишние волосы на лице и теле.
Чаще всего это происходит на:
- лице и шее
- груди
- животе
- бедрах
Кроме того, женщины с синдромом Кушинга также могут испытывать нерегулярные менструации.
 В некоторых случаях менструация вообще отсутствует. Отсутствие лечения синдрома Кушинга у женщин может затруднить беременность.
В некоторых случаях менструация вообще отсутствует. Отсутствие лечения синдрома Кушинга у женщин может затруднить беременность.У мужчин
Как и в случае с женщинами и детьми, мужчины с синдромом Кушинга также могут испытывать некоторые дополнительные симптомы.
Мужчины с синдромом Кушинга могут иметь:
Синдром Кушинга вызван избытком гормона кортизола. Ваши надпочечники вырабатывают кортизол.
Он помогает выполнять ряд функций вашего организма, в том числе:
Ваше тело может вырабатывать высокий уровень кортизола по разным причинам, в том числе:
Кортикостероиды
Наиболее частой причиной синдрома Кушинга является прием кортикостероидных препаратов. , например, преднизон, в высоких дозах в течение длительного периода.Медицинские работники могут назначать их для лечения воспалительных заболеваний, таких как волчанка, или для предотвращения отторжения пересаженного органа.
Высокие дозы инъекционных стероидов для лечения боли в спине также могут вызывать синдром Кушинга.
 Однако более низких доз стероидов в форме ингалянтов, таких как те, которые используются при астме, или кремов, например, прописанных при экземе, обычно недостаточно, чтобы вызвать состояние.
Однако более низких доз стероидов в форме ингалянтов, таких как те, которые используются при астме, или кремов, например, прописанных при экземе, обычно недостаточно, чтобы вызвать состояние.Опухоли
Некоторые виды опухолей также могут приводить к повышению выработки кортизола.
Вот некоторые из них:
Болезнь Кушинга
Если синдром Кушинга вызван гипофизом, вырабатывающим АКТГ, который, в свою очередь, превращается в кортизол, это называется болезнью Кушинга.
Как и синдром Кушинга, болезнь Кушинга поражает больше женщин, чем мужчин.
Общая цель лечения синдрома Кушинга — снизить уровень кортизола в организме. Этого можно добиться несколькими способами. Лечение, которое вы получите, будет зависеть от причины вашего заболевания.
Ваш лечащий врач может прописать лекарство для контроля уровня кортизола. Некоторые лекарства снижают выработку кортизола в надпочечниках или снижают выработку АКТГ в гипофизе. Другие лекарства блокируют действие кортизола на ваши ткани.

Примеры включают:
- кетоконазол (Низорал)
- митотан (Лизодрен)
- метирапон (Метопирон)
- пасиреотид (Сигнифор)
- мифепристон (Корлым, Мифепрекс)
0 у лиц с диабетом 982 типа или непереносимостью глюкозы 982 Если вы принимаете кортикостероиды, может потребоваться изменение лекарства или дозировки.Не пытайтесь самостоятельно изменить дозировку. Делать это следует под тщательным медицинским наблюдением.
Опухоли могут быть злокачественными, что означает злокачественные, или доброкачественными, что означает доброкачественные.
Если ваше состояние вызвано опухолью, ваш лечащий врач может захотеть удалить опухоль хирургическим путем. Если опухоль не может быть удалена, ваш лечащий врач может также порекомендовать лучевую терапию или химиотерапию.
Синдром Кушинга бывает особенно сложно диагностировать. Это связано с тем, что многие симптомы, такие как увеличение веса или усталость, могут иметь другие причины.
 Кроме того, сам синдром Кушинга может иметь множество различных причин.
Кроме того, сам синдром Кушинга может иметь множество различных причин.Ваш лечащий врач изучит вашу историю болезни. Они зададут вопросы о симптомах, любых состояниях вашего здоровья и лекарствах, которые вам могут прописать.
Они также проведут медицинский осмотр, на котором будут искать такие признаки, как буйволиный горб, растяжки и синяки.
Затем они могут заказать лабораторные тесты, в том числе:
- 24-часовой тест на свободный кортизол в моче: Для этого теста вам будет предложено собрать мочу в течение 24-часового периода.Затем будут проверены уровни кортизола.
- Измерение кортизола в слюне: У людей без синдрома Кушинга уровень кортизола падает вечером. Этот тест измеряет уровень кортизола в образце слюны, который был собран поздно ночью, чтобы увидеть, не слишком ли высокий уровень кортизола.
- Тест на подавление низких доз дексаметазона: Для этого теста вам дадут дозу дексаметазона поздно вечером.
 Утром ваша кровь будет проверена на уровень кортизола.Обычно дексаметазон вызывает снижение уровня кортизола. Если у вас синдром Кушинга, этого не произойдет.
Утром ваша кровь будет проверена на уровень кортизола.Обычно дексаметазон вызывает снижение уровня кортизола. Если у вас синдром Кушинга, этого не произойдет.
Диагностика причины синдрома Кушинга
После того, как вам поставили диагноз синдрома Кушинга, ваш лечащий врач все равно должен определить причину избыточного производства кортизола.
Тесты, помогающие определить причину, могут включать:
- Тест на адренокортикотропиновый гормон (АКТГ) в крови: Измеряются уровни АКТГ в крови.Низкий уровень АДТГ и высокий уровень кортизола могут указывать на наличие опухоли надпочечников.
- Тест на стимуляцию высвобождающего гормона кортикотропина (CRH): В этом тесте делается укол CRH. Это повысит уровень АКТГ и кортизола у людей с опухолями гипофиза.
- Тест подавления с высокой дозой дексаметазона: Это то же самое, что и тест с низкой дозой, за исключением того, что используется более высокая доза дексаметазона.
 Если уровень кортизола падает, возможно, у вас опухоль гипофиза.В противном случае у вас может быть внематочная опухоль.
Если уровень кортизола падает, возможно, у вас опухоль гипофиза.В противном случае у вас может быть внематочная опухоль. - Взятие пробы каменной пазухи: Кровь берется из вены рядом с гипофизом, а также из вены, расположенной далеко от гипофиза. Дан снимок CRH. Высокий уровень АКТГ в крови возле гипофиза может указывать на опухоль гипофиза. Сходные уровни в обоих образцах указывают на внематочную опухоль.
- Визуализирующие исследования: Сюда могут входить такие вещи, как компьютерная томография и МРТ. Они используются для визуализации надпочечников и гипофиза в поисках опухолей.
Хотя изменения в диете не излечивают ваше состояние, они могут помочь предотвратить еще больший рост уровня кортизола или предотвратить некоторые осложнения.
Вот несколько советов по питанию для людей с синдромом Кушинга:
- Следите за потреблением калорий. Отслеживать количество потребляемых калорий важно, поскольку увеличение веса является одним из основных симптомов синдрома Кушинга.

- Старайтесь избегать употребления алкоголя. Согласно исследованию 2007 года, потребление алкоголя связано с повышением уровня кортизола, особенно у сильно пьющих.
- Следите за уровнем сахара в крови. Синдром Кушинга может привести к повышению уровня глюкозы в крови, поэтому старайтесь не есть продукты, которые могут вызвать повышение уровня сахара в крови. Примеры продуктов, на которых стоит сосредоточиться, включают овощи, фрукты, цельнозерновые продукты и рыбу.
- Уменьшите потребление натрия. Синдром Кушинга также связан с высоким кровяным давлением (гипертонией). Из-за этого постарайтесь ограничить потребление натрия. Вот несколько простых способов сделать это: не добавлять соль в пищу и внимательно читать этикетки продуктов, чтобы проверить содержание натрия.
- Убедитесь, что вы получаете достаточно кальция и витамина D. Синдром Кушинга может ослабить ваши кости, что сделает вас склонными к переломам.
 И кальций, и витамин D могут помочь укрепить ваши кости.
И кальций, и витамин D могут помочь укрепить ваши кости.
Основным фактором риска развития синдрома Кушинга является длительный прием высоких доз кортикостероидов. Если ваш лечащий врач прописал кортикостероиды для лечения какого-либо заболевания, спросите его о дозировке и о том, как долго вы будете их принимать.
Другие факторы риска могут включать:
Некоторые случаи синдрома Кушинга связаны с образованием опухоли.Хотя может быть генетическая предрасположенность к развитию эндокринных опухолей (семейный синдром Кушинга), предотвратить образование опухолей невозможно.
Если у вас синдром Кушинга, важно правильно лечить его. Если вы не лечитесь от него, синдром Кушинга может привести к множеству потенциально серьезных осложнений для здоровья.
Сюда могут входить:
Чем раньше вы начнете лечение, тем лучше ожидаемый результат. Важно отметить, что ваше индивидуальное мировоззрение зависит от конкретной причины и лечения, которое вы получаете.

Для улучшения симптомов может потребоваться некоторое время. Обязательно спросите своего врача о рекомендациях по здоровому питанию, записывайтесь на прием к врачу и постепенно повышайте уровень активности.
Группы поддержки могут помочь вам справиться с синдромом Кушинга. Ваша местная больница или поставщик медицинских услуг может предоставить вам информацию о группах, которые встречаются в вашем районе.
Синдром Кушинга — (гиперкортизолизм) — Эндокринный центр UCLA, Лос-Анджелес, Калифорния
Что такое синдром Кушинга (гиперкортизолизм)?
Определение:
Синдром Кушинга — это заболевание, вызванное повышенной выработкой кортизола или чрезмерным употреблением кортизола или других стероидных гормонов.Альтернативные названия: Гиперкортизолизм
Причины, заболеваемость и факторы риска:
Синдром Кушинга — это состояние, которое возникает в результате избытка кортизола, гормона, вырабатываемого надпочечниками. Наиболее частой причиной синдрома Кушинга является болезнь Кушинга, вызванная чрезмерной выработкой гипофизом гормона АКТГ. АКТГ стимулирует надпочечники вырабатывать кортизол.
Наиболее частой причиной синдрома Кушинга является болезнь Кушинга, вызванная чрезмерной выработкой гипофизом гормона АКТГ. АКТГ стимулирует надпочечники вырабатывать кортизол.Синдром Кушинга может быть вызван опухолью гипофиза, опухолью надпочечников, опухолью где-то еще, кроме гипофиза или надпочечников (эктопический синдром Кушинга), или длительным приемом кортикостероидов (обычно применяемых препаратов). для лечения таких состояний, как ревматоидный артрит и астма).
Факторами риска синдрома Кушинга являются опухоли надпочечников или гипофиза, длительная терапия кортикостероидами и женское начало.
См. Также:
- Болезнь Кушинга (гипофизарный синдром Кушинга)
- Синдром Кушинга — экзогенный
- Эктопический синдром Кушинга
- Синдром Кушинга, вызванный опухолью надпочечников
Симптомы:
- лунное лицо (круглое, красное) и полный)
- буйволиный горб (скопление жира между плечами)
- центральное ожирение с выступающим животом и тонкими конечностями
- увеличение веса (непреднамеренное)
- слабость
- боль в спине
- головная боль
- угри или поверхностные кожные инфекции
- тонкая кожа с легкими синяками
- жажда
- учащенное мочеиспускание
- фиолетовые полосы на коже живота, бедер и груди
- психические изменения
- импотенция или прекращение менструаций
- рост волос на лице
дополнительные симптомы, которые может быть связано с этим заболеванием ase:
- пятна на коже, красные
- покраснение / покраснение кожи
- атрофия мышц
- усталость
- боль или болезненность в костях
- высокое кровяное давление
Признаки и тесты:
Тесты для подтверждения высокого уровня кортизола :
- кортизол, моча
- тест на подавление дексаметазона
- серийные уровни кортизола в сыворотке
Тесты для определения причины:
- ACTH
- МРТ черепа или КТ черепа могут показать опухоль гипофиза
- КТ брюшной полости может показать надпочечники масса
- Общие результаты:
- уровень глюкозы повышен
- анализ калия может быть низким
- количество лейкоцитов может быть повышено
Лечение:
Лечение зависит от причины расстройства. При синдроме Кушинга, вызванном медикаментозной терапией кортикостероидами, дозу препарата необходимо постепенно снижать под наблюдением врача.
При синдроме Кушинга, вызванном медикаментозной терапией кортикостероидами, дозу препарата необходимо постепенно снижать под наблюдением врача.При болезни Кушинга, вызванной опухолью гипофиза, рекомендуется операция по удалению опухоли. Иногда также требуется облучение. После операции необходима заместительная терапия гидрокортизоном (кортизолом). В некоторых случаях становится необходимой пожизненная заместительная терапия кортизолом.
Синдром Кушинга, вызванный опухолью надпочечников, обычно лечится путем хирургического удаления опухоли.Если опухоль не может быть удалена, некоторые лекарства могут подавить секрецию кортизола.
При синдроме Кушинга, вызванном опухолью, секретирующей АКТГ, удаление опухоли — лучший способ лечения синдрома Кушинга. Заместительная терапия кортизолом необходима после операции до возобновления выработки кортизола. В некоторых случаях становится необходимой пожизненная терапия препаратами кортизона.
Группы поддержки:
Ожидания (прогноз):
Удаление опухоли может привести к полному выздоровлению, но есть вероятность рецидива. Выживание людей с внематочными опухолями зависит от общего результата, связанного с конкретным типом опухоли. Без лечения синдром Кушинга может привести к смерти.
Выживание людей с внематочными опухолями зависит от общего результата, связанного с конкретным типом опухоли. Без лечения синдром Кушинга может привести к смерти.Осложнения:
- сахарный диабет
- высокое кровяное давление
- серьезные инфекции
- переломы из-за остеопороза
- камни в почках
- увеличение опухоли гипофиза
Позвоните своему врачу:
поставщик медицинских услуг, если развиваются симптомы, указывающие на синдром Кушинга.Профилактика:
Синдром Кушинга можно предотвратить, зная о связанных с ним симптомах, чтобы можно было обнаружить его на ранней стадии.Болезнь Кушинга (гипофизарный синдром Кушинга)
Что такое болезнь Кушинга (гипофизарный синдром Кушинга)?
Определение:
Гипофиз Кушинга — это состояние, при котором гипофиз (орган эндокринной системы) секретирует избыток адренокортикотропного гормона (АКТГ).
Причины, частота возникновения и факторы риска:
Болезнь Кушинга — это форма синдрома Кушинга, при которой выделяется избыток кортизола (гормона стресса).В случае болезни Кушинга проблема вызвана опухолью или гиперплазией (избыточным ростом) гипофиза. Гипофиз расположен в основании черепа и регулирует деятельность многих желез и процессы в организме.Когда АКТГ секретируется гипофизом, надпочечники выделяют кортизол. При болезни Кушинга слишком много АКТГ, что приводит к избыточному выбросу кортизола. Этот гормон, обычно выделяемый во время стрессовых ситуаций, контролирует использование организмом углеводов, жиров и белков, а также играет роль в подавлении реакции организма на воспаление.
Симптомы:
- Лунное лицо (круглое, красное и полное)
- Буйволиный горб (скопление жира на задней части шеи)
- Центральное ожирение с выступающим животом и тонкими конечностями
- Увеличение веса
- Слабость
- Боль в спине
- Головная боль
- Угри или поверхностные инфекции кожи
- Жажда
- Повышенное мочеиспускание
- Фиолетовые полосы на коже живота, бедер и груди
- Психические изменения
- Импотенция или прекращение менструации
- Чрезмерный рост волос у женщин
Признаки и тесты:
Тесты проводятся для подтверждения гиперкортизолизма, а затем для определения причины. В общем, уровень глюкозы натощак может быть повышен (непереносимость глюкозы), а уровень калия в сыворотке может быть низким.
В общем, уровень глюкозы натощак может быть повышен (непереносимость глюкозы), а уровень калия в сыворотке может быть низким.Эти тесты подтверждают гиперкортизолизм:
- Суточный кортизол мочи
- Суточный креатинин мочи
- Тест на подавление дексаметазона (низкая доза)
- Серийные уровни кортизола в сыворотке, которые не показывают суточных изменений
Уровни кортизола в слюне в ночное время
- Уровни АКТГ в сыворотке
- МРТ-сканирование черепа, показывающее опухоль гипофиза
- Тест CRH
- Взятие пробы каменной пазухи
- Тест на подавление дексаметазона (высокая доза)
- Высокое кровяное давление
- Диабет
- Инфекции
- Компрессионные переломы
- Камни в почках
- Психоз
Эти тесты определяют причину:
Лечение:
Лечение по возможности хирургическим удалением опухоли гипофиза.После операции функция гипофиза может постепенно прийти в норму.Потребность в заместительной терапии гидрокортизоном может стать очевидной в процессе выздоровления.
 Также может использоваться облучение гипофиза.
Также может использоваться облучение гипофиза.Если опухоль не реагирует на хирургическое вмешательство или облучение, назначаются лекарства, подавляющие синтез кортизола.
Группы поддержки:
Ожидания (прогноз):
Без лечения болезнь Кушинга может вызвать тяжелое заболевание, даже смерть.Удаление опухоли может привести к полному выздоровлению, но может произойти повторный рост опухоли.Осложнения:
Звонок своему врачу:
Если у вас появятся симптомы, позвоните своему врачу гипофиза Кушинга.Если вам удалили опухоль гипофиза, позвоните, если появятся признаки осложнений, в том числе признаки рецидива опухоли.
Синдром Кушинга — familydoctor.org
Самая частая причина синдрома Кушинга — прием кортикостероидных препаратов (таблеток) каждый день в течение недель или месяцев.
 Эти лекарства обычно используются для лечения воспалительных заболеваний, таких как астма, волчанка и ревматоидный артрит.
Эти лекарства обычно используются для лечения воспалительных заболеваний, таких как астма, волчанка и ревматоидный артрит.Ингаляционные стероидные препараты от астмы и стероидные кремы для кожи обычно не вызывают синдром Кушинга. Эти формы используются для лечения экземы, и других кожных заболеваний. Даже таблетки, принимаемые каждый день в течение короткого периода времени или через день в течение длительного периода, не часто вызывают синдром Кушинга.
Следующей по частоте причиной синдрома Кушинга является выработка организмом слишком большого количества кортизола. Это может быть один надпочечник, производящий слишком много кортизола, или оба надпочечника. Это перепроизводство может быть вызвано опухолью » rel=»tooltip»> на гипофизе. Опухоли гипофиза, вызывающие синдром Кушинга, обычно не являются злокачественными (раковыми). Однако, если эти опухоли станут слишком большими, они могут вызвать проблемы со зрением.
Синдром Кушинга также может быть вызван другими опухолями в вашем теле.Внематочные опухоли, продуцирующие АКТГ, могут быть злокачественными или доброкачественными, (не злокачественными). Они выделяют слишком много гормона АКТГ. Это говорит вашему организму вырабатывать больше кортизола. Не так много известно о причинах возникновения опухолей. Если ваше тело не получает достаточного количества АКТГ, уровень кортизола снизится. Когда это происходит, надпочечники сокращаются. Это может привести к другому заболеванию, называемому болезнью Аддисона.
Первичное заболевание или расстройство надпочечников также может вызывать синдром Кушинга.При этом типе заболевания ваши железы вырабатывают слишком много или слишком мало кортизола.

- 24-часовой тест на свободный кортизол в моче: Для этого теста вам будет предложено собрать мочу в течение 24-часового периода.

 (моча), сут.
(моча), сут. Если причиной развития синдрома Кушинга является опухоль, врач рекомендует ее полное удаление. Опухолями питуитарной железы обычно занимаются нейрохирурги. Они проводят трансназальное удаление опухоли. Опухоли надпочечников, легких и поджелудочной железы удаляют хирурги. Проводятся полостные операции, реже используются малоинвазивные хирургические техники, предполагающие небольшие разрезы.
Если причиной развития синдрома Кушинга является опухоль, врач рекомендует ее полное удаление. Опухолями питуитарной железы обычно занимаются нейрохирурги. Они проводят трансназальное удаление опухоли. Опухоли надпочечников, легких и поджелудочной железы удаляют хирурги. Проводятся полостные операции, реже используются малоинвазивные хирургические техники, предполагающие небольшие разрезы.  Если в ходе операции опухоль не была полностью удалена, врач может назначить вам курс лучевой терапии. Кроме того, лучевая терапия проводится тем больным, у кого есть противопоказания к операции.
Если в ходе операции опухоль не была полностью удалена, врач может назначить вам курс лучевой терапии. Кроме того, лучевая терапия проводится тем больным, у кого есть противопоказания к операции. Происходит истончение кожи, ухудшается заживление ран.
Происходит истончение кожи, ухудшается заживление ран. У некоторых людей причиной синдрома Иценко-Кушинга является нарушение функции надпочечников. Наиболее распространенная патология – доброкачественная опухоль коры надпочечников, или аденома. У женщин она встречается в 4-5 раз чаще, чем у мужчин. Средний возраст, в котором аденома образуется чаще всего – 40 лет.
У некоторых людей причиной синдрома Иценко-Кушинга является нарушение функции надпочечников. Наиболее распространенная патология – доброкачественная опухоль коры надпочечников, или аденома. У женщин она встречается в 4-5 раз чаще, чем у мужчин. Средний возраст, в котором аденома образуется чаще всего – 40 лет.


 Кроме того, сам синдром Кушинга может иметь множество различных причин.
Кроме того, сам синдром Кушинга может иметь множество различных причин. Утром ваша кровь будет проверена на уровень кортизола.Обычно дексаметазон вызывает снижение уровня кортизола. Если у вас синдром Кушинга, этого не произойдет.
Утром ваша кровь будет проверена на уровень кортизола.Обычно дексаметазон вызывает снижение уровня кортизола. Если у вас синдром Кушинга, этого не произойдет. Если уровень кортизола падает, возможно, у вас опухоль гипофиза.В противном случае у вас может быть внематочная опухоль.
Если уровень кортизола падает, возможно, у вас опухоль гипофиза.В противном случае у вас может быть внематочная опухоль.
 И кальций, и витамин D могут помочь укрепить ваши кости.
И кальций, и витамин D могут помочь укрепить ваши кости.
 Согласно исследованию 2019 года, около 10 процентов новых случаев синдрома Кушинга ежегодно возникают у детей.
Согласно исследованию 2019 года, около 10 процентов новых случаев синдрома Кушинга ежегодно возникают у детей. Ваши надпочечники вырабатывают кортизол.
Ваши надпочечники вырабатывают кортизол.

 Затем будут проверены уровни кортизола.
Затем будут проверены уровни кортизола.

 Синдром Кушинга также связан с высоким кровяным давлением (гипертонией). Из-за этого постарайтесь ограничить потребление натрия. Вот несколько простых способов сделать это: не добавлять соль в пищу и внимательно читать этикетки продуктов, чтобы проверить содержание натрия.
Синдром Кушинга также связан с высоким кровяным давлением (гипертонией). Из-за этого постарайтесь ограничить потребление натрия. Вот несколько простых способов сделать это: не добавлять соль в пищу и внимательно читать этикетки продуктов, чтобы проверить содержание натрия.

 В некоторых случаях менструация вообще отсутствует. Отсутствие лечения синдрома Кушинга у женщин может затруднить беременность.
В некоторых случаях менструация вообще отсутствует. Отсутствие лечения синдрома Кушинга у женщин может затруднить беременность. Однако более низких доз стероидов в форме ингалянтов, таких как те, которые используются при астме, или кремов, например, прописанных при экземе, обычно недостаточно, чтобы вызвать состояние.
Однако более низких доз стероидов в форме ингалянтов, таких как те, которые используются при астме, или кремов, например, прописанных при экземе, обычно недостаточно, чтобы вызвать состояние.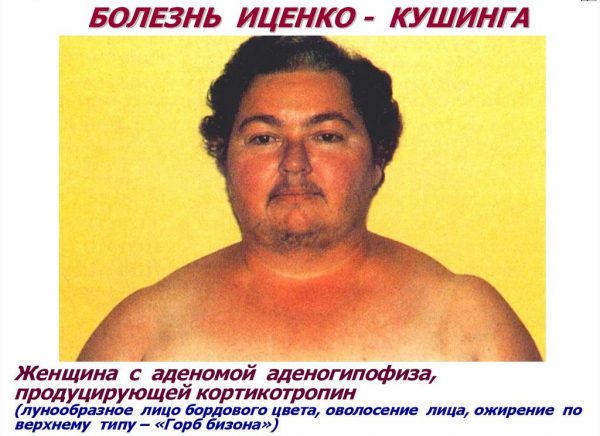
 Кроме того, сам синдром Кушинга может иметь множество различных причин.
Кроме того, сам синдром Кушинга может иметь множество различных причин. Утром ваша кровь будет проверена на уровень кортизола.Обычно дексаметазон вызывает снижение уровня кортизола. Если у вас синдром Кушинга, этого не произойдет.
Утром ваша кровь будет проверена на уровень кортизола.Обычно дексаметазон вызывает снижение уровня кортизола. Если у вас синдром Кушинга, этого не произойдет. Если уровень кортизола падает, возможно, у вас опухоль гипофиза.В противном случае у вас может быть внематочная опухоль.
Если уровень кортизола падает, возможно, у вас опухоль гипофиза.В противном случае у вас может быть внематочная опухоль.
 И кальций, и витамин D могут помочь укрепить ваши кости.
И кальций, и витамин D могут помочь укрепить ваши кости.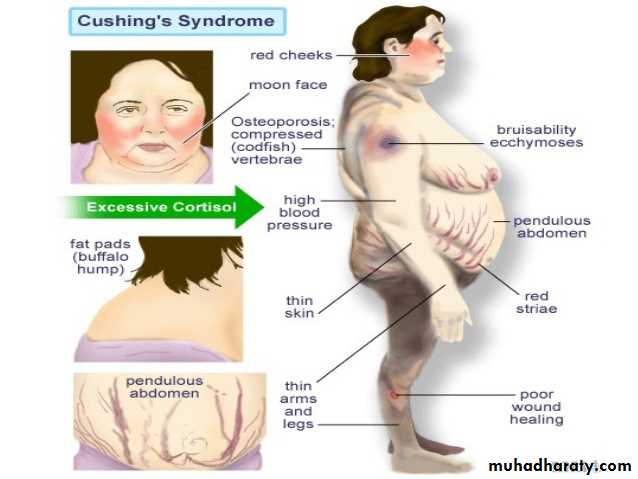
 Наиболее частой причиной синдрома Кушинга является болезнь Кушинга, вызванная чрезмерной выработкой гипофизом гормона АКТГ. АКТГ стимулирует надпочечники вырабатывать кортизол.
Наиболее частой причиной синдрома Кушинга является болезнь Кушинга, вызванная чрезмерной выработкой гипофизом гормона АКТГ. АКТГ стимулирует надпочечники вырабатывать кортизол. При синдроме Кушинга, вызванном медикаментозной терапией кортикостероидами, дозу препарата необходимо постепенно снижать под наблюдением врача.
При синдроме Кушинга, вызванном медикаментозной терапией кортикостероидами, дозу препарата необходимо постепенно снижать под наблюдением врача. Выживание людей с внематочными опухолями зависит от общего результата, связанного с конкретным типом опухоли. Без лечения синдром Кушинга может привести к смерти.
Выживание людей с внематочными опухолями зависит от общего результата, связанного с конкретным типом опухоли. Без лечения синдром Кушинга может привести к смерти.
 В общем, уровень глюкозы натощак может быть повышен (непереносимость глюкозы), а уровень калия в сыворотке может быть низким.
В общем, уровень глюкозы натощак может быть повышен (непереносимость глюкозы), а уровень калия в сыворотке может быть низким. Также может использоваться облучение гипофиза.
Также может использоваться облучение гипофиза. Эти лекарства обычно используются для лечения воспалительных заболеваний, таких как астма, волчанка и ревматоидный артрит.
Эти лекарства обычно используются для лечения воспалительных заболеваний, таких как астма, волчанка и ревматоидный артрит.