УФ-светодиоды в сельском хозяйстве
За последнее десятилетие рынок ультрафиолетовых (УФ) светодиодов увеличился в пять раз и к 2025 году, согласно прогнозам, превысит $1 млрд. Ключевой тенденцией, которая, как ожидается, будет влиять на рынок, является возникновение новых областей применения таких устройств, например сельское хозяйство. Ультрафиолетовый свет, при подходящей частоте и дозе, может увеличить производство активных веществ в лекарственных растениях и традиционных культурах и способствовать поддержанию здоровой среды для роста растений. Но для того, чтобы воспользоваться преимуществами УФ-светодиодов в полной мере, при проектировании необходимо учитывать некоторые значимые аспекты.
Вследствие бурного роста, происходящего в тепличном и городском растениеводстве, светодиоды становятся привлекательными источниками света, прежде всего из-за их энергоэкономичности, однако достижения в области УФ-светодиодов позволяют получить дополнительные преимущества от УФ-А- и УФ-В-излучения. Доказано, что воздействие ультрафиолета приводит к увеличению активных веществ в лекарственных растениях, включая антиоксидантные свойства многочисленных растений и содержание ТГК (тетрагидроканнабинола) в конопле. Ультрафиолетовый свет также помогает поддерживать здоровую среду, подавляя плесень, ложную мучнистую росу и некоторых вредителей растений во всех случаях, когда необходима альтернатива химическим веществам из-за повышения устойчивости к фунгицидам. В то время как многие из распространенных светильников, используемых в тепличном сельском хозяйстве, имеют в спектре определенный (хотя и небольшой) уровень ультрафиолетового излучения, материалы линз блокируют большую, если не всю часть этого УФ-света. Поскольку цена УФ-светодиодов продолжает снижаться, улучшается возможность экономически эффективно включать в процесс выращивания растений целенаправленное облучение ультрафиолетом с требуемой длиной волны, правильной дозой и в соответствующий период жизненного цикла конкретных видов растений.
Доказано, что воздействие ультрафиолета приводит к увеличению активных веществ в лекарственных растениях, включая антиоксидантные свойства многочисленных растений и содержание ТГК (тетрагидроканнабинола) в конопле. Ультрафиолетовый свет также помогает поддерживать здоровую среду, подавляя плесень, ложную мучнистую росу и некоторых вредителей растений во всех случаях, когда необходима альтернатива химическим веществам из-за повышения устойчивости к фунгицидам. В то время как многие из распространенных светильников, используемых в тепличном сельском хозяйстве, имеют в спектре определенный (хотя и небольшой) уровень ультрафиолетового излучения, материалы линз блокируют большую, если не всю часть этого УФ-света. Поскольку цена УФ-светодиодов продолжает снижаться, улучшается возможность экономически эффективно включать в процесс выращивания растений целенаправленное облучение ультрафиолетом с требуемой длиной волны, правильной дозой и в соответствующий период жизненного цикла конкретных видов растений.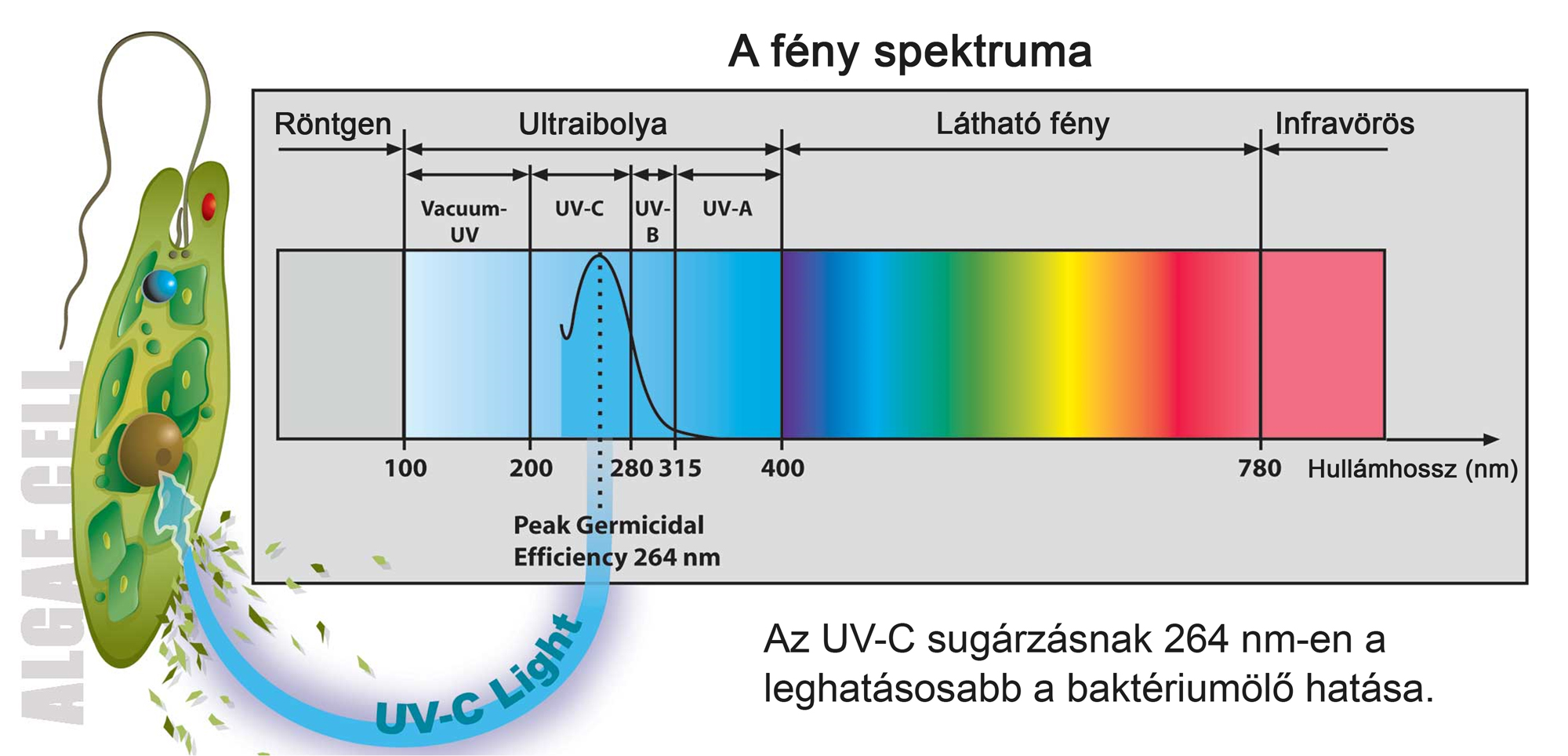 Однако УФ-светодиоды по-прежнему необходимо применять в сочетании с подходящими линзами, которые могут пропускать УФ-излучение без риска деградации или разрушения линзы и/или самого светодиода.
Однако УФ-светодиоды по-прежнему необходимо применять в сочетании с подходящими линзами, которые могут пропускать УФ-излучение без риска деградации или разрушения линзы и/или самого светодиода.
Введение
История и длины волн Ультрафиолетовый (УФ) свет является основной частью электромагнитного спектра с длиной волны 10-400 нм (рис. 1), невидимой для человеческого глаза, хотя некоторые области УФ-излучения воспринимаются насекомыми и птицами. Большая часть ультрафиолетового спектра, включая весь экстремальный ультрафиолетовый (10-100 нм) и большую часть спектра с длиной волны менее 280 нм, поглощается атмосферой.
Рис. 1 Шкала видимого и ультрафиолетового излучения с диапазонами УФ-излучения
Т
ем не менее по-прежнему важно понимать преимущества каждой области УФ-спектра, учитывая нашу способность искусственно воспроизводить эти длины волн.
Классификация УФ-спектра, использование и преимущества
•УФ-С (200-280 нм) — почти полностью поглощается земной атмосферой, обычно применяется для обеззараживания;
•УФ-В (280-320 нм) — приблизительно 95% УФ-В поглощается земной атмосферой. Широко известен в связи с повышенным риском развития рака кожи, однако также было обнаружено, что он имеет противомикробное действие, включая борьбу с сельскохозяйственными инфекциями и вредителями, такими как мучнистая роса и паутинные клещи; кроме того, он инициирует ответную реакцию растений, которые увеличивают производство флавоноидов и каннабиноидов;
Широко известен в связи с повышенным риском развития рака кожи, однако также было обнаружено, что он имеет противомикробное действие, включая борьбу с сельскохозяйственными инфекциями и вредителями, такими как мучнистая роса и паутинные клещи; кроме того, он инициирует ответную реакцию растений, которые увеличивают производство флавоноидов и каннабиноидов;
•УФ-А (320-400 нм) — часто называемый черным светом, УФ-А имеет самую большую длину волны в УФ-спектре и считается наименее вредным. Он наиболее известен своим применением в УФ-отверждении, обнаружении подделок и судебной экспертизе, но также применяется в сельском хозяйстве из-за его способности запускать желаемые реакции у растений.
Последние достижения
В индустрии ультрафиолетового освещения в основном преобладают источники, отличные от светодиодов, обычно это ртутные лампы. Однако в последние годы наблюдается значительный прогресс УФ-светодиодов не только благодаря достижениям в производстве твердотельных УФ-устройств, но и в результате повышенного внимания к поиску более экологически чистых и энергосберегающих способов получения УФ-излучения.
Однако только недавно светодиоды смогли покрыть все диапазоны ультрафиолетового излучения. Светодиоды, излучающие ультрафиолет в верхней части диапазона УФ-А (390-420 нм), доступны с конца 1990-х годов, они, как правило, используются для обнаружения фальшивых купюр, проверки водительских прав и документов, а также в судебной экспертизе. Фактически на большой части рынка УФ-светодиодов преобладают такие применения, как отверждение красок, покрытий или адгезивов с помощью УФ-А-излучения в диапазоне 350-390 нм.
При переходе на более короткие длины волн — UV-В и UV-C — область применения меняется на дезинфекцию продуктов питания, воздуха, воды и поверхностей. Хотя УФ-излучение имеет долгую, хорошо известную историю обеззараживающего воздействия, светодиоды в этом диапазоне стали использоваться совсем недавно (первая коммерческая система обеззараживания воды на основе УФ-С-светодиодов введена в эксплуатацию в 2012 году). Для многих отраслей промышленности, таких как очистка воды, привлекательна не только экономия энергии, которую дают светодиоды; чрезвычайно маленькие размеры светодиодов делают их очень гибкими в использовании, включая возможность создания переносных систем дезинфекции.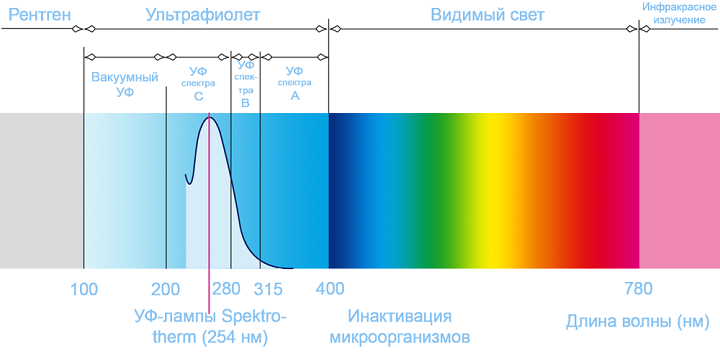 Благодаря этим достижениям за последнее десятилетие рынок УФ-светодиодов увеличился в пять раз, и прогнозируется, что к 2025 году вырастет до $1,3 млрд. Ключевая тенденция, которая, как ожидается, будет влиять на рынок, — это способность находить новые применения, включая изделия для солнечной энергетики, пищевую промышленность и производство напитков, а также сельское хозяйство. Однако по-прежнему необходимы дополнительные улучшения (особенно в том, что касается линз для этих изделий), позволяющие гарантировать, что технология может достичь желаемых результатов в каждой отрасли экономически эффективным образом.
Благодаря этим достижениям за последнее десятилетие рынок УФ-светодиодов увеличился в пять раз, и прогнозируется, что к 2025 году вырастет до $1,3 млрд. Ключевая тенденция, которая, как ожидается, будет влиять на рынок, — это способность находить новые применения, включая изделия для солнечной энергетики, пищевую промышленность и производство напитков, а также сельское хозяйство. Однако по-прежнему необходимы дополнительные улучшения (особенно в том, что касается линз для этих изделий), позволяющие гарантировать, что технология может достичь желаемых результатов в каждой отрасли экономически эффективным образом.
Преимущества ультрафиолетового излучения для сельского хозяйства
С бурным развитием, происходящим в тепличном и городском сельском хозяйстве, растет стремление продолжать совершенствовать процесс выращивания растений экономически эффективным способом, который по-прежнему будет давать положительные результаты. Значительная часть существующих исследований по использованию светодиодов в сельском хозяйстве сосредоточена на длинах волн видимого света и спектра, который необходим растениям для различных процессов. В ходе масштабных исследований «NASA определило, что светодиодные светильники являются лучшими источниками света для выращивания растений как на Земле, так и в космосе». Фактически выполнена большая работа по изучению того, как различные длины волн влияют на рост растений. Эта информация позволит обеспечить дальнейшее развитие освещения со специализированным спектром, которое дает более высокие результаты в выращивании растений при меньших затратах энергии. Например, было определено, что красный свет (630-660 нм) необходим для роста стебля и увеличения размера листьев. Эта же длина волны регулирует периоды цветения и покоя.
В ходе масштабных исследований «NASA определило, что светодиодные светильники являются лучшими источниками света для выращивания растений как на Земле, так и в космосе». Фактически выполнена большая работа по изучению того, как различные длины волн влияют на рост растений. Эта информация позволит обеспечить дальнейшее развитие освещения со специализированным спектром, которое дает более высокие результаты в выращивании растений при меньших затратах энергии. Например, было определено, что красный свет (630-660 нм) необходим для роста стебля и увеличения размера листьев. Эта же длина волны регулирует периоды цветения и покоя.
В то время как первые светодиоды были далеки от того, чтобы удовлетворять потребности и растений, и самих растениеводов, самые современные светодиоды стали основой практичных решений для выращивания в помещениях, обеспечивая значительную экономию средств (при условии использования линз из правильного материала), особенно по сравнению с традиционными системами освещения, такими как натриевые газоразрядные лампы высокого давления (НЛВД).
Одновременно непрерывное улучшение УФ-светодиодов позволяет получать преимущества, которые дает ультрафиолетовый свет, особенно УФ-А и УФ-В, в процессе выращивания растений в помещении (рис. 2). Исследователи обнаружили, что в отсутствие ультрафиолетового света у некоторых видов растений могут «развиваться наросты на листьях и наблюдаться деформация тканей». Например, обычное стекло блокирует более 90% УФ-В излучения, поэтому выращивание растений в теплицах или других подобных средах без дополнительного освещения может иметь неблагоприятные последствия.
Рис. 2 УФ-излучение может увеличить количество активных веществ в лекарственных растениях, например повысить антиоксидантные свойства розмарина или уровень ТГК в конопле
Было также показано, что воздействие ультрафиолетового света приводит к увеличению производства активных веществ в лекарственных растениях, в частности к повышению антиоксидантных свойств многих растений или уровня ТГК в конопле. В растениях протекают химические процессы, при этом разные длины волн света вызывают определенные реакции, включая реакции на УФ-излучение, которые могут приводить к изменению формы растения и его химического состава. Однако, чтобы действительно понять все последствия, включая лучшие методы внедрения, эта область фотоники по-прежнему нуждается в проведении огромного объема исследований.
В растениях протекают химические процессы, при этом разные длины волн света вызывают определенные реакции, включая реакции на УФ-излучение, которые могут приводить к изменению формы растения и его химического состава. Однако, чтобы действительно понять все последствия, включая лучшие методы внедрения, эта область фотоники по-прежнему нуждается в проведении огромного объема исследований.
Одной из наиболее распространенных реакций растений на УФ-излучение является синтез и накопление УФ- поглощающих соединений. Эти соединения, в том числе фенольные вещества, действуют как солнцезащитный крем для растений, предотвращая повреждение из-за чрезмерного воздействия УФ- излучения. Однако фенольные соединения не только защищают растения, они полезны для здоровья человека, включая антиоксидантные свойства и профилактику различных хронических заболеваний,таких как некоторые виды рака и сердечно-сосудистые заболевания. Изучается воздействие ресвератрола, найденного в винограде и красном вине, на здоровье сердца, иммунную систему и даже функции мозга. Исследование розмарина показало, что общее содержание в нем фенольных соединений приблизительно удваивается при выращивании с использованием УФ-В-излучения. Аналогично увеличилось содержание эфирных масел при таком выращивании Mentha spicata (мяты).
Исследование розмарина показало, что общее содержание в нем фенольных соединений приблизительно удваивается при выращивании с использованием УФ-В-излучения. Аналогично увеличилось содержание эфирных масел при таком выращивании Mentha spicata (мяты).
Другой вид растений, известный увеличением лекарственных соединений под УФ-излучением, это конопля посевная. Исследования показали, что более высокие уровни каннабиноидов обнаружены у растений на самых низких экваториальных широтах и на больших высотах (на 32% больше на высоте 3350 м, чем на 1500 м). Было установлено, что эти регионы имеют более высокие уровни УФ-В. Последующие исследования показали, что облучение растений УФ-В повышает на 48% в тканях листьев и 32% в цветах уровень Д9-тетрагидроканнабинола (А9-ТГК), который имеет широкое лекарственное применение.
Ультрафиолетовый свет также помогает поддерживать здоровую среду, подавляя плесень, ложную мучнистую росу и некоторых вредителей растений во всех случаях, когда необходима альтернатива химическим веществам из-за повышения устойчивости к фунгицидам. УФ-поглощающие соединения, производимые растениями для их защиты от слишком большого количества УФ- излучения, также могут помочь в защите растений от инфекций, травм и некоторых вредителей. Эти соединения как будто изменяют «привлекательность» растений для вредителей.
УФ-поглощающие соединения, производимые растениями для их защиты от слишком большого количества УФ- излучения, также могут помочь в защите растений от инфекций, травм и некоторых вредителей. Эти соединения как будто изменяют «привлекательность» растений для вредителей.
Одной из основных угроз для производителей, выращивающих растения в помещениях, является мучнистая роса. Было доказано, что УФ-излучение значительно уменьшает поражение растений мучнистой росой, начиная от винограда, роз, огурцов, розмарина и заканчивая клубникой. Исследователи успешно уменьшили тяжесть поражения мучнистой росой на 90-99%, используя подходящие дозы УФ-В- излучения.
УФ-В-излучение доказало свою эффективность и для сокращения выживаемости и количества яиц паутинных клещей — вредителей, которые, как известно, разрушают целые посевы. В исследовании Ohtsuka и Osakabe менее 6% подвергшихся воздействию доз УФ-В личинок выжили на второй день, а на третий день эксперимента погибли все личинки.
Третьей серьезной угрозой является Botrytis cinerea, тип серой плесени, часто называемой серой гнилью, которая может поражать 200 различных видов, как правило, это фрукты или цветы, включая клубнику, виноград и коноплю. Этот вредитель заносится, как правило, с улицы, в помещение для выращивания растений он попадает по воздуху или на обуви и одежде. Борьба с этим вредителем может включать использование системы дезинфекции воздуха и/или дезинфекции пола. Исследования показали, что очищение от спор Botrytis cinerea наиболее эффективно происходит с помощью облучения УФ-С. Mercier и соавторы (2001) с дозами УФ-С 440-2200 Дж/м2 достигли уровня дезинфекции более 90 %.
Этот вредитель заносится, как правило, с улицы, в помещение для выращивания растений он попадает по воздуху или на обуви и одежде. Борьба с этим вредителем может включать использование системы дезинфекции воздуха и/или дезинфекции пола. Исследования показали, что очищение от спор Botrytis cinerea наиболее эффективно происходит с помощью облучения УФ-С. Mercier и соавторы (2001) с дозами УФ-С 440-2200 Дж/м2 достигли уровня дезинфекции более 90 %.
За последние несколько десятилетий значительно увеличился объем данных, подтверждающих пользу УФ-излучения для защиты сельскохозяйственных культур от плесени, ложной мучнистой росы и других вредителей растений, а также способность повышать лекарственные свойства растений (рис. 3). Однако по-прежнему существуют серьезные проблемы с тем, как успешно внедрить УФ-излучение в помещения для выращивания растений.
Рис. 3 Мучнистая роса и клещи представляют серьезную угрозу для многих культур но их количество может быть существенно уменьшено с помощью УФ-излучения
Соображения по интеграции УФ в освещение для теплиц
Ультрафиолетовая светодиодная система должна учитывать специфические требования к дозе ультрафиолетового излучения, необходимой длине волны и размещению источника излучения относительно растений.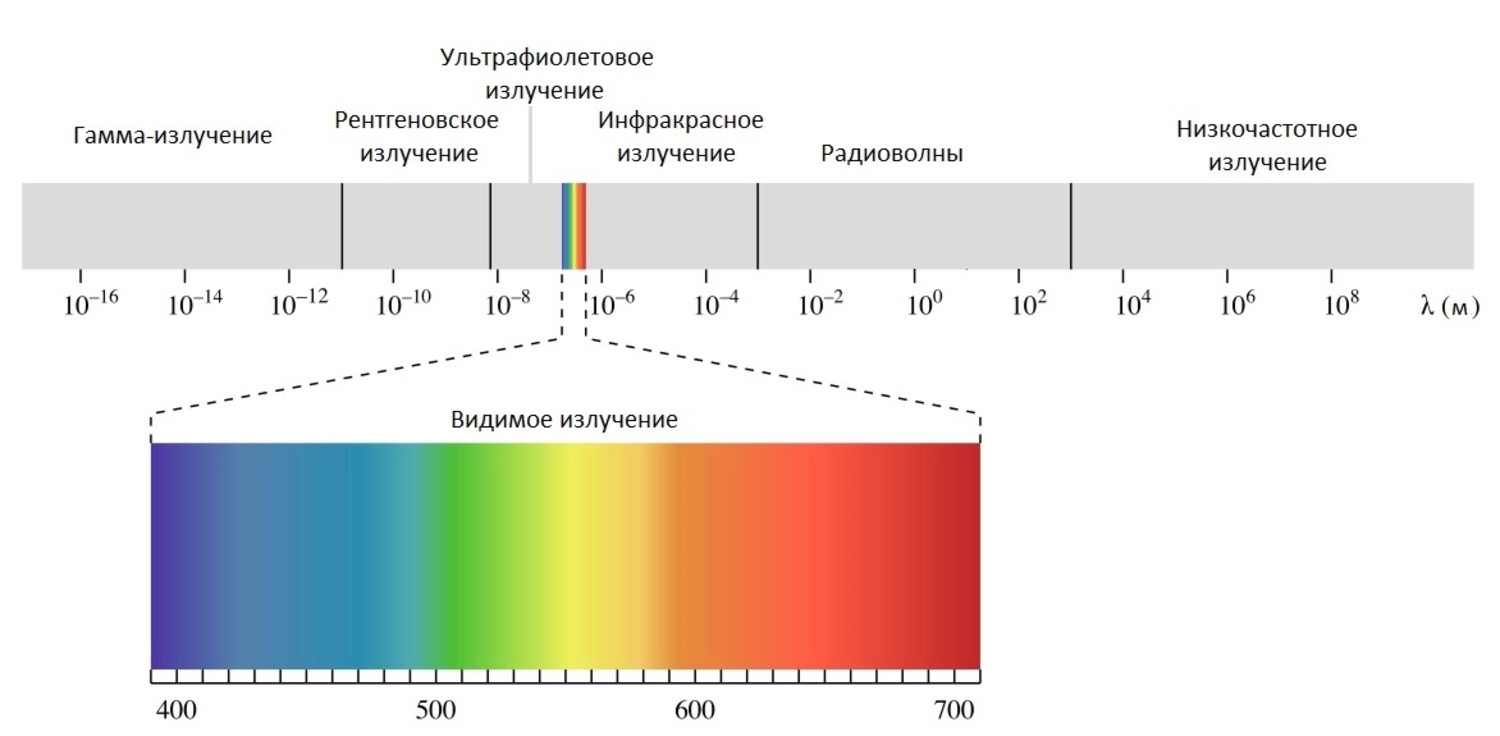 Также следует помнить об отведении тепла, конструкции оптики, источнике питания и драйвере и, самое главное, о материале линзы.
Также следует помнить об отведении тепла, конструкции оптики, источнике питания и драйвере и, самое главное, о материале линзы.
Определение необходимой дозы и длины волны
При выращивании растений в помещениях важно определить спектр, который наилучшим образом отвечает потребностям растений, поскольку потребность в разных длинах волн зависит от того, на какой стадии роста находятся растения и какого они вида. Например, в видимом спектре небольшой процент зеленого света (до 24% для некоторых видов) может быть полезен для стимуляции роста растений, но исследования показали, что он видоспецифичен и доле свыше 50% может вызывать пагубные последствия. То же самое верно и при включении УФ-излучения в сельскохозяйственное освещение — надо четко понимать, в чем именно нуждаются растения.
В некоторых случаях может потребоваться интеграция источника УФ-излучения в первичный источник освещения. Например, ресвератрол, лекарственное вещество, производимое растениями в ответ на стресс, получается в ходе химической реакции, которая требует УФ-А- излучения с длиной волны ниже 360 нм. Производители, заинтересованные в повышении уровня специфических флавоноидов или каннабиноидов, скорее всего, захотят использовать УФ-А, УФ-В или их комбинацию для достижения необходимого эффекта.
Производители, заинтересованные в повышении уровня специфических флавоноидов или каннабиноидов, скорее всего, захотят использовать УФ-А, УФ-В или их комбинацию для достижения необходимого эффекта.
Если производитель заинтересован в предотвращении заражения конкретными вредителями растений, таких как мучнистая роса и паутинные клещи, в борьбе с ними решающее значение может иметь дополнительное облучение конкретными дозами УФ-В-излучения. Для лечения Botrytis cinerea ультрафиолетовое излучение можно интегрировать в системы, предназначенные для дезинфекции воздуха помещений, или использовать в качестве отдельного дополнительного облучения, применяемого в рамках регулярных циклов лечения растений дозами УФ-С. Принимая во внимание различные потребности и применения УФ-излучения в сельском хозяйстве, важно сотрудничать с компаниями — изготовителями облучающих устройств, которые понимают тонкости применения УФ-излучения как для увеличения роста растений, так и для дезинфекции и борьбы с вредителями.
Измерение светового потока
Независимо от того, оцениваете ли вы светильник или отдельные светодиодные компоненты, общая методология включает сравнение значений потока излучения, указываемых различными производителями. Однако следует проявлять особую осторожность и убедиться, что вы действительно сравниваете одно и то же измерение по различным параметрам, и имейте в виду, что многие компании недостаточно раскрывают параметры испытаний, включая наиболее важный фактор, называемый расстоянием. Не контролируя различия в этих параметрах, сравнивать числа бессмысленно.
Кроме того, многие из датчиков, представленных на рынке, предназначены только для измерения конкретных частей электромагнитного спектра и могут не правильно измерять отдельные части спектра, нередко включающие дальнюю красную часть видимого спектра и дальнюю УФ-часть невидимого спектра. Так, при оценке параметров освещения с помощью плотности фотосинтетического фотонного потока (PPFD) важно понимать, что датчик будет давать результат, пропорциональный числу фотонов, без учета того, что фотоны разных длин волн несут разную энергию. Разные длины волн имеют неодинаковую ценность и привлекательность для выращивания растений, при этом часть спектра может оказаться за границами диапазона чувствительности фотометра.
Разные длины волн имеют неодинаковую ценность и привлекательность для выращивания растений, при этом часть спектра может оказаться за границами диапазона чувствительности фотометра.
Энергия каждого фотона обратно пропорциональна длине его волны. Чем короче длина волны, тем более энергетичным является фотон, чем длиннее длина волны, тем менее энергетичен фотон. Поэтому красный свет несет меньше энергии, чем желтый или зеленый, хотя и является более желательным для растений с точки зрения фотосинтеза и других химических процессов, происходящих в растении. Другими словами, светильники, излучающие много желтого и зеленого света, могут давать более высокие значения PPFD, но при этом они не могут производить свет, необходимый растениям.
Если оценивать только параметры УФ-освещения, следует отметить, что, хотя существует широкий спектр УФ- радиометров, предназначенных для измерения УФ-излучения, создаваемого традиционными широкополосными ртутными газоразрядными лампами, которые в первую очередь генерируют УФ-С, эти радиометры не смогут должным образом измерить УФ-излучение, создаваемое УФ-светодиодами, особенно если конструкция светильника предполагает несколько полос ультрафиолетового излучения, не совпадающих с целевым спектром используемого датчика. Многие производители УФ-светодиодных чипов будут измерять поток УФ-излучения светодиодов в интегрирующей сфере, также известной как сфера Ульбрихта, однако это измерение не даст ответа на вопрос, что на самом деле будут испытывать растения.
Многие производители УФ-светодиодных чипов будут измерять поток УФ-излучения светодиодов в интегрирующей сфере, также известной как сфера Ульбрихта, однако это измерение не даст ответа на вопрос, что на самом деле будут испытывать растения.
Влияние линз
При выборе светодиодного освещения для растений очень важно помнить, что, хотя растения не могут получить слишком много света, они, безусловно, могут получить слишком много тепла. В то время как светодиоды более эффективны, чем ртутные лампы, исследования показывают, что УФ-светодиоды преобразуют только 15-25 % входной мощности в излучение. Оставшаяся часть мощности превращается в тепло, поэтому отведение тепла должно стать существенным элементом системы.
Кроме того, когда светильники испускают излучение с длинами волн в областях спектра, не требуемых растениями, фотоны, не поглощенные растением, в конечном итоге преобразуются в тепло, нагревая окружающую среду, в результате требуются более высокие затраты на охлаждение — это и постоянное потребление электроэнергии, и расходы на инфраструктуру.
Подобно покрытиям теплиц, некоторые типы линз, такие как внешний стеклянный колпак натриевого газоразрядного светильника, фактически блокируют большую часть ультрафиолетового излучения, переводя его в тепло.
Другим важным фактором при использовании ультрафиолетовых или даже синих светодиодов является то, что с течением времени большинство материалов линз подвержено значительной деградации, а это приведет к снижению эффективности и даже может стать причиной поглощения существенного количества тепла и в конечном итоге способно уничтожить сам светодиод (рис. 4).Однако новые достижения, в частности запатентованная технология компании Violet Gro, позволяют сочетать источник ультрафиолетового излучения с особым классом прозрачного для ультрафиолета материала линз, не подверженного указанным негативным эффектам. Эта уникальная линза, имеющая непосредственный контакт с УФ-светодиодами, позволяет выводить больше ультрафиолетового излучения и направлять его на освещаемые объекты, увеличивая эффективность и уменьшая тепловую мощность.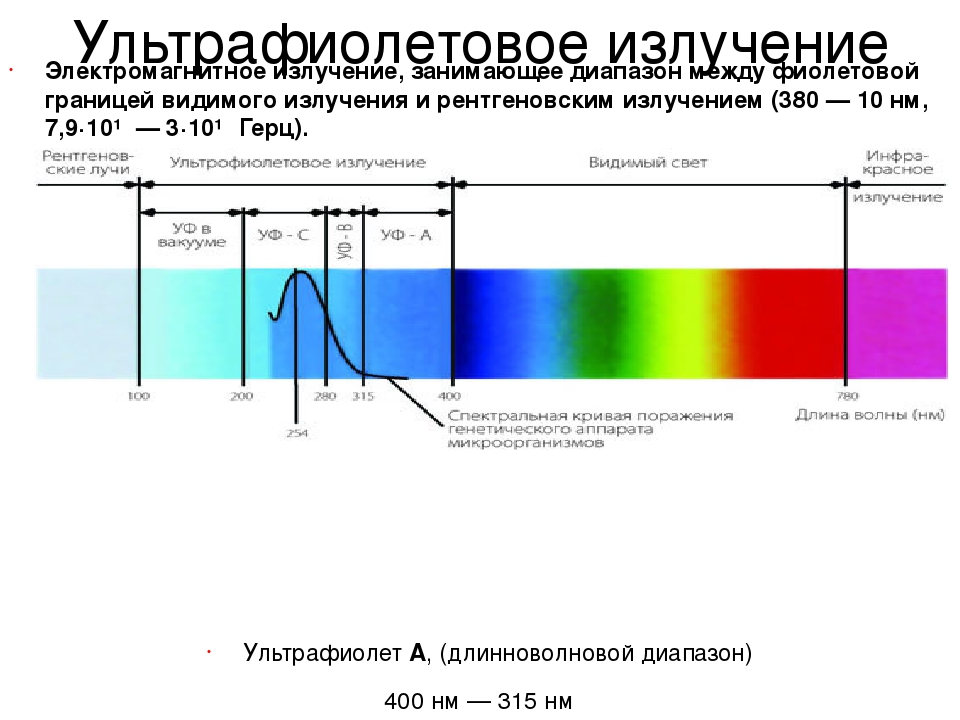 Это выгодно как для срока службы светодиодов, так и для значительного снижения требований к охлаждению в помещении для выращивания растений.
Это выгодно как для срока службы светодиодов, так и для значительного снижения требований к охлаждению в помещении для выращивания растений.
Рис. 4 Пример светодиодов, разрушенных из-за избыточного тепла внутри линзы
Что дальше
Поскольку стоимость УФ-светодиодов продолжает снижаться, резко возрастает возможность эффективно включать УФ-излучение в процесс выращивания растений с учетом выбора правильных длин волн, дозировки и нужного времени жизненного цикла конкретных видов растений. Это позволит провести дальнейшие исследования и разработку УФ-решений, в том числе определение оптимальных комбинаций ультрафиолетовых длин волн и доз для достижения желаемых эффектов для конкретных видов растений.
Независимо от желаемых результатов — роста растений или борьбы с вредителями — для эффективности и долговечности светильников УФ- светодиоды по-прежнему необходимо сочетать с соответствующей пропускающей ультрафиолет линзой, которая позволяет передавать УФ-излучение без риска деградации или разрушения линзы и самого светодиода.
Источник:
Журнал «Полупроводниковая светотехника»
Новый мобильный девайс, отслеживающий воздействие ультрафиолетового излучения
Разработка исследователей из университета Granada (Испания) и RMIT (Мельбурн, Австралия), привела к появлению новых светочувствительных браслетов для отслеживания воздействия ультрафиолетового излучения в режиме реального времени.
Ультрафиолетовые лучи представляют собой спектр света, не видимый человеческому глазу. В соответствии с диапазоном они подразделяются на три категории: УФ-A, УФ-B и УФ-C. Солнце излучает полный спектр УФ-лучей, некоторые из которых поглощаются земной атмосферой. Однако часть лучей, в частности УФ-А и УФ-В лучи, проникает в атмосферу и может вступить в контакт с кожей. Именно эти лучи оказывают вредное воздействие на кожу, вызывая повреждение ДНК ее клеток и увеличивая риск развития рака кожи. УФ-В лучи оказывают более разрушительное воздействие на кожу, чем УФ-А, и вызывают значительные солнечные ожоги.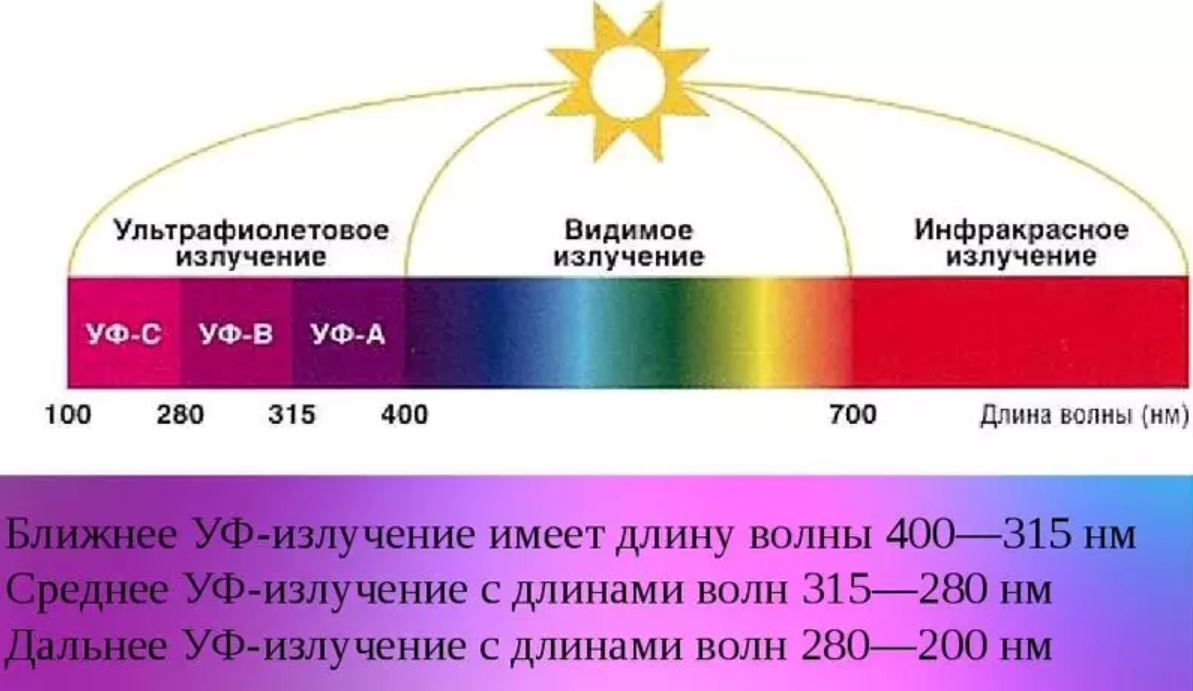 Однако, следует помнить, что все виды УФ-лучей не являются безопасными.
Однако, следует помнить, что все виды УФ-лучей не являются безопасными.
УФ-облучение увеличивает риск развития рака кожи
Рак кожи является одним из наиболее распространенных видов рака во всем мире. Это часто происходит из-за избыточного количества ультрафиолетового облучения. И хотя солнечный свет является основным источником ультрафиолетового излучения, не следует забывать и о других его источниках, таких как солярии и лампы. Сила воздействия ультрафиолетовых лучей зависит от ряда факторов, в числе которых — время суток, сезон, географическое положение, высота и другие. Помимо развития рака, воздействие ультрафиолетовых лучей может иметь другие неблагоприятные последствия для кожи, такие как ее старение, появление морщин, гиперпигментация и многое другое. Люди, которые более чувствительны к воздействию ультрафиолетовых лучей, подвергаются большему риску развития рака кожи.
Мониторинг экспозиции и профилактика повреждения кожи
Хотя солнечный свет вреден для кожи, его не следует избегать полностью. Небольшое количество солнечного света весьма полезно, поскольку УФ-В лучи способствуют образованию в организме витамина D. Ограничение воздействия ультрафиолетового излучения и принятие профилактических мер, таких как применение солнцезащитного крема и использование надлежащей одежды, помогут избежать возникновения рака кожи.
Небольшое количество солнечного света весьма полезно, поскольку УФ-В лучи способствуют образованию в организме витамина D. Ограничение воздействия ультрафиолетового излучения и принятие профилактических мер, таких как применение солнцезащитного крема и использование надлежащей одежды, помогут избежать возникновения рака кожи.
Обнаружение ультрафиолетовых лучей с помощью невидимых чернил, используемых в браслете
Датчики представляют собой недорогие изделия, изготовленные из предметов домашнего обихода с использованием фильтровальной бумаги, перьевой ручки и прозрачных листов. С целью обнаружения УФ-лучей, команда исследователей разработала невидимые чернила, способные обнаружить УФ-лучи различного спектра. Они наносили чернила для фильтрации на бумажные диски, рисуя на каждом из них улыбающиеся или нахмуренные лица. Диски затем подвергались воздействию каждого из подтипов ультрафиолетового излучения. При воздействии ультрафиолетовых лучей нарисованные невидимые лица постепенно проявлялись и приобретали цвет. В последующем, при создании переносного устройства, исследователи прикрепили диски к гибкой ленте.
В последующем, при создании переносного устройства, исследователи прикрепили диски к гибкой ленте.
В результате были созданы шесть типов полос УФ-датчика в соответствии с определенным тоном кожи. Лица на ленте переносного устройства появляются последовательно в соответствии с длительностью экспозиции ультрафиолетового излучения, при этом на каждом из 25%, 50%, 75% и 100% от рекомендуемого количества ежедневного УФ-излучения, появляется изображение нового лица. Изображение нахмуренного лица появляется при рекомендуемой 100% УФ-экспозиции, предупреждая пользователя о необходимости принятия мер предосторожности с целью предотвращения повреждения кожи.
Сохранение здоровой кожи
Поскольку ультрафиолетовое излучение не видимо человеческому глазу, его эффекты трудно своевременно обнаружить. Ожоги и другие вредные воздействия на кожу не проявляются до тех пор, пока не будет достигнута максимальная экспозиция ультрафиолетового излучения. Новый мобильный девайс позволяет пользователям отслеживать воздействие вредных лучей в режиме реального времени. Возможность его применения при различных тонах кожи делает его эффективным устройством для защиты и профилактики. Этот браслет обеспечивает простой и доступный способ снижения риска различных повреждений кожного покрова и возникновения рака.
Возможность его применения при различных тонах кожи делает его эффективным устройством для защиты и профилактики. Этот браслет обеспечивает простой и доступный способ снижения риска различных повреждений кожного покрова и возникновения рака.
Источник:
https://www.medicalnewsbulletin.com/new-wearable-device-uv-exposure/
Материал подготовила Ольга Заднипряная
Ультрафиолетовый фонарь Дозор-Спектр 365
Профессиональный источник ультрафиолетового излучения
Предназначен для решения широкого круга задач в сфере неразрушающего контроля, криминалистики, и других областей связанных с выявлением визуальной информации под действием УФ излучения
Поиск микрочастиц и биологических следов
Обнаружение скрытых дефектов в материалах
Утечки технических жидкостей
Ультрафиолетовое излучение в диапазоне А, длина волны — 365 н.м.*
Интенсивность излучения УФ на расстоянии 38см, не менее 190000 мВт/м2
Время непрерывной работы не менее 6 часов
IP65
Ударопрочный алюминиевый сплав с анодированием, устойчив к механическим воздействиям и изменениям температур
Электронный стабилизатор сохраняет неизменную интенсивность излучения, по мере разряда источников питания
Профессиональный источник УФ излучения Дозор предназначен для решения широкого спектра задач как в области инспекционной криминалистики (поиск микрочастиц и биологических следов на месте происшествия, визуализация естественных и УФ-флуоресцентных красок и порошков) так и неразрушающего контроля (обнаружения поврежденных образцов материалов, экспертизы художественных произведений)
Ультрафиолетовое излучение определенного спектра, генерируется использованием инновационных полупроводников на базе УФ светодиодов, что позволяет производить экспертизу даже в условиях хорошей освещенности. Высокая мощность прибора и длительное время работы от одного заряда аккумуляторов достигается с помощью использования современных LED технологий .
Высокая мощность прибора и длительное время работы от одного заряда аккумуляторов достигается с помощью использования современных LED технологий .
* Возможны модификации длины волны прибора:
365нм — УФ 405нм — Фиолетовый 450нм — Синий 500нм — Голубой 525нм — Зеленый 590нм — Золотой 630нм – Красный
Состав изделия Дозор-Спектр365 Кол-во
Источник света с длиной волны 365нм ДС-365-01.0001 1шт
Очки защитные ОЗ-365-01.0001 1 шт
Штатив ШЭ-01.0001 1 шт
Автоматическое зарядное устройство ЗУ-02.000RLi 1 шт
Кабель питания 220В ЗУ-02.0001 1 шт
Кабель питания 12В ЗУ-03.0001 1 шт
Аккумулятор типоразмера 18650 АКК-18650.000R 1 шт
Кейс защищенный пластиковый К-W12.0001 1 шт
Руководство по эксплуатации/паспорт — 1 шт
Как сбалансировать вкус, питательные свойства и урожайность с помощью освещения в УФ-спектре
ЭЛИЗЕБЕТ КОЛМОС (ELSEBETH KOLMOS) из центра LESA рассказывает о влиянии ультрафиолетового излучения на растения и отмечает, что еще многие аспекты такого влияния остаются неизученными.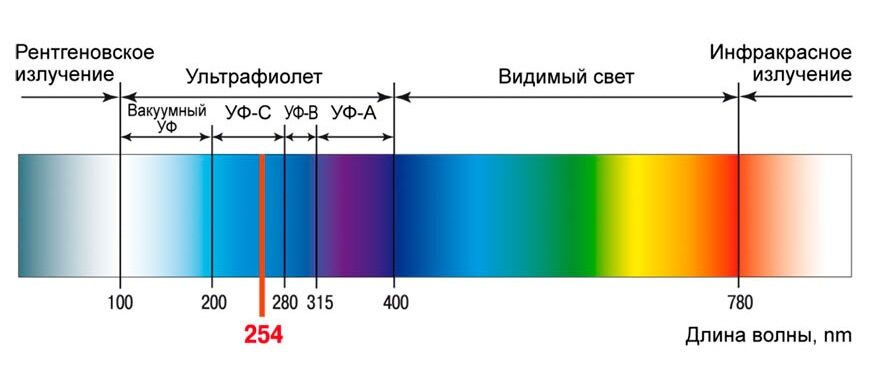
В летнее время нам напоминают, что солнечный свет может быть вреден. Мы наносим солнцезащитные лосьоны и надеваем солнцезащитные очки с линзами, блокирующими ультрафиолетовое (УФ) излучение. Мы прячемся, потому что знаем, что ультрафиолетовое излучение от Солнца может нанести вред живым клеткам и даже убить некоторых из них.
Солнечный свет включает в себя свет с длинами волн вне видимого спектра: длинноволновое излучение [>700 нм, дальний красный свет и инфракрасное (ИК) излучение] и коротковолновое излучение (<400 нм или УФ-свет). При длине волны короче 400 нм ультрафиолетовое излучение обладает все большей энергией по мере уменьшения длины волны, а способность ультрафиолетового света разрушать химические связи постепенно увеличивается по мере того, как УФ-волны становятся короче. Из-за разницы таких химических эффектов спектр УФ-излучения обычно делится на УФ-A (400‒315 нм), УФ-B (315‒280 нм) и УФ-C (280‒100 нм) спектры.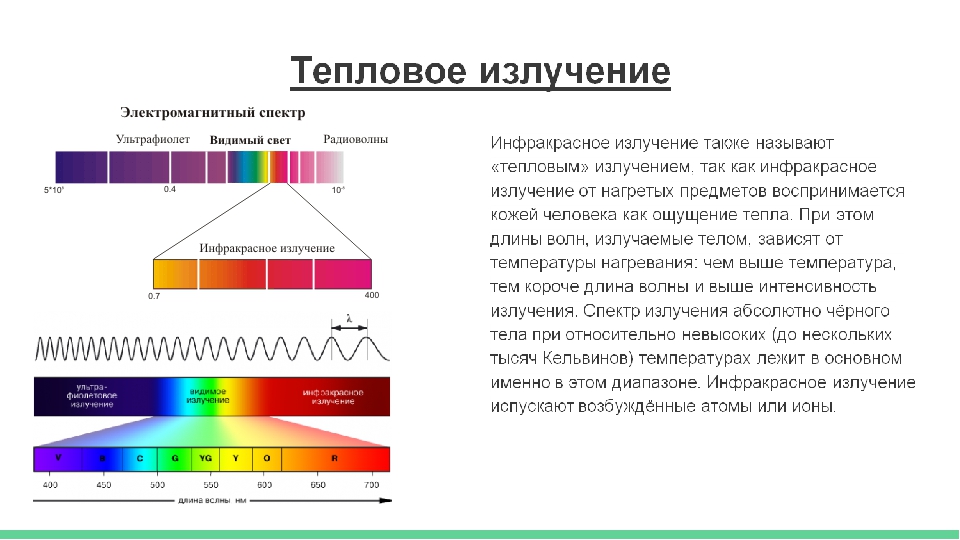 Поскольку верхние слои атмосферы Земли поглощают почти все ультрафиолетовое излучение на длинах волн короче 300 нм, на уровне поверхности в отношении воздействия на живые организмы обычно рассматривают только биохимическое воздействие ультрафиолетового излучения в диапазоне между 300 и 400 нм.
Поскольку верхние слои атмосферы Земли поглощают почти все ультрафиолетовое излучение на длинах волн короче 300 нм, на уровне поверхности в отношении воздействия на живые организмы обычно рассматривают только биохимическое воздействие ультрафиолетового излучения в диапазоне между 300 и 400 нм.
Процесс воздействия УФ-излучения на уровне поверхности на растения и животных может быть сложен для понимания. В то время как УФ-B излучение (315 нм и короче) может вызвать более сильные повреждения открытых тканей (например, солнечный ожог), оно поглощается прямо на поверхности. УФ-A излучение, с другой стороны, по мере увеличения длины волны постепенно становится менее опасным для тканей, подвергнутых воздействию, но все более глубоко проникает в подвергнутые воздействию ткани, вызывая другие фотохимические эффекты. Эти эффекты воздействуют на все живые ткани, подвергнутые такому воздействию.
Растения имеют развитые комплексные биохимические средства для управления воздействием со стороны всего спектра солнечного света, достигающего поверхности. Они прекрасно научились ощущать и использовать свет различных спектров. Например, самый известный растительный пигмент, хлорофилл, в основном поглощает синий и красный спектр и преобразует фотоны в биохимическую энергию (молекулы сахара) посредством фотосинтеза. Другие пигментные молекулы поглощают свет в коротковолновой части спектра. Растения воспринимают свет, используя специализированные белки. Растительные фоторецепторы специфичны для разных длин волн, например, фитохромы отвечают за восприятие красного света, а криптохромы – синего. Был открыт один УФ-рецептор — UVR8, который обнаруживает УФ-B-свет — но еще многое предстоит изучить в отношении молекулярного восприятия УФ-света растениями.
Они прекрасно научились ощущать и использовать свет различных спектров. Например, самый известный растительный пигмент, хлорофилл, в основном поглощает синий и красный спектр и преобразует фотоны в биохимическую энергию (молекулы сахара) посредством фотосинтеза. Другие пигментные молекулы поглощают свет в коротковолновой части спектра. Растения воспринимают свет, используя специализированные белки. Растительные фоторецепторы специфичны для разных длин волн, например, фитохромы отвечают за восприятие красного света, а криптохромы – синего. Был открыт один УФ-рецептор — UVR8, который обнаруживает УФ-B-свет — но еще многое предстоит изучить в отношении молекулярного восприятия УФ-света растениями.
Фото: Изображение предоставлено центром LESA.
Восприятие УФ-излучения очень важно для роста и развития растений. Например, на стадии рассады рост должен быть ориентирован на оптимальное поглощение света, распределение длин волн и фотосинтез. В сельском хозяйстве с контролируемыми условиями также есть и другие факторы влияния. Растения, выращенные в теплицах, получают фильтрованный солнечный свет, поскольку ультрафиолетовый свет с длиной волны примерно короче 350 нм не проходит сквозь стекло или пластиковые материалы, а отсутствие света в диапазоне между 300 и 350 нм может оказывать различное воздействие на растения либо непосредственно, либо вызывая изменения в развитии других организмов (например, насекомых, микробов, грибов) в их экосистеме.
В сельском хозяйстве с контролируемыми условиями также есть и другие факторы влияния. Растения, выращенные в теплицах, получают фильтрованный солнечный свет, поскольку ультрафиолетовый свет с длиной волны примерно короче 350 нм не проходит сквозь стекло или пластиковые материалы, а отсутствие света в диапазоне между 300 и 350 нм может оказывать различное воздействие на растения либо непосредственно, либо вызывая изменения в развитии других организмов (например, насекомых, микробов, грибов) в их экосистеме.
Ультрафиолетовый свет может спровоцировать биосинтез вторичных метаболитов, таких как флавоноиды. Этот биохимический ответ является, главным образом, защитным механизмом, поскольку окрашенные флавоноиды, такие как антоцианы, поглощают ультрафиолетовый свет и поэтому действуют в качестве защиты от повреждающих лучей. В то же время вкусовой профиль плодов или листьев изменяется, но часто востребованным образом, например, усиливая приятный аромат помидоров или уменьшая горечь салата.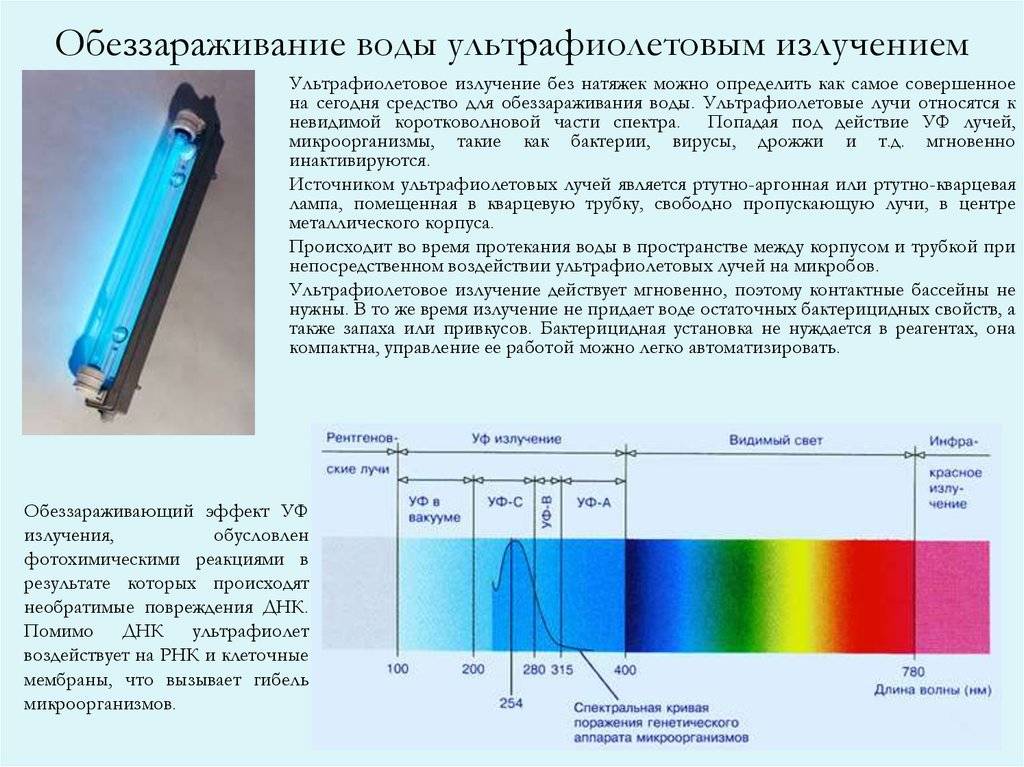
Другими соединениями, вырабатываемыми в ответ на стресс и способствующими хемотипу растения, являются терпеноиды, которые также важны для аромата и пигментации растений и их плодов. Вторичные метаболиты в целом, как полагают, улучшают питательные качества культур, в первую очередь за счет антиоксидантных и антимикробных свойств этих соединений.
Развитие светодиодного освещения в сельском хозяйстве с контролируемыми условиями обеспечивает возможность добавления с помощью светодиодов УФ-света в режим освещения посадок сельскохозяйственными лампами, но исследования относительно того, может ли дополнительное УФ-освещение улучшить аромат и вкус овощей, все еще находятся в зачаточном состоянии. В последних докладах таких как «Управление сенсорными и фитохимическими профилями тепличных томатов с использованием экологически значимых доз ультрафиолетового излучения» (“Manipulating Sensory and Phytochemical Profiles of Greenhouse Tomatoes Using Environmentally Relevant Doses of Ultraviolet Radiation”) (август 2016 г. ) и «Изменения в морфологии, антиоксидантной способности и содержании летучих веществ в базилике камфорном (Ocimum basilicum)» (“Light Quality Dependent Changes in Morphology, Antioxidant Capacity, and Volatile Production in Sweet Basil (Ocimum basilicum)”) (сентябрь 2016 г.), было обнаружено, что дополнительное воздействие УФ-излучения действительно улучшает вкусовые качества некоторых трав (например, базилика) и помидоров.
) и «Изменения в морфологии, антиоксидантной способности и содержании летучих веществ в базилике камфорном (Ocimum basilicum)» (“Light Quality Dependent Changes in Morphology, Antioxidant Capacity, and Volatile Production in Sweet Basil (Ocimum basilicum)”) (сентябрь 2016 г.), было обнаружено, что дополнительное воздействие УФ-излучения действительно улучшает вкусовые качества некоторых трав (например, базилика) и помидоров.
Конечно же, могут возникать дополнительные проблемы, которые необходимо учитывать при применении дополнительного УФ-освещения в растениеводстве. Нуждаются ли растения в постоянном воздействии для улучшения качеств конечного урожая? Могут ли растения достичь правильного сочетания вкуса, питательных свойств и размера? Могут возникнуть и другие проблемы безопасности — насколько УФ-облучение безопасно для работников объекта, если УФ-свет требуется в процессе контроля условий для растениеводства? Мы уже знаем, что слишком большое воздействие излучения в УФ-B спектре может вызвать серьезные проблемы с глазами и кожей.
Будущие исследования в LESA (Центр изучения систем и приложений на основе освещения (Lighting Enabled Systems and Applications) при Ренсселеровском политехническом институте) помогут проанализировать влияние различных длин волн ультрафиолетового света на качество продукции, вкус, питательные свойства, объем биомассы и урожайность сельскохозяйственных культур с целью производства более ценных продуктов растениеводства в контролируемых условиях, над чем как раз работает команда ученых-растениеводов LESA.
Cтатьи — Ультрафиолет — Биологическое действие ультрафиолетового излучения — Электронная Медицина
Излучение солнца имеет электромагнитную колебательную природу и носит непрерывный характер. Этот спектр излучений можно разделить на несколько областей:
- рентгеновское излучение – ниже 2 нм,
- УФ-излучение – от 2 нм до 400 нм,
- видимый участок спектра – от 400 нм до 750 нм,
- инфракрасное излучение – выше 750 нм.

Биологическая роль каждого вида излучений имеет свои характерные особенности. В нашем обзоре мы остановимся на рассмотрении роли и механизмов биологического действия УФ-излучения, которое имеет лишь часть ультрафиолетового электромагнитного спектра в области 180 ÷ 400 нм. Энергия квантов этого излучения (70–140 ккал/моль) превосходит энергию активации большинства химических реакций. Поэтому УФ-радиация является весьма фотохимически активной частью спектра. Ультрафиолетовое излучение в области 2 ÷ 180 нм интенсивно поглощается кислородом воздуха. Поэтому оно реально существует лишь в космическом пространстве или в специальных лабораторных условиях. Рассматриваемый нами спектр УФ-излучений, имеющих биологическое значение, подразделяется на три диапазона по своей проникающей способности и фотохимической активности:
- область А (320÷400 нм),
- область В (275÷320 нм),
- область С (180÷275 нм).

В настоящее время в фотобиологии принято также выделять так называемый экологический диапазон (295÷400 нм) и УФ-излучение искусственных источников (короче 295 нм). В атмосфере Земли коротковолновое излучение Солнца, рентгеновское, и короткий ультрафиолет, взаимодействуя с молекулярным кислородом, приводят к образованию озонового слоя на высоте от 20 до 30 км. Озон поглощает все виды излучений с длиной волны короче 295 нм и экранирует поверхность Земли и нижележащие слои атмосферы от нежелательных воздействий этих излучений.
С другой стороны, экологическое УФ-излучение является постоянно действующим фактором внешней среды, оказывающим мощное воздействие на многие физиологические процессы, протекающие в организме. Также оно сыграло важную роль в эволюционных процессах, протекавших на Земле.
Прежде всего, УФ-излучение, наряду с космическими лучами и радиоактивными элементами земной коры, с электрическими разрядами в атмосфере, извержениями вулканов и ударами метеоритов, было важнейшим фактором, способствовавшим абиогенному синтезу органических соединений на Земле. Мутагенное действие УФ-излучения на простейшие формы жизни стимулировало ход биологической эволюции, способствовало увеличению разнообразия жизненных форм.
Мутагенное действие УФ-излучения на простейшие формы жизни стимулировало ход биологической эволюции, способствовало увеличению разнообразия жизненных форм.
В ходе эволюции земные организмы приобрели способность использовать для своих нужд энергию различных частей солнечного спектра. Хорошо известна роль видимой части солнечного света – фотосинтез, зрение, инфракрасной – тепло. Оказалось, что используются и ультрафиолетовые компоненты солнечного диапазона и, в частности, при фотохимическом синтезе витамина D, важнейшего регулятора обмена кальция и фосфора в организме. Предшественники витамина D, такие как 7,8-дегидрохолестерин, эргостерин и другие, поступающие в организм с пищей, выносятся на поверхность кожи в составе секрета сальных желез – кожной смазки. Кванты УФ-излучения в ходе инсоляции взаимодействуют с молекулами провитамина D. Полученный в результате фотохимического преобразования витамин D всасывается обратно в кровь. Эта реакция используется в промышленности для получения витамина D из провитаминов и при обогащении им природных источников (китового жира и др. ).
).
Дефицит витамина D в организме приводит к развитию рахита в детском возрасте и остеомаляции (уменьшению содержания кальция в костной ткани) во взрослом организме. Характерными симптомами нарушения минерального обмена являются повышенная утомляемость, головные боли, повышение заболеваемости простудными и другими воспалительными заболеваниями. Наиболее физиологический метод профилактики и лечения этих состояний – инсоляция, а также освещение эритемными лампами совместно с приемом препаратов – витамина D или богатых им продуктов. В то же время дефицит УФ-облучения, наблюдаемый у жителей крайнего Севера, зимовщиков и, периодически (в зимне-весенний период), у всех жителей умеренного географического пояса, в крупных городах с пониженной прозрачностью атмосферы для УФ-излучения, проявляется не только в нарушениях минерального обмена и не устраняются полностью только назначением витамина D.
Этот синдром светового голодания означает, что физиологическая роль УФ-излучения не ограничивается синтезом витамина D. Так, умеренное облучение кожи человека в дозах порядка 0,1-1,5 пороговых эритемных доз оказывает на весь организм неспецифическое стимулирующее действие. Увеличивается продукция и активность клеточных и гуморальных факторов иммунитета, сопротивляемость простудным и другим заболеваниям, интоксикациям, ускоряется заживление ран и срастание переломов. В физиологических дозах УФ-радиация стимулирует функции кроветворной, иммунокомпетентной и эндокринной систем организма. Предварительное УФ-облучение повышает устойчивость к воздействию рентгеновских и гамма-лучей, т.е. радиорезистентность. На фоне иммунодепрессии, вызванной опухолевым процессом и лучевой терапией, стимулирующее действие профилактического курса УФ-облучения проявляется в сокращении сроков заживления лучевых дерматитов и язв на 40-50%. Клинические испытания на больных раком кожи и нижней губы подтвердили высокую эффективность метода. Наблюдалось смягчение тяжести лучевых изменений и ускорение ликвидации последствий на 3-4 недели и хороший косметический эффект.
Так, умеренное облучение кожи человека в дозах порядка 0,1-1,5 пороговых эритемных доз оказывает на весь организм неспецифическое стимулирующее действие. Увеличивается продукция и активность клеточных и гуморальных факторов иммунитета, сопротивляемость простудным и другим заболеваниям, интоксикациям, ускоряется заживление ран и срастание переломов. В физиологических дозах УФ-радиация стимулирует функции кроветворной, иммунокомпетентной и эндокринной систем организма. Предварительное УФ-облучение повышает устойчивость к воздействию рентгеновских и гамма-лучей, т.е. радиорезистентность. На фоне иммунодепрессии, вызванной опухолевым процессом и лучевой терапией, стимулирующее действие профилактического курса УФ-облучения проявляется в сокращении сроков заживления лучевых дерматитов и язв на 40-50%. Клинические испытания на больных раком кожи и нижней губы подтвердили высокую эффективность метода. Наблюдалось смягчение тяжести лучевых изменений и ускорение ликвидации последствий на 3-4 недели и хороший косметический эффект.
В основе общестимулирующего действия УФ-излучения заложено несколько механизмов. Во-первых, это нормализация минерального обмена и повышение барьерных свойств тканей, т.к. кальций уплотняет клеточные и сосудисто-тканевые мембраны. Во-вторых, стимуляция иммунокомпетентной системы и всей физиологической системы соединительной ткани. В-третьих, повышение реактивности и трофики органов и систем органов. Очевидно, УФ-излучение в физиологических дозах вызывает такую степень неспецифического раздражения, которая необходима для оптимальной жизнедеятельности организма. Естественно, что стимулирующее действие УФ-излучения максимально проявляется на фоне его недостаточности и выражается в резком повышении работоспособности, устойчивости к разнообразным вредным агентам, в нормализации повышенной или аллергической реактивности, в десенсибилизирующем эффекте. Поэтому применение УФ-радиации показано не только для профилактики и лечения рахита и синдрома светового голодания, но и во всех многочисленных случаях, когда необходимы стимуляция и нормализация иммунореактивности, мобилизация защитных сил и систем регуляции обмена веществ и гомеостаза в организме. Знание и целенаправленное использование УФ-излучения как физиологического стимулятора жизненных функций и мощного природного средства закаливания, повышения сопротивляемости и оптимизации жизнедеятельности организма уже дают и способны дать еще больший профилактический и лечебный эффект.
Знание и целенаправленное использование УФ-излучения как физиологического стимулятора жизненных функций и мощного природного средства закаливания, повышения сопротивляемости и оптимизации жизнедеятельности организма уже дают и способны дать еще больший профилактический и лечебный эффект.
Обобщив в первой части обзора положительную роль УФ-излучения в регуляции разнообразных процессов в организме, перейдем к рассмотрению вопросов, связанных с механизмами повреждающего действия ультрафиолета на различные молекулярные и клеточные структуры, бактерицидного, мутагенного и канцерогенного действия. Поэтому в начале коротко остановимся на молекулярных основах биологического действия УФ-излучения.
Права на статью принадлежат ООО «Электронная Медицина».
Источники УФ-излучения | Всё о красках
В качестве источника УФ-излучения используют микроволновые безэлектродные УФ-излучатели, ртутные лампы низкого давления и ртутные излучатели высокого давления. В кварцевой трубке (кварц имеет небольшое поглощение в УФ-области) находится заполняющий материал (ртуть, инертный газ и галогеновая добавка) под давлением от 1 до 10 бар, возбуждаемый для эмиссии излучения. В момент действия разряда в насыщенном ртутью газе лампа должна иметь оптимальную рабочую температуру, чтобы можно было добиться высокого коэффициента полезного действия. В этом случае ртутный излучатель высокого давления эмитирует характерный спектр с основными линиями при 254, 302,313, 366, 405 и 456 нм.
В кварцевой трубке (кварц имеет небольшое поглощение в УФ-области) находится заполняющий материал (ртуть, инертный газ и галогеновая добавка) под давлением от 1 до 10 бар, возбуждаемый для эмиссии излучения. В момент действия разряда в насыщенном ртутью газе лампа должна иметь оптимальную рабочую температуру, чтобы можно было добиться высокого коэффициента полезного действия. В этом случае ртутный излучатель высокого давления эмитирует характерный спектр с основными линиями при 254, 302,313, 366, 405 и 456 нм.
Излучение в этой волновой области обладает высокой энергией, достаточной для расщепления фотоинициатора и инициирования радикальной полимеризации. Мощность используемых излучателей обычно составляет от 80 до 160 Вт/см. Продолжительность их жизни в среднем 1500-2000 ч до того, как мощность упадет на 80%. Обычно изготавливают лампы с длиной дуги от 50 до 2500 мм. Длиной дуги называется расстояние между двумя электродами. Диаметр ламп варьируется от 19 до 28 мм в зависимости от мощности
В энергетическом балансе УФ-излучения на УФ-С, УФ-В и УФ-А диапазон приходится 25-30% энергии, видимая область спектра имеет 10-15% и 50-60% приходится на ИК-излучение. При этом излучатели с микроволновым возбуждением имеют 35-40% энергии в ИК-диапазоне, а в УФ-области около 36%, что значительно выше, чем у разрядных ртутных ламп. Для сравнения мощности УФ-излучателей получила признание специфическая величина мощности излучения Вт/см.
При этом излучатели с микроволновым возбуждением имеют 35-40% энергии в ИК-диапазоне, а в УФ-области около 36%, что значительно выше, чем у разрядных ртутных ламп. Для сравнения мощности УФ-излучателей получила признание специфическая величина мощности излучения Вт/см.
Мощность излучения не может характеризовать интенсивность и энергетическую плотность попадающего на отверждаемую пленку УФ-излучения, так как в данном случае необходимо также принимать во внимание следующие факторы: геометрию рефлектора и силу фокусировки, расстояние от излучателя до подложки , а также атмосферу, в которой происходит отверждение, УФ-спектр.
Для фокусировки УФ-излучения на подложке применяют рефлекторы, которые собирают УФ-излучение в пучок или отражают. В основном используют два типа рефлекторов. Самым сильным является эллиптический рефлектор, создающий фокальную линию, на которой находится максимум УФ-излучения. Расстояние до окрашенной подложки должно быть точно установлено. В параболическом рефлекторе излучение отражается параллельно и фокальной линии не образуется.
В параболическом рефлекторе излучение отражается параллельно и фокальной линии не образуется.
Так как эмитируемая излучателем мощность ни в коем случае не равна интенсивности попадающего на поверхность субстрата излучения, то УФ-установки характеризуются двумя величинами, для точного измерения которых можно установить один прибор (УФ-фотометр).
Такими величинами являются облучение (Е, доза энергии) и сила облучения (H, УФ-интенсивность). В общем случае эти величины зависят от длины волны. Единицы измерения Е и Н относятся к определенному диапазону длин волн и называются спектральной силой облучения и спектральным облучением. В разных спектральных областях получаются разные значения Е и Н.
Облучение (доза энергии). Доза (облучение) – это общая энергия излучения, которая попадает на объект. Она измеряется в Дж/см2 и связана с интенсивностью через время.Сила облучения (УФ-интенсивность). Понятие интенсивности описывает по определению собственно эмиссию излучения от источника. Но на практике обычно отклоняются от этого определения. Вошло в обычай измерять интенсивность излучения на поверхности деталей.
Но на практике обычно отклоняются от этого определения. Вошло в обычай измерять интенсивность излучения на поверхности деталей.
Интенсивность – это максимальная мощность излучения, достигшая поверхности субстрата. Она измеряется в Вт/см2. Интенсивность является характеристикой излучателя и рефлектора и не зависит от скорости продвижения изделий на линии окраски. Сила облучения является важным параметром химической сшивки и установления степени блеска для УФ-материалов.
На скорость отверждения также влияет состав атмосферы, в которой происходит отверждение. Коротковолновое УФ-С излучение, обладающее наиболее высокой энергией абсорбции, интенсивно поглощается кислородом воздуха (λ < 200 нм). При снижении количества кислорода в зоне отверждения за счет введения азота или углекислого газа скорость отверждения возрастает.
УФ-отверждение в атмосфере инертного газа позволяет существенно снизить содержание фотоинициатора, уменьшить количество продуктов расщепления фотоинициаторов, отказаться от добавления аминных синергетиков, что уменьшает пожелтение покрытия, не использовать высокофункциональные мономеры, снизить мощность и дозу УФ-облучения.
Польза, вред, старение кожи и защита — Wonderzine
При выборе солнцезащитного крема по показателю SPF следует учитывать не только так называемый фототип кожи (как мы уже выяснили, это довольно условный ориентир), но и степень её тонкости, эластичности и чувствительности. Важно и ваше местонахождение: чем ближе к экватору вы находитесь, тем выше солнечная активность и, следовательно, тем выше риск получить солнечный ожог. Рекомендуем выбирать кремы, спреи и декоративную косметику с защитой широкого спектра (broad spectrum) — они блокируют излучение спектров А и В. Защищаясь от лучей cпектра А, вы в определённой степени жертвуете загаром, зато обеспечиваете здоровье кожи. Оптимальным соотношением считается пропорция фильтров УФБ к УФА в количестве 3:1.
Солнцезащитные средства производят на основе двух типов ингредиентов: это либо поглощающие органические фильтры, либо экраны — неорганические твёрдые частицы, отражающие УФ-лучи (как правило, диоксид титана, оксид цинка или их комбинация). Фильтры проникают в кожу и трансформируют солнечную энергию в тепловую. В отличие от фильтров экраны остаются на поверхности кожи.
Некоторые фильтры, например оксибензон и ретинола пальмитат, считаются опасными и онкогенными, так что их следует избегать. К слову, Environmental Working Group, американская некоммерческая организация, занимающаяся исследованиями в области токсических веществ и корпоративной ответственности, не признаёт ни один действующий ингредиент в солнцезащитных средствах стопроцентно безопасным, но всё равно настоятельно рекомендует ими пользоваться и даже предлагает свой топ относительно безопасных средств.
Если ваша кожа чувствительна, склонна к акне, гиперпигментации или имеет какие-либо другие особенности, при выборе солнечной защиты не пренебрегайте консультацией дерматолога: доктор поможет подобрать некомедогенное, гипоаллергенное средство или специальный продукт, призванный более эффективно препятствовать образованию пигментных пятен. В любом случае не ленитесь пользоваться базовой защитой от солнца — это такая же естественная забота о здоровье, как регулярное мытьё рук. А подробнее о том, как выбрать солнцезащитные средства для разных целей и бюджетов, мы еще расскажем.
Фотографии: Weekday, Oséa
4.4: УФ-видимая спектроскопия — Chemistry LibreTexts
Ультрафиолетовая-видимая (УФ-видимая) спектроскопия используется для получения спектров поглощения соединения в растворе или в твердом виде. На самом деле спектроскопически наблюдается поглощение световой энергии или электромагнитного излучения, которое переводит электроны из основного состояния в первое синглетное возбужденное состояние соединения или материала. Энергия в УФ-видимой области электромагнитного спектра составляет 1,5–6,2 эВ, что соответствует диапазону длин волн 800–200 нм.Закон Бера-Ламберта, уравнение \ ref {1}, лежит в основе спектроскопии поглощения. Для одной длины волны A — оптическая плотность (без единицы измерения, обычно обозначаемая как произвольные или произвольные единицы), ε — молярная поглощающая способность соединения или молекулы в растворе (M -1 см -1 ), b — длина пути кюветы или держателя образца (обычно 1 см), а c — концентрация раствора (М).
\ [A \ = \ \ varepsilon b c \ label {1} \]
Все эти инструменты имеют источник света (обычно дейтериевую или вольфрамовую лампу), держатель образца и детектор, но некоторые имеют фильтр для выбора одной длины волны за раз.Однолучевой прибор (рисунок \ (\ PageIndex {1} \)) имеет фильтр или монохроматор между источником и образцом для анализа одной длины волны за раз. Двухлучевой прибор (рис. \ (\ PageIndex {2} \)) имеет единственный источник и монохроматор, а затем есть делитель и серию зеркал, чтобы направить луч на эталонный образец и образец для анализа, это позволяет получить более точные показания. Напротив, синхронный прибор (рисунок \ (\ PageIndex {3} \)) не имеет монохроматора между образцом и источником; вместо этого он имеет детектор с диодной матрицей, который позволяет прибору одновременно определять оптическую плотность на всех длинах волн.Синхронный прибор обычно намного быстрее и эффективнее, но все эти типы спектрометров работают хорошо.
Рисунок \ (\ PageIndex {1} \) Изображение однолучевого прибора для УФ-видимости. Рисунок \ (\ PageIndex {2} \) Изображение двухлучевого прибора для УФ-видимости. Рисунок \ (\ PageIndex {3} \) Иллюстрация одновременного УФ-видимого прибора.
Какую информацию можно получить с помощью спектров УФ-видимой области?
УФ-видимые спектроскопические данные могут дать качественную и количественную информацию о данном соединении или молекуле.Независимо от того, требуется ли количественная или качественная информация, важно использовать контрольную ячейку для обнуления прибора для растворителя, в котором находится соединение. Для получения количественной информации о соединении калибровка прибора с использованием известных концентраций рассматриваемого соединения в растворе. с тем же растворителем, что и неизвестный образец. Если необходимая информация является просто доказательством того, что соединение находится в анализируемой пробе, калибровочная кривая не нужна; однако, если проводится исследование разложения или реакция и требуется концентрация соединения в растворе, то необходима калибровочная кривая.
Для построения калибровочной кривой потребуются по крайней мере три концентрации соединения, но пять концентраций были бы наиболее идеальными для более точной кривой. Концентрации должны начинаться чуть выше расчетной концентрации неизвестного образца и должны снижаться примерно на порядок ниже максимальной концентрации. Растворы для калибровки должны быть расположены относительно одинаково друг от друга, и их следует готовить как можно точнее с использованием цифровых пипеток и мерных колб вместо градуированных цилиндров и мензурок.Пример спектров поглощения калибровочных растворов Rose Bengal (4,5,6,7-тетрахлор-2 ‘, 4’, 5 ‘, 7’-тетраиодофлуоресцеин, рисунок \ (\ PageIndex {4} \) можно увидеть на рисунке \ (\ PageIndex {5} \). Чтобы построить калибровочную кривую, значение оптической плотности каждой из спектральных кривых на самой высокой длине волны поглощения нанесено на график, аналогичный приведенному на рисунке \ (\ PageIndex { 6} \) поглощения в зависимости от концентрации. Коэффициент корреляции приемлемой калибровки составляет 0,9 или лучше. Если коэффициент корреляции ниже этого значения, попробуйте найти решение еще раз, поскольку проблема может заключаться в человеческой ошибке.Однако, если после приготовления растворов несколько раз калибровка по-прежнему неудовлетворительна, возможно, с прибором что-то не так; например, лампы могут выйти из строя.
Рисунок \ (\ PageIndex {4} \) Молекулярная структура розового бенгальского (4,5,6,7-тетрахлор-2 ‘, 4’, 5 ‘, 7’-тетраиодофлуоресцеин). Рисунок \ (\ PageIndex {5} \) УФ-видимые спектры различных концентраций Rose Bengal. Рисунок \ (\ PageIndex {6} \) Калибровочная кривая Rose Bengal. Уравнение линии: y = 0,0977x — 0,1492 (R 2 = 0,996)
Ограничения УФ-видимой спектроскопии
Образец
Спектроскопия
UV-vis хорошо работает с жидкостями и растворами, но если образец больше представляет собой суспензию твердых частиц в жидкости, образец будет больше рассеивать свет, чем поглощать свет, и данные будут сильно искажены.Большинство приборов УФ-видимого диапазона могут анализировать твердые образцы или суспензии с помощью дифракционного прибора (рис. \ (\ PageIndex {7} \)), но это не является обычным явлением. УФ-видимые приборы обычно наиболее эффективно анализируют жидкости и растворы.
Рисунок \ (\ PageIndex {7} \) Схематическое изображение устройства для сбора УФ-видимых спектров твердых материалов.
Калибровка и ссылка
Пустой эталон потребуется в самом начале анализа используемого растворителя (вода, гексаны и т. Д.), И если необходимо провести анализ концентрации, калибровочные растворы должны быть приготовлены точно.Если растворы приготовлены недостаточно точно, фактическая концентрация рассматриваемого образца не будет точно определена.
Выбор растворителя или емкости
Каждый растворитель имеет длину волны отсечки УФ-видимой абсорбции. Граница для растворителя — это длина волны, ниже которой сам растворитель поглощает весь свет. Поэтому при выборе растворителя следует учитывать предел его поглощения и место, которое, как предполагается, будет поглощать исследуемое соединение. Если они близки, выберите другой растворитель.В таблице \ (\ PageIndex {1} \) приведен пример отсечки растворителя.
| Растворитель | Отсечка УФ-поглощения (нм) |
|---|---|
| Ацетон | 329 |
| Бензол | 278 |
| Диметилформамид | 267 |
| этанол | 205 |
| Толуол | 285 |
| Вода | 180 |
Материал, из которого сделана кювета (держатель образца), также будет иметь предел поглощения УФ-видимой области.Стекло будет поглощать весь свет с более высокой энергией, начиная примерно с 300 нм, поэтому, если образец поглощает в УФ, кварцевая кювета будет более практичной, поскольку отсечка поглощения составляет около 160 нм для кварца (Таблица \ (\ PageIndex {2 } \)).
| Материал | Диапазон длин волн (нм) |
|---|---|
| Стекло | 380-780 |
| Пластик | 380-780 |
| Плавленый кварц | <380 |
Концентрация раствора
Для получения надежных данных пик поглощения данного соединения должен быть по крайней мере в три раза выше по интенсивности, чем фоновый шум прибора.Очевидно, что использование более высоких концентраций соединения в растворе может бороться с этим. Кроме того, если образец очень маленький и его разбавление не даст приемлемого сигнала, существуют кюветы, которые вмещают образцы меньшего размера, чем 2,5 мл стандартных кювет. Некоторые кюветы рассчитаны только на 100 мкл, что позволяет анализировать небольшой образец без необходимости разбавлять его до большего объема, что снижает отношение сигнал / шум.
14.9: Интерпретация ультрафиолетовых спектров — эффект конъюгации
Цель
После завершения этого раздела вы сможете использовать данные ультрафиолетовых спектров, чтобы помочь в выяснении неизвестных молекулярных структур.
Учебные заметки
Важно понимать, что максимум поглощения ультрафиолетового излучения конъюгированной молекулы зависит от степени конъюгации в молекуле.
Когда молекула с двойной связью, такая как этен (обычное название этилен), поглощает свет, она претерпевает переход π — π *. Поскольку π- π * энергетические щели уже, чем σ — σ * щели, этен поглощает свет с длиной волны 165 нм — более длинной волны, чем молекулярный водород.
Электронные переходы как молекулярного водорода, так и этена слишком энергичны, чтобы их можно было точно зарегистрировать стандартными УФ-спектрофотометрами, которые обычно имеют диапазон 220-700 нм. УФ-видимая спектроскопия становится полезной для большинства химиков-органиков и биологов при изучении молекул с сопряженными пи-системами. В этих группах энергетическая щель для π -π * переходов меньше, чем для изолированных двойных связей, и, таким образом, длина поглощаемой волны больше.Молекулы или части молекул, которые сильно поглощают свет в УФ-видимой области, называются хромофорами .
Давайте вернемся к МО-картине 1,3-бутадиена, простейшей сопряженной системы (см. Раздел 2.1B). Напомним, что мы можем нарисовать диаграмму, показывающую четыре МО пи, которые возникают в результате объединения четырех атомных орбиталей 2p z . Две нижние орбитали связывают, а две верхние — разрыхляют.
Сравнивая эту МО-картину с этеном, нашим примером изолированной пи-связи, мы видим, что запрещенная зона ВЗМО-НСМО действительно меньше для сопряженной системы.1,3-бутадиен поглощает УФ-свет с длиной волны 217 нм.
По мере того, как сопряженные пи-системы становятся больше, энергетическая щель для перехода π — π * становится все более узкой, и длина волны поглощенного света соответственно увеличивается. Поглощение из-за перехода π — π * в 1,3,5-гексатриене, например, происходит при 258 нм, что соответствует Δ E 111 ккал / моль.
В молекулах с протяженными пи-системами энергетическая щель ВЗМО-НСМО становится настолько малой, что поглощение происходит в видимой, а не в ультрафиолетовой области электромагнитного спектра.Бета-каротин с его системой из 11 сопряженных двойных связей поглощает свет с длинами волн в синей области видимого спектра, позволяя передавать другие длины волн видимого света, в основном в красно-желтой области. Вот почему морковь оранжевого цвета.
Конъюгированная пи-система в 4-метил-3-пентен-2-оне дает сильное УФ-поглощение при 236 нм из-за перехода π — π *. Однако эта молекула также поглощает на длине волны 314 нм. Это второе поглощение связано с переходом несвязывающего электрона (неподеленной пары) на кислород до π * разрыхляющей МО:
Это называется переходом n — π * .Несвязывающие (n) МО имеют более высокую энергию, чем самые высокие связывающие p-орбитали, поэтому запрещенная зона для перехода n — π * меньше, чем у перехода π — π *, и, таким образом, пик n — π * находится на более длинная длина волны. В общем, переходы n — π * слабее (меньше поглощается света), чем переходы, обусловленные переходами π — π *.
Глядя на УФ-видимые спектры
Мы говорили в общих чертах о том, как молекулы поглощают УФ и видимый свет — теперь давайте посмотрим на некоторые реальные примеры данных спектрофотометра поглощения УФ и видимой области спектра.Базовая установка такая же, как и для ИК-спектроскопии: излучение с диапазоном длин волн направляется через интересующий образец, и детектор регистрирует, какие длины волн были поглощены и в какой степени произошло поглощение. Ниже представлен спектр поглощения важной биологической молекулы, называемой никотинамидадениндинуклеотидом, сокращенно NAD + (мы узнаем, что он делает в разделе 16.4). Это соединение поглощает свет в УФ-диапазоне из-за наличия конъюгированных пи-связывающих систем. .
Вы заметите, что этот УФ-спектр намного проще, чем ИК-спектры, которые мы видели ранее: у него только один пик, хотя многие молекулы имеют более одного пика. Также обратите внимание, что в УФ-видимой спектроскопии принято показывать базовую линию внизу графика с пиками, направленными вверх. Значения длины волны на оси x обычно измеряются в нанометрах (нм), а не в см -1 , как принято в ИК-спектроскопии.
Пики в УФ-спектрах имеют тенденцию быть довольно широкими, часто охватывая более 20 нм на половине максимальной высоты.Обычно есть две вещи, которые мы ищем и записываем в УФ-видимом спектре. Первая — это λ, max, — длина волны при максимальном поглощении света. Как видите, NAD + имеет λ max , = 260 нм. Мы также хотим записать, сколько света поглощается при λ max . Здесь мы используем безразмерное число, называемое оптической плотностью , сокращенно «А». Он содержит ту же информацию, что и число «процент пропускания», используемое в ИК-спектроскопии, только выраженное в несколько других терминах.Для расчета оптической плотности на заданной длине волны компьютер спектрофотометра просто измеряет интенсивность света на этой длине волны до того, как он проходит через образец (I 0 ), делит это значение на интенсивность той же длины волны после . он проходит через образец (I), затем берет журнал 10 из этого числа:
A = лог I 0 / I
Вы можете видеть, что значение поглощения при 260 нм (A 260 ) составляет около 1.0 в этом спектре.
Пример 14.8.1
Express A = 1,0 в процентах пропускания (% T, единица измерения, обычно используемая в ИК-спектроскопии (а иногда и в УФ-видимой области).
Решение
Вот спектр поглощения обычного пищевого красителя Красный # 3:
Здесь мы видим, что расширенная система сопряженных пи-связей заставляет молекулу поглощать свет в видимом диапазоне. Поскольку λ max из 524 нм попадает в зеленую область спектра, соединение кажется нам красным.
А теперь взгляните на спектр другого пищевого красителя, Синий # 1:
.
Здесь максимальное поглощение составляет 630 нм, в оранжевом диапазоне видимого спектра, и соединение выглядит синим.
Пример 14.8.2
Насколько велик переход π — π * в 4-метил-3-пентен-2-оне?
Решение
Пример 14.8.3
Какие из следующих молекул вы ожидаете, что они будут поглощать более длинные волны в УФ-области электромагнитного спектра? Поясните свой ответ.
Решение
Упражнение
Вопросы
Q14.8.1
Что из следующего может показывать поглощение УФ-излучения в диапазоне 200–300 нм?
Решения
S14.8.1
B и D будут в этом диапазоне.
Авторы и авторство
Что такое УФ-видимая спектроскопия? И как это применимо к спряжению?
Понимание УФ-видимой спектроскопии сделает вас веселее на вечеринках
В сегодняшнем посте мы обсудим, почему большинство молекул бесцветны, познакомимся с полезной техникой УФ-видимой спектроскопии и, наконец, объясним , почему молекул, таких как хлорофилл и β-каротин окрашены.В заключение мы даже покажем вам, как использовать УФ-видимый спектр для предсказания цвета молекулы, что является отличным трюком для использования на коктейльных вечеринках. Нет, серьезно, это невероятно. Мы говорим о понимании химии цвета, всем! Нет ничего лучше этого.
Во-первых, резюме. Мы рассмотрим детали ниже.
Содержание
- Преобразование единиц частоты в единицы энергии
- Электроны основного состояния могут быть переведены в возбужденное состояние посредством поглощения света
- Практический пример: молекулярная орбитальная диаграмма h3
- Почему большинство молекул Содержат только одиночные связи, являются бесцветными
- Pi-связи поглощают на более длинных и энергетически доступных длинах волн
- УФ-видимый спектрометр
- Как конъюгация Pi-связей влияет на Lambda Max?
- Как лямбда-макс соотносится с цветом, который мы воспринимаем?
- Заключение: УФ-видимая спектроскопия
- Примечания
1.Преобразование частоты света в единицы энергии
Если вы хотите, чтобы кто-то прочитал то, что вы написали, начинать с уравнения — плохая идея. Однако мы собираемся начать с одного из самых красивых, удивительных и простых полезных уравнений во всей науке. Так что если вы уйдете после прочтения этого, это действительно ваша проблема.
Из общей химии вы можете вспомнить бессмертное уравнение
E = hν
, где E — энергия, h — постоянная Планка (6.626 × 10 -34 м 2 кг / с) и ν — частота (в м -1 ).
Почему это уравнение так чертовски полезно? Потому что он связывает энергию с частотой света.
Чтобы быть более конкретным, когда я говорю «свет», я имею в виду «фотон», как носитель электромагнитного излучения. Для целей сегодняшней публикации, вот часть электромагнитного спектра, которую мы будем обсуждать сегодня: УФ и видимые частоты.
2. Электроны основного состояния могут быть переведены в возбужденное состояние посредством поглощения света
Вернувшись в общую химию (модель Бора атома водорода, кто-нибудь?… Кто-нибудь?), Вы видели, как электрон может быть продвинут из основное состояние , , орбиталь к возбужденному состоянию , орбиталь через поглощение фотона с частотой:
ν = ΔE / h
[где ΔE — разница в энергии между основным и возбужденным состояниями ].
Поскольку электрон перемещается с одного энергетического уровня на другой, мы называем эти « электронных переходов ». Обычно частота излучения, необходимая для электронных переходов, находится в ультрафиолетовой и видимой части электромагнитного спектра.
Это имеет практическое значение во многих отношениях, но для наших целей мы увидим, что наиболее важным из них является то, что свет может продвигать электроны с , связывающих орбиталей, на анти-связывающих орбиталей , и, следовательно, потенциально может привести к разрыв химических связей.
Это поможет нам понять:
- почему молекулы в первую очередь поглощают УФ-свет (переходы сигма -> сигма *)
- почему УФ-излучение чрезвычайно вредно (особенно дальнее УФ-излучение)
- и, в конечном итоге, почему определенные молекулы имеют цвет (переходы pi -> pi *)
Начнем с простейшей молекулы, водорода (H 2 ) и построим оттуда.
3. Практический пример: диаграмма молекулярных орбиталей молекулярного водорода (H
2 )
В начале курса органической химии вы, вероятно, видели, как атомные орбитали могут перекрываться, образуя молекулярных орбиталей.
В водороде (H 2 ), например, две 1s атомные орбитали перекрываются, образуя две сигма (σ) молекулярные орбитали . Число орбиталей всегда сохраняется: поскольку мы начинаем с двух атомных орбиталей, мы получаем две молекулярные орбитали.
Конструктивное перекрытие приводит к образованию более низкоэнергетической сигма (σ) орбитали. Деструктивное перекрытие приводит к образованию орбитали сигма-звезды с более высокой энергией (σ *).Эти две орбитали различаются по энергии ΔE .
Поскольку каждый атом водорода приносит на вечеринку по одному электрону, у нас есть два электрона, которыми мы заполняем наши молекулярные орбитали, и они сначала заполняют орбитали с более низкой энергией — так же, как никто не предпочитает стоять в проходе городского автобуса. (более высокая энергия), когда присутствует свободное место (более низкая энергия).
Это дает нам диаграмму, которая выглядит следующим образом: (Если вас это пугает, просто сосредоточьтесь на этом красном ΔE ).
То, что ΔE важно: по аналогии с моделью Бора, если молекулярный водород (H 2 ) подвергается воздействию света с частотой
ν = ΔE / h
, электрон будет продвигаться из молекулярная орбиталь в основном состоянии (сигма) (самая высокая занятая молекулярная орбиталь или HOMO) на возбужденную сигма * молекулярную орбиталь (самая низкая незанятая молекулярная орбиталь или LUMO ).
Это немного похоже на то, как малыши поднимаются по лестнице, по одной ступеньке за раз: одна ступня поднимается с самой высокой занятой ступени до самой низкой незанятой ступени , и энергия, необходимая для этого, определяется разницей в высоте между ними. шаги.
Теперь мы можем преобразовать частоту в длину волны с помощью уравнения
c = ν λ (c — скорость света, λ — длина волны).
Для связи H-H в H 2 , ΔE соответствует измеренному максимуму длины волны поглощения 112 нм , который является глубоким, глубоким, глубоким в УФ-области электромагнитного спектра.
4. Почему большинство молекул, содержащих только одинарные связи, являются бесцветными
112 нм — это не совсем область солярия УФ.Нет, это часть ультрафиолетового спектра с лучами смерти. Это потому, что УФ-излучение ниже 120 нм также является местом, где поглощаются обычные сигма-связи, такие как CH и CC, и, следовательно, воздействие дальнего УФ-света быстро фрагментирует связи, которые составляют белки, сахара и ДНК, присутствующие в нашем организме, и нам слизь.
Давайте проясним это.
Большинство одинарных (то есть сигма) связей, таких как C-C, C-H, O-H и C-O, имеют значения ΔE, которые соответствуют свету в глубокой УФ-части спектра. Они кажутся нам бесцветными, потому что свет в видимой области (400-700 нм) просто не имеет достаточно энергии, чтобы перевести их связывающие электроны в возбужденное состояние.
Поэтому вода бесцветная. Вот почему этанол бесцветен. Вот почему диэтиловый эфир, гексаны, хлороформ и множество других молекул, с которыми вы сталкиваетесь как в лаборатории, так и в повседневной жизни, бесцветны: ΔE для связывающих орбиталей слишком велико для фотонов видимого света с относительно низкой энергией возбуждают их. [Вставьте шутку с Джебом Бушем?]
На самом деле УФ в области ниже 120 нм настолько энергичен, что полностью поглощается атмосферным O 2 и N 2 . Другими словами, если вы хотите измерить точные длины волн, на которых, скажем, поглощает этанол, вам нужно будет поместить его в вакуумную камеру и подвергнуть воздействию жесткого ультрафиолетового света. Это, конечно, представляет академический интерес, но выходит за рамки типичного вводного курса. Для наших целей мы не будем далее обсуждать переходы сигма → сигма *.
Итог: мы обычно не наблюдаем переходы сигма → сигма *.
[Единственное исключение, с которым мы действительно сталкиваемся, — это дигалогены, такие как Cl 2 и I 2 , которые могут поглощать видимый свет и генерировать свободные радикалы за счет гомолитического расщепления сигма-связей. Это пример разрыва сигма-связей за счет поглощения УФ или видимого света, что стало возможным благодаря тому, что эти связи довольно слабые, около 50-60 ккал / моль, и соответствующее ΔE невелико].
5.Связи Pi (π) поглощают на более длинных и доступных длинах волн
Хорошо: мы собираемся игнорировать переходы σ → σ *. Так что давайте вместо этого поговорим о переходах π-π *.
Вот где становится интересно и актуально.
Давайте вспомним, о чем мы говорим, начав с простой молекулы. Вот этен (он же «этилен»), простейший алкен. Беглый взгляд на его структуру показывает 5-сигма облигаций и однопи-облигаций .
- Напомним, что сигма-связи являются результатом «на конце» перекрытия между s или sp n (sp, sp 2 или sp 3 ) орбиталями, тогда как пи-связи являются результатом «сбоку» соединение соседних p-орбиталей.
- При прочих равных π-связи на слабее , чем сопоставимые сигма-связи, потому что существует меньшее перекрытие орбиталей.
- Более слабые связи означают, что энергетическая щель ΔE между π (HOMO) и π * (LUMO) будет соответственно на меньше .[В нашей аналогии более короткая ступенька лестницы требует меньше энергии для подъема].
- Поскольку ΔE на меньше для пи-связи, это соответствует более длинной на длине волны (из более низкой частоты ), необходимой для возбуждения электрона с пи на орбиталь пи *.
Для этена максимальная длина волны поглощения для этого перехода pi-pi * составляет около 170 нм: все еще находится в глубоком УФ-диапазоне, но не так сильно, как для соответствующей сигма-связи C-C.
Мы ожидаем, что этилен будет бесцветным, и это так: он просто поглощает немного ближе к видимой части спектра, чем, скажем, этан.
Давайте проиллюстрируем это фигурой, которая часто выглядит пугающей для студентов: диаграммой орбитальной энергии.
* Предупреждение о срабатывании триггера * Все, что этот рисунок пытается показать, это то, что ΔE для π-связи C-C ( в зеленом цвете ) меньше, чем ΔE для σ-связи C-C ( в сером) . Если вы это поняли, значит, вы уловили ключевой момент.*
Подождите, можно сказать. Откуда мы, , знаем , что этен поглощает УФ свет около 170 нм?
Рад, что вы спросили. Давайте представим очень важное устройство под названием UV-Vis Spectrometer .
6. Спектрометр УФ-видимой области
Основная идея спектроскопии УФ-видимой области состоит в том, чтобы направить свет с различной длиной волны через образец и с помощью прибора измерить оптическую плотность на каждой длине волны . Только длины волн, соответствующие ΔE для электронного перехода, будут сильно поглощаться.[Схематическое изображение работы спектрометра: посмотрите на эту отличную страницу , , которая также является отличным альтернативным объяснением УФ].
Спектр UV-Vis отображает оптическую плотность (или обратную ей, пропускание) образца в зависимости от длины волны. Вот спектр этена. [В этом случае длина волны отображается в зависимости от коэффициента пропускания , обратной величины поглощения (высокое поглощение = низкое пропускание, и наоборот). ]
Обратите внимание, что длина волны с максимальным коэффициентом пропускания составляет 174 нм. Мы называем это λ max , произносится как «lambda max». Очень мало света проходит через образец на этой длине волны, потому что длина волны очень близко соответствует ΔE для перехода от π к π *.
Спектрометр UV-Vis — полезный инструмент, потому что он позволяет нам точно определить, где образцы поглощают свет, и, таким образом, количественно определить электронных переходов. Например, зная, что λ max для этена находится на длине волны 174 нм, мы можем рассчитать ширину запрещенной зоны ΔE, которая составляет около 164 ккал / моль.
7. Как конъюгация связей Pi влияет на λ max ?
В нашей предыдущей публикации о природных пигментах, мы отметили, что их большое количество конъюгированных пи-связей отвечает за их цвет.
УФ-видимая спектроскопия помогает нам понять , как именно конъюгация связана с λ max молекулы — и, следовательно, с ее цветом (или его отсутствием).
Например, давайте посмотрим, что происходит с λ max , когда мы увеличиваем длину сопряжения с 1 (этен) до 2 (бутадиен) до 3 (гексатриен).
По мере увеличения количества сопряженных пи-связей, λ max также увеличивается!
Поскольку более высокая частота = меньшая энергия, это означает, что энергетический зазор ΔE между наиболее занятой молекулярной орбиталью (ВЗМО) и самой низкой незанятой молекулярной орбиталью (НСМО) уменьшается на по мере увеличения количества сопряженных пи-связей .
Вот как выглядит склеивающее изображение (примерно).Опять же, просто сосредоточьтесь на ΔE: он становится меньше по мере увеличения количества сопряженных пи-связей.
Поскольку эта тенденция продолжается и дальше от гексатриена к молекулам с большей длиной сопряжения, λ max начинает проникать в видимую область спектра. Он уже составляет 258 нм для длины сопряжения, равной 3. Цвет начинает появляться, когда длина сопряжения приближается к 7 или около того. [Например, амфотерицин B имеет 7 конъюгированных пи-связей и поглощает около 403 нм в фиолетовом цвете.]
Наши старые друзья ликопин (λ макс. 471 нм), β-каротин (λ макс. 452 нм) и лютеин (λ макс. 445 нм) имеют еще большие пи-системы (10 и 11) и поглощают видимые свет дальше в сторону красного. [Примечание 4]
Таким образом, λ max молекул в значительной степени зависит от длины конъюгации: по мере увеличения числа конъюгации увеличивается и λ max .
Но остается один вопрос:
8. Как λ
max соотносится с цветом, который мы воспринимаем?
Последний кусочек головоломки.Как длина волны максимального поглощения (λ max ) соотносится с фактическим цветом ?
Во-первых, напоминание из последнего поста. Мы видим дополнительный цвет к основному поглощаемому цвету. Молекула, которая поглощает синий , будет выглядеть оранжевым , потому что мы воспринимаем цвета, которые отражаются , а оранжевый является дополнительным цветом синего.
Например, эта молекула, родамин B [примечание 2] поглощает около 560 нм ( зеленый ) и выглядит красным , дополнительным зеленым цветом.
Знание того, где молекула поглощает видимый свет, позволяет нам делать прогнозы относительно ее цвета. Интересно!
Думаю, это довольно крутой трюк с коктейльной вечеринкой. Подумайте об этом, когда в следующий раз посмотрите на лист, помидор, морковь или кровь желтого рака.
Мы могли бы продолжить (и будем!). Но пока оставим это.
BTW: Фантастическая обработка УФ-видимой спектроскопии с меньшим количеством болтовни была написана Тимом Содербергом в LibreText.Проверить это.
Кроме того, статья Ройша в онлайн-учебнике по УФ-видимой спектроскопии более детальна и богата деталями по этой теме, чем эта статья.
9. Заключение: УФ-видимая спектроскопия
В этом посте были рассмотрены некоторые теории, лежащие в основе спектров УФ-видимого диапазона.
В следующем посте мы рассмотрим некоторые из более практических аспектов УФ-видимой спектроскопии. На какие вопросы УФ-видимое излучение может помочь нам ответить о неизвестной молекуле?
Примечания
Дополнительные примечания:
Чего не хватает в этом обсуждении?
λ max не является исключительно функцией количества пи-связей.Если бы это было правдой, ликопин (11 конъюгированных пи-связей) и b-каротин (также с 11 конъюгированными пи-связями) имели бы точно такой же цвет. Это не так, поскольку на λ max также влияют заместители, такие как присоединенные алкильные группы, независимо от того, является ли пи-связь внутренней или внешней по отношению к кольцу (эндоциклическим / экзоциклическим) и присоединенными гетероатомами.
Еще в 1940-х годах, когда УФ-видимое излучение было практически единственным доступным спектроскопическим методом, Вудвард и Физер разработали набор эмпирических правил (правила Вудворда-Физера), направленных на прогнозирование λ max на основе ряда структурных факторов. .Существуют также варианты этих правил для более сложных сопряженных систем (правила Физера-Куна).
[Примечание 2] Я бы хотел использовать УФ-видимые спектры природных пигментов, таких как ликопин и хлорофилл, в качестве примеров, но они содержат более одного максимума. Это непросто объяснить. Следовательно, не так просто перевести в цвет, как Родамин B. Вот, например, ликопин (источник: wikipedia)
[Примечание 3] Также здесь не хватает того, почему спектры UV-Vis являются широкими, а не прямыми линиями.Например, если, скажем, родамин имеет дельту E, которая соответствует свету с длиной волны 560 нм, почему он также поглощает свет с длиной волны 559 и 561 нм? Частично ответ заключается в том, что связи находятся в постоянной вибрации, и это регулирует значение дельта E, так что поглощается диапазон энергий.
[Примечание 4] [Как далеко мы можем зайти? В крайнем случае, у вас есть графен, который представляет собой просто большую плоскую сопряженную пи-систему с почти бесконечным числом сопряженных пи-связей. В этой ситуации почти каждая длина волны света соответствует некоторому переходу пи-пи *, и в результате получается черный цвет.]
УФ-ВИДИМЫЕ СПЕКТРЫ ПОГЛОЩЕНИЯ На этой странице объясняется, что происходит, когда органические соединения поглощают УФ или видимый свет, и почему длина волны поглощаемого света варьируется от соединения к соединению. | |||||||||||||||||||
Важно: Если вы перешли прямо на эту страницу из поисковой системы, вы должны знать, что она следует из вводной страницы, объясняющей некоторые важные связи для УФ-видимой спектрометрии.Вам необходимо прочитать это, прежде чем переходить к этой странице. | |||||||||||||||||||
Что происходит, когда свет поглощается молекулами? Продвижение электронов Когда мы говорили на вводной странице о различных типах орбиталей, присутствующих в органических соединениях (см. Выше), вы натолкнулись на эту диаграмму, показывающую их относительные энергии: Помните, что диаграмма не предназначена для масштабирования — она просто показывает относительное расположение различных орбиталей. Когда свет проходит через соединение, энергия света используется для продвижения электрона с связывающей или несвязывающей орбитали на одну из пустых антисвязывающих орбиталей. | |||||||||||||||||||
Важно: Если вы не совсем понимаете, что я имею в виду под связывающими, несвязывающими и анти-связывающими орбиталями, или не помните диаграмму, вернитесь и прочтите вводную страницу еще раз. | |||||||||||||||||||
Возможные скачки электрона, которые может вызвать свет: В каждом возможном случае электрон возбуждается с полной орбитали на пустую антисвязывающую орбиталь.Каждый прыжок забирает энергию от света, и, очевидно, для большого прыжка требуется больше энергии, чем для маленького. С каждой длиной волны света связана определенная энергия. Если это конкретное количество энергии как раз подходит для совершения одного из этих энергетических скачков, тогда эта длина волны будет поглощена — ее энергия будет использована для продвижения электрона. Нам нужно выяснить, какова взаимосвязь между шириной запрещенной зоны и длиной поглощенной волны. Означает ли, например, большую энергетическую щель, что свет с меньшей длиной волны будет поглощаться — или что? Проще начать с соотношения между частотой поглощенного света и его энергией: Как видите, если вы хотите совершить прыжок с высокой энергией, вам придется поглощать свет более высокой частоты.Чем выше частота, тем больше энергия. Это легко, но, к сожалению, спектры поглощения в УФ и видимой областях всегда даются с использованием длин волн света, а не частоты. Это означает, что вам нужно знать соотношение между длиной волны и частотой. Из этого видно, что чем выше частота, тем меньше длина волны. Итак. . . Если у вас больший энергетический скачок, вы будете поглощать свет с более высокой частотой — это то же самое, что сказать, что вы будете поглощать свет с более низкой длиной волны. Важная информация Чем больше скачок энергии, тем меньше длина волны поглощаемого света. | |||||||||||||||||||
Примечание: Очевидно, лучше, если вы сможете решить это на случай, если вы его забудете, но вы можете почувствовать, что намного проще выучить последнее утверждение. Как бы то ни было, вы должны быть уверены в этих отношениях. Если вам нужна дополнительная помощь в выяснении этих взаимосвязей, вы найдете их более медленное обсуждение на странице этого раздела, посвященной электромагнитному излучению. Если вы решите перейти по этой ссылке, используйте кнопку НАЗАД в браузере, чтобы вернуться на эту страницу. | |||||||||||||||||||
Некоторые скачки важнее других для абсорбционной спектрометрии Абсорбционный спектрометр работает в диапазоне от примерно 200 нм (в ближнем ультрафиолетовом диапазоне) до примерно 800 нм (в самом ближнем инфракрасном диапазоне). Только ограниченное количество возможных электронных прыжков поглощает свет в этой области. | |||||||||||||||||||
Примечание: Если вам интересно, на другой странице этого раздела есть описание того, как работает двухлучевой абсорбционный спектрометр. Это не обязательно знать об этом, чтобы понять остальную часть этой страницы. | |||||||||||||||||||
Посмотрите еще раз на возможные прыжки. На этот раз важные прыжки показаны черным, а менее важные — серым. Серые пунктирные стрелки показывают скачки, которые поглощают свет за пределами области спектра, в которой мы работаем. Помните, что для больших прыжков требуется больше энергии, поэтому они поглощают свет с более короткой длиной волны.Скачки, показанные серыми пунктирными стрелками, поглощают УФ-свет с длиной волны менее 200 нм. Важные прыжки:
Это означает, что для поглощения света в области от 200 до 800 нм (где измеряются спектры) молекула должна содержать либо пи-связи, либо атомы с несвязывающими орбиталями.Помните, что несвязывающая орбиталь — это неподеленная пара, скажем, на кислороде, азоте или галогене. Группы в молекуле, которые поглощают свет, известны как хромофоры . | |||||||||||||||||||
Примечание: Сайт канадского университета описывает «хромофор» как «одно из тех полезных, но небрежных слов, значение которых в некоторой степени зависит от контекста». Как вы вскоре узнаете, сильно делокализованные системы в молекуле часто ответственны за поглощение света в видимой области и придание составу цветного вида.Делокализация может включать несколько различных типов групп — бензольные кольца, двойные связи углерод-углерод, двойные связи углерод-кислород, неподеленные пары азота или кислорода — и так далее. Некоторые люди говорят так, как будто вся делокализованная система является хромофором; другие склонны думать о вкладе отдельных частей системы. Мне кажется более логичным думать о системе в целом, потому что именно скачки электрона внутри системы в целом вызывают поглощение.Однако, если ваши экзаменаторы придерживаются другой точки зрения, очевидно, что вам следует придерживаться того, что они хотят. Единственный способ узнать это — посмотреть на недавние экзаменационные работы и схемы оценок. Если вы студент уровня A (или эквивалент) в Великобритании, перейдите по этой ссылке на страницу учебных программ, чтобы узнать, как их получить, если вы их еще не получили. | |||||||||||||||||||
Как выглядит спектр поглощения На диаграмме ниже показан простой спектр поглощения в УФ и видимой областях бута-1,3-диена — молекулы, о которой мы поговорим позже.Поглощение (по вертикальной оси) — это просто мера количества поглощенного света. Чем выше значение, тем больше поглощается волны определенной длины. Вы увидите, что поглощение достигает пика при значении 217 нм. Он находится в ультрафиолетовом диапазоне, поэтому видимых признаков поглощения света не будет — бута-1,3-диен бесцветен. Вы читаете символ на графике как «лямбда-макс». В бута-1,3-диене, CH 2 = CH-CH = CH 2 , нет несвязывающих электронов.Это означает, что происходят только скачки электронов (в пределах диапазона, который может измерить спектрометр) от пи-связывания к пи-антисвязывающим орбиталям. | |||||||||||||||||||
Примечание: Показанный спектр представляет собой упрощенный схематический график — он не претендует на большую точность! Если вы действительно бодрствуете, вы можете задаться вопросом, почему график выглядит так, как будто он имеет широкий пик поглощения, а не одну линию на 217 нм. Переход с пи-связывающей орбитали на пи-анти-связывающую орбиталь должен иметь фиксированную энергию и, следовательно, поглощать фиксированную длину волны.На самом деле соединение поглощает во всем диапазоне длин волн, что предполагает целый диапазон энергетических скачков. Эта проблема возникает из-за того, что вращения и колебания в молекуле постоянно изменяют энергии орбиталей — и это, конечно, означает, что промежутки между ними также постоянно меняются. В результате поглощение происходит в диапазоне длин волн, а не в одном фиксированном диапазоне. На этом уровне вам не нужно беспокоиться об этом. | |||||||||||||||||||
Хромофор, дающий два пика Хромофор, такой как двойная связь углерод-кислород в этанале, например, очевидно, имеет пи-электроны как часть двойной связи, но также имеет неподеленные пары на атоме кислорода. Это означает, что возможны оба важных поглощения из последней энергетической диаграммы. | |||||||||||||||||||
Примечание: Если вы не слишком уверены в связи в двойной связи углерод-кислород, перед продолжением стоит перейти по этой ссылке. Используйте кнопку НАЗАД в браузере, чтобы вернуться на эту страницу, когда будете готовы. | |||||||||||||||||||
Вы можете возбудить электрон от пи-связи к пи-антисвязывающей орбитали, или вы можете возбудить электрон от неподеленной кислородной пары (несвязывающей орбитали) на пи-антисвязывающую орбиталь. | |||||||||||||||||||
Примечание: Прежде чем продолжить чтение, выясните, какие из них будут поглощать свет с большей длиной волны.Попытайся! Если вы можете решить это сами, значит, вы раскрыли одну из самых сложных вещей в этой теме. | |||||||||||||||||||
Несвязывающая орбиталь имеет более высокую энергию, чем связывающая пи-орбиталь. Это означает, что прыжок с неподеленной кислородной пары на орбиталь с антисвязыванием пи требует меньше энергии. Это означает, что он поглощает свет с более низкой частотой и, следовательно, с более высокой длиной волны. Таким образом, Ethanal может поглощать свет двух разных длин волн: Оба этих поглощения находятся в ультрафиолетовом диапазоне, но большинство спектрометров не улавливают поглощение на 180 нм, потому что они работают в диапазоне от 200 до 800 нм. Важность сопряжения и делокализации на длине волны поглощения Рассмотрим эти три молекулы: Этен содержит простую изолированную двойную связь углерод-углерод, но два других имеют сопряженные двойные связи. В этих случаях происходит делокализация пи-связывающих орбиталей по всей молекуле. | |||||||||||||||||||
Важно: Если вы не знаете, что такое спряжение, вернитесь и прочтите этот раздел вводной страницы еще раз. | |||||||||||||||||||
Теперь посмотрите на длины волн света, которые поглощает каждая из этих молекул.
Все молекулы дают одинаковые спектры поглощения в УФ и видимой областях спектра с той лишь разницей, что поглощение перемещается в сторону более длинных и длинных волн по мере увеличения степени делокализации в молекуле. Почему это? Вы действительно можете понять, что должно происходить.
. . . и вот что происходит. Сравните этен с бута-1,3-диеном. В этене есть одна пи-связывающая орбиталь и одна пи-анти-связывающая орбиталь. В бута-1,3-диене есть две пи-связывающие орбитали и две анти-связывающие пи-орбитали. Все это подробно обсуждается на вводной странице, которую вы должны были прочитать. Наивысшую занятую молекулярную орбиталь часто называют HOMO — в этих случаях это пи-связывающая орбиталь.Самая низкая незанятая молекулярная орбиталь (НСМО) — это пи-антисвязывающая орбиталь. Обратите внимание, что разрыв между ними уменьшился. В случае бута-1,3-диена для возбуждения электрона требуется меньше энергии, чем в случае этена. В случае гекса-1,3,5-триена еще меньше. | |||||||||||||||||||
Примечание: В этом случае вам придется решить для себя, почему в гекса-1,3,5-триене есть 3 связывающих и 3 антисвязывающих пи-орбитали.Если вам интересно, вы можете решить это так же, как я использовал для бута-1,3-диена на вводной странице. Это не обязательно — важно только то, что вы можете видеть узор — чем больше делокализация, тем длиннее поглощаемая длина волны. Если вы решите перейти по этой ссылке, используйте кнопку НАЗАД в браузере, чтобы вернуться сюда позже. | |||||||||||||||||||
Если вы распространите это на соединения с действительно сильной делокализацией, длина поглощенной волны в конечном итоге будет достаточно высокой, чтобы находиться в видимой области спектра, и тогда соединение будет рассматриваться как окрашенное.Хорошим примером этого является оранжевый растительный пигмент, бета-каротин, присутствующий, например, в моркови. Почему бета-каротин оранжевый? Бета-каротин имеет вид делокализации, который мы только что рассмотрели, но в гораздо большем масштабе с 11 двойными связями углерод-углерод, сопряженными вместе. На диаграмме показана структура бета-каротина с чередующимися двойными и одинарными связями, показанными красным. Чем больше делокализация, тем меньше зазор между связывающей орбиталью pi с самой высокой энергией и антисвязывающей орбиталью pi с самой низкой энергией.Следовательно, для продвижения электрона в бета-каротине требуется меньше энергии, чем в случаях, которые мы рассмотрели до сих пор, потому что промежуток между уровнями меньше. Помните, что меньшая энергия означает поглощение света меньшей частоты — и это эквивалентно большей длине волны. Бета-каротин поглощает всю ультрафиолетовую область в фиолетовую, но особенно сильно в видимой области между 400 и 500 нм с пиком примерно 470 нм. Если вы читали страницу в этом разделе об электромагнитном излучении, вы могли вспомнить, что длины волн, связанные с различными цветами, приблизительно равны:
Итак, если поглощение больше всего в диапазоне от фиолетового до голубого, какой цвет вы на самом деле увидите? Заманчиво думать, что вы можете решить это по оставшимся цветам — и в этом конкретном случае вы не ошибетесь.К сожалению, это не так просто! Иногда то, что вы видите на самом деле, бывает довольно неожиданным. Смешивание разных длин волн света не дает такого же результата, как смешивание красок или других пигментов. Однако иногда можно получить некоторую оценку цвета, который вы бы увидели, используя идею дополнительных цветов . Дополнительные цвета Если вы расставите несколько цветов по кругу, вы получите «цветовой круг».На схеме показан один из возможных вариантов этого. Поиск в Интернете подбросит много разных версий! Цвета, расположенные прямо напротив друг друга на цветовом круге, называются дополнительными цветами. Синий и желтый — дополнительные цвета; красный и голубой дополняют друг друга; а также зеленый и пурпурный. Смешивание двух дополнительных цветов света даст вам белый свет. | |||||||||||||||||||
Осторожно: Это НЕ то же самое, что смешивание цветов краски.Если смешать желтую и синюю краски, не получится белая краска. Это сбивает с толку? ДА! | |||||||||||||||||||
Все это означает, что если определенный цвет поглощается из белого света, то, что ваш глаз обнаруживает, смешивая все другие длины волн света, является его дополнительным цветом. В случае с бета-каротином ситуация более запутанная, потому что вы поглощаете такой диапазон длин волн. Однако, если вы думаете о пиковом поглощении, переходящем от синего к голубому, было бы разумно думать о цвете, который вы бы увидели, как о противоположном цвету, где желтый переходит в красный — другими словами, оранжевый. Вы найдете цвета немного более четкими в двух других примерах, о которых мы поговорим ниже. | |||||||||||||||||||
Примечание: Если вам интересно понять взаимосвязь между поглощенным цветом и видимым цветом (помимо самого основного описания выше), перейдите к уроку 2 («Цвет и зрение») «Световые волны и зрение» на сайте The Кабинет физики. Я не даю прямую ссылку на эти страницы, потому что этот сайт все еще развивается, и безопаснее давать ссылку на главную страницу сайта.Это наиболее понятное объяснение, которое я нашел в Интернете. | |||||||||||||||||||
Применяя это к изменению цвета двух индикаторов Фенолфталеин Вы, вероятно, использовали фенолфталеин в качестве кислотно-основного индикатора и знаете, что он бесцветен в кислой среде и пурпурный (ярко-розовый) в щелочном растворе. Как это изменение цвета связано с изменениями в молекуле? Структуры двух разноцветных форм: Оба они поглощают свет в ультрафиолетовом диапазоне, но тот, что справа, также поглощает в видимом диапазоне с пиком на 553 нм. Молекула в растворе кислоты бесцветна, потому что наши глаза не могут обнаружить тот факт, что часть света поглощается ультрафиолетом. Однако наши глаза действительно обнаруживают поглощение при 553 нм, производимое формой в щелочном растворе. 553 нм находится в зеленой области спектра. Если вы посмотрите на цветовое колесо, вы обнаружите, что дополнительный цвет зеленого — пурпурный — и это тот цвет, который вы видите. Так почему же цвет меняется при изменении структуры? То, что мы имеем, — это переход к поглощению на более высокой длине волны в щелочном растворе.Как мы уже видели, переход к более высокой длине волны связан с большей степенью делокализации. Вот модифицированная диаграмма строения формы в кислом растворе — бесцветная форма. Степень делокализации показана красным. Обратите внимание, что есть делокализация по каждому из трех колец, простирающихся по двойной связи углерод-кислород и к различным атомам кислорода из-за их неподеленных пар. Но делокализация не распространяется на всю молекулу.Атом углерода в центре с его четырьмя одинарными связями предотвращает взаимодействие трех делокализованных областей друг с другом. Теперь сравните это с пурпурной формой: Теперь перегруппировка позволяет делокализации распространиться на весь ион. Эта большая делокализация уменьшает энергетический зазор между самой высокой занятой молекулярной орбиталью и самой низкой незанятой антисвязывающей пи-орбиталью. Чтобы совершить прыжок, требуется меньше энергии, поэтому поглощается свет с большей длиной волны. Помните: увеличение степени делокализации смещает пик поглощения в сторону большей длины волны. | |||||||||||||||||||
Примечание: Не паникуйте при мысли, что вам, возможно, придется рисовать эти структуры на экзамене. На уровне стандарта UK A (и его эквивалента) этого не произойдет. Однако, если бы вам дали структуры двух форм фенолфталеина и попросили объяснить изменение цвета, это могло бы стать хорошим вопросом (в зависимости, конечно, от того, что именно ваша программа ожидает от вас). | |||||||||||||||||||
Метиловый оранжевый Вы знаете, что метиловый оранжевый желтый в щелочных растворах и красный в кислых. Структура в щелочном растворе: В кислотном растворе ион водорода (возможно, неожиданно) захватывается одним из атомов азота в двойной связи азот-азот. Теперь все становится намного сложнее! Положительный заряд азота делокализован (распределяется по структуре), особенно по направлению к правому концу молекулы, как мы это писали.Обычно нарисованная структура для красной формы метилового оранжевого — это. . . Но это может серьезно ввести в заблуждение относительно степени делокализации в структуре по причинам, обсуждаемым ниже (после красного поля предупреждения), если вас это интересует. | |||||||||||||||||||
Важно: Если вы читали вводную страницу, вы знаете, что делокализация не распространяется на сульфонатную группу. Это никоим образом не влияет на остальную часть этого аргумента.Эта группа не изменяется при добавлении иона водорода. Все, что нас действительно интересует, — это влияние на делокализацию остальной части молекулы — двух бензольных колец и двух азотсодержащих групп. | |||||||||||||||||||
Итак, какая структура более делокализована — красная или желтая? Давайте вернемся к спектрам поглощения и посмотрим, поможет ли это. Желтая форма имеет пик поглощения около 440 нм.Это синяя область спектра, а дополнительный синий цвет — желтый. Это именно то, что вы ожидали. Красная форма имеет пик поглощения около 520 нм. Это край голубой области спектра, а дополнительный цвет голубого — красный. Опять же, здесь нет ничего неожиданного. Обратите внимание, что изменение желтой формы на красную привело к увеличению длины поглощаемой волны. Увеличение длины волны предполагает увеличение делокализации. Это означает, что в красной форме должно быть больше делокализации, чем в желтой. Почему? Для целей UK A level (и его эквивалентов) на это, вероятно, невозможно ответить. Однако, если вам интересно, ниже есть возможный ответ. . . | |||||||||||||||||||
Внимание! Остальная часть этой страницы будет серьезно затруднена. Если вы студент британского уровня A (или эквивалентный), это выходит далеко за рамки того уровня понимания, который вам может понадобиться. Причина включения его состоит в том, чтобы попытаться устранить впечатление, что красная форма менее делокализована, чем желтая, из-за того, как обычно рисуется структура. Был даже вопрос о бумаге уровня OCR A относительно метилового оранжевого, в котором говорилось (ошибочно!), Что в красной форме было на делокализаций меньше, чем в желтой. Если вы студент OCR из Великобритании, пожалуйста, не используйте Q3 (b) (ii) на бумаге 2815-04 июня 2005 года для практики — на него невозможно ответить, потому что вся основа вопроса неверна. | |||||||||||||||||||
Вот снова структура желтой формы: Делокализация будет распространяться на большую часть структуры — вплоть до неподеленной пары на правом атоме азота. Если вы используете обычную структуру для красной формы, то кажется, что делокализация нарушена посередине — схема чередования одинарных и двойных связей кажется потерянной. Но это означает неправильное понимание того, что представляет собой эта последняя структура. Канонические формы Если вы нарисуете две возможные структуры Кекуле для бензола, вы узнаете, что реальная структура бензола не похожа ни на одну из них. Реальная структура находится где-то посередине — все связи идентичны и имеют что-то среднее между одинарным и двойным характером. Это из-за делокализации бензола. Эти две структуры известны как канонические формы , и каждая из них может рассматриваться как добавление некоторого знания к реальной структуре.Например, связь, нарисованная в правом верхнем углу молекулы, не является ни одинарной, ни двойной, а находится где-то посередине. Аналогично со всеми остальными облигациями. | |||||||||||||||||||
Примечание: Если вы не встречали канонические формы как способ представления делокализации, важно, чтобы вы не воображали, что молекула быстро переключается с одной структуры на другую. Двуглавые стрелки означают совсем другое. Мул — это гибрид осла и лошади.В этих обозначениях вы могли бы изобразить мула, написав осла и лошадь , соединенные двуглавой стрелкой. Ни осел , ни лошадь точно не представляют, как выглядит мул, но проявив немного воображения, вы можете создать довольно хорошее изображение мула, объединив вместе характеристики осла и лошади. Но очевидно, что мул не тратит свое время на то, чтобы быстро переключаться между ослом и лошадью! | |||||||||||||||||||
Две структуры, которые мы ранее нарисовали для красной формы метилового оранжевого, также являются каноническими формами — две из множества форм, которые можно было нарисовать для этой структуры.Мы могли бы представить делокализованную структуру следующим образом: Эти две формы можно рассматривать как результат движений электронов в структуре, и фигурные стрелки часто используются, чтобы показать, как одна структура может вести к другой. На самом деле электроны не сдвинулись полностью ни в ту, ни в другую сторону. Как и в случае с бензолом, реальная структура находится где-то посередине. Вы также должны понимать, что рисование канонических форм не влияет на базовую геометрию конструкции.Типы скрепления, длина или углы не меняются в реальной структуре. Например, неподеленные пары на атомах азота, показанные на последней диаграмме, — это , обе из которых участвуют в делокализации. Чтобы это произошло, все связи вокруг этих атомов азота должны находиться в одной плоскости, а неподеленная пара торчит вверх, чтобы она могла сбоку перекрываться с орбиталями соседних атомов. Тот факт, что в каждой из двух канонических форм один из этих атомов азота показан так, как если бы он имел аммиакоподобное расположение связей, потенциально вводит в заблуждение — и создает впечатление, что делокализация нарушена. Проблема в том, что не существует простого способа представить сложную делокализованную структуру на простых структурных диаграммах. С бензолом и так плохо — с чем-то таким сложным, как метиловый оранжевый, любой метод просто приведет к возможной путанице, если вы не привыкли работать с каноническими формами. Все становится еще сложнее! Если бы вы делали это правильно, было бы множество других канонических форм с другим расположением двойных и одинарных связей и с положительным зарядом, расположенным в разных местах вокруг колец и на другом атоме азота. Реальная структура не может быть правильно представлена ни одной из этого множества канонических форм, но каждая дает намек на то, как работает делокализация. Если мы возьмем две формы, которые мы записали как, возможно, две наиболее важные, это предполагает, что существует делокализация электронов по всей структуре, но что плотность электронов немного мала вокруг двух атомов азота, несущих положительный заряд на одном из них. каноническая форма или другая. Так почему же красная форма более делокализована, чем желтая? Наконец, мы подошли к попытке объяснить, почему делокализация больше в красной форме метилового оранжевого в кислотном растворе, чем в желтой форме в щелочном растворе. Ответ может заключаться в том, что неподеленная пара на азоте в правом конце структуры, как мы ее нарисовали, более полно участвует в делокализации в красной форме. Каноническая форма с положительным зарядом этого азота предполагает значительное движение неподеленной пары к остальной части молекулы. Разве не то же самое происходит с неподеленной парой на одном и том же азоте в желтой форме метилового оранжевого? Не в такой степени. Любая каноническая форма, которую вы рисуете, в которой это происходит, порождает другой отрицательно заряженный атом где-то в остальной части структуры.Такое разделение отрицательных и положительных зарядов энергетически невыгодно. В красной форме мы не производим новое разделение зарядов, а просто перемещаем положительный заряд по структуре. Помните: Это высокоуровневый материал. Чтобы по-настоящему понять это, вам нужно заранее познакомиться с каноническими формами и попрактиковаться в их рисовании. Это химия на уровне степени, а не на уровне A (или его эквиваленте). Вам НЕ нужно ничего из этого (снизу красного предупреждения), если, возможно, вы не читаете это как студент университета.
© Джим Кларк 2007 (изменено в мае 2016 г.) | |||||||||||||||||||
УФ-видимые спектрофотометры — УФ-видимые часто задаваемые вопросы — Свет и теория
Что такое свет?
Хотя обычно говорят, что свет является волной, в отличие от волн, которые возникают на поверхности воды, для него не требуется среда.Как показано здесь, свет состоит из электрического поля и магнитного поля, которые пересекаются друг с другом под прямым углом при движении в вакууме. Расстояние между последовательными пиками электрического или магнитного поля и есть длина волны.
Почему важна длина световой волны?
Чтобы ответить на этот вопрос, нам нужно знать некоторые важные характеристики света в целом. Любая волна — это, по сути, просто способ перемещения энергии из одного места в другое, будь то довольно очевидная передача энергии в волнах на море или в гораздо более трудных для представления волнах в свете.В случае волн на воде энергия передается за счет массового движения молекул воды; однако конкретная молекула воды не проходит через Атлантику или даже через пруд. В зависимости от глубины воды волны следуют примерно по круговой траектории от точки происхождения. По мере того, как они продвигаются к вершине круга, волна переходит в гребень; когда они снова спустятся, вы получите желоб. Энергия передается относительно небольшими локальными движениями в окружающей среде.С волнами на воде довольно легко нарисовать диаграммы, чтобы показать, как это происходит с реальными молекулами. Со светом сложнее. Энергия в свете распространяется из-за локальных флуктуирующих изменений электрических и магнитных полей; отсюда «электромагнитное» излучение. (Вверху слева)
Если вы нарисуете луч света в форме волны, не слишком заботясь о том, что именно вызывает волну, расстояние между двумя гребнями называется длиной волны света. Это также может быть расстояние между двумя впадинами или двумя другими одинаковыми позициями на волне.Вы должны представить себе эти гребни волн движущимися слева направо. Если вы посчитали количество гребней, проходящих через определенную точку в секунду, у вас есть частота света. Он измеряется в том, что раньше называлось «циклами в секунду», а теперь называется герцами, Гц. Циклы в секунду и Герц означают одно и то же. Свет проходит через данное вещество с постоянной скоростью. Например, он всегда движется со скоростью примерно 3 x 108 метров в секунду в вакууме. На самом деле это скорость, с которой распространяется все электромагнитное излучение, а не только видимый свет.Существует простая связь между длиной волны и частотой определенного цвета света и скоростью света. (Внизу слева)
Это соотношение означает, что если вы увеличиваете частоту, вы должны уменьшать длину волны, и, конечно же, верно обратное. Если длина волны больше, частота ниже. Очень важно, чтобы вы чувствовали себя комфортно с соотношением частоты и длины волны. С каждой конкретной частотой света связана определенная энергия.Чем выше частота, тем выше энергия света. Свет с длинами волн от 380 до 435 нм рассматривается как последовательность фиолетовых цветов. Различные красные цвета имеют длину волны от 625 до 740 нм. У кого самая высокая энергия? Свет с наивысшей энергией будет светом с самой высокой частотой, то есть светом с наименьшей длиной волны. (Справа)
Как классифицируются световые волны различной длины?
Свет состоит из определенных типов электромагнитных волн.Электромагнитные волны имеют разные названия в соответствии с их длиной волны, как показано здесь, «свет» обычно относится к электромагнитным волнам в диапазоне, охватывающем инфракрасное и ультрафиолетовое излучение, но в некоторых случаях это относится только к видимому свету. Свет с длинами волн в диапазоне приблизительно от 400 до 800 нм называется «видимым светом» и представляет собой свет, который мы, люди, можем видеть невооруженным глазом. Например, свет с длиной волны 470 нм — синий, свет с длиной волны 540 нм — зеленый, а свет с длиной волны 650 нм — красный.Видимый свет можно охарактеризовать как вид света, с которым мы, люди, знакомы из-за нашей способности его видеть.
Какие диапазоны длин волн света используются?
В УФ / видимой / ближней ИК-спектроскопии используются ультрафиолет (от 170 до 380 нм), видимый (от 380 до 780 нм) и ближний инфракрасный (от 780 до 3300 нм). Нанометр (нм) равен 10 -9 метра. Большинство спектрофотометров сконфигурированы либо как инструменты УФ / видимого диапазона, которые покрывают диапазон длин волн от 190 до 900 нм (или 1100 нм), либо как инструменты УФ / видимого света / ближнего ИК-диапазона, которые покрывают диапазон длин волн от 175 до 3300 нм.
Люди хорошо знакомы с областью видимого света, так как это длины волн, которые может видеть человеческий глаз. На диаграмме «Видимый спектр» выше показано приближение к спектру видимого света. Порядок цветов в видимой области легко запомнить с помощью мнемоники Roy G Biv. Итак, от длинных волн к коротким — красный, оранжевый, желтый, зеленый, синий, индиго, фиолетовый. Теперь мы должны поместить область видимого света в остальную часть электромагнитного спектра.Этот электромагнитный спектр не ограничивается цветами, которые вы видите. Вполне возможно, что длина волны будет короче фиолетового или длиннее красного. На приведенном выше рисунке показаны крайние значения ультрафиолета и инфракрасного излучения, но их можно распространить еще дальше на рентгеновские лучи и радиоволны, среди прочего. На приведенной выше диаграмме показано примерное положение некоторых из них на спектре.
Не беспокойтесь о точных границах между различными видами электромагнитного излучения, потому что границ нет.Как и в случае с видимым светом, один вид излучения переходит в другой. Просто помните об общей закономерности. Также имейте в виду, что энергия, связанная с различными видами излучения, увеличивается по мере увеличения частоты (или уменьшения длины волны).
Как работает «абсорбционная» спектроскопия?
Рассмотрим поглощение света веществом. Это тесно связано с квантовой механикой. Решение уравнений квантовой механики, относящихся к электронам в атоме, дает модель, подобную показанной здесь, в которой электроны имеют дискретные энергетические состояния.E0 называется «основным состоянием», а E1, E2 и т. Д. — «возбужденными состояниями». Чтобы электрон переключился с E0 на E1, свет с энергией (E1 — E0) должен попасть на электрон. Это «поглощение» света. Электроны имеют определенные уровни энергии, а лучи ультрафиолетового и видимого света обладают энергией для изменения энергетических состояний электронов.
Поскольку состояние с более высокой энергией, E1, нестабильно, электрон вскоре возвращается в основное состояние E0. Энергия, выделяемая при возвращении электрона из E1 в E0 (E1 — E0), преобразуется в тепло.Если по какой-то причине она не превращается в тепло, энергия выделяется в виде света. Явление излучения света хорошо известно как флуоресценция или фосфоресценция.
Что касается количественного измерения, выполняемого с помощью спектроскопии, следствием этого явления является то, что существует большое количество поглощения, если в растворе существует большое количество целевых молекул, и только небольшое количество поглощения, если имеется только небольшое количество молекул. целевых молекул. Определение количества и, следовательно, концентрации вещества по степени абсорбции является фундаментальным принципом количественного измерения.
Какую информацию выдает спектрофотометр?
Спектроскопия
UV / Vis обычно используется в аналитической химии для количественного определения различных аналитов, таких как ионы переходных металлов, сильно сопряженные органические соединения и некоторые биологические макромолекулы. Измерение обычно проводят в растворе. Растворы ионов переходных металлов могут быть окрашены (т. Е. Поглощать видимый свет), потому что d-электроны внутри атомов металла могут переходить из одного электронного состояния в другое.На цвет растворов ионов металлов сильно влияет присутствие других частиц, таких как определенные анионы или лиганды. Например, разбавленный раствор сульфата меди имеет светло-голубой цвет; добавление аммиака усиливает цвет и изменяет длину волны максимального поглощения (λmax). Органические соединения, особенно с высокой степенью конъюгации, также поглощают свет в УФ или видимой областях электромагнитного спектра. Растворителями для этих определений часто являются вода для водорастворимых соединений или этанол для органических растворимых соединений.Некоторые органические растворители могут иметь значительное УФ-поглощение; не все растворители подходят для использования в УФ-спектроскопии. Этанол очень слабо поглощает в более низких длинах волн ультрафиолета. Полярность растворителя и pH могут влиять на спектр поглощения некоторых органических соединений.
Выход спектрофотометра — это спектр (обычно). Спектр (множественные спектры) — это график, на котором отображаются значения прошедшего, поглощенного или отраженного света (ось Y) в зависимости от различных значений длины волны света (ось X).
Какие существуют режимы сбора данных типичного спектрофотометра?
Существует четыре основных режима сбора данных на типичном спектрофотометре УФ / видимой / ближней ИК-области. Ниже представлено главное меню инструментов Shimadzu.
1) Режим сканирования — наиболее часто используемый режим — сканирование по длине волны. Здесь длина волны сканируется, а значение ординаты записывается для получения спектра, как показано выше. Приборы сканируют от самой длинной волны к самой короткой.Это необходимо для уменьшения воздействия на образец ультрафиолетового излучения высокой энергии, которое может вызвать фоторазложение.
2) Квантовый режим — квантование обычно выполняется на основном пике образца. Данные могут быть собраны как по высоте пика, так и по площади. Закон Бера гласит, что поглощение пробы прямо пропорционально концентрации. Сначала измеряются стандарты, которые могут состоять из одной или нескольких различных концентраций. Затем концентрации стандарта анализируются и наносятся на график с использованием статистического анализа наименьших квадратов (см. Выше).Неизвестные образцы могут быть рассчитаны с помощью уравнения подбора линии. Если используется только один стандарт, предполагается линейность.
3) Фотометрический режим — Иногда сканирование длины волны не требуется, но необходимо собирать данные с несколькими прерывистыми длинами волн. Фотометрический режим позволяет определять и собирать таблицу длин волн. Этот процесс обычно выполняется для экономии времени, поскольку эта функция выполняется быстрее, чем сканирование по длине волны.
4) Режим Time Drive — в этом режиме собираются данные по ординате с фиксированной длиной волны как функция времени.Часто используется для кинетического анализа для исследования изменений образцов во времени.
Как спектрофотометр измеряет образец?
Для каждой длины волны света, проходящего через спектрометр, измеряется интенсивность света, проходящего через ячейку для образца. Интенсивность света, попадающего в образец, обычно обозначается как I 0 . Интенсивность света, проходящего через кювету с образцом и выходящего с другой стороны, обычно обозначается I 1 .Если мы теперь вычислим процент отношения этих двух значений (I 1 / I 0 ) * 100, мы получим значение процента передачи (% T). Значение% T является мерой света, который проходит через образец и попадает на детектор. Если I 1 меньше, чем I 0 , то очевидно, что образец поглотил часть падающего света. Затем на компьютере выполняется простая математическая операция, чтобы преобразовать это значение в так называемую оптическую плотность образца, обозначенную символом A (иногда абс).Поглощение — это мера количества света, который исчезает (взаимодействует) с образцом. Закон Бера-Ламберта (см. Выше) — это соотношение между оптической плотностью как функцией концентрации образца c, коэффициентом экстинкции образца a, длиной пути образца L, I 0 и I 1 определяется по формуле:
Для большинства недорогих спектрофотометров, которые вы встретите, поглощение колеблется от 0 до 3, но оно может быть выше, чем у более дорогих приборов. UV-3600i Plus и Solid Spec 3700i могут измерять до 8, а иногда и выше.Поглощение 0 означает, что образец не поглощает свет данной длины волны. Интенсивность света, входящего и выходящего из образца, одинакова, поэтому отношение I 1 / I 0 равно 1, поэтому -log 10 из 1 равно нулю. Поглощение, равное 1, происходит, когда было поглощено 90% света на этой длине волны, что означает, что интенсивность составляет 10% от того, что было бы в противном случае. В этом случае I 1 / I 0 равно 10/100 = 0,1) и -log 10 из 0.1 равно 1.
Поглощение — это логарифмическая шкала, аналогичная шкале Рихтера, используемой для землетрясений. Увеличение на 1 единицу по шкале абсорбции означает уменьшение в 10 раз по шкале% T. Другое название, которое люди обычно используют для логарифмической связи (изменение в 10 раз), — «порядок величины». Таким образом, прибор, который может измерять до 3 единиц поглощения, имеет диапазон значений в 3 порядка. Помните также, что по мере уменьшения значения% T значение оптической плотности увеличивается. Выше представлена простая таблица, которая суммирует соотношение между% T и поглощением.
Что такое «молярная поглощающая способность»?
Итак, как насчет ξ (иногда обозначаемого a) в уравнении закона Бера? ξ — молярная поглощающая способность, также известная как коэффициент экстинкции образца. Это уникальная физическая константа химического состава образца, которая связана со способностью образца поглощать свет с заданной длиной волны. Подобно длине пути (b) и концентрации образца (c), ξ также прямо пропорционален поглощению.
Для начала переставим уравнение:
А = ξbc
до
ξ = A / bc
2) Квантовый режим — квантование обычно выполняется на основном пике образца.Данные могут быть собраны как по высоте пика, так и по площади. Закон Бера гласит, что поглощение пробы прямо пропорционально концентрации. Сначала измеряются стандарты, которые могут состоять из одной или нескольких различных концентраций. Затем концентрации стандарта анализируются и наносятся на график с использованием статистического анализа наименьших квадратов (см. Выше). Неизвестные образцы могут быть рассчитаны с помощью уравнения подбора линии. Если используется только один стандарт, предполагается линейность.
Проще говоря, это соотношение можно сформулировать как «ξ» — это мера количества света, поглощенного на единицу концентрации на определенной длине волны.Молярная поглощающая способность является константой для конкретного вещества, поэтому, если концентрация раствора уменьшается вдвое, поглощение уменьшается, а это именно то, что вы ожидаете. Соединение с высокой молярной поглощающей способностью очень эффективно поглощает свет с указанной длиной волны, и, следовательно, низкие концентрации соединения с высокой молярной поглощающей способностью могут быть обнаружены при более низких концентрациях. Кроме того, значение оптической плотности при заданной длине волны можно рассчитать, если вы знаете молярную поглощающую способность, длину пути и концентрацию.
Как использовать закон Бера-Ламберта для количественного анализа?
A = -log
10 (I 1 / I 0 ) = a * b * c
А = а * б * в
Давайте посмотрим на закон Бера-Ламберта и исследуем его значение. Это важно, потому что люди, использующие закон, часто не понимают его, даже если уравнение, представляющее закон, простое. До сих пор мы рассматривали только количество света, попадающего в образец и выходящего из него.Есть три других важных фактора, связанных с образцом, которые определяют оптическую плотность.
Эти факторы:
- длина пути образца (обозначена буквой b)
- концентрация образца (обозначена буквой c)
- — коэффициент экстинкции выборки (обозначен a). Иногда a также называют молярной поглощающей способностью.
Коэффициент экстинкции — это физическое свойство молекулярных связей (химическая структура) исследуемого соединения.Одна и та же молекула всегда будет иметь одно и то же значение a на указанной длине волны. Например, слабо поглощающий пик (связь n-pi *) может иметь значение только 1000; тогда как сильно поглощающий пик (связь пи-пи *) может иметь значения 600 000 значений, а может находиться в диапазоне от нескольких 100 до 1 000 000. Важной особенностью значения a является то, что оно является постоянным для уникального химического состава образца и будет изменяться только при изменении химического состава.
Причина, по которой мы предпочитаем выражать закон в виде оптической плотности (а не% T) с помощью этого уравнения… A = a * b * c
объясняется тем, что оптическая плотность прямо пропорциональна другим параметрам, если соблюдается закон. Вывод:
- если я удваиваю длину пути образца, я удваиваю значение оптической плотности и
- , если я удваиваю концентрацию образца, я удваиваю значение оптической плотности.
Концентрация и длина пути линейно пропорциональны величине оптической плотности.
В чем разница между «количеством» и «концентрацией»?
В химии очень важно понимать разницу между количеством пробы и концентрацией пробы.Количество — это количество чего-либо; концентрация — это количество чего-то в объеме чего-то другого. Итак, 10 граммов сахара — это количество, а 10 граммов сахара, растворенные в 100 миллилитрах воды, — это концентрация. В химии количества обычно выражаются в молях; тогда как концентрации используют термин молярный. Моль чего-либо — это молекулярная масса соединения, выраженная в граммах. Итак, если молекулярная масса соединения 245, то один моль этого соединения будет 245 граммов.Одномолярный раствор будет 245 граммов, растворенных в одном литре растворителя (воды).
Почему количественный анализ всегда выполняется по абсорбции, а не по% передачи?
В качестве примера предположим, что у нас есть раствор сульфата меди (который выглядит синим, потому что имеет максимум поглощения при 600 нм). Мы смотрим, как изменяется интенсивность света, когда он проходит через раствор в кювете диаметром 1 см. Мы будем смотреть на уменьшение каждые 0.2 см, как показано на схеме выше. Закон Бера гласит, что доля света, поглощаемая каждым слоем раствора, одинакова. Для нашей иллюстрации предположим, что эта доля составляет 0,5 для каждого «слоя» 0,2 см, и рассчитаем таблицу данных (вверху справа).
Эти данные можно изобразить в виде графика, чтобы лучше увидеть взаимосвязь. Для% T на графике отображается кривая (вверху слева). Однако для оптической плотности соотношение представляет собой прямую линию (внизу слева). Это принципиальное отличие от% T. Ученые любят прямые линии, а не кривые.Почему? Потому что проще математически смоделировать прямую линию, чем кривую.
Уравнение A = abc говорит нам, что поглощение зависит от общего количества поглощающего соединения на пути света через кювету (внизу справа). Если мы построим график зависимости поглощения на длине волны пика от концентрации, мы получим прямую линию, проходящую через начало координат (0,0). Линейная зависимость между концентрацией и поглощением проста и понятна, поэтому мы предпочитаем выражать закон Бера-Ламберта, используя поглощение как меру поглощения, а не% T.Отсюда ясно, что можно было бы использовать оптическую плотность в качестве шкалы для любого УФ / видимого / ближнего ИК-диапазона, включающего количественный анализ. С оптической плотностью мы можем использовать спектроскопию, чтобы измерить, сколько чего-то присутствует.
Какие химические вещества может измерять спектрофотометр в УФ / видимой области?
Здесь мы рассмотрим электронные переходы УФ / видимой области спектра. Этот высокоэнергетический свет по сравнению с ближним инфракрасным светом имеет достаточно энергии, чтобы вызвать электронные переходы.Эти типы переходов перемещают электроны с низких энергетических уровней в атоме или молекуле на более высокие энергетические уровни.
Сначала мы объясним, что происходит, когда органические соединения поглощают УФ или видимый свет, и почему длина волны поглощаемого света варьируется от соединения к соединению. Проще говоря, энергия света передается электронам, участвующим в химической связи. Это заставляет электроны продвигаться (перемещаться) на более высокий энергетический уровень; тем самым поглощая световую энергию.Эти энергетические уровни связаны со связывающими и антисвязывающими орбиталями сопряженных двойных и тройных атомов углерода или кольцевых систем ароматического бензольного типа в органических молекулах. Помните, что диаграмма выше не предназначена для масштабирования, она просто показывает относительное расположение различных орбиталей. Когда свет проходит через соединение, энергия света используется для продвижения электрона от связывающей или несвязывающей орбитали с более низкой энергией на пустые антисвязывающие орбитали с более высокой энергией.Возможные скачки электронов, которые может вызвать свет, показаны на этом рисунке слайдов (вверху справа).
Длина стрелки пропорциональна количеству энергии, необходимой для перемещения электрона между уровнями энергии. Итак, если у вас есть больший скачок энергии, вы будете поглощать свет с более высокой частотой, что равносильно утверждению, что вы будете поглощать свет с более низкой длиной волны.
Аналогия с реальным миром: Перемещение электрона на более высокий энергетический уровень подобно подбрасыванию мяча в воздух.Энергия от мышц вашей руки (свет) передается (продвижение) к шару (электрону), заставляя его подниматься против силы тяжести (основное состояние). Затем мяч достигает определенной высоты (возбужденное состояние), которая определяется количеством усилия (длиной световой волны), которое вы использовали при броске. В двух словах, это процесс поглощения света, кроме! Шар (электрон) не просто зависает на более высоких энергетических уровнях, он падает обратно на нижний уровень с того места, где он был первоначально продвинут.То же самое происходит с продвинутым электроном при отключении световой энергии. Электрон возвращается в основное состояние. Потенциальная энергия падающего электрона выделяется в виде тепла или может повторно излучаться в виде света (флуоресценция или фосфоресценция). Этот переизлученный свет можно изучить с помощью люминесцентной спектроскопии.
Наиболее важные скачки электронных орбиталей для УФ / видимой спектроскопии:
1) От пи-связывающих орбиталей к пи-антисвязывающим орбиталям (от π к π *)
2) От несвязывающих орбиталей к пи-антисвязывающим орбиталям (от n до π *)
3) От несвязывающих орбиталей к сигма антисвязывающим орбиталям (от n до σ *)
Это означает, что для поглощения света в области от 200 до 800 нм (где измеряются спектры) молекула должна содержать либо пи-связи, двойные связи, либо ароматические кольцевые системы) или атомы с несвязывающими орбиталями.Помните, что несвязывающая орбиталь — это неподеленная электронная пара, скажем, на кислороде, азоте или галогене. Группы в молекуле, которые поглощают свет, известны как хромофоры. Помимо органических молекул, могут поглощать как отдельные неорганические атомы, так и комплексы ионов металлов. Неорганические комплексы имеют тенденцию давать более острые спектральные пики с узкой полушириной полосы. Пример неорганического соединения редкоземельного элемента, оксида гольмия, показан внизу слева.
Какая связь между спектроскопией поглощения и полиароматической кольцевой структурой?
Есть много органических соединений, которые имеют системы сопряженных двойных связей (далее именуемые «сопряженные системы»), в которых каждая другая связь является двойной связью.Эти сопряженные системы имеют большое влияние на максимальную длину волны и интенсивность поглощения.
На верхнем рисунке показаны структуры бензола, нафталина и антрацена. На нижнем рисунке показаны спектры поглощения, полученные при растворении этих соединений в этаноле и анализе полученных растворов. Концентрации были отрегулированы так, чтобы интенсивности поглощения компонентов были примерно одинаковыми. На рисунке видно, что пиковые длины волн имеют тенденцию смещаться в длинноволновую область по мере увеличения размера сопряженной системы.
Почему же тогда длина волны пика имеет тенденцию смещаться в длинноволновую область по мере увеличения размера сопряженной системы? Рассмотрим связь между энергией света и движением электронов.
Свет проявляет свойства как волн, так и частиц (фотонов). Энергия одного фотона выражается как hc / λ, где h — постоянная Планка, c — скорость света, а λ — длина волны. Поглощение в ультрафиолетовой и видимой областях связано с переходом электронов.«Переход» относится к переключению электрона из одного состояния движения в другое. Состояние движения π-электронов в сопряженной системе изменяется легче, чем состояние σ-электронов, образующих молекулярные каркасы. Если фотон сталкивается с π-электроном, этот π-электрон легко переходит в другое состояние движения. Это верно, даже если фотон имеет лишь небольшое количество энергии. На π-электроны в относительно больших сопряженных системах легче воздействовать фотонами низкой энергии.Переход выражает способ поглощения энергии фотонов электронами. Если фотон имеет относительно небольшое количество энергии, значение hc / λ для этого фотона относительно мало, и, следовательно, значение λ относительно велико. λ наблюдается как длина волны поглощения, и поэтому, если имеется сопряженная система, пики имеют тенденцию появляться в областях, где λ велика, то есть в длинноволновой области.
Как пи-орбитальное сопряжение влияет на длину волны пика?
В таблице приведены длины волн пиков и молярные коэффициенты поглощения различных органических соединений.Молярный коэффициент поглощения — это показатель того, насколько сильно вещество поглощает свет. Чем больше его значение, тем больше поглощение. В более крупных сопряженных системах длины волн пиков поглощения имеют тенденцию смещаться в сторону длинноволновой области, а пики поглощения имеют тенденцию к увеличению.
Какая связь между абсорбционной спектроскопией и сигма-орбитальной связью?
На верхнем рисунке показана структура пищевых красителей New Coccine (Red No.102) и бриллиантовый синий FCF (синий № 1), а на нижнем рисунке показаны их спектры поглощения. Пищевые красители, как правило, имеют большие сопряженные системы, подобные тем, которые показаны на рисунке, и поэтому их пиковые длины волн имеют тенденцию смещаться в длинноволновую область, а пики появляются в видимой области (от 400 до 700 нм). Поэтому они признаны цветами. Между прочим, цвет, который мы видим, — это цвет, который не поглощается веществом (который называется «дополнительным цветом»). Как показано на рисунке, New Coccine поглощает синий и зеленый свет в диапазоне от 450 до 550 нм, поэтому человеческий глаз видит дополнительный красный цвет.Brilliant Blue FCF поглощает желтый свет в диапазоне от 560 до 650 нм, поэтому синий виден человеческим глазом.
Какое влияние оказывают функциональные группы?
На пики поглощения также влияют функциональные группы. На верхнем рисунке показаны спектры поглощения бензола, фенола, который состоит из гидроксильной группы, связанной с бензольным кольцом, и п-нитрофенола, который состоит из гидроксильной группы и нитрогруппы, связанной с бензольным кольцом.Функциональные группы влияют на сопряженные системы, вызывая появление пиков поглощения на более длинных волнах, чем длина волны пика бензола, хотя они не выходят за пределы 400 нм и попадают в видимую область. Таким образом, на цвет органических соединений сильнее влияет размер конъюгированной системы.
Имеет ли значение размер молекулы, если это не пи-электроны?
На рисунках показаны спектры поглощения преднизолона, который используется в качестве фармацевтического средства, и бензола.Хотя преднизолон имеет большой молекулярный каркас, его сопряженная система мала, поэтому длины волн его пиков не сильно смещены в длинноволновую область, а его пики появляются примерно в том же положении, что и пики бензола.
Электронная теория химии в ближней инфракрасной области (БИК)?
Как видно из рисунка вверху, как средняя, так и ближняя инфракрасная области спектра имеют более длинные волны (более низкую энергию), чем УФ / видимый свет.Эта энергия настолько ниже, что от нее не возникает промотирования электронов. Но пока электроны не продвигаются, химические связи могут быть затронуты.
Энергетическая диаграмма выше показывает довольно большую разницу в энергии между связывающими электронными переходами по сравнению с деформирующими связь колебательными и вращательными уровнями энергии, вызванными средними инфракрасными частотами. Таким образом, инфракрасная спектроскопия дает информацию о том, какие атомы связаны с другими атомами в молекуле. Это очень полезно для идентификации и описания материалов.
Какие типы химии может измерять спектрофотометр в ближней инфракрасной области (NIR)?
Ближний инфракрасный диапазон спектра является не чем иным, как «обертонным зеркалом» среднего инфракрасного диапазона. Ближний инфракрасный диапазон содержит ту же информацию, что и средний инфракрасный диапазон. Так зачем использовать регион NIR, если там нет новой информации? Обертоны обычно гораздо менее интенсивны по амплитуде, чем их первичные аналоги.Это еще один способ сказать, что их коэффициент экстинкции (молярная поглощающая способность) меньше. Таким образом, согласно закону Бера, это означает, что длина пути, используемого для ближней ИК-спектроскопии, может быть больше. Типичная длина пути MIR составляет порядка микрон, тогда как длина пути для NIR-спектроскопии находится в диапазоне миллиметров. Эта более длинная длина пути может быть полезна в определенных режимах определения характеристик материалов.
Интересным фактом БИК-спектроскопии является ее большая чувствительность к небольшим количествам воды или вообще к любой группе -ОН.Как видно из спектра справа, группа -ОН имеет три полосы в ближнем ИК-диапазоне около 1450 нм, 1900 нм и 2600 нм. Это может создать проблему для любого образца со значительным компонентом группы -ОН.
Руководство пользователя базы данных
UV / Vis
В. Талроуз, А. Ермаков, А. Лескин,
А.А. Усов, А.А. Гончарова, Н.А. Мессинева, Н.В. Усова,
М.В. Ефимкина, Е.В. Аристова
Институт Энергетических Проблем Химической
Физика РАН
Источники данных
Подавляющее большинство спектров взяты из оригинальных
научные статьи с точными ссылками.Некоторые данные
взяты из нескольких опубликованных сборников. Эти коллекции включают:
- «Атлас спектров ароматических и гетроциклических соединений.
соединения », Коптюг В.А. (редактор), Наука , Сибирский
Отделение АН СССР, Новосибирск, т. 28-35 (1984-1986). - «Спектры поглощения в видимой области», Ланг,
Л. (редактор) тома 1-20, Будапешт, 1959-1975. - «УФ-атлас органических соединений», опубликованный в
сотрудничество с группой фотоэлектрической спектрометрии, Лондон, и
Институт Spectrochemie un Angewandte Sspectroskopie,
Дортмунд, тома 1-5, Лондон, Баттервортс и Вайнхайм, Chemie,
1966–1971. - «Ультрафиолетовые спектры поглощения ароматических
углеводороды », Кусов М.М., Шиманко Н.А., Шишкина М.В.
АН СССР, Москва. - «Ультрафиолетовые спектры поглощения гетероорганических
соединения », Большаков Г.В., Ватаго В.С., Агрест Ф.
Химия , Ленинградское отделение, Ленинград, 1969.
Данные из «Ультрафиолетовых спектров ароматических
соединений », Friedel, R.A., and Milton, M.O., U.S. Bureau of
Майнс, Брюсетон, Пенсильвания, Джон Уайли и сыновья, Нью-Йорк, 1951.60 из 600
вещества в публикации были исследованы, и было обнаружено, что они
отличается от спектров в более поздней литературе и имеет более узкую
расхождение по длине волны.
Обработка данных
- УФ / видимый свет
собранные спектры снимаются в основном в жидкой фазе (это
отражает характер литературы спектры абстрагированы
из). Следовательно, включены данные об использованном растворителе. В
некоторые редкие случаи, когда опубликованные данные были получены в газе или
паровые фазы именно такие спектры и вошли в сборник. - В литературе по спектрам УФ / видимой
сокращенная форма с упоминанием только поглощения для некоторого графика спектров
особенности (пары логарифма ε и длины волны). Данные
используются только в том случае, если источник содержит спектр в форме графика или (a
очень редкий случай) подробная цифровая форма. - Для осей X и Y, нм и логарифма ε (логарифм
является основанием 10), как правило, используются в недавних
литература для представления УФ-спектров. Любые другие единицы были
пересчитано в соответствии с этим соглашением.Если данные о впитывающей способности в
литературный источник не может быть представлен в количественной форме,
источник был опущен. - Используемый спектрометр описан в строгом соответствии с
оригинальная бумага. Эффективное спектральное разрешение, заявленное для
измерения обрабатываются аналогично.
Вспомогательные данные
- УФ ID
- Регистрационный номер в сборе данных UV / Vis.
- ТОЧКА ПЛАВЛЕНИЯ
- Данные шкалы Цельсия, обновленные с учетом информации из CRC Hanbdbook of
Химия и физика, Дэвид Р.Лиде (главный редактор),
78 th edition 1997-1998, CRC Press, Boca Raton, FL. - ТОЧКА КИПЕНИЯ
- То же, что и данные по температуре плавления. Сокращения «подп.»
и «дек.» означают сублимацию и разложение. - СОВЛЕНТ / ФАЗА
- Как указано в первоисточнике. Когда указывается только pH,
означает, что растворитель — вода. Аббревиатура «н.у.г.»
означает, что в первоисточнике нет данных о растворителе. - ПРИБОР
- Как указано в первоисточнике.Сокращение
«н.и.г.» означает, что данные о приборе не указаны в
первоисточник.
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie.Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.
Чтобы принять файлы cookie с этого сайта, используйте кнопку «Назад» и примите файлы cookie. - Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г.,
браузер автоматически забудет файл cookie.Чтобы исправить это, установите правильное время и дату на своем компьютере. - Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.
Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie
потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.


