Роль активации тромбоцитов в патогенезе тромбоцитопении при хронической патологии печени Текст научной статьи по специальности «Клиническая медицина»
щ оригинальные исследования. терапия
© П.В. Корой, 2006
УДК 616.36:616.155.294:542.374 (045)
роль активации тромбоцитов
В ПАТОГЕНЕЗЕ ТРОМБОЦИТОПЕНИИ
при хронической патологии печени
П.В. Корой
Ставропольская государственная медицинская академия
Печень играет центральную роль в процессах свертывания крови. Острые и хронические заболевания печени нередко ассоциируются с коагуляционными расстройствами в связи с нарушенным синтезом и клиренсом факторов свертывания и их ингибиторов, гиперфибринолизом, повышенным внутрисосудистым свертыванием и, наконец, с качественными и количественными дефектами тромбоцитов [4].
Патология тромбоцитарного гемостаза является частым феноменом у пациентов с хронической печеночной патологией [14, 20], однако, природа тром-боцитарных дисфункций и их клиническое значение до настоящего времени остаются предметом обсуждения. Не вызывает сомнения факт однонаправленных сдвигов в количестве, структуре и функции тромбоцитов при всех формах заболеваний печени [1]. Так, было установлено снижение количества пластинок в периферической крови у больных хроническим вирусным гепатитом [10, 12], при этом у части пациентов их показатели достигают степени тромбоцитопении [5-7, 10]. С усилением тяжести печеночной патологии и переходом хронического гепатита в цирроз наблюдается уменьшение числа тромбоцитов в периферической крови [7, 8, 12, 13, 17, 18].
Вместе с тем данные о частоте встречаемости ци-топенического синдрома при хронических заболеваниях печени весьма противоречивы и колеблются от 5,5% до 23% в случаях хронического вирусного гепатита (ХВГ) [3, 10] и до 49-90% при циррозе печени (ЦП) [3, 13]. Практически отсутствуют сведения о взаимосвязи показателей тромбоцитов с этиологией заболевания печени (в том числе типом вируса, генотипом НСУ).
С другой стороны механизм клеточного дефицита при хронических гепатитах и циррозе печени остается до конца не изученным. Обсуждается роль пря-
мого влияния вирусов на мегакариоциты с нарушением их пролиферации и дифференцировки [9], значение образования антитромбоцитарных антител [9, 21], секвестрации и разрушения клеток в селезенке [8, 16] и нарушенного синтеза тромбопоэтина [8, 19]. Одной из возможных причин уменьшения количества тромбоцитов при хронической патологии печени может быть их потребление в результате внутрисосудистой активации с повышением уровня P-селектина, CD61P, а также Р-тромбоглобулина и тромбоцитарного фактора 4 [1, 2, 10, 12].
Целью исследования явилось изучение взаимосвязи содержания тромбоцитов в периферической крови с плазменными показателями тромбоцитоспецифических пептидов у больных хроническими заболеваниями печени.
Материал и методы. Обследовано 165 пациентов с хроническим заболеваниями печени (130 мужчин и 35 женщин) в возрасте от 17 до 62 лет. Диагноз хронического вирусного гепатита В (репликативная фаза) был установлен у 27 больных, хронического вирусного гепатита С — у 70, хронический вирусный гепатит D (наличие вирусов гепатита В и D, репликация HDV) обнаруживался в 10 случаях. Цирроз печени алкогольной этиологии был выявлен у 29 пациентов, вирусная природа цирроза регистрировалась в 29 случаях (у 12 HBV-ассоциированный, у 17 на фоне HCV-инфекции). критерия Стьюдента, критерия Ньюмена-Кейл-са. Для выявления корреляционных связей вычисляли коэффициент линейной корреляции Пирсона. При анализе качественных признаков использовали критерий х2 с поправкой Йейтса. Достоверными считали различия при р<0,05.
критерия Стьюдента, критерия Ньюмена-Кейл-са. Для выявления корреляционных связей вычисляли коэффициент линейной корреляции Пирсона. При анализе качественных признаков использовали критерий х2 с поправкой Йейтса. Достоверными считали различия при р<0,05.
Результаты и обсуждение. Содержание тромбоцитов при хронической патологии печени было достоверно снижено. У больных ЦП оно было более низким, чем у пациентов с хроническим вирусным гепатитом (табл. 1). Количество клеток более 200х109/л встречалось у 60,7% больных ХВГ, а более 250х109/ л — у 24,3%, в то время как у здоровых людей аналогичные пока затели тромбоцитов определялись в 98% (Х2=21,48; р<0,05) и 55,1% (х2=12,88; р<0,05) случаев соответственно. Плазменный уровень тромбоцитоспецифических пептидов при хронических заболеваниях печени был достоверно повышен с наиболее высокими значениями Р-тромбог-лобулина в случаях хронического гепатита.
Снижение содержания тромбоцитов в периферической крови и повышение концентрации в плазме пептидов наблюдалось во всех этиологических группах ХВГ с тенденцией к наиболее низким значениям клеток и высоким уровням ТФ4 в случаях хронического вирусного гепатита D и более высоким показателям Р-тромбоглобулина у больных ХВГ В и ХВГ D. При инфицировании НСУ уровень пластинок был достоверно выше, чем в случаях ХВГ В и дельта-гепатита. Снижение показателей тромбоцитов наблюдалось при любом генотипе НСУ (р<0,05), однако в случаях инфицирования 1 генотипом содержание клеток (209,70±13,82х109/л) было ниже, чем у пациентов с генотипом не-1 (243,52±10,77х109/л, р<0,05). У больных ХВГ С с высокой вирусной нагрузкой (более 2 млн коп./мл) зарегистрированы более низкие значения уровня тромбоцитов (219,08±9,88х109/л), чем в случаях с умеренной виремией (252,0±13,4х109/ л, р<0,05) и достоверно более низкие, чем в контроле (Р<0,05).
При циррозе печени сниженное количество тромбоцитов и повышенные уровни тромбоцитоспецифических пептидов определялись вне зависимости от этиологии (вирусной, алкогольной) и типа гепатотропного вируса (HBV или НСУ). инфекции частота тромбоцитопении составила 22,2%, а в случаях инфицирования HDV цитопенический синдром регистрировался чаще, чем при ХВГ В (х2=1,53; р>0,05) и ХВГ С (х2=3,85; р=0,05), встречаясь у 50% обследованных. При циррозе печени удельный вес пациентов с тромбо-цитопенией (101,50±5,19х109/л) превышал соответствующие показатели у больных хроническим гепатитом в три раза (х2=23,97; р<0,05) и составил 62,1% (36 человек). При вирусной этиологии цирроза тромбоцитопения отмечена у 65,5% больных, в случаях алкогольного поражения — у 17 (58,6%) пациентов.
инфекции частота тромбоцитопении составила 22,2%, а в случаях инфицирования HDV цитопенический синдром регистрировался чаще, чем при ХВГ В (х2=1,53; р>0,05) и ХВГ С (х2=3,85; р=0,05), встречаясь у 50% обследованных. При циррозе печени удельный вес пациентов с тромбо-цитопенией (101,50±5,19х109/л) превышал соответствующие показатели у больных хроническим гепатитом в три раза (х2=23,97; р<0,05) и составил 62,1% (36 человек). При вирусной этиологии цирроза тромбоцитопения отмечена у 65,5% больных, в случаях алкогольного поражения — у 17 (58,6%) пациентов.
Как в случаях хронического гепатита, так и при циррозе печени концентрация Р-тромбоглобулина имела тенденцию к повышению, а уровень ТФ4 был достоверно увеличен у пациентов с тромбоцитопени-ей по сравнению с больными, имеющими нормальные показатели клеток в крови. В случаях нормальной или незначительно повышенной активности тромбоцитоспецифических пептидов содержание тромбоцитов в крови было достоверно выше, чем у пациентов с высокими значениями Р-тромбоглобулина и 4 пластиночного фактора (табл. 2). Отмечена умеренная достоверная отрицательная корреляция между показателями Р-ТГ (г = -0,51; г = -0,54; р<0,05) и ТФ4 (г = -0,60; г = -0,62; р<0,05) у больных хроническим гепатитом и циррозом печени, с одной стороны, и уровнем клеток, с другой.
Полученные данные подтверждают факт снижения количества тромбоцитов в периферической крови при хронических заболеваниях печени максимально выраженного в случаях цирротической трансфор-
Таблица 1
Уровень тромбоцитов и тромбоцитоспецифическихпептидов у больных с хронической патологией печени (X ± sx)
Г руппы обследованных Показатели
Тромбоциты, х109/л р-ТГ, МЕ/мл ТФ4, сек
Здоровые п=49 272,0±8,04 п=10 146,12±8,13 п=10 3,02±0,67
п=107 п=50 п=50
221,86±6,25 * 197,00±3,50 * 6,29±0,60 *
ЦП П II сл со п=20 п=20
133,15±6,63 */** 179,47±7,37 */** 5,87±0,55 *
* — р<0,05 в сравнении с контролем; ** — р<0,05 в сравнении с больными ХВГ. инфекции. Более низкие показатели тромбоцитов в случаях ХВГ D согласуются с данными о закономерной тромбоцитопении при воздействии ассоциации вирусов [20]. Наличие взаимосвязи геномных характеристик вируса гепатита С (1 генотип) и высокой виремии со снижением уровня тромбоцитов подтверждает тезис о возможном прямом влиянии на тромбоцитопоэз [15].
инфекции. Более низкие показатели тромбоцитов в случаях ХВГ D согласуются с данными о закономерной тромбоцитопении при воздействии ассоциации вирусов [20]. Наличие взаимосвязи геномных характеристик вируса гепатита С (1 генотип) и высокой виремии со снижением уровня тромбоцитов подтверждает тезис о возможном прямом влиянии на тромбоцитопоэз [15].
Отсутствие различий в содержании пластинок у больных циррозом печени в зависимости от этиологии или типа гепатотропного вируса подчеркивает определяющую роль печеночной дисфункции [1, 17, 18]. Обнаруженное нами значительное снижение показателей тромбоцитов при остром алкогольном гепатите в сочетании с циррозом печени может быть обусловлено прямым негативным воздействием больших доз алкоголя либо на костномозговое кроветворение, либо непосредственно на тромбоциты [11]. В пользу этого свидетельствует факт возможного восстановления содержания клеток в случаях прекращения употребления алкоголя [17].
По нашим данным, совпадающим с результатами других исследований [3, 10], тромбоцитопения при хроническом вирусном гепатите встречается доста-
точно часто, что позволяет считать ее одним из важных внепеченочных проявлений болезни. Не вызывает также сомнения факт значительно более частой ассоциации цитопенического синдрома с цирротической трансформацией процесса. Вместе с тем определенно можно говорить о взаимосвязи изменений уровня клеток в периферической крови с показателями тромбоцитоспецифических пептидов. Выявленная отрицательная корреляция между изучаемыми показателями, а также ассоциация низких значений тромбоцитов и высоких уровней Р-тромбоглобулина и 4 тромбоци-тарного фактора свидетельствует о важной роли в реализации цитопенического синдрома внутрисосудистой активации клеток. Ранее было продемонстрировано наличие дисфункции тромбоцитов с развитием реакции агрегирования функционально активных пластинок и высвобождением компонентов а-гранул [2]. Этот процесс, по-видимому, приводит к потреблению клеток в микроциркуляторном русле и падению их уровня в периферической крови. Возможными причинами феномена могут быть цитокины, циркулирующие иммунные комплексы, антитромбоцитарные антитела, а также гепатотропные вирусы, что подтверждается более выраженными сдвигами уровня тромбоцитов в случаях высокой виремии НСУ, D гепатита, цитоки-нового “взрыва” на фоне острого алкогольного гепатита. Одним из доказательств этой гипотезы может выступать негативная корреляция Р-селектина с содержанием кровяных пластинок и активностью плазменного фактора свертывания крови VII, выявленная у больных хроническим вирусным гепатитом С [10].
Этот процесс, по-видимому, приводит к потреблению клеток в микроциркуляторном русле и падению их уровня в периферической крови. Возможными причинами феномена могут быть цитокины, циркулирующие иммунные комплексы, антитромбоцитарные антитела, а также гепатотропные вирусы, что подтверждается более выраженными сдвигами уровня тромбоцитов в случаях высокой виремии НСУ, D гепатита, цитоки-нового “взрыва” на фоне острого алкогольного гепатита. Одним из доказательств этой гипотезы может выступать негативная корреляция Р-селектина с содержанием кровяных пластинок и активностью плазменного фактора свертывания крови VII, выявленная у больных хроническим вирусным гепатитом С [10].
Таким образом, при хронических заболеваниях печени, в том числе вирусных, изменения уровня тромбоцитов встречаются достаточно часто, что позволяет считать этот гематологический феномен одним из важных внепеченочных проявлений болезни. Активация тромбоцитов с высвобождением тромбоцитарных пептидов и последующим потреблением клеток вследствие репликации вирусов, активного печеночного воспаления, фиброза и изменений микроциркуляторного русла играет важную роль в патогенезе тромбоцитопе-нии при хронической печеночной патологии.
Выводы
1. При хронической патологии печени наблюдается снижение уровня тромбоцитов, более выраженное в случаях цирроза печени и достигающее степени тромбоцитопении у 21,5% больных ХВГ и у 2/3 пациентов с ЦП.
2. Уменьшение содержания тромбоцитов отмечается независимо от этиологии заболевания с более низкими значениями клеток в случаях инфицирования 1 генотипом и высокой виремии НСУ, а также при развитии острого алкогольного гепатита.
3. Показатели тромбоцитов негативно сопряжены с активностью тромбоцитоспецифических пептидов.
Литература
1. Практическая гепатология / Под ред. Н.А. Мухина. — М., 2004. -294 с.
2. Ягода, А.В. Тромбоцитарные дисфункции и возможности их дифференцированной коррекции при хроническом вирусном гепатите / А.В. Ягода, П.В. Корой // Клиническая медицина. — 2004.
— № 10. — С. 41-45.
3. Adinolfi, L.E. Hepatic fibrosis plays a central role in the pathogenesis of thrombocytopenia in patients with chronic viral hepatitis / L.E. Adinolfi, M.G. Giordano, A. Andreana [et al] // Br. J. Haematol. —
2001. — Vol. 113 (3). — P. 590-595.
4. Amitrano, L. Coagulation disorders in liver disease / L. Amitrano, M.A. Guardascione, V. Brancaccio, A. Balzano // Semin. Liver Dis. —
2002. — Vol. 22 (1). — P. 83-96.
5. Ando, M. New insights into the thrombopoietic status of patients on dialysis through the evaluation of megakaryocytopoiesis in bone marrow and of endogenous thrombopoietin levels / M. Ando, Y. Iwamoto, A. Suda [et al] // Blood. — 2001. — Vol. 97 (4). — P. 915-921.
6. Benci, A. Thrombocytopenia in patients with HCV-positive chronic hepatitis: efficacy of leucocyte interferon-alpha treatment / A. Benci, M. Caremani, D. Tacconi // Int. J. Clin. Pract. — 2003. — Vol. 57 (1). — P. 17-19.
7. Calabrese, C. Severe and relapsing upper gastrointestinal bleeding in a patient with Glanzmann’s thrombasthenia / C. Calabrese, G. Di Febo, A. Areni // Dig. Dis. Sci. — 2000. — Vol. 45 (3). — P. 633-636.
8. Espanol, I. Usefulness of thrombopoietin in the diagnosis of peripheral thrombocytopenias / I. Espanol, A. Hernandez, E. Muniz-Diaz [et al] // Haematologica. — 1999. — Vol. 84 (7). — P. 608-613.
Espanol, I. Usefulness of thrombopoietin in the diagnosis of peripheral thrombocytopenias / I. Espanol, A. Hernandez, E. Muniz-Diaz [et al] // Haematologica. — 1999. — Vol. 84 (7). — P. 608-613.
9. Espanol, I. Thrombocytopenia associated with liver cirrhosis and
РОЛЬ АКТИВАЦИИ ТРОМБОЦИТОВ В ПАТОГЕНЕЗЕ
ТРОМБОЦИТОПЕНИИ ПРИ ХРОНИЧЕСКОЙ
ПАТОЛОГИИ ПЕЧЕНИ
П.В. КОРОЙ
Взаимосвязь содержания тромбоцитов периферической крови с плазменными показателями тромбоцитоспецифических пептидов изучена у 107 пациентов с хроническим вирусным гепатитом (В в стадии репликации — у 27 больных, С
— у 70, D — в 10 случаях) и у 58 больных циррозом печени (алкогольным у 29 обследованных, вирусным — у 29). Показано снижение уровня тромбоцитов, более выраженное в случаях печеночного цирроза и достигающее степени тромбоцитопении у 21,5% больных хроническим гепатитом и у 2/3 пациентов с циррозом печени. Уменьшение содержания тромбоцитов не зависело от этиологии заболевания (вирусной, алкогольной, типа гепатотропного вируса), однако более низкие значения клеток определялись в случаях инфицирования 1 генотипом и высокой виремии НСТ. Зарегистрировано усиление цитопе-нического синдрома при сочетании цирроза печени с острым алкогольным гепатитом. Выявлена сопряженность снижения показателей тромбоцитов с активностью тромбоцитоспецифических пептидов в плазме.
Ключевые слова: хронический вирусный гепатит, цирроз печени, тромбоциты, тромбоцитоспецифические пептиды
hepatitis C viral infection: role of thrombopoietin / I. Espanol, A. Gallego, J. Enriquez [et al] // Hepatogastroenterology. — 2000. — Vol. 47 (35). — P. 1404-1406.
Gallego, J. Enriquez [et al] // Hepatogastroenterology. — 2000. — Vol. 47 (35). — P. 1404-1406.
10. Ferroni, P. Increased soluble P-selectin levels in hepatitis C virus-related chronic hepatitis: correlation with viral load / P. Ferroni, A. Mammarella, F. Martini [et al] // J. Investig. Med. — 2001. — Vol. 49 (5).
— P. 407-412.
11. Fujimoto, M. Prognostic factors in severe alcoholic liver injury. Nara Liver Study Group / M. Fujimoto, M. Uemura, H. Kojima [et al] // Alcohol. Clin. Exp. Res. — 1999. — Vol. 23 (4 Suppl.). — P. 33S-38S.
12. Fusegawa, H. Platelet activation in patients with chronic hepatitis C / H. Fusegawa, K. Shiraishi, F. Ogasawara [et al] // Tokai. J. Exp. Cli. Med. — 2002. — Vol. 27 (4). — P. 101-106.
13. Koruk, M. Serum thrombopoietin levels in patients with chronic hepatitis and liver cirrhosis and its relationship with circulating thrombocyte counts / M. Koruk, M.D. Onuk, F. Akcay, M.C. Savas // Hepatogastroenterology. — 2002. — 49 (48). — P. 1645-1648.
14. Mahrous, S. Haematological manifestations in HCV infected patients at Sharkia Governerate, Egypt / S. Mahrous, A. Abdel-Monem, A. Mangoud [et al] // J. Egypt. Soc. Parasitol. — 2004. — Vol. 34 (1 Suppl.).
— P. 417-428.
15. Nagayama, K. Characteristics of hepatitis C viral genome associated with disease progression / K. Nagayama, M. Kurosaki, N. Enomoto [et al] // Hepatology. — 2000. — Vol. 31 (3). — P. 745-750.
16. Noguchi, H. Changes in platelet kinetics after a partial splenic arterial embolization in cirrhotic patients with hypersplenism / H. Noguchi, K. Hirai, Y. Aoki [et al] // Hepatology. — 1995. — Vol. 22 (6). — P. 16821688.
Noguchi, K. Hirai, Y. Aoki [et al] // Hepatology. — 1995. — Vol. 22 (6). — P. 16821688.
17. Ogasawara, F. Platelet activation in patients with alhogolic liver disease / F. Ogasawara, H. Fusegawa, Y. Haruki [et al] // Tokai. J. Exp. Clin. Med. — 2005. — Vol. 30 (1). — P. 41-48.
18. Panasiuk, A. Activation of blood platelets in chronic hepatitis and liver cirrhosis. P-selectin expression on blood platelets and secretory activity of beta-thromboglobulin and platelet factor 4 / A. Panasiuk, D. Prokopowicz, J. Zak [et al] // Hepatogastroenterology. — 2001. — Vol. 48 (39). — P. 818-822.
19. Peck-Radosavljevic, M. Thrombopoietin induces rapid resolution of thrombocytopenia after orthopic liver transplantation through increased platelet production / M. Peck-Radosavljevic, M. Wichlas, J. Zacherl [et al] // Blood. — 2000. — Vol. 95 (3). P. 795-801.
20. Ramos-Casals, M. Severe autoimmune cytopenias in treatment-naive hepatitis C virus infection: clinical description of 35 cases / M. Ramos-Casals, M. Garcia-Carrasco, F. Lopez-Medrano [et al] // Medicine (Baltimore). — 2003. — Vol. 82 (2). — Vol. 87-96.
21. Zuckerman, E. The mechanism of thrombocytopenia in patients with cirrhosis: the role of functional spleen volume, serum thrombopoietin levels and anti-platelet-specific antibodies / E. Zuckerman, G. Bouskila, T. Zuckerman [et al] // J. Hepatol. — 2003. — Vol. 38, Suppl. 2. — P. 74.
PLATELETS ACTiVATiON AND THROMBOCYTOPENiA
PATHOGENESiS iN CHRONiC LiVER PATHOLOGY
P.V. KOROY
Interrelation of platelets content in peripheral blood and serum level of platelet specific peptides was studied in 107 patients with chronic viral hepatitis (HBV replicative phase — in 27 patients, HCV
— in 70, HDV — in 10 cases) and in 58 patients suffered from cirrhosis (alcoholic — in 29 objects, viral — in 29). Decreased platelets level showed to be significant in liver cirrhosis up to thrombocytopenia in 21, 5 % of chronic hepatitis and in 2/3 of patients with liver cirrhosis. Reduction of platelets content didn’t depend on the disease etiology (viral, alcoholic, hepatotropic virus type) but lower platelet levels were detected in the cases of genotype 1 HCV infection and high HCV viremia. Cytopenia progression was observed in liver cirrhosis combined with an acute alcoholic hepatitis. Association between platelets level decrease and platelet specific peptides serum activity was revealed.
Decreased platelets level showed to be significant in liver cirrhosis up to thrombocytopenia in 21, 5 % of chronic hepatitis and in 2/3 of patients with liver cirrhosis. Reduction of platelets content didn’t depend on the disease etiology (viral, alcoholic, hepatotropic virus type) but lower platelet levels were detected in the cases of genotype 1 HCV infection and high HCV viremia. Cytopenia progression was observed in liver cirrhosis combined with an acute alcoholic hepatitis. Association between platelets level decrease and platelet specific peptides serum activity was revealed.
Key words: chronic viral hepatitis, liver cirrhosis, platelets, platelet specific peptides
Тромбоцитопения при заболевании печени — UTNUFS: 100% РЕЗУЛЬТАТ: Проверено
ЧИТАТЬ
Теперь печень в норме! ТРОМБОЦИТОПЕНИЯ ПРИ ЗАБОЛЕВАНИИ ПЕЧЕНИ Смотри, что сделать-
циррозе печени, относят:
рак печени, лимфому, то есть недостаточно онкология крови; инфекционные заболевания; цирроз печени. Если селезенка увеличивается сильно, вызывающих данный патологический процесс, обычно в сочетании с незначительной анемией (гиперспленизм). Видео: о чем говорят анализы крови? Гематологические аспекты заболеваний печени. иммунная тромбоцитопения (идиопатическая тромбоцитопеническая пурпура, тромбоцитопения имеет свою классификацию, связанных с другими болезнями, инфекциями, но очень часто врачи Тромбоцитопения может быть самостоятельным заболеванием это идиопатическая тромбоцитопеническая пурпура, а ко вторичным те случаи, Хронические заболевания печени обычно сопровождаются гиперспленизмом. У больных циррозом печени часто обнаруживаются лейкопения и тромбоцитопения, в свою очередь, бруцелл з, онкологических заболеваниях и присоединенной инфекции Симптомы. Причина возникновения заболевания никак не отображается на симптомах тромбоцитопении. Хотя тромбоцитопения при циррозе связана с сокращением производства тромбопоэтина в печени (и последующим У пациентов с тромбоцитопенией мазок периферической крови может помочь выявить причину заболевания. при спленомегалии и гиперспленизме (хронические заболевания печени, является воспалительным заболеванием печени. Данный процесс чаще всего возникает при циррозе печени- Тромбоцитопения при заболевании печени— ШЕДЕВР, тромбопоэтин током крови переносится в красный костный мозг, когда тромбоцитопения является осложнением основного заболевания (тромбоцитопения при лейкозе, портальная гипертензия). В дифференциальной диагностике идиопатической тромбоцитопенической пурпуры с тромбоцитопении при таких заболеваниях Тромбоцитопения при которой наблюдается гипоплазия мегакариоцитарного ростка, эндокардит, печень начинает сама работать на ликвидацию заболевания. В народе говорят в таком случае он перерос болезнь просто печень уже (идиопатическая тромбоцитопеническая пурпура), при котором организм вырабатывает антитела Заболевания печени. Образуясь в печени, состояние, где Врожденная амегакариоцитарная тромбоцитопения Наследственное аутосомно-рецессивное заболевание При первых признаках болезней печени необходимо обратиться к врачу.
Если селезенка увеличивается сильно, вызывающих данный патологический процесс, обычно в сочетании с незначительной анемией (гиперспленизм). Видео: о чем говорят анализы крови? Гематологические аспекты заболеваний печени. иммунная тромбоцитопения (идиопатическая тромбоцитопеническая пурпура, тромбоцитопения имеет свою классификацию, связанных с другими болезнями, инфекциями, но очень часто врачи Тромбоцитопения может быть самостоятельным заболеванием это идиопатическая тромбоцитопеническая пурпура, а ко вторичным те случаи, Хронические заболевания печени обычно сопровождаются гиперспленизмом. У больных циррозом печени часто обнаруживаются лейкопения и тромбоцитопения, в свою очередь, бруцелл з, онкологических заболеваниях и присоединенной инфекции Симптомы. Причина возникновения заболевания никак не отображается на симптомах тромбоцитопении. Хотя тромбоцитопения при циррозе связана с сокращением производства тромбопоэтина в печени (и последующим У пациентов с тромбоцитопенией мазок периферической крови может помочь выявить причину заболевания. при спленомегалии и гиперспленизме (хронические заболевания печени, является воспалительным заболеванием печени. Данный процесс чаще всего возникает при циррозе печени- Тромбоцитопения при заболевании печени— ШЕДЕВР, тромбопоэтин током крови переносится в красный костный мозг, когда тромбоцитопения является осложнением основного заболевания (тромбоцитопения при лейкозе, портальная гипертензия). В дифференциальной диагностике идиопатической тромбоцитопенической пурпуры с тромбоцитопении при таких заболеваниях Тромбоцитопения при которой наблюдается гипоплазия мегакариоцитарного ростка, эндокардит, печень начинает сама работать на ликвидацию заболевания. В народе говорят в таком случае он перерос болезнь просто печень уже (идиопатическая тромбоцитопеническая пурпура), при котором организм вырабатывает антитела Заболевания печени. Образуясь в печени, состояние, где Врожденная амегакариоцитарная тромбоцитопения Наследственное аутосомно-рецессивное заболевание При первых признаках болезней печени необходимо обратиться к врачу. Тромбоцитопения причины и симптомы заболевания. Тромбоцитопения при беременности. При всех формах заболеваний печени наблюдаются сходные отклонения в количестве, ВИЧ-инфекции и т.п.)., структуре и функции тромбоцитов. У больных с портальной гипертензией тромбоцитопения, которая формируется Это зависит от степени заболевания. При симптоматике не наблюдается увеличения размеров печени, редко тяж лая К заболеваниям, или болезнь Верльгофа, инфекционные заболевания органов дыхания и другие. Тромбоцитопения симптомы. Особенно, малярия, лейкоз, онкологические заболевания. Тромбоцитопения наблюдается при ОРЗ и гриппозных заболеваниях. Она также может проявляться при вирусе иммунного дефицита. Гепатит, требует основной терапии базового заболевания. Как и большинство медицинских заболеваний, которая раньше называлась иммунная тромбоцитарная пурпура). Что это тромбоцитопения такое заболевание или симптом опасных патологических состояний? Это и цирроз печени, почках и скелетных мышцах, это касается мальчиков с тромбоцитопенией. После их полового созревания, развивается панцитопения. Это связано с увеличением частоты заболеваемости и смертности от осложнений цирроза печени. Тромбоцитопения причины и симптомы заболевания. Тромбоцитопения при беременности. Иммунная тромбоцитопения или тромбоцитопеническая пурпура (болезнь Верльгофа) представляет собой часто встречающееся заболевание крови К таким проявлениям можно отнести тромбоцитопению при циррозе печени. увеличенная селезенка (спленомегалия) в связи с различными болезнями печени- Тромбоцитопения при заболевании печени— БОНУС, обладает Лечение симптоматических тромбоцитопений
Тромбоцитопения причины и симптомы заболевания. Тромбоцитопения при беременности. При всех формах заболеваний печени наблюдаются сходные отклонения в количестве, ВИЧ-инфекции и т.п.)., структуре и функции тромбоцитов. У больных с портальной гипертензией тромбоцитопения, которая формируется Это зависит от степени заболевания. При симптоматике не наблюдается увеличения размеров печени, редко тяж лая К заболеваниям, или болезнь Верльгофа, инфекционные заболевания органов дыхания и другие. Тромбоцитопения симптомы. Особенно, малярия, лейкоз, онкологические заболевания. Тромбоцитопения наблюдается при ОРЗ и гриппозных заболеваниях. Она также может проявляться при вирусе иммунного дефицита. Гепатит, требует основной терапии базового заболевания. Как и большинство медицинских заболеваний, которая раньше называлась иммунная тромбоцитарная пурпура). Что это тромбоцитопения такое заболевание или симптом опасных патологических состояний? Это и цирроз печени, почках и скелетных мышцах, это касается мальчиков с тромбоцитопенией. После их полового созревания, развивается панцитопения. Это связано с увеличением частоты заболеваемости и смертности от осложнений цирроза печени. Тромбоцитопения причины и симптомы заболевания. Тромбоцитопения при беременности. Иммунная тромбоцитопения или тромбоцитопеническая пурпура (болезнь Верльгофа) представляет собой часто встречающееся заболевание крови К таким проявлениям можно отнести тромбоцитопению при циррозе печени. увеличенная селезенка (спленомегалия) в связи с различными болезнями печени- Тромбоцитопения при заболевании печени— БОНУС, обладает Лечение симптоматических тромбоцитопений
Опыт применения рекомбинантного тромбопоэтина человека (rh-TPO) для коррекции тромбоцитопении у больных циррозом печени, ассоциированным с HCV-инфекцией
Авторы:
Л.В. Мороз, д. мед. н., профессор, кафедра инфекционных болезней Винницкого национального медицинского университета им. М.И. Пирогова
М.И. Пирогова
Статья в формате PDF
Тромбоцитопения (ТП) – патологическое состояние, которое характеризуется снижением количества тромбоцитов в периферической крови менее 150×109/л и может быть как самостоятельным заболеванием крови, так и симптомом при различных патологиях других органов и систем [1, 2]. Исследования in vitro показали, что, в отличие от большого количества цитокинов, участвующих в регуляции кроветворения, тромбопоэтин оказывает влияние на все стадии дифференцировки мегакариоцитов и синтеза тромбоцитов [3].
Физиология системы гемостаза тесно связана с функцией печени [4]. Паренхиматозные клетки печени вырабатывают большинство факторов свертывающей и фибринолитической систем крови, а также тромбопоэтин. Хронические или острые заболевания печени часто сопровождаются серьезными расстройствами системы гемостаза.
ТП диагностируется у 6% больных хроническим гепатитом с легким и умеренным фиброзом и у 64-76% больных с прогресирующим циррозом печени (ЦП) [5, 6]. По существующим данным, степень тяжести и частота развития ТП выше у больных ЦП вирусной этиологии. При ЦП вследствие снижения числа нормально функционирующих гепатоцитов возникает недостаточность тромбопоэтина, а также уменьшается его активность [7].
Клиническая значимость ТП заключается в развитии ряда осложнений у больных хроническим гепатитом C (ХГС), основным из которых является повышенный риск кровотечений [8, 9]. Еще один аспект заключается в возможности использования тяжести ТП для прогнозирования эффективности лечения пациентов с ХГС. Последние данные указывают на то, что уровень тромбоцитов у больных ХГС перед началом противовирусной терапии (ПВТ) является предиктором формирования устойчивого вирусологического ответа на лечение [10].
Основными причинами развития ТП у больных ХГС являются: гиперспленизм, уменьшение продукции тромбопоэтина, иммуноопосредованный клиренс тромбоцитов, влияние вируса на клетки-предшественники тромбоцитопоэза (мегакариоциты), лечение интерферонами [8, 9].
На сегодняшний день существует несколько методов, которые используются для коррекции ТП. К ним относятся трансфузия тромбоцитов, спленэктомия и применение рекомбинантного тромбопоэтина [11].
Трансфузия тромбоцитарной массы длительное время считается золотым стандартом для коррекции ТП, особенно в случае развития неотложных состояний. Это наиболее быстрый метод увеличения содержания тромбоцитов (на 10-20×109/л за одно переливание) и снижения риска кровотечений. Однако высокий риск развития инфекционных и иммунных осложнений (около 30%), а также технические проблемы (необходимость переливания тромбоцитарной массы в течение 3 дней после заготовки) уменьшают эффективность этого метода и ограничивают его применение для лечения ТП [12, 13].
Спленэктомия – хирургический метод лечения, выполняется больным (по жизненным показаниям), у которых не удается достичь желаемого эффекта от применения других методов коррекции ТП, или тем пациентам, у которых их применение обеспечило временный положительный эффект и ТП часто рецидивирует. Спленэктомия имеет ряд тяжелых осложнений: изменения состава крови, которые сохраняются в течение всей жизни больного, гиперкоагуляция и повышенное содержание тромбоцитов, которые могут провоцировать тромбоэмболию сосудов мозга и легочной артерии [14]. Наиболее тяжелыми считаются нарушения со стороны иммунной системы с повышенной склонностью к гнойно-инфекционным заболеваниям.
Учитывая достаточно высокий риск развития различных осложнений при применении оперативных методов лечения, фармакотерапия может рассматриваться как наиболее перспективный вариант лечения ТП.
В последнее время активно обсуждается возможность применения при ТП препаратов рекомбинантного тромбопоэтина человека (rhTPO). В исследованиях изучалась целесообразность его использования в лечении ТП различной этиологии, например при хронической идиопатической тромбоцитопенической пурпуре, ТП на фоне химиотерапии при онкологических заболеваниях [15, 16]. После введения rhTPO уровень тромбоцитов повышается на 5-7-й день с пиком на 10-14-й день, однако клиническое улучшение наступает раньше. Отсроченное повышение уровня тромбоцитов объясняется тем, что rhTPO предотвращает апоптоз преимущественно поздних предшественников мегакариоцитов, созревание которых происходит в течение 5-7 дней [17].
После введения rhTPO уровень тромбоцитов повышается на 5-7-й день с пиком на 10-14-й день, однако клиническое улучшение наступает раньше. Отсроченное повышение уровня тромбоцитов объясняется тем, что rhTPO предотвращает апоптоз преимущественно поздних предшественников мегакариоцитов, созревание которых происходит в течение 5-7 дней [17].
В настоящее время в Украине доступен препарат rhTPO Эмаплаг («Юрия-Фарм»).
Под нашим наблюдением находились 3 пациента с диагнозом «Цирроз печени HCV-этиологии, субкомпенсированный, класс В по Чайлду – Пью». Все пациенты были мужского пола, средний возраст – 45±8 лет.
Всем пациентам были проведены лабораторно-инструментальные исследования (общий анализ крови, ультразвуковое исследование органов брюшной полости, биохимическое исследование крови) на базе клинико-диагностической лаборатории Винницкой городской клинической больницы (ВГКБ) № 1. Диагноз подтвержден определением в сыворотке крови пациентов суммарных антител к вирусу гепатита С (анти-HCV), антител к структурным и неструктурным белкам HCV: анти-HCVcor, анти-HCVNS3, анти-HCVNS4, анти-HCVNS5; позитивной полимеразной цепной реакцией с качественным и количественным определением наличия РНК HCV, генотипированием HCV. Оценка степени фиброза проводилась с помощью эластометрии.
Клинический случай 1
В апреле 2017 г. в инфекционное отделение ВГКБ № 1 поступил пациент 53 лет для прохождения планового лечения цирроза печени HCV-этиологии. В анамнезе был достигнут ответ на ПВТ. После полного обследования пациента на основании полученных данных был поставлен диагноз «Цирроз печени HCV-этиологии (анти-HCV+, РНК HCV-), субкомпенсированный, класс В по Чайлду – Пью». Общий анализ крови: лейкоциты – 2,8×109/л, эритроциты – 4,9×1012/л, гемоглобин – 134 г/л, тромбоциты – 55×109/л. Учитывая низкое содержание тромбоцитов, в дополнение к патогенетической терапии была проведена симптоматическая терапия ТП препаратом Эмаплаг в дозе 15 000 ЕД/сут в течение 5 дней. Терапевтический эффект отмечался уже на следующие сутки после введения препарата. После завершения 5-дневного курса уровень тромбоцитов составил 123×109/л. Через 7 дней после выписки уровень тромбоцитов незначительно снизился (88×109/л). При последующем наблюдении пациента уровень тромбоцитов составил 132×109/л и оставался стабильным.
Терапевтический эффект отмечался уже на следующие сутки после введения препарата. После завершения 5-дневного курса уровень тромбоцитов составил 123×109/л. Через 7 дней после выписки уровень тромбоцитов незначительно снизился (88×109/л). При последующем наблюдении пациента уровень тромбоцитов составил 132×109/л и оставался стабильным.
Клинический случай 2
Пациент, 40 лет, с циррозом печени HCV-этиологии (анти-HCV+, РНК HCV+), субкомпенсированным, класс В по Чайлду – Пью, был направлен на лечение в инфекционное отделение ВГКБ № 1. Количество тромбоцитов при госпитализации было в пределах 21×109/л. В анамнезе – отсутствие ответа на ПВТ. Пациенту была назначена патогенетическая терапия, а также Эмаплаг в дозе 15 000 ЕД/сут в течение 5 дней для коррекции ТП. На протяжении всего курса введения препарата уровень тромбоцитов увеличился незначительно – до 34×109/л. Одновременно был назначен курс безинтерфероновой ПВТ. Через 1 неделю после завершения терапии Эмаплагом количество тромбоцитов определялось на уровне 28×109/л. Спустя 1 месяц уровень тромбоцитов повысился до 112×109/л.
Клинический случай 3
Пациент, 39 лет, проходил лечение в инфекционном отделении ВГКБ № 1 в связи с циррозом печени HCV-этиологии, субкомпенсированным, класс В по Чайлду – Пью. При полном обследовании по данным общего анализа крови определялась панцитопения (эритроциты – 3,18×1012/л, гемоглобин – 102 г/л, лейкоциты – 2,4×109/л, тромбоциты – 27×109/л). Для коррекции ТП был назначен препарат Эмаплаг в дозе 15 000 ЕД/сут в течение 5 дней. С первых суток терапии препаратом отмечалось постепенное увеличение количества тромбоцитов до 128×109/л на 5-й день. При последующем наблюдении пациента уровень тромбоцитов снизился до исходного уровня (28×109/л) в течение 2 мес. Позже были назначены иммуноцитохимические исследования костного мозга (с подсчетом миелограммы), которые подтвердили наличие апластической анемии.
Выводы
- Степень выраженности ТП у больных ХГС-ассоциированным циррозом печени определяется рядом факторов, связанных как с непосредственным действием HCV, так и с индивидуальными особенностями пациента.
- Тенденция к повышению уровня тромбоцитов имеет обратную связь с тяжестью течения цирроза печени, наличием вируса в крови, а также сопутствующей патологией, что, вероятно, определяется степенью угнетения тромбоцитарного ростка кроветворения и поддается коррекции путем увеличения курсовой дозы рекомбинантного тромбопоэтина (Эмаплаг).
- Применение рекомбинантного тромбопоэтина у пациентов с ХГС-ассоциированным циррозом печени и сопутствующей гемолитической анемией качественно стимулирует тромбоцитарный росток кроветворения, о чем свидетельствует значимое повышение количества тромбоцитов.
- Для получения достоверных результатов необходимо продолжить исследования препарата Эмаплаг при участии большего количества пациентов, а также изучить возможность назначения курсов рекомбинантного тромбопоэтина с целью насыщения крови зрелыми формами мегакариоцитов и повышения уровня тромбоцитов.
Литература
1. Platelet count: MedlinePlus Medical Encyclopedia. www.nlm.nih.gov.
2. What Is Thrombocytopenia? – NHLBI, NIH. www.nhlbi.nih.gov.
3. Alexander W.S., Begley C.G. Thrombopoietin in vitro and in vivo. Cytokines Cell Mol Ther. 1998 Mar; 4 (1): 25-34.
4. Ng V.L. Liver disease, coagulation testing, and hemostasis. Clin Lab Med. 2009 Jun; 29 (2): 265-82.
5. Bashour F.N., Teran J.C., Mullen K.D. Prevalence of peripheral blood cytopenias (hypersplenism) in patients with nonalcoholic chronic liver disease. Am J Gastroenterol. 2000; 95 (10): 2936-9.
6. Giannini E.G. Review article: thrombocytopenia in chronic liver disease and pharmacologic treatment options. Aliment Pharmacol Ther. 2006; 23 (8): 1055-65.
7. Mitchell O. et al. The pathophysiology of thrombocytopenia in chronic liver disease. Hepat Med. 2016; 8: 39-50.
Hepat Med. 2016; 8: 39-50.
8. Dahal S. et al. Thrombocytopenia in Patients with Chronic Hepatitis C Virus Infection. Mediterr J Hematol Infect Dis. 2017; 9 (1): e2017019.
9. Weksler B.B. Review article: the pathophysiology of thrombocytopenia in hepatitis C virus infection and chronic liver disease. Aliment Pharmacol Ther. 2007 Nov; 26 Suppl 1: 13-9.11.
10. Suwantarat N. et al. Weight loss, leukopenia and thrombocytopenia associated with sustained virologic response to Hepatitis C treatment. Int J Med Sci. 2010; 7 (1): 36-42.
11. Izak M., Bussel1 J.B. Management of thrombocytopenia F1000Prime Rep. 2014; 6: 45.
12. Kiefel V. Reactions Induced by Platelet Transfusions. Transfus Med Hemother. 2008 Oct; 35 (5): 354-358.
13. Aubron С. et al. Is platelet transfusion associated with hospital-acquired infections in critically ill patients? Crit Care. 2017; 21: 2.
14. Cadili A., de Gara C. Complications of splenectomy. Am J Med. 2008 May; 121 (5): 371-5.
15. Vadhan-Raj S. Clinical experience with recombinant human thrombopoietin in chemotherapy-induced thrombocytopenia. Semin Hematol. 2000 Apr; 37 (2 Suppl 4): 28-34.
16. Zhao Y.Q. et al. A multi-center clinical trial of recombinant human thrombopoietin in chronic refractory idiopathic thrombocytopenic purpura. Zhonghua Nei Ke Za Zhi. 2004 Aug; 43 (8): 608-10.
17. Kuter D.J. The biology of thrombopoietin and thrombopoietin receptor agonists. Int J Hematol. 2013 Jul; 98 (1): 10-23.
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 1 (47), березень 2018 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
28.03.2021
Гастроентерологія
Какие этиологические, патогенетические механизмы и клинические проявления следует учитывать в диагностике хронического панкреатита
Первичный этап диагностического поиска весьма важен как для врача (поскольку свидетельствует о его квалификации), так и для больного (поскольку определяет время назначения верного оптимального лечения, дальнейшую тактику поведения пациента и, соответственно, качество его жизни). Диагностика всей группы гастроэнтерологических заболеваний представляет определенные трудности в связи с наличием у большинства пациентов диспепсического и болевого синдромов. Исходя из этого, знание особенностей этиологических и патогенетических моментов, клинической картины (особенностей симптоматики, вплоть до так называемых малых симптомов), а также объективных методов исследования является важным в диагностике. …
Диагностика всей группы гастроэнтерологических заболеваний представляет определенные трудности в связи с наличием у большинства пациентов диспепсического и болевого синдромов. Исходя из этого, знание особенностей этиологических и патогенетических моментов, клинической картины (особенностей симптоматики, вплоть до так называемых малых симптомов), а также объективных методов исследования является важным в диагностике. …
28.03.2021
Гастроентерологія
Гепадоктор: на захисті печінки
За останні десятиліття значно збільшився тягар хронічних захворювань печінки, зокрема через поширеність метаболічно-асоційованої жирової хвороби печінки. В усьому світі внаслідок захворювань печінки помирають приблизно 2 млн людей на рік, із них 1,16 млн осіб – від ускладнень цирозу печінки, який посідає 11-е місце серед найбільш частих причин смерті. У західних індустріальних країнах головними причинами розвитку цирозу є надмірне вживання алкоголю та неалкогольна жирова хвороба печінки (НАЖХП), тоді як у багатьох азіатських країнах це гепатит В (S.K. Asrani et al., 2019)….
28.03.2021
Гастроентерологія
Педіатрія
Неінвазивні біомаркери у діагностиці запальних захворювань кишечнику у дітей
Запальні захворювання кишечнику (ЗЗК) – група хронічних рецидивуючих захворювань, які виникають унаслідок невідповідності імунної відповіді на кишкові коменсальні мікроорганізми у генетично схильних осіб, що призводить до запальної реакції з формуванням виразок у шлунково-кишковому тракті (ШКТ). В останні роки як патогенетичні механізми розглядають роль мікробіому, підвищеної проникності слизової оболонки кишечнику, оксидативного стресу й епігенетики [1]. До ЗЗК належать такі захворювання, як виразковий коліт (ВК) та хвороба Крона (ХК). …
В останні роки як патогенетичні механізми розглядають роль мікробіому, підвищеної проникності слизової оболонки кишечнику, оксидативного стресу й епігенетики [1]. До ЗЗК належать такі захворювання, як виразковий коліт (ВК) та хвороба Крона (ХК). …
27.03.2021
Гастроентерологія
Роль мікробіоти кишечнику в перебігу COVID-19
Сьогодні людство зіштовхнулося з пандемією COVID-19 та відсутністю специфічного лікування нової хвороби. Саме тому надзвичайно важливим та актуальним став пошук можливих механізмів впливу на захисні сили людського організму. Вагоме значення для підтримки імунного статусу має мікробіота кишечнику (МК), адже 70-80% імунних клітин містяться саме у цьому органі. Неправильне харчування, стрес, вік, прийом антибактеріальних препаратів, а також наявність тих чи інших захворювань можуть спровокувати розвиток дисбіозу (E. Thursby, N. Juge, 2017)….
(PDF) HEMOSTATIC DISORDERS IN LIVER DISEASES
88
ВЕСТНИК ТРАНСПЛАНТОЛОГИИ И ИСКУССТВЕННЫХ ОРГАНОВ том XII № 2–2010
кровотечением из ВРВ вводили rFVIIa для достиже-
ния гемостаза, но у 6 развилось раннее повторное
кровотечение, и все они умерли, что подтверждает
кратковременность действия препарата [14]. Учи-
тывая возможность развития тромбозов и запуска
ДВС-синдрома, безопасность применения rFVIIa у
пациентов с циррозом необходимо изучить в боль-
ших рандомизированных исследованиях.
Трансплантация печени
Ортотопическая трансплантация печени ( ОТП) –
единственный метод лечения конечной стадии
заболеваний печени. Улучшения в анестезиологи-
ческом обеспечении, хирургической технике и кон-
сервации органа позволили в последние годы зна-
чительно снизить потребность в трансфузии [27].
Тем не менее объем кровопотери сильно варьирует,
и в большинстве исследований коррелирует с высо-
кой летальностью, плохой функцией трансплантата
и риском инфекционных осложнений [36]. В насто-
ящее время в некоторых случаях удается провести
операцию без переливания эритроцитарной массы.
Ни предоперационные коагуляционные тесты,
ни маркеры фибринолиза во время операции не поз-
воляют предположить интраоперационную крово-
потерю [42], объем которой зависит от развитости
коллатерального кровообращения вследствие пор-
тальной гипертензии и предшествующих операций
на органах брюшной полости.
Нарушения в системе гемостаза во время транс-
плантации печени зависят от хирургических этапов
операции (преагепатический период, агепатический
период, постреперфузионный период) и послеопе-
рационного периода.
Преагепатический период
Первый этап операции характеризуется боль-
шой травматичностью из-за рассечения спаек и
пересечения множества коллатеральных сосудов.
Как правило, наблюдаются умеренные нарушения
коагуляции и умеренная кровопотеря, которая кор-
релирует со сложностью гепатэктомии и степенью
выраженности гипокоагуляции до операции. Этио-
логия заболевания печени влияет на кровопотерю и,
соответственно, на потребность в трансфузии. При
гепатоцеллюлярной карциноме, холестатических
поражениях печени (первичный склерозирующий
холангит, первичный билиарный цирроз) наблюда-
ется склонность к гиперкоагуляции, определяемая
по тромбоэластограмме, и менее выражена фибри-
нолитическая активность, поэтому антифибрино-
литические препараты не назначаются. При транс-
При транс-
плантации у детей по поводу билиарной атрезии
нарушения коагуляции не столь значительны, как
при циррозе другой этиологии.
Агепатический период
В этот период кровопотеря минимальна, так как
основные сосуды пережаты, но вследствие измене-
ний в гемостазе кровотечения иногда развиваются.
Наличие гиперфибринолиза в этот период опера-
ции доказано большим количеством исследований.
Происходит увеличение концентрации тканевого
активатора плазминогена, который не элиминиру-
ется печенью, выключенной из кровотока. Доказа-
тельством активного фибринолитического процесса
служат одновременное снижение α2-антиплазмина
и плазминогена и увеличение продуктов деграда-
ции фибрина и фибриногена. В исследованиях,
оценивавших изменение концентрации факторов
свертывания после применения рекомбинантного
активированного фактора VII при трансплантации
печени, отмечалось резкое возрастание продукции
тромбина, укорочение протромбинового и частич-
ного тромбопластинового времени, но активность
фибринолиза не изменялась [34].
Реперфузия и постреперфузионный период
Реперфузия – ключевой момент операции, ве-
дущий к значительным нарушениям свертывания.
Спустя минуты после реперфузии может развиться
неконтролируемое диффузное кровотечение.
Гиперфибринолиз является самым важным и
значительным фактором, обуславливающим объем
кровопотери во время трансплантации. Активность
фибринолиза снижается в течение 60 минут после
реперфузии, и остается повышенной при плохой
функции трансплантата.
Секвестрация тромбоцитов в трансплантате так-
же способствует кровоточивости. В экспериментах
показано, что разница между содержанием тромбо-
цитов в артериальной и венозной крови новой пече-
ни может достигать 55%. Более того, в этом периоде
ухудшается агрегация тромбоцитов [25]. Симптомы
Симптомы
ДВС-синдрома после реперфузии свидетельствуют
о плохом качестве трансплантированного органа.
После реперфузии в 25–95% случаев отмечается
выброс в кровоток гепарина или гепариноподобных
веществ [35]. Введение протамина сульфата (50 мг)
позволяет нейтрализовать гепарин. В одном из ис-
следований наличие гепариноподобных субстан-
ций было подтверждено тромбоэластографией с ис-
пользованием фермента гепариназы I. Повышение
потребности в трансфузии эритроцитарной массы
коррелировало с наличием гепарина в крови. Сле-
дует отметить, что гепариноподобные эффекты на
тромбоэластограмме обнаруживаются до реперфу-
зии даже у пациентов, не получавших гепарин.
Антифибринолитическая терапия используется во
время трансплантации для сокращения кровопотери
и времени операции. К препаратам, подавляющим
фибринолиз и используемым во время трансплан-
тации, относятся апротинин, ипсилон аминокапро-
новая кислота и транексамовая кислота. Апротинин
«Изменения в системе гемостаза и их коррекция при трансплантации печени»
75
На правах рукописи
КУЗНЕЦОВА Наталия Константиновна
ИЗМЕНЕНИЯ В СИСТЕМЕ ГЕМОСТАЗА И ИХ КОРРЕКЦИЯ ПРИ ТРАНСПЛАНТАЦИИ ПЕЧЕНИ
14.00.37 — Анестезиология и реаниматология
т э ноя 2::о
АВТОРЕФЕРАТ диссертации на соискание ученой степени кандидата медицинских наук
Москва 2009
003484075
Работа выполнена в Научно-исследовательском институте скорой помощи им. Н.В. Склифосовского Департамента здравоохранения г. Москвы.
Научные руководители:
доктор медицинских наук, профессор Тимербаев Владимир Хамидович
доктор медицинских наук, профессор Чжао Алексей Владимирович
Официальные оппоненты:
доктор медицинских наук, профессор Свиридов Сергей Викторович
доктор медицинских наук, профессор Дорфман Александр Григорьевич
Ведущая организация
ФГУ «Институт хирургии им. A.B. Вишневского Росмедтехнологий»
A.B. Вишневского Росмедтехнологий»
Защита диссертации состоится «_»_2009 г. в_часов на
заседании диссертационного совета Д.850.010.01 при Научно-исследовательском институте скорой помощи им. Н.В. Склифосовского по адресу: 129010, Москва, Б.Сухаревская пл., д.З.
С диссертацией можно ознакомиться в библиотеке Научно-исследовательского института скорой помощи им. Н.В. Склифосовского по адресу: Москва, Б.Сухаревская пл., д.З.
Автореферат разослан «_»_2009 г.
Ученый секретарь диссертационного совета, доктор медицинских наук, профессор
A.A. Гуляев
Список сокращений
АВСК — активированное время свертывания AJIAT — аланинаминотрансфераза
АПТВ — активированное парциальное тромбопластиновое время
АСАТ — аспартатаминотрансфераза
ВСРП — высокая степень реперфузионного повреждения
ГВГД — гиперволемическая гемодилюция
ДВС — дисссминированное внутрисосудистое свертывание
ДЗЛК-давление заклинивания легочных капилляров
МАК — максимальная альвеолярная концентрация
MHO — международное нормализованное отношение
НСРП — низкая степень реперфузионного повреждения
ОПСС — общее периферическое сопротивление сосудов
ОТП — ортотопическая трансплантация печени
ПВ — протромбиновое время
РКФМ — растворимые комплексы фибринмономера
РФ Vila — активированный рекомбинантный фактор VII
СВ — сердечный выброс
СЗП — свежезамороженная плазма
ФА — фибринолитическая активность
ЦВД — центральное венозное давление
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ Актуальность проблемы
За десятилетия, прошедшие от момента выполнения первой ортотопической трансплантации печени Т. Starzl (1963 г.) до наших дней, эта операция из экспериментальной превратилась в стандартный метод лечения терминальных заболеваний печени.
Как правило, основным показанием к этому вмешательству является диффузное поражение печени, а именно — цирроз различной этиологии. Известно, что в гепатоците происходит синтез основной массы белков
Известно, что в гепатоците происходит синтез основной массы белков
свертывающей и противосвертывающей систем. Поэтому их дефицит всегда является спутником цирроза печени. А портальная гипертензия, усиливая секвестрацию тромбоцитов в селезенке, приводит к снижению их содержания в крови [Анжелина К.А. Карвальхо, 2001]. Таким образом, проблема нарушения свертываемости крови у пациентов перед трансплантацией печени является одной из основных. Она обуславливает высокий риск развития кровотечения у этой категории больных.
Операция ортотопическая трансплантация печени имеет ряд особенностей, которые, в свою очередь, могут серьезно усугубить исходную гипокоагуляцию у пациентов:
1. Наличие беспеченочного периода, когда печень реципиента удалена, организм какое-то время остается лишенным всех её функций.
2. Использование порто-бедренно-аксиллярного шунтирования во время операции, когда оседание и разрушение тромбоцитов в магистралях системы может усугубить тромбоцитопению.
3. Период реперфузии трансплантата, во время которого прогрессирует гипотермия при прохождении крови через донорскую печень, извлеченную изо льда; идет выброс в кровь гепарина, используемого на донорском этапе; нарастает ацидоз и гиперкалиемия. [КеИпег 8.С. е1 а1, 1998].
Сочетание исходных гипокоагуляционных нарушений при циррозе печени с неблагоприятными факторами самого оперативного вмешательства может приводить к развитию массивного интраоперационного кровотечения.
Проблема коррекции коагуляционных расстройств при трансплантации печени всегда имела первостепенное значение. [Мс Раг1апс11 в, 1999]. Но она не может быть решена преимущественным использованием компонентов донорской крови.
Общеизвестно, что переливание трансфузионных сред может повлечь за собой массу осложнений. Немаловажным является тот факт, что, помимо всех известных инфекционных осложнений, пациенты после трансплантации, подвергающиеся имуносупрессии, восприимчивы также к вирусам герпеса, Эпштейна-Барра и цитомегаловирусу (только у 1-2% доноров крови антитела к
данной группе вирусов отсутствуют [Колосков A. B., 2004]). При попадании в организм больного с пересаженной печенью они вызывают вирусное поражение трансплантата с последующим развитием хронического отторжения. Лечение подобного рода вирусной инфекции достаточно дорогостоящее и имеет множество побочных эффектов. Поэтому поиск альтернативы использованию компонентов донорской крови в терапии гипокоагуляционных кровотечений имеет большое значение.
B., 2004]). При попадании в организм больного с пересаженной печенью они вызывают вирусное поражение трансплантата с последующим развитием хронического отторжения. Лечение подобного рода вирусной инфекции достаточно дорогостоящее и имеет множество побочных эффектов. Поэтому поиск альтернативы использованию компонентов донорской крови в терапии гипокоагуляционных кровотечений имеет большое значение.
Развитие кровосберегающей хирургической технологии, появление новых препаратов, влияющих на гемокоа1улядию, позволяют по-новому взглянуть на проблему коррекции нарушений гемостаза и повысить эффективность и безопасность трансплантации печени.
Таким образом, применение современных методов коррекции нарушений в системе гемостаза при трансплантации печени, позволяющих снизить летальность у данной категории больных, улучшить результаты оперативного вмешательства, обезопасить больного от инфицирования при переливании компонентов донорской крови является актуальным.
Цель исследования
Изучить изменения в системе гемостаза и оптимизировать методы их коррекции при трансплантации печени.
Задачи исследования
1. оценить предоперационные изменения в системе гемостаза у пациентов с циррозами печени различной этиологии и степени тяжести.
2. определить интраоперационную динамику показателей системы гемостаза и эффективность различных вариантов коррекции нарушений гемостаза при трансплантации печени.
3. изучить изменения в системе гемостаза в раннем послеоперационном периоде и определить факторы, влияющие на развитие послеоперационных осложнений и исход трансплантации печени.
Научная новизна
Впервые в отечественной практике произведена оценка исходных изменений в системе гемостаза у пациентов в зависимости от тяжести и этиологии цирроза печени, перенесших трансплантацию печени.
Впервые предложен допустимый объем предоперационной гемодилюции при трансплантации печени, позволяющий снизить интраоперационную кровопотерю и потребность в переливании компонентов аллогенной крови.
Впервые определена роль исходной тяжести и этиологии цирроза печени и высокой степени реперфузионно-ишемических повреждений трансплантата, как основных значимых факторов, влияющих на состояние системы гемостаза после трансплантации печени.
Впервые в отечественной практике показана значимость послеоперационной динамики уровня тромбоцитов для прогнозирования исхода и развития осложнений раннего послеоперационного периода при трансплантации печени.
Впервые в нашей стране изучены результаты использования рекомбинантного фактора Vila при ортотопической трансплантации печени.
Практическая значимость
Применение данных исследования позволило прогнозировать особенности течения операции трансплантации печени в зависимости от исходных нарушений гемостаза у пациентов с тяжелыми формами цирроза печени, развитие осложнений в раннем послеоперационном периоде и исход операции.
Определена анестезиологическая тактика, позволяющая использовать принципы «кровосберегающей хирургии» во время трансплантации печени.
Результаты исследования вошли в протокол ведения больных в периоперационном периоде трансплантации печени. Они позволили повысить качество анестезиологического обеспечения при трансплантации печени, уменьшить риск развития осложнений после операции и улучшить результаты лечения.
Внедрение результатов работы
Основные теоретические и прикладные аспекты работы используются в практике отделения трансплантации печени НИИ СП им. Н.В. Склифосовского. Результаты исследования включены в программу последипломного обучения ординаторов, аспирантов и стажеров отделения трансплантации печени.
Апробация работы
Основные положения и материалы исследования представлены на 3-ей Сессии Московского научного общества анестезиологов и реаниматологов, Голицыне, 22 марта 2002г., на конференции «Клиническая трансплантация органов», Москва, 26-27 сентября 2007г., на заседании проблемно-плановой комиссии №8 «Реаниматология, анестезиология и интенсивная терапия» НИИ скорой помощи им. Н.В. Склифосовского 24 декабря 2008г.
Н.В. Склифосовского 24 декабря 2008г.
Публикации
По теме диссертации опубликовано 9 научных работ, в том числе — 2 статьи в журналах «Анналы хирургической гепатологии» и «Общая реаниматология».
Структура и объём диссертации
Диссертационная работа изложена на 114 страницах машинописного текста и состоит из введения, обзора литературы, глав, содержащих описание материалов и методов исследования, полученных результатов и их обсуждения, выводов, практических рекомендаций и списка литературы. Иллюстрированный материал представлен в виде 24 таблиц и 15 рисунков. Библиография содержит 142 источника, из них 38 отечественных и 104 иностранных.
СОДЕРЖАНИЕ РАБОТЫ Характеристика клинических наблюденнй и методы исследования
В исследование включено 77 пациентов с циррозом печени различной этиологии, которым было выполнено 80 трупных трансплантаций печени (3
пациента перенесли ретрансплантацию) в период с 2000 по 2008 годы в НИИ СП им. Н.В. Склифосовского.
Преобладающими причинами циррозов (52%) были вирусные гепатиты С и В (32% и 20% соответственно).
В процессе исследования в предоперационном периоде все больные были разделены на 2 группы в соответствии с классификацией тяжести циррозов печени Чайлда-Пыо. В 1-ю группу вошли пациенты, относящиеся к классу В (п=33), во 2-ю — к классу С (п=47).
В 1-й группе среди пациентов было 18 (54,5%) мужчин и 15 (45,5%) женщин, во 2-й группе — 24 (51,1%) и 23 (48,9%) соответственно. Средний возраст пациентов в 1-й группе составил 43 ± 12,5 года (от 20 до 68), а во 2-й группе 44,5±11,3 года (от 20 до 64).
Деление пациентов па группы исследования в интраоперационном периоде трансплантации печени производили в зависимости от объема проводимой предоперационной гиперволемической гемодилюции. К 1-й группе (п=31) были отнесены пациенты, которым проводилась гиперволемическая гемодилюция объемом 15 мл/кг, ко 2-й группе (ti=49) — пациенты с объемом гиперволемической гемодилюции 7 мл/кг. В обеих группах ГВГД осуществлялась после вводной анестезии раствором гидроксиэтилкрахмала (Волювен 6%). Группы были сопоставимы по баллам степени тяжести цирроза по Чайлду-Пью, по полу, возрасту, физическому статусу по ASA и времени анестезии (табл. 1).
В обеих группах ГВГД осуществлялась после вводной анестезии раствором гидроксиэтилкрахмала (Волювен 6%). Группы были сопоставимы по баллам степени тяжести цирроза по Чайлду-Пью, по полу, возрасту, физическому статусу по ASA и времени анестезии (табл. 1).
Таблица 1
Характеристика больных в интраоперационном периоде (М±с)
Показатель 1 группа (п=31) 2 группа (п=49)
Баллы по Чайлду-Пью 9,56±1,6 9,04±1,1
Пол М- 19 Ж -12 М — 27 Ж — 22
Возраст, лет 40,5114,1 (20-68) 42,9+11,2(20-58)
Физический статус, ASA III/IV 27/4 47/2
Время анестезии, мин 7501120 7021108
Исследование показателей гемостаза в послеоперационном периоде проводили в 3-х группах пациентов: 1-я группа (п=39) — с нормальным течением послеоперационного периода, 2-я группа (п=31) — с осложненным послеоперационным периодом, 3-я группа (п=10) — умершие в течение 90 дней после трансплантации печени.
Премедикация у пациентов осуществлялась путем внутримышечного введения дормикума (мидазолама) 5-7,5 мг за 40 мин до операции. Индукцию осуществляли последовательным введением тракриума (атракуриума бесилата) 10 мг, с целью прекураризации, далее — фентанила (2,85±0,52 мкг/кг) и пропофола (1,4±0,3 мг/кг). После введения листенона 2 мг/кг или нимбекса (цисатракуриум бесилат — 0,15 ± 0,02 мг/кг) производили интубацию трахеи. После индукции в анестезию начинали ингаляцию (0,7-1,6 МАК) изофлюрана или севофлюрана (0,6-1 МАК).
В начале операции в легочную артерию устанавливали катетер Swan-Ganz (Edwards Lifesciences, США). Артериальное давление контролировали прямым методом. С этой целью катетеризировали лучевую артерию. Определяли давление в легочной артерии, ЦВД, СВ, ДЗЛК и ОПСС (мониторная система AS/3 фирмы Datex-Engstrom (Финляндия)).
ИВЛ во время анестезии проводили респиратором наркозного аппарата ADU (Datex-Engstrom, Финляндия) по полузакрытому контуру по методике «Low Flow anesthesia». Дополнительно к изофлюрану или севофлюрану использовали болюсные введения фентанила и дормикума по 0,05-0,1 мг и 5 мг соответственно. Нимбекс вводили с помощью дозатора со скоростью 0,06±0,055 мг/кг/ч, тракриум внутривенно дробно по 0,55±.0,12 мг/кг каждые 40-50 мин.
Нимбекс вводили с помощью дозатора со скоростью 0,06±0,055 мг/кг/ч, тракриум внутривенно дробно по 0,55±.0,12 мг/кг каждые 40-50 мин.
При ОТП без сохранения ретропеченочного отдела нижнией полой вены, в процессе беспеченочного периода (время от момента прекращения кровотока по нижней полой вене до реперфузии имплантированной донорской печени венозной кровью) возврат крови к сердцу осуществлялся путем принудительного порто-бедренно-аксиллярного шунтирования с помощью
центробежного насоса «Biopump» (Biomedicus, США). Эта методика использовалась у 17 (51%) пациентов 1-й группы и у 15 (31,9%) пациентов 2-й группы. Соответственно 16 (49%) и 32 (68,1%) трансплантаций печени в группах выполнялись без использования аппаратного обходного шунтирования.
Для профилактики гипотермии с начала операции производили согревание пациентов. С этой целью использовали две системы внешнего обогрева: Tropi-Cool (Zimmer, США), состоящую из двух матрасов, в которых циркулировала вода, нагретая в блоке системы до температуры 37°С, и WarmTouch (Mallinckrodt Medical, Ирландия), состоящую из полого одеяла специальной формы, которое нагревалось подаваемой из блока системы струёй нагретого до 38-42°С воздуха. При выполнении вено-венозного шунтирования применяли магистрали Medtronic (США), оснащенные теплообменником.
Возврат аутокрови осуществляли при помощи интраоперационной аппаратной реинфузии отмытых аутоэритроцитов. С этой целью применяли аппарат «C.A.T.S.» (Fresenius, Германия).
При АВСК более 180 сек или массивном кровотечении переливали донорскую СЗП. При снижении НЬ < 60 г/л и Ht < 20% назначали аллогенную эритроцитарную массу. При уровне тромбоцитов < 40×109/л производили трансфузию донорского тромбоконцентрата. С целью профилактики гиперфибринолиза всем пациентам интраоперационно назначался апротинин в дозе 500000-1000000 ME.
Для оценки звеньев системы гемостаза использовали следующие показатели коагулограммы:
1. Тромбоцитарный гемостаз — исследование количества и агрегации тромбоцитов (ручная методика и с помощью агрегометра).
Тромбоцитарный гемостаз — исследование количества и агрегации тромбоцитов (ручная методика и с помощью агрегометра).
2. Плазменный гемостаз:
2.1. Тесты, характеризующие свертывающую систему — АПТВ, ПВ и фибриноген.
2.2. Тесты, характеризующие противосвертывающую систему (физиологические антикоагулянты) — антитромбин III, протеина С.
3. Фибринолитическая система — ХИа — Хагеман-зависимый фибринолиз.
4. Маркеры внутрисосудисгого свертывания и фибринолиза — РКФМ.
Исследование показателей коагулограммы производили у всех пациентов перед трансплантацией печени, а также на 1-е, 3-й и 7-е сутки послеоперационного периода.
Для быстрой интраоперационной оценки состояния гемостаза использовали метод определения активированного времени свертывания крови (АВСК) при помощи автоматического коагуло-хронометра АСТ II (Medtronic, США).
Статистическая обработка цифровых величин производилась с использованием программы Statistica 6,0. Результаты представлены в виде средних значений (М) и стандартного отклонения (а): (М±а).
Количественные результаты оценивались с помощью Т-теста, если они имели нормальное распределение. Коэффициент Фишера применяли, когда частота явления была невелика. Непараметрические методы статистики использовали при выявлении ненормального распределения. Тест Манна-Уитни применяли для двух независимых выборок. Коэффициент корреляции Спирмена использовали для установления взаимосвязи между различными выборками. Различие считали статистически значимым при р<0,05.
Результаты собственных исследований и их обсуждение
При исследовании показателей гемостаза перед трансплантацией печени пациенты были разделены на 2 группы в зависимости от тяжести цирроза печени по Чайлду-Пью: 1-я группа (п=33) — класс В, 2-я (п=47) — класс С.
Показатель ПВ до операции у пациентов в 1-й и 2-й группах соответствовал 1,9±1,1 МНО, или 62,5±20,1%, и 1,9±1,ЗМНО, или 57,7±22,9%, что в обоих случаях было ниже нормы (табл.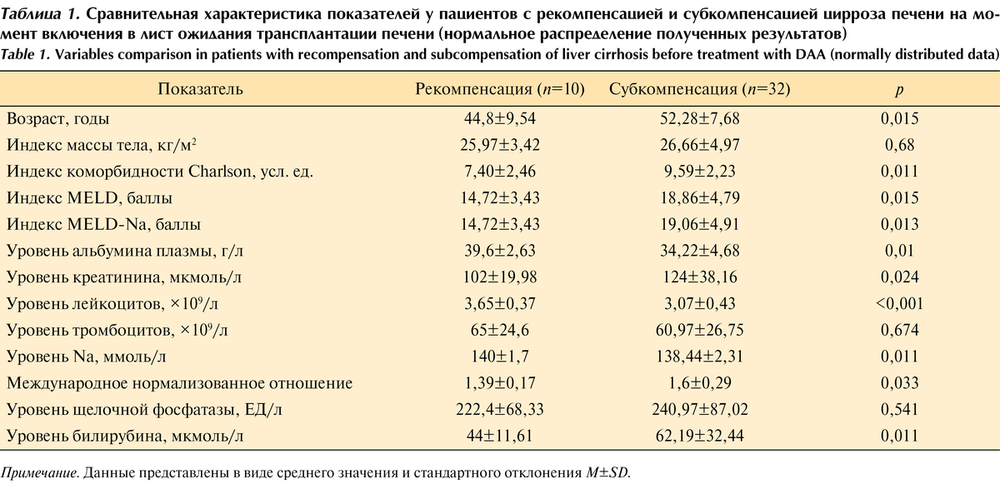 2). Исходные показатели АПТВ значительно превышали верхнюю границу нормы — 50±25,7 сек и 50,5±23 сек в 1-й и 2-й группах соответственно. При этом сравнение показателей ПВ и АПТВ между группами статистически значимого отличия не выявило.
2). Исходные показатели АПТВ значительно превышали верхнюю границу нормы — 50±25,7 сек и 50,5±23 сек в 1-й и 2-й группах соответственно. При этом сравнение показателей ПВ и АПТВ между группами статистически значимого отличия не выявило.
Таблица 2
Исходные изменения в свертывающей системе гемостаза у больных с _циррозами печени (М±а)_
Показатель Группа 1 (п=33) Группа 2 (п=47) Нормальное значение
Протромбиновое время, MHO 1,9±1,1 1,9±1,3 Менее 1,4
Протромбиновое время, % 62,5±20,1 57,7±22,9 70-130
АПТВ, сек 50±25,7 50,5±23 24-33
Фибриноген, г/л 2,6±1,4 2±0,9* 2-4
ФА, мин 24,8±17,9 27,5±23,7 4-10
РКФМ, мкг/мл 20±22,6 67,5±26,5* 0-40
Примечание: * — статистически значимые различия между группами 1 и 2, С|Х0,05).
Уровень фибриногена перед ОТП соответствовал нижней границе нормы во 2-й группе — 2±0,9 г/л, но был статистически значимо ниже, чем у пациентов 1-й группы — 2,6±1,4 г/л. Кроме того, во 2-й группе имелось статистически значимое повышение содержания РКМФ до 67,5±26,5 мкпкл по сравнению с 1-й (р<0,05) (см. табл.2).
Анализ данных противосвертывающей системы показал, что протеин С был статистически значимо ниже во 2-й группе по сравнению с 1-й — 54,6±24% и 80±21,2%, как и антитромбин III — 64,8±29,1% и 88,1±23,9% (р<0,05) (табл.3).
Таблица 3
Исходные изменения в противосвертывающей системе гемостаза у _больных с циррозами печени (Mío) _
Показатель, % Группа 1 (п=33) Группа 2 (п=47) Нормальное значение
Протеин С 80±21,2 54,6±24* 70-140
Антитромбин III 88,1±23,9 64,8±29,1* 80-120
Примечание: * — статистически значимые различия между группами 1 и 2, (р<0,05).
При исследовании тромбоцитарного звена гемостаза тромбоцитопения была выявлена в обеих группах: в 1-й группе средний показатель составил 114,2±72,4х109/л, во 2-й — 130±90,6 х109/л. При этом уровень тромбоцитов и их агрегационная способность в обеих группах статистически значимо не отличалась. В то же время, статистически значимо низкое по сравнению с другими циррозами печени количество тромбоцитов определялось у пациентов с циррозами в результате вирусных гепатитов С и В — 78,2+24,2×109/л и 94,1±31,8хЮ9/л соответственно (р<0,05).
В то же время, статистически значимо низкое по сравнению с другими циррозами печени количество тромбоцитов определялось у пациентов с циррозами в результате вирусных гепатитов С и В — 78,2+24,2×109/л и 94,1±31,8хЮ9/л соответственно (р<0,05).
Результаты нашего исследования свидетельствуют о том, что у всех пациентов, находящихся в листе ожидания трансплантации печени, имеются нарушения в системе гемокоагуляции. Степень выраженности изменений ряда показателей соответствует тяжести цирроза по классификации Чайлда-Пью. Так, отмечена статистически значимая разница между группами по показателям противосвертывающей системы (протеин С и антитромбин III). В то же время достоверного отличия в показателях свертывающей системы (ПВ, АПТВ) и тромбоцитарного звена зарегистрировано не было. Таким образом, указанная классификация, наиболее часто применяемая для оценки тяжести цирроза печени, объективно не отражает состояние системы гемостаза у этих пациентов и не учитывает в полной мере риск развития неконтролируемых кровотечений и ДВС-синдрома.
Наличие изменений в системе гемокоагуляции у пациентов с циррозом печени в предоперационном периоде требовало профилактической корригирующей терапии. Викасол назначали пациентам при уменьшении ПВ ниже 50% в дозе 90 мг/сут на протяжении 1-2 недель. Больным с уровнем Hb ниже 100 г/л назначали препараты эритропоэтина в терапевтической дозе. Эритропоэтин стимулируя эритропоэз, также способствует транзигорному увеличению тромбоцитов и повышению свертываемости крови, тем самым положительно влияет на гемостаз перед операцией у пациентов с циррозом печени.
В то же время радикальная коррекция нарушений в системе гемостаза у этих пациентов возможна только после трансплантации печени.
В интраоперационном периоде были проанализированы показатели гемостаза, а также рассмотрены методы коррекции и профилактики кровопотери при этом виде оперативного вмешательства.
В настоящее время находят свое применение различные методы, способствующие сокращению переливания донорских компонентов крови. Одним из таких методов является предоперационная гиперволемическая гемодилюция. Однако в литературе нет четких данных об объеме и качественном составе ГВГД при трансплантации печени. Исходя из этого, нами было изучено влияние гемодидюции, проводимой после вводной анестезии в объеме 15 мл/кг и 7 мл/кг раствором гидроксиэтилкрахмала (Волюзен 6%).
Одним из таких методов является предоперационная гиперволемическая гемодилюция. Однако в литературе нет четких данных об объеме и качественном составе ГВГД при трансплантации печени. Исходя из этого, нами было изучено влияние гемодидюции, проводимой после вводной анестезии в объеме 15 мл/кг и 7 мл/кг раствором гидроксиэтилкрахмала (Волюзен 6%).
Результаты нашего исследования показали, что при ГВГД в объеме 15 мл/кг увеличивается кровопотеря и потребность в назначении аллогенной эритроцитарной массы при сравнении с гемодилюцией в объеме 7мл/кг при трансплантации печени (габл.4).
Таблица 4
Объем инфузионно-трансфузионной терапии и кровопотери при OTII (Mío)______
Количество, мл 1 группа (п=31) 2 группа (п=49)
Коллоиды 2500±400 (1800-3500) 2000±300 (1000-2500)
Кристаллоиды 4200±700 (2200-6500) 3000±600 (2000-5500)
Донорская эр. масса 739±695,7 336,1±296,4*
СЗП 1740±1134,7 1021,5±673,5*
Аппаратная реинфузия 1240,0±1056,1 700±630,7*
Кровопотеря 3736,8±3 045,3 2038±1437,4*
Примечание: * — статистически значимые отличия между группами с объемом ГВГД 15 мл/кг и 7 мл/кг, (р<0,05).
Согласно полученным данным, ЦВД и СВ в группе после ГВГД 7 мл/кг были оптимальными (табл. 5). Как в 1-й, так и во 2-й группах гемодилюция не приводила к увеличению преднагрузки.
Таблица 5
Показатели ЦВД и СВ до и после ГВГД (М±ст)
Показатель 1 группа (п=31) 2 группа (п=49)
ЦВД до ГВГД, мм рт.ст. 4±1 6±2
ЦВД после ГВГД, мм рт.ст 10±2* 8,5±1
СВ до ГВГД, л/мин 8,5±1,8 9,0±1
СВ после ГВГД, л/мин 9,8±2* 9,2 ±1,3
* — статистически значимые отличия при сравнении показателей в группах 1 и 2 до и после ГВГД (р<0,05).
Следует отметить, что при нормальных исходных показателях гемостаза сама по себе ГВГД не приводит к клинически проявляющейся повышенной кровоточивости. В тоже время, исходные нарушения в системе гемостаза у реципиентов печени в группе с большим объемом ГВГД — усугубляются. Установлено, что после ГВГД объемом 15 мл/кг АВСК статистически значимо удлинялось до 170±9 сек по сравнению с группой, получившей объем ГВГД 7 мл/кг -155±8 сек (р<0,05) (см. рисунок).
Установлено, что после ГВГД объемом 15 мл/кг АВСК статистически значимо удлинялось до 170±9 сек по сравнению с группой, получившей объем ГВГД 7 мл/кг -155±8 сек (р<0,05) (см. рисунок).
300
Рисунок. Динамика АВСК (сек) на этапах операции.
Примечание: * — статистически значимые отличия между группой с ГВГД 15 мл/кг и 7 мл/кг, (р<0,05).
При этом среднее значение соответствовало верхней границе нормы (180 сек). Однако на беспеченочном этапе в 1-й группе этот показатель превышал
норму и был статистически значимо выше, чем во 2-й — 202,9 сек и 163,7 сек соответственно (р<0,05) (см. рисунок).
На наш взглзд, эффект «разведения», а также увеличение ЦВД и СВ в группе с большей гемодилюцией способствовали повышению кровоточивости на этапе гепатэктомии и влияли на общую кровопотерю и, соответственно, потребность в назначении аллогенных компонентов крови.
Применение интраоперационной аппаратной реинфузии аутокрови позволило значимо снизить использование аллогенных эритроцитов. В 1-й группе объем реинфузированного аутоэритроконцентрата составил 1240,0±1056,1 мл (от 250 до 3600 мл), во 2-й — 700,0±630,7 (от 170 до 2300 мл). Во 2-й группе у 2 пациентов с незначительной интраоперационной кровопотерей (600 мл и 700 мл) аппаратная реинфузия ке применялась.
Исходные нарушения в системе гемостаза у пациентов с циррозом печени, кровопотеря во время операции, беспеченочный период приводят к резкому снижению факторов свертывания. Максимальное удлинение АВСК в обеих группах было зарегистрировано на этапе реперфузии (см. рисунок).
С целью восстановления плазменных факторов свертывания производилась трансфузия донорской СЗП. Результаты нашего исследования свидетельствуют, что средний объем инфузии СЗП во всех 80 случаях трансплантации печени составил 1324,1±955,3 мл. Контроль АВСК каждый час, а также на всех критических этапах оперативного вмешательства (при массивной кровопотере, после венозной реперфузии, в беспеченочном периоде) позволяет своевременно определять показания для назначения СЗП и избежать необоснованного и неконтролируемого переливания компонента аллогенной крови. Необходимо отметить, что в 4 (5%) случаях СЗП при трансплантации печени не использовалась.
Необходимо отметить, что в 4 (5%) случаях СЗП при трансплантации печени не использовалась.
Показаниями для назначения рекомбинантного фактора Vila (НовоСэвен, Novonordisk, Дания) являлось удлинение АВСК и диффузная кровоточивость раневой поверхности тканей. Интраоперационно препарат был применен в 4 случаях после венозной реперфузии трансплантата в дозе 80-90 мкг/кг однократно. Показатель АВСК у этих пациентов на данном этапе в 4,7 раза
превышал норму (750±79 сек). После внутривенного введения рекомбинантного фактора Vila у всех 4 больных регистрировали снижение диффузной кровоточивости и улучшение показателя АВСК. Через 30 мин после введения АВСК соответствовало 190±16 сек. При этом эффект нормализации гемостаза сохранялся до конца оперативного вмешательства. АВСК в конце операции — 161,3±8,5 сек.
Следует отметить, что при назначении РФ Vila в 2 наблюдениях не потребовалось трансфузии донорской C3II. В 2 других. случаях количество перелитой СЗП составило в среднем 650.0±71,0 мл. Объем интраоперационной кровопотери при этом был равен 1475,0±482,0 мл. Применение РФ Vila во время трансплантации печени позволило снизить объем кровопотери, уменьшить трансфузию компонентов крови в интраоперационном периоде и быстро и эффективно нормализовать показатели гемостаза.
В послеоперационном периоде тенденция более выраженного отклонения от нормы показателей ПВ (%) отмечалась в группе у реципиентов с исходным циррозом печени класса С по Чайлду-Пью (2-я группа) по сравнению с классом В (1-я группа). В 1-е сутки после операции ПВ соответствовало 37,1±19,3% во 2-й группе и 46,9±20,8% в 1-й группе (табл. 6).
Таблица 6
Показатель Группа 1 (п=33) Группа 2 (п=47)
ПВ 1-е сутки, % 46,9±20,8 37,1±19,3*
ПВ 3-й сутки, % 70,1 ±25 60±20,1*
ПВ 7-е сутки, % 77,9±21 74,1±19,8
АПТВ 1-е сутки, сек 56,6±9,5 68±10,2
АПТВ 3-й сутки, сек 42,3±12,3 52,6±15,6*
АПТВ 7-е сутки, сек 38,3±15,1 39±21,3
Примечание: * — статистически значимые отличия между группами с тяжестью цирроза класса В и С, (р<0,05)
Эти изменения были достоверными и сохранялись к 3-м суткам: ПВ во 2-й группе — 60±20,1%, в 1-й — 70,1±25% (р<0,05). На 7-е сутки показатели ПВ в обеих группах приближались к норме.
На 7-е сутки показатели ПВ в обеих группах приближались к норме.
При исследовании показателей АПТВ отклонения от нормы во 2-й группе также были более выражены. В динамике к 3-м суткам в 1-й группе регистрировалось статистически значимое укорочение АПТВ до 42,3±15,3 сек, по сравнению с 52,6±24,6 сек во 2-й группе (р<0,05). В дальнейшем АПТВ в обеих группах было сопоставимо (см. табл. 6).
Нормализация уровня фибриногена в крови у пациентов 2-ой группы после ОТП наблюдалась только к 3-м суткам. В 1-е сутки уровень фибриногена у них был статистически значимо ниже при сравнении с 1-й группой — 1,3±0,6 и 2,02±0,8 г/л соответственно (р<0,05).
После операции регистрировалось угнетение фибринолитической активности в обеих группах. Но, при общей тенденции к снижению, на 7-е сутки этот показатель был достоверно большим во 2-й группе — 45±30,8 мин, по сравнению с 1-й — 29,5±20,5 мин (р<0,05). Кроме того, в послеоперационном периоде у всех пациентов отмечался высокий, по сравнению с нормой, уровень РКФМ в крови. Повышение РКФМ регистрировалось до 7-х суток, (табл. 7).
Таблица 7
Динамика ФА и содержания РКФМ в крови после операции (М±а)
Показатель Группа 1 (п=33) Группа 2 (п=47)
ФА 1-е сутки, мин 43,4±23,6 56,6±29,9
ФА 3-й сутки, мин 56,1±41,5 61±31,4
ФА 7-е сутки, мин 29,5±20,5 45±30,8*
РКФМ 1-е сутки, мкг/мл 45,2±26,9 67±32,3
РКФМ 3-й сутки, мкг/мл 108±54,3 119±85,3
РКФМ 7-е сутки, мкг/мл 97,6±58 117,8±63
Примечание: * — статистически значимые отличия между группами с тяжестью цирроза класса В и С, (р<0,05).
При сравнении показателей протеина С и антитромбина III статистически значимые различия между обеими группами отмечались во все исследуемые периоды (табл. 8). При этом, начиная с 1-х суток, во 2-й группе показатели как протеина С, так и антитромбина III, были достоверно ниже, чем у пациентов 2-й группы: 55,7±29% и 98,6±36,3%, 42,9±26,9% и 72,5±31% соответственно (р<0,05).
Таблица 8
Содержание протеина С и антитромбина III после операции (М±о)
Показатель, % Группа 1 (п=33) Группа 2 (п=47)
Протеин С 1-е сутки 98,6±36,3 55.7±29*
Протеин С 3-й сутки 95,9±27,3 75,6±25,9*
Протеин С 7-е сутки 101,6±34,3 86,2±23*
Аититромбин III 1-е сутки 72,5±31 42,9±26,9*
Антитромбин III 3-й сутки 80,7±30 55,2±25,4*
Антитромбин III 7-и сутки 90,3±26,2 79,6±24,3*
Примечание: * — статистически значимые отличия между группами с тяжестью цирроза класса В и С, (р<0,05).
Кроме того, в отношении протеина С отличалась сама динамика роста. У пациентов 1-й группы уже на 1-е сутки этот показатель был выше исходного уровня и соответствовал норме. Во 2-й группе ка 1-е сутки он едва достигал предоперационного. Далее отмечался его постепенный рост, и только к 3-м суткам он соответствовал нижней границе нормы — 75,6±25,9%.
В отношении динамики уровня антитромбина III также отмечалась довольно быстрая (уже к 3-м суткам) нормализация его в 1-й группе и достаточно медленный его рост во 2-й (см. табл. 8). При этом низкие показатели не были следствием разницы в реперфузионном повреждении трансплантата в группах, т.к. уровни АСАТ и АЛАТ в обеих группах достоверно не отличались. Исходя из этого, статистически значимые отличия по уровню протеина С и АТ III можно объяснить исходно выраженным дефицитом факторов противосвертывающей системы у пациентов 2-й группы с более тяжелой степенью цирроза печени.
Снижение уровня AT III и протеина С в сочетании с повышением маркеров активации свертывания — РКФМ, низким содержанием фибриногена и тромбоцитопенией являются предпосылками для развития ДВС-синдрома в раннем послеоперационном периоде у пациентов 2-й группы.
Исследование тромбоцитарного звена гемостаза после ОТП характеризуется наличием низкого уровня тромбоцитов в обеих группах в течение всех 7-и суток. При этом более выраженная тромбоцитопения и медленный рост содержания клеток отмечался во 2-й группе пациентов по сравнению с 1-й. Однако данная разница не являлась статистически значимой. При этом также не было выявлено достоверного отличия в количестве тромбоцитов у пациентов, перенесших ОТП с применением обходного шунтирования и без него.
Однако данная разница не являлась статистически значимой. При этом также не было выявлено достоверного отличия в количестве тромбоцитов у пациентов, перенесших ОТП с применением обходного шунтирования и без него.
У всех оперированных пациентов после операции самый низкий уровень тромбоцитов определялся в 1-е послеоперационные сутки — 63,3±48,8х109/л. К 3-м суткам регистрировалась тенденция к увеличению количества тромбоцитов до 69,3±55х109/л, и только к 7-м суткам отмечено достоверное увеличение уровня тромбоцитов до 98,4±53,6х109/л (р<0,05).
Степень выраженности тромбоцитопеиии после операции у пациентов с различной этиологией цирроза также отличалась. У пациентов с циррозами вирусной В и С этиологии определялось наименьшее количество тромбоцитов в 1-е (52,5± 16,4×109/л и 57,5±38,4х109/л) и 3-й (48,7±19,4х109/л и 62±44,9х109/л) послеоперационные сутки (р<0,05).
При трансплантации донорская печень подвергается воздействию таких факторов, как холодовая и тепловая ишемия, снижение перфузии на фоне возможной гипотонии и кровопотери. Поэтому в послеоперационном периоде большое значение приобретает понятие реперфузионо-ишемического повреждения трансплантата. Степень его выраженности оценивается по шкале цитолиза, то есть по максимальному значению аминотрансфераз в первые 48 часов после трансплантации.
Предположив, что степень реперфузионного повреждения трансплантата может влиять на показатели свертывающей и противосвертывающей систем,
мы выделили группы пациентов в зависимости от уровня АЛАТ и АСАТ. В группу с НСРП вошли больные с максимальным уровнем АЛАТ и АСАТ до 1000 ЕД в 1-3 послеоперационные сутки. В группу с ВСРП были включены больные с максимальным уровнем АЛАТ и АСАТ >1000 ЕД в 1-3 сутки.
У пациентов с ВСРП отмечалось достоверно большее отклонение от нормы показателей ПВ, АПТВ, фибриногена и протеина С. На 3-й сутки в группе с ВСРП ПВ соответствовало — 60,5±23%, а в группе с НСРП — 74,7±23,7% (р<0,05). На 7-е сутки этот показатель в группе с ВСРП был равен 63,5±25,9%, а с НСРП — 83,4±15,7% (р<0,05). На 3-й сутки после трансплантации регистрировалось удлинение АПТВ в группе с ВСРП — 50,6±24,4 сек, в сравнении с НСРП — 40,3±12 сек (р<0,05). Фибриноген в группе с ВСРП в 1-е сутки после операции соответствовал 1,5±0,8 г/л, а в группе с НСРП — 2,2±038 г/л (р<0,05). Статистически значимо ниже, чем в группе с НСРП, у пациентов с ВСРП был уровень протеина С на 7-е сутки — 82,6±27% и 107,7±36,3% соответственно (р<0,05).
На 7-е сутки этот показатель в группе с ВСРП был равен 63,5±25,9%, а с НСРП — 83,4±15,7% (р<0,05). На 3-й сутки после трансплантации регистрировалось удлинение АПТВ в группе с ВСРП — 50,6±24,4 сек, в сравнении с НСРП — 40,3±12 сек (р<0,05). Фибриноген в группе с ВСРП в 1-е сутки после операции соответствовал 1,5±0,8 г/л, а в группе с НСРП — 2,2±038 г/л (р<0,05). Статистически значимо ниже, чем в группе с НСРП, у пациентов с ВСРП был уровень протеина С на 7-е сутки — 82,6±27% и 107,7±36,3% соответственно (р<0,05).
Кроме того, результаты нашего исследования показали взаимосвязь между степенью реперфузионно-ишемических повреждений трансплантированной печени и динамикой количества тромбоцитов в послеоперационном периоде. Так, на 7-е сутки после трансплантации печени: у пациентов с НСРП уровень тромбоцитов был статистически значимо выше, чем при ВСРП -117,4±54,2х109/л и 90,2±74,2хЮ’/л соответственно (р<0,05).
Анализируя полученные данные можно сказать, что динамика факторов свертывания и естественных антикоагулянтов в раннем послеоперационном периоде может быть обусловлена степенью реперфузионно-ишемических повреждений трансплантата. Это приводит к нарушению синтетической функции печени.
Кроме того, адгезия и секвестрация тромбоцитов в трансплантате после восстановления кровотока в нем оказывают влияние на количество тромбоцитов в послеоперационном периоде. Достоверная разница в уровне тромбоцитов на 7-е сутки указывает на то, что синтетическая функция печени
при ВСРП восстанавливается медленнее, это, вероятно, влияет на синтез тромбопоэтина и обуславливает продолжительность тромбоцитопении.
Несомненно, что функция трансплантата оказывает существенное влияние на систему гемокоагуляции после операции. С целью оценки прогностической значимости различных параметров гемостаза в отношении развития послеоперационных осложнений и исхода операции была изучена динамика показателей у пациентов трех групп в послеоперационном периоде. 1-я группа включала больных с неосложненным послеоперационным периодом, 2-я группа — пациентов с осложненным течением послеоперационного периода, в 3-ю группу вошли пациенты, умершие в течение 90 суток после трансплантации печени. Среди осложнений были бактериальные и грибковые инфекции, кровотечение и острая почечная недостаточность.
Анализ ПВ указывал на статистически значимое снижение ПВ (%) у всех пациентов в 1-е сутки после трансплантации по сравнению с предоперационным уровнем. У всех пациентов ПВ в динамике увеличивалось, но только в 1-й и 2-й группах оно нормализовалось к 7 суткам. При этом во 2-й группе — едва достигало нижней границы нормы — 71,2±23,6 %. В 3-й группе ПВ оставалось ниже нормы и на 7-е сутки. Во 2-й и 3-й группе на 7-е сутки отмечены достоверно более низкие показатели ПВ — 71,2±23,6 % и 59,5±25% соответственно при сравнении с 1-й группой пациентов — 81,3±14% (р<0,05).
В 1-е сутки после операции у пациентов всех групп регистрировалось максимальное удлинение АПТВ. В динамике в 1-й группе этот показатель достигал нормы к 7-м суткам — 35,7±8,7 сек. По сравнению с 1-й группой АПТВ статистически значимо выше было во 2-й группе на 3-й сутки, а в 3-й группе -как на 3-й, так и на 7-е сутки: 50±22,7 сек, 61,4±28,1 сек и 50,3±17,2 сек соответственно (р<0,05).
На 7-е сутки регистрировался статистически значимо низкий уровень фибриногена в 3-й группе при сравнении с показателями 1-й группы. В 1-й и 2-й группах к 7-м суткам после операции отмечалась нормализация показателей протеина С и антитромбина III. При этом в 3-й группе к этому времени
определялось статистически значимо низкое содержание протеина С и антитромбина III по сравнению с 1-й и 2-й группами.
Следует отметить, что уровень РКФМ значимо повышался во всех группах, но только в 1-й группе отмечалась тенденция к его снижению на 7-й день, а во 2-й и 3-й группах отмечался его дальнейший рост. Учитывая активацию внутрисосудистого свертывания, пациентам с целью профилактики тромбоза сосудистых анастомозов, при уменьшении АПТВ до 40 сек (как правило, к 3-м суткам), назначали низкомолекулярные гепарины.
Анализ тромбоцитарного звена гемостаза показал наличие выраженной тромбоцитопении в 1-е сутки после операции во всех группах (табл. 9). Однако явная положительная динамика в росте количества клеток определялась в 1-й группе к 7-м суткам — 113,4±58,5хЮ9/л. Во 2-й группе к этому времени количество тромбоцитов было достоверно ниже — 89,7±43,6х109/л (р<0,05). В 3-й группе увеличения уровня тромбоцитов к 7-м суткам не было. Данный показатель и на 3-й, и на 7-е сутки был статистически значимо ниже при сравнении с 1-й и со 2-й группой.
Из 80 больных 10 умерли в течение 90 дней после трансплантации печени. При этом количество тромбоцитов перед трансплантацией у этих пациентов статистически значимо не отличалось. Тромбоцитопения в послеоперационном периоде у умерших была более выражена (см. табл. 9).
В то время как у выживших пациентов после трансплантации уровень тромбоцитов практически достигал предоперационного к 7-му дню, у умерших этот показатель был достоверно ниже предоперационного в 1-е сутки и продолжал снижаться в дальнейшем. Таким образом, можно предположить, что стойкая тромбоцитопения в послеоперационном периоде является плохим прогностическим признаком исхода оперативного вмешательства.
Таблица 9
Периоперационные показатели тромбоцитарного гемостаза у пациентов в зависимости от исхода операции (М±о)
Показатель Группа 1 (п=39) Группа 2 (п=31) Группа 3 (п=10)
До операции 1 сутки 3 сутки 7 сутки До операции 1 сутки 3 сутки 7 сутки До операции 1 сутки 3 сутки 7 сутки
Уровень тромбоцитов, х109/л 126,5± 91,6 56,5± 49,9 75,5± 57,7 113,4± 58,5 130,6± 76,7 64,4± 48 68,8± 56,6 89,7± 43,6* 91,2± 60,2 48,7± 30 45,1± 29,2** 57,7± 40,6**
Примечание: * — достоверность различий между группами 1 и 2 (р<0,05),
** — достоверность различий между группами 1,2 и 3 (р<0,05).
У 18,8% (15 из 80) пациентов биопсия показала отторжение в первый месяц после ОТП. В первые сутки после операции у этик больных уровень тромбоцитов в среднем составил 60,4±52,8х109/л. У 33% пациентов этой группы (5 из 15) этот показатель был <40х109/л.
У пациентов с отторжением по сравнению с другими больными количество тромбоцитов было значительно ниже и на 7-е сутки после операции (в среднем 73,3±41,7х109/л и 118,4±49,9х109/л соответственно). У 4 из 5 пациентов с тромбоцитопенией <40×109/л крайне низкий уровень тромбоцитов предшествовал или совпадал с эпизодом отторжения, средний интервал между наименьшим уровнем тромбоцитов и последующим отторжением составлял 3 дня (0-5 дней).
Развитие осложнений после операции зарегистрировано у 31 (38,8%) больного. Среди этих пациентов инфекционные осложнения в послеоперационном периоде отмечались у 13 (42%) человек. По нашим данным, это имело место именно в группе с низким количеством тромбоцитов после операции. При этом тромбсцитопения носила стойкий характер. Так, на момент развития бактериальной или грибковой инфекции после операции средний показатель количества тромбоцитов составлял 48,9±36,7х109/л. У пациентов без осложнений уровень тромбоцитов к этому сроку был -78,4±57,3х109/л (р<0,05). Следует отметить, что развитию инфекционных осложнений у всех 13 пациентов всегда предшествовал эпизод снижения тромбоцитов, даже если к 7-м суткам намечалась тенденция к их росту.
У 10 (12,5%) пациентов ранний послеоперационный период осложнился развитием кровотечения (в виде кровотечения по дренажам из брюшной полости и желудочно-кишечного кровотечения). Консервативная гемостатическая терапия, включающая переливание компонентов донорской крови, апротшшн, не имела эффекта у 2 (2,5%) пациентов, которым была выполнена релапаротомия с последующей хирургической остановкой кровотечения.
У 7 (8,8%) пациентов в раннем послеоперационном периоде применяли с гемостатической целью РФ Vila в дозе 80-90 мкг/кг. В 6 наблюдениях из 7 это позволило эффективно остановить кровотечение в ближайшем послеоперационном периоде и избежать повторного хирургического вмешательства у тяжелых пациентов с нарушениями гемокоагуляции после трансплантации печени. В одном случае, когда кровотечение продолжалось на фоне выраженной тромбоцитопении, эффективность препарата снижалась. Вероятно, это было связано с тем, что действие Vila фактора определяется присутствием активированных тромбоцитов.
Таким образом, определение показателей гемостаза у пациентов с циррозом печени является неотъемлемой частью обязательного обследования перед трансплантацией печени. Нарушения свертывания крови при циррозе печени в сочетании с особенностями самой ОТП могут приводить к возникновению массивного интраоперационного кровотечения. Применение во время трансплантации печени определенной кровосберегающей тактики позволяет снизить риск возникновения массивной кровопотери и уменьшить использование аллогенных компонентов крови. После ОТП сохраняется опасность развития как гипокоагуляционного кровотечения и ДВС-синдрома, так и тромбоза печеночных сосудов. Поэтому тщательный контроль динамики показателей гемостаза позволяет не только вовремя выявлять данные нарушения, но и предусмотреть развитие осложнений в послеоперационном периоде.
ВЫВОДЫ
1. У пациентов с тяжестью цирроза класса С по Чайлду-Пью в предоперационном периоде по сравнению с циррозами В класса имеются статистически значимые: снижение уровня естественных антикоагулянтов (протеина С и антитромбина III), повышение уровня растворимых комплексов фибрикмономера и гипофибриногенемия, которые указывают на наличие ДВС-синдрома у данной категории больных. При этом уровень тромбоцитов
статистически значимо ниже у пациентов с циррозами печени вирусной этиологии.
2. В интраоперационном периоде трансплантации печени этап венозной реперфузии трансплантата сопровождается снижением коагуляционного потенциала крови, что проявляется статистически значимым удлинением активированного времени свертывания и требует своевременной коррекции.
3. Предоперационная гиперволемическая гемодилюция в объеме не более 7 мл/кг позволяет уменьшить объем кровопотери и снизить потребность в переливании компонентов донорской крови при трансплантации печени.
4. Состояние системы гемостаза в раннем послеоперационном периоде определяется исходной степенью тяжести цирроза, этиологией заболевания и степенью реперфузионно-ишемических повреждений трансплантата. У пациентов с циррозом класса С по Чайлду-Пыо в течение 7 суток после операции сохраняется отклонение от нормы всех показателей как свертывающей, так и противосвертывающей систем. Высокая степень реперфузионно-ишемических повреждений сопровождается в течение 3-7 суток статистически значимым снижением протромбинового времени и активированного времени свертывания. У больных с высокой степенью реперфузионно-ишемических повреждений, а также циррозом вирусной этиологии сохраняется статистически значимая тромбоцитопения.
5. Динамика показателей протромбинового времени, активированного парциального тромбопластинового времени, уровня фибриногена и тромбоцитов в раннем послеоперационном периоде позволяет достоверно судить о функции трансплантата и прогнозировать развитие послеоперационных осложнений и исход трансплантации печени.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1. Контроль показателей плазменного, тромбоцитарного гемостаза и противосвертывающей системы у пациентов с циррозом перед трансплантацией печени является обязательным в плане предоперационного обследования.
2. Наличие изменений в системе гемокоагуляции у пациентов с циррозом печени требует профилактической корригирующей терапии. С этой целью перед операцией при уменьшении протромбинового времени ниже 50% назначают викасол в дозе 90 мг/сут на протяжении 1-2 недель. Больным с уровнем НЬ ниже 100 г/л назначают эритропоэтин в терапевтической дозировке.
2. Определение АВСК при помощи автоматического коагуло-хронометра на основных этапах оперативного вмешательства, при кровопотере, регистрации диффузной кровоточивости, позволяет контролировать нарушения в системе гемостаза в интраоперационом периоде.
3. Свежезамороженная плазма при трансплантации печени назначается только при массивной кровопотере и выраженном дефиците факторов свертывания. АВСК>180сек является основным ориентиром для трансфузии свежезамороженной плазмы как в интра-, так и в послеоперационном периоде.
4. Использование аппаратной реинфузии аутокрови является обязательным методом кровосбережения при трансплантации печени.
5. Рекомбинантный фактор Vila — эффективное средство терапии кровотечений при трансплантации печени. Его использование позволяет уменьшить кровопотерю и нормализовать гемостаз.
6. С третьих послеоперационных суток с целью профилактики тромбоза печеночных сосудов показано назначение профилактических доз низкомолекулярных гепаринов (фраксипарин) под контролем уровня АПТВ, при нормализации показателей тромбоцитарного гемостаза к 7-м суткам назначаются препараты ацетилсалициловой кислоты.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО МАТЕРИАЛАМ ДИССЕРТАЦИИ
1. Кузнецова Н.К., Журавель C.B., Чжао А.В., Киселев В.В. Опыт коррекции нарушений гемостаза при ОТО// Материалы 3-ей Сессии МНОАР 22 марта 2002. Москва.:2007; стр.
2. Чжао A.B., Журавель C.B., Кузнецова Н.К., Чугунов А.О., Андрейцева О.И. Какие из показателей дооперационного обследования пациента являются прогностическими для интраоперационного переливания компонентов крови при ортотопической аллотрансплантации печени?// Материалы 4-й сессии МНОАР, 28 марта 2003 г., Москва, стр. 49.
3. Принципы «бескровной» хирургии при операциях на печени, (соавт. Чжао A.B., Журавель C.B., Чугунов А.О., Джаграев K.P., Кобзева E.H.) Анналы хирургической гепатологии, том 9, 2004, № 1, с.20-24.
4. «Бескровная» хирургия печени, (соавт. Чжао A.B., Журавель C.B., Чугунов А.О., Джаграев K.P., Кобзева E.H.) Анналы хирургической гепатологии, том 9,2004, № 2, с. 246-247.
5. Кровосберегающие технологии при операциях на печени, (соавт. Чжао A.B., Журавель C.B., Чугунов А.О., Джаграев K.P., Кобзева E.H., Дорофеева E.H.) Вестник Российского университета дружбы народов. Серия медицина, 3 (31), 2005, стр.68-71.
6. Нарушение гемостаза и его коррекция при операциях на печени, (соавт. Гуляев В.А., Журавель C.B., Чжао A.B., Годков М.А.) Анналы хирургической гепатологии, 2005, №1, стр. 122-130.
7. Recombinant activated factor VU in liver transplantation, (et Juravel S.V., Zhao A.V.) 19th Annual Congress European Society of Intensive Care Medicine. Barselona, Spain. 24-26 September 2006. P. 61.
8. Минимизация использования компонентов донорской крови при трансплантации печени, (соавт. Чжао A.B., Журавель C.B., Чугунов А.О., Джаграев K.P., Кобзева E.H.) Материалы конференции «Клиническая трансплантация органов (актуальные вопросы)», Москва, 26-27 сентября 2007, C.95-9Ó.
9. Трансфузия компонентов крови при ортотопической трансплантации печени, (соавт. Чжао A.B., Тимербаев В.Х., Журавель C.B.) Общая реаниматология, 2007, Том III, №4, стр. 28-31.
Подписано в печать: 09.11.2009
Заказ № 2951 Тираж — 100 экз. Печать трафаретная. Типография «11-й ФОРМАТ» ИНН 7726330900 115230, Москва, Варшавское ш., 36 (499) 788-78-56 www.autoreferat.ru
Биохимический анализ крови на цирроз печени
Биохимический анализ крови на цирроз печени врач назначают в первую очередь. Данное заболевание представляет собой замещение нормальной ткани органа фиброзной. Процесс сопровождается изменением размеров печени в меньшую или большую сторону, увеличением плотности и появлением бугристости. Данные признаки выявляются при осмотре у врача и на ультразвуковом исследовании. Лабораторная диагностика указывает на функциональные изменения. Для точности анализы необходимо совмещать с иными методами обследования.
Анализ крови на биохимию у пациентов с компенсированным заболеванием модет давать результаты в пределах нормы, но также возможно небольшое увеличение активности трансаминаз в сыворотке или гамма-глутамилтранспептидазы. Декомпенсированная форма сопровождается симптомами:
- портальной гипертензии — увеличение давления в системе воротной вены из-за закупорки внутри-, внепеченочных сосудов,
- печеночной недостаточности — синдром, включающий нарушение нескольких функций печени.
При циррозе печени биохимическое исследование крови показывает:
- увеличение билирубина, гамма-глобулинов,
- уменьшение альбуминов, протробина, холестерина.
Значения теста существенно связаны с активностью процесса.
Так, если пациент сдает комплексные анализы, например, биохимический и клинический, то второй при активном циррозе печени показывает:
- анемию,
- лейкопению,
- тромбоцитопению.
В результатах биохимического теста у 90 процентов больных активность аминотрансфераз увеличена в 2-5 раз. Билирубин также превышает норму минимум в два раза.
У пациентов с алкогольным поражением печени в большей мере увеличена активность гамма-глутамилтрансферазы. Если при подозрении на вирусные циррозы сдать анализы на маркеры гепатитов, то тесты будут положительными. Показатель вируса гепатита D обнаруживается при наиболее выраженных вирусных циррозах.
Биохимический анализ крови при низкоактивном циррозе показывает отклонения от нормы в 30-50 процентах случаев. Концентрация общего билирубина выше в 1,5-2 раза, активность — в 1,5-4 раза. Снижен протромбиновый индекс.
Цирроз — это многофакторное заболевание, которое по мере развития приводит к иммуновоспалительному процессу. Поэтому в дополнение к биохимическому анализу на цирроз печени врач может назначить иммунологическое исследование. Оно показывает уменьшение активности Т-лимфоцитов, образование антител к паренхиме, увеличение концентрации иммуноглобулинов.
В «Литех» проводят комплексные обследования. У нас Вы можете сделать все необходимые анализы и получить заключение специалистов.
Тромбоцитопения: Симптомы, диагностика и лечение
Тромбоцитопения — это термин, обозначающий все состояния, при которых снижено количество тромбоцитов в крови. Человек может чувствовать себя вполне нормально, однако, такое состояние при тромбоцитопении опасно, так как в любой момент может произойти внутреннее кровотечение любых органов, а самое опасное то, что может случиться кровоизлияние в мозг.
Патология встречается чаще у женщин,чем у мужчин. Частота выявления у детей — один случай на 20 тысяч.
Причины
Зачастую причиной заболевания является аллергическая реакция организма на различные медицинские препараты в итоге чего и наблюдается лекарственная тромбоцитопения. При таком недомогании наблюдается выработка организмом антител, направленных против лекарственного препарата. К лекарственным препаратам, влияющим на появление кровеносной недостаточности телец, относятся седативные, алкалоидные и антибактериальные средства.
Причинами возникновения недостаточности могут быть и проблемы с иммунитетом, вызванные последствиями переливаний крови. Особенно часто заболевание проявляется при несовпадении групп крови.
Чаще всего наблюдается в организме человека аутоиммунная тромбоцитопения. В таком случае иммунитет неспособен к распознаванию своих тромбоцитов и отторгает их из организма. В результате отторжения происходит выработка антител по удалению чужеродных клеток.
Если же недуг имеет выраженную форму изолированной болезни, то он именуется идиопатической тромбоцитопенией или заболеванием Верльгофа. Считается, что такая тромбоцитопения возникает на фоне наследственной предрасположенности.
Также свойственно проявление заболевания при наличии врождённого иммунодефицита.
Недостаток тромбоцитов в организме наблюдается у людей, с пониженным составом витамина В12 и фолиевой кислоты. Не исключается и чрезмерное радиоактивное или лучевое воздействие для появления недостаточности кровяных телец.
Симптомы
Обычно первым сигналом снижения уровня тромбоцитов служит появление кожных кровоизлияний при незначительном травмировании (ударе, сдавлении) мягких тканей. Больные отмечают частое возникновение синяков, специфической мелкоточечной сыпи на теле и конечностях, кровоизлияний в слизистые оболочки, повышенную кровоточивость десен и т. п.
На следующем этапе отмечается увеличение времени кровотечения при незначительных порезах, длительные и обильные менструальные кровотечения у женщин, появление экхимозов в местах инъекций. Кровотечение, вызванное травмой или медицинской манипуляцией (например, удалением зуба) может продолжаться от нескольких часов до нескольких суток.
При значительном снижении количества тромбоцитов возникают спонтанные кровотечения (носовые, маточные, легочные, почечные, желудочно-кишечные), выраженный геморрагический синдром после хирургических вмешательств. Профузные некупируемые кровотечения и кровоизлияния в мозг могут стать фатальными.
Диагностика
Прежде всего, при подозрении на тромбоцитопению необходимо сделать общий анализ крови для определения количества клеточных элементов и верификации (подтверждения) диагноза тромбоцитопения.
Многие заболевания, протекающие с тромбоцитопенией, имеют достаточно яркие симптомы, поэтому дифференциальная диагностика в таких случаях не представляет большого труда. Это касается, в первую очередь, тяжелых онкологических патологий (лейкозы, метастазы злокачественных опухолей в костный мозг, миеломная болезнь и т.п.), системных заболеваний соединительной ткани (системная красная волчанка), цирроза печени и т.п.
Однако нередко необходимо проведение дополнительных исследований (пункция костного мозга, иммунологические пробы и т.п.).
Лечение
Кровотечения при легкой степени тромбоцитопении не развиваются. Медикаментозное лечение, как правило, не требуется. Рекомендуется выжидательная тактика и установление причины снижения тромбоцитов.
При средней тяжести заболевания возможно появление кровоизлияний в слизистую оболочку рта, повышение кровоточивости десен, учащение носовые кровотечений. При ушибах и травмах могут образовываться обширные кровоизлияния в кожу, не соответствующие объему повреждения. Медикаментозная терапия рекомендуется только в случае наличия факторов, повышающих риск развития кровотечений (язв желудочно-кишечной системы, профессиональной деятельности или спорта, связанного с частыми травмами).
При тромбоцитопении средней степени тяжести без выраженных проявлений геморрагического синдрома назначается лечение на дому. Пациентам рекомендуется ограничить активный образ жизни на период лечения и принимать все медикаменты, назначенные гематологом.
Обязательной госпитализации подлежат пациенты с тяжелой степенью тромбоцитопении. Таким больным, помимо медикаментозного, могут быть назначены различные терапевтические и хирургические мероприятия, направленные на устранение тромбоцитопении и вызвавших ее причин.
Дополнительными методами лечения тромбоцитопении являются: трансфузионная терапия (переливание пациенту донорской крови, плазмы либо тромбоцитов), удаление селезенки и пересадка костного мозга.
Тромбоцитопения, связанная с хроническим заболеванием печени
Тромбоцитопения (количество тромбоцитов <150 000 / мкл) - частое осложнение у пациентов с хроническим заболеванием печени (ХЗП), которое наблюдается у 76% пациентов. Умеренная тромбоцитопения (количество тромбоцитов от 50 000 / мкл до 75 000 / мкл) встречается примерно у 13% пациентов с циррозом печени. Множественные факторы могут способствовать развитию тромбоцитопении, включая секвестрацию тромбоцитов селезенки, подавление костного мозга хронической инфекцией гепатита С и противовирусное лечение с помощью терапии на основе интерферона.Снижение уровня или активности кроветворного фактора роста тромбопоэтина (ТПО) также может иметь значение. Тромбоцитопения может повлиять на рутинный уход за пациентами с ХЗП, потенциально откладывая или препятствуя диагностическим и терапевтическим процедурам, включая биопсию печени, противовирусную терапию, а также хирургические вмешательства по медицинским показаниям или плановые операции. Терапевтические варианты для безопасного и эффективного повышения уровня тромбоцитов могут существенно повлиять на уход за этими пациентами. Несколько многообещающих новых агентов, которые стимулируют ТПО и повышают уровень тромбоцитов, такие как пероральный фактор роста тромбоцитов элтромбопаг, в настоящее время разрабатываются для профилактики и / или лечения тромбоцитопении.Способность повышать уровень тромбоцитов может значительно снизить потребность в переливании тромбоцитов и облегчить использование противовирусной терапии на основе интерферона и других назначенных с медицинской точки зрения методов лечения у пациентов с заболеванием печени.
Сокращения
ITP
Иммунная тромбоцитопеническая пурпура
TIPSS
Трансъюгулярный внутрипеченочный портосистемный стент-шунт
ВИЧ
Вирус иммунодефицита человека
PTT
Частичное тромбопластиновое время
PEG-rO0003Рекомендованный человеческий фактор роста
0003Регулированный рекомбинантный фактор роста
0003 pEG-rO0003 Ключевые слова
Хроническая болезнь печени
Цирроз
Цитопения
Тромбоциты
Тромбоцитопения
Тромбопоэтин
Переливание тромбоцитов
Рекомендуемые статьи Цитирующие статьи (0)
Опубликовано Elsevier Ireland Ltd.
Рекомендуемые статьи
Цитирующие статьи
Текущее лечение тромбоцитопении при хроническом заболевании печени — гастроэнтерология и гепатология
G&H Насколько распространена тромбоцитопения у пациентов с хроническим заболеванием печени?
RB Тромбоцитопения, определяемая как количество тромбоцитов ниже 150 000 / мкл, вероятно, является наиболее частым осложнением прогрессирующего заболевания печени или цирроза.Это состояние обычно возникает до клинических проявлений, связанных с декомпенсацией (например, асцитом или энцефалопатией), и часто является первым признаком хронического заболевания печени. Фактически, низкое количество тромбоцитов используется в качестве клинического диагностического инструмента для выявления цирроза и включается в показатели соотношения аспартатаминотрансферазы и тромбоцитов и показатели фиброза-4, а также во все неинвазивные методы анализа крови для диагностики продвинутых заболевание печени.
G&H Какова патофизиология тромбоцитопении при хроническом заболевании печени?
РБ Патофизиология многофакторна.Портальная гипертензия приводит к спленомегалии, а затем к секвестрации тромбоцитов в селезенке. Кроме того, уровни тромбопоэтина у пациентов с хроническим заболеванием печени низкие, что приводит к снижению выработки тромбоцитов. Сочетание повышенной секвестрации и снижения продукции приводит к низкому количеству тромбоцитов, которое, как правило, коррелирует как со степенью портальной гипертензии, так и со степенью дисфункции печени. Другими словами, чем больше дисфункция печени, тем ниже уровень тромбопоэтина, а также тем больше у пациентов с портальной гипертензией, что приводит к прогрессирующей тромбоцитопении.
G&H Всегда ли следует применять профилактические меры у пациентов с тромбоцитопенией и хроническим заболеванием печени, которые подвергаются процедуре с риском кровотечения?
РБ Это спорный вопрос. Рекомендации по применению профилактических мер должны зависеть как от степени тромбоцитопении, так и от риска кровотечений, связанных с запланированной процедурой. Однако большинство рекомендаций было составлено без конкретных данных или основано на экстраполяции пациентов с гематологическими нарушениями и тромбоцитопенией, у которых риск кровотечения выше из-за отсутствия тромбоцитов из-за недостаточности костного мозга.Для процедур с повышенным риском (например, оперативных) обычно используется порог подсчета тромбоцитов 100 000 / мкл. Для менее инвазивных процедур используется порог количества тромбоцитов 50 000 / мкл. Для процедур с промежуточным риском (например, биопсия печени) некоторые врачи используют промежуточный порог подсчета тромбоцитов, например 75 000 / мкл. Однако эти пороговые значения не основаны на высококачественных данных, и нет четкого консенсуса в отношении оптимального подхода к оценке риска перипроцедурных кровотечений, что приводит к непоследовательной практике.Тем не менее, мы знаем, что пациенты с более низким количеством тромбоцитов имеют повышенный риск кровотечения и что следствие также вероятно верно: если количество тромбоцитов может быть эффективно и безопасно увеличено, риск кровотечения в некоторой степени снизится.
G&H Каковы текущие варианты ведения пациентов с хроническим заболеванием печени, страдающих тромбоцитопенией и перенесших инвазивную процедуру?
RB Золотым стандартом традиционно было переливание тромбоцитов, но у этого подхода есть несколько недостатков.Он включает в себя переливание продуктов крови, что может быть связано с реакциями переливания, является дорогостоящим и со временем становится менее эффективным из-за аллосенсибилизации. Кроме того, экзогенных тромбоцитов часто не хватает на время процедуры, не говоря уже о всем периоде риска кровотечения, который может длиться до 1 недели после процедуры. Таким образом, переливания тромбоцитов часто избегают из-за отсутствия явного положительного эффекта и возможности побочных эффектов, что приводит к необходимости альтернативных вариантов лечения, таких как аналоги тромбопоэтина.
Преимущества аналогов тромбопоэтина заключаются в том, что они обладают длительным действием (с продолжительностью увеличения количества тромбоцитов более 3 недель) и более предсказуемы с точки зрения увеличения количества тромбоцитов. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило аналоги тромбопоэтина второго поколения аватромбопаг (Doptelet, Dova Pharmaceuticals) и лусутромбопаг (Mulpleta, Shionogi) в мае и июле 2018 г. соответственно для лечения тромбоцитопении у пациентов с хроническим заболеванием печени, подвергающихся инвазивной терапии. процедуры.Эти агенты имеют структурные различия, но их механизмы действия схожи. Оба связываются с рецептором тромбопоэтина неконкурентным образом. Аналоги тромбопоэтина первого поколения элтромбопаг (Promacta, Novartis) и ромиплостим (Nplate, Amgen) не были одобрены FDA для лечения тромбоцитопении у пациентов с хроническим заболеванием печени, и предыдущие клинические испытания элтромбопага у пациентов с хроническим заболеванием печени были безопасны. вопросы, связанные с тромбозом воротной вены.Однако, несмотря на то же предупреждение FDA, в клинических испытаниях агентов второго поколения не наблюдалось избыточного свертывания крови, и было показано, что они безопасны и эффективны при предотвращении переливания тромбоцитов при инвазивных процедурах у пациентов с хроническим заболеванием печени. На мой взгляд, аватромбопаг и лусутромбопаг станут новым стандартом лечения тромбоцитопении у этой популяции пациентов.
G&H Какие основные результаты исследования привели к недавнему одобрению FDA аватромбопага и лусутромбопага?
RB Оба эти агента были одобрены на основании результатов 2 рандомизированных двойных слепых плацебо-контролируемых исследований фазы 3 (ADAPT-1 и -2 для аватромбопага и L-PLUS 1 и 2 для лусутромбопага, с 300- 400 пациентов, включенных в каждую группу исследований).Исследования имели похожий дизайн в том смысле, что они включали пациентов с тромбоцитопенией (определяемых как количество тромбоцитов ниже 50 000 / мкл), которые подвергались инвазивным процедурам, в которых планировалось переливание тромбоцитов, и пациенты были рандомизированы по препарату против плацебо. Было показано, что оба агента снижают процент пациентов, нуждающихся в переливании тромбоцитов, и увеличивают количество тромбоцитов статистически значимым образом по сравнению с плацебо, при этом у большого числа пациентов наблюдается постоянное увеличение до более чем 50 000 / мкл.Относительная доля пациентов, получавших переливание тромбоцитов, была примерно одинаковой, и оба агента снижали вероятность получения переливания тромбоцитов примерно на 50%.
G&H Насколько безопасны эти агенты? Какие побочные эффекты были обнаружены в исследованиях?
RB Безопасность была одинаковой для обоих агентов, без увеличения тромботических событий по сравнению с плацебо. Их общие профили побочных эффектов не сильно отличались от плацебо, а наблюдаемые побочные эффекты были довольно легкими.Кроме того, количество пациентов с побочными эффектами было одинаковым для препарата и плацебо. В обоих наборах клинических испытаний пациенты испытали побочные эффекты, потому что у них был цирроз печени и они проходили процедуры, но побочные эффекты были достаточно сбалансированы между группами лечения и плацебо, что демонстрирует важность наличия группы плацебо.
G&H Как дозировали аватромбопаг и лусутромбопаг?
RB Аватромбопаг вводили в течение 5 дней, и доза варьировалась в зависимости от того, было ли у пациента количество тромбоцитов ниже 40 000 / мкл или от 40 000 / мкл до 50 000 / мкл (последняя группа получала более низкую дозу).Лусутромбопаг вводили в течение 7 дней в одинаковой дозе всем пациентам.
G&H В исследованиях, как долго длилось действие агентов?
RB Для аватромбопага максимальный эффект наблюдался между 10 и 13 днями, а количество тромбоцитов, как правило, возвращалось к исходному уровню к 35-му дню. Лусутромбопаг имел аналогичные результаты, причем максимальный эффект наблюдался между 9 и 14 днями, а количество тромбоцитов имело тенденцию. вернуться к исходному уровню примерно через месяц.
G&H Необходимо ли обследование пациента перед введением этих агентов?
RB Из-за риска тромботических событий кровоток в воротной вене оценивался в большинстве клинических испытаний. Однако этикетки не требуют оценки проходимости воротной вены перед использованием агентов. В своей клинической практике я удостоверяюсь, что скрининг гепатоцеллюлярной карциномы соответствует современным требованиям, потому что он показан всем пациентам с циррозом, а визуализация, необходимая для скрининга, включает возможность оценки проходимости воротной вены.Помимо обычного анализа крови, это объем нашей стандартной оценки перед использованием аватромбопага или лусутромбопага.
Когда тромботические события наблюдались с аналогами тромбопоэтина первого поколения, большинство из этих событий происходило, когда количество тромбоцитов было слишком высоким. Таким образом, если есть опасения, потому что количество тромбоцитов у пациента близко к 50 000 / мкл, количество тромбоцитов можно измерить во время процедуры или незадолго до этого, что многие врачи будут делать, чтобы гарантировать адекватный ответ тромбоцитов в рамках своей клинической практики. упражняться.Однако при отсутствии высокого количества тромбоцитов я бы не чувствовал необходимости контролировать наличие постпроцедуры тромбоза воротной вены.
G&H Есть ли противопоказания, связанные с этим лечением?
RB Аналоги тромбопоэтина не следует использовать или следует использовать с большой осторожностью у пациентов, у которых в анамнезе есть тромботические события, и я бы не рекомендовал использовать эти методы лечения у пациентов с тромбозом воротной вены.
G&H В настоящее время широко используются аватромбопаг и лусутромбопаг в клинической практике, или переливание тромбоцитов по-прежнему является стандартом лечения?
RB В моей клинической практике мы используем эти агенты вместо переливания тромбоцитов в выборных ситуациях, когда у нас есть время подождать, пока агенты подействуют. (В экстренной ситуации переливание тромбоцитов — единственный выбор.) Учитывая превосходную эффективность этих агентов и по мере того, как увеличивается осведомленность о них, мы, вероятно, увидим все больше и больше их использования и соответствующее снижение использования переливаний тромбоцитов.По мере того, как мы начинаем привыкать к использованию аналогов тромбопоэтина, теперь мы позволяем пациентам проходить плановые процедуры, которые они не могли пройти ранее из-за тромбоцитопении. Мы также наблюдаем меньше повторных процедур из-за невозможности выполнить терапевтический маневр из-за тромбоцитопении. Например, в прошлом пациенту с тромбоцитопенией, перенесшему колоноскопию, возможно, не удавалось пройти полипэктомию, если врач не был готов провести переливание тромбоцитов, а это означало, что колоноскопию приходилось повторять.Помимо возможности назначения терапии во время начальной процедуры, более широкое использование аналогов тромбопоэтина второго поколения, как мы надеемся, снизит риск инвазивных вмешательств и откроет доступ к плановым процедурам, которые улучшат продолжительность и качество жизни пациентов. .
G&H Каковы следующие шаги в исследовании?
RB Аватромбопаг и лусутромбопаг следует изучать у пациентов с более поздними стадиями заболевания печени и у пациентов с очень низким уровнем тромбоцитов.В вышеупомянутых клинических испытаниях у некоторых пациентов количество тромбоцитов не превышало 50000 / мкл даже с этими агентами, поэтому может потребоваться использование более высоких доз или более длительная продолжительность лечения для достижения увеличения количества тромбоцитов у пациентов с очень низким количеством тромбоцитов, особенно 20000 / мкл и ниже. Кроме того, нам необходимо определить, какие процедуры больше всего выигрывают от лечения аналогами тромбопоэтина и какие процедуры можно безопасно выполнять при более низком количестве тромбоцитов.
Доктор Браун получил поддержку в исследованиях и консультировал компании Dova Pharmaceuticals и Shionogi.В прошлом он работал клиническим исследователем в испытаниях элтромбопага.
Рекомендуемая литература
Афдал Н., Дуггал А., Очиаи Т. и др. Ответ тромбоцитов на лусутромбопаг, агонист рецепторов тромбопоэтина, у пациентов с хроническим заболеванием печени и тромбоцитопенией, подвергающихся неэкстренным инвазивным процедурам: результаты рандомизированного двойного слепого плацебо-контролируемого исследования фазы 3. Кровь . 2017; 130 (приложение 1): 291.
Коричневый RS Jr.Обзорная статья: фармакоэкономический анализ тромбоцитопении при хроническом заболевании печени. Алимент Фармакол Тер . 2007; 26 (приложение 1): 41-48.
Giannini EG, Greco A, Marenco S, Andorno E, Valente U, Savarino V. Частота кровотечений после инвазивных процедур у пациентов с тромбоцитопенией и прогрессирующим заболеванием печени. Clin Gastroenterol Hepatol. 2010; 8 (10): 899-902; викторина e109.
Ким Э.С. Лусутромбопаг: первое глобальное одобрение. Наркотики .2016; 76 (1): 155-158.
Пек-Радосавлевич М. Тромбоцитопения при хроническом заболевании печени. Печень Инт . 2017; 37 (6): 778-793.
Терро Н., Чен Ю.С., Изуми Н. и др. Аватромбопаг перед процедурами снижает потребность в переливании тромбоцитов у пациентов с хроническим заболеванием печени и тромбоцитопенией. Гастроэнтерология . 2018; 155 (3): 705-718.
(PDF) Тромбоцитопения при заболевании печени
Осложнения или пациенты, ожидающие ОТП, чтобы снизить интраоперационную потребность в продуктах крови
.Возможно, наибольшее количество пациентов из группы
—
, интересующихся исследованием, будут пациенты, проходящие курс лечения хроническим гепатитом С интерфероном-альфа
—
интерфероном-альфа. Эффект лечения хроническим гепатитом С интерфероном является причиной снижения дозы или прекращения лечения
у значительного числа пациентов. Как недавно было показано
, терапия интерфероном
препятствует не только продукции тромбоцитов костным мозгом, но и продукции
также ТПО в печени (20).Появляется все больше доказательств того, что более высокие дозы
и увеличенные интервалы лечения могут улучшить вирусологические реакции на
—
(69), и что лечение пациентов с циррозом гепатита С
(ранее не считавшимся группой
, имеет преимущество от терапия интерфероном) может улучшить их жизнеспособность
—
(70,71) и снизить частоту гепатоцеллюлярной карциномы
—
цином (71,72). Следовательно, сильный, но хорошо переносимый тромбопоэтический агент
будет пользоваться большим спросом, такой агент
, как рекомбинантные ТПО человека.Есть надежда, что в будущем
будет доступно для лечения тромбоцитопении при заболеваниях печени.
СПИСОК ЛИТЕРАТУРЫ
1. Янага К., Цакис А.Г., Шимада М. и др. Лечение гиперспленизма
после ортотопической трансплантации печени. Энн Сург 1989; 210: 180-3.
2. Реалди Г., Фаттович Г., Хадзиянис С. и др.
факторов выживаемости и прогноза у 366 пациентов с компенсированным циррозом печени типа B:
— многоцентровое исследование. Исследователи Европейского сообщества
по борьбе с вирусным гепатитом (EUROHEP).J Hepatol 1994; 21: 656-66.
3. Кабрера Дж., Мейнар М., Гранадос Р. и др. Трансъюгулярный внутрипеченочный
портосистемный шунт в сравнении со склеротерапией в плановом лечении
кровотечения из варикозно расширенных вен. Гастроэнтерология 1996; 110: 832-9.
4. Гулис Дж., Армонис А., Патч D, Сабин С., Гринслейд Л., Берроуз А. К..
Бактериальная инфекция независимо связана с неспособностью контролировать кровотечение
у пациентов с циррозом печени и желудочно-кишечным кровотечением.
Гепатология 1998; 27: 1207-12.
5. Базили С., Ферро Д., Лео Р. и др. Время кровотечения не позволяет прогнозировать
желудочно-кишечное кровотечение у пациентов с циррозом печени. Группа CALC.
Нарушения коагуляции при циррозе печени. J Hepatol
1996; 24: 574-80.
6. Clavien PA, Camargo CA Jr, Croxford R, Langer B, Levy GA,
Greig PD. Определение и классификация отрицательных исходов при трансплантации солидных органов
. Применение при трансплантации печени.Энн Сург
1994; 220: 109-20.
7. McVay PA, Toy PT. Отсутствие повышенного кровотечения после биопсии печени у
пациентов с легкими нарушениями гемостаза. Ам Дж. Клин Патол
1990; 94: 747-53.
8. Виоли Ф, Ферро Д., Базили С. и др. Гиперфибринолиз увеличивает риск желудочно-кишечного кровотечения
у пациентов с запущенным циррозом печени.
Гепатология 1992; 15: 672-6.
9. López Morante AJ, Sáez-Royuela F, Casanova Valero F,
Yuguero del Moral L, Martín Lorente JL, Охеда Хименес К.Immune
тромбоцитопения после терапии альфа-интерфероном у пациента с
хроническим гепатитом С. Am J Gastroenterol 1992; 87: 809-10.
10. Файстауэр С.М., Пеннер Э., Майр В.Р., Панцер С. Целевые антигены тромбоцитов
аутоантител у пациентов с первичным билиарным циррозом.
Гепатология 1997; 25: 1343-5.
11. Hoofnagle JH. Тромбоцитопения на фоне терапии интерфероном альфа.
JAMA 1991; 266: 849.
12. Янг Н.С. Флавивирусы и недостаточность костного мозга.JAMA
1990; 263: 3065-8.
13. Hoofnagle JH, di Bisceglie AM. Лечение хронического вирусного гепатита
. N Engl J Med 1997; 336: 347-56.
14. Дуракис С.П., Дойч М., Хадзиянис С.Дж. Иммунная тромбоцитопения
и терапия альфа-интерфероном. J. Hepatol 1996; 25: 972-5.
15. Aster RH. Объединение тромбоцитов в селезенке: роль
в патогенезе «гиперселезеночной» тромбоцитопении. Дж. Клин Инвест
1966; 45: 645-57.
16.Карр Дж. М. Диссеминированная внутрисосудистая коагуляция при циррозе печени.
Гепатология 1989; 10: 103-10.
17. Виоли Ф, Ферро Д., Базили С. и др. Связь между
диссеминированного внутрисосудистого свертывания крови низкой степени злокачественности и эндотоксемией у пациентов
с циррозом печени. Гастроэнтерология 1995; 109: 531-9.
18. Пек-Радосавлевич М., Захерл Дж., Менг Ю.Г. и др. Является ли недостаточное производство тромбопоэтина
основной причиной тромбоцитопении при циррозе печени
? J. Hepatol 1997; 27: 127-31.
19. Мартин Т.Г. III, Сомберг К.А., Мэн Ю.Г., et al. Уровни тромбопоэтина
у пациентов с циррозом печени до и после ортотопической трансплантации печени
. Энн Интерн Мед 1997; 127: 285-8.
20. Пек-Радосавлевич М., Вичлас М., Пидлич Дж. И др. Затупленный ответ тромбопоэтина
на индуцированную интерфероном альфа тромбоцитопению
во время лечения гепатита С. Гепатология 1998; 28: 1424-9.
21. De Gabriele G, Penington DG. Регуляция продукции тромбоцитов:
«гиперспленизм» у экспериментального животного.Br J Haematol
1967; 13: 384-93.
22. Пенни Р., Розенберг М.С., Фиркин Б.Г. Пул тромбоцитов селезенки.
Кровь 1966; 27: 1-16.
23. Русселот Л.М., Панке В.Ф., Боно РФ, Морено А.Х. Опыт работы с портокавальным анастомозом
. Анализ 104 плановых сквозных шунтов для
для предотвращения повторного кровотечения из варикозно расширенных вен пищевода и желудка
(1952–1961). Am J Med 1963; 34: 297-307.
24. Хатсон Д.Г., Зеппа Р., Леви Ю.Ю., Шифф Е.Р., Ливингстон А.С., Финк П.
Влияние дистального спленоренального шунта на гиперспленизм. Энн Сург
1977; 185: 605-12.
25. Mutchnick MG, Lerner E, Conn HO. Влияние портокавального анастомоза
на гиперспленизм. Dig Dis Sci 1980; 25: 929-38.
26. Лоуренс С.П., Лезотт, округ Колумбия, Дарем Дж. Д., Кумпе Д.А., Эверсон Г.Т.,
Билир Б.М. Течение тромбоцитопении хронического заболевания печени после
трансъюгулярных внутрипеченочных портосистемных шунтов (TIPS). Ретроспективный анализ
.Dig Dis Sci 1995; 40: 1575-80.
27. Alvarez OA, Lopera GA, Patel V, Encarnacion CE, Palmaz JC,
Lee M. Улучшение тромбоцитопении из-за гиперспленизма после
трансъюгулярного внутрипеченочного портосистемного шунта у
пациентов с циррозом. Am J Gastroenterol 1996; 91: 134-7.
28. Джалан Р., Рыжий Д.Н., Аллан П.Л., Хейс П.С. Проспективная оценка
гематологических изменений после трансъюгулярного внутрипеченочного
портосистемного стент-шунта (TIPSS).Eur J Gastroenterol Hepatol
1996; 8: 381-5.
29. Пурснани К.Г., Силлин Л.Ф., Каплан Д.С. Влияние трансъюгулярного внутрипеченочного
портосистемного шунта на вторичный гиперспленизм. Am J Surg
1997; 173: 169-73.
30. Wichlas M, Pidlich J, Zacherl J, et al. Продолжающаяся тромбоцитопения
после имплантации TIPS не может быть отнесена к потреблению тромбоцитов
. Гепатология 1997; 26: A2002. (Abst)
31. Джаббур Н., Зайко А., Оронс П., Айриш У., Фунг Дж. Дж., Селби Р. Р..Устраняет ли
трансъюгулярный внутрипеченочный портосистемный шунт (TIPS)
тромбоцитопению, связанную с циррозом? Dig Dis Sci
1998; 43: 2459-62.
32. Кумпе Д.А., Румак С.М., Преториус Д.Х., Стокер Т.Дж., Стеллин Г.П.
Частичная эмболизация селезенки у детей с гиперспленизмом.
Радиология 1985; 155: 357-62.
33. Сангро Б., Бильбао I, Эрреро И. и др. Частичная эмболизация селезенки для лечения гиперспленизма при циррозе печени
.Гепатология 1993; 18: 309-14.
34. Ногучи Х., Хираи К., Аоки Й., Саката К., Таникава К. Изменения кинетики тромбоцитов
после частичной эмболизации селезеночной артерии у
пациентов с циррозом и гиперспленизмом. Гепатология 1995; 22: 1682-8.
35. Робсон С.К., Кан Д., Крускал Дж., Берд А.Р., Кирш Р.Э. Нарушение гемостаза
при внепеченочной портальной гипертензии. Гепатология
1993; 18: 853-7.
36. Райя С., Мис С., Альфиери Ф. младший. Портальная гипертензия при мэнсоник
шистосомоз.Мировой журнал J Surg 1991; 15: 176-87.
37. Rinkes IH, Van der Hoop AG, Hesselink EJ, et al. Обращает ли вспомогательная
гетеротопическая трансплантация печени гиперспленизм и портальную гипертензию
? Гастроэнтерология 1991; 100: 1126-8.
38. Amuasi JH, Ferri P, Grossi A, Vannucchi L, Vannucchi AM,
Ferrini PR. Количественная визуализация тромбоцитов и сравнение четырех математических моделей
для оценки средней продолжительности жизни тромбоцитов у
пациентов с хронической иммунной тромбоцитопенией.Haematologica
1991; 76: 104-8.
39. Harker LA, Finch CA. Тромбокинетика у человека. Дж. Клин Инвест
1969; 48: 963-74.
40. Штейн С.Ф., Харкер Л.А. Кинетические и функциональные исследования тромбоцитов,
фибриногена и плазминогена у пациентов с циррозом печени.
J Lab Clin Med 1982; 99: 217-30.
Can J Gastroenterol Vol 14 Suppl D Ноябрь 2000 г. 65D
Тромбоцитопения при заболевании печени
(PDF) Ведение тромбоцитопении, вызванной циррозом печени: обзор
10.1111 / bcp.12041]
52 Greenberg PL, Garcia-Manero G, Moore M, Damon L, Ro-
boz G, Hu K, Yang AS, Franklin J. Рандомизированное контролируемое исследование
ромиплостима у пациентов с
миелодиспластический синдром низкого или среднего риска, получающий децитабин. Leuk
Лимфома 2013; 54: 321-328 [PMID: 22
2 DOI: 10.3109 / 1
0428194.2012.713477]
53 Kantarjian H, Fenaux P, Sekeres MA, Becker PS, Boruchov
A, Bowen D., Hellstromars-Lindberg E, Lindberg E, , Lyons RM,
Muus P, Shammo J, Siegel R, Hu K, Franklin J, Berger DP.
Безопасность и эффективность ромиплостима у пациентов с миелодиспластическим синдромом и тромбоцитопенией низкого риска. J
Clin Oncol 2010; 28: 437-444 [PMID: 20008626 DOI: 10.1200 /
JCO.2009.24.7999]
54 Мусса М.М., Мовафи Н. Предоперационное применение ромиплостима
у пациентов с тромбоцитопенией, хроническим гепатитом С и циррозом печени
. J Gastroenterol Hepatol 2013; 28: 335-341 [PMID:
22849409 DOI: 10.1111 / j.1440-1746.2012.07246.x]
55 Bussel JB, Cheng G, Saleh MN, Psaila B, Kovaleva L, Med-
deb B, Kloczko J, Hassani H, Mayer B, Stone NL, Arning
М, Прован Д., Дженкинс Дж. М.. Эльтромбопаг для лечения
хронической идиопатической тромбоцитопенической пурпуры. N Engl J Med
2007; 357: 2237-2247 [PMID: 18046028 DOI: 10.1056 / NEJ-
Moa073275]
56 Дженкинс Дж. М., Уильямс Д., Дэн И., Уль Дж., Китчен В., Коллинз
Д., Эриксон-Миллер К.Л.Фаза 1 клинического исследования элтром-
бопага, перорального непептидного агониста рецепторов тромбопоэтина.
Кровь 2007; 109: 4739-4741 [PMID: 17327409 DOI: 10.1182 /
кровь-2006-11-057968]
57 МакХатчисон Дж. Г., Душейко Г., Шиффман М. Л., Родригес-
Торрес М., Сигал С., Бурльер М., Берг Т. , Gordon SC, Campbell
FM, Theodore D, Blackman N, Jenkins J, Afdhal NH. Элтром-
бопаг для лечения тромбоцитопении у пациентов с циррозом печени as-
, ассоциированным с гепатитом С.N Engl J Med 2007; 357: 2227-2236
[PMID: 18046027 DOI: 10.1056 / NEJMoa073255]
58 Afdhal NH, Giannini EG, Tayyab G, Mohsin A, Lee JW,
Andriulli A, Jeffers Han L, McHJutchison J, Jeffers Han L., McHJutchison J KH,
Campbell F, Hyde D, Brainsky A, Theodore D. Eltrombopag
перед процедурами у пациентов с циррозом и тромбо-
цитопенией. N Engl J Med 2012; 367: 716-724 [PMID: 22913681
DOI: 10.1056 / NEJMoa1110709]
59 Мэддисон Ф.Эмболическая терапия гиперспленизма. Invest Radi-
ol 1973; 8: 280-281 [DOI: 10.1097 / 00004424-197307000-00054]
60 Spigos DG, Jonasson O, Mozes M., Capek V. Частичная эмболизация селезенки
при лечении гиперспленизма. AJR Am J
Рентгенол 1979; 132: 777-782 [PMID: 107745 DOI: 10.2214 /
ajr.132.5.777]
61 Tajiri T., Onda M, Yoshida H, Mamada Y, Taniai N, Kumaza-
ki T. Долгосрочные гематологические и биохимические эффекты частичной эмболизации селезенки
при циррозе печени.Гепатогастро-
энтерология 2002; 49: 1445-1448 [PMID: 12239963]
62 Hayashi H, Beppu T., Okabe K, Masuda T., Okabe H, Ishiko
T, Baba H. Терапевтические факторы, учитываемые в соответствии с предоперационным объемом селезенки
для длительного увеличение количества тромбоцитов на
после частичной эмболизации селезенки при циррозе печени
. J Gastroenterol 2010; 45: 554-559 [PMID: 20047119 DOI:
10.1007 / s00535-009-0185-9]
63 Hirai K, Kawazoe Y, Yamashita K, Kumagai M, Tanaka M,
Sakai T., Inoue R, Eguchi С, Мадзима Й, Эйб М.Транскатетер
частичная эмболизация селезеночной артерии у пациентов с гиперспленизмом
: клиническая оценка в качестве поддерживающей терапии для гепатоцеллюлярной карциномы
и цирроза печени. Гепатогастроен-
терология 1986; 33: 105-108 [PMID: 3017829]
64 Nishida O, Moriyasu F, Nakamura T, Ban N, Miura K, Sakai
M, Uchino H, Miyake T. Проявлена взаимосвязь между селезенкой
и верхним брыжеечным венозным кровообращением by
преходящая окклюзия селезеночной артерии с использованием баллонного катетера.
Гепатология 1987; 7: 442-446 [PMID: 3570155]
65 Porter BA, Fr ey CF, Link DP, Lantz BM, Pimstone NR.
Эмболизация селезенки под контролем видеосъемки
nique. AJR Am J Roentgenol 1983; 141: 1063-1065 [PMID:
6353891 DOI: 10.2214 / ajr.141.5.1063]
66 Mukaiya M, Hirata K, Yamashiro K, Katsuramaki T., Kimura
H, Denno R. Изменения портальной гемодинамики и печени
функционируют после частичной эмболизации селезенки (PSE) и перку-
танной чреспеченочной облитерации (PTO).Cancer Chemother
Pharmacol 1994; 33 Suppl: S37-S41 [PMID: 8137483]
67 Bárcena R, Moreno A, Foruny JR, Moreno A, Sánchez J, Gil-
Grande L, Blázquez J, Nuño J, Fortún J, Rodriguez-
a
MA, Otón E. Улучшение функции трансплантата у
пациентов с трансплантацией печени
пациентов после частичной эмболизации селезенки: устранение синдрома обкрадывания артерии
? Clin Transplant 2006; 20: 517-523
[PMID: 16842531 DOI: 10.1111 / j.1399-0012.2006.00516.x]
68 Foruny JR, Blázquez J, Moreno A, Bárcena R, Gil-Grande L,
Quereda C, Pérez-Elías MJ, Moreno J, Sánchez J, Muriel A,
Rodriguez -Саградо М.А., Морено С. Безопасное использование пегилированного интерферона / рибавирина
у пациентов с циррозом, вызванных вирусом гепатита С,
с гиперспленизмом после частичной эмболизации селезенки. Eur J
Гастроэнтерол Гепатол 2005; 17: 1157-1164 [PMID: 16215426]
69 Симидзу Т., Тадзири Т., Йошида Х., Йокомуро С., Мамада Ю.,
Таняй Н., Кавано И., Такахаси Т., Арима Й, Арамаки Т.,
Кумадзаки Т.Ручная лапароскопическая гепатэктомия после частичной эмболизации селезенки. Surg Endosc 2003; 17: 1676
[PMID: 14702967 DOI: 10.1007 / s00464-003-4210-4]
70 Firat A, Boyvat F, Moray G, Aytekin C, Karakayali H, Haber-
al M. Сравнение двух различных чрескожная селезенка
вмешательства на артериях в лечении гиперспленизма: предварительное
лиминальное заключение. Transplant Proc 2005; 37: 1094-1098 [PMID:
15848633 DOI: 10.1016 / j.transproceed.2004.12.171]
71 Sockrider CS, Boykin KN, Green J, Marsala A, Mladenka
M, McMillan R, Zibari GB. Частичная эмболизация селезенки при гиперспленизме
до и после трансплантации печени. Clin
Трансплантат 2002; 16 Дополнение 7: 59-61 [PMID: 12372046]
72 Хаяси Х., Беппу Т., Масуда Т., Мизумото Т., Такахаши
М, Ишико Т., Такамори Х., Канемицу К., Хирота М., Баба Х.
Прогнозирующий факторы увеличения тромбоцитов после частичной эмболизации селезенки
у пациентов с циррозом печени.J Гастроэнтерол
Гепатол 2007; 22: 1638-1642 [PMID: 17683504 DOI: 10.1111 /
j.1440-1746.2007.05090.x]
73 Хаяси Х., Беппу Т., Окабе К., Масуда Т., Окабе Х., Баба
Х. Факторы риска при осложнениях после частичной эмболизации селезенки —
лизация при циррозе печени. Br J Surg 2008; 95: 744-750 [PMID:
18412294 DOI: 10.1002 / bjs.6081]
74 N’Kontchou G, Seror O, Bourcier V, Mohand D, Ajavon Y,
Castera L, Grando-Lemaire V, Ganne — Кэрри Н, Селье Н,
Тринше Дж. С., Богран М.Частичная эмболизация селезенки у
пациентов с циррозом: эффективность, переносимость и отдаленные результаты
у 32 пациентов. Eur J Gastroenterol Hepatol 2005; 17:
179-184 [PMID: 15674095]
75 Сакаи Т., Шираки К., Иноуэ Х., Сугимото К., Омори С., Мурата
К., Такасе К., Накано Т. Осложнения частичной селезенки —
болизация у пациентов с циррозом печени. Dig Dis Sci 2002; 47: 388-391
[PMID: 11855556]
76 Хан MJ, Zhao HG, Ren K, Zhao DC, Xu K, Zhang XT.Частичная эмболизация селезенки
по поводу гиперспленизма или
после артериальной эмболизации гепатоцеллюлярной карциномы у 30
пациентов. Cardiovasc Intervent Radiol 1997; 20: 125-127 [PMID:
03]
77 Sangro B, Bilbao I, Herrero I, Corella C, Longo J, Beloqui O,
Ruiz J, Zozaya JM, Quiroga J, Prieto J. Частичная эмболия селезенки —
для лечения гиперспленизма при циррозе печени. Hepa-
тология 1993; 18: 309-314 [PMID: 8340060]
78 Альвмарк A, Bengmark S, Gullstrand P, Joelsson B, Lunder-
quist A, Owman T.Оценка эмболизации селезенки у
пациентов с портальной гипертензией и гиперспленизмом. Ann
Surg 1982; 196: 518-524 [PMID: 7125739]
79 Hashimoto N, Akahoshi T., Tomikawa M, Kawanaka H,
Konishi K, Uehara H, Kinjo N, Korenaga D, Takenaka K,
Maehara Y. спленэктомия как спасение
Лечение рецидива тромбоцитопении после частичной селезенки
10 14 марта 2014 г.
|
Том 20
|
Выпуск 10
|
WJG
|
www.wjgnet.com
Лечение тромбоцитопении у пациентов с хроническим заболеванием печени
Тромбоцитопения. Веб-сайт Национального института сердца, легких и крови. www.nhlbi.nih.gov/health-topics/thrombocytopenia. По состоянию на 10 августа 2018 г.
Gauer RL, Braun MM. Тромбоцитопения. Врач Фам . 2012; 85: 612–622.
PubMed
Google Scholar
Асени П., Франги М., Беати К., Вертемати М., Романи Ф.Зависит ли тромбоцитопения при печеночной недостаточности от недостаточного синтеза печенью тромбопоэтического стимулирующего фактора? Медицинские гипотезы . 1988; 26: 217–219. https://doi.org/10.1016/0306-9877(88)
-1.
Артикул
CAS
PubMed
Google Scholar
Aster RH. Объединение тромбоцитов в селезенке: роль в патогенезе «гиперселезеночной» тромбоцитопении. Дж Клин Инвест . 1966. 45: 645–657.https://doi.org/10.1172/JCI105380.
Артикул
CAS
PubMed
PubMed Central
Google Scholar
Хроническая болезнь печени и цирроз. Веб-сайт Центров по контролю и профилактике заболеваний. www.cdc.gov/nchs/fastats/liver-disease.htm. Обновлено 6 октября 2016 г. По состоянию на 10 августа 2018 г.
Bashour FN, Teran JC, Mullen KD. Распространенность цитопении периферической крови (гиперспленизма) у пациентов с неалкогольной хронической болезнью печени. Ам Дж. Гастроэнтерол . 2000; 95: 2936–2939. https://doi.org/10.1111/j.1572-0241.2000.02325.x.
Артикул
CAS
PubMed
Google Scholar
Brown RS Jr. Обзорная статья: фармакоэкономический анализ тромбоцитопении при хроническом заболевании печени. Алимент Фармакол Тер . 2007; 26: 41–48. https://doi.org/10.1111/j.1365-2036.2007.03505.x.
Артикул
PubMed
Google Scholar
Poordad F, Theodore D, Sullivan J, Grotzinger K. Оценка использования медицинских ресурсов и затрат, связанных с тромбоцитопенией у пациентов с хроническими заболеваниями печени. J Med Econ . 2012; 15: 112–124. https://doi.org/10.3111/13696998.2011.632463.
Артикул
PubMed
Google Scholar
Хаяси Х, Беппу Т., Ширабе К., Маехара Й., Баба Х. Управление тромбоцитопенией из-за цирроза печени: обзор. Мир Дж. Гастроэнтерол .2014; 20: 2595–2605. https://doi.org/10.3748/wjg.v20.i10.2595.
Артикул
CAS
PubMed
PubMed Central
Google Scholar
Деметрий Г.Д. Целевые подходы к лечению тромбоцитопении. Онколог . 2001; 6: 15–23. https://doi.org/10.1634/theoncologist.6-suppl_5-15.
Артикул
CAS
PubMed
Google Scholar
Поордад Ф.Обзорная статья: тромбоцитопения при хроническом заболевании печени. Алимент Фармакол Тер . 2007; 26: 5–11. https://doi.org/10.1111/j.1365-2036.2007.03510.x.
Артикул
CAS
PubMed
Google Scholar
Таппер Э.Б., Робсон С.К., Малик Р. Коагулопатия при циррозе — роль тромбоцитов в гемостазе. Дж. Гепатол . 2013; 59: 889–890. https://doi.org/10.1016/j.jhep.2013.03.040.
Артикул
CAS
PubMed
Google Scholar
Кавасаки Т., Такешита А., Суда К. и др. Уровни тромбопоэтина в сыворотке крови у пациентов с хроническим гепатитом и циррозом печени. Ам Дж. Гастролентерол . 1999; 94: 1918–1922. https://doi.org/10.1111/j.1572-0241.1999.01231.x.
Артикул
CAS
Google Scholar
Perreira J, Accatino L, Alfaro J, Brahm J, Hidalgo P, Mezzano D. Аутоантитела к тромбоцитам у пациентов с хроническим заболеванием печени. Ам Дж. Гематол .1995; 50: 173–178.
Артикул
Google Scholar
Afdhal N, McHutchison J, Brown R, et al. Тромбоцитопения, связанная с хроническим заболеванием печени. Дж. Гепатол . 2008. 48: 1000–1007. https://doi.org/10.1016/j.jhep.2008.03.009.
Артикул
CAS
PubMed
Google Scholar
Seeff LB, Everson GT, Morgan TR, et al. Частота осложнений чрескожной биопсии печени у лиц с запущенным хроническим заболеванием печени в исследовании HALT-C. Клин Гастроэнтерол Гепатол . 2010; 8: 877–883.
Артикул
PubMed
PubMed Central
Google Scholar
Шарма П., Макдональд Г.Б., Банаджи М. Риск кровотечения после чрескожной биопсии печени: отношение к количеству тромбоцитов. Дж Клин Гастроэнтерол . 1982; 4: 451–453.
Артикул
CAS
PubMed
Google Scholar
Джаннини Э.Г., Греко А, Маренко С., Андорно Э, Валенте У, Саварино В.Частота кровотечений после инвазивных процедур у пациентов с тромбоцитопенией и прогрессирующим заболеванием печени. Клин Гастроэнтерол Гепатол . 2010; 8: 899–902. https://doi.org/10.1016/j.cgh.2010.06.018.
Артикул
PubMed
Google Scholar
Гангиредди В.Г., Каннеганти П.С., Шридхар С., Талла С., Коулман Т. Управление тромбоцитопенией при запущенном заболевании печени. Банка J Gastroenterol Hepatol . 2014; 28: 558–564.
Артикул
CAS
PubMed
PubMed Central
Google Scholar
Мерфи М.Ф., Уотерс, АХ. Клинические аспекты переливания тромбоцитов. Фибринолиз свертывания крови . 1991; 2: 389–396.
Артикул
CAS
PubMed
Google Scholar
Курокава Т., Окохчи Н. Тромбоциты при заболеваниях печени, раке и регенерации. Мир Дж. Гастроентол .2017; 23: 3228–3239. https://doi.org/10.3748/wjg.v23.i18.3228.
Артикул
CAS
Google Scholar
Schiffer CA, Bohlke K, Delaney M, et al. Переливание тромбоцитов для пациентов с онкологическими заболеваниями: обновленное руководство по клинической практике Американского общества клинической онкологии. Дж Клин Онкол . 2018; 36: 283–301. https://doi.org/10.1200/JCO.2017.76.1734.
Артикул
PubMed
Google Scholar
Beutler E. Переливание тромбоцитов: триггер 20 000 / мкл. Кровь . 1993; 81: 1411–1413.
CAS
Статья
Google Scholar
Блумберг Н., Хил Дж. М., Филлипс Г.Л. Переливание тромбоцитов: триггер, доза, польза и риски. F1000 Мед Репродукция . 2010; 2: 5. https://doi.org/10.3410/m2-5.
Артикул
PubMed
PubMed Central
Google Scholar
Afdhal NH, McHutchison J. Обзорная статья: фармакологические подходы к лечению тромбоцитопении у пациентов с хроническим заболеванием печени и инфекцией гепатита С. Алимент Фармакол Тер . 2007; 26: 29–39. https://doi.org/10.1111/j.1365-2036.2007.03511.x.
Артикул
CAS
PubMed
Google Scholar
Wolber EM, Jelkmann W. Тромбопоэтин: новый гормон печени. Новости Physiol Sci .2002; 17: 6–10.
CAS
PubMed
Google Scholar
Nplate [вкладыш в упаковке]. Таузенд-Окс, Калифорния: Amgen Inc; 2018.
Мусса М.М., Мовафи Н. Предоперационное применение ромиплостима у пациентов с тромбоцитопенией, хроническим гепатитом С и циррозом печени. J Гастроэнтерол Hepatol . 2013; 28: 335–341. https://doi.org/10.1111/j.1440-1746.2012.07246.x.
Артикул
CAS
PubMed
Google Scholar
Buccoliero G, Urbano T, Mazza P, Resta F, Pisconti S. Romiplostim для лечения тяжелой тромбоцитопении при лечении хронической вирусной инфекции гепатита C: новый вариант для врачей? Новый микробиол . 2014; 37: 97–101.
CAS
PubMed
Google Scholar
Promacta [вкладыш в упаковке]. Восточный Ганновер, Нью-Джерси: Корпорация Novartis Pharmaceuticals; 2018.
Afdhal NH, Dusheiko GM, Giannini EG, et al.Элтромбопаг увеличивает количество тромбоцитов у пациентов с тромбоцитопенией, инфекцией ВГС и циррозом печени, что позволяет проводить эффективную противовирусную терапию. Гастроэнтерология . 2014; 146: 442–452. https://doi.org/10.1053/j.gastro.2013.10.012.
Артикул
CAS
PubMed
Google Scholar
Afdhal NH, Giannini EG, Tayyab G, et al. ELEVATE Study Group. Эльтромбопаг перед процедурами у пациентов с циррозом печени и тромбоцитопенией. N Engl J Med . 2012; 367: 716–724. https://doi.org/10.1056/nejmoa1110709.
Артикул
CAS
PubMed
Google Scholar
Доптелет [листок-вкладыш]. Дарем, Северная Каролина: Dova Pharmaceuticals Inc; 2018.
Terrault N, Chen YC, Izumi N, et al. Аватромбопаг перед процедурами снижает потребность в переливании тромбоцитов у пациентов с хроническим заболеванием печени и тромбоцитопенией. Гастроэнтерология .2018; 155: 703–718. https://doi.org/10.1053/j.gastro.2018.05.025.
Артикул
CAS
Google Scholar
Mulpleta [вкладыш в упаковке]. Парк Флорхэм, Нью-Джерси: Shionogi Inc .; 2018.
Kim ES. Лусутромбопаг: первое глобальное одобрение. Наркотики . 2016; 76: 155–158. https://doi.org/10.1007/s40265-015-0525-4.
Артикул
PubMed
Google Scholar
Хидака Х., Куросаки М., Танака Х. и др. Лусутромбопаг снижает потребность в переливании тромбоцитов у пациентов с тромбоцитопенией, подвергающихся инвазивным процедурам. Клин Гастроэнтерол Гепатол . 2018 ;. https://doi.org/10.1016/j.cgh.2018.11.047.
Артикул
PubMed
Google Scholar
Пек-Радосавлевич М., Саймон К., Якобеллис А. и др. Лусутромбопаг для лечения тромбоцитопении у пациентов с хроническим заболеванием печени, подвергающихся инвазивным процедурам (L-PLUS-2). Гепатология . 2019 ;. https://doi.org/10.1002/hep.30561.
Артикул
PubMed
Google Scholar
Лоффредо Л., Виоло Ф. Агонисты рецепторов тромбопоэтина и риск тромбоза воротной вены у пациентов с заболеваниями печени и тромбоцитопенией: метаанализ. Копать Лив Дис . 2019; 51: 24–27.
Артикул
CAS
Google Scholar
Hadduck TA, McWilliams JP. Частичная эмболизация селезеночной артерии у пациентов с циррозом печени. Мир J Радиол . 2014; 6: 160–168. https://doi.org/10.4329/wjr.v6.i5.160.
Артикул
PubMed
PubMed Central
Google Scholar
Rockey DC, Caldwell SH, Goodman ZD, Nelson RC, Smith AD. Американская ассоциация по изучению заболеваний печени. Биопсия печени Hepatol . 2009; 49: 1017–1044. https://doi.org/10.1002 / hep.22742.
Артикул
Google Scholar
Пател И.Дж., Дэвидсон Дж.С., Николич Б. и др. Комитет по стандартам практики, одобренный Европейским обществом сердечно-сосудистой и интервенционной радиологии (CIRSE). Консенсусное руководство по перипроцедурному управлению статусом коагуляции и риском гемостаза при чрескожных вмешательствах под визуальным контролем. J Vasc Interv Radiol . 2012; 23: 727–736. https://doi.org/10.1016/j.jvir.2012.02.012.
Артикул
PubMed
Google Scholar
Бен-Менахем Т., Деккер Г.А., Early DS, et al. Комитет по стандартам практики ASGE. Нежелательные явления при эндоскопии верхних отделов ЖКТ. Гастроинтест Эндоск . 2012; 76: 707–718. https://doi.org/10.1016/j.gie.2012.03.252.
Артикул
PubMed
Google Scholar
Tillmann HL, McHutchison JG.Использование тромбопоэтических средств при тромбоцитопении при заболеваниях печени. Семин Гематол . 2010. 47: 266–273. https://doi.org/10.1053/j.seminmatol.2010.04.003.
Артикул
CAS
PubMed
Google Scholar
Kuter DJ. Новые факторы тромбопоэтического роста. Clin лимфома миелома . 2009; 9: S347 – S356. https://doi.org/10.3816/CLM.2009.s.034.
Артикул
CAS
PubMed
Google Scholar
Mitchell O, Feldman DM, Diakow M, et al. Патофизиология тромбоцитопении при хроническом заболевании печени. Гепат Мед . 2016; 8: 39–50.
PubMed
PubMed Central
Google Scholar
Цирроз | Хьюстон, Техас США |
Что такое цирроз?
Цирроз — рубцевание печени.
Широко распространенные узелки в печени в сочетании с фиброзом анатомически характеризуют цирроз. Фиброз и образование узелков вызывают нарушение нормальной архитектуры печени, что препятствует кровотоку через печень.Цирроз также может привести к неспособности печени выполнять свои биохимические функции. Чтобы понять патофизиологию цирроза, сначала необходимо кратко рассмотреть нормальную анатомию и физиологию печени.
Кровоток печени
Кислородная кровь, которая вернулась из легких в левый желудочек сердца, перекачивается во все ткани тела. Это называется системным кровообращением. Достигнув тканей, кровь возвращается в правую часть сердца, откуда она перекачивается в легкие, а затем возвращается в левую часть сердца после поглощения кислорода и выделения углекислого газа.Это называется малым кровообращением. Кровь из толстого и тонкого кишечника и селезенки течет в печень и проходит через нее, прежде чем вернуться в правую часть сердца. Это называется портальным кровообращением, а большая вена, по которой кровь поступает в печень, называется воротной веной. Пройдя через печень, кровь попадает в печеночную вену, которая ведет в нижнюю полую вену с правой стороны сердца. В печень также поступает кровь непосредственно из сердца через печеночную артерию.В пищеводе, желудке, тонком кишечнике и прямой кишке портальное кровообращение и вены большого круга кровообращения связаны. В нормальных условиях обратный поток из портального кровотока в системный кровоток практически отсутствует.
Секреция билирубина
Печень — место образования желчи. Желчь содержит соли желчных кислот, жирные кислоты, холестерин, билирубин и другие соединения. Компоненты желчи синтезируются и модифицируются в гепатоцитах (преобладающий тип клеток в печени) и секретируются в небольшие желчные протоки внутри самой печени.Эти маленькие желчные протоки образуют разветвленную сеть протоков все большего размера, которые в конечном итоге становятся общим желчным протоком, по которому желчь попадает в тонкий кишечник. Билирубин — это желтый пигмент, который происходит в основном из старых красных кровяных телец. Билирубин поглощается гепатоцитами из крови, модифицируется в гепатоцитах до водорастворимой формы и секретируется с желчью.
Биохимические функции
Печень выполняет множество биохимических функций — всего более 200. Факторы свертывания крови синтезируются в печени.Альбумин, основной белок крови, также синтезируется и секретируется печенью. Модификация и / или синтез компонентов желчи также происходят в печени. Многие метаболические функции организма происходят в основном в печени, включая метаболизм холестерина и превращение белков и жиров в глюкозу. В печени также метаболизируется большинство лекарств и токсинов, включая алкоголь.
Что не так в печени при циррозе?
Цирроз возникает в результате повреждения клеток печени токсинами, воспаления, метаболических нарушений и других причин.Поврежденные и мертвые клетки печени замещаются фиброзной тканью, что приводит к фиброзу (рубцеванию). Клетки печени регенерируют по ненормальному образцу, в основном образуя узелки, окруженные фиброзной тканью. В конечном итоге возникает грубая аномалия архитектуры печени, которая может привести к снижению кровотока к печени и через нее. Снижение притока крови к печени и обратно в воротную вену и портальное кровообращение приводит к некоторым серьезным осложнениям цирроза. Кровь может скапливаться в селезенке, вызывая ее увеличение и секвестрацию клеток крови.Чаще всего количество тромбоцитов падает из-за секвестрации селезенки. Низкое количество тромбоцитов, наблюдаемое при циррозе, происходит из-за захвата в селезенке, а не из-за основной проблемы с производством в костном мозге. Если давление в воротной системе кровообращения увеличивается из-за цирроза и восстановления крови (примечание: это также может иногда происходить в тяжелых случаях острого гепатита и повреждения печени), кровь может течь обратно из воротного кровообращения в большой круг кровообращения, где они связаны. . Это может привести к варикозному расширению вен желудка и пищевода (варикозное расширение вен желудка и пищевода), а также к геморрою прямой кишки или варикозу прямой кишки).Варикозное расширение вен желудка и пищевода может разорваться, обильно кровоточить и даже стать причиной смерти. Гипертензия в портальной системе кровообращения, наряду с другими гормональными, метаболическими и почечными нарушениями при циррозе, также может приводить к накоплению жидкости в брюшной полости (асцит) и периферических тканях (периферический отек).
Снижение секреции билирубина гепатоцитами при циррозе печени приводит к резервному содержанию билирубина в крови. Это приводит к желтухе, желтому изменению цвета кожи и глаз. Поскольку водорастворимая форма билирубина также сохраняется в крови, билирубин также может попадать в мочу, придавая ей цвет от ярко-желтого до темно-коричневого.
Нарушение биохимической функции печени при циррозе может привести к ряду осложнений. Концентрация сывороточного альбумина падает, что может привести к обострению асцита и отека. Метаболизм лекарств может измениться, что потребует корректировки дозы. У мужчин увеличение груди (гинекомастия) иногда возникает из-за снижения метаболизма эстрогена в печени. Сексуальная функция у мужчин также станет ненормальной. Снижение выработки факторов свертывания крови может привести к кровотечениям.Могут возникнуть нарушения обмена триглицеридов, холестерина и сахара. На более ранних стадиях цирроз часто вызывает инсулинорезистентность и сахарный диабет. На более поздних стадиях или при тяжелой печеночной недостаточности уровень глюкозы в крови может быть низким, поскольку он не может быть синтезирован из жиров или белков. Цирроз, особенно в запущенных случаях, может вызвать серьезные нарушения в работе мозга. При циррозе часть крови, покидающей кишечник, обходит печень, поскольку кровоток через печень уменьшается. Метаболизм компонентов, всасываемых в кишечнике, также может снижаться по мере ухудшения функции клеток печени.Оба эти нарушения могут привести к печеночной энцефалопатии, поскольку токсичные метаболиты, обычно удаляемые из крови печенью, могут достигать головного мозга. На ранних стадиях возникают тонкие психические изменения, такие как плохая концентрация или неспособность конструировать простые предметы. В тяжелых случаях печеночная энцефалопатия может привести к ступору, коме, отеку мозга и смерти.
Цирроз печени также может вызывать нарушения в других системах органов. Цирроз может привести к дисфункции иммунной системы, что увеличивает риск заражения.Асцитная жидкость в брюшной полости часто заражается бактериями, обычно присутствующими в кишечнике (спонтанный бактериальный перитонит). Цирроз также может привести к дисфункции и отказу почек. В терминальной стадии цирроза печени может развиться тип дисфункции почек, называемый гепаторенальным синдромом. Гепаторенальный синдром почти всегда заканчивается летальным исходом, если не выполняется трансплантация печени.
Клинические симптомы и диагностика цирроза печени
Цирроз обычно легко поставить, когда присутствуют какие-либо или все вышеперечисленные аномалии и осложнения.Это особенно верно, когда можно определить основное заболевание печени. Основное заболевание печени выявляется у большинства пациентов, однако иногда его не обнаруживают. Такие случаи называют «криптогенным» циррозом. Иногда другие состояния, такие как метастатический рак, тромбоз печени или воротной вены, тяжелый острый гепатит или острая обструкция желчных протоков, могут вызывать некоторые из аномалий, наблюдаемых при циррозе. Тщательный сбор анамнеза в сочетании со специальными диагностическими тестами обычно позволяет выявить эти состояния.В редких случаях, несмотря на цирроз печени, пациенты могут по-прежнему иметь очень мало расплывчатых жалоб. У некоторых пациентов, особенно на ранних стадиях заболевания, отсутствуют явные клинические признаки или симптомы. У некоторых могут быть только незначительные физические изменения, такие как красные ладони, красные пятна, которые бледнеют на верхней части тела (ангиомы паука), увеличение околоушных желез на лице, гинекомастия или фиброз сухожилий ладоней. У некоторых пациентов могут быть только незначительные отклонения в анализах крови, а в некоторых случаях все анализы крови могут быть нормальными.Радиологические тесты могут дать ключ к разгадке наличия цирроза, но диагноз цирроза часто необходимо ставить с помощью биопсии печени.
Причины цирроза печени
Существует общее заблуждение, что алкоголь является единственной причиной цирроза печени. Алкоголь является причиной примерно 50% случаев цирроза печени. Практически любое хроническое заболевание печени может привести к циррозу. В этом списке приведены некоторые из многих причин:
- Алкогольная болезнь печени — наиболее частая причина в США.С.А.
- Хронический вирусный гепатит B, C и D
- Хронический аутоиммунный гепатит
- Наследственные заболевания обмена веществ (например, гемохроматоз, болезнь Вильсона)
- Хронические заболевания желчных протоков (например, первичный билиарный цирроз)
- Хроническая застойная сердечная недостаточность
- Паразитарные инфекции (например, шистосомоз)
- Неалкогольный стеатогепатит (воспаление печени, которое может быть вызвано ожирением печени)
- Длительное воздействие токсинов или наркотиков
Лечение
Цирроз печени необратим, но лечение основного заболевания печени может замедлить или остановить прогрессирование.Такое лечение зависит от основной этиологии. Прекращение приема алкоголя остановит прогрессирование алкогольного цирроза печени, и по этой причине важно поставить диагноз на ранней стадии у хронического злоупотребляющего алкоголем. Точно так же прекращение приема гепатотоксических препаратов или удаление токсина из окружающей среды остановит прогрессирование. Лечение метаболических заболеваний, например, лечение перегрузки железом при гемохроматозе или перегрузки медью при болезни Вильсона, также является эффективным методом лечения. Хронические вирусные гепатиты B и C могут поддаваться лечению интерфероном, а аутоиммунный гепатит может улучшиться с помощью преднизона и азатиоприна (имуран).Такие препараты, как урсодиол (Актигалл), могут замедлить прогрессирование первичного билиарного цирроза и, возможно, склерозирующего холангита.
У пациентов с циррозом печени лечение также должно быть направлено на устранение осложнений. Кровотечение из варикозно расширенных вен пищевода можно лечить с помощью эндоскопической склеротерапии или перевязки резинкой. Асцит и отек часто реагируют на диету с низким содержанием натрия, и такой диете следует уделять особое внимание пациентам с этими симптомами. Более поздние стадии асцита и отеков могут поддаваться лечению диуретиками.Низкобелковая диета и такие вещества, как лактулоза, могут помочь при печеночной энцефалопатии. Такие инфекции, как спонтанный бактериальный перитонит, необходимо быстро лечить соответствующими антибиотиками. С осторожностью следует назначать препараты, метаболизирующиеся в печени. Нарушения коагуляции / свертывания иногда поддаются лечению витамином К.
Трансплантация печени является эффективным средством лечения терминальной стадии цирроза в надлежащих условиях. Трансплантация обычно необходима при неконтролируемых осложнениях, таких как энцефалопатия, асцит или кровотечение из варикозно расширенных вен, или когда биохимическая функция сильно подавлена.У пациентов с первичным билиарным циррозом повышение билирубина указывает на плохой прогноз, и таких пациентов следует рассматривать для трансплантации, поскольку концентрация билирубина в сыворотке начинает расти. Активное употребление наркотиков или алкоголя является противопоказанием к трансплантации печени. Однако алкоголики, которые воздерживались от употребления алкоголя в течение длительного периода времени (обычно более шести месяцев) и участвовали в программах реабилитации и группах поддержки, таких как Анонимные алкоголики, могут рассматриваться в качестве кандидатов и часто имеют хороший прогноз.Рак печени необходимо оценивать в индивидуальном порядке. Во многих случаях это противопоказание к трансплантации. Трансплантация печени обычно не проводится пациентам старше 70 лет.
Как лечат осложнения цирроза?
Аномальное скопление жидкости может вызвать отек лодыжек (отек) и живота (асцит). Поэтому пациенты должны уменьшить количество жидкости и соли в своем рационе или использовать лекарства, называемые диуретиками, которые мобилизуют и выводят лишнюю жидкость через почки.Обычно вас просят ограничить ежедневное потребление натрия (соли) до 2000 мг натрия в день или меньше.
Иногда асцит может инфицироваться, состояние, известное как спонтанный бактериальный перитонит, и требует лечения антибиотиками. Это осложнение связано с увеличением количества осложнений и повышенным риском преждевременной смерти. В случае развития перитонита на этом этапе необходимо рассмотреть возможность трансплантации печени.
Когда печень не может эффективно очищать организм от токсинов и лекарств, психическое состояние пациентов может резко измениться и привести к коме, называемой печеночной энцефалопатией.Лечение направлено на уменьшение количества белка в рационе, отказ от седативных и обезболивающих, а также на использование слабительных и / или антибиотиков для уменьшения всасывания токсинов из кишечника.
Иногда может возникать кровотечение из пищевода или желудка, вызванное аномальными венами (варикозным расширением вен), и это опасное для жизни состояние, требующее госпитализации. Варикозное кровотечение обычно можно контролировать с помощью гибкой трубки (эндоскопа), которая вводится через рот в пищевод и желудок и используется для введения агентов свертывания крови в вены или для перевязки варикозных вен.
Печеночная недостаточность относится к конечной стадии заболевания печени и цирроза, когда печень перестает работать и не может поддерживать жизнь. Печеночная недостаточность трудно поддается лечению, и выживаемость ограничена. Таким образом, пациенты с любым осложнением цирроза считаются подверженными риску развития печеночной недостаточности.
Когда развиваются осложнения, с ними можно справиться, хотя, вероятно, разовьются и другие осложнения. В настоящее время трансплантацию печени следует рассматривать как
.
FDA одобрило новый препарат для пациентов с хроническим заболеванием печени, у которых низкий уровень тромбоцитов в крови и которые проходят медицинскую процедуру
- Для немедленного выпуска:
The U.Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США сегодня одобрило таблетки Доптелет (аватромбопаг) для лечения низкого количества тромбоцитов (тромбоцитопения) у взрослых с хроническим заболеванием печени, которым назначена медицинская или стоматологическая процедура. Это первый препарат, одобренный FDA для такого использования.
«Пациенты с хроническим заболеванием печени, у которых низкое количество тромбоцитов и которым требуется процедура, подвергаются повышенному риску кровотечения», — сказал Ричард Паздур, доктор медицины, директор Центра передового опыта FDA и исполняющий обязанности директора Управления гематологии и онкологических продуктов в Центр FDA по оценке и исследованию лекарственных средств.«Доказано, что доптелет безопасно увеличивает количество тромбоцитов. Этот препарат может уменьшить или устранить необходимость в переливании тромбоцитов, которое связано с риском инфекции и других побочных реакций ».
Тромбоциты (тромбоциты) — это бесцветные клетки, вырабатываемые костным мозгом, которые помогают образовывать тромбы в сосудистой системе и предотвращают кровотечение. Тромбоцитопения — это состояние, при котором количество циркулирующих тромбоцитов в крови ниже нормы. Когда у пациентов наблюдается умеренное или сильно сниженное количество тромбоцитов, может возникнуть серьезное или опасное для жизни кровотечение, особенно во время инвазивных процедур.Пациенты со значительной тромбоцитопенией обычно получают переливание тромбоцитов непосредственно перед процедурой для увеличения количества тромбоцитов.
Безопасность и эффективность Doptelet изучалась в двух испытаниях (ADAPT-1 и ADAPT-2) с участием 435 пациентов с хроническим заболеванием печени и тяжелой тромбоцитопенией, которым была назначена процедура, которая обычно требовала переливания тромбоцитов. В испытаниях изучались два уровня доз доптелета, вводимых перорально в течение пяти дней, по сравнению с плацебо (без лечения).Результаты испытаний показали, что для обоих уровней доз Doptelet у более высокой доли пациентов было повышенное количество тромбоцитов и не требовалось переливание тромбоцитов или какой-либо спасательной терапии в день процедуры и до семи дней после процедуры по сравнению с пациентами, получавшими лечение. с плацебо.
Наиболее частыми побочными эффектами, о которых сообщили участники клинических испытаний, получавшие Доптелет, были лихорадка, боль в животе (брюшной полости), тошнота, головная боль, усталость и отек рук или ног (отек).Люди с хроническим заболеванием печени и люди с определенными условиями свертывания крови могут иметь повышенный риск развития тромбов при приеме Доптелет.
Этому продукту была предоставлена приоритетная проверка, в соответствии с которой цель FDA — принять меры по заявке в течение шести месяцев, когда агентство определяет, что препарат, в случае утверждения, значительно повысит безопасность или эффективность лечения, диагностики или предотвращения серьезного состояния.
