Вертеброгенный болевой синдром (боль в спине из-за проблем с позвоночником): отчего возникает и как проявляется
Как правило, к врачу по поводу болей в позвоночнике обращаются пациенты с комплексными дистрофическими изменениями. Проще говоря, у них уже поражены все кости, суставы и мягкие ткани позвоночного столба. Всего есть пять типов таких изменений:
1. остеохондроз (нарушения в суставных хрящах),
2. деформирующий спондилез (разрастание ткани позвонков в виде выступов и шипов),
3. межпозвонковый артроз (разрушение межпозвоночных суставов),
4. анкилозирующий гиперостоз (окостенение связок с ограничением их подвижности),
5. кальциноз диска (отложение солей в позвоночнике).
Общей причиной боли в любом отделе позвоночника – шейном, грудном, поясничном или крестцовом – является компрессия (сдавливание) спинного мозга, его оболочек и корешков, отходящих от него нервов. Сдавливание вызвано центральным или боковым стенозом (сужением)позвоночного канала.
Слабое развитие мускулатуры шеи и спины ведет к перегрузке позвоночника. Добавим к ней разнообразные патологические процессы и получим дегенеративно-дистрофические, то есть разрушительные изменения в межпозвонковых дисках и суставах. В суставах они начинаются с синовитов (воспаление с выделением излишней жидкости) и переходят в подвывихи. В дисках изменения проявляются в уплощении дисков и нарушении их функции, отчего при движении они становятся нестабильными. Все это ведет к динамическому стенозу (сужению) позвоночного канала, который возникает при сгибании, разгибании или ротации (поворотам) позвонков.
Чем дальше, тем больше сужается позвоночный канал, пока не стабилизируется в этом сдавленном состоянии. Иногда это происходит из-за костных разрастаний или увеличения суставных отростков — они занимают пространство. Еще одна частая причина — хрящевая грыжа. Грыжа — выпячивание части диска назад, что влечет за собой центральный стеноз позвоночного канала, или в сторону, что приводит к боковому стенозу и сужению канала, в котором находится нервный корешок.
Увидеть функциональную недостаточность межпозвонкового диска можно на функциональных рентгенограммах. Обычно их делают в боковой проекции, лежа, при максимальном сгибании и разгибании позвоночника. Гораздо лучше, если есть возможность получить рентгенограмму в положении стоя или сидя.
Как выглядит рентгенограмма «проблемного» позвоночника? При сгибании, разгибании или ротационных движениях заметна либо блокада, либо нестабильность пораженного сегмента. Это означает, что на функциональных снимках либо совершенно не меняются взаимоотношения между двумя соседними позвонками, либо, наоборот, возникает усиленная подвижность их вплоть до соскальзывания одного из позвонков по отношению к другому.
Для успешного лечения болей в спине (в позвоночнике) крайне важно правильно определить причину. Основным способом диагностики вертеброгенного болевого синдрома стала магнитно-резонансная томография. Измерение позвоночного канала, определение степени и типа его деформации, выявление обызвествлений (отложения солей), гипертрофии связок, хрящевых грыж, артроза межпозвонковых суставов, опухолей в позвоночном канале, оценка состояния спинного мозга – вот далеко не полный перечень возможностей МРТ позвоночника.
Вертеброгенный болевой синдром Текст научной статьи по специальности «Клиническая медицина»
М.В.ПУТИЛИНА, д.м.н., профессор, РГМУ, Москва
Вертеброгенный болевой синдром
В настоящее время до 80% населения нашей планеты страдают различными заболеваниями позвоночника. К этому приводят урбанизация, низкая двигательная активность, изменение режима и качества питания, ухудшение экологических условий окружающей среды. В России каким-либо заболеванием позвоночника страдает каждый 9-й человек. Боли в спине являются одной из наиболее частых причин потери трудоспособности людей 30—45-летнего возраста.
Среди многочисленных форм поражений суставов, по данным В. К.Велитченко (2002), первое место занимают дегенеративно-дистрофические заболевания позвоночника и суставов, которыми страдают от 8 до 12% населения различных стран. При этом за медицинской помощью обращаются только 40% больных. Острая боль переходит в хроническую у трети пациентов [5, 6]. Болеют чаще женщины. У мужчин короче ремиссии, выше процент оперированных по поводу грыж дисков и ухода на пенсию по инвалидности. По данным статистических исследований патология пояснично-крестцового отдела составляет около 30% общей заболеваемости, 20—30% всех заболеваний нервной системы и более 80% заболеваний периферической нервной системы. Ежегодно она регистрируется у 15—25% взрослого населения страны. Около 84% мирового населения в течение жизни хотя бы раз переживали относительно длительный эпизод боли в спине. В ходе проведенного в Швеции почтового опроса 1806 человек были получены следующие результаты: 55% респондентов жаловались на боли продолжительностью более 3 месяцев, 49% — не менее 6 месяцев [22].
К.Велитченко (2002), первое место занимают дегенеративно-дистрофические заболевания позвоночника и суставов, которыми страдают от 8 до 12% населения различных стран. При этом за медицинской помощью обращаются только 40% больных. Острая боль переходит в хроническую у трети пациентов [5, 6]. Болеют чаще женщины. У мужчин короче ремиссии, выше процент оперированных по поводу грыж дисков и ухода на пенсию по инвалидности. По данным статистических исследований патология пояснично-крестцового отдела составляет около 30% общей заболеваемости, 20—30% всех заболеваний нервной системы и более 80% заболеваний периферической нервной системы. Ежегодно она регистрируется у 15—25% взрослого населения страны. Около 84% мирового населения в течение жизни хотя бы раз переживали относительно длительный эпизод боли в спине. В ходе проведенного в Швеции почтового опроса 1806 человек были получены следующие результаты: 55% респондентов жаловались на боли продолжительностью более 3 месяцев, 49% — не менее 6 месяцев [22].
Первичные вертеброгенные боли, как правило, связаны с дегенеративно-дистрофическими изменениями позвоночника (дорсопатией, спондилезом и спондилоартрозом). На их развитие влияют генетическая предрасположенность, возраст, факторы риска. Дегенеративно-дистрофические изменения приводят к появлению функциональных блокад и других нарушений биомеханики позвоночного столба. Это может спровоцировать заболевания внутренних органов, сегментарно связанных с пораженным отделом позвоночника. Но следует учитывать, что внутренние органы не имеют строгой сегментарной иннервации. Например, желудок, печень, почки, поджелудочная железа получают иннервацию из одного и того же чревного сплетения. Все физиологические и патологические реакции не ограничиваются только одним сегментом, а пере-
ходят в зоны соседних метамеров. В связи с тем, что патология позвоночника служит причиной многосторонних расстройств нервной регуляции и трофики различных внутренних органов, она может привести к развитию функциональных нарушений и органической патологии и вызвать соматическое заболевание [4].
Дорсопатии являются наиболее частой причиной вертеброгенных болей. При инфекционных, онкологических, травматических поражениях позвоночника возникают вторичные вертеброгенные боли. Чаще к ним приводят травматические и инфекционные (спондилиты) заболевания, анкилози-рующий спондилоартрит (болезнь Бехтерева), реже — опухоли и идиопатическая спондилопатия (юношеский дорсальный кифоз или болезнь Шайерманна—Мау.
Дорсопатии — группа заболеваний костно-мы-шечной системы и соединительной ткани, ведущим симптомокомплексом которых является боль в туловище и конечностях невисцеральной этиологии. Это заболевание является серьезной проблемой во всем мире. Например, в США общие потери национальной экономики от дорсопатии оцениваются в 85—90 млрд долларов в год, а на лечение этого заболевания приходится до 80% затрат здравоохранения [17].
В связи с тем, что в клинической практике для лечения как острой, так и хронической боли часто используют общий алгоритм, в настоящее время особенно актуальна проблема адекватно подобранной терапии дорсопатий. Причем при выборе тактики лечения необходимо учитывать, что речь идет о дегенеративном поражении позвоночника, о его сложном патогенетическом каскаде и времени возникновения патологии. Поэтому лечение больных с дорсопатией должно быть комплексным, с использованием лекарственных средств и методов немедикаментозной терапии. В острый и межприс-тупный период болезни проводятся разные лечебные мероприятия. В первую очередь необходимо
предпринять меры, направленные на снятие или уменьшение болевого синдрома [1, 9, 23].
При острой боли пациенту рекомендуют соблюдать постельный режим в течение 1—3 дней. Также сразу назначают нестероидные противовоспалительные средства (НПВС), анальгетики, миорелак-санты.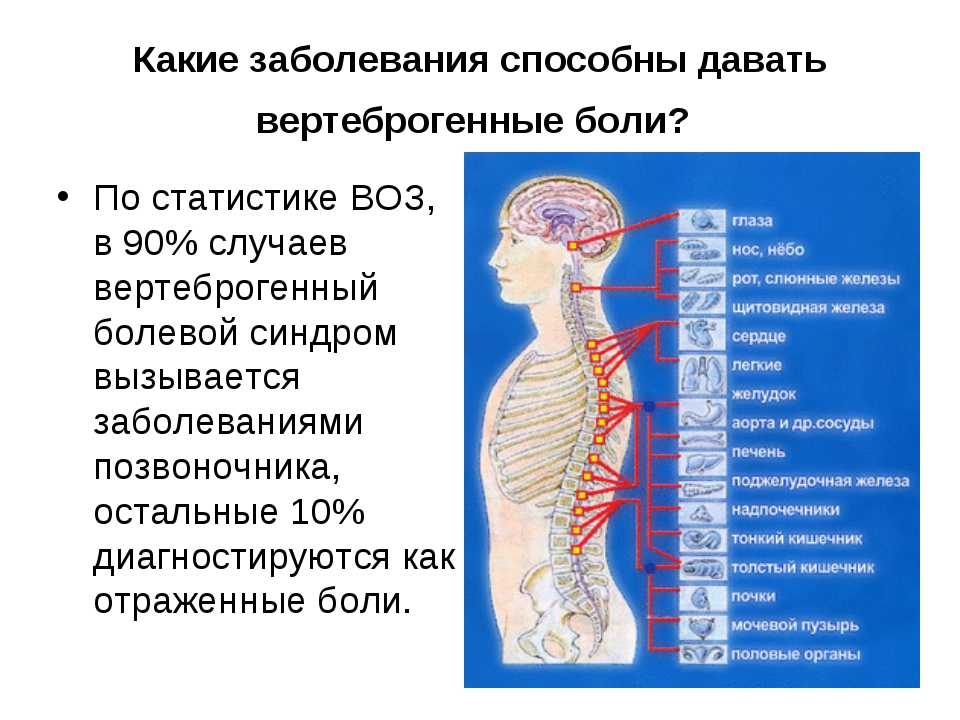 Для повышения эффективности препарата и скорости наступления обезболивания НПВС лучше назначать в виде внутривенных инъекций [13]. Показанием для назначения противоишемических препаратов: антиоксидантов, антигипоксантов, ва-зоактивных препаратов является наличие компрессионного синдрома. Вопрос о применении антидепрессантов решается индивидуально для каждого пациента [7, 12].
Для повышения эффективности препарата и скорости наступления обезболивания НПВС лучше назначать в виде внутривенных инъекций [13]. Показанием для назначения противоишемических препаратов: антиоксидантов, антигипоксантов, ва-зоактивных препаратов является наличие компрессионного синдрома. Вопрос о применении антидепрессантов решается индивидуально для каждого пациента [7, 12].
Медикаментозное лечение дорсопатий — сложная задача, требующая глубоких знаний патогенеза, клинических проявлений болезни. Помимо этого врач должен придерживаться алгоритмов, разработанных с учетом стадии процесса (рис.). При лечении острой дорсопатии следует ожидать значительного регресса боли в течение 1—2 недель. Существовавшая раньше установка об ограничении двигательной активности вплоть до строгого постельного режима в настоящее время пересмотрена: частичное ограничение рекомендуется при умеренной боли, постельный режим в течении 1—3 дней — при интенсивной боли. Пациента необходимо научить правильно сидеть, вставать, идти, а также запретить поднимать тяжести и т.д. При отсутствии результатов от проводимой терапии в течение 1—2 недель необходимо назначить другие препараты в оптимальных дозах. Если боль сохраняется более 1 месяца — это свидетельствует о хро-низации процесса или о неправильной постановке диагноза.
Решение об оперативном вмешательстве принимается при:
■ сдавлении конского хвоста с нижним парапаре-зом и тазовыми нарушениями;
■ нарастающем парезе;
■ тяжелом болевом синдроме, не поддающемся консервативному лечению.
К основным принципам медикаментозной терапии вертеброгенной боли в спине относятся раннее начало, снятие болевого синдрома, сочетание патогенетической и симптоматической терапии. В первую очередь патогенетическая терапия должна быть направлена на борьбу с оксидантным стрессом, а также воздействовать на микроцирку-ляторное русло, улучшать кровоснабжение пораженного участка, снимать признаки нейрогенного воспаления. С этой целью применяются антиокси-дантные, вазоактивные и нестероидные противовоспалительные препараты [8, 14, 15]. Для купирования алгических проявлений назначают симпто-
В первую очередь патогенетическая терапия должна быть направлена на борьбу с оксидантным стрессом, а также воздействовать на микроцирку-ляторное русло, улучшать кровоснабжение пораженного участка, снимать признаки нейрогенного воспаления. С этой целью применяются антиокси-дантные, вазоактивные и нестероидные противовоспалительные препараты [8, 14, 15]. Для купирования алгических проявлений назначают симпто-
матическую терапию. При выраженном тревожно-депрессивном расстройстве, а также при наличии хронической боли показано применение антидепрессантов.
Сложность проведения медикаментозной терапии в большинстве случаев заключается в запутанной анатомо-физиологической иерархии структур, вовлеченных в патологический процесс. С одной стороны, это обусловлено особенностями строения и функционирования структур пояснично-крестцового сплетения. С другой стороны, базисным механизмом, лежащим в основе дорсопатии, является четкая корреляция между компрессией и ишемией нерва и развитием оксидантного стресса [16, 18].
Важное место в механизмах развития заболеваний периферической нервной системы занимают нарушения гемодинамики, ишемия, расстройства микроциркуляции, нарушения энергообмена в ишемизированных нейронах со снижением аэробного энергообмена, метаболизма АТФ, утилизации кислорода, глюкозы. Проведения коррекции вазо-активными препаратами требуют патогенетические процессы, происходящие в нервных волокнах. Для улучшения процессов микроциркуляции, активизации процессов обмена и гликолиза применяют следующие лекарственные средства: Весел Дуэ Ф, трентал (пентоксифиллин), кавинтон (вин-поцетин), кортексин.
Оксидантный стресс — это нарушение равновесия между продукцией свободных радикалов и активностью антиоксидантных систем. Возникший в результате этого дисбаланс приводит к усиленной продукции соединений (нейротрансмиттеров), выделяющихся поврежденными тканями: гистамина, серотонина, АТФ, лейкотриенов, интерлейкинов, простогландинов, окиси азота и т. д. Они приводят к развитию нейрогенного воспаления, увеличивая проницаемость сосудистой стенки, а также способствуют высвобождению тучными клетками и лейкоцитами простагландина Е2, цитокинов и биогенных аминов, повышая возбудимость ноцицепторов.
д. Они приводят к развитию нейрогенного воспаления, увеличивая проницаемость сосудистой стенки, а также способствуют высвобождению тучными клетками и лейкоцитами простагландина Е2, цитокинов и биогенных аминов, повышая возбудимость ноцицепторов.
В настоящее время появились клинические работы по использованию препаратов, улучшающих реологические свойства крови и эндотелий-зависимые реакции стенки сосудов у пациентов с компрессионными невропатиями. Для уменьшения проявлений оксидантного стресса успешно применяются производные липоевой кислоты (октоли-пен), мексидол, актовегин и др.
Мексидол — современный отечественный препарат, действующим веществом которого является этилметилгидроксипиридина сукцинат. Он относится к группе гетероароматических антиоксидан-тов-антигипоксантов и обладает ноотропными и анксиолитическими свойствами. Механизм его дей-
ствия обусловлен антиоксидантным и мембрано-протекторным действием. Он ингибирует перекис-ное окисление липидов, повышает активность су-пероксидоксидазы, повышает соотношение липид-белок, уменьшает вязкость мембраны, увеличивает ее текучесть. Препарат модулирует активность мем-
браносвязанных ферментов (кальцийнезависимой фосфодиэстеразы, аденилатциклазы, ацетилхоли-нэстеразы), рецепторных комплексов (бензодиазе-пинового, ГАМК, ацетилхолинового), что усиливает их способность связывания с лигандами, способствует сохранению структурно-функциональной ор-
ганизации биомембран, транспорта нейромедиато-ров и улучшению синаптической передачи. Диапазон терапевтических эффектов препарата составляет от 10 до 300 мг/кг. При вертеброгенной патологии препарат назначают по 400 мг 1 раз в день внутримышечно, курс 10—15 дней с последующим переходом на пероральное применение в течение 1—3 месяцев.
Актовегин — антиоксидант, представляющий собой депротеинизированный экстракт крови молодых телят, улучшает утилизацию кислорода и глюкозы. Под влиянием препарата значительно улучшается диффузия кислорода в нейрональных структурах, что приводит к уменьшению выраженности вторичных трофических расстройств. При приеме актовегина также отмечается значительное улучшение церебральной и периферической микроциркуляции на фоне улучшения аэробного энергообмена сосудистых стенок и высвобождения простациклина и оксида азота. Происходящая при этом вазодилатация и снижение периферического сопротивления являются вторичными по отношению к активации кислородного метаболизма сосудистых стенок. При дорсопатии целесообразно назначать актовегин как в острой, так и в подострой стадиях заболевания, особенно при отсутствии эффекта от других методов лечения. Препарат вводят в дозе 400—800 мг в течение 5 дней, с последующим переходом на пероральное применение. Акто-вегин можно также использовать для проведения лечебных блокад совместно с анестетиком.
Кортексин — препарат пептидной природы, содержащий комплекс аминокислот, полипептидов, сбалансированный витаминный и минеральный комплекс. Его производят из коры головного мозга телят (свиней). Пептиды препарата оказывают прямое и опосредованное нейротрофическое воздействие на клетки. Кортексин через систему противовоспалительных цитокинов улучшает нейротрофи-ческое обеспечение нервного волокна и уменьшает аутоиммунную агрессию, способствуя восстановлению и росту аксонов. При дорсопатиях препарат назначают в дозе 10 мг внутримышечно ежедневно в течение 10—15 дней.
Октолипен (а-липоевая кислота) — эндогенный антиоксидант, образующийся в организме при окислительном декарбоксилировании альфа-кето-кислот. Он способствует снижению концентрации глюкозы в крови и увеличению содержания гликогена в печени, а также преодолению инсулинорези-стентности. Октолипен участвует в регулировании липидного и углеводного обмена, стимулирует обмен холестерина, улучшает функцию печени. Также он оказывает гепатопротекторное, гиполипидеми-ческое, гипохолестеринемическое, гипогликемиче-ское действие, улучшает трофику нейронов и аксо-
Октолипен участвует в регулировании липидного и углеводного обмена, стимулирует обмен холестерина, улучшает функцию печени. Также он оказывает гепатопротекторное, гиполипидеми-ческое, гипохолестеринемическое, гипогликемиче-ское действие, улучшает трофику нейронов и аксо-
нальную проводимость, уменьшает проявление по-линейропатии. Октолипен применяют внутрь по 600 мг (2 капсулы) 1 раз в день натощак, за 30 минут до первого приема пищи, не разжевывая и запивая достаточным количеством воды. Препарат назначают в комплексе с НПВП, курс лечения составляет 1—3 месяца.
Кавинтон — препарат полимодального механизма действия. Препарат угнетает фосфодиэсте-разу, что способствует накоплению в тканях цАМФ и повышению концентрации АТФ. Его отличительным свойством является нормализация сосудистого тонуса, положительное воздействие на макро- и микроциркуляцию. Кавинтон оказывает мощный антиоксидантный эффект. Также он является эффективным ангиопротектором. Пациентам с дорсо-патией его назначают как средство патогенетической терапии. Кавинтон назначают ежедневно внутривенно капельно по 2 мл на 200 мл 0,9% раствора хлорида натрия в течение 10—15 дней с последующим переходом на пероральный прием.
Средством первого выбора для снятия болевого синдрома являются нестероидные противовоспалительные препараты (НПВП). Механизм действия НПВП заключается в ингибировании циклооксиге-назы (ЦОГ-1,2), ключевого фермента каскада метаболизма арахидоновой кислоты, приводящего к синтезу простагландинов, простациклинов и тром-боксанов. НПВП широко используются в неврологической практике, так как метаболизм ЦОГ играет главную роль в индукции боли в очаге воспаления и передаче ноцицептивной импульсации в спинной мозг. По данным некоторых авторов, их принимают 300 млн пациентов [2, 14, 19]. Все НПВП обладают противовоспалительным, анальгезирующим и жаропонижающим эффектом, способны тормозить миграцию нейтрофилов в очаг воспаления и агрегацию тромбоцитов, а также активно связываться с белками сыворотки крови. Различия в действии НПВП носят количественный характер, но именно они обусловливают выраженность терапевтического эффекта, переносимость и наличие побочных эффектов у больных. Высокая гастротоксичность НПВП, коррелирующая с выраженностью их сано-генетического действия, связана с неизбирательным ингибированием обеих изоформ циклооксиге-назы. В зависимости от действия, оказываемого НПВС на циклооксигеназу, в настоящее время они делятся на две группы. Неселективные НПВС блокируют как конституциональную циклооксигеназу-1, с которой связывают желудочно-кишечные побочные эффекты этих лекарств, так и индуцибельную цик-лооксигеназу-2, образование которой активируют противовоспалительные цитокины. Селективные препараты воздействуют преимущественно на цик-лооксигеназу-2. К неселективным НПВС относятся
Различия в действии НПВП носят количественный характер, но именно они обусловливают выраженность терапевтического эффекта, переносимость и наличие побочных эффектов у больных. Высокая гастротоксичность НПВП, коррелирующая с выраженностью их сано-генетического действия, связана с неизбирательным ингибированием обеих изоформ циклооксиге-назы. В зависимости от действия, оказываемого НПВС на циклооксигеназу, в настоящее время они делятся на две группы. Неселективные НПВС блокируют как конституциональную циклооксигеназу-1, с которой связывают желудочно-кишечные побочные эффекты этих лекарств, так и индуцибельную цик-лооксигеназу-2, образование которой активируют противовоспалительные цитокины. Селективные препараты воздействуют преимущественно на цик-лооксигеназу-2. К неселективным НПВС относятся
Таблица. Основные НПВС, применяемые при лечении боли в спине
Препарат Дозы/способ применения Анальгетический эффект Побочные действия Примечания
Диклофенак 75—150 мг/сут внутрь, в/м, в/в 1—2 раза в день, 3—5 дней +++ ++ Препарат выбора при выраженном болевом синдроме
Индометацин 25—50 мг/сут внутрь, 100—160 мг/сут, в/м 1 раз в день, ректально ++ +++ Частые побочные эффекты, отрицательно влияет на метаболизм хряща, может вызвать психические нарушения
Кетопрофен 100—320 мг/сут внутрь, 100—160 мг в/м, ректально 1 раз в день +++ ++ Возникает диарея, метеоризм, тошнота при применении высоких доз
Нимесулид 200—400 мг/сут внутрь ++ ++ Препарат выбора при умеренной боли
Кеторолак 10 мг 2—4 раза в день внутрь, 30 мг в/м 2—3 раза в день +++ +++ Риск побочного действия возрастает при приеме препарата в течение более 7 суток
Лорноксикам Внутрь 16—24 мг в первые сутки, затем 8 мг 2 раза; 8—16 в/в или в/м 2 раза в день +++ +++ Препарат выбора при сильной боли
Мелоксикам 7,5—15 мг 1 раз в сутки, внутрь, в/м ++ + Препарат выбора при хроническом болевом синдроме
Пироксикам 20—40 мг внутрь 1 раз в сутки ++ ++ Медленное начало действия
Целекоксиб 200—400 мг внутрь 2 раза в сутки ++ + Показан при наличии в анамнезе заболеваний ЖКТ
лорноксикам (ксефокам), ацеклофенак (аэртал) ибупрофен, индометацин, к селективным ингибиторам ЦОГ — мелоксикам (мовалис, мирлокс, артро-зан), нимесулид, целекоксиб (целебрекс).
Ксефокам — препарат, оказывающий выраженное антиангинальное действие за счет сочетания противовоспалительных эффектов НПВП и сильного обезболивающего эффекта, сопоставимого с опиатами. Фармакокинетика ксефокама не отличается у пациентов различных возрастных групп. Достоверно доказана эффективность перорального применения препарата по схеме: 1-й день — 16 и 8 мг; 2—4 день — 8 мг 2 раза в день, 5 день — 8 мг/сут при острых болях в спине [10]. Анальгетический эффект от применения ксефокама в дозе 2—16 мг 2 раза в сутки в несколько раз выше напроксена. При дорсопатии рекомендуется использование препарата в дозе 16—32 мг. Препарат можно вводить внутримышечно, внутривенно, назначать внутрь, обкалывать триггерные точки, делать лечебные блокады. Курс лечения составляет не менее 5—7 дней при одноразовой ежедневной процедуре. Средние дозы препарата эффективны так же, как высокие
дозы других НПВС. При выраженном болевом синдроме в первый день назначают по 16 мг в/м или в/в 2 раза в день, затем дозу уменьшают до 8 мг в день в течение 3—5 дней.
Артрозан (мелоксикам) — нестероидный противовоспалительный препарат, оказывающий противовоспалительное, жаропонижающее и анальгети-ческое действие. Противовоспалительное действие препарата связано с торможением ферментативной активности циклооксигеназы-2, участвующей в биосинтезе простагландинов в области воспаления [20, 21]. В меньшей степени он действует на цикло-оксигеназу-1, участвующую в синтезе простаглан-дина, защищающего слизистую оболочку пищеварительного тракта и принимающего участие в регуляции кровотока в почках. Артрозан хорошо всасывается из желудочно-кишечного тракта, абсолютная биодоступность мелоксикама — 89%. Одновременный прием пищи не влияет на всасывание. При использовании Артрозана внутрь в дозах 7,5 и 15 мг его концентрации пропорциональны дозам. Равновесные концентрации достигаются в течение 3—5 дней.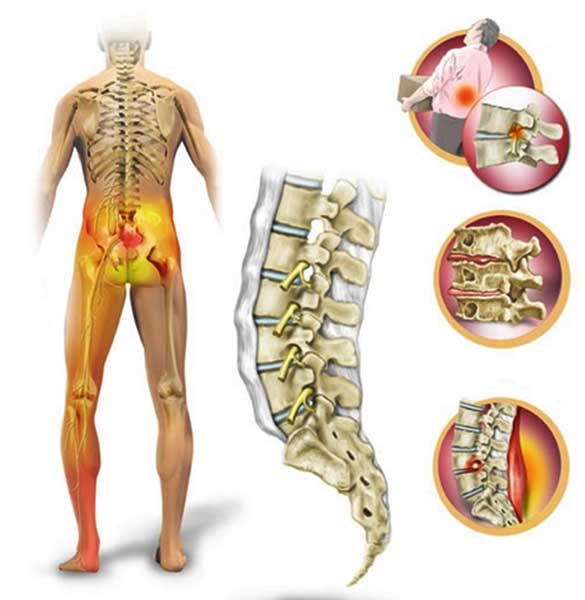 Курс лечения составляет не менее 5—7
Курс лечения составляет не менее 5—7
пги медицинский МС советв-,-№3 2009
дней при одноразовой ежедневной процедуре. Мелоксикам принимают внутрь во время еды 1 раз в день или вводят внутримышечно. В зависимости от выраженности клинической картины суточная дозировка препарата составляет 7,5—15 мг/сут.
Основные НПВС, применяемые при лечении боли в спине, приведены в таблице.
В ОСНОВНЫЕ НПВС, ПРИМЕНЯЕМЫЕ
ПРИ ЛЕЧЕНИИ БОЛИ В СПИНЕ
Важную роль в комплексной терапии болей в спине, особенно при наличии миофасциального синдрома, играют центральные миорелаксанты (мидокалм). За счет уменьшения патологического гипертонуса они не только уменьшают боль и снижают потребность в НПВП, но и значительно сокращают сроки нетрудоспособности. Лечебное действие этих препаратов обусловлено потенцированием ГАМК-ергической системы спинного мозга, что приводит к торможению систем возбуждающих медиаторов, угнетению спинальных рефлексов, релаксации мышечного гипертонуса [3]. Их обезболивающее действие обусловлено ликвидацией мышечного спазма.
Миорелаксанты применяют как для купирования болевого эпизода, так и для предупреждения хронизации боли. Препараты данной группы мож-
но назначать на срок не более 7—14 дней, за исключением мидокалма, терапию которым можно продолжать 21 день. Основными представителями группы миорелаксантов являются толперизон (ми-докалм), баклофен, тизанидин (сирдалуд).
Самым назначаемым миорелаксантом в России является мидокалм. Мидокалм тормозит спиналь-ные моно- и полисинаптические рефлексы, благодаря чему оказывает прямое миорелаксирующее действие и снимает болезненный мышечный спазм. |>_п ‘■*—■ |ц|,Ч4«: ?И| :-тп■зс тпни
|>_п ‘■*—■ |ц|,Ч4«: ?И| :-тп■зс тпни
жилых пациентов и пациентов с сопутствующими заболеваниями, получающих другие лекарственные препараты. При резко выраженных мышечно-то-нических болевых синдромах препарат вводят внутримышечно по 100 мг дважды в день, в остальных случаях назначают таблетки мидокалма по 150 мг 3 раза в день.
Сирдалуд относится к производным имидазоли-на и имеет структурное и биохимическое сходство с клонидином. Препарат влияет на а2 адренорецеп-торы в головном и спинном мозге, за счет чего оказывает миорелаксирующее действие. Высвобождая возбуждающие нейромедиаторы (норадреналин и аспартат) в спинном и головном мозге, он уменьшает их воздействие на рецепторы, что приводит к уменьшению возбудимости а- и у-мотонейронов. Тизанидин преимущественно угнетает полисинап-тические рефлексы спинного мозга, отвечающие за гипертонус мышц, и вызывает снижение тонуса сгибательной и разгибательной мускулатуры, уменьшая болезненный мышечный спазм. К наиболее частым побочным эффектам препарата относятся сухость во рту, головокружение и сонливость. Препарат следует с осторожностью назначать лицам пожилого возраста и больным с нарушениями функции печени и почек. Средняя доза сирдалуда составляет 12—24 мг/сут. Начальная доза препарата при выраженном болезненном мышечном спазме составляет 2 мг утром и 4 мг вечером внутрь, с последующим увеличением дозы.
Невропатическая боль при дорсопатии часто имеет необычный характер, сопровождается нарушениями чувствительности (гиперестезиями, ди-зестезиями, аллодинией), другими неврологическими нарушениями или локальной вегетативной дисфункцией. Это может быть связано с ограничением притока сенсорной импульсации из-за повреждения проводящих путей (деафферентацион-ная боль), эктопической спонтанной генерацией сенсорных импульсов в поврежденных нейронах, а также усилением симпатических влияний на болевую сенсорную мотивацию. С целью диагностики наличия синдрома болевой невропатии, а также идентификации патофизиологических механизмов развития боли и гипералгезии необходимо провести клиническое обследование, направленное на определение характера боли и выявление различных видов гипералгезии. Знание механизмов, лежащих в основе развития патологического процесса, позволяет выработать логически обоснованную стратегию лечения. В лечении синдрома невропатической боли используются антиконвуль-санты и антидепрессанты.
С целью диагностики наличия синдрома болевой невропатии, а также идентификации патофизиологических механизмов развития боли и гипералгезии необходимо провести клиническое обследование, направленное на определение характера боли и выявление различных видов гипералгезии. Знание механизмов, лежащих в основе развития патологического процесса, позволяет выработать логически обоснованную стратегию лечения. В лечении синдрома невропатической боли используются антиконвуль-санты и антидепрессанты.
Антиконвульсанты являются препаратами выбора при лечении невропатической боли. Данные лекарственные средства блокируют натриевые кана-
лы, генерирующие патологическую импульсацию; стимулируют ГАМК-ергическую активность; действуют как антагонисты глутамата. Для лечения невропатических болей используют следующие препараты: карбамазепин в дозе 400—600 мг/сут, фе-нитоин — 300 мг/сут, клоназепам — 4—6 мг/сут, вальпроевую кислоту — 1500—2000 мг/сут, ламот-риджин — 25—100 мг/сут, габапентин — 1200— 3600 мг/сут. Средние дозы препаратов подбирают индивидуально в каждом случае.
Трициклические антидепрессанты и ингибиторы обратного захвата серотонина усиливают нисходящие (серотонинергические) тормозные влияния на 5НТ рецепторы на уровне заднего рога спинного мозга. Применяют следующие препараты: амитриптилин — до 75 мг/сут; флуоксетин — 20— 40 мг/сут; паксил, рексетин — 20 мг/сут. В случаях недостаточной эффективности монотерапии амит-риптилином добиться более высокого антиноци-цептивного эффекта позволяет сочетанное использование амитриптилина (50 мг/сут) и антиконвуль-сантов типа клоназепама (4—6 мг/сут) или карбамазепина (400—600 мг/сут). Трициклические антидепрессанты могут снижать выраженность болевого синдрома или устранять его независимо от их антидепрессивного эффекта.
Основными принципами лечения психогенной дорсалгии являются коррекция психической, вегетативной и соматической сфер с учетом специфики каждого конкретного синдрома и индивидуальных особенностей пациента. Для коррекции психических расстройств с успехом применяют психотерапию (гипноз, поведенческую и аутогенную терапию), ориентированную на осознание больным связи боли с психогенными факторами. Психотропный препарат подбирают с учетом структуры синдрома психических нарушений. При преобладании тревожно-фобических расстройств назначают бензодиазепиновые анксиолитики (кло-назепам, ксанакс и др.), при депрессивных расстройствах — антидепрессанты (амитриптилин, фе-варин, паксил и т.д.), при ипохондрических расстройствах — нейролептики (эглек, сонапакс).
Для коррекции психических расстройств с успехом применяют психотерапию (гипноз, поведенческую и аутогенную терапию), ориентированную на осознание больным связи боли с психогенными факторами. Психотропный препарат подбирают с учетом структуры синдрома психических нарушений. При преобладании тревожно-фобических расстройств назначают бензодиазепиновые анксиолитики (кло-назепам, ксанакс и др.), при депрессивных расстройствах — антидепрессанты (амитриптилин, фе-варин, паксил и т.д.), при ипохондрических расстройствах — нейролептики (эглек, сонапакс).
При вегетативных нарушениях назначают веге-токорректоры (афобазол, грандаксин, атаракс).
Афобазол — производное 2-меркаптобензими-дазола, селективный анксиолитик, не относящийся к классу агонистов бензодиазепиновых рецепторов. Препарат обладает анксиолитическим и легким активирующим действием, при этом не оказывая гипноседативного и миорелаксирующего. При применении Афобазола не формируется лекарственная зависимость и не развивается синдром отмены. На 5—7 день лечения наблюдаются уменьшение или устранение тревоги, напряженности, соматических и вегетативных нарушений. Максимальный эффект
достигается к концу 4 недели лечения и сохраняется в послетерапевтическом периоде, в среднем 1—2 недели. Для лечения вегетативных нарушений вер-теброгенной природы Афобазол назначают по 10 мг в 3 приема в течение дня. Курс лечения — 2—4 недели. При необходимости суточная доза препарата может быть увеличена до 60 мг, а длительность лечения — до 3 месяцев.
При лечении вертеброгенной боли используют не только медикаментозные средства, но и методы мануальной терапии и физиотерапевтические процедуры. Однако следует помнить, что их можно назначать только через 5—10 дней после купирования болевого синдрома. Особую роль в терапии, преимущественно при стенозах и артрозах фасеточных суставов, играют препараты хондропротек-торного ряда, способствующие торможению дегенеративного процесса и снижаюшие вероятность хронизации боли. В неврологической практике предпочтение отдается препаратам для парентерального введения (алфлутопу). В комплексном лечении традиционно используются витаминосодержащие комплексы (амбене, бенфолипен, комбили-пен, мильгамма), гомеопатические препараты, дегидрационная терапия, препараты локального воздействия на очаг поражения.
В неврологической практике предпочтение отдается препаратам для парентерального введения (алфлутопу). В комплексном лечении традиционно используются витаминосодержащие комплексы (амбене, бенфолипен, комбили-пен, мильгамма), гомеопатические препараты, дегидрационная терапия, препараты локального воздействия на очаг поражения.
В неврологии очень широко применяются препараты витамина В (тиамин, пиридоксин, цианоко-
баламин) [24]. Перспективы в лечении дорсопатии связаны с разработкой новых лекарственных форм витаминов группы В — «нейротропных» витаминов, оказывающих специфическое влияние на функцию нервной системы. Биологически активным веществом бенфотиамина является тиаминдифос-фат, который ранее назывался тиаминпирофосфа-том. ТДФ — это кофермент различных многоферментных комплексов, среди которых наибольшее значение для нервных клеток имеют ферменты, участвующие в углеводном обмене. Тиамин-зависимые ключевые ферменты играют важную роль в окислительных процессах расщепления глюкозы. Путем изменения направления метаболизма промежуточных продуктов распада глюкозы — фруктозо-6-фосфата и глицеральдегид-3-фосфата, бенфотиамин препятствует активации патогенетических механизмов. Наряду с описанными эффектами, тиамину и пиридоксину в сочетании с цианоко-баламином может быть свойственно антиноцицеп-тивное действие. Пиродиксальфосфат, в качестве кофермента, участвует в синтезе серотонина, а тиамин выполняет важную функцию при его депонировании и транспорте. Именно здесь, возможно, находится точка реализации анальгетического действия фармакологических доз тиамина и пиридоксина. Тиамин, посредством усиления энергообеспечения в форме АТФ, поддерживает аксоплазматический
ШрММЧНЧм’н и СНУШМЮТ p&»*ntf РтмойСЧн -Ь&М1НЦ»Н ТЦПШфВЫИННИ пц-щга РЬос1*<срл4 4чие|иц|*<
BlflpUHt lUyiHLH У r:. низапар
низапар
Запив и прщачма коиОнренцни на сайге WWW.Cipodjta.ru
f h ч г Инирнгг-пацдсрма-
транспорт, пиридоксин участвует в синтезе транспортных белков, а цианокобаламин обеспечивает доставку жирных кислот для клеточных мембран и миелиновой оболочки. Жирорастворимые формы витамина В1 (бенфотиамин) имеют преимущества по сравнению с водорастворимыми.
Бенфолипен — комбинированный поливитаминный комплекс. В его состав входят: бенфотиа-мин (жирорастворимая форма витамина В1, 100 мг), пиридоксина гидрохлорид (витамин В6, 100 мг), цианокобаламин (витамин В12, 2 мкг). Препарат принимают после еды, не разжевывая и запивая небольшим количеством жидкости.
Комбилипен — комбинированный поливитаминный препарат. Действие препарата определяется свойствами витаминов, входящих в его состав: тиамина гидрохлорида (100 мг), пиридоксина гидрохлорида (100 мг), цианокобаламина (1 мг). Препарат также содержит лидокаина гидрохлорид (20 мг). Комбилипен выпускается в ампулах по 2 мл. Максимальный клинический эффект достигается при его назначении в комбинации с НПВП. При выраженных проявлениях заболевания комбилипен вводят внутримышечно по 2 мл ежедневно в течение 5—7 дней, затем по 2 мл 2—3 раза в неделю в течение 2 недель; в легких случаях по 2 мл 2—3 раза в неделю в течение 7—10 дней. Продолжительность
курса инъекций не должна превышать 2 недели. В дальнейшем для поддерживающей терапии рекомендуется прием бенфолипена по 1 таблетке 1—3 раза в день курсом, не превышающим 4 недели.
Оптимальным средством воздействия на периферический источник боли — как первичный, так и рефлекторный — являются мазевые и гелевые формы лекарственных средств, обладающих противовоспалительным и миорелаксирующим действием. исок литературы вы можете запросить в редакции.
исок литературы вы можете запросить в редакции.
Диагностика и лечение вертеброгенных болевых синдромов шейной локализации в условиях поликлиники
Боль в области шеи распространенной жалобой, предъявляемой пациентами неврологу. Первичные обращения в поликлинику по поводу шейных болевых синдромов составляет около 12% по отношению ко всем неврологическим больным и часто являются причиной временной утраты трудоспособности.
Клинические проявления вертеброгенных заболеваний формируются из неврологических, ортопедических и рентгенологических феноменов. Неврологические расстройства развиваются вследствие рефлекторных и компрессионных изменений, вызванных дегенеративно-дистрофическими изменениями позвоночника. Рефлекторные синдромы на шейном уровне занимают значительное место и отличаются своим многообразием. Среди них выделяют цервикалгию, мышечно-тонические, вазомоторные и нейродистрофические синдромы. Синдром цервикалгии, проявляющийся болями в виде «прострелов» или постоянных болевых ощущений в области шеи, или шеи и головы (цервикокраниалгия) часто наблюдается при дорсопатии шейного отдела позвоночника. Одновременно отмечается ограничение подвижности шеи. Иногда при движении головой пациент ощущает треск, который слышен на расстоянии. Такие шейные прострелы могут предшествовать возникновению различных рефлекторных нейродистрофических синдромов. Из нейродистрофических синдромов наиболее часто диагностируется плечелопаточный пери-артроз, который в свою очередь, может явиться причиной вторичного вовлечения окружающих мышц, нервов, сосудов. Клиническое течение плечелопаточного периартроза в значительной мере определяется его неврологическими осложнениями. В развитии симптоматики большое значение имеет как непосредственное поражение вегетативных структур, так и включение патологических импульсов через эти структуры. Заболевание протекает длительно, часто приводит к утрате временной трудоспособности, следовательно, требует к себе внимания неврологов в плане профилактики, правильности диагностики и лечения. По поликлиническим наблюдениям чаще страдают женщины в возрасте приблизительно от 40 до 65 лет. Давность болевого синдрома может составлять от нескольких месяцев до нескольких лет. Ведущими жалобами являются боли в области плечевого сустава, усиливающиеся при движениях (особенно при отведении плеча кзади и в сторону) и иррадиирующими в руку и шею. При осмотре отмечается болезненность при пальпации паравертебральных точек и остистых отростков шейно-грудного отдела позвоночника, пораженного плечевого сустава, ограничение подвижности в этом суставе. Вегетативные расстройства проявляются в виде отечности, похолодания и синюшности руки. Клинические проявления в большинстве случаев сопровождаются рентгенологическими изменениями в шейном отделе позвоночника. Средняя длительность временной нетрудоспособности при данном заболевании составляет 21 день.
По поликлиническим наблюдениям чаще страдают женщины в возрасте приблизительно от 40 до 65 лет. Давность болевого синдрома может составлять от нескольких месяцев до нескольких лет. Ведущими жалобами являются боли в области плечевого сустава, усиливающиеся при движениях (особенно при отведении плеча кзади и в сторону) и иррадиирующими в руку и шею. При осмотре отмечается болезненность при пальпации паравертебральных точек и остистых отростков шейно-грудного отдела позвоночника, пораженного плечевого сустава, ограничение подвижности в этом суставе. Вегетативные расстройства проявляются в виде отечности, похолодания и синюшности руки. Клинические проявления в большинстве случаев сопровождаются рентгенологическими изменениями в шейном отделе позвоночника. Средняя длительность временной нетрудоспособности при данном заболевании составляет 21 день.
Компрессионные синдромы, обусловленные изменениями шейного отдела позвоночника в зависимости от числа поврежденных корешков, подразделяются на моно, бирадикулярные и плексопатии. Корешковый синдром отличается стадийностью течения. В первой стадии, дискалгической (невралгической; стадии симптомов раздражения), преобладают резкие боли, гиперестезия, оживление сухожильных рефлексов, защитное напряжение мышц, болезненность паравертебральных точек. Для второй невритической стадии (стадии симптомов выпадения) характерны менее резкие боли, выпадение чувствительности в зоне соответствующего корешка, угасание периостальных рефлексов, локальные гипотрофии, сохраняющееся локальное мышечное напряжение и болезненность паравертебральных точек.
Диагностический процесс при спондилогенных болевых синдромах шейной локализации включает субъективную оценку боли пациентом, опрос и осмотр: исследование функции мышц, суставно-связочного аппарата, а также корешков спинного мозга и нервов. При исследовании мышц, суставно-связочного аппарата шейно-грудного отдела позвоночника определяются степень нарушения функции пораженного отдела и суставов (плечевых, локтевых), наличие болезненных(триггерных) зон и очагов миогелоза, степень мышечного напряжения.
Кроме клинического обследования проводится рентгенологическое исследование шейного отдела позвоночника в двух стандартных проекциях с функциональными пробами; при исследовании суставов проводятся обзорные снимки в двух проекциях.
Компьютерная рентгеновская томография (КТ) позвоночника в сагитальной и аксиальной проекциях позволяет анализировать состояние структур позвоночного канала и межпозвонковых отверстий, определять направление и величину грыжевых выпячиваний и остеофитов, степень компрессии нервного корешка.
Магнитнорезонансная томография (МРТ) проводится в сагитальной проекции и позволяет визуализировать позвоночный столб, спинной мозг, дуральный мешок на большом протяжении. Реконструкция срезов в горизонтальной проекции позволяет уточнить анатомические особенности межпозвонковых дисков, дугоотросчатых суставов и нервных корешков. Эффективность лечения пациентов с шейными болевыми синдромами во многом зависит от своевременности начатого лечения.
В острой стадии назначается ортопедический режим, фармакотерапия с учетом переносимости препаратов и показаний в зависимости от выраженности симптомов (НСПВС, миорелаксанты, витамины группы В, сосудистые препараты, антидепрессанты, местно применяются растирания мазями). Хороший терапевтический эффект получен от внутримышечного комплексного применения гомеопатических препаратов ( цель Т, траумель С, дискус композитум). Значительные улучшения у пациентов наступают от физиотерапевтического лечения диадинамическими токами, электрофорезом, фонофорезом гидрокортизона на зоны нейромиоостеофиброза. В ряде случаев применяется инфильтрационная терапия, иглотерапия. После уменьшения спонтанных болей назначается массаж, лечебная физкультура. Мануальная терапия проводится по показаниям с целью нормализации нарушенного мышечно-тонического дисбаланса на шейно-грудном уровне. Наиболее эффективным является применение мобилизационной методики с постизометрической релаксацией и техники миофасциального расслабления при мышечно-тоническом напряжении. -Ч’ О /
-Ч’ О /
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
АКТУАЛЬНОСТЬ. На современных предприятиях цветной металлургии растет количество рабочих мест с воздействием комплекса неблагоприятных факторов физической и химической природы, а также увеличивается время их воздействия на организм работника.
Несмотря на проводимые инженерно-технические мероприятия, рабочие металлургических предприятий продолжают подвергаться воздействию неблагоприятных факторов производственной среды, ведущими из которых являются тяжелый физический труд, нагревающий микроклимат и сложные аэрозоли металлов и других веществ. На некоторых рабочих местах максимальная температура воздуха в теплый период года достигает 50°С, а максимальное значение инфракрасного спектра излучения — превышает ПДУ в 10 и более раз. При этом значительную часть рабочего времени (28,6-57,1%) вышеуказанный контингент занят выполнением тяжелого физического труда в условиях загазованности, запыленности, воздействия физических факторов. Такие условия труда негативно отражаются на состоянии здоровья работающих (Шпигель A.C., 1990; Лях Г.Д., 1992; Семенникова Т.К. с соавт., 1992, 1995; Косарев В.В., 1993, 2001; Коневских Л.А., 1996; Карханин Н.П., 1998; Рослый О.Ф., 2000; Чащин М.В., 2000).
Имеются убедительные результаты экспериментальных, клинико-физиологических, эпидемиологических, исследований, свидетельствующих о значительной роли вредных факторов металлургического производства в развитии болезней различных органов и систем: сердечно-сосудистой патологии (Монаенкова A.M. с соавт., 1980; Крюков H.H., 1997; Черкесов В.В., 2000; P.G. Lund-Larsen et al„ 1991; Galloway S., 1999), заболеваний легких пылевой этиологии, в том числе и пылевого бронхита (Крушевский В.Д., 1994; Величковский В.Т., 1997; Осипов Ю.А. с соавт., 1997), заболеваний пищеварительного тракта (Агибалов А.Н., 1988; Абламунец Н.Г., 1996), неврологической патологии, связанной с дегенеративно-дистрофическими
нарушениями (Каратай Ш. С., Иванов В.В.1991; Романова В.М., 1993; Бараев И. А., 1995).
С., Иванов В.В.1991; Романова В.М., 1993; Бараев И. А., 1995).
Однако, в литературе мы не нашли сведений, отражающих функциональное состояние органов дыхания, пищеварения, сердечнососудистой системы и вегетативной регуляции сердечной деятельности у работников металлургических предприятий по вторичной переработке алюминия, работающих в неблагоприятных производственных условиях.
В связи с этим изучение нарушений адаптационно-компенсаторных реакций организма у работников предприятия по вторичной переработке алюминия является актуальной проблемой, т.к. позволит выявить доклинические стадии заболеваний, разработать мероприятия, направленные на профилактику их развития.
ЦЕЛЬ ИССЛЕДОВАНИЯ. Оценить состояние здоровья работников металлургического предприятия по вторичной переработке алюминия, разработать комплекс диагностических и лечебно-профилактических мер для своевременной коррекции нарушений сердечно-сосудистой, дыхательной, пищеварительной систем и вертеброгенных расстройств.
ЗАДАЧИ ИССЛЕДОВАНИЯ.
1. Определить структуру общей заболеваемости работников, подвергающихся воздействию вредных факторов производственной среды металлургического предприятия, установить нозологические формы, преобладающие в ней.
2. Выявить нарушения вегетативной регуляции сердечной деятельности, связанные с большим стажем работы во вредных условиях у лиц, не имеющих клинико-инструментальных признаков патологии сердечно-сосудистой системы.
3. Установить влияние длительного воздействия вредных профессиональных факторов на сократимость миокарда у работников
прессового и литейного производств и выявить у них скрытую патологию сердечно-сосудистой системы.
4. Определить влияние вредных факторов металлургического производства на систему внешнего дыхания и выявить среди работников алюминиевого производства лиц со скрыто протекающей патологией легких.
5. Изучить заболеваемость с временной утратой трудоспособности, обусловленную болезнями пищеварительной системы, связанную с влиянием на нее комплекса вредных факторов современного металлургического предприятия.
6. Оценить патогенность биомеханики производственных движений различных групп работающих и ее влияние на возникновение у них патологии позвоночника
7. Установить зависимость между заболеваниями внутренних органов и дегенеративно-дистрофическим поражением соответствующих сегментов позвоночника у работников металлургического производства, а также разработать комплекс диагностических и лечебно-профилактических мероприятий для своевременной коррекции нарушений сердечно- сосудистой, дыхательной, пищеварительной систем и дегенеративно- дистрофических изменений позвоночника.
НАУЧНАЯ НОВИЗНА.
В работе впервые оценено воздействие комплекса неблагоприятных факторов производственной среды металлургического предприятия по вторичной переработке алюминия на организм работника.
Выявлены скрытые закономерности повреждающего воздействия комплекса вредных факторов производственной среды металлургического предприятия на сердечно-сосудистую, дыхательную, пищеварительную системы и позвоночник.
Впервые выявлена зависимость распространенности соматической патологии от нарушений в соответствующем отделе позвоночника у работников металлургического производства.
Предложены комплексные методики профилактики и лечения профессиональной и соматической патологии в условиях современного металлургического предприятия.
ПРАКТИЧЕСКАЯ ЗНАЧИМОСТЬ.
Материалы проведенного исследования составили основу отчета и заключительного акта обследования работников Самарского металлургического завода и использовались при разработке и внедрении мер профилактики заболеваний и охраны здоровья трудящихся.
Оценена эффективность предложенного комплекса лечебно-профилактических мероприятий по лечению и реабилитации больных с поражением позвоночника профессионального генеза на базе санатория-профилактория «Металлург».
Информативность использованных в ходе работы методик позволит рекомендовать их для включения в периодический профилактический медосмотр на крупном промышленном предприятии с целью оценки состояния внутренних органов у лиц, контактирующих с производственными вредностями.
Предложенные методы лечения и профилактики вертеброгенных и соматических расстройств позволят уменьшить вероятность развития как неспецифической, так и профессиональной патологии, что в условиях промышленного предприятия приводит к снижению общей и профессиональной заболеваемости, распространенности заболеваний сердечно-сосудистой, дыхательной, пищеварительной систем и опорно-двигательного аппарата, а также связанного с этим экономического ущерба.
Материалы и результаты исследований также включены в программу обучения студентов курса профессиональных болезней на кафедре профзаболеваний и клинической фармакологии СамГМУ.
АПРОБАЦИЯ РАБОТЫ.
По материалам диссертации опубликовано 9 работ. Основные положения работы представлены в виде докладов на конференции «Актуальные проблемы профилактики неинфекционных заболеваний» (Москва, 1999), на VII Национальном Конгрессе по болезням органов дыхания (Москва, 1997), на Всероссийской научно-практической конференции «Медико-биологические и эколого-гигиенические проблемы оценки и прогнозирования воздействия факторов окружающей среды» (Санкт-Петербург, 1998), на VI Международном Конгрессе «Экология и здоровье человека» (Самара, 1999).
ОСНОВНЫЕ ПОЛОЖЕНИЯ, ВЫНОСИМЫЕ НА ЗАЩИТУ.
1. Методика и результаты комплексной неинвазивной доклинической диагностики нарушений сердечно-сосудистой, дыхательной и пищеварительной систем с целью выявления влияния комплекса вредных факторов производства по переработке на регуляцию сердечной деятельности, состояния органов кровообращения, дыхания и пищеварения, а также позвоночника у различных групп работников.
2. Особенности биомеханики производственных движений у различных групп рабочих металлургического предприятия в связи с поражением позвоночника и соматической патологией. Разработанный с их учетом комплекс мероприятий по лечению и реабилитации больных с поражением позвоночника и соматической патологией и результаты его применения.
ОБЪЕМ И СТРУКТУРА РАБОТЫ.
Диссертация включает следующие разделы: введение, обзор литературы, материалы и методы исследования, гигиеническую оценку условий труда прессового и литейного производств, результаты проведенных клинических и физиологических исследований, обсуждение результатов, выводы,
практические рекомендации, список литературы, включающий труды 285 отечественных и 78 иностранных авторов. Изложена на 153 страницах машинописи, иллюстрирована 1 рисунком и 17 таблицами.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ.
Основу клинических наблюдений составил углубленный медицинский осмотр рабочих, подвергающихся воздействию комплекса вредных производственных факторов Самарского металлургического завода, выявивший группу больных общесоматическими заболеваниями и группу риска по их возникновению. В 1997-2001 годах на базе областного профпатологического центра было проведено комплексное обследование и лечение данных групп рабочих. За период проведения клинических наблюдений большинство обследованных было осмотрено 2 и более раз.
По профессиональным группам обследованные распределились следующим образом: литейщики — 860 человек (51,8%), прессовщики 800 человек (48,2%).
Производственный стаж работы составлял от 1 до 15 и более лет, причем 27,7 % обследованных имели стаж работы во вредных условиях более 15 лет.
По данным санитарно-гигиенических характеристик условий труда все обследованные в процессе работы подвергались воздействию комплекса идентичных вредных факторов производственной среды. По принятой в настоящее время классификации условий труда по степени вредности и опасности («Гигиенические критерии оценки и классификация условий труда по показателям вредности и опасности производственной среды, тяжести и напряженности трудового процесса» Р.2.2.755-99) изученные профессии отнесены к классам 3 (вредному) и 4 (опасному), т.е. к таким, при которых возможно развитие профессиональной патологии.
При проведении клинического исследования наряду с общеклиническими методами скринингового контроля, проводимого в ходе периодических профилактических медосмотров, а также углубленных
исследований в условиях клиники профессиональных болезней и амбулаторно, нами были использованы адекватные инструментальные тесты. Углубленное обследование специалистами — терапевтом, невропатологом, пульмонологом, гастроэнтерологом проводилось по общепринятой методике.
Сократительную способность миокарда изучали с помощью комплекса неинвазивных методов: тетраполярной реографии, М-эхокардиографии, визуально-поисковой допплерэхо-кардиографии. М-эхокардиография проводилась на аппарате Hewlett Packard «SANOS»-1000 (Япония). Тетраполярная реография аорты и реокардиография проводились на реоплетизмографе РПГ2-02 с определением фазовой структуры сердечного цикла, оценки сократительной функции миокарда для определения ударного и минутного объема кровообращения (УО). Анализ реограмм проводился с учетом качественных и количественных характеристик. Качественная характеристика учитывала амплитуду, регулярность кривой, количество и выраженность дополнительных волн.
С целью изучения функциональных расстройств сердечной деятельности применялся автокорреляционный и спектральный анализ волновой периодики сердечного ритма по Д. Жемайтите (1987). Выбор метода обусловливался его информативностью, неинвазивностью, а также доказанным формированием вегетативных дизрегуляторных сдвигов в сердечно-сосудистой системе, реализующейся при длительном воздействии комплекса неблагоприятных факторов производственной среды.
Для оптимизации функциональной диагностики респираторных расстройств при скрининговых исследованиях у работников, подвергающихся длительному воздействию комплекса неблагоприятных факторов металлургического производства проведено анкетирование 450 рабочих прессового цеха. По результатам анкетирования была отобрана группа из 300 человек, у которых выявлялся ряд симптомов заболеваний органов дыхания, либо имеющих стаж работы по специальности более 10 лет. В данной группе
В данной группе
работников проведено клинико-инструментальное обследование с применением вентилометрии на приборе фирмы Клемент Кларк. Флоуметрия проводилась на аппарате «Флоускрин» фирмы Эрих Егер 245 рабочим.
Анализ показателей заболеваемости с временной утратой трудоспособности (ЗВУТ) по поводу заболеваний желудочно-кишечного тракта проведен по числу болевших лиц, случаев и дней нетрудоспособности на 100 работающих в среднем за 2 года в целях апостериорной оценки риска возникновения патологии пищеварения у работников, занятых во вредных профессиях на металлургическом предприятии.
Биомеханическое исследование проводилось с применением теле- и киносъемки рабочих операций, томографии, с последующей кодировкой типа биомеханики. При этом детальному визуальному изучению подвергнуты отдельные элементы кинематических цепей основных операций у рабочих.
Комплекс примененных методов исследования позволяет наряду с углубленным обследованием работников выявлять доклинические нарушения сердечно-сосудистой, дыхательной систем. Использованная методика изучения биомеханики производственных движений позволила выявить факторы, влияющие на развитие патологии позвоночника и сочетания ее с соматической.
Полученные результаты были подвергнуты математической обработке с использованием методов вариационной статистики с учетом стажа работы по специальности, возрасту, полу. Достоверность различия между изучаемыми показателями оценивалась по критерию «ь> Стьюдента. Различия считали достоверными при величине I = 1,96 и более, что соответствует заданной надежности не ниже 95%.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ.
В результате проведенных исследований установлено, что жалобы, связанные с функциональными расстройствами сердечной деятельности и вегетативно-сосудистыми нарушениями предъявляли 40% обследованных. Нами у работников металлургического предприятия установлена более
высокая по сравнению с контролем и другими популяциями распространенность нейроциркуляторной дистопии и других заболеваний сердечно-сосудистой системы (соответственно 7,8±0,034 и 7,4±0,033 у обследуемых прессовщиков; 8,5±0,032 и 6,6±0,029 у литейщиков и 5,5±0,057 и 5,510,057 у контрольной группы.
Оценка показателей сократительной способности миокарда работников показала достоверный рост у них массы миокарда, снижение диастолического объема левого желудочка, фракций выброса и ударного объема с увеличением стажа работы со специальности (достоверность р<0,05). В контрольной же группе с увеличением стажа работы сократимость миокарда существенно не менялся. Причем, этот процесс протекает неравномерно. Вслед за напряжением адаптационных резервов сердца на первом году работы в условиях металлургического предприятия происходит постепенное их истощение. В результате у лиц, выполняющих тяжелую физическую работу в нагревающем микроклимате, при воздействии сложных аэрозолей и шума более 10 лет, эти показатели достоверно (р<0,05) ниже, чем у рабочих контрольной группы с аналогичным стажем работы, что можно считать ранней доклинической стадией сердечной недостаточности. В литературе имеются данные о целесообразности использования эхокардиографического метода с целью выявления доклинических изменений сердечной деятельности (Обухова A.A. с соавт., 1995).
Примененный нами метод автокорреляционного анализа ритмограмм также известен как наиболее информативный в плане выявления нарушений вегетативной регуляции сердечного ритма и скрытой патологии сердечнососудистой системы (Шестаков В.Н., 1999; Мачерет E.JI. с соавт., 2000; von Speidel Т., 1999).
При автокорреляционном анализе ритмограмм работников обследуемой группы, у которых при электрокардиографическом исследовании не выявилось значимых отклонений от нормы, выяснилось, что регуляция сердечного ритма
у них достоверно отличалась от контроля снижением парасимпатического влияния, известного своей протектирующей ролью.
С помощью активной ортостатической пробы определялась способность
7
сердечно-сосудистой системы адаптироваться к физической нагрузке. Целесообразность использования этой пробы в качестве стандарта физического напряжения подтверждается многими исследователями (Миронова Т.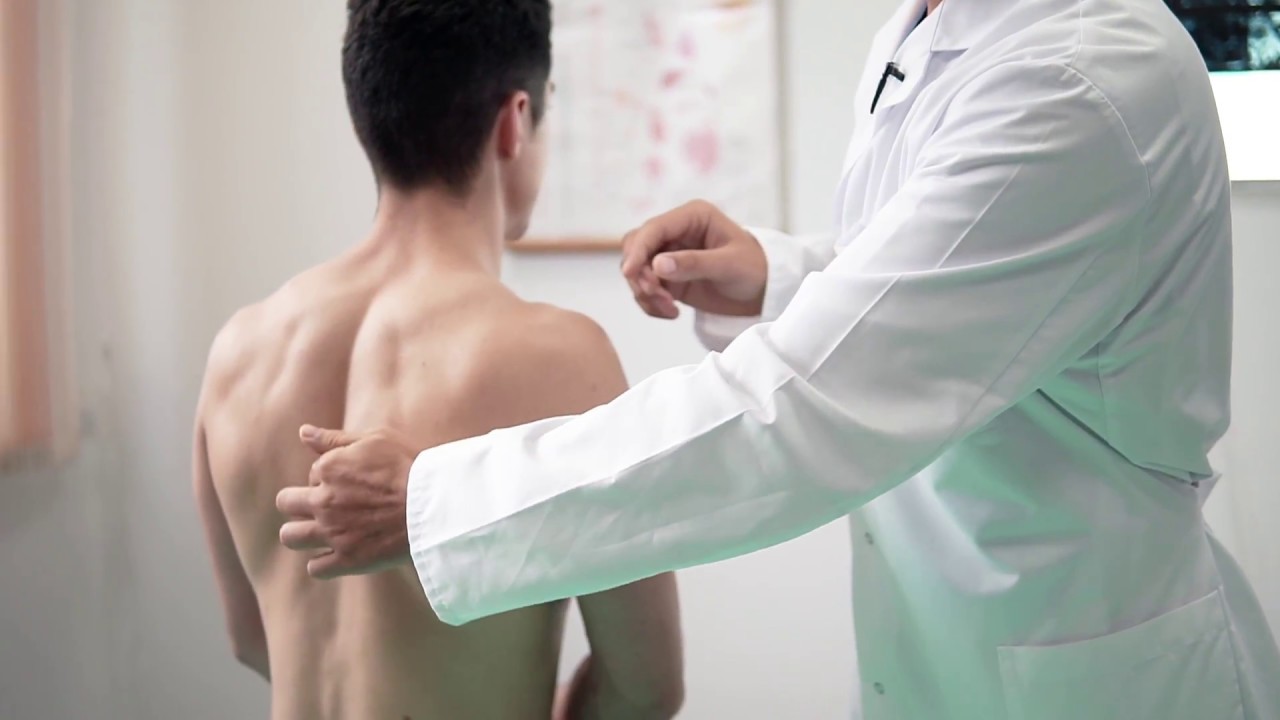 Ф., 2000; Кирячков Ю.Ю. с соавт., 2000; Laitnen Toni et al„ 1999; Lollgen H., 1999). Изменения сердечной деятельности при этом были разнонаправлены, во всех случаях свидетельствуя о патологических изменениях вегетативной регуляции сердечного ритма и формировании кардиоваскулярной автономной нейропатии (КВАН). Клинически это явление представлено «ригидным пульсом» на фоне тахикардии и предшествует манифестации нескольких нозологических единиц сердечно-сосудистой патологии (Маколкин В.Н., Аббакумов С.А., Романов М.М., 1975; Иванова С.Н., 2000). Она предшествует манифестированным формам сердечно-сосудистой патологии, нозологическая принадлежность которой определяется, по-видимому, сочетанным патогенетическим эффектом или первичным поражением. В одних случаях, например, сочетание неспецифической КВАН с атеросклеротической несостоятельностью венечных сосудов приводит к клиническим проявлениям ишемической болезни сердца, во других — к миокардиодистрофическому процессу. На рис.1 демонстрируются ритмограммы и спектрограммы частотной характеристики волновой структуры СР у работника ремонтно-механического цеха (а) и прессовщика со стажем работы во вредных условиях более 10 лет (б). У первого заметны трехкомпонентная структура волн, а у второго — отсутствие модуляций ритма а ритмограммах и спектрограммах
Ф., 2000; Кирячков Ю.Ю. с соавт., 2000; Laitnen Toni et al„ 1999; Lollgen H., 1999). Изменения сердечной деятельности при этом были разнонаправлены, во всех случаях свидетельствуя о патологических изменениях вегетативной регуляции сердечного ритма и формировании кардиоваскулярной автономной нейропатии (КВАН). Клинически это явление представлено «ригидным пульсом» на фоне тахикардии и предшествует манифестации нескольких нозологических единиц сердечно-сосудистой патологии (Маколкин В.Н., Аббакумов С.А., Романов М.М., 1975; Иванова С.Н., 2000). Она предшествует манифестированным формам сердечно-сосудистой патологии, нозологическая принадлежность которой определяется, по-видимому, сочетанным патогенетическим эффектом или первичным поражением. В одних случаях, например, сочетание неспецифической КВАН с атеросклеротической несостоятельностью венечных сосудов приводит к клиническим проявлениям ишемической болезни сердца, во других — к миокардиодистрофическому процессу. На рис.1 демонстрируются ритмограммы и спектрограммы частотной характеристики волновой структуры СР у работника ремонтно-механического цеха (а) и прессовщика со стажем работы во вредных условиях более 10 лет (б). У первого заметны трехкомпонентная структура волн, а у второго — отсутствие модуляций ритма а ритмограммах и спектрограммах
Рис.1 Ритмограммы и спектрограммы работника из контрольной группы (а) и работника прессового производства (б) в состоянии покоя и в активной ортостатической пробе.
В области диагностики хронических неспецифических заболеваний легких достигнуты значительные успехи. Однако, попытки раннего выявления этой группы патологий, в том числе хронического бронхита, не привели к полному успеху. Это объясняется тем, что клиническая и инструментально-лабораторная объективизация его ранних признаков недостаточно результативна (Артамонова В.Г., 1998; Осадчук М.А. с соавт., 1999; Христенко И.Д., 1999; Кулакова Н.В. с соавт., 2000). Функциональные легочные тесты широко применяются при диагностике хронических болезней легких. Однако, чаще всего, они не используются во время периодических медицинских осмотров, а только на этапе пребывания больного в стационаре, то есть в фазе
Однако, чаще всего, они не используются во время периодических медицинских осмотров, а только на этапе пребывания больного в стационаре, то есть в фазе
манифестации заболевания. При этом, еще одна причина диагностики этой патологии в позднем периоде в том, что у пациентов могут отсутствовать клинические симптомы даже при низком показателе объема форсированного выдоха за 1 секунду — ОФВ 1 (ХОБЛ, 1998).
Проведенный нами анализ функции внешнего дыхания рабочих с воспалительной формой хронического пылевого бронхита определил, что имела место достоверно фиксируемая обструкция дыхательных путей. При этом происходило снижение по сравнению с контрольной группой, таких параметров ФВД: ЖЕЛ, ОФВ 1, ФЖЕЛ (р>0,05). Обструктивные нарушения у пациентов с астматической формой пылевого бронхита достоверно выявлялись не только на уровне средних (ФЖЕЛ, ОФВ 1,ОФВ 1/ФЖЕЛ, ППВ), но и мелких (МОС25, МОС75) бронхов.
Среди рабочих с эмфизематозной формой ХПБ также выявлена обструкция дыхательных путей, при этом ЖЕЛ, ФЖЕЛ, ОФВ1 и ППВ были достоверно ниже, чем в контрольной группе (р>0,05).
Однако спирограмма без динамических проб не всегда позволяет выявить ранние респираторные нарушения. Весьма важно, что тест с бронходилататором в случае диагностики астматической формы пылевого бронхита являлся высокоинформативным признаком. Кроме этого, скрытая бронхиальная обструкция выявлялась с помощью бронходилатационного теста (р>0,05) в группе больных с другими формами бронхита.
Таким образом, спирометрия, включенная в периодический медицинский осмотр на предприятии, позволяет раньше обнаружить признаки хронического пылевого бронхита даже при отсутствии клинических симптомов, а применение теста с бронхолитиком дает возможность установить скрытые обструктивные нарушения. Поэтому серийные скрининговые измерения функции внешнего дыхания — наилучший метод раннего выявления хронического пылевого бронхита, что подтверждает литературные данные (Антонов Н. С., Чучалин А.Г., 1996).
С., Чучалин А.Г., 1996).
Согласно современным представлениям о патогенезе, хронический бронхит — это воспалительное заболевание дыхательных путей. Причем, в период ремиссии оно имеет небактериальный характер. При воспалении происходит активация лейкоцитарного пула, что является неспецифической реакцией организма на воспалительный процесс. По данным литературы, в период обострения воспаления при хроническом бронхите происходит активация эозинофилов (Кулакова Н.В. с соавт., 2000). Полученные нами результаты подтверждают имеющиеся сведения об участии эозинофилов в патогенезе хронического бронхита. Более того, по уровню повышения эозинофильного катионного белка можно судить о клинической форме пылевого бронхита: астматическая, воспалительная, эмфизематозная.
Результаты анализа крови на содержание эозинофильного катионного белка (ЭКБ) показали, что он достоверно превышал допустимый уровень не только при манифестных формах пылевого бронхита, но и при ранних («латентных»). Это свидетельствует о том, что на начальном этапе развития патологического процесса при пылевом бронхите имеет место эозинофильное воспаление. Можно также сказать, что у больных хроническим пылевым бронхитом с клинически определяемой обструкцией, по сравнению с другими субъектами концентрация ЭКБ выше, в связи с тем, что при этом заболевании имеет место эозинофильная активация, которая сравнима с таковой при астме, что подтверждает литературные данные (Ando F., Ruggieri А., 1996; Kroegel С., 1994, Borchers Michael Т. et al., 1999). Таким образом, следует признать определенное участие эозинофилов в воспалении при хроническом пылевом бронхите, что не противоречит литературным данным (Keatings V.M., 1996) и открывает перспективу использования данного маркера при скрининге данной патологии.
Повышение показателя муцинового антигена (р<0,05) во всех нозологически значимых группах свидетельствует о том, что степень его
возрастания может сыграть определенную роль в установлении как манифестных, так и ранних форм хронического пылевого бронхита.
Регрессионный анализ показал, что наиболее значимым показателем вентиляционной функции легких в диагностике наиболее часто встречающихся в клинической практике манифестных форм хронического бронхита: воспалительной и эмфизематозной — явились ФЖЕЛ и ФЖЕЛ, ППВ соответственно. Это совпадает с последними литературными данными (Чучалин А.Г., 1998). Для астматической формы ХПБ из функциональных показателей первостепенную диагностическую значимость имел положительный результат теста с бронходилататором и МОС50, поскольку при астматической форме пылевого бронхита одним из основных патогенетических моментов является гиперреактивность бронхов, в результате которой формируется обратимый (в том числе под влиянием бронхолитика) спазм гладкой мускулатуры бронхов.
При ранней стадии ХПБ выявлялись достоверные изменения таких параметров ФВД, как ППВ, тест с бронходилататором, МОС25. Отсюда следует, что идентификация хронического бронхита в более ранней стадии вполне реальна. Она наиболее актуальна когда есть обратимый, пусть даже скрытый бронхоспазм. Это не противоречит литературным сведениям о выделении латентного пылевого бронхита, при котором могут отмечаться либо очень скудные клинические данные, либо отсутствие таковых, однако, при этом уже могут определяться функциональные нарушения (Измеров Н.Ф., Монаенкова A.M., 1996).
Анализ состояния пищеварительного тракта у работников, занятых во вредных условиях металлургического производства показал, что распространенность основных нозологических форм патологии ЖКТ (хронический гастрит, гастродуоденит, язвенная болезнь, хронический холецистит) у них достоверно выше по сравнению с контрольной группой (соответственно 9,9±0,038 и 6,5±0,065).
Метод, выбранный нами для углубленного исследования патологии пищеварительной системы, позволяет оценить как клинический, так и эпидемиологический и экономический аспекты данных нозологических форм (Г.Д. Лях, 1992). Уровень заболеваемости, обусловленный болезнями системы пищеварения, в целом по изучаемому контингенту работающих оказался достоверно выше, чем в контроле и составил 4,0 случая и 77,0 дней нетрудоспособности на 100 работающих. В контрольной группе эти показатели составили 3,7 случая и 56,9 дня нетрудоспособности. Это свидетельствует и о том, что у рабочих изучаемых производств заболевания пищеварительной системы протекают более тяжело и длительно.
В контрольной группе эти показатели составили 3,7 случая и 56,9 дня нетрудоспособности. Это свидетельствует и о том, что у рабочих изучаемых производств заболевания пищеварительной системы протекают более тяжело и длительно.
Наиболее частой патологией у работников металлургического производства оказался остеохондроз позвоночника, связанный по нашему мнению с нефизиологичной биомеханикой производственных движений. Большинство обследованных жаловались на боли в области позвоночника при стаже работы более 5 лет. Как правило, боли начинались в связи с подъемом тяжести. По мере увеличения стажа частота жалоб на боли в поясничной области нарастала.
Патология опорно-двигательного аппарата встречалась у 27,1+0,1% рабочих обследуемой группы. В контрольной группе этот показатель был достоверно ниже и составил 20,0±0,4%. Многолетние обследования работников металлургического производства показали, что у них остеохондроз поясничного отдела позвоночника встречается в 1,5 раза чаще, чем у работников других предприятий, на 20% продолжительнее пребывание на больничном листе, в 2 раза больше больных, направленных на стационарное лечение, более 3% ежегодно направляется на МСЭК (Косарев В.В. и соавт., 1998; БиасНсаш Р. е1 а1„ 1997; УовЫтига №эпсо « а1„ 2000).
Анализ патологического воздействия биомеханики производственных движений работников, занятых в металлургическом производстве позволил выявить некоторые их особенности. Они обуславливают возникновение
начальных проявлений дегенеративно-дистрофических изменений позвоночника металлургов, ранее относившиеся к доклиническим.
Биомеханические исследования рабочих мест и операций для установления влияния различных производственных движений на возникновение и развитие проявлений остеохондроза применялись наряду с клиническими приемами выявления ранних признаков дегенеративно-дистрофических изменений.
Начальные проявления и течение поясничного остеохондроза у рабочих металлургического производства также имеют ряд особенностей. При раннем распознавании придавалось значение не столько органическому поражению позвоночника, что возникало, как уже указывалось, значительно позже, а так называемым предвестникам, то есть первичным патологическим отклонениям со стороны мышц спины и поясничной области. Общепризнанным является то, что дегенеративно-дистрофические изменения в позвоночнике клинико-рентгенологически проявляются и выявляются лишь через 12-18 месяцев с момента заболевания (Van der Weide W.E. et al., 1997). Значимость рентгенологического исследования поэтому на ранних этапах фактически сводится к нулю (Бараев И.А., 1995). Учитывая это, от рентгеновского исследования с целью диагностики остеохондроза, особенно на ранних стадиях, мы отказались. Основные симптомы остеохондроза — боль, болезненность при пальпации, обездвиженность, однако, не постоянны. Поэтому мы пользовались для выявления начальных стадий болезни методом определения повышенного мышечного тонуса в области пораженного сегмента по сравнению с выше и ниже лежащими отделами позвоночника, вызываемое поколачиванием молоточка, особенно асимметричность напряжения при одностороннем поражении. Этот симптом выявлялся у 90 % пациентов.
При раннем распознавании придавалось значение не столько органическому поражению позвоночника, что возникало, как уже указывалось, значительно позже, а так называемым предвестникам, то есть первичным патологическим отклонениям со стороны мышц спины и поясничной области. Общепризнанным является то, что дегенеративно-дистрофические изменения в позвоночнике клинико-рентгенологически проявляются и выявляются лишь через 12-18 месяцев с момента заболевания (Van der Weide W.E. et al., 1997). Значимость рентгенологического исследования поэтому на ранних этапах фактически сводится к нулю (Бараев И.А., 1995). Учитывая это, от рентгеновского исследования с целью диагностики остеохондроза, особенно на ранних стадиях, мы отказались. Основные симптомы остеохондроза — боль, болезненность при пальпации, обездвиженность, однако, не постоянны. Поэтому мы пользовались для выявления начальных стадий болезни методом определения повышенного мышечного тонуса в области пораженного сегмента по сравнению с выше и ниже лежащими отделами позвоночника, вызываемое поколачиванием молоточка, особенно асимметричность напряжения при одностороннем поражении. Этот симптом выявлялся у 90 % пациентов.
Отсутствие или скудность клиники в начальной стадии заболевания можно объяснить воздействием вредных факторов непосредственно на позвоночник и межпозвонковые диски (Тещук В.И., Ярош О.О., 1999; Fautrel
В., Rozenberg S„ Bourgeois P., 1998; Armstrong N„ 1999). У работников же основных цехов металлургического производства в связи с особенностями рабочих операций патология чаще начинается с мышц, преимущественно поясничной области и спины. Хроническое утомление, переутомление, перенапряжение их нередко заканчивается миалгией или даже миозитом, что, разумеется, снижает стабилизирующие их функции, а это в свою очередь снижает амортизирующие возможности позвоночника, способствует микротравматизации диска. Возникает и развивается остеохондроз позвоночника с пагубным, в свою очередь, влиянием на соответствующий регионарный мышечный аппарат и сегментарно расположенные внутренние органы (Вейн A.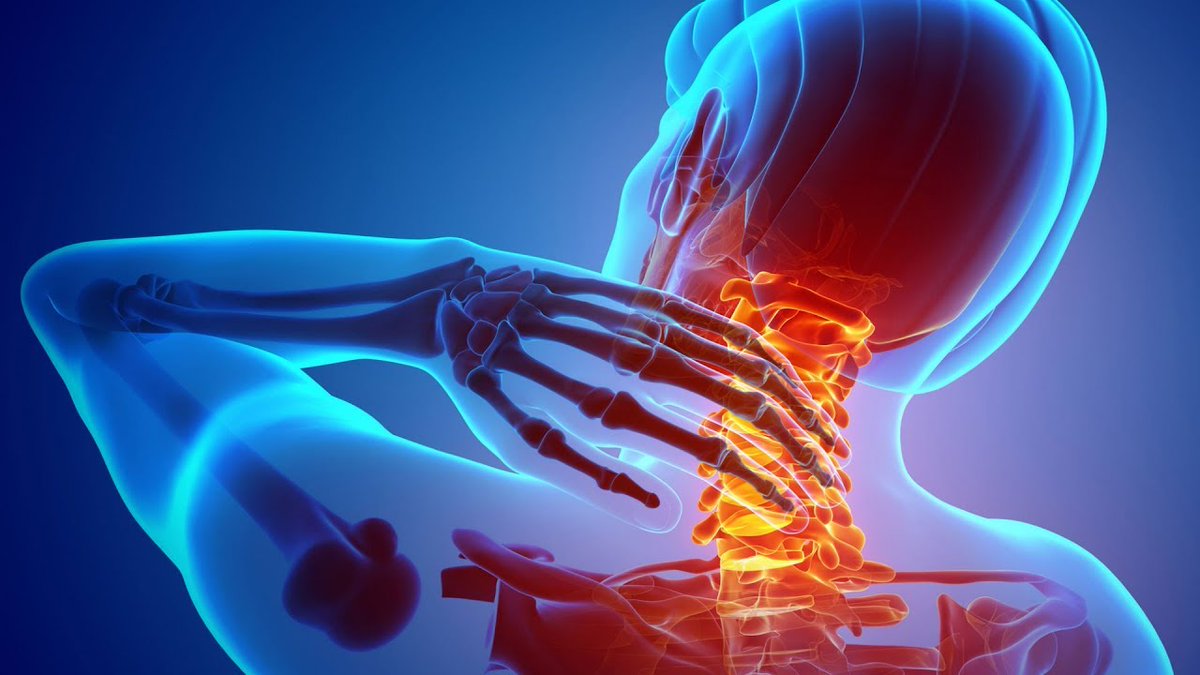 M., 1991; Вартанян И.А., 1999).
M., 1991; Вартанян И.А., 1999).
Таким образом, для развития клинических проявлений остеохондроза позвоночника необходима совокупность способствующих, реализующих и вызывающих факторов. К реализующим факторам мы относим мышечные перегрузки, обусловленные неоптимальным двигательным стереотипом. Если началом заболевания считается возникновение органических изменений в сегменте позвоночника, то реализующие факторы существуют уже длительное время (6-12 месяцев), чаще не проявляя себя клинически, на что указывают и Шардакова Э.В. с соавт. (1999), и Рыжов А.Я. с соавт. (2000). Эта особенность учитывалась нами при диагностике, профилактике и лечении.
Еще одной особенностью поясничного остеохондроза у рабочих металлургического производства является его более частое (в 2-2,5 раза чаще, чем на других производствах) сочетание с нарушениями подвижности крестцово-подвздошных сочленений, сакроилеитом. Объясняется это особенностью взаимодействия рабочих операций и анатомии этой области. Наиболее часто сакроилеитом поражены рабочие, трудовой процесс которых связан не столько со сгибанием и разгибанием позвоночника, сколько с ротацией поясничного и пояснично-крестцового отдела позвоночника.
Перечисленные особенности, присущие поясничному остеохондрозу позвоночника у работников алюминиевого производства, учитывались при проведении лечебных и оздоровительно-профилактических мероприятий.
После определения локализации степени выраженности патологического процесса работники обследуемого контингента группировались для проведения рациональных лечебно-профилактических мероприятий. Работникам профессиональных групп «повышенного риска», где биомеханика производственных движений определялась как наиболее нефизиологичная, индивидуально подбирался благоприятный режим труда с вводной гимнастикой, микропаузами, физкультурными паузами. Таким образом, осуществлялось воздействие уже на этапе предболезни. С этой целью применялось ношение поясов-корсетов, фиксирующих позвончно-двигательный сегмент (Попелянский Я. Ю., 1992, 1997). Аппликации с димексидом на пораженные участки позвоночника улучшали микроциркуляцию и снижали мышечный тонус. Важным направлением в комплексном лечении сочетанной патологии опорно-двигательного аппарата и сердечно-сосудистой систем являлось повышение адаптивных возможностей организма работника в сочетании с компенсацией периферических сосудистых и трофических нарушений. С этой целью использовалось устройства для тепловых суховоздушных и гидровакуумных жемчужных ванн. Нами использовалось разработанное Д.К.Макридиным, В.В.Косаревым, И.А.Бараевым (1995) устройство для проведения гидровакуумных ванн, сочетающее в себе весь комплекс физиопроцедур с лекарственными средствами предназначенное для лечения периферических гемодинамических нарушений различного генеза. На полезную модель «Устройства для проведения гидровакуумных жемчужных ванн» получено Свидетельство РОСПАТЕНТА N 1426 от 26.06.1995. Оно впервые применено нами для коррекции ранней стадии поражения позвоночника. Жемчужные ванны улучшают реактивность, нормализуют возбудимость периферических и
Ю., 1992, 1997). Аппликации с димексидом на пораженные участки позвоночника улучшали микроциркуляцию и снижали мышечный тонус. Важным направлением в комплексном лечении сочетанной патологии опорно-двигательного аппарата и сердечно-сосудистой систем являлось повышение адаптивных возможностей организма работника в сочетании с компенсацией периферических сосудистых и трофических нарушений. С этой целью использовалось устройства для тепловых суховоздушных и гидровакуумных жемчужных ванн. Нами использовалось разработанное Д.К.Макридиным, В.В.Косаревым, И.А.Бараевым (1995) устройство для проведения гидровакуумных ванн, сочетающее в себе весь комплекс физиопроцедур с лекарственными средствами предназначенное для лечения периферических гемодинамических нарушений различного генеза. На полезную модель «Устройства для проведения гидровакуумных жемчужных ванн» получено Свидетельство РОСПАТЕНТА N 1426 от 26.06.1995. Оно впервые применено нами для коррекции ранней стадии поражения позвоночника. Жемчужные ванны улучшают реактивность, нормализуют возбудимость периферических и
ig
центральных звеньев нервной системы, улучшают кровоснабжение тканей, активизируют обменные процессы. Кроме того, они оказывают механическое (массажное) и тепловое воздействие (температура воды 36-38С°) на область позвоночника. В состав применяемых фитосмесей входит ментол, оказывающий местное обезболивающие действие. Выраженный терапевтический эффект констатирован у 84,5% обследованных, из них с начальной стадией процесса было 64,4%.
Как известно, вертеброгенная патология существенным образом влияет на течение соматических заболеваний (Михайлов М.К., Ларюкова Е.К., 1990; Трунова С.В., 1990; Густов A.B., 1991). Это обуславливает важность, прежде всего, раннего выявления, целенаправленной профилактики и лечения больных остеохондрозом позвоночника с вторичной корешковой и вегетативно-сосудистой симптоматикой (Агальцев М.В., Федорова С.И., 1997). Помимо результатов скринингового обследования нами была проведена оценка состояния различных отделов позвоночника у рабочих, занятых тяжелым физическим трудом (прессовщики, кузнецы, вальцовщики, резчики).
Таблица 1.
Соматическая и вертеброгенная патология у работников металлургического предприятия
Пораженная система Контроль <В%) (М±ш, п = 100) Остеохондроз позвоночника(в %)
шейный отдел (М±ш, п = 60) грудной отдел (M±m, п = 42) Поясничный отдел (M±m, п = 74)
Органы дыхания 2,04+0,07 5,50±0,36* 2,41±0,31 2,74±0,22
Сердечнососудистая система 9,03 ±0,2 9 8,38±0,46 10,63±0,65* 9,58±0,40
Органы пищеварения 5,00±0,22 3,23±0,30 4,32±0,43 6,72+0,34*
* р < 0,05
В результате проведенной статистической обработки выяснилось, что у работников металлургического производства, находящихся в контакте с профессиональными вредностями и вследствие этого чаще страдающих остеохондрозом позвоночника, достоверно чаще по сравнению с контрольной группой встречается соматическая патология (см. табл. 1). Причем у больных с диагнозом «остеохондроз шейного отдела позвоночника» достоверно чаще, чем у здоровых лиц встречаются заболевания органов дыхания (хронический бронхит, бронхиальная астма).
Сердечно-сосудистая система страдает чаще у работников с остеохондрозом грудного отдела позвоночника. Это выражается в большей распространенности у них НЦД, ИБС, нарушений сердечного ритма по сравнению с группой контроля. При диагностике остеохондроза поясничного отдела позвоночника чаще обнаруживаются заболевания желудочно-кишечного тракта, которые включают хронический гастрит, язвенную болезнь желудка и двенадцатиперстной кишки, хронический дуоденит, хронический холецистит. Патогенетической основой выявленной взаимозависимости можно считать нарушение регуляции вегетативных функций внутренних органов вследствие обменно-дистрофических изменений в соответствующих сегментах спинного мозга, как следствие остеохондроза позвоночника (Вейн A.M., Данилова А.Б., 1999; Li Li et al., 1998).
В соответствии с установленной связью патогенной биомеханики производственных движений с заболеваниями внутренних органов разработан алгоритм наиболее эффективного применения существующих методов лечебного воздействия применительно к условиям труда металлургов.
Своевременное подключение адекватных лечебно — профилактических мер на всех этапах (выявление «зон риска», подбор режимов труда, неспецифическое оздоровительное воздействие, рационально подобранные физиопроцедуры) позволили приостановить развитие патологических
процессов, предупредить их возникновение, вызвать регрессирующее течение заболевания, снизить заболеваемость, особенно на начальных стадиях.
ВЫВОДЫ.
1. По данным углубленного медосмотра работников металлургического предприятия по вторичной переработке алюминия, подвергающихся воздействию комплекса вредных факторов, частота патологии сердечнососудистой, дыхательной, пищеварительной систем и позвоночника у них достоверно выше общепопуляционного уровня, что свидетельствует о неблагоприятном влиянии производственной среды предприятия на состояние здоровья.
2. В основе выявляемых у 40% обследованных рабочих нарушений вегетативной регуляции деятельности сердечно-сосудистой системы является несоответствие интенсивности физической нагрузки в условиях перегревания ее адаптивным возможностям, что выражается в синдроме кардио-васкулярной автономной нейропатии.
3. Комплексное клинико-функциональное исследование дыхательной системы позволяет выявить скрытые формы ее патологии (пылевого бронхита, например), не диагностируемые при профилактическом медицинском осмотре. Наиболее информативным методом скринингового исследования дыхательной системы является флоуметрия с пробой с бронходилататором, т.к. она дает наиболее полное представление о функции внешнего дыхания даже на ранних этапах ее нарушений..
4. В комплексном подходе к диагностике патологии органов дыхания как при периодических медицинских осмотрах на промышленных предприятиях, так и в клинической практике, целесообразно использование таких серологических маркеров, как эозинофильный катионный белок и муцин-антиген.
5. У рабочих металлургического производства заболеваемость с временной утратой трудоспособности, обусловленная болезнями пищеварительной системы, выше, чем в группе контроля. Кроме того, эти заболевания протекают у названного контингента более тяжело и длительно.
Кроме того, эти заболевания протекают у названного контингента более тяжело и длительно.
6. В результате комплексного обследования работников алюминиевого производства установлено, что 27,1% из них страдает остеохондрозом позвоночника, что связано с особенностями биомеханики производственных движений. У работников литейных цехов чаще страдают шейный и грудной отделы позвоночника, а у прессовщиков — поясничный.
7. С увеличением стажа работы во вредных условиях у работников алюминиевого производства возникает патология позвоночника, что, возможно, приводит к нарушениям внутренних органов. При этом повреждение шейного отдела позвоночника чаще сочетается с нарушением дыхательной системы, грудного — сердечно- сосудистой, поясничного -пищеварительной.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ.
1. Для ранней диагностики соматических заболеваний у работников металлургического производства со стажем более 10 лет рекомендуется комплекс неинвазивных методов исследования систем кровообращения и дыхания, включающий эхокардиографию, тетраполярную реографию, автокорреляционный и спектральный анализ сердечного ритма, флоуметрию с тестом с бронходилататором.
2. Для выявления нарушений регуляции деятельности сердечнососудистой системы у работников алюминиевого производства, подвергающихся воздействию комплекса вредных факторов целесообразно использовать методы эхокардиографии и автокорреляционного анализа ритмограмм и спектрограмм, особенно у лиц, имеющих большой производственный стаж (свыше 10 лет).
3. Включить в периодический профилактический медосмотр комплексное клинико-функциональное исследование дыхательной системы с применением флоуметрии с пробой с бронходилататором, что позволит выявить начальные формы ее поражений.
4. В комплексном подходе к диагностике патологии органов дыхания как при периодических медицинских осмотрах на промышленных предприятиях, так и в клинической практике, целесообразно использование таких серологических маркеров, как эозинофильный катионный белок и муцин-антиген.
5. Оздровительно-лечебные мероприятия должны применяться строго дифференцированно, с учетом биомеханики трудовых операций, а также стадий патологического процесса. В комплексном лечении основная роль отводится дистракционному воздействию на позвоночник в сочетании с местными физиотерапевтическими факторами (тепловыми суховоздушными и гидровакуумными жемчужными ваннами).
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ.
1. Эпидемиологические, клинико-функциональные и лабораторные аспекты различных клинических форм профессионального пылевого бронхита. //Сборник резюме VII национального конгресса по болезням органов дыхания. — Москва. — 1997 год. — С. 309. (совместно с H.A. Мокиной).
2. Лечение компрессионных пояснично-крестцовых радикулопатий местными тепловыми суховоздушными ваннами. // Сборник статей II Самарской конференции неврологов и нейрохирургов. — Самара. — 1997. — с. 324. (совместно с В.В.Косаревым, Д.К.Макридиным)
3. Состояние здоровья работающих в металлургическом производстве. // Гигиена и санитария. — 1998. — №1. — С.39-41. (совместно с В.В.Косаревым, Д.К.Макридиным, И.А.Бараевым).
4. Диагностика и лечение периферических ангиодистонических нарушений от воздействия физических факторов. // Тезисы докладов на Всероссийской научно-практической конференции «Медико-биологические и эколого-гигиенические проблемы оценки и прогнозирования воздействия факторов окружающей среды». Санкт-Петербург. — 1998. — С.131. (совмесно с Д.К.Макридиным)
5. Плотность костной ткани и фосфорно-кальциевый обмен у рабочих металлургического производства. // Тезисы докладов Всероссийской научно-практической конференции «Актуальные проблемы профилактики неинфекционных заболеваний». Москва. — 1999. — Т.Н. — С.97. (совместно с
A.Ф.Вербовым)
6. Фармакофизотерапевтические методы реабилитации больных с вертеброгенными заболеваниями. // Тезисы докладов VI Международного Конгресса «Экология и здоровье человека». — Самара. — 1999. — С.12.
— Самара. — 1999. — С.12.
7. Ранние признаки профессиональной патологии у рабочих металлургического производства (диагностика, профилактика и лечение). Методические рекомендации. — Самара. — 2000. — 24 с. (совместно с
B.В.Косаревым, Д.К.Макридиным).
8. Влияние стажа работы во вредных условиях прессового производства на сократимость миокарда. // Сб. тез. и докл. конф. молодых исследователей «Аспирантские чтения — 2000». — Самара. — 2000. — С. 60-61.
9. Клинико-эпидемиологическая диагностика хронического пылевого бронхита. // Гигиена и санитария. — №2. — 2001.- С. 31-33. (совместно с В.В. Косаревым, H.A. Мокиной).
Полезная информация о дорсопатии позвоночника
Полезная информация о дорсопатии позвоночника
Дорсопатия (от лат. dorsum — спина) – термин, которым обозначают все возможные патологии позвоночника и поражения мягких тканей спины. В определении «вертеброгенная дорсопатия» заложена суть проблемы — это патология спины, вызванная заболеваниями позвоночника (от латинского «vertebra» — «позвонок»). Около 80% взрослого населения переживали ощущения боли в спине, обусловленной данной паталогией, и примерно 50% людей трудоспособного возраста эту боль испытывают ежегодно .
Дорсопатия дословно с латыни – заболевание спины. Это по сути патологическое состояние, характерное для травм этих отделов позвоночника, остеохондроза и специфического повреждения позвонков при туберкулезе, опухолях, сифилисе. При дорсопатии патологически изменяется не только хрящевая и костная ткань позвонка и межпозвонкового диска, но и рядом находящиеся кровеносные сосуды, нервы, мышцы, связочный аппарат.
Дорсопатия позвоночника аналогично понятию «остеохондроз позвоночника»
В первой четверти 20 столетия дрезденским патологоанатомом К. Шморлем было установлено, что позвоночник человека, или, как его еще называют, столб жизни, сформировавшись к 22 годам, уже вскоре начинает изнашиваться, перерождаться, стареть. Процесс дистрофии суставного хряща и костной ткани называется остеохондрозом. В процессе этого прогрессирующего заболевания поражаются позвонки, межпозвонковые суставы и связки.
Процесс дистрофии суставного хряща и костной ткани называется остеохондрозом. В процессе этого прогрессирующего заболевания поражаются позвонки, межпозвонковые суставы и связки.
Дорсопатия пояснично-крестцового отдела позвоночника
Дорсопатия пояснично-крестцового отдела позвоночника встречается чаще всего, так как в функциональном плане поясничные позвонки наиболее уязвимы: поясница максимально испытывает механическую нагрузку, «выдерживая» большую часть массы тела.
По сути дела, дорсопатия поясничного отдела – аналог остеохондроза того же отдела, — длительное хроническое заболевание, протекающее при наличии характерных обострений с проявлением резких болевых ощущений. Поясничный отдел позвоночника страдает чаще других из-за механической нагрузки. Дегенеративные изменения при этом касаются не только хрящевой и костной ткани позвонков и межпозвонковых дисков, но и рядом находящихся кровеносных сосудов, нервов, мышц, связочного аппарата. Как правило, проявляется заболевание с 45 — 50 лет.
Цервикальная дорсопатия (дорсопатия шейного отдела позвоночника
Дорсопатия шейного отдела позвоночника — это общее название для большой группы патологий позвоночника, связанных с дегенеративными изменениями костной и мышечных структур и характеризующихся хроническим болевым синдромом. Самым частым случаем дорсопатии является остеохондроз. В условиях современного образа жизни и нездоровой окружающей среды, редкий человек старше 40 не сталкивался с болью в области спины.
По сути, термином «цервикальная дорсопатия» заменили ранее применявшийся термин “остеохондроз шейного отдела позвоночника”. Среди причин болевых синдромов, проявляющихся в спине, это заболевание — на втором месте (более 30%) после дорсопатий нижних отделов спины (42%)
Дорсопатия грудного отдела позвоночника
Дорсопатия грудного отдела позвоночника – распространенная патология у пациентов различных возрастов. Под дорсопатией в медицине понимается комплекс болезней, возникающих в результате патологии соединительной и костно-мышечной ткани основным симптомом, которых является боль в конечностях и спине. Грудной отдел позвоночника является одним из самых подвижных в сравнении с другими отделами. Большое количество образований (позвонки, ребра, реберно-позвоночные и реберно-поперечные суставы) определяют функционирование грудного отдела.
Грудной отдел позвоночника является одним из самых подвижных в сравнении с другими отделами. Большое количество образований (позвонки, ребра, реберно-позвоночные и реберно-поперечные суставы) определяют функционирование грудного отдела.
|
Неврологическое отделение для больных с острыми нарушениями мозгового кровообращения
Жизнь после инсульта может быть комфортной! Задача отделения – сделать всё для этого.
Неврологическое отделение ГКБ им Ф.И. Иноземцева для больных с ОНМК и перенесших инсульт создано на базе нейрососудистого отделения с более, чем 20-летним опытом лечения пациентов с неврологической патологией. В состав Регионального сосудистого центра отделение входит с января 2013 г.
Руководство отделением осуществляет Савкова О.Н. – врач невролог высшей категории, стаж работы по специальности 30 лет.
В лечении больных также принимает участие Заслуженный врач РФ, доктор медицинских наук, заведующая кафедрой внутренних болезней МГМСУ им.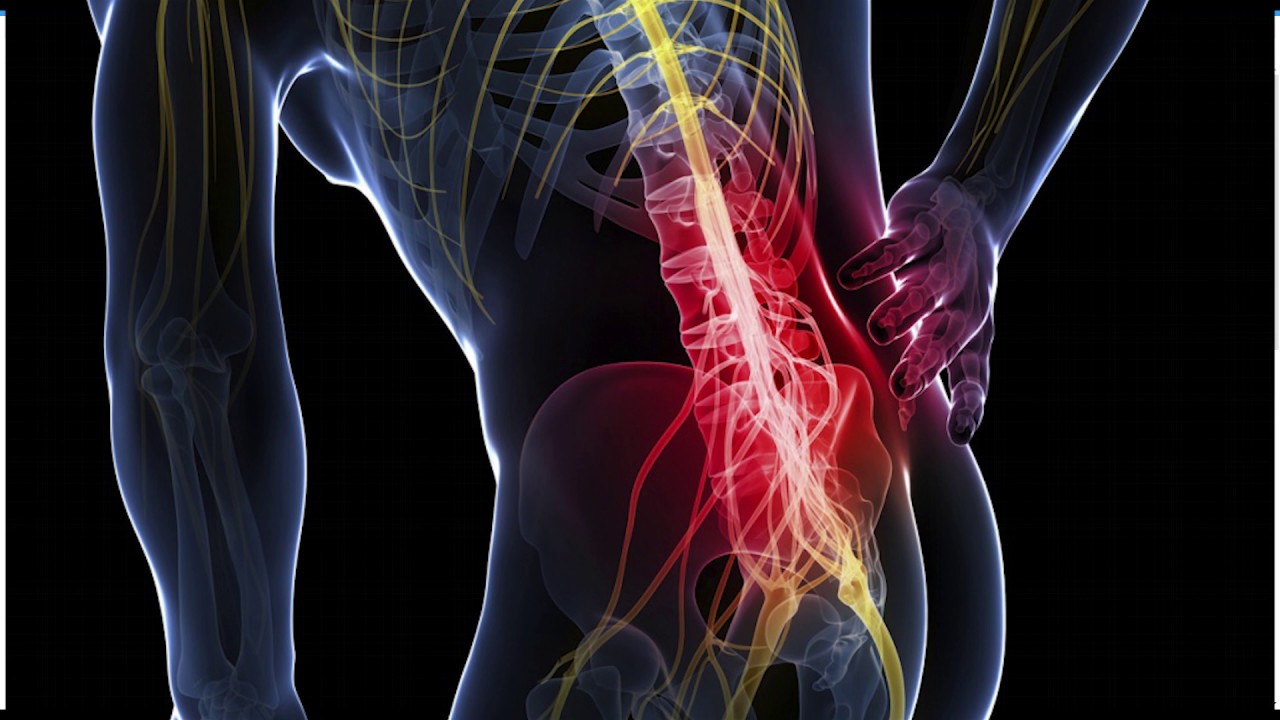 А.И. Евдокимова, профессор Стрюк Раиса Ивановна.
А.И. Евдокимова, профессор Стрюк Раиса Ивановна.
В настоящее время в отделении есть 48 мест для пациентов, из них 6 – это палаты интенсивного наблюдения для «тяжелых» больных с отдельным сестринским постом. Эти палаты специально оборудованы для ежечасного наблюдения и мониторирования показателей жизнедеятельности больных с нарушениями функции глотания, мочеиспускания, другими осложнениями ОНМК.
Оборудовано 3 сестринских поста, имеются палаты повышенной комфортности на 1-2 койки, оснащенные санузлами, душевыми кабинами, бытовой техникой, и 14 общих палат на 3-4 пациента, имеется все необходимым оборудованием для качественного оказания медицинской помощи больным с острыми нарушениями мозгового кровообращения.
ГОСПИТАЛИЗАЦИЯ
Основной вид госпитализации по скорой медицинской помощи и по направлению невролога. Основная задача отделения – оказание специализированной медицинской помощи больным с ОНМК в круглосуточном режиме.
Возможна госпитализация пациентов по каналу ПМУ, ДМС с целью проведения диагностического поиска, обследования, лечения и ранней реабилитации с использованием всех имеющихся в клинике ресурсов. Отделение активно участвует в программе «Москва – Столица Здоровья», предусматривающей лечение и обследование иногородних пациентов.
В отделение могут быть госпитализированы больные со следующими заболеваниями:
- все виды острых нарушений мозгового кровообращения;
- другие неотложные неврологические состояния;
- хроническая ишемия головного мозга;
- вертеброгенная патология – заболевания позвоночника или окружающих тканей;
- мононевропатия – поражение отдельного нервного ствола;
- полинейропатия – множественное поражение периферических нервов;
- энцефалопатия – поражение головного мозга;
- подозрение на опухоли мозга;
- оперированные сосудистые мальформации;
- обследования и отбор для высокотехнологичных операций при заболеваниях нервной системы и позвоночника.

Основные принципы лечения:
- ранняя диагностика;
- максимально раннее начало лечения и реабилитации больных;
- внедрение новых передовых методов лечения.
БЕЗБАРЬЕРНАЯ СРЕДА
Специально созданное «безбарьерное пространство» создает удобство передвижения для маломобильных категорий пациентов и больных с нарушением функции ходьбы. Помещения оборудованы специальными поручнями для больных с двигательными нарушениями, нарушением функции ходьбы. В работе используются ресурсы всех параклинических и лечебно-диагностических подразделений больницы. Максимально приближены к пациенту параклинические диагностические службы (кабинеты УЗИ, ЭЭГ, УЗДГ) размещены непосредственно на базе отделения.
СПЕЦИАЛИСТЫ
С пациентами работают специалисты высокого класса, с большим опытом ведения «сосудистых» больных: неврологи, нейрохирурги, сосудистые хирурги, терапевты, офтальмолог, кардиолог, врач восстановительной медицины, логопед, психолог – в составе мультидисциплинарной бригады. Данные специалисты работают не по отдельности, а как единая команда с четкой согласованностью и координированностью действий, обеспечивая целенаправленный подход к проведению реабилитации постинсультных пациентов.
Опытные медицинские сестры, младший медицинский персонал создают в отделении благоприятную обстановку тепла и взаимопонимания, обучают родственников и пациентов приемам ухода.
КОМПЛЕКСНЫЙ ПОДХОД
Совместно с сосудистыми хирургами проводится отбор и дообследование пациентов для оказания высокотехнологичной помощи – каротидной эндартерэктомии, стентирования.
Проводится отбор, дообследование и предоперационная подготовка больных с нейрохирургической патологией (сосудистая патология, опухоли, вертеброгенная патология).
Пациенты с вертебральной патологией могут пройти полноценный курс комплексной консервативной терапии с определением тактики лечения, в том числе оперативного.
По завершении курса стационарного лечения, всем больным определяется реабилитационный прогноз и потенциал с целью перевода на 2 этап реабилитации в специализированных стационарах Москвы и санаториях Подмосковья.
Проблемы пациентов – это наша забота!
ГАЛЕРЕЯ
Патология позвоночника — обзор
Патология грудного отдела позвоночника часто сопровождается отсутствием или минимальными жалобами и может имитировать шейный диск, сердечно-легочную, абдоминальную, аортальную, внутреннюю миопатию или почечную калькулезную болезнь, требующую тщательной оценки всех патологий.
У большинства пациентов с заболеванием грудного диска симптомы отсутствуют, но магнитно-резонансная томография грудной клетки (МРТ) показывает, что примерно у 73% взрослых пациентов есть положительные аномалии МРТ, включая деформацию спинного мозга у 29%.
Разнообразные клинические проявления являются нормой для пациентов с симптоматическими дисками и включают боль в грудной клетке (передняя полосатая корешковая боль в груди), осевая боль в спине, слабость, частое опорожнение кишечника или мочевого пузыря, недержание мочи или позывы.
Физикальное обследование может выявить слабость верхних конечностей, онемение, синдром Горнера (диск Т1), онемение и слабость нижних конечностей (нижний грудной диск), миелопатические признаки удлиненного тракта, спастичность и гиперрефлексию, нарушения походки и дисфункцию сфинктера. .
Визуализация обычно состоит из рентгенограмм с простой пленкой, компьютерной томографии (КТ), МРТ или КТ миелограммы (если МРТ противопоказана).
Простые снимки важны для определения количества поясничных и грудных сегментов на 3-футовых снимках стоя и обеспечивают полезную меру подсчета количества ребер и поясничных сегментов, которые будут использоваться во время предоперационной и интраоперационной рентгеноскопии. Сагиттальную и коронарную деформацию лучше всего оценить на простых снимках.Патологические переломы, а также кальцинированные диски можно отметить на рентгенограммах (рис. 18.1).
Сагиттальную и коронарную деформацию лучше всего оценить на простых снимках.Патологические переломы, а также кальцинированные диски можно отметить на рентгенограммах (рис. 18.1).
МРТ наиболее полезно для оценки нормальных и патологических мягких тканей (связок, диска) и нервных элементов. TDH, опухоли, инфекции, корни или внутренние поражения спинного мозга лучше всего распознаются на МРТ. Сагиттальная полноразмерная скаутская МРТ позвоночника помогает в интраоперационной идентификации уровня с помощью рентгеноскопии.
КТ-сканирование часто полезно для оценки переломов, OPLL, кальцинированных TDH, костной анатомии и ориентиров, степени нарушения позвоночного канала, а также планирования идеальных резекций и инструментов для корпэктомии (ориентация или расположение, длина, размер) (Рисунок.18.2). Планирование смежной гемикорэктомии и инструментария (кейдж-винт) может быть выполнено на основе предоперационных сагиттальных и коронарных реконструкций.
Предоперационный прием полиметилметакрилата (ПММА) может быть проведен за один или два дня до операции у пациентов с патологическим ожирением с помощью компьютерной томографии или рентгеноскопии, чтобы обеспечить адекватную идентификацию уровня во время операции. Кроме того, ПММА можно использовать для усиления фиксации винтами у пациентов с остеопорозом, независимо от того, используется ли он спереди (перед установкой переднего инструментария) или сзади (перед инструментарием с помощью педикулярного винта) (рис.18.3).
Тесты функции легких (PFT) могут идентифицировать и количественно определять предоперационные сердечно-легочные обструктивные, рестриктивные или ограничивающие диффузию патологии у маргинальных кандидатов.
Сосудистые исследования (МРТ, КТ или стандартная ангиография) могут помочь в локализации нормальной сосудистой сети спинного мозга или эмболизации гиперваскулярных поражений (метастатических поражений).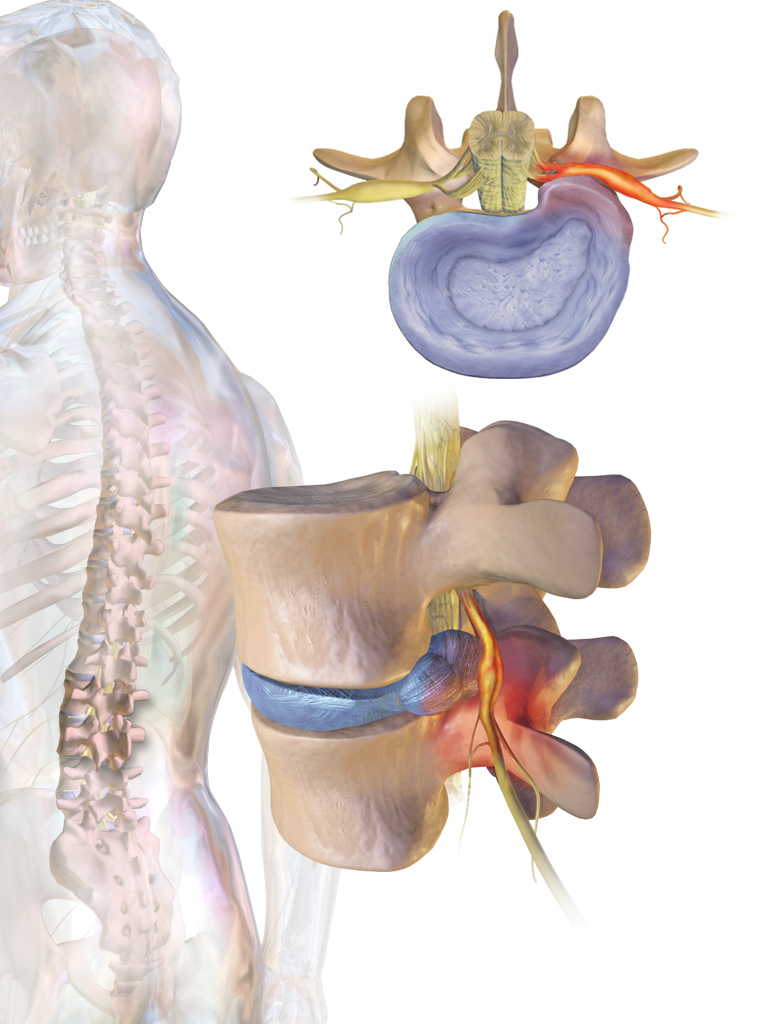
Некоторые выступают за провокационную дискографию, чтобы обозначить, какой диск (диски) может быть генератором боли при многоуровневых грыжах грудного диска, обнаруженных на МРТ после неудач консервативных вариантов лечения боли в грудной оси.
Предоперационная или интраоперационная электромиография (ЭМГ), исследования нервной проводимости (NCS), транскраниальные моторные вызванные потенциалы (tcMEP) и соматосенсорные вызванные потенциалы (SSEP) полезны в установлении и мониторинге базовой нервной функции.
Заболевания поясничного отдела позвоночника: Патология
Миелома
Злокачественная опухоль плазматических клеток, наиболее часто встречающаяся первичная опухоль кости; почти всегда задействован позвоночник.Диссеминированная форма — это множественная миелома , и на ее долю приходится 45% всех злокачественных опухолей костей (Dahlin and Unni: 70 pp. 193–207). Пациенты обычно относятся к более старшей возрастной группе, поскольку заболевание редко встречается в возрасте до 50 лет. Плазмацитома является солитарной формой и поражает позвоночник примерно у 50% пациентов. 96
Наиболее частая жалоба — боль в спине, которая не меняется от нагрузки, хотя сначала может немного уменьшиться постельным режимом.О злокачественном заболевании свидетельствует неуклонное усиление боли в спине, которая со временем становится постоянной, независимо от позы или движения. По мере усиления боли в спине появляется ишиас, который часто бывает двусторонним. 97 Тот факт, что боль в спине не прекращается после появления корневой боли и что боль в корне является двусторонней, сразу обращает внимание на возможность расширения поражения. Как вариант, боль в спине возникает внезапно в результате патологического перелома.
Результаты клинического обследования зависят от степени заболевания.На ранней стадии обычно наблюдается только спазм поясничных мышц и локальная болезненность. На более поздних стадиях можно увидеть угловой кифоз и признаки сдавления нервных корешков на разных уровнях. Наконец, становятся заметными признаки общего заболевания, такие как лихорадка, потеря веса и бледность.
На более поздних стадиях можно увидеть угловой кифоз и признаки сдавления нервных корешков на разных уровнях. Наконец, становятся заметными признаки общего заболевания, такие как лихорадка, потеря веса и бледность.
Рентгенологически множественная миелома характеризуется наличием круглых литических дефектов в кости без какого-либо окружающего реактивного склероза. Иногда литические дефекты могут быть неочевидными, и рентгенограмма показывает не что иное, как диффузную остеопению. 98 В таких обстоятельствах дифференциальный диагноз должен быть поставлен с помощью лабораторных исследований, 99 , которые постоянно выявляют повышенную скорость оседания эритроцитов — редко менее 100 мм / ч. Характерно, что аномальные белки Бенс-Джонса могут быть обнаружены в моче. 100 Наиболее важным тестом является электрофорез сывороточного белка, который выявляет моноклональный всплеск у более чем 75% пациентов и гипогаммаглобулинемию у 9%. 101
Обычное течение множественной миеломы — это постепенное прогрессирование.Системная терапия мелфаланом и кортизоном может улучшить клинические симптомы, но средняя выживаемость редко превышает 5 лет. 102
Поясничный отдел позвоночника: распространенная патология и вмешательства
Аннотация и введение
Поясничная грыжа пульпозного ядра (HNP) и поясничный стеноз позвоночного канала (LSS) являются частыми патологиями позвоночника с различными клиническими проявлениями и различными вмешательствами. HNP обычно имеет острое начало, часто без провоцирующего события. Если нет значительного или возникающего неврологического дефицита, нехирургическое лечение оправдано в течение 6 или более недель после появления симптомов.Если через 6 недель улучшения не наступит, может быть показано хирургическое вмешательство. Микродискэктомия — это золотой стандарт лечения неосложненного ГНП. LSS имеет коварное начало. Часто клинические проявления представляют собой длительную историю перемежающейся боли в спине и постепенного уменьшения возможности передвигаться из-за боли в ногах, которая быстро проходит после сидения. Медикаментозное лечение является первым выбором лечения. Если состояние пациента не улучшается, может потребоваться операция. Как и при любой операции на позвоночнике, симптомы пациента, клиническое обследование и диагностика должны коррелировать.Послеоперационный уход отличается от микродискэктомии и декомпрессивной ламинэктомии, потому что хирургическая патология и вмешательства различны. Обычные возрастные колебания пациентов, проходящих любую из двух процедур, также изменят потребности в послеоперационном уходе. Медсестры-неврологи проводят постоянное обучение пациентов и обеспечивают полное понимание предлагаемого хирургического вмешательства и результата, которого могут ожидать пациент и его семья. Конгруэнтные ожидания между пациентом и врачом жизненно важны.Кроме того, крайне важна точная оценка физического и функционального прогресса пациента медсестрами-неврологами.
Медикаментозное лечение является первым выбором лечения. Если состояние пациента не улучшается, может потребоваться операция. Как и при любой операции на позвоночнике, симптомы пациента, клиническое обследование и диагностика должны коррелировать.Послеоперационный уход отличается от микродискэктомии и декомпрессивной ламинэктомии, потому что хирургическая патология и вмешательства различны. Обычные возрастные колебания пациентов, проходящих любую из двух процедур, также изменят потребности в послеоперационном уходе. Медсестры-неврологи проводят постоянное обучение пациентов и обеспечивают полное понимание предлагаемого хирургического вмешательства и результата, которого могут ожидать пациент и его семья. Конгруэнтные ожидания между пациентом и врачом жизненно важны.Кроме того, крайне важна точная оценка физического и функционального прогресса пациента медсестрами-неврологами.
Симптоматика корешковой боли, связанная с поясничной грыжей пульпозного ядра (HNP), может быть мучительной. В большинстве случаев через 4 недели после появления симптомов боль достигается, и можно возобновить обычную деятельность. Примерно у 16% пациентов симптомы все еще проявляются через 7 недель после появления симптомов (Rosomoff & Rosomoff, 1999).
Стеноз поясничного отдела позвоночника (LSS) — это сужение центрального канала и, часто, латерального углубления из-за гипертрофии фасеточного сустава, утолщения и выпячивания желтой связки, выпячивания межпозвонкового диска, образования остеофитов или спондилолистеза. Симптомы включают боль в ногах и ягодицах при физической активности, которая облегчается отдыхом или маневрами, увеличивающими размер позвоночного канала, такими как наклон вперед для ходьбы.
Эти распространенные патологии поясницы очень разные.Поэтому медсестрам-нейробиологам необходимы базовые знания о HNP и LSS, а также различиях в клинической картине и нейрохирургическом лечении каждого из них, чтобы обеспечить оптимальную помощь и консультации. В этой статье описываются HNP и LSS, признаки и симптомы, оперативное лечение и уход. Представлен краткий обзор функциональной анатомии поясницы.
В этой статье описываются HNP и LSS, признаки и симптомы, оперативное лечение и уход. Представлен краткий обзор функциональной анатомии поясницы.
заболеваний позвоночника | Состояние | Юго-западный медицинский центр UT
Расширенное лечение заболеваний позвоночника
Позвоночник состоит из 26 костей, называемых позвонками, которые защищают и поддерживают спинной мозг и нервы.Ряд состояний и травм могут повлиять на позвоночник, что может повредить позвонки, вызвать боль и ограничить подвижность.
Наши нейрохирурги, хирурги-ортопеды, физиотерапевты, болеутоляющие, психологи и другие специалисты обладают обширным опытом в лечении даже самых сложных заболеваний позвоночника, что дает нашим пациентам доступ к целому ряду экспертных знаний, которые помогают уменьшить боль и улучшить качество жизни.
Типы заболеваний позвоночника
Многие заболевания могут поражать позвоночник в любом месте от шеи до поясницы.Вот некоторые из многих заболеваний позвоночника, которые мы лечим:
Дегенеративные заболевания позвоночника и диска:
Другие состояния и заболевания позвоночника:
Причины заболеваний позвоночника
Заболевания позвоночника имеют широкий спектр причин в зависимости от конкретного состояния. Причины некоторых состояний неизвестны. К распространенным причинам относятся:
- Несчастные случаи или падения
- Врожденные нарушения (присутствующие с рождения)
- Воспаление
- Инфекция
- Наследственные заболевания
- Травмы от легких до травм
- Дегенеративный износ, возникающий при старении
- Избыточный вес или ожирение
- Неправильная техника подъема тяжестей
- Питание и привычки образа жизни, такие как малоподвижный образ жизни, низкое потребление кальция или курение
- Другие состояния, такие как остеоартрит, ревматоидный артрит или заболевание щитовидной железы
- Чрезмерное использование упражнений или профессиональных движений
- Плохая осанка
- Повторяющаяся физическая активность
- Аномально округлые плечи или спина
- Боль в спине или шее, которая может быть острой и колющей, тупой и ноющей или жгучей
- Дисфункция мочевого пузыря или кишечника
- Тошнота и / или рвота
- Боль, излучающая в руки или ноги
- Скованность или скованность
- Неравномерный внешний вид, например, одно плечо или бедро выше другого
- Слабость, онемение или покалывание в руках или ногах
- Физический осмотр
- Обсуждение личного и семейного медицинского анамнеза
- Обсуждение симптомов и факторов риска
- Неврологическое обследование при подозрении на повреждение или нарушение нерва
- 902 21 Магнитно-резонансная томография (МРТ) : При МРТ используются радиоволны и сильный магнит для получения детальных изображений позвоночника.МРТ полезна при обнаружении повреждений и нарушений в мягких тканях, таких как мышцы, связки, сухожилия, спинной мозг и нервы.
- Компьютерная томография (КТ) : При КТ используются специальные рентгеновские лучи с контрастным веществом или без него для получения трехмерных изображений поперечного сечения позвоночника. КТ обеспечивает более подробные изображения, чем обычные рентгеновские снимки, для оценки повреждений или нарушений костей.
- Рентген : Мы используем рентгеновские снимки шеи или различных областей спины для выявления проблем с костями, таких как переломы, другие травмы и хронические заболевания.
- Биопсия: При подозрении на рак наши нейрохирурги могут взять небольшой образец ткани для анализа под микроскопом.
- Электромиография (ЭМГ): Электродиагностические исследования измеряют электрическую активность, генерируемую мышцами и нервами.
 Обычно они включают наблюдение за тем, как разные части тела реагируют на раздражители.
Обычно они включают наблюдение за тем, как разные части тела реагируют на раздражители. - Подтяжка спины
- Лечение рака, такое как операция по удалению опухолей, лучевая терапия, радиохирургия и химиотерапия
- Ледяная или тепловая терапия для травм
- Инъекции, такие как кортикостероиды или блокада нервов, для лечения боли
- Лекарства, такие как противовоспалительные, болеутоляющие или миорелаксанты
- Реабилитация с использованием физиотерапии для укрепления и растяжения мышц спины и живота
- Операция по замене дисков, сращению (соединению) позвонков, открытию позвоночного канала или восстановлению нервы
Автор: M.H. и Э. спланированное исследование; М.Х., Э. Т., К. Ф., Н. Б. и Н. Ф. проведенное исследование; M.H., E.T., C.F., N.B. и T.B. внесены новые реагенты / аналитические инструменты; M.H., E.T., J.M., N.B., T.B. и N.F. проанализированные данные; и M.H., E.T. и N.F. написал газету.
Рецензенты: К.Р., Университет штата Делавэр; и B.M.R., Медицинский колледж Северо-Восточного Университета Огайо.
Авторы заявляют об отсутствии конфликта интересов.
Эта статья содержит вспомогательную информацию на сайте www.pnas.org/lookup/suppl/doi:10.1073/pnas.1820745116/-/DCSupplemental.
- Пожилой возраст. Процесс старения дисков в нижней части спины, а также повторяющиеся травмы дисков и спинных мышц повышают вероятность возникновения у человека проблем с поясницей, которые обычно начинаются в среднем возрасте
- Мужчины старше женщин
- История предыдущей травмы спины
- Ваша работа или другая деятельность, повышающая риск развития грыжи межпозвоночного диска, например, длительное сидение, подъем или тяга тяжелых предметов, частое сгибание или скручивание спина, тяжелые физические нагрузки, повторяющиеся движения или воздействие постоянной вибрации (например, вождение)
- Регулярные упражнения, длительное выполнение напряженных упражнений или начало чрезмерных упражнений после длительного периода бездействия
- Курение.Никотин и другие токсины могут ухудшить способность дисков позвоночника поглощать необходимые им питательные вещества из крови, делая диски более склонными к травмам.
- Избыточный вес. Избыточный вес тела (особенно в области живота) вызывает дополнительную нагрузку на поясницу.
- Частый кашель
Факторы риска заболеваний позвоночника
Факторы, которые могут увеличить риск развития заболевания позвоночника, включают:
Симптомы заболеваний позвоночника
Признаки и симптомы заболевания позвоночника часто зависят от характера влияют на другие части тела, в зависимости от пораженной области позвоночника или спинного мозга. Общие симптомы включают:
Общие симптомы включают:
Диагностика заболеваний позвоночника
В Юго-Западном Юго-Западном наши специалисты по позвоночнику проводят тщательную оценку, включая:
В каждом индивидуальном случае наши врачи могут порекомендовать один или несколько тестов, например:
Лечение заболеваний позвоночника
Наши специалисты по позвоночнику часто используют одно или несколько методов лечения, в зависимости от конкретного состояния или травмы.Мы предлагаем следующие виды лечения:
Клинические испытания
UT Southwestern проводит клинические испытания, направленные на улучшение диагностики и лечения всех типов заболеваний позвоночника.Поговорите с нашими врачами, чтобы узнать, доступно ли клиническое исследование.
Морфология, патология и положение позвоночника у La Chapelle-aux-Saints Neandertal
Значение
Полностью прямая и уравновешенная осанка является одним из отличительных признаков человечества, и долгое время считалось, что она присутствует среди всех членов общества. род Homo . Однако недавние исследования позвонков неандертальцев привели к выводу, что эти поздние архаичные люди, которые были близки к нам как в поведении, так и в филогенетическом плане, не обладали полностью развитыми искривлениями позвоночника и, следовательно, имели шаткую позу.Переоценка и виртуальная реконструкция скелетов неандертальцев в Ла-Шапель-о-Святых 1 предоставляет прямые анатомические доказательства того, что он, а также другие неандертальцы, обладали обычным человеческим искривлением нижней части спины и шеи (лордоз).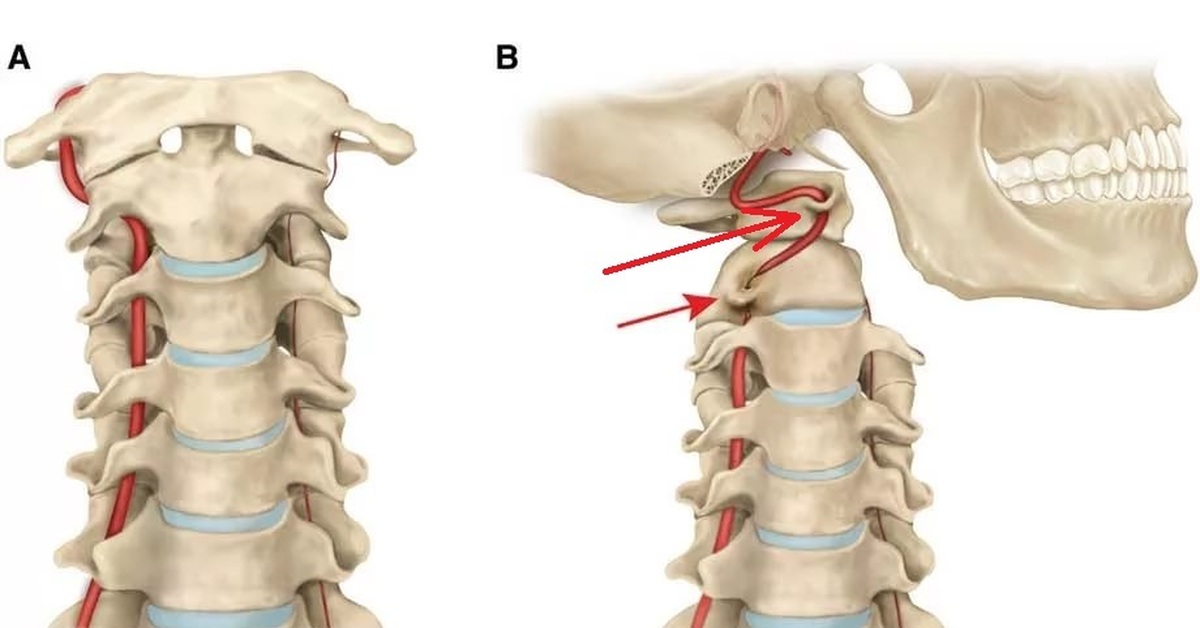 Следовательно, пора выйти за рамки того, чтобы делать неандертальцев менее человечными, и сосредоточиться на тонких сдвигах в биологии и поведении человека в позднем плейстоцене.
Следовательно, пора выйти за рамки того, чтобы делать неандертальцев менее человечными, и сосредоточиться на тонких сдвигах в биологии и поведении человека в позднем плейстоцене.
Abstract
Хотя ранние постуральные реконструкции неандертальцев как неполностью эрегированные были отвергнуты полвека назад, недавние исследования неандертальских позвоночных останков сделали вывод о гиполордозе, плоской нижней части спины и дисбалансе позвоночника, включая La Chapelle-aux- Святые 1 скелет.Эти исследования являются частью устойчивой тенденции рассматривать неандертальцев как менее «человечных», чем мы, несмотря на растущие доказательства незначительных, если вообще никаких различий в базовой функциональной анатомии и поведенческих способностях. Поэтому мы пересмотрели положение позвоночника Ла Шапель-о-Сэйнтс 1, используя новую реконструкцию таза, чтобы сделать вывод о поясничном лордозе, сочленении нижних поясничных (L4-S1) и шейных (C4-T2) позвонках, а также с учетом его широко распространенного возраста. связанный остеоартроз. La Chapelle-aux-Saints 1 демонстрирует поражение таза (и, следовательно, поясничный лордоз), аналогичное современному человеку, сочленение поясничных и шейных позвонков указывает на выраженный лордоз и болезнь Бааструпа как результат его преклонного возраста, остеоартрита и лордоза.Наши результаты ставят под сомнение представление о небольших искривлениях позвоночника у неандертальцев. Если оставить в стороне аномальный позвоночный столб Кебара 2, к Ла Шапель-о-Сэйнтс 1 присоединяются другие неандертальцы с достаточным количеством позвоночных остатков, обеспечивающих им полностью прямую (и человеческую) осевую осанку.
Постуральные реконструкции неандертальцев в конце 19-го и начале 20-го веков (1, 2), и особенно обширный скелет неандертальца La Chapelle-aux-Saints 1 Буля (2), создали устойчивые изображения этих позднеархаичных людей как примитивных людей. и неполностью возведенный.Предполагалось, что у неандертальцев отсутствует современный человеческий поясничный и шейный лордоз, а также слабый грудной кифоз, привычно согнутые бедра и колени и расходящиеся галлюцинации. В сочетании с их предполагаемой комбинацией наследственных и уникально полученных особенностей (2), а также их временной близости к ранним современным людям, эта постуральная реконструкция служила для того, чтобы дистанцироваться от этих людей позднего плейстоцена.
В сочетании с их предполагаемой комбинацией наследственных и уникально полученных особенностей (2), а также их временной близости к ранним современным людям, эта постуральная реконструкция служила для того, чтобы дистанцироваться от этих людей позднего плейстоцена.
В середине 20-го века серия переоценок (3-5) выявила ошибки более ранних реконструкций, при этом одна (5) сосредоточила внимание на остеоартрите останков Ла-Шапель-о-Сент.Вместе эти и более поздние анализы (6⇓⇓ – 9) предоставили неандертальцам полностью прямую (человеческую) позу с нормальным искривлением позвоночника. Однако в серии недавних работ (10–16) утверждается, что неандертальцы, в том числе Ла Шапель-о-Сент 1, обладали поясничными позвонками и углами падения таза, что свидетельствует об уменьшении поясничного лордоза, более плоском шейном лордозе и грудном кифозе. чем у современных людей, и небольшой наклон таза, связанный с двуногой позой (и поясничным лордозом) у недавних людей.Такая плоская кривая позвоночника у современных людей связана с передним смещением линии тяжести и нестабильностью, приводящей к хронической боли в спине (17), что вызывает вопросы о ее пригодности для неандертальцев.
Таким образом, цель здесь состоит в том, чтобы переоценить патологию и осанку одного из ключевых экземпляров в этих рассуждениях, «vieillard» из Ла Шапель-о-Сен. Первоначально основное внимание уделяется поражению таза, определенному после реконструкции таза, чтобы определить степень поясничного лордоза до развития обширного остеоартрита позвоночника.Он сочетается с оценкой наклона таза на основании распределения дегенеративных изменений в тазобедренном суставе. Выравнивание шейных и поясничных позвонков на основе их остеоартрозных изменений затем используется в качестве альтернативного средства для определения искривления позвоночника в более позднем возрасте. Эти оценки имеют значение как для вертикального положения неандертальцев, так и для нашего восприятия поведения этих немодернистских людей в контексте их позднего плейстоцена.
Результаты
Заболеваемость тазом и осанка.
Виртуальная реконструкция таза La Chapelle-aux-Saints 1 ( SI Приложение , рис. S2) показывает, что непатологические части двух сторон полностью симметричны. Угол падения таза (угол в сагиттальной плоскости между лучом от центра тазобедренного сустава до верхней крестцовой поверхности и перпендикуляром к крестцовой поверхности; ссылка 18) не зависит от дегенерации левой вертлужной впадины, учитывая симметричное соответствие эквивалентные левая и правая части вертлужной впадины и, следовательно, точное расположение центроида головки бедренной кости.Полученный таз показывает угол падения таза 56 ° (рис. 1), что тривиально выше среднего (52,4 ° ± 11 °, n = 131) для современного человеческого образца и находится в пределах 27 °. 82 ° (18).
Рис. 1.
Левый вид сбоку левой вертлужной впадины La Chapelle-aux-Saints 1, медиальный вид правой бедренной кости и срединно-сагиттальный разрез крестца. (Масштабная линейка, 3 см.) Угол падения таза (PI) = 56 °. Розовый: части правой бедренной кости, реконструированные в гипсе Боулем (11⇓ – 13).Обратите внимание, что реконструированный крестцовый мыс выступает над телом S1 выше, чем сохранившаяся часть; реконструкция поэтому консервативна, потому что только сохранившаяся часть обеспечит более высокий индекс PI.
Левая вертлужная впадина демонстрирует серию дегенеративных изменений, отражающих прогрессирующий остеоартрит. Наблюдается массивный периартикулярный рост по дорсальному краю вертлужной впадины и образование новой кости на полулунной суставной поверхности, но, что наиболее важно, есть полоса отлива шириной 10–12 мм, идущая от области передней нижней подвздошной ости (AIIS) до миддорсальный край (рис.2), или из секторов ∼2–5 после разделения полулунной поверхности вертлужной впадины на семь анатомически определенных секторов (19) ( SI Приложение , рис. S5). Степень этой дегенерации обеспечивает средний балл 3,5, что близко к медиане (3,25) недавнего образца трупа человека и находится в пределах его диапазона (2,75–3,75, n = 81). Более ограниченная, но отчетливая депрессия в правой верхней вертлужной впадине (Fig. 2) простирается от только дорсальной части AIIS до миддорсального края, или 2.5–4,5, что дает среднее значение 3,5. Все эти ископаемыхи и последних значения человека указует на среднюю точку для веса несущих сила реакции сустава через тазобедренный сустав около или слегка спинной от АИИСА, область, в которой вертлужное давление наибольшие в течение статического или динамической нагрузки в нормальном вертикальном положении человека и локомоциях (например, ссылки 20⇓⇓⇓ – 24; SI Приложение , раздел V ).
Более ограниченная, но отчетливая депрессия в правой верхней вертлужной впадине (Fig. 2) простирается от только дорсальной части AIIS до миддорсального края, или 2.5–4,5, что дает среднее значение 3,5. Все эти ископаемыхи и последних значения человека указует на среднюю точку для веса несущих сила реакции сустава через тазобедренный сустав около или слегка спинной от АИИСА, область, в которой вертлужное давление наибольшие в течение статического или динамической нагрузки в нормальном вертикальном положении человека и локомоциях (например, ссылки 20⇓⇓⇓ – 24; SI Приложение , раздел V ).
Рис. 2.
Виды La Chapelle-aux-Saints 1 правая ( A ) и левая ( B ) вертлужные впадины, ориентированные приблизительно анатомически.Зона пониженной нагрузки очевидна на правом, а широкая полоса опалившейся суставной кости в области воздействия нагрузки видна слева.
Таким образом, очевидно, что общая осанка таза Ла Шапель-о-Сэйнтс 1 вполне соответствовала диапазону вариаций современных людей на протяжении всей его жизни. Кроме того, ориентация черепной поверхности S1, которая должна была быть установлена во время развития, была неотличима от таковой у современных людей.
Искривление позвоночника и остеоартроз позвоночника.
Заболеваемость тазом по La Chapelle-aux-Saints 1 предсказывает хорошо развитый угол поясничного лордоза 52 ° с 95% доверительным интервалом 35 ° — 69 °, в соответствии с уравнением регрессии из (15). Недавний образец человека (18) дает среднее значение 55,6 ° (± 11,2 °, n = 131). Характер и степень его позвоночного остеоартрита подтверждают это предсказанное нормальное искривление позвоночника у человека.
Наблюдаются заметные изменения, в частности, в нижнем шейном и верхнегрудном отделах позвоночника, а также в средней и нижней части грудного отдела, включая отлив и подвывихи телескопических фасеточных суставов ( SI Приложение , рис.S1; см. также исх. 25). Однако включение незначительных изменений указывает на то, что все сохранившиеся фасеточные суставы поражены остеоартрозом.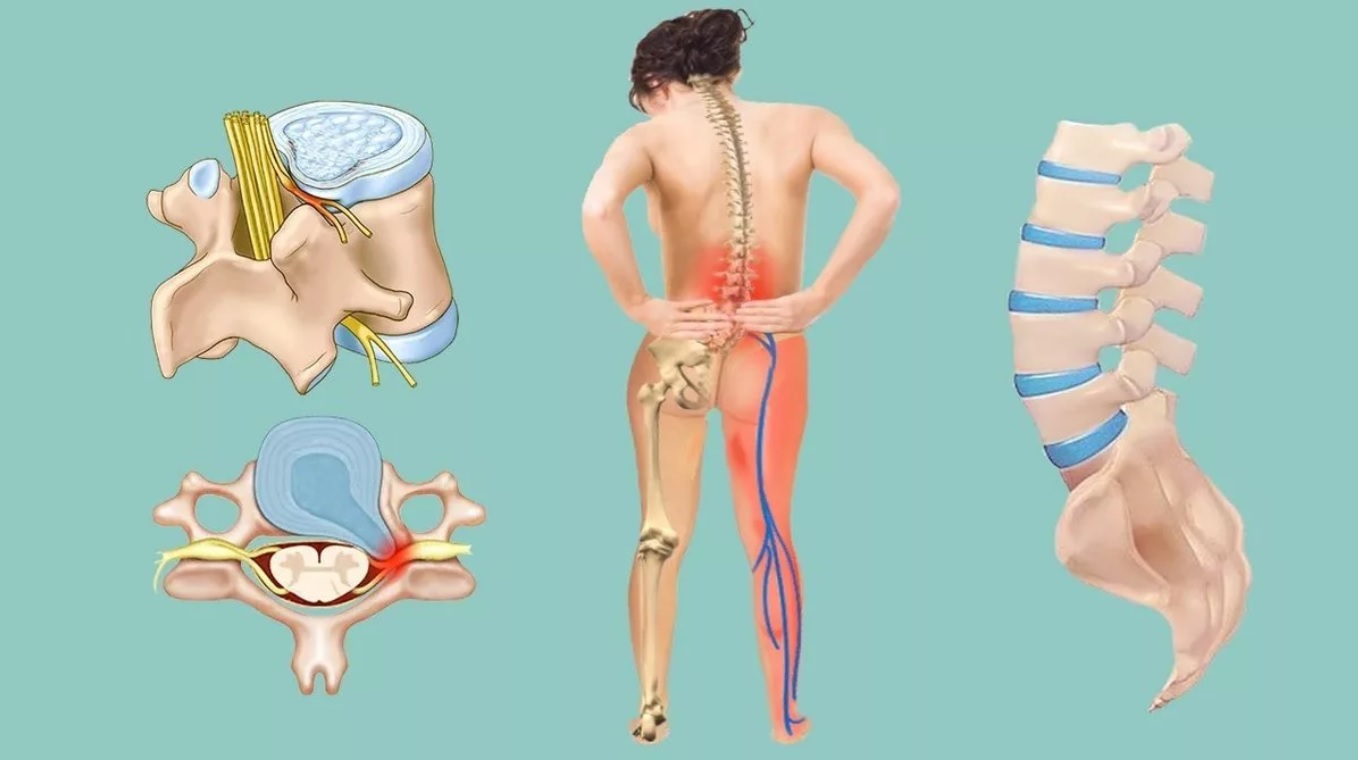 В шейной области верхушка остистого отростка C6 была уплощена, а небольшое углубление на его левой нижней части соответствует верхушке остистого отростка C7, что указывает на ремоделирование кости из-за болезни Бааструпа (рис. 3). Сочленение шейных позвонков также свидетельствует об уменьшении межпозвонковых дисковых пространств и тесном контакте между остистыми отростками C4 / C5 и C5 / C6, но явных признаков ремоделирования остеофита не наблюдалось.Сочленение шейных позвонков (рис. 3) также обеспечивает отчетливый лордоз от C4 до T1, также очевидный в шейных позвонках La Ferrassie 1 и Krapina 107 и 106 / 108–110 (26, 27).
В шейной области верхушка остистого отростка C6 была уплощена, а небольшое углубление на его левой нижней части соответствует верхушке остистого отростка C7, что указывает на ремоделирование кости из-за болезни Бааструпа (рис. 3). Сочленение шейных позвонков также свидетельствует об уменьшении межпозвонковых дисковых пространств и тесном контакте между остистыми отростками C4 / C5 и C5 / C6, но явных признаков ремоделирования остеофита не наблюдалось.Сочленение шейных позвонков (рис. 3) также обеспечивает отчетливый лордоз от C4 до T1, также очевидный в шейных позвонках La Ferrassie 1 и Krapina 107 и 106 / 108–110 (26, 27).
Рис. 3.
Шарнирно-сочлененные шейные и верхнегрудные серии C4-T3 по La Chapelle-aux-Saints 1, модели, созданные поверхностным сканированием. ( A ) вид сверху, ( B ) вид сбоку. Обратите внимание на болезнь Бааструпа остистых отростков C6-C7 (стрелка) и умеренное дегенеративное сколиотическое смещение.
Подвывих фасеточного сустава также наблюдался на L4 / L5 и L5 / S1, где он был связан с умеренными остеоартритическими изменениями фасеток. Эти подвывихи привели к формированию дополнительных суставов на нижних сторонах оснований правых реберных отростков L4 и L5, которые сочленялись с выемчатыми ложными суставами на правых верхних суставных отростках L5 и S1 соответственно (рис. 4). Кроме того, в остистых отростках L4, L5 и S1 наблюдались признаки болезни Бааструпа с обширным ремоделированием остеофитов.Сочленение нижних поясничных позвонков (рис. 4) показывает, что межпозвоночное пространство L4 / L5 заметно сократилось, что привело к привычному тесному контакту соответствующих остистых отростков. Нижний остистый отросток L5 эродирован, но между остистыми отростками L5 и S1 имеется небольшая точка соприкосновения. Типичным следствием асимметричных подвывихов с ложными суставами на правой стороне L4, L5 и S1 является правовыпуклое дегенеративное сколиотическое смещение этих позвонков (28, 29), которое в меньшей степени также присутствует в шейном отделе позвоночника.
Рис. 4.
Шарнирные нижние части позвоночника и крестца пиломатериалов Ла Шапель-о-Сент 1, ( A ) вид сверху, ( B ) вид сбоку. Обратите внимание на ложные суставы в форме выемки между L4 и L5, а также между L5 и S1 (кружки), ведущие к дегенеративному сколиотическому смещению и болезни Бааструпа между остистыми отростками L4-L5 и L5-S1 (стрелки; нижняя часть остистого L5 процесс размывается).
Угол сегментарного лордоза от L4 до S1 (55,5 ° ± 2,3 °) предсказывает очень высокий средний угол поясничного лордоза 73 ° — 79 ° на основе его сочлененных позвонков (SEest = 3.4 °, r = 0,721; SI Приложение , рис. S4). В сочетании с углом лордоза, предсказанным на основе его таза, эти соображения подтверждают наличие отчетливо человеческого поясничного лордоза для La Chapelle-aux-Saints 1.
Артикуляция нижних поясничных позвонков также демонстрирует, что подвывих фасеточных суставов с последующим ложные суставы в L4 / L5 и L5 / S1 в сочетании с болезнью Бааструпа этих позвонков должны были привести к лордотически фиксированной и практически неподвижной нижней части поясничного отдела позвоночника, неспособной к разгибанию и с очень ограниченной способностью сгибаться и сгибаться влево. сторона.Вероятно, что эта ригидность поясницы привела к ранее отмеченной (25) меньшей степени дегенерации поясничных фасеток по сравнению с выраженными шейными и грудными изменениями.
Обсуждение
La Chapelle-aux Saints 1 играет важную роль в обсуждениях позы неандертальцев с момента ее первоначального анализа Боулем (2). Наша оценка подтверждает наличие хорошо развитого шейного и поясничного лордоза у этого человека, как предполагалось ранее (3, 5, 8, 9). Это ставит под сомнение недавние реконструкции, предполагающие ограниченное искривление позвоночника неандертальцев (10–16).Мы основываем наши выводы на двух линиях доказательств: ( и ) заболеваемость тазом, связанная с нормальной осанкой таза человека, близкая к среднему значению для современных людей, и ( II ) сочленение шейного и нижнего поясничного отделов. позвонки. Дополнительные выводы из базикрания La Chapelle-aux-Saints 1 и других неандертальских позвонков ( SI Приложение , раздел IV ) подтверждают этот вывод.
позвонки. Дополнительные выводы из базикрания La Chapelle-aux-Saints 1 и других неандертальских позвонков ( SI Приложение , раздел IV ) подтверждают этот вывод.
Заболеваемость тазом и осанка.
La Chapelle-aux-Saints 1 представляет собой единственный достаточно полный таз неандертальца, неискаженный и непатологический в соответствующих частях.Таким образом, это позволяет точно определить поражение таза. Эта заболеваемость не только полностью соответствует современным требованиям, но и значительно превышает угол падения таза на 34 ° для таза Кебара 2 (15) и 28 ° для таза Атапуэрка-Сима-де-лос-Уэсос (AT-SH) 1 (11). .
Однако задняя подвздошная кость и крестец Kebara 2 были раздавлены и нуждались в обширной реконструкции (30), а от L2 до L5 произошел ряд пороков развития дисрафизма позвоночника и (вероятно, вторичных) дегенеративных аномалий (31, 32).Пациент в области таза 1 AT-SH также страдал от дефекта спинномозгового дисрафизма L5, приводящего к диспластическому спондилолистезу в процессе развития, и имел обширный набор остеоартрозных дегенеративных изменений (11). Полученная куполообразная верхняя крестцовая поверхность таза 1 AT-SH не позволяет правильно измерить его угол падения в таз. Кроме того, как у Kebara 2, так и у AT-SH таза 1 крестца обнаруживаются пояснично-крестцовые переходные аномалии; Пояснично-крестцовые переходные позвонки, как известно, приводят к ошибочно малым углам падения таза и, следовательно, к неправильной оценке поясничного лордоза (18, 33, 34).
Таким образом, таз Кебары и Атапуэрка не подходит для оценки заболеваемости тазом и корреляционной кривизны поясничного отдела у более широких популяций неандертальцев (или среднего плейстоцена). Таз La Chapelle-aux-Saints 1 обеспечивает по крайней мере одного неандертальца с полностью нормальной человеческой конфигурацией в осанке, углах наклона и подразумеваемом поясничном искривлении.
Дополнительная поддержка обеспечивается местами более легкой дегенерации других тазобедренных костей неандертальцев, которые параллельны локализации остеоартрита вертлужной впадины La Chapelle-aux-Saints 1. Вертлужные впадины Feldhofer 1, Kebara 2 и Krapina 208 и 209 имеют среднюю точку дегенерации поверхности в секторе 3, La Ferrassie 1 — 3,25, а Krapina 207 — 3,5 (27). Все эти средние точки дегенерации с опорой на вес тела отчетливо расположены дорсальнее AIIS, что указывает на то, что положение таза у неандертальцев в целом было таким же, как у современных людей.
Вертлужные впадины Feldhofer 1, Kebara 2 и Krapina 208 и 209 имеют среднюю точку дегенерации поверхности в секторе 3, La Ferrassie 1 — 3,25, а Krapina 207 — 3,5 (27). Все эти средние точки дегенерации с опорой на вес тела отчетливо расположены дорсальнее AIIS, что указывает на то, что положение таза у неандертальцев в целом было таким же, как у современных людей.
Болезнь Бааструпа и остеоартрит.
Еще одним важным руководством по восстановлению осанки позвоночника является наличие болезни Бааструпа в La Chapelle-aux-Saints 1 (см. Также исх.35). Он присутствует в C6 / C7, L4 / L5 и L5 / S1. Болезнь Бааструпа («целующиеся шипы»; ссылка 36) вызывается контактом соседних остистых отростков во время вертикальной позы и повторяющимися нагрузками на межостистую связку. Вначале это приводит к межостистой сумке и, при длительном стрессе, к остеофитическому увеличению кончиков остистых отростков. Они становятся уплощенными и склеротическими, между ними развиваются ложные суставы (37–39). Клинически это может быть связано с болезненностью в средней линии и болью в спине при вертикальном положении, которая усиливается при разгибании позвоночника и исчезает при сгибании.Чаще всего поражается L4 / L5, но в более тяжелых случаях также могут быть затронуты L3 / L4 (не сохранившиеся в La Chapelle-aux-Saints 1) и L5 / S1, а также весь поясничный отдел позвоночника, а также шейные позвонки (39 , 40). Часто (до 50% пациентов с запущенной болезнью Бааструпа; ссылка 37) может наблюдаться дегенеративное сколиотическое смещение поясничного отдела позвоночника, поскольку остистые отростки пытаются отклонить напряжение. Такое сколиотическое смещение подразумевается односторонними ложными суставами между L4 / L5 и L5 / S1 в La Chapelle-aux-Saints 1 и в меньшей степени, по-видимому, присутствует в шейном отделе позвоночника.
Факторы риска болезни Бааструпа включают крупные остистые отростки, усиление лордоза (например, в качестве компенсации за усиление грудного кифоза в пожилом возрасте), уменьшение межпозвонкового пространства и другие дегенеративные изменения стареющего позвоночника (37–41). В La Chapelle-aux-Saints 1 остистый отросток L5 не особенно велик, и степень грудного кифоза оценить невозможно. Однако уменьшение межпозвонковых промежутков проявляется телескопическим подвывихом шейных и нижних поясничных позвонков.Более того, сочленение нижних поясничных позвонков с крестцом предполагает, что угол лордоза находится в верхнем диапазоне у современного человека, если принять во внимание ложные суставы между остистыми отростками и основаниями реберных отростков. Кроме того, La Chapelle-aux-Saints 1 — один из старейших из известных экземпляров позднего плейстоцена, как неандертальцев, так и людей раннего современности.
В La Chapelle-aux-Saints 1 остистый отросток L5 не особенно велик, и степень грудного кифоза оценить невозможно. Однако уменьшение межпозвонковых промежутков проявляется телескопическим подвывихом шейных и нижних поясничных позвонков.Более того, сочленение нижних поясничных позвонков с крестцом предполагает, что угол лордоза находится в верхнем диапазоне у современного человека, если принять во внимание ложные суставы между остистыми отростками и основаниями реберных отростков. Кроме того, La Chapelle-aux-Saints 1 — один из старейших из известных экземпляров позднего плейстоцена, как неандертальцев, так и людей раннего современности.
Возраст смерти и патология.
Повторная оценка возраста на момент смерти Ла Шапель-о-Сэйнтс с использованием наиболее хорошо сохранившегося индикатора возраста (правая подвздошно-ушная поверхность) дает возраст в шестом или даже седьмом десятилетии ( SI Приложение , раздел II ).Поэтому вполне вероятно, что обширные остеоартритические изменения в его позвоночнике, а также очевидные в его грудино-ключичных, плечевых, локтевых, лучезапястных, тазовых и межфаланговых суставах педалей (8) связаны с совокупным влиянием возраста и в меньшей степени его кормовое существование в плейстоцене (42, 43). Таким образом, дегенерация позвоночника может быть использована как продукт нормальных возрастных процессов при оценке положения его позвоночника.
Выводы
После более чем столетия альтернативных взглядов должно быть очевидно, что в морфологии таза или позвоночника неандертальцев нет ничего, что отвергало бы наличие искривлений позвоночника в пределах диапазонов вариаций здоровых недавних людей.Остатки таза La Chapelle-aux-Saints 1 обеспечивают угол падения таза и осанку, что указывает на нормальную человеческую конфигурацию и, как следствие, на хорошо развитый поясничный лордоз в вертикальном положении. Последнее усилено сочленением его позвонков L4-S1, которые обеспечивают повышенный угол лордоза, отчасти из-за подвывиха фасеток, ложных суставов и болезни Бааструпа. Сочленение C4 с T3 свидетельствует о хорошо развитом шейном лордозе. Остеоартрозные изменения его позвонков и бедра поддерживают эту осанку таза и позвоночника, поскольку они отражают нормальные возрастные дегенерации человека.Другие, непатологические, тазовые и позвоночные останки неандертальцев подтверждают закономерность, очевидную в La Chapelle-aux-Saints 1.
Сочленение C4 с T3 свидетельствует о хорошо развитом шейном лордозе. Остеоартрозные изменения его позвонков и бедра поддерживают эту осанку таза и позвоночника, поскольку они отражают нормальные возрастные дегенерации человека.Другие, непатологические, тазовые и позвоночные останки неандертальцев подтверждают закономерность, очевидную в La Chapelle-aux-Saints 1.
Этот пересмотр останков La Chapelle-aux-Saints 1, связанный с позой и патологией позвонков, должен подчеркнуть то, что было принято полвека назад, но ставится под сомнение, поскольку отношения между неандертальцами и современными людьми (44, 45) стали (что неудобно для некоторых) близкими. Несмотря на очевидные морфологические контрасты, палеонтологически или археологически мало что указывает на различия в базовой функциональной анатомии и поведенческих способностях между ними и их современными соседями позднего плейстоцена (46, 47).Поэтому есть надежда, что эта переоценка подтвердит то, что уже давно было очевидным.
Материалы и методы
Анализ основан в первую очередь на оригинальном частичном скелете La Chapelle-aux-Saints 1 (2, 48) ( SI Приложение , раздел I ). Правая подвздошная кость отсутствует, гипсовая повязка [сверена с размерами оригинала; (49)]. Он представляет собой пожилого мужчины, возраст смерти которого находится в шестом или седьмом десятилетии ( SI Приложение , раздел II ).
Остатки таза не деформированы. Крестец включает в себя частичные первое и второе крестцовые тела, правую крылышко и смещенную пластинку. Левая тазовая кость сохраняет нижнюю подвздошную, седалищную и заднюю половину остеоартрозной вертлужной впадины. Правая тазовая кость удерживает большую часть подвздошной кости с ушной поверхностью и вертлужной впадиной подвздошной кости. Его недостающие части были реконструированы в гипсе по оригиналу (2), а сочленение с крестцом указывает на соответствующие размеры седалищно-лобкового отдела (49).Остается 19 пресакральных позвонков различной формы (50). Они включают C1 и C2, C4 – T2 (обозначены как C5 – T3 в ссылке 2), два фрагментарных верхних грудных позвонка (T3 или T4 и T6 или T7), T8 – T12, L1 и L3 – S2 (приложение SI. , рис. S1). У большинства тел позвонков отсутствуют вентральные края, но их дорсальные тела и нервные дуги в основном не повреждены. С C4 по T2 целы, с незначительными повреждениями.
Они включают C1 и C2, C4 – T2 (обозначены как C5 – T3 в ссылке 2), два фрагментарных верхних грудных позвонка (T3 или T4 и T6 или T7), T8 – T12, L1 и L3 – S2 (приложение SI. , рис. S1). У большинства тел позвонков отсутствуют вентральные края, но их дорсальные тела и нервные дуги в основном не повреждены. С C4 по T2 целы, с незначительными повреждениями.
3D-сканирование поверхности позвонков и тазовых останков с высоким разрешением было получено с помощью сканера PT-M4c (Polymetric).Сканер позволяет получать 3D-модели с максимальным разрешением по глубине 0,006 мм при поле сканирования 62 × 62 мм.
Виртуальная реконструкция таза (Рис. 1 и SI Приложение , Рис. S2) была выполнена с использованием Geomagic Design X (3dsystems.com) и Amira 6.7 (fei.com). Крестец отображали в зеркале, реконструкция контура передней части верхней крестцовой поверхности проводилась по контуру сохранившихся частей и сравнивалась с размерами тела L5.Разрушенное переднее крестцовое тело с мысом было зафиксировано с использованием поверхностной модели современного человека hemi-S1, которая была деформирована на тело S1 La Chapelle-aux-Saints 1 с использованием 167 ориентиров; ископаемого S1 искривления не было. Смещенная пластинка и срединный крестцовый гребень уменьшены. Отсутствующая каудальная часть крестца не реконструировалась. Зеркальное отображение двух бедренных костей позволило повторно собрать таз. Виртуальной реконструкции способствовала ручная реконструкция таза с использованием 3D-печати элементов.Основываясь на виртуальной реконструкции таза, мы измерили угол падения таза и оценили поясничный лордоз, следуя уравнению регрессии, которое было описано ранее (15).
Чтобы предсказать форму позвоночника La Chapelle-aux-Saints, его позвоночные остатки были сочленены цифровым способом с использованием Rhinoceros 5.4 (rhino3d.com), так что поверхности смежных фасеток показали максимальное совпадение с учетом телескопических подвывихов фасеточных суставов. Для цифровой реконструкции использовалась ручная артикуляция 3D-отпечатков позвонков.
Для цифровой реконструкции использовалась ручная артикуляция 3D-отпечатков позвонков.
Сочленения L4 и L5 и крестец использовались для оценки угла поясничного лордоза (18) на основе регрессии по методу наименьших квадратов угла лордоза L4-S1 по сравнению с углом лордоза L1-S1 на 63 рентгенограммах бокового поясничного отдела в вертикальном положении современного человека. из больницы Университета Балгрист, Цюрих ( SI Приложение , рис. S4). Рентгенограммы поясничного отдела получали в соответствии со стандартными протоколами (51) (Утверждение Комитета по этике кантона Цюрих KEK-ZH-№ 2014–0309). 95% интервалы прогноза были рассчитаны, как описано ранее (52).
Изменения при остеоартрите оценивались (в соответствии с ссылками 53 и 54) на отсутствующие, дискретно-легкие, умеренные и тяжелые с эбурналом. Распределение дегенеративных изменений вертлужной впадины оценивали в соответствии с разделением поверхности полулунной кости на семь секторов (19), в которых передняя и задняя степени дегенерации оценивались относительно обозначенных линий (2,5 с центром на AIIS) и Средняя точка между этими величинами используется для отражения основной области привычной совместной силы реакции.
Благодарности
Мы благодарим Д. Гримо-Эрве, А. Форта, Л. Юэ, В. Лаборда и А. Бальзо (Musée de l’Homme, Muséum Nationale d’Histoire Naturelle, Париж) за доступ к музею La Ископаемые останки Шапель-о-Святых. Финансовая поддержка была предоставлена Швейцарским национальным научным фондом №№ 31003A_156299 и 31003A_176319, а также Фондом Mäxi, Швейцария.
Сноски
Патология поясничного диска | Lifecare
Анатомия поясничного отдела позвоночника
Между каждым из пяти поясничных позвонков (костей) находится диск — прочная волокнистая амортизирующая прокладка. Диск представляет собой комбинацию прочных соединительных тканей, которые удерживают один позвонок за другим и действуют как амортизатор между позвонками. Диск состоит из жесткого внешнего слоя, называемого «фиброзное кольцо», и гелеобразного центра, называемого «пульпозное ядро».По мере того, как вы становитесь старше, центр диска может начать терять влагу, что делает диск менее эластичным и менее эффективным в качестве подушки.
Нервные корешки выходят из позвоночного канала через небольшие проходы между позвонками и дисками. Боль и другие симптомы могут развиться, когда поврежденный диск попадает в позвоночный канал или нервные корешки.
Дифференциальная диагностика — Дегенерация против пролапса против грыжи против компрессии нерва
Дегенерация диска — Дегенерация диска относится к синдрому, при котором болезненный диск может вызывать сопутствующую боль в пояснице.Состояние обычно начинается с травмы дискового пространства. Травма ослабляет диск и вызывает чрезмерное движение, потому что диск больше не может удерживать вместе позвонки выше и ниже диска, как раньше. Чрезмерное движение в сочетании с воспалительной реакцией раздражает локальную область, обычно вызывая симптомы боли в пояснице (см. Этап 1 на рисунке). В отличие от мышц спины, поясничный диск не имеет кровоснабжения и, следовательно, не может излечиться самостоятельно, а болезненные симптомы остеохондроза могут стать хроническими и привести к дальнейшим проблемам, таким как грыжа и сдавление нервных корешков.
Важно отметить, что дегенерация диска является частью естественного процесса старения и не обязательно приводит к болям в пояснице. МРТ-сканирование документально подтвердило, что примерно у 30% 30-летних есть признаки дегенерации диска на МРТ-сканировании, даже если у них нет симптомов боли в спине. Поэтому необходимо подчеркнуть, что не все дегенерированные диски, которые видны на МРТ, являются генераторами боли.
Грыжа межпозвоночного диска — Грыжа межпозвоночного диска часто называют «соскользнувшим диском», «выпуклым диском» или «выпавшим диском».Этот термин происходит от действия ядра ткани, когда оно выталкивается из центра диска. Сам диск не скользит. Однако ядро (мягкий внутренний слой) тканей, расположенное в центре диска, может быть подвергнуто такому давлению, что это может вызвать грыжу или разрыв фиброзного кольца (внешнего жесткого слоя). Это видно по разной степени выраженности на соседнем снимке со 2 по 4 стадии. Тяжесть межпозвоночной грыжи может привести к сдавливанию выпуклой тканью одного или нескольких спинномозговых нервов, что может вызвать локальную и отраженную боль, онемение или слабость в нижней части спины.нога или ступня. Приблизительно 90% грыж диска возникает в L4-L5 (поясничные сегменты 4 и 5) или L5-S1 (поясничный сегмент 5 и крестцовый сегмент 1), что вызывает боль в нерве L5 или нерве S1, соответственно.
Сдавление нерва / ишиас — Седалищный нерв — это большой нерв, который проходит вниз по позвоночнику до точки его выхода в тазу и переносит нервные волокна к ноге. Ишиас — это состояние, при котором грыжа или разрыв межпозвоночного диска давит на седалищный нерв. Это сжатие вызывает шоковую или жгучую боль в пояснице в сочетании с болью в ягодицах и вниз по ноге ниже колена, иногда достигая стопы.В самых крайних случаях, когда нерв защемлен между диском и прилегающей костью, симптомы включают не боль, а онемение и некоторую потерю контроля над движением в ноге из-за прерывания передачи нервных сигналов. Состояние также может быть вызвано опухолью, кистой, метастатическим заболеванием или дегенерацией корешка седалищного нерва.
Признаки и симптомы травмы поясничного диска Патология поясничного диска может проявляться широким спектром признаков и симптомов, при этом основной жалобой является боль в пояснице.Первоначальные признаки и симптомы могут включать централизованную боль в пояснице, скованность ранним утром, защемление и хватание, мышечный спазм, боль при движении (в основном при сгибании и скручивании) и ограниченный диапазон движений в пояснице. Если состояние прогрессирует и поясничный диск еще больше ухудшается, вызывая компрессию нервов, симптомы могут проявляться в виде излучающей боли в пояснице, стреляющих болей по ноге и стопе, онемения, булавок и игл, жжения, мышечной слабости и дальнейшего уменьшения диапазона поясницы движения.
Что увеличивает ваш риск? Факторы, которые нельзя изменить
Факторы, которые вы можете изменить
Лечение — В большинстве случаев, если боль в пояснице и / или ноге у пациента проходит после поясничной грыжи межпозвоночного диска, она проходит в течение примерно шести недель. В ожидании того, что диск заживет сам по себе, несколько консервативных вариантов лечения могут помочь уменьшить боль в спине, ногах и дискомфорт, вызванные грыжей межпозвоночного диска.
Физиотерапевтическое лечение при жалобе на поясничный диск может включать в себя ультразвук, электрическую стимуляцию, горячие компрессы, холодные компрессы, вытяжение поясничных суставов и мануальные («ручные») мобилизации, чтобы уменьшить боль и мышечный спазм, что облегчит его чтобы начать программу упражнений. Манипуляция может обеспечить кратковременное облегчение неспецифической боли в пояснице, но ее следует избегать в большинстве случаев грыжи межпозвоночного диска, чтобы избежать дальнейших травм и / или компрессии. Нестероидные противовоспалительные препараты (НПВП) e.грамм. Нурофен и аспирин могут быть полезны для облегчения воспаления, связанного с болью в пояснице, и для лечения тяжелых обострений могут быть назначены более сильные методы лечения, такие как пероральные стероиды или эпидуральная анестезия.
Сначала ваш физиотерапевт может прописать вам легкую растяжку или изменение позы, чтобы уменьшить боль в спине или симптомы в ногах. Когда у вас будет меньше боли, вы будете выполнять более энергичные упражнения для улучшения гибкости и силы поясницы, устойчивости корпуса, выносливости и обеспечения безопасного возврата к полной активности.В тяжелых случаях, когда дегенерация диска и / или компрессия нерва не поддаются консервативному лечению, может потребоваться хирургическое вмешательство.
Для получения дополнительной информации обратитесь к местному практикующему врачу.
Щелкните здесь, чтобы найти ближайшую клинику LifeCare.
Для получения дополнительной информации обратитесь к специалисту ближайшей к вам клиники Lifecare.
Найти клинику
Искривление позвоночника | патология
Искривление позвоночника , любое из группы отклонений нормального искривления позвоночника, включая сколиоз, лордоз и кифоз.
сколиоз
Рентгеновский снимок бокового отклонения позвоночника при сколиозе.
© Энтони Риччи / Shutterstock.com
Британская викторина
Болезни, расстройства и многое другое: медицинская викторина
Какое состояние вызвано отложением солей мочевой кислоты? Как еще называют перелом костей? Узнайте, что вы знаете о болезнях, расстройствах и многом другом.
Сколиоз — это боковое или боковое отклонение позвоночника или позвоночника. Состояние обычно включает две кривые — исходную аномальную кривую и развивающуюся позже компенсационную кривую. Возможные причины сколиоза включают асимметричное развитие мускулатуры спины, груди или живота, что может наблюдаться при полиомиелите или церебральном параличе; значительная разница в длине ног; или порок развития или заболевание позвоночного столба и связанных структур, например, при спондилите, расщеплении позвоночника, переломах, вывихах, полупозвонках или рахите.Лечение, которое зависит от причины, обычно включает ортопедическую операцию, использование вытяжения, ношение скобок для тела или шеи и упражнения.
Лордоз, или раскачивание, представляет собой увеличенное искривление в поясничной (от середины к низу) области позвоночного столба, и это может быть связано со спондилолистезом, воспалением межпозвонкового диска или ожирением. Кифоз, обычно называемый круглым, горбатым или горбатым, представляет собой увеличенное искривление грудного (верхнего) позвоночного столба; это может быть вызвано врожденной аномалией позвоночника, развитием клиновидных позвонков в подростковом возрасте (болезнь Шейермана) или другими состояниями, такими как остеопороз или туберкулезный спондилит (болезнь Потта).

 При лечении используются: бальнеологические, физиотерапевтические кабинеты, кабинеты лечебной физ.культуры и функциональной диагностики, кабинеты мануальной терапии и массажа, кабинет гипербарической оксигенации. В отделении 15 палат. В палатах имеется централизованная подача кислорода. Достаточное обеспечение твердым и мягким инвентарем. Стерилизация медицинских инструментов проводится централизовано в автоклавной. В процедурном кабинете имеются шкафы для хранения инъекционных и таблетированных препаратов, сейф для хранения наркотических и сильнодействующих препаратов, холодильник для хранения сывороток и медикаментов. Имеются наборы инструментов для выполнения люмбальной и подключичной пункции, аппараты ЭХО-скопии, реокартограф, доплерограф, столы для тракции позвоночника, аппарат для тракции шейного отдела позвоночника, наборы для ИРТ, два массажных кабинета с массажными столами и электромассажерами, физиоаппаратура для анестезии и электросна, ЭЛАП, мониторы прикроватного наблюдения в палате интенсивной терапии.
При лечении используются: бальнеологические, физиотерапевтические кабинеты, кабинеты лечебной физ.культуры и функциональной диагностики, кабинеты мануальной терапии и массажа, кабинет гипербарической оксигенации. В отделении 15 палат. В палатах имеется централизованная подача кислорода. Достаточное обеспечение твердым и мягким инвентарем. Стерилизация медицинских инструментов проводится централизовано в автоклавной. В процедурном кабинете имеются шкафы для хранения инъекционных и таблетированных препаратов, сейф для хранения наркотических и сильнодействующих препаратов, холодильник для хранения сывороток и медикаментов. Имеются наборы инструментов для выполнения люмбальной и подключичной пункции, аппараты ЭХО-скопии, реокартограф, доплерограф, столы для тракции позвоночника, аппарат для тракции шейного отдела позвоночника, наборы для ИРТ, два массажных кабинета с массажными столами и электромассажерами, физиоаппаратура для анестезии и электросна, ЭЛАП, мониторы прикроватного наблюдения в палате интенсивной терапии.

 Обычно они включают наблюдение за тем, как разные части тела реагируют на раздражители.
Обычно они включают наблюдение за тем, как разные части тела реагируют на раздражители.