Пороки развития легких — причины, симптомы, диагностика и лечение
Пороки развития легких – грубые изменения нормальной анатомической структуры легких, возникающие на этапе эмбриональной закладки и развития бронхолегочной системы и вызывающие нарушение или потерю ее функций. Пороки развития легких могут проявиться в детстве или взрослом возрасте, сопровождаясь цианозом, одышкой, кашлем с выделением гнойной мокроты, кровохарканьем, деформацией грудной клетки и др. С целью диагностики пороков развития легких выполняется рентгенография, КТ, бронхоскопия и бронхография, АПГ. Лечение пороков развития легких может быть хирургическим (резекция легкого, пульмонэктомия) или консервативным (медикаменты, ФТЛ, массаж, санация бронхиального дерева).
Общие сведения
Пороки развития легких – врожденные анатомические аномалии и дефекты функционирования легких, бронхов и легочных сосудов. Частота выявления пороков развития легких у детей варьирует от 10 до 20%. Среди врожденных дефектов легких и бронхов встречаются аномалии их развития, которые, в отличие от пороков, не проявляются клинически и не влияют на функцию измененного органа (например, аномалии деления крупных и средних бронхов). Пороки развития легких, сопровождающиеся дыхательной недостаточностью, проявляются уже в раннем детском возрасте и сопровождаются задержкой в физическом развитии ребенка.
На фоне пороков развития легких нередко развиваются воспалительные и нагноительные процессы, вызывающие клинику острых или хронических неспецифических заболеваний, которые могут принимать очень тяжелое течение. Более половины хронических неспецифических заболеваний легких патогенетически связаны с имеющимися пороками развития легких.
Пороки развития легких
Причины
Формирование аномалий и пороков развития легких в пренатальном периоде может происходить под влиянием ряда экзогенных и эндогенных тератогенных (повреждающих плод) факторов. К экзогенным факторам, оказывающим тератогенное воздействие на эмбрион, относятся физические (механическая или термическая травма, электромагнитное или радиоактивное излучение), химические (любые яды), биологические (вирусные или иные инфекции, бактериальные токсины) повреждающие механизмы.
К числу эндогенных тератогенных факторов принадлежат наследственность, аномалии генов и хромосом, эндокринные патологии, биологически неполноценные половые клетки (при поздней беременности у женщин или пожилом возрасте у мужчин). Вид развивающегося порока легкого зависит не столько от характера тератогенного фактора, сколько от срока беременности, на котором организм женщины испытывает его воздействие.
Если воздействие тератогенного фактора приходится на первые 3-4 недели беременности, когда происходит закладка трахеи и главных бронхов, возможно развитие пороков эти структур вплоть до нарушения формирования целого легкого. Тератогенное воздействие на эмбрион в период с 6 по 10 недели беременности может вызвать пороки формирования сегментарных и субсегментарных бронхов по типу кистозной или простой гипоплазии, а также развитие врожденных бронхоэктазов. Поздние пороки развития легких у плода могут сформироваться на 6-8 месяце беременности, когда закладывается альвеолярная ткань.
Классификация
По степени недоразвития легкого или его отдельных анатомических, тканевых, структурных элементов в пульмонологии различают:
- Агенезию – порок развития, характеризующийся полным отсутствием легкого и соответствующего ему главного бронха.
- Аплазию – порок развития, при котором отсутствует легкое или его часть при наличии культи рудиментарного главного бронха.
- Гипоплазию – одновременное недоразвитие элементов легкого (бронхов, легочной паренхимы, сосудов), встречающееся на уровне сегмента, доли или всего легкого. Простая гипоплазия характеризуется равномерным уменьшением размеров легкого без существенного нарушения его структуры с сохранением отчетливой редукции бронхиального дерева. Кистозная гипоплазия (кистозное или сотовое легкое, поликистоз) встречается среди всех пороков развития легкого наиболее часто (в 60-80% случаев) и сопровождается одновременным недоразвитием бронхов, легочной паренхимы и сосудов с формированием бронхогенных полостей в дистальных отделах субсегментарных бронхов, где обычно развивается хронический воспалительно-нагноительный процесс.
Среди пороков развития стенок трахеи и бронхов выделяют:
- Трахеоброхомегалию (трахеоцеле, мегатрахея, синдром Мунье-Куна) – расширение просвета трахеи и крупных бронхов вследствие врожденного недоразвития мышечных и эластических волокон их стенок. Наличие трахеобронхомегалии сопровождается упорным течением трахеобронхита.
- Трахеобронхомаляцию – несостоятельность хрящей трахеи и бронхов, вызывающую их аномальное спадание в процессе дыхания. Проявляется стридорозным дыханием, грубым кашлем, приступами апноэ.
- Синдром Вильямса-Кемпбелла – гипоплазия хрящей и эластических тканей бронхов III -VI-го порядков, проявляющаяся генерализованным развитием бронхоэктазов на уровне средних бронхов и бронхообструктивным синдромом.
- Бронхиолоэктатическую эмфизему Лешке – врожденную слабость стенок бронхиол, сопровождающуюся бронхиолоэктазиями и центрилобулярной эмфиземой.
Ограниченные (локализованные) дефекты строения стенок бронхов и трахеи включают:
- Стеноз трахеи и бронхов – резкое сужение бронхов и трахеи, возникающее вследствие нарушения развития хрящевых колец или внешнего сдавления трахеобронхиального дерева сосудами. Клинически проявляются стридорозным дыханием, приступами цианоза, нарушением глотания, рецидивирующими ателектазами.
- Врожденную долевую (лобарную) эмфизему – нарушение бронхиальной проходимости на уровне бронхов III-V порядков с образованием вентильного (клапанного) механизма, вызывающего резкое вздутие соответствующей доли. Сужение просвета бронха может развиваться в результате дефекта хряща, складок слизистой оболочки, сдавления опухолью или аномально расположенными сосудами и т. д. Лобарная эмфизема проявляется дыхательной недостаточностью различной степени, которая развивается в первые часы после рождения.
- Трахео- и бронхопищеводные свищи – открытое сообщение между трахеей (или бронхами) и пищеводом. Диагностируются вскоре после рождения, сопровождаются аспирацией пищи, кашлем, цианозом, приступами удушья при кормлениях, развитием аспирационной пневмонии.
- Дивертикулы бронхов и трахеи – формируются вследствие гипоплазии мышечного и эластического каркаса бронхов.
К врожденным порокам развития легких, связанным с наличием добавочных (избыточных) дизэмбриогенетических структур, относят:
- Добавочную долю (или легкое) – наличие дополнительного скопления легочной ткани, независимого от нормально сформировавшегося легкого.
- Секвестрацию легкого – наличие аномального участка легочной ткани, развивающегося независимо от основного легкого и снабжаемого кровью собственными артериями большого круга. Секвестрация может располагаться вне доли (внедолевая) и внутри нее (внутридолевая). Долгие годы клиника секвестрации может отсутствовать, проявления в виде рецидивирующей пневмонии возникают при инфицировании секвестра.
- Кисты легкого – парабронхиальные полостные образования, связанные с нарушениями эмбриогенеза мелких бронхов. Встречаются дренирующиеся и недренирующиеся кисты по признаку наличия или отсутствия сообщения с бронхиальным деревом. Кисты могут достигать гигантских размеров, при этом сдавливая окружающую паренхиму легкого.
- Гамартомы – дизэмбриональные образования, состоящие из бронхиальных стенок и легочной паренхимы; прогрессирующий рост и малигнизация не характерны.
Среди пороков развития легких, характеризующихся аномальным расположением анатомических структур, наиболее часто встречаются:
- Синдром Картагенера – обратное расположение внутренних органов, в т. ч. и легких. Обычно сочетается с хроническим бронхитом, бронхоэктазами и хроническим синуситом, протекает с частыми обострениями гнойного бронхолегочного процесса. Возможны видоизменения концевых фаланг и ногтей по типу «часовых стекол», «барабанных палочек».
- Трахеальный бронх – наличие аномального бронха, отходящего от трахеи выше верхнедолевого бронха.
- Доля непарной вены – часть верхней доли правого легкого, отделенная непарной веной.
К наиболее распространенным порокам развития кровеносных сосудов легких относятся:
- Стенозы легочной артерии – изолированными бывают крайне редко, обычно встречаются вместе с пороками сердца.
- Артериовенозные аневризмы – наличие патологических сообщений между венозным и артериальным руслом, сопровождающееся смешением венозной крови с артериальной и ведущее к возникновению гипоксемии. Наличие множественных артериовенозных сообщений характерно для болезни Рандю-Ослера. Поражение крупных и средних артерий протекает с формированием артериовенозных свищей — расширений по типу аневризмы. У пациентов развиваются выраженные гипоксемия и дыхательная недостаточность, кровохарканье.
- Гипоплазия и агенезия легочной артерии – недоразвитие или отсутствие ветвей легочной артерии часто встречается в сочетании с пороками сердца и гипоплазией легкого.
Симптомы пороков развития легких
Многообразию видов пороков развития легких соответствует полиморфность их возможных клинических проявлений. Скрытое течение многих пороков легких обусловливает вариабельность сроков их выявления. В первое десятилетие жизни обнаруживается 3,8% всех встречающихся пороков развития легких, во второе десятилетие — 18,2%, в третье — 26,6%, в четвертое — 37,9%, у лиц после 40 лет -14%.
Бессимптомное течение пороков развития легких встречается у 21,7% пациентов, симптомами нагноения проявляется 74,1% пороков, осложнениями других заболеваний — 4,2%.
Наиболее рано, в первые дни жизни ребенка, проявляются пороки развития легких, сопровождающиеся признаками дыхательной недостаточности: лобарная эмфизема, выраженный стеноз главных бронхов и трахеи, бронхо- и трахеопищеводные свищи, агенезия, аплазия и выраженная гипоплазия легкого. Они характеризуются стридорозным дыханием, приступами асфиксии, цианозом.
Кисты легкого, легочная секвестрация, гипоплазия легкого, бронхоэктазы могут впервые проявить себя развитием острого воспалительного процесса и нагноения. Характер воспалительных процессов при пороках развития легких носит затяжное рецидивирующее течение и сопровождается кашлем с выделением значительного количества гнойной мокроты, эпизодами кровохарканья, интоксикацией, нарушением самочувствия в периоды обострений. Тяжелые пороки развития легких вызывают отставание физического развития детей, асимметрию и деформацию грудной клетки.
Диагностика пороков развития легких
Диагностирование пороков развития легких требует комплексного специализированного обследования. Заподозрить пороки развития легких следует у пациентов, с детства страдающих стойкими хроническими бронхолегочными процессами. Решающее значение в диагностике пороков легких занимают рентгенологическое и бронхологическое исследования.
Рентгенологическое исследование позволяет выявить пороки развития легких даже при их бессимптомном течении. По данным рентгенографии и КТ легких можно определить изменения сосудистого и бронхиального рисунка (при гипоплазии), повышение прозрачности (при лобарной эмфиземе), смещение органов средостения (при гипоплазии или агенезии), контуры теней (при гамартоме или секвествации), обратную топографию легких (при синдроме Картагенера) и др. При бронхоскопии и бронхографии проводится оценка анатомического строения трахеи и бронхов, выявляются деформации (стеноз, свищи и др.) и изменения бронхиального дерева. При пороках развития сосудов легкого целесообразно проведение ангиопульмонографии.
Лечение пороков развития легких
Выбор адекватной тактики лечения пороков развития легких осуществляется пульмонологоми и торакальными хирургами. Он диктуется оценкой состояния пациента, степенью выраженности имеющихся нарушений и возможным прогнозом. Неотложная операция показана при выраженной дыхательной недостаточности в случаях лобарной эмфиземы, аплазии и агенезии легких, при трахеопищеводном свище и стенозах трахеи и бронхов.
При бронхоэктазах и кистозной гипоплазии выбор хирургического или консервативного лечения определяется количеством измененных сегментов в обоих легких, частотой рецидивов и характером изменений легочной ткани. Как правило, при таких пороках развития легких проводят резекцию измененного участка легкого.
При распространенных изменениях в легких проводится консервативная терапия, направленная на предупреждение обострений гнойного процесса. Она включает в себя ежегодные курсы противовоспалительной терапии, улучшение дренажа бронхиального дерева (бронхоальвеолярный лаваж, отхаркивающие, муколитические препараты, массаж, ингаляции, ЛФК), санаторно-курортную реабилитации.
Прогноз и профилактика пороков развития легких
При пороках развития легких, не связанных с развитием дыхательной недостаточности и не сопровождающихся гнойно-воспалительными осложнениями, прогноз удовлетворительный. Частые обострения бронхолегочного процесса могут вызывать ограничение трудоспособности пациентов. Меры профилактики врожденных пороков развития легких включают: исключение неблагоприятных тератогенных воздействий на протяжении беременности, медико-генетическое консультирование и обследование пар, планирующих рождение ребенка.
Врожденные пороки развития легких у новорожденных > Клинические протоколы МЗ РК
Пороки легких и бронхов могут быть результатом отклонений в развитии на всех стадиях формирования органа: между 3-й и 6-й неделями эмбрионального развития, когда на первичной кишке появляется дивертикул трахей, между 6-й и 16-й неделями, когда происходит быстрое деление бронхов, после 16-й недели, когда начинается активное формирование альвеолярного аппарата.
Врожденная гипоплазия и дисплазия лёгкого (синонимы: Врожденная кистозно-аденоматозная мальформация легкого, КАМЛ). Порок, при котором происходит разрастание терминальных бронхиол с образованием кист разного размера, не затрагивающих альвеолы. Вовлеченная в патологический процесс ткань легкого снабжается воздухом из магистральных дыхательных путей через узкие поры Кона, а кровью из легочной артерии. Практический во всех случаях заболевание поражает одно легкое (80-95%).
Врожденная секвестрация легкого (СЛ) представляет собой порок развития, характеризующийся тем, что часть легочной ткани, обычно ано-мально развитой и представляющей собой кисту или группу кист, оказывается отделенной от нормальных анатомо-физиологических связей (бронхи, легочные артерии) и васкуляризуется артериями большого круга кровообращения отходящими от аорты. Масса нефункционирующей эмбриональной или кистозной ткани, не имеющей связи с функционирующими дыхательными путями и снабжаемой кровью из большого круга кровообращения, носит название секвестра. Частота возникновения этого порока варьирует 0,15 до 6,4% среди всех пороков развития легкого. Почти во всех случаях поражение одностороннее и располагается в нижней доле легкого; около 2/3-слева.
Врожденная киста легкого (ВКЛ) (синонимы: бронхогенная, бронхолегочная, бронхиальная, воздушная бронхогенная и др.) киста легкого является пороком развития одного из мелких бронхов и представляет собой округлое полостное тонкостенное образование, выстланное изнутри эпителием и содержащее слизистую жидкость или воздух.
Врожденная лобарная эмфизема (ВЭЛ) — Врожденная лобарная эмфизема (синонимы — врожденная локализованная эмфизема, гигантская эмфизема, эмфизема напряжения) — порок развития, характеризующийся растяжением паренхимы доли легкого или сегмента и выявляющийся преимущественно в раннем детском возрасте. Врожденная лобарная эмфизема может быть обусловлена следующими тремя пороками развития: 1) аплазией гладких мышц терминальных и респираторных бронхов, в которых отсутствуют пучки гладких мышц и имеются лишь единичные мышечные клетки; 2) отсутствием промежуточных генераций бронхов; 3) агенезией всего респира-торного отдела доли. Изменения заключаются в отсутствии внутридольковых бронхов, терминальных респираторных бронхиол и альвеол.
I. ВВОДНАЯ ЧАСТЬ
Название протокола: Врожденные пороки развития легких у новорожденных
Код протокола:
Код(ы) МКБ-10:
Q33.6 гипоплазия и дисплазия легкого
Q33.2 секвестрация лекого
Q33.0 Врожденная киста лекого
Q33.8 Другие врожденные аномалии легкого
Сокращения, используемые в протоколе:
АЛТ -аланинаминотрансфераза
БЛД – бронхолегочная дисплазия
ВДГ-врожденная диафрагмальная грыжа
ИФА-иммуноферментный анализ
КЩР-кислотно-щелочное основание
КАМЛ– кисто- аденоматозная мальформация лекгого
МВ – механическая вентиляция
ОАК – общий анализ крови
ОАП – открытый артериальный проток
ОЦК-обьем циркулирующей крови
ПЦР – полимеразная цепная реакция
РКИ-рандамизированные контролируемые исследования
См Н2О – сантиметры водного столба
СРАР — постоянное положительное давление в дыхательных путях
СРБ – С-реактивный белок
ТБИ – тяжелая бактериальная инфекция
ЧД − частота дыхания
ЧСС – частота сердечных сокращений
ЭКМО -экстракорпоральная мембранная оксигенация
ЭхоКГ – эхокардиография
PIP- пиковое давление на вдохе,
PEEP- пиковое давление на выдохе
Tin –время вдох
FiO2 – концентрация подаваемого кислорода
LHR- легочно-головное отношение
SIMV- Synchronizedintermittentmandatoryventilation —синхронизированная принудительная перемежающаяся вентиляция легких (СППВЛ).
HFO (HFLO) –High fre quency oscillation —— высокочастотная осцилляция (осцилляторная ВЧ ИВЛ).
IPPV- Intermittent positive pressure ventilation (принудительная вентиляция без возможности спонтанного дыхания
CDP–Continuous disten din gpressure —самостоятельное дыхание с постоянно положительным давлением в дыхательных путей (СДППД)
СРАР –Contionuouspositiveail-waypressure —самостоятельное дыхание с положительным давлением в дыхательных путях (СДППД).
Дата разработки протокола: 2014 год.
Категория пациентов*: новорожденные дети.
Пользователи протокола: врачи неонатологи, анестезиологи-реаниматологи детские, детский (неонатальный) хирург стационаров.
Пороки развития легких — Знаешь как
Пороки развития легких у детей
Это врожденное или недоразвитая часть одного или сразу двух, недоразвитие всех структурных элементов: бронхов, паренхимы, сосудов и т.д.
Содержание статьи
Агенезия легких
Это врожденное отсутствие одного или обоих легких. При двустороннем агенезии ребенок рождается мертвым или погибает сразу после рождения. При односторонней агенезии он жизнеспособен.
Клиника. При агенезии легкого отмечается асимметрия грудной клетки, ее сплющивание на стороне агенезии, отсутствие участия в акте дыхания. На пораженной стороне межреберные промежутки сужены, сердце смещено в сторону отсутствующего легкого в связи со снижением давления в этой области, а также прессорного влияния компенсаторно увеличенного другого легкого. Перкуторный звук укорочен, аускультативно — дыхание резко ослаблено. На здорововой стороне — легочный звук с коробочным оттенком, дыхание существенно не изменено.
Диагностика агенезии
Рентгенологически определяют смещение органов средостения в сторону поражения, гомогенное интенсивное затемнение на месте отсутствующего легкого. Диафрагма смещена кверху и ограничена в движении. Воздушность здорового легкого повышена, отмечается усиление рисунка за счет компенсаторного увеличения кровообращения. На суперэкспонированных и послойных снимках видно отсутствие одного из главных бронхов, что подтверждается и бронхоскопически. Определенное диагностическое значение имеет также ангиопульмонография, при помощи которой выявляют отсутствие одноименной ветви легочной артерии и расширение общего ствола, а также единственной ветви легочной артерии. Бронхографию следует проводить крайне осторожно, так как может возникнуть нарушение бронхиальной проводимости единственного легкого. Агенезия часто сочетается с пороками развития других органов (врожденные пороки сердца, пищевода, дефект диафрагмы, расщелины тел позвонков и др.).
Аплазия легкого
Это порок развития, при котором имеется только рудиментарный главный бронх, паренхима легкого и сосудов отсутствует. Клинически и рентгенологически аплазия имеет симптоматику, аналогичную агенезии. Их разграничение может быть проведено с помощью бронхографии.
Лечение. При агенезии и аплазии легкого необходимости в хирургическом лечении нет. Особое значение имеет предупреждение заболеваний органов дыхательной системы, ликвидация очагов хронической инфекции в носоглотке, околоносовых полостях.
Прогноз. Длительность жизни с данными пороками развития различна. Значительная часть больных не доживает до 20 лет. Описаны единичные случаи, когда лица с подобной аномалией доживали до 70 лет и более.
Гипоплазия легких кистозная
Это недоразвитие всех структурных элементов: бронхов, паренхимы, сосудов. Гипоплазия может быть одно- и двусторонней. Может сочетаться с патологией развития других органов и систем (пороки развития диафрагмы, сердечно-сосудистой системы и др.). При кистозной форме гипоплазии наряду со значительным уменьшением объема легкого или его доли отмечаются выраженные изменения в бронхиальном дереве (кистозное расширение сегментарных и субсегментарных бронхов), а также агенезия альвеол и гипоплазия легочных сосудов в месте поражения.
Клиника. Проявления кистозной гипоплазии возникают в случае присоединения воспалительного процесса, обычно приобретающего хроническое течение. Наблюдается кашель с выделением мокроты, при физической нагрузке появляется одышка. Односторонняя гипоплазия характеризуется асимметрией грудной клетки с западанием пораженной стороны и сужением межреберных промежутков, искривлением позвоночника в грудном отделе в здоровую сторону, смещением органов средостения в пораженную сторону. Аускультативно в области кист выслушиваются сухие и влажные хрипы. При двусторонней гипоплазии асимметрия грудной клетки отсутствует. Степень дыхательной недостаточности зависит от объема пораженных легких. Рентгенологически наряду с уменьшением пораженного участка наблюдается картина фиброателектаза. При бронхографии обнаруживают уменьшение угла бифуркации, удлинение и сужение главного бронха, в участке поражения — множественные кистозные полости, которыми заканчиваются бронхи. С помощью ангиопульмонографии выявляют гипоплазию ветви легочной артерии, аномальное отхождение ветви артерии гипоплазированного легкого, обеднение кровотока в нем.
Лечение гипоплазии легких
Хирургическое (удаление измененной ткани легкого). В связи с тем, что кистозная гипоплазия прогрессирует, необходимо раннее хирургическое лечение. При двусторонней долевой гипоплазии лечение консервативное, такое же, как и при бронхоэктатической болезни.
Прогноз. Зависит от степени распространенности нарушения развития, своевременности диагностики и лечения.
Гипоплазия легких простая
Возникает при остановке развития легкого в конце второго месяца внутриутробной жизни. Простая форма гипоплазии характеризуется равномерным уменьшением легкого, доли или сегмента в результате недоразвития бронхов и паренхимы легкого.
Клиника. Сходна с таковой при кистозной гипоплазии. Рентгенологически при простой гипоплазии отмечается снижение прозрачности легочной ткани в зонах нарушения, обеднение ее рисунка, более высокое стояние купола диафрагмы на пораженной стороне. Здоровое легкое гипертрофируется, прозрачность его повышена. При значительном уменьшении измененного легкого возможно частичное смещение другого легкого в пораженную сторону. При бронхографии обнаруживают обеднение рисунка бронхиального дерева, уменьшение диаметра бронхов, слабое заполнение периферических отделов.
Лечение и прогноз. См. Гипоплазия легкого кистозная.
Кисты легких не паразитарные
Это одиночные или множественные тонкостенные кистозные образования в легочной паренхиме.
Этиология. Различают непаразитарные кисты врожденные, обусловленные нарушением эмбриогенеза бронхолегочного аппарата, и приобретенные, сформированные в результате стафилококковой и коклюшной пневмонии в виде булл, которые в редких случаях не имеют тенденции к облитерации, эпителизируются и приобретают черты врожденной кисты. Поэтому отличить истинную врожденную кисту от приобретенной трудно не только клинически и рентгенологически, но и морфологически, и помочь здесь могут анамнестические сведения.
Патогенез. Вследствие нарушения закладки бронха в процессе эмбриогенеза или в результате эпителизации буллы, оставшейся после острой деструкции легких, образуются кисты, которые могут сохранять связь с бронхом. Скапливающийся в их полости секрет может инфицироваться и нагнаиваются.
Классификация. Кисты бывают единичными (солитарными) и множественными, врожденными и приобретенными. Врожденные кисты подразделяют на бронхогенные, альвеолярные и межуточные в зависимости от порока развития бронха, альвеолярного аппарата или межуточной ткани. Врожденные й приобретенные кисты делят на неосложненные и осложненные (нагноение, напряжение, прорыв в плевральную полость) .
Клиника. Неосложненные кисты в большинстве случаев не имеют характерных клинических симптомов, протекают бессимптомно и диагностируются случайно при профилактических рентгенологических осмотрах. Нагноение кисты характеризуется болью в соответствующей половине грудной клетки, кашлем, сухим или влажным (при дренировании кисты бронхом), гнойной интоксикацией (ухудшение состояния, вялость, потеря аппетита, гектическая температура, лейкоцитоз со сдвигом лейкоцитарной формулы влево до нейтрофильных гранулоцитов). При осмотре пораженная сторона может отставать в дыхании, перкуторно здесь определяют притупление звука, аускультативно — ослабление везикулярного дыхания, хрипы. Напряжение кисты обусловлено вентильным механизмом в месте соединения ее с дренирующим бронхом, диаметр которого определяет быстроту нарастания напряжения и его степень. Сдавление паренхимы легкого и смещение средостения в здоровую сторону приводит к развитию дыхательной недостаточности (одышка, цианоз носогубного треугольника, тахикардия, беспокойство ребенка). Перкуторно над напряженной кистой определяют коробочный звук с притуплением вокруг, границы сердца смещены в противоположную сторону, выслушивается бронхиальное дыхание с амфорическим оттенком, а в окружности кисты — ослабление везикулярного дыхания, хрипы. Рентгенологически видна большая тонкостенная округлая воздушная полость с четкими контурами. Легкое оттеснено к периферии, медиастинальная плевра выпячена в здоровую сторону — медиастинальная грыжа. При прорыве напряженной кисты в плевральную полость развивается клиническая картина пневмоторакса—острая боль в боку, кашель, нарастающая дыхательная и сердечно-сосудистая недостаточность вследствие внезапного поступления воздуха в плевральную полость, коллабирования легкого, смещения средостения в здоровую сторону с ограничением экскурсии второго легкого (см. Пневмоторакс). Перкуторно на стороне поражения определяют тимпанит и смещение границ средостения в противоположную сторону, аускультативно-бронхиальное дыхание. На рентгенограмме виден воздух в плевральной полости, легкое поджато к корню, а средостение смещено в здоровую сторону. Иногда напряженный пневмоторакс сочетается с пневмомедиастинумом (эмфиземой средостения).
Диагностика кисты легких
Распознают на основании рентгенологического исследования, при котором устанавливают единичные или множественные кистозные образования, их размеры и локализацию. При необходимости производится томография. Для уточнения отношения кист к бронхиальному дереву в неосложненных случаях целесообразна бронхография.
Дифференциальная диагностика. Легочные кисты следует дифференцировать с буллами, оставшимися после острой деструкции легких, врожденной лобарной эмфиземой, а при нагноении — с абсцессом легкого или ограниченным пиопневмотораксом.
Лечение кисты легких
Хирургическое. Отсрочка операции или отказ от нее допустимы у новорожденных и грудных детей, при невозможности сразу дифференцировать с буллами стафилококкового генеза, что можно сделать лишь в процессе динамического наблюдения. Радикальное оперативное вмешательство не показано при множественных кистах в обоих легких. В случае нагноения кист радикальной операции может предшествовать бронхоскопическая катетеризация полости через дренирующий бронх или чрескожная пункция (катетеризация), отсасывание гноя и санация полости растворами антибиотиков широкого спектра и антисептиков (нитрофураны и др.). Напряженная киста может быть дренирована для уменьшения явлений дыхательной недостаточности перед транспортировкой в специализированный стационар или перед торакотомней.
Радикальная операция заключается в цистэктомии или лобэктомии. При прорыве кисты в плевральную полость последнюю дренируют по общим правилам, а вопрос о радикальной операции решают с учетом анамнестических данных и состояния больного.
Статья на тему Пороки развития легких
4.5.1 Классификация пороков развития легких.
Наиболее
детальной следует признать классификацию
ПРЛ, разработанную Н. В. Путовым с соавт.
(1980) как классификацию, наиболее полно
отражающую все многообразие этой сложной
патологии.
Пороки
развития (дисплазии) легких.
1. Пороки,
связанные с недоразвитием органа в
целом или его анатомических, структурных,
тканевых элементов.
§ Агенезия
легкого.
§ Аплазия
легкого.
§ Гипоплазия
легкого простая.
§ Гипоплазия
легкого кистозная (поликистоз).
§ Синдром
гиалиновых мембран (респираторный
дистресс-синдром новорожденных).
§ Трахео
– бронхиальная дискинезия (экспираторный
стеноз).
§ Синдром
Вильямса – Кемпбелла.
§ Врожденная
долевая эмфизема новорожденных.
§ Трахеобронхомегалия
(синдром Мунье – Куна).
§ Врожденная
односторонняя эмфизема (синдром
Маклеода).
2. Пороки,
связанные с наличием избыточных
(добавочных) дизэмбриогенетических
формирований.
§ Добавочное
легкое (доля) с обычным кровоснабжением.
§ Добавочное
легкое (доля) с аномальным кровоснабжением
(внедолевая секвестрация).
§ Киста
легкого.
§ Киста
(кисты) легкого с аномальным кровоснабжением
(внутридолевая секвестрация).
§ Гамартома
и другие врожденные опухолевидные
образования.
3. Необычное
расположение анатомических структур
легкого, имеющее клиническое значение.
§ Доля
непарной вены.
§ «Зеркальное»
легкое.
§ Обратное
расположение легких.
§ Трахеальный
бронх.
4. Локализованные
аномалии строения трахеи и бронхов.
§ Дивертикулы
трахеи и бронхов.
§ Стенозы
трахеи и бронхов.
§ Трахео-
(бронхо) пищеводные свищи.
§ Сочетания
перечисленных поражений.
5. Аномалии
кровеносных и лимфатических сосудов
легких.
§ Аневризмы
легочной артерии и ее ветвей.
§ Артериовенозные
свищи (аневризмы) локализованные.
§ Артериовенозные
свищи множественные без четкой локализации
(при синдроме Рандю–Ослера).
§ Варикозное
расширение легочных вен.
§ Стенозы
легочной артерии и ее ветвей.
§ Лимфангиоэктазии
и прочие аномалии лимфатической системы
легких.
Эффективность
лечения больных с пороками развития
легких во многом зависит от раннего
выявления этих заболеваний, тщательного
анализа результатов специальных методов
исследования и своевременного
использования всего арсенала лечебных
мероприятий, включая хирургическое
лечение.
4.4.2 Пороки, связанные с недоразвитием органа в целом или его анатомических, структурных, тканевых элементов.
Агенезия
легкого (врожденное
отсутствие) относится к наиболее редким
порокам развития дыхательной системы.
С эмбриологической точки зрения агенезия
объясняется отсутствием первичной
бронхиальной почки. При этом пороке
развития отсутствуют все структурные
единицы легкого: бронхи, сосуды, паренхима
(Рис. 17)
Рис.
17 Агенезия левого легкого. Обзорная
рентгенограмма. Срединная тень смещена
влево. Межреберные промежутки сужены.
Купол диафрагмы приподнят.
Односторонняя
агенезия легкого совместима с жизнью,
но часто сочетается с тяжелыми врожденными
пороками других органов – сердца,
сосудов, пищевода, скелета.
Клиника
диагностика. Дети
с двусторонней агенезией нежизнеспособны
и погибают сразу после рождения.
При
односторонней агенезии и отсутствии
воспалительного процесса в единственном
легком клинические проявления скудные.
Явных признаков дыхательной недостаточности
не отмечается. При осмотре выявляется
асимметрия грудной клетки с уплощением
и отставанием при дыхании на стороне
поражения. Органы средостения смещаются
в сторону порочно развитого легкого.
Сердце при этом состоянии обычно
повернуто вокруг вертикальной оси.
Здоровое легкое расширяется, проникает
на другую половину грудной клетки и
образует так называемую медиастинальную
грыжу. Над медиастинальной грыжей в
верхних и медиальных отделах грудной
клетки на стороне порочно развитого
легкого прослушиваются дыхательные
шумы.
При рентгенографии отмечаются
следующие признаки:
1) интенсивное
затемнение легочного поля на стороне
агенезии;
2) тень
купола диафрагмы не контурируется;
3) резкое
смещение тени средостения;
4) декстракардия
при агенезии справа и ротация сердца
при агенезии слева;
5) обнажение
и кифосколиоз позвоночника;
6) медиастинальная
грыжа на стороне поражения;
7) усиление
корня и легочного рисунка единственного
легкого за счет полного перекровотока.
При трахеобронхоскопии определяются
девиация трахеи, отсутствие карины и
мембранозной части в нижних отделах
трахеи с замкнутыми хрящевыми кольцами.
Трахея непосредственно переходит в
главный бронх единственного легкого.
Наибольшую
ценность в диагностике агенезии легкого
имеет трахеобронхография,
при которой выявляется смещение и
удлинение трахеи, переходящей в бронхи
единственного легкого. Культя главного
бронха на стороне агенезии отсутствует.
При ангиопульмонографии отмечаются
смещение тени сердца, легочного ствола
и отсутствие легочной артерии на стороне
поражения.
Дифференциальная
диагностика проводится с ателектазом
легкого, аплазией или гипоплазией,
инородным телом главного бронха. В
некоторых случаях картину агенезии
легкого может напоминать фибриноторакс
после перенесенной острой гнойной
деструктивной пневмонии.
Несмотря
на исключительную редкость агенезии
легкого, функция внешнего дыхания и
гемодинамика в малом круге при этой
патологии изучены достаточно подробно.
В значительной части опубликованных
наблюдений агенезии представлены
результаты изучения вентиляции,
газообмена и гемодинамики, которые
свидетельствуют об отсутствии у
большинства пациентов существенных
отклонений от нормы.
При
отсутствии врожденной патологии со
стороны других органов и систем, а также
заболеваний единственного легкого
пациенты с агенезией практически
здоровы. Так, Emery (1970)
наблюдал пациентку, дожившую с агенезией
легкого до 81 года.
Лечение. При
воспалительном процессе в единственном
легком – показана массивная
антибактериальная терапия. В остальных
случаях – симптоматическое лечение.
Хирургическое лечение не проводится.
Аплазия
легкого.
Аплазия
легкого отличается от агенезии наличием
рудиментарного бронха, заканчивающегося
слепо или имеющего рудименты долевых
бронхов, а иногда соответствующей
артерии. Порок развития встречается
крайне редко. Клинические симптомы
практически не отличаются от агенезии
легкого. Иногда при ревизии воспалительного
процесса в слепо заканчивающемся бронхе
наблюдается кашель со скудной слизисто
– гнойной мокротой.
Возможна
аплазия одной или двух долей. Чаще
встречается отсутствие верхней и средней
долей справа.
Рентгенологически
отмечается смещение средостения в
сторону поражения. При бронхоскопии
выявляется культя соответствующего
бронха. В диагностике решающее значение
имеет бронхо – и ангиопульмонография.
Хирургическое
лечение при данном пороке не требуется.
Гипоплазия
легкого.
Гипоплазия
легкого представляет собой недоразвитие
всех структурных единиц легкого,
зависящее от той стадии развития
глоточно–трахеального зачатка, на
которой оно закончилось. В зависимости
от этого гипоплазия легкого имеет разные
клинико–рентгенологические проявления.
Принято
считать (И. К. Есипова), что в основе
гипоплазии лежит не столько остановка,
сколько извращение развития всех
структур легкого, причем структуры
легочной ткани, остановившись в развитии
на одном из этапов эмбриогенеза, не
могут абсолютно стабилизироваться.
Дисгенезия тканевых структур (термин
предложен Roche и Chemin в
1962) является почвой, на которой формируются
различные анатомические и гистоморфологические
проявления порока, зависящие от этапа
эмбриогенеза и условий развития, и
проявляющиеся анатомическими и
функциональным недоразвитием всех
элементов легкого.
При
остановке развития до деления на
сегментарные бронхи респираторный
отдел практически не дифференцирован,
и легкое имеет значительно уменьшенные
размеры в виде комочка легочной ткани.
При нарушении развития легкого на уровне
деления сегментарных бронхов последние
деформированы и заканчиваются слепо
без последующих генераций. Нарушение
развития легкого на уровне деления
сегментарных и субсегментарных бронхов
бронхографически проявляется в виде
кистообразных, слепо заканчивающихся
субсегментарных бронхов. Остановка
развития внутридольковых бронхов
сопровождается образованием множества
мелких кист (микрополикистоз).
Большинство
клиницистов описывают две наиболее
распространенные формы гипоплазии
легких — простую и кистозную.
Простая
гипоплазия —
этот порок развития состоит в равномерном
уменьшении легкого без существенного
нарушения структуры органа с отчетливой
редукцией бронхиального дерева до 10 –
14 генераций вместо 18 – 24 генераций в
норме.
Анатомически
легкое или его доли при простой гипоплазии
уменьшены в объеме, «мясистой»
консистенции, с отсутствием пигмента,
без внешних признаков деления на доли
и сегменты. При рассечении бронхиального
дерева во всех случаях обнаруживается
уменьшение числа сегментарных бронхов
и их ветвлений. Узкие субсегментарные
бронхи продолжаются до субплевральных
отделов, где располагаются в виде
спиралей и рассыпаются на мелкие
стволики, образуя фигуру «кисточек».
Клиника
и диагностика. Простая
гипоплазия часто сочетается с другими
аномалиями легких – агенезия доли,
секвестрация и др., а также с расщеплением
грудины, аномалией впадения легочных
вен и т.д.
Клиническая
картина определяется вторичным
нагноительным процессом – жалобы на
влажный, реже сухой кашель, со
слизисто–гнойной мокротой, повторные
обострения бронхолегочного процесса,
одышку при физической нагрузке. В раннем
возрасте дети слаборазвиты, отстают в
физическом развитии от сверстников.
При обширном поражении выражены симптомы
гнойной интоксикации и хронической
гипоксии. При аускультации в фазе
ремиссии выслушиваются рассеянные или
локализованные сухие хрипы. Следует
отметить, что в ряде случаев этот порок
развития может протекать и бессимптомно.
При
исследовании больных обращает на себя
внимание ассиметрия грудной клетки,
из–за западения и уплощения одной ее
половины, что сопровождается сужением
межреберных промежутков и перемещением
органов средостения в пораженную
сторону. Над уменьшенной в объеме и
уплощенной половиной грудной клетки
перкуторный звук укорочен, дыхание
резко ослаблено.
При рентгенографии выявляется
уменьшение гемиторакса, сужение
межреберных промежутков, смещение тени
средостения в пораженную сторону,
высокое стояние купола диафрагмы на
стороне пораженного легкого. При
бронхоскопии выявляется катаральный
эндобронхит, нетипичное расположение
устьев сегментарных и долевых бронхов,
часто суженных. На бронхограммах у
больных с простой гипоплазией
контрастируются лишь бронхи 3 – 6 порядка
в виде «обгоревшего дерева» или имеет
место картина пропуска генераций, когда
непосредственно от крупных бронхов
отходят очень мелкие бронхиальные
веточки (Рис.18)
Рис.
18 Простая гипоплазия. Бронхограмма.
Недоразвитие бронхов средней и нижней
доли правого легкого.
В
ряде случаев имеет место древовидное
ветвление бронхов или в виде «пучка»
(в норме – дихотомическое). Ангиопульмонограмма дает
контрастирование равномерно суженных
артериальных стволов с задержкой фаз
заполнения капилляров и вен. Радиологические
методы позволяют
определить степень функциональных
нарушений (вентиляции и кровотока) в
зонах, соответствующих локализации
порока.
Лечение хирургическое,
при этом своевременная операция у детей
позволяет избежать вовлечения в процесс
интактных отделов этого же легкого. У
взрослых дифференциальная диагностика
простой гипоплазии, осложненной
нагноением и приобретенной хронической
патологией, затруднена, но это
обстоятельство не имеет большого
практического значения, поскольку
хирургическая тактика лечения в обоих
случаях одинакова, т. е. и в том и в другом
случаях показано удаление доли или
всего легкого.
Кистозная
гипоплазия –
один из наиболее (до 60 – 80%) встречающихся
пороков развития легких, характеризуется
кистозным превращением легкого на
уровне ветвлений сегментарных и
субсегментарных бронхов. Многообразие
клинических и анатомических проявлений
служит причиной множества терминов,
применяемых для обозначения этой
патологии в литературе (поликистоз,
кистозные бронхоэктазы, сотовое легкое,
множественные кисты, кистозный фиброз,
мышечный фиброз легких и т. д.). Е. В.
Рыжков собрал в литературе около 40
наименований кистозной гипоплазии. Это
объясняется еще и отсутствием единых
представлений о сущности кистозных
форм пороков, трудностью дифференциальной
диагностики этой патологии с приобретенными
кистами легких.
Клиника
и диагностика. Поскольку
в абсолютном большинстве случаев
кистозная гипоплазия легких осложняется
присоединением инфекции, это обстоятельство
и определяет клиническую картину
заболевания. Больные предъявляют жалобы
на постоянный влажный кашель со слизистой
или (чаще) со слизисто–гнойной мокротой,
частые повторные обострения бронхолегочного
процесса, признаки выраженной гнойной
интоксикации.
Первые
проявления хронического бронхолегочного
процесса отмечаются в раннем детском
возрасте, реже – в юношеском и взрослом
возрасте. В дальнейшем заболевание
сразу приобретает характер хронического,
неуклонно прогрессирующего воспалительного
процесса, протекающего на фоне довольно
стертой симптоматики со скудными
клиническими проявлениями. Раннее
выявление больных с кистозной гипоплазией
имеет решающее значение, поскольку
своевременно выполненная операция
может предотвратить распространение
воспалительного процесса с вовлечением
интактных участков пораженного легкого,
а нередко и противоположного легкого.
В
состоянии ремиссии больные предъявляют
жалобы на одышку, вначале при физической
нагрузке, затем и при незначительных
физических усилиях, а также на постоянно
беспокоящий кашель со скудной мокротой.
При осмотре грудной
клетки отмечается неравномерность
участия в акте дыхания, с запаздыванием
и отставанием на вдохе той половины,
где процесс более выражен. Перкуторно над
очагом поражения можно отметить
укорочение звука, смещение органов
средостения в сторону хронического
процесса в легком. При аускультации выявляются
локализованные (постоянно) или рассеянные
сухие и разнокалиберные влажные хрипы.
Решающее
значение в установлении диагноза
имеют рентгенологические
и бронхологические методы
исследования. На рентгенограммах
определяется деформация и усиление
легочного рисунка, уменьшение легочного
поля на стороне измененной доли и
смещение органов средостения в сторону
поражения. Обращает также внимание
различная прозрачность легочных полей
в зоне поражения, в интактных участках
легкого и в противоположном легком за
счет неравномерности легочного рисунка,
который в зоне поражения приобретает
характер ячеистого.
При бронхоскопии слизистая
оболочка бронхов гиперемирована, отечна,
легко кровоточит, в просвете бронхов
наблюдается слизисто–гнойное или
гнойное отделяемое в большом количестве;
устья долевых и сегментарных бронхов
деформированы, шпоры сглажены, дыхательная
подвижность уменьшена.
Бронхографическая картина
зачастую бывает сложной из–за
присоединения к врожденной гипоплазии
вторичных деформаций бронхов. В зоне
кистозной гипоплазии отмечается
объемное уменьшение доли, контрастируются
полостные образования в виде «гроздьев
винограда» или четкообразные расширения
сегментарных и субсегментарных бронхов
(Рис. 18).
Рис.
18. Кистозная гипоплазия. Бронхограмма.
Недоразвитие бронхов нижней доли левого
легкого с кистозным их расширением.
Эти
изменения могут сочетаться, а в ряде
случаев и дополняться вторичными
изменениями в интактных участках
пораженного легкого и в противоположном
легком из-за выраженного обструктивного
синдрома, поэтому зачастую требуется
повторная бронхография после курса
санационных бронхоскопий.
Во
многом облегчает задачу точного
определения границ поражения перфузионная
гамма – сцинтиграфия,
результаты которой достаточно четко
указывают на изменения в артериоло–капиллярных
структурах пораженного участка легкого
в виде отсутствия контрастирования на
сцинтипневмограммах и перераспределения
кровотока в противоположное легкое при
раздельном подсчете импульсов.
Ангиопульмонография выявляет
недоразвитие сосудов в пораженном
легком или доле. При этом определяется
резкое обеднение сосудистой сети в
артериальной фазе, артерии истончены
и огибают воздушные полости, отмечается
резкая задержка капиллярной и венозной
фаз контрастирования.
Лечение.
При кистозной гипоплазии доли без
вовлечения в процесс соседних участков
и противоположного легкого лечение
должно быть оперативным, не допускающим
диффузного распространения хронического
воспаления на соседние участки.
Консервативное лечение в таких случаях
(эндобронхиальные санации, ингаляции,
физиотерапевтические процедуры,
использование санаторных факторов и
др.) может только на время задержать
течение вторичного неспецифического
воспаления и ограничить экспансию
процесса. Самостоятельное значение
этот метод имеет в тех случаях, когда
распространенность патологического
процесса превышает объем 10 – 11 сегментов,
и сопровождается наличием выраженной
дыхательной недостаточности и гипертензий
в малом круге кровообращения.
Результаты
хирургического лечения в большинстве
случаев удовлетворительные. Функциональные
нарушения у таких больных после операции
выражены меньше, так как они не теряют
большого объема функционирующей легочной
паренхимы и уже до операции имеют
достаточно развитые компенсаторные
механизмы.
Синдром
гиалиновых мембран (респираторный
дистресс–синдром новорожденных;
врожденная альвеолярная дисплазия).
Проявляется с первых часов жизни
прогрессирующей одыщкой, приступами
асфиксии, цианозом. Заболевание связано
с недостаточным развитием у недоношенных
детей антиателектатического фактора
–сурфактанта и формированием гиалиновых
мембран, состоящих из фибрина, гемоглобина,
нуклео – и монопротеиновых субстанций.
Все это приводит к резкому нарушению
периферической вентиляции, газообмена
и гипоксемии.
Диагностика
синдрома гиалиновых мембран основывается
на рентгенологических исследованиях,
при которых первоначально определяется
сетчатая деформация легочного рисунка
с множественными сегментарными
ателектазами, затем – очаговая
диссеминация и развитие тотального
затемнения (белое легкое).
Лечение. Назначаются
патогенетические и симптоматические
средства (корригирование ацидоза, ИВЛ,
гормональная терапия, сердечные
гликозиды).
Прогноз
неблагоприятный в большинстве случаев.
Врожденная
долевая эмфизема новорожденных (синонимы:
лобарная эмфизема, обструктивная
эмфизема, гипертрофическая эмфизема,
напряженная эмфизема новорожденных и
др.). Этот порок развития характеризуется
растяжением части легкого (чаще одной
доли). Истинные причины порока остаются
невыясненными. Однако некоторые авторы
связывают его возникновение с аплазией
хрящевых элементов бронхов, гипоплазией
эластических волокон, гипоплазией
гладких мышц терминальных и респираторных
бронхиол и другими нарушениями в
структурных единицах легочной ткани.
Эти факторы создают предпосылки для
возникновения клапанного механизма,
способствующего чрезмерному вздутию
соответствующей части легкого и развитию
дыхательных нарушений. Чаще поражаются
верхние доли, реже – средняя. Резкая
гиперэкстензия доли ведет к сдавлению
остальных отделов легкого, часто
перемещается в сторону контрлатерального
легкого, образуя медиастинальную грыжу.
Ю.
Ф. Исаков, Э. А. Степанов с соавт. (1978) на
основании патоморфологических
исследований выделяют три типа порока,
приводящих к локализованной эмфиземе:
1) гипоплазия
гладких мышц терминальных и респираторных
бронхиол с гипертрофией эпителиальной
выстилки;
2) агенезия
всего респираторного отдела с отсутствием
респираторных бронхиол и альвеолярной
ткани. При этом обнаруживается множество
атипичных макроскопических полостей,
формирующихся из междольковых бронхов,
которые и создают картину повышенной
воздушной доли;
3) отсутствие
промежуточных генераций бронхов. Это
влечет за собой резкое расширение
просветов внутридольковых бронхов и
отсутствие генераций терминальных и
респираторных бронхиол, эмфизематозная
паренхима является при этом непосредственным
продолжением внутридольковых бронхов.
Во
всех случаях в патогенезе синдрома
напряжения в альвеолах играет клапанный
механизм, возникающий вследствие
неправильной закладки респираторных
отделов и нарушений вентиляции.
Клиника
и диагностика. Превалирующими
симптомами у большинства больных
являются одышка, затрудненное дыхание,
приступы цианоза, кашель. Это обусловлено
тем, что эмфизематозно раздутая доля
коллабирует здоровые участки легкого,
частично выключая их из дыхания, вызывает
смещение органов средостения, затрудняя
приток крови к сердцу и отток ее.
Компрессия и флотация средостения могут
быть выражены в различной степени, они
усиливаются при беспокойстве, крике,
плаче и приводят к периодическому
ухудшению состояния ребенка,
сопровождающемуся приступами кашля,
цианоза.
В
течении болезни принято различать три
стадии:
1) Острая
(или декомпенсированная) – проявляется
с первых дней или недель жизни. У больного
развивается картина острой дыхательной
и сердечно – сосудистой недостаточности.
Состояние больных с декомпенсированной
формой крайне тяжелое, при этом дети
адинамичны, грудная клетка на стороне
поражения выбухает, дыхательные экскурсии
снижены или отсутствуют. Отмечается
коробочный перкуторный звук, дыхание
не выслушивается. При поражении левого
легкого перкуторно и аускультативно
отмечается резкое смещение сердца
вправо. Заболевание быстро прогрессирует
и при неадекватном лечении заканчивается
летально;
2) Субкомпенсированная
– характеризуется эпизодически
возникающими приступами удушья,
дыхательной недостаточности, сопровождается
локальным цианозом, кашлем и самостоятельно
купируются. Постоянным симптомом
является одышка. Критическим
периодом жизни ребенка является первое
полугодие, после чего наступает период
относительного равновесия, однако дети
склонны к частым воспалительным
заболеваниям легких, при этом состояние
их резко ухудшается, и быстро выявляются
признаки декомпенсации. Перкуторные и
аускультативные данные аналогичны
декомпенсированной стадии, но выражены
в меньшей степени.
3) Компенсированная
– спокойное течение заболевания без
приступов удушья или выраженной одышки.
Чаще симптомы возникают к концу первого
года жизни, нередко порок развития
диагностируется при присоединении
воспалительных заболеваний. Прогрессирование
заболевания с возрастом не отмечается,
но дети, как правило, отстают в физическом
развитии, иногда у них развиваются
вторичные деформации грудной клетки и
искривление позвоночника.
В
диагностике врожденной локализованной
эмфиземы решающим является рентгенологическое
исследование. Уже на обзорных
рентгенограммах выявляются следующие
характерные признаки: повышенная
прозрачность легочнго поля на стороне
поражения, выраженное смещение средостения
в противоположную сторону. Диафрагма
уплощена, межреберные промежутки
расширены. В нижнемедиальном отделе
легочного поля определяется тень
оттесненной части легкого (Рис. 19).
Рис.
19. Врожденная лобарная эмфизема верхней
доли правого легкого. Обзорная
рентгенограмма. Определяется повышенная
прозрачность легочного поля справа,
смещение органов средостения влево с
образованием «медиастинальной грыжы».
Выраженный синдром «напряжения» в
правом гемитораксе.
Бронхография показана
только при компенсированной форме
заболевания для топической диагностики.
На бронхограммах обнаруживают деформацию
или сужение долевого бронха и обрыв
периферических бронхов со смещением
сдавленных отделов к низу. Бронхи
коллабированных долей хорошо
контрастированы, сближены и собраны в
«кисточку» (Рис. 20).
Рис.
20.Врожденная лобарная эмфизема верхней
доли правого легкого. Бронхограмма.
Бронхи нижних коллабировааныых долей
правого легкого хорошо контрастированны,
сближены и собраны в «кисточку».
Бронхоскопия,
как правило, не выявляет заболевания,
иногда обнаруживают сужение бронха,
гипертрофию слизистой оболочки и другие
изменения.
Перфузионная
гамма – сцинтиграфия выявляет
почти полное отсутствие накопления
радиофармпрепарата в области измененной
доли и значительное диффузное снижение
его накопления в пограничных с пораженными
бронхолегочных сегментах.
При
ангиопульмонографическом
исследовании устанавливается
локализация поражения и степень
компенсации гемодинамики в малом круге
кровообращения. На ангиограммах
выявляется обеднение сосудистого
рисунка эмфизематозной доли с истончением
и оголенностью артериальных ветвей;
сосудистая сеть веерообразно раздвинута.
Сосуды прилежащих здоровых отделов
сближены, углы ветвления уменьшены.
Дифференциальную
диагностику проводят с эмфиземой,
вызванной вентильным инородным телом,
с компенсаторной эмфиземой при пневмонии,
ателектазе или гипоплазии нижней доли
легкого, с напряженным пневмотораксом,
легочными кистами, диафрагмальной
грыжей, синдромом Маклеода (врожденная
односторонняя эмфизема).
Лечение. Радикальным
вмешательством может быть только
удаление пораженных участков легкого.
Экстренность оперативного вмешательства
определяется формой поражения. Неотложная
операция показана при декомпенсированной
эмфиземе. При субкомпенсированной
эмфиземе операция может быть отложена
на некоторое время для более тщательного
исследования и подготовки больного.
При компенсированной форме выполняется
плановая операция.
Врождённые пороки развития бронхолегочной системы
Врождённые заболевания лёгких являются одной из наиболее сложных диагностических, патогенетических и терапевтических проблем современной пульмонологии.
Распознавание их представляет немалые трудности.
Нередко их ошибочно принимают за обычные формы хронических неспецифических заболеваний лёгких. Вместе с тем только четкое определение истинного характера патологического процесса обеспечивает успех терапевтических мероприятий.
Диагностический арсенал пульмонологической клиники, обогащение её современными методами функциональных и бронхологических исследований, клинической генетики, биохимии, иммунологии, радиологии и морфологии позволяют расшифровать и дифференцировать различные формы патологии лёгких врождённого и наследственного характера.
Врожденными пороками (аномалиями) развития, по определению Г.И. Лазюка (1983), называют стойкие морфологические изменения органа или организма, выходящие за пределы вариаций их строения и возникающие внутриутробно в результате нарушений развития зародыша, плода или, иногда, после рождения ребёнка как следствие нарушения дальнейшего формирования органов. Подавляющее большинство пороков связано с наследственной патологией.
Сведения о частоте пороков развития среди других заболеваний лёгких противоречивы: на их долю приходится от 1,5 до 50 % и более всей легочной патологии. Столь существенные различия объясняются объективными трудностями дифференциальной и морфологической диагностики антенатальных и постнатальных (приобретённых) изменений в лёгких.
При некоторых аномалиях бронхолёгочной системы тяжёлые клинические признаки наблюдаются сразу после рождения. Другие пороки определенное время протекают бессимптомно и проявляются в более поздние сроки, в том числе у взрослых, главным образом, вследствие присоединения инфекционного процесса или постепенного нарастания функциональных нарушений. Наконец, у части больных на протяжении всей жизни аномалия дыхательной системы может клинически не проявиться.
Классификация
Существует много вариантов классификации аномалий развития лёгких. В НИИ пульмонологии МЗ РФ разработана следующая классификация пороков развития бронхолегочной системы, основанная на морфологических критериях:
I. Пороки, связанные с недоразвитием органа в целом или его анатомических, структурных, тканевых элементов:
1. Агенезия лёгкого.
2. Аплазия лёгкого.
3. Гипоплазия лёгкого простая.
4. Гипоплазия лёгкого кистозная.
5. Синдром Вильямса-Кемпбелла.
6. Врождённая долевая эмфизема.
7. Трахеобронхомегалия (синдром Мунье-Куна).
II. Пороки, связанные с наличием избыточных дизэмбриогенетических формирований:
1. Легочная секвестрация (внедолевая и внутридолевая).
2. Кисты лёгких.
3. Гамартома и другие врождённые опухолевидные образования.
III. Необычное расположение структур лёгкого, которое может иметь клиническое значение:
1. «Зеркальное» лёгкое.
2. Обратное расположение лёгких (в том числе триада Зиверта-Картагенера).
3. Трахеальный бронх.
4. Доля непарной вены.
5. Прочие.
IV. Локализованные нарушения строения трахеи и бронхов:
1. Стенозы трахеи и крупных бронхов.
2. Дивертикулы трахеи и бронхов.
3. Трахео(бронхо)пищеводные свищи.
4. Сочетания перечисленных аномалий.
V. Аномалии кровеносных и лимфатических сосудов:
1. Стенозы легочной артерии и её ветвей.
2. Аневризмы легочной артерии и её ветвей.
3. Варикозные расширения легочных вен.
4. Артериовенозные свищи (аневризмы) локализованные.
5. Артериовенозные свищи без чёткой локализации (синдром Ослера-Рандю).
6. Лимфангиэктазии и другие аномалии лимфатической системы.
Агенезия и аплазия лёгкого
Агенезией легкого принято называть отсутствие его вместе с главным бронхом. Аплазия характеризуется отсутствием ткани лёгкого при наличии рудиментарного главного бронха.
Указанные пороки встречаются редко и во многих случаях сочетаются с другими врождёнными пороками и аномалиями развития.
Во многих случаях агенезия и аплазия легкого как у детей, так и у взрослых, если нет поражения других органов, не имеет выраженных клинических проявлений. В относительно редких случаях сразу после рождения развивается дыхательная недостаточность, которая либо приводит к летальному исходу, либо постепенно компенсируется.
У многих больных отмечаются снижение толерантности к нагрузкам, частое развитие острых респираторных заболеваний (ОРЗ), одышка при быстрой ходьбе и беге, цианоз, а также периодический кашель со скудной мокротой, связанный со скоплением бронхиального секрета в культе главного бронха и развитием в ней хронического воспалительного процесса.
При объективном обследовании обнаруживают уплощение половины грудной клетки, сколиоз позвоночника с выпуклостью в здоровую сторону, притупление перкуторного звука и ослабленное дыхание на стороне поражения, особенно выраженное сзади, резкое смещение сердца в больную сторону.
Рентгенологическое исследование показывает сужение легочного поля из-за смещения органов средостения, интенсивное затемнение половины грудной клетки, из-за которого тени сердца и купола диафрагмы не дифференцируются, симптомы пролабирования здорового легкого в противоположную сторону (медиастинальная легочная грыжа), полосу просветления, идущую паравертебрально на стороне поражения за счёт смещения трахеи. Бронхография выявляет смещение трахеи и бронхов в больную сторону, непосредственный переход трахеи в главный бронх при агенезии и культю главного бронха при аплазии легкого. В единственном легком нередко обнаруживаются бронхоэктазы.
Лечение, как правило, не требуется.
Гипоплазия легкого и его долей
Гипоплазией легкого принято называть одновременное недоразвитие бронхов и легочной паренхимы. Большинство авторов разделяют гипоплазию на простую и кистозную.
Простая гипоплазия легкого (доли) представляет собой относительно равномерное уменьшение числа разветвлений бронхов, которые не имеют выраженных кистозных и веретенообразных расширений. Респираторный отдел недоразвит, воздушность его снижена, хотя описаны случаи эмфизематозной трансформации.
Клинические проявления порока зависят от выраженности и длительности вторичного хронического воспаления. Больные часто жалуются на кашель со слизисто-гнойной мокротой в умеренном количестве, иногда на одышку при физической нагрузке. При обострениях увеличивается количество мокроты, повышается температура тела, появляются симптомы интоксикации.
Физикально обнаруживается асимметрия грудной клетки, сужение межреберных промежутков, высокое стояние диафрагмы — на стороне поражения, а также смещение органов средостения в больную сторону. Нарушение нормального оттока бронхиального секрета при минимальных воспалительных изменениях и даже без них обусловливает постоянные хрипы в области поражённого участка легкого.
При простой гипоплазии долей или сегментов легкого рентгенологически и бронхографически выявляется уменьшение его поражённых отделов. Бронхи резко сближены между собой, в отдельных случаях напоминают «метёлку». Число генераций бронхов может быть уменьшено. Без воспалительных изменений просвет бронхов может быть нормальным или незначительно расширенным. Бронхи непоражённых отделов легкого смещены в сторону гипоплазированных сегментов, а иногда подворачиваются под них, компенсируя их уменьшенный объём.
В других случаях при бронхографии выявляется грубая деформация бронхов поражённой доли и/или заполнение контрастным веществом лишь начальных отделов бронхиальных разветвлений, что не всегда можно связать с длительностью и тяжестью воспалительного процесса.
Ангиопульмонографическое исследование обнаруживает гипоплазию легочных сосудов.
Кистозная гипоплазия (син.: кистозная болезнь легкого, поликистоз, врождённые бронхоэктатические кисты, врождённое «сотовое легкое» и др.) представляет собой аномалию легкого или его части, обусловленную антенатальным недоразвитием легочной паренхимы, бронхов и сосудов с формированием кистозных полостей на различных уровнях бронхиального дерева.
По мнению большинства авторов, кистозная гипоплазия составляет не менее 60-80 % всех пороков развития легкого.
При морфологическом исследовании удалённых легких выявляется множество тонкостенных полостей, выстланных изнутри бронхиальным эпителием (цилиндрическим мерцательным или кубическим), аплазия или уменьшение легочной паренхимы без признаков предшествующего воспаления, отсутствие в субсегментарных и более мелких бронхах хрящевых пластинок, что отличает кистозную гипоплазию от кистозных постнатальных бронхоэктазов.
Течение заболевания при кистозной гипоплазии лёгких может быть относительно доброкачественным, однако чаще в связи с неизбежным присоединением инфекции появляются симптомы хронического нагноительного процесса.
Первые проявления болезни очень часто возникают уже в раннем детстве, но иногда пациенты узнают о своём заболевании в юношеском или даже зрелом возрасте. В анамнезе у детей отмечаются повторные респираторные заболевания, острая респираторная вирусная инфекция (ОРВИ), осложнённые бронхитом, затяжные бронхиты, пневмонии. Обычно такие больные предъявляют жалобы на кашель со слизисто-гнойной или гнойной мокротой, одышку, повышение температуры тела, имеются признаки интоксикационного синдрома.
В связи с уменьшением объёма пострадавшего легкого физикально отмечается асимметрия грудной клетки, ограничение дыхательных экскурсий на стороне поражения. Перкуторно в области кистозных изменений выявляется тимпанит. Аускультативно — дыхание жёсткое, над кистами выслушиваются разнокалиберные влажные и сухие хрипы.
Главную роль в диагностике играет рентгенологическое исследование. Характерными рентгенологическими признаками кистозной гипоплазии являются множественные тонкостенные, наслаивающиеся друг на друга просветления (полости) диаметром от 1 до 5 см. Поражённые отделы легкого в большинстве случаев уменьшены в размерах, определяется деформация или усиление легочного рисунка по ячеистому типу. Преобладает односторонняя локализация процесса. Чаще процесс локализуется в нижней доле левого легкого и язычковых сегментах, а также в верхней доле правого легкого.
При бронхографическом исследовании выявляются деформированные и расширенные бронхи, множественные, наслаивающиеся друг на друга тонкостенные полости, частично или полностью заполненные контрастным веществом. Иногда хорошо контрастированное бронхиальное дерево в зоне поражения напоминает украшенную шарами новогоднюю ёлку.
Ангиопульмонография показывает, что при кистозной гипоплазии кровоток в легком либо резко обеднён, либо прекращён. У большинства больных отмечается недоразвитие сосудов малого круга кровообращения в поражённом легком или доле легкого. Субсегментарные и прелобулярные артерии и вены обычно равномерно истончены и огибают кистоподобные образования, как бы подчёркивая их границы.
Бронхоскопически при поражении всего легкого отмечаются смещение трахеи и бифуркации в больную сторону, гнойный эндобронхит; при поражении долей или сегментов — слизисто-гнойный или гнойный эндобронхит.
При исследовании функции внешнего дыхания чаще обнаруживаются смешанные нарушения вентиляции.
Лечение кистозной гипоплазии обычно хирургическое. Операция при кистозной гипоплазии заключается в удалении недоразвитой доли или же всего легкого (пульмонэктомия показана лишь при тяжёлых клинических проявлениях). Больных с установленным диагнозом обычно оперируют в возрасте 7-8 лет и старше.
Консервативное лечение (эндобронхиальные санации, постуральный дренаж, антибактериальная терапия) показано в период обострения с целью подготовки больных к операции, а также пациентам, которым оперативное вмешательство по тем или иным причинам не показано (в случае полного отсутствия симптомов, при двусторонних обширных изменениях, исключающих возможность резекции, при наличии общих противопоказаний к операции на легких).
Саперов В.Н., Андреева И.И., Мусалимова Г.Г.
Опубликовал Константин Моканов
Лечение пороков развития легких и бронхов у детей | Середа Е.В.
Пороки развития бронхов и легких составляют значительную группу в структуре хронической бронхолегочной патологии у детей. По данным литературы и собственных наблюдений, частота пороков развития легких у детей колеблется от 10 до 20%, что связано с недостаточно четкими критериями их диагностики.
Многие из пороков развития подлежат хирургической коррекции. Неоперабельные больные при наличии у них хронического инфекционного процесса, а также дети в до- и послеоперационных периодах должны лечиться подобно больным хронической пневмонией.
| ПОРОКИ РАЗВИТИЯ БРОНХОВ И ЛЕГКИХ:
o агенезия легких;
|
Клиническая картина
Гипоплазии долей легких являются наиболее частой формой из всех пороков развития легких, встречающихся у детей. В зависимости от формы гипоплазии (простая, кистозная) значительно различаются их клинические проявления и рентгено-бронхологическая картина, а в связи с этим тактика лечения (консервативное или хирургическое). Консервативная терапия как при отсутствии показаний к хирургическому лечению, так и в до- и послеоперационном периодах должна включать в себя в качестве важнейшего компонента антибиотикотерапию.
| Основные патогеныпри пороках развития легких — гемофильная палочка, пневмококки бранхамелла |
Эмфизема часто захватывает долю легкого (лобарная). В основе заболевания лежит дефект развития хрящевых колец долевого или сегментарного бронха, в результате этого развивается вентильный механизм, способствующий резкому вздутию паренхимы легких, которая определяет клинико-рентгенологическую картину порока. Наслоение инфекционного воспалительного процесса (пневмония) вызывает резкое утяжеление заболевания.
Кисты легкого могут быть одиночными и множественными. Неосложненные кисты могут протекать бессимптомно. Инфицированные, дренирующиеся через бронхи кисты характеризуются частыми обострениями, протекающими нередко по типу пневмонической вспышки, по клиническому течению близки к бронхоэктазам.
| Основные принципы применения антибиотиков у детей, страдающих хроническими бронхолегочными заболеваниями: 1) определение тяжести болезни и активности воспаления; 2) этиологическая диагностика — определение этиологически значимого возбудителя воспаления путем посева мокроты или промывных вод бронхов с использованием количественного метода; 3) определение чувствительности к антибиотикам выделенной флоры; 4) выбор оптимальной дозы; 5) учет возраста ребенка, переносимость различных лекарственных средств, наличие аллергических реакций; 6) учет характера побочных действий у назначаемого антибиотика; 7) выбор наиболее эффективного и щадящего метода введения препарата. |
Секвестрация — порок легкого, связанный с аномальным кровоснабжением. Рудиментарный зачаток легкого, не имеющий сообщения с бронхами, кровоснабжается осуществляется аномальной артерией, отходящей непосредственно от аорты. Клиническое течение зависит от инфицирования.
Распространенные пороки развития бронхов
| Возбудитель является этиологически значимым, если его концентрация в мокроте не менее 106/мл |
Основной формой из группы распространенных пороков развития стенки бронхов является синдром Вильямса — Кемпбелла. В его основе лежит отсутствие хряща в бронхах с 3-4-го до 6-8-го порядков. В результате слабость бронхиальной стенки приводит к выраженной дискинезии бронхов, нарушению вентиляции легких, застою бронхиального секрета и его инфицированию. При этом развивается тяжелый хронический бронхит и характерные (баллонные) бронхоэктазы. Заболевание характеризуется тяжелым течением. У больных развивается деформация грудной клетки и концевых фаланг пальцев по типу (барабанных палочек). Отмечается постоянный влажный кашель с мокротой, хроническая интоксикация, нарушение вентиляции комбинированного типа. Бронхоскопически определяется катарально-гнойный или гнойный эндобронхит. Характерна хроническая гипоксемия и формирование легочного сердца у части больных. Процесс обычно двусторонний, хотя в отдельных случаях он бывает односторонним. В таких случаях заболевание протекает легче.
Синдром Картагенера представляет собой комбинированный (системный), наследственно-обусловленный порок развития с триадой симптомов: обратное расположение сердца (декстракардия) и других внутренних органов, хронический бронхолегочный процесс и синусоринопатия. В основе легочного компонента порока лежит анатомическая и функциональная патология ресничек мерцательного эпителия слизистой оболочки бронхов, что приводит к нарушению мукоцилиарного клиренса, являющегося основным механизмом их самоочищения. В результате у больных развивается тяжелый бронхолегочный процесс, в основе которого лежит распространенный хронический бронхит. Наряду с этим у больных синдромом Картагенера могут обнаруживаться участки пневмосклероза с деформацией бронхов и бронхоэктазами. Типичным является упорное, трудно поддающееся лечению поражение носоглотки (рецидивирующий синусит, ринит). Нарушение вентиляции легких и бронхоскопические изменения близки к обнаруживаемым у детей с синдромом Вильямса — Кемпбелла. Показания к оперативному лечению крайне ограничены в связи с распространенностью основного дефекта.
| При нетяжелом обострении назначают перорально: амоксициллин/клавуланат, цефалоспорины или макролиды |
К описанному пороку примыкает синдром неподвижности (или дисфункции) ресничек. Как и при синдроме Картагенера, у больных имеется врожденный дефект ресничек мерцательного эпителия бронхов в виде их неподвижности или асинхронного биения, нарушающий нормальную работу эскалатора. Бронхолегочные изменения при этом аналогичны обнаруживаемым у детей с синдромом Картагенера. Если диагноз последнего не вызывает трудностей, то для подтверждения описываемого синдрома требуется электронно-микроскопическое исследование ресничек.
Лечение
| Бронхообструкция у детей с распространенными пороками развития легких может приводить к ошибочному диагнозу |
Консервативная терапия, как упоминалось, занимает существенное место в лечении пороков развития легких как подлежащих, так и не подлежащих хирургическому лечению. В случаях, при которых показано хирургическое лечение, консервативная терапия должна проводиться в дооперационном периоде для снятия обострения и снижения активности воспалительного процесса. В послеоперационном периоде она показана для профилактики осложнений и более быстрой реабилитации больного.
Антибиотики
Антибиотикотерапия является одним из важнейших компонентов комплексного лечения хронических бронхолегочных заболеваний, включая пороки развития легких. Оптимизация антибиотикотерапии при лечении заболеваний органов дыхания должна, с одной стороны, основываться на строгих показаниях и адекватном выборе наиболее эффективного препарата с учетом антибиотикограммы, а с другой стороны, на отказе от необоснованного назначения антибиотика. При пороках развития легких назначают антибиотик при обострении инфекционного воспалительного процесса или наличии его активности; а также в до- и послеоперационные периоды. В связи с тем, что обострение чаще возникает при заболевании ребенка ОРВИ, назначение антибиотиков и в этих случаях оправдано.
Для оценки этиологически значимой микрофлоры, выделенной из мокроты или бронхиального содержимого (при бронхоскопии) при хронических бронхолегочных заболеваниях, необходимо использовать количественный метод посева.
Этиологически значимыми являются те микробы, которые находятся в биоматериале (мокроте) в концентрации не менее 106-107 клеток в 1 мл.
У детей, у которых воспалительный процесс в бронхолегочной системе развился на основе врожденных пороков легких и бронхов, микробный спектр представлен в основном тремя пневмотропными микробами: Haemophilus influenzae, Str. pneumoniae и Moraxella catarrhalis.
Доминирующим агентом обострения является гемофильная палочка, составляющая 76-88%, второе место занимает пневмококк (31 — 38%). Бранхамелла катаралис при ограниченных и распространенных пороках легких и бронхов составляет 3,4%. В 0,1% случаев выделяется клебсиелла, в редких случаях при тяжелом течении заболевания можно обнаружить анаэробные бактерии.
Основными отличиями микрофлоры у детей с синдромом Зиверта-Картагенера является большая частота высева патогенов (96%) при высоком проценте выделения бранхамеллы катаралис (32%), превышающем почти в 10 раз частоту ее высева при других хронических заболеваниях легких. Обращает внимание более частая ее ассоциация с пневмококком и гемофильной палочкой (41%). Ассоциация пневмококка и гемофильной палочки составляет 25%.
Мониторинг чувствительности основных бактерий к антибиотикам позволяет выявить, что гемофильная палочка сохраняет высокую чувствительность к ампициллину, амоксициллину (в т. ч. с клавулановой кислотой), азитромицину, хлорамфениколу, препаратам аминогликозидной группы и цефалоспоринам II-III поколений.
Практически все штаммы гемофильной палочки обладают резистентностью к таким антибиотикам, как оксациллин (84%), олеандомицин (97%), линкомицин (100%), что подтверждает нецелесообразность их применения в этих случаях. Низкой и средней активностью обладают цефалоспорины I поколения при сохранении высокой чувствительности к препаратам II и III поколений.
Пневмококк сохраняет высокую чувствительность к препаратам пенициллинового ряда, макролидам, цефалоспоринам и обладает высокой резистентностью к аминогликозидам. Среди штаммов бранхамеллы катаралис резистентность к пенициллинам составляет 70-80%.
Наиболее адекватное лечение предполагает определение этиологии и чувствительности выделенных микроорганизмов к антибиотикам. При невозможности получения антибиотикограммы и в экстренных случаях рекомендуется использование антибиотиков широкого спектра действия.
В настоящее время фармацевтическая промышленность предлагает огромный арсенал антибактериальных пероральных средств широкого спектра действия: амоксициллин (в т. ч. с клавулановой кислотой), мидекамицин, рокситромицин, спирамицин, азитромицин, цефалексин, цефадроксил, цефуроксим, цефаклор, цефтибутен и другие, в том числе детские лекарственные формы (суспензии, капли, таблетки в соответствущей дозировке), эффективность которых убедительно доказана при хронических воспалительных бронхолегочных заболеваниях у детей.
Путь введения антибиотиков. При легком и среднетяжелом обострении хронического воспаления в аномальных бронхах и легких, чаще у детей с поражением, ограниченным одним-тремя сегментами, ограниченной деформацией бронхов без выраженных бронхоэктазов, наличием катарального или катарально-гнойного эндобронхита может быть рекомендовано лечение пероральными антибиотиками. При отсутствии эффекта следует заменить препарат или перейти на парентеральное введение антибиотика.
При тяжелом течении обострения, выраженной активности воспаления у детей с полисегментарными или двусторонними поражениями, наличием грубой деформации бронхов — бронхоэктазов, распространенного гнойного эндобронхита, что чаще наблюдается у детей с распространенными пороками развития бронхов (синдром Вильямса-Кемпбелла и другие недифференцированные пороки, при синдроме Зиверта-Картагенера, кистозной гипоплазии, кистах легкого и др.) показано назначение преимущественно парентеральных антибиотиков (внутривенно, внутримышечно) широкого спектра действия. К ним относятся пенициллины с ингибиторами b-лактамаз, цефалоспорины II-III поколений — цефуроксим, цефтриаксон, цефотаксим, цефтазидим и др. При недостаточной эффективности показаны комбинации цефалоспоринов с макролидами, аминогликозидами, комбинация методов введения: парентерального и перорального с учетом тяжести заболевания и его этиологии.
Наиболее щадящим методом в этих случаях является использование пролонгированных антибиотиков (вводимых 1-2 раза в сутки) и применение ступенчатого метода, при котором в первые 1-3 дня антибиотик вводят парентерально, а в последующем, при наметившемся положительном эффекте, осуществляют переход на пероральное применение адекватных препаратов.
Возрастание роли грибковой колонизации, преимущественно Candida albicans (37,5%), у детей с данной патологией диктует необходимость назначения противогрибковых препаратов (кетоконазол, флюконазол) в случаях выявления в мокроте грибковой инфекции.
При врожденной патологии важным является проведение санационной бронхоскопии (бронхоальвеолярный лаваж, эндобронхиальное введение антибиотиков, муколитиков и др.), эффективность которой в сочетании с парентеральным введением антибиотиков доказана.
С определенной осторожностью следует подходить к назначению левомицетина и аминогликозидов с учетом возможного влияния этих препаратов на кроветворную систему (левомицетин), нефротоксического и ототоксического эффекта (аминогликозиды). Хотя назначение последних оправдано в случаях тяжелого обострения заболевания, вызванного преимущественно грамотрицательной флорой, в ряде подобных случаев рекомендуется назначение цефалоспоринов II и III поколений, при необходимости в сочетании с аминогликозидами.
Сложность выбора антибиотиков и метода введения при обострении хронического бронхолегочного процесса у ребенка с врожденной патологией легких и бронхов обусловлено тем, что эти дети нередко получают повторные и длительные курсы антибиотикотерапии в связи с частыми обострениями.
Муколитики
Наряду с антибактериальной терапией важное место в лечении занимают муколитические средства, действие которых направлено на улучшение дренажной и вентиляционной функции легких и бронхов, мукоцилиарного клиренса.
В настоящее время имеется большое число препаратов, обладающих муколитическими свойствами. Основными из них являются ацетилцистеин, карбоцистеин, бромгексин, амброксол, а также лекарственные отхаркивающие травы. Выбор препарата определяется возрастом ребенка, тяжестью и периодом заболевания, индивидуальной чувствительностью.
Бронхолитики
При пороках развития легких и бронхов, особенно у детей при распространенных пороках трахеобронхиального дерева (синдром Вильямса-Кемпбелла и др.), при генетически детерминированных заболеваниях (первичная цилиарная дискинезия — синдром неподвижных ресничек, синдром Зиверта-Картагенера) нередко ведущим в клинической картине является синдром бронхиальной обструкции, торпидный к базовой терапии (антибиотики, муколитики, дренажи, массаж, ЛФК), что нередко приводит к ошибочной диагностике. При этом клинические проявления обструкции нередко сходны с бронхиальной астмой, однако механизмы обструктивного синдрома могут существенно отличаться.
Среди детей с синдромом Вильямса-Кемпбелла, обследованных в отделении пульмонологии НИИ педиатрии НЦЗД РАМН, 10% больных ранее наблюдались с диагнозом (бронхиальная астма). Механизм бронхиальной обструкции при данной патологии сложный и обусловлен как наличием стойких необратимых морфологических изменений (врожденные дефекты бронхов и легких), так и наличием частично обратимых компонентов (хронического воспаления, вызванного и поддерживаемого бактериальной флорой, гиперсекрецией слизи, рефлекторных и аллергических механизмов).
С целью оптимизации терапевтической тактики при наличии выраженной бронхообструкции важным является воздействие на обратимые или частично обратимые механизмы воспаления и обструкции.
Наиболее эффективным препаратом является беродуал (дозированный аэрозоль или раствор с использованием небулайзера) — бронхолитическое средство двойного действия, содержащее b2-адренергический препарат — фенотерол и антихолинергическое вещество — ипратропиум бромид. Эти вещества по своему бронхолитическому действию дополняют и усиливают друг друга и способствуют мукоцилиарному очищению. Бронхорасширяющий эффект в ряде случаев оказывает ипратропиум бромид, а также сальбутамол, являющийся b2-адреностимулятором. При отсутствии эффекта от применения дозированных аэрозолей рекомендуется назначение пролонгированных препаратов теофиллина. В ряде случаев показано назначение фенспирида, обладающего бронхолитическим и противовоспалительным действием, а также способностью снижать гиперчувствительность бронхов.
Неотъемлемой составляющей комплекса лечения и реабилитации детей с пороками развития легких является постоянное проведение ЛФК и специальных ее методов (дренажное положение, вибромассаж грудной клетки, упражнения на больших гимнастических мячах, батуте, дыхательная гимнастика и др.), а также дозированных спортивных упражнений.
В последние годы особое внимание уделяется стимуляции противоинфекционной защиты, особенно при обострениях хронического воспалительного процесса, возникающих на фоне частых ОРВИ при врожденных пороках развития легких. С этой целью применяются различные вакцины (бронхомунал, рибомунил), а также лейкинферон (природный a-интерферон в комплексе с цитокинами) и циклоферон (индуктор интерферонов).
Хирургическое лечение
Хирургическому лечению подлежат дети преимущественно с ограниченными пороками развития легких, кистозными и бронхоэктатическими формами гипоплазии долей легких, кистами легких, легочной секвестрацией, врожденной долевой эмфиземой.
Оперативные вмешательства должны проводиться после тщательного обследования больных, с учетом выраженности морфологических и функциональных изменений, объема поражения, эффективности консервативной терапии. Решение о целесообразности хирургического лечения и сроков его проведения должно приниматься совместно хирургом и педиатром-пульмонологом. Распространенные пороки развития легких, синдром Зиверта-Картагенера, синдром Вильямса-Кемпбелла оперативному лечению не подлежат в связи с распространенностью врожденных дефектов бронхов и легких.
Ввиду того, что субстратом хронического воспаления при аномалиях развития бронхов и легких являются стойкие необратимые морфологические изменения, заболевание не может в принципе быть излечено консервативными методами, и тем не менее, проведение целенаправленного лечения и реабилитации позволяет улучшить прогноз этих тяжелых инвалидизирующих заболеваний, способствовует уменьшению частоты обострении и улучшению качества жизни ребенка.
Фенспирид:
ЭРЕСПАЛ
(Laboratoires SERVIER)
Фенотерол+ипратропиум бромид:
БЕРОДУАЛ
(Boehringer Ingelheim)
Фенотерол:
БЕРОТЕК
(Boehringer Ingelheim)
Ипратропиума бромид:
АТРОВЕНТ
(Boehringer Ingelheim)
.
Пороки развития бронхолегочной системы
Пороки развития бронхолегочной системы появляются из-за неправильно сформированной системы бронхов и легких у эмбриона. Наиболее часто встречающиеся аномалии можно разделить на три категории: бронхолегочные аномалии, сосудистые аномалии и комбинированные аномалии легких и сосудов. Бронхолегочные аномалии включают в себя комплекс агнезии -гипоплазии легких (легочное недоразвитие), врожденные пороки развития дыхательных путей легких, бронхиальную атрезию и бронхогенную кисту. Сосудистые аномалии включают отсутствие основной легочной артерии, аномальное происхождение левой легочной артерии, аномальный легочный венозный дренаж и легочные артериовенозные мальформации.

К таким отклонениям относится видоизменение структуры бронхов (их ветвления).
Из-за чего появляется порок бронхолегочной системы?
Эту проблему могут спровоцировать многие факторы. В основном это происходит из-за тлетворного воздействия на организм малыша в то время, когда он находится в утробе матери.
Эта система формируется на ранних этапах беременности – от четырех до восьми недель. Этот недуг спровоцирован видоизмененными хромосомами карапуза или генами, передавшимися от родителей.
Пороки развития бронхолегочной системы
Было выдвинуто предположение, что аномальный кровоток в дорсальной аортальной арке в течение 4-й недели беременности (эмбриональная фаза) вызывает легочное агенезирование
Более 50% пораженных плодов имеют другие аномалии, связанные с сердечно-сосудистой системой, желудочно-кишечным трактом, аномалии мочеполовой системы или скелета.
Существует три типа простых аномалий, связанных с легкими.
- Агенезия. Одного из легких у ребенка нет с рождения. Либо у него отсутствует бронх. Вследствие этого часто наблюдается недостаточность дыхательных путей.
- Аплазия. Основной бронх представлен в виде рудимента.
- Гилоплазия дольки или легкого. Легочная гипоплазия определяется как недостаточное или неполное развитие легких. Характеризуется наличием как бронхов, так и альвеол в слаборазвитой доле легкого, и это вызвано факторами, прямо или косвенно нарушающими торакальное пространство, доступное для роста легких, такое как врожденная диафрагмальная грыжа. Легочная гипоплазия также отмечается при агенезии диафрагмы, большом плевральном выпоте и других состояниях.
Бронхи

Основные типы аномалий, связанных с бронхами.
-
Трахеобронхомаляция. Трахеомаляция у новорожденного развивается, когда хрящ в трахеи не развился должным образом. Вместо того, чтобы быть жестким, стены трахеи остаются гибкими. Поскольку трахея является основным воздухопроводящим путём, проблемы с дыханием начинаются вскоре после рождения.
-
Синдром Вильямса-Кэмпбэла. Синдром Уильямса-Кэмпбелла — это редкий врожденный синдром, характеризующийся дефектным или полностью отсутствующим хрящем в стенке субсегментарных бронхов, приводящим к дистальному колапсу дыхательных путей, что приводит к механическим нарушениям, которые в свою очередь, приводят к образованию бронхоэктазов, дистальнее спавшихся бронхов. Дефект обычно находится между бронхиальными отделами четвертого и шестого порядков, но он может простираться от первого до восьми поколений проксимальных бронхов. Дефицит хряща происходит в раннем возрасте, когда легкие все еще развиваются и растут. Точный механизм до сих пор не совсем понятен. Пациенты имеют трахею нормального калибра и центральные бронхи. Симптомы и прогноз в конечном счете зависят от степени развития хряща бронхов.
-
Бронхиолоэктатическая эмфизема Лешке – передающееся по аутосомно-рецессивному типу поражение периферических отделов бронхиального дерева с развитием бронхоэктазов и эмфиземы вследствие врожденной слабости стенок мелких бронхов. Клинически проявляется рецидивирующими пневмониями и бронхитами с усиливающейся со временемм дыхательной недостаточностью, нарастающей одышкой.
Аномалии развития трахеи
Существует три типа аномалий, связанных с трахеей.
-
Стенозы трахеи. Врожденный стеноз трахеи является редким заболеванием, характеризующимся наличием фокальных или диффузных полных колец хряща трахеи, что приводит к фиксированному сужению трахеи. Патоология может развиваться изолированно или совместно с другими аномалиями
-
Лобарная эмфизема. Врожденная лобальная эмфизема — редкая врожденная аномалия, характеризующаяся альвеолярным растяжением вздутием легочной ткани, с контралатеральным легочным ателектазом (спадением легочной ткани). Чаще всего диагностируется в неонатальном периоде, у 5% пациентов диагностируется в возрасте около шести месяцев. Диагноз также может быть установлен пренатально при ультразвукавом исследовании.
-
Свищи, расположенные в трахеи, бронхах, пищеводе. Этот порок тоже можно диагностировать сразу после рождения. Он проявляется в первые часы жизни карапуза. Симптоматика следующая: ребенок начинает сильно кашлять, и задыхаться, когда вы вскармливаете его грудью. Часто эта болезнь провоцирует воспаление легких.
Другие аномалии развития легких
Существует еще шесть типов аномалий, связанных с легкими.
-
Кисты легких. Кисты этого органа могут быть врожденными. Они появляются из-за того, что легкие развиты неправильно. Проблема может появиться даже в развитом легком. По типу они бывают либо одиночными, либо множественными. Последнее называется поликистозом. Они могут проявляться либо без симптомов, либо в виде воспаления легких. Обычно это происходит в одном и том же месте.
-
Секвестрация. Секвестрация это анатомически и функционально обособленный участок гипоплазированной легочной ткани, которая не имеет нормальной связи с бронхиальным деревом или с легочными артериями. Артериальная кровоснабжение возникает из системных артерий, обычно грудной или брюшной части аорты, а ее венозный дренаж осуществляется через легочные вены или нижнюю полой веной . Секвестрация разделена на два типа: экстралобарную и внутрилегочную
-
Синдром Картагенера. Эта болезнь подразумевает неправильное положение органов. Они размещены в обратную сторону. Проявляется в виде бронхита и синусита. Это происходит из-за того, что реснички имеют аномальное строение. Однако, синдром Картагенера может появиться и у тех детей, которые имеют правильное расположение органов. Болезнь проявляется в виде гноя в бронхах и легких.
-
Агенезия и гипоплазия. Появляется в участках легочной артерии, которые находятся удаленно от остальных элементов. Болезнь проявляется следующим образом: легочное поле становится более прозрачным, чем должно быть. Отток и приток крови нарушается, либо и вовсе отсутствует.
-
Артериовенозные аневризмы и свищи. Из-за этой болезни поток крови между артериями и венами нарушается. В результате, кровь из вен переливается в артерии, вызывая гипоксемию. Когда средние и большие сосуды функционируют неправильно, появляются свищи на венах. В некоторых случаях появляются аневризмы. Проявляется в виде тяжести в процессе дыхания и отхаркивания крови.
Как проявляются пороки развития бронхолегочной системы?
Симптомы проявляются в зависимости от иммунитета и того, насколько развит организм.
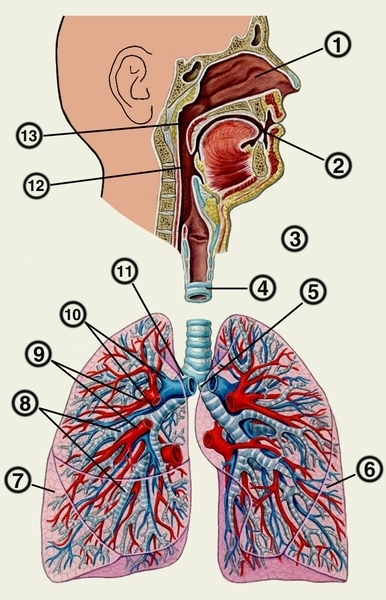
-
Отдельные пороки могут протекать без симптомов. Среди таких недугов: секвестрация и кисты, которые появляются с рождения.
-
Цианоз при затруднении дыхания
-
Если ребенок задыхается в процессе дыхания, то это может быть признаком стенозов, которые образовались в трахеи.
-
При некоторых пороках у малыша могут быть проблемы с развитием, видоизменяться форма грудной клетки.
Какие процедуры нужно проводить, чтобы диагностировать болезнь?
Для диагностики большинства болезней такого типа, помимо физикального осмотра, нужно использовать рентгенологические методы исследования. С помощью них можно увидеть агенезию, гипоплазию, секвестрацию, аномальное размещение органов, находящихся внутри (они расположены наоборот).
Чтобы выявить различные проблемы с бронхами, нужно провести бронхологическое обследование. С помощью него можно увидеть различные свищи и другие серьезные проблемы с этим органом.
Чтобы заметить проблемы с сосудистой системой, доктора выписывают направление на ангиопульмонографию.
Лечение
Доктора прописывают различные курсы лечения. Их интенсивность зависит от того, насколько тяжелой является болезнь, и какой орган она охватила.
В некоторых случаях проводятся и хирургическое лечение.
На портале Vikids вы можете:
1. Найти врача и записаться на прием
2. Найти клинику и записаться на прием, или зарегистрировать свою
3. Перейти на Форум
4. Почитать похожие статьи или написать свою
PPT — Врожденные дефекты легких Презентация PowerPoint, скачать бесплатно
Врожденные дефекты легких BIO361.001 Group 9 Evan Kinney Charlee Pittman Mina Yegani
Кистозный фиброз Charlee Pittman
000
14
фиброз — это наследственное хроническое заболевание слизистых желез, которое может поражать различные системы организма • Легкие и пазухи • Желудочно-кишечный тракт • Печень • Поджелудочная железа • Эндокринная система • Репродуктивная система • Одно из наиболее распространенных и сокращающих жизнь генетических заболеваний
The Genetics • Муковисцидоз был связан с мутацией в одном гене и его ассоциативном белке: регулятор трансмембранной проводимости при муковисцидозе, или CFTR • Включает мутацию на хромосоме 7 гена CFTR • Унаследован по аутосомно-рецессивному типу.
The Genetics • Делеция трех пар оснований, известная как ΔF508, является наиболее распространенной мутацией, вызывающей кистозный фиброз. • Это приводит к удалению одной аминокислоты (фенилаланин) в положении 508.
Пять типов мутаций CFTR Дефектная продукция белка Дефектная обработка белка Дефектная регуляция белка Дефектная проводимость белка Снижение количества функционирующего белка CFTR
Ген CFTR • Предоставляет инструкции, необходимые для создания активного ионного канала, который транспортирует отрицательные ионы хлорида внутрь и из клеток • Поток этих ионов помогает контролировать движение воды в различных тканях, что помогает производить тонкие и свободнотекущая слизь
Ген CFTR • Различные мутации в гене CFTR нарушают работу хлоридных каналов, не позволяя им регулировать поток хлорид-ионов и воды через клеточные мембраны
Слизь • Не регулируется поток приводит к появлению множества ячеек, выстилающих разные проходы поджелудочной железы, легких и других органов • Способствует выработке густой и липкой слизи
Слизь • Вызывает хронический кашель, хрипы и воспаления • В течение длительного периода времени скопление слизи вызывает повреждение легких и других органов • Образование рубцовой ткани (фиброз) • Рост кисты
Симптомы • Более частые, жирные и / или пахнущие испражнения • Мясистые наросты внутри носа (носовые полипы) • Увеличенные или неровные кончики пальцев / пальцы ног • Усталость • Кожа с соленым привкусом • Обезвоживание • Постоянный или тянущий кашель • Возможны кровяные прожилки • Густая / вязкая слизь в легких • Повторные инфекции (напр.г. бронхит, пневмония, синусит) • Проблемы с набором веса • Боль в животе • Метеоризм • Астма
Диагноз • Наблюдение за симптомами • Генетическое тестирование (дефектная хромосома 7) • Амниоцентез • Биопсия ворсин хориона • Новорожденных можно проверить с помощью простого анализ крови (трипсиноген) • Потовый тест ([NaCl])
Лечение • В настоящее время нет лекарства от муковисцидоза • Цели лечения включают: • Профилактика и контроль инфекций в легких • Предотвращение закупорки кишечника • Разжижение и удаление слизи из легких • Обеспечение адекватного питания
Лечение [Антибиотики] • Первичное лечение • Помогает лечить инфекции дыхательных путей в легких • Используемый антибиотик будет зависеть от • различных штаммов присутствующих бактерий • Общая тяжесть состояния • Предыдущее применение антибиотиков
Лечение [грудная терапия] • Также известно как постуральное дренаж • В грудную клетку и спину постоянно наносят удары, чтобы вывести слизь из легких, чтобы ее можно было кашлять • Обычно выполняется три-четыре раза в день, сидя или лежа на животе с опущенной головой
Лечение [Грудь Терапия] Демонстрация техники, используемой для разжижения слизи.
Лечение [упражнения] • Помогает разжижить слизь в легких, вызывая кашель • Улучшает общее физическое здоровье
Лечение [кислородные добавки]
Лечение [ Трансплантация] Выполняется только в самых тяжелых случаях.
Врожденная кистозная аденоматоидная мальформация Эван Кинни
Обзор • Врожденное заболевание • Результат аномального образования легочной ткани • Обычно проявляется в виде полного замещения доли • Причина в настоящее время неизвестна • Методы обнаружения в основном неинвазивные • Результаты обычно хорошие • Редко требует хирургического вмешательства
Происхождение и диагноз • Повышенная экспрессия локализованных факторов роста фибробластов (например,г. FGF10) • Мезенхимные клетки легких • Гестационный возраст 35-55 дней • Диагностика с помощью сомнографии или МРТ • Максимальный размер поражения ~ 25-28 недель беременности
Классификация • Система Стокера • Тип I • Наиболее часто • Множественные кисты> 2 см в диаметр • Одиночная большая киста, окруженная более мелкими кистами • Тип II • 40% случаев • Множественные кисты <1 см в диаметре • Тип III • 5% случаев • Множественные микрокисты • Выглядит как сплошная масса
Рис. 1 Stocker врожденная аденоматоидная мальформация I типа.
Рис.2 Врожденная аденоматоидная мальформация Стокера II типа.
Рис.3 Врожденная аденоматоидная мальформация Стокера III типа.
Лечение • Обычно не требуется • В большинстве случаев разрешается в утробе матери • Показано хирургическое вмешательство • Кардиомиопатии, вызванные ростом кисты • Наличие водянки • Рентгенография показала послеродовой период, даже если поражение рассасывается • Может увеличить вероятность развития сопутствующие заболевания, если не лечить
Исследования [Происхождение] • Исследование 2008 г. • Вызванная избыточная экспрессия FGF10 на обеих стадиях развития легочной ткани у крыс • Связь между образованием кисты и временем / местом экспрессии • Поддерживает теорию FGF10 как индуктор CCAM в моделях человека
Рис.4 Мезенхимальная сверхэкспрессия FGF10 совпадает с локализацией кистозных пороков развития. Легкие от инъецированных плодов на ст. E15.5 и E18.5 анализировали с помощью полной гибридизации in situ (wISH) для fgf10 через 24 часа после инъекции (E16.5, f – j и E19.5, k – o, соответственно) . Макроскопическое изображение (a, f, k) и изображения флуоресцентной стереомикроскопии для GFP (b, g, l) показаны рядом с изображениями wISH для сравнения. FGF10 сверхэкспрессируется в мезенхиме кистозной области (h – j; m – o).
Рис.5 Количественная ПЦР на FGF10 в легких. Экспрессию FGF10 в инъецированных легких на E15.5 анализировали на E16.5, E18.5 и E21.5. Количественную ПЦР проводили в контроле PBS, инъецированном AdGFP-FGF10 и контралатеральных легких. Уровни мРНК Fgf10 были значительно выше на E16.5 в ипсилатеральных легких AdGFP-FGF10 по сравнению с PBS и контрлатеральными легкими. Однако на E18.5 и E21.5 экспрессия FGF10 существенно не различалась между группами. Масштабные полосы соответствуют 50 мм для метакрилатных срезов гибридизированных легких.
Исследования [ретроспективный анализ] • Исследование 1993 г. • В подавляющем большинстве случаев затрагивалась только одна доля • Чаще встречается у мужчин, чем у женщин • Обычно диагностируется до истечения шести месяцев • Два аномальных случая • Патологические рентгенологические проявления; не обнаруживается до третьего дня рождения • Мертворожденный младенец; единственно вероятный случай двусторонней CCAM • Пациенты, не нуждающиеся в хирургическом вмешательстве, не имели значимых клинических событий (в среднем через 12 лет наблюдения)
Рис.6 Сводка зарегистрированных случаев врожденной кистозной аденоматоидной мальформации.
Список литературы • Фонд кистозного фиброза [домашняя страница в Интернете]. Bethesda (Мэриленд): Schaner & Lubitz, PLLC; 2010. [цитируется 12 ноября 2010 г.]. Доступно по адресу: http://www.cff.org/index.cfm. • Домашний справочник по генетике [домашняя страница в Интернете]. Бетесда (Мэриленд): Национальная медицинская библиотека США, Национальные институты здравоохранения; 1 января 1993 г. [цитировано 12 ноября 2010 г.]. Доступно по адресу: http: // ghr.nlm.nih.gov/condition/cystic-fibrosis. • Кобольдт Д. Генетика кистозного фиброза [домашняя страница в Интернете]. 2010. [цитируется 10 ноября 2010 г.]. Доступно по адресу: http: //snp.wustl.edu/snp-and-fp … / Koboldt_Cystic_Fibr …. • Муковисцидоз [домашняя страница в Интернете]. Фонд Мэйо медицинского образования и исследований; 2010. [цитируется 13 ноября 2010 г.]. Доступно по адресу: http: //www.mayoclinic.com/health/cystic-fibrosis/DS002 …. • Cystic-Fibrosis-Symptom.com [домашняя страница в Интернете]. Ashland (OR): Web Ring Incorporated; 2007 г.[цитировано 13 ноября 2010 г.]. Доступно по адресу: http://cystic-fibrosis-symptom.com/index.htm. • Cloutier, M. M., D. A. Schaeffer, et al. (1993). «Врожденный кистозный аденоматоидный порок». Сундук 103 (3): 761-764. • Gonzaga, S., T. Henriques-Coelho, et al. (2008). «Кистозные аденоматоидные мальформации вызваны локализованной сверхэкспрессией FGF10 в легких эмбриона крысы». Американский журнал респираторной клетки и молекулярной биологии 39 (3): 346-355. • Матхай, А., Х. Кини и др. (2010). «Врожденный кистозный аденоматоидный порок легкого 1 типа.»Журнал детской хирургии 45 (2): E25-28. • Мур, Л. и Р. Хэнди (2009).» Врожденная кистозная аденоматоидная мальформация: краткий обзор с изображениями «. Журнал диагностической медицинской сонографии 25 (168): 168-172.
Вопросы
.
Врожденные пороки сердца | Бэбицентр
Эта статья была адаптирована на основе информации, опубликованной Национальным институтом сердца, легких и крови, входящим в состав Национальных институтов здравоохранения США.
Поделитесь историями и получите совет от других родителей, чей ребенок имеет врожденный порок сердца, в нашей группе «Дети и дети с проблемами сердца».
Что такое врожденные пороки сердца?
Врожденные пороки сердца (кон-JEN-i-tal) — это проблемы со структурой сердца, которые присутствуют при рождении.Эти дефекты могут включать:
- Внутренние стенки сердца
- Клапаны внутри сердца
- Артерии и вены, по которым кровь идет к сердцу или оттуда к телу
Врожденные пороки сердца изменяют нормальный кровоток через сердце.
Есть много видов врожденных пороков сердца. Они варьируются от простых дефектов без симптомов до сложных дефектов с серьезными, опасными для жизни симптомами.
Врожденные пороки сердца — самый распространенный вид врожденных пороков.Они поражают 8 из каждых 1000 новорожденных. Ежегодно в США рождается более 35 000 детей с врожденными пороками сердца.
Многие из этих дефектов являются простыми состояниями, которые легко исправить или не нуждаются в лечении. Небольшое количество детей рождается со сложными врожденными пороками сердца, требующими особой медицинской помощи вскоре после рождения.
За последние несколько десятилетий диагностика и лечение этих сложных дефектов значительно улучшились. В результате почти все дети со сложными пороками сердца доживают до взрослого возраста и могут жить активной и продуктивной жизнью.
Большинство людей со сложными пороками сердца продолжают нуждаться в особой сердечной помощи на протяжении всей жизни. Им может потребоваться обратить особое внимание на то, как их состояние может повлиять на медицинское страхование, занятость, беременность и контрацепцию, а также на другие вопросы, связанные со здоровьем.
В Соединенных Штатах около 1 миллиона взрослых живут с врожденными пороками сердца.
Что вызывает врожденные пороки сердца?
Если у вас есть ребенок с врожденным пороком сердца, вы можете подумать, что вы сделали что-то не так во время беременности, чтобы вызвать проблему.Однако в большинстве случаев врачи не знают, почему развиваются врожденные пороки сердца.
Наследственность может играть роль в некоторых пороках сердца. Например, родитель с врожденным пороком сердца с большей вероятностью, чем другие люди, родит ребенка с этим заболеванием. В редких случаях в семье рождается более одного ребенка с пороком сердца.
Дети с генетическими нарушениями, такими как синдром Дауна, часто имеют врожденные пороки сердца. Фактически, половина детей с синдромом Дауна имеет врожденные пороки сердца.
Курение во время беременности также связано с несколькими врожденными пороками сердца, включая дефекты перегородки.
Ученые продолжают поиск причин врожденных пороков сердца.
Каковы признаки и симптомы врожденных пороков сердца?
Многие врожденные пороки сердца имеют несколько признаков или симптомов или вообще не имеют их. Врач может даже не обнаружить признаков порока сердца во время медицинского осмотра.
У некоторых пороков сердца есть признаки и симптомы. Они зависят от количества, типа и серьезности дефектов.Тяжелые дефекты могут вызывать признаки и симптомы, обычно у новорожденных. Они могут включать:
- Учащенное дыхание
- Цианоз (синюшный оттенок кожи, губ и ногтей)
- Утомляемость (усталость)
- Плохое кровообращение
Врожденные пороки сердца не вызывают боли в груди и т. Д. болезненные симптомы.
Пороки сердца могут вызвать нарушение кровотока через сердце, которое будет издавать определенный звук, называемый сердечным шумом. Ваш врач может услышать шум в сердце с помощью стетоскопа.Однако не все шумы являются признаками врожденных пороков сердца. У многих здоровых детей шумы в сердце.
Нормальный рост и развитие зависят от нормальной нагрузки на сердце и нормального притока богатой кислородом крови ко всем частям тела. Младенцы с врожденными пороками сердца могут иметь цианоз или легко уставать при кормлении. В результате они могут не набирать вес или расти так, как должны.
Дети старшего возраста с врожденными пороками сердца могут легко уставать или одышки во время физических нагрузок.
Многие виды врожденных пороков сердца заставляют сердце работать тяжелее, чем следовало бы. При тяжелых дефектах это может привести к сердечной недостаточности. Сердечная недостаточность — это состояние, при котором сердце не может перекачивать кровь, достаточную для удовлетворения потребностей организма. Симптомы сердечной недостаточности включают:
- Усталость при физической активности
- Одышка
- Накопление крови и жидкости в легких
- Накопление жидкости в ступнях, лодыжках и ногах
Как происходит врожденное сердце диагностированы дефекты?
Тяжелые врожденные пороки сердца обычно обнаруживаются во время беременности или вскоре после родов.Менее серьезные дефекты диагностируются только у детей.
Незначительные дефекты часто не имеют признаков или симптомов и диагностируются на основании результатов медицинского осмотра и тестов, проведенных по другой причине.
Привлеченные специалисты
Врачи, специализирующиеся на уходе за младенцами и детьми с проблемами сердца, называются детскими кардиологами. Кардиохирурги — другие специалисты, которые лечат пороки сердца. Эти врачи исправляют пороки сердца хирургическим путем.
Физический осмотр
Во время медицинского осмотра врач:
- Слушайте сердце и легкие вашего ребенка с помощью стетоскопа
- Обратите внимание на признаки порока сердца, такие как цианоз (синюшный оттенок кожи, губ или ногтей), одышку, учащенное дыхание, задержку роста или признаки сердечной недостаточности
Диагностические тесты
Эхокардиография
Эхокардиография (эхо) — это безболезненный тест, который использует звуковые волны для создания движущегося изображения сердца.Во время теста звуковые волны (называемые ультразвуком) отражаются от структур сердца. Компьютер преобразует звуковые волны в изображения на экране.
Эхо позволяет врачу четко увидеть любую проблему, связанную с формированием сердца или его работой.
Эхо — важный тест как для диагностики проблемы с сердцем, так и для отслеживания проблемы с течением времени. У детей с врожденными пороками сердца эхо может показать проблемы со структурой сердца и то, как сердце реагирует на эти проблемы.Эхо поможет кардиологу вашего ребенка решить, когда и когда необходимо лечение.
Во время беременности, если ваш врач подозревает, что у вашего ребенка врожденный порок сердца, может быть выполнено эхо-исследование плода. В этом тесте используются звуковые волны, чтобы создать изображение сердца ребенка, пока ребенок еще находится в утробе матери.
Эхо плода обычно проводится примерно на 18–22 неделе беременности. Если у вашего ребенка диагностирован врожденный порок сердца до рождения, ваш врач может спланировать лечение до рождения ребенка.
ЭКГ (электрокардиограмма)
ЭКГ — это простой безболезненный тест, который регистрирует электрическую активность сердца. Тест показывает, насколько быстро бьется сердце и его ритм (устойчивый или нерегулярный). Он также регистрирует силу и синхронизацию электрических сигналов, проходящих через каждую часть сердца.
ЭКГ может определить, увеличена ли одна из камер сердца, что может помочь диагностировать проблемы с сердцем.
Рентген грудной клетки
Рентген грудной клетки — это безболезненный тест, позволяющий получить изображения структур грудной клетки, таких как сердце и легкие.Этот тест может показать, увеличено ли сердце, есть ли в легких дополнительный кровоток или дополнительная жидкость, что является признаком сердечной недостаточности.
Пульсоксиметрия
Пульсоксиметрия показывает количество кислорода в крови. Для этого теста небольшой датчик прикрепляется к пальцу руки или ноги (например, липкой повязкой). Датчик дает оценку количества кислорода в крови.
Катетеризация сердца
Во время катетеризации сердца (KATH-e-ter-i-ZA-shun) тонкая гибкая трубка, называемая катетером, вводится в вену на руке, паховой области (верхней части бедра), или шею и продетую к сердцу.
Специальный краситель вводится через катетер в кровеносный сосуд или камеру сердца. Краситель позволяет врачу увидеть кровоток через сердце и сосуды на рентгеновском снимке.
Врач также может использовать катетеризацию сердца для измерения давления и уровня кислорода в камерах сердца и кровеносных сосудах. Это может помочь врачу определить, смешивается ли кровь между двумя сторонами сердца.
Катетеризация сердца также используется для восстановления некоторых пороков сердца.
Как лечат врожденные пороки сердца?
Хотя многие дети с врожденными пороками сердца не нуждаются в лечении, некоторым это необходимо. Врачи устраняют врожденные пороки сердца с помощью катетерных процедур или хирургического вмешательства.
Лечение, которое получает ваш ребенок, зависит от типа и тяжести его или ее порока сердца. Другие факторы включают возраст, размер и общее состояние вашего ребенка.
Некоторым детям со сложными врожденными пороками сердца может потребоваться несколько катетеров или хирургических вмешательств в течение нескольких лет, или им может потребоваться принимать лекарства в течение многих лет.
Катетерные процедуры
Катетерные процедуры намного проще для пациентов, чем хирургические операции, поскольку они включают только прокол иглой в коже, когда катетер (тонкая гибкая трубка) вводится в вену или артерию.
Врачам не нужно открывать грудную клетку хирургическим путем или оперировать сердце, чтобы исправить дефект. Это означает, что восстановление может быть проще и быстрее.
Использование катетерных процедур значительно выросло за последние 20 лет.Они стали предпочтительным способом лечения многих простых пороков сердца, таких как дефект межпредсердной перегородки (ДМПП) и стеноз легочного клапана.
При ДМПП врач вводит катетер через вену и продвигает его в сердце до перегородки. Катетер имеет крошечное устройство, похожее на зонтик, свернутое внутри.
Когда катетер достигает перегородки, устройство выталкивается из катетера. Он расположен так, что закрывает отверстие между предсердиями. Устройство закрепляется на месте, а затем катетер извлекается из тела.
При стенозе клапана легочной артерии врач вводит катетер через вену и вводит его в сердце к легочному клапану. Крошечный баллончик на конце катетера быстро надувается, чтобы раздвинуть створки или «двери» клапана. Затем баллон сдувается, а катетер и баллон извлекаются. Эта процедура может использоваться для восстановления любого суженного клапана в сердце.
Чтобы направить катетер, врачи часто используют эхокардиографию (эхо) или чреспищеводную (tranz-ih-sof-uh-JEE-ul) эхокардиографию (TEE) и ангиографию (an-jee-OG-ra-fee).
TEE — это особый тип эхо-сигнала, при котором снимается задняя часть сердца через пищевод (проход, ведущий изо рта в желудок). ЧВЭ также часто используется для исследования сложных пороков сердца.
Иногда врачи комбинируют катетерные и хирургические процедуры для устранения сложных пороков сердца, которые могут включать в себя несколько видов дефектов.
Хирургия
Операция на открытом сердце может потребоваться, если порок сердца у ребенка не может быть исправлен с помощью катетерной процедуры.Иногда одна операция может полностью исправить дефект. Если это невозможно, ребенку могут потребоваться дополнительные операции в течение месяцев или лет, чтобы решить проблему.
Операцию на открытом сердце можно сделать по телефону:
- Закройте отверстия в сердце швами или пластырем
- Отремонтируйте или замените сердечные клапаны
- Расширьте артерии или отверстия сердечных клапанов
- Устраните сложные дефекты, такие как проблемы с тем, где расположены кровеносные сосуды рядом с сердцем или как они разработали
В редких случаях дети рождаются с множественными дефектами, которые слишком сложно исправить.Этим младенцам может потребоваться пересадка сердца. В этой процедуре сердце ребенка заменяется здоровым сердцем умершего ребенка, подаренным семьей этого ребенка. .
Подход к цианотическим врожденным порокам сердца у новорожденных
Щелкните для pdf: цианотический врожденный порок сердца
Введение в цианоз
Цианоз — это синюшное или пурпурное изменение цвета кожи и слизистых оболочек, связанное с плохой оксигенацией. Это заметно, когда присутствует> 5 г / дл дезоксигенированного гемоглобина, и обычно оценивается с помощью пульсоксиметрии. Его очень трудно обнаружить, если сатурация артерий не превышает 85% и лучше всего не видна на языке и слизистой оболочке полости рта.Акроцианоз (цианоз только периферических частей), обычно наблюдаемый в холодных условиях или после купания, всегда является нормальным явлением и не является истинным цианозом. Давний цианоз приводит к цифровым клубам.
Причины цианоза: сердечные и внесердечные
Несердечные причины неонатального цианоза
Легочный | Неврологический |
Болезнь гиалиновой мембраны | Нарушение функции ЦНС |
Аспирация мекония / пневмония | Дыхательная нервно-мышечная дисфункция |
Пневмоторакс / плевральный выпот | Тяжелая седация для беременных |
Стойкая легочная гипертензия новорожденного | Перинатальная асфиксия |
Атрезия или стеноз хоан | Внутриутробный дистресс плода |
Диафрагмальная грыжа |
Обратите внимание, что подробный подход к неонатальному цианозу доступен на сайте LearnPediatrics.com
Кардиальные причины цианоза можно разделить на протоковозависимые и протоковонезависимые поражения. Зависимые от протоков поражения требуют артериального протока для адекватного легочного кровообращения и включают: тетралогию Фалло, атрезию трикуспидального клапана или аномалию Эбштейна, а также атрезию или стеноз легочной артерии. Независимые от протоков поражения приводят к легочному и системному смешиванию, что приводит к дезоксигенации артериальной крови; отсюда цианоз. Эти поражения включают: артериальный ствол, транспозицию магистральных артерий и полное аномальное соединение легочных вен.В этих условиях смешение обычно происходит через дефект межпредсердной перегородки (ASD), открытое овальное отверстие (PFO) или дефект межжелудочковой перегородки (VSD).
Дифференциальная диагностика цианотических врожденных пороков сердца
Зависимые от протоков поражения | Протоковонезависимые поражения |
Тетралогия Фалло | Артериальный ствол |
Атрезия трикуспидального клапана или аномалия Эбштейна | Транспозиция магистральных артерий |
Атрезия или стеноз легочной артерии | Общий аномальный возврат по легочной вене |
Синдром гипоплазии левых отделов сердца |
Сбор анамнеза: основные симптомы
Необходимо собрать подробный сердечный анамнез, включая пренатальный, перинатальный и семейный анамнез.Для детей старшего возраста полезно иметь в анамнезе шум в сердце, респираторную недостаточность и непереносимость физических упражнений. Важные отметки в истории включают:
Цианоз
- Время и локализация (периферическая или центральная) цианоза, дубинки
- Рефрактерный цианоз, если кислородная терапия не помогает
Обмороки или синюшные приступы
- Цианоз, возникающий при нагрузке, эмоциях и / или давлении вниз, что свидетельствует о динамической и увеличивающейся обструкции выводного тракта правого желудочка, что приводит к увеличению шунтирования справа налево через внутрисердечный шунт (VSD, ASD)
Нетерпимость к физическим упражнениям
- Непереносимость физических упражнений в анамнезе, включая одышку и / или потоотделение при незначительной физической нагрузке или учащенное сердцебиение при нагрузке
Гестационный и семейный анамнез
- Пренатальный скрининг важен, так как многие генетические синдромы связаны с врожденными пороками сердца
- Заболевания матери: сахарный диабет, краснуха, тератогенные препараты.
- В последнее время матери или плоды с риском врожденных пороков сердца обычно нуждаются в эхокардиограмме плода для выявления сердечных дефектов
- Семейный анамнез врожденных пороков сердца важен, поскольку все больше и больше людей с врожденными пороками сердца доживают до своего репродуктивного возраста.
Обратите внимание, что подход к сбору сердечного анамнеза доступен на LearnPediatrics.com
Физикальное обследование: основные выводы
Необходимо провести тщательное физическое обследование, включая полное кардиологическое и респираторное обследование.Следует отметить, что важные выводы включают:
Инспекция
- Дисморфические признаки генетических / врожденных пороков развития (например, синдром Дауна связан с дефектами эндокардиальной подушки, синдром Тернера связан с коарктацией аорты)
- Ищите признаки периферического (ногтевые ложа) и центрального (слизистые оболочки) цианоза
- Дифференциальный цианоз (насыщение кислородом нижних конечностей <верхних конечностей)
Обследование сердца
- Частота сердечных сокращений, пульсоксиметрия, пальпация центрального и периферического пульса и / или измерение артериального давления в верхних и нижних конечностях
- Пальпируйте для выявления громких сердечных тонов, парастернального подъема, апикального импульса и трепета.
- Выслушайте аномальные (например, одиночный или раздельный S2) и лишние сердечные тоны и шумы (степень, время, местоположение, радиация, интенсивность и маневры)
- Признаки сердечной недостаточности: парастернальная приподнятость и пальпируемый P2 (легочная гипертензия), повышенный JVP, гепатомегалия и периферический отек (правосторонняя недостаточность), смещение апикального импульса (увеличенный ЛЖ)
Респираторное обследование
- Обратите внимание на признаки респираторного дистресса, такие как тахипноэ, одышка (т.е.добавочные мышцы, парадоксическая диафрагма) и гиповентиляция
- Пальпация для асимметричного расширения диафрагмы, а у детей старшего возраста перкуссия для консолидации, плеврального выпота и пневмоторакса
- Аускультативно выслушать воздух, послушать хрипы / потрескивания (соответствующие выпотам и / или уплотнениям)
- Застойная сердечная недостаточность: затрудненное поступление воздуха и притупление перкуссии в основании (плевральный выпот) вместе с базальными хрипами / хрипами (отек легких)
Обратите внимание, что подход к шумам доступен на сайте LearnPediatrics.com
Исследования цианотического врожденного порока сердца
При подозрении на цианотический порок сердца для подтверждения основного диагноза доступны следующие исследования:
Электрокардиограмма (ЭКГ)
Гипертрофия правого желудочка: транспозиция магистральных артерий, общий аномальный возврат легочных вен, тетралогия фаллота, правый желудочек с двойным выходом, PPHN
Гипертрофия левого или двухжелудочкового ствола: артериальный ствол, транспозиция магистральных артерий, атрезия легких или трехстворчатого клапана, синдром асплениии
Блокада правой ножки пучка Гиса: аномалия Эбштейна
Рентген грудной клетки (CXR)
Рентген грудной клетки покажет размер сердца и легочную васкулярность.
Цианотические поражения сердца с повышенной васкуляризацией включают простой TGA, TAPVR, DORV и синдром полисплени.
Цианотические поражения сердца со сниженной васкуляризацией включают TOF, комплексный TGA, аномалию Эбштейна, атрезию легких и трехстворчатого клапана, а также синдром асплени.
Некоторые уникальные результаты рентгенографии грудной клетки могут быть более полезными и включают:
| « Яйцевидный » сердечная транспозиция магистральных артерий | Сердце « В форме сапога » в Тетралогии Фалло |
| « Снеговик » при полном аномальном оттоке легочной вены | При аномалии Эбштейна может возникнуть крайняя кардиомегалия. |
Тест на гипероксию:
Тест на гипероксию проводится для демонстрации реакции артериальной PaO 2 новорожденного на 100% кислород.Как правило, если причина цианоза не сердечная, артериальное PaO 2 будет увеличиваться до ≥ 100 мм рт. Ст. При воздействии 100% кислорода. Однако, если есть сердечная причина цианоза, PaO2 останется ниже 100 мм рт.
Пре-протоковая и пост-протоковая пульсоксиметрия:
Пульсоксиметрия из верхней (преддуктальной) и нижней / пупочной (постпротоковой) артерий может помочь идентифицировать шунт справа налево, проходящий через артериальный проток. Как правило, разница> 5% при наличии нормальной сатурации кислорода в пре- и пост-протоковых измерениях в верхних конечностях предполагает шунт справа налево.Кроме того, дифференциальный цианоз (т.е. цианоз нижних конечностей) является проявлением экстремального пред- и пост-протокового градиента PaO 2 , который может возникать при PPHN с прерванной дугой аорты и коарктацией аорты. Интересно, что обратный цианоз верхних, но не нижних конечностей может быть проявлением коарктации аорты или прерывания с одновременной транспозицией магистральных артерий.
Трансторакальная эхокардиограмма (ТЭЭ)
Трансторакальная эхокардиограмма точно идентифицирует врожденное поражение сердца, вызывающее цианоз.Например, двумерная эхокардиограмма может идентифицировать анатомические поражения, такие как дефекты перегородки (предсердные или желудочковые), тетралогия Фалло и т. Д. Дополнительная спектральная допплерография может определять степень и направление шунта и классификацию обструкции оттока.
Дополнительные возможности
Дополнительные методы визуализации включают катетеризацию сердца и магнитный резонанс сердца для дальнейшего уточнения аномальной анатомии при подготовке к кардиохирургии.
Краткое описание цианотических врожденных пороков сердца
Здесь мы представляем краткое изложение патофизиологии распространенных врожденных пороков сердца.Чтобы получить более подробное описание врожденных пороков сердца, прочтите статью Детская кардиология для практикующих врачей Мён К. Парк.
Транспозиция магистральных артерий
При транспозиции магистральных артерий аорта выходит из правого желудочка, а главная легочная артерия — из левого желудочка. Системное и легочное кровообращение идут параллельно со значительным цианозом, возникающим вскоре после рождения. В результате большинство новорожденных зависят от открытого артериального протока или дефекта межжелудочковой перегородки (30-40% случаев) для поддержания соответствующей насыщенности кислородом.У большинства детей с этим заболеванием в настоящее время проводится операция по переключению артерий (аорта соединяется с левым желудочком, а легочная артерия — с правым желудочком) наряду с коррекцией сопутствующих поражений, таких как закрытие дефекта межжелудочковой перегородки.
Тетралогия Фалло
Тетралогия Фалло — это совокупность четырех врожденных сердечных поражений, включая: обструкцию выводного тракта правого желудочка (инфундибулярный стеноз легкого), перекрывающую аорту, дефект межжелудочковой перегородки и гипертрофию правого желудочка.В результате возникает переменный шунт дезоксигенированной крови справа налево из-за динамической обструкции выводного тракта правого желудочка. Как правило, у младенцев цианоз появляется вскоре после рождения или у них появляются приступы цианоза, сопровождающиеся плачем, физическим напряжением, приводящим к частому приседанию на корточки. Важно отметить, что вариация тетралогии Фалло с атрезией легочной артерии приводит к тяжелому цианозу сразу же при рождении. Большинство пациентов восстанавливаются хирургическим путем в возрасте 4-6 месяцев.
Полный или частичный аномальный возврат в легочную вену (TAPVR или PAPVR):
В этом состоянии легочные вены имеют ненормальное соединение или дренаж в системные вены, что приводит к объемной перегрузке сердца.Младенцы с TAPVR (все легочные вены) могут иметь симптомы сердечной недостаточности или тяжелый цианоз и легочную гипертензию при обструкции. Аномальный дренаж легочной вены можно разделить на: надкардиальный (верхняя полая вена), сердечный (коронарный синус, правое предсердие), инфракардиальный (воротная вена, печеночная вена, нижняя полая вена) и смешанный дренаж. Обструкция TAPVR требует срочного хирургического вмешательства.
Трикуспидальная или легочная атрезия
Наличие трикуспидальной или легочной атрезии обычно требует сопутствующей аномалии, такой как дефект межпредсердной или желудочковой перегородки и / или открытый артериальный проток, для выживания.Младенцы страдают цианозом и нуждаются в хирургическом лечении.
Аномалия Эбштейна
Аномалия Эбштейна включает смещение перегородки и задней створки трехстворчатого клапана в правый желудочек, что приводит к тяжелой регургитации трикуспидального клапана и функциональной гипоплазии правого желудочка. В результате происходит расширение правого предсердия, которое можно увидеть на рентгенограмме грудной клетки. Лечение обычно хирургическое, в зависимости от степени тяжести.
Гипопластический синдром левых отделов сердца
Гипоплазия левого желудочка приводит к тому, что левый желудочек становится маленьким и нефункциональным, чтобы поддерживать системное кровообращение.Несмотря на то, что он переносится внутриутробно из-за компенсации правого желудочка, гипоплазированный левый желудочек не может поддерживать адекватный системный кровоток после рождения. Обычно артериальный проток защищен простагландинами до тех пор, пока не будет проведено этапное хирургическое паллиативное лечение (операции Норвуда) с последующим разделением системного и легочного кровообращения с помощью операции Фонтана.
Артериальный ствол
Устойчивый артериальный ствол возникает из раннего ствола плода, единственного артериального ствола, обеспечивающего легочное и системное кровообращение.Если этот единственный артериальный ствол не может разделиться, остается единый тракт оттока от правого и левого желудочков с стволовым клапаном. Обычно это связано с VSD.
Правый желудочек с двойным выходом
Правый желудочек с двойным выходом просто означает, что и аорта, и легочная артерия выходят из правого желудочка, а выход из левого желудочка проходит через большой межжелудочковый промежуток. Пациенты могут иметь сердечную недостаточность или тяжелый цианоз. Это состояние лечится с помощью различных хирургических вмешательств в зависимости от другого связанного поражения.
Гетеротаксия: синдромы асплении (изомерия правого предсердия) и полисплении (изомерия левого предсердия)
Гетеротаксия относится к неспособности дифференцировать правосторонний и левосторонний орган, что приводит не только к сложным поражениям сердца, но и ко многим другим несердечным порокам развития, особенно органов брюшной полости. Эти два синдрома наиболее точно суммированы и сопоставлены в следующей таблице:
АСПЛЕНИЯ | ПОЛИСПЛЕНИЯ | |
| Сердечно-сосудистая система | Двусторонний ВПВ, аномальный возврат в легочную вену, отсутствие коронарного синуса, дефект эндокардиальной подушки, стеноз легочной артерии, транспозиция магистральных артерий, | Прерванная нижняя полая вена с непродолжительным продолжением, легочный стеноз, стеноз или коарктация аорты, дефекты эндокардиальной подушки |
| Селезенка | Агенезия селезенки (** риск инфекции **) | Множественные, но нефункциональные селезенки |
| Легкие | Легкие трехлопастные с эпартериальным бронхом | Двустворчатые легкие с гипартериальным бронхом |
| Печень | Средняя линия печени, независимая печеночная вена на противоположной стороне от НПВ | Обычно нормальная, но может быть средней линии, прямой дренаж печеночных вен в предсердие |
| Желудочно-кишечный | Правосторонний или средний желудок, мальротация желудочно-кишечного тракта | Мальротация или аномалии желчевыводящих путей |
Синдром Эйзенменгера:
Синдром Эйзенменгера — это цианоз, вызванный шунтированием внутрисердечного шунта справа налево.Ацианотические поражения (такие как дефекты межпредсердной или межжелудочковой перегородки) обычно способны поддерживать соответствующую насыщенность кислородом, несмотря на шунт слева направо. Однако постоянное шунтирование слева направо с течением времени вызывает избыточное кровообращение в легких, что приводит к увеличению сопротивления легочных сосудов. Сопротивление легочных сосудов увеличивается до такой степени, что правостороннее давление становится больше, чем левостороннее, что приводит к шунту справа налево (обратное шунтирование), вызывая цианоз. Признаки синдрома Эйзенменгера, помимо центрального цианоза, включают признаки легочной гипертензии и правосторонней сердечной недостаточности, такие как припухлость правого желудочка, пальпируемый P2, легочная или трикуспидальная регургитация, повышенный JVP, застой в печени / пальпируемая печень и периферический отек.
Лечение цианотических врожденных пороков сердца
Ниже приводится краткое изложение острого и длительного лечения цианотических врожденных пороков сердца. Для более глубокого подхода к лечению конкретных врожденных поражений, рассмотрите возможность чтения Детская кардиология для практикующих врачей Мён К. Парк.
Медицинский менеджмент
Помимо дополнительного кислорода, медикаментозное лечение цианотических заболеваний сердца включает в себя инфузию простагландина E 1 в протоковозависимых поражениях для поддержания открытого артериального протока.Это обычно служит промежуточным лечением к вмешательству или кардиохирургии.
Септостомия предсердий
В случаях опасного для жизни цианоза и / или легочной гипертензии баллонная септостомия предсердий проводится путем продевания проволоки через овальное отверстие и надувания баллона для открытия овального отверстия. Это позволяет обеспечить адекватное перемешивание в случае транспозиции магистральных артерий и снимает правостороннее давление при легочной гипертензии.
Кардиохирургия
С помощью ряда хирургических процедур можно исправить врожденные аномалии или стабилизировать состояние ребенка с врожденными аномалиями.Эти паллиативные процедуры часто могут служить долгосрочными вариантами и включают шунтирование Блэлока-Тауссига, процедуру Гленна и другие.
Глобальные ссылки
- Парк, мкр. Детская кардиология для практиков. 5 -е издание . Филадельфия: Мосби Эльзевьер; 2008.
Дополнительные ссылки
- Парк, мкр. Справочник по детской кардиологии. 4 -е издание . Филадельфия: Мосби Эльзевьер; 2010.
- Rose V, Izukawa T, Moës CA.Синдромы асплении и полисплении. Обзор сердечных и внесердечных пороков развития в 60 случаях с особым упором на диагностику и прогноз. Br Heart J. 1975, август; 37 (8): 840–852.
- Marton T, Cesko I., Hajdu J et al. Синдром гетеротаксии, разбор 13 случаев и обзор литературы. Орв Хетиль. 2002 Feb 10; 143 (6): 299-301.
- Cesko I, Hajdu J, Marton T., Tarnai L, Zs Toth E. Синдром семейной гетеротаксии. Отчет о болезни и обзор международного. Литература.Орв Хетиль. 1998 Nov 15; 139 (46): 2775-8.
- Лейте, Дж. Синдромы асплени-полисплени. 2006 [обновлено 18 января 2006 г .; цитируется 1 декабря 2012 г.]. Доступно на: www.thefetus.net.
- Фондер Мюлл I. Цианотическая болезнь сердца и синдром Эйзенменгера. Эдмонтон: Университет Альберты; 2011 [обновлено 9 сентября 2011 г .; цитируется 1 декабря 2012 г.]. Доступно по адресу: www.medicine.med.ualberta.ca.
Благодарности
Сценарист: Кристофер Чунг
Редактор: Сантох Диллон, доктор медицины, MBBS
.

