Цитомегаловирус: Симптомы, диагностика и лечение
Цитомегаловирус – это достаточно распространенное вирусное заболевание, которое, между тем, известно далеко не каждому. Цитомегаловирус, симптомы и характерные признаки которого определяются, прежде всего, состоянием иммунной системы, при нормальном ее состоянии может вообще никак себя не проявлять. Не проявлять и не оказывая никакого вредного воздействия на организм вирусоносителя. Примечательно, что в этом случае единственной особенностью вирусоносителя является возможность передачи цитомегаловирусной инфекции к другому человеку.
Причины и симптомы
Заражение цитомегаловирусом происходит через сперму, слизь канала шейки матки, слюну, кровь и грудное молоко. Младенцы заражаются от своих матерей во время родов или через грудное молоко. Дети заражаются друг от друга в детских садах (обычно через слюну). Взрослые нередко заражаются при половых контактах и поцелуях.
Стоит отметить, что для заражения требуются длительное, тесное общение или многократные контакты, поэтому подхватить вирус не так уж просто.
Этот вирус широко распространен среди людей. Антитела к цитомегаловирусу выявляют у 10-15% подростков. К возрасту 35 лет эти антитела выявляют уже у 50% людей.
У людей с нормальным иммунитетом цитомегаловирус в подавляющем большинстве случаев протекает бессимптомно, не причиняя никакого вреда.
Иногда у лиц с нормальным иммунитетом этот вирус вызывает так называемый мононуклеозоподобный синдром. Этот синдром возникает спустя 20-60 суток после заражения и длится 2-6 недель. Проявляется он высокой температурой, ознобом, утомляемостью, недомоганием и головной болью. В большинстве случаев мононуклеозоподобный синдром заканчивается полным выздоровлением.
У лиц с ослабленным иммунитетом (ВИЧ-инфицированные; химиотерапия по поводу злокачественных новообразований; иммуносупрессивная терапия при трансплантации внутренних органов) цитомегаловирус вызывает тяжелые заболевания (поражение глаз, легких, пищеварительной системы и головного мозга), которые могут приводить к смерти.
При заражении плода во время беременности (но не во время родов) возможно развитие врожденной цитомегаловирусной инфекции. Последняя приводит к тяжелым заболеваниям и поражениям центральной нервной системы (отставание в умственном развитии, тугоухость). В 20-30% случаев ребенок погибает. Врожденная цитомегаловирусная инфекция наблюдается почти исключительно у детей, матери которых во время беременности впервые заражаются цитомегаловирусом.
Лишь порядка 17% из общего числа зараженных детей испытывает различную симптоматику, соответствующую инфекции. Цитомегаловирус проявляется в виде желтухи, увеличения внутренних органов в размерах (селезенка, печень), понижения гемоглобина и изменения состава крови на биохимическом уровне, в тяжелых формах своего течения может спровоцировать нарушения в ЦНС. Помимо этого, как нами уже отмечено ранее, могут развиться поражения слухового аппарата и глаз.
Часто отмечается появление обильной сыпи у детей уже в течение первых часов с момента рождения при наличии у них инфекции. Затрагивает она кожные покровы в области туловища, лица, ног и рук. Кроме того, цитомегаловирус нередко сопровождается и кровоточивостью пупочной ранки наряду с обнаружением в кале крови.
Затрагивает она кожные покровы в области туловища, лица, ног и рук. Кроме того, цитомегаловирус нередко сопровождается и кровоточивостью пупочной ранки наряду с обнаружением в кале крови.
Поражение головного мозга приводит к дрожанию ручек и к судорогам, отмечается повышенная сонливость.
Диагностика
Диагностирование заболевания производится с помощью ряда специфических исследований, ориентированных на обнаружение рассматриваемого вируса. Сюда входят не только лишь лабораторные методы, но также и изучение клинических особенностей.
Культуральный посев — с его помощью определяется возможность выявления вируса во взятых образцах слюны, спермы, крови, мочи, общего мазка. Здесь не только выявляется актуальность наличия вируса, но и составляется комплексная картина, указывающая на его активность. Кроме того, за счет проведения этого анализа становится понятно, насколько эффективна используемая против действия вируса терапия.
Световая микроскопия. С помощью данного метода с использованием в нем микроскопа имеется возможность обнаружения гигантских клеток цитомегаловируса.
С помощью данного метода с использованием в нем микроскопа имеется возможность обнаружения гигантских клеток цитомегаловируса.
ИФА. Данный метод основывается на выявлении антител к цитомегаловирусной инфекции. При иммунодефиците его не используют, потому, как это состояние исключает возможность выработки антител.
Диагностика ДНК. Ткани организма исследуются на предмет обнаружения ДНК рассматриваемого вируса.
Лечение
На сегодняшний день метода лечения, с помощью которого полностью устраняется из организма цитомегаловирус, не существует. При нормальном состоянии иммунной системы и отсутствии активности со стороны вируса, лечения, как такового, не требуется. В случае обнаружения в организме цитомегаловирусной инфекции, в обязательном порядке применять антивирусную терапию не нужно.
Курс лечения требуется в обязательном порядке при гепатите, расстройстве слуховых и зрительных органов, пневмонии, энцефалите, желтухе, подкожных кровоизлияниях и недоношенности (в случае врожденной формы цитомегаловируса). Лечение, как правило, предполагает использование препаратов в виде свечей, а также ряда противовирусных препаратов. Длительность приема, как и дозировка, определяются исходя из индивидуальных особенностей и состояния больного.
Лечение, как правило, предполагает использование препаратов в виде свечей, а также ряда противовирусных препаратов. Длительность приема, как и дозировка, определяются исходя из индивидуальных особенностей и состояния больного.
Для подробной консультации обращайтесь в нашу клинику.
Цитомегаловирус
Цитомегаловирус (ЦМВ) — это род вирусов группы герпесвирусов.
Вирус имеет сродство к тканям слюнных желез, что зачастую позволяет находить и локализовывать его именно там. Данный вирус, как и все вирусы герпеса, имеет свойство постоянно находиться (персистировать) в организме человека при однократном заражении, однако сам по себе он не сильно заразен, поскольку для этого требуются частые и тесные контакты с носителем.
Заражение происходит:
- воздушно-капельным путем, а также через слюну при поцелуях;
- половым путем — при контакте со спермой и слизистой матки;
- при переливании крови;
- при родах и во время пребывания ребенка в утробе в процессе беременности;
- через молоко матери при грудном кормлении ребенка.

Клинические проявления
Срок от 20 до 60 дней считается инкубационным для ЦМВ, тогда как острая фаза заболевания длится от 2 до 6 недель. При этом проявляются: повышение температуры тела, признаки общей интоксикации, слабость, ознобы, головные боли, боли в мышцах, явления бронхита. Впоследствии под действием вируса происходит перестройка иммунной системы организма, готовящейся к отражению атаки. Однако в случае нехватки сил организма острая фаза переходит в более спокойную форму, когда зачастую проявляются сосудисто-вегетативные расстройства, а также поражения внутренних органов. В данном случае возможны три проявления заболевания:
- ОРВИ (острая респираторная вирусная инфекция) — в данном случае представлены все симптомы ОРВИ (слабость, общее недомогание, быстрая утомляемость, немного повышенная температура тела, головные боли, насморк, увеличение и воспаление слюнных желез, белесоватые налеты на языке и деснах; иногда возможно наличие воспаленных миндалин;
- генерализованная форма — поражение ЦМВ внутренних органов (воспаление печеночной ткани, надпочечников, почек, селезенки, поджелудочной железы).
 Данные поражения органов могут стать причиной бронхита, пневмонии, что ещё более ухудшает состояние и оказывает повышенное давление на иммунную систему. При этом лечение антибиотиками оказывается менее эффективным, нежели при обычном протекании бронхита и/или пневмонии. Вместе с тем может наблюдаться уменьшение тромбоцитов в периферийной крови, поражение стенок кишечника, сосудов глазного яблока, головного мозга и нервной системы. Внешне проявляется, в дополнении к увеличенным слюнным железам, кожной сыпью;
Данные поражения органов могут стать причиной бронхита, пневмонии, что ещё более ухудшает состояние и оказывает повышенное давление на иммунную систему. При этом лечение антибиотиками оказывается менее эффективным, нежели при обычном протекании бронхита и/или пневмонии. Вместе с тем может наблюдаться уменьшение тромбоцитов в периферийной крови, поражение стенок кишечника, сосудов глазного яблока, головного мозга и нервной системы. Внешне проявляется, в дополнении к увеличенным слюнным железам, кожной сыпью; - поражение органов мочеполовой/мочевыводящей системы — проявляется в виде неспецифического и периодического воспаления. При этом, как и в случае бронхита и пневмонии, воспаления плохо поддаются лечению традиционными для данного локального заболевания антибиотиками.
Также в случае заражения беременной женщины возможна патология плода, когда плод заражается поступившим в кровь извне ЦМВ, что приводит к невынашиванию плода (одна из наиболее частых причин). Также возможна активизация латентной формы вируса, заражающего плод через кровь матери. Заражение приводит либо к гибели ребенка в утробе/после родов, либо к поражению нервной системы и головного мозга, что проявляется в различных психологических и физических заболеваниях.
Также возможна активизация латентной формы вируса, заражающего плод через кровь матери. Заражение приводит либо к гибели ребенка в утробе/после родов, либо к поражению нервной системы и головного мозга, что проявляется в различных психологических и физических заболеваниях.
Лечение
Лечение вируса имеет общий характер, когда требуется укрепление иммунной системы человека для противостояния развитию заболевания даже в случае заражения. Также лечение антибиотиками сопутствующих заболеваний в комплексе с противовирусной и общеукрепляющей терапией позволяет излечиться или вывести вирус в латентную (неактивную) форму, когда деятельность вируса контролируется иммунной системой человека.
Правильно подобранное лечение современными препаратами, а также лечение сопутствующих заболеваний антибиотиками и иммуномодуляторами, в комплексе с общеукрепляющей (здоровый образ жизни, обязательные прогулки, витаминотерапия и т. п.) терапией позволяет излечиться полностью
п.) терапией позволяет излечиться полностью
противовирусные препараты — клиника «Добробут»
Методы лечения цитомегаловируса у детей и взрослых
Цитомегаловирусная инфекция относится к семейству герпесвирусов. Заболевание протекает латентно у здоровых людей, но весьма опасно для пациентов с иммунодефицитом (ВИЧ-инфицированных, принимающих иммуносупрессоры после трансплантации органов и тканей). Врожденная цитомегаловирусная инфекция может привести к серьезным патологиям и даже смерти. После инфицирования вирус остается в организме на протяжении всей жизни и способен к реактивации в любое время, что может вызвать развитие мукоэпидермоидной карциномы и других злокачественных образований. Вот почему так важно своевременно сдать анализ крови на антитела к цитомегаловирусу во время беременности.
Причины и симптомы заболевания
Заражение происходит при непосредственном контакте с носителем инфекции или больным через различные биологические жидкости: кровь, сперму, слюну, влагалищные выделения, мочу, грудное молоко. Еще один путь передачи инфекции – от матери к плоду во время беременности. При инфицировании плода может развиться врожденная цитомегалия.
Еще один путь передачи инфекции – от матери к плоду во время беременности. При инфицировании плода может развиться врожденная цитомегалия.
У пациентов с нормальным иммунитетом ЦМВ-инфекция через 30-60 суток после заражения часто проявляется мононуклеозоподобным синдромом. Могут отмечаться слабость, лихорадка, боль в мышцах. После выработки антител против вируса симптомы заболевания исчезают, но вирус остается в организме в неактивной форме.
У пациентов с ослабленным иммунитетом цитомегаловирусная инфекция вызывает поражение легких, поджелудочной железы, печени, почек и других органов. Внутриутробное инфицирование плода чревато развитием серьезного заболевания – врожденной цитомегалии.
Симптомы цитомегалии:
- увеличение селезенки, печени;
- хориоретинит;
- пневмония;
- тугоухость;
- аномалии развития зубов.
Вирус Эпштейна-Барр тоже относится к семейству герпесвирусов. Симптомы поражения вирусом Эпштейна-Барр у мужчин:
- повышение температуры тела;
- воспаление миндалин;
- увеличение лимфоузлов на шее, затылке, в паховой области.

Что значит положительный цитомегаловирус IgG
Наличие антител IgM к цитомегаловирусу у женщин при отрицательном IgG говорит о недавнем инфицировании и начале развития болезни. Положительный результат анализа на определение антител IgG и IgM свидетельствует об острой стадии заболевания.
Что значит положительный цитомегаловирус IgG? Положительный анализ свидетельствует о носительстве цитомегаловируса. Наличие антител к цитомегаловирусу – признак выработки устойчивого иммунитета к возбудителю. То есть положительный результат анализа считается благоприятным при условии, что пациент не страдает иммунодефицитом. Детальную расшифровку анализа проводит врач. Подробную информацию о методах диагностики цитомегаловируса вы найдете на нашем сайте https://www.dobrobut.com.
Обнаружен цитомегаловирус при беременности – что делать
Как лечить цитомегаловирус? Вирусоносительство и мононуклеозоподобный синдром у пациентов с нормальным иммунитетом обычно не требуют лечения. Терапию назначают при выявлении генерализованных форм инфекции. Поскольку применяемые для лечения цитомегаловируса препараты достаточно токсичные, их назначают только по жизненным показаниям. Для профилактики цитомегаловирусной инфекции, развивающейся на фоне иммунодепрессивной терапии, назначают иммуноглобулин антицитомегаловирусный (один или в сочетании с противовирусным препаратом). Это позволяет предупредить ухудшение состояния и снизить риск летального исхода.
Терапию назначают при выявлении генерализованных форм инфекции. Поскольку применяемые для лечения цитомегаловируса препараты достаточно токсичные, их назначают только по жизненным показаниям. Для профилактики цитомегаловирусной инфекции, развивающейся на фоне иммунодепрессивной терапии, назначают иммуноглобулин антицитомегаловирусный (один или в сочетании с противовирусным препаратом). Это позволяет предупредить ухудшение состояния и снизить риск летального исхода.
Если обнаружен цитомегаловирус при беременности, то для профилактики передачи вируса плоду проводят десенсибилизирующую и общеукрепляющую терапию. Назначают иммуномодуляторы, витамины. В качестве специфического средства применяют нормальный человеческий иммуноглобулин. Число мертворождений при такой схеме лечения снижается в пять раз. Препараты с выраженным противовирусным действием токсичны, а потому не применяются для лечения ЦМВ-инфекции у беременных.
Лечение цитомегаловируса у детей проводят с использованием специфических иммуноглобулинов и противовирусных препаратов. Эффективным средством для лечения ЦМВ-инфекции признан ганцикловир – пуриновый ациклический нуклеозид. Однако препарат обладает высокой токсичностью, поэтому его не применяют для лечения цитомегаловируса у новорожденных. В других возрастных группах ганцикловир назначают только при непосредственной угрозе жизни ребенка. Применение препарата оправдано при подтвержденном диагнозе и наличии четких показаний.
Эффективным средством для лечения ЦМВ-инфекции признан ганцикловир – пуриновый ациклический нуклеозид. Однако препарат обладает высокой токсичностью, поэтому его не применяют для лечения цитомегаловируса у новорожденных. В других возрастных группах ганцикловир назначают только при непосредственной угрозе жизни ребенка. Применение препарата оправдано при подтвержденном диагнозе и наличии четких показаний.
Цитомегаловирус — «СМ-Клиника» Санкт-Петербург
Цитомегаловирус (ЦМВ) – это широко распространенный вирус, относящийся к семейству герпесных. Более половины взрослых в нашей стране имеют его в организме примерно к 40 годам. ЦМВ легко распространяется через слюну инфицированного человека или другие биологические жидкости организма Источник:
Цитомегаловирусная инфекция. Луценко М.Т. Бюллетень физиологии и патологии дыхания №44, 2012. с. 131-136.
Особенности вируса и инфекции
Цитомегаловирус (CMV, вирус герпеса человека 5 типа) может провоцировать инфекции разной степени тяжести. Наиболее распространен синдром инфекционного мононуклеоза без развития тяжелого фарингита. У ВИЧ-инфицированных пациентов, реципиентов органов и других пациентов с ослабленным иммунитетом может развиваться тяжелая очаговая форма инфекции, включая ретинит. У новорожденных и пациентов с ослабленным иммунитетом может формироваться и тяжелое системное поражение.
Наиболее распространен синдром инфекционного мононуклеоза без развития тяжелого фарингита. У ВИЧ-инфицированных пациентов, реципиентов органов и других пациентов с ослабленным иммунитетом может развиваться тяжелая очаговая форма инфекции, включая ретинит. У новорожденных и пациентов с ослабленным иммунитетом может формироваться и тяжелое системное поражение.
Цитомегаловирусная инфекция (ЦМВ) очень распространена. Анализы крови на антитела показывают, что от 60 до 90% взрослых когда-либо были инфицированы ЦМВ и у них остались антитела к инфекции и клетки памяти Источник:
Морфологические особенности цитомегаловирусной инфекции. Кузьмичев Д.Е., Скребов Р.В., Вильцев И.М. Здравоохранение Югры: опыт и инновации №1, 2020. с. 57-59.
Пути заражения
Цитомегаловирусная инфекция – это достаточно распространенная герпесвирусная инфекция с широким спектром симптомов: от бессимптомного носительства, легкой лихорадки и усталости (напоминающих инфекционный мононуклеоз) до тяжелых симптомов, затрагивающих глаза, мозг или другие внутренние органы.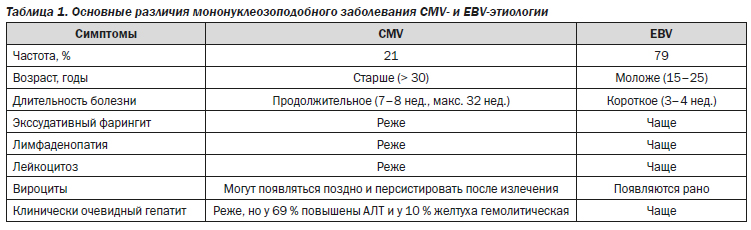 Этот вирус распространяется половым путем и через другие биологические жидкости тела (слеза, слюна, кровь или моча).
Этот вирус распространяется половым путем и через другие биологические жидкости тела (слеза, слюна, кровь или моча).
Обычно инфекция ЦМВ протекает бессимптомно. Серьезные инфекции обычно развиваются только у младенцев, инфицированных до рождения (внутриутробно), и у людей с ослабленной иммунной системой, например, у пациентов со СПИДом или у тех, кто перенес трансплантацию органов. У людей с ослабленной иммунной системой заболевание часто возникает в результате реактивации спящего вируса.
Инфицированные люди могут периодически выделять цитомегаловирус с мочой или слюной. Вирус также выделяется со слизью шейки матки (нижняя часть матки), спермой, стулом и грудным молоком. Таким образом, вирус распространяется половым и несексуальным путем. Если беременная женщина инфицирована, плод может заразиться во время беременности или родов.
ЦМВ-инфекция может развиться у людей, которым переливают инфицированную кровь или трансплантируют инфицированный орган. Люди, которым была проведена трансплантация органов, особенно восприимчивы к ЦМВ-инфекции, потому что им дают лекарства, подавляющие иммунную систему (иммунодепрессанты), чтобы предотвратить отторжение трансплантата.
Клинические проявления
У большинства людей симптомы отсутствуют, но некоторые чувствуют себя плохо и у них поднимается температура, а у людей с ослабленной иммунной системой могут быть серьезные симптомы, включая возможную слепоту.
Если это активная инфекция, ЦМВ может вызвать симптомы вскоре после заражения. Также он остается бездействующим (неактивным) в различных тканях на всю жизнь. Различные стимулы могут реактивировать спящий ЦМВ, что приводит к размножению вируса, который иногда может вызывать повторное заболевание. Могут быть инфицированы легкие, желудочно-кишечный тракт, головной, спинной мозг или глаза.
У большинства людей, инфицированных цитомегаловирусом, даже минимальные симптомы отсутствуют. Некоторые инфицированные люди заболевают, и у них поднимается температура. Инфекция ЦМВ, как и инфекция вирусом Эпштейна-Барра (EBV, вирус герпеса 4 типа), может вызывать инфекционный мононуклеоз у подростков и молодых людей. Мононуклеоз ЦМВ и ВЭБ вызывает лихорадку и усталость. Но EBV также вызывает сильную боль в горле. CMV – нет. У неинфицированного человека, которому переливают кровь, содержащую ЦМВ, может подняться температура, а иногда через 2-4 недели развивается воспаление печени. У людей с ослабленной иммунной системой ЦМВ может вызвать серьезное заболевание или смерть. У людей со СПИДом инфекция ЦМВ является частым вирусным осложнением. Вирус может поразить сетчатку глаза. Эта инфекция (ЦМВ-ретинит) может вызвать слепоту. Также может развиться инфекция головного мозга (энцефалит), пневмония или болезненные язвы кишечника или пищевода Источник:
Но EBV также вызывает сильную боль в горле. CMV – нет. У неинфицированного человека, которому переливают кровь, содержащую ЦМВ, может подняться температура, а иногда через 2-4 недели развивается воспаление печени. У людей с ослабленной иммунной системой ЦМВ может вызвать серьезное заболевание или смерть. У людей со СПИДом инфекция ЦМВ является частым вирусным осложнением. Вирус может поразить сетчатку глаза. Эта инфекция (ЦМВ-ретинит) может вызвать слепоту. Также может развиться инфекция головного мозга (энцефалит), пневмония или болезненные язвы кишечника или пищевода Источник:
Клинико-патоморфологическая характеристика цитомегаловирусной инфекции. Жетписбаев Б.Б., Баешева Д.А.
Журнал «Нейрохирургия и неврология Казахстана» №3, 2013. с. 16-18
. Если беременная женщина передает ЦМВ плоду, может произойти следующее:
- выкидыш;
- мертворождение;
- смерть новорожденного.
У новорожденных ЦМВ-инфекция может вызвать обширное повреждение печени или мозга. Выжившие новорожденные могут иметь потерю слуха и умственную отсталость.
Выжившие новорожденные могут иметь потерю слуха и умственную отсталость.
Классификация ЦМВ
Существуют разные типы цитомегаловирусной инфекции:
- Врожденная. Это когда ребенок получает ЦМВ от матери до рождения.
- Первичная. Это первый случай заражения ЦМВ. Обычно это не вызывает симптомов, но у некоторых людей могут быть признаки, похожие на мононуклеоз.
- Реактивация. Спящая инфекция может снова стать активной, когда иммунная система ослабевает. Это может произойти, если имеются различные состояния, подавляющие активность иммунной системы Источник:
Факторы реактивации цитомегаловирусной инфекции. Божбанбаева Н. С., Байгазиева Г. Ж., Абдуллаева Г. М. Вестник Казахского Национального медицинского университета №2, 2012. с. 128-130.
Симптомы ЦМВИ: как проявляется
Большинство здоровых людей, заразившихся ЦМВ, ничего не ощущают. Если возникают симптомы первичного ЦМВ, они мягкие и включают:
Если возникают симптомы первичного ЦМВ, они мягкие и включают:
- усталость;
- воспаление и небольшую отечность лимфоузлов;
- невысокую температуру;
- боль в горле;
- боль в мышцах.
В редких случаях ЦМВ также может вызывать:
- изменения в настроении;
- головные боли;
- проблемы с концентрацией;
- одышку;
- сухой кашель.
Младенцы с ЦМВ могут появляться на свет ранее срока, имеют маленький рост или низкий вес при рождении, страдают от сыпи, похожей на синяки, у них желтая кожа или глаза (желтуха), увеличенная печень и селезенка, маленькая голова (микроцефалия). Для врожденной ЦМВИ типичны судороги, потеря слуха, пневмония и воспаление печени (гепатит).
Если у пациента ВИЧ на поздней стадии, ЦМВ может поражать разные части тела. Возможные проявления:
- слепые пятна или движущиеся черные точки (плавающие пятна) в полях зрения;
- нечеткое зрение;
- слепота;
- диарея;
- боль в животе;
- проблемы с глотанием или болезненное глотание из-за язв во рту или пищеводе;
- спутанность сознания;
- боль в пояснице;
- потеря веса;
- усталость;
- слабость в ногах.

Методы диагностики
Цитомегаловирусную инфекцию нельзя распознать сразу. У здоровых взрослых и детей в диагностике ЦМВ-инфекции часто нет необходимости, поскольку им не требуется лечения. Однако врачи рассматривают возможность заражения ЦМВ у людей с ослабленной иммунной системой и инфекциями глаза, головного мозга или желудочно-кишечного тракта, а также у новорожденных, которые кажутся больными.
При подозрении на инфекцию ЦМВ врач проводит тесты для обнаружения вируса в жидкостях или тканях организма. У новорожденных диагноз обычно ставится при исследовании образца мочи в лаборатории идентификации вируса.
Анализы крови, обнаруживающие антитела к ЦМВ, могут подтвердить свежую инфекцию. (Антитела вырабатываются иммунной системой, чтобы помочь защитить организм от конкретного вируса.) Но эти тесты не могут подтвердить наличие болезни. Например, болезнь может быть вызвана реактивацией вируса, как у людей с ослабленной иммунной системой. В этих случаях часто необходима биопсия тканей для подтверждения заболевания ЦМВ Источник:
В этих случаях часто необходима биопсия тканей для подтверждения заболевания ЦМВ Источник:
Лабораторная диагностика цитомегаловирусной инфекции. Смирнова А.И., Россихина Е.В., Колеватых Е.П. Вятский медицинский вестник, 2010.
Анализы крови и мочи. К ним относятся антиген ЦМВ (часть вируса), вирусная культура или ПЦР (молекулярный тест). Серологические тесты ищут антитела IgM и IgG, которые иммунная система создает для борьбы с ЦМВ, хотя они также есть у большинства здоровых людей.
Биопсия. Врач берет небольшой образец ткани из кишечника, пищевода или легкого и рассматривает его под микроскопом.
Визуализирующие обследования, такие как компьютерная томография, для выявления изменений в легких или головном мозге.
ЦМВ ретинит может быть идентифицирован офтальмологом, который исследует внутренние структуры глаза для выявления характерных аномалий с помощью офтальмоскопа Источник:
Лабораторная диагностика цитомегаловирусной инфекции. Сижажева А.М. Инновационная наука №12, 2015. с. 289-292.
с. 289-292.
Лечение
Легкая форма цитомегаловирусной инфекции обычно не лечится,иммунитет сам справляется с возбудителем. Когда инфекция угрожает жизни или зрению, может быть назначен противовирусный препарат («Валганцикловир», «Ганцикловир», «Цидофовир», «Фоскарнет» или их комбинация). Эти препараты можно вводить перорально или внутривенно. При очень тяжелой форме ЦМВ-ретинита препараты также можно вводить непосредственно в глаз. Эти препараты имеют серьезные побочные эффекты и не лечат инфекцию. Однако лечение замедляет прогрессирование болезни и может сохранить зрение. Противовирусные препараты используются для лечения других тяжелых симптомов, вызванных ЦМВ, но они менее эффективны, чем при лечении ретинита.
Если ЦМВ-инфекция возникает у людей, чья иммунная система временно ослаблена или подавлена (заболеванием или лекарством), инфекция обычно проходит после восстановления иммунной системы или прекращения приема препарата. Лечение людей, инфицированных ВИЧ/СПИДом, с помощью лекарств, используемых для борьбы с ВИЧ (антиретровирусные препараты), помогает защитить от инфекции ЦМВ.
Людям, перенесшим трансплантацию органов, часто назначают противовирусные препараты (например, «Ганцикловир», «Валганцикловир» или «Фоскарнет») для предотвращения инфекции ЦМВ.
Методы профилактики
ЦМВ когда-то был самой распространенной вирусной оппортунистической инфекцией – заболеванием, которое обостряется или чаще возникает у людей с ослабленной иммунной системой, что связано с ВИЧ. Сегодня антиретровирусная терапия может помочь поддерживать уровень CD4 и укреплять иммунную систему. Это также может помочь предотвратить повторение ретинита.
У здоровых людей каких-либо особых мер профилактики, кроме стандартных рекомендаций, не имеется.
Источники статьи:
- Цитомегаловирусная инфекция. Луценко М.Т. Бюллетень физиологии и патологии дыхания №44, 2012. с. 131-136
- Морфологические особенности цитомегаловирусной инфекции. Кузьмичев Д.Е., Скребов Р.В., Вильцев И.М. Здравоохранение Югры: опыт и инновации №1, 2020.
 с. 57-59
с. 57-59 - Лабораторная диагностика цитомегаловирусной инфекции. Смирнова А.И., Россихина Е.В., Колеватых Е.П. Вятский медицинский вестник, 2010
- Факторы реактивации цитомегаловирусной инфекции. Божбанбаева Н. С., Байгазиева Г. Ж., Абдуллаева Г. М. Вестник Казахского Национального медицинского университета №2, 2012. с. 128-130
- Лабораторная диагностика цитомегаловирусной инфекции. Сижажева А.М. Инновационная наука №12, 2015. с. 289-292
- Клинико-лабораторная диагностика цитомегаловирусной инфекции. Бегайдарова Р.Х., Бейсенова Г.Р., Карпова Л.В., Карпова Е.В., Перевертова Е.С., Файзуллина А.М. Медицина и экология №1, 2010. с. 69-73
- Клинико-патоморфологическая характеристика цитомегаловирусной инфекции. Жетписбаев Б.Б., Баешева Д.А.Журнал «Нейрохирургия и неврология Казахстана» №3, 2013. с. 16-18
Цитомегаловирусная инфекция в практике врача: современный алгоритм диагностики и лечения | #04/18
Цитомегаловирус (ЦМВ) — чрезвычайно распространенный вирус, поражающий людей всех возрастов и формирующий пожизненную персистенцию в организме инфицированного человека. Считается, что в большинстве случаев персистенция начинается в ранние годы жизни и протекает латентно, не оказывая выраженного патологического влияния на состояние здоровья инфицированного. С другой стороны, доказано, что персистенция вируса может сопровождаться хроническим воспалением, формировать разнообразные многочисленные иммунные дисфункции и определять развитие вторичных иммунных, аутоиммунных и дегенеративных нарушений. Различного рода иммунокомпрометации могут приводить к рецидивам размножения вируса и многообразным клиническим проявлениям с поражением любых органов и систем в любом возрасте.
Считается, что в большинстве случаев персистенция начинается в ранние годы жизни и протекает латентно, не оказывая выраженного патологического влияния на состояние здоровья инфицированного. С другой стороны, доказано, что персистенция вируса может сопровождаться хроническим воспалением, формировать разнообразные многочисленные иммунные дисфункции и определять развитие вторичных иммунных, аутоиммунных и дегенеративных нарушений. Различного рода иммунокомпрометации могут приводить к рецидивам размножения вируса и многообразным клиническим проявлениям с поражением любых органов и систем в любом возрасте.
Особое значение имеют врожденные инфекции детей, которые отличаются высоким риском развития тяжелых генерализованных форм и инвалидизирующих исходов заболевания, таких как потеря слуха, зрения, умственная отсталость, микроцефалия, судорожный синдром и пр. Такие пожизненные проблемы со здоровьем развиваются примерно у каждого пятого ребенка с врожденной цитомегаловирусной инфекцией (ЦМВИ), что определяет потребность в своевременном пренатальном выявлении беременных и плодов с высоким риском развития врожденной ЦМВИ и ранней диагностике и лечении инфекций у новорожденных.
Теоретические дискуссии по вопросам адекватной диагностики антенатальной и постнатальной ЦМВИ, а также лечению острых ЦМВИ у беременной, плода и новорожденного продолжаются с 1990-х гг., но отсутствие единых руководящих принципов затрудняет практическую работу врачей. Российской ассоциацией специалистов перинатальной медицины в 2016 г. выработаны отечественные клинические рекомендации по диагностике и лечению врожденной ЦМВИ. Созданная в рамках 5-й Международной конференции по ЦМВИ (Брисбен, Австралия, 19 апреля 2015) международная группа экспертов на основе консенсусных дискуссий и обзора литературы выработала первые неофициальные международные рекомендации по вопросам диагностики и лечения врожденной ЦМВИ, которые опубликованы в Lancet Infect Dis в марте 2017. Все эти рекомендации будут нуждаться в постоянном обновлении по мере поступления дополнительных данных.
История
Исходя из теории ко-эволюции вирусов с их хозяевами, считается, что герпетические вирусы появились в кембрийский период. В человеческой популяции герпетические вирусы распространены на протяжении тысячелетий. 24 ноября 1974 г. американским антропологом Д. Джохансоном в Великой рифтовой долине был обнаружен скелет афарского австралопитека Люси — предполагается, что это ветвь прародителей Homo sapiens [1]. Возраст Люси определен как 3,2–3,5 млн лет. В «слюне» Люси найдены три герпетических вируса — ЦМВ, вирус Эпштейна–Барр (ВЭБ), вирус простого герпеса 1-го типа (ВПГ 1-го типа). «Современные» люди, мигрировавшие из Африки от 60 до 100 тысяч лет назад, были уже носителями ЦМВ, ВЭБ, ВПГ 1-го типа и ВПГ 2-го типа. Человек со времен афарского австралопитека инфицировался вирусами в раннем детстве в семьях с большим количеством детей; вирусы передавались контактным путем со слюной, в грудном молоке и пр. Под воздействием, в том числе, и герпетических вирусов как компонентов комменсальной микробиоты, передаваемой от матери, эволюционировала иммунная система человека [2].
В человеческой популяции герпетические вирусы распространены на протяжении тысячелетий. 24 ноября 1974 г. американским антропологом Д. Джохансоном в Великой рифтовой долине был обнаружен скелет афарского австралопитека Люси — предполагается, что это ветвь прародителей Homo sapiens [1]. Возраст Люси определен как 3,2–3,5 млн лет. В «слюне» Люси найдены три герпетических вируса — ЦМВ, вирус Эпштейна–Барр (ВЭБ), вирус простого герпеса 1-го типа (ВПГ 1-го типа). «Современные» люди, мигрировавшие из Африки от 60 до 100 тысяч лет назад, были уже носителями ЦМВ, ВЭБ, ВПГ 1-го типа и ВПГ 2-го типа. Человек со времен афарского австралопитека инфицировался вирусами в раннем детстве в семьях с большим количеством детей; вирусы передавались контактным путем со слюной, в грудном молоке и пр. Под воздействием, в том числе, и герпетических вирусов как компонентов комменсальной микробиоты, передаваемой от матери, эволюционировала иммунная система человека [2].
Характеристика возбудителя
ЦМВ — двухцепочечный ДНК-вирус, член семейства герпес-вирусов (β-герпесвирус человека). Синтез вирусного генома ДНК происходит в ядре клетки-хозяина. Исследования последних лет подтверждают гипотезу о том, что штаммы ЦМВ могут варьировать в их вирулентности, тропизме и патогенном потенциале, который, в свою очередь, вероятно, связан с генетической изменчивостью ключевых для патогенеза генов. Внешняя оболочка вируса содержит множественные гликопротеины, кодируемые вирусом. Гликопротеин B и гликопротеин H, по-видимому, являются основными факторами для формирования гуморального иммунитета — антитела к ним способны нейтрализовать вирус. Эти гликопротеины используют сегодня при разработке анти-ЦМВ-вакцин [3].
Синтез вирусного генома ДНК происходит в ядре клетки-хозяина. Исследования последних лет подтверждают гипотезу о том, что штаммы ЦМВ могут варьировать в их вирулентности, тропизме и патогенном потенциале, который, в свою очередь, вероятно, связан с генетической изменчивостью ключевых для патогенеза генов. Внешняя оболочка вируса содержит множественные гликопротеины, кодируемые вирусом. Гликопротеин B и гликопротеин H, по-видимому, являются основными факторами для формирования гуморального иммунитета — антитела к ним способны нейтрализовать вирус. Эти гликопротеины используют сегодня при разработке анти-ЦМВ-вакцин [3].
Патогенез
Вирус распространяется различными способами: через продукты крови (переливание, трансплантация органов), грудное вскармливание, пролиферацию в местах контактов (кожа, любые слизистые оболочки), перинатально и половым путем. ЦМВИ может протекать в виде первичной инфекции ранее неинфицированных (серонегативных) пациентов, реинфекции или реактивации у инфицированных (серопозитивных) людей; может вызывать острое, латентное и хроническое течение врожденных или приобретенных форм болезни [4].
При острой ЦМВ-инфекции могут поражаться практически все типы клеток человеческого организма — эндотелиальные клетки, эпителиальные клетки, клетки гладкой мускулатуры, фибробласты, нейронные клетки, гепатоциты, трофобласты, моноциты/макрофаги, дендритные клетки и пр. Все типы клеток поражаются и в мозге: нейроны, астроциты, клетки эпендимы, выстилающие желудочки, макроглия, эндотелий капилляров, оболочек, микроглия, сплетения сосудистой оболочки, дендриты и аксоны — т. е. вирус в мозге не имеет избирательной клеточной цели, что объясняет многообразие клинических форм поражения нервной системы у больных [5].
Считается, что ЦМВ реплицируется в эндотелиальных клетках с низкой скоростью, вызывая преимущественно подострые инфекции, однако истинная скорость репликации вируса в клетках определяется эффективностью цитотоксического Т-клеточного иммунитета и степенью иммуносупрессии хозяина. Так, например, на моделях ЦМВИ у животных продемонстрировано, что отсутствие CD4 Т-клеток сопровождалось более тяжелым и стремительным заболеванием ЦМВИ. Известно также, что ВИЧ-инфицированные новорожденные имеют очень высокую частоту врожденной ЦМВИ с высоким риском смерти, неврологических дефектов и прогрессии ВИЧ-инфекции [6–7].
Известно также, что ВИЧ-инфицированные новорожденные имеют очень высокую частоту врожденной ЦМВИ с высоким риском смерти, неврологических дефектов и прогрессии ВИЧ-инфекции [6–7].
Особое свойство ЦМВИ — способность вызывать депрессию практически всех звеньев иммунитета, резко угнетать продукцию интерферонов (ИНФ), в первую очередь ИНФ-α. Внедрение ЦМВ приводит к иммунной перестройке в виде снижения реакции лимфоцитов на вирусы в связи с угнетением экспрессии антигена макрофагами, подавлением пролиферативной активности лимфоцитов (что коррелирует с тяжестью болезни), угнетением фагоцитарной активности и завершенности фагоцитоза [7].
Доказано, что и первичные и латентные ЦМВИ сами могут индуцировать хронические воспалительные системные реакции с устойчивой иммунной активацией, запускать и поддерживать аутоиммунные процессы, усиливать аллореактивность Т-клеток после трансплантации и, возможно, участвовать в комплексе причин повышения частоты нейродегенеративных состояний с возрастом человека (Jones R.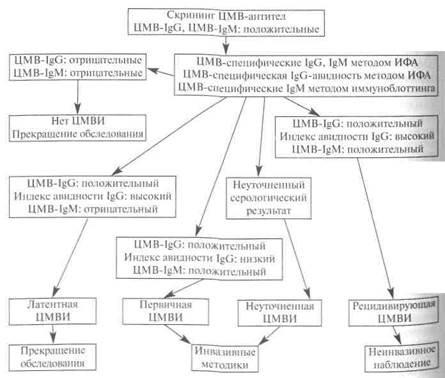 P. The debility cascade in neurological degenerative disease). Установлено также, что ЦМВ-индуцированные иммунные изменения в пожилом возрасте могут отвечать, например, за замедленную элиминацию вируса гриппа из легких, сниженный поствакцинальный иммунитет на гриппозные вакцины, измененную реакцию организма на терапию интерферонами [8].
P. The debility cascade in neurological degenerative disease). Установлено также, что ЦМВ-индуцированные иммунные изменения в пожилом возрасте могут отвечать, например, за замедленную элиминацию вируса гриппа из легких, сниженный поствакцинальный иммунитет на гриппозные вакцины, измененную реакцию организма на терапию интерферонами [8].
Многие годы риск развития врожденных инфекций плода ассоциировали преимущественно с первичной инфекцией матери, однако к настоящему моменту не вызывает сомнения, что большая доля врожденных ЦМВИ (до 75%) встречается в условиях рецидивирующей во время беременности материнской инфекции. Допускаются также и экзогенные реинфекции с новыми штаммами ЦМВ — доказательства основываются на молекулярных данных, подтверждающих получение нового штамма вируса.
Вместе с тем степень риска вертикального инфицирования плода в условиях первичной инфекции матери рассматривают по-прежнему как чрезвычайно высокую — в 30–50% случаев острой первичной инфекции беременной развивается врожденная инфекция ребенка. Показано, что ранее существовавший материнский иммунитет хоть и не гарантирует полной защиты, тем не менее обеспечивает снижение риска врожденной ЦМВИ при следующих беременностях на 69% [9].
Показано, что ранее существовавший материнский иммунитет хоть и не гарантирует полной защиты, тем не менее обеспечивает снижение риска врожденной ЦМВИ при следующих беременностях на 69% [9].
Недавними исследованиями установлено, что ЦМВ может поражать амниотическую мембрану, ухудшая цитотрофобласт-индуцированный лимфангиогенез и ремоделирование сосудов в плаценте и задерживая правильное развитие клеток — предшественников трофобласта, одновременно вызывает врожденную провоспалительную иммунную реакцию. Это приводит к гипоксии плода, задержке внутриутробного развития и возможным последующим гипоксическим повреждениям головного мозга. Степень поражения плода определяется сроками антенатального инфицирования и вирусной нагрузкой в размножающихся клетках — чем меньше гестационный возраст, тем более выражена альтерация (разрушение) тканей с формированием пороков развития [10]. Особенно быстро ЦМВ достигает максимума в астроцитарных и глиальных клетках, при этом максимальная экспрессия вируса найдена в глиальных клетках развивающегося мозга мышат (что объясняет микрогирию, микроцефалию и другие пороки ЦМВ-инфицированного мозга детей). По мере увеличения срока гестации в клинической картине инфекционного заболевания плода преобладают симптомы системного воспаления с выраженной пролиферацией и экссудацией. У 1/3 умерших от ЦМВИ новорожденных (из них 60% — недоношенные) при морфологическом исследовании выявляют различные пороки развития. У 43% — признаки генерализованной внутриутробной инфекции с геморрагическими и ишемическими инфарктами (в том числе в головном и спинном мозге) [11].
По мере увеличения срока гестации в клинической картине инфекционного заболевания плода преобладают симптомы системного воспаления с выраженной пролиферацией и экссудацией. У 1/3 умерших от ЦМВИ новорожденных (из них 60% — недоношенные) при морфологическом исследовании выявляют различные пороки развития. У 43% — признаки генерализованной внутриутробной инфекции с геморрагическими и ишемическими инфарктами (в том числе в головном и спинном мозге) [11].
Клиника ЦМВИ
Способность вируса реплицироваться в любых клетках человеческого организма определяет многообразие клинических форм болезни; ЦМВ может вызывать как генерализованные инфекции, так и поражения отдельных органов: печени, головного мозга, сердца, легких, мочеполовых органов, желудочно-кишечного тракта и др.
У беременных острая первичная ЦМВИ протекает чаще бессимптомно (25–50%) или малосимптомно — с неспецифическими проявлениями (обычно лихорадка, астения и головная боль).
Как первичная, так и рецидивирующая ЦМВИ матери может стать причиной антенатальных ультразвуковых признаков поражения плода в результате трансплацентарной инфекции. Самые частые УЗИ-признаки: задержка роста плода, вентрикуломегалия, микроцефалия, перивентрикулярная гиперэхогенность, кальцификаты в мозге, плевральный выпот или асцит, гепатоспленомегалия, гиперэхогенный кишечник и мекониальный илеус и др. Эти УЗИ-аномалии эмбриона прогнозируют тяжелую генерализованную манифестную врожденную ЦМВИ новорожденного с высоким риском формирования инвалидизирующих исходов болезни и смерти. Поэтому первичная острая ЦМВИ во время беременности может являться показанием к ее искусственному прерыванию. Установлено, что около 4% детей с антенатальной ЦМВИ умрут в утробе матери или вскоре после рождения, среди остальных около 60% будут иметь когнитивные дефекты, нейросенсорную потерю слуха и другие неврологические и прочие проблемы [11–12].
Самые частые УЗИ-признаки: задержка роста плода, вентрикуломегалия, микроцефалия, перивентрикулярная гиперэхогенность, кальцификаты в мозге, плевральный выпот или асцит, гепатоспленомегалия, гиперэхогенный кишечник и мекониальный илеус и др. Эти УЗИ-аномалии эмбриона прогнозируют тяжелую генерализованную манифестную врожденную ЦМВИ новорожденного с высоким риском формирования инвалидизирующих исходов болезни и смерти. Поэтому первичная острая ЦМВИ во время беременности может являться показанием к ее искусственному прерыванию. Установлено, что около 4% детей с антенатальной ЦМВИ умрут в утробе матери или вскоре после рождения, среди остальных около 60% будут иметь когнитивные дефекты, нейросенсорную потерю слуха и другие неврологические и прочие проблемы [11–12].
Сегодня установлено также, что нейросенсорная тугоухость является прогрессирующим заболеванием и может формироваться в течение 5–6 лет жизни даже у детей, родившихся с бессимптомной ЦМВИ (это связывают с многолетней репликацией ЦМВ в перилимфе), что требует соответствующей длительности наблюдения ребенка.
У новорожденного антенатальная ЦМВИ проявляется симптомами «тяжелой инфекции» с полисистемным поражением: задержкой внутриутробного развития, часто — недоношенностью, гепатоспленомегалией, затяжной неконъюгационной и конъюгационной желтухой, тромбоцитопенической пурпурой, анемией, ДВС-синдромом с кровоизлиянием во внутренние органы, прежде всего в мозг, пневмонией, микроцефалией, хориоретинитом, увеитом, кардитом, различными вариантами поражения центральной нервной системы, в том числе продуктивным вентрикулоэнцефалитом с прогрессирующей гидроцефалией, а также — кортикальными или мозжечковыми пороками развития [13]. В дальнейшем этим детям присущи недостаточная прибавка веса, задержки психического и моторного развития, мышечная слабость, часто — длительная субфебрильная температура, стойкая анемия и тромбоцитопения, длительный гепатит с холестатическим синдромом и высоким риском фиброза и цирроза печени, мальабсорбция.
При инфицировании в поздние сроки гестации ЦМВИ у новорожденного может проявляться и как генерализованная инфекция, и как поражение отдельных органов с нетяжелыми транзиторными симптомами болезни, например, умеренной гепатомегалией, изолированным снижением количества тромбоцитов или повышенным уровнем аланинаминотрансферазы. Возможна и клинически бессимптомная ЦМВИ с изолированной нейросенсорной тугоухостью.
Возможна и клинически бессимптомная ЦМВИ с изолированной нейросенсорной тугоухостью.
У 10% всех новорожденных в течение первого месяца жизни возникают инфекционные заболевания в результате в основном семейных контактов, в том числе грудного вскармливания. Экскреция ЦМВ с грудным молоком в течение первых недель после родов бывает низкой, достигает максимума к 4–8 неделям, завершается к 9–12 неделям. Считается, что риск трансмиссии вируса коррелирует с вирусной нагрузкой в молоке, передача максимальна при высокой экскреции. У доношенных детей в результате инфицирования ЦМВ через молоко матери формируется, как правило, субклиническое течение инфекции без остаточных явлений; в клинической картине более вероятно развитие энтероколита и транзиторного холестатического гепатита с минимальным цитолизом. Недоношенные дети (вес < 1000 г, срок гестации — < 30 недель) имеют более высокий риск инфицирования с риском развития острой ЦМВИ с полисистемным поражением (сепсис-подобные формы) и формированием распространенного эрозивно-язвенного поражения кишечника. Интересно, что отдаленные исходы ЦМВИ, приобретенных с грудным молоком матери, как правило, благоприятные — без когнитивных нарушений и нейросенсорной тугоухости.
Интересно, что отдаленные исходы ЦМВИ, приобретенных с грудным молоком матери, как правило, благоприятные — без когнитивных нарушений и нейросенсорной тугоухости.
Приобретенная ЦМВИ даже в раннем возрасте протекает чаще в виде субклинической (малосимптомной) формы или в виде бессимптомной сероконверсии. Считается, что только 10–15% детей развивают манифестные формы заболевания в виде локального или генерализованного лимфопролиферативного синдрома в сочетании с длительным катаральным синдромом и различными органными поражениями: гепатит, энтероколит, энцефалит, множественные мононейропатии, пневмония, кардит, ретинит и пр.
Независимо от возраста, в котором развивается приобретенная ЦМВИ в клинической картине, возможны длительная преимущественно субфебрильная лихорадка, стойкий астенический синдром, лимфаденопатия (чаще цервикальная), гепато- и спленомегалия, гепатит с минимальной степенью активности цитолитического синдрома, дерматиты, васкулиты, интерстициальный пневмонический процесс, тромбоцитоз или тромбоцитопения, лимфомоноцитоз,
У пожилых пациентов ЦМВ может вызывать тяжелые инфекции с развитием стойкой лихорадки, экзантемы, гепатита, поражения желудочно-кишечного тракта, центральной и периферической нервной системы, органов дыхания, почек.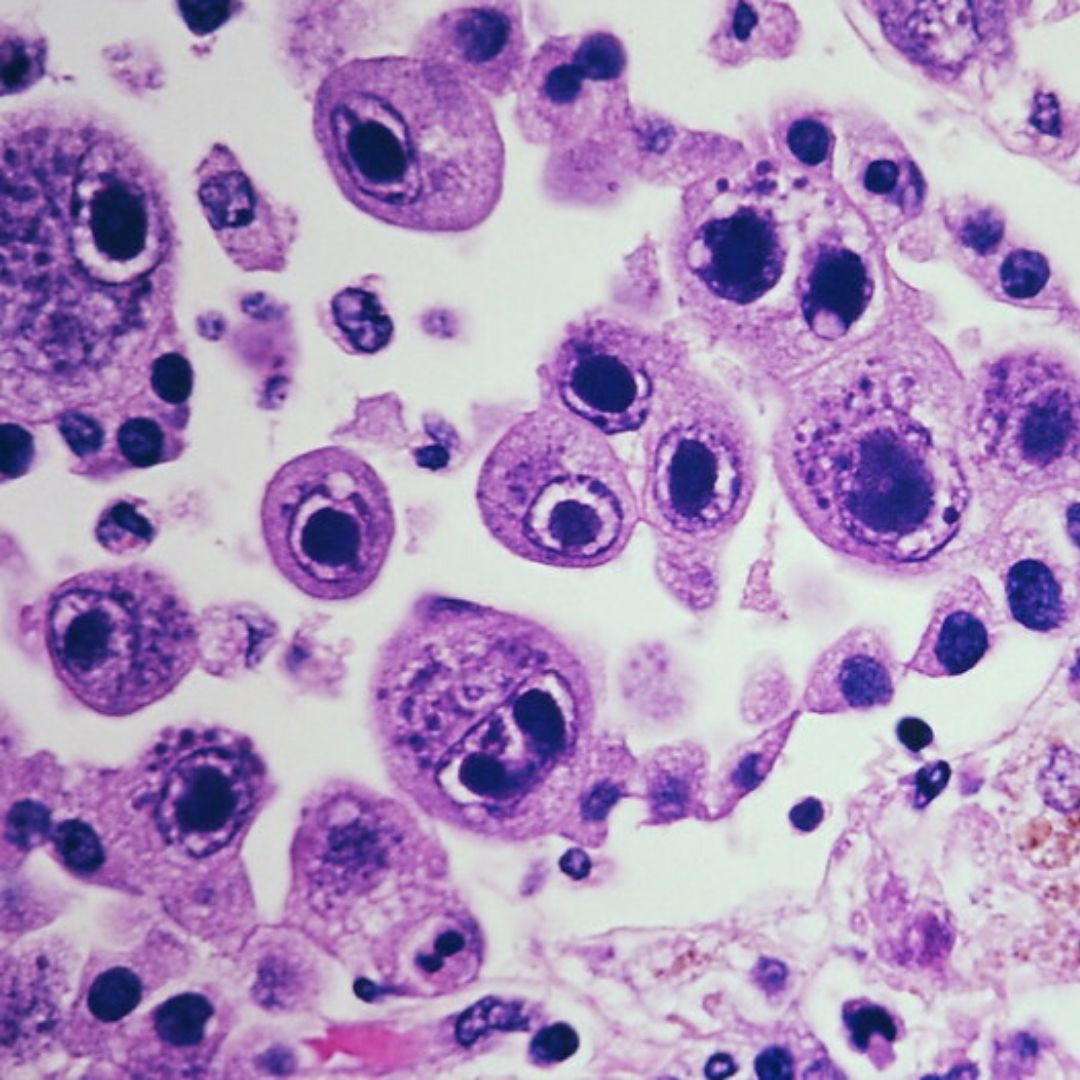 В иностранной литературе принят диагноз «синдром лихорадящей бабушки» (Feverish granny syndrome) — ЦМВИ женщин старшего возраста, заражающихся от собственных внуков [14].
В иностранной литературе принят диагноз «синдром лихорадящей бабушки» (Feverish granny syndrome) — ЦМВИ женщин старшего возраста, заражающихся от собственных внуков [14].
Диагностика ЦМВИ
Скрининг всех беременных для выявления ЦМВ серонегативных пациенток не является обязательным ни в одной стране мира, это связано с различными экономическими, практическими и юридическими причинами. Однако выборочные обследования отдельных беременных проводятся во всех странах. В случае наличия у беременной исходных данных серологического исследования до наступления беременности идеально провести сравнение данных иммуноферментным анализом (ИФА). Диагностика первичной инфекции у беременных женщин выполняется прежде всего с целью своевременного выявления и прогноза ЦМВИ плода. «Золотым стандартом» является определение анти-ЦМВ IgG с низкой авидностью в крови матери и обнаружение с количественной оценкой вируса в амниотической жидкости с помощью полимеразной цепной реакции (ПЦР) в реальном времени [15].
В последнее время много дискуссий вызывают рекомендации по определению анти-ЦМВ IgМ в крови матери и новорожденного, исследование ПЦР в материнской крови, моче и амниотической жидкости, а также сама инвазивная процедура амниоцентеза, которая может привести к разрыву мембран, внутриутробному инфицированию или выкидышу. Показано, например, что истинная первичная ЦМВИ диагностируется только у 20–25% беременных женщин с положительными результатами на анти-ЦМВ IgM. Это связано с тем, что анти-ЦМВ IgM могут сохраняться в течение 6–9 месяцев после первичной инфекции, а также могут быть обнаружены при латентной реактивации. На практике редко удается отследить и истинную сероконверсию. С другой стороны, результаты ПЦР и антигенных анализов в материнской крови и моче не коррелируют с риском врожденной инфекции или тяжестью заболевания плода. В 2016 г. японскими учеными предложен неинвазивный подход к прогнозированию врожденной ЦМВИ плода. Проанализировав данные лабораторного и инструментального обследования 300 анти-ЦМВ IgM позитивных беременных женщин, они установили, что наиболее результативным является выявление УЗИ признаков аномалий внутриутробного развития плода в сочетании с положительными результатами ПЦР секрета шейки матки беременной. В этом случае, по мнению исследователей, врачи имеют возможность начать раннее противовирусное лечение новорожденного и таким образом улучшить неврологический прогноз врожденной ЦМВИ.
В этом случае, по мнению исследователей, врачи имеют возможность начать раннее противовирусное лечение новорожденного и таким образом улучшить неврологический прогноз врожденной ЦМВИ.
Однако не вызывает сомнения факт, что одновременное использование анти-ЦМВ IgM вместе с анти-ЦМВ IgG с низкой авидностью улучшает раннюю диагностику первичной инфекции матери еще до появления УЗИ-признаков и при положительном результате указывает на более высокий риск развития врожденной ЦМВИ — это важно особенно в срок до 12–16 недель гестации [15–18].
Согласно Консенсусу 2017, обследование на анти-ЦМВ IgG, IgM и IgA должно быть предложено беременной женщине при наличии гриппоподобных симптомов (как правило, лихорадка, астения и головная боль), не связанных с какой-то конкретной инфекцией, или когда результаты визуализации (УЗИ или МРТ) подозрительны на врожденную инфекцию плода (уровень доказательности 3). Для ЦМВ-серонегативных беременных женщин диагностика первичной ЦМВИ должна включать обнаружение анти-ЦМВ IgG в сыворотке (уровень доказательности 2b). Когда иммунный статус до беременности неизвестен, диагноз первичной ЦМВИ матери должен основываться на обнаружении анти-ЦМВ IgM и анти-ЦМВ IgG с низкой авидностью (уровень доказательности 2b) [19].
Когда иммунный статус до беременности неизвестен, диагноз первичной ЦМВИ матери должен основываться на обнаружении анти-ЦМВ IgM и анти-ЦМВ IgG с низкой авидностью (уровень доказательности 2b) [19].
Диагностика подтвержденной ЦМВИ плода, согласно Консенсусу 2017, может быть выполнена после 20–21 недели гестации или, по крайней мере, через 6 недель с момента диагностики материнской инфекции, путем тестирования амниотической жидкости на ДНК ЦМВ с помощью ПЦР в реальном времени (уровень доказательности 2b) [19].
Диагностика ЦМВИ новорожденного имеет свои особенности: серологические исследования информативны редко и особенно при манифестной клинике, так как врожденная иммунная система ко времени требуемого серологического ответа еще не эффективна, и отсутствие специфических фетальных IgM даже на фоне острой тяжелой ЦМВИ («серологическая ниша») — общая черта этого периода, они начинают продуцироваться только через несколько месяцев. Специфическая детекция инфекции у детей возможна только с помощью культуральных исследований или ПЦР. Диагноз врожденной ЦМВИ требует положительного результата слюны и/или мочи на ПЦР в первые 21 день жизни (пуповинную кровь не исследуют, так как она может быть контаминирована). Рекомендуется забирать материал на исследование так быстро, как возможно, идеально — в первые 24 часа жизни. При наличии признаков инфекции с полисистемным вовлечением этих данных ПЦР бывает достаточно для принятия решения о начале специфической противовирусной терапии. В диагностически сложных ситуациях, а также для мониторинга эффективности терапии ЦМВИ информативно выполнение ПЦР в реальном времени в стерильных средах (ликвор, кровь, биопсийный материал) с оценкой вирусной нагрузки ДНК ЦМВ в динамике.
Диагноз врожденной ЦМВИ требует положительного результата слюны и/или мочи на ПЦР в первые 21 день жизни (пуповинную кровь не исследуют, так как она может быть контаминирована). Рекомендуется забирать материал на исследование так быстро, как возможно, идеально — в первые 24 часа жизни. При наличии признаков инфекции с полисистемным вовлечением этих данных ПЦР бывает достаточно для принятия решения о начале специфической противовирусной терапии. В диагностически сложных ситуациях, а также для мониторинга эффективности терапии ЦМВИ информативно выполнение ПЦР в реальном времени в стерильных средах (ликвор, кровь, биопсийный материал) с оценкой вирусной нагрузки ДНК ЦМВ в динамике.
В отличие от того, что в настоящее время не рекомендуется обязательный скрининг всех беременных женщин на ЦМВИ, международная группа экспертов считает необходимым проведение скрининга на ЦМВИ у всех новорожденных. И особенно важно проведение такого скрининга у всех детей с глухотой. Согласно Консенсусу 2017, диагноз врожденной ЦМВИ у новорожденных требует проведения ПЦР в реальном времени в слюне и/или моче как можно скорее после рождения, но не позднее первых 3 недель жизни, при этом предпочтительно исследование слюны (уровень доказательности 2b). У детей старше 3-недельного возраста отличить врожденную от постнатальной ЦМВИ с помощью ПЦР и ИФА практически невозможно [19–20].
У детей старше 3-недельного возраста отличить врожденную от постнатальной ЦМВИ с помощью ПЦР и ИФА практически невозможно [19–20].
В случае проведения серологического обследования ребенка требуется одновременное серологическое обследование и матери. Поступательное снижение уровня IgG и его исчезновение к 6–9-месячному возрасту при отрицательной ПЦР свидетельствуют об имевшихся у ребенка материнских трансплацентарных антителах (пассивный специфический транзиторный иммунитет) и неинфицированности.
Диагностика острой ЦМВИ в других возрастных группах проводится по общим принципам — выявление острофазовых анти-ЦМВ IgM, низкоавидных анти-ЦМВ IgG с последующей сероконверсией, а также детекция вирусного генома в ПЦР и/или антигенов вируса в ИФА в исследуемых материалах от больного.
Применение анти-ЦМВ-иммуноглобулина с целью предотвращения вертикальной передачи ЦМВ от инфицированной матери к плоду
Специфический анти-ЦМВ-иммуноглобулин неоднократно пытались использовать с целью профилактики ЦМВИ плода, однако результаты этих исследований не однозначные и не окончательные. Несмотря на сообщения о возможной эффективности, в настоящее время не определены ни оптимальные дозы, ни схемы лечения. Опубликованы результаты рандомизированного исследования, в котором не найдено никакой значимой пользы от введения иммуноглобулина, но выявлены акушерские осложнения (преждевременные роды, преэклампсия, задержка роста плода) у 7 (13%) из 53 женщин в группе, получавшей ЦМВ-иммуноглобулин (в сравнении с 1 (2%) из 51 женщины в группе плацебо). Рандомизированные исследования эффективности ЦМВ-иммуноглобулина у беременных в настоящее время в мире продолжаются. Согласно рекомендациям Консенсуса 2017, анти-ЦМВ-иммуноглобулин не следует вводить беременным женщинам с первичной ЦМВИ для профилактики врожденной инфекции плода в связи недостаточностью доказательств (уровень доказательности 2c). Если же такое лечение проводится, результаты следует отслеживать для дальнейшего понимания безопасности этого подхода [19, 21–23].
Несмотря на сообщения о возможной эффективности, в настоящее время не определены ни оптимальные дозы, ни схемы лечения. Опубликованы результаты рандомизированного исследования, в котором не найдено никакой значимой пользы от введения иммуноглобулина, но выявлены акушерские осложнения (преждевременные роды, преэклампсия, задержка роста плода) у 7 (13%) из 53 женщин в группе, получавшей ЦМВ-иммуноглобулин (в сравнении с 1 (2%) из 51 женщины в группе плацебо). Рандомизированные исследования эффективности ЦМВ-иммуноглобулина у беременных в настоящее время в мире продолжаются. Согласно рекомендациям Консенсуса 2017, анти-ЦМВ-иммуноглобулин не следует вводить беременным женщинам с первичной ЦМВИ для профилактики врожденной инфекции плода в связи недостаточностью доказательств (уровень доказательности 2c). Если же такое лечение проводится, результаты следует отслеживать для дальнейшего понимания безопасности этого подхода [19, 21–23].
Преимущества и вред противовирусных препаратов для предотвращения вертикальной передачи у беременных женщин исследованы мало. В настоящее время в одном рандомизированном, двойном слепом клиническом исследовании продолжается оценка эффективности валацикловира для предотвращения вертикальной передачи ЦМВ при первичной инфекции матери. Результаты этого исследования могут предоставить доказательства безопасности и эффективности противовирусной терапии во время беременности. Согласно же современным рекомендациям Консенсуса 2017, противовирусная терапия для предотвращения врожденной ЦМВИ плода также не рекомендуется на основе недостаточности текущих данных (уровень доказательности 3) [19].
В настоящее время в одном рандомизированном, двойном слепом клиническом исследовании продолжается оценка эффективности валацикловира для предотвращения вертикальной передачи ЦМВ при первичной инфекции матери. Результаты этого исследования могут предоставить доказательства безопасности и эффективности противовирусной терапии во время беременности. Согласно же современным рекомендациям Консенсуса 2017, противовирусная терапия для предотвращения врожденной ЦМВИ плода также не рекомендуется на основе недостаточности текущих данных (уровень доказательности 3) [19].
Антенатальное лечение врожденной ЦМВИ плода
Такие препараты, как ганцикловир, валганцикловир, фоскарнет, цидофовир, доказано эффективны в лечении ЦМВИ у пациентов с ослабленным иммунитетом. Однако фоскарнет и цидофовир непригодны для лечения во время беременности, так как нефротоксичны и потенциально канцерогенны. Данные же о безопасности и эффективности ганцикловира и валганцикловира при беременности ограничены: опубликованы результаты применения ганцикловира у беременных реципиентов трансплантаций и у пациентки с ВИЧ/СПИДом — в обоих случаях тератогенных эффектов выявлено не было [24, 25]. Тем не менее из-за результатов исследования на животных (риск гонадного дисгенеза и нейтропении у плода) ганцикловир в настоящее время не рекомендуется для использования во время беременности. Результаты двух небольших наблюдательных исследований с выявленной низкой частотой неблагоприятных эффектов при беременности и слабой анти-ЦМВ-активностью стали основой для применения у беременных ацикловира и валацикловира в качестве профилактики ЦМВИ плода. Предполагается, что лечение валацикловиром может способствовать снижению вирусной нагрузки ЦМВ в фетальной крови, хотя окончательный результат пока не ясен [26–27]. Согласно консенсусу 2017, противовирусная терапия для предотвращения или лечения врожденной ЦМВИ плода также не рекомендуется в связи с недостаточными доказательствами безопасности и эффективности (уровень доказательности 2c).
Тем не менее из-за результатов исследования на животных (риск гонадного дисгенеза и нейтропении у плода) ганцикловир в настоящее время не рекомендуется для использования во время беременности. Результаты двух небольших наблюдательных исследований с выявленной низкой частотой неблагоприятных эффектов при беременности и слабой анти-ЦМВ-активностью стали основой для применения у беременных ацикловира и валацикловира в качестве профилактики ЦМВИ плода. Предполагается, что лечение валацикловиром может способствовать снижению вирусной нагрузки ЦМВ в фетальной крови, хотя окончательный результат пока не ясен [26–27]. Согласно консенсусу 2017, противовирусная терапия для предотвращения или лечения врожденной ЦМВИ плода также не рекомендуется в связи с недостаточными доказательствами безопасности и эффективности (уровень доказательности 2c).
Лечение ЦМВИ новорожденных
Несмотря на токсичность противовирусных анти-ЦМВ препаратов при развитии у ребенка угрожающей жизни манифестной генерализованной ЦМВИ применение ганцикловира и валганцикловира показано и необходимо после обязательного предварительного анализа риска и пользы. Ганцикловир впервые применен в лечении новорожденных в конце 1980-х гг.; в последующем было многократно показано, что в целом он безопасен, хорошо переносится детьми и эффективен особенно при ЦМВ-поражении центральной нервной системы и глаз. Препарат назначается в дозе 5–6 мг/кг два раза в день в среднем в течение 6 недель. Ограничения применения ганцикловира на практике связаны не столько с токсичностью, сколько с необходимостью постоянных катетеров для его инфузии. Альтернативой к инвазивному использованию ганцикловира стало введение валганцикловира, рандомизированное исследование эффективности которого завершено в 2015 г. [28]. Согласно Консенсусу 2017, лечение валганцикловиром (моновалиловый эфир — пролекарство ганцикловира с высокой пероральной биодоступностью) показано детям со среднетяжелой врожденной ЦМВИ — 16 мг/кг 2 раза в сутки, до (но не более) 6 месяцев [19, 28]. Во время лечения обязателен контроль нейтрофилов (еженедельно до 6 недель, затем на 8-й неделе, затем ежемесячно) и трансаминаз (ежемесячно).
Ганцикловир впервые применен в лечении новорожденных в конце 1980-х гг.; в последующем было многократно показано, что в целом он безопасен, хорошо переносится детьми и эффективен особенно при ЦМВ-поражении центральной нервной системы и глаз. Препарат назначается в дозе 5–6 мг/кг два раза в день в среднем в течение 6 недель. Ограничения применения ганцикловира на практике связаны не столько с токсичностью, сколько с необходимостью постоянных катетеров для его инфузии. Альтернативой к инвазивному использованию ганцикловира стало введение валганцикловира, рандомизированное исследование эффективности которого завершено в 2015 г. [28]. Согласно Консенсусу 2017, лечение валганцикловиром (моновалиловый эфир — пролекарство ганцикловира с высокой пероральной биодоступностью) показано детям со среднетяжелой врожденной ЦМВИ — 16 мг/кг 2 раза в сутки, до (но не более) 6 месяцев [19, 28]. Во время лечения обязателен контроль нейтрофилов (еженедельно до 6 недель, затем на 8-й неделе, затем ежемесячно) и трансаминаз (ежемесячно). Аудиологическое обследование необходимо проводить 1 раз в 6 месяцев — до 3 лет, затем — в подростковом возрасте (10–12 лет). Противовирусная терапия не рекомендована новорожденным с бессимптомной и легкой врожденной ЦМВИ, а также с изолированной сенсоневральной глухотой [29].
Аудиологическое обследование необходимо проводить 1 раз в 6 месяцев — до 3 лет, затем — в подростковом возрасте (10–12 лет). Противовирусная терапия не рекомендована новорожденным с бессимптомной и легкой врожденной ЦМВИ, а также с изолированной сенсоневральной глухотой [29].
Отношение к грудному вскармливанию
ЦМВ был впервые выделен из грудного молока матери в 1967 г., длительное время трансмиссия вируса в молоке рассматривалась как естественная иммунизация без развития клинически значимых форм ЦМВИ. С течением времени выяснилось, что проблему может составлять грудное вскармливание младенцев с экстремально низким весом при рождении (менее 1500 г). Сегодня при выборе вскармливания рекомендовано учитывать, что потенциальные преимущества материнского молока превышают риск развития острой ЦМВИ. Замораживание и пастеризация грудного молока могут снизить риск передачи вируса; при этом кратковременная пастеризация (5 с, 62 °C) оказалась более эффективной, чем замораживание [30].
Профилактика ЦМВИ матери и ребенка
Вакцинация: несколько ЦМВ-вакцин находятся сегодня в фазе клинических испытаний, завершение которых ожидается между 2017 и 2019 гг. Эффективность рекомбинантной ЦМВ-вакцины против гликопротеина В была исследована у серонегативных женщин, продемонстрировав 50% эффективность в достижении сероконверсии. Однако долгосрочная эффективность этой вакцины вызывает много вопросов, в связи с поступательным ослаблением приобретенного иммунитета. Близкие результаты получены и у подростков, в рандомизированном, двойном слепом, плацебо-контролируемом исследовании фазы 2 этой вакцины [31].
Гигиеническая профилактика ЦМВИ у беременных
Фактор высокого риска инфицирования беременных женщин — контакт с инфицированными детьми первых лет жизни, которые могут длительно выделять ЦМВ в слюне и моче. В многочисленных исследованиях показано, что только изменение гигиенических поведенческих навыков с уменьшением контактов беременной женщины с инфицированными жидкостями (моча, слюна, кровь) детей раннего возраста сокращают частоту сероконверсии к ЦМВ, а значит, и риск врожденной ЦМВИ плода. Согласно Консенсусу 2017, все медицинские работники должны обладать знаниями о ЦМВИ и ее профилактике. Учитывая потенциальный риск врожденной ЦМВИ у беременных, все беременные женщины должны получать информацию о ЦМВИ и ее профилактике [19, 29].
Заключение
Клиническая диагностика ЦМВИ представляет большие трудности. При наличии у ребенка клиники врожденной инфекции с поражением разных органов и систем в план дифференциально-диагностического поиска необходимо включать обследование на ЦМВИ. При этом большое значение имеют анамнестические данные (мать — плод), результаты клинических и инструментальных методов обследования, патоморфологические исследования плаценты, плодных оболочек, пуповины. Выявление в крови и/или моче ДНК ЦМВ в высокой или средней концентрации методом ПЦР в сочетании с определением специфических IgM (у новорожденных выявляются редко) и низкоавидных IgG методом ИФА. Применение противовирусных препаратов с доказанной клинической эффективностью — ганцикловира и валганцикловира показано детям с тяжелой ЦМВИ при угрозе для жизни и при высокой вероятности потери функции органов.
Литература
- Grose С., Johanson D. C. Transmission of Cytomegalovirus, Epstein–Barr Virus, and Herpes Simplex Virus Infections: From the Lucy Australopithecus Epoch to Modern-Day Netherlands // The Journal Of Pediatrics. 2016, vol. 170. www.jpeds.com.
- Rook G. A. W., Raison C. L., Lowry C. A. Microbial ‘old friends’, immunoregulation and socioeconomic status // Clinical and Experimental Immunology. 2014; 177: 1–12.
- Gandhi M. K., Khanna R. Human cytomegalovirus: clinical aspects, immune regulation, and emerging treatments // Lancet Infect Dis. 2004; 4: 725–738.
- Gossman W. G., Bhimji S. S. Cytomegalovirus. [Updated 2017 Oct 22]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2017.
- Jun van den Pol A. N. Cytomegalovirus Cell Tropism, Replication, and Gene Transfer in Brain // The Journal of Neuroscience. 1999, 19 (24): 10948–10965.
- Kallemeijn1 M. J., Boots А. M. H., van der Klift1 M. Y. et al. Ageing and latent CMV infection impact on maturation, differentiation and exhaustion profiles of T-cell receptor gamma-delta T-cells. www.nature.com/scientificreports2017.
- Юлиш Е. И. Цитомегаловирусная инфекция у детей: подходы к лечению при различном течении инфекционного процесса // Здоровье ребенка. 2015, 4 (64).
- Jones R. P., Goldeck D. Unexpected and unexplained increase in death due to neurological disorders in 2012 in England and Wales: Is cytomegalovirus implicated? // Medical Hypotheses. 2014, 83, 25–31.
- Schleiss M. R. Congenital Cytomegalovirus Infection: Improved Understanding of Maternal Immune Responses That Reduce the Risk of Transplacental Transmission // Clinical Infectious Diseases. 2017, vol. 65, Issue 10, p. 1666–1669. https://doi.org/10.1093/cid/cix626.
- Emery V. C., Lazzarotto T. Cytomegalovirus in pregnancy and the neonate [version 1; referees: 2 approved] // F1000 Research. 2017, 6 (F1000 Faculty Rev): 138. DOI: 10.12688/f1000 research.10276.1.
- Dreher A. M., Arora N., Fowler K. B. et al. Spectrum of Disease and Outcome in Children with Symptomatic Congenital Cytomegalovirus Infection // J Pediatr. 2014. http://dx.doi.org/10.1016/j.jpeds.2013.12.007.
- Malinger G., Lev D., Lerman-Sagie T. Imaging of fetal cytomegalovirus infection // Fetal Diagn Ther. 2011; 29 (2): 117–126.
- Lazzarotto T., Guerra B., Gabrielli L., Lanari M., Landini M. P. Update on the prevention, diagnosis and management of cytomegalovirus infection during pregnancy // Clin Microbiol Infect: the official publication of the European Society of Clinical Microbiology and Infectious Diseases. 2011; 17 (9): 1285–1293.
- McGregor Alastair. Diagnostics in fever of unknown origin — an introduction. Новости с конгресса ECCMID 2017. Сессия «Встреча с экспертом», 23 апреля 2017.
- Toriyabe K., Morikawa F., Minematsu T. Anti-cytomegalovirus immunoglobulin M titer for congenital infection in first-trimester pregnancy with primary infection: a multicenter prospective cohort study // Journal of Perinatology, 2017, 12 October. DOI: 10.1038/jp.2017.133.
- Tanimura К., Tairaku S. et al. Prediction of congenital cytomegalovirus infection in high-risk pregnant women // Clin Infect Dis. 2017; 64 (2): 159–165. DOI: https://doi.org/10.1093/cid/ciw707.
- Tanimura K., Tairaku S., Morioka I. et al. Universal screening with use of IgG avidity for congenital cytomegalovirus infection // Clin Infect Dis. 2017; 65 (10). https://doi.org/10.1093/cid/cix626.
- Sonoyama A., Ebina Y., Morioka I. et al. Low IgG avidity and ultrasound fetal abnormality predict congenital cytomegalovirus infection // J Med Virol. 2012; 84 (12): 1928–1933.
- Rawlinson W. D., Boppana S. B., Fowler K. B., Kimberlin D. W. et al. Congenital cytomegalovirus infection in pregnancy and the neonate: consensus recommendations for prevention, diagnosis, and therapy // Lancet Infect Dis. 2017. http://dx.doi.org/10.1016/S1473–3099 (17)30143–3.
- Nishida K., Morioka I., Nakamachi Y. et al. Neurological outcomes in symptomatic congenital cytomegalovirus-infected infants after introduction of newborn urine screening and antiviral treatment // Brain Dev. 2016; 38 (2): 209–216.
- Nigro G., Capretti I., Manganello A. M., Best A. M., Adler S. P. Primary maternal cytomegalovirus infections during pregnancy: association of CMV hyperimmune globulin with gestational age at birth and birth weight // J Matern Fetal Neonatal Med. 2015; 28: 1–4.
- Revello M. G. et al. A randomized, phase 2 trial of prevention of congenital cytomegalovirus // N Engl J Med. 2014, Apr 2; 370: 1316. http://dx.doi.org/10.1056/NEJMoa1310214.
- Blázquez-Gamero D. et al. Prevention and treatment of fetal cytomegalovirus infection with cytomegalovirus hyperimmune globulin: a multicenter study in Madrid // The Journal of Maternal-Fetal & Neonatal Medicine. 2017, Oct, р. 1–9. http://dx.doi.org/10.1080/14767058.2017.1387890.
- Puliyanda D. P., Silverman N. S., Lehman D. et al. Successful use of oral ganciclovir for the treatment of intrauterine cytomegalovirus infection in a renal allograft recipient // Transpl Infect Dis. 2005; 7: 71–74.
- Brandy R. C., Schleiss M. R., Witte D. P., Siddiqi T. A., Fame P. T. Placental transfer of ganciclovir in a woman with acquired immunodeficiency syndrome and cytomegalovirus disease // Pediatr Infect Dis. J. 2002; 21: 796–797.
- Jacquemard F., Yamamoto M., Costa J. M. et al. Maternal administration of valaciclovir in symptomatic intrauterine cytomegalovirus infection // BJOG. 2007; 114: 1113–1121.
- Leruez-Ville M., Ghout I., Bussieres L. et al. In utero treatment of congenital cytomegalovirus infection with valacyclovir in a multicenter, open-label, phase II study // Am J Obstet Gynecol. 2016; 215: 462 e1–462.
- Kimberlin D. W, Jester P. M, Sanchez P. J. et al. Valganciclovir for symptomatic congenital cytomegalovirus disease // N Engl J Med. 2015; 372: 933–943.
- Marsico С., Kimberlin D. W. Congenital Cytomegalovirus infection: advances and challenges in diagnosis, prevention and treatment // Italian Journal of Pediatrics. 2017, 43: 38.
- Hamprecht К., Goelz R. Postnatal Cytomegalovirus Infection Through Human Milk in Preterm Infants // Clinics in Perinatology. 2016, vol. 44, is. 1, p. 121–130.
- Schleiss M. R., Permar S. R., Plotkin S. A. Progress Toward Development of a Vaccine Against Congenital Cytomegalovirus Infection // Clin. Vaccine Immunol. 2017. DOI: 10.1128/CVI.00268–17.
И. Я. Извекова1, доктор медицинских наук, профессор
М. А. Михайленко
Е. И. Краснова, доктор медицинских наук, профессор
ФГБОУ ВО НГМУ МЗ РФ, Новосибирск
1 Контактная информация: [email protected]
Цитомегаловирусная инфекция в практике врача: современный алгоритм диагностики и лечения/ И. Я. Извекова, М. А. Михайленко, Е. И. Краснова
Для цитирования: Лечащий врач № 4/2018; Номера страниц в выпуске: 90-95
Теги: новорожденные, беременность, инфекция, персистирование
Цитомегаловирусная инфекция. Симптомы и диагностика.
Цитомегаловирусная инфекция (цитомегалия) — распространенное инфекционное заболевание, которое может долго не проявляться либо вызвать поражение внутренних органов и центральной нервной системы. Распространение цитомегаловируса может происходить через сперму, слюну, кровь, грудное молоко. Поэтому инфицирование возможно при любом тесном контакте: при поцелуе и во время полового акта, а также в быту при использовании одной посуды, зубной щетки и предметов гигиены. Заражение происходит при длительном контакте с инфицированным человеком. Возможна передача цитомегаловируса при переливании инфицированной крови или трансплантации инфицированного органа. Ребенок может заразиться от матери через плаценту во время беременности, во время родов или через грудное молоко.
Проявления
Цитомегаловирус, попав в организм, остается в нем навсегда. Обычно вирус бездействует, находится в неактивном состоянии и может длительное время никак себя не проявлять. Если по каким-либо причинам произошел сбой иммунной системы, тогда вирус активизируется и развивается цитомегалия разной степени тяжести. Тяжелая форма заболевания возникает у ВИЧ-инфицированных, у больных СПИДом, при химиотерапии у онкобольных, а также у перенесших трансплантацию органов. Во время беременности, когда отмечается снижение иммунитета, цитомегаловирус начинает активно размножаться, проникать через плаценту и поражать плод.
Симптомы
У большинства людей цитомегалия протекает без каких-либо симптомов либо отмечаются признаки схожие с ОРЗ: повышенная температура, озноб, увеличение лимфатических узлов, головная боль, слабость, плохое самочувствие. Если заражение вирусом произошло при переливании крови, тогда спустя 2-4 недели наблюдается длительное повышение температуры, возможно развитие гепатита и желтухи, появление сыпи. При тяжелой форме заболевания вирус вызывает поражение целого ряда органов и может привести к развитию слепоты, энцефалита, язвы кишечника или пищевода, поражению легких и головного мозга, которые могут привести к смерти.
У беременных
Наиболее опасен вирус для беременных женщин, которые заразились во время беременности. Инфицирование в первом триместре беременности может вызвать выкидыш или смерть ребенка. У младенцев с врожденной цитомегалией отмечаются увеличенные размеры печени, селезенки, пониженный гемоглобин, желтуха. Для данных детей характерна задержка психического развития, церебральный паралич, эпилепсия, слепота, поражение слуха.
Где сдать анализы
Медицинская лаборатория «Синэво» рекомендует пройти обследование на цитомегаловирус при подозрениях на половые инфекции, при длительных воспалительных заболеваниях, а также при планировании беременности.
Для диагностики заражения организма цитомегавирусной инфекцией, оценки риска возникновения острой стадии заболевания предлагаем:
- анализ крови на антитела к цитомегаловирусу IgG и анализ крови на антитела к цитомегаловирусу IgM;
- ДНК-диагностика вируса в мазке и ДНК-диагностика вируса в крови.
Помните, что своевременное обследование на цитомегаловирусную инфекцию позволит избежать серьезных последствий, а также предотвратить инфицирование близких.
Цитомегаловирусная инфекция. Особенности клинического течения у детей раннего возраста Текст научной статьи по специальности «Клиническая медицина»
¡нфекцм в д1тей
УДК 616.988-07-085-053.2
МАКСИМОВА С.М, САМОЙЛЕНКО И.Г., НИКОНЕЦ Л.Д. Донецкий национальный медицинский университет им. М. Горького
ЦИТОМЕГАЛОВИРУСНАЯ ИНФЕКЦИЯ. ОСОБЕННОСТИ КЛИНИЧЕСКОГО ТЕЧЕНИЯ У ДЕТЕЙ РАННЕГО ВОЗРАСТА
Резюме. Описан случай наблюдения за больным ребенком с цитомегаловирусной инфекцией (ЦМВИ) в раннем возрасте. Особенностью данного случая являются прогрессирование и генерализация ЦМВИ на фоне тяжелого иммунодефицита — врожденной нейтропении Костманна. Наличие этого синдрома создавало дополнительные трудности для диагностики ЦМВИ и сопутствующих этой инфекции гематологических симптомов. Ключевые слова: ЦМВИ, дети.
Цитомегаловирусная инфекция (ЦМВИ) относится к подсемейству бета-герпесвирусов и является одним из крупных вирусов, ядро которого состоит из двухцепочечной ДНК [1].
Цитопатический эффект вируса проявляется образованием гигантских клеток диаметром 24—40 мкм с внутриядерными включениями («совиный глаз»).
Источником инфекции является человек, зараженный цитомегаловирусом (ЦМВ). После первичной инфекции экскреция вируса продолжается обычно несколько месяцев, до тех пор пока не переходит в латентную форму. При врожденных и перинатальных инфекциях непрерывная экскреция вируса может продолжаться 4—8 лет. Как у взрослых, так и у детей состояние латентной инфекции нередко прерывается периодическими рецидивами, во время которых вновь начинается выделение вируса [2].
У инфицированного человека вирус находится в слюне, моче, влагалищном секрете, сперме, грудном молоке, слезах, крови и многих внутренних органах [1].
В большинстве случаев ЦМВИ протекает в субклинической форме, ее источники не выявляются, не изолируются и длительное время остаются резервуаром вируса.
Механизм передачи ЦМВИ контактный, а пути передачи такие же, как и при вирусном гепатите В, простом герпесе. Передача ЦМВ от матери реализуется чаще, чем других вирусов. Врожденная ЦМВИ встречается у 1—2,5 % новорожденных. По мере роста популярности грудного вскармливания частота перинатальной инфекции ЦМВ будет возрастать [3].
Серьезная проблема — заражение ЦМВ реципиентов крови. В нашей стране доноры пока не обследуются на ЦМВИ. В то же время известно, что при переливании крови от серопозитивных доноров заражаются от 15 до 40 % детей и 2—3 % взрослых. Еще более сложная проблема связана с трансплантацией органов, так как фактором передачи инфекции может быть не только перелитая кровь, но и пересаженный орган. Так, например, при трансплантации костного мозга ЦМВ заражаются около 5 % реципиентов [2].
Вследствие большого числа источников инфекции, множества путей и факторов ее передачи ЦМВИ чрезвычайно широко распространена среди людей.
Во всем мире от 90 до 100 % детского населения оказываются зараженными уже в возрасте до 5 лет. Установлено, что основными причинами являются низкий уровень жизни, отсутствие гигиенических навыков и особенно большая скученность. Скученность детей в различных детских учреждениях, школах, способствует распространению инфекции [4].
Различают ЦМВИ врожденную и приобретенную (первичную и вторичную). Врожденная инфекция возникает, если во время беременности происходит первичное заражение матери ЦМВ или реактивация имеющейся латентной инфекции. Околоплодные воды, кровь, влагалищный секрет содержат вирус. Входными воротами при врожденной инфекции являются плацента, плодные оболочки, внешние покровы плода, дыхательные пути, желудочно-кишечный тракт. Вероятность инфицирования плода при этом составляет 25—50 %. При этом у 15—18 % инфицированных детей отмечается манифестная врожденная ЦМВИ с тяжелым течением и нередко заканчивающаяся летальным исходом. А среди выживших детей в последующем сохраняются серьезные осложнения, приводящие к инвалидизации [1].
Наиболее активно инфекция передается в перинатальный период через зараженное грудное молоко, давая около 60 % всех случаев перинатальной инфекции.
При антенатальном инфицировании плода чаще имеет место трансплацентарный путь передачи ЦМВ.
При вторичной инфекции в период беременности, когда происходит реактивация латентно-персистирующей ЦМВИ или инфицирование новым штаммом вируса серопозитив-ной женщины, риск инфицирования плода и развития тяжелой ЦМВИ значительно ниже и не превышает 2 %. Это объясняется тем, что у большинства таких женщин сформировался достаточно эффективный анти-ЦМВ-иммунитет. И поэтому факторы специфического иммунитета матери
6(27) • 2010
1нфекцН в дтей
(анти-ЦМВ-антитела и анти-ЦМВТ(СD-8)-лимфоциты) обеспечивают действенную защиту плода от инфицирования и развития тяжелой ЦМВИ [1].
В случае постнатального инфицирования инкубационный период болезни составляет 3—8 недель. После проникновения вируса через слизистую оболочку респираторного или генитального тракта и его локального размножения наступает виремическая фаза. При этом поражаются основные органы-мишени: почки, слюнные железы, сердце, печень, респираторный и генитальный тракт с последующим размножением в фибробластах, эпителии и эндотелии. Попав в организм человека, ЦМВ размножается и выделяется из него в течение недель, месяцев и даже лет. Проникая в лимфоциты, вирус сохраняется в организме человека на протяжении всей его жизни и может передаваться, как уже было сказано, при переливании крови или трансплантации органов.
Первичная инфекция в детском возрасте часто протекает незаметно. Выздоровление после первичного эпизода ЦМВИ наступает, как правило, через несколько недель.
Приобретенная первичная инфекция у большинства (> 90 %) детей и взрослых протекает латентно. И только у небольшой части инфицированных возникают клинические симптомы: сиалоаденит — увеличение слюнных желез и мононуклеозоподобный синдром. Последний характеризуется умеренной лихорадкой, недомоганием, гепатоспле-номегалией, редко наблюдается тонзиллит. В крови обнаруживают лимфоцитоз и атипичные мононуклеары.
Особенно часто возникает пневмония, которая характеризуется общеинфекционным синдромом, умеренными физикальными и рентгенологическими (по типу интерсти-циальной пневмонии) данными, гепатоспленомегалией, лейкопенией. При этом стандартная антибактериальная терапия не дает эффекта [5].
Поражения печени возможны от гепатомегалии до тяжелого гепатита и деструктивного холангита с холестазом.
Поражения ЖКТ могут длительно протекать под маской дуоденита, энтероколита и других, а также возможны язвенно-некротические поражения.
Нервная система часто вовлекается в процесс. Наряду с тяжелыми энцефалитами развиваются вялотекущие энцефалопатии со слабоумием, периферические нейропатии.
Кроме того, ЦМВИ может сопровождаться васкулита-ми, тромбоцитопенией и другими симптомами. Характерный клинический признак цитомегалии — геморрагический синдром. Обычно уже в течение первых суток после рождения у ребенка на лице, туловище, конечностях появляются множественная петехиальная сыпь, кровоизлияния в кожу, слизистые оболочки, кровотечения из пупочной ранки, кровь в стуле. Как правило, через 8—10 дней геморрагический синдром бесследно проходит и может снова возникнуть через несколько недель [5].
У некоторых детей с первых дней жизни возникает желтуха вследствие поражения гепатоцитов, гемолиза эритроцитов.
Возможно поражение почек по типу нефрозонефрита.
При врожденной ЦМВИ отмечаются хориоретиниты, катаракта, атрофия зрительного нерва, полная слепота.
Больные с наследственным иммунодефицитом, принимающие иммунодепрессанты, ВИЧ-инфицированные в стадии СПИДа подвергаются более высокому риску развития висцеральных и диссеминированных форм ЦМВИ. По мере прогрессирования иммунодефицита утяжеляются поражения, вызванные ЦМВ [4].
В настоящее время известно, что ЦМВ сам снижает уровень клеточного иммунитета, то есть обладает иммуносу-прессивным действием.
Приводим случай наблюдения из нашей практики за ребенком с врожденной ЦМВИ.
Ребенок К. родился от первой беременности 40 недель, протекавшей с угрозой прерывания в первой половине, анемией, пиелонефритом, дрожжевым кольпитом; от срочных родов, с однократным обвитием пуповины вокруг шеи, признаками морфофункциональной незрелости, оценкой по шкале Апгар 7 баллов. Масса при рождении 2850 г, длина тела 49 см, окружность головы 34 см, окружность груди 33 см. Приложен к груди в первые сутки, сосал активно. Пуповина отпала на 3-и сутки, вакцинирован БЦЖ на 5-е сутки. Выписан из роддома на 6-е сутки с массой 2780 г, с чистой кожей, мокнущим пупком. В течение последующих 3 недель после выписки из роддома у ребенка сохранялось мокнутие пупка (гранулема). Получал местное лечение, после чего через месяц наступила полная эпителизация пупочной ранки. Находился на грудном вскармливании до 4 месяцев, затем получал питание искусственными смесями.
В возрасте одного месяца перенес везикулопустулез, дисбиоз кишечника на фоне перинатального гипоксиче-ского поражения ЦНС с вентрикуломегалией (по данным нейросонографии).
В возрасте 2 месяцев у ребенка появились отечность и гиперемия правого века, беспокойство, высокая температура тела. Госпитализирован в областную детскую больницу, где находился около 4 месяцев на стационарном лечении. Диагностированы детский генетический агранулоцитоз (нейтропения Костманна), врожденный иммунодефицит, эндофтальмит, некроз тканей века правого глаза, двусторонняя пневмония, гипотрофия III степени.
В возрасте 4 месяцев произведена операция — эвисцера-ция (энуклеация) правого глаза и секвестротомия нижнего края орбиты и скуловой кости справа. Послеоперационный период протекал с крайне вялой регенерацией. После выписки перенес повторно пневмонию, абсцесс левой ягодицы, стоматит, рецидивы пиодермии, фурункулез. Лечился в разных стационарах города.
С 7 месяцев жизни отмечалось прогрессирующее увеличение размеров живота за счет паренхиматозных органов (печени и селезенки).
В 1 год 2 месяца был госпитализирован в отделение челюстно-лицевой хирургии и реанимации по поводу сепсиса, тромбофлебита поверхностных вен щеки и лба слева, пневмонии, пиелонефрита, с отставанием в психомоторном развитии на фоне тяжелого врожденного иммунодефицита. Выписан с улучшением.
В 1 год 7 месяцев госпитализирован в местную больницу по поводу пневмонии, выявлены изменения в гемограмме и миелограмме. В последней отмечено увеличение бластов до 16 %, нейтропения. При повторных исследованиях периферической крови отмечалось также увеличение количества бластов до 8 %. Предполагался миелодиспластический синдром, переведен в детский онкогематологический центр. При поступлении состояние ребенка тяжелое. Выражена бледность кожи и слизистых, пониженного питания, отмечались рахитические стигмы, отставание в психофизическом и статическом развитии. Геморрагий на коже нет. Периферические лимфатические узлы по типу микрополи-адении. В легких дыхание пуэрильное, хрипов нет. Одышка умеренная. Границы сердца расширены в поперечнике. Тоны ритмичны, учащены, систолический шум у верхуш-
www.pediatric.mif-ua.com
95
1нфекцН в dimeu
6(27) • 2010
ки. Отмечается значительное увеличение размеров живота. Печень пальпировалась на 10 см ниже правого подреберья, край заострен, занимает эпигастральную область. Селезенка занимает левую половину брюшной полости, плотная, нижний край до 2 см ниже пупочной линии.
В миелограмме: индекс созревания эритробластов 0,9; красный ряд имеет мегалобластоидный оттенок, функция мегакариоцитарного ростка снижена.
На ЭКГ: синусовая тахикардия.
На УЗИ сердца: листки перикарда уплотнены, количество жидкости в перикарде до 60 мл, резкая дилатация всех полостей сердца. Снижение насосной функции миокарда левого желудочка. При цветном картировании выявлен шунтовый поток на межжелудочковой перегородке в области средней трети по типу Толочинова — Роже.
Статическая сцинтиграфия печени: диффузное поражение печени. Спленомегалия. Значительная активизация РЭС селезенки. Четких признаков очагового поражения печени и портальной гипертензии нет.
Трепанобиопсия: гиперплазия костного мозга за счет в основном эритроидного ряда. Гранулоцитарный ряд от миелоцитов до сегментоядерных форм (нейтрофилы, эози-нофилы) малоклеточный. Мегакариоциты немногочисленны. Ретикулярные клетки большей частью вытянутой формы — фибробласты, образующие соединительнотканные волокна.
За время пребывания в онкогематологическом отделении у ребенка повторялись носовые кровотечения. Выполнялись передние тампонады обоих носовых ходов. В периферической крови отмечалось снижение числа лейкоцитов и бластных клеток вплоть до полного их отсутствия. В последующем вновь нарастало количество бластных клеток и лейкоцитов. Мазки периферической крови и костного мозга консультированы в лаборатории цитохимической иммунологии Института проблем онкологии и радиобиологии г. Киева. Предполагалась наследственная дизэритропоэти-ческая анемия. Но клинические данные (нарастание числа лейкоцитов, бластов, гепатоспленомегалия) позволили подтвердить основной диагноз: врожденный агранулоцитоз (нейтропения Костманна).
Осложнение: экссудативный перикардит.
Сопутствующий: дефект мышечной части межжелудочковой перегородки, перинатальное постгипоксическое поражение ЦНС, рахит II степени, гипотрофия II степени, синдром отставания психического и моторно-статического развития.
На фоне лечения состояние ребенка несколько стабилизировалось: купирован геморрагический синдром, но сохранялись явления гепатоспленомегалии, тромбоцитопении, анемии.
Максимова С.М., Самойленко 1.Г., Нконець Л.Д. Аонецький нацональний медичний ун!верситет 1м. М. Горького
ЦИТОМЕГАЛОВ^УСНА ¡НФЕЩЯ. В ДЛЕЙ РАННЬОГО ВкУ
Резюме. Описаний випадок спостереження за хворою дитиною з цитомегаловiрусною шфекщею (ЦМВ1) в ранньому вщ. Особливютю даного випадку е прогресування й генералiзацiя ЦМВ1 на фош тяжкого iмунодефiциту — природжено! нейтропенii Костманна. Наявнiсть цього синдрому створювала додатеош труднощi для дiагностики ЦМВ1 та супутн1х цiй шфекци гематологiчних симптомiв. Ключовi слова: ЦМВ1, дiти.
96
Диагноз хронического миелолейкоза не был исключен. Предполагалось исследование в Институте молекулярной биохимии и генетики, г. Киев (определение Rh-хромосомы), от которого родители отказались.
Состояние ребенка резко ухудшилось в 1 год 11 месяцев, когда после перенесенного сальмонеллеза был переведен в реанимационное отделение в тяжелом состоянии с явлениями сердечной и легочной недостаточности. Консультирован кардиохирургом, произведена пункция перикарда, извлечено 350 мл зловонной жидкости из полости перикарда.
В последующие дни состояние ребенка прогрессивно ухудшалось. Реанимационные мероприятия не дали положительного эффекта. Ребенок умер при явлениях сердечной и легочной недостаточности.
Основной патологоанатомический диагноз: врожденная генерализованная цитомегаловирусная инфекция — хронический сиалоаденит, энцефалит с внутренней гидроцефалией, микрополигирией, нарушением цитоархитектоники коры головного мозга, хронический цитомегалический гепатит (620,0 г), спленомегалия с периспленитом (200,0), хронический очаговый нефрит, панкардит с организацией экссудата серозной оболочки, очаговая межуточная и пе-рибронхиальная пневмония. Стигмы дизэмбриогенеза. Состояние после энуклеации правого глазного яблока.
Осложнение: общая анемия, акцидентальная инволюция тимуса, гипотрофия, дистрофические изменения паренхиматозных органов, отек головного мозга.
Причина смерти: двусторонняя очаговая пневмония.
Таким образом, мы полагаем, что особенностью данного случая являются прогрессирование и генерализация ЦМВИ на фоне тяжелого иммунодефицита — врожденной ней-тропении Костманна. Наличие этого синдрома создавало дополнительные трудности для диагностики ЦМВИ и сопутствующих этой инфекции гематологических симптомов. Именно для ЦМВИ характерен полиморфизм клинических проявлений, обязывающий врача проводить тщательное обследование таких пациентов для подтверждения или исключения этой инфекции.
Список литературы
1. Чернышева Л.И. Цитомегаловирусная инфекция (лекция) //Сучаст шфекци. — 1999. — №3. — С. 71-79.
2. Рахманова А., Пригожина В., Неверов В. Цитомегаловирусная инфекция //Инфекционный контроль. — Январь — март 2002. — № 1. — С. 25-27.
3. Иммунология детского возраста / Под ред. А.Ю. Щербины и Е.Д. Пашанова // Дефекты фагоцитоза, врожденные нейтропении. — Москва, 2006. — Глава 12. — С. 191-197.
4. Сидорова И.С, Макаров И.О., Матвиенко Н.А. Внутриутробные инфекции: Учебное пособие. — Москва, 2006. — С. 36-48.
5. Диагностика, дифференциальная диагностика и лечение детских инфекций: Справочник. — 2-е изд. — С.-Петербург, 2007. — С. 88-100, 199-212.
Получено 26.08.10 □
Maksimova S.M., Samoylenko I.G., Nikonets L.D. Donetsk National Medical University named after M. Gorky, Donetsk, Ukraine
CYTOMEGALOVIRUS INFECTION. FEATURES OF CLINICAL COURSE IN CHILDREN OF EARLY AGE
Summary. In the article there is presented the case ofobservation of sick child with cytomegalovirus infection (CMVI) in early age. The features of this case are progression and generalization of CMVI secondary to severe immunodeficiency — congenital neutropenia of Kostmann. The presence of this syndrome made additional difficulties in diagnostics of CMVI and hematological symptoms concomitant to this infection.
Key words: CMVI, children.
Цитомегаловирусные (ЦМВ) инфекции — HealthyChildren.org
Цитомегаловирус (ЦМВ) — распространенный вирус, который является частью семейства вирусов герпеса. Он заражает большинство людей в какой-то момент их жизни. Он может передаваться детям через жидкости организма, такие как слюна, слезы, моча, кровь и даже грудное молоко. Он часто передается при смене подгузников, во время купания и при других близких контактах. Подростки и взрослые передают вирус при тесном контакте, например, при поцелуях и половом акте.
Цитомегаловирус является причиной наиболее распространенной врожденной (присутствующей при рождении) инфекции в США. Младенцы могут заразиться ЦМВ-инфекцией от инфицированных матерей, иногда до рождения, когда вирус передается плоду через плаценту, или во время родов, если инфицированы половые пути матери. Он также может передаваться через грудное молоко, инфицированное ЦМВ.
Дети, инфицированные вирусом иммунодефицита человека (ВИЧ) или чья иммунная система ослаблена по другой причине (например,g., из-за лечения рака) также особенно восприимчивы к ЦМВ-инфекциям и их осложнениям.
Когда человек инфицирован, ЦМВ остается внутри человека, обычно в состоянии покоя или в неактивном (латентном) состоянии, и может периодически становиться активным и появляться в выделениях этого человека. Вирус может реактивироваться и вызывать болезнь, если иммунная система человека ослабляется болезнью или лекарством.
Признаки и симптомы
Когда ребенок заражается ЦМВ-инфекцией, у него обычно проявляются легкие симптомы или даже симптомы отсутствуют совсем.Однако некоторые инфекции действительно вызывают симптомы. Например, когда у подростков развивается ЦМВ-инфекция, это может выглядеть как инфекционный мононуклеоз из-за продолжительной лихорадки, боли в горле, ломоты в теле и усталости.
Большинство детей, рожденных с ЦМВ-инфекцией, не имеют явных симптомов при рождении и остаются здоровыми. Однако у некоторых обнаруживается потеря слуха или нарушение обучаемости. В меньшем количестве случаев у этих детей при рождении наблюдаются такие симптомы, как низкий вес при рождении, желтуха (пожелтение кожи и глаз), увеличение лимфатических узлов и кожная сыпь.У этих младенцев могут быть проблемы на протяжении всей жизни, такие как глухота и умственная отсталость. У детей с ослабленной иммунной системой инфекция ЦМВ может поражать многие органы тела, включая легкие, печень, почки, костный мозг и кишечник. У детей, перенесших трансплантацию органов, инфекции ЦМВ связаны с отторжением или нарушением функции трансплантата.
Инкубационный период большинства инфекций ЦМВ составляет от 4 до 16 недель.
Как ставится диагноз?
Признаки ЦМВ-инфекции могут быть обнаружены с помощью специальных вирусных культур мочи, слюны или других биологических жидкостей.Анализы крови покажут, выработал ли человек антитела к вирусу. Существует множество специальных тестов, которые измеряют части вируса и позволяют врачам предсказать, является ли ЦМВ причиной определенного заболевания.
Лечение
У большинства детей нет необходимости в специфическом лечении ЦМВ-инфекций. Однако серьезные инфекции у детей с ослабленной иммунной системой, например, у детей с ВИЧ-инфекцией или после трансплантации органов, можно лечить с помощью лекарства под названием ганцикловир.В настоящее время проводятся исследования, чтобы выяснить, может ли помочь лечение новорожденных с серьезной инфекцией ЦМВ.
Каков прогноз?
У большинства детей с ЦМВ-инфекцией симптомы отсутствуют, и они ведут совершенно нормальный образ жизни, даже если вирус остается неактивным в организме. Однако у молодых людей, заразившихся ЦМВ-инфекцией при рождении, может развиться нарушение слуха или умственная отсталость.
Профилактика
Соблюдение правил личной гигиены, особенно регулярное мытье рук, может снизить риск распространения ЦМВ.Когда вы ухаживаете за ребенком с ЦМВ-инфекцией, не забывайте часто мыть руки, особенно после смены подгузников. У большинства детей с ЦМВ нет никаких симптомов, но вирус передается с мочой, поэтому важно не забывать мыть руки каждый раз, когда вы меняете детский подгузник. Детей следует попросить не делиться своими чашками и посудой, потому что они загрязнены слюной и могут передавать вирусы от человека к человеку.
Информация, содержащаяся на этом веб-сайте, не должна использоваться вместо медицинской помощи и рекомендаций вашего педиатра.Ваш педиатр может порекомендовать различные варианты лечения в зависимости от индивидуальных фактов и обстоятельств.
Цитомегаловирус или ЦМВ
Цитомегаловирус или ЦМВ — распространенный вирус, который в какой-то момент жизни поражает почти всех. Большинство инфекций, вызванных ЦМВ, протекают «бессимптомно» и не вызывают никаких признаков или симптомов. Если CMV вызывает симптомы, это обычно лихорадка, усталость и боли или «моно» синдром мононуклеоза. ЦМВ может вызывать тяжелые заболевания и повреждение органов и зрения у людей с ослабленной иммунной системой.ЦМВ при беременности представляет особый риск, поскольку вирус может передаваться еще не родившемуся ребенку, особенно если беременная мать впервые заразится ЦМВ во время беременности. Младенцы, рожденные с ЦМВ, называются «врожденно инфицированными ЦМВ». Большинство младенцев с врожденным ЦМВ выглядят нормальными, они просто незаметно инфицированы и будут жить нормальной жизнью. Однако у некоторых младенцев, рожденных с ЦМВ, могут быть проблемы, включая глухоту, потерю зрения, сыпь, увеличение печени или селезенки и аномалии развития мозга.
Как распространяется ЦМВ?
ЦМВ — это вирус, который передается от человека к человеку при тесном контакте, например при поцелуях, совместном использовании еды, питья или посуды. Малыши и маленькие дети обычно болеют тихой ЦМВ-инфекцией и могут иметь ЦМВ в слюне и моче. ЦМВ также передается при переливании крови и трансплантации органов.
Каковы симптомы ЦМВ?
У большинства людей с ЦМВ нет симптомов, и они никогда не узнают, что инфицированы.У других есть легкое гриппоподобное заболевание или мононуклеоз с симптомами, которые могут включать:
- Лихорадка
- Головная боль
- Боль в горле
- Увеличение лимфатических узлов
- Мышечные боли
- Усталость
- Сыпь
Каковы симптомы врожденного ЦМВ?
Здоровые дети могут рождаться с тихой врожденной ЦМВ и протекать бессимптомно. У некоторых детей с врожденной ЦМВ глухота бывает при рождении.Новорожденные с более тяжелым поражением и врожденным ЦМВ могут иметь сыпь, увеличенную печень и селезенку, проблемы со зрением или аномалии развития мозга, такие как микроцефалия (маленькая голова), кальцификаты или полимикрогирия (PMG).
Как диагностируется ЦМВ?
Медицинские работники могут запросить простой анализ крови для определения уровня антител к ЦМВ для диагностики ЦМВ-инфекции у детей старшего возраста и взрослых.
Врожденная ЦМВ-инфекция диагностируется путем обнаружения вируса в моче, слюне или крови новорожденного.Поскольку ЦМВ очень распространен, врожденный ЦМВ необходимо диагностировать в течение первого месяца жизни.
Как лечится ЦМВ?
Лечение ЦМВ у здоровых людей не требуется. Большинство людей полностью выздоравливают без лечения. При тяжелых симптомах может потребоваться стационарное лечение. ЦМВ-инфекции у людей с аномальной иммунной системой или новорожденных с тяжелым заболеванием, вызванным врожденным ЦМВ, можно лечить противовирусными препаратами, такими как ганцикловир, внутривенными инфузиями, таблетками валганцикловира или раствором, принимаемым перорально.В особых случаях ЦМВ-инфекцию во время беременности можно лечить с помощью инфузий ЦМВ-гипер иммуноглобулина. Вы можете спросить своего врача об этих специальных методах лечения.
Как можно предотвратить ЦМВ?
ЦМВ встречается часто и обычно не поддается профилактике.
Лицензированной вакцины против ЦМВ не существует.
Однако, если вы беременны, вам следует соблюдать меры предосторожности, чтобы снизить риск заражения ЦМВ в первый раз во время беременности, чтобы избежать риска врожденной инфекции ЦМВ у вашего ребенка.
Если вы беременны и хотите избежать заражения ЦМВ, сделайте следующее:
- Не делитесь едой и напитками с кем-либо, особенно с малышами или маленькими детьми.
- Тщательно мойте руки после смены подгузников или вытирания выделений из носа или слюны изо рта младенцев и маленьких детей.
- Не целуйте маленьких детей в рот или рядом с ним. Вместо этого обнимите их или поцеловайте в макушку.
Факты о CMV
Большинство ЦМВ-инфекций протекает бессимптомно и бессимптомно
ЦМВ может вызывать у некоторых людей гриппоподобное заболевание или мононуклеоз
ЦМВ может быть опасным для людей с ослабленной иммунной системой или беременных
Большинство новорожденных с ЦМВ здоровы, но у некоторых новорожденных может быть серьезное заболевание, вызванное ЦМВ.
Серьезное заболевание, вызванное ЦМВ, можно лечить с помощью противовирусных препаратов или инфузий иммуноглобулина
Вакцины против ЦМВ нет
Беременным женщинам рекомендуются меры предосторожности в отношении ЦМВ для предотвращения передачи ЦМВ между людьми —
Не делитесь едой и напитками с маленькими детьми
Не целуйте маленьких детей в рот или вокруг него
хорошо вымыть руки после смены подгузников и вытирания насморка и слюни у детей
Цитомегаловирусных инфекций | Американская академия педиатрии
Цели
После завершения этой статьи читатели должны иметь возможность:
Обсудить факторы риска заражения матери цитомегаловирусной (ЦМВ) инфекцией во время беременности.
Диагностика первичной ЦМВ-инфекции у беременных и здоровых людей.
Опишите физические данные плода и новорожденного, указывающие на врожденную ЦМВ-инфекцию.
Перечислите критерии диагностики ЦМВ-болезни у пациентов с ослабленным иммунитетом.
Определите методы лечения, наиболее эффективные для лечения ЦМВ-инфекций у беременных женщин, новорожденных и пациентов с ослабленным иммунитетом.
Введение
Цитомегаловирус (ЦМВ), член семейства герпесвирусов, имеет самый большой геном среди всех вирусов, поражающих людей.Поскольку геном содержит около 230 т.п.н. двухцепочечной ДНК и кодирует более 100 белков, трудно определить, как происходит инфекция ЦМВ. ЦМВ адаптировался к иммунной системе человека и распространяется среди людей через вирусную экскрецию почти со всеми жидкостями организма, включая мочу, слюну и сперму. В большинстве случаев ЦМВ-инфекция не оказывает видимого воздействия на иммунную систему, и у большинства инфицированных людей болезнь отсутствует. Заболевание, связанное с ЦМВ-инфекцией, обычно возникает при нарушении иммунной системы, например, у пациентов, инфицированных вирусом иммунодефицита человека (ВИЧ) или перенесших трансплантацию органов.Недавние наблюдения показывают, что ЦМВ-инфекция, связанная с врожденной инфекцией, может быть частично связана с плацентарной дисфункцией, вызванной ЦМВ-инфекцией плаценты.
Вирус и передача
Вирусные частицы ЦМВ структурно сходны с другими вирусами герпеса человека. Вирус имеет внутреннее ядро размером 65 нм, содержащее вирусную ДНК. Внутреннее ядро находится внутри икосаэдрического белкового капсида, состоящего из 162 капсомеров. Эта структура окружена слоем тегумента и внешней оболочкой мембраны, содержащей гликопротеины.Гликопротеины оболочки являются антигенными и ответственны за запуск иммунного ответа. Большинство нейтрализующих антител, индуцированных антигенами ЦМВ, направлены против основного гликопротеина ЦМВ gB, хотя другие…
Цитомегаловирус (ЦМВ)
Последняя редакция: октябрь 2011 г.
Что такое цитомегаловирус (ЦМВ)?
ЦМВ — распространенный вирус, которым в какой-то момент в течение жизни заражается от 50 до 80 процентов людей, но редко вызывает явное заболевание. Это член семейства вирусов герпеса.Другие члены семейства герпесвирусов вызывают ветряную оспу, инфекционный мононуклеоз, лихорадку (простой герпес типа I) и генитальный герпес (простой герпес типа II). Как и другие герпесвирусы, ЦМВ-инфекция может на время бездействовать, а затем может снова активироваться. Вирус переносится людьми и не связан с пищей, водой или животными.
Кто заразился ЦМВ?
Заразиться ЦМВ может любой человек. Практически все люди подверглись воздействию ЦМВ к тому времени, когда они достигли совершеннолетия.
Как распространяется ЦМВ?
Хотя вирус не очень передается, он может передаваться от человека к человеку при прямом контакте. Вирус выделяется с мочой, слюной, спермой и, в меньшей степени, с другими жидкостями организма. Передача также может происходить от инфицированной матери ее плоду или новорожденному, а также при переливании крови и трансплантации органов.
Каковы симптомы ЦМВ-инфекции?
У большинства детей и взрослых, инфицированных ЦМВ, симптомы отсутствуют.Те, у кого развиваются симптомы, могут страдать от болезни, напоминающей инфекционный мононуклеоз, и иметь жар, опухшие железы и чувство усталости. Люди с ослабленной иммунной системой (например, люди с ВИЧ / СПИДом или получающие химиотерапию) могут испытывать более серьезные заболевания, включая лихорадку, пневмонию и другие симптомы.
Является ли инфекция ЦМВ очень серьезной для младенцев?
Примерно 8 из каждых 1000 детей, рожденных в Соединенных Штатах, будут инфицированы ЦМВ, из которых 1-2 могут иметь серьезные заболевания, связанные с повреждением нервной системы или нарушениями развития.
Как скоро после контакта появляются симптомы?
Хотя у большинства людей симптомы никогда не появляются после контакта, инкубационный период составляет от 3 до 12 недель.
Как долго инфицированный человек может переносить ЦМВ?
ЦМВ остается в организме на протяжении всей жизни. Инфицированные люди могут иногда выделять вирус с мочой или слюной. Несколько исследований показали, что от трех до 11 процентов нормальных взрослых и до 50 процентов здоровых детей выделяют вирус либо с мочой, либо с слюной.После выхода из организма вирус быстро умирает.
Как диагностируется ЦМВ?
Существуют специальные лабораторные тесты для культивирования вируса, но такие тесты трудны, дороги и не являются широко доступными. Специфические анализы крови могут быть полезны врачу при постановке диагноза или определении того, подвергся ли человек воздействию, но результаты иногда бывают неточными.
Как лечить ЦМВ-инфекцию?
В настоящее время лечение ЦМВ-инфекции у здоровых людей не показано.Противовирусное лечение используется для лиц с ослабленным иммунитетом, у которых есть глазные инфекции или опасные для жизни заболевания, вызванные ЦМВ.
Следует ли исключить инфицированного ребенка из школы или детского сада?
Нет причин исключать детей с ЦМВ.
Какие меры предосторожности следует соблюдать беременным женщинам при уходе за пациентами или детьми?
Беременным женщинам следует соблюдать правила гигиены и тщательно мыть руки после ухода за пациентами или детьми. Это особенно важно при работе с подгузниками или при контакте с мочой или слюной ребенка.
Риск заражения ЦМВ у больничных работников не выше, чем у других людей, и, вероятно, низок из-за практики тщательного мытья рук. В детских садах, где практика мытья рук может быть не такой хорошей, может быть более высокий риск заражения. В обоих случаях наиболее важными мерами контроля являются хорошая гигиена и тщательное мытье рук. Беременным женщинам, работающим в детских учреждениях, следует свести к минимуму прямое воздействие слюны и избегать поцелуев младенцев или маленьких детей в губы.Объятия — это нормально и не фактор риска.
Обычно не рекомендуется рутинный анализ крови во время беременности на антитела к ЦМВ. Беременным женщинам следует индивидуально проконсультироваться со своим врачом по этому поводу.
Что можно сделать, чтобы предотвратить распространение ЦМВ?
Хорошее мытье рук — лучшая профилактическая мера. При работе с бельем или нижним бельем, загрязненным фекалиями или мочой, следует надевать одноразовые пластиковые перчатки.
Цитомегаловирус и беременность
Цитомегаловирус (также называемый ЦМВ) — это разновидность вируса герпеса.Есть много видов герпесвирусов. Некоторые из них являются заболеваниями, передающимися половым путем, некоторые могут вызывать такие проблемы, как герпес, а некоторые могут вызывать инфекции, такие как ЦМВ. Многие люди заболевают ЦМВ в какой-то момент своей жизни, чаще всего в детстве.
Если у вас есть ЦМВ во время беременности, у вас есть шанс 1 из 3 (33 процента) передать его вашему ребенку. ЦМВ — наиболее распространенный вирус, передающийся от матери младенцу во время беременности. Примерно от 1 до 4 из 100 женщин (от 1 до 4 процентов) имеют ЦМВ во время беременности. Большинство детей, рожденных с ЦМВ, не имеют проблем со здоровьем, вызванных вирусом.Но ЦМВ может вызвать проблемы у некоторых младенцев, включая микроцефалию. Это врожденный дефект, при котором голова ребенка меньше, чем ожидалось, по сравнению с младенцами того же пола и возраста.
Вы можете передать ЦМВ своему ребенку на любом сроке беременности. Более вероятно, что это вызовет проблемы у вашего ребенка, если это произойдет на ранних сроках беременности. Вы также можете передать ЦМВ своему ребенку во время схваток и родов, а также во время кормления грудью. Если ваш ребенок заразится вирусом в это время, у него меньше шансов иметь проблемы со здоровьем, чем если он заразится вирусом во время беременности.
Около половины всех беременных женщин в прошлом болели цитомегаловирусом. Если он у вас уже был, вам не нужно беспокоиться о его получении снова. После заражения ЦМВ остается в вашем организме на всю жизнь. Вы все еще можете передать инфекцию своему ребенку, но это случается редко и обычно не причиняет никакого вреда вашему ребенку.
Как узнать, есть ли у вас ЦМВ?
У большинства людей с ЦМВ нет никаких признаков или симптомов. Но у некоторых может быть:
- Боль в горле
- Повышенная температура в течение нескольких дней
- Увеличение лимфоузлов
- Усталость (постоянное чувство усталости)
Сообщите своему врачу, если вы думаете, что у вас может быть ЦМВ.Ваш врач может сдать вам анализ крови, чтобы узнать, есть ли он у вас.
Если у вас слабая иммунная система, ЦМВ может вызвать серьезные проблемы со здоровьем, включая пневмонию или глазные инфекции. Например, ЦМВ может вызывать такие проблемы у людей с ВИЧ.
Как лечат ЦМВ во время беременности?
Если ваш анализ крови положительный на ЦМВ, ваш поставщик может проверить вашего ребенка на вирус с помощью амниоцентеза (также называемого амнио). Во время этого теста ваш врач вводит тонкую иглу в живот, чтобы удалить небольшое количество околоплодных вод.Амниотическая жидкость — это жидкость, которая окружает вашего ребенка в утробе матери. Лаборатория проверяет жидкость на ЦМВ. Ваш врач также может использовать ультразвук для проверки физических признаков того, что ваш ребенок инфицирован. Ультразвук использует звуковые волны и экран компьютера, чтобы показать изображение вашего ребенка в утробе матери.
Ученые работают над созданием вакцины от ЦМВ. Они также ищут другие способы предотвратить рождение детей с цитомегаловирусом.
Как можно заразиться ЦМВ?
Вы можете заразиться цитомегаловирусом при контакте с биологической жидкостью человека, который вызывает вирусный кариес.Жидкости организма включают слюну, грудное молоко, сперму, слизь, мочу и кровь.
Женщины обычно заражаются половым путем с кем-либо, кто инфицирован ЦМВ, или контактируя с маленькими детьми, инфицированными ЦМВ. Целых 7 из 10 детей (70 процентов) в возрасте от 1 до 3 лет, посещающих детский сад, могут иметь ЦМВ. Они могут передать его своим семьям, опекунам и другим детям.
У вас может быть больше шансов заразиться ЦМВ, если вы:
- Иметь детей дома
- Работа с маленькими детьми, например, воспитателем или учителем
- Работа в сфере здравоохранения.Если вы медицинский работник и общаетесь с людьми, инфицированными ЦМВ, включая новорожденных, примите стандартные меры предосторожности, чтобы не заразиться самостоятельно. Вы можете пройти тестирование до беременности, чтобы узнать, есть ли у вас ЦМВ.
Как защитить себя от ЦМВ?
Вот что вы можете сделать:
- Если вы находитесь рядом с детьми, хорошо мойте руки после контакта с жидкостями их тела. Например, мойте руки после смены подгузников, вытирания носов и сбора игрушек.
- Осторожно выбрасывайте использованные подгузники и салфетки.
- Не целуйте маленьких детей в губы или в щеку.
- Не делитесь едой, стаканами, чашками, вилками или другой посудой с маленькими детьми или с кем-либо, кто может заразиться цитомегаловирусом.
- Если у вашего партнера ЦМВ, используйте латексный презерватив во время секса.
Дополнительная информация
nationalcmv.org
Последняя проверка: ноябрь 2013 г.
Цитомегаловирус (ЦМВ) во время беременности | Беременность, рождение и рождение ребенка
Цитомегаловирус — это инфекция, вызываемая вирусом.Обычно его называют ЦМВ.
ЦМВ часто не вызывает каких-либо явных симптомов, поэтому вы можете не знать, что инфицированы. Еще не родившийся ребенок может заразиться ЦМВ. Это может вызвать серьезные проблемы, хотя обычно этого не происходит. Есть способы снизить риски.
Что такое ЦМВ?
ЦМВ — распространенный вирус, особенно у младенцев и детей младшего возраста. Его переносят только люди, а не другие животные.
CCMV — один из вирусов семейства вирусов герпеса.Вирусы этого семейства вызывают ветряную оспу, герпес и железистую лихорадку. Все эти вирусы, включая ЦМВ, могут оставаться живыми, хотя и неактивными, в течение многих лет после того, как вы впервые заразились.
Как можно заразиться ЦМВ?
ЦМВ передается от человека к человеку при контакте с биологическими жидкостями, такими как слюна, слизистые носа, моча, вагинальные выделения, сперма и грудное молоко.
Считается, что около половины всех австралийских женщин были инфицированы цитомегаловирусом к моменту беременности.
Некоторые женщины заражаются ЦМВ во время беременности. Это происходит при обращении с инфицированными детскими игрушками, грязными салфетками или грязными пеленками. Также возможно заразиться ЦМВ при половом акте, переливании крови или трансплантации органов.
Нерожденные дети могут заразиться ЦМВ от матери, находясь в утробе матери. В очень редких случаях дети могут заразиться ЦМВ во время кормления грудью.
Как узнать, есть ли у вас ЦМВ?
ЦМВ обычно не вызывает заметных симптомов. Однако у некоторых людей это может вызывать легкие симптомы, похожие на симптомы железистой лихорадки, такие как лихорадка, увеличение лимфатических узлов, кашель или простуда.
ЦМВ может вызывать серьезные заболевания у людей, инфицированных ВИЧ или получающих химиотерапию от рака. Но большинство людей никогда не узнают, что у них ЦМВ-инфекция или была ли она раньше.
Могу ли я дать ребенку ЦМВ?
Да. Если вы беременны и инфицированы ЦМВ, ваш ребенок может родиться с ЦМВ. Это называется врожденной ЦМВ.
Есть тест на ЦМВ-инфекцию. Беременным женщинам, у которых развиваются симптомы вирусной инфекции, указывающие на ЦМВ, рекомендуется пройти обследование.Тестирование на ЦМВ следует предлагать женщинам, которые часто контактируют с большим количеством очень маленьких детей (например, работники по уходу за детьми).
Даже если у вас нет никаких симптомов, вы можете поговорить со своим врачом о тестировании на ЦМВ, если у вас есть какие-либо проблемы.
Как ЦМВ влияет на нерожденных детей?
Младенцы, рожденные с ЦМВ, не обязательно заболевают. Но некоторые дети с ЦМВ могут родиться с инвалидностью, например, с плохим слухом или зрением или интеллектуальными нарушениями.
Это, по-видимому, более вероятно у детей, чьи матери заразились новой инфекцией, чем у матерей, которые носили вирус в течение длительного времени.
Можно ли предотвратить ЦМВ?
Лучший способ избежать заражения ЦМВ — это соблюдать правила гигиены.
Если вы беременны, рекомендуется:
- Регулярно и тщательно мойте руки водой с мылом, особенно при уходе за детьми или при работе с предметами, на которых есть жидкости организма
- Регулярно очищайте поверхности и предметы, на которых могут быть жидкости организма
- Надевайте перчатки при смене подгузников
- избегать контакта со слюной детей
- Не делитесь едой, чашками, посудой или зубными щетками
Вакцины для предотвращения ЦМВ-инфекции не существует.
Для получения дополнительной информации
Пожалуйста, обратитесь к своему врачу или акушерке, чтобы обсудить любые вопросы, которые могут у вас возникнуть. Дополнительная информация доступна в этом информационном листке CMV.
Цитомегаловирусная инфекция, в том числе врожденная — Советник по терапии рака
ОБЗОР: Что нужно знать каждому практикующему врачу
Вы уверены, что у вашего пациента цитомегаловирус? Каковы типичные проявления этого заболевания?
Представление цитомегаловирусной (ЦМВ) инфекции в педиатрической практике зависит от возраста ребенка и времени заражения.Наиболее важное влияние ЦМВ-инфекции вызывает врожденная ЦМВ-инфекция, которая может протекать как симптоматическая, так и бессимптомная при рождении. Приобретенные ЦМВ-инфекции обычно протекают бессимптомно, но могут вызывать недифференцированные фебрильные синдромы и гетерофил-отрицательный мононуклеоз. Клинические проявления этих форм ЦМВ-инфекции кратко изложены ниже:
Симптоматическая врожденная ЦМВ-инфекция
Микроцефалия
Гепатоспленомегалия
Петехии
Тромбоцитопения
Желтуха
Задержка внутриутробного развития
Нейросенсорная тугоухость (СНХЛ)
Нарушения развития нервной системы: умственная отсталость, церебральный паралич, судороги
Бессимптомная врожденная ЦМВ-инфекция
Обычно младенец выглядит нормальным; следовательно, бессимптомные инфекции не учитываются.
Примерно 10% младенцев страдают нейросенсорной тугоухостью, которая может не проявляться при рождении.
Могут возникать тонкие хронические нарушения развития нервной системы.
Приобретенная ЦМВ-инфекция
ЦМВ-инфекция обычно передается в послеродовой период при грудном вскармливании.
Инфекции, приобретенные через грудное молоко, у здоровых доношенных детей протекают бессимптомно.
Первичные инфекции часто передаются малышам в детских садах.
ЦМВ передается половым путем у подростков и молодых людей.
Обычно бессимптомный у взрослых ЦМВ может вызывать «гетерофил-отрицательный» мононуклеоз.
Какое другое заболевание / состояние имеет некоторые из этих симптомов?
Ряд так называемых TORCH-инфекций (токсоплазмоз, другие возбудители, краснуха, цитомегаловирус, простой герпес) могут имитировать врожденный ЦМВ. К ним относятся синдром врожденной краснухи, врожденный токсоплазмоз и вирусная инфекция врожденного лимфоцитарного хориоменингита.
У маленьких детей с первичной ЦМВ-инфекцией симптомы могут имитировать симптомы, связанные со многими вирусными инфекциями, такими как лихорадка, боль в горле и недомогание.
У подростков и молодых людей с первичной ЦМВ-инфекцией может отмечаться синдром мононуклеоза. Как правило, он неотличим от мононуклеоза вируса Эпштейна-Барра (EBV), хотя чаще спленомегалия связана с мононуклеозом CMV. Сыпь, связанная с приемом β-лактамных антибиотиков (особенно амоксициллина, а также родственных агентов), может возникать как при мононуклеозе ЦМВ, так и при мононуклеозе ВЭБ.
Факторы, связанные с передачей врожденного цитомегаловируса
ЦМВ-инфекция плода, вероятно, происходит трансплацентарным путем.Заражение плода может произойти в результате первичного инфицирования матери или повторного заражения новым штаммом ЦМВ. Заражение плода чаще происходит в контексте первичной материнской инфекции (~ 40%), чем в контексте рецидивирующей материнской инфекции (частота передачи ЦМВ у женщин с иммунитетом до зачатия составляет примерно 0,7%).
Существующий материнский иммунитет может снизить риск осложнений, связанных с развитием нервной системы, у врожденно инфицированных младенцев.
Какие лабораторные исследования следует запросить для подтверждения диагноза? Как следует интерпретировать результаты?
Многие врачи ошибочно полагают, что «TORCH-титры» предоставляют полезную диагностическую информацию, но они редко имеют какое-либо значение при диагностике врожденной ЦМВ-инфекции.
Краеугольным камнем диагностики является использование вирусологических исследований
Посев мочи или слюны
Исследование мочи, слюны и крови с помощью полимеразной цепной реакции (ПЦР)
ЦМВ-специфические исследования IgM иногда дают положительные результаты
Время получения образцов имеет решающее значение при интерпретации исследований; Для постановки диагноза врожденной инфекции необходимо провести вирусологические исследования в течение первых 14 дней жизни, поскольку обнаружение ЦМВ после этого момента времени может отражать передачу инфекции через грудное молоко при рождении.
Другие важные лабораторные исследования включают общий анализ крови, количество тромбоцитов и сывороточные уровни трансаминаз.
Какие лабораторные исследования следует запросить, чтобы подтвердить диагноз натального цитомегаловируса?
Натальные ЦМВ-инфекции могут передаваться в родовые пути во время родов через естественные родовые пути, но гораздо чаще передаются при грудном вскармливании. Получение ЦМВ из грудного молока не имеет клинического значения у здоровых доношенных детей, и диагностические исследования не требуются.
У недоношенных детей с низкой массой тела при рождении ЦМВ, полученный из грудного молока или в результате переливания крови (с кровью, не подвергнутой лейкофильтрации), может вызвать серьезное симптоматическое заболевание, поэтому необходимы диагностические исследования:
Слюна, трахеальный аспират, моча для вирусного посева и исследования ПЦР
ПЦР крови для определения вирусной нагрузки
Иногда бывает трудно исключить диагноз врожденного ЦМВ у некоторых младенцев.
Какие лабораторные исследования следует запросить для подтверждения диагноза цитомегаловирусной инфекции у подростков и молодых людей?
Подавляющее большинство ЦМВ-инфекций в этой возрастной группе протекает бессимптомно, и диагностические исследования не требуются или не требуются.
ЦМВ может быть связан с «гетерофил-отрицательным» мононуклеозом.
Исследования
CMV IgG и IgM иногда могут быть полезны, когда желателен окончательный диагноз.
Роль вирусного посева и ПЦР в постановке этого диагноза неясна.
Использование серологических тестов на ЦМВ может сыграть определенную роль для определения статуса ЦМВ-инфекции беременных женщин или женщин, планирующих беременность.
Нет четкой роли рутинного скрининга на антитела к ЦМВ во время беременности.
Женщины, работающие в групповых дневных стационарах, и матери маленьких детей, посещающие групповые дневные стационары, могут подвергаться высокому риску, поэтому можно рассмотреть возможность проведения серологического скрининга и мониторинга.
Медицинские работники не подвергаются повышенному риску заражения ЦМВ-инфекцией, и нет никакой роли для скрининга или переназначения на работу на основе серологического статуса.
Демонстрация сероконверсии и / или появления IgM к ЦМВ во время беременности может представлять собой ситуацию высокого риска.
Помимо сероконверсии (исследования IgG) и демонстрации антител IgM, определение индекса авидности IgG к CMV может быть важным исследованием для прогнозирования риска передачи плоду (высокая авидность коррелирует со снижением риска передачи).
Могут ли быть полезны визуализирующие исследования? Если да, то какие?
Визуализирующие исследования имеют большое значение в диагностике врожденного ЦМВ с поражением центральной нервной системы (ЦНС) и помогают прогнозировать прогноз.
Визуализация может быть выполнена с помощью ультразвукового исследования или компьютерной томографии (КТ) головы.
Важные результаты визуализации ЦНС в неонатальном периоде включают следующее (Рисунок 1):
Рисунок 1.
Визуализация ЦНС: УЗИ врожденного ЦМВ (верхняя панель) и МРТ (нижняя панель) новорожденного с врожденной ЦМВ-инфекцией, демонстрирующие лизэнцефалию, вентрикуломегалию и перивентрикулярные кальцификации (стрелка).
Незначительные отклонения от нормы не могут быть обнаружены с помощью визуализации до тех пор, пока магнитно-резонансная томография не будет выполнена позже в детстве.
Отсутствие внутричерепных кальцификаций при УЗИ и / или КТ не исключает возможности повреждения ЦНС и отдаленных последствий.
Если вы можете подтвердить, что у пациента цитомегаловирусная инфекция, какое лечение следует начать?
Лечение цитомегаловирусных инфекций в педиатрической практике
Симптоматическая врожденная ЦМВ-инфекция
Противовирусным препаратом, наиболее часто используемым при ЦМВ-инфекциях у младенцев и детей, является ганцикловир.Ганцикловир — это аналог нуклеозидов, подавляющий репликацию вирусной ДНК.
Было продемонстрировано, что при симптоматической врожденной ЦМВ-инфекции с поражением ЦНС 6-недельный курс ганцикловира снижает риск СНХЛ и, возможно, других последствий для нервного развития.
Валганцикловир (валиновый эфир ганцикловира) менее изучен, чем ганцикловир, но, по-видимому, он является приемлемой пероральной биодоступной терапией для лечения симптоматического врожденного ЦМВ.
Оптимальная доза неизвестна, но представляется подходящей 16 мг / кг каждые 12 часов
Рекомендуемая продолжительность терапии: 6 недель (можно начать с внутривенного введения ганцикловира и перейти на пероральный валганцикловир)
Длительная терапия валганцикловиром перорально (~ 6 месяцев) может дополнительно снизить риск осложнений со стороны СНВЛ и ЦНС, и эта терапия в настоящее время оценивается в рамках контролируемого исследования, спонсируемого Национальными институтами здравоохранения.
Отсутствие каких-либо данных относительно долгосрочной терапии (например, 6 месяцев) пероральным валганцикловиром при симптоматической врожденной ЦМВ-инфекции исключает возможность получения окончательных рекомендаций в настоящее время; Рекомендуется консультация специалиста по лечению перинатальной вирусной инфекции.
Симптоматическая постнатальная инфекция, вызванная ЦМВ
Показания к терапии ганцикловиром при постнатально приобретенных ЦМВ-инфекциях (симптоматическое заболевание у недоношенных детей) не ясны.
Ганцикловир показан при тяжелых заболеваниях, включая пневмонию и тяжелый гепатит.
Ганцикловир может быть назначен для младенцев с симптомами, стойкими к тромбоцитопении или тяжелой виремией.
Продолжительность терапии 14-21 день; дольше, если заболевание органов-мишеней сохраняется.
Нет четкой роли использования иммуноглобулина CMV в этих условиях.
Другие ЦМВ-инфекции
Ганцикловир показан для профилактики и лечения ЦМВ-инфекций у пациентов с трансплантацией твердых органов и гемопоэтических стволовых клеток с ослабленным иммунитетом.
Лицензированные альтернативные агенты для пациентов с ослабленным иммунитетом включают цидофовир и фоскарнет; Эти агенты обычно используются для устранения побочных эффектов ганцикловира или выявления устойчивости к ганцикловиру.
ЦМВ иммуноглобулин может рассматриваться у беременных пациенток в условиях документально подтвержденной инфекции плода (подтверждение амниоцентеза или ультразвуковые аномалии с серологическими и / или вирусологическими данными о первичной материнской инфекции).
Нет показаний для противовирусной терапии у детей и подростков с первичной ЦМВ-инфекцией, включая ЦМВ-мононуклеоз.
Какие побочные эффекты связаны с каждым вариантом лечения?
Терапия ганцикловиром связана со значительным риском нейтропении
Почти две трети младенцев имели нейтропению при лечении ганцикловиром от врожденной ЦМВ-инфекции.
Нейтропения легко обратима после прекращения терапии.
Если в этих условиях желательно продолжение лечения, введение гранулоцитарного колониестимулирующего фактора может исправить нейтропению и позволить продолжить терапию.
Ганцикловир также может быть связан с подавлением костным мозгом других клеточных линий (например, анемии, тромбоцитопении).
Лечение цидофовиром или фоскарнетом может быть связано со значительной токсичностью, особенно нефотоксичностью, с соответствующими изменениями гомеостаза жидкости и электролитов.
Каковы возможные исходы цитомегаловирусной инфекции?
Цитомегаловирусные инфекции распространены повсеместно и практически всегда протекают бессимптомно у здоровых людей.
Важно подчеркнуть распространенную и латентную природу ЦМВ среди пациентов и их семей, которые, как правило, никогда не слышали о вирусе.
Заражение происходит на протяжении всей жизни, и можно подчеркнуть аналогию с другими Herpesviridae (например, ветряной оспой, простым герпесом).
Мононуклеоз
ЦМВ имеет различное клиническое течение, как и мононуклеоз ВЭБ, и, хотя для некоторых пациентов подходят некоторые ограничения (например, снижение учебной / рабочей нагрузки, отказ от контактных видов спорта при наличии спленомегалии), прогноз для полного выздоровления отличный.
У пациентов с ослабленным иммунитетом после трансплантации (солидный орган и гемопоэтические стволовые клетки) ЦМВ может вызывать опасное для жизни заболевание органов-мишеней, является фактором, способствующим реакции «трансплантат против хозяина», и увеличивает риск оппортунистических грибковых инфекций и несостоятельности трансплантата.
У беременной пациентки исход ЦМВ-инфекции для плода зависит от иммунного статуса матери до установления беременности.
Для первичных материнских инфекций риск передачи плоду составляет приблизительно одну треть (32% в недавнем метаанализе), тогда как для рецидивирующих материнских инфекций риск передачи составляет 1.4%.
У инфицированного плода отдаленный исход инфекции зависит от того, проявляются ли у ребенка симптомы при рождении.
Приблизительно 10% врожденно инфицированных младенцев имеют признаки и симптомы болезни при рождении.
У младенцев с симптомами 40% -90% риск последующих неврологических осложнений, включая умственную отсталость, микроцефалию, задержку развития, судорожные расстройства и церебральный паралич.
Девяносто процентов врожденно инфицированных младенцев не имеют симптомов при рождении.
По сообщениям, от 7% до 20% бессимптомно инфицированных младенцев имеют риск необратимых последствий, наиболее частым из которых является сенсоневральная потеря слуха.
Эпидемиология цитомегаловируса и тенденции заболевания
Распространенность серотипа наиболее высока в развивающихся странах, где инфекция передается в раннем возрасте. Нет никаких сезонных колебаний.
Распространенность в развитых странах выше среди афроамериканцев и лиц с более низким социально-экономическим статусом.
Инфекции в развитых странах распространены в группах дневного ухода, где до 70% малышей могут выделять вирус с мочой.
Уровень врожденной ЦМВ-инфекции напрямую зависит от распространенности серотипа среди населения.
Чем выше распространенность материнских антител против ЦМВ в популяции, тем выше частота врожденной инфекции ЦМВ.
Большинство этих инфекций будут повторными.
Наибольшее влияние врожденный ЦМВ на нарушение развития нервной системы у детей (особенно нарушение слуха) наблюдается у детей, рожденных женщинами с предзачатыми антителами к ЦМВ.
Эта проблема усложняет разработку вакцины.
Скрининг новорожденных на наличие слюны или высохших пятен крови может дать лучшее представление о текущей эпидемиологии врожденных инфекций.
Серологический скрининг матери во время беременности является спорным вопросом и в настоящее время не рекомендуется Американским колледжем акушерства и гинекологии.
Взаимодействие между хозяином и патогенами и влияние генетики
CMV кодирует гены, которые вызывают апоптоз, уклоняются от иммунных ответов хозяина и модулируют клеточный цикл; эти гены могут играть роль в патогенезе инфекции.
Нет четких доказательств повышенной генетической предрасположенности к тяжелой ЦМВ-инфекции, но есть некоторые предположения о том, что полиморфизмы рецепторов Toll связаны с более тяжелым заболеванием после трансплантации солидных органов.
ЦМВ может способствовать длительному пребыванию в отделении интенсивной терапии взрослых пациентов, может играть роль в патогенезе артериальных заболеваний и злокачественных новообразований, а также может быть причиной иммунного старения и нарушения иммунитета у пожилых людей. Эти ассоциации противоречивы, но могут служить основанием для универсальной вакцинации против ЦМВ, как только вакцина будет доступна, а не только для селективной иммунизации женщин детородного возраста.
Перспективы профилактики цитомегаловирусной инфекции
Мытье рук, тщательные гигиенические меры и избегание инфекционных выделений (моча, слюна, носоглоточные выделения) могут защитить как от первичной инфекции, так и от повторного заражения.
Гигиенические меры предосторожности должны быть подчеркнуты с молодыми женщинами, которые беременны или могут быть беременны.
ЦМВ-иммуноглобулин для беременных с признаками внутриутробной инфекции может защитить плод от ЦМВ-болезни; это вмешательство недоказано, но доступно.
ЦМВ передается половым путем, и это еще один источник заражения, о котором пациенты могут быть осведомлены.
Лейкофильтрация продуктов крови по существу устранила ЦМВ-инфекцию и заболевание, вызванное переливанием крови.
Ряд вакцин против ЦМВ проходит клинические испытания, но ни одна из них не лицензирована для использования.
Недавнее исследование субъединичной гликопротеиновой вакцины продемонстрировало 50% защитную эффективность в клинических испытаниях на молодых женщинах детородного возраста.
Какие доказательства?
Веллер, TH. «Цитомегаловирусы: повсеместные агенты с разнообразными клиническими проявлениями». N Engl J Med. об. 285. 1971. С. 203-14, 267-74.
Коэн, Д.И., Кори, Г.Р. «Цитомегаловирусная инфекция у нормального хозяина». Медицина (Балтимор). об. 64. 1985. С. 100-14.
Horwitz, CA, Henle, W., Henle, G. «Клиническая и лабораторная оценка мононуклеоза, вызванного цитомегаловирусом, у ранее здоровых людей.Отчет о 82 случаях ». Медицина (Балтимор). об. 65. 1986. pp. 124–34.
Бравендер Т. «Вирус Эпштейна-Барра, цитомегаловирус и инфекционный мононуклеоз». Adolesc Med State Art Rev. vol. 21. 2010. С. 251–64.
Cheeran, MC, Lokensgard, JR, Schleiss, MR. «Нейропатогенез врожденной цитомегаловирусной инфекции: механизмы заболевания и перспективы вмешательства». Clin Microbiol Rev. vol. 22. 2009. С. 99–126.
Demmler-Harrison, GJ.«Врожденный цитомегаловирус: действия общественного здравоохранения, направленные на повышение осведомленности, профилактику и лечение». J Clin Virol. об. 46. 2009. С. S1-5.
Арвин, AM, Фаст, П., Майерс, М. «Разработка вакцины для предотвращения цитомегаловирусной болезни: отчет Национального консультативного комитета по вакцинам». Clin Infect Dis. об. 39. 2004. С. 233–9.
Kimberlin, DW, Lin, CY, Sánchez, PJ. «Влияние терапии ганцикловиром на слух при симптоматическом врожденном цитомегаловирусном заболевании с поражением центральной нервной системы: рандомизированное контролируемое исследование». J Pediatr. об. 143. 2003. С. 16-25.
Söderberg-Nauclér, C. «Играет ли цитомегаловирус причинную роль в развитии различных воспалительных заболеваний и рака». J Intern Med. об. 259. 2006. С. 219–46.
Осава, Р., Сингх, Н. «Цитомегаловирусная инфекция у пациентов в критическом состоянии: систематический обзор». Crit Care. об. 13. 2009. pp. R68
.
Фаулер, КБ, Стагно, С, Пасс, РФ. «Исход врожденной цитомегаловирусной инфекции в зависимости от статуса материнских антител». N Engl J Med. об. 326. 1992. pp. 663-7.
Sung, H, Schleiss, MR. «Обновленная информация о текущем статусе цитомегаловирусных вакцин». Exp Rev Vaccine. об. 9. 2010. С. 1303-14.
Schleiss, MR. «Врожденная цитомегаловирусная инфекция: молекулярные механизмы, опосредующие вирусный патогенез». Целевые препараты для инфицирования расстройств. об. 11. 2011. С. 449–65.
Copyright © 2017, 2013 ООО «Поддержка принятия решений в медицине».


 Данные поражения органов могут стать причиной бронхита, пневмонии, что ещё более ухудшает состояние и оказывает повышенное давление на иммунную систему. При этом лечение антибиотиками оказывается менее эффективным, нежели при обычном протекании бронхита и/или пневмонии. Вместе с тем может наблюдаться уменьшение тромбоцитов в периферийной крови, поражение стенок кишечника, сосудов глазного яблока, головного мозга и нервной системы. Внешне проявляется, в дополнении к увеличенным слюнным железам, кожной сыпью;
Данные поражения органов могут стать причиной бронхита, пневмонии, что ещё более ухудшает состояние и оказывает повышенное давление на иммунную систему. При этом лечение антибиотиками оказывается менее эффективным, нежели при обычном протекании бронхита и/или пневмонии. Вместе с тем может наблюдаться уменьшение тромбоцитов в периферийной крови, поражение стенок кишечника, сосудов глазного яблока, головного мозга и нервной системы. Внешне проявляется, в дополнении к увеличенным слюнным железам, кожной сыпью;

 с. 57-59
с. 57-59