Болезнь Аддисона. Причины, симптомы, диагностика и лечение патологии :: Polismed.com
Сайт предоставляет справочную информацию. Адекватная диагностика и лечение болезни возможны под наблюдением добросовестного врача. У любых препаратов есть противопоказания. Необходима консультация специалиста, а также подробное изучение инструкции!
Болезнь Аддисона является достаточно редкой эндокринной патологией. В основе ее развития лежит деструкция (разрушение) тканей внешнего (коркового) слоя надпочечников. Такое разрушение может быть спровоцировано разнообразными факторами. Ими могут быть вредоносные бактерии (например, микобактерии), грибки (кандиды, криптококки), вирусы (цитомегаловирус, герпес и др.), генетические, иммунные, микроциркуляторные (нарушение кровоснабжения коры надпочечников) нарушения (ДВС-синдром, антифосфолипидный синдром).
Повреждение коркового слоя надпочечников приводит к нарушению секреции ими стероидных гормонов, в первую очередь, альдостерона и кортизола, которые регулируют водно-солевой, белковый, углеводный, липидный обмены в организме. Они также участвуют в реализации стрессовых реакций, влияют на артериальное давление, общий объем циркулирующей крови.
При болезни Аддисона могут возникать различные симптомы, такие как повышенная утомляемость, общая слабость, головокружение, снижение трудоспособности, головная боль, чувство жажды, влечения к соленой пище, мышечная слабость, миалгия (боли в мышцах), мышечные судороги, боли в животе, тошнота, рвота, нарушение менструального цикла, низкое артериальное давление, гиперпигментация (потемнение кожи), витилиго, тахикардия (учащенное сердцебиение), боли в области сердца и др.
Строение и функции надпочечников
Надпочечники представляют собой парные эндокринные железы. Каждый надпочечник (правый или левый) размещен на верхнемедиальной (верхней внутренней боковой) поверхности верхнего конца (полюса) соответствующей почки (правой или левой).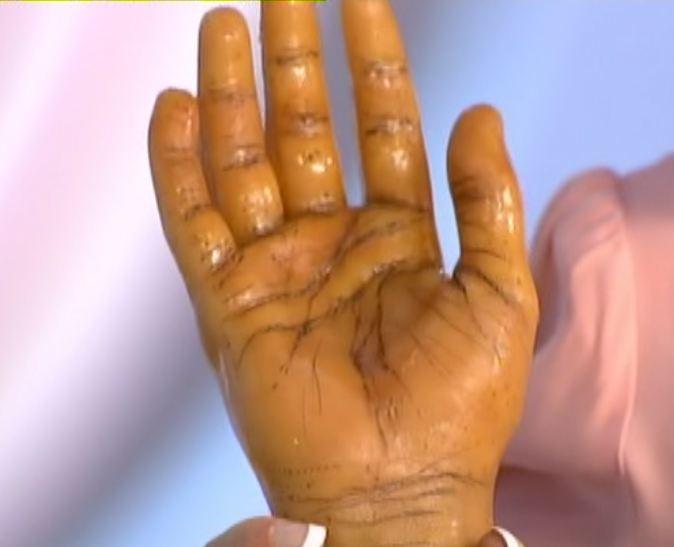 Оба надпочечника имеют примерно одинаковую массу (около 7 – 20 г каждый). У детей надпочечники весят чуть меньше (6 г). Данные железы располагаются в забрюшинной жировой клетчатке на уровне XI – XII грудных позвонков. Забрюшинная клетчатка находится в ретроперитонеальном пространстве – области, локализованной позади заднего листка париетальной (пристеночной) брюшины, выстилающей заднюю стенку брюшной полости. Ретроперитонеальное пространство тянется от диафрагмы (дыхательная мышца, разделяющая грудную и брюшную полости) до малого таза (анатомическая область, находящаяся чуть ниже брюшной полости). В нем помимо надпочечников расположены почки, поджелудочная железа, аорта, нижняя полая вена и другие органы.
Оба надпочечника имеют примерно одинаковую массу (около 7 – 20 г каждый). У детей надпочечники весят чуть меньше (6 г). Данные железы располагаются в забрюшинной жировой клетчатке на уровне XI – XII грудных позвонков. Забрюшинная клетчатка находится в ретроперитонеальном пространстве – области, локализованной позади заднего листка париетальной (пристеночной) брюшины, выстилающей заднюю стенку брюшной полости. Ретроперитонеальное пространство тянется от диафрагмы (дыхательная мышца, разделяющая грудную и брюшную полости) до малого таза (анатомическая область, находящаяся чуть ниже брюшной полости). В нем помимо надпочечников расположены почки, поджелудочная железа, аорта, нижняя полая вена и другие органы.
Левый надпочечник имеет полулунную форму, правый – треугольную. В каждом из них выделяют переднюю, заднюю и почечную поверхности. Задней своей поверхностью оба надпочечника прилежат к диафрагме. Почечная (нижняя) их поверхность соприкасается с верхним полюсом соответствующей почки.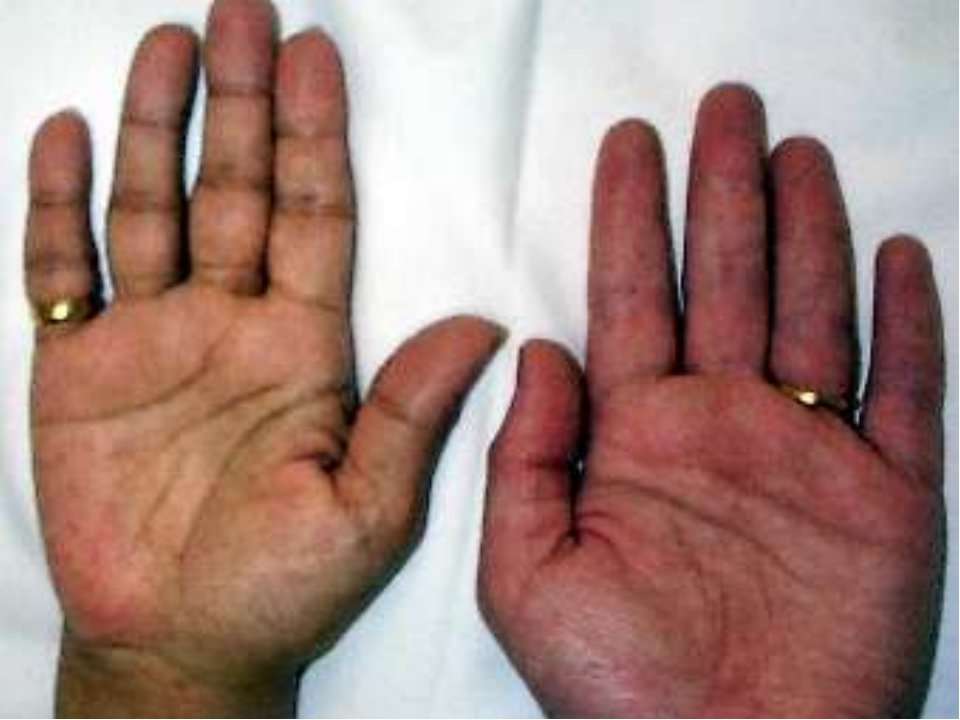 Правый надпочечник в ретроперитонеальном пространстве расположен чуть выше левого. Передней своей поверхностью он примыкает к нижней полой вене, печени и брюшине. Левый надпочечник спереди контактирует с поджелудочной железой, кардиальным отделом желудка и селезенкой. На переднемедиальной (передней внутренней боковой) поверхности каждого из надпочечников находятся так называемые ворота (hilum), через которые из них (из надпочечников) выходят центральные вены (в дальнейшем они называются надпочечниковыми венами).
Правый надпочечник в ретроперитонеальном пространстве расположен чуть выше левого. Передней своей поверхностью он примыкает к нижней полой вене, печени и брюшине. Левый надпочечник спереди контактирует с поджелудочной железой, кардиальным отделом желудка и селезенкой. На переднемедиальной (передней внутренней боковой) поверхности каждого из надпочечников находятся так называемые ворота (hilum), через которые из них (из надпочечников) выходят центральные вены (в дальнейшем они называются надпочечниковыми венами).
Из каждого надпочечника выходит по одной центральной вене. Левая надпочечниковая вена затем впадает в левую почечную вену. Венозная кровь из правого надпочечника транспортируется через правую надпочечниковую вену сразу в нижнюю полую вену. В воротах надпочечников можно обнаружить и лимфатические сосуды, по которым лимфатическая жидкость попадает поясничные лимфатические узлы (nodi lymphatici lumbales), расположенные вокруг брюшной аорты и нижней полой вены.
Артериальная кровь проникает в надпочечники через ветви верхней, средней и нижней надпочечниковых артерий (a. suprarenalis superior, a. suprarenalis media, a. suprarenalis inferior). Верхняя надпочечниковая артерия является продолжением нижней диафрагмальной артерии. Средняя надпочечниковая артерия отходит от брюшной аорты. Нижняя надпочечниковая артерия служит ветвью почечной артерии. Все три надпочечниковые артерии под соединительнотканной капсулой, которая покрывает каждый из надпочечников, образуют густую артериальную сеть. От этой сети отходят мелкие сосудики (около 20 — 30), проникающие в толщу надпочечников через их переднюю и заднюю поверхности. Таким образом, артериальная кровь поступает к надпочечникам по многочисленным сосудам, тогда как венозная кровь удаляется из этих эндокринных желез только через один сосуд – центральную (надпочечниковую) вену.
Иннервация надпочечников осуществляется за счет ветвей, отходящих из солнечного, почечного и надпочечникового нервных сплетений, а также ветвей диафрагмального и блуждающего нервов.
Кнутри от соединительнотканной капсулы располагается корковое вещество (наружный слой) надпочечника, на долю которого приходится около 90% всей паренхимы (ткани) данного органа. Остальные 10% в надпочечнике занимает его мозговое вещество (внутренний слой надпочечника), которое находится под корковым веществом, непосредственно, в самой глубине железы. Корковое и мозговое вещество имеют различное строение, функции и эмбриональное происхождение. Корковое вещество (кора надпочечников) представлено рыхлой соединительной и железистой тканью. Этот слой на анатомических срезах имеет желтовато-коричневый цвет.
Наружный слой каждого из надпочечников принято делить на три зоны – клубочковую, пучковую и сетчатую. Клубочковая зона является самым внешним слоем коркового вещества и локализуется, непосредственно, под капсулой надпочечника. Сетчатая зона граничит с мозговым веществом надпочечника. Пучковая зона занимает срединное положение между клубочковой и сетчатой. В клубочковой зоне вырабатываются минералокортикоиды (альдостерон, дезоксикортикостерон, кортикостерон), в пучковой – глюкокортикостероиды (кортизол и кортизон), а в сетчатой – андрогены. Мозговое вещество надпочечников имеет буровато-красный цвет и не разделяется ни на какие зоны. В этой области в надпочечниках синтезируются катехоламины (адреналин и норадреналин).
В клубочковой зоне вырабатываются минералокортикоиды (альдостерон, дезоксикортикостерон, кортикостерон), в пучковой – глюкокортикостероиды (кортизол и кортизон), а в сетчатой – андрогены. Мозговое вещество надпочечников имеет буровато-красный цвет и не разделяется ни на какие зоны. В этой области в надпочечниках синтезируются катехоламины (адреналин и норадреналин).
Надпочечники являются жизненно необходимым органами и выполняют разнообразные функции посредством выработки ряда гормонов, обладающих специфическими свойствами. Как было уже сказано немного выше, в этих эндокринных железах вырабатываются минералокортикоиды (альдостерон, дезоксикортикостерон, кортикостерон), глюкокортикостероиды (кортизол и кортизон), андрогены и катехоламины (адреналин и норадреналин). Жизненно необходима для человека секреция надпочечниками альдостерона и кортизола. Альдостерон является единственным минералокортикоидом, который надпочечники выделяют в кровь. Этот стероидный гормон способствует задержке в организме натрия, хлоридов и воды и выделению калия вместе с мочой. Он способствует увеличению системного артериального давления, общего объема циркулирующей крови, влияет на ее кислотно-основное состояние и осмолярность. Альдостерон регулирует правильную работу потовых и желудочно-кишечных желез.
Этот стероидный гормон способствует задержке в организме натрия, хлоридов и воды и выделению калия вместе с мочой. Он способствует увеличению системного артериального давления, общего объема циркулирующей крови, влияет на ее кислотно-основное состояние и осмолярность. Альдостерон регулирует правильную работу потовых и желудочно-кишечных желез.
Кортизол, как и альдостерон, также относится к стероидным гормонам. Он оказывает разностороннее действие на обмен веществ (метаболизм) в органах и тканях организма. Кортизол стимулирует образование большого количества глюкозы и гликогена в печени и ингибирует (блокирует) утилизацию их в периферических тканях. Это способствует развитию гипергликемии (увеличению в крови уровня глюкозы). В жировой, лимфоидной, костной и мышечной ткани данный гормон стимулирует распад белков. В печени он, наоборот, активирует синтез новых протеинов. Кортизол регулирует и жировой обмен. В частности, он способствует распаду жиров в одних тканях (например, жировой) и липогенез (образование новых жиров) в других (туловище, лицо). Этот глюкокортикоид является главным гормоном стресса, который помогает организму приспособиться к действию различных стрессовых факторов (инфекциям, физическому перенапряжению, психическим или механическим травмам, хирургическим вмешательствам и др.).
Этот глюкокортикоид является главным гормоном стресса, который помогает организму приспособиться к действию различных стрессовых факторов (инфекциям, физическому перенапряжению, психическим или механическим травмам, хирургическим вмешательствам и др.).
Андрогены вырабатываются клетками сетчатой зоны коры надпочечников. Основными их представителями являются дегидроэпиандростерон, этиохоланолон, андростендиол и андростендион.
Тестостерон и эстрогены надпочечниками практически не вырабатываются. Андрогены, которые вырабатываются в больших количествах в надпочечниках, оказывают на ткани организма гораздо меньшее действие, чем это делают основные половые гормоны. Так, например, тестостерон по своей активности превосходит действие андростендиона в 10 раз. Андрогены отвечают за развитие вторичных половых признаков, таких как изменение голоса, оволосение на теле, развитие половых органов и др., регулируют обмен веществ, повышают либидо, то есть сексуальное влечение.
Катехоламины (адреналин и норадреналин), которые образуются в мозговом веществе надпочечников, отвечают за адаптацию организма к острым стрессовым воздействиям со стороны окружающей среды. Эти гормоны увеличивают частоту сердечных сокращений, регулируют артериальное давление. Также они участвуют в тканевом метаболизме (обмен веществ), посредством ингибирования выброса инсулина (гормон, который нормализует уровень глюкозы в крови) из поджелудочной железы, активации липолиза (расщепления жиров) в жировой ткани и распада гликогена в печени.
Эти гормоны увеличивают частоту сердечных сокращений, регулируют артериальное давление. Также они участвуют в тканевом метаболизме (обмен веществ), посредством ингибирования выброса инсулина (гормон, который нормализует уровень глюкозы в крови) из поджелудочной железы, активации липолиза (расщепления жиров) в жировой ткани и распада гликогена в печени.
Причины развития болезни Аддисона
Болезнь Аддисона – это эндокринное заболевание, возникающее в результате разрушения тканей коры надпочечников под действием определенных вредоносных факторов. По-другому данную болезнь еще называют первичным гипокортицизмом (или первичной надпочечной недостаточностью). Эта патология является достаточно редким заболеванием и по статистике встречается только в 50 – 100 новых случаев на 1 миллион взрослых в год. Первичный гипокортицизм возникает гораздо чаще, чем вторичный.
Вторичная надпочечниковая недостаточность является отдельным эндокринным заболеванием и не относится к болезни Аддисона, так как она появляется в результате нарушения секреции гипофизом адренокортикотропного гормона (АКТГ), который служит естественным стимулятором функционирования коры надпочечников. Этот гормон контролирует выработку и секрецию гормонов (в основном, глюкокортикостероидов и андрогенов) коры надпочечников. В условиях дефицита АКТГ пучковая (средняя) и сетчатая (внутренняя) зоны коры надпочечников подвергаются постепенной атрофии, что приводит к надпочечниковой недостаточности, но уже вторичной (так как первопричина заболевания не в самих надпочечниках).
Этот гормон контролирует выработку и секрецию гормонов (в основном, глюкокортикостероидов и андрогенов) коры надпочечников. В условиях дефицита АКТГ пучковая (средняя) и сетчатая (внутренняя) зоны коры надпочечников подвергаются постепенной атрофии, что приводит к надпочечниковой недостаточности, но уже вторичной (так как первопричина заболевания не в самих надпочечниках).
При болезни Аддисона поражаются сразу все три зоны коры (коркового вещества) надпочечников – клубочковая, пучковая и сетчатая, поэтому, считается, что первичный гипокортицизм клинически протекает тяжелее, чем вторичный. Следует также отметить тот факт, что все симптомы, которые имеют место у пациента при болезни Аддисона, связаны только с деструкцией коры надпочечников, а не их мозгового вещества, возможное разрушение которого (в зависимости от причины первичного гипокортицизма) не играет никакой роли в механизме развития данной патологии. Как было уже сказано немного выше, болезнь Аддисона возникает в результате действия на кору надпочечников определенных повреждающих факторов. Ими могут быть различные микроорганизмы (бактерии, грибки, вирусы), аутоиммунные процессы, новообразования (опухолевое или метастатическое поражение надпочечников), генетические нарушения (например, адренолейкодистрофия), нарушение кровоснабжения коры надпочечников (ДВС-синдром, антифосфолипидный синдром).
Ими могут быть различные микроорганизмы (бактерии, грибки, вирусы), аутоиммунные процессы, новообразования (опухолевое или метастатическое поражение надпочечников), генетические нарушения (например, адренолейкодистрофия), нарушение кровоснабжения коры надпочечников (ДВС-синдром, антифосфолипидный синдром).
Наиболее частыми причинами болезни Аддисона являются:
- аутоиммунное поражение тканей коры надпочечников;
- туберкулез;
- адреналэктомия;
- метастатическое поражение коры надпочечников;
- грибковые инфекции;
- ВИЧ-инфекция;
- адренолейкодистрофия;
- антифосфолипидный синдром;
- ДВС-синдром;
- синдром Уотерхауса-Фридериксена.
Аутоиммунное поражение тканей коры надпочечников
В подавляющем большинстве всех новых случаев (в 80 — 90%) болезнь Аддисона возникает в результате аутоиммунного разрушения коры надпочечников. Такое разрушение появляется вследствие нарушения нормального развития иммунной системы. Клетки иммунной системы (лимфоциты) у таких пациентов при контакте с тканью надпочечников (через кровь) начинают воспринимать ее как чужеродную. Из-за этого они активируются и инициируют деструкцию коры надпочечников. Важную роль в процессе аутоиммунной деструкции играют аутоантитела, которые секретируют в кровь лимфоциты.
Такое разрушение появляется вследствие нарушения нормального развития иммунной системы. Клетки иммунной системы (лимфоциты) у таких пациентов при контакте с тканью надпочечников (через кровь) начинают воспринимать ее как чужеродную. Из-за этого они активируются и инициируют деструкцию коры надпочечников. Важную роль в процессе аутоиммунной деструкции играют аутоантитела, которые секретируют в кровь лимфоциты.
Аутоантитела – это антитела (белковые, защитные молекулы), направленные против собственных тканей (в данном случае против тканей коры надпочечников), которые специфически связываются с различными структурами на клетках коры надпочечников и, тем самым, вызывают их гибель. Основными типами аутоантител, наблюдающихся в крови у больных с аутоиммунной болезнью Аддисона, являются антитела к ферментам надпочечникового стероидогенеза (процесса образования стероидных гормонов) – 21-гидроксилазе (P450c21), 17а-гидроксилазе (P450c17), ферменту отщепления боковой цепи (P450scc).
Туберкулез
Туберкулез – это инфекционное заболевание, вызываемое микобактериями (обычно микобактерией туберкулеза). Туберкулез надпочечников является второй по статистике причиной развития первичного гипокортицизма. В подавляющем большинстве случаев данная форма туберкулеза является вторичной, то есть инфицирование тканей коры надпочечников происходит уже при имеющемся в организме пациента туберкулезном очаге, который расположен в каком-либо другом органе (например, легких, костях, печени, почках и др.). Занос инфекции (вредоносных микобактерий) в надпочечники из первично пораженных органов чаще всего происходит гематогенно (посредством крови). Попадая внутрь надпочечников, микобактерии начинают размножаться и разрушать их нормальную ткань, при этом нередко отмечается деструкция не только коры, но и мозгового вещества этих эндокринных желез. Первые симптомы болезни Аддисона, спровоцированной туберкулезным поражением, начинают возникать у пациента только после того как микобактерии разрушат значительную долю тканей коры надпочечников (около 80 – 90%). Именно поэтому диагностировать эту форму заболевания на ранних стадиях довольно трудно.
Именно поэтому диагностировать эту форму заболевания на ранних стадиях довольно трудно.
Адреналэктомия
Болезнь Аддисона также может возникать в результате двусторонней адреналэктомии. Адреналэктомия – это хирургическое удаление одного или обоих надпочечников по медицинским показаниям. Чаще всего двусторонняя адреналэктомия производится у пациентов, имеющих опухолевое поражение обоих надпочечников. Удаление двух надпочечников нередко осуществляется у лиц, страдающих болезнью Иценко-Кушинга. При данном эндокринном заболевании ткани гипофиза производят в избыточном количестве адренокортикотропный гормон (АКТГ), который заставляет работать кору надпочечников интенсивнее, что сопровождается развитием гиперкортицизма (повышенное выделение корой надпочечников своих гормонов).
Метастатическое поражение коры надпочечников
В некоторых случаях кора надпочечников может поражаться опухолевыми метастазами. Метастазирование – это ситуация, при которой опухолевые клетки из первичного очага рака, расположенного в одном органе, заносятся с током крови (или, например, через лимфу) в другие органы (не обязательно соседние). Проникнув во вторичные органы, злокачественные клетки начинают интенсивно размножаться, что сопровождается образованием новых (но уже вторичных — дочерних) опухолей, которые называются метастазами. Метастазирование служит одним из осложнений большинства злокачественных новообразований и абсолютно не характерно для доброкачественных опухолей. Метастазы в коре надпочечников отмечаются в 57% случаев рака молочной железы, в 32% случаев меланомы (злокачественная опухоль из пигментных клеток — меланоцитов), в 38% случаев бронхогенного рака легкого. Также довольно частой причиной болезни Аддисона, связанной с метастатическим поражением коры надпочечников, служит неходжкинская крупноклеточная лимфома (злокачественное заболевание крови).
Проникнув во вторичные органы, злокачественные клетки начинают интенсивно размножаться, что сопровождается образованием новых (но уже вторичных — дочерних) опухолей, которые называются метастазами. Метастазирование служит одним из осложнений большинства злокачественных новообразований и абсолютно не характерно для доброкачественных опухолей. Метастазы в коре надпочечников отмечаются в 57% случаев рака молочной железы, в 32% случаев меланомы (злокачественная опухоль из пигментных клеток — меланоцитов), в 38% случаев бронхогенного рака легкого. Также довольно частой причиной болезни Аддисона, связанной с метастатическим поражением коры надпочечников, служит неходжкинская крупноклеточная лимфома (злокачественное заболевание крови).
Грибковые инфекции
Грибковая инфекция довольно редко служит причиной развития болезни Аддисона. Первичный гипокортицизм чаще всего отмечается при паракокцидиомикозе, кокцидиомикозе, системном (распространенном) гистоплазмозе, кандидозе, бластомикозе, криптококкозе. Самой распространенной причиной болезни Аддисона из всех вышеперечисленных видов микозов является паракокцидиомикоз, вызываемый грибками рода Paracoccidioides Brasiliensis. Этот тип микоза, в основном, встречается у населения стран Латинской Америки. При паракокцидиомикозе поражаются легкие, слизистая оболочка верхних дыхательных путей, лимфатические узлы, в некоторых случаях кожа и надпочечники. В поврежденных вредоносными грибками тканях образуются гранулемы (воспалительные узелки), микроабсцессы (мелкие полости заполненные гноем) и участки очагового некроза (зоны с мертвой тканью).
Самой распространенной причиной болезни Аддисона из всех вышеперечисленных видов микозов является паракокцидиомикоз, вызываемый грибками рода Paracoccidioides Brasiliensis. Этот тип микоза, в основном, встречается у населения стран Латинской Америки. При паракокцидиомикозе поражаются легкие, слизистая оболочка верхних дыхательных путей, лимфатические узлы, в некоторых случаях кожа и надпочечники. В поврежденных вредоносными грибками тканях образуются гранулемы (воспалительные узелки), микроабсцессы (мелкие полости заполненные гноем) и участки очагового некроза (зоны с мертвой тканью).
ВИЧ-инфекция
Наличие у пациента ВИЧ-инфекции (болезнь, возникающая в результате инфицирования вирусом иммунодефицита человека) может служить причиной развития болезни Аддисона. Дело в том, что при ВИЧ-инфекции у пациентов появляется серьезное иммунодефицитное состояние, при котором их организм достаточно тяжело борется с любыми инфекциями, вследствие чего они часто страдают разнообразными инфекционными заболеваниями. Наличие нарушенного иммунитета и частых системных инфекций (например, грибковых инфекций, цитомегаловирусной инфекции и др.) при определенных обстоятельствах может служить причиной первичного гипокортицизма (так как присутствие в организме какой-либо инфекции, рано или поздно, приведет к повреждению тканей коры надпочечников). Считается, что у пациентов с ВИЧ-инфекцией латентно (скрыто) протекающая болезнь Аддисона отмечается в 8 – 11% всех случаев.
Наличие нарушенного иммунитета и частых системных инфекций (например, грибковых инфекций, цитомегаловирусной инфекции и др.) при определенных обстоятельствах может служить причиной первичного гипокортицизма (так как присутствие в организме какой-либо инфекции, рано или поздно, приведет к повреждению тканей коры надпочечников). Считается, что у пациентов с ВИЧ-инфекцией латентно (скрыто) протекающая болезнь Аддисона отмечается в 8 – 11% всех случаев.
Адренолейкодистрофия
Адренолейкодистрофия (АЛД) – это наследственное заболевание, возникающее в результате делеции (удаления) определенного участка на длинном плече X-хромосомы. В этом участке локализуется ген ALD, который кодирует структуру фермента лигноцероил-КоА-синтетазы, участвующего в окислении длинноцепочечных жирных кислот (ДЖК) в клетках центральной нервной системы, надпочечников и в других тканях. При адренолейкодистрофии этот фермент не вырабатывается, в результате чего в нервной ткани и в коре надпочечников накапливается большое количество жира (ДЖК вместе с эфирами холестерина), что постепенно приводит к их дегенерации и отмиранию. Данная патология чаще всего регистрируется у мужчин (адренолейкодистрофия является X-сцепленным рецессивным заболеванием).
Данная патология чаще всего регистрируется у мужчин (адренолейкодистрофия является X-сцепленным рецессивным заболеванием).
Существуют различные клинические варианты течения адренолейкодистрофии и не всегда при данной болезни могут серьезно поражаться ткани коры надпочечников. Например, у части таких пациентов преобладает неврологическая симптоматика (ювенильная форма адренолейкодистрофии), тогда как признаки болезни Аддисона могут долго отсутствовать (особенно в начале заболевания).
Помимо надпочечников и центральной нервной системы при адренолейкодистрофии нередко развивается первичный мужской гипогонадизм (недостаточность функции яичек), что может сказаться на репродуктивной способности мужчин. Адренолейкодистрофия является третьей по статистике причиной развития болезни Аддисона (после аутоиммунной деструкции коркового вещества надпочечников и туберкулеза надпочечников). Сопутствующая неврологическая симптоматика, встречающаяся при АЛД, делает прогноз болезни Аддисона менее благоприятной, по сравнению с другими причинами первичного гипокортицизма.
Антифосфолипидный синдром
Антифосфолипидный синдром (АФС) является патологическим состоянием, характеризующимся нарушением свертываемости крови и появлением в различных сосудах тромбов. Причиной появления АФС служат антитела (белковые, защитные молекулы) к фосфолипидам клеточных мембран тромбоцитов, эндотелиоцитов (клеток, выстилающих внутреннюю поверхность сосудов). Считается, что возникновение таких антител в крови у пациентов связано с нарушением работы иммунной системы.
Антифосфолипидные антитела оказывают прямое повреждающее действие на эндотелий (внутреннюю стенку) сосудов, подавляют производство эндотелиоцитами специальных белков (простациклина, тромбомодулина, антитромбина III), обладающих антикоагулянтными (противосвертывающими) свойствами, вследствие чего они (антитела) способствуют развитию тромбозов. При антифосфолипидном синдроме, в очень редких случаях, может иметь место двусторонний тромбоз надпочечниковых вен, что может послужить причиной повреждения тканей коры надпочечников (из-за нарушения венозного оттока из тканей надпочечников) и развития болезни Аддисона.
ДВС-синдром
Ткани коркового вещества надпочечников довольно часто поражаются при синдроме диссеминированного внутрисосудистого свертывания крови (ДВС-синдроме), который является одной из патологий системы гемостаза (система, контролирующая жидкое состояние крови и остановку кровотечений). На первых стадиях ДВС-синдрома в различных тканях и органах образуются многочисленные мелкие тромбы (гиперкоагуляция крови), что впоследствии (на более поздних стадиях данного синдрома) осложняется коагулопатией потребления (то есть истощением системы свертывания), сопровождающейся тяжелым нарушением свертывания крови и развитием геморрагического синдрома (в различных органах и тканях возникают спонтанные трудно останавливаемые кровотечения).
Причинами ДВС-синдрома могут служить разнообразные состояния, такие как тяжелые механические травмы, гемолитические анемии (снижение количества эритроцитов в крови на фоне их чрезмерного разрушения), лейкозы, опухоли, системные бактериальные, вирусные, грибковые инфекции, аутоиммунные заболевания, внутриутробная гибель плода, преждевременная отслойка плаценты, переливание несовместимой крови и др. При ДВС-синдроме в сосудах тканей коры надпочечников можно обнаружить многочисленные мелкие тромбы, которые служат непосредственной причиной расстройства микроциркуляции, нарушения кровоснабжения, гибели клеток клубочковой, пучковой и сетчатой зон и развития первичной надпочечниковой недостаточности (болезни Аддисона).
При ДВС-синдроме в сосудах тканей коры надпочечников можно обнаружить многочисленные мелкие тромбы, которые служат непосредственной причиной расстройства микроциркуляции, нарушения кровоснабжения, гибели клеток клубочковой, пучковой и сетчатой зон и развития первичной надпочечниковой недостаточности (болезни Аддисона).
Синдром Уотерхауса-Фридериксена
Синдром Уотерхауса-Фридериксена представляет собой патологию, возникающую в результате острого геморрагического инфаркта обоих надпочечников (то есть массивного кровоизлияния внутрь тканей надпочечников) и обычно наблюдающуюся при сепсисе (тяжелое, системное, воспалительное состояние, вызванное распространением инфекции по всему организму из первичного очага). При сепсисе нередко развивается ДВС-синдром, который, по сути, и служит непосредственной причиной кровоизлияния внутрь надпочечников. При таком внутреннем кровотечении ткани надпочечников быстро переполняются кровью. Кровоток в них резко замедляется, венозная кровь из надпочечников не удаляется, а новая артериальная кровь не поступает в достаточных количествах.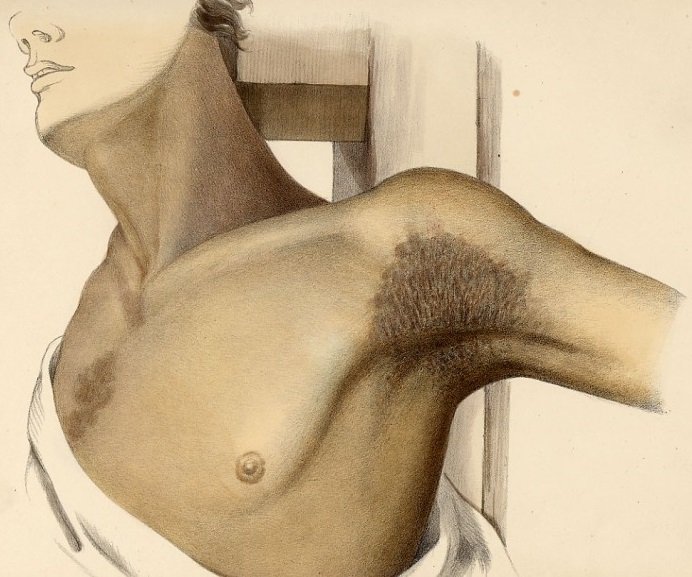 Из-за этого клетки коры надпочечников быстро погибают. Развивается надпочечниковая недостаточность. Быстрое переполнение надпочечников кровью при синдроме Уотерхауса-Фридериксена спровоцировано не только нарушением свертываемости крови (причиной которого служит ДВС-синдром), но и особенностями кровоснабжения самих надпочечников.
Из-за этого клетки коры надпочечников быстро погибают. Развивается надпочечниковая недостаточность. Быстрое переполнение надпочечников кровью при синдроме Уотерхауса-Фридериксена спровоцировано не только нарушением свертываемости крови (причиной которого служит ДВС-синдром), но и особенностями кровоснабжения самих надпочечников.
Чаще всего синдром Уотерхауса-Фридериксена встречается при сепсисе, развивающимся на фоне менингококковой инфекции.
Патогенез болезни Аддисона
Патогенез (механизм развития) болезни Аддисона обусловлен дефицитом в организме альдостерона, кортизола и избытком секреции меланоцитостимулирующего гормона. Альдостерон является важным гормоном, который регулирует в организме уровень натрия и воды, количество калия и состояние гемодинамики. Он действует на почки и заставляет их задерживать в организме натрий и воду (в обмен на калий), что, тем самым, предотвращает их быстрое удаление из организма. При дефиците альдостерона почки начинают быстро выводить с мочой натрий и воду, что приводит к быстрому обезвоживанию организма, нарушению водно-электролитного баланса в организме, сгущению крови, замедлению циркуляции крови и кровоснабжения периферических тканей. На фоне этих изменений серьезнее всего страдают сердечно-сосудистая система (повышается частота сердечных сокращений, боли в сердце, снижается артериальное давление и др.), желудочно-кишечный тракт (появляются боли в животе, тошнота, запоры, рвота и др.), центральная нервная система (возникают обмороки, судороги, психические расстройства, головная боль и др.). Нарушение выведения калия из организма при первичном гипокортицизме способствует его накоплению в крови и развитию так называемой гиперкалиемии, которая оказывает вредное воздействие на работу сердца и скелетных мышц.
На фоне этих изменений серьезнее всего страдают сердечно-сосудистая система (повышается частота сердечных сокращений, боли в сердце, снижается артериальное давление и др.), желудочно-кишечный тракт (появляются боли в животе, тошнота, запоры, рвота и др.), центральная нервная система (возникают обмороки, судороги, психические расстройства, головная боль и др.). Нарушение выведения калия из организма при первичном гипокортицизме способствует его накоплению в крови и развитию так называемой гиперкалиемии, которая оказывает вредное воздействие на работу сердца и скелетных мышц.
Отсутствие в организме кортизола делает его очень чувствительным к стрессовым для него факторам (например, инфекциям, физическому перенапряжению, механическим травмам и др.), при действии которых, собственно говоря, и происходит декомпенсация болезни Аддисона.
Кортизол является одним из гормонов, регулирующих углеводный обмен в организме. Он стимулирует образование глюкозы из других химических веществ (глюконеогенез), гликолиз (распад гликогена). Кроме того кортизол оказывает похожее с альдостероном действие на почки (то есть он способствует задержке в организме воды и натрия и удалению калия). Данный гормон также влияет на белковый и жировой обмен, усиливая распад белков и накопление жиров в периферических тканях. Кортизол хорошо взаимодействует с гормонами щитовидной железы и катехоламинами, то есть гормонами мозгового вещества надпочечников. Дефицит кортизола при болезни Аддисона приводит к нарушению углеводного, белкового, жирового обмена и снижению общей резистентности, то есть сопротивляемости организма стрессу.
Кроме того кортизол оказывает похожее с альдостероном действие на почки (то есть он способствует задержке в организме воды и натрия и удалению калия). Данный гормон также влияет на белковый и жировой обмен, усиливая распад белков и накопление жиров в периферических тканях. Кортизол хорошо взаимодействует с гормонами щитовидной железы и катехоламинами, то есть гормонами мозгового вещества надпочечников. Дефицит кортизола при болезни Аддисона приводит к нарушению углеводного, белкового, жирового обмена и снижению общей резистентности, то есть сопротивляемости организма стрессу.
При болезни Аддисона у пациентов часто наблюдается гиперпигментация кожных покровов (повышенное отложение в коже пигмента меланина). Она вызвана избытком в крови меланоцитостимулирующего гормона, который стимулирует меланоциты (пигментные клетки) кожи к производству меланина. Такой избыток возникает вследствие того, что при первичном гипокортицизме в гипофизе увеличивается концентрация общего для меланоцитостимулирующего и адренокортикотропного гормонов предшественника – проопиомеланокортина. Проопиомеланокортин не обладает гормональными свойствами. По химической структуре он является большой белковой молекулой, которая при расщеплении (определенными ферментами) разделяется на несколько пептидов-гормонов (адренокортикотропный, меланоцитостимулирующий, бета-липотропный гормоны и др.). Увеличенное содержание в крови меланоцитостимулирующего гормона постепенно вызывает потемнение кожи, поэтому болезнь Аддисона еще называют бронзовой болезнью.
Проопиомеланокортин не обладает гормональными свойствами. По химической структуре он является большой белковой молекулой, которая при расщеплении (определенными ферментами) разделяется на несколько пептидов-гормонов (адренокортикотропный, меланоцитостимулирующий, бета-липотропный гормоны и др.). Увеличенное содержание в крови меланоцитостимулирующего гормона постепенно вызывает потемнение кожи, поэтому болезнь Аддисона еще называют бронзовой болезнью.
Симптомы и признаки болезни Аддисона
Пациенты с болезнью Аддисона при обращении к врачу чаще всего предъявляют жалобы на имеющуюся у них общую слабость, повышенную утомляемость, хроническую усталость, периодическую головную боль, головокружения, обморочные состояния. Они нередко испытывают беспокойство, тревогу, повышенное внутреннее напряжение. У части больных можно обнаружить неврологические и психические расстройства (нарушение памяти, снижение мотивации, негативизм, потерю интереса к происходящим событиям, повышенную раздражительность, подавленность, депрессию, оскудение мышления и др.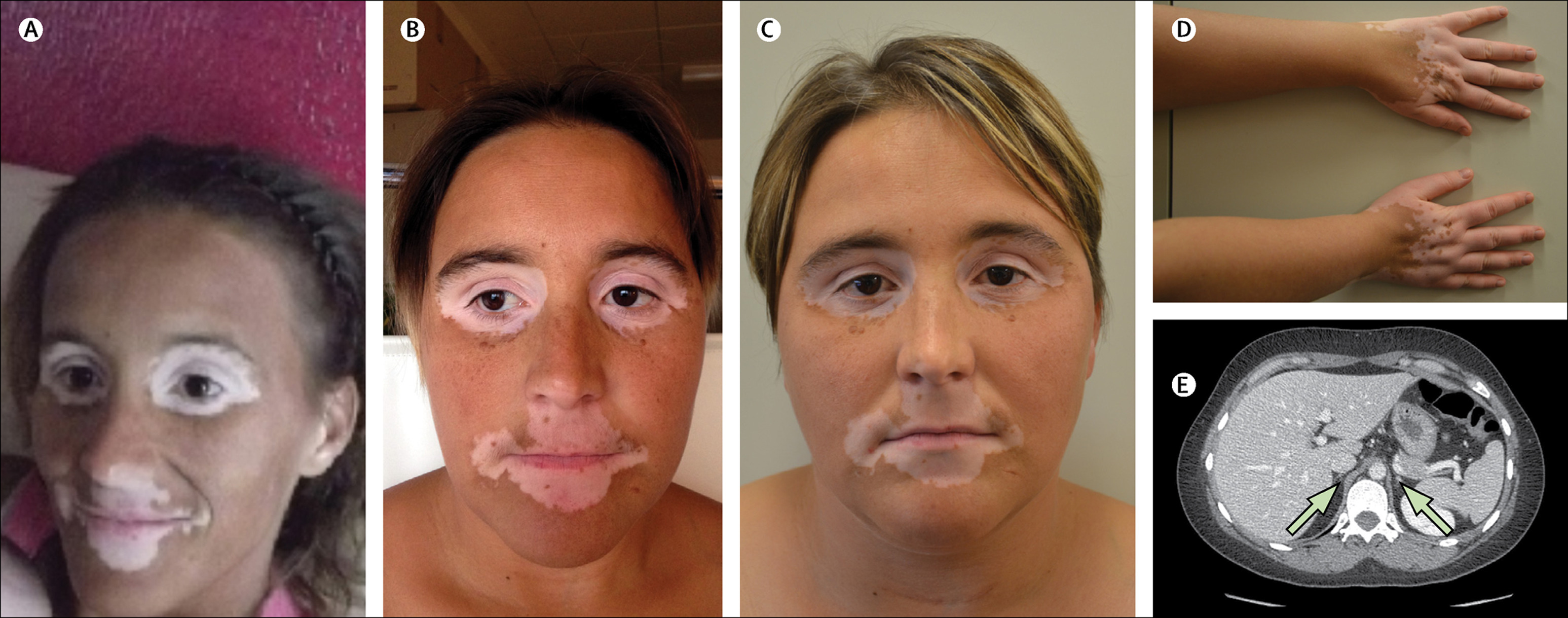 ). Вся эта симптоматика обусловлена нарушениями во всех типах обмена (углеводного, белкового, липидного, водно-электролитного) в головном мозге.
). Вся эта симптоматика обусловлена нарушениями во всех типах обмена (углеводного, белкового, липидного, водно-электролитного) в головном мозге.
При первичном гипокортицизме у пациентов наблюдается прогрессирующая потеря массы тела. Это связано с постоянными потерями организмом жидкости, присутствием у них анорексии (отсутствия аппетита) и истинным снижением количества мышечной массы. У них часто отмечается мышечная слабость, миалгия (боли в мышцах), мышечные судороги, тремор (непроизвольное дрожание пальцев рук), нарушение чувствительности конечностей. Мышечную симптоматику можно объяснить нарушениями водно-электролитного баланса (в частности, повышенным содержанием калия и кальция в крови), которые обычно отмечаются у таких больных.
Достаточно распространенной при болезни Аддисона является разнообразная гастроинтестинальная (желудочно-кишечная) симптоматика в виде тошноты, рвоты, запоров (иногда диареи), диффузных (распространенных) болей в животе. Больные постоянно испытывают влечение к соленой пище. Кроме этого их постоянно беспокоит чувство жажды, поэтому они часто пьют воду. Нередко такие пациенты долгое время наблюдаются у гастроэнтеролога в связи с тем, что у их выявляют различные заболевания желудочно-кишечной системы (например, язву желудка, двенадцатиперстной кишки, спастический колит, гастрит), а надпочечниковая недостаточность остается продолжительное время необнаруженной. Гастроинтестинальная симптоматика при болезни Аддисона, как правило, коррелирует со степенью анорексии (отсутствия аппетита) и снижения массы тела.
Больные постоянно испытывают влечение к соленой пище. Кроме этого их постоянно беспокоит чувство жажды, поэтому они часто пьют воду. Нередко такие пациенты долгое время наблюдаются у гастроэнтеролога в связи с тем, что у их выявляют различные заболевания желудочно-кишечной системы (например, язву желудка, двенадцатиперстной кишки, спастический колит, гастрит), а надпочечниковая недостаточность остается продолжительное время необнаруженной. Гастроинтестинальная симптоматика при болезни Аддисона, как правило, коррелирует со степенью анорексии (отсутствия аппетита) и снижения массы тела.
Одним из основных признаков болезни Аддисона служит гипотония (низкое артериальное давление). У большинства больных систолическое артериальное давление колеблется в пределах 110 – 90 мм.рт.ст., а диастолическое может падать ниже 70 мм.рт.ст. На начальных этапах болезни гипотония может иметь только ортостатический характер (то есть артериальное давление будет падать при смене положения тела с горизонтального на вертикальное). В дальнейшем артериальная гипотония начинает возникать при воздействии на организм практически любого для человека стрессового фактора. Кроме низкого артериального давления также может наблюдаться тахикардия (учащенное сердцебиение), боли в области сердца, одышка. Иногда артериальное давление может оставаться в пределах нормальных значений, в редких случаях оно может быть повышенным (особенно у пациентов с гипертонической болезнью). У женщин, страдающих болезнью Аддисона, порой нарушается менструальный цикл. Месячные либо исчезают полностью (то есть наступает аменорея), либо становятся нерегулярными. Это нередко серьезно сказывается на их репродуктивной функции и выливается в различные проблемы, связанные с беременностью. У мужчин при этом заболевании появляется импотенция (нарушение эрекции полового члена).
В дальнейшем артериальная гипотония начинает возникать при воздействии на организм практически любого для человека стрессового фактора. Кроме низкого артериального давления также может наблюдаться тахикардия (учащенное сердцебиение), боли в области сердца, одышка. Иногда артериальное давление может оставаться в пределах нормальных значений, в редких случаях оно может быть повышенным (особенно у пациентов с гипертонической болезнью). У женщин, страдающих болезнью Аддисона, порой нарушается менструальный цикл. Месячные либо исчезают полностью (то есть наступает аменорея), либо становятся нерегулярными. Это нередко серьезно сказывается на их репродуктивной функции и выливается в различные проблемы, связанные с беременностью. У мужчин при этом заболевании появляется импотенция (нарушение эрекции полового члена).
Гиперпигментация при болезни Аддисона
Гиперпигментация (потемнение кожи) при болезни Аддисона является одним из важнейших симптомов, характерных для данной патологии. Обычно существует четкая корреляция (зависимость) между давностью присутствия у пациента надпочечниковой недостаточности, ее тяжестью и интенсивностью окраски кожных покровов и слизистых оболочек, так как этот признак возникает у больных одним из первых. В большинстве случаев, сначала начинают темнеть открытые участки тела, которые постоянно контактируют с солнечным светом. Чаще всего ими являются кожа рук, лица и шеи. Кроме того наблюдается усиление пигментации (отложения меланина) в области тех участков тела, которые в норме имеют достаточно интенсивную темную окраску. Речь идет о коже мошонки, сосков, перианальной зоны (кожный покров вокруг ануса). Затем начинает темнеть кожа складок на ладонях (ладонных линий), а также тех участков, о которых постоянно трутся складки одежды (такое наблюдается в области воротника, пояса, локтевых сгибов и др.).
Обычно существует четкая корреляция (зависимость) между давностью присутствия у пациента надпочечниковой недостаточности, ее тяжестью и интенсивностью окраски кожных покровов и слизистых оболочек, так как этот признак возникает у больных одним из первых. В большинстве случаев, сначала начинают темнеть открытые участки тела, которые постоянно контактируют с солнечным светом. Чаще всего ими являются кожа рук, лица и шеи. Кроме того наблюдается усиление пигментации (отложения меланина) в области тех участков тела, которые в норме имеют достаточно интенсивную темную окраску. Речь идет о коже мошонки, сосков, перианальной зоны (кожный покров вокруг ануса). Затем начинает темнеть кожа складок на ладонях (ладонных линий), а также тех участков, о которых постоянно трутся складки одежды (такое наблюдается в области воротника, пояса, локтевых сгибов и др.).
В некоторых случаях у части пациентов может темнеть слизистая оболочка десен, губ, щек, мягкого и твердого неба.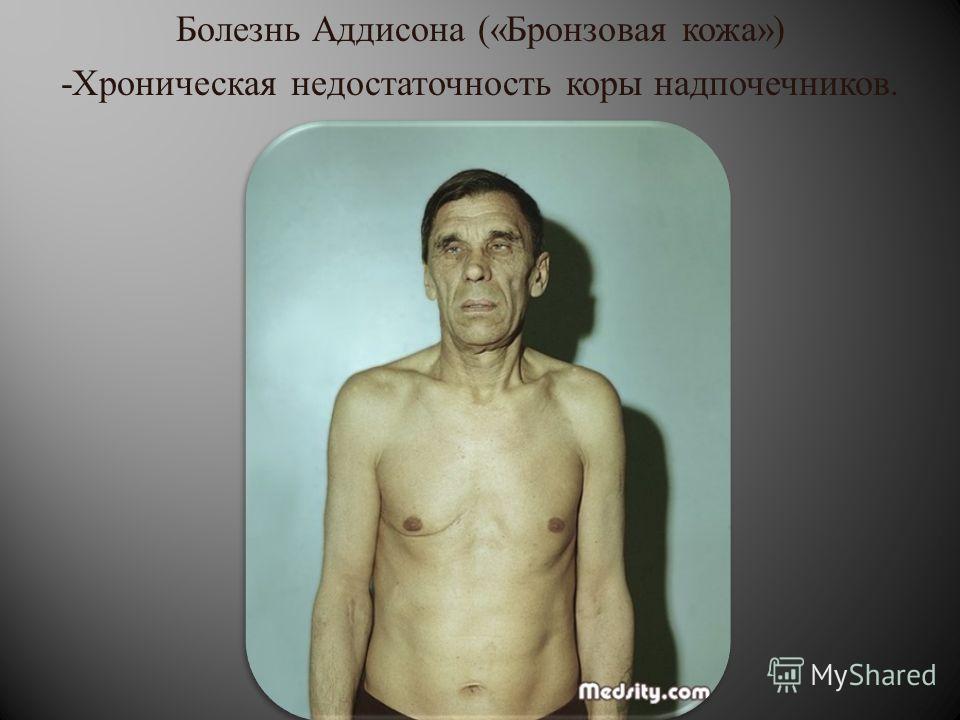 В более поздних стадиях отмечается диффузная гиперпигментация кожи, которая может иметь различную выраженность. Кожный покров может приобретать дымчатый, бронзовый, бурый оттенок. Если болезнь Аддисона вызвана аутоиммунным разрушением коры надпочечников, то нередко на фоне пигментации на коже у пациентов может появляться витилиго (беспигментные, белые пятна). Витилиго может возникать практически в любом месте на теле и иметь различные размеры и очертания. Его достаточно легко обнаружить, так как кожа у таких больных гораздо темнее, чем сами пятна, что создает между ними четкий контраст. Очень редко при болезни Аддисона гиперпигментация кожи может отсутствовать или быть минимально выраженной (незаметной), такое состояние называется «белый аддисонизм». Поэтому отсутствие потемнения кожи еще не является доказательством того, что у данного пациента нет надпочечниковой недостаточности.
В более поздних стадиях отмечается диффузная гиперпигментация кожи, которая может иметь различную выраженность. Кожный покров может приобретать дымчатый, бронзовый, бурый оттенок. Если болезнь Аддисона вызвана аутоиммунным разрушением коры надпочечников, то нередко на фоне пигментации на коже у пациентов может появляться витилиго (беспигментные, белые пятна). Витилиго может возникать практически в любом месте на теле и иметь различные размеры и очертания. Его достаточно легко обнаружить, так как кожа у таких больных гораздо темнее, чем сами пятна, что создает между ними четкий контраст. Очень редко при болезни Аддисона гиперпигментация кожи может отсутствовать или быть минимально выраженной (незаметной), такое состояние называется «белый аддисонизм». Поэтому отсутствие потемнения кожи еще не является доказательством того, что у данного пациента нет надпочечниковой недостаточности.
Диагностика болезни Аддисона
Диагностика болезни Аддисона в настоящее время не является трудной задачей. Диагноз данной патологии ставится на основании клинических (сбор анамнеза, внешний осмотр), лабораторных и лучевых методов исследований. На первом этапе диагностики врачу важно понять, являются ли на самом деле симптомы (например, гиперпигментация кожных покровов, сниженное артериальное давление, общая слабость, боли в животе, тошнота, рвота, нарушение менструального цикла и др.), обнаруживаемые (с помощью клинических обследований) у обратившегося к нему пациента, признаками первичной надпочечниковой недостаточности. Чтобы это подтвердить, он назначает ему прохождение некоторых лабораторных исследований (общий анализ крови и биохимический анализ крови, анализ мочи). Эти исследования должны выявить наличие у больного в моче и в плазме крови сниженного уровня гормонов надпочечников (альдостерона, кортизола), повышенной концентрации адренокортикотропного гормона (АКТГ), ренина, а также нарушенное состояние водно-электролитного состояния крови, углеводного обмена и определенные нарушения в клеточном составе крови.
Диагноз данной патологии ставится на основании клинических (сбор анамнеза, внешний осмотр), лабораторных и лучевых методов исследований. На первом этапе диагностики врачу важно понять, являются ли на самом деле симптомы (например, гиперпигментация кожных покровов, сниженное артериальное давление, общая слабость, боли в животе, тошнота, рвота, нарушение менструального цикла и др.), обнаруживаемые (с помощью клинических обследований) у обратившегося к нему пациента, признаками первичной надпочечниковой недостаточности. Чтобы это подтвердить, он назначает ему прохождение некоторых лабораторных исследований (общий анализ крови и биохимический анализ крови, анализ мочи). Эти исследования должны выявить наличие у больного в моче и в плазме крови сниженного уровня гормонов надпочечников (альдостерона, кортизола), повышенной концентрации адренокортикотропного гормона (АКТГ), ренина, а также нарушенное состояние водно-электролитного состояния крови, углеводного обмена и определенные нарушения в клеточном составе крови.
Кроме того, помимо лабораторных тестов для подтверждения первичного гипокортицизма назначают кратковременные и длительные диагностические пробы. Эти пробы являются стимуляционными. Пациенту вводят внутримышечно или внутривенно искусственно синтезированный адренокортикотропный гормон (АКТГ), который выпускается под коммерческим названием синактен, синактен-депо или цинк-кортикотропин. В норме, при попадании в организм, данные препараты должны простимулировать кору надпочечников, вследствие чего ее ткани начнут интенсивно выделять гормоны (кортизол), концентрацию которых и определяют в крови через 30 и 60 минут после введения препаратов. Если пациент болен болезнью Аддисона, то надпочечники не смогут адекватно отвечать на стимуляцию синактеном (или синактеном-депо, или цинк-кортикотропином), в результате чего уровень надпочечниковых гормонов в плазме крови останется неизменным.
После того как было осуществлено подтверждение присутствия у пациента болезни Аддисона, врачу важно установить ее этиологию. Поскольку в подавляющем большинстве случаев (в 80 — 90%) причиной этого эндокринного заболевания служит аутоиммунное поражение тканей коры надпочечников, то больному необходимо сдать кровь на иммунологическое исследование. С помощью него можно будет выявить антитела к ферментам надпочечникового стероидогенеза (процесса образования стероидных гормонов) – 21-гидроксилазе (P450c21), 17а-гидроксилазе (P450c17), ферменту отщепления боковой цепи (P450scc), являющихся маркерами (индикаторами) первичного аутоиммунного гипокортицизма. Если такие антитела не были обнаружены, то следующим диагностическим тестом, который должен быть назначен – это биохимическое исследование крови на содержание в ней длинноцепочечных жирных кислот (ДЖК).
Поскольку в подавляющем большинстве случаев (в 80 — 90%) причиной этого эндокринного заболевания служит аутоиммунное поражение тканей коры надпочечников, то больному необходимо сдать кровь на иммунологическое исследование. С помощью него можно будет выявить антитела к ферментам надпочечникового стероидогенеза (процесса образования стероидных гормонов) – 21-гидроксилазе (P450c21), 17а-гидроксилазе (P450c17), ферменту отщепления боковой цепи (P450scc), являющихся маркерами (индикаторами) первичного аутоиммунного гипокортицизма. Если такие антитела не были обнаружены, то следующим диагностическим тестом, который должен быть назначен – это биохимическое исследование крови на содержание в ней длинноцепочечных жирных кислот (ДЖК).
Выявление ДЖК является важным диагностическим признаком адренолейкодистрофии, которая является третьей по статистике причиной развития болезни Аддисона. В случае отрицательного результата на наличие в крови ДЖК пациенту обычно назначают прохождение лучевых исследований (компьютерной томографии, магнитно-резонансной томографии), необходимых для визуализации структуры тканей коры надпочечников. Эти исследования, как правило, подтверждают наличие в надпочечниках метастазов рака или туберкулезного очага.
Эти исследования, как правило, подтверждают наличие в надпочечниках метастазов рака или туберкулезного очага.
Диагностические мероприятия в отношении ДВС-синдрома, синдрома Уотерхауса-Фридериксена, антифосфолипидного синдрома, грибковых инфекций, ВИЧ-инфекции довольно сложно рассматривать, так как существует множество факторов, влияющих на выбор того или иного диагностического метода. Все зависит от конкретной ситуации. К тому же все эти патологии являются довольно редкими причинами болезни Аддисона, и заподозрить присутствие надпочечниковой недостаточности при них не всегда так просто.
Диагностические методы, применяемые для обнаружения болезни Аддисона
| Название метода | Зачем проводиться данное исследование? |
| Анамнез | При сборе анамнеза врач расспрашивает пациента о беспокоящих его жалобах и об условиях, которые способствовали их появлению. Основными симптомами болезни Аддисона являются повышенная утомляемость, общая слабость, головокружение, головная боль, обморочные состояния, чувство беспокойства, тревоги, жажды, влечения к соленой пище, мышечная слабость, миалгия (боли в мышцах), мышечные судороги, боли в животе, тошнота, рвота, нарушение менструального цикла и др. Основными симптомами болезни Аддисона являются повышенная утомляемость, общая слабость, головокружение, головная боль, обморочные состояния, чувство беспокойства, тревоги, жажды, влечения к соленой пище, мышечная слабость, миалгия (боли в мышцах), мышечные судороги, боли в животе, тошнота, рвота, нарушение менструального цикла и др. |
| Внешний осмотр | При внешнем осмотре пациентов, страдающих болезнью Аддисона, можно выявить повышенную пигментацию кожных покровов, витилиго, снижение веса, артериальную гипотонию (пониженное артериальное давление), различные психические расстройства (нарушение памяти, снижение мотивации, потерю интереса к происходящим событиям, повышенную раздражительность, подавленность, депрессию и др.), тремор (непроизвольное дрожание пальцев рук), нарушение чувствительности конечностей. |
| Рентгенография и компьютерная томография | Компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) используются с целью выявления в надпочечниках метастазов, туберкулезных очагов. Рентгенография обычно назначается с целью выявления в легких туберкулезного процесса. КТ и МРТ головного и спинного мозга назначаются для подтверждения диагноза адренолейкодистрофии. Рентгенография обычно назначается с целью выявления в легких туберкулезного процесса. КТ и МРТ головного и спинного мозга назначаются для подтверждения диагноза адренолейкодистрофии. |
| Магнитно-резонансная томография | |
| Общий анализ крови | При болезни Аддисона в общем анализе крови можно обнаружить анемию (снижение количества эритроцитов и гемоглобина), лимфоцитоз (увеличение количества лимфоцитов), нейтропению (снижение количества нейтрофилов), эозинофилию (увеличение количества эозинофилов), повышенное СОЭ (скорость оседания эритроцитов). |
| Биохимический анализ крови | Биохимическое исследование крови позволяет обнаружить гипогликемию (низкий уровень глюкозы), гипонатриемию (снижение уровня натрия), гипохлоремию (снижение уровня хлора), гиперкальциемию (повышенное содержание кальция), гиперкалиемию (повышенное содержание калия), сниженный уровень кортизола, альдостерона, повышенную концентрацию адренокортикотропного гормона (АКТГ), ренина. Если врач подозревает у пациента адренолейкодистрофию как причину развития болезни Аддисона, то он ему также может назначить анализ на содержание в крови длинноцепочечных жирных кислот (ДЖК). Если врач подозревает у пациента адренолейкодистрофию как причину развития болезни Аддисона, то он ему также может назначить анализ на содержание в крови длинноцепочечных жирных кислот (ДЖК). |
| Иммунологический анализ крови | Иммунологический анализ крови назначается для подтверждения аутоиммунного генеза (происхождения) надпочечниковой недостаточности. В таких случаях пациент должен пройти тестирование на содержание в крови антител к ферментам надпочечникового стероидогенеза (процесса образования стероидных гормонов) – 21-гидроксилазе (P450c21), 17а-гидроксилазе (P450c17), ферменту отщепления боковой цепи (P450scc). Такое исследование также может выявить антитела к вирусу иммунодефицита человека (ВИЧ) и системным грибковым инфекциям, которые могут быть одной из причин развития болезни Аддисона. Кроме того иммунологический анализ часто назначается при подозрении на антифосфолипидный синдром, при котором в плазме крови можно обнаружить антикардиолипиновые антитела, антитела к В-2-гликопротеину 1 и волчаночный антикоагулянт (ВА). |
| Общий и биохимический анализ мочи | В анализе мочи можно выявить увеличение ее суточного объема, гипостенурию (снижение относительной плотности мочи), повышенное содержание натрия, сниженное количество альдостерона, 17-оксикортикостероидов (общее содержание различных типов глюкокортикоидов, образующихся в коре надпочечников), а также 17-кетостероидов (андрогенов, синтезируемых корой надпочечников). |
| Диагностические пробы | Кратковременные (с синактеном) и длительные (с синактеном-депо или цинк-кортикотропином) диагностические пробы при болезни Аддисона выявляют существенное снижение секреции гормонов корой надпочечников при их стимуляции. |
| Биопсия ткани надпочечников | Биопсия (микрохирургическая операция, направленная на взятие кусочка ткани для цитологического исследования) ткани надпочечников производится крайне редко. В большинстве случаев, ее делают для уточнения характера поражения тканей коры надпочечников. В большинстве случаев, ее делают для уточнения характера поражения тканей коры надпочечников. |
| Общий анализ мокроты | Общий анализ мокроты назначается в тех случаях, когда у врача имеется подозрение на туберкулезное поражение коры надпочечников пациента. |
Лечение болезни Аддисона
Для лечения болезни Аддисона назначают пожизненную медикаментозную терапию, позволяющую постоянно восполнять дефицит гормонов коры надпочечников (кортикостероидов). С этой целью больным прописывают заместительные гормональные средства, которые бывают двух видов. Первый вид гормональных препаратов, включает медикаменты, корректирующие в организме баланс минералокортикоидов. Второй вид гормонов, назначаемых при болезни Аддисона, включает средства, повышающие в крови уровень глюкокортикоидов. Оба типа гормонов необходимо всегда комбинировать и употреблять параллельно.
В качестве заместительных минералокортикоидов обычно назначается препарат кортинефф (или флудрокортизон). Его нужно пить по утрам (один раз в сутки). Суточная доза, как правило, подбирается индивидуально и всегда колеблется в пределах от 0,05 до 0,2 мг. Адекватность назначения кортинеффа должна постоянно находиться под клиническим и лабораторным контролем.
Его нужно пить по утрам (один раз в сутки). Суточная доза, как правило, подбирается индивидуально и всегда колеблется в пределах от 0,05 до 0,2 мг. Адекватность назначения кортинеффа должна постоянно находиться под клиническим и лабораторным контролем.
У пациентов, проходящих медикаментозное лечение с помощью данного гормонального препарата, должно быть нормальное артериальное давление, уровень калия, натрия и концентрации ренина (специфический фермент, вырабатывающийся почками) в плазме крови. Кроме того у них не должно быть выявлено признаков отечности (например,
АДДИСОНОВА БОЛЕЗНЬ — Большая Медицинская Энциклопедия
АДДИСОНОВА БОЛЕЗНЬ (morbus Addisoni; син.: бронзовая болезнь, хроническая первичная недостаточность надпочечников, недостаточность надпочечников) — заболевание, обусловленное двусторонним поражением коры надпочечников и выключением (акортицизм) или уменьшением (гипоадренокортицизм) продукции гормонов коры надпочечников. Названо по имени английского врача Аддисона (см.), впервые описавшего его в 1849 году. Заболевание выявляется чаще в возрасте 20—40 лет, одинаково часто среди мужчин и женщин. Распространение Аддисоновой болезни колеблется от 0,03 до 0,1 на 10 000 населения.
Названо по имени английского врача Аддисона (см.), впервые описавшего его в 1849 году. Заболевание выявляется чаще в возрасте 20—40 лет, одинаково часто среди мужчин и женщин. Распространение Аддисоновой болезни колеблется от 0,03 до 0,1 на 10 000 населения.
Этиология
Аддисонова болезнь возникает в результате деструктивных процессов различного происхождения в коре надпочечников. Наиболее частой причиной первичного поражения коры надпочечников является туберкулез (50—85% случаев), который развивается в результате гематогенного диссеминирования; у больных Аддисоновой болезнью обычно обнаруживают специфические изменения в легких и других органах. Иногда наблюдаются случаи изолированного поражения надпочечников.
Причиной Аддисоновой болезни также могут быть кровоизлияния в надпочечники, тромбоз сосудов, сифилис, двусторонние опухоли или метастазы рака в надпочечники, амилоидов, гнойное воспаление надпочечников, лимфогранулематоз, гистоплазмоз. Аддисонова болезнь может развиться и в результате аутоиммунного поражения надпочечников, что подтверждается повышением титра циркулирующих аутоантител к ткани надпочечников. В отдельных случаях заболевание может быть обусловлено нарушениями в гипоталамо-гипофизарной системе, приводящими к уменьшению секреции АКТГ или кортикотропин-рилизинг-фактора. Редко встречающиеся семейные формы Аддисоновой болезни, связанные с атрофией коры надпочечников, имеют наследственный характер и выявляются у гомозиготов в результате аутосомно-рецессивной мутации.
В отдельных случаях заболевание может быть обусловлено нарушениями в гипоталамо-гипофизарной системе, приводящими к уменьшению секреции АКТГ или кортикотропин-рилизинг-фактора. Редко встречающиеся семейные формы Аддисоновой болезни, связанные с атрофией коры надпочечников, имеют наследственный характер и выявляются у гомозиготов в результате аутосомно-рецессивной мутации.
Патологическая анатомия и патогенез
Поражение надпочечников при Аддисоновой болезни носит характер распространенных деструктивных или атрофических изменений.
Деструктивные изменения могут быть вызваны различными причинами. Чаще всего они связаны с двусторонним туберкулезом надпочечников. На рисунке видны увеличенные и уплотненные надпочечники, с обширными полями творожистого некроза, которые нередко содержат отложения солей извести. При микроскопическом исследовании по периферии участков творожистого некроза обнаруживается специфическая воспалительная инфильтрация из светлых эпителиоидных клеток с примесью лимфоидных элементов. Здесь же можно встретить единичные туберкулезные гранулемы, содержащие многоядерные эпителиоидные клетки Пирогова—Лангханса. При специальных окрасках примерно в половине случаев в краевых зонах творожистого некроза выявляются микобактерии туберкулеза. Туберкулезный процесс приводит к почти полному поражению надпочечников; корковая и мозговая ткань сохраняется лишь в виде единичных мелких разбросанных очажков. В сохранившихся участках коры отмечается атрофия клеток. При гистохимическом исследовании в этих клетках обнаруживается снижение содержания холестерина. При выраженной петрификации творожистых масс наблюдается развитие рубцовых изменений в забрюшинной клетчатке с образованием грубых сращений надпочечников с почками и печенью.
Рис. Туберкулез надпочечников, вызвавший аддисонову болезнь.
Первичные опухоли надпочечников, так же как и метастазы рака в эти железы, могут быть причиной Аддисоновой болезни лишь в случаях почти полного разрушения надпочечниковой ткани бластоматозным процессом, что наблюдается очень редко.
Деструктивные изменения в надпочечниках как причина Аддисоновой болезни могут быть вызваны также амилоидозом, гистоплазмозом, диссеминированным кокцидиомикозом. При этом отмечается распространенное двустороннее поражение преимущественно коркового слоя надпочечников.
Атрофические изменения. При атрофии надпочечников находят выраженное снижение веса желез. Уменьшение размеров органов происходит главным образом за счет толщины коры. Микроскопически наблюдается значительное истончение коркового слоя с нарушением нормальной архитектоники пучковой и сетчатой зон. В пучковой зоне коры, помимо уменьшения числа клеток и их размеров, отмечается дезорганизация расположения клеточных столбов, снижение содержания липидов и ферментативной активности в спонгиоцитах. Понижение активности стероид-3-бета-олдегидрогеназы указывает на недостаточный синтез стероидов. В наружных слоях пучковой зоны появляются псевдотубулярные структуры. В сетчатой зоне возникают дистрофические изменения с обильным отложением липофусцина в клетках. Клубочковая зона коры остается чаще всего интактной. Мозговое вещество надпочечников претерпевает незначительные изменения. Они заключаются в уменьшении количества хромаффинных клеток и некотором увеличении стромальных волокнистых структур.
Согласно современным представлениям, в основе развития атрофии надпочечников при Аддисоновой болезни лежат нарушения в иммунологических системах организма. Подтверждением такого взгляда является почти постоянно обнаруживаемая при Аддисоновой болезни с атрофией надпочечников выраженная гиперплазия зобной железы и лимфоидная инфильтрация в тканях многих паренхиматозных органов.
В некоторых наблюдениях имело место сочетание Аддисоновой болезни с аутоиммунными заболеваниями. По другим данным, атрофия надпочечников развивается на почве интоксикации организма, возможно, вирусного происхождения.
Клинические проявления заболевания являются следствием резкого снижения гормональной активности коры надпочечников. В эксперименте на животных проявления, аналогичные Аддисоновой болезни, возникают после удаления коркового вещества надпочечников.
Пигментация кожи и слизистых оболочек при Аддисоновой болезни возникает вследствие усиленного образования пигмента меланина, что связано действием внутриклеточного фермента ДОФА-оксидазы на дериваты бренцкатехина (диоксифенилаланин). Отмечают тесную связь меланодермии с дефицитом аскорбиновой кислоты и с меланоформным гормоном. В гипофизе при Аддисоновой болезни находят уменьшение числа базофильных элементов дегрануляцию базофилов, главным образом из дельта-форм. Сердце бывает уменьшено размерах. Микроскопически определяется бурая атрофия миокарда Обращает на себя внимание сужение просвета аорты и крупных магистральных сосудов, обусловленное приспособлением сосудистого ложа к условиям длительной гипотонии. В поджелудочной железе иногда отмечается гиперплазия островкового аппарата; изредка встречаются инсулярные аденомы. В этих случаях клинически определяется появление гипогликемии. В щитовидной железе нередко находят лимфоидноклеточную инфильтрацию некоторое увеличение интерстициальной ткани. В желудке обнаруживается атрофия слизистой оболочке и уменьшение числа обкладочных клеток. Иногда возникают поверхностные эрозии и небольшие язвы. В печени и почках наблюдаются дистрофические изменения. Половые железы претерпевают незначительные изменения. В них обнаруживаются умеренные атрофические процессы. Изменения в нервной системе при Аддисоновой болезни касаются некоторых симпатических ганглиев и выражаются в процессах склероза и атрофии. Такие изменения иногда обнаруживаются в области чревного (солнечного) сплетения.
Аддисонова болезнь обусловлена выключением или резким снижением продукции глюко- и минералокортикоидов (кортизола, альдостерона и кортикостерона).
Клиническая картина
Заболевание развивается медленно. Первые признаки — немотивированная слабость и быстрая физическая утомляемость, похудание. У 99% больных постепенно появляется пигментация кожи (цвета загара, золотисто-коричневая, грязно-коричневая, бронзовая), имеющая диффузный характер.
Рис. 2. Пигментация слизистой оболочки рта и меланодермия при аддисоновой болезни
Пигментация кожи усиливается участках тела, подвергающихся соляции или усиленному трению. Характерно усиление пигментации ладонных линий, тыльной поверхности кистей и стоп, области ожоговых и послеоперационных рубцов. в местах физиологического отложения пигмента (соски молочных желез, половые органы). У 80% больных наблюдается пигментация слизистой оболочки полости рта (цветн. рис. 2), влагалища и прямой кишки.
Одним из характерных признаков Аддисоновой болезни является гипотония со снижением преимущественно систолического давления. Наблюдается уменьшение пульсового давления, минутного объема крови. Сердце уменьшено в размерах, на ЭКГ отмечается снижение вольтажа зубцов, смещение ST-интервала вниз, отрицательный зубец T.
У больных нередко наблюдаются желудочно-кишечные нарушения (сиижение аппетита, топшота, рвота, понос, боли в области живота). Кислотность желудочного сока снижена, внешняя секреция поджелудочной железы уменьшена. Нарушаются функции печени (белковообразовательная, антитоксическая, гликогенообразовательная). Характерно увеличение толерантности к глюкозе и признаки относительного гиперинсулинизма в результате недостатка глюкокортикоидов.
Нарушение электролитного обмена сопровождается увеличением уровня калия и уменьшением концентрации натрия и хлоридов в сыворотке крови. Выделение калия с мочой уменьшается, а натрия и хлоридов увеличивается.
Изменения функции центральной нервной системы характеризуются психической истощаемостью, головными болями, понижением памяти. В отдельных случаях могут развиваться острые психозы. На электроэнцефалограмме наблюдается снижение активности коры головного мозга и появление дельта- и тэта-волн.
Функция половых желез при легкой форме Аддисоновой болезни нарушается редко, при тяжелой форме наблюдается нарушение менструального цикла у женщин и снижение потенции у мужчин. Выделение с мочой 17-кето- и 17-оксикортикостероидов, а также альдостерона значительно снижено. В крови выявляются эозинофилия и лимфоцитоз.
К нетипичным (стертым) формам заболевания относят Аддисонову болезнь с характерной клинической симптоматикой, но без пигментации. Пигментация настолько слабо выражена, что обычно не фиксируется при обследовании. Диагноз этой формы возможен только на основании данных лабораторного исследования.
К нетипичным формам Аддисоновой болезни относят и заболевание, протекающее по типу гипоальдостеронизма (резкое снижение секреции и выделения альдостерона с мочой при нормальной секреции глюкокортикоидов). Эта форма Аддисоновой болезни обусловлена изолированным поражением клубочковой зоны коры неизвестной этиологии. Клинически при этом наблюдается гипотония и менее выраженная пигментация.
Изолированная недостаточность секреции АКТГ или кортикотропин-рилизинг-фактора (диэнцефально-гипофизарная форма Аддисоновой болезни) характеризуется менее выраженными проявлениями заболевания, положительной пробой Торна — Лабхарта (см. Торна проба).
При неправильном лечении может развиться аддисонический криз, особенно на фоне острой инфекции, интоксикации, токсикоинфекции, операции, физической травмы. Нарастание признаков криза Аддисоновой болезни может быть постепенным (в течение нескольких дней) и быстрым (несколько часов).
При кризе наблюдается обострение всех клинических проявлений заболевания, появляется неукротимая рвота, прострация, нарастают признаки обезвоживания, артериальное давление снижается, появляется запах ацетона изо рта и ацетонурия, нередко — клонические судороги и менингеальный синдром, ошибочно диагностируемый как туберкулезный менингит. Без лечения сознание исчезает, и больной впадает в кому, которая может закончиться летальным исходом. Во время криза наблюдается снижение уровня сахара в крови до 50—30 мг%, увеличение остаточного азота и мочевины крови, лейкоцитоз, ускорение РОЭ, появление в моче гиалиновых, зернистых цилиндров, белка. Выделение с мочой метаболитов андрогенов и глюкокортикоидов уменьшается.
Диагноз
Диагноз основывается на характерной клинической картине и лабораторных тестах. Пигментацию кожи при Аддисоновой болезни необходимо дифференцировать с солнечным загаром, сочетающимся с гипотоническим синдромом, с пигментацией кожи при токсическом диффузном зобе, при гемохроматозе, пеллагре, акантозе, зудящих дерматозах, хронической малярии, склеродермии, сольтеряющей форме нефрита. Пигментация слизистой оболочки полости рта наблюдается также при хронических отравлениях мышьяком, азотнокислым серебром, ртутью, свинцом.
Прогноз
На фоне правильно проводимого лечения длительность жизни больных превышает 15—20 лет, трудоспособность сохраняется; для больных, выполняющих тяжелую физическую работу, необходимы некоторые трудовые ограничения.
Лечение
Лечение направлено на замещение недостаточности функции коры надпочечников при помощи индивидуально подбираемых дозировок глюкокортикоидных и минералокортикоидных препаратов. Назначают обычно преднизолон по 5—20 мг или кортизон в таблетках по 25—50 мг в день, или гидрокортизон и кортизон внутримышечно по 12,5—50 мг в день.
Если вышеуказанное лечение не способствует нормализации артериального давления, добавляют минералокортикоиды — дезоксикортикостерон в таблетках по 5—20 мг в день сублингвально или в виде 0,5% масляного раствора внутримышечно 2—3 раза в неделю, в виде подкожных имплантаций 100—200 мг (стерильные таблетки) один раз в 3—6 месяцев, а также в виде 2,5% раствора триметилового ацетата ДОК по 25— 50 мг внутримышечно один раз в 2—3 нед. Лечение проводится под контролем общего самочувствия, веса тела, артериального давления и выделения 17-кето- и 17-оксикортикостероидов с мочой. Рекомендуется добавление к пище поваренной соли (до 10 г в день).
Противотуберкулезное лечение проводится только при наличии активного туберкулезного процесса в надпочечниках или других органах.
Лечение кризаАддисоновой болезни заключается во внутривенном введении капельным способом 2—3 л изотонического раствора хлорида натрия с 5% раствором глюкозы, 100—300 мг кортизона или гидрокортизона или 100—200 мг преднизолона в день. При резком снижении артериального давления в указанный выше раствор добавляют 1 —3 мл 0,2% раствора норадреналина.
Масляный раствор дезоксикортикостерона вводят по 20—40 мг в день внутримышечно с интервалами в 6— 8 часов. Рекомендуется одновременно проведение антибактериальной терапии. Через 2—3 дня в зависимости от состояния больного глюкокортикоиды назначают внутримышечно в убывающих дозах, а затем переводят на поддерживающие дозы минерало- и глюкокортикоидов. В комплексную терапию Аддисоновой болезни входит санаторно-курортное лечение, проводимое в санаториях общего типа. При наличии туберкулеза показания к санаторно-курортному лечению основываются на характере туберкулезного процесса.
Профилактика
Профилактика Аддисоновой болезни заключается главным образом в правильно и своевременно проводимом лечении туберкулеза (см.) и других заболеваний, являющихся этиологическими факторами Аддисоновой болезни.
Библиография: Баранов В. Г. Болезни эндокринной системы и обмена веществ, Л., 1955; Зефирова Г. С. Аддисонова болезнь, М., 1963, библиогр.; Соффер Л., Дорфман Р. и Гебрилав А. Надпочечные железы человека, пер. с англ., с. 207, М., 1966; Шерешевский Н. А. Клиническая эндокринология, с. 185, М., 1946; Addison Т. On the constitutional and local effects of disease of the suprarenal capsules, L., 1855; Brenner O. Addison’s disease with atrophy of the cortex of the suprarenale, Quart. J. Med., v. 22, p. 121, 1928—1929; Guttman P. H. Addison’s disease, Arch. Path., v. 10, p. 742, 895, 1930; Hall R., Anderson J. a. Smart G. A. Fundamentals of clinical endocrinology, L., 1969; Human adrenal cortex, ed. by A. R. Currie a. o., Baltimore, 1062; К & d a s I. Die latente Addisonische Krankheit, Z. gee. inn. Med., S. 140, 1970; Paschkis К. E.. Ra-koff A.E. a. Gantarow A. Clinical endocrinology, N. Y., 1958; Textbook of endocrinology, ed. by R. Ы. Williams, Philadelphia — L., 1963.
Г. С. Зефирова; В. Б. Зайратъянц (пат. ан.).
Болезнь Рота: причины, признаки, симптомы и лечение | Лечение болезней
Содержание:
- Основные причины
- Признаки
- Диагностика
- Лекарственная терапия
Болезнь Рота – это одна из самых частых разновидностей туннельного синдрома. Появляется он в том случае, когда происходит сдавление нерва в области паховой связки или в районе передней подвздошной кости.
При этом страдает латеральный кожный нерв бедра, который образуется из некоторых ветвей нервов, выходящих из спинного мозга. Проходит он по каналу и обеспечивает нервную чувствительность передней поверхности бедра, а заканчивается в области колена. Чаще всего это состояние диагностируется у женщин. А само заболевание получило название по имени двух врачей, которые впервые его описали – В.К.Рот и М. Бернгардт.
Основные причины
Компрессионная невропатия при болезни Рота — Бернгардта может возникать в связи с некоторыми анатомическими особенностями строения тела человека. Чаще всего сдавление происходит в туннеле при его трении во время наклона туловища вперёд или при движении ног.
Чаще всего эту болезнь можно обнаружить у беременных в связи с тем, что во время вынашивания ребёнка увеличивается поясничный лордоз и разгибание в области тазобедренного сустава. Также изменяется и угол наклона таза, что приводит к компрессии нерва.
Ещё одна причина – избыточное количество жировых отложений в области бёдер и передней брюшной стенке. К прочим причинам можно отнести:
- Опухоли.
- Гематомы забрюшинного пространства.
- Оперативные вмешательства.
- Воспалительные процессы в брюшной полости.
- Ношение тесного нижнего белья.
- Частое ношение поясов.
- Применение корсетов.
- Нарушение питания нерва.
- Малоподвижный образ жизни.
- Дегенеративные заболевания позвоночника.
Также причинами могут стать травмы спины и позвоночника и длительное нахождение в одной позе. К тому же иногда такое состояние выявляется у людей некоторых профессий и может считаться профессиональным недугом.
Признаки
Болезнь Бернгардта – Рота можно отличить от других заболеваний по специфическим симптомам, хотя в большинстве случаев пациенты с этим диагнозом описывали самые разные его проявления. Так, например, чаще всего были жалобы на:
- Онемение.
- Ощущение холода.
- Ощущения жжения на передней поверхности бедра.
- Ползание мурашек на коже.
- Покалывание в области поражения.
- Небольшое нарушение питания кожи.
- Полное отсутствие чувствительности.
Что же касается болезненности, то у всех пациентов она разная. Кто-то описывает боль как терпимую, а для кого-то она жгучая и непереносимая.
Если заболевание длительно не лечить, то в самых запущенных случаях может начать появляться перемежающаяся хромота, которая также бывает из-за болевых ощущений. И в крайне редких случаях боль бывает настолько сильной, что приходится прибегать к оперативному лечению.
Болезнь Рота после установления диагноза по симптомам, должна обязательно быть пролечена, в противном случае могут возникнуть серьёзные нарушения в питании кожи, что приведёт к трофическим язвам и другим патологическим состояниям, которые потом будет трудно вылечить.
Диагностика
Лечение болезни Рота должно начинаться с диагностических мероприятий, которые помогут поставить точный диагноз, так как иногда этот недуг может быть принят либо за ушиб, либо за другое патологическое состояние.
Диагностика начинается с выяснения жалоб пациента, после этого могут понадобиться такие исследования, как:
- Электронейромиография.
- МРТ.
- УЗИ.
- Рентгенологический снимок.
- КТ.
Если диагноз очевиден, то для его подтверждения чаще всего проводится рентгенологическое исследование. Если же есть какие-то сомнения, то лучше всего сделать МРТ и точно понять причину боли в области бедра.
Лекарственная терапия
Лечение болезни Бернгардта — Рота нужно начинать с применения лекарственных препаратов, а также с использования гимнастических упражнений и физиопроцедур. Если говорить о лекарствах, то основное лечение направлено на то, чтобы убрать отёк и воспаление там, где проходит нерв, а также уменьшить болевые ощущения. Поэтому идеальными здесь станут препараты из группы НПВП. Также нередко назначаются витамины из группы В. К операции прибегают только в очень запущенных случаях, да и то очень редко.
Из физиопроцедур рекомендуется использовать для снятия симптомов болезни Рота — Бернгардта следующие методики:
Дарсонвализацию для улучшения венозного тока крови и для снятия спазмов.
- Иглорефлексотерапию.
- Радоновые ванны, которые укрепляют организм, помогают снизить болевые ощущения, улучшают кровоснабжение органов.
- Сероводородные ванны.
- Массаж.
- Грязелечение.
Также рекомендуется проводить и самостоятельные упражнения по лечебной физкультуре — сгибание ног в коленях, разведение их в стороны, махи. Если болезнь Рота, симптомы которой могут проявляться по-разному, не запущена, то выздоровление наступит буквально за несколько недель, после чего наступает длительная ремиссия, но если заболевание запущено, то здесь не обойтись без операции.
В качестве профилактики необходимо перестать вести сидячий образ жизни, больше двигаться, совершать пешие прогулки пешком, ездить на велосипеде и заниматься плаванием.
Стадии болезни Паркинсона
По мере того, как число клеток в коре головного мозга, которые вырабатывают определённый гормон, уменьшается, болезнь Паркинсона прогрессирует всё более активно. В результате снижается работа тех участков головного мозга, которые контролируют непроизвольные движения конечностей.
По степени выраженности симптомов заболевания, паркинсонизм разделяют на несколько стадий. Каждая стадия характеризуется своими особенностями, спецификой лечения. В разделении стадий болезни Паркинсона используется шкала Хен-Яру. Согласно этой шкале выделяют следующие этапы заболевания:
- Нулевая – у человека отсутствуют явные признаки патологии.
- Первая – наблюдаются небольшие нарушения в движениях пальцев, кистей рук, дрожание некоторых конечностей, которое прекращается в состоянии сна или покоя, появляется депрессия, вялость, нарушается сон.
- Вторая – двигательные нарушения появляются с обеих сторон, ухудшается мимика лица, ухудшается работа потовых желёз, нарушаются процессы, связанные с выделением пота. Человек выполняет свою повседневную работу, но его движения уже становятся замедленными.
- Третья – лицо принимает форму маски; человек приобретает определённую позу, в которой начинает находиться постоянно, это поза именуется как поза просителя; повышается тонус, напряжение в мышцах; двигательная активность становится очень низкой.
- Четвёртая – наблюдаются нарушения координации движений при ходьбе, снижается способность человека удерживать равновесие в той или иной позе, появляются проблемы с работой вестибулярного аппарата, в обычной жизни человеку необходимо помощь и поддержка со стороны. На этой стадии могут проявляться признаки слабоумия.
- Пятая – явные признаки нарушения нервной системы – человек
Болезнь Аддисона, что это такое? Фото, симптомы и прогноз
Болезнь Аддисона (гипокортицизм, бронзовая болезнь) – редкое заболевание эндокринной системы, при котором секреция гормонов (прежде всего, кортизола) корой надпочечников снижается.
Заболевание впервые было описано в 2019 году британским врачом Томасом Аддисоном. Оно с одинаковой частотой поражает мужчин и женщин; чаще диагностируется у людей молодого и среднего возраста.
Причины и факторы риска
К развитию болезни Аддисона приводит поражение клеток коры надпочечников или гипофиза, вызванное разными патологическими состояниями и заболеваниями:
- аутоиммунным поражением коры надпочечников;
- туберкулезом надпочечников;
- удалением надпочечников;
- кровоизлияниями в ткани надпочечников;
- адренолейкодистрофией;
- саркоидозом;
- длительной заместительной гормональной терапией;
- грибковыми инфекциями;
- сифилисом;
- амилоидозом;
- СПИДом;
- опухолями;
- облучением.
Опухоль почки может привести к поражению клеток коры надпочечника и как следствие – болезни Аддисона
Примерно в 70% случаев причиной болезни Аддисона является аутоиммунное поражение коры надпочечников. В силу различных причин в иммунной системе происходит сбой, и она начинает распознавать клетки надпочечников как чужеродные. В результате вырабатываются антитела, атакующие кору надпочечников и повреждающие ее.
Синдром Аддисона сопровождает ряд наследственных патологий.
Формы заболевания
В зависимости от причины болезнь Аддисона бывает:
- Первичной. Обусловлена недостаточным функционированием или повреждением непосредственно коры надпочечников.
- Вторичной. Передняя доля гипофиза секретирует недостаточное количество адренокортикотропного гормона, что приводит к уменьшению секреции гормонов корой надпочечников.
- Ятрогенной. Длительный прием кортикостероидных препаратов влечет атрофию надпочечников, кроме того, нарушает связь между гипоталамусом, гипофизом и надпочечниками.
Болезнь Аддисона — причины, симптомы, осложнения, лечение
На чтение 7 мин. Просмотров 4.4k. Обновлено
Сегодня мы поговорим о бронзовой болезни — болезни Аддисона, вскроем ее причины, опишем на alter-zdrav.ru симптомы, диагностику и лечение.
Что это такое болезнь Аддисона
Болезнь Аддисона, которую также называют недостаточностью надпочечников (гипокортицизм), является весьма редким заболеванием, возникающим, когда происходит разрушение внешнего слоя коры надпочечников и, следовательно, она перестаёт производить достаточно стероидных гормонов. При этой болезни гормоны кортизол и альдостерон, ответственные за обмен веществ в организме, вырабатываются в очень малом количестве.
Пусковым механизмом деструкции может быть вирусные, грибковые инфекции, интоксикации, генетические, аутоиммунные нарушения, новообразования.
Эта болезнь встречается во всех возрастных группах, заболеть ею могут и мужчины, и женщины. В лечение, в основном входит приём недостающих гормонов.
Симптомы болезни Аддисона
Они развиваются довольно медленно, срок развития около нескольких месяцев. Часто болезнь прогрессирует настолько медленно, что симптоматика игнорируется. Ухудшить её проявления может другое заболевание или травма.
Признаки и симптомы включают в себя:
- Крайнюю утомляемость, слабость, обморочные состояния.
- Потерю веса и снижение аппетита.
- Головокружение, головная боль.
- Гиперпигментацию (Потемнение верхнего слоя кожи) — повышенное отложение в коже пигмента меланина. Иногда на фоне темного бронзового оттенка появляются и пятна витилиго (белые депигментированные участки).
- Низкое давление, приводящее порой к полуобморочному состоянию.
- Зависимость от употребления соли и ощущение жажды.
- Понижение уровня сахара в крови (гипогликемия).
- Тошнота, рвота, диарея.
- Боли в животе.
- Боли в мышцах и суставах, судороги, тремор рук, нарушение чувствительности.
- Боль в области сердца, учащенное сердцебиение.
- Раздражительность беспокойство, тревога, негативизм.
- Нарушение памяти и внимания.
- Депрессивные состояния.
- Выпадения волос по всему телу.
- Нарушение менструального цикла, всей репродуктивной функции.
- Сексуальная дисфункция (в случае, если болезнь развивается у женщины).
Острая недостаточность надпочечников (аддисонический криз)
Иногда перечисленная выше симптоматика может проявляться внезапно.
За неотложной медицинской помощью следует обращаться в тех случаях, когда человек испытывает следующие признаки этого заболевания:
- Сильную слабость.
- Затруднения в мышлении.
- Боли в пояснице или голенях.
- Сильные болезненные ощущения в животе, рвота, диарея, доходящие до обезвоживания.
- Бред.
- Симптоматика проявляющаяся в аддисоническом кризе:
- Снижение давления.
- Повышение уровня калия в организме и снижение уровня натрия.
Причины болезни Аддисона
Аддисонова болезнь вызвана повреждением надпочечников, недостатком гормона кортизола и альдостерона. Так как надпочечники являются частью эндокринной системы, то они вырабатывают гормоны, воздействующие на каждый орган и ткань в организме.
Надпочечники состоят из двух секций. Продолговатый мозг, его внутренняя сторона, вырабатывает «адреналиноподобные» гормоны — катехоламины (адреналин и норадреналин). Внешний слой коры этого мозга производит ряд гормонов, зовущихся кортикостероидами.
Они в себя включают:
- Глюкокортикоиды (кортизол и кортизон). Эти гормоны, в них входит тот же кортизол, влияющий на способность организма к превращению пищи в энергию, блокировку воспалительных процессов при аллергических реакциях. Однако при этом он оказывает угнетающее действие на иммунную систему, недаром же его называют гормоном стресса.
- Минералокортикоиды (альдостерон, дезоксикортикостерон, кортикостерон). Гормоны, включающие в себя альдостерон и поддерживающие баланс калия и натрия в организме призваны нормализовать кровяное давление, поддерживать общий объем циркулирующей крови, влиять на ее кислотное состояние. Альдостерон регулирует правильную работу потовых и желудочно-кишечных желез.
- Андрогены . Мужские половые гормоны, вырабатывающиеся в малом количестве надпочечниками, как мужчин так и женщин. Они крайне необходимы в момент полового созревания для мальчиков, при этом они так же оказывают влияние на мышечную массу и либидо.
Первичная недостаточность коры надпочечников
При повреждении этой коры, она перестаёт выработку в достаточном количестве адренокортикальных гормонов. В большинстве случаев это состояние является результатом, нападения организма на самого себя (аутоиммунные заболевания).
По неизвестным причинам иммунная система пациента начинает рассматривать кору надпочечников, как чуждое организму явление, которое нужно уничтожить. Люди с болезнью Аддисона часто имеют ещё какое-либо аутоиммунное заболевание.
Другие причины недостаточности надпочечников включают в себя:
- Туберкулёз.
- Иные инфекционные заболевания надпочечников.
- Вич.
- Рак надпочечников.
- Внутреннее кровотечение этого органа. В таком случае у пациента возникает аддисонический криз без каких-либо предшествующих симптомов.
Вторичная надпочечниковая недостаточность
Гипофиз вырабатывает адренокортикотропный гормон (АКТГ). А он в свою очередь стимулирует выработку гормонов коры надпочечников. Частой причиной их недостатка является операции на доброкачественную опухоль гипофиза.
Дефицит АКТГ способен привести к малой выработке глюкокортикоидов и андрогенов, даже в том случае, когда сами надпочечники не повреждены. Это состояние и называется вторичной надпочечниковой недостаточностью. Большая часть её симптоматики схожа с симптомами первичной недостаточности. Тем не менее пациенты со вторичной в меньшей степени подвержены обезвоживанию, не имеют гиперпигментации, у них не понижается давление и уровень сахара в крови более стабилен.
Иногда причина вторичной недостаточности возникает при приёме кортикостероидов (к таким препаратам относят преднизолон), нужных для лечения хронических состояний, подобных астме и артриту. В таком случае следует прекратить приём гормонов сразу, без уменьшения дозировки.
Осложнения болезни Аддисона
Аддисонический криз
Он может развиться при отсутствии лечения болезни Аддисона, а так же в результате стресса тела (такого, как травма, болезнь или инфекция). В нормальном состоянии надпочечники производят в два-три раза больше кортизола. Это их ответ на физический стресс.
При кризе у них нет возможности выработать больше гормона. Эта ситуация опасна тем, что она приводит к понижению давления, падению частоты сердечных сокращений, неукротимой рвоте, поносу, сильным болям в животе и пояснице, отвращению к пище, неврологическим и психиатрическим проявлениям — галлюцинациям, заторможенности, бреду, судорогам, ступору, может иметь место потеря сознания.
Болезнь Аддисона предотвратить пока невозможно, но существуют меры по предотвращению аддисонического криза. При сильной выраженности заболевания, когда появляется рвота, а вместе с ней и неспособность принять лекарство, следует срочно обратится за неотложной помощью.
При аддисоническом кризе неотложная медицинская помощь, оказываемая в стационаре, может включать в себя инъекции:
- Кортикостероиды (внутривенное введение пациенту больших доз гидрокортизона (100 мг) несколько раз в сутки).
- Регидратационная терапия включает в себя введение физиологического раствора, раствора глюкозы.
Диагностика болезни Аддисона
Заболевание диагностируют путем сбора анамнеза, жалоб пациента, внешнего осмотра, общего анализа крови и мочи, биохимии, крови на уровень кортизола, уровень калия, натрия, также с помощью КТ и МРТ брюшной полости.
Они помогают узнать не увеличен ли размер надпочечников, что бывает в тех случаях, когда проблемы со здоровьем вызваны туберкулёзом. Уменьшение размеров органа свидетельствует о том, что болезнь проявляется из-за аутоиммунных процессов проходящих в организме.
Также проводятся диагностические пробы с АКТГ. Адренокортикотропные гормоны усиливают секрецию кортизола. И, если сделать инъекцию синактена, синтетического аналога АКТГ, можно измерить уровень кортизола в крови до и после её введения.
Если пациент болен болезнью Аддисона, то надпочечники не смогут ответить на стимуляцию синактеном, и уровень надпочечниковых гормонов в крови останется прежним.
Также назначается иммунологический анализ крови для выявление возможных аутоиммунных процессов.
Лечение болезни Аддисона
Лечится болезнь Аддисона только медикаментозно. Больному назначается гормональная терапия, необходимая для корректировки уровня стероидных гормонов. В неё входят гидрокортизон, преднизолон и его аналоги, метилпреднизолон.
Если болезнь Аддисона вызвана туберкулезной инфекцией, дополнительно назначаются антибиотики. Если заболевание спровоцировали грибки — назначаются параллельно противогрибковые препараты (флуконазол).
Иногда назначаются препараты для разжижения крови при сильно выраженном ее сгущении (проявление обезвоживания организма).
Диета при болезни Аддисона
Пациенту нужно получать из рациона много соли (натрия) особенно в жаркую погоду и при физических упражнениях. Желательно повышенное содержание белка в пищи, продуктов, стимулирующих аппетит — солений, мясных бульонов, соусов. Можно есть мясо, рыбу, яйца, молочные продукты, каши, маринованные и соленые овощи, соки, фрукты, ягоды.
Так как у больных болезнью Аддисона задерживается в организме много калия, не стоит налегать на продукты, пусть и калорийные, но с высоким содержанием этого минерала в составе — исключить сухой изюм, курагу, орехи, шоколад, грибы, чай, кофе, свеклу, шпинат, бобовые.
Дополнительные рекомендации к лечению:
Имейте при себе назначенные лекарства. Пропуск даже одного единственного дня при их приёме может стать опасным для пациента.
возможные причины, симптомы и лечение Бронзовая болезнь гормон
Кора надпочечников вырабатывает жизненно важные гормоны – глюкокортикоиды и минералокортикоиды. Кроме того, в этом эндокринном органе вырабатывается и небольшое количество половых гормонов.
Если кору поражает какой-либо патологический процесс, то у пациента развивается серьезное заболевание – первичная надпочечниковая недостаточность (болезнь Аддисона). Эта хроническая патология имеет много последствий для всего организма и даже угрожает жизни.
Распространенность заболевания небольшая. На 100 тысяч населения приходится 40–60 случаев патологии. Женщины страдают болезнью Аддисона значительно чаще. Особенно это различие в структуре заболеваемости по полу пациентов стало заметно в последнее время.
Почему возникает заболевание
Причиной болезни Аддисона в большинстве случаев является аутоиммунное воспаление. Антитела к собственным клеткам организма вырабатывают защитные системы. Иммунитет ошибочно принимает кору надпочечников за чужеродную ткань и начинает ее разрушать. Когда большая часть эндокринных клеток уже погибла, появляются первые симптомы бронзовой болезни.
Что может спровоцировать аутоиммунную агрессию? Медики не могут однозначно ответить на этот вопрос. Вероятно, патология защитных сил организма связана с наследственностью, генетическими мутациями, избыточной инсоляцией (солнечные лучи, солярий), неблагоприятными условиями окружающей среды.
Аутоиммунный процесс является причиной 80–90% случаев развития заболевания. Разрушение коры надпочечников может произойти и по другим причинам. Так, в неблагоприятных социальных условиях болезнь провоцирует туберкулез. На сегодняшний день эта инфекция является причиной около 10% всех случаев хронической надпочечниковой недостаточности.
Реже причиной болезни является травма, хирургическое разрушение, тромбоз, доброкачественная или злокачественная опухоль.
Чем бы ни была вызвана первичная надпочечниковая недостаточность, ее клиническая картина и принципы лечения отличаются незначительно.
Признаки болезни
Симптомы болезни связаны с недостаточностью глюкокортикоидов и минералокортикоидов. Часть признаков появляется из-за избыточного стимулирующего влияния гипофиза. Эндокринные клетки в головном мозге пытаются усилить работу коры надпочечников, выделяя большое количество тропных гормонов (в первую очередь адренокортикот
Анемия хронических заболеваний; Причины, симптомы, лечение, профилактика
Что такое анемия при хроническом заболевании?
Анемия хронического заболевания — это низкий уровень красных кровяных телец в результате аутоиммунных заболеваний (заболеваний, при которых иммунная система организма атакует суставы и / или органы) или других хронических заболеваний. Хронические заболевания — это те, которые длятся более 3 месяцев. Это состояние также называется анемией воспаления или анемией воспаления и хронического заболевания (AI / ACD).
Насколько распространена анемия при хроническом заболевании?
Это второй по распространенности тип анемии после анемии, вызванной дефицитом железа.
Кто подвержен риску развития этого состояния?
Наиболее частые заболевания, которые могут вызывать анемию:
- Любые инфекции
- Рак
- Хроническая болезнь почек (Практически каждый пациент с этим типом заболевания заболеет анемией, потому что почки вырабатывают эритропоэтин (ЭПО), гормон, который контролирует производство эритроцитов в костном мозге.)
- Аутоиммунные болезни
- Хроническое отторжение пересаженного органа
- Сердечная недостаточность
- Ожирение
Что вызывает анемию при хроническом заболевании?
Хронические заболевания могут вызывать изменения в красных кровяных тельцах, переносящих кислород кровяных тельцах, производимых костным мозгом. Эти изменения могут привести к более ранней смерти красных кровяных телец и замедлению их производства.
При хронической анемии железо, которое обычно перерабатывается из старых красных кровяных телец для создания новых красных кровяных телец, сохраняется в системе клеток, называемых макрофагами.Это ограничивает количество доступного железа, которое помогает создавать новые эритроциты.
Кроме того, метаболизм железа в клетках нарушается. (Метаболизм — это серия организованных химических реакций, необходимых организму для выживания.)
Каковы симптомы анемии при хроническом заболевании?
Симптомы аналогичны симптомам, вызванным железодефицитной анемией, и включают:
- Чувство усталости или слабости
- С бледной кожей
- При одышке
- Потение
- Головокружение или слабость
- Учащенное сердцебиение
- Головная боль
У некоторых людей симптомы отсутствуют.У некоторых людей симптомы появляются только во время тренировок.
Далее: Диагностика и тесты
Последний раз проверял медицинский работник Cleveland Clinic 23.07.2018.
Ссылки
Получите полезную, полезную и актуальную информацию о здоровье и благополучии
е Новости
Клиника Кливленда — некоммерческий академический медицинский центр.Реклама на нашем сайте помогает поддерживать нашу миссию. Мы не поддерживаем продукты или услуги, не принадлежащие Cleveland Clinic.
Политика
Симптомы и причины | NIDDK
Каковы симптомы болезни Вильсона?
Симптомы болезни Вильсона различны. Болезнь Вильсона присутствует при рождении, но симптомы не проявляются, пока медь не накапливается в печени, головном мозге или других органах.
Некоторые люди не имеют симптомов болезни Вильсона до того, как им поставят диагноз и не начнут лечение. Если у вас есть симптомы, они могут быть связаны с вашей печенью, нервной системой и психическим здоровьем, глазами или другими органами.
Печеночные симптомы
У людей с болезнью Вильсона могут развиться симптомы гепатита или воспаления печени. В некоторых случаях у людей появляются эти симптомы при острой печеночной недостаточности. Эти симптомы могут включать
- чувство усталости
- тошнота и рвота
- плохой аппетит
- боль над печенью, в верхней части живота
- потемнение цвета мочи
- Осветление стула
- Желтоватый оттенок белков глаз и кожи, называемый желтухой
У некоторых людей с болезнью Вильсона симптомы появляются только в том случае, если у них развивается хроническое заболевание печени и осложнения в результате цирроза.Эти симптомы могут включать
- чувство усталости или слабости
- худеем не пытаясь
- Вздутие живота из-за скопления жидкости в брюшной полости, называемое асцитом
- Отек голеней, щиколоток или стоп, называемый отеком
- кожный зуд
- желтуха
Нервная система и симптомы психического здоровья
У людей с болезнью Вильсона могут развиться симптомы нервной системы и психического здоровья после накопления меди в организме.Эти симптомы чаще встречаются у взрослых, но иногда встречаются у детей. 7 Симптомы нервной системы могут включать
- Проблемы с речью, глотанием или физической координацией
- жесткие мышцы
- тремор или неконтролируемые движения
Симптомы психического здоровья могут включать
Глазные симптомы
Многие люди с болезнью Вильсона имеют кольца Кайзера-Флейшера, которые представляют собой зеленоватые, золотые или коричневатые кольца по краям роговицы.Скопление меди в глазах вызывает появление колец Кайзера-Флейшера. Врач может увидеть эти кольца во время специального осмотра зрения, называемого осмотром с помощью щелевой лампы.
Среди людей с симптомами болезни Вильсона со стороны нервной системы более 9 из 10 имеют кольца Кайзера-Флейшера. Однако среди людей, у которых есть только симптомы со стороны печени, 5 или 6 из 10 имеют кольца Кайзера-Флейшера. 7
У многих людей с болезнью Вильсона есть кольца Кайзера-Флейшера.
Источник: Получено от Ассоциации болезни Вильсона.
Другие симптомы и проблемы со здоровьем
Болезнь Вильсона может поражать другие части вашего тела и вызывать симптомы или проблемы со здоровьем, в том числе
Что вызывает болезнь Вильсона?
Мутации гена ATP7B вызывают болезнь Вильсона.Эти генные мутации не позволяют организму выводить лишнюю медь. Обычно печень выделяет дополнительную медь в желчь. Желчь выносит медь вместе с другими токсинами и продуктами жизнедеятельности из организма через пищеварительный тракт. При болезни Вильсона печень выделяет меньше меди в желчь, и в организме остается больше меди.
Мутации ATP7B , вызывающие болезнь Вильсона, передаются по наследству, то есть передаются от родителей к ребенку. Эти мутации являются аутосомно-рецессивными, что означает, что человек должен унаследовать два гена ATP7B с мутациями, по одному от каждого родителя, чтобы иметь болезнь Вильсона.Люди, у которых есть один ген ATP7B без мутации и один ген ATP7B с мутацией, не страдают болезнью Вильсона, но они являются носителями этой болезни.
Люди могут быть врожденными от болезни Вильсона, если оба родителя являются носителями, у которых нет болезни. В таблице ниже показана вероятность наследования болезни Вильсона от родителей-носителей.
Мутации, вызывающие болезнь Вильсона
являются аутосомно-рецессивными, что означает, что человек
должен унаследовать два гена с мутациями
есть болезнь Вильсона.
Список литературы
[7] Щильский М.Л. Болезнь Вильсона: диагностические тесты. До настоящего времени. Доступно по ссылке https://www.uptodate.com/contents/wilson-disease-diagnostic-tests. Обновлено 1 декабря 2015 г. Проверено 14 мая 2018 г.
ученых открывают «разрушительное» НОВОЕ генетическое заболевание, от которого погибло 40% известных пациентов, поражая легкие и иммунную систему — RT World News
По словам исследователей, новое заболевание, вызванное генетическими мутациями, продемонстрировало особенно высокий уровень смертности, поскольку пациенты не реагировали на какие-либо доступные в настоящее время методы лечения.
Заболевание — «вакуоли, фермент E1, Х-связанный, аутовоспалительный и соматический синдром» — получило название VEXAS. Он вызывает симптомы, которые включают сгустки крови в венах, периодические лихорадки, аномалии в легких и вакуоли — необычные полые структуры — в миелоидных клетках, которые играют решающую роль в иммунной системе человека.
Исследователи из Национального института здоровья США (NIH) обнаружили это заболевание после анализа последовательностей генома более 2500 человек с недиагностированными воспалительными заболеваниями.Сравнивая данные, они обнаружили, что 25 взрослых мужчин имели определенные мутации в гене UBA1, который, как полагают, является источником VEXAS.
«Вместо того, чтобы смотреть на клинические сходства, мы вместо этого использовали преимущества общих геномных сходств, которые могли помочь нам открыть совершенно новое заболевание», — сказал Дэниел Кастнер, научный директор программы внутренних исследований Национального исследования генома человека. Институт.
Также на RT.com
Южная Корея сообщила о 83 случаях смерти среди людей, которым сделали прививки от гриппа на фоне опасений по поводу безопасности, связанных с программой вакцинации правительства
Национальный институт здравоохранения сообщил, что новое заболевание «может быть опасным для жизни» , поскольку 40 процентов пациентов с VEXAS, изученных исследователями, умерли. Большое количество погибших выявило «разрушительных последствий тяжелого состояния», — заявила группа человек.
Кастнер сообщил NBC News, что пациенты с VEXAS становятся «действительно больными», и «не реагируют ни на какое лечение, от высоких доз стероидов до различных химиотерапевтических препаратов.”
Думаете, вашим друзьям будет интересно? Поделись этой историей!
Причина и симптомы болезни Хантингтона
Обзор болезни Хантингтона
Симптомы могут включать проблемы с движением или равновесием, когнитивные проблемы и проблемы с психическим здоровьем, имеющие широкий спектр признаков и симптомов. Существуют лекарства для лечения, и теперь доступен диагностический тест для диагностики этого заболевания.
Этим заболеванием страдают от 5 до 10 человек на 100 000 человек во всем мире.Очевидно, это больше влияет на белых людей, чем на азиатов или чернокожих. На головной мозг больше всего влияет группа нервных клеток, расположенных в основании мозга, которая известна как базальные ганглии. Эта область отвечает за организацию движений тела, управляемых мышцами (называемых двигательными движениями).
Blueprint of Huntington’s Disease
Болезнь Хантингтона унаследована с одним геном, который является аутосомно-доминантной мутацией. По данным Национального института здоровья, «болезнь Хантингтона (БХ) — это прогрессирующее аутосомно-доминантное нейродегенеративное заболевание, вызываемое 36 или более тринуклеотидными (CAG) повторами на коротком плече хромосомы.«Чтобы упростить это описание, вы просто помните, что это наследственное заболевание, вызванное аномальным геном.
Итак, если у одного из родителей есть этот ген, вероятность унаследовать это генетическое заболевание у ребенка составляет 50%. Неважно, мужчина вы или женщина, риск одинаков.
Обычно это заболевание вызывает симптомы у пациентов в возрасте от 30 до 40 лет. Однако заболевание может возникнуть раньше, и если у кого-то развивается это заболевание в возрасте до 20 лет, это называется ювенильной болезнью Хантингтона.
Ювенильная болезнь Хантингтона
Ювенильная болезнь Гентингтона обычно вызывает несколько иные симптомы и более быстрое развитие болезни. Дефектный ген вызывает изменения в головном мозге. Также могут возникать непроизвольные движения, депрессия и другие изменения настроения
Снижается успеваемость в школе. По мере развития болезни ребенок будет проявлять неуклюжесть, жесткость, частые падения, невнятную речь и слюнотечение. Судороги также являются проблемой у 30-50% этих детей.Поскольку это заболевание у детей прогрессирует быстрее, они живут от 10 до 15 лет после появления симптомов.
Первые симптомы болезни Хантингтона
Начальные симптомы могут включать:
- Чрезмерное беспокойство
- Различные формы нервной деятельности, которая может проявляться как ерзание, подергивание в пальцах рук и ног
- Малые непроизвольные движения
- Сильное беспокойство
- Раздражительность или депрессия
- Некоторая неуклюжесть
- Плохая координация
- Мелкие правки почерка
- Затруднения в усвоении новой информации
- Некоторые трудности с обычными повседневными физическими навыками, такими как вождение
Если человек испытывает один или несколько из этих симптомов, было бы неплохо обратиться к семейному врачу.Конечно, это особенно верно, если вы знаете, что эта болезнь присутствует в вашей семье.
Симптомы болезни
Неконтролируемое движение ног. руки, голова, лицо или верхняя часть тела являются отличительными признаками этого заболевания. Кроме того, может произойти снижение способности рассуждать или снижение мышления. Могут влиять память, концентрация, способность планировать и организовывать, а также суждение. Первоначальные симптомы у разных людей различаются.
Болезнь Хантингтона обычно вызывает двигательные, когнитивные и психические расстройства с широким спектром признаков и симптомов.Познание — это ваше восприятие, осознание, суждение, мышление и рассуждение. Эти изменения происходят из-за потери нейронов в головном мозге. Какие симптомы появляются первыми, у разных людей сильно различаются. Во время болезни некоторые нарушения становятся более доминирующими или имеют большее влияние на функциональные способности.
Изменения в головном мозге могут привести к изменениям настроения, в частности, к депрессии, тревоге или раздражительности или гневу без каких-либо провокаций. Также может иметь место обсессивно-компульсивное поведение, которое заставляет человека повторять действие снова и снова или повторять один и тот же вопрос.Неизвестно, как остановить или хотя бы замедлить изменения мозга, вызываемые этим заболеванием.
Больше тревожных симптомов болезни
Международные эксперты рекомендовали следующие методы лечения некоторых из наиболее серьезных симптомов:
- Раздражительность может включать сильный гнев или даже угрожающее поведение, и для лечения этого поведения лучше всего лечить атипичным антипсихотическим препаратом. Более умеренное поведение, которое не представляет угрозы, обычно лечится селективным ингибитором обратного захвата серотонина (SSR), который является антидепрессантом.
- Хорею, то есть непроизвольные движения, часто лечат атипичными антипсихотическими препаратами, такими как оланзапин. Тетрабеназин — это недавно одобренный (в 2008 г.) препарат для лечения этого заболевания.
- Еще одна проблема для многих пациентов — это навязчивые действия и мысли. SSR также рекомендуются при этом психотическом расстройстве.
Депрессия, беспокойство или бессонница лечатся в соответствии с принятыми рекомендациями. Дистония в конечном итоге может заменить хорею, то есть мышечные спазмы, возникающие в руках, плечах, шее и ногах.
Кроме того, возможны неправильные позы, скручивания и повторяющиеся движения. В конце концов, движения пациента замедлятся из-за скованности и жесткости в конечностях.
Это заболевание трудно поддается лечению, поэтому лечат только симптомы, поскольку не существует специальных лекарств от болезни Гентингтона.
Состояние продвинутой стадии болезни
Люди с болезнью Гентингтона на продвинутой стадии претерпевают изменение личности. В конце концов у этих людей возникают трудности с речью, ходьбой или глотанием.Смерть может наступить из-за болезни сердца, пневмонии, аспирации или травмы в результате падения. Около 9% смертей от этой болезни происходят из-за суицида.
Взрослые пациенты с болезнью Хантингтона с дебютом обычно живут от 15 до 30 лет после появления первых признаков и симптомов.
Резюме
Это действительно душераздирающая болезнь. Симптомы тяжелы для пациента и членов его семьи. Членам семьи очень трудно принять изменение личности.
Тот факт, что на самом деле нет лекарств для лечения болезни, очень трудно принять пострадавшим и их семьям.Надеюсь, ученый найдет лекарство, так как ведется много исследований.
Симптомы болезни Лайма — Canada.ca
Узнайте о симптомах болезни Лайма, на что обращать внимание и что делать, если вы заболеете.
Симптомы болезни Лайма могут отличаться от человека к человеку.
Ранние признаки и симптомы болезни Лайма обычно проявляются через 3–30 дней после укуса инфицированного черноногого клеща.Большинство людей испытывают легкие симптомы гриппа вскоре после укуса, в то время как у небольшого числа людей могут быть более серьезные симптомы, иногда через несколько недель после укуса.
Ранние признаки и симптомы болезни Лайма могут включать:
- Сыпь, иногда в форме яблока (мигрирующая эритема (ЭМ сыпь))
- Лихорадка
- Озноб
- Головная боль
- Усталость
- Боли в мышцах и суставах
- Увеличение лимфатических узлов
Если не лечить, могут возникнуть более серьезные симптомы, которые могут длиться от месяцев до лет.Тяжелые симптомы могут включать:
- Сильная головная боль
- Дополнительные высыпания на коже ЭМ
- Паралич лицевого нерва (то есть паралич Белла)
- Периодические боли в мышцах, суставах, сухожилиях и костях
- Сердечные расстройства (учащенное сердцебиение, аномальное сердцебиение), известные как кардит Лайма
- Неврологические расстройства (головокружение, спутанность сознания или неспособность ясно мыслить, а также потеря памяти, воспаление головного и спинного мозга, нервная боль, онемение или покалывание в руках или ногах)
- Артрит с сильной болью в суставах и отеком, особенно в коленях и, реже, в других суставах, таких как лодыжка, локоть и запястья.
В редких случаях болезнь Лайма может привести к смерти, обычно из-за осложнений, связанных с инфекцией сердца.
Симптомы после лечения
Вы можете испытывать симптомы, которые длятся от месяцев до лет после лечения. Это состояние известно как синдром болезни Лайма после лечения (PTLDS).
Симптомы PTLDS могут включать:
- Нарушение сна
- Усталость (утомление)
- Боль в мышцах и суставах
- Психическое замешательство или неспособность ясно мыслить с небольшими когнитивными изменениями
Немедленно проконсультируйтесь со своим врачом, если у вас появятся симптомы болезни Лайма после укуса клеща или если вы посетили район, известный как зона риска по болезни Лайма.Чем раньше будет поставлен диагноз, тем больше шансов на успешное лечение.
Если вы сохранили клеща, который вас укусил, принесите его на прием к врачу. Сообщите своему врачу:
- как долго вы оцениваете, что галочка была прикреплена к вам
- где ты был, когда тебя укусил клещ
Заболевания щитовидной железы — причины, симптомы, лечение, диагностика
Факты
Щитовидная железа — это небольшая железа, расположенная под адамовым яблоком на вашей шее. Он выделяет гормоны, тироксин, (T4) и трийодтиронин, (T3), которые увеличивают количество кислорода, которое ваше тело использует, и стимулируют ваши клетки к производству новых белков. Контролируя выброс этих гормонов, щитовидная железа определяет скорость метаболизма большинства органов вашего тела.
Щитовидная железа регулируется тиреотропным гормоном (ТТГ), который вырабатывается гипофизом в головном мозге. Обычно, когда уровень гормонов щитовидной железы в организме высок, они «отключают» производство ТТГ, что, в свою очередь, не позволяет щитовидной железе производить больше Т4 и Т3.
Проблемы возникают, когда щитовидная железа становится либо недостаточной ( гипотиреоз, ), либо гиперактивной ( гипертиреоз ). Проблемы с щитовидной железой чаще встречаются у женщин, чем у мужчин. Рак также может развиться в щитовидной железе.
Причины
Заболевания щитовидной железы иногда возникают из-за несоответствующего уровня ТТГ или могут быть вызваны проблемами самой щитовидной железы.
Наиболее частой причиной гипотиреоза является тиреоидит Хашимото, аутоиммунное заболевание, при котором организм вырабатывает антитела, которые разрушают части щитовидной железы.Хирургическое удаление и некоторые лекарства (например, амиодарон, литий) также могут вызывать гипотиреоз. Лечение гипертиреоза также может вызвать гипотиреоз.
Другие причины гипотиреоза включают проблемы с гипофизом, гипоталамусом и дефицит йода (редко в Северной Америке, но затрагивает почти 2 миллиарда человек во всем мире). Некоторые дети рождаются с гипотиреозом — это называется врожденный гипотиреоз .
Есть разные причины гипертиреоза. Болезнь Грейвса — наиболее частая причина гипертиреоза. Это состояние возникает, когда иммунная система вырабатывает антитело, которое стимулирует всю щитовидную железу; это приводит к гиперактивности и повышению уровня гормонов щитовидной железы.
Другая форма гипертиреоза — токсический узловой зоб или токсическая аденома щитовидной железы . Аденомы, аномальные узелки ткани в щитовидной железе, постоянно производят гормоны щитовидной железы, даже когда они не нужны.
Вторичный гипертиреоз возникает, когда гипофиз вырабатывает слишком много ТТГ, что приводит к постоянной стимуляции щитовидной железы. Опухоль гипофиза может вызвать повышение уровня ТТГ. Реже гипофиз становится нечувствительным к гормонам щитовидной железы, больше не реагируя на высокие уровни.
Другой возможной причиной гипертиреоза является состояние, называемое тиреоидитом . Это состояние возникает, когда воспаляется щитовидная железа. В зависимости от типа тиреоидита это может привести к временному гипертиреозу, за которым может последовать гипотиреоз.
Существует четыре типа рака щитовидной железы: папиллярный, фолликулярный, анапластический, и медуллярный рак. Они связаны с лучевой терапией головы, шеи или груди. Лучевая терапия доброкачественных (незлокачественных) состояний больше не проводится в этих областях, но в прошлом была более распространенной. В других случаях генетическая мутация может быть связана с раком щитовидной железы либо отдельно, либо в сочетании с другими типами рака (например,, множественная эндокринная неоплазия, мутации гена BRAF). Реже другие виды рака могут метастазировать в щитовидную железу (например, лимфома, рак груди).
Симптомы и осложнения
Гипотиреоз приводит к низкому уровню Т4 и Т3 в крови. Недостаток Т4 и Т3 в крови замедляет метаболизм.
Общие симптомы включают:
- грубые и сухие волосы
- спутанность сознания или забывчивость (часто ошибочно принимается за деменцию у пожилых людей)
- запор
- депрессия
- веки отвисшие
- Сухая, чешуйчатая кожа
- усталость или чувство вялости
- отечность лица
- Выпадение волос
- хриплая речь
- Увеличение менструального цикла (женщины)
- Непереносимость низких температур
- Раздражительность
- мышечные судороги
- медленнее пульс
- слабость
- прибавка в весе
Если гипотиреоз не лечить, симптомы будут прогрессировать. Редко может развиться тяжелая форма гипотиреоза, называемая микседема . Симптомы микседемы включают:
- низкая температура тела
- притупление психических процессов
- Застойная сердечная недостаточность, состояние, при котором сердце не может перекачивать кровь, достаточную для удовлетворения потребностей организма
Микседема кома возникает у людей с тяжелым гипотиреозом, которые подвергались дополнительным физическим нагрузкам, таким как инфекции, низкие температуры, травмы или употребление седативных средств.Симптомы включают потерю сознания, судороги и замедленное дыхание.
Гипертиреоз приводит к высокому уровню Т4 и Т3, циркулирующих в крови. Эти гормоны ускоряют метаболизм. Некоторые из наиболее распространенных симптомов включают:
- учащение пульса с ненормальным ритмом или стуком (учащенное сердцебиение)
- высокое кровяное давление
- Повышенная температура тела (ощущение необычно теплого)
- Повышенное потоотделение
- липкость
- чувство возбуждения или нервозности
- тремор в руках
- чувство беспокойства, даже если человек устал или слаб
- Повышение аппетита с похуданием
- прерывистый сон
- Частое опорожнение кишечника, иногда с диареей
- отечность вокруг глаз, усиление слез, чувствительность к свету или пристальный взгляд
- Потеря костной массы (остеопороз)
- прекращение менструального цикла
Болезнь Грейвса, помимо общих симптомов гипертиреоза, может вызывать выпуклость на шее (зоб) в месте увеличения щитовидной железы.Это также может вызвать выпучивание глаз, что может привести к двоению в глазах. Иногда кожа на голенях становится приподнятой.
Если гипертиреоз не лечить или не лечить должным образом, может возникнуть опасное для жизни осложнение, называемое тиреоидным штормом (крайняя гиперактивность щитовидной железы). Симптомы включают:
- путаница
- кома
- диарея
- лихорадка
- высокое кровяное давление
- Нерегулярное сердцебиение, которое может быть фатальным
- Желтуха, связанная с увеличением печени
- перепады настроения
- Истощение мышц
- тошнота
- психоз
- беспокойство
- амортизатор
- рвота
- слабость
Тиреоидный шторм, считающийся неотложной медицинской помощью, также может быть вызван травмой, инфекцией, хирургическим вмешательством, неконтролируемым диабетом, беременностью или родами или приемом слишком большого количества препаратов для лечения щитовидной железы.
Диагностика
Заболевание щитовидной железы, заподозренное на основании анамнеза и физикального обследования, подтверждено лабораторными исследованиями. Лабораторные тесты обычно измеряют уровни ТТГ и гормонов щитовидной железы. Серологические тесты могут измерять уровни антител, связанных с гипотиреозом и гипертиреозом. Если ваш врач подозревает рак щитовидной железы, можно использовать биопсию, чтобы взять образец ткани щитовидной железы и проверить на рак.
Другой метод, называемый тестом функциональной стимуляции , может использоваться для определения того, являются ли гипофиз и щитовидная железы источником медицинских симптомов.Ультразвук и ядерное сканирование щитовидной железы позволяют визуально и функционально исследовать щитовидную железу или узелки.
Лечение и профилактика
Обычное лечение гипотиреоза — заместительная терапия гормонами щитовидной железы. При таком лечении синтетический гормон щитовидной железы (например, левотироксин *) принимается внутрь для восполнения недостающего гормона щитовидной железы. Лечение обычно пожизненное.
Большинство людей, принимающих заместительную терапию щитовидной железы, не испытывают побочных эффектов.Однако при приеме слишком большого количества гормона щитовидной железы симптомы могут включать дрожь, учащенное сердцебиение и проблемы со сном. Беременным женщинам может потребоваться увеличение замены щитовидной железы на 50%. Для того чтобы эффект начальной дозы или изменение дозы отразился в лабораторных исследованиях, требуется от 4 до 6 недель.
Гипертиреоз можно лечить йодом (включая радиоактивный йод), антитероидными препаратами или хирургическим вмешательством.
Радиоактивный йод может разрушить части щитовидной железы. Этого может быть достаточно, чтобы взять под контроль гипертиреоз. По крайней мере, в 80% случаев одна доза радиоактивного йода способна вылечить гипертиреоз. Однако, если разрушается слишком большая часть щитовидной железы, возникает гипотиреоз. Радиоактивный йод используется в достаточно низких количествах, чтобы не причинить вред остальным частям тела. Беременным женщинам его не дают, потому что он может разрушить щитовидную железу развивающегося плода.
Более высокие дозы обычного йода, , который не разрушает щитовидную железу, помогают блокировать выброс гормонов щитовидной железы.Он используется для неотложного лечения тиреоидного шторма и для уменьшения избыточной выработки гормонов щитовидной железы перед операцией.
Антитреоидные препараты (например, пропилтиоурацил * или метимазол) могут контролировать гипертиреоз в течение 6 недель — 3 месяцев. Эти препараты вызывают снижение выработки щитовидной железой новых гормонов щитовидной железы. Большие дозы действуют быстрее, но могут вызывать побочные эффекты, включая кожную сыпь, тошноту, потерю вкусовых ощущений, повреждение клеток печени и, в редких случаях, снижение выработки клеток крови в костном мозге.
Иногда необходимо хирургическое удаление щитовидной железы, которое называется тиреоидэктомией . Может потребоваться при наличии злокачественных узлов; если незлокачественный узел вызывает проблемы с дыханием или глотанием; если человек не может принимать радиоактивный йод или антитиреоидные препараты, или если они не работают; или если узелок, содержащий жидкость, продолжает вызывать проблемы. Удаление щитовидной железы приводит к гипотиреозу, который необходимо лечить гормональной терапией щитовидной железы до конца жизни человека.
Иногда ваш врач может порекомендовать другие лекарства, которые помогают контролировать симптомы гипертиреоза, такие как дрожь, учащенное сердцебиение, беспокойство и нервозность. Однако это не вылечит дисфункцию щитовидной железы.
Лечение рака щитовидной железы часто включает комбинацию тиреоидэктомии (хирургическое удаление щитовидной железы), радиоактивного йода, лучевой терапии (реже), противоопухолевых препаратов и подавления гормонов.
