Чрескожные коронарные вмешательства у больных стабильной ИБС – 2012 | Буза В.В., Карпов Ю.А.
В Российской Федерации, как и во многих экономически развитых странах мира, основной причиной смертности населения остается ишемическая болезнь сердца (ИБС) [1]. В этой ситуации огромное значение имеет реализация основных положений рекомендаций экспертов по диагностике и современному лечению больных с ИБС. В последние годы все более широко используются чрескожные коронарные вмешательства (ЧКВ), направленные на полное или частичное восстановление коронарного кровотока. Первичная ангиопластика в остром периоде инфаркта миокарда (ИМ) с подъемом сегмента ST снижает смертность и риск повторного ИМ [2]. Кроме того, у больных с нестабильной стенокардией и ИМ без подъема сегмента ST проведение ЧКВ также сопровождается улучшением краткосрочного и отдаленного прогноза [3]. В то же время оптимальная современная стратегия применения инвазивного лечения ИБС вне обострения, т.е. при стабильной стенокардии, и влияние на прогноз до сих пор точно не определены. Частично это связано со значительным прогрессом как в области медикаментозного, так и инвазивного лечения, произошедшим за последние два десятилетия (табл. 1).
Существует ряд теоретических предпосылок для положительного влияния ЧКВ на прогноз пациентов со стабильной ИБС. Доказана четкая связь степени выраженности каждого отдельного гемодинамически значимого стеноза при коронароангиографии (КАГ), а также количества пораженных артерий и риска развития отдаленных неблагоприятных событий (табл. 2) [4].
Выявление ишемии миокарда у больных с подтвержденной или предполагаемой ИБС увеличивает риск общей и сердечно–сосудистой смертности, частоты развития ИМ, даже при отсутствии стенокардии. Проведение реваскуляризации у бессимптомных больных со значительной массой ишемизированного миокарда приводит к улучшению их отдаленного прогноза. С другой стороны, отрицательный тест на ишемию при нагрузочной сцинтиграфии миокарда даже при наличии болевого синдрома в грудной клетке является маркером благоприятного отдаленного прогноза. Кроме того, ишемия миокарда является пусковым механизмом, запускающим полиморфную желудочковую тахикардию/фибрилляцию желудочков и, соответственно, приводит к развитию внезапной смерти. Поэтому неудивительно, что степень поражения коронарного русла коррелирует с выживаемостью в отдаленном периоде. Учитывая указанные теоретические предпосылки, были проведены несколько клинических исследований, в которых сравнивались консервативная – оптимальная медикаментозная терапия (ОМТ) и инвазивная тактики, при которой наряду с ОМТ проводилось ЧКВ.
Современная ОМТ
В соответствии с рекомендациями по лечению больных ИБС для снижения риска развития осложнений используются такие классы препаратов, как антитромбоцитарные (ацетилсалициловая кислота, клопидогрел), липидснижающие (статины и др.), ингибиторы ангиотензинпревращающего фермента (АПФ), β–блокаторы (после перенесенного ИМ).
Для лечения стенокардии применяются препараты, направленные либо на увеличение доставки кислорода к сердечной мышце, либо на уменьшение потребности в нем миокарда (табл. 3). Препараты, традиционно используемые для этих целей, – β–блокаторы, антагонисты кальция и нитраты, оказывают свое антиангинальное/антиишемическое действие через изменение гемодинамических параметров деятельности сердца (ЧСС, коронарный кровоток, пред– и постнагрузка и др.) и АД, а также средства метаболического или цитопротективного действия.
β–блокаторы уменьшают ЧСС и АД во время нагрузки, задерживают или предотвращают развитие болей и ишемических изменений по данным ЭКГ. При подборе дозы ориентируются на частоту приступов, обычно стараются замедлить ЧСС до 55–60 уд./мин. Антагонисты кальция обычно назначаются при недостаточном антиангинальном эффекте нитратов или β–блокаторов. Этот класс препаратов обладает различным гемодинамическим эффектом (группа дигидропиридинов и препараты с ритм–замедляющими эффектами – верапамил и дилтиазем) и, соответственно, спектром побочного действия, что необходимо учитывать при выборе препарата. Антагонисты кальция, в основном верапамил и дилтиазем, особенно показаны для лечения вазоспастической стенокардии. При применении нитратов уменьшаются частота и тяжесть приступов стенокардии, однако назначение длительно действующих нитратов после перенесенного ИМ не приводит к улучшению прогноза. При развитии толерантности к нитратам ухудшается контроль за приступами стенокардии.
Ивабрадин – ингибитор If–тока клеток синусового узла, рекомендуется для клинического применения как антиангинальное средство у больных стабильной стенокардией с синусовым ритмом как при непереносимости или противопоказаниях к применению β–блокаторов, так и для совместного применения с β–блокаторами, если последние не контролируют ЧСС, а увеличение их дозы невозможно.
Активатор калиевых каналов – препарат никорандил – одновременно обладает свойствами органических нитратов и активирует АТФ–зависимые калиевые каналы. Никорандил расширяет коронарные артериолы и вены, воспроизводит защитный эффект ишемического прекондиционирования.
Миокардиальный цитопротектор триметазидин в монотерапии и в комбинации с любым из антиангинальных средств не только уменьшает количество приступов стенокардии и число потребляемых таблеток нитроглицерина, но и достоверно увеличивает время физической нагрузки на велоэргометре и тредмиле, объем выполненной работы, толерантность к физической нагрузке. Триметазидин может с успехом применяться у лиц пожилого и молодого возраста, с нарушениями углеводного обмена и при сопутствующей недостаточности кровообращения. Получены данные о том, что триметазидин до и после процедур реваскуляризации миокарда может оказать благоприятное влияние на ишемическое повреждение миокарда и быть эффективным в лечении стенокардии, возобновившейся после ЧКВ.
Первые исследования по изучению влияния ЧКВ на отдаленный прогноз у больных стабильной ИБС
В исследовании ACME [5] пациенты с одно– и двухсосудистым поражением и верифицированной ишемией миокарда или перенесенным ИМ в анамнезе при наличии подходящих для ЧКВ стенозов были рандомизированы к медикаментозной терапии, или им выполнялась транслюминальная баллонная коронарная ангиопластика (ТБКА). При анализе больных с однососудистым поражением оказалось, что в группе ТБКА через 6 мес. было достоверно больше пациентов без приступов стенокардии (64 против 46%), что сопровождалось большей толерантностью к физической нагрузке. Вместе с тем достоверной разницы при длительном наблюдении отмечено не было. Через 3 года наблюдения преимущество ТБКА перед медикаментозной терапией по приступам стенокардии сохранялось, и также без влияния на прогноз. В подгруппе пациентов с двухсосудистым поражением через 6 мес. ТБКА и медикаментозная терапия были одинаково эффективны в плане избавления от стенокардии, повышения толерантности к физической нагрузке и качества жизни.
В крупном исследовании RITA–2 (1018 участников) пациенты со стенозами коронарных артерий, подходящими для проведения ЧКВ, были рандомизированы в группу медикаментозного лечения, или им дополнительно проводилась ТБКА [6]. У значительного числа включенных больных было многососудистое поражение (40%), в том числе у 34% – гемодинамически значимое поражение проксимального сегмента передней нисходящей артерии. Через 3 мес. у пациентов в группе инвазивного лечения на 16,5% реже встречалась стенокардия II–IV ФК (р=0,001), достоверно выше (на 35 с) было общее время нагрузки при повторном проведении нагрузочной пробы, а также выше качество жизни. В группе медикаментозной терапии 23% пациентов потребовалось проведение ТБКА вследствие неэффективности медикаментозного лечения. Однако через 2,7 лет наблюдения в группе ТБКА суммарная частота смерти/ИМ была достоверно выше (6,3 против 3,3%) в группе консервативной терапии за счет частоты перипроцедуральных ИМ; разница по частоте стенокардии снизилась до 7,6%, хотя и сохранялась достоверность в пользу ТБКА. При более длительном (7–летнем) наблюдении частота смерти/ИМ между группами уже достоверно не различалась.
В исследовании MASS (у пациентов с поражением проксимального отдела передней нисходящей артерии) и MASS II (у пациентов с многососудистым поражением) ТБКА была также более эффективной в плане уменьшения симптомов стенокардии и показателей нагрузочных проб как через 12 мес., так и при длительном наблюдении (4–5 лет). При этом достоверной разницы по частоте развития смерти/ИМ между группой медикаментозной терапии и ТБКА отмечено не было [7,8]. У пожилых больных в исследовании TIME (старше 75 лет) лечение с помощью ЧКВ снова оказалось более эффективным, чем медикаментозная терапия в плане уменьшения приступов стенокардии и улучшения качества жизни. Указанная разница сохранилась и после 4 лет наблюдения [9].
Все ранее описанные исследования были проведены до внедрения в клиническую практику стентов и современных стандартов медикаментозного лечения. Кроме того, число включенных больных не позволяло сделать точный вывод при сравнении влияния ЧКВ и медикаментозной терапии на отдаленный прогноз.
Современные исследования
по изучению влияния ЧКВ на прогноз при стабильной ИБС
Наиболее современными и крупными из завершенных на данный момент исследований являются COURAGE, BARI 2D, JSAP. В исследование COURAGE было включено 2287 пациентов с ишемией миокарда, доказанной при проведении нагрузочных проб, и гемодинамически значимыми стенозами, выявленными во время КАГ [10]. После заключения экспертов о том, что выявленные стенозы подходят для проведения ЧКВ, больные были рандомизированы к ОМТ, или помимо ОМТ им дополнительно проводилось ЧКВ. ОМТ включала в себя антиангинальные препараты, антиагреганты, агрессивную липидснижающую и гипотензивную терапию. Важной особенностью исследования было частое (90%) применение стентов, хотя стенты с лекарственным покрытием использовались менее чем в 3% случаев. В течение длительного периода наблюдения (в среднем 4,6 лет) достоверной разницы по частоте смерти, развития ИМ, инсульта, потребности в госпитализации из–за развития ОКС отмечено не было. Как и ожидалось, ЧКВ оказалось более эффективным в плане избавления от стенокардии (табл. 4), а также повышения качества жизни (согласно различным опросникам), однако через 5 лет разница и по уровню качества жизни, и доле пациентов без стенокардии между группами не различалась, во многом за счет высокой частоты внеплановой реваскуляризации в группе исходно медикаментозного лечения вследствие развития рефрактерной стенокардии (33% в группе ОМТ и 21% в группе ЧКВ, р<0,001).
Надо отметить, что в исследование COURAGE не включались пациенты высокого риска. Так, в частности, критериями исключения в нем было сохранение стенокардии IV ФК, несмотря на проведение антиангинальной терапии, не включались также пациенты, у которых во время нагрузочной пробы отмечалась резко положительная проба (выраженная депрессия сегмента ST или падение АД на первой стадии нагрузки), пациенты с недавно перенесенным ИМ, у которых сохранялись приступы покоя, пациенты со сниженной ФВ, а также больные, у которых в предшествующие 6 мес. проводилось ЧКВ или КШ, больные с гемодинамически значимым поражением ствола ЛКА. Частота включения больных с 3–сосудистым поражением также была низкой – 30%. Кроме того, рандомизация проводилась после проведения КАГ, что снизило число пациентов с критическими стенозами, т.к. врачам–исследователям психологически было трудно их рандомизировать в исследование, где с 50% вероятностью они могли попасть в группу медикаментозного лечения.
Интересные данные были получены при отдельном анализе небольшой группы (n=300) пациентов, участвовавших в исследовании COURAGE, которым проводилась сцинтиграфия миокарда. Оказалось, что у небольшой группы пациентов (n=100) с большой и умеренной областью ишемии (с 10% и более объемом ишемизированного миокарда, согласно данным исходной сцинтиграфии миокарда) проведение ЧКВ привело к более выраженному снижению объема ишемизированного миокарда, что сопровождалось достоверным снижением смертности и частоты ИМ.
В исследование BARI 2D было включено 2368 пациентов со стабильной ИБС, страдающих СД 2 типа [11]. Пациенты были рандомизированы к ОМТ, или помимо ОМТ им проводилась реваскуляризация миокарда в виде ЧКВ или коронарного шунтирования (КШ) на усмотрение лечащего врача. Через 5 лет выживаемость между группами достоверно не различалась: 88,3% в группе реваскуляризации и 87,8% в группе медикаментозного лечения (p=0,97). Доля пациентов без неблагоприятных сердечно–сосудистых событий (смерть, ИМ, инсульт) также достоверно не различалась (77,2% в группе реваскуляризации против 75,9% в группе медикаментозной терапии, p=0,70). При отдельном анализе групп ЧКВ и медикаментозной терапии также достоверной разницы выявлено не было. Таким образом, в группе больных СД 2 типа проведение ЧКВ также не приводит к улучшению отдаленного прогноза по сравнению с ОМТ.
В относительно небольшом рандомизированном исследовании JSAP (Japanese Stable Angina Pectoris), проведенном в Японии, 384 пациента со стабильной ИБС низкого риска, направляемые лечащими врачами на инвазивное лечение, были рандомизированы к проведению ОМТ, или наряду с ОМТ им выполнялось ЧКВ [12]. Через 3,3 года наблюдения частота смерти достоверно не различалась между группами (2,9% в группе инвазивного лечения против 3,9% в группе ОМТ), однако частота комбинированной конечной точки (смерть + ОКС) достоверно реже встречалась в группе инвазивного лечения (7,9 и 14,9%, p=0,018). Недостатком данного исследования является небольшое число включенных пациентов, а также использование внутрисосудистого ультразвукового исследования при всех ЧКВ. Этим объясняется увеличение частоты первоначального успеха ЧКВ в исследовании JSAP (99,5%) по сравнению с COURAGE (93%), что, возможно, и является причиной различий в полученных результатах.
Результаты метаанализов
После публикации результатов исследований COURAGE, BARI 2D, JSAP был выполнен ряд метаанализов по той же тематике. В ряде из них были получены противоречащие COURAGE результаты. Так, в метаанализе A. Schomig и соавт., в который вошли данные 17 исследований, было выявлено 20% снижение общей смертности при проведении ЧКВ по сравнению с медикаментозной терапией [13]. Однако в указанный метаанализ был включен ряд исследований, в которых участвовали пациенты с недавно перенесенным ИМ, где ЧКВ, как было указано выше, улучшает прогноз пациентов, а также исследования пациентов с безболевой ишемией миокарда. Поэтому правомочность указанного метаанализа по отношению к больным со стабильной стенокардией вызывает сомнения. В метаанализ A. Jeremias был включен 13 121 пациент из исследований, где сравнивались реваскуляризация миокарда (ЧКВ или КШ) и медикаментозная терапия [14]. Согласно данным этого метаанализа, у больных после реваскуляризации миокарда отмечено снижение общей смертности, но не частоты ИМ. Указанный эффект был более выраженным в группе КШ по сравнению с ЧКВ (OP=0,62 95% CI 0,5–0,77 против OP=0,82 95% CI 0,68–0,99). При этом даже после исключения больных с недавним ИМ указанные различия сохранялись. В 2012 г. был выполнен еще ряд метаанализов, где были получены несколько иные результаты. В метаанализе, выполненном Stergiopoulos, проведение ЧКВ не только не привело к снижению смертности, ИМ и потребности в экстренной реваскуляризации, но и не оказалось более эффективным в плане снижения частоты стенокардии по сравнению с ОМТ [15]. Однако в данный метаанализ были включены не все исследования со стабильной ИБС, кроме того, в некоторые из них также были включены пациенты со стенокардией после перенесенного ИМ. Этого недостатка лишен метаанализ Pursnani, куда были включены исследования, в которых участвовали только пациенты со стабильной стенокардией и не включались больные с ОКС. Строгие критерии отбора больных только со стабильной ИБС, исключение пациентов с КШ, включение в анализ данных по длительности последующего наблюдения за больными делают данный метаанализ самым лучшим на данный момент [16]. Согласно полученным результатам, частота ССС при применении ЧКВ не снижается по сравнению с ОМТ, однако оно действительно на 20% снижает долю пациентов без стенокардии, при этом указанная разница сохранялась во всех проанализированных временных точках 1, 1–5 лет и 5 лет. Была выявлена также интересная временная закономерность: по мере включения более современных исследований, где чаще применялись стенты и более агрессивная медикаментозная терапия, влияние ЧКВ на улучшение прогноза уменьшалось.
После публикации данных исследования COURAGE, BARI 2D, JSAP, а также указанных метаанализов во всем мире отмечается снижение частоты инвазивных вмешательств у больных со стабильной ИБС. Какие же тенденции наблюдаются в нашей стране? Согласно данным статистики, в РФ наблюдается непрерывный рост числа выполняемых ЧКВ [17]: с 2001 по 2011 г. отмечено 16–кратное увеличение числа выполняемых ЧКВ на 1 млн населения (рис. 1). Несмотря на это, мы все еще отстаем по данному показателю от многих стран Европы. Кроме того, доля ЧКВ, проводимых при ОКС, составляет всего 40,1% от всех ЧКВ при ИБС, что ниже среднеевропейского уровня, который составляет 60%. Т.е. в нашей стране сохраняется парадоксальная ситуация, когда в условиях ограниченного финансирования ЧКВ чаще применяется у больных со стабильной ИБС, где его прогностическая роль не ясна.
В то же время наблюдается рост приверженности пациентов к лечению препаратами, положительное влияние большинства из которых при стабильной ИБС не вызывает сомнений. Хотя надо отметить, что мы и по этим показателям отстаем от лучших центров США, где проводилось исследование COURAGE (табл. 5).
Таким образом, в настоящее время нет убедительных данных, что проведение ЧКВ у больных со стабильной ИБС, получающих ОМТ, приводит к снижению общей, сердечно–сосудистой смертности, нефатального ИМ или потребности в экстренной реваскуляризации. В то же время проведение ЧКВ приводит к значительному снижению выраженности стенокардии по сравнению с медикаментозной терапией. Следует отметить, что дискуссия о прогностическом влиянии ЧКВ продолжается. Критики исследования COURAGE утверждают, что незначительная частота использования СЛП, отсутствие СЛП нового поколения, которые, как было показано в ряде исследований, не только снижают частоту рестеноза стента, но и снижают частоту ИМ по сравнению с непокрытыми стентами и СЛП первого поколения, недостатки дизайна (в частности рандомизация после КАГ и нечеткие критерии ишемии), данные подысследования пациентов с большим объемом ишемизированного миокарда, не позволяет заключить, что данное исследование дало окончательный ответ на вопрос о влиянии ЧКВ на прогноз больных со стабильной ИБС. Кроме того, как уже отмечалось ранее, за последнее время произошел качественный скачок как в медикаментозном лечении, так и технике и фармакологии инвазивного лечения. Поэтому было инициировано крупнейшее исследование International Study of Comparative Health Effectiveness with Medical and Invasive Approaches (ISCHEMIA), в котором ЧКВ + ОМТ и ОМТ будут сравниваться у больных с верифицированной, по крайней мере умеренной, ишемией. При этом будет использоваться весь арсенал современной медикаментозной и инвазивной терапии (в частности СЛП). Планируется включить как минимум 8000 пациентов, что позволит определить даже небольшую разницу в исходах [20].
Литература
1. The World Health Organization the top ten causes of death fact sheet. 2004. Available at: http://www.who.int/mediacentre/factsheets/fs310/en/ index.html. Accessed February 2, 2012.
2. Ribeiro E.E., Silva L.A., Carneiro R. et al. Randomized trial of direct coronary angioplasty versus intravenous streptokinase in acute myocardial infarction // J. Am. Coll. Cardiol. 1993. Vol. 22. P. 376–380.
3. The Fragmin and Fast Revascularization During Instability in Coronary Artery Disease (FRISC) Investigators. Invasive compared with non–inva–sive treatment in unstable coronary–artery disease: FRISC–II prospective randomised multicentre study // Lancet. 1999. Vol. 354. P. 708.
4. 2011 ACCF/AHA/SCAI Guideline for Percutaneous Coronary Intervention: A Report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines and the Society for Cardiovascular Angiography and Interventions // Circulation. 2011. Vol. 124(23). P. e574–e651.
5. Folland E.D., Hartigan P.M., Parisi A.F. Percutaneous transluminal coronary angioplasty versus medical therapy for stable angina pectoris: outcomes for patients with double–vessel versus single–vessel coronary artery dis–ease in a Veterans Affairs Cooperative randomized trial. Veterans Affairs ACME InvestigatorS // J. Am. Coll. Cardiol. 1997. Vol. 29. P.1505–1511.
6. Coronary angioplasty versus medical therapy for angina: the second Randomised Intervention Treatment of Angina (RITA2) trial // Lancet. 1997. Vol. 350. P. 461468.
7. Hueb W.A., Soares P.R., Almeida De Oliveira S. et al. Five–year follow–op of the medicine, angioplasty, or surgery study (MASS): A prospective, random¬ized trial of medical therapy, balloon angioplasty, or bypass surgery for single proximal left anterior descending coronary artery stenosis // Circulation. 1999. Vol. 100(19 Suppl). P. II107–II113.
8. Hueb W., Lopes N.H., Gersh B.J. et al. Five–year follow–up of the Medicine, Angioplasty, or Surgery Study (MASS II): a randomized controlled clinical trial of 3 therapeutic strategies for multivessel coronary artery disease // Circulation. 2007. Vol.115. P.1082–1089.
9. Pfisterer M. Trial of Invasive versus Medical therapy in Elderly patients Investigators. Long–term outcome in elderly patients with chronic an¬gina managed invasively versus by optimized medical therapy: four–year follow–up of the randomized Trial of Invasive versus Medical therapy in Elderly patients (TIME) // Circulation. 2004. Vol. 110. P.1213–1218.
10. Boden W.E., O’Rourke R.A., Teo K.K. et al. Optimal medical therapy with or without PCI for stable coronary disease // N. Engl. J. Med. 2007. Vol. 356. P. 15031516.
11. Dagenais G.R., Lu J., Faxon D.P. et al. Bypass Angioplasty Revascularization Investigation2 Diabetes (BARI 2D) Study Group. Effects of optimal medical treatment with or without coronary revascularization on angina and subsequent revascularizations in patients with type 2 diabetes mellitus and stable ischemic heart disease // Circulation. 2011. Vol. 123. P.1492–1500.
12. Nishigaki K., Yamazaki T., Kitabatake A. et al. Japanese Stable Angina Pectoris Study Investigators. Percutaneous coronary intervention plus medical therapy reduces the incidence of acute coronary syndrome more effectively than initial medical therapy only among patients with low–risk coronary artery disease a randomized, comparative, multicenter study // JACC Cardiovasc. Interv. 2008. Vol. 1. P. 469–479.
13. Schomig A., Mehilli J., de Waha A. et al. A meta–analysis of 17 randomized trials of a percutaneous coronary intervention–based strategy in patients with stable coronary artery disease // J. Am. Coll. Cardiol. 2008. Vol. 52.
14. Jeremias A., Kaul S., Rosengart T.K. et al. The impact of revascularization on mortality in patients with nonacute coronary artery disease // Am. J. Med. 2009. Vol. 122. P. 152–161.
15. Stergiopoulos K., Brown D.L. Initial coronary stent implantation with medical therapy vs medical therapy alone for stable coronary artery disease // Arch. Intern. Med. 2012. Vol. 172. P. 312–319.
16. Pursnani S., Korley F., Gopaul R. et al. Coronary Intervention Versus Optimal Medical Therapy in Stable Coronary Artery Disease. A Systematic Review and Meta–Analysis of Randomized Clinical Trials. // Circ. Cardiovasc. Interv. 2012. Vol. 5. P. 476–490.
17. Бокерия Л.А., Алекян Б.Г. Рентгенэндоваскулярная диагностика и лечение заболеваний сердца и сосудов в Российской Федерации – 2011 год.– М.: Издательство НЦССХ им. А.Н. Бакулева РАМН, 2012.
18. Карпов Ю.А., Самко А.Н., Буза В.В. Коронарная ангиопластика и стентирование. – М.: Медицинское информационное агентство, 2010.
19. Karpov Y., Buza V. Pre–procedure C–reactive Protein and Erythrocyte Sedimentation Rate but not Lipoprotein–associated Phospholipase A2 Predict Clinical Outcomes after Drug–eluting Stents Implantation in Patients with Stable Coronary Disease on Chronic Statin Therapy .. AHA 2012. Abstract Poster Board Number: 2026.
20. International Study of Comparative Health Effectiveness with Medical and Invasive Approaches (ISCHEMIA) home page. 2012. Available at: https://www.ischemiatrial.org. Accessed June 11, 2012.
.
Чкв показания и противопоказания
Кто из больных с ОКС без подъема ST нуждается в ранней катетеризации сердца и реваскуляризации? В соответствии с рекомендациями, содержащимися в руководствах АСС/АНА (2007), ранняя инвазивная стратегия (т.е. диагностическая ангиография с намерением реваскуляризации) показана тем пациентам с ОКС без подъема ST, у которых имеются клинические характеристики, указывающие на высокий риск. Такими факторами риска являются:
— Рецидивирующая стенокардия и/или ишемия миокарда в покое или при минимальной активности
— Повышение уровня биохимических маркеров некроза миокарда (тропонины Т или I)
— Появление свежей (или предположительно свежей) депрессии сегмента ST на ЭКГ
— Прогрессирование СН, свежая или прогрессирующая митральная регургитация, артериальная гипотензия
— Признаки высокого риска при неинвазивном обследовании
— Снижение ФВ ЛЖ ниже 40%
— Нестабильность гемодинамики (артериальная гипотензия)
— Устойчивая желудочковая тахикардия
— ЧKB в течение последних 6 месяцев или ранее выполненное коронарное шунтирование
— Высокий риск по данным балльной оценки по различным шкалам (TIMI, GRACE)
При условии успешной первичной стабилизации состояния больного и при отсутствии вышеупомянутых факторов риска (группа низкого риска) может быть выбрана первично консервативная (или селективно инвазивная) стратегия лечения.
Каковы противопоказания для ЧKB и предикторы неблагоприятного исхода?
Единственными абсолютными противопоказаниями для ЧKB являются невозможность сосудистого доступа и активное тяжелое кровотечение, не позволяющее использовать антикоагулянтные и антитромбоцитарные средства. К относительным противопоказаниям относятся:
— Геморрагический диатез или другие состояния, предрасполагающие к кровотечению на фоне антитромбоцитарной терапии
— Тяжелая почечная недостаточность
— Сепсис
— Неудовлетворительное соблюдение пациентом рекомендаций по лечению
— Наличие терминального состояния, резко ограничивающего ожидаемую продолжительность жизни
— Наличие других состояний, являющихся показаниями для операции на открытом сердце
— Анатомические особенности, резко снижающие вероятность успешной манипуляции
— Неэффективность предшествующего чрескожного коронарного вмешательства (ЧКВ). В следующих ситуациях чрескожное коронарное вмешательство (ЧКВ), как правило, не должно выполняться:
— Если зона миокарда, кровоснабжаемого через пораженный сосуд, очень мала
— Если объективные признаки ишемии миокарда отсутствуют (за исключением случаев, когда у пациента имеются убедительные клинические признаки стенокардии, а нагрузочная проба по каким-то причинам не выполнена)
— Если вероятность успешной манипуляции низкая
— Если поражение ствола левой коронарной артерии выявлено у пациента, который является кандидатом на коронарное шунтирование
— Если стеноз сосуда гемодинамически незначим (менее 50%)
Клиническими предикторами неблагоприятного исхода чрескожного коронарного вмешательства (ЧКВ) являются пожилой возраст, нестабильность состояния (наличие ОКС, острого ИМ, декомпенсированной СН, КШ), многососудистый характер поражения коронарного русла, наличие дисфункции ЛЖ, сахарного диабета, почечной недостаточности, выраженного атеросклероза периферических артерий и небольшие размеры тела.
Ангиографическими предикторами неблагоприятного исхода вмешательства являются наличие интракоронарного тромба, обнаружение дегенерации коронарного шунта, «незащищенного» поражения ствола левой коронарной артерии, протяженных (более 20 мм) поражений коронарного русла, выраженной извилистости просвета проксимального сегмента, углового поражения артерии (90°), поражения в зоне бифуркации с вовлечением крупных периферических ветвей или в зоне хронической тотальной окклюзии.
— Вернуться в оглавление раздела «кардиология»
Оглавление темы «Лечение инфаркта миокарда, кардиогенного шока»:
- Антитромбоцитарные препараты. Механизмы действия, контроль
- Антикоагулянтная терапия. Механизмы действия гепарина
- Антикоагулянты при инфаркте миокарда без подъема сегмента ST. Ингибиторы тромбина
- Кардиогенный шок (КШ). Определение, признаки
- Что значит пансистолический шум при кардиогенном шоке? Как кардиогенный шок можно отличить от септического шока?
- Патогенез кардиогенного шока. Причины
- Лечение кардиогенного шока. Оптимальная тактика
- Лекарственная, механическая терапия кардиогенного шока. Принципы
- Чрескожное коронарное вмешательство (ЧКВ) при стенокардии. Показания
- Чрескожное коронарное вмешательство (ЧКВ) при инфаркте миокарда. Противопоказания к ЧКВ
Коронарная ангиография (КАГ). Стентирование коронарных артерий.
Ангиографией называется визуализация сосуда каким-либо
способом. Коронароангиография или коронарография (КАГ) – диагностическая (не
лечебная) визуализация коронарных (венечных) артерий сердца. Методом
визуализации служит введение (рентген)контрастного вещества в коронарную артерию и одновременное проведение рентгеноскопии – запись фильма, на котором видно, как контраст проходит по артериям.
Строение коронарного русла:
Коронарных артерий у человека три. От
аорты отходят правая и левая коронарная артерия, левая сперва идет одним стволом
(ствол левой коронарной артерии), а затем делится на переднюю нисходящую (или
переднюю межжелудочковую ветвь) и огибающую артерию. Эти три артерии дают ветви
первого порядка (передняя нисходящая – диагональную артерию, огибающая –
артерию тупого края, правая – артерию острого края и т.д.).
Существует
несколько анатомических вариантов строения коронарного русла. Например, между
передней нисходящей и огибающей артериями может отходить интермедиарная
артерия. Также различают правый, левый и сбалансированный тип кровоснабжения.
В настоящее время КАГ является полипозиционной, то есть рентгеновскую трубку
поворачивают в разные позиции и в каждой проводят рентгеноскопию, вводя
контраст. Это нужно для точной оценки поражения коронарной артерии, так как
съемка эксцентрического стеноза только в одной проекции даст ложную информацию.
Слева стеноз (сужение) коронарной артерии концентрический и даже в одной
проекции степень стеноза определена правильно. Справа стеноз эксцентрический.
При съемке только одной проекции степень стеноза недооценена. На самом деле
изображенный стеноз около 50%.
Сужение артерии называется стенозом. Как правило, стеноз
возникает за счет атеросклеротической бляшки.
Атеросклеротическая бляшка
Показаниями к КАГ является подозрение на ишемическую болезнь
сердца. Прежде всего, это характерные жалобы пациента – давящие или сжимающие
боли за грудиной, возникающие при физической нагрузке и купирующиеся в покое
или при приеме нитратов, длительность – до 20 мин. Иногда клиническая картина
стенокардии может быть атипичной – боль в эпигастрии, одышка, «комок в горле”.
Боль может иррадиировать в лопатку, руки, челюсть. Иногда боль может не
возникать – безболевая ишемия миокарда.
Длительная боль (несколько часов),
связанная с положением тела, скорее всего, является проявлением остеохондроза.
Обычно перед КАГ проводят неинвазивное обследование – велоэргометрию или
тредмил-тест (на беговой дорожке), стресс-эхокардиографию, перфузионную
сцинтиграфию миокарда, холтеровское (суточное) мониторирование ЭКГ. На
основании этих обследований решают вопрос о проведении КАГ.
КАГ может быть экстренной или плановой. Плановая КАГ проводится при подозрении
на стабильную ИБС. Экстренная проводится при остром коронарном синдроме или при
инфаркте миокарда в первые часы заболевания. За экстренной КАГ, как правило,
следует транслюминальная баллонная ангиопластика со стентированием.
Ангиограмма До и ПОСЛЕ стентирования
Противопоказание к КАГ
Абсолютное – тяжелые психические нарушения. Относительные –
инфекционное заболевание, почечная недостаточность (в этом случае проводят
специальную подготовку), аллергия на йод, анемия, коагулопатии, обострение
хронических заболеваний и т.д. В этом случае врач взвешивает риск и пользу КАГ и
принимает решение.
Проведение КАГ
КАГ проводится под местной анастезией (подкожно вводится
анестетик, например, лидокаин). Место пункции – бедренная артерия (в районе
паховой складки) или лучевая артерия (кисть руки). Бедренная артерия большего
диаметра и стенки ее не травмируются. При пункции лучевой артерии пациенту не
надо соблюдать постельный режим. (Возможно проведение КАГ через локтевую, подмышечную,
подключичную артерию, но эти доступы используются крайне редко).
Отделение интервенционной радиологии
Перед КАГ делают внутримышечный укол (транквилизатор+антигистаминный препарат)
и затем в операционной после местной анестезии пунктируют артерию. После этого
вводят проводник (напоминает тонкую гитарную струну) и по ней тонкую трубку –
катетер. Кончик катетера под контролем рентгеноскопии подводят к устью
коронарной артерии. Затем делают ряд записей с введением контраста. Все это
видно на мониторе. После удаляют катетер, накладывают давящую повязку.
Процедура закончена.
После нее рекомендуют обильное питье для лучшего вымывания
контраста.
На основании полученных данных выявляют поражение коронарных артерий,
определяют количество, локализацию и степень стеноза. И решают вопрос о
необходимости инвазивного лечения — транслюминальная баллонная ангиопластика со
стентированием (ТБКА, другое сокращение ЧКВ), реже без установки стента, или
коронарное шунтирование.
Если у пациента значимо поражены все три артерии, или
имеется терминальный стеноз ствола и стеноз передней нисходящей артерии, то скорее
рекомендуют проведение коронарного шунтирования.
Осложнения КАГ
Встречаются редко, примерно в 0,1% (1 случай из 1000). К ним
относят аллергию, кровотечение, прокол/разрыв артерии, закрытие артерии,
гематому в месте пункции, почечную недостаточность. Раньше могли возникать
инсульты, которые сейчас практически не встречаются (используются качественные
расходные материалы). Инфаркт миокарда может произойти только при крайне
тяжелом поражении коронарного русла, то есть когда состояние пациента
критическое.
Несмотря на перечень возможных осложнений, следует отметить, что
он указывается скорее по этическим причинам, так как осложнения при КАГ в
настоящее время встречаются крайне редко.
Амбулаторно или стационарно?
Чаще КАГ выполняют стационарно (при госпитализации), так как
возможно одномоментное проведение транслюминальной баллонной ангиопластики, а
также для проведения перед КАГ вышеуказанных обследований. Однако в ряде
случаев возможно и амбулаторное выполнение КАГ. Решить данный вопрос должен
врач.
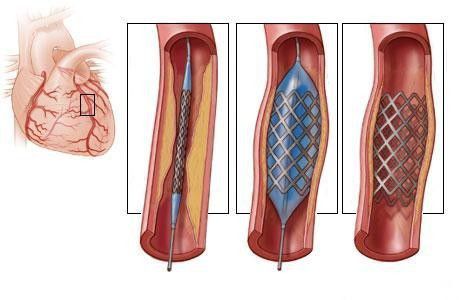
Процедура баллонной ангиопластики со стентированием (ТБКА).
В последние годы увеличивается число случаев внезапной смерти у пациентов с
поражением коронарных артерий. Поражение артерий, кровоснабжающих сердце ведёт
к их стенозу и обструкции; в результате нарушается кровоснабжение сердечной
мышцы. Как правило, причиной подобного сужения является наличие атеросклеротической
бляшки на стенке артерии.
Эти жировые отложения и ведут к уменьшению поступления кислорода к сердцу. Когда
кровоснабжение миокарда опускается ниже определённого уровня требуется
проводить медикаментозное лечение. На фото представлено поражение коронарной
артерии.
Основным не хирургическим путём восстановления просвета
коронарной артерии является проведение Чрезкожной транслюминарной коронарной
баллонной ангиопластики. Вы можете судить о сути этой манипуляции исходя из её
названия:
Чрезкожная – обозначает, что введение катетера в сосуд
осуществляется через прокол кожи.
Транслюминарная – означает, что все манипуляции
проводятся через коронарные артерии.
Коронарная – означает, что воздействию подвергается
коранарная артерия, то есть артерия, кровоснабжающая сердце.
Ангиопластика – означает, что производится
восстановление просвета сосуда (при помощи баллона).
Термин «баллонная» означает, что восстановление просвета
поражённой артерии (показана на рисунке) происходит путём проведения катетера с
баллоном и последующем его раздуванием.
Для установки стента используется специальный катетер.
Вопрос о проведении баллонной ангиопластики и стентирования решается после
получения результатов коронарографии – изображения коронарных артерий. Для этого
в просвет коронарной артерии при помощи катетера вводится контраст.
Процедура баллонной ангиопластики может быть выполнена как одномоментно при
коронарографии, так и через некоторое время (но не более чем через 6 месяцев,
так как за это время могут произойти изменеия ангиографической картины).
Преимуществом одномоментной ангиопластики является меньшая травматичность
(артерия пунктируется один раз). Преимуществом отсроченной ангиопластики
является возможность более точно подобрать стент (тип, длина, диаметр). Выбор
процедуры в каждом конкретном определяется врачом, проводящим коронарографию.
Ниже пошагово предоставлена информация о технике проведения Транслюминарной
Баллонной Коронарной Ангиопластики (ТБКА).
Процедура проведения ТБКА
Подготовка
После проведения предварительного обследования (анализы,
ЭКГ, ЭХО КГ, изотопная диагностика), Вам необходимо принять душ, сбрить волосы
в области паха (при доступе через бедренную артерию). Следует отказаться от
завтрака, или завтрак должен быть лёгким. Нужно иметь 1.5-2 литра минеральной
воды без газа и новую видеокассету (или чистый CD-диск с возможностью записи).
Процедура
Продолжительность процедуры различная в каждом конкретном
случае, в среднем 1-2 часа.
Пациента доставляют в лабораторию ангиографии после предварительной
премедикации (в/м введение седативных препаратов). В лаборатории производиться
укладка пациента на хирургический стол и установка кубитального катетера (в
вену руки).
В лаборатории поддерживается стерильная чистота, поэтому
родственники и друзья не могут присутствовать при процедуре. На руки и ноги
накладываются электроды для постоянного мониторирования ЭКГ. Место пункции
обрабатывается антисептиком, затем вводится анестетик (новокаин, лидокаин и
др.). Процедура проводится под местной анестезией. При проведении анестезии
пациент может чувствовать «покалывание иголочек». Через кубитальный катетер
вводятся необходимые препараты. Помните – Вы можете говорить в процессе
процедуры, сообщайте о любых изменениях в Вашем самочувствии врачу.
Вся процедура проводится под рентгеновским контролем. Катетер с баллоном на
конце вводится через место пункции и продвигается по направлению к сердцу.
Когда катетер достигнет места стеноза, Вы можете
почувствовать дискомфорт за грудиной, это является нормальным явлением. Во
время раздувания баллона может появиться боль. Врач может попросить задержать
дыхание на несколько секунд.
После проведения процедуры пациент переводиться в блок
интенсивной терапии для динамического наблюдения за ЭКГ, показателями крови и
местом пункции. В артерии в течение нескольких часов находится маленький гибкий
катетер (интродьюсер), который затем удаляется врачом. Накладывается давящая
повязка на место пункции. В это время не разрешается сгибать ногу. На следующий
день пациента переводят в палату, снимают повязку и разрешают ходить.
Есть и пить можно сразу после процедуры. Рекомендуется
выпить 1-1.5 литра минеральной воды для лучшего выведения контраста.
Первые несколько дней после проведения ТБКА нужно несколько
ограничить физическую активность (нагрузку на нижние конечности).
Так выглядит стент
Возможные осложнения и риск.
Если Вы следуете рекомендациям врачей, риск от процедуры
минимален. В случае осложнений немедленно будет оказана помощь в полном объёме
(вплоть до экстренной операции коронарного шунтирования.).
Возможные осложнения:
- Кровотечение в месте пункции.
- Нарушение ритма сердца.
- Аллергическая реакция на контраст.
- Тромбоз коронарной артерии в месте баллонирования.
- Развитие инфаркта миокарда.
После процедуры
Врач может изменить терапию (например отменить нитраты,
бета-блокаторы, назначить средства, влияющие на свёртываемость крови).
Впоследствии мы рекомендуем периодически проходить обследование – лабораторные
исследования, ЭКГ, нагрузочный тест, изотопная диагностика и др.
В некоторых случаях возможно возникновение рестеноза коронарной артерии.
Поэтому, сли Вы почувствуете загрудинную боль, сообщите своему лечащему врачу.
Помните, что процедура ТБКА является наиболее безопасным методом лечения
ишемической болезни сердца и находит всё более широкое применение.
Рекомендации после операции стентирования коронарных артерий
После выписки избегайте напряженной деятельности и тяжелой
физической работы несколько дней. Место пункции, скорее всего, останется
напряженным на некоторое время. Оно может быть слегка припухлым иметь небольшие
кровоподтеки.
Обратитесь к врачу, если:
— Вы заметили кровотечение, новые кровоподтеки или сильную припухлость в
области пункции и установки катетера;
— Вы чувствуете нарастающую боль или дискомфорт в области пункции и установки
катетера;
— В области пункции и установки катетера появилось покраснение и возникла
лихорадка;
— Изменилась температура или цвет ноги / руки, через которую была проведена
процедура;
— Вы чувствуете боль в груди или одышку.
Источник: noatero.ru
Что такое спасительное чрезкожное коронарное вмешательство (ЧКВ)
Последнее обновление статьи: Апрель , 2019
Все мероприятия при медикаментозном лечении инфаркта миокарда не решают проблему радикально, а направлены только на возвращения болезни в ремиссию, и часто такие меры бывают не достаточно эффективными. Это приводит либо к гибели пациента, либо к его инвалидизации.
В настоящее время, как за рубежом так и в нашей стране, лечение инфаркта миокарда проводится все чаще с помощью интервенционных технологий – то есть уже в острый период проводят коронарографию, обнаруживают инфаркт-зависимую артерию и стентируют ее или хотя бы временно расширяют специальным баллоном. Эта процедура и называется спасительное чрезкожное коронарное вмешательство (ЧКВ), так как проводится сразу при поступлении пациента в лечебное учреждение, не дожидаясь эффекта от терапии, либо когда другие методы уже исчерпаны.
Конечно, при остром инфаркте миокарда риск осложнений при коронарографии значительно возрастает по сравнению с плановой процедурой, но ни один из препаратов не сможет так восстановить кровоток в пораженной артерии как механическое устранение этой проблемы. Однако, ввиду отсутствия дорогостоящего оборудования, клиники, где могут провести такое лечение, есть не везде. Кроме того, такое радикальное лечение гораздо дороже консервативного и не по карману большинству пациентов. Хорошо когда эти затраты может взять на себя государство как например в Санкт — Петербурге.
The following two tabs change content below.
Автор статьи, доктор Гохман Александр.
врач- кардиолог/терапевт интернист медицинский центр Каплан (Израиль)
Чрезкожное коронарное вмешательство — Percutaneous coronary intervention
Чрескожное коронарное вмешательство ( PCI ) не является хирургической процедура используется для лечения сужения из коронарных артерий в сердце находится в болезни коронарной артерии . Процесс включает в себя сочетание коронарной ангиопластики со стентированием, которое представляет собой введение постоянной проволочной сетки, которая либо выделяется лекарственным средством (DES), либо состоит из чистого металла (BMS). Баллон для доставки стента из катетера для ангиопластики надувается средой для обеспечения контакта между стойками стента и стенкой сосуда (наложение стента), таким образом увеличивая диаметр кровеносного сосуда. После получения доступа к кровотоку через бедренную или лучевую артерию в процедуре используется коронарная катетеризация для визуализации кровеносных сосудов на рентгеновских снимках. После этого интервенционный кардиолог может выполнить коронарную ангиопластику , используя баллонный катетер, в котором спущенный баллон продвигается в закупоренную артерию и надувается, чтобы уменьшить сужение; некоторые устройства, такие как стенты, могут быть развернуты, чтобы кровеносный сосуд оставался открытым. Также могут быть выполнены различные другие процедуры.
Первичное ЧКВ — это неотложное применение ЧКВ у людей с острым сердечным приступом , особенно если на электрокардиограмме есть доказательства поражения сердца . ЧКВ также используется у людей после других форм инфаркта миокарда или нестабильной стенокардии, когда существует высокий риск дальнейших событий. Наконец, ЧКВ можно использовать у людей со стабильной стенокардией , особенно если симптомы трудно контролировать с помощью лекарств. ЧКВ является альтернативой аортокоронарному шунтированию (АКШ, часто называемым «шунтирование»), которое позволяет обойти стенозированные артерии путем пересадки сосудов из других частей тела. При определенных обстоятельствах, таких как обширная закупорка, фон диабета , АКШ может быть лучше.
Коронарная ангиопластика была впервые введена в 1977 году Андреасом Грунцигом в Швейцарии.
Медицинское использование
Коронарная ангиография и ангиопластика при остром инфаркте миокарда (слева: ПКА закрыта, справа: ПКА успешно расширена)
ЧКВ используется в первую очередь для открытия закупоренной коронарной артерии и восстановления артериального кровотока в ткани сердца без операции на открытом сердце. У пациентов с суженной или заблокированной коронарной артерией ЧКВ может быть лучшим вариантом для восстановления кровотока, а также предотвращения стенокардии (боли в груди), инфаркта миокарда (сердечного приступа) и смерти. Сегодня ЧКВ обычно включает установку стентов, таких как металлические стенты, стенты с лекарственным покрытием и полностью рассасывающиеся сосудистые каркасы (или естественно растворяющиеся стенты). Было показано, что использование стентов важно в течение первых трех месяцев после ЧКВ; после этого артерия может оставаться открытой сама по себе. Это предпосылка для разработки биорезорбируемых стентов, которые растворяются естественным образом, когда они больше не нужны.
Целесообразность использования PCI зависит от многих факторов. ЧКВ может быть подходящим для пациентов со стабильной ишемической болезнью сердца, если они соответствуют определенным критериям, таким как наличие коронарного стеноза более 50 процентов или симптомы стенокардии, не поддающиеся лечению. Хотя ЧКВ не может оказать большей помощи в предотвращении смерти или инфаркта миокарда по сравнению с пероральными препаратами для пациентов со стабильной ИБС, оно, вероятно, обеспечивает лучшее облегчение стенокардии.
У пациентов с острым коронарным синдромом может быть целесообразным ЧКВ; руководящие принципы и лучшие практики постоянно развиваются. У пациентов с тяжелой блокадой, такой как инфаркт миокарда с подъемом сегмента ST (ИМпST), ЧКВ может иметь решающее значение для выживания, поскольку оно снижает смертность, инфаркты миокарда и стенокардию по сравнению с лекарствами. Для пациентов с инфарктом миокарда без подъема сегмента ST (nSTEMI) или нестабильной стенокардией лечение медикаментами и / или ЧКВ зависит от оценки риска пациента. Время от двери до баллона используется в больницах как критерий качества для определения своевременности первичного ЧКВ.
Использование ЧКВ в дополнение к лекарствам от стенокардии при стабильной стенокардии может снизить количество пациентов с приступами стенокардии на срок до 3 лет после терапии, но не снижает риск смерти, инфаркта миокарда в будущем или необходимости других вмешательств.
Неблагоприятные события
Коронарная ангиопластика широко практикуется и сопряжена с рядом рисков; однако серьезные процедурные осложнения случаются редко. Коронарная ангиопластика обычно выполняется с использованием инвазивных катетерных процедур интервенционным кардиологом, врачом, имеющим специальную подготовку в области лечения сердца.
Во время ангиопластики пациент обычно не спит, и во время процедуры может возникнуть дискомфорт в груди. Пациент не спит, чтобы следить за симптомами пациента. Если симптомы указывают на то, что процедура вызывает ишемию, кардиолог может изменить или прервать часть процедуры. Кровотечение из точки введения в пах (бедренная артерия) или запястье (лучевая артерия) является обычным явлением, отчасти из-за приема антиагрегантов . Некоторые кровоподтеки поэтому следует ожидать, но иногда гематомы может образоваться. Это может задержать выписку из больницы, так как кровоток из артерии в гематому может продолжаться (псевдоаневризма), что требует хирургического вмешательства. Инфекция в месте прокола кожи встречается редко, а расслоение (разрыв) доступного кровеносного сосуда — нечасто. Возможна аллергическая реакция на используемый контрастный краситель, но она уменьшилась с помощью новых средств. Ухудшение функции почек может произойти у пациентов с уже существующим заболеванием почек, но почечная недостаточность, требующая диализа, встречается редко. Осложнения сосудистого доступа менее распространены и менее серьезны, когда процедура проводится через лучевую артерию.
Наиболее серьезными рисками являются смерть , инсульт , фибрилляция желудочков ( часто бывает неустойчивая желудочковая тахикардия ), инфаркт миокарда (сердечный приступ, инфаркт миокарда ) и расслоение аорты . Инфаркт во время или вскоре после процедуры возникает в 0,3% случаев; для этого может потребоваться экстренное аортокоронарное шунтирование . Повреждение сердечной мышцы, характеризующееся повышенными уровнями CK-MB , тропонина I и тропонина T, может наблюдаться до 30% всех процедур ЧКВ. Повышенные ферменты были связаны с более поздними клиническими исходами, такими как более высокий риск смерти, последующий ИМ и необходимость повторных процедур реваскуляризации. Ангиопластика, проводимая вскоре после инфаркта миокарда, имеет риск возникновения инсульта , но он меньше, чем риск инсульта после тромболитической терапии.
Как и в случае с любой процедурой на сердце, осложнения иногда, хотя и редко, могут привести к смерти. Летальность при ангиопластике — 1,2%. Иногда во время ангиопластики может возникнуть боль в груди, потому что баллон на короткое время перекрывает кровоснабжение сердца. Риск осложнений выше:
- Люди в возрасте 65 лет и старше
- Людям с заболеванием почек или диабетом
- женщины
- Люди с плохой насосной функцией сердца
- Людям с обширными сердечными заболеваниями и закупорками
Процедура
Термин баллонная ангиопластика обычно используется для описания надувания баллона в коронарной артерии с целью раздавливания бляшки на стенках артерии. Хотя баллонная ангиопластика до сих пор проводится как часть почти всех чрескожных коронарных вмешательств, это редко бывает единственной процедурой.
Другие процедуры, выполняемые во время чрескожного коронарного вмешательства, включают:
Процедура ангиопластики обычно состоит из большинства следующих шагов и выполняется группой, состоящей из врачей, помощников врача , практикующих медсестер , медсестер , рентгенологов и специалистов по эндоваскулярным заболеваниям ; все они прошли обширную специализированную подготовку по этим типам процедур.
- Бедренная артерия в ноге или лучевой артерии в руке прокалывается с помощью иглы и небольшой провод проходит в артерию. Эту процедуру часто называют чрескожным доступом.
- Как только доступ в артерию получен, «интродьюсер» помещается поверх проволоки в артерию, чтобы позволить катетерам продвинуться в артерию и остановить кровотечение.
- Через эту оболочку проталкивается длинная гибкая мягкая пластиковая трубка, называемая «направляющим катетером». Наконечник направляющего катетера помещается в устье коронарной артерии. Направляющий катетер позволяет вводить рентгеноконтрастные красители (обычно на основе йода) в коронарную артерию, так что состояние и местонахождение заболевания можно легко оценить с помощью рентгеновской визуализации в реальном времени.
- Во время рентгеновской визуализации кардиолог оценивает размер коронарной артерии и выбирает тип баллонного катетера и коронарного проводника, которые будут использоваться во время исследования. Гепарин («разжижитель крови» или лекарство, используемое для предотвращения образования тромбов) назначают для поддержания кровотока. Бивалирудин при использовании вместо гепарина вызывает более высокий уровень инфаркта миокарда, но более низкий уровень кровотечений.
- Коронарный проводник, который представляет собой очень тонкий провод с рентгеноконтрастным гибким наконечником, вводится через направляющий катетер в коронарную артерию. При повторной визуализации с помощью рентгеновских снимков в реальном времени кардиолог направляет провод через коронарную артерию к месту стеноза или закупорки. Затем конец проволоки пропускают через засорение. Кардиолог контролирует движение и направление проволочного направителя, осторожно манипулируя концом, который находится вне пациента, путем скручивания проволочного проводника.
- Пока проволочный проводник находится на месте, он действует как путь к стенозу. Кончик катетера для ангиопластики или баллонного катетера является полым и затем вставляется в заднюю часть проволочного направителя — таким образом, проводник теперь находится внутри катетера для ангиопластики. Катетер для ангиопластики осторожно продвигается вперед, пока спущенный баллон не окажется внутри закупорки.
- Затем баллон надувается, он сжимает атероматозную бляшку и растягивает стенку артерии для расширения.
- Если на баллоне был стент, то он будет имплантирован (оставлен) для поддержки нового растянутого открытого положения артерии изнутри.
Типы стентов
Традиционные металлические стенты (BMS) представляют собой механический каркас, который удерживает стенку артерии открытой, предотвращая стеноз или сужение коронарных артерий.
Новые стенты с лекарственным покрытием (DES) представляют собой традиционные стенты с полимерным покрытием, содержащим лекарства, предотвращающие пролиферацию клеток. Антипролиферативные препараты высвобождаются медленно с течением времени, чтобы помочь предотвратить рост ткани, который может возникать в ответ на стент, который может блокировать артерию. Было показано, что эти типы стентов помогают предотвратить рестеноз артерии с помощью физиологических механизмов, которые зависят от подавления роста ткани в месте стента и местной модуляции воспалительных и иммунных реакций организма. Первые два стента с лекарственным покрытием, которые были использованы, были стент с покрытием паклитакселом и стент с покрытием сиролимусом , оба из которых получили одобрение Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США. Большинство современных одобренных FDA стентов с лекарственным покрытием используют сиролимус (также известный как рапамицин), эверолимус и зотаролимус . Стенты с покрытием Biolimus A9, в которых используются биоразлагаемые полимеры, одобрены за пределами США.
Однако в 2006 году клинические испытания показали возможную связь между стентами с лекарственным покрытием и событием, известным как «поздний тромбоз стента», когда свертывание крови внутри стента может происходить через один или несколько лет после имплантации стента. Поздний тромбоз стента возникает у 0,9% пациентов и заканчивается летальным исходом примерно в одной трети случаев, когда возникает тромбоз. Повышенное внимание к продолжительности приема антитромбоцитарных препаратов и стентам нового поколения (например, стентам, выделяющим эверолимус) резко снизило опасения по поводу позднего тромбоза стентов.
Технологии ЧКВ нового поколения направлены на снижение риска позднего тромбоза стента или других долгосрочных нежелательных явлений. Некоторые продукты DES продают биоразлагаемое полимерное покрытие, полагая, что стойкие полимерные покрытия DES способствуют долгосрочному воспламенению. Другие стратегии: в более недавнем исследовании предполагается, что в случае популяции с сахарным диабетом — группы особого риска — лечение баллонным препаратом с паклитакселом с последующим БМС может снизить частоту коронарного рестеноза или инфаркта миокарда по сравнению с применением только БМС.
После установки стента или каркаса пациенту необходимо принимать два антиагрегантных препарата (аспирин и один из нескольких других вариантов) в течение нескольких месяцев, чтобы предотвратить образование тромбов. Продолжительность приема двойной антитромбоцитарной терапии зависит от индивидуального риска ишемических событий и риска кровотечения.
Аспирация тромба
При первичном ЧКВ ангиография может выявить тромб (сгустки крови) внутри коронарных артерий. Были проведены различные исследования, чтобы определить, полезна ли аспирация этих сгустков (аспирация тромба или ручная тромбэктомия). На данный момент нет доказательств того, что обычная аспирация сгустка улучшает результаты.
использование
Чрескожная коронарная ангиопластика — одна из наиболее распространенных процедур, выполняемых во время пребывания в больнице в США; на его долю приходилось 3,6% от всех операций в операционных, выполненных в 2011 году. Однако с 2001 по 2011 год его объем снизился на 28%, с 773 900 операционных процедур, выполненных в 2001 году, до 560 500 процедур в 2011 году.
Сравнение с АКШ
Большинство исследований показали, что АКШ дает преимущества в снижении смертности и инфаркта миокарда у людей с многососудистой блокадой по сравнению с ЧКВ. Различные исследования моделирования пришли к противоположным выводам об относительной рентабельности ЧКВ и АКШ у людей с ишемией миокарда, которая не улучшается при медикаментозном лечении.
История
Коронарная ангиопластика, также известная как чрескожная транслюминальная коронарная ангиопластика (ЧТКА), потому что она проводится через кожу и через просвет артерии, была впервые разработана в 1977 году Андреасом Грунцигом . Первая процедура прошла в пятницу 16 сентября 1977 года в Цюрихе , Швейцария . Принятие процедуры ускорилось после переезда Грюнцига в Университет Эмори в США. Первым сотрудником Грюнцига в Эмори был Меррил Кнудтсон , который к 1981 году уже представил его в Калгари , Альберта , Канада . К середине 1980-х годов многие ведущие медицинские центры по всему миру начали применять эту процедуру для лечения ишемической болезни сердца .
Ангиопластика иногда называют «Dottering», после интервенционный радиолог , д — р Чарльз Теодор Dotter , который вместе с доктором Melvin П. Джудкинс, впервые была описана в 1964 году ангиопластики Поскольку спектр процедур , выполняемых при коронарной артерии лм расширился, имя процедуры заменено чрескожным коронарным вмешательством.
Исследовательская работа
Современные концепции признают, что через три месяца артерия адаптировалась, зажила и больше не нуждается в стенте. Полная реваскуляризация всех стенозированных коронарных артерий после ИМпST более эффективна с точки зрения серьезных неблагоприятных сердечных событий и общей смертности, но при этом безопаснее, чем подход с использованием только виновных сосудов.
Полемика
В 2007 году Медицинский журнал Новой Англии опубликовал результаты исследования COURAGE. В исследовании сравнивали стентирование, используемое при ЧКВ, и только медикаментозную терапию при симптоматической стабильной ишемической болезни сердца (ИБС). Это показало, что при стабильной ИБС не было преимущества в отношении смертности по сравнению со стентированием, хотя наблюдалось более раннее облегчение симптомов, которое выровнялось на пять лет. После этого испытания были широко опубликованы отчеты отдельных врачей, выполняющих ЧКВ пациентам, которые не соответствовали никаким традиционным критериям. Метаанализ 2014 года показал, что использование стентов второго поколения с лекарственным покрытием , которые не были доступны во время исследования COURAGE, может снизить смертность . С тех пор медицинские общества выпустили рекомендации относительно того, когда целесообразно проводить чрескожное коронарное вмешательство. В ответ на это было замечено, что частота несоответствующего стентирования снизилась в период с 2009 по 2014 год. Опубликованные статистические данные о тенденциях в госпитальных процедурах в США показали 28% -ное снижение общего количества ЧКВ, выполненных в период с 2001 по 2011 год, с самое большое снижение, заметное с 2007 года.
Исследование ORBITA 2017 года также вызвало много споров, поскольку оно показало, что после чрескожного коронарного вмешательства не было статистически значимой разницы во времени упражнений по сравнению с медикаментозной терапией. Авторы исследования считают, что облегчение стенокардии с помощью ЧКВ во многом является эффектом плацебо. Другие отметили небольшой размер выборки, недостаточную мощность для выявления различий в результатах и короткую 6-недельную продолжительность испытания. 85% пациентов в группе медикаментозной терапии выбрали ЧКВ в конце исследования.
Исследование ISCHEMIA 2019 подтвердило, что инвазивные процедуры (ЧКВ или АКШ) не снижают смертность или сердечные приступы по сравнению с одной медикаментозной терапией стабильной стенокардии. У пациентов со стенокардией улучшилось качество жизни после ЧКВ по сравнению с медикаментозной терапией.
Ссылки
внешние ссылки
Проведение кардиографии (КАГ) сердца: что это такое?
Проведение КАГ сердца может быть назначено пациентам по многим причинам. Коронарография (КАГ) позволяет выявить множественные заболевания сердечной мышцы, в частности, ишемическую болезнь.
Коронарография в кардиологии часто назначается пациентам перед тем, как провести хирургическую операцию на данном органе. В процессе такого обследования врач может определить, какую тактику лечения выбрать, возможно ли проводить оперативное вмешательство, и если да, то как лучше его произвести.
1
Коронарная ангиография и ее назначение
Данный диагностический способ относят к малоинвазивным методикам инструментального исследования. В ходе диагностики устанавливается степень проходимости коронарных сосудов, которые снабжают сердечную мышцу кислородом. Если происходит сужение их просвета, то, соответственно, ухудшается кровоснабжение сердца. Причиной сужения сосудов могут быть: атеросклеротические бляшки, спазм сосудов, врожденная патология развития сосудов.
В основе коронарографии лежит обычное рентгенологическое исследование с применением контрастного вещества, которое заполняет просветы сосудов и отображает их на рентгеновском снимке.
Коронарография назначается пациенту врачом на основании следующих причин:
- 1. Нахождение пациента в группе риска возникновения осложнений, которые подтверждаются другими диагностическими мероприятиями, что проводились ранее.
- 2. Малоэффективное или полное отсутствие положительных результатов после медикаментозного лечения ишемической болезни сердца.
- 3. Если пациент перенес инфаркт миокарда, который сопровождался гипотонией, отеком легких или дисфункцией левого желудочка, и у него наблюдается нестабильная стенокардия, что не поддается медикаментозному лечению.
- 4. Невозможность выявить патологические процессы другими исследовательскими методиками.
- 5. Предоперационное обследование. Если пациенту назначается хирургическая операция на открытом сердце проводимая, к примеру, с целью протезирования и лечения сердечных клапанов.
Правила и техника снятия ЭКГ
2
Подготовка к коронароангиографии
Коронароангиография — это достаточно сложная исследовательская методика, перед проведением которой следует пройти специальную подготовку. Но бывают и ситуации, когда пациент нуждается в проведении экстренной коронароангиографии.
После того, как человеку было назначено КАГ, на подготовительном этапе ему предстоит сдать следующие анализы:
- ЭКГ в 12 отделах;
- тест на ВИЧ-инфекцию;
- анализ на гепатит грубы С,В;
- RW-исследование;
- общий анализ крови.

Дополнительно может быть назначен анализ определяющий группу крови и резус-фактор, если человек ранее его не сдавал и не имеет соответствующих записей в медицинской карте.
После того, как кардиолог проведет опрос пациента и расшифрует результаты предыдущих анализов, он может направить больного на обследование к другим специалистам. Это делается с той целью, чтобы получить максимально детальные результаты и выявить сопутствующие заболевания, наличие которых может отражаться на результатах коронарографии.
Если в процессе подготовительного обследования не выявлено причин, которые могут во время процедуры коронарной ангиографии отрицательно повлиять на состояние пациента, назначается дата проведения коронарографии.

Как проводят ЭФИ сердца?
3
Техническая сторона исследования
Во время выполнения процедуры исследования пациент будет находиться в лежачем положении, на спине. Чтобы исследование было максимально комфортным, пациенту делается местный наркоз, при котором пациент остается в сознании.

Чтобы ввести в организм рентгенологическое контрастное вещество, потребуется сделать прокол. Его могут выполнить в верхней части бедра, в редких случаях местом прокола является предплечье.
В образовавшееся отверстие вводится катетер. Его аккуратно продвигают вглубь, пока он не достигнет сосудов. После того, как катетер достигнет своего место назначения, через него в просвет коронарных сосудов вводят контрастное вещество.
С помощью специального аппарата, который называется ангиограф, врач отслеживает, как движется контрастное вещество с током крови по коронарным сосудам. Получаемая картинка выводится на мониторе врача. Также все данные сохраняются на цифровом носителе.
На мониторе рентгено-контрастное вещество отображается в виде теней. Получаемая картинка точно передает все проблемные участки, что позволяет оценить степень сложности патологии. Врач может рассмотреть, где именно произошло сужение просвета коронарных сосудов, а где кровь вовсе не циркулирует.
Если во время диагностики врач обнаружит закупорку сосудистого просвета, которую называют окклюзией, пациенту рекомендуется как можно быстрее провести операцию по устранению такого патологического состояния, ведь оно представляет собой угрозу для жизни пациента.
Чтобы минимально травмировать пациента, в ходе коронарографии производится баллонная дилатация или стентирование коронарных сосудов в местах их сужения. Данные действия обговариваются с пациентом еще на подготовительном этапе.

Когда нужно делать МРТ сердца и коронарных сосудов?
4
Существующие противопоказания
Коронарная ангиография имеет множество преимуществ, но есть и недостатки, за счет которых не всем пациентам может проводиться данный способ обследования.
Перечень противопоказаний к данной процедуре может несколько отличаться, все будет зависеть от индивидуальных особенностей организма пациента.
При наличии аллергической реакции организма на контрастное рентгенологическое вещество, что вводится для проведения исследования, пациенту коронарную ангиографию не делают. Также процедура исследования не назначается:
- 1. При диагностировании у пациента сердечной или почечной недостаточности. В данной ситуации, пациенту может быть изначально назначен курс медикаментозной терапии, который будет направлен на стабилизацию состояния больного. При положительном результате лечения такое исследование, как коронарография становится возможной.
- 2. Проблемы с процессом свертывания крови или анемия. Процедура исследования станет возможной, как и в предыдущем случае, только после предварительного курса лечения, который нормализует состояние пациента.
- 3. При сахарном диабете.
- 4. Различные инфекционные заболевания, особенно те, что протекают в острой форме.
- 5. Эндокардит.
- 6. Язвенная болезнь в стадии обострения.
- 7. Повышенное артериальное давление, лечение которого малоэффективно медикаментозно. То есть, состояние пациента нельзя стабилизировать.
После того, как будет проведена коронарография, у пациента могут возникнуть следующие осложнения:
- открытие кровотечения в месте, где был сделан прокол для катетера;
- появление аллергической реакции на контрастное вещество;
- различного рода аритмии;
- развитие инфаркта миокарда;
- острое отслоение интимы артерии.
Несмотря на профессионализм врачей и все меры предосторожностей, осложнения все же могут быть. Поэтому перед тем, как назначить коронарографию, врач обязан изучить клиническую картину состояния больного и проинформировать пациента о возможных последствиях такого диагностического вмешательства в организм.
PCI для ИМпST — Советчик по кардиологии
Общее описание процедуры, оборудования, техники
Чрескожное коронарное вмешательство (ЧКВ) — широко применяемая инвазивная процедура, предназначенная для лечения обструктивных поражений эпикардиальных коронарных артерий и их основных ветвей. После введения сосудистой оболочки в периферическую артерию (лучевую, плечевую или бедренную) катетеры специальной формы продвигаются к устью коронарных артерий, и выполняется коронарная ангиография с использованием рентгеноконтрастного материала.После того, как обструктивные поражения будут идентифицированы и охарактеризованы, проводится адекватная антикоагуляция и начинается ЧКВ.
Сначала направляемый провод проводится через препятствие и дистальнее, а над ним устанавливаются баллоны, аспирационные катетеры, устройства для атерэктомии и стенты для лечения. В настоящее время более 90% ЧКВ включают имплантацию коронарного стента — металлического каркаса, предназначенного для проталкивания внутрипросветного материала (атеросклеротической бляшки, тромба, кальция) к стенке сосуда, одновременно способствуя заживлению сосудов и восстановлению эндотелиальной функции.Большинство используемых в настоящее время стентов покрыты антирестенотическими соединениями (стенты с лекарственным покрытием), такими как паклитаксел, сиролимус или его модифицированные родственные соединения, которые в значительной степени предотвращают естественную миграцию и пролиферацию гладкомышечных клеток, присущие повреждению и заживлению сосудов. Еще больше новых стентов имеют либо биорезорбируемые полимеры, которые растворяются после элюирования лекарственного средства, либо полностью состоят из биорезорбируемых каркасов из полимолочной кислоты (без металлического каркаса), которые исчезают через 1-3 года после имплантации.
Показания и выбор пациента
ЧКВ выполняется более чем одному миллиону пациентов ежегодно только в Соединенных Штатах и примерно у двух миллионов человек во всем мире. Почти две трети этих пациентов имеют острый коронарный синдром (ОКС), включающий в себя такие разнообразные клинические проявления, как нестабильная стенокардия, инфаркт миокарда без подъема сегмента ST (ИМбпST) и инфаркт миокарда с подъемом сегмента ST (ИМпST). Другая треть — это плановые пациенты со стабильной ишемической болезнью сердца (ИБС), аномальными стресс-тестами или симптомами, которые недопустимы, несмотря на интенсивную медикаментозную терапию.
пациентов с ИМпST составляют особенно важный сегмент общей популяции ЧКВ. Хотя в Соединенных Штатах ежегодно в нее входят от 350 000 до 400 000 пациентов, именно в этой группе достигается максимальная польза от ЧКВ с точки зрения снижения смертности, заболеваемости и продолжительности пребывания в больнице.
Пациенты с ИМпST — это пациенты, у которых внезапное разрушение атеросклеротической бляшки приводит к интенсивной коагуляции и образованию богатого тромбоцитами тромба, который превращается в окклюзионный богатый фибрином тромб, построенный вокруг начальной тромбоцитарной пробки.Для этих пациентов немедленная реперфузионная терапия имеет решающее значение для ограничения размера инфаркта, содействия благоприятному ремоделированию пораженной территории и прилегающих сегментов и предотвращения ухудшения гемодинамического статуса.
Реперфузия может быть обеспечена либо путем введения фибринолитических агентов, либо путем выполнения экстренного (первичного — поскольку это основной метод реперфузии) ЧКВ. Более 25 клинических исследований и многочисленные метаанализы продемонстрировали, что по сравнению с фибринолизом ЧКВ предотвращает две смерти, шесть нефатальных инфарктов миокарда, 15 эпизодов рецидивирующей ишемии и один инсульт (преимущественно геморрагический инсульт) на каждые 100 пациентов, получавших лечение. .В каждой из этих категорий наблюдается очень статистически значимое снижение относительного риска от 20 до 75% и сопутствующее сокращение пребывания в больнице примерно на 1 день. Такое глубокое клиническое преимущество объясняется уникальными особенностями первичного ЧКВ, а именно его способностью восстанавливать нормальный антеградный кровоток (тромболизис при инфаркте миокарда [TIMI] 3 flow) в артерии, связанной с инфарктом, примерно у 90% пациентов. Это очень выгодно отличается от 40–60% успеха при фибринолизе.
Но помимо эпикардиального кровотока, первичное ЧКВ чрезвычайно полезно для восстановления перфузии миокарда или нормального кровотока к инфарктным миокардиальным клеткам. Именно этот исход с высокой степенью предсказуемости позволяет уменьшить размер инфаркта, отсутствие кардиогенного шока или сердечной недостаточности и снизить смертность. Напротив, только 25% пациентов, получавших фибринолиз, достигают успешной реперфузии на уровне миокарда. Индекс спасения (функция восстановления миокарда как доля миокарда, подверженного риску в начале ИМпST), связанный с фибринолизом, составляет лишь приблизительно 0.25, а с первичным PCI — от 0,50 до 0,60. Мы можем оценить этот успех реперфузии путем качественной и количественной оценки степени покраснения миокарда (MBG), разрешения подъема сегмента ST и восстановления функции движения регионарной стенки.
Противопоказания
Особенности
В то время как первичное ЧКВ чрезвычайно важно для большинства пациентов с ИМпST, могут существовать некоторые особые сценарии, которые диктуют альтернативную стратегию.
Некоторые пациенты вообще не подходят для реперфузионной терапии.Старые, ослабленные пациенты с запущенной деменцией, незначительными симптомами и гемодинамически незначимым инфарктом миокарда (ИМ) лучше всего лечить с помощью соответствующей медикаментозной терапии. Точно так же те, у кого инфаркт миокарда произошел более чем за 24–36 часов до прибытия, и которые находятся в критическом состоянии с гемодинамической точки зрения, могут оказаться безнадежными, особенно если они очень старые и ослабленные. Вмешательство в этих случаях может только ускорить неизбежное.
Пациенты с очевидной остановкой сердца и реанимационными мероприятиями в полевых условиях должны быть немедленно доставлены для первичного ЧКВ при наличии ИМпST, независимо от неврологического статуса.Тем не менее, следует рассмотреть возможность использования протоколов охлаждения, чтобы улучшить шансы на неврологическое восстановление.
Иногда оперативная бригада не может быть собрана своевременно из-за продолжающихся случаев высокого риска или неподконтрольных обстоятельств (экстремальные погодные условия, движение транспорта и т. Д.). Затем пациентов следует быстро обследовать на предмет фибринолиза и лечить им, если подходят кандидаты. . Окончательная механическая терапия может быть назначена позже, без ущерба для потенциальной пользы своевременной реперфузии.
Подробная информация о том, как выполняется процедура
Выполнение первичного ЧКВ требует от интервенционного кардиолога дополнительных навыков помимо тех, которые необходимы во время планового ЧКВ. Поскольку время до реперфузии имеет решающее значение для обеспечения ее эффективности, а показатели эффективности и клинические руководства рекомендуют своевременное и быстрое вмешательство, больницы, выполняющие первичное ЧКВ, должны соответствовать требованиям специального персонала и оборудования.
Должна существовать возможность круглосуточно, 7 дней в неделю высококвалифицированных интервенционных кардиологов, медсестер и техников, которые могут выполнить первичное ЧКВ (первое устройство, развернутое в артерии, связанной с инфарктом [IRA]) в течение 90 минут после первого медицинский контакт в соответствии с последними рекомендациями по ИМпST и ЧКВ.Независимо от того, прибывает ли пациент на машине скорой помощи (предпочтительно) или самостоятельно, немедленную сортировку и сканирование электрокардиографии (ЭКГ) необходимо выполнить в течение 10 минут. Ожидается, что врач отделения неотложной помощи правильно определит ИМпST и предупредит команду ИМпST без необходимости консультации кардиолога. Этот шаг имеет решающее значение для обеспечения своевременного вмешательства, особенно в нерабочее время. Получены быстрые кардиологические ферменты и базовые лабораторные тесты (предпочтение отдается тестированию в месте оказания медицинской помощи), а краткий анамнез и обследование гарантируют отсутствие значительных противопоказаний к первичному ЧКВ.
Ожидается, что после того, как бригада лаборатории катетеризации (CL) будет оповещена, пациент прибудет в CL в течение максимум 45 минут после прибытия в больницу. Команда CL должна работать как команда с четко определенными задачами, возложенными на каждого члена, такими как гемодинамический мониторинг, подготовка зоны доступа и стерильного покрытия, а также открытие и подготовка процедурного набора. После выбора пути сосудистого доступа важны квалифицированные и быстрые пункции и введение интродьюсера, чтобы минимизировать риск кровотечения.У большинства пациентов должна быть проведена подготовка к использованию вспомогательных устройств для левого желудочка, например, очистка двух участков доступа, адекватные возможности мониторинга и т. Д.
В последнее время радиальный доступ приобрел популярность при ИМпST из-за снижения риска кровотечения из основных участков доступа и возможности, таким образом, снизить смертность. Подсчитано, что до 25% случаев первичного ЧКВ с подъемом сегмента ST выполняется этим путем, особенно в Европе. Рандомизированные клинические испытания подтвердили более низкую частоту кровотечений, но не обнаружили устойчивой разницы в смертности.
Некоторые интервенционные кардиологи начинают процедуру с ангиограммы левого желудочка, чтобы обнаружить неожиданные механические осложнения, требующие немедленной операции на открытом сердце и гемодинамической поддержки, а также для оценки степени повреждения миокарда. Это особенно важно для пациентов с неустойчивым гемодинамическим статусом и для тех, у кого клинический статус тяжелее, чем ожидалось, исходя из предполагаемого размера ИМ.
Если гемодинамика нарушена или присутствует явный кардиогенный шок, следует начать с введения вспомогательного устройства левого желудочка и даже рассмотреть возможность эндотрахеальной интубации.Процедура продолжается с визуализации не-IRA, чтобы установить общую тяжесть ИБС, выявить коллатерали, которые обеспечивают перфузию в инфарктную область, и оценить гемодинамический риск невозможности реканализации IRA. Если ЭКГ предполагает передний ИМ, для этой цели должен быть подходящим диагностический катетер Judkins Right 4.0 (JR4), чтобы канюлировать плотную коронарную артерию (ПКА).
Если подозревается нижний инфаркт миокарда, оператору необходимо оценить сканирование ЭКГ на предмет вероятности того, что IRA представляет собой ПКА (большее повышение ST в отведениях II или aVF, чем депрессия ST в V2 – V3) или левой огибающей коронарной артерии, чтобы выбрать подходящий стартовый катетер.Помните, что у подавляющего большинства пациентов ПКА является доминирующей и снабжает нижнюю стенку. После того, как оператор удовлетворится визуализацией без ИРА, следует выбрать направляющий катетер, чтобы задействовать ИРА. Я предпочитаю катетер 6F XB 3.5 для левой коронарной артерии и катетер JR4 для ПКА. Изменения вносятся, если размер аорты кажется необычно маленьким или большим при введении первого диагностического катетера.
Я выбираю эти катетеры, потому что они позволяют быстро задействовать IRA.IRA берут столько изображений, сколько достаточно для планирования PCI. Дальнейшее подробное изображение поражений, не связанных с IRA, может быть выполнено после реперфузии. Чаще всего (70–80% случаев) ИРА полностью окклюзирована и имеется поток TIMI 0 или 1.
Во время определения анатомии коронарных артерий оператору необходимо убедиться, что проводится адекватная антикоагулянтная и антитромбоцитарная терапия. Поскольку примерно 90% пациентов с ИМпST проходят ЧКВ, я предпочитаю, чтобы пациенты с подозрением на ИМпST получали двойную антитромбоцитарную терапию (ДАТ) и болюсное введение гепарина (нефракционированный гепарин [НФГ] или эноксапарин) в отделении неотложной помощи в соответствии с заранее написанными протоколами.В настоящее время наша схема включает аспирин (четыре жевательные таблетки по 81 мг), ударную дозу тикагрелора 180 мг и 60 Ед / кг НФГ — максимум 4000 единиц. После того, как принято решение о проведении ЧКВ (имеется подозрение на поражение и нет неотложных показаний к операции), можно инициировать дополнительное ингибирование гликопротеина IIb / IIIa с помощью абциксимаба, эптифибатида или высоких доз тирофибана или переключить режим антитромбина на бивалирудин. Быстрая оценка риска кровотечения (возраст, пол, исходный уровень гемоглобина и функция почек) может помочь в этом решении.Абциксимаб, введенный в очаг поражения через специальные «мокрые» баллончики, может уменьшить размер инфаркта.
PCI IRA начинается с быстрого электромонтажа судна с использованием одного из любимых проводов рабочей лошади. Если после нескольких попыток прогресс не заметен, быстро замените его на другой провод! Важно попытаться пересечь поражение один раз, чтобы избежать создания или увеличения существующих плоскостей рассечения вокруг разрыва бляшки.
Иногда большое количество тромбов препятствует прохождению проволоки.Этот процесс редко занимает более 3-5 минут. Проводка часто приводит к восстановлению некоторого потока в IRA. Это позволяет оператору оценить размер сосуда и длину поражения. Если используется аспирационный катетер, такой как EXPORT ™ (Medtronic) или аналогичный, его готовят, сначала промывая порт аспирации физиологическим раствором и применяя к нему вакуум перед введением.
Аспирация должна начаться до того, как будет достигнуто поражение, чтобы создать «фору». Это первое введение устройства — аспирационного катетера, баллона или стента — которое определяет время от двери до баллона, которое следует более правильно называть временем от двери до устройства.Я обычно процеживаю аспират в прилагаемом фильтре, чтобы увидеть тромб.
Более чем в 50% случаев аспирация приводит к восстановлению потока TIMI 3 в IRA, и у пациента обычно наблюдается разрешение или заметное уменьшение боли в груди и подъема сегмента ST. Если позволяет гемодинамика, интракоронарный нитроглицерин и аденозин могут дополнительно улучшить кровоток и позволить точно оценить длину поражения и диаметр сосуда для установки стента. Первоначальные данные исследования TAPAS показали снижение смертности при ручной аспирации тромба по сравнению с традиционным ЧКВ.Два более крупных исследования — TASTE и TOTAL — проведенные с участием почти 20 000 пациентов, опровергли этот вывод и даже предположили, что может быть более высокая частота раннего инсульта у пациентов, получавших аспирацию. Из-за этих последних данных энтузиазм по поводу рутинной аспирации тромба снизился.
Выбор типа стента — с лекарственным покрытием или без покрытия — основан на нашей оценке способности и готовности пациента принимать ДАТТ в течение как минимум года, планах проведения некардиальных операций в ближайшем будущем, соблюдении медикаментозной терапии в целом, и сопутствующие заболевания, такие как сахарный диабет, хроническое заболевание почек или потребность в хронических антикоагулянтах.Недавние данные свидетельствуют о преимуществах некоторых стентов с лекарственным покрытием второго поколения по сравнению с металлическими стентами при первичном ЧКВ. Имплантация стента почти всегда дает отличный ангиографический результат. В областях поражения можно увидеть остаточный тромб, но до тех пор, пока поток быстрый и стент установлен хорошо, дальнейшая терапия не требуется.
Интерпретация результатов
В конце IRA PCI оператор должен формально оценить, помимо статуса симптомов (полный, неполный или отсутствие изменений боли), эпикардиальный кровоток IRA (степень TIMI), а также покраснение миокарда и разрешение элевации ST как маркеры реперфузия миокарда.Если результаты ангиографии и ЭКГ неудовлетворительны, можно рассмотреть возможность дополнительной вазоактивной терапии.
Результаты (относится только к терапевтическим процедурам)
Первичное ЧКВ успешно более чем у 90% пациентов. Как показано на Рисунке 1, Рисунке 2 и Рисунке 3, преимущество первичного ЧКВ превосходит другие стратегии реперфузии, особенно когда пациенты обращаются за помощью в течение 2 часов с момента появления симптомов.
Рисунок 1.

Рисунок 2.

Рисунок 3.

Осложнения и их лечение
Следует уделять особое внимание дистальному отделу IRA и его ветвям, чтобы определить возможную дистальную эмболизацию, которая могла возникнуть после аспирационной тромбэктомии или развертывания стента. Если такое осложнение обнаружено, проводка сосуда (если ветвь IRA) может сместить небольшой тромб и восстановить кровоток. Дополнительные полезные маневры включают прохождение баллона без надувания или повторную аспирационную тромбэктомию, если размер сосуда позволяет это.Если этих механических вмешательств и агрессивной фармакологии недостаточно, может потребоваться ЧКВ области со стентированием или без него, особенно если покрываемая область достаточно велика.
Помимо дистальной эмболизации, необходимо оценить другие важные внутрипроцедурные осложнения. Медленный кровоток в IRA не редкость, особенно в IRA с большой тромбовидной нагрузкой. Могут потребоваться повторные проходы с аспирационным катетером и даже механическая тромбэктомия в случае большой ПКА.
Может потребоваться агрессивное фармакологическое вмешательство с использованием интракоронарных вазоактивных веществ, таких как нитроглицерин, аденозин, верапамил или нитропруссид. Никардипин широко используется в Японии для этой цели, и в некоторых сообщениях указывается, что адреналин, как это ни парадоксально, помогает, стимулируя бета-2-адренорецепторы. Не забудьте ввести эти вещества в дистальный сосуд, вставив аспирационный катетер или проводной баллон, и ввести через них. Проксимальное введение в сосуд без быстрого кровотока не решит проблему и приведет только к проксимальному распространению вводимого вещества и нарушению гемодинамики.
В последнее время обращают внимание на «новое» осложнение — внутрипроцедурный тромбоз стента (IPST). Это появление нового или более тяжелого тромба после его первоначального разрешения или улучшения. IPST не входит в классические определения тромбоза стента, которые оценивают осложнения только после завершения процедуры. Тем не менее, IPST ассоциируется с заметным увеличением последующей смерти и тромбоза стента, даже когда поток TIMI 3 достигается в конце процедуры. Наиболее важным выводом из этих наблюдений является то, что этим пациентам может потребоваться более продолжительная или интенсивная антитромботическая терапия.Быстрый внутривенный ингибитор рецептора P2Y12 — кангрелор — недавно был одобрен FDA и EMA для специфического снижения IPST и предотвращения перипроцедурного инфаркта миокарда у пациентов, ранее не получавших пероральный ингибитор P2Y12, как это часто бывает у пациентов с ИМпST.
Какие доказательства?
Bhatt, DL, Stone, GW, Mahaffey, KW. «Влияние ингибирования тромбоцитов кангрелором во время ЧКВ на ишемические события». N Engl J Med. об. 368. 2013.С. 1303-13. (CHAMPION PHOENIX оценил кангрелор во время ЧКВ, включая пациентов с ИМпST.)
Brener, SJ, Barr, LA, Burchenal, JE. ”Рандомизированное плацебо-контролируемое исследование блокады тромбоцитов гликопротеина IIb / IIIa с первичной ангиопластикой по поводу острого инфаркта миокарда. ReoPro и исследователи организации и рандомизированного исследования (RAPPORT) первичной PTCA ». Тираж. об. 98. 1998. pp. 734-41. (Первое рандомизированное испытание абциксимаба в качестве дополнения к первичному ЧКВ.)
Де Лука, G, Сурьяпраната, H, Стоун, GW.«Абциксимаб в качестве дополнительной терапии реперфузии при остром инфаркте миокарда с подъемом сегмента ST: метаанализ рандомизированных исследований». JAMA. об. 293. 2005. С. 1759–65. (Вклад дополнительного абциксимаба в улучшение результатов у пациентов, получающих первичное ЧКВ или фибринолиз.)
Jolly, SS, Cairns, JA, Yusuf, S. «Рандомизированное исследование первичного ЧКВ с рутинной ручной тромбэктомией или без нее». N Engl J Med. об. 372. 2015. С. 1389–98. (ВСЕГО оценивали рутинную мануальную аспирационную тромбэктомию при ИМпST.)
Кили, EC, Бура, JA, Гринс, CL. «Первичная ангиопластика по сравнению с внутривенной тромболитической терапией при остром инфаркте миокарда: количественный обзор 23 рандомизированных исследований». Ланцет. об. 361. 2003. С. 13-20. (Метаанализ исследований, сравнивающих первичное ЧКВ с фибринолизом.)
Кумбхани, ди-джей, Баври, AA, Десаи, MY. «Аспирационная тромбэктомия у пациентов, перенесших первичную ангиопластику: совокупность данных до 2013 г.». Катетер Cardiovasc Interv. об.84. 2014. С. 973-7. (Метаанализ исследований, сравнивающих мануальную аспирационную тромбэктомию с обычным лечением при ИМпST.)
Lagerqvist, B, Frobert, O, Olivecrona, GK. «Результаты через 1 год после аспирации тромба при инфаркте миокарда». N Engl J Med. об. 371. 2014. С. 1111-20. (TASTE оценил рутинную мануальную аспирационную тромбэктомию при ИМпST.)
Левин, GN, Бейтс, ER, Бланкеншип, JC. «Руководство ACCF / AHA / SCAI по чрескожному коронарному вмешательству 2011 г .: отчет Фонда Американского колледжа кардиологов / Целевой группы Американской кардиологической ассоциации о практических рекомендациях и Общества сердечно-сосудистой ангиографии и вмешательств». Тираж. об. 124. 2011. С. e574-651. (Обновленные инструкции по ЧКВ, в том числе при ИМпST.)
О’Гара, П.Т., Кушнер, Ф.Г., Ашейм, ДД. «Руководство ACCF / AHA 2013 г. по ведению инфаркта миокарда с подъемом сегмента ST: краткое изложение: отчет Фонда Американского колледжа кардиологов / Целевой группы Американской кардиологической ассоциации по практическим рекомендациям». J Am Coll Cardiol. об. 61. 2013. С. 485-510. (Обновленные рекомендации по ведению ИМпST.)
Schömig, A, Kastrati, A, Dirschinger, J. «Коронарное стентирование плюс блокада тромбоцитарного гликопротеина IIb / IIIa в сравнении с тканевым активатором плазминогена при остром инфаркте миокарда. Стент против тромболизиса окклюзированных коронарных артерий у пациентов с острым инфарктом миокарда. Исследователи ». N Engl J Med. об. 343. 2000. С. 385–91. (В исследовании «Стент против тромболизиса для окклюзированных коронарных артерий у пациентов с острым инфарктом миокарда» сравнивали спасение миокарда у пациентов, получавших первичное ЧКВ или фибринолиз.)
Schömig, A, Ndrepepa, G, Mehilli, J. «Зависимое от терапии влияние интервала времени до лечения на спасение миокарда у пациентов с острым инфарктом миокарда, получавших стентирование коронарной артерии или тромболизис». Тираж. об. 108. 2003. pp. 1084-8. (Влияние времени от двери до баллона и от двери до иглы на результат — сравнение первичного ЧКВ с фибринолизом.)
Stone, GW, Witzenbichler, B, Godlewski, J. «Внутриочаговая аспирация абциксимаба и тромба у пациентов с большим передним инфарктом миокарда: результаты исследования INFUSE-AMI за один год». Circ Cardiovasc Interv. об. 6. 2013. С. 527-34. (INFUSE AMI оценил роль абциксимаба в очаге поражения в уменьшении размера инфаркта при большом переднем ИМпST.)
Stone, GW, Witzenbichler, B, Guagliumi, G. «Бивалирудин во время первичного ЧКВ при остром инфаркте миокарда». N Engl J Med. об. 358. 2008. С. 2218-30. (Бивалирудин в сравнении с гепарином и GPI при ИМпST.)
Валлентин, Л., Беккер, Р. К., Будай, А. «Тикагрелор по сравнению с клопидогрелем у пациентов с острыми коронарными синдромами». N Engl J Med. об. 361. 2009. С. 1045-57. (Новая антиагрегантная терапия тикагрелором при ИМпST.)
Wiviott, SD, Braunwald, E, McCabe, CH. «Прасугрел в сравнении с клопидогрелом у пациентов с острыми коронарными синдромами». N Engl J Med. об. 357. 2007. С. 2001-15. (Новая антиагрегантная терапия прасугрелом при ИМпST.)
Copyright © 2017, 2013 ООО «Поддержка принятия решений в медицине». Все права защищены.
Ни один спонсор или рекламодатель не участвовал, не одобрял и не платил за контент, предоставляемый Decision Support in Medicine LLC.Лицензионный контент является собственностью DSM и защищен авторским правом.
.
Выбор ЧКВ, АКШ или медикаментозного лечения: Текущие рекомендации
Общее описание процедуры, оборудования, техники
1.) Оптимальная медикаментозная терапия (ОМТ)
OMT включает в себя спектр лекарств (и упражнений), снижающих заболеваемость и смертность от процесса ишемической болезни сердца (ИБС). По сравнению с реваскуляризацией основное внимание часто уделяется лекарствам, назначаемым для уменьшения бремени стенокардии, в первую очередь за счет расширения сосудов и уменьшения нагрузки на сердце (произведение давления на скорость).
Традиционные методы лечения, которые достигают этой цели, включают нитраты, блокаторы кальциевых каналов и бета-блокаторы. Появился ряд новых агентов, которые можно использовать даже в сочетании с традиционными методами лечения. Однако единственным нетрадиционным лекарством, одобренным FDA в США для лечения стенокардии, является ранолазин, который действует через ингибирование позднего внутреннего натриевого канала, тем самым снижая внутриклеточную концентрацию кальция. Никорандил одобрен для лечения стенокардии в Европе и Азии и опосредует открытие калиевых каналов и эффекты нитратов.Ивабрадин является специфическим ингибитором электрокардиостимулятора синусового узла и оказывает антиангинальное действие за счет снижения частоты сердечных сокращений.
Другие подходы частично совпадают с оптимальным лечением профиля сердечно-сосудистых факторов риска и улучшают здоровье сердечно-сосудистой системы, особенно здоровье эндотелия. Эти другие подходы включают терапию высокими дозами статинов, ингибирование рецептора типа I блокатора рецепторов ангиотензина (АПФ) или блокатора рецепторов ангиотензина (БРА) и даже аллопуринола. Антиагрегантная терапия аспирином или клопидогрелом также является стандартной практикой.
2.) Реваскуляризация
2a.) Чрескожное коронарное вмешательство (ЧКВ)
PCI влечет за собой устранение ограничивающего кровоток аспекта стеноза коронарной артерии посредством катетерного сжатия и стабилизации бляшек с помощью металлических каркасов. Стандартные устройства включают баллоны разного размера и податливости, а также стенты без или с определенным полимерным покрытием и способностью выделять лекарство (так называемые стенты из чистого металла и стенты с лекарственным покрытием). К другим устройствам, которые используются реже, относятся режущие баллоны и ротабляторы.Выбор устройства зависит от анатомических особенностей поражения.
2b.) Аортокоронарное шунтирование (АКШ)
АКШ выполняет «обход» стеноза коронарной артерии с помощью кондуитного сосуда от аорты или ее дополнительных сосудов, то есть внутренней артерии молочной железы. Эта процедура выполняется либо как операция на открытом сердце со стернотомией, либо как минимально инвазивная операция прямого коронарного шунтирования (MIDCAB) с ограниченной передней торакотомией и использованием эндоскопических или роботизированных методов.Оба эти типа операций могут выполняться с использованием искусственного кровообращения или без него.
«Гибридные процедуры» предполагают комбинацию операции MIDCAB и ЧКВ, особенно MIDCAP левой внутренней молочной артерии (LIMA) с трансплантацией левой передней нисходящей (LAD) коронарной артерии в сочетании с ЧКВ левой огибающей артерии (LCX) и / или правой коронарной артерии (ПКА) поражения.
Показания и выбор пациентов
1.) ОМТ
Все пациенты с ИБС должны получать ОМТ, как описано выше.Это служит двум целям: 1) уменьшение прогрессирования процесса атеросклеротического заболевания и «стабилизация» бляшек коронарных артерий и сердечной функции, тем самым снижая частоту серьезных побочных эффектов, и 2) улучшение симптомов и качества жизни. Очевидно, что это единственная терапия для пациентов, которые явно выражают желание не проводить инвазивные методы лечения.
2.) Реваскуляризация
Стратегии реваскуляризации должны выполняться, если две указанные выше цели не могут быть достигнуты только с помощью медикаментозной терапии, т.е.е., по прогностическим или симптоматическим показаниям, при отсутствии противопоказаний. При остром коронарном синдроме обычно выполняются оба показания, и чаще всего предпочтительной стратегией является ЧКВ.
Ни при каких других обстоятельствах показания к реваскуляризации не являются более сильными, чем при острой сердечной недостаточности, осложняющей острый инфаркт миокарда, особенно при кардиогенном шоке, и в этом случае реваскуляризация должна быть максимально полной.
Другие четкие показания для реваскуляризации с прогностическими последствиями включают стеноз левой основной артерии> 50%, любой проксимальный стеноз ПМЖВ> 50%, заболевание 2 или 3 сосудов с нарушением функции ЛЖ или единственный оставшийся проходимый сосуд со стенозом> 50% ПЛЮС задокументированный фракционный резерв расхода (FFR) <0.80 или задокументированная ишемия.
В частности, если неинвазивное тестирование демонстрирует большое бремя ишемии (формально> 10% ЛЖ или неофициально более 3 сегментов при эхо-тестировании или ядерном стресс-тесте), рассматривается возможность реваскуляризации.
Для контроля симптомов реваскуляризация показана при любом стенозе> 50% с ограничением стенокардии или эквивалентом стенокардии, не отвечающим на ОМТ.
Выбор наилучшей стратегии реваскуляризации зависит от ряда факторов. Одним из лучших инструментов для принятия обоснованного решения в настоящее время является оценка SYNTAX.Особенно у пациентов со сложной ишемической болезнью сердца (ИБС) решение должно приниматься с использованием подхода кардиологической бригады, который включает ценное мнение интервенционного кардиолога и сердечно-сосудистого хирурга. Команда кардиологов может определить предпочтительную стратегию реваскуляризации для любого конкретного пациента. Однако часто могут быть выполнены обе процедуры, и решение будет за пациентом и его / ее лечащим врачом в контексте общей клинической картины.
2а.) PCI
ЧКВ
обычно является предпочтительным вариантом при поражении одного или двух сосудов, не затрагивающего проксимальную ПМЖВ.
ЧКВ почти эквивалентно АКШ при поражении 1 или 2 сосудов, включающем проксимальную ПМЖВ, изолированном поражении устья или ствола левой основной артерии, и поражении 3 сосудов с простыми поражениями и технической осуществимостью полной реваскуляризации. Все эти обстоятельства можно обобщить по шкале SYNTAX <23.
ЧКВ может быть выполнено, но, как правило, уступает АКШ при дистальном левом главном (бифуркационном) поражении, особенно в сочетании с поражением 2 или 3 сосудов и оценкой SYNTAX <32.
2b.) АКШ
АКШ является предпочтительным вариантом при поражении основного левого ствола с поражением 2 и 3 сосудов и показателем SYNTAX> 32.
АКШ также является предпочтительным вариантом даже при наличии более низкого балла по шкале SYNTAX, когда присутствуют множественные сложные поражения, а ЧКВ остается технически ограниченным для достижения полной реваскуляризации. АКШ также предпочтительнее у больных сахарным диабетом с многососудистым поражением.
Противопоказания
1.) ОМТ
Нет никаких противопоказаний для продолжения какого-либо из перечисленных медицинских методов лечения, за исключением случаев, когда пациенту было предложено комфортное лечение.
2.) Реваскуляризация
Ни PCI, ни CABG не подлежат преследованию, если компетентный пациент или доверенность отказывается от информированного согласия или выражает безотзывные приказы DNR / DNI.
В противном случае инвазивная стратегия не рекомендуется при неблагоприятном соотношении пользы и риска. Это влечет за собой клинические проявления с очень низким риском и тяжелые сопутствующие заболевания, ограничивающие ожидаемую продолжительность жизни независимо от кардиологического вмешательства, при этом риск процедуры выше, чем любая значимая клиническая польза.В частности, реваскуляризация не рекомендуется при отсутствии (ограничивающих) симптомов при ОМТ или поражении одного сосуда без поражения проксимального отдела ПМЖВ и ишемической нагрузки <10%. Точно так же инвазивная стратегия может иметь чрезвычайно высокий риск, несмотря на предполагаемую пользу, например, ЧКВ при чрезвычайно сложной ИБС без хирургического вмешательства.
Даже первичное ЧКВ не должно выполняться в больницах без возможности кардиохирургии на месте и проверенного плана быстрого переноса для неотложной АКШ в ближайшем учреждении, включая применение соответствующих режимов гемодинамической поддержки.
Подробная информация о том, как проводится процедура
1.) PCI
Эта процедура выполняется интервенционными кардиологами совместно с группой обученных медсестер и техников в лаборатории катетеризации.
После соответствующего отбора и анализа показаний и противопоказаний получено информированное согласие (письменное, если у пациента нет инфаркта миокарда с подъемом сегмента ST (ИМпST) или кардиогенный шок, и в этом случае достаточно устного согласия или согласия семьи, чтобы избежать задержек ).
Большинство лекарств продолжаются для процедуры с некоторыми важными характеристиками. Прием метформина следует прекратить как можно раньше перед процедурой, особенно при почечной дисфункции (которая может потребовать дополнительной гидратации). С другой стороны, антитромбоцитарная терапия является обязательной, и ее нельзя прекращать. Фактически, двойная антитромбоцитарная терапия должна применяться при ЧКВ в случае острого коронарного синдрома. Чаще всего назначают аспирин (325 мг) и, в зависимости от клинической ситуации, либо клопидогрел (300 мг, по крайней мере, за 6 часов или 600 мг, как минимум за 2-3 часа), либо другой тиенопиридин, такой как прасугрел или тикагрелор или гликопротеин IIb. / Ингибиторы IIIa.
Инфузия гепарина прекращается до начала процедуры, и, как правило, все же используется нефракционированный гепарин для достижения времени активированного свертывания крови 250–300 секунд. Этот режим антикоагуляции начинается после получения доступа к сосуду (лучевая или бедренная артерия, реже плечевая артерия) и должен применяться до входа устройства в коронарную артерию. В качестве альтернативы можно использовать бивалирудин.
Серия ангиографических изображений определяет серьезность поражения и анатомию, которые определяют интервенционный подход.Иногда для помощи в планировании процедуры используются дополнительные методы, такие как межсосудистое ультразвуковое исследование. В зависимости от этих оценок проводится либо прямая имплантация стента в очаг поражения, либо баллонная ангиопластика, либо ротационная атерэктомия с последующей имплантацией стента. Все эти устройства продвигаются через направляющий катетер, помещенный в начале коронарной артерии, и проводник, который проходит от внешней стороны направляющего катетера к коронарной сосудистой сети за пределы участка поражения.
После процедуры используются методы визуализации для подтверждения результата, и все оборудование удаляется, за исключением оболочки сосудистого доступа, которая будет удалена после того, как состояние антикоагуляции будет признано безопасным. Все пациенты находятся под наблюдением в течение нескольких часов после процедуры.
Пациенты с низким риском осложнений и в непосредственной близости от медицинских учреждений могут быть выписаны при тщательном наблюдении, включая визит на следующий день. В противном случае пациенты находятся под наблюдением в специализированном отделении с выпиской на следующий день при отсутствии осложнений.
2.) АКШ
Эта процедура выполняется специализированной бригадой сердечно-сосудистых хирургов, в которую входят не только хирургический персонал, но также анестезиологи, медсестры, техники и перфузиологи. АКШ выполняется в операционной, встроенной в структуру больницы.
После изучения показаний, противопоказаний, рисков, преимуществ и альтернатив команда получает информированное согласие. Часто пациент также посещает анестезиолога при подготовке к операции.Обычно приемлем аспирин; однако для большинства хирургов клопидогрель и, безусловно, ингибиторы GPIIb / IIIa неприемлемы, поскольку они приводят к неприемлемо высокому риску кровотечения. По той же причине следует отменить прием гепарина перед процедурой.
Часто продолжают принимать другие лекарства. В частности, следует продолжить терапию бета-блокаторами, чтобы снизить частоту периоперационной фибрилляции предсердий. Пациентам с противопоказаниями к терапии бета-адреноблокаторами и из группы высокого риска (предшествующая фибрилляция предсердий и операция на митральном клапане) рекомендуется амиодарон (600 мг перорально в течение одной недели до операции и 200 мг в день до выписки после нее; в противном случае — 400 мг. мг внутрь 2 раза в день x 7 дней или 1 г внутривенно в день x 2 дня после операции).
Процедура начинается с интубации и индукции общей анестезии, после чего следует срединная стернотомия. Затем мобилизуют внутреннюю артерию (и) молочной железы или забирают лучевую артерию или шунтирующие трансплантаты подкожной вены. Затем вскрывают перикардиальный мешок и обнажают сердце. Чтобы сделать возможным безопасное наложение обходных путей на артериях с минимальным диаметром просвета в диапазоне миллиметров, необходимо вызвать «неподвижное состояние» путем погружения сердца в кардиоплегический раствор после подключения пациента к экстракорпоральному кровообращению через сердечно-легочный обход. насосом или фиксацией устройства «без насоса».Пережатие аорты позволяет построить проксимальные анастомозы.
После того, как эти подготовительные меры выполнены, мобилизованный конец внутренней молочной артерии или один конец канала трансплантата пришивают к коронарным артериям дистальнее стенозов. В случае трансплантатов лучевой артерии или подкожной вены другой конец пришивают к устью, образующейся в восходящей аорте. Последнее можно проводить даже при частично закупоренной аорте и бьющемся сердце. Постепенно разрешают кровоток, чтобы отслеживать возможные утечки.Состояние функционального обходного трансплантата затем проверяется с помощью допплеровского зонда после введения вазодилататора (папаверина). Когда все удовлетворительно, все устройства удаляются и проводится закрытие, включая грудную проводку.
После этого пациент переводится в отделение интенсивной терапии для послеоперационного ухода, включая экстубацию и мониторинг стабилизации гемодинамики. Часто даже на следующий день пациента переводят в приемное отделение и отпускают домой через четыре дня с проведением кардиологической реабилитации.
Интерпретация результатов
1.) ОМТ
Пациенты, получающие ОМТ, нуждаются в регулярном наблюдении и должны быть проинструктированы обращаться за медицинской помощью при любом изменении симптомов. Регулярное стресс-тестирование таких пациентов не рекомендуется. Следовательно, клиническая картина — это интерпретация успеха ОМТ.
2.) Реваскуляризация
Как и в случае с ОМТ, клиническое течение определяет результат процедуры реваскуляризации. Очевидно, что заранее хотелось бы установить цели и преимущества процедуры; результаты процедуры должны соответствовать этим целям.
Исходы (относится только к терапевтическим процедурам)
1.) ОМТ
Как указано выше, все пациенты должны получать ОМТ. При отсутствии веских показаний реваскуляризация не меняет прогностический и / или симптоматический исход.
Пригодность подхода первичной ОМТ была подчеркнута в исследовании COURAGE, которое, однако, потребовало коронарной ангиографии для определения определенной подгруппы пациентов, которым реваскуляризация не подойдет лучше.За период наблюдения в 5 лет пациенты без нестабильной стенокардии, значительного основного заболевания левого отдела, явно ненормального стресс-теста, фракции выброса (ФВ) <30% и поражений, не подходящих для ЧКВ, устойчивой смерти или нефатального ИМ, как это часто бывает при ОМТ отдельно, как и при предварительном ОМТ + ЧКВ (почти 20% пациентов), и так же часто госпитализировались по поводу острого коронарного синдрома (примерно 12%). Однако, если не совмещать с ЧКВ во время ангиографии, пациенты, которым лечили только ОМТ, сталкивались с абсолютным на 10% более высоким риском прохождения будущих процедур реваскуляризации и развития стенокардии в течение первого года.
Эти данные полностью согласуются с самим процессом атеросклеротического заболевания, поскольку поражения, вызывающие фатальный и нефатальный инфаркт миокарда, часто демонстрируют внешнее ремоделирование и, следовательно, остаются вне поля зрения симптомов и традиционных методов оценки. Именно по этой причине ОМТ остается ключевым фактором, влияющим на общий исход пациентов с ИБС, независимо от их представления и оценки.
2.) Реваскуляризация
Важным элементом интерпретации имеющихся данных является функциональная значимость стенозов коронарных артерий.Это часто не учитывается при расчете преимуществ реваскуляризации.
Симптоматическая или нет, но большое бремя ишемии предвещает плохой прогноз, особенно внезапную сердечную смерть, которую можно предотвратить с помощью реваскуляризации. Пороговое значение ишемического бремени, при котором появляется преимущество в отношении смертности при реваскуляризации, составляет примерно 10%, и наиболее определенно оно заметно на уровне 20%. Сердце с пониженным уровнем функционирования может быть даже более восприимчивым к негативным последствиям повторяющихся эпизодов ишемии, особенно обширной ишемии.
Поскольку обычно в основе этих представлений лежит сложная ИБС, большинству этих пациентов будет выполнена АКШ, хотя некоторым можно управлять с помощью ЧКВ, как описано выше. По этой причине данные стабильного CAD в целом не так убедительны для ЧКВ, как для АКШ. Это отличается от пациентов с острым коронарным синдромом, которым в основном проводят ЧКВ. Однако применяются те же принципы стратификации риска и пользы.
Хотя данные различных исследований не согласуются друг с другом, общее мнение состоит в том, что пациенты с ИМ без сегмента ST или нестабильной стенокардией и показателем риска тромболизиса при инфаркте миокарда (TIMI)> 2 получают пользу от инвазивного подхода и реваскуляризации.В этих условиях реваскуляризация приводит к относительному снижению смертности, ИМ и повторных госпитализаций на 20% по сравнению с ОМТ. Это преимущество может проявиться только после выписки. Выгода как минимум вдвое больше и более очевидна при инфаркте миокарда сегмента ST. Наконец, преимущества еще более значительны при кардиогенном шоке, при котором реваскуляризация приводит к снижению абсолютной смертности на 20%.
Альтернативные и / или дополнительные процедуры для рассмотрения
Усиленная внешняя контрпульсация (УНКП)
В этом методе используются три пары манжет вокруг нижних конечностей, которые накачиваются до высокого давления (300 мм рт. Ст.) Последовательно от дистального к проксимальному отделу во время диастолы, что обеспечивает ретроградный кровоток в аорте и увеличение диастолической коронарной перфузии.Обсуждается также ряд других механизмов, которые могут способствовать наблюдаемому клиническому эффекту, который включает снижение бремени стенокардии у 70% пациентов с прекращением использования нитроглицерина у 50% пациентов. Эта процедура не имеет нежелательных последствий и покрывается программой Medicare / Medicaid для пациентов со стенокардией III / IV уровня Канадского сердечно-сосудистого общества (CCS), проходящих лечение, которые не являются кандидатами на реваскуляризационную терапию.
Стимуляция спинного мозга на уровне Th2 / Th3
Этот метод подавляет активность внутренних нейронов сердца во время ишемии миокарда и, следовательно, оказывает в первую очередь обезболивающее действие.Это безопасно и эффективно для улучшения симптомов и качества жизни пациентов с рефрактерной стенокардией. Тем не менее, этот метод следует использовать только для избранных пациентов.
Трансмиокардиальная лазерная реваскуляризация
Этот метод использует лазер для создания трансмуральных каналов в ишемизированном миокарде. Считалось, что это обеспечит пассивную перфузию миокарда насыщенной кислородом кровью из полости левого желудочка (ЛЖ). Однако в течение одного дня практически все каналы закрываются, и не может быть дано никаких объективных доказательств исходной теории.Обсуждались и другие механизмы, такие как симпатическая денервация и индукция ангиогенеза. Клинически часто наблюдается отсрочка получения положительного результата, если таковая имеется, а уровень смертности от процедуры составляет 3–5% (по сообщениям до 12%). Следовательно, несмотря на то, что эта стратегия одобрена FDA, ее следует применять только с особой осторожностью.
Осложнения и их лечение
1.) ОМТ
Медикаментозная терапия всегда требует контроля на предмет возможных осложнений, то есть побочных эффектов. Антитромбоцитарная терапия увеличивает риск кровотечений, а терапия статинами в высоких дозах может вызвать гепатоцеллюлярное повреждение и миопатию, а также — и что наиболее опасно — рабдомиолиз.Терапия ингибиторами АПФ может привести к ангионевротическому отеку. Это примеры осложнений медикаментозной терапии. Для каждого отдельного пациента необходимо обсудить профиль, признаки и симптомы побочных эффектов, а также предупредить пациента о необходимости обращения за медицинской помощью с любыми проблемами. Последующая лабораторная оценка, такая как панель ферментов печени, должна быть рутинной при терапии статинами. Лечение любого из этих осложнений заключается в прекращении приема лекарств и обсуждении альтернативных вариантов.
2.) Реваскуляризация
2а.) PCI
Рассечение / резкое закрытие: чаще всего надувание баллона вызывает разрыв или расслоение интимы (до 50%), которое может быть незначительным с последующим безболезненным заживлением, вплоть до значительной степени, которое приводит к острому закрытию (4–9%) ) в течение нескольких минут после надувания или до нескольких часов спустя, когда действие антикоагуляции против гепарина прекратится (усугубляется тромбом и вазоспазмом). Стентирование снизило частоту этих событий; Однако для облегчения ишемии иногда требуется экстренная операция.
Внутримуральная гематома: скопление крови в медиальном пространстве, обычно дистальнее и проксимальнее места поражения, чаще встречается при баллонной ангиопластике (7%). На ангиографии это выглядит как расслоение, и лечение таково.
Перфорация: проводники могут проходить вне просвета, или устройства могут нарушать целостность стенки коронарной артерии. Перфорация может быть локализованной, незначительной с внесосудистым окрашиванием или большой (> 1 мм) с явным высыпанием (<1%).Риск снижения перфузии дистально и инфаркта миокарда, а также повышенного наполнения перикардиального пространства и тампонады возрастает с увеличением степени перфорации. Немедленное действие заключается в перекрытии притока крови и места перфорации с помощью надувания баллона низкого давления, обратной антикоагуляции и выполнения перикардиоцентеза. После этого может быть выполнено быстрое размещение покрытого стента или спиральная эмболизация дистальных перфораций проволочного направителя. Экстренное хирургическое вмешательство необходимо выполнить, если кровотечение продолжается или перикардиоцентез остается неэффективным для облегчения нарушения гемодинамики.
Нет повторного потока: Причиной отсутствия повторного потока может быть функциональная (вазоспазм) или структурная (атеросклеротический мусор или тромб) обструкция микроциркуляции, которая приводит к снижению коронарного кровотока, несмотря на широко открытый эпикардиальный сосуд (от 0,5% до 5% в зависимости от по сложности поражения / ЧКВ). Лечением выбора являются прямые вазодилататоры (аденозин, нитропруссид, верапамил) и ингибиторы гликопротеина (GP) IIb / IIIa, вводимые интракоронарно (IC), даже через инфузионный катетер.
Окклюзия боковой ветви: в основном это связано с смещением зубного налета (20%).Чаще всего стеноз уже имел место. Дальнейшее вмешательство не проводится, если только оно не вызвано симптомами ишемии, размером боковой ветви и предоставленной территорией. Большинство из них спонтанно реканализируются.
Смещение стента: это потенциально серьезное осложнение стало редким явлением (<2%), но все еще является наиболее частой причиной в настоящее время экстренной АКШ.
Перипроцедурный ИМ: в настоящее время это определяется как повышение уровня сердечного биомаркера (тропонина) после процедуры> 5-кратного верхнего предела нормы при наличии нормы и повышение> 20% при наличии аномальных исходных значений в сочетании с одним признаком или симптомом миокарда. ишемия.В основном это связано с процедурными осложнениями (с вмешательствами на сложных поражениях). Терапия поддерживающая. Повторная ангиография требуется только в том случае, если перипроцедуральный ИМ связан с болью в груди и заметными ишемическими изменениями сегмента ST.
Аритмии: желудочковые тахикардии нечасты при ЧКВ (0,8%). Чаще всего они наблюдаются после введения контрастного вещества. Немедленная дефибрилляция.
Инсульт: чаще всего является следствием разрыва атеромы по дуге аорты с прохождением направляющего катетера.Реже это происходит из-за выхода атеротромботического материала и воздуха при промывке катетера. Это редко является следствием прохождения проволоки в мозговой кровоток. Инсульт имеет равную долю поражения переднего и заднего кровообращения (по 0,2% каждый). Терапия в основном поддерживающая.
Кровотечение: наиболее опасным является забрюшинное кровотечение (<1%). Кровотечение может проявляться «необъяснимой» гипотонией, потоотделением и брадикардией. Кровотечение часто принимают за вагусную реакцию.Боль в паху, животе и спине возникает реже, но настораживает. Заметное падение гемоглобина может отсутствовать на ранней стадии; следовательно, необходим высокий уровень клинического подозрения. Требуются компьютерная томография и иногда ангиография. Лечение заключается в отмене антикоагулянтной +/- антиагрегантной терапии, внутривенного введения жидкостей, переливания крови или консультации по сосудистой хирургии по сравнению с рассмотрением возможности установки покрытого стента. Другие кровотечения из сосудистого доступа обычно вызывают меньшее беспокойство, если, например, кровотечение из несжатой лучевой артерии не приводит к синдрому предплечья, который требует неотложной хирургической помощи.Кровотечения из желудочно-кишечного тракта и мочевого пузыря требуют дальнейшего обследования специалистами консультационной службы.
Острое повреждение почек: в основном это связано с нефропатией, вызванной контрастированием (особенно если было использовано> 200 мл контрастного вещества и у пациента уже есть заболевание почек и диабет), атероэмболия (часто с другими признаками, такими как эозинофилия, синие пальцы ног или livedo reticularis, боль в животе или церебральные нарушения) или гипотензия. Лечение направлено на основную этиологию и в основном включает гидратацию.
2b.) АКШ
Периоперационный ИМ: определяется повышением сердечных биомаркеров после процедуры> 10-кратного верхнего предела нормы (ULN) или наличием новых зубцов Q (4–5%) и отражает либо повреждение миокарда во время операции, либо трансплантат. отказ в начале после этого. В то время как риск худшего исхода возникает при установленном пороге определения, влияние тем сильнее, чем больше степень повреждения миокарда, и в несколько раз выше при очень обширных ИМ (ИМ с зубцом Q или CK-MB> 10x ULN).Лечение состоит из стандартной поддерживающей терапии и направления на коронарную ангиографию с дальнейшими вмешательствами по показаниям.
Ранняя окклюзия трансплантата: Обычно это происходит из-за тромботической окклюзии, вызванной техническими трудностями с подготовкой трансплантата или анастомоза (3–6% в остром послеоперационном периоде). Во избежание ранней повторной операции обычно проводится ангиография с ЧКВ; однако, особенно при расширении баллона под высоким давлением и стентировании анастомоза вскоре после операции существует высокий риск перфорации, а при стентировании высоки кровотечения.Следовательно, когда это возможно, баллонная ангиопластика низкого давления выполняется только для восстановления кровотока +/- дистальное защитное устройство.
Низкий выходной недостаточность: это может быть связано с остановкой кардиоплегии и ишемическим повреждением, включая инфаркт миокарда, аритмии, механические осложнения (включая выпот / тампонаду перикарда), снижение преднагрузки или увеличение постнагрузки (частота варьируется в зависимости от ФВЛЖ от 5% до 25%). Управление направлено на первопричину. Часто достаточно гидратации и / или кратковременной инотропной поддержки.Нитропруссид с гипертонией, внутриаортальный баллонный насос или введение вспомогательного устройства левого желудочка может потребоваться вместе с ангиографией и вернуться в операционную для лечения механических проблем.
Сосудорасширяющий (распределительный) шок: это осложнение искусственного кровообращения. Он легко поддается лечению низкими дозами норэпинефрина и, если нет ответа, вазопрессином.
Аритмии. Наиболее распространенным типом аритмий является неустойчивая желудочковая тахикардия (ЖТ) (17–97%).Обычно это доброкачественно. Второй по распространенности тип аритмии — фибрилляция предсердий (15–40%). У пациентов без анамнеза он обычно проходит самостоятельно; в противном случае можно использовать терапию бета-блокаторами, соталолом или амиодароном. Устойчивая ЖТ или ФЖ (1–3%) возникает при периоперационном инфаркте миокарда (полиморфный) или в анамнезе перенесенного инфаркта миокарда, сердечной недостаточности или низкого ФВ (мономорфный). Лечение является поддерживающим и направлено на устранение первопричины, как при брадиаритмии (<1–4%).
Кровотечение: это наиболее частое несердечное осложнение (прибл.10–90% пациентов с АКШ получают переливание крови), особенно у пожилых пациентов, женщин, пациентов с низким ИМТ, анемией перед операцией и приемом антиагрегантов непосредственно перед операцией. Хотя уровень гемоглобина, при котором переливание крови улучшает исход, неизвестен, рекомендуется переливать кровь при Hb <6 г / дл. Пороговое значение <7 г / дл является разумным, в то время как некоторые рекомендуют уровень 8 г / дл. Предпочтительны свеже хранящиеся продукты крови с пониженным содержанием лейкоцитов.
Неврологические осложнения: Нежелательные церебральные явления после АКШ равномерно разделены на события типа I (очаговое повреждение, кома или ступор) и события типа II (снижение когнитивных функций, дефект памяти, судороги) и резко возрастают с возрастом (> 5% с возрастом> 75, иначе 1% –2%).
Инфекции: Наибольшее беспокойство вызывает медиастинит (примерно 1%), который клинически проявляется обычно после латентного периода от нескольких дней до недель после операции. Стрептококк и стафилококк — основные виды. Риск увеличивается при сложных операциях и сопутствующих заболеваниях, таких как ожирение, ХОБЛ и диабет, а также при проведении двойных антиагрегантных операций. Целлюлит встречается чаще (4%) и проявляется типично; антибиотикотерапия — основа лечения.
Острое повреждение почек: оно может иметь несколько этиологий и диагностируется по увеличению креатинина до> 2 мг / дл с минимальным удвоением предоперационного значения.Риск увеличивается с увеличением исходного уровня почечной функции (0,2% при нормальной рСКФ, 2% при рСКФ от 30 до 59 и 11% с рСКФ <30) и близости коронарной ангиографии к операции. Стандартные лечебные меры включают гемодиализ при необходимости.
Какие доказательства?
Fihn, SD, Gardin, JM, Abrams, J. «2012 ACCF / AHA / ACP / AATS / PCNA / SCAI / STS, руководство по диагностике и ведению пациентов со стабильной ишемической болезнью сердца: отчет Американского колледжа кардиологов. Рабочая группа Фонда / Американской кардиологической ассоциации по практическим руководствам, а также Американский колледж врачей, Американская ассоциация торакальной хирургии, Ассоциация профилактических сердечно-сосудистых медсестер, Общество сердечно-сосудистой ангиографии и вмешательств и Общество торакальных хирургов ». Обращение. т. 126. 2012 декабрь 18, стр. E354-471. (Самый последний обзор рекомендаций и рекомендаций по ведению пациентов с САД, включая оптимальную медикаментозную терапию.)
Hillis, LD, Smith, PK, Anderson, JL. «Руководство ACCF / AHA 2011 г. по хирургии шунтирования коронарной артерии. Отчет Фонда Американского колледжа кардиологов / Целевой группы Американской кардиологической ассоциации по практическим рекомендациям. Разработано в сотрудничестве с Американской ассоциацией торакальной хирургии, Обществом сердечно-сосудистых анестезиологов и Обществом торакальных хирургов ». J Am Coll Cardiol. т. 58. 2011. С. e123-210. (Справочная публикация по хирургической реваскуляризации ИБС.)
Левин, GN, Бейтс, ER, Бланкеншип, JC. «Руководство ACCF / AHA / SCAI по чрескожному коронарному вмешательству, 2011 г.». Отчет Фонда Американского колледжа кардиологов / Целевой группы Американской кардиологической ассоциации по практическим рекомендациям и Общества сердечно-сосудистой ангиографии и вмешательств ». J Am Coll Cardiol. т. 58. 2011. С. e44-122. (Современные размышления о катетерных вмешательствах при ИБС.)
Wijns, W, Kolh, P, Danchin, N. «Рекомендации по реваскуляризации миокарда». Eur Heart J. vol. 31. 2010. С. 2501-55. (Превосходный помощник по клиническим показателям процедур коронарной реваскуляризации.)
Copyright © 2017, 2013 ООО «Поддержка принятия решений в медицине». Все права защищены.
Ни один спонсор или рекламодатель не участвовал, не одобрял и не платил за контент, предоставляемый Decision Support in Medicine LLC. Лицензионный контент является собственностью DSM и защищен авторским правом.
.
Что вам нужно знать
Нарушение требований PCI может привести к крупным штрафам для вас и вашего бизнеса. Узнайте больше о соответствии требованиям PCI DSS и узнайте, как Square защищает вас — бесплатно.
Содержание
Введение
Введение в соответствие требованиям PCI
Когда дело доходит до растущего бизнеса, безопасность вашей конфиденциальной информации и данных ваших клиентов, вероятно, является главным приоритетом, особенно когда речь идет о платежах.
Новые достижения в сфере торговли и платежных технологий часто сопровождаются новыми правилами и положениями, которые помогают обеспечить защиту как предприятий, так и потребителей.Введите стандарт безопасности данных индустрии платежных карт (PCI DSS), стандарт, предложенный пятью крупнейшими компаниями, выпускающими кредитные карты, чтобы помочь сократить дорогостоящие утечки данных потребителей и банков.
Понимание соответствия стандарту PCI DSS может показаться сложным для лиц, принимающих деловые решения. В этом руководстве мы расскажем о том, что нужно знать о соответствии стандарту PCI DSS, и проведем вас через шаги, необходимые для защиты вашего бизнеса и клиентов.
FAQ
Шесть часто задаваемых вопросов о соответствии стандарту PCI
Что означает соответствие PCI DSS?
PCI DSS — это стандарт безопасности данных индустрии платежных карт, который устанавливает требования для организаций и продавцов по безопасному и надежному приему, хранению, обработке и передаче данных держателей карт во время транзакций по кредитным картам для предотвращения мошенничества и утечки данных.
Кому нужна сертификация на соответствие PCI DSS?
Хотя технически не существует такой вещи, как «сертификация PCI», продавцы всех размеров, поставщики услуг, банки и любые другие организации, которые обрабатывают платежи по кредитным картам, должны доказать, что они соответствуют требованиям PCI.
Каковы уровни соответствия PCI DSS?
Существует четыре уровня соответствия PCI; каждый уровень предъявляет уникальные требования к бизнесу для подтверждения соответствия. Уровень вашего бизнеса зависит от общего объема ваших транзакций за год.
Сколько стоит соответствие PCI DSS?
Плата за соответствие требованиям PCI и поддержание этого статуса ежегодно может варьироваться от примерно 1000 долларов в год до более 50 000 долларов в год, в зависимости от размера вашего бизнеса.
Отвечаю ли я за заполнение анкеты для самооценки соответствия требованиям PCI DSS (SAQ)?
Анкета для самооценки PCI DSS — это контрольный список объемом от 19 до 87 страниц, созданный и распространяемый Советом по стандартам безопасности PCI.Он используется как механизм, позволяющий продавцам самостоятельно подтверждать соответствие требованиям PCI DSS. Square не требует, чтобы продавцы заполняли опросный лист или проходили самопроверку, поскольку оборудование и программное обеспечение Square соответствуют Стандарту безопасности данных индустрии платежных карт (PCI DSS).
Взимается ли плата за несоблюдение требований PCI?
Да, обычно за несоблюдение требований PCI. Если ваш бизнес не соответствует стандартам PCI, вы можете столкнуться с риском утечки данных, штрафов, затрат на замену карты, дорогостоящих судебно-медицинских аудитов и расследований в отношении вашего бизнеса, ущерба бренду и т. Д.
Сколько вы на самом деле платите?
От дорогого оборудования до высоких тарифов и дополнительных сборов вы можете платить за обработку платежей больше, чем вы думаете.
Глубокое погружение
Соответствие PCI: глубокое погружение
Square продавец или нет, но все же неплохо понять соответствие требованиям PCI, поскольку соблюдение этого правила является частью защиты финансовой информации ваших клиентов и вашего бизнеса.
Контрольный список соответствия стандарту
PCI на 2019 год
| # | Требование соответствия |
| 1 | Установите и поддерживайте конфигурацию брандмауэра для защиты данных держателей карт. |
| 2 | Не используйте заводские настройки по умолчанию для системных паролей и других параметров безопасности. |
| 3 | Защита сохраненных данных о держателях карт. |
| 4 | Шифрование передачи данных о держателях карт в открытых общедоступных сетях. |
| 5 | Используйте и регулярно обновляйте антивирусное программное обеспечение. |
| 6 | Разрабатывать и поддерживать безопасные системы и приложения. |
| 7 | Ограничьте доступ к данным держателей карт по служебной необходимости. |
| 8 | Назначьте уникальный идентификатор каждому человеку, имеющему доступ к компьютеру. |
| 9 | Ограничить физический доступ к данным держателей карт. |
| 10 | Отслеживайте и контролируйте любой доступ к сетевым ресурсам и данным держателей карт. |
| 11 | Регулярно тестируйте системы и процессы безопасности. |
| 12 | Поддерживайте политику безопасности и убедитесь, что все сотрудники знают об этом. |
* Этот контрольный список соответствия PCI был получен в июле 2018 года и может быть устаревшим, поэтому убедитесь, что вы соблюдаете его, продавая через Square или посетив веб-сайт Совета по стандартам безопасности PCI.
Понимание истории стандарта безопасности данных индустрии платежных карт
Стандарт безопасности данных индустрии платежных карт (PCI DSS) родился в 2006 году, когда Интернет стал необходимым и ценным инструментом для предприятий любого размера.Когда эпоха Интернета начала достигать зрелости, компании, решившие использовать ее возможности, начали выводить свои системы обработки платежей в онлайн, подключая их по беспроводной сети как к своим физическим, так и к виртуальным терминалам. Между тем, потребители стали более комфортно использовать кредитные карты для покупок как в Интернете, так и за его пределами.
Историческая актуальность этих стандартов безопасности имеет решающее значение для того, как и почему развивались стандарты PCI. Эти новые направления коммерции подвергали предприятия и потребителей все большему и большему риску, и возможность мошенников украсть информацию о кредитных картах из незащищенных сетей и платежных систем стала более распространенной.
В ответ на рост кражи данных пять крупнейших брендов кредитных карт — Visa, MasterCard, Discover, American Express, JCB — внедрили стандарт безопасности данных индустрии платежных карт (PCI DSS) для предотвращения дорогостоящих утечек данных потребителей и банков. Именно с появлением этого постановления и Совета по стандартам безопасности PCI соблюдение требований PCI стало и остается важным шагом в регулировании безопасности индустрии платежей по кредитным картам.
Чтобы помочь в управлении стандартами соответствия, платежные бренды также учредили Совет по стандартам безопасности PCI в качестве независимого органа, призванного «отслеживать угрозы и совершенствовать отраслевые средства борьбы с ними посредством усовершенствования стандартов безопасности PCI и обучения сотрудников безопасности. профессионалы.”
Важно отметить, однако, что компании, выпускающие кредитные карты, сделали соблюдение требований PCI в качестве саморегулируемого мандата — это означает, что они переложили ответственность за соблюдение требований на всех этапах жизненного цикла обработки платежей на продавцов и организации.
Таким образом, хотя Совет несет ответственность за установление стандартов и установление требований к продавцам, которых они должны придерживаться, таких как PCI-совместимые приложения и анкеты самооценки (SAQ) или контрольные списки, платежные бренды несут ответственность за соблюдение их среди продавцов и организаций. которые принимают кредитные карты.
Прежде чем мы начнем более подробно изучать стандарты соответствия PCI, важно отметить, что в целом кредитные карты безопасны, а благодаря новым правилам и стандартам, таким как чиповые карты EMV, они становятся еще более безопасными (мы поговорим об этом позже). Но даже крупнейшие бренды все еще могут подвергаться риску серьезных утечек данных, связанных с кредитными картами.
Независимо от того, являетесь ли вы корпоративной корпорацией или имеете небольшой побочный бизнес, вы, вероятно, слышали термин PCI DSS.Поддерживая соответствие PCI, вы можете помочь защитить свой бизнес от хакеров, которые могут получить конфиденциальные данные о держателях карт и использовать их для выдачи себя за держателей карт или кражи их личности.
Что такое соответствие PCI DSS?
Стандарт безопасности данных индустрии платежных карт (PCI DSS) относится к стандартам безопасности платежей, которые гарантируют, что все продавцы безопасно и надежно принимают, хранят, обрабатывают и передают данные держателей карт (также известные как информация о кредитных картах ваших клиентов) во время транзакции по кредитной карте. .
Любой продавец с идентификатором продавца, который принимает платежные карты, должен соблюдать эти правила соответствия PCI для защиты от утечки данных. Требования варьируются от установления политик безопасности данных для вашего бизнеса и сотрудников до удаления данных карт из вашей процессинговой системы и платежных терминалов.
«Владелец карты» или платежные данные включают такую информацию, как полный номер основного счета (PAN), имя держателя карты, а также код обслуживания кредитной карты и дату истечения срока действия.Продавцы также несут ответственность за защиту конфиденциальных данных аутентификации в данных магнитной полосы (например, CAV2, CVC2, CVV2, CID, PIN-коды, блоки PIN-кодов и т. Д.).
На приведенной выше схеме кредитной карты показано, где на кредитной карте содержатся уникальные и конфиденциальные данные держателя карты. Вашему бизнесу следует избегать хранения каких-либо данных на этой диаграмме; Если вы это сделаете, то вам, скорее всего, потребуется представить вескую коммерческую причину для хранения и продемонстрировать, что у вас есть надлежащие механизмы для его защиты.
Чтобы определить, где ваш бизнес может быть уязвим для атаки, важно знать, откуда могут быть украдены конфиденциальные данные о держателях карт. Например, данные могут быть украдены:
- Взломанные считыватели карт
- Базы данных небезопасных платежных систем
- Скрытые камеры, записывающие ввод данных аутентификации
- Секретный доступ к беспроводной или проводной сети вашего магазина
- Бумага, хранящаяся в картотеке, или письменные записи
Таким образом, важно обеспечить безопасность на протяжении всего жизненного цикла платежа, от приема кредитной карты до обработки платежа, путем защиты данных о держателях карт, когда они собираются в точке продажи и по мере поступления в платежную систему на ваш торговый счет.
Стандарты
PCI применяются к:
Как вы, наверное, догадались, обеспечение соответствия требованиям PCI и поддержание этого соответствия может оказаться сложным процессом; он может включать в себя реализацию мер безопасности, наем дорогостоящего стороннего консультанта для установки дорогостоящего программного и аппаратного обеспечения и подписание дорогостоящего и имеющего обязательную силу контракта, в соответствии с которым вы соглашаетесь с условиями банка для ежегодного соответствия требованиям PCI, проведения ежегодной самооценки и т.
Сколько вы на самом деле платите?
От дорогого оборудования до высоких тарифов и дополнительных сборов вы можете платить за обработку платежей больше, чем вы думаете.
Каковы уровни соответствия и требования PCI?
Если ваша компания принимает платежные карты с любым из пяти брендов кредитных карт PCI SSC (American Express, Discover, JCB, MasterCard и Visa), то вы должны соответствовать требованиям PCI на различных уровнях, как это определено вашим объем транзакции.
Шестьдесят пять процентов малых предприятий не соответствуют минимальным требованиям соответствия.
Имейте в виду, что не все требования к отчетности о соответствии одинаковы — они могут различаться в зависимости от объема обработки.Например, продавцы с большим объемом транзакций (как описано в таблице ниже) должны работать с внутренними оценщиками безопасности (ISA), квалифицированными оценщиками безопасности (QSA) и поставщиками сканирования, утвержденными PCI (ASV).
Существует четыре различных уровня соответствия; эти уровни устанавливают требования, за выполнение которых несут ответственность продавцы. Совет PCI считает, что пройденный балл соответствует 100% критериям . Из-за этой сложной ответственности многие крупные компании предпочитают работать с консультантом по соблюдению требований PCI по вопросам стандартов и того, как соответствовать этим требованиям уровня соответствия требованиям PCI.
Каждый продавец попадает в одну из четырех категорий в зависимости от объема их транзакций в течение 12-месячного периода. Хотя у каждого бренда кредитных карт есть свои собственные критерии, немного отличающиеся друг от друга, обычно уровни соответствия PCI следующие *:
Уровни соответствия PCI
| Уровень торговца | Применимо к | Требования PCI * |
|---|---|---|
| 1 | 1) Продавцы, которые обрабатывают более 6 миллионов транзакций в год |
2) Любой продавец, у которого была утечка данных или атака, которая привела к компрометации данных учетной записи
| 3) Любой продавец, идентифицированный какой-либо ассоциацией карт как Уровень 1 | о соответствии (ROC) квалифицированным оценщиком безопасности (QSA) — также широко известный как оценка уровня 1 на месте — или внутренним аудитором, если он подписан должностным лицом компании |
Ежеквартальное сетевое сканирование утвержденным поставщиком сканирования (ASV)
| Форма подтверждения соответствия | |||
| 2 | Продавцы, обрабатывающие от 1 до 6 млн транзакций в год | Заполните анкету для самооценки PCI DSS в соответствии с содержащимися в ней инструкциями. |
Завершите и получите доказательства прохождения сканирования уязвимостей с помощью утвержденного поставщика сканирования PCI SSC (ASV)
Полностью заполнить соответствующий Сертификат соответствия (находится в инструменте ОЛС)
| Отправьте свой опросный лист, подтверждение прохождения сканирования (если применимо) и Подтверждение соответствия вместе с любой другой запрошенной документацией своему эквайеру | |||
| 3 | Продавцы, которые обрабатывают от 20000 до 1 млн транзакций электронной торговли в год | Заполните анкету для самооценки PCI DSS в соответствии с содержащимися в ней инструкциями. |
Завершите и получите доказательства прохождения сканирования уязвимостей с помощью утвержденного поставщика сканирования PCI SSC (ASV)
Полностью заполните соответствующий Сертификат соответствия (находится в инструменте ОЛС)
| Отправьте свой опросный лист, подтверждение прохождения сканирования (если применимо) и Подтверждение соответствия вместе с любой другой запрошенной документацией своему эквайеру | |||
| 4 | Продавцы, которые обрабатывают менее 20000 транзакций электронной торговли, и все остальные продавцы, которые обрабатывают до 1 миллиона транзакций в год | Заполните анкету для самооценки PCI DSS в соответствии с содержащимися в ней инструкциями. |
Завершите и получите доказательства прохождения сканирования уязвимостей с помощью утвержденного поставщика сканирования PCI SSC (ASV)
Полностью заполните соответствующий Сертификат соответствия (находится в инструменте ОЛС)
| Отправьте свой опросный лист, подтверждение прохождения сканирования (если применимо) и Подтверждение соответствия вместе с любой другой запрошенной документацией своему эквайеру |
* Каждый из пяти платежных брендов имеет свои собственные программы защиты данных, которые требуют от продавцов защиты данных обработки кредитных карт.Вот полезный пример требований Visa PCI DSS.
Каковы последствия несоблюдения?
Если вы не знаете правил соблюдения PCI или последствий несоблюдения, вы не одиноки.
Хотя соблюдение требований PCI не является законом, это не означает, что нарушение правил не имеет большого значения. Фактически, отчет Verizon о взломе данных за 2019 год показал, что в этом году произошло почти 42 068 инцидентов, связанных с безопасностью данных. Поэтому как никогда важно, чтобы жизненный цикл обработки платежей был безопасным.
Если ваш бизнес не соответствует стандартам PCI, вы можете подвергнуться риску утечки данных, штрафов, затрат на замену карты, дорогостоящих судебно-медицинских аудитов и расследований вашего бизнеса, ущерба бренду и т. Д. В случае нарушения.
На самом деле, 30% малых предприятий сообщают, что им неизвестны штрафы за несоблюдение требований PCI DSS 3.0.
Штрафы не получают широкой огласки, но они могут быть разрушительными для бизнеса. Например, если ваша компания нарушает стандарты соответствия PCI, бренды кредитных карт могут взимать штрафы от 5000 до 100000 долларов в месяц в ваш банк-эквайер.Банки часто перекладывают эти расходы на продавца и могут расторгнуть контракты или увеличить комиссию за транзакции в ответ на нарушения и нарушения
Помимо финансовых затрат, существуют и другие потенциальные обязательства, которые могут повлиять на ваш бизнес. Согласно Стандартам безопасности PCI, несоблюдение стандартов PCI и связанное с этим нарушение данных может привести к:
- Доверие утрачено, покупатели переходят к другим торговцам
- Снижение продаж
- Стоимость перевыпуска новых платежных карт
- Убытки от мошенничества
- Более высокие последующие затраты на соблюдение требований
- Судебные издержки, урегулирования и судебные решения
- Штрафы и пени
- Прекращение приема платежных карт
- Потерянные рабочие места (CISO, CIO, CEO и зависимые профессиональные должности)
- Выход из бизнеса
Сколько стоит соответствие стандарту PCI?
Создание и поддержание бизнеса, соответствующего требованиям PCI, может быть дорогостоящим, в зависимости от типа и размера вашей компании, а также уровня соответствия, которого вы придерживаетесь.
По уровню затраты обычно колеблются от:
Уровень 4: от 60 до 75 долларов в месяц и выше
В ваши расходы входит утвержденный поставщик сканирования (ASV), который должен выполнять регулярное сканирование сети или веб-сайта, а также заполнять анкету самооценки (SAQ) и подтверждение соответствия вами или вашим персоналом.
Уровень 3: 1200 долларов в год и выше
Ваши расходы включают регулярное сканирование с помощью ASV и увеличиваются в зависимости от размера вашей компьютерной сети и количества IP-адресов, плюс стоимость заполнения ежегодной анкеты для самооценки и подтверждения соответствия.
Уровень 2: 10 000 долларов в год и выше
Ваши расходы включают регулярное сканирование с помощью ASV и увеличиваются в зависимости от размера вашей компьютерной сети и количества IP-адресов, плюс стоимость заполнения ежегодной анкеты для самооценки и подтверждения соответствия.
Уровень 1: 50 000 долларов в год и выше
Ваши расходы включают регулярное сканирование сети утвержденным поставщиком сканирования, годовой отчет о соответствии требованиям квалифицированного специалиста по оценке безопасности и подтверждение соответствия.
Остерегайтесь хищных поставщиков услуг, которые взимают дорогую плату, но удовлетворяют лишь часть ваших требований PCI.
Square позаботится о соответствии требованиям PCI для вашего бизнеса
Square соответствует стандарту безопасности данных индустрии платежных карт (PCI DSS), поэтому вам не нужно индивидуально подтверждать свое состояние соответствия.
Наше оборудование / считыватели имеют готовое к эксплуатации сквозное шифрование без необходимости настройки и дополнительных затрат — без ежемесячной платы или требований ежегодной оценки. Мы поддерживаем программное обеспечение, соответствующее стандарту PCI, без дополнительных затрат для вас, без ежемесячных контрактов или долгосрочных обязательств. Если вы используете Square для хранения, обработки и передачи данных карт ваших клиентов, вам не нужно предпринимать никаких действий для проверки соответствия требованиям PCI к Square, и вам не нужно платить какие-либо сборы за соблюдение требований PCI.
Square является продавцом каждой транзакции. Мы работаем с банками от вашего имени, включая соответствие требованиям PCI, регулирование и обработку.Мы от вашего имени выступаем за то, чтобы простые и честные ошибки и споры разрешались справедливо.
Технический подход Square к безопасности также разработан для защиты как вас, так и ваших клиентов. Мы придерживаемся ведущих отраслевых стандартов PCI для управления нашей сетью, защиты наших веб-приложений и клиентских приложений, а также установления политик в нашей организации. Интегрированная платежная система Square обеспечивает сквозное шифрование для каждой транзакции в точке смахивания, падения или касания и токенизирует данные, когда они достигают наших серверов.Кроме того, мы отслеживаем каждую транзакцию от ее принятия до платежа, постоянно внедряем инновации в области предотвращения мошенничества и защищаем ваши данные так, как от этого зависит наш бизнес — потому что это так.
Сколько вы фактически платите?
От дорогого оборудования до высоких тарифов и дополнительных сборов вы можете платить за обработку платежей больше, чем вы думаете.
.
| PCI | Интерфейс периферийных компонентов Академия и наука »Электроника — и многое другое … | Оцените: | |||
| PCI | Индустрия платежных карт Бизнес »Общий бизнес — и многое другое … | Оцените: | |||
| PCI | Доход на душу населения Правительство» Правительство США | Оцените: | |||
| PCI | Чрескожное коронарное вмешательство Медицина »Кардиология — и многое другое… | Оцените это: | |||
| PCI | PC Zone Бизнес »Компании и фирмы | ||||
| PCI | Информация для управления протоколом Вычислительная техника »Сети — и многое другое … | Оцените: | |||
| PCI | Профилактическое лечение Краниальное облучение Медицина »Физиология | Оценить: | |||
| PCI | Инициатива до колледжа Сообщество» Некоммерческие организации | ||||
| PCI | Подготовительный курс Инициатива Сообщество »Образовательные | Оцените это: | |||
| PCI | Пылевидный уголь Бизнес» Продукты | : | |||
| PCI | Идентификация конфигурации продукта Правительственный »Военный | Оцените: | |||
| PCI | Программируемое прерывание вычислений | Оцените: | |||
| PCI | Элемент физической конфигурации Правительственный »Военный — и многое другое… | Оцените: | |||
| PCI | Инструменты для персональных компьютеров Вычислительная техника »Сеть | 9005 | |||
| PCI | Prosound Communications, Inc. Бизнес »Компании и фирмы | Оцените: | |||
| PCI | Prunuske Chatham, Inc. Бизнес »Компании и Фирмы | Оцените: | |||
| PCI | Photo-Certified Coin Institute Разное» Монеты | 9000 9000 9000 | Оцените: | ||
| PCI | Потенциальный криминальный информатор Правительственные »Файлы ФБР | Оцените: | |||
| Оцените: | |||||
| PCI | Осмотр перед подключением Сообщество» Жилье и удобства | 4 | Оцените: | ||
Population Council, Inc. Сообщество »Некоммерческие организации | Оцените: | ||||
| PCI | Чистый импорт на заказ Государственный» Транспорт | Оцените: | |||
| PCI | Индикатор личных изменений Сообщество | Оцените: | |||
| PCI | Разное Разное Разное Разное | Оцените: | |||
| PCI | Чрескожное кардиологическое вмешательство Медицинское »Кардиология | 415 |
