Трудности дифференциальной диагностики в практике врача-пульмонолога: гранулематоз с полиангиитом | Демко И.В., Гордеева Н.В., Мамаева М.Г., Матвеева И.В., Крапошина А.Ю., Соловьева И.А., Собко Е.А., Зеленый С.В., Локтионова М.М.
Статья посвящена трудностям диагностики гранулематоза с полиангиитом
Гранулематоз с полиангиитом (Вегенера) (ГПА) относится к системным васкулитам, ассоциированным с антинейтрофильными цитоплазматическими антителами (АНЦА), – тяжелым полиорганным заболеваниям, при которых прогноз во многом определяет скорость диагностики и правильное назначение индукционной терапии. Отличительным признаком ГПА является сочетание патогенетически связанного с АНЦА некротизирующего васкулита, преимущественно сосудов мелкого и среднего калибра различной локализации, и сопутствующего ему гранулематозного воспаления, прежде всего в органах респираторного тракта [1].
Поражение легких в целом встречается у 85–100% больных, причем у 45% – в дебюте заболевания.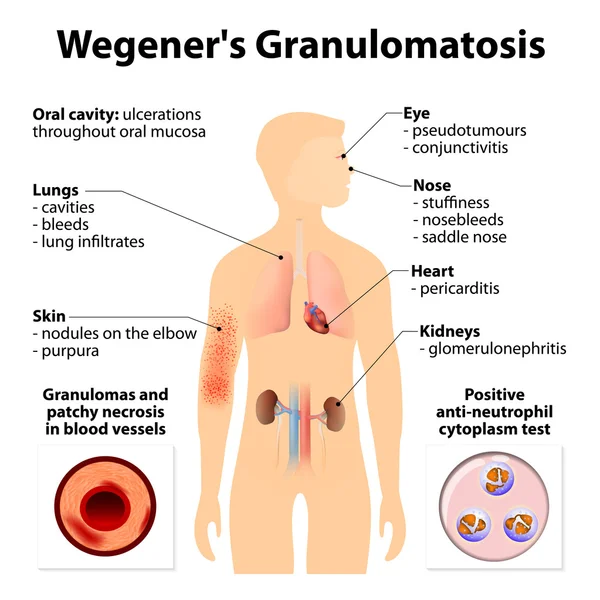 Патоморфологическая картина поражения легких при болезни Вегенера характеризуется широким вовлечением в процесс сосудов микроциркуляторного русла органа с образованием изолированных гранулем и полей диффузного гранулирования ткани, подвергающихся некрозу. Патологический процесс, как правило, бывает двусторонним и развивается преимущественно в средних и нижних отделах легких. Только у половины больных с рентгенологическими изменениями в легких имеются клинические признаки (кашель, кровохарканье), в остальных случаях поражение легких может протекать бессимптомно [2].
Патоморфологическая картина поражения легких при болезни Вегенера характеризуется широким вовлечением в процесс сосудов микроциркуляторного русла органа с образованием изолированных гранулем и полей диффузного гранулирования ткани, подвергающихся некрозу. Патологический процесс, как правило, бывает двусторонним и развивается преимущественно в средних и нижних отделах легких. Только у половины больных с рентгенологическими изменениями в легких имеются клинические признаки (кашель, кровохарканье), в остальных случаях поражение легких может протекать бессимптомно [2].
При выявлении инфильтративных изменений в легких прежде всего проводится дифференциальная диагностика с неспецифическим воспалительным процессом (пневмония), туберкулезом, онкопатологией. А о таком редком заболевании, как гранулематоз Вегенера, забывают, особенно если поражение верхних дыхательных путей и почек выражено незначительно [3].
В настоящее время, несмотря на то что накоплено достаточное количество случаев, хорошо описанных и проанализированных, заболевание выявляется достаточно редко, а своевременная диагностика его вызывает большие трудности [4].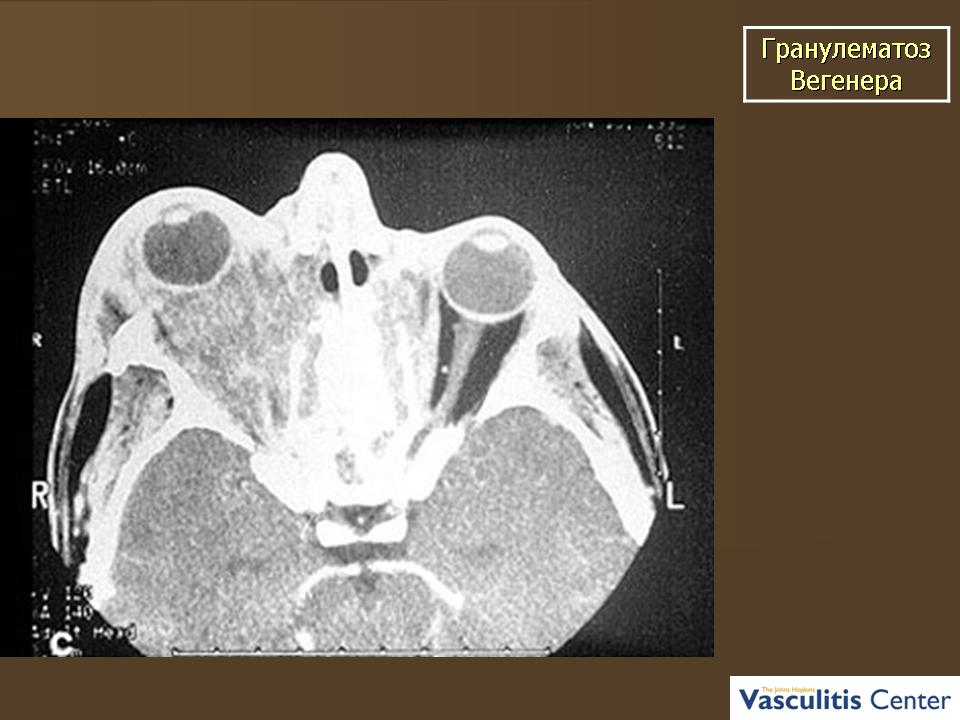
Далее приводим клиническое наблюдение данного заболевания, иллюстрирующее сложности дифференциальной диагностики.
Пациент С. был госпитализирован в отделение пульмонологии Краевой клинической больницы Красноярска с жалобами на кашель с отделением белой пенистой мокроты до 20 мл/сут, затруднение носового дыхания, повышение температуры тела до 38,9°С, снижение массы тела на 5 кг в течение 1 мес. при сохраненном аппетите, болезненность в коленных, голеностопных суставах в состоянии покоя, усиливающуюся при физической нагрузке, слабость, снижение работоспособности.
Из анамнеза: считает себя больным в течение 1 мес. (с 20.11.2015), когда впервые поднялась температура до 38°С (связывает с переохлаждением на рабочем месте), появился кашель, заложенность носа. Лечился самостоятельно: нестероидные противовоспалительные препараты (НПВП), сосудосуживающие капли в нос, антибактериальные препараты (левофлоксацин). Продолжал ходить на работу. Несмотря на проводимое лечение, сохранялась лихорадка до 38°С, нарастала слабость, появился кашель с отхождением мокроты. В связи с ухудшением состояния, 01.12.2015 обратился к терапевту по месту жительства. Выполнена рентгенография органов грудной клетки в 2-х проекциях. Рентгенологически выявлена инфильтрация в проекции верхней доли справа. С подозрением на специфический процесс больной был направлен на консультацию в Краевой противотуберкулезный диспансер Красноярска. В результате проведенного обследования специфический процесс был исключен. С диагнозом «правосторонняя верхнедолевая пневмония» пациент был направлен в стационар по месту жительства с рекомендацией провести курс антибактериальной терапии. С 04.12.2015 по 21.12.2015 лечился по месту жительства в отделении терапии ЦРБ. Повторно консультирован фтизиатром в противотуберкулезном диспансере. Дано заключение об отсутствии туберкулеза легких, высказано предположение о саркоидозе легочно-медиастинальной формы. Для уточнения диагноза пациент направлен на консультацию к пульмонологу в краевую клиническую больницу и 21.12.2015 госпитализирован в отделение пульмонологии для дальнейшего уточнения диагноза и лечения.
В связи с ухудшением состояния, 01.12.2015 обратился к терапевту по месту жительства. Выполнена рентгенография органов грудной клетки в 2-х проекциях. Рентгенологически выявлена инфильтрация в проекции верхней доли справа. С подозрением на специфический процесс больной был направлен на консультацию в Краевой противотуберкулезный диспансер Красноярска. В результате проведенного обследования специфический процесс был исключен. С диагнозом «правосторонняя верхнедолевая пневмония» пациент был направлен в стационар по месту жительства с рекомендацией провести курс антибактериальной терапии. С 04.12.2015 по 21.12.2015 лечился по месту жительства в отделении терапии ЦРБ. Повторно консультирован фтизиатром в противотуберкулезном диспансере. Дано заключение об отсутствии туберкулеза легких, высказано предположение о саркоидозе легочно-медиастинальной формы. Для уточнения диагноза пациент направлен на консультацию к пульмонологу в краевую клиническую больницу и 21.12.2015 госпитализирован в отделение пульмонологии для дальнейшего уточнения диагноза и лечения.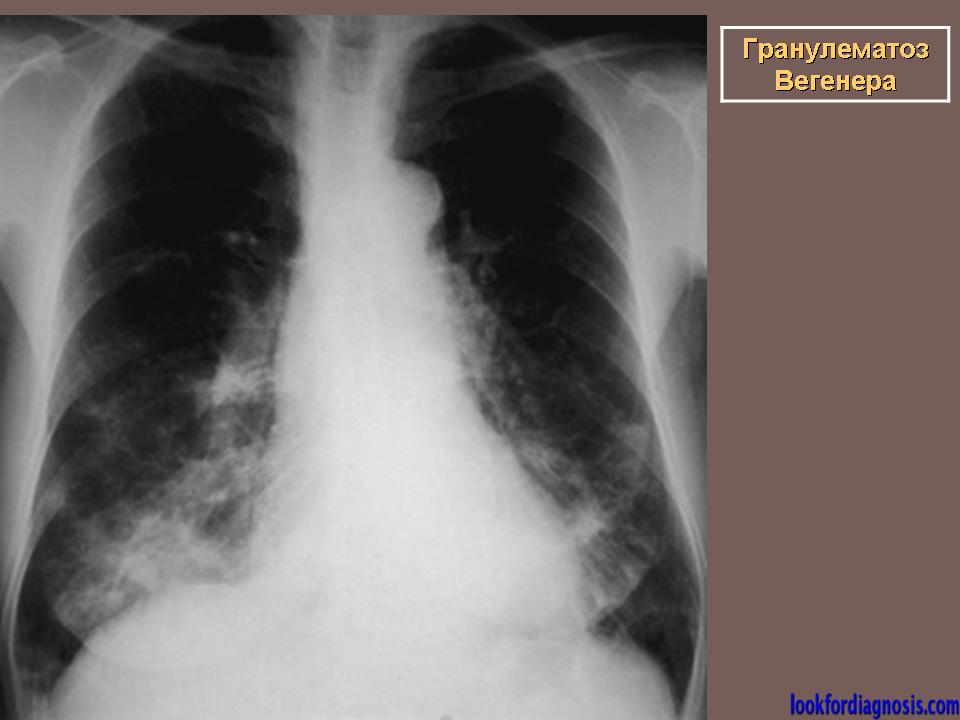
При поступлении: состояние средней степени тяжести, телосложение нормостеническое (ИМТ – 26,06 кг/м2), кожные покровы влажные, горячие (t=38,5°С), слизистые бледно-розовые, сухие. На коже в проекции голеностопных суставов единичные элементы язвенно-некротической сыпи (рис. 1). Костно-мышечная система без особенностей. Носовое дыхание затруднено. Болезненность при пальпации в проекции лобных, гайморовых пазух справа. ЧДД – 21 в минуту, SpO2 – 98%. Грудная клетка правильной формы, голосовое дрожание несколько ослаблено в правых верхних отделах. По средней аксиллярной линии при аускультации выслушиваются рассеянные инспираторные хрипы. Над остальными легочными полями дыхание везикулярное, хрипов нет. Тоны сердца: ясные, ритмичные; шумов нет; ЧСС – 81 уд/мин; АД – 120/85 мм рт.ст. Живот мягкий, безболезненный; стул регулярный, оформленный. Мочеиспускание: свободное, безболезненное.
В анализах крови отмечается лейкоцитоз, увеличение СОЭ (67 мм/ч), гипохромная анемия (108 г/л), а также повышение СРБ (128,3 г/л) и фибриногена (7,9 г/л).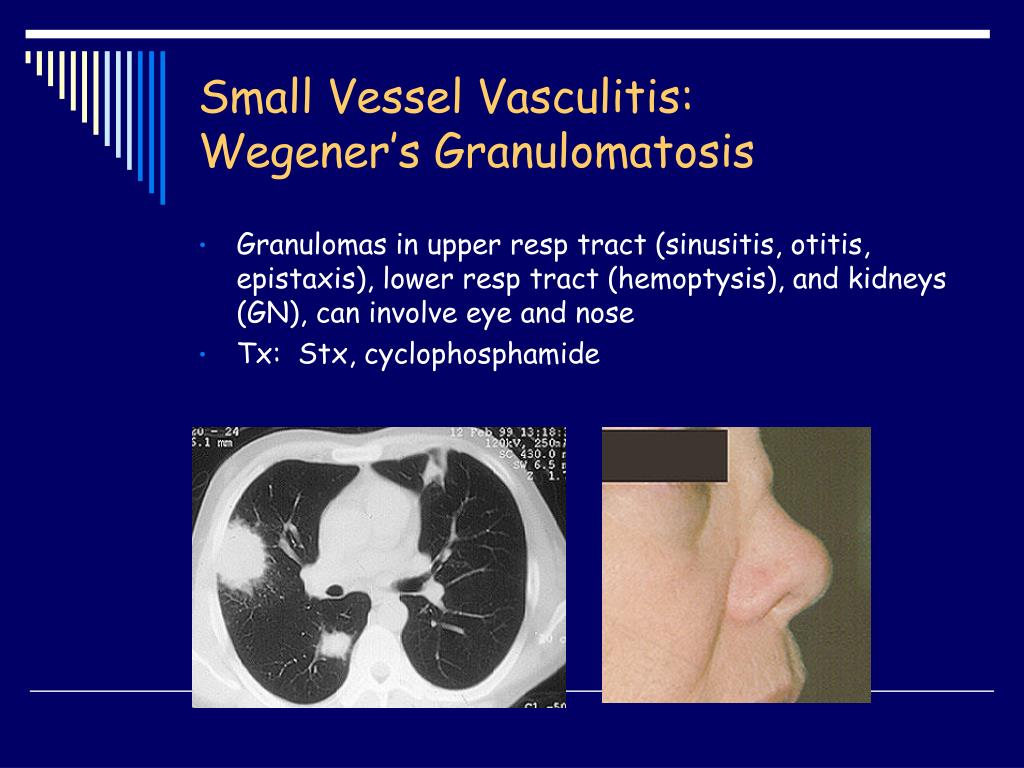 При цитологическом исследовании мокроты изменений не выявлено. На рентгенограмме легких – участки инфильтрации легочной ткани в проекции верхней, нижней долей справа и нижней доли слева с наличием мелких полостей деструкции справа. Учитывая симптомы со стороны верхних дыхательных путей, пациенту проведена рентгенография придаточных пазух носа. Установлено тотальное затемнение правой гайморовой пазухи, затемнение клеток решетчатого лабиринта и носовых ходов справа – гемипансинусит. Консультирован отоларингологом, проведена пункция правой гайморовой пазухи, получено большое количество слизисто-гнойного отделяемого.
При цитологическом исследовании мокроты изменений не выявлено. На рентгенограмме легких – участки инфильтрации легочной ткани в проекции верхней, нижней долей справа и нижней доли слева с наличием мелких полостей деструкции справа. Учитывая симптомы со стороны верхних дыхательных путей, пациенту проведена рентгенография придаточных пазух носа. Установлено тотальное затемнение правой гайморовой пазухи, затемнение клеток решетчатого лабиринта и носовых ходов справа – гемипансинусит. Консультирован отоларингологом, проведена пункция правой гайморовой пазухи, получено большое количество слизисто-гнойного отделяемого.
Таким образом, согласно вышепредставленным результатам, в клинической картине преобладали синдромы инфильтрации легочной ткани и интоксикационного лихорадочного активного воспалительного процесса. Установлен рабочий диагноз: двухсторонняя полисегментарная пневмония тяжелого течения с сопутствующим острым гнойным правосторонним верхнечелюстным синуситом.
В отделении пациенту проводилась антибактериальная (цефтриаксон+азитромицин), дезинтоксикационная (электролитные растворы), симптоматическая (парацетамол), муколитическая (бромгексин) терапия.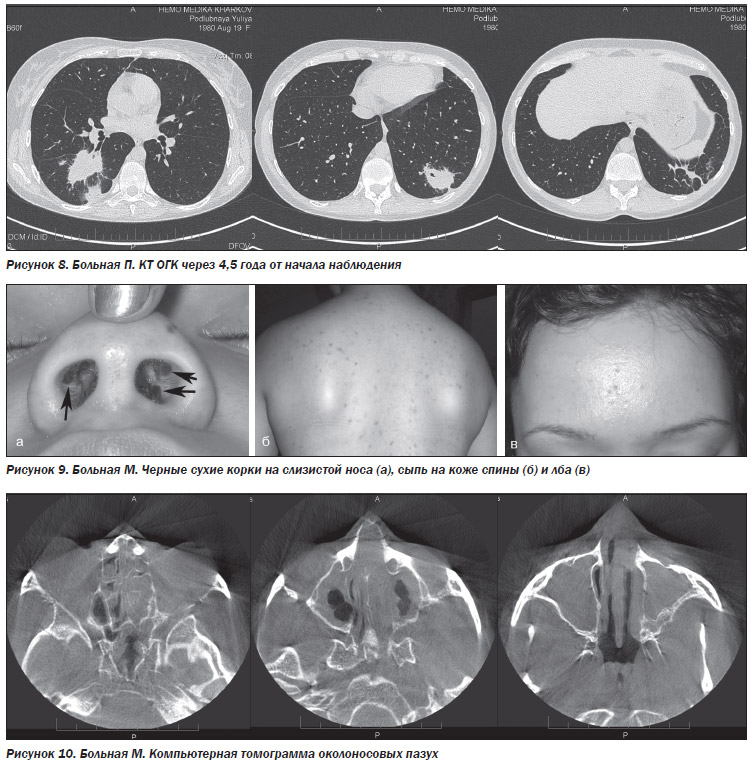 Однако на фоне проводимой терапии наблюдалась отрицательная динамика: нарастали симптомы интоксикации, сохранялась фебрильная температура до 39°С с кратковременным эффектом от введения НПВП, появились кровохарканье, признаки дыхательной недостаточности (ЧДД 26 в минуту, снижение SpO2 до 91%), увеличилось количество язвенно-некротических элементов в проекции голеностопных суставов. 26.12.15. у пациента отмечен эпизод легочного кровотечения (появилась мокрота ржавого цвета, при цитологическом исследовании выявлено множество эритроцитов, фибробронхоскопия (ФБС) показала гемопноэ справа).
Однако на фоне проводимой терапии наблюдалась отрицательная динамика: нарастали симптомы интоксикации, сохранялась фебрильная температура до 39°С с кратковременным эффектом от введения НПВП, появились кровохарканье, признаки дыхательной недостаточности (ЧДД 26 в минуту, снижение SpO2 до 91%), увеличилось количество язвенно-некротических элементов в проекции голеностопных суставов. 26.12.15. у пациента отмечен эпизод легочного кровотечения (появилась мокрота ржавого цвета, при цитологическом исследовании выявлено множество эритроцитов, фибробронхоскопия (ФБС) показала гемопноэ справа).
При проведении мультиспиральной компьютерной томографии (МСКТ) легких 28.12.15 выявлена диффузная альвеолярная инфильтрация легочной ткани, занимающая практически весь объем правого легкого с видимыми просветами бронхов в толще (рис. 2). Аналогичные изменения, но менее выраженные, определялись в левом легком, преимущественно в прикорневой зоне и в нижней доле. Немногочисленные лимфатические узлы средостения – до 1,6 см.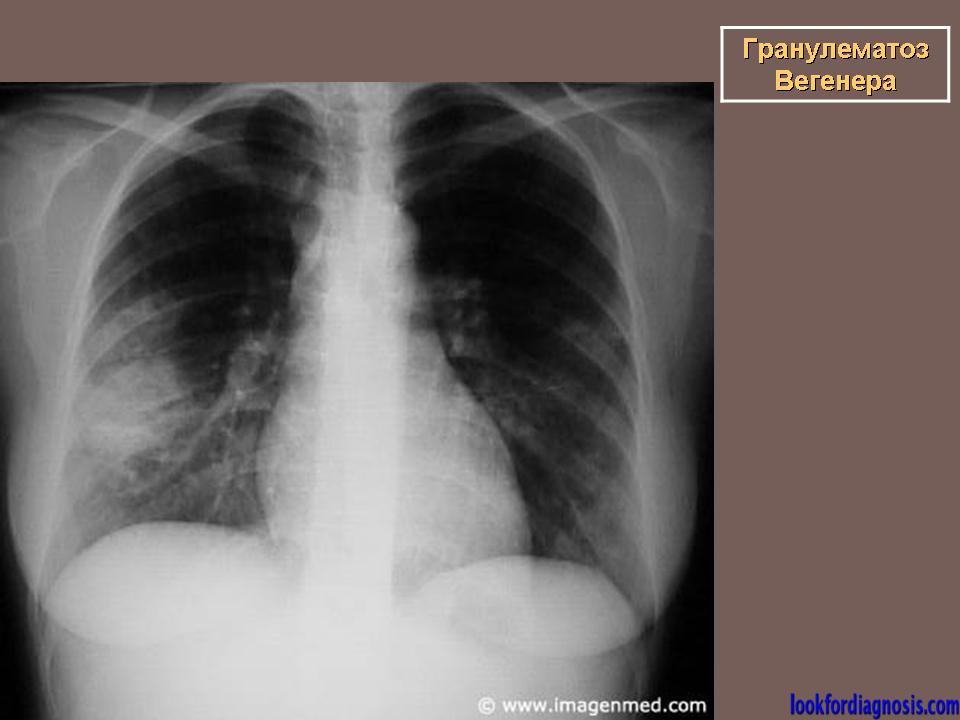
Учитывая отрицательную динамику, было принято решение о смене антибактериальной терапии (назначены карбапенемы+аминогликозиды), проведены диагностическая ФБС (установлен двусторонний диффузный умеренно выраженный бронхит со слабо выраженной слизисто-гнойной гиперсекрецией), рентгенография органов дыхания в динамике (положительной динамики не отмечено).
Проводилась дифференциальная диагностика между сепсисом, инфекционным эндокардитом, ВИЧ-инфекцией, паранеопластическим синдромом, системными заболеваниями. В этих целях были проведены: Эхо-КГ (расширена полость левого предсердия до 4,1 см, недостаточность трикуспидального клапана I–II степени, среднее давление в легочной артерии 52 мм рт.ст., заднее эхопространство – 0,4 см, дополнительные эхосигналы на клапанных структурах четко не выявлены), бактериологическое исследование крови на стерильность (рост микроорганизмов не выявлен), определение суммарных антител к ВИЧ-инфекции (отрицательно).
Отсутствие эффекта у пациента от проводимой неспецифической антибактериальной терапии, сочетание в клинической картине инфильтративного поражения легких с гемипансинуситом, легочное кровотечение, кожный синдром по типу элементов пурпуры с изъязвлениями в области голеностопных суставов, высокая активность воспалительного процесса (СОЭ – до 70 мм/ч, фибриноген – 7,8 г/л, СРБ – 128 мг/мл), лихорадочный синдром, суставной синдром, мочевой синдром (измененные эритроциты 0-2-4 в п/зр, протеинурия 0,065 г/л), анемия (эритроциты 3,55×1012/л, гемоглобин 88 г/л), тромбоцитоз (до 557×109/л) со снижением агрегации тромбоцитов – все это позволило предположить наличие системного заболевания.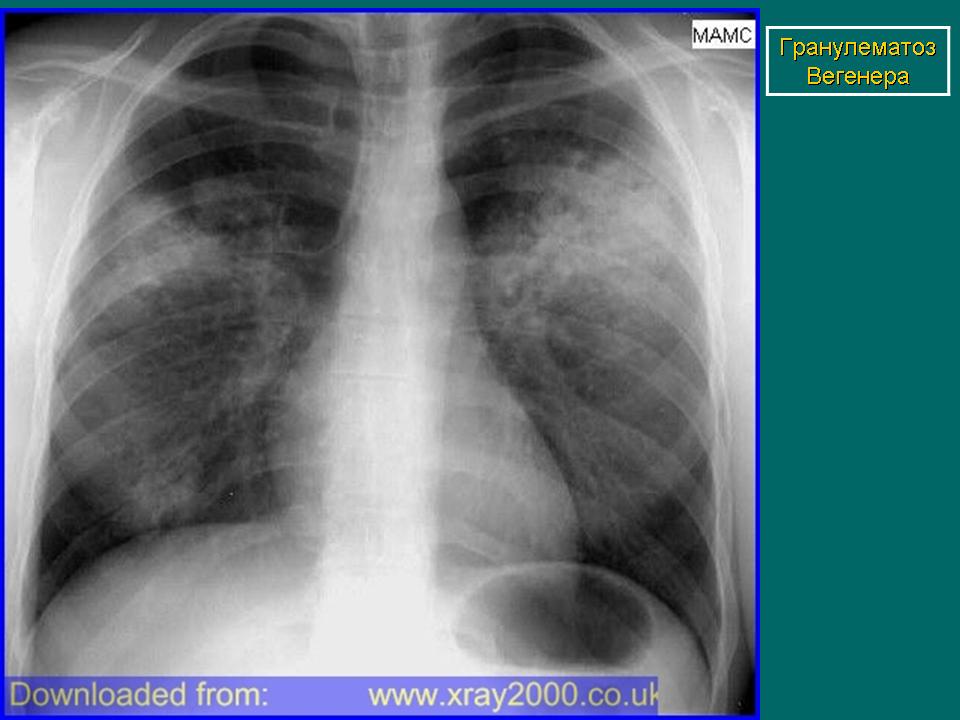 Для подтверждения диагноза назначено иммунологическое исследование: антитела к протеиназе 3, миелопероксидазе, ANCA. Получен положительный результат: АТ к PR-3 – 252,6 МЕ/мл, ANCA – положительно, позволивший подтвердить диагноз «гранулематоз с полиангиитом». Проведен консилиум для определения дальнейшей тактики ведения пациента.
Для подтверждения диагноза назначено иммунологическое исследование: антитела к протеиназе 3, миелопероксидазе, ANCA. Получен положительный результат: АТ к PR-3 – 252,6 МЕ/мл, ANCA – положительно, позволивший подтвердить диагноз «гранулематоз с полиангиитом». Проведен консилиум для определения дальнейшей тактики ведения пациента.
Таким образом, с учетом клинико-анамнестических данных, дополнительных исследований, МСКТ-картины, иммунологических показателей выставлен диагноз: Системный васкулит, гранулематозный ангиит.
После проведенного курса пульс-терапии медилпреднизолоном 1000 мг № 3 и циклофосфамидом 1000 мг № 1, с последующим переходом на пероральный прием преднизолона в дозе 60 мг/сут отмечалась положительная клиническая, лабораторная и рентгенологическая динамика. Уменьшилась одышка, нормализовались показатели оксигенации крови, повысилась толерантность к физической нагрузке, исчезло кровохарканье. Снизились уровень лейкоцитов и СОЭ, повысились показатели гемоглобина.
При выписке пациенту рекомендовано: наблюдение участкового терапевта, госпитализация в отделение нефрологии через 2 нед. для проведения повторного курса пульс-терапии циклофосфамидом, прием преднизолона внутрь в суточной дозе 60 мг, омепразола 20 мг по 1 капсуле утром и на ночь, аспаркама по 2 таб. 2 раза в день ежедневно, бисептола 480 мг по 1 таб. 2 раза в день в течение 3-х недель, сорбифера 100 мг по 1 таб. 2 раза в день до повышения уровня гемоглобина выше 130 г/л. Повторить МСКТ легких в динамике через 3 мес. (см. рис. 2).
Обсуждение
Таким образом, данный случай демонстрирует определенные диагностические сложности у больного с системным васкулитом, связанные с преобладанием поражения верхних и нижних дыхательных путей (в связи с чем пациент неоднократно был обследован фтизиатром) и отсутствием поражения почек на начальном этапе развития заболевания. Однако сопоставление клинической картины, тщательный анализ симптомов заболевания, диагностический поиск с исследованием специфических иммунологических маркеров гранулематозного полиангиита, совместное обсуждение больного специалистами разного профиля позволили не только своевременно установить правильный диагноз, назначить адекватную терапию, но и способствовать улучшению прогноза этого тяжелого заболевания.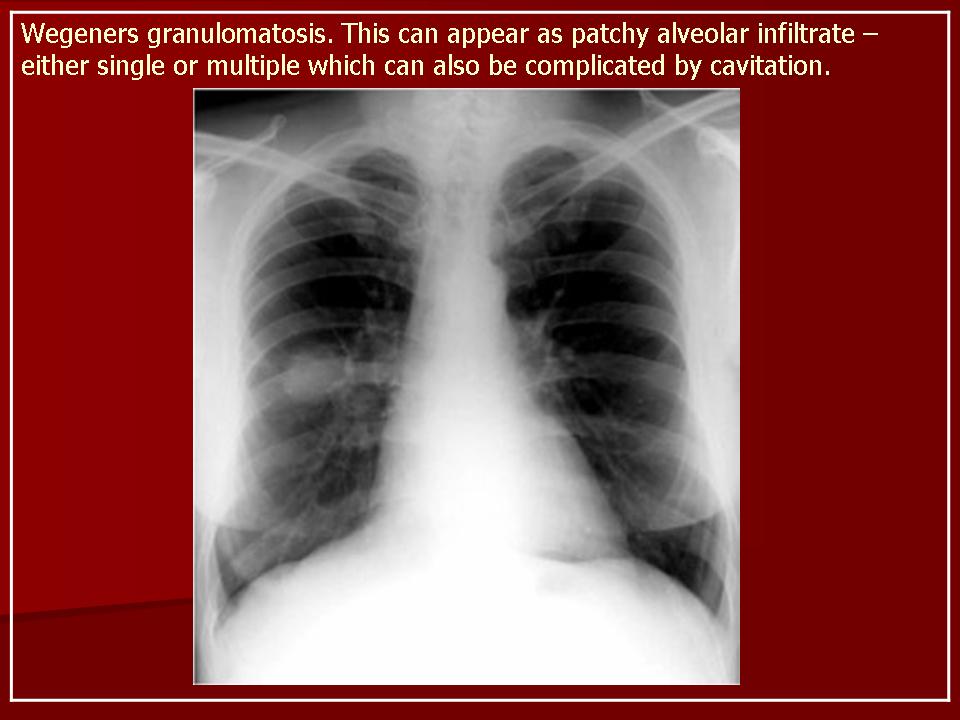
.
Дифференциальная диагностика гранулематоза Вегенера и болезни Бехчета | Голоева
1. <div><p>Алекберова 3. С. Болезнь Бехчета, М., 2007, 90с.</p><p>Насонов Е. Л., Баранов А. А., Шилкина Н. П. Васкулиты и васкулопатии. Ярославль, 1999, 321с.</p><p>Насонова В. А., Насонов Е. Л. Ревматология. М., ГЭОТАР- Медиа, 2008, 528 с.</p><p>Семенкова Е. Н. Системные некротизирующие васкулиты. М., Русский врач, 2001, 96 с.</p><p>Bacon P. The spectrum of Wegener’s granulomatosis and disease relapse. N. Engl. J. Med., 2005, 352 (4), 330-332</p><p>Chen N.t Francois A., Moguelet P. et al. Difficult diagnosis for a lingual ulceration. Wegener granulamotosis. Rev. Stomatol. Chir. Maxillofac., 2002, 103 (5), 304-306.</p><p>Glass E., Lawton L., True love E. Oral presentation of Wegener granulomatosis. J. Am. Dent. Assoc.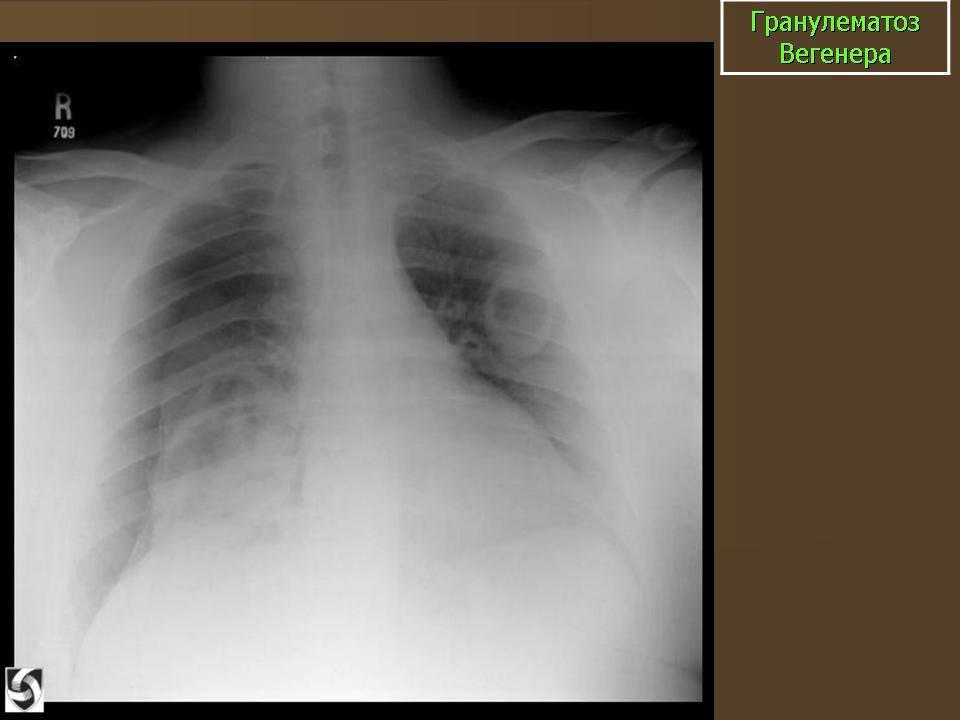 , 1990, 120(5), 523-525.</p><p>Lamprecht P., Lerin-Lozano C., Reinhold-Keller E. et al. Retinal artery occlusion in Wegener’s</p><p>Langford С., Hoffman G. Rare diseases. 3: Wegener’sgranulomatosis. Thorax, 1999, 54(7), 629-637.</p><p>Lee S., Bang D., Lee E. et al. Behcet’s disease.Textbook and Atlas. Springer, 2001, 210p.</p><p>Sakemi Т., Yoshiyuki Т., Ikeda I. et al. End-stagerenal failure due to crescentic glomerulonephritis in patients with Behcet’s syndrome. Am. J. Nephrol.,1998, 18, 321-324</p><p>Seyahi E., Melikoglu М., Akman C. et al. Pulmonaryvascular involvement in Behcet’s syndrome. Clin. Exp. Rheumat., 2006, 24, suppl. 42, 22.</p><p>Stewart C., Cohen D., Bhattacharyya I. et al. Oral manifestations of Wegener’s granulomatosis: A report of three cases and a literature review. Am. Dent.Assoc., 2007, 138, 338-348.</p><p>YaziciH, YardakulS., Hamuryudan V. etal. Behcet’s syndrome. Int. Rheumatology Third edition, 2003, 1665-1669.
, 1990, 120(5), 523-525.</p><p>Lamprecht P., Lerin-Lozano C., Reinhold-Keller E. et al. Retinal artery occlusion in Wegener’s</p><p>Langford С., Hoffman G. Rare diseases. 3: Wegener’sgranulomatosis. Thorax, 1999, 54(7), 629-637.</p><p>Lee S., Bang D., Lee E. et al. Behcet’s disease.Textbook and Atlas. Springer, 2001, 210p.</p><p>Sakemi Т., Yoshiyuki Т., Ikeda I. et al. End-stagerenal failure due to crescentic glomerulonephritis in patients with Behcet’s syndrome. Am. J. Nephrol.,1998, 18, 321-324</p><p>Seyahi E., Melikoglu М., Akman C. et al. Pulmonaryvascular involvement in Behcet’s syndrome. Clin. Exp. Rheumat., 2006, 24, suppl. 42, 22.</p><p>Stewart C., Cohen D., Bhattacharyya I. et al. Oral manifestations of Wegener’s granulomatosis: A report of three cases and a literature review. Am. Dent.Assoc., 2007, 138, 338-348.</p><p>YaziciH, YardakulS., Hamuryudan V. etal. Behcet’s syndrome. Int. Rheumatology Third edition, 2003, 1665-1669. </p></div><br />
</p></div><br />
Гранулематоз Вегенера
Гранулематоз Вегенера — аутоиммунное гранулематозное воспаление стенок сосудов (васкулит), захватывающее мелкие и средние кровеносные сосуды: капилляры, венулы, артериолы и артерии, с вовлечением верхних дыхательных путей, глаз, почек, лёгких и других органов. Относится к системным АНЦА-ассоциированным некротизирующим васкулитам.
Гранулематоз Вегенера — тяжелое быстро прогрессирующее заболевание. Без своевременно начатого лечения приводит к смертельному исходу в течение 6 — 12 мес. Подразделяется на две формы: локальную и генерализованную, которые по мнению ряда авторов являются стадиями заболевания.
При локальной форме поражаются ЛОР органы (90 % случаев) и глаза (10 % случаев) с развитием ринита, назофарингита, синусита, евстахиита, отита, склерита, эписклерита, а также увеита.
При генерализованной форме к вышеуказанным симптомам присоединяется поражение легких (80 % случаев) в виде легочного гранулематозного васкулита, обычно заканчивающегося образованием легочных гранулём. Гранулемы подвержены распаду с образованием каверн, что нередко сопровождается легочным кровотечением. У 2/3 пациентов наблюдается поражение почек в виде некротизирующего быстропрогрессирующего гломерулонефрита.
Достаточно часто гранулематоз Вегенера протекает с развитием кожного васкулита (у 40 % пациентов) и поражения периферической нервной системы (15 %) с развитием асимметричной полинейропатии. У 5 % больных описан перикардит.
Заболевание чаще всего манифестирует с поражения верхних дыхательных путей и глаз. Поражение внутренних органов обычно наступают позже.
Эпидемиология
Гранулематоз Вегенера поражает в равной степени как мужчин, так и женщин. Средний возраст заболевших составляет 40 лет.
Клиническая картина
Общие проявления
Заболевание начинается с общей слабости, пониженного аппетита и похудения. В последующем присоединяются лихорадка, артралгии и миалгии. Иногда выявляют симптомы реактивных артритов.
В последующем присоединяются лихорадка, артралгии и миалгии. Иногда выявляют симптомы реактивных артритов.
Поражение глаз
При гранулематозе Вегенера воспалительный процесс затрагивает в основном белочную и радужную оболочку глаз. Нередко развитие увеита, иридоциклита, эписклерита, склерита, приводящих к перфорации роговицы и слепоте. Возможно образование периорбитальной гранулёмы с развитием экзофтальма.
<Поражение верхних дыхательных путей, ротовой полости и органов слуха
Проявляется в виде упорного насморка с гнойно-геморрагическим отделяемым. В последующем развивается изъязвление слизистой оболочки. Возможна перфорация перегородки с развитием седловидной деформации носа. Помимо язвенно-некротического ринита возможно поражение трахеи, гортани, придаточных пазух носа, слуховых труб и ушей. Нередко возникновение язвенного стоматита. Иногда встречается резистентный к консервативному и хирургическому лечению мастоидит
<Поражение кожи
Наблюдается кожный васкулит с язвенно-геморрагическими высыпаниями.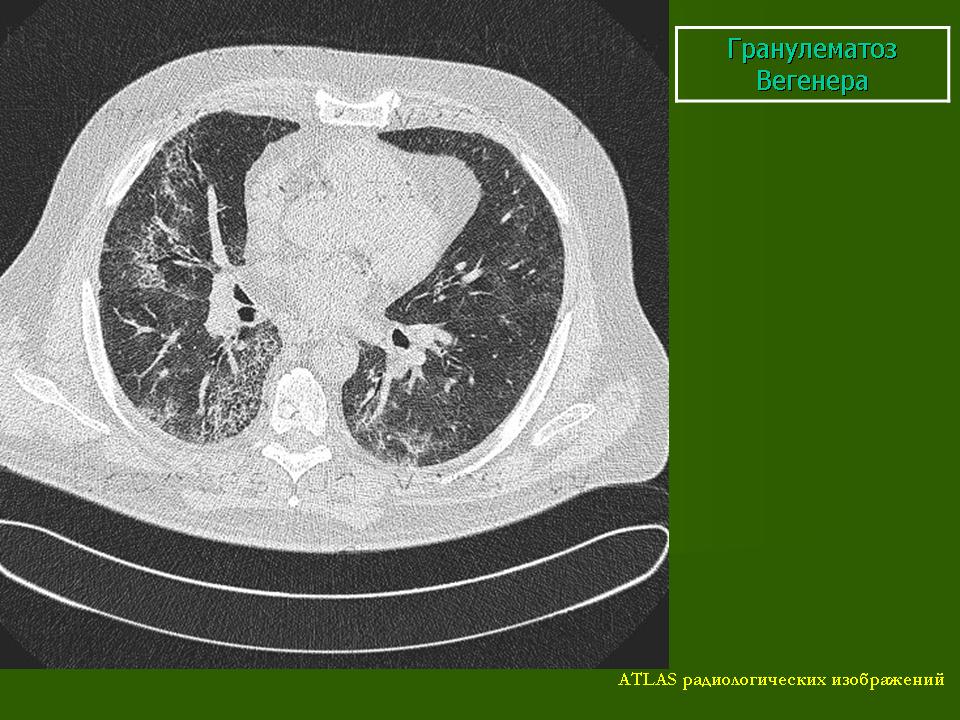
Поражение нервной системы
Протекает в виде асимметричной полинейропатии.
Поражение лёгких
В легких образуются гранулемы, нередко распадающиеся, что приводит к кровохарканию и развитию дыхательной недостаточности. У 1/3 пациентов гранулёмы клинически ничем себя не проявляют. Возможно развитие плеврита, аускультативно проявляющегося шумом трения плевры. Также может наблюдаться выпотной плеврит
Поражение почек
Одной из излюбленных локализаций гранулематоза Вегенера являются почечные клубочки. Возникающий гломерулонефрит проявляется гематурией, массивной протеинурией, нередко имеет быстро прогрессирующее течение и приводит к быстро нарастающей почечной недостаточности.
Поражение оболочек сердца
Проявляется в виде различных видов перикардита. Поражение миокарда и эндокарда нехарактерно
Диагностика
У больных с развернутой клинической картиной диагноз обычно несложен, однако в связи с разнообразием форм и вариантов течения возникают трудности на ранних стадиях заболевания. Примерно 25 % больных в начальной стадии не имеют признаков поражения легких или почек.
Примерно 25 % больных в начальной стадии не имеют признаков поражения легких или почек.
Классификационные критерии диагностики гранулематоза Вегенера
| Критерий | Определение |
| 1. Воспаление носа и полости рта | Язвы в полости рта. Гнойные или кровянистые выделения из полости носа |
| 2. Изменения при рентгенографическом исследовании лёгких | Узелки, инфильтраты или полости |
| 3. Изменения мочи | Микрогематурия (>5 эритроцитов в поле зрения) или скопления эритроцитов в осадке мочи |
| 4. Биопсия | Гранулематозное воспаление в стенке артерии или в периваскулярном и экстраваскулярном пространствах |
При наличии двух и более критериев чувствительность постановки диагноза составляет 88 %, а специфичность — 92 %. Для подтверждения диагноза определяют наличие в крови классических антинейтрофильных цитоплазматических антител (кАНЦА).
Дифференциальная диагностика
С целью правильной диагностики следует исключить заболевания, также протекающие с лёгочно-почечным синдромом: микроскопическим полиангиитом, синдромом Чарга-Стросса, узелковым периартериитом, синдромом Гудпасчера, геморрагическим васкулитом, системной красной волчанкой; редко — стрептококковой пневмоней с гломерулонефритом. Также проводят дифференциальный диагноз с другими заболеваниями: лимфоидный гранулематоз, ангиоцентрическая злокачественная лимфома, злокачественные опухоли, срединная гранулёма носа, саркоидоз, туберкулёз, бериллиоз, системные микозы, сифилис, проказа, СПИД и др. При преимущественно почечном течении дифференциальную диагностику проводят с идиопатическим быстропрогрессирующим гломерулонефритом.
Лечение
Поскольку заболевание имеет аутоиммунный генез, препаратами выбора являются иммунодепрессанты: цитостатики в сочетании с глюкокортикоидами. Из цитостатиков хорошо себя зарекомендовал циклофосфамид в дозе 2 мг/кг/сут. При поражении почек дозу повышают до 3-5 мг/кг/сут. Глюкокортикоиды назначаются в эквивалентной преднизолону дозе 1 мг/кг/сут. Хорошие результаты показала пульс-терапия циклофосфамида в дозе 1000 мг. Определённые надежды возлагаются на антицитокиновую терапию.
При поражении почек дозу повышают до 3-5 мг/кг/сут. Глюкокортикоиды назначаются в эквивалентной преднизолону дозе 1 мг/кг/сут. Хорошие результаты показала пульс-терапия циклофосфамида в дозе 1000 мг. Определённые надежды возлагаются на антицитокиновую терапию.
Прогноз
Без лечения прогноз неблагоприятен: средняя продолжительность жизни не превышает 5 мес, а летальность в течение первого года болезни составляет 80 %. При своевременно начатой терапии циклофосфамидом и глюкокортикостероидами у 93 % пациентов ремиссия длится около 4-х лет, иногда у некоторых больных — более 10 лет.
Лечение гранулематоза вегенера — стоимость приема, запись к врачу на DocDoc.ru
Лоры (отоларингологи) Москвы — последние отзывы
Владислав Олегович, спасибо! Приёмом очень осталась довольна, все подробно расспросил, весь анамнез составил, очень тщательно посмотрел, а главное очень понятно и подробно разъяснил, мне прям полегчало психологически, а это очень важно ‘разгрузиться’, когда тебе ставят разные непонятные диагнозы. .. Надеюсь, что и назначенное лечение будет таким же продуктивным!
.. Надеюсь, что и назначенное лечение будет таким же продуктивным!
На модерации,
12 марта 2021
Доктор выслушала мои жалобы, осмотрела и провела процедуру. Она так же мне прописала лекарства и всё объяснила. По моему мнению достаточно квалифицированный врач.
Вараздат,
07 марта 2021
супер-врач, четко поставила диагноз и дала все необходимые советы и рекомендации! Цена за приём тоже приемлемая.
Никита,
28 февраля 2021
Хороший и вежливый врач. Ольга Владимировна проверила меня, всё объяснила и назначила лечение. Я доволен и пойду к ней повторно!
Бактбек,
25 февраля 2021
Приятный в общении врач. Елена Юрьевна прочистила ухо и назначила мне лечение.
Елена Юрьевна прочистила ухо и назначила мне лечение.
Мария,
09 февраля 2021
Очень хороший, замечательный, профессиональный и участливый доктор. Во всех отношениях мне понравилась Татьяна Борисовна. Она очень хорошо со мной поговорила, сделала всё, что мне нужно было и помогла. Спасибо ей большое!
Нина,
19 марта 2020
Мне очень понравился приём, подход врача и как она мне все понятно разъяснила. Во многом меня успокоила. Остались самые приятные впечатления. Что самое главное, что в Клинике я не испытала чувство вымогательства, что меня хотят развести или что-то подобное. т.к. устала с этим постоянно сталкиваться, в других клиниках, и этот развод сразу чую. Я однозначно бы ещё туда вернулась. Спасибо
Во многом меня успокоила. Остались самые приятные впечатления. Что самое главное, что в Клинике я не испытала чувство вымогательства, что меня хотят развести или что-то подобное. т.к. устала с этим постоянно сталкиваться, в других клиниках, и этот развод сразу чую. Я однозначно бы ещё туда вернулась. Спасибо
На модерации,
12 марта 2021
Доктор высокопрофессиональный. Она провела качественный осмотр, доступно, на понятном языке все мне объяснила и выписала необходимые лекарства.
На модерации,
12 марта 2021
Был второй раз на приёме у данного врача. Выслушала меня, назначила препараты для лечения и посоветовала дальнейшее рекомендации по восстановлению. Рассказала из-за чего у меня обострение происходит. Плохого ничего не могу сказать.
Выслушала меня, назначила препараты для лечения и посоветовала дальнейшее рекомендации по восстановлению. Рассказала из-за чего у меня обострение происходит. Плохого ничего не могу сказать.
Хороший врач.
Аноним,
12 марта 2021
Доктор хороший, внимательный, отзывчивый, компетентный и корректный. Он провел обследование, визуальный осмотр и проконсультировал нас, по результатам анализов, по дальнейшему лечению.
На модерации,
12 марта 2021
Показать 10 отзывов из 13400
Особенности диагностики и лечения гранулематоза Вегенера Текст научной статьи по специальности «Клиническая медицина»
УДК 616.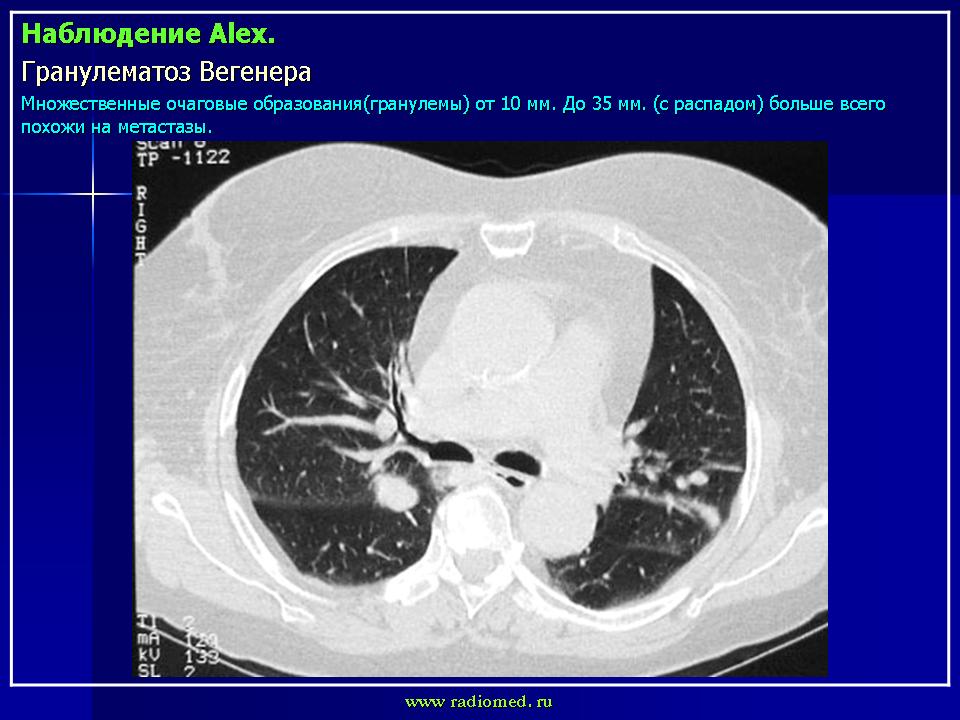 13-002:616-006.443 DOI 10.21685/2072-3032-2019-1-2
13-002:616-006.443 DOI 10.21685/2072-3032-2019-1-2
Т. М. Левина, М. Д. Романов, Е. М. Киреева
ОСОБЕННОСТИ ДИАГНОСТИКИ И ЛЕЧЕНИЯ ГРАНУЛЕМАТОЗА ВЕГЕНЕРА
Аннотация.
Актуальность и цели. Цель исследования — изучение особенностей ранней диагностики и лечения гранулематоза Вегенера (гранулематоз с полиангиитом).
Материалы и методы. Проведен анализ особенностей диагностики и лечения гранулематоза Вегенера по материалам публикаций и собственного клинического наблюдения ограниченного варианта этого заболевания, предвестником которого явилось торпидное течение рецидивирующего ринита с образованием «корочек с геморрагиями» без повышения температуры тела. Развитие пневмонии с абсцедированием на фоне других минимальных признаков (синусит, отит, боли в суставах) позволило заподозрить наличие гранулематоза Вегенера и назначить адекватную комплексную терапию, которая позволила приостановить процессы деструкции и воспаления и привела к стойкой ремиссии заболевания.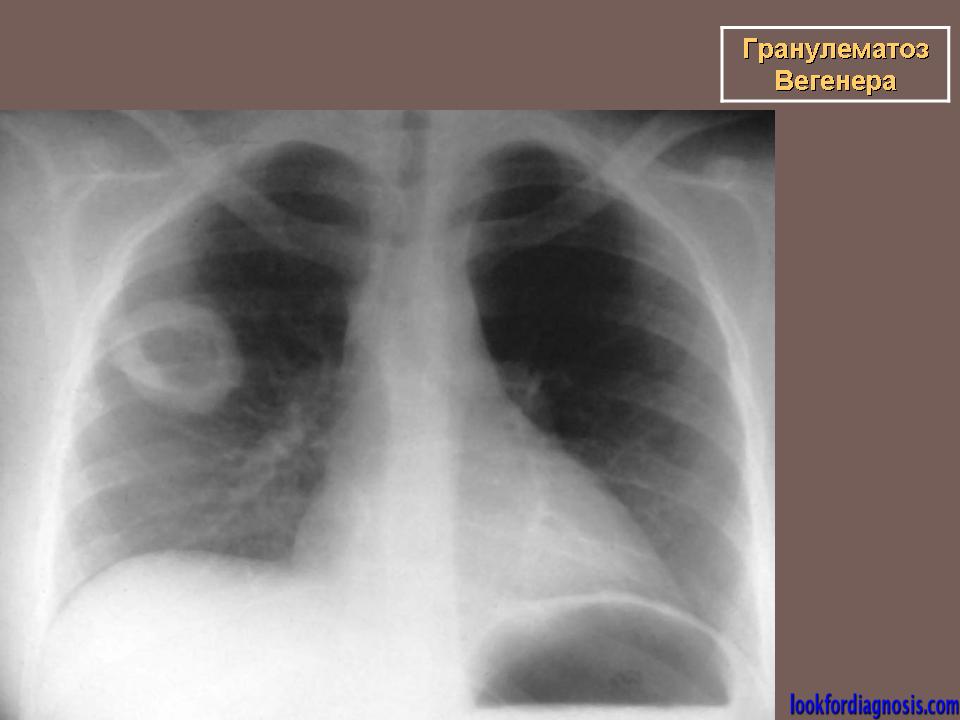
Результаты и выводы. Приведенный материал демонстрирует необходимость комплексного подхода специалистов в оценке совокупности ранних клинических признаков (синусита, отита и патологии верхних дыхательных путей и др.), характерных для этого заболевания. Раннее назначение стартовой комплексной (в том числе иммуносупрессивной) терапии ex juvantibus, направленной на предупреждение прогрессирования необратимых изменений органов, несмотря на ее нежелательные побочные эффекты, при наличии хотя бы двух диагностических критериев гранулематоза Вегенера позволит предотвратить дальнейшее драматическое развитие событий и улучшить клинические результаты и прогноз.
Ключевые слова: гранулематоз Вегенера, ранняя диагностика, иммуносу-прессивная терапия, циклофосфан, ритуксимаб.
T. M. Levina, M. D. Romanov, E. M. Kireeva
FEATURES OF DIAGNOSTICS AND TREATMENT OF VEGENER’S GRANULOMATOSIS
Abstract.
Background. The aim of the study was to study the features of early diagnosis and treatment of Wegener’s granulomatosis (granulomatosis with polyangiitis).
Materials and methods. The analysis of the features of diagnosis and treatment of Wegener’s granulomatosis (WH) based on the materials of publications and own clinical observation of a limited variant of this disease, the harbinger of which was the torpid course of recurrent rhinitis with the formation of «crusts with hemorrhages» without increasing body temperature. The development of pneumonia with abscess formation compared to other minimal signs (sinusitis, otitis media, pain in the
© Левина Т. М., Романов М. Д., Киреева Е. М., 2019. Данная статья доступна по условиям всемирной лицензии Creative Commons Attribution 4.0 International License (http://creativecommons.Org/licenses/by/4.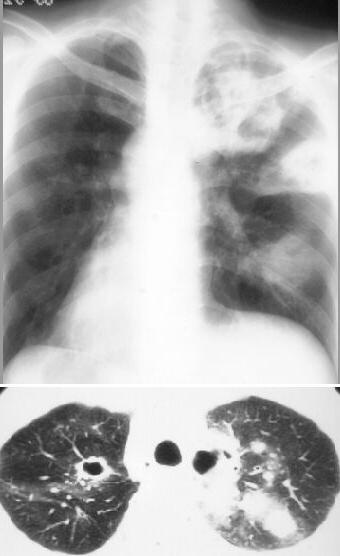 0/), которая дает разрешение на неограниченное использование, копирование на любые носители при условии указания авторства, источника и ссылки на лицензию Creative Commons, а также изменений, если таковые имеют место.
0/), которая дает разрешение на неограниченное использование, копирование на любые носители при условии указания авторства, источника и ссылки на лицензию Creative Commons, а также изменений, если таковые имеют место.
joints) allowed to suspect the presence of Wegener’s granulomatosis and adequate complex therapy, which allowed to stop the processes of destruction and inflammation, and led to a stable remission of the disease.
Results and conclusions. An analysis of the features of the diagnosis and treatment of Wegener’s granulomatosis based on publications and in the presented clinical observation demonstrates the need for an integrated approach in assessing the totality of early clinical signs (sinusitis, otitis, and upper respiratory tract pathology, etc.) characteristic of this disease. Early assignment of the starting complex (including immunosuppressive) ex juvantibus therapy aimed at preventing the progression of irreversible organ changes, despite its undesirable side effects, if at least two diagnostic criteria for WH are present, it will prevent further dramatic development of events and improve clinical results and prognosis.
Keywords: Wegener’s granulomatosis, early diagnosis, immunosuppressive therapy, cyclophosphamide, rituximab.
Введение
Гранулематоз Вегенера (ГВ) — редкое иммунологически опосредованное мультисистемное заболевание неизвестной этиологии, морфологической основой которого является гигантоклеточный гранулематозно-некротизирую-щий васкулит мелких артерий, артериол и венул с сочетанным поражением нескольких органов (преимущественно верхних дыхательных путей, органов дыхания, зрения, слуха и почек). Классическая клиническая триада ГВ включает в себя гайморит, деструктивную пневмонию и гломерулонефрит. Впервые клинику ГВ в виде варианта узелкового полиартрита описал H. Klinger в 1931 г., а в виде самостоятельного синдрома — F. Wegener в двух статьях, опубликованных в 1936 и 1939 гг. [1].
Распространенность ГВ в популяции составляет 25-60 на 1 млн, заболеваемость — 3-12 на 1 млн человек; в Европе распространенность ГВ составляет пять случаев на 100 тыс. населения, а в Северной Европе этот показатель еще выше. В европейских странах за последние 30 лет отмечен рост заболеваемости ГВ в 4 раза. Прогноз заболевания при запоздалой диагностике и отсутствии адекватного лечения всегда плохой: у 40 % больных развивается хроническая почечная недостаточность, смертность достигает 12 % [1, 2].
населения, а в Северной Европе этот показатель еще выше. В европейских странах за последние 30 лет отмечен рост заболеваемости ГВ в 4 раза. Прогноз заболевания при запоздалой диагностике и отсутствии адекватного лечения всегда плохой: у 40 % больных развивается хроническая почечная недостаточность, смертность достигает 12 % [1, 2].
Классификационные критерии ГВ были разработаны сотрудниками Американского колледжа ревматологии в 1990 г. по данным 85 пациентов при сравнении с другими формами васкулитов. Они основаны на выявлении признаков васкулита при наличии не менее двух из четырех признаков:
1. Воспаление носа с гнойными или кровянистыми выделениями и развитием в полости рта язв.
2. Выявление на рентгенограмме легких небольших узелков, фиксированных инфильтратов или полостей деструкции.
3. Обнаружение в мочевом осадке микрогематурии (>5 эритроцитов в поле зрения) или скоплений эритроцитов.
Обнаружение в мочевом осадке микрогематурии (>5 эритроцитов в поле зрения) или скоплений эритроцитов.
4. Биопсийный материал представлен в виде гранулематозного воспаления в сосудистой стенке артерий или артериол, в периваскулярной или в экстравазальной области.
Чувствительность: 88,2 %, специфичность: 92 % [3].
Иммунологическим маркером заболевания является превышение рефе-ренсных значений уровня антител к цитоплазме нейтрофилов в сыворотке
крови (ANCA) — anti-PR3 ANCA (антитела к протеиназе-3, с-ANCA) и anti-MPO ANCA (антитела к миелопероксидазе, p-ANCA), однако у 10-30 % пациентов с гистологически доказанным ГВ ANCA не определяются, что обусловлено различной степенью тяжести и активности заболевания; кроме того, данные антитела встречаются и при других формах васкулитов [2, 4]. «Золотым стандартом» в диагностике ГВ считается биопсия в органах-мишенях, в материале которых обнаруживается картина фибриноидного некроза и воспаления сосудистых стенок в сочетании с периваскулярными и экстравазаль-ными гранулемами. Диагностическая ценность биопсии пораженных структур неравноценна: информативность биопсии почек составляет 91,5 %, чувствительность трансбронхиальной биопсии легкого достигает только 12 %, а биопсия ЛОР-органов не всегда информативна [5, 6]. Кроме того, указанные процедуры являются достаточно инвазивными, сопровождаются осложнениями, а в тяжелых случаях их выполнение связано с риском для жизни.
«Золотым стандартом» в диагностике ГВ считается биопсия в органах-мишенях, в материале которых обнаруживается картина фибриноидного некроза и воспаления сосудистых стенок в сочетании с периваскулярными и экстравазаль-ными гранулемами. Диагностическая ценность биопсии пораженных структур неравноценна: информативность биопсии почек составляет 91,5 %, чувствительность трансбронхиальной биопсии легкого достигает только 12 %, а биопсия ЛОР-органов не всегда информативна [5, 6]. Кроме того, указанные процедуры являются достаточно инвазивными, сопровождаются осложнениями, а в тяжелых случаях их выполнение связано с риском для жизни.
В течении ГВ выделяют период начальных проявлений с локальными изменениями верхних дыхательных путей, среднего уха или глаз; период генерализации с системным поражением внутренних органов и терминальный период, в котором происходят развитие и прогрессирование почечной или сердечно-легочной недостаточности. В течении заболевания зафиксированы три клинических варианта: локальный, с поражением верхних дыхательных путей, глаз, кожи, мышц и суставов; ограниченный, в котором к локальным проявлениям присоединяются гипертермия и поражение легких; при генерализованном варианте наблюдается системное поражение практически всех органов и систем [2].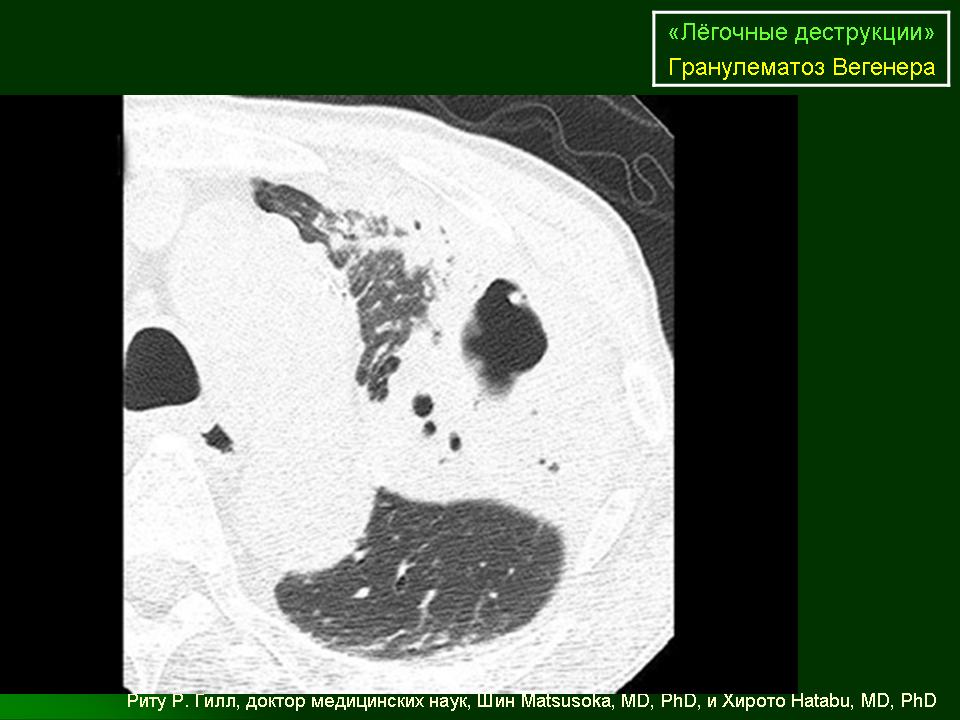
Диагностика ГВ при наличии характерных клинических, гистологических и лабораторных признаков воспаления не представляет особых затруднений, лишь в дебюте и при подострой форме заболевания с отсутствием классических сочетаний клинических проявлений возникает необходимость в дифференциальной диагностике с другими васкулитами, протекающими с легочно-почечным синдромом, а также со злокачественными опухолями, саркоидозом, туберкулезом, системными микозами, сифилисом, СПИД и др. [7-9]. Клиническая картина ГВ также довольно часто бывает скрыта под разными масками, запоздалая диагностика при этом сопровождается неудовлетворительными результатами лечения.
Ранняя диагностика особенно важна до развития патологии почек. Стартовыми предикторами вовлечения почек в патологический процесс являются микрогематурия, протеинурия и гипопротеинемия, которые наблюдаются примерно у 20 % пациентов в дебюте заболевания; повреждение почек значительно возрастает (до 80 %) при прогрессировании ГВ и в значительной мере определяет неблагоприятный прогноз [2, 10].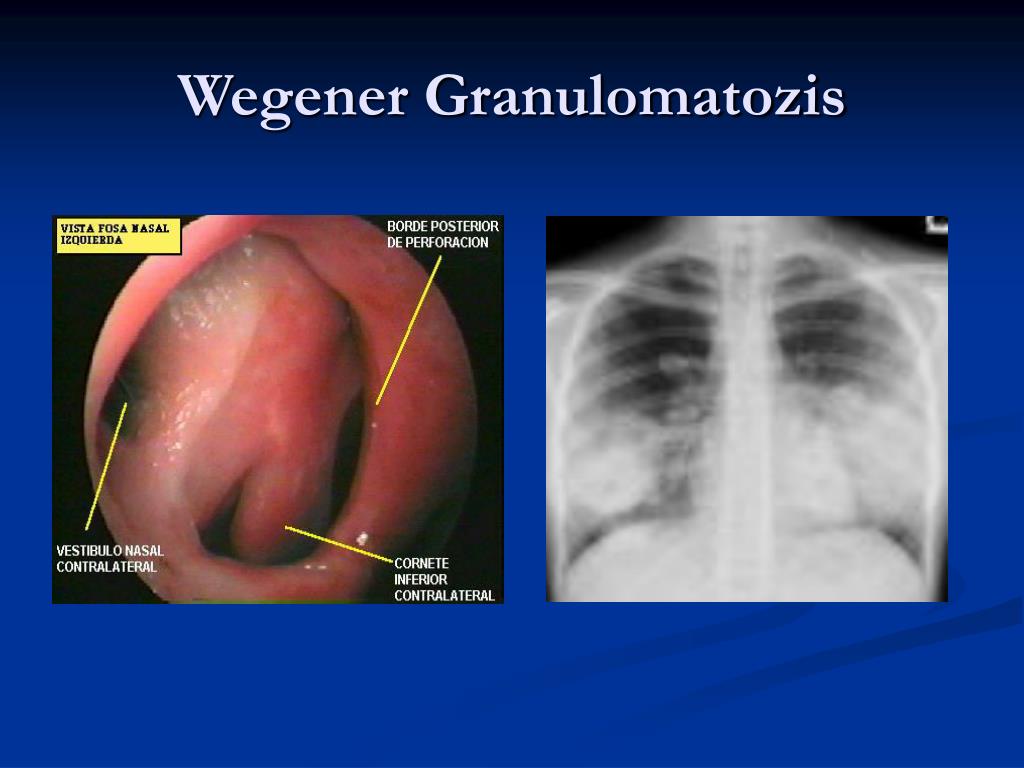
Основу лечения ГВ составляет иммуносупрессивная терапия (глюко-кортикоидные гормоны, циклофосфамид, ритуксимаб и др.), препараты про-стагландинов, низкомолекулярные гепарины и др.; по показаниям применяют плазмаферез и другие методы детоксикации и эфферентной терапии. Выбор препаратов и схем лечения зависит от клинической формы и стадии заболевания, активности процесса, состояния организма и эффективности комплексной терапии [2]. Мы солидарны с мнением K. Westman (2015) о том, что
интенсивность иммуносупрессии, с одной стороны, должна адекватно купировать проявления болезни, предупреждать развитие осложнений и обеспечивать стойкость ремиссии и, с другой стороны, не провоцировать развития инфекционных осложнений [11], особенно при прогрессировании деструктивных процессов в легких, обусловленных высоковирулентной неспецифической и анаэробной неклостридиальной микрофлорой, и других возможных последствий данной терапии из-за побочного действия препаратов.
Цель исследования: изучение особенностей ранней диагностики и лечения гранулематоза Вегенера (гранулематоза с полиангиитом).
Для иллюстрации особенностей диагностики и лечебной тактики при ограниченном варианте ГВ приводим клиническое наблюдение.
Клиническое наблюдение
Больная Б., 32 года, в течение 5 лет наблюдалась у отоларинголога по поводу хронического рецидивирующего ринита с образованием «корочек с геморрагиями» без повышения температуры тела. Ухудшение отмечает после переохлаждения в июле 2017 г., когда на фоне беременности была пунктирована гайморова пазуха, после чего, со слов больной, развилась седловидная деформация спинки носа. Больная в течение 12 лет работает на газовой АЗС. В детстве перенесла корь, ветряную оспу; пароксизмальная наджелу-дочковая тахикардия возникла после беременности 3 года тому назад.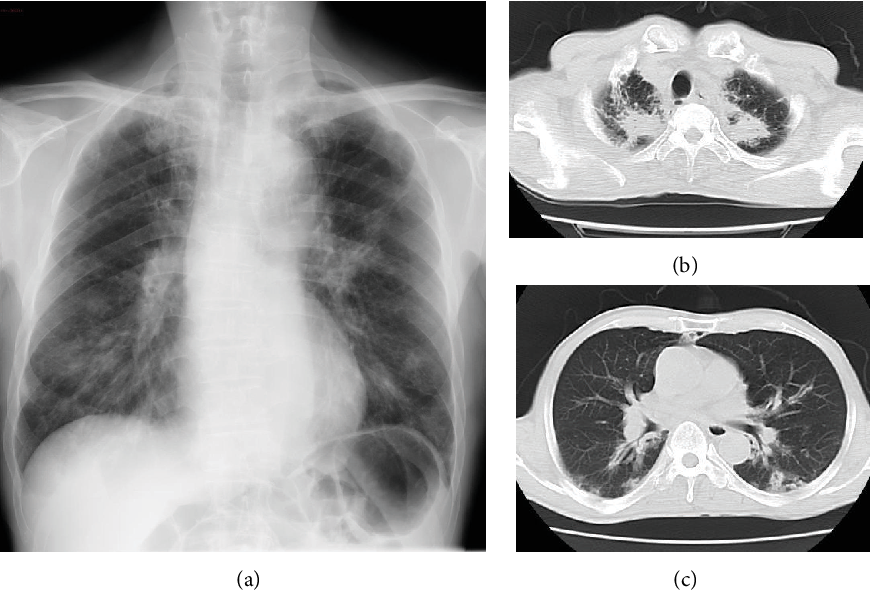 15.09.2017 — срочные роды путем кесарева сечения.
15.09.2017 — срочные роды путем кесарева сечения.
18.10.2017 появились боли в ушах, заложенность носа, боли в суставах, повысилась температура тела до 38 °С. На рентгенограммах (рис. 1) органов грудной клетки от 18.10.2017 установлена картина правосторонней верхнедолевой пневмонии с формированием полости деструкции в 82, лимфаденопатия средостения.
Рис. 1. Рентгенограмма органов грудной клетки в прямой и правой боковой проекциях от 18.10.2017. Полость деструкции в 82 на фоне инфильтрации легочной ткани в верхней доле правого легкого
Госпитализирована по поводу абсцедирующей пневмонии правого легкого, двустороннего отита и мастоидита в терапевтическое отделение ГБУЗ РМ «Республиканская клиническая больница» № 3; где были назначены в суточной дозировке цефтриаксон, амикацин, метрогил. Осмотрена ревматологом, заподозрен гранулематоз Вегенера, к лечению добавлен дексаметазон 8 мг/сут.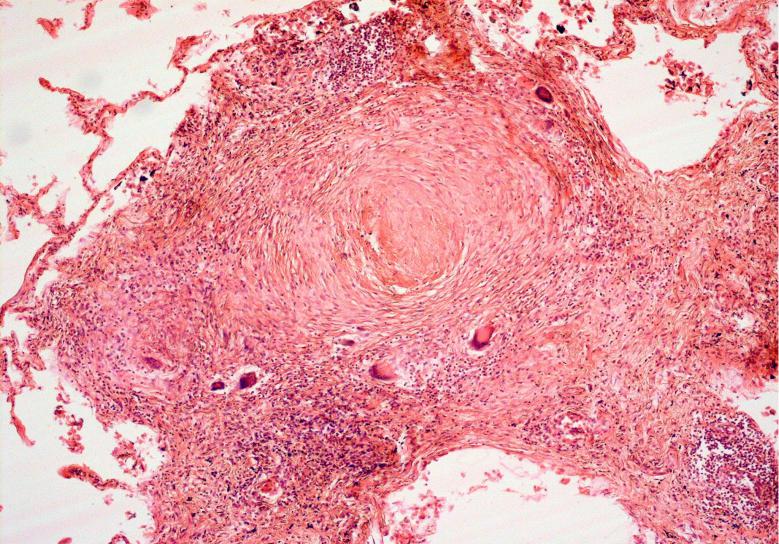 внутривенно капельно, на фоне которого температура тела снизилась, уменьшились боли в суставах.
внутривенно капельно, на фоне которого температура тела снизилась, уменьшились боли в суставах.
Анализ крови от 18.10.2017: гемоглобин — 106 г/л, эритроциты -3,92 • 10 /л, тромбоциты — 247 • 107л, гематокрит -31%, лейкоциты -14,2 • 109/л, эозинофилы — 2, с/я нейтрофилы — 74, лимфоциты — 22, моноциты — 2 %, скорость оседания эритроцитов (СОЭ) — 66 мм/ч. Маркеры вирусного гепатита и анализ крови на ВИЧ — отрицательные. Креатинин -0,062 ммоль/л, мочевина — 3,7 ммоль/л, глюкоза — 5,5 ммоль/л, билирубин (непрямой) — 17,0 ммоль/л. В анализе мочи белка нет, уд. вес — 1030, эритроциты, лейкоциты, эпителий — 0-1 в поле зрения.
29.10.2017: снова повысилась температура тела до 39 °С. Назначены: кламосар 1,2 внутривенно 3 раза в сутки, лефлобакт по 0,5 2 раза в сутки, ке-торолак, диклофенак 75 мг внутримышечно № 3, далее ибуклин 0,725 2 раза в сутки, метронидазол 1,5 в сутки внутривенно капельно, омепразол 0,02, бронхорус 0,03 3 раза в сутки.
В связи с ухудшением состояния 31.10.2017 переведена в отделение торакальной хирургии ГБУЗ РМ «Республиканская клиническая больница» № 4 с диагнозом «Внегоспитальная правосторонняя верхнедолевая пневмония, тяжелое течение». При поступлении состояние средней тяжести, кожные покровы бледные, на нижних конечностях имеются множественные геморрагические высыпания, выступающие над поверхностью кожи. При осмотре обращает на себя внимание седловидная деформация спинки носа, энантема твердого неба. Язык сухой, единичные геморрагии. Отмечается снижение слуха (шепотная речь — 3 м). Резкая болезненность при пальпации суставов кистей, плечевых, коленных и голеностопных суставов, ограничение в них пассивных и активных движений, пастозность голеней. Пальпация грудной клетки безболезненна. При перкуссии отмечается притупление над верхней долей правого легкого, при аускультации выслушивается жесткое дыхание, ослабленное над верхней долей правого легкого, здесь же выслушиваются мелко- и среднепузырчатые влажные хрипы, над нижней долей правого легкого — единичные сухие жужжащие хрипы.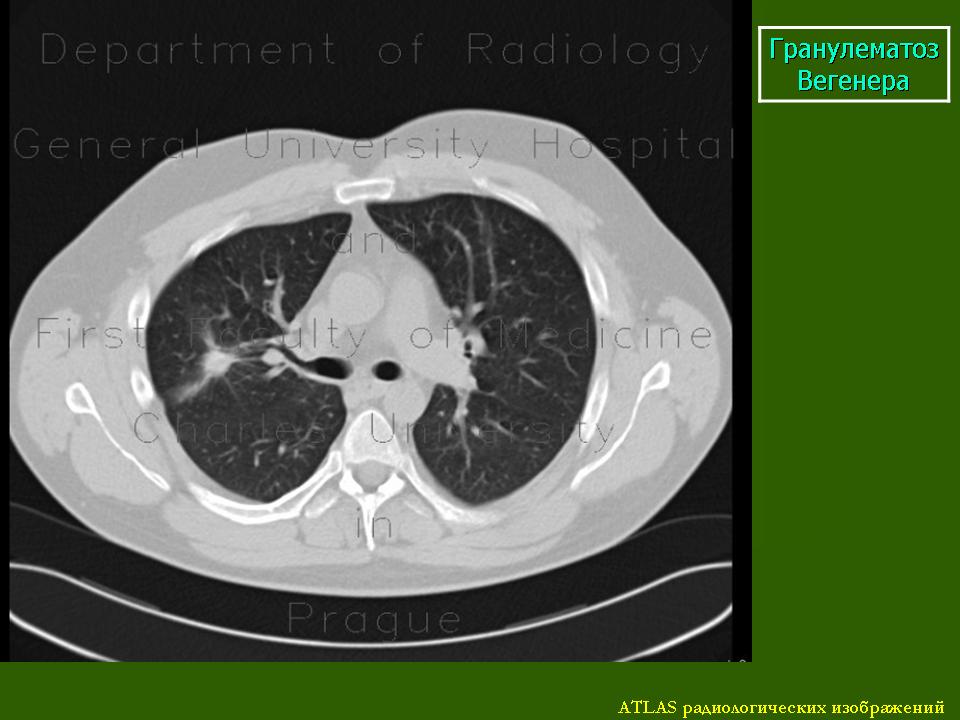 Тоны сердца приглушены, ритм сердечных сокращений правильный. Пульс — 76 уд./мин. Частота дыхания -17 в 1 мин. SpO2 — 97 %. Живот мягкий, умеренно болезнен в правом подреберье, печень выступает из-под края реберной дуги на 1 см. Пальпация почек безболезненна.
Тоны сердца приглушены, ритм сердечных сокращений правильный. Пульс — 76 уд./мин. Частота дыхания -17 в 1 мин. SpO2 — 97 %. Живот мягкий, умеренно болезнен в правом подреберье, печень выступает из-под края реберной дуги на 1 см. Пальпация почек безболезненна.
В анализе крови от 01.11.2017: гемоглобин — 80 г/л, гематокрит — 25 %, СОЭ — 34 мм/ч; эритроциты — 3,1 • 10/л, тромбоциты — 310 • 109/л, лейкоциты — 8,8 • 109/л, нейтрофилы — 72, лимфоциты -25 и моноциты -3 %. 01.11.2017 при бактериологическом исследовании крови роста аэробных бактерий не обнаружено. 01.11.2017 в биохимическом анализе крови: креатинин -0,069 ммоль/л, мочевина — 2,42 ммоль/л, глюкоза — 5,08 ммоль/л, билирубин (непрямой) — 5,23, (прямой) — 2,62 ммоль/л, АсАТ — 36,6 u/l, АлАТ — 24,1 u/l, серомукоид — 1,2, С-реактивный белок — 60 мг/л. Альбумины — 31,37 %, а1 —
6,46, а2 — 15,29, ß — 13,13, у — 33,75 %. Общий белок — 77 г/л, А/Г — 0,46.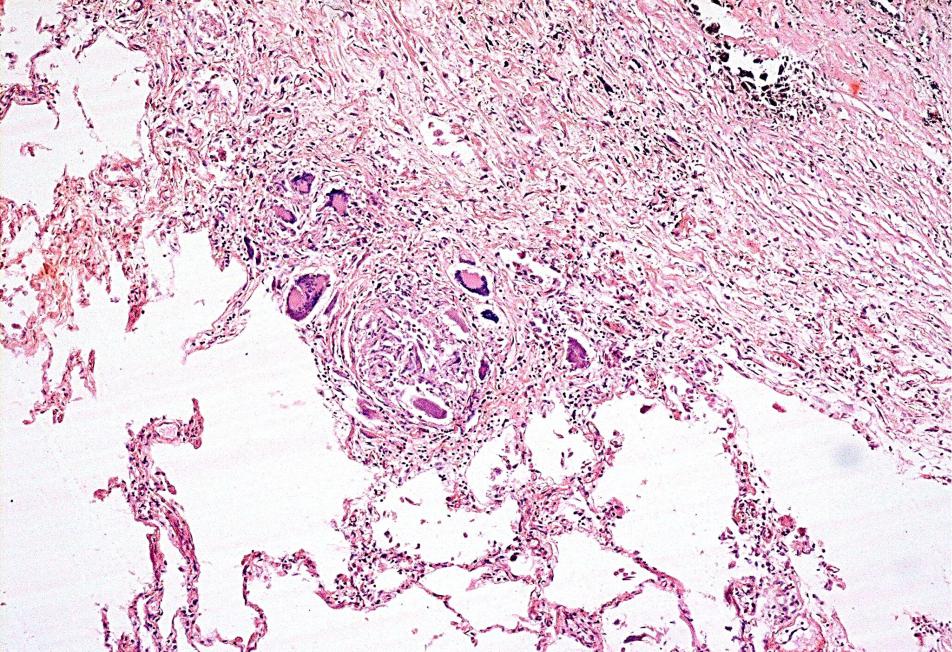 В анализе мочи белка нет, уд. вес — 1012, эритроциты, лейкоциты, эпителий -0-1 в поле зрения, ураты (++), белок Бенс-Джонса отсутствует.
В анализе мочи белка нет, уд. вес — 1012, эритроциты, лейкоциты, эпителий -0-1 в поле зрения, ураты (++), белок Бенс-Джонса отсутствует.
В мокроте 01.11.2017 выделены Str. haemolyticus 105 КОЕ/мл. чувствительны к ванкомицину, клиндамицину, кларитромицину; устойчивы к офлок-сацину, цефтиазидину. В материале, полученном при биопсии слизистой носовой перегородки, обнаружены нейтрофилы, эозинофилы, лимфоциты, гистиоциты, плазмоциты и единичные гигантские многоядерные клетки типа Пирогова — Лангханса, расположенные вокруг участка некроза.
На ЭКГ 01.11.2017: Синусовый ритм с частотой сердечных сокращений (ЧСС) = 98 уд./мин. Нормальное положение ЭОС. ЭхоКС 03.11.2017: камеры сердца не расширены, систолическая функция левого желудочка удовлетворительная. Фракция выброса — 69 %. СДЛА — 25 мм рт.ст. Фибробронхоско-пия 01.11.2017: слизистая бронхов бледно-розовой окраски с участками пятнистой гиперемии, на слизистой левого главного бронха и угла карины единичные острые эрозии с налетом фибрина и слизи, в долевых бронхах левого легкого — синяя пигментация, в устье S2 правого легкого скопление гнойной мокроты в виде пробки, слизистая отечная, просвет бронха сужен.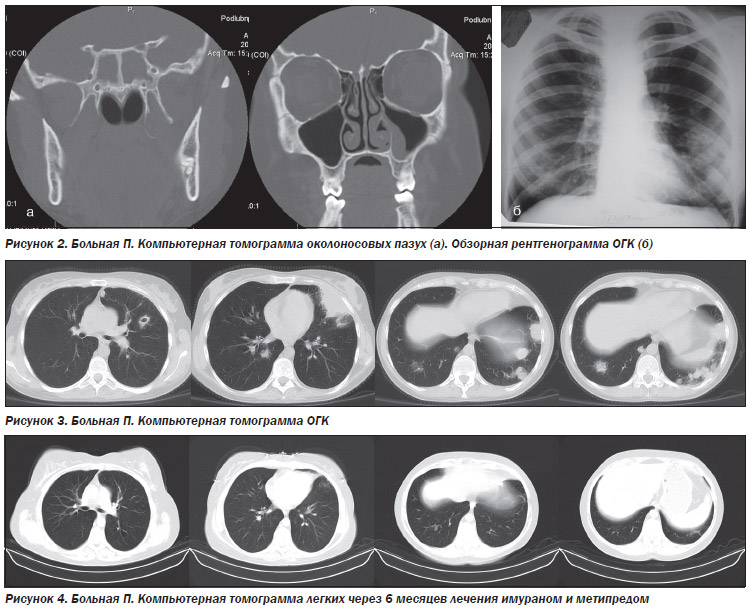
Получала сумамед 500 мг внутривенно капельно 2 раза в сутки, реопо-лиглюкин 10 % 200 мл внутривенно капельно ежедневно. В 10 ч 02.11.2017 появились боли в левой половине грудной клетки, сердцебиение, слабость, артериальное давление (АД) снизилось до 90 и 60 мм рт.ст.; на ЭКГ зафиксированы признаки наджелудочковой тахикардии с ЧСС = 150 уд./мин. Нарушение ритма купировано внутривенной инфузией амиодарона. На ЭхоКГ 03.11.2017 — без патологии.
03.11.2017 возобновились боли в плечевых, локтевых, голеностопных суставах, появилась сгибательная контрактура левого локтевого сустава. Движения в суставах ограниченны, болезненны. Установлен диагноз: Грану-лематоз Вегенера с поражением верхних дыхательных путей (ринит), органа слуха (двусторонний отит), легких (множественные двусторонние инфильтраты, полости распада в верхней доле правого легкого), гематологическим синдромом, поражением суставов (полиартрит) и геморрагическим васкули-том.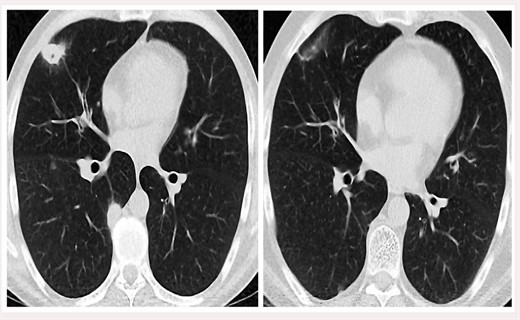 Пароксизм наджелудочковой тахикардии. 06.11.2017 антитела к натив-ной и денатурированной ДНК не обнаружены, антитела к миелопероксидазе кл. pANCA — 3,0 Ед/мл, антитела к нуклеосомам кл. cANCA -1,8 Ед/мл. К лечению добавлены меропенем 1,0 внутривенно капельно 3 раза в сутки. Декс-аметазон 4 % 2 мл и диклофенак 1,5 % 3 мл внутривенно капельно.
Пароксизм наджелудочковой тахикардии. 06.11.2017 антитела к натив-ной и денатурированной ДНК не обнаружены, антитела к миелопероксидазе кл. pANCA — 3,0 Ед/мл, антитела к нуклеосомам кл. cANCA -1,8 Ед/мл. К лечению добавлены меропенем 1,0 внутривенно капельно 3 раза в сутки. Декс-аметазон 4 % 2 мл и диклофенак 1,5 % 3 мл внутривенно капельно.
07.11.2017 на контрольных рентгенограммах грудной клетки определяется отрицательная динамика: интенсивное негомогенное затенение верхней доли, S6 и Si0 правого легкого за счет инфильтрации легочной ткани с наличием на этом фоне неправильной формы сливающихся полостей в S1 и S2. Левое легкое — без патологии (рис. 2). При УЗИ органов брюшной полости и за-брюшинного пространства 08.11.2017 патологии не обнаружено.
На мультиспиральной компьютерной томографии грудной клетки 09.10.2017 выявлено увеличение зон инфильтрации по всем легочным полям, преимущественно в верхней доле левого легкого с образованием трех полостей. Бронхи проходимы. Увеличение лимфатических узлов в корнях легких. Жидкости в плевральной полости не выявлено.
Бронхи проходимы. Увеличение лимфатических узлов в корнях легких. Жидкости в плевральной полости не выявлено.
Рис. 2. Рентгенограмма органов грудной клетки в прямой и правой боковой проекциях от 07.11.2017: интенсивное негомогенное затенение верхней доли,
86 и Б10 правого легкого за счет инфильтрации легочной ткани с наличием на этом фоне неправильной формы сливающихся полостей в Б1 и 82
09.11.2017 к лечению с иммуносупрессивной целью назначены пульс-терапия метипредом в дозе 1000 мг внутривенно капельно в течение 3 дней, циклофосфан 600 мг внутривенно капельно во второй день пульс-терапии, нимесулид 100 мг 2 раза в день, омепразол 20 мг 2 раза в день, затем после проведения пульс-терапии преднизолон в дозе 1 мг/кг массы тела.
10.11.2017 переведена в ревматологическое отделение для продолжения специфической терапии в ГБУЗ РМ «Республиканская клиническая больница», где после завершения полного курса лечения выписана под наблюдение ревматолога с выраженной положительной динамикой. В стационаре по месту жительства получала циклофосфан по 1000 мг № 6 каждые 3 недели и преднизолон по схеме. 12.04.2018 была госпитализирована для индукции ремиссии с помощью ритуксимаба 1000 мг внутривенно однократно; лечение с положительным эффектом.
В стационаре по месту жительства получала циклофосфан по 1000 мг № 6 каждые 3 недели и преднизолон по схеме. 12.04.2018 была госпитализирована для индукции ремиссии с помощью ритуксимаба 1000 мг внутривенно однократно; лечение с положительным эффектом.
При МСКТ органов грудной клетки 09.10.2018 признаков активного воспаления и деструкции в легких не определяется. В 81 82 правого легкого определяется тонкостенная полость без содержимого размерами 32*40*21 мм, вокруг полости определяются участки пневмофиброза с округлыми кальци-натами и деформированными мелкими бронхами (рис. 3). Апикальная плевра уплотнена, деформирована плевральными швартами. Лимфатические узлы прикорневой зоны и средостения не увеличены; диафрагма, средостение и перикард без особенностей.
Больная госпитализирована 10.11.2018 в ревматологическое отделение для повторного введения ритуксимаба. При осмотре предъявляет жалобы на сердцебиение и одышку при физической нагрузке; носовое дыхание восстановилось полностью, боли в коленных суставах беспокоят только при большой физической нагрузке.63 мм, контуры почек четкие, ровные, чашеч-но-лоханочная система уплотнена, без деформации, толщина паренхимы на полюсах 14 мм, в средней части 18 мм, конкрементов нет. Печень, поджелудочная железа без патологии, лимфатические узлы основных групп не увеличены.
Рис. 3. МСКТ органов грудной клетки от 09.10.2018. В Б1 82 правого легкого тонкостенная полость без содержимого размерами 32*40*21 мм, вокруг полости участки пневмофиброза с кальцинатами и деформированными мелкими бронхами
В анализе крови от 10.11.2018: гемоглобин — 112 г/л, СОЭ — 20 мм/ч; эритроциты — 4,3 • 10 /л, тромбоциты — 290 • 109/л, лейкоциты — 5,8 • 10 /л, эозинофилы — 3, нейтрофилы — 68, лимфоциты — 24 и моноциты — 5 %. В биохимическом анализе крови: креатинин — 0,08 ммоль/л, мочевина -5,3 ммоль/л, билирубин (непрямой) — 11,5 ммоль/л, АсАТ — 52 и/1, АлАТ -120 и/1, общий белок — 72 г/л. В анализе мочи белка нет, уд. вес — 1018, эритроциты, лейкоциты, эпителий — 0-1 в поле зрения.
Обсуждение
Приведенный клинический случай примечателен тем, что сочетание патологии верхних и нижних дыхательных путей, органов слуха даже при отсутствии иммунологических маркеров (антитела к протеиназе-3 и к миело-пероксидазе в цитоплазме нейтрофилов) и изменений со стороны почек, поз-
волило констатировать дебют ГВ и назначить специфическую иммуносу-прессивную терапию, которая привела к значительному улучшению состояния и стойкой ремиссии. Указанные иммунологические маркеры не являются абсолютно специфичными и чувствительными [7].
В Европейских (EULAR/ERA-EDTA) рекомендациях по диагностике и лечению системных васкулитов, ассоциированных с антинейтрофильными цитоплазматическими антителами для подтверждения диагноза как в дебюте, так и при рецидиве заболевания рекомендуется выявление гистологических признаков васкулита. Выполнение открытой биопсии легкого у пациентов, находящихся в тяжелом состоянии, сопряжено с неблагоприятными последствиями торакотомии и развитием интра- и послеоперационных осложнений; использование видеоторакоскопических технологий в данном случае также не было показано из-за необходимости однолегочной вентиляции. Биопсия почек при отсутствии клинических, ультразвуковых, лабораторных и биохимических признаков их поражения из-за риска развития осложнений (кровотечение и др.) в данном клиническом случае нами также признана нецелесообразной.
В то же время типичная клиническая картина с системным поражением органов и систем, характерных для ГВ при отсутствии признаков поражения мочевыделительной системы, позволила установить верный диагноз, правомерность которого была подтверждена результатами лечения ex juvantibus, что согласуется с рекомендациями EULAR/ERA-EDTA по диагностике и лечению АНЦА-ассоциированных системных васкулитов [6]. Кроме того, в микропрепаратах из материалов, полученных при биопсии слизистой носовой перегородки, были обнаружены гигантские многоядерные клетки типа Пирогова — Лангханса, расположенные вокруг участка некроза, что характерно для гранулематоза с полиангиитом.
Наличие хронического рецидивирующего ринита в течение 5 лет и нерациональный прием антибиотиков при его обострениях, длительное воздействие неблагоприятного производственного фактора (работа на газовой АЗС) в данном наблюдении могли послужить основой для развития данного заболевания. A. Greco et al. (2016) в дебюте ГВ в большинстве случаев наблюдали клинические признаки среднего отита при недостаточной эффективности длительной антибактериальной терапии [1]. В роли триггеров могут выступать также острые респираторные вирусные инфекции, хроническая очаговая носоглоточная бактериальная инфекция.
Заключение
Объективный анализ сочетания минимальных клинических признаков начальной стадии заболевания при появлении немотивированного другими причинами сухого кашля и одышки при физической нагрузке, при скудной аускультативной картине и отсутствии рентгенологических признаков со стороны легких позволяют с высоким уровнем достоверности предположить наличие ГВ. Одновременное выявление признаков патологии верхних дыхательных путей, синусита, отита у пациентов, резистентных к антибактериальной терапии должно побуждать врачей различных специальностей (терапевтов, врачей общей практики, отоларингологов, ревматологов, офтальмологов, пульмонологов, торакальных хирургов и др.) к целенаправленному диагно-
стическому поиску других признаков ГВ, в том числе гистологических и иммунологических маркеров.
Своевременное выявление ранних признаков ограниченного варианта ГВ и назначение комплексной иммуносупрессивной терапии, направленной на предупреждение прогрессирования необратимых изменений органов, имеют решающее значение для исхода заболевания. Раннее назначение стартовой комплексной терапии ex juvantibus, несмотря на ее нежелательные побочные эффекты, при прогрессировании заболевания с наличием хотя бы двух диагностических критериев ГВ, позволит предотвратить дальнейшее драматическое развитие событий и улучшить клинические результаты и прогноз.
Библиографический список
1. Clinic manifestations in granulomatosis with polyangiitis / A. Greco, C. Marinelli, M. Fusconi, G. F. Macri, A. Gallo, A. De Virgilio, G. Zambettii and M. de Vincentiis // International Journal of Immunopathology and Pharmacology. — 2016. — Vol. 29, № 2. — P. 151-159. — DOI 10.1177/0394632015617063.
2. Гранулематоз Вегенера / А. А. Баранов, Е. И. Алексеева, С. И. Валиева, Т. М. Бза-рова, Г. А. Лыскина, В. Г. Часнык, М. М. Костик // Клинические рекомендации МЗ РФ. — Москва : МЗ РФ, 2017. — 73 с.
3. The American College of Rheumatology 1990 criteria for the classification of Wegener’s granulomatosis / R. Y. Leavitt, A. S. Fauci, D. A. Bloch, B. A. Michel, G. G. Hunder, W. P. Arend, L. H. Calabrese, J. F. Fries, J. T. Lie, R. W. Lightfoot, A. T. Masi, D. J. Mcshane, J. A. Mills, M. B. Stevens, S. L. Wallace and N. J. Zvaifler // Arthr. Rheum. — 1990. — Vol. 33. — P. 1101-1107.
4. Румянцев, А. Г. Лечение васкулитов, ассоциированных с антинейтрофиль-ными цитоплазматическими антителами / А. Г. Румянцев // Вопросы гематологии/онкологии и иммунопатологии в педиатрии. — 2016. — № 2. — С. 6-14. — DOI 10.20953/1726-1708-2016-2-5-13.
5. Бекетова, Т. В. Европейские (EULAR/ERA-EDTA) рекомендации по диагностике и лечению АНЦА-ассоциированных системных васкулитов — 2016 / Т. В. Бекетова // Научно-практическая ревматология. — 2017. — Т. 55, № 1. -С. 12-16.
6. EULAR/ERA-EDTA recommendations for the management of ANCA-associated vas-culitis / M. Yates, R. A. Watts, I. M. Bajema, M. C. Cid, B. Crestani, T. Hauser,
B. Hellmich, J. U. Holle, M. Laudien, M. A. Little, R. A. Luqmani, A. Mahr, P. A. Merkel, J. Mills, J. Mooney, M. Segelmark, V. Tesar, K. Westman, A. Vaglio, N. Yalgindag, D. R. Jayne and C. Mukhtyar // Ann. Rheum. Dis. — 2016. — Vol. 75. -P. 1583-1594. — DOI 10.1136/annrheumdis-2016-209133 originally published online June 23, 2016.
7. Моисеев, С. В. АНЦА-ассоциированные васкулиты: спорные вопросы классификации, диагностики и оценки активности и современные подходы к лечению /
C. В. Моисеев, П. И. Новиков, А. Д. Мешков, Л. В. Иваницкий // Клиническая фармакология и терапия. — 2014. — Т. 23, № 1. — С. 44-50.
8. Крутько, В. С. Гранулематоз Вегенера (распространенность, причина, диагностика, собственные наблюдения) / В. С. Крутько, П. И. Потейко, Э. М. Ходош // Новости медицины и фармации. Пульмонология. Аллергология. Антимикробная терапия. — 2015. — № 1 (530). — С. 63-72.
9. Ходош, Э. М. Гранулематоз с полиангиитом (Вегенера) и системные васкулиты: многосторонний взгляд на проблему (обзор литературы) / Э. М. Ходош, В. С. Крутько, О. А. Ефремова // Научные ведомости Белгородского государ-
ственного университета. Сер.: Медицина. Фармация. — 2017. — № 19 (268), вып. 39. — С. 40-53.
10. Lutalo, P. M. Diagnosis and classification of granulomatosis with polyangiitis (aka Wegener’s granulomatosis) / P. M. Lutalo, D. P. D’Cruz // J. Autoimmun. — 2014. -Vol. 48-49. — P. 94-98.
11. Westman, K. The long-term outcomes of systemic vasculitis / K. Westman, O. Flossmann and G. Gregorini // Nephrol. Dial. Transplant. — 2015. — Vol. 30. — P. 6066. — DOI 10.1093/ndt/gfu392.
References
1. Greco A., Marinelli C., Fusconi M., Macri G. F., Gallo A., De Virgilio A., Zambetti1 G. and de Vincentiis M. International Journal of Immunopathology and Pharmacology. 2016, vol. 29, no. 2, pp. 151-159. DOI 10.1177/0394632015617063.
2. Baranov A. A., Alekseeva E. I., Valieva S. I., Bzarova T. M., Lyskina G. A., Chasnyk V. G., Kostik M. M. Klinicheskie rekomendatsii MZ RF [Clinical recommendations of the Ministry of Health of the Russian Federation]. Moscow: MZ RF, 2017, 73 p. [In Russian]
3. Leavitt R. Y., Fauci A. S., Bloch D. A., Michel B. A., Hunder G. G., Arend W. P., Cal-abrese L. H., Fries J. F., Lie J. T., Lightfoot R. W., Masi A. T., Mcshane D. J., Mills J. A., Stevens M. B., Wallace S. L. and Zvaifler N. J. Arthr. Rheum. 1990, vol. 33, pp. 1101-1107.
4. Rumyantsev A. G. Voprosy gematologii/onkologii i immunopatologii v pediatrii [He-matology/oncology and immunopathology in pediatrics]. 2016, no. 2, pp. 6-14. DOI 10.20953/1726-1708-2016-2-5-13. [In Russian]
5. Beketova T. V. Nauchno-prakticheskaya revmatologiya [Scientific and practical rheumatology]. 2017, vol. 55, no. 1, pp. 12-16. [In Russian]
6. Yates M., Watts R. A., Bajema I. M., Cid M. C., Crestani B., Hauser T., Hellmich B., Holle J. U., Laudien M., Little M. A., Luqmani R. A., Mahr A., Merkel P. A., Mills J., Mooney J., Segelmark M., Tesar V., Westman K., Vaglio A., Yalgindag N., Jayne D. R. and Mukhtyar C. Ann. Rheum. Dis. 2016, vol. 75, pp. 1583-1594. DOI 10.1136/annrheumdis-2016-209133 originally published online June 23, 2016.
7. Moiseev S. V., Novikov P. I., Meshkov A. D., Ivanitskiy L. V. Klinicheskaya farma-kologiya i terapiya [Clinical pharmacy and therapy]. 2014, vol. 23, no. 1, pp. 44-50. [In Russian]
8. Krut’ko V. S., Poteyko P. I., Khodosh E. M. Novosti meditsiny i farmatsii. Pul’mon-ologiya. Allergologiya. Antimikrobnaya terapiya [News of medicine and pharmacy. Pulmonology. Allergology. Antimicrobial therapy]. 2015, no. 1 (530), pp. 63-72. [In Russian]
9. Khodosh, E. M., Krut’ko V. S., Efremova O. A. Nauchnye vedomosti Belgorodskogo gosudar-stvennogo universiteta. Ser.: Meditsina. Farmatsiya [Scientific bulletin of Belgorod State University. Series: Medicine. Pharmacy]. 2017, no. 19 (268), iss. 39, pp. 40-53. [In Russian]
10. Lutalo P. M., D’Cruz D. P. J. Autoimmun. 2014, vol. 48-49, pp. 94-98.
11. Westman K., Flossmann O. and Gregorini G. Nephrol. Dial. Transplant. 2015, vol. 30, pp. 60-66. DOI 10.1093/ndt/gfu392.
Левина Татьяна Михайловна
кандидат медицинских наук, доцент, кафедра госпитальной терапии, Медицинский институт, Национальный исследовательский Мордовский государственный университет имени Н. П. Огарёва (Россия, г. Саранск, ул. Большевистская, 68)
E-mail: [email protected]
Levina Tat’yana Mikhaylovna Candidate of medical sciences, associate professor, sub-department of hospital therapy, Medical Institute, National Research Mordovia State University (68 Bolshevistskaya street, Saransk, Russia)
Романов Михаил Дмитриевич
доктор медицинских наук, профессор, кафедра госпитальной хирургии, Медицинский институт, Национальный исследовательский Мордовский государственный университет имени Н. П. Огарёва (Россия, г. Саранск, ул. Большевистская, 68)
E-mail: [email protected]
Romanov Mikhail Dmitrievich Doctor of medical sciences, professor, sub-departmet of hospital surgery, Medical Institute, National Research Mordovia State University (68 Bolshevistskaya street, Saransk, Russia)
Киреева Екатерина Михайловна
кандидат медицинских наук, доцент, кафедра госпитальной хирургии, Медицинский институт, Национальный исследовательский Мордовский государственный университет имени Н. П. Огарёва (Россия, г. Саранск, ул. Большевистская, 68)
E-mail: [email protected]
Kireeva Ekaterina Mikhaylovna Candidate of medical sciences, associate professor, sub-department of hospital surgery, Medical Institute, National Research Mordovia State University (68 Bolshevistskaya street, Saransk, Russia)
Образец цитирования:
Левина, Т. М. Особенности диагностики и лечения гранулематоза Вегенера / Т. М. Левина, М. Д. Романов, Е. М. Киреева // Известия высших учебных заведений. Поволжский регион. Медицинские науки. — 2019. -№ 1 (49). — С. 15-26. — DOI 10.21685/2072-3032-2019-1-2.
ИЦ РИОР
Гранулематоз Вегенера (ГВ) – аутоиммунное гранулематозное воспаление стенок сосудов, захватывающее мелкие и средние кровеносные сосуды – капилляры, венулы, артериолы и артерии, с вовлечением верхних дыхательных путей, глаз, почек, легких и других органов [10, 11]. Относится к системным некротизирующим васкулитам.
Первое сообщение об этом заболевании принадлежит H.Klinger. В 1939 г. F.Wegener детально описал синдром, включающий язвенно-некротические поражения верхних дыхательных путей и кожи, быстропрогрессирующий гломерулонефрит.
Точных данных о распространенности ГВ в Российской Федерации нет [13]. В США распространенность ГВ в популяции составляет 25-60 случаев на 1 млн населения, заболеваемость – 3-12 случаев на 1 млн человек [16]. ГВ может быть диагностирован в любом возрасте, но чаще в 40-65 лет. Очень редко выявляется в детском возрасте [17]. Считается, что заболевание одинаково часто встречается у мужчин и женщин [1]. В Европе ГВ несколько чаще выявляется у мужчин, чем у женщин 1,5:1 [21]. По данным С.В.Клименко [3] ГВ наблюдался в 1,6 раза чаще у женщин, чем у мужчин.
Причины развития этого злокачественного некротического васкулита до настоящего времени неизвестны. Выявлена генетическая предрасположенность пациентов, но роль наследственности в настоящее время не доказана. Придают значение развитию острой носоглоточной инфекции, длительному лечению антибиотиками, наличию очагов хронической инфекции. Роль инфекции бесспорна в качестве стимула рецидивов заболевания. Чаще всего они возникают при заражении пациента стафилококками, вирусами. Высказывается предположение, что существует сложное взаимодействие между факторами окружающей среды и организмом человека [4]. Повреждение тканей ассоциируется с активацией клеточных иммунных реакций и воспалительных процессов.
Важнейшим звеном патогенеза ГВ являются процессы, связанные с синтезом антител к цитоплазме нейтрофилов (АНЦА). АНЦА – это гетерогенная популяция аутоантител, реагирующих с различными ферментами цитоплазмы нейтрофилов, в первую очередь, с протеиназой-3 (эта разновидность антител выявляется при васкулите Вегенера чаще) и миелопероксидазой (при выявлении которой прогноз хуже) [18].
Протеиназа-3 и миелопероксидаза непосредственно связываются с нейтрофилами и моноцитами, циркулирующими в кровотоке. На мембранах последних локализованы рецепторы для связи с указанными иммуноглобулинами. Когда антитело связывается с рецептором, клетки становятся очень активными, они приобретают высокую протеолитическую активность. Данный факт обеспечивает воспаление и некротическую деструкцию сосудистой стенки. Эти процессы сопровождаются увеличением концентрации провоспалительных цитокинов, которые, в свою очередь, поддерживают воспалительный процесс, вовлекая новые клеточные и гуморальные элементы. Морфологический субстрат заболевания – гранулёмы, сопровождающиеся некрозом.
ГВ – тяжелое, быстро прогрессирующее заболевание и без своевременно начатого лечения приводящее к смертельному исходу в течение 6-12 мес. [11]. Подразделяется на две формы: локальную и генерализованную. При локальной форме поражаются ЛОР органы (90% случаев) и глаза (15% случаев) с развитием ринита, назофарингита, синусита, евстахиита, отита, склерита, эписклерита, а также увеита [10, 11]. При генерализованной форме к вышеуказанным симптомам присоединяется поражение легких (80% случаев) в виде легочного гранулематозного васкулита, обычно заканчивающегося образованием легочных гранулём [10, 11]. Гранулёмы подвержены распаду с образованием каверн, что нередко сопровождается легочным кровотечением. У 2/3 пациентов наблюдается поражение почек в виде некротизирующего быстропрогрессирующего гломерулонефрита [10, 11]. Достаточно часто ГВ протекает с развитием кожного васкулита (у 40% пациентов) и поражения периферической нервной системы (15%) с развитием асимметричной полинейропатии [10, 11]. У 5% больных описан перикардит [10, 11]. Заболевание начинается с общей слабости, пониженного аппетита и похудания. В последующем присоединяются лихорадка, артралгии и миалгии. Иногда выявляют симптомы реактивных артритов.
Основной морфологический признак ГВ – гранулёмы, определяется только при гистологическом исследовании после биопсии пораженной ткани. Начальные изменения обнаруживаются в мелких артериях и венах. В результате последовательного чередования стадий отека, фибриноидного некроза в стенке сосуда и в окружающих тканях скапливаются гигантские многоядерные клетки. Они образуют особую структуру – гранулёму. ГВ характеризуется наличием васкулита малых и средних сосудов, «географическим» некрозом и гранулематозным воспалением, особенно дыхательных путей. Предполагается, что основу начального патологического поражения (гранулёмы) составляют клеточные иммунные процессы [1, 19].
Поражение глаз. При ГВ воспалительный процесс затрагивает в основном белочную и радужную оболочку глаз. Нередко развитие увеита, иридоциклита, эписклерита, склерита, приводящих к перфорации роговицы и слепоте. Возможно образование периорбитальной гранулёмы и экзофтальма.
Поражение лёгких. В легких образуются гранулёмы, нередко распадающиеся, что приводит к кровохарканью и развитию дыхательной недостаточности. У 1/3 пациентов гранулёмы клинически ничем себя не проявляют [12]. Возможно развитие плеврита, аускультативно проявляющегося шумом трения плевры. Также может наблюдаться выпотной плеврит.
Гранулематозное воспаление альвеолярных капилляров и артериол легких приводит к развитию тяжелого легочного капиллярита. Развиваются инфильтраты, которые подвергаются деструкции с образованием полостей, что способствует появлению кровохарканья и легочного кровотечения. Инфильтраты, которые могут расти и уменьшаться, часто вначале ошибочно принимают за пневмонию. При рентгенологическом исследовании наряду с инфильтратами может быть картина легочной диссеминации. Одностороннее выявление теней мелких узелков часто ошибочно интерпретируют как рак легкого. Как правило, отмечаются множественные узелки, расположенные билатерально и часто с наличием полости. Кроме того, установлено, что венозный тромбоз (в частности, тромбозы глубоких вен) и тромбоэмболии легочной артерии являются частым осложнением ГВ [1, 9]. Поэтому у пациентов с ГВ, предъявляющих жалобы на одышку, боль в груди или другие характерные симптомы, следует исключить тромбоэмболию легочной артерии [2, 9].
При определении степени поражения легких значительные преимущества имеют данные компьютерной томографии по сравнению с рентгенографией грудной клетки [2, 5]. Пациентам с подозрением на ГВ в числе основных исследований необходимо проведение компьютерной томографии (КТ) грудной клетки. При КТ у пациентов с ГВ выявляются различные изменения (за редким исключением прикорневых лимфоузлов и средостения), включая плевральный выпот и неспецифические инфильтраты. В легких, как правило, определяются множественные и двусторонние узелки и полости распада. Изменения часто располагаются на периферии легких и могут иметь клиновидную или округлую форму, что может быть ошибочно расценено как тромбоэмболия легочной артерии или злокачественное новообразование. [1].
Поражение верхних дыхательных путей, ротовой полости и органов слуха. Проявляется в виде упорного насморка с гнойно-геморрагическим отделяемым. В последующем развивается изъязвление слизистой оболочки. Возможна перфорация перегородки с развитием седловидной деформации носа (рис. 4). Помимо язвенно-некротического ринита возможно поражение трахеи, гортани, придаточных пазух носа, слуховых труб и ушей. Нередко возникновение язвенного стоматита.
Поражение нервной системы. Протекает в виде асимметричной полинейропатии.
Поражение кожи. Наблюдается кожный васкулит с язвенно-геморрагическими высыпаниями.
Поражение почек. Одной из излюбленных локализаций ГВ являются почечные клубочки. Гломерулонефрит проявляется гематурией и протеинурией, нередко имеет быстропрогрессирующее течение и приводит к быстро нарастающей почечной недостаточности. Быстропрогрессирующий нефрит является показанием к проведению биопсии почки. Поражение почек – третий главный признак ГВ, отмечаемый у 80-90% больных [7]. При этом в дебюте болезни симптомы почечной патологии присутствуют менее чем у 20% пациентов. В острую фазу заболевания размеры почек нормальные или несколько увеличены, их поверхность часто имеет мелкие кровоизлияния; паренхима бледная, отёчная. При аутопсии примерно в 20% случаев отмечают папиллярный некроз, который клинически не был диагностирован [7]. Для острой стадии ГВ характерна картина фокального сегментарного некротизирующего гломерулонефрита с полулуниями. В наиболее тяжёлых случаях отмечают поражение практически всех клубочков, в которых, как правило, выявляют сегментарный некроз, охватывающий отдельные капиллярные петли, хотя возможен и тотальный некроз клубочковых капилляров. Количество клубочков с полулуниями варьирует в зависимости от тяжести процесса от 10 до 100%. По характеру расположения в клубочке, полулуния могут быть сегментарными, занимающими менее 50% окружности капсулы, или циркулярными. У 15-50% больных ГВ с поражением почек, по данным разных авторов, в биоптатах обнаруживают гранулематозные полулуния, содержащие многочисленные эпителиоидные и гигантские клетки. У некоторых больных гранулематозные полулуния сочетаются с обычными клеточными. В хронической стадии патологического процесса отмечают сегментарный или диффузный гломерулосклероз, фиброзные полулуния. В связи с быстрой эволюцией морфологических изменений явления гломерулосклероза могут сосуществовать с активным гломерулитом [7].
Тубулоинтерстициальные изменения при ГВ у небольшого числа больных могут быть представлены типичными интерстициальными гранулёмами. При аутопсийном исследовании примерно в 20% случаев выявляют васкулит восходящих vasa recta с развитием сосочкового некроза, который практически невозможно выявить при помощи чрескожной пункционной нефробиопсии и который, по-видимому, развивается чаще, чем диагностируется [8]. Хроническая стадия процесса характеризуется атрофией канальцев и фиброзом интерстиция. При иммуногистохимическом исследовании не обнаруживают депозитов иммуноглобулинов в сосудах и клубочках почек, что служит характерной особенностью малоиммунных васкулитов и гломерулонефрита, ассоциированных с наличием АНЦА [8].
Поражение оболочек сердца. Проявляется в виде различных видов перикардита. Поражение миокарда и эндокарда нехарактерно.
Диагностика. Критериями диагностики ГВ согласно Американской Коллегии Ревматологов являются: 1) воспаление носа и ротовой полости, развитие болезненных или безболезненных язв полости рта, гнойные или кровянистые выделения из носа; 2) патологические изменения на рентгенограмме легких, наличие узелков, фиксированных инфильтратов или полостей распада; 3) изменение мочевого осадка – микрогематурия или эритроцитарные цилиндры; 4) гранулематозное воспаление при биопсии, гистологические изменения в виде гранулематозного воспаления в пределах сосудистой стенки артерии или в периваскулярной или экстравазальной области (артерий или артериол) [16]. Необходимо наличие двух критериев [16].
Исследование АНЦА. В настоящее время для выявления АНЦА широко используется методы иммунофлюоресценции и иммуноферментного анализа. В диагностике ГВ оба исследования являются взаимодополняющими и их рекомендуется применять при подозрении на это заболевание [2, 14]. Отрицательные тесты АНЦА не исключают диагноз ГВ. Однако следует учитывать, что до 10% пациентов с активным нелеченным генерализованным ГВ при тестировании на АНЦА могут иметь отрицательные результаты, а при ограниченном ГВ в 30% и более случаев АНЦА могут не определяться [2, 15].
Для окончательного подтверждения диагноза ГВ требуется биопсия пораженного органа. Среди органов, поражение которых обычно происходит при ГВ, наиболее часто проводят биопсию следующих тканей: легкие, почки и верхние дыхательные пути (нос или его пазухи). При ГВ зоны некроза тканей часто настолько обширны, что их иногда называют «географическим некрозом». При этом даже при наличии всех трех патологических признаков (гранулематозного воспаления, васкулита и некроза) диагноз ГВ требует тщательной интеграции с клинической симптоматикой, лабораторными и радиологическими данными. Далеко не во всех случаях ГВ результаты биопсии дают положительный результат. Это зависит от стадии болезни, предшествующей терапии и частого присоединения инфекции. Так, полная диагностическая триада при биопсии верхних дыхательных путей (носа, придаточных пазух носа и подсвязочной области) определяется лишь в 15% случаев [13]. Однако биопсия верхних дыхательных путей, как правило, безопаснее, чем легких или почек. При типичной симптоматике ГВ отрицательные результаты гистологического исследования не опровергают клинического диагноза. Но даже выявление нескольких признаков триады при биопсии носа или синусов подтверждает диагноз ГВ только при условии наличия других признаков заболевания. При биопсии легкого у больных с ГВ патологический процесс представлен наиболее полно, что связано с забором большего количества ткани [13].
При ГВ некротизирующий васкулит характеризуется возможным вовлечением артерий, вен и капилляров с наличием или без признаков гранулёмы. Некроз сосудов начинается со скопления нейтрофилов в стенке кровеносных сосудов (микроабсцессы), происходит перерождение тканей стенки сосуда с окружением из гистиоцитов. Слияние таких нейтрофильных микроабсцессов приводит к географическим некрозам. Однако результаты биопсии легкого далеко не всегда диагностически значимы, а тяжесть состояния больных может не позволить провести торакотомию; более показана трансбронхиальная биопсия с исследованием слизистой оболочки бронхов при их поражении [4]. Данные биопсии почки при ГВ являются неспецифичными (результаты могут быть подобны другим формам аутоиммунного гломерулонефрита). Обычно наблюдается некротизирующий гломерулит или гломерулонефрит. Описаны случаи капиллярного некроза [20]. Пятилетняя выживаемость 18 больных ГВ с быстропрогрессирующим гломерулонефритом составила 67% [6].
Терапия. Комбинированная терапия системными глюкокортикоидами (СГК) и циклофосфамидом – основа лечения ГВ. Стандартная терапия основана на пероральном приеме циклофосфамида (2-3 мг/кг/сут) в сочетании с преднизолоном (1 мг/кг/сут). Лечение СГК в этой дозе продолжают до развития иммуносупрессивного эффекта цитостатика (около 4 недель), затем дозу преднизолона постепенно снижают (по 5 мг каждые 2 недели) или переводят больного на альтернирующий прием препарата (60 мг через день). Длительность такой терапии СГК зависит от индивидуального ответа пациента на нее.
У больных с быстропрогрессирующим заболеванием начальная доза цитостатика составляет не менее 3-5 мг/кг/сут. Одновременно назначаются СГК (2-15 мг/кг/сут). Такое лечение проводится в течение нескольких дней с последующим переводом больного на стандартный режим терапии.
Эффективной является ежемесячная пульс-терапия циклофосфамидом, особенно в течение первых месяцев от начала заболевания.
В последнее время для лечения больных ГВ без угрожающих для их жизни осложнений используют метотрексат (0,15-0,3 мг/кг/нед) в сочетании с высокими дозами преднизолона (1 мг/кг/сут). Низкие дозы метотрексата (0,3 мг/кг в/в 1 раз в нед) во многих случаях позволяют эффективно поддерживать индуцированную циклофосфамидом ремиссию у больных ГВ, но не могут использоваться в качестве основного метода лечения у пациентов с тяжелыми проявлениями заболевания.
В последние годы для лечения ГВ используют ритуксимаб [11].
При субглоточном стенозе гортани развитие угрожающих жизни осложнений может потребовать экстренной трахеотомии или плановой хирургической коррекции в сочетании с местным введением глюкокортикоидов. Развитие острой дыхательной недостаточности на фоне диффузных альвеолярных геморрагий может потребовать искусственной вентиляции легких.
Учитывая значительную редкость заболевания, приводим клиническое наблюдение из личной практики авторов.
Больная Б., 1960 г.р. поступила в пульмонологическое отделение Амурской областной клинической больницы (АОКБ). Жалобы при поступлении: на выраженную слабость, повышение температуры тела до 39ºС, кашель с мокротой слизистого характера, боли в горле и грудной клетке, усиливающиеся при кашле, одышку при незначительной физической нагрузке. Считает себя больной с июня 2010 г., когда стали беспокоить заложенность носа, боли в левой половине лица, глазах, отмечалось повышение температуры тела до 38ºС. В июле 2010 г. была госпитализирована в гинекологическое отделение городской больницы, где проведено диагностическое выскабливание и рекомендовано оперативное лечение по поводу миомы матки. Операция была отсрочена в связи с нарушением сердечного ритма (экстрасистолия). Жалобы со стороны ЛОР-органов и лихорадка сохранялись. Получала лечение по поводу нарушения ритма в кардиохирургическом цетре, ритм восстановился, но сохранялись боли в области лица, носа и лихорадка до 38ºС. Амбулаторно лечилась у ЛОР-врача, неоднократно проводились пункции гайморовых пазух, сопровождающиеся носовыми кровотечениями. В августе 2010 г. лечилась в ЛОР-отделении с диагнозом «хронический гайморит». Получала антибиотики, физиолечение. Отмечалось незначительное улучшение, уменьшились боли в области носа и лица, временно нормализовалась температура.
В октябре 2010 г. после сильного переохлаждения повысилась температура тела, появились озноб, сухой кашель. Лечилась самостоятельно, принимала парацетамол, аспирин, но температура не понижалась, появились боли в горле и грудной клетке, кашель с мокротой слизистого характера, одышка при незначительной физической нагрузке, выраженная слабость. Самостоятельно обратилась в ЦРБ Ивановского района, где после рентгенографии органов грудной клетки был выставлен диагноз «двусторонняя пневмония», назначены антибиотики пенициллинового ряда, аминогликозиды. На фоне лечения состояние не улучшалось, и в ноябре 2010 г. больная была госпитализирована в пульмонологическое отделение АОКБ в крайне тяжелом состоянии (наблюдались выраженная слабость, снижение массы тела, гектическая лихорадка, кровохарканье, одышка до 26 дыханий в минуту). При осмотре: бледность кожного покрова, единичные подкожные кровоизлияния в области предплечий, правой ягодицы, пастозность голеней, стоп. В легких дыхание везикулярное, слева под ключицей – бронхиальное, хрипов нет. Границы относительной тупости сердца в пределах нормы, тоны сердца ритмичные, ЧСС 114 уд/мин., АД 130 и 80 мм рт. ст. Живот при пальпации мягкий, безболезненный, нижний край печени не выступает из-под реберной дуги, селезенка не увеличена. Симптом поколачивания отрицательный с обеих сторон.
Клинический анализ крови: гемоглобин – 77 г/л, эритроциты – 2,68×1012/л, СОЭ – 30 мм/час, лейкоциты – 16,8×109/л, палочкоядерные – 3%, сегментоядерные – 72%, эозинофилы – 12%, лимфоциты – 8%, моноциты – 7%, тромбоциты – 540×109/л.
Биохимический анализ крови: глюкоза – 5,0 ммоль/л, билирубин общий – 8,6 мкм/л, непрямой – 7,0 мкм/л, прямой – 1,4 мкм/л, АЛАТ – 2,8, АСАТ – 9,5, мочевина – 3,2 ммоль/л, креатинин – 135 ммоль/л, сиаловые кислоты – 160, церулоплазмин – 183, тимоловая проба – 1,0, холестерин – 5,5 ммоль/л, щелочная фосфатаза – 160, фибриноген – 4652 г/л, ПТИ – 100%. Общий анализ мочи: белок – 1275 г/л, сахар – нет, эритроциты – много, лейкоциты – до 15 в поле зрения. Анализ мочи по Нечипоренко: лейкоциты – 16200, эритроциты – 125100.
Посев крови на гемокультуру (трехкратно) – стерильная. Общий анализ мокроты: характер – слизистый, вязкая, плоский эпителий – сплошь, КУМ (трехкратно) – не обнаружены. Посев мокроты на микрофлору и чувствительность к антибиотикам: пневмококк ×108, клебсиелла ×108, чувствительные к пенициллинам, цефалоспоринам, аминогликозидам.
ЭКГ: Синусовая тахикардия, 100 уд. в мин., эл. ось расположена горизонтально, повышена нагрузка на правый желудочек.
На рентгенограмме органов грудной клетки: справа, на фоне диффузного усиления легочного рисунка, в средних и нижних отделах определяются мелкоочаговые множественные тени, сливающиеся между собой; снижена пневматизация легочной ткани нижних отделов левого легкого за счет инфильтрации, корни легких расширены (рис. 1).
При КТ (кроме изменений, выявленных на рентгенограммах) – признаки шаровидного инфильтрата нижней доли (S10) левого легкого с явлениями распада, как проявление основного заболевания (рис. 2).
|
|
|
|
Рис. 1. Больная Б., гранулематоз Вегенера. Обзорная рентгенограмма. Справа легочный рисунок диффузно усилен, в средних и нижних отделах определяются мелкоочаговые множественные тени, сливающиеся между собой. В нижних отделах левого легкого снижена пневматизация легочной ткани за счет инфильтрации. Корни легких расширены.
|
Рис. 2. Больная Б., гранулематоз Вегенера. Компьютерная томография. Признаки шаровидного инфильтрата нижней доли (S10) левого легкого с явлениями распада.
|
Учитывая, что у пациентки уже с сентября 2010 г. наблюдались изменения в легких при отсутствии выраженных клинических проявлений, больная была осмотрена фтизиатром. Резистентность к антибактериальной терапии позволила заподозрить в данном случае туберкулез легких, в связи с чем пациентка была переведена в областной противотуберкулезный диспансер для проведения терапии ex juvantibus. На фоне лечения противотуберкулезными препаратами положительной динамики не отмечалось, состояние больной прогрессивно ухудшалось, появились боли в коленных суставах, дистальных фалангах пальцев кистей рук, цианотичная окраска ногтевой фаланги III пальца правой кисти и II—III – левой, рентгенологически – отрицательная динамика, увеличение инфильтрации легочной ткани. Заключение КЭК: по клинико-лабораторным, рентгенологическим данным – активного туберкулеза легких нет.
Больная вновь переведена в пульмонологическое отделение АОКБ. При бронхоскопии: слизистая трахеи и всех бронхов гиперемирована, истончена, с участками изъязвлений; на слизистой, в основном, правых бронхов, мелкобугристые образования, покрытые фибрином, с гнойным налетом; заключение: язвенный эндобронхит, преимущественно справа, ИВ II ст. По данным трансбронхиальной браш-биопсии выявлены клетки, подозрительные на низкодифференцированный рак.
Однако клиническая картина заболевания с его полисиндромностью, вовлечением в патологический процесс многих систем организма, не укладывалась в данный диагноз, в связи с чем была проведена повторная трансбронхиальная биопсия. Гистологическое исследование биоптата: на фоне некротических масс, увеличенного количества лимфоцитов имеется выраженная пролиферации цилиндрического эпителия, бóльшая часть клеток изменена, обнаружена полиморфноклеточная гранулёма с многоядерными гигантскими клетками.
ЭхоКГ: Камеры сердца не расширены, сократительная способность миокарда сохранена, небольшое количество свободной жидкости в полости перикарда.
УЗИ: размеры печени в пределах нормы, дополнительных образований в паренхиме не выявлено, структурные изменения поджелудочной железы, в левой плевральной полости – свободная жидкость.
Учитывая жалобы на боли в горле и полости носа, пациентка осмотрена ЛОР-врачом, на поверхности языка, задней стенке глотки, носовой перегородки отмечены язвенно-некротические участки с кровоточивостью.
Консультация офтальмолога: глазное дно – диск зрительного нерва бледно-розового цвета, границы четкие, соотношение сосудов сохранено, очаговых изменений нет. УЗИ орбит: структура ретробульбарной клетчатки неоднородная, больше справа, дополнительных образований нет.
С учетом анамнеза и клинической картины заболевания, острого начала с лихорадкой, артралгиями, поражения слизистой носа и ротовой полости, легких, почек, синдрома Рейно, геморрагических высыпаний, дигитального васкулита, данных гистологического исследования материала трансбронхиальной биопсии ткани легкого выставлен диагноз: Гранулематоз Вегенера, генерализованная форма, с поражением верхних дыхательных путей, трахеобронхиального дерева, легких, сердца, почек, острое течение. Вторичная двусторонняя пневмония, ДН II—III ст.
Назначено лечение: преднизолон – 60 мг/сут. per os, 90 мг – в/в №5, циклофосфан – 200 мг/сут в/в, ципрофлоксацин – 400 мг/сут в/в, пентоксифиллин – 5,0 в/в, панангин – 10,0 в/в, дезинтоксикационная и другая симптоматическая терапия. В стационаре у пациентки развилась клиника сухой гангрены концевой фаланги IV пальца правой кисти (рис. 3), в связи с чем была произведена экзартикуляция фаланги. В дальнейшем, на фоне проводимой терапии наблюдалась положительная динамика, уменьшились одышка, кашель, боли в грудной клетке, нормализовалась температура тела, улучшилось общее самочувствие.
В клиническом анализе крови нормализовались показатели гемоглобина, эритроцитов, уменьшились СОЭ и лейкоцитоз, в анализах мочи снизилась протеинурия до 50 г/л. Отмечена также положительная динамика при бронхоскопии, рентгенологическая динамика – в виде уменьшения инфильтрации легочной ткани, количества жидкости в плевральной полости. В связи с улучшением состояния больная была выписана из стационара с дальнейшим лечением по месту жительства, рекомендована доза преднизолона – 60 мг в сутки, с последующим снижением до поддерживающей, циклофосфан – 200 мг 2 раза в неделю.
В течение последующего времени больная наблюдалась ревматологом АОКП, терапевтом по месту жительства, находилась на плановом лечении в ревматологическом отделении АОКБ. Получала поддерживающую дозу циклофосфана 200 мг 1 раз в 2 недели, затем – 1 раз в месяц, преднизолон в дозе 5 мг/сут. Получала также нестероидные противовоспалительные препараты, препараты кальция, калия – курсами, симптоматическую терапию. На фоне проводимого лечения отмечалась непродолжительная временная положительная динамика. Однако в дальнейшем гранулематозный процесс рецидивировал. Со временем сформировалась седловидная деформация носовой перегородки (рис. 4).
В дальнейшем присоединился двусторонний экссудативный плеврит. Анализ плевральной жидкости: геморрагического характера, мутная, уд. вес – 1016, белок 1,65%, проба Ривальта положительная; цитологическое исследование: в мазках на фоне эритроцитов определяется большое количество лимфоцитов – 98%.
|
|
|
|
Рис. 3. Больная Б., гранулематоз Вегенера. Сухая гангрена концевой фаланги IV пальца правой кисти.
|
Рис. 4. Больная Б., гранулематоз Вегенера. Седловидная деформация носа.
|
В феврале 2012 г. в связи с появлением одышки при незначительной физической нагрузке, сердцебиения, повышения температуры тела до 38-39ºС, больная была госпитализирована в ревматологическое отделение АОКБ, где при проведении рентгенографии, эхокардиографии был выявлен выпот в полости перикарда (60-70 мл). В анализе крови: анемия, лейкоцитоз, эозинофилия (25%), увеличение СОЭ, увеличение АСАТ. В анализах мочи — протеинурия, гематурия. В связи с этим было решено увеличить дозу циклофосфана до 200 мг через день, преднизолона – до 30 мг в сутки. К лечению был присоединен ритуксимаб. В начале 2012 г. появились боли в правом тазобедренном суставе, усиливающиеся вечером, повышение АД до 140 и 100 мм рт. ст. Рентгенограмма тазобедренных суставов: умеренное сужение суставной щели в правом тазобедренном суставе, стушеванность контуров головки и нижнего отдела суставной впадины, в головке бедренной кости справа – участки просветления размерами до 11 мм. Заключение: рентгенологические признаки асептического некроза головки правой бедренной кости. Двусторонний коксартроз II ст. Консультирована ортопедом: Асептический некроз головки бедренной кости справа. Двусторонний коксартроз, R— II ст., НФС II. Оперативное лечение не показано.
Заболевание прогрессировало, присоединялись новые осложнения ГВ. В 2012 г. диагноз звучал так: Гранулематоз Вегенера, активность III степени, генерализованная форма, с поражением верхних дыхательных путей (атрофический ринит, в слизистой носа гранулематозное воспаление, поражение носовой перегородки с формированием седловидной деформации носа, рецидивирующие носовые кровотечения), глаз (двусторонний экзофтальм), сердца (перикардит), печени (гранулематозный процесс), легких (прогрессирующий гранулематозный процесс в обоих легких с формированием инфильтратов и образованием очагов деструкции и полостей распада, двусторонний плеврит), слизистой полости рта (генерализованный катаральный гингивит), околоушных желёз (двусторонний паротит), суставов и костной ткани (сухая гангрена концевой фаланги IV пальца правой кисти, олигоартрит, асептический некроз головки бедренной кости), почек (прогрессирующий гломерулонефрит). Осложнения: Хроническая почечная недостаточность; анемия хронического заболевания, тяжелой степени.
Несмотря на проводимую терапию, заболевание прогрессировало. Присоединились сепсис и ДВС-синдром. В мае 2012 г. был констатирован летальный исход. Патологоанатомический диагноз полностью соответствовал прижизненному.
Данный случай представляет сложности диагностики редкого некротизирующего васкулита – гранулематоза Вегенера. Проводился сложный дифференциальный диагноз между пневмониями различной этиологии, туберкулезом, раком легкого и гранулематозным заболеванием. С учетом анамнеза и клинической картины заболевания, острого начала с лихорадкой, артралгиями, поражением слизистой носа и ротовой полости, легких, почек, синдрома Рейно, геморрагических высыпаний, дигитального васкулита, данных гистологического исследования материала трансбронхиальной биопсии ткани легкого, был выставлен диагноз: гранулематоз Вегенера, генерализованная форма, с поражением верхних дыхательных путей, трахеобронхиального дерева, легких, сердца, почек, острое течение. Несмотря на адекватное лечение, заболевание прогрессировало с присоединением различных осложнений, и был констатирован летальный исход. Авторы выражают надежду, что изложение данного клинического случая гранулематоза Вегенера окажет помощь коллегам при необходимости диагностики и дифференциальной диагностики некротизирующих васкулитов.
Терапия » Пульмонологические «маски» системных васкулитов
Пульмонологические «маски» системных васкулитов
DOI: https://dx.doi.org/10.18565/therapy.2019.8.157-162
З.Д. Михайлова, П.Ф. Климкин, Н.В. Новицкая, П.Н. Обухов, Н.Б. Митрясова
1) ГБУЗ Нижегородской области «Городская клиническая больница № 38», г. Нижний Новгород;
2) ГБУЗ Нижегородской области «Городская клиническая больница № 5», Нижний Новгород
В статье представлены клинические наблюдения за пациентами с системными васкулитами (гранулематоз с полиангиитом и эозинофильный гранулематоз с полиангиитом), протекающими под «маской» другой соматической патологии. Заболевания дебютировали с патологии верхних дыхательных путей и легких (пневмония, бронхиальная астма). Проведение диагностического поиска позволило установить в кратчайшие сроки причину поражения внутренних органов.
Ключевые слова: поражение органов дыхания, АНЦА-ассоциированный васкулит, гранулематоз с полиангиитом, эозинофильный гранулематоз с полиангиитом
Литература
- Ревматология: национальное руководство. Под ред. Е.Л. Насонова, В.А. Насоновой. М.: ГЭОТАР-Медиа, 2008: 528–572 с.
- Российские клинические рекомендации. Ревматология. Под ред. Е.Л. Насонова. М.: ГЭОТАР-Медиа. 2017: 180–204.
- Федеральные клинические рекомендации по диагностике и лечению системных васкулитов. М., 2014; 29 с.
- Falk R.J., Gross W.L., Guillevin L., Hoffman G.S., Jayne D.R., Jennette J.C., Kallenberg C.G., Luqmani R., Mahr A.D., Matteson E.L., Merkel P.A., Specks U., Watts R.A. American College of Rheumatology; American Society of Nephrology; European League Against Rheumatism. ArthritisRheum. 2011; 63(4): 863–64.
- Анаев Э.Х. Легочные васкулиты: дифференциальная диагностика. Практическая пульмонология. 2017; 1: 51–57.
- Бабаева А.Р., Калинина Е.В., Звоноренко М.С. Трудности диагностики гранулематоза Вегенера у взрослых в современной клинической практике (Клиническое наблюдение). Волгоградский научно-медицинский журнал. 2016; 3: 49–54.
- Бекетова Т.В. Гранулематоз с полиангиитом, патогенетически связанный с антинейтрофильными цитоплазматическими антителами: особенности клинического течения. Научно-практическая ревматология. 2012; 50(6): 19–28.
- Щеголева Е.М., Зыкова А.С., Буланов Н.М., Новиков П.И., Моисеев С.В., Мухин Н.А. Современные подходы к диагностике и лечению микроскопического полиангиита. Клиническая медицина. 2018; 1: 66–72.
- Фернандо Д., Шпотин В., Гостюнин А., Кудаев С. Случай молниеносного течения АНЦА-негативного варианта гранулематоза Вегенера с первичным поражением лор-органов. Врач. 2018; 1: 76–78.
- Макарьянц Н., Шмелев Е., Куклина Г., Лепеха Л., Березовский Ю., Романов В., Багиров М. Сложный случай дифференциальной диагностики гранулематозного полиангиита (гранулематоз Вегенера) у пациента с длительной медикаментозной иммуносупрессией. Врач. 2018; 7: 43–47.
- Зайцева А.С., Шмелев Е.И., Степанян И.Э., Шабалина И.Ю., Дмитриева Л.И., Евгущенко Г.В. Особенности диагностики системных васкулитов в практике врача-пульмонолога. Consilium Medicum. 2017; 19(3): 50–54.
- Ходош Э.М., Крутько В.С., Ефремова О.А. Гранулематоз с полиангиитом (Вегенера) и системные васкулиты: многосторонний взгляд на проблему (обзор литературы). Научные ведомости БелГУ. Сер. Медицина. Фармация. 2017. 19(268), вып. 39: 40–53.
- Novikov P., Smitienko I., Bulanov N., Zykova A., Moiseev S., Testing for antineutrophil cytoplasmic antibodies (ANCAs) in patients with systemic vasculitides and other diseases. Ann. Reum. Dis. 2017; 76(8): e23. doi: 10.1136/annrheumdis-2016-210890.
- Кашкун А.А. Руководство по лабораторным методам диагностики. М.: ГЭОТАР-Медиа. 2009: 800 с.
- Николаева С.С., Енисеева Е.С., Тигунцева О.Д., Растомпахова Т.А. Синдром Чарга–Стросса в терапевтической практике. Сибирский медицинский журнал. 2010; 1: 128–130.
Об авторах / Для корреспонденции
Зинаида Дмитриевна Михайлова, д.м.н., доцент, консультант ГБУЗ НО «Городская клиническая больница № 38». Адрес: 603000, г. Нижний Новгород, ул. Чернышевского, д. 22. E-mail: [email protected]
Павел Федорович Климкин, к.м.н., консультант ГБУЗ НО «Городская клиническая больница № 5». Адрес: 603005, г. Нижний Новгород, ул. Нестерова, д. 34. E-mail: [email protected]
Наталья Витальевна Новицкая, зав. 2 терапевтическим отделением ГБУЗ НО «Городская клиническая больница № 38». Адрес: 603000, г. Нижний Новгород, ул. Чернышевского, д. 22. E-mail: [email protected]
Павел Николаевич Обухов, врач-терапевт ГБУЗ НО «Городская клиническая больница № 38». Адрес: 603000, г. Нижний Новгород, ул. Чернышевского, д. 22. E-mail: [email protected]
Наталья Борисовна Митрясова, зав. рентген-кабинетом – врач-рентгенолог ГБУЗ НО «Городская клиническая больница № 38». Адрес: 603000, г. Нижний Новгород, ул. Чернышевского, д. 22. E-mail: natbaldina @yandex.ru
Гранулематоз с полиангиитом (GPA, ранее назывался Wegener’s)
Обзор
Что такое гранулематоз с полиангиитом (GPA, ранее называвшийся синдромом Вегенера)?
Гранулематоз с полиангиитом (GPA, ранее называвшийся болезнью Вегенера) — редкое заболевание неизвестной причины. Это результат воспаления в тканях, называемого гранулематозным воспалением и воспалением кровеносных сосудов («васкулит»), которое может повредить системы органов.Области, наиболее часто поражаемые GPA, включают пазухи, легкие и почки, но может быть поражен любой участок.
Что такое васкулит?
Васкулит — это общий термин, обозначающий воспаление кровеносных сосудов. При воспалении кровеносный сосуд может ослабнуть и растянуться, образуя аневризму, или стать настолько тонким, что разорвется, что приведет к кровотечению в ткани. Васкулит также может вызвать сужение кровеносных сосудов до полного закрытия сосуда.Это может привести к повреждению органов из-за потери кислорода и питательных веществ, поступающих с кровью.
Каковы особенности гранулематоза с полиангиитом (ГПА)?
GPA в первую очередь влияет на верхние дыхательные пути (пазухи, нос, трахею [верхний воздуховод]), легкие и почки. Также может быть поражен любой другой орган в организме.
Симптомы GPA и их тяжесть у разных пациентов различаются. Общие признаки заболевания могут включать:
- Потеря аппетита
- Похудание
- Лихорадка
- Усталость
Большинство пациентов сначала замечают симптомы в дыхательных путях.Симптомы могут включать:
- Постоянный насморк (также называемый ринореей) или образование корок и язв в носу
- Боль в носу или лице
- Носовое кровотечение или необычные выделения из носа, вызванные воспалением носа или пазух
- Кашель, который может включать кровавую мокроту, вызванную воспалением верхних или нижних дыхательных путей (легких)
- Дискомфорт в груди с одышкой или без нее
- Воспаление среднего уха (также называемое средним отитом), боль или потеря слуха
- Изменение голоса, хрипы или одышка, вызванные воспалением трахеи
Другие возможные функции:
- Воспаление глаза и / или давление за глазом, затрудняющее движение глаз, с потерей зрения или без нее
- Боль в суставах (артрит) или боль в мышцах
- Сыпь или кожные язвы
- Воспаление почек (хотя воспаление почек является обычным явлением, обычно оно не связано с такими симптомами, как боль).
Кто страдает гранулематозом с полиангиитом (ГПА)?
GPA может быть у людей любого возраста. Пиковая возрастная группа заболевания — от 40 до 60 лет. Похоже, это одинаково влияет на мужчин и женщин.
Симптомы и причины
Что вызывает гранулематоз при полиангиите (ГПА)?
Причина GPA неизвестна.GPA не является формой рака, не заразен и обычно не возникает в семьях. Данные исследовательских лабораторий убедительно подтверждают идею о том, что иммунная система играет решающую роль в GPA, так что иммунная система вызывает воспаление и повреждение кровеносных сосудов и тканей.
Диагностика и тесты
Как диагностируется гранулематоз с полиангиитом (ГПА)?
GPA имеет симптомы, схожие с рядом других расстройств, что может затруднить диагностику.Однако для наиболее эффективного и успешного лечения критически важна ранняя диагностика.
При подозрении на диагноз ГПД часто выполняется биопсия (образец ткани) пораженного участка, чтобы попытаться подтвердить наличие васкулита. Биопсия рекомендуется только для тех участков органов, в которых обнаружены отклонения от нормы при осмотре, лабораторных исследованиях или визуализации.
Это сочетание симптомов, результатов медицинского осмотра, лабораторных тестов, рентгеновских лучей, а иногда и биопсии (образца) пораженной ткани (кожи, носовых оболочек, пазух, легких, почек или других участков), которые вместе подтверждают диагноз. GPA.После лечения эти факторы также имеют решающее значение при оценке активности заболевания или ремиссии.
Положительный анализ крови на антинейтрофильные цитоплазматические антитела (ANCA) может подтвердить подозрение на диагноз заболевания. Однако этот анализ крови сам по себе не подтверждает диагноз GPA и не определяет активность заболевания.
GPA часто поражает легкие. У пациентов с ГПД, у которых нет легочных симптомов (кашель или одышка), визуализирующие тесты (обычные рентгеновские снимки или компьютерная томография) выявляют аномалии легких примерно в одной трети случаев.Следовательно, важно выполнять снимки легких при подозрении на активный ГПД, даже если у вас нет никаких симптомов заболевания легких.
Ведение и лечение
Как лечится гранулематоз с полиангиитом (ГПА)?
Поскольку GPA часто представляет собой опасное для жизни заболевание, его лечат различными мощными лекарствами, которые, как было доказано, спасают жизнь.Лекарства, подавляющие иммунную систему, составляют основу лечения GPA. Степень тяжести заболевания в каждом отдельном случае определяет, какие иммуносупрессивные препараты используются. Существует множество иммуносупрессивных препаратов, которые используются при GPA, каждое из которых имеет индивидуальные побочные эффекты.
Людей с ГПД с поражением критических систем органов обычно лечат кортикостероидами в сочетании с другими иммуносупрессивными препаратами, такими как циклофосфамид (Cytoxan®) или ритуксимаб (Rituxan®).У пациентов с менее тяжелым ГПД вначале можно использовать кортикостероиды и метотрексат. Цель лечения — остановить все травмы, возникающие в результате GPA. Если активность болезни можно полностью «выключить», это называется «ремиссией». Как только становится очевидным, что болезнь улучшается, врачи постепенно снижают дозу кортикостероидов и в конечном итоге надеются полностью отменить ее. Когда используется циклофосфамид, его назначают только до момента ремиссии (обычно от 3 до 6 месяцев), после чего его переключают на другой иммунодепрессант, такой как метотрексат, азатиоприн (Imuran®) или микофенолят мофетил (Cellcept®). ) для поддержания ремиссии.Продолжительность лечения поддерживающими иммуносупрессивными препаратами может варьироваться в зависимости от человека. В большинстве случаев его дают как минимум в течение 2 лет, прежде чем будет рассмотрен вопрос о медленном снижении дозы до прекращения приема.
Все эти лекарства также используются для лечения других заболеваний. Азатиоприн и микофенолят мофетил используются для предотвращения отторжения трансплантата органов. Метотрексат используется для лечения ревматоидного артрита и псориаза. И циклофосфамид, и метотрексат назначаются в высоких дозах для лечения определенных типов рака и поэтому иногда называются «химиотерапией».«При лечении рака эти лекарства работают, убивая или замедляя рост быстро размножающихся раковых клеток. При васкулите эти лекарства вводятся в дозах, которые от 10 до 100 раз ниже, чем те, которые используются для лечения рака, и их основной эффект заключается в том, чтобы влиять на поведение иммунной системы таким образом, что приводит к иммуносупрессии. Ритуксимаб относится к классу лекарств, называемых биологическими агентами, которые нацелены на определенный элемент иммунной системы. Недавние исследования показали, что ритуксимаб был так же эффективен, как циклофосфамид, для лечения тяжелого активного GPA.
Какие побочные эффекты связаны с лечением гранулематоза с полиангиитом (ГПА)?
Поскольку эти лекарства подавляют иммунную систему, существует повышенный риск развития серьезных инфекций. Каждый иммунодепрессивный препарат также имеет уникальный набор потенциальных побочных эффектов. Мониторинг побочных эффектов, связанных с каждым лекарством, имеет решающее значение для предотвращения или минимизации их возникновения. Кроме того, тот факт, что пациент может изначально переносить лечение, не гарантирует, что переносимость останется неизменной с течением времени.
Независимо от того, какое лекарство используется, постоянный контроль за лабораторными работами пациента имеет важное значение при лечении этих заболеваний. Метотрексат, азатиоприн и циклофосфамид могут подавлять способность пациента вырабатывать клетки крови. Если пациент проходит регулярные лабораторные исследования, за которыми тщательно наблюдают, это подавление производства клеток будет обнаружено, и доза лекарства может быть скорректирована или отменена в зависимости от степени тяжести. Циклофосфамид также имеет важные побочные эффекты, такие как снижение фертильности у более молодых пациентов, а также повышенный риск развития рака мочевого пузыря.Использование ритуксимаба в редких случаях связано с повышенным риском инфекции головного мозга, которая может быть опасной для жизни.
Перспективы / Прогноз
Каковы перспективы для людей с гранулематозом и полиангиитом (ГПД)?
После достижения ремиссии возможно повторение GPA (часто называемое «рецидивом»).Рецидивы могут быть похожи на те, которые испытывал пациент во время постановки диагноза, или симптомы могут отличаться. Вероятность серьезного рецидива можно свести к минимуму, если незамедлительно сообщать врачу о любых новых симптомах, регулярно осматривать врача и проводить постоянный мониторинг с помощью лабораторных тестов и визуализации. Подход к лечению рецидивов аналогичен лечению недавно диагностированного заболевания.
GPA — очень серьезное заболевание, лечение которого сопряжено со значительными рисками. Однако лечение может спасти жизнь, если диагноз поставлен своевременно и начато соответствующее лечение.
До признания эффективной терапии в 1970-х годах половина всех пациентов с этим заболеванием умирала в течение 5 месяцев после постановки диагноза. Сегодня более 80% пролеченных пациентов живы по крайней мере восемь лет спустя. Многие люди со средним баллом успеваемости продемонстрировали долгосрочное выживание, когда многие из них могут вести относительно нормальный образ жизни. Если прошлое является прелюдией к будущему, текущие исследования приведут к дальнейшим открытиям и даже лучшему лечению.
Гранулематоз с полиангиитом (GPA, ранее назывался Wegener’s)
Обзор
Что такое гранулематоз с полиангиитом (GPA, ранее называвшийся синдромом Вегенера)?
Гранулематоз с полиангиитом (GPA, ранее называвшийся болезнью Вегенера) — редкое заболевание неизвестной причины.Это результат воспаления в тканях, называемого гранулематозным воспалением и воспалением кровеносных сосудов («васкулит»), которое может повредить системы органов. Области, наиболее часто поражаемые GPA, включают пазухи, легкие и почки, но может быть поражен любой участок.
Что такое васкулит?
Васкулит — это общий термин, обозначающий воспаление кровеносных сосудов. При воспалении кровеносный сосуд может ослабнуть и растянуться, образуя аневризму, или стать настолько тонким, что разорвется, что приведет к кровотечению в ткани.Васкулит также может вызвать сужение кровеносных сосудов до полного закрытия сосуда. Это может привести к повреждению органов из-за потери кислорода и питательных веществ, поступающих с кровью.
Каковы особенности гранулематоза с полиангиитом (ГПА)?
GPA в первую очередь влияет на верхние дыхательные пути (пазухи, нос, трахею [верхний воздуховод]), легкие и почки. Также может быть поражен любой другой орган в организме.
Симптомы GPA и их тяжесть у разных пациентов различаются.Общие признаки заболевания могут включать:
- Потеря аппетита
- Похудание
- Лихорадка
- Усталость
Большинство пациентов сначала замечают симптомы в дыхательных путях. Симптомы могут включать:
- Постоянный насморк (также называемый ринореей) или образование корок и язв в носу
- Боль в носу или лице
- Носовое кровотечение или необычные выделения из носа, вызванные воспалением носа или пазух
- Кашель, который может включать кровавую мокроту, вызванную воспалением верхних или нижних дыхательных путей (легких)
- Дискомфорт в груди с одышкой или без нее
- Воспаление среднего уха (также называемое средним отитом), боль или потеря слуха
- Изменение голоса, хрипы или одышка, вызванные воспалением трахеи
Другие возможные функции:
- Воспаление глаза и / или давление за глазом, затрудняющее движение глаз, с потерей зрения или без нее
- Боль в суставах (артрит) или боль в мышцах
- Сыпь или кожные язвы
- Воспаление почек (хотя воспаление почек является обычным явлением, обычно оно не связано с такими симптомами, как боль).
Кто страдает гранулематозом с полиангиитом (ГПА)?
GPA может быть у людей любого возраста. Пиковая возрастная группа заболевания — от 40 до 60 лет. Похоже, это одинаково влияет на мужчин и женщин.
Симптомы и причины
Что вызывает гранулематоз при полиангиите (ГПА)?
Причина GPA неизвестна.GPA не является формой рака, не заразен и обычно не возникает в семьях. Данные исследовательских лабораторий убедительно подтверждают идею о том, что иммунная система играет решающую роль в GPA, так что иммунная система вызывает воспаление и повреждение кровеносных сосудов и тканей.
Диагностика и тесты
Как диагностируется гранулематоз с полиангиитом (ГПА)?
GPA имеет симптомы, схожие с рядом других расстройств, что может затруднить диагностику.Однако для наиболее эффективного и успешного лечения критически важна ранняя диагностика.
При подозрении на диагноз ГПД часто выполняется биопсия (образец ткани) пораженного участка, чтобы попытаться подтвердить наличие васкулита. Биопсия рекомендуется только для тех участков органов, в которых обнаружены отклонения от нормы при осмотре, лабораторных исследованиях или визуализации.
Это сочетание симптомов, результатов медицинского осмотра, лабораторных тестов, рентгеновских лучей, а иногда и биопсии (образца) пораженной ткани (кожи, носовых оболочек, пазух, легких, почек или других участков), которые вместе подтверждают диагноз. GPA.После лечения эти факторы также имеют решающее значение при оценке активности заболевания или ремиссии.
Положительный анализ крови на антинейтрофильные цитоплазматические антитела (ANCA) может подтвердить подозрение на диагноз заболевания. Однако этот анализ крови сам по себе не подтверждает диагноз GPA и не определяет активность заболевания.
GPA часто поражает легкие. У пациентов с ГПД, у которых нет легочных симптомов (кашель или одышка), визуализирующие тесты (обычные рентгеновские снимки или компьютерная томография) выявляют аномалии легких примерно в одной трети случаев.Следовательно, важно выполнять снимки легких при подозрении на активный ГПД, даже если у вас нет никаких симптомов заболевания легких.
Ведение и лечение
Как лечится гранулематоз с полиангиитом (ГПА)?
Поскольку GPA часто представляет собой опасное для жизни заболевание, его лечат различными мощными лекарствами, которые, как было доказано, спасают жизнь.Лекарства, подавляющие иммунную систему, составляют основу лечения GPA. Степень тяжести заболевания в каждом отдельном случае определяет, какие иммуносупрессивные препараты используются. Существует множество иммуносупрессивных препаратов, которые используются при GPA, каждое из которых имеет индивидуальные побочные эффекты.
Людей с ГПД с поражением критических систем органов обычно лечат кортикостероидами в сочетании с другими иммуносупрессивными препаратами, такими как циклофосфамид (Cytoxan®) или ритуксимаб (Rituxan®).У пациентов с менее тяжелым ГПД вначале можно использовать кортикостероиды и метотрексат. Цель лечения — остановить все травмы, возникающие в результате GPA. Если активность болезни можно полностью «выключить», это называется «ремиссией». Как только становится очевидным, что болезнь улучшается, врачи постепенно снижают дозу кортикостероидов и в конечном итоге надеются полностью отменить ее. Когда используется циклофосфамид, его назначают только до момента ремиссии (обычно от 3 до 6 месяцев), после чего его переключают на другой иммунодепрессант, такой как метотрексат, азатиоприн (Imuran®) или микофенолят мофетил (Cellcept®). ) для поддержания ремиссии.Продолжительность лечения поддерживающими иммуносупрессивными препаратами может варьироваться в зависимости от человека. В большинстве случаев его дают как минимум в течение 2 лет, прежде чем будет рассмотрен вопрос о медленном снижении дозы до прекращения приема.
Все эти лекарства также используются для лечения других заболеваний. Азатиоприн и микофенолят мофетил используются для предотвращения отторжения трансплантата органов. Метотрексат используется для лечения ревматоидного артрита и псориаза. И циклофосфамид, и метотрексат назначаются в высоких дозах для лечения определенных типов рака и поэтому иногда называются «химиотерапией».«При лечении рака эти лекарства работают, убивая или замедляя рост быстро размножающихся раковых клеток. При васкулите эти лекарства вводятся в дозах, которые от 10 до 100 раз ниже, чем те, которые используются для лечения рака, и их основной эффект заключается в том, чтобы влиять на поведение иммунной системы таким образом, что приводит к иммуносупрессии. Ритуксимаб относится к классу лекарств, называемых биологическими агентами, которые нацелены на определенный элемент иммунной системы. Недавние исследования показали, что ритуксимаб был так же эффективен, как циклофосфамид, для лечения тяжелого активного GPA.
Какие побочные эффекты связаны с лечением гранулематоза с полиангиитом (ГПА)?
Поскольку эти лекарства подавляют иммунную систему, существует повышенный риск развития серьезных инфекций. Каждый иммунодепрессивный препарат также имеет уникальный набор потенциальных побочных эффектов. Мониторинг побочных эффектов, связанных с каждым лекарством, имеет решающее значение для предотвращения или минимизации их возникновения. Кроме того, тот факт, что пациент может изначально переносить лечение, не гарантирует, что переносимость останется неизменной с течением времени.
Независимо от того, какое лекарство используется, постоянный контроль за лабораторными работами пациента имеет важное значение при лечении этих заболеваний. Метотрексат, азатиоприн и циклофосфамид могут подавлять способность пациента вырабатывать клетки крови. Если пациент проходит регулярные лабораторные исследования, за которыми тщательно наблюдают, это подавление производства клеток будет обнаружено, и доза лекарства может быть скорректирована или отменена в зависимости от степени тяжести. Циклофосфамид также имеет важные побочные эффекты, такие как снижение фертильности у более молодых пациентов, а также повышенный риск развития рака мочевого пузыря.Использование ритуксимаба в редких случаях связано с повышенным риском инфекции головного мозга, которая может быть опасной для жизни.
Перспективы / Прогноз
Каковы перспективы для людей с гранулематозом и полиангиитом (ГПД)?
После достижения ремиссии возможно повторение GPA (часто называемое «рецидивом»).Рецидивы могут быть похожи на те, которые испытывал пациент во время постановки диагноза, или симптомы могут отличаться. Вероятность серьезного рецидива можно свести к минимуму, если незамедлительно сообщать врачу о любых новых симптомах, регулярно осматривать врача и проводить постоянный мониторинг с помощью лабораторных тестов и визуализации. Подход к лечению рецидивов аналогичен лечению недавно диагностированного заболевания.
GPA — очень серьезное заболевание, лечение которого сопряжено со значительными рисками. Однако лечение может спасти жизнь, если диагноз поставлен своевременно и начато соответствующее лечение.
До признания эффективной терапии в 1970-х годах половина всех пациентов с этим заболеванием умирала в течение 5 месяцев после постановки диагноза. Сегодня более 80% пролеченных пациентов живы по крайней мере восемь лет спустя. Многие люди со средним баллом успеваемости продемонстрировали долгосрочное выживание, когда многие из них могут вести относительно нормальный образ жизни. Если прошлое является прелюдией к будущему, текущие исследования приведут к дальнейшим открытиям и даже лучшему лечению.
Гранулематоз с полиангиитом (GPA, ранее назывался Wegener’s)
Обзор
Что такое гранулематоз с полиангиитом (GPA, ранее называвшийся синдромом Вегенера)?
Гранулематоз с полиангиитом (GPA, ранее называвшийся болезнью Вегенера) — редкое заболевание неизвестной причины.Это результат воспаления в тканях, называемого гранулематозным воспалением и воспалением кровеносных сосудов («васкулит»), которое может повредить системы органов. Области, наиболее часто поражаемые GPA, включают пазухи, легкие и почки, но может быть поражен любой участок.
Что такое васкулит?
Васкулит — это общий термин, обозначающий воспаление кровеносных сосудов. При воспалении кровеносный сосуд может ослабнуть и растянуться, образуя аневризму, или стать настолько тонким, что разорвется, что приведет к кровотечению в ткани.Васкулит также может вызвать сужение кровеносных сосудов до полного закрытия сосуда. Это может привести к повреждению органов из-за потери кислорода и питательных веществ, поступающих с кровью.
Каковы особенности гранулематоза с полиангиитом (ГПА)?
GPA в первую очередь влияет на верхние дыхательные пути (пазухи, нос, трахею [верхний воздуховод]), легкие и почки. Также может быть поражен любой другой орган в организме.
Симптомы GPA и их тяжесть у разных пациентов различаются.Общие признаки заболевания могут включать:
- Потеря аппетита
- Похудание
- Лихорадка
- Усталость
Большинство пациентов сначала замечают симптомы в дыхательных путях. Симптомы могут включать:
- Постоянный насморк (также называемый ринореей) или образование корок и язв в носу
- Боль в носу или лице
- Носовое кровотечение или необычные выделения из носа, вызванные воспалением носа или пазух
- Кашель, который может включать кровавую мокроту, вызванную воспалением верхних или нижних дыхательных путей (легких)
- Дискомфорт в груди с одышкой или без нее
- Воспаление среднего уха (также называемое средним отитом), боль или потеря слуха
- Изменение голоса, хрипы или одышка, вызванные воспалением трахеи
Другие возможные функции:
- Воспаление глаза и / или давление за глазом, затрудняющее движение глаз, с потерей зрения или без нее
- Боль в суставах (артрит) или боль в мышцах
- Сыпь или кожные язвы
- Воспаление почек (хотя воспаление почек является обычным явлением, обычно оно не связано с такими симптомами, как боль).
Кто страдает гранулематозом с полиангиитом (ГПА)?
GPA может быть у людей любого возраста. Пиковая возрастная группа заболевания — от 40 до 60 лет. Похоже, это одинаково влияет на мужчин и женщин.
Симптомы и причины
Что вызывает гранулематоз при полиангиите (ГПА)?
Причина GPA неизвестна.GPA не является формой рака, не заразен и обычно не возникает в семьях. Данные исследовательских лабораторий убедительно подтверждают идею о том, что иммунная система играет решающую роль в GPA, так что иммунная система вызывает воспаление и повреждение кровеносных сосудов и тканей.
Диагностика и тесты
Как диагностируется гранулематоз с полиангиитом (ГПА)?
GPA имеет симптомы, схожие с рядом других расстройств, что может затруднить диагностику.Однако для наиболее эффективного и успешного лечения критически важна ранняя диагностика.
При подозрении на диагноз ГПД часто выполняется биопсия (образец ткани) пораженного участка, чтобы попытаться подтвердить наличие васкулита. Биопсия рекомендуется только для тех участков органов, в которых обнаружены отклонения от нормы при осмотре, лабораторных исследованиях или визуализации.
Это сочетание симптомов, результатов медицинского осмотра, лабораторных тестов, рентгеновских лучей, а иногда и биопсии (образца) пораженной ткани (кожи, носовых оболочек, пазух, легких, почек или других участков), которые вместе подтверждают диагноз. GPA.После лечения эти факторы также имеют решающее значение при оценке активности заболевания или ремиссии.
Положительный анализ крови на антинейтрофильные цитоплазматические антитела (ANCA) может подтвердить подозрение на диагноз заболевания. Однако этот анализ крови сам по себе не подтверждает диагноз GPA и не определяет активность заболевания.
GPA часто поражает легкие. У пациентов с ГПД, у которых нет легочных симптомов (кашель или одышка), визуализирующие тесты (обычные рентгеновские снимки или компьютерная томография) выявляют аномалии легких примерно в одной трети случаев.Следовательно, важно выполнять снимки легких при подозрении на активный ГПД, даже если у вас нет никаких симптомов заболевания легких.
Ведение и лечение
Как лечится гранулематоз с полиангиитом (ГПА)?
Поскольку GPA часто представляет собой опасное для жизни заболевание, его лечат различными мощными лекарствами, которые, как было доказано, спасают жизнь.Лекарства, подавляющие иммунную систему, составляют основу лечения GPA. Степень тяжести заболевания в каждом отдельном случае определяет, какие иммуносупрессивные препараты используются. Существует множество иммуносупрессивных препаратов, которые используются при GPA, каждое из которых имеет индивидуальные побочные эффекты.
Людей с ГПД с поражением критических систем органов обычно лечат кортикостероидами в сочетании с другими иммуносупрессивными препаратами, такими как циклофосфамид (Cytoxan®) или ритуксимаб (Rituxan®).У пациентов с менее тяжелым ГПД вначале можно использовать кортикостероиды и метотрексат. Цель лечения — остановить все травмы, возникающие в результате GPA. Если активность болезни можно полностью «выключить», это называется «ремиссией». Как только становится очевидным, что болезнь улучшается, врачи постепенно снижают дозу кортикостероидов и в конечном итоге надеются полностью отменить ее. Когда используется циклофосфамид, его назначают только до момента ремиссии (обычно от 3 до 6 месяцев), после чего его переключают на другой иммунодепрессант, такой как метотрексат, азатиоприн (Imuran®) или микофенолят мофетил (Cellcept®). ) для поддержания ремиссии.Продолжительность лечения поддерживающими иммуносупрессивными препаратами может варьироваться в зависимости от человека. В большинстве случаев его дают как минимум в течение 2 лет, прежде чем будет рассмотрен вопрос о медленном снижении дозы до прекращения приема.
Все эти лекарства также используются для лечения других заболеваний. Азатиоприн и микофенолят мофетил используются для предотвращения отторжения трансплантата органов. Метотрексат используется для лечения ревматоидного артрита и псориаза. И циклофосфамид, и метотрексат назначаются в высоких дозах для лечения определенных типов рака и поэтому иногда называются «химиотерапией».«При лечении рака эти лекарства работают, убивая или замедляя рост быстро размножающихся раковых клеток. При васкулите эти лекарства вводятся в дозах, которые от 10 до 100 раз ниже, чем те, которые используются для лечения рака, и их основной эффект заключается в том, чтобы влиять на поведение иммунной системы таким образом, что приводит к иммуносупрессии. Ритуксимаб относится к классу лекарств, называемых биологическими агентами, которые нацелены на определенный элемент иммунной системы. Недавние исследования показали, что ритуксимаб был так же эффективен, как циклофосфамид, для лечения тяжелого активного GPA.
Какие побочные эффекты связаны с лечением гранулематоза с полиангиитом (ГПА)?
Поскольку эти лекарства подавляют иммунную систему, существует повышенный риск развития серьезных инфекций. Каждый иммунодепрессивный препарат также имеет уникальный набор потенциальных побочных эффектов. Мониторинг побочных эффектов, связанных с каждым лекарством, имеет решающее значение для предотвращения или минимизации их возникновения. Кроме того, тот факт, что пациент может изначально переносить лечение, не гарантирует, что переносимость останется неизменной с течением времени.
Независимо от того, какое лекарство используется, постоянный контроль за лабораторными работами пациента имеет важное значение при лечении этих заболеваний. Метотрексат, азатиоприн и циклофосфамид могут подавлять способность пациента вырабатывать клетки крови. Если пациент проходит регулярные лабораторные исследования, за которыми тщательно наблюдают, это подавление производства клеток будет обнаружено, и доза лекарства может быть скорректирована или отменена в зависимости от степени тяжести. Циклофосфамид также имеет важные побочные эффекты, такие как снижение фертильности у более молодых пациентов, а также повышенный риск развития рака мочевого пузыря.Использование ритуксимаба в редких случаях связано с повышенным риском инфекции головного мозга, которая может быть опасной для жизни.
Перспективы / Прогноз
Каковы перспективы для людей с гранулематозом и полиангиитом (ГПД)?
После достижения ремиссии возможно повторение GPA (часто называемое «рецидивом»).Рецидивы могут быть похожи на те, которые испытывал пациент во время постановки диагноза, или симптомы могут отличаться. Вероятность серьезного рецидива можно свести к минимуму, если незамедлительно сообщать врачу о любых новых симптомах, регулярно осматривать врача и проводить постоянный мониторинг с помощью лабораторных тестов и визуализации. Подход к лечению рецидивов аналогичен лечению недавно диагностированного заболевания.
GPA — очень серьезное заболевание, лечение которого сопряжено со значительными рисками. Однако лечение может спасти жизнь, если диагноз поставлен своевременно и начато соответствующее лечение.
До признания эффективной терапии в 1970-х годах половина всех пациентов с этим заболеванием умирала в течение 5 месяцев после постановки диагноза. Сегодня более 80% пролеченных пациентов живы по крайней мере восемь лет спустя. Многие люди со средним баллом успеваемости продемонстрировали долгосрочное выживание, когда многие из них могут вести относительно нормальный образ жизни. Если прошлое является прелюдией к будущему, текущие исследования приведут к дальнейшим открытиям и даже лучшему лечению.
Гранулематоз с полиангиитом (Вегенера) — Johns Hopkins
Первое описание
Первый случай был описан Хайнцем Клингером, немецким студентом-медиком, в 1931 году.Несколько лет спустя немецкий патолог Фридрих Вегенер описал еще 3 случая и признал заболевание отдельной формой васкулита. Другие названия, которые иногда используются для гранулематоза с полиангиитом, — это артериит Вегенера или болезнь Вегенера .
Кто заболевает гранулематозом и полиангиитом?
Гранулематоз с полиангиитом почти одинаково распространен между полами, с небольшим преобладанием мужчин. Гранулематоз с полиангиитом обычно возникает в среднем возрасте, но встречается у людей всех возрастов.Хотя гранулематоз с полиангиитом возникает в детстве, это не является необычным для пациента, страдающего гранулематозом с полиангиитом, на момент постановки диагноза в возрасте 70 или даже 80 лет.
На фото ниже представлен рентген грудной клетки, показывающий двусторонние узелки в легких у 27-летнего индийского мужчины с гранулематозом с полиангиитом.
На рисунке ниже показана компьютерная томография того же пациента. Изображение представляет собой поперечный разрез легких пациента.Компьютерная томография не только позволяет лучше оценить размер поражений, но и выявляет больше поражений.
Гранулематоз с полиангиитом может поражать практически любой участок тела, но имеет предрасположенность к определенным органам. Классическими органами, участвующими в гранулематозе с полиангиитом, являются верхние дыхательные пути (пазухи, нос, уши и трахея [«дыхательное горло»]), легкие и почки. Ниже перечислены органы, обычно участвующие в гранулематозе с полиангиитом, и конкретные проявления заболевания в каждом органе.
Ухо
Ушные инфекции, которые медленно проходят. Рецидивирующий средний отит. Снижение слуха.
Глаз
Воспаление может возникать в разных частях глаза. Воспаление белой части глаза известно как склера («склерит»). «Увеит» — это воспаление глаза. Воспаление за глазом известно как «псевдоопухоль глазницы». Псевдоопухоль орбиты, например, вызванная гранулематозом с полиангиитом, может вызывать «проптоз» или выпячивание одного глаза.
На рисунке ниже показано сканирование глаз с помощью компьютерной томографии (CAT) пациента с ретроорбитальной массой (массой за глазом) у мужчины с гранулематозом с полиангиитом. Подобные образования иногда вызывают резкую потерю зрения из-за растяжения или сжатия зрительного нерва, который входит в заднюю часть глаза.
Нос
Могут образовываться корки в носу и частые носовые кровотечения. Эрозия и перфорация носовой перегородки. Переносица может разрушиться, что приведет к «седловидной деформации носа». На фото ниже показан пример этой деформации до и после косметической операции. Это произошло в результате разрушения носовой перегородки, вызванного воспалением хряща. У этого пациента гранулематоз с полиангиитом, но идентичное поражение может возникнуть при рецидивирующем полихондрите.
Пазух
Хроническое воспаление носовых пазух, которое иногда приводит к разрушению тканей вокруг носовых пазух.
Трахея
Характерное осложнение дыхательных путей при гранулематозе с полиангиитом: сужение «дыхательного горла» чуть ниже голосовых связок, состояние, называемое «стенозом подсвязочного канала».Это сужение, вызванное воспалением и рубцеванием, вызывает затруднение дыхания и может после подострого прогрессирования потребовать экстренной трахеостомии. На рисунке ниже показаны два рисунка, которые показывают стеноз подсвязочного канала до (слева) и после (справа) операции, выполненной специалистом по уху, носу и горлу. Операция позволила резко улучшить дыхание пациента.
Легкие
Синдром, похожий на пневмонию, с «инфильтратами» легких можно увидеть на рентгенограмме грудной клетки.Может возникнуть кровотечение из легких.
Почки
Воспаление может возникать в почках, что приводит к небольшому (или, в редких случаях, большому) количеству крови и белка в моче. Это состояние называется гломерулонефритом. Если не лечить агрессивно, гранулематоз с поражением почек полиангиитом может привести к почечной недостаточности. Почечные образования могут возникать, но очень необычны при этом заболевании.
Изображение ниже является результатом анализа мочи пациента с воспалением почек.Когда гранулематоз с полиангиитом активен, эритроциты образуют комок или «слепок» (в белых скобках) в канальцах воспаленных почек. Эти «цилиндры» проходят через почечную систему и могут просматриваться под микроскопом в моче пациента.
Кожа
Гранулематоз с полиангиитом может вызывать многие виды кожной сыпи. Чаще всего сыпь возникает в виде маленьких пурпурных или красных точек на нижних конечностях (известная как «пальпируемая пурпура»).Недостаточный приток крови к пальцам рук и ног может привести к феномену Рейно (чрезмерная чувствительность пальцев к холоду) и даже к инфарктам кончиков пальцев рук и ног с развитием гангрены.
Суставы
Может возникнуть артрит с опуханием суставов и болью.
Нервы
Поражение периферических нервов приводит к онемению, покалыванию, стреляющей боли в конечностях, а иногда и к слабости в ступне, руке, руке или ноге.
Разное
Описан гранулематоз с полиангиитом, поражающим почти все органы, включая мозговые оболочки (слои защитной ткани вокруг головного и спинного мозга), предстательную железу и мочеполовые пути.Помимо поражения определенных органов, гранулематоз с полиангиитом также часто приводит к генерализованным симптомам усталости, субфебрильной температуре и потере веса.
Причина гранулематоза с полиангиитом неизвестна. По сравнению с заболеваниями с очевидной генетической предрасположенностью, генетика играет относительно небольшую роль в этиологии гранулематоза с полиангиитом. Очень редко гранулематоз с полиангиитом возникает у двух человек в одной семье.(Однако возможно, что существуют менее очевидные генетические факторы риска, например гены, которые могут предрасполагать пациента к инфицированию этиологическим организмом). Некоторое время подозревали, что инфекция вызывает (или, по крайней мере, способствует) гранулематоз с полиангиитом, но не было выявлено конкретной инфекции (бактериальной, вирусной, грибковой или другой).
Как диагностируется гранулематоз при полиангиите?
По возможности, важно подтвердить диагноз гранулематоза и полиангиита путем биопсии пораженного органа и выявления патологических признаков этого заболевания под микроскопом.Поскольку многие заболевания могут имитировать гранулематоз с полиангиитом (и наоборот), перед началом курса лечения важно быть как можно более уверенным в диагнозе. Мы обсуждаем некоторые из конкретных процедур биопсии, используемых для диагностики гранулематоза с полиангиитом, в разделе этого веб-сайта «Что такое васкулит: диагноз?».
Поскольку гранулематоз с полиангиитом очень часто поражает верхние дыхательные пути (носовые пазухи, нос, уши и трахею [«дыхательное горло»]), и поскольку биопсия этих тканей является неинвазивной процедурой относительно , то эти участки часто подвергаются биопсии у пациентов. подозревается на гранулематоз с полиангиитом.К сожалению, количество биопсий из этих участков довольно низкое: вероятно, менее 50%. Поэтому иногда для постановки диагноза требуются более инвазивные процедуры.
Биопсия легкого (открытая или торакоскопическая) часто является лучшим способом диагностики гранулематоза с полиангиитом. Достаточное количество ткани, получаемой с помощью этих процедур, обычно позволяет подтвердить гранулематоз с диагнозом полиангиит. Точно так же, хотя количество ткани, полученной при биопсии почки, обычно намного меньше, обнаружение определенных патологических особенностей в контексте общих симптомов, признаков и лабораторных тестов пациента часто является диагностическим.
С 1982 года, когда были впервые описаны ANCA (антинейтрофильные цитоплазматические антитела), роль этих антител в диагностике гранулематоза с полиангиитом возросла. Тестирование ANCA, которое включает в себя выполнение простого анализа крови, стало широко доступным в 1990-х годах. Это и хорошо, и плохо: использование тестов ANCA во многих случаях привело к более ранней диагностике и более быстрому назначению соответствующего лечения, но также привело к неправильному диагнозу и неправильному лечению, когда тесты не выполняются или интерпретируются неправильно.
Как следует из их названия, ANCA направлены против цитоплазмы (неядерной части) белых кровяных телец. Их точная роль в процессе болезни остается неясной, но представляет значительный исследовательский интерес. ANCA бывают двух основных форм: 1) C – ANCA [C означает цитоплазматический] и 2) P – ANCA [P означает перинуклеарный]. C – ANCA имеют особенно сильную связь с гранулематозом с полиангиитом (до 80% пациентов — и, возможно, больше пациентов с активным заболеванием — имеют эти антитела).Когда C – ANCA присутствуют в крови пациента, симптомы или признаки которого указывают на гранулематоз с полиангиитом, вероятность диагноза значительно возрастает. Однако в большинстве случаев ОЧЕНЬ ВАЖНО провести биопсию пораженного органа для подтверждения диагноза.
Лечение и курс гранулематоза с полиангиитом
До 1970-х годов гранулематоз с полиангиитом почти всегда был смертельным заболеванием. Использование преднизона и других стероидов помогло продлить жизнь пациентам, но большинство пациентов в конечном итоге умерли от болезни в течение нескольких месяцев или лет.Первое применение циклофосфамида в конце 1960-х годов изменило ужасный прогноз этого заболевания. Используя комбинацию циклофосфамида и преднизона, более 90% пациентов с тяжелым заболеванием реагируют на лечение, а 75% могут достичь ремиссии заболевания. К сожалению, гранулематоз с полиангиитом — заболевание, при котором часто возникают рецидивы. Примерно половина всех пациентов, достигших ремиссии болезни, в конечном итоге страдают рецидивами («обострениями»). Обострения гранулематоза с полиангиитом обычно поддаются лечению, вызвавшему ремиссию, но иногда требуется интенсификация лечения (например, переход на более сильные лекарства).
В течение 1990-х годов врачи все чаще использовали комбинацию метотрексата и преднизона, а не циклофосфамида и преднизона для лечения гранулематоза у пациентов с полиангиитом, у которых нет немедленного опасного для жизни заболевания (особенно заболевания, которое не затрагивает серьезно почки) из-за частоты серьезных побочных эффектов, связанных с последним режимом.
Бактрим (или Септра), комбинация двух антибиотиков (триметоприма и сульфаметоксазола) также может быть полезной при лечении гранулематоза с полиангиитом, особенно у пациентов, заболевание которых ограничено в основном верхними дыхательными путями.Большое многоцентровое исследование показало, что Бактрим полезен для предотвращения обострений гранулематоза с полиангиитом в верхних дыхательных путях.
Что нового при гранулематозе с полиангиитом?
За последние несколько лет в понимании гранулематоза и полиангиита были достигнуты значительные успехи, хотя многие важные вопросы остаются. В дополнение к лучшему пониманию того, как использовать имеющиеся в настоящее время лекарства от гранулематоза и полиангиита, вполне вероятно, что в ближайшие несколько лет будут разработаны новые лекарства от этого заболевания.Научные открытия могут привести к разработке более специфических модуляторов иммунной системы, которые принесут большую пользу пациентам с гранулематозом и полиангиитом.
С медицинской точки зрения, Дэвид Хеллманн, доктор медицины
Обсуждение гранулематоза с полиангиитом, написанное в медицинских терминах Дэвидом Хеллманном, доктором медицины (FACP), Центр васкулита Джонса Хопкинса, для отдела ревматологии Программы самооценки медицинских знаний, опубликованное и защищенное авторским правом Американского колледжа врачей (издание 11, 1998).Американский колледж врачей дал нам разрешение сделать эту информацию доступной для пациентов, обращающихся к нашему веб-сайту
Гранулематоз с полиангиитом — это заболевание, включающее гранулематозное воспаление, некроз и васкулит, которое чаще всего поражает верхние дыхательные пути, нижние дыхательные пути и почки. Хотя гранулематоз с полиангиитом может начаться в любом возрасте, средний возраст возникновения составляет около 40 лет. Другие органы, часто поражаемые гранулематозом с гранулематозом полиангиита, включают глаз (проптоз и двоение в глазах из-за ретроорбитальной псевдоопухоли, склерит), кожу (язвы, пурпура).или периферический нерв (множественный мононеврит). Гранулематоз с полиангиитом может быть ограничен одним местом в течение многих месяцев или лет до распространения. Системные симптомы (лихорадка, утомляемость, потеря веса) также нередки. Анемия, легкий лейкоцитоз и повышенная скорость оседания эритроцитов (СОЭ) являются неспецифическими лабораторными данными. Рентгенограммы грудной клетки часто показывают инфильтраты, узелки, образования или полости; только внутригрудная лимфаденопатия несовместима с диагнозом гранулематоз с полиангиитом. КТ грудной клетки более чувствительна, чем рентгенография грудной клетки, и может быть ненормальной при отрицательной рентгенограмме грудной клетки.Гломерулонефрит вызывает гематурию, цилиндры эритроцитов и протеинурию.
Новая группа аутоантител, ANCA, помогает в диагностике гранулематоза, полиангиита и родственных форм васкулита и дает представление о патогенезе этих заболеваний. ANCA направлены против ферментов, содержащихся в первичных гранулах нейтрофилов и моноцитов. Различают два основных типа ANCA. C-ANCA направлены против сериновой протеиназы 3 и относительно чувствительны и высокоспецифичны для гранулематоза с полиангиитом.P-ANCA направлены против миелопероксидазы и других антигенов и не являются специфичными для какой-либо отдельной формы васкулита, но были замечены у некоторых пациентов с гранулематозом с полиангиитом, узловым полиартериитом, васкулитом Чарджа-Стросса и некоторыми формами слабого иммунного гломерулонефрита. (так называемый микроскопический узелковый полиартериит). Некоторые пациенты с легочно-почечными синдромами, которые могут не соответствовать критериям гранулематоза с полиангиитом, также являются серопозитивными по отношению к ANCA. Некоторые пациенты с воспалительным заболеванием кишечника, ревматоидным артритом или СКВ могут иметь атипичные результаты теста P-ANCA, основанные на аутоантителах, направленных против других компонентов нейтрофилов, таких как лактоферрин.
ANCA могут быть не только маркерами гранулематоза с полиангиитом и родственными заболеваниями, но они также могут быть участниками патогенеза. Исследования показывают, что когда нейтрофилы подвергаются воздействию цитокинов, таких как фактор некроза опухоли, небольшие количества сериновой протеиназы и миелопероксидазы, мишени для ANCA, экспрессируются на поверхности нейтрофилов. Добавление ANCA к этим цитокин-примированным нейтрофилам заставляет их генерировать кислородные радикалы и высвобождать ферменты, способные повредить кровеносные сосуды.
Диагноз «Гранулематоз и полиангиит» наиболее надежно устанавливается с помощью биоптатов, показывающих триаду васкулита, гранулем и обширных участков некроза (известного как географический некроз), смешанных с острыми и хроническими воспалительными клетками. Только большие срезы легочной ткани, полученные с помощью торакоскопической или открытой биопсии легких, вероятно, покажут все гистологические особенности. Однако более легко получаемые образцы биопсии носа или носовых пазух могут показать некоторые изменения, которые сильно указывают на гранулематоз с полиангиитом.Такой образец биопсии в сочетании с совместимой клинической картиной и серопозитивностью на C-ANCA должен быть достаточным для подтверждения диагноза. Серопозитивность только на C-ANCA недостаточно специфична для установления диагноза гранулематоза с полиангиитом.
Не леченный гранулематоз с полиангиитом приводит к летальному исходу. Преднизон может замедлить прогрессирование болезни, но сам по себе недостаточен для купирования болезни. Заболевание дыхательных путей обычно прогрессирует медленно, но заболевание почек может прогрессировать быстро и поэтому требует срочного обследования и лечения.При традиционном лечении преднизоном (начальное с 1 мг / кг в день в течение 1-2 месяцев, затем с постепенным снижением) и циклофосфамидом (2 мг / кг в день в течение как минимум 12 месяцев) более чем у 90% пациентов наблюдается улучшение, а у 75% — ремиссия. Однако у 50% пациентов, у которых позже наступает рецидив, также наблюдаются рецидивы, а ежедневный пероральный прием циклофосфамида вызывает серьезную токсичность. Кратковременная токсичность включает цитопению, инфекцию и геморрагический цистит. Длительное применение циклофосфамида у пациентов с гранулематозом и полиангиитом более чем вдвое увеличивает риск рака в целом, увеличивает риск рака мочевого пузыря в 33 раза и риск лимфомы в 11 раз.Ежемесячное внутривенное введение циклофосфамида менее токсично, но и менее эффективно. Еженедельно метотрексат является эффективной альтернативой гранулематозу с полиангиитом, который не представляет непосредственной угрозы для жизни, а также полезен для поддержания ремиссии. Роль триметоприм-сульфаметоксазола в лечении активного заболевания противоречива: одни считают его эффективным при гранулематозе с полиангиитом, ограниченным дыхательными путями, а другие — нет. У пациентов, достигших ремиссии, триметоприм-сульфаметоксазол снижает частоту рецидивов.
Анализ подхода
, обнаружение ANCA, рентгенография и компьютерная томография
Фаучи А.С., Хейнс Б.С., Кац П., Вольф С.М. Гранулематоз Вегенера: проспективный клинический и терапевтический опыт с 85 пациентами в течение 21 года. Энн Интерн Мед. . Январь 1983 г. 98 (1): 76-85. [Медлайн].
Manganelli P, Fietta P, Carotti M, Pesci A, Salaffi F. Участие дыхательной системы в системном васкулите. Clin Exp Rheumatol . Март-апрель 2006 г.24: S48-S59. [Медлайн].
Hoffman GS, Kerr GS, Leavitt RY, et al. Гранулематоз Вегенера: анализ 158 больных. Энн Интерн Мед. . 1992 15 марта. 116 (6): 488-98. [Медлайн].
Мухтяр С., Гильевин Л., Сид М.К. и др. Рекомендации EULAR по лечению первичного васкулита малых и средних сосудов. Энн Рум Дис . March 2009. 68: 310-317. [Медлайн].
Джейн Д., Расмуссен Н., Андрасси К. и др.Рандомизированное исследование поддерживающей терапии васкулита, связанного с антинейтрофильными цитоплазматическими антителами. N Engl J Med . Июль 2003. 349 (1): 36-44. [Медлайн].
Metzler C, Miehle N, Manger K и др. Повышенная частота рецидивов при пероральном приеме метотрексата по сравнению с лефлуномидом для поддержания ремиссии при гранулематозе Вегенера. Ревматология (Оксфорд) . Июль 2007. 46 (7): 1087-1091. [Медлайн].
Falk RJ, Gross WL, Guillevin L, et al.Гранулематоз с полиангиитом (болезнь Вегенера): альтернативное название гранулематоза Вегенера. Энн Рум Дис . 2011. 70: 704. [Медлайн].
Ливитт Р.Ю., Фаучи А.С., Блох Д.А. и др. Критерии классификации гранулематоза Вегенера, принятые в 1990 г. Американским колледжем ревматологии. Революционный артрит . August 1990. 33 (8): 1101-1107. [Медлайн].
Исследовательская группа по исследованию гранулематоза и этанерцепта Вегенера (WGET).Ограниченный гранулематоз Вегенера по сравнению с тяжелым: исходные данные о пациентах в исследовании гранулематоза Вегенера с этанерцептом. Революционный артрит . Август 2003. 48 (8): 2299-2309. [Медлайн].
Финкельман Дж. Д., Ли А. С., Хаммел А. М. и др. ANCA выявляются почти у всех пациентов с активным тяжелым гранулематозом Вегенера. Am J Med . Июль 2007. 120: 643.e9-14. [Медлайн].
Boomsma MM, Stegeman CA, van der Leij MJ, et al.Прогнозирование рецидивов гранулематоза Вегенера путем измерения уровней антинейтрофильных цитоплазматических антител: проспективное исследование. Революционный артрит . Сентябрь 2000. 43 (9): 2025-33. [Медлайн].
Финкельман Дж. Д., Меркель П. А., Шредер Д. и др. Антинейтрофильные цитоплазматические антитела к антипротеиназе 3 и активность заболевания при гранулематозе Вегенера. Энн Интерн Мед. . Ноябрь 2007. 147 (9): 611-9. [Медлайн].
Исследовательская группа по исследованию гранулематоза и этанерцепта Вегенера (WGET).Этанерцепт плюс стандартная терапия гранулематоза Вегенера. N Engl J Med . 2005 27 января. 352 (4): 351-61. [Медлайн].
Schlieben DJ, Korbet SM, Kimura RE, Schwartz MM, Lewis EJ. Легочно-почечный синдром у новорожденного с плацентарной передачей ANCA. Am J Kidney Dis . 2005 апр. 45 (4): 758-61. [Медлайн].
Stegeman CA, Tervaert JW, Sluiter WJ, Manson WL, de Jong PE, Kallenberg CG. Связь хронического носительства Staphylococcus aureus через нос и более высокой частоты рецидивов гранулематоза Вегенера. Энн Интерн Мед. . Январь 1994. 120 (1): 12-17. [Медлайн].
Stone JH, Merkel PA, Spiera R, Seo P, Langford CA, Hoffman GS, et al. Ритуксимаб в сравнении с циклофосфамидом при ANCA-ассоциированном васкулите. N Engl J Med . 15 июля 2010 г. 363 (3): 221-32. [Медлайн].
Джонс Р. Б., Терверт Дж. В., Хаузер Т. и др. Ритуксимаб в сравнении с циклофосфамидом при ANCA-ассоциированном почечном васкулите. N Engl J Med . Июль 2010. 363 (3): 211-20.[Медлайн].
Калленберг CGM. Патогенез PR3-ANCA-ассоциированного васкулита. J Аутоиммунный . Февраль-март 2008. 30: 29-36. [Медлайн].
Falk RJ, Terrell RS, Charles LA, Jennett C. Антинейтрофильные цитоплазматические аутоантитела индуцируют дегрануляцию нейтрофилов и выработку кислородных радикалов in vitro. Proc Natl Acad Sci USA . June 1990. 87: 4115-4119.
Калленберг CGM. Патофизиология ANCA-ассоциированного васкулита мелких сосудов. Curr Rheumatol Rep . Декабрь 2010. 12 (6): 399-405. [Медлайн].
Сяо Х., Херинга П., Лю З. и др. Роль нейтрофилов в индукции гломерулонефрита антителами против миелопероксидазы. Ам Дж. Патол . Июль 2005. 167 (1): 39-45. [Медлайн].
Kallenberg CGM, Heeringa P, Stegeman CA. Механизмы заболевания: патогенез и лечение ANCA-ассоциированного васкулита. Нат Клин Практик Ревматол .Декабрь 2006. 2: 661-670. [Медлайн].
Moosig F, Lamprecht P, Gross WL. Гранулематоз Вегенера: современная точка зрения. Clin Rev Allergy Immunol . Октябрь 2008. 35 (1-2): 19-21. [Медлайн].
Spagnolo P, Richeldi L, DuBois RM. Триггеры окружающей среды и факторы восприимчивости при идиопатических гранулематозных заболеваниях. Semin Respir Crit Care Med . Декабрь 2008. 29: 610-619. [Медлайн].
Carr EJ, Niederer HA, Williams J, et al.Подтверждение генетической ассоциации CTLA4 и PTPN22 с ANCA-ассоциированным васкулитом. BMC Med Genet . Декабрь 2009. 10: 121. [Медлайн].
Ягайло П., Овен П., Арнинг Л. и др. Аллель PTPN22 620W является фактором риска гранулематоза Вегенера. Революционный артрит . Декабрь 2005. 52 (12): 4039-43. [Медлайн].
Heckmann M, Holle JU, Arning L, et al. Локус количественного признака гранулематоза Вегенера на хромосоме 6p21.3, что характеризует генотипирование tagSNP. Энн Рум Дис . Июль 2008. 67 (7): 972-9. [Медлайн].
Pendergraft WF 3rd, Preston GA, Shah RR, et al. Аутоиммунитет запускается cPR-3 (105-201), белком, комплементарным аутоантигенной протеиназе-3 человека. Нат Мед . Январь 2004. 10 (1): 72-9. [Медлайн].
Каин Р., Экснер М., Брандес Р. и др. Молекулярная мимикрия при слабоммунном фокально-некротическом гломерулонефрите. Нат Мед .Октябрь 2008. 14 (10): 1088-96. [Медлайн].
Hogan SL, Cooper GS, Savitz DA, et al. Связь воздействия диоксида кремния с антинейтрофильными цитоплазматическими аутоантителами васкулитом мелких сосудов: популяционное исследование случай-контроль. Clin J Am Soc Nephrol . Март 2007. 2 (2): 290-9. [Медлайн].
Watts RA, Lane SE, Koldingsnes W. et al. Эпидемиология васкулитов в Европе. Энн Рум Дис . Декабрь 2001. 60 (12): 1156-7.[Медлайн].
Lane SE, Watts R, Scott DGI. Эпидемиология системных васкулитов. Curr Rheumatol Rep . Август 2005. 7: 270-275. [Медлайн].
Iudici M, Quartier P, Terrier B, Mouthon L, Guillevin L, Puéchal X. Детский гранулематоз с полиангиитом и микроскопическим полиангиитом: систематический обзор и метаанализ. Орфанет J Редкие Dis . 2016 22 октября. 11 (1): 141. [Медлайн]. [Полный текст].
Мухтяр С, Флоссманн О, Хельмих Б и др.Результаты исследований васкулита, ассоциированного с антинейтрофильными цитоплазматическими антителами: систематический обзор целевой группы Европейской лиги против ревматизма по системному васкулиту. Энн Рум Дис . Июль 2008. 67: 1004-1010. [Медлайн].
Haroun MK, Stone JH, Nair R, Racusen L, Hellmann DB, Eustace JA. Корреляция процента нормальных клубочков с почечным исходом при гранулематозе Вегенера. Ам Дж. Нефрол . Сентябрь-декабрь 2002. 22 (5-6): 497-503.[Медлайн].
Hauer HA, Bajema IM, Van Houwelingen HC, et al. Детерминанты исхода при ANCA-ассоциированном гломерулонефрите: проспективный клинико-гистопатологический анализ 96 пациентов. Почки Инт . Ноябрь 2002. 62 (5): 1732-1742. [Медлайн].
Renaudineau Y, Le Meur Y. Поражение почек при гранулематозе Вегенера. Клиника Рев Аллерг Иммунол . Октябрь 2008. 35: 22-29. [Медлайн].
Walsh M, Merkel PA, Mahr A, Jayne D.Влияние продолжительности терапии глюкокортикоидами на частоту рецидивов при васкулите, ассоциированном с антинейтрофильными цитоплазматическими антителами: метаанализ. Центр по уходу за артритом (Хобокен) . 2010 августа 62 (8): 1166-73. [Медлайн].
Филипп Р., Лукмани Р. Смертность при системном васкулите: систематический обзор. Clin Exp Rheumatol . Сентябрь-октябрь 2008 г. 26: S94-S104. [Медлайн].
Seo P, Min Y-I, Holbrook JT, et al. Повреждения, вызванные гранулематозом Вегенера, и его лечение: проспективные данные исследования гранулематоза Вегенера с этанерцептом (WGET). Революционный артрит . July 2005. 52: 2168-2178. [Медлайн].
Le Guenno G, Mahr A, Pagnoux C, Dhote R, Guillevin L. Частота и предикторы уротоксических нежелательных явлений у пациентов с системными некротическими васкулитами, принимающих циклофосфамид. Революционный артрит . 2011 17 февраля [Medline].
Heijl C, Harper L, Flossmann O, et al. Заболеваемость злокачественными новообразованиями у пациентов, получавших лечение по поводу васкулита, ассоциированного с антинейтрофильными цитоплазматическими антителами: последующие данные клинических испытаний Европейской группы изучения васкулита. Энн Рум Дис . Август 2011. 70 (8): 1415-1421. [Медлайн].
Суппиа Р., судья А., Батра Р. и др. Модель для прогнозирования сердечно-сосудистых событий у пациентов с впервые диагностированным гранулематозом Вегенера и микроскопическим полиангиитом. Центр по уходу за артритом (Хобокен) . 2011 14 января [Medline].
Aviña-Zubieta JA, Mai A., Amiri N, Dehghan N, Ann Tan J, Sayre EC, et al. Риск инфаркта миокарда и инсульта у пациентов с гранулематозом с полиангиитом (Вегенера): популяционное исследование. Ревматический артрит . 2016 ноябрь 68 (11): 2752-2759. [Медлайн].
Литтл М.А., Найтингейл П., Вербург, Калифорния и др. Ранняя смертность при системном васкулите: относительный вклад нежелательных явлений и активного васкулита. Энн Рум Дис . Июнь 2010. 69 (6): 1036-43. [Медлайн].
Wallace ZS, Lu N, Miloslavsky E, Unizony S, Stone JH, Choi HK. Общенациональные тенденции госпитализации и госпитальной смертности от гранулематоза с полиангиитом. Центр по уходу за артритом (Хобокен) . 2016 г. 7 июля [Medline].
Holle JU, Gross WL. Неврологические нарушения при гранулематозе Вегенера. Curr Opin Rheumatol . 2011 23 января (1): 7-11. [Медлайн].
Флориан А., Славич М., Блокманс Д., Дымарковский С., Богерт Дж. Поражение сердца при гранулематозе с полиангиитом (гранулематоз Вегенера). Тираж . 2011 27 сентября. 124 (13): e342-4. [Медлайн].
McGeoch L, Carette S, Cuthbertson D, Hoffman GS, Khalidi N, Koening CL, et al.Поражение сердца при гранулематозе с полиангиитом. Дж. Ревматол . 2015 июл.42 (7): 1209-12. [Медлайн].
Hazebroek MR, Kemna MJ, Schalla S, Sanders-van Wijk S, Gerretsen SC, Dennert R, et al. Распространенность и прогностическая значимость поражения сердца при ANCA-ассоциированном васкулите: эозинофильный гранулематоз с полиангиитом и гранулематоз с полиангиитом. Инт Дж. Кардиол . 2015 15 ноября. 199: 170-9. [Медлайн].
Аль-Хаким Д.А., Феделе С., Карлос Р., Портер С.Экстранодальная NK / Т-клеточная лимфома носового типа. Оральный онкол . Январь 2007. 43 (1): 4-14. [Медлайн].
Франкель С.К., Косгроув Г.П., Фишер А. Последние данные по диагностике и лечению легочного васкулита. Сундук . Февраль 2006. 129 (2): 452-65. [Медлайн].
Bossuyt X, Cohen Tervaert JW, Arimura Y, et al. Документ с изложением позиции: Пересмотренный международный консенсус 2017 года по тестированию ANCA при гранулематозе с полиангиитом и микроскопическим полиангиитом. Нат Ревматол . 2017 13 ноября (11): 683-692. [Медлайн].
Rottem M, Fauci AS, Hallahan CW, Kerr GS, Lebovics R, Leavitt RY, et al. Гранулематоз Вегенера у детей и подростков: клиническая картина и исходы. Дж. Педиатр . 1993, январь 122 (1): 26-31. [Медлайн].
Polychronopoulos VS, Prakash UBS, Golbin JM, Edell ES, Specks U. Участие дыхательных путей в гранулематозе Вегенера. Rheum Dis Clin N Am .Ноябрь 2007. 33: 755-775. [Медлайн].
Эрвье Б., Дюран С, Массо А, Понге Т, Хамиду М., Муссини Дж. М.. Использование биопсии мышц для диагностики системных васкулитов. Дж. Ревматол . 2011 Март 38 (3): 470-4. [Медлайн].
Нунокава Т., Йокогава Н., Шимада К., Энацу К., Суги С. Использование мышечной биопсии в диагностике системного васкулита, поражающего сосуды малого и среднего размера: перспективная оценка в Японии. Scand J Rheumatol .2015 8. 1-5 октября. [Медлайн].
DeGroot K, Harper L, Jayne DRW и др. Импульс против ежедневного перорального приема циклофосфамида для индукции ремиссии при васкулите, ассоциированном с антинейтрофильными цитоплазматическими антителами: рандомизированное исследование. Энн Интерн Мед. . May 2009. 150: 670-680. [Медлайн].
Monach PA, Arnold LM, Merkel PA. Частота и профилактика токсичности циклофосфамида для мочевого пузыря при лечении ревматических заболеваний: обзор, основанный на данных. Революционный артрит . 2010 Январь 62 (1): 9-21. [Медлайн].
Clowse ME, Copland SC, Hsieh TC, Chow SC, Hoffman GS, Merkel PA и др. Резерв яичников снижается пероральной терапией циклофосфамидом при гранулематозе с полиангиитом (Вегенера). Центр по уходу за артритом (Хобокен) . 2011 декабрь 63 (12): 1777-81. [Медлайн].
Langford CA. Циклофосфамид как индукционная терапия гранулематоза Вегенера и микроскопического полиангиита. Клин Экспер Иммунол . Май 2011. 164 (Дополнение 1): 31-4. [Медлайн].
Specks U, Merkel PA, Seo P, Spiera R, Langford CA, Hoffman GS, et al. Эффективность схем индукции ремиссии при ANCA-ассоциированном васкулите. N Engl J Med . 2013 авг., 1. 369 (5): 417-27. [Медлайн].
Garcia-Valladares I, Espinoza LR. Ритуксимаб превосходит циклофосфамид при ANCA-ассоциированном васкулите по индукции ремиссии и имеет лучший профиль безопасности? Curr Rheumatol Rep . Декабрь 2010. 12 (6): 395-8. [Медлайн].
Овен PM, Hellmich B, Voswinkel J, et al. Недостаточная эффективность ритуксимаба при гранулематозе Вегенера с рефрактерными гранулематозными проявлениями. Энн Рум Дис . Июль 2006 г. 65 (7): 853-858. [Медлайн].
Seo P, Specks U, Keogh KA. Эффективность ритуксимаба при ограниченном гранулематозе Вегенера с рефрактерными гранулематозными проявлениями. Дж. Ревматол .Октябрь 2008. 35 (10): 2017-2023. [Медлайн].
Gottenberg JE, Ravaud P, Bardin T, et al. Факторы риска тяжелых инфекций у пациентов с ревматоидным артритом, получавших ритуксимаб в аутоиммунном реестре и регистре ритуксимаба. Революционный артрит . 2010 сентябрь 62 (9): 2625-32. [Медлайн].
Джонс Р. Б., Ферраро А. Дж., Чаудри А. Н. и др. Многоцентровое исследование терапии ритуксимабом рефрактерного антинейтрофильного цитоплазматического васкулита. Революционный артрит . 2009 Июль 60 (7): 2156-68. [Медлайн].
Tesfa D, Ajeganova S, Hägglund H и др. Поздняя нейтропения после терапии ритуксимабом при ревматических заболеваниях: связь с истощением B-лимфоцитов и инфекциями. Революционный артрит . Август 2011. 63 (8): 2209-2214. [Медлайн].
McGregor JG, Hogan SL, Hu Y, Jennette CE, Falk RJ, Nachman PH. Глюкокортикоиды, частота рецидивов и инфекций при заболевании, связанном с цитоплазматическими антителами нейтрофилов. Clin J Am Soc Nephrol . 2012 Февраль 7 (2): 240-7. [Медлайн]. [Полный текст].
Klemmer PJ, Chalermskulrat W, Reif MS, Hogan SL, Henke DC, Falk RJ. Плазмаферез при диффузном альвеолярном кровотечении у пациентов с васкулитом мелких сосудов. Am J Kidney Dis . Декабрь 2003. 42 (6): 1149-1153. [Медлайн].
Пьюзи CD, Рис AJ, Эванс DJ, Питерс Д.К., Локвуд CM. Плазмообмен при очаговом некротическом гломерулонефрите без антител против GBM. Почки Инт . Октябрь 1991. 40 (4): 757-763. [Медлайн].
Джейн Д. Р., Гаскин Г., Расмуссен Н. и др. Рандомизированное исследование плазмафереза или высоких доз метилпреднизолона в качестве дополнительной терапии тяжелого почечного васкулита. Дж. Ам Соц Нефрол . Июль 2007. 18 (7): 2180-2188. [Медлайн].
Casian A, Jayne D. Плазмообмен в лечении гранулематоза Вегенера, микроскопического полиангиита, синдрома Черга-Стросса и почечно-ограниченного васкулита. Curr Opin Rheumatol . 2011 23 января (1): 12-7. [Медлайн].
ДеГрут К., Расмуссен Н., Бэкон П.А. и др. Рандомизированное испытание циклофосфамида по сравнению с метотрексатом для индукции ремиссии при раннем системном васкулите, ассоциированном с цитоплазматическими антителами к антинейтрофилам. Революционный артрит . Август 2005. 52: 2461-2469. [Медлайн].
Rhee EP, Laliberte KA, Niles JL. Ритуксимаб в качестве поддерживающей терапии васкулита, ассоциированного с антинейтрофильными цитоплазматическими антителами. Clin J Am Soc Nephrol . 2010 5 (8): 1394-400. [Медлайн]. [Полный текст].
Sanders JS, Slot MC, Stegeman CA. Поддерживающая терапия васкулита, связанного с антинейтрофильными цитоплазматическими аутоантителами. N Engl J Med . Ноябрь 2003. 349 (21): 2072-2073. [Медлайн].
Slot MC, Tervaert JW, Boomsma MM, Stegeman CA. Положительный титр классических антинейтрофильных цитоплазматических антител (C-ANCA) при переходе на терапию азатиоприном, связанный с рецидивом васкулита, связанного с протеиназой 3. Революционный артрит . April 2004. 51 (2): 269-273. [Медлайн].
Pagnoux C, Mahr A, Hamidou MA, et al. Поддерживающая терапия азатиоприном или метотрексатом при ANCA-ассоциированном васкулите. N Engl J Med . Декабрь 2008. 359: 2790-2803. [Медлайн].
Puéchal X, Pagnoux C, Perrodeau É, Hamidou M, Boffa JJ, et al. Отдаленные результаты исследования WEGENT по поддержанию ремиссии гранулематоза с полиангиитом или микроскопическим полиангиитом. Ревматический артрит . 2015 16 октября [Medline].
Reinhold-Keller E, Fink CO, Herlyn K, Gross WL, De Groot K. Высокая частота рецидивов почек у 71 пациента с гранулематозом Вегенера при поддержании ремиссии низкими дозами метотрексата. Революционный артрит . Июнь 2002. 47 (3): 326-32. [Медлайн].
Langford CA, Talar-Williams C, Barron KS, Sneller MC. Использование циклофосфамидной индукционной схемы поддерживающей терапии метотрексатом для лечения гранулематоза Вегенера: длительное наблюдение и частота рецидивов. Am J Med . April 2003. 114 (6): 463-9. [Медлайн].
Langford CA, Talar-Williams C, Barron KS, Sneller MC. Поэтапный подход к лечению гранулематоза Вегенера: индукция ремиссии глюкокортикоидами и ежедневный переход на метотрексат для поддержания ремиссии. Революционный артрит . Декабрь 1999. 42 (12): 2666-73. [Медлайн].
Снеллер М.С., Хоффман Г.С., Талар-Уильямс К., Керр Г.С., Халлахан К.В., Фаучи А.С.Анализ 42 пациентов с гранулематозом Вегенера, получавших метотрексат и преднизон. Революционный артрит . May 1995. 38 (5): 608-13. [Медлайн].
Guillevin L, et al; Французская группа по изучению васкулита. Сравнение ритуксимаба и азатиоприна при лечении ANCA-ассоциированного васкулита. N Engl J Med . 2014 6 ноября. 371 (19): 1771-80. [Медлайн]. [Полный текст].
Terrier B, et al; Французская группа по изучению васкулита. Долгосрочная эффективность поддерживающих режимов ремиссии ANCA-ассоциированных васкулитов. Энн Рум Дис . 2018 августа 77 (8): 1150-1156. [Медлайн].
Чарльз П. и др .; Французская группа по изучению васкулита. Сравнение индивидуально подобранного и фиксированного режима ритуксимаба для поддержания ремиссии ANCA-ассоциированного васкулита: результаты многоцентрового рандомизированного контролируемого исследования III фазы (MAINRITSAN2). Энн Рум Дис . 2018 Август 77 (8): 1143-1149. [Медлайн].
Stegeman CA, Tervaert JW, de Jong PE, Kallenberg CG.Триметоприм-сульфаметоксазол (ко-тримоксазол) для профилактики рецидивов гранулематоза Вегенера. Голландская исследовательская группа по ко-тримоксазолу Вегенера. N Engl J Med . 1996 г., 4 июля, 335 (1): 16-20. [Медлайн].
Bosch X, Guilabert A, Espinosa G, Mirapeix E. Лечение васкулита, связанного с антинейтрофильными цитоплазматическими антителами: систематический обзор. ЯМА . Август 2007. 298: 655-669. [Медлайн].
Martinez V, Cohen P, Pagnoux C, et al.Внутривенные иммуноглобулины при рецидивах системных васкулитов, связанных с антинейтрофильными цитоплазматическими аутоантителами: результаты многоцентрового проспективного открытого исследования 22 пациентов. Революционный артрит . Январь 2008. 58 (1): 308-371. [Медлайн].
Сильва Ф., Спекс Ю., Калра С. и др. Микофенолата мофетил для индукции и поддержания ремиссии при микроскопическом полиангиите с поражением почек от легкой до умеренной степени — проспективное открытое пилотное исследование. Clin J Am Soc Nephrol . Март 2010. 5 (3): 445-53. [Медлайн].
Joy MS, Hogan SL, Jennette JC, Falk RJ, Nachman PH. Пилотное исследование с использованием микофенолятмофетила при рецидивирующем или резистентном ANCA васкулите мелких сосудов. Циферблат нефрола . Декабрь 2005. 20 (12): 2725-2732. [Медлайн].
Коукулаки М, Джейн ДР. Микофенолят мофетил при системном васкулите, ассоциированном с антинейтрофильной цитоплазмой и антителами. Нефрон Клиническая Практика .2006. 102 (3-4): c100-7. [Медлайн].
Nowack R, Göbel U, Klooker P, Hergesell O, Andrassy K, van der Woude FJ. Микофенолят мофетил для поддерживающей терапии гранулематоза Вегенера и микроскопического полиангиита: пилотное исследование с участием 11 пациентов с поражением почек. Дж. Ам Соц Нефрол . 1999 Сентябрь 10 (9): 1965-71. [Медлайн].
Hiemstra TF, Walsh M, Mahr A, et al. Микофенолятмофетил против азатиоприна для поддержания ремиссии при васкулите, ассоциированном с антинейтрофильными цитоплазматическими антителами: рандомизированное контролируемое исследование. ЯМА . Декабрь 2010 г. 304 (21): 2381-2388. [Медлайн].
Stone JH, Uhlfelder ML, Hellmann DB, Crook S, Bedocs NM, Hoffman GS. Этанерцепт в сочетании с традиционным лечением гранулематоза Вегенера: открытое шестимесячное исследование для оценки безопасности. Революционный артрит . May 2001. 44 (5): 1149-1154. [Медлайн].
Бут А, Харпер Л., Хаммад Т., Бэкон П., Гриффит М., Леви Дж. И др. Проспективное исследование блокады TNF-альфа инфликсимабом при системном васкулите, ассоциированном с антинейтрофильными цитоплазматическими антителами. Дж. Ам Соц Нефрол . 2004 15 марта (3): 717-21. [Медлайн].
Ли Р.У., Д’Круз Д.П. Новые методы лечения васкулита, ассоциированного с антинейтрофильными цитоплазматическими антителами. Наркотики . 2008. 68: 747-770. [Медлайн].
Sangle SR, Hughes GR, D’Cruz DP. Инфликсимаб у пациентов с трудно поддающимся лечению системным васкулитом: неблагоприятный исход и значительные побочные эффекты. Энн Рум Дис . April 2007. 66 (4): 564-565. [Медлайн].
Hinze CH, Colbert RA. Истощение В-клеток при гранулематозе Вегенера. Clin Rev Allergy Immunol . Июнь 2008. 34: 372-379. [Медлайн].
Schmitt WH, Birck R, Heinzel PA, et al. Длительное лечение рефрактерного гранулематоза Вегенера с 15-дезоксиспергуалином: открытое исследование с участием семи пациентов. Циферблат нефрола . Июнь 2005. 20 (6): 1083-1092. [Медлайн].
Бирк Р., Варнац К., Лоренц Х. М. и др.15-Деоксиспергуалин у пациентов с рефрактерным ANCA-ассоциированным системным васкулитом: открытое шестимесячное исследование для оценки безопасности и эффективности. Дж. Ам Соц Нефрол . Февраль 2003. 14 (2): 440-7. [Медлайн].
Schmitt WH, Hagen EC, Neumann I, et al. Лечение рефрактерного гранулематоза Вегенера антитимоцитарным глобулином (АТГ): открытое исследование с участием 15 пациентов. Почки Инт . Апрель 2004. 65 (4): 1440-1448. [Медлайн].
Уолш М., Чаудри А., Джейн Д.Долгосрочное наблюдение за рецидивирующим / рефрактерным васкулитом, ассоциированным с антителами к цитоплазме нейтрофилов, леченным алемтузумабом (CAMPATH-1H), истощающим лимфоциты. Энн Рум Дис . Сентябрь 2008 г. 67 (9): 1322-1327. [Медлайн].
Рейнольдс Дж., Там Ф. В., Чандракер А. и др. Блокада CD28-B7 предотвращает развитие экспериментального аутоиммунного гломерулонефрита. Дж. Клин Инвест . March 2000. 105 (5): 643-51. [Медлайн].
Girard C, Charles P, Terrier B, Bussonne G, Cohen P, Pagnoux C, et al.Трахеобронхиальные стенозы при гранулематозе с полиангиитом (Вегенера): отчет о 26 случаях. Медицина (Балтимор) . 2015 август 94 (32): e1088. [Медлайн].
Hoffman GS, Thomas-Golbanov CK, Chan J, Akst LM, Eliachar I. Лечение субгортального стеноза, вызванного гранулематозом Вегенера, кортикостероидами внутри очага поражения и дилатацией. Дж. Ревматол . May 2003. 30 (5): 1017-21. [Медлайн].
Langford CA, Sneller MC, Hallahan CW, et al.Клинические особенности и лечение стеноза подсвязочного канала у пациентов с гранулематозом Вегенера. Революционный артрит . Октябрь 1996. 39 (10): 1754-60. [Медлайн].
Мартинес Дель Перо М., Джейн Д., Чаудри А., Сивазоти П., Яни П. Долгосрочный исход стеноза дыхательных путей при гранулематозе с полиангиитом (гранулематоз Вегенера): обсервационное исследование. JAMA Otolaryngol Head Neck Surg . 2014 ноябрь 140 (11): 1038-44. [Медлайн].
Ezzat WH, Compton RA, Basa KC, Levi J.Реконструктивные методы при седловидной деформации носа при гранулематозе с полиангиитом: систематический обзор. JAMA Otolaryngol Head Neck Surg . 2017 1 мая. 143 (5): 507-512. [Медлайн].
Wallace ZS, Wallwork R, Zhang Y, Lu N, Cortazar F, Niles JL, et al. Повышение выживаемости с трансплантацией почек при терминальной стадии почечной недостаточности из-за гранулематоза с полиангиитом: данные Системы данных по почкам США. Энн Рум Дис . 2018 сен.77 (9): 1333-1338. [Медлайн].
Эспозито Д., Тримпоу П., Джульяно Д., Делин М., Рагнарссон О. Дисфункция гипофиза при гранулематозе с полиангиитом. Гипофиз . 2017 20 октября (5): 594-601. [Медлайн]. [Полный текст].
Петерс Дж. Э., Гупта В., Саид ИТ, Оффиа К., Джавад АСМ. Тяжелый локализованный гранулематоз с полиангиитом (гранулематоз Вегенера), проявляющийся обширным параличом черепных нервов и несахарным черепным диабетом: отчет о болезни и обзор литературы. BMC Neurol . 2018 1 мая. 18 (1): 59. [Медлайн]. [Полный текст].
Гранулематоз с полиангиитом — NORD (Национальная организация редких заболеваний)
УЧЕБНИКИ
Specks U. Легочный васкулит. В: Интерстициальная болезнь легких, 5-е изд. Schwarz MI, King Jr. TE, ред. Народное медицинское издательство, Шелтон, Коннектикут. 2011: 765-793.
СТАТЬИ В ЖУРНАЛЕ
Уолш М., Меркель П.А., Пех С.-А и др. Плазмаферез и глюкокортикоиды при тяжелом ANCA-ассоциированном васкулите.N Engl J Med. 2020 13 февраля; 382 (7): 622-631. https://www.ncbi.nlm.nih.gov/pubmed/32053298
Сингхал М., Гупта П., Шарма А. Визуализация при васкулите малых и средних сосудов. Int J Rheum Dis. 2019 Янв; 22 Приложение 1: 78-85. https://www.ncbi.nlm.nih.gov/pubmed/30698353
Берти А., Дежако С. Обновленная информация об эпидемиологии, факторах риска и исходах системных васкулитов. Лучшая практика Res Clin Rheumatol. 2018 Апрель; 32 (2): 271-294. https://www.ncbi.nlm.nih.gov/pubmed/30527432
Cansu DÜ, Özbülbül NI, Akyol G, Arık D, Korkmaz C.Подвержены ли легочные признаки гранулематоза с полиангиитом противотуберкулезному лечению? Rheumatol Int. 2018 июн; 38 (6): 1131-1138. https://www.ncbi.nlm.nih.gov/pubmed/29632976
Coordes A, Loose SM, Hofmann VM. Седловидная деформация носа и перфорация перегородки при гранулематозе с полиангиитом. Клин Отоларингол. 2018 Февраль; 43 (1): 291-299. https://www.ncbi.nlm.nih.gov/pubmed/28881107
Iudici M, Pagnoux C, Quartier P, et al. ANCA-ассоциированные васкулиты в детском возрасте и взрослые: вложенное исследование случай-контроль из реестра французских групп по изучению васкулита.Autoimmun Rev.2018 февраля; 17 (2): 108-114. https://www.ncbi.nlm.nih.gov/pubmed/29180123
Zonozi R, Niles JL, Cortazar FB. Вовлечение почек в васкулит, связанный с антинейтрофильными цитоплазматическими антителами. Rheum Dis Clin North Am. 2018 ноя; 44 (4): 525-543. https://www.ncbi.nlm.nih.gov/pubmed/30274621
Bossuyt X, Cohen Tervaert JW, Arimura Y, et al. Документ с изложением позиции: Пересмотренный международный консенсус 2017 года по тестированию ANCA при гранулематозе с полиангиитом и микроскопическим полиангиитом.Nat Rev Rheumatol. 2017 ноя; 13 (11): 683-692. https://www.ncbi.nlm.nih.gov/pubmed/28
6
Cornec D, Cornec-Le Gall E, Specks U. Клинические испытания васкулита, ассоциированного с антинейтрофильными цитоплазматическими антителами: что мы узнали и что нам еще нужно учиться. Пересадка нефрола Dial. 2017; [Epub перед печатью]. https://www.ncbi.nlm.nih.gov/pubmed/28087591
Lee PY, Adil EA, Irace AL, et al. Проявление и лечение гранулематоза с полиангиитом (гранулематоз Вегенера) в дыхательных путях у детей.Ларингоскоп. 2017; 127: 233-340. https://www.ncbi.nlm.nih.gov/pubmed/27113905
Singer O, McCune WJ. Обновленная информация о поддерживающей терапии гранулематоза с полиангиитом и микроскопическим полиангиитом. Curr Opin Rheumatol. 2017 Май; 29 (3): 248-253. https://www.ncbi.nlm.nih.gov/pubmed/28306595
Авина-Зубиета Дж. А., Май А., Амири Н. и др. Риск инфаркта миокарда и инсульта у пациентов с гранулематозом с полиангиитом (Вегенера): популяция исследование на основе. Arthritis Rheumatol.2016; 68: 2752-2759. https://www.ncbi.nlm.nih.gov/pubmed/27213713
Cabral DA, Canter DL, Muscal E, et al. Сравнение клинических проявлений у 48 детей с микроскопическим полиангиитом и 183 детей с гранулематозом с полиангиитом (Вегенера): когортное исследование ARChiVe. Arthritis Rheumatol. 2016; 68: 2514-2526. https://www.ncbi.nlm.nih.gov/pubmed/27111558
Iudici M, Quartier P, Terrier B и др. Детский гранулематоз с полиангиитом и микроскопическим полиангиитом: системный обзор и метаанализ.Orphanet J Rare Dis. 2016; 11: 141. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5075395/
Кубаиси Б., Абу-Самра К., Фостер CS. Гранулематоз с полиангиитом (гранулематоз Вегенера): обновленный обзор проявлений глазных болезней. Непреодолимый редкий диск Res. 2016; 5: 61-69. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4869584/
Pagnoux C. Обновления по ANCA-ассоциированному васкулиту. Eur J Rheumatol. 2016; 3: 122-133. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5058451/
Relle M, Fohr B, Fasola F, Schwarting A.Генетика и патофизиология гранулематоза с полиангиитом (ГПА) и его основной аутоантигенной протеиназой 3. Mol Cell Probes. 2016; 30: 366-373. https://www.ncbi.nlm.nih.gov/pubmed/27559009
Войцеховская Ю., Краевски В., Краевский П., Крецицкий Т. Гранулематоз с полиангиитом отоларингологической практики: обзор современных знаний. Clin Exp Otorhinolaryngo. 2016; 9: 8-13. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4792240/
Geetha D, Specks U, Stone JH, et al. Ритуксимаб в сравнении с циклофосфамидом при ANCA-ассоциированном васкулите с поражением почек.J Am Soc Nephrol. 2015; 26: 976-985. https://www.ncbi.nlm.nih.gov/pubmed/25381429
Pagnoux C, Guillevin L. Лечение гранулематоза с полиангиитом (Вегенера). Эксперт Рев Клин Иммунол. 2015 Март; 11 (3): 339-48. https://www.ncbi.nlm.nih.gov/pubmed/25644677
Содерстром А., Реваз С., Дудлер Дж. Черепные невропатии при гранулематозе с полиангиитом (Вегенера): обзор конкретных случаев. Clin Rheum. 2015; 34: 591-596. https://www.ncbi.nlm.nih.gov/pubmed/24352751
Stone JH, Merkel PA, Spiera R, et al.Ритуксимаб в сравнении с циклофосфамидом при ANCA-ассоциированном васкулите. N Engl J Med. 2015; 363: 221-232. https://www.ncbi.nlm.nih.gov/pubmed/20647199
de Joode AA, Sanders JS, Smid WH, Stegeman CA. Спасательная терапия плазмаферезом при прогрессирующем системном ANCA-ассоциированном васкулите: одноцентровые результаты ступенчатого нарастания иммуносупрессии. Дж. Клин Афер. 2014; 29: 266-272. https://www.ncbi.nlm.nih.gov/pubmed/24497412
Silva-Fernández L, Loza E, Martínez-Taboada VM, et al. Биологическая терапия системного васкулита: систематический обзор.Semin Arthritis Rheum. 2014 Февраль; 43 (4): 542-57. https://www.ncbi.nlm.nih.gov/pubmed/23978781
Jennette JC. Обзор номенклатуры васкулитов, пересмотренной в 2012 г. на международной конференции Chapel Hill Consensus Conference. Clin Exp Nephrol. 2013; 17: 603-606. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4029362/
Флориан А., Славич М., Блокманс Д., Дымарковский С., Богерт Дж. Циркуляция. Поражение сердца при гранулематозе с полиангиитом (гранулематоз Вегенера). Тираж. 2011; 124: e342-344.https://www.ncbi.nlm.nih.gov/pubmed/21947937
Kallenberg CGM. Васкулит, связанный с антинейтрофильными цитоплазматическими антителами (ANCA): куда идти? Clin Exp Immunol. 2011; 164 (Приложение 1): 1-3. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3095854/
ИНТЕРНЕТ
Микроскопический полиангиит. Веб-сайт Центра васкулита Джонса Хопкинса. https://www.hopkinsvasculitis.org/types-vasculitis/microscopic-polyangiitis/ По состоянию на 28 апреля 2020 г.
Гранулематоз с полиангиитом. Веб-сайт Центра васкулита Джонса Хопкинса.https://www.hopkinsvasculitis.org/types-vasculitis/granulomatosis-with-polyangiitis/ По состоянию на 28 апреля 2020 г.
Гильевен Л. Гранулематоз с полиангиитом. Энциклопедия Orphanet, январь 2019 г. Доступно по адресу: http://www.orpha.net/consor/cgi-bin/OC_Exp.php?lng=EN&Expert=900 Проверено 28 апреля 2020 г.
McKusick VA., Ed. Интернет-Менделирующее наследование в человеке (OMIM). Балтимор. MD: Университет Джона Хопкинса; Запись №: 608710; Последнее обновление: 08.09.2018. Доступно по адресу: https: // www.omim.org/entry/608710. По состоянию на 28 апреля 2020 г.
Gota CE. Гранулематоз с полиангиитом (ГПА). Веб-сайт профессиональной онлайн-версии руководства Merck Manual. Обновлено в марте 2019 г. https://www.merckmanuals.com/professional/musculoskeletal-and-connective-tissue-disorders/vasculitis/granulomatosis-with-polyangiitis-gpa По состоянию на 28 апреля 2020 г.
Falk RJ, Merkel PA, King Jr. TE. Клинические проявления и диагностика гранулематоза с полиангиитом и микроскопическим полиангиитом. UpToDate, Inc.23 января 2019 г. Доступно по адресу: http://www.uptodate.com/contents/clinical-manifestations-and-diagnosis-of-granulomatosis-with-polyangiitis-and-microscopic-polyangiitis По состоянию на 28 апреля 2020 г.
Гранулематоз с полиангиитом (GPA): симптомы, причины и многое другое
Гранулематоз с полиангиитом (GPA), ранее известный как гранулематоз Вегенера, является редким и опасным для жизни заболеванием, которое ограничивает кровоток к нескольким органам, включая легкие, почки, и верхние дыхательные пути.
Это разновидность васкулита, воспаления и повреждения кровеносных сосудов.
GPA требует длительной иммуносупрессии. Некоторые пациенты умирают из-за токсичности лечения.
GPA затрагивает только 3 из каждых 100 000 человек в Соединенных Штатах.
Он может развиться в любом возрасте, но обычно симптомы появляются у пациентов в возрасте от сорока до пятидесяти. Он затрагивает мужчин и женщин в равной степени, и белые люди кажутся более восприимчивыми, чем другие этнические группы.
Помимо воспаления кровеносных сосудов, GPA производит гранулемы вокруг кровеносных сосудов. Гранулема или грануляция — это своего рода локализованное узловое воспаление, обнаруживаемое в тканях, тип воспалительной ткани.
Причина неизвестна, но GPA не является типом рака или инфекции.
При своевременном лечении и диагностике симптомы GPA могут перейти в ремиссию. Без лечения это может привести к почечной недостаточности и смерти.
GPA является частью большой группы васкулитных синдромов.
Все они характеризуются аутоиммунной атакой аномального типа циркулирующих антител, называемых антинейтрофильными цитоплазматическими антителами (ANCA).
Эти антитела атакуют мелкие и средние кровеносные сосуды.
Помимо GPA, другие примеры васкулитных синдромов включают:
- Синдром Чурга-Стросса
- микроскопический полиангиит
Согласно описанию, опубликованному на конференции Chapel Hill Consensus Conference 2012 (CHCC2012), GPA имеет вид:
«Некротическое гранулематозное воспаление, обычно затрагивающее верхние и нижние дыхательные пути, и некротический васкулит, поражающий преимущественно сосуды малого и среднего размера (например,g., капилляры, венулы, артериолы, артерии и вены). Некротический гломерулонефрит — обычное дело ».
CHCC2012 также согласился переименовать гранулематоз Вегенера в гранулематоз с полиангиитом (GPA).
Признаки и симптомы GPA могут развиваться постепенно или внезапно.
Первым симптомом у большинства пациентов является ринит, насморк и заложенность носа, как в тяжелом случае простуды.
Другие признаки и симптомы могут включать:
- стойкий насморк
- кашель, который может включать кровь
- инфекции уха
- боли в суставах
- потеря аппетита
- недомогание или общее недомогание
- кровотечение из носа
- одышка
- синусит
- кожные язвы
- опухоль суставов
- боль в глазах
- ощущение жжения в глазах
- покраснение глаз
- проблемы со зрением
- лихорадка
- слабость, часто вызванная анемией
- непреднамеренная потеря веса
- кровь в моче
Это может привести к быстро прогрессирующему гломерулонефриту, почечному синдрому, который, если его не лечить, быстро переходит в острую почечную или почечную недостаточность.Около 75 процентов людей с этим заболеванием развивают заболевание почек.
Специалисты не знают, что вызывает GPA.
По всей видимости, он возникает, когда первоначальное событие, вызывающее воспаление, вызывает ненормальную реакцию иммунной системы. Это приводит к воспалению и сужению кровеносных сосудов и гранулем или воспалительных тканевых массах.
Рецидив может быть вызван инфекцией.
Другими способствующими факторами могут быть токсины окружающей среды, генетическая предрасположенность или их комбинация.
Он был связан с парвовирусом и долгосрочным присутствием золотистого стафилококка (S. aureus) в носовом проходе.
Диагностика может быть затруднена, потому что у пациента могут отсутствовать симптомы на ранних стадиях или симптомы могут быть неспецифическими. Для постановки диагноза в первичной медико-санитарной помощи может потребоваться от 2 до 20 месяцев.
Врач может заподозрить GPA, если у пациента в течение длительного периода наблюдались соответствующие необъяснимые симптомы.
Врач спросит о признаках и симптомах, проведет медицинский осмотр и изучит историю болезни пациента.
Анализы крови могут обнаружить ANCA, антитела, которые присутствуют у более чем 90 процентов пациентов с активным GPA.
ANCA сами по себе не могут подтвердить диагноз, но они могут указывать на то, что состояние может присутствовать.
Анализ крови также может измерить скорость оседания эритроцитов (седиментация) у пациента. Это скорость, с которой эритроциты падают на дно пробирки. Обычно это занимает около часа.
Тест уровня седативности может помочь определить, есть ли в организме воспаление, и если да, то насколько оно серьезное.При воспалении эритроциты опускаются на дно быстрее.
Анализ крови также может выявить анемию, частую проблему у пациентов с этим заболеванием. Это также может показать, правильно ли работают почки.
Другие диагностические тесты могут включать следующее:
- Анализ мочи, чтобы определить, поражены ли почки
- Рентген грудной клетки, чтобы помочь определить, связана ли проблема с GPA или другим заболеванием легких
- биопсия
Биопсия это единственный надежный способ определения среднего балла.Он включает в себя взятие небольшого кусочка ткани пораженного органа для исследования под микроскопом. Образцы тканей могут быть взяты из дыхательных путей, носовых ходов или легких, и результаты могут исключить или подтвердить наличие гранулем и васкулита.
Образцы также могут быть взяты с кожи или почек, если у пациента есть почечная или почечная недостаточность или кожный васкулит.
Лечение GPA обычно делится на два этапа:
- Вызвание ремиссии болезни, которая включает в себя избавление от всех признаков и симптомов.
- Поддержание ремиссии заболевания для предотвращения рецидива.
Ранняя диагностика и лечение повышают шансы пациента на ремиссию в течение нескольких месяцев. Некоторым пациентам может потребоваться больше времени.
Важно наблюдать за пациентом после того, как признаки и симптомы исчезнут, во время стадии ремиссии, поскольку болезнь может рецидивировать.
Кортикостероиды, такие как преднизон, могут быть назначены при начальных признаках и симптомах. В некоторых случаях это единственное необходимое лекарство.
В большинстве случаев также назначаются другие иммунодепрессанты, такие как циклофосфамид (Цитоксан), азатиоприн (Имуран) или метотрексат (Ревматрекс). Цель состоит в том, чтобы остановить чрезмерную реакцию иммунной системы.
До того, как стало доступно лечение стероидами и циклофосфамидом, 82 процента пациентов с ГПД умерли в течение первого года, а средняя выживаемость составила 5 месяцев. Прогресс, достигнутый за последние 50 лет, означает, что 90 процентов пациентов выживут, а некоторые могут ожидать еще 20 лет без ремиссии.
Можно использовать ритуксимаб или ритуксан. Это лекарство, которое изначально было разработано для лечения неходжкинской лимфомы, одного из видов рака. Позже он был одобрен для лечения ревматоидного артрита (РА). Ритуксимаб снижает количество В-клеток в организме. В-клетки участвуют в воспалении. Если стандартные методы лечения неэффективны, некоторые врачи могут назначить Ритуксимаб.
Многие лекарства, используемые для лечения этого состояния, ослабляют иммунную систему пациента, поэтому очень важно следить за пациентом.Сниженная иммунная система менее способна бороться с инфекцией.
Следующие препараты могут помочь поддержать иммунную систему во время лечения:
- Триметоприм-сульфаметоксазол, например Бактрим, Септра, может обеспечить защиту от инфекций легких.
- Бисфосфонаты, такие как Fosamax, помогают предотвратить остеопороз или потерю костной массы, которая может возникнуть при использовании кортикостероидов.
- Фолиевая кислота может предотвратить появление язв и других проблем, которые могут возникнуть при низком уровне фолиевой кислоты, например, в результате лечения метотрексатом.
Некоторым пациентам может потребоваться операция. При возникновении почечной недостаточности врач может порекомендовать пересадку почки.
Осложнения обычно возникают из-за отсутствия лечения.
Они могут включать любое из следующего:
- глухота из-за воспаления гранулированной ткани в среднем ухе
- рубцевание кожи, если на коже появляются язвы
- сердечный приступ, если поражены артерии сердца
- повреждение почек, так как невылеченные случаи GPA часто приводят к проблемам с почками.
