Диарея — Заболевания желудочно-кишечного тракта
При острой диарее (продолжительностью < 4 дней), как правило, нет необходимости в специальном обследовании. Исключение составляют пациенты, у которых определяются признаки дегидратации, кровь в стуле, лихорадка, интенсивная боль, гипотензия, симптомы выраженной интоксикации, в особенности пациенты детского, подросткового и пожилого, старческого возраста. Таким больным необходимо провести общий анализ крови, исследовать содержание электролитов, азота мочевины и креатинина в крови. Необходимо провести микроскопический анализ образцов стула, включая оценку содержания лейкоцитов, культуральное исследование кала и, если антибиотики были приняты недавно, исследовать содержание токсинов C. difficile в кале.
При хронической диарее (продолжительностью > 4 недель), а также более коротких (от 1 до 3 недель) эпизодах диареи у пациентов с нарушениями иммунной системы и при тяжелом общем состоянии больного необходимо дополнительное обследование. Первый этап оценки стула подразумевает культуральное исследование, исследование на наличие лейкоцитов (в мазке или методом исследования содержания лактоферрина), микроскопическое исследование на предмет выявления яиц глист и паразитов, оценку рН (ферментация бактериями неабсорбированных углеводов способствует снижению рН < 6,0), наличия жира (окраска судановым красителем) и электролитов (натрия и калия). Если не обнаружено обычных возбудителей, проводятся специальные исследования на антигены Giardia и Aeromonas, Plesiomonas, кокцидии и микроспоридии. Следующий шаг – проведение сигмоскопии или колоноскопии с множественной биопсией для исключения воспалительных заболеваний. После острой кишечной инфекции у 10% пациентов развивается хроническая диарея (постинфекционный синдром раздраженного кишечника).
Первый этап оценки стула подразумевает культуральное исследование, исследование на наличие лейкоцитов (в мазке или методом исследования содержания лактоферрина), микроскопическое исследование на предмет выявления яиц глист и паразитов, оценку рН (ферментация бактериями неабсорбированных углеводов способствует снижению рН < 6,0), наличия жира (окраска судановым красителем) и электролитов (натрия и калия). Если не обнаружено обычных возбудителей, проводятся специальные исследования на антигены Giardia и Aeromonas, Plesiomonas, кокцидии и микроспоридии. Следующий шаг – проведение сигмоскопии или колоноскопии с множественной биопсией для исключения воспалительных заболеваний. После острой кишечной инфекции у 10% пациентов развивается хроническая диарея (постинфекционный синдром раздраженного кишечника).
Если определенный диагноз не удается установить, а с помощью окраски суданом определяется наличие стеатореи, проводят количественную оценку потери жира с калом и затем исследуют состояние тонкой кишки методами энтероклизиса либо КТ-энтерографии (патологические изменения структуры) и эндоскопической биопсии (заболевания слизистой оболочки). Если патология тонкой кишки не выявлена, при наличии «необъяснимой» стеатореи проводится оценка структуры и функции поджелудочной железы ( Острый панкреатит : Лабораторные методы). В ряде случаев капсульная эндоскопия позволяет обнаружить изменения, не выявленные другими методами (преимущественно болезнь Крона и энтеропатию, ассоциированную с приемом НПВС).
Если патология тонкой кишки не выявлена, при наличии «необъяснимой» стеатореи проводится оценка структуры и функции поджелудочной железы ( Острый панкреатит : Лабораторные методы). В ряде случаев капсульная эндоскопия позволяет обнаружить изменения, не выявленные другими методами (преимущественно болезнь Крона и энтеропатию, ассоциированную с приемом НПВС).
Такая характеристика кала, как осмотический «провал», который рассчитывается 290 − 2 × (концентрация натрия в кале + концентрация калия в кале), указывает, носит ли диарея характер секреторной или осмотической. Осмотический «провал» < 50 мЭкв/л указывает, что диарея носит секреторный характер; при большем значении — осмотический. При осмотической диарее необходимо заподозрить скрытый прием магний-содержащих слабительных (определяемый по содержанию магния в кале) или мальабсорбцию углеводов (диагностируемую с помощью водородного дыхательного теста, исследования активности лактазы и пересмотра диеты).
При секреторной диарее неуточненного происхождения необходимо обследование для исключения эндокринной патологии (в частности, исследование на содержание гастрина, кальцитонина, вазоактивного интестинального пептида в сыворотке, гистамина, 5-гидроксииндолилуксусной кислоты [5-ГИУК] в моче). Необходимо дополнительно оценить симптоматику для выявления признаков болезней щитовидной железы и надпочечников. Следует рассмотреть возможность тайного приема слабительных средств, что можно выяснить с помощью исследования кала на примесь слабительных.
Необходимо дополнительно оценить симптоматику для выявления признаков болезней щитовидной железы и надпочечников. Следует рассмотреть возможность тайного приема слабительных средств, что можно выяснить с помощью исследования кала на примесь слабительных.
Вирусная диарея
Причины вирусных диарей. О том, что вирусы могут вызывать диарею, стали говорить еще в тридцатые годы прошлого века на основании описаний вспышек диарей среди детей, было высказано предположение о том, что поносы вызывают именно вирусы, и данные диареи стали называть «кишечным гриппом», «эпидемическим поносом», вирусной дизентерией или зимним поносом. На сегодня накоплено достаточно данных о том, что вирусы могут провоцировать поносы и расстройства пищеварения у детей и у взрослых. Как причина развития вирусного поноса сегодня рассматривается энтеровирусная, ротавирусная и реовирусная этиологии болезни. Вирусные диареи широко распространены во всем мире, ими ежегодно переболевают до миллионов детей и взрослых, они могут возникать как единичные случаи, так и эпидемические вспышки, в основном среди детей раннего возраста или среди закрытых организованных коллективов. Особенности вирусов Одной из самых характерных особенностей вирусов, которые способны вызвать поражения пищеварения и диарею, является их относительная устойчивость во внешней среде, а также хорошая способность к сохранению при низкой температуре воды и воздуха. Они выживают при 20˚С воды более 2 недель, а при 10˚С – до нескольких месяцев. Многим вирусам безразлична кислая среда желудка, они спокойно проходят ее, не разрушаясь., сохраняются вирусы в открытых водоемах и водохранилищах, морях и реках, а оттуда могут попадать в источники питьевого водоснабжения. Также вирусы выделяются из организма пораженных с фекалиями, где сохраняются длительное время, и могут загрязнять окружающую среду и воду водоемов. Как можно заразиться? — источниками инфекции при любой вирусной диарее могут стать люди, которые болеют, или выздоравливающие, выделяющие вирусы в окружающую среду, либо носители вируса, сами не болеющие, но вирусы выделяющие. При некоторых из вирусных диарей актуальным путем заражения может стать перенос инфекции от домашних животных и крупного рогатого скота, такие вирусы в зависимости от способа попадания в организм могут давать разные симптомы – при воздушно-капельном инфицировании — клинику простудной инфекции с поражением органов дыхания, а при попадании в пищеварение фекально-оральным путем – поражение системы пищеварения.
Особенности вирусов Одной из самых характерных особенностей вирусов, которые способны вызвать поражения пищеварения и диарею, является их относительная устойчивость во внешней среде, а также хорошая способность к сохранению при низкой температуре воды и воздуха. Они выживают при 20˚С воды более 2 недель, а при 10˚С – до нескольких месяцев. Многим вирусам безразлична кислая среда желудка, они спокойно проходят ее, не разрушаясь., сохраняются вирусы в открытых водоемах и водохранилищах, морях и реках, а оттуда могут попадать в источники питьевого водоснабжения. Также вирусы выделяются из организма пораженных с фекалиями, где сохраняются длительное время, и могут загрязнять окружающую среду и воду водоемов. Как можно заразиться? — источниками инфекции при любой вирусной диарее могут стать люди, которые болеют, или выздоравливающие, выделяющие вирусы в окружающую среду, либо носители вируса, сами не болеющие, но вирусы выделяющие. При некоторых из вирусных диарей актуальным путем заражения может стать перенос инфекции от домашних животных и крупного рогатого скота, такие вирусы в зависимости от способа попадания в организм могут давать разные симптомы – при воздушно-капельном инфицировании — клинику простудной инфекции с поражением органов дыхания, а при попадании в пищеварение фекально-оральным путем – поражение системы пищеварения. Источником вирусов при вирусных диареях могут стать продукты питания и вода, обсемененные вирусами, вещи и игрушки детей, которые они тянут в рот, ротавирусы можно выделить из водопроводной воды, которую не кипятили и пили дети.
Источником вирусов при вирусных диареях могут стать продукты питания и вода, обсемененные вирусами, вещи и игрушки детей, которые они тянут в рот, ротавирусы можно выделить из водопроводной воды, которую не кипятили и пили дети.
Входными воротами для диарейных вирусных инфекций является ротовая полость и желудочно-кишечный тракт.
Механизм развития вирусных диарей — вирусы попадают в эпителий в области верхних дыхательных путей, и заглатываются со слюной, проникая в желудок и кишечник. Там происходит поражение клеток эпителия желудка, кишки, и вирусы начинают размножаться на эпителии энтероцитов, клеток кишки, они проникают в кровь, вызывая проявления общего токсикоза и лихорадку, могут поражать отдельные органы и системы – нервную, легочную, печень. Идеальными условиями для размножения кишечных вирусов являются двенадцатиперстная и тонкая кишка, происходит формирование обильных и частых диарей. Нарушается всасывание воды клетками, происходит реакция брожения из-за проблем с расщеплением пищи, это и дает в комплексе симптомы диареи ( диареи обильные, водянистые, без примесей крови и зелени).
Проявления вирусных диарей зависят от того, каким вирусом и в каком возрасте вызвана диарея. При энтеровирусных диареях поражаются дети до 2 лет, может быть как только диарея, так и сочетание ее с поражением мышц, менингитом, ангиной или миокардитом. Изолированные формы энтеровируса дают легкую не длительную диарею, проходят самостоятельно. Опасны только энтеровирусы с диарейным синдромом у новорожденных и ослабленных детей. При диареях, вызванных вирусом Коксаки, может быть различная клиническая картина, зависит от возраста ребенка (легкие диареи у детей от 2 до 5 лет практически без температуры и токсикоза, с приступообразными болями животе и жидким стулом до 3-10 раз в сутки без примесей). Через 1-2 дня состояние нормализуется.
Иногда болезнь протекает с повышением температуры, простудными явлениями, с болями в животе, жидким стулом и повторной рвотой, состояние с лихорадкой длится до 3 суток, а понос первые 2-3 суток. Тяжело вирусы Коксаки протекают в первые 2 года жизни, лечение только в условиях стационара. Вирусные повреждения ЕСНО-этиологии возникают в любом возрасте, протекают не тяжело, обычно проявляясь в форме гастрита и энтерита, при этом дисфункции кишечника бывают незначительными и не длительными (тошнота, рвота , учащение стула в пределах 1-2 дней, нарушение аппетита, невысокая температура, стул разжиженный, без примесей, 5-6 раз в сутки) . В грудном возрасте или у детей в период новорожденности вирусные заболевания могут протекать тяжело, но обычно они начинаются как простудные заболевания, а кишечная симптоматика возникает позднее (повторное срыгивание, рвота, вздутие живота, разжижение стула). За счет потерь жидкости развивается токсикоз с эксикозом, обезвоживанием, нарастает тяжесть состояния.
Вирусные повреждения ЕСНО-этиологии возникают в любом возрасте, протекают не тяжело, обычно проявляясь в форме гастрита и энтерита, при этом дисфункции кишечника бывают незначительными и не длительными (тошнота, рвота , учащение стула в пределах 1-2 дней, нарушение аппетита, невысокая температура, стул разжиженный, без примесей, 5-6 раз в сутки) . В грудном возрасте или у детей в период новорожденности вирусные заболевания могут протекать тяжело, но обычно они начинаются как простудные заболевания, а кишечная симптоматика возникает позднее (повторное срыгивание, рвота, вздутие живота, разжижение стула). За счет потерь жидкости развивается токсикоз с эксикозом, обезвоживанием, нарастает тяжесть состояния.
Респираторные инфекции с кишечными синдромом
Расстройства кишечника могут быть одним из симптомов острых респираторных вирусных инфекций, изначально начинающимся как простуда. Расстройства кишечника при них возникают как результат токсического воздействия на кишку, нарушения ферментов, присоединение микробной флоры на фоне ослабления иммунитета, формирование дисбактериоза. В таких случаях как таковой вирусной диареи быть уже не может, но говорят тога об ОРВИ с кишечными проявлениями.
В таких случаях как таковой вирусной диареи быть уже не может, но говорят тога об ОРВИ с кишечными проявлениями.
Особенность вирусных диарей — расстройства работы кишечника, при которых в процесс поражения вовлекается тонкий кишечник, течение протекает по типу гастроэнтерита или энтерита (с рвотой или без нее). При вирусных диареях в крови детей — лимфоцитоз и лейкопения, нет выраженного воспаления стенок кишки (толстой), возникает диарея без примесей (слизь, кровь, зелень, в копрограмме нет лейкоцитов и эритроцитов). Стул с частицами непереваренной пищи, жирный из-за проблем с поджелудочной железой, обильный. Вирусные диареи протекают не длительно, не дают тяжелого течения и нарушения микробного равновесия. Ротавирусные диареи м.б. достаточно тяжелыми ( в раннем детском возрасте), поэтому, сегодня и в отношении вирусных диарей ведется разработка активных методов профилактики и разработка вакцин.
Автор: гл. м/с Стрига Т.В.
Дополнительное пероральное введение цинка для лечения диареи у детей
В странах с низким и средним уровнем дохода миллионы детей ежегодно страдают от тяжелой диареи и многие умирают от дегидратации (обезвоживания). Было показано, что приём жидкости через рот (с использованием раствора для пероральной регидратации) спасает жизни детей, но не оказывает влияния на продолжительность страдания детей от диареи. Дополнительное введение цинка может помочь уменьшить продолжительность и тяжесть диареи, и, следовательно, приносит дополнительную пользу по отношению к пероральным регидратационным растворам в снижении детской смертности.
Было показано, что приём жидкости через рот (с использованием раствора для пероральной регидратации) спасает жизни детей, но не оказывает влияния на продолжительность страдания детей от диареи. Дополнительное введение цинка может помочь уменьшить продолжительность и тяжесть диареи, и, следовательно, приносит дополнительную пользу по отношению к пероральным регидратационным растворам в снижении детской смертности.
Что такое пероральный цинк и как он может сократить продолжительность и тяжесть диареи
Цинк обычно применяют в виде сульфата цинка, ацетата цинка или глюконата цинка, все они являются водорастворимыми соединениями. Всемирная организация здравоохранения (ВОЗ) и Детский Фонд Организации Объединенных Наций (ЮНИСЕФ) рекомендует детям с диареей от 10 мг до 20 мг цинка в сутки. Существует несколько механизмов действия цинка при острой диарее, некоторые из которых являются специфичными для желудочно-кишечного тракта: цинк восстанавливает целостность барьера слизистых оболочек и активность ферментов щеточной каёмки энтероцитов, он способствует выработке антител и циркулирующих лимфоцитов против кишечных патогенов и непосредственно влияет на ионные каналы, действуя как блокатор калиевого канала секреции хлора, опосредованной 3-5-циклическим аденозинмонофосфатом. Исследователи Кокрейн изучили доказательства, доступные на 30 сентября 2016 года.
Исследователи Кокрейн изучили доказательства, доступные на 30 сентября 2016 года.
Какие доказательства представлены в этом обзоре
Тридцать три клинических испытания, которые включали 10841 ребёнка, соответствовали критериям включения этого обзора.
Мы не знаем, влияет ли лечение цинком на смертность или число госпитализированных детей среди детей с острой диареей ( очень низкая уверенность в доказательствах). У детей старше 6 месяцев дополнительное введение цинка может сокращать среднюю продолжительность диареи примерно на половину суток (низкая уверенность в доказательствах) и, вероятно, уменьшает число детей, у которых диарея сохраняется на седьмые сутки ( умеренная уверенность в доказательствах). У детей с симптомами недостаточности питания эффект был более выраженным, продолжительность диареи сокращалась примерно на сутки (высокая уверенность в доказательствах). И наоборот, у детей младше шести месяцев, имеющиеся данные свидетельствуют о том, что добавки цинка могут не влиять на среднюю продолжительность диареи (низкая
уверенность в доказательствах), или на число детей, у которых сохраняется диарея на седьмой день (низкая
уверенность в доказательствах). Дополнительное введение цинка увеличивает риск развития рвоты в обеих возрастных группах (умеренная уверенность в доказательствах). О других неблагоприятных эффектах не сообщали.
Дополнительное введение цинка увеличивает риск развития рвоты в обеих возрастных группах (умеренная уверенность в доказательствах). О других неблагоприятных эффектах не сообщали.
Среди детей с сохраняющейся диареей дополнительное введение цинка, вероятно, сокращает среднюю продолжительность диареи примерно на 16 часов (умеренная уверенность в доказательствах) но, вероятно, увеличивает риск развития рвоты ( умеренная уверенность в доказательствах).
В районах с высокой распространенностью дефицита цинка или недостаточности питания цинк может быть полезным у детей в возрасте шести месяцев или старше. Имеющиеся в настоящее время доказательства не поддерживают использование дополнительного введения цинка у детей младше 6 месяцев, хорошо питающихся детей и в условиях, где дети имеют низкий риск дефицита цинка.
S. boulardii CNCM I-745 устраняют причины и симптомы диареи с помощью специфического механизма действия
В доклинических исследованиях на животных моделях или моделях эпителиальных клеток кишечника продемонстрировано, что Saccharomyces boulardii CNCM I-745 нейтрализуют вредные бактериальные токсины путем блокирования активных центров рецепторов, непосредственного связывания с токсинами или синтеза белков, разрушающих их. 3
3
Например, один белок, синтезируемый Saccharomyces boulardii CNCM I-745, подавляет цАМФ-индуцированное увеличение продукции хлоридов, вызываемое токсином холеры и приводящее к увеличению экскреции воды. Кроме того, Saccharomyces boulardii CNCM I-745 могут непосредственно связывать токсины, предотвращая повреждение клеток.3
Другой антитоксический белок, секретируемая протеазарасщепляет токсины А и В Clostridium difficile, а также соответствующие рецепторы.3
Наконец, доклинические исследования на животных показали, что Saccharomyces boulardii CNCM I-745 вырабатывают протеинфосфатазу, которая дефосфорилирует липополисахарид Escherichia coli, снижая интенсивность воспаления.3
Помимо нейтрализации вредных токсинов, вырабатываемых болезнетворными бактериями, Saccharomyces boulardii CNCM I-745 также предотвращают их проникновение в стенку кишечника, выступая в качестве барьера и сохраняя плотные контакты клеток. 3 Дрожжи ингибируют фосфорилированиелегкой цепи миозина (связанного с формированием плотных контактов), предотвращая повышение проницаемости стенки кишечника.3 Было продемонстрировано, что это препятствует проникновению бактерий, таких как Shigella.3
3 Дрожжи ингибируют фосфорилированиелегкой цепи миозина (связанного с формированием плотных контактов), предотвращая повышение проницаемости стенки кишечника.3 Было продемонстрировано, что это препятствует проникновению бактерий, таких как Shigella.3
Исследования In vitro и исследования с помощью микроскопии показали, что Saccharomyces boulardii CNCM I-745 могут связываться с клетками бактериальных штаммов, например, E. coli, S. typhimurium, предотвращая их адгезию к клеткам кишечника.3 Визуализирующие исследования in vivo продемонстрировали, что Saccharomyces boulardii CNCM I-745 могут увеличивать скорость выведения некоторых патогенных бактерийчерез пищеварительный тракт.3 Также сообщалось о том, Saccharomyces boulardii CNCM I-745 могут напрямую подавлять рост бактерий, например, Yersinia enterocolitium.2
Опосредованные трофические эффекты
Saccharomyces boulardii CNCM I-745
Доклинические исследования показали, что Saccharomyces boulardii CNCM I-745 увеличивают ферментативную активность кишечника. 2 Сообщалось, что введение Saccharomyces boulardii CNCM I-745 связано с увеличением :
2 Сообщалось, что введение Saccharomyces boulardii CNCM I-745 связано с увеличением :
- лактазы, α-глюкозидазы и щелочной фосфатазы, которые участвуют в поддержании нормальной деятельности кишечника ; 1
- выработки полиаминов, веществ, участвующих в созревании энтероцитов ; 1,2
- дисахаридазы, которая улучшает усвоение глюкозы1, что может противодействовать процессам нарушения всасывания глюкозы и развитию осмотической диареи при ротавирусной инфекции ; 4
- активного всасывания D-глюкозы, сопряженной с Na+, и экспрессии натрий-глюкозного котранспортера-1 (НГЛТ-1) которые участвуют в транспорте глюкозы внутрь клеток.5
Кроме того, Saccharomyces boulardii CNCM I-745 опосредованно увеличивают протеолиз малых N-концевых пептидовпутем выработки лейцинаминопептидазы, принадлежащ ей к семейству цинковых металлопротеаз, что противодействует замедлению процессов пищеварения. 6
6
Другим трофическим воздействием является иммунное действие — Saccharomyces boulardii CNCM I-745 обладают способностью усиливать ответ организма на присутствие болезнетворных бактерий путем стимуляции выработки секреторного иммуноглобулина A (sIgA). Например, у мышей введение Saccharomyces boulardii CNCM I-745 повышает уровень циркулирующих антител IgA к токсину А C. difficile, связывающих и нейтрализующих этот токсин.3
Чем нас лечат: Смекта. Наноглина от диареи
Всемирная организация гастроэнтерологов написала такую рекомендацию по поводу каолина, активированного угля и других сорбентов: «Несостоятельные доказательства эффективности при диарее у взрослых, дополнительные траты, поэтому использоваться не должны». При инфекционной диарее сорбенты не лечат причину заболевания, а просто устраняют симптом — слишком частый жидкий стул. Поскольку этот симптом — не просто побочное действие, а механизм, который должен в прямом смысле устранить причину заболевания, есть вероятность, что лечиться от инфекции любителям таких препаратов придется дольше. Они сгодятся как разовая экстренная мера, скажем, если болезнь застала вас в путешествии, а вам срочно нужно сесть в автобус, который несколько часов будет ехать без остановок.
Они сгодятся как разовая экстренная мера, скажем, если болезнь застала вас в путешествии, а вам срочно нужно сесть в автобус, который несколько часов будет ехать без остановок.
С другой стороны, при отравлении, когда нужно не дать вредному веществу попасть в кровоток из кишечника, сорбент может быть очень полезен. Есть некоторые данные в пользу того, что Смекта помогает при изжоге и гастроэнтерите, однако их довольно мало.
При этом нужно понимать, что впитывающие способности Смекты помогут ей поглотить многие вещества, включая лекарства. Так что, если вы собрались выпить антибиотик, а потом принять еще и Смекту, пусть после приема первого лекарства пройдет хотя бы два часа, чтобы оно успело проникнуть в кровь и подействовать. Иначе оно свяжется в кишечнике и просто выйдет из организма, не причинив вам вреда, но и не успев принести пользу. Подробнее про отдельные лекарства можно почитать, например, в статье французских ученых.
Главным, самым проверенным (и чаще всего достаточным) средством лечения этого состояния остается регидратационный раствор. Если диарея мучает вас или вашего ребенка дольше трех-четырех дней без видимых признаков улучшения (в хронических случаях она длится не менее 10-14 дней) или в стуле есть кровь, нужно обратиться к врачу и сдать анализы. Не установив причину инфекции, подобрать лечение наугад бывает непросто. Тревожными симптомами можно считать признаки сильного обезвоживания, очень сильную рвоту, лихорадку, пониженное давление, ослабевший пульс, потерю сознания. В остальных случаях специфических медикаментов, как и определения, кого так усердно пытался изгнать ваш кишечник, не требуется.
Если диарея мучает вас или вашего ребенка дольше трех-четырех дней без видимых признаков улучшения (в хронических случаях она длится не менее 10-14 дней) или в стуле есть кровь, нужно обратиться к врачу и сдать анализы. Не установив причину инфекции, подобрать лечение наугад бывает непросто. Тревожными симптомами можно считать признаки сильного обезвоживания, очень сильную рвоту, лихорадку, пониженное давление, ослабевший пульс, потерю сознания. В остальных случаях специфических медикаментов, как и определения, кого так усердно пытался изгнать ваш кишечник, не требуется.
А вот прекращать кормить больного (и лишать грудного ребенка молока), даже если он не чувствует голода, ВОЗ не советует, выражая общий консенсус международного медицинского сообщества.
Профилактика: NICE guideline, анти- и пробиотики
Большинство состояний и болезней легче и приятнее предотвращать, чем лечить, и диарея явно не исключение. Принимать Смекту или антибиотики заранее (например, собираясь в страну с не самым высоким уровнем санитарии или во время радиотерапии) — бесполезная затея, объясняют авторы обзора о диарее путешественников и гайдлайна британского Национального института здоровья и клинического совершенствования (National Institute for Health and Care Excellence, или NICE). Те же рекомендации представлены и в виде интерактивной схемы.
Те же рекомендации представлены и в виде интерактивной схемы.
Так что, если вы не хотите устроить своим микробам войну с их туземными родственниками, которые, вполне возможно, давно стали безобидными для местного населения, лучше позаботьтесь о гигиене: мойте руки и следите за тем, что вы едите и пьете. Не забывайте и о прививках от распространенных в этом регионе заболеваний.
Диарея после антибиотиков: причины и лечение
В кишечнике каждого человека живет множество разнообразных микроорганизмов. Какие-то приносят безусловную пользу, участвуя, например, в синтезе витамина В12: какие-то абсолютно индифферентны и проходят ЖКТ транзитом; некоторые вызывает болезни.
Есть особенная группа микроорганизмов, которые мы называем «условно патогенными». Это грамположительные облигатные анаэробы, название которых происходит от греческого «клостед» — веретено. Клостридии спокойно живут в кишечнике множества людей, не принося никакого вреда. До определенного момента.
До определенного момента.
Своеобразным «пусковым механизмом» для активизации патогенных свойств антибиотиков клостридий становится прием антибиотиков. Антибиотики имеют свойство убивать микроорганизмы, причем — все без разбора. Но для клостридий, в большинстве своем, они безвредны. Из-за отсутствия конкурирующих микроорганизмов, «условно патогенные» клостридии переходят в разряд «патогенных». Микроорганизмы активно размножаются, создают колонии. А потом, в один момент, как по команде, все члены «клостридиального сообщества» начинают выделять токсины, которые и вызывают заболевание, именуемое «псевдомембранозный колит».
Клостридиальная инфекция опасна тем, что эти микроорганизмы выделяют сразу 2 токсина — цитотоксин и энтеротоксин. Один вызывает разрушение клеток слизистой кишечник, вплоть до изъязвления и перфорации.
Второй токсин через разрушенную слизистую кишечника беспрепятственно проникает в кровяное русло, разносится по всему организму и вызывает общую интоксикацию.
Клиническая картина псевдомембранозного колита может развиваться как на 3 день с начала приема антибиотика, так и спустя 1-10 дней с момента окончания его приема. А возможно и более отсроченное развитие колита — до 8 недель после антибиотикотерапии. Поэтому сложно бывает выявить этиологию диареи и поставить диагноз.
Типичным проявлением псевдомембранозного колита является жидкий стул, иногда с зеленоватой, бурой или кровянистой слизью. Больного мучают режущие боли в животе, усиливающиеся при пальпации. Боль объясняется повреждениями слизистой и воспалительным процессом в кишечнике.
В отдельных случаях манифестация заболевания может начинаться с лихорадки. Температура может подниматься до 40°С, а в некоторых случаях и выше.
Степень проявления симптомов у разных пациентов сильно варьирует.
При исследовании кишечника на всем протяжении слизистой обнаруживаются беловато-желтые псевдомембранозные бляшки. В тяжелых случаях видны фокальные некрозы, глубокие язвы с перфорацией. Неизмененная слизистая оболочка в виде мостиков перекинута между участками изъязвления.
Неизмененная слизистая оболочка в виде мостиков перекинута между участками изъязвления.
Чаще всего причиной активации становится прием таких антибиотиков, как линкомицин, клиндамицин, тетрациклин, ампициллин, цефалоспорины. Даже однократный прием антибиотиков, может привести к появлению псевдомембранозного колита. При легких проявлениях антибиотикоассоциированной диареи иногда для излечения достаточно отмены антибиотика. При более тяжелых терапия состоит в назначен ванкомицина и/или метронидазола. Важную роль в лечении больно: играет регидратация и восстановление электролитического баланса. Пациенту необходимо рекомендовать больше теплого питья и щадящую диету.
Но прием антибиотика — это полумера. Одновременно с антибиотиками необходимо назначение пробиотиков (препаратов, содержащих живые микроорганизмы.) Если бы врачи помнили об этом и назначали пробиотики одновременно с назначением антибиотикотерапии, то развития псевдомембранозного колита в большинстве случаев удалось бы избежать.
Среди врачей ведутся споры по поводу корректности термина «дисбактериоз». Но к какому бы выводу в итоге не пришли спорящие стороны, реальность остается реальностью — в результате приема антибиотиков нормальная микрофлора кишечника нарушается и на смену привычным для организма бактериям приходят вредоносные микробы.
С 1995 г. микроорганизмы со специфическими терапевтическими свойствами, ингибирующие рост патогенных бактерий, используются в официальной медицине и называются пробиотиками. Эти микроорганизмы при естественном способе введения оказывают положительное действие на физиологические, метаболические функции, а также биохимические и иммунные реакции организма.
Если верить не рекламным проспектам, а контролируемым рандомизированным исследованиям, то наиболее эффективными в лечении антибиотик-ассоциированных поражений кишечника являются дрожжевые грибы — сахаромицеты. Не зря издавна людям с расстройством пищеварения рекомендовали принимать кефир — сбраживающим агентом кефира является симбионт лактобактерий и сахаромицес. Но содержание полезных дрожжей в молочнокислых продуктах недостаточно, чтобы оказать терапевтический эффект. Поэтому в качестве профилактики развития нарушения баланса бактериальной флоры в кишечнике и для лечения антибиотик-ассоциированных диарей рекомендуется принимать препараты с живыми сахаромицетами.
Но содержание полезных дрожжей в молочнокислых продуктах недостаточно, чтобы оказать терапевтический эффект. Поэтому в качестве профилактики развития нарушения баланса бактериальной флоры в кишечнике и для лечения антибиотик-ассоциированных диарей рекомендуется принимать препараты с живыми сахаромицетами.
Предрасполагающие факторы для развития псевдомембранозного колита
- Антибиотикотерапия
- Возраст старше 60 лет.
- Нахождение в стационаре (особенно в одной палате с инфекционным больным или в реанимационном отделении).
- Недавно перенесенная операция на органах брюшной полости.
- Применения цитостатических препаратов (особенно метотрексата).
- Гемолитико-уремический синдром.
- Злокачественные заболевания.
- Ишемия кишечника.
- Почечная недостаточность.
- Некротический энтероколит
- Хронические воспалительные заболевания кишечника.
Острая диарея, ассоциированная с Clostridium difficile
Содержание номера
Т. А. Соломенцева,
А. Соломенцева,
ГУ «Институт терапии имени Л.Т. Малой АМН Украины», г. Харьков
Диарейный синдром, особенно острая диарея, которая не проходит самостоятельно, является труднокурируемой патологией, требующей скорой помощи пациенту, так как влечет за собой нарушение электролитного баланса и трофологическую недостаточность. При острой диарее быстро развивается значительно выраженная дегидратация организма. Иногда она приобретает катастрофическое значение и может угрожать жизни пациента. Возникновение острой диареи требует проведения неотложных мероприятий для правильной постановки диагноза и назначения адекватной терапии.
В зависимости от причины возникновения диареи и ведущего механизма развития необходим дифференцированный подход к лечению. Поэтому важным этапом является установление причины острой диареи для назначения своевременного и успешного лечения, от которого зависит прогноз больного.
Диарея (понос) — это учащение дефекаций и одновременно изменение консистенции кала (кал становится жидким и кашицеобразным). Диагностическим критерием диареи является повышение содержания жидкости в фекалиях с 60–75 до 85–90% или увеличение их массы более 200 г в сутки. Острой диарея считается, если ее продолжительность не превышает 2–3 недель, хронической — если жидкий стул продолжается более 3 недель [1].
Диагностическим критерием диареи является повышение содержания жидкости в фекалиях с 60–75 до 85–90% или увеличение их массы более 200 г в сутки. Острой диарея считается, если ее продолжительность не превышает 2–3 недель, хронической — если жидкий стул продолжается более 3 недель [1].
Причинами развития острой диареи чаще всего являются прием лекарственных препаратов, инфекционные возбудители или их токсины, воспалительные или ишемические заболевания кишечника, воспаление в органах малого таза.
Инфекционная диарея является наиболее угрожающей для жизни пациента и наиболее сложной для выбора тактики лечения. Часто этиологический фактор поноса, обусловленного инфекционными агентами, установить не удается. Очень важным в этой связи является выделение из спектра инфекционной диареи колита, обусловленного инфекцией Clostridium difficile (С. difficile), так как данная патология требует особого подхода к тактике ведения пациентов. Предполагать наличие С. difficile как этиологического фактора диареи необходимо у любого больного, прошедшего курс антибиотикотерапии в течение предшествующих 4–8 недель. Симптомы могут возникать в первые дни приема антибиотиков и до 2 месяцев после прекращения лечения.
Симптомы могут возникать в первые дни приема антибиотиков и до 2 месяцев после прекращения лечения.
Антибиотикоассоциированный колит — воспалительное заболевание толстой кишки, ассоциированное с антибиотикотерапией, чаще всего вызванное инфекцией С. difficile и варьирующее от кратковременной диареи до тяжелого псевдомембранозного колита с образованием фибринозных бляшек на слизистой оболочке толстой кишки. Иногда используется также неофициальное название — С. difficile-колит.
Актуальность проблемы антибиотикоассоциированных диарей связана с неконтролируемым применением антибиотиков, что обусловливает усиление побочных эффектов антибиотикотерапии. Частым осложнением антибиотикотерапии является диарея, которая регистрируется в 3–25% от всех случаев применения антибиотиков. Виновником острой диареи у половины пациентов, принимающих антибиотики или другие антибактериальные агенты, является С. difficile.
Инфекция С. difficile — наиболее частая причина госпитальной диареи. В лечебных учреждениях и домах престарелых С. difficile выделяется у 30% больных с бессимптомным течением заболевания и в настоящее время признана основной причиной госпитальной диареи. При внутрибольничных вспышках наблюдается наиболее тяжелое течение данной инфекции [1]. Распространенность антибиотикоассоциированной диареи у амбулаторных больных также высока и cоставляет 22 случая на 100 тысяч населения [3].
В лечебных учреждениях и домах престарелых С. difficile выделяется у 30% больных с бессимптомным течением заболевания и в настоящее время признана основной причиной госпитальной диареи. При внутрибольничных вспышках наблюдается наиболее тяжелое течение данной инфекции [1]. Распространенность антибиотикоассоциированной диареи у амбулаторных больных также высока и cоставляет 22 случая на 100 тысяч населения [3].
Фактором риска развития колита, обусловленного С. difficile, служит прием антибиотиков и некоторых других лекарственных средств, обладающих антибактериальными свойствами. Прием практически любого антибиотика может быть связан с риском возникновения антибиотикоассоциированной диареи, но чаще всего тяжелое воспаление в кишечнике вызывают антибиотики широкого спектра действия. К наиболее опасным в этом отношении относятся клиндамицин, цефалоспорины (цефазолин, цефалексин и др.), производные пенициллина, клавулановая кислота. Клиндамицин — один из антибиотиков, который вызывает классические нарушения в кишечнике, характерные для псевдомембранозного колита. Совместное применение антибиотиков и лекарственных препаратов с антихолинергическими эффектами увеличивает риск развития псевдомембранозного колита в несколько раз. Препараты данной группы замедляют кишечный транзит и увеличивают время контакта бактерий со слизистой оболочкой кишки, задерживают токсины, усиливают эффекты антибиотиков широкого спектра действия.
Совместное применение антибиотиков и лекарственных препаратов с антихолинергическими эффектами увеличивает риск развития псевдомембранозного колита в несколько раз. Препараты данной группы замедляют кишечный транзит и увеличивают время контакта бактерий со слизистой оболочкой кишки, задерживают токсины, усиливают эффекты антибиотиков широкого спектра действия.
Лица старше 60 лет более подвержены этому заболеванию. Пациенты, имеющие сопутствующую патологию, особенно сахарный диабет, аутоиммунные заболевания, цирроз печени, также попадают в группу риска развития псевдомембранозного колита. У больных, получающих иммуносупрессивную терапию, рост С. difficile наблюдается в 2 раза чаще, чем в общей популяции. К другим факторам риска относят последствия оперативного вмешательства и инвазивные процедуры на органах брюшной полости. Следует отметить, что сам факт госпитализации в стационар увеличивает риск развития псевдомембранозного колита.
В некоторых опубликованных источниках имеются единичные сведения о том, что длительный прием ингибиторов протонной помпы может усиливать размножение C. difficile в кишечнике и провоцировать развитие псевдомембранозного колита [2]. На сегодняшний день этот вопрос остается недостаточно изученным. Для более убедительного подтверждения данного предположения необходимо проведение широкомасштабных клинических исследований. Данные недавно проведенного многоцентрового контролируемого исследования показали, что ингибиторы протонной помпы не являются факторами риска развития псевдомембранозного колита. [4]
difficile в кишечнике и провоцировать развитие псевдомембранозного колита [2]. На сегодняшний день этот вопрос остается недостаточно изученным. Для более убедительного подтверждения данного предположения необходимо проведение широкомасштабных клинических исследований. Данные недавно проведенного многоцентрового контролируемого исследования показали, что ингибиторы протонной помпы не являются факторами риска развития псевдомембранозного колита. [4]
Реакция микрофлоры кишки на прием антибиотиков связана с нарушением нормального функционирования кишечной микробиоты. Под воздействием антибиотиков широкого спектра действия уменьшается количество анаэробов нормальной кишечной микрофлоры, нарушаются переваривание и всасывание углеводов и клетчатки, что обусловливает возникновение осмотической диареи. Неабсорбированные углеводы в просвете кишки создают избыточное осмотическое давление, способствуя повышенной секреции воды в просвет кишечника. Нарушение нормальной бактериальной флоры кишечника вызывает снижение синтеза короткоцепочечных жирных кислот и также приводит к нарушению адсорбции воды и электролитов, что усиливает диарейный синдром.
Важным механизмом развития диареи при приеме антибиотиков является снижение защитной функции кишки за счет снижения колонизационной резистентности, способности нормальной кишечной микрофлоры эффективно подавлять рост и размножение патогенных микроорганизмов. В результате этого снижаются местный иммунитет, синтез иммуноглобулина А, лизоцима. В условиях снижения конкуренции за жизненное пространство и питательные вещества появляется возможность для гораздо более бурного роста патогенных бактерий, в частности С. difficile [3]. С. difficile — это грамположительный спорообразующий анаэроб, являющийся представителем условно-патогенной кишечной микрофлоры. Повреждающее воздействие на кишечную стенку наносится посредством выработки токсинов А и В, которые действуют синергически и потенцируют друг друга. [3].
Спектр заболеваний, связанных с размножением в толстой кишке С. difficile, варьирует от легкой диареи до тяжелых форм псевдомембранозного колита, который при нераспознанных случаях может осложняться токсическим мегаколоном и перфорацией толстой кишки. Необходимо помнить, что симптомы заболевания могут возникать как в первые дни приема антибиотиков, так и в течение 2 месяцев после прекращения лечения.
Необходимо помнить, что симптомы заболевания могут возникать как в первые дни приема антибиотиков, так и в течение 2 месяцев после прекращения лечения.
Псевдомембранозный колит характеризуется поносом до 7–10 раз в сутки, в тяжелых случаях — до 15–20 раз в сутки, абдоминальной болью и лихорадкой. Обычно понос не сопровождается выделением крови, хотя кровь может появляться, если больной принимает антикоагулянты или антитромбоцитарные препараты либо имеет сопутствующее заболевание кишечника, например геморрой. Боль в животе почти всегда присутствует, носит схваткообразный характер и может быть достаточно интенсивной. Иногда наблюдаются перитонеальные симптомы, положительный симптом раздражения брюшины при пальпации живота. В легких случаях температура тела субфебрильная, однако у некоторых пациентов может повышаться до 38–40°С. Конституциональные симптомы типа лихорадки, дегидратации, потери аппетита также выражены в развернутой фазе заболевания. Общая астенизация очень характерна для пациентов с колитом, ассоциированным с патологическим ростом С. difficile. Фактически один из основных способов заподозрить псевдомембранозный колит у лиц с диарей, вызванной антибиотиками, — это правильная оценка астенического состояния. Пациенты часто выглядят обессиленными, сонливыми и вообще нездоровыми, имеют «больной» внешний вид. Однако подобная клиническая картина может наблюдаться при любой острой инфекционной диарее, тяжелых формах воспалительных заболеваний кишечника. Отсутствие четких типичных клинических симптомов может затруднить диагностику и отсрочить начало этиотропной терапии.
difficile. Фактически один из основных способов заподозрить псевдомембранозный колит у лиц с диарей, вызванной антибиотиками, — это правильная оценка астенического состояния. Пациенты часто выглядят обессиленными, сонливыми и вообще нездоровыми, имеют «больной» внешний вид. Однако подобная клиническая картина может наблюдаться при любой острой инфекционной диарее, тяжелых формах воспалительных заболеваний кишечника. Отсутствие четких типичных клинических симптомов может затруднить диагностику и отсрочить начало этиотропной терапии.
Диагностика псевдомембранозного колита строится на классических принципах. Для постановки правильного диагноза существенно важны данные анамнеза заболевания. Тщательный сбор анамнеза является ключом к выбору дальнейшей тактики обследования и лечения пациентов с острой диареей. В большинстве случаев пациент, заболевший псевдомембранозным колитом, недавно принимал антибиотики. Любое применение пациентом антибактериальных средств в течение последних месяцев должно привлечь внимание врача. Болезнь может развиться уже после одного или двух месяцев использования антибиотиков. Хотя есть некоторая зависимость между дозой и продолжительностью приема антибиотика и вероятностью развития псевдомембранозного колита, заболевание может возникнуть даже после однократного приема антибиотика. Профилактическое назначение антибиотика перед оперативным вмешательством у пациентов с хирургической патологией также может быть причиной развития пседомембранозного колита в послеоперационный период.
Болезнь может развиться уже после одного или двух месяцев использования антибиотиков. Хотя есть некоторая зависимость между дозой и продолжительностью приема антибиотика и вероятностью развития псевдомембранозного колита, заболевание может возникнуть даже после однократного приема антибиотика. Профилактическое назначение антибиотика перед оперативным вмешательством у пациентов с хирургической патологией также может быть причиной развития пседомембранозного колита в послеоперационный период.
Тщательный осмотр больного и правильная интерпретация клинических симптомов позволяют предположить наличие у пациента псевдомембранозного колита.
Результаты лабораторных исследований могут лишь незначительно дополнить информацию, полученную при сборе анамнеза и объективном осмотре. При оценке результатов лабораторных исследований в крови выявляют анемию, лейкоцитоз со сдвигом формулы крови влево, увеличение скорости оседания эритроцитов (СОЭ), низкий сывороточный альбумин. Лейкоцитоз иногда может достигать высоких значений. Копрологическое исследование показывает наличие лейкоцитоза, обильной йодофильной микрофлоры, иногда — небольшого количества эритроцитов.
Копрологическое исследование показывает наличие лейкоцитоза, обильной йодофильной микрофлоры, иногда — небольшого количества эритроцитов.
Стандартом диагностики служит исследование кала на наличие токсинов А и В С. difficile методом иммуноферментного анализа, результаты которого можно получить в течение нескольких часов, а чувствительность и специфичность метода приближаются к 100%. В редких случаях определить наличие токсинов не удается; это связано с тем, что часть штаммов C. difficile вырабатывает другие токсины. В стандартные панели для диагностики входит исследование только двух токсинов — А и B.
В таких случаях диагностика должна базироваться на данных колоноскопии и микробиологического исследования кала.
Диагностика заболевания при помощи получения культуры стула ограничивается временными интервалами, а также микробиологическими особенностями С. difficile. Выделить культуру из фекалий пациента и получить рост колоний С. difficile удается приблизительно в 20% случаев антибиотикоассоциированной диареи. Поэтому иммуноферментный метод диагностики является более информативным.
Поэтому иммуноферментный метод диагностики является более информативным.
Колоноскопия и сигмоскопия используются для проведения дифференциальной диагностики с воспалительными заболевания толстой кишки, опухолями. Чаще воспалительные изменения при псевдомембранозном колите локализуются преимущественно в дистальных отделах ободочной кишки, в некоторых случаях могут поражаться и правые отделы толстого кишечника. При эндоскопическом исследовании при колите, ассоциированном с С. difficile, определяется выраженный отек, гиперемия слизистой оболочки, контактная кровоточивость. Характерными являются патологические образования на стенках ободочной или прямой кишки, в виде желтых фибринозных пленок (псевдомембран) на слизистой оболочке. До появления результатов иммуноферментного и бактериологического исследований стула диагноз устанавливается на основании характерной картины эндоскопии.
Осложнениями псевдомембранозного колита являются электролитные нарушения, дегидратация, снижение артериального давления, перфорация толстой кишки. Угрожающее жизни осложнение — развитие токсического мегаколона. Дилатация кишки более 6 см и рефрактерное течение проводимой терапии являются показанием к срочной тотальной колэктомии.
Угрожающее жизни осложнение — развитие токсического мегаколона. Дилатация кишки более 6 см и рефрактерное течение проводимой терапии являются показанием к срочной тотальной колэктомии.
Выбор лечения во многом зависит от тяжести состояния пациента, сопутствующей патологии, наличия осложнений. Препаратами этиотропной терапии являются метранидазол и ванкомицин.
Обычно при легких и среднетяжелых формах колита лечение начинают с метронидазола, который назначается перорально по 250 мг 4 раза в сутки в течение 7–10 дней. В качестве альтернативного препарата может применяться ванкомицин перорально по 125 мг 4 раза в сутки в течение 10 дней. При тяжелых формах псевдомембранозного колита, угрозе развития осложнений дозы антибиотиков повышаются. Так, метранидазол назначается по 500 мг внутривенно каждые 6 часов, доза ванкомицина также может быть увеличена до 2 г в сутки, разделенная на четыре приема внутрь. Внутривенное введение ванкомицина неэффективно, так как при таком способе не достигается необходимая концентрация препарата в полости толстой кишки. При необходимости можно вводить препарат через назогастральный зонд.
При необходимости можно вводить препарат через назогастральный зонд.
Ванкомицин для лечения данной патологии является препаратом резерва. Ограничение применения ванкомицина связано с его высокой стоимостью и высоким риском развития устойчивого к нему энтерококка. Поэтому круг назначения ванкомицина ограничивается группой пациентов, нечувствительных к метронидазолу, или с известной непереносимостью препарата. Также ванкомицин назначается в качестве терапии первой линии беременным женщинам, лицам, употребляющим алкоголь во время лечения, пациентам с рецидивом псевдомембранозного колита после курса метронидазола.
Применение пробиотиков в качестве этиотропного лечебного средства не привело к желаемым результатам. Рандомизированное контролируемое исследование, в котором применялся пробиотический напиток, содержащий Lactobacillus casei, L. bulgaricus и Streptococcus thermophilus, показало невысокую эффективность данной терапии по сравнению с традиционными методами лечения [6].
Более удовлетворительные результаты были получены при использовании грибов Saccharomyces boulardii для лечения 124 пациентов с рецидивом псевдомембранозного колита [5].
В качестве альтернативы традиционного лечения была предложена фекальная бактериотерапия — процедура, связанная со введением бактериальной флоры, полученной от здорового донора, в толстую кишку больного. Данный метод лечения основан на ликвидации бактериального дисбаланса, который наблюдается у пациентов с рецидивированием инфекции С. difficile. Высокая вероятность успеха — почти 95% — делает ее эффективным методом резервной терапии для антибиотикоустойчивых и рецидивирующих форм C. difficile-инфекции.
Сопутствующая терапия может включать холестирамин, сорбенты, способные связывать токсины С. difficile.
Регидратационная терапия показана всем пациентам с наличием электролитных нарушений.
Несмотря на проводимую терапию, нерешенной проблемой антибиотикоассоциированной диареи является рецидив инфекции С. difficile. Она становится причиной рецидивирующей диареи у 12–20% пациентов. Причиной рецидива может быть как сохранение в споровой форме первичного штамма, так и повторное заражение другим штаммом. Рецидивы возникают обычно через 28 недель после окончания специфической терапии, направленной на уничтожение С. difficile.
Рецидивы возникают обычно через 28 недель после окончания специфической терапии, направленной на уничтожение С. difficile.
Острая диарея, вызванная ростом С. difficile, является достаточно распространенным заболеванием, которое отягощает течение основного заболевания, особенно у лиц с наличием сочетанной патологии. Поэтому дифференцированное назначения антибиотиков по строгим показаниям позволит уменьшить риск развития С. difficile и будет способствовать профилактике возникновения антибиотикоассоциированной диареи.
Литература
1. Парфенов А.И. Энтерология. – М.: Триада Х, 2002. – 724 с.
2. Dial S., Delaney C., Schneider V., Suissa S. Proton pump inhibitor use and risk of community-acquired Clostridium difficile-associated disease defined by prescription for oral vancomycin therapy // CMAJ. – 2006. – Vol. 175 (7). – P. 745–748.
3. Pepin J., Saheb N., Coulombe M. et al. Emergence of fluoroquinolones as the predominant risk factor for Clostridium difficile associated diarrhea: a cohort study during an epidemic in Quebec // Clin. Infect. Dis. – 2005. – Vol. 41. – P. 1254–1260.
Infect. Dis. – 2005. – Vol. 41. – P. 1254–1260.
4. Lowe D.O., Mamdani M.M., Kopp A. et al. Proton pump inhibitors and hospitalization for Clostridium difficile-associated disease: a population-based study // Clin. Infect. Dis. – 2006. – Vol. 43 (10). – P. 1272–1276.
5. McFarland L.V., Surawicz C.M., Greenberg R.N. et al. A randomized placebo-controlled trial of Saccharomyces boulardii in combination with standard antibiotics for Clostridium difficile disease // JAMA. – 1994. – Vol. 271 (24). – P. 1913–1918.
6. Hickson M., D’Souza A.L., Muthu N. et al. Use of probiotic Lactobacillus preparation to prevent diarrhoea associated with antibiotics: randomized double blind placebo controlled trial // BMJ. – 2007. – Vol. 335 (7610). – P. 80.
Диарея: основы практики, предпосылки, патофизиология
King CK, Glass R, Bresee JS, Duggan C. Ведение острого гастроэнтерита у детей: пероральная регидратация, поддерживающая терапия и нутритивная терапия. MMWR Recomm Rep . 2003 21 ноября. 52: 1-16. [Медлайн].
Ведение острого гастроэнтерита у детей: пероральная регидратация, поддерживающая терапия и нутритивная терапия. MMWR Recomm Rep . 2003 21 ноября. 52: 1-16. [Медлайн].
Фишер Т.К., Вибоуд К., Парашар Ю., Малек М., Штайнер С., Гласс Р. и др. Госпитализации и смерти детей от диареи и ротавируса J Infect Dis . 2007 15 апр.195 (8): 1117-25. [Медлайн].
Cortese MM, Tate JE, Simonsen L, Edelman L, Parashar UD. Снижение заболеваемости гастроэнтеритом у детей в США и корреляция с ранним использованием ротавирусной вакцины из национальных баз данных медицинских заявлений. Pediatr Infect Dis J . 29 июня 2010 г. (6): 489-94. [Медлайн].
Talbert A, Thuo N, Karisa J, Chesaro C, Ohuma E, Ignas J, et al. Диарея, осложняющая тяжелую острую недостаточность питания у кенийских детей: проспективное описательное исследование факторов риска и исходов. PLoS One . 2012. 7 (6): e38321. [Медлайн]. [Полный текст].
PLoS One . 2012. 7 (6): e38321. [Медлайн]. [Полный текст].
Любберт С., Циммерманн Л., Борхерт Дж., Хорнер Б., Муттерс Р., Родлофф А.С. Эпидемиология и частота рецидивов инфекций Clostridium difficile в Германии: анализ вторичных данных. Инфекция Dis Ther . 2016 21 октября [Medline].
Эспозито Д.Х., Холман Р.С., Хаберлинг Д.Л., Тейт Дж.Э., Подевилс Л.Дж., Гласс Р.И. и др. Исходные оценки смертности от диареи среди детей в США до внедрения ротавирусной вакцины. Pediatr Infect Dis J . 2011 30 ноября (11): 942-7. [Медлайн].
Mehal JM, Esposito DH, Holman RC, Tate JE, Sinden LL, Parashar UD. Факторы риска детской смертности, связанной с диареей, в США, 2005–2007 гг. Pediatr Infect Dis J . 2012 9 марта. [Medline].
Хейман М.Б., Абрамс С.А., СЕКЦИЯ ГАСТРОЭНТЕРОЛОГИИ, ГЕПАТОЛОГИИ И ПИТАНИЯ. КОМИТЕТ ПО ПИТАНИЮ. Фруктовый сок у младенцев, детей и подростков: современные рекомендации. Педиатрия . 2017 22 мая. [Medline].
Йи Дж., Седердал Б.К., Валь К. и др. Ротавирус и норовирус в педиатрическом гастроэнтерите. Открытый форум Infect Dis .2016 30 августа. 3 (4): ofw181. [Медлайн]. [Полный текст].
Гуарино А., Альбано Ф., Ашкенази С. и др. Европейское общество детской гастроэнтерологии, гепатологии и питания / Европейское общество педиатрических инфекционных заболеваний, основанное на фактических данных, руководство по ведению острого гастроэнтерита у детей в Европе: резюме. J Педиатр Гастроэнтерол Нутр . 2008 май. 46 (5): 619-21. [Медлайн].
J Педиатр Гастроэнтерол Нутр . 2008 май. 46 (5): 619-21. [Медлайн].
[Рекомендации] Атия А.Н., Бухман А.Л.Растворы для пероральной регидратации при нехолерной диарее: обзор. Ам Дж. Гастроэнтерол . 2009 октябрь 104 (10): 2596-604; викторина 2605. [Medline].
Kling J. Зеленый чай и экстракт граната помогают бороться с диареей у детей. Медицинские новости Medscape. Доступно на http://www.medscape.com/viewarticle/833747. Доступ: 24 октября 2014 г.
Гуандалини С. Пробиотики для профилактики и лечения диареи. Дж Клин Гастроэнтерол .2011 ноябрь 45 Дополнение: S149-53. [Медлайн].
Ruiz-Palacios GM, Perez-Schael I, Velazquez FR, et al. Безопасность и эффективность аттенуированной вакцины против тяжелого ротавирусного гастроэнтерита. N Engl J Med . 2006, 5 января. 354 (1): 11-22. [Медлайн]. [Полный текст].
N Engl J Med . 2006, 5 января. 354 (1): 11-22. [Медлайн]. [Полный текст].
Соарес-Вайзер К., МакЛехоз Х, Бергман Х, Бен-Аарон И., Нагпал С., Голдберг Э и др. Вакцины для предотвращения ротавирусной диареи: используемые вакцины. Кокрановская база данных систематических обзоров .2012.
Platts-Mills JA, Babji S, Bodhidatta L, et al. Патоген-специфическое бремя общинной диареи в развивающихся странах: многопрофильное когортное исследование (MAL-ED). Ланцетный шар Здоровье . 2015 Сентябрь 3 (9): e564-75. [Медлайн].
Абубакар I, Алию Ш., Арумугам Ц, Усман Н.К., Хантер пр. Лечение криптоспоридиоза у лиц с ослабленным иммунитетом: систематический обзор и метаанализ. Br J Clin Pharmacol .2007 апр. 63 (4): 387-93. [Медлайн].
Bellemare S, Hartling L, Wiebe N и др. Пероральная регидратация по сравнению с внутривенной терапией для лечения обезвоживания из-за гастроэнтерита у детей: метаанализ рандомизированных контролируемых исследований. BMC Med . 2004 15 апреля 2:11. [Медлайн]. [Полный текст].
Брайс Дж, Боски-Пинто C, Сибуя К, Черный RE ,.Оценки ВОЗ причин смерти детей. Ланцет . 2005 26 марта — 1. 365 (9465): 1147-52. [Медлайн].
Чарльз М.Д., Холман Р.К., Кернс А.Т. и др. Госпитализации, связанные с ротавирусным гастроэнтеритом в США, 1993-2002 гг. Pediatr Infect Dis J . 2006 июн.25 (6): 489-93. [Медлайн].
Girard MP, Steele D, Chaignat CL, Kieny MP. Обзор исследований и разработок вакцин: кишечные инфекции человека. Вакцина . 2006 Apr 5. 24 (15): 2732-50. [Медлайн].
Гуандалини С. Лечение острой диареи в новом тысячелетии. J Педиатр Гастроэнтерол Нутр . 2000 Май. 30 (5): 486-9. [Медлайн].
Guandalini S, Dincer AP.Управление питанием при диарейных заболеваниях. Байер Клин Гастроэнтерол . 1998 12 декабря (4): 697-717. [Медлайн].
Guandalini S, Kahn S. Острая диарея. Уокер А., Гуле О., Клейнман Дж. И др. Заболевания желудочно-кишечного тракта у детей . Онтарио, Канада: Брайан К. Декер; 2008. Том 1: 252-64 / Глава 15.
Онтарио, Канада: Брайан К. Декер; 2008. Том 1: 252-64 / Глава 15.
Matson DO, Staat MA, Azimi P, Itzler R, Bernstein DI, Ward RL, et al. Бремя госпитализаций детей раннего возраста в связи с ротавирусом в трех педиатрических больницах США определено путем активного наблюдения по сравнению со стандартными косвенными методами. J Детский педиатр . 2012 25 апреля. [Medline].
Mayo-Wilson E, Junior JA, Imdad A, Dean S, Chan XH, Chan ES, et al. Добавка цинка для предотвращения смертности, заболеваемости и задержки роста у детей в возрасте от 6 месяцев до 12 лет. Кокрановская база данных Syst Rev . 2014 15 мая. 5: CD009384. [Медлайн].
Миллер Р.К., Петерейт Д.Г., Слоан Дж. А. и др. Рандомизированное исследование фазы III сравнения сульфасалазина с плацебо в профилактике острой диареи у пациентов, получающих лучевую терапию тазовых органов [аннотация LBA2]. Представлено на 55-м ежегодном собрании Американского общества радиационной онкологии (ASTRO); 22 сентября 2013 г .; Атланта, Джорджия.
Представлено на 55-м ежегодном собрании Американского общества радиационной онкологии (ASTRO); 22 сентября 2013 г .; Атланта, Джорджия.
Mulcahy N. Рекомендуемый препарат может вызвать диарею с лучевой терапией. 3 октября 2013 года. Medscape Medical News. Доступно на http://www.medscape.com/viewarticle/812057. Доступ: 7 октября 2013 г.
Sandhu BK, Isolauri E, Walker-Smith JA и др. Многоцентровое исследование от имени Рабочей группы по острой диарее Европейского общества педиатрической гастроэнтерологии и питания.Раннее вскармливание в детском гастроэнтерите. J Педиатр Гастроэнтерол Нутр . 1997 Май. 24 (5): 522-7. [Медлайн].
Салливан ПБ. Питание при острой диарее. Питание . 1998, 14 октября (10): 758-62. [Медлайн].
[Рекомендации] Уокер-Смит Дж. А., Сандху Б. К., Исолаури Э. и др. Рекомендации подготовлены Рабочей группой ESPGAN по острой диарее. Рекомендации по кормлению при детском гастроэнтерите. Европейское общество детской гастроэнтерологии и питания. J Педиатр Гастроэнтерол Нутр . 1997 Май. 24 (5): 619-20. [Медлайн].
А., Сандху Б. К., Исолаури Э. и др. Рекомендации подготовлены Рабочей группой ESPGAN по острой диарее. Рекомендации по кормлению при детском гастроэнтерите. Европейское общество детской гастроэнтерологии и питания. J Педиатр Гастроэнтерол Нутр . 1997 Май. 24 (5): 619-20. [Медлайн].
Арасараднам Р.П., Браун С., Форбс А., Фокс М.Р., Хангин П., Кельман Л. и др. Рекомендации по исследованию хронической диареи у взрослых: Британское общество гастроэнтерологов, 3-е издание. Кишечник . 13 апреля 2018 г. [Medline].
Олортеги М.П., Рухани С., Йори П.П. и др. Астровирусная инфекция и диарея в 8 странах. Педиатрия . 2018 Янв.141 (1): [Medline].
[Руководство] Садовски Д.К., Камиллери М., Чей В.Д., Леонтиадис Г.И., Маршалл Дж. К., Шаффер Е.А. и др. Руководство Канадской ассоциации гастроэнтерологов по клинической практике по лечению диареи, вызванной желчными кислотами. Клин Гастроэнтерол Гепатол . 2020 18 января (1): 24-41.e1. [Медлайн].
Клин Гастроэнтерол Гепатол . 2020 18 января (1): 24-41.e1. [Медлайн].
Обезвоживание: общие сведения, патофизиология, этиология
Bettari L, Fiuzat M, Shaw LK, et al. Гипонатриемия и отдаленные исходы хронической сердечной недостаточности — обсервационное исследование из Duke Databank for Cardiovascular Diseases. J Card Fail . 2012 18 января (1): 74-81. [Медлайн].
Guarner J, Hochman J, Kurbatova E, Mullins R. Исследование исходов, связанных с гипонатриемией и гипернатриемией у детей. Педиатр Дев Патол . 2011 март-апрель. 14 (2): 117-23. [Медлайн].
Заки С.А., Мондкар Дж., Шанбаг П., Верма Р. Гипернатремическое обезвоживание из-за недостаточности лактации у новорожденных, вскармливаемых исключительно грудью. Saudi J Kidney Dis Transpl . 2012 Янв.23 (1): 125-8. [Медлайн].
[Медлайн].
Арора СК. Гипернатремические расстройства в отделении интенсивной терапии. J Intensive Care Med . 2013 янв-фев. 28 (1): 37-45. [Медлайн].
Colletti JE, Brown KM, Sharieff GQ, Barata IA, Ishimine P, ACEP Pediatric Emergency Medicine Committee. Ведение детей с гастроэнтеритом и обезвоживанием в отделении неотложной помощи. J Emerg Med . 2010 июн. 38 (5): 686-98. [Медлайн].
Parkin PC, Macarthur C, Khambalia A, Goldman RD, Friedman JN.Клинико-лабораторная оценка степени обезвоживания у детей с острым гастроэнтеритом. Clin Pediatr (Phila) . 2010 Март 49 (3): 235-9. [Медлайн].
Костер С., Клингельхофер Д., Гронеберг Д.А., Шварцер М. Ротавирус — Глобальное исследование, выравнивающее картирование плотности и гендерный анализ. Вакцина . 2016 г. 2 января. 34 (1): 90-100. [Медлайн].
Вакцина . 2016 г. 2 января. 34 (1): 90-100. [Медлайн].
Cheuvront SN, Kenefick RW, Montain SJ, Sawka MN. Механизмы снижения аэробной работоспособности при тепловом стрессе и обезвоживании. J Appl Physiol . 2010 декабрь 109 (6): 1989-95. [Медлайн].
[Рекомендации] Голдман Р.Д., Фридман Дж. Н., Паркин П.С. Валидация клинической шкалы обезвоживания у детей с острым гастроэнтеритом. Педиатрия . 2008 сентябрь 122 (3): 545-9. [Медлайн].
Каруджи С., Росси М., Де Джакомо С. и др. Оценка обезвоживания у детей при сортировке: проспективное исследование времени восстановления. Гастроэнтерол Педиатр Hepatol Nutr .2018 21 октября (4): 278-88. [Медлайн].
Штайнер MJ, DeWalt DA, Byerley JS. Этот ребенок обезвожен? JAMA ._5.jpg) 2004, 9 июня. 291 (22): 2746-54. [Медлайн].
2004, 9 июня. 291 (22): 2746-54. [Медлайн].
Штайнер MJ, Nager AL, Wang VJ. Удельный вес мочи и другие показатели мочи: неточные тесты на обезвоживание. Скорая педиатрическая помощь . 2007 май. 23 (5): 298-303. [Медлайн].
Brandt KG, de Castro Antunes MM, da Silva GA. Острая диарея: лечение, основанное на доказательствах. Дж. Педиатр (Рио Дж.) . 2015 ноябрь-декабрь. 91 (6 доп. 1): S36-43. [Медлайн].
[Рекомендации] Карсон Р.А., Мадд С.С., Мадати П.Дж. Руководство по клинической практике лечения острого гастроэнтерита у детей в амбулаторных условиях. J Педиатр здравоохранения . 2016 ноябрь — декабрь 30 (6): 610-6. [Медлайн].
Ли Г.О., Ричард С.А., Канг Джи и другие, для исследователей сети MAL-ED. Сравнение показателей тяжести диареи в многоцентровом когортном исследовании MAL-ED на базе сообщества. J Педиатр Гастроэнтерол Нутр . 2016 ноябрь 63 (5): 466-73. [Медлайн].
J Педиатр Гастроэнтерол Нутр . 2016 ноябрь 63 (5): 466-73. [Медлайн].
Всемирная организация здравоохранения. Информация ВОЗ о лекарствах Vol. 16, No. 2, 2002: новая формула солей для пероральной регидратации. Доступно по адресу http://apps.who.int/medicinedocs/en/d/Js4950e/2.4.html. 10 мая 2002 г .; Дата обращения: 29 ноября 2018 г.
ЮНИСЕФ. Новая формула солей для пероральной регидратации (ПРС) с пониженной осмолярностью — отчет совещания экспертов, организованного совместно ЮНИСЕФ и ВОЗ.WHO / CAH / 01.22. Технический бюллетень № 9 . 10 мая 2002 г. Доступно по адресу https://www.unicef.org/supply/files/Oral_Rehydration_Salts(ORS)_.pdf.
Кумар Р., Кумар П., Анея С., Кумар В., Рехан Х.С. Безопасность и эффективность ПРС с низкой осмолярностью по сравнению с модифицированным раствором для регидратации для детей с недостаточным питанием для лечения детей с тяжелой острой недостаточностью питания и диареей: рандомизированное контролируемое исследование. Дж. Троп Педиатр . 2015 Декабрь 61 (6): 435-41. [Медлайн].
Дж. Троп Педиатр . 2015 Декабрь 61 (6): 435-41. [Медлайн].
Atherly-John YC, Каннингем SJ, Crain EF. Рандомизированное испытание пероральной и внутривенной регидратации в педиатрическом отделении неотложной помощи. Arch Pediatr Adolesc Med . 2002 Декабрь 156 (12): 1240-3. [Медлайн].
Hartling L, Bellemare S, Wiebe N, Russell K, Klassen TP, Craig W. Пероральная регидратация в сравнении с внутривенной регидратацией для лечения обезвоживания из-за гастроэнтерита у детей. Кокрановская база данных Syst Rev . 2006, 19 июля: CD004390.[Медлайн].
Данева А.С., Шах Д., Батра П., Бхаттачарья С.К., Гупта П. Оральный ондансетрон в лечении обезвоживающей диареи с рвотой у детей в возрасте от 3 месяцев до 5 лет: рандомизированное контролируемое исследование. J Педиатр . 2016 Февраль 169: 105-9. e3. [Медлайн].
e3. [Медлайн].
Freedman SB, Adler M, Seshadri R, Powell EC. Ондансетрон для приема внутрь при гастроэнтерите в педиатрическом отделении неотложной помощи. N Engl J Med . 2006 20 апреля. 354 (16): 1698-705.[Медлайн].
Маркетти Ф., Бонати М., Маэстро А. и др., Для исследователей SONDO (Исследование ONdansetron vs DOmperidone). Пероральный прием ондансетрона в сравнении с домперидоном при остром гастроэнтерите в педиатрических отделениях неотложной помощи: многоцентровое двойное слепое рандомизированное контролируемое исследование. PLoS One . 2016 23 ноября. 11 (11): e0165441. [Медлайн].
Uhlig U, Pfeil N, Gelbrich G, et al. Дименгидринат у детей с инфекционным гастроэнтеритом: проспективное, РКИ. Педиатрия . 2009 Октябрь 124 (4): e622-32. [Медлайн].
Prasetyo D, Sabaroedin IM, Ermaya YS, Soenarto Y. Связь между тяжелым обезвоживанием при ротавирусной диарее и исключительно грудным вскармливанием среди младенцев в Dr.Больница общего профиля Хасана Садыкина, Бандунг, Индонезия. Дж Троп Мед . 2015. 2015: 862578. [Медлайн].
Шенли Л., Миттал В., Флорес Г. Предотвращение госпитализаций, связанных с обезвоживанием: исследование родителей, стационаров и врачей первичной медико-санитарной помощи с использованием смешанных методов. Госпиталь Педиатр . 2013 июл.3 (3): 204-11. [Медлайн].
Bellemare S, Hartling L, Wiebe N и др. Пероральная регидратация по сравнению с внутривенной терапией для лечения обезвоживания из-за гастроэнтерита у детей: метаанализ рандомизированных контролируемых исследований. BMC Med . 2004 15 апреля 2:11. [Медлайн]. [Полный текст].
Бендер Б.Дж., Озуах PO, Crain EF. Оральная регидратационная терапия: кто-нибудь пьёт ?. Скорая педиатрическая помощь . 2007 сентября 23 (9): 624-6. [Медлайн].
Бхатнагар С., Бахл Р., Шарма П.К. и др.Цинк при пероральной регидратационной терапии снижает количество стула и продолжительность диареи у госпитализированных детей: рандомизированное контролируемое исследование. J Педиатр Гастроэнтерол Нутр . 2004, январь, 38 (1): 34-40. [Медлайн].
2004, январь, 38 (1): 34-40. [Медлайн].
Choice Study Group. Многоцентровое рандомизированное двойное слепое клиническое испытание для оценки эффективности и безопасности раствора солей для пероральной регидратации с пониженной осмолярностью у детей с острой водянистой диареей. Педиатрия . 2001 апр. 107 (4): 613-8.[Медлайн].
Дейл Дж. Растворы для пероральной регидратации в лечении острого гастроэнтерита у детей. J Педиатр здравоохранения . 2004 июль-авг. 18 (4): 211-2. [Медлайн].
Дагган С., Фонтейн О., Пирс Н.Ф. и др. Научное обоснование изменения состава раствора для пероральной регидратации. JAMA . 2 июня 2004 г. 291 (21): 2628-31. [Медлайн].
Дугган С., Рефат М., Хашем М. и др.Насколько достоверны клинические признаки обезвоживания у младенцев? J Педиатр Гастроэнтерол Нутр . 1996, 22 января (1): 56-61. [Медлайн].
1996, 22 января (1): 56-61. [Медлайн].
Duke T, Molyneux EM. Внутривенные жидкости для тяжелобольных детей: пора пересмотреть. Ланцет . 18 октября 2003 г. 362 (9392): 1320-3. [Медлайн].
Fonseca BK, Holdgate A, Craig JC. Энтеральная и внутривенная регидратационная терапия для детей с гастроэнтеритом: метаанализ рандомизированных контролируемых исследований. Arch Pediatr Adolesc Med . 2004 г., май. 158 (5): 483-90. [Медлайн].
Горелик MH, Шоу, К.Н., Мерфи, КО. Обоснованность и достоверность клинических признаков в диагностике обезвоживания у детей. Педиатрия . 1997. May; (5): 99: E6. [Медлайн].
Холлидей М. Эволюция терапии обезвоживания: следует ли по-прежнему преподавать дефицитную терапию ?. Педиатрия . 1996 август 98 (2, часть 1): 171-7. [Медлайн].
1996 август 98 (2, часть 1): 171-7. [Медлайн].
Холлидей М.А., Фридман А.Л., Сегар В.Е. и др.Острая госпитальная гипонатриемия у детей: физиологический подход. J Педиатр . 2004 ноябрь 145 (5): 584-7. [Медлайн].
Холлидей М.А., Фридман А.Л., Васснер С.Дж. Восстановление внеклеточной жидкости при обезвоживании: критика быстрого и медленного. Педиатр Нефрол . 1999 Май. (4): 292-7. [Медлайн].
Хорн Э.Дж., Гири Д., Робб М. и др. Острая гипонатриемия, связанная с внутривенным введением жидкости у госпитализированных детей: обсервационное исследование. Педиатрия . 2004 г., май. 113 (5): 1279-84. [Медлайн].
King CK, Glass R, Bresee JS и др. Лечение острого гастроэнтерита у детей: пероральная регидратация, поддерживающая терапия и диетотерапия. MMWR Recomm Rep . 2003 21 ноября. 52 (RR-16): 1-16. [Медлайн].
MMWR Recomm Rep . 2003 21 ноября. 52 (RR-16): 1-16. [Медлайн].
Миясака К., Симидзу Н., Кодзима Дж. Последние тенденции в детской инфузионной терапии. Методы Найдите Exp Clin Pharmacol . 2004 г., май. 26 (4): 287-94. [Медлайн].
Moritz ML, Ayus JC. Профилактика неврологических осложнений от диснатремий у детей. Педиатр Нефрол . 2005 20 декабря (12): 1687-700. [Медлайн].
Moritz ML, Ayus JC. Профилактика внутрибольничной гипонатриемии: случай использования изотонического раствора. Педиатрия . 2003 Февраль 111 (2): 227-30. [Медлайн].
Moritz ML, Manole MD, Bogen DL, Ayus JC. Гипернатриемия, связанная с грудным вскармливанием: мы упускаем из виду диагноз ?. Педиатрия . 2005 сентябрь 116 (3): e343-7. [Медлайн].
[Медлайн].
Мерфи С., Хан С., Волминк Дж. Раствор для пероральной регидратации с пониженной осмолярностью для лечения холеры. Кокрановская база данных Syst Rev . 2004. CD003754. [Медлайн].
Нагер А.Л., Ван В.Дж. Сравнение назогастрального и внутривенного методов регидратации у детей с острым обезвоживанием. Педиатрия . 2002 апр. 109 (4): 566-72. [Медлайн].
Налин Д.Р., Хиршхорн Н., Гриноу В. и др.Клинические опасения по поводу раствора для пероральной регидратации с пониженной осмолярностью. JAMA . 2 июня 2004 г. 291 (21): 2632-5. [Медлайн].
Ozuah PO, Avner JR, Stein RE. Оральная регидратация, врачи неотложной помощи и параметры практики: национальное исследование. Педиатрия . 2002 Февраль 109 (2): 259-61. [Медлайн].
[Медлайн].
Phin SJ, McCaskill ME, Browne GJ, Lam LT. Клинический путь использования быстрой регидратации у детей с гастроэнтеритом. J Детский педиатр .2003 июл. 39 (5): 343-8. [Медлайн].
Play для SD. Гипотонические растворы для внутривенного введения детям. Мнение экспертов по наркотикам Saf . 2004 г., 3 (1): 67-73. [Медлайн].
Рейд С.Р., Бонадио, Вашингтон. Быстрая внутривенная регидратация в амбулаторных условиях для коррекции обезвоживания и устранения рвоты у детей с острым гастроэнтеритом. Энн Эмерг Мед . 1996 Сентябрь, 28 (3): 318-23. [Медлайн].
Сантошем М., Кинан Э.М., Таллох Дж. И др.Пероральная регидратационная терапия диареи: пример обратной передачи технологии. Педиатрия . 1997 Ноябрь 100 (5): E10. [Медлайн].
[Медлайн].
Сарнаик А.П., Меерт К., Хакбарт Р., Флейшманн Л. Лечение гипонатриемических припадков у детей с помощью гипертонического раствора: безопасная и эффективная стратегия. Crit Care Med . 1991. Jun; 19 (6): 758-62. [Медлайн].
Spandorfer PR, Alessandrini EA, Joffe MD, et al. Пероральная регидратация в сравнении с внутривенной регидратацией у детей с умеренным обезвоживанием: рандомизированное контролируемое исследование. Педиатрия . 2005 февраль 115 (2): 295-301. [Медлайн].
Wathen JE, MacKenzie T, Bothner JP. Полезность панели электролитов сыворотки при лечении обезвоживания у детей, получавшего внутривенно вводимые жидкости. Педиатрия . 2004 ноябрь 114 (5): 1227-34. [Медлайн].
Эндрюс Дж. Р., Леунг Д. Т., Ахмед С. и др. Детерминанты тяжелого обезвоживания в результате диарейного заболевания при обращении в больницу: данные за 22 года госпитализации в Бангладеш. PLoS Negl Trop Dis . 2017 г., 11 (4): e0005512. [Медлайн].
и др. Детерминанты тяжелого обезвоживания в результате диарейного заболевания при обращении в больницу: данные за 22 года госпитализации в Бангладеш. PLoS Negl Trop Dis . 2017 г., 11 (4): e0005512. [Медлайн].
Boskabadi H, Akhondian J, Afarideh M, et al. Отдаленные результаты неврологического развития новорожденных с гипернатремической дегидратацией. Мед. Грудного вскармливания . 2017 Апрель 12: 163-8. [Медлайн].
Какова патофизиология диареи при гастроэнтерите?
Автор
Артур Дискин, доктор медицины Вице-президент, главный медицинский директор Royal Caribbean Cruise Lines; Доцент-добровольец Университета Майами, Медицинская школа Леонарда М. Миллера
Артур Дискин, доктор медицины, является членом следующих медицинских обществ: Американский колледж врачей скорой помощи
Раскрытие: нечего раскрывать.
Соавтор (ы)
Лилиан Гутьеррес-Альварес, магистр здравоохранения Аналитик общественного здравоохранения, Департамент медицины и общественного здравоохранения, Royal Caribbean Cruises, Ltd
Лилиан Гутьеррес-Альварес, магистр здравоохранения, является членом следующих медицинских обществ: Американской ассоциации общественного здравоохранения, Golden Key International Honor Общество
Раскрытие: Ничего не раскрывать.
Специальная редакционная коллегия
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: Получил зарплату от Medscape за работу.для: Medscape.
BS Ананд, доктор медицины Профессор, кафедра внутренней медицины, отделение гастроэнтерологии, Медицинский колледж Бейлора
BS Ананд, доктор медицинских наук, является членом следующих медицинских обществ: Американской ассоциации по изучению заболеваний печени, Американского колледжа гастроэнтерологии , Американская гастроэнтерологическая ассоциация, Американское общество эндоскопии желудочно-кишечного тракта
Раскрытие: Ничего не разглашать.
Главный редактор
Стивен Дронен, доктор медицины, FAAEM Председатель, отделение неотложной медицины, Медицинский центр ЛеКонт
Стивен Дронен, доктор медицины, FAAEM является членом следующих медицинских обществ: Американской академии неотложной медицины, Общества академической неотложной медицины
Раскрытие: Ничего не раскрывать.
Благодарности
Мишель Эрвин, доктор медицины , заведующая отделением неотложной медицины, больница Ховардского университета
Мишель Эрвин, доктор медицины, является членом следующих медицинских обществ: Американской академии неотложной медицины, Американского колледжа врачей неотложной помощи, Американской медицинской ассоциации, Национальной медицинской ассоциации и Общества академической неотложной медицины
webmd.com»> Раскрытие: Ничего не раскрывать.Юджин Хардин, доктор медицины, FAAEM, FACEP Бывший председатель и доцент кафедры неотложной медицины Медицинского и научного университета Чарльза Дрю; Бывший председатель отделения неотложной медицины, Медицинский центр Мартина Лютера Кинга / Дрю
Раскрытие: Ничего не раскрывать.
Диарея — обзор | ScienceDirect Topics
Хроническая неспецифическая диарея
Хроническая неспецифическая диарея, также известная как функциональная или детская диарея , обычно поражает детей в возрасте от 1 до 3 лет и характеризуется ежедневным выделением нескольких водянистых и несформированных стула. Стул обычно относительно хорошо сформирован утром, но с течением дня становится более жидким. Стул часто содержит непереваренные растительные вещества, но без крови, слизи или избыточного жира.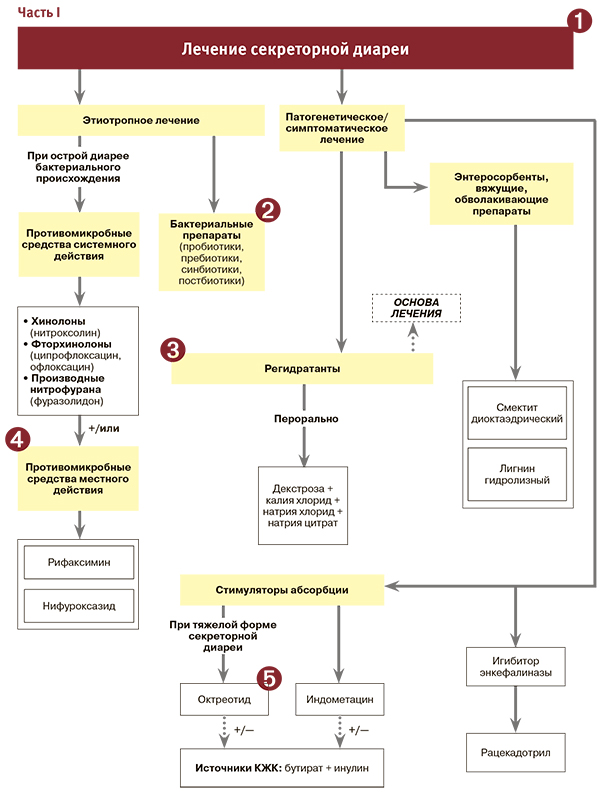 Дети с функциональной диареей, если им предлагается неограниченная и соответствующая возрасту диета, обычно набирают вес. Однако в попытке вылечить диарею многих детей помещают на ограничительные диеты, в которых могут отсутствовать молочные продукты, жиры и иногда крахмалы; такие ограничения приводят к невозможности процветания. Диагностические критерии Rome-III указывают на то, что должно присутствовать все следующее:
Дети с функциональной диареей, если им предлагается неограниченная и соответствующая возрасту диета, обычно набирают вес. Однако в попытке вылечить диарею многих детей помещают на ограничительные диеты, в которых могут отсутствовать молочные продукты, жиры и иногда крахмалы; такие ограничения приводят к невозможности процветания. Диагностические критерии Rome-III указывают на то, что должно присутствовать все следующее:
- 1.
Ежедневное безболезненное повторяющееся отхождение 3 или более крупных несформированных стула
- 2.
Симптомы длятся более 4 недель
- 3.
Начало симптомов, которые начинаются в возрасте от 6 до 36 месяцев
- 4.
Прохождение стула в часы бодрствования
- 5
При адекватном потреблении калорий не может быть отказа от роста.
Считается, что хроническая неспецифическая диарея является вариантом синдрома раздраженного кишечника (СРК), и СРК в семейном анамнезе является обычным явлением. Патофизиология может включать нарушение перистальтики кишечника с уменьшением времени прохождения от рта к анусу. Чрезмерное потребление фруктового сока также может способствовать диарее, подавляя всасывающую способность кишечника по углеводам. Хроническая неспецифическая диарея — доброкачественное и самоограничивающееся состояние, которое обычно проходит без вмешательства к 3-4 годам. Родителей следует успокаивать и поощрять к тому, чтобы они сидели с ребенком на регулярной неограниченной диете, чтобы обеспечить достаточное количество калорий. Диарея часто проходит после снятия предшествующих диетических ограничений и ограничения потребления фруктового сока.У некоторых пациентов может улучшиться содержание жира в рационе (например, при переходе с обезжиренного молока на цельное), что может замедлить прохождение через желудочно-кишечный тракт.
Патофизиология может включать нарушение перистальтики кишечника с уменьшением времени прохождения от рта к анусу. Чрезмерное потребление фруктового сока также может способствовать диарее, подавляя всасывающую способность кишечника по углеводам. Хроническая неспецифическая диарея — доброкачественное и самоограничивающееся состояние, которое обычно проходит без вмешательства к 3-4 годам. Родителей следует успокаивать и поощрять к тому, чтобы они сидели с ребенком на регулярной неограниченной диете, чтобы обеспечить достаточное количество калорий. Диарея часто проходит после снятия предшествующих диетических ограничений и ограничения потребления фруктового сока.У некоторых пациентов может улучшиться содержание жира в рационе (например, при переходе с обезжиренного молока на цельное), что может замедлить прохождение через желудочно-кишечный тракт.
Избыточный бактериальный рост в тонком кишечнике (SIBO)
Нормальный тонкий кишечник заселен относительно небольшим количеством бактерий, обычно менее 10 4 организмов / мл.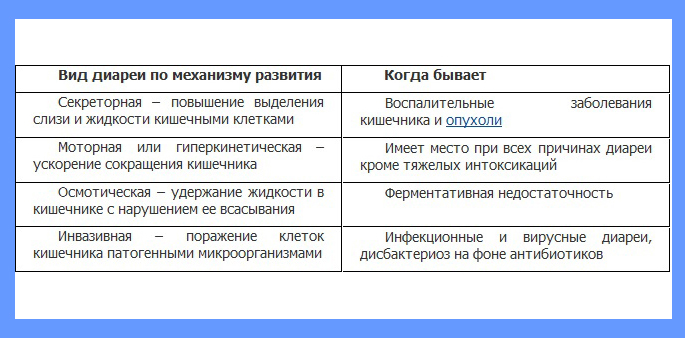 Различные состояния, такие как синдром короткой кишки, недоедание, псевдообструкция, стриктуры кишечника и ахлоргидрия, вызванные лекарствами, такими как ингибиторы протонной помпы, могут привести к чрезмерному росту аэробных и анаэробных бактерий в тонкой кишке.Симптомы боли в животе, вздутие живота, вздутие живота и диарея возникают из-за деконъюгирования желчных кислот и гидроксилирования жирных кислот бактериями, что приводит к осмотической диарее. Диагноз может быть поставлен путем анализа содержания водорода в выдыхаемом воздухе, показывающего раннее и позднее повышение содержания водорода в выдыхаемом воздухе после приема лактулозы. Количественные культуры аспирата тощей кишки, показывающие более 10 5 организмов / мл, наводят на мысль о SIBO, хотя установленные диапазоны отсечения и специфичность несовершенны.
Различные состояния, такие как синдром короткой кишки, недоедание, псевдообструкция, стриктуры кишечника и ахлоргидрия, вызванные лекарствами, такими как ингибиторы протонной помпы, могут привести к чрезмерному росту аэробных и анаэробных бактерий в тонкой кишке.Симптомы боли в животе, вздутие живота, вздутие живота и диарея возникают из-за деконъюгирования желчных кислот и гидроксилирования жирных кислот бактериями, что приводит к осмотической диарее. Диагноз может быть поставлен путем анализа содержания водорода в выдыхаемом воздухе, показывающего раннее и позднее повышение содержания водорода в выдыхаемом воздухе после приема лактулозы. Количественные культуры аспирата тощей кишки, показывающие более 10 5 организмов / мл, наводят на мысль о SIBO, хотя установленные диапазоны отсечения и специфичность несовершенны.
Синдром раздраженного кишечника (СРК)
Синдром раздраженного кишечника характеризуется периодическими болями в животе и измененными привычками кишечника, которые обычно проявляются в подростковом возрасте. Симптомы включают ненормальную частоту стула (4 или более стула в день или 2 или меньше стула в неделю), ненормальную форму стула (жидкий и водянистый или комковатый и твердый), ненормальное отхождение стула (например, напряжение, позывы к позывам, чувство одышки). неполное опорожнение), отхождение слизи, вздутие живота или вздутие живота. Для постановки диагноза необходимо, чтобы пациенты имели нормальный физический осмотр и кривую роста и соответствовали обоим следующим критериям не реже одного раза в неделю в течение как минимум 2 месяцев до постановки диагноза:
Симптомы включают ненормальную частоту стула (4 или более стула в день или 2 или меньше стула в неделю), ненормальную форму стула (жидкий и водянистый или комковатый и твердый), ненормальное отхождение стула (например, напряжение, позывы к позывам, чувство одышки). неполное опорожнение), отхождение слизи, вздутие живота или вздутие живота. Для постановки диагноза необходимо, чтобы пациенты имели нормальный физический осмотр и кривую роста и соответствовали обоим следующим критериям не реже одного раза в неделю в течение как минимум 2 месяцев до постановки диагноза:
- 1.
Дискомфорт в животе (неприятное ощущение, не описываемое как боль) или боль, связанная с 2 или более из следующих, по крайней мере, 25% случаев:
- a.
Улучшение при дефекации
- б.
Начало связано с изменением частоты стула
- c.
Начало, связанное с изменением формы (внешнего вида) стула
- 2.

Нет свидетельств воспалительного, анатомического, метаболического или неопластического процесса, объясняющего симптомы субъекта
Этиология и патогенез синдрома раздраженного кишечника изучен недостаточно.Висцеральная гиперчувствительность хорошо известна у детей с СРК. Генетическая предрасположенность, ранние стрессовые события и неэффективные механизмы преодоления — все это усугубляющие факторы. Дополнительные механизмы могут включать инфекцию, воспаление, травму кишечника, аллергию и нарушение моторики кишечника.
Целиакия
Целиакия — это иммуноопосредованное системное заболевание, вызываемое воздействием глютена и родственных белков у генетически предрасположенных лиц. Клинические проявления различаются, хотя признаки целиакии включают энтеропатию и наличие специфических антител.Распространенность достигает 1% в западных странах, при этом наиболее пораженные люди проявляются в детстве. Генетическая предрасположенность подтверждается семейной агрегацией и высокой конкордантностью у монозиготных близнецов, которая приближается к 100%. Обнаружена сильная связь с человеческим лейкоцитарным антигеном (HLA) -DQ2.5 и, в меньшей степени, с HLA-DQ8. Семейный или личный анамнез аутоиммунных заболеваний и определенных генетических состояний представляет более высокий риск (Таблица 11.15).
Обнаружена сильная связь с человеческим лейкоцитарным антигеном (HLA) -DQ2.5 и, в меньшей степени, с HLA-DQ8. Семейный или личный анамнез аутоиммунных заболеваний и определенных генетических состояний представляет более высокий риск (Таблица 11.15).
Патогенез целиакии сначала включает воздействие глиадина , белкового компонента глютена пшеницы, или структурно связанных запасных белков ( проламинов ), обнаруженных в ржи и ячмене.Измененный процессинг внутрипросветными ферментами, изменения кишечной проницаемости и активация врожденного иммунного ответа предшествуют развитию адаптивного иммунного ответа, который приводит к системному аутоиммунитету и воспалительной энтеропатии, характеризующейся атрофией ворсинок , удлиненными криптами и интраэпителиальным лимфоцитозом.
Симптомы целиакии разнообразны и отражают ее системный характер. Возраст начала варьирует, и требуется высокая степень подозрения.Проявления включают периодические боли в животе, тошноту и рвоту, дефицит железа с анемией или без нее, низкий рост, афтозный стоматит, хроническую усталость, артрит, повышение уровня аминотрансферазы и снижение минеральной плотности костей. Редкие проявления включают атаксию, герпетиформный дерматит , , пузырчатую сыпь с патогномоничными кожными отложениями IgA, и , глютеновый криз , который представляет собой редкий опасный для жизни синдром, чаще всего наблюдаемый у детей, который характеризуется тяжелой диареей, гипопротеинемией и метаболический и электролитный дисбаланс.Классические проявления у малыша с хронической диареей, вздутием живота и неспособностью нормально развиваться нечасто. Большинство пациентов выявляются с помощью серологического скрининга в контексте сильного семейного анамнеза или других факторов риска.
Редкие проявления включают атаксию, герпетиформный дерматит , , пузырчатую сыпь с патогномоничными кожными отложениями IgA, и , глютеновый криз , который представляет собой редкий опасный для жизни синдром, чаще всего наблюдаемый у детей, который характеризуется тяжелой диареей, гипопротеинемией и метаболический и электролитный дисбаланс.Классические проявления у малыша с хронической диареей, вздутием живота и неспособностью нормально развиваться нечасто. Большинство пациентов выявляются с помощью серологического скрининга в контексте сильного семейного анамнеза или других факторов риска.
Серологические тесты являются краеугольным камнем скрининга на целиакию у пациентов с факторами риска или с подозрительным анамнезом (таблица 11.16). Установление диагноза зависит от обнаруженных уровней специфических антител. Для исключения дефицита IgA необходимо получить общий сывороточный IgA.Если общий сывороточный IgA в норме, а антитела IgA к тканевой трансглутаминазе отрицательны, целиакия маловероятна. Пациентам с положительными антителами IgA к тканевой трансглутаминазе, которые менее чем в 10 раз превышают верхний предел нормы, следует пройти верхнюю эндоскопию с множественными биопсиями. Если биопсия демонстрирует полную или частичную атрофию ворсинок, удлиненные крипты и увеличение интраэпителиальных лимфоцитов (> 25 лимфоцитов / 100 энтероцитов), диагноз подтверждается. Пациентам с положительными антителами IgA к тканевой трансглутаминазе, которые в 10 раз превышают верхний предел нормы, должны быть выполнены антиэндомизиальные антитела IgA и проведено тестирование HLA.Если у пациента положительный результат на антиэндомизиальные антитела IgA и положительный результат на DQ2 или DQ8 HLA, диагноз подтверждается; если один или оба отрицательные результаты, пациенту следует пройти биопсию.
Пациентам с положительными антителами IgA к тканевой трансглутаминазе, которые менее чем в 10 раз превышают верхний предел нормы, следует пройти верхнюю эндоскопию с множественными биопсиями. Если биопсия демонстрирует полную или частичную атрофию ворсинок, удлиненные крипты и увеличение интраэпителиальных лимфоцитов (> 25 лимфоцитов / 100 энтероцитов), диагноз подтверждается. Пациентам с положительными антителами IgA к тканевой трансглутаминазе, которые в 10 раз превышают верхний предел нормы, должны быть выполнены антиэндомизиальные антитела IgA и проведено тестирование HLA.Если у пациента положительный результат на антиэндомизиальные антитела IgA и положительный результат на DQ2 или DQ8 HLA, диагноз подтверждается; если один или оба отрицательные результаты, пациенту следует пройти биопсию.
У пациентов с глютеновой болезнью симптомы облегчаются при соблюдении строгой безглютеновой диеты. Осложнения, связанные с нелеченой целиакией, включают остеопороз, нарушение функции селезенки, неврологические расстройства, бесплодие или повторный аборт, язвенный еюноилеит и рак. Связанная с энтеропатией Т-клеточная лимфома и аденокарцинома тощей кишки являются редкими осложнениями целиакии. Рефрактерная глютеновая болезнь диагностируется при наличии стойких или повторяющихся симптомов мальабсорбции и признаков атрофии ворсинок при биопсии, несмотря на строгое соблюдение безглютеновой диеты в течение более 12 месяцев. Рефрактерная целиакия может быть классифицирована как тип 1, (характеризуется наличием нормальных интраэпителиальных лимфоцитов) или тип 2 (характеризуется аномальными внутриэпителиальными лимфоцитами; клональные интраэпителиальные лимфоциты, лишенные поверхностных маркеров CD3, CD8 и рецепторов Т-клеток; или оба).Рефрактерная целиакия 2 типа связана с более высоким риском язвенного еюноилеита и лимфомы.
Связанная с энтеропатией Т-клеточная лимфома и аденокарцинома тощей кишки являются редкими осложнениями целиакии. Рефрактерная глютеновая болезнь диагностируется при наличии стойких или повторяющихся симптомов мальабсорбции и признаков атрофии ворсинок при биопсии, несмотря на строгое соблюдение безглютеновой диеты в течение более 12 месяцев. Рефрактерная целиакия может быть классифицирована как тип 1, (характеризуется наличием нормальных интраэпителиальных лимфоцитов) или тип 2 (характеризуется аномальными внутриэпителиальными лимфоцитами; клональные интраэпителиальные лимфоциты, лишенные поверхностных маркеров CD3, CD8 и рецепторов Т-клеток; или оба).Рефрактерная целиакия 2 типа связана с более высоким риском язвенного еюноилеита и лимфомы.
Воспалительное заболевание кишечника (ВЗК)
Воспалительное заболевание кишечника в широком смысле делится на язвенный колит и болезнь Крона , идиопатические системные хронические воспалительные заболевания, основные симптомы которых связаны с рецидивирующим воспалением желудочно-кишечного тракта.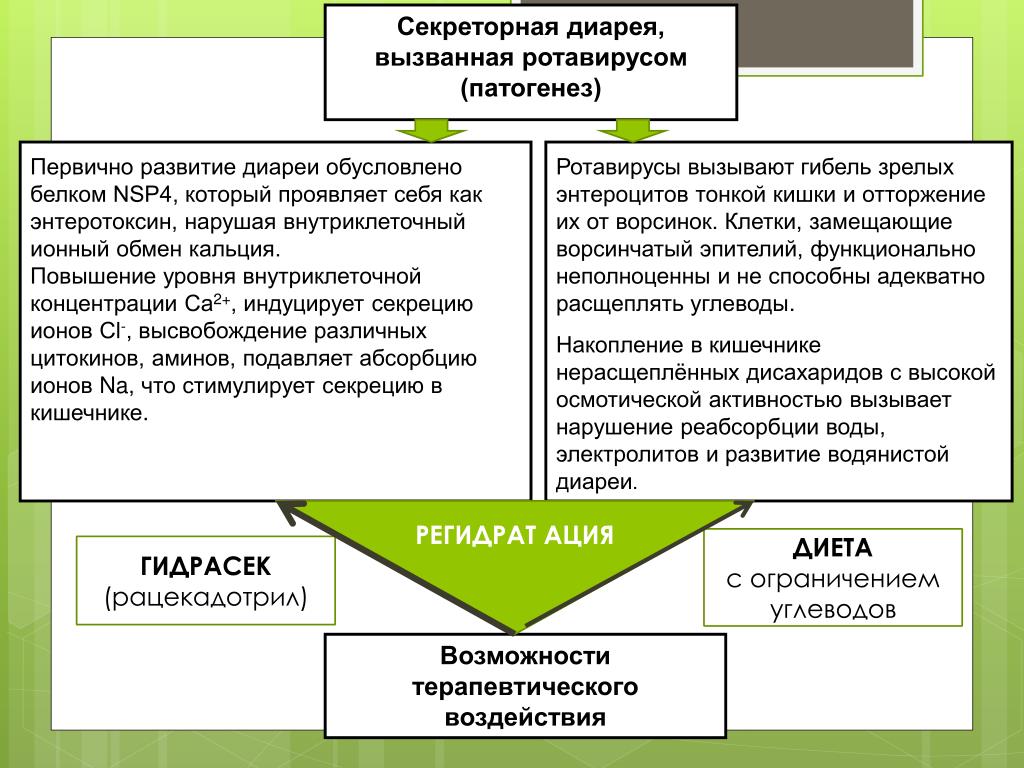 Общие признаки и симптомы включают диарею, боль в животе, кровь в стуле и нарушение питания.Язвенный колит представляет собой воспаление слизистой оболочки, ограниченное толстой кишкой, тогда как болезнь Крона представляет собой трансмуральное воспаление , которое поражает все слои стенки кишечника и может поражать любую часть желудочно-кишечного тракта от рта до ануса. Язвенный колит поражает толстую кишку непрерывно, обычно начиная с прямой кишки и распространяясь проксимально до различной степени. Болезнь Крона характеризуется пропущенными поражениями , в которых есть участки слизистой оболочки нормального вида, перемежающиеся воспалительными поражениями.
Общие признаки и симптомы включают диарею, боль в животе, кровь в стуле и нарушение питания.Язвенный колит представляет собой воспаление слизистой оболочки, ограниченное толстой кишкой, тогда как болезнь Крона представляет собой трансмуральное воспаление , которое поражает все слои стенки кишечника и может поражать любую часть желудочно-кишечного тракта от рта до ануса. Язвенный колит поражает толстую кишку непрерывно, обычно начиная с прямой кишки и распространяясь проксимально до различной степени. Болезнь Крона характеризуется пропущенными поражениями , в которых есть участки слизистой оболочки нормального вида, перемежающиеся воспалительными поражениями.
Распространенность язвенного колита достигает 246 на 100 000 человек, а распространенность болезни Крона достигает 199 на 100 000 человек. Приблизительно 25% всех ВЗК диагностируется у детей и подростков, хотя до 6-летнего возраста проявления заболевания встречаются редко.
Клиническая картина.

До 80% детей с болезнью Крона будут иметь диарею. Стул может содержать микроскопическую кровь, хотя и не может быть сильно кровоточащим, особенно при отсутствии значительного поражения левой толстой кишки.Диарея чаще встречается при заболеваниях толстой кишки и может вообще отсутствовать в случаях изолированного воспаления тонкой кишки. При язвенном колите диарея — более постоянный признак, часто незаметный в своем развитии, но в конечном итоге прогрессирующий до гематохезии. Ночная диарея с позывами может быть признаком левостороннего воспаления толстой кишки в обоих случаях. Желудочно-кишечные и внекишечные проявления в остальном варьируют в зависимости от болезни Крона и язвенного колита (таблица 11.17). Внекишечные проявления присутствуют у 23% детей при постановке диагноза, с большей частотой у детей старше 6 лет.
Физикальное обследование должно установить статус питания и включать оценку параметров роста, в том числе обзор предыдущих диаграмм роста. Также следует регистрировать пубертатный статус. При обследовании полости рта необходимо выявить афтозные язвы, которые присутствуют примерно у 10% пациентов с ВЗК (чаще при болезни Крона). При обследовании глаз необходимо выявить эписклерит , болезненное воспаление внешнего слоя склеры, а пациентов с известной ВЗК должен сопровождать офтальмолог для оценки увеита и кератопатии .Детальное обследование брюшной полости должно выявить вздутие живота, массу, болезненность и гипер- или гипоактивные шумы кишечника. Особое внимание следует уделить оценке перианальной области на предмет абсцессов или свищей. При обследовании кожи необходимо выявить узловатую эритему , болезненные приподнятые красные высыпания около 1-3 см в диаметре, обычно обнаруживаемые на голенях; гангренозная пиодермия , сильная язвенная сыпь; и псориатические поражения. Две клинические особенности предполагают диагноз болезни Крона по сравнению с язвенным колитом: наличие перианальной болезни и наличие структурирующей и фистулизирующей болезни кишечника.
При обследовании полости рта необходимо выявить афтозные язвы, которые присутствуют примерно у 10% пациентов с ВЗК (чаще при болезни Крона). При обследовании глаз необходимо выявить эписклерит , болезненное воспаление внешнего слоя склеры, а пациентов с известной ВЗК должен сопровождать офтальмолог для оценки увеита и кератопатии .Детальное обследование брюшной полости должно выявить вздутие живота, массу, болезненность и гипер- или гипоактивные шумы кишечника. Особое внимание следует уделить оценке перианальной области на предмет абсцессов или свищей. При обследовании кожи необходимо выявить узловатую эритему , болезненные приподнятые красные высыпания около 1-3 см в диаметре, обычно обнаруживаемые на голенях; гангренозная пиодермия , сильная язвенная сыпь; и псориатические поражения. Две клинические особенности предполагают диагноз болезни Крона по сравнению с язвенным колитом: наличие перианальной болезни и наличие структурирующей и фистулизирующей болезни кишечника. Никакие другие системные или внекишечные проявления не позволяют достоверно предположить один диагноз по сравнению с другим (таблица 11.18).
Никакие другие системные или внекишечные проявления не позволяют достоверно предположить один диагноз по сравнению с другим (таблица 11.18).
Диагностика.
ВЗК — это клинический диагноз, который объединяет анамнез и физические данные с объективными данными визуализационных исследований, лабораторной оценки и эндоскопических данных, включая гистопатологию. Диагноз не следует подтверждать или исключать по какой-либо одной переменной или результату: до 54% пациентов с язвенным колитом легкой степени и 21% пациентов с болезнью Крона легкой степени имеют нормальные уровни гемоглобина, альбумина, СРБ и СОЭ на момент постановки первоначального диагноза. .Важные имитаторы ВЗК включают синдром раздраженного кишечника, болезнь Бехчета, инфекционный энтероколит (особенно энтеровирус и Yersinia ) и туберкулез (таблицы 11.19 и 11.20). Таким образом, каждый пациент с анамнезом и обследованием, позволяющим предположить ВЗК, должен пройти исследования стула на инфекционные организмы, и следует сделать особый запрос на культуру Yersinia , если мультиплексные ПЦР-анализы, включающие тестирование Yersinia , недоступны.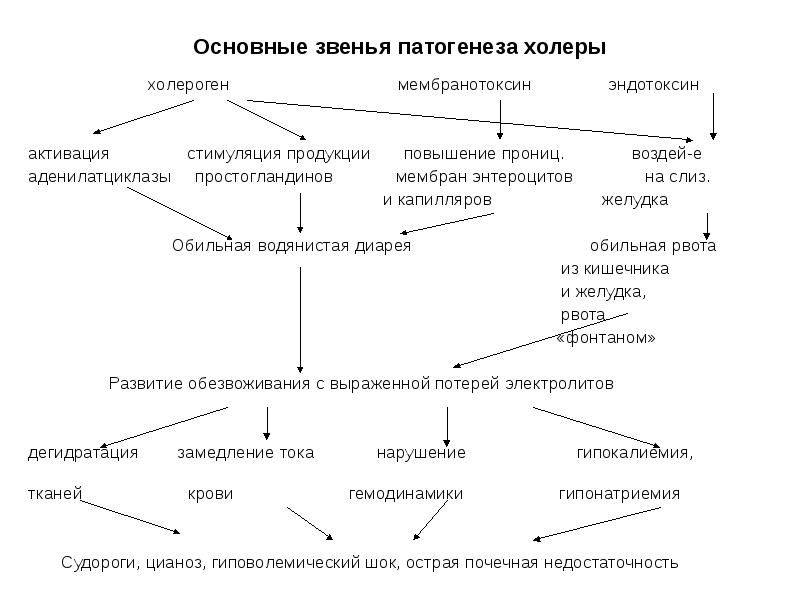 Пациентам с подозрительными симптомами в возрасте до 6 лет может потребоваться оценка основного нарушения иммунной дисрегуляции в качестве дополнительной имитации ВЗК (Таблица 11.21). Перед проведением эндоскопических процедур следует использовать биомаркеры стула, такие как кальпротектин и лактоферрин, чтобы исключить невоспалительные причины. Предлагаемая диагностическая оценка подозреваемого воспалительного заболевания кишечника представлена в таблице 11.22.
Пациентам с подозрительными симптомами в возрасте до 6 лет может потребоваться оценка основного нарушения иммунной дисрегуляции в качестве дополнительной имитации ВЗК (Таблица 11.21). Перед проведением эндоскопических процедур следует использовать биомаркеры стула, такие как кальпротектин и лактоферрин, чтобы исключить невоспалительные причины. Предлагаемая диагностическая оценка подозреваемого воспалительного заболевания кишечника представлена в таблице 11.22.
Секреторная диарея | SpringerLink
Schiller LR: Секреторная диарея . В Гастроэнтерология и гепатология: Комплексный визуальный справочник , том 7, Тонкий кишечник. Под редакцией Фельдмана М., Шиллера Л.Р.Филадельфия: современная медицина; 1997: 4.1–4.24.
Google ученый

Венцл Х.Х., Файн К.Д., Шиллер Л.Р., Фордтран Дж.С.: Детерминанты снижения консистенции кала у пациентов с диареей . Гастроэнтерология 1995, 108 : 1729–1738.
PubMed
Статья
CAS
Google ученый
Eherer AJ, Fordtran JS: Фекальный осмотический разрыв и pH при экспериментальной диарее различных причин . Гастроэнтерология 1992, 103 : 545–551.
PubMed
CAS
Google ученый
Fordtran JS, Санта-Ана, Калифорния, Моравски С.Г., et al. : Патофизиология хронической диареи: выводы, полученные в результате исследований перфузии кишечника у 31 пациента . Gastroenterol Clin North Am 1986, 15 : 477–490.
CAS
Google ученый
Guerrant RL: Уроки диарейных болезней: от демографии к молекулярной фармакологии . J Infect Dis 1994, 169 : 1206–1218.
PubMed
CAS
Google ученый
DuPont HL: Обзорная статья: инфекционная диарея . Aliment Pharmacol Ther 1994, 8 : 3–13.
PubMed
CAS
Статья
Google ученый
Giannella RA: Инфекции кишечника . В Гастроэнтерология и гепатология: Комплексный визуальный справочник , том 7, Тонкий кишечник. Под редакцией Фельдмана М., Шиллера Л. Р. Филадельфия: современная медицина; 1997: 12.1–12.19.
Р. Филадельфия: современная медицина; 1997: 12.1–12.19.
Google ученый
Popoff MR: Взаимодействие между бактериальными токсинами и клетками кишечника . Toxicon 1998, 36 : 665–685.
PubMed
Статья
CAS
Google ученый
Phalipon A, Sansonetti PJ: Взаимодействия микробов с хозяевами на участках слизистой оболочки. Ответ хозяина на патогенные бактерии на участках слизистой оболочки . Curr Top Microbiol Immunol 1999, 236 : 163–189.
PubMed
CAS
Google ученый
Lundgren O: 5-гидрокситриптамин, энтеротоксины и секреция кишечной жидкости [редакционная статья] .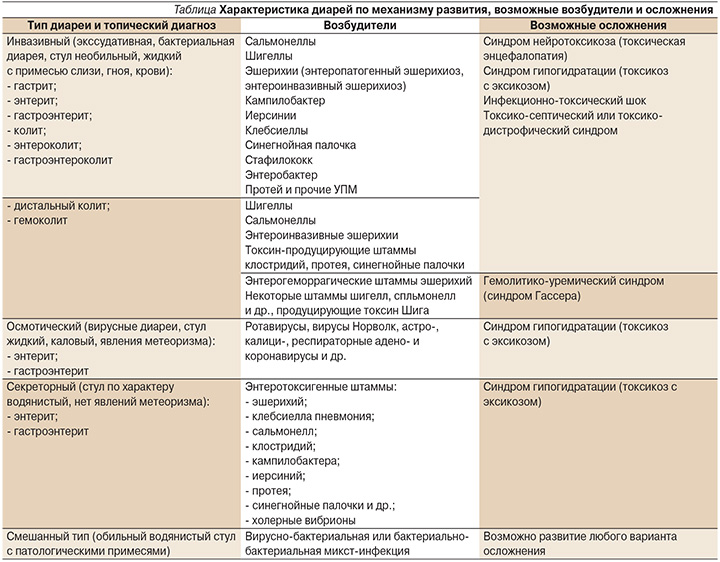 Гастроэнтерология 1998, 115 : 883–890.
Гастроэнтерология 1998, 115 : 883–890.
Артикул
Google ученый
Forte LR, Currie MG: Гуанилин: пептидный регулятор эпителиального транспорта . FASEB J 1995, 9 : 643–650.
PubMed
CAS
Google ученый
Blaser MJ: Эпидемиологические и клинические особенности инфекций Campylobacter jejuni . J Infect Dis 1997, 176 ( доп. 2 ): S103-S105.
PubMed
Google ученый
Слуцкер Л., Райс А.А., Мэлони К., и др. : Общенациональное исследование методом случай-контроль инфекции Escherichia coli O157: H7 в США .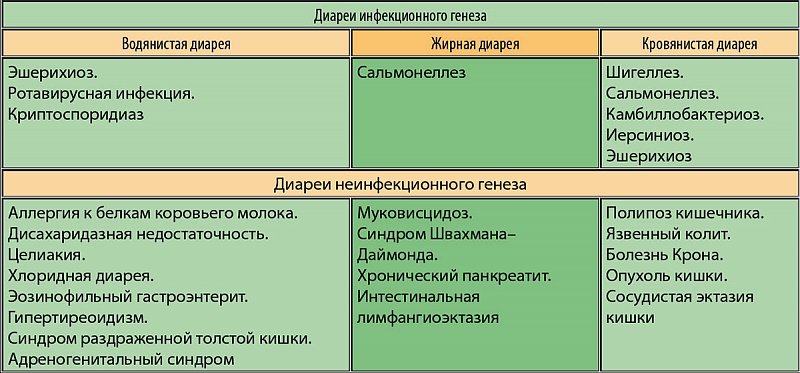 J Infect Dis 1998, 177 : 962–966.
J Infect Dis 1998, 177 : 962–966.
PubMed
CAS
Google ученый
Слуцкер Л., Райс А.А., Грин К.Д., и др. : Диарея, вызванная Escherichia coli O157: H7 в США: клинические и эпидемиологические особенности . Ann Intern Med 1997, 126 : 505–513.
PubMed
CAS
Google ученый
Kelly CP, LaMont JT: Инфекция Clostridium difficile . Ann Rev Med 1998, 49 : 375–390.
PubMed
Статья
CAS
Google ученый
Fekety R: Руководство по диагностике и лечению диареи и колита, связанных с Clostridium difficile, . Am J Gastroenterol 1997, 92 : 739–750.
Am J Gastroenterol 1997, 92 : 739–750.
PubMed
CAS
Google ученый
Arrambide KA, Santa Ana CA, Schiller LR, et al. : Потеря абсорбционной способности хлорида натрия как причина диареи после частичной резекции подвздошной и правой ободочной кишки . Dig Dis Sci 1989, 34 : 193–201.
PubMed
Статья
CAS
Google ученый
Aichbichler BW, Zerr CH, Santa Ana CA, et al. : Краткий отчет: подавление секреции хлорида желудка с помощью протонной помпы при врожденной хлоридореи . N Engl J Med 1997, 336 : 106–109.
PubMed
Статья
CAS
Google ученый
Perdue MH, McKay DM: Интегративная иммунофизиология слизистой оболочки кишечника . Am J Physiol 1994, 267 : G151-G165.
PubMed
CAS
Google ученый
Селлин Дж. Х .: Функциональная анатомия, абсорбция жидкости и электролитов . В Гастроэнтерология и гепатология: Комплексный визуальный справочник , том 7, Тонкий кишечник. Под редакцией Фельдмана М., Шиллера Л.Р. Филадельфия: современная медицина; 1997: 1.1–1.14.
Google ученый
Lee E, Schiller LR, Fordtran JS: Количественная оценка клеток собственной пластинки толстой кишки с помощью метода морфометрического точечного подсчета . Гастроэнтерология 1988, 94 : 409–418.
PubMed
CAS
Google ученый
Каррас П.Дж., Пфайфер МА: Диабетическая желудочно-кишечная вегетативная нейропатия . Curr Ther Endocrinol Metab 1997, 6 : 462–465.
PubMed
CAS
Google ученый
Saslow SB, Camilleri M: Диабетическая диарея . Semin Gastrointest Dis 1995, 6 : 187–193.
PubMed
CAS
Google ученый
Rosa-e-Silva L, Troncon LE, Oliveira RB, et al. : Быстрый дистальный транзит тонкой кишки, связанный с симпатической денервацией при сахарном диабете I типа . Кишечник 1996, 39 : 748–756.
PubMed
CAS
Google ученый
Шиллер Л. Р., Ривера Л. М., Сантанджело В. К., и др. : Диагностическая ценность концентраций пептидов в плазме натощак у пациентов с хронической диареей . Dig Dis Sci 1994, 39 : 2216–2222.
PubMed
Статья
CAS
Google ученый
Fine KD, Schiller LR: Технический обзор Американской гастроэнтерологической ассоциации по оценке и лечению хронической диареи . Гастроэнтерология 1999, 116 : 1464–1486. Подробный обзор диагностических тестов, используемых при оценке хронической диареи, который также предлагает предлагаемый подход.
PubMed
Статья
CAS
Google ученый
Брандт Л.Дж., Гринвальд D: Острая и хроническая диарея: учебник по диагностике и лечению . Арлингтон, Вирджиния: Американский колледж гастроэнтерологии; 1997.
Комитет по клинической практике и экономике: Заявление о медицинской позиции Американской гастроэнтерологической ассоциации: Руководство по оценке и лечению хронической диареи . Гастроэнтерология 1999, 116 : 1461–1464.
Артикул
Google ученый
Доновиц М., Кокке Ф. Т., Саиди Р: Оценка пациентов с хронической диареей . N Engl J Med 1995, 332 : 725–729.Экспертный обзор практических подходов к этой группе пациентов.
PubMed
Статья
CAS
Google ученый
Пауэлл DW: Подход к пациенту с диареей . В Учебник гастроэнтерологии , изд. 2. Под редакцией Ямады Т. Филадельфия: Lippincott; 1995: 813–863. Научно обоснованный обзор оценки пациентов с острой и хронической диареей.
Google ученый
Fine KD: Диарея . В Желудочно-кишечные и печеночные заболевания: патофизиология, диагностика, лечение , изд. 6. Под редакцией Фельдмана М., Шаршмидта Б.Ф., Слейзенгера М.Х. Филадельфия: Сондерс; 1998: 128–152. Клинически ориентированный подход к этому сложному симптому.
Google ученый
DuPont HL: Рекомендации по острой инфекционной диарее у взрослых . Am J Gastroenterol 1997, 92 : 1962–1975.
PubMed
CAS
Google ученый
Дженкинс Д., Гудолл А., Скотт ББ: Простые объективные критерии диагностики причин острой диареи при ректальной биопсии . J Clin Pathol 1997, 50 : 580–585.
PubMed
CAS
Google ученый
Маршалл Дж. Б., Сингх Р., Диаз-Ариас AA: Хроническая диарея необъяснимой причины: необходима ли биопсия, если колоноскопия в норме?
Am J Gastroenterol 1995, 90 : 372–376.
PubMed
CAS
Google ученый
Robinson RJ, Stone M, Mayberry JF: Нормальная слизистая оболочка прямой кишки. Следует ли делать биопсию?
Гепатогастроэнтерология 1997, 44 : 703–705.
PubMed
CAS
Google ученый
Патель Ю., Петтигрю Н.М., Грэм Г.Р., Бернштейн CN: Диагностическая ценность эндоскопии нижних отделов плюс биопсия при диарее без крови . Gastrointest Endosc 1997, 46 : 338–343.
PubMed
Статья
CAS
Google ученый
Bini EJ, Weinshel EH: Эндоскопическая оценка диареи, связанной с вирусом хронического иммунодефицита человека: превосходит ли колоноскопия гибкую сигмоидоскопию?
Am J Gastroenterol 1998, 93 : 56–60.
PubMed
Статья
CAS
Google ученый
Schiller LR, Hogan RB, Morawski SG, et al. : Исследования распространенности и значимости мальабсорбции желчных кислот с радиоактивной меткой в группе пациентов с идиопатической хронической диареей . Гастроэнтерология 1997, 92 : 151–160.
Google ученый
Potter GD: Желчная кислотная диарея . Dig Dis 1998, 16 : 118–124.
PubMed
Статья
CAS
Google ученый
Фартинг MJ: Пероральная регидратационная терапия . Pharmacol Ther 1994, 64 : 477–492.
PubMed
Статья
CAS
Google ученый
Шиллер Л. Р., Санта-Ана, Калифорния, Портер Дж. А., и др. : Стимулированный глюкозой транспорт натрия в кишечнике человека во время экспериментальной холеры . Гастроэнтерология 1997, 112 : 1529–1535.
PubMed
Статья
CAS
Google ученый
Thillainayagam AV, Hunt JB, Farthing MJ: Повышение клинической эффективности пероральной регидратационной терапии: является ли низкая осмоляльность ключевым фактором?
Гастроэнтерология 1998, 114 : 197–210.
PubMed
Статья
CAS
Google ученый
Шиллер LR: Обзорная статья: антидиарейная фармакология и терапия . Aliment Pharmacol Ther 1995, 9 : 87–106.Обзор доступных в настоящее время и исследуемых противодиарейных средств.
PubMed
CAS
Google ученый
Roge J, Baumer P, Berard H, et al. : Ингибитор энкефалиназы ацторфан при острой диарее: двойное слепое контролируемое клиническое испытание в сравнении с лоперамидом . Scand J Gastroenterol 1993, 28 : 352–354.
PubMed
CAS
Google ученый
Schiller LR, Santa Ana CA, Morawski SG, et al. : Исследования противодиарейного действия клонидина: влияние на моторику и кишечную абсорбцию . Гастроэнтерология 1985, 89 : 982–988.
PubMed
CAS
Google ученый
Фартинг MJ: Роль аналогов соматостатина в лечении рефрактерной диареи . Пищеварение 1996, 57 ( доп. 1 ): 107–113.
PubMed
CAS
Статья
Google ученый
Саймон Д.М., Виолончель JP, Валенсуэла Дж., и др. : Многоцентровое исследование октреотида у пациентов с диареей, связанной с рефрактерным синдромом приобретенного иммунодефицита . Гастроэнтерология 1995, 108 : 1753–1760.
PubMed
Статья
CAS
Google ученый
Инфекционная диарея | Pathway Medicine
Инфекционная диарея | Pathway Medicine
- Инфекционные агенты являются причиной подавляющего большинства случаев «острой диареи», определяемой как течение диареи продолжительностью менее 3 недель.Следует отметить, что многие механизмы, с помощью которых микроорганизмы вызывают диарею, можно отнести к категории других патофизиологий диареи; однако мы группируем под этим заголовком любую инфекционную причину диареи, независимо от ее молекулярного механизма.
- Подробный анамнез, физические данные и панель лабораторных результатов имеют решающее значение для сужения списка возможных инфекционных организмов. Определенные продукты питания часто связаны с определенными инфекционными агентами, поэтому следует составить список недавно проглоченных продуктов.Конституциональные симптомы указывают на то, что микроорганизм проник в слизистую оболочку желудочно-кишечного тракта и, таким образом, инициировал системный иммунный ответ. Присутствие крови в диарейных фекалиях указывает на то, что микроб повредил слизистую толстой или тонкой кишки либо путем производства цитотоксинов, либо путем физического проникновения в слизистую оболочку. Посев кала чрезвычайно полезен для прямой микобиологической диагностики инфекционной диареи.
- Обзор
- Вирулентные кишечные микробы могут вызывать диарею из-за целого ряда возможных патофизиологических механизмов.Ниже мы обсуждаем исключительно некоторые общие темы, в то время как конкретные молекулярные механизмы описаны на страницах причинных организмов.
- Повышение кишечной секреции
- Обычно это вызвано микробными энтеротоксинами, которые вызывают чрезмерную активацию путей регуляции секреции тонкой или толстой кишки. Поскольку эти микроорганизмы обычно не проникают в слизистую оболочку желудочно-кишечного тракта, они обычно не вызывают лихорадки, конституциональных симптомов или кровавой диареи.
- Нарушение абсорбции воды и электролита в ЖКТ
- Различные процессы могут нарушать всасывание воды и электролитов в кишечнике, что приводит к диарее. Прилипание микробов к эпителию толстой или тонкой кишки обычно вызывает только водянистую диарею, поскольку не происходит гибели или инвазии клеток слизистой оболочки. Производство цитотоксинов бактериями-виновниками может привести к образованию крови и присутствию воспалительных клеток в стуле, но без конституциональных симптомов, так как фактического вторжения в слизистую оболочку нет.Микробная инвазия слизистой оболочки кишечника приведет к образованию крови и воспалительных клеток в кале, а также к запуску системного иммунного ответа, который будет проявляться в виде конституциональных симптомов, таких как лихорадка.
- Широкое разнообразие бактерий, вирусов и простейших может вызывать инфекционную диарею, поэтому в качестве ориентира следует использовать взаимосвязи, хотя ниже мы классифицируем несколько организмов по патофизиологическому механизму, с помощью которого они вызывают диарею
- Производство энтеротоксина: Staphylococcus aureus, Clostridium perfringens, Vibrio cholera
- Продукция цитотоксина: Clostridium difficile, ETEC и STEC Escherichia coli
- Инвазия: Salmonella, Campylobacter jejuni, Vibrioella 9000, Vibrioella parelis 9000, Vibrioella p. : Лямблии лямблии
Диарея — AMBOSS
Последнее обновление: 8 декабря 2020 г.
Резюме
Диарейные заболевания очень распространены и в большинстве случаев проходят самостоятельно.Диарея определяется как наличие более трех испражнений в день, содержание воды более 75% или количество стула не менее 200–250 г в день. Острая диарея длится не более 14 дней и обычно вызвана вирусной или бактериальной инфекцией или пищевым отравлением. Хроническая диарея часто вызывается основными желудочно-кишечными или эндокринологическими состояниями, такими как воспалительное заболевание кишечника или гипертиреоз. Дополнительные симптомы могут включать жар, кровавый стул, боль в животе, тошноту и рвоту в случаях гастроэнтерита.Диагностические тесты при острой диарее обычно не нужны, но они могут включать общий анализ крови, образцы стула или колоноскопию в тяжелых или хронических случаях. В большинстве случаев диарея требует только симптоматического лечения, такого как пероральная регидратация, в то время как в тяжелых случаях может потребоваться введение антибиотиков и госпитализация для внутривенного замещения жидкости.
Определение
- Диарея присутствует, если выполняется один из следующих критериев: [1] [2]
- Частая дефекация: ≥ 3 раз в день
- Изменение консистенции стула: повышенное содержание воды
- Увеличение в количестве стула: более 200–250 г в сутки
- Острая диарея: продолжительностью ≤ 14 дней
- Стойкая диарея: длится> 14 дней
- Хроническая диарея: длится> 30 дней
Этиология
Инфекционные причины
[1] [3]
Неинфекционные
[5] [6] [7]
| Условия | |||||
|---|---|---|---|---|---|
| Пищевые токсины | |||||
|
Передача заболеваний и факторы риска
[1]
- Фекально-оральная передача
- Проглатывание зараженной пищи или напитков (см. «Диарея путешественников»)
- Прямой контакт с загрязненными поверхностями или предметами
- Прямой контакт с больным (например,г., рукопожатие, разделение еды)
- Факторы риска
- Посещение детских садов, резиденция в доме престарелых, госпитализация
- Плохая гигиена
- Воздействие на животных
Классификация
| Патофизиология [1] | ||
|---|---|---|
| Экссудативно-воспалительная диарея |
| |
| Секреторная диарея |
| |
| Осмотическая диарея |
| |
| Моторная диарея |
|
Потеря жидкости, богатой бикарбонатом, при тяжелой диарее может вызвать метаболический ацидоз без анионной щели.
Клинические особенности
- Острая или хроническая диарея (см. «Определение» выше)
- Дальнейшие возможные симптомы [9]
- Течение заболевания может варьироваться от легкого до тяжелого с необходимостью госпитализации.
Подтипы и варианты
Диарея путешественников
[10]
- Определение: инфекции, которые обычно возникают у пациентов, недавно путешествовавших
- Эпидемиология
- Очень часто встречается во время путешествий по странам Азии («живот Дели»), Африки и Латинской Америки («Месть Монтесумы»)
- Основная причина диареи среди детей в развивающихся странах
- Этиология
- Клинические признаки: экссудативно-воспалительная диарея или секреторная диарея.
Мнимая диарея
- Определение: диарея, вызванная собой, обычно в результате злоупотребления слабительными (часто возникает у людей с искусственными расстройствами)
- Эпидемиология
- Наиболее часто встречается у женщин
- Пациенты обычно работают в сфере здравоохранения.
- История нескольких госпитализаций
- Клинические признаки: хроническая водянистая диарея без установленной причины.
- Диагностика
- Лечение
Злоупотребление слабительными
- Вещества
- Клинические особенности
Диагностика
Обследование при диарее включает подробный анамнез пациента (например, недавние поездки), физический осмотр и лабораторные тесты для оценки тяжелых случаев.
Лабораторные тесты
Лабораторные тесты обычно не требуются в острых случаях, а используются для диагностики тяжелых или хронических заболеваний.
- Показания
- Тесты
- Общий анализ крови: может выявить анемию или лейкоцитоз.
- Образцы стула
- Посев стула: тест, используемый для выявления бактерий, вирусов, грибков или паразитов в кале, часто в контексте подозрения на желудочно-кишечную инфекцию.
- Посев кала обычно не рекомендуется, поскольку тесты дороги и имеют низкую чувствительность.
- Показания: подозрение на инвазивный бактериальный энтерит, тяжелое заболевание или лихорадка (> 38,5 °), требуется госпитализация и / или положительный результат анализа стула на лейкоциты / скрытую кровь / лактоферрин
- Анализ на токсин C. difficile
- Осмотический зазор стула: уравнение, используемое для определения, имеет ли водянистая диарея осмотическую или секреторную этиологию
- Уравнение: 290 — [2x (натрий в стуле + калий в стуле)]
- Интерпретация
Визуализация
Лечение Поскольку в большинстве случаев острая диарея проходит самостоятельно, наиболее распространено симптоматическое лечение с упором на пероральную регидратацию.Терапия редко предполагает прием лекарств.
- Регидратация (особенно у детей)
- Легкое или умеренное обезвоживание: пероральная регидратационная терапия электролитосодержащими жидкостями, например яблочным соком или раствором для пероральной регидратации
- Тяжелые случаи: рассмотреть возможность госпитализации; гидратация с внутривенным введением 0,9% хлорида натрия
- Противодиарейные средства (например, лоперамид)
- Можно назначать в легких и умеренных случаях
- Следует избегать, если в стуле высокая температура или кровь (что свидетельствует о системном заболевании).
- Антибиотики: обычно не показаны
- Другое: лечение основного заболевания в случае хронической диареи
Ссылки
Барр В., Смит А.Острая диарея у взрослых. Ам Фам Врач . 2014; 89
(3): с.180-189.- Диарея путешественников.
https://wwwnc.cdc.gov/travel/yellowbook/2016/the-pre-travel-consultation/travelers-diarrhea .
Обновлено: 10 июля 2015 г.
Доступ: 1 марта 2017 г. - Каспер Д.Л., Фаучи А.С., Хаузер С.Л., Лонго Д.Л., Ламесон Дж.Л., Лоскальцо Дж. Принципы внутренней медицины Харрисона .
McGraw-Hill Education
; 2015 г. - Уокер Х. К., Холл В. Д., Херст В. Дж., Сильверман М. Е., Моррисон Г. Клинические методы: история, физикальные и лабораторные исследования .
Баттервортс
; 1990 г. Цю Ф.З., Шен ХХ, Ли Г.Х. и др. Аденовирус, связанный с острой диареей: исследование случай-контроль .. BMC Infect Dis . 2018; 18
(1): с.450.
DOI: 10.1186 / s12879-018-3340-1. | Открыть в режиме чтения QxMD- Токсичность гистамина.
https://www.aaaai.org/conditions-and-treatments/related-conditions/histamine-toxicity .Обновлено: 1 марта 2017 г.
Доступ: 1 марта 2017 г. - Обзор пищевого отравления.
http://www.msdmanuals.com/home/injuries-and-poisoning/poisoning/overview-of-food-poisoning .
Обновлено: 1 марта 2017 г.
Доступ: 1 марта 2017 г. Джакетт Дж., Триведи Р. Оценка хронической диареи. Ам Фам Врач . 2011; 84
(10): с.1119-1126.- Диарейное заболевание. http://www.who.int/mediacentre/factsheets/fs330/en/ .
Обновлено: 1 апреля 2013 г.
Доступ: 1 марта 2017 г. - Диарея.
http://www.merckmanuals.com/professional/gastrointestinal-disorders/symptoms-of-gi-disorders/diarrhea .
Обновлено: 1 марта 2016 г.
Доступ: 1 марта 2017 г. - Герольд Г. Внутренняя медицина .
Герольд Дж.
; 2014 г. - Агабеги СС, Агабеги ЭД. Шаг вперед в медицину .
Липпинкотт Уильямс и Уилкинс
; 2013 - Агабеги СС, Агабеги ЭД. Шаг вперед в медицину .
Wolters Kluwer Health
; 2015 г. - Ле Т, Бхушан В, Багга Х.С. Первая помощь для USMLE Step 2 CK .
McGraw-Hill Medical
; 2009 г. - Гуандалини С. Диарея. Диарея . Нью-Йорк, штат Нью-Йорк: WebMD. http: // emedicine.medscape.com/article/928598-overview . Обновлено: 11 ноября 2016 г. Дата обращения: 19 февраля 2017 г.
- Диарея.
http://www.who.int/topics/diarrhoea/en/ .
Обновлено: 1 марта 2017 г.
Доступ: 1 марта 2017 г. - Вальд А. Мнимая диарея: клинические проявления, диагностика и лечение. В: Post TW, ed. Дата обновления . Уолтем, Массачусетс: UpToDate. https://www.uptodate.com/contents/factitious-diarrhea-clinical-manifestations-diagnosis-and-management?source=search_result&search=factitious%20diarrea&selectedTitle=1~28 .

