Контроль качества стерилизации — Студопедия
1. Краткосрочный (оперативный) метод контроля стерилизации:
· Химический метод – использование химических индикаторов стерильности или химических тестов (для паровой, воздушной и газовой стерилизации)
· Физический метод – использование: термометров, максимальных термометров, индикаторных устройств на панели, мановакуометров, секундомеров, часов, таймеров на панели аппарата (для паровой, воздушной и химической стерилизации).
Химические индикаторы стерильности для паровой стерилизации: мочевина, бензойная кислота, сера, ИС – Винар (120, 132 гр.)
Химические индикаторы стерильности для воздушной стерилизации: винная кислота, гидрохинон, тиомочевина, ИС — Винар (160, 180 гр.)
2. Долгосрочный метод контроля стерилизации — использование бактериологического метода (бактериальных тестов со споровой культурой)
Самоконтроль работы стерилизаторов проводит персонал ЛПУ физическим и химическим методом при каждой загрузке стерилизатора.
Для регистрации контроля качества стерилизации ведется журнал —
форма 257/у.
Причины неудовлетворительных результатов контроля стерилизации в паровых и воздушных стерилизаторах: неисправность стерилизатора, неполное удаление воздуха из камеры парового стерилизатора перед стерилизацией (образование паровоздушной смеси вместо насыщенного пара), избыточная, неравномерная или неправильная загрузка камеры стерилизатора, нарушение режима стерилизатора, использование несоответствующего упаковочного материала.
| Уровень освоения компетенции | Исходный
балл | Полученный
балл |
Дан полный, развернутый ответ на поставленный вопрос, показана совокупность знаний; в ответе прослеживается логическая последовательность, отражающая сущность раскрываемых понятий. Знание демонстрируется на фоне понимания его в системе данного модуля и междисциплинарных связей. Ответ изложен грамотно с использованием медицинской терминологии. Могут быть допущены недочеты в определении понятий, исправленные студентом самостоятельно в процессе ответа. Ответ изложен грамотно с использованием медицинской терминологии. Могут быть допущены недочеты в определении понятий, исправленные студентом самостоятельно в процессе ответа.
| 10 — 8 | |
| Дан недостаточно полный и недостаточно развернутый ответ. Логика и последовательность изложения имеют нарушения. Допущены ошибки в раскрытии понятий, употреблении терминов. Умение раскрыть значение обобщенных знаний не показано. Речевое оформление требует поправок, коррекции. | 7 — 5 | |
| Дан недостаточно полный и недостаточно развернутый ответ. Логика и последовательность изложения имеют нарушения. Допущены ошибки в раскрытии понятий, употреблении медицинских терминов. Умение раскрыть значение обобщенных знаний не показано. Речевое оформление требует поправок, коррекции. | 4 — 2 | |
| Ответ представляет собой разрозненные знания с существенными ошибками по вопросу. Присутствуют фрагментарность, нелогичность изложения Речь неграмотная, медицинская терминология не используется. Дополнительные и уточняющие вопросы преподавателя не приводят к коррекции ответа студента; или ответ на вопрос полностью отсутствует
или имеется отказ от ответа. | ||
| Максимальное количество баллов |
Этапы контроля качества стерилизации
Нужна помощь в написании работы?
|
Этап контроля
|
цель
|
Используемые
Методы
контроля
|
Кто проводит
|
|
Контроль работы оборудования
|
Оценить качество работы оборудования Внимание! Если вам нужна помощь в написании работы, то рекомендуем обратиться к
|
физический
|
Персонал, обслуживающий стерилизационное оборудование
|
|
Контроль качества стерилизации всей загрузки
|
Оценить качество стерилизации всего объема стерилизуемых материалов для чего используется тестовая упаковка
|
Химический,
биологический
| |
|
Контроль качества стерилизации упаковки с материалами
|
Оценить достижение параметров стерилизации внутри каждой из упаковок, проводится в момент вскрытия упаковки непосредственно перед применением
|
Химический, биологический
|
Персонал отделений при использовании стерильных материалов
|
|
Протоколирование полученных результатов
|
Письменно подтвердить качество стерилизационного процесса
|
физический
|
Вышеуказанные категории персонала
|
Функции оператора стерилизационного оборудования по контролю качества проводимой стерилизации
Персонал, обслуживающий стерилизацию изделий медицинского назначения, обязан:
-знать действующие нормативные документы по вопросам стерилизации изделий мед. назначения
-знать основные принципы работы стерилизационного оборудования
-знать принципы работы стерилизационного процесса
-уметь анализировать полученные данные
-соблюдать правила техники безопасности.
Поможем написать любую работу на аналогичную
тему
Получить выполненную работу или консультацию специалиста по вашему
учебному проекту
Узнать стоимость
Поделись с друзьями
Химические индикаторы
Химические индикаторы контроля качества стерилизации
Эксплуатация стерилизаторов в учреждениях здравоохранения и производстве медицинских изделий должна находится под контролем. Процесс уничтожения патогенных спор и бактерий невозможно оценить визуально. Для этой цели применяют специальные индикаторы качества стерилизационнх процессов, которые основаны на разных технологиях. Биологические индикаторы используют живые споры для теста, инактивация контрольных микроорганизмов моделирует уничтожение микроорганизмов на стерилизуемых изделиях. Химические индикаторы – основаны на принципе изменения цвета контрольной индикаторной полоски при воздействии определенных факторов для проверки работы стерилизационного оборудования.
Индикаторы химического типа должны соответствовать ГОСТ ISO 11140-1-2011, этот стандарт действует с 2002 года.
Как работают химические индикаторы стерилизации?
Наиболее распостранены паровой, газовый и радиационные методы стерилизации. Если вы приобретаете химические индикаторы для контроля качества стерилизации, они будут различными для данных технологий. Принцип их работы прост — химические индикаторы контрастно изменяют свой цвет после прохождения цикла стерилизации (химические индикаторы 1 типа) или после соблюдения заданных стандартом параметров стерилизации (индикаторы 4 типа и индикаторы 5 типа) и позволяют определить, соответствуют ли реальные условия стерилизации требуемым нормам.
Преимущества этого метода проверки:
- мгновенное получение информации, без ожидания анализа данных;
- нет необходимости использовать дополнительные инкубаторы для проверки результатов;
- возможность проверки достаточности концентрации газа при стерилизации оксидом этилена, а также дополнительно относительной влажности;
- возможность проверки радиационного воздействия, поглощенной дозы излучения;
- наличие шести отдельных типов индикаторных лент, которые применяются в разных условиях.
ГОСТ ISO 11140-1-2011 выделяет 6 типов индикаторов. Первый – самый простой тип, он визуально показывает, что поверхность или изделие были подвергнуты стерилизации. Вторая группа проверяет качество вывода воздуха из камеры паровой стерилизации. К третьему классу относятся более точные индикаторы, но лишь с одним измеряемым параметром. В случае с четвертым классом параметров уже может быть несколько, есть ряд отдельно реагирующих красителей. Пятый и шестой тип наиболее четко реагируют на параметры цикла стерилизации и любые изменения при стерилизации или на достижение поставленного результата.
Где купить качественные химические индикаторы?
Химические индикаторы для проверки качества стерилизационных процессов можно приобрести в компании «СтериПро» http://steri-pro.ru/. В каталоге доступны различные типы тестов, которые сертифицированы по государственному стандарту и отвечают высоким требованиям по качеству. Мы поставляем товары от ведущих мировых брендов, предоставляем сопроводительные документы для каждой партии. Накопленный опыт продаж, поставок, предоставления в аренду и самостоятельного использования стерилизационного оборудования позволяет нам подбирать для клиентов оптимальные средства контроля качества и предоставлять детальные консультации. Чтобы уточнить информацию, заказать подбор индикаторов или оформить заказ на продукцию, звоните менеджерам компании по телефону или электронной почте, будем рады обсудить с Вами вопросы качества стерилизации!
Контроль качества и эффективности дезинфекции и стерилизации
Для профилактики инфекционных заболеваний в помещениях осуществляют контроль качества дезинфекции. Мероприятия по дезинфекции проводятся визуальными, химическими и бактериологическим методами. Нередко этими методами пользуются одновременно.
Мероприятия по дезинфекции проводятся визуальными, химическими и бактериологическим методами. Нередко этими методами пользуются одновременно.
Метод визуального контроля определяет своевременность дезинфекции, имеющиеся основания, спектр мероприятий и объем работ по стерилизации предметов, объектов и помещений.
Химический контроль дезинфекции и стерилизации выбирают, когда нужно определить содержание веществ и соответствие инструкции. В данном методе важно установить, когда и кем был приготовлен раствор, определяют качество стерилизации поверхностей эпидемиологически опасных предметов – посуды, мебели, помещения, бытовых предметов, которые следует увлажнить во время уборки хлорсодержащими растворами.
Бактериологический контроль качества стерилизации и дезинфекции предполагает снятие проб с бытовых предметов, предметов одежды, постельного белья, мебели и поверхностей. Данный метод специалистами осуществляется без предупреждения рабочего персонала. Его цель — контроль эффективности дезинфекции и всех мероприятий, проводимых в дошкольных, школьных, медицинских и общесвтенных учреждениях.
Контроль качества дезинфекции осуществляется комиссией специалистов санитарно-эпидемиологической станции в установленные сроки, либо без предупреждения. Цель таких мероприятий – свести к минимуму и предотвратить возникновение очагов опасных инфекционных заболеваний среди населения. Эти мероприятия проводятся в три этапа:
1. проверка уровня чистоты поверхностей, увлажненность и защита приборов;
2. смотр режима стерилизации включает в себя учет температуры раствора, равномерности увлажнения поверхностей, качество распыления средства, его концентрацию и специфику и проводится с привлечением специалистов;
3. данный этап предполагает проверку качества дезинфекции со вниманием на специфику производства, определенных особенностей и остановки предприятия, где осуществляется контроль.
Опыт проведения контроля качества стерилизации и дезинфекции показывает, что такие мероприятия позволяют избежать и предотвратить непоправимые ситуации, которые могут угрожать жизни и здоровью населения. Поэтому они являются обязательными для поликлиник, предприятий общепита и детских учреждений.
Поэтому они являются обязательными для поликлиник, предприятий общепита и детских учреждений.
Контроль качества стерилизации оксидом этилена
Контроль качества стерилизации осуществляется с помощью биологических и химических индикаторов
Есть несколько способов проверки эффективности стерилизации. Соответствующая упаковка, время стерилизации, температура, влажность, концентрация, давление газа важны для физического контроля. С другой стороны, если требуется быстрый ответ о соблюдении параметров стерилизации, лучшее решение – химические индикаторы. При использовании химических индикаторов смена цвета показывает насколько эффективно прошла стерилизация. В качестве биологических индикаторов часто используют споры Bacillus subtilis, B. stearothermophilus, B. atrophaeus.
Биологический индикатор — в качестве биологического индикатора в СтериПак Сервис используются споры Bacillus atrophaeus. Биологический индикатор 3M™ Attest™ состоит из полоски со спорами (споры закреплены на бумажной полоске), заключённой в пластиковый контейнер с питательной средой, содержащейся в хрупкой стеклянной ампуле. Крышка создана таким образом, чтобы газ проникал в пластиковый контейнер, убивая споры и тем самым подтверждая соблюдение необходимых условий стерилизации.
Химический индикатор 3M™ Comply™ 1251 — полоска с химическим индикатором. Это внешний индикатор, который обеспечивает мгновенный точный и легкий для отображения метод мониторинга газовой стерилизации. Качество стерилизации подтверждается изменением цвета с красного на зелёный.
Устройства регистрации данных — небольшые электронные устройства, которые помещаются в камеру стерилизации, где они отслеживают и регистрируют внутренние условия. Они малогабаритные, запитываются от батарейки, портативные и оборудованы микропроцессором, внешним устройством хранения информации и датчиками. Наши устройства регистрации данных связанны с компьютером и используют программное обеспечение для активации устройства регистрации данных, просмотра и анализа полученных данных.
Наши специалисты используют биологические, химические индикаторы, а также устройства регистрации данных для оценки качества стерилизации.
Стерилизация. Устройство и функции ЦСО
1. Стерилизация. Устройство и функции ЦСО
2. Стерилизация
– полное освобождение какого-либо вещества или
предмета от микроорганизмов, в том числе и от спор
(спороцидное действие), как патогенных, так и не
патогенных микроорганизмов
Дезинфекция
ПСО
Стерилизация
Стерилизации подвергаются все изделия,
соприкасающиеся с раневой поверхностью,
контактирующие с кровью или инъекционными
препаратами, медицинские инструменты,
которые соприкасаются со слизистыми и могут
вызвать их повреждение.
Стерилизация важное звено неспецифической
профилактики ВБИ
4. Нормативно-правовая база
ОСТ 42-21-2-85 «Стерилизация и дезинфекция
изделий медицинского назначения» Этим
стандартом установлены методы, средства и
режимы дезинфекции и стерилизации
СанПиН 2.1.3.2630-10 «Санитарноэпидемиологические требования к
ООМД»Определяют организацию
стерилизационных мероприятий в ООМД
5. Методы стерилизации
Методы стерилизации
Физические
Термические
(паровой,
воздушный,
глассперленовый)
Промышленные
(плазменный,
радиационный)
Химические
Газовый,
химическими
растворами
6. Методы стерилизации
Выбор метода стерилизации конкретных изделий
зависит от
свойств объекта
самого метода, его достоинств и недостатков.
В практике ЛПУ наиболее широко используется
термический метод стерилизации с использованием
насыщенного пара и сухого горячего воздуха
(паровой и воздушный стерилизаторы).
7. ТЕРМИЧЕСКИЕ МЕТОДЫ СТЕРИЛИЗАЦИИ
Преимущества:
надежность,
удобство и оперативность работы персонала;
возможность использования разных видов упаковок,
отсутствие необходимости удаления остатков
химических средств с изделий
Недостатки:
специальное оборудование,
высокие температуры
8.
 Термические методы стерилизации
Термические методы стерилизации
Паровой метод
Для достижения температур выше
точки кипения воды пользуются
автоклавом. Автоклав представляет
собой установку для стерилизации
паром под давлением. Температура
насыщенного пара зависит от
давления.
Компактный переносной
автоклав
9. ПАРОВОЙ МЕТОД СТЕРИЛИЗАЦИИ
стерилизующим средством является
водяной пар под избыточным
давлением, температурой 120- 134
градуса
стерилизацию осуществляют в паровых
стерилизаторах (автоклавах)
10. ПАРОВОЙ МЕТОД СТЕРИЛИЗАЦИИ
Стерилизуют:
общие хирургические и специальные инструменты,
детали приборов и аппаратов из коррозионностойких
металлов,
стекло,
шприцы с пометкой 200 град. С,
хирургическое белье,
перевязочный и шовный материал,
изделия из резин (перчатки, трубки, катетеры, зонды и
т.д.), латекса, отдельных видов пластмасс.
11. ПАРОВОЙ МЕТОД СТЕРИЛИЗАЦИИ
УПАКОВКА:
стерилизационные коробки
пергамент
оберточные бумаги
12. ПАРОВОЙ МЕТОД СТЕРИЛИЗАЦИИ
Режимы стерилизации:
2 атм. — 132 градуса – 20 минут;
1,1 атм. – 120 градусов — 45 минут.
Контроль стерильности
бензойная кислота,
термоиндикаторная лента фирмы
«Винар» ИС-120, ИС-132.
13. ПАРОВОЙ МЕТОД СТЕРИЛИЗАЦИИ
Преимущества:
недорогой, надежный, нетоксичный,
обеспечивает стерильность не только на
поверхности изделий, но и всего изделия,
сравнительно невысокая температура,
можно использовать упаковку
Недостатки:
вызывает коррозию металлов,
увлажняет стерилизуемые изделия
14. Термические методы стерилизации
Воздушный метод
Стерилизация осуществляется в
специальных аппаратах — сухожаровых шкафах-стерилизаторах.
Стерилизация в сухожаровом шкафу
происходит при помощи циркуляции
внутри него горячего воздуха
15. ВОЗДУШНЫЙ МЕТОД СТЕРИЛИЗАЦИИ
стерилизующим средством
является сухой горячий воздух
температурой 160-180 градусов,
стерилизацию осуществляют в
воздушных стерилизаторах
(сухожаровых шкафах)
16.
 ВОЗДУШНЫЙ МЕТОД СТЕРИЛИЗАЦИИ
ВОЗДУШНЫЙ МЕТОД СТЕРИЛИЗАЦИИ
Режимы стерилизации:
180 градусов – 60 минут;
160 градусов – 150 минут.
Индикаторами будут:
янтарная кислота, тиомочевина, сахароза, винокаменная кислота,
термоиндикаторная лента фирмы «Винар» ИС-160;
ИС-180,
17. ВОЗДУШНЫЙ МЕТОД СТЕРИЛИЗАЦИИ
Преимущества метода:
не вызывает коррозии инструментов,
не происходит увлажнения упаковки.
Недостатки:
необходимость использования высоких температур,
нельзя использовать для стерилизации изделий из
пластмассы и резины, многие упаковочные
материалы.
18. Сроки хранения
6 часов:
без упаковки
3 суток, включая дату стерилизации:
в биксах без фильтра,
в двойной упаковке из бязи,
крафт-бумаге
20 суток, включая дату стерилизации:
в биксах с фильтром,
в крепированоой бумаге
19. Термические методы стерилизации
Глассперленовый метод
стерилизации: стерилизуют
цельнометаллические
стоматологические,
косметологические инструменты,
погружая их в среду стеклянных
шариков, нагретых до Т 190-250о С.
Время обработки указано в
инструкции по эксплуатации
конкретного стерилизатора
20. Промышленные методы стерилизации
Плазменный метод
позволяет создать биоцидную среду на основе
водного раствора пероксида водорода, а также
низкотемпературной плазмы
(ионизированный газ, образующийся при
низком давлении).
Это самый современный метод стерилизации.
Он позволяет стерилизовать любые
медицинские изделия, от полых инструментов
до кабелей, электроприборов, к которым в
ряде случаев вообще не удается применить ни
один из известных методов стерилизации.
21. Промышленные методы стерилизации
22. Промышленные методы стерилизации
Плазменный метод
Плазма образуется под воздействием сильного
электромагнитного излучения в атмосфере паров
перекиси водорода. При отключении
При отключении
электромагнитного поля свободные радикалы
преобразуются в молекулы воды и кислорода, не
оставляя никаких токсичных отходов.
Минимальное время обработки в плазменном
стерилизаторе – от 35 минут, рабочая температура
– 36-60°С. Одно из основных преимуществ этого
метода – отсутствие токсичных отходов,
образуются только кислород и водный пар.
Плазменная стерилизация уничтожает все формы
и виды микроорганизмов
23. Промышленные методы стерилизации
Радиационный метод
стерилизации
Радиационное излучение
применяют для
термолабильных полимерных
материалов, биологических
(вакцины и сыворотки) и
лекарственных препаратов.
Стерилизующим объектом
являются гамма- и бета- лучи
24. Обязательные условия сохранения стерильности одноразовых ИМН:
целостность упаковки;
соблюдение срока годности
25. Химический метод стерилизации:
стерилизация растворами
является вспомогательным
методом, который применяют
при невозможности
использования других
26. Химический метод стерилизации:
Преимущества:
легкость в применении
Недостатки:
изделия стерилизуют без
упаковки,
их необходимо
промывать.
27. Химический метод стерилизации:
Стерилизацию проводят при полном погружении
изделий в раствор, свободно их раскладывая, при
большой длине укладывая по спирали.
Разъемные изделия стерилизуют в разобранном виде,
заполняя каналы и полости.
Погружаемые изделия должны быть сухими, во
избежание разбавления раствора стерилянта.
Извлекают изделия с помощью стерильных пинцетов
или корнцангов, удаляют раствор из каналов и
полостей, а затем промывают дважды в стерильной
жидкости выдерживая экспозицию 5 минут.
28. Химический метод стерилизации:
Промытые стерильные изделия
сразу же используют по
назначению или помещают с
помощью стерильных пинцетов в
стерильный бикс, выложенный
стерильной простыней.
Срок хранения изделий не более 3
суток
29. Средства для химической стерилизации
6% раствор перекиси водорода,
дезоксон,
лизоформин,
сайдекс.
30. Контроль качества стерилизации
Технический
Химический
Бактериологический
31. Контроль качества стерилизации
это регулярные мероприятия по получению,
документированию и интерпретации данных,
необходимых для доказательства надежности
стерилизации
Физические и химические методы предназначены для
оперативного контроля и позволяют контролировать
соблюдение параметров режимов паровой, газовой,
воздушной стерилизации, температуру, давление,
экспозицию. Недостаток этих методов заключается в
том, что они не могут служить доказательством
эффективной стерилизации. Достоверным для
определения эффективности является только
бактериологический метод.
32. Контроль качества стерилизации Технический контроль
осуществляется путем
наблюдения за
показаниями приборов
(температура, давление,
время экспозиции и др.)
33. Контроль качества стерилизации Химический контроль
осуществляется с помощью химических тестов и
термохимических индикаторов.
Химический тест представляет запаянную с обоих
концов стеклянную трубку, заполненную смесью
химического соединения или только химическим
соединением (веществом), изменяющим свое
агрегатное состояние и цвет при достижении
определенной для него температуры плавления,
близкой к контролируемой.
34. Контроль качества стерилизации Химический контроль
1) для режима парового стерилизатора 120±2°С —
бензойная кислота с красителем, сера элементарная
(высокопробная) без красителя;
2) для режима парового стерилизатора 132±2°С —
мочевина с красителем, никотинамид с красителем,
Д(+)манноза с красителем;
3) для режима воздушного стерилизатора 180±2°С —
винная кислота без красителя, тиомочевина без
красителя, гидрохинон без красителя;
4) для режима воздушного стерилизатора 160±10°С —
левомицетин без красителя.
35. Контроль качества стерилизации Химический контроль
Термохимический индикатор представляет собой полоску
бумаги, на которую нанесена термоиндикаторная краска, цвет
которой необратимо меняется только при
регламентированных режимах стерилизации.
Термохимические индикаторы повышают эффективность
оперативного контроля, так как обеспечивают оценку
температуры и времени стерилизации
С января 2002 года в России введен в действие ГОСТ Р ИСО
11140-1 «Стерилизация медицинской продукции. Химические
индикаторы. Общие требования». Согласно этому документу
химические индикаторы распределены на шесть классов.
36. Контроль качества стерилизации Химический контроль
Химические индикаторы позволяют
осуществлять контроль условий стерилизации
внутри упаковок и изделий, а также контроль
условий в камере парового стерилизатора, вне
стерилизуемых изделий и упаковок — так
называемый «наружный» контроль – контроль
загрузки камеры стерилизатора.
Класс 1. Индикаторы процесса
Класс 2. Индикаторы для специальных
испытаний
Класс 4. Многопеременные индикаторы
Класс 5. Интегрирующие индикаторы
37. Индикаторы 1-го класса- «Свидетели»
Индикаторы 1-го класса«Свидетели»
Они позволяют визуально отличить изделия,
прошедшие стерилизацию, от нестерилизованных в тех
случаях, когда стерилизация осуществляется в
односторонних стерилизаторах и существует риск
смешения потоков стерилизованных и
нестерилизованных изделий, и тем самым уменьшить
вероятность применения нестерилизованных изделий
38. Индикаторы 2-го класса
Индикаторы 2-го класса
Самый характерный представитель этого класса
индикаторов — индикатор теста Бовье-Дика
Он предназначен для испытания эффективности
вакуумной системы парового стерилизатора.
Другими словами, с помощью теста Бовье-Дика
можно оценить равномерность распределения пара в
камере стерилизатора.
Индикатор предназначен для использования
персоналом ЛПУ, эксплуатирующих и
контролирующих стерилизационное оборудование
39. Индикаторы 3-го класса
Индикаторы 3-го класса являются индикаторами
одного параметра. Они оценивают максимальную
температуру, но не дают представления о времени
ее воздействия. (бензойная кислота, тиомочевина
и др.)
40. Индикаторы 4-го класса (Внутри упаковки )
Индикаторы 4-го класса
(Внутри упаковки )
Индикаторы рекомендуется применять при
каждом цикле стерилизации. Индикаторы
помещают в трудно стерилизуемые места
стерилизуемых изделий и стерилизационных
упаковок с изделиями.
41. Индикаторы 4-го класса (Снаружи упаковки)
Закрепление индикаторов производится:
— при использовании комбинированных упаковок (прозрачная
синтетическая пленка плюс бумага) – на пленку;
— при использовании бумажных пакетов – на заклеивающийся
клапан пакета;
— при использовании листовых бумажных оберточных материалов
– на оставшийся свободным после завертывания угол бумаги;
— при использовании стерилизационных коробок – на бирку
коробки.
Индикаторы рекомендуется применять в каждом цикле
стерилизации. Количество индикаторов, закладываемых в
стерилизатор, зависит от объема камеры стерилизатора
42. Индикаторы 4-го класса (Снаружи упаковки)
Количество точек, в
которые закладываются
индикаторы
До 100 включительно
5
От 100 до 750
включительно
11
Свыше 750
13
ВНИМАНИЕ! Не допускается размещать
наружные индикаторы внутри стерилизуемых
изделий и упаковок.
43. Индикаторы 5-го класса-интеграторы
Индикаторы 5-го классаинтеграторы
Эти индикаторы называются интеграторами.
Индикатор предназначен для использования
персоналом ЛПУ, эксплуатирующих и
контролирующих стерилизационное
оборудование.
Действие интеграторов анологично
биологическим тестам.
Применяются как и биологические тесты- 1раз в
месяц для биологического контроля работы
стерилизационной аппаратуры.
44. Индикаторы 6-го класса
Теоретически эти индикаторы (эмуляторы)
реагируют на все, а не только на критические
параметры процесса стерилизации
45. Контроль качества стерилизации Бактериологический контроль
самый точный и достоверный метод, является
объективным методом оценки эффективности
работы паровых, воздушных стерилизаторов и
основан на выявлении гибели спор тесткультур.
Для контроля паровых стерилизаторов
используются высушенные споры тест-культуры
Bacillus stearothermophilus ВКМ В-718; для
контроля воздушных стерилизаторов — Bacillus
licheniformis штамм G.
46. Биологические индикаторы
Они представляют собой пластиковый контейнер с
крышечкой, содержащий хрупкую ампулу с
восстанавливающей средой и бумажную полоску,
зараженную спорами контрольных микроорганизмов.
Индикатор размещается непосредственно в
стерилизационной камере, либо закладывается в
контейнеры и упаковки, предназначенные к стерилизации,
в процессе их подготовки. После извлечения из камеры
стерилизатора надо раздавить находящуюся внутри ампулу
и инкубировать при рекомендованной температуре в
течение необходимого времени — обычно это 24 часа.
Ошибка стерилизации проявляется изменением
цвета и/или помутнением
среды.
47. Ситуационная задача
Старшая медсестра ЛПУ проводит
обход и предлагает
медицинской сестре процедурного кабинета вскрыть
стерилизационную коробку с универсальной укладкой,
срок стерильности которой не истек. При вскрытии
обнаружили, что одна из индикаторных лент ИС-132 не
изменила свой цвет.
Что произошло?
Какими индикаторами осуществляется
контроль стерильности?
Что необходимо проверить в связи с данным
нарушением?
Ваши действия?
48.
 Эталон ответа
Эталон ответа
Допущены нарушения при подготовке к стерилизации и (или) процесса
стерилизации. Этими нарушениями могут быть: неправильная
установка параметров стерилизации, сбой в работе стерилизатора,
грубое нарушение норм загрузки бикса или правил размещения их в
камере автоклава
Контроль стерильности осуществляется индикаторными лентами
фирмы «Винар», которые позволяют проконтролировать все параметры
стерилизации
В связи с этим нарушением необходимо проверить:
1.
2.
3.
1.
2.
3.
4.
срок годности индикатора
плотность укладки бикса, если не изменил цвет один из индикаторов,
значит бикс уложен не правильно: не вертикально, не рыхло.
работу автоклава – необходимо вызвать специалиста «Медтехники» для
ремонта автоклава, или правильной установки параметров
стерилизации
Пользоваться данной укладкой нельзя, отправить на повторную
стерилизацию в ЦСО.
49. Домашнее задание
Лекция
2. Учебник
3. Реферат:
«Почему ЦСО лучше?»
1.
Контроль качества стерилизации
Контроль качества стерилизации проводится персоналом центров дезинфекции и стерилизации и дезинфекционных отделов центров гигиены и эпидемиологии, а также персоналом лечебно-профилактических учреждений.
В функции персонала центров дезинфекции и стерилизации и дезинфекционных отделов входит контроль работы стерилизаторов на объектах надзора с использованием физического, химического и бактериологического методов: после монтажа и ремонта аппаратов; плановый контроль в порядке государственного санитарного надзора не реже 2 раз в год; по показаниям при обнаружении неудовлетворительных результатов контроля стерильности изделий медицинского назначения.
В функции персонала лечебно-профилактических учреждений входит самоконтроль работы стерилизаторов, который проводится при каждой загрузке аппаратов. Контроль осуществляется физическим и химическим методами.
Физический метод контроля осуществляется с помощью приборов измерения температуры (термометр, термометр максимальный), давления (мановакуумметры) и времени (часы). Максимальные термометры размещают в контрольных точках стерилизаторов для определения максимальной температуры, достигнутой в ходе стерилизационного цикла и распределения температуры внутри загруженной стерилизационной камеры.
Максимальные термометры размещают в контрольных точках стерилизаторов для определения максимальной температуры, достигнутой в ходе стерилизационного цикла и распределения температуры внутри загруженной стерилизационной камеры.
Химический метод контроля осуществляется с помощью химических тестов и термохимических индикаторов. Химический тест представляет запаянную с обоих концов стеклянную трубку, заполненную смесью химического соединения или только химическим соединением (веществом), что меняет свое агрегатное состояние и цвет при достижении определенной для него температуры плавления, близкой к контролируемой. При достижении заданной температуры химические тесты плавятся, необратимо меняя цвет.
работы паровых и воздушных стерилизаторов наиболее показательны такие химические тесты:
1) для режима парового стерилизатора 120 ± 2 ° С — бензойная кислота с красителем, сера элементарная (высокопробная) без красителя;
2) для режима парового стерилизатора 132 ± 2 ° С — мочевина с красителем, никотинамид с красителем, Д (+) манноза с красителем;
3) для режима воздушного стерилизатора 180 ± 2 ° С — винная кислота без красителя, тиомочевина без красителя, гидрохинон без красителя;
4) для режима воздушного стерилизатора 160 ± 10 ° С — левомицетин без красителя.
В настоящее время для контроля работы паровых и воздушных стерилизаторов находят широкое применение термохимические индикаторы. Термохимический индикатор представляет собой полоску бумаги, на которую нанесена Термоиндикаторная краска, цвет которой необратимо меняется только при регламентированных режимах стерилизации. Термохимические индикаторы повышают эффективность оперативного контроля, так как обеспечивают оценку температуры и времени стерилизации.
Контроль качества стерилизации в условиях клиники
Август 2018
CBSPD (Сертификационный совет по стерильной обработке и распространению) предварительно утвердил это обслуживание на один (1) контактный час в течение пяти (5) лет с даты первоначальной публикации.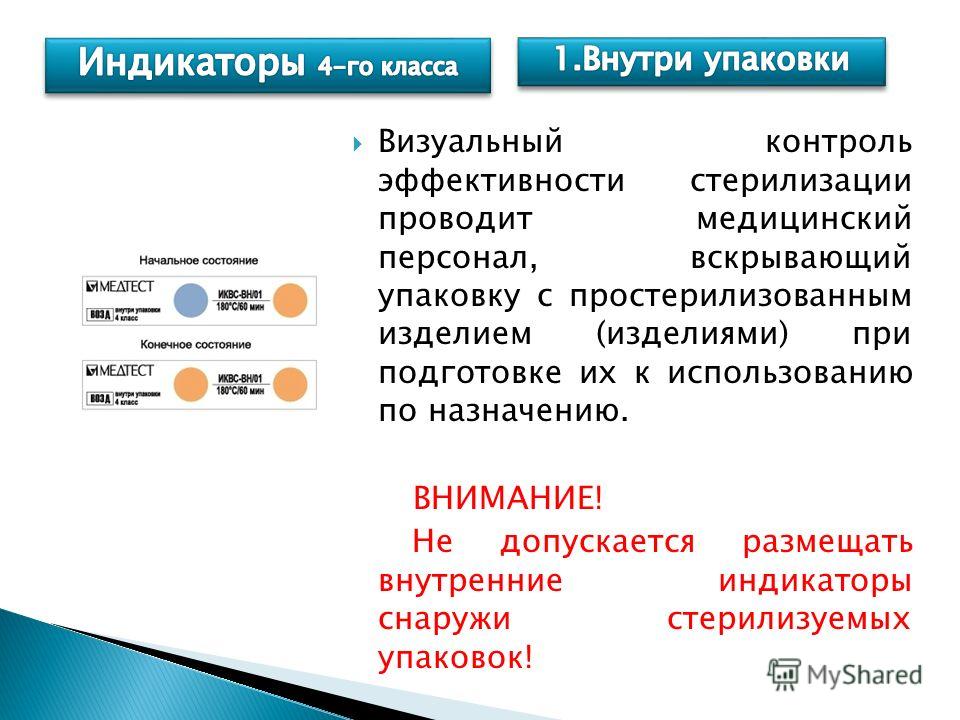 Успешное завершение урока и последующего тестирования должно быть задокументировано руководством учреждения, и эти записи должны храниться индивидуально до тех пор, пока не потребуется повторная сертификация. НЕ ОТПРАВЛЯЙТЕ УРОКИ ИЛИ ТЕСТ В CBSPD.
Успешное завершение урока и последующего тестирования должно быть задокументировано руководством учреждения, и эти записи должны храниться индивидуально до тех пор, пока не потребуется повторная сертификация. НЕ ОТПРАВЛЯЙТЕ УРОКИ ИЛИ ТЕСТ В CBSPD.
За дополнительной информацией о сертификации обращайтесь в CBSPD — 148 Main Street, Suite C-1, Lebanon, NJ 08833 www.sterileprocessing.org.
IAHCSMM (Международная ассоциация управления материальными ресурсами центральных служб здравоохранения) предварительно утвердила это без отрыва от производства для получения 1,0 кредита на непрерывное образование в течение трех лет, до 5 июля 2021 г.
Номер утверждения для этого урока: 3M-HPN 180507 . www.iahcsmm.org
Для получения дополнительной информации обращайтесь по телефону Healthcare Purchasing News (941) 927-9345, доб.202.
Скачать статью и тест.
Чтобы обеспечить наилучшие возможные исходы для пациентов и поскольку органы аккредитации уделяют более пристальное внимание обработке медицинских устройств многократного использования, важно, чтобы клиники, занимающиеся переработкой медицинских устройств, независимо от того, занимаются ли они независимой практикой или офисом, связанным с более крупной системой здравоохранения знаком с текущими рекомендуемыми практиками. ANSI / AAMI ST79, Всеобъемлющее руководство по стерилизации паром и обеспечению стерильности в медицинских учреждениях — это «переходный» документ по стерилизации паром, включая настольные стерилизаторы, часто используемые в клиниках.
Настольный стерилизатор определяется в AAMI ST79 как «Компактный паровой стерилизатор с объемом камеры менее или равным 2 кубических футам, который вырабатывает собственный пар при добавлении дистиллированной или деионизированной воды пользователем». 1 Это необходимое оборудование во многих офисных медицинских и стоматологических кабинетах и небольших амбулаторных клиниках. По всей стране многие системы здравоохранения выступают с инициативами по стандартизации обработки медицинских изделий во всей своей системе.В рамках этих усилий по стандартизации менеджеры по стерильной обработке и / или специалисты по профилактике инфекций обычно определяют все различные места, где выполняется повторная обработка устройств в их системе, и работают над тем, чтобы общие политики и процедуры были приняты в масштабах всей системы. 3M Sterilization Tech Line часто получает информацию от систем, которые недавно обнаружили или приобрели клиники, использующие настольные паровые стерилизаторы. Мы также часто обсуждаем с клиниками, которые стремятся внедрить передовой опыт.У обеих групп есть вопросы о соответствующих процедурах контроля качества стерилизации. В этой статье будут рассмотрены методы контроля качества, характерные для настольных стерилизаторов, представленные в недавно опубликованном AAMI ST79: 2017.
По всей стране многие системы здравоохранения выступают с инициативами по стандартизации обработки медицинских изделий во всей своей системе.В рамках этих усилий по стандартизации менеджеры по стерильной обработке и / или специалисты по профилактике инфекций обычно определяют все различные места, где выполняется повторная обработка устройств в их системе, и работают над тем, чтобы общие политики и процедуры были приняты в масштабах всей системы. 3M Sterilization Tech Line часто получает информацию от систем, которые недавно обнаружили или приобрели клиники, использующие настольные паровые стерилизаторы. Мы также часто обсуждаем с клиниками, которые стремятся внедрить передовой опыт.У обеих групп есть вопросы о соответствующих процедурах контроля качества стерилизации. В этой статье будут рассмотрены методы контроля качества, характерные для настольных стерилизаторов, представленные в недавно опубликованном AAMI ST79: 2017.
Совместная комиссия
Одним из факторов, побуждающих системы здравоохранения стандартизировать обработку устройств в масштабах всей системы, является Стандарт IC 02.02.01 Объединенной комиссии, который гласит: «Больница снижает риск инфекций, связанных с медицинским оборудованием, устройствами и расходными материалами.” 2 Обоснование этого стандарта основано на риске инфицирования пациентов в случае неправильной очистки и стерилизации медицинских устройств. Стандарт рекомендует внедрение стандартных процессов по адресу:
- «Ориентация, обучение и компетентность медицинских работников, занимающихся обработкой медицинского оборудования, устройств и расходных материалов.
- Уровень укомплектования персоналом и надзор за медицинскими работниками, которые обрабатывают медицинское оборудование, устройства и расходные материалы
- Стандартизация процесса независимо от того, централизованный он или децентрализованный
- Усиление процесса (например, использование табличек, на которых перечислены шаги, которые необходимо выполнить в соответствии с инструкциями производителя)
- Постоянный контроль качества » 2
Центры по контролю за заболеваниями
Признавая возможность улучшения практики профилактики инфекций вне больниц, в 2016 году CDC опубликовал версию 2. 3 их краткого руководства, озаглавленного «Руководство по профилактике инфекций в амбулаторных условиях: минимальные ожидания для безопасного ухода». “ 3 Сопутствующий Контрольный список для профилактики инфекций в амбулаторных условиях (включен в документ как Приложение A) напоминает читателю, что:
3 их краткого руководства, озаглавленного «Руководство по профилактике инфекций в амбулаторных условиях: минимальные ожидания для безопасного ухода». “ 3 Сопутствующий Контрольный список для профилактики инфекций в амбулаторных условиях (включен в документ как Приложение A) напоминает читателю, что:
- «Важнейшие предметы (например, хирургические инструменты) — это предметы, которые попадают в стерильные ткани или сосудистую систему и должны быть стерильными перед использованием».
- «Очистка всегда должна выполняться перед стерилизацией и / или дезинфекцией.”
- «Одноразовые устройства (SUD) маркируются производителем для одноразового использования и не имеют инструкций по обработке. Их нельзя перерабатывать для повторного использования, за исключением организаций, которые выполнили нормативные требования FDA и получили разрешение FDA на переработку определенных SUD ». 3
Контрольный список может быть использован специалистами в офисе для проведения самопроверки повторной обработки устройств многократного использования. В дополнение к пунктам контрольного списка, относящимся к контролю качества стерилизатора, более общие вопросы о повторной обработке устройств включают:
- «Политики, процедуры и инструкции производителя по переработке медицинских изделий многократного использования, используемых на предприятии, доступны в зоне (ах) обработки.
- HCP {Медицинский персонал], ответственный за переработку медицинских устройств многократного использования, проходит практическое обучение по правильному выбору и использованию СИЗ, а также по рекомендуемым шагам для обработки назначенных устройств: i.При аренде, до получения разрешения на переработку устройств ii. Ежегодно iii. Когда вводятся новые устройства или меняются политики / процедуры.
- После очистки инструменты соответствующим образом оборачиваются / упаковываются для стерилизации (например, выбранная система упаковки совместима с выполняемым процессом стерилизации, предметы правильно помещаются в корзину, полку или тележку стерилизатора, чтобы не препятствовать проникновению стерилизатора.
 стерилизатора, инструменты на шарнирах открыты, инструменты разбираются, если это указано производителем).
стерилизатора, инструменты на шарнирах открыты, инструменты разбираются, если это указано производителем). - Стерильные упаковки маркируются номером загрузки, который указывает используемый стерилизатор, цикл или номер загрузки, дату стерилизации и, если применимо, срок годности.
- После стерилизации медицинские изделия и инструменты хранят так, чтобы стерильность не нарушалась ». 3
Полный контрольный список доступен бесплатно по ссылке, указанной в ссылке 3 в конце этой статьи. Почему бы не запланировать на этой неделе время для проведения самопроверки?
Стандартное снятие нагрузки
Все паровые стерилизаторы, используемые для обработки предметов ухода за пациентами, включая настольные паровые стерилизаторы в офисных помещениях, должны регулярно контролироваться с помощью различных инструментов мониторинга, включая физические мониторы, химические индикаторы (ХИ), биологические индикаторы (БИ). , и устройства для обработки вызовов (PCD).Персонал, работающий с настольными паровыми стерилизаторами, должен сознательно принимать решение о выпуске каждой загрузки на основе результатов этих инструментов мониторинга.
Физические мониторы — это диаграммы, датчики и распечатки на оборудовании, которые обеспечивают измерения времени, температуры и давления в реальном времени. Физические мониторы проверяют правильность параметров цикла стерилизации и сообщают оператору, был ли выбран правильный цикл стерилизации. После каждого цикла обученный и знающий оператор должен прочитать и запустить распечатку цикла, чтобы убедиться, что был выбран правильный цикл и цикл прошел правильно.AAMI ST79, раздел 13.5.1 гласит: «Стерилизаторы, не имеющие записывающих устройств, не должны использоваться, за исключением стерилизаторов, используемых вместе с дополнительными записывающими устройствами или распечатками». 1
Самооценка
Ваш стерилизатор оборудован принтером? Если нет, можно ли его приобрести как аксессуар?
Внешние КЭ используются для того, чтобы с первого взгляда отличить обработанные медицинские устройства от необработанных. Индикаторная лента паровой стерилизации является примером внешнего химического индикатора. Раздел 13.5.2.2.1 AAMI ST79 рекомендует, чтобы все пакеты имели внешний CI типа 1, если внутренний CI не является видимым. Если внешний CI не изменен, пакет использовать не следует. Внутренние КИ подтверждают, что пар проник к инструментам внутри каждой упаковки. Раздел 13.5.2.2.2 стандарта AAMI ST79 рекомендует: «Один или несколько внутренних химических индикаторов должны быть помещены в каждую упаковку, лоток или жесткий контейнер.Эти индикаторы могут быть любого типа (Тип 3, 4, 5 или 6), но предпочтительно индикатор Типа 5 или Типа 6, потому что эти типы КИ предоставляют пользователю дополнительную информацию о критических параметрах стерилизации паром ». 1 Результаты внутренних КЭ должны интерпретироваться обученными и знающими специалистами в области здравоохранения в месте использования до того, как предметы будут использоваться для ухода за пациентом. Если внутренний CI не показывает приемлемого результата, элементы в пакете использовать не следует.
Индикаторная лента паровой стерилизации является примером внешнего химического индикатора. Раздел 13.5.2.2.1 AAMI ST79 рекомендует, чтобы все пакеты имели внешний CI типа 1, если внутренний CI не является видимым. Если внешний CI не изменен, пакет использовать не следует. Внутренние КИ подтверждают, что пар проник к инструментам внутри каждой упаковки. Раздел 13.5.2.2.2 стандарта AAMI ST79 рекомендует: «Один или несколько внутренних химических индикаторов должны быть помещены в каждую упаковку, лоток или жесткий контейнер.Эти индикаторы могут быть любого типа (Тип 3, 4, 5 или 6), но предпочтительно индикатор Типа 5 или Типа 6, потому что эти типы КИ предоставляют пользователю дополнительную информацию о критических параметрах стерилизации паром ». 1 Результаты внутренних КЭ должны интерпретироваться обученными и знающими специалистами в области здравоохранения в месте использования до того, как предметы будут использоваться для ухода за пациентом. Если внутренний CI не показывает приемлемого результата, элементы в пакете использовать не следует.
Самооценка
Полагаться на предварительно напечатанный химический индикатор на отслаиваемых пакетах для внутреннего CI? Если это так, обратитесь к производителю, чтобы убедиться, что это CI типа 5 или 6.В противном случае, как рекомендовано AAMI ST79, поместите дополнительный CI в каждый пакет.
Биологические индикаторы (BI) содержат большую популяцию живых спор, которые обладают высокой устойчивостью к процессу стерилизации. В случае паровых стерилизаторов рекомендуется использовать БИ, содержащие спор Geobacillus stearothermophilus . Раздел 13.5.3.1 AAMI ST79 гласит: «Биологические индикаторы — единственное устройство для мониторинга процесса стерилизации, которое обеспечивает прямую оценку летальности процесса стерилизации.” 1 Автономные БИ состоят из спор на носителе и ампулы со средой для выращивания, заключенных во внешнюю оболочку. После стерилизации BI активируется (подвергая споры воздействию питательной среды) и инкубируется. Если микроорганизмы не могут расти в течение указанного периода инкубации, регистрируется отрицательный результат и делается вывод, что процесс стерилизации прошел успешно. Проконсультируйтесь с производителями стерилизатора и BI, чтобы убедиться, что вы используете подходящий BI для тестируемого цикла (ов) настольного стерилизатора.Использование биологических индикаторов с быстрым считыванием данных облегчает выполнение биологических тестов и документирование прямо в клинике в течение нескольких часов.
После стерилизации BI активируется (подвергая споры воздействию питательной среды) и инкубируется. Если микроорганизмы не могут расти в течение указанного периода инкубации, регистрируется отрицательный результат и делается вывод, что процесс стерилизации прошел успешно. Проконсультируйтесь с производителями стерилизатора и BI, чтобы убедиться, что вы используете подходящий BI для тестируемого цикла (ов) настольного стерилизатора.Использование биологических индикаторов с быстрым считыванием данных облегчает выполнение биологических тестов и документирование прямо в клинике в течение нескольких часов.
Регулярные испытания эффективности стерилизатора
Чтобы гарантировать, что они могут эффективно стерилизовать медицинские изделия, все стерилизаторы должны регулярно проверяться с помощью BI PCD. AAMI ST79 рекомендует использовать BI PCD еженедельно и предпочтительно каждый день использования стерилизатора. Хотя частота рутинного тестирования BI PCD является элементом, который крупные системы могут попытаться стандартизировать, сам BI PCD не может быть стандартизован.Для настольных стерилизаторов пользователь создает PCD, представляющий тип упаковки или лотка, которые обычно обрабатываются (см. AAMI ST79, раздел 13.7.3). PCD должен содержать как BI, так и CI, и предметы, обычно присутствующие в упаковке или лотке. Каждый используемый тип цикла должен быть протестирован. Например, если стерилизатор используется для обработки небольших упакованных пакетов при температуре 250 ° C (121 ° F) и упакованных предметов при температуре 270–275 ° F (132–135 ° C), каждый цикл следует тестировать с помощью типичного BI PCD. PCD помещается с полной нагрузкой в «холодную точку», обычно в центре нагрузки.AAMI ST79, раздел 13.7.3.2, рекомендует размещать PCD «на краю, если это маленькая упаковка, или плоской, если это лоток или большая упаковка». 1 В дополнение к стандартному тестированию эффективности, BI PCD следует использовать в каждой партии, содержащей имплантаты, и имплантаты должны быть помещены в карантин до тех пор, пока не станет известен результат BI.
Сбои в процессе стерилизации
На сбой процесса стерилизации может указывать отказ физического монитора, отказ CI от PCD или положительный результат тестового BI.AAMI ST79 предоставляет руководство по действиям, которые следует предпринять при расследовании сбоя процесса стерилизации, в Разделе 13.7.5. В этом разделе говорится: «Если причину сбоя не удается сразу определить, нагрузку следует поместить в карантин и отозвать все нагрузки, вернувшиеся к последнему отрицательному BI. Элементы в этих партиях следует по возможности извлекать и повторно обрабатывать (см. 13.7.5.2). Данный стерилизатор следует вывести из эксплуатации до тех пор, пока не будет выявлена и устранена причина неисправности ». 1 Многие клиники учитывают влияние отзыва при определении частоты мониторинга BI.
Документация
Процесс контроля качества стерилизатора включает в себя задачи по документации. Каждая упаковка должна соответствовать загрузке, в которой она была стерилизована. Обычно это достигается путем маркировки каждой упаковки контрольным номером партии, включая дату стерилизации, номер стерилизатора и номер загрузки. AAMI ST79 рекомендует записывать и хранить следующую информацию для каждого цикла стерилизации:
- номер лота;
- конкретное содержимое партии или груза;
- — время воздействия и температура, если они не указаны в таблице записи стерилизатора;
- наименование или инициалы оператора;
- результаты биологического тестирования, если применимо;
- — результаты тестирования Боуи-Дика, если применимо;
- — ответ CI, помещенного в BI PCD, если применимо; и
- — любые отчеты о неубедительных или неотвечающих КЭ, обнаруженные позже в загрузке. 1
Как упоминалось ранее, лента принтера стерилизатора должна быть проверена и подписана оператором.
В дополнение к записям цикла стерилизации, AAMI ST79 рекомендует вести записи обслуживания для каждого стерилизатора. Руководство по эксплуатации стерилизатора должно содержать указания по текущему уходу, профилактическому обслуживанию и калибровке стерилизатора. Протокол технического обслуживания может быть в бумажном или электронном формате и должен обеспечивать непрерывную историю всех запланированных и внеплановых услуг.(Раздел 12.7)
Независимая оценка / аудит
Обсуждая необычные методы обработки устройств, мы иногда слышим: «Потому что мы всегда так поступали». Хотя самопроверки могут быть очень полезными, иногда свежая группа экспертов, оценивающих методы обработки устройств в клинике, может помочь определить возможности для улучшения. Фактически, в 2015 году CDC выпустил предупреждение CDCHAN-00383, в котором рекомендовалось: «Медицинским учреждениям следует нанять медицинского специалиста, обладающего опытом обработки устройств, для немедленной оценки их процедур обработки.Эта оценка должна гарантировать правильность повторной обработки, в том числе предоставить персоналу, занимающемуся переработкой, достаточно времени для выполнения всех шагов, рекомендованных производителем устройства ». 4 Итак, для тех клиник, которые являются частью более крупной системы здравоохранения, если «они» еще не нашли вас, возможно, пришло время поднять руку и пригласить эксперта учреждения для ознакомления с вашей практикой стерилизации.
Сводка
Критические устройства необходимо стерилизовать перед использованием. Настольные паровые стерилизаторы играют ключевую роль в стерилизации устройств в офисных медицинских и стоматологических клиниках.Поэтому методы контроля качества настольных стерилизаторов в клиниках заслуживают того же внимания к деталям, что и в отделениях стерильной обработки больниц и амбулаторных хирургических центров. К счастью, AAMI ST79 предоставляет руководство по тестированию и документированию результатов тестирования паровых стерилизаторов, используемых в клиниках. Комплексная программа контроля качества включает рутинное тестирование эффективности стерилизатора, стандартную загрузку (с использованием физических мониторов, CI и BI PCD), квалификационные испытания и надлежащую документацию.Органы по аккредитации продолжают уделять пристальное внимание повторной обработке устройств, где бы она ни проводилась. Чтобы начать подготовку к следующему аккредитационному обследованию, воспользуйтесь бесплатным «Контрольным списком профилактики инфекций для амбулаторных больных: минимальные ожидания для безопасного ухода» от CDC 3 , чтобы оценить соответствие вашего учреждения рекомендуемым методам обработки устройств.
Обычная стерилизация
вопросы контроля качества из настройки клиники
В.Следует ли нам использовать коммерческий пакет тестов BI, как это делает главная больница, для тестирования
наш настольный стерилизатор?
А. Нет,
коммерчески доступные предварительно собранные устройства проверки процесса бизнес-аналитики (BI PCD) являются
эквивалентны по вызову PCD с 16 полотенцами и используются для контроля стерилизаторов
больше 2 кубических футов. Не существует стандартизированного предварительно собранного PCD для
настольные стерилизаторы. Раздел 13.7.3 AAMI ST79 рекомендует использовать
репрезентативной PCD, то есть, что пользователь создает PCD того же типа
пакет или лоток, которые обычно обрабатываются в стерилизаторе.Например,
если типичная нагрузка в клинике состоит из инструментов, упакованных в пакеты для пилинга,
тогда соответствующий BI PCD будет состоять из BI, CI и представителя
инструмент помещен в мешочек для кожуры.
В. Как часто мы должны проверять стерилизатор с помощью биологического индикатора?
А. ААМИ
ST79 рекомендует рутинный мониторинг эффективности стерилизатора с помощью BI PCD.
проводится еженедельно, но предпочтительно каждый день использования стерилизатора. Наиболее
Настольные стерилизаторы имеют несколько вариантов цикла, и AAMI ST79 рекомендует
тестирование каждого используемого типа цикла.Любые грузы, содержащие имплантаты, также должны
контролироваться с помощью BI PCD, а имплантат должен быть помещен в карантин до тех пор, пока BI
результат имеется. В случае сбоя процесса стерилизации AAMI
рекомендует отозвать все нагрузки до последнего отрицательного биологического
индикатор. Многие учреждения предпочитают проводить мониторинг чаще, чем рекомендует AAMI.
чтобы обеспечить единообразный уход за пациентами и избежать сложных и дорогостоящих отзывов, которые могут
включать уведомления врача и пациента.
В. Следует ли проводить тест Боуи-Дика в нашем настольном стерилизаторе?
А. А
Испытание типа Боуи-Дика используется для проверки способности пара с динамическим удалением воздуха.
стерилизатор для удаления воздуха из камеры и предотвращения повторного вовлечения воздуха. Ежедневно
Следовательно, испытание Боуи-Дика не требуется для столешницы с гравитационным смещением.
паровые стерилизаторы. Многие настольные стерилизаторы обладают функцией динамического удаления воздуха и
использовать либо импульс давления с продувкой паром (SFPP), либо метод предварительного вакуума
удаление воздуха. В этом случае циклов SFPP AAMI ST79 предлагает проконсультироваться с
производителя стерилизатора, чтобы определить, рекомендуется ли ежедневный тест Боуи-Дика.
В. Что такое контрольный BI? Где взять контрольную BI?
A. A управление
BI — это биологический индикатор из той же партии, что и для
тестирование стерилизатора, который не подвергается воздействию стерилизатора и инкубируется до
проверьте жизнеспособность спор, правильную температуру инкубации
инкубатор, а также способность питательной среды поддерживать рост спор.
Положительный контроль следует инкубировать каждый день, пока инкубируется тест BI.В
контрольный БИ должен давать положительный результат, чтобы результат теста
BI считается действительным.
Практическое применение: будет использоваться минимум два биологических индикатора каждый.
день испытания настольного стерилизатора. Один БИ служит контролем и принимается
прямо из коробки, активируется и инкубируется. Другой «тестовый» БИ помещается в
репрезентативный PCD, обработанный с полной загрузкой, затем активированный и инкубированный
следуя инструкциям производителя BI. Критерии приемлемости для этого
стандартное тестирование включает положительный результат для положительного контроля BI и
отрицательный результат по тесту БИ.
В. Как мы квалифицируем наш новый настольный стерилизатор?
A. Квалификация
тестирование настольных стерилизаторов следует проводить после стерилизации.
установка, перемещение, неисправности, капитальный ремонт и процесс стерилизации
неудачи. Как и при обычном тестировании, выбираются репрезентативные BI PCD и
собран. BI PCD помещается в «холодное пятно» камеры и запускается в
три последовательные полные нагрузки. Загрузить предметы из трех квалификационных заездов
следует помещать в карантин до получения отрицательных результатов BI.Для динамического удаления воздуха
настольные стерилизаторы, уточните у производителя, рекомендуют ли они
это квалификационное тестирование также включает три последовательных цикла с
Набор тестов Боуи-Дика. Критерии приемки включают распечатки стерилизатора.
с указанием полных циклов, соответствующих результатов химических индикаторов и отрицательных
результаты тестов BI. 1
В. Как добиться прослеживаемости грузовых единиц?
А. ААМИ
ST79 рекомендует маркировать каждую единицу контрольным идентификатором партии до
стерилизация.Наклейка загрузки может использоваться для документирования идентификационного номера стерилизатора;
дата стерилизации и номер цикла.
Скачать статью и протестировать ..
Артикул:
- Ассоциация развития медицинского оборудования. Подробное руководство по стерилизации паром и обеспечению стерильности в медицинских учреждениях. ANSI / AAMI ST79: 2017. Арлингтон (Вирджиния): AAMI, 2017.
- Совместная комиссия. Стандарты аккредитации больниц 2018.
- Центров по контролю и профилактике заболеваний.Руководство по профилактике инфекций в амбулаторных условиях: минимальные ожидания для безопасного ухода, 2016 г. Дата обращения: 6 декабря 2018 г. https://www.cdc.gov/infectioncontrol/pdf/outpatient/guide.pdf
- Центров по контролю и профилактике заболеваний. CDC / FDA Health Update о немедленной необходимости для медицинских учреждений пересмотреть процедуры очистки, дезинфекции и стерилизации многоразовых медицинских устройств. Дата обращения 6.12.2018. https://emergency.cdc.gov/han/han00383.asp
Управление отходами — Портал pSMILE
Приносим извинения за неудобства, но страница, к которой вы пытались получить доступ, находится не по этому адресу.Вы можете использовать приведенные ниже ссылки, чтобы помочь вам найти то, что вы ищете.
Если вы уверены, что имеете правильный веб-адрес, но столкнулись с ошибкой, пожалуйста,
связаться с Администрацией сайта.
Спасибо.
Возможно, вы искали…
Управление отходами
- Гематология Диаграмма Леви-Дженнингса СОП
- Ссылка на аудит: Раздел статей о тестировании и контроле
- Процедура построения карты CD4 Леви-Дженнингса
- Ссылка на аудит: Раздел
- Процедура построения диаграммы Леви-Дженнингса для химии
- Ссылка на аудит: Раздел
- СОП по контролю документов Anglo Lab
- Ссылка на аудит: Раздел
- Приложение A QSE 1 — Документы и записи
- Ссылка на аудит: Раздел управления качеством
- Приложение C QSE 3- Персонал.
- Ссылка на аудит: Раздел управления качеством
- SmartLab Tools: часто задаваемые вопросы
- Справка по аудиту — Раздел статьи о тестировании и контроле
Этот часто задаваемый вопрос предназначен для следующих документов: Рассчитать среднее значение, SD, CV%, контрольный диапазон -… - CAPRISA Lab Написание СОП и управление документами
- Ссылка на аудит: Раздел
- СОП по обучению и оценке компетентности
- Ссылка на аудит: организация и персонал
- Приложения и рекомендации по разработке плана управления качеством
- Ссылка на аудит: Раздел управления качеством
статей о тестировании и контроле
статей о тестировании и контроле
«Эксплуатация средств тестирования»
«Эксплуатация средств тестирования»
Применение модели управления специальностями улучшает контроль качества в центральном отделении стерильного снабжения | BMC Health Services Research
Дизайн исследования и участники исследования
Это ретроспективное исследование, в котором сравниваются 2 модели управления в нашей больнице.С сентября 2015 года по апрель 2016 года в нашей больнице применялась традиционная рутинная модель управления (описанная ниже), которая была выбрана в качестве контрольного лечения. В отличие от этого, модель управления наблюдением применялась на основе модели управления специальностями, которая применялась с июля 2016 года по февраль 2017 года. Специализированное устройство было определено как устройство, используемое одним конкретным клиническим отделением. Участниками исследования были медицинский персонал, выбранный случайным образом из следующих отделений: операционная, стоматология, гинекология, ортопедия, торакальная хирургия, хирургия мочевыводящих путей и общая хирургия.
В общей сложности 92 сотрудника были отобраны случайным образом, чтобы составить контрольную группу, и 100 сотрудников были случайным образом отобраны для группы наблюдения. Анкеты были отправлены контрольной группе в мае 2016 г. и группе наблюдения в марте 2017 г. Анкеты были разработаны на основе соответствующих исследований в литературе с некоторыми исправлениями, внесенными нашим центром [11, 12]. Всем набранным сотрудникам в периоды контроля и наблюдения было предложено ответить на нашу анкету.
Анкета была модифицированной версией, основанной на предыдущей работе Shan et al. [13] с хорошей надежностью и достоверностью (α Кронбаха = 0,978; достоверность = 0,963). Анкета в основном состояла из 3 областей (переработка, упаковка и стерилизация), включая 21 пункт, в которых участники оценивали свое удовлетворение услугами, предоставленными CSSD в течение предыдущих 6 месяцев. В ходе опроса участников просили ответить, выбрав одну оценку из пяти категорий, от «полностью удовлетворен» до «полностью не удовлетворен».Ответ «Полностью удовлетворен» получил 5 баллов, а «Совершенно не удовлетворен» — 1. Оценка удовлетворенности была суммой этих баллов. В анкете также были собраны данные об общей информации участников (возраст, пол, клиническое отделение, высший уровень образования и профессиональное звание). В нашей больнице все специалисты были разделены на 3 группы по профессиональному уровню: низкий, средний или высокий.
Мы также провели тестирование знаний и навыков среди профессиональных сотрудников ( n = 27) в марте 2016 г. и январе 2017 г. в периоды контроля и наблюдения, соответственно, в ЦСО.
Модели управления
Контрольная обработка
Для контрольной обработки (рутинное управление) CSSD состоял из 3 рабочих зон: очистки; стерилизация и упаковка; и стерильное хранение. К каждой зоне был назначен руководитель группы, который помогал главному руководителю ЦСО выполнить всю работу в зоне. Работающие специалисты в ЦСО были случайным образом распределены по разным рабочим зонам.
Лечение под наблюдением
Лечение под наблюдением (т.е., модель управления специальностями) дополнила традиционную модель различными модулями для улучшения контроля качества. На основании результатов оценки шкалы, связанной с медицинскими изделиями, в ЦСО специализированные медицинские изделия были разделены на 3 под-специальности: лапароскопические; стоматология; или аренда. Персонал в ЦСО был распределен по различным подгруппам специальностей на основе их профессионального звания, лет работы в ЦСО, высшего образовательного уровня, трудоспособности и личного желания.
Каждая подгруппа специализации взяла на себя полную ответственность за очистку, дезинфекцию, стерилизацию и упаковку медицинских изделий в рамках этой подспециализации. Специалисты CSSD в каждой группе работали в тесном сотрудничестве с соответствующими клиническими отделами. Клиницистов из соответствующих отделений регулярно приглашали для выступлений по клиническому использованию и обслуживанию конкретных медицинских устройств. Все члены подгруппы специализации работали в зоне очистки, а также в зоне стерилизации и упаковки.Смены между различными подгруппами специальностей происходили каждые 6–12 месяцев.
Статистический анализ
Размер выборки был рассчитан исходя из α = 5% и β = 90%. Увеличение степени удовлетворенности на ≥10 баллов было определено как клиническое улучшение; ожидаемый образец был ≥81. Принимая во внимание возможное 10% -ное отсутствие ответов, мы определили, что письмо-приглашение следует отправить ≥90 участникам.
t-тест использовался для сравнения возраста, оценки удовлетворенности, количества жалоб, степени повреждения устройства, оценки навыков и частоты ошибок.Тест хи-квадрат (χ2) применялся для сравнения уровня образования и профессионального уровня. Статистически значимым считалось двустороннее значение P <0,05. Все анализы проводились с использованием программного обеспечения SPSS 17.0 (SPSS, Чикаго, Иллинойс, США).
Контроль качества и обеспечение качества
Целью данного раздела не является полный обзор контроля качества стерильных продуктов или химических анализов и требований к лекарствам и вспомогательным веществам перед составлением рецептуры. Здесь представлены только те методы, которые важны либо для микробиологии, либо для подтверждения стерильности конечного продукта.
КАЧЕСТВО КОНТРОЛЬ И КАЧЕСТВО
ОБЕСПЕЧЕНИЕ
Это не
цель этого
раздел для обзора
полный контроль качества стерильных
продуктов или химических анализов и требований к лекарствам и вспомогательным веществам до
формулировка. Только те
методы, имеющие значение либо для микробиологии, либо для подтверждения стерильности конечного продукта
представлены здесь.
A) Бионагрузка
Следует
быть очевидным из
В предыдущих разделах говорилось, что успешный процесс стерилизации зависит от продукта, имеющего низкую бионагрузку перед стерилизацией. Это будет
также относиться к отдельным ингредиентам, которые должны
иметь низкий уровень микробного заражения, или есть
опасность, что
загрязнители будут
найти свой путь к конечному продукту или стать источником
пирогенов.
Стерилизация должна
обычно рассматривается как удаление бионагрузки, но высокая термостойкость бактериальных эндотоксинов означает, что успешная стерилизация паром не обязательно гарантирует
что продукт пропускает фармакопейный эндотоксин
тестовое задание; мертвые бактерии, вероятно, останутся пирогенными.
Недооценка
Уровень микробного загрязнения до завершения процесса стерилизации приведет к неправильному расчету требований к стерилизующей дозе для достижения желаемой SAL.Бионагрузка должна
поддерживаться в определенных
пределы для оправдания
выбранный процесс стерилизации. Когда выше
количество организмов или более
при производстве партий встречаются устойчивые микроорганизмы, чем было определено во время первоначальной валидации, т.е.
предполагается, что партии не
быть бесплодным. Бионагрузка является приблизительной.
от общего
жизнеспособное количество присутствующих микроорганизмов
перед стерилизацией и знание характеристик устойчивости
этих организмов часто является неотъемлемой частью
расчета гарантии стерильности.Строить
некоторая степень безопасности в
процесс стерилизации
должны быть установлены условия стерилизации для разрушения
всю бионагрузку, предполагая, что все
загрязняющий
микроорганизмы являются наиболее устойчивыми из видов, идентифицированных в этой бионагрузке. Гарантия стерильности, как подразумевается
в схемах, показанных на рисунках 22.1 и
22.2, может быть достигнуто только с
низкая бионагрузка и полностью проверенные, правильно работающие стерилизаторы.
B)
Тест
Для стерильности
Широкий
Основа теста на стерильность заключается в том, что он исследует
образцы конечного продукта
на наличие микроорганизмов.Теоретически тест на стерильность должен
применяться ко всем продуктам, обозначенным как стерильные. Однако тест не исследует
все образцы в партии и ее результаты
можно только считать действительным
если все позиции в партии
обрабатываются аналогично ( британских
Фармакопея , 2010 г.). Четко,
для продуктов, которые окончательно стерилизованы, это может
кажется разумным предположением, но только если
есть униформа
распределение тепла в автоклаве
или духовка с горячим воздухом
или единообразная доставка
дозы облучения.С
произведено в асептических условиях
продукты есть опасности, потому что не все предметы
в партии могли быть обработаны
так же. Успешный тест
только показывает, что
в пробах не было обнаружено микробного загрязнения
проверено по тесту
условия. Продление результата
на целую партию
требует уверенности в том, что каждый
единица в
партия была изготовлена таким образом, чтобы
также прошли проверку с большой долей вероятности.Это подчеркивает слабость теста.
на бесплодие и почему
элементы управления
процессов стерилизации
очень важны и, вероятно, имеют большую уверенность в подтверждении
стерильность замеса.
Однако испытание остается
один из немногих аналитических методов, проверяющих продукт на стерильность.
C) Параметрическое разрешение
Поскольку существуют значительные ограничения теста на стерильность, многие органы власти помещают
значительная опора на
проверка и надежная работа стерилизаторов и их циклов стерилизации.Параметрический выпуск занимает
эта уверенность — еще один шаг вперед, позволяя партиям
окончательно стерилизованных продуктов, подлежащих выпуску
не подвергаясь испытаниям
на бесплодие. Цикл стерилизации
будет подтверждено наличие SAL 10 −6 или меньше как минимум
коэффициент безопасности. Валидационные исследования будут включать
распределение тепла, проникновение тепла, бионагрузка, закрытие контейнера
и исследования летальности цикла.
Чтобы продукт подлежал параметрической
выпуск, предстерилизационные испытания бионагрузки на каждую партию
будет завершена, и сравнительная устойчивость изолированных спорообразователей проверена.Каждый цикл будет
включать использование химических
или биологические индикаторы. Есть надежда, что эти действия обеспечат значительно более высокую
уровень гарантии стерильности, чем обеспечивается испытанием на
бесплодие. Этот
требует подтверждения, что
каждая часть
производственный процесс
удовлетворительно завершена, первоначальная бионагрузка перед стерилизацией находится в согласованных пределах, что
контроль цикла стерилизации был удовлетворительным, и правильное время
циклы были достигнуты.На практике параметрический выпуск
следует использовать только после накопления опыта
на надежно контролируемом и адекватно подтвержденном процессе
и где отношения были
подтверждено между тестированием конечного продукта и производственным мониторингом.
Очевидно,
воспроизводимость,
Требуются регулярный мониторинг и документация. Однако параметрический
освобождение означало бы отказ от испытания на стерильность,
вариант, которого у многих производителей еще нет
принято, возможно, из-за боязни судебного разбирательства
исходя из того, что любой стерильный
продукт при тестировании имел бы
прошел испытание на стерильность.
D)
Пирогены
Открытие, что
водные растворы могут привести к повышению температуры тела при введении пациенту еще в 19 веке. Агенты, ответственные за эту лихорадку
были названы «пирогенами». Теоретически пироген — это любое вещество, которое при введении
в млекопитающее, вызывает повышение температуры тела и вырабатываемые вещества
некоторыми грамположительными бактериями, микобактериями, грибами, а также вирусами соответствуют
к этому определению.Самый распространенный
пирогены, однако, и те, которые имеют большое значение для
фармацевтической промышленности, производятся грамотрицательными
бактерии и известны
как эндотоксинов ; они липополисахариды (ЛПС)
найдено в
клеточная оболочка. В
присутствие пирогенов в водных растворах было первым
продемонстрировано путем инъекции кроликам, чьи
регистрировалась температура тела. С тех пор были разработаны более чувствительные методы, в основном основанные на открытии того факта, что часть крови подковообразного краба вступает в реакцию.
с ЛПС в качестве
свертывающий агент.
Две фармакопеи
существуют предельные тесты.
Что для пирогенов используют кролики для оценки фармакологической
активность и, следовательно, наличие пирогенов всех видов.
В тесте на бактериальные эндотоксины используется лизированный
амебоциты (клетки крови) подковообразного краба, поэтому его называют
тест на лизат амебоцитов (LAL) Limulus . Это может быть распространено на многие лекарственные препараты и устройства.
и явно будет развиваться в будущем
оценить
наличие эндотоксинов в биотехнологических продуктах.
i) Физиологические эффекты пирогенов
Самый характерный
эффект после инъекции пирогенов человеку
рост тела
температура, но это только одна из нескольких
дозозависимых разнообразных эффектов. Пирогены повышают
циркулирующие уровни
воспалительных цитокинов, которые могут сопровождаться лихорадкой,
коагуляция крови,
гипотензия, лимфопения, нейтрофилия, повышенный уровень кортизола в плазме и белков острой фазы.Низкие дозы пирогенов вызывают бессимптомные воспалительные реакции. Умеренные дозы вызывают
лихорадка и изменение состава плазмы. Введение высоких пирогенных доз вызывает шок, характеризующийся дисфункцией сердечно-сосудистой системы, расширением сосудов и др.
сужение сосудов, дисфункция эндотелия и множественные
органная дисфункция или отказ и смерть.
ii) Характеристики бактериального эндотоксина
Выпуск ЛПС от
бактерии имеют место
после смерти и лизиса.Много
Грамотрицательные бактерии, например Escherichia coli и Proteus,
Виды Pseudomonas, Enterobacte r и Klebsiella производят пирогенный ЛПС, который состоит из двух
основные части: гидрофильная полисахаридная цепь с антигенными участками, и
гидрофобный липид
группа, названная липидом А, ответственная за многие биологические активности. Молекулярный
размер полисахаридной цепи очень варьируется, и, следовательно, молекулярная масса LPS может варьироваться от нескольких тысяч
до нескольких миллионов дальтон.LPS
необычайно термостабилен и чувствителен к изменениям pH. Молекулы способны выдерживать 120 ° C более
3 часа. Для быстрого разрушения ЛПС требуются крайние значения pH.
iii)
Источники
Источники
пирогенов в продуктах для парентерального введения включает воду, используемую в конце
стадии очистки и
кристаллизация препарата или вспомогательных веществ; вода
используется при обработке; компоненты упаковки; и
химикаты, сырье
или оборудование, использованное при приготовлении
товар.Наличие эндотоксинов на устройствах может быть
приписывается воде
в процессе производства промывка таких компонентов, как фильтр
СМИ, которые будут использоваться
для изготовления фильтров или промывки / ополаскивания трубок или других
пластиковые устройства приор
их стерилизации. Кроме того, если препарат биологически произведен, неполное удаление микроорганизмов при очистке
может привести
в высоких уровнях эндотоксина.
iv)
Измерение пирогенов
Пирогенов есть
традиционно оценивалась с использованием кроликов, которых бережно хранят в
контролируемые условия и чьи
температура контролируется перед введением тестируемого продукта. Британская фармакопея (2010) описывает тест изначально
на основе трех кроликов;
число постепенно увеличивается, если результаты
находятся между двумя значениями (таблица 22.4). Образцы
тестируемого продукта вводятся
в маргинальное
ушная вена в дозе не более
10 мл / кг. За животными наблюдают в течение 3 часов сразу после инъекции с 30-минутными интервалами. Тест предполагает, что
будет обнаружен максимальный рост температуры
в эти 3 часа
период сразу после инъекции.В таблице 22.4 описаны критерии прохождения или неудачи в виде числа.
использованных кроликов увеличивается до максимума
из 12.
Номер
ограничений кролика
пирогенный тест. Повторное использование животных приводит
к толерантности к эндотоксинам. Низкая реактивность по отношению к эндотоксину, продуцируемому некоторыми
виды, например Легионелла .Там
также изменчивость
в результатах контроля
при использовании идентичных стандартизированных препаратов эндотоксина, что
вероятно, связано с межлабораторными факторами и вариациями из-за сезона, вида кроликов
и другие биологические источники. Необходимо соблюдать осторожность при тестировании радиофармпрепаратов,
и некоторые лекарства
могут сами выявить
повышение температуры при администрации. Следовательно, этот тест не подходит для радиофармпрепаратов.
химиотерапевтические агенты против рака, снотворные и наркотические средства, витамины, стероиды и некоторые
антибиотики.Наличие пирогенов может быть скрыто
по фармакологической активности компонентов продукта. Наконец, тест на кроликах недостаточно чувствителен для обнаружения эндотоксина в интратекальных продуктах.
где только низкий уровень пирогенов
приемлемы.
EMA (2009 г.)
поощрять замену теста на кроликах на
тест активации моноцитов (Hoffmann,
2005) для лекарственных средств, полученных из плазмы.
Моноциты человека из культивированных
клеточные линии имитируют реакцию лихорадки человека in vitro
, продуцируя цитокины.Высвобождение цитокинов можно определить, как правило, с помощью иммуноферментного анализа (ELISA).
в)
Измерение бактериальных эндотоксинов
Тест LAL значительно больше
чувствительнее, чем пирогенный тест. Как указано выше,
хотя Legionella
Эндотоксин не очень пирогенен для кроликов, его легко обнаружить с помощью теста LAL.Это было
по оценкам, существует 1000-кратная разница в чувствительности между
два теста, но только тест LAL
обнаруживает эндотоксины грамотрицательных бактерий
и не все пирогены. Однако LAL
тест может быть использован
для радиофармпрепаратов.
LAL тестовый реагент
происходит от американского подковообразного краба Limulus
полифем. Свертывание крови, вызванное эндотоксинами, основано на ферментно-опосредованном взаимодействии.
ЛАЛ с эндотоксинами.Реагенты получают из крови только что отловленных.
подковообразные крабы, чьи
амебоциты концентрируются, промываются
и лизируется водой, не содержащей эндотоксинов. LAL отделен
от оставшегося клеточного мусора и его активность оптимизирована
с использованием катионов металлов, регулирования pH и
добавки, а затем
сублимированный. Некоторые препараты препятствуют взаимодействию КЛЛ и эндотоксина. Химическая
ингибиторы могут вызвать хелатирование
двухвалентные катионы, необходимые для реакции, денатурация белков
или несоответствующие изменения pH.Физическое ингибирование может быть результатом адсорбции эндотоксина или вязкости продукта.
Даже тип стеклянной посуды может повлиять на тест. Посуда из силиконизированного стекла или пластиковая банка
ингибировать образование гелевых сгустков или препятствовать получению точных спектрофотометрических показаний реакции
конечная точка.
Образцы
продуктов инкубируют с LAL при 37 ° C. Если эндотоксины
представить твердую
гелеобразные формы, свидетельствующие о наличии
эндотоксинов.Британская фармакопея
(2010) описывает шесть
отдельные методологии для
тест на эндотоксин. Эти
(A) гель-сгусток
предельный тест; (B) гельклот: полуколичественный; (C) турбидиметрический
кинетический метод; (D) хромогенный
кинетический метод; (E)
хромогенный метод конечных точек;
и (F) турбидиметрический метод конечной точки.
Есть проверки на наличие мешающих факторов. Любые проверенные
метод может быть использован, но гель-сгусток
Метод — это проверка рефери в случае возникновения спора.Цветные продукты не могут быть протестированы
турбидиметрическими и хромогенными
методы, так как образование осадка может быть ошибочно принято за
положительный ответ.
Кинетические методы LAL призваны повысить эффективность крупномасштабных испытаний,
вероятно, важно при валидации циклов депирогенизации
или подготовка компонентов для асептики
требуется обработка. Для всех процедур необходимо провести валидацию теста, чтобы исключить помехи, которые могут быть либо
торможение или усиление.Посуда из депирогенного стекла должна быть
используется повсюду.
Метод гель-сгустка
чаще всего используется. Тест проводится путем добавления реагента LAL.
к равному объему теста
раствор, перемешивание и хранение при 37 ° C в течение
1 час, когда
конечная точка определяется инверсией
трубок. Если твердый сгусток остается неповрежденным,
считается, что продукт содержит эндотоксины.
Хромогенные методы используют
колориметрия но не зависит
на свертывающийся белок.Синтетический субстрат
используется, содержащий амино
кислотная последовательность аналогична
коагулогену свертываемый
белок. Активированный
проклоттинг фермент расщепляет
p -нитроанилидный хромофор из
синтетическая подложка и цвет
продуцируется пропорционально количеству эндотоксина. Турбидиметрический
Метод LAL основан на том, что
что увеличение концентрации эндотоксина вызовет пропорциональное увеличение
в результате помутнения
путем осаждения свертывающегося белка, коагулогена.Оптическая плотность
считывается спектрофотометрически либо в фиксированное время, либо постоянно для кинетических анализов
по мере развития помутнения. Кинетические методы зависят от
соотношение между логарифмом
ответ и логарифм концентрации эндотоксина. Конечная точка
методы относятся к эндотоксину
уровни к количеству
хромофора высвобождено
или сумма
осадков.
vi)
Эндотоксины в
парентеральные фармацевтические препараты
Пределы
для эндотоксина основаны на дозе
продукта.Проще говоря, предел эндотоксина,
EL, которая представляет собой максимальное количество эндотоксина, допустимое в определенной дозе,
обратно связано
в дозе
Наркотик; это может быть оценено из
следующее уравнение ( Фармакопея США , 2010):
EL = К / М (2)
где K —
порог человека
пирогенная доза эндотоксина на кг тела
вес и M составляет
максимальная человеческая доза продукта в кг массы тела, которая будет вводиться
за 1 час
период. M признает, что фармакологические эффекты эндотоксина
дозозависимый. Предел эндотоксина — это
уровень, на котором
продукт
признано пирогенным или апирогенным. Чувствительность к реагентам гель-лота обычно находится в диапазоне
0,015–0,5 ЕЭ / мл. В качестве примеров пределов эндотоксинов:
США Фармакопея США (2010) устанавливает ограничения
не более 0,5 ЕС / мл для инфузии декстрозы, не более 5 ЕС / мг прометазина для инъекций прометазина
USP, не более 10 EU / мг митомицина в митомицине для
Инъекции USP и не более 24 ЕЭ / мг варфарина.
натрия в варфарине натрия для инъекций.Британская фармакопея
(2010) имеет ограничение
0,25 МЕ / мл
в внутривенной инфузии глюкозы; это
значение аналогично
для многих АД внутривенное
настои. Другой пример:
инсулин должен содержать
не более 10 МЕ / мг
эндотоксина. Предел эндотоксина для приема лекарств
доступ к спинномозговой жидкости
снижается до 0,2 ЕС / кг
потому что интратекальный путь является наиболее токсичным для эндотоксинов.
vii)
Депирогенизация и
Производство Апирогенных продуктов
Пирогены и эндотоксины
трудно удалить с продуктов, когда они присутствовали
и легче сохранить компоненты относительно свободными от эндотоксинов, чем удалять их из конечного продукта.Промывание или разбавление — один из способов
устранение пирогенной активности при условии полоскания
жидкость апирогенная. Закрытие
и флаконы следует промывать апирогенной водой.
перед стерилизацией. Пирогены во флаконах или стакане
компоненты могут быть разрушены стерилизацией сухим жаром при высоких температурах. А
Рекомендуемое условие для депирогенизации стеклянной посуды и оборудования — нагревание при 250 ° C в течение 45 минут.
Пирогены также разрушаются при 650 ° C за 1 минуту.
или при 180 ° C за 4 часа. Британская фармакопея (2010) утверждает, что сухой жар при
температура выше 220
° C может использоваться для
депирогенизация посуды. Стерилизационные туннели спроектированы
не только стерилизовать при 250–300 ° C, но и
удалить пирогены. Эти процессы приравниваются к сжиганию, хотя удаление
может использоваться промывание, также называемое разбавлением. Фильтрация, облучение или обработка оксидом этилена ограничены.
значение в снижении пирогенных или эндотоксиновых нагрузок.
Удаление
пирогенов из
Вода для инъекций может быть подвергнута дистилляции или обратному осмосу.Дистилляция — самый надежный метод удаления эндотоксина. уход
необходимо принять меры, чтобы избежать разбрызгивания в кубе, так как пирогены переносятся
по каплям. Другой источник
эндотоксинов — это система «Вода для инъекций». Как правило, циркуляция горячей воды при температуре выше 75 ° C обеспечивает
среда, которая
не способствует росту микробов
и, таким образом, формирование
эндотоксина. Циркуляция воды с температурой около 60 ° C вызывает некоторые опасения.
как некоторые грамотрицательные организмы, например.грамм. Легионелла
pneumophila , выживет и будет расти при 57 ° C. Системы производства воды
можно продезинфицировать циркулирующей водой при 75–80
° C.
Вода без пирогенов
может производиться с использованием ультрафильтрационной мембраны с номинальным
предел молекулярной массы, который
достаточно низкий, чтобы обеспечить удаление эндотоксинов при любых условиях. Пустой
мембраны из волоконного полисульфона можно дезинфицировать
с гидроксидом натрия, который эффективно разрушает пирогены.Номинальный
предел молекулярной массы 5000 Да должен эффективно
удалить эндотоксины. Однако многие продуцирующие эндотоксины
микроорганизмы размножаются при температуре окружающей среды. Вода для систем впрыска, особенно систем обратного осмоса (RO), в которых фильтры
не абсолютны
и могут использоваться последовательно для производства апирогенной воды.
Химические индикаторы подтверждают обработку инструментов во время цикла стерилизации
Крис Миллер, PHD
Стерилизация — это процесс, предназначенный для уничтожения всех микробов.В стоматологическом кабинете стерилизация в основном включает термическую обработку очищенных и упакованных инструментов в паровом автоклаве, стерилизаторе сухим жаром или ненасыщенном стерилизаторе химическим паром. Кроме того, в некоторых частях страны используются процедуры стерилизации для обработки определенных видов регулируемых отходов, образующихся в офисе, до их утилизации.
Мониторинг стерилизации включает оценку эффективности процесса стерилизации, чтобы можно было обнаружить и исправить проблемы с использованием или функционированием стерилизатора.Это помогает обеспечить безопасность пациента.
Три формы мониторинга стерилизации — это физический мониторинг, химический мониторинг и биологический мониторинг. Следует использовать все три типа мониторинга, поскольку каждый предоставляет разную информацию.
Физический мониторинг включает периодическое наблюдение за стерилизаторами во время их работы, чтобы убедиться, что манометры показывают правильную температуру и / или давление. Он также может оценить правильность времени цикла и прислушаться к необычным звукам, которые могут выявить проблему (например, шипение из парового автоклава может указывать на необходимость новой дверной прокладки).
Биологический мониторинг включает демонстрацию воздействия процесса стерилизации на споры живых бактерий, уничтожить которые труднее, чем все обычные болезнетворные микробы. Споры имеют форму полосок со спорами или флаконов со спорами, которые называются тестами на споры или биологическими индикаторами. После обработки в стерилизаторе их анализируют на наличие живых спор.
Несмотря на то, что эти споры обладают высокой устойчивостью к уничтожению, они обычно очень быстро уничтожаются в правильно функционирующем стерилизаторе.Хотя тестирование на споры является основной гарантией стерилизации, оно проводится только периодически (обычно еженедельно или ежемесячно). А на анализ теста на споры уходит от одного до семи дней. Таким образом, важно продолжать регулярный физический и химический мониторинг, который дает немедленные результаты.
Химический мониторинг в стоматологии включает использование термочувствительных химикатов, которые указывают на воздействие определенной температуры, сочетание температуры и времени или присутствие пара.Эти химические вещества меняют цвет или форму после соответствующего воздействия. Их реакцию на воздействие можно определить (наблюдать визуально) сразу после извлечения предметов из стерилизатора.
Индикаторы процесса — индикаторы процесса (также называемые индикаторами производительности) меняют цвет очень быстро после воздействия определенной температуры (например, 250 градусов по Фаренгейту). Примеры индикаторов процесса включают точки, стрелки или другие специальные отметки на стерилизационных пакетах, трубках и обертке.Другими примерами являются автоклавная лента, используемая для запечатывания упаковок и полосок или язычков, которые могут быть помещены внутрь обрабатываемых упаковок или кассет.
Поскольку индикаторы процесса быстро меняют цвет, они могут указывать только на то, что предмет подвергался воздействию температуры стерилизации (например, 250 градусов по Фаренгейту) в течение некоторого неизвестного времени. Они не могут указывать на то, что обработанные предметы стерильны.
Когда индикаторы процесса находятся на внешней стороне упаковки или обернутой кассеты, они могут показать, был ли предмет обработан в стерилизаторе.Пакеты, готовые к обработке в стерилизаторе, могут выглядеть точно так же, как уже обработанные. Таким образом, внешние индикаторы процесса могут быть единственным способом идентифицировать пакеты инструментов, которые готовы к использованию на пациентах, и предотвратить смешивание стерильных предметов с нестерильными предметами.
В стерилизационной комнате эти индикаторы подтверждают стерилизационному персоналу, какие упаковки были обработаны. Они также показывают другим сотрудникам, входящим в палату, какие пакеты готовы для использования пациентами.
Это может быть особенно важно, если человек, который обычно раздает стерилизованные предметы в кресле, недоступен, и другие должны забирать эти предметы из помещения для обработки инструментов. Простой взгляд на пакеты инструментов или кассеты, содержащие внешние индикаторы процесса, дает стоматологам, гигиенистам и ассистентам быструю уверенность в том, что установка соответствует требованиям и что поставленные инструменты действительно прошли термическую обработку.
Интеграторы — химическому интегратору (также называемому многопараметрическим индикатором) для изменения цвета требуется нечто большее, чем просто температура.Температура должна поддерживаться в течение определенного периода времени или должен присутствовать пар в дополнение к соответствующей температуре, чтобы произошло химическое изменение.
Таким образом, эти индикаторы предоставляют немного больше информации, чем индикаторы процесса. Они показывают, были ли достигнуты комбинации времени и температуры или времени, температуры и пара.
Внешние химические индикаторы идентифицируют упаковки, которые были обработаны и готовы к использованию с пациентами. Химические индикаторы, помещенные внутри упаковок или кассет (внутренние химические индикаторы), показывают, что подходящая температура или стерилизующий агент проник в упаковочный материал и достигли инструментов.
В текущих рекомендациях ADA по инфекционному контролю указано, что «индикаторы процесса должны использоваться при каждой загрузке». В текущих рекомендациях CDC говорится: «Простым и недорогим методом подтверждения проникновения тепла ко всем инструментам во время каждого цикла является использование химического индикатора внутри и в центре партии неупакованных инструментов или в каждой упаковке из нескольких инструментов; это процедуру рекомендуется использовать во всех стоматологических кабинетах ». Фонд исследования процедур безопасности и асептики офиса рекомендует, чтобы «химические индикаторы использовались внутри каждой упаковки во время каждой загрузки стерилизатора.»
Таким образом, использование химических индикаторов в сочетании с физическим и биологическим мониторингом является важной частью контроля качества для обеспечения безопасности пациентов, при условии, что выполняются другие аспекты обеспечения стерильности.
Крис Миллер — директор отдела исследований и услуг по инфекционному контролю и профессор биологии полости рта Университета Индианы
Методы контроля качества стерилизации медицинских инструментов Контроль качества стерилизации
В комплексе мер по стерилизации изделий медицинского назначения большое значение имеют организация и мониторинг его эффективности.Используемые до сих пор методы и средства контроля не всегда позволяют выявить дефекты стерилизации, что влечет за собой повышение уровня внутрибольничных инфекций.
Наиболее частыми ошибками при ручной очистке и дезинфекции являются. Откладывание этих процессов, что приводит к высыханию загрязняющих веществ, особенно на труднодоступных поверхностях. Для заключительного полоскания используйте обычную воду, которая вызывает отложение на инструментах.
Неправильный выбор моющих и дезинфицирующих средств, несовместимых с материалами, из которых изготовлены инструменты.Растворы дезинфицирующих средств недостаточной концентрации. Минимальная эффективная концентрация дезинфицирующих средств не контролируется регулярно.
Контроль эффективности стерилизационного оборудования осуществляется физическими, химическими и биологическими (бактериологическими) методами. Надежность этих методов неодинакова. Физико-химические методы предназначены для оперативного контроля и позволяют контролировать соблюдение параметров пара, газа, стерилизации воздуха, температуры, давления, выдержки.Недостатком этих методов является то, что они не могут служить доказательством эффективной стерилизации. Только бактериологический метод надежен для определения эффективности.
Процесс очистки и дезинфекции необходимо контролировать и контролировать соответствующим образом. Моющие средства для автоматической дезинфекции следует тестировать с помощью различных проверок валидации процесса. Эффективность очистки. Микробиологические показатели.
Дозирование химикатов. Качество воды. Провода. Рабочий цикл. Важно использовать объективные, стандартные и воспроизводимые методы контроля.Ежедневные тесты. Свободное движение форсунок. Еженедельные тесты. Испытания остатков.
Физические методы
Физические методы контроля осуществляются посредством измерения температуры (термометры, термопары), давления (манометры, мановакуумметры) и времени (таймеры). Современные стерилизаторы также оснащены записывающими устройствами, которые фиксируют индивидуальные параметры каждого цикла стерилизации.
Ежеквартальные тесты. Ежегодные испытания и переаттестация. Водный тест.Химическая дозировка. Термометры для термодезинфекции. Тщательная промывка и эффективная дезинфекция инструментов перед стерилизацией необходимы для обеспечения безопасности пациента во время операции. Неправильно очищенные инструменты и эндоскопы могут привести к инфицированию операционного поля и вызвать пирогенные эффекты.
После очистки и дезинфекции хирургические инструменты необходимо проверить на чистоту и качество работы, износ и работоспособность. При получении стерилизационного оборудования обычно невозможно контролировать износ и правильную работу инструментов, так как инструменты грязные и по соображениям безопасности необходимо вмешиваться.По этой причине трудно определить, что стало причиной отказа медицинского устройства. Событие может происходить в хирургическом отделении, во время транспортировки или в отделении стерилизации.
Химические методы
На протяжении десятилетий химические вещества использовались для проведения химического контроля, изменения их агрегатного состояния или цвета при температуре, близкой к температуре стерилизации (бензойная кислота для контроля паровой стерилизации, сахароза, гидрохинон и ряд других веществ для контроля стерилизации воздуха) .При изменении цвета и плавлении этих веществ результат стерилизации был признан удовлетворительным. Однако многолетние наблюдения и данные литературы показывают, что при удовлетворительных результатах химического контроля с использованием этих показателей бактериологический контроль в некоторых случаях (до 12%) выявляет неудовлетворительный результат стерилизации.
Независимо от того, где он был поврежден, система управления предназначена для поиска всех поврежденных инструментов, ссылок на них для ремонта, обслуживания или удаления, так что конечный пользователь имеет только безопасные и надежные инструменты.Хирургические инструменты должны быть упакованы в прямом или шарнирном положении, в открытом или сжатом положении, в хирургических наборах или по отдельности. Открытые шарнирные инструменты должны быть защищены от случайного закрытия, например, с помощью специальных корпусов для инструментов.
Кроме того, у этих веществ есть существенный недостаток. Их переход в другое агрегатное состояние не дает представления о продолжительности воздействия температуры, при которой они плавятся.
Учитывая недостаточную надежность использования этих индикаторов для мониторинга, а также значительную сложность и неудобство их практического применения, в 70-е годы были разработаны химические индикаторы, цвет которых меняется при воздействии принятой для этого температуры. режим, на время, необходимое для стерилизации.По изменению цвета этих индикаторов можно судить о том, что основные параметры процесса стерилизации — температура и время — поддерживаются. Многолетнее использование таких индикаторов показало их высокую надежность.
Метод упаковки должен позволять открывать упаковку в асептических условиях и обеспечивать стерильность продукта при использовании конечным пользователем. Просто, чтобы легко удалить содержимое, оберните бумажные пакеты, а также пакеты и мешочки из фольги. Сохранение размера упаковки обычно приводит к увеличению расхода материала и затрат, поскольку при открытии большие части продукта загрязняются, и их необходимо повторно стерилизовать или утилизировать.
Процессы стерилизации в больницах намного сложнее и, следовательно, более рискованны, чем ошибки в промышленности или аптеке. В больницах используются различные методы стерилизации: пар, оксид этилена, газовая плазма, перекись водорода, стерилизация параформальдегидом, надуксусной кислотой, горячим сухим воздухом. У каждого из этих методов есть ограничения и критические моменты. При стерилизации паром существуют различные способы удаления воздуха и водяного пара. Паровая баня обычно стерилизует комбикорма: пористые материалы, твердые инструменты, инструменты с подсветкой.
Более сложные индикаторы предназначены для контроля критических параметров процесса стерилизации. Критическими параметрами являются: для метода стерилизации паром — температура, время воздействия заданной температуры, насыщенный водяной пар; для метода стерилизации воздуха — температура и время воздействия заданной температуры; для методов газовой стерилизации — концентрация используемого газа, температура, время воздействия, уровень относительной влажности; для радиационной стерилизации — общая поглощенная доза.
Эффективность этого процесса зависит от контакта водяного пара со всеми поверхностями стерилизованных продуктов и материалов. Многие стерилизаторы, используемые в Польше, старше 10 лет. Часто они не оснащены системой записи параметров стерилизации или работают неточно. Такие стерилизаторы следует тщательно контролировать и контролировать.
Достижение температуры стерилизации, давления в камере, теоретической температуры пара во время экспонирования. Температура и давление в камере хотя бы для одной фазы цикла.В первом цикле одного из вышеперечисленных методов контроля и мониторинга недостаточно. Все эти методы следует использовать в каждом цикле стерилизации.
До конца 80-х не существовало стандартов на химические индикаторы, выпускаемых различными компаниями, и не было попыток их классифицировать. Только в 1995 году Международная организация по стандартизации (ISO) опубликовала документ «Стерилизация медицинских изделий. Химические индикаторы. Часть 1».
С января 2002 г. в России введен ГОСТ Р ИСО 11140-1 «Стерилизация медицинских изделий.Химические индикаторы. Общие требования ». В соответствии с этим документом химические индикаторы делятся на шесть классов.
Во многих больницах проблема заключается в обеспечении надлежащего функционирования стерилизатора. Отсутствие периодических проверок приводит к тому, что стерилизаторы не находятся в хорошем состоянии, калибруются датчики и магнитолы. Это может снизить эффективность процесса стерилизации. Снижение эксплуатационных расходов приводит к меньшему количеству контроллеров процесса и меньшему контролю.Чтобы гарантировать высокий уровень безопасности пациента, во многих странах проводится все больше и больше проверок для каждого цикла.
Из-за частой нехватки оборудования и хирургических инструментов стерильное хранилище обычно служит для кратковременного хранения материалов перед передачей конечному пользователю. Большинство больниц расположены в зданиях, приспособленных к их потребностям, или имеют необъяснимую конструкцию, что затрудняет распространение стерильных материалов. При транспортировке необходимо обеспечить стерильность упаковки.Не всякая упаковка подходит для перевозки в любых условиях.
Показатели 1-й класс являются показателями («свидетелями») процесса. Примером такого индикатора является термоиндикаторная лента, наклеенная перед стерилизацией на текстильную упаковку или стерилизационные коробки. Изменение цвета ленты указывает на то, что упаковка была стерилизована. Эти же индикаторы можно размещать в наборах хирургических инструментов или хирургическом белье.
Дополнительные функции безопасности, такие как.Транспортировка в закрытых контейнерах. Правильная транспортная маркировка. Деактивация транспортных средств. Неправильная дезактивация хирургического инструмента — серьезная проблема в любой больнице. Снижение количества внутрибольничных инфекций — цель всех больниц по всему миру. Перекрестное заражение после использования неправильно продезинфицированных хирургических инструментов часто является причиной широко распространенного инфекционного заболевания.
Неправильно обработанные хирургические инструменты, эндоскопы и другие медицинские материалы и устройства повышают риск заражения патогенными микроорганизмами и прионами.Разработайте подробные процедуры для каждого этапа подготовки инструментов и материалов, мониторинга и контроля всех процессов стерилизации, а также обучения персонала, занимающегося не только дезинфекцией, но и использованием стерильных медицинских изделий.
2-й класс индикаторов, предназначенных для использования в специальных процедурах тестирования, например, при проведении теста Боуи-Дика (Bowie-Dick test). Этот тест не контролирует параметры стерилизации; он оценивает эффективность удаления воздуха из камеры парового стерилизатора.
Показатели 3-й класс — показатели одного параметра. Они оценивают максимальную температуру, но не дают представления о времени ее воздействия. Примерами таких индикаторов являются описанные выше химические вещества.
Контроль устройств — это продукт, используемый для контроля надлежащего функционирования медицинских устройств путем контроля соблюдения установленного времени, температуры, давления, удаления воздуха, увлажнения и воздействия стерилизующего агента.
Контроль экспозиции дает оператору уверенность в том, что каждая упаковка была открыта, без необходимости открывать упаковку для проверки внутренней скорости или поиска пакета в результатах контроля партии.Химические индикаторы, размещенные на внешней упаковке, меняют цвет из-за воздействия стерилизатора. Хорошая практика требует, чтобы каждая стерилизованная упаковка имела индикатор воздействия. Рукава и стерилизационные пакеты обычно имеют внешний химический индикатор.
4 класс — Это многопараметрические индикаторы. Они содержат красители, которые меняют цвет в сочетании с несколькими параметрами стерилизации, чаще всего температурой и временем. Примером таких индикаторов являются тепловые индикаторы для контроля стерилизации воздуха.
5 класс — интегрирующие показатели. Эти индикаторы реагируют на все критические параметры метода стерилизации. Характеристика этого класса индикаторов сравнивается с инактивацией высокорезистентных микроорганизмов.
Другие типы стерилизационной упаковки требуют использования дополнительных индикаторов. Это наиболее важный метод мониторинга эффективности процессов стерилизации в больницах с использованием биологических индикаторов. Только использование спор бактерий, наиболее устойчивых к определенному стерилизующему агенту, гарантирует, что этот процесс эффективен с бактерицидной активностью.Эта информация не содержит физических или химических показателей, и это самая важная информация о цикле стерилизации.
Управление упаковками основано на использовании химических индексов внутри упаковок. Стандарты стерилизации требуют, чтобы стерилизационный персонал установил и применил все стандарты и стандарты, гарантирующие качество предоставляемых услуг. А также вести учет стерилизованных материалов, методов стерилизации, результатов контроля. Циклический регистр обеспечивает свидетельство стерилизации медицинских изделий и включает результаты проверки эффективности процесса стерилизации.Правильный регистр позволяет документировать весь процесс стерилизации.
6 класс — индикаторы, эмуляторы. Эти показатели должны реагировать на все контрольные значения критических параметров метода стерилизации.
Биологический метод
Наряду с физико-химическим применяется бактериологический метод стерилизационного контроля. Он предназначен для контроля эффективности стерилизационного оборудования. До недавнего времени образцы садовой почвы, содержащие микроорганизмы, обладающие высокой устойчивостью к стерилизующим факторам, использовались для контроля стерилизации паром и воздухом.Однако устойчивость микроорганизмов в разных образцах неодинакова, что не позволяет стандартизировать результаты контроля.
Контроль остатков протеина
Это должно позволить вам отслеживать путь возврата каждой разветвленной упаковки перед стерилизацией. Обеспечивает легкий отбор проб с труднодоступных поверхностей. Его эффективность основана на реакции на биурет и позволяет оценить количество белка по цветовой реакции. Тест на чистый белок очень прост в использовании.
Не прикасайтесь к прибору или тестируемой жидкости, чтобы исключить ошибочные результаты.После инкубации прочитайте результат, сравнив цвет теста с шаблоном.
- Нанесите на тампон 4 капли увлажняющего крема.
- Загрузите прибор тампоном.
- Вставьте пробирку с образцом в прибор и сильно нажмите, чтобы активировать образец.
- Встряхните боком в течение 5 секунд.
Если цвет зеленый, инструменты чистые. Если цвет фиолетовый или серый, значит, инструменты загрязнены.
В настоящее время для проведения бактериологического контроля используются биотесты, содержащие отмеренное количество спор тест-культур.Контроль эффективности стерилизации с помощью биотестов рекомендуется проводить 1 раз в 2 недели. В зарубежной практике принято применять биологическое тестирование не реже 1 раза в неделю.
В результате стерилизации материал теоретически свободен от жизнеспособных микроорганизмов. На практике этот материал определяется как тот, для которого вероятность нестерильности равна 1: тогда первая стерилизация была проведена с использованием пара и тепловой обработки. Стерилизация — это технологический процесс, который включает уничтожение всех, как вегетативных, так и споровых форм микроорганизмов.Стерилизаторы вызывают изменения в клетках за счет коагуляции, денатурации и окисления белка.
Это необратимые изменения, способствующие разрушению клетки. Отжиг или сжигание Отжиг используется для небольших предметов, таких как те, которые используются для микробных модификаторов, и состоит из пламени горелки на металлической части этого продукта для удаления микроорганизмов. В настоящее время все чаще используются разовые выбытия. Сжигание можно использовать для полного уничтожения загрязненных материалов, таких как больничные отходы.Однако по санитарным и экологическим причинам существуют альтернативы сжиганию медицинских отходов.
В некоторых случаях возникает необходимость проводить контроль с помощью биотестов каждой загрузки стерилизатора. В первую очередь, это стерилизация инструментов, используемых для проведения сложных хирургических вмешательств, требующих использования высоконадежных стерильных материалов. Каждая загрузка имплантируемых продуктов также должна подвергаться бактериологическому контролю. Более того, использование стерилизованных материалов откладывается до получения отрицательных результатов контроля.Рекомендуется придерживаться тех же принципов при определении периодичности контроля в отношении газовой стерилизации, которая более сложна по сравнению с другими методами.
Если наша статья была вам полезна, пожалуйста. Вам не потребуется никаких сложных действий, платежей или отправки SMS, звоните на номер
.
Методы контроля эффективности стерилизации
В комплексе мероприятий по стерилизации медицинских изделий важное значение имеют организация и контроль ее эффективности.Используемые до сих пор методы и средства контроля не всегда позволяют выявить дефекты стерилизации, что влечет за собой повышение уровня внутрибольничных инфекций. Контроль эффективности стерилизационного оборудования осуществляется физическими, химическими и биологическими (бактериологическими) методами. Надежность этих методов неодинакова. Физико-химические методы предназначены для оперативного контроля и позволяют контролировать соблюдение параметров пара, газа, стерилизации воздуха, температуры, давления, выдержки.Недостатком этих методов является то, что они не могут служить доказательством эффективной стерилизации. Только бактериологический метод надежен для определения эффективности.
Физические методы
Физические методы контроля осуществляются посредством измерения температуры (термометры, термопары), давления (манометры, мановакуумметры) и времени (таймеры). Современные стерилизаторы также оснащены записывающими устройствами, которые фиксируют индивидуальные параметры каждого цикла стерилизации.
Химические методы контроля
Использование химикатов или их комбинаций, которые меняют свое состояние или цвет под воздействием процесса стерилизации, называется химическим контролем. Вещества, используемые для контроля стерилизации, называются химическими индикаторами. Химические индикаторы могут реагировать на один, несколько или все критические параметры процесса стерилизации.
Индикаторы процесса (класс 1)
Индикаторы процесса предназначены для использования с продуктами или индивидуальной упаковкой (например, мешками, коробками), чтобы подтвердить, что эти продукты или упаковка прошли стерилизационную обработку.Они позволяют отличить стерилизованную продукцию (упаковку) от нестерилизованной.
Показатели для специальных испытаний (класс 2)
Эти индикаторы предназначены для использования в специальных тестах стерилизационного оборудования, определенных соответствующими стандартами. Самый распространенный индикатор этого класса — тест Боуи и Дика.
Однопараметрические индикаторы (класс 3)
Однопараметрические индикаторы должны реагировать на один из критических параметров и указывать на стерилизационную обработку, когда установлено значение выбранного параметра.
Многопараметрические индикаторы (класс 4)
Многопараметрические индикаторы стерилизации должны реагировать на два или более критических параметра и указывать на достижение заданных значений выбранных параметров во время стерилизации.
«Внешние» химические индикаторы класса 4 для контроля стерилизации паром размещаются на стерилизационных упаковках или в контрольных точках в камере стерилизатора.
Обеспечить соблюдение критических параметров паровой стерилизации (температура, время, насыщенный пар) в стерилизаторах с гравитационным методом удаления воздуха.
«Внутренние» химические индикаторы класса 4 для контроля стерилизации паром помещаются внутри упаковки продуктов и предоставляют информацию о соблюдении параметров стерилизации паром в непосредственной близости от продуктов. Они позволяют выбрать лучший способ и материал для упаковки продукции.
ВНЕШНИЕ ХИМИЧЕСКИЕ ПОКАЗАТЕЛИ КЛАССА 4 КЛАСС ICPS
«ВНУТРЕННИЕ» ХИМИЧЕСКИЕ ПОКАЗАТЕЛИ 4 КЛАССА СЕРИИ ИКПС-ВН / 01
Интегрирующие индикаторы (класс 5)
Интегрирующие индикаторы должны реагировать на все критические параметры метода стерилизации.Контрольные значения параметров для индикаторов 5 класса определяются заданной степенью инактивации тестовых микроорганизмов с определенными значениями значения D и, при необходимости, значения z в соответствии с ГОСТ Р ИСО 11138. -1 и ГОСТ Р ИСО 11138-3.
Химические индикаторы
класса 5 предназначены для обеспечения высочайшего уровня контроля за соблюдением параметров паровой стерилизации. Срабатывание химических индикаторов 5 класса соответствует полной гибели тестовых микроорганизмов, что позволяет сразу после завершения цикла стерилизации судить о качестве стерилизации.
КЛАСС ХИМИЧЕСКИХ ПОКАЗАТЕЛЕЙ ДЛЯ ПАРОВОЙ СТЕРИЛИЗАЦИИ (ИНТЕГРАЦИЯ)
Мнемосхемы (класс 6)
Эти индикаторы должны реагировать на все критические параметры метода стерилизации (определенная группа режимов). Контрольные значения параметров определяются соответствующими режимами стерилизации.
Реагирует на все критические параметры паровой стерилизации. Предназначен для точной проверки стерилизатора и соблюдения параметров стерилизации.Реагируйте только в присутствии пара требуемой температуры с соответствующим временем выдержки.
ХИМИЧЕСКИЕ ПОКАЗАТЕЛИ КЛАССА 6 ДЛЯ ПАРОВОЙ СТЕРИЛИЗАЦИИ
Цвет химического индикатора, приобретенный после использования во время хранения, может вернуться к исходному состоянию. Такие индикаторы не архивируются.
медицинская контрольная стерилизация
Биологический метод
Наряду с физико-химическим применяется бактериологический метод стерилизационного контроля.Он предназначен для контроля эффективности стерилизационного оборудования. До недавнего времени образцы садовой почвы, содержащие микроорганизмы, обладающие высокой устойчивостью к стерилизующим факторам, использовались для контроля стерилизации паром и воздухом. Однако устойчивость микроорганизмов в разных образцах неодинакова, что не позволяет стандартизировать результаты контроля.
В настоящее время для проведения бактериологического контроля используются биотесты, содержащие отмеренное количество спор тест-культур.Контроль эффективности стерилизации с помощью биотестов рекомендуется проводить 1 раз в 2 недели. В зарубежной практике принято применять биологическое тестирование не реже 1 раза в неделю.
В результате стерилизации материал теоретически свободен от жизнеспособных микроорганизмов. На практике этот материал определяется как тот, для которого вероятность нестерильности равна 1: тогда первая стерилизация была проведена с использованием пара и тепловой обработки. Стерилизация — это технологический процесс, который включает уничтожение всех, как вегетативных, так и споровых форм микроорганизмов.Стерилизаторы вызывают изменения в клетках за счет коагуляции, денатурации и окисления белка.
Это необратимые изменения, способствующие разрушению клетки. Отжиг или сжигание Отжиг используется для небольших предметов, таких как те, которые используются для микробных модификаторов, и состоит из пламени горелки на металлической части этого продукта для удаления микроорганизмов. В настоящее время все чаще используются разовые выбытия. Сжигание можно использовать для полного уничтожения загрязненных материалов, таких как больничные отходы.Однако по санитарным и экологическим причинам существуют альтернативы сжиганию медицинских отходов.
Биологический контроль с использованием биологических индикаторов (биотестов). Биологический метод контроля процесса стерилизации основан на гибели определенного количества тест-организмов, устойчивых к стерилизующему агенту микроорганизмов.
Единственным недостатком этого метода является то, что биопробы нельзя использовать как средство оперативного контроля. Для получения результата биологический индикатор необходимо термостатировать двое суток.При этом стерильный материал, в присутствии которого проводился биологический контроль, также необходимо законсервировать и не передавать в работу до получения результата.
По информативности результата биологический контроль превосходит описанные выше методы контроля, так как является средством прямого контроля и дает однозначный ответ о гибели микроорганизмов при стерилизации.
Ошибочная работа биологического индикатора при эффективной стерилизации стремится к нулю, естественно, если при работе с биотестами соблюдается главное требование — исключение из технологического процесса работы с ними возможности их повторного загрязнения.
Биологические индикаторы используются для определения эффективности стерилизации. Если сравнить это определение с определением назначения химических индикаторов, то сразу бросается в глаза разница в формулировках функциональности, а, следовательно, и в точности принимаемых мер контроля.
Химические индикаторы показывают, была ли проведена стерилизационная обработка, а биологические индикаторы определяют эффективность процесса стерилизации.«
Чтобы понять и понять, что такое биологический контроль и что он позволяет решать проблемы, вам необходимо познакомиться с концепциями и определениями.
Биологический индикатор — это готовый к использованию инокулированный носитель в первичной упаковке, обеспечивающий определенную устойчивость (устойчивость) к определенному режиму стерилизации.
Здесь носитель представляет собой удерживающий материал, на который наносятся тестовые микроорганизмы. А первичная упаковка — это система, которая защищает инокулированный носитель от повреждений и загрязнения, но не препятствует проникновению стерилизующих агентов.Носитель, на который нанесено определенное количество тестовых микроорганизмов, называется инокулированным.
Кроме того, использование постоянно периодического мониторинга в практике центрального стерилизационного центра значительно облегчает анализ причин неэффективности стерилизации. Это, в свою очередь, позволяет установить, что данные причины являются результатом ряда скрытых факторов, действующих по отдельности или в сочетании друг с другом (неисправность технического оборудования, несоблюдение технологии стерилизации, ошибки персонала, в том числе при проведении контрольных мероприятий, и т.п.Далее) [
И что самое главное, этот анализ может быть проведен самостоятельно специалистами ЦО без привлечения сторонних организаций, что, как следствие, может существенно сэкономить средства для ЛПУ. Еще один важный аспект использования биологических индикаторов — возможность их использования во всех существующих режимах стерилизации. К ним относятся классические российские режимы автоклавирования и стерилизации воздуха, так называемая импортная «короткая» стерилизация паром, режимы стерилизации лекарств, а также режимы дезинфекции (так называемые «режимы убийства») и обработки в дезинфекционных камерах.Рассмотрим подробно все возможные режимы стерилизации, где необходим биологический контроль.
Ø Стерилизация растворов лекарственных сред в автоклавах. Режимы стерилизации: 112 ° С с временной выдержкой 8 минут и более; 120 ° C при временном воздействии 10 минут и более.
Ш Стерилизация паром (автоклавирование). Режимы стерилизации: 110 ° / 180м; 120 ° / 45м; 121 ° / 20м; 126 ° / 10м; 132 ° / 20м; 134 ° / 5м.
Ø Стерилизация воздуха. Режимы стерилизации: 160 ° / 150м; 180 ° / 60м.
Ш Стерилизация паром (автоклавирование). Режимы дезинфекции 110 ° / 45м; 120 ° / 30м; 120 ° / 60м; 126 ° / 45м; 126 ° / 60м; 132 ° / 45м; 132 ° / 60м; 132 ° / 90м.
Ø Режимы обработки для дезинфекционных камер.
· Режимы паро-формалиновой дезинфекции: 58 ° / 45м; 50 ° / 150м; 58 ° / 60м; 58 ° / 210м; 126 ° / 60м; 132 ° / 45м; 132 ° / 60м; 132 ° / 90м.
· Режимы дезинфекции паром: 100 ° / 30м; 100 ° / 60м; 108 ° / 40м.
Ш Плазменная и газовая (оксид этилена, озон) стерилизация.
Контроль стерильности медицинских изделий
Осуществляется взятием мазков на стерильность и посевом на питательную среду.
Контроль стерильности осуществляется путем прямого посева (погружения) всего продукта (с их небольшими размерами) или в виде отдельных частей (отделяемые изделия) и фрагментов (кусочки шовного материала, перевязочный материал, разрезанный стерильными ножницами и т. Д.) в питательных средах. Объем питательной среды в пробирке (колбе, флаконе) должен быть достаточным для полного погружения продукта (частей или фрагментов продукта).При проверке стерильности более крупных изделий отбор проб проводится путем промывания с разных частей поверхности изделия: стерильными щипцами (щипцами) тщательно протирают каждую область марлевой салфеткой (размер полотенца 5,5 см), смоченной стерильной питьевой водой. либо стерильный 0,9% раствор натрия хлорида, либо раствор нейтрализатора (при стерилизации раствором химического агента). Каждая салфетка помещается в отдельную пробирку с питательной средой. Для продуктов с функциональными каналами рабочий конец опускают в пробирку с питательной средой и 1-2 раза промывают стерильным шприцем или пипеткой Посевы в тиогликолевой среде выдерживают в термостате при температуре 32 ° С, посевы в среде Сабуро при температуре 20 — 22 ° С в течение 14 дней при контроле продуктов, стерилизованных растворами химикатов и газовым методом, в течение 7 дней — стерилизованными термическими (пар, воздух) методами.При отсутствии роста микроорганизмов во всех пробирках (колбах, флаконах) делается вывод о стерильности продукции.
Мониторинг стерилизации с помощью тестов на споры: вопросы и ответы с координатором инфекционного контроля
По данным Центров по контролю и профилактике заболеваний (CDC), способность стерилизатора достигать условий, необходимых для стерилизации, следует контролировать с помощью комбинации механических и химических методов. , и биологические индикаторы (БИ).Механические индикаторы оценивают время цикла, температуру и давление, отображаемые на дисплеях и распечатках автоклавов. Эти параметры можно наблюдать во время цикла стерилизации, и они могут служить первым признаком неисправности.
Химические индикаторы (ХИ) используют чувствительные химические вещества для оценки физических условий во время процесса стерилизации. Ленты, полоски или ярлыки с химическими индикаторами и маркировка на упаковочных материалах меняют цвет при воздействии высоких температур или сочетания времени и температуры.Тем не менее, ни один из этих методов не гарантирует стерилизации — они просто обнаруживают процедурные ошибки и неисправности оборудования. В этом интервью выясняется, почему БИ — лучшая гарантия того, что стерилизация произошла.
Координатор инфекционного контроля (ICC): Во-первых, если механические и химические индикаторы не «подтверждают» стерилизацию, зачем нужны эти методы мониторинга?
Доктор Флюент (MTF): Это отличный вопрос! Как механические, так и химические индикаторы являются первыми шагами в обеспечении качества и должны выполняться для каждого цикла стерилизации.Эти методы мониторинга могут быть первым признаком того, что что-то пошло не так, и могут различать обработанные и необработанные элементы. Используя механический и химический мониторинг, стоматологический персонал может быть уверен, что нестерилизованные инструменты , а не будут использоваться для ухода за пациентами.
ICC: Я слышал о «биологических индикаторах» и «тестах на споры». Это такие же?
MTF: Да, тесты BI и споры относятся к одной и той же процедуре мониторинга.БИ и тесты на споры остаются лучшей гарантией того, что стерилизационное оборудование работает, а процедуры обработки инструментов выполняются правильно. Этот процесс мониторинга оценивает гибель высокорезистентных микроорганизмов (например, Geobacillus stearothermophilus для автоклавов и химических паров или Bacillus atrophaeus для сухих тепловых автоклавов). Инактивация BI строго означает, что другие потенциальные патогены в нагрузке были убиты.Другими словами, если споры Geobacillus и Bacillus уничтожены, все другие патогены также должны быть уничтожены в цикле стерилизации.
ICC: Я видел инкубационные системы в офисе для тестирования спор и услуг по мониторингу по почте. Как лучше?
MTF: Тестирование спор может быть инкубировано с использованием систем инкубации в офисе или с помощью служб мониторинга по почте, предоставляемых медицинскими компаниями, университетами и стоматологическими школами.Ни один из вариантов не лучше другого, однако есть несколько соображений, которые следует учитывать при выборе службы мониторинга в офисе или по почте. Были некоторые опасения, что задержки с отправкой по почте могут привести к тому, что тесты на споры будут доставлены в службу мониторинга через несколько дней после процесса стерилизации, однако они не влияют на инкубацию спор или окончательные результаты тестов.
Таким образом, нет необходимости беспокоиться о неточных результатах из-за задержек с обычной почтой. Для тестирования спор в офисе важно использовать надлежащую температуру и время инкубации, указанные производителем.При использовании любого метода записи мониторинга стерилизации (механические, химические и биологические) должны вестись в соответствии с государственными и местными правилами. При использовании почтовых услуг учет ведется службой мониторинга, тогда как ведение документации в офисных системах должно выполняться стоматологическим персоналом. Это дополнительный шаг, требующий усердия и соблюдения.
ICC: Вы можете рассказать мне, как проводить тест на споры?
MTF: Конечно.Прежде всего, всегда следуйте инструкциям производителя по применению (IFU). IFU определит размещение и расположение тестового BI в автоклаве. Второй контрольный BI также играет важную роль в тестировании спор. Контрольный BI должен быть от того же производителя и той же партии, что и тестовый BI, но , а не , должны быть обработаны в стерилизаторе. И тестовый, и контрольный БИ следует инкубировать одновременно. Окончательные результаты должны показать, что контрольный BI имеет положительные результаты на рост бактерий, а тест BI — нет.Другими словами, споры из тестового BI должны быть убиты, тогда как споры из контрольного BI должны быть живыми. Прохождение теста на споры называется отрицательным тестом на споры. Если уничтожены и тестовый, и контрольный БИ, это указывает на то, что с партией спор что-то не так, и тест следует повторить с другой партией. Если и тестовый, и контрольный BI живы, это называется положительным тестом на споры или неудачей BI. Это означает, что с вашим процессом стерилизации что-то пошло не так.
ICC: Теперь, когда у нас есть положительный тест на споры (сбой BI), что теперь?
MTF: Сначала посмотрите на свои механические и химические индикаторы. Если они демонстрируют, что ваш стерилизатор функционирует должным образом (время, температура и давление), то один положительный тест на споры, вероятно, не указывает на неисправность стерилизатора, но важно вспомнить все элементы с момента последнего отрицательного теста на споры. Стерилизатор должен быть выведен из эксплуатации, а все записи механического и химического мониторинга должны быть пересмотрены с момента последнего отрицательного теста BI.Затем повторите тест сразу после загрузки стерилизатора, используя тот же цикл, в котором произошел сбой. Если повторный тест отрицательный (тест BI пройден), можно снова ввести стерилизатор в эксплуатацию. На этом этапе следует пересмотреть рабочие процедуры стерилизатора, чтобы определить, возможна ли ошибка оператора.
ICC: Что делать, если положительный результат теста на споры был вызван ошибкой оператора?
MTF: Большинство положительных тестов на споры происходит из-за ошибки оператора, такой как перегрузка, отсутствие разделения между упаковками и неправильный или избыточный упаковочный материал.В таких случаях пересмотрите рабочие процедуры стерилизатора (включая упаковку, загрузку, тестирование спор) и включите весь персонал, занимающийся обработкой инструментов. Рассмотрите возможность приглашения представителя производителя для проведения тренинга и проверки работы стерилизатора и технического обслуживания. Кроме того, именно поэтому рекомендуется держать ваши IFU для оборудования для обработки в легкодоступном месте, в идеале — в зоне обработки или рядом с ней.
ICC: Как вспомнить пакеты инструментов?
MTF: Центры по контролю и профилактике заболеваний (CDC) рекомендуют маркировать упаковки инструментов с указанием используемого стерилизатора, номера цикла или загрузки, даты стерилизации и, если применимо, срока годности.Если эта информация будет записана на упаковках инструментов, стоматологический персонал сможет быстро определить инструменты, которые были обработаны во время или после положительного теста на споры.
ICC: Что делать, если у нас был положительный результат BI и повторный сбой?
MTF: Если повторный тест BI положителен и процедуры упаковки, загрузки и эксплуатации были выполнены правильно, стерилизатор должен оставаться в нерабочем состоянии до тех пор, пока он не будет проверен, отремонтирован и повторно проверен с помощью тестов BI в три последовательных цикла стерилизации пустой камеры.Важно определить и устранить причину неисправности стерилизатора. По возможности вспомните пакеты инструментов, относящиеся к последнему отрицательному BI. Эти предметы следует повторно очистить, снова обернуть и повторно стерилизовать. Имейте в виду, что текущее обслуживание стерилизационного оборудования должно выполняться в соответствии с инструкциями производителя и что записи о техническом обслуживании должны вестись.
ICC: Как часто следует проводить тестирование спор всех стерилизаторов?
MTF: CDC рекомендует проверять все стерилизаторы на споры не реже чем раз в неделю.По возможности следует использовать биологический индикатор для каждой загрузки стерилизатора, содержащей имплантируемое устройство, и для проверки результатов перед использованием имплантируемого устройства. Эксперты также рекомендуют тестирование спор при использовании новых упаковочных материалов, после обучения нового персонала, во время первого запуска после ремонта в стерилизаторе и после любых других изменений в процедурах стерилизации инструментов.
В заключение, мониторинг стерилизации должен представлять собой комбинацию параметров процесса, включая механические, химические и биологические, для оценки как условий стерилизации, так и эффективности процедуры.Механические и химические индикаторы являются первыми шагами в обеспечении качества и должны выполняться для каждого цикла стерилизации, однако биологические индикаторы (BI) обеспечивают наилучшую уверенность в том, что стерилизация произошла.

 Более 70 000 авторов готовы помочь вам прямо сейчас. Бесплатные
Более 70 000 авторов готовы помочь вам прямо сейчас. Бесплатные стерилизатора, инструменты на шарнирах открыты, инструменты разбираются, если это указано производителем).
стерилизатора, инструменты на шарнирах открыты, инструменты разбираются, если это указано производителем).