Задание 3. Предстерилизационная очистка. — Студопедия.Нет
Изучив информационное пособие, перечислите этапы ПСО и цель каждого этапа и заполните таблицу.
№
| Этапы проведения очистки
| Режим очистки
| Применяемое оборудование
| |
| Температура | Мин. Время | |||
| 1 | Предварительная ……
Цель: | |||
| 2 | Ополаскивание…….
Цель: | |||
| 3 | Замачивание ……
Цель: | |||
| 4 | Мойка …. . .
Цель: | |||
| 5 | Ополаскивание ….
Цель:. | |||
| 6 | Ополаскивание ….
Цель: | |||
| 7 | Сушка ….
Цель: | |||
Задание 4. Моющие растворы.
Изучите таблицу приготовление моющего раствора и восстановите недостающие компоненты и их количество.
| № | Компоненты раствора | % | Объём | Темпереатура |
| 1 | Вода
…… Использовать однократно |
5гр | 40-45 | |
| 2 | Вода
Раствор пергидроля Н2О2 ……. 
Использовать в течение суток 6 раз |
33% | 978 мл.
…… 5 гр. | ….. |
| 3 | Вода
Раствор пергидроля Н2О2 Моющее средство «Лотос», «Астра» и др. Использовать в течение суток 6 раз |
….. | 835
160 …. | 50-55 |
Задание 5. Контроль качества ПСО.
Контроль качества ПСО изделий медицинского назначения. Найдите соответствие.
| № | Название проб:
| Цель применения:
| Положительная реакция:
|
| 1 | фенолфталеиновая
| А. наличие остатков дезинфицирующих средств | а. розовое окрашивание |
| 2 | азопирамовая
| Б. наличие остатков моющего средства наличие остатков моющего средства
| б. сине-зеленое окрашивание |
| 3 | с суданом | В. на жиры | в. сине – фиолетовое окрашивание |
| 4 | амидопириновая | С. наличие скрытой крови | г. жёлтое |
Тема: « Организация работы централизованного стерилизационного отделения с целью профилактики ВБИ»
Студенты должен знать:
цели, задачи, принципы работы ЦСО
методы, средства и режимы стерилизации
виды контроля режима и качества стерилизации
Студент должен уметь:
пользоваться стерильным биксом
Задание 1. Определите понятия.
Установите соответствие термина и его формулировки.
| Термин | Формулировка термина |
| Стерилизация | комплекс мер направленных на предупреждение попадания инфекции в рану и организм больного.
|
| Асептика | комплекс мер направленных на уничтожение микроорганизмов на предметах окружающей среды и медицинских инструментах. |
| Антисептика | процесс уничтожения всех форм (обеззараживание) микробной жизни.
2 формы жизни микробов – вегетативная и споровая. |
Задание 2. Распределите методы стерилизации на 2 способа стерилизации. Способы и методы стерилизации.
| Способы | Методы | Стерилизующий агент
|
Ф
И
З
И
Ч
Е
С
К
И
Й
|
|
Водяной насыщенный пар под избыточным давлением |
| Сухой горячий воздух
| ||
| Инфракрасное излучение
| ||
| Среда нагретых стеклянных шариков | ||
Х
И
М
И
Ч
Е
С
К
И
Й
|
| Окись этилена
|
| Формальдегид
| ||
| Озон
| ||
| Пары перекиси водорода в сочетании с их низкотемпературной плазмой | ||
| Растворы химических средств |
· паровой,
· инфракрасный,
· гласперленовый;
· химических средств (жидкостной),
· применение растворов,
· воздушный ,
· газовый,
· плазменный
Задание 3. Укажите виды упаковок и сроки их использования. Выполните задания.
Укажите виды упаковок и сроки их использования. Выполните задания.
Упаковки:
· бумажные,
· комбинированные,
· пластиковые,
· в неупакованном виде.
Срок хранения в бактерицидных камерах — ….?
Задание 4 .Зоны ЦСО и объём работы.
Заполните следующую схему:
Задание 5 . Заполните таблицы.
Методы стерилизации:
Физический:
Паровой – называется ……….?
| 1 режим:
| 2 режим:
|
| Изделия из:
| Изделий из: |
| Химический контроль…? | Химический контроль…? |
Виды упаковок и сроки сохранения стерильности….?
| |
Воздушный – воздействие высокой температуры. Сухожаровой шкаф.
Сухожаровой шкаф.
| 1 режим:
| 2 режим:
|
| Изделия из | Изделия из
|
| Химический контроль…? | Химический контроль…?
|
Виды упаковок и сроки сохранения стерильности….?
| |
Задание 6 . Укажите какие инструменты и материалы стерилизуют данные методы.
· Инфракрасный:
· Гласперленовый:
· Радиационный:
Задание 7. Установите соответствие между методом и химическим веществом для стерилизации.
Химический:
· А) Жидкостной
· Б) Плазменный
· В) Газовый
1. Окись этилена, формальдегиды, озон.
2. Парами перекиси водорода
Парами перекиси водорода
3. глутаровый альдегид, альдегид янтарной кислоты.
4. перекись водорода, надкислоты, активный кислород.
5. Аналит
Задание 8. Вставьте пропущенное.
Режимы 6℅ перекиси водорода:
| Т — 18 градусов- ? часов – 360 минут. | Т – 50 градусов – 3 часа- ? минут. |
Задание 9. Установите соответствие между методом контроля качества и его содержанием.
| Метод контроля качества | Содержание метода |
| 1. Биологический
| · Г) Индикаторы изменяют цвет под влиянием процесса стерилизации |
| 2. Физический
| · А) Осуществляется контрольно-измерительными приборами, которые фиксируют: температуру, давление и время
|
3. Химический Химический
| · В) Взятие смывов с поверхности стерильных предметов.
|
| 4. Бактериологический
| · Б) Использование биотестов, биологических индикаторов основанных на процессе тепловой инактивации спор тестовых культур. Биотест — пробирка, в которой помещено определенное количество высушенных спор |
Учебники. Основная литература:
1. Л.И. Кулешова, Е.В. Пустоветова, «Оновы сестринского дела». Курс лекций, сестринские технологии. Издание 7-е: Ростоа-на-Дону, Феникс, 2017 год.
2. Т.П.Обуховец, «Основы сестринского дела: практикум» год издания 2013
3. Мухина С.А. Тарновская И.И. Теоретические основы сестринского дела: Учебник.-2-е изд., исп. и доп.-М.: ГЭОТАР-Медиа, 2012. Островская И.В., Широкова Н.В. Основы сестринского дела: Учебник.-М.: ГЭОТАР-Медиа, 2012.
4. Осипова В.Л. «Дезинфекция» Учебное пособие для медицинских училищ и колледжей. Москва. Издательская группа «ГЭОТАР-Медиа»2009г.
Москва. Издательская группа «ГЭОТАР-Медиа»2009г.
Дополнительные источники:
1. Абрамова И.М. Комментарии к методическим указаниям по дезинфекции, предстерилизационной очистке и стерилизации изделий медицинского назначения.
2. Акимкин В.Г. «Санитарно-эпидемиологические требования к организации сбора, обеззараживания, временного хранения и удаления отходов в ЛПУ». Методическое пособие. Москва. Издательство РАМН 2004г.
3. ВБИ. Меры профилактики. Приложение к журналу «СД» №1, 2004г.
4. Веткина И.Ф. Продлим молодость наших рук: новый взгляд на обеззараживание рук медицинского персонала. «Главная медицинская сестра», 2005, №4, стр.121-124.
Законы,СанПины,ОСТы:
1. Приказ МЗ СССР № 770 от 1985 г. ОСТ 42-21-2-85 «Стерилизация и дезинфекция изделий медицинского назначения. Методы, средства и режимы».
2. Санитарно-эпидемиологические правила и нормативы СанПиН 2.1.3.2630–10 «Санитарно-эпидемиологические требования к организациям, осуществляющим медицинскую деятельность».
3. Санитарно-эпидемиологические правила и нормативы СанПиН 2.1.7.2790-10 «Санитарно-эпидемиологические требования к обращению с медицинскими отходами.
4. Санитарно-эпидемиологические правила и нормативы СанПиН 3.2.3215-14 «Профилактика паразитарных болезней на территории Российской Федерации»
5. «Санитарно-эпидемические требования к организации и осуществлению дезинфекционной деятельности» СП 3.5.1378 – 03.
6. Методические указания 287–113 от 30.12.98г. «Дезинфекция, предстерилизационная очистка и стерилизация изделий медицинского назначения».
7. Руководство «Использование ультрафиолетового бактерицидного излучения для обеззараживания воздуха в помещениях»: Р 3.5.1904 – 04.
Предстерилизационная очистка — Мегаобучалка
ОТРАСЛЕВОЙ СТАНДАРТ
СТЕРИЛИЗАЦИЯ И ДЕЗИНФЕКЦИЯ ИЗДЕЛИЙ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ
МЕТОДЫ, СРЕДСТВА И РЕЖИМЫ
ОСТ 42-21-2-85
Дата введения — 1 января 1986 года
Взамен ОСТ 42-2-2-77
Настоящий стандарт распространяется на изделия медицинского назначения, подвергаемые в процессе эксплуатации стерилизации и (или) дезинфекции.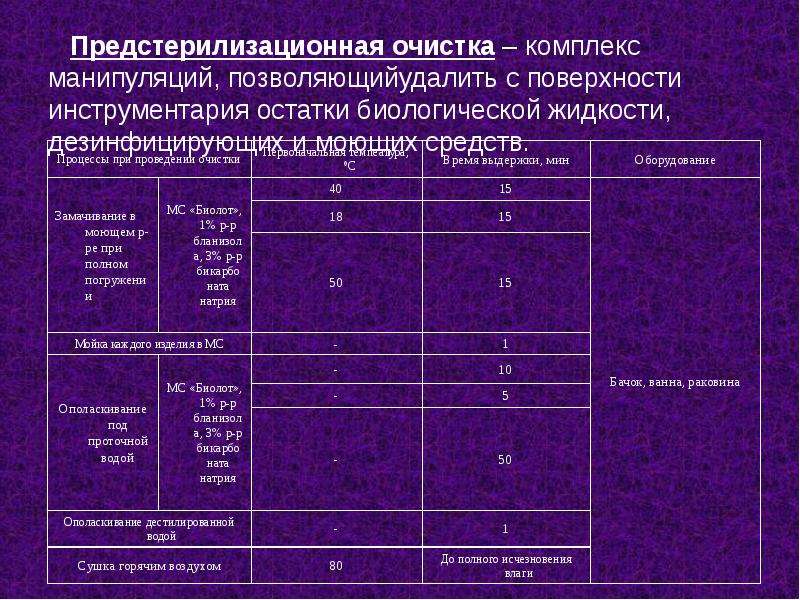
Стандарт обязателен для учреждений, эксплуатирующих изделия медицинского назначения, а также для организаций и предприятий, разрабатывающих и изготовляющих данные изделия.
Стандарт не распространяется на лекарственные препараты и средства их упаковки, на изделия, выпускаемые промышленностью стерильными, на изделия из текстильных материалов (в части дезинфекции), предметы ухода за больными, мебель медицинскую.
Стандарт устанавливает методы, средства и режимы предстерилизационной очистки, стерилизации и дезинфекции.
Основные понятия из области предстерилизационной очистки, стерилизации и дезинфекции по ГОСТ 25375-82 (СТ СЭВ 3188-81).
Перечень нормативно-технических документов на химические реактивы и вспомогательные материалы дан в справочном Приложении 1 к настоящему стандарту.
Перечень инструктивно-методических документов Минздрава СССР по вопросам стерилизации и дезинфекции дан в справочном Приложении 2 к настоящему стандарту.
Общие положения
1. 1. Установленные в настоящем стандарте методы, средства и режимы предстерилизационной очистки, стерилизации и дезинфекции являются равнозначными по эффективности для каждого вида обработки.
1. Установленные в настоящем стандарте методы, средства и режимы предстерилизационной очистки, стерилизации и дезинфекции являются равнозначными по эффективности для каждого вида обработки.
Примечание. Предпочтение следует отдавать термическим методам стерилизации (паровому и воздушному).
1.2. На основе положений настоящего стандарта должны разрабатываться инструкции, устанавливающие методы, средства и режимы предстерилизационной очистки, стерилизации и дезинфекции применительно к конкретным изделиям или группам изделий с учетом их назначения и конструктивных особенностей.
1.3. При разработке изделий должен выбираться метод, средство и режим, исходя из устойчивости изделий к средствам предстерилизационной очистки, стерилизации и дезинфекции в зависимости от материала, степени обработки поверхности, конструктивного исполнения.
Выбранные методы, средства и режимы не должны вызывать изменения внешнего вида, эксплуатационных качеств и других показателей изделия, обработанные изделия не должны оказывать токсического действия.
1.4. Требования устойчивости изделий к средствам предстерилизационной очистки, стерилизации и дезинфекции должны нормироваться в технических заданиях (медико-технических требованиях) на разработку новых изделий, технических условиях, стандартах, а также указываться в эксплуатационной документации и должны контролироваться на стадии разработки и изготовления изделия.
В технических условиях и стандартах на серийно выпускаемую продукцию требование устойчивости изделий к предстерилизационной очистке и конкретному методу стерилизации или дезинфекции должно нормироваться с учетом положений настоящего стандарта по результатам предварительно проведенных испытаний.
1.5. В процессе эксплуатации изделий предстерилизационная очистка, стерилизация и (или) дезинфекция должны проводиться в соответствии с настоящим стандартом и инструкциями Министерства здравоохранения СССР, разработанными на основании настоящего стандарта, устанавливающими порядок проведения предстерилизационной очистки, стерилизации, дезинфекции конкретных видов изделий, а также эксплуатационной документации.
1.6. Положения технической документации (в том числе эксплуатационной) части предстерилизационной очистки, стерилизации и дезинфекции должны соответствовать настоящему стандарту, инструкциям Министерства здравоохранения СССР, а при отсутствии указанных инструкций по тем или иным видам изделий должны быть согласованы с Министерством здравоохранения СССР.
1.7. При проведении предстерилизационной очистки, стерилизации и дезинфекции химическим методом (за исключением газовой стерилизации), дезинфекции методом кипячения допускается применение ингибиторов и других добавок, способствующих снижению коррозии, разрешенных Министерством здравоохранения СССР и не снижающих эффективности предстерилизационной очистки, стерилизации и дезинфекции.
1.8. Контроль стерильности должен осуществляться бактериологическими лабораториями санитарно-эпидемиологических станций и лечебно-профилактических учреждений в соответствии с инструкциями Министерства здравоохранения СССР.
1. 9. Контроль работы стерилизаторов осуществляется дезинфекционными станциями и дезинфекционными отделами (отделениями) санитарно-эпидемиологических станций в соответствии с инструкциями Министерства здравоохранения СССР.
9. Контроль работы стерилизаторов осуществляется дезинфекционными станциями и дезинфекционными отделами (отделениями) санитарно-эпидемиологических станций в соответствии с инструкциями Министерства здравоохранения СССР.
1.10. Контроль качества предстерилизационной очистки и дезинфекции должен проводиться лечебно-профилактическими учреждениями, санитарно-эпидемиологическими и дезинфекционными станциями в соответствии с инструкциями Министерства здравоохранения СССР.
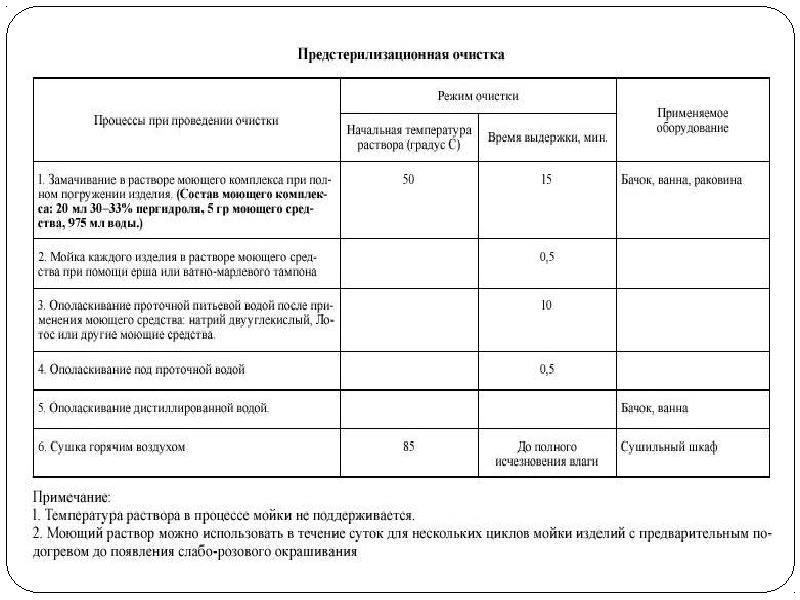
Предстерилизационная очистка
2.1. Предстерилизационной очистке должны подвергаться все изделия перед их стерилизацией с целью удаления белковых, жировых и механических загрязнений, а также лекарственных препаратов.
2.2. Разъемные изделия должны подвергаться предстерилизационной очистке в разобранном виде.
2.3. Предстерилизационная очистка должна осуществляться ручным или механизированным (с помощью специального оборудования) способом.
2.4. Механизированная предстерилизационная очистка должна производиться струйным, ротационным методами, ершеванием или с применением ультразвука с использованием поверхностно-активных веществ по п. 2.8 настоящего стандарта и других добавок.
2.8 настоящего стандарта и других добавок.
Методика проведения механизированной очистки должна соответствовать инструкции по эксплуатации, прилагаемой к оборудованию.
Примечание. Ершевание резиновых изделий не допускается.
2.5. Предстерилизационная очистка ручным способом должна осуществляться в последовательности в соответствии с табл. 1.
2.6. При использовании моющего раствора, содержащего 0,5% перекиси водорода и 0,5% синтетического моющего средства «Лотос», применяют ингибитор коррозии — 0,14% олеата натрия.
2.7. По окончании рабочей смены оборудование должно быть очищено механическим способом путем мытья с применением моющих средств.
2.8. Моющий раствор должен включать компоненты в соответствии с табл. 2.
2.9. Инструменты в процессе эксплуатации, предстерилизационной очистки, стерилизации могут подвергаться коррозии. Инструменты с видимыми пятнами коррозии, а также с наличием оксидной пленки подвергаются химической очистке не более 1 — 2 раз в квартал.
Стерилизация
3.1. Стерилизации должны подвергаться все изделия, соприкасающиеся с раненой поверхностью, контактирующие с кровью или инъекционными препаратами, и отдельные виды медицинских инструментов, которые в процессе эксплуатации соприкасаются со слизистой оболочкой и могут вызвать ее повреждения.
3.2. Стерилизация должна осуществляться одним из методов, приведенных в табл. 4 — 9.
Дезинфекция
4.1. Дезинфекции должны подвергаться все изделия, не имеющие контакта с раненой поверхностью, кровью или инъекционными препаратами.
Изделия, используемые при проведении гнойных операций или
операционных манипуляций у инфекционного больного, подвергают
дезинфекции перед предстерилизационной очисткой и стерилизацией.
Кроме того, дезинфекции подлежат изделия медицинского назначения
после операций, инъекций и т.п., лицам, перенесшим гепатит В или
гепатит с неуточненным диагнозом (вирусный гепатит), а также
являющимся носителями HB -антигена.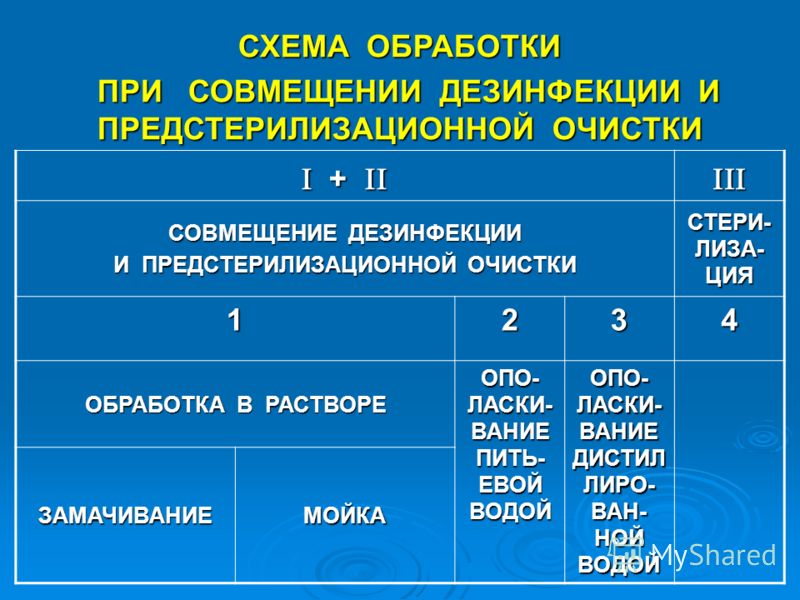
S
Дезинфекция должна осуществляться одним из методов, указанных в табл. 10.
Таблица 1
| На главную | База 1 | База 2 | База 3 |
| Поиск по реквизитамПоиск по номеру документаПоиск по названию документаПоиск по тексту документа |
Искать все виды документовДокументы неопределённого видаISOАвиационные правилаАльбомАпелляционное определениеАТКАТК-РЭАТПЭАТРВИВМРВМУВНВНиРВНКРВНМДВНПВНПБВНТМ/МЧМ СССРВНТПВНТП/МПСВНЭВОМВПНРМВППБВРДВРДСВременное положениеВременное руководствоВременные методические рекомендацииВременные нормативыВременные рекомендацииВременные указанияВременный порядокВрТЕРВрТЕРрВрТЭСНВрТЭСНрВСНВСН АСВСН ВКВСН-АПКВСПВСТПВТУВТУ МММПВТУ НКММПВУП СНЭВУППВУТПВыпускГКИНПГКИНП (ОНТА)ГНГОСТГОСТ CEN/TRГОСТ CISPRГОСТ ENГОСТ EN ISOГОСТ EN/TSГОСТ IECГОСТ IEC/PASГОСТ IEC/TRГОСТ IEC/TSГОСТ ISOГОСТ ISO GuideГОСТ ISO/DISГОСТ ISO/HL7ГОСТ ISO/IECГОСТ ISO/IEC GuideГОСТ ISO/TRГОСТ ISO/TSГОСТ OIML RГОСТ ЕНГОСТ ИСОГОСТ ИСО/МЭКГОСТ ИСО/ТОГОСТ ИСО/ТСГОСТ МЭКГОСТ РГОСТ Р ЕНГОСТ Р ЕН ИСОГОСТ Р ИСОГОСТ Р ИСО/HL7ГОСТ Р ИСО/АСТМГОСТ Р ИСО/МЭКГОСТ Р ИСО/МЭК МФСГОСТ Р ИСО/МЭК ТОГОСТ Р ИСО/ТОГОСТ Р ИСО/ТСГОСТ Р ИСО/ТУГОСТ Р МЭКГОСТ Р МЭК/ТОГОСТ Р МЭК/ТСГОСТ ЭД1ГСНГСНрГСССДГЭСНГЭСНмГЭСНмрГЭСНмтГЭСНпГЭСНПиТЕРГЭСНПиТЕРрГЭСНрГЭСНсДИДиОРДирективное письмоДоговорДополнение к ВСНДополнение к РНиПДСЕКЕНВиРЕНВиР-ПЕНиРЕСДЗемЕТКСЖНМЗаключениеЗаконЗаконопроектЗональный типовой проектИИБТВИДИКИМИНИнструктивное письмоИнструкцияИнструкция НСАМИнформационно-методическое письмоИнформационно-технический сборникИнформационное письмоИнформацияИОТИРИСОИСО/TRИТНИТОсИТПИТСИЭСНИЭСНиЕР Республика КарелияККарта трудового процессаКарта-нарядКаталогКаталог-справочникККТКОКодексКОТКПОКСИКТКТПММ-МВИМВИМВНМВРМГСНМДМДКМДСМеждународные стандартыМетодикаМетодика НСАММетодические рекомендацииМетодические рекомендации к СПМетодические указанияМетодический документМетодическое пособиеМетодическое руководствоМИМИ БГЕИМИ УЯВИМИГКМММНМОДНМонтажные чертежиМос МУМосМРМосСанПинМППБМРМРДСМРОМРРМРТУМСанПиНМСНМСПМТМУМУ ОТ РММУКМЭКННАС ГАНБ ЖТНВННГЭАНДНДПНиТУНКНормыНормы времениНПНПБНПРМНРНРБНСПНТПНТП АПКНТП ЭППНТПДНТПСНТСНЦКРНЦСОДМОДНОЕРЖОЕРЖкрОЕРЖмОЕРЖмрОЕРЖпОЕРЖрОКОМТРМОНОНДОНКОНТПОПВОПКП АЭСОПНРМСОРДОСГиСППиНОСНОСН-АПКОСПОССПЖОССЦЖОСТОСТ 1ОСТ 2ОСТ 34ОСТ 4ОСТ 5ОСТ ВКСОСТ КЗ СНКОСТ НКЗагОСТ НКЛесОСТ НКМОСТ НКММПОСТ НКППОСТ НКПП и НКВТОСТ НКСМОСТ НКТПОСТ5ОСТНОСЭМЖОТРОТТПП ССФЖТПБПБПРВПБЭ НППБЯПВ НППВКМПВСРПГВУПереченьПиН АЭПисьмоПМГПНАЭПНД ФПНД Ф СБПНД Ф ТПНСТПОПоложениеПорядокПособиеПособие в развитие СНиППособие к ВНТППособие к ВСНПособие к МГСНПособие к МРПособие к РДПособие к РТМПособие к СНПособие к СНиППособие к СППособие к СТОПособие по применению СППостановлениеПОТ РПОЭСНрППБППБ-АСППБ-СППБВППБОППРПРПР РСКПР СМНПравилаПрактическое пособие к СППРБ АСПрейскурантПриказПротоколПСРр Калининградской областиПТБПТЭПУГПУЭПЦСНПЭУРР ГазпромР НОПРИЗР НОСТРОЙР НОСТРОЙ/НОПР РСКР СМНР-НП СРО ССКРазъяснениеРаспоряжениеРАФРБРГРДРД БГЕИРД БТРД ГМРД НИИКраностроенияРД РОСЭКРД РСКРД РТМРД СМАРД СМНРД ЭОРД-АПКРДИРДМРДМУРДПРДСРДТПРегламентРекомендацииРекомендацияРешениеРешение коллегииРКРМРМГРМДРМКРНДРНиПРПРРТОП ТЭРС ГАРСНРСТ РСФСРРСТ РСФСР ЭД1РТРТМРТПРУРуководствоРУЭСТОП ГАРЭГА РФРЭСНрСАСанитарные нормыСанитарные правилаСанПиНСборникСборник НТД к СНиПСборники ПВРСборники РСН МОСборники РСН ПНРСборники РСН ССРСборники ценСБЦПСДАСДАЭСДОССерияСЗКСНСН-РФСНиПСНиРСНККСНОРСНПСОСоглашениеСПСП АССП АЭССправочникСправочное пособие к ВСНСправочное пособие к СНиПСправочное пособие к СПСправочное пособие к ТЕРСправочное пособие к ТЕРрСРПССНССЦСТ ССФЖТСТ СЭВСТ ЦКБАСТ-НП СРОСТАСТКСТМСТНСТН ЦЭСТОСТО 030 НОСТРОЙСТО АСЧМСТО БДПСТО ВНИИСТСТО ГазпромСТО Газпром РДСТО ГГИСТО ГУ ГГИСТО ДД ХМАОСТО ДОКТОР БЕТОНСТО МАДИСТО МВИСТО МИСТО НААГСТО НАКССТО НКССТО НОПСТО НОСТРОЙСТО НОСТРОЙ/НОПСТО РЖДСТО РосГеоСТО РОСТЕХЭКСПЕРТИЗАСТО САСТО СМКСТО ФЦССТО ЦКТИСТО-ГК «Трансстрой»СТО-НСОПБСТПСТП ВНИИГСТП НИИЭССтП РМПСУПСССУРСУСНСЦНПРТВТЕТелеграммаТелетайпограммаТематическая подборкаТЕРТЕР Алтайский крайТЕР Белгородская областьТЕР Калининградской областиТЕР Карачаево-Черкесская РеспубликаТЕР Краснодарского краяТЕР Мурманская областьТЕР Новосибирской областиТЕР Орловской областиТЕР Республика ДагестанТЕР Республика КарелияТЕР Ростовской областиТЕР Самарской областиТЕР Смоленской обл. ТЕР Ямало-Ненецкий автономный округТЕР Ярославской областиТЕРмТЕРм Алтайский крайТЕРм Белгородская областьТЕРм Воронежской областиТЕРм Калининградской областиТЕРм Карачаево-Черкесская РеспубликаТЕРм Мурманская областьТЕРм Республика ДагестанТЕРм Республика КарелияТЕРм Ямало-Ненецкий автономный округТЕРмрТЕРмр Алтайский крайТЕРмр Белгородская областьТЕРмр Карачаево-Черкесская РеспубликаТЕРмр Краснодарского краяТЕРмр Республика ДагестанТЕРмр Республика КарелияТЕРмр Ямало-Ненецкий автономный округТЕРпТЕРп Алтайский крайТЕРп Белгородская областьТЕРп Калининградской областиТЕРп Карачаево-Черкесская РеспубликаТЕРп Краснодарского краяТЕРп Республика КарелияТЕРп Ямало-Ненецкий автономный округТЕРп Ярославской областиТЕРрТЕРр Алтайский крайТЕРр Белгородская областьТЕРр Калининградской областиТЕРр Карачаево-Черкесская РеспубликаТЕРр Краснодарского краяТЕРр Новосибирской областиТЕРр Омской областиТЕРр Орловской областиТЕРр Республика ДагестанТЕРр Республика КарелияТЕРр Ростовской областиТЕРр Рязанской областиТЕРр Самарской областиТЕРр Смоленской областиТЕРр Удмуртской РеспубликиТЕРр Ульяновской областиТЕРр Ямало-Ненецкий автономный округТЕРррТЕРрр Ямало-Ненецкий автономный округТЕРс Ямало-Ненецкий автономный округТЕРтр Ямало-Ненецкий автономный округТехнический каталогТехнический регламентТехнический регламент Таможенного союзаТехнический циркулярТехнологическая инструкцияТехнологическая картаТехнологические картыТехнологический регламентТИТИ РТИ РОТиповая инструкцияТиповая технологическая инструкцияТиповое положениеТиповой проектТиповые конструкцииТиповые материалы для проектированияТиповые проектные решенияТКТКБЯТМД Санкт-ПетербургТНПБТОИТОИ-РДТПТПРТРТР АВОКТР ЕАЭСТР ТСТРДТСНТСН МУТСН ПМСТСН РКТСН ЭКТСН ЭОТСНэ и ТЕРэТССЦТССЦ Алтайский крайТССЦ Белгородская областьТССЦ Воронежской областиТССЦ Карачаево-Черкесская РеспубликаТССЦ Ямало-Ненецкий автономный округТССЦпгТССЦпг Белгородская областьТСЦТСЦ Белгородская областьТСЦ Краснодарского краяТСЦ Орловской областиТСЦ Республика ДагестанТСЦ Республика КарелияТСЦ Ростовской областиТСЦ Ульяновской областиТСЦмТСЦО Ямало-Ненецкий автономный округТСЦп Калининградской областиТСЦПГ Ямало-Ненецкий автономный округТСЦэ Калининградской областиТСЭМТСЭМ Алтайский крайТСЭМ Белгородская областьТСЭМ Карачаево-Черкесская РеспубликаТСЭМ Ямало-Ненецкий автономный округТТТТКТТПТУТУ-газТУКТЭСНиЕР Воронежской областиТЭСНиЕРм Воронежской областиТЭСНиЕРрТЭСНиТЕРэУУ-СТУказУказаниеУказанияУКНУНУОУРврУРкрУРррУРСНУСНУТП БГЕИФАПФедеральный законФедеральный стандарт оценкиФЕРФЕРмФЕРмрФЕРпФЕРрФормаФорма ИГАСНФРФСНФССЦФССЦпгФСЭМФТС ЖТЦВЦенникЦИРВЦиркулярЦПИШифрЭксплуатационный циркулярЭРД ТЕР Ямало-Ненецкий автономный округТЕР Ярославской областиТЕРмТЕРм Алтайский крайТЕРм Белгородская областьТЕРм Воронежской областиТЕРм Калининградской областиТЕРм Карачаево-Черкесская РеспубликаТЕРм Мурманская областьТЕРм Республика ДагестанТЕРм Республика КарелияТЕРм Ямало-Ненецкий автономный округТЕРмрТЕРмр Алтайский крайТЕРмр Белгородская областьТЕРмр Карачаево-Черкесская РеспубликаТЕРмр Краснодарского краяТЕРмр Республика ДагестанТЕРмр Республика КарелияТЕРмр Ямало-Ненецкий автономный округТЕРпТЕРп Алтайский крайТЕРп Белгородская областьТЕРп Калининградской областиТЕРп Карачаево-Черкесская РеспубликаТЕРп Краснодарского краяТЕРп Республика КарелияТЕРп Ямало-Ненецкий автономный округТЕРп Ярославской областиТЕРрТЕРр Алтайский крайТЕРр Белгородская областьТЕРр Калининградской областиТЕРр Карачаево-Черкесская РеспубликаТЕРр Краснодарского краяТЕРр Новосибирской областиТЕРр Омской областиТЕРр Орловской областиТЕРр Республика ДагестанТЕРр Республика КарелияТЕРр Ростовской областиТЕРр Рязанской областиТЕРр Самарской областиТЕРр Смоленской областиТЕРр Удмуртской РеспубликиТЕРр Ульяновской областиТЕРр Ямало-Ненецкий автономный округТЕРррТЕРрр Ямало-Ненецкий автономный округТЕРс Ямало-Ненецкий автономный округТЕРтр Ямало-Ненецкий автономный округТехнический каталогТехнический регламентТехнический регламент Таможенного союзаТехнический циркулярТехнологическая инструкцияТехнологическая картаТехнологические картыТехнологический регламентТИТИ РТИ РОТиповая инструкцияТиповая технологическая инструкцияТиповое положениеТиповой проектТиповые конструкцииТиповые материалы для проектированияТиповые проектные решенияТКТКБЯТМД Санкт-ПетербургТНПБТОИТОИ-РДТПТПРТРТР АВОКТР ЕАЭСТР ТСТРДТСНТСН МУТСН ПМСТСН РКТСН ЭКТСН ЭОТСНэ и ТЕРэТССЦТССЦ Алтайский крайТССЦ Белгородская областьТССЦ Воронежской областиТССЦ Карачаево-Черкесская РеспубликаТССЦ Ямало-Ненецкий автономный округТССЦпгТССЦпг Белгородская областьТСЦТСЦ Белгородская областьТСЦ Краснодарского краяТСЦ Орловской областиТСЦ Республика ДагестанТСЦ Республика КарелияТСЦ Ростовской областиТСЦ Ульяновской областиТСЦмТСЦО Ямало-Ненецкий автономный округТСЦп Калининградской областиТСЦПГ Ямало-Ненецкий автономный округТСЦэ Калининградской областиТСЭМТСЭМ Алтайский крайТСЭМ Белгородская областьТСЭМ Карачаево-Черкесская РеспубликаТСЭМ Ямало-Ненецкий автономный округТТТТКТТПТУТУ-газТУКТЭСНиЕР Воронежской областиТЭСНиЕРм Воронежской областиТЭСНиЕРрТЭСНиТЕРэУУ-СТУказУказаниеУказанияУКНУНУОУРврУРкрУРррУРСНУСНУТП БГЕИФАПФедеральный законФедеральный стандарт оценкиФЕРФЕРмФЕРмрФЕРпФЕРрФормаФорма ИГАСНФРФСНФССЦФССЦпгФСЭМФТС ЖТЦВЦенникЦИРВЦиркулярЦПИШифрЭксплуатационный циркулярЭРД |
| Показать все найденныеПоказать действующиеПоказать частично действующиеПоказать не действующиеПоказать проектыПоказать документы с неизвестным статусом |
| Упорядочить по номеру документаУпорядочить по дате введения |
| Тема 1.14. Предстерилизационная очистка. Контроль качества предстерилизационной очистки Прежде чем перейти к изучению новой темы необходимо обратиться к материалу предыдущего занятия и вспомнить этапы обработки медицинского инструментария многоразового применения. Этапы обработки изделий медицинского назначения (пинцет, зажим, корнцанг) Очистка Дезинфекция с предстерилизационной очисткой Стерилизация Использование Приготовить: инструмент для обработки, лоток, два контейнера с дезинфектантом. Последовательность действий:
Предстерилизационная обработка — промежуточный этап обработки изделий медицинского назначения многоразового использования с целью удаления с их поверхностей белковых, жировых, механических загрязнений и остатков лекарственных средств. Предстерилизационную обработку изделий медицинского назначения проводят после 8 этапа очистки и дезинфекции. Общие требования к предстерилизационной очистке
Предстерилизационную очистку ручным способом осуществляют, используя емкости из пластмасс, стекла или покрытых эмалью (без повреждений).
Методика проведения предстерилизационной очистки совмещенной с дезинфекцией Этапы проведения очистки:
Предстерилизационная очистка изделий медицинского назначения Приготовить: инструмент для обработки, контейнер, лотки/сетки, салфетки, ватно-марлевые тампоны/щетки, перчатки. Последовательность действий:
Моюще-дезинфицирующий раствор можно использовать многократно в течение срока, установленного инструкцией по применению данного препарата, или до изменения его внешних свойств (изменение цвета, появление осадка). Усовершенствование процесса предстерилизационной очистки изделий возможно за счет обработки изделий моющими или моюще-дезинфицирующими средствами в сочетании с ультразвуком. Это позволяет сократить трудоемкость и повысить качество стерилизации инструментов, а также обеспечить охрану здоровья медицинских работников. Основные преимущества ультразвуковых моек: — снижение риска инфицирования, — существенное снижение трудоемкости, — улучшение качества очистки, в том числе труднодоступных участков изделий, — сокращение времени обработки, особенно в больших объемах, — соблюдение экологической чистоты процессов, — щадящий режим воздействия, не допускающий повреждения инструментов. Контроль качества предстерилизационной обработки Качество предстерилизационной очистки проверяют пробами: — азопирамовой (универсальной) – проверяют наличие остатков крови, дезсредства, моющих средств; — фенолфталеиновой – проверяют наличие остатков моющего средства. Контроль качества предстерилизационной обработки проводят специалисты центров гигиены и эпидемиологии 1 раз в квартал. Самоконтроль в ЛПУ проводят: — в центральных стерилизационных отделениях ежедневно, — в отделениях ЛПУ – не реже одного раза в неделю (организует и контролирует старшая сестра отделения, старшая акушерка). Контролю качества подлежит 1% обработанных изделий, но не менее 3-5единиц, выбирая изделия разной конфигурации. В случае положительной пробы на кровь или остаточное количество моющих средств, всю партию контролируемых изделий подвергают повторной очистке до получения отрицательных результатов. Результаты контроля фиксируются в журнале. Журнал учета качества предстерилизационной обработки Начат «__»______20__г. Окончен «__»______20__г.
Азопирамовая проба Раствор готовят из 1-1,5% раствора солянокислого анилина и 95% этилового спирта. Непосредственно перед проведением пробы готовят рабочий раствор: смешивают равные части азопирама и 3% раствор перекиси водорода в стерильной емкости. Инструменты, на которых будет проведена проба, размещаются на белой салфетке. Затем с помощью стерильной пипетки или шприца раствор наносится на поверхности инструментов, им наполняются каналы, заполняются полости. Результат оценивают в течение 1 минуты. Окрашивание, появившееся после 1 минуты, не учитывается. Если раствор окрашивается в розовый цвет – это говорит о наличии остатков моющего вещества, в сине-фиолетовый цвет – остатков крови, в бурый цвет – наличие остатков хлора и ржавчины. Контроль качества считается положительным. Рабочий раствор может быть использован в течение 1-2 часов. При более длительном хранении может появиться спонтанное розовое окрашивание рабочего раствора. При температуре выше 25˚С рабочий раствор розовеет быстрее, поэтому его рекомендуют использовать в течение 30-40 минут. Нельзя подвергать проверке горячие инструменты; а также держать раствор на ярком свету или вблизи нагревательных приборов. Задания для закрепления и систематизации знаний, предварительного контроля по теме 1.14. Предстерилизационная очистка. Контроль качества предстерилизационной очистки Дайте ответы на вопросы:
Решите тестовые задания:
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
| |||||||
Этапы предстерилизационной очистки
А С Е П Т И К А
Асептика — комплекс профилактических мероприятий, направленных на предупреждение попадания микроорганизмов в рану, ткани, органы и полости тела больного /раненого/ при хирургических операциях, перевязках, эндоскопических и других лечебных и диагностических манипуляциях.
Асептика включает:
— стерилизацию инструментов, приборов, операционного
белья, шовного материала;
— обеззораживание рук участников операции;
— обеззараживание кожи операционного поля;
— дезинфекцию предметов ухода за больными, постельных
принадлежностей, термометров, инструментов и приборов для
неинвазивных исследований и манипуляций;
— соблюдение определенных правил проведения операций,
манипуляций и поведения при них медперсонала и больного;
— специальные санитарно-гигиенические и организационные
мероприятия в лечебных учреждениях, расположение и
устройство операционного блока, функциональных
подразделений хирургического отделения и палат, очередность
перевязок, санацию медперсонала.
Основные термины и понятия
Обеззараживание /деконтаминация / — общий термин, обозначающий процесс обработки для удаления возбудителей инфекционных заболеваний, в результате чего использование обработанного предмета становится безопасным.
Очистка — процесс удаления видимой пыли, органических /кровь, биологические жидкости/ и неорганических загрязнений,
остатков медикаментозных средств и других инородных материалов. Обычно осуществляется водой с мылом, детергентами и ферментными препаратами. Очистка всегда предшествует дезинфекции и стерилизации.
Дезинфекция — процесс уничтожения большинства патогенных и непатогенных форм микроорганизмов /бактериоцидность/, а бактериальные споры, отличающиееся особой устойчивостью к воздействию внешней среды, остаются жизнеспособными. Этот термин применяется исключительно только по отношению к неодушевленным предметам. Уничтожение микроорганизмов в биологических тканях называется «антисептика».
Стерилизация /обеспложивание/ — процесс уничножения всех форм микробной жизни, включая патогенные и непатогенные бактерии, вирусы, споры и грибы, с помощью различных физических и химических методов.
Выбор адекватного уровня обеззараживания определяется:
— предназначением изделия и материалов /вид процедуры/;
— видом материала, из которого изготовлен инструмент;
— финансовыми возможностями.
СТЕРИЛИЗАЦИИ ПОДЛЕЖАТ:
1. Изделия и материалы, соприкасающиеся с раневой
поверхностью — инструменты, шовный материал, операционное белье, перевязочный материал и пр..
2. Изделия и материалы, контактирующие с кровью или инъекционными препаратами — системы для переливания крови, шприцы, инъекционные иглы, сердечные и сосудистые катетеры и т.д..
3. Отдельные виды инструментов, которые в процессе эксплуатации соприкасаются со слизистой оболочкой органа и могут вызвать ее повреждение — цистоскоп, мочевые катетеры, внутриматочные устройства и пр..
/Из отраслевого стандарта СССР ОСТ 42-21-2-85/.
Предметы, подлежащие стерилизации, получили название «критические изделия», поскольку их применение связано с высоким риском развития инфекции.
ДЕЗИНФЕКЦИИ ПОДВЕРГАЮТСЯ:
— изделия, не имеющие контакта с раневой поверхностью, кровью или инъекционными препаратами;
— инструменты, использованные на операции, перед их предстерилизационной очисткой для повторного применения.
/Из отраслевого стандарта СССР ОСТ 42-21-2-85/.
Различается дезинфекция высокого /полукритические предметы/ и низкого уровня /некритические предметы/.
Дезинфекции высокого уровня подлежат изделия, контактирующие со слизистой оболочкой органа или с интактной кожей — наркозные аппараты, эндоскопы желудочно-кишечного тракта, аэротерапевтические установки, инструменты для иссле-дования влагалища и пр..
Дезинфекции низкого уровня подлежат предметы, контак-тирующие только с интактной кожей и не входящие в контакт со слизистыми оболочками, а так же предметы окружающей среды, не находящиеся в непосредственном контакте с пациентом — подмышечные термометры, подкладное судно, постельное белье, медицинская мебель, полы, костыли и пр..
МЕТОДЫ АСЕПТИКИ
— использование высоких температур /автоклавирование, в сухожаровом шкафу, обжигание, кипячение/;
— низкотемпературные методы асептики:
а/ физические методы /ионизирующее излучение, ультразвук,
УФО/;
б/ химические методы /газами, парами или растворами
химических веществ/;
— микроволновая фильтрация;
— специальные санитарно-гигиенические и организационные
мероприятия.
Стерилизация достигается автоклавированием паром под давлением, горячим воздухом в сухожаровом шкафу, ионизирую-щим излучением, в газовой камере (окисью этилена, смесью ОБ, озоном, парами формалина), жидкими химическими антисептика-ми, воздействием ультразвука.
Дезинфекция достигается в сухожаровом шкафу, кипячением, обжиганием, УФО, растворами химических антисептиков, микроволновой фильтрацией.
Таким образом, горячим воздухом в сухожаровом шкафу, в зависимости от режима работы аппарата, можно достигнуть как стерилизации, так и дезинфекции.
ПРЕДСТЕРИЛИЗАЦИОННАЯ ОЧИСТКА МЕДИЦИНСКИХ ИЗДЕЛИЙ
Предстерилизационная очистка является подготовительным этапом к стерилизации.
Предстерилизационной очистке подвергаются все изделия для механического удаления белковых, жировых и механических загрязнений, обеззараженных биосред, лекарственных препаратов, окислов металлов.
Микроорганизмы, укрытые свернувшейся кровью или остат-ками других органических жидкостей, или механическими загряз-нениями, защищены от воздействия высоких температур и многих химических антисептиков.
Разъемные изделия подвергаются предстерилизационной очистке в разобранном виде. Разборка и мытье инструментария проводится только в резиновых перчатках с строгим соблюдением правил личной гигиены.
Предстерилизационная очистка осуществляется ручным или механизированным способом с помощью специального оборудо-вания /Рис.2.13/.
Рис.2.13. Машина моечная для хирургического
инструментария, шприцев, игл
Этапы предстерилизационной очистки
1. Дезинфекция медицинских изделий путем погружения в
3% растор хлорамина или 1% раствор гипохлорита кальция на 60 мин, или раствор Пресепта на 90 мин. Перчатки после операции дезинфи-цируются путем погружения их в 3% раствор хлорамина или 6% перекись водорода на 1 час.
2. Тщательное промывание изделий под проточной водой,
удаляя все загрязнения щетками. Изделия с каналами и полостями промывают с помощью шприцев, резиновых баллонов и пр..
3. Замачивание изделий в разобранном виде с заполнением каналов и полостей в горячем моющем растворе /температура 40% — 50% C/ в течение 15 минут. В процессе обработки температура моющего раствора не поддерживается.
Для замачивания могут использоваться:
— 0.5% моющий раствор порошка «Билот» /5 г порошка и 995 мл воды температуры 40% — 45% C/;
— раствор, содержащий 5 г моющего средства /»Прогресс», «Астра», «Лотос»/ + 20 мл 33% раствора перекиси водорода /пергидроль/ + 975 мл воды температуры 50-55% С;
— 3% натрий двууглекислый /питьевая сода/;
— 0,5% перекись водорода с моющими средствами «Лотос», «Лотос-автомат», «Астра», «Айна», «Маричка», «Професс». К этому комплексу добавляется ингибитор коррозии – 0,14% раствор олеата натрия. Моющий комплекс с перекисью водорода можно использовать в течение суток до 6 раз с момента приготовления при условии, что цвет раствора не изменился. Другие моющие растворы используются однократно.
4. Кипячение в течение 15 мин. при полном погружении изделий в один из следующих растворов:
— сода питьевая 2%;
— моющие средства «Лотос», «Лотос-автомат» 1,5%.
При использовании кипячения предстерилизационная очистка объединяется в один процесс с дезинфекцией.
5. Мойка инструментов в использовавшемся моющем растворе ершами или ватно-марлевыми тампонами в течение 0,5 минуты. Изделия с внутренними каналами промывают с помощью шприцев или баллонов, иглы прочищают мандренами. Механизированная предстерилизационная очистка медицинских изделий с использованием моечных машин и ультразвуковых установок мо-жет производиться только с применением разрешенных для этих целей препаратов в соответствии с инструкцией, прилагаемой к оборудованию.
6. Промывание инструментов под проточной водой для уда-ления остатков моющих средств. При использовании порошка «Биолот» в течение 3 минут, «Прогресс» — 5-6 минут, «Бланизол» — 5 минут, «Астра» и «Лотос» – 10 минут, натрий двууглекистый — 50 минут.
7. Ополаскивание изделий в дистиллированной воде в тече-ние 0,5-1 минуты для обессоливания.
8. Подсушка инструментария — проводится в сухожаровом
шкафу при температуре 80-90 гр.С в течение 15-20 мин. /до полного исчезновения влаги при визуальном контроле/.
Предстерилизационная очистка шприцев, игл и инструментария
Предстерилизационная очистка шприцев, игл и инструментария
Последовательность выполнения процедуры:
1) приготовить моющий раствор (5 г синтетического моющего средства, 15 мл 33 %-ного раствора перекиси водорода, 980 мл воды), электроплиту, ершик, мандрен, гемотесты (бензидиновый, амидопириновый, орттолуидиновый, азопирамовый или стандартный реактив), 1 %-ный спиртовой раствор фенолфталеина, лоток для шприцев, резиновые перчатки, клеенчатый передник;
2) надеть резиновые перчатки и передник;
3) промывать под проточной водой на протяжении 1 мин обеззараженные шприцы, иглы или инструментарий;
4) подогреть моющий раствор до температуры 45–50 °C;
5) окунуть в моющий раствор на 15 мин поршни, цилиндры, иглы или инструментарий;
6) промыть каждый цилиндр и поршень в моющем растворе ершиком, а иглы – мандреном, пропустить моющий раствор через каждую иглу;
7) промывать инструменты под струей холодной проточной воды на протяжении 3 мин;
8) провести контрольные пробы на выявление остатков крови и моющего средства;
9) только при получении отрицательного результата во время проведения контрольных проб промывать инструментарий на протяжении 1 мин в дистиллированной воде;
10) обсушить инструменты в разобранном виде в сухожаровом шкафу при температуре 75–85 °C.
Данный текст является ознакомительным фрагментом.
Читать книгу целиком
Поделитесь на страничке
Очистка, стерилизация, осмотр и техническое обслуживание … · Инструкции по очистке, стерилизации,
Инструкции для:
Очистка, стерилизация, осмотр и техническое обслуживание многоразовых медицинских устройств Инструкции для Stryker Orthopaedics
Содержание
1. Введение Предупреждения и меры предосторожности
2. Обзор обработки 3. Подготовка к очистке 4. Ручная очистка
Предварительная очистка Очистка Ручная дезинфекция
5.Автоматическая очистка 6. Осмотр 7. Упаковка 8. Стерилизация 9. Хранение перед использованием 10. Ссылки
Приложение 1 Инструкции по очистке
Приложение 2 Параметры США Совместимость с жесткими контейнерами
Приложение 3 Параметры США Совместимость с жесткими контейнерами (старые лотки)
Приложение Параметры 4OUS Совместимость с синей пленкой (устаревшие лотки)
Приложение 5 Параметры OUS Совместимость с жесткими контейнерами
1. Введение
Этот документ предназначен для
, в котором содержатся подробные инструкции
по обработке многоразовых
хирургических инструментов
производства Stryker
Ортопедия.Все инструменты многоразового использования Stryker
Orthopaedics
необходимо очистить
и стерилизовать, чтобы подготовить их
к использованию. Этот документ также
дает инструкции по проверке
, чтобы определить, когда
инструмент достиг конца срока службы
и
необходимо заменить.
В этом документе представлены инструкции по сборке и разборке
многокомпонентных инструментов, которые
необходимо разобрать перед очисткой и / или стерилизацией.
Компания Stryker Orthopaedics проверила
, чтобы процессы
, представленные в этих инструкциях, были эффективными.
Оборудование, операторы, очистка
агентов и процедуры — все
способствуют повышению эффективности обработки
. Медицинское учреждение
должно гарантировать, что выбранные этапы обработки
будут безопасными и эффективными.
Альтернативные методы обработки
, выходящие за рамки этого документа, могут быть подходящими для повторной обработки
; однако эти
должны быть утверждены конечным пользователем.
В случае противоречия между национальными требованиями
по очистке и стерилизации, такие требования имеют преимущественную силу над рекомендациями
Stryker Orthopaedics.
В соответствии с ISO 17664,
два метода очистки Stryker
Ортопедия многоразового использования
Инструменты представлены в
настоящей инструкции, полностью ручной метод
(раздел 4) и метод
с использованием автоматическая мойка-дезинфектор
(секция 5).По возможности
следует использовать автоматизированный метод
. Автоматический процесс очистки
более воспроизводимый и, следовательно, более надежный.
Кроме того, персонал
менее подвержен воздействию загрязненных устройств и
используемых чистящих средств.
Какой бы метод не использовался, персонал
должен всегда использовать подходящую защитную одежду и оборудование
. В частности, обратите внимание на
инструкции, предоставленные производителем чистящего средства
для правильного обращения и использования продукта.
Предупреждения и меры предосторожности
Одноразовые устройства
нельзя использовать повторно, поскольку они не предназначены для работы по назначению
после первоначального использования
, если только они не прошли переработку
на переработчике
, прямо разрешенном Stryker
Ортопедия. Только тогда
может быть уверен, что устройство
подходит для повторной обработки
и что используются правильные методы проверки
.Пожалуйста, обратитесь к
на этикетке устройства, чтобы идентифицировать
одно- или многоразовых устройств
и компонентов.
Некоторые материалы устройства могут изменять механические, физические или химические характеристики в условиях многократного использования, очистки и повторной стерилизации, что может поставить под угрозу целостность конструкции и / или материала, что приведет к снижению безопасности, производительности и / или соблюдению соответствующих требований. технические характеристики.
Stryker Orthopaedics многоразового использования
Инструменты обычно не используются в хирургических процедурах
там, где они контактируют с инфекционными тканями TSE
(Transcept Spongiform
Encephalopathies) в соответствии с определением
Всемирной организации здравоохранения
(ВОЗ).
Следовательно, дезактивация
процедур с использованием сильно агрессивных агентов
[т.е. гидроксид натрия
(NaOH) или гипохлорит натрия
(NaClO)] не являются необходимыми
и для нормальной обработки не рекомендуются
, поскольку может произойти разложение материала
. Параметры стерилизации
, рекомендуемые в этом документе, не предназначены, а параметры
не подходят для инактивации прионов
.
2. Обзор повторной обработки
Последовательность шагов, необходимых для подготовки многоразовых инструментов для повторного использования или для подготовки новых устройств к первоначальному использованию, обобщена в таблице ниже. Более подробные инструкции для каждого шага приведены на следующих страницах.
Примечание. Следует тщательно учитывать качество воды, используемой для разбавления чистящих и / или дезинфицирующих средств, а также для ополаскивания инструментов многоразового использования.
Применение свежеприготовленной очищенной воды / воды высокой степени очистки или стерильной воды для промывки с содержанием менее 100 КОЕ / мл и 0.Настоятельно рекомендуется 5 EU / мл.
Минеральные остатки жесткой воды, а также повышенное загрязнение микроорганизмами и эндотоксинами могут привести к окрашиванию устройства или помешать эффективной очистке и стерилизации.
3. Подготовка к очистке (точка использования для всех инструментов)
Место использования
После использования (максимум 2 часа
после операции) удалите крупные загрязнения с помощью салфеток из впитывающей бумаги
. Настоятельно рекомендуется интенсивное ополаскивание
многоразовых инструментов проточной водой
или перенос медицинских устройств в ванну
с дезинфицирующим раствором без альдегидов
.
Транспортировка в зону обработки Избегайте механических повреждений, следя за тем, чтобы тяжелые устройства не смешивались с хрупкими. Уделяйте особое внимание режущим кромкам, чтобы избежать травм и повреждения инструментов многократного использования. Транспортируйте инструменты многоразового использования в то место, где должна быть проведена очистка, как можно скорее. Если перенос в зону обработки может быть отложен, подумайте о том, чтобы накрыть инструменты влажной тканью, чтобы избежать высыхания почвы.
Подготовка к очистке В Приложении 1 приведены конкретные инструкции для инструментов, требующих разборки, и для некоторых инструментов, которые не следует разбирать перед очисткой.
Осторожно:
Лотки Stryker Orthopaedics и
чемоданы предназначены для транспортировки
и хранения многоразовых инструментов
. Они не предназначены для очистки и / или дезинфекции
в полностью собранном состоянии. Инструменты
необходимо вынуть из лотка
для получения надлежащих результатов очистки.
4. Ручная очистка
Предварительная очистка
Удалите крупные загрязнения, используя салфетки и раствор чистящего средства.
Погрузите многоразовый инструмент в раствор чистящего средства.
Убедитесь, что все поверхности тщательно увлажнены. Используйте шприц или пипетку, чтобы чистящий раствор достиг всех частей канюль.
При погружении в раствор убедитесь, что воздух не попадает в детали устройства.
Выдержите в течение минимального времени, рекомендованного инструкциями производителя моющего средства.
Используя подходящие щетки с мягкой щетиной, тщательно очистите инструмент многократного использования,
уделяя особое внимание шероховатым поверхностям и
деталям, на которые может попасть грязь или которые могут быть защищены от процесса очистки.
Используйте щетку с твердой щетиной для чистки режущих элементов, например наконечников сверл, канавок разверток и зубьев протяжек.
Для катетеризации используйте бутылочную щетку подходящего диаметра и длины. Убедитесь, что кисть проходит по всей длине каждой канюляции.
Управляйте шарнирно-сочлененными устройствами
и с подвижными частями.
Промойте в проточной воде, пока не будут удалены все следы чистящего раствора.
Обратите особое внимание на канюли и глухие отверстия, а также петли и стыки между сопрягаемыми деталями.
Визуально проверьте, нет ли остатков грязи, и при необходимости повторите описанные выше действия.
Дайте стечь абсорбирующей бумаге
или немедленно перенесите
на этап очистки.
Осторожно:
Никогда не используйте для чистки металлические щетки или стальную мочалку
.
Ручная очистка
Необходимое оборудование:
Ультразвуковая ванна, достаточно большая, чтобы позволить полностью погрузить инструмент многократного использования. (Рекомендуется частота 25–50 кГц.Не превышайте температуру, указанную производителем моющего средства.)
Чистящее средство, предназначенное для ручной очистки и подходящее для обработки ультразвуком. Не превышайте концентрацию, указанную производителем моющего средства.
Подходящие щетки или чистящие проволоки для доступа ко всем частям устройства. Осторожно: Никогда не используйте для чистки металлические щетки или стальную мочалку.
Шприцы (объемы от 1 до 50 мл, в зависимости от размера промываемых каналов).
Свежая очищенная вода, вода высокой степени очистки или стерильная вода для ополаскивания.
Инструкции:
Подготовьте ультразвуковую ванну
с чистящим раствором при концентрации
и температуре
, указанной производителем моющего средства
.
Полностью погрузите устройство и активируйте ванну минимум на 15 минут.
Используя подходящие щетки или чистящую проволоку, очистите устройство, уделяя особое внимание шероховатым поверхностям и деталям, которые могут быть защищены от УФ-стерилизационной системы
Заявление о методе тестирования и ввода в эксплуатацию — Заявление о методе HQ
Система УФ-стерилизации
может использоваться во многих случаях. системы очистки воды для дезинфекции и борьбы с бактериями.Ультрафиолетовая или УФ-энергия находится в электромагнитном спектре между видимым светом и рентгеновскими лучами и лучше всего может быть описана как невидимое излучение. Ультрафиолетовый свет имеет длину волны от 200 до 390 нанометров (нм). Наиболее эффективная длина волны с точки зрения микробиологической дезинфекции составляет 254 нм, поскольку именно здесь находится оптимальная энергоемкость.
Принцип системы УФ-стерилизации
Типичные системы УФ-дезинфекции включают прохождение воды через сосуд, содержащий УФ-лампу.• Когда вода проходит через этот сосуд, микроорганизмы подвергаются воздействию интенсивной энергии ультрафиолетового света, которая вызывает повреждение генетических молекул (например, нуклеиновых кислот: ДНК или РНК), необходимых для репродуктивных функций.
Чтобы уничтожить микроорганизмы, УФ-лучи УФ-системы стерилизации должны действительно попадать на клетку. Ультрафиолетовая энергия проникает через внешнюю клеточную мембрану, проходит через тело клетки и разрушает ее ДНК, предотвращая размножение. Это повреждение предотвращает размножение или репликацию микроорганизма в организме человека или животного-хозяина.Поскольку микроорганизм не может размножаться, не может возникнуть инфекция. Обеззараживание воды достигается, когда УФ-свет вызывает инактивацию микробов.
Преимущества системы УФ-стерилизации
УФ-дезинфекция не добавляет химикатов в воду. Система УФ-стерилизации эффективна против бактерий и вирусов. Криптоспоридиумы, лямблии и другие биологические патогены инактивируются, а возобновление роста бактерий прекращается. Большинство УФ-устройств имеют звуковой детектор УФ-излучения, который уведомляет пользователя о недостаточной интенсивности лампы.
Есть и недостатки, такие как регулярное обслуживание и замена лампы. УФ-устройства убивают бактерии только в одной точке системы полива и не оказывают никакого остаточного бактерицидного эффекта ниже по течению. Трубопровод системы полива, обработанный УФ-дезинфекцией, необходимо периодически дезинфицировать химическим дезинфицирующим средством. Обрабатываемая вода не должна быть мутной или мутной. Любой уровень цвета, присутствующий в воде, будет препятствовать способности УФ-излучения проникать в нее и уничтожать микроорганизмы внутри.
Дезинфекция — это обычно окончательный процесс очистки воды. Цель дезинфекции — уничтожить патогенные микроорганизмы в воде и обеспечить дополнительную защиту от последующего заражения.
Ниже приводится точное описание метода, которое может быть полезно, когда кто-то хочет провести тестирование и ввод в эксплуатацию УФ-системы стерилизации.
Пусконаладочные работы системы и проверки завершения строительства фильтра
Перед вводом системы в эксплуатацию необходимо убедиться в следующем.
- Система была проверена по утвержденным монтажным чертежам.
- Убедитесь, что давление на входе в фильтр превышает 2,5 бар (38 фунтов на кв. Дюйм) во время цикла промывки.
- Убедитесь, что фильтр установлен в правильном направлении потока.
- Убедитесь, что все контрольные трубки подключены правильно и все соединения затянуты.
- Убедитесь, что трехходовой мини-клапан установлен в автоматическое положение. Стрелка на ручке должна указывать на АВТО, а наклейка ο на фильтре.
- Убедитесь, что установленная труба соответствует утвержденному чертежу или номинальный диаметр должен составлять 3 дюйма (75 мм).
- Если были установлены рекомендуемые запорные клапаны на входе и выходе, убедитесь, что они закрыты.
Проверки системы перед вводом в эксплуатацию УФ-стерилизатора
Проверьте радиационную камеру на герметичность и вентиляцию в соответствии со следующей процедурой:
- Ослабьте (откройте) вентиляционный винт на радиационной камере
- Медленно откройте запорный клапан на входе радиационной камеры
- Заполните радиационную камеру до тех пор, пока вода не начнет выходить из вентиляционного винта
- Закройте вентиляционный винт, приложив небольшое усилие
- Проверьте радиационную камеру на герметичность
- Откройте запорный клапан после радиационной камеры (необходимо только для ручного закрытия) запорный клапан)
Этап ввода в эксплуатацию системы УФ-стерилизации
При вводе системы фильтрации в эксплуатацию необходимо выполнить следующие шаги:
- Медленно откройте запорный клапан на входе фильтра.Вода потечет в фильтр.
- Проверить герметичность и при необходимости отремонтировать.
- Убедитесь, что минимальное давление на входе остается 2,5 бара (38 фунтов на кв. Дюйм) или выше.
- Медленно откройте запорный клапан на выходе из фильтра.
- Если есть перепускной клапан, закройте его медленно.
- Убедитесь, что поток через фильтр не превышает заявленный максимальный расход фильтра.
- Начните промывку вручную, повернув трехходовой клапан в положение ОТКРЫТО на несколько секунд, а затем снова поверните его в положение АВТО.
- Во время цикла самоочистки проверьте давление на входе фильтра и в камере ротора.
Примечание. Минимальное давление в камере ротора должно быть на 1,5 бара (22 фунта на квадратный дюйм) ниже, чем давление на входе.
Ввод в эксплуатацию УФ-системы фильтрации , необходимо выполнить следующие шаги:
- Включить главный выключатель или подсоединить сетевой штекер
- Проверьте параметры в режиме программирования системы управления и при необходимости измените их, см. Настройки рабочего состояния.
- Включить систему УФ-дезинфекции кнопкой СТАРТ / СТОП; нажмите кнопку START / STOP и удерживайте не менее 2 секунд.
- Если система управления переходит в состояние ПАУЗА, задействуйте контакт паузы. После зажигания УФ-лампам может потребоваться несколько минут, чтобы они достигли своего полного УФ-излучения.
Рекомендации по стерилизации | ASCRS
В феврале 2015 года CMS опубликовала в информационном бюллетене электронного провайдера Medicare Learning Network (MLN) 26 февраля, в котором разъясняется их позиция в отношении использования короткоцикловой стерилизации паром.В частности, путаница возникла после того, как CMS выпустила Меморандум об изменении терминологии и обновлении опроса и сертификации (S&C) 09-55 относительно немедленного использования паровой стерилизации (IUSS) в хирургических учреждениях в августе 2014 года. В результате этой путаницы ASCRS, американец Академия офтальмологии (AAO) и Общество амбулаторной офтальмохирургии (OOSS) дважды встречались с CMS, чтобы выразить нашу озабоченность по поводу новой политики, сосредоточив внимание на обучении персонала CMS в отношении этиологии синдрома токсического переднего сегмента (TASS) и эндофтальмита. и предоставление результатов недавнего обзора ASC их текущей практики стерилизации и очистки инструментов.Как мы уже сообщали, путаница связана с номенклатурой, используемой для описания процессов стерилизации. CMS считает, что термин IUSS, который сейчас запрещен на регулярной основе, относится к практике, ранее известной как «мгновенная стерилизация».
Это разъяснение рекомендаций 2014 г. явилось прямым результатом поддержки со стороны ASCRS, AAO и OOSS. В своем заявлении CMS отметила, что IUSS — это термин, принятый в настоящее время для описания процесса паровой стерилизации инструмента, который необходим немедленно и не предназначен для хранения для последующего использования, и который допускает минимальную сушку или ее отсутствие после цикла стерилизации.IUSS неприемлем для использования в качестве стандартного метода стерилизации. Он заменяет гораздо менее точный и устаревший термин «мгновенная стерилизация».
CMS подчеркнула, что IUSS — это не то же самое, что стерилизация «коротким циклом», которая представляет собой форму конечной стерилизации, приемлемую для рутинного использования упакованных / содержащихся загрузок, когда предварительная очистка инструментов выполняется в соответствии с требованиями производителей. Инструкции и загрузка соответствуют инструкциям производителя устройства по применению (IFU), включают использование времени полного высыхания и упакованы в обертку или жесткий стерилизационный контейнер, утвержденный для дальнейшего использования.CMS заявила, что «использование коротких циклов стерилизации особенно распространено в учреждениях, где проводятся операции на глазах, и допустимо, когда соблюдаются все IFU (т.е. стерилизатор, устройство и производитель контейнеров)».
Если у вас есть вопросы, обращайтесь к Нэнси Макканн, директору ASCRS / ASOA по связям с государственными органами, по адресу [email protected].
Сравнение стерилизации ЭО и VPA
По мере развития медицинских технологий производители устройств должны рассматривать методы стерилизации, которые не повредят электронике, лекарствам или биопрепаратам.
Мэтт Конлон, Решения для стерилизации Revox
[Изображение любезно предоставлено Revox Sterilization Solutions]
Индустрия медицинского оборудования претерпела впечатляющие преобразования за последние несколько лет, результатом которых стали новые инновационные устройства и решения. По мере того, как компании продолжают вводить новшества, они обнаруживают, что обычно используемые методы стерилизации накладывают ограничения с точки зрения эффективности, качества или производственных процессов многих новых компонентов устройств (электроника), покрытий (лекарств) или содержимого (лекарств или биопрепаратов).Новые подходы могут помочь преодолеть ограничения устаревших методов стерилизации.
(Сеть с экспертами Revox на DeviceTalks West, 11–12 декабря в округе Ориндж, Калифорния)
Проблемы окиси этилена
Правильная и тщательная стерилизация медицинских изделий имеет решающее значение. Одним из наиболее часто используемых методов стерилизации является воздействие этиленоксида (ЭО) для уничтожения микроорганизмов. Хотя другие методы сопряжены со своими проблемами, ЭО представляет наибольший риск с точки зрения безопасности пациентов и работников, а также затрат, связанных с требованиями по снижению рисков.
Следующие три области представляют собой наиболее серьезные проблемы для производителей медицинского оборудования, связанные с ЭО:
1. Совместимость материалов
Новые материалы для производства медицинских устройств, такие как биосенсоры, биоабсорбируемые материалы и электроника, не могут противостоять методам стерилизации, вызывающим нагревание и влажность, таким как ЭО. Кроме того, любые химические реакции, которые могут происходить при более высоких температурах и с влажностью, могут вызвать неблагоприятные химические реакции, которые ускоряют разрушение и коррозию устройства.В ситуациях, когда лекарство или биологический препарат присутствует во время стерилизации, например, с предварительно заполненными шприцами или стентами, покрытыми лекарством, лекарство также подвергается риску. Тепло может повлиять на активный фармацевтический ингредиент (API) или биологический препарат и повлиять на стабильность или pH, что угрожает его общей функциональности.
2. Безопасность пациентов и сотрудников
Ограничения, изложенные в стандарте ISO 10993-07, устанавливают правила относительно того, сколько ЭО можно оставить на медицинских устройствах. Эта сумма зависит от предполагаемого использования устройства.Особое внимание этому вопросу уделяется во Франции, где 85% одноразовых стерильных устройств в отделениях для новорожденных стерилизуются с использованием ЭО. Из-за этого в процесс предложения ISO входят более строгие правила, чтобы еще больше препятствовать использованию ЭО, требуя, чтобы производители предоставили документацию с обоснованием выбора ЭО для стерилизации (в отличие от альтернативного метода), а также количественной оценки и ограничения совокупности (несколько продуктов) потенциальное воздействие на особые группы пациентов, например новорожденных.Из-за сложности выполнения этих расчетов (с потенциально несколькими продуктами производителя, используемыми для одного пациента) большинство предпочло бы подход «риск против пользы». Это позволяет продолжать использовать процессы стерилизации ЭО на жизненно важных устройствах, для которых нет других коммерчески осуществимых методов стерилизации.
Другой стороной этого вопроса является опасность ЭО для здоровья и безопасности сотрудников производственного предприятия, использующего его для стерилизации.OSHA имеет строгие правила в отношении воздействия ЭО, которых производители медицинского оборудования должны придерживаться при использовании его на своих предприятиях. Например, в камерах ЭО должны использоваться взрывобезопасные средства содержания, а сотрудники должны принимать всесторонние меры предосторожности в отношении здоровья и безопасности. Хотя защитные меры являются стандартными операционными процедурами, когда процесс / материал представляет опасность для сотрудников, эти меры могут оказаться дорогостоящими. Немногие производители, которые еще не имеют опыта работы с риском и стоимостью обработки ЭО на месте, готовы взять на себя нормативные требования и препятствия, связанные с безопасностью, которые это создает.
3. Производственная эффективность
Хотя время самого процесса стерилизации сильно варьируется в зависимости от стерилизуемого продукта, каждый процесс ЭО требует периодов до стерилизации и аэрации после обработки. Это может значительно продлить весь процесс, от нескольких дней до недель. Из-за рисков и затрат, связанных со стерилизацией ЭО на месте, примерно 75% медицинских изделий отправляется контрактным компаниям, предоставляющим услуги по стерилизации.В зависимости от местоположения стерилизационного помещения и логистики распределения самого продукта, это также может значительно увеличить время транспортировки и потребности в запасах, что повлияет на стоимость проданных товаров. Операции по ЭО на месте сопряжены с затратами на необходимое снижение рисков.
VPA как альтернатива
Новые методы стерилизации могут включать свет высокой интенсивности / импульсный свет, микроволновое излучение, звуковые волны, ультрафиолетовый свет и испаренную перуксусную кислоту (VPA).
Если производитель хочет перейти на один из этих новых методов, изменение требует, чтобы продукт и процесс стерилизации были повторно отправлены на разрешение 510 (k). Тем не менее, имеет смысл рассмотреть эти альтернативные методы, если компания разрабатывает новый продукт, претерпевает изменения, которые все равно необходимо будет отправить на разрешение FDA 510 (k), или планирует новые производственные процессы / участки.
VPA может улучшить совместимость материалов и обеспечить интеграцию менее дорогих конструкций и материалов за счет исключения использования тепла для стерилизации, которое может повредить новые, чувствительные к теплу материалы, такие как датчики и биопрепараты.Вместо использования тепла запатентованный биоцид перуксусной кислоты (PAA) вводится в вакуумную камеру при комнатной температуре (от 18 ° C до 30 ° C) в виде пара, аккуратно стерилизуя продукт с общим временем обработки от двух до четырех часов. Процесс VPA не канцерогенный, невзрывоопасный / огнеопасный, не требует внешней вентиляции и в течение нескольких часов разрушается до H 2 0, CO 2 и O 2 .
Кроме того, хотя новые методы стерилизации, такие как газовая плазма и испаренная перекись водорода (VHP), доказали свою эффективность и полезность для различных применений, они не предлагают коммерческой применимости в промышленном стерилизационном пространстве с точки зрения их пропускной способности.Благодаря вместимости камеры до восьми поддонов и короткому времени обработки VPA теперь является коммерчески осуществимой альтернативой, которая может помочь производителям еще больше снизить риск в дереве принятия решений о соотношении рисков и выгод. VPA также может использоваться в качестве ценного инструмента для снижения бионагрузки при предтерминальной стерилизации, устраняя колебания бионагрузки перед стерилизацией и обеспечивая более низкую степень воздействия при конечной стерилизации при любом используемом методе.
Мэтт Конлон — вице-президент и генеральный директор Revox Sterilization Solutions (Миннеаполис).
.

 14. Предстерилизационная очистка. Контроль качества предстерилизационной очистки
14. Предстерилизационная очистка. Контроль качества предстерилизационной очистки
 Предстерилизационную обработку проводят в центральном стерилизационном отделении в ЛПУ при его наличии или в лечебном отделении ЛПУ.
Предстерилизационную обработку проводят в центральном стерилизационном отделении в ЛПУ при его наличии или в лечебном отделении ЛПУ. Мойку осуществляют с помощью ерша, ватно-марлевых тампонов, тканевых салфеток; каналы изделий промывают с помощью шприца. Использование ерша при очистке изделий из резины не допускается.
Мойку осуществляют с помощью ерша, ватно-марлевых тампонов, тканевых салфеток; каналы изделий промывают с помощью шприца. Использование ерша при очистке изделий из резины не допускается.
 Ватно-марлевые тампоны, используемые для обработки, меняются для каждой обработки.
Ватно-марлевые тампоны, используемые для обработки, меняются для каждой обработки.
 Готовый раствор может храниться в плотно закрытом флаконе в темноте при +4˚С (в холодильнике) 2 месяца; при комнатной температуре 18-23˚С не более месяца. Умеренное пожелтение раствора в процессе хранения без выпадения осадков не снижает его рабочих свойств.
Готовый раствор может храниться в плотно закрытом флаконе в темноте при +4˚С (в холодильнике) 2 месяца; при комнатной температуре 18-23˚С не более месяца. Умеренное пожелтение раствора в процессе хранения без выпадения осадков не снижает его рабочих свойств. Если раствор не изменил свой цвет, контроль качества отрицательный, инструменты могут быть подвергнуты стерилизации.
Если раствор не изменил свой цвет, контроль качества отрицательный, инструменты могут быть подвергнуты стерилизации. …
…