Микроскопический колит — что такое, симптомы и лечение
Микроскопический колит представляет собой группу хронических заболеваний, характеризующихся водянистой диареей, отсутствием макроскопических изменений при проведении колоноскопии и специфическими гистологическими признаками, обнаруживаемыми при микроскопическом исследовании биоптатов (отсюда и происхождение названия данной патологии)
Содержание статьи
Подробнее о патологии
С 1984 года начались исследования в центрах Европы, которые показали увеличение случаев микроскопического колита. Распространенность его стала сопоставима с неспцифическим язвенным колитом и болезнью Крона. При наличии у пациентов хронической диареи наряду с классическими диагностическими признаками необходимо исключать микроскопический колит.
Считается, что это заболевание пожилых людей, чаще женщин, отягощенных различными аутоиммунными заболеваниями такими, как сахарный диабет, тиреоидит (заболевание щитовидной железы) и др.
По данным эпидемиологических исследований заболеваемость и распространенность микроскопическим колитом сопоставимы с таковыми при болезни Крона и язвенном колите. Тем не менее, в клинической практике микроскопический колит до сих пор относится к редко диагностируемым заболеваниям, поскольку большинство клиницистов и патологоанатомов имеют лишь смутное представление о морфологических принципах его диагностики.
Как правило, микроскопический колит является болезнью пожилых – на момент постановки диагноза средний возраст пациентов составляет 65 лет. Однако возраст 25% среди заболевших не достигает 45 лет. Именно поэтому у молодых пациентов с хронической диареей при проведении дифференциально-диагностического поиска не стоит забывать и о микроскопическом колите. Появление МК в детском возрасте является казуистикой, однако в литературе опубликованы и такие клинические случаи.
В структуре заболеваемости МК преобладают женщины. Клинические проявления ЛК и КК не имеют каких бы то ни было различий. Основным клиническим проявлением данных нозологий является хроническая диарея без примесей крови, как правило, имеющая водянистый характер, приводящая к императивным позывам (70% пациентов) и даже к недержанию кала (40% пациентов). В тяжелых случаях примерно у половины пациентов дефекация может достигать 15-ти раз в сутки (включая ночные позывы). Несмотря на значительные потери жидкости, дегидратация организма и электролитные нарушения встречаются достаточно редко.
Естественное течение заболевания недостаточно изучено, но по данным последних проспективных исследований риск развития рецидива после отмены терапии буденофальком достаточно высок и составляет 60–80%, что свидетельствует в пользу хронически рецидивирующего течения МК.
Причины возникновения патологии
Механизмы формирования микроскопического колита неизвестны. Данные литературы свидетельствуют о взаимосвязи болезни с патологическими процессами защитных сил организма, нарушением всасывания желчных кислот и курением. В основе болезни может лежать патологическая реакция иммунной системы эпителия толстой кишки. Она связана с поступлением в избыточном количестве бактериальных, пищевых, лекарственных веществ. Иммунитет реагирует на них как на чужеродные и атакует здоровые ткани организма. Развивается хронический воспалительный процесс.
Провоцирующую роль в возникновении микроскопического колита может играть прием лекарственных препаратов:
- нестероидных противовоспалительных средств ─ жаропонижающих и обезболивающих препаратов типа аспирин, ибупрофен, диклофенак;
- лекарств при лечении болезней, связанных с увеличением выработки соляной кислоты в желудке, ─ лансопразол, омепразол;
- препаратов, перечисленных в пункте 1 и 2, одновременно;
- психотропных лекарств третьего поколения для терапии тревожных расстройств и депрессии.
Однако взаимосвязь между принятием перечисленных лекарственных средств и воспалением остается пока малоизученной.
Виды заболевания
Существует два вида микроскопического колита: коллагеновый и лимфоцитарный.
Лимфоцитарный колит. Патология определяется рассеянным повышением количества лимфоцитов слизистой поверхности толстой кишки. Число главных клеток иммунной системы возрастает с 4,4 – 5,2 до 24 и более штук на 100 клеток эпителия. Распределение этих клеток по кишечнику идет неравномерно. Они скапливаются по большей части в куполе слепой кишки, начальном сегменте ободочной кишки. На некоторых сегментах слизистой поверхности происходит шелушение и сплющивание эпителия. Диагноз подтверждается на основе типичных изменений в тканях внутренней оболочки.
Лимфоцитарный колит не перерастает в злокачественные опухоли. При тщательном врачебном исследовании значительных ухудшений в организме не обнаруживается. Только чуть повышается скорость оседания эритроцитов (СОЭ). Толстая кишка продолжает полноценно функционировать. Потеря питательных веществ вследствие недостаточности всасывания кишечника бывает нечасто. Упорное продолжение жидкого стула бывает только у 7% пациентов. Лимфоцитарный колит может с течением времени преобразоваться в коллагеновый колит.
Коллагеновый колит. При коллагеновом колите происходит уплотнение слоя коллагена, находящегося под поверхностным эпителием толстой кишки. Кишка при этом становится неправильной формы, у нее неровные границы. Как и в предыдущем типе колита, повреждается часть слизистой оболочки кишки, содержание лимфоцитов и эозинофилов также увеличивается.
Причины возникновения коллагенового колита тоже неизвестны. Есть версия, что уплотнение коллагенового слоя происходит из-за нарушения работы клеток соединительной ткани (фибробластов) как реакция на стимуляцию неизвестным раздражителем. Возможно, раздражающим фактором могут быть нестероидные противовоспалительные лекарственные средства. При этом от начала принятия этих лекарств до появления симптомов проходит приблизительно 5 лет. Во врачебной практике был эпизод формирования коллагенового колита после назначения симвастатина — лекарства для профилактики сердечно-сосудистых болезней.

Коллагеновый колит зачастую сочетается с эндокринными заболеваниями, что предполагает его аутоиммунное происхождение — идет патологическая выработка агрессивных клеток против здоровых тканей организма. Заболевание в 10 – 20 раз чаще встречается у женщин, чем у мужчин. Колит протекает остро в 35% клинических случаев.
Коллагеновый колит в основном протекает хронически, опасность перерождения в злокачественную опухоль маловероятна. Значительное перерождение слизистой поверхности толстого кишечника отсутствует. Изредка бывает отек, нарушение сосудистого рисунка.
Симптомы патологии
Главными проявлениями лимфоцитарного колита являются:
- Жидкий стул, который носит периодический характер, возможны улучшения с последующим повторением поноса. Диарея может длиться от нескольких месяцев до нескольких лет. Стул жидкого характера не содержит следов крови.
- Повторяющиеся болевые ощущения в животе.
- Уменьшение веса на фоне течения заболевания и постоянной диареи.
Диагностика
Микроскопический колит (МК) остается гистологическим диагнозом. При этом информация о клиническом течении всегда должна быть предоставлена морфологу.
Анализ данных крупных ретроспективных исследований показал, что наличие диареи непосредственно не позволяет идентифицировать пациентов с высоким риском обнаружения МК при гистологическом исследовании. Но у пациентов старше 60 лет значительно повышается вероятность обнаружения патологических изменений при морфологическом исследовании, а наиболее вероятным диагнозом будет являться именно МК.

Проведение гистологического исследования необходимо не только для постановки диагноза и проведения дифференцировки между двумя главными подтипами (лимфоцитарным колитом и коллагеновым), но и для исключения других возможных причин развития хронической диареи. В ходе эндоскопической диагностики слизистая оболочка толстого кишечника практически всегда соответствует норме, но изредка можно обнаружить незначительные изменения, такие как отек, эритема, нарушение сосудистого рисунка или даже дефекты слизистой оболочки.
При МК морфологические изменения могут быть диффузными и очаговыми. Анализ данных проспективных мультицентровых исследований показывает, что коллагеновые тяжи толщиной более 10 мм чаще встречаются в правой половине кишечника, (достигая максимальных значений в слепой и восходящей ободочной кишке) и значительно реже в сигмовидной и прямой кишке, тогда как мононуклеарное воспаление в собственной пластинке равномерно распределено среди различных сегментов толстого кишки.
Рекомендуется брать материалы для гистологического исследования на протяжении всей толстой кишки, тогда как биопсии, полученные только из прямой кишки или из прямой кишки и сигмовидной могут привести к ложноотрицательным результатам в 41% или 21% случаев соответственно. При этом, предпочтительно, чтобы биоптаты были помещены в различные контейнеры.
Дифференциальный диагноз
Были опубликованы ряд случаев, когда у пациентов были клинические черты микроскопического колита, но для постановки диагноза не «выполнялись» все морфологические критерии лимфоцитарного или коллагенового колита. В этих случаях, в собственной пластинке слизистой наблюдается воспалительная инфильтрация, а расположение коллагеновых волокон отличается от нормы, но их толщина не достигает 10 μм, а увеличение количества ИЭЛ не достигает 20 клеток на 100 эпителиальных клеток.
В связи с этим были предложены следующие термины, которые отражают изменения в гистологической картине, но не отражают клинические различия: пограничный ЛК, частичный МК, МК неуточненный и неполный ЛК. Атипичные формы до сих пор остаются спорными и не являются общепринятыми. Кроме того, в ряде случаев этим больным клинически был установлен диагноз синдрома раздраженного кишечника.
Лечение патологии
Подходы к лечению лимфоцитарного и коллагенового колита идентичны. В первую очередь, следует отменить больному лекарственные препараты, которые могли спровоцировать развитие микроскопического колита, в частности — НПВП, блокаторы Н2-рецепторов гистамина, ингибиторы протонной помпы, статины, карбамазепин.
Проводится коррекция диеты с исключением из рациона продуктов, способствующих усилению перистальтики толстой кишки (крепкий кофе, шоколад, жирные сорта мяса и рыбы, копченые продукты, свежие овощи и фрукты, сдоба, изделия с кремом, концентрированные соки, алкоголь, холодные и газированные напитки, кулинарные жиры, изделия из пшенной, перловой, ячменной крупы, цельное молоко, кислый творог, жирная сметана, мороженое).
Используются немедикаментозные фитотерапевтические методы лечения. Рекомендуются отвары растений, содержащих дубильные вещества: кровохлебки корневище и корень (иван-чай) применяют по 1 столовой ложке 5–6 раз в день, лапчатки корневища — по 1 столовой ложке 3 раза в день, черемухи плоды — по полстакана 2–3 раза в день, настой соплодий ольхи (1:20) — по 1 столовой ложке 3–4 раза в день, отвар плодов черники или коры дуба — по 2 столовые ложки 3 раза в день.
Касательно медикаментозной терапии, в настоящее время базисным препаратом для коррекции микроскопических колитов, эффективность которого оправдана с позиций доказательной медицины, является топический стероид будесонид. Он легко проникает через клеточные мембраны, высвобождается в подвздошной кишке, быстро подвергается метаболизму в печени и становится биологически неактивным.
Преимуществом будесонида (буденофалька) является его максимальная концентрация в очаге воспаления, в слизистой оболочке толстой кишки, а также отсутствие его системного действия, что обусловливает минимальное количество побочных эффектов. При коллагенозных колитах буденофальк назначают внутрь в дозе 9 мг (3 раза по 3 мг) в сутки до достижения ремиссии.
В рамках трех плацебо-контролируемых исследований, в которых приняли участие 94 пациента, показано, что будесонид является высокоэффективным препаратом для лечения коллагенозного колита. Самое крупное из этих исследований охватывало 51 пациента с гистологически подтвержденным коллагеновым колитом, которых в течение 6 недель лечили будесонидом в дозе 9 мг в сутки или плацебо. В группе, принимавшей будесонид, клинической ремиссии достигли 87% пациентов, в то время как в группе, принимавшей плацебо, — всего 14%.
Гистологическое улучшение достигнуто в 61 и 4,5% случаев соответственно. Данные мета-анализа выявили клиническое улучшение у 81% пациентов с улучшением гистологических показателей у 72%. Эти данные недавно были подтверждены анализом Cochrane. Предварительное исследование, контролируемое плацебо, лимфоцитарного колита дало такие же положительные результаты с уровнем клинической ремиссии через 5 недель 86 и 47%.
Эффективность будесонида доказана не только для лечения обострений микроскопических колитов, но и для поддержания клинической ремиссии коллагенозного колита. В ходе рандомизированного исследования, контролируемого плацебо (O. Bonderup и соавт., 2009), в котором приняли участие 42 пациента с гистологически подтвержденным коллагенозным колитом, клинически проявляющимся диареей более 3 раз в сутки, в течение 6 недель назначали будесонид перорально в дозе 9 мг в сутки.
В дальнейшем больных, достигших ремиссии, рандомизировали на 2 группы по 17 человек: больным основной группы в течение 24 недель проводили поддерживающую терапию будесонидом в дозе 6 мг в сутки, пациенты второй группы получали плацебо. Результаты исследования продемонстрировали, что поддерживающая терапия будесонидом позволила сохранить состояние клинической ремиссии у 76,5% больных, прием плацебо — лишь у 12% (р < 0,001).
Через 48 недель (по окончании периода последующего наблюдения, когда пациенты обеих групп не принимали никаких препаратов) этот показатель составил 23,5 и 12% соответственно. Также было продемонстрировано, что длительное применение будесонида у пациентов, страдающих коллагенозным колитом, характеризуется хорошей переносимостью. Таким образом, будесонид может рассматриваться в качестве препарата первой линии для лечения коллагенозного колита.
При сохраняющейся диарее на фоне вышеперечисленной терапии хорошего эффекта можно достичь с помощью применения препаратов 5-аминосалициловой кислоты (5-АСА), например месалазина. Препараты 5-AСК уменьшают активность воспалительного процесса, ингибируя синтез метаболитов арахидоновой кислоты, активность нейтрофильной липоксигеназы. Они также тормозят миграцию, дегрануляцию и фагоцитоз нейтрофилов.
Иммуномодуляторное действие 5-AСК проявляется и в подавлении секреции лимфоцитами иммуноглобулинов. Месалазин (салофальк, пентаса и др.) назначают в дозе 1,5–4 г в сутки в течение 1–2 месяцев до достижения клинического эффекта, после чего продлевают поддерживающую терапию еще на 2–3 месяца с постепенным снижением суточной дозы вплоть до полной отмены.
В качестве симптоматической терапии при минимальной выраженности клинической симптоматики достаточно хороший эффект достигается с помощью назначения антидиарейных препаратов, например, лоперамида в дозе 2–4 мг внутрь однократно с последующим приемом по 2 мг после каждого акта дефекации, не превышая суточную дозу — 16 мг, а также дополнительное назначение энтеросорбентов (холестирамин, полифепан, энтеросгель). Эти препараты способствуют связыванию желчных кислот и бактериальных токсинов в толстом кишечнике, которые могут участвовать в патогенезе диареи. Холестирамин назначают в дозе 4 г (1 пакетик) 1–3 раза в сутки перед едой, энтеросгель — по 1 столовой ложке 3 раза в день через 2 часа после приема пищи.
Хороший эффект в коррекции легких форм микроскопического колита достигается при назначении вяжущих и обволакивающих средств, обладающих антидиарейным, противовоспалительным и антибактериальным действием: препаратов висмута, смекты, таннальбина. Доза висмута субсалицилата составляет 0,35 г внутрь 3 раза в сутки, смекты — по 1 пакетику 3–4 раза в день перед едой. Продолжительность терапии – до 2 месяцев.
В случаях, когда заболевание имело острое начало, сопровождалось повышением количества лейкоцитов в кале и увеличением скорости оседания эритроцитов, возможно применение антибактериальных препаратов: метронидазола по 500 мг внутрь 3 раза в день, ципрофлоксацина по 500 мг внутрь 2 раза в сутки, тетрациклина по 200 мг внутрь 4 раза в сутки.
При выраженной клинической активности, а также при отсутствии эффекта от лечения топическими стероидами и препаратами 5-АСК показано применение преднизолона. Начальная доза составляет обычно 30–40 мг в сутки. Через 4–6 недель лечения при достижении ремиссии дозу постепенно снижают в течение 8 недель (на 5 мг в неделю) до достижения поддерживающей дозы 5–10 мг в сутки или полной отмены с переходом на препараты 5-АСК. Длительность приема системных стероидов ограничивают системные побочные проявления, а также малая эффективность в поддержании клинической ремиссии.
В качестве нового направления терапии микроскопических колитов изучается возможность применения пробиотиков, в частности штамма E.coli Nissle 1917. В пилотном исследовании, проведенном A. Tromm (2004), на 14 больных коллагенозным колитом, получавшим 100 мг E. coli Nissle 1917 два раза в день, получены следующие результаты: у 11 больных (78,6%) на фоне терапии отмечалось достоверное уменьшение частоты стула, тогда как 3 пациента (21,4%) не ответили на лечение. Частота стула уменьшилась с 7,6±4,8 до 3,7±5,8 в день (р = 0,0034). Эти результаты послужили основанием для проведения контролируемых исследований, которые продолжаются в настоящее время.
По данным пилотного исследования Madisch и соавторов (2005) попытки применения экстракта Boswellia serrata (ладана) у больных коллагенозным колитом не подтвердили эффективность этого препарата.
В случаях рефрактерного течения коллагенового и лимфоцитарного колита проводится хирургическое лечение — наложение илеостомы, которое позволяет достичь клинической и гистологической ремиссии у данной категории больных.
Диета
Конкретных диет не существует. Пищевые продукты, содержащие кофеин, или лактоза должны быть исключены из рациона, так как они стимулируют секрецию жидкости в толстой кишке. Если пациент не в состоянии переваривать жиры, низкое содержание жиров в рационе может быть полезным. Следует избегать приема НПВП (ибупрофен и пр.), так как исследования показали, что они могут быть связаны с коллагеновым колитом. Однако прием парацетамола (ацетаминофен) является допустимым.
Организация лечебного питания предполагает диету, способствующую снижению секреторной и моторной функции кишечника. Рекомендуют нежирные мясо и рыбу (вареные или приготовленные на пару), паровые омлеты. Количество жиров следует ограничить до 55-60 г, углеводов — до 250 г. Исключают молоко и ограничивают поступление клетчатки. Из рациона также исключают продукты, в отношении которых существует непереносимость. Возможно применение отваров растений, содержащих дубильные вещества и обладающих вяжущим действием (гранат, отвар плодов черники, черемухи, коры дуба).
Лечение народными средствами
Кроме средств традиционной медицины, в борьбе с микроскопическим колитом эффективны народные средства. Широкое применение имеют рецепты с содержанием дубильных веществ:
- Смесь из шалфея, василька и ромашки. Для приготовления необходимы по 1 части каждого растения в сухом измельченном виде. Смеси должно получиться в расчете 1 ложка трав на стакан кипятка. Отвар кипятить 15 минут, затем профильтровать и дать остыть. Принимать по 1 ложке каждые два часа, исключая ночное время. Курс терапии может быть длительный, постепенно можно уменьшать дозу выпиваемого отвара и промежутки между приемами.
- Чай из малины. На 1 стакан напитка необходимо 2 ложки ягод или листьев. После закипания настаивать чай около получаса. Пить по полстакана до еды 3-4 раза в день.
- Чай из мяты. На стакан чая необходимы две ложки мяты. После закипания отвара дать настояться около 20 минут. Чай пить по полстакана за 20 минут до приема пищи 2-3 раза в день.
- Смесь шалфея и полыни. Для приготовления отвара необходимы 1 ст. л. смеси в равных долях каждого ингредиента. Вскипятить смесь в стакане кипятка, затем настаивать полчаса. Отвар процедить, остудить, принимать по столовой ложке каждые 2 часа.
- Настойка прополиса. Ее следует развести стаканом кипятка (на 1 стакан необходимо 30-40 капель). Пить за час до приема пищи 3 раза в день.
- Спиртовая настойка ольхи. Для ее приготовления нужно 50 г. шишек ольхи и пол литра спирта. Настаивать около 3 недель. Периодически взбалтывать содержимое, по готовности процедить. Принимать по 30 капель до еды трижды в день.
Прогноз
Прогноз для микроскопического колита при современном лечении благоприятный. Симптомы у большинства пациентов постепенно разрешаются полностью. При этом, как правило, нормализуется гистологическая картина.
Профилактика не разработана. При возникновении заболевания, для последующего успешного его лечения и достижения ремиссии, пациенту необходимо изменить характер питания и не принимать НПВП.
Источники:
bredihina.ru/tolstaya-kishka/mikroskopicheskii-kolit/
https://medprosvita.com.ua/mikroskopicheskijj-kolit-sovremennoe/
med.vesti.ru/articles/zabolevaniya/vospalenie-tolstoj-kishki-simptomy-i-lechenie-kolita/
https://www.kronportal.ru/forum/showthread.php/19802-Микроколиты-Лимфоцитарный-и-коллагеновый-колит
gastritam.net/bolezni/kolit/limfotsitarnyj-2.html
https://diseases.medelement.com/disease/другие-уточненные-неинфекционные-гастроэнтериты-и-колиты-k52-8/4696
Данный материал носит исключительно субъективный характер и не является руководством к действию. Определить точный диагноз и назначить лечение может только квалифицированный специалист.
Последнее изменение: 19.03.2020
Микроскопический колит — диагностика и лечение
 Микроскопический колит — редко диагносцируемая патология толстой кишки, проявлением которой являются поносы. При проведении колоноскопического исследования при микроскопическом колите не обнаруживается изменений слизистой оболочки толстой кишки. Только биопсия слизистой выявляет специфические микроскопические изменения — именно отсюда и возникло название микроскопический колит.
Микроскопический колит — редко диагносцируемая патология толстой кишки, проявлением которой являются поносы. При проведении колоноскопического исследования при микроскопическом колите не обнаруживается изменений слизистой оболочки толстой кишки. Только биопсия слизистой выявляет специфические микроскопические изменения — именно отсюда и возникло название микроскопический колит.
С 1984 года начались исследования в центрах Европы, которые показали увеличение случаев микроскопического колита. Распространенность его стала сопоставима с неспцифическим язвенным колитом и болезнью Крона. При наличии у пациентов хронической диареи наряду с классическими диагностическими признаками необходимо исключать микроскопический колит.
Считается, что это заболевание пожилых людей, чаще женщин, отягощенных различными аутоиммунными заболеваниями такими, как сахарный диабет, тиреоидит (заболевание щитовидной железы) и др.
Симптомы микроскопического колита
Основным клиническим проявлением заболевания является хронический понос без примесей крови, который может носить водянистый характер, приводить к ложным позывам на стул и недержанию кала. Количество дефекаций может быть от 3 и более раз, и в тяжелых случаях до 15 раз в сутки и чаще. Обращается внимание не на частоту стула, а его консистенцию (водянистый стул).
Другими симптомами могут быть боль в животе, дискомфорт, спазм, потеря в массе тела за счет поносов и ограничения приема пищи, что требует исключения целиакии. Клинические признаки наиболее выражены в период обострения заболевания и уменьшаются после лечения.
Микроскопический колит — это морфологический диагноз, гистологические изменения чаще встречаются в правой половине толстой кишки, но не исключаются и другие ее отделы, в связи с чем, при колоноскопии рекомендуется брать биопсию на всем протяжении всей толстой кишки. Различают две гистологические формы микроскопического колита: лимфоцитарный и коллагеновый колит.
Факторы риска микроскопического колита
- Лекарственные препараты.
Предполагается, что некоторые лекарственные препараты могут быть запускающими моментами в развитии микроскопического колита, что не исключает лекарственно-ассоциированный колита. К препаратам с высокой степенью вероятности запускающего механизма колита отнесены следующие препараты:- аспирин,
- лансопразол,
- нестероидные противовоспалительные препараты,
- ранитидин и др,
- ингибиторы протонной помпы, снижающие кислотность желудочного сока,
- нестероидные противовоспалительные средства. В побочных проявлениях при приеме этих препаратов указывается диарея.
- Курение.
Доказательств по этому вопросу мало, но известно, что у курящих развитие заболевания начинается раньше, чем у некурящих.
Микроскопический колит. Лечение
Лечение ставит основной своей целью достижение клинической ремиссии и улучшение качества жизни пациента.
До назначения лекарственной терапии следует отказаться от лекарств, которые, возможно, могут стать причиной микроскопического колита. Уже этот отказ может привести к исчезновению клинических признаков диареи.
Медикаментозное лечение микроскопического колита является трудной клинической задачей. На основании имеющихся в настоящее время доказательств, Европейской группой по изучению микроскопического колита предложен алгоритм ведения пациента с данной болезнью.
При легком течении болезни назначаются антидиарейные средства, такие как лоперамид, который может применяться в виде монотерапии или в сочетании с другими видами лечения.
При активной форме заболевания лечение начинается с применения местного кортикостероида – Буденофалька, который не обладает системным действием и превосходит по своему действию гормоны типа преднизолона. Продолжительность курса 6-8 недель, по 3 мг принимать 2-3 раза в день за 30 минут до еды. Эффект наблюдается через 2-4 недели и далее постепенно препарат отменяется. Пациентам, которые ответили на лечение, возможно назначать короткие курсы или пролонгированное лечение низкими дозами препарата.
При средней тяжести обострения заболевания, если нет эффекта от приема буденофалька, применяются препараты висмута, лоперамид, холестероламин в виде комбинированного лечения или монотерапии.
В процессе разработки и изучения находятся применение биологических препаратов (инфликсимаба), азатиопринна, метотрексата и др.
Таким образом, научные исследования показывают, что микроскопический колит становится распространенным заболеванием. У всех больных при наличии хронической диареи при проведении колоноскопии должна быть взята биопсия для гистологического исследования для подтверждения или исключения микроскопического колита, особенно у пожилых людей. У каждого конкретного больного необходимо провести анализ возможных провоцирующих факторов – лекарственные препараты, инфекции, режим питания, состояние гормонального фона.
Микроскопический колит
Современные принципы и схемы морфологической оценки микроскопического колита. Колоноскопия.
А.С. Тертычный1, Х.М. Ахриева2, О.В. Зайратьянц3, Л.С. Селиванова1,Ж.В. Шароян1, Е.И. Епифанова4, Е.А. Таширова4, Н.С. Маренич51 Кафедра патологической анатомии имени академика А.И. Струкова Первого МГМУ имени И.М. Сеченова2 Кафедра факультетской терапии медицинского факультета ФГБОУ ВПО «Ингушский государственный университет»3 Кафедра патологической анатомии ГБОУ ВПО «Московский государственный медико-стоматологический университетимени А.И. Евдокимова» Минздрава России4 Кафедра патологической анатомии педиатрического факультета №2 ГБОУ ВПО «Российский научно-исследовательский медицинский университет имени Н.И. Пирогова» Минздрава России5 Морозовская детская городская клиническая больница
В данной статье рассматриваются современные принципы и схемы морфологической оценки МК. На протяжении последнего десятилетия МК расценивается как основная причина хронической водянистой диареи, особенно в старшей возрастной группе. При проведении колоноскопии не выявляется существенных отклонений от нормы, и только при проведении морфологического исследования возможна постановка диагноза, а также определение варианта колита – коллагеновый (КК) или лимфоцитарный (ЛК). Этиология МК на данный момент остается неизвестной, но триггерная роль приписывается неконтролируемому иммунному ответу при наличии генетической предрасположенности. В связи с тем, что к МК не проявляют такой же интерес как к другим ВЗК, например как к язвенному колиту (ЯК) или болезни Крона (БК), осведомленность о данном заболевании, как среди врачей клинических специальностей, так и среди патологоанатомов весьма ограничена.
Микроскопический колит представляет собой группу хронических заболеваний, характеризующихся водянистой диареей, отсутствием макроскопических изменений при проведении колоноскопии и специфическими гистологическими признаками, обнаруживаемыми при микроскопическом исследовании биоптатов (отсюда и происхождение названия данной патологии) [1]. По данным эпидемиологических исследований заболеваемость и распространенность микроскопическим колитом сопоставимы с таковыми при болезни Крона и язвенном колите. Тем не менее, в клинической практике микроскопический колит до сих пор относится к редко диагностируемым заболеваниям, поскольку большинство клиницистов и патологоанатомов имеют лишь смутное представление о морфологических принципах его диагностики.
До сегодняшнего дня не известна этиология и точные механизмы патогенеза. Более того, в диагностике и лечении пациентов остается много спорных моментов [2-4].
Эпидемиология
Эпидемиологические исследования проводились в основном в Европе, Северной Америке и в Канаде. Однако, даже публикации отдельных клинических наблюдений и исследования небольших групп из Африки, Азии, Латинской Америки и Австралии свидетельствую о том, что МК является повсеместно распространенным заболеванием. [1, 5] Наиболее обширные популяционные исследования проводились в Олмстеде, Миннесота и в Örebro, Швеция.
Оценка непрерывно получаемых результатов с 1984 года начала исследований в обоих центрах показали тенденцию к увеличению заболеваемости МК, которая стабилизировалась лишь в течение последнего десятилетия. В целом, ежегодная заболеваемость коллагеновым колитом составляет от 2,6 до 10,8 случаев на 100 тысяч населения и от 2,2 до 14 случаев лимфоцитарного колита. [Munch A, 2012] По данным 2010 года распространенность МК в Олмстеде составляет 219 человек на 100 тысяч населения [6], и 123 человека на 100 тысяч населения по данным Örebro на 2008 год [7]. Таким образом, можно говорить, что распространенность МК сопоставима с таковой при «классических» воспалительных заболеваниях кишечника – язвенном колите и болезни Крона.
Как правило, микроскопический колит является болезнью пожилых – на момент постановки диагноза средний возраст пациентов составляет 65 лет. Однако возраст 25% среди заболевших не достигает 45 лет. Именно поэтому у молодых пациентов с хронической диареей при проведении дифференциально-диагностического поиска не стоит забывать и о микроскопическом колите. [8]. Появление МК в детском возрасте является казуистикой, однако в литературе опубликованы и такие клинические случаи. [9].
В структуре заболеваемости МК преобладают женщины. Клинические проявления ЛК и КК не имеют каких бы то ни было различий. Основным клиническим проявлением данных нозологий является хроническая диарея без примесей крови, как правило, имеющая водянистый характер, приводящая к императивным позывам (70% пациентов) и даже к недержанию кала (40% пациентов) [10]. В тяжелых случаях примерно у половины пациентов дефекация может достигать 15-ти раз в сутки (включая ночные позывы). Несмотря на значительные потери жидкости, дегидратация организма и электролитные нарушения встречаются достаточно редко.
Естественное течение заболевания недостаточно изучено, но по данным последних проспективных исследований риск развития рецидива после отмены терапии буденофальком достаточно высок и составляет 60–80%, что свидетельствует в пользу хронически рецидивирующего течения МК. [5, 11].
В период обострения качество жизни пациентов значительно снижается и может послужить причиной их социальной дезадаптации. [3]. При этом по данным исследований, не столько частота дефекаций, сколько консистенция испражнений определяет степень ухудшения качества жизни [3, 12]. Именно поэтому стадия обострения МК по Hjortswang [13] устанавливается при наличии стула 3 и более раз в день или при наличии хотя бы однократного воднястого стула (данные оцениваются в течении недели). Таким образом, при решении вопроса о целесообразности назначении терапии в первую очередь обращают внимание не на количество дефекаций, а на их консистенцию (лечение может быть назначено и в случае, если количество дефекаций менее трех, при условии, что стул является водянистым). По данным некоторых рандомизированно контролируемых исследований буденофальк значительно улучшает качество жизни пациентов, а вышеперечисленные жалобы (количество дефекаций и консистенция испражнений) могут послужить критериями оценки активности заболевания в ходе клинических испытаний. [12].
Еще одним распространенным симптомом при МК является боли в животе. [8, 10]. Чувство дискомфорта или спазмы могут встречаться у 50% пациентов. В этих случаях проведение дифференциальной диагностики с синдромом раздраженного кишечника может представлять определенную сложность. На основании последних проспективных исследований у 43% пациентов при использовании «римских критериев III» может быть поставлен диагноз «синдром раздраженного кишечника». [14]. Как правило, болевой синдром наиболее выражен в стадию обострения и регрессирует на фоне лечения буденофальком [неопубликованные данные, 2013 год]. Также при обострении у половины пациентов может наблюдаться потеря веса [8, 10]. Хотя остается неясным вследствие чего происходит уменьшение массы тела – из-за потери жидкости или же из-за ограничения
питания самими пациентами с целью уменьшения количества дефекаций. При значительной потере веса следует исключать целиакию как сопутствующее заболевание.
Часто МК ассоциирован и с другими аутоиммуными патологиями. По данным шведского многоцентрового исследования другие аутоиммунные заболевания встречаются у трети больных. Среди них преобладают целиакия (12%), аутоиммунный тиреоидит (10,3%), синдром Шегрена (3,4%), сахарный диабет (1,7%), а также заболевания кожи и суставов (6%). В большинстве случаев их диагностика предшествует установлению диагноза МК. Примечательно, что в этих случаях МК имеет более раннюю манифестацию и более выраженные симптомы со стороны желудочно-кишечного тракта [15].
Риск развития злокачественный новообразований и общая смертность у больных МК не отличается от таковых по сравнению с общей популяцией. [16].
Гистопатология
Микроскопический колит (МК) остается гистологическим диагнозом. При этом информация о клиническом течении всегда должна быть предоставлена морфологу.
Анализ данных крупных ретроспективных исследований показал, что наличие диареи непосредственно не позволяет идентифицировать пациентов с высоким риском обнаружения МК при гистологическом исследовании. Но у пациентов старше 60 лет значительно повышается вероятность обнаружения патологических изменений при морфологическом исследовании, а наиболее вероятным диагнозом будет являться именно МК. [17].
Проведение гистологического исследования необходимо не только для постановки диагноза и проведения дифференцировки между двумя главными подтипами (лимфоцитарным колитом и коллагеновым), но и для исключения других возможных причин развития хронической диареи. В ходе эндоскопической диагностики слизистая оболочка толстого кишечника практически всегда соответствует норме, но изредка можно обнаружить незначительные изменения, такие как отек, эритема, нарушение сосудистого рисунка или даже дефекты слизистой оболочки. [18].
При МК морфологические изменения могут быть диффузными и очаговыми. Анализ данных проспективных мультицентровых исследований показывает, что коллагеновые тяжи толщиной более 10 мм чаще встречаются в правой половине кишечника, (достигая максимальных значений в слепой и восходящей ободочной кишке) и значительно реже в сигмовидной и прямой кишке, тогда как мононуклеарное воспаление в собственной пластинке равномерно распределено среди различных сегментов толстого кишки. [19]. Именно поэтому рекомендуется брать материалы для гистологического исследования на протяжении всей толстой кишки, тогда как биопсии, полученные только из прямой кишки или из прямой кишки и сигмовидной могут привести к ложноотрицательным результатам в 41% или 21% случаев соответственно. При этом, предпочтительно, чтобы биоптаты
были помещены в различные контейнеры [1, 19, 20].
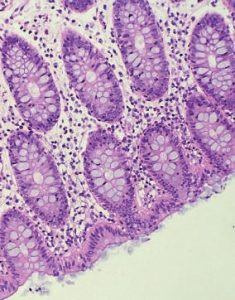
Лимфоцитарный колит
Патогномоничным признаком лимфоцитарного колита является интраэпителиальный лимфоцитоз, то есть увеличение количества поверхностных интраэпителиальных лимфоцитов с незначительным нарушением цитоархитектоники или без него [21, 23]. По данным большинства исследователей диагностическим считается увеличение ИЭЛ от 20 и более на 100 поверхностных эпителиальных клеток (тогда как в норме количество ИЭЛ составляет не более 5), но ряд авторов предполагает, что и 15 ИЭЛ уже могут указывать на наличие ЛК [24]. С целью стандартизации критериев морфологической диагностики Европейским Обществом Патологов и Европейским Обществом по изучении Болезни Крона и Язвенного Колита было рекомендовано считать пороговым значением, обладающим диагностической ценностью, увеличение количества ИЭЛ от 20 и более. [20].
Терминальный отдел подвздошной кишки считается вовлеченным в процесс (ЛК, КК) при среднем количестве интраэпителиальных клеток на ворсину превышающем 5 клеток. [25].
На препаратах, окрашенных гематоксилином и эозином, интраэпителиальные лимфоциты представляют собой преимущественно округлые клетки с компактным ядром и с компактным строением хроматина, немного неправильным контуром ядра и перинуклеарным гало.
Поверхностные эпителиальные клетки могут отражать дистрофические и/или регенеративные изменения, такие как вакуолизация и уменьшение муцина. [26]. По сравнению с нормой, количество клеток в собственной пластинке слизистой диффузно увеличено. Воспалительная инфильтрация состоит преимущественно из лимфоцитов и плазматических клеток, но также могут присутствовать эозинофилы и даже единичные нейтрофилы.
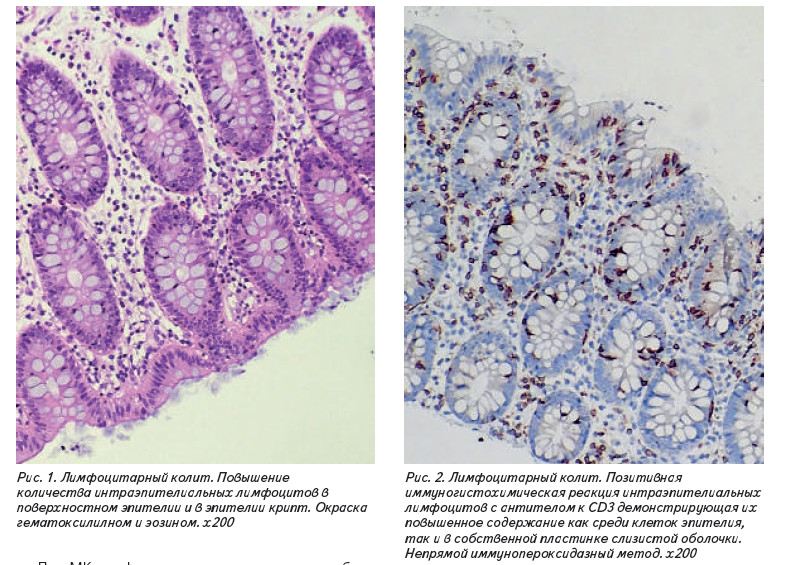
В большинстве случаев окрашивание биоптатов гемотоксилином и эозином достаточно для постановки диагноза, и ИГХ окрашивание с АТ к CD3 не является рутинным методом (Рис.1 и 2).
Коллагеновый колит
Диагностическим гистологическим признаком КК является утолщение слоя коллагена, расположенного сразу под поверхностным эпителием. Особенно хорошо эти изменения определяются между криптами. Отложения коллагена могут иметь неправильные очертания и неровную границу с подлежащей собственной пластинкой слизистой оболочки.
Коллагеновые массы могут содержать капилляры, эритроциты, а также клетки воспаления, в частности, лимфоциты [21, 23]. Повреждение поверхностного эпителия при КК встречается намного чаще, чем при ЛК, и, как правило, оно достаточно отчетливо выражено. Также характерным признаком КК является десквамация эпителиоцитов с субэпителиального коллагенового слоя. Хотя при КК наблюдается увеличение количества интраэпителиальных лимфоцитов, степень их увеличения не достигает таких значений, как при ЛК. Изменение клеточного состава собственной пластинки слизистой оболочки происходит в основном за счет мононуклеарной инфильтрации, а в редких случаях за счет изменений, сходных с ВЗК – обнаруживается активный воспалительный процесс в криптах с возможным формированием крипт-абсцессов.
Согласно Европейскому Консенсусу по Гистопатологии Воспалительных Заболеваний Кишечника, на правильно ориентированных биопсийных материалах толщина коллагенового тяжа должна превышать 10 мм (тогда как в норме это значение не превышает 3 мм) (гистологические срезы должны быть выполнены строго перпендикулярно поверхности слизистой оболочки [20]).
В большинстве случаев диагноз без затруднений может быть поставлен при окраске препаратов гематоксилинэозином. В сомнительных случаях может потребоваться окраска гистологических препаратов по Ван Гизону или ИГХ-окрашивание с АТ к тенасцину, который синтезируется субэпителиальными миофибробластами и отсутствует в слизистой оболочке в норме [28] (Рис.3 и 4).

Дифференциальный диагноз
Были опубликованы ряд случаев, когда у пациентов были клинические черты микроскопического колита, но для постановки диагноза не «выполнялись» все морфологические критерии лимфоцитарного или коллагенового колита. В этих случаях, в собственной пластинке слизистой наблюдается воспалительная инфильтрация, а расположение коллагеновых волокон отличается от нормы, но их толщина не достигает 10 μм, а увеличение количества ИЭЛ не достигает 20 клеток на 100 эпителиальных клеток.
В связи с этим были предложены следующие термины, которые отражают изменения в гистологической картине, но не отражают клинические различия: пограничный ЛК [29], частичный МК [1, 10], МК неуточненный [30] и неполный ЛК [31]. Атипичные формы до сих пор остаются спорными и не являются общепринятыми [32]. Кроме того, в ряде случаев этим больным клинически был установлен диагноз синдрома раздраженного кишечника.
Генетические факторы
Хотя в ряде случаев наблюдается семейная предрасположенность, точная роль генетических факторов остается еще не определенной. [35, 36]. В ходе исследований было показано наличие связи заболеваемости МК и обнаружением у пациентов HLA-DQ2 или DQ1/3МК локусов комплекса гистосовместимости 2 класса. Установлено, что по сравнению с контрольной группой, МК встречается чаще при идентификации DR3DQ2 гаплотипа или TNF2 аллелей. [37]. К тому же предполагается наличие связи между различными вариациями генов металлопротеиназ-9 и коллагеновым колитом [38]. В отличие от болезни Крона, не был установлен функциональный полиморфизм нуклеотидсвязывающего домен-содержащего белка 2 и набора каспаз, содержащих протеин 15 (гены NOD2/CARD15).
Барьерная функция эпителия
Еще одним возможным звеном в патогенезе МК является нарушение барьерной функции эпителия, что приводит к увеличению проницаемости слизистой оболочки для антигенов и бактериальных агентов. Таким образом, происходит стимуляция и поддержания воспалительного процесса. В ходе экспериментов в биопсийном материале толстой кишки даже в стадию ремиссии наблюдается значительное нарушение барьерной функции слизистой оболочки, проявляющееся повышенной проницаемостью для непатогенных бактерий. Данная дисфункция сохраняется, несмотря на клинически эффективные краткосрочные курсы лечения буденофальком. [40]. По данным Tagkalidis и его коллег при КК наблюдается снижение экспрессии Е-кадгерина и образования межклеточных соединений zonula occludens (в норме индуцируемые интерферономгамма), что свидетельствует об изменении барьерной функции эпителия. Burgel и другие отметили снижение синтеза клаудина-4 и окклудина – белков, участвующих в формировании плотных контактов в эпителиальных тканях. Эти данные коррелируют со сведениями о снижении эпителиальной резистентности, что проявляется увеличением парацеллюлярной проницаемости.
Иммунология
CD8+ T-лимфоциты превалируют как в эпителиальном слое, так и в собственной пластинке слизистой, при этом наблюдается увеличение соотношения Ki67 + и CD45RO+CD8+ Т-лимфоцитов, а CD4+ Т-лимфоциты сравнительно редко встречаются в собственной пластинке. [45].
«Цитокиновый профиль» представляет собой преимущественное увеличение Th2-цитокинов слизистой и ИНФ-гамма при КК, а при ЛК – ФНО-альфа. Также увеличивается количество ИЛ-8 и ИЛ-15 [41, 46]. Более поздние исследования в области иммунологии показали комбинированное увеличение Th27/Nc17 и Th2/Tc1 цитокинов. Уровни матричной РНК ИНФ-гамма, ИЛ-12, ИЛ-17А, ИЛ21 И ИЛ-22 значительно выше у пациентов с МК (по сравнению с контрольной группой), кроме того наблюдается прямая зависимость между степенью активации мРНК и степенью активности клинических проявлений. Значительное увеличение ИЛ-21 и ФНО-альфа отмечено как при КК, так и при ЛК [47].
Факторы риска
Лекарственные препараты
Предполагается, что употребление некоторых лекарственных препаратов можно рассматривать в качестве триггерного фактора при развитии микроскопического колита. [48].
Beaugerie и Pardi [49] была предположена шкала балльной оценки с различной степени достоверности участия того или иного препарата в развитии колита.
К препаратам, с высокой степенью вероятности «запускающими» МК были отнесены акарбоза, аспирин, цикло-3форт, лансопразол, НПВС, ранитидин, серталин и тиклопидин. В недавно опубликованных обзорных статьях, двумя препаратами, которые с наибольшей вероятность могут рассматривать в качестве триггерных факторов для МК являются ингибиторы протонной помпы и нестероидные противовоспалительные средства.
Некоторые ученые озадачены тем фактом, что до сих пор отсутствует такое понятие как лекарственно-ассоциированный микроскопический колит. [50]. У большинства лекарственных препаратов, рассматриваемых в качестве триггерных факторов микроскопического колита, одним из побочных эффектов является развитие диареи. [51].
Чем чаще проводить колоноскопию со взятием биопсий у пациентов с лекарственно-ассоциированной диареей, тем чаще будет устанавливаться диагноз МК, тогда как не всегда препараты, вызвавшиеся диарею можно рассматривать в качестве триггера. Поэтому, нельзя рассматривать лекарственный препарат как причину развития МК основываясь только на клинических данных.
Курение
По данным исследований, развитие заболевание у курильщиков начинается раньше, чем у некурящих людей (медиана составляет 14 лет). Курение является равноправным фактором риска для мужчин и женщин. [52-54].
Лечение
Основной целью лечения являются достижение клинической ремиссии, а также улучшение качества жизни пациентов. [13]. Является ли необходимым достижение гистологической ремиссии в настоящий момент не известно.
До начала медикаментозной терапии, всегда необходимо исключать возможность развития лекарственно-ассоциированного МК – особое внимание следует обратить на препараты, которые с высокой долей вероятности могут стать причинным фактором развития МК. [49]. В этих случаях уже отказ от приема данных препаратов может привести к исчезновению симптомов. Может быть также рассмотрен вопрос об отказе от курения, но доказательная база в настоящее время все еще слаба. Пациентам рекомендуется вести дневник, в котором они будут регистрировать стул до начала лечения и во время него.
Доказанной эффективностью обладает будесонид – местный кортикостероид, который активно метаболизируется в печени и практически не оказывает системного действия. При проведении мета-анализа, будесонид показал высокую эффективность: процент пациентов, положительно ответивших на лечение, был выше 80; препарат также хорошо подходит для индукции и поддержания ремиссии (количество пациентов, нуждающихся в поддерживающей терапии среди больных с КК достигало 2 пациентов, а при ЛК – 3).
При краткосрочном курсе терапии или при использовании препарата в качестве поддерживающей терапии, его отмена с высокой вероятностью приводит к развитию рецидива (60% случаев). [5,11].
В настоящее время нет других препаратов, обладающих доказательной базой. При микроскопическом колите часто используют антидиарейные препараты, такие как лоперамид, хотя фактически не было ни одного рандомизированного контролируемого исследования в отношении данного препарата. Однако клинический опыт показывает клиническое улучшение у некоторых пациентов. [8, 57]. Как бы то ни было, очень редко возможно достижение долгосрочной ремиссии, а воздействие на воспалительный процесс в кишечники – маловероятно.
Таким образом, в зависимости от тяжести течения антидиарейные препараты могут быть использованы в качестве монотерапии или в сочетании с другими видами лечения.
Эффективность преднизолона оценивалась в основном в ретроспективно. [8, 57]. В последних популяционных исследованиях было показано, что будесонид по сравнению с преднизолоном с большей частотой приводит к «полному ответу» (82,5% и 52,9% соответственно). Кроме того, рецидив развивался чаще у пациентов, лечившихся преднизолоном. [58]. Поэтому преднизолон не имеет никакого значения для пациентов, если они резистенты к терапии будесонидом.
Клиническая и гистологическая ремиссия была достигнута у всех 7 пациентов, получавших салицилат висмута по сравнению с контрольной группой плацебо-контролируемых пациентов [59]. Для определения значения висмута в терапии МК необходимо проведение более крупных исследований.
Недавние рандомизированные контролируемые исследования, показывающие, что достижение ремиссии при назначении месалазина пациентам с КК сопоставимо с плацебо, указывают на то, что не следует начинать лечение пациентов с данного препарата. [55].
Несмотря на тот факт, что данные ограничены, иммуноспупрессивная терапия может быть рассмотрена у пациентов с тяжелым течением, которые проявляют резистентность или непереносимость терапии будесонидом. Согласно результатам, предполагается, что пациенты с МК в течение 4 недель достигают клинической ремиссии при назначении индукционной терапии будесонидом в дозе 9 мг в сутки или поддерживающей терапии в дозе 6 мг в сутки.
Около 10-20% пациентов проявляют резистентность при краткосрочном лечении будесонидом; именно они и являются кандидатами для имунносупрессивной терапии [12, 55]. Процент пациентов, проявляющих резистентность к будесониду или его непереносимость при длительной поддерживающей терапии, нигде не опубликован.
На сегодняшний день можно найти несколько клинических публикаций, указывающих на благоприятный эффект у некоторых пациентов с КК при использовании ингибиторов ФНО-альфа (инфликсимаб, адалимумаб).
Схемы лечения и дозы соответствуют таковым при классическом течении ВЗК [60, 62]. Часто пациенты, резистентные к терапии будесонидом, длительно получали неэффективное лечение. Хронически активное заболевание с высокой частотой водянистого стула нередко «привязывает» пациента к туалету, тем самым значительно снижая качество его жизни. Но несмотря ни на что, начало биологической терапии всегда должно рассматриваться индивидуально, принимая во внимание возраст больного и наличие сопутствующих заболеваний. Чтобы избежать серьезных побочных эффектов, необходимо тщательно взвешивать риск и пользу. Опыт применения биологических препаратов ограничен, а данные по длительному приему ингибиторов ФНО-альфа тоже отсутствуют.
Азатиоприн или меркаптопурин были протестированы на небольшой группе пациентов (9 человек) со стероидозависимым или резистентным КК. Лечение дало 89% положительных ответов и стероидощадящий эффект [63]. В крупных ретроспективных мультицентровых исследованиях, 28% пациентов, принимающих азатиоприн достигли ремиссии в течение 57 месяцев, однако у большинства пациентов препарат был отменен в связи с его непереносимостью. 13 из 31 пациентов, которые не могли продолжать лечение азатиоприном, начали получать меркаптопурин, и 6 из них (48%) восстановили клиническую ремиссию, в результате чего общее количество положительных ответов достигло 41%. [64]. Эти данные указывают на то, что тиопурины могут быть использованы в первую очередь в качестве поддерживающей терапии при хроническом активном МК, но проспективные рандомизированные клинические исследования не только ожидаемы, но и необходимы.
При ретроспективном исследовании случаев прием метотрексата показал хороший эффект у пациентов, ранее не получающих терапию будесонидом [65].
Однако, анализ недавней серии случаев показал, что 9 больных, непереносящих терапию будесонидом или резистентные к ней, получали метотрексат в дозе 15–25 мг/нед в течение 12 недель подкожно. Но ни у одного из этих пациентов не была достигнута ремиссия, более того, у четверых из них были показания для отмены метотрексата. [65]. Эти данные весьма противоречивы и проведение дальнейших исследований необходимо.
На основе имеющихся в настоящее время доказательств, Европейской группой по МК был предложен алгоритм ведения пациентов с микроскопическим колитом.
Согласно данному алгоритму назначение антидиарейных препаратов и/ или холестероламина может быть оправдано только в случаях легкого течения. Тем не менее, при активной форме заболевания лечение стоит начинать с короткого курса будесонидо (6–8 недель). У пациентов, чувствительных к такой терапии, будесонид в дальнейшем может быть использован при рецидиве заболевания в качестве интермитиррующей терапии или непрерывной низкодозированной поддерживающей терапии, целью которой является определение самой низкой дозы, позволяющей достичь клиническую ремиссию.
В случаях МК средней тяжести, когда отсутствует положительная динамика при приеме будесонида, возможно назначение холестероламина, препаратов бисмута или лоперамида в виде монотерапии или комбинированно.
Заключение
Появившиеся в последнее время данные четко указывают на тот факт, что микроскопический колит становится распространенным заболеванием, поэтому как врачи, так и морфологи должны быть осведомлены о нем. У всех пациентов при наличии хронической диареи должна быть проведена колоноскопия со взятием материала для гистологического ния микроскопического колита, причем особое внимание следует уделять пациентам пожилого возраста.
Предполагается, что новые исследования должны быть нацелены не только на изучение заболеваемости – особое внимание следует уделять возможным провоцирующим факторам, таким как прием лекарственных препаратов, инфекционные заболевания, режим питания. В связи с доминированием женщин среди пациентов, необходимо также рассмотреть предположение о патогенетической роли некоторых гормонов или же просто отнести заболевание к аутоиммунным, поскольку женщины более склонных к их развитию. Масштабные генетические исследования нацелены на выявление генов, ассоциированных с МК, и особое внимание уделяют обнаружению генов предрасположенности. Хотя большинство больных положительно реагируют на терапию будесонидом, все же есть определенная группа пациентов, резистентных к такому лечению.
Углубление знаний в области иммунологических процессов может стать ключом для разработки новых стратегий лечения.
Микроскопический (лимфоцитарный и коллагенозный) колит: что не показывает колоноскопия |
Одной из множественных причин хронической диареи, не сопровождающейся примесью крови в кале, но с болями в животе, служит микроскопический колит.
Это собирательный диагноз, под которым объединены воспалительные заболевания толстой кишки, не имеющие явных симптомов при эндоскопии и рентгеновском исследовании. Диагноз подтверждается микроскопией гистологического образца.
К микроскопическому колиту относят лимфоцитарный и коллагеновый колит.
Это довольно редкая патология и причина достоверно не ясна. Может наблюдаться лимфоцитарный и коллагеновый колит у больных с синдромом Шегрена, ревматоидным артритом, целиакией, сахарным диабетом.
Сейчас такие формы колита выявляются чаще, но это связано с более совершенной диагностикой. По данным A.Trom (2005г), если у больных с хронической диареей не обнаруживается изменений при колоноскопии, то биопсия показывает микроскопический колит в 11,7% случаев.
Лимфоцитарный колит
В норме у человека на 100 клеток эпителия приходится около 5 лимфоцитов, иммунных клеток, находящихся в подслизистом слое. По данным G.Adler, при лимфоцитарном колите на 100 эпителиальных клеток насчитывается более 24 лимфоцитов. Сильнее всего инфильтрация иммунными клетками наблюдается в слепой и восходящем отделе толстой кишки.
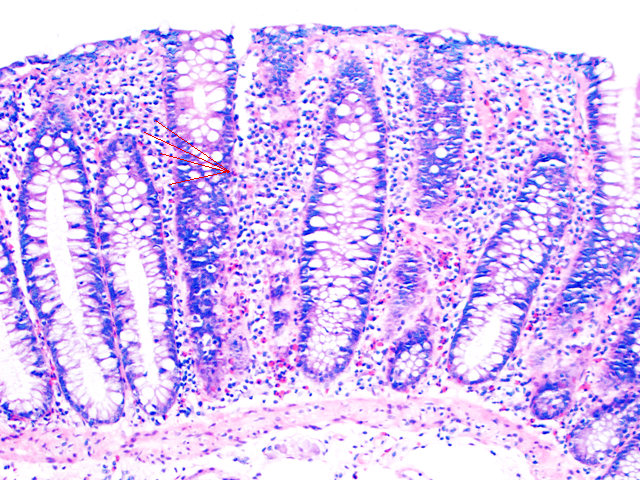
При микроскопии видна лимфоцитарная инфильтрация. Автор фото: Андреас Мюнх (Andreas Munch, USA)
Заболевание чаще всего развивается у людей старше 50 лет. Женщины болеют в 2-4 раза чаще, чем мужчины.
Болезнь проявляется частым (до 4-6 раз в сутки) и жидким стулом, сопровождающимся схваткообразными болями в животе.
Лимфоцитарный колит обычно имеет доброкачественное течение. Диарея возникает периодически, причем возможны довольно длительные бессимптомные периоды.
Диагностика. В лабораторных анализах может не быть существенных отклонений от нормы. Чаще всего отмечается небольшое повышение СОЭ и С-реактивного белка. При эндоскопии и на рентгене ничего не выявляется. Диагноз ставится по биопсии.
Иногда с течением времени лимфоцитарный колит может перейти в коллагеновый.
Коллагеновый колит
Для этого заболевания характерно отложение волокнистого белка коллагена в подслизистом слое толстого кишечника. В норме коллагеновый слой имеет толщину 2-5 мкм. При болезни эта цифра увеличивается в 2-100 раз.
прим.
Коллаген — это фибриллярный белок, участвующий в формировании волокон сухожилий, мышц, костей. Формирует трехмерную «сетку» внутренних органов (строму), определяя его форму и плотность. Это самый распространенный белок в нашем теле, на его массу приходится 25-35%.
Кстати, именно подслизистый слой в кишечнике самый прочный, благодаря этой коллагеновой прослойке. Поэтому при наложении кишечного шва хирурги его всегда захватывают.
Известно 28 типов этого белка. В норме в подслизистом слое кишки строма состоит из коллагена 4 типа. При коллагеновом колите накапливается другой, 3 тип. Это важно для диагностики.

Видны скопления коллагена. Толщина слоя при патологическом процессе может тостигать 10 мм! (обычно 1-3 мм). Автор фото: Андреас Мюнх (Andreas Munch,USA)
Причины коллагенового колита неясны. Есть предположения, что синтез коллагена 3 типа, который обычно выявляется в регенерирующих тканях, — это защита от неизвестного раздражителя.
Причем таким раздражителем могут быть нестероидные противовоспалительные средства (НПВС). Развитие симптомов коллагенового колита иногда наблюдается после длительного (не менее 5 лет) приема НПВС. Что же получается? Аспирин, у которого при продолжительном приеме выявлена способность снижать риск рака толстого кишечника, может провоцировать другую проблему… Исследования в этом направлении продолжаются. Тем более, что длительный прием НПВС обычно характерен для пациентов с другими хроническими заболеваниями, в том числе ревматическими. Поэтому виноваты ли в этом НПВС, предстоит еще разобраться.
Сообщается о повышении частоты болезни при длительном приеме селективных ингибиторов обратного захвата серотонина (СИОЗС) — большинство современных антидепрессантов.
Считается, что наиболее вероятной причиной является аутоиммунное происхождение. В пользу этого говорит нередкое сочетание аутоиммунного тиреоидита, ревматоидного артрита, сахарного диабета. К тому же, обнаруживаются антинуклеарные антитела.
Симптомы. Основной симптом — водянистая диарея, причем объем стула достигает 4 литров в сутки. Возникает это по причине выделения большого количества жидкости и солей в просвет кишечника. Конечно, до симптомов холеры далеко, когда потери жидкости могут достигать 15-20 литров, но все же у многих пациентов довольно быстро наступает истощение. Они теряют массу тела. Часты и диспепсические расстройства (тошнота, рвота, боли в животе).
Диагностика. Практически то же, что и при лимфоцитарном колите. В анализах может быть небольшое повышение СОЭ. Диагноз подтверждается гистологически. Причем биопсию лучше всего брать в правых отделах толстой кишки, так как в прямой и сигмовидной кишке утолщение коллагенового слоя может не наблюдаться.
Лечение. Если имеет место прием НПВС, то их отменяют (предполагают, что они могут быть причиной). Проводится корректировка питания, исключаются продукты, стимулирующие перистальтику (например, кофе, алкоголь, молочные продукты.
Применяются антидиарейные препараты, например лоперамид (имодиум).
Имеются исследования по применению препарата холестирамина, который связывает желчные кислоты (желчь стимулирует перистальтику). В отдельных случаях клинический эффект был достигнут приемом антибиотиков (метронидазол), что может натолкнуть на мысль о возможно какой-то бактерии как этиологического фактора.
В более тяжелых случаях назначается сульфасалазин (салофальк), препараты группы кортикостероидов (лучше всего зарекомендовал препарат будезонид).
Если микроскопический колит не отвечает на курс терапии при тяжелых состояниях пациента проводится хирургическое вмешательство — накладывается стома с целью выключить функцию пораженного отдела. Когда кишка выключается из кишечного пассажа, в ней наблюдается регресс патологических изменений (при восстановлении пассажа вновь возникают характерные микрокопичеcкие изменения). Что-то в кишечном содержимом все же есть…
В целом, микроскопические колиты протекают благоприятно, нередко наблюдается длительная ремиссия даже без лечения.
Это одно или два заболевания?
Клиническое и гистологическое сходство между двумя болезнями, а также факты перехода лимфоцитарного колита в колалгенозный, привело к предположению, что это разные стадии одной болезни. Пока все же большинством исследователей признаются как два отдельных, но тесно связанных заболевания.
В заключение
Микроскопический колит довольно часто лечится как синдром раздраженного кишечника, поэтому при лечении длительно протекающей диареи показана биопсия. У пациента с «синдромом раздраженного кишечника» может быть другой диагноз.
Если вы нашли опечатку в тексте, пожалуйста, сообщите мне об этом. Выделите фрагмент текста и нажмите Ctrl+Enter.
Поделиться новостью в соцсетях
Метки: диарея, колит

« Предыдущая запись
Следующая запись »
Микроскопический колит и синдром раздраженной кишки с диареей: трудности дифференциального диагноза
Микроскопический колит (МК) представляет собой особую форму хронических воспалительных заболеваний кишечника, для которой характерны особые изменения в толстой кишке.
Относительно гистологических изменений выделяют лимфоцитарный колит (наличие значительной инфильтрации слизистой толстой кишки интраэпителиальными лимфоцитами при сохраненной архитектонике слизистой) и коллагеновый колит (утолщение базальной мембраны за счет депозитов коллагена в ней). Доминирующим, а часто и единственным клиническим проявлением у таких больных является диарея без патологических примесей.
Первое описание микроскопического колита было сделано Lindstrom и Freeman в 1976 году, что позволило разграничить данную патологию с инфекционными и заболеваниями кишечника. С тех пор данных о МК получено мало, заболевание продолжает оставаться малоизученным, а причины его возникновения и прогрессирования до конца не выяснены. Возможно, это связано с невысокой распространенностью МК (103, 00 на 100 000 человек, M. Storr et al. Microscopic Colitis: Epidemiology, Pathophysiology, Diagnosis and Current Management—An Update 2013. ISRN Gastroenterol. 2013).
Предполагают, что лимфоцитарный и коллагеновый колит развивается в результате взаимодействия нескольких факторов, среди которых определенное значение имеют наследственность, состояние кишечной микрофлоры, иммунные нарушения. В качестве возможных триггерных механизмов развития болезни рассматривают курение и влияние лекарственных веществ (аспирин, лизиноприл, ранитидин, мадопар, симвастатин) .
На сегодня разработаны методы терапии, которые позволяют если не излечивать таких больных, то улучшать качество их жизни. В клинической практике одним из самых частых заболеваний, при котором наблюдается диарея без патологических примесей, является синдром раздраженной кишки (СРК). Таким образов, практикующие врачи нередко сталкиваются с необходимостью дифференциального диагноза в случае выявления подобной диареи. Для уточнения и описания различий между МК и СРК во Франции проведено масштабное мультицентровое исследование.
Цели и методы
Целью данного проспективного исследования являлось описание характеристик когорты пациентов с МК и сравнение их с пациентами с СРК с диареей. Проводилось данное исследование в 26 медицинских центрах во Франции. Критериями включение были: диарея без патологических примесей как минимум 3 раза в день, продолжительность заболевания более 3 недель и отсутствие органической патологии при колоноскопии. При этом каждому пациенту выполнялись биопсии из области слепой кишки и всех отделов толстой кишки при колоноскопии, а также проводилась эзофагогастродуоденоскопия с взятием биопсийного материала из желудка и двенадцатиперстной кишки.
Диагноз «лимфоцитарный колит» устанавливался на основании обнаружения более 20% интраэпителиальных лимфоцитов слизистой толстой кишки и «коллагеновый колит» на основании утолщения базальной мембраны более чем 10 микрон за счет депозитов коллагена. Полученные данные были статистически обработаны и сравнены друг с другом.
Результаты
Из включенных в исследование 433 человек, у 129 обнаруживался МК (лимфоцитарный колит у 87 и коллагеновый колит у 42 больных), у 278 исследуемых диагностирован СРК с диареей, вследствие чего они отнесены в контрольную группу. У 26 участников выявлена органическая патология. Диагностическая ценность биопсии была выше в поперечной кишке, при лимфоцитарном колите 96% и коллагеновом колите 98.5%, и ниже в прямой кишке, 83% и 78% соответственно. Прием лекарств отмечен у 53% пациентов с МК, связь с аутоиммунными заболеваниями выявлялась в 34% случаев.
При статистическом анализе существенная разница между группами больных с МК и СРК наблюдалась в таких характеристиках, как: средний возраст (61 г для МК vs. 47 лет для СРК, p
Заключение
В представленном мультицентровом проспективном исследовании были выявлены следующие наиболее достоверные факторы, позволяющие установить диагноз «микроскопический колит»: возраст старше 50 лет, появление диареи ночью, потеря веса, получение новых лекарств за перод не более 3 месяцев и наличие аутоиммунных заболеваний. Связь с приемом лекарств и аутоиммунной патологией чаще ассоциирована с коллагеновым колитом. Также установлено, что диагностическая точность биопсий была максимальна в поперечной кишке и минимальна в прямой. Полученные данные призваны помочь практикующим врачам в диагностике МК и его лечении.
Источник: Microscopic colitis or irritable bowel syndrome with diarrhea: prospective multicenter study. G. Macaigne et al. UEG journal, 2013. p. A78.
Гастрошколы. Микроскопический колит: пособие для врачей
Главная » Микроскопический колит: пособие для врачей
Кучерявый Юрий Александрович, Андреев Дмитрий Николаевич
УДК 616.34−002−07−08(07) | ББК 54.133я7 | К95 | ISBN 978−5-905 757−56−3
В пособии изложены современные данные о микроскопическом колите, включая вопросы его эпидемиологии, этиопатогенеза, особенностей клинической картины и критериев диагностики. Особое внимание уделено терапии микроскопического колита с позиций доказательной медицины. Пособие рекомендовано для врачей общей практики, терапевтов, гастроэнтерологов, колопроктологов и патоморфологов.
Сведения об авторах:
Кучерявый Юрий Александрович — доцент кафедры пропедевтики внутренних болезней и гастроэнтерологии МГМСУ им. А. И. Евдокимова, кандидат медицинских наук.
Андреев Дмитрий Николаевич — ассистент кафедры пропедевтики внутренних болезней и гастроэнтерологии МГМСУ им. А. И. Евдокимова.
Понятие «микроскопический колит» объединяет в себе два патологических состояния известных как коллагенозный и лимфоцитарный колит. В клинической практике данную патологию нередко называют синдромом водянистой диареи ввиду доминирующего симптома.
Микроскопический колит является относительно молодым заболеванием, которое привлекает к себе все большее внимание медицинского сообщества. В настоящее время существует четкое понимание того, что, подобно язвенному колиту и болезни Крона, микроскопический колит представляет собой хроническое воспалительное заболевание кишечника, значение которого долго оставалось недооцененным. Сравнительно недавно Европейская организация по изучению болезни Крона и язвенного колита (European Crohn´s and Colitis Organisation; ECCO) признала микроскопический колит как самостоятельное заболевание и разработала рекомендации по его диагностике и лечению. В 2010 году с целью комплексного мультидисциплинарного изучения данной патологии была образована Европейская группа по изучению микроскопического колита (European Microscopic Colitis Group; EMCG).
В настоящем пособии мы постарались отразить эволюцию клинических представлений о микроскопическом колите, прошедшую в течение последних десятилетий.
Искренне Ваши,
авторы
- ЭПИДЕМИОЛОГИЯ:
коллагенозный колит, лимфоцитарный колит - ПАТОМОРФОЛОГИЯ:
дефиниция, коллагенозный колит, лимфоцитарный колит, микроскопический колит: «верхушка айсберга», «Новая сущность» микроскопического колита? - ЭТИОЛОГИЯ И ПАТОГЕНЕЗ:
инфекционные и иммунологические механизмы, мальабсорбция желчных кислот, прием лекарственных препаратов, курение, генетическая предрасположенность, нарушения метаболизма коллагена, патогенез диареи 20 - КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ:
симптоматика, естественное течение и осложнения, сопутствующие заболевания - ДИАГНОСТИКА:
подходы к диагностике, дифференциальная диагностика - ЛЕЧЕНИЕ:
доказанные методы лечения: колит, лимфоцитарный колит, эмпирические подходы к лечению - ЛИТЕРАТУРА:
литература к главе «Эпидемиология», «Патоморфология»,»Этиология и патогенез», «Клинические проявления», «Диагностика», «Лечение»
Поделитесь страницей
Лечение микроскопического колита: обзор клинических рекомендаций
Авторы:
Т.А. Соломенцева

Микроскопический колит характеризуется хронической водянистой диареей неинфекционного генеза. Заболевание диагностируется на основании выявления воспаления в ткани толстой кишки при гистологическом исследовании. Микроскопический колит имеет два основных подтипа – лимфоцитарный и коллагеновый, у которых много общего. В частности, практически одинаковые клинические симптомы: водянистая диарея, отсутствие макроскопических изменений на слизистой оболочке толстой кишки. При обеих формах заболевания гистологическое исследование выявляет интраэпителиальный лимфоцитоз, увеличение воспалительных клеток в собственной пластинке слизистой оболочки, сохранение архитектоники крипт, при коллагеновом колите наблюдается утолщение подэпителиального коллагенового слоя [13].
 Т.А. Соломенцева
Т.А. Соломенцева
Первые описания случаев микроскопического колита опубликованы в медицинской печати в начале 80-х годов прошлого столетия [11, 12]. В начале изучения анализу подвергались единичные спорадические случаи данного заболевания. За последние 30 лет диагностика микроскопического колита существенно улучшилась, заболевание интенсивно изучается и интерес к нему только растет.
До недавнего времени микроскопический колит считался редким заболеванием, было мало известно о его распространенности, этиологии, патогенезе. Благодаря широкому внедрению в медицинскую практику эндоскопической диагностики и морфологических исследований стало очевидно, что микроскопические колиты являются частой причиной хронической неинфекционной диареи [6]. На сегодняшний день микроскопический колит диагностируется в 4-13% случаев диарейного синдрома [8].
Количество публикаций, посвященных микроскопическому колиту, в последнее время увеличивается, и это свидетельствует о том, что данное заболевание диагностируется гораздо чаще. С одной стороны, это связано с улучшением диагностики, с другой – с истинным ростом заболеваемости. Новые эпидемиологические исследования, проведенные в этом столетии, подтвердили высокие цифры заболеваемости, показывающие, что фактическая заболеваемость и распространенность микроскопического колита выше, чем предполагалось первоначально [26]. Показатели заболеваемости и распространенности коллагенового колита в странах Западной Европы несколько выравниваются, в то время как показатели заболеваемости лимфоцитарного колита по-прежнему растут [23]. Эпидемиологические данные, полученные из различных регионов мира, преимущественно Северной Америки и стран Европейского региона, свидетельствуют о том, что заболеваемость коллагеновым колитом составляет 0,8-6,2 случаев на 100 тыс. населения, лимфоцитарным – 0,5-12,9 случаев на 100 тыс. населения [10, 25]. Обе формы микроскопического колита по темпам заболеваемости и распространенности приближаются к классическим воспалительным заболеваниям кишечника, таким как язвенный колит и болезнь Крона [22]. Последние эпидемиологические исследования показали, что микроскопический колит является заболеванием в основном пожилых людей, особенно пожилых пациентов женского пола [27].
Крайне редко микроскопический колит диагностируется в развивающихся странах Азии. Есть немногочисленные публикации, посвященные описанию отдельных случаев микроскопического колита в странах Восточного региона, в частности Индии [14], Турции [4], Бангладеш [21]. В настоящее время нет эпидемиологических данных относительно этого заболевания из стран Африки, где инфекционные заболевания являются наиболее распространенными. Единичные случаи были зарегистрированы в Нигерии [3]. В этом регионе микроскопический колит диагностируется крайне редко из-за отсутствия средств для колоноскопии, а также в результате низкого обращения за медицинской помощью в целом.
В нашей стране, даже в специализированных клиниках, где ежегодно проводится большое количество колоноскопий по поводу хронической диареи неинфекционного генеза, редко устанавливается диагноз «микроскопический колит». «Упущение» этого диагноза происходит по многим причинам, одна из которых связана с тем, что врач-эндоскопист просто не проводит забор биопсийного материала при нормальной визуальной картине слизистой оболочки толстой кишки. Однако при взятии гистологического материала микроскопическое заключение носит часто не конкретный, обтекаемый характер, как например «хронический колит», «неопределенный колит», и т.д. На основании отсутствия визуальных патологических изменений в толстой кишке и таких неопределенных гистологических заключений, как правило, устанавливается диагноз «синдром раздраженной толстой кишки».
В диагностике микроскопического колита ведущая роль, конечно, принадлежит врачу-эндоскописту и морфологу. Однако врач общей практики или гастроэнтеролог, направивший больного на колоноскопию с целью диагностики микроскопического колита, также должен правильно поставить задачу перед врачом-эндоскопистом и морфологом для максимально четкой диагностики данного заболевания.
Микроскопический колит – заболевание, которое не представляет особого риска для пациента, поскольку не связано с повышенной смертностью, не приводит к прогрессированию, развитию осложнений и инвалидизации. В отличие от других воспалительных заболеваний кишечника, не получено доказательств того, что имеющиеся гистологические изменения при микроскопическом колите могут привести к неблагоприятным последствиям, таким как колоректальный рак или необходимость хирургического вмешательства [15]. Однако клинические симптомы могут быть упорными, рецидивирующими и привести к ухудшению качества жизни пациентов [18].
Соответственно, целью медикаментозной терапии является облегчение симптомов и улучшение качества жизни пациентов с микроскопическим колитом при одновременной минимизации негативных последствий, связанных с применением лекарственных препаратов.
Лечение микроскопического колита претерпело существенные изменения за последние десять лет. Первоначально основными лекарственными средствами для лечения данного заболевания были антидиарейные и противовоспалительные препараты [2]. Клинические исследования и метаанализы последних лет установили эффективность новых препаратов для лечения микроскопического колита [7].
В 2015 г. вышли официальные рекомендации Американской гастроэнтерологической ассоциации (American Gastroenterological Association, AGA) по лечению микроскопического колита [19]. Данное руководство было разработано ведущими экспертами в области гастроэнтерологии и утверждено советом AGA. В основу документа положены руководящие принципы доказательной медицины [1, 9, 24]. Результаты клинических исследований проанализированы, оценены экспертами, и на их основе сформулированы основные рекомендации по лечению микроскопического колита.
Это руководство фокусируется на лечении микроскопического колита, а не на его диагностике. Поскольку результаты анализа эффективных методов лечения существенно не отличались между лимфоцитарным и коллагеновым колитом, в данных рекомендациях не проводится различия между подтипами микроскопического колита.

Авторы данного обзора 25 апреля 2015 г. обсудили качество доказательств (табл. 1) и рассмотрели другие факторы, имеющие значение для оценки риска и пользы рекомендаций.
Впоследствии авторы сформулировали основные положения рекомендаций. Хотя качество доказательств является наиболее важным фактором в определении прочности рекомендации, экспертами также учитывался баланс между их пользой и негативными последствиями (табл. 2).
Рекомендация № 1. У пациентов с симптоматикой микроскопического колита для индукции клинической ремиссии AGA рекомендует лечение с применением будесонида. Сильная рекомендация, среднее качество доказательств.

Метаанализ шести рандомизированных клинических исследований продемонстрировал очевидные преимущества будесонида в индукции клинической ремиссии. В пяти исследованиях также был достигнут гистологический ответ. Два исследования показали улучшение качества жизни пациентов, хотя разница не имела статистической значимости. Пациенты, получавшие 9 мг будесонида ежедневно, более чем в два раза чаще достигали клинической ремиссии в течение 7-13 дней по сравнению с группой не получавших лечение (относительный риск – ОР 2,52, 95% доверительный интервал – ДИ 1,45-4,40). При приеме будесонида риск серьезных побочных эффектов был низким. В связи с благоприятным профилем безопасности и эффективности, а также удобством приема (1 р/день) будесонид следует считать препаратом первой линии лечения микроскопического колита. Учитывая то, что будесонид является дорогостоящим препаратом, могут быть рассмотрены альтернативные методы терапии, если стоимость лечения является определяющим фактором. В большинстве случаев нет необходимости выполнять колоноскопию для оценки гистологического ответа на проводимую терапию. Тем не менее для пациентов, у которых сохраняются клинические симптомы после лечения будесонидом, рекомендуется проведение гистологического исследования. Отсутствие патологических изменений в биоптатах ободочной кишки является причиной для верификации другого диагноза – синдрома раздраженного кишечника или целиакии. Прекращение терапии будесонидом может быть рассмотрено после 8 недель терапии. У трети пациентов удается достигнуть клинической ремиссии и не требуется поддерживающей терапии.
Рекомендация № 2. У пациентов с клиническими симптомами микроскопического колита для индукции клинической ремиссии AGA отдает предпочтение лечению будесонидом по сравнению с месалазином. Сильная рекомендация, высокое качество доказательств.
Анализ большого количества высококачественных клинических испытаний при условии прямых доказательств показал преимущество будесонида над месалазином. Поэтому будесонид следует считать препаратом первой линии по сравнению с месалазином для лечения микроскопического колита. У пациентов с симптомами микроскопического колита, которых ежедневно лечили 9 мг будесонида, клиническая и гистологическая ремиссия была достигнута в 2 раза чаще, чем у пациентов, получавших месалазин 3 г ежедневно. Кроме того, не было выявлено статистически значимых различий в возникновении побочных эффектов.
Рекомендация № 3. У пациентов с симптоматикой микроскопического колита, которым противопоказана терапия будесонидом, для индукции клинической ремиссии AGA считает целесообразным применение месалазина. Условная рекомендация, среднее качество доказательств.
Согласно результатам одного рандомизированного клинического исследования терапия месалазином показала более низкую вероятность достижения клинического эффекта по сравнению с отсутствием лечения (отношение шансов 0,74; 95% ДИ 0,44-1,24), хотя результаты данного исследования не были статистически значимыми. На основании этих данных сделано заключение, что польза месалазина в достижении клинической ремиссии больных с микроскопическим колитом является неопределенной. Из-за недостаточно определенного баланса между эффективностью и потенциальными побочными эффектами месалазин рекомендуется условно, в качестве препарата второй линии, который может быть использован при некоторых обстоятельствах. Например, пробная терапия месалазином может подходить для пациентов, которые имеют противопоказания для назначения будесонида или показали плохой клинический ответ.
Рекомендация № 4. Для пациентов с симптоматикой микроскопического колита, у которых терапия будесонидом является недопустимой, AGA предлагает лечение преднизолоном с целью индукции клинической ремиссии. Условная рекомендация, очень низкое качество доказательств.
В небольшом рандомизированном клиническом исследовании эффективность преднизолона при лечении микроскопического колита достигла 22%. В связи с небольшой выборкой пациентов клинический эффект системных стероидов является неопределенным. Несмотря на нехватку доказательств, AGA считает, что системные кортикостероиды, в частности преднизолон, скорее всего уменьшают клинические симптомы. Хотя качество фактических данных об эффективности относительно безопасности также является низким. Обширный клинический опыт применения системных стероидов для других заболеваний позволяет предположить, что риск развития побочных эффектов при лечении микроскопического колита также будет значимым. AGA предложила условную рекомендацию для использования системных стероидов при лечении микроскопического колита из-за неопределенного баланса между клинической пользой и потенциальными побочными реакциями. Хотя в большинстве случаев системные кортикостероиды не следует использовать в качестве терапии первой линии, могут быть случаи, при которых лечение преднизолоном может стать целесообразным. Прежде всего претендентами для терапии системными стероидами становятся пациенты, которые не ответили на лечение будесонидом, при условии, что были исключены другие причины неинфекционной диареи, такие, например, как целиакия. С другой стороны, преднизолон значительно дешевле, чем будесонид, это может служить альтернативным выбором для пациентов с низкими материальными возможностями.
Рекомендация № 5. У пациентов с симптомами микроскопического колита, которым противопоказана терапия будесонидом, AGA предлагает лечение салицилатом висмута для индукции клинической ремиссии. Условная рекомендация, низкое качество доказательств.
В небольшом рандомизированном контролируемом исследовании с использованием салицилата висмута для лечения микроскопического колита все 7 пациентов показали клинический ответ, в то время как ни один из 7 пациентов контрольной группы не ответил на лечение. Пациенты, получавшие салицилат висмута, имели в 3 раза более высокую вероятность достижения гистологического ответа, хотя это не было статистически значимым. Отсутствуют данные о побочных эффектах салицилата висмута при длительной терапии микроскопического колита. По этим причинам AGA условно рекомендует салицилат висмута в качестве терапии второй линии либо как альтернативный метод лечения для отдельных лиц, которые могут иметь противопоказания к лечению стероидными гормонами или для которых стоимость лечения является определяющим фактором.
Рекомендация № 6. У пациентов с симптомами микроскопического колита AGA не рекомендует комбинированную терапию холестирамином и месалазином в сравнении с монотерапией месалазином с целью индукции клинической ремиссии. Условная рекомендация, низкое качество доказательств.
Низкое качество доказательств основано на результатах одного рандомизированного клинического исследования, которое не показало увеличения клинического эффекта от добавления холестирамина к терапии месалазином. При предоставлении условной рекомендации в отношении комбинированной терапии холестирамином и месалазином AGA учитывает не только неопределенный баланс между пользой и риском, но и возможности нарушения всасывания других лекарственных препаратов при приеме холестирамина, что является особенно важным в лечении пожилых пациентов, когда полипрагмазия является обычным делом. AGA не может прокомментировать целесообразность монотерапии холестирамином, так как отсутствуют данные о клинических исследованиях, которые оценили подобное лечение у больных с микроскопическим колитом.
Рекомендация № 7. У пациентов с микроскопическим колитом AGA не рекомендует лечение Boswellia serrata для индукции клинической ремиссии. Условная рекомендация, низкое качество доказательств.
В одном рандомизированном контролируемом исследовании 44% из 16 пациентов с микроскопическим колитом показали клиническое улучшение в ответ на терапию Boswellia serrata, тогда как только у 27% из 15 пациентов клиническая ремиссия достигнута в группе плацебо. Не было выявлено никакой разницы в качестве жизни между двумя группами, побочные эффекты были более частыми в группе приема Boswellia serrata. Все полученные результаты не были статистически значимыми в дополнение к неопределенности баланса между пользой и риском терапии Boswellia serrata. Группа экспертов также высказала опасение относительно возможности доступа к стандартизованной формуле Boswellia serrata, учитывая многочисленные продукты, доступные для применения на фармацевтическом рынке, содержащие компоненты Boswellia serrata. По этим причинам AGA предоставила условную рекомендацию против рутинного использования Boswellia serrata для лечения микроскопического колита.
Рекомендация № 8. У пациентов с микроскопическим колитом AGA не рекомендует лечение пробиотиками для индукции клинической ремиссии. Условная рекомендация, низкое качество доказательств.
Основанием для данной рекомендации стали результаты небольшого рандомизированного исследования, сравнивающего пробиотические продукты (Lactobacillus acidophilus, Bifidobacterium animalis, lactis strains) с плацебо при лечении микроскопического колита. Полученные данные показали неопределенное преимущество в отношении клинической ремиссии, гистологического ответа и качества жизни пациентов с микроскопическим колитом при лечении пробиотиками. Из-за неопределенности баланса между пользой и риском побочных эффектов AGA условно не рекомендует использование пробиотиков для лечения микроскопического колита. Эксперты признают неопределенность полученных результатов в одном исследовании с применением конкретного пробиотического препарата и делают заключение о том, что полученные результаты не могут быть обобщены для всех доступных пробиотических продуктов.
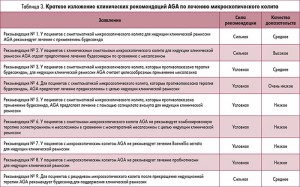
Рекомендация № 9. Для пациентов с рецидивом микроскопического колита после прекращения индукционной терапии AGA рекомендует будесонид для поддержания клинической ремиссии. Сильная рекомендация, среднее качество доказательств.
Умеренное качество доказательств получено из 2 рандомизированных клинических исследований, которые показали, что поддерживающая терапия препаратом будесонид (6 мг ежедневно в течение 6 мес) в 66% случаев приводила к снижению ОР клинического рецидива (ОР 0,34; 95% ДИ 0,19-0,60). Данный режим терапии также эффективно поддерживал гистологическую ремиссию и улучшал качество жизни пациентов с микроскопическим колитом. Прием более низких доз будесонида (чередование 3 и 6 мг в сутки) в течение 12 мес показал одинаковую эффективность в поддержании клинического ответа. Группа экспертов отмечает, что поддерживающая терапия должна быть предложена только пациентам с микроскопическим колитом, у которых развился рецидив клинических симптомов после прекращения индукционной терапии. Треть пациентов не нуждаются в проведении поддерживающей терапии, а ее прекращение может быть рассмотрено после 6-12 мес лечения.
Эти рекомендации по лечению микроскопического колита были разработаны в рамках методологии GRADE (Grading of Recommendations Assessment, Development and Evaluation) и согласованы с Институтом стандартов медицины. В результате анализа исследований можно сделать вывод о том, что для лечения микроскопического колита препаратом первой линии является будесонид – как для индукционной терапии, так и для поддержания ремиссии. Представленные прочие методы лечения могут быть использованы как альтернативные варианты лечения из-за низкого качества доказательств. Из-за отсутствия данных клинических испытаний эти рекомендации не рассматривали лечение стероидорефрактерных форм микроскопического колита [5]. Получены ограниченные данные о пользе иммунодепрессантов, таких как азатиоприн и антитела к фактору некроза опухоли, в лечении микроскопического колита [16, 17, 19, 20]. Дальнейшие клинические испытания с целью продолжения изучения новых методов позволят улучшить лечение микроскопического колита.
Литература
1. AGA Institute clinical practice guideline development process. http://www.gastro.org/guidelines/guidelines-policies.
2. Chande N., McDonald J.W., Macdonald J.K. Interventions for treating lymphocytic colitis. Cochrane Database of Systematic Reviews. 2008; (2)CD006096.
3. Ekrikpo U.E., Otegbayo J.A., Oluwasola A.O. Lymphocytic colitis presenting as difficult diarrhoea in an African woman: a case report and review of the literature. J Med Case Reports. 2010; 4: 31.
4. Erdem L., Yildirim S., Akbayir N., Yilmaz B., Yenice N., Gultekin O.S., Peker O. Prevalence of microscopic colitis in patients with diarrhea of unknown etiology in Turkey. World J Gastroenterol. 2008; 14: 4319-4323.
5. Esteve M., Mahadevan U., Sainz E. et al. Efficacy of anti-TNF therapies in refractory severe microscopic colitis. J Crohns Colitis 2011; 5: 612-618.
6. Fernandez-Ban~ares F., de Sousa M.R., Salas A. et al. Epidemiological risk factors in microscopic colitis: a prospective case-control study. Inflamm Bowel Dis. 2013; 19 (2): 411-417.
7. Gentile N.M., Abdalla A.A., Khanna S. et al. Outcomes of patients with microscopic colitis treated with corticosteroids: a population-based study. Am J Gastroenterol. 2013; 108 (2): 256-259.
8. Gentile N.M., Khanna S., Loftus E.V. Jr. et al. The epidemiology of microscopic colitis in Olmsted County from 2002 to 2010: a population-based study. ClinGastroenterolHepatol. 2014; 12 (5): 838-842.
9. Graham R., Mancher M., Wolman D.M. et al. Clinical practice guidelines we can trust. Washington, DC: Institute of Medicine; The National Academies Press, 2011.
10. Guagnozzi D., Lucendo A.J., Angueira-Lapena T., Gonzalez-Castillo S., Tenias Burillo J.M. Prevalence and incidence of microscopic colitis in patients with diarrhoea of unknown aetiology in a region in central Spain. Digestive and Liver Disease. 2012; 44 (5): 384-388.
11. Lazenby A.J., Yardley J.H., Giardiello F.M., Jessurun J., Bayless T.M. Lymphocytic (‘microscopic’) colitis: a comparative histopathologic study with particular reference to collagenous colitis. Human Pathology. 1989; 20 (1): 18-28.
12. Lindstrom C.G. ‘Collagenous colitis’ with watery diarrhoea. A new entity? Pathologia Europaea. 1976; 11 (1): 87-89.
13. Malekian V., Amirfattahi R., Sadri S., Mokhtari M., Aghaie A., Rezaeian M. Computer aided measurement of sub-epithelial collagen band in colon biopsies for collagenous colitis diagnosis. Micron. 2013; 45: 59-67.
14. Misra V., Misra S.P., Dwivedi M., Singh P.A., Agarwal V. Microscopic colitis in patients presenting with chronic diarrhea.Indian J Pathol Microbiol. 2010; 53: 15-19.
15. Munch A., Aust D., Bohr J. et al. Microscopic colitis: Current status, present and future challenges: statements of the European Microscopic Colitis Group. Journal of Crohn’s & colitis. 2012 Oct; 6 (9): 932-945.
16. Munch A., Fernandez-Banares F., Munck L.K. Azathioprine and mercaptopurine in the management of patients withchronic, active microscopic colitis. Aliment Pharmacol Ther. 2013; 37: 795-798.
17. Munch A., Ignatova S., Strom M. Adalimumab in budesonide and methotrexate refractory collagenous colitis. Scand J Gastroenterol. 2012; 47: 59-63.
18. O’Toole A., Coss A., Holleran G. et al. Microscopic colitis: clinical characteristics, treatment and outcomes in an Irish population. Int J Colorectal Dis. 2014; 29 (7): 799-803.
19. Pardi D.S., Tremaine W.J., Carrasco-Labra A. American Gastroenterological Association institute technical re-view on the medical management of microscopic colitis. Gastroenterology 2016; 150: 247-274.
20. Pola S., Fahmy M., Evans E. et al. Successful use of infliximab in the treatment of corticosteroid dependentcollagenous colitis. Am J Gastroenterol 2013; 108: 857-858.
21. Rahman M.A., Raihan A.S., Ahamed D.S. et al. Symptomatic overlap in patients with diarrhea predominant irritable bowel syndrome and microscopic colitis in a sub group of Bangladeshi population. Bangladesh Medical Research Council Bulletin. 2012; 38 (1): 33-38.
22. Sonnenberg A., Genta R.M. Geographic distributions of microscopic colitis and inflammatory bowel disease in the United States.Inflammatory Bowel Diseases. 2012; 18 (12): 2288-2293.
23. Stewart M., Andrews C.N., Urbanski S., Beck P.L., Storr M. The association of coeliac disease and microscopic colitis: a large population-based study.Alimentary Pharmacology and Therapeutics. 2011; 33 (12): 1340-1349.
24. Sultan S., Falck-Ytter Y., Inadomi J.M. The AGA Institute process for developing clinical practice guidelines part one: grading the evidence. ClinGastroenterolHepatol. 2013; 11: 329-332.
25. Tysk C., Bohr J., Nyhlin N., Wickbom A., Eriksson S. Diagnosis and management of microscopic colitis. World J Gastroenterol. 2008; 14: 7280-7288.
26. Vigren L., Olesen M., Benoni C., Sjoberg K. An epidemiological study of collagenous colitis in southern Sweden from 2001-2010. World Journal of Gastroenterology. 2012; 18 (22): 2821-2826.
27. Williams J.J., Beck P.L., Andrews C.N., Hogan D.B., Storr M.A. Microscopic colitis – a common cause of diarrhoea in older adults. Age and Ageing. 2010; 39 (2): 162-168.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Симптомы, причины, тесты и лечение
Что такое микроскопический колит?
Микроскопический колит — воспалительное заболевание кишечника, при котором толстая кишка воспаляется (опухает, раздражается). Существует два типа микроскопического колита, лимфоцитарного колита и коллагенозного колита:
- У пациентов с лимфоцитарным колитом наблюдается увеличение лимфоцитов (белых кровяных телец) в эпителии (слизистой оболочке толстой кишки).
- У пациентов с коллагеновым колитом слой коллагена (волокнистая соединительная ткань) под эпителием становится толще.
Женщины, люди старше 50 лет и люди с аутоиммунными заболеваниями (иммунная система атакует организм) более подвержены микроскопическому колиту.
Что вызывает микроскопический колит?
Микроскопический колит может иметь несколько различных причин, в том числе следующие:
- Некоторые аутоиммунные заболевания, включая целиакию, заболевания щитовидной железы, ревматоидный артрит и псориаз
- Лекарства, включая нестероидные противовоспалительные препараты, такие как аспирин, ибупрофен и напроксен; антациды и препараты от изжоги; антидепрессанты; и некоторые лекарства для лечения рака или болезней сердца
- Инфекции (вызванные бактериями или вирусами)
- Генетика (наследственность)
- Курение
Каковы симптомы микроскопического колита?
Основным симптомом микроскопического колита является диарея без крови, которая может сохраняться у пациента в течение некоторого времени.Другие симптомы включают:
- Всегда ощущение, что вам нужно опорожнить кишечник
- Похудание
- Боль и спазмы в животе
- Недержание кала (подтекание стула, вызванное неспособностью контролировать дефекацию)
- Тошнота
- Обезвоживание (сильная жажда)
- Мальабсорбция желчных кислот. Желчь вырабатывается и выделяется печенью, а затем отправляется через трубчатые структуры, называемые желчными протоками, в тонкий кишечник, где помогает организму расщепляться и усваивать пищу.При мальабсорбции желчной кислоты что-то, например камень, блокирует поток желчи из печени и желчного пузыря в кишечник.
Далее: Диагностика и тесты
Последний раз проверял медицинский работник Cleveland Clinic 25.01.2018.
Ссылки
Получите полезную, полезную и актуальную информацию о здоровье и благополучии
е Новости
Клиника Кливленда — некоммерческий академический медицинский центр.Реклама на нашем сайте помогает поддерживать нашу миссию. Мы не поддерживаем продукты или услуги, не принадлежащие Cleveland Clinic.
Политика
.
Микроскопический колит и диета: руководство по лечению для начинающих
[Последнее обновление 14 августа 2018 г.]
Хроническая и частая диарея может сделать жизнь любого человека несчастной.
Это то, с чем люди с микроскопическим колитом сталкиваются почти ежедневно.
Это воспалительное заболевание толстой кишки, разделенное на две формы — коллагеновый и лимфоцитарный колит, — становится все более распространенным явлением, и все больше людей ищут быстрого облегчения.
Здесь мы исследуем лучшие методы лечения обеих форм микроскопического колита и то, как изменение диеты и образа жизни может быть вашим лучшим долгосрочным курсом действий.
Что такое микроскопический колит?
 Микроскопический колит — это воспаление толстой кишки (толстой кишки), которое вызывает хроническую водянистую диарею.
Микроскопический колит — это воспаление толстой кишки (толстой кишки), которое вызывает хроническую водянистую диарею.
Больные могут испражняться более 10 раз в день.
Он называется «микроскопическим», потому что его можно определить только под микроскопом. Колоноскопия или ректороманоскопия его не обнаружит.
Как правило, для точного диагноза требуется биопсия толстой кишки.
Помимо воспаления, это состояние не связано с другими воспалительными заболеваниями кишечника (ВЗК), такими как язвенный колит или болезнь Крона, или инфекциями, такими как псевдомембранозный колит (C. diff колит).
Микроскопический колит подразделяется на два конкретных типа:
- Лимфоцитарный колит (ЛК): Эта форма определяется по чрезмерному количеству воспалительных клеток или лимфоцитов, в частности, более одной пятой клеток, обнаруженных в тканях толстой кишки.
- Коллагеновый колит (CC): Эта форма также включает накопление лимфоцитов вместе с утолщенным слоем коллагена в lamina propria , части соединительной ткани в толстой кишке.
В чем разница между коллагенозным колитом и лимфоцитарным колитом?
Хотя коллагеновый колит (КК) также включает образование избыточного коллагена в толстой кишке, на самом деле обе формы могут быть просто разными фазами одного и того же состояния.
По этой причине симптомы, факторы риска и лечение как CC, так и лимфоцитарного колита (LC) одинаковы.
Однако частота ЦП немного выше, чем частота ЦК, и у женщин риск развития ЦК выше, чем у мужчин (1).
Резюме: Микроскопический колит — это воспаление толстой кишки (толстой кишки), которое вызывает хроническую водянистую диарею. При лимфоцитарном колите (LC) и коллагенозном колите (CC) наблюдается обилие воспалительных клеток, но последние также показывают утолщенный слой коллагена в ткани толстой кишки. Обе формы имеют одинаковые симптомы, факторы риска и протоколы лечения.
Симптомы и причины микроскопического колита
 Основным симптомом обеих форм микроскопического колита является хроническая диарея, водянистая, но не кровянистая.
Основным симптомом обеих форм микроскопического колита является хроническая диарея, водянистая, но не кровянистая.
Другие симптомы могут включать:
- Боль в животе, спазмы или вздутие живота
- Недержание кала
- Непреднамеренная потеря веса
- Усталость
- Обезвоживание (от потери жидкости из-за диареи)
Что вызывает микроскопический колит и кто больше всего подвержен риску?
Хотя причина обоих типов микроскопического колита до сих пор неизвестна, похоже, что возраст, аутоиммунные заболевания и прием определенных лекарств увеличивают риск этого заболевания.
Люди, страдающие аутоиммунными заболеваниями, такими как артрит и целиакия, имеют более высокий шанс развития симптомов микроскопического колита.
Фактически, у людей с целиакией риск микроскопического колита в 70 раз выше, особенно у женщин среднего возраста.
Возраст также является фактором риска, 75% людей старше 50 лет. История курения также была связана с этим заболеванием (1).
Существует также сильная связь между микроскопическим колитом и использованием различных лекарств, в том числе:
- Нестероидные противовоспалительные препараты (НПВП), такие как аспирин и ибупрофен
- Селективные ингибиторы обратного захвата серотонина (СИОЗС), такие как Celexa, Paxil и Zoloft
- Ингибиторы протонной помпы (ИПП), такие как Prilosec и Prevacid
Другие препараты, такие как статины, бета-блокаторы и блокаторы рецепторов ангиотензина, также могут увеличить ваш риск.
В целом, все, что может раздражать толстую кишку — бактериальная или вирусная инфекция или нарушение всасывания желчной кислоты — может привести к любой из форм микроскопического колита.
Резюме: Основным симптомом обеих форм микроскопического колита является водянистая некровавая хроническая диарея. Другие также могут испытывать боль в животе, потерю веса и усталость. Возраст, аутоиммунные заболевания (например, артрит и глютеновая болезнь), курение и употребление определенных лекарств увеличивают ваш риск этого.
Лечение микроскопического колита
 Хотя от микроскопического колита нет лекарств, было обнаружено, что различные методы лечения его симптомов эффективны.
Хотя от микроскопического колита нет лекарств, было обнаружено, что различные методы лечения его симптомов эффективны.
Лечение одинаково для LC и CC и включает в себя лекарства, отпускаемые по рецепту и без рецепта.
Будесонид, кортикостероид (или стероидный гормон), часто называют одним из наиболее эффективных методов лечения. Было доказано, что он помогает контролировать диарею и предотвращать рецидивы.
Однако он имеет побочные эффекты, включая мышечную боль, тошноту, головную боль и расстройство желудка. И это не лучшее долгосрочное решение, поскольку после отмены чаще случаются рецидивы (2).
Сульфасалазин и месалазин, известные как аминосалицилаты, представляют собой противовоспалительные препараты, часто используемые для лечения язвенного колита и болезни Крона. Они также показали свою эффективность при микроскопическом колите.
Одно исследование показало, что 85% пациентов с ЦП испытали ремиссию через 6 месяцев приема месалазина (некоторые в комбинации с холестирамином, который помогает при мальабсорбции желчных кислот).У пациентов с КК дела обстоят еще лучше: 91% завершили испытание в состоянии ремиссии (3).
Безрецептурные противодиарейные средства, такие как субсалицилат висмута (включая такие продукты, как Pepto-Bismol и Kaopectate), также могут помочь облегчить симптомы.
Фактически, одно исследование показало, что прием Пепто-Бисмола в течение 8 недель разрешил диарею у 100% пациентов с LC по сравнению с 0% в группе плацебо. При этом размер выборки был очень маленьким — всего 9 участников (4).
Натуральные средства для лечения микроскопического колита
Конечно, перечисленные выше лекарства часто имеют побочные эффекты, поэтому добавление пробиотиков или таких трав, как boswellia serrata, может быть хорошим вариантом.
На данный момент исследования пробиотиков сосредоточены только на очень небольших выборках.
Одно небольшое исследование показало, что пробиотики (AB — Cap — 10, смесь Lactobacillus acidophilus LA-5 и Bifidobacterium lactis BB-12), принимаемые дважды в день в течение 3 месяцев, помогли избавиться от диареи у 29% пациентов с CC по сравнению с 13%, принимавшими плацебо (5).
Другой показал, что использование пробиотиков было эффективным у пациентов с ЦП, но не так сильно у пациентов с ЦК (6).
Экстракт босвеллии пильчатой, одно лечебное средство, известное своими противовоспалительными свойствами, также было протестировано при лечении микроскопического колита.
Одно исследование показало, что 6-недельное лечение boswellia serrata привело к ремиссии у 63% пациентов по сравнению с 27% в группе плацебо.
Однако в испытании был протестирован только 31 пациент; опять же, необходимы более масштабные исследования, чтобы доказать, что boswellia serrata является эффективным лечением (7).
Другие популярные противовоспалительные добавки, такие как куркумин, имбирь и омега-3 жирные кислоты, еще не изучались при микроскопическом колите.
Резюме: Лечение одинаково для LC и CC.Будесонид, отпускаемый по рецепту, оказался наиболее эффективным, в то время как безрецептурные антидиарейные препараты, такие как Пепто-Бисмол, также могут помочь облегчить симптомы. Пробиотики и экстракт босвеллии пильчатой также могут помочь при диарее, хотя необходимы дополнительные исследования.
Лучшая диета для лечения микроскопического колита

Вышеуказанные методы лечения могут помочь облегчить микроскопический колит в краткосрочной перспективе, но наиболее эффективный способ справиться с симптомами — это диета и образ жизни.
Интересно, что диетические факторы не увеличивают риск микроскопического колита, но внесение значительных изменений в свой рацион может помочь справиться с этим (8).
Для облегчения диареи часто рекомендуют диету с низким содержанием жиров и клетчатки.
Вы также можете съесть несколько небольших приемов пищи, а не несколько больших приемов пищи. Такой подход намного щадит ваше пищеварение.
Поскольку микроскопический колит чаще встречается у пациентов с целиакией, может быть целесообразно исключить глютен из своего рациона, чтобы посмотреть, помогает ли это облегчить какие-либо симптомы (9).
Хотя никаких исследований конкретных диет и микроскопического колита еще не проводилось, возможно, стоит попробовать диету с низким содержанием FODMAP. Он с низким содержанием клетчатки, почти без глютена по умолчанию, без лактозы, и первые данные показали, что он эффективен при других воспалительных заболеваниях кишечника.
Что есть и пить
Для облегчения пищеварения лучше всего подходят мягкие продукты с низким содержанием жира и клетчатки, в том числе:
- Яблочное пюре
- Бананы
- Белый рис
- Суп
- Хорошо прожаренные овощи с низким содержанием клетчатки (морковь, свекла, стручковая фасоль, пюре из шпината)
Убедитесь, что вы пьете много воды и восполняете электролиты, потерянные из-за диареи.Оставайтесь гидратированными с помощью таких напитков, как:
- Разбавленные фруктовые соки
- Вода с лимоном и морской солью
- Соки овощные фильтрованные
- Бульоны
Продукты, которых следует избегать
Определенные продукты и напитки только усугубляют диарею и обезвоживание, например:
- Продукты с высоким содержанием клетчатки, такие как бобы, орехи и сырые овощи
- Жареные и жирные продукты
- Острая пища
- Сладкие продукты и напитки (включая искусственные подсластители)
- Кофеин (кофе, чай, газированные напитки)
- Алкоголь
Как упоминалось выше, вы также можете попробовать избегать глютена и, возможно, лактозы (содержится в молочных продуктах).
Резюме: Ешьте мягкую пищу с низким содержанием жира и клетчатки, чтобы облегчить диарею. Избегайте жареной, жирной и сладкой пищи, а также кофеина и алкоголя. Вы также можете удалить глютен и лактозу (молочные продукты) из своего рациона. Обязательно оставайтесь гидратированными и восполняйте потерянные электролиты.
Возможно ли лечение вашего микроскопического колита?
Хорошая новость в том, что вы легко справитесь со своим микроскопическим колитом.
В отличие от других воспалительных заболеваний кишечника, таких как ЯК и болезнь Крона, он не увеличивает риск заболевания раком толстой кишки.
В любом случае, с его основным симптомом — хронической водянистой диареей — трудно справиться. И лимфоцитарный, и коллагенозный колит имеют этот симптом, а также факторы риска и методы лечения.
Хотя лекарства нет, лекарства, отпускаемые по рецепту, такие как будесонид, и безрецептурные противодиарейные средства, такие как Пепто-Бисмол, могут помочь облегчить симптомы.
Натуральные добавки, включая пробиотики и экстракт босвеллии пильчатой, также могут избавить от диареи, хотя необходимы дополнительные исследования.
В целом, наиболее эффективным способом лечения микроскопического колита является диета и образ жизни.
Ешьте продукты, которые легко усваиваются, в том числе продукты с низким содержанием жиров и клетчатки. Избегайте жареной, жирной и сладкой пищи, а также кофеина и алкоголя.
Вы также можете удалить глютен и лактозу (молочные продукты) из своего рациона. Обязательно поддерживайте водный баланс и восполняйте запасы электролитов, которые вы могли потерять из-за диареи.
Кроме того, поскольку ряд рецептурных препаратов (включая НПВП, СИОЗС и ИПП) связан с микроскопическим колитом, вы можете обсудить с врачом альтернативные лекарства.
В конечном итоге облегчение ваших симптомов вполне возможно. Это просто требует немного дополнительной работы, но, по крайней мере, это означает меньшее количество посещений туалета.
.
Микроскопический колит | Крона и колит, Великобритания
Микроскопический колит — это воспалительное заболевание кишечника (ВЗК), поражающее толстый кишечник — толстую и прямую кишку. Это не всегда так хорошо известно, как болезнь Крона или язвенный колит , другие формы ВЗК.
Диагноз «Микроскопический колит» может занять некоторое время. А справиться с водянистым фулом, спазмами в животе и спешкой в туалет может быть непросто. Но вы не одиноки; мы здесь, чтобы поддержать вас.Многие люди хорошо поддаются лечению, и часто симптомы исчезают, когда вы находите то, что подходит вам.
Микроскопический колит поражает часть кишечника, известную как толстая кишка, — толстая и прямая кишки. Основная задача толстой кишки — поглощать воду из фекалий, чтобы вы могли выделять твердый, но мягкий и хорошо сформированный фекалий.
Стенки кишечника многослойны. При микроскопическом колите воспаляется внутренняя оболочка. Но это изменение можно увидеть только тогда, когда образец ткани (биопсия) взят из вашей толстой кишки и рассмотрен под микроскопом.
Существует два типа микроскопического колита:
- Лимфоцитарный колит (ЛК) — внутренняя оболочка содержит больше лейкоцитов (лимфоцитов), чем обычно.
- Коллагеновый колит (CC) — внутренняя подкладка имеет более толстый слой коллагена, белка, важного для обеспечения структуры тела, чем обычно. Также может быть больше лейкоцитов.
Микроскопический колит — это общий термин для LC и CC.Хотя под микроскопом они выглядят по-разному, симптомы и лечение одинаковы. Однако несколько больше людей имеют ЦП, а женщины чаще имеют ЦК. У некоторых людей могут быть даже оба типа микроскопического колита, но в разное время.
Обычно толстый кишечник поглощает большую часть воды из оставшихся отходов пищеварения и образует твердые фекалии. Но когда толстая кишка поражена микроскопическим колитом, она не может абсорбировать столько жидкости из отходов. Это может привести к дисбалансу определенных химических веществ в кишечнике и к тому, что будет накапливаться еще больше жидкости, что приведет к образованию большого объема водянистых фекалий (диарея).
Основной симптом микроскопического колита — непрекращающаяся водянистая диарея. Это когда водянистый или жидкий стул выделяется более трех раз в день в течение более четырех недель. Для некоторых людей это может быть до пятнадцати раз в течение дня и ночи. Это может начаться внезапно или постепенно, может произойти в любое время и может происходить каждый раз, когда вы идете в туалет, или только время от времени.
Понос может:
- внезапно — не всегда успеешь дойти до туалета
- быть взрывоопасным — это когда в вашей прямой кишке водянистых фекалий и газов больше, чем она может удержать, и она выталкивает фекалии с большой силой, часто громко
- случаются несколько раз в день и ночью.
Крови в помете обычно нет.
Другие симптомы могут включать:
- Боль в области живота, которая может быть схваткообразной или тупой
- Усталость или сильная усталость — это может быть вызвано тем, что ночью встает, чтобы сходить в туалет, но многие люди испытывают это, даже если спят всю ночь.
- боль в суставах
- вздутие живота и ветер
- потеря веса.
Мои симптомы включают резкую диарею, спазмы желудка и усталость.Я тоже сильно похудела.
Lyn , 60 лет
Жизнь с микроскопическим колитом
Жизнь с симптомами
Эти симптомы могут реально повлиять на жизнь. Колеблющийся характер может означать, что некоторые дни плохие, и вы можете почувствовать, что больше не знаете свое собственное тело. Это может сильно затруднить общение с друзьями, работу и планирование мероприятий. Справившись с этими симптомами, вы также можете почувствовать себя изолированным и подавленным.
Наша информация о Fatigue , Joints , Bloating and Wind и Managing Incontinence может помочь вам найти способы справиться с этими симптомами.
Никто не сказал мне, что я могу испытать, например, усталость или боли в суставах.
Хелен, 73 года
Живет с микроскопическим колитом
Мы еще не знаем, что вызывает микроскопический колит. Считается, что сочетание факторов заставляет иммунную систему организма атаковать здоровые клетки слизистой оболочки толстой кишки.
Сюда входят:
- Повреждение слизистой оболочки кишечника — это может быть вызвано вирусами, бактериями или некоторыми лекарствами.
- Гены, унаследованные человеком.
- Другие факторы, такие как курение, возраст и пол.
У вас больше шансов заболеть микроскопическим колитом, если вы:
- Возраст старше 50 лет . Большинство людей заболевают микроскопическим колитом в возрасте от 50 до 60 лет. Но каждый четвертый человек моложе 25 лет, и у детей также диагностировано это заболевание.
- Женский
- Имеете аутоиммунное заболевание (см. Ниже)
- Дымные сигареты
- Используйте определенные лекарства , см. Список в разделе Лечение микроскопического колита.
Считается, что по крайней мере 1 из 1000 человек в Великобритании страдает микроскопическим колитом, но реальное число может быть намного выше, потому что о нем часто не сообщают и не диагностируют. Это менее известно как специалистам в области здравоохранения, так и широкой публике, что может означать, что многие люди с микроскопическим колитом справляются с этим молча.
Аутоиммунные заболевания
Около 4 из 10 человек с микроскопическим колитом также страдают заболеванием, вызванным атакой иммунной системы на другие части тела (аутоиммунное состояние).
Сюда входят:
- Сахарный диабет 1 типа
- Заболевание щитовидной железы
- глютеновая болезнь
- Ревматоидный артрит
Мальабсорбция желчных кислот (BAM)
Примерно 4 из 10 человек с микроскопическим колитом также имеют BAM. Желчные соли помогают переваривать жиры. Когда вы едите пищу, особенно с жиром, эти желчные соли выделяются из печени и желчного пузыря в верхнюю часть кишечника. Они помогают переваривать пищу по мере ее прохождения по тонкому кишечнику.Когда желчные соли достигают дальнего конца, они в основном всасываются обратно в ваше тело и возвращаются в вашу печень с кровотоком.
Мальабсорбция желчной кислоты возникает, когда кишечник не может направить желчную кислоту обратно в печень. Считается, что это раздражает слизистую оболочку толстой кишки и означает, что ваше тело не поглощает воду должным образом. Это означает, что вы производите большое количество водянистых фекалий. Узнайте больше в Diarrhea and Constipation .
История ваших симптомов
Ваш врач тщательно изучит историю всех ваших симптомов, поскольку некоторые из них могут быть похожи на другие состояния, такие как синдром раздраженного кишечника (СРК).
Колоноскопия с биопсией
При микроскопическом колите изменения в кишечнике можно увидеть только под микроскопом. Итак, чтобы диагностировать заболевание, во время колоноскопии из толстой кишки берется небольшой образец ткани (биопсия). Затем это рассматривается под микроскопом.
При колоноскопии длинная гибкая трубка (толщиной с ваш мизинец) с ярким светом и камерой на конце вводится через задний проход, позволяя специалисту исследовать слизистую оболочку толстой кишки.В ходе исследования специалист безболезненно удалит небольшие кусочки ткани со слизистой оболочки толстой кишки, чтобы исследовать их в лаборатории под микроскопом.
Врач не увидит никаких видимых признаков воспаления, если осмотрит вашу толстую и прямую кишки. Это отличается от болезни Крона или язвенного колита, когда видны воспаление или язвы. Узнайте больше в Tests and Investigations .
Мне поставили диагноз на основании биопсии, взятой во время колоноскопии.Это последовало за 6 месяцами необъяснимой потери веса, постоянной частой диареи и болей в животе.
Микаэла, , возраст 54
Живет с микроскопическим колитом
Другие анализы, которые вы можете сдать
Вы можете пройти тест на мальабсорбцию желчных кислот. Обычно это проводится в амбулаторном отделении ядерной медицины больницы. Вам дадут проглотить небольшую капсулу синтетических солей желчных кислот, содержащую небольшое количество безвредного радиоактивного материала, известного как SeHCAT.Затем вам сделают сканирование, а через неделю — еще одно. Они будут измерять поглощение радиоактивных солей желчных кислот. Узнайте больше о диарее желчных кислот в нашей информации на Diarrhea and Constipation .
Задержка в получении диагноза
Диагноз «Микроскопический колит» может занять некоторое время, и это может расстраивать.
Это может быть потому, что:
- Тест на экскременты (калпротектин) обычно бесполезен — он обнаруживает признаки воспаления в кишечнике, но при микроскопическом колите уровни часто довольно низкие.
- Ободочная и прямая кишки при колоноскопии будут выглядеть нормально — для обнаружения микроскопического колита необходимо провести биопсию.
- Симптомы могут быть аналогичны другим состояниям, таким как синдром раздраженного кишечника (СРК) или целиакия, с которыми врачи могут быть более знакомы.
Трудно было получить диагноз и лечение. Даже после этого микроскопия все еще не считается таким серьезным заболеванием, как другие условия.
Lyn , 60 лет
Жизнь с микроскопическим колитом
Прежде чем вам предложат какое-либо лечение от микроскопического колита, ваш врач рассмотрит лекарства, которые вы уже принимаете, от других заболеваний.
Лекарства, которые могут вызвать микроскопический колит, включают:
- нестероидные противовоспалительные препараты (НПВП), такие как ибупрофен, диклофенак
- некоторые ингибиторы протонной помпы (ИПП), такие как омепразол и лансопразол, используемые для снижения кислотности желудка
- селективные ингибиторы обратного захвата серотонина (СИОЗС), используемые для лечения депрессии
- аспирин
- акарбоза при диабете
- ранитидин при расстройстве желудка и изжоге
- тиклопидин для лечения заболеваний крови
- статинов для контроля холестерина.
Многие из этих лекарств также могут вызывать диарею как побочный эффект. Но если вы принимаете какие-либо из них, не прекращайте их принимать, пока не поговорите со своим врачом.
Изменение образа жизни
Сокращение употребления алкоголя и кофеина может помочь уменьшить диарею. Часто бывает полезно записывать, когда вы останавливаетесь или сокращаете дозу, и как меняются ваши симптомы, например, в дневнике питания в Food .
- Попробуйте сократить потребление кофеина — пейте чай, кофе, безалкогольные напитки или воду без кофеина и уменьшите количество потребляемого шоколада.
- Сократите употребление алкоголя — было показано, что меньше употребления алкоголя помогает облегчить симптомы.
- Бросьте курить — курение увеличивает риск микроскопического колита, и у курящих людей симптомы ухудшаются и с меньшей вероятностью выздоровеют после лечения. Ваш терапевт может предложить помощь в отказе от курения.
Лекарства
В зависимости от тяжести имеющихся у вас симптомов может быть несколько вариантов лечения.
- Лоперамид. Если у вас микроскопический колит легкой степени, могут оказаться эффективными лекарства от диареи, такие как лоперамид. Это замедляет мышечные сокращения кишечника, что заставляет пищу двигаться медленнее и позволяет впитывать больше воды. Пу становится более твердым и менее актуальным. Они также могут помочь контролировать симптомы, в то время как другим лекарствам нужно время, чтобы подействовать. Узнайте больше в нашей информации о Diarrhea and Constipation .
- Секвестранты желчных кислот. К ним относятся колестирамин, колестипол или колесевелам.Если микроскопический колит связан с мальабсорбцией желчных кислот (БАМ) или у вас по-прежнему наблюдается диарея, несмотря на другое лечение, вам могут предложить этот тип лекарства. Они связываются с желчными кислотами в кишечнике и помогают облегчить симптомы диареи. Было высказано предположение, что это может быть эффективным даже там, где BAM отсутствует.
- Будесонид. Этот стероид оказался эффективным средством лечения микроскопического колита средней и тяжелой степени. Было показано, что примерно у 8 из 10 человек улучшается состояние при приеме этого лекарства, и обычно наблюдается небольшое количество побочных эффектов.
Обычная доза составляет 9 мг будесонида в день в течение 6-8 недель. Вам также могут предложить лоперамид для контроля диареи, в то время как будесонид помогает контролировать ваше состояние. Ваши симптомы могут начать улучшаться в течение одного или двух дней, но для некоторых людей это может занять от трех до шести недель.
Более половины людей, принимающих будесонид, обнаруживают, что их симптомы возвращаются после прекращения лечения. Если это произойдет с вами, можно попробовать более низкую дозу, и это можно будет продолжать до года.Как и в случае со всеми стероидами, это обычно не долгосрочный вариант. Узнайте больше в Стероиды
Большинство людей поправляются с помощью этих подходов, но если они не работают для вас, можно попробовать другие методы лечения.
- Биологические препараты. В небольших исследованиях было показано, что Инфликсимаб и адалимумаб улучшают симптомы у некоторых людей, у которых будесонид не был эффективным. Небольшие исследования также показывают, что ведолизумаб может быть полезным. Эти лекарства принимаются вливанием или инъекциями, и вы можете узнать больше в нашей информации о Biologic Medicines .
- Иммунодепрессанты. Азатиоприн и меркаптопурин показали свою эффективность у некоторых людей, у которых будесонид не помог. Узнайте больше в Азатиоприн и Меркаптопурин .
Хирургия
Хирургия требуется очень редко, но для тех немногих людей, у которых другие подходы не увенчались успехом, это может быть вариантом. Вы можете узнать больше о возможных операциях в Хирургия язвенного колита .
Микроскопический колит НЕ повышает вероятность заболевания раком толстой кишки, чем население в целом.
Диета при микроскопическом колите у всех разная. Нет никаких доказательств того, что определенные продукты влияют на людей с микроскопическим колитом, но вы можете обнаружить, что определенные продукты являются спусковым крючком для вас. Жирная, острая и богатая клетчаткой пища ухудшает самочувствие некоторых людей, но все люди разные, поэтому ведение дневника питания может помочь. Диетолог может помочь вам подобрать здоровую диету, которая вам подходит.Попробуйте дневник питания в Food .
Многие спрашивают:
Следует ли избегать глютена? — Люди с микроскопическим колитом более чем в 50 раз чаще страдают целиакией, чем население в целом. Это означает, что вы не можете переваривать белок, называемый глютеном, который содержится в пшенице, ячмене и ржи. Чтобы узнать, нужно ли вам избегать глютена, ваш врач сделает анализ крови, чтобы проверить это. Если ваш анализ крови положительный, вам также может потребоваться эндоскопия верхних отделов желудочно-кишечного тракта.Узнайте больше в Food и Tests and Investigations.
- Следует ли избегать молочных продуктов? — Если диарея усиливается после употребления молочных продуктов, у вас могут возникнуть проблемы с перевариванием лактозы — типа сахара, который содержится в основном в молоке, сыре и других молочных продуктах. Ведение дневника питания, чтобы увидеть, как вы себя чувствуете, может помочь вам узнать, так ли это для вас — попробуйте дневник из Food. Иногда используется простой дыхательный тест, чтобы определить, есть ли у вас непереносимость лактозы.
Проконсультируйтесь с врачом или диетологом, прежде чем вносить какие-либо серьезные изменения в свой рацион. Они могут помочь вам спланировать, как отказаться от молочных продуктов или глютена, получая при этом необходимые питательные вещества.
После многих лет экспериментов я обнаружил, что молочные продукты вызывают у меня симптомы, поэтому я заменил молоко соевым или миндальным молоком.
Lyn , 57
Коллагенозный колит диагностирован в 2014 г.
Наша горячая линия принимает множество звонков от людей с микроскопическим колитом, поэтому вы не одиноки.Мы не можем посоветовать, но это может помочь вам разрешить ваши опасения. Ваш врач поддержит вас, и вам следует обратиться за помощью к медсестре, работающей с ВЗК.
Медсестра, работающая с ВЗК, может предложить поддержку и совет о вариантах лечения, повседневной жизни с микроскопическим колитом и помочь вам хорошо жить с ВЗК. Но службы поддержки NHS различаются — в некоторых регионах до сих пор нет медсестры по ВЗК, в то время как в других ресурсы ограничены, и они могут быть не в состоянии оказать вам поддержку, если у вас микроскопический колит.
Узнайте, есть ли в вашей больнице медсестра IBD .
Мы предлагаем более 50 публикаций по многим аспектам болезни Крона , Язвенного колита и других форм воспалительного заболевания кишечника. Вас могут заинтересовать наши подробные буклеты по каждому заболеванию, а также следующие публикации:
• Жизнь с болезнью Крона или колитом
• Усталость
• Прием лекарств
• Лечение недержания кишечника
The It Takes Talking Toolkit — это интерактивный инструмент со всей информацией, советами и ресурсами, которые вам понадобятся, чтобы с уверенностью начать разговор о микроскопическом колите.Существует множество индивидуальных вариантов, в зависимости от того, с кем вы хотите поговорить и что вас больше всего беспокоит.
Специалисты в области здравоохранения могут заказать несколько публикаций оптом с помощью нашей системы онлайн-заказов . Если вам нужна распечатанная копия буклета или информационного листа, обратитесь по нашей горячей линии.
Наша телефонная линия — это конфиденциальная служба, предоставляющая информацию и поддержку всем, кто страдает болезнью Крона или колитом. Наша команда может:
• помочь вам узнать больше о болезни Крона или колите, вариантах диагностики и лечения
• предоставить информацию, которая поможет вам хорошо жить с вашим заболеванием
• помочь вам понять и получить доступ к пособиям по инвалидности
• быть рядом, чтобы выслушать, если вам нужно кто-нибудь, с кем можно поговорить с
• свяжет вас с обученным волонтером службы поддержки, который лично сталкивался с болезнью Крона или колитом
Позвоните нам по телефону 0300 222 5700
Телефон доверия по электронной почте @ crohnsandcolitis.org.uk
Воспользуйтесь нашим LiveChat
Crohn’s & Colitis UK Forum
Это сообщество закрытых групп на Facebook предназначено для всех, кто страдает болезнью Крона или колитом. Вы можете поделиться своим опытом и получить поддержку от других.
Группы пациентов Crohn’s & Colitis UK
Панели пациентов IBD, которые поддерживаются Crohn’s & Colitis UK, представляют собой группы людей с болезнью Крона или колита, которые используют свою точку зрения как пациента, чтобы работать со своей командой здравоохранения IBD, чтобы помочь улучшить их больничные услуги.Для получения дополнительной информации о панелях пациентов, пожалуйста, прочтите нашу информационную брошюру или свяжитесь с нашей группой взаимодействия с пациентами .
Локальные сети Crohn’s & Colitis в Великобритании
Наши локальные сети волонтеров по всей Великобритании организуют мероприятия и предоставляют возможности познакомиться с другими людьми в неформальной обстановке, а также участвовать в образовательной, просветительской деятельности и сборе средств виды деятельности. Возможно, вы обнаружите, что просто общение с другими людьми и осознание того, что вы не одиноки, успокаивает.Семьям и родственникам также может быть полезно познакомиться с другими людьми с болезнью Крона или колитом. Все мероприятия открыты для членов Crohn’s & Colitis UK
.
Помогите нам улучшить нашу информацию — дайте нам знать, что вы думаете, заполнив короткий опрос .
.
все, что вам нужно знать
Автор:
Д-р Атаван Логанаягам
Опубликовано: 19.12.2019
Отредактировал: Лаура Берджесс
Микроскопический колит — хроническое заболевание, вызывающее воспаление толстой кишки или толстой кишки , которое приводит к симптомам водянистой диареи и спазм желудка .Состояние может быть очень болезненным, но после правильного диагноза хорошая новость состоит в том, что его можно вылечить, и качество жизни значительно улучшится.
К счастью, один из наших ведущих гастроэнтерологов доктор Атаван Логанаягам расскажет все, что вам нужно знать о микроскопическом колите; от причин до вариантов лечения.
Что такое микроскопический колит?
Микроскопический колит на самом деле включает два состояния; коллагеновый и лимфоцитарный колит .
Эти состояния называются «микроскопическими», потому что, в отличие от других воспалительных заболеваний кишечника, таких как болезнь Крона и Язвенный колит , при обследовании во время процедуры колоноскопии не наблюдается признаков воспаления слизистой оболочки кишечника.
Микроскопический колит можно диагностировать только с помощью биопсии толстой кишки, которая демонстрирует воспаление на микроскопе.
В чем причина микроскопического колита?
Существует ряд теорий относительно причины микроскопического колита, хотя точная причина неизвестна.Считается, что ряд лекарств может быть связан с микроскопическим колитом, и прекращение приема этих лекарств может привести к улучшению симптомов. Хотя симптомы коллагенозного колита и лимфоцитарного колита схожи, также неясно, связаны ли эти два состояния.
Какие симптомы микроскопического колита?
Микроскопический колит обычно вызывает хроническую водянистую диарею. Эти симптомы могут возникать либо периодически (чаще), либо постоянно.Другие сопутствующие симптомы могут включать дискомфорт в животе, потерю веса и летаргию . Он не вызывает кровавой диареи или ректального кровотечения.
Кто заболевает микроскопическим колитом?
Микроскопический колит — относительно редкое заболевание, обычно диагностируемое у людей среднего и пожилого возраста. Коллагенозный колит чаще встречается у женщин (соотношение женщин и мужчин 15: 1). Лимфоцитарный колит не имеет гендерного перевеса.
Как диагностируется микроскопический колит?
Микроскопический колит, диагностированный на основании обычной колоноскопии с биопсией толстой кишки, демонстрирующей характерные «коллагеновые» изменения или повышенное количество «лимфоцитов» в слизистой оболочке кишечника.
Коллаген — это белок, который является частью рубцовой ткани, а лимфоциты — это особый тип лейкоцитов в иммунной системе. Воспалительные изменения, наблюдаемые при микроскопическом колите, могут быть только очагами и не затрагивать всю толстую кишку, поэтому рекомендуется выполнить несколько биопсий из разных частей толстой кишки.
Как лечится микроскопический колит?
Лечение микроскопического колита зависит от тяжести симптомов и может включать антидиарейные (например, лоперамид) и стероиды (например, будесонид). Некоторые люди могут прекратить прием лекарств без повторения симптомов, хотя также может произойти рецидив, требующий повторной медикаментозной терапии.
Может ли микроскопический колит вызвать рак?
Нет данных о связи между микроскопическим колитом и раком.
Если вас беспокоят симптомы микроскопического колита, запишитесь на прием к доктору Логанаягаму прямо сейчас.
Гастроэнтерология
В Лондоне
.

