Пути введения лекарств в организм больного
Контрольные тесты по теме «Пути введения лекарств в организм больного»
1. Документ, в котором врач записывает назначения пациенту:
а) журнал назначений
б) рецептурный бланк
в) лист назначений
г) больничный лист
2. К энтеральному пути введения лекарств относится введение:
а)внутримышечно
б) внутривенно
в) внутрикожно
г) перорально
3. Преимуществом перорального способа введения лекарств перед инъекционным является:
а)медленное и неполное всасывание лекарств
б)инактивация лекарства печенью
в)местное воздействие лекарств на слизистую оболочку желудка
г) простота, возможность приёма лекарств в нестерильном виде
4. Медсестра делает выборку назначений из листа назначений:
а) через день
б) ежедневно
в)еженедельно
г) при поступлении пациента в лечебное отделение
5. К списку «А» относятся лекарственные вещества:
К списку «А» относятся лекарственные вещества:
а) наркотические анальгетики
б) снотворные
в) сильнодействующие
г) гипотензивные
6. К списку «В» относятся лекарственные вещества:
а) дорогостоящие
б) ядовитые
в)сильнодействующие
г)снотворные
7. К энтеральному способу введения лекарств относится:
а) ректальный
б) пероральный
в) сублингвальный
г) всё перечисленное вернo
8.Более удобными в применении являются лекарства
имеющие низкую токсичность
имеющие малую широту терапевтического действия
обладающие избирательным действием
9.Основной механизм всасывания лекарственных веществ в желудочно-кишечном тракте
активный транспорт
облегченная диффузия
пассивная диффузия
10.Особенности ректального пути введения лекарств в сравнении с пероральным
более физиологичный путь
лекарство не подвергается действию хлористоводородной кислоты и ферментов
лекарство меньше обезвреживается в печени
можно назначать в любом объеме
11. Побочное действие лекарств может быть
Побочное действие лекарств может быть
12.Энтерально применяются лекарственные формы
свечи
капли
мази
таблетки
13.Дисбактериоз, возникающий при назначении некоторых противомикробных средств, можно характеризовать как:
основное действие лекарства
побочный эффект препарата
мутагенное действие
заместительную терапию
14.К понятию «привыкание» имеют отношение
15.Тератогенное действие – это
токсическое действие на нервную систему больного
отрицательное действие на эмбрион и плод с нарушением органогенеза
токсическое действие на систему кроветворения
привыкание к препарату при повторном приеме
16.
 Энтеральными путями введения считаются
Энтеральными путями введения считаются
17.Особенности сублингвального пути введения лекарственных веществ
более быстрое, чем при внутримышечном введении, всасывание
отсутствие контакта с ферментами желудка и двенадцатиперстной кишки
лекарственное вещество при первичном прохождении минует печеночный баpьеp
отсутствие местного раздражающего действия
18.Запрещено внутривенное введение
больших объемов жидкости
нерастворимых соединений
осмотически активных соединений
масляных растворов
19.Факторы, воздействующие на лекарство в желудке
пепсин
липаза
кислая среда
20.Теpмином «побочное» действие лекарств можно характеризовать
нежелательное действие, возникающее в процессе лечения
синергистическое
антагонистическое
аллергенное
21.
 Пpи теpмических поpажениях pотовой полости можно пpименить наружно
Пpи теpмических поpажениях pотовой полости можно пpименить наружно
22.В основе механизма анестезиpующего действия местных анестетиков лежит
понижение чувствительности окончаний эффеpентных неpвов
наpушение пpоницаемости мембpан неpвных клеток для ионов натpия
угнетение центpов болевой чувствительности
понижение чувствительности рецепторов афферентных нервов
23.Ментол можно пpименять
пpи воспалительных заболеваниях веpхних дыхательных путей
в качестве вяжущего сpедства
для удаления боpодавок
для pефлектоpного pасшиpения сосудов сеpдца
24.Обволакивающие сpедства
пpепятствуют pаздpажению окончаний чувствительных неpвов
защищают слизистую оболочку
пpименяются пpи воспалительных пpоцессах желудочно-кишечного тpакта
оказывают pезоpбтивное действие
оказывают местное pаздpажающее действ
Выбеpите обволакивающие сpедства
слизь кpахмала
слизь из семян льна
тальк
танинВыбеpите адсоpбиpующие сpедства
тальк
уголь активиpованный
слизь кpахмальная
смектаПеpедозиpовка новокаина может пpивести к
угнетению дыхательного центpа
pезкому падению аpтеpиального давления
психической зависимости
pезкому повышению аpтеpиального давления
При местном применении этиловый спирт
может вызвать привыкание
оказывает противомикробное действие
оказывает раздражающее действие
вызывает анестезию
задерживает регенерацию
При попадании 10 % хлорида кальция в ткани развивается осложнение
тромбофлебит
некроз
абсцесс
гепатит
Ответы на контрольные тесты по теме «Пути введения лекарств в организм больного»
1.
 Документ, в котором врач записывает назначения пациенту:
Документ, в котором врач записывает назначения пациенту:
а) журнал назначений
б) рецептурный бланк
в) лист назначений
г) больничный лист
2. К энтеральному пути введения лекарств относится введение:
а) внутримышечно
б) внутривенно
в) внутрикожно
г) перорально
3. Преимуществом перорального способа введения лекарств перед инъекционным является:
а) медленное и неполное всасывание лекарств
б) инактивация лекарства печенью
в) местное воздействие лекарств на слизистую оболочку желудка
г) простота, возможность приёма лекарств в нестерильном виде
4. Медсестра делает выборку назначений из листа назначений:
а) через день
б)ежедневно
в)еженедельно
г) при поступлении пациента в лечебное отделение
5.
 К списку «А» относятся лекарственные вещества:
К списку «А» относятся лекарственные вещества:
а) наркотические анальгетики
б) снотворные
в) сильнодействующие
г) гипотензивные
6. К списку «В» относятся лекарственные вещества:
а) дорогостоящие
б) ядовитые
в) сильнодействующие
г) снотворные
7. К энтеральному способу введения лекарств относится:
а) ректальный
б) пероральный
в) сублингвальный
г)всё перечисленное вернo
а) некроз
б) абсцесс
в) сепсис
г) флебит
30. Настойки дозируют
а) граммами
б) миллилитрами
в) ложками
г) каплями
Биодоступность лекарственных средств. Что это такое, от чего зависит, примеры при различных путях введения
Что это такое, от чего зависит, примеры при различных путях введения
Большинство лекарственных средств назначают в виде пероральных препаратов или внесосудистых инъекций для лечения системных заболеваний. Следовательно, эти лекарства должны быть абсорбированы, чтобы транспортироваться к тканям-мишеням и вызывать их фармакологические действия.
Биодоступность играет ключевую роль в определении того, оказывает ли лекарство клинический эффект и как быстро он наступает.
Содержание записи:
Что такое биодоступность лекарств?
Биодоступность лекарственных средств – это количество активного вещества, которое достигло основного места действия в организме человека. Этот термин обозначает количество потерянных и сохраненных питательных или лекарственных веществ, которые необходимы для организма.
Распространенным средством определения биодоступности является измерение концентрации препарата в крови или моче через определенные промежутки времени. Врачи знают спектр биодоступности препаратов и рассчитывают дозировку для получения желаемой терапевтической концентрации лекарства.
Часто 2 термина, абсорбция и биодоступность, рассматриваются как синонимы, но между ними существует небольшая разница. Возможно, что лекарственные препараты будут быстро всасываться перорально из-за хорошей растворимости в липидах, но не будут обладать хорошей биодоступностью из-за обширной пресистемной потери.
Это относится к лекарству, потерянному между пероральным введением и первым появлением в системном кровообращении. Препарат должен пережить среду в желудочно-кишечном тракте, пересечь стенку кишки и затем пройти через воротную вену в печень.
Если молекула лекарства выживет на этом пути, она достигнет системного кровообращения. Метаболизм печени — самая большая проблема с увеличением доступности. Чтобы преодолеть слабую биодоступность, врачи увеличивают введенную дозу, изменяют фармацевтическую композицию или используют другой путь введения.
Типы биодоступности
Не все компании могут производить оригинальные лекарства, и не каждый потребитель может их себе позволить, поэтому необходимы качественные универсальные заменители активных веществ. Чтобы они соответствовали всем стандартам, необходимо проводить исследование биоэквивалентности.
Чтобы они соответствовали всем стандартам, необходимо проводить исследование биоэквивалентности.
Согласно определению ВОЗ, 2 препарата считаются биоэквивалентными, если они фармацевтически эквивалентны, имеют одинаковую биодоступность и при использовании в одинаковой дозе обеспечивают надлежащую эффективность и безопасность.
Понятие относительной биологической доступности
Биодоступность лекарственных средств — это доля вводимой дозы медицинского препарата, которая в неизменном виде попадает в кровоток. В медицинской практике чаще определяют относительную биодоступность. Стандартом измерения в этом случае является пероральная форма исследуемого препарата, которая хорошо изучена и успешно всасывается.
Относительная биодоступность лекарственных средств
Относительную доступность препарата определяют при сравнительной оценке лекарственного средства, вводимого в стандартной лекарственной форме (стандартным может быть клинически доказанный препарат) и тестового лекарственного препарата.
Оба препарата должны быть введены одним и тем же путем. Вычисление относительной доступности необходимо в случае изменения технологии производства лекарственного средства, при изготовлении различных лекарственных форм. Относительная биодоступность выражается в процентах.
Понятие абсолютной биологической доступности
Абсолютную биодоступность можно рассчитать путем сравнения общего количества лекарственного средства, которое попадает в системный кровоток после ректального, перорального и других путей введения с общим количеством, которое достигает системного кровообращения после внутривенного введения.
Оно используется в качестве стандарта, эталона, для сравнения системной доступности лекарства, вводимого различными путями.
Когда лекарство вводится внутривенно, введенная доза напрямую поступает в системный кровоток, она не будет сталкиваться с барьерами поглощения, и, следовательно, считается, что она полностью (на 100%) биодоступна. Абсолютная биодоступность также выражается в процентах.
Факторы, влияющие на биодоступность лекарств
Есть много факторов, которые влияют на биодоступность:
- Возраст.
- Сексуальная активность.
- Физическая подготовленность.
- Генетика.
- Качество производимого препарата.
- Скорость опорожнения желудка.
- Желудочно-кишечная мальабсорбция.
- Состояние функциональности системы (почки, печень).
Другими факторами, влияющими на биодоступность, являются взаимодействия с пищевыми продуктами, другими лекарственными средствами, а также с лекарственными травами и растительными средствами.
Что такое биоэквивалентность?
Биоэквивалентный лекарственный продукт означает, что биодоступность и клинические результаты тестируемого продукта и лекарственного средства, указанного в перечне как оригинала, существенно не отличаются. Фармакокинетические исследования проводятся для определения общих характеристик коммерчески доступного бренда и версии дженерика.
Фармакокинетические исследования проводятся для определения общих характеристик коммерчески доступного бренда и версии дженерика.
При этом биоэквивалентность или фармацевтическая эквивалентность должны присутствовать, показывая, что два препарата высвобождают активный ингредиент в кровоток в одинаковом количестве, с одинаковой скоростью и имеют одинаковое качество.
Биоэквивалентность не требует полного процесса клинических испытаний, через который должна была пройти версия оригинального бренда. Вместо этого препараты должны быть только биоэквивалентными. Биоэквивалентность позволяет назначать более дешевые дженерики.
Биоэквивалентность не может быть заявлена на основании только испытаний invitro или только исследований на животных. Биологическая эквивалентность человеческих лекарств должна быть определена у людей с помощью установленных показателей биодоступности. Точно так же препараты для животных должны быть проверены на биоэквивалентность у животных, для которых предназначен препарат.
После того как биоэквивалентность была установлена путем тестирования биодоступности статистически значимым образом, последующие партии одного и того же продукта считаются биоэквивалентными на основе мер invitro, таких как растворение лекарственного средства.
Утверждение о повышенной биологической эквивалентности не имеет смысла. Продукт не может быть более биоэквивалентным или менее биоэквивалентным.
Как определяется показатель?
Биодоступность лекарственных средств – это количество молекул действующего вещества, дошедших до назначенного места. Определяется она путем вычисления фармакокинетической кривой.
Абсолютная биодоступность:
[ППК] по* ДОЗА в/в
F= ───────────────
[ППК] вв* ДОЗА п/о:
- ППК – кривая «концентрация-время».
- ВВ – внутривенное введение препарата.
- ПО – пероральное введение препарата.
Площадь под кривой представляет собой область концентрации лекарства в плазме крови в зависимости от времени. Эта площадь показывает общее воздействие активного вещества на организм. С её помощью оценивается и сравнивается биодоступность препарата. Символ Тмакс. обозначает время самой высокой концентрации в крови, а C макс. означает максимальную концентрацию.
Эта площадь показывает общее воздействие активного вещества на организм. С её помощью оценивается и сравнивается биодоступность препарата. Символ Тмакс. обозначает время самой высокой концентрации в крови, а C макс. означает максимальную концентрацию.
За меру биодоступности принимается процентное соотношение количества всосавшегося препарата исследуемой формы к количеству абсорбированного средства в той же дозе эталонной формы. Стандартом служит в/в инъекция или раствор. Биодоступность лекарственных средств устанавливается различными путями.
Это 3 основных метода:
- in vitro (в пробирке) с помощью приборов;
- in vivo (внутри живого организма) на животных;
- in vivo у здоровых людей-добровольцев.
Доклинические исследования препарата на людях охватывают несколько фаз:
| Число участников | Продолжительность | Цель |
| Фаза I | ||
| От 12 до 24 человек | Несколько месяцев | Выявление максимально безопасной дозы препарата. |
Фаза II | ||
| От нескольких десятков до нескольких сотен человек | От 1–6 месяцев до 2 лет | Выявление побочных эффектов и проверка эффективности воздействия. |
Фаза III | ||
| От 1 сотни до нескольких тысяч | От 1 года до нескольких лет | Подтверждение эффективности, выявление побочных действий препарата, которые не были выявлены в предыдущие фазы. |
Фаза IV | ||
| Несколько тысяч человек | В зависимости от препарата продолжительность опыта может | |
Отрицательные виды действия лекарственных веществ. — Студопедия.Нет
Лекция №5
Тема: Основные понятия фармакокинетики: пути введения и всасывание лекарственных средств.
Фармакология – это наука о взаимодействии лекарственных средств с организмом человека и о путях изыскания новых лекарственных средств.
Как медицинская дисциплина фармакология тесно связана с другими фармацевтическими дисциплинами (фарм. химией, фармакогнозией, фарм. технологией), с общемедицинскими (физиологией, микробиологией, биохимией) и со всеми клиническими дисциплинами (терапией, педиатрией, хирургией и др.).
Задачи фармакологии:
1. Совершенствование лекарственных средств в уже известных классах химических соединений с целью приближения к идеальному препарату в каждой из таких групп.
2. Изыскание лекарственных средств с принципиально новыми или использовавшимися в прошлом, механизмами действия, которые на основании данных патофизиологии и патобиохимии могут вывести на новые, более эффективные способы фармакологического воздействия на патологический процесс.
3. Получение синтетических аналогов гормонов, медиаторов передачи нервных импульсов, местных тканевых регуляторов обмена и функций органов.
4. Анализ и освоение многовекового опыта народной медицины в области фитотерапии.
Общая фармакология – это раздел науки фармакологии, в которой суммированы сведения об общих принципах взаимодействия лекарств с организмом больного человека.
Этот раздел можно разбить на два основных подраздела: фармакокинетику и фармакодинамику.
Фрамакокинетика изучает движение лекарственных средств по организму человека, а именно пути введения лекарственных средств, их всасывание, распределение, метаболизм (биотрансформацию) и выделение из организма.
Основные положения фармакокинетики.
Пути введения лекарственных средств в организм человека.
Все пути введения можно разделить на две основные группы:
1. Энтеральные – через желудочно-кишечный тракт;
2. Парентеральные – минуя желудочно-кишечный тракт.
Энтеральные пути введения удобны в применении, не требуют стерильности препаратов и присутствия медперсонала, однако их невозможно исподьзовать во многих экстренных ситуациях, а также если больной без сознания или у него неукротимая рвота. К энтеральным путям введения лекарственных средств относятся:
1. Пероральный (через рот, внутрь) – самый распространенный путь введения вследствие его удобства. Однако эффект развивается медленно, т.к. скорость всасывания лекарственного вещества зависит от качества и количества содержимого желудка и кишечника, от свойств слизистой кишечника, его моторики. Также часть лекарственного вещества разрушается при прохождении через печеночный барьер и только после этого поступает в кровь.
2. Сублингвальный (под язык) – самый быстрый по наступлению эффекта из энтеральных путей введения, т.к. ротовая полость хорошо кровоснабжается, и лекарственное вещество попадает непосредственно в кровь, не разрушаясь пищеварительными ферментами и ферментами печени.
3. Ректальный (через прямую кишку) – путь, который используется при невозможности применения лекарств пероральным или сублингвальным способом или при необходимости воздействия непосредственно на прямую кишку. При этом лекарственное вещество не разрушается пищеварительными ферментами и ферментами печени, поэтому при всасывании в общий кровоток эффект развивается быстрее, чем при пероральном введении.
Парентеральные пути введения лекарственных средств можно разделить на инъекционные и не инъекционные.
Инъекционные пути введения лекарственных средств требуют стерильности лекарственного препарата, а также присутствия медперсонала, однако эффект лекарственного средства при этих путях введения развивается быстрее, поэтому данные пути введения могут использоваться в экстренных ситуациях. К инъекционным путям введения лекарственных средств относятся:
1. Подкожный – вводятся изотонические водные растворы, масляные растворы, крайне редко суспензии. Нельзя вводить раздражающие и гипертонические растворы. При введении масляных растворов и суспензий их подогревают до температуры тела, а после введения делают легкий массаж во избежание образования болезненных инфильтратов. Эффект развивается относительно медленно, т.к. препарат депонируется в подкожно-жировой клетчатке.
2. Внутримышечный – вводятся изотонические водные растворы, масляные растворы и суспензии. Нельзя вводить гипертонические растворы, не рекомендуется вводить раздражающие растворы. Масляные растворы и суспензии перед введением подогревают до температуры тела. Эффект развивается быстрее, чем при подкожном пути введения препаратов.
3. Внутривенный – самый быстрый путь введения по наступлению эффекта, поэтому часто используется в экстренных ситуациях. Вводят только водные растворы, как изотонические, так и гипертонические и раздражающие. Нельзя вводить масляные растворы и суспензии. При многократном введении раздражающих растворов рекомендуется использовать разные вены для профилактики развития тромбофлебитов.
4. Спинномозговой (субарахноидальный, эпидуральный) – введение лекарственных средств в спинномозговой канал. Используется для введения местных анестетиков при спинномозговой анестезии нижних конечностей и органов малого таза и для введения противомикробных средств при менингитах и энцефалитах. Можно вводить только водные изотонические и не раздражающие лекарственные средства.
Также к инъекционным относятся более редкие пути введения лекарственных средств, такие как внутриартериальный, внутрисердечный, внутрикостный и др.
К не инъекционным путям введения лекарственных средств относятся:
1. Ингаляционный – для лечения инфекционно воспалительных и аллергических заболеваний верхних дыхательных путей и в хирургии для введения ингаляционного наркоза. Таким способом могут вводиться газообразные вещества, летучие жидкости и аэрозоли.
2. Накожный (трансдермальный) – используется как для поверхностного воздействия на кожу, так и для лечения поражений глубоких слоев кожи и подкожной клетчатки. Эффект того или иного лекарственного средства зависит во многом от свойств самой кожи, а также от способа приготовления лекарственного препарата.
Также к не инъекционным путям введения лекарственных средств относятся интраназальный, конъюнктивальный и другие пути введения.
Всасываниелекарственных веществ.
Существует несколько механизмов прохождения лекарственных веществ через клеточные мембраны (биологические барьеры).
1. Диффузия – перемещение веществ через клеточную мембрану по градиенту концентрации без затрат энергии. Существует обыкновенная и облегченная диффузия. Этот вид транспорта во многом зависит от липофильности (степени поляризации) лекарственного вещества, которая в свою очередь может завесить от рН среды, в которой находится вещество. Таким образом всасываются в основном жирорастворимые, неполярные лекарственные вещества.
2. Фильтрация – перемещение лекарственных веществ через поры клеточных мембран. Таким образом переносятся чаще всего некрупные, незаряженные и водорастворимые молекулы.
3. Активный транспорт – перемещение лекарственных веществ с помощью специальных транспортных систем против градиента концентрации с затратой энергии. Этот вид транспорта отличается высокой специфичностью.
4. Пиноцитоз – захват крупных молекул лекарственного вещества с образованием вакуоли. Имеет небольшое значение для транспорта.
Лекция 6.
Тема: Основные понятия фармакокинетики: распределение, биотрансформация и выведение лекарственных средств.
Распределение лекарственных веществ.
Распределение лекарственных веществ в организме после всасывания во многом зависит от их способности проникать через биологические барьеры и связываться с белками плазмы крови, что во многом зависит от их липофильности. Вещества могут распределяться равномерно (в большинстве случаев) и неравномерно. Липофильные лекарственные вещества в большей степени поглащаются жировой тканью и создают в ней депо. Некоторые вещества обладают избирательным химическим сродством к тем или иным органам (тканям) и способны создавать депо в этих органах.
Биотрансформация – это превращение лекарственного вещества в организме. В процессе биотрансформации, как правило, активные вещества переходят в неактивные, липофильные в гидрофильные, неполярные в полярные, что способствует их скорейшему выведению из организма. Биотрансформация может осуществляться при помощи следующих типовых процессов: окисление, восстановление, гидролиз, конъюгация. Наиболее активно процессы биотрансформации осуществляются в печени. При пероральном пути введения лекарственные вещества начинают подвергаться биотрансформации уже в кишечнике и при первом прохождении через печень, т.е. до попадания в системный кровоток. Этот процесс называется пресистемной элиминацией и способен существенно снизить их биодоступность, и таким образом ослабить фармакологический эффект лекарственного вещества. Биодоступность – это количество активного (не связанного с белками плазмы) вещества в плазме крови через определенный промежуток времени после его введения относительно исходной дозы препарата. Величина биодоступности зависит от пути введения лекарственного вещества, от его лекарственной формы, физико-химических свойств, особенностей всасывания и других условий.
Выведение лекарственных веществ из организма.
Наибольшая часть лекарственных веществ выводятся из организма с калом через желудочно-кишечный тракт, с мочой через мочевыделительную систему, а также легкими через выдыхаемый воздух, секретом экзокринных желез (потовых, сальных, слезных, слюнных, бронхиальных, молочных и др.). На выделение лекарственных веществ почками во многом влияет рН мочи, т.к. она определяет степень поляризации выводимого вещества. Полярные вещества выводятся мочой быстрее. Процесс освобождения организма от лекарственного вещества характеризуется термином элиминация. Элиминация – это суммарный результат инактивации лекарственного вещества в тканях организма и его выведения (экскреции) различными путями. Для количественной характеристики процесса элиминации существует показатель период полужизни, или период полувыведения, (Т1/2) – время, за которое из организма элиминирует половина введенной дозы препарата. Знание данного показателя позволяет более рационально и безопасно подбирать дозы и кратность введения лекарственных веществ в течение курса лечения.
Вопросы для самоконтроля:
- Что изучает фармакология? Каковы теоретические и практические задачи фармакологии?
- Что изучает фармакокинетика?
- Что означает термин энтеральные пути введения?
- Перечислите и дайте характеристику энтеральных путей введения лекарственных средств.
- Что означает термин парентеральные пути введения лекарственных средств? Какие они бывают?
- Перечислите инъекционные пути введения лекарственных средств и дайте их характеристику. Перечислите не инъекционные путей введения лекарственных средств и дайте их характеристику.
- Охарактеризуйте основные механизмы всасывания лекарственных средств (пассивная диффузия, фильтрация, активный транспорт, пиноцитоз).
- Каковы особенности распределения различных лекарственных средств в организме, от чего зависит распределение?
- Что такое биодоступность?
- Что такое биотрансформация, каковы ее цели и механизмы?
- Назовите основные пути выведения лекарственных веществ из организма.
- Дайте определение терминам экскреция, элиминация, период полужизни.
Лекция №7
Тема: Основные понятия фармакодинамики.
Фармакодинамика – это раздел общей фармакологии, изучающий действие и механизмы действия лекарственных средств на организм человека.
Изменения, которые происходят в организме под действием лекарственных веществ, называются фармакологическими эффектами (видами действия). Способы, которыми достигаются те или иные фармакологические эффекты, называются механизмами действия.
Виды действия лекарственных веществ:
1. Основное – действие, ради которого лекарственное вещество применяется в медицине.
2. Побочное – нежелательные, иногда опасные, эффекты, возникающие в организме при применении лекарственного вещества в лечебных дозах.
3. Местное – действие, проявляющееся на месте применения препарата при непосредственном контакте с тканями организма.
4. Резорбтивное – действие, развивающееся после всасывания лекарственного вещества в кровь, независимо от пути введения.
5. Прямое – действие, проявляющееся при непосредственном взаимодействии лекарственного вещества с определенным органом, приводящее к изменению его функций.
6. Косвенное – действие, развивающееся вторично, вследствие реализации прямого действия. Одной из разновидностей косвенного действия является рефлекторное, осуществляемое с участием нервной системы.
7. Избирательное – действие, направленное на изменение функций определенного органа или системы органов.
8. Неизбирательное – действие, направленное на изменение функций многих органов и систем одновременно.
9. Обратимое – временное действие, которое прекращается после выведения или разрушения лекарственного вещества.
10. Необратимое – действие, сохраняющееся даже после инактивации и выведения лекарственного вещества.
Большинство лекарственных средств при осуществлении своего фармакологического действия вступают во взаимодействие с определенными участками клеточных мембран, которые называются рецепторами. Рецепторы обладают высокой специфичностью. В организме существуют естественные химические вещества (медиаторы, гормоны и др.), регулирующие работу рецепторов, их принято называть лигандами. Соответственно лекарственные вещества, действующие в организме также как лиганды, т.е. стимулирующие работу определенных рецепторов, называются стимуляторами, миметиками или агонистами. Вещества, которые блокируют взаимодействие лигандов с рецепторами, называются блокаторами, литиками или антагонистами.
Некоторые лекарственные вещества не взаимодействуют ни с какими рецепторами, а осуществляют свое действие, накапливаясь в липидном слое клеточных мембран, или вступают в чисто химические реакции с веществами, образующимися при физиологических процессах в организме.
Лекция 8.
Характеристика разновидностей фармакологического действия ЛВ при их повторном и комбинированном применении. Отрицательные виды действия ЛВ.
При повторном введении лекарственных веществ в организм человека могут возникать следующие явления:
1. Привыкание (толерантность) – постепенное ослабление эффекта препарата, вплоть до его полного отсутствия. Это может быть связано с постепенным снижением чувствительности рецепторов к данному лекарственному веществу, с ускорением его метаболизма и выведения, а также с усилением компенсаторных механизмов организма в ответ на изменения, вызванные лекарством. При этом приходится увеличивать дозу препарата или один препарат заменять другим. Одним из вариантов привыкания является тахифилаксия – очень быстрое развитие толерантности, иногда уже после второго-третьего приема препарата.
2. Кумуляция – накопление лекарственного препарата (физическая, или материальная, кумуляция) или его эффекта (функциональная кумуляция) в организме. Физическая кумуляция может быть связана с медленной инактивацией и выведением лекарственного вещества и может приводить к развитию токсических эффектов.
3. Лекарственная зависимость – болезненное пристрастие, непреодолимое стремление к приему препарата. Чаще всего развивается при приеме препаратов, вызывающих эйфорию, т.е. психотропных средств. При этом может формироваться психическая зависимость, когда резкая отмена препарата вызывает у человека депрессию, чувство подавленности, неустойчивость настроения, снижение работоспособности. Также может формироваться физическая зависимость, когда резкая отмена препарата приводит не только к эмоциональным нарушениям, но и к тяжелым расстройствам органов и функциональных систем организма, которые могут повлечь за собой смерть пациента. Такие тяжелые расстройства называются абстиненцией и проходят после возобновления приема лекарственного средства.
4. Сенсибилизация – это иммунопатологическая реакция организма, при которой формируется повышенная чувствительность к лекарственному средству, что приводит к развитию лекарственной аллергии.
Комбинированная фармакотерапия – это одновременное применение нескольких лекарственных средств. При комбинированном назначении лекарственных средств, они могут взаимодействовать на фармакокинетическом, фармакодинамическом и физико-химическом уровнях. При этом могут наблюдаться следующие виды взаимодействия лекарственных средств друг с другом.
1. Синергизм – это взаимодействие лекарственных веществ, которое приводит к увеличению конечного эффекта. Он бывает суммарным, когда величина конечного эффекта равна простой сумме эффектов каждого из лекарств, и потенцированным, когда конечный эффект превышает простую сумму эффектов каждого из лекарственных веществ.
2. Антагонизм – это взаимодействие лекарственных веществ, которое приводит к ослаблению эффекта одного вещества другим. Антагонизм бывает функциональный (лекарственные вещества изменяют функции того или иного органа в прямо противоположные стороны), конкурентный (вещества со сходной химической структурой конкурируют за транспортные и ферментативные системы или рецепторы) и химический (вещества изменяют химическую структуру друг друга). В последнем случае такие антагонисты называются антидотами (противоядиями).
Отрицательные виды действия лекарственных веществ.
Побочное действие – это нежелательные эффекты, возникающие при применении лекарственных веществ в лечебных дозах. Они могут быть неаллергические – специфичны для каждого вещества и во многом зависят от его дозы, и аллергические – неспецифичны, не зависят от дозы препарата и возникают вследствие сенсибилизации организма к данному веществу.
Токсические эффекты – это нежелательные, часто опасные для жизни, эффекты, возникающие в организме при применении лекарственных препаратов в дозах, превышающих лечебные, или при их кумуляции.
Идиосинкразия – индивидуальная, генетически обусловленная непереносимость некоторых лекарственных веществ. При этом лекарство может оказывать токсическое, быстро развивающееся действие даже в небольших дозах.
По способности лекарственных веществ оказывать негативное действие на тот или оной орган или физиологических процесс выделяют следующие виды отрицательного действия: органотоксическое – отрицательное действие на тот или иной орган или систему органов; канцерогенное – способность вызывать развитие злокачественных новообразований; мутагенное – способность вызывать мутации в клетках организма человека, в том числе в половых.
По способности вызывать токсическое действие на плод беременной женщины на различных сроках беременности выделяют следующие виды отрицательного действия лекарственных веществ: тератогенное – действие, возникающее при применении лекарственных веществ в первые 12 недель беременности и приводящее к развитию у плода уродств, часто несовместимых с жизнью; эмбриотоксическое – действие, возникающее при применении лекарственных веществ в период с 12 по 30 недели беременности и приводящее к формированию врожденных пороков развития органов и систем; фетотоксическое – действие лекарственных веществ в период с 30 недель до родов, приводящее к формированию малых аномалий развития, гипотрофию или задержку развития.
Вопросы для самоконтроля:
- Что изучает фармакодинамика?
- Дайте определение основных видов действия лекарственных средств в организме:
· основного,
· побочного,
· местного,
· резорбтивного,
· прямого,
· косвенного,
· избирательного,
· неибирательного,
· обратимого,
· необратимого.
- Что такое агонисты и антогонисты?
- Какие явления могут возникать в организме при повторном введении лекарственных веществ?
- Что такое лекарственная зависимость?
- Что такое сенсибилизация?
- Что такое толерантность, тахифилаксия?
- Какие эффекты могут наблюдаться при комбинированном применении лекарственных средств?
- Дайте определение понятиям синергизм и антагонизм.
- Что такое идиосинкразия?
- Перечислите виды отрицательного действия лекарственных препаратов на организм и дайте их характеристику.
Лекция №9
Тема: Классификация ЛС, влияющих на афферентную нервную систему.
Характеристика местноанестезирующих средств.
Афферентная (чувствительная) нервная система – это отдел периферической нервной системы, отвечающий за различные виды чувствительности. Этот отдел состоит из чувствительных нервных окончаний (рецепторов) и чувствительных нервов, которые проводят нервный импульс (информацию о раздражителе) в центральную нервную систему, где этот импульс обрабатывается и на него формируется ответная реакция. Существует несколько видов чувствительности: болевая, температурная, тактильная, проприоцептивная, зрительная, вкусовая, обонятельная, слуховая.
Классификация лекарственных средств, влияющих на афферентную нервную систему:
I. Вещества, угнетающего типа действия:
1. Местноанестезирующие средства;
2. Вяжущие средства;
3. Обволакивающие средства;
4. Адсорбирующие средства.
II. Вещества, возбуждающего типа действия:
1. Местнораздражающие средства;
2. Отхаркивающие средства;
3. Рвотные средства;
4. Горечи;
5. Слабительные средства.
Побочные и токсические действия препаратов : Farmf
Побочные и токсические действия препаратов
Что такое минимальная токсическая доза?
– максимальное количество препарата, не вызывающее токсическое действие
– доза, которая вызывает оптимальное терапевтическое или профилактическое действие у большинства больных
+ доза, которая вызывает минимальные патофизиологические изменения
– доза, которая вызывает летальный исход в 10% наблюдений
– доза, которая вызывает интоксикацию или отравление в 50% наблюдений
Мутагенное действие лекарственных веществ – это:
– врожденная повышенная чувствительность к какому-либо лекарственному веществу
– способность вызывать развитие злокачественных опухолей
+ способность вызывать изменения в генетическом аппарате
– врожденная повышенная чувствительность к какому-либо лекарственному веществу
Что такое эмбриотоксическое действие лекарственных средств:
+ неблагоприятное действие на плод, возникающее до периода имплантации
– нежелательное влияние на плод в 3 триместре беременности
Что такое фетотоксическое действие:
+ нежелательное действие на плод, приводящее к наследственным ферментопатиям
– действие на эмбрион, приводящее к врожденным уродствам
Тератогенное действие – это:
+ возникновение врожденных уродств у детей при приеме лекарственных средств в период беременности
– врожденная повышенная чувствительность к какому-либо лекарственному веществу
– способность вызывать развитие злокачественных опухолей
– раздражающие эффекты
– способность индуцировать мутации
Лекарственные вещества могут не оказывать побочного действия
– верно
+ не верно
Лекарственная аллергия:
+ нежелательна
+ относится к побочным эффектам
+ возникает даже в терапевтических дозах
– возникает только в токсических дозах
Нежелательные эффекты лекарственного вещества, возникающие при его применении в дозах, превышающих терапевтические, называют:
– побочным действием
+ токсическим действием
– идиосинкразией
– тератогенным действием
– мутагенным действием
Токсическое действие возникает:
+ при передозировке
+ при кумуляции
+ при патологии печени и почек
+ из-за недоучета индивидуальных особенностей больного
Как называется врожденная гиперчувствительность организма к ЛС:
– аллергия
+ идиосинкразия
– тератогенность
– эмбриотоксичность
Как называется приобретенная гиперчувствительность организма к ЛС:
– идиосинкразия
+ аллергия
– индивидуальная непереносимость
– сенсибилизация
Что лежит в основе идиосинкразии:
– рожденная патология внутренних органов
– тяжелая черепно-мозговая травма
+ врожденное отсутствие или нарушение активности определенных ферментов
На какой по счету прием ЛС развивается идиосинкразия:
+ на первый прием ЛС
– на повторный прием ЛС
– по завершении курса приема ЛС
Относительная передозировка возникает:
– при введении большей дозы препарата
+ при кумуляции
+ при патологии печени и почек
+ из-за недоучета индивидуальных особенностей больного
Определить вид нежелательных эффектов лекарственных веществ: мало зависят от дозы, возникают, как правило, при повторных введениях лекарственных веществ:
– побочные эффекты неаллергической природы
+ побочные эффекты аллергической природы
– токсические эффекты
– идиосинкразия
Определить вид нежелательных эффектов лекарственного вещества: усиливаются с увеличением дозы, возникают при введении вещества в терапевтических дозах:
+ побочные эффекты неаллергической природы
– побочные эффекты аллергической природы
– токсические эффекты
Что характерно для побочных эффектов неаллергической природы?
+ возникают при применении вещества в терапевтических дозах
+ относятся к спектру фармакологического действия лекарственного вещества
– их выраженность не зависит от дозы
+ их выраженность возрастаете увеличением дозы
Что характерно для побочных эффектов аллергической природы?
+ возникают при использовании вещества в любой дозе
– относятся к спектру фармакологического действия лекарственного вещества
+ обычно возникают при повторном введении лекарственного вещества
– обычно возникают при первом введении лекарственного вещества
Каким термином обозначают нежелательное действие лекарственных средств при их применении в терапевтических дозах?
+ побочное действие
– токсическое действие
Выраженность каких побочных эффектов мало зависит от дозы вещества?
+ аллергической природы
– неаллергической природы
Побочные эффекты не аллергической природы при увеличении дозы лекарственного средства:
+ усиливаются
– не изменяются
– уменьшаются
Строго дозозависимым является следующая группа побочных эффектов:
– фармацевтические;
– фармакогенетические;
– аллергические;
– мутагенные;
+ синдром отмены.
К отсроченным относится следующая группа побочных эффектов:
– токсические
– развитие лекарственной зависимости
– фармакогенетические
+ канцерогенные
– синдром отмены
Увеличение специфического эффекта лекарства при его повторном введении наблюдается при:
+ кумуляции
– привыкании
– лекарственной зависимости
– сенсибилизации
– феномене отмены
Снижение эффекта при повторном введении лекарственных препаратов наблюдается при:
+ привыкании
– кумуляции
– сенсибилизации
– психической лекарственной зависимости
– физической лекарственной зависимости
Привыкание характеризуется:
– усилением эффекта при повторном введении
+ снижением эффективности при повторном применении
– непреодолимым желанием повторно принять лекарство
– развитием сенсибилизации
– синдромом отмены
Чем характеризуется кумуляция:
– Возникает только при приеме внутрь
+ Развивается при повторном введении лекарственного препарата
+ Усиление эффекта лекарственного препарата
+ Необходимость коррекции дозы
+ Повышение риска развития побочных эффектов
Кумуляция – это:
– повышение чувствительности организма к лекарственному веществу
+ накопление в организме лекарственного вещества
– необычная реакция организма на лекарственное вещество
Как изменяется эффект лекарственного вещества в случае его кумуляции:
– ослабляется
+ усиливается
– извращается
– не изменяется
– укорачивается
“Накопление” фармакологического эффекта лекарственного вещества при его повторных введениях обозначается как:
+ функциональная кумуляция
– материальная кумуляция
– потенцирование
– тахифилаксия
Быстрое привыкание к лекарственному средству обозначается как:
– идиосинкразия
– сенсибилизация
– кумуляция
+ тахифилаксия
– абстиненция
Накопление в организме лекарственного вещества при повторных его введениях обозначается как:
– функциональная кумуляция
+ материальная кумуляций
– аддитивный эффект
– потенцирование
Что характерно для лекарственной зависимости
– развитие тахифилаксии
– увеличение эффекта при повторном введении
+ непреодолимое стремление к повторному приему лекарства с целью улучшения самочувствия и повышения настроения
– возникновение сенсибилизации
– кумуляция
Каким термином обозначают необычные реакции на лекарственные средства, связанные с генетически обусловленными энзимопатиями?
– сенсибилизация
– тахифилаксия
+ идиосинкразия
– абстиненция
– привыкание
Идиосинкразия – это:
– накопление в организме лекарственного вещества
– повышение чувствительности организма к лекарственным препаратам
+ необычная реакция организма на лекарственное вещество
– аллергическая реакция
Лекарственная зависимость проявляется:
– только при внутривенном введении
– ослаблением эффекта при повторном введении
+ не преодолимым желанием повторно принять лекарство
– усилением эффекта при повторном введении
– развитием кумуляции
Что такое тахифилаксия:
– проявление взаимодействия лекарств
– лекарственная зависимость
+ разновидность привыкания
– вид кумуляции
– синоним десенсибилизации
Синдром абстиненции характерен для:
– привыкания к лекарственному средству
+ физической зависимости
– кумуляции лекарственного средства
Стремление к повторным приемам какого-либо средства характерно для:
– привыкания к лекарственному средству
+ психической лекарственной зависимости
Г. выведение лекарственных веществ — Студопедия
29. При сублингвальном введении эффект развивается через:
А. 1-2 мин.
Б. 10-15 мин.
В. 3-4-5мин
Г. 30-60 мин.
30.При ингаляционном введении эффект развивается через:
А. 1-2 мин. В. 3-4-5мин
Б. 10-15 мин. Г. 30-60 мин.
31. Пути введения через ж-к-т:
1. Внутримышечно А. Верно 2,3,4
2. Внутрь Б. Верно 1,2
3. Под язык В. Верно 2,4
4. Ректально Г. Верно 1,3
32. Понятие «фармакодинамика» включает:
1. Механизмы действия А. Верно 1,2,3
2. Виды действия Б. Верно 2,3,4
3.Локализация действия В. Верно 1,2,4
4.Фармакологические эффекты Г. Верно все
33. При каком механизме всасывания необходима энергия?
А. Пассивная диффузия В. Активный транспорт
Б. Облегченная диффузия Г. Фильтрация
34. Местное действие лекарственных препаратов возникает:
А. через рефлекторную дугу
Б. на месте нанесения
В. через ЦНС
Г. через всасывание в кровь
35. Энтеральные пути введения:
1.Внутрикожный А. Верно 1,2
2. Перлингвальный Б. Верно 2,3
3. Ректальный В. Верно 1,3,4
4. Внутривенный Г. Верно все
36. Депонирование – это:
А. превращение лекарственных веществ В. накопление лекарственных веществ
Б. распределения лекарственных веществ Г. выведение лекарственных веществ
37. Пероральный прием препаратов характеризуется:
1. Быстрое развитие эффекта
2. Раздражение слизистой ЖКТ
3. Всасывание ЛП зависит от рН желудка, интенсивности моторики
4.Невозможность применения при бессознательном состоянии больного
А. Верно 2,3,4 В. Верно1,4
Б. Верно все Г. Верно 1,2
38. При подкожном введении эффект развивается через:
А. 1-2 мин. В. 3-4-5мин
Б. 10-15 мин. Г. 30-60 мин.
39. Метаболизм – это:
А. всасывание лекарственных веществ В. депонирование лекарственных веществ
Б. распределения лекарственных веществ Г. превращение лекарственных веществ
40.Фильтрация (облегченная диффузия) лекарственного вещества осуществляется:
А. до выравнивания концентрации Б. через поры мембран
В. С помощью белков – переносчиков пермеазов Г. с помощью пузырька
41. Основные пути выведения лекарственных веществ из организма:
1. Желудочно-кишечный тракт А. Верно 1,4
2. Потовые железы Б. Верно 2,3
3. Легкие В. Верно 2,4
4. Почки Г. Верно 1,3
42. Парентеральные пути введения:
1. Субарахноидальный А. Верно 2,4
2. Внутриполостной Б. Верно 1,3
3. Ингаляционный В. Верно 1,2,3
4. Буккальный Г. Верно 3,4
42. При пассивной диффузии транспорт лекарственных веществ осуществляется:
А. до выравнивания концентрации Б. через поры мембран
В. С помощью белков – переносчиков пермеазов Г. с помощью пузырька
43. Элиминация – это:
А. всасывание лекарственных веществ
Б. распределения лекарственных веществ
В. депонирование лекарственных веществ
Г. выведение лекарственных веществ
43.Метаболизм – это:
Введение в биохимическую фармакологию и открытие лекарств
1. Введение
Эта глава знакомит с биохимической фармакологией и освещает реакции всасывания и превращения лекарств, а также общее введение в фармакологию, открытие новых лекарств и клинические испытания новых лекарственных препаратов-кандидатов. Он также вводит концепцию индивидуализации лекарственной терапии. После изучения этой главы ожидается, что каждый продемонстрирует понимание следующего: (i) связь между различными фармакологическими процессами (ii) пути введения лекарственного средства, (iii) механизмы абсорбции лекарственного средства (iv) кинетика распределения лекарственного средства и концепции, такие как как объем распределения, начальная доза и период полувыведения; (v) биотрансформация и выведение лекарств.(vi) Роль биохимических знаний в открытии и разработке лекарственных соединений-кандидатов в полезные лекарства (vii) Базовый дизайн клинических испытаний новых лекарств и процесс утверждения лекарств. (viii) Связь между генетическими вариациями и различными реакциями на лекарства в разные люди (ix) Различные побочные реакции на лекарства у разных пациентов (x) Как рассчитываются разные режимы дозирования с учетом преобладающего состояния здоровья людей и как проводятся корректировки у пожилых пациентов или пожилых людей.
2. Фармакология
Фармакология — это наука, изучающая лекарства, их свойства, действие и судьбу в организме. Он охватывает такие науки, как фармацевтика (приготовление лекарств), терапия (лечение заболеваний с помощью лекарств) и токсикоз или побочные эффекты, возникающие в результате терапевтических вмешательств. Фармакологию можно разделить на следующие процессы: —
Фармацевтический процесс лекарственных средств; занимается химическим синтезом, рецептурой и распространением лекарств.
Фармакокинетический процесс; занимается изменением концентрации лекарства в организме с течением времени. Этот процесс можно подразделить на следующие: абсорбция, распределение, биотрансформация и выведение препарата.
Фармакодинамический процесс; занимается механизмом действия лекарств: то есть взаимодействием лекарств с молекулярными структурами в организме.
Лечебный процесс; имеет дело с клиническим ответом, возникающим в результате фармакодинамического процесса.
Токсикологический процесс; имеет дело с побочными эффектами лекарств, возникающими в результате передозировки или вмешательства в биохимические пути, не связанные с намеченной мишенью. Эти пять процессов связаны между собой, как показано на Рисунке 1.
3. Биохимическая фармакология
Биохимическая фармакология изучает влияние лекарств на биохимические пути, лежащие в основе фармакокинетических и фармакодинамических процессов, а также последующих терапевтических и токсикологических процессов.Однако фармацевтический процесс выходит за рамки биохимической фармакологии.
4. Пути введения лекарственного средства и системная доступность
Это зависит от фактических биохимических характеристик лекарственного средства и взаимодействия молекул лекарственного средства с жидкостями и тканями организма. Основные пути введения лекарств — местное, парентеральное и энтеральное.
Способ применения лекарства определяет, как быстро лекарство достигает места действия.Таким образом, выбор способа введения лекарственного средства зависит от терапевтических целей лечения. Например, внутривенная инъекция или ингаляция могут быть выбраны для получения интенсивных, но довольно краткосрочных эффектов, в то время как пероральное дозирование может быть лучше и удобнее для длительных эффектов и даже интенсивности. К различным типам введения лекарств относятся:
4.1. Местное применение
Это наиболее прямой и простой способ введения лекарства.Он включает местное нанесение препарата на место действия, например растворы глазных капель, спреи и лосьоны для перорального, ректального, вагинального и уретрального применения. Эти препараты всасываются через клеточные мембраны. Всасывание лекарств через кожу пропорционально их растворимости в липидах, поскольку эпидермис ведет себя как гидрофильный барьер. Поэтому нерастворимые в липидах лекарственные средства суспендируют в масляных носителях для повышения растворимости и, следовательно, абсорбции.
Рисунок 1.
Взаимосвязь между пятью фармакологическими процессами, начиная с поступления лекарственного средства и заканчивая клиническим ответом и / или токсическими эффектами
4.2. Пероральный прием
Препараты, вводимые перорально, всасываются в различных участках желудочно-кишечного тракта (ЖКТ):
4.2.1. Слизистая оболочка полости рта или подъязычно
Всасывание лекарств обычно происходит быстро из-за обильного кровоснабжения слизистой оболочки и отсутствия рогового слоя. Препараты, доставляемые этим путем, не подвергаются воздействию желудочного и кишечного пищеварительного сока и не подвергаются немедленному прохождению через печень. Следовательно, перед попаданием лекарств в системный кровоток не происходит предварительной биотрансформации или первого эффекта.
4.2.2. Желудок и кишечник
Всасывание зависит от различных факторов, таких как pH, опорожнение желудка, перистальтика кишечника и растворимость твердых лекарств. Скорость, с которой лекарство достигает тонкого кишечника, увеличивается, если лекарство запивать водой и когда желудок относительно пустой. Однако лекарства, всасываемые в желудке и кишечнике, подвергаются эффекту первого прохождения.
4.3. Ректальное введение
Это предпочтительный путь, когда пероральный путь не подходит из-за тошноты или если лекарства имеют неприятный вкус или запах.Этот путь также защищает чувствительные лекарства от реакций биотрансформации в печени. Однако абсорбция этим путем часто бывает нерегулярной и неполной. Такие препараты, как суппозитории или клизмы, применяются ректально.
4.4. Парентеральное введение
Этот способ введения также известен как инъекция. Как правило, это происходит быстрее и позволяет более точно выбирать дозу и предсказуемую абсорбцию. Парентеральные пути включают;
4.4.1. Подкожная инъекция
Этот способ введения в основном используется для нераздражающих лекарств.Он обеспечивает равномерное и замедленное всасывание, вызывая стойкий лекарственный эффект. Сосудосуживающие агенты, такие как адреналин, могут быть добавлены к раствору лекарства для уменьшения скорости абсорбции.
Однако большие количества лекарств могут быть болезненными из-за растяжения тканей.
4.4.2. Внутримышечная инъекция
Этот способ доставки лекарства обеспечивает быстрое всасывание лекарства в водных растворах. Медленное и равномерное всасывание возможно при суспендировании лекарств в масляных носителях.
4.4.3. Внутривенное введение
Этот путь обеспечивает быструю доставку нужной концентрации препарата в крови, которая может быть получена точно и немедленно, и является предпочтительным путем доставки в экстренных ситуациях. Раздражающие препараты вводятся внутривенно, потому что вены имеют низкую чувствительность к боли. Этот способ доставки также предпочтителен для таких лекарственных средств, как барбитураты и фенитоин, противосудорожных препаратов, которые растворяются только в довольно сильном щелочном растворе и, следовательно, нуждаются в крови для буферизации рН раствора лекарственного средства для лучшей растворимости.Лекарства, такие как этилендиаминтетрауксусная кислота (ЭДТА), для лечения отравления тяжелыми металлами вводятся внутривенно или в виде инфузии, поскольку они плохо всасываются в кишечнике. Другим преимуществом этого способа доставки является предотвращение эффекта первого прохождения через печень и легкие. Как правило, свойства препарата могут определять путь, который следует использовать для достижения разумной эффективности.
5. Механизмы всасывания лекарств через мембраны
Для того, чтобы лекарственные препараты проявили свои фармакологические эффекты, они должны проникнуть через биологические мембраны в системный кровоток и достичь места действия.Таким образом, понимание структуры и функции мембраны приводит к лучшему пониманию абсорбции лекарственного средства. Мембраны представляют собой двухслойные фосфолипиды с вкраплениями интегральных и периферических белков, которые действуют как молекулярные «ворота» или «насосы». Молекулярные ворота неспецифичны. Поступление молекул в клетку зависит от заряженных групп в поре и размера молекулы, которая переносится через мембрану. Молекулярные насосы, однако, очень специфичны и требуют энергии для молекулярного транспорта.Существует несколько механизмов, с помощью которых лекарственные средства проходят через мембраны, чтобы достичь намеченного целевого сайта, и они включают следующие:
5.1. Простая диффузия
Это включает прохождение полярных, но незаряженных веществ через заполненные водой каналы в ответ на градиент концентрации. Простая диффузия — это механизм выбора для водорастворимых лекарств и лекарств с низкой молекулярной массой, таких как эстетическая закись азота (44 кДа) и этанол (46 кДа). Большинство липидорастворимых лекарств проникают через клеточные мембраны за счет пассивной диффузии между липидными молекулами мембраны.Скорость проникновения липидорастворимого лекарственного средства зависит от концентрации лекарственного средства, его коэффициента распределения липид / вода, концентрации протонов и площади поверхности абсорбирующей мембраны. Коэффициент распределения липида / воды лекарственного средства является основным фактором, определяющим его абсорбцию.
Чем выше значение коэффициента распределения липид / вода в лекарстве, тем быстрее оно абсорбируется, и наоборот. Химическая сила, которая заставляет жирорастворимые лекарства легко перемещаться через мембраны, называется гидрофобной силой, поскольку молекулы воды отталкивают жирорастворимые лекарства.В большинстве случаев абсорбция лекарственного средства может быть усилена усилителями абсорбции, такими как жирные кислоты, фосфолипиды и мукоадгезивные полимеры. Эти соединения разрушают липидный бислой, делая его более проницаемым, а также повышают растворимость нерастворимых лекарств.
5.2. Облегченная диффузия
Этот тип диффузии достигается молекулами-носителями, которые объединяются с рассматриваемым лекарственным средством с образованием комплексов, которые могут диффундировать через мембрану быстрее, чем это могло бы сделать свободное лекарство в одиночку.Примером является транспорт нуклеотидных антиметаболитов, используемый в химиотерапии вирусов или рака.
5.3. Активный транспорт наркотиков
Это транспорт, связанный с источником энергии. Примерами конкретных активных транспортных систем являются натриевая помпа, которая поддерживает высокий уровень ионов калия и низкий уровень ионов натрия внутри клетки относительно внешней среды, и кальциевый насос, который поддерживает высокую концентрацию кальция внутри саркоплазматического ретикулума и низкую концентрацию вокруг миофибрилл.Обнаружен активный транспорт лекарств через мембраны, и примером является поглощение пентазоцина (антагониста наркотических средств) лейкоцитами, которое зависит от поступления энергии (глюкозы) и может подавляться циклазоцином, который конкурирует за тот же механизм транспорта.
5.4. Пиноцитоз и фагоцитоз лекарственных средств
Белки, бактериальные токсины и лекарственные средства с высокой молекулярной массой (1000 кДа и более) проникают в клетки посредством пиноцитоза и эндоцитоза. Эти вещества окончательно попадают в лизосомальную систему.
6. Факторы, влияющие на абсорбцию лекарственных средств
6.1. Площадь поверхности
Для любого вещества, которое может проникать через ЖКТ в измеримых количествах, тонкий кишечник представляет собой наибольшую область абсорбции. Например, этанол может всасываться в желудке, но в тонком кишечнике он всасывается в восемь раз быстрее из-за большой площади поверхности, обеспечиваемой ворсинками. Скорость, с которой содержимое желудка опорожняется в тонкий кишечник, также заметно влияет на общую скорость, с которой лекарства попадают в общую циркуляцию после перорального приема.По этой причине многие агенты вводятся натощак с достаточным количеством воды, чтобы обеспечить их быстрое проникновение в тонкий кишечник.
6.2. PH ткани
Лекарства можно классифицировать как органические амины или органические кислоты, и поэтому их абсорбция сильно зависит от pH. Третичные амины не заряжаются при высоком pH и имеют высокий коэффициент распределения липид / вода и, следовательно, легко проникают через мембраны.
При низком pH третичный амин протонируется и имеет низкий коэффициент распределения липид / вода, что снижает скорость проникновения.
В случае органической кислоты применяется тот же общий принцип. Непротонированная органическая кислота при низком pH легче проникает в ткани по сравнению с заряженной формой лекарства при высоком pH.
Низкий pH Высокий pHR-COOH ⇌ R — COO- + H + Желудок Кишечник
Следовательно, органические кислоты, такие как барбитураты и ацетилсалициловая кислота (аспирин), имеют более высокую скорость абсорбции в желудке.
Степень ионизации лекарственного средства в желудочно-кишечном тракте или других жидкостях организма является основным фактором, определяющим количество лекарственного средства в незаряженной форме, и это зависит от соотношения между pH жидкости и pKa лекарственного средства:
Кислотные препараты:
RCOOH⇌KaRCOO- + H +
Основные препараты:
R — + Nh4⇌Ka RNh3 + H +
Если pH жидкости низкий, ионизация кислых препаратов меньше, а ионизация базовые лекарства будут высокими.Когда pKa лекарства равно pH окружающей жидкости, происходит 50% ионизация.
7. Типы тканевых барьеров для лекарств
Большинство из этих барьеров, как правило, являются теми же системами, которые животные используют для защиты от вторжения чужеродных агентов. Эти барьеры включают кожу, оболочки ЖКТ, гематоэнцефалический барьер и плаценту.
7.1. Кожа
Поверхностный слой кожи, роговой слой, особенно непроницаем для большинства лекарств. Проницаемость кожи для лекарств увеличивается за счет использования системы сорастворителей, такой как этанол / вода, которая увеличивает распределение лекарственного средства в коже.Липидные домены слизистой оболочки щек и носа также ограничивают проникновение лекарств, и лекарственные средства, которые проникают, могут делать это посредством пассивной диффузии с использованием гидрофильных трансклеточных пространств и прямого проникновения через мембрану.
7.2. Плотные соединения
Щелевые соединения между клетками в разных типах клеток внутри ткани могут образовывать каналы для прохождения лекарств между эпителиальными, эндотелиальными и мезотелиальными клетками одной и той же ткани. Эти каналы состоят из группы белков, известных как коннексин.Однако клетки в разных тканях связаны плотными контактами, и это может нарушать транспорт между клетками в разных тканях. Плотные контакты — это динамические структуры, которые обычно регулируют перемещение питательных веществ, соединений среднего размера между клетками и образуют регулируемый барьер в промежутках между клетками. Следовательно, существует необходимость в использовании усилителей всасывания лекарств, таких как соли желчных кислот и длинноцепочечные ацилкарнитины, которые действуют как хелаторы Ca 2+ и разрушают плотные контакты, тем самым улучшая транспорт через соединения.Плотные соединения показаны на рисунке 2.
Рисунок 2.
Расположение эпителиальных клеток с плотными контактами
7.3. Барьер спинномозговой жидкости (CSF)
Эпителиальные клетки, которые находятся в контакте с желудочковыми пространствами головного мозга, создают барьер для движения лекарств. Эти эпителиальные клетки связаны закрывающими зонулами (гематоэнцефалический барьер), как показано на рисунке 3. Зонулы сильно ограничивают прохождение большинства молекул между кровотоком и паренхимой центральной нервной системы.Проникновение лекарств через этот барьер осуществляется либо посредством пассивной диффузии, либо посредством транспорта, опосредованного носителями. Только липидорастворимые препараты проникают в спинномозговую жидкость из крови.
Рис. 3.
Эпителиальные клетки с плотными контактами как часть гематоэнцефалического барьера
Эпителиальные клетки, которые отделяют спинномозговую жидкость от мозга, связаны плотными контактами и характеризуются заметным дефицитом пиноцитарных пузырьков. Однако эпителиальные клетки, выстилающие мозг, не соединены закрывающими зонулами, и, следовательно, существует неограниченный проход молекул лекарства из спинномозговой жидкости в мозг.Такие препараты, как пенициллин, которые плохо растворимы в жирах и требуются в высоких концентрациях для лечения абсцессов головного мозга, вводятся путем интратекальных инъекций непосредственно в CFS.
7.4. Плацентарный барьер
Плацентарная мембрана ограничивает количество материнской крови, идущей через плаценту к плоду, а пассивная диффузия является основным механизмом попадания лекарств из материнской крови к плоду. Наименьшее время, необходимое для уравновешивания лекарственного средства между матерью и плодом, составляет около десяти минут, и эта задержка полезна, поскольку она может позволить матери провести анестезию на заключительных этапах родов.
8. Системная доступность лекарств
Препарат достигнет системного артериального кровообращения только в том случае, если он абсорбируется из ЖКТ и не подвергается метаболизму в кишечнике, печени и легких. Когда концентрацию лекарственного средства в плазме измеряют через определенные интервалы времени, можно построить график зависимости концентрации от времени и, следовательно, определить степень доступности лекарственного средства, как показано на рисунке 4.
Доступность зависит как от степени абсорбции и степени пресистемного метаболизма и включает три аспекта; Пиковая концентрация (C max ), время, необходимое для достижения пика (T max ), и площадь под кривой (AUC), как показано на рисунке 4.C max и T max являются показателями степени доступности, в то время как AUC является мерой степени доступности (т. Е. Доли введенного лекарственного средства, которая достигает системного кровообращения в неизменном виде). Для трех кривых, показанных для составов a, b и c; AUC одинакова, но степень доступности в каждом случае разная; a имеет самый низкий уровень доступности, за которым следует b, а c — самый высокий уровень доступности.
Рисунок 4.
Кривые зависимости концентрации в плазме от времени для различных лекарственных форм
Скорость, с которой конкретное лекарство необходимо для достижения места действия, будет определять тип используемой композиции.Лекарства с одинаковой относительной биодоступностью, которые можно использовать для лечения одного и того же состояния с использованием тех же способов или дозировок, известны как биоэквивалентные препараты.
9. Дозировка и эффект
Конкретная доза вводимого лекарства зависит от биохимических процессов в организме, как показано на рисунке 5. Желаемый эффект лекарства пропорционален концентрации лекарства в месте его действия. который описывается следующими кинетическими параметрами: (i) Кажущийся объем распределения (V d ), который представляет собой объем гидрофильных и гидрофобных пространств в организме, в которых распространяется лекарство.Его получают делением введенной дозы (D o ) на исходную концентрацию (C o ) в плазме крови. Лекарства, которые связываются с тканями, имеют низкие концентрации в плазме и, следовательно, имеют более высокий V d по сравнению с теми, которые в основном связываются белками плазмы крови. В среднем человек весом 70 кг имеет общий объем воды в организме ~ 50 л, из которых ~ 10 л занимает внеклеточное пространство.
Рис. 5.
Пути распределения лекарства от абсорбции к экскреции
Кажущийся объем распределения не может сказать нам, где на самом деле находится лекарство в организме.(C tox ) — это максимальная концентрация лекарственного средства, при превышении которой могут возникнуть токсические эффекты в организме, в то время как (C до ) — это концентрация лекарства в плазме, при которой достигается терапевтический эффект или эффективный клинический ответ. Концентрация устойчивого состояния (C ss ) — это концентрация, которая должна поддерживаться между любыми двумя интервалами введения лекарства. Эти фармакокинетические данные важны, поскольку они характеризуют судьбу лекарственных средств в организме и требуются фармакологам для расчета доз и частоты введения лекарств.Однако в некоторых клинических ответах интенсивность фармакологического действия лучше коррелирует с концентрацией свободного лекарства в плазме, в то время как в других ответах нет прямой зависимости между концентрацией лекарства и клиническим ответом. Основные вариации эффектов реакции на наркотики включают:
Лекарства, которые соединяются со своими рецепторами так же быстро, как они отделяются от них; для этой категории препаратов фармакологический эффект увеличивается или уменьшается одновременно с концентрацией препарата в плазме.
Лекарства, которые плохо отделяются от своих рецепторов. В этом случае фармакологический эффект сохраняется, несмотря на падение концентрации в плазме.
Лекарства, которые сочетаются с рецепторами и независимо от скорости их ассоциации / диссоциации, запускают каскад событий, который продолжается, несмотря на падение концентрации в плазме.
10. Кинетика процесса распределения лекарства
Процесс распределения лекарства в большинстве случаев соответствует кинетике порядка 1 st , в которой распределение пропорционально концентрации лекарства в любой момент времени.Следовательно, концентрация лекарственного средства в плазме будет снижаться со скоростью, которая всегда пропорциональна самой концентрации. Следовательно;
-d [C] dt = K [C]
∫-d [C] [C] = ∫Kdt
Более удобная форма этого уравнения получается, если взять log10
Так как
lnx = 2.303log10xE1
Отсюда следует, что;
2.303log10C = 2.30.3log10C0-Kt
и log10C = log10C0 — Kt2.303
Линейная зависимость получается, когда логарифм концентраций (log10C) наносится на график относительно (t), время наблюдения (рисунок 6).
Рисунок 6.
Логарифмический временной ход концентрации лекарственного средства
Период полувыведения (t 1/2 ) лекарственного средства: это период времени, в течение которого концентрация снижается до половины от своего предыдущего значения. T 1/2 можно определить по константе скорости исключения.
Когда t = t1 / 2, C t = C02
, следовательно,
C02 = C0e-Kt1 / 2
12 = e-Kt1 / 2 но, Kt1 / 2 = loge2
t1 / 2 = loge2K = 0,693K
11.Реакции биотрансформации лекарств
Лекарства и другие чужеродные вещества (ксенобиотики) претерпевают ряд реакций биотрансформации в организме. Реакции биотрансформации действуют как стратегия защиты первой линии против этих ксенобиотиков. Он оснащен батареей ферментов, которые превращают жирорастворимые ксенобиотики в более водорастворимые метаболиты, чтобы обеспечить более эффективное выведение лекарств в ограниченном объеме воды с мочой или желчью.
Ферменты, участвующие в биотрансформации эндогенных химических веществ, являются теми же ферментами, которые используются в биотрансформации ксенобиотиков.Следовательно, существует тесная связь между биотрансформацией лекарств и фундаментальными гомеостатическими процессами.
Реакция биотрансформации лекарственного средства может привести к следующим потенциальным эффектам в отношении фармакологической активности:
11.1. Активация
Неактивный предшественник может быть преобразован в фармакологически активное лекарство. Например, аналог нуклеозида, используемый в качестве лекарственного средства против ВИЧ, должен подвергнуться фосфорилированию in vivo и для образования активных трифосфатов, которые действуют, чтобы ингибировать фермент обратной транскриптазы, в то время как L-допа (неактивный), который используется в лечении. болезни паркинсона, превращается в дофамин (активный) в базальных ганглиях.Футамид, лекарство, используемое для лечения рака простаты, подвергается гидроксилированию в боковой алкильной цепи с образованием гидроксифлутамида, метаболита, который является более активным и имеет более длительную продолжительность действия по сравнению с исходным лекарственным средством.
11.2. Поддержание активности
Активное лекарство превращается в другую форму, которая также является активной, например, диазепам, снотворное седативное средство, метаболизируется до столь же активного метаболита, оксазепама.
11.3. Инактивация
Активное лекарство превращается в неактивные продукты, например, пентобарбитал гидроксилируется до форминоактивных метаболитов.
11.4. Реакции фазы I
Они включают реакции окисления, восстановления и гидролиза, и такие реакции обычно вводят или демаскируют функциональную группу (гидроксил, амин, сульфгидрил и т. Д.), Которая делает лекарство более полярным.
11,5. Реакции фазы II
Состоят из реакций синтеза / конъюгирования, в которых эндогенное вещество, такое как глюкуроновая кислота или глутатион, объединяется с функциональной группой, полученной в результате реакций фазы I, с образованием высокополярного конъюгата лекарственного средства.Все ткани обладают некоторой способностью проводить реакции биотрансформации лекарств, но наиболее важные органы биотрансформации включают: печень, желудочно-кишечный тракт, легкие, кожа и почки в таком порядке, и большинство реакций фазы II приводят к снижению фармакологической активности препарата. Тот факт, что желудочно-кишечный тракт и печень являются основными участками биотрансформации лекарств, означает, что лекарства, которые вводятся перорально, будут экстенсивно биотрансформированы, прежде чем они в конечном итоге попадут в системный кровоток. Этот эффект первого прохождения может серьезно ограничить пероральную биодоступность некоторых лекарств.Кроме того, кишечные микроорганизмы способны катализировать реакции биотрансформации лекарств, например глюкуронидный конъюгат лекарственного средства может выводиться через кишечник с желчью, где кишечные бактерии могут преобразовывать конъюгат обратно в свободное лекарственное средство. Затем свободное лекарство реабсорбируется и снова попадает в печень через воротную вену, где повторяется процесс конъюгации. Это приводит к явлению, известному как энтеро-печеночная циркуляция.
На субклеточном уровне ферменты биотрансформации лекарств расположены в эндоплазматическом ретикулуме, митохондриях, цитозоле и лизосомах.Основным местом биотрансформации лекарств в гепатоцитах и других клетках является мембрана гладкого эндоплазматического ретикулума. Гладкая эндоплазматическая сеть представляет собой фракцию микросом во время дифференциального центрифугирования цельной крови. Фракцию микросом можно использовать для проведения многих реакций биотрансформации лекарственных средств in vitro.
11.6. Механизмы реакций I фазы
11.6.1. Окисление
Является наиболее важной категорией микросомальных систем окисления лекарств и требует участия двух различных белков в эндоплазматическом ретикулуме; цитохромы P 450 (которые функционируют как терминальная оксидаза) и цитохром P 450 редуктаза.Название Cyt 450 происходит от того факта, что восстановленная форма этого гемопротеина комплексов с монооксидом углерода с образованием комплекса, который имеет уникальный спектр поглощения с максимумом при 450 нм. Редуктаза цитохрома Р 450 служит для переноса восстанавливающего эквивалента из НАДФН в цитохром Р 450 оксидаза:
DrugRH + O2 + NADPH + H + → DrugROH (гидроксилированный продукт) + h3O + NADP +
Последовательность реакций, которые превращают лекарство в его гидроксилированный продукт, показана ниже (Рисунок 7).
Рис. 7.
Фаза 1 реакций биотрансформации лекарств в микросомальной фракции печени, в которых лекарство превращается в более полярную форму.
Фосфолипиды эндоплазматического ретикулума необходимы для связывания субстрата, переноса электронов и облегчения взаимодействия между CytP 450 и его редуктазой. Однако цитохром P 450 не катализирует все реакции окисления. Микросомальные флавинсодержащие монооксигеназы (FMO) катализируют НАДФН-зависимую оксигенацию нуклеофильных атомов фосфора, азота и серы.Эти атомы присутствуют в большом количестве ксенобиотиков, включая карбамат-содержащие пестициды и терапевтические агенты, такие как фенотиазины, эфедрин и N-метиламфетамин. Другой важной лекарственно-окислительной системой является зависимое от простагландинсинтетазы совместное окисление.
Многие ксенобиотики, включая фенитоин, могут подвергаться совместному окислению вместе с указанной выше реакцией восстановления. Этот путь имеет большое токсикологическое значение, поскольку часто приводит к образованию токсичных реактивных метаболитов.Другие ферменты, катализирующие окисление ксенобиотиков, включают алкогольдегидрогеназу, альдегиддегидрогеназу, ксантиноксидазу и моноаминоксидазу.
11.6.2. Восстановление
Некоторые препараты с азосвязями (RN = NR, например пронтозил) и азотными группами (RNO 2 , такие как хлорамфеникол) трансформируются восстановительными путями. Ферменты редуктазы Cyt P 450 и NADPH-cyt P 450 , которые катализируют реакции окисления, также участвуют в реакциях восстановления лекарств, содержащих хининовые фрагменты.Эта трансформация приводит к образованию свободных радикалов семихинона, показанных на фиг.8. Образующиеся свободные радикалы вызывают окислительный стресс, перекисное окисление липидов, повреждение ДНК и, следовательно, цитотоксичность. Эти эффекты особенно ответственны за противоопухолевые свойства такого лекарства, как доксорубицин.
11.6.3. Гидролиз
Лекарства, содержащие сложноэфирные функции (R 1 COOR 2 ), такие как прокаин, гидролизуются множеством неспецифических эстераз в печени и плазме, в то время как лекарства с амидными связями гидролизуются амидазами в лив
Первый — и препараты второго ряда и лекарственная устойчивость
1.Введение
Туберкулез (ТБ) вызывается инфекцией, вызванной Mycobacterium tuberculosis , которая передается при вдыхании аэрозольных капель. Туберкулез в основном поражает легкие, но может поражать и другие части тела. Туберкулез очень заразен во время активной стадии заболевания и может заразить человека при вдыхании всего 10 бактерий Mycobacterium tuberculosis (MTB). После ингаляции эти бактерии в основном захватываются альвеолярными макрофагами, но они могут уклоняться от иммунной системы хозяина и оставаться в стадии покоя в течение длительного периода времени, после чего они могут реактивироваться до вирулентной формы в условиях ослабленного иммунитета. гостья.Это возможно, потому что M. tuberculosis может сохраняться как на медленных, так и на быстрых стадиях роста, что затрудняет лечение. Почти все антибиотики, которые можно использовать для лечения туберкулеза, работают, когда бактерии активно делятся. В интенсивной фазе лечения туберкулеза антибиотики в основном убивают быстрорастущие бактерии, что вызывает быстрое превращение мокроты и устранение клинических симптомов. Однако для того, чтобы убить устойчивые или медленно растущие штаммы MTB, необходима фаза продолжения лечения.Туберкулез можно эффективно лечить с помощью препаратов первого ряда (FLD), изониазида (INH), рифампицина (RIF), пиразинамида (PZA), этамбутола (EMB) и стрептомицина (SM). Однако эта терапия первой линии часто не помогает вылечить туберкулез по нескольким причинам. Рецидив и распространение болезни способствуют появлению устойчивых к лекарствам бактерий. Возникновение туберкулеза с множественной лекарственной устойчивостью (МЛУ-ТБ), т. Е. Устойчивого как минимум к изониазиду (INH) и рифампицину (RIF), вызывает серьезную озабоченность, поскольку требует использования препаратов второго ряда, которые трудно приобрести и намного токсичнее и дороже, чем FLD [1].Таким образом, выявление и лечение лекарственно-чувствительного или одного лекарственно-устойчивого ТБ является важной стратегией предотвращения возникновения МЛУ-ТБ [2]. M. tuberculosis штаммов ТБ с широкой лекарственной устойчивостью (ШЛУ-ТБ), устойчивых к изониазиду или рифампицину (например, к туберкулезу с множественной лекарственной устойчивостью), любому фторхинолону и по крайней мере к одному из трех инъекционных противотуберкулезных препаратов второго ряда — т.е. ., Капреомицин, канамицин и амикацин [3].
Препараты первого и второго ряда, минимальные ингибирующие концентрации (МПК) и механизмы лекарственной устойчивости представлены в таблице 1 [4].Противотуберкулезные препараты в основном делятся на две части.
Противотуберкулезные препараты первого ряда — изониазид (INH), рифампицин (RIF), этамбутол (EMB), пиразинамид (PZA) и стрептомицин (SM).
Противотуберкулезные препараты второго ряда — подразделяются на две части:
Фторхинолоны: офлоксацин (OFX), левофлоксацин (LEV), моксифлоксацин (MOX) и ципрофлоксацин (CIP).
Инъекционные противотуберкулезные препараты — канамицин (KAN), амикацин (AMK) и капреомицин (CAP).
Менее эффективные противотуберкулезные препараты второго ряда — этионамид (ETH) / протионамид (PTH), циклосерин (CS) / теризидон, P-аминосалициловая кислота (PAS).
| Лекарственное средство | МИК (мг / л) | Ген | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| katG | каталаза / пероксидаза | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| inhA | еноилредуктаза | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ahperC 426 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ahperC42 | rpoB | β-субъединица РНК-полимеразы | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Пиразинимид | 16–50 (LJ) | pncA | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| rpsL | Рибосомный белок S12 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| rrs | 16S rRNA | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| gidB | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| gidB 7 -transferos6 5 (7H9 / 7h20) | embB | арабинозилтрансфераза | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Фторхинолоны | 0.5–2.0 (7H9 / 7h20) | gyrA / gyrB | ДНК-гираза | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Канамицин | 2–4 (7H9 / 7h20) | rrs | аминогликозидацетилтрансфераза | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Амикацин | 2–4 (7H9 / 7h20) | rrs | 16S rRNA | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
RRNA | 9404 9404 | 9402 | 9404 | 9402 9402 | 9402 9402 | 9402 9402 9402 16S рРНК | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| tylA | рРНК метилтрансфераза | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Этионамид | 2.5–10 (7h21) | inhA | еноилредуктаза | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| p -аминосалициловая кислота | 0,5 (LJ) | tyA | thyA | 3 synthaseymidylate Препараты первого и второго ряда, МПК и механизмы лекарственной устойчивости2. Противотуберкулезные препараты первого ряда2.1. ИзониазидИзониазид (INH) — одно из наиболее эффективных и специфических противотуберкулезных препаратов, которое стало ключевым в лечении с момента его появления в 1952 году [5]. M. tuberculosis очень чувствителен к INH (MIC 0,02–0,2 мкг / мл). INH активен только против растущих туберкулезных бацилл и не активен против нереплицирующихся бацилл или в анаэробных условиях. INH проникает в микобактериальную клетку путем пассивной диффузии [6]. Наиболее значительными побочными реакциями, связанными с приемом изониазида, являются гепатотоксичность и нейротоксичность. Устойчивость к изониазиду — сложный процесс. Мутации в нескольких генах, включая katG , ahpC и inhA , все были связаны с устойчивостью к изониазиду.INH — пролекарство, активируемое микобактериальным ферментом KatG [7]. Резистентные к INH клинические изоляты M. tuberculosis часто теряют каталазу и фермент пероксидазу, кодируемый kat G [8], особенно в штаммах с высокой устойчивостью (MIC> 5 мкг / мл) [9]. Штаммы с низким уровнем устойчивости (МИК <1 мкг / мл) часто все еще обладают активностью каталазы [9]. Хотя мутации в katG , как было показано, ответственны за устойчивость к INH [10], неясно, играет ли регуляция экспрессии katG роль в устойчивости к INH.Ген katG кодирует бифункциональную каталазу-пероксидазу, которая превращает INH в его активную форму [7]. Активированный INH подавляет синтез незаменимых миколиновых кислот путем инактивации NADH-зависимой еноилацильной протеин-редуктазы, кодируемой inhA [11]. Исследование Hazbo´n et al. [12] проанализировали 240 аллелей и обнаружили, что мутации в katG , inhA и ahpC были наиболее сильно связаны с устойчивостью к изониазиду. Снижение или полная потеря активности каталазы / пероксидазы в результате мутации katG являются наиболее частыми генетическими изменениями, связанными с устойчивостью к изониазиду [7].Ser315Thr является наиболее распространенной мутацией katG в клинических изолятах, но существует множество мутаций, которые приводят к инактивации каталазы-пероксидазы с МИК в диапазоне от 0,2 до 256 мг / л. Мутации в inh A или его промоторной области обычно связаны с низким уровнем устойчивости (MIC = 0,2–1 мкг / мл) и встречаются реже, чем мутации kat G [10, 12]. INH-устойчивый M. tuberculosis , несущий inh A мутации, может иметь дополнительные мутации в kat G, обеспечивая более высокие уровни устойчивости к INH [13].Наиболее распространенная мутация inhA встречается в его промоторной области (-15C → T), и было обнаружено, что она чаще связана с монорезистентными штаммами [14]. В M. tuberculosis , ahpC кодирует редуктазу алкилгидропероксидазы, которая участвует в устойчивости к реактивному кислороду и промежуточным соединениям реактивного азота. Первоначально было предложено использовать мутации в промоторе ahpC в качестве суррогатных маркеров для выявления устойчивости к изониазиду [15].Однако в нескольких других исследованиях было обнаружено, что увеличение экспрессии ahpC , по-видимому, является скорее компенсаторной мутацией для потери активности каталазы / пероксидазы, а не основой устойчивости к изониазиду [4, 16]. 2.2. РифампицинРифампицин (RIF) был представлен в 1972 году в качестве противотуберкулезного препарата и обладает отличной стерилизующей активностью. Рифампицин действует путем связывания с β-субъединицей РНК-полимеразы ( rpoB ) [17], фермента, ответственного за транскрипцию и экспрессию микобактериальных генов, что приводит к ингибированию активности транскрипции бактерий и тем самым уничтожает организм.Важной характеристикой рифампицина является то, что он активен в отношении активно растущих и медленно метаболизирующихся (нерастущих) бацилл [18]. РИФ вызывает относительно мало побочных реакций. Это может вызвать расстройство желудочно-кишечного тракта. Гепатотоксичность возникает реже, чем при приеме изониазида. МИК рифампицина колеблется от 0,05 до 1 мкг / мл на твердой или жидкой среде, но МПК выше в яичной среде (МПК = 2,5–10 мкг / мл). Штаммы с МПК <1 мкг / мл в жидкой или агаровой среде или МПК <40 мкг / мл в среде Левенштейна-Йенсена (LJ) считаются чувствительными к RIF.Подавляющее большинство клинических изолятов M. tuberculosis , устойчивых к рифампицину, обнаруживают мутации в гене rpoB , который кодирует β-субъединицу РНК-полимеразы. Это приводит к конформационным изменениям, которые определяют низкое сродство к лекарству и, как следствие, развитие устойчивости [19]. Мутации в «горячей точке» из 81 п.н. rpoB были обнаружены примерно в 96% изолятов M. tuberculosis , устойчивых к рифампицину. Эта область, охватывающая кодоны 507–533 (нумерация в соответствии с последовательностью Escherichia coli rpoB ), также известна как область, определяющая устойчивость к рифампицину (RRDR) [17].Мутации в кодонах 531, 526 и 516 (Ser531Leu, His526Tyr и Asp516Val) являются наиболее часто встречающимися мутациями в большинстве исследований [20, 21]. В некоторых исследованиях также сообщалось о мутациях за пределами горячей области rpoB в устойчивых к рифампицину изолятов M. tuberculosis [22]. 2.3. ПиразинамидПиразинамид (PZA) — важный противотуберкулезный (противотуберкулезный) препарат первой линии, который используется в краткосрочной химиотерапии и является одним из краеугольных препаратов при лечении МЛУ-ТБ [23].Одной из ключевых характеристик пиразинамида является его способность подавлять полуактивные бациллы, обитающие в кислой среде [23]. Пиразинамид является структурным аналогом никотинамида и является пролекарством, которое необходимо преобразовать в его активную форму, пиразиновую кислоту, с помощью фермента пиразинамидаза / никотинамидаза (PZase) [24]. PZA активен только против M. tuberculosis при кислом pH (например, 5,5) [25]. Даже при кислом pH (5,5) активность PZA довольно низка, с МИК в диапазоне 6,25–50 мкг / мл [26].При приеме PZA могут возникать реакции гиперчувствительности и желудочно-кишечные расстройства. PZase кодируется в M. tuberculosis геном pncA [27]. Мутации в гене pncA могут вызывать снижение активности PZase, что может быть основным механизмом устойчивости к PZA у MTB [28, 29]. Мутации гена pncA в PZA-устойчивых изолятах MTB хорошо охарактеризованы, однако корреляция варьируется в зависимости от географических регионов, включая миссенс-мутации, одну или несколько вставок или делеций оснований и полную делецию [28–32].Несмотря на очень разнообразное и разрозненное распределение мутаций pnc A, существует некоторая степень кластеризации мутаций в различных областях гена pncA , таких как аминокислотные остатки 3–17, 61–85 и 132–142. сообщил [33, 34]. Очень разнообразный профиль мутаций в гене pncA , наблюдаемый в штаммах, устойчивых к PZA, является уникальным среди генов устойчивости к лекарствам в M. tuberculosis [28]. Хотя причина такого разнообразия до сих пор неясна, считается, что это может быть связано с адаптивным мутагенезом или с дефицитом механизмов репарации ошибочного спаривания ДНК [23].Большинство PZA-устойчивых штаммов M. tuberculosis (72–97%) имеют мутации в pnc A; [28, 29, 34, 35] однако; некоторые устойчивые штаммы не имеют мутаций pnc A. 2.4. ЭтамбутолЭтамбутол (EMB) [декстро-2,2 ‘- (этилендиимино) ди-1-бутанол], который является важным препаратом первой линии при лечении туберкулеза, играет важную роль в химиотерапии лекарственно-устойчивого туберкулеза [ 36]. EMB также является важным антимикобактериальным препаратом, поскольку он усиливает действие других сопутствующих препаратов, включая аминогликозиды, рифамицины и хинолоны.Наиболее частыми побочными эффектами, наблюдаемыми при применении этамбутола, являются головокружение, помутнение зрения, дальтонизм, тошнота, рвота, боль в животе, потеря аппетита, головная боль, сыпь, зуд, одышка, отек лица, губ или глаз, онемение или покалывание в пальцы рук или ног. Пациентам, принимающим этамбутол, следует проверять остроту зрения и цветовое зрение не реже одного раза в месяц. МИК EMB для M. tuberculosis находится в диапазоне 0,5–2 мкг / мл. EMB — бактериостатический агент, который активен в отношении растущих бацилл и не действует на нереплицирующиеся бациллы.EMB нарушает биосинтез арабиногалактана клеточной стенки [37]. Он ингибирует полимеризацию арабинана в клеточной стенке арабиногалактана и липоарабиноманнана и индуцирует накопление D-арабинофуранозил-P-декапренола, промежуточного продукта в биосинтезе арабинана [38, 39]. Арабинозилтрансфераза, кодируемая с помощью embB , фермента, участвующего в синтезе арабиногалактана, была предложена в качестве мишени для EMB в M. tuberculosis [40] и M.avium [41]. В M. tuberculosis , embB организован в оперон с embC и embA в порядке embCAB . embC, embB и embA имеют более 65% аминокислотной идентичности друг с другом и, как предполагается, кодируют трансмембранные белки [40]. Мутации в опероне embCAB , в частности, embB , и иногда embC , ответственны за устойчивость к EMB [40]. Точечные мутации гена embABC обычно встречаются в кодоне embB 306 [40, 42, 43], а мутации в кодоне embB306 были предложены в качестве маркера устойчивости к EMB в диагностических тестах [44].Однако точечные мутации в локусе embB306 встречаются только в 50–60% всех клинических изолятов, устойчивых к EMB [42, 45-47], а мутации embB306 также могут возникать в клинических изолятах, чувствительных к EMB [46, 47 ]. В этом кодоне было обнаружено пять различных мутаций (ATG → GTG / CTG / ATA, ATC и ATT), что привело к трем различным аминокислотным сдвигам (Met → Val, Leu или Ile) [43]. Хотя связь между мутацией embB306 и устойчивостью к этамбутолу или широкой лекарственной устойчивостью наблюдалась в нескольких исследованиях групп с клиническими или лабораторными изолятами [48, 49], точная роль мутации embB306 играет в развитии устойчивости к этамбутолу. и множественная лекарственная устойчивость у M.tuberculosis полностью не изучен. Около 35% штаммов, устойчивых к EMB (MIC <10 мкг / мл), не имеют мутаций embB [39, 45], что позволяет предположить, что могут быть другие механизмы устойчивости к EMB. Необходимы дальнейшие исследования для выявления потенциальных новых механизмов устойчивости к EMB. 2,5. СтрептомицинСтрептомицин (SM), аминоциклитолгликозидный антибиотик, был первым лекарством, которое было использовано для лечения туберкулеза в 1948 году [50]. SM убивает активно растущие туберкулезные палочки с МИК 2–4 мкг / мл, но неактивен против нерастущих или внутриклеточных бацилл [23].Препарат связывается с 16S рРНК, мешает проверке трансляции и тем самым подавляет синтез белка [51, 52]. Ототоксичность и нефотоксичность связаны с введением SM. Вестибулярная дисфункция встречается чаще, чем слуховые нарушения. Почечная токсичность встречается реже, чем при приеме канамицина или капреомицина. У пациентов, получающих СМ, следует контролировать слух и функцию почек. Мутации, связанные с устойчивостью к стрептомицину, были идентифицированы в генах, кодирующих 16S рРНК ( rrs ) [53] и рибосомный белок S12 ( rpsL ) [54-57].Рибосомный белок S12 стабилизирует высококонсервативную структуру псевдоузла, образованную 16S рРНК [58]. Аминокислотные замены в RpsL влияют на структуру более высокого порядка 16S рРНК [51] и придают устойчивость к стрептомицину. Изменения в структуре 16S рРНК нарушают взаимодействия между 16S рРНК и стрептомицином, процесс, который приводит к устойчивости [59]. Мутации в rps L и rrs являются основным механизмом устойчивости к SM [54, 56, 57], составляя соответственно около 50 и 20% устойчивых к SM штаммов [54, 56, 57].Наиболее частая мутация в rps L — это замена в кодоне 43 лизина на аргинин [54, 56, 57], вызывающая высокий уровень устойчивости к SM. Мутация в кодоне 88 также обычна [54, 56, 57]. Мутации гена rrs происходят в петлях 16S рРНК и группируются в двух областях вокруг нуклеотидов 530 и 915 [39, 54, 56, 57]. Однако около 20–30% устойчивых к SM штаммов с низким уровнем устойчивости (MIC <32 мкг / мл) не имеют мутаций в rps L или rrs [60], что указывает на другой механизм (ы). сопротивления.Было обнаружено, что мутация в gid B, кодирующая консервативную 7-метилгуанозин (m (7) G) метилтрансферазу, специфичную для 16S рРНК, вызывает низкий уровень устойчивости к SM у 33% устойчивых изолятов M. tuberculosis [61 ]. Последующее исследование показало, что хотя изменение Leu16Arg является полиморфизмом, не участвующим в устойчивости к SM, другие мутации в gid B, по-видимому, участвуют в низком уровне устойчивости к SM [62]. Кроме того, некоторый низкий уровень резистентности к SM, по-видимому, вызван повышенным оттоком, поскольку ингибиторы отводящего насоса вызывают повышенную чувствительность к SM, хотя точный механизм еще предстоит идентифицировать [62]. 3. Противотуберкулезные препараты второго ряда3.1. ФторхинолоныФторхинолоны (FQ) обладают антимикробным действием широкого спектра и поэтому широко используются для лечения бактериальных инфекций дыхательных путей, желудочно-кишечного тракта и мочевыводящих путей, а также заболеваний, передающихся половым путем, и хронического остеомиелита [63]. В отличие от многих других антибиотиков, используемых для лечения бактериальных инфекций, FQ обладают превосходной активностью in vitro и in vivo против M.tuberculosis [64, 65]. FQ включают ципрофлоксацин, офлоксацин, левофлоксацин и моксифлоксацин. Итак, в настоящее время FQ используются как препараты второго ряда при лечении туберкулеза. Побочные эффекты относительно нечасты (0,5–10% пациентов) и включают желудочно-кишечную непереносимость, сыпь, головокружение и головную боль. Большинство исследований побочных эффектов фторхинолонов было основано на относительно кратковременном применении при бактериальных инфекциях, но теперь испытания показали относительную безопасность и переносимость фторхинолонов, вводимых в течение нескольких месяцев во время лечения туберкулеза у взрослых. Клеточной мишенью для FQ в M. tuberculosis является ДНК-гираза, топоизомераза типа II, состоящая из двух А и двух субъединиц В, кодируемых генами gyrA и gyrB соответственно [66]. Мутации в небольшой области gyrA , называемой областью, определяющей устойчивость к хинолонам (QRDR), и, реже, в gyrB , являются первичным механизмом устойчивости к FQ у M. tuberculosis [66, 67]. Было высказано предположение, что анализ только QRDR с помощью генотипических тестов достаточен для быстрой идентификации подавляющего большинства FQ-устойчивых M.tuberculosis , поскольку дополнительное нацеливание на gyrB не привело к значительному повышению чувствительности [67, 68]. Мутации в пределах QRDR gyr A были идентифицированы в клинических и лабораторно отобранных изолятах M. tuberculosis , в основном сгруппированных по кодонам 90, 91 и 94 [69-73], причем относительно часто встречается Asp94 [71 , 74]. Кодон 95 (Ser95Thr) содержит природный полиморфизм, не связанный с устойчивостью к фторхинолонам, поскольку он встречается как у чувствительных к фторхинолонам, так и у устойчивых к фторхинолонам штаммов [75].Менее распространен кодон 88 [76]. Для клинических изолятов мутации gyr B встречаются гораздо реже [72, 73]. Обычно две мутации в gyr A или сопутствующие мутации в gyr A плюс gyr B необходимы для развития более высоких уровней устойчивости [69, 77]. 3.2. Аминогликозиды (канамицин, амикацин и капреомицин)Аминогликозиды амикацин (AMK) / канамицин (KAN) и циклический полипептид капреомицин (CAP) являются важными инъекционными препаратами в лечении туберкулеза с множественной лекарственной устойчивостью.Хотя они принадлежат к двум разным семействам антибиотиков, все они проявляют свою активность на уровне трансляции белков. Эти препараты вызывают почечную токсичность. Рекомендуется регулярный контроль слуха и функции почек. АМК и КАН — аминогликозиды, между которыми наблюдается высокий уровень перекрестной резистентности [78-80]. Циклический полипептид CAP структурно не связан с аминогликозидами и, таким образом, является потенциальным кандидатом на замену AMK или KAN, если есть подозрение на устойчивость к любому из них [81, 82].Было продемонстрировано, что риск неэффективности лечения и смертности увеличиваются, когда возникает устойчивость к ВП среди больных МЛУ-ТБ [83]. Однако перекрестная резистентность M. tuberculosis между AMK / KAN и CAP наблюдалась как у клинических изолятов, так и у мутантов, полученных в лаборатории [79, 80, 84, 85]. AMK / KAN и CAP в первую очередь влияют на синтез белка в M. tuberculosis , и устойчивость к этим препаратам связана с изменениями в 16S рРНК ( rrs ) [78, 80, 81, 85, 86].Мутация rrs A1401G вызывает высокий уровень AMK / KAN и низкий уровень устойчивости к CAP. C1402T связан с сопротивлением CAP и низким уровнем сопротивления KAN. G1484T связан с высоким уровнем устойчивости к AMK / KAN и CAP [79, 80, 84, 86]. Низкий уровень устойчивости к канамицину коррелировал с мутациями в промоторной области гена eis , кодирующего аминогликозидацетилтрансферазу, белок повышенной внутриклеточной выживаемости Eis [87]. Устойчивость к циклическому пептиду капреомицину также была связана с мутациями в tlyA [86].Ген tlyA кодирует предполагаемую 2′-O-метилтрансферазу (TlyA), которая, как предполагается, метилирует нуклеотид C1402 в спирали 44 16S рРНК и нуклеотид C2158 в спирали 69 23S рРНК в M. tuberculosis [81, 88 ]. Капреомицин связывается с рибосомой 70S и ингибирует транслокацию мРНК-тРНК [89]. Считается, что метилирование TlyA усиливает антимикробную активность капреомицина [81] и что нарушение tlyA приводит к устойчивости к капреомицину, поскольку неметилированные рибосомы нечувствительны к лекарству [81, 86, 88].Выявленный механизм устойчивости к капреомицину на основе отобранных in vitro мутантов показал, что мутации tlyA были обычными [80, 86], тогда как нечастыми в клинических изолятах M. tuberculosis [79, 80]. 3.3. Этионамид / протионамидЭтионамид (ETH, 2-этилизоникотинамид) представляет собой производное изоникотиновой кислоты и используется в качестве противотуберкулезного средства с 1956 года. МИК ETH для M. tuberculosis составляет 0,5–2 мкг / мл в жидкой среде. , 2.5–10 мкг / мл в агаре 7h21 и 5–20 мкг / мл в среде LJ. Этионамид и аналогичный протионамид лекарственного средства (ПТГ, 2-этил-4-пиридинкарботиоамид) действуют как пролекарства, как изониазид. Который активируется EtaA / EthA (моно-оксигеназой) [90, 91] и ингибирует ту же мишень, что и INH, InhA пути синтеза миколиновой кислоты [92]. Попав в бактериальную клетку, этионамид претерпевает несколько изменений. Его сульфогруппа окисляется флавинмонооксигеназой, а затем лекарство превращается в 2-этил-4-аминопиридин.Промежуточные продукты, образовавшиеся перед 2-этил-4-аминопиридином, кажутся токсичными для микобактерий, но их структура неизвестна (могут быть очень нестабильными соединениями). Мутанты, устойчивые к этионамиду, обладают перекрестной устойчивостью к протионамиду. ETH часто вызывает побочные эффекты со стороны желудочно-кишечного тракта, такие как боль в животе, тошнота, рвота и анорексия. Он может вызвать гипотиреоз, особенно если он используется с аминосалициклической кислотой пара . 3.4. p- Аминосалициловая кислотаp- Аминосалициловая кислота (ПАСК) была одним из первых антибиотиков, проявивших противотуберкулезную активность, и использовалась для лечения ТБ в комбинации с изониазидом и стрептомицином [93].Позже, с открытием других более сильных препаратов, включая рифампицин, его использование в схемах первого ряда было прекращено. ПАСК по-прежнему полезен как часть схемы лечения ШЛУ-ТБ, хотя его польза ограничена и он чрезвычайно токсичен. Тимидилатсинтаза А, кодируемая thyA , ферментом, участвующим в биосинтезе тимина, была недавно предложена в качестве мишени для PAS в M. bovis BCG [94]. Наиболее частой мутацией в thyA была Thr202Ala, хотя несколько чувствительных изолятов также показали ту же мутацию [95].Однако механизм его действия так и не был выяснен. Наиболее частыми побочными реакциями, связанными с ПАВ, являются желудочно-кишечные расстройства. 3.5. ЦиклосеринЦиклосерин (CS) — это антибиотик, который используется для лечения туберкулеза. Точный механизм действия циклосерина неизвестен, но считается, что он предотвращает выработку бактериями туберкулеза веществ, называемых пептидогликанами, которые необходимы для формирования клеточной стенки бактерий. Это приводит к ослаблению клеточной стенки бактерий, которая затем убивает бактерии.Циклосерин обладает высокой желудочной толерантностью (по сравнению с другими препаратами) и не обладает перекрестной резистентностью к другим соединениям. Но это вызывает неблагоприятные психиатрические эффекты; [96, 97], что является его основным недостатком. Итак, перед назначением циклосерина необходимо пройти обследование у психиатра. Циклосерин — один из краеугольных камней лечения туберкулеза с множественной и множественной лекарственной устойчивостью [96, 97, 98]. Теризидон (комбинация двух молекул циклосерина) может быть менее токсичным [96, 97], хотя исследования этого препарата немногочисленны. 4. ВыводыНесмотря на все успехи, достигнутые в лечении и ведении, туберкулез по-прежнему остается одной из основных проблем общественного здравоохранения, от которых человечество страдает на протяжении тысячелетий. Проблемы, создаваемые инфекцией M. tuberculosis из-за ее взаимодействия с иммунной системой и ее механизмов уклонения, требуют еще многих достижений, чтобы оказать значительное влияние на мировую проблему туберкулеза. Внедрение штаммов МЛУ и ШЛУ M.tuberculosis создает несколько проблем в генетике микобактерий и фтизиатрии. Среди приоритетов ответных мер первостепенное значение имеют быстрое выявление устойчивости к противотуберкулезным препаратам, использование соответствующих схем лечения и разработка новых лекарств. Однако, что касается динамики передачи туберкулеза, а также с точки зрения рациональной разработки новых противотуберкулезных препаратов, чрезвычайно важно расширить наши знания о молекулярной основе лекарственной устойчивости и всей ее сложности.Необходимо прояснить связь между конкретными мутациями и развитием МЛУ-ТБ или связь между лекарственной устойчивостью и приспособленностью. Это позволит лучше оценить динамику передачи устойчивых штаммов и более точно предсказать сценарий будущего заболевания. Адекватный мониторинг лекарственной устойчивости, особенно МЛУ / ШЛУ-ТБ у новых пациентов и его передачи, молекулярная характеристика лекарственно-устойчивых штаммов, а также анализ иммунного статуса и генетической предрасположенности пациентов также необходимы для решения проблемы приспособленности и вирулентности. и трансмиссивность лекарственно-устойчивого M.tuberculosis штамма. Антипсихотики второго поколения и экстрапирамидные побочные эффектыЭкстрапирамидные побочные эффекты, вызванные антипсихотиками, хорошо известны в контексте антипсихотических препаратов первого поколения. Однако введение антипсихотиков второго поколения с атипичным механизмом действия, особенно с более низким сродством к дофаминовым рецепторам, вызвало большие ожидания среди клиницистов в отношении их потенциально более низкой склонности к экстрапирамидному синдрому.В этом обзоре дается краткое изложение недавней литературы, относящейся к антипсихотикам второго поколения и экстрапирамидному синдрому. Многочисленные исследования изучали частоту и тяжесть экстрапирамидного синдрома при применении антипсихотических средств первого и второго поколения. Большинство этих исследований ясно показывают, что экстрапирамидный синдром действительно возникает при приеме препаратов второго поколения, хотя и с меньшей частотой по сравнению с первым поколением. Факторами риска являются выбор конкретного агента второго поколения (клозапин несет самый низкий риск, а рисперидон — самый высокий), высокие дозы, предшествующие экстрапирамидные симптомы в анамнезе и сопутствующие заболевания.Кроме того, в сравнительных исследованиях выбор компаратора первого поколения существенно влияет на результаты. Экстрапирамидный синдром остается клинически важным даже в эпоху антипсихотических средств второго поколения. Частота и тяжесть экстрапирамидного синдрома у этих нейролептиков различаются, но факт в том, что эти препараты не оправдали ожиданий относительно их переносимости. 1. ПредпосылкиАнтипсихотические препараты — краеугольный камень фармакологического лечения шизофрении.Появление первого антипсихотического препарата хлорпромазина в 1952 г. ознаменовало новую эру в психофармакологии [1]. Тем не менее, эти ранние нейролептики, теперь называемые антипсихотиками первого поколения (FGA), такие как хлорпромазин, галоперидол или флуфеназин, хотя и эффективны для облегчения положительных симптомов болезни, имеют некоторые серьезные ограничения. Отсутствие эффективности в отношении негативных симптомов и побочных эффектов, особенно экстрапирамидных симптомов (ЭПС), является серьезным недостатком этих препаратов.Разработка новых антипсихотических средств (рисперидон, оланзапин, кветиапин и др.) С 1990-х годов оправдала большие ожидания. Эти новые нейролептики, теперь называемые антипсихотиками второго поколения (SGA), были смоделированы на основе прототипа препарата клозапина [2]. Клозапин был первым нейролептиком, который оказался эффективным при резистентной к лечению шизофрении [3], но он также был первым антипсихотическим средством, лишенным ЭПС. Однако способность клозапина вызывать агранулоцитоз в качестве серьезного побочного эффекта привела к добровольной отмене препарата производителем с последующим его повторным введением в 1989 г. с последующим строгим регулированием показаний и последующего контроля количества лейкоцитов [4].Эффективность клозапина и его неспособность продуцировать ЭПС были мотивами для разработки аналогичных нейролептиков, но с более безопасным профилем. Антипсихотики второго поколения, такие как оланзапин, рисперидон, кветиапин, а в последнее время зипразидон и арипипразол, вскоре стали основой лечения шизофрении, несмотря на их более высокую стоимость и несогласованность данных, показывающих их более высокую эффективность по сравнению с FGA [5, 6]. Клозапин, как первый SGA, фактически дискредитировал теорию о том, что EPS являются неизбежным дополнением антипсихотической эффективности.Ранее ЭПС рассматривались как важнейший компонент антипсихотического «нейролептического» эффекта. Связь антидофаминергической (D2) активности, антипсихотического эффекта и ЭПС (из-за потери дофамина в экстрапирамидной части центральной нервной системы) была основой допаминовой гипотезы шизофрении [7, 8]. Способность вещества вызывать ЭПС экспериментально считалась доказательством его антипсихотического потенциала. Однако дофаминовая гипотеза шизофрении устарела с введением клозапина и других SGA. Все антипсихотические агенты обладают некоторой степенью антагонистического сродства к дофаминергическим рецепторам D2. Было показано, что нейролептики первого поколения, хотя известно, что они блокируют другие рецепторы, оказывают не только свои антипсихотические, но и экстрапирамидные эффекты, в первую очередь за счет связывания с рецепторами D2 в центральной нервной системе. Нейролептики первого поколения оказывают терапевтический (антипсихотический) эффект при 60–80% занятости D2, в то время как 75–80% занятости рецептора D2 приводит к острой ЭПС [9–11].Следовательно, совпадение между желаемой и неблагоприятной занятостью рецептора D2 в большинстве случаев неизбежно при использовании FGA. С другой стороны, терапевтические эффекты SGA также в некоторой степени связаны с антагонизмом к D2, но больше с блокадой определенных рецепторов серотонина (в основном 5HT2A). Удивительно, но клозапин, как наиболее эффективный антипсихотический препарат, имеет самое низкое сродство к D2 (таблица 1). Также было предположено и показано на животных моделях, что SGA действительно связываются с рецепторами D2 и диссоциируют от них нетипичным образом (Kapur, 2001).Слабое связывание и быстрая диссоциация SGA от рецепторов D2 может быть причиной их более низкой склонности к EPS [12]. Сродство антипсихотических препаратов к рецепторам D2 показано в таблице 1. Хотя антипсихотический эффект FGA коррелирует с аффинностью D2, это не относится к SGA.
Эффективность фармакологического лечения не может быть интерпретирована независимо от профиля его побочных эффектов.Лучшая переносимость SGA считалась одним из их основных преимуществ как класса [7]. Идея лечения шизофрении без возникновения ЭПС была очень привлекательной для специалистов в области психиатрической помощи, а также для пациентов. Однако постклозапиновые SGA не полностью оправдали эти ожидания и непереносимость из-за того, что EPS остается значительной проблемой при лечении шизофрении [7, 13]. Теперь очевидно, что все SGA, кроме клозапина, имеют склонность вызывать определенную степень ЭПС.Результаты недавних клинических испытаний и метаанализов показали, что нет преимущества SGA в отношении переносимости и эффективности по сравнению с FGA [13, 14]. Кроме того, постмаркетинговое наблюдение за SGA выявило другие побочные эффекты, такие как увеличение веса и метаболические побочные эффекты. Однако заметные метаболические побочные эффекты также вызываются FGA, и более высокий кардиометаболический риск SGA по сравнению с FGA не подтвержден [15]. Следовательно, чрезмерно упрощенное разделение классов нейролептиков, в которых FGA ответственны за EPS, а SGA за метаболические побочные эффекты, хотя и укоренилось в клинической практике, на самом деле не подтверждается недавними открытиями [1, 16]. В этом обзоре обобщены недавно опубликованные результаты относительно риска развития ЭПС у пациентов, получавших различные классы антипсихотических препаратов. EPS включают острую дистонию, акатизию, паркинсонизм и позднюю дискинезию (TD). ЭПС являются серьезными, иногда изнуряющими и стигматизирующими побочными эффектами и требуют дополнительной фармакотерапии. EPS развивается в два этапа. Ранние острые ЭПС чаще всего развиваются в начале лечения нейролептиками или при увеличении дозы.Позднее возникновение ЭПС обычно возникает после длительного лечения и проявляется в виде поздней дискинезии (ПД). Моторные проявления включают акатизию (беспокойство и ритм), острую дистонию (устойчивые аномальные позы и мышечные спазмы, особенно головы или шеи) и паркинсонизм (тремор, ригидность скелетных мышц и / или брадикинезию) [13, 17]. TD характеризуется непроизвольными повторяющимися движениями лица, такими как гримаса, высунутый язык, окулогирический криз и сморщивание губ, а также движения туловища и конечностей.Острый ЭПС является одной из основных причин плохой приверженности к лечению антипсихотиками из-за обратимости симптомов, в то время как поздняя ПД оказывает наиболее серьезное влияние на качество жизни пациентов и лиц, осуществляющих уход [18, 19]. ТД может сохраняться после прекращения лечения или даже быть необратимой. По оценкам, примерно у 50% пациентов, получавших высокоактивные FGA (например, галоперидол), в течение первых нескольких дней лечения развивается острый EPS. Распространенность TD несколько менее известна из-за различий в дизайне и методологиях исследований, в которых изучалась эта проблема [13, 20, 21].Сообщалось, что распространенность TD составляет от 0,5% до 70% пациентов, получающих FGA, при средней частоте от 24% до 30% [22, 23]. Острый ЭПС обычно реагирует на снижение дозы антипсихотического средства или требует дополнительного фармакологического лечения. Острая дистония возникает в течение первых нескольких дней после начала лечения антипсихотиками и может быть эффективно предотвращена или купирована антихолинергическими препаратами, такими как бипериден [24–26]. Факторами риска острой дистонии являются молодой возраст и мужской пол, злоупотребление психоактивными веществами и семейный анамнез дистонии [27, 28].Острая дистония часто встречается при АГП, таких как галоперидол [29], и реже — при АПГ. Сообщается, что примерно у 7,2% пациентов, получавших парентеральный рисперидон длительного действия, развиваются острые дистонические реакции [30]. Также были опубликованы сообщения о случаях острой дистонии после начала антипсихотической терапии арипипразолом и зипразидоном [31, 32]. Акатизия очень распространена (примерно половина всех случаев ЭПС), плохо изучена и трудно поддается лечению. В основном это происходит в течение первых трех месяцев лечения.Акатизия не реагирует на антихолинергические препараты, но снижение дозы антипсихотиков, жирорастворимые бета-адреноблокаторы и бензодиазепины доказали свою эффективность [24, 25]. По приблизительным оценкам, примерно у 25% пациентов, получавших FGA, развивается акатизия, но она также характерна для SGA. Некоторые исследователи предполагают, что частота акатизии не различается между FGA и SGA [24]. Ранее предполагалось, что SGA клозапин и кветиапин несут наименьший риск развития акатизии, однако это не было подтверждено в некоторых слепых обзорах [33].Кроме того, исследование Clinical Antipsychotic Trials of Intervention Effectiveness (CATIE) как рандомизированное, частично открытое исследование, в котором эффективность и побочные эффекты нескольких SGA с перфеназином FGA показало, что акатизия остается проблемой для SGA, хотя и с более низкой частотой по сравнению с FGAs [24, 34]. На основании исследования CATIE выяснилось, что, например, рисперидон и перфеназин вызывают акатизию у 7% пациентов. Дальнейший анализ данных исследования CATIE не выявил различий между какими-либо антипсихотиками, протестированными в этом исследовании, в отношении частоты акатизии и других ЭПС у пациентов с хронической шизофренией во время поддерживающего лечения антипсихотиками в течение до 18 месяцев [35].Однако при интерпретации этих результатов следует учитывать хорошо известные ограничения CATIE (выбор перфеназина FGA с промежуточной эффективностью, нерандомизированное распределение пациентов с поздней дискинезией для лечения SGA). Паркинсонизм, вызванный антипсихотическими средствами, возникает в период от нескольких дней до нескольких месяцев после начала лечения. Факторами риска для этого типа паркинсонизма являются возраст (пожилой), пол (женщины), когнитивный дефицит и раннее начало ЭПС [36].Паркинсонизм, вызванный антипсихотиками, считается обратимым заболеванием, хотя его продолжительность может варьироваться. Лечение выбора не установлено, но могут быть полезны снижение дозы и антихолинергические препараты. Однако пожилым пациентам следует избегать приема антихолинергических средств из-за их побочных эффектов, таких как ухудшение когнитивных функций, задержка мочи, сухость во рту и риск обострения глаукомы. Хотя переход на SGA часто рекомендуется в случаях паркинсонизма, частота паркинсонизма, вызванного SGA (например,g., 26% с оланзапином) ниже, чем с FGA (55% с галоперидолом), но не незначительны [37]. Другие данные показывают практически отсутствие преимуществ SGA по сравнению с FGA в отношении паркинсонизма в качестве побочного эффекта, особенно если принять во внимание эффективность и дозу. Было показано, что высокие дозы SGA (таких как оланзапин, рисперидон или кветиапин) вызывали паркинсонизм в высоких дозах с той же скоростью, что и низкоактивные FGA (хлорпромазин), но риск был на 50% выше в группе с высокой активностью FGA [ 38].В исследовании CATIE результаты относительно паркинсонизма также были противоречивыми. В исследование CATIE включены пациенты с предшествующей поздней дискинезией, которые на исходном уровне были исключены из группы перфеназина. Это могло привести к потенциальной предвзятости, означая, что пациенты с предыдущей уязвимостью к EPS были распределены исключительно в отделение SGA. Чтобы избежать этой потенциальной систематической ошибки, в сравнения на паркинсонизм были включены только пациенты без предшествующей TD. Доля пациентов, у которых не было признаков паркинсонизма на исходном уровне, которые соответствовали хотя бы одному из трех критериев паркинсонизма в течение последующего периода наблюдения, не выявила существенных различий между группами лечения.При 12-месячном наблюдении частота паркинсонизма с поправкой на ковариаты составила 37–44% для SGA и 37% для перфеназина [35]. Однако выбор FGA (перфеназина) с промежуточной эффективностью в качестве средства сравнения в умеренных дозах при CATIE, вероятно, может быть причиной отсутствия значимой разницы между FGA и SGA в отношении частоты паркинсонизма. Экономическая полезность новейших антипсихотических препаратов в группе 1 исследования шизофрении (CUtLASS-1) в качестве рандомизированного контролируемого исследования (РКИ), в котором проверялась гипотеза о том, что клиническая и экономическая эффективность SGA превосходит людей, чье антипсихотическое лечение было изменено из-за недостаточного эффективность или побочные эффекты предыдущего лечения.Это исследование также не показало статистически значимых различий между группами лечения с точки зрения паркинсонизма между пациентами с SGA и FGA [39] между пациентами с SGA и FGA. В отношении акатизии результаты были аналогичными. Как и в исследовании CATIE, основным ограничением этого исследования является выбор компаратора FGA. Галоперидол как высокоактивный FGA был редким выбором на исходном уровне, в то время как сульпирид был наиболее распространенным. Сульпирид считается FGA с нетипичными свойствами, и его низкая склонность к EPS хорошо известна [40]. Поздняя дискинезия возникает после нескольких месяцев или лет антипсихотической терапии. Риск развития TD является самым высоким в первые пять лет лечения FGA [24]. Ведущими факторами риска развития TD являются пожилой возраст, некавказская раса, женский пол, наличие диабета в анамнезе, органическое поражение головного мозга и наличие негативных симптомов шизофрении [41]. TD может также возникать спонтанно у пациентов с диагнозом шизофрения со скоростью 0,5% в год [42]. Лечение TD отличается от лечения острого EPS.Антихолинергические препараты не рекомендуются (на самом деле было показано, что эти препараты усиливают ТД). Согласно руководящим принципам, первичным этапом является переключение с возбудителя на SGA с последующим, при необходимости, дополнительным фармакологическим лечением. Эмпирический алгоритм лечения от Margolese et al. предлагает снизить дозу холинолитиков, перейти на SGA и, при необходимости, добавить тетрабеназин. Наконец, следует рассмотреть возможность добавления экспериментальной терапии, включающей донепезил / мелатонин / витамин E / витамин B6 / аминокислоты с разветвленной цепью (BCAA), если предыдущие шаги не принесли облегчения [43].Клозапин считается наиболее безопасным и даже полезным препаратом для лечения ТД из-за его способности улучшать непроизвольные симптомы [41]. Недавнее проспективное когортное исследование заболеваемости TD среди амбулаторных пациентов, получающих антипсихотическую поддерживающую терапию, показало некоторые неутешительные результаты в отношении SGA и заболеваемости TD. В то время как большинство ранее проведенных исследований показали, что риск TD с SGA составляет одну четверть от риска FGA, результаты этого исследования показывают, что риск с SGA более чем вдвое меньше, чем у FGA (за исключением пациентов с клозапином) или более двух ~ трети риска (включая пациентов с клозапином) [44].Обнаружение удивительно высокой частоты TD среди пациентов с клозапином в этом исследовании было связано с определенными смешивающими факторами, такими как искажение по показаниям (назначение клозапина пациентам с TD или с риском TD), и должно интерпретироваться с осторожностью. В исследовании CATIE пациенты с TD были исключены из рандомизации для лечения перфеназином. Статистически значимых различий в частоте новых дебютов TD в группе антипсихотических препаратов не было. Частота варьировала от 13% (кветиапин) до 17% (перфеназин) [13].Поскольку пациенты в группе FGA (перфеназин) не были ранее перенесены TD, исследование CATIE не дает возможности достоверного сравнения между FGA и SGA в отношении TD, но оно предлагает некоторые ценные сведения о факторах предрасположенности к TD, зарегистрированных в качестве исходного уровня. Этими факторами являются пожилой возраст, предыдущее воздействие FGA и холинолитиков, предшествующее более длительное лечение антипсихотиками и острый EPS [13, 24]. Исследование CUtLASS-1 неожиданно показало увеличение заболеваемости TD в группе пациентов с SGA в течение 12-й недели лечения, но это, вероятно, было связано с переключением лечения (отмена препарата, блокирующего D2, и начало SGA с большим антихолинергическим действием. ).Эта разница в частоте ДП уменьшилась к 52-й неделе наблюдения [39]. Недавние исследования склонности FGA и SGA вызывать EPS дали противоречивые результаты [35, 37, 39, 45]. При интерпретации этих исследований крайне важно учитывать методологические вопросы и ограничения, некоторые из которых включают дозы антипсихотических средств, выбор компаратора FGA, продолжительность исследования, критерии включения и исключения, исходные характеристики пациентов и чувствительность критерии для EPS. EPS остаются самой серьезной проблемой среди пациентов, страдающих шизофренией, даже в эпоху новых нейролептиков с меньшим сродством к рецепторам D2. После введения антипсихотических средств второго поколения эти агенты были признаны атипичными на основании их механизма действия. Атипичные нейролептики проявляли меньшее сродство к рецепторам полосатого тела D2, чем типичные, FGA, и различные уровни антагонизма 5-HT2A, антагонизма альфа-1 или холинергического антагонизма. Тем не менее, все SGA все еще в некоторой степени влияют на рецепторы D2, при этом клозапин имеет наименьшее сродство [7, 46] и, следовательно, имеет некоторые незначительные проблемы с EPS. 3. ЗаключениеSGA не полностью оправдали ожидания того, что они будут антипсихотическими препаратами без ЭПС. Несмотря на то, что они рекомендованы действующими руководящими принципами в качестве терапии первой линии при лечении шизофрении [47], превосходство этих препаратов с точки зрения лучшей эффективности и переносимости не ясно. Недавние исследования показали, что SGA существенно не отличаются от FGA с точки зрения эффективности (за исключением клозапина для лечения резистентных пациентов) и в целом имеют более низкую склонность вызывать ЭПС, чем FGA, но с большими вариациями внутри класса [48]. Вероятность возникновения EPS из-за SGA существует и зависит от многих факторов. Характеристики пациента (возраст, пол и сопутствующие состояния), история болезни, предыдущее лечение, выбор конкретного антипсихотика, его дозы, а также продолжительность лечения и адъювантной терапии должны быть приняты во внимание, чтобы минимизировать риск. EPS и обеспечить лучшее качество обслуживания. На данный момент рекомендуется метод проб и ошибок, поскольку терапевтический результат и побочные эффекты трудно предсказать.Будем надеяться, что недавние многообещающие достижения в фармакогеномике и нейробиологии могут предоставить прогностические маркеры антипсихотического ответа и побочных эффектов и привести к индивидуализированной терапии [48]. Конфликт интересовАвторы заявляют об отсутствии конфликта интересов в отношении публикации данной статьи. Авторский вкладВсе авторы прочитали и одобрили окончательный вариант статьи. БлагодарностьРабота поддержана Министерством образования, науки и технологического развития Сербии (грант №175023). Стратегии составления препаратов для улучшения биодоступности плохо абсорбируемых лекарственных средств с особым упором на самоэмульгирующиеся системыПлохо растворимые в воде лекарственные препараты становятся все более распространенными. Было подсчитано, что примерно 60–70% молекул лекарственного средства недостаточно растворимы в водной среде и / или имеют очень низкую проницаемость, чтобы обеспечить их адекватное и воспроизводимое всасывание из желудочно-кишечного тракта (ЖКТ) после перорального приема.Ученые, занимающиеся разработкой рецептур, должны применять различные стратегии для улучшения их усвоения. Было обнаружено, что липидные препараты являются многообещающим подходом к решению проблем. В этой обзорной статье обсуждаются потенциальные преимущества и недостатки различных традиционных методов и новейших подходов, в частности, самоэмульгирующихся систем. Критически рассмотрены различные компоненты самоэмульгирующихся систем и критерии их выбора. Попытки различных ученых превратить жидкие самоэмульгирующиеся системы доставки лекарств (SEDDS) в твердые SEDDS путем адсорбции, распылительной сушки, лиофилизации, грануляции из расплава, экструзии и т. Д. С целью создания различных лекарственных форм, таких как самоэмульгирующиеся капсулы, таблетки, Гранулы с контролируемым высвобождением, шарики, микросферы, наночастицы, суппозитории, имплантаты и так далее также были включены.Составление SEDDS представляет собой потенциальную стратегию доставки новых молекул лекарств с повышенной биодоступностью, в основном проявляющих плохую растворимость в воде. Самоэмульгирующаяся система предлагает различные преимущества по сравнению с другими системами доставки лекарств, имеющими потенциал для решения различных проблем, связанных с лекарствами всех классов биофармацевтической системы классификации (BCS). 1. ВведениеРазличные стратегии были широко исследованы для повышения биодоступности плохо всасываемых лекарственных средств с целью повышения их клинической эффективности при пероральном введении.Подсчитано, что от 40% до 70% всех новых химических соединений, выявленных в программах открытия лекарств, недостаточно растворимы в водных средах [1, 2]. Увеличение доли плохо растворимых кандидатов часто связывают с усовершенствованием технологии синтеза, что позволило создавать очень сложные соединения, а также с изменением стратегии открытия с так называемого фенотипического подхода на подход, основанный на мишенях [3] . Различные физико-химические свойства, которые способствуют плохой растворимости различных лекарств, включают их сложную структуру, размер, высокую молекулярную массу, высокую липофильность, Н-связывание соединения с растворителем, внутримолекулярное Н-связывание, межмолекулярное Н-связывание (кристаллическую упаковку), кристалличность, полиморфность. формы, ионный заряд, pH и форма соли [4]. Правило пяти Липински широко предлагалось в качестве качественной прогностической модели для оценки абсорбции плохо всасываемых соединений. В настройке открытия «правило 5» предсказывает, что плохое поглощение или проницаемость более вероятно, когда имеется более 5 доноров Н-связи, 10 акцепторов Н-связи, молекулярная масса больше 500, а рассчитанный Log P равен больше 5. Правило пяти справедливо только для соединений, которые не являются субстратами для активных транспортеров и механизмов оттока [5].Таким образом, in vivo оценка новых лекарственных препаратов-кандидатов на животных моделях выполняется для оценки абсорбции лекарственного средства. Плохо всасываемые лекарственные средства создают проблему для ученых, разрабатывающих рецептуру, при разработке подходящей лекарственной формы, которая может повысить их биодоступность. В целом, плохо растворимые лекарственные препараты могут быть составлены в трех различных формах, чтобы преодолеть проблему плохой абсорбции: кристаллические твердые препараты, аморфные препараты и липидные препараты [6]. 1.1. Кристаллические твердые составыМодификация физико-химических свойств, таких как образование солей и микронизация кристаллического соединения, для увеличения площади поверхности и, таким образом, растворения может быть одним из подходов к повышению скорости растворения лекарственного средства.Размер частиц около 2–5 9 · 1031 мкм · 9 · 1032 мкм может быть получен путем микронизации с использованием воздушно-струйной мельницы. Технология нанокристаллов позволяет уменьшить размер кристаллических частиц до 100–250 нм с помощью шаровой мельницы [7], технологий плотного газа [8] и так далее. Однако у этих методов есть свои ограничения. Например, образование солей нейтральных соединений невозможно. Уменьшение размера частиц может быть нежелательным в ситуациях, когда очень мелкие порошки испытывают плохую смачиваемость и трудности с обращением [9]. 1.2. Аморфные составыАморфные составы включают «твердые растворы», которые могут быть образованы с использованием различных технологий, включая распылительную сушку и экструзию из расплава [9–11]. Аморфные составы могут включать поверхностно-активные вещества и полимеры, обеспечивающие поверхностную активность во время диспергирования. Другие стратегии составления, которые наиболее широко используются для повышения биодоступности таких лекарств, включают комплексообразование с циклодекстринами [12], составление полимерных конъюгатов [13], наночастиц, твердых липидных наночастиц (SLN) [14], использование усилителей проникновения , и ПАВ [15]. 1.3. Липидные составыВ последние годы большой интерес был сосредоточен на системах носителей на основе липидов. Наиболее популярным подходом является включение активного, плохо растворимого в воде компонента в инертные липидные носители, такие как масла, дисперсии поверхностно-активных веществ [16], твердые дисперсии, твердые липидные наночастицы, эмульсии, микроэмульсии, наноэмульсии, самоэмульгирующиеся составы (SEF), микроэмульсии. / наноэмульгирующие препараты [17] и липосомы [18]. В таблице 1 кратко представлены основные стратегии формулирования, а также основные преимущества и недостатки каждого подхода [6].
2.Липидные составыЛипидные составы для перорального введения лекарственных средств представляют собой разнообразную группу составов, имеющих широкий диапазон свойств. Использование солюбилизирующих составов на основе липидов для улучшения всасывания в желудочно-кишечном тракте (ЖКТ) плохо растворимых в воде гидрофобных лекарственных средств хорошо документировано в литературе. Как правило, они состоят из лекарства, растворенного в смеси вспомогательных веществ (5 классов вспомогательных веществ) с широким спектром физико-химических свойств, начиная от чистых триглицеридных масел, моно- и диглицеридов и значительной части липофильных или гидрофильных поверхностно-активных веществ и сорастворителей.В таблице 2 представлена широкая система классификации различных липидных составов [19].
Основным механизмом действия, с помощью которого липидный состав приводит к улучшенной биодоступности, обычно является предотвращение процесса медленного растворения, который ограничивает биодоступность гидрофобных лекарственных средств из твердых лекарственных форм. Предпочтительно композиция позволяет лекарству оставаться в растворенном состоянии на протяжении всего пути его прохождения через ЖКТ.Абсорбция лекарственного средства может быть увеличена путем приготовления лекарственного средства в виде солюбилизата в коллоидной дисперсии. Эта цель может быть достигнута путем создания препарата в самоэмульгирующейся системе. Среди различных подходов больше внимания привлекла самоэмульгирующаяся система доставки лекарств из-за повышенной пероральной биодоступности, позволяющей снизить дозу, более согласованных временных профилей всасывания лекарства, избирательного нацеливания лекарства (ов) на определенное окно всасывания в ЖКТ и защиты наркотики из агрессивной среды в кишечнике [17]. 2.1. Типы самоэмульгирующихся систем: самоэмульгирующиеся, самоэмульгирующиеся и самонаноэмульгирующиеся системы доставки лекарств (SEDDS, SMEDDS и SNEDDS)SEDDS, SMEDDS и SNEDDS представляют собой физически стабильные изотропные смеси масла, поверхностно-активного вещества, соурфактанта и солюбилизированное лекарственное вещество, которое быстро и самопроизвольно образует тонкодисперсное масло в водных эмульсиях, микроэмульсиях или наноэмульсиях, соответственно, при введении в водные фазы при осторожном перемешивании. Таким образом, самоэмульгирующиеся составы легко диспергируются в желудочно-кишечном тракте, где моторика желудка и тонкого кишечника обеспечивает возбуждение, необходимое для эмульгирования. Потенциальные преимущества самоэмульгирующихся систем включают 100% способность захватывать лекарство, физически стабильный состав (также может быть заполнен капсулами), отсутствие необходимости в стадии растворения, образование капель субмикронного размера, что увеличивает площадь абсорбционной поверхности, увеличение скорости и степень абсорбции, и, следовательно, повышенная биодоступность. SEDDS эффективно доставляет препараты класса II BCS. Они также обладают потенциалом для эффективной доставки BCS класса III, BCS класса IV и гидролитически чувствительных препаратов.Они обеспечивают защиту от деградации желудка. Кроме того, они обеспечивают постоянный временной профиль с уменьшенной дозировкой, частотой дозирования. Их легко производить и масштабировать. Он также направляет распределение лекарства в лимфатическую систему. SEDDS были описаны как системы, которые производят эмульсии с размером капель от 100 до 300 нм, в то время как SMEDDS образуют прозрачные микроэмульсии с размером капель менее 50 нм [20]. Однако SEDDS обычно относится ко всем типам самоэмульгирующихся систем, если не указано иное, в то время как SNEDDS описывает системы, которые образуют наноэмульсии при диспергировании в водной среде [21]. По сравнению с эмульсиями, которые являются чувствительными и метастабильными дисперсными формами, эти самоэмульгирующиеся составы физически стабильны, легко производятся и подходят для пероральной доставки в виде стандартной лекарственной формы в мягких или твердых желатиновых капсулах из-за безводной природы. Таким образом, для липофильных лекарственных соединений, которые демонстрируют абсорбцию с ограниченной скоростью растворения, эти системы могут предлагать улучшение скорости и степени абсорбции и приводить к более воспроизводимым профилям времени крови.Будучи безводными, эти системы также обладают большим потенциалом для приготовления и введения гидролитически чувствительных лекарств. Также обнаружено, что SEDDS увеличивает проницаемость кишечника и минимизирует влияние pH на абсорбцию лекарств [22]. В то время как основной механизм, с помощью которого эти препараты, как считается, улучшают абсорбцию лекарственного средства, заключается в устранении необходимости в преабсорбционной солюбилизации лекарственного средства в желудочно-кишечном тракте (ЖКТ), другие механизмы могут включать защиту от химического и ферментативного распада, локализованного в водной среде организма. желудочно-кишечный тракт и стимулирование лимфатического транспорта лекарств, что препятствует метаболизму первого прохождения через печень [2].На рисунке 1 представлена схематическая диаграмма кишечного транспорта лекарств из составов на основе липидов через портальный и мезентериальный лимфатические пути [23].
Физико-химические характеристики лекарственного вещества, сами липидные наполнители и диспергируемость препарата in vivo будут определять как поглощение лекарственного средства в ЖКТ, так и степень участия воротной вены и мезентериальные лимфатические пути в общем всасывании лекарства. 2.2. Выбор вспомогательных веществ в самоэмульгирующихся составахОсновное внимание при выборе подходящих вспомогательных веществ для любого состава на основе липидов заключается в идентификации вспомогательного вещества или их комбинации, обладающих способностью солюбилизировать всю дозу лекарственного средства в объеме, приемлемом для единичного перорального введения. Было показано, что самоэмульгирование зависит от природы пары масло / поверхностно-активное вещество; концентрация поверхностно-активного вещества и соотношение масло / поверхностно-активное вещество; и температура, при которой происходит самоэмульгирование [33].В подтверждение этих фактов также было продемонстрировано, что только очень специфические комбинации фармацевтических наполнителей могут привести к эффективным самоэмульгирующимся системам. Лекарственное средство также должно быть физически и химически стабильным в составе, а характеристики высвобождения лекарственного средства должны оставаться постоянными в течение срока хранения состава. Последнее требование зависит от физической и химической стабильности наполнителей, которую необходимо тщательно контролировать во время разработки рецептуры.Вспомогательное вещество следует выбирать из списка обычно считающихся безопасными вспомогательных веществ «GRAS», опубликованного USFDA, или из других неактивных ингредиентов, одобренных и опубликованных регулирующими органами. Основные вспомогательные вещества в самоэмульгирующейся системе включают липиды (масла), поверхностно-активное вещество и дополнительное поверхностно-активное вещество. Несколько примеров различных вспомогательных веществ, используемых в различных коммерческих продуктах, приведены в таблице 3.
2.2.1. Липиды / маслаМасло представляет собой один из наиболее важных наполнителей в самоэмульгирующихся составах, поскольку оно может солюбилизировать заметные количества липофильного лекарственного средства, способствовать самоэмульгированию и увеличивать долю липофильного лекарственного средства, транспортируемого через лимфатическую систему кишечника. тем самым увеличивая абсорбцию из желудочно-кишечного тракта в зависимости от молекулярной природы триглицерида [16, 46]. Несмотря на значительный потенциал, который предлагают эти липидные эксципиенты, на фармацевтическом рынке появилось очень мало составов на основе липидов.Это может быть связано с недостаточной информацией об относительно сложном физико-химическом составе липидов и опасениями по поводу химической и физической стабильности лекарственного препарата. В дополнение к этим проблемам, также важно взаимодействие липидной композиции со средой желудочно-кишечного тракта и ее влияние на абсорбцию лекарственного средства [2]. Например, было показано, что перевариваемые липиды являются значительно более эффективными усилителями всасывания плохо растворимых лекарств по сравнению с неперевариваемыми липидами (например,г., жидкий парафин). Длина цепи жирных кислот липида также влияет на абсорбцию лекарственного средства [47]. Масла с триглицеридами с длинной и средней цепью с разной степенью насыщения использовались для создания самоэмульгирующихся составов. Пищевые масла, которые представляют собой логичный и предпочтительный выбор липидных эксципиентов для разработки SEDDS, не часто выбираются из-за их низкой способности растворять большие количества липофильных лекарственных средств. Модифицированные или гидролизованные растительные масла широко используются, поскольку эти эксципиенты образуют хорошие эмульгирующие системы с большим количеством поверхностно-активных веществ, одобренных для перорального введения, и демонстрируют лучшие свойства растворимости лекарств [48].Они обладают лечебными и физиологическими преимуществами, а продукты их разложения напоминают естественные конечные продукты кишечного пищеварения. Новые полусинтетические производные со средней длиной цепи, которые можно определить как амфифильные соединения с поверхностно-активными свойствами, постепенно и эффективно заменяют обычные триглицеридные масла со средней длиной цепи в самоэмульгирующихся системах доставки лекарств [49]. Липиды оказывают свое действие, возможно, посредством нескольких сложных механизмов, которые могут привести к изменению биофармацевтических свойств лекарственного средства, таких как повышенная скорость растворения лекарственного средства и растворимость в кишечной жидкости, защита лекарственного средства от химических и ферментативных деградация в каплях масла и образование липопротеинов, способствующих лимфатическому транспорту высоколипофильных лекарств [48]. Количество липидов, содержащихся в препарате, также влияет на абсорбцию лекарственного средства, прежде всего за счет солюбилизации в ЖКТ и, возможно, за счет активации переваривания липидов ЖКТ, что приводит к увеличению секреции панкреатического сока и желчи [50]. Таким образом, необходимо учитывать влияние любого состава на основе липидов на процессы переваривания липидов, особенно когда несколько единиц дозирования состава на основе липидов вводятся в виде одной дозы, что является обычным для многих лекарств против ВИЧ. 2.2.2. Поверхностно-активные веществаСамоэмульгирующие свойства требуют включения в состав относительно больших количеств поверхностно-активного вещества в дополнение к маслянистому носителю лекарственного средства. Поверхностно-активные вещества могут улучшать сродство между липидами и кишечной мембраной или увеличивать проницаемость кишечной мембраны. Поверхностно-активные вещества увеличивают проницаемость, разделяясь на клеточную мембрану и нарушая структурную организацию липидного бислоя, что приводит к усилению проницаемости [51].Следовательно, большинство лекарств всасывается пассивным трансклеточным путем. Они также усиливают абсорбцию за счет увеличения скорости растворения лекарства. Некоторые соединения, проявляющие свойства поверхностно-активных веществ, могут быть использованы для создания самоэмульгирующихся систем, из которых наиболее широко рекомендуются неионные поверхностно-активные вещества с относительно высокими значениями гидрофильно-липофильного баланса (HLB) [2, 51, 52]. Безопасность — главный определяющий фактор при выборе поверхностно-активного вещества. Эмульгаторы природного происхождения (напр.g., лецитин, среднецепочечные моноглицериды Akoline (MCM) и Peceol) обычно предпочтительны, поскольку они считаются более безопасными, чем синтетические поверхностно-активные вещества. Однако эти вспомогательные вещества обладают ограниченной эффективностью самоэмульгирования [49]. Различные производные растительного масла, такие как Акрозил (производное касторового масла), все еще могут давать оптимальную самоэмульгирующую способность [53]. Неионогенные поверхностно-активные вещества обычно предпочтительнее их ионных аналогов из-за более благоприятных профилей безопасности и большей стабильности эмульсии в более широком диапазоне pH и ионной силы.Кроме того, неионогенные поверхностно-активные вещества могут вызывать обратимые изменения проницаемости слизистой оболочки кишечника [51], дополнительно облегчая абсорбцию совместно вводимого лекарства. Гидрофобные поверхностно-активные вещества могут проникать через мембраны, вызывая изменения их текучести и проницаемости. Обычно одиночные алкильные цепи обладают большей проницаемостью, поэтому объемные поверхностно-активные вещества, такие как полисорбаты и этоксилаты триглицеридов, менее токсичны. Обычно концентрация поверхностно-активного вещества составляет от 30 до 60% от общей композиции для образования стабильных SEDDS [33].Очень важно правильно определить концентрацию поверхностно-активного вещества, так как большое количество поверхностно-активного вещества может вызвать раздражение желудочно-кишечного тракта. Однако чрезвычайно малый размер липидных капель, производимых составами SMEDDS и SNEDDS, способствует быстрому опорожнению желудка и широкой дисперсии по ЖКТ, сводя к минимуму воздействие высоких локальных концентраций поверхностно-активного вещества и, таким образом, снижая потенциал раздражения. Поверхностно-активное вещество, входящее в состав SEDDS, должно иметь относительно высокий уровень ГЛБ и гидрофильность, чтобы обеспечить быстрое и легкое диспергирование в водной жидкости GI в виде очень тонкой эмульсии масло-в-воде, и, следовательно, могут быть достигнуты хорошие самоэмульгирующие свойства [2 ].Использование смесей поверхностно-активных веществ для достижения значения гидрофильно-липофильного баланса (HLB), необходимого для эмульгирования, часто доказывает, что обеспечивает превосходные самоэмульгирующие свойства по сравнению с использованием одного поверхностно-активного вещества, обладающего желаемым HLB [54]. В состав часто добавляют один или несколько сорастворителей, чтобы способствовать растворению высоких концентраций лекарственного средства. Поверхностно-активные вещества имеют амфифильную природу и могут растворять или солюбилизировать относительно большие количества гидрофобных лекарственных соединений.Существует взаимосвязь между размером капель и концентрацией используемого поверхностно-активного вещества. Во многих случаях увеличение концентрации поверхностно-активного вещества может привести к образованию капель с меньшим средним размером капель. Это можно объяснить стабилизацией капель масла в результате локализации молекул поверхностно-активного вещества на границе раздела нефть-вода. С другой стороны, в некоторых случаях средний размер капель может увеличиваться с увеличением концентрации поверхностно-активного вещества [55]. Это явление может быть связано с нарушением межфазной поверхности, вызванным усиленным проникновением воды в капли масла, опосредованным повышенной концентрацией поверхностно-активного вещества и приводящим к выбросу капель масла в водную фазу.Были предприняты попытки оценить токсичность фармацевтических эксципиентов и препаратов SEDDS или SMEDDS in vitro в монослоях клеток Caco-2 [20, 56]. 2.2.3. КосурфактантыПроизводство оптимального самоэмульгирующегося состава требует относительно высоких концентраций (обычно более 30% мас. / Мас.) Поверхностно-активных веществ. Добавление дополнительных поверхностно-активных веществ способствует самоэмульгированию. Присутствие дополнительных поверхностно-активных веществ снижает напряжение изгиба границы раздела и обеспечивает достаточную гибкость межфазной пленки, чтобы принимать различные кривизны, необходимые для образования наноэмульсий в широком диапазоне составов [57].Органические растворители, такие как этанол, пропиленгликоль (PG) и полиэтиленгликоль (PEG), подходят для пероральной доставки, и они позволяют растворять большие количества либо гидрофильного поверхностно-активного вещества, либо лекарственного средства в липидной основе. С другой стороны, спирты и другие летучие сорастворители имеют недостаток, заключающийся в том, что они испаряются в оболочки мягких желатиновых или твердых герметичных желатиновых капсул в обычных самоэмульгирующихся препаратах, что приводит к осаждению лекарственного средства. Таким образом, также были разработаны препараты без спирта [49], но их способность растворять липофильные лекарства может быть ограничена. 3. Механизм самоэмульгированияМеханизм, с помощью которого происходит самоэмульгирование, еще недостаточно изучен. Рейсс предположил, что самоэмульгирование имеет место, когда изменение энтропии, благоприятствующее дисперсии, превышает энергию, необходимую для увеличения площади поверхности дисперсии [58]. Свободная энергия обычного состава эмульсии является прямой функцией энергии, необходимой для создания новой поверхности между двумя фазами (масляной и водной фазами), и может быть описана следующим образом: где — свободная энергия, связанная с процессом (без учета свободной энергии перемешивания), — количество капель, — радиус глобул и — межфазная энергия. Две фазы эмульсии имеют тенденцию разделяться со временем, чтобы уменьшить площадь поверхности раздела и, следовательно, свободную энергию систем. Обычные эмульгирующие агенты стабилизируют эмульсии, полученные в результате водного разбавления, путем образования монослоя вокруг капель эмульсии, снижения межфазной энергии и создания барьера для коалесценции. Напротив, в самоэмульгирующихся составах эмульгирование происходит самопроизвольно, поскольку свободная энергия, необходимая для образования эмульсии, либо мала и положительна, либо отрицательна [17, 49].Эмульгирование, требующее очень небольшого количества подводимой энергии, включает дестабилизацию за счет сжатия локальных межфазных областей. Для эмульгирования необходимо, чтобы межфазная структура не оказывала сопротивления поверхностному сдвигу. На рисунке 2 схематично показан механизм, происходящий при добавлении воды в SEDDS, в упрощенном виде.
Было высказано предположение, что легкость эмульгирования связана с легкостью проникновения воды в различные жидкие кристаллы (ЖК) или гелевые фазы, образующиеся на поверхности капли.Граница раздела между масляной и водной непрерывными фазами образуется при добавлении бинарной смеси (масло / неионогенное поверхностно-активное вещество) к воде. За этим следует солюбилизация воды в масляной фазе в результате проникновения воды через границу раздела. Это будет происходить до тех пор, пока предел солюбилизации не будет достигнут близко к границе раздела фаз. Дальнейшее проникновение воды приведет к образованию дисперсной ЖК-фазы. В конечном итоге все, что находится в непосредственной близости от границы раздела, будет ЖК, фактическое количество которого зависит от концентрации поверхностно-активного вещества в бинарной смеси.Таким образом, после осторожного перемешивания самоэмульгирующейся системы вода будет быстро проникать в водные ядра и приводить к разрушению границы раздела и образованию капель. Вследствие образования границы раздела жидкостей вокруг капель масла самоэмульгирующиеся составы становятся очень устойчивыми к слипанию. Также были проведены детальные исследования для определения участия ЖК фазы в процессе образования эмульсии [31, 33, 59]. Кроме того, анализ размера частиц и низкочастотная диэлектрическая спектроскопия (LFDS) были использованы для изучения самоэмульгирующих свойств серии Imwitor 742 (смесь моно- и диглицеридов каприновой и каприловой кислот) / систем Tween 80 [60].Результаты показали, что может существовать сложная взаимосвязь между образованием ЖК и образованием эмульсии. Более того, присутствие лекарственного соединения может изменить характеристики эмульсии, вероятно, за счет взаимодействия с ЖК-фазой. Тем не менее, корреляция между образованием ЖК и спонтанным эмульгированием до сих пор не установлена. 4. Новые подходы к самоэмульгирующейся системе доставки лекарствСамоэмульгирующиеся системы доставки лекарств предлагают преимущества в решении проблем растворимости и абсорбции лекарств; Следующей проблемой остается доставка лекарства в приемлемой лекарственной форме.Пероральные лекарственные формы являются предпочтительным путем введения лекарств, а липидные составы обеспечивают гибкость для пероральных дозированных форм, поскольку они могут быть приготовлены в виде растворов, полутвердых и твердых форм. Однако обычные самоэмульгирующиеся системы доставки лекарств в основном готовятся в жидкой форме, что может иметь некоторые недостатки, например, низкую стабильность, необратимое осаждение лекарств / вспомогательных веществ, большой объем дозы, сложность в обращении и переносимости, а также мало вариантов выбора. лекарственных форм. Для решения этих проблем были исследованы твердые SEDDS (S-SEDDS) в качестве альтернативных подходов. Такие системы требуют отверждения жидких самоэмульгирующихся систем в порошки для получения различных твердых лекарственных форм (капсулы SE, таблетки SE, гранулы SE, шарики SE и так далее). Жидкие SEDDS могут быть преобразованы в твердую лекарственную форму, не влияя на свойство высвобождения лекарственного средства. Самоэмульгирование происходит в ЖКТ высвобожденным содержимым. Таким образом, S-SEDDS сочетают в себе преимущества SEDDS (т.е.д., улучшенная растворимость и биодоступность) по сравнению с твердыми лекарственными формами (например, высокая стабильность и воспроизводимость, компактная лекарственная форма, простота обращения и переносимость, а также лучшее соблюдение пациентом режима лечения). Зная преимущества твердых лекарственных форм, S-SEDDS в последние годы широко исследовались, поскольку они часто соответствуют более эффективным альтернативам традиционным жидким SEDDS. Примеры включают разработку S-SEDDS дексибупрофена [36], нимодипина [45] и гидрохлоротиазида [28].С точки зрения лекарственных форм, S-SEDDS означают твердые лекарственные формы со свойствами самоэмульгирования. S-SEDDS фокусируются на включении жидких / полутвердых ингредиентов SE в порошки / наночастицы с помощью различных методов отверждения. Также была исследована концепция супер-SNEDDS малорастворимого лекарственного средства Симвастатин. Супер-SNEDDS (с 200% -ной загрузкой лекарственного средства) получали, подвергая предварительные концентраты SNEDDS циклу нагревания и охлаждения. Относительная биодоступность препарата из супер-SEDDDS значительно увеличилась (180 ± 53.3%) по сравнению с обычными SNEDDS. Наблюдалась длительная абсорбция в тонком кишечнике [61]. В одном более раннем исследовании также был разработан сверхнасыщаемый SEDDS с использованием небольшого количества HPMC (гидроксипропилметилцеллюлозы или других полимеров) в составе для предотвращения осаждения лекарственного средства путем создания и поддержания перенасыщенного состояния in vivo . Эта система содержала пониженное количество поверхностно-активного вещества, тем самым сводя к минимуму побочные эффекты со стороны ЖКТ и [62]. Для повышения пероральной биодоступности лекарственных средств с высокой растворимостью и низкой проницаемостью также исследуются двойные эмульсии вода-в-масле-в-воде (w / o / w).Новый состав, самодвойные эмульгирующиеся системы доставки лекарств (SDEDDS) были составлены путем смешивания гидрофильных поверхностно-активных веществ и эмульсий вода-в-масле (w / o). SDEDDS может спонтанно эмульгироваться в двойные эмульсии в / в / в в смешанной водной среде желудочно-кишечного тракта с лекарствами, инкапсулированными во внутренней водной фазе двойных эмульсий [63]. 4.1. Методы отверждения для преобразования жидких SEDDS в твердые SEDDS (S-SEDDS)Твердые SEDDS разрабатываются из жидких / полутвердых SEDDS в основном путем адсорбции на твердых носителях [64], распылительной сушки [45], лиофилизации [65], экструзии расплава [66] и технологии наночастиц.Такие порошки / наночастицы, которые называются наночастицами SE / сухими эмульсиями / твердыми дисперсиями, обычно далее перерабатываются в другие твердые лекарственные формы SE или, альтернативно, заполняются в капсулы (т.е. капсулы SE). Капсулы SE также включают те капсулы, в которые непосредственно заполняются жидкие / полутвердые SEDDS без какого-либо затвердевающего наполнителя. Другие твердые лекарственные формы SE, появившиеся в последние годы, включают гранулы / таблетки SE, микросферы / наночастицы SE и суппозитории / имплантаты SE [67]. 4.1.1. Адсорбция на твердых носителяхЛегкосыпучие порошки могут быть получены из жидких составов SE путем адсорбции на твердых носителях. Процесс адсорбции прост и включает лишь добавление жидкого состава на инертные носители и их перемешивание в смесителе. Затем полученный порошок может быть помещен непосредственно в капсулы или, альтернативно, смешан с подходящими наполнителями перед прессованием в таблетки. SEDDS могут адсорбироваться в высоких концентрациях (до 70% по массе) на подходящих носителях [64].Твердые носители могут быть микропористыми неорганическими веществами, коллоидными неорганическими адсорбентами с большой площадью поверхности, сшитыми полимерами или адсорбентами наночастиц, например диоксидом кремния, силикатами, трисиликатом магния, силикатом алюминия и магния (Neusilin), микропористым силикатом кальция (Florite TM RE). гидроксид магния, тальк, кросповидон, сшитая карбоксиметилцеллюлоза натрия и сшитый полиметилметакрилат. Самоэмульгирующийся порошок был приготовлен путем адсорбции жидкого SEDDS на нейсилине в качестве носителя для улучшения растворимости плохо растворимого гидрохлорида лерканидипина [35].Сшитые полимеры создают благоприятную среду для растворения лекарства. Адсорбенты наночастиц включают пористый диоксид кремния [36], углеродные нанотрубки, углеродные нанороги, древесный уголь и так далее. 4.1.2. Распылительная сушкаВ этой методике жидкий SEDDS добавляется к раствору подходящего твердого носителя при перемешивании для получения эмульсии масло / вода. Затем он распыляется в виде спрея капель в сушильной камере, где летучая фаза (например, вода, содержащаяся в эмульсии) испаряется, образуя сухие частицы при контролируемой температуре и условиях воздушного потока [36, 45].Из таких частиц могут быть дополнительно изготовлены таблетки или капсулы. Распылитель, температура, наиболее подходящий режим воздушного потока и конструкция сушильной камеры выбираются в соответствии с характеристиками сушки продукта и спецификацией порошка. Твердотельные эмульсии описаны Майерсом и Шивли (1993). Шивли использовал сахарозу и минеральное масло для приготовления твердых эмульсий [68]. 4.1.3. Метод лиофилизацииЛиофилизация или сублимационная сушка включает передачу тепла и массы к готовому продукту и от него.Сублимационная сушка эмульсии типа масло в воде может быть альтернативным методом производства сухих эмульсий. Лиофилизация рассматривалась как метод молекулярного смешения, при котором лекарство и носитель совместно растворяются в общем растворителе, замораживаются и сублимируются для получения лиофилизированной молекулярной дисперсии. Потенциальные применения лиофилизации в производстве твердых дисперсий успешно исследованы [65, 69, 70]. Сообщалось, что медленная скорость охлаждения и добавление аморфных криопротекторов имеют лучший стабилизирующий эффект во время лиофилизации эмульсий масло-в-воде [71].Мальтодекстрины также являются полезным образующим матрицу агентом при приготовлении лиофилизированных таблеток [28]. 4.1.4. Гранулирование в расплавеГранулирование в расплаве — это метод, при котором агломерация порошка достигается за счет добавления липида в качестве связующего, который плавится или размягчается при относительно низких температурах. Гранулирование из расплава предлагает несколько преимуществ по сравнению с обычным влажным гранулированием, поскольку не используются добавление жидкости и последующая фаза сушки. Кроме того, это также хорошая альтернатива использованию растворителя.Основными параметрами, контролирующими процесс гранулирования, являются частота вращения крыльчатки, время перемешивания, размер частиц связующего и вязкость связующего. В качестве плавких связующих может применяться широкий спектр твердых и полутвердых липидов. Например, Gelucires, семейство носителей, полученных из смесей моно- / ди- / триглицеридов и сложных эфиров полиэтиленгликоля (PEG) и жирных кислот, способно увеличивать скорость растворения по сравнению с PEG, обычно используемым ранее, вероятно, благодаря его SE собственность. Другие наполнители на основе липидов, оцененные для грануляции из расплава для создания твердых SES, включают лецитин, частичные глицериды или полисорбаты.Во всех случаях используемые липидные вспомогательные вещества должны быть полутвердыми при комнатной температуре [66]. 4.1.5. Экструзия расплава / экструзия СферонизацияЭкструзия расплава — это процесс без использования растворителей, который обеспечивает высокую загрузку лекарственного средства (60%), а также однородность содержимого. Экструзия — это процедура превращения сырья с пластическими свойствами в продукт однородной формы и плотности путем пропускания его через фильеру в условиях контролируемой температуры, потока продукта и давления. Размер апертуры экструдера будет определять приблизительный размер получаемых сфероидов.Процесс экструзии-сферонизации обычно используется в фармацевтической промышленности для изготовления сфероидов (гранул) одинакового размера. Процесс экструзии-сферонизации требует следующих этапов: сухое смешивание активных ингредиентов и наполнителей для получения гомогенного порошка; влажное массирование со связующим; экструзия в жгутовый экструдат; сферонизация экструдата до сфероидов одинакового размера; сушка; просеивание для достижения желаемого гранулометрического состава и покрытия [34, 66]. 4.2.Проблемы, связанные с технологиями отвержденияСуществуют различные проблемы, связанные с технологиями отверждения. Примеры таких проблем включают следующее. (1) Количество затвердевающих вспомогательных веществ может повлиять на высвобождение лекарственного средства. (2) Природа используемых вспомогательных веществ может повлиять на абсорбцию лекарственного средства. (3) Вероятность необратимого разделения фаз при восстановлении. (4) ) Засорение форсунок из-за содержания масла в методе распылительной сушки. (5) Разложение лекарственного средства в процессе затвердевания.(6) Снижение загрузки лекарственного средства. (7) Трудность в обеспечении однородности содержимого. (8) Вероятность использования остаточных растворителей во время гранулирования. 4.3. Подходы к преодолению проблем, связанных с технологиями отверждения(1) Чтобы уменьшить количество затвердевающих наполнителей, необходимых для преобразования SEDDS в твердые лекарственные формы, был разработан гель SEDDS. Коллоидный диоксид кремния (Аэросил 200) был выбран в качестве гелеобразующего агента для систем на масляной основе, который служил двойной цели — уменьшению количества необходимых затвердевающих наполнителей и помощи в замедлении высвобождения лекарства [72].(2) После введения капсул, содержащих обычные жидкие составы SE, образуются капли эмульсии, которые затем диспергируются в желудочно-кишечном тракте, достигая мест абсорбции. Однако, если происходит необратимое фазовое разделение эмульсии, нельзя ожидать улучшения абсорбции лекарственного средства. (A) Для решения этой проблемы в состав SE был добавлен додецилсульфат натрия [73]. (B) С той же целью, Перенасыщаемый SEDDS был разработан с использованием небольшого количества HPMC (или других полимеров) в составе для предотвращения осаждения лекарственного средства путем создания и поддержания перенасыщенного состояния in vivo .Эта система содержит пониженное количество поверхностно-активного вещества, тем самым сводя к минимуму побочные эффекты GI [62]. (3) Самоэмульгирующиеся твердые дисперсии . Они включают диспергирование лекарственного средства в самоэмульгирующихся твердых наполнителях. Эти эксципиенты могут увеличивать абсорбцию плохо растворимых в воде лекарственных средств по сравнению с ранее использовавшимися твердыми дисперсиями ПЭГ, а также могут быть заполнены непосредственно в твердые желатиновые капсулы в расплавленном состоянии, тем самым устраняя прежнее требование измельчения и смешивания перед заполнением.Вспомогательные вещества SE, такие как Gelucire1 44/14, Gelucire150 / 02, Labrasol1, Transcutol1 и токоферилполиэтиленгликоль 1000 сукцинк (TPGS), широко используются в этой области [10, 11, 26, 69]. 5. Лекарственные формы из самоэмульгирующих систем5.1. Самоэмульгирующиеся капсулыЗаполнение капсул — это самая простая и наиболее распространенная технология инкапсулирования жидких, полутвердых или твердых составов SE для перорального введения. Преимущества наполнения капсул заключаются в простоте производства, пригодности для сильнодействующих лекарственных средств с низкими дозами и высокой потенциальной загрузке лекарственного средства (до 50% мас. / Мас.). Для жидких составов он включает в себя двухэтапный процесс: заполнение рецептурой капсул с последующим запечатыванием корпуса и крышки капсулы с помощью бинтов или запечатывания с помощью микроспрей. Помимо жидкого наполнения SEDDS, в капсулы могут быть помещены твердые SEDDS, полученные различными способами, описанными выше, такими как распылительная сушка, сублимационная сушка и так далее. После введения капсул, содержащих обычные жидкие составы SE или твердые составы SE, образуются капли эмульсии / наноэмульсии / микроэмульсии, которые затем диспергируются в желудочно-кишечном тракте, достигая участков абсорбции [19]. 5.2. Самоэмульгирующиеся таблеткиКомбинации липидов и поверхностно-активных веществ представляют большой потенциал для получения таблеток SE, которые широко исследовались. Nazzal et al. разработали самоэмульгирующуюся таблетированную лекарственную форму убихинона [67]. Сначала была приготовлена система самоэмульсии, содержащая убихинон; эту наноэмульсию абсорбировали на гранулированном материале, а затем прессовали с образованием таблеток. Полиэтиленоксид успешно продемонстрировал свою пригодность для матриц с контролируемым высвобождением.Полученные в результате таблетки SE постоянно поддерживали более высокую концентрацию активного ингредиента в плазме крови в течение того же периода времени по сравнению с неэмульгирующей таблеткой. Новейшим достижением в области исследований таблеток SE является таблетка с осмотическим насосом SE, в которой элементарная система осмотической помпы была выбрана в качестве носителя SES. Эта система обладает выдающимися характеристиками, такими как стабильная концентрация в плазме и контролируемая скорость высвобождения лекарства, что обеспечивает биодоступность 156,78% по сравнению с коммерческими таблетками карведилола [74]. 5.3. Самоэмульгирующиеся гранулы с замедленным / контролируемым высвобождениемГранулы представляют собой многокомпонентные лекарственные формы, которые обладают многими преимуществами по сравнению с обычными твердыми лекарственными формами, такими как гибкость в производстве, снижение внутрипредметной и межсубъектной вариабельности плазменных профилей и минимизация раздражения желудочно-кишечного тракта без снижения лекарственного средства. биодоступность [75]. Таким образом, очень интересно объединить преимущества гранул с преимуществами гранул SEDDS by SE. Гранулы SE с контролируемым высвобождением получали путем включения лекарств в SES, которые увеличивали скорость их высвобождения, а затем путем покрытия гранул нерастворимым в воде полимером, который снижал скорость высвобождения лекарственного средства.Пеллеты можно получить путем экструзии / сферонизации. Комбинации покрытия и SES могут контролировать высвобождение лекарства in vitro и обеспечивать диапазон скоростей высвобождения [76]. В некоторых исследованиях твердые самоэмульгирующиеся системы доставки лекарств (твердые SEDDS) были приготовлены посредством процесса влажной грануляции в лабораторном смесителе с большими сдвиговыми усилиями, чтобы улучшить скорость растворения плохо растворимого в воде лекарства. Обычное связующее для жидкой грануляции было заменено на микроэмульсию типа «масло в воде», наполненную лекарственным средством [34, 42]. 5.4. Самоэмульгирующиеся шарикиСамоэмульгирующаяся система может быть приготовлена в виде твердой лекарственной формы с использованием минимального количества затвердевающих наполнителей. Патил и Парадкар исследовали загрузку SES в микроканалы пористых полистирольных шариков (PPB), используя метод испарения растворителя. PPB имеет сложные структуры внутренних пустот, которые обычно образуются путем сополимеризации стирола и дивинилбензола. Он инертен и стабилен в широком диапазоне pH, температуры и влажности. Было обнаружено, что PPB является потенциальным носителем для затвердевания SES с достаточно высокими отношениями SES к PPB, необходимыми для получения твердой формы.Было обнаружено, что размер гранул и структура пор PPB влияют на эффективность загрузки и высвобождение in vitro лекарственного средства из загруженного SES PPB [77]. В другом исследовании были разработаны плавающие альгинатные шарики, содержащие SEDDS тетрагидрокуркумина, для увеличения растворимости лекарства и увеличения времени пребывания в желудке. Было обнаружено, что использование различных пропорций альгината натрия, хлорида кальция и водорастворимого порообразователя (сополимер поливинилового спирта-полиэтиленгликоля) в составах гранул по-разному влияет на плавучесть и скорость высвобождения лекарства in vitro [78]. 5.5. Самоэмульгирующиеся микросферы с замедленным высвобождениемТвердые микросферы с замедленным высвобождением SE были получены с использованием метода диффузии квазиэмульсии в растворителе по технологии сферической кристаллизации. Масло куркумы Zedoary (ZTO) обладает мощным фармакологическим действием. При использовании ZTO в качестве масляной фазы поведение ZTO при высвобождении контролировалось соотношением сукцината ацетата гидроксипропилметилцеллюлозы и Aerosil 200 в составе. Профили «концентрация в плазме — время», полученные после перорального введения таких микросфер кроликам, показали биодоступность 135.6% по отношению к обычным жидким SEDDS [79]. 5.6. Самоэмульгирующиеся наночастицыМетоды наночастиц полезны в производстве наночастиц SE. Введение растворителя — один из таких методов. В этом методе липид, поверхностно-активное вещество и лекарственные средства плавятся вместе и вводятся по каплям в перемешиваемый нерастворитель. Полученные наночастицы SE отфильтровывают и сушат. Этот подход позволил получить наночастицы (около 100 нм) с высокой эффективностью загрузки лекарственного средства 74% [80]. Второй метод — это ультразвуковое распыление эмульсии с испарением. Смесь сополимера полилактид-гликолида (PLGA) и O-карбоксиметил-хитозана (O-CMC) имела SE-эффект без необходимости добавления другого стабилизатора поверхностно-активного вещества. В конце концов, эффективность инкапсуляции 5-FU и плазмиды составила 94,5% и 95,7% соответственно, а активность высвобождения 5-FU из наночастиц была обнаружена в течение трех недель [81]. Trickler et al. разработала новую систему доставки лекарств в виде наночастиц, состоящую из хитозана и глицерилмоноолеата, для доставки паклитаксела.Эти наночастицы хитозана / ГМО, обладающие биоадгезивными свойствами и увеличенной клеточной ассоциацией, были приготовлены с помощью методов испарения нескольких эмульсионных (м / м / м) растворителей. Свойство SE увеличивает растворимость паклитаксела и обеспечивает основу для агрегации хитозана, в то же время вызывая почти 100% эффективность загрузки и захвата паклитаксела. Эти преимущества позволяют использовать более низкие дозы паклитаксела для достижения эффективного терапевтического окна, тем самым сводя к минимуму неблагоприятные побочные эффекты, связанные с химиотерапевтическими средствами, такими как паклитаксел [82]. 5.7. Самоэмульгирующаяся суспензия фосфолипидов (SEPS)Самоэмульгирующаяся суспензия фосфолипидов (SEPS), состоящая из большого количества фосфолипидов, обладает способностью сохранять лекарство в солюбилизированной форме in vivo , что важно для повышения биодоступности. Фосфолипиды представляют собой эндогенный липид с эффективной способностью in vivo к эмульгированию . Они требуют относительно небольшого количества поверхностно-активного вещества / вспомогательного поверхностно-активного вещества и, таким образом, создают меньше проблем со здоровьем [83]. 5.8. Самоэмульгирующиеся суппозиторииНекоторые исследователи доказали, что S-SEDDS может увеличивать не только адсорбцию GI, но также адсорбцию ректально / вагинально [84]. Лекарства, которые не могут легко достичь терапевтических концентраций в плазме при пероральном введении, могут достигать удовлетворительных терапевтических уровней при хронических заболеваниях печени с помощью вагинальных или ректальных суппозиториев SE. Таких запатентованных продуктов тоже немного. Самоэмульгирующиеся суппозитории β -артеметера были составлены и оценены с целью более быстрого начала действия и пролонгированного эффекта при ректальном введении [85]. 5.9. Самоэмульгирующиеся имплантатыИсследования имплантатов SE значительно расширили возможности применения S-SEDDS. Например, 1,3-бис (2-хлорэтил) -1-нитрозомочевина (кармустин) представляет собой химиотерапевтическое средство, используемое для лечения злокачественных опухолей головного мозга. Однако на его эффективность влияет короткий период полураспада. Чтобы повысить его стабильность по сравнению со стабильностью, высвобождаемой из пластин-имплантатов из поли (d, l-лактид-гликолида) (PLGA), в состав SES входили трибутирин, Cremophor RH 40 (гидрированное касторовое масло полиоксил 40) и Лабрафил 1944 ( полигликолизированный глицерид).Затем из самоэмульгированного кармустина были изготовлены пластины с плоской и гладкой поверхностью методом компрессионного формования. В конечном итоге, SES увеличил период полувыведения in vitro кармустина до 130 мин. In vitro высвобождение кармустина из пластин SE PLGA было продлено до 7 дней. Такие пластины имели более высокую противоопухолевую активность in vitro и были менее подвержены гидролизу, чем пластины, лишенные SES [86]. 6. Физико-химические характеристики самоэмульгирующихся составов6.1.% Коэффициент пропусканияОсновным средством оценки самоэмульгирования является визуальная оценка [87]. Чтобы избежать каких-либо субъективных изменений, процент прозрачности полученной микро / наноэмульсии, полученной при разбавлении / восстановлении самоэмульгирующихся составов, измеряется с помощью спектрофотометра в УФ-видимом диапазоне [22]. 6.2. Размер глобул и PDIРазмер глобул эмульсии является решающим фактором в эффективности самоэмульгирования, поскольку он определяет скорость и степень высвобождения лекарственного средства, а также абсорбцию [54, 88, 89].Сообщается, что распределение частиц по размерам является одной из наиболее важных характеристик судьбы in vivo лекарственной эмульсии [37]. Размер глобул восстановленных составов обычно измеряется с помощью Malvern Zeta Sizer, основанного на принципе динамического светорассеяния (DLS). 6.3. Устойчивость к разбавлениюУстойчивость к разбавлению важна для SEDDS / SNEDDS, чтобы гарантировать, что образованная эмульсия / наноэмульсия имеет аналогичные свойства при различных разбавлениях, чтобы достичь однородного профиля высвобождения лекарственного средства и гарантировать, что лекарственное средство не будет осаждаться при более высоких разведениях in vivo , что может значительно замедлить всасывание лекарства из состава [49, 90].SEDDS следует оценивать, разбавляя их разными разбавлениями и исследуя их влияние на свойства образованной эмульсии / наноэмульсии [22]. 6.4. Дзета-потенциалИспользуется для определения заряда капель. Заряд масляных капель SEDDS — это свойство, которое необходимо оценить [46]. Как правило, увеличение электростатических сил отталкивания между каплями наноэмульсии предотвращает слияние капель наноэмульсии. Напротив, уменьшение электростатических сил отталкивания вызывает разделение фаз.Дзета-потенциал восстановленного SEDDS обычно измеряется с помощью Malvern Zeta Sizer Nano на основе электрофореза и электропроводности образованной наноэмульсии. 6.5. Влияние pHpH водной фазы существенно влияет на фазовое поведение самопроизвольно эмульгирующихся систем [33, 84]. В связи с этим следует также исследовать влияние pH водной фазы на полученную наноэмульсию. 6.6. Влияние температурыБыло показано, что самоэмульгирование зависит от температуры, при которой происходит самоэмульгирование [33, 52].Следовательно, влияние температуры на размер глобулы также можно исследовать [22]. 6.7. ВязкостьВязкость жидкого SEDDS используется для оценки его способности заполнять твердые или мягкие желатиновые капсулы. Если система имеет очень низкую вязкость, это может увеличить вероятность утечки из капсулы, а система со слишком высокой вязкостью может создать проблемы с текучестью [91]. 6,8. Тест центрифугированияЭтот тест можно использовать для определения стабильности SEDDS после образования эмульсии.Для этого образцы, разбавленные дистиллированной водой, центрифугируются при заданных оборотах в течение заданного времени и затем исследуются на разделение фаз [92, 93]. 6.9. Тест на солюбилизацию красителяХарактеристика самоэмульгирующейся системы доставки лекарственного средства может быть проведена с использованием солюбилизации красителя [49]. Этот тест используется для определения природы образовавшейся наноэмульсии и ее непрерывной фазы. Для этого водорастворимый краситель разбрызгивается на поверхность приготовленной наноэмульсии.Наблюдая за дисперсией красителя или образованием комков, можно определить природу внутренней и внешней фазы эмульсии. 6.10. Измерение точки помутненияТемпература помутнения является необходимым фактором в SEDDS, состоящем из неионных поверхностно-активных веществ. Когда температура выше точки помутнения, произойдет необратимое разделение фаз, и помутнение препарата будет плохо влиять на абсорбцию лекарственного средства из-за обезвоживания его ингредиентов.Следовательно, температура помутнения для SNEDDS должна быть выше 37 ° C, что позволит избежать разделения фаз в желудочно-кишечном тракте [22, 94, 95]. 6.11. Просвечивающая электронная микроскопияМорфология наноэмульсии, полученной из SEDDS, исследуется с помощью просвечивающей электронной микроскопии. 7. ВыводыРазвитие технологий, разработка и разработка новых химических компонентов, обладающих таргетным потенциалом, приводит к появлению новых молекул лекарственных средств, обладающих терапевтическим эффектом, но неблагоприятных физико-химическими свойствами для их абсорбции в организме.Эффективная доставка таких молекул лекарств, которые в большинстве своем обладают плохой растворимостью в воде, становится самой большой проблемой для ученых, разрабатывающих рецептуры. Липидные составы являются многообещающим подходом для различных категорий молекул лекарств, имеющих сложные лекарственные свойства. Среди различных липидных составов самоэмульгирующиеся системы доставки предлагают дополнительные преимущества, связанные с более высокой стабильностью, пригодностью для гидролитически чувствительных лекарств, высокой способностью загрузки лекарственного средства, возможностью пероральной доставки лекарственного средства (твердый SEDDS), простотой производства и масштабирования, а также и так далее, если они составлены соответствующим образом с правильным подбором вспомогательных веществ. SEDDS в основном исследуются для лекарств BCS класса II, имеющих низкую растворимость в воде для повышения их биодоступности, и показали многообещающий успех. Они могут решить проблемы, связанные с лекарствами всех других классов BCS, как показано в таблице 4. Некоторые исследования уже были выполнены с положительными результатами. Необходимы дополнительные исследования, чтобы лучше разобраться в этой области.
Проблемы, связанные с составом самоэмульгирующейся системы, включают выбор правильных вспомогательных веществ с учетом их растворяющей способности, смешиваемости, химической стабильности , капсула co мобильность, самодисперсность, вопросы регулирования и так далее.Основными вспомогательными веществами, необходимыми для их рецептуры, являются масло, поверхностно-активное вещество и вспомогательное поверхностно-активное вещество для жидких самоэмульгирующихся систем. Критерии выбора комбинации вспомогательных веществ для составов SEDDS должны включать их способность к растворению для необходимой дозы лекарственного средства, способность к самоэмульгированию системы при контакте с желудочной жидкостью (с использованием фазовой диаграммы), их одобрение регулирующими органами. состояние для перорального применения с учетом их разрешенной концентрации и т. д.Материал, используемый для преобразования жидких SEDDS в твердые формы, должен быть инертным, совместимым и не должен влиять на эмульгирующие свойства и профиль высвобождения лекарства. Различные методы, используемые для отверждения, также могут влиять на качество продукта. Различные авторы сообщают о незначительном влиянии на эмульгирующие свойства твердых SEDDS, полученных распылительной сушкой, свободной сушкой (лиофилизацией) или методами адсорбции и экструзии, в отношении соответствующих жидких SEDDS [34, 36, 45, 65].Распылительная сушка может быть предпочтительной из-за их способности быстро производить гладкие, хорошо разделенные сферические частицы. Но он может не подходить для термолабильных лекарств, когда метод лиофилизации может оказаться полезным. Другая проблема, связанная с SEDDS, заключается в том, что их оценка in vivo затруднена на мелких животных из-за небольшого объема желудочного сока по сравнению с людьми, которого может быть недостаточно для надлежащего самоэмульгирования.Можно предвидеть хорошие возможности для роста самоэмульгирующихся систем доставки лекарств в ближайшем будущем, если будут разработаны некоторые средства для оценки их эффективности in vivo . Существует потребность в средствах, которые обладают даже лучшими самоэмульгирующими свойствами при более низких концентрациях, чтобы свести к минимуму любую возможность нежелательных эффектов, таких как раздражение желудка, которые могут быть связаны с этой системой доставки лекарственного средства из-за сравнительно большего количества используемых поверхностно-активного вещества и дополнительного поверхностно-активного вещества. в их постановке.В этой области было проведено множество исследований, однако существует потребность в более предсказательных моделях in vitro для прогнозирования изменений, связанных с лекарством в SEDDS в кишечнике, так что судьба лекарственного средства in vivo может быть под более надежным контролем. Будущие исследования могут также включать исследования биодоступности человека. Список сокращений
Конфликт интересовАвторы заявляют об отсутствии конфликта интересов в отношении публикации этой статьи. Наркомания (расстройство, вызванное употреблением психоактивных веществ) — симптомы и причиныОбзорНаркомания, также называемая расстройством, связанным с употреблением психоактивных веществ, — это заболевание, которое влияет на мозг и поведение человека и приводит к неспособности контролировать использование легальных или незаконных наркотиков или медикаментов.Такие вещества, как алкоголь, марихуана и никотин также считаются наркотиками. Когда у вас есть зависимость, вы можете продолжать употреблять наркотик, несмотря на причиненный им вред. Наркомания может начаться с экспериментального использования рекреационного наркотика в социальных ситуациях, а для некоторых людей употребление наркотиков становится более частым. Для других, особенно при употреблении опиоидов, наркомания начинается с приема прописанных лекарств или приема лекарств от друга или родственника, которому прописали лекарство. Риск зависимости и то, как быстро вы становитесь зависимым, зависит от препарата. Некоторые препараты, такие как опиоидные обезболивающие, имеют более высокий риск и вызывают привыкание быстрее, чем другие. По прошествии времени вам могут потребоваться большие дозы препарата, чтобы получить кайф. Вскоре вам может понадобиться этот препарат, чтобы чувствовать себя хорошо. По мере роста употребления наркотиков вы можете обнаружить, что обходиться без них становится все труднее. Попытки прекратить употребление наркотиков могут вызвать сильную тягу к еде и физическое недомогание (симптомы отмены). Для преодоления наркозависимости и отказа от наркотиков вам может потребоваться помощь врача, семьи, друзей, групп поддержки или организованной программы лечения. Продукты и услугиПоказать больше продуктов от Mayo Clinic СимптомыСимптомы или поведение наркомании включают, среди прочего:
Распознавание нездорового употребления наркотиков у членов семьиИногда бывает трудно отличить нормальное настроение подростка или тревогу от признаков употребления наркотиков.Возможные признаки того, что ваш подросток или другой член семьи употребляет наркотики, включают:
Распознавание признаков употребления наркотиков или интоксикацииПризнаки и симптомы употребления наркотиков или интоксикации могут различаться в зависимости от типа наркотика.Ниже вы найдете несколько примеров. Марихуана, гашиш и другие вещества, содержащие каннабис.Люди употребляют каннабис путем курения, еды или вдыхания испаренной формы наркотика. Каннабис часто предшествует употреблению или употребляется вместе с другими веществами, такими как алкоголь или запрещенные наркотики, и часто является первым наркотиком, который пробуют. Признаки и симптомы недавнего употребления могут включать:
Долгосрочное (хроническое) употребление часто связано с:
K2, Специи и соли для ваннДве группы синтетических наркотиков — синтетические каннабиноиды и замещенные или синтетические катиноны — запрещены в большинстве штатов.Воздействие этих препаратов может быть опасным и непредсказуемым, поскольку отсутствует контроль качества, а некоторые ингредиенты могут быть неизвестны. Синтетические каннабиноиды, также называемые K2 или Spice, распыляют на сушеные травы, а затем коптят, но их можно приготовить как травяной чай. Несмотря на заявления производителя, это химические соединения, а не «натуральные» или безвредные продукты. Эти наркотики могут вызывать «кайф», аналогичный марихуане, и стали популярной, но опасной альтернативой. Признаки и симптомы недавнего употребления могут включать:
Замещенные катиноны, также называемые «солями для ванн», представляют собой изменяющие сознание (психоактивные) вещества, похожие на амфетамины, такие как экстази (МДМА) и кокаин.Пакеты часто маркируются как другие продукты, чтобы избежать обнаружения. Несмотря на название, это не продукты для ванн, такие как английская соль. Замещенные катиноны можно есть, вдыхать, вдыхать или вводить инъекциями, и они вызывают сильное привыкание. Эти препараты могут вызвать тяжелую интоксикацию, которая может привести к опасным последствиям для здоровья или даже смерти. Признаки и симптомы недавнего употребления могут включать:
Барбитураты, бензодиазепины и снотворныеБарбитураты, бензодиазепины и снотворные средства являются депрессантами центральной нервной системы, отпускаемыми по рецепту.Их часто используют и неправильно используют в поисках ощущения расслабления или желания «выключиться» или забыть мысли или чувства, связанные со стрессом.
Признаки и симптомы недавнего употребления могут включать:
Мет, кокаин и другие стимуляторыСтимуляторы включают амфетамины, мет (метамфетамин), кокаин, метилфенидат (Риталин, Концерта и другие) и амфетамин-декстроамфетамин (Аддералл, Аддералл XR, другие).Их часто используют и неправильно используют в поисках «кайфа» или для повышения энергии, для повышения успеваемости на работе или в школе, или для похудания или контроля аппетита. Признаки и симптомы недавнего употребления могут включать:
Клубные наркотикиКлубные наркотики обычно используются в клубах, на концертах и вечеринках.Примеры включают экстази или молли (МДМА), гамма-гидроксимасляную кислоту (ГОМК), флунитразепам (рогипнол — торговая марка, используемая за пределами США, также называемая рутином) и кетамин. Эти препараты не относятся к одной и той же категории, но они имеют схожие эффекты и опасности, включая долгосрочные вредные эффекты. Поскольку GHB и флунитразепам могут вызывать седативный эффект, расслабление мышц, спутанность сознания и потерю памяти, с использованием этих препаратов связана вероятность сексуальных проступков или сексуального насилия. Признаки и симптомы употребления клубных наркотиков могут включать:
ГаллюциногеныИспользование галлюциногенов может вызывать различные признаки и симптомы в зависимости от препарата.Наиболее распространенными галлюциногенами являются диэтиламид лизергиновой кислоты (LSD) и фенциклидин (PCP). Использование LSD может вызвать:
Использование PCP может вызвать:
ИнгалянтыПризнаки и симптомы употребления ингалянтов различаются в зависимости от вещества.Некоторые часто вдыхаемые вещества включают клей, разбавители для краски, корректирующую жидкость, жидкость для фломастеров, бензин, чистящие жидкости и бытовые аэрозоли. Из-за токсичности этих веществ у пользователей может развиться повреждение мозга или внезапная смерть. Признаки и симптомы употребления могут включать:
Опиоидные обезболивающиеОпиоиды — наркотические обезболивающие, производимые из опия или синтетические.Этот класс наркотиков включает, среди прочего, героин, морфин, кодеин, метадон и оксикодон. Иногда называемая «опиоидной эпидемией» зависимость от рецептурных опиоидных обезболивающих достигла угрожающих темпов в Соединенных Штатах. Некоторым людям, которые употребляли опиоиды в течение длительного периода времени, может потребоваться назначенная врачом временная или долгосрочная заместительная терапия во время лечения. Признаки и симптомы употребления наркотиков и зависимости могут включать:
Когда обращаться к врачуЕсли употребление наркотиков вышло из-под контроля или вызывает проблемы, обратитесь за помощью.Чем раньше вы обратитесь за помощью, тем больше у вас шансов на долгосрочное выздоровление. Поговорите со своим лечащим врачом или обратитесь к специалисту по психическому здоровью, например, к врачу, специализирующемуся на наркологической медицине или психиатрии, или к лицензированному консультанту по алкоголю и наркотикам. Запишитесь на прием к врачу, если:
Если вы не готовы обратиться к врачу, можно узнать о лечении по телефону помощи или горячей линии.Эти линии можно найти в Интернете или в телефонной книге. Когда обращаться за неотложной помощьюОбратитесь за неотложной помощью, если вы или кто-то из ваших знакомых принимали наркотики и:
Подготовка вмешательстваЛюди, страдающие зависимостью, обычно отрицают, что их употребление наркотиков является проблемой, и не хотят обращаться за лечением.Вмешательство предоставляет близкому человеку структурированную возможность внести изменения, прежде чем ситуация станет еще хуже, и может побудить кого-то обратиться за помощью или принять ее. Вмешательство должно быть тщательно спланировано и может проводиться семьей и друзьями после консультации с врачом или профессионалом, например, лицензированным консультантом по алкоголю и наркотикам, или под руководством специалиста по вмешательству. В нем участвуют семья и друзья, а иногда и коллеги, священнослужители или другие люди, которым небезразличен человек, борющийся с зависимостью. Во время вмешательства эти люди собираются вместе, чтобы напрямую поговорить с человеком по душам о последствиях зависимости и попросить его или ее принять лечение. ПричиныКак и многие психические расстройства, несколько факторов могут способствовать развитию наркозависимости. Основными факторами являются:
Изменения в мозгеФизическая зависимость, по-видимому, возникает, когда повторное употребление наркотика меняет способ ощущения удовольствия в мозгу. Наркотик вызывает физические изменения в некоторых нервных клетках (нейронах) вашего мозга. Нейроны для общения используют химические вещества, называемые нейротрансмиттерами.Эти изменения могут сохраняться еще долго после прекращения приема препарата. Факторы рискаЛюди любого возраста, пола или экономического положения могут стать зависимыми от наркотиков. Определенные факторы могут повлиять на вероятность и скорость развития зависимости:
ОсложненияУпотребление наркотиков может иметь серьезные и разрушительные краткосрочные и долгосрочные последствия. Прием некоторых лекарств может быть особенно опасным, особенно если вы принимаете высокие дозы или сочетаете их с другими наркотиками или алкоголем. Вот несколько примеров.
Другие осложнения, изменяющие жизньЗависимость от наркотиков может вызвать ряд опасных и разрушительных осложнений, в том числе:
ПрофилактикаЛучший способ предотвратить зависимость от наркотиков — это вообще отказаться от них. Если ваш врач прописывает лекарство, потенциально способное вызвать привыкание, соблюдайте осторожность при приеме этого препарата и следуйте инструкциям врача. Врачи должны назначать эти лекарства в безопасных дозах и количествах и контролировать их использование, чтобы вам не давали слишком большую дозу или слишком долго.Если вы чувствуете, что вам необходимо принять лекарство в дозе, превышающей предписанную, обратитесь к врачу. Профилактика злоупотребления наркотиками у детей и подростковПримите следующие меры, чтобы помочь предотвратить злоупотребление наркотиками у ваших детей и подростков:
Предотвращение рецидиваПосле того, как вы пристрастились к наркотику, вы подвергаетесь высокому риску снова стать зависимым.Если вы все же начнете использовать это лекарство, скорее всего, вы снова потеряете контроль над его использованием — даже если вы прошли курс лечения и какое-то время не принимали его.
26 октября 2017 г. Границы | Повышение эффективности за счет потенциальной пластичности мозга: нейронные ответвления ноотропных препаратов в здоровом развивающемся мозгеВведениеУлучшение когнитивных функций и связанные с этим этические соображения — одна из самых актуальных тем в неврологическом сообществе.Люди искали вещества для улучшения нашей когнитивной функции на протяжении веков, от древних цивилизаций, использовавших галлюциногены в попытке поднять свое сознание, чтобы общаться со своими богами, до появления кофе и новейших лекарств, таких как стимуляторы и активаторы глутамата. Поэтому некоторые могут возразить, что стремление к самосовершенствованию — это человеческая черта, и поэтому когнитивные улучшения — это не что иное, как применение нами новых научных подходов для удовлетворения нашего извечного стремления к самосовершенствованию и развитию.Однако другие утверждают, что искусственное усиление когнитивных способностей несправедливо и дает непревзойденное преимущество для более богатых слоев населения, которые будут иметь более свободный доступ к лекарствам (Butcher, 2003; Cakic, 2009). Проблему улучшения когнитивных функций даже сравнивают с дискуссией о стероидах в спорте (Cakic, 2009). Опубликовано множество всесторонних обзоров и статей по этическим вопросам улучшения когнитивных способностей; однако литературы о безопасности употребления этих наркотиков среди молодежи крайне не хватает, несмотря на значительный рост злоупотребления стимуляторами подростками, о котором сообщалось в недавнем национальном исследовании (Goldberg, 2013).Поэтому для целей этого обзора мы сконцентрируемся на изучении потенциальных нейробиологических ответвлений популярных усилителей когнитивных функций и выделим последние данные о действиях этих препаратов на развитие мозга. Вероятно, что большая часть населения подвергается воздействию препаратов, улучшающих когнитивные функции, и давление с целью их приема может быть особенно сильным среди студентов колледжей и старших классов; эти люди сталкиваются с более строгими критериями приема в колледж и аспирантуру, ограниченным кругом вакансий и постоянно растущим давлением, чтобы работать лучше и лучше, если они надеются на успех (Goodman, 2010; Franke et al., 2011; Lynch et al., 2011). Однако люди в этой популяции могут быть наиболее подвержены риску потенциальных неврологических последствий из-за их все еще развивающегося мозга. Мы выражаем сожаление по поводу того, что мы не можем процитировать много других хороших статей из-за тематической специфичности и редкости существующих исследований; однако интересную информацию о когнитивных усилителях, выходящую за рамки этого обзора, можно найти в этих дополнительных ссылках (Dresler et al., 2013; Pang and Hannan, 2013; Ragan et al., 2013; Мадан, 2014). Метилфенидат и развивающийся мозгОдин из наиболее популярных рассматриваемых препаратов для улучшения когнитивных функций был первоначально разработан для лечения синдрома дефицита внимания с гиперактивностью (СДВГ). Метилфенидат (риталин ©; MPH; рис. 1A) в настоящее время является наиболее часто назначаемым препаратом для лечения СДВГ (Challman and Lipsky, 2000; Spiller et al., 2013). MPH является психостимулятором, связанным с амфетамином и кокаином, и проявляет свое действие, блокируя переносчики, которые повторно захватывают дофамин и норадреналин в пресинаптический нейрон после их высвобождения; таким образом, он увеличивает уровни или продлевает доступность этих нейротрансмиттеров в синапсах, чтобы оказывать влияние на постсинаптические нейроны (Kuczenski and Segal, 2005). Рисунок 1. (A) Химическая структура метилфенидата (риталин ©). (B) Химическая структура модафинила (Provigil ©). Препарат поразительно похож на метилфенидат и другие стимуляторы. Однако большая часть литературы по безопасности и эффективности MPH основана на исследованиях, проведенных на нормальных, здоровых взрослых животных, поскольку в настоящее время не существует достаточно надежной животной модели для СДВГ. Несколько десятилетий назад начали появляться исследования, которые предположили, что снижение гиперактивности и импульсивности у пациентов с СДВГ, принимающих стимуляторы, не было «парадоксальным» эффектом, но фактически также наблюдалось у здоровых людей, получавших те же дозы (Rapoport et al., 1978, 1980). Более поздние исследования MPH как на людях, так и на крысах показали, что низкие дозы MPH, которые соответствуют тем, которые вводятся пациентам с СДВГ в клинике, по-видимому, улучшают префронтально-зависимые функции и когнитивные способности во многом так же у здоровых людей и крыс, как и в Пациенты с СДВГ и модельные линии крыс (Mehta et al., 2001; Askenasy et al., 2007; Dow-Edwards et al., 2008; Agay et al., 2010; Linssen et al., 2012). Эти факты привели не только к признанию исследования MPH на нормальных предметах, но и к рассмотрению этого лекарства как усилителя когнитивных функций. Подавляющее большинство исследований влияния MPH на улучшение когнитивных функций и его воздействия на нормальный мозг проводилось на взрослых животных или людях. Более высокие дозы (дозы выше, чем для лечения СДВГ; 5–10 мг / кг внутрибрюшинно у крыс) увеличивают двигательную активность и ухудшают внимание и производительность при выполнении когнитивных задач, зависящих от префронтальной коры; однако более низкие дозы (дозы, эквивалентные диапазону, назначаемому пациентам с СДВГ; 0,5–2 мг / кг внутрибрюшинно у крыс) улучшают когнитивные функции и снижают двигательную активность у здоровых людей (Mehta et al., 2001). Аналогичным образом, более низкие дозы MPH (0,25–1 мг / кг, внутрибрюшинно, внутрибрюшинно) у нормальных взрослых крыс приводили к повышению производительности при выполнении задач на концентрацию внимания, но не влияли на двигательную активность, тогда как более высокие дозы снижали работоспособность и вызывали гиперактивность; дозы более 10 мг / кг приводили к «стереотипам» (повторяющимся мелким моторным движениям, сходным с тиками, наблюдаемыми при таких расстройствах, как синдром Туретта) (Mehta et al., 2001). Низкие дозы MPH приводят к небольшому увеличению дофамина и норадреналина избирательно в префронтальной коре, не влияя при этом на другие области мозга (Berridge et al., 2006). Это позволяет улучшить исполнительный контроль и рабочую память (WM), не вызывая двигательной активности или стереотипов. Однако опасность улучшения когнитивных функций такими стимуляторами, как MPH, заключается в их потенциальном воздействии на регуляцию дофамина и норэпинефрина (рис. 2). В оптимальных дозах дофамин связывается с D1-подобными рецепторами с более высоким сродством, а норэпинефрин связывается с рецепторами α2, что приводит к увеличению отношения сигнал / шум префронтальной коры головного мозга и усилению потока информации и укреплению нейронной связи (Arnsten and Li, 2005).Когда уровни дофамина и норадреналина превышают оптимальные уровни, они начинают активировать дофаминовые рецепторы класса D2 и норадренергические рецепторы α1 и β, что приводит к ослаблению отношения сигнал / шум за счет активации нейронов, которые могут не участвовать в текущей задаче (Arnsten, Li, 2005; Arnsten, 2009b). Эта неспецифическая активация нарушает избирательность внимания и приводит к проявлению двигательной гиперактивности, отвлекаемости и плохому контролю над импульсами. Рисунок 2.Связь дофамина / норэпинефрина с префронтальной функцией. При уровне ниже оптимального, PFC является недостаточно активным, и человек страдает от симптомов СДВГ (импульсивность, плохое суждение, невнимательность, двигательная гиперактивность). По мере повышения уровня функция улучшается, пока когнитивные и исполнительные функции не достигнут максимальной производительности при оптимальном уровне дофамина / норэпинефрина. По мере того, как уровни нейротрансмиттеров продолжают подниматься выше оптимальной точки, познавательная способность снова ухудшается, при этом человек демонстрирует отвлекаемость, импульсивность, стереотипное поведение и когнитивную негибкость. Уровни дофамина и норэпинефрина в нормальном здоровом мозге не универсальны и могут незначительно изменяться со временем у одного и того же человека в зависимости от сезона, времени дня или активности (Otter and Nurmand, 1980; Petrović et al., 1980) . В настоящее время не существует надежного метода определения оптимальных уровней этих нейромедиаторов в мозге живого человека; таким образом, прогнозирование того, как определенная доза MPH повлияет на конкретного человека, в значительной степени является обоснованным приближением. Также возможно, что, хотя многие исследования не обнаружили явных когнитивных различий между эффектами низких доз MPH на нормальных людей и пациентов с СДВГ, могут существовать молекулярные или клеточные различия, которые ожидают обнаружения с помощью разработки более продвинутых технологий.Таким образом, следует с осторожностью рассматривать исследования MPH как когнитивного усилителя и исследования с участием нормальных людей. В настоящее время миль в час наиболее часто злоупотребляют и продают на черном рынке среди подростков, особенно в средних школах и университетских городках (Goodman, 2010; Franke et al., 2011). Студенты ищут лекарство, когда у них есть экзамены или им нужно бодрствовать в течение долгих часов, чтобы повысить свою энергию и память. Это довольно обычное употребление среди подростков особенно пугает в свете графика развития префронтальной коры.Эта область мозга, центр контроля суждений, сдерживания поведения и эмоций, логического мышления и принятия решений, развивается только в юном возрасте; у людей это приходится на конец второго или начало третьего десятилетия жизни (Casey et al., 2008). Во время подросткового развития уровни норадреналина и дофамина резко падают и падают, что позволяет созреть механизмы исполнительного контроля и вознаграждения (Kanitz et al., 2011). Введение вещества, которое изменяет уровни дофамина и норэпинефрина, например MPH, может нарушить созревание префронтальной коры и иметь долгосрочные поведенческие последствия. Действительно, в последнее время исследования начали сдвигаться в сторону понимания действий MPH в мозге подростка. Эти новаторские исследования дали поразительные результаты, показывающие, что лечение MPH в раннем возрасте может изменять циркадные ритмы, вызывать тревогу, сохраняющуюся в зрелом возрасте, и даже ухудшать память на распознавание объектов (Lee et al., 2009; Algahim et al., 2010). Однако во многих исследованиях режим дозирования не был особенно строгим, и читатель должен очень внимательно изучить количество препарата, использованного в каждом исследовании.У взрослых крыс терапевтическая, клинически значимая доза MPH — это такая доза, которая обеспечивает уровни в плазме крови 8-40 нг / дл; это, по-видимому, находится в диапазоне 0,25–1 мг / кг при внутрибрюшинной инъекции (внутрибрюшинно) (Berridge et al., 2006). Недавно мы завершили несколько исследований, в которых изучали влияние низкой терапевтической дозы (1 мг / кг, внутрибрюшинно) на молодых крыс. Мы сообщили, что однократная доза MPH привела к значительному снижению возбудимости нейронов и синаптической передачи в префронтальной коре; лечение по хроническому режиму продолжительностью 3 недели привело к еще большей депрессии (Urban et al., 2012). Однако у взрослых крыс такая же низкая доза увеличивала нейрональную активность (Urban et al., 2012). Эти результаты предполагают, что существует возрастная разница в действиях MPH, и что у здоровых подростков и подростков дозы, ранее считавшиеся терапевтическими и улучшающими когнитивные функции, на самом деле могут вызывать чрезмерный уровень дофамина и норадреналина и фактически ухудшать определенные аспекты. познания. В поддержку этой теории мы обнаружили, что подавление нейрональной активности было вызвано, по крайней мере частично, активацией канала, известного как активируемый гиперполяризацией неспецифический катионный канал (HCN; Urban et al., 2012). Канал HCN позволяет потоку положительно заряженных ионов, в частности калия, из нейрона, снижая его потенциал напряжения и затрудняя для нейрона запуск потенциалов действия. Также известно, что канал HCN активируется гипердофаминергическим состоянием; таким образом, его роль в лечении молодых людей с помощью MPH предполагает, что эта доза индуцирует чрезмерное количество дофамина и, возможно, также норэпинефрина (Arnsten, 2009a). Одним из важных уникальных свойств префронтальной коры является ее высокий уровень пластичности, позволяющий выполнять управляющие функции, такие как WM и активное принятие решений; эта пластичность может быть результатом медленного созревания этой области (Jernigan et al., 1991; Кубосима-Амемори и Савагути, 2007; Спенсер-Смит и Андерсон, 2009 г .; Ньюман и МакГоги, 2011 г .; Теффер и Семендефери, 2012; Селемон, 2013). Пластичность регулируется уровнями рецепторов α-амино-3-гидрокси-5-метил-4-изоксазолепропионовой кислоты (AMPA) и рецепторов n-метил-d-аспартата (NMDA). Рецепторы NMDA содержат две субъединицы NR1 с комбинацией NR2A или NR2B; NR2B передает каналу более медленную кинетику, позволяя ему оставаться частично открытым во время нескольких стимуляций (Cull-Candy et al., 2001). Это свойство приводит к суммированию ответов и продолжению нейронной активности на короткое время после прекращения ввода, что считается нейрональным коррелятом WM (Wang et al., 2008, 2013). В большинстве областей коры головного мозга соотношение NR2B / NR2A высокое при рождении и снижается по мере развития; однако в префронтальной коре он остается высоким (Wang et al., 2008). Это позволяет сохранять пластичность на протяжении всей жизни, позволяя префронтальной коре постоянно адаптироваться к поступающей информации и корректировать поведенческий результат.Недавно мы обнаружили, что обработка низкими дозами (1 мг / кг, внутрибрюшинно) молодых крыс с MPH индуцировала избирательное снижение уровней NR2B, не затрагивая субъединицы NR2A (Urban et al., 2013). Это открытие подтверждает нашу теорию о том, что мозг подростка может быть сверхчувствительным к уровням дофамина; чрезмерные уровни дофамина вызывают интернализацию рецепторов NR2B через активацию киназы гликогенсинтазы (GSK) -3β, которая вызывает фосфорилирование β-катенина, нарушая взаимодействие β-катенин-NR2B, которое стабилизирует субъединицу NR2B (Li et al., 2009). При несвязанном β-catenin субъединицы NR2B становятся мишенями для интернализации. Что наши результаты означают для здорового подростка, принимающего MPH? Уникально высокие уровни субъединиц NR2B в префронтальной коре на протяжении всей жизни придают нейронам способность суммировать ответы на входящие стимулы, что приводит к кратковременному усилению нейронной активности, необходимой для WM; таким образом, снижение уровней NR2B в префронтальной коре приводит к уменьшению суммирования, что должно ухудшать WM (Wang et al., 2008, 2013; Urban et al., 2013). Однако было обнаружено, что длительная потенциация (ДП) усиливается после лечения несовершеннолетних MPH (Urban et al., 2013). Точные роли NR2A по сравнению с субъединицами рецептора NR2B в регуляции LTP в префронтальной коре не совсем понятны, но в настоящее время считается, что направление пластичности в префронтальной коре (потенциация или депрессия) зависит, скорее, от соотношения NR2A / NR2B. чем точные уровни каждой субъединицы (Massey et al., 2004; Xu et al., 2009; Foster et al., 2010). Таким образом, снижения уровней NR2B без изменения уровней NR2A, как было замечено после лечения ювенильных MPH, было достаточно, чтобы изменить направление долгосрочной пластичности ПФК (Urban et al., 2013). Поведенческие последствия изменения LTP и долговременной депрессии (LTD) в префронтальной коре неясны, поскольку точно не известно, что LTP представляет в этой области. Однако была выдвинута гипотеза, что если кратковременная потенциация является клеточным компонентом WM, то LTP может быть маркером устойчивого внимания и консолидации долговременной памяти.Таким образом, возможно, лечение здорового ювенильного мозга этими низкими дозами MPH приводит к нарушению WM и поведенческой гибкости, но улучшает устойчивое внимание и долговременную память? Если это так, это может указывать на то, что дети, проходящие лечение MPH, которые на самом деле не имеют СДВГ, будут успешно лечиться в классе — эти дети будут обращать внимание на учителя, станут менее гиперактивными и могут улучшиться обучение. Однако тщательное тестирование их поведенческой гибкости и WM может выявить незначительные недостатки, которые могут повлиять на их жизнь.Например, для вождения автомобиля необходима поведенческая гибкость — водитель должен уметь быстро переключать внимание с дороги на дорожные знаки, другие приближающиеся автомобили, обратно на дорогу и так далее. Пристальное внимание и недостаток гибкости потенциально могут привести к невнимательному или отвлеченному вождению. Поведенческая гибкость также является важным компонентом навыков межличностного общения; нужно уметь адаптироваться к разным людям и в рабочей обстановке менять планы и роли в группе, чтобы достичь цели.Опять же, поведенческая и когнитивная негибкость может нарушить работу человека и привести к снижению заработной платы, безработице или дисциплинарным мерам. Наконец, поведенческая гибкость является важнейшим компонентом противодействия злоупотреблению наркотиками и восстановления после него. Каливас и Волков определили изменения в глутаматергической передаче сигналов, которые приводят к неспособности изменить свое поведение у кокаиновых наркоманов (Kalivas and Volkow, 2005, 2011; Kalivas et al., 2005). Было показано, что MPH снижает вероятность последующего злоупотребления наркотиками у людей с диагнозом СДВГ, но, поскольку препарат, по-видимому, влияет на глутаматергическую сигнализацию, он потенциально может привести к аналогичной поведенческой ригидности и повысить вероятность обсессивно-компульсивного или аддиктивного поведения. (Ньюман и МакГоуи, 2011). Модафинил — потенциал для эффектов, подобных стимуляторам?Воздействие миль в час на развитие мозга, безусловно, интересно и потенциально пугающе; однако это не единственное лекарство, улучшающее когнитивные способности, которое изменяет передачу дофамина и глутамата. Еще один усилитель познавательной способности, который начал привлекать внимание в научном сообществе, — модафинил (Provigil ©), который имеет поразительное структурное сходство с метилфенидатом (MPH) и другими стимуляторами (рис. 1B). Первоначально разработанный во Франции в 1970-х годах модафинил повышает уровень гистамина в гипоталамусе, но также, по-видимому, обладает поразительным сродством с переносчиками дофамина на клеточной поверхности (Engber et al., 1998; Ishizuka et al., 2008; Zolkowska et al., 2009). Его точный механизм действия остается предметом споров, хотя были высказаны аргументы в пользу того, что он действует больше как реагент, способствующий пробуждению через систему гипокретин / орексин гипоталамуса, и как классический психостимулятор благодаря его блокаде ингибитора обратного захвата дофамина (Ishizuka et al., 2003; Zolkowska et al., 2009). Однако модафинил по-прежнему способствует бодрствованию у мышей с нокаутом орексина, поэтому оказывается, что система орексина не требуется для терапевтического эффекта (Willie et al., 2005). Каким бы ни был механизм или механизмы действия, модафинил в настоящее время является хорошо изученным лекарством с множеством применений. В настоящее время он одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) для лечения нарколепсии, нарушений при сменной работе и обструктивного апноэ во сне (Erman and Rosenberg, 2007; Cephalon, 2013). Было показано, что он уменьшает смену часовых поясов и улучшает настроение у сменных рабочих, которые часто борются с депрессией и хронической усталостью, забывчивостью и общими когнитивными нарушениями, вызванными их рабочим временем, не позволяющим поддерживать устойчивый цикл сна и бодрствования (O’Connor, 2004 ; Харт и др., 2006). Модафинил также изучался как альтернатива амфетаминам для использования в военных целях — военные предоставляют стимуляторы солдатам, страдающим от недосыпания или в ситуациях сильного стресса, которые требуют крайней бдительности в течение длительного времени. В настоящее время он одобрен для миссий ВВС США, а также используется в Великобритании и Индии (Taylor and Keys, 2003; Wheeler, 2006; Sharma, 2011). Хотя модафинил считается терапией первой линии при чрезмерной дневной сонливости (EDS), связанной с нарколепсией, у взрослых; он также широко используется при лечении СЭД у детей (Иваненко и др., 2003; Салливан, 2012). Осторожность снова является правилом, особенно в более молодом возрасте, из-за сообщений о серьезных побочных эффектах (таких как тахикардия, бессонница, возбуждение, головокружение и беспокойство) при приеме повышенных доз модафинила (Spiller et al., 2009), и фактически производитель рекомендует не использовать модафинил у детей младшего возраста. Несмотря на эти сообщения, модафинил одобрен FDA для использования у детей старше 16 лет (Sullivan, 2012). Полезность модафинила в улучшении бодрствования и бодрствования у здоровых людей, не страдающих недосыпом, и его военное участие привели к рассмотрению этого препарата как усилителя когнитивных функций (Turner et al., 2003; Барански и др., 2004; Randall et al., 2005b). Большинство исследований сходятся во мнении, что модафинил способствует улучшению памяти распознавания образов, воспоминаний о размахе цифр и умственных манипуляций с цифрами (выполнение сложения / вычитания / умножения в уме), но влияние на пространственную память, внимание и другие аспекты исполнительной функции более неоднозначно, и по всей видимости, зависят от исходных показателей данного человека (Turner et al., 2003; Baranski et al., 2004; Müller et al., 2004; Randall et al., 2005b). В исследовании здоровых студентов-добровольцев модафинил улучшал чувствительность цели в задаче быстрой обработки визуальной информации (RVIP), а также скорость обозначения цветов и рисования, но только у людей с «низким» (среднее значение 106 + 6) IQ; он не оказал значительного влияния на людей с «более высоким» (в среднем 115 + 5) IQ (Randall et al., 2005a). У крыс эти результаты повторяются, при этом крысы с низким ответом показывают улучшение времени реакции стоп-сигнала после модафинила; у более эффективных крыс не наблюдалось никаких улучшений (Eagle et al., 2007). Интересно, что MPH также показывает чувствительность к базовой производительности; многие исследования показали, что MPH вызывает большее улучшение у людей с низкими показателями, чем у людей с более высокими показателями, и в некоторых случаях может фактически вызывать дефицит у более эффективных людей (Eagle et al., 2007; Finke et al., 2010). Недавнее исследование, проведенное на здоровых людях, показало, что модафинил отличается от других агентов, усиливающих возбуждение, химической структурой, нейрохимическим профилем и поведенческими эффектами (Rasetti et al., 2010). В отличие от большинства исследований функциональной нейровизуализации, которые фокусировались на влиянии модафинила только на обработку информации, лежащую в основе исполнительного познания, в этом исследовании изучалось влияние модафинила на нейронные цепи, лежащие в основе аффективной обработки и когнитивных функций. Они прошли функциональную магнитно-резонансную томографию (МРТ, или функциональную МРТ, фМРТ), зависящую от уровня кислорода в крови (жирный шрифт), при выполнении задачи обработки эмоциональной информации, которая активирует миндалевидное тело, и двух префронтально зависимых когнитивных задач — задачи WM и переменной внимательности. задача управления (VAC).BOLD фМРТ выявила значительно сниженную реактивность миндалины на раздражающие стимулы на модафиниле по сравнению с плацебо. Во время задач исполнительного познания, задачи WM и задачи VAC модафинил уменьшал BOLD-сигнал в префронтальной коре и передней поясной извилине. Это исследование показало, что модафинил в низких дозах обладает уникальным физиологическим профилем по сравнению со стимуляторами: он повышает эффективность обработки когнитивной информации префронтальной коры головного мозга, снижая при этом реактивность на угрожающие стимулы в миндалине, области мозга, вызывающей тревогу (Rasetti et al., 2010). Базовая функциональная чувствительность и аффинность переносчика обратного захвата дофамина указывают на то, что модафинил может вызывать аналогичные эффекты на мозг, что и психостимуляторы, такие как MPH. В этом случае повод для беспокойства возникает, когда модафинил рассматривается как усилитель когнитивных функций у подростков и молодых людей. Чтобы поступить на службу в ВВС, где модафинил в настоящее время используется для пилотов, необходимо быть в возрасте от 17 до 27 лет (ВВС США, 2013 г.). Префронтальная кора головного мозга, которая жестко регулируется уровнями дофамина и норэпинефрина и является главным центром внимания и исполнительной обработки мозга, у людей не завершает свое развитие до конца 20–30-х годов; таким образом, молодые пилоты могут подвергаться риску того, что модафинил вызывает чрезмерный уровень дофамина в этой области мозга (Casey et al., 2008). Можно ожидать, что потенциальные последствия применения модафинила у здоровых молодых людей и подростков будут аналогичны тем, которые наблюдаются при применении MPH подростками / подростками (Urban et al., 2012, 2013). Таким образом, модафинил может вызывать изменения в пластичности или поведенческой ригидности и потенциально вредить WM, логическому мышлению и принятию решений. Сообщалось, что длительное бодрствование вызывает зависящую от опыта синаптическую пластичность в гипокретиновых / орексиновых нейронах мышей (Rao et al., 2007). В частности, острое и хроническое длительное бодрствование у мышей, вызванное лечением модафинилом, вызывало LTP глутаматергических синапсов на гипокретин / орексиновых нейронах в латеральном гипоталамусе, хорошо известном центре возбуждения / пробуждения.Подобное усиление синаптической силы в глутаматергических синапсах гипокретин / орексиновых нейронов также наблюдалось, когда мышей лишали сна в течение 4 часов. Эти результаты показывают, что синаптическая пластичность из-за длительного бодрствования возникает в цепях, ответственных за возбуждение, и может способствовать изменениям в головном мозге животных, страдающих от потери сна. Поэтому вполне вероятно, что неправильное употребление модафинила и злоупотребление им у подростков в конечном итоге приведет к пластичности мозга, особенно к областям мозга, связанным со сном и мотивацией, таким как гипоталамус и богатая дофамином префронтальная кора, гиппокамп и прилежащее ядро.В будущих исследованиях необходимо будет устранить эти недостатки, чтобы определить безопасность и эффективность модафинила как истинного усилителя когнитивных функций. В недавних обзорах предложены некоторые интересные механизмы, которые могут объяснить вероятность улучшения когнитивных функций (Lynch et al., 2011; Roesler and Schröder, 2011; Lynch and Gall, 2013), но эксперименты заслуживают дальнейшего изучения. Текущие исследования противоречивы в том, что некоторые исследования отметили явное улучшение устойчивого внимания у людей, в то время как другие не обнаружили какого-либо эффекта препарата (Turner et al., 2003; Randall et al., 2005b). Подобные расхождения можно найти в исследованиях на грызунах; однако более поздние исследования указывают на возможность того, что модафинил избирательно усиливает WM, не влияя на консолидацию воспоминаний в долговременное хранилище (Béracochéa et al., 2002; Turner et al., 2003; Müller et al., 2004; Randall et al., ., 2005b; Минзенберг, Картер, 2008). Эти исследования интересны и показывают поразительную полезность модафинила в качестве усилителя когнитивных функций; однако они были выполнены на взрослых людях и грызунах.В исследованиях здоровых взрослых и детей с СДВГ было также показано, что MPH явно усиливает WM (Mehta et al., 2004; Pietrzak et al., 2006; Kobel et al., 2009; Marquand et al., 2011), но недавно Исследования на молодых крысах показывают, что в здоровом развивающемся мозге препарат может фактически ухудшать WM в низких дозах, которые считаются клинически значимыми, т. е. дозах, которые производят уровни в плазме крови 8-40 нг / дл (Urban et al., 2013) . Профиль модафинила, демонстрирующий улучшения в WM у здоровых взрослых и лиц, лишенных сна (группа населения, для которой препарат был первоначально разработан), аналогичен MPH, способствующему улучшениям у здоровых взрослых и детей с СДВГ; поскольку оба препарата, по-видимому, влияют на уровень дофамина посредством блокады транспортеров обратного захвата и изменяют передачу сигналов глутамата, очевидно, что они могут вызывать аналогичные эффекты на WM в здоровом мозге подростков.Таким образом, модафинил в определенных дозах может вызывать снижение уровней рецепторов NMDA, ухудшение краткосрочной пластичности и изменения долгосрочной пластичности, как и MPH (Urban et al., 2013). Будущие исследования модафинила как усилителя когнитивных функций должны изучить эту возможность и установить, проявляет ли препарат возрастной и дозозависимый профиль эффектов, как у классических психостимуляторов. Ампакины — препараты для лечения болезни Альцгеймера — улучшающие когнитивные функцииПоследними классами лекарств, которые мы обсудим в этом обзоре, являются ампакины, которые также обладают потенциалом значительного воздействия на развивающуюся глутаматергическую систему.Ампакины — это класс лекарств, которые связываются с глутаматергическим рецептором AMPA, повышая его активность за счет замедления деактивации и ослабления десенсибилизации токов рецептора AMPA, увеличения синаптических ответов и усиления LTP (Arai and Kessler, 2007). Рецепторы AMPA критически вовлечены в регуляцию пластичности коры; Доставка рецепторов AMPA в синапс имеет решающее значение для поддержания возбудимости, которая приводит к LTP (Malinow and Malenka, 2002; Huganir and Nicoll, 2013). Однако это еще не все, о том, как AMPA регулирует возбудимость; он действует не в одиночку в этом процессе.Второй класс ионотропных рецепторов глутамата, рецепторы NMDA, фактически запускают индукцию LTP; однако эти рецепторы обычно блокируются магнием при мембранных потенциалах покоя (Dingledine et al., 1999; Cull-Candy et al., 2001; Paoletti et al., 2013). Активация рецепторов AMPA индуцирует EPSC, которые деполяризуют нейрон и удаляют магниевый блок NMDA, обеспечивая индукцию LTP. Затем рецепторы NMDA увеличивают доставку большего количества рецепторов AMPA в синапс, поддерживая LTP (Lu et al., 2001; Паолетти и др., 2013). В настоящее время никакие ампакины не одобрены Управлением по контролю за продуктами и лекарствами, но они исследуются в качестве средств лечения старческой болезни Альцгеймера, болезни Паркинсона, СДВГ, синдрома Ретта, шизофрении, депрессии, аутизма и синдрома Ангельмана (AS; Goff et al., 2001; Arai and Kessler, 2007 ; Ogier et al., 2007; Wezenberg et al., 2007; Simmons et al., 2009; Baudry et al., 2012; Silverman et al., 2013). Однако они также показали эффективность в улучшении памяти и познания у здоровых взрослых добровольцев и крыс (Ingvar et al., 1997; Hampson et al., 1998; Линч и Галл, 2006; Wezenberg et al., 2007). Американские военные также изучают ампакины для использования в качестве усилителей когнитивных способностей и стимуляторов бдительности для солдат в условиях длительных боевых действий с высоким стрессом; отсутствие стимуляции центральной нервной системы (например, при применении модафинила, амфетаминов или MPH, делает ампакины очень привлекательными (Saletan, 2008). Хотя ампакины имеют мало побочных эффектов при терапевтически значимых концентрациях и защищают нейроны от нейротоксических поражений у взрослых (Arai and Kessler , 2007), ампакин фарамптор может вызывать головную боль, сонливость и тошноту (Wezenberg et al., 2007). В то время как ампакины представляют собой, пожалуй, наиболее многообещающую группу фармацевтических препаратов для улучшения когнитивных функций с низким риском, а также потенциального облегчения для людей, страдающих психическими заболеваниями, они, вероятно, небезопасны для подростков, подростков и молодых людей. Во-первых, об этих препаратах известно очень мало; Единственным примером, прошедшим клинические испытания на людях, является CX-717 Cortex Pharmaceuticals, который оценивался в фазе I для лечения болезни Альцгеймера; гистологические повреждения были замечены в исследованиях на животных, но Cortex заявила, что это артефакт фиксации ткани (Stoll and Griesel, 2007).FDA отклонило заявку, и одобрение CX-717 было приостановлено. Ни один из других ампакинов в настоящее время не проходит испытания на людях, поэтому мало что может быть доказано об их эффективности или безопасности у здоровых людей. Однако мы можем строить предположения, основываясь на знаниях пластичности и глутаматной системы. Первая проблема при стимуляции передачи глутамата в мозге — это возможность эксайтотоксичности. Токсичность глутамата обычно возникает, когда избыток глутамата атакует рецепторы AMPA и NMDA, вызывая массовый приток кальция.Этот избыток кальция в клетках активирует ряд ферментов, таких как протеазы и фосфолипазы, которые вызывают повреждение органелл, клеточной мембраны и ДНК (Manev et al., 1989; Ankarcrona et al., 1995). Однако прямая активация рецепторов AMPA вызовет аналогичный массовый приток катионов, а также может вызвать эксайтотоксичность. Недавнее исследование показало, что ампакины способствуют полимеризации актина позвоночника, LTP и обучению на мышиной модели AS (Baudry et al., 2012). AS представляет собой нарушение нервного развития, в основном из-за аномальной материнской экспрессии гена UBE3A, ведущей к делеции E6-ассоциированного белка.Субъекты с АС имеют серьезные когнитивные нарушения, для которых нет терапевтических вмешательств. Мышиные модели (нокаут материнского гена UBE3A: «мыши AS») нарушения имеют существенный дефицит LTP и обучения. Baudry et al. Сообщили, что ампакин CX929 значительно усиливает LTP и, в частности, уменьшает аномалии дендритного позвоночника и нарушения обучения (Baudry et al., 2012). Это минимально инвазивное медикаментозное лечение, безусловно, является многообещающим для лечения АС и, вероятно, других нарушений развития нервной системы, таких как синдром ломкой Х-хромосомы и аутизм (Rueda et al., 2009; Silverman et al., 2013). Однако такой масштаб воздействия на синаптическую пластичность и целостность дендритных позвонков также вызывает серьезную озабоченность в отношении незрелого мозга маленьких детей, использующих ампакины в качестве усилителей когнитивных функций. Нетрудно представить, что ампакины будут иметь аналогичные эффекты на синаптическую передачу и нейронную связь в нормальном мозге, в конечном итоге вызывая пластичность мозга в областях, которые связаны с эмоциональными и аффективными функциями. Это может потенциально привести к плохой эмоциональной регуляции и нарушению поведенческого торможения, если пластичность чрезмерна и не регулируется.Действительно, одним из важных механизмов, с помощью которых поддерживаются и настраиваются мозговые связи, является сокращение синапсов, при котором высокоактивные синапсы усиливаются, а менее активные синапсы удаляются посредством ретракции аксонов (Luo and O’Leary, 2005; Gazzaniga and Mangum, 2009 ; Колб и др., 2012). На первый взгляд, повышенная пластичность может показаться преимуществом, выражающимся в более быстром обучении и улучшении когнитивных функций; однако чрезмерная пластичность может также привести к высокой активности всех синапсов и, следовательно, уменьшить синаптическую обрезку.Нарушения синаптической обрезки на самом деле были связаны с расстройствами аутистического спектра (Belmonte et al., 2004). Чрезмерная связность приводит к повышенной общей активации мозга, но снижение избирательности активации таково, что отношение сигнал / шум значительно снижается (Belmonte, 2000; Belmonte and Yurgelun-Todd, 2003). Таким образом, можно ясно увидеть потенциальные опасности, связанные с нерегулируемой пластичностью, и то, как ампакины (которые укрепляют синапсы и повышают пластичность, способствуя росту дендритных позвонков) могут приводить к синдромам, подобным аутизму. Хотя никакие исследования еще не отметили этого на людях, дозы ампакинов, вводимых людям, до сих пор строго контролировались. Если лекарство станет доступным как усилитель когнитивных функций или попадет на черный рынок, люди могут легко превысить безопасные дозы и пострадать от нейронального поражения из-за токсичности глутамата. Кроме того, основное предполагаемое терапевтическое действие ампакинов — изменение пластичности; известно, что они снижают порог индукции ДП, а также увеличивают величину достигнутой ДП (Lynch and Gall, 2006).Хотя это изменение пластичности может улучшить многие аспекты обучения и познания, такие как бдительность, усиление LTP, вероятно, будет сопровождаться одновременным снижением в противоположном направлении пластичности, то есть LTD. LTD имеет решающее значение для формирования пространственных карт и может также играть роль в моторном обучении мозжечка (хотя исследования двигательной активности после нарушения LTD были несколько противоречивыми) (Aiba et al., 1994; Manahan-Vaughan, 2005; Kemp and Manahan-Vaughan, 2007). Таким образом, смещение пластичности в пользу LTP может приводить к нарушениям пространственной памяти и, возможно, двигательной функции.В будущем необходимо будет завершить тщательное определение кривой доза-ответ, эксайтотоксических эффектов и видовых различий в метаболизме / реакции на ампакины, чтобы определить их истинную полезность в качестве усилителей познавательной способности. Заключение и перспективы на будущееВ этом обзоре мы рассмотрели три основных фармацевтических препарата, которые рассматриваются как усилители когнитивных функций: MPH, модафинил и ампакины. Мы сообщили о поразительном и глубоко касающемся влиянии клинически значимых доз MPH на функцию и пластичность ювенильной префронтальной коры, сравнили их с потенциальными последствиями лечения модафинилом и предложили несколько потенциальных рисков воздействия ампакина на здоровых людей.Из-за отсутствия в настоящее время исследований в этой области очевидно, что необходимо проделать большую работу для определения безопасности усилителей познавательной способности, особенно среди подростков, население, которое, скорее всего, воспользуется преимуществами этих препаратов, если они станут доступны. В кампусах колледжей и средних школах уже существует высокий спрос на MPH; таким образом, многие здоровые подростки и молодые люди уже подвергаются нерегулируемым дозам этого вещества. Понимание поведенческих и функциональных ответвлений клеточных и молекулярных изменений в еще незрелом мозге имеет первостепенное значение для снижения рисков потенциальной пластичности мозга и, как следствие, эмоциональных и поведенческих изменений (Urban and Gao, 2012, 2013). В настоящее время неясно, будет ли диапазон доз стимуляторов, который приводит к эффективному облегчению симптомов СДВГ и улучшению когнитивных функций у здорового взрослого человека, приводить к таким же поведенческим эффектам у подростков; тем не менее, наши недавние исследования показывают, что мозг молодых людей сверхчувствителен к воздействию MPH (Urban et al., 2012). Таким образом, даже низкая, предположительно клинически значимая доза может вызвать чрезмерный уровень дофамина и норадреналина и ухудшить исполнительные функции и WM.Этот чрезмерный допамин / норэпинефрин, вероятно, также является потенциальным риском лечения несовершеннолетних модафинилом. Гораздо менее ясно, как ампакины могут влиять на функцию мозга молодых людей, но их влияние на пластичность через глутаматергическую систему требует дальнейшего изучения. Стремление к развитию веществ, улучшающих когнитивные способности, вряд ли уменьшится со временем; он может представлять собой следующий этап эволюции — стремление человека к самосовершенствованию, приводящее к искусственному усилению врожденных способностей.Поэтому ученые и медицинское сообщество несут ответственность за тщательную оценку и исследование каждого нового вещества-кандидата, способствуя нашему пониманию работы мозга в процессе. Возможно, наиболее важным является то, что роль возраста и стадии развития в индивидуальной реакции на вещества, улучшающие когнитивные функции, требует тщательного изучения. Показатели метаболизма у молодых людей по сравнению со взрослыми не ясны на моделях людей или грызунов; Кривая доза-ответ для подростков по сравнению со взрослыми для MPH, модафинила и ампакинов, а также многих других психоактивных препаратов не изучалась.Наконец, потенциальное долгосрочное разветвление воздействия этих веществ на мозг здорового подростка в раннем возрасте — это только недавно возникшая тема исследования, и для того, чтобы оперативно ответить на поставленные вопросы, необходимо проявить большую осторожность. Когнитивные улучшения больше не являются научной фантастикой; мы должны учитывать уникальную динамику развивающегося мозга и действовать осторожно, пока не будут установлены точные параметры безопасности и эффективности. Заявление о конфликте интересовАвторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов. БлагодарностиЭто исследование было поддержано грантом R01MH085666 Вен-Цзюнь Гао из Национального института здравоохранения США. Список литературыAgay, N., Yechiam, E., Carmel, Z., and Levkovitz, Y. (2010). Неспецифические эффекты метилфенидата (риталина) на когнитивные способности и принятие решений у СДВГ и здоровых взрослых. Психофармакология (Berl) 210, 511–519. DOI: 10.1007 / s00213-010-1853-4 Pubmed Аннотация | Pubmed Полный текст | CrossRef Полный текст Айба, А., Кано, М., Чен, К., Стэнтон, М. Э., Фокс, Г. Д., Херруп, К. и др. (1994). Долговременная депрессия мозжечка и нарушение моторного обучения у мутантных мышей mGluR1. Cell 79, 377–388. DOI: 10.1016 / 0092-8674 (94) -4 Pubmed Аннотация | Pubmed Полный текст | CrossRef Полный текст Альгахим, М. Ф., Янг, П. Б., Бурау, К. Д., Суон, А. С. и Дафни, Н. (2010). Повторяющееся лечение риталином изменяет суточную активность молодых самцов крыс SD. Cent.Nerv. Syst. Agents Med. Chem. 10, 247–257. DOI: 10.2174 / 1871524 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

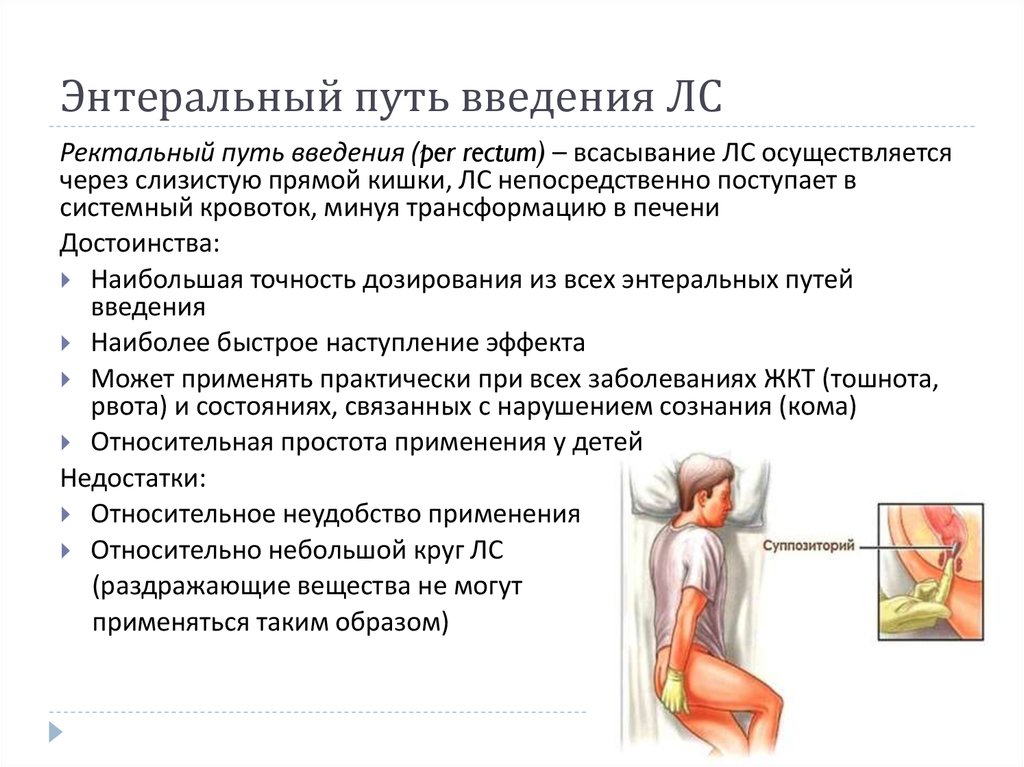 Энтеральными путями введения считаются
Энтеральными путями введения считаются Пpи теpмических поpажениях pотовой полости можно пpименить наружно
Пpи теpмических поpажениях pотовой полости можно пpименить наружно Документ, в котором врач записывает назначения пациенту:
Документ, в котором врач записывает назначения пациенту: К списку «А» относятся лекарственные вещества:
К списку «А» относятся лекарственные вещества: Что это такое, от чего зависит, примеры при различных путях введения
Что это такое, от чего зависит, примеры при различных путях введения