ГИПЕРТРОФИЧЕСКАЯ ОБСТРУКТИВНАЯ КАРДИОМИОПАТИЯ | Осиев
1. Караськов АМ, Осиев АГ. Гипертрофическая кардиомиопатия с обструкцией выходного отдела левого желудочка. Новосибирск: Дизайн науки; 2012. 187 с. Karas’kov AM, Osiev AG. Gipertroficheskaya kardiomiopatiya s obstruktsiey vykhodnogo otdela levogo zheludochka [Hypertrophic cardiomyopathy with left ventricular outlet obstruction]. Novosibirsk: Dizayn nauki; 2012. 187 p. (in Russian).
2. Бокерия ЛА, Борисов КВ, Синев АФ, Черникова НА, Злочевская ЕВ. Хирургическая коррекция гипертрофической обструктивной кардиомиопатии у детей при помощи оригинального способа. Грудная и сердечно-сосудистая хирургия. 2003;(2):22–8. Bokeriya LA, Borisov KV, Sinev AF, Chernikova NA, Zlochevskaya EV. Khirurgicheskaya korrektsiya gipertroficheskoy obstruktivnoy kardiomiopatii u detey pri pomoshchi original’nogo sposoba [Surgical correction of hypertrophic obstructive cardiomyopathy in children: an original method].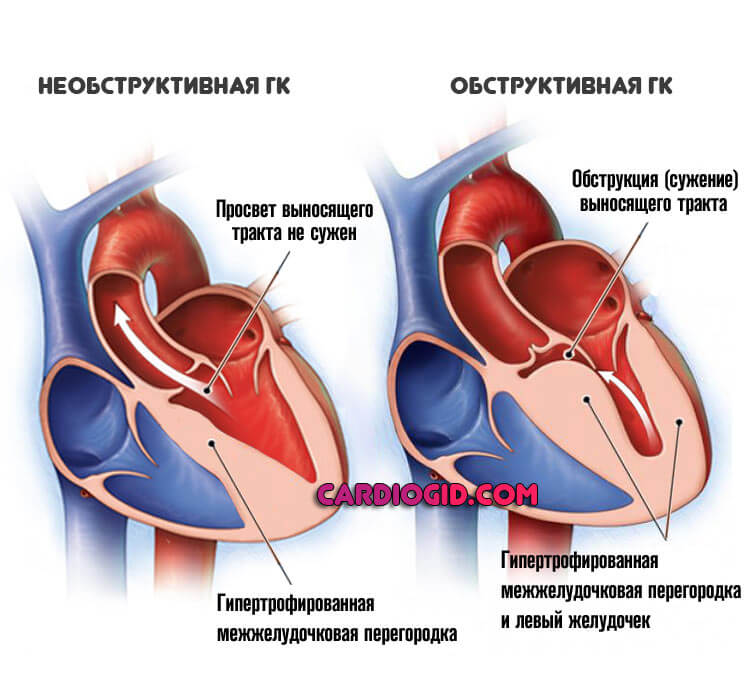 Grudnaya i serdechno-sosudistaya khirurgiya [Thoracic and Cardiovascular Surgery]. 2003;(2):22–8 (in Russian).
Grudnaya i serdechno-sosudistaya khirurgiya [Thoracic and Cardiovascular Surgery]. 2003;(2):22–8 (in Russian).
3. Gruver EJ, Fatkin D, Dodds GA, Kisslo J, Maron BJ, Seidman JG, Seidman CE. Familial hypertrophic cardiomyopathy and atrial fibrillation caused by Arg663His beta-cardiac myosin heavy chain mutation. Am J Cardiol. 1999;83(12A):13H–18H.
4. Gersh BJ, Maron BJ, Bonow RO, Dearani JA, Fifer MA, Link MS, Naidu SS, Nishimura RA, Ommen SR, Rakowski H, Seidman CE, Towbin JA, Udelson JE, Yancy CW. 2011 ACCF/AHA guideline for the diagnosis and treatment of hypertrophic cardiomyopathy: executive summary: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol. 2011;58(25):2703–38.
5. Authors/Task Force members, Elliott PM, Anastasakis A, Borger MA, Borggrefe M, Cecchi F, Charron P, Hagege AA, Lafont A, Limongelli G, Mahrholdt H, McKenna WJ, Mogensen J, Nihoyannopoulos P, Nistri S, Pieper PG, Pieske B, Rapezzi C, Rutten FH, Tillmanns C, Watkins H. 2014 ESC Guidelines on diagnosis and management of hypertrophic cardiomyopathy: the Task Force for the Diagnosis and Management of Hypertrophic Cardiomyopathy of the European Society of Cardiology (ESC). Eur Heart J. 2014;35(39):2733–79.
Authors/Task Force members, Elliott PM, Anastasakis A, Borger MA, Borggrefe M, Cecchi F, Charron P, Hagege AA, Lafont A, Limongelli G, Mahrholdt H, McKenna WJ, Mogensen J, Nihoyannopoulos P, Nistri S, Pieper PG, Pieske B, Rapezzi C, Rutten FH, Tillmanns C, Watkins H. 2014 ESC Guidelines on diagnosis and management of hypertrophic cardiomyopathy: the Task Force for the Diagnosis and Management of Hypertrophic Cardiomyopathy of the European Society of Cardiology (ESC). Eur Heart J. 2014;35(39):2733–79.
6. Maron BJ. Hypertrophic cardiomyopathy: a systematic review. JAMA. 2002;287(10): 1308–20.
7. Maron BJ, Maron MS. Hypertrophic cardiomyopathy. Lancet. 2013;381(9862):242–55..
8. Maron MS, Olivotto I, Betocchi S, Casey SA, Lesser JR, Losi MA, Cecchi F, Maron BJ. Effect of left ventricular outflow tract obstruction on clinical outcome in hypertrophic cardiomyopathy. N Engl J Med. 2003;348(4):295–303.
Effect of left ventricular outflow tract obstruction on clinical outcome in hypertrophic cardiomyopathy. N Engl J Med. 2003;348(4):295–303.
9. Maron MS, Olivotto I, Zenovich AG, Link MS, Pandian NG, Kuvin JT, Nistri S, Cecchi F, Udelson JE, Maron BJ. Hypertrophic cardiomyopathy is predominantly a disease of left ventricular outflow tract obstruction. Circulation. 2006;114(21):2232–9.
10. Olivotto I, Cecchi F, Casey SA, Dolara A, Traverse JH, Maron BJ. Impact of atrial fibrillation on the clinical course of hypertrophic cardiomyopathy. Circulation. 2001;104(21):2517–24.
11. Geske JB, Sorajja P, Nishimura RA, Ommen SR. Evaluation of left ventricular filling pressures by Doppler echocardiography in patients with hypertrophic cardiomyopathy: correlation with direct left atrial pressure measurement at cardiac catheterization. Circulation. 2007;116(23):2702–8.
Circulation. 2007;116(23):2702–8.
12. Maron MS, Zenovich AG, Casey SA, Link MS, Udelson JE, Aeppli DM, Maron BJ. Significance and relation between magnitude of left ventricular hypertrophy and heart failure symptoms in hypertrophic cardiomyopathy. Am J Cardiol. 2005;95(11):1329–33.
13. Bonow RO, Frederick TM, Bacharach SL, Green MV, Goose PW, Maron BJ, Rosing DR. Atrial systole and left ventricular filling in hypertrophic cardiomyopathy: effect of verapamil. Am J Cardiol. 1983;51(8):1386–91.
14. Spirito P, Maron BJ, Bonow RO, Epstein SE. Occurrence and significance of progressive left ventricular wall thinning and relative cavity dilatation in hypertrophic cardiomyopathy. Am J Cardiol. 1987;60(1):123–9.
15. McKenna WJ, England D, Doi YL, Deanfield JE, Oakley C, Goodwin JF. Arrhythmia in hypertrophic cardiomyopathy. I: Influence on prognosis.Br Heart J. 1981;46(2):168–72.
McKenna WJ, England D, Doi YL, Deanfield JE, Oakley C, Goodwin JF. Arrhythmia in hypertrophic cardiomyopathy. I: Influence on prognosis.Br Heart J. 1981;46(2):168–72.
16. Skinner JR, Manzoor A, Hayes AM, Joffe HS, Martin RP. A regional study of presentation and outcome of hypertrophic cardiomyopathy in infants. Heart. 1997;77(3):229–33.
17. Houston BA, Stevens Gerin R. Hypertrophic cardiomyopathy: a review. Clin Med Insights Cardiol. 2014;8(Suppl 1):53–65.
18. Ghosh S, Avari JN, Rhee EK, Woodard PK, Rudy Y. Hypertrophic cardiomyopathy with preexcitation: insights from noninvasive electrocardiographic imaging (ECGI) and catheter mapping. J Cardiovasc Electrophysiol. 2008;19(11):1215–7.
19. Абдулаев РЯ, Соболь ЮС, Шиллер НБ, Фостер Э. Современная эхокардиография.Харьков: Фортуна-Пресс; 1998. 240 с. Abdulaev RYa, Sobol’ YuS, Shiller NB, Foster E. Sovremennaya ekhokardiografiya [Modern echocardiography]. Kharkov: Fortuna-Press; 1998. 240 p. (in Russian).
Абдулаев РЯ, Соболь ЮС, Шиллер НБ, Фостер Э. Современная эхокардиография.Харьков: Фортуна-Пресс; 1998. 240 с. Abdulaev RYa, Sobol’ YuS, Shiller NB, Foster E. Sovremennaya ekhokardiografiya [Modern echocardiography]. Kharkov: Fortuna-Press; 1998. 240 p. (in Russian).
20. Габрусенко СА, Сафрыгина ЮВ, Наумов ВГ, Беленков ЮН. Современные подходы к лечению больных гипертрофической кардиомиопатией. Лечащий врач. 2004;(2):32–7. Gabrusenko SA, Safrygina YuV, Naumov VG, Belenkov YuN. Sovremennye podkhody k lecheniyu bol’nykh gipertroficheskoy kardiomiopatiey [Modern approaches to treatment of patients with hypertrophic cardiomyopathy]. Lechashchiy vrach. 2004;(2):32–7 (in Russian).
21. Ларина ОМ. Диагностическое значение магнитно-резонансной томографии при гипертрофии миокарда левого желудочка различного генеза. Литературный обзор. Вестник РНЦР. 2010;(10). Доступно на: http://vestnik.rncrr.ru/vestnik/v10/papers/larina_v10.htm Larina OM. Diagnosticheskoe znachenie magnitnorezonansnoy tomografii pri gipertrofii miokarda levogo zheludochka razlichnogo geneza. Literaturnyy obzor [Diagnostic significance of magnetic resonance imaging in left ventricular hypertrophy of various causes. Literature review]. Vestnik RNCRR. 2010;(10). Available from: http://vestnik.rncrr.ru/vestnik/v10/papers/larina_v10.htm (in Russian).
2010;(10). Доступно на: http://vestnik.rncrr.ru/vestnik/v10/papers/larina_v10.htm Larina OM. Diagnosticheskoe znachenie magnitnorezonansnoy tomografii pri gipertrofii miokarda levogo zheludochka razlichnogo geneza. Literaturnyy obzor [Diagnostic significance of magnetic resonance imaging in left ventricular hypertrophy of various causes. Literature review]. Vestnik RNCRR. 2010;(10). Available from: http://vestnik.rncrr.ru/vestnik/v10/papers/larina_v10.htm (in Russian).
22. Синицын ВЕ, Стукалова ОВ, Ларина ОВ, Смирнова МД, Агеев ФТ, Терновой СК. Магнитно-резонансная томография сердца с отсроченным контрастированием в оценке очаговых изменений в миокарде левого желудочка у больных с гипертрофической кардиомиопатией. Кардиологический вестник. 2008;(2):54–7. Sinitsyn VE, Stukalova OV, Larina OV, Smirnova MD, Ageev FT, Ternovoy SK. Magnitno-rezonansnaya tomografiya serdtsa s otsrochennym kontrastirovaniem v otsenke ochagovykh izmeneniy v miokarde levogo zheludochka u bol’nykh s gipertroficheskoy kardiomiopatiey [Magnetic resonance imaging
23. of the heart with delayed contrast filling for assessment of focal lesion of left ventricular myocardium in patients with hypertrophic cardiomyopathy]. Kardiologicheskiy vestnik. 2008;(2):54–7.
of the heart with delayed contrast filling for assessment of focal lesion of left ventricular myocardium in patients with hypertrophic cardiomyopathy]. Kardiologicheskiy vestnik. 2008;(2):54–7.
24. Bogaert J, Goldstein M, Tannouri F, Golzarian J, Dymarkowski S. Original report. Late myocardial enhancement in hypertrophic cardiomyopathy with contrast-enhanced MR imaging. AJR Am J Roentgenol. 2003;180(4):981–5.
25. Moon JC, Reed E, Sheppard MN, Elkington AG, Ho SY, Burke M, Petrou M, Pennell DJ. The histologic basis of late gadolinium enhancement cardiovascular magnetic resonance in hypertrophic cardiomyopathy. J Am Coll Cardiol. 2004;43(12):2260–4.
26. Keng FY, Chang SM, Cwajg E, He ZX, Lakkis NM, Nagueh SF, Spencer WH 3rd, Verani MS. Gated SPECT in patients with hypertrophic obstructive cardiomyopathy undergoing transcoronary ethanol septal ablation. J Nucl Cardiol. 2002;9(6):594–600.
J Nucl Cardiol. 2002;9(6):594–600.
27. Jiang TY, Wu XS, Han ZH, Jia CQ, Mi HZ, Gao YC, Zhang XL. Myocardial condition after transcoronary ablation predicts the curative effect in patients with hypertrophic obstructive cardiomyopathy. Chin Med J (Engl). 2006;119(3):246–9.
28. Veselka J, Prochazkova S, Duchonova R, Bolomova-Homolova I, Palenickova J, Tesar D, Cervinka P, Honek T. Alcohol septal ablation for hypertrophic obstructive cardiomyopathy: Lower alcohol dose reduces size of infarction and has comparable hemodynamic and clinical outcome. Catheter Cardiovasc Interv. 2004;63(2):231–5.
29. Spoladore R, Maron MS, D’Amato R, Camici PG, Olivotto I. Pharmacological treatment options for hypertrophic cardiomyopathy: high time for evidence. Eur Heart J. 2012;33(14):1724–33.
30. Pollick C. Muscular subaortic stenosis: hemodynamic and clinical improvement after disopyramide. N Engl J Med. 1982;307(16):997–9.
31. Pollick C, Kimball B, Henderson M, Wigle ED. Disopyramide in hypertrophic cardiomyopathy. I. Hemodynamic assessment after intravenous administration. Am J Cardiol. 1988;62(17):1248–51.
32. Sherrid MV, Barac I, McKenna WJ, Elliott PM, Dickie S, Chojnowska L, Casey S, Maron BJ. Multicenter study of the efficacy and safet of disopyramide in obstructive hypertrophic cardiomyopathy. J Am Coll Cardiol.2005;45(8):1251–8.
33. Lim DS, Lutucuta S, Bachireddy P, Youker K, Evans A, Entman M, Roberts R, Marian AJ. Angiotensin II blockade reverses myocardial fibrosis in a transgenic mouse model of human hypertrophic cardiomyopathy. Circulation. 2001;103(6):789–91.
Circulation. 2001;103(6):789–91.
34. Tsybouleva N, Zhang L, Chen S, Patel R, Lutucuta S, Nemoto S, DeFreitas G, Entman M, Carabello BA, Roberts R, Marian AJ. Aldosterone, through novel signaling proteins, is a fundamental molecular bridge between the genetic defect and the cardiac phenotype of hypertrophic cardiomyopathy. Circulation. 2004;109(10):1284–91.
35. Davies MJ, McKenna WJ. Hypertrophic cardiomyopathy – pathology and pathogenesis. Histopathology. 1995;26(6):493–500.
36. Flores-Ramirez R, Lakkis NM, Middleton KJ, Killip D, Spencer WH 3rd, Nagueh SF. Echocardiographic insights into the mechanisms of relief of left ventricular outflow tract obstruction after nonsurgical septal reduction therapy in patients with hypertrophic obstructive cardiomyopathy. J Am Coll Cardiol. 2001;37(1):208–14.
J Am Coll Cardiol. 2001;37(1):208–14.
37. Maron BJ, Peterson EE, Maron MS, Peterson JE. Prevalence of hypertrophic cardiomyopathy in an outpatient population referred for echocardiographic study. Am J Cardiol. 1994;73(8):577–80.
38. Brock R. Functional obstruction of the left ventricle; acquired aortic subvalvar stenosis. Guys Hosp Rep. 1957;106(4):221–38.
39. Morrow AG, Brockenbrough EC. Surgical treatment of idiopathic hypertrophic subaortic stenosis: technic and hemodynamic results of subaorticventriculomyotomy. Ann Surg. 1961;154:181–9.
Гипертрофическая кардиомиопатия
«Чем меньше компетентность, тем больше энтузиазм» Правило Де’Кашола
ОПРЕДЕЛЕНИЕ
Утолщение стенки левого желудочка (≥15 мм), которое нельзя объяснить перегрузкой (ESC).
Эпидемиология кардиомиопатий
КМП — кардиомиопатия. European Cardiomyopathy Pilot Registry. Eur Heart J. 2016;37:164–73.
ЭТИОЛОГИЯ ГИПЕРТРОФИЧЕСКОЙ КАРДИОМИОПАТИИ
• Наследственное аутосомно-доминантное заболевание, связанное с мутацией генов, кодирующих белки саркомера: 60–70%.
• Неуточненная причина: 30–40%.
Морфология
КЛИНИКА
• Одышка: сердечная недостаточность.
• Ангинозная боль: типичная или атипичная (неадекватное кровоснабжение, микроваскулярная дисфункция, вазоспазм, атеросклероз, мышечный мостик).
• Синкопе, пресинкопе, головокружение.
• Сердцебиение.
Электрокардиограмма
Апикальная гипертрофическая кардиомиопатия
Электрокардиограмма
Переднесептальная гипертрофическая кардиомиопатия
ДИАГНОСТИКА
• Шкала HCM Risk-SCD.
• Эхокардиография: оценка гипертрофии и градиента давления в выходном отделе левого желудочка в тест Вальсальвы (сидя, стоя).
• Магнитно-резонансная томография: дифференциальная диагностика, прогноз (позднее гадолиниевое усиление).
• Холтеровское мониторирование ЭКГ: 48 ч, каждые 12–24 мес, если не имплантирован кардиовертер.
• Стресс-тест с эхокардиографией: симптомным пациентам, если не достигнут провоцируемый пик ΔP ≥50 мм рт. ст. в выходном отделе левого желудочка.
• Коронарная ангиография: стенокардия III–IV ФК, устойчивая ЖТ, выжившие после остановки сердца.
• Генетическое тестирование: при атипичной клинике или подозрении на другие генетические дефекты, скрининг родственников 1 степени родства.
Эхокардиография
ВОЛЖ — выходной отдел левого желудочка, ЛЖ — левый желудочек, ЛП — левое предсердие, МКл — митральный клапан.
ФОРМЫ ГИПЕРТРОФИЧЕСКОЙ КАРДИОМИОПАТИИ
• Асимметричная гипертрофия (межжелудочковая перегорода, передняя стенка левого желудочка): 70%.
• Септальная гипертрофия: 15–20%.
• Концентрическая гипертрофия: 8–10%.
• Апикальная гипертрофия или боковой стенки: <2%.
Эхокардиография
ЭХОКАРДИОГРАФИЧЕСКИЕ ПРИЗНАКИ
• Асимметричная гипертрофия межжелудочковой перегородки ≥15 мм.
• Диффузная концентрическая или локальная в области передней стенки гипертрофия или верхушки.
• Систолическое движение передней створки митрального клапана.
• Митральная регургитация.
• Обструктивная форма: максимальный провоцируемый пик ΔP ≥50 мм рт. ст. в выходном отделе левого желудочка (скорость потока ≥2.7 м/сек).
Диагностика спортивного сердца (EAPC/EACVI)
Отсутствуют в «серой зоне» гипертрофии левого желудочка (13–16 мм):
• Семейный анамнез внезапной сердечной смерти или гипертрофической кардиомиопатии.
• Выраженные аномалии ЭКГ: инверсия ST/Т, широкий и глубокий Q.
• Нормальный или уменьшенный конечно-диастолический размер левого желудочка (<54 мм).
• Аномальная геометрия или сегментарная (≥2 мм) гипертрофия левого желудочка.
• Обструкция выходного отдела левого желудочка.
• Аномальное диастолической расслабление/наполнение левого желудочка (E/A <1.0, септальная e0 <8 см/с).
• Диспропорция увеличения левого предсердия и желудочка.
• Положительное гадолиниевое усиление при магнитно-резонансной томографии сердца.
• Отсутствие изменений толщины стенки левого желудочка после прекращения тренировок.
Магнитно-резонансная томография
B — гетероганная зона рубца в перегородке, D — нет позднего усиления гадолиния, F — субэндокардиальное усиление обоих желудочков. Kumar P, et al. Future Cardiol. 2013;9:697–709.
ПРИЧИНЫ ГИПЕРТРОФИИ ЛЕВОГО ЖЕЛУДОЧКА
Без перегрузки
• Врожденные нарушения метаболизма: болезни накопления гликогена, лизосомальные (болезнь Данона).
• Нейромышечные болезни: атаксия Фридриха.
• Митохондриальные болезни.
• Синдромы мальформации.
• Амилоидоз: после 65 лет, прогрессирующая АВ блокада, синдром запястного канала, снижен QRS, эхокардиография (утолщены межпредсердная стенка, свободная стенка правого желудочка, АВ клапан), МРТ, аномальные легкие цепи иммуноглобулинов в плазме.
• Лекарства: анаболические стероиды, гидроксихлорохин, такролимус.
• Эндокринные болезни: феохромоцитома, акромегалия.
С перегрузкой
• Артериальная гипертензия.
• Аортальный стеноз.
• Спортивное сердце.
• Ожирение.
Прогноз гипертрофической кардиомиопатии
Maron M, et al. NEJM. 2003;348:295.
ФОРМУЛИРОВКА ДИАГНОЗА
□ Гипертрофическая кардиомиопатия, обструктивная (35 мм рт. ст.). ХСН II ФК. Пароксизмальная фибрилляция предсердий, EHRA 2б. [I42.1]
□ Гипертрофическая кардиомиопатия, септальная, необструктивная. Пароксизмальная устойчивая мономорфная желудочковая тахикардия с синкопе. [I42.2]
Пароксизмальная устойчивая мономорфная желудочковая тахикардия с синкопе. [I42.2]
□ Гипертрофическая кардиомиопатия с формированием дилатационной кардиомиопатии, ХСН со сниженной ФВЛЖ (21% 10.06.2019), II ФК, 2Б. Имплантированный кардиовертер-дефибриллятор (2018). [I42.0]
Тактика ведения пациентов с гипертрофической кардиомиопатией (ESC)
ВОЛЖ — выходной отдел левого желудочка сердца, ЛЖ — левый желудочек.
ФАКТОРЫ РИСКА ВНЕЗАПНОЙ СМЕРТИ (AHA/ACC)
При наличии ≥1 большого фактора риска целесообразно рекомендовать ИКД:
• Внезапная смерть определенно или верятно обусловленная гипертрофической кардиомиопатией у ближайших родственников в возрасте ≤50 лет.
• Массивная гипертрофия левого желудочка ≥30 мм в любом сегменте.
• Недавний (<6 мес) предположительно аритмогенный обморок (нехарактерный для вазовагального или связанного с обструкцией выводного тракта левого желудочка).
• Апикальная аневризма левого желудочка любого размера.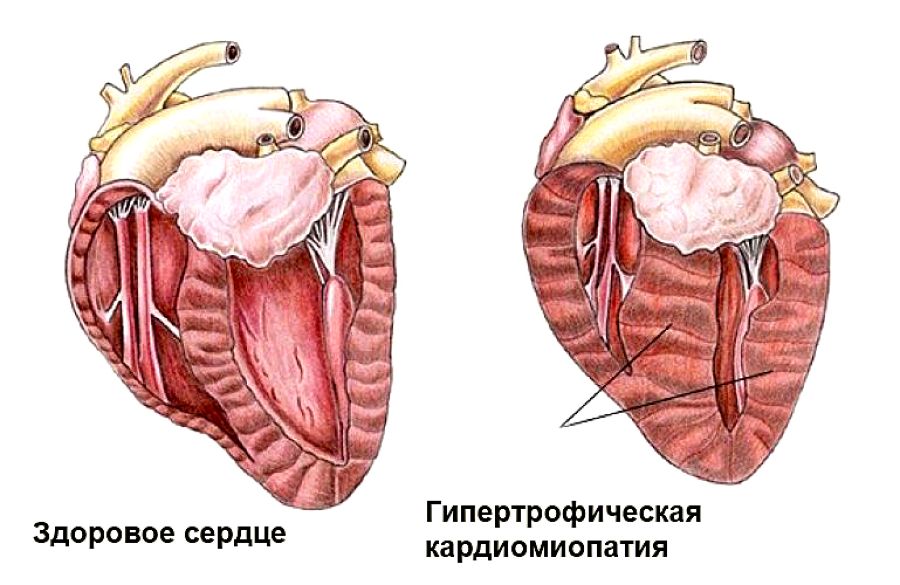
• Дисфункция левого желудочка с ФВЛЖ <50%.
ОТБОР ДЛЯ ИМПЛАНТАЦИИ КАРДИОВЕРТЕРА-ДЕФИБРИЛЛЯТОРА (ESC)
ВОЛЖ — выходной отдел левого желудочка сердца, ВСС — внезапная сердечная смерть,
ЖТ — желудочковая тахикардия, ИКД — имплантируемый кардиовертер-дефибриллятор, ЛЖ — левый желудочек,
ЛП — левое предсердие, НЖТ — наджелудочковая тахикардия, ФЖ — фибрилляция желудочков.
ЛЕЧЕНИЕ
Обструктивная форма
• Бета-блокаторы невазодилатирующие (до 400–600 мг/сут, ЧСС <60 в мин) или верапамил пролонгированный (до 320–480 мг/сут) в максимально переносимых дозах, ± дизопирамид.
• Мавакамтен 10–20 мг/сут (Heitner S, et al, 2019).
• Септальная миомэктомия, септальная абляция.
• Двухкамерная кардиостимуляция.
Ангинозные боли
• Бета-блокаторы, верапамил/дилтиазем, ранолазин.
• Мышечный мостик: миомэктомия, коронарное шунтирование, не показаны нитраты.
Лечение сердечной недостаточности II–IV ФК без обструкции
• Сохраненная ФВЛЖ: бета-блокаторы/верапамил, низкие дозы диуретиков (тиазиды, петлевые).
• Сниженная ФВЛЖ: ИАПФ/БРА, бета-блокаторы, петлевые диуретики, антагонисты альдостерона.
Лечение аритмий
• Риск внезапной смерти: амиодарон, кардиовертер-дефибриллятор.
• Фибрилляции предсердий: амиодарон, соталол, дизопирамид, бета-блокаторы/верапамил, катетерная абляция.
• Оральные антикоагулянты при фибрилляции предсердий независимо от CHA2DS2-VASc (AHA/ACC).
Прогресс в лечение заболевания
ИКД — имплантируемый кардиовертер-дефибриллятор. Maron B, et al. JAMA Cardiol. 2016;1:98–105.
Спиртовая септальная абляция при гипертрофической кардиомиопатии с обструкцией выходного тракта левого желудочка под контролем контрастной эхокардиографии | Николаева
Введение
Гипертрофическая кардиомиопатия (ГКМП) — генетическая патология, выражающаяся структурной и функциональной аномалией миокарда левого желудочка, проявляющаяся утолщением стенок по данным ЭхоКГ, КТ или МРТ. У части пациентов гипертрофия миокарда может приводить к обструкции выходного тракта левого желудочка (ВТЛЖ), что обуславливает высокий риск неблагоприятных сердечно-сосудистых исходов. Критерием обструкции ВТЛЖ является максимальный градиент давления (ГДmax) в ВТЛЖ > 25 мм рт. ст. по данным ЭхоКГ. При ГДmax > 50 мм рт. ст. рассматривается вопрос о выполнении коррекции ВТЛЖ [1-3]. Показания к коррекции ВТЛЖ определяются высокими цифрами градиента давления, недостаточностью кровообращения 3-4-го функционального класса по NYHA, наличием синкопальных состояний и неэффективностью медикаментозной терапии [1].
У части пациентов гипертрофия миокарда может приводить к обструкции выходного тракта левого желудочка (ВТЛЖ), что обуславливает высокий риск неблагоприятных сердечно-сосудистых исходов. Критерием обструкции ВТЛЖ является максимальный градиент давления (ГДmax) в ВТЛЖ > 25 мм рт. ст. по данным ЭхоКГ. При ГДmax > 50 мм рт. ст. рассматривается вопрос о выполнении коррекции ВТЛЖ [1-3]. Показания к коррекции ВТЛЖ определяются высокими цифрами градиента давления, недостаточностью кровообращения 3-4-го функционального класса по NYHA, наличием синкопальных состояний и неэффективностью медикаментозной терапии [1].
В настоящее время устранение субаортальной обструкции выполняется двумя способами: миоэктомии на открытом сердце и эндоваскулярным способом. В нашей статье мы хотели описать вариант лечения обструктивной формы ГКМП с помощью транскатетерного метода [4].
Впервые септальная абляция у больных с обструктивной формой ГКМП была осуществлена в 1994 г. F. Gietzen и его коллегами [5]. Они использовали технику чрескожной транслюминальной ангиопластики с последующим введением 96 % этанола в перфорантную септальную ветвь, что приводило к локализованному инфаркту и уменьшению толщины МЖП с последующим снижением субаортальной обструкции.
Они использовали технику чрескожной транслюминальной ангиопластики с последующим введением 96 % этанола в перфорантную септальную ветвь, что приводило к локализованному инфаркту и уменьшению толщины МЖП с последующим снижением субаортальной обструкции.
Рисунок 1. Передняя межжелудочковая артерия отдает множественные мелкие септальные ветви. Случай, не подходящий для септальной абляции
Figure 1. Anterior interventricular artery with multiple small septal branches. Septal ablation contraindicated
Рисунок 2. Передняя межжелудочковая артерия отдает крупную септальную ветвь
Figure 2. Anterior interventricular artery with a large septal branch
Сегодня во всем мире операция спиртовой септальной абляции выполняется в немногих медицинских центрах, включая ГБУЗ «Республиканский кардиологический центр».
Техническая возможность выполнения септальной абляции определяется наличием перфорантных внутриперегородочных ветвей более 1 мм и отсутствием их участия в кровоснабжении папиллярных мышц. Оценка строения септальных ветвей выполняется при коронарографии.
Оценка строения септальных ветвей выполняется при коронарографии.
В связи с тем что расположение септальных артерий в миокарде индивидуально, информация об участке миокарда, который нужно разрушить инъекцией спирта, крайне необходима перед выполнением абляции, чтобы исключить повреждение гемодинамически значимых структур миокарда, таких как папиллярные мышцы.
Оценка зоны кровоснабжения септальной ветви выполняется методом селективной контрастной трансторакальной эхокардиографии. Выполняется следующими образом: в септальную ветвь в приустьевом отделе over the wire (OTW) баллонным катетером через просвет OTW-баллонного катетера вводится ультразвуковое контрастное средство, распределяющееся в зоне кровоснабжения септальной ветви. В течение времени, необходимого для выполнения эхокардиографического определения зоны распределения контрастного вещества, баллонный катетер должен оставаться достаточно раздутым, препятствуя смыванию ультразвукового контраста (рис. 3) [6, 7].
Рисунок 3. Определяется контрастное вещество в пределах базального сегмента межжелудочковой перегородки
Определяется контрастное вещество в пределах базального сегмента межжелудочковой перегородки
Figure 3. Contrast agent in basal segment of interventricular septum
Материалы и методы
Собственный клинический случай
Пациентка В., 50 лет, с 2008 г. наблюдалась с диагнозом «гипертрофическая кардиомиопатия». С ноября 2018 г. отмечала ухудшение самочувствия в виде выраженной одышки, давящих болей за грудиной, преимущественно при физической нагрузке (при ходьбе до 100 м и подъеме на 2-й этаж), неоднократных эпизодах синкопальных состояний. По данным ЭхоКГ обращали внимание следующие показатели: толщина межжелудочковой перегородки 1,7-1,9 см, градиент давления на выходном тракте ЛЖ 130 мм рт. ст. в покое, систолическое давление в правом желудочке (СДПЖ) 90 мм рт. ст., умеренная митральная недостаточность, незначительное количество выпота в полости перикарда, фракция выброса составляла 67 % Sim. Принимаемое лечение — метопролол сукцинат 100 мг утром, периндоприл 2,5 мг вечером, кардиомагнил 150 мг. Назначить более высокие дозы метопролола не позволяло низкое артериальное давление.
Назначить более высокие дозы метопролола не позволяло низкое артериальное давление.
Также в анамнезе у пациентки отмечалась диагностированная кавернозная ангиома головного мозга. Состояние при поступлении средней тяжести. Сознание ясное. Кожные покровы физиологической окраски. Дыхание жесткое, хрипов нет. ЧД 17 в минуту. Сердечные тоны усилены, расщепление 2 тона и систолический шум на аортальном клапане типа crescendo-decrescendo. Пульс 65 ударов в минуту. АД 120/90 мм рт. ст. Отечность нижних конечностей до середины голеней.
Учитывая высокую степень субаортальной обструкции, клиническое состояние пациентки, отсутствие эффективности медикаментозной терапии и наличие высокого риска осложнений при открытой миоэктомии, было решено провести спиртовую септальную абляцию.
На коронарографии определись интактные коронарные артерии, выраженная первая септальная ветвь (СВ1) передней межжелудочковой артерии (ПМЖА), мышечный мост в среднем сегменте ПМЖА с систолической компрессией до 40 % (видео 1).
Видео 1. Селективное контрастирование левой коронарной артерии
Video 1. Selective contrast enhancement of left coronary artery
Правая коронарная артерия была интактна (видео 2).
Видео 2. Селективное контрастирование правой коронарной артерии
Video 2. Selective contrast enhancement of right coronary artery
Премедикация в операционной — диазепам 10 мг, промедол 20 мг.
Ход операции. Электрод временного электрокардиостимулятора (ЭКС) установлен в правый желудочек, контроль положения электрода пробным навязыванием ритма. Инвазивное измерение градиента давления в ВТЛЖ, ГД в покое 105 мм рт. ст., при пробе Вальсальвы 125 мм рт. ст.
ст.
Устье ЛКА канюлировано проводниковым катетером. По коронарному проводнику в септальную ветвь проведен OTW-баллонный катетер, проводник удален (видео 3). Раздутием баллона окклюзирована септальная ветвь, в септальную ветвь введено ультразвуковое контрастное вещество серы гексафторид (соновью) 2,0 мл (видео 4). На ЭхоКГ контрастное вещество распределилось в пределах базального сегмента межжелудочковой перегородки (видео 5 и 6). После чего в септальную ветвь введено 2,0 мл 96 % раствора этилового спирта с экспозицией 20 минут (видео 7 и 8). Баллон сдут и удален. На контрольной коронарографии первая септальная ветвь не контрастируется, контрастирование передней межжелудочковой артерии не изменено (видео 9). Интраоперационно по данным ЭхоКГ ГД в ВТЛЖ снизился до 53-60 мм рт. ст.
В раннем послеоперационном периоде суточное наблюдение в условиях отделения реанимации и интенсивной терапии (ОРИТ). Двукратное срабатывание ЭКС. Тропониновый тест положительный.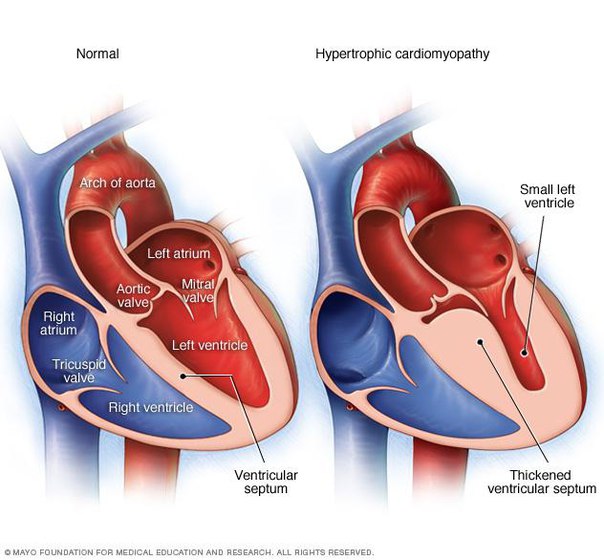 Электрод ЭКС удален на 2-е сутки.
Электрод ЭКС удален на 2-е сутки.
На 3-е сутки по данным ЭхоКГ отмечалась локальная редукция толщины базальной части МЖП до 1,3 см с гипокинезом на небольшом участке с сохранением общей сократительной способности левого желудочка (ФВ 60 % Sim), ГД на выходном тракте ЛЖ составлял 65 мм рт. ст., наблюдалось уменьшение степени регургитации на митральном клапане и снижение СДПЖ до 45 мм рт. ст.
Через 2 мес. при проведении контрольной ЭхоКГ было зафиксировано увеличение ГД до 85 мм рт. ст. У пациентки, несмотря на улучшение самочувствия (повысилась толерантность к физической нагрузке, уменьшились отеки на ногах, перестали беспокоить кардиальные боли) и принимаемую медикаментозную терапию (в т. ч. максимальные для нее дозы β-блокаторов), сохранялась выраженная одышка.
Учитывая высокую степень обструкции на выходном тракте ЛЖ, жалобы пациентки на одышку, оптимальное строение и расположение второй ветви, было решено провести повторную абляцию.
После абляции второй септальной ветви интраоперационно ГД в ВТЛЖ составил 43 мм рт. ст.
ст.
На контрольной ЭхоКГ через 3 суток отмечалась гипертрофия базального сегмента МЖП до 1,2 см с локальным истончением на небольшом протяжении до 0,8 см с уменьшением контрактильной способности на этом участке и сохранением общей сократительной способности левого желудочка (ФВ 62 % Sim), ГД в выходном тракте ЛЖ 20-22 мм рт. ст., СДПЖ 35 мм рт. ст. (рис. 4). Данные показатели сохранялись при проведении контрольной ЭхоКГ через 1, 3, 6 мес.
Клинически у больной отмечалось улучшение самочувствия, в том числе значительное уменьшение одышки.
Рисунок 4. Доплерограмма выходного тракта левого желудочка после септальной абляции
Figure 4. Left ventricular outflow tract Doppler post septal ablation
Обсуждение
По данным литературы, устранение или значительное снижение градиента давления в выходном тракте левого желудочка наблюдается более чем у 90 % больных ГКМП после хирургического вмешательства, что приводит к значительному улучшению клинической картины в 70-80 % случаев [8, 9]. Несмотря на большой опыт лечения этого заболевания, остается высокая летальность у пациентов с ХСН 3-4 ФК (42 %) [10]. В нашем случае, несмотря на проводимую адекватную медикаментозную терапию с высокими дозами β-блокаторов, у пациентки наблюдалась клиническая картина выраженной сердечной недостаточности и сохранялись высокие значения градиента давления в выходном тракте ЛЖ. Ситуацию усугубляло наличие установленной кавернозной ангиомы головного мозга. После продолжительного обсуждения, учитывая высокий риск осложнений при открытой миоэктомии, было решено провести септальную миоабляцию. Хирургическая коррекция была эффективной, несмотря на двукратное вмешательство. Повышение субаортального ГД после первой операции, видимо, было связано с редукцией базальной части МЖП на недостаточном протяжении и ремоделированием миокарда.
Несмотря на большой опыт лечения этого заболевания, остается высокая летальность у пациентов с ХСН 3-4 ФК (42 %) [10]. В нашем случае, несмотря на проводимую адекватную медикаментозную терапию с высокими дозами β-блокаторов, у пациентки наблюдалась клиническая картина выраженной сердечной недостаточности и сохранялись высокие значения градиента давления в выходном тракте ЛЖ. Ситуацию усугубляло наличие установленной кавернозной ангиомы головного мозга. После продолжительного обсуждения, учитывая высокий риск осложнений при открытой миоэктомии, было решено провести септальную миоабляцию. Хирургическая коррекция была эффективной, несмотря на двукратное вмешательство. Повышение субаортального ГД после первой операции, видимо, было связано с редукцией базальной части МЖП на недостаточном протяжении и ремоделированием миокарда.
После второй абляции были достигнуты оптимальные значения градиента давления, которые сохранялись в течение 6 месяцев, и улучшение других показателей по данным ЭхоКГ. Также хотелось отметить, что, несмотря на индуцированный локализованный инфаркт, общая сократительная способность миокарда не пострадала. Одновременно с положительным изменением показателей данных инструментальных обследований отмечалось выраженное улучшение самочувствия больной и компенсация хронической сердечной недостаточности.
Также хотелось отметить, что, несмотря на индуцированный локализованный инфаркт, общая сократительная способность миокарда не пострадала. Одновременно с положительным изменением показателей данных инструментальных обследований отмечалось выраженное улучшение самочувствия больной и компенсация хронической сердечной недостаточности.
Заключение
Спиртовая септальная абляция является малоинвазивным, эффективным и относительно безопасным методом лечения гипертрофической обструктивной кардиомиопатии при резистентности к медикаментозной терапии. Также может быть лечением выбора при наличии высокого риска осложнений операции на открытом сердце. А выполнение контрастной эхо-кардиографии позволяет диагностировать зоны, допустимые для введения этанола, исключить повреждение гемодинамически значимых структур миокарда и этим самым повысить безопасность хирургического лечения.
1. ESC Guidelines on diagnosis and management of hypertrophic cardiomyopathy. Eur Heart J. 2014;35(39):2733–79. DOI: 10.1093/eurheartj/ ehu284
ESC Guidelines on diagnosis and management of hypertrophic cardiomyopathy. Eur Heart J. 2014;35(39):2733–79. DOI: 10.1093/eurheartj/ ehu284
2. Mischi M. Contrast echocardiography for cardiac quantifications [dissertation]. Eindhoven: Technische Universiteit Eindhoven; 2004. DOI: 10.6100/IR579395
3. Бокерия Л.А. Гипертрофическая обструктивная кардиомиопатия. Анналы хирургии. 2013;(5):5–14.
4. Каплунова В.Ю., Шакарьянц Г.А., Кожевникова М.В., Хабарова Н.В., Привалова Е.В., Беленков Ю.Н. Современные подходы к проблеме гипертрофической кардиомиопатии. Клиническая медицина. 2016;94(10):754–63. DOI: 10.18821/0023-2149-2016-94- 10-754-763
5. Gietzen F., Leuner C., Gerenkapm T., Kuhn H. Relief of obstruction in hypertrophic cardiomyopathy by transient occlusion of the first septal branch of the left coronary artery. Eur Heart J. 1994;15(Suppl.):125. DOI: 10.1093/eurheartj/15.Abstract_Supplement.1
Gietzen F., Leuner C., Gerenkapm T., Kuhn H. Relief of obstruction in hypertrophic cardiomyopathy by transient occlusion of the first septal branch of the left coronary artery. Eur Heart J. 1994;15(Suppl.):125. DOI: 10.1093/eurheartj/15.Abstract_Supplement.1
6. Mukherjee D., Bates E.R., Roffi M., Lange R.A., Moliterno D.J. Cardiovascular catheterization and intervention: a textbook of coronary, peripheral, and structural heart disease. 2nd ed. Boca Raton: CRC Press; 2018.
7. Осиев А.Г., Гегенава Б.Б., Палеев Ф.Н., Григорьева Н.М. Спиртовая септальная аблация межжелудочковой перегородки с контрастным эхокардиографическим контролем. Российский кардиологический журнал. 2017;22(8):122–7. DOI: 10.15829/1560-4071-2017- 8-122-127
8. Осиев А.Г., Кретов Е.И., Курбатов В.П., Мироненко С.П., Найденов Р.А., Артамонова Е.А. и др. Новый подход к оценке результатов транскоронарной септальной аблации у больных с гипертрофической обструктивной кардиомиопатией. Патология кровообращения и кардиохирургия. 2013;17(3):46–9. DOI: 10.21688/1681-3472-2013-3-46-49
Осиев А.Г., Кретов Е.И., Курбатов В.П., Мироненко С.П., Найденов Р.А., Артамонова Е.А. и др. Новый подход к оценке результатов транскоронарной септальной аблации у больных с гипертрофической обструктивной кардиомиопатией. Патология кровообращения и кардиохирургия. 2013;17(3):46–9. DOI: 10.21688/1681-3472-2013-3-46-49
9. Maron B.J., Tpstein S.E., Morrow A.G. Symptomatic status and prognosis of patients after operation for hypertrophic obstructive cardiomyopathy: efficacy of ventricular septal myotomy and myectomy. Eur Heart J. 1983;4(Suppl. F):175–85. DOI: 10,1093 / eurheartj / 4.suppl_f.175
10. Schulte H.D., Gramsch-Zabel H., Schwartzkopff R. Hypertrophic obstructive cardiomyopathy: surgical management. Schweiz Med Wochenschr. 1995;125(41):1940–9. PMID: 7481652
СПИРТОВАЯ СЕПТАЛЬНАЯ АБЛЯЦИЯ МЕЖЖЕЛУДОЧКОВОЙ ПЕРЕГОРОДКИ С КОНТРАСТНЫМ ЭХОКАРДИОГРАФИЧЕСКИМ КОНТРОЛЕМ | Осиев
1. Maron BJ, Ommen SR, Semsarian C, Spirito P, Olivotto I, Maron MS. Hypertrophic cardiomyopathy: present and future, with translation into contemporary cardiovascular medicine. J Am Coll Cardiol 2014;64(1):83–99. doi: 10.1016/j.jacc.2014.05.003.
Maron BJ, Ommen SR, Semsarian C, Spirito P, Olivotto I, Maron MS. Hypertrophic cardiomyopathy: present and future, with translation into contemporary cardiovascular medicine. J Am Coll Cardiol 2014;64(1):83–99. doi: 10.1016/j.jacc.2014.05.003.
2. Maron MS, Olivotto I, Betocchi S, Casey SA, Lesser JR, Losi MA, Cecchi F, Maron BJ. Effect of left ventricular outflow tract obstruction on clinical outcome in hypertrophic cardiomyopathy. N Engl J Med 2003;348(4):295–303. doi: 10.1056/NEJMoa021332.
3. Osiev AG, Naydenov RA, Kretov EI, Obedinskaya NR, Kurbatov VP. Hypertrophic obstructive cardiomyopathy. Almanac of Clinical Medicine 2015;38:95–104. Russian. doi:10.18786/2072-0505-2015-38-95-104 (Осиев АГ, Найденов РА, Кретов ЕИ, Обединская НР, Курбатов ВП. Гипертрофическая обструктивная кардиомиопатия. Альманах клинической медицины 2015;38:95–104).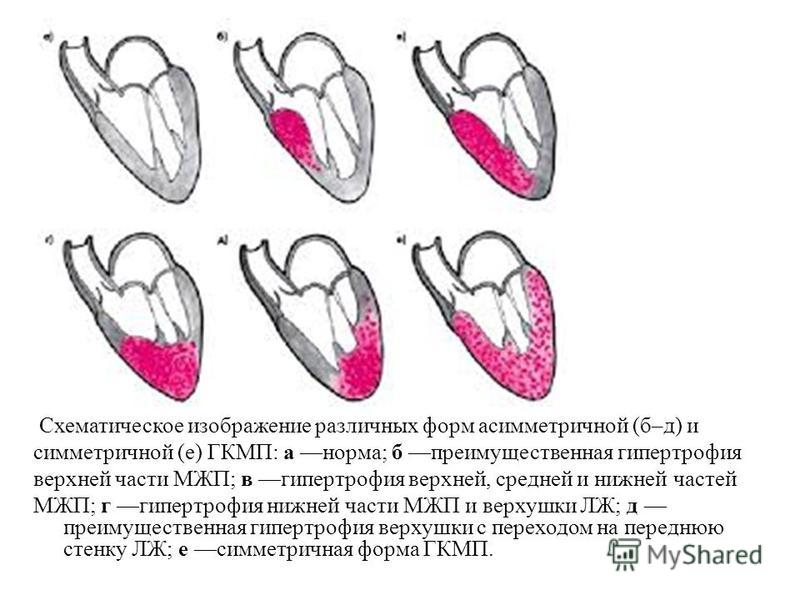
4. Maron BJ, Bonow RO, Cannon RO 3rd, Leon MB, Epstein SE. Hypertrophic cardiomyopathy. Interrelations of clinical manifestations, pathophysiology, and therapy (2). N Engl J Med 1987;316(14):844–52. doi: 10.1056/NEJM198704023161405.
5. Smedira NG, Lytle BW, Lever HM, Rajeswaran J, Krishnaswamy G, Kaple RK, Dolney DO, Blackstone EH. Current effectiveness and risks of isolated septal myectomy for hypertrophic obstructive cardiomyopathy. Ann Thorac Surg 2008;85(1):127–33. doi: 10.1016/j.athoracsur.2007.07.063.
6. Maron BJ. Hypertrophic cardiomyopathy: a systematic review. JAMA 2002;287(10):1308–20. doi:10.1001/jama.287.10.1308.
7. Maron BJ, McKenna WJ, Danielson GK, Kappenberger LJ, Kuhn HJ, Seidman CE, Shah PM, Spencer WH 3rd, Spirito P, Ten Cate FJ, Wigle ED; Task Force on Clinical Expert Consensus Documents. American College of Cardiology; Committee for Practice Guidelines. European Society of Cardiology. American College of Cardiology/European Society of Cardiology clinical expert consensus document on hypertrophic cardiomyopathy. A report of the American College of Cardiology Foundation Task Force on Clinical Expert Consensus Documents and the European Society of Cardiology Committee for Practice Guidelines. J Am Coll Cardiol 2003;42(9):1687–713. doi: https://doi.org/10.1016/S0735-1097(03)00941-0.
American College of Cardiology; Committee for Practice Guidelines. European Society of Cardiology. American College of Cardiology/European Society of Cardiology clinical expert consensus document on hypertrophic cardiomyopathy. A report of the American College of Cardiology Foundation Task Force on Clinical Expert Consensus Documents and the European Society of Cardiology Committee for Practice Guidelines. J Am Coll Cardiol 2003;42(9):1687–713. doi: https://doi.org/10.1016/S0735-1097(03)00941-0.
8. Robbins RC, Stinson EB. Long-term results of left ventricular myotomy and myectomy for obstructive hypertrophic cardiomyopathy. J Thorac Cardiovasc Surg 1996;111(3):586–94. doi: https://doi.org/10.1016/S0022-5223(96)70310-0.
9. Sigwart U. Non-surgical myocardial reduction for hypertrophic obstructive cardiomyopathy. Lancet 1995;346(8969):211–4. doi: https://doi.org/10.1016/S0140-6736(95)91267-3.
doi: https://doi.org/10.1016/S0140-6736(95)91267-3.
10. Brugada P, de Swart H, Smeets JL, Wellens HJ. Transcoronary chemical ablation of ventricular tachycardia. Circulation 1989;79(3):475–82. doi: https://doi.org/10.1161/01.CIR.79.3.475.
11. Inoue H, Waller BF, Zipes DP. Intracoronary ethyl alcohol or phenol injection ablates aconitine-induced ventricular tachycardia in dogs. J Am Coll Cardiol 1987;10(6):1342–9.
12. Li ZQ, Cheng TO, Zhang WW, Qiao SB, Zhao LY, Jin YZ, Guan RM, Liu L. Percutaneous transluminal septal myocardial ablation for hypertrophic obstructive cardiomyopathy; The Chinese experience in 119 patients from a single center. Int J Cardiol 2004;93(2-3):197–202. doi: 10.1016/j.ijcard.2003.03.005.
13. Fifer MA. Controversies in cardiovascular medicine. Most fully informed patients choose septal ablation over septal myectomy. Circulation 2007;116(2):207–16. doi: 10.1161/CIRCULATIONAHA.107.688135.
Fifer MA. Controversies in cardiovascular medicine. Most fully informed patients choose septal ablation over septal myectomy. Circulation 2007;116(2):207–16. doi: 10.1161/CIRCULATIONAHA.107.688135.
14. Harthorne JW, Pohost GM. Electrical therapy of cardiac dysrhythmias. In: HJ Levine (Ed.). Clinical Cardiovascular Physiology. New York: Grune & Stratton, 1976:853–82.
15. Aksu T, Guler T, Yalin K, Golcuk SE, Ozcan K. Septal ablation for hypertrophic obstructive cardiomyopathy: transcoronary and endocardial approach. Am J Med Sci 2016;352(5):466–71. doi: 10.1016/j.amjms.2016.08.025.
16. Gietzen FH, Leuner CJ, Obergassel L, Strunk-Mueller C, Kuhn H. Role of transcoronary ablation of septal hypertrophy in patients with hypertrophic cardiomyopathy, New York Heart Association functional class III or IV, and outflow obstruction only under provocable conditions. Circulation 2002;106(4):454–9. doi: https://doi.org/10.1161/01.CIR.0000022845.80802.9D.
Circulation 2002;106(4):454–9. doi: https://doi.org/10.1161/01.CIR.0000022845.80802.9D.
17. Sathyamurthy I, Nayak R, Oomman A, Subramanyan K, Kalarical MS, Mao R, Ramachandran P. Alcohol septal ablation for hypertrophic obstructive cardiomyopathy – 8 years follow up. Indian Heart J. 2014;66(1):57–63. doi: 10.1016/j.ihj.2013.12.008.
18. Faber L, Seggewiss H, Welge D, Fassbender D, Schmidt HK, Gleichmann U, Horstkotte D. Echo-guided percutaneous septal ablation for symptomatic hypertrophic obstructive cardiomyopathy: 7 years of experience. Eur J Echocardiogr 2004;5(5):347–55. doi: 10.1016/j.euje.2004.01.001.
19. Okayama H, Sumimoto T, Morioka N, Yamamoto K, Kawada H. Usefulness of selective myocardial contrast echocardiography in percutaneous transluminal septal myocardial ablation: a case report. Jpn Circ J 2001;65(9):842–4. doi: http://doi.org/10.1253/jcj.65.842.
Jpn Circ J 2001;65(9):842–4. doi: http://doi.org/10.1253/jcj.65.842.
20. Geske JB, Sorajja P, Ommen SR, Nishimura RA. Variability of left ventricular outflow tract gradient during cardiac catheterization in patients with hypertrophic cardiomyopathy. JACC Cardiovasc Interv 2011;4(6):704–9. doi: 10.1016/j.jcin.2011.02.014.
21. Harada T, Ohtaki E, Sumiyoshi T. Papillary muscles identified by myocardial contrast echocardiography in preparation for percutaneous transluminal septal myocardial ablation. Acta Cardiol 2002;57(1):25–7. doi: 10.2143/AC.57.1.2005377.
22. Kuhn H, Lawrenz T, Lieder F, Leuner C, Strunk-Mueller C, Obergassel L, Bartelsmeier M, Stellbrink C. Survival after transcoronary ablation of septal hypertrophy in hypertrophic obstructive cardiomyopathy (TASH): a 10 year experience. Clin Res Cardiol 2008;97(4):234–43. doi: 10.1007/s00392-007-0616-7.
Clin Res Cardiol 2008;97(4):234–43. doi: 10.1007/s00392-007-0616-7.
23. Gietzen FH, Leuner CJ, Raute-Kreinsen U, Dellmann A, Hegselmann J, Strunk-Mueller C, Kuhn HJ. Acute and long-term results after transcoronary ablation of septal hypertrophy (TASH). Catheter interventional treatment for hypertrophic obstructive cardiomyopathy. Eur Heart J. 1999;20(18):1342–54. doi: 10.1053/euhj.1999.1520.
24. Veselka J, Duchonová R, Procházková S, Homolová I, Pálenícková J, Zemánek D, Pernisová Z, Tesar D. The biphasic course of changes of left ventricular outflow gradient after alcohol septal ablation for hypertrophic obstructive cardiomyopathy. Kardiol Pol 2004;60(2):133–6.
25. Yoerger DM, Picard MH, Palacios IF, Vlahakes GJ, Lowry PA, Fifer MA. Time course of pressure gradient response after first alcohol septal ablation for obstructive hypertrophic cardiomyopathy. Am J Cardiol 2006;97(10):1511–4. doi: 10.1016/j.amjcard.2005.12.040.
Am J Cardiol 2006;97(10):1511–4. doi: 10.1016/j.amjcard.2005.12.040.
26. Veselka J, Zemánek D, Tomasov P, Duchonová R, Linhartová K. Alcohol septal ablation for obstructive hypertrophic cardiomyopathy: ultra-low dose of alcohol (1 ml) is still effective. Heart Vessels 2009;24(1):27–31. doi: 10.1007/s00380-008-1083-4.
27. Liebregts M, Steggerda RC, Vriesendorp PA, van Velzen H, Schinkel AF, Willems R, van Cleemput J, van den Berg MP, Michels M, ten Berg JM. Long-term outcome of alcohol septal ablation for obstructive hypertrophic cardiomyopathy in the young and the elderly. JACC Cardiovasc Interv 2016;9(5):463–9. doi: 10.1016/j.jcin.2015.11.036.
28. Angelini P. The «1st septal unit» in hypertrophic obstructive cardiomyopathy: a newly recognized anatomo-functional entity, identified during recent alcohol septal ablation experience. Tex Heart Inst J 2007;34(3):336–46.
Tex Heart Inst J 2007;34(3):336–46.
29. Holmes DR Jr, Valeti US, Nishimura RA. Alcohol septal ablation for hypertrophic cardiomyopathy: indications and technique. Catheter Cardiovasc Interv 2005;66(3):375–89. doi: 10.1002/ccd.20500.
30. Faber L, Seggewiss H, Gleichmann U. Percutaneous transluminal septal myocardial ablation in hypertrophic obstructive cardiomyopathy: results with respect to intraprocedural myocardial contrast echocardiography. Circulation 1998;98(22):2415–21. doi: https://doi.org/10.1161/01.CIR.98.22.2415.
31. Lakkis NM, Nagueh SF, Dunn JK, Killip D, Spencer WH 3rd. Nonsurgical septal reduction therapy for hypertrophic obstructive cardiomyopathy: one-year follow-up. J Am Coll Cardiol 2000;36(3):852–5. doi: https://doi.org/10.1016/S0735-1097(00)00767-1.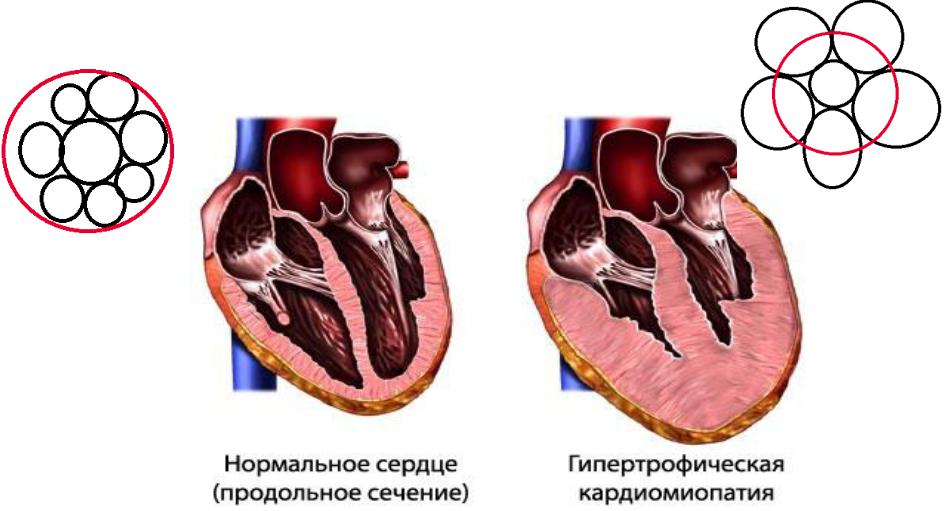
32. Kim JJ, Lee CW, Park SW, Hong MK, Lim HY, Song JK, Jin YS, Park SJ. Improvement in exercise capacity and exercise blood pressure response after transcoronary alcohol ablation therapy of septal hypertrophy in hypertrophic cardiomyopathy. Am J Cardiol 1999;83(8):1220–3. doi: https://doi.org/10.1016/S0002-9149(99)00063-6.
33. Fernandes VL, Nagueh SF, Wang W, Roberts R, Spencer WH 3rd. A prospective follow-up of alcohol septal ablation for symptomatic hypertrophic obstructive cardiomyopathy – the Baylor experience (1996-2002). Clin Cardiol 2005;28(3):124–30. doi: 10.1002/clc.4960280305.
34. Jensen MK, Almaas VM, Jacobsson L, Hansen PR, Havndrup O, Aakhus S, Svane B, Hansen TF, Køber L, Endresen K, Eriksson MJ, Jørgensen E, Amlie JP, Gadler F, Bundgaard H. Long-term outcome of percutaneous transluminal septal myocardial ablation in hypertrophic obstructive cardiomyopathy: a Scandinavian multicenter study. Circ Cardiovasc Interv 2011;4(3):256–65. doi: 10.1161/CIRCINTERVENTIONS.110.959718.
Long-term outcome of percutaneous transluminal septal myocardial ablation in hypertrophic obstructive cardiomyopathy: a Scandinavian multicenter study. Circ Cardiovasc Interv 2011;4(3):256–65. doi: 10.1161/CIRCINTERVENTIONS.110.959718.
35. Alam M, Dokainish H, Lakkis N. Alcohol septal ablation for hypertrophic obstructive cardiomyopathy: a systematic review of published studies. J Interv Cardiol 2006;19(4):319–27. doi: 10.1111/j.1540-8183.2006.00153.x.
36. Kuhn H, Lawrenz T, Lieder F, Leuner C, Strunk-Mueller C, Obergassel L, Bartelsmeier M, Stellbrink C. Survival after transcoronary ablation of septal hypertrophy in hypertrophic obstructive cardiomyopathy (TASH): a 10 year experience. Clin Res Cardiol 2008;97(4):234–43.
37. Sitges M, Shiota T, Lever HM, Qin JX, Bauer F, Drinko JK, Agler DA, Martin MG, Greenberg NL, Smedira NG, Lytle BW, Tuzcu EM, Garcia MJ, Thomas JD. Comparison of left ventricular diastolic function in obstructive hypertrophic cardiomyopathy in patients undergoing percutaneous septal alcohol ablation versus surgical myotomy/myectomy. Am J Cardiol 2003;91(7):817–21. doi: https://doi.org/10.1016/S0002-9149(03)00016-X.
Comparison of left ventricular diastolic function in obstructive hypertrophic cardiomyopathy in patients undergoing percutaneous septal alcohol ablation versus surgical myotomy/myectomy. Am J Cardiol 2003;91(7):817–21. doi: https://doi.org/10.1016/S0002-9149(03)00016-X.
38. Reinhard W, Ten Cate FJ, Scholten M, De Laat LE, Vos J. Permanent pacing for complete atrioventricular block after nonsurgical (alcohol) septal reduction in patients with obstructive hypertrophic cardiomyopathy. Am J Cardiol 2004;93(8):1064–6. doi: 10.1016/j.amjcard.2003.12.065.
39. Chen AA, Palacios IF, Mela T, Yoerger DM, Picard MH, Vlahakes G, Lowry PA, Fifer MA. Acute predictors of subacute complete heart block after alcohol septal ablation for obstructive hypertrophic cardiomyopathy. Am J Cardiol 2006;97(2):264–9. doi: 10.1016/j.amjcard.2005.08.032.
40. Lawrenz T, Lieder F, Bartelsmeier M, Leuner C, Borchert B, Meyer zu Vilsendorf D, Strunk-Mueller C, Reinhardt J, Feuchtl A, Stellbrink C, Kuhn H. Predictors of complete heart block after transcoronary ablation of septal hypertrophy: results of a prospective electrophysiological investigation in 172 patients with hypertrophic obstructive cardiomyopathy. J Am Coll Cardiol 2007;49(24):2356–63. doi: 10.1016/j.jacc.2007.02.056.
Lawrenz T, Lieder F, Bartelsmeier M, Leuner C, Borchert B, Meyer zu Vilsendorf D, Strunk-Mueller C, Reinhardt J, Feuchtl A, Stellbrink C, Kuhn H. Predictors of complete heart block after transcoronary ablation of septal hypertrophy: results of a prospective electrophysiological investigation in 172 patients with hypertrophic obstructive cardiomyopathy. J Am Coll Cardiol 2007;49(24):2356–63. doi: 10.1016/j.jacc.2007.02.056.
41. Chang SM, Lakkis NM, Franklin J, Spencer WH 3rd, Nagueh SF. Predictors of outcome after alcohol septal ablation therapy in patients with hypertrophic obstructive cardiomyopathy. Circulation 2004;109(7):824–7. doi: 10.1161/01.CIR.0000117089.99918.5A.
42. Talreja DR, Nishimura RA, Edwards WD, Valeti US, Ommen SR, Tajik AJ, Dearani JA, Schaff HV, Holmes DR Jr. Alcohol septal ablation versus surgical septal myectomy: comparison of effects on atrioventricular conduction tissue. J Am Coll Cardiol 2004;44(12):2329–32. doi: 10.1016/j.jacc.2004.09.036.
J Am Coll Cardiol 2004;44(12):2329–32. doi: 10.1016/j.jacc.2004.09.036.
Обструктивная гипертрофическая кардиомиопатия | Справка.Неинвалид.ru
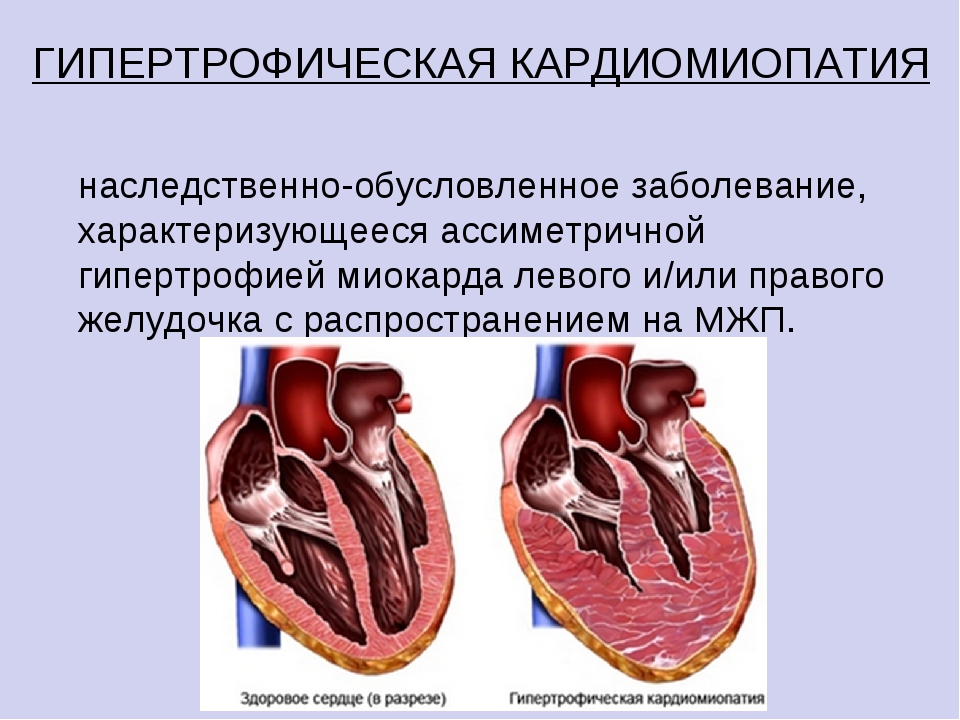
Гипертрофическая кардиомиопатия (ГКМП) — наследственное заболевание, которое передается по аутосомно-доминантному признаку. Это означает, что если один из родителей болен, то вероятность, что заболеет ребенок, составляет 50%.
Генетический дефект возникает при мутации в одном из 10 генов, каждый из которых кодирует синтез сократительных белков в мышечных волокнах миокарда. В сердечной мышце в результате мутаций нарушается расположение волокон, мелкие сосуды сердца сужаются, появляются разрастания соединительной ткани. Такие структурные изменения и называются кардиомиопатией.
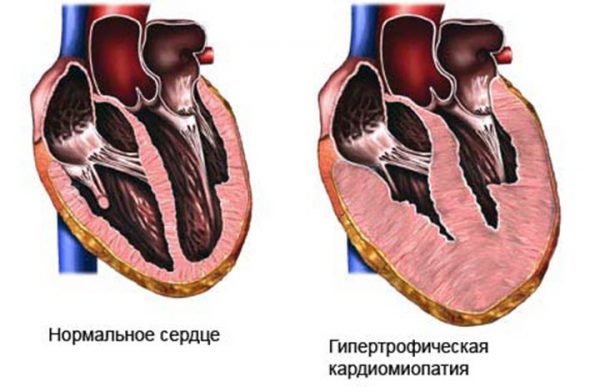
Термин «гипертрофическая» означает, что в результате этих изменений сердце заметно увеличивается. Перегородка между правым и левым желудочками (межжелудочковая перегородка) при этом утолщается – и створка митрального клапана оказывается в опасной близости к ней. В результате затрудняется ток крови из левого желудочка сердца в аорту, и давление в полости левого желудочка повышается. Этот вид кардимиопатии, когда существует препятствие для тока крови, называется обструктивной (obstructio — помеха, преграда).
В результате затрудняется ток крови из левого желудочка сердца в аорту, и давление в полости левого желудочка повышается. Этот вид кардимиопатии, когда существует препятствие для тока крови, называется обструктивной (obstructio — помеха, преграда).
Сердечная мышца, вынужденная бороться с повышенным давлением крови, еще больше утолщается, и в работе сердца начинаются перебои. В конце концов развивается сердечная недостаточность, когда сердце уже не способно справиться с перекачиванием крови.
ГКМП встречается с частотой примерно у 1 из 1000 людей и относится к редким заболеваниям. Мужчины заболевают чаще женщин. Болезнь может обнаружиться в подростковом возрасте, но чаще ее симптомы начинают проявляться после 30 лет.
Диагностика
Строго специфических диагностических и клинических признаков обструктивной ГКМП не существует.
ЭКГ в 12 отведениях может выявить признаки гипертрофии левого желудочка, гипертрофии и перегрузки левого предсердия, нарушение сердечной проводимости и др. Эти признаки можно обнаружить у более чем 90% больных ГКМП. Но, чтобы дифференцировать ГКМП от других сердечно-сосудистых заболеваний, требуются дополнительные обследования:
Эти признаки можно обнаружить у более чем 90% больных ГКМП. Но, чтобы дифференцировать ГКМП от других сердечно-сосудистых заболеваний, требуются дополнительные обследования:
- Фонокардиография – графическая регистрация «шумов» сердца (обычно эту диагностику проводят одновременно с ЭКГ).При ГКМП выявляется патологическое усиление III и IV тонов.
- ЭХО-кардиография.На ней выявляются увеличение стенок левого желудочка и повышение давления в нем.
- Стресс-ЭхоКГиспользуется для выявления коронарной болезни сердца, сопутствующей ГКМП, что позволяет оценить прогноз и назначить правильное лечение.
- Биохимическое исследование крови позволяет дифферинцировать ГКМП от других сердечно-сосудистых заболеваний (липидный спектр – для выявления атеросклероза, биомаркеры некроза миокарда – для диагностики инфаркта миокарда).
- Холтеровское суточное мониторирование ЭКГ обязательно для больных с высоким риском внезапной смерти (обмороки, случаи внезапной смерти в семье) и при признаках недостаточного кровоснабжения сердца.

- Магнитно-резонансная томография (МРТ) – золотой стандарт для оценки распространенности и выраженности гипертрофии миокарда.
- КТ сердца назначается пациентам, у которым противопоказано проведение МРТ, или данные МРТ и ЭХО-кардиографии противоречивы.
- Коронарная ангиография.Её выполняют при ГКМП, осложненной ишемической болезнью сердца, перед оперативным вмешательством – чтобы оценить его объем и возможные осложнения.
- Определение концентрации N-терминального про-мозгового натрийуретического пептида (Nt-proBNP) в плазме. У больных ГКМП его содержание в плазме крови повышено и является показателем тяжести заболевания.
- Генетическая диагностика.Тесты на наличие мутаций в генах MYBPC3, MYH7, TNNI3, TNNT2, TPM1 дают возможность поставить точный диагноз ГКМП. При положительных тестах нужно обследовать близких родственников пациента для исключения диагноза ГКМП.
Cимптомы
Зачастую болезнь развивается бессимптомно и выявляется случайно при плановом ЭКГ. Но иногда ГКМП способна привести к внезапной смерти от остановки сердца, особенно при больших физических нагрузках. Как известно, американский атлет Миклош Фехер – прямо во время матча. Оба они страдали недиагностированной ГКМП с бессимптомным течением.
Но иногда ГКМП способна привести к внезапной смерти от остановки сердца, особенно при больших физических нагрузках. Как известно, американский атлет Миклош Фехер – прямо во время матча. Оба они страдали недиагностированной ГКМП с бессимптомным течением.
Все симптомы ГКМП не являются специфическими, но в любом случае являются поводом немедленно обратиться к кардиологу:
- Загрудинные боли при физической нагрузке,
- Одышка при нагрузке,
- Обмороки.
- Внезапные приступы слабости, ощущение нехватки воздуха.
- Тупая, тянущая, сдавливающая боль в грудной клетке.
Прогноз во многом зависит от формы заболевания и возраста пациента. Он благоприятнее у больных, которые прошли хирургическое лечение.
Лечение
К настоящему моменту специфического лечения ГКМП, которое устраняло бы генетические дефекты, не существут. Однако ученые разрабатывают методы генной терапии этого заболевания.
Сейчас основная цель лечения – уменьшить тяжесть симптомов и замедлить течение болезни, улучшить качество и увеличить продолжительность жизни больных, предупредить внезапную смерть. Для этого в первую очередь используются возможности лекарственной терапии.
Для этого в первую очередь используются возможности лекарственной терапии.
Основными препаратами являются β-адреноблокаторы, которые уменьшают силу сокращения сердца (обзидан, анаприлин). Если к их назначению есть противопоказания или их эффект недостаточен, то назначаются блокаторы кальциевых каналов (препарат выбора — верапамил). Специалисты пока не пришли к единому выводу, стоит ли назначать β-адреноблокаторы при бессимптомном течении ГКМП. Врач принимает решение в каждом конкретном случае, в зависимости от множества факторов.
Для лечения аритмий используются антиаритмические препараты. Лучший препарат, применение которого действительно снижает частоту внезапной смерти и улучшает прогноз заболевания — амиодарон.
Диуретики и вазодилататоры (нитроглицерин, натрия нитропруссид) при ГКМП не назначаются.
Основной метод хирургического лечения ГКМП – это чрезаортальная септальная миэктомия по A. Morrow: в основании утолщенной межжелудочковой перегородки иссекается участок ткани. В результате давление внутри левого желудочка нормализуется или значительно снижается. Одномоментно, если к тому есть показания, делается реконструкция или протезирование митрального клапана. Операция показана молодым пациентам, при значительном повышении давления в левом желудочке, с осложнениями в виде патологии митрального клапана, коронарных артерий, врожденных пороках сердца. Пятилетняя выживаемость больных составляет, в среднем, 91%, 10-летняя – 83%.
В результате давление внутри левого желудочка нормализуется или значительно снижается. Одномоментно, если к тому есть показания, делается реконструкция или протезирование митрального клапана. Операция показана молодым пациентам, при значительном повышении давления в левом желудочке, с осложнениями в виде патологии митрального клапана, коронарных артерий, врожденных пороках сердца. Пятилетняя выживаемость больных составляет, в среднем, 91%, 10-летняя – 83%.
В НЦССХ им. А. Н. Бакулева разработана оригинальная методика операции, которая применяется в случаях, когда препятствия для тока крови и увеличение давления есть в обоих желудочках.
У пожилых пациентов, когда оперативное вмешательство слишком опасно, применяется транскатетерная алкогольная септальная аблация – искусственный инфаркт утолщенного отдела межжелудочковой перегородки. В ветвь коронарной артерии вводится несколько миллилитров 95-процентного этилового спирта, в результате толщина перегородки уменьшается.
Операции при ГКМП относятся к высокотехнологичной медицинской помощи.
Широко применяемый в недавнем прошлом метод последовательной двухкамерной электрокардиостимуляции не подтвердил своей эффективности и в наше время применяется редко.
Как с этим жить
ГКМП, чаще всего, прогрессирует медленно. Чтобы жить с этим заболеванием полноценно и долго, необходимо смириться с ограничениями в образе жизни и тщательно выполнять предписания врачей.
Если в семье уже есть человек, страдающий ГКМП, то прямые родственники по восходящей и нисходящей линии (родители, дети, братья и сестры) должны пройти обследование. Диагноз будет абсолютно достоверным, если он подтвержден генетическим тестом.
При стабильном доброкачественном течении заболевания пациент и его близкие могут потерять бдительность. Необходимо бережно относиться к больному сердцу и избегать физического напряжения (показатель – появление одышки). Занятия спортом однозначно запрещаются. Работа не должна вызывать физического и умственного переутомления. Нельзя работать на высоте, у движущихся механизмов (чтобы в случае внезапной потери сознания не навредить себе и другим). Запрещена работа, связанная с постоянной и длительной ходьбой.
Нельзя работать на высоте, у движущихся механизмов (чтобы в случае внезапной потери сознания не навредить себе и другим). Запрещена работа, связанная с постоянной и длительной ходьбой.
При быстро прогрессирующем течении заболевания, плохом прогнозе, риске внезапной сердечной смерти, тромбоэмболических осложнениях (инсульт, эмболический инфаркт миокарда, эмболии почечной артерии и крупных периферических сосудов) медико-санитарная экспертиза может установить инвалидность II и III степени.
Женщины с ГКМП при желании иметь ребенка должны пройти углубленное обследование. При легкой или умеренной симптоматике, которая хорошо контролируется медикаментами, беременность не представляет опасности для здоровья матери и ребенка. Во время беременности необходим постоянный мониторинг показателей сердечной деятельности. В случае, если течение ГКМП осложняется сердечной недостаточностью, беременность может привести к резкому ухудшению состояния и летальному исходу.
Полезные сайты
Куда обратиться
- Филатовская детская больница, отделение кардиохирургии и интенсивной терапии http://www.
 childheart.ru/ (для детей)
childheart.ru/ (для детей) - Отделение кардиохирургии ДКБ N 1 (Санкт-Петербург) http://www.cardiospb.ru/ (для детей)
- Федеральное государственное бюджетное научное учреждение «Томский национальный исследовательский медицинский центр РАН», «Научно-исследовательский институт кардиологии» 8 (3822) 56-58-30 (отдел госпитализации) e-mail: [email protected] (для детей)
- Морозовская детская городская клиническая больница http://xn--90adclrioar.xn--p1ai/kontakty/ (для детей)
- ФГБУ «НМИЦ им. В. А. Алмазова» Минздрава России http://www.almazovcentre.ru/ (для детей и взрослых)
- Федеральный медицинский научный центр кардиологии МЗ РФ (им.А.Л.Мясникова) https://www.cardioweb.ru/ (для взрослых)
- Научный центр сердечно-сосудистой хирургии им.А.Н.Бакулева https://bakulev.ru/ (для взрослых)
- Благотворительный фонд «Детские сердца» — адресная помощь детям с врожденными заболеваниями сердца — https://www.detis.ru/
- Благотворительный фонд «Краблик» www.
 korablik-fond.ru
korablik-fond.ru - Благотворительный Фонд помощи тяжело больным детям, сиротам и инвалидам «РУСФОНД» (Русфонд.Сердце) https://www.rusfond.ru/list-intro/04#text
- Благотворительный фонд «Путь к сердцу» — помощь детям и взрослым с болезнями сердца https://fond.pravmir.ru/causes/put-k-serdtsu/
- Межрегиональная благотворительная организация инвалидов «Союз пациентов и пациентских организаций по редким заболеваниям» http://spiporz.ru/
- Всероссийское общество орфанных заболевний http://www.rare-diseases.ru/about
Первый опыт расширенной миоэктомии при хирургическом лечении обструктивной гипертрофической кардиомиопатии: непосредственные и промежуточные результаты | Богачев-Прокофьев
Литература
Rick A. Nishimura, Steve R. Ommen. Septal Reduction Therapy for Obstructive Hypertrophic Cardiomyopathy and Sudden Death: What Statistics Cannot Tell You // Circ. Cardiovasc. Interv. 2010. Vol. 3. P. 91–93.
Robert A. Leonardi, Evan P. Kransdorf, David L. Simel and Andrew Wang. Meta-Analyses of Septal Reduction Therapies for Obstructive Hypertrophic Cardiomyopathy Comparative Rates of Overall Mortality and Sudden Cardiac Death After Treatment // Circ. Cardiovasc. Interv. 2010. Vol. 3. P. 97–104.
Kransdorf, David L. Simel and Andrew Wang. Meta-Analyses of Septal Reduction Therapies for Obstructive Hypertrophic Cardiomyopathy Comparative Rates of Overall Mortality and Sudden Cardiac Death After Treatment // Circ. Cardiovasc. Interv. 2010. Vol. 3. P. 97–104.
A report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. 2011 ACCF/AHA guideline for the diagnosis and treatment of hypertrophic cardiomyopathy // J. Thorac. Cardiovasc. Surg. 2011. Vol. 142. P. 153–203.
Morrow A.F. Hypertrophic subaortic stenosis. Operative methods utilized to relieve left ventricular outflow obstruction // J. Thorac. Cardiovasc. Surg. 1978. Vol. 76. P. 423–30.
Balaram S.K., Sherrid M.V., Derose J.J. Jr., Hillel Z., Winson G, Swistel D.G. Beyond extended myectomy for hypertrophic cardiomyopathy: resection-plication-release (RPR) repair // Ann. Thorac. Surg. 2005. Vol. 80. P. 217–23.
Cooley D.A. Surgical technique for hypertrophic left ventricular obstructive myopathy including mitral valve plication // J.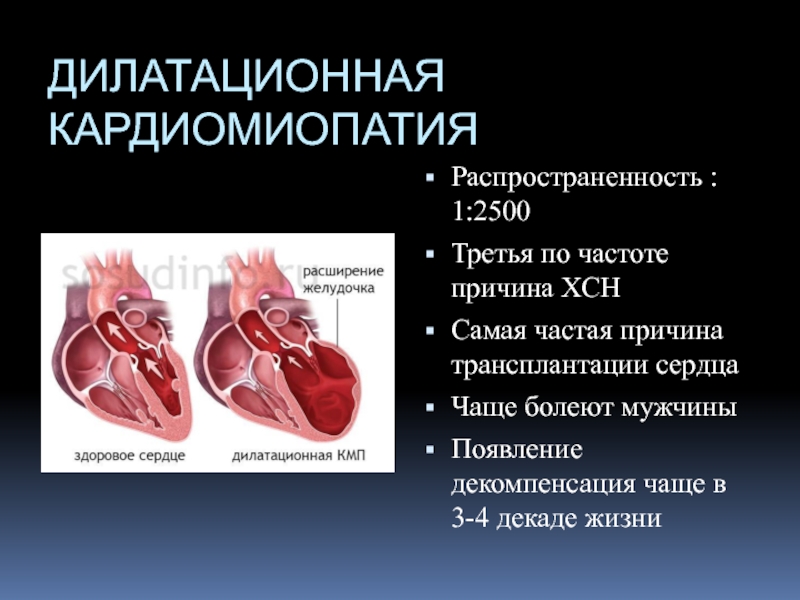 Cardiac.Surg. 1991. Vol. 6. P. 29–33.
Cardiac.Surg. 1991. Vol. 6. P. 29–33.
Maslow A.D., Regan M.M., Haering J.M., Johnson R.G., Levine R.A. Echocardiographic predictors of left ventricular outflow tract obstruction and systolic anterior motion of the mitral valve after mitral valve reconstruction for myxomatous valve disease // J. Am. Coll. Cardiol. 1999. Vol. 34. P. 2096–104.
Lee K.S., Stewart W.J., Lever H.M., Underwood P.L., Cosgrove D.M. Mechanism of outflow tract obstruction causing failed mitral valve repair. Anterior displacement of leaflet coaptation //Circulation. 1993. Vol. 88. P. II24–9.
Kaple R.K., Murphy R.T., DiPaola L.M., et al. Mitral valve abnormalities in hypertrophic cardiomyopathy: echocardiographic features and surgical outcomes // Ann. Thorac. Surg. 2008. Vol. 85. P. 1527–35, 1535.e1–2.
Balaram S.K., Tyrie L., Sherrid M.V., et al. Resection-plicationrelease for hypertrophic cardiomyopathy: clinical and echocardiographic follow-up // Ann. Thorac. Surg. 2008. Vol. 86. P. 1539–44.
Schaff H. V., Suri R.M., Enriquez-Sarano M. Indications for surgery in degenerative mitral valve disease // Semin. Thorac. Cardiovasc. Surg. 2007. Vol. 19. P. 97–102.
V., Suri R.M., Enriquez-Sarano M. Indications for surgery in degenerative mitral valve disease // Semin. Thorac. Cardiovasc. Surg. 2007. Vol. 19. P. 97–102.
Enriquez-Sarano M., Avierinos J.F., Messika-Zeitoun D., et al. Quantitative determinants of the outcome of asymptomatic mitral regurgitation // N. Engl. J. Med. 2005. Vol. 352. P. 875–83.
Calvin K.N. Wan, Joseph A. Dearani, Thoralf M. Sundt, et al. What Is the Best Surgical Treatment for Obstructive Hypertrophic Cardiomyopathy and Degenerative Mitral Regurgitation? // Ann. Thorac. Surg. 2009. Vol. 88. P. 727–32.
Minakata K., Dearani J.A., Nishimura R.A., et al. Extended septal myectomy for hypertrophic obstructive cardiomyopathy with anomalous mitral papillary muscles or chordae // J. Thorac. Cardiovasc. Surg. 2004. Vol. 127. P. 481–9
Железнев С.И., Богачев-Прокофьев А.В., Емешкин М.И., Караськов А.М. Отдаленные результаты хирургического лечения фибрилляции предсердий у больных с приобретенными пороками митрального клапана // Патология кровообращения и кардиохирургия.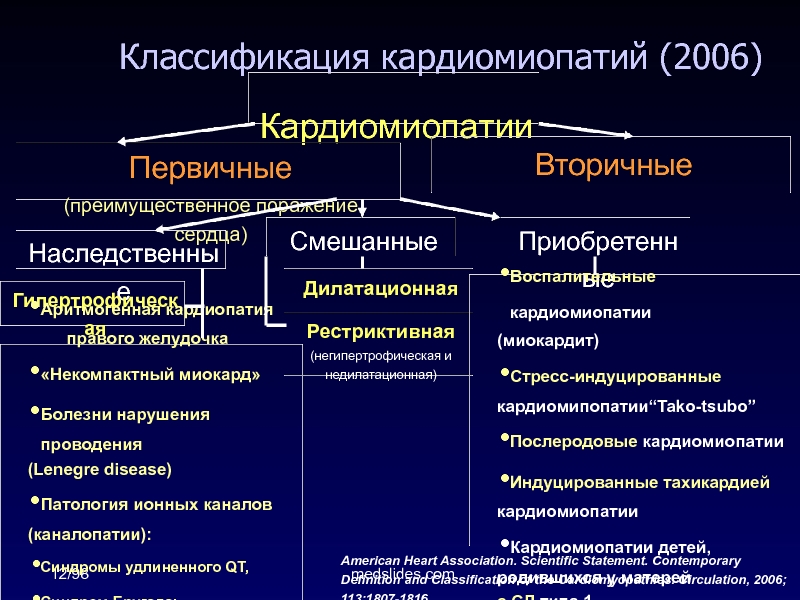 2014. № 1. С. 5–10.
2014. № 1. С. 5–10.
Тулеутаев Р.М., Богачев-Прокофьев А.В., Железнев С.И., АфанасьевА.В., Караськов А.М. Обратное ремоделирование левых камер сердца после реконструкции митрального клапана при мезенхимальной дисплазии // Патология кровообращения и кардиохирургия. 2015. Т. 19, № 1. С. 66–71.
Sandhya K. Balaram, Ronald E. Ross, Mark V. Sherrid, Gary S. Schwartz, Zak Hillel, Glenda Winson, and Daniel G. Swistel. Role of Mitral Valve Plication in the Surgical Management of Hypertrophic Cardiomyopathy // Ann. Thorac. Surg. 2012. Vol. 94. P. 1990–1998.
Дилатационная кардиомиопатия
Кардиомиопатии -это первичные поражения мышцы сердца невоспалительного характера.
Формы кардиомиопатий: гипертрофическая, дилатационная и рестриктивная. Гипертрофическая кардиомиопатия — ГКМП: обструктивная и необструктивная, дилатационная кардиомиопатия — ДКМП- еще называется застойная. Рестриктивная кардиомиопатия — РКМП-встречается редко.
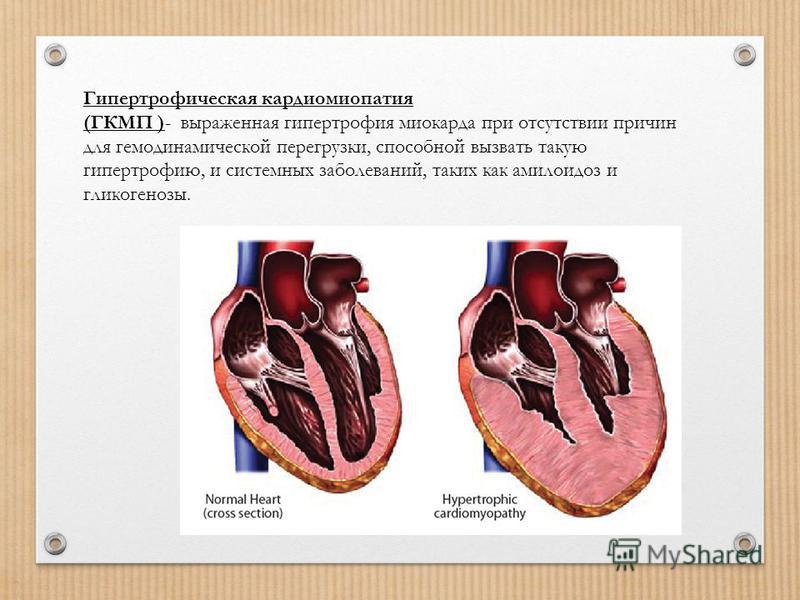
Гипертрофическая кардиомиопатия (ГКМП) характеризуется выраженной (более 15 мм) гипертрофией миокарда левого желудочка, утолщением межжелудочковой перегородки (МЖП), или только верхушки сердца, в редких случаях-гипертрофией правого желудочка. Обструктивная ГКМП развивается, если сужаются пути оттока левого желудочка и развивается стеноз аортального отверстия .
Дилатационная кардиомиопатия — поражение миокарда, которое характеризуется расширением всех полостей сердца, нарушением сократительной функции миокарда. ДКМП проявляется застойной сердечной недостаточностью, тромбоэмболическим синдромом, нарушениями ритма сердца. Диагностика основывается на клинической картине, ЭКГ, ЭхоКГ, рентгенографии, МРТ, сцинтиграфии, биопсии миокарда). В кардиологии дилатационной кардиомиопатии существует около 60% от всех кардиомиопатий. ДКМП чаще возникает в возрасте 20−50 лет. Среди заболевших преобладают мужчины (60−90%).
Определяют несколько причин дилатационной кардиомиопатии: наследственная, токсическая, метаболическая, аутоиммунная, вирусная. В 20−30% случаев ДКМП является семейным заболеванием (синдром Барта). Этот синдром имеет неблагоприятное течение, кроме дилатационной кардиомиопатии, характеризуется миопатиями, сердечной недостаточностью, фиброэластозом эндокарда, задержкой роста, пиодермиями.
В 20−30% случаев ДКМП является семейным заболеванием (синдром Барта). Этот синдром имеет неблагоприятное течение, кроме дилатационной кардиомиопатии, характеризуется миопатиями, сердечной недостаточностью, фиброэластозом эндокарда, задержкой роста, пиодермиями.
В анамнезе у трети пациентов с дилатационной кардиомиопатией — злоупотребление алкоголем. Этанол токсично воздействует на миокард, повреждает митохондрии, уменьшает синтез сократительных белков, образует свободные радикалы, а также нарушает метаболизм в клетках сердца-кардиомиоцитах. Также из токсических факторов можно выделить профессиональный контакт с аэрозолями, красками, промышленной пылью, металлами.
Недостаточность питания, дефицит белка, гиповитаминоз витамина В1, нехватка селена, дефицит карнитина также усугубляют развитие ДКМП .
Доказаны теории развития ДКМП- метаболическая, аутоимунная, вирусная (энтеровирус, аденовирус, вирус герпеса, цитомегаловирус). Часто дилатационная кардиомиопатия- исход вирусного миокардита.
Факторами риска послеродовой дилатационной кардиомиопатии считаются возраст старше 30 лет, негроидная раса, наличие в анамнезе более 3-х родов, поздний токсикоз беременности, многоплодная беременность.
В редких случаях причины дилатационной кардиомиопатии неизвестны (идиопатическая дилатационная кардиомиопатия), вероятно, имеет значение генетическая предрасположенность.
Патогенез дилатационной кардиомиопатии:
Под действием определенных факторов снижается количество полноценных кардиомиоцитов, что ведёт расширению полостей сердца и снижению насосной функции миокарда. Это приводит к диастолической и систолической дисфункции желудочков, развивается застойная сердечная недостаточность в малом, а затем и в большом круге кровообращения.
Сначала увеличивается ЧСС, уменьшается периферическое сопротивление. Затем истощается миокард, нарастает систолическая дисфункция, уменьшается минутный и ударный объем, нарастает конечное диастолическое давление в левом желудочке развивается относительная митральная и трикуспидальная недостаточность.
Снижается сердечный выброс, уменьшается почечная перфузия, активизируются симпатическая нервная и ренин-ангиотензиновая системы. Из-за выброса катехоламинов возникает тахикардия, аритмия. Развивается периферическая вазоконстрикция, происходит задержка ионов натрия, увеличивается ОЦК, развиваются отеки. У части пациентов в полостях сердца формируются пристеночные тромбы, которые впоследствии вызывают тромбоэмболический синдром.
Симптомы дилатационной кардиомиопатии:
ДКМП развивается постепенно. Длительное время у пациентов жалобы могут отсутствовать. Реже она возникает подостро, после пневмонии, бронхита или ОРВИ. Синдромами дилатационной кардиомиопатии являются сердечная недостаточность, нарушения ритма и проводимости, а также тромбоэмболии.
Клиника дилатационной кардиомиопатии :
- одышка;
- быстрая утомляемость;
- ортопноэ;
- сухой кашель и удушье.
У некоторых пациентов жалобы на ангинозные боли — это приступы стенокардии. Появляется тяжесть в правом подреберье, отеки ног, асцит из-за застойных явлений в большом круге кровообращения .
Появляется тяжесть в правом подреберье, отеки ног, асцит из-за застойных явлений в большом круге кровообращения .
При нарушениях ритма и проводимости возникают головокружение, синкопальные состояния. Как осложнение может возникнуть ишемический инсульт, ТЭЛА, что может явиться причиной внезапной смерти больных. Риск эмболии увеличивается при мерцательной аритмии.
Течение заболевания может быть быстро прогрессирующим, медленно прогрессирующим, рецидивирующим. При быстро прогрессирующем варианте дилатационной кардиомиопатии терминальная стадия сердечной недостаточности наступает в течение 1,5 лет от появления первых признаков заболевания. Чаще всего встречается медленно прогрессирующее течение.
Диагностика дилатационной кардиомиопатии:
Признаки дилатационной кардиомиопатии — кардиомегалия, тахикардия, ритм галопа, шумы относительной недостаточности митрального и трикуспидального клапанов. Увеличивается Ч. Д., появляются застойные хрипы в нижних отделах легких, набухают вены шеи, увеличивается печень .
На ЭКГ — перегрузка и гипертрофия левых отделов сердца, нарушения ритма по типу мерцательной аритмии, нарушения проводимости по типу блокады левой ножки пучка Гиса, АВ — блокады. По Холтеру определяются угрожающие для жизни аритмии .
По Эхокардиографии можно обнаружить основные признаки дилатационной кардиомиопатии — расширение полостей сердца, снижение фракции выброса левого желудочка, обнаруживаются пристеночные тромбы и оценивается риск развития тромбоэмболии.
На рентгене выявляется увеличение размеров сердца, признаки легочной гипертензии, гидроперикард. МРТ, ПЭТ, сцинтиграфия выполняются для оценки структурных изменений и сократимости миокарда. Биопсия миокарда берется для дифференциальной диагностики ДКМП с другими заболеваниями.
Лечение дилатационной кардиомиопатии:
Лечебная тактика заключается в коррекции сердечной недостаточности, нарушений ритма. Рекомендуется постельный режим, ограничивается потребление соли и жидкости .
Медикаментозно назначают ингибиторы АПФ (эналаприла, каптоприла, и др. ), диуретики (фуросемид), при нарушениях ритма сердца — b-адреноблокаторы (карведилол, метопролол, бисопролол), сердечные гликозиды (дигоксин), для снижения притока крови к правым отделам сердца-пролонгированные нитраты.
), диуретики (фуросемид), при нарушениях ритма сердца — b-адреноблокаторы (карведилол, метопролол, бисопролол), сердечные гликозиды (дигоксин), для снижения притока крови к правым отделам сердца-пролонгированные нитраты.
Профилактика тромбоэмболических осложнений проводится антикоагулянтами. Радикальное лечение дилатационой кардиомиопатии -трансплантация сердца.
Прогноз и профилактика дилатационной кардиомиопатии:
Чаще течение дилатационной кардиомиопатии неблагоприятное. Средняя продолжительность жизни около 4−7 лет после появления симптомов сердечной недостаточности.
Профилактика дилатационной кардиомиопатии: медико-генетическое консультирование, лечение респираторных инфекций, сбалансированное питание, отсутствие алкоголя.
Берегите себя!
Гипертрофическая кардиомиопатия: причины. Симптомы и лечение
Обзор
Гипертрофическая кардиомиопатия (ГКМ) — это заболевание, которое поражает сердечную мышцу, вызывая ее увеличение или «гипертрофию».
В Семейном институте сердца, сосудов и грудной клетки Миллера клиники Кливленда мы проявляем особый интерес к лечению гипертрофической кардиомиопатии (ГКМП).С 1978 года мы вылечили сотни пациентов, и их число с каждым годом увеличивается.
Что такое гипертрофическая кардиомиопатия (ГКМП)?
Гипертрофическая кардиомиопатия (ГКМП) — это сложный тип сердечного заболевания, поражающего сердечную мышцу. Это вызывает утолщение сердечной мышцы (особенно желудочков или нижних камер сердца), жесткость левого желудочка, изменения митрального клапана и клеточные изменения.
Утолщение сердечной мышцы (миокарда) чаще всего происходит в области перегородки.Перегородка — это мышечная стенка, разделяющая левую и правую стороны сердца. Проблемы возникают, когда перегородка между нижними камерами сердца или желудочками утолщается. Утолщенная перегородка может вызвать сужение, которое может блокировать или уменьшать кровоток от левого желудочка к аорте — состояние, называемое «обструкцией оттока». Желудочки должны работать сильнее, чтобы преодолеть сужение или закупорку. Этот тип гипертрофической кардиомиопатии можно назвать гипертрофической обструктивной кардиомиопатией (ГОКМ).
Желудочки должны работать сильнее, чтобы преодолеть сужение или закупорку. Этот тип гипертрофической кардиомиопатии можно назвать гипертрофической обструктивной кардиомиопатией (ГОКМ).
HCM также может вызывать утолщение в других частях сердечной мышцы, таких как нижняя часть сердца, называемая верхушкой, правым желудочком или во всем левом желудочке.
Нормальное сердце
Жесткость в левом желудочке возникает в результате клеточных изменений, которые происходят в сердечной мышце при ее утолщении. Левый желудочек не может нормально расслабиться и наполняться кровью. Поскольку в конце наполнения остается меньше крови, к органам и мышцам перекачивается меньше крови, богатой кислородом.Жесткость левого желудочка вызывает повышение давления в сердце и может привести к симптомам, описанным ниже.
Изменения митрального клапана: Сужение выходного тракта левого желудочка нарушает правильную функцию митрального клапана, что приводит к обструкции оттока и повышению давления в левом желудочке.
Обструкция является результатом удара митрального клапана о перегородку. Когда это происходит, митральный клапан часто протекает, в результате чего кровь возвращается в левое предсердие.
Клеточные изменения, или изменения в клетках сердечной мышцы, происходят при ГКМП. Под микроскопом клетки кажутся неорганизованными и нерегулярными (так называемый «беспорядок»), а не организованными и параллельными. Этот беспорядок может вызвать изменения в электрических сигналах, проходящих через нижние камеры сердца, и привести к желудочковой аритмии (разновидность нарушения сердечного ритма).
Неорганизованная структура
Нормальный образец ячеек
Кто страдает гипертрофической кардиомиопатией (ГКМП)?
Гипертрофическая кардиомиопатия поражает примерно 600 000: 1.5 миллионов американцев, или каждый 500 человек. Это более распространено, чем рассеянный склероз, которым страдает каждый 700 человек.
Симптомы и причины
Что вызывает гипертрофическую кардиомиопатию (ГКМП)?
- HCM может передаваться по наследству из-за отклонения от нормы в гене, который кодирует характеристики сердечной мышцы.Есть много генов, которые могут вызвать HCM. При наличии генного дефекта тип развивающейся HCM сильно варьируется в семье. Кроме того, у некоторых людей, у которых есть ген HCM, болезнь может никогда не развиться.
- Гипертрофия может быть приобретена в результате высокого кровяного давления или старения.
- В других случаях причина гипертрофии и ГКМП неизвестна.
Поскольку причины HCM различны, часто бывает трудно определить группу высокого риска.
Какие состояния связаны с гипертрофической кардиомиопатией (ГКМП)?
Многие люди с HCM живут нормальной жизнью и не имеют проблем со здоровьем.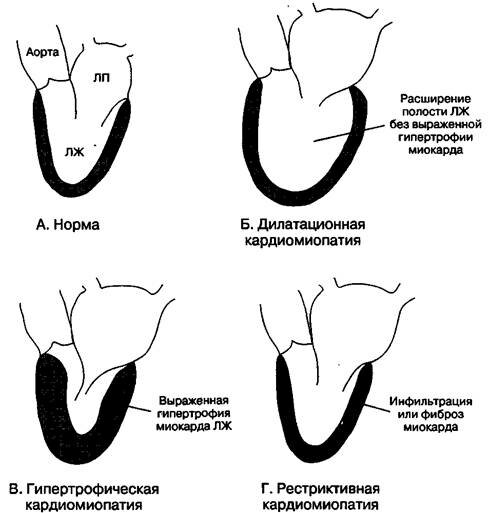
У других людей с HCM могут развиться сердечные заболевания, которые сокращают продолжительность жизни или снижают качество жизни человека, в том числе:
- Внезапная остановка сердца и внезапная сердечная смерть: Внезапная остановка сердца — это внезапная потеря функции сердца, вызванная опасно учащенным сердечным ритмом, называемым желудочковой тахикардией. Если неотложное лечение, включая СЛР и дефибрилляцию, не начато сразу после появления симптомов, может произойти внезапная сердечная смерть.
Большинство людей с HCM имеют низкий риск внезапной сердечной смерти.Однако ГКМП является наиболее частой причиной внезапной сердечной смерти у людей в возрасте до 30 лет. ГКМП, возможно, наиболее известен своей ролью в остановке сердца и последующей смерти у некоторых молодых профессиональных спортсменов.
- Сердечная недостаточность: Состояние, при котором насосная мощность сердца ниже, чем обычно.
Сопутствующие симптомы
Симптомы, связанные с наличием желудочковой тахикардии или сердечной недостаточности, включают:
- Боль в груди или давление, которое обычно возникает при физических упражнениях или физической активности, но также может возникать во время отдыха или после еды.

- Одышка и утомляемость, особенно при физической нагрузке. Эти симптомы чаще встречаются у взрослых с гипертрофической кардиомиопатией и, скорее всего, вызваны резервным давлением в левом предсердии и легких.
- Обморок (обморок или потеря сознания) может повлиять на пациентов с HCM. Обморок при ГКМП может быть вызван нерегулярным сердечным ритмом, аномальной реакцией кровеносных сосудов во время упражнений или может быть не обнаружено никакой причины.
- Сердцебиение (трепетание в груди) из-за нарушений сердечного ритма (аритмии), таких как фибрилляция предсердий или желудочковая тахикардия.Фибрилляция предсердий встречается примерно у 25% больных ГКМП и увеличивает риск образования тромбов и сердечной недостаточности.
Диагностика и тесты
Как диагностируется гипертрофическая кардиомиопатия (ГКМП)?
Диагноз HCM основан на:
- История болезни: Ваш врач задаст вам вопросы о ваших симптомах и семейном анамнезе.

- Осмотр: Ваш врач послушает ваше сердце и легкие. У пациентов с гипертрофической обструктивной кардиомиопатией (HOCM) может быть шум в сердце.
- Тесты: Эхокардиограмма — это наиболее распространенный тест, используемый для диагностики ГКМП, так как характерное утолщение стенок сердца обычно видно на эхосигнале. Другие тесты могут включать анализы крови, электрокардиограмму, рентген грудной клетки, эхо-тест с физической нагрузкой, катетеризацию сердца и магнитно-резонансную томографию (МРТ).
Ведение и лечение
Тип назначаемого лечения HCM зависит от:
- Имеется ли сужение оттока (путь, по которому кровь выходит из сердца)
- Как работает сердце
- Симптомы пациента
- Возраст и уровень активности пациента
- Наличие аритмий
Лечение направлено на минимизацию или предотвращение симптомов и снижение риска осложнений, таких как сердечная недостаточность и внезапная сердечная смерть.
Лечение включает выявление рисков и регулярное наблюдение, изменение образа жизни, прием лекарств и процедур по мере необходимости.
Скрининг и идентификация рисков
Проверка
Гипертрофическая кардиомиопатия (ГКМП) — это заболевание, которое может передаваться из поколения в поколение. Для вас или членов вашей семьи важно пройти обследование, если у вас есть родственник первой степени родства с этим заболеванием. Ближайшие родственники — это ваши родители, братья, сестры и дети.
Первый шаг — сделать электрокардиограмму (ЭКГ) и эхокардиограмму (эхо), чтобы проверить свое сердце.
Если результаты теста показывают признаки гипертрофической кардиомиопатии, вам необходимо обратиться к кардиологу, специализирующемуся на ГКМП. Чтобы получить список врачей клиники Кливленда, которые лечат пациентов с этим заболеванием, посетите наш Центр гипертрофической кардиомиопатии.
Если результаты ваших анализов нормальные, мы предлагаем повторное эхо-исследование и ЭКГ каждые три года, пока вам не исполнится 30 лет, а затем каждые 5 лет.
Риск внезапной сердечной смерти
Большинство людей с ГКМП имеют низкий риск внезапной сердечной смерти. Тем не менее, важно выявить небольшое количество пациентов с ГКМП, которые имеют более высокий риск внезапной сердечной смерти, чтобы можно было принять профилактические меры.
К людям с ГКМП, имеющим более высокий риск внезапной сердечной смерти, относятся:
- Пациенты, у которых в семейном анамнезе была внезапная сердечная смерть
- Молодые пациенты, перенесшие несколько эпизодов обморока (обморока)
- Пациенты, у которых наблюдается ненормальная реакция артериального давления на упражнения
- Пациенты с аритмией в анамнезе с учащенным сердечным ритмом
- Пациенты с тяжелыми симптомами и нарушением функции сердца
Ваш врач может обсудить ваш личный риск.Если у вас есть два или более фактора риска внезапной смерти, ваш врач может назначить профилактическое лечение, такое как антиаритмические препараты или имплантируемый кардиовертер-дефибриллятор (ICD), чтобы снизить ваш риск.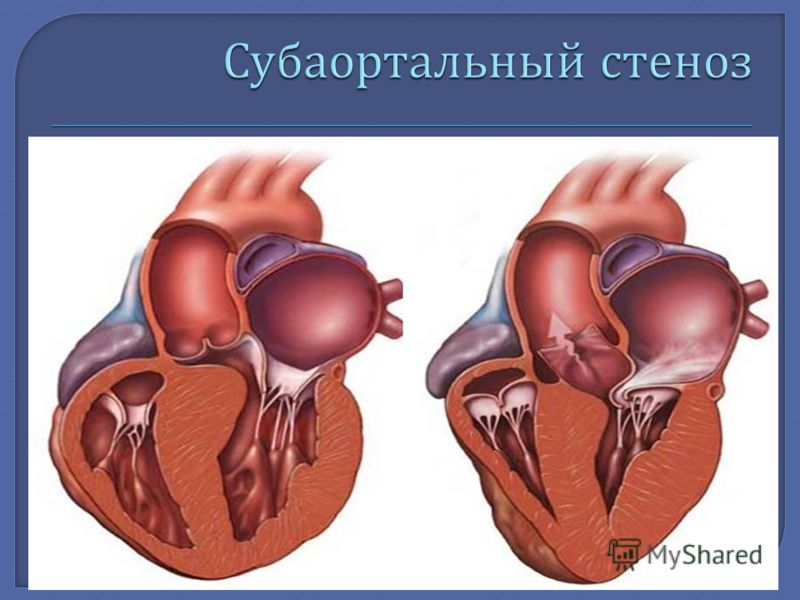
Лекарства
Лекарства часто назначают для лечения симптомов и предотвращения дальнейших осложнений. Лекарства, такие как бета-блокаторы и блокаторы кальциевых каналов, расслабляют сердечную мышцу, позволяя ей лучше наполняться и перекачивать кровь более эффективно. При необходимости могут быть прописаны другие лекарства, чтобы контролировать частоту сердечных сокращений или уменьшить частоту аритмий.
Вам могут посоветовать избегать некоторых лекарств, таких как нитраты, потому что они снижают кровяное давление, или дигоксина, потому что он увеличивает силу сокращения сердца.
Антибиотики могут быть прописаны для снижения риска бактериального эндокардита, потенциально опасного для жизни состояния (см. Другие меры предосторожности, перечисленные на следующей странице).
Процедуры
Процедуры лечения гипертрофической обструктивной кардиомиопатии включают миэктомию перегородки, абляцию этанолом, имплантируемый кардиовертер-дефибриллятор (ИКД) и, при необходимости, лечение сердечной недостаточности.
Миэктомия перегородки
Во время миэктомии перегородки, хирургической процедуры, хирург удаляет небольшую часть утолщенной перегородки, чтобы расширить отток крови (путь, по которому проходит кровь) от левого желудочка до аорты. Миэктомия рассматривается, когда лекарства не эффективны при лечении ГКМП. Это часто устраняет регургитацию митрального клапана.
Абляция этанолом
Эта процедура, также называемая аблацией перегородки, предназначена для пациентов, которые не соответствуют критериям для проведения миэктомии перегородки.Процедура абляции проводится в лаборатории катетеризации сердца.
Во-первых, во время процедуры катетеризации сердца располагается малая коронарная артерия, которая снабжает кровоток верхней частью перегородки. В артерию вводится баллонный катетер и надувается. Контрастное вещество вводится, чтобы определить местонахождение утолщенной стенки перегородки, которая сужает проход от левого желудочка к аорте.
При обнаружении выпуклости через катетер вводится небольшое количество чистого спирта. Спирт убивает клетки при контакте, в результате чего перегородка сокращается до более нормальных размеров в течение следующих месяцев, расширяя проход для кровотока.
Спирт убивает клетки при контакте, в результате чего перегородка сокращается до более нормальных размеров в течение следующих месяцев, расширяя проход для кровотока.
Имплантируемые кардиовертер-дефибрилляторы (ICD)
ИКД рекомендованы людям с риском угрожающих жизни аритмий или внезапной сердечной смерти. ИКД — это небольшое устройство, которое помещается прямо под кожу и подключается к проволочным выводам, которые проходят через вену к сердцу. ИКД постоянно контролирует сердечный ритм.Когда он обнаруживает очень быстрый, ненормальный сердечный ритм, он доставляет энергию (небольшой, но мощный разряд) в сердечную мышцу, чтобы сердце снова билось в нормальном ритме. Ваш врач скажет вам, рекомендуется ли использовать ИКД.
Изменения образа жизни
Определенные изменения образа жизни, перечисленные ниже, необходимы для правильного ведения HCM.
- Ограничение количества жидкости и натрия может потребоваться некоторым пациентам при наличии симптомов сердечной недостаточности.
 Спросите своего врача о конкретных рекомендациях по употреблению жидкости и диете, включая информацию об алкогольных напитках и продуктах с кофеином.
Спросите своего врача о конкретных рекомендациях по употреблению жидкости и диете, включая информацию об алкогольных напитках и продуктах с кофеином. - Упражнение. Ваш врач обсудит с вами рекомендации по упражнениям. Большинство людей с гипертрофической кардиомиопатией могут заниматься неконкурентной аэробной нагрузкой. Не рекомендуется поднимать тяжести и заниматься многими видами спорта высокой интенсивности.
- Регулярные контрольные посещения. Пациенты с ГКМП должны регулярно посещать своего кардиолога, как рекомендовано, для наблюдения за своим состоянием.
- Снижение риска заражения. См. Ниже меры предосторожности, которые следует предпринять, если вы подвержены риску развития инфекционного эндокардита.
Меры предосторожности при инфекционном эндокардите
Если у вас ГКМП, у вас повышенный риск развития бактериального или инфекционного эндокардита.
Бактериальный или инфекционный эндокардит — это инфекция сердечных клапанов или внутренней оболочки сердца (эндокарда). Это происходит, когда микробы (особенно бактерии, но иногда грибки и другие микробы) попадают в кровоток и атакуют внутреннюю оболочку сердца или сердечные клапаны. Бактериальный эндокардит вызывает разрастания или отверстия на клапанах или рубцевание клапанной ткани, что чаще всего приводит к утечке сердечного клапана.Без лечения бактериальный эндокардит может быть смертельным заболеванием.
Это происходит, когда микробы (особенно бактерии, но иногда грибки и другие микробы) попадают в кровоток и атакуют внутреннюю оболочку сердца или сердечные клапаны. Бактериальный эндокардит вызывает разрастания или отверстия на клапанах или рубцевание клапанной ткани, что чаще всего приводит к утечке сердечного клапана.Без лечения бактериальный эндокардит может быть смертельным заболеванием.
Чтобы снизить риск
- Соблюдайте правила гигиены полости рта каждый день. Позаботьтесь о своих зубах и деснах: каждые шесть месяцев обращайтесь за профессиональной стоматологической помощью, регулярно чистите зубы щеткой и зубной нитью и следите за тем, чтобы протезы подходили правильно.
- Позвоните своему врачу, если у вас есть симптомы инфекции, включая жар выше 100 градусов по Фаренгейту; пот или озноб; кожная сыпь; боль, нежность, покраснение или припухлость; рана или порез, которые не заживают; красная, теплая или дренирующая рана; боль в горле, першение в горле или боль при глотании; дренаж носовых пазух, заложенность носа, головные боли или болезненность вдоль верхних скул; стойкий сухой или влажный кашель, который длится более двух дней; белые пятна во рту или на языке; тошнота, рвота или диарея.

- Не медлите, чтобы обратиться за лечением. Простуда и грипп не вызывают эндокардит, но инфекции, которые могут иметь одинаковые симптомы, вызывают эндокардит. На всякий случай позвоните своему врачу.
- Cleveland Clinic считают, что для пациентов с HCM важно принимать профилактические антибиотики перед определенными медицинскими и стоматологическими процедурами, а также выполнять указанные выше действия для снижения риска. Пожалуйста, поговорите со своим врачом о типе и количестве антибиотиков, которые вам следует принимать, а также о том, для каких процедур вы должны их принимать.
- Идентификационная карта бактериального эндокардита доступна в Американской кардиологической ассоциации, и ее следует носить с собой. Попросите у врача карточку или зайдите на сайт www.americanheart.org и найдите «бумажник с карточкой от бактериального эндокардита».
Кардиологи клиники
Ресурсы
Как мне найти врача, если у меня гипертрофическая кардиомиопатия?
Чтобы найти врача, записаться на прием или узнать больше о лечении гипертрофической кардиомиопатии в клинике Кливленда, посетите Центр гипертрофической кардиомиопатии.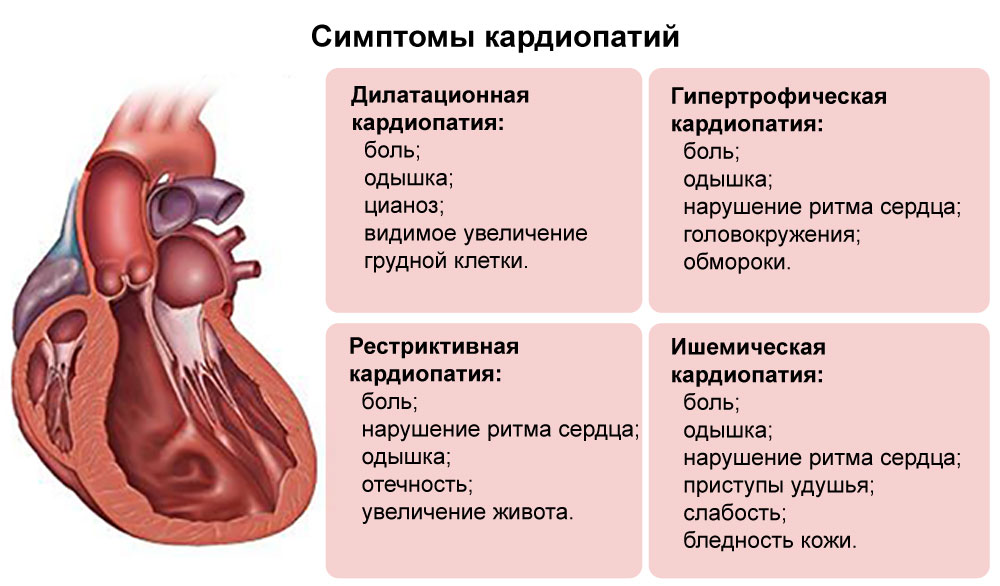
По вопросам педиатрии посетите веб-сайт Центра детских и врожденных пороков сердца.
Ассоциация гипертрофической кардиомиопатии (HCMA)
Ассоциация гипертрофической кардиомиопатии (HCMA) занимается поддержкой и обучением людей с HCM, их семей и других медицинских работников. С ними можно связаться по телефону:
P.O. Box 306,
Hibernia, NJ 07842
Телефон: 973.983.7429
Электронная почта: поддержка @ 4hcm.org
www.4hcm.org *
Дополнительные ресурсы
Гипертрофическая кардиомиопатия: для пациентов, их семей и заинтересованных врачей
Очень полезное руководство для людей с гипертрофической кардиомиопатией. Книги можно заказать на www.4hcm.org
* В новом окне браузера откроется эта ссылка. Включение ссылок на другие веб-сайты не означает какого-либо одобрения материалов на веб-сайтах или какой-либо связи с их операторами
- Предикторы отдаленных исходов у пациентов с симптоматической гипертрофической обструктивной кардиомиопатией, перенесших хирургическое лечение обструкции выходного тракта левого желудочка.

- Desai MY, Bhonsale A, Smedira NG, Naji P, Thamilarasan M, Lytle BW, Lever HM. Тираж. 2013, 14 июня [Epub до печати]
- Взаимосвязь между исходной диастолической функцией в состоянии покоя и переносимостью физической нагрузки у пациентов с гипертрофической кардиомиопатией, перенесших стресс-эхокардиографию на беговой дорожке: когортное исследование.
- Альджароуди, Вашингтон, Десаи, М.С. Алрайес, Тамиларасан, М., Менон, В., Родригес, Л.Л., Смедира, Н., Гримм, Р.А., Левер, М.М., Джабер, ВА BMJ Open. 2012 декабря 12; 2 (6).doi: pii: e002104. 10.1136 / bmjopen-2012-002104. Печать 2012.
- Разнообразие аномалий митрального клапана при обструктивной гипертрофической кардиомиопатии.
- Cavalcante JL, Barboza JS, рычаг HM. Prog Cardiovasc Dis. 2012 май-июнь; 54 (6): 517-22. DOI: 10.1016 / j.pcad.2012.03.002. Рассмотрение.
- Корреляция между функциональным статусом, воспринимаемым врачом, состоянием здоровья, воспринимаемым пациентом, и сердечно-легочной нагрузкой приводит к гипертрофической кардиомиопатии.

- Huff CM, Turer AT, Wang A. Qual Life Res. 2013 Апрель; 22 (3): 647-52. DOI: 10.1007 / s11136-012-0182-у. Epub 2012 29 апреля
Гипертрофическая кардиомиопатия: основы практики, основы, патофизиология
Ly HQ, Greiss I, Talakic M, et al. Внезапная смерть и гипертрофическая кардиомиопатия: обзор. Банка Кардиол . 2005 21 апреля (5): 441-8. [Медлайн].
Коломбо М.Г., Ботто Н., Витторини С., Парадосси Ю., Андреасси М.Г.Клиническая полезность генетических тестов при наследственных гипертрофических и дилатационных кардиомиопатиях. Кардиоваск Ультразвук . 2008 декабрь 19, 6:62. [Медлайн]. [Полный текст].
Моримото С. Саркомерные белки и наследственные кардиомиопатии. Cardiovasc Res . 2008 г. 1. 77 (4): 659-66. [Медлайн].
Soor GS, Luk A, Ahn E, Abraham JR, Woo A, Ralph-Edwards A и др. Гипертрофическая кардиомиопатия: современное понимание и цели лечения. Дж. Клин Патол . 2009 Март 62 (3): 226-35. [Медлайн].
Ван Дрист С.Л., Акерман М.Дж., Оммен С.Р., Шакур Р., Уилл М.Л., Нишимура Р.А. и др. Распространенность и тяжесть «доброкачественных» мутаций тяжелой цепи бета-миозина, сердечного тропонина Т и альфа-тропомиозина при гипертрофической кардиомиопатии. Тираж . 2002 декабрь 10. 106 (24): 3085-90. [Медлайн].
[Рекомендации] Марон Б.Дж., Маккенна В.Дж., Дэниэлсон Г.К., Каппенбергер Л.Дж., Кун Г.Дж., Зейдман К.Э. и др.Согласованный документ клинических экспертов Американского колледжа кардиологов / Европейского общества кардиологов по гипертрофической кардиомиопатии. Отчет целевой группы Фонда Американского колледжа кардиологов по согласованным документам клинических экспертов и Практические рекомендации Комитета кардиологов Европейского общества. Джам Колл Кардиол . 5 ноября 2003 г. 42 (9): 1687-713. [Медлайн].
Марон Б.Дж., Петерсон Е.Е., Марон М.С., Петерсон Дж. Распространенность гипертрофической кардиомиопатии в амбулаторных условиях, направленных на эхокардиографическое исследование. Ам Дж. Кардиол . 1994 15 марта. 73 (8): 577-80. [Медлайн].
Марон Б.Дж., Гардин Дж. М., Флэк Дж. М. и др. Распространенность гипертрофической кардиомиопатии в общей популяции молодых людей. Эхокардиографический анализ 4111 пациентов в исследовании CARDIA. Развитие риска коронарной артерии у (молодых) взрослых. Тираж . 1995 15 августа. 92 (4): 785-9. [Медлайн].
Марон Б.Дж. Гипертрофическая кардиомиопатия: систематический обзор. ЯМА .2002 13 марта. 287 (10): 1308-20. [Медлайн].
Эллиотт П.М., Гимено Дж. Р., Таман Р., Шах Дж., Уорд Д., Дики С. и др. Исторические тенденции в выживаемости пациентов с гипертрофической кардиомиопатией. Сердце . 2006 июнь 92 (6): 785-91. [Медлайн].
Minami Y, Kajimoto K, Terajima Y, et al. Клинические последствия обструкции среднего желудочка у пациентов с гипертрофической кардиомиопатией. Джам Колл Кардиол . 2011 июн 7.57 (23): 2346-55. [Медлайн].
DeRose JJ Jr, Banas JS Jr, Winters SL. Современные взгляды на внезапную сердечную смерть при гипертрофической кардиомиопатии. Программа Cardiovasc Dis . 1994 май-июнь. 36 (6): 475-84. [Медлайн].
Марон Б.Дж., Робертс В.С., Эпштейн SE. Внезапная смерть при гипертрофической кардиомиопатии: профиль 78 пациентов. Тираж . 1982 июн. 65 (7): 1388-94. [Медлайн].
[Рекомендации] Elliott PM, Anastasakis A, Borger MA и др., Для Целевой группы по диагностике и лечению гипертрофической кардиомиопатии Европейского общества кардиологов (ESC).Рекомендации ESC по диагностике и лечению гипертрофической кардиомиопатии, 2014 г. Eur Heart J . 2014 14 октября. 35 (39): 2733-79. [Медлайн].
Мусат Д., Шерид М.В. Эхокардиография в лечении гипертрофической кардиомиопатии. Анадолу Кардиёл Дерг . 2006 г., 6, Дополнение 2: 18–26. [Медлайн].
Peteiro J, Bouzas-Mosquera A, Fernandez X и др. Прогностическое значение Эхокардиографии с нагрузкой у пациентов с гипертрофической кардиомиопатией. J Am Soc Echocardiogr . 2012 25 февраля (2): 182-9. [Медлайн].
Bruder O, Wagner A, Jensen CJ, Schneider S, Ong P, Kispert EM. Рубцы миокарда, визуализируемые с помощью магнитно-резонансной томографии сердечно-сосудистой системы, позволяют прогнозировать серьезные нежелательные явления у пациентов с гипертрофической кардиомиопатией. Джам Колл Кардиол . 2010 сентября 7. 56 (11): 875-87. [Медлайн].
Soor GS, Luk A, Ahn E, Abraham JR, Woo A, Ralph-Edwards A и др. Гипертрофическая кардиомиопатия: современное понимание и цели лечения. Дж. Клин Патол . 2009 Март 62 (3): 226-35. [Медлайн].
Verlinden NJ, Coons JC. Дизопирамид при гипертрофической кардиомиопатии: прагматическая переоценка старого препарата. Фармакотерапия . 2015 Декабрь 35 (12): 1164-72. [Медлайн].
Boggs W. Поэтапная антигипертензивная терапия, эффективная при гипертрофической кардиомиопатии. Медицинские новости Medscape. 4 февраля 2013 г. Доступно по адресу http://www.medscape.com/viewarticle/778707. Доступ: 26 февраля 2013 г.
Аргулиан Э., Мессерли Ф. Х., Азиз Э. Ф., Винсон Дж., Агарвал В., Каддаха Ф. и др. Антигипертензивная терапия при гипертрофической кардиомиопатии. Ам Дж. Кардиол . 2013 19 января [Medline].
[Рекомендации] Герш Б.Дж., Марон Б.Дж., Боноу Р.О. и др. Для ACCF / AHA, AATS и др. Руководство ACCF / AHA 2011 г. по диагностике и лечению гипертрофической кардиомиопатии: краткое содержание: отчет Фонда Американского колледжа кардиологов / Целевой группы Американской кардиологической ассоциации по практическим рекомендациям. Тираж . 2011 декабрь 13, 124 (24): 2761-96. [Медлайн].
[Рекомендации] Герш Б.Дж., Марон Б.Дж., Боноу Р.О. и др. Для Фонда Американского колледжа кардиологов / Целевой группы Американской кардиологической ассоциации по практическим рекомендациям. Руководство ACCF / AHA 2011 г. по диагностике и лечению гипертрофической кардиомиопатии: отчет Фонда Американского колледжа кардиологов / Целевой группы Американской кардиологической ассоциации по практическим рекомендациям. Разработан в сотрудничестве с Американской ассоциацией торакальной хирургии, Американским обществом эхокардиографии, Американским обществом ядерной кардиологии, Американским обществом сердечной недостаточности, Обществом сердечного ритма, Обществом сердечно-сосудистой ангиографии и вмешательств и Обществом Тхо… J Am Coll Cardiol . 2011 13 декабря. 58 (25): e212-60. [Медлайн].
Эллиотт П.М., Анастасакис А., Боргер М.А. и др., Для членов Целевой группы Европейского общества кардиологов. Руководство ESC 2014 г. по диагностике и лечению гипертрофической кардиомиопатии: Целевая группа по диагностике и лечению гипертрофической кардиомиопатии Европейского общества кардиологов (ESC). Eur Heart J . 2014 14 октября. 35 (39): 2733-79. [Медлайн].
Гиллинов АМ.Обновленные рекомендации по аппаратной терапии нарушений сердечного ритма. J Thorac Cardiovasc Surg . 2012 декабрь 144 (6): 1285. [Медлайн].
Schaff HV, Dearani JA, Ommen SR, Sorajja P, Nishimura RA. Расширение показаний к миэктомии перегородки у пациентов с гипертрофической кардиомиопатией: результаты операции у пациентов со скрытой обструкцией. J Thorac Cardiovasc Surg . 2012 февраль 143 (2): 303-9. [Медлайн].
Panaich SS, Badheka AO, Chothani A, et al.Результаты миэктомии межжелудочковой перегородки и гипертрофической кардиомиопатии (из общенациональной стационарной выборки [1998-2010]). Ам Дж. Кардиол . 2014 г. 1. 114 (9): 1390-5. [Медлайн].
Vriesendorp PA, Schinkel AF, Soliman OI, et al. Долгосрочные преимущества миэктомии и удлинения передней митральной створки при обструктивной гипертрофической кардиомиопатии. Ам Дж. Кардиол . 2015 г. 1. 115 (5): 670-5. [Медлайн].
Сингх К., Кутб М., Карсон К., Хибберт Б., Гловер К.Метаанализ текущего состояния абляции алкогольной перегородки и хирургической миэктомии при обструктивной гипертрофической кардиомиопатии. Катетер Cardiovasc Interv . 2015 3 ноября [Medline].
Qintar M, Morad A, Alhawasli H, et al. Электрокардиостимуляция при лекарственной рефрактерной или непереносимой лекарственной гипертрофической кардиомиопатии Кокрановская база данных Syst Rev . 2012 16 мая. 5: CD008523. [Медлайн].
Хагеж А.А., Деснос М. Новые тенденции в лечении гипертрофической кардиомиопатии. Арка Кардиоваск Дис . 2009 Май. 102 (5): 441-7. [Медлайн].
Jassal DS; Нейлан Т.Г.; Fifer MA; Palacios IF; Lowry PA; Vlahakes GJ; Picard MH; Йоргер Д.М., Лаборатория ультразвукового исследования сердца, отделение кардиологии, Массачусетская больница общего профиля, Бостон, Массачусетс 02114, и др. Устойчивое улучшение диастолической функции левого желудочка после абляции спиртовой перегородки при гипертрофической обструктивной кардиомиопатии. Eur Heart J. 2006; 27 (15): 1805-10 (ISSN: 0195-668X) .
Streit S, Walpoth N, Windecker S, Meier B, Hess O. Связана ли алкогольная абляция перегородки с рецидивирующими тахиаритмиями ?. Швейцарский Мед Вкли . 2007 декабрь 1. 137 (47-48): 660-8. [Медлайн].
Lin G, Nishimura RA, Gersh BJ, et al. Осложнения устройства и несоответствующие разряды имплантируемого кардиовертера-дефибриллятора у пациентов с гипертрофической кардиомиопатией. Сердце . 2009 Май. 95 (9): 709-14. [Медлайн].
Пилларисетти Дж., Кондур А., Алани А. и др.Перипартальная кардиомиопатия: предикторы выздоровления и текущее состояние использования имплантируемого кардиовертера-дефибриллятора. Джам Колл Кардиол . 2014 июл 1. 63 (25, балл A): 2831-9. [Медлайн].
Ашихмина Э, Фарбер М.К., Мидзугути К.А. Роженицы с гипертрофической кардиомиопатией: серия случаев и обзор исходов беременности и анестезиологическое ведение родов и родоразрешения. Int J Obstet Anesth . 2015 24 ноября (4): 344-55. [Медлайн].
[Директива] Федеральное управление безопасности автотранспортных средств (FMCSA).Рекомендации медицинской экспертной комиссии. (См. Раздел 9: ЦМВ-факторы при кардиомиопатии). Доступно на https://www.fmcsa.dot.gov/regulations/medical/recommendations-medical-expert-panel. Обновлено 28 августа 2015 г .; Доступ: 22 декабря 2015 г.
Федеральное управление гражданской авиации. Руководство для авиационных медицинских экспертов. Соображения по поводу решения — аэрокосмические медицинские диспозиции. Пункт 36. Сердце. Доступно по адресу https://www.faa.gov/about/office_org/headgency_offices/avs/offices/aam/ame/guide/app_process/exam_tech/item36/amd/.Изменено 20 июня 2014 г .; Доступ: 22 декабря 2015 г.
Марон Б.Дж., Барри Д.А., Пул Р.С. Пилоты, гипертрофическая кардиомиопатия и вопросы авиационной и общественной безопасности. Ам Дж. Кардиол . 2004 15 февраля. 93 (4): 441-4. [Медлайн].
Pack C. Гипертрофическая кардиомиопатия у первоклассного летчика. Федеральный медицинский бюллетень воздушного хирурга. Том 51, № 2 . Отредактировано 29 апреля 2013 г. Проверено 22 декабря 2015 г. Доступно на https: // www.faa.gov/other_visit/aviation_industry/designees_delegations/designee_types/ame/fasmb/media/201302.pdf.
Федеральное управление гражданской авиации. Руководство для авиационных медицинских экспертов. Соображения по поводу решения — аэрокосмические медицинские диспозиции. Пункт 36. Сердце — другие сердечные заболевания. Доступно по адресу http://www.faa.gov/about/office_org/headgency_offices/avs/offices/aam/ame/guide/app_process/exam_tech/item36/amd/occ/. Изменено 20 июня 2014 г .; Доступ: 22 декабря 2015 г.
Марон Б.Дж., Иснер Дж. М., Маккенна В. Дж..26-я конференция Bethesda: рекомендации по определению допуска к соревнованиям спортсменов с сердечно-сосудистыми заболеваниями. Целевая группа 3: гипертрофическая кардиомиопатия, миокардит и другие миоперикардиальные заболевания и пролапс митрального клапана. Джам Колл Кардиол . 1994 24 октября (4): 880-5. [Медлайн].
Томпсон П.Д., Франклин Б.А., Балади Г.Дж., Блэр С.Н., Коррадо Д., Эстес Н.А., 3-й и др. Физические упражнения и острые сердечно-сосудистые события, рассматривающие риски в перспективе: научное заявление Совета Американской кардиологической ассоциации по питанию, физической активности и метаболизму и Совета по клинической кардиологии. Тираж . 2007 1 мая. 115 (17): 2358-68. [Медлайн].
Каунихан П.Дж., Маккенна В.Дж. Низкие дозы амиодарона для лечения аритмий при гипертрофической кардиомиопатии. Дж Клин Фармакол . 1989 Май. 29 (5): 436-8. [Медлайн].
Fananapazir L, Leon MB, Bonow RO, et al. Внезапная смерть во время эмпирической терапии амиодароном при симптоматической гипертрофической кардиомиопатии. Ам Дж. Кардиол . 1991 15 января. 67 (2): 169-74.[Медлайн].
[Рекомендации] Эпштейн А.Е., Димарко Дж. П., Элленбоген К.А., Эстес Н.А., 3-й, Фридман Р.А., Геттес Л.С. и др. Руководство ACC / AHA / HRS 2008 по аппаратной терапии нарушений сердечного ритма: краткое содержание. Ритм сердца . 2008 июн. 5 (6): 934-55. [Медлайн].
Topilski I; Шерез Дж; Керен Г; Копперман I, отделение кардиологии, Тель-Авивский медицинский центр Сураски, Тель-Авив, Израиль. [email protected]. Долгосрочные эффекты двухкамерной кардиостимуляции с периодической эхокардиографической оценкой оптимальной атриовентрикулярной задержки у пациентов с гипертрофической кардиомиопатией> 50 лет. Ам Дж. Кардиол . 2006. 97 (12): 1769-1775.
Galve E, Sambola A, Saldaña G, Quispe I, Nieto E, Diaz A и др. Поздние преимущества двухкамерной кардиостимуляции при обструктивной гипертрофической кардиомиопатии. Последующее 10-летнее исследование. Сердце . 2009 28 мая. [Medline].
Силва Л.А., Фернандес Е.А., Мартинелли Филхо М., Коста-Р, Сикейра С., Янни Б.М. и др. Кардиостимуляция при гипертрофической кардиомиопатии: когорта с периодом наблюдения 24 года. Арк Бюстгальтер Кардиол . 2008 Октябрь 91 (4): 250-6, 274-80. [Медлайн].
You JJ, Woo A, Ko DT, Cameron DA, Mihailovic A, Krahn M. Увеличение продолжительности жизни и экономическая эффективность имплантируемых кардиовертеров / дефибрилляторов для первичной профилактики внезапной сердечной смерти у пациентов с гипертрофической кардиомиопатией. Am Heart J . 2007 ноябрь 154 (5): 899-907. [Медлайн].
Дженсен М.К., Принц С., Хорсткотте Д., ван Бюрен Ф., Биттер Т., Фабер Л. и др.Абляция алкогольной перегородки у пациентов с гипертрофической обструктивной кардиомиопатией: низкая частота внезапной сердечной смерти и сниженный профиль риска. Сердце . 2013 июл.99 (14): 1012-7. [Медлайн].
McKinney AM, Lohman BD, Sarikaya B, Benson M, Benson MT, Lee MS. Точность стандартных изображений FLAIR с подавлением жира и взвешенных по диффузии изображений при обнаружении клинически очевидного неврита зрительного нерва. Акта Радиол . 2013 5 февраля. [Medline].
Tracy CM, Epstein AE, Darbar D и др., Для Фонда Американского колледжа кардиологов, Целевой группы Американской кардиологической ассоциации по практическим рекомендациям и др.2012 г. ACCF / AHA / HRS, посвященное обновлению рекомендаций 2008 г. по аппаратной терапии нарушений сердечного ритма: отчет Фонда Американского колледжа кардиологов / Целевой группы Американской кардиологической ассоциации по практическим рекомендациям и Общества сердечного ритма. [исправлено]. Тираж . 2 октября 2012 г. 126 (14): 1784-800. [Медлайн].
Чжао Д.С., Шэнь И, Чжан Кью и др. Результаты катетерной аблации фибрилляции предсердий у пациентов с гипертрофической кардиомиопатией: систематический обзор и метаанализ. Europace . 2015 26 ноября. [Medline].
Гипертрофическая кардиомиопатия | Анестезиология | Американское общество анестезиологов
ГИПЕРТРОФИЧЕСКАЯ кардиомиопатия (ГКМП) — это генетическое заболевание сердца, вызванное мутациями в одном из по крайней мере 12 саркомерных или несаркомерных генов, и признано наиболее частой причиной внезапной сердечной смерти (ВСС) у молодых и важным субстратом для инвалидности в любом возрасте. возраст.1,2 Широкое фенотипическое проявление и сложность заболевания постоянно вызывают неопределенность в отношении этого расстройства.Технологические разработки в сочетании с глубоким пониманием эпидемиологии, клинического течения и молекулярных дефектов, ответственных за ГКМП, способствовали развитию новых стратегий управления диагностикой.2 Провайдеры анестезии, ухаживающие за пациентами с этим гетерогенным заболеванием, должны осознавать его потенциальную опасность для жизни и должны быть знакомы с новыми методами лечения. клинические данные для обеспечения оптимального лечения в периоперационный период. И наоборот, анестезиологи могут столкнуться с клинически нераспознанной ГКМП и должны быть готовы предвидеть гемодинамические изменения и сердечно-сосудистую нестабильность, которые могут возникнуть у таких пациентов.
Гипертрофическая кардиомиопатия является уникальной среди сердечно-сосудистых заболеваний в силу ее потенциальной клинической картины на любом этапе жизни, от младенчества до старше 90 лет.3 Хотя неблагоприятные клинические последствия заболевания, особенно внезапная сердечная смерть, хорошо документированы, более сбалансированная В последнее время появилась перспектива прогноза, согласно которой нормальная продолжительность жизни признается у значительной части пациентов.3
Клинический диагноз ГКМП обычно устанавливается с помощью двумерной эхокардиографии, демонстрируя гипертрофию левого желудочка (ЛЖ), обычно асимметричную по распределению и связанную с недилатированной камерой при отсутствии другого сердечного или системного заболевания, способного вызвать выраженную гипертрофию. .2,4 Это определение ГКМП не зависит от наличия обструкции оттока ЛЖ или сердечных симптомов.
В течение последних нескольких десятилетий многочисленные исследования привели к эволюции нашего понимания клинического, генетического и патологического спектра ГКМП.1 В процессе это заболевание приобрело множество названий, в значительной степени связанных с его существенными клиническими, функциональными проявлениями. и морфологическое разнообразие. Гипертрофическая кардиомиопатия — предпочтительное название, потому что оно описывает общую степень заболевания, не вводя вводящего в заблуждение вывода о том, что обструкция выводного тракта является неизменной характеристикой.1,2,4
Эпидемиологические исследования с различными дизайнами исследований показали аналогичные оценки распространенности фенотипически выраженной ГКМП среди взрослого населения в целом около 0,2% (1: 500) .5 Таким образом, ГКМП не является редкостью и, фактически, является наиболее распространенной. генетическое сердечно-сосудистое заболевание, передающееся по аутосомно-доминантному признаку.2 В настоящее время очевидно, что, основываясь на несоответствиях между распространенностью ГКМП в общей популяции и кардиологической практикой, большинство пациентов, страдающих этим заболеванием, нераспознаны клинически, в том числе многие пациенты с высоким риском SCD.1–3 Кроме того, поскольку в Северной Америке более 30 миллионов пациентов ежегодно подвергаются хирургической операции, можно ожидать, что значительное число пациентов с ГКМП получат периоперационную и анестезиологическую помощь по крайней мере один раз в течение своей жизни.
Можно рассматривать большую часть клинического спектра ГКМП как единое целое заболевание и первичное нарушение саркомера. Мутации в генах тяжелой цепи β-миозина и миозин-связывающего протеина C составляют почти половину генотипированных пациентов на сегодняшний день, в то время как шесть других генов саркомеров на каждый составляют небольшое количество случаев, i.е. , сердечный тропонин Т, сердечный тропонин I, α, тропомиозин, сердечная α-актин регуляторная легкая цепь миозина, основная легкая цепь миозина. 2 Это генетическое разнообразие усугубляется внутригенной гетерогенностью, в настоящее время идентифицировано более 400 мутаций2. мутации с заменой одного аминокислотного остатка на другой, но также включают вставки, делеции и мутации сплайсинга (расщепления сайтов), кодирующие усеченные саркомерные белки.
Совсем недавно мутации в двух несаркомерных генах были признаны вызывающими заболевания с гипертрофией ЛЖ (часто связанные с паттерном Вольфа-Паркинсона-Уайта на электрокардиограмме), которые имитируют ГКМП, но связаны с накоплением гликогена в миокарде, i.е. , ген, кодирующий γ 2 -регуляторную субъединицу аденозинмонофосфат-активируемой протеинкиназы (PRKAG2) и мутантный ген болезни Данона, включающий связанный с лизосомами мембранный белок 2-α-галактозидазу или кислоту α-1,4 -глюкозидаза, как правило, с большой степенью гипертрофии.6 Фенотипическая экспрессия HCM, как полагают, является продуктом не только вызывающей болезнь мутации, но также генов-модификаторов и факторов окружающей среды. Следовательно, большое количество генов и мутаций (включая многие еще не идентифицированные) могут влиять на экспрессию фенотипа HCM.
Недавние исследования признали роль генетики в генезе электрофизиологических нарушений, связанных с ГКМП. Например, повышенный риск фибрилляции предсердий при HCM был связан с конкретной миссенс-мутацией в гене тяжелой цепи β-миозина. Однако многие подростки (и некоторые взрослые) с генетическим дефектом ГКМП не обязательно проявляют типичные клинические и фенотипические особенности, хотя электрокардиографические аномалии или свидетельства диастолической дисфункции по данным тканевой допплерографии могут предшествовать появлению гипертрофии ЛЖ на эхокардиограмме.7
Хотя лабораторный анализ ДНК на мутантные гены является наиболее окончательным методом для установления диагноза ГКМП, остаются важные препятствия для трансформации таких основанных на исследованиях генетических технологий в практические клинические стратегии на широко распространенной и рутинной основе. Эти факторы включают вышеупомянутую генетическую гетерогенность HCM, а также методологические трудности, связанные с идентификацией одной вызывающей заболевание мутации среди по меньшей мере 12 возможных генов HCM.Однако, когда мутация HCM выявляется у пробанда, определение генетического статуса может быть достигнуто у всех членов семьи эффективно и недорого. Диагностические молекулярные лаборатории§ недавно начали решать эти проблемы, предлагая быстрое прямое секвенирование ДНК для подмножества генов болезни ГКМП.8 Тем не менее, остается значительный потенциал ложноотрицательных результатов (, т. Е. , в которых нельзя исключать диагноз ГКМП). ).
Клиническая идентификация ГКМП по-прежнему обычно основывается на трансторакальном двумерном эхокардиографическом распознавании фенотипа заболевания с гипертрофией ЛЖ (толщина стенки ≥ 15 мм), не связанной с увеличением полости желудочка.Однако корреляции генотип-фенотип у членов семьи показали, что практически любая толщина стенки ЛЖ (включая нормальную) совместима с присутствием мутантного гена HCM4. Максимальные значения толщины стенки ЛЖ имеют особенно широкий диапазон, достигая 60 мм и больше всего. существенен при любом сердечном заболевании. Средняя толщина стенки ЛЖ в популяции пациентов с ГКМП составляет 21–22 мм, что в среднем намного превышает показатель, наблюдаемый при системной гипертензии или стенозе аортального клапана.
Степень обструкции выводного тракта ЛЖ оценивается с помощью непрерывно-волновой допплеровской эхокардиографии в состоянии покоя или с физиологической провокацией в условиях физической нагрузки на основании характерной среднесистолической пиковой формы волны.Митральная регургитация, обычно от легкой до умеренной степени, сопровождает обструкцию оттока, при этом регургитационная струя обычно направляется назад. Продолжительность потока, максимальная скорость и доплеровская спектральная конфигурация отличают струю митральной регургитации от струи оттока ЛЖ. Характерно выраженное нарушение релаксации миокарда из-за гипертрофированного миокарда. Увеличивается время изоволюмической релаксации, снижается пиковая скорость раннего наполнения и увеличивается время замедления. Как правило, чреспищеводная эхокардиография играет лишь ограниченную клиническую роль при ГКМП, но полезна в операционной для мониторинга обструкции оттока и гемодинамических изменений, связанных с оттоком жидкости и введением лекарств, а также оперативной стратегии и оценки результатов во время перегородочной миэктомии.15
Электрокардиограмма в 12 отведениях отклоняется от нормы у 75–90% пациентов с ГКМП, показывая множество патологических паттернов, ни одна из которых не является патогномоничной или высокоспецифичной для этого заболевания. Наиболее распространенными являются высокие напряжения, соответствующие гипертрофии ЛЖ, изменениям сегмента ST и инверсии зубца Т, увеличению левого предсердия, аномальным зубцам Q и уменьшенным или отсутствующим зубцам R в левых прекардиальных отведениях. Кроме того, существует небольшая корреляция между электрокардиографическим напряжением и величиной гипертрофии ЛЖ, оцененной с помощью эхокардиографии; гетерогенные паттерны, наблюдаемые на электрокардиограмме, имеют мало прогностической ценности для клинического результата.Тем не менее аномальные электрокардиограммы могут иметь диагностическое значение, поскольку вызывают подозрение на ГКМП у молодых членов семьи, у которых на эхокардиограмме еще не обнаружена гипертрофия ЛЖ2
Современная магнитно-резонансная томография сердца позволяет получить томографические изображения всего ЛЖ с высоким разрешением и представляет собой дополнительный метод диагностики ГКМП. Магнитный резонанс особенно важен для пациентов с технически неоптимальными эхокардиографическими исследованиями или иногда, когда гипертрофия ограничивается необычными участками внутри стенки ЛЖ ( e.грамм. , переднебоковая свободная стенка или вершина). Следовательно, магнитный резонанс играет все более важную роль в качестве дополнительного метода клинической визуализации и может превосходить эхокардиографию у отдельных пациентов с ГКМП2
Несмотря на то, что ранее это было предметом периодических споров, в настоящее время широко распространено мнение, что субаортальный градиент и связанное с ним повышение внутриполостного давления в ЛЖ отражают истинное механическое сопротивление оттоку и, следовательно, имеют прогностическое значение для пациентов с ГКМП.16 Недавнее многоцентровое исследование показало, что обструкция оттока ЛЖ является независимым долгосрочным детерминантом прогрессирования сердечной недостаточности, сердечной недостаточности и смерти от инсульта, хотя слабо связана с внезапной смертью. 16 Более того, большая часть пациентов с ГКМП подвержена физиологически провоцируемому оттоку ЛЖ. градиенты тракта со стрессом, в том числе многие без систолического переднего движения или обструкции в состоянии покоя (базальные) .16 Обструкция оттока при ГКМП определяется рядом структурных аномалий, включая небольшую площадь оттока ЛЖ, степень выпуклости перегородки в тракт оттока и удлинение и смещенные кпереди митральные створки в сочетании с гипердинамическим выбросом ЛЖ, подтягивая (и / или толкая) митральный клапан к перегородке.
Обструкция характерно динамична, то есть , у большинства пациентов не наблюдается обструкции в условиях покоя (базальных), хотя у многих наблюдается развитие субаортальных градиентов различной величины с различными провокационными маневрами, которые включают упражнения или Вальсальву, а также нефизиологические фармакологические вмешательства, такие как внутривенное введение инотропных и мощных препаратов, индуцирующих катехоламины ( e.грамм. , добутамин или изопротеренол). Градиент оттока при ГКМП также может быть спонтанно лабильным и может даже значительно варьироваться в зависимости от гидратации или потребления тяжелой еды или умеренного количества алкоголя.16,17 Градиенты оттока ответственны за шумы систолического выброса на левой нижней границе грудины и верхушке, которые могут присутствуют в положении лежа на спине или провоцируются стоянием (или Вальсальвой) и уменьшаются при приседании.18 Систолическое переднее движение отвечает не только за субаортальную обструкцию, но также и за сопутствующую митральную регургитацию из-за неполного прилегания створок.18 Последствия заболевания, связанные с хроническими градиентами оттока, такие как прогрессирующая сердечная недостаточность, вероятно, опосредованы повышенным напряжением стенки ЛЖ, ишемией миокарда и, в конечном итоге, гибелью миоцитов и замещающим фиброзом. динамические и возникают резко и неожиданно, спровоцированы или усугублены условиями, которые увеличивают сократимость миокарда (, например, , тахикардия и стресс) или уменьшают преднагрузку и объем желудочков ( e.грамм. , вазодилататоры, гиповолемия и гипотензия). Митральная регургитация при ГКМП отвечает на фармакологическое вмешательство парадоксальным образом по сравнению с тем, что наблюдается при врожденном пороке клапана. Следовательно, при ГКМП вазодилататоры увеличивают субаортальный градиент, в результате чего увеличивается MR, тогда как вазоконстрикторы уменьшают обструкцию и объем регургитации.
Клиническое течение ГКМП обычно непостоянно, и пациенты могут оставаться стабильными в течение длительных периодов времени, при этом значительная часть пациентов достигает нормальной продолжительности жизни.3 Хотя неблагоприятные клинические последствия, в том числе преждевременная смерть, хорошо задокументированы, в последнее время появился более сбалансированный взгляд на прогноз. Риски HCM ранее были переоценены из-за зависимости от отчетов из специализированных центров (уровень смертности до 6% ежегодно) .1,2
Более поздние исследования, проведенные за последние 10 лет с участием менее отобранных региональных или местных когорт пациентов с ГКМП, указывают на гораздо более низкие общие годовые показатели смертности, составляющие примерно 1%, что не отличается от ожидаемого для взрослого U.S. популяция. 3,6 Таким образом, HCM может быть связан с важными симптомами и преждевременной смертью, но часто с отсутствием или относительно легкой инвалидностью и без необходимости серьезных терапевтических вмешательств.
Пациенты, у которых наблюдаются симптомы как следствие ГКМП, имеют клиническое течение, которое развивается по одному или нескольким направлениям: прогрессирующая сердечная недостаточность с одышкой при физической нагрузке; утомляемость и боль в груди; случайная эволюция до конечной стадии; AF; и внезапная смерть (некоторые группы высокого риска, связанные с ежегодной смертностью ≥ 5%).Внезапная смерть часто возникает как начальное проявление болезни, часто у молодых пациентов с бессимптомными или слабо выраженными симптомами, и остается наиболее частым способом смерти и наиболее разрушительным и непредсказуемым осложнением ГКМП.2 Хотя пациенты с высоким риском составляют лишь меньшинство в общем спектре заболеваний. Исторически сложилось так, что основное внимание в исследованиях уделялось клинической идентификации этой важной подгруппы пациентов по признанным факторам риска (рис. 4). Хотя имеется значительный объем данных о стратификации риска и достигнут большой объем понимания, критерии точной идентификации всех пациентов с высоким риском по клиническим маркерам риска не являются полными.Значительное меньшинство внезапно умирающих пациентов с ГКМП не имеют или не имеют только одного фактора риска2
Рис. 4. Оценка риска внезапной сердечной смерти в общей популяции с гипертрофической кардиомиопатией. Лечение для предотвращения внезапной смерти ограничивается той небольшой подгруппой пациентов, которые считаются подверженными наивысшему риску по сравнению со всеми другими пациентами с гипертрофической кардиомиопатией на основе анализа факторов риска.ICD = имплантируемый кардиовертер-дефибриллятор; ГЛЖ = гипертрофия левого желудочка; NSVT = неустойчивая желудочковая тахикардия; SD = внезапная смерть.
Рис. 4. Оценка риска внезапной сердечной смерти в общей популяции с гипертрофической кардиомиопатией. Лечение для предотвращения внезапной смерти ограничивается той небольшой подгруппой пациентов, которые считаются подверженными наивысшему риску по сравнению со всеми другими пациентами с гипертрофической кардиомиопатией на основе анализа факторов риска. ICD = имплантируемый кардиовертер-дефибриллятор; ГЛЖ = гипертрофия левого желудочка; NSVT = неустойчивая желудочковая тахикардия; SD = внезапная смерть.
Несмотря на то, что имеется значительный объем данных относительно сердечно-сосудистых рисков для пациентов с атеросклеротической болезнью коронарных артерий, которым проводится анестезия для внесердечных операций, имеется мало информации о таких рисках для пациентов с ГКМП.26 Это, вероятно, в значительной степени связано с относительной редкостью, с которой пациенты с подтвержденной ГКМП диагноз встречаются у анестезиологов.Тем не менее, пациенты с ГКМП (с обструкцией оттока ЛЖ или без нее), перенесшие внесердечное хирургическое вмешательство, нередко имеют неблагоприятные периоперационные исходы. Зарегистрированные события включают застойную сердечную недостаточность, ишемию миокарда, системную гипотензию, а также наджелудочковые или желудочковые аритмии26. Продолжительность и тип хирургического вмешательства (большое по сравнению с незначительным ) являются прогностическими факторами неблагоприятного сердечного исхода у пациентов с ГКМП26
Хотя смерть и инфаркт миокарда кажутся редкими, такие катастрофы во время внесердечной хирургии у молодых пациентов с недиагностированным ГКМП продолжают представлять серьезную проблему для анестезиологов.У пациентов с нераспознанной ГКМП может возникнуть внезапная и неожиданная системная гипотензия (, например, , из-за кровопотери и гиповолемии) и вызвать динамическую обструкцию оттока ЛЖ. Об этом сценарии может свидетельствовать усиление интенсивности или появление систолического шума и раздвоения артериального контура. идентифицируемые по трассировке артериальной линии или парадоксальные реакции на вазоактивные препараты и анестетики. В таких обстоятельствах следует рассмотреть возможность применения ГКМП и маневров для сохранения ударного объема, таких как уменьшение сократимости и симпатических выделений ( i.е. , с β-блокадой) и увеличения давления наполнения и постнагрузки (, т.е. , с гидратацией, α 1 агонистов). Острая застойная сердечная недостаточность иногда возникает у пациентов с ГКМП, перенесших внесердечное хирургическое вмешательство, что, вероятно, связано с диастолической дисфункцией26
Эти соображения подчеркивают важность предоперационной идентификации HCM для обеспечения надлежащих профилактических стратегий ведения.Учитывая распространенность ГКМП 1: 500 среди населения в целом, частоту, с которой это заболевание не диагностируется клинически, и растущее число амбулаторных операций, выполняемых каждый год в Соединенных Штатах, можно ожидать, что определенная подгруппа пациентов с ГКМП представит на операцию и анестезию без установленного диагноза. Этот вопрос представляет собой проблему для анестезиолога, на которого возложена клиническая ответственность за пациентов с ГКМП, которые часто молоды, в остальном здоровы и обычно подвергаются относительно несложным оперативным процедурам.
Стандартный предоперационный личный и семейный анамнез (, т. Е. , нацелены на сердечные симптомы одышки при физической нагрузке, утомляемость, стенокардию, обмороки или семейный анамнез ГКМП) и физикальное обследование (, т. Е. , шум систолического выброса, особенно если он усиливается при стоянии и снижается при приседании) может вызвать клиническое подозрение на ГКМП, тем самым инициируя полное сердечно-сосудистое обследование, при этом диагноз в конечном итоге подтверждается эхокардиографией до введения анестезии.Необструктивную форму HCM может быть сложно идентифицировать, учитывая отсутствие громкого шума в сердце16
Инвазивный мониторинг артериального давления и давления наполнения ЛЖ важен для пациентов с ГКМП, перенесших внесердечную операцию. Перед индукцией следует провести артериальную линию, чтобы распознать гипотензивные события, что позволит своевременно начать терапевтическое вмешательство. Давление заклинивания легочных капилляров может переоценить истинный объем в результате снижения диастолической податливости.Чреспищеводная эхокардиография с допплеровской визуализацией цветного потока позволяет наблюдать за морфологией тракта оттока ЛЖ, а также геометрией митрального клапана и камеры и может определять интраоперационное ведение, предоставляя информацию о развитии динамической обструкции оттока ЛЖ, митральной регургитации и диастолической дисфункции, а также а также свидетельство ишемии миокарда (в силу аномального движения стенки ЛЖ). Эти изменения важно распознать на ранней стадии, учитывая, что механические изменения часто предшествуют электрическим аномалиям, о которых свидетельствует электрокардиограмма.
У пациентов с известной ГКМП клиническая оценка должна быть сосредоточена на прогнозировании возможности динамической обструкции ЛЖ, злокачественных аритмий и ишемии миокарда, к которым эти пациенты могут быть особенно чувствительны в периоперационном периоде и под влиянием анестезии. Правильная гидратация и препараты, которые слегка снижают сократимость миокарда и снижают потребность в кислороде при сохранении объема внутрисосудистой жидкости и системного сосудистого сопротивления, являются основой предотвращения провокации обструкции выходного тракта ЛЖ.Увеличение или уменьшение внутрижелудочкового объема потенциально угрожает пациенту с HCM, а чрезмерно агрессивная инфузионная терапия в попытке выдержать преднагрузку может иметь негативные последствия, вызывая сердечную недостаточность.
Пациенты без признаков обструкции оттока ЛЖ в состоянии покоя до операции не должны рассматриваться как свободные от возможности развития динамической обструкции при введении анестетиков.Хотя нет никаких доказательств того, что величина толщины стенки ЛЖ напрямую связана с риском периоперационного события, массивная степень гипертрофии ЛЖ (толщина стенки ≥ 30 мм) является независимым фактором риска внезапной аритмической смерти, 27 и, следовательно, разумное предположение, что такие пациенты с ГКМП могут быть предрасположены к потенциально летальным тахиаритмиям в операционной.
Анксиолитики (бензодиазепины) показаны для подавления активации симпатической нервной системы, хотя следует избегать применения холинолитиков, таких как атропин или гликопирролат, из-за возможности развития тахикардии.Скополамин является предпочтительным из-за меньшего воздействия на частоту сердечных сокращений и при использовании в сочетании с другими депрессантами центральной нервной системы. При выборе индукционного агента следует учитывать возможность лекарственной гипотензии или повышенной симпатической активации при начале анестезии, и следует использовать медленное титрование этих препаратов. Перед попыткой интубации необходимо добиться достаточной депрессии симпатической системы, в то же время поддерживая адекватную постнагрузку.При использовании миорелаксантов следует учитывать последствия выделения гистамина, ваголитической и мускариновой активности и предотвращения обратного захвата катехоламинов, производимого этими препаратами. В этом отношении приемлемым агентом является векуроний.
Поскольку депрессия миокарда обычно желательна во время поддерживающей анестезии, летучие анестетики показаны пациентам с ГКМП, хотя важна бдительность в отношении внезапных гемодинамических изменений или узлового ритма.Изофлуран имеет тенденцию к увеличению частоты сердечных сокращений вследствие снижения системного сосудистого сопротивления при быстром введении. Более того, в высоких концентрациях изофлуран, похоже, увеличивает как частоту сердечных сокращений, так и артериальное давление, как и десфлуран. Закись азота может иногда вызывать симпатическую стимуляцию и повышенное давление в легочной артерии, тогда как при введении десфлурана резкое повышение концентрации может привести к тахикардии и системной артериальной гипертензии, а также к нежелательному высвобождению катехоламинов.Севофлуран является мягким депрессантом миокарда, и его введение приводит к более умеренному снижению системного сосудистого сопротивления и артериального давления, чем при приеме изофлурана или десфлурана, в то же время вызывая лишь небольшое увеличение частоты сердечных сокращений или вообще не увеличивая его.
Отрицательные инотропные агенты (эсмолол и метопролол) полезны при периоперационном ведении, поскольку повышение инотропии считается неблагоприятным при ГКМП.Снижение венозного возврата, которое происходит при высоком давлении в дыхательных путях, вызванном механической вентиляцией, плохо переносится и может вызвать острую обструкцию оттока ЛЖ. Для поддержания достаточной минутной вентиляции следует использовать малые дыхательные объемы и более высокую частоту дыхания. Адекватная гидратация особенно важна перед началом этих маневров.
Лечение острой гипотензии в операционной требует быстрого восполнения объема и введения агонистов α 1 ( e.грамм. , фенилэфрин). Лекарства с активностью агонистов β-адренорецепторов, такие как дофамин, добутамин или эфедрин, являются плохим выбором, поскольку повышенная инотропия и хронотропия, связанная с их применением, вероятно, будет способствовать обструкции оттока ЛЖ и увеличению потребности миокарда в кислороде. Системную гипертензию следует лечить увеличением концентрации ингаляционных анестетиков или введением β-антагонистов. Сосудорасширяющие средства, такие как нитроглицерин или нитропруссид, не показаны для снижения артериального давления, поскольку они вызывают снижение преднагрузки и системного сосудистого сопротивления.
Гипертрофическая кардиомиопатия представляет собой потенциал для различных аритмий во время индукции или поддерживающей анестезии, включая брадиаритмию, наджелудочковую тахикардию (включая ФП) и потенциально летальную желудочковую тахикардию / фибрилляцию. Поддержание синусового ритма важно, потому что наполнение желудочков в значительной степени зависит от сокращения левого предсердия, и, следовательно, пациенты могут быть ослаблены во время ФП.В операционной или в периоперационном периоде ФП следует купировать с помощью кардиоверсии на постоянном токе, а не фармакологически.
Приоритетом остается бдительность во время выхода из наркоза и в палате восстановления в отношении усиления симпатической реакции. Повышенное высвобождение катехоламинов на фоне боли или переохлаждения может привести к увеличению потребности миокарда в кислороде, способствуя ишемии, динамической обструкции оттока ЛЖ и, возможно, злокачественным аритмиям.
Сердечно-легочная реанимация после остановки сердца у пациентов с ГКМП требует знания патофизиологии заболевания. Инотропные агенты (адреналин) противопоказаны при ГКМП, потому что этим пациентам требуется пониженное инотропное и хронотропное состояние для смягчения обструкции оттока, диастолической дисфункции и ишемии миокарда. Сепсис и геморрагический шок значительно снижают постнагрузку и преднагрузку, соответственно, и могут предрасполагать пациентов с ГКМП к динамической обструкции со всеми присущими ей пагубными последствиями.
Беременность у пациентов с ГКМП поднимает вопросы ведения из-за уникальных сердечно-сосудистых изменений, которые могут произойти. На поздних этапах родов аортокавальная компрессия или большая кровопотеря во время родов и родоразрешения могут заметно снизить преднагрузку. Более того, боль и стресс при родах вызывают симпатическую стимуляцию, тем самым увеличивая частоту сердечных сокращений и сократительную способность, что, в свою очередь, может способствовать ухудшению гемодинамического состояния.Недавние исследования показывают, что абсолютная материнская смертность при ГКМП очень низка и, по-видимому, ограничивается женщинами, которые подвергаются особенно высокому риску из-за лежащей в основе ГКМП.28 Большое прогрессирование симптомов, ФП и обмороков возникают редко и в значительной степени связаны с предыдущим заболеванием пациентки. Клиническое состояние. 28 Нет доказательств того, что региональная анестезия увеличивает риск у женщин с ГКМП при использовании во время стандартных вагинальных родов. Как общая, так и региональная анестезия успешно использовались без осложнений при кесаревом сечении у родильниц с ГКМП.29 Успешное применение эпидуральной, комбинированной спинальной и эпидуральной анестезии и непрерывной спинальной анестезии зарегистрировано в клинических случаях 30
Гипертрофическая кардиомиопатия: симптомы, причины и многое другое
Что такое гипертрофическая кардиомиопатия?
Гипертрофическая кардиомиопатия (ГКМП) — это состояние, при котором сердечная мышца или миокард становится толще, чем обычно. Это мешает вашему сердцу перекачивать кровь.
В большинстве случаев HCM не вызывает никаких симптомов.Люди с HCM обычно могут вести нормальный образ жизни. Однако некоторые случаи могут стать серьезными. Серьезные случаи могут развиваться медленно или внезапно.
HCM встречается примерно у каждого 500 человек в США.
Многие люди с HCM не испытывают никаких симптомов. Однако во время физической активности могут возникнуть следующие симптомы:
- боль в груди
- одышка
- обморок
- головокружение
Другие симптомы, которые могут возникнуть в любое время, включают:
- усталость
- одышка дыхание
- учащенное сердцебиение, которое представляет собой учащенное или трепещущее сердцебиение
- высокое кровяное давление
Генетика
ГКМП обычно является наследственным заболеванием.Дефектные гены могут вызвать утолщение сердечной мышцы. У вас есть 50-процентный шанс унаследовать один из этих генов, если один из ваших родителей болен HCM.
Наследование гена не обязательно означает, что у вас будет симптоматическое заболевание. HCM следует доминантному типу наследования. Однако симптомы не всегда развиваются у людей с дефектным геном.
Другие причины
Другие возможные причины HCM включают старение и высокое кровяное давление. В некоторых случаях причина HCM никогда не устанавливается.
Для диагностики HCM можно использовать различные тесты.
Физический осмотр
Ваш врач выслушает шум в сердце или необычное сердцебиение. Шумы в сердце могут возникнуть, если утолщенная сердечная мышца нарушает приток крови к сердцу.
Эхокардиограмма
Это наиболее распространенный диагностический тест на ГКМП. Эхокардиограмма создает изображения вашего сердца с помощью звуковых волн. Ваш врач будет искать необычные движения.
Электрокардиограмма
Электрокардиограмма используется для измерения электрической активности сердца.HCM может вызвать отклонения от нормы.
Монитор Холтера
Монитор Холтера — это портативный электрокардиограмма, который можно носить в течение дня. Ваш врач попросит вас носить его от 24 до 48 часов. Это позволяет вашему врачу увидеть, как изменяется ваше сердцебиение во время различных занятий.
МРТ сердца
МРТ сердца использует магнитное поле для получения детальных изображений вашего сердца.
Катетеризация сердца
Этот тест используется для измерения давления кровотока в сердце и поиска закупорок.Чтобы выполнить этот тест, ваш врач поместит катетер в одну из ваших артерий на руке или около вашего паха. Катетер осторожно продвигается через артерии к сердцу. Как только он достигает сердца, вводится краситель, чтобы врач мог сделать подробные рентгеновские снимки.
Лечение ГКМП направлено на облегчение симптомов и предотвращение осложнений, особенно внезапной сердечной смерти. Используемые методы зависят от вашего:
- симптомов
- возраста
- уровня активности
- сердечной функции
Лекарств
Бета-блокаторы и блокаторы кальциевых каналов расслабляют сердечную мышцу.Расслабление помогает ему работать лучше.
Если у вас нерегулярный сердечный ритм, врач может прописать антиаритмические препараты, например амиодарон.
Возможно, вам придется принимать антибиотики перед стоматологическими процедурами или операцией, чтобы снизить риск инфекционного эндокардита.
Миэктомия перегородки
Миэктомия перегородки — это операция на открытом сердце, которая проводится для удаления части утолщенной перегородки. Перегородка — это стенка сердечной мышцы между двумя нижними камерами сердца, которые являются желудочками.Это помогает улучшить кровоток в сердце.
Миэктомия перегородки выполняется только в том случае, если лекарства не уменьшают ваши симптомы.
Абляция перегородки
Абляция перегородки включает использование алкоголя для разрушения части утолщенной сердечной мышцы. Спирт вводится через катетер, помещенный в артерию, которая питает часть вашего сердца, которая подвергается лечению.
Аблация перегородки часто выполняется людям, которым не может быть проведена миэктомия перегородки.
Имплантация кардиостимулятора
Если у вас нерегулярный пульс и ритм, крошечное электронное устройство, называемое кардиостимулятором, можно поместить под кожу на груди.Кардиостимулятор помогает регулировать частоту сердечных сокращений, посылая электрические сигналы вашему сердцу.
Эта процедура менее инвазивна, чем миэктомия и абляция перегородки. К тому же это обычно менее эффективно.
Имплантируемый кардиовертер-дефибриллятор (ICD)
Имплантируемый кардиовертер-дефибриллятор (ICD) — это небольшое устройство, которое с помощью электрического разряда отслеживает ваше сердцебиение и фиксирует опасные аномальные сердечные ритмы. Он находится в твоей груди.
ИКД часто используется у людей с высоким риском внезапной сердечной смерти.
Изменения образа жизни
Если у вас HCM, ваш врач может порекомендовать изменить образ жизни, чтобы снизить риск осложнений. Это включает:
- здоровое питание
- поддержание веса на здоровом уровне
- выполнение низкоинтенсивных физических нагрузок
- ограничение потребления алкоголя, поскольку алкоголь может вызвать нарушение сердечного ритма
Многие люди с ГКМП никогда не будут иметь любые серьезные проблемы со здоровьем, вызванные им. Однако у некоторых людей HCM может вызывать серьезные осложнения.Наиболее частыми осложнениями HCM являются:
Внезапная остановка сердца
Внезапная остановка сердца происходит, когда ваше сердце внезапно перестает работать. Это состояние также называют «внезапной сердечной смертью». Обычно это вызвано учащенным сердечным ритмом, известным как желудочковая тахикардия. Без неотложной помощи внезапная остановка сердца может быть фатальной. ГКМП является основной причиной внезапной сердечной смерти у людей моложе 30 лет.
Вы можете подвергаться более высокому риску внезапной сердечной смерти, если у вас есть одно или несколько из следующих:
- семейный анамнез внезапной сердечной смерти
- нарушение функции сердца
- тяжелые симптомы
- нарушение сердечного ритма в анамнезе с учащенным пульсом
- несколько случаев обморока в анамнезе, и вы молоды
- необычная реакция артериального давления на физическую активность
сердечная недостаточность
Когда ваше сердце не перекачивает столько крови, сколько нужно вашему организму, у вас сердечная недостаточность.
Дилатационная кардиомиопатия
Этот диагноз означает, что ваша сердечная мышца стала слабой и увеличенной. Увеличение заставляет ваше сердце работать менее эффективно.
Инфекционный эндокардит
Когда внутренняя оболочка вашего сердца или сердечные клапаны инфицированы, это называется инфекционным эндокардитом. Это может произойти, когда бактерии или грибки попадают в ваш кровоток и попадают в ваше сердце. Инфекционный эндокардит может вызвать рубцевание тканей, отверстия или разрастания в сердечных клапанах.Без лечения это может привести к летальному исходу.
Наличие такого заболевания, как тяжелая форма HCM, может повысить риск эмоциональных проблем. Некоторым людям трудно справиться с необходимостью корректировки, например, ограничить физические упражнения и полагаться на лекарства всю оставшуюся жизнь.
Если вам трудно справиться с HCM, ваш врач может порекомендовать обратиться к терапевту или присоединиться к группе поддержки. Вам также могут помочь лекарства, которые используются для лечения тревоги или депрессии.
Ведение обструктивной гипертрофической кардиомиопатии | Royal Brompton & Harefield Specialist Care
Лечение обструктивной гипертрофической кардиомиопатии
Обструкция выводящего тракта левого желудочка (LVOTO)
Программа управления LVOTO в RB&HH Specialist Care основана на высочайшем уровне диагностических знаний и предлагает все варианты лечения, доступные на международном уровне.Вмешательства LVOTO считаются подходящими для пациентов со значительной степенью обструкции LVOT, которые не улучшают лечение и имеют симптомы, ограничивающие их повседневную активность.
В настоящее время доступны два метода: абляция спиртовой перегородки и хирургическая миэктомия . Перед вмешательством пациенту предстоит пройти ряд тестов, включая динамическую эхокардиограмму и МРТ сердца, для оценки ОВЛЖ, анатомии и геометрии как левого желудочка, так и митрального клапана.
Хирургическая миэктомия
Хирургическая миэктомия для лечения обструктивной гипертрофической кардиомиопатии — это процедура, которая влечет за собой хирургическую резекцию мышцы для устранения ОВЛЖ.
Операция планируется тщательно с помощью специальной визуализации для оценки LVOTO и анатомии левого желудочка и митрального клапана. Во время процедуры хирург достигает внутренней части сердца через аорту и аортальный клапан. Затем внутренняя поверхность сердечной мышцы будет резецирована под прямым наблюдением, чтобы снять закупорку в тех областях, где она утолщена.
Количество удаляемой мышцы варьируется от 3 до 15 г, и резекция тщательно планируется и проводится с учетом всех индивидуальных анатомических характеристик сердца пациента. Иногда резекции мышцы недостаточно, и тогда может потребоваться восстановление или замена митрального клапана.
Спиртовая абляция перегородки
Алкогольная абляция перегородки (ASA) — это нехирургическое уменьшение толщины мышцы желудочка в области оттока.В отдельных случаях это клинически эффективный терапевтический вариант. Во время процедуры кончик катетера вклинивается в небольшую артерию, которая снабжает кровью толстую мышцу. Затем область кровоснабжения тщательно проверяется с помощью специальной визуализации.
Если возможно, инфаркт создается в этой области путем введения небольшого количества этанола (спирта) через катетер. Это приводит к образованию рубцов и уменьшению толщины стенки, что уменьшает или даже устраняет препятствие.Однако улучшение может проявиться не сразу после процедуры.
ASA может воздействовать только на толщину мышц, а не на другие компоненты внутренней анатомии сердца, и степень уменьшения мышечной массы также ограничена. В случаях, когда потребуется значительное уменьшение толщины стенки, это будет означать индукцию большого инфаркта миокарда, что может увеличить риск процедуры.
Семейная гипертрофическая кардиомиопатия: MedlinePlus Genetics
Мутации в одном из нескольких генов могут вызвать семейную гипертрофическую кардиомиопатию; наиболее часто задействованы гены MYH7 , MYBPC3 , TNNT2 и TNNI3 .Другие гены, в том числе некоторые, которые не были идентифицированы, также могут быть вовлечены в это состояние.
Белки, продуцируемые генами, связанными с семейной гипертрофической кардиомиопатией, играют важную роль в сокращении сердечной мышцы, образуя структуры мышечных клеток, называемые саркомерами. Саркомеры, которые являются основными единицами сокращения мышц, состоят из толстых и тонких белковых нитей. Перекрывающиеся толстые и тонкие нити прикрепляются друг к другу и отпускаются, что позволяет нитям перемещаться относительно друг друга, так что мышцы могут сокращаться.В сердце регулярные сокращения сердечной мышцы перекачивают кровь к остальному телу.
Белок, продуцируемый геном MYH7 , называемый тяжелой цепью сердечного бета (β) -миозина, является основным компонентом толстой нити в саркомерах. Белок, продуцируемый геном MYBPC3 , сердечным миозин-связывающим белком C, связывается с толстым филаментом, обеспечивая структурную поддержку и помогая регулировать мышечные сокращения.
Гены TNNT2, и TNNI3 предоставляют инструкции по производству сердечного тропонина Т и сердечного тропонина I, соответственно, которые являются двумя из трех белков, составляющих комплекс тропониновых белков, обнаруженных в клетках сердечной мышцы.Комплекс тропонинов ассоциируется с тонкой нитью саркомеров. Он контролирует сокращение и расслабление мышц, регулируя взаимодействие толстых и тонких волокон.
Неизвестно, как мутации в генах, связанных с саркомерами, приводят к гипертрофии сердечной мышцы и нарушениям сердечного ритма. Мутации могут привести к изменению белка саркомера или снижению количества белка. Нарушение или нехватка любого из этих белков может нарушить функцию саркомера, нарушая нормальное сокращение сердечной мышцы.Исследования показывают, что у пораженных людей сокращение и расслабление сердечной мышцы является ненормальным даже до того, как разовьется гипертрофия. Однако неясно, как эти проблемы с сокращениями связаны с гипертрофией или симптомами семейной гипертрофической кардиомиопатии.
Гипертрофическая кардиомиопатия (ГКМП) | BHF
Ищете информацию о коронавирусе (Covid-19)?
Если вы или кто-то, кого вы любите, страдаете сердечным заболеванием и нарушением кровообращения, или если вы подвергаетесь повышенному риску заражения коронавирусом (Covid-19), посетите нашу страницу о коронавирусе для получения регулярно обновляемой информации по ряду тем.
Получить информацию о коронавирусе
HCM — это генетическое заболевание, вызванное изменением или мутацией в одном или нескольких генах, и передается через семьи. Каждый ребенок кого-то с HCM имеет 50-процентный шанс унаследовать это заболевание.
Около 1 из 500 жителей Великобритании страдает этим заболеванием, хотя у большинства людей симптомы отсутствуют.
Как HCM влияет на мое сердце?
Если у вас HCM, мышечная стенка вашего сердца — миокард — утолщается, что делает сердечную мышцу жесткой.
Из-за этого утолщения сердцу становится труднее перекачивать кровь из сердца и по всему телу.
Толщина ваших мышц и их поражение варьируется от человека к человеку. Левый желудочек (одна из четырех камер сердца) почти всегда поражен, а у некоторых людей утолщается и мышца правого желудочка.
Укол от гриппа
Всем, у кого есть проблемы с сердцем и кровообращением, рекомендуется делать прививку от гриппа ежегодно, и в этом году это важно, как никогда.
Узнать больше
Каковы симптомы HCM?
Общие симптомы включают:
- Одышка
- Боль в груди
- Сердцебиение
- Головокружение и обмороки
Вы можете обнаружить, что у вас никогда не было серьезных проблем, связанных с вашим состоянием, и с помощью лечения ваши симптомы следует контролировать. Однако некоторые люди могут обнаружить, что их симптомы ухудшаются или их становится труднее контролировать в более позднем возрасте.
Область сердечной мышцы, на которую влияет HCM, и степень ее жесткости определяют, как симптомы влияют на вас.
У некоторых людей в результате HCM может развиться ряд других состояний. Они могут включать нарушения сердечного ритма или аритмии, включая блокаду сердца и эндокардит.
Как диагностируется ГКМП?
Наиболее распространенные тесты на гипертрофическую кардиомиопатию:
- ЭКГ — регистрирует электрическую активность вашего сердца.
- Эхокардиограмма — показывает пульсирующую активность вашего сердца.
- Тест с физической нагрузкой — в этом тесте ЭКГ записывается, когда вы находитесь на беговой дорожке или велотренажере, чтобы увидеть, как работает ваше сердце, когда оно более активно.
- МРТ — создает подробные изображения ваших внутренних органов, например сердца.
Генетическое тестирование на HCM
Гипертрофическая кардиомиопатия — это наследственное заболевание сердца, что означает, что оно передается через семьи.Если ваш врач считает, что у вас HCM, вам могут предложить генетический тест для выявления дефектного гена, который может вызывать ваше заболевание.
Если у вас обнаружится дефектный ген, ваш специалист может попросить вас помочь в определении близких родственников, таких как родители, братья и сестры или дети, которые также могли унаследовать этот ген.
Как можно скорее пройти тестирование означает, что лечение можно начать как можно быстрее, что снизит риск развития опасных для жизни нарушений сердечного ритма.
Для получения информации о ближайшей клинике по поводу наследственных заболеваний сердца и поддержки в отношении генетического тестирования позвоните в Службу генетической информации BHF по телефону 0300 456 8383 .
Фонд Майлза Фроста
Майлз Фрост, сын сэра Дэвида Фроста, скончался в возрасте 31 года после остановки сердца, вызванной недиагностированной гипертрофической кардиомиопатией.
Его семья и BHF объединили свои усилия для создания Фонда Майлза Фроста, который собрал 1,5 миллиона фунтов стерлингов для организации служб генетического тестирования по всей стране.
Фонд Майлза Фроста
Как лечится HCM?
В настоящее время не существует лекарства от HCM, но существуют методы лечения, которые помогают контролировать ваши симптомы и предотвращать осложнения. Ваше лечение будет зависеть от того, как поражено ваше сердце и какие у вас симптомы.
Вам может понадобиться:
- Лекарства — для контроля артериального давления, нарушения сердечного ритма или других симптомов, которые у вас могут быть
- Кардиостимулятор — для контроля частоты пульса
- МКБ — если вы подвержены риску опасного для жизни нарушения сердечного ритма.
Как HCM повлияет на меня?
Исследования показали, что при правильном лечении и последующем наблюдении большинство людей с этим заболеванием живут нормальной жизнью.
Однако, поскольку существует очень небольшой риск развития опасного для жизни нарушения сердечного ритма, небольшое количество людей с ГКМП подвержены риску внезапной сердечной смерти. Важно обсудить этот риск со своим врачом, который может предложить лекарства или посоветовать вам установить ИКД, если вы находитесь в группе повышенного риска.
Возможно, вам придется внести небольшие изменения в свой образ жизни, например, отказаться от соревновательных видов спорта, но вы должны иметь возможность продолжать работать и, например, водить машину.
Однако вы не сможете управлять грузовым автомобилем или коммерческим пассажирским транспортным средством, и вам, возможно, придется пересмотреть ручную работу, которая связана с тяжелой деятельностью.
Удар сердца от гипертрофической кардиомиопатии
Наше финансирование исследований уже помогло ученым лучше понять сердечные заболевания, такие как гипертрофическая кардиомиопатия.
Это исследование стало возможным только благодаря щедрым пожертвованиям общественности. Ваши пожертвования помогают нам финансировать сотни ведущих ученых по всей Великобритании, работающих над более чем тысячей различных исследовательских проектов, но еще многое предстоит сделать.
Пожертвовать
Для получения дополнительной информации
Позвоните в нашу Службу генетической информации BHF по номеру 0300 456 8383 , чтобы поговорить с одной из наших медсестер, чтобы получить информацию о наследственных заболеваниях сердца и о том, как они могут повлиять на вас и вашу семью.
Хотите узнать больше?
Закажите или скачайте наши публикации:
.


 childheart.ru/ (для детей)
childheart.ru/ (для детей)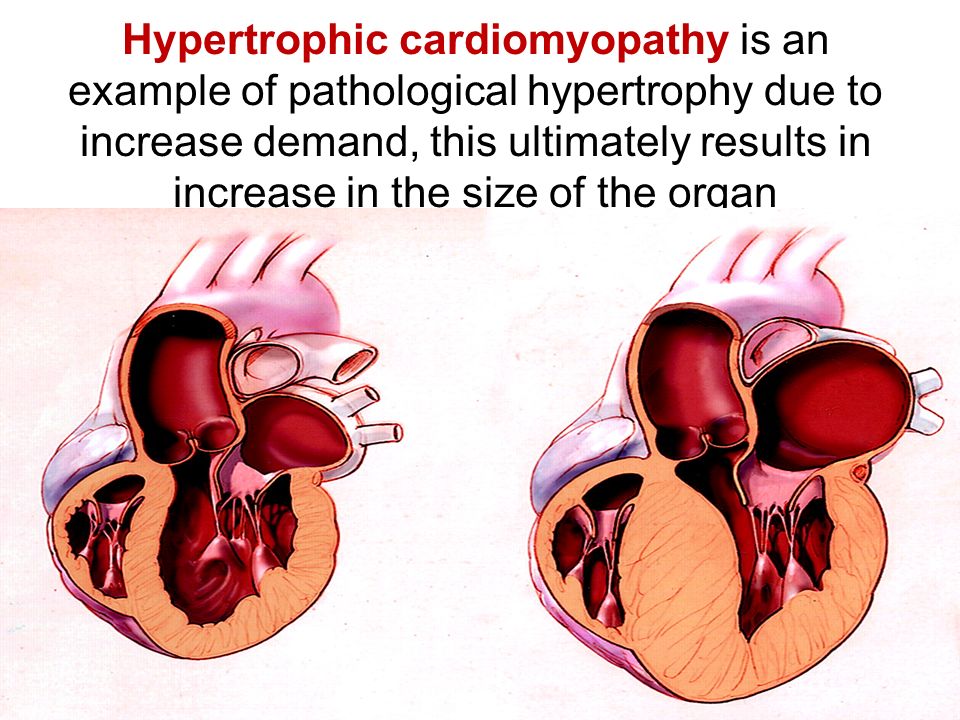 korablik-fond.ru
korablik-fond.ru
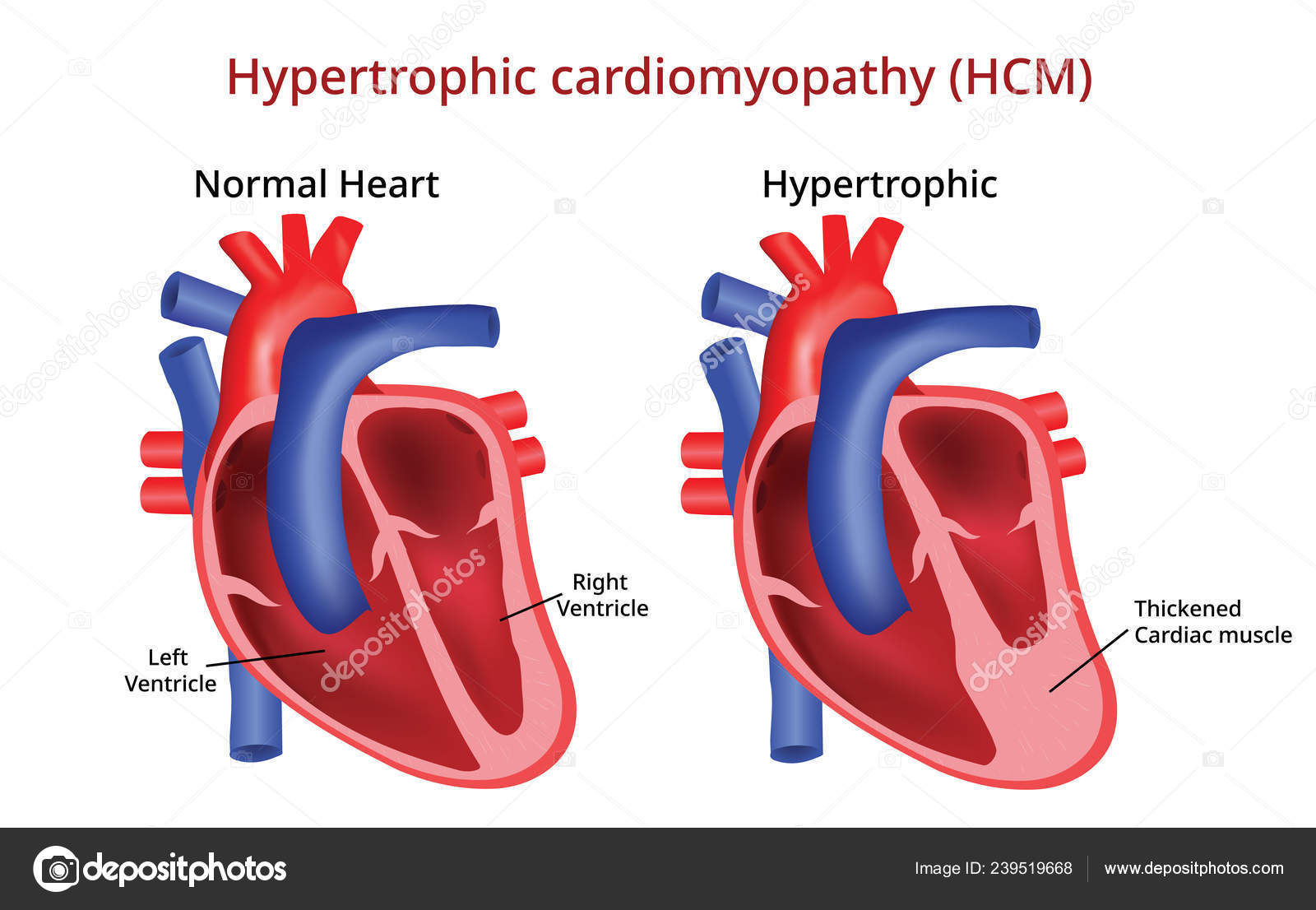
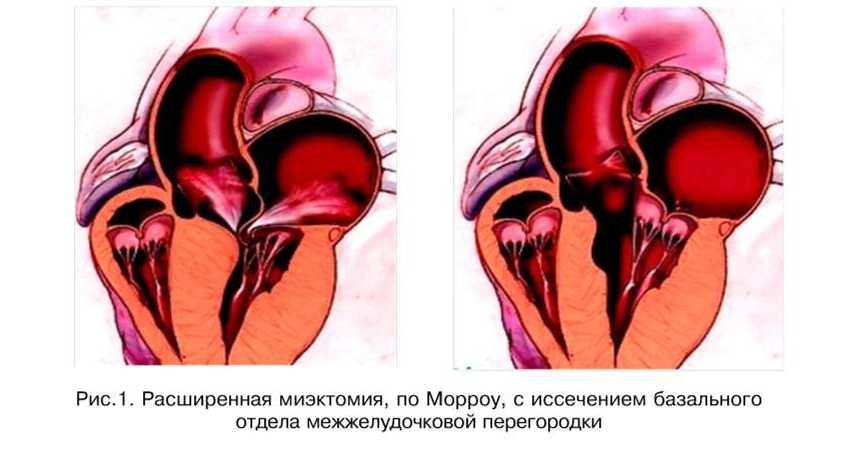 Спросите своего врача о конкретных рекомендациях по употреблению жидкости и диете, включая информацию об алкогольных напитках и продуктах с кофеином.
Спросите своего врача о конкретных рекомендациях по употреблению жидкости и диете, включая информацию об алкогольных напитках и продуктах с кофеином.