Резекция желудка: осложнения, противопоказания, реабилитация
Часто резекция желудка — единственный способ сохранить жизнь пациента. Эта тяжелая операция имеет ряд противопоказаний и способна привести к развитию послеоперационных осложнений. Поэтому ее проведение — это крайняя мера, на которую идут врачи, после использования всевозможных консервативных методов лечения.
Показания и противопоказания
Резекция (код по международной классификации К91.1) проводится с целью спасти жизнь пациента или предотвратить развитие серьезных заболеваний. Но бывают ситуации, когда проведение операции по удалению желудка невозможно. Такое случается, если состояние пациента осложнено асцитом, метастазами, туберкулезом или эндокринными заболеваниями. Показания к проведению операции принято разделять на абсолютные, когда речь идет о немедленном оперативном вмешательстве, и относительные, например, ожирение, ХЯБ, разрастание полипов в желудке. При синдроме Золлингера-Эллисона, когда опухоль, диагностируемая в поджелудочной железе, провоцирует усиленный синтез гастрина, также показано удаление желудка или железы. Абсолютные показания, это такие заболевания, как:
Абсолютные показания, это такие заболевания, как:
- рак;
- большие доброкачественные опухоли;
- длительные язвенные кровотечения;
- сужение пилоруса;
- пенетрация или перфорация язвы.
Вернуться к оглавлению
Предоперационная подготовка
Непосредственно перед процедурой больной повторно проходит полную лабораторную диагностику.
Операции проводится после полного и комплексного обследования пациента, включающего такие диагностические процедуры, как:
- анализы крови, определение ее группы и свертываемости;
- ФГДС;
- УЗИ желудка, щитовидки, желчных протоков и печени;
- определение функционального состояния легких;
- анализ мочи;
- ЭКГ;
- печеночные пробы;
- рентген органов грудной клетки.
Непосредственная подготовка пациента к операции начинается с установления ему специального режима дня и питания. Для профилактики осложнений пациенту рекомендуют не принимать медикаменты на основе ацетилсалициловой кислоты и нормализовать вес. За день до вмешательства прекращают прием пищи и делают очистительную клизму.
За день до вмешательства прекращают прием пищи и делают очистительную клизму.
Вернуться к оглавлению
Виды и методы резекции
Существует много разных техник проведения операции.
Проведя полное обследование пациента и выяснив локализацию проблемного участка в органе, врач определяется с методикой проведения операции. Эндоскопическое вмешательство наименее травматичное и быстрое. Учитывая размер патологии и ее локализацию (в дистальной, проксимальной или срединной части), проводят такие виды резекции:
- частичная;
- обширная;
- субтотальная;
- тотальная.
Формируют анастомоз, используя две методики. Первая — резекция желудка по Бильрот 1. Она предусматривает соединение оставшейся части желудка с отверстием двенадцатиперстной кишки. Резекция желудка по Бильрот 2, при которой соединение происходит с тощей кишкой, применяется чаще. Возможны использования этих методов в модификации. Например, операция по Гофмейстеру Финстереру предусматривает формирование искусственного антрального клапана, а резекция желудка по Бальфуру — создание межкишечного соустья.
При ожирении удаляется бо́льшая часть органа, но сохраняются все его сфинктеры и клапаны. Этот вид операции называется рукавная или продольная резекция желудка (иные названия «слив» или вертикальная).
Вернуться к оглавлению
Техника выполнения полостной операции
Схему проведения операции определяют индивидуально в зависимости от поставленного диагноза.
Обследовав пациента, врач определяет метод резекции. Непосредственно перед хирургическим вмешательством, проводят очищение органов ЖКТ. Резекция желудка проводится под общей анестезией, но если существуют противопоказания к нему, то используют миорелаксанты для локального блокирования мышц и нервных окончаний.
Лапаротомическая операция начинается с верхнесрединного рассечения абдоминальной стенки. Сначала отделяют большой и малый сальники от ободочной кишки, большой кривизны и печени. Перевязывают правую и левую желудочные артерии и определяют уровень резекции органа. Дальнейшая схема действий зависит от того проксимальная, дистальная, рукавная или субтотальная резекция желудка требуется.
Непосредственное иссечение органа и формирование анастомоза проводят с помощью жома Пайра. Ним ограничивают место резекции с двух сторон, после чего электрокаутером разрезают стенку желудка и «запаивают» сосуды. Такую же процедуру проводят и с 12-перстной кишкой. Накладывают швы и формируют анастомоз. При неоперабельном раке ход операции меняется, накладывают обходной анастомоз, а брюшную полость зашивают.
Вернуться к оглавлению
Лапароскопический метод вмешательства
Такая техника позволит избежать больших разрезов.
Лапароскопическая клиновидная операция проводится эндоскопическим инструментарием через 5 отверстий в брюшной стенке. Удаление онкологического очага в слизистой желудка можно провести с помощью новых технологий, которые успешно внедрены в практику не только за границей, но и в отечественных клиниках. Эндоскопическая резекция слизистой и эндоскопическая диссекция подслизистого шара позволяют удалять полипы и онкологические новообразования, проводить рукавную операцию (слив), используя такие варианты, как:
- петлевая биопсия;
- аспирация слизистой;
- трансгастральная резекция;
- методика с использованием двух- или трехканального эндоскопа.

Эндоскопическая операция имеет ряд преимуществ. Устранение проблемы слизистой оболочки без нарушения физиологического строения желудка предупреждает многие возможные последствия, а пациент восстанавливается быстрее.
Вернуться к оглавлению
Осложнения после оперативного вмешательства
Возможно появление воспалительного процесса.
Постгастрорезекционные осложнения могут возникнуть сразу после операции или спустя время. Ранние из них, например, кровотечения или инфицирование раны, провоцирует воспаление, перитонит, шок. Часто повышается температура, падает АД, в результате чего наступает кома. Жизнь пациента после гастрэктомии меняется, возникают проблемы с пищеварением. Рассмотрим некоторые последствия резекции желудка подробнее.
Боль в животе, нарушение перистальтики и непроизвольная отрыжка возникают после приема небольшого количества еды. Излишек соли в рационе вызывает у пациента понос, а чрезмерно жирная еда — стеаторею и быструю потерю веса. Желудочный сок, проявляющий бактерицидные свойства, секретируется в недостаточном количестве, что потенцирует рост бактерий и такие осложнения после резекции желудка, как:
Желудочный сок, проявляющий бактерицидные свойства, секретируется в недостаточном количестве, что потенцирует рост бактерий и такие осложнения после резекции желудка, как:
- интоксикация;
- разрушение ворсинчатого эпителия кишечника и нарушение его всасывающей функции;
- панкреатит или недостаточность поджелудочной железы;
- рефлюкс желчи, в результате чего возникает изжога и рвота;
- кишечная непроходимость.
Если присутствуют 2 и более симптомов, говорят про пострезекционные синдромы. Среди них часто диагностируют, такие как:
- анастомозит;
- язвенное образование;
- постваготомическая диарея;
- демпинг-синдром;
- синдром приводящей петли;
- малокровие;
- синдром малого желудка (после тотальной или субтотальной резекции).
Вернуться к оглавлению
Синдром приводящей петли
После приема пищи болевые ощущения резко усиливаются.
Осложнение, возникающее после операции по Б2 способу. Загиб в месте соединения затрудняет отток кишечных соков и пищи, которые накапливаются здесь. Это провоцирует нарастающую боль, тошноту и рвоту. Медикаментозные средства при этом состоянии не эффективны. Пациенту рекомендуют питаться маленькими порциями. Если это не дает результата, то нужно сделать повторную операцию и новый анастомоз.
Это провоцирует нарастающую боль, тошноту и рвоту. Медикаментозные средства при этом состоянии не эффективны. Пациенту рекомендуют питаться маленькими порциями. Если это не дает результата, то нужно сделать повторную операцию и новый анастомоз.
Вернуться к оглавлению
Анастомозит
Наиболее частое органическое изменение после операции на желудке. Застойные явления и нарушение трофики слизистой оболочки приводят к стойкому болевому синдрому после еды, возникают расстройства пищеварения и всасывания, которые сопровождают вздутие, тошнота, слабость. Длительное раздражающее воздействие заканчивается хронизацией процесса, развитием эрозии или язвы. Такие типы осложнений требуют повторного оперативного вмешательства.
Вернуться к оглавлению
Демпинг-синдром
Удаление пилоруса нарушает эвакуаторную работу желудка. Ранняя его форма характеризуется появлением в течение часа после еды спазмов, поноса, учащенного сердцебиения и гипотонии. Поздний демпинг-синдром возникает спустя 2—3 часа, и вызван чрезмерным поступлением в кровь инсулина. Падение при этом уровня глюкозы сопровождается тахикардией, слабостью и помутнением сознания.
Падение при этом уровня глюкозы сопровождается тахикардией, слабостью и помутнением сознания.
Вернуться к оглавлению
Реабилитация
Первое время рекомендовано пищу измельчать.
Использование обезболивающих средств, нормализация кровообращения и метаболизма, а также качественный уход и профилактика осложнений — все это ускорит восстановление пациента. Успех реабилитации зависит от психоэмоционального благополучия, диеты, физической формы. Послеоперационный период требует покоя. Физические нагрузки должны быть минимальны, а движения нерезкими, со временем могут быть рекомендованы занятия ЛФК и пешие недлительные прогулки.
Полная реабилитация пациента длится 6—8 месяцев, в течение которых обязательно ношение бандажа, прием энзимов и регулярный, несколько раз в год, осмотр врача.
Вернуться к оглавлению
Особенности диеты
При удаленном желудке нужно соблюдать особый режим и рацион. Сначала пища вливается больному через зонд. Если застойных явлений не наблюдается, то постепенно вводят полужидкую отварную еду: бульоны, каши, супы. Частота приема — 4—6 раз в день. Категорически запрещены копчености, соленья, маринады, специи и другие продукты, стимулирующие желудочную секрецию.
Частота приема — 4—6 раз в день. Категорически запрещены копчености, соленья, маринады, специи и другие продукты, стимулирующие желудочную секрецию.
Вернуться к оглавлению
Послеоперационный прогноз
Успешная операция и реабилитация дает хорошие шансы для полного выздоровления. Если пациент не будет переходить границы дозволенного, вести правильный образ жизни и прислушиваться к мнению врача и диетолога, то сможет жить полноценной жизнью. Если операция проводилась для устранения онкологического заболевания, то в 80% случаев рецидива не случается.
Операция на желудке при раке: виды, реабилитация, последствия
Выполнение операции при раке желудка зависит от тяжести онкологического процесса и общего состояния пациента. Перед ее проведением необходимо пройти комплексное медицинское обследование. Существуют различные виды операций.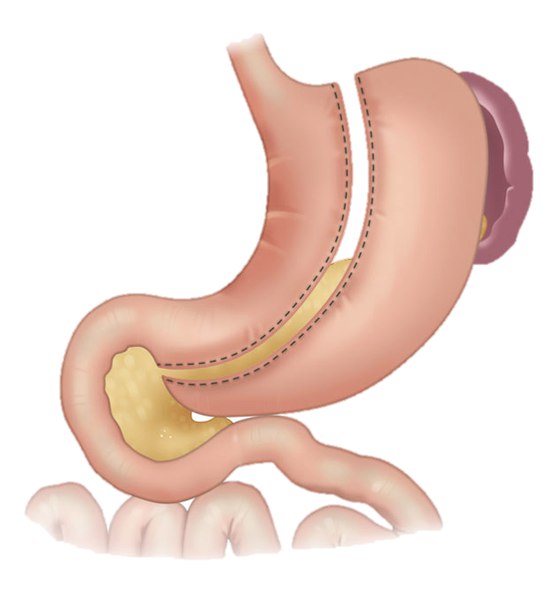 Выбор одного из них определяется локализацией и распространенностью новообразования.
Выбор одного из них определяется локализацией и распространенностью новообразования.
Показания к проведению
Операция по удалению желудка выполняется при наличии у пациента:
- злокачественного образования;
- поражение слизистой полипами;
- длительно протекающей язвы;
- массивного кровотечения;
- перфорации стенки органа;
- тяжелого ожирения.
При раковых опухолях показано полное удаление желудка. Однако, процедура проводится только в том случае, если в результате вмешательства удастся удалить большую часть атипичных клеток. Когда опухолевый процесс распространен и затрагивает другие жизненно важные органы, то процедура не выполняется. Субтотальное или удаление части желудка с сохранением культи проводится в случае распространенных полипов или язвенного дефекта с кровотечением. Это позволяет сохранить минимальную функциональную активность.
Удаление желудка может быть частичным или тотальным.
Вернуться к оглавлению
Подготовка к операции
Перед удалением опухоли пациент проходит ряд обязательных лабораторных и инструментальных исследований:
Подготовительный этап к такому лечению – прохождение флюорографии.
- исследование каловых масс на скрытую кровь;
- общий анализ крови;
- коагулограмма;
- моча на исследование;
- ультразвуковая диагностика органов брюшной полости;
- флюорография;
- фиброгастродуоденоскопия с выполнением биопсии.
Перед тем как проводится резекция желудка пациенту необходимо полностью остановить прием кроверазжижающих и противотромботических препаратов, а также нестероидных противовоспалительных средств. При наличии очагов хронической инфекции назначается курс антибактериальных препаратов. Также необходим отказ от курения и употребления алкогольных напитков. Больному назначается строгая диета с ограничением жирной, жареной и острой пищи. Необходимо начать дробное питание небольшими порциями. За день перед выполнением резекции желудка пациенту полностью запрещено есть и пить, что связано с возможной непереносимостью наркоза.
Вернуться к оглавлению
Виды и методика выполнения
Удаляют желудок под общим наркозом. Эта процедура является травматичной и проводится в несколько этапов. Сначала хирург выполняет вскрытие брюшной полости с ее ревизией. После делается мобилизация или отделение органа от брюшины и других образований. Далее соединяется пищевод с тонким кишечником, а после этого выполняется иссечение тканей органа. Модификации процедуры зависят от особенностей онкологии у больного.
Эта процедура является травматичной и проводится в несколько этапов. Сначала хирург выполняет вскрытие брюшной полости с ее ревизией. После делается мобилизация или отделение органа от брюшины и других образований. Далее соединяется пищевод с тонким кишечником, а после этого выполняется иссечение тканей органа. Модификации процедуры зависят от особенностей онкологии у больного.
Вернуться к оглавлению
Частичная проксимальная резекция
При удалении верхней части органа вместе с опухолью пациенту оставляют нижнюю.
Проводится если онкология расположена в верхней части желудка. Является органосохраняющей процедурой, при которой остается культя. Ее выполнение возможно при экзофитных образованиях до 4 сантиметров. При этом необязательно проводить полное удаление желудка при раке, а можно оставить небольшой участок непораженных тканей. Это ускоряет восстановление после оперативного вмешательства и улучшает прогнозы пациента. Данная манипуляция предусматривает то, что нижняя часть пищевода помещается в культю органа.
Вернуться к оглавлению
Частичная дистальная резекция
Необходимо делать при расположении новообразования в пилорическом отделе и незначительных размерах образования. Часто вместе с желудком в таком случае удаляют селезенку. С этой целью используют кибер нож, так как он помогает уменьшить выраженность кровопотери и осложнения, связанные с гиповолемией. Органосохраняющее лечение, к которому относится эта процедура, улучшает качество жизни пациента в послеоперационный период и уменьшает отрицательные последствия, вызванные нарушением пищеварения.
Вернуться к оглавлению
Полная резекция
Проводится при значительных размерах новообразования и эндофитном характере роста опухоли. Часто вместе с желудком удаляется и селезенка, так как именно в этот орган происходит преимущественное метастазирование атипичных клеток. В таком случае частичное удаление будет являться паллиативной процедурой, не приносящей необходимого лечения. После тотального удаления желудка пациенту потребуется пожизненный курс заместительной терапии препаратами желудочного сока.
Вернуться к оглавлению
Лапароскопическая операция
Удаление опухоли таким методом целесообразно при ее небольшом размере.
Лапароскопия является эндоскопической процедурой, выполняется через незначительные отверстия в брюшной полости с применением специальной камеры и инструментария. При этом вместо значительной травматизации тканей и широкого разреза у пациента остаются малозаметные шрамы. К такому лечению прибегают в случае незначительных размеров новообразования или при выполнении превентивной операции для предотвращения рака. Лапароскопическая гастрэктомия проводится крайне редко, так как при значительных размерах опухоли она длится очень долго. Это обуславливает также поздний срок постановки диагноза.
Вернуться к оглавлению
Удаление лимфоузлов
Проводится в том случае, если произошло метастазирование атипичных клеток в лимфатическую систему. Основные узлы, отходящие от желудка, находятся в области селезенки и иссекаются вместе с этим органом. Процедура проводится после удаления желудка или его части и может длиться недолго. В результате этого онкология не распространяется по всему организму. Прогноз для таких пациентов является более благоприятным.
В результате этого онкология не распространяется по всему организму. Прогноз для таких пациентов является более благоприятным.
Вернуться к оглавлению
Паллиативная помощь
Такая гастрэктомия при раке желудка выполняется в случае обширного поражения тканей онкологическим процессом. Она призвана улучшить качество жизни пациента и восстановить пищеварение. Проводится при нарушении эвакуации пищи из желудка или значительных размерах новообразования. При этом атипичные клетки иссекаются только частично, что не приводит к выздоровлению пациента, а только уменьшает симптомы рака.
Вернуться к оглавлению
Восстановление после операции
После такого лечения больному назначается курс химии.
После хирургического вмешательства пациенту требуется длительный период реабилитации. Он включает в себя заживление послеоперационного рубца и соблюдение диеты. Иногда прооперированным больным требуется заместительная терапия препаратами соляной кислоты и желудочного сока. Необходимо дробное питание часто и малыми порциями, что позволит желудку справиться с нагрузкой. Онкологическим больным после хирургического вмешательства проводится курс химиотерапии или облучение. Реабилитация после рака желудка требуется длительная и включает в себя физиопроцедуры и санаторно-курортное лечение.
Онкологическим больным после хирургического вмешательства проводится курс химиотерапии или облучение. Реабилитация после рака желудка требуется длительная и включает в себя физиопроцедуры и санаторно-курортное лечение.
Вернуться к оглавлению
Осложнения
При выполнении операции возможна сильная кровопотеря, что может вызвать гиповолемию, резкое падение артериального давления и летальный исход для пациента. Кроме этого, удаление раковой опухоли не гарантирует избавление от злокачественного процесса. В последующем возможно повторное развитие новообразования. Больные после вмешательства испытывают сильную боль и дискомфорт в брюшной полости, нарушается процесс пищеварения и усвоение основных компонентов пищи.
При неправильном питании после операции происходит истощение организма или кахексия.
Вернуться к оглавлению
Когда нельзя лечить рак желудка хирургически?
Удаление или комбинированные резекции желудка не выполняются в таких случаях:
Удалять орган нельзя, если больной неподвижен.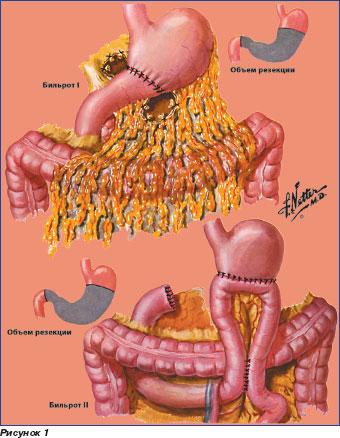
- наличие метастазов в других органах;
- тяжелая соматическая патология;
- спаечный процесс желудка;
- кахексия;
- неподвижность и отеки конечностей;
- тяжелая инфекция.
Вернуться к оглавлению
Прогнозы и последствия
После того как желудок удален и значительная часть атипичных клеток устранена из организма, пациенту становиться проще побороть онкологическую патологию. Исход заболевания зависит от общего состояния здоровья больного и степени мутации клеток. При наличии метастазов в другие органы прогноз для жизни человека неблагоприятный. Если они отсутствуют, то может наступить продолжительная ремиссия.
ПОСЛЕ ОПЕРАЦИИ РАКА ЖЕЛУДКА
MedTravel Лечение за рубежом » Онкология » После операции рака желудка
ПОСЛЕ ОПЕРАЦИИ РАКА ЖЕЛУДКА
После окончания операции пациент приходит в себя в реанимационной палате или отделении интенсивной терапии. Это стандартное мероприятие после крупных операций. Как только врач убедиться в том, что состояние пациента стабильно, его переводят в обычную палату. Чаще всего это происходит через день или два. В отделении интенсивной терапии за пациентом непрерывно наблюдают медицинские сестры, и его состояние тщательно контролируется. Важно понимать, что это стандартный прием, который не означает каких-либо нарушений состояния пациента.
Это стандартное мероприятие после крупных операций. Как только врач убедиться в том, что состояние пациента стабильно, его переводят в обычную палату. Чаще всего это происходит через день или два. В отделении интенсивной терапии за пациентом непрерывно наблюдают медицинские сестры, и его состояние тщательно контролируется. Важно понимать, что это стандартный прием, который не означает каких-либо нарушений состояния пациента.
Хирург и анестезиолог внимательно отслеживают восстановление пациента после операции. Вы можете чувствовать сонливость после наркоза и обезболивающих препаратов.
Внутривенное введение жидкостей и дренаж
Приходя в себя после наркоза, пациент может обнаружить несколько установленных катетеров. Это немного странно. Однако к этому будет легче адаптироваться, зная, для чего они нужны.
У пациента могут быть установлены:
Вокруг операционной раны могут быть установлены один или несколько дренажей: они предотвращают скопление в месте операции крови, желчи и тканевой жидкости.
Назогастральный зонд проводится через нос в желудок: по нему отводится желудочное содержимое для уменьшения тошноты.
Катетеры для внутривенной инфузии: они нужны для переливания крови и жидкостей, пока пациент не сможет снова нормально питаться и пить.
В мочевой пузырь устанавливается катетер (трубка) для выведения мочи и измерения ее объема.
Дренажная трубка также устанавливается в грудную клетку, если пациенту проводилась эзофагогастрэктомия. Она может соединяться с отсосным резервуаром. Его работа обеспечивает восстановление равномерного раздувания легких воздухом после операции на грудной клетке.
После пробуждения от наркоза пациент также может обнаружить на руке манжету для измерения артериального давления. На одном из пальцев кисти будет установлен пульсоксиметр — маленький зажим, который измеряет пульс и содержание кислорода в крови. На лице некоторое время может находиться кислородная маска. После выхода из наркоза давление измеряется довольно часто в первые несколько часов. Средний медицинский персонал измеряет количество выделяемой мочи, поскольку это показывает наличие дегидратации (обезвоживания) или, напротив, избыток жидкости в организме.
Средний медицинский персонал измеряет количество выделяемой мочи, поскольку это показывает наличие дегидратации (обезвоживания) или, напротив, избыток жидкости в организме.
Обезболивающие препараты
К внутривенному катетеру может быть присоединено несколько автоматизированных помп. Одна из них контролирует введение в организм обезболивающего препарата. Пациенту может быть предоставлено ручное управление этой помпой. При необходимости нажатие кнопки обеспечивает дополнительное введение болеутоляющего средства. Такой принцип обезболивания называется «аналгезией, контролируемой пациентом». Если система для самостоятельного введения болеутоляющих средств находится у вас под рукой, используйте ее при первой же необходимости. Вы не сможете передозировать препарат: система настроена так, чтобы избежать таких ситуаций. Если вам слишком часто приходится прибегать к помощи системы с анальгетиком, сообщите об этом врачу. Возможно, потребуется увеличение дозы препарата.
В первые дни после операции в некоторых больницах проводится эпидуральная анестезия. Обычно она очень хорошо помогает пациенту. При этом в спинномозговой канал вводится очень тонкая трубка и соединяется с помпой, которая обеспечивает постоянное поступление обезболивающих препаратов в организм. При сохранении боли медицинская сестра может увеличить дозу поступающего препарата.
В течение недели после операции или около того, практически во всех случаях вас будут беспокоить боли. Однако самые различные обезболивающие средства помогают справиться с этим. Очень важно сразу же после возникновения болевых ощущений сообщить об этом медицинскому персоналу. Врачу нужна ваша помощь, для того, чтобы выбрать подходящий вам препарат и его дозу. Обычно при регулярном введении обезболивающие препараты действуют лучше.
Прием жидкостей и пищи
Деятельность кишечника приостанавливается на некоторое время после операции на любом отделе желудочно-кишечного тракта. Нельзя пить, и есть до того, как он не начнет снова нормально работать.
Нельзя пить, и есть до того, как он не начнет снова нормально работать.
Перед тем, как пациенту разрешается возобновить прием пищи и жидкости примерно через неделю после операции, проводится рентгенологическое исследование. Это необходимо для обнаружения несостоятельности хирургического соединения желудка с кишечником. Перед проведением исследования пациент выпивает краситель под названием Гастрографин. Это вещество хорошо видно на рентгенограмме, а поэтому врач легко увидит его утечку из кишечника.
Питание проводится внутривенно и через центральный катетер до тех пор, пока пациенту не разрешается самостоятельно принимать пищу и жидкости. Этот катетер устанавливается в крупную вену грудной клетки. Такой тип питания называется парентеральным. Кроме этого, с помощью так называемой «питающей» стомы, жидкая пища может вводиться непосредственно в кишечник. Другой способ введения жидкой пищи заключается в использовании трубки, которая проходит через нос в кишечник, так называемого назоеюнального зонда.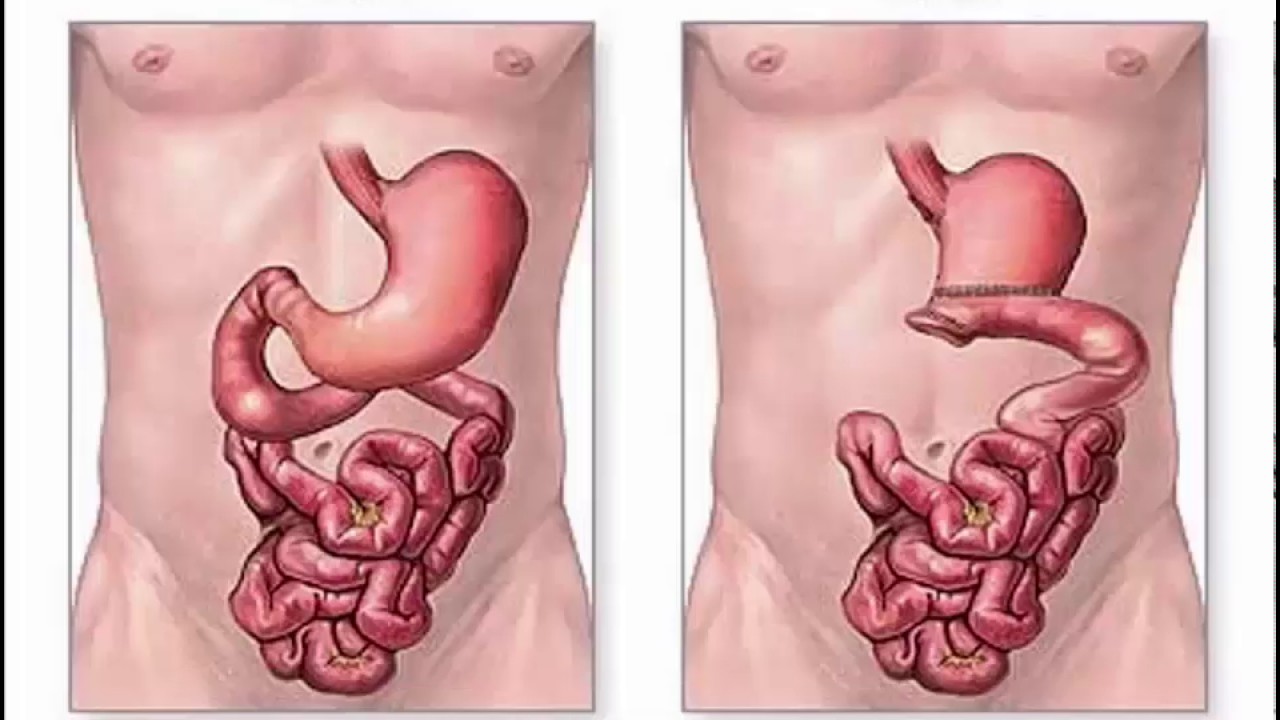
Самостоятельное питание после операции на желудке, которая может сопровождаться его полным удалением, должно начинаться очень медленно и осторожно. Сначала разрешается пить обычную воду маленькими глотками. Если пациент хорошо это переносит, то объем жидкости очень медленно увеличивается. Затем можно перейти на другие жидкости, например, молоко, чай или суп. После того, как пациент начинает переносить жидкость без тошноты или рвоты, катетер для внутривенной инфузии и назогастральный зонд удаляются.
Рана после операции
После операции на рану накладывается стерильная повязка. Рана будет закрыта ею в течение нескольких дней. Затем проводиться перевязка со сменой повязки и очисткой раны. до тех пор, пока из ране не перестанет выходить отделяемое, в ней будет находиться дренаж. Если дренаж соединяется с флаконом, то его необходимо менять каждый день. Обычно, дренажные трубки извлекаются через 3-7 дней после операции. Шовный материал или хирургические клипсы обычно остаются, по крайней мере, на 10 дней.
Физическая активность
В первые дни после операции движение будет казаться просто невозможным. Однако для восстановления организма движение крайне необходимо и должно начинаться постепенно. После операции каждый день пациента должен посещать физиотерапевт. Он проводит с пациентом дыхательные упражнения и тренировку для нижних конечностей.
Врач должен мотивировать пациента садиться в кровати и вставать уже через 1-2 дня после операции. Обращению с катетерами и дренажами обучат медицинские сестры. Постепенно, через несколько дней после операции трубки, флаконы и мешки начнут удаляться. После этого двигаться станет намного проще, и вы действительно ощутите, что идете на поправку.
Улучшение послеоперационного состояния
Вы сможете вставать с кровати и начнете двигаться через несколько дней. Ваше самочувствие постепенно улучшится. Скоро вы начнете, есть больше. Сначала вам потребуется множество небольших приемов пищи вместо привычных трех больших приемов пищи в день. Может потребоваться много времени для того, чтобы вернуться к трехразовому питанию. Некоторые пациенты предпочитают продолжать принимать пищу понемногу и часто. Диетолог проконсультирует вас перед выпиской и поможет составить план вашего нового питания. Он обязательно посоветует вам регулярно принимать витамины и есть больше богатой железом пищи.
Может потребоваться много времени для того, чтобы вернуться к трехразовому питанию. Некоторые пациенты предпочитают продолжать принимать пищу понемногу и часто. Диетолог проконсультирует вас перед выпиской и поможет составить план вашего нового питания. Он обязательно посоветует вам регулярно принимать витамины и есть больше богатой железом пищи.
Во время пребывания в больнице вам будет вводиться витамин B12. Вы не сможете больше получать витамин B12 из пищи, если в ходе операции была удалена значительная часть желудка или орган целиком. Вот поэтому, чтобы избежать его дефицит в организме, этот витамин нужно будет регулярно вводить в виде уколов.
Очень многие люди считают, что после удаления желудка или его большей части уже невозможно вернуться к прежней активной жизни. Что человек навсегда остается, зависим от строгой диеты, ему нельзя путешествовать, заниматься спортом и необходимо большую часть времени проводить дома (зимой прятаться от холода, весной от слякоти, летом от солнца, осенью от дождя).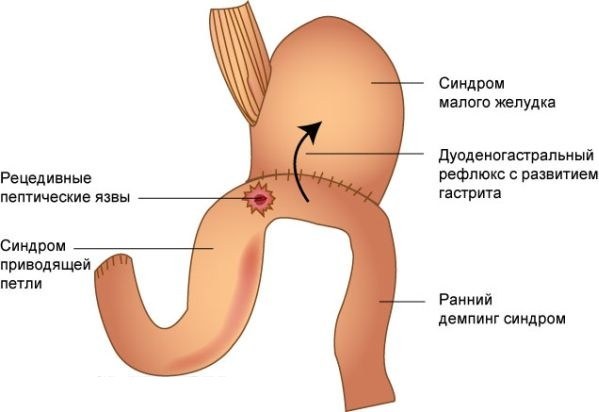 Бытует мнение, что человек, перенесший такую операцию, остается инвалидом навсегда.
Бытует мнение, что человек, перенесший такую операцию, остается инвалидом навсегда.
Это совершенно неправильно. Если правильно себя вести в первые несколько месяцев и соблюдать ряд простых правил в дальнейшем, возврат к полноценной жизни не только возможен, но и обязателен.
Режим дня не должен быть «охранительным», то есть направленным на максимальное оберегание человека от движения, работы по дому. Наоборот, выполнение домашних обязанностей, прогулки на свежем воздухе, активное поведение и общение очень полезно как для социологической реабилитации, так и для физической. Но не стоит перетруждаться. В первые месяцы после операции сил у организма еще не так много, чтобы взваливать на него непосильную ношу (тяжелый физический труд, постоянные общение с людьми, насыщенная трудовая деятельность). В то же время не стоит забывать о том, что окончательное срастание апоневроза (сухожильный «корсет» брюшной полости) проходит за несколько месяцев и поэтому врачи рекомендуют на 6 месяцев ограничивать физические нагрузки.
Действия, связанные с поднятием тяжести (работа в саду, профессиональная и бытовая деятельность) могут привести к образованию послеоперационной грыжи, что нередко требует повторной операции по ее ликвидации.
Также для профилактики грыжи необходимо избегать запоров, сильного кашля и чихания. Легкая общеукрепляющая гимнастика допускается, но без тренировки брюшного пресса. Для дополнительного укрепления послеоперационной раны на период формирования рубца рекомендуется ношение так называемого абдоминального бандажа – эластического пояса, подобного радикулитному. Это особенно необходимо, если Вы не спортсмен и мышечный «корсет» живота не тренирован.
Помимо физической активности очень важен и правильный психологический настрой. Необходимо максимальное количество положительных эмоций (книги, фильмы, юмор, приятные Вам родственники, соседи, знакомые).
Любимое хобби – очень полезный механизм, помогающий восстановить привычки и образ жизни, который был до операции. Разумеется, и здесь необходимо помнить про «золотую середину» — ежедневные гости и походы в кино, и театры очень скоро могут вызвать психологическую усталость.
Разумеется, и здесь необходимо помнить про «золотую середину» — ежедневные гости и походы в кино, и театры очень скоро могут вызвать психологическую усталость.
Очень важно следить и за дефекацией (так называется опорожнение кишечника). Эта, как кажется, далекая от желудка и деликатная проблема тоже очень важна. Необходимо стремиться и добиваться ежедневного стула (не менее 1 раза в сутки) диетой, эпизодически — легкими слабительными (длительный прием слабительных средств вреден). При сохраняющейся склонности к запорам необходимо обратиться к врачу-колопроктологу, который расскажет о продуктах питания, помогающих регулировать стул, и, при необходимости, подберет необходимые лекарственные препараты.
Особенно важно избегать запоров в первые 2-3 месяца после операции. Это связано с тем, что во время дефекации при запоре значительно повышается давление в брюшной полости (при постоянном и сильном натуживании), что еще более способствует образованию послеоперационной грыжи.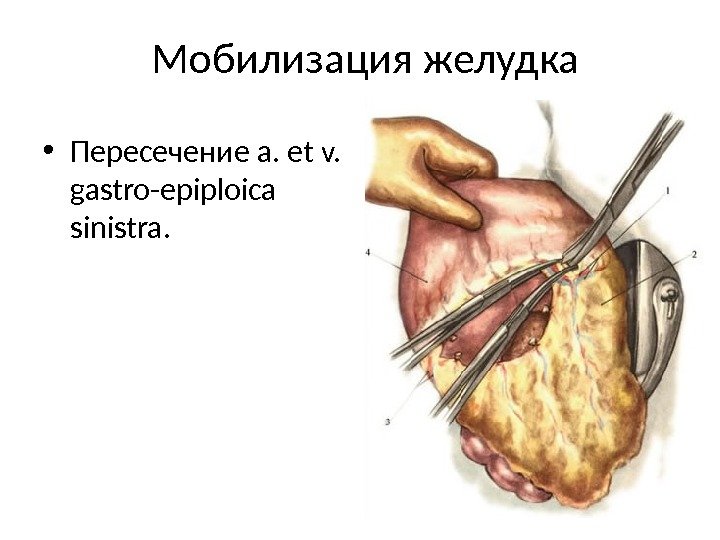 Кроме этого, повышение внутрибрюшного давления приводит к различного рода рефлюксам (обратным забросам), вызывают рефлюкс-гастрит культи (оставшейся части) желудка или рефлюкс-эзофагит (воспаление слизистой оболочки пищевода).
Кроме этого, повышение внутрибрюшного давления приводит к различного рода рефлюксам (обратным забросам), вызывают рефлюкс-гастрит культи (оставшейся части) желудка или рефлюкс-эзофагит (воспаление слизистой оболочки пищевода).
Ограничения после операции
Категорически запрещается проведение такому больному физиотерапии.
Очень нежелательно посещение солярия или загар под солнцем. Не нужно часто подвергаться тепловым нагрузкам (баня, сауна и тому подобное). Эти процедуры создают ненужную нагрузку на ослабленный после операции организм, на сердце и сосуды, а некоторые из вышеперечисленных воздействий (наиболее это касается физиотерапии) могут даже спровоцировать возврат болезни и появление метастазов или рецидива.
Особо следует сказать о беременности. Если женщина, перенесшая операцию по поводу рака желудка, хочет иметь ребенка, то такую ситуацию необходимо обязательно обсудить как с гинекологом, так и обязательно с онкологом. Такая настороженность связана с тем, что при беременности в организме женщины наступает сильнейшая гормональная перестройка, что тоже может дать толчок к возврату онкологического заболевания (нередко на фоне беременности раковые опухоли растут особенно быстро и агрессивно). В общем можно сказать, что очень нежелательна беременность в первые 3-5 лет после операции.
В общем можно сказать, что очень нежелательна беременность в первые 3-5 лет после операции.
Санаторно-курортное лечение не противопоказано, если операция прошла успешно и опухоль удалена полностью. После осмотра онкологом, терапевтом и другими необходимыми специалистами, как правило, можно пройти санаторно-курортное лечение в санатории гастроэнтерологического профиля в своей климатической зоне, то есть в каком-то местном учреждении, естественно, воздержавшись от физиотерапевтических процедур. Чистый воздух, вкусное и диетическое питание, красивая природа и приятное общение очень благотворно отражаются как на психологическом состоянии человека, так и на его физической форме.
Особенности питания после операции
Наиболее частые операции, выполняемые по поводу рака желудка – это резекция желудка (удаление большей части желудка) и гастрэктомия (удаление всего желудка).
Преследуя своей целью избавление человек от опухоли, при выполнении этих операций часто не удается избежать расстройств пищеварительной деятельности, так как теряется функция желудка как резервуара для пищи, дозировано пропускающего съеденное в кишечник. Следствием этого является более быстрое поступление пищи из пищевода в кишечник, что может служить причиной неприятных ощущений — у больного могут возникать ощущение тяжести в подложечной области, слабость, потливость, головокружение, учащенное сердцебиение, сухость во рту, вздутие живота (метеоризм), сонливость, желание прилечь. Эти явления называются демпинг-синдром. При тяжелом течении он может приводить к потере трудоспособности.
Следствием этого является более быстрое поступление пищи из пищевода в кишечник, что может служить причиной неприятных ощущений — у больного могут возникать ощущение тяжести в подложечной области, слабость, потливость, головокружение, учащенное сердцебиение, сухость во рту, вздутие живота (метеоризм), сонливость, желание прилечь. Эти явления называются демпинг-синдром. При тяжелом течении он может приводить к потере трудоспособности.
Чтобы избежать такого состояния или уменьшить интенсивность его проявления, те, кто перенес операцию на желудке, должны соблюдать следующие правила:
Питание при раке желудка является важной частью лечебного процесса. Для поддержания сил и восстановления вам необходимо получать достаточно калорий, белка, витаминов и минералов. После операции на желудке вам потребуются пищевые добавки с витаминами и минералами, такими как витамин D, кальций и железо. Также необходимы инъекции витамина B12. Принимать пищу небольшими порциями, но часто (6-8 раз в день). Есть не спеша, тщательно пережевывая пищу.
Необходимо ограничить прием тех продуктов, которые содержать в себе легко- и быстровсасывающиеся углеводы. Это варенья, сладкие молочные каши, мед, сахар и тому подобное. Полностью отказываться от этих продуктов не требуется.
Третье блюдо целесообразно принимать не сразу, а через ½ -1 час после приёма пищи, чтобы не перегружать желудок (если небольшая часть его сохранена) или начальные отделы кишечника, если желудок удален полностью. Количество жидкости за один прием не должно превышать 200 мл.
Очень важно, чтобы питание после операции на желудке было вкусным, разнообразным, включало все основные пищевые вещества. Особое значение придается полноценным животным белкам (содержащимся в нежирном мясе, курице, рыбе, яйцах, твороге, сыре) и витаминам (входящим в блюда из овощей, являющимися составными элементами фруктов, ягод, овощных и фруктовых соков, отвара шиповника и т. д.).
Особое внимание нужно уделять питанию в первые 2-3 месяца после выписки из больницы: именно в это время происходит приспособление системы пищеварения и организма в целом к новым условиям в связи с перенесенной операцией. Диета физиологически полноценная, с высоким содержанием белка, резким ограничением легкоусвояемых углеводов, нормальным содержанием жира. Ограничены химические раздражители слизистой оболочки и рецепторного аппарата желудочно-кишечного тракта. Исключены продукты и блюда, способные вызвать демпинг-синдром. Пища готовится в вареном, паровом, запеченном виде без грубой корки, непротёртая. Избегать употребления избыточно горячих и холодных блюд – они могут оказывать дополнительное раздражающее действие на слизистую оболочку кишечника.
В первое время питание должно быть дробным: 6 – 7 – 8 – 9 раз в сутки небольшими порциями. Диета должна быть полноценной по составу, особенно в плане белков (мясо, рыба). Обязательно свежие овощи и фрукты, кроме тех, которые вызывают выраженное «брожение» в кишечнике, супы и каши. В первое время необходимо стараться избегать жареной пищи. Еда должна быть щадящей термически (не горячей), механически (не грубой, хорошо прожеванной, или предварительно проваренной, прокрученной и т.п.) и химически (не острой, не жирной). Необходимо иметь в виду плохую переносимость после резекций желудка цельного молока (а вот кисломолочное можно все) и сладостей — конфеты, шоколад, халва и т.д. Ограничения в основном на первые 2-3 месяца, затем диету надо настойчиво расширять. Также надо будет постепенно увеличивать разовый объем (не взирая на болезненность, тошноту — культю желудка надо тренировать, что бы к концу года после операции вернуться к обычному 3 — 4-х разовому питанию) с сокращением кратности приема пищи. Если хотите попробовать какой-то новый продукт, то съешьте небольшой кусочек и подождите некоторое время (около 30 минут). Если не появилось никаких неприятных ощущений (боль, тошнота, рвота, вздутие живота, спазмы), то можно понемногу вводить этот продукт в рацион питания.
Как правило, в ближайшее время после операции полезно пройти курс любого препарата, восстанавливающего нормальную кишечную микрофлору (эуфлорин, нормофлорин, бактисубтил, колибактерин, лактобактерин, бификол — и тому подобных). Этот особенно актуально, если до или после операции пациенту назначали антибиотики. Чтобы правильно выбрать препарат и подобрать дозу и длительность приема, необходимо посоветоваться с гастроэнтерологом.
Разумеется, из употребляемых продуктов исключается алкоголь, особенно крепкие (водка, коньяк и т.п.) и газированные (пиво, шампанское) напитки. Обладая сильным раздражающим действием, он способен усиливать расстройства пищеварения.
Таким образом, правила питания после операции по поводу рака желудка достаточно просты и доступны. Следование им позволит избежать многих проблем, связанных с послеоперационным нарушением процессов пищеварения. Очень важную роль играет дисциплинированность пациента, так как необходимо избегать не только пренебрежения режима питания (это ведет к еще большим нарушениям функции кишечника), но и сознательного ужесточения его из-за боязни возвращаться в прежние рамки прима пищи.
Необходимо помнить, что разрешить любые вопросы, связанные с питанием, диетой и помогающим пищеварению лечением сможет Ваш врач — гастроэнтеролог.
(495) 50-253-50 — бесплатная консультация по клиникам и специалистам
ОФОРМИТЬ ЗАЯВКУ на ЛЕЧЕНИЕ
РАК ЖЕЛУДКА
|
На вопросы наших читателей, страдающих раком желудка, отвечает заместитель директора МНИОИ им. П.А. Герцена, профессор, доктор медицинских наук
СТАРИНСКИЙ ВАЛЕРИЙ ВЛАДИМИРОВИЧ | |
|
Профессор В.В. Старинский – ведущий специалист по организации противораковой борьбы в России. Много лет занимается изучением эпидемиологической ситуации, разработкой мер профилактики рака, совершенствованием принципов организации онкологической службы и формированием программ научных исследований по этим направлениям, разработкой федеральных стандартов диагностики и лечения злокачественных новообразований.
| |
Вопросы:
- Соглашаться ли на операцию по удалению желудка, если человек пожилой? Говорят, что после нее не выживают.
- Пациента выписали домой после операции на пищеводе/желудке. В больнице все было хорошо, а дома, даже если он выпьет воды, начинается неукротимая рвота, ничего не может есть.
- Если начался асцит, есть ли шанс провести какую-то терапию?
- Какую диету надо соблюдать после операции на желудке?
- Долго лечили от язвы, а оказался рак желудка. Можно ли заставить больницу оплатить лечение по раку желудка?
- Рецидив рака желудка после частичной операции, снова развилась непроходимость кишечника, больной ничего не ест и не хочет лечиться. Как его убедить?
1. Соглашаться ли на операцию по удалению желудка, если человек пожилой? Говорят, что после нее не выживают.
Рак желудка характерен для старшей возрастной группы, наиболее высокий уровень заболеваемости у мужчин от 70 лет и старше, что много больше, чем у 30-летних. У женщин отмечена та же тенденция, но они болеют в 2 раза реже мужчин. Правда, в молодом возрасте до 30 лет чаще болеют женщины.
Радикальное лечение рака желудка заключается в хирургическом удалении части желудка с опухолью и лимфатическими узлами – зонами возможного метастазирования. И именно хирургическое лечение отнесено к «золотому» стандарту, позволяющему добиться излечения. Отсюда ясно, что, отказавшись от операции, невозможно надеяться на мало-мальски продолжительную жизнь. В России такое лечение получают только 34% заболевших раком желудка. Все остальные не подлежат оперативному лечению из-за позднего обращения и большой распространённости процесса.
Нельзя серьёзно относиться к утверждению «после операции не выживают», поскольку в случае только такой альтернативы вряд ли лечащим онкологом предлагалась бы операция. Действительно, ещё в конце ХХ века отличная техника отечественных хирургов, но очень ограниченный спектр лекарственных препаратов, в том числе для анестезиологического пособия, не позволяли снизить планку послеоперационной смертности ниже 25%. Сейчас совершенно другие возможности, притом, что качественный состав больных остался практически без изменений: у 60-90% диагностируется III-IV стадии заболевания. На лечение попадают преимущественно пожилые больные с сопутствующими возрасту хроническими болезнями. Послеоперационные осложнения возникают у четверти пациентов, при распространённом раке – у трети, что понятно: большой объём и длительность операции; сложные биохимические нарушения, сопровождающие опухолевые процессы желудочно-кишечного тракта; наличие сопутствующих возрастных заболеваний.
Современное предоперационное обследование с использованием лапароскопической аппаратуры позволяет избежать более серьёзного вмешательства, что снижает послеоперационную летальность до 10%. Но нельзя сказать, что исключение хирургического вмешательства у непростого контингента улучшило бы результаты, поскольку при местно-распространённом раке расширились показания и частота выполнения паллиативных операций, позволяющих ликвидировать не только осложнения, вызываемые опухолью, но и саму опухоль. Неуклонно совершенствуются и операционная техника, и аппаратура, и лекарственные средства, используемые в анестезиологии и реанимации, что в совокупности и отражается на послеоперационных результатах.
2. Пациента выписали домой после операции на пищеводе/желудке. В больнице все было хорошо, а дома, даже если он выпьет воды, начинается неукротимая рвота, ничего не может есть.
Почти у каждого четвертого больного, оперированного по поводу данных заболеваний, развиваются нарушения процесса пищеварения в различных формах и проявлениях. Пострезекционные синдромы значительно ухудшают качество жизни, не только снижают работоспособность, но могут привести к инвалидизации. Термин «болезнь оперированного желудка», предложенный видным желудочным хирургом Е.Л. Березовым, получил широкое распространение и наиболее точно отражает патологическую сущность страдания.
Значительная часть постгастрорезекционных синдромов возникает вследствие наличия хронического сопутствующего патологического процесса: грыжа пищеводного отверстия диафрагмы, хронические нарушения дуоденальной проходимости, хронический панкреатит, желчнокаменная болезнь и другие.
Болезни оперированного желудка подразделяются на органические и функциональные. Органические: пептические язвы анастомоза или тощей кишки, рубцовое сужение анастомоза, свищи, каскадная деформация желудка, синдром приводящей петли и пр. Лечение их, как правило, хирургическое. Группа функциональных расстройств обусловлена новыми анатомо-физиологическими взаимоотношениями, создающимися после операции на желудке. К ним относятся: демпинг-синдром, гипогликемия и гипергликемия, энтерогенный синдром, диарея, гастростаз. У ряда больных развиваются стойкие гематологические расстройства, гиперхромная и пернициозная анемия.
Демпинг-синдром проявляется приступами резкой слабости с сосудистыми и нейровегетативными расстройствами. Обычно они возникают через 15-20 минут после еды, особенно сладких и молочных блюд. Тяжесть приступов колеблется от кратковременной общей слабости до пароксизмов полного физического бессилия. Легкая степень выраженности синдрома поддаётся корригирующей терапии, тяжёлая – оперативному лечению.
После резекции желудка по Бильрот-2 может развиться своеобразное страдание, получившее название синдрома приводящей петли: тошнота, горечь во рту, нарастающее чувство тяжести в подложечной области, больше справа, отрыжка. Симптомы постепенно нарастают, особенно после приема молока и жирной пищи, затем возникает обильная рвота с примесью желчи и без нее, дающая значительное облегчение. В тяжелых случаях рвота носит изнуряющий характер, нарушается переваривание и усвоение пищи, больные постепенно теряют в весе и слабеют.
В результате ускоренного опорожнения культи желудка в тонкую кишку попадает сразу большое количество углеводов. В крови резко повышается уровень сахара – гипергликемия, на что организм реагирует быстрым и избыточным выделением инсулина. Увеличение инсулина приводит к падению концентрации сахара и развитию гипогликемии. Синдром характеризуется мучительным чувством голода, слабостью, усиленным потоотделением, чувством жара, сердцебиением, головокружением, потемнением в глазах, дрожью в теле. Приступ возникает через 2-3 ч после еды и длится от нескольких минут до 1,5-2 часов. Может осложняться потерей сознания.
Функциональный гастростаз возникает из-за нарушения ритма перистальтической (сокращение) волны желудка и ведёт к дискоординации по времени и направлению движений. Оставшаяся после операции часть желудка не может своевременно и правильно опорожняться и растягивается. Гастростаз проявляется ощущением полноты в подложечной области, тошнотой, тупой болью, обильной рвотой застойным желудочным содержимым. Рвота облегчает состояние больного, что побуждает вызывать её искусственно.
В половине случаев имеются сочетанные осложнения. Наиболее часто наблюдается сочетание демпинг-синдрома с синдром приводящей петли. Демпинг-синдром нередко сопровождается гипогликемией. Демпинг-синдром и гипогликемия легкой и средней степени успешно лечатся правильной организацией питания, режима труда и отдыха. Тяжелая степень синдрома нередко требует оперативного вмешательства.
Постгастрорезекционные и постгастрэктомические синдромы весьма частые осложнения: около трети оперированных больных страдают рефлюкс-эзофагитом (заброс желудочного содержимого в пищевод), нарушением аппетита, демпинг-синдромом, гипогликемией, дисфагией, а также расстройством стула. По мере удаления срока операции клинические проявления этих расстройств уменьшаются. Раннее выявление этих синдромов, установление причины их развития и определение лечебной тактики позволяют избавить большинство больных от тяжелых страданий.
3. Если начался асцит, есть ли шанс провести какую-то терапию?
Распространение опухоли за пределы желудка и вовлечение в этот процесс брюшины, тончайшего серозного листка, покрывающего органы, может способствовать выработке большого количества жидкости. Асцит – скопление жидкости в брюшной полости. Нет закономерности между скоростью накопления, количеством вырабатываемой жидкости и размерами или количеством опухолевых узлов. Нередко метастазы по брюшине диагностируются только при хирургическом вмешательстве, именно с целью их выявления в обязательный алгоритм предоперационного обследования входит лапароскопия. Источником образования жидкости является капиллярная сеть листков брюшины, всасывание же идёт через лимфатические сосуды. Нарушение равновесия между скоростью образования и всасывания приводит к увеличению количества жидкости. Метастазы по брюшине увеличивают проницаемость кровеносных и вызывают обструкцию лимфатических сосудов, которые в норме могут вывести жидкости в 20 раз больше, чем её выработалось. Вторая причина асцита – нарушение оттока лимфы – «блок» – при опухолевом поражении лимфатических узлов брюшной полости.
В зависимости от количества жидкости асцит подразделяют на минимальный, умеренный и выраженный. Минимальный выявляется только при инструментальном исследовании – УЗИ или КТ брюшной полости. Умеренный асцит определяется при обычном осмотре. Асцит нередко приводит к появлению жидкости в плевральных полостях за счёт пропотевания из брюшной полости через диафрагму. Высокое стояние диафрагмы при асците способствует нарушению воздушности нижних отделов лёгких, где возможна активизация инфекции. Всё это усугубляет легочно-сердечную недостаточность. Повышение внутрибрюшного давления приводит к дальнейшим нарушениям со стороны пищеварительного тракта, тошноте и рвоте. Прогрессирует варикозное расширение геморроидальных вен и отёчность нижних конечностей.
На первом этапе асцит пытаются уменьшить сокращением приёма жидкости, соли и мочегонными. Но результаты такой терапии более чем скромны. Накопление жидкости требует её удаления – лапароцентеза – через небольшой прокол передней брюшной стенки. Беда в том, что в жидкости содержится большое количество белка – более 30 г/л, который восполнить у больного раком желудка практически невозможно, даже внутривенным введением альбумина. Получается замкнутый круг, когда из-за значительного ухудшения состояния не удалять жидкость невозможно, но и удаление несёт малое облегчение, так как влечёт усугубление белковой недостаточности.
Хирургическое удаление метастатических узлов нереально. Успехи химиотерапии при раке желудка вообще весьма скромны. Предпринимались попытки введения цитостатиков в брюшную полость после удаления излишней жидкости, но не то что не было позитивных результатов, напротив, превалировали только токсические реакции, ухудшающие и без того плохое самочувствие. Поэтому в настоящее время признано неразумным проведение химиотерапии у пациентов, страдающих раком желудка с асцитом. Остаётся только коррекция патологических симптомов – симптоматическая терапия.
4. Какую диету надо соблюдать после операции на желудке?
Во время пребывания в стационаре о питании расскажет лечащий врач. В ранний послеоперационный период каждый день в питании происходят перемены, приспосабливающие оставшуюся часть желудка к приёму пищи. С 14 дня на ближайшие 4 месяца, при отсутствии болезней оперированного желудка, предполагается частый приём богатой белком, негрубой пищи, желательно имеющей температуру тела.
Более подробно вопросы питания освещены на портале Help-Patient.ru
5. Долго лечили от язвы, а оказался рак желудка. Можно ли заставить больницу оплатить лечение по раку желудка?
Ежегодно на земном шаре заболевает раком желудка около 1 млн. человек. Уровень заболеваемости колеблется в достаточно широких пределах: максимальный отмечен у мужчин Японии (114,7 на 100 тыс. населения), а минимальный – у белых женщин США (3,1 на 100 тыс. населения).
Первичной профилактике рака желудка мешает отсутствие четкого специфического причинного фактора. Замечено, что на величину показателя заболеваемости раком желудка оказывает влияние характер и режим питания. Наличие в рационе достаточного количества растительной пищи и фруктов, животных и растительных белков существенно снижает риск возникновения рака желудка. Найден канцероген, способствующий развитию рака – Helicobacter pylori, заражение которой происходит в детстве через продукты питания. Показано, что рак развивается только у малого числа инфицированных H.pylori, но инфицированность повышает риск рака в 3-6 раз. Нитраты и нитриты, содержащиеся в овощах, также способствуют развитию рака. К предрасполагающим факторам относится атрофический гастрит, аденоматозные полипы размером свыше 2 см, послеоперационные рубцовые изменения желудка.
Позитивные результаты государственной программы скрининга рака отмечены в Японии. Программа довольно дорогостоящая, включает рентгенологическое исследование с барием и гастроскопию. В Европейских странах скрининг не практикуется, за исключением Англии, где его выполняют только страдающим хроническими заболеваниями желудка.
Ранний рак желудка бессимптомен, клиническая картина стёрта и ничем не отличается от клиники многочисленных неопухолевых заболеваний. Зачастую язвенная болезнь желудка, имеет более выраженную симптоматику. Все больные язвенной болезнью подлежат динамическому наблюдению с периодической гастроскопией, хоть по своей сути язвенная болезнь желудка не является предраковым процессом, но рак и язва могут сосуществовать и 70% ранних раков имеет форму язвы. При гастроскопии берётся ткань из подозрительных мест для гистологического исследования.
Но для выявления рака одной гастроскопии недостаточно, опухоль может распространяться под слизистой оболочкой, не нарушая её, и увидеть её можно при рентгеновском исследовании с барием, и то при достаточном распространении. Только комбинация обоих исследований позволяет с большой долей вероятности выявить опухолевое поражение желудка. КТ используется в основном для определения распространённости процесса перед операцией. Метод информативен, но очень дорог и, опять-таки, на некоторые вопросы не даёт однозначного ответа.
К сожалению, мы утратили позитивные стороны советской медицины, а именно, проведение обязательной бесплатной диспансеризации. Сейчас диспансеризация встречает затруднения как финансовые, так и со стороны работодателя, тем более что речь идёт о таких исследованиях как рентген желудка и гастроскопия.
Что касается Вашего конкретного случая, то нужно разбираться. На первом этапе достаточно написать претензию главному онкологу Вашего региона. Компетентная комиссия проведёт служебное расследование и сообщит свои выводы, которые могут иметь или не иметь судебную перспективу. Но и в случае признания вины лечебного учреждения в несвоевременной диагностике заболевания, достаточно сложно компенсировать финансовые траты, понесённые при лечении. Вы должны знать, что лечение онкологического заболевания в РФ обеспечивается бюджетом государства, то есть бесплатно всё: от таблетки до операции. Платное лечение рассматривается только как альтернатива бесплатному, обеспечивающее лучший сервис. И суд будет исходить из этих предпосылок. Если вы оплачивали лечение самостоятельно, то необходимо представить все чеки. Разбирательство потребует много сил и времени, а удовлетворение, как показывает жизнь, никогда не бывает полным.
6. Рецидив рака желудка после частичной операции, снова развилась непроходимость кишечника, больной ничего не ест и не хочет лечиться.
Как его убедить?
Выделяют ранние рецидивы рака желудка, развивающиеся в первые 3 года после хирургического лечения и поздние – по прошествии 3 лет. В 60% случаев повторная опухоль возникает в зоне анастомоза – хирургического соединения желудка с кишечной трубкой. Место расположения рецидивной опухоли и её размеры определяют клиническую картину и возможность её удаления. Чаще всего при расположении опухоли в зоне анастомоза возникает клиническая картина стеноза – непроходимости желудка, что усугубляется его малыми размерами в результате первого оперативного вмешательства. Клиническая картина стеноза характеризуется болевыми ощущениями после еды, чувством тяжести в подложечной области. Рвота – типична для непроходимости, она возникает через 4–6 часов после еды при скоплении в желудке большого количества пищевых масс. Рвота со временем приобретает постоянный характер, повторяясь ежедневно и принося значительное чувство облегчения. В рвотных массах отсутствует желчь, определяются прожилки свежей или измененной крови, а также остатки непереваренной пищи. Опухолевый стеноз желудка является жизненным показанием к хирургическому лечению, однако, операция возможна только после проведения полноценной предоперационной подготовки.
Основной радикальной операцией является экстирпация – полное удаление – оставшейся части желудка. Но предпринимаются и паллиативные вмешательства для ликвидации угрожающих жизни состояний, преимущественно кровотечения и восстановления проходимости желудочно-кишечного соустья. Выживаемость после повторных операций при раке резецированного желудка существенно не отличается от выживаемости после операций по поводу первичного рака желудка. Только 26% проживают после лечения рецидива 5 лет и более. Минимальная продолжительность жизни в среднем – около 17 месяцев, и здесь важная роль отводится гистологической структуре. Более неблагоприятная форма рака перстневидно-клеточная, менее – низкодифференцированная, при аденокарциноме минимальная продолжительность жизни в среднем 33,5 месяца.
Разумеется, человек вправе самостоятельно решать, как ему поступать: соглашаться на лечение или нет. Чаще при выборе нами управляют эмоции, и трезво подойти к оценке собственного состояния и своих перспектив поможет опытный психолог.
% PDF-1.4
%
112 0 объект
>
endobj
xref
112 81
0000000016 00000 н.
0000002443 00000 н.
0000002611 00000 н.
0000002646 00000 н.
0000003150 00000 н.
0000003263 00000 н.
0000003375 00000 н.
0000003488 00000 н.
0000003601 00000 п.
0000003715 00000 н.
0000003828 00000 н.
0000003941 00000 н.
0000004054 00000 н.
0000004167 00000 п.
0000004280 00000 н.
0000004394 00000 н.
0000005291 00000 п.
0000005929 00000 н.
0000006093 00000 н.
0000006130 00000 н.
0000006233 00000 н.
0000007397 00000 н.
0000008567 00000 н.
0000009287 00000 н.
0000009430 00000 н.
0000010066 00000 п.
0000010127 00000 п.
0000023635 00000 п.
0000024956 00000 п.
0000026121 00000 п.
0000026918 00000 п.
0000027557 00000 п.
0000028723 00000 п.
0000029571 00000 п.
0000029712 00000 п.
0000030575 00000 п.
0000031411 00000 п.
0000032246 00000 п.
0000032409 00000 п.
0000032709 00000 п.
0000032941 00000 п.
0000033811 00000 п.
0000034439 00000 п.
0000037132 00000 п.
0000047590 00000 н.
0000057953 00000 п.
0000069239 00000 п.
0000079163 00000 п.
0000082461 00000 п.
0000082521 00000 п.
0000092499 00000 п.
0000093610 00000 п.
0000093896 00000 п.
0000093950 00000 п.
0000105712 00000 н.
0000106532 00000 н.
0000106594 00000 п.
0000111400 00000 н.
0000113021 00000 н.
0000113306 00000 н.
0000113378 00000 н.
0000113547 00000 н.
0000113672 00000 н.
0000113772 00000 н.
0000113886 00000 н.
0000114023 00000 н.
0000114148 00000 п.
0000114261 00000 н.
0000114411 00000 н.
0000114509 00000 н.
0000114619 00000 п.
0000114734 00000 н.
0000114846 00000 н.
0000114987 00000 н.
0000115118 00000 п.
0000115246 00000 н.
0000115373 00000 п.
0000115474 00000 н.
0000115576 00000 н.
0000115687 00000 н.
0000001916 00000 н.
трейлер
] / Назад 206246 >>
startxref
0
%% EOF
192 0 объект
> поток
hb«f`Pa`c` Ȁ
Рак желудка: симптомы, осложнения и лечение
Содержание
В этой статье мы рассмотрим:
Вы можете нажать на любую из ссылок выше, чтобы перейти к интересующему вас разделу.
Что такое рак желудка?
Рак желудка или рак желудка — это рост аномальных клеток в слизистой оболочке желудка. Это относительно редкий тип рака, и пациенты редко проявляют какие-либо симптомы на ранних стадиях, что делает его одним из самых сложных злокачественных новообразований для диагностики на стадии 1.
Существует четыре основных типа рака желудка: аденокарцинома, лимфома, желудочно-кишечный тракт. Стромальная опухоль (GIST) и карциноидная опухоль.
Аденокарцинома
Это наиболее распространенный вид рака желудка, под эту категорию попадает примерно 90-95 процентов рака желудка.Здесь клетки внутренней оболочки желудка или слизистой оболочки ненормально размножаются, образуя опухоль.
Лимфома
Лимфома обычно поражает иммунную систему человека. В некоторых случаях этот вид рака развивается на стенках желудка.
Желудочно-кишечная стромальная опухоль (GIST)
Это редкая форма рака желудка, которая начинается в интерстициальных клетках Кахаля в желудке. Здесь одни клетки опухоли доброкачественные, а другие злокачественные.
Карциноидная опухоль
Этот тип рака желудка развивается в клетках желудка, вырабатывающих гормоны, и он также известен как желудочно-кишечные карциноидные опухоли. Преимущество этого рака в том, что он обычно не распространяется на другие органы.
Как возникает рак желудка?
Точная причина рака желудка до сих пор не известна. Онкологи считают, что заражение Helicobacter pyroli может быть вероятной причиной развития рака желудка.Это вызывает язвы в желудке, которые в будущем часто становятся злокачественными. В дополнение к этому, гастрит (воспаление в желудке), злокачественная анемия (разновидность хронической анемии) и полипы в кишечнике также могут вызывать рак желудка.
Как и все другие формы рака, рак желудка имеет 4 стадии.
Стадия 0: На этой стадии накопление нездоровых клеток развивается во внутренней оболочке желудка пациента, что имеет более высокую вероятность злокачественного образования в будущем.
Этап 1: Здесь у пациента уже есть небольшая злокачественная опухоль на внутренней оболочке желудка. Раковые клетки могут распространяться на близлежащие лимфатические узлы на стадии 1.
Стадия 2: На этой стадии злокачественные клетки распространяются в лимфатические узлы желудка, а также в более глубокие слои стенки желудка.
Стадия 3: Теперь раковые клетки присутствуют во всех слоях желудка, а также в некоторых прилегающих органах, таких как селезенка или толстая кишка.
Стадия 4: Это последняя стадия рака желудка, при которой раковые клетки присутствуют во многих органах, таких как печень, легкие и даже мозг.
Кто предрасположен к раку желудка?
Люди со следующими факторами риска более склонны к раку желудка, чем другие:
- История желудочно-кишечного рефлюкса (ГЭРБ)
- Дымный табак
- Употребляйте соленую и копченую пищу
- Включите в рацион меньше фруктов и овощей
- История инфекции Helicobacter pyroli
- Семейная история рака желудка
- История полипов и пернициозной анемии
Каковы симптомы рака желудка? Как диагностируется рак желудка?
Симптомы рака желудка включают:
- Тошнота и рвота
- Усталость
- Чувство переполнения или вздутия живота даже после приема небольших порций пищи
- Стойкая изжога
- Необъяснимая потеря веса
- Тяжелое несварение желудка в течение длительного периода
- Боль в желудке, потеря аппетита
- Кровавый стул
- Желтуха
Диагноз
У пациентов редко появляются какие-либо симптомы на ранних стадиях рака желудка.В большинстве случаев к тому моменту, когда онколог диагностирует это заболевание, опухоль уже достигла запущенной стадии. Врач сначала физически осматривает брюшную полость пациента, чтобы заметить какие-либо нарушения, и назначает тщательный анализ крови, в том числе обнаружение бактериальной инфекции H. pylori. Если отчет об анализе крови указывает на какие-либо отклонения в системе, онколог рекомендует дальнейшие исследования, такие как рентген, эндоскопия верхних отделов желудочно-кишечного тракта, ПЭТ-КТ и, наконец, биопсия.Биопсия может подтвердить или исключить наличие рака желудка.
Каковы осложнения рака желудка?
Если рак желудка прогрессирует до поздней стадии, это может привести к множеству осложнений, например:
- Желудочно-кишечное кровотечение
- Перфорация желудка
- Непроходимость тонкого кишечника
Как лечить рак желудка?
Лечение рака желудка зависит от того, как долго пациент был поражен этой болезнью.Если онколог диагностирует злокачественное новообразование на стадии 0 или стадии 1, то хирургическое вмешательство — лучший способ избавить пациента от рака.
На этапе 2 врачи проводят операцию вместе с последующей химиотерапией.
На третьем этапе химиотерапия является основным методом лечения. Врачи также могут порекомендовать полную гастрэктомию для удаления всего желудка вместе с химиолучевой терапией для лечения заболевания или уменьшения дискомфорта.
На 4 стадии трудно вылечить болезнь.Врачи назначают лечение для облегчения осложнений, например, установку стента для устранения закупорки желудочно-кишечного тракта или операцию обходного желудочного анастомоза для создания альтернативного маршрута прохождения пищи вокруг опухоли.
Операционный день в будние дни влияет на послеоперационные осложнения и долгосрочную выживаемость пациентов с раком желудка в Китае после лечебной гастрэктомии
Сообщается, что на долгосрочную выживаемость пациентов с карциномой желудка после гастрэктомии влияют многие факторы; В настоящем исследовании была предпринята первая попытка выяснить потенциальную роль хирургических вмешательств в будние дни в послеоперационном прогнозе пациентов с раком желудка.463 пациента с раком желудка успешно наблюдались. Для одномерного анализа использовался критерий Пирсона. Кривые выживаемости были построены с использованием метода Каплана-Мейера и оценены с использованием критерия логарифмического ранга. Модель пропорциональной регрессии рисков Кокса использовалась для определения факторов риска, а анализ подгрупп был проведен для исключения мешающих факторов. Мы обнаружили, что пациенты, перенесшие гастрэктомию в более поздний рабочий день (среда – пятница), легче страдали от более высокой послеоперационной заболеваемости.Рабочий день операции был одним из независимых индикаторов прогноза для пациентов после операции по поводу рака желудка. Однако в группе осложнений роль рабочего дня операции была существенно ослаблена. В заключение следует отметить, что операция, проведенная в более поздний будний день, с большей вероятностью приведет к увеличению послеоперационных осложнений и неблагоприятной роли в прогнозе пациентов с раком желудка в Китае после лечебной гастрэктомии.
1. Введение
При уровне смертности 498,0 / 100 000 рак желудка считается четвертым по значимости смертельным заболеванием, связанным с раком, и входит в пятерку наиболее часто диагностируемых онкологических заболеваний в Китае [1].Хотя ранняя диагностика рака желудка достигла большого прогресса благодаря быстрому развитию эндоскопической техники, исход злокачественного новообразования желудка остается неудовлетворительным [1]. Следовательно, исследователи заняты выяснением того, какие контролируемые факторы действительно влияют на прогноз, чтобы улучшить текущую безрадостную ситуацию с раком желудка. Долгосрочный результат после резекции желудка зависит от нескольких универсальных хорошо известных факторов, таких как дифференциация опухоли, количество пораженных лимфатических узлов, стадия TNM, техника операции и адъювантная терапия [2, 3].Сообщается, что даже экстремальный индекс массы тела и гипопротеинемия указывают на худший прогноз [4–6]. В настоящее время гастрэктомия по-прежнему является основным и широко распространенным методом лечения излечимой карциномы желудка. Хотя хирургия всегда дает более удовлетворительные результаты в опытных руках и в специализированных центрах [7], сообщается, что сопутствующие послеоперационные осложнения по-разному повышают качество послеоперационного периода и выживаемость [8–10]. Это указывает на то, что контроль послеоперационных осложнений может значительно улучшить неутешительную выживаемость.
Интересно, что в предыдущих исследованиях также сообщалось, что выбор хирургического дня в будний день действительно играл значительную роль в прогнозе после опухолевой резекции. При анализе 4 133 346 госпитализаций для плановых операций в операционной, Aylin et al. сообщили, что операция на более поздней неделе или в выходные увеличила послеоперационную 30-дневную смертность [11]. Пятилетняя смертность от излечимого рака пищевода увеличилась после операции в конце недели [12, 13]. Однако неясно, играет ли операционный день роль в послеоперационных осложнениях или в прогнозе рака желудка.
Таким образом, настоящее исследование было направлено на определение потенциальной роли операционного дня в будние дни в послеоперационных осложнениях, а также на долгосрочную выживаемость после гастрэктомии. В этом исследовании мы обнаружили, что пациенты, перенесшие операцию в более поздний будний день (со среды по пятницу), более легко страдали от повышенной послеоперационной заболеваемости и худшего прогноза рака желудка, чем пациенты в более ранний будний день. В совокупности наши результаты показали, что более строгий контроль послеоперационных осложнений и надлежащее планирование улучшат прогноз рака желудка.
2. Материалы и методы
2.1. Критерий отбора пациентов
Во-первых, мы получили одобрение Институционального наблюдательного совета Третьей больницы Сянъя Центрального Южного университета, Хунань, Китай. С 1 января 2012 г. мы ретроспективно собирали медицинскую и клинико-патологическую информацию о пациентах, которым был поставлен диагноз карцинома желудка и которые перенесли гастрэктомию в период с 1 января 2004 г. по 1 января 2010 г. в отделении желудочно-кишечной хирургии, Xiangya Third. Больница.Детали для набранных пациентов относятся к ранее описанным методам [14]. Критерии отбора были следующими: (1) у пациента была диагностирована карцинома желудка, гистологически подтвержденная по крайней мере двумя патологами, без отдаленных метастазов, и пациенту была проведена резекция желудка; (2) при необходимости выполнялась лимфаденэктомия с границей R0; (3) подробные сведения о клинико-патологических особенностях, послеоперационных осложнениях и информация о последующем наблюдении были доступны и сохранены; (4) продолжительность жизни после операции составила более 60 суток.Как следствие, в наш анализ было включено 463 пациента. Клинико-патологические данные были подробно собраны из оригинальных медицинских карт, как показано в Таблице 1; они были сгруппированы по клиническим, патологическим и терапевтическим признакам. Кроме того, стадия метастазов опухолевых узлов (TNM) была классифицирована в соответствии с 7-м изданием Американского объединенного комитета по раку, AJCC [15]. Вся личная информация была скрыта для обеспечения конфиденциальности. Дизайн и методы этого исследования соответствовали требованиям соответствующих нормативных документов и процедур (таких как GCP, ICH-GCP), а также этическим принципам.IRB Третьей больницы Xiangya Центрального Южного университета одобрил проведение исследования, номер разрешения — 2016-S232. Все авторы имели доступ к информации, которая могла идентифицировать отдельных участников во время или после сбора данных.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
2.2. Осложнения
Любое отклонение от нормального течения в течение 30 дней после операции рассматривалось как послеоперационное осложнение, которое детально фиксировалось (медицинские, хирургические, инфекционные осложнения и т. Д.). Согласно пересмотренной системе классификации Clavien-Dindo [16], конкретность была следующей: Осложнения I степени включают любое отклонение от протекшего без осложнений послеоперационного течения без необходимости фармакологического лечения или хирургических, эндоскопических и радиологических вмешательств, за исключением следующих лекарственных препаратов. : жаропонижающие, противорвотные, анальгетики, электролиты, диуретики, физиотерапия.Также были включены раневые инфекции и нутритивная поддержка. Осложнения II степени можно лечить только с помощью лекарств, переливания крови и парентерального питания. Осложнение III степени потребовало эндоскопического, радиологического или хирургического вмешательства. Степень IV включала опасные для жизни осложнения (включая осложнения со стороны ЦНС), которые требовали обращения в отделение интенсивной терапии. Степень III или IV в целом рассматривалась как тяжелое осложнение. V степень означала смерть пациента, которая была исключена из нашего анализа.Подробная информация представлена в Таблице 2.
| ||||||||||||||||||||||||||||||||||||||||
2.3. Последующее наблюдение
Включенные в исследование объекты наблюдались каждые 3 месяца в течение первого послеоперационного года и, по крайней мере, через 6 месяцев после этого для проверки выживаемости и рецидива. Данные были получены по телефону, письмом, сообщением и повторным посещением. Данные последующего наблюдения рассчитывались от даты операции до смерти или окончания сбора данных. Наблюдение прекращено 1 января 2015 года.
2.4. Статистика
Программное обеспечение SPSS (версия 16.0, Чикаго, Иллинойс) и призма GraphPad 5.0 были использованы для завершения всех статистических анализов и графиков. Чтобы прояснить возможные переменные, влияющие на послеоперационную заболеваемость, клинические, патологические и терапевтические характеристики были сгруппированы и сопоставлены между теми, у кого были осложнения или нет. При необходимости для одномерного анализа использовался критерий Пирсона или точный критерий Фишера. Кривые выживаемости были построены с использованием метода Каплана-Мейера и оценены с помощью критерия логарифмического ранга. Анализ подгрупп был проведен, чтобы исключить смешивающие факторы.Модель регрессии пропорциональных рисков Кокса использовалась для выявления факторов, которые были независимо связаны с общей выживаемостью и выживаемостью без болезней. Переменные со значением p менее 0,05 в одномерном анализе считались потенциальными кандидатами на основные эффекты и оценивались в пошаговом многомерном анализе Кокса. В многофакторном анализе статистически значимыми считались значения p менее 0,05.
3. Результаты
(1) Пациенты, которым была сделана гастрэктомия в более поздние будние дни, были предрасположены к послеоперационным осложнениям .С января 2004 г. по январь 2010 г. в исследование было включено 495 последовательных пациентов с карциномой желудка, перенесших гастрэктомию; из них 32 пациента умерли через 30 дней (степень V, <30 дней) после операции, и они были исключены из этого анализа. Как показано в Таблице 1, 198 пациентов перенесли операцию в предыдущий будний день (понедельник или вторник) и 265 пациентов в более поздний будний день (среда – пятница). Пациенты, перенесшие гастрэктомию в более поздний будний день, легче страдали от более длительной операции или большей кровопотери, связанной с операцией.Более того, пациенты, перенесшие гастрэктомию в более поздний будний день, имели более высокий риск послеоперационных осложнений. Однако мы обнаружили, что не было значительной разницы в распределении общего состояния (возраст, пол, история курения и ИМТ), болезненного состояния (сопутствующие патологии и степень ASA), состояния опухоли (дифференциация, размер, уровень CEA в сыворотке и TNM. этап) и терапевтический график (операция и адъювантная терапия) между двумя группами.
Около 21,8% (101/463) пациентов в конечном итоге испытали послеоперационные осложнения.У 34 пациентов в более ранний будний день были послеоперационные осложнения, а у 67 — в более поздний будний день. Они были разделены на 4 группы в соответствии с пересмотренной системой классификации Clavien-Dindo [16] (степень I; степень II; степень III; степень IV). Кроме того, мы обнаружили, что послеоперационная заболеваемость постепенно увеличивалась с понедельника по пятницу. Хотя это не является статистически значимым, степень тяжести осложнений увеличивалась со среды по четверг по пятницу. Более того, тяжелые осложнения (Grade III + Grade IV) в основном были сосредоточены в четверг или пятницу (Таблица 2).
(2) Хирургический рабочий день был связан с долгосрочным выживанием больных раком желудка после гастрэктомии . Для оценки потенциальных факторов, влияющих на прогноз рака желудка, была введена модель регрессии пропорциональных рисков Кокса. Однофакторный анализ (таблица 3) показал, что послеоперационная 5-летняя выживаемость была связана с сопутствующими заболеваниями, размером опухоли, временем операции, интраоперационной кровопотерей, послеоперационным уровнем СРБ в сыворотке крови, стадией TNM, адъювантной терапией и послеоперационными осложнениями.Стоит отметить, что операция в конце рабочего дня также способствовала неблагоприятному прогнозу после гастрэктомии. Затем переменные со значением p менее 0,05 в одномерном анализе были дополнительно объединены в многомерный анализ. По результатам многомерного анализа выживаемости, будний день операции (
Химиотерапия рака желудка | Химиотерапия рака желудка
В химиотерапии (химиотерапии) используются противораковые препараты, которые вводятся в вену или вводятся внутрь в виде таблеток. Эти препараты попадают в кровоток и достигают всех участков тела, что делает это лечение полезным для лечения рака, который распространился на органы, находящиеся за пределами того места, где оно началось.
Chemo можно использовать по-разному для лечения рака желудка:
- Химиотерапия может быть проведена перед операцией по поводу рака желудка. Это, известное как неоадъювантное лечение , может уменьшить опухоль и, возможно, облегчить операцию. Это также может помочь предотвратить рецидив рака и помочь пациентам прожить дольше. При некоторых стадиях рака желудка неоадъювантная химиотерапия является одним из стандартных вариантов лечения. Часто после операции снова проводят химиотерапию.
- Химиотерапия может быть проведена после операции по удалению рака. Это называется адъювант лечение . Цель адъювантной химиотерапии — убить любые раковые клетки, которые могли остаться, но слишком малы, чтобы их можно было увидеть. Это может помочь предотвратить возвращение рака. Часто при раке желудка после операции назначают химиотерапию вместе с лучевой терапией. Эта комбинация называется химиолучевой . Это может быть особенно полезно при раковых заболеваниях, которые нельзя полностью удалить хирургическим путем.
- Химиотерапия может применяться в качестве основного (основного) лечения рака желудка, который распространился (метастазировал) в отдаленные органы. Это может помочь уменьшить рак или замедлить его рост, что может облегчить симптомы у некоторых пациентов и помочь им прожить дольше.
Врачи проводят химиотерапию циклами, с каждым периодом лечения, за которым следует период отдыха, чтобы дать организму время на восстановление. Каждый цикл обычно длится несколько недель.
Ряд химиопрепаратов можно использовать для лечения рака желудка, в том числе:
- 5-ФУ (фторурацил), часто назначаемый вместе с лейковорином (фолиевая кислота)
- Капецитабин (Кселода)
- Карбоплатин
- Цисплатин
- Доцетаксел (Таксотер)
- Эпирубицин (Элленс)
- Иринотекан (Камптозар)
- Оксалиплатин (Элоксатин)
- Паклитаксел (Таксол)
- Трифлуридин и типирацил (Лонсурф), комбинированное лекарственное средство в форме таблеток
В зависимости от ситуации (включая стадию рака, общее состояние здоровья человека и то, сочетается ли химиотерапия с лучевой терапией), эти препараты могут использоваться отдельно или в сочетании с другими химиотерапевтическими или целевыми лекарствами.
Некоторые распространенные комбинации препаратов, используемые при планировании операции, включают:
- ECF (эпирубицин, цисплатин и 5-FU), которые можно вводить до и после операции
- Доцетаксел или паклитаксел плюс 5-ФУ или капецитабин в сочетании с лучевой терапией перед операцией
- Цисплатин плюс 5-ФУ или капецитабин в сочетании с лучевой терапией перед операцией
- Паклитаксел и карбоплатин в сочетании с лучевой терапией перед операцией
При проведении химиотерапии с лучевой терапией после операции можно использовать одно лекарственное средство, такое как 5-ФУ или капецитабин.
Для лечения запущенного рака желудка можно использовать ECF, но могут быть полезны и другие комбинации. Некоторые из них включают:
- DCF (доцетаксел, цисплатин и 5-ФУ)
- Иринотекан плюс цисплатин
- Иринотекан плюс 5-ФУ или капецитабин
- Оксалиплатин плюс 5-ФУ или капецитабин
- Трифлуридин и типирацил (Лонсурф), комбинированное лекарственное средство в форме таблеток
Многие врачи предпочитают использовать комбинации двух химиопрепаратов для лечения запущенного рака желудка.Комбинации из трех препаратов могут иметь больше побочных эффектов, поэтому они обычно предназначены для людей с очень хорошим здоровьем, за которыми может внимательно следить их врач.
Побочные эффекты химиотерапии
Химиопрепараты атакуют клетки, которые быстро делятся, поэтому они действуют против раковых клеток. Но другие клетки в организме, такие как клетки костного мозга (где образуются новые клетки крови), слизистой оболочки рта и кишечника и волосяных фолликулов, также быстро делятся.Эти клетки также могут быть затронуты химиотерапией, что может привести к побочным эффектам. Тип побочного эффекта зависит от типа лекарств, принимаемого количества и продолжительности лечения. Краткосрочные побочные эффекты, общие для большинства химиотерапевтических препаратов, могут включать:
- Тошнота и рвота
- Потеря аппетита
- Выпадение волос
- Диарея
- Язвы во рту
- Повышенная вероятность заражения (из-за нехватки лейкоцитов)
- Кровотечение или синяк после небольших порезов или травм (из-за нехватки тромбоцитов)
- Утомляемость и одышка (от недостатка эритроцитов)
Эти побочные эффекты обычно кратковременны и проходят после окончания лечения.Например, после окончания лечения волосы обычно отрастают. Обязательно сообщайте своим специалистам по лечению рака о любых побочных эффектах, которые у вас есть, потому что часто есть способы уменьшить их. Например, вам могут назначить лекарства для предотвращения или уменьшения тошноты и рвоты.
Некоторые химиотерапевтические препараты имеют определенные побочные эффекты. Вам следует предоставить конкретную информацию о каждом лекарстве, которое вы принимаете, и вы должны ознакомиться с ней перед началом лечения.
Невропатия: Цисплатин, оксалиплатин, доцетаксел и паклитаксел могут повреждать нервы вне головного и спинного мозга.Иногда это может приводить к появлению таких симптомов (в основном в руках и ногах), как боль, жжение или покалывание, чувствительность к холоду или теплу или слабость. В большинстве случаев это проходит после прекращения лечения, но у некоторых пациентов оно может длиться долго. Оксалиплатин также может влиять на нервы в горле, вызывая боль в горле, которая усиливается при попытке есть или пить холодные жидкости или продукты. Эта боль может привести к проблемам с глотанием или даже дыханию и может длиться несколько дней после лечения.
Поражение сердца: Доксорубицин, эпирубицин и некоторые другие препараты могут вызвать необратимое повреждение сердца при длительном применении или в высоких дозах.По этой причине врачи тщательно контролируют дозы и используют тесты сердца, такие как эхокардиограммы или сканирование MUGA, для контроля функции сердца. Лечение этими препаратами прекращают при первых признаках поражения сердца.
Синдром ладони-стопы может возникнуть во время лечения капецитабином или 5-ФУ (при введении в виде инфузии). Это начинается с покраснения рук и ног, которое затем может перерасти в боль и чувствительность в ладонях и подошвах. При ухудшении состояния могут появиться волдыри или шелушение кожи, что иногда приводит к открытию болезненных язв.Специального лечения не существует, хотя некоторые кремы могут помочь. Эти симптомы постепенно улучшаются при прекращении приема препарата или уменьшении дозы. Лучший способ предотвратить тяжелый синдром кисти-стопы — сообщить врачу о первых симптомах, чтобы можно было изменить дозу препарата.
Чтобы узнать больше, см. Химиотерапия.
Рак желудка: лечение и осложнения
Что такое рак желудка?
Также известное как рак желудка, рак кишечника или рак желудка — это заболевание, при котором клетки желудка начинают бесконтрольно размножаться, образуя опухоль.Опухоль может распространяться вдоль стенки желудка или прорастать прямо через нее и попадать в кровоток или лимфатическую систему, откуда она может распространиться на другие органы.
Существуют различные типы рака кишечника в зависимости от типа кишечной ткани, из которой они происходят:
- Аденокарцинома — Самая распространенная форма рака желудка. Аденокарцинома возникает в железистой оболочке желудка. Клетки железы, присутствующие во внутренней оболочке желудка (слизистой оболочке), производят слизистые и желудочные соки.Опухоль может проникать глубже в стенку желудка и пересекать ее, вторгаясь в окружающие органы, такие как поджелудочная железа или печень, или распространяться вверх или вниз в пищевод или тонкий кишечник, или проникать в кровоток или лимфатическую систему и распространяться на отдаленные части тело (метастаз).
- Лимфома — Эта форма рака кишечника возникает в лимфатической ткани стенки желудка.
- Саркома — Этот тип рака желудка возникает из-за соединительной ткани (мышцы, жир или кровеносные сосуды) в стенке желудка.
- Желудочно-кишечная стромальная опухоль (GIST) — Это редкая форма рака желудка, которая возникает из клеток нервной системы, обнаруженных в желудке.
- Карциноидный рак — Это еще одна редкая форма рака желудка, возникающая из-за продуцирующих гормоны клеток желудка.
Каковы причины расстройства?
Точная причина того, что клетки желудка начинают бесконтрольно размножаться, неизвестна, но определенные факторы риска делают одних людей более склонными к раку кишечника, чем других.К ним относятся:
- Инфекция Helicobacter pyroli (заражение слизистой оболочки желудка)
- Хроническое воспаление желудка
- Диета с высоким содержанием соли и копченостей; диета бедная фруктами и овощами
- Курение
- Недостаток физической активности
- Семейный анамнез рака желудка
Что нужно знать о симптомах и признаках?
По мере прогрессирования рака развиваются следующие симптомы:
- Дискомфорт и боли в животе
- Вздутие живота после еды
- Чувство сытости даже после небольших приемов пищи
- Затруднение глотания
- Постоянная тошнота, рвота
- Изжога
К какому специалисту следует проконсультироваться при появлении признаков и симптомов?
Лица, страдающие аномальными желудочно-кишечными проблемами, которые не проходят, должны проконсультироваться с терапевтом, который направит их к гастроэнтерологу (специализирующемуся на лечении желудочно-кишечных заболеваний).Для дальнейшего диагноза и подтверждения также может потребоваться помощь онколога (специалиста по лечению рака).
Какие скрининговые тесты и исследования проводятся для подтверждения или исключения заболевания?
Диагностические процедуры рака желудка включают:
- Физикальное обследование — Врач будет искать опухоль, скопление жидкости или другие изменения в брюшной полости, а также любые опухоли в лимфатических узлах.
- Эндоскопия — Тонкая трубка с крошечной камерой на конце вставляется в рот и проходит через пищевод, чтобы добраться до желудка.Эта процедура позволяет выявить злокачественный рост, а также собрать образцы для дальнейшего лабораторного исследования (биопсия).
- Визуализирующие тесты — Компьютерная томография (компьютерная томография) может обнаруживать и создавать изображения аномальных раковых опухолей в кишечнике.
Стадия рака желудка
Врач также проводит тесты, чтобы определить степень роста рака, которые будут полезны при составлении правильного плана лечения для пациента. Это делается с помощью визуализационных тестов, таких как компьютерная томография, позитронно-эмиссионная томография (ПЭТ-сканирование) или лапароскопическая хирургия.
Какие методы лечения доступны для лечения расстройства?
Врач составляет план лечения в зависимости от расположения и размера опухоли, степени ее распространения и общего состояния здоровья пациента. Рак кишечника можно лечить следующими методами:
Доступны различные варианты хирургического удаления рака кишечника:
- Хирургическое удаление опухоли на ранней стадии — Эндоскопическая резекция слизистой оболочки — это эндоскопическая процедура, при которой удаляются небольшие опухоли, ограниченные внутренней оболочкой стенки желудка.
- Субтотальная гастрэктомия — Удаляется только часть желудка, пораженная опухолью.
- Тотальная гастрэктомия — Удаляется весь желудок и окружающие здоровые ткани. Врач соединяет пищевод напрямую с тонкой кишкой.
- Удаление лимфатического узла — Лимфатические узлы в брюшной полости исследуются и удаляются, если обнаружены раковые клетки.
- Хирургия для облегчения симптомов — При запущенном раке кишечника удаляется часть желудка, чтобы облегчить симптомы у пациентов.
- Химиотерапия — Химиотерапия использует лекарства для уничтожения раковых клеток. Его можно назначить перед операцией для уменьшения опухоли (неоадъювантная химиотерапия) или после операции для уничтожения всех оставшихся клеток (адъювантная химиотерапия). Обычно его назначают вместе с лучевой терапией.
- Лучевая терапия — Энергетические лучи высокой мощности, такие как рентгеновские лучи, используются для уничтожения раковых клеток. Облучение может использоваться в сочетании с хирургическим вмешательством до (неоадъювантное облучение) или после (адъювантное облучение), а также обычно используется вместе с химиотерапией.
Какие известные осложнения при лечении расстройства?
Рак желудка и его лечение могут повлиять на пищеварительную способность организма пациента. Пациенты могут испытывать тошноту, рвоту, диарею и запор. Жидкости могут слишком быстро попасть в тонкий кишечник после операции.
Каковы требования к питанию и физической активности во время лечения?
Выздоравливающим пациентам, возможно, потребуется внести некоторые изменения в свой рацион, чтобы обеспечить беспрепятственное переваривание и усвоение пищи:
- Небольшое, более частое питание
- Ограничение сладких продуктов и напитков
- Жидкости питьевые до и после еды
Регулярные медицинские осмотры после лечения гарантируют, что любые изменения в состоянии здоровья можно будет вылечить в самое ближайшее время.
рака желудочно-кишечного тракта | CancerIndex
В этом исследовании изучали клинико-патологические факторы, связанные с поглощением 2- [F] фтор-2-дезокси-D-глюкозы (F-FDG) при раннем раке желудка (EGC), и использовали их для разработки метода клинической оценки для прогнозирования FDG. -видность EGC. Двадцать девять ретроспективно включенных пациентов прошли предоперационную позитронно-эмиссионную томографию / компьютерную томографию F-FDG (ПЭТ / КТ). Гистологическая информация была получена при резекции желудка (n = 195) или эндоскопической диссекции слизистой оболочки (n = 34).Была определена связь между клинико-патологическими факторами и поглощением F-FDG первичной опухолью. Результаты были использованы для разработки метода клинической оценки. Поглощение F-FDG было обнаружено у 49 (17,5%) пациентов. Согласно однофакторному анализу, местоположение, общий тип, классификация Всемирной организации здравоохранения, классификация Лорен, размер, глубина инвазии и лимфатическая инвазия были значимыми переменными, влияющими на поглощение F-FDG (все P
Чжоу К., Чен Ю.Г., Сяо Дж. И др.
Традиционная китайская медицина (отвар Xiaoai Jiedu) в качестве адъювантного лечения для предотвращения появления нового колоректального аденоматозного полипа после полипэктомии: протокол исследования для рандомизированного контролируемого исследования.
Медицина (Балтимор). 2019; 98 (31): e16680 [PubMed] Связанные публикации
ИСТОРИЯ: Колоректальный аденоматозный полип (КАП) был одним из предшественников колоректального рака (КРР) и имел высокую вероятность развития КРР. Не было убедительных доказательств химиопрофилактики для предотвращения новых случаев ВП после полипэктомии. Отвар Сяоай Цзеду, разработанная китайским национальным профессором медицины (Чжоу Чжунъин), использовался для лечения новых случаев ВП после полипэктомии в 20 веке в Китае.Однако клинических исследований отвара Сяоай Цзеду в лечении рецидива ВП не проводилось. Мы планируем это исследование, чтобы оценить эффективность и безопасность отвара Xiaoai Jiedu в лечении новых случаев ВП после полипэктомии при колоноскопии.
МЕТОДЫ / КОНСТРУКЦИЯ: Предлагается рандомизированное, контролируемое, слепое и многоцентровое исследование для оценки эффективности и безопасности отвара Xiaoai Jiedu. Пациенты с ВП (после полной полипэктомии при колоноскопии) будут случайным образом разделены на группу отвара Xiaoai Jiedu и группу миметиков отвара Xiaoai Jiedu.Пациенты пройдут курс лечения из 6 курсов и последующее наблюдение в течение 2 лет. Ожидается, что последующая колоноскопия будет проведена через 1 и 2 года после базовых обследований. Первичным показателем результата является появление новой ВП через 1 и 2 года. Вторичным критерием оценки является возникновение аденомы на поздней стадии через 1 и 2 года.
ОБСУЖДЕНИЕ: Это исследование предоставит объективные доказательства для оценки эффективности и безопасности отвара Xiaoai Jiedu в качестве адъювантного лечения новых случаев ВП после полипэктомии.
ПРОБНАЯ РЕГИСТРАЦИЯ: NCT03616444.
Се М., Рао В., Чжан П. и др.
Эндоскопическая резекция на всю толщину стромальной опухоли желудочно-кишечного тракта у реципиента трансплантата печени: клинический случай.
Медицина (Балтимор). 2019; 98 (31): e16669 [PubMed] Связанные публикации
ОБОСНОВАНИЕ: С развитием эндоскопической техники и усовершенствованием доступных принадлежностей эндоскопическая терапия стала играть важную роль в лечении подслизистых опухолей желудочно-кишечного тракта (SMT).
ЗАБОЛЕВАНИЯ ПАЦИЕНТОВ: СМТ желудка, подозреваемая в опухоли стромы желудочно-кишечного тракта (GIST), была диагностирована у реципиента трансплантата печени, которому была проведена операция по трансплантации 11 месяцев назад.
ДИАГНОСТИКА: SMT желудка, посттрансплантация печени. ВМЕШАТЕЛЬСТВА :: Для удаления опухоли была выполнена эндоскопическая резекция на всю толщину (EFR). Продолжительность операции составила 50 минут, прием перорального иммунодепрессанта в послеоперационном периоде не прерывался.
ИСХОДЫ: Клиническое течение было без осложнений, на четвертый день после операции наблюдалось незначительное повышение уровня печеночного фермента.Патологический диагноз — ГИСО с полной капсулой.
УРОКОВ: Наш успешный опыт показал, что EFR является выполнимым, безопасным и эффективным методом лечения малых (
Ян Ф., Сюй Ю.Л., Чжу РФ
Инфекция Helicobacter pylori и риск колоректальной карциномы: систематический обзор и метаанализ.
Минерва Мед. 2019; 110 (5): 464-470 [PubMed] Связанные публикации
ВВЕДЕНИЕ: Helicobacter pylori — это грамотрицательная бактерия, которая колонизируется в желудке.Инфекция H. pylori может привести к ряду заболеваний желудка. Однако связь между инфекцией H. пилори и колоректальным раком в настоящее время спорная. Поэтому мы провели этот метаанализ, чтобы лучше понять взаимосвязь между инфекцией H. pylori и колоректальным раком.
СОБЫТИЕ ДОКАЗАТЕЛЬСТВ: Мы провели всесторонний поиск из электронных баз данных, включая базы данных PubMed, Medline, China National Knowledge Infrastructure (CNKI) и China Wanfang Data Knowledge Service Platform (Wanfang Databases) до 1 мая 2018 года.Мы использовали поисковые запросы H. pylori и колоректальный рак или колоректальный рак и собрали все соответствующие исследования, чтобы изучить связь между инфекцией H. pylori и колоректальным раком.
СИНТЕЗ ДАННЫХ: Было включено 27 исследований, включающих 14357 случаев. Инфекция H. pylori была связана с повышенным риском колоректального рака. Объединенное отношение шансов (OR) 1,27 с 95% доверительным интервалом 1,17-1,37 (P ВЫВОДЫ: Настоящий метаанализ предоставляет доказательства того, что положительная связь между H.pylori и риск развития колоректального рака.
Хисака Т., Исикава Х., Сакаи Х. и др.
Синдром синусоидальной обструкции и послеоперационные осложнения, возникшие в результате предоперационной химиотерапии метастазов в печень колоректального рака.
Anticancer Res. 2019; 39 (8): 4549-4554 [PubMed] Публикации по теме
Предпосылки / цель: Целью этого исследования было изучить влияние предоперационной химиотерапии на здоровую, свободную от метастазов часть печени у пациентов с колоректальным раком с метастазами в печень, а также взаимосвязь между химиотерапией и послеоперационными осложнениями.
ПАЦИЕНТЫ И МЕТОДЫ: В наше исследование было включено 90 случаев метастазов в печень колоректального рака, удаленных после предоперационной химиотерапии. Пациенты были разделены на три группы в соответствии с полученным режимом химиотерапии: 20 пациентов получали mFOLFOX6, 54 случая — комбинацию mFOLFOX6 с бевацизумабом и 16 пациентов — комбинацию mFOLFOX6 и цетуксимаба или панитумумаба.
РЕЗУЛЬТАТЫ: Сравнивали среднее количество синусоидальных повреждений для каждого типа химиотерапии.Группа, получавшая комбинацию mFOLFOX6 и бевацизумаба, показала меньшую степень синусоидального повреждения по сравнению с другими группами; эта межгрупповая разница становилась все более заметной по мере увеличения количества курсов химиотерапии. Осложнения различной степени были обнаружены во всех трех группах, но между тремя группами не наблюдалось значительных различий.
ЗАКЛЮЧЕНИЕ: В тех случаях, когда предоперационная химиотерапия была продлена на длительный период, комбинированное использование бевацизумаба считалось эффективным из-за стабилизации нарушенной гемодинамики печени, вызванной эффектами подавления синусоидального повреждения, что позволяет эффективно распределять противораковые агенты в опухолях. .
Фукуока Э., Ямасита К., Танака Т. и др.
Неоадъювантная химиотерапия увеличивает экспрессию PD-L1 и CD8
Anticancer Res. 2019; 39 (8): 4539-4548 [PubMed] Связанные публикации
Предпосылки / цель: Целью этого исследования было изучить экспрессию PD-L1 и ее связь с прогнозом при плоскоклеточной карциноме пищевода (ESCC) до и после неоадъювантной химиотерапии (5-фторурацил и цисплатин, NAC-FP).
ПАЦИЕНТЫ И МЕТОДЫ: Используя базу данных 69 пациентов с ESCC, мы проанализировали экспрессию PD-L1 на опухолевых клетках (TC) и иммунных клетках (IC), а также плотность CD8
РЕЗУЛЬТАТЫ: Доля ESCC содержащие IC, экспрессирующие PD-L1 и имеющие высокий уровень CD8
ВЫВОД: NAC-FP индуцировал экспрессию PD-L1 на IC и CD8
Такимото Р., Камигаки Т., Окада С. и др.
Факторы прогноза для пациентов с колоректальным раком, леченных с помощью комбинации иммуноклеточной терапии и химиотерапии первой линии: ретроспективное исследование.
Anticancer Res. 2019; 39 (8): 4525-4532 [PubMed] Публикации по теме
Предпосылки / цель: В этом ретроспективном исследовании мы стремились изучить эффективность иммуноклеточной терапии с использованием Т-лимфоцитов, активированных in vitro с вакцинацией дендритными клетками (DC) или без нее, в сочетании с химиотерапией 1-й линии с точки зрения выживаемость пациентов с распространенным колоректальным раком (CRC).
ПАЦИЕНТЫ И МЕТОДЫ: Всего в этом исследовании приняли участие 198 пациентов, у которых был диагностирован прогрессирующий CRC и которым вводили химиотерапию 1-й линии. Корреляция между общей выживаемостью (ОС) и различными клиническими факторами была изучена с помощью одномерного и многомерного анализов.
РЕЗУЛЬТАТЫ: Однофакторный анализ показал, что прогноз улучшился у пациентов с CRC, получавших иммуноклеточную терапию с PS 0, бевацизумабом (BV) и схемами, включающими капецитабин (Cap).Наконец, многомерный анализ показал, что PS = 0, а комбинация иммуноклеточной терапии и Cap обеспечила улучшение выживаемости у пациентов с запущенным CRC.
ЗАКЛЮЧЕНИЕ: Повышение выживаемости может быть потенциально получено с лучшим PS путем комбинации иммуноклеточной терапии и Cap в качестве настройки 1-й линии у пациентов с CRC.
Танака Ю., Уэно Т., Йошида Н. и др.
Правильно ли рассмотрено возникновение мукозита полости рта во время химиотерапии у пациентов с раком пищевода? Наблюдательное когортное исследование EPOC.
Anticancer Res. 2019; 39 (8): 4441-4448 [PubMed] Связанные публикации
Предпосылки / цель: Мукозит полости рта (ОМ) — одно из частых побочных эффектов, с которыми сталкиваются пациенты, получающие химиотерапию. Большинство диагнозов ОМ основано на жалобах пациентов. Целью этого исследования было разработать инструмент для точной диагностики ОМ.
МАТЕРИАЛЫ И МЕТОДЫ: Была создана центральная система обзора (CRS), позволяющая судить, когда история пациента полностью неизвестна.Первичной конечной точкой была степень ОМ 2 или выше, а вторичной конечной точкой была разница в степени между оценкой клинициста каждого учреждения и оценкой CRS.
РЕЗУЛЬТАТЫ: Всего на учете было 53 пациента из четырех учреждений. CRS успешно выявила ОМ 2 и выше степени у 16 (30,2%) из 53 пациентов. Частота выявления всех степеней ОМ составила 41,5% (22 из 53 пациентов) по оценке врачей каждого учреждения и 84,9% (45 из 53 пациентов) по оценке CRS (p ВЫВОД: ОМ во время химиотерапии может быть занижена.
Ашизава Н., Симидзу Х., Судо М. и др.
Клиническое значение НАДФН-оксидазы 5 при раке толстой кишки человека.
Anticancer Res. 2019; 39 (8): 4405-4410 [PubMed] Публикации по теме
Предпосылки / цель: Недавние исследования сообщили об участии НАДФН-оксидазы (NOX) в прогрессировании опухоли. Однако роль NOX5 при раке толстой кишки неясна. Мы изучили клиническое значение экспрессии NOX5 при раке толстой кишки.
ПАЦИЕНТЫ И МЕТОДЫ. Экспрессия NOX5 была оценена иммуногистохимически у 119 пациентов с раком толстой кишки II или III стадии, и была проанализирована взаимосвязь между экспрессией NOX5 и клинико-патологическими данными.
РЕЗУЛЬТАТЫ: Из всех тканей 39,5% были отрицательными, а 60,5% были положительными по экспрессии NOX5. Положительная экспрессия была значимо связана с недифференцированной гистологией (p = 0,037) и метастазами в лимфатические узлы (p = 0,023). 5-летняя выживаемость без прогрессирования заболевания у NOX5-положительных пациентов была значительно хуже, чем у NOX5-отрицательных пациентов (p = 0,046). Частота местных рецидивов, наблюдаемая у NOX5-положительных пациентов, была выше, чем у NOX5-отрицательных пациентов.
ВЫВОД. Экспрессия NOX5 может быть связана с плохими прогностическими факторами и может быть полезна в качестве прогностического биомаркера.
Осава М., Хамай Ю., Ибуки Ю. и др.
Долгосрочный выживший после рака пищевода, пролеченный шунтированием по поводу пищеводно-бронхиальной фистулы после химиолучевой терапии: отчет о болезни.
Anticancer Res. 2019; 39 (8): 4399-4403 [PubMed] Связанные публикации
СПРАВОЧНАЯ ИНФОРМАЦИЯ: Эзофагореспираторный свищ (ЭСП) является смертельным осложнением для пациентов с трахеобронхиальной инвазией рака пищевода. Мы сообщаем о случае длительного выживания после рака пищевода, которому была проведена операция обходного пищеводного анастомоза по поводу ERF после химиолучевой терапии (CRT).
СЛУЧАЙНЫЙ ОТЧЕТ: 44-летнему мужчине была проведена радикальная СРТ-терапия (лучевая терапия 66 Гр, химиотерапия цисплатином и 5-фторурацилом) по поводу неоперабельного местнораспространенного рака пищевода с массивной инвазией в главный левый бронх. Хотя был получен полный клинический ответ, у пациента развилась пневмония из-за ERF. Для снятия симптомов было выполнено шунтирование пищевода. Симптомы пациента улучшились, и стал возможен пероральный прием. Рецидивов не было за 12 лет.
ЗАКЛЮЧЕНИЕ: Хирургия шунтирования пищевода может помочь в облегчении симптомов и может быть связана с долгосрочным выживанием пациентов с раком пищевода с ERF после хорошего ответа на CRT. Таким образом, шунтирование — это полезный вариант лечения рака пищевода с помощью ERF.
Найери М., Искандер О., Табчури Н. и др.
Низкая связь по сравнению с высокой. Перевязка сосудов нижней брыжеечной артерии при хирургии рака прямой кишки снижает послеоперационные осложнения, не влияя на общую выживаемость.
Anticancer Res. 2019; 39 (8): 4363-4370 [PubMed] Связанные публикации
ИСТОРИЯ ВОПРОСА / ЦЕЛЬ: Целью данного исследования было определить клиническое влияние перевязки низкой связки (LT) нижней брыжеечной артерии (IMA) ниже левой колической артерии по сравнению с перевязкой высокой связки (HT) в месте возникновения IMA у пациентов, перенесших операцию по поводу рака прямой кишки.
ПАЦИЕНТЫ И МЕТОДЫ: В период с января 2005 г. по декабрь 2017 г. ретроспективно были включены все пациенты, прошедшие резекцию прямой кишки по поводу неметастатического рака.Пациентов с ТТ сравнивали с пациентами с АГ.
РЕЗУЛЬТАТЫ: Всего было идентифицировано 200 пациентов (101 HT и 99 LT). Послеоперационная 30-дневная летальность в обеих группах была нулевой. Было значительно больше тяжелых послеоперационных осложнений у пациентов с HT по сравнению с пациентами с LT (Clavien-Dindo III-IV) (18,8% против 9,1%, p = 0,048). Медиана последующего наблюдения составила 38,5 месяцев, а общая выживаемость через 5 лет составила 91,5%, и не было никакой разницы между двумя группами (90,1% против 92,9%; HT против LT p = 0.640).
ЗАКЛЮЧЕНИЕ: LT лигирование IMA значительно снизило частоту тяжелых послеоперационных осложнений, не влияя на безрецидивную или общую выживаемость.
Мацуда А., Ямада Т., Мацумото С. и др.
Отношение нейтрофилов к лимфоцитам перед лечением прогнозирует выживаемость пациентов с метастатическим колоректальным раком после лечения TAS-102.
Anticancer Res. 2019; 39 (8): 4343-4350 [PubMed] Связанные публикации
ИСТОРИЯ ВОПРОСА / ЦЕЛЬ: TAS-102 рекомендуется в качестве терапии линии спасения метастатического колоректального рака (mCRC), но практических предикторов его эффективности нет.
ПАЦИЕНТЫ И МЕТОДЫ: В ретроспективном исследовании 33 пациентов, получавших TAS-102, мы изучали прогностическую ценность предобработки нейтрофилов-лимфоцитов (NLR), тромбоцитов-лимфоцитов (PLR) и Соотношение лимфоцитов и моноцитов (LMR) для выживаемости без прогрессирования (PFS) и общей (OS) выживаемости. Сравнивали прогностическую способность с использованием пороговых значений среднего значения (3,14) и 5 для NLR.
РЕЗУЛЬТАТЫ: При одномерном анализе показатели эффективности Восточной кооперативной онкологической группы, NLR и PLR были отрицательно значимо связаны с PFS и OS.Количество линий лечения было отрицательно связано с ВБП. Пороговое значение NLR, равное 5, превышало медианное значение. Многофакторный анализ показал значительное прогностическое влияние на NLR при пороговом значении 5 (отношение рисков (HR) = 6,26, p = 0,02 для PFS; HR = 6,97, p = 0,07 для OS).
ВЫВОД: NLR перед лечением является прогностическим биомаркером для пациентов с мКРР, получающих лечение TAS-102.
Ямамото К., Хирао М., Нисикава К. и др.
Саркопения связана с нарушением общей выживаемости после гастрэктомии по поводу рака желудка у пожилых людей.
Anticancer Res. 2019; 39 (8): 4297-4303 [PubMed] Связанные публикации
ИСТОРИЯ ВОПРОСА / ЦЕЛЬ: Целью данного исследования было оценить влияние саркопении, диагностированной алгоритмом Европейской рабочей группы по саркопении у пожилых людей (EWGSOP), на отдаленные результаты после гастрэктомии.
ПАЦИЕНТЫ И МЕТОДЫ: Всего в текущий анализ были включены 90 пожилых пациентов с раком желудка без отдаленных метастазов в возрасте 65 лет и старше, перенесших гастрэктомию в Национальной больнице Осаки в период с июля 2012 года по январь 2015 года.
РЕЗУЛЬТАТЫ: Группа саркопении (n = 19) имела более низкую общую выживаемость (OS) (p ВЫВОД: Саркопения — потенциальная цель для предоперационного вмешательства у пожилых пациентов с раком желудка для улучшения прогноза после гастрэктомии (UMIN-CTR). : R000041532).
Sdralis EK, Davakis S, Syllaios A, et al.
Прогностическое значение субкаринальных лимфатических узлов при минимально инвазивной эзофагэктомии при раке.
Anticancer Res. 2019; 39 (8): 4291-4295 [PubMed] Связанные публикации
ИСТОРИЯ ВОПРОСА / ЦЕЛЬ: Хирургическая резекция рака пищевода остается золотым стандартом лечения во всем мире.Субкаринальные лимфатические узлы классифицируются как периэзофагеальные узлы, и их рассечение может выполняться во время 2- или 3-этапной эзофагэктомии. Необходимость и прогностическая ценность субкаринальной лимфаденэктомии до сих пор остаются дискуссионными. Целью этого исследования было изучить процент пораженных субкаринальных лимфатических узлов из общего количества удаленных лимфатических узлов. Обнаружение пораженных узлов коррелировало с клинической стадией и дифференцировкой опухоли.
ПАЦИЕНТЫ И МЕТОДЫ: Это ретроспективный анализ последовательных эзофагэктомий по поводу рака, выполненных в медицинском центре Великобритании.Исследование проводилось в течение 3 лет.
РЕЗУЛЬТАТЫ: Скорость инвазии субкаринальных лимфатических узлов была чрезвычайно низкой по результатам нашего анализа.
ЗАКЛЮЧЕНИЕ: Лимфаденэктомия не лишена клинического воздействия на пациентов, и поэтому решение должно фактически быть результатом динамического баланса между осложнениями и преимуществом в отношении выживаемости.
Джингу К., Такахаши Н., Мураками Ю. и др.
Является ли одновременная химиотерапия с лучевой терапией при раке пищевода полезной для пациентов в возрасте 80 лет и старше?
Anticancer Res.2019; 39 (8): 4279-4283 [PubMed] Связанные публикации
Предпосылки / цель: Определить, следует ли проводить одновременную химиотерапию с лучевой терапией у пожилых пациентов с раком пищевода.
ПАЦИЕНТЫ И МЕТОДЫ: В исследование были включены 185 пациентов в возрасте 80 лет и старше, которые получали только радикальную лучевую терапию или комбинированную химиолучевую терапию по поводу рака пищевода в семи учреждениях. Чтобы сравнить показатели выживаемости пациентов, получавших химиолучевую терапию, с показателями выживаемости пациентов, получавших только лучевую терапию, было выполнено сопоставление показателей предрасположенности для гомогенизации двух популяций.
РЕЗУЛЬТАТЫ: Для всей когорты пациентов 3-летняя общая выживаемость (ОС) составила 52,6%, а медиана выживаемости составила 42,5 месяца. После сопоставления оценок предрасположенности показатель общей выживаемости в течение 3 лет для группы химиолучевой терапии не был значительно лучше, чем для группы, получавшей только лучевую терапию (53,7% против 59,9%, p = 0,876).
ЗАКЛЮЧЕНИЕ: Одновременная химиотерапия с лучевой терапией при раке пищевода у пациентов в возрасте 80 лет и старше не давала значительного улучшения общей выживаемости по сравнению с одной лучевой терапией.
Rubio CA, Schmidt PT
Рассечение микроскопической анатомии крипт толстой кишки при недиспластических седалищных зубчатых полипах.
Anticancer Res. 2019; 39 (8): 4259-4263 [PubMed] Связанные публикации
ПРЕДПОСЫЛКИ / ЦЕЛЬ: Зазубренные полипы сечений (SSP) характеризуются криптами искаженной формы (CCS).
МАТЕРИАЛЫ И МЕТОДЫ: Исследовали количество CCS и латеральный размер 60 недиспластических SSP (NDSSP).
РЕЗУЛЬТАТЫ: Из 60 NDSSP 34 были маленькими (≤9 мм) и 26 — большими (≥10 мм). Всего было зарегистрировано 1101 CCS: 547 CCS были подключены к просвету (CCSL), а 554 CCS не были (CCSNL). Латеральный размер NDSSP, общее количество CCS и количество CCSNL были значительно выше в большом NDSSP, чем в маленьком NDSSP. Напротив, количество CCS, соединенных с просветом / мм (CCSL / мм), и крипт нормальной формы, соединенных с просветом / мм (CCSNL / мм), было значительно ниже в больших NDSSP, чем в маленьких NDSSP.
ЗАКЛЮЧЕНИЕ: Боковое расширение большого NDSSP происходит за счет увеличения количества CCS за счет уменьшения количества CCSL / мм и CCSNL / мм.
Мацумото А., Юда М., Танака Ю. и др.
Эффективность чрескожной эндоскопической гастростомии у пациентов с раком пищевода во время предоперационной терапии.
Anticancer Res. 2019; 39 (8): 4243-4248 [PubMed] Связанные публикации
Предпосылки / цель: Это исследование было направлено на выяснение преимуществ и недостатков чрескожной эндоскопической гастростомии (ПЭГ) у пациентов с раком пищевода (ЭК) во время предоперационной терапии.
МАТЕРИАЛЫ И МЕТОДЫ: Мы ретроспективно рассмотрели 92 пациента, перенесших эзофагэктомию по поводу ЭК после предоперационной терапии. Пациенты были разделены на группу ПЭГ (n = 14) и контрольную группу (n = 78) и сравнивались в отношении характеристик пациентов, статуса питания, операционных переменных и послеоперационных осложнений.
РЕЗУЛЬТАТЫ: В группе ПЭГ первый статус питания и стадия опухоли были значительно хуже, но изменения статуса питания от первого визита до операции были значительно лучше.По данным интраоперационной тепловизии, пациентов с нарушением кровотока в желудочном канале из-за ПЭГ не было. Ближайшие хирургические исходы достоверно не различались.
ЗАКЛЮЧЕНИЕ. ПЭГ оказывает меньшее неблагоприятное воздействие на продукцию желудочного зонда при эзофагэктомии и может рассматриваться у высокоселективных пациентов во время предоперационной терапии.
Ито Й, Кобучи С., Такесада В., Такахаши С.
Оценка индуцированной оксалиплатином хронической невропатии и противораковой эффективности посредством фармакокинетической и токсикодинамической оценки крысиной модели колоректального рака.
Anticancer Res. 2019; 39 (8): 4207-4213 [PubMed] Связанные публикации
Предпосылки / цель: Хроническая невропатия, вызванная оксалиплатином, является важным фактором снижения дозы и не завершения всех циклов химиотерапии для пациентов с колоректальным раком (CRC). Целью исследования было изучить фармакокинетику и токсикодинамику вызванной оксалиплатином хронической нейропатии у крыс CRC для обеспечения эффективного лечения.
МАТЕРИАЛЫ И МЕТОДЫ: Модель CRC на крысах была разработана с использованием 1,2-диметилгидразина и сульфата декстрана.Оксалиплатин (L-OHP) вводили внутривенно крысам CRC каждую неделю. Фармакокинетические профили и распределение L-OHP и хронических невропатий в опухолях изучались в течение более четырех недель.
РЕЗУЛЬТАТЫ: Средние значения площади под кривой зависимости концентрации от времени для L-OHP показали дозозависимое увеличение. Хроническая невропатия возникла с 14-го дня в группе 8 мг / кг и с 19-го дня в группах 3 и 5 мг / кг.
ВЫВОД: Эти результаты предоставляют предварительную информацию для разработки фармакокинетической и токсикодинамической модели L-OHP для циклов терапии CRC.
Итикава Х., Ниши Х., Яно С. и др.
Противоопухолевый эффект новой фотодинамической терапии с ацетилированным глюкозо-конъюгированным хлорином при раке желудочно-кишечного тракта.
Anticancer Res. 2019; 39 (8): 4199-4206 [PubMed] Связанные публикации
Предпосылки / цель: Ранее мы синтезировали соединение хлорина е6, конъюгированное с глюкозой (G-хлорин е6), и сообщили, что оно обладает очень сильным противоопухолевым действием. Целью настоящего исследования был синтез ацетилированного глюкозо-конъюгированного хлорина (AcN003HP) и оценка его противоопухолевого эффекта и выведения.
МАТЕРИАЛЫ И МЕТОДЫ: Для оценки противоопухолевого эффекта AcN003HP его IC
РЕЗУЛЬТАТЫ: AcN003HP показал более сильное противоопухолевое действие и накопление в раковых клетках по сравнению с талапорфином натрия, традиционным фотосенсибилизатором. AcN003HP был локализован в эндоплазматическом ретикулуме. В модели мыши с ксенотрансплантатом опухоли AcN003HP показал более длительное время выведения из организма, чем G-хлорин e6, а фотодинамическая терапия с использованием AcN003HP показала очень сильные противоопухолевые эффекты.
ЗАКЛЮЧЕНИЕ: Безопасность, улучшенная управляемость и устойчивые противоопухолевые эффекты позволяют предположить, что AcN003HP является хорошим фотосенсибилизатором следующего поколения.
Накадзава Н., Огата К., Йокобори Т. и др.
Низкие уровни IRBIT связаны с устойчивостью к химиотерапии у больных раком желудка.
Anticancer Res. 2019; 39 (8): 4111-4116 [PubMed] Связанные публикации
Предпосылки / цель: Мы исследовали, может ли экспрессия инозитол-1,4,5-трифосфатного рецепторного белка, высвобождаемого с инозитол-1,4,5-трифосфатом (IRBIT) у пациентов с клиническим раком желудка (GC), предсказать терапевтический эффект. ответ на послеоперационную адъювантную химиотерапию.
МАТЕРИАЛЫ И МЕТОДЫ: Иммуногистохимия была использована для исследования экспрессии IRBIT у 115 пациентов с ГК. Чтобы выяснить, имеет ли IRBIT связь с терапевтическими эффектами химиотерапии, мы сравнили две группы — 62 пациента, получавших послеоперационную адъювантную химиотерапию, и 53 пациента, получавших послеоперационную адъювантную химиотерапию.
РЕЗУЛЬТАТЫ: Что касается группы послеоперационной адъювантной химиотерапии, мы не обнаружили какой-либо статистически значимой корреляции между клинико-патологическими особенностями и рецидивом независимо от экспрессии IRBIT.Напротив, в группе, получавшей послеоперационную адъювантную химиотерапию, была обнаружена значимая связь между экспрессией IRBIT и как общей, так и безрецидивной выживаемостью.
ЗАКЛЮЧЕНИЕ: IRBIT может использоваться как полезный прогностический маркер для химиотерапии.
Юн С.Н., Пак Дж. Х., Лвин TM и др.
Хирургическая ортотопическая имплантация опухоли при раке толстой кишки у голых мышей вызывает клинически значимые метастазы без раннего перитонеального карциноматоза.
Anticancer Res. 2019; 39 (8): 4065-4071 [PubMed] Связанные публикации
ИСТОРИЯ ВОПРОСА: Хирургическая ортотопическая имплантация ткани рака толстой кишки человека в слепую кишку мышей была использована для имитации поведения рака у пациентов с целью развития точной медицины рака. Однако при нынешнем методе имплантации серозной поверхности (SSI) кусочков ткани рака толстой кишки человека раковые клетки подвергаются воздействию брюшины, что может искусственно увеличивать частоту перитонеального карциноматоза (PC) в течение болезни.Целью настоящего исследования было представить метод герметизации опухоли (TSM) и сравнить его с SSI на предмет способности вызывать клинически значимые метастазы без искусственного ПК.
МАТЕРИАЛЫ И МЕТОДЫ. клеток рака толстой кишки HCT116, трансфицированных зеленым флуоресцентным белком (GFP), культивировали и затем вводили в подкожный слой бестимусных голых мышей. Подкожным опухолям давали возможность вырасти в достаточной степени, чтобы обеспечить адекватную опухоль для ортотопической имплантации. Для SSI, 1 мм
РЕЗУЛЬТАТЫ: Через 20 дней после имплантации частота ПК в группе SSI и TSM составила 80% (12/15) и 20% (3/15) соответственно (p ВЫВОД: Эти результаты предполагают, что TSM может быть более подходящим для пациента и полезным методом в качестве модели метастатического рака толстой кишки, чем SSI.
Вирджилио Э., Джарнери Э., Монтаньини М. и др.
Достижения во внутрипросветной эксфолиативной цитологии рака желудка: онкологические последствия шестого метастатического пути (метастаз VI).
Anticancer Res. 2019; 39 (8): 4019-4022 [PubMed] Связанные публикации
Исторически анализ внутрижелудочной эксфолиативной цитологии (IEC) рака желудка (GC) использовался только с диагностической целью. С успешным появлением эндоскопической биопсии во всем мире повысилась скорость обнаружения GC, и, как следствие, от IEC постепенно отказались.Однако сегодня наблюдается возобновление интереса к этой области исследований, о чем свидетельствуют несколько соответствующих публикаций. Как обсуждалось в этом обзоре, на самом деле в настоящее время важность анализа IEC у пациентов с ранними и поздними стадиями GC, по-видимому, заключается в его клинико-патологическом и прогностическом значении. Фактически, по сравнению с не шелушащимися опухолями, GC, демонстрирующая внутрижелудочное эксфолиацию, недавно была связана с агрессивным фенотипом опухоли (характеризуется более глубокой инфильтрацией стенки желудка, лимфатическими узлами или отдаленными метастазами, ангиолимфатической и периневральной инвазией) и более плохим прогнозом.Внедрение ИЭК в рутинную практику может помочь выявить пациентов с повышенным риском развития местного рецидива и перитонеальных метастазов в результате раннего и позднего РЖ, оптимизируя их лечение и улучшая качество жизни и продолжительность жизни.
Кан Б.В., Пэк Д.В., Кан Х. и др.
Новые терапевтические подходы к раку желудка, ассоциированному с вирусом Эпштейна-Барра.
Anticancer Res. 2019; 39 (8): 4003-4010 [PubMed] Связанные публикации
Рак желудка (РЖ), ассоциированный с вирусом Эпштейна-Барра (EBV) (EBVaGC), классифицируется как один из четырех подтипов GC по всесторонней молекулярной характеристике.Хотя механизм туморогенеза при инфицировании ВЭБ еще полностью не выяснен, инфекция ВЭБ может вносить вклад в злокачественную трансформацию клеток GC, вовлекая различные клеточные процессы и сигнальные пути. EBVaGC продемонстрировал следующие отличительные характеристики в отличие от других подтипов: крайнее гиперметилирование ДНК, повторяющиеся мутации альфа-изоформы каталитической субъединицы фосфатидилинозитол-4,5-бифосфат-3-киназы (PIK3CA), сверхэкспрессия лиганда 1/2 запрограммированной гибели клеток (PD-L1 / 2), а также периодической активации сигналов иммунных клеток.

