Пероральные лекарственные средства | Medtronic Diabetes Russia
Пероральные лекарственные средства при диабете 2 типа
С диабетом 2 типа и гестационным диабетом зачастую можно бороться с помощью всего лишь изменений диеты, физической нагрузки и образа жизни. Правильное питание может помочь Вам поддерживать уровень глюкозы в крови в пределах целевого диапазона, регулярная физическая нагрузка может повысить эффективность инсулина, а изменения образа жизни — посодействовать снижению стресса и кровяного давления. Хотя все это принесет Вам значительную пользу, через некоторое время Вы станете менее восприимчивыми к инсулину, потому что диабет — прогрессирующее заболевание. На этом этапе Вам могут выписать таблетки от диабета, которые помогут контролировать уровень сахара в Вашей крови. В зависимости от состояния некоторым больным диабетом выписывают пероральные препараты от сахарного диабета сразу после постановки диагноза.
Существует несколько различных препаратов, которые Вам могут выписать для борьбы с диабетом и которые помогают снизить уровень глюкозы в крови. Наиболее распространенные таблетки при диабете 2 типа — метформин, помогающий организму повысить восприимчивость к вырабатываемому им инсулину, помогая таким образом снизить уровень сахара в крови. Как и все другие лекарственные средства, его нужно принимать в соответствии с рекомендациями врача, и подходит он не для всех.
Как работают пероральные лекарственные средства?
Пероральные лекарственные средства могут помочь больным диабетом 2 типа контролировать уровень сахара в крови и работают одним из пяти основным способов2:
Снижение инсулинрезистентности
Метформин уменьшает количество глюкозы, вырабатываемой клетками печени, и снижает скорость всасывания глюкозы из кишечника после еды.
Повышение секреции инсулина
Препараты сульфонилмочевины и меглитиниды стимулируют секрецию инсулина бета-клетками поджелудочной железы.
Снижение скорости всасывания сахара из кишечника
Акарбоза представляет собой препарат, нацеленный на ферменты, который активно воздействует на альфа-глюкозидазу. Этот фермент критически важен для разрушения углеводов на сахара, что замедляет всасывание сахаров после еды и предотвращает резкие скачки уровня сахара в крови.
Увеличение осадка глюкозы в моче
Глифлозины — относительно новая форма лекарственных средств, которые начинают после того, как почки отфильтровали глюкозу. Они ингибируют натрий-зависимый переносчик глюкозы, предотвращая реабсорбцию глюкозы в кровоток, что позволяет организму выделять глюкозу с мочой и снижает уровень сахара в крови.
Ингибирование дипептидилпептидазы
Глиптины, представляющие собой ингибиторы дипептидилпептидазы, предотвращают разрушение глюкагоноподобного пептида-1, что, в свою очередь, обеспечивает более высокую выработку инсулина после приема пищи.
Пероральные лекарства для лечения женщин с гестационным диабетом
В чем суть проблемы?
Во всем мире растет число женщин, у которых диагностирован гестационный сахарный диабет (ГСД). ГСД — это непереносимость глюкозы, приводящая к повышению сахара в крови, впервые возникающая во время беременности, которая обычно разрешается после родов. Стандартная помощь включает в себя изменение образа жизни — советы по диете и упражнения. Лечение для некоторых женщин включает пероральные противодиабетические препараты, такие, как метформин и глибенкламид, которые являются альтернативой и могут использоваться вместе с инсулином для контроля уровня сахара в крови. Целью этого обзора стало исследование пользы от приема пероральных средств для лечения ГСД у беременных женщин. Другой Кокрейновский обзор сравнивает эффект инсулина с пероральными противодиабетическими фармакологическими видами лечения (
Brown 2016).
Почему это важно?
Женщины с диагнозом ГСД подвержены большему риску возникновения таких осложнений, как высокое кровяное давление во время беременности и родов. Они имеют повышенный риск развития диабета в дальнейшей жизни. Младенцы, рожденные у матерей, которым был диагностирован ГСД, могут быть крупнее, чем обычно, и это может привести к травмам матери и ребенка при родах. Вероятнее всего, роды придется индуцировать или делать кесарево сечение. Эти дети находятся в группе риска по развитию диабета в детском или молодом возрасте. Поэтому так важно найти лучшие лекарственные средства для лечения женщин и предотвращения осложнений, которые связаны с ГСД.
Они имеют повышенный риск развития диабета в дальнейшей жизни. Младенцы, рожденные у матерей, которым был диагностирован ГСД, могут быть крупнее, чем обычно, и это может привести к травмам матери и ребенка при родах. Вероятнее всего, роды придется индуцировать или делать кесарево сечение. Эти дети находятся в группе риска по развитию диабета в детском или молодом возрасте. Поэтому так важно найти лучшие лекарственные средства для лечения женщин и предотвращения осложнений, которые связаны с ГСД.
Какие доказательства мы обнаружили?
Мы провели поиск исследований по 14 мая 2016 года. Мы включили 11 рандомизированных контролируемых клинических испытаний с участием 1487 матерей и их детей (но только 8 испытаний внесли данные для наших анализов). Доказательства были ограничены качеством и числом исследований, и мы советуем с осторожностью относиться к этим результатам.
Критерии диагностики ГСД и цели лечения варьировали в разных исследованиях, и каждый исход основывался на нескольких исследованиях с небольшим числом женщин. Три исследования сравнивали пероральные препараты с плацебо/стандартной помощью, но следующие результаты были получены из одного исследования (375 женщин). Качество доказательств было очень низким или низким. Мы не обнаружили никаких различий между применением пероральных препаратов и плацебо по их влиянию на риск развития высокого кровяного давления, травм промежности, необходимости кесарева сечения или индукции родов. Число младенцев, родившихся крупными для своего гестационного возраста, с низким уровнем сахара в крови или умерших при рождении, в двух группах не отличалось. Два исследования (434 женщины) сообщили об отсутствии различий в потребности в инсулине между группой перорального приема препаратов и группой плацебо.
Три исследования сравнивали пероральные препараты с плацебо/стандартной помощью, но следующие результаты были получены из одного исследования (375 женщин). Качество доказательств было очень низким или низким. Мы не обнаружили никаких различий между применением пероральных препаратов и плацебо по их влиянию на риск развития высокого кровяного давления, травм промежности, необходимости кесарева сечения или индукции родов. Число младенцев, родившихся крупными для своего гестационного возраста, с низким уровнем сахара в крови или умерших при рождении, в двух группах не отличалось. Два исследования (434 женщины) сообщили об отсутствии различий в потребности в инсулине между группой перорального приема препаратов и группой плацебо.
Шесть исследований сравнивали метформин с глибенкламидом. Качество доказательств было от очень низкого до среднего (умеренного). Мы не нашли каких-либо различий между метформином и глибенкламидом по риску развития высокого кровяного давления (3 исследования, 508 женщин, доказательства умеренного качества), по необходимости кесарева сечения (4 исследования, 554 женщины, доказательства низкого качества), по травмам промежности (2 исследования, 308 женщин, доказательства низкого качества), или по необходимости индукции родов (1 исследование, 159 женщин, доказательства низкого качества).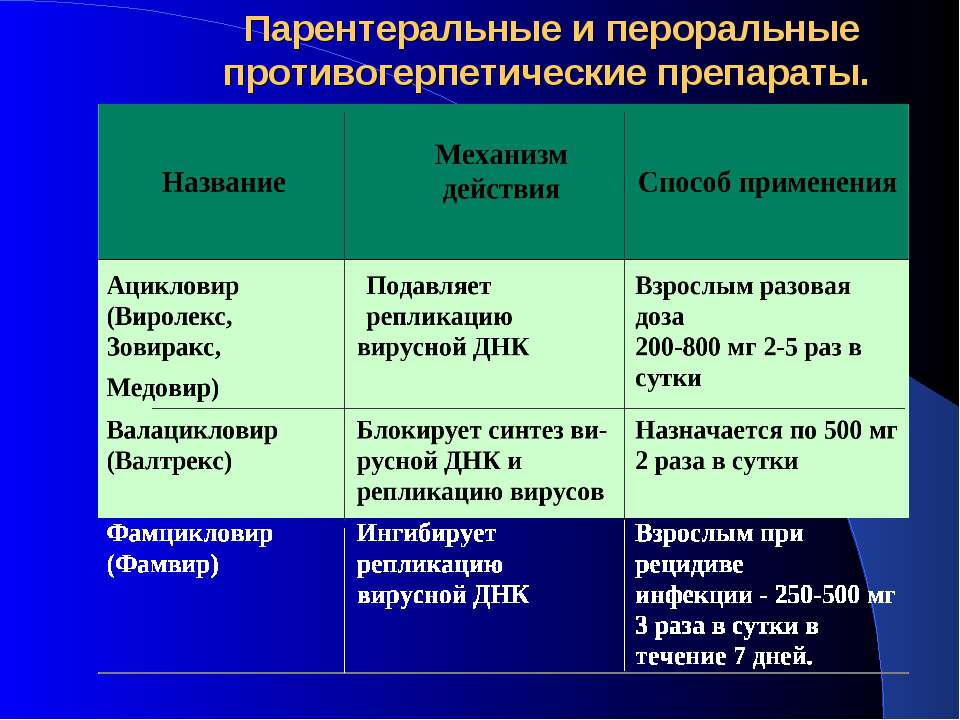 Мы не нашли никаких различий между метформином и глибенкламидом в отношении числа детей, рожденных с низким уровнем сахара крови (4 исследования, 554 младенца, доказательства низкого качества), родившихся крупными для своего гестационного возраста (2 исследования, 246 младенцев) или умерших при родах (все доказательства — низкого и очень низкого качества). В одном из исследований дети, рожденные от матерей, принимавших метформин, имели меньший риск любого серьезного исхода (низкий уровень сахара в крови, желтуха, крупный размер при рождении, проблемы с дыханием, родовые травмы или смерть при родах) (доказательства низкого качества). Одно небольшое исследование (43 женщины) по сравнению глибенкламида с акарбозой сообщило об отсутствии различий в исходах для матерей и их младенцев.
Мы не нашли никаких различий между метформином и глибенкламидом в отношении числа детей, рожденных с низким уровнем сахара крови (4 исследования, 554 младенца, доказательства низкого качества), родившихся крупными для своего гестационного возраста (2 исследования, 246 младенцев) или умерших при родах (все доказательства — низкого и очень низкого качества). В одном из исследований дети, рожденные от матерей, принимавших метформин, имели меньший риск любого серьезного исхода (низкий уровень сахара в крови, желтуха, крупный размер при рождении, проблемы с дыханием, родовые травмы или смерть при родах) (доказательства низкого качества). Одно небольшое исследование (43 женщины) по сравнению глибенкламида с акарбозой сообщило об отсутствии различий в исходах для матерей и их младенцев.
Ни одно из включенных исследований не предоставило каких-либо данных об исходах, упомянутых ранее в этом обзоре, в том числе и о долгосрочных исходах для матери и ребенка в детском и зрелом возрасте.
Что это значит?
Нет доступных доказательств достаточно высокого качества, чтобы дать ответ на вопрос, дают ли пероральные препараты лучшие исходы для женщин с гестационным диабетом и их младенцев по сравнению с плацебо, или действительно ли один пероральный препарат дает лучшие исходы для здоровья, чем другой пероральный препарат. Поскольку вопрос до сих пор остается неясным, необходимы дальнейшие исследования. Будущие исследования должны помочь получить сведения об исходах, предложенных в этом обзоре, и, в особенности, о долгосрочных исходах для женщин и их младенцев, о которых скудно сообщалось на сегодняшний день.
Поскольку вопрос до сих пор остается неясным, необходимы дальнейшие исследования. Будущие исследования должны помочь получить сведения об исходах, предложенных в этом обзоре, и, в особенности, о долгосрочных исходах для женщин и их младенцев, о которых скудно сообщалось на сегодняшний день.
|
Ацетогексамид*
|
250 мг 1 раз/день — 750 мг 2 раза/день
|
|
Больше не доступно в США
|
|
Хлорпропамид*
|
100 мг 1 раз/день — 750 мг 1 раз/день
|
|
Хлорпропамид: может вызвать гипонатриемию и приливы после употребления алкоголя
|
|
|
100 мг 1 раз/день — 500 мг 2 раза/день
|
|
Больше не доступно в США
|
|
|
250 мг 1 раз/день — 1500 мг 2 раза/день
|
|
|
|
Глибурид, с равномерным выделением действующего вещества
|
1,25 мг 1 раз/день — 10 мг 2 раза/день
|
|
Глипизид и глибенкламид: нет доказательств повышения эффективности при дозах выше 10 мг/день
|
|
Глибурид, микронизированный
|
0,75 мг 1 раз/день — 6 мг 2 раза/день
|
| |
|
Глипизид, с равномерным выделением действующего вещества
|
2,5 мг 1 раз/день — 20 мг 2 раза/день
|
| |
|
Глипизид, с длительным выделением действующего вещества
|
2,5-20 мг 1 раз/день
|
| |
|
|
1-8 мг 1 раз/день
|
|
|
Усиливающие секрецию инсулина: короткого действия
|
Усиливают секрецию инсулинаbeta-клетками поджелудочной железы
Могут применяться отдельно или в комбинации с другими пероральными препаратами и инсулином
| ||
|
|
60-120 мг три раза в день во время еды
|
| |
|
|
0,5-4 мг три раза в день во время еды
|
| |
Сенсибилизаторы инсулина: бигуаниды
|
Усиливают подавление выработки глюкозы в печени инсулином
Могут применяться отдельно или в комбинации с другими пероральными препаратами и инсулином
Противопоказаны всем пациентам группы риска, в том числе пациентам с почечной недостаточностью, метаболическим ацидозом, гипоксией, алкоголизмом или обезвоживанием
Не вызывают гипогликемию
Другие побочные эффекты: поражения желудочно-кишечного тракта (диарея, тошнота, боли), мальабсорбцию витамина B12
Усиливают потерю веса
| ||
|
Метформин, с равномерным выделением действующего вещества
|
500 мг 1 раз/день — 1250 мг 2 раза/день
|
| |
|
Метформин, с длительным выделением действующего вещества
|
500 мг — 2 г 1 раз/день
|
| |
Сенсибилизаторы инсулина: Тиазолидиндионы
|
Усиливают подавление выработки глюкозы в печени инсулином
Могут применяться отдельно или в комбинации с другими пероральными препаратами и инсулином
Основные побочные эффекты: увеличение веса, задержка жидкости, анемия (легкая)
Гепатотоксичность встречается редко, но необходимо контролировать показатели функции печени
| ||
|
|
15-45 мг 1 раз/день
|
|
Пиоглитазон: может повышать риск развития рака мочевого пузыря, сердечной недостаточности, переломов
|
|
|
2-8 мг 1 раз/день
|
|
Розиглитазон: может увеличивать уровень холестерина липопротеина низкой плотности и риск развития сердечной недостаточности, стенокардии, инфаркта миокарда, инсульта и переломов
|
Ингибиторы альфа-глюкозидазы
|
Ингибиторы кишечных ферментов
Используется в качестве монотерапии или в составе комбинированной терапии с другими пероральными препаратами или инсулином для уменьшения постпрандиальных уровней глюкозы в плазме
Следует принимать в самом начале приема пищи
Нежелательные эффекты в ЖКТ (метеоризм, диарея, вздутие живота) встречаются часто, но с течением времени могут уменьшаться
Терапию начинают с небольшой дозы (25 мг/день) и постепенно подбирают дозу в течение нескольких недель
| ||
|
|
25-100 мг три раза в день во время еды
|
| |
|
|
25-100 мг три раза в день во время еды
|
| |
Ингибиторы дипептидилпептидазы-4 (DPP4)
| |||
|
|
6,25–25 мг 1 раз/день
|
|
Все ингибиторы ДПП-4 могут быть использованы при почечной недостаточности средней или тяжелой степени.
Хорошо переносится, но вызывает лишь незначительные улучшения в гемоглобине A1C
В нескольких исследованиях наблюдалось небольшое увеличение риска панкреатита
|
|
|
По 5 мг 1 раз/день
|
| |
|
|
2,5-5 мг 1 раз/день
|
| |
|
|
25-100 мг 1 раз/день
|
| |
Ингибиторы натрий-глюкозного котранспортера 2 типа (SGLT2)
| |||
|
Канаглифлозин
|
100 или 300 мг 1 раз/день
|
|
Ингибиторы натрийзависимого переносчика глюкозы 2 типа могут вызывать гангрену Фурнье, снижение веса, ортостатическую гипотонию, инфекции дрожжами, инфекции мочеполовых путей
С осторожностью применяют у пожилых людей и при почечной недостаточности.
Возможно увеличение риска диабетического кетоацидоза
Канаглифлозин связан с более высокой долей ампутаций конечностей.
Эмпаглифлозин может оказывать положительное воздействие на сердечно-сосудистую систему.
|
|
Дапаглифлозин
|
5-10 мг 1 раз/день
|
| |
|
Эмпаглифлозин
|
|
| |
|
Эртуглифлозин
|
5–15 мг ежедневно
|
| |
Способы введения медикаментов
На сегодняшний день существует несколько способов введения медикаментов, которые можно разделить на два вида: энтеральный и парентеральный. Метод введения влияет на то, как быстро лекарственный препарат попадёт в очаг воспаления, а также на скорость и продолжительность его действия. Aprūpes Birojs осуществляет все нижеперечисленные виды введения лекарств на дому.
Метод введения влияет на то, как быстро лекарственный препарат попадёт в очаг воспаления, а также на скорость и продолжительность его действия. Aprūpes Birojs осуществляет все нижеперечисленные виды введения лекарств на дому.
Энтеральный способ подразумевает собой принятие лекарств через слизистую оболочку желудочно-кишечного тракта. Можно выделить следующие варианты введения:
- Пероральное введение – самый привычный и удобный способ принятия лекарств. Медикаменты попадают в организм через рот. Чаще всего таким способом принимают таблетки, капсулы, растворы, порошки, сиропы и др.
- Сублингвальное введение – таблетки, порошки, капли, и аэрозоли наносятся под язык, где расположено много капилляров и происходит активное кровоснабжение. Это позволяет лекарству в короткие сроки попадать в организм и мгновенно оказывать своё действие.
- Ректальное введение – введение лекарств через анальное отверстие в прямую кишку. Таким образом, лекарства гораздо быстрее попадают в кровь, чем при пероральном способе.
 Ректально принимаются свечи, мази и растворы, вводимые с помощью клизмы.
Ректально принимаются свечи, мази и растворы, вводимые с помощью клизмы.
При парентеральном способе введения лекарств препараты напрямую попадают в кровь, минуя желудочно-кишечный тракт.
Преимущества парентерального введения:
- Быстрота поступления лекарственных веществ в кровь.
- Большая точность дозировки.
- Исключается барьерная роль печени.
Данный метод осуществляется в виде различных инъекций и подходит в тех случаях, когда лекарство разрушается или не всасывается под воздействием желудочного сока. Инъекции можно проводить не только в стационаре, но и дома с помощью опытной медсестры.
• Интровенозные инъекции – через шприц лекарство сразу же попадает в системный кровоток, а эффект наступает мгновенно.
- Инфузионные инъекции – внутривенные вливания препарата объёмом более 100 мл, осуществляются с помощью капельницы.
- Внутримышечные инъекции, как правило, вводятся в зону ягодиц, живота или предплечья.
 Эффект от лекарства наступает в течение 10-15 минут.
Эффект от лекарства наступает в течение 10-15 минут. - Субкутанные инъекции или подкожные инъекции вводятся в подлопаточную область или наружную поверхность плеча. Действие лекарства проявляется в течение 15-20 минут.
Какие бы препараты не были назначены пациенту, медицинский персонал Aprūpes Birojs обеспечит надлежащее введение медикаментов на дому с соблюдением всех санитарных норм и врачебных предписаний.
На сегодняшний день существует несколько способов введения медикаментов, которые можно разделить на два вида: энтеральный и парентеральный. Метод введения влияет на то, как быстро лекарственный препарат попадёт в очаг воспаления, а также на скорость и продолжительность его действия. Aprūpes Birojs осуществляет все нижеперечисленные виды введения лекарств на дому.
Энтеральный способ подразумевает собой принятие лекарств через слизистую оболочку желудочно-кишечного тракта. Можно выделить следующие варианты введения:
- Пероральное введение – самый привычный и удобный способ принятия лекарств.
 Медикаменты попадают в организм через рот. Чаще всего таким способом принимают таблетки, капсулы, растворы, порошки, сиропы и др.
Медикаменты попадают в организм через рот. Чаще всего таким способом принимают таблетки, капсулы, растворы, порошки, сиропы и др. - Сублингвальное введение – таблетки, порошки, капли, и аэрозоли наносятся под язык, где расположено много капилляров и происходит активное кровоснабжение. Это позволяет лекарству в короткие сроки попадать в организм и мгновенно оказывать своё действие.
- Ректальное введение – введение лекарств через анальное отверстие в прямую кишку. Таким образом, лекарства гораздо быстрее попадают в кровь, чем при пероральном способе. Ректально принимаются свечи, мази и растворы, вводимые с помощью клизмы.
При парентеральном способе введения лекарств препараты напрямую попадают в кровь, минуя желудочно-кишечный тракт.
Преимущества парентерального введения:
- Быстрота поступления лекарственных веществ в кровь.
- Большая точность дозировки.
- Исключается барьерная роль печени.
Данный метод осуществляется в виде различных инъекций и подходит в тех случаях, когда лекарство разрушается или не всасывается под воздействием желудочного сока.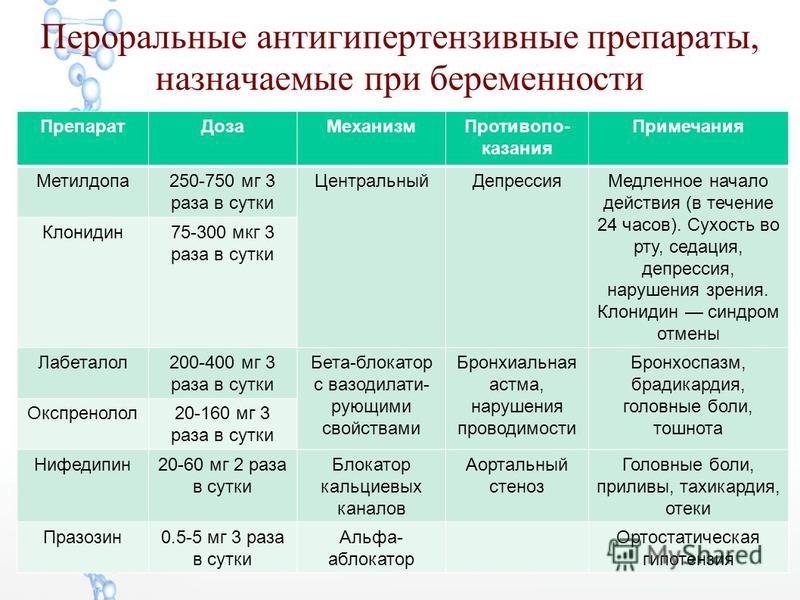 Инъекции можно проводить не только в стационаре, но и дома с помощью опытной медсестры.
Инъекции можно проводить не только в стационаре, но и дома с помощью опытной медсестры.
• Интровенозные инъекции – через шприц лекарство сразу же попадает в системный кровоток, а эффект наступает мгновенно.
- Инфузионные инъекции – внутривенные вливания препарата объёмом более 100 мл, осуществляются с помощью капельницы.
- Внутримышечные инъекции, как правило, вводятся в зону ягодиц, живота или предплечья. Эффект от лекарства наступает в течение 10-15 минут.
- Субкутанные инъекции или подкожные инъекции вводятся в подлопаточную область или наружную поверхность плеча. Действие лекарства проявляется в течение 15-20 минут.
Какие бы препараты не были назначены пациенту, медицинский персонал Aprūpes Birojs обеспечит надлежащее введение медикаментов на дому с соблюдением всех санитарных норм и врачебных предписаний.
Современные сахароснижающие средства в лечении сахарного диабета 2 типа | Майоров А.Ю., Науменкова И. В.
В.
Эндокринологический научный центр РАМН, Москва
Эндокринологический научный центр РАМН, Москва
Количество больных сахарным диабетом 2 типа (СД2) неуклонно возрастает. По данным Diabetes Atlas 2000, в мире зарегистрирован 151 миллион больных СД2. В то же время эксперты говорят о том, что количество невыявленного сахарного диабета (СД) может превышать регистрируемый сегодня уровень в 2–3 раза. Поэтому рациональная фармакотерапия этого заболевания является предметом многочисленных научных и клинических исследований. Одним из самых крупных исследований последнего времени явилось Британское проспективное исследование по контролю сахарного диабета и развитию осложнений (UKPDS). Оно продолжалось около 20 лет, в нем участвовало более 5000 больных СД2. Больные были разделены на группы, получавшие с момента выявления СД разные виды лечения: только диету, различные пероральные сахароснижающие препараты, инсулинотерапию.
Исследование показало возможность уменьшения частоты осложнений заболевания при интенсивной тактике лечения. Было продемонстрировано, что снижение уровня гликированного гемоглобина HbA1c на 1% (в результате интенсивного лечения СД с применением различных методов в течение 10 лет) снижает частоту осложнений СД в целом на 21%, микрососудистые осложнения на 35%, инфаркт миокарда на 18%, инсульт на 15%, смертность по диабету на 25%, общую смертность на 17%. С учетом большой опасности хронической (и часто не осознаваемой пациентами и даже врачами) декомпенсации СД в плане развития сосудистых осложнений, в последние годы разработаны более жесткие критерии компенсации (точнее сказать, цели лечения) СД2 (табл. 1) и пересмотрены некоторые терапевтические подходы к данной группе больных. Последний пересмотр этих критериев был проведен в 1998–99 гг. после изучения результатов исследования UKPDS.
Было продемонстрировано, что снижение уровня гликированного гемоглобина HbA1c на 1% (в результате интенсивного лечения СД с применением различных методов в течение 10 лет) снижает частоту осложнений СД в целом на 21%, микрососудистые осложнения на 35%, инфаркт миокарда на 18%, инсульт на 15%, смертность по диабету на 25%, общую смертность на 17%. С учетом большой опасности хронической (и часто не осознаваемой пациентами и даже врачами) декомпенсации СД в плане развития сосудистых осложнений, в последние годы разработаны более жесткие критерии компенсации (точнее сказать, цели лечения) СД2 (табл. 1) и пересмотрены некоторые терапевтические подходы к данной группе больных. Последний пересмотр этих критериев был проведен в 1998–99 гг. после изучения результатов исследования UKPDS.
Дополнительная цель: прекращение курения или уменьшение, насколько это возможно.
Одной из целей лечения сахарного диабета следует считать и снижение веса при его избытке.
Основными принципами лечения СД2 в настоящее время являются:
- диета
- физические нагрузки
- сахароснижающие препараты
– пероральные сахароснижающие препараты
– инсулин - обучение больных
- самоконтроль показателей обмена веществ
- раннее лечение осложнений и сопутствующих заболеваний (например, адекватный контроль артериального давления, липидов крови).
Диетотерапия
Эффективное лечение СД2 невозможно без соблюдения диеты, вне зависимости от того, получает больной дополнительно какие–либо сахароснижающие средства (в том числе инсулин) или нет. Питание больного СД2 должно отвечать ряду требований:
1. Оптимизация массы тела (для 80–90% больных с избытком массы – ее снижение).
2. Предотвращение постпрандиальной (после еды) гипергликемии.
3. Профилактика или лечение факторов риска сердечно–сосудистых заболеваний (дислипидемии, артериальной гипертонии).
4. Соблюдение всех принципов здорового питания, включая правильные соотношения всех необходимых нутриентов, достаточное количество витаминов, минеральных веществ и т.д.
Основную причину нарушения углеводного обмена при СД2 составляет избыточная масса тела. Многочисленными исследованиями уже давно доказано, что у большинства больных снижение массы тела позволяет достичь устойчивой компенсации углеводного обмена, уменьшить инсулинорезистентность, а также получить положительный эффект в отношении часто сопутствующих артериальной гипертонии и дислипидемии. Достигнуть снижения веса можно только путем ограничения калорийности рациона. Физическая нагрузка при СД2 играет, как правило, вспомогательную роль и особенно важна для длительного поддержания полученного эффекта.
Следует помнить, что не имеет смысла рекомендовать больному точный подсчет калоража. Во–первых, это практически невозможно. Человек питается смешанной пищей, а таблицы калорийности содержат информацию лишь о продуктах в чистом виде, что ведет к грубым ошибкам при попытках подсчета калорийности реального питания. Во–вторых, взвешивание каждого куска, постоянная сверка с таблицами калорийности, лишают процесс питания гедонической (доставляющей удовольствие) ценности. Собственно говоря, важно не столько само по себе рекомендуемое количество калорий, сколько реальное сокращение калорийности по сравнению с предшествующим питанием, которое и привело к избытку веса. Информация о низкокалорийной диете для больного должна быть простой, ясной и применимой в его повседневной жизни. Исходя из калорийности компонентов пищи (вода – 0 ккал, 1 г белка – 4 ккал, 1 г углеводов – 4 ккал, 1 г жира – 9 ккал, 1 г алкоголя – 7 ккал), основные принципы низкокалорийной диеты сводятся к следующему: во–первых, необходимо исключить или резко ограничить высококалорийные продукты – богатые жирами, алкоголь, сахар и сладости; во–вторых, употреблять в меньшем по сравнению с прежним (т.е. привычным для данного больного) количестве продукты средней калорийности – белки и крахмалы; в–третьих, свободно, без всяких ограничений, употреблять (замещая уменьшившийся за счет перечисленных ограничений объем питания) низкокалорийные продукты – овощи, зелень, некалорийные напитки.
Во–вторых, взвешивание каждого куска, постоянная сверка с таблицами калорийности, лишают процесс питания гедонической (доставляющей удовольствие) ценности. Собственно говоря, важно не столько само по себе рекомендуемое количество калорий, сколько реальное сокращение калорийности по сравнению с предшествующим питанием, которое и привело к избытку веса. Информация о низкокалорийной диете для больного должна быть простой, ясной и применимой в его повседневной жизни. Исходя из калорийности компонентов пищи (вода – 0 ккал, 1 г белка – 4 ккал, 1 г углеводов – 4 ккал, 1 г жира – 9 ккал, 1 г алкоголя – 7 ккал), основные принципы низкокалорийной диеты сводятся к следующему: во–первых, необходимо исключить или резко ограничить высококалорийные продукты – богатые жирами, алкоголь, сахар и сладости; во–вторых, употреблять в меньшем по сравнению с прежним (т.е. привычным для данного больного) количестве продукты средней калорийности – белки и крахмалы; в–третьих, свободно, без всяких ограничений, употреблять (замещая уменьшившийся за счет перечисленных ограничений объем питания) низкокалорийные продукты – овощи, зелень, некалорийные напитки.
Большинству больных СД2 следует рекомендовать дробное питание (5–6 раз в день малыми порциями). Оно позволяет избежать сильного чувства голода при уменьшении привычного объема питания, а также препятствует как постпрандиальной гипергликемии (порция углеводов в каждом приеме пищи должна быть невелика), так и гипогликемиям у больных на медикаментозной сахароснижающей терапии (частый прием небольших количеств углеводов).
Предотвращение постпрандиальной гипергликемии является вторым принципом диеты для больного СД2. Часто ему придают первостепенное значение, забывая, что патогенетически более важной является нормализация массы тела. Кроме дробного режима питания, снизить постпрандиальную гликемию помогают следующие меры: исключение из диеты легкоусвояемых углеводов в чистом виде (сахара, меда, сладких напитков, фруктовых соков), увеличение количества растительных волокон в пище, минимальная кулинарная обработка.
Диетические рекомендации для больных с нормальной массой тела сводятся, в конечном итоге, только к устранению высокой постпрандиальной гликемии. Сокращения калорийности рациона им, разумеется, не требуется.
Сокращения калорийности рациона им, разумеется, не требуется.
Физические нагрузки
Физические упражнения рассматриваются как важный метод в структуре комплексной терапии СД2. Кроме ускорения снижения веса, физическая активность сама по себе улучшает чувствительность к инсулину и, как следствие этого – показатели состояния углеводного обмена, а также нормализует липидемию. Считается, что наиболее приемлемой и безопасной (в связи с наличием сопутствующих заболеваний) тактикой физических упражнений являются занятия с начальной продолжительностью 5 – 10 минут и постепенным увеличением времени до 30–40 минут по крайней мере 2–3 раза в неделю. Если больной получает сахароснижающие препараты, на первый план должна выдвигаться осторожность в связи с возможной гипогликемией.
Пероральные сахароснижающие препараты
Подбор адекватной сахароснижающей терапии и достижение желаемой степени компенсации заболевания у больных СД2 представляют определенные сложности. Это обусловлено значительной гетерогенностью СД2, которая затрудняет поиск патогенетического лечения в каждом конкретном случае.
Это обусловлено значительной гетерогенностью СД2, которая затрудняет поиск патогенетического лечения в каждом конкретном случае.
Назначение пероральных сахароснижающих препаратов (ПССП) при впервые выявленном СД2 рекомендуется, если правильное соблюдение диеты в сочетании с физическими нагрузками не приводит к компенсации углеводного обмена. К сожалению, зачастую приходится назначать ПССП при сохраняющейся декомпенсации СД на фоне явного несоблюдения диеты. Альтернативой здесь могло бы быть направление в «Школу диабета» для группового обучения с целью изменения отношения к питанию или привлечение психолога к процессу изменения поведения пациента.
На сегодняшний день в клинической практике применяются ПССП следующих классов:
1. Производные сульфонилмочевины
2. Бигуаниды
3. Ингибиторы a-глюкозидаз
4. Прандиальные регуляторы гликемии
5. Тиазолидиндионы
6. Комбинированные препараты.
Механизмы действия этих классов препаратов различны, но в целом направлены на устранение трех основных метаболических нарушений, приводящих к гипергликемии: нарушение секреции инсулина поджелудочной железой, периферическая инсулинорезистентность, избыточная продукция глюкозы печенью. Дополнительный механизм действия – замедление всасывания глюкозы в тонком кишечнике и за счет этого уменьшение постпрандиального подъема гликемии.
Дополнительный механизм действия – замедление всасывания глюкозы в тонком кишечнике и за счет этого уменьшение постпрандиального подъема гликемии.
Производные сульфонилмочевины
Невзирая на факт наличия у больных СД2 гиперинсулинемии (по крайней мере, в начале заболевания), для преодоления имеющейся инсулинорезистентности собственного инсулина оказывается недостаточно и необходимо медикаментозно увеличивать концентрацию гормона в крови. Производные сульфонилмочевины (ПСМ) относятся к группе секретогогов, т.е. их действие основано прежде всего на способности стимулировать секрецию инсулина b-клетками поджелудочной железы, особенно в присутствии глюкозы. Препараты данной группы связываются со специфическими рецепторами на поверхности мембран b-клеток. Это связывание приводит к закрытию АТФ–зависимых калиевых каналов и деполяризации мембран b-клеток, что, в свою очередь, способствует открытию кальциевых каналов и быстрому поступлению кальция внутрь этих клеток. Указанный процесс приводит к дегрануляции и секреции инсулина. Таким образом, ПСМ активируют тот же естественный механизм, посредством которого глюкоза стимулирует секрецию инсулина. Повышение уровня инсулина в крови обеспечивает утилизацию глюкозы инсулинзависимыми тканями и подавление продукции глюкозы печенью.
Указанный процесс приводит к дегрануляции и секреции инсулина. Таким образом, ПСМ активируют тот же естественный механизм, посредством которого глюкоза стимулирует секрецию инсулина. Повышение уровня инсулина в крови обеспечивает утилизацию глюкозы инсулинзависимыми тканями и подавление продукции глюкозы печенью.
ПСМ делятся на препараты первой и второй генерации. Основное отличие препаратов второй генерации от первой заключается в их большей активности. Так, препараты второго поколения оказывают в 50–100 раз более выраженный сахароснижающий эффект по сравнению с таковыми первой генерации, в связи с чем применяются в значительно меньших дозах. Соответственно, риск побочных эффектов у препаратов второй генерации ниже, чем у первой. В настоящее время в клинической практике (во всяком случае в России) применяются только ПСМ второй генерации. Все ПСМ имеют в целом сходную структуру, и их фармакологический эффект опосредуется через единый механизм. Но некоторые различия в химической структуре приводят к тому, что каждый из них имеет свои особенности действия, которые позволяют оптимально использовать их в тех или других ситуациях.
Назначают ПСМ с минимальных доз, постепенно (с интервалом в 1–2 недели) оценивая эффект и увеличивая дозу по мере необходимости. В каждом конкретном случае дозу препарата следует подбирать индивидуально, помня о высоком риске гипогликемичеких состояний у лиц старческого возраста.
Глибенкламид остается одним из наиболее широко применяемых в мире ПСМ. Он обладает максимальным сродством к АТФ–зависимым К–каналам b-клеток, в связи с чем оказывает мощный сахароснижающий эффект, нередко являющийся причиной гипогликемии, обычно в случае нарушения режима питания или показаний к его применению. В настоящее время в России применяются как немикронизированные формы глибенкламида, так и микронизированные.
Биодоступность немикронизированной формы составляет до 70%, а концентрация в крови достигает максимума через 4–6 ч после приема препарата внутрь. Период полувыведения составляет от 10 до 12 ч, сахароснижающий эффект сохраняется до 24 ч. Выводится из организма на 50% почками и на 50% с желчью. Суточная доза может варьировать от 2,5 до 20 мг (обычно составляя 10–15 мг) и назначается обычно в 1–2 приема. Часто применяемое в обычной практике назначение в 3 приема не является обоснованным в отношении увеличения его эффективности. Обычно соотношение утренней и вечерней дозы составляет 1:1 или 2:1. Препарат принимается за 30 мин до еды.
Суточная доза может варьировать от 2,5 до 20 мг (обычно составляя 10–15 мг) и назначается обычно в 1–2 приема. Часто применяемое в обычной практике назначение в 3 приема не является обоснованным в отношении увеличения его эффективности. Обычно соотношение утренней и вечерней дозы составляет 1:1 или 2:1. Препарат принимается за 30 мин до еды.
Появившиеся в последние годы микронизированные формы (1,75 и 3,5) характеризуются почти полной биодоступностью, особенными фармакокинетикой, фармакодинамикой и большей эффективностью при употреблении в меньшей разовой и суточной дозе. Микронизированная форма глибенкламида обеспечивает полное высвобождение действующего вещества в течение 5 мин после растворения и быстрое всасывание, в связи с чем может быть сокращен интервал между приемом препарата и пищи. Максимальная концентрация микронизированного глибенкламида также наступает раньше, т.е. лучше совпадает с пиком постпрандиальной гликемии. Длительность сахароснижающего эффекта микронизированных форм – до 24 ч, а в связи с полной биодоступностью препарата потребность в глибенкламиде оказывается ниже на 30–40%, что в итоге обеспечивает адекватную секрецию инсулина в течение суток и снижает риск гипогликемических состояний. Максимальная доза микронизированного глибенкламида составляет 14 мг/сут.
Максимальная доза микронизированного глибенкламида составляет 14 мг/сут.
Глипизид в настоящее время представлен двумя основными формами: традиционной и новой – ГИТС (гастроинтестинальная терапевтическая система).
Начальная доза препарата – 2,5 – 5 мг, максимальная суточная – 20 мг. Время действия традиционной формы препарата составляет 12–24 ч, поэтому он назначается в основном 2 раза в день перед приемами пищи. Новая форма глипизида ГИТС выпускается под названием ретард. Отличие ее от традиционной формы глипизида заключается в наличии осмотически активного ядра препарата, который окружен полупроницаемой для воды мембраной. Ядро разделено на два слоя: «активный», содержащий препарат, и слой, содержащий инертные компоненты, однако обладающие осмолярной активностью. Вода из кишечного тракта поступает в таблетку, увеличивая давление в осмотическом слое, которое «выдавливает» активную часть препарата из центральной зоны. Это ведет к выходу препарата через мельчайшие, образованные лазером отверстия в наружной мембране таблетки. Таким образом, поступление препарата из таблетки в желудочно–кишечный тракт осуществляется постоянно и постепенно, до тех пор, пока не изменяется осмотический градиент. После приема препарата пролонгированного действия концентрация его в плазме повышается постепенно, достигая максимума через 6–12 ч. Терапевтическая концентрация в крови поддерживается в течение 24 часов, что позволяет принимать препарат 1 раз в сутки. Это более удобно и повышает приверженность больного лечению. ГИТС– форма достаточно безопасна в плане гипогликемических реакций. Это качество препарата особенно ценно для пациентов старше 65 лет – риск развития гипогликемий у которых выше.
Таким образом, поступление препарата из таблетки в желудочно–кишечный тракт осуществляется постоянно и постепенно, до тех пор, пока не изменяется осмотический градиент. После приема препарата пролонгированного действия концентрация его в плазме повышается постепенно, достигая максимума через 6–12 ч. Терапевтическая концентрация в крови поддерживается в течение 24 часов, что позволяет принимать препарат 1 раз в сутки. Это более удобно и повышает приверженность больного лечению. ГИТС– форма достаточно безопасна в плане гипогликемических реакций. Это качество препарата особенно ценно для пациентов старше 65 лет – риск развития гипогликемий у которых выше.
Гликлазид (Диабетон), помимо сахароснижающего эффекта (более мягкого, чем у глибенкламида), оказывает положительное влияние на микроциркуляцию, систему гемостаза, некоторые гематологические показатели и реологические свойства крови, что является крайне актуальным для больных СД. Также считается, что гликлазид наиболее хорошо стимулирует раннюю фазу секреции инсулина, которая нарушена при СД2. Период полувыведения составляет 12 ч, поэтому чаще всего применяется в 2 приема. Метаболизируется в печени, большая часть выводится почками. Начальная суточная доза – 40–80 мг, максимальная – 320 мг. Совсем недавно появилась новая форма гликлазида с модифицированным высвобождением – Диабетон МВ. Почти 100% биодоступность позволила снизить дозу гликлазида при использовании такой формы до 30–120 мг в сутки. Длительность действия составляет 24 ч, поэтому препарат принимается 1 раз в сутки перед завтраком, чтобы профиль действия соответствовал нормальному суточному ритму выделения инсулина. Такой режим применения, а также действие гликлазида преимущественно на первую фазу секреции инсулина обеспечивают меньший риск гиперинсулинемии. Результатом такого, более мягкого, действия является низкая частота гипогликемий, отсутствие прибавки веса и относительно более позднее развитие вторичной резистентности к препарату.
Период полувыведения составляет 12 ч, поэтому чаще всего применяется в 2 приема. Метаболизируется в печени, большая часть выводится почками. Начальная суточная доза – 40–80 мг, максимальная – 320 мг. Совсем недавно появилась новая форма гликлазида с модифицированным высвобождением – Диабетон МВ. Почти 100% биодоступность позволила снизить дозу гликлазида при использовании такой формы до 30–120 мг в сутки. Длительность действия составляет 24 ч, поэтому препарат принимается 1 раз в сутки перед завтраком, чтобы профиль действия соответствовал нормальному суточному ритму выделения инсулина. Такой режим применения, а также действие гликлазида преимущественно на первую фазу секреции инсулина обеспечивают меньший риск гиперинсулинемии. Результатом такого, более мягкого, действия является низкая частота гипогликемий, отсутствие прибавки веса и относительно более позднее развитие вторичной резистентности к препарату.
Гликвидон является единственным сахароснижающим препаратом, назначение которого возможно у лиц с заболеваниями почек: 95% полученной дозы препарата выводится через желудочно–кишечный тракт и лишь 5% – через почки. В связи с тем, что другие сахароснижающие препараты выводятся в значительной мере через почки, при диабетической нефропатии или сопутствующем поражении почек высок риск их кумуляции с развитием тяжелых гипогликемий. Начальная доза 30 мг, при отсутствии эффекта ее постепенно увеличивают (при необходимости до 120–180 мг). Также следует отметить, что по сравнению с другими препаратами гликвидон является более короткодействующим, поэтому кратность приема может быть увеличена до 3 раз в день.
В связи с тем, что другие сахароснижающие препараты выводятся в значительной мере через почки, при диабетической нефропатии или сопутствующем поражении почек высок риск их кумуляции с развитием тяжелых гипогликемий. Начальная доза 30 мг, при отсутствии эффекта ее постепенно увеличивают (при необходимости до 120–180 мг). Также следует отметить, что по сравнению с другими препаратами гликвидон является более короткодействующим, поэтому кратность приема может быть увеличена до 3 раз в день.
Глимепирид имеет ряд специфических особенностей. Он отличается от других ПСМ тем, что связывается не с классическим рецептором сульфонилмочевины (с молекулярной массой 177 кД), а с другим белком, сопряженным с АТФ–зависимыми К–каналами b-клеток и имеющим молекулярную массу 65 кД. В связи с этим препарат в 2,5–3 раза быстрее, чем глибенкламид, вызывает высвобождение инсулина b-клетками. С другой стороны, диссоциация его комплекса со связывающим белком происходит в 8–9 раз быстрее, чем у других ПСМ. Большая продолжительность эффекта (24 часа) делает достаточным прием 1 раз в сутки, что снижает вероятность пропуска приема лекарства. При этом усиление секреции инсулина происходит почти исключительно во время приемов пищи, что значительно снижает риск гипогликемических состояний. Широкий спектр доз таблетированных форм глимепирида (1, 2, 3, 4, 6 мг) облегчает подбор необходимой суточной дозы и его прием пациентами. Максимальная доза – 8 мг.
Большая продолжительность эффекта (24 часа) делает достаточным прием 1 раз в сутки, что снижает вероятность пропуска приема лекарства. При этом усиление секреции инсулина происходит почти исключительно во время приемов пищи, что значительно снижает риск гипогликемических состояний. Широкий спектр доз таблетированных форм глимепирида (1, 2, 3, 4, 6 мг) облегчает подбор необходимой суточной дозы и его прием пациентами. Максимальная доза – 8 мг.
При терапии больных ПСМ в ряде случаев наблюдается резистентность к препаратам данной группы. В том случае, когда отсутствие ожидаемого сахароснижающего эффекта наблюдается с первых дней лечения, несмотря на смену препаратов и увеличение суточной дозы до максимально возможной, принято говорить о первичной резистентности к ПСМ, которая наблюдается у 5% впервые диагносцированных больных. Как правило, первичная резистентность к ПСМ обусловлена снижением остаточной секреции собственного инсулина и диктует необходимость перевода пациентов на инсулинотерапию. Вторичная резистентность к ПСМ обычно развивается через несколько лет от начала лечения. Ежегодно это явление обнаруживается у 5–10% больных с СД2. У некоторых из этих больных имеет место более медленно прогрессирующий СД1. При лечении таких больных обязательна инсулинотерапия. У другой группы больных снижение остаточной секреции инсулина наблюдается лишь при стимуляции глюкозой, а не аргинином, что указывает на снижение чувствительности глюкорецепторов b-клеток к глюкозе. У части из этих больных назначение инсулинотерапии на небольшой срок восстанавливает чувствительность глюкорецепторов и позволяет вновь вернуться к пероральной сахароснижающей терапии. Вторичная резистентность к ПСМ может быть вызвана обострением сопутствующих заболеваний. После купирования этих состояний эффективность ПСМ может восстановиться. В ряде случаев имеет место не истинная вторичная резистентность к ПСМ, а ухудшение их эффекта вследствие несоблюдения диеты.
Вторичная резистентность к ПСМ обычно развивается через несколько лет от начала лечения. Ежегодно это явление обнаруживается у 5–10% больных с СД2. У некоторых из этих больных имеет место более медленно прогрессирующий СД1. При лечении таких больных обязательна инсулинотерапия. У другой группы больных снижение остаточной секреции инсулина наблюдается лишь при стимуляции глюкозой, а не аргинином, что указывает на снижение чувствительности глюкорецепторов b-клеток к глюкозе. У части из этих больных назначение инсулинотерапии на небольшой срок восстанавливает чувствительность глюкорецепторов и позволяет вновь вернуться к пероральной сахароснижающей терапии. Вторичная резистентность к ПСМ может быть вызвана обострением сопутствующих заболеваний. После купирования этих состояний эффективность ПСМ может восстановиться. В ряде случаев имеет место не истинная вторичная резистентность к ПСМ, а ухудшение их эффекта вследствие несоблюдения диеты.
Всегда необходимо помнить о риске гипогликемических реакций при использовании ПСМ и предупреждать больных о необходимости ношения с собой легкоусвояемых углеводов. Гипогликемия является, скорее, не побочным, а прямым эффектом ПСМ, но свидетельствует о неправильном подборе дозы или нарушении режима питания. Особенностью гипогликемий, вызванных ПСМ (в отличие от большинства «инсулиновых» гипогликемий), является их пролонгированность в связи с длительным периодом полувыведения этих препаратов, особенно в пожилом возрасте. Поэтому после успешного выведения из состояния гипогликемии, она, тем не менее, может рецидивировать в течение 12–72 часов.
Гипогликемия является, скорее, не побочным, а прямым эффектом ПСМ, но свидетельствует о неправильном подборе дозы или нарушении режима питания. Особенностью гипогликемий, вызванных ПСМ (в отличие от большинства «инсулиновых» гипогликемий), является их пролонгированность в связи с длительным периодом полувыведения этих препаратов, особенно в пожилом возрасте. Поэтому после успешного выведения из состояния гипогликемии, она, тем не менее, может рецидивировать в течение 12–72 часов.
Побочные эффекты при применении ПСМ чаще всего нетяжелые. Как правило, они появляются в первые 2 месяца от начала терапии и проявляются диспептическими расстройствами в виде тошноты, иногда рвоты, болей в эпигастрии, ощущением металлического вкуса во рту. Значительно реже встречаются более тяжелые побочные эффекты, которые требуют снижения дозы или полной отмены препаратов. Это кожные аллергические реакции, лейко– и тромбоцитопения, агранулоцитоз, гемолитическая анемия, токсическое поражение печени и почек. К побочным эффектам ПСМ следует относить и увеличение веса, однако этот эффект можно минимизировать или предотвратить правильным соблюдением диеты.
К побочным эффектам ПСМ следует относить и увеличение веса, однако этот эффект можно минимизировать или предотвратить правильным соблюдением диеты.
Бигуаниды
Препараты этой группы не изменяют секрецию инсулина, однако в присутствии последнего увеличивают периферическую утилизацию глюкозы тканями. Второй важный механизм действия бигуанидов – снижение глюконеогенеза и уменьшение продукции глюкозы печенью. Также считается, что они могут уменьшать всасывание углеводов в кишечнике. Влияние бигуанидов на уровень сахара в крови можно оценить, скорее, как антигипергликемическое, нежели как сахароснижающее.
Наиболее опасным побочным эффектом бигуанидов является развитие лактацидоза, в связи с этим долгое время отношение к этой группе было очень негативным, но в 90–е годы один из представителей группы бигуанидов – метформин – был реабилитирован. Было доказано, что он обладает минимальным риском развития лактацидоза.
Mетформин относительно быстро всасывается из желудочно–кишечного тракта. При суточной дозе 0,5–1,5 г биодоступность составляет 50–60%. Максимальное насыщение препаратом обычно достигается при дозе 3 г. В связи с этим назначение более высоких доз метформина считается нецелесообразным, так как не способствует дальнейшему усилению антигипергликемического эффекта. Полное выведение препарата обычно происходит в течение 8–20 ч. Начальная суточная доза метформина не должна превышать 500 мг. Препарат принимается вместе с пищей. При необходимости через неделю от начала терапии (при условии отсутствия побочных эффектов) доза препарата может быть увеличена до 500 мг дважды в сутки и далее. Оптимальная суточная доза метформина составляет 1500–1700 мг (500 мг трижды или 850 мг дважды в день). Максимальный эффект при лечении метформином наступает через несколько недель – его не следует ожидать слишком рано. При монотерапии снижение HbA1c составляет 0,9–1,5%.
При суточной дозе 0,5–1,5 г биодоступность составляет 50–60%. Максимальное насыщение препаратом обычно достигается при дозе 3 г. В связи с этим назначение более высоких доз метформина считается нецелесообразным, так как не способствует дальнейшему усилению антигипергликемического эффекта. Полное выведение препарата обычно происходит в течение 8–20 ч. Начальная суточная доза метформина не должна превышать 500 мг. Препарат принимается вместе с пищей. При необходимости через неделю от начала терапии (при условии отсутствия побочных эффектов) доза препарата может быть увеличена до 500 мг дважды в сутки и далее. Оптимальная суточная доза метформина составляет 1500–1700 мг (500 мг трижды или 850 мг дважды в день). Максимальный эффект при лечении метформином наступает через несколько недель – его не следует ожидать слишком рано. При монотерапии снижение HbA1c составляет 0,9–1,5%.
Помимо перечисленного действия метформина на углеводный обмен, следует подчеркнуть его положительное влияние на метаболизм липидов, что не менее важно при СД2: снижение общего холестерина на 10%, триглицеридов на 20–30%. Метформин – практически единственный сахароснижающий препарат, лечение которым может приводить не к повышению, а даже к снижению массы тела пациентов (в среднем – на 1,5 кг в год). По данным исследования UKPDS, если повышение веса со временем все же происходит, то оно минимально по сравнению с другими препаратами. Поэтому показанием к применению метформина является невозможность достижения компенсации заболевания у лиц с СД2 (в первую очередь с ожирением) на фоне диетотерапии только или в сочетании с применением ПСМ.
Метформин – практически единственный сахароснижающий препарат, лечение которым может приводить не к повышению, а даже к снижению массы тела пациентов (в среднем – на 1,5 кг в год). По данным исследования UKPDS, если повышение веса со временем все же происходит, то оно минимально по сравнению с другими препаратами. Поэтому показанием к применению метформина является невозможность достижения компенсации заболевания у лиц с СД2 (в первую очередь с ожирением) на фоне диетотерапии только или в сочетании с применением ПСМ.
Среди побочных действий метформина следует отметить диарею и другие диспепсические явления (металлический вкус во рту, тошнота, анорексия), которые в начале терапии наблюдаются почти у 20% больных, а затем самостоятельно проходят через несколько дней. Риск побочных эффектов можно свести к минимуму медленным титрованием дозы, приемом препарата во время еды и снижением доз при их возникновении. При длительном приеме метформина в больших дозах следует помнить о возможности снижения всасывания в желудочно–кишечном тракте витаминов В12 и фолиевой кислоты, что в исключительных случаях может привести к развитию мегалобластной анемии.
Риск развития лактацидоза при применении метформина минимален по сравнению с остальными бигуанидами и не превышает 8,4 случая на 100 000 больных в год. Тем более, что при развитии лактацидоза речь, как правило, идет не о метформин–индуцированном, а метформин–ассоциированном ацидозе. Лактацидоз той или иной степени тяжести может развиваться и без приема медикаментов – на фоне сердечной, почечной и печеночной недостаточности, а также при употреблении алкоголя. Однако следует иметь в виду даже столь незначительную опасность развития лактацидоза и контролировать содержание лактата (оптимально – около двух раз в год), регулярно оценивать скорость клубочковой фильтрации (развитие почечной недостаточности любого происхождения приведет к кумуляции метформина). При появлении жалоб на мышечные боли следует немедленно исследовать уровень лактата, а при возрастании содержания в крови лактата или креатинина, лечение метформином следует прекратить. К положительным аспектам действия метформина относится то, что сам по себе он практически не способен вызвать гипогликемию.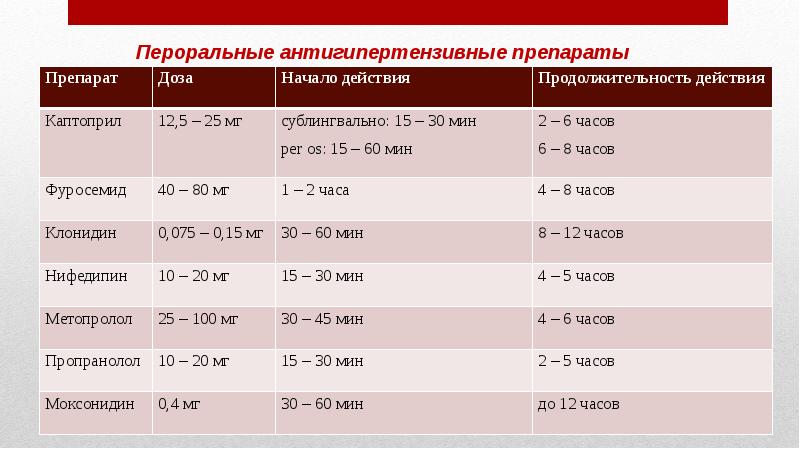
Противопоказаниями к назначению метформина являются гипоксические состояния любой природы, нарушение функции печени и почек, сердечная недостаточность, склонность к злоупотреблению алкоголем и указание на наличие лактацидоза в анамнезе. Прием метформина должен быть приостановлен за 1–2 дня до проведения любого контрастного исследования в связи с опасностью развития почечной недостаточности после внутривенного введения контраста.
Метформин может применяться как в виде монотерапии с диетой у лиц с СД2 и ожирением, так и в сочетании с ПСМ или инсулином. Указанная комбинированная терапия назначается в том случае, если желаемый терапевтический эффект на фоне монотерапии не достигается.
Ингибиторы a-глюкозидаз
Ингибиторы a-глюкозидаз (акарбоза) представляют собой псевдотетрасахариды, которые, конкурируя с ди–, олиго– и полисахаридами за места связывания на пищеварительных ферментах (сахаразе, гликоамилазе, мальтазе, декстразе и др. ), замедляют процессы последовательного ферментирования и всасывания углеводов по всему тонкому кишечнику. Указанный механизм действия приводит к снижению уровня постпрандиальной гипергликемии, т.е. препараты этой группы являются антигипергликемическими, а не сахароснижающими. Таким образом, акарбоза наиболее эффективна при высоком уровне гликемии после еды и нормальном – натощак. Для достижения нормального уровня чаще всего приходится использовать другие ПССП. К сожалению, в реальной клинической практике эффективность монотерапии акарбозой не столь значительна и проявляется в основном у больных с впервые выявленным СД.
), замедляют процессы последовательного ферментирования и всасывания углеводов по всему тонкому кишечнику. Указанный механизм действия приводит к снижению уровня постпрандиальной гипергликемии, т.е. препараты этой группы являются антигипергликемическими, а не сахароснижающими. Таким образом, акарбоза наиболее эффективна при высоком уровне гликемии после еды и нормальном – натощак. Для достижения нормального уровня чаще всего приходится использовать другие ПССП. К сожалению, в реальной клинической практике эффективность монотерапии акарбозой не столь значительна и проявляется в основном у больных с впервые выявленным СД.
Побочные эффекты акарбозы не опасны, но могут быть очень неприятны для больных. В толстый кишечник поступает значительно большее, чем обычно количество углеводов, которые перерабатываются бактериальной флорой с повышенным газообразованием. У пациентов возникает метеоризм и диарея. Пациент должен быть информирован о том, что возникновению побочных эффектов способствует в основном отклонение от рекомендованной диеты: употребление большого количества углеводов, как медленно, так и быстроусвояемых. Поэтому у некоторых больных побочные эффекты акарбозы являются дополнительным фактором, требующим соблюдения диеты.
Поэтому у некоторых больных побочные эффекты акарбозы являются дополнительным фактором, требующим соблюдения диеты.
Начальная доза акарбозы составляет 50 мг трижды в день перед едой или непосредственно в самом начале приема пищи. В случае хорошей переносимости препарата и отсутствия побочных эффектов дозу препарата можно увеличивать до 300–600 мг/сут.
Противопоказанием для назначения акарбозы являются такие заболевания желудочно–кишечного тракта, как грыжи различной локализации, язвенный колит, а также хронические заболевания кишечника, протекающие с выраженными нарушениями пищеварения и всасывания, острые и хронические гепатиты, панкреатиты, колиты.
Гипогликемии на фоне терапии акарбозой не развиваются. Однако следует учесть, что если гипогликемия развилась по другим причинам (передозировка ПСМ, в комбинации с которыми применялся препарат), акарбоза замедляет всасывание перорально принимаемых для ее коррекции углеводов. Пациентов необходимо информировать, что в этой ситуации они должны принимать препараты или продукты, содержащие глюкозу: виноградный сок, таблетированную глюкозу. Обычный сахар оказывается неэффективным.
Обычный сахар оказывается неэффективным.
Прандиальные регуляторы гликемии (меглитиниды)
Репаглинид – первый зарегистрированный в России препарат из этой группы. Он стимулирует секрецию инсулина b-клетками, но является представителем принципиально иного класса химических соединений, нежели ПСМ. Относится к производным карбамоил–метил–бензоевой кислоты. Препарат стимулирует секрецию инсулина, связываясь со своим собственным специфичным участком (молекулярная масса 36 кД), являющимся частью АТФ–зависимого К–канала. Все это и обуславливает специфические фармакологические свойства препарата.
Репаглинид in vitro (в отличие от ПСМ) не стимулирует секрецию инсулина b-клетками при отсутствии в среде глюкозы, но при концентрации глюкозы выше 5 ммоль/л оказывается в несколько раз более активным, чем ПСМ. Другой особенностью репаглинида является скорость его действия. Препарат быстро всасывается, начало действия наступает через 5–10 мин, что позволяет больному принимать его непосредственно перед едой.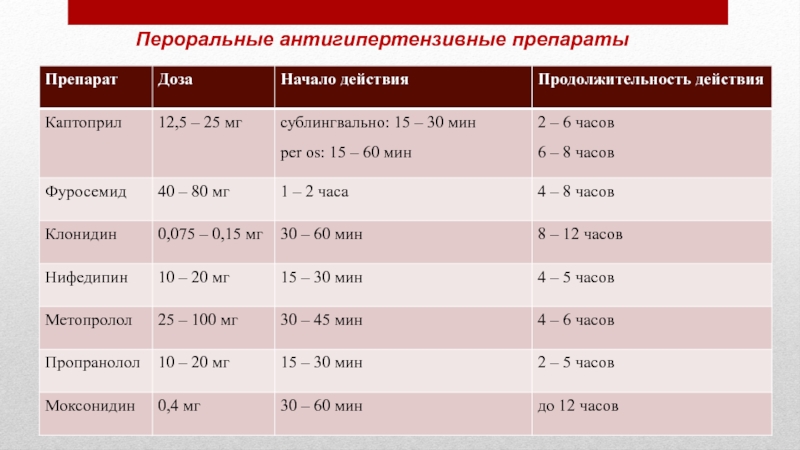 Пик концентрации в плазме достигается через 40 мин – 1 ч, что позволяет лучше регулировать уровень постпрандиальной гликемии. Препарат столь же быстро инактивируется (период полувыведения 40 мин – 1 ч), поэтому уровень инсулина возвращается к исходному через 3 часа после приема препарата, что имитирует нормальную секрецию инсулина во время еды и позволяет снизить вероятность гипогликемии в промежутках между едой. Также к положительным свойствам репаглинида можно отнести то, что он не вызывает прямого экзоцитоза и не подавляет биосинтез инсулина в b-клетке. Все это ведет к значительно более медленному истощению b-клеток. Инактивация препарата происходит в печени, более 90% выводится с желчью, что позволяет принимать препарат больным не только с легкой, но даже с умеренной степенью поражения почек. На фоне применения новонорма не зарегистрировано случаев гипогликемической комы.
Пик концентрации в плазме достигается через 40 мин – 1 ч, что позволяет лучше регулировать уровень постпрандиальной гликемии. Препарат столь же быстро инактивируется (период полувыведения 40 мин – 1 ч), поэтому уровень инсулина возвращается к исходному через 3 часа после приема препарата, что имитирует нормальную секрецию инсулина во время еды и позволяет снизить вероятность гипогликемии в промежутках между едой. Также к положительным свойствам репаглинида можно отнести то, что он не вызывает прямого экзоцитоза и не подавляет биосинтез инсулина в b-клетке. Все это ведет к значительно более медленному истощению b-клеток. Инактивация препарата происходит в печени, более 90% выводится с желчью, что позволяет принимать препарат больным не только с легкой, но даже с умеренной степенью поражения почек. На фоне применения новонорма не зарегистрировано случаев гипогликемической комы.
Дозировка – от 0,5 до 4 мг перед основными приемами пищи (обычно 2–4 раза в день). Таким образом, препарат позволяет больному более гибко подходить к вопросу соблюдения режима питания.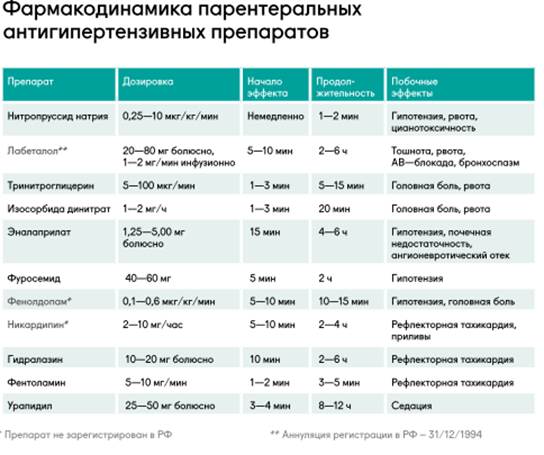 В случае пропуска приема пищи (например, обеда) прием препарата также пропускается. Это очень важно для относительно молодых пациентов с активным образом жизни, т.к. при лечении ПСМ в этом случае возникал бы риск гипогликемии. Максимальная доза составляет 16 мг в сутки.
В случае пропуска приема пищи (например, обеда) прием препарата также пропускается. Это очень важно для относительно молодых пациентов с активным образом жизни, т.к. при лечении ПСМ в этом случае возникал бы риск гипогликемии. Максимальная доза составляет 16 мг в сутки.
Наилучшие результаты репаглинид показывает у больных с небольшим стажем СД2, т.е. у больных с сохраненной секрецией инсулина. Если на фоне использования препарата происходит улучшение постпрандиальной гликемии, а гликемии натощак остается повышенной, его можно успешно комбинировать с метформином или пролонгированным инсулином перед сном.
Натеглинид является еще одним представителем прандиальных регуляторов гликемии. Он представляет собой производное аминокислоты D–фенилаланина. Механизм действия и все основные фармакокинетические и фармакодинамические свойства схожи с репаглинидом. Можно отметить, что натеглинид практически не требует подбора дозы. Стандартная разовая доза – 120 мг перед каждым основным приемом пищи.
Тиазолидиндионы
Препараты тиазолидиндионового ряда (пиоглитазон, розиглитазон) вошли в клиническую практику только в последние годы. Подобно бигуанидам, эти препараты не стимулируют секрецию инсулина, но повышают чувствительность к нему периферических тканей. Соединения этого класса выступают в роли агонистов ядерных PPAR-g рецепторов (peroxisome proliferator–activated receptor). PPAR-g рецепторы обнаруживаются в жировой, мышечной тканях и в печени. Активация PPAR-g рецепторов модулирует транскрипцию ряда генов, связанных с передачей эффектов инсулина на клетки и участвующих в контроле уровня глюкозы и метаболизме липидов. Помимо снижения уровня гликемии, улучшение чувствительности тканей к инсулину благоприятно влияет на липидный профиль (повышается уровень липопротеидов высокой плотности, снижается содержание триглицеридов). Учитывая, что эти препараты действуют, стимулируя транскрипцию генов, для получения максимального эффекта требуется до 2–3 мес. В клинических исследованиях эти препараты обеспечивали снижение уровня HbA1c при монотерапии примерно на 0,5–2%. Препараты данного класса могут применяться в сочетании с ПСМ, инсулином или метформином. Сочетание с метформином обосновано в связи с тем, что действие бигуанидов направлено в большей степени на подавление глюконеогенеза, а действие тиазолидиндионов – на повышение периферической утилизации глюкозы. Гипогликемии они практически не вызывают (но как и бигуаниды, способны повышать частоту гипогликемий в сочетании с секретогогами).
В клинических исследованиях эти препараты обеспечивали снижение уровня HbA1c при монотерапии примерно на 0,5–2%. Препараты данного класса могут применяться в сочетании с ПСМ, инсулином или метформином. Сочетание с метформином обосновано в связи с тем, что действие бигуанидов направлено в большей степени на подавление глюконеогенеза, а действие тиазолидиндионов – на повышение периферической утилизации глюкозы. Гипогликемии они практически не вызывают (но как и бигуаниды, способны повышать частоту гипогликемий в сочетании с секретогогами).
В настоящее время в России зарегистрирован препарат из группы тиазолидиндионов пиоглитазон. У препарата, который относится ко второму поколению тиазолидиндионов, не было обнаружено гепатотоксического действия (применение препарата «первого поколения» троглитазона было из–за этого запрещено). На фоне лечения рекомендуется контроль уровня аланин– и аспартаттрансферазы и прекращение приема препарата при уровне ферментов, вдвое превышающем норму. Пиоглитазон инактивируется в печени, выделяется преимущественно с желчью. Одним из побочных эффектов может быть появление отеков, а также прибавка веса. Препарат назначают один раз в сутки вне зависимости от приемов пищи. Суточная доза варьирует от 15 до 45 мг.
Пиоглитазон инактивируется в печени, выделяется преимущественно с желчью. Одним из побочных эффектов может быть появление отеков, а также прибавка веса. Препарат назначают один раз в сутки вне зависимости от приемов пищи. Суточная доза варьирует от 15 до 45 мг.
Комбинированные препараты
Традиционно лечение СД2 начинают с монотерапии метформином или ПСМ и только при выраженном ухудшении гликемического контроля добавляют второй препарат или инсулин. Такая тактика приводит к тому, что достаточно большая часть больных СД2 постоянно находится в состоянии неудовлетворительной компенсации, имея гликированный гемоглобин HbA1c на уровне не ниже 9%. В исследовании UKPDS также была отмечена ограниченная возможность монотерапии при длительном поддержании хорошего гликемического контроля. Через 3 года после установления диагноза только 50% были в состоянии достичь рекомендуемого уровня HbA1c при использовании монотерапии, а к 9 году эта цифра составила менее 25%. Логичным представляется интенсивное терапевтическое воздействие в возможно более ранние сроки одновременно на оба патогенетических звена, вызывающих гипергликемию для того, чтобы добиться постоянного уровня HbA1c менее 7%, рекомендуемого в качестве цели для профилактики осложнений.
Логичным представляется интенсивное терапевтическое воздействие в возможно более ранние сроки одновременно на оба патогенетических звена, вызывающих гипергликемию для того, чтобы добиться постоянного уровня HbA1c менее 7%, рекомендуемого в качестве цели для профилактики осложнений.
Применение двух препаратов разных классов в средних дозах более оправдано не только патогенетически: такая терапия создает меньший риск тяжелых побочных эффектов, чем высокие дозы одного препарата. Но, с другой стороны, комбинированная терапия может приводить к снижению комплаентности больных в отношении лечения. В связи с этим встал вопрос о производстве готовых комбинаций. В настоящее время используются готовые комбинации ПСМ и метформина.
Инсулинотерапия
Число больных СД2, требующих лечения инсулином, неуклонно возрастает, уже давно превысив количество больных СД1. К сожалению, существует множество причин (скорее психологических, чем объективных), из–за которых инсулинотерапия при СД2 зачастую назначается слишком поздно и рассматривается, как «последняя возможность» в лечении СД. На самом деле, помня о гетерогенности СД2, можно сказать, что в ряде случаев инсулин должен назначаться очень рано, если не вообще с самого начала заболевани
На самом деле, помня о гетерогенности СД2, можно сказать, что в ряде случаев инсулин должен назначаться очень рано, если не вообще с самого начала заболевани
.
Клинический фармаколог в помощь эндокринологу: выбор пероральной сахароснижающей терапии | #03/16
В настоящее время имеется широкий арсенал стационарных и амбулаторных средств, способных воздействовать практически на все известные звенья патогенеза сахарного диабета (СД) 2-го типа. Существует множество их классификаций, среди которых разделение по основному эффекту, по точкам приложения, по механизму действия, по длительности и т. д.
Выделяют гипогликемические средства и антигипергликемические средства. Целью гипогликемических препаратов (производные сульфонилмочевины и меглитиниды) является стимуляция синтеза эндогенного инсулина, в результате чего среди положительных сторон лечения происходят и отрицательные события: прибавка в весе и увеличение риска развития гипогликемических состояний.
Антигипергликемические препараты (ингибиторы α-глюкозидаз, бигуаниды, тиазолидиндионы, инкретиномиметики) улучшают периферическую утилизацию глюкозы, но не оказывают стимулирующего действия на β-клетки поджелудочной железы. Благодаря этому уровень инсулина в крови не повышается и снижения глюкозы в крови ниже нормы не происходит [1].
Сахароснижающие средства, влияющие на тонкую кишку, препятствуют полному всасыванию углеводов в кишечнике за счет ингибирования ферментов α-глюкозидаз, влияющих на поджелудочную железу (секретогены), — заставляют ее β-клетки выделять эндогенный инсулин, а влияющие на гепатоциты, жировую и другие периферические ткани (сенситайзеры) — увеличивают чувствительность органов-мишеней к инсулину.
Примерами секретогенных сахароснижающих лекарственных средств являются препараты сульфонилмочевины (глибенкламид, гликлазид, глимепирид) и прандиальные регуляторы глюкозы — меглитиниды (натеглинид, репаглинид). Сенситайзеры представлены бигуанидами (метформин) и тиазолидиндионами (пиоглитазон, росиглитазон).
Относительно новым классом сахароснижающих препаратов являются инкретиномиметики (вилдаглиптин, саксаглиптин, эксенатид, лираглутид), инсулинотропное действие которых является глюкозозависимым и реализуется только при повышенном уровне гликемии. При достижении нормогликемии концентрация инсулина возвращается к базальному уровню, что способствует снижению риска развития гипогликемии на фоне приема данных лекарственных средств. Механизм действия этих препаратов является глюкозозависимым и не нарушает нормального глюкагонового ответа на гипогликемию [2]. Основные классы пероральных сахароснижающих препаратов и механизмы их действия представлены в табл. 1 и на рис. 1.
Перед читателем десятки наименований лекарственных средств, принадлежащих к разным фармакологическим группам, обладающим своим механизмом действия, доказательной базой и стоимостью. При таком обилии лекарств, в рамках короткого режима общения с пациентом, а также в условиях коморбидности и вынужденной полипрагмазии, выбор нужного медикамента в адекватном режиме дозирования сделать очень нелегко — практически невозможно, что диктует необходимость в обозначении клинико-фармакологических ниш данных препаратов, а также их преимуществ и недостатков (рис. 2–8).
2–8).
Ингибиторы a-глюкозидазы должны применяться в основном с целью профилактики сахарного диабета 2-го типа у пациентов с начальными проявлениями инсулинорезистентности. Кроме того, они являются препаратами выбора для лиц с предиабетом, сопровождающимся именно постпрандиальной гипергликемией при нормальных тощаковых уровнях (снижение уровня HbA1c на 0,5–0,8%).
Показаниями для назначения глинидов являются сахарный диабет 2-го типа при неэффективности диеты и физических нагрузок. Также они предназначены для преимущественного снижения постпрандиальной гипергликемии (снижение уровня HbA1c на 0,5–1,5%).
Клиническая ниша для назначения глитазонов (тиазолидиндионов) сводится к сахарному диабету 2-го типа, в качестве монотерапии или в комбинации с препаратом сульфонилмочевины, бигуанидами или инсулином при отсутствии эффекта от диетотерапии, физических упражнений и монотерапии одним из вышеперечисленных средств (снижение уровня HbA1c на 0,5–1,4%).
Бигуаниды являются препаратами выбора как для лиц с предиабетом, сопровождающимся тощаковой гипергликемией и с нормальным уровнем сахара после еды, что косвенно свидетельствует об инсулинорезистентности, так и для пациентов с сахарным диабетом 2-го типа. Их назначение возможно в виде монотерапии и в комбинациях прежде всего с секретогенами (когда последние не дают полной коррекции гипергликемии) и с инсулином (при наличии инсулинорезистентности) (снижение уровня HbA1c на 1–2%).
Назначение производных сульфанилмочевины, как правило, ассоциировано с наличием СД 2-го типа в тех случаях, когда диета и физические нагрузки, назначение ингибиторов α-глюкозидаз и бигуанидов оказались неэффективными (снижение уровня HbA1c на 1–2%).
Препараты с инкретиновой активностью (рис. 7), влияющие преимущественно на ГПП1, назначаются при СД 2-го типа в качестве дополнения к терапии бигуанидами, производными сульфонилмочевины, тиазолидиндионами в случае неадекватного гликемического контроля (снижение уровня HbA1c на 0,8–1,8%).
Другая разновидность инкретиномиметиков — препараты, влияющие на ДПП4 (рис. 8), которые целесообразно назначать при сахарном диабете 2-го типа в качестве монотерапии в сочетании с диетотерапией и физическими упражнениями; в комбинации с бигуанидами в качестве начальной медикаментозной терапии при недостаточной эффективности диетотерапии и физических упражнений; а также в составе двухкомпонентной комбинированной терапии с бигуанидами, производными сульфонилмочевины, тиазолидиндионами или инсулином в случае неэффективности диетотерапии, физических упражнений и монотерапии этими препаратами (снижение уровня HbA1c на 0,5–1,0%).
Механизм действия ингибиторов ДПП4 максимально приближен к естественным процессам, происходящим в здоровом человеческом организме. Под их действием происходит уменьшение частоты защитных перекусов, которые пациенты употребляют во избежание гипогликемий, уменьшение всасывания жира из кишечника, повышение расхода энергии, а также повышение окисления липидов во время приема пищи [3]. Кроме того, при СД в результате повышенного апоптоза β-клетки теряют свою массу, что выражается в значительных нарушениях их функций, основной из которых является синтез инсулина. Физиологичное действие данной группы препаратов поддерживает жизнеспособность β-клеток поджелудочной железы, увеличивает их массу на 75% и на 65% уменьшает апоптоз [4]. Сравнение основных представителей ингибиторов ДПП4 представлено в табл. 2.
Кроме того, при СД в результате повышенного апоптоза β-клетки теряют свою массу, что выражается в значительных нарушениях их функций, основной из которых является синтез инсулина. Физиологичное действие данной группы препаратов поддерживает жизнеспособность β-клеток поджелудочной железы, увеличивает их массу на 75% и на 65% уменьшает апоптоз [4]. Сравнение основных представителей ингибиторов ДПП4 представлено в табл. 2.
Сердечно-сосудистые эффекты ингибиторов ДПП4 сводятся к уменьшению ремоделирования миокарда, улучшению функции эндотелия, снижению атерогенных фракций липопротеидов, снижению артериального давления (АД), уменьшению симптомов недостаточности кровообращения, защите миокарда от ишемии, а также к функциональному восстановлению миокарда после ишемии и увеличению числа рецепторов к инсулину в кардиомиоцитах [5]. Кардиометаболизм ингибиторов ДПП4 представлен в табл. 3.
Сводные данные, отражающие преимущества и недостатки основных классов сахароснижающих препаратов, представлены в табл. 4.
4.
Как видно из представленной таблицы:
- при сердечно-сосудистых заболеваниях пациентам следует избегать препаратов с высокой вероятностью развития гипогликемии, которая может оказаться весьма опасной для них;
- больным с избыточной массой тела необходимо назначать сахароснижающие препараты, не способствующие дальнейшей прибавке веса;
- при лечении женщин детородного возраста следует принимать во внимание возможность беременности, при которой таблетированные сахароснижающие препараты противопоказаны;
- все таблетированные сахароснижающие препараты противопоказаны лицам с диабетическим кетоацидозом;
- у больных алкогольной висцеропатией и циррозом печени выбор сахароснижающей терапии должен основываться на особенностях метаболизма препарата, а также длительности его действия;
- у пациентов с ХБП (в т. ч. в результате диабетической нефропатии) коррекцию гликемии следует осуществлять под контролем скорости клубочковой фильтрации (СКФ).

Невозможность поддержания компенсации углеводного обмена у пациентов на монотерапии, а также высокий риск развития острых и хронических осложнений сахарного диабета у коморбидных больных являются достаточными основаниями для проведения комбинированного лечения. В случае комбинированной сахароснижающей терапии улучшение эффективности лечения является следствием сложения механизмов действия препаратов (например, секретогенов и сенситайзеров) [6]. Комбинированная терапия сопровождается улучшением качества жизни больных и хорошо переносится ими, что связано с параллельным воздействием на разные звенья патогенеза СД и с уменьшением количества одномоментного приема таблетированных препаратов при одновременном улучшении компенсации углеводного обмена (рис. 9).
Однако эволюция пероральных сахароснижающих средств продолжается — еще в ноябре 2012 г. в Европе был одобрен первый представитель новейшего класса пероральных ингибиторов натрий-глюкозного котранспортера 2-го типа (SGLT2) — дапаглифлозин, а в марте 2013 г. Управление по контролю за продуктами питания и лекарственными средствами (Food and Drug Administration, FDA) одобрило канаглифлозин для лечения взрослых пациентов с сахарным диабетом 2-го типа. В американские, европейские и азиатские регуляторные органы также поданы заявки на регистрацию эмпаглифлозина, ипраглифлозина и лузеоглифлозина, масштабные исследования которых продолжаются в настоящее время.
Управление по контролю за продуктами питания и лекарственными средствами (Food and Drug Administration, FDA) одобрило канаглифлозин для лечения взрослых пациентов с сахарным диабетом 2-го типа. В американские, европейские и азиатские регуляторные органы также поданы заявки на регистрацию эмпаглифлозина, ипраглифлозина и лузеоглифлозина, масштабные исследования которых продолжаются в настоящее время.
Механизм их действия заключается в следующем. Из-за активной системы реабсорбции эта глюкоза практически полностью реабсорбируется в проксимальном канальце нефрона. Моча, поступающая в петлю Генле, свободна от глюкозы. Повышение концентрации глюкозы в плазме крови приводит к увеличению ее фильтрации в клубочках. При увеличении скорости поступления глюкозы в проксимальный каналец выше 260–350 мг/мин/1,73 м2, например у пациентов с СД, избыток глюкозы превышает реабсорбтивный потенциал, и она начинает выделяться с мочой. У здорового взрослого человека это соответствует концентрации глюкозы в крови около 10–11 ммоль/л (180–200 мг/дл). Поскольку глюкоза не способна свободно проникать через клеточную мембрану, то во всасывании ее в кишечнике и реабсорбции в почках участвуют натрийзависимые переносчики глюкозы (SGLT1 и 2) [7]. Соответственно, ингибиторы SGLT снижают концентрацию глюкозы в крови за счет стимуляции ее выведения с мочой.
Поскольку глюкоза не способна свободно проникать через клеточную мембрану, то во всасывании ее в кишечнике и реабсорбции в почках участвуют натрийзависимые переносчики глюкозы (SGLT1 и 2) [7]. Соответственно, ингибиторы SGLT снижают концентрацию глюкозы в крови за счет стимуляции ее выведения с мочой.
Мнение экспертов по поводу зарегистрированных ингибиторов SGLT2, ставших альтернативой метформину, в том числе в случае его непереносимости, неоднозначно. С одной стороны, препараты этого класса предлагают новые возможности в лечении СД: прежде всего новый, не зависимый от инсулина механизм действия, отсутствие негативного влияния на массу тела и даже небольшое ее снижение, благоприятные фармакокинетические свойства и в целом хорошую переносимость [8]. С другой стороны, механизм действия ингибиторов SGLT2 направлен на клинические проявления СД, а не на его причину [9]. Вследствие угнетения SGLT2 степень глюкозурии зависит от функции почек, а поскольку у больных СД она снижается по мере прогрессирования заболевания, эффективность этих препаратов в отдаленном периоде остается неизвестной. Кроме того, присутствие глюкозы в моче всегда рассматривалось как нежелательное явление, и многие врачи не готовы назначать лекарственные средства, вызывающие глюкозурию. Последняя является и причиной наиболее распространенных побочных эффектов — инфекций мочевыводящих путей и грибковых поражений гениталий [10].
Кроме того, присутствие глюкозы в моче всегда рассматривалось как нежелательное явление, и многие врачи не готовы назначать лекарственные средства, вызывающие глюкозурию. Последняя является и причиной наиболее распространенных побочных эффектов — инфекций мочевыводящих путей и грибковых поражений гениталий [10].
Клинико-фармакологические ниши данного класса препаратов расставит время, а ответы на многие вопросы должны развеять результаты клинических исследований этих лекарств, однако уже сегодня не вызывает сомнений постулат, гласящий о том, что, выбирая сахароснижающий препарат, врачу необходимо помнить, что в каждом конкретном случае адекватная терапия СД возможна только при учете возраста, пола, гендерных особенностей, массы тела пациента, а также этиологических и патогенетических механизмов развития заболевания.
Литература
- De Fronzo R. Pharmacologic therapy for type 2 diabetes mellitus // Ann Inter Med. 1999; 131: 281–303.
- Дедов И.
 И., Шестакова М. В. Инкретины: новая веха в лечении сахарного диабета 2-го типа. М., 2010. С. 55–62.
И., Шестакова М. В. Инкретины: новая веха в лечении сахарного диабета 2-го типа. М., 2010. С. 55–62. - Rosenstock J. Comparison of vildagliptin and rosiglitazone monotherapy in patients with type 2 diabetes: double-blind, randomized trial // Diabetes Care. 2007, 30 (2): 217–223.
- Matikainen N. Vildagliptin therapy reduces postprandial intestinal triglyceride-rich lipoprotein particles in patients with type 2 diabetes // Diabetologia. 2006, 49: 2049–2057.
- Duttaroy A. The DPP-4 inhibitor vildagliptin increases pancreatic beta-cell neogenesis and decreases apoptosis / Poster № 572 presented at ADA, 2005.
- Балаболкин М. И., Клебанова Е. М., Креминская В. М. Комбинированная сахароснижающая терапия и возможность достижения длительной компенсации углеводного обмена у больных сахарным диабетом 2-го типа // Русский медицинский журнал. 2007, № 17, с. 492–496.
- Hardman T. C., Dubrey S.
 W. Development and Potential Role of Type-2 Sodium-Glucose Transporter Inhibitors for Management of Type 2 Diabetes // Diabetes Ther. 2011; 2 (3): 133–145.
W. Development and Potential Role of Type-2 Sodium-Glucose Transporter Inhibitors for Management of Type 2 Diabetes // Diabetes Ther. 2011; 2 (3): 133–145. - Experts Express Mixed Thoughts on Canagliflozin Approval. Medscape Medical News. Apr 18, 2013. http://www.medscape.com/viewarticle/782712.
- Kim Y., Babu A. R. Clinical potential of sodium-glucose cotransporter 2 inhibitors in the management of type 2 diabetes // Diabetes Metab Syndr Obes. 2012; 5: 313–327.
- Ушкалова Е. А. Новый класс антидиабетических препаратов — ингибиторы натрий-глюкозных котранспортеров // Фарматека. 2013, № 16, с. 33–36.
А. С. Скотников*, 1, кандидат медицинских наук
М. Г. Селезнёва**
* ГБОУ ВПО Первый МГМУ им. И. М. Сеченова, Москва
** ГБУЗ ГКБ № 5 ДЗМ, Москва
1 Контактная информация: skotnikov. [email protected]
[email protected]
Комбинированная пероральная сахароснижающая терапия в современной стратегии лечения сахарного диабета 2 типа
В обзорной статье описаны современные подходы к выбору сахароснижающей терапии у пациентов с впервые диагностированным сахарным диабетом 2 типа согласно рекомендациям Международной диабетической федерации (IDF) 2012 г. и Российского общества эндокринологов 2013 г. Акцент сделан на выборе оптимальной комбинации пероральных сахароснижающих препаратов.
Таблица 1. Индивидуальные цели лечения (критерии контроля) СД
Рис. 1. Алгоритм лечения СД 2 типа IDF 2012 г. (адаптировано по [27])
Таблица 2. Клиническая эффективность различных классов пероральных сахароснижающих препаратов [33]
Рис. 2. Алгоритм контроля гликемии у больных СД 2 типа с исходным уровнем HbA1c 6,5–7,5%, РАЭ 2013 (адаптировано по [15])
Рис. 3. Алгоритм контроля гликемии у больных СД 2 типа с исходным уровнем HbA1c 7,6–9,0%, РАЭ 2013 (адаптировано по [15])
3. Алгоритм контроля гликемии у больных СД 2 типа с исходным уровнем HbA1c 7,6–9,0%, РАЭ 2013 (адаптировано по [15])
Рис. 4. Алгоритм контроля гликемии у больных СД 2 типа с исходным уровнем HbA1c > 9,0%, РАЭ 2013 (адаптировано по [15])
Рост распространенности сахарного диабета (СД) 2 типа в мире превосходит все прогнозы. Если 15 лет назад эксперты Всемирной организации здравоохранения (ВОЗ) предполагали, что к 2025 г. количество больных СД в мире будет равняться 380 млн [1], то, по данным Международной диабетической федерации (International Diabetes Federation, IDF), в 2011 г. их численность уже достигла 366 млн, а в соответствии с новым прогнозом ВОЗ к 2030 г. составит 552 млн человек [2]. Продолжительность жизни больных СД 2 типа в среднем на 5 лет меньше, чем в общей популяции. Это в первую очередь обусловлено быстрым прогрессированием атеросклероза, который повышает смертность лиц с СД 2 типа от сердечно-сосудистых заболеваний в 4–5 раз [3]. В целом от ассоциированных с атеросклерозом заболеваний умирает больше больных СД, чем от всех других причин, вместе взятых [4]. Считается, что такое выраженное поражение сосудистого русла вызывается гипергликемией. Метаанализ 20 исследований с участием 95 783 пациентов (период наблюдения составил 12 лет) позволил сделать вывод о том, что повышенный уровень глюкозы крови является таким же фактором риска развития атеросклероза и сердечно-сосудистых событий, как и повышенный уровень общего холестерина и артериального давления [5].
В целом от ассоциированных с атеросклерозом заболеваний умирает больше больных СД, чем от всех других причин, вместе взятых [4]. Считается, что такое выраженное поражение сосудистого русла вызывается гипергликемией. Метаанализ 20 исследований с участием 95 783 пациентов (период наблюдения составил 12 лет) позволил сделать вывод о том, что повышенный уровень глюкозы крови является таким же фактором риска развития атеросклероза и сердечно-сосудистых событий, как и повышенный уровень общего холестерина и артериального давления [5].
В серии крупных рандомизированных исследований [6–10] доказано большое значение жесткого контроля гликемии в снижении риска развития сердечно-сосудистых осложнений СД, что требует применения сразу после диагностики заболевания агрессивной тактики лечения пациентов с СД 2 типа с использованием эффективных и безопасных сахароснижающих препаратов и их комбинаций, позволяющих достичь целевого уровня гликемии. Длительные наблюдения показали, что такой терапевтический подход позволяет предупредить быстрое прогрессирование атеросклероза [11, 12].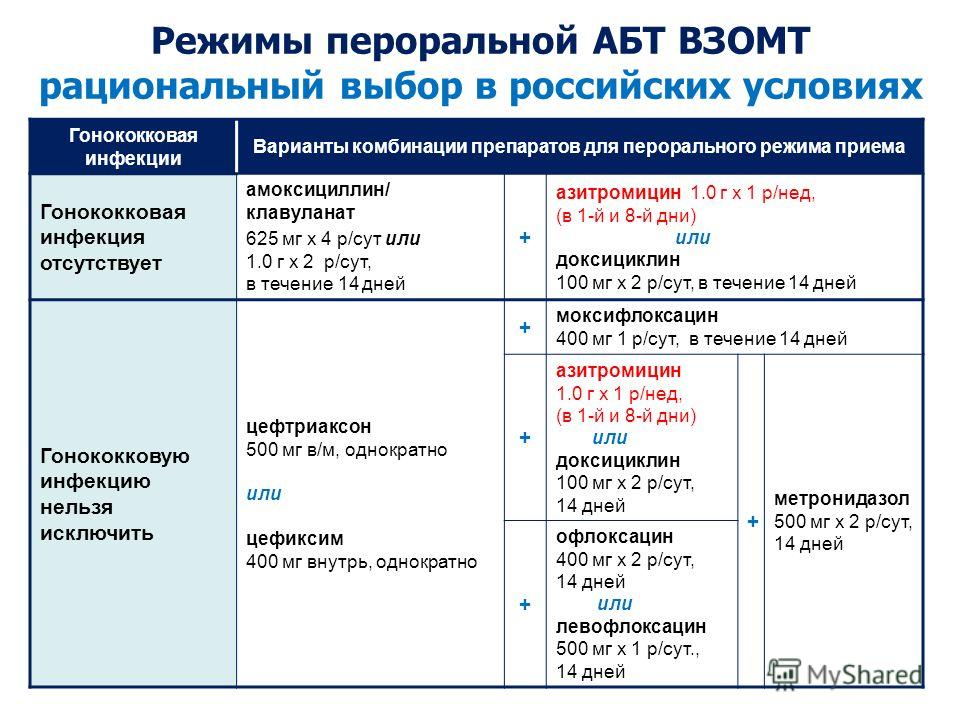
Однако интенсификация сахароснижающей терапии ограничивается риском развития гипогликемических состояний, увеличения массы тела и, как следствие, повышением смертности от острых сосудистых катастроф. В ходе исследования AСCORD (Action to Control Cardiovascular Risk in Diabetes – Действия по контролю сердечно-сосудистого риска у пациентов с сахарным диабетом) в группе интенсивного лечения эпизоды гипогликемии выявляли в 3 раза чаще по сравнению с группой стандартной терапии [13], а в исследовании VADT (Veterans Affairs Diabetes Trial – Исследование сахарного диабета у ветеранов войн США) – в 2 раза чаще [14], что сопровождалось увеличением общей летальности на 22% в исследовании АССORD и повышением числа сердечно-сосудистых событий в последующие 3 месяца после тяжелой гипогликемии у пожилых людей в исследовании VADT.
В связи с вышеизложенным Российская ассоциация эндокринологов (РАЭ) в конце 2011 г. предложила индивидуализировать целевые уровни гликемического контроля [15] в зависимости от возраста пациента, ожидаемой продолжительности жизни (ОПЖ), риска развития гипогликемических состояний и наличия или отсутствия тяжелых сердечно-сосудистых осложнений (табл. 1).
1).
СД 2 типа характеризуется двумя основными патогенетическими дефектами: снижением чувствительности к инсулину, или инсулинорезистентностью (ИР), и неадекватной секрецией инсулина для преодоления барьера ИР. Инсулинорезистентность зачастую в течение многих лет предшествует развитию СД 2 типа и обычно является генетически обусловленной, хотя и усугубляется такими факторами, как ожирение, снижение физической активности, беременность и избыток контринсулярных гормонов. Изначально ИР компенсируется за счет гиперинсулинемии, что поддерживает нормальную толерантность к углеводам. Нарушение толерантности к углеводам наблюдается при возрастании тяжести ИР или при снижении компенсаторных возможностей инсулиновой секреции, либо при прогрессировании обоих дефектов [16, 17]. По современным представлениям, СД 2 типа манифестирует, когда секреторная функция бета-клеток истощается, то есть бета-клетки становятся не способны поддерживать достаточно высокий уровень секреции инсулина, чтобы преодолеть барьер ИР. Основная роль в этой несостоятельности инсулярного аппарата отводится генетическим нарушениям [17], однако немаловажное значение в снижении секреторных резервов инсулярного аппарата имеет так называемый феномен глюкозотоксичности, за счет которого развиваются апоптоз и гибель бета-клеток. По статистическим данным, к моменту манифестации заболевания у пациентов функционируют только 50% бета-клеток, что подтверждает теорию постепенного прогрессирования нарушений углеводного обмена: от нормогликемии в условиях ИР и гиперинсулинемии до манифестации СД 2 типа через последовательные стадии нарушения гликемии натощак и нарушенную толерантность к глюкозе [18].
Основная роль в этой несостоятельности инсулярного аппарата отводится генетическим нарушениям [17], однако немаловажное значение в снижении секреторных резервов инсулярного аппарата имеет так называемый феномен глюкозотоксичности, за счет которого развиваются апоптоз и гибель бета-клеток. По статистическим данным, к моменту манифестации заболевания у пациентов функционируют только 50% бета-клеток, что подтверждает теорию постепенного прогрессирования нарушений углеводного обмена: от нормогликемии в условиях ИР и гиперинсулинемии до манифестации СД 2 типа через последовательные стадии нарушения гликемии натощак и нарушенную толерантность к глюкозе [18].
На основании вышеизложенного напрашивается вполне логичный вывод о том, что основным стратегическим направлением в лечении СД 2 типа должно быть воздействие на ИР как главное патогенетическое звено в развитии заболевания. Снижая ИР, или, иными словами, повышая чувствительность к инсулину, мы уменьшаем нагрузку на инсулярный аппарат, сохраняя тем самым его секреторные возможности и снижая негативное влияние гиперинсулинемии на повышение аппетита, увеличение массы тела, состояние сердечно-сосудистой системы. Самый простой способ повышения чувствительности к инсулину – уменьшение массы тела путем изменения образа жизни и характера питания. Однако на практике эти меры позволяют достичь целевого уровня гликемии менее чем у 30% пациентов с впервые выявленным СД 2 типа [6]. Таким образом, большинству пациентов необходима медикаментозная терапия, воздействующая на основное патогенетическое звено заболевания – ИР.
Самый простой способ повышения чувствительности к инсулину – уменьшение массы тела путем изменения образа жизни и характера питания. Однако на практике эти меры позволяют достичь целевого уровня гликемии менее чем у 30% пациентов с впервые выявленным СД 2 типа [6]. Таким образом, большинству пациентов необходима медикаментозная терапия, воздействующая на основное патогенетическое звено заболевания – ИР.
Выбор сахароснижающей терапии согласно алгоритму IDF (2012)
Первая линия терапии
Наиболее доступным и эффективным лекарственным средством на сегодняшний день является метформин. Основной механизм действия метформина направлен на снижение ИР за счет повышения активности тирозинкиназы инсулинового рецептора в периферических тканях, вследствие чего улучшается периферическая утилизация и окисление глюкозы [19, 20], подавляется липолиз и окисление свободных жирных кислот как альтернативного энергосубстрата [21, 22]. Именно с повышением чувствительности ткани печени к инсулину связывают снижение активности процессов глюконеогенеза и гликогенолиза [23, 24]. Таким образом, сахароснижающий эффект метформина является не столько гипогликемическим, сколько антигипергликемическим, так как приводит к уменьшению продукции глюкозы печенью и уровня гликемии натощак. С повышением чувствительности периферических тканей к инсулину связывают и снижение потребности в инсулине, и улучшение функциональных возможностей бета-клеток в связи с уменьшением глюкозотоксичности [25]. Кроме того, как показали недавние исследования, метформин может способствовать повышению уровня глюкагоноподобного пептида 1 (ГПП-1), стимулирующего, как известно, секрецию инсулина за счет улучшения абсорбции глюкозы в дистальных отделах тонкой кишки, где в основном и локализованы L-клетки, секретирующие ГПП-1 [26].
Именно с повышением чувствительности ткани печени к инсулину связывают снижение активности процессов глюконеогенеза и гликогенолиза [23, 24]. Таким образом, сахароснижающий эффект метформина является не столько гипогликемическим, сколько антигипергликемическим, так как приводит к уменьшению продукции глюкозы печенью и уровня гликемии натощак. С повышением чувствительности периферических тканей к инсулину связывают и снижение потребности в инсулине, и улучшение функциональных возможностей бета-клеток в связи с уменьшением глюкозотоксичности [25]. Кроме того, как показали недавние исследования, метформин может способствовать повышению уровня глюкагоноподобного пептида 1 (ГПП-1), стимулирующего, как известно, секрецию инсулина за счет улучшения абсорбции глюкозы в дистальных отделах тонкой кишки, где в основном и локализованы L-клетки, секретирующие ГПП-1 [26].
В случае непереносимости метформина или при наличии противопоказаний у пациентов, не имеющих избыточной массы тела, возможно применение препаратов сульфонилмочевины (ПСМ) в качестве первой линии лечения, исходя из предположения о том, что основным патогенетическим дефектом в развитии СД 2 типа без ожирения является неадекватная секреция инсулина.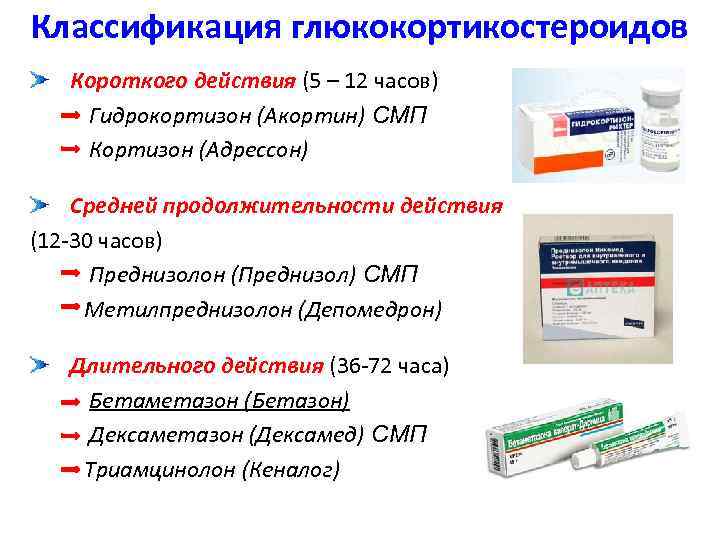 Данный вариант начала медикаментозного лечения не только патогенетически обоснован, но и имеет достаточную доказательную базу в отношении эффективности и безопасности применения ПСМ, а также отличается относительной дешевизной и доступностью.
Данный вариант начала медикаментозного лечения не только патогенетически обоснован, но и имеет достаточную доказательную базу в отношении эффективности и безопасности применения ПСМ, а также отличается относительной дешевизной и доступностью.
Как указывалось выше, у большинства больных СД 2 типа мероприятия по изменению образа жизни не обеспечивают достижения целевых параметров углеводного обмена либо из-за недостаточного снижения или повторного увеличения массы тела, либо из-за прогрессирования заболевания, а также вследствие сочетания перечисленных и ряда других факторов. Именно поэтому начинать терапию метформином рекомендуется вместе с изменением образа жизни сразу после установления диагноза [27]. В отсутствие противопоказаний метформин необходимо назначать в первую очередь, благодаря его влиянию на снижение гипергликемии, отсутствию на фоне его применения увеличения массы тела и гипогликемических состояний, обычно хорошему профилю переносимости с низкой частотой побочных эффектов, высокой приверженности пациентов лечению и относительно низкой стоимости. Доза метформина должна быть постепенно (в течение одного-двух месяцев) увеличена до максимально эффективной и переносимой.
Доза метформина должна быть постепенно (в течение одного-двух месяцев) увеличена до максимально эффективной и переносимой.
Вторая линия терапии
Однако даже максимальные терапевтические дозы метформина далеко не всегда позволяют добиться целевого уровня гликемии и снижения показателя HbA1c до
При невозможности достижения целевого уровня гликемического контроля с помощью ПСМ в качестве второй линии терапии предлагается применение метформина, если он не был назначен ранее, либо иДПП-4, или ТЗД, или ингибиторов альфа-глюкозидазы (в качестве альтернативного варианта).
Третья линия терапии
Если изменение образа жизни, лечение метформином и добавление к терапии второго препарата не способствовали достижению целевых параметров контроля углеводного обмена, начинают инсулинотерапию (см. рис. 1). В случае если уровень HbА1с близок к целевому (
Четвертая линия терапии
Интенсивная инсулинотерапия обычно заключается во введении дополнительных инъекций инсулина короткого или ультракороткого действия перед отдельными приемами пищи для уменьшения постпрандиальных колебаний гликемии (см. рис. 1). При переходе на интенсивную инсулинотерапию с инъекциями инсулина короткого или быстрого действия следует отменить секретогены инсулина (ПСМ или глиниды), поскольку они действуют синергично с вводимым инсулином.
рис. 1). При переходе на интенсивную инсулинотерапию с инъекциями инсулина короткого или быстрого действия следует отменить секретогены инсулина (ПСМ или глиниды), поскольку они действуют синергично с вводимым инсулином.
Стратификация лечебной тактики по алгоритму РАЭ (2013)
Эндокринологи-клиницисты нередко сталкиваются с ситуацией, когда добиться целевого уровня контроля гликемии в течение двух-трех месяцев лечения больного невозможно, что связано с сильными колебаниями исходного уровня HbA1c у пациентов – от 6,5 до 10% и выше. В связи с этим в конце 2011 г. эксперты РАЭ предложили дифференцированный подход к назначению и коррекции сахароснижающей терапии в зависимости от исходного уровня HbA1c с последующим изменением лечения при недостижении цели не ранее чем через 6 месяцев от начала проводимой терапии.
Тактика ведения пациентов с исходным уровнем HbА1с от 6,5 до 7,5%
Если уровень HbA1c не превышает 7,5%, вполне реально достичь целевого значения ниже 6,5% на фоне монотерапии метформином, пиоглитазоном, иДПП-4 или альфа-глюкозидазой, как это представлено на рис. 2. Двойная комбинация при неэффективности монотерапии предполагает добавление препаратов, влияющих на секрецию инсулина вследствие либо стимуляции секреторной функции бета-клеток (ПСМ, глиниды и аналоги ГПП-1), либо блокады расщепления нативного ГПП-1 ингибиторами фермента ДПП-4. В любом случае такая комбинация воздействует на оба патогенетических звена развития СД 2 типа: ИР и неадекватную секрецию инсулина, в результате чего обеспечивается адекватный гликемический контроль не только по параметру «уровень гликемии натощак», но и по показателю «уровень постпрандиальной гликемии», что и приводит к быстрому достижению терапевтической цели.
2. Двойная комбинация при неэффективности монотерапии предполагает добавление препаратов, влияющих на секрецию инсулина вследствие либо стимуляции секреторной функции бета-клеток (ПСМ, глиниды и аналоги ГПП-1), либо блокады расщепления нативного ГПП-1 ингибиторами фермента ДПП-4. В любом случае такая комбинация воздействует на оба патогенетических звена развития СД 2 типа: ИР и неадекватную секрецию инсулина, в результате чего обеспечивается адекватный гликемический контроль не только по параметру «уровень гликемии натощак», но и по показателю «уровень постпрандиальной гликемии», что и приводит к быстрому достижению терапевтической цели.
Возникает вопрос, какая комбинация предпочтительнее у пациентов с исходным уровнем HbA1c от 6,5 до 7,5%. Если брать за основу критерии переносимости и безопасности, то возможный риск гипогликемии при применении секретогенов у больных с исходно невысоким уровнем HbA1c превышает выраженность побочных эффектов со стороны желудочно-кишечного тракта и отечного синдрома, связанных с применением инкретинов и ТЗД соответственно. Именно поэтому авторы алгоритма РАЭ 2013 г. предлагают в качестве наиболее рациональных комбинаций в первую очередь сочетание метформина с иДПП-4 или аналогами ГПП-1, а во вторую – метформина с секретогенами (ПСМ или глинидами). Если изменение образа жизни, применение метформина и второго препарата не способствовали достижению целевых параметров контроля углеводного обмена, на следующем этапе начинают или интенсифицируют инсулинотерапию (рис. 2). Если уровень HbА1с близок к целевому (
Именно поэтому авторы алгоритма РАЭ 2013 г. предлагают в качестве наиболее рациональных комбинаций в первую очередь сочетание метформина с иДПП-4 или аналогами ГПП-1, а во вторую – метформина с секретогенами (ПСМ или глинидами). Если изменение образа жизни, применение метформина и второго препарата не способствовали достижению целевых параметров контроля углеводного обмена, на следующем этапе начинают или интенсифицируют инсулинотерапию (рис. 2). Если уровень HbА1с близок к целевому (
Тактика ведения пациентов с исходным уровнем HbА1с от 7,6 до 9%
Подавляющее большинство пациентов с СД 2 типа имеют на момент диагностики заболевания уровень HbА1с > 7,6%. При таком повышении показателя HbА1с на сегодняшний день не существует препаратов, которые бы были способны обеспечить достижение целевого уровня контроля при монотерапии в течение двух-трех месяцев (табл. 2).
Именно поэтому авторы алгоритма РАЭ 2013 г. предлагают изначально использовать комбинированную «двойную» терапию для достижения быстрого и эффективного контроля гликемии (рис. 3). Такой подход основан на данных многочисленных исследований, показавших, что одновременное назначение препаратов с разными точками приложения действия обеспечивает более значимое снижение HbА1с не только за более короткие сроки, но и в значительно меньших дозировках, нежели начальная монотерапия метформином с последующим добавлением второго препарата [29–31]. Метформин является основой всех возможных комбинаций, из которых наиболее безопасная – сочетание метформина с инкретиновыми миметиками (благодаря отсутствию риска гипогликемических состояний и увеличения массы тела), а самая эффективная – сочетание метформина с ПСМ (поскольку обеспечивает хороший контроль не только гликемии, но и уровня холестерина и липидного спектра крови) [31].
3). Такой подход основан на данных многочисленных исследований, показавших, что одновременное назначение препаратов с разными точками приложения действия обеспечивает более значимое снижение HbА1с не только за более короткие сроки, но и в значительно меньших дозировках, нежели начальная монотерапия метформином с последующим добавлением второго препарата [29–31]. Метформин является основой всех возможных комбинаций, из которых наиболее безопасная – сочетание метформина с инкретиновыми миметиками (благодаря отсутствию риска гипогликемических состояний и увеличения массы тела), а самая эффективная – сочетание метформина с ПСМ (поскольку обеспечивает хороший контроль не только гликемии, но и уровня холестерина и липидного спектра крови) [31].
В случае неэффективности «двойной» терапии рекомендуется добавить третий препарат. Руководствуясь принципами эффективности и безопасности, и в этой ситуации метформин следует выбрать в качестве основы терапии. С точки зрения риска развития гипогликемических состояний наиболее безопасным представляется добавление к комбинации метформина с инкретиновыми миметиками ТЗД. А наиболее эффективным считается присоединение ПСМ к комбинации метформина с инкретиновыми миметиками. Таким образом, пациентам с уровнем HbА1с, близким к 7,5%, целесообразно назначать комбинацию метформина с ТЗД и инкретиновыми миметиками, тогда как лицам с более высоким уровнем HbА1с – комбинацию метформина с ПСМ и инкретиновыми миметиками. Следующим этапом достижения целевого уровня гликемии при неэффективности комбинации трех препаратов является назначение инсулинотерапии сначала в фоновом, а затем и фоново-болюсном режиме, при переходе к которому необходимо отменить препараты, стимулирующие секрецию инсулина.
А наиболее эффективным считается присоединение ПСМ к комбинации метформина с инкретиновыми миметиками. Таким образом, пациентам с уровнем HbА1с, близким к 7,5%, целесообразно назначать комбинацию метформина с ТЗД и инкретиновыми миметиками, тогда как лицам с более высоким уровнем HbА1с – комбинацию метформина с ПСМ и инкретиновыми миметиками. Следующим этапом достижения целевого уровня гликемии при неэффективности комбинации трех препаратов является назначение инсулинотерапии сначала в фоновом, а затем и фоново-болюсном режиме, при переходе к которому необходимо отменить препараты, стимулирующие секрецию инсулина.
Тактика ведения пациентов с исходным уровнем HbА1с > 9%
В клинической практике нередко уже при диагностике СД 2 типа у пациентов имеется значительная гипергликемия и уровень HbA1c превышает 9%, однако отсутствует клиническая симптоматика заболевания, что свидетельствует о достаточной секреторной активности инсулярного аппарата. Тактикой выбора в этой ситуации, по предложению авторов алгоритма, может быть не интенсивная инсулинотерапия, которая абсолютно показана при HbА1с > 10% и выраженной клинической симптоматике, а изначальная «тройная» терапия. Наиболее эффективной при этом считается комбинация метформина с ПСМ и инкретиновыми миметиками, наиболее безопасной в отношении риска гипогликемии – комбинация метформина с инкретиновыми миметиками и ТЗД (рис. 4).
Тактикой выбора в этой ситуации, по предложению авторов алгоритма, может быть не интенсивная инсулинотерапия, которая абсолютно показана при HbА1с > 10% и выраженной клинической симптоматике, а изначальная «тройная» терапия. Наиболее эффективной при этом считается комбинация метформина с ПСМ и инкретиновыми миметиками, наиболее безопасной в отношении риска гипогликемии – комбинация метформина с инкретиновыми миметиками и ТЗД (рис. 4).
Фиксированные комбинации сахароснижающих препаратов как способ повышения приверженности пациентов лечению
Практикующим врачам хорошо известно о неблагоприятном влиянии сложных схем сахароснижающей терапии на соблюдение пациентами режима терапии. Как показали результаты исследования DARTS (The diabetes audit and research in Tayside Scotland – Аудит и исследование сахарного диабета в области Тейсайд (Шотландия)) [32], только 30% пациентов твердо придерживаются терапии одним лекарственным средством и менее 13% – бóльшим количеством препаратов и в высоких дозах (раздельная комбинация). Этим объясняется появление официнальных комбинированных сахароснижающих препаратов, состоящих из сочетания метформина с различными препаратами других классов. Самой эффективной является комбинация метформина с ПСМ, позволяющая добиться наиболее быстрого и значимого снижения уровня HbА1с при использовании меньших доз каждого из составляющих, чем в случае раздельной комбинации, что, безусловно, снижает риск развития и выраженность побочных эффектов (нарушения со стороны желудочно-кишечного тракта, увеличение массы тела, гипогликемические состояния). Первой фиксированной комбинацией метформина и ПСМ, зарегистрированной в России, стал препарат Глибомет, не утративший своей популярности более чем за 10 лет применения благодаря высокой эффективности, относительной дешевизне и хорошему профилю безопасности. Глибомет представляет собой фиксированную комбинацию 2,5 мг глибенкламида и 400 мг метформина гидрохлорида. Сочетание глибенкламида, стимулятора секреции инсулина, и метформина, повышающего чувствительность тканей к действию гормона, обеспечивает воздействие на оба патофизиологических механизма развития заболевания.
Этим объясняется появление официнальных комбинированных сахароснижающих препаратов, состоящих из сочетания метформина с различными препаратами других классов. Самой эффективной является комбинация метформина с ПСМ, позволяющая добиться наиболее быстрого и значимого снижения уровня HbА1с при использовании меньших доз каждого из составляющих, чем в случае раздельной комбинации, что, безусловно, снижает риск развития и выраженность побочных эффектов (нарушения со стороны желудочно-кишечного тракта, увеличение массы тела, гипогликемические состояния). Первой фиксированной комбинацией метформина и ПСМ, зарегистрированной в России, стал препарат Глибомет, не утративший своей популярности более чем за 10 лет применения благодаря высокой эффективности, относительной дешевизне и хорошему профилю безопасности. Глибомет представляет собой фиксированную комбинацию 2,5 мг глибенкламида и 400 мг метформина гидрохлорида. Сочетание глибенкламида, стимулятора секреции инсулина, и метформина, повышающего чувствительность тканей к действию гормона, обеспечивает воздействие на оба патофизиологических механизма развития заболевания. По современным представлениям, глибенкламид – препарат сульфонилмочевины второй генерации. Применяющийся в клинической практике с 1969 г., глибенкламид до сих пор остается «золотым стандартом», по которому оцениваются все остальные пероральные сахароснижающие препараты. Это объясняется тем, что глибенкламид обладает самой высокой константой сродства к SUR1-субъединице КАТФ-канала бета-клетки, связываясь с ней как сульфонилмочевинной, так и бензамидной группировкой. В 2010 г. глибенкламиду была присуждена Премия лекарственных средств им. Г.Г. Крейтцфельдта (Германия) как лекарственному препарату, который благодаря своему принципу действия сыграл центральную роль в оптимизации фармакотерапии. Особое значение при этом имеют эффективность препарата, его профиль безопасности и возможные долгосрочные благоприятные эффекты. В свою очередь метформин входит в Перечень жизненно необходимых и важнейших лекарственных препаратов, его эффективность и безопасность доказаны многочисленными исследованиями.
По современным представлениям, глибенкламид – препарат сульфонилмочевины второй генерации. Применяющийся в клинической практике с 1969 г., глибенкламид до сих пор остается «золотым стандартом», по которому оцениваются все остальные пероральные сахароснижающие препараты. Это объясняется тем, что глибенкламид обладает самой высокой константой сродства к SUR1-субъединице КАТФ-канала бета-клетки, связываясь с ней как сульфонилмочевинной, так и бензамидной группировкой. В 2010 г. глибенкламиду была присуждена Премия лекарственных средств им. Г.Г. Крейтцфельдта (Германия) как лекарственному препарату, который благодаря своему принципу действия сыграл центральную роль в оптимизации фармакотерапии. Особое значение при этом имеют эффективность препарата, его профиль безопасности и возможные долгосрочные благоприятные эффекты. В свою очередь метформин входит в Перечень жизненно необходимых и важнейших лекарственных препаратов, его эффективность и безопасность доказаны многочисленными исследованиями.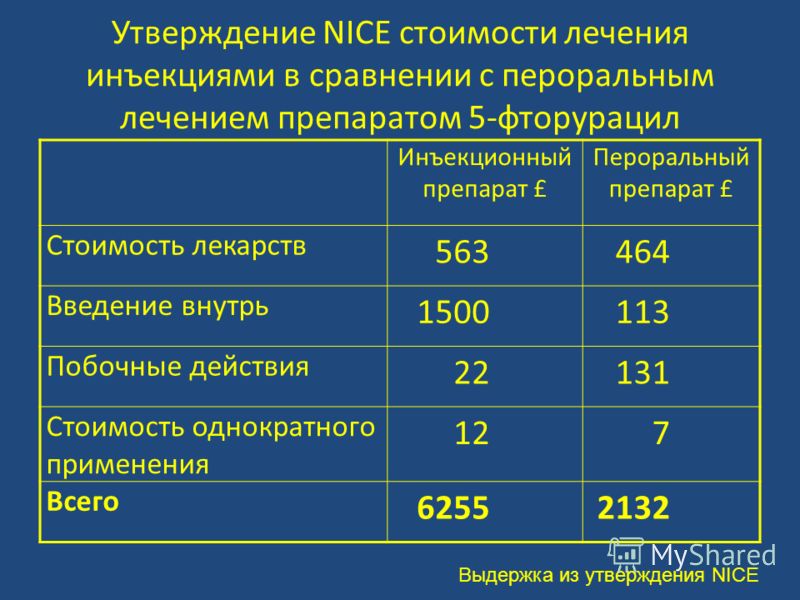 Отметим еще одно важное преимущество фиксированной комбинации: фармакокинетические параметры позволяют применять оба препарата 2 раза в день. Глибомет не уступает по эффективности комбинированной терапии двумя сахароснижающими препаратами. При расчете показателя «затраты – эффективность» было показано, что наименьшие затраты на достижение хорошего и удовлетворительного контроля были в группе лечения Глибометом, а наибольшие – в группе комбинированной терапии двумя сахароснижающими средствами [34].
Отметим еще одно важное преимущество фиксированной комбинации: фармакокинетические параметры позволяют применять оба препарата 2 раза в день. Глибомет не уступает по эффективности комбинированной терапии двумя сахароснижающими препаратами. При расчете показателя «затраты – эффективность» было показано, что наименьшие затраты на достижение хорошего и удовлетворительного контроля были в группе лечения Глибометом, а наибольшие – в группе комбинированной терапии двумя сахароснижающими средствами [34].
Таким образом, применение Глибомета в терапии СД 2 типа позволяет достичь целевого уровня контроля гликемии как у пациентов, не ответивших на лечение максимальными дозами метформина, либо в случае его непереносимости, так и у лиц, которым изначально показана «двойная» терапия при уровне HbА1с > 8,0% либо «тройная» терапия при уровне HbА1с > 9,0% в сочетании с инкретиновыми миметиками или ТЗД. Глибомет не только оказывает воздействие на оба основных патогенетических звена СД 2 типа, но и позволяет добиться эффекта с использованием меньших доз препарата и низким риском побочных явлений, а также обеспечивает лучшую комплаентность пациентов. Глибомет может быть использован в любой когорте пациентов с СД 2 типа вне зависимости от исходного уровня HbA1c, разумеется, с учетом индивидуальных целей лечения, определяемых исходя из возраста и ожидаемой продолжительности жизни пациента в отсутствие риска развития гипогликемических состояний и тяжелых сосудистых осложнений в анамнезе.
Глибомет может быть использован в любой когорте пациентов с СД 2 типа вне зависимости от исходного уровня HbA1c, разумеется, с учетом индивидуальных целей лечения, определяемых исходя из возраста и ожидаемой продолжительности жизни пациента в отсутствие риска развития гипогликемических состояний и тяжелых сосудистых осложнений в анамнезе.
1. The World Health Report 1998. Life in 21st Century – a Vision for all. Geneva: World Health Organisation, 1998.
2. Cунцов Ю.И. Современные сахароснижающие препараты, используемые в России при лечении сахарного диабета 2 типа // Сахарный диабет. 2012. № 1. С. 6–10.
3. Hsueh W.A., Law R.E. Cardiovascular risk continuum: Implications of insulin resistance and diabetes // Am. J. Med. 1998. Vol. 105. № 1А. P. 4S–14S.
4. Доборджгинидзе Л.М., Грацианский Н.А. Роль статинов в коррекции диабетической дислипидемии // Сахарный диабет. 2001. № 2. С. 41–47.
Доборджгинидзе Л.М., Грацианский Н.А. Роль статинов в коррекции диабетической дислипидемии // Сахарный диабет. 2001. № 2. С. 41–47.
5. Coutinho M., Gerstein H.C., Wang Y., Yusuf S. The relationship between glucose and incident cardiovascular events: a metaregression analysis of published data from 20 studies of 95,783 individuals followed for 12.4 years // Diabetes Care. 1999. Vol. 22. № 2. P. 233–240.
6. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complication in patients with type 2 diabetes (UKPDS 33). UK Prospective Diabetes Study (UKPDS) Group // Lancet. 1998. Vol. 352. № 9131. P. 837–853.
7. Ohkubo Y., Kishikawa H., Araki E. et al. Intensive insulin therapy prevents the progression of diabetic microvascular complications in Japanese patients with non-insulin-dependent diabetes mellitus: a randomized prospective 6-year study // Diabetes Res. Clin. Pract. 1995. Vol. 28. P. 103–117.
Clin. Pract. 1995. Vol. 28. P. 103–117.
8. Kahn S.E., Zinman B., Lachin J.M. et al. Rosiglitazone-associated fractures in type 2 diabetes: an analysis from a Diabetes Outcome Progression Trial (ADOPT) // Diabetes Care. 2008. Vol. 31. № 5. P. 845–851.
9. Patel A., MacMahon S., Chalmers J. et al. Intensive blood glucose control and vascular outcomes in patients with type 2 diabetes // N. Engl. J. Med. 2008. Vol. 358. № 24. P. 2560–2572.
10. Wilcox R., Kupfer S., Erdmann E. (PROactive Study Investigators). Effects of pioglitazone on major adverse cardiovascular events in high-risk patients with type 2 diabetes: results from PROspective pioglitAzone Clinical Trial In macro Vascular Events (PROactive 10) // Am. Heart J. 2008. Vol. 155. № 4. P. 712–717.
11. Holman R. R., Paul S.K., Bethel M.A. et al. 10-year follow-up of intensive glucose control in type 2 diabetes // N. Engl. J. Med. 2008. Vol. 359. № 15. P. 1577–1589.
R., Paul S.K., Bethel M.A. et al. 10-year follow-up of intensive glucose control in type 2 diabetes // N. Engl. J. Med. 2008. Vol. 359. № 15. P. 1577–1589.
12. Gaede P., Valentine W.J., Palmer A.J. et al. Cost-effectiveness of intensified versus conventional multifactorial intervention in type 2 diabetes: results and projections from the Steno-2 study // Diabetes Care. 2008. Vol. 31. № 8. P. 1510–1515.
13. Gerstein H.C., Miller M.E., Byington R.P. et al. Effects of intensive glucose lowering in type 2 diabetes // N. Engl. J. Med. 2008. Vol. 358. № 24. P. 2545–2559.
14. Duckworth W., Abraira C., Moritz T. et al. Glucose control and vascular complications in veterans with type 2 diabetes // N. Engl. J. Med. 2009. Vol. 360. № 2. P. 129–139.
15. Алгоритмы специализированной медицинской помощи больным сахарным диабетом.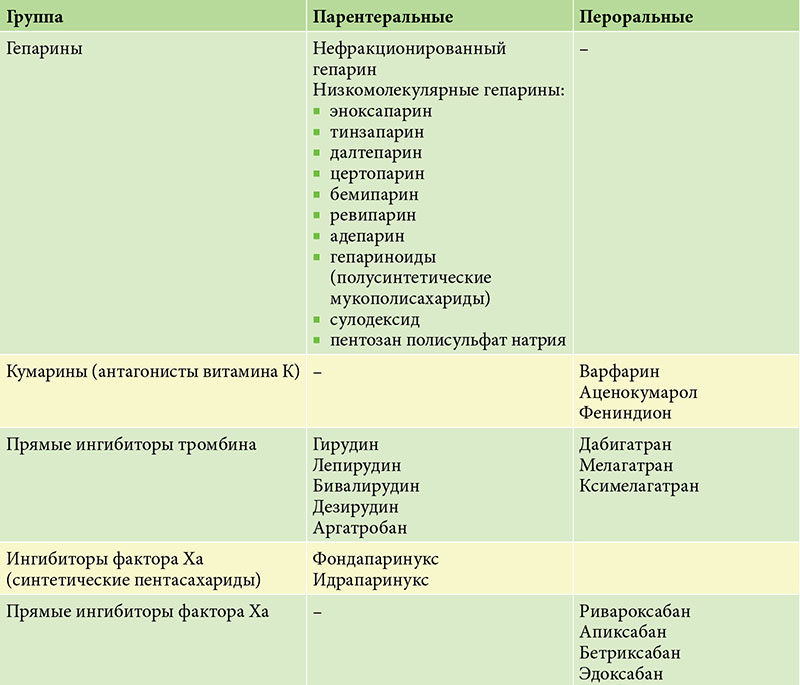 Вып. 6 / Российская ассоциация эндокринологов; под ред. И.И. Дедова, М.В. Шестаковой. М.: Информполиграф, 2013. 119 с.
Вып. 6 / Российская ассоциация эндокринологов; под ред. И.И. Дедова, М.В. Шестаковой. М.: Информполиграф, 2013. 119 с.
16. DeFronzo R.A. Pathogenesis of type 2 diabetes: metabolic and molecular implications for identifying diabetes genes // Diabetes Rev. 1997. Vol. 5. № 3. P. 177–269.
17. Kahn C.R., Vicent D., Doria A. Genetics of non-insulin-dependent (type-II) diabetes mellitus // Annual Rev. Med. 1996. Vol. 47. P. 509–531.
18. Kahn C.R. Banting Lecture. Insulin action, diabetogenes, and the cause of type II diabetes // Diabetes. 1994. Vol. 43. № 8. P. 1066–1084.
19. Kirpichnikov D., McFarlane S.I., Sowers J.R. Metformin: an update // Ann. Intern. Med. 2002. Vol. 137. P. 25–33.
20. Riccio A., Del Prato S. , Vigili de Kreutzenberg S., Tiengo A. Glucose and lipid metabolism in non-insulin-dependent diabetes. Effect of metformin // Diabetes Metab. 1991. Vol. 17. № 1. Pt. 2. P. 180–184.
, Vigili de Kreutzenberg S., Tiengo A. Glucose and lipid metabolism in non-insulin-dependent diabetes. Effect of metformin // Diabetes Metab. 1991. Vol. 17. № 1. Pt. 2. P. 180–184.
21. Perriello G., Misericordia P., Volpi E. et al. Acute antihyperglycemic mechanisms of metformin in NIDDM. Evidence for suppression of lipid oxidation and hepatic glucose production // Diabetes. 1994. Vol. 43. № 7. P. 920–928.
22. Radziuk J., Bailey C.J., Wiernsperger N., Yudkin J.S. Metformin and its liver targets in the treatment of type 2 diabetes // Curr. Drug Targets. Immune Endocr. Metabol. Disord. 2003. Vol. 3. № 2. P. 151–169.
23. Wollen N., Bailey C.J. Inhibition of hepatic gluconeogenesis by metformin. Synergism with insulin // Biochem. Pharmacol. 1988. Vol. 37. № 22. P. 4353–4358.
24. Ferner R.E., Rawlins M.D., Alberti K.G. Impaired B-cell responses improve when fasting blood glucose concentrate is reduced in non-insulin-dependent diabetes // Q. J. Med. 1988. Vol. 66. № 250. P. 137–146.
Ferner R.E., Rawlins M.D., Alberti K.G. Impaired B-cell responses improve when fasting blood glucose concentrate is reduced in non-insulin-dependent diabetes // Q. J. Med. 1988. Vol. 66. № 250. P. 137–146.
25. Lindsay J.R., Duffy N.A., McKillop A.M. et al. Inhibition of dipeptidyl peptidase IV activity by oral metformin in Type 2 diabetes // Diabet. Med. 2005. Vol. 22. № 5. P. 654–657.
26. Sinha Roy R., Bergeron R., Zhu L. et al. Metformin is a GLP-1 secretagogue, not a dipeptidyl peptidase-4 inhibitor // Diabetologia. 2007. Vol. 50. Suppl. 1. P. S284.
27. International Diabetes Federation Clinical Guidelines Task Force. Global Guideline for type 2 diabetes. Brussels, 2012. 117 p.
28. Schwartz S., Sievers R., Strange P. et al. Insulin 70/30 mix plus metformin versus triple oral therapy in the treatment of type 2 diabetes after failure of the two oral drugs // Diabetes Care. 2003. Vol. 26. № 8. P. 2238–2243.
2003. Vol. 26. № 8. P. 2238–2243.
29. De Fronzo R.A., Goodman A.M. Efficacy of metformin in patients with non-insulin-dependent diabetes mellitus. Multicenter Metformin Study Group // N. Engl. J. Med. 1995. Vol. 333. № 9. P. 541–549.
30. Hermann L.S., Schersten B., Bitzen P.-O. et al. Therapeutic comparison of metformin and sulphonylurea alone and in various combinations. A double-blind controlled study // Diabetes Care. 1994. Vol. 17. № 10. P. 1100–1109.
31. Tosi F., Muggeo M., Brun E. et al. Combination treatment with metformin and glibenclamide versus single-drug therapies in type 2 diabetes mellitus: a randomized, double-blind, comparative study // Metabolism. 2003. Vol. 52. № 7. P. 862–867.
32. Morris A.D. Considerations in assessing effectiveness and costs of diabetes care: lessons from DARTS // Diabetes Metab. Res. Rev. 2002. Vol. 18. Suppl. 3. P. S32–S35.
Res. Rev. 2002. Vol. 18. Suppl. 3. P. S32–S35.
33. Nathan D.M., Buse J.B., Davidson M.B. et al. Management of hyperglycemia in type 2 diabetes: A consensus algorithm for the initiation and adjustment of therapy: a consensus statement from the American Diabetes Association and the European Association for the Study of Diabetes // Diabetes Care. 2006. Vol. 29. № 8. P. 1963–1972.
34. Тюрина И.В., Воробьев П.А., Авксентьева М.В. Клинико-экономический анализ применения препарата глибомет по сравнению с альтернативными схемами лечения сахарного диабета 2 типа // Проблемы стандартизации в здравоохранении. 2003. № 8. С. 36–40.
The role of oral antidiabetic drugs combinations in the current treatment strategy of type 2 diabetes mellitus
State Budgetary Educational Institution for Higher Professional Education ‘I. M. Sechenov First Moscow State Medical University’ of the Ministry of Health of Russia, Endocrinology Department of the Faculty for Postgraduate Professional Training of Physicians
M. Sechenov First Moscow State Medical University’ of the Ministry of Health of Russia, Endocrinology Department of the Faculty for Postgraduate Professional Training of Physicians
Contact person: Lyudmila Viktorovna Nedosugova, [email protected]
The review addresses current strategies of hypoglycemic treatment in patients with new-onset type 2 diabetes mellitus according to the 2012 International Diabetes Federation (IDF) clinical guidelines and 2013 Russian Endocrinology Society guidelines, with special focus on the choice of optimal combinations of oral hypoglycemic agents.
Управление пероральными препаратами | Encyclopedia.com
Определение
Пероральное введение лекарств — это процесс, при котором лекарства доставляются перорально через пищеварительный тракт.
Цель
Лекарства принимаются этим путем из-за удобства, абсорбции препарата, простоты использования и низкой стоимости. Таким образом, это наиболее распространенный метод.
Таким образом, это наиболее распространенный метод.
Меры предосторожности
Другие способы используются, когда человек ничего не может принять внутрь или лекарство плохо всасывается в желудочно-кишечном тракте.Медсестра должна проверить, есть ли у пациента какие-либо известные аллергии . При приеме любого лекарства полезно помнить о следующих проверках: правильный пациент, правильное лекарство, правильный путь, правильная доза, правильное место и правильное время.
Описание
Пероральные препараты можно назначать для приема через разные промежутки времени, до или после еды. Они могут быть в жидкой или твердой форме. Вопросы о частоте приема лекарств следует адресовать лечащему врачу.
Подготовка
Вымойте руки. Следует проверить лист заказа пациента, чтобы убедиться, что доза еще не была введена. Как только это будет подтверждено, следует выбрать правильный препарат и дозу. Соответствующее количество таблеток следует встряхнуть на крышке контейнера и бросить в небольшую мерную чашку, чтобы передать пациенту. Это следует делать непосредственно перед введением препарата, а не заранее.
Это следует делать непосредственно перед введением препарата, а не заранее.
Если лекарство жидкое, флакон следует встряхнуть, снять крышку и держать флакон на уровне глаз этикеткой вверх, чтобы предотвратить образование пятен.Правильную дозу следует налить в мерный стаканчик.
Следует проинформировать пациента о том, что его или ее врач прописал ему или ей какое-либо лекарство. Медсестра должна еще раз сверить лекарство и дозу с таблицей рецептов пациента, а затем подтвердить имя пациента на его или ее браслете. Затем лекарство можно передать пациенту, которому также следует предложить выпить воды для облегчения проглатывания таблеток.
Жидкие лекарства, содержащие железа , следует принимать через соломинку, чтобы минимизировать окрашивание зубов.
Убедившись, что лекарство было принято, медсестра должна записать время и введенную дозу.
Последующий уход
Медсестра должна следить за реакцией пациента и при необходимости успокаивать.
Осложнения
Возможные осложнения включают:
- Препарат может взаимодействовать с другими лекарствами, которые принимает пациент, и изменять желаемый эффект.
- Пациент может отказаться от препарата.
- Могут возникнуть трудности с глотанием.
- Препарат может вызвать раздражение желудочно-кишечного тракта.
- Препарат может быстро проходить через организм, и его преимущества могут быть потеряны.
КЛЮЧЕВЫЕ УСЛОВИЯ
Пищевые продукты —в отношении системы питания.
Пищеварительный тракт — Пищеварительный тракт и другие органы, участвующие в пищеварении и абсорбции.
Gastro — относительно желудка.
Желудочно-кишечный тракт —Желудок и кишечник, участвующие в пищеварении и удалении продуктов жизнедеятельности.
Кишечник — Что касается кишечника.
Результаты
Введение пероральных препаратов должно привести к тому, что пациент получит надлежащую дозу препарата безопасно и без осложнений. Пероральные препараты также могут взаимодействовать с другими лекарствами, которые принимает пациент, например, с инъекциями. Медсестра должна проверить наличие каких-либо побочных реакций, если препарат вводится впервые.
Пероральные препараты также могут взаимодействовать с другими лекарствами, которые принимает пациент, например, с инъекциями. Медсестра должна проверить наличие каких-либо побочных реакций, если препарат вводится впервые.
Роли группы здравоохранения
Персонал должен установить, принимает ли пациент какие-либо лекарства, прежде чем ему будут назначены какие-либо дополнительные лекарства.Важно, чтобы медсестра понимала действие, побочные эффекты и несовместимость лекарств, знала нормальные дозы и знала о любых реакциях, которые может испытывать пациент. Медсестра должна сообщать о любых необычных эффектах медицинскому персоналу и регистрировать любые побочные эффекты или негативные реакции на введенное лекарство.
Если лекарство назначается регулярно для лечения определенного заболевания, пациента можно направить в группу самопомощи, члены которой имеют такое же заболевание.Пациенту следует помочь почувствовать уверенность в том, что его или ее конфиденциальность обеспечена.
Если этикетки на бутылках с жидкими лекарствами окрашены и неразборчивы, лекарство использовать нельзя.
Ресурсы
КНИГИ
Денвилл, Нью-Джерси Книга с источниками самопомощи. American Self Help Clearinghouse, 1998.
ORGANIZATIONS
Американская академия практикующих медсестер. AANP, а / я 12846, Остин, Техас, 78711. (512) 442-4262. [адрес электронной почты защищен]
Американская ассоциация медсестер, 600 Мэриленд-авеню, юго-запад, люкс 100 Запад, Вашингтон, округ Колумбия 20024.(202) 651-7000.
Национальная ассоциация медицинских сестер-специалистов, 3969 Green Street, Harrisburg, PA, 17110. (717) 234-6799. [адрес электронной почты защищен]
Национальная лига медсестер, 61 Broadway, 33rd Floor, New York, NY 10006. (212) 363-5555 или (800) 669-1656.
ДРУГОЕ
«Как вводить лекарства».
Маргарет А. Стокли, RGN
Как правильно принимать пероральные препараты
Чаще всего люди принимают лекарства орально (внутрь). В зависимости от того, что прописал врач, пероральные лекарства можно проглотить, разжевать или положить под язык для растворения.
В зависимости от того, что прописал врач, пероральные лекарства можно проглотить, разжевать или положить под язык для растворения.
Лекарства, которые вы проглатываете, попадают из желудка или кишечника в кровоток, а затем разносятся по всем частям вашего тела. Этот процесс известен как абсорбция. Скорость, с которой происходит всасывание, зависит от нескольких факторов:
- Тип лекарства, которое вы принимаете (например, жидкость или таблетка)
- Принимаете ли вы лекарство во время еды, после еды или натощак
- Способность вашего лекарства попадать в кровоток (некоторые лекарства имеют специальное покрытие и медленно растворяются в желудке.)
- Как ваше лекарство реагирует на кислотную среду в желудке
- Взаимодействует ли ваше лекарство с другими лекарствами, которые вы принимаете одновременно
Если желателен быстрый эффект, врач может назначить лекарство, которое растворяется во рту и быстро попадает в кровоток.
AsiaVision / Getty Images
Таблетки и капсулы
Как правило, следует принимать таблетки и капсулы, запивая водой. Прием некоторых таблеток, таких как Липитор (аторвастатин) и Виагра (силденафил), с грейпфрутовым соком может вызвать потенциально опасные побочные эффекты.Молоко может блокировать всасывание многих антибиотиков, таких как ципро (ципрофлоксацин).
Ваш врач или фармацевт скажет вам, следует ли принимать лекарство натощак, до или после еды. Эта информация очень важна, потому что переваривание пищи может помешать растворению лекарств и их попаданию в кровоток. Всегда следуйте инструкциям по рецепту.
Ни в коем случае не ломайте, не раздавливайте и не жуйте капсулы или таблетки, если они не рекомендованы вашим врачом или фармацевтом.Многие лекарства имеют длительный срок действия или имеют специальную оболочку, поэтому их нужно глотать целиком. Если у вас есть вопросы по этому поводу, спросите своего фармацевта.
Если у вас возникли проблемы с проглатыванием лекарства, сообщите об этом своему врачу и фармацевту. Они могут предложить вам жидкую форму лекарства или таблетку меньшего размера, которую легче проглотить.
Они могут предложить вам жидкую форму лекарства или таблетку меньшего размера, которую легче проглотить.
Жидкие лекарства
Жидкие лекарства подходят детям и взрослым (особенно пожилым), которые не могут глотать таблетки или капсулы.
Многие жидкие лекарства, в том числе лекарства, отпускаемые по рецепту и без рецепта, предназначены для детей и имеют ароматизаторы, чтобы маскировать вкус лекарства. Кроме того, многие аптеки могут добавлять в жидкие лекарства различные ароматизаторы без дополнительного рецепта врача.
Перед тем, как отмерить нужную дозу жидкого лекарства, не забудьте встряхнуть бутылку, так как часть лекарства может «осесть» на дне.
Чаще всего вам дадут дозировку лекарства в чайных ложках (помните, что чайные ложки меньше столовых).В медицине чайная ложка означает ровно 5 миллилитров (мл).
В ваших домашних чайных ложках может содержаться больше или меньше 5 мл. Попросите у фармацевта ложку, чашку с лекарством, капельницу для лекарств или шприц без иглы, специально предназначенный для отмеривания лекарств. Они могут показать вам, как их правильно использовать.
Многие безрецептурные жидкие лекарства поставляются с небольшой чашкой для лекарств, прикрепленной к верхней части бутылки.
Если лекарство было прописано младенцу или маленькому ребенку, обязательно обсудите со своим педиатром правильную дозировку или количество жидких лекарств для вашего ребенка.
Сублингвальные и буккальные препараты
Некоторые лекарства вводятся под язык (сублингвально) или между зубами и щекой (буккально). Эти лекарства быстро всасываются в кровоток через слизистую оболочку рта и используются для почти мгновенного облегчения симптомов.
Некоторыми примерами сублингвальных препаратов являются нитростат и другие препараты нитроглицерина, используемые для лечения стенокардии (боли в груди) и субоксон (бупренорфин с налоксоном), который используется для лечения зависимости от героина и / или наркотических обезболивающих.
Другие формы пероральных препаратов
Хотя большинство пероральных лекарств проглатывается, некоторые из них выделяются во рту при жевании, медленно растворяются или тают на языке. Многие из этих лекарств продаются без рецепта.
Жевательные таблетки
Жевательные таблетки следует жевать до полного растворения. Они не предназначены для проглатывания целиком.
Примеры жевательных таблеток включают Tylenol Chewable и многие марки детских витаминов.
Лекарства для жевательной резинки
У лекарств жевательной резинки есть минимальное время, в течение которого они должны быть разжеваны, чтобы обеспечить высвобождение всего количества лекарства, часто до 30 минут.
Примеры лечебных жевательных резинок включают Nicorette Gum (никотин) и Aspergum (аспирин).
Пастилки
Пастилки предназначены для «всасывания», как леденцы, и позволяют медленно растворяться во рту. Их нельзя глотать.
Примеры лекарственных пастилок включают Commit (никотин) и Cepacol (бензокаин).
Медикаменты для мягкого жевания
Лекарства для мягкого жевания предназначены для таяния во рту или для жевания.
Примером препарата Softchew является Rolaids Soft Chew (карбонат кальция).
Наконечник для глотания таблеток
Для некоторых глотание таблеток может быть неприятным и неприятным переживанием. Если вам трудно глотать таблетки, вы можете сделать это, чтобы облегчить этот процесс.
Например, немецкие исследователи добились успеха с помощью следующей техники, называемой «методом лопания бутылки».«Этот метод был протестирован с таблетками.
- Откройте бутылку с водой или бутылку содовой, наполненную водой.
- Положите таблетку на язык и закройте рот вокруг отверстия флакона.
- Откиньте голову назад и держите рот закрытым вокруг бутылки с водой. Не допускайте попадания воздуха в рот. Наберите воду в рот и проглотите таблетку с водой.
Обратите внимание, что это вмешательство не было тщательно протестировано, и, если вам интересно, вы должны обсудить этот метод со своим врачом, прежде чем попробовать его.Кроме того, если у вас вообще проблемы с глотанием, вам, вероятно, следует пройти обследование на предмет дисфагии.
И последнее: всегда внимательно читайте инструкции и принимайте лекарства в соответствии с рекомендациями. Если у вас есть какие-либо сомнения или опасения, обратитесь к врачу или фармацевту.
Приготовление и введение пероральных таблеток и жидких лекарств
Пероральное введение лекарств — один из наиболее предпочтительных и часто используемых медицинскими специалистами способов для пациентов.Большинство пероральных лекарств дается в твердой или жидкой форме. Как и при любой процедуре введения лекарств, медсестра должна следовать и выполнять пять «прав» на трех контрольных точках безопасности. Кроме того, перед приемом медсестра также должна знать показания, назначение и возможные побочные эффекты конкретного лекарства, которое вводится пациенту.
В этом видеоролике будут показаны основные этапы приготовления и приема твердых и жидких форм пероральных препаратов.
Прежде чем углубляться в процесс приема, давайте взглянем на различные типы пероральных препаратов, которые обычно встречаются в больничных условиях.Твердые формы включают таблетки, капсулы, каплеты и таблетки с энтеросолюбильным покрытием. Жидкие формы включают сиропы, эликсиры, спиртные напитки и суспензии.
Некоторые формы обладают уникальными лечебными свойствами. Например, таблетки с энтеросолюбильным покрытием покрыты материалом, который всасывается в тонком кишечнике только один раз. Эти таблетки нельзя разбивать или изменять на этапах приготовления. Менее распространены две другие оральные формы: сублингвальная и буккальная. В сублингвальной форме пациенту дают лекарство, которое помещают под язык для растворения.При буккальном приеме лекарство помещается в области щек для растворения.
Теперь, когда вы знаете о различных типах, давайте рассмотрим процедуру приготовления пероральных лекарств. Войдя в палату пациента, вымойте руки теплой водой с мылом не менее 20 секунд или нанесите дезинфицирующее средство для рук, используя сильное трение. Затем подойдите к прикроватному компьютеру и войдите в электронную медицинскую карту или EHR. Изучите историю болезни пациента и любые зарегистрированные аллергии, чтобы подтвердить возможные побочные реакции.
В EHR просмотрите электронную запись приема лекарств, или MAR. На MAR найдите лекарства, которые будут вводить в это время. Спросите пациента, есть ли у него предпочтения по приготовлению лекарств. Обратите внимание, что некоторые пациенты не могут глотать таблетки, а некоторые могут предпочесть измельченные таблетки. Медсестра должна знать эти подробности перед приготовлением лекарств. После подтверждения с пациентом выйдите из EHR и выйдите из комнаты и выполните гигиену рук, как описано ранее.
Затем получите лекарство в таблетках для приема внутрь из устройства для выдачи лекарств, используя пять «прав», как описано в первом видео этой коллекции.На этом завершается первая из трех проверок безопасности. Теперь в области подготовки лекарств приготовьте лекарство, как указано в MAR пациента, инструкциях по аптеке, справочнике по лекарствам медсестры, предпочтениях пациента и в соответствии с передовой практикой, политиками и процедурами учреждения. Предварительно расфасованные пероральные таблетки или капсулы, не требующие подготовки, останутся в оригинальной упаковке.
Откройте упаковку таблеток, если есть трудности с глотанием, требуется частичное дозирование или если пациент предпочитает разделенные таблетки.Некоторые предписанные дозы требуют разделения таблетки, чтобы получить желаемую дозу лекарства. Для разделения сначала определите, есть ли на планшете отметки — с помощью видимой линии, где она может быть разбита пополам, или без отметок. Разделите большие таблетки с насечками на две равные части, взявшись за обе стороны таблетки и сломав по линии с надрезами. Для таблеток без насечек равномерно поместите таблетку в резак для таблеток и быстро закройте устройство, чтобы убедиться, что таблетка разрезается равномерно. Если требуется частичное дозирование, утилизируйте оставшиеся частичные дозы в соответствии с политикой учреждения.Если у пациентов с затрудненным глотанием таблетки режутся и / или ломаются, поместите все кусочки лекарства в чашку для лекарства.
Приготовление капсул для перорального применения для пациентов, которые не могут проглотить капсулу, потребует получения мягкой пищи, например пюре или пудинга, из комнаты питания. Чтобы опорожнить содержимое пероральной капсулы с лекарством, возьмитесь за оба конца капсулы, осторожно поверните и потяните и вылейте содержимое в чашку для лекарства. Будьте осторожны, чтобы не потерять содержащиеся в нем лекарства.
Для жидких пероральных премиксов осторожно встряхните лекарство в течение нескольких секунд, чтобы обеспечить равномерное распределение лекарства в жидкости. Затем рассчитайте соответствующий объем для вывода, учитывая концентрацию, указанную на этикетке жидкого лекарства. Если MAR указывает на дозу 200 мг, а предоставленная концентрация составляет 32 мг / мл, то вам необходимо извлечь 6,25 мл из контейнера. Для этого поставьте чашку с лекарством на ровную поверхность и присядьте, пока не окажетесь на уровне глаз с измерением объема.Затем налейте жидкий предварительно приготовленный лекарственный препарат в емкость для лекарств, пока он не достигнет нужного объема. Жидкость, налившаяся, когда вы стоите и смотрите на чашку с лекарством, вызовет выдачу недостаточного объема и ошибку приема лекарства.
Если лекарство указывает точное измерение, например жидкий дигоксин, возьмите пероральный шприц из ящика для лекарств. Всегда используйте пероральный шприц для отмены перорального лекарства, так как шприц для внутривенного введения можно легко принять за внутривенное, что может привести к ошибкам при приеме лекарств.При извлечении из многодозового контейнера поместите чашку с лекарством на ровную поверхность и налейте объем, превышающий предписанную дозу. Выливание объема, который будет использоваться перед извлечением, сохраняет контейнер для нескольких доз чистым, если не используется стерильный оральный шприц.
При использовании стерильного орального шприца можно набирать непосредственно из контейнера. Всегда отбирайте немного больше, чем предписано. Затем поверните кончик шприца вверх и переместите его на уровень глаз. Теперь медленно нажимайте на плунжер, пока не выйдет весь воздух и верхняя часть уплотнения плунжера не достигнет желаемого объема.Если используется контейнер для однократной дозы, медсестра может извлечь его прямо из контейнера и утилизировать оставшийся объем в соответствии с политикой учреждения. Выбросьте всю упаковку с лекарствами в контейнер для мусора.
Затем, используя ленту или заранее напечатанную этикетку лекарства, напишите название лекарства и количество дозировки на этикетке и поместите ее на шприц. Обратите внимание, что все лекарства, которые были извлечены из оригинальной упаковки, должны быть помечены перед тем, как покинуть комнату для приготовления лекарств.
В зоне приготовления лекарств выполните вторую проверку безопасности, используя пять «прав» приема лекарств. После второй проверки безопасности соберите все необходимые принадлежности, в том числе чашку с водой, соломинку, нестерильные перчатки, пероральные лекарства и чашки с лекарствами, и пройдите в палату пациента.
При первом входе в палату пациента положите лекарства на стойку и выполните гигиену рук, как описано выше, с сильным трением в течение не менее 20 секунд.В палате пациента выполните третью и последнюю проверку безопасности приема лекарств, соблюдая пять «прав» приема лекарств. Убедитесь, что пациент носит правильную именную полосу, попросив его указать свое имя и дату рождения. Сравните эту информацию с тем, что указано на именной полосе.
На этом этапе расскажите пациенту о пероральном приеме лекарств. Сообщите пациенту название лекарства, показания и действие. Просмотрите все побочные эффекты, связанные с приемом лекарства.Обсудите любые опасения, которые могут возникнуть у пациента по поводу лекарства. Если пациент отказывается от приема лекарства, убедитесь, что он осознает потенциальное физиологическое или психологическое воздействие своего отказа на его здоровье и выздоровление.
Перед тем, как дать лекарство, попросите пациента сделать небольшой глоток воды, чтобы убедиться, что он может без труда проглотить. Теперь откройте упакованные лекарства, поместите их в чашку с лекарствами и дайте пациенту в соответствии с его или ее предпочтениями и возможностями.
После введения укажите следующие данные в MAR пациента: дозу лекарства, способ введения, дату и точное время введения с вашими инициалами. Любые оценки, необходимые перед администрированием, должны быть включены в документацию. Перед тем как покинуть палату, напомните пациенту о любых побочных эффектах или соображениях, о которых он должен сообщить медсестре. Выйдите из палаты пациента и при выходе не забудьте выполнить гигиену рук, как описано ранее.
«Поскольку вариации дозировки в институциональной аптеке могут быть ограничены, важно, чтобы медсестра проверила правильную дозу лекарства, полученную из устройства для выдачи лекарств, и подготовила лекарство в соответствии с дозой, указанной в записи приема лекарства пациентом».
«Распространенной ошибкой при пероральном приеме жидких лекарств является заливка жидкого лекарства, не находясь на уровне глаз или на ровной поверхности. В обоих случаях это может привести к ошибке дозирования, при которой недозировка может привести к потенциально опасным последствиям. эффекты как передозировка, в зависимости от введенного лекарства и желаемого эффекта.»
Вы только что посмотрели видео JoVE о проверке и применении пероральных препаратов, включая таблетки, капсулы и жидкие препараты. Теперь вы должны понимать различные формы пероральных препаратов, как подготовить лекарства для приема и безопасные методы. применения лекарств с использованием пяти «прав». Как всегда, спасибо за просмотр!
Устные проявления общепринятых лекарств
1. Кантор Э.Д.,
Рем CD,
Haas JS,
и другие.Тенденции употребления рецептурных лекарств среди взрослого населения США в 1999–2012 гг. ЯМА .
2015; 314 (17): 1818–1831 ….
2. Чон Н.,
Сорокина М,
Хенриксен С,
и другие.
Измерение выбранных предотвратимых нежелательных явлений, связанных с лекарственными средствами, в электронных медицинских картах: к разработке шкалы сложности [опубликованные исправления появляются в Am J Health Syst Pharm. 2017; 74 (23): 1928 и Am J Health Syst Pharm. 2017; 74 (24): 2030]. Am J Health Syst Pharm .2017; 74 (22): 1865–1877.
3. Лаван АХ,
Галлахер П.
Прогнозирование риска побочных реакций на лекарства у пожилых людей. Тер Адвен Лекарственный Сейф .
2016; 7 (1): 11–22.
4. ClinCalc. 200 лучших препаратов 2019 года. По состоянию на 28 апреля 2020 г. https://clincalc.com/blog/2018/11/the-top-200-drugs-of-2019/?s=the+top+200+drugs+ из + 2019
5. Lexicomp для стоматологии. По состоянию на 18 сентября 2019 г. http://online.lexi.com.libdb.db.uth.tmc.edu
6. Hahnel S,
Шварц С,
Земан Ф,
и другие.Распространенность ксеростомии и гипосаливации и их связь с качеством жизни у пожилых пациентов в зависимости от стоматологического статуса и ортопедической реабилитации: пилотное исследование. Дж Дент .
2014. 42 (6): 664–670.
7. Gaur S,
Агнихотри Р.
Является ли зубной налет единственным этиологическим фактором разрастания десен, вызванного амлодипином? Систематический обзор доказательств. Дж. Клин Эксп Дент .
2018; 10 (6): e610 – e619.
8. Брюне Л,
Миранда Дж.,
Фарре М.,
и другие.Увеличение десен, вызванное лекарствами. Лекарственная безопасность .
1996. 15 (3): 219–231.
9. Ранганатан К.,
Редди Б.В.,
Кумарасами Н,
и другие.
Поражения полости рта и состояния, связанные с инфекцией вируса иммунодефицита человека, у 300 пациентов из Южной Индии. Устный диск .
2000. 6 (3): 152–157.
10. Ранганатан К.,
Умадеви М,
Сарасвати TR,
и другие.
Поражения полости рта и состояния, связанные с инфекцией вируса иммунодефицита человека, у 1000 пациентов из Южной Индии. Анн Акад Мед Сингапур .
2004; 33 (4 доп.): 37–42.
11. Bahloul E,
Джаллоули М,
Гарбаа S,
и другие.
Гиперпигментация, вызванная гидроксихлорохином, при системных заболеваниях: распространенность, клинические особенности и факторы риска: перекрестное исследование 41 случая. Волчанка .
2017; 26 (12): 1304–1308.
12. Петушков Ю.М.,
Savage NW.
Миноциклин и пигментация полости рта. Aust Dent J .
1998. 43 (1): 14–16.
13. Невилл Б.В., Дамм Д.Д., Аллен С.М. и др. Патология полости рта и челюстно-лицевой области. 4-е изд. Эльзевир; 2016.
14. Бамиас А,
Кастрит E,
Бамиа С,
и другие.
Остеонекроз челюсти при раке после лечения бисфосфонатами: частота и факторы риска. Дж. Клин Онкол .
2005. 23 (34): 8580–8587.
15. Уолтер К.,
Ан-Навас Б,
Грётц К.А.,
и другие.
Распространенность и факторы риска бисфосфонат-ассоциированного остеонекроза челюсти у пациентов с раком простаты с запущенной стадией заболевания, получавших золедронат. евро Урол .
2008. 54 (5): 1066–1072.
16. Ци В-Х,
Тан Л-Н,
Он А-Н,
и другие.
Риск остеонекроза челюсти у онкологических больных, получающих деносумаб: метаанализ семи рандомизированных контролируемых исследований. Инт Дж. Клин Онкол .
2014. 19 (2): 403–410.
17. Сиволелла С,
Люмачи Ф,
Стеллини Э,
и другие.
Деносумаб и остеонекроз челюсти, связанный с антиангиогенетическими лекарственными средствами: необычное, но потенциально тяжелое заболевание. Противораковое лечение .
2013; 33 (5): 1793–1797.
18. Lo JC,
О’Райан Ф.С.,
Гордон Н.П.,
и другие.;
Прогнозирование риска остеонекроза челюсти с помощью орального воздействия бисфосфонатов (PROBE).
Распространенность остеонекроза челюсти у пациентов, получавших пероральный прием бисфосфонатов. Дж. Орал Максиллофак Сург .
2010. 68 (2): 243–253.
19. Мур Р.А.,
McQuay HJ.
Распространенность побочных эффектов опиоидов при хронической незлокачественной боли: систематический обзор рандомизированных исследований пероральных опиоидов. Артрит Ресурс .
2005; 7 (5): R1046 – R1051.
20. Эллис Дж. С.,
Сеймур Р.А.,
Стил Дж. Г.,
и другие.
Распространенность избыточного роста десен, вызванного блокаторами кальциевых каналов: исследование на уровне сообщества. Дж Периодонтол .
1999. 70 (1): 63–67.
21. Пури П.К.,
Лунцис Н.И.,
Тайлер В,
и другие.
Гиперпигментация, вызванная гидроксихлорохином: характер окрашивания. Дж. Кутан Патол .2008. 35 (12): 1134–1137.
22. Barclay S,
Томасон Дж. М.,
Холостой JR,
и другие.
Частота и тяжесть разрастания десен, вызванного нифедипином. Дж Клин Периодонтол .
1992. 19 (5): 311–314.
23. Вт A,
Эдди М.
Изменение цвета и окрашивание зубов: обзор литературы. Br Dent J .
2001. 190 (6): 309–316.
24. Clementini M,
Витторини Г,
Crea A,
и другие.Эффективность терапии AZM у пациентов с избыточным ростом десен, вызванным циклоспорином A: систематический обзор. BMC Здоровье полости рта .
2008; 8: 34.
25. Коричневый RS,
Араны PR.
Пересмотр механизма медикаментозного разрастания десен: объединяющая гипотеза. Устный диск .
2015; 21 (1): e51 – e61.
26. Bondon-Guitton E,
Багери Х,
Montastruc J-L.
Разрастание десен, вызванное лекарствами: исследование в базе данных французского фармаконадзора. Дж Клин Периодонтол .
2012. 39 (6): 513–518.
27. Chatzopoulos GS,
Койду В.П.,
Вольф LF.
Систематический обзор разрастания десен, вызванного циклоспорином А, и генетической предрасположенности. Квинтэссенция Инт .
2017; 48 (9): 711–724.
28. Уокер Р.Г.,
Коттрелл С,
Sharp K,
и другие.
Превращение циклоспорина в такролимус у стабильных реципиентов почечного аллотрансплантата: количественная оценка влияния на тяжесть увеличения десны и гирсутизма, а также результаты, сообщаемые пациентами. Нефрология (Карлтон) .
2007. 12 (6): 607–614.
29. Ливада р,
Шилоа Дж.
Увеличение десен, вызванное блокаторами кальциевых каналов. Дж Хум Гипертенс .
2014; 28 (1): 10–14.
30. Сеймур РА,
Томасон Дж. М.,
Эллис Дж. С..
Патогенез медикаментозного разрастания десен. Дж Клин Периодонтол .
1996. 23 (3 ч. 1): 165–175.
31. Моффитт М.Л.,
Бенчивенни Д.,
Коэн RE.
Увеличение десен, вызванное лекарственными средствами: обзор. Компенд Контин Образов Дент .
2013. 34 (5): 330–336.
32. Пиллони А,
Камарго П.М.,
Carere M,
и другие.
Хирургическое лечение увеличения десен, вызванного циклоспорином А и нифедипином: гингивэктомия по сравнению с пародонтальным лоскутом. Дж Периодонтол .
1998. 69 (7): 791–797.
33. Mehta J,
Бакутра Г,
Чандран С,
и другие.
Различные методы лечения медикаментозного разрастания десен: серия случаев. Натл Дж. Интегр Рес Мед .
2018; 9 (2): 1-6-109.
34. Savage NW,
Барбер М.Т.,
Адкинс К.Ф.
Пигментные изменения слизистой оболочки полости рта крыс после противомалярийной терапии. Дж. Устный Патол. .
1986. 15 (9): 468–471.
35. Хасан С,
Хан Н,
Шервани ДУБ,
и другие.
Лекарства, вызывающие орофациальную пигментацию: обзор литературы. Int Res J Pharm .
2013. 4 (5): 40–43.
36.Глик А,
Тебризи М,
Latortue MC,
и другие.
Распознавание пигментных поражений полости рта. J Gt Houst Dent Soc .
2019; 90 (1): 34–36.
37. Силлер Г.М.,
Тод М.А.,
Savage NW.
Пигментация полости рта, вызванная миноциклином. Дж. Ам Акад Дерматол .
1994. 30 (2 ч. 2): 350–354.
38. Абдулджаббар Т,
Vohra F,
Акрам З,
и другие.
Эффективность хирургической лазерной терапии в лечении пигментных поражений полости рта: систематический обзор. J Photochem Photobiol B .
2017; 173: 353–359.
39. Аласмари Д.С.
Знакомство с методами депигментации десен: плюсы и минусы. Int J Health Sci (Кассим) .
2018; 12 (5): 84–89.
40. Алави Ф.
Пигментные поражения полости рта: актуальная информация. Дент Клин Норт Ам .
2013. 57 (4): 699–710.
41. Хаммисса РАГ,
Чандран Р,
Масилана А,
и другие.
Неблагоприятные иммунологически опосредованные реакции слизистой оболочки полости рта на системные лекарства: лихеноидная тканевая реакция / интерфейсный дерматит-стоматит, аутоиммунная везикулобуллезная болезнь, а также IgE-зависимые и иммунные комплексные реакции. Дж. Иммунол Рес .
2018; (2018): 1–10.
42. Феллер Л,
Вуд NH,
Хаммисса Р.А.,
и другие.
Отзыв: аллергический контактный стоматит. Oral Surg Oral Med Oral Pathol Oral Radiol .
2017; 123 (5): 559–565.
43. Каплан А.П.,
Наголенники MW.
Ангионевротический отек. Дж. Ам Акад Дерматол .
2005; 53 (3): 373–388, викторина 389–392.
44. Летко Э.,
Папалиодис DN,
Папалиодис Г.Н.,
и другие.Синдром Стивенса-Джонсона и токсический эпидермальный некролиз: обзор литературы. Ann Allergy Asthma Immunol .
2005; 94 (4): 419–436, викторина 436–438, 456.
45. Paulmann M,
Моккенгаупт М.
Тяжелые кожные реакции, вызванные лекарственными средствами: клиника, диагностика, этиология и терапия. J Dtsch Dermatol Ges .
2015; 13 (7): 625–645.
46. Mockenhaupt M,
Viboud C,
Дюнан А,
и другие.
Синдром Стивенса-Джонсона и токсический эпидермальный некролиз: оценка медикаментозных рисков с акцентом на недавно появившихся на рынке лекарствах.EuroSCAR-исследование. Дж Инвест Дерматол .
2008. 128 (1): 35–44.
47. Гарсия-Доваль I,
LeCleach L,
Боке H,
и другие.
Токсический эпидермальный некролиз и синдром Стивенса-Джонсона: снижает ли ранняя отмена лекарств, вызывающих заболевание, риск смерти? Арка Дерматол .
2000. 136 (3): 323–327.
48. Хоминский А,
Лим М.
«Спонтанный» медикаментозный остеонекроз челюсти; два отчета о случаях болезни и систематический обзор. Aust Dent J .
2018; 63 (4): 441–454.
49. Кот В.С.,
Фигейредо Массачусетс,
Салум ФГ,
и другие.
Связанный с бисфосфонатами остеонекроз челюсти: от sine qua non условия воздействия на костную ткань необлученного BRONJ. Дентомаксиллофак Радиол .
2016; 45 (7): 20160049.
50. Ruggiero SL,
Додсон ТБ,
Фантазия J,
и другие.
Документ с изложением позиции Американской ассоциации челюстно-лицевых хирургов по поводу лекарственного остеонекроза челюсти — обновление 2014 г. [опубликованные исправления представлены в J Oral Maxillofac Surg.2015; 73 (7): 1440, и J Oral Maxillofac Surg. 2015; 73 (9): 1879]. Дж. Орал Максиллофак Сург .
2014. 72 (10): 1938–1956.
51. Эль-Раббани М,
Сгро А,
Лам Д.К.,
и другие.
Эффективность лечения медикаментозного остеонекроза челюсти: систематический обзор и метаанализ. J Am Dent Assoc .
2017; 148 (8): 584–594.e2.
52. Aparecida Cariolatto F,
Карелли Дж.,
де Кампос Морейра Т,
и другие.Рекомендации по профилактике остеонекроза челюсти, связанного с бисфосфонатами: систематический обзор. Дж. Эвид Дент Практик .
2018; 18 (2): 142–152.
53. Вилла А,
Коннелл К.Л.,
Абати С.
Диагностика и лечение ксеростомии и гипосаливации. Центр управления рисками в клинике .
2014; 11: 45–51.
54. Леал СК,
Биттар Дж,
Португалия А,
и другие.
Лекарства у пожилых людей: его влияние на слюноотделение, признаки и симптомы сухости во рту. Геродонтология .
2010. 27 (2): 129–133.
55. Алико А,
Вольф А,
Доус С,
и другие.
Всемирный семинар по оральной медицине VI: клинические последствия медикаментозной дисфункции слюнных желез. Oral Surg Oral Med Oral Pathol Oral Radiol .
2015; 120 (2): 185–206.
56. Портер СР,
Скалли Си,
Хегарти AM.
Обновленная информация об этиологии и лечении ксеростомии. Oral Surg Oral Med Oral Pathol Oral Radiol Endod .2004. 97 (1): 28–46.
57. Вилла А,
Вольф А,
Афрамян Д,
и другие.
Всемирный семинар по оральной медицине VI: систематический обзор медикаментозной дисфункции слюнных желез: распространенность, диагностика и лечение. Клин Оральное Исследование .
2015; 19 (7): 1563–1580.
58. Лю Б,
Дион MR,
Юрский ММ,
и другие.
Ксеростомия и гипофункция слюны у уязвимых пожилых людей: распространенность и этиология. Oral Surg Oral Med Oral Pathol Oral Radiol .
2012. 114 (1): 52–60.
59. Дас П,
Challacombe SJ.
Системы оценки сухости во рту и клинической сухости полости рта. Прим Дент J .
2016; 5 (1): 77–79.
60. Лопес-Хорнет М.П.,
Гарсия-Тереза Дж.,
Виньяс М,
и другие.
Клиническая и антимикробная оценка жидкости для полоскания рта и зубной пасты при ксеростомии: рандомизированное двойное слепое перекрестное исследование. Дж Дент .2011. 39 (11): 757–763.
61. Gil-Montoya JA,
Сильвестр Ф.Дж.,
Barrios R,
и другие.
Лечение ксеростомии и гипосаливации у пожилых людей: систематический обзор. Med Oral Patol Oral Cir Bucal .
2016; 21 (3): e355 – e366.
62. Aframian DJ,
Хелцер М,
Ливни Д,
и другие.
Лечение пилокарпином в смешанной когорте пациентов с ксеростомией. Устный диск .
2007. 13 (1): 88–92.
63. Гётрик Б,
Окерман С,
Эриксон Д,
и другие.
Пилокарпин для перорального применения для лечения сухости полости рта, вызванной опиоидами, у здоровых взрослых. Дж Дент Рес .
2004. 83 (5): 393–397.
64. Hanchanale S,
Адкинсон Л,
Даниэль С,
и другие.
Систематический обзор литературы: ксеростомия у больных раком на поздних стадиях. Служба поддержки рака .
2015; 23 (3): 881–888.
65. Ноаисех Г.,
Бейкер Дж. Ф.,
Vivino FB.Сравнение частоты отмены и профилей побочных эффектов пилокарпина и цевимелина при ксеростомии при первичном синдроме Шегрена. Clin Exp Rheumatol .
2014. 32 (4): 575–577.
Оральные препараты | ADA
Первым лечением диабета 2 типа для контроля уровня глюкозы в крови (сахара) часто является планирование приема пищи, снижение веса и физические упражнения.
Иногда этих мер недостаточно, чтобы снизить уровень глюкозы в крови до нормального уровня.Следующий шаг — прием лекарства, снижающего уровень глюкозы в крови.
Могут ли мне помочь таблетки от диабета?
Только люди с диабетом 2 типа могут использовать таблетки для лечения своего диабета, люди с диабетом 1 типа должны использовать инсулин.
Эти таблетки лучше всего работают при планировании еды и физических упражнениях. Таким образом, у вас есть три терапии, работающих вместе, чтобы снизить уровень глюкозы в крови.
Таблетки от диабета работают не на всех. Хотя большинство людей обнаруживают, что уровень глюкозы в крови снижается, когда они начинают принимать таблетки, уровень глюкозы в крови может не приближаться к нормальному диапазону.Начните с рассмотрения ваших вариантов и посмотрите, что лучше всего подойдет вам.
И для многих важным фактором является стоимость. Получите факты и изучите наши советы по сравнению стоимости.
Помогут?
Каковы шансы, что таблетки от диабета подействуют на вас? Ваши шансы невелики, если вы страдаете диабетом более 10 лет или уже принимаете более 20 единиц инсулина каждый день. С другой стороны, у вас хорошие шансы, если вы недавно заболели диабетом или вам было мало инсулина или совсем его не было, чтобы поддерживать уровень глюкозы в крови около нормы.
Таблетки от диабета иногда перестают действовать через несколько месяцев или лет. Причина часто неизвестна. Это не значит, что ваш диабет хуже. В этом случае может помочь комбинированная пероральная терапия.
Даже если таблетки от диабета действительно позволяют приблизить уровень глюкозы в крови к нормальному диапазону, вам все равно может потребоваться прием инсулина, если у вас тяжелая инфекция или вам нужна операция. Таблетки могут быть не в состоянии контролировать уровень глюкозы в крови в эти стрессовые времена, когда уровень глюкозы в крови резко повышается.
Кроме того, если вы планируете забеременеть, вам нужно будет контролировать свой диабет с помощью диеты и физических упражнений или с помощью инсулина. Беременным женщинам небезопасно принимать пероральные лекарства от диабета.
Не существует «лучших» таблеток или лекарств от диабета 2 типа. Возможно, вам придется попробовать несколько типов таблеток, комбинацию таблеток или таблетки плюс инсулин.
Есть ли опасность взаимодействия?
В целом таблетки от диабета безопасны и хорошо работают. Но, как и любой другой препарат, их нужно использовать с осторожностью.
Все таблетки от диабета могут взаимодействовать с другими лекарствами. Из-за возможности взаимодействия лекарств вам необходимо сообщить врачу обо всех лекарствах, которые вы принимаете. Пока вы принимаете таблетки от диабета, вам следует проконсультироваться с врачом, прежде чем начинать что-то новое, даже безрецептурные.
Любая сульфонилмочевина или меглитинид могут вызвать слишком низкое падение уровня глюкозы в крови (гипогликемия).
Метформин или глитазоны редко вызывают гипогликемию, если их не принимать вместе со стимуляторами инсулина (сульфонилмочевиной или репаглинидом) или инъекциями инсулина.
Акарбоза или миглитол, принятые по назначению, не вызывают гипогликемии. Однако гипогликемия может возникнуть при приеме акарбозы или меглитола в сочетании с другими лекарствами от диабета.
Получение пероральной или местной химиотерапии
Хотя многие химиотерапевтические (химиотерапевтические) препараты вводятся в виде инфузий или инъекций, существуют также пероральные химиопрепараты (принимаемые внутрь) или химиотерапевтические препараты местного действия (втираемые в кожу).
Информация, приведенная ниже, описывает традиционную или стандартную химиотерапию, которую можно вводить перорально или наносить на кожу. Существуют также другие препараты, которые используются для лечения рака различными способами, включая таргетную терапию, гормональную терапию и иммунотерапию.
Химиотерапия для перорального применения
Если химиотерапия принимается внутрь, вы проглатываете таблетку, капсулу или жидкость так же, как и другие лекарства. Как и другие виды химиотерапии, иногда химиотерапия проводится циклами. Это снижает вред здоровым клеткам и позволяет химиотерапии убивать больше раковых клеток.
Оральная химиотерапия обычно проводится дома.Поэтому очень важно точно знать, как его следует принимать. Если вы и ваш врач решили, что пероральная химиотерапия — лучший вариант лечения для вас, обязательно спросите и получите инструкции о:
- Как и когда брать. У вас должны быть четкие инструкции о том, сколько и когда принимать химиотерапию. Вам необходимо принимать точную дозировку в нужное время и ровно столько, сколько вы должны это делать. Дозы пероральной химиотерапии устанавливаются таким образом, чтобы в вашем организме оставался тот же уровень лекарства, который убивает раковые клетки.Неправильное применение химиотерапии может повлиять на ее эффективность. Иногда необходимо изменить дозу, но не вносите никаких изменений, если это вам не скажет врач. Если вы пропустите дозу или поздно ее приняли, сообщите об этом своему врачу или медсестре. Им необходимо знать об этом, когда решают, подействует ли лечение. Это также может помочь врачу решить, следует ли изменить количество лекарства, которое вы принимаете, или когда вы его принимаете.
- Специальное обращение . Химиотерапия, которую вы проглатываете, так же сильна, как и другие формы химиотерапии.Многие также считаются опасными. Обычно существуют особые меры предосторожности при хранении и обращении с химиопрепаратами. Вам могут посоветовать соблюдать осторожность и не позволять другим контактировать с ним или с жидкостями вашего тела во время приема и в течение некоторого времени после приема. Иногда при прикосновении к таблеткам или капсулам нужно надевать перчатки. Некоторые лекарства нужно хранить в бутылке или коробке, в которой они пришли. А некоторые лекарства и упаковки, в которых они поступают, нужно утилизировать определенным образом. Некоторые, возможно, придется отнести обратно в аптеку, чтобы их благополучно выбросить.Чтобы узнать больше, см. Безопасность химиотерапии.
- Стоимость. Пероральные химиопрепараты могут быть дорогими. Обязательно спросите своего врача о стоимости вашего лечения, чтобы вы не удивились, когда придете в аптеку или когда получите счет, если лечение недоступно в аптеках. В зависимости от типа лекарства некоторые страховки не покрывают полную стоимость или могут не покрывать ее вовсе. Иногда вы можете получить помощь, но многим людям приходится платить за них больше своих денег, чем они платили бы за химиотерапию, проводимую с помощью иглы в больнице или клинике.Если у вас есть медицинская страховка, это может означать более высокую доплату. Убедитесь, что вы знаете, сколько вам придется платить за каждое лечение. Вы можете позвонить в Американское онкологическое общество по телефону 1-800-227-2345 для получения дополнительной информации о финансовой помощи.
Обязательно сообщите своему врачу или медсестре о любых проблемах, которые возникают у вас при приеме химиотерапии. Например, если вас рвет или вы чувствуете тошноту, возможно, вы почувствуете себя слишком больным, чтобы принимать химиотерапию. Или вы не сможете сдерживать химиотерапию и можете ее вырвать.Ваш врач должен знать обо всех проблемах, чтобы при необходимости изменить ваш план лечения.
Местная химиотерапия
Местная химиотерапия наносится прямо на кожу в области определенных раковых образований. Местная химиотерапия может быть кремом, гелем или мазью.
Химиотерапия, которую вы наносите на кожу, столь же сильна, как и другие формы химиотерапии. Многие также считаются опасными. Если вы используете местную химиотерапию, убедитесь, что вы знаете меры предосторожности, которые необходимо соблюдать при хранении, обращении и утилизации тюбика или контейнера, в котором они находятся.Также необходимо соблюдать меры предосторожности при нанесении на кожу, например надевать специальные перчатки. Чтобы узнать больше, см. Безопасность химиотерапии.
Мне все равно нужно будет обратиться к врачу?
Даже если вы принимаете пероральную и местную химиотерапию дома, вам все равно нужно будет посещать свою бригаду по лечению рака. Они будут следить за изменениями в раке и следить за тем, как у вас дела с планом химиотерапии. Будут сделаны анализы крови и сканирование, чтобы увидеть, как ваше тело и рак переносят химиотерапию.
Как часто мне нужно будет проходить пероральную или местную химиотерапию?
Как часто вы принимаете пероральную или местную химиотерапию и как долго длится ваше лечение, зависит от типа рака, целей лечения, используемых лекарств и реакции вашего организма на них.
Вам может потребоваться лечение ежедневно, еженедельно или ежемесячно, но обычно оно проводится циклически. Это означает, например, что вы можете проходить химиотерапию в течение первых 2 недель, а затем делать перерыв на неделю, что делает этот цикл циклом, который будет начинаться каждые 3 недели.Свободное время позволяет вашему телу создавать новые здоровые клетки и восстанавливать свои силы.
Ваша команда по лечению рака может сказать вам, сколько циклов запланировано и как долго, по их мнению, продлится ваше лечение.
Многие люди задаются вопросом, как долго лекарства остаются в их организме и как они удаляются. Ваши почки и печень расщепляют большинство химиопрепаратов, которые затем выводятся из организма с мочой или стулом. Сколько времени потребуется вашему организму, чтобы избавиться от лекарств, зависит от многих факторов, в том числе от типа химиотерапии, которые вы принимаете, других лекарств, которые вы принимаете, вашего возраста и того, насколько хорошо работают ваши почки и печень.Ваша команда по лечению рака сообщит вам, нужно ли вам принимать какие-либо особые меры предосторожности из-за принимаемых вами лекарств.
Если рак вернется, возможно, вам снова сделают химиотерапию. На этот раз вам могут назначить разные лекарства для облегчения симптомов или замедления роста или распространения рака. Побочные эффекты могут быть разными в зависимости от лекарств, доз и способа их приема.
Чего мне ожидать от пероральной или местной химиотерапии?
Побочные эффекты любой формы химиотерапии варьируются от лекарства к лекарству и от человека к человеку.Ваша онкологическая бригада может не сказать вам, какие у вас будут побочные эффекты, но они подскажут, на что обращать внимание.
Если вы сообщите своей команде о побочных эффектах, как только они возникнут, это поможет убедиться, что они не слишком серьезны. Вашему врачу, возможно, придется изменить дозировку или назначить вам другие лекарства, чтобы вы почувствовали себя лучше. Если вы не уверены в побочном эффекте и не можете связаться с врачом, не принимайте химиотерапию, пока не поговорите с кем-нибудь из своей бригады по лечению рака.
Принятие химиотерапии дома дает вам больше свободы без частых посещений врача.Возможно, вы не часто посещаете врача и медсестер, но обязательно звоните им, если у вас возникнут какие-либо вопросы или опасения.
Вы готовы начать пероральную или местную химиотерапию?
Вот некоторые вещи, о которых вы, возможно, захотите поговорить со своей бригадой по лечению рака, когда начнете пероральную или местную химиотерапию:
- Как называется химиотерапия? Существует ли несколько названий одного и того же препарата?
- Как использовать или взять?
- Когда мне использовать или брать?
- Безопасно ли принимать его с другими лекарствами, едой, витаминами, травами, добавками, лосьонами для кожи или другими лекарствами, которые я использую?
- Что мне делать, если я пропустил дозу?
- Как мне его хранить?
- Нужно ли обращаться с ним по-особенному, чтобы защитить меня и других?
- Что вы от него ожидаете?
- Каковы вероятные побочные эффекты? Что делать, если у меня появились побочные эффекты?
- Как я могу с вами связаться, если у меня возникнут проблемы поздно ночью или в выходные?
- Как долго мне нужно будет проходить химиотерапию?
- Будет ли моя страховка оплачивать мою химиотерапию? Если нет, сколько это будет стоить? Как я буду за это платить?
- Могут ли другие проблемы со здоровьем помешать мне принимать химию должным образом? Есть ли шанс, что из-за других проблем со здоровьем я забуду про химиотерапию?
- Вы позвоните мне, чтобы узнать, как у меня дела с химиотерапией?
- Как часто вам нужно будет видеть меня лично?
Для пероральной химиотерапии обязательно задавайте некоторые вопросы о таблетках, например:
- Что делать, если у меня проблемы с глотанием или удержанием таблеток?
- Можно ли их открыть, сломать или раздавить?
- Можно ли смешать с едой или жидкостью?
Перед тем, как начать химиотерапию, поговорите со своим врачом или медсестрой о любых проблемах или вопросах, которые у вас есть. Получите ответы на все свои вопросы о химиотерапии до того, как вы начнете ее принимать.
Успех химиотерапии дома действительно во многом зависит от вас — важно принять правильную дозу препарата в нужное время, как вам и сказали. Ваша онкологическая бригада поможет вам в этом.
Эректильная дисфункция: Виагра и другие пероральные препараты
Пероральные препараты часто являются первой линией лечения эректильной дисфункции.Для большинства мужчин, у которых есть проблемы с поддержанием эрекции, достаточной для секса (эректильная дисфункция), эти лекарства работают хорошо и вызывают мало побочных эффектов.
Силденафил (Виагра), варденафил (Левитра, Стаксин), тадалафил (Сиалис) и аванафил (Стендра) — это пероральные препараты, которые обращают вспять эректильную дисфункцию, усиливая действие оксида азота, естественного химического вещества, которое вырабатывается вашим организмом и расслабляет мышцы полового члена. Это увеличивает кровоток и позволяет получить эрекцию в ответ на сексуальную стимуляцию.
Чем отличаются пероральные препараты
Хотя они действуют одинаково, каждый пероральный препарат имеет немного разный химический состав. Эти незначительные различия влияют на то, как работает каждое лекарство, например, на скорость его действия и истечение срока его действия, а также на возможные побочные эффекты. Ваш врач учтет эти факторы, а также другие состояния, которые у вас есть, и возможные взаимодействия с другими лекарствами, которые вы принимаете.
- Силденафил (Виагра). Этот препарат наиболее эффективен при приеме натощак за час до секса.Он эффективен в течение четырех-пяти часов или более, если у вас эректильная дисфункция легкой или средней степени тяжести.
Варденафил (Левитра, Стаксин). Этот препарат также наиболее эффективен при приеме за час до секса, его можно принимать с едой или без нее. Еда с высоким содержанием жиров может помешать ему так быстро усвоиться.
Варденафил эффективен в течение четырех-пяти часов и более, если у вас эректильная дисфункция легкой или средней степени тяжести. Более новая форма препарата, которая растворяется на языке, может действовать быстрее, чем таблетка, которую вы проглатываете.
- Тадалафил (Сиалис). Это лекарство принимают вместе с едой или без еды за один-два часа до секса. Эффективен до 36 часов. Его можно принимать в небольшой дозе ежедневно или в большей дозе, если необходимо.
- Аванафил (Стендра). Это лекарство принимают с пищей или без нее за 30 минут до секса, в зависимости от дозы. Длится до шести часов.
Поскольку эти препараты одинаково эффективны, Американский колледж врачей рекомендует делать выбор на основе ваших предпочтений, включая стоимость, простоту использования, продолжительность действия препарата и побочные эффекты.Доступны дженерики силденафила, верденафила и тадалафила.
Когда пероральные препараты могут быть небезопасными
Прежде чем принимать какие-либо лекарства от эректильной дисфункции, проконсультируйтесь с врачом. Лекарства от эректильной дисфункции могут не работать или быть опасными, если вы:
- Принимайте нитратные препараты — обычно назначаемые при боли в груди (стенокардия) — такие как нитроглицерин (Nitro-Dur, Nitrostat, другие), изосорбид мононитрат (Monoket) и динитрат изосорбида (Dilatrate-SR, Isordil)
- У вас очень низкое кровяное давление (гипотония) или неконтролируемое высокое кровяное давление (гипертония)
- У тяжелой болезни печени
- У вас заболевание почек, требующее диализа
Побочные эффекты
Большинство мужчин, принимающих оральные препараты для лечения эректильной дисфункции, не обеспокоены побочными эффектами.Когда возникают побочные эффекты, они могут включать:
- Промывка
- Головная боль
- Несварение
- Визуальные изменения, такие как синий оттенок зрения, чувствительность к свету или нечеткость зрения
- Душный или насморк
- Боль в спине
Редко могут возникать более серьезные побочные эффекты, в том числе:
- Потеря слуха или потеря зрения. У некоторых мужчин внезапная потеря слуха или зрения после приема одного из этих лекарств.Однако неясно, была ли потеря зрения или слуха напрямую вызвана приемом лекарства или уже существовавшим заболеванием. Если вы принимаете лекарство от оральной эректильной дисфункции и внезапно потеряли слух или зрение, немедленно обратитесь за медицинской помощью.
- Эрекция, которая не проходит сама по себе. Это редкое заболевание, называемое приапизмом, может быть болезненным и требует лечения, чтобы избежать повреждения полового члена. Если у вас эрекция, которая длится более четырех часов, немедленно обратитесь за медицинской помощью.
Покупка лекарств от оральной эректильной дисфункции в Интернете
Лекарства от эректильной дисфункции — это большой бизнес, и в Интернете существует множество мошенников. Если вы все же покупаете лекарства через Интернет:
- Проверьте, является ли интернет-аптека законной. Никогда не заказывайте лекарства в интернет-аптеке, если нет возможности связаться с аптекой по телефону, если цены кажутся слишком хорошими, чтобы быть правдой, или если вам сказали, что рецепт не требуется. Некоторые незаконные предприятия продают поддельные версии законных лекарств, которые могут быть неэффективными или опасными.В США Национальная ассоциация фармацевтических советов может сказать вам, имеет ли интернет-аптеку лицензию и хорошую репутацию.
- Убедитесь, что вы получили правильный рецепт и правильную дозу. Когда вы заказываете лекарства — и когда получаете их по почте — убедитесь, что они соответствуют точной дозе и типу, прописанным вашим врачом.
- Не обманывайтесь, покупая «травяную виагру». Никогда не принимайте лекарства, которые считаются «травяными» или безрецептурными эквивалентами пероральных лекарств от эректильной дисфункции.Это не эффективная альтернатива, а некоторые содержат вредные вещества.
11 июня 2019 г.,
Показать ссылки
- Wein AJ, et al., Eds. Оценка и лечение эректильной дисфункции. В: Урология Кэмпбелла-Уолша. 11 изд. Филадельфия, Пенсильвания: Эльзевир; 2016 г. https://www.clinicalkey.com. По состоянию на 7 мая 2019 г.
- Khera M, et al. Лечение мужской сексуальной дисфункции. https://www.uptodate.com/contents/search. По состоянию на 7 мая 2019 г.
- Найдите безопасные веб-сайты, чтобы купить лекарства или найти информацию и услуги, связанные с лекарствами.Национальная ассоциация советов по фармацевтике. https://safe.pharmacy/. По состоянию на 7 мая 2019 г.
- Универсальный препарат Левитры в таблетках Тева. Тева. https://www.tevagenerics.com/product/vardenafil-hydrochloride-tablets. По состоянию на 7 мая 2019 г.
- Teva объявляет об эксклюзивном первом поступлении на рынок дженериковой версии Сиалиса в США. Тева. https://seekingalpha.com/pr/17284017-teva-announces-exclusive-first-file-launch-generic-version-cialis-united-states.

 Все, кроме линаглиптина, нуждаются в коррекции дозы для рассчитанной СКФ.
Все, кроме линаглиптина, нуждаются в коррекции дозы для рассчитанной СКФ.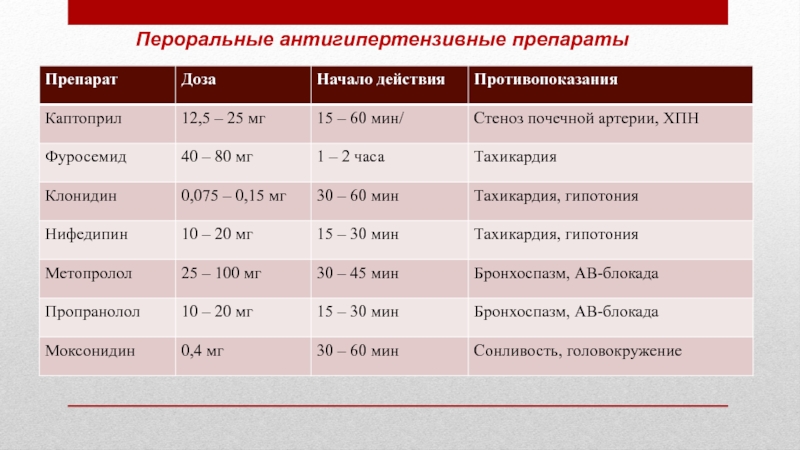
 Ректально принимаются свечи, мази и растворы, вводимые с помощью клизмы.
Ректально принимаются свечи, мази и растворы, вводимые с помощью клизмы. Эффект от лекарства наступает в течение 10-15 минут.
Эффект от лекарства наступает в течение 10-15 минут. Медикаменты попадают в организм через рот. Чаще всего таким способом принимают таблетки, капсулы, растворы, порошки, сиропы и др.
Медикаменты попадают в организм через рот. Чаще всего таким способом принимают таблетки, капсулы, растворы, порошки, сиропы и др. В.
В.
 И., Шестакова М. В. Инкретины: новая веха в лечении сахарного диабета 2-го типа. М., 2010. С. 55–62.
И., Шестакова М. В. Инкретины: новая веха в лечении сахарного диабета 2-го типа. М., 2010. С. 55–62. W. Development and Potential Role of Type-2 Sodium-Glucose Transporter Inhibitors for Management of Type 2 Diabetes // Diabetes Ther. 2011; 2 (3): 133–145.
W. Development and Potential Role of Type-2 Sodium-Glucose Transporter Inhibitors for Management of Type 2 Diabetes // Diabetes Ther. 2011; 2 (3): 133–145.