Мастер-класс по коллапсотерапии на кафедре фтизиопульмонологии
Ассистентом кафедры фтизиопульмонологии ВолгГМУ С.Г. Гагариной на базе 1 легочного отделения ГКУЗ ВОКПД 1 октября был проведен мастер-класс по коллапсотерапии для клинических интернов и ординаторов.
В последние годы наблюдается снижение эффективности лечения больных туберкулезом органов дыхания, несмотря на применение новых схем, и режимов химиотерапии с использованием современных противотуберкулезных препаратов. Это связано в первую очередь с нарастанием количества больных деструктивным туберкулезом легких, вызванным лекарственно-устойчивыми микобактериями туберкулеза. В этих условиях одними из важных методов лечения является искусственный пневмоторакс и пневмоперитонеум. В современных условиях следует учитывать и экономический эффект при использовании коллапсотерапии как доступного по простоте применения, дешевизне и быстроте получаемого терапевтического эффекта.
«Основанием для лечения искусственным пневмотораксом должно служить выделение больными лекарственно-устойчивых МВТ, плохая переносимость химиопрепаратов, нерегулярный их прием мало дисциплинированными больными, неблагоприятные эпидемиологические условия, в частности контакт с детьми, отказ больного от операции» (А. Е. Рабухин).
Суть искусственного пневмоторакса заключается во введении газа в плевральную полость. При этом нарушается сцепление между листками плевры и легкое спадается. Благоприятное течение туберкулезного процесса в легких при искусственном пневмотораксе обосновывается уменьшением эластического напряжения легкого, созданием относительного покоя пораженному участку, изменениями лимфо- и кровообращения, что создает предпосылки для усиления репаративных процессов и положительно сказывается на течении туберкулезного процесса. В результате этого в легком под пневмотораксом рассасываются инфильтративно-воспалительные изменения, заживают полости распада с образованием на их месте рубцов.
Современные аппараты для наложения искусственного пневмоторакса состоят из двух сообщающихся между собой цилиндров, на которых имеются деления для определения объема воздуха в них, водяного манометра и системы резиновых трубок, соединяющих газометр и манометр с полостью плевры. Газометры рассчитаны на вмещение 500 мл жидкости и через трехходовой кран могут соединяться друг с другом. Перемещение жидкости в цилиндрах приводит к вытеснению воздуха в полость плевры. В последние годы использовался пневмотораксный аппарат системы Качкачева.
Газометры рассчитаны на вмещение 500 мл жидкости и через трехходовой кран могут соединяться друг с другом. Перемещение жидкости в цилиндрах приводит к вытеснению воздуха в полость плевры. В последние годы использовался пневмотораксный аппарат системы Качкачева.
Для проведения манипуляции введения газа в плевральную полость больного укладывают на здоровый бок, под который подкладывается валик. Кожу места прокола смазывают йодом или спиртом. Чаще прокол делается в четвертом-шестом межреберьях по одной из подмышечных линий. Специальную тупоскошенную иглу вводят в выбранное и фиксированное левой рукой межреберье по верхнему краю нижележащего ребра, что исключает возможность повреждения межреберных сосудов.
Основываясь на показаниях манометра, определяют местонахождение иглы. Колебания манометра совпадают со вдохом и выдохом. При вдохе отрицательное давление в плевральной полости повышается, при выдохе — понижается. Поэтому цифры манометра левого колена кверху от 0 называются отрицательными, книзу от 0 — положительными.
Устойчивое отрицательное давление в плевральной полости, меняющееся на входе и выходе, свидетельствует о том, что игла находится в плевральной полости и газ можно вводить. При первичном поддувании вводят обычно 200-300 мл воздуха. После окончания процедуры врач вновь фиксирует кожу левой рукой, а правой извлекает иглу. После этого кожу места прокола сдвигают в сторону левой рукой и смазывают йодом или спиртом
При формировании пневмоторакса в течение первых 10 дней инсуфляции производятся с интервалом 2—3 дня при рентгеноскопическом контроле и только послеформирования газового пузыря, поджимающего легкое не менее чем на 1/3, интервалы между поддуваниями увеличиваются до 5-7 дней, а количество вводимого газа составляет 400-500 см3.
По данным ЦНИИТ РАМН применение искусственного пневмоторакса у больных деструктивным туберкулезом легких с лекарственной устойчивостью МБТ к основным и резервным препаратам позволяет через 12 месяцев лечения добиться прекращения бактериовыделения в 100% случаев и закрытия каверн – в 85-95%. При применении только химиотерапии резервными препаратами эти показатели составляют, соответственно, 5-25% и 20-30%. Длительность применения пневмоторакса составляет в среднем 6-8 месяцев.
При применении только химиотерапии резервными препаратами эти показатели составляют, соответственно, 5-25% и 20-30%. Длительность применения пневмоторакса составляет в среднем 6-8 месяцев.
А.А. Калуженина,
ассистент кафедры фтизиопульмонологии, к.м.н.
Роль и значение искусственного пневмоторакса у больных
деструктивным туберкулезом легких с лекарственной
устойчивостью возбудителя | Мишин
1. АлексееваГ.С.,Михайлова Ю.В.,Скачкова Е.И. и др. Отраслевые показатели противотуберкулезной работы в 2007-2008 гг.: Стат.материалы.М.:ТРИАДА;2009.
2. Андренко А. А., Федорова М.В., Грищенко Н.Г., Таджиев Н.В. Роль искусственного пневмоторакса в компле ксной терапии деструктивного туберкулеза легких. Пробл. туб. 1995; 1: 43-45.
3. Баранчукова А. А. Возможности 2-4 месячного кол лапса легкого при внутривенной интермиттирующей терапии больных распространенным деструктивным туберкулезом: Автореф. дис. … канд. мед. наук. Ново сибирск; 1998.
4. Кильдюшева Е. И. Эффективность комбинированной химиотерапии деструктивного туберкулеза легких в со четании с краткосрочным искусственным пневмото раксом: Автореф. дис. … канд. мед. наук. М.; 2001.
5. Краснов В.А., Андренко А.А., Белявский В.Е. и др. Воз можности искусственного пневмоторакса в хирургии прогрессирующего двустороннего деструктивного ту беркулеза легких. Пробл. туб. 1994; 6: 31-34.
6. Мишин В.Ю. Чуканов В.И. Эффективность лечения ту беркулеза легких, вызванного микобактериями с мно жественной лекарственной устойчивостью. Пробл. туб. 2002; 12: 18-23.
Пробл. туб. 2002; 12: 18-23.
7. Мишин В.Ю. Туберкулез легких с лекарственной устой чивостью возбудителя. М.: ГЭОТАРМедиа; 2009.
8. Михайлов Ф.А. Теория и практика лечебного пневмото ракса. М.: Медицина; 1952.
9. Приказ МЗ РФ от 21.03.03 № 109. «О совершенствова нии противотуберкулезных мероприятий в Российской Федерации». М.; 2003.
10. Рабухин А.Е. Химиотерапия больных туберкулезом лег ких. М.: Медицина; 1970.
11. Хоменко А.Г. Химиотерапия туберкулеза легких. М.: Медицина; 1980.
12. Перельман М.И. (ред.). Фтизиатрия. Нац. руководство. М.: ГЭОТАР Медиа; 2007.
13. Шебанов Ф.В. Коллапсотерапия легочного туберкулеза. М.: Медицина; 1950.
14. Шилова М.В. Туберкулез в России в 2008 году. М.: РПЦ Прима; 2009.
15. Штернберг А.Я. Искусственный пневмоторакс при ту беркулезе легких. М.: Медицина; 1921.
16. Эйнис В.Л. Коллапсотерапия при туберкулезе легких. Пробл. туб. 1945; 2: 12-14.
23.3 Искусственный пневмоторакс и пневмоперитонеум
а б в
Рис. 23.15. Посттуберкулезный стеноз левого главного бронха.
а — бронхограмма с отчетливо выявленным стенозом; б — схема верхней лобэктомии с резекцией главного бронха и бронхиальным анастомозом; в — по слеоперационная бронхограмма. Просвет бронха восстановлен.
Просвет бронха восстановлен.
тельств при туберкулезе легких значительно снизилась, воз росла их эффективность. Сформировался крупный и важный раздел торакальной хирургии — фтизиохирургия. На ее долю в России приходится около половины всех операций на легких. Эффективность хирургического лечения больных туберкуле зом легких приблизилась к 90 %.
Искусственный пневмоторакс (ИП) — это введение воздуха в плевральную полость для создания коллапса пораженного легкого. До открытия специфических химиопрепаратов ИП считали наиболее эффективным методом лечения больных ту беркулезом легких, особенно его деструктивных форм.
Широкое применение противотуберкулезных препаратов и оперативных вмешательств у больных туберкулезом значи тельно сократили показания к лечению ИП. В настоящее вре мя его применяют у ограниченной группы больных каверноз ными формами туберкулеза легких в случаях недостаточной эффективности химиотерапии.
Лечебный эффект ИП обусловлен уменьшением эластиче ского растяжения легкого. В условиях относительного коллап са частично или полностью спадаются каверны, снижается интенсивность всасывания токсинов и рассеивания МБТ, ус коряются репаративные процессы.
Основным показанием к наложению ИП является деструк тивный туберкулез со свежей каверной без значительного
| фиброзного уплотнения пора | ||||||
| женного | легкого. | Срочным | ||||
| показанием | может | быть | ле | |||
| гочное | кровотечение, | если | ||||
| известно при этом, из какого | ||||||
| легкого. |
|
|
|
|
| |
| Ранее наложение ИП ино | ||||||
| гда производили с диагности | ||||||
| ческой | целью для | уточнения | ||||
| локализации различных обра | ||||||
| зований — в | легком | или | в | |||
| грудной | стенке. | Частичное | ||||
| спадение легкого и появление | ||||||
| воздушной | прослойки | между | ||||
| ним и грудной стенкой по | ||||||
| зволяли четко определить ло | ||||||
| кализацию | патологической | |||||
| тени. В настоящее время это | ||||||
| достигается с помощью КТ. | ||||||
Рис. 23.16. Аппарат для наложе | Воздух в плевральную по | ||||||
лость вводят через иглу, соеди | |||||||
ния искусственного пневмото | ненную | с | пневмотораксным | ||||
ракса. | |||||||
аппаратом. Аппарат состоит из | |||||||
| |||||||
двух взаимно передвигающих ся по вертикали сосудов, частично заполненных водой, водя ного манометра, крана и мягких трубок, связывающих мано метр с иглой и иглу с сосудом-газометром (рис. 23.16). В поло жении больного на здоровом боку прокалывают грудную стенку в четвертом—шестом межреберье по подмышечной линии. О нахождении иглы в полости плевры судят по колебаниям ма нометра, который на вдохе фиксирует отрицательное (т. е. ниже атмосферного) давление. При первой пункции в плевральную полость вводят 250—300 мл воздуха. В дальнейшем, по мере рассасывания воздуха, повторяют его введение через 5—10 дней. Объем воздуха в плевральной полости контролируют рентгено логическим методом. Лечебным коллапсом считают спадение легкого на 1/3 первоначального размера легочного поля.
Типичным, но не опасным осложнением искусственного пневмоторакса является подкожная эмфизема. Она возникает в случаях проникновения воздуха по пункционному каналу в мягкие ткани грудной стенки. Тяжелее протекает медиастинальная эмфизема, при которой воздух из плевральной полос ти поступает в клетчатку средостения, затрудняя движение крови по венам. При попадании воздуха в кровеносный сосуд может возникнуть эмболия, исход которой во многом зависит от конечной локализации воздушного эмбола (сетчатка глаза, головной мозг).
Длительность лечения ИП от 2 мес до 1 года и зависит от
Рис. 23.17. Коррекция искусственного пневмоторакса.
а — сращения между париетальной и висцеральной плеврой; б — пережигание термокаутером. Схема.
срока закрытия каверны. Все это время больной должен при нимать противотуберкулезные препараты.
Нередко под действием ИП легкое спадается лишь час тично из-за сращений между висцеральной и париетальной плеврой. В таких случаях пневмоторакс неэффективен. Для его коррекции ранее широко применяли разрушение плев ральных сращений путем их пережигания или торакокаустики. После осмотра плевральной полости торакоскопом выяс няли возможность их разрушения и намечали место для вве дения термокаутера. Сращения пережигали платиновой пет лей, раскаленной электрическим током (рис. 23.17). После достижения коллапса легкого пневмоторакс считали эффек тивным.
После осмотра плевральной полости торакоскопом выяс няли возможность их разрушения и намечали место для вве дения термокаутера. Сращения пережигали платиновой пет лей, раскаленной электрическим током (рис. 23.17). После достижения коллапса легкого пневмоторакс считали эффек тивным.
В настоящее время коррекция неэффективного ИП обычно нецелесообразна. Однако при необходимости она может быть выполнена видеоторакоскопическим методом.
Пневмоперитонеум — введение воздуха в брюшную полость для подъема и ограничения подвижности диафрагмы. При поднятая диафрагма уменьшает дыхательную экскурсию лег ких, преимущественно их нижних отделов. Эластическое на пряжение легких, как и при наложении ИП, снижается. Ме тод используют в основном как дополнение к химиотерапии и оперативным вмешательствам.
Для введения воздуха в брюшную полость используют ап парат для наложения ИП. Прокол брюшной стенки произво дят в нижнем левом квадранте у латерального края прямой мышцы на уровне пупка или на 3—4 см ниже. Вначале вводят
Рис. 23.18. Пневмоперитонеум. Рентгенограммы легких в прямой проекции.
Искусственный пневмоторакс в комплексном лечении больных туберкулезом легких Текст научной статьи по специальности «Клиническая медицина»
ОБМЕН ОПЫТОМ
Искусственный пневмоторакс в комплексном лечении больных туберкулезом легких
Гельберг И.С.1, Шейфер Ю.А.2
1 Гродненский государственный медицинский университет
2 Гродненский областной клинический центр«Фтизиатрия»
Gelberg I.S.1, Sheifer YA.2
1 Grodno State Medical University, Belarus 2 Grodno Regional Clinical Center«Phthiziatria», Belarus
Artificial pneumothorax in complex treatment in tuberculosis patients in present time
Резюме. Под наблюдением находились 60 больных деструктивным туберкулезом легких, у которых применялся искусственный пневмоторакс (ИП) на фоне химиотерапии. Непосредственные результаты изучены у 56 пациентов, отдаленные — у 54. У больных деструктивным туберкулезом при сохранении в условиях химиотерапии полостей распада применение ИП позволило добиться их заживления у 51 пациента из 56, т.е. в 91,0% случаев. Прекращение бактериовыделения достигнуто у 49 из 53 бактериовыделителей (92,4%). Отдаленные результаты, изученные у 54 больных при сроках наблюдения от 6 мес. до 8 лет, оказались следующими: полный клинический эффект при лекарственной чувствительности микобак-терий туберкулеза (28 пациентов) получен в 100% случаев, при множественной лекарственной устойчивости — у 22 из 28 больных, т.е. в 78,6% случаев, в целом у 50 из 56 (89,3%). Летальность — 1,85% (одна пациентка). Ключевые слова: туберкулез легких, лечение, искусственный пневмоторакс.
Под наблюдением находились 60 больных деструктивным туберкулезом легких, у которых применялся искусственный пневмоторакс (ИП) на фоне химиотерапии. Непосредственные результаты изучены у 56 пациентов, отдаленные — у 54. У больных деструктивным туберкулезом при сохранении в условиях химиотерапии полостей распада применение ИП позволило добиться их заживления у 51 пациента из 56, т.е. в 91,0% случаев. Прекращение бактериовыделения достигнуто у 49 из 53 бактериовыделителей (92,4%). Отдаленные результаты, изученные у 54 больных при сроках наблюдения от 6 мес. до 8 лет, оказались следующими: полный клинический эффект при лекарственной чувствительности микобак-терий туберкулеза (28 пациентов) получен в 100% случаев, при множественной лекарственной устойчивости — у 22 из 28 больных, т.е. в 78,6% случаев, в целом у 50 из 56 (89,3%). Летальность — 1,85% (одна пациентка). Ключевые слова: туберкулез легких, лечение, искусственный пневмоторакс.
Summary. Undergoing 60 patients with lungs destructive tuberculosis treat by artificial pneumothorax accompanying with medicine therapy The direct results were observed in 56 patients, the distant results — 54. Closing oi disintegration cavity appears to be achieve in 51 patient oi 56, by using oi artificial pneumothorax (91.0%), as well as interruption oi bacteria producing in 48 cases oi 52 (92.4%). Aiter long term observing (irom 6 month to 8 years) distant results were the next in 54 inspected patients: total clinical effect was achieved in 100% (28 patients) cases in the patients wtth drug sensitive tuberculosis mycobacteria, in 78.6% (22 patients) cases with multiply drug resistance (MDR) (in total group proportion: in 50 oi 56 patients — 89.3%). Lethality composed 1.85% (1 womiin).
Keywords: lungs tuberculosis, treatment, artlilclal pneumothorax.
Искусственный пневмоторакс (ИП) как метод лечения больных туберкулезом легких широко применялся во фтизиатрии до середины 1960-х гг. В дальнейшем ввиду эффективности химиотерапии примерно в течение 35 лет он практически не использовался, и современное поколение фтизиатров с этим методом мало знакомо.
В дальнейшем ввиду эффективности химиотерапии примерно в течение 35 лет он практически не использовался, и современное поколение фтизиатров с этим методом мало знакомо.
Однако с конца XX в. в большинстве стран мира, в том числе в Восточной Европе и государствах бывшего СССР отмечается неблагоприятный патоморфоз туберкулеза, выражающийся в увеличении его распространенности, ухудшении клинической структуры, повышении частоты наличия отягощающих факторов, среди которых особое место занимает нарастание множественной лекарственной устойчивости (МЛУ) микобактерий туберкулеза (МБТ), а также снижении эффективности химиотерапии.
Учитывая вышеизложенное, представляется целесообразным использование ИП с пересмотром показаний и методики его применения в современных условиях.
Об этом свидетельствуют немногочисленные литературные данные последних десятилетий [1-5].
Цель исследования — оценка эффективности ИП у больных деструктивным туберкулезом при сохраняющихся в условиях химиотерапии полостях распада в легких.
Материалы и методы
Под наблюдением находились 60 пациентов с туберкулезом легких, в комплексном лечении которых использовался или используется ИП в сочетании с химиотерапией. Характеристика больных представлена в таблице.
Как видно из таблицы, пациенты преимущественно молодого возраста, с небольшим преобладанием мужского пола, с инфильтративным и кавернозным туберкулезом легких. Подавляющее большинство — бактериовыделители, почти у половины имела место МЛУ МБТ в половине случаев отмечается злоупотребление алкоголем. Полости распада в легких обнаружены у всех больных. Отягощающие факторы отсутствовали лишь у одной пятой обследованных.
Всем пациентам проводилась химиотерапия согласно существующим в соответствующий период инструкциям, в последние годы — по I, II и IV категориям. Вопрос о наложении ИП решался при сохранении полости распада после трех и более месяцев лечения. Как показывает опыт, при длительных сроках консервативного лечения стенки полости утолщаются, вокруг нее постепенно развиваются фиброзные изменения, легочная ткань теряет эластичность и эффективность лечения ИП снижается.
Результаты и обсуждение
К настоящему времени курс лечения ИП закончили 56 пациентов. Из них антибактериальная терапия по 1-й категории проводилась 18 больным (32,1%), по 2-й — 13 (23,2%), по 4-й — 25 (44,6%). Показанием к наложению ИП было сохранение полости распада без явной положительной динамики в течение трех и более месяцев лечения, иногда — до 8-9 мес. Дополнительные показания к наложению ИП: наличие МЛУ МБТ зависимости от алкоголя, сахарного диа-
№7 • 2012
МЕДИЦИНСКИЕ НОВОСТИ |дэ
Обмен опытом! мн
Таблица 1 Характеристика больных туберкулезом легких с ИП
Наименование показателя Число больных Процент
Всего больных 60 100
Пол:
мужской 34 56,7
женский 26 43,3
Возраст:
до 30 лет 30 50,0
30-39 лет 25 41,7
40-49 лет 4 6,7
50 лет и старше 1 1,7
Клиническая форма туберкулеза:
инфильтративный 45 75,0
кавернозный 15 25,0
Бактериовыделение:
МБТ плюс 53 88,3
МБТ минус 7 10,7
Лекарственная устойчивость МБТ
(к числу бактериовыделителей):
чувствительность ко всем антибактериальным препаратам 19 35,8
к 1 препарату 5 9,4
к 2 препаратам 1 1,9
МЛУ 28 52,8
Наличие полости распада 60 100
в т. ч. свыше 4 см в диаметре 7 11,6
ч. свыше 4 см в диаметре 7 11,6
в т.ч. 2 полости и более 8 13,6
Выявление туберкулеза:
впервые выявлены 37 61,7
рецидив (обострение) 23 38,3
Факторы риска (отягощающие факторы):
без факторов риска 11 18,3
контакт 10 16,7
сахарный диабет 4 6,7
хронические неспецифические заболевания органов 6 10,0
дыхания
заболевания ЖКТ 6 10,0
злоупотребление алкоголем (не состоит на учете) 17 28,3
зависимость от алкоголя (на учете) 14 23,8
Работа:
работает 40 66,6
не работает 19 31,7
инвалид 1 1,7
бета и т.п. Имеет значение и возраст: у больных старше 50 лет ИП применяется редко, среди наших пациентов — только в одном случае. При выраженном пнев-москлерозе, эмфиземе даже в более молодом возрасте ИП противопоказан. Методика наложения и ведения ИП осуществлялась согласно разработанной авторами инструкции по применению, утвержденной Министерством здравоохранения Республики Беларусь 27.09.20l0 г. В настоящее время при адекватной анти-
бактериальной терапии отпадает необходимость в длительном, по 2 года и более, поддерживании ИП, как это было ранее. Время его использования определяется эффективностью, т.е. сроками прекращения бактериовыделения, закрытия полостей распада. Имеют значение исходный размер полости, наличие плевральных спаек, МЛУ МБТ и других отягощающих факторов, например сахарного диабета. До 4 мес. ИП продолжался у 9 пациентов (16,1%), 4-6 мес. — у 36 (64,3%), 6-8
Время его использования определяется эффективностью, т.е. сроками прекращения бактериовыделения, закрытия полостей распада. Имеют значение исходный размер полости, наличие плевральных спаек, МЛУ МБТ и других отягощающих факторов, например сахарного диабета. До 4 мес. ИП продолжался у 9 пациентов (16,1%), 4-6 мес. — у 36 (64,3%), 6-8
мес. у 11 (19,6%). Как свидетельствует наш опыт и данные других авторов [2], в настоящее время в значительной части случаев ИП со спайками между париетальной и висцеральной плеврой оказывается эффективным, поэтому вопрос о хирургическом удалении плевральных спаек целесообразно решать лишь при сохранении полости распада в процессе лечения ИП. Оно было проведено у 4 больных.
При первичном наложении и дальнейшем ведении ИП возможны осложнения. У 4 из 60 пациентов (6,6%) возник спонтанный пневмоторакс, что может быть связано с отрывом плевральных сращений при спадении легкого, травмой легочной ткани иглой. У всех больных последствия спонтанного пневмоторакса ликвидированы, ИП продолжен.
После первого введения воздуха в плевральную полость (рекомендуется не более 150-200 мл) практически все пациенты ощущали чувство давления, небольшую боль, которые через 1-3 дня проходили и при последующих введениях воздуха не ощущались. У двух больных (3,3%) болевая реакция была выражена, ее купировали обезболивающими средствами, ИП продолжен.
Ввиду раздражения плевральных листков при введении воздуха нередко появляется экссудат в плевральной полости — пневмоплеврит, в нашем случае возникший у 14 пациентов (23,3%). Количество экссудата обычно было небольшим, клинические проявления отсутствовали или были незначительными. Лишь в одном случае, где ИП накладывался по расширенным показаниям, отмечен переход в эмпиему, ИП пришлось прекратить.
Непосредственные результаты ИП оказались достаточно высокими: прекращение бактериовыделения наступило у 49 пациентов из 53, выделявших МБТ (92,4%), закрытие полостей — у 51 из 56 (91,0%), положительная рентгенодинами-ка — у всех больных.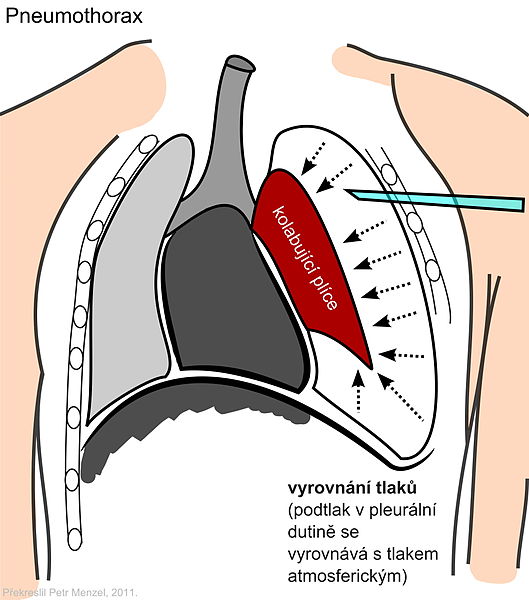
Таким образом, эффективность ИП к моменту его прекращения составила 91,0%. Из пяти пациентов, у которых ИП признан неэффективным, МЛУ МБТ имела место у четверых.
Отдаленные результаты изучены у 54 больных, срок наблюдения за которыми после выписки из стационара составил 6-12 мес. (9 человек), 1-2 года (20 чел.), 3-4 года (17 чел.), 5-8 лет (8 чел.), всего более года наблюдались 83,3% пациентов.
В период наблюдения обострения и рецидивы туберкулеза легких были выявлены у 15 больных, т.е. в 27,7% случа-
44 МЕДИЦИНСКИЕ НОВОСТИ
№7 • 2012
мн Обмен опытом
ев, из них связанные с МЛУ МБТ — у 12 человек, с ЛЧ МБТ — у 3, в том числе у одной пациентки с сахарным диабетом 1-го типа и лекарственной устойчивостью к изониазиду. К настоящему времени у 12 больных достигнуто клиническое излечение или значительное улучшение, трое продолжают лечение, из них одна пациентка оперирована. У троих пока сохраняются полости распада и бактерио-выделение. Из 5 пациентов с исходно неэффективным пневмотораксом у одной женщины выполнена пульмонэктомия с последующим клиническим излечением, одна продолжает лечение восстановленным ИП в сочетании с пневмоперитонеу-мом, достигнуто прекращение бактерио-выделения и закрытие полости распада. У одной больной с МЛУ МБТ — летальный исход из-за прогрессирования туберкулезного процесса.
В целом полный клинический эффект получен у 50 пациентов из 56, т.е. в 89,3% случаев, летальность составила 1,85% (одна больная). У больных с наличием ЛЧ МБТ или лекарственной устойчивости к
одному препарату (28 человек) эффективность достигнута в 100% случаев, при наличии МЛУ МБТ — у 22 из 28 пациентов, т. е. в 78,6% случаев, летальность составила 3,6%. У 2 больных с МЛУ МБТ при наличии полостей распада в верхних и нижних долях использовалась сочетан-ная коллапсотерапия — ИП в сочетании с пневмоперитонеумом с благоприятным результатом. У 4 пациентов с обострениями или рецидивами туберкулеза накладывался повторно ИП, у 3 из них закончен эффективно.
е. в 78,6% случаев, летальность составила 3,6%. У 2 больных с МЛУ МБТ при наличии полостей распада в верхних и нижних долях использовалась сочетан-ная коллапсотерапия — ИП в сочетании с пневмоперитонеумом с благоприятным результатом. У 4 пациентов с обострениями или рецидивами туберкулеза накладывался повторно ИП, у 3 из них закончен эффективно.
Выводы:
1. Искусственный пневмоторакс -ценный метод в комплексном лечении деструктивных форм туберкулеза легких при недостаточной эффективности химиотерапии.
2. Показания к наложению ИП: преимущественно инфильтративный в фазе распада и кавернозный туберкулез легких при сохранении полости распада в условиях химиотерапии в течение трех месяцев и более. Наличие МЛУ МБТ и других отягощающих
факторов — дополнительные показания к наложению ИП.
3. Сроки лечения ИП в настоящее время составляют в среднем 4-6 мес.
4. Применение ИП при отсутствии успеха химиотерапии позволило получить полный клинический эффект, по данным отдаленных результатов — в 100% случаев у больных без МЛУ и в 76,9% случаев у пациентов с МЛУ МБТ в целом — у 88,9% пролеченных больных.
Л И Т Е Р А Т У Р А
1. Андренко А.А., Федорова М.В., Грищенко Н.Г., Тафилева Н.В. // Пробл. туберкулеза и болезней легких. — 1995. — № 1. — С. 43-45.
2. ВинникЛ.А. Современная газовая коллапсотера-пия туберкулеза легких. — Астрахань, 1999. — 38 с.
3. Мотус И.Я., Скорняков С.Н., Кильдюшева Е.И. и др. // Пробл. туберкулеза и болезней легких. -2005. — № 12. — С. 23-26.
23-26.
4. Соколов В.А., Кильдюшева Е.И, Егоров Е.А. и др. // Пробл. туберкулеза и болезней легких. -2002. — № 5. — С. 16-19.
5. Чуканов В.И., Мишин В.Ю., Сигаев А.Т. и др. // Пробл. туберкулеза и болезней легких. — 2004. -№ 8. — С. 22-24.
Поступила 14.03.2011 г.
Диагностика и хирургическое лечение больных с новообразованиями крестца
Воронович И.Р., Пашкевич Л.А.
РНПЦ травматологии и ортопедии, Минск
Voronovich I.R., Pashkevich L.A.
RSPC of Traumatology and Orthopedics, Minsk
Diagnostics and surgical treatment of patients with tumors of sacrum
Резюме. Описаны редкие признаки в диагностике новообразований крестца, определен характер течения опухолевого процесса,, выявлены возможности злокачественной трансформации некоторых доброкачественных опухолей, определены наиболее рациональные методы хирургического лечения в зависимости от структуры, локализации и агрессивности опухолевого процесса. Ключевые слова: новообразования крестца, остеохондрома, остеосаркома, хондрома, лимфома.
Summary. The rare signs in the diagnostics of sacral bone tumors are described; the nature of tumor process is determined; the possibilities of malignant transformation of some benign tumors are identified; the most rational methods of surgical treatment depending on the structure, localization and aggressiveness of tumor process are defined.
Keywords: sacral bone tumors, osteochondroma, osteosarcoma, chondroma, lymphoma.
Диагностика опухолей крестца в раннем периоде представляет большие трудности в связи с многообразием форм и неспецифичностью симптоматики. В повседневной практике нередко встречаются диагностические ошибки и позднее направление пациентов в специализированные учреждения. В большинстве случаев они получают
тепловые процедуры и физиолечение по поводу остеохондроза пояснично-крестцо-вого отдела позвоночника, люмбоишиалгии и т.д. Наиболее часто приходится дифференцировать опухоль верхнего отдела крестца с дегенеративно-дистрофическими изменениями этого отдела позвоночника, а также с различными формами новообразований, несколько реже — с
воспалительными процессами и туберкулезным поражением.
Оперативные вмешательства при доброкачественных опухолях заднего отдела крестца (остеоидная остеома, остеохондрома) не представляют особых затруднений, но при больших опухолях переднего отдела крестца в верхней части с распространением в полость мало-
№7 • 2012
МЕДИЦИНСКИЕ НОВОСТИ |45
Коллапсотерапия при туберкулезе легких: возвращение к истокам | Шаповалов
1. Базаров Д.В. Обоснование показаний и объема резекции при хирургическом уменьшении легкого у больных диффузной эмфиземой: дис.. канд. мед. наук. М., 2007. 163 с.
2. Барканова О. Н., Гагари С.Г., Калуженина А.А. Применение коллапсотерапии в лечении деструктивного туберкулеза легких с лекарственной устойчивостью возбудителя // Вестник Волгоградского государственного медицинского университета. 2014. № 4. С. 121-123.
№ 4. С. 121-123.
3. Богуш Л.К., Калиничев Г.А. Корригирующие операции при резекции легких: Тбилиси: Сабчота Сакартвело, 1979. 122 с.
4. Васильева И.А., Кузьмина Н.В., Ерохин В.В. Коллапсотерапия в комплексном лечении больных деструктивным туберкулезом легких с лекарственной устойчивостью возбудителя. М.: ГЭОТАР-Медиа. 2014. 237 с.
5. Винник, Л.А. Современная газовая коллапсотерапия туберкулеза легких: метод. рекомендации для врачей и студентов. Астрахань, 1999. 39 с.
6. Гусейнов Г.К., Адзиев А.А., Муталихов М.А. [и др.]. Коллапсотерапия и местное введение противотуберкулезных препаратов в комплексном лечении деструктивных и лекарственно-устойчивых форм туберкулеза легких // Юбилейный сборник научных трудов, посвященный 80-летию Дагестанской государственной медицинской академии. Махачкала, 2012. С. 382-384.
7. Кильдюшева Е.И., Мотус И.Я., Скорняков С.Н. [и др.]. Сочетанное применение методов коллапсотерапии при деструктивном лекарственно-устойчивом туберкулезе легких — один из путей повышения эффективности лечения // Фтизиатрия и пульмонология. 2015. № 2. С. 20-21.
8. Краснов В.А., Андренко А.А., Белявский В.Е. [и др.]. Возможности искусственного пневмоторакса в хирургии прогрессирующего двустороннего деструктивного туберкулеза легких // Проблемы туберкулеза. 1994. № 6. С.31-34.
9. Левин А.В., Кагаловский Г.М., Максименко А.А., Самуйленков А.М Хирургическое лечение туберкулеза и других заболеваний легких: мат. юбил. науч. -практ. конф. Челябинск, 2001. С. 35-37.
-практ. конф. Челябинск, 2001. С. 35-37.
10. Мотус И.Я., Скорняков С.Н., Кильдюшева Е.И. Искусственный пневмоторакс в лечении деструктивного туберкулеза легких, осложненного лекарственной устойчивостью возбудителя // Проблемы туберкулеза. 2005. № 12. С. 22-26.
11. Полежаев А.А., Шаповалов А.С., Белов С.А. [и др.]. Применение латексного клея во фтизиохирурги // Тихоокеанский медицинский журнал. 2014. № 1. С. 88-90.
12. Салмаханов А.Р. Коллапсотерапия в комплексном лечении деструктивного туберкулеза легких: дис. канд. мед. наук. Махачкала, 2009. 142 с.
13. Соколов В.А., Кильдюшева Е.И., Егоров Е.А. [и др.]. Возможности коллапсотерапии при лечении деструктивного туберкулеза легких // Проблемы туберкулеза. 2002. № 5. С. 16-19.
14. Чуканов В.И., Мишин В.Ю., Сигаев А.Т. Эффективность искусственного пневмоторакса в лечении больных с множественной лекарственной устойчивостью микобактерий // Проблемы туберкулеза. 2004. № 8. С. 22-24.
15. Шевченко А.А., Жила Н.Г., Шевченко А.В., Коллапсохирургическое лечение деструктивного туберкулеза легких // Якутский медицинский журнал. 2014. № 1. С. 9-11.
Отделение лечения больных туберкулезом легких с множественной лекарственной устойчивостью
Отделение лечения больных туберкулезом легких с множественной лекарственной устойчивостью
Основной профиль деятельности: основной профиль деятельности: лечение больных туберкулезом легких с множественной лекарственной устойчивостью (МЛУ), подготовка к хирургическому лечению больных с МЛУ и лечение в послеоперационном периоде, применение коллапсотерапии (лечебный пневмоперитонеум, искусственный пневмоторакс, КББ — клапанная бронхоблокация) у больных с МЛУ.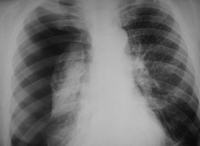 Лечение больных с (широкой лекарственной устойчивостью) ШЛУ, лечение больных туберкулезом легких с МЛУ, осложненное токсической непереносимостью противотуберкулёзных припаратов (ПТП).
Лечение больных с (широкой лекарственной устойчивостью) ШЛУ, лечение больных туберкулезом легких с МЛУ, осложненное токсической непереносимостью противотуберкулёзных припаратов (ПТП).
Заведующая отделением: Кильдюшева Елена Ивановна врач – фтизиатр, высшая квалификационная категория по специальности – фтизиатрия кандидат медицинских наук.
Технологии, применяемые в отделении:
подбор схемы химиотерапии на основании определения чувствительности МБТ быстрыми методами: молекулярно -генетические методы с определением чувствительности к препаратам 1 и 2 ряда, посевы на жидких питательных средах с тестом лекарственной чувствительности (ТЛЧ) через 3 недели от момента забора, посевы на плотных питательных средах с охватом ТЛЧ всех противотуберкулезных препаратов. Лечение больных с деструктивным туберкулезом методом ингаляций с ПТП, сурфактанта, перибронхиальных блокад. Определение показаний к лечебному пневмотораксу на основании данных компьютерной томографии легких, оценки ФВД методом спирометрии, диффузионной способности легких, оценки центральной гемодинамики. Наложение лечебного пневмоперитонеума и искусственного пневмоторакса, подготовка к торакокаустике при линейных и ограниченных плоскостных сращениях. КББ с целью рубцевания каверн, гемостатической целью в сочетании с пневмоперитонеумом.
Комплексное лечение больных туберкулезом легких с МЛУ, ШЛУ с использованием эндобронхиального лечения, коллапсотерапии, КББ, подготовки к хирургическому лечению.
Лечение туберкулеза в Санкт-Петербурге в доинститутский период
Изучение туберкулеза началось в Петербурге в конце XVIII века. 5 апреля 1796г. адъюнкт-профессор Иван Андреевич Смеловский (1762 — 1808) прочел первую в России лекцию по туберкулезу «О болезненных причинах вообще и о чахотке» в Петербургском Медико-Хирургическом Училище, на базе которого через 2 года была создана Медико-Хирургическая Академия (ныне — Военно-медицинская академия), ставшая первым центром противотуберкулезных исследований в России.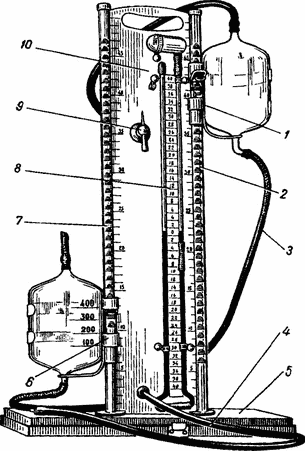
В первой половине XIX века, работая в Петербургском сухопутном госпитале, Н.И.Пирогов у 60-70% умерших от различных причин солдат обнаружил туберкулезные бугорки в легких, лобарные или лобулярные сливные очаги.
Кроме больных туберкулезом легких Н.И.Пирогов наблюдал много больных туберкулезом лимфатических узлов, костно-суставного аппарата и больных с быстро прогрессирующими генерализованными формами. В лекции «О болезнях коленного сустава» Н.И.Пирогов дал замечательное для того времени описание клинических и патологоанатомических изменений при туберкулезных заболеваниях коленного сустава. Приготовленные им сухие патологоанатомические препараты туберкулеза костей и сделанные с препаратов цветные рисунки хранятся на кафедре патанатомии ВМА. Все это свидетельствовало о высокой пораженности туберкулезом. Уже впервые полученные статистические данные показали, что в 1881 году в Петербурге умерло от туберкулеза 60,7 на 100 000 жителей.
С 60-х годов XIX века центром интенсивной научной работы в области туберкулеза становится Медико-хирургическая академия и ее научно-учебные базы.
Из исследований Вильмена и Коха, доказавших инфекционный характер туберкулеза, казалось, следовал неопровержимый вывод, что противоэпидемические мероприятия в борьбе с туберкулезом являются самыми основными. Однако отечественная медицинская мысль Петербурга не пошла по этому исключительному пути. Разделяя точку зрения о микробной этиологии туберкулеза, великий клиницист С.П.Боткин писал: «Теперь надо совершенно серьезно считаться и с микробами, из-за которых начинают забывать не только клинику, но и патологическую анатомию тканей, забывают значение реакции организма на микробы». Аналогичную мысль высказал другой знаменитый клиницист Петербурга В.А.Манассеин: «Из-за палочек не следует забывать организма, в котором эти палочки разводятся. Причина туберкулеза лежит не только в заразительности, но и в неблагоприятных условиях быта и труда».
Проводившиеся по мысли В. А.Манассеина с 1889 года массовые обследования населения на туберкулез в разных местностях нашей страны показали громадное значение в возникновении туберкулеза санитарно-бытовых и профессиональных факторов. Этим самым отечественные исследователи приблизились к пониманию социальных корней в возникновении и распространении туберкулеза.
А.Манассеина с 1889 года массовые обследования населения на туберкулез в разных местностях нашей страны показали громадное значение в возникновении туберкулеза санитарно-бытовых и профессиональных факторов. Этим самым отечественные исследователи приблизились к пониманию социальных корней в возникновении и распространении туберкулеза.
С конца 1890 года ученые и врачи Петербурга приступили к испытанию туберкулинотерапии, но уже к 1891 году были обнаружены побочные вредные воздействия препарата и интерес к нему как к терапевтическому практическому средству значительно ослабевает. Однако научное изучение его лечебных и иммунных свойств продолжается, о чем свидетельствует ряд научных статей.
В 1891 году при Русском обществе охранения народного здравия была организована «Комиссия по изысканию мер против чахотки». Такая же комиссия была создана в 1900 году Обществом русских врачей в память Н.И.Пирогова. И только в 1909 году был утвержден устав Всероссийской лиги для борьбы с туберкулезом. Торжественное открытие Лиги произошло 20 апреля 1910 года в Петербурге в здании ВМА.
Среди первоочередных задач выдвигались распространение сведений в народе о путях заражения туберкулезом, о необходимости своевременного и настойчивого лечения. Лига будет стремиться создавать для своих целей специальные лечебные и попечительские учреждения. В заключении говорилось, что туберкулез является одной из основных причин вымирания и вырождения народа.
Источником финансовой деятельности Лиги должны стать частные благотворительные и денежные сборы в ежегодно организуемые повсеместно по предложению крупного врача-бактериолога А.А.Владимирова так называемые «дни белого цветка» или «дни белой ромашки». Таким образом, Лига борьбы с туберкулезом составила объединение ученых, общественников, врачей, дам-патронесс.
С 1906 года основным центром научного исследования туберкулеза становится Обуховская больница, которую возглавлял талантливый терапевт проф. А.А.Нечаев. Эта была больница, обслуживающая контингент бедноты. А.А.Нечаев добился, что Обуховская больница стала образцовым лечебным учреждением. В ней работали многие известные клиницисты и ученые. Ее называли «Большой академией медицинских наук». Профессор А.А.Нечаев предложил заведование 15-м мужским легочным отделением больницы профессору А.Я.Штернбергу, который здесь продолжил изучение туберкулиноте-рапии и дал теоретическое обоснование ее минимальным и все возрастающим дозам. Особенно тщательные многолетние исследования были проведены в области пневмоторакса. Профессор А.Я.Штенберг ввел в терапевтическую практику искусственный пневмоторакс, усовершенствовал соответствующую аппаратуру и методику ведения пневмоторакса. Результаты этих исследований в 1921 году нашли свое отражение в монографии А.Я.Штенберга «Искусственный пневмоторакс», которая стала настольной книгой фтизиатров и была переиздана в 1929 году. Много врачей из различных городов приезжали в Петербург, чтобы под его руководством освоить лечение этим методом.
А.А.Нечаев. Эта была больница, обслуживающая контингент бедноты. А.А.Нечаев добился, что Обуховская больница стала образцовым лечебным учреждением. В ней работали многие известные клиницисты и ученые. Ее называли «Большой академией медицинских наук». Профессор А.А.Нечаев предложил заведование 15-м мужским легочным отделением больницы профессору А.Я.Штернбергу, который здесь продолжил изучение туберкулиноте-рапии и дал теоретическое обоснование ее минимальным и все возрастающим дозам. Особенно тщательные многолетние исследования были проведены в области пневмоторакса. Профессор А.Я.Штенберг ввел в терапевтическую практику искусственный пневмоторакс, усовершенствовал соответствующую аппаратуру и методику ведения пневмоторакса. Результаты этих исследований в 1921 году нашли свое отражение в монографии А.Я.Штенберга «Искусственный пневмоторакс», которая стала настольной книгой фтизиатров и была переиздана в 1929 году. Много врачей из различных городов приезжали в Петербург, чтобы под его руководством освоить лечение этим методом.
Изучалась проблема иммунитета при туберкулезе, причем было указано на приспособляемость туберкулезной палочки и ее изменчивость в условиях пребывания в человеческом организме, чем объяснялись периоды клинического затишья и многообразие клинических проявлений. Разрабатывался вопрос об иммунизации живыми и мертвыми возбудителями болезни. Был выполнен ряд работ по токсемии при туберкулезе, намечены пути рациональной терапии.
Параллельно и независимо по научному исследованию туберкулеза работал другой ученый Петербурга А.Н.Рубель. Монография А.Н.Рубеля «Искусственный пневмоторакс при лечении туберкулеза легких» (1912г.) была первым в русской медицинской литературе исследованием, посвященным теории и практике пневмоторакса. Он одним из первых стал изучать начальные формы туберкулеза легких. Заслугой А.Н.Рубеля в отечественной фтизиатрии является еще и то, что он обосновал различные организационные формы борьбы с туберкулезом. В 1881 году недалеко от Выборга был открыт санаторий «Халила» для больных туберкулезом легких.
Необходимо упомянуть еще одного Петербургского ученого — хирурга, профессора Н.А.Вельяминова, который много внимания уделял изучению хирургического туберкулеза. Хирургический туберкулез был широко распространен среди детей. По предположениям Н.А.Вельяминова в России было около 200 000 больных детей. Он считал, что успех лечения больных костно-суставным туберкулезом зависит от применения комплексного метода лечения, наряду с хирургическо-ортопедическими методами применялся режим, морской и лесной воздух. Были организованы санатории в Гатчине и Стрельне. В 1898 году было учреждено Общество приморских санаториев для хронически больных детей, вице-председателем Н.А.Вельяминов. При его участии в апреле 1900 года Общество открыло первый в России санаторий для больных хирургическим туберкулезом — Виндавский санаторий на 40 коек. В санатории широко применялись все виды консервативного лечения детей с хирургическим туберкулезом, широко использовались морские купания и ванны с морской водой для детей до 5 лет. В 1901 году на II съезде российских хирургов Вельяминов выступил с докладом о наиболее целесообразных приемах борьбы с хирургическим туберкулезом на Севере.
На IV съезде российских хирургов программным был вопрос «О хирургической бугорчатке вообще и о бугорчатки костей и суставов в особенности». Вельяминов подчеркивал, что лечение хирургического туберкулеза вообще, а костей и суставов в частности, преследует 2 цели: лечение всего организма и местного проявления болезни. Он настаивал на сугубо индивидуальном подходе к больному.
В 1904 году он докладывает хирургической секции IX Пироговского съезда о блестящих результатах лечения в первом русском приморском санатории и приходит к твердому убеждению, что «факты стоят на стороне приморских санаториев». В 1912 году Н.А.Вельяминов выступает с докладом на Международном конгрессе по бугорчатке в Риме.
Таким образом, изучение туберкулеза в Петербурге велось весьма интенсивно и в конце XIX века, и в начале XX.
Хирургических процедур — Искусственный пневмоторакс
Туберкулез легких на сегодняшний день является наиболее частым проявлением туберкулеза, зафиксированным во всех записях Стэннингтона. До разработки и использования любых эффективных средств лечения антибиотиками наиболее распространенной формой вмешательства была индукция искусственного пневмоторакса. Многие из различных методов лечения, применяемых в то время для лечения туберкулеза всех типов, основывались на принципах отдыха и изоляции пораженной области, и подход к искусственному пневмотораксу не отличался.
Через грудную стенку вводится игла, позволяющая ввести воздух в плевральную полость. Количество вводимого воздуха будет зависеть от размера пациента, а также от того, сколько лечащий врач может реально справиться с этим за один раз, и насколько быстро они хотели, чтобы легкое коллапсировало. После введения давление воздуха заставит легкое сжаться само и перестать функционировать должным образом. Необязательно, чтобы все легкое разрушилось сразу, либо потому, что это не было необходимо для лечения, либо потому, что фиброзные спайки между легким и грудной стенкой в результате заболевания не позволили этому сделать это.Там, где поражена только часть легкого, нежелательно коллапсировать все легкое, и в таких случаях может случиться коллапс только одной доли. Возможен также двусторонний искусственный пневмоторакс, при котором часть обоих легких разрушается одновременно. Состояние коллапса могло сохраняться в течение месяцев или даже лет, и для этого пациенту требовалось регулярно дозаправляться воздухом.
Большое количество рентгенографических иллюстраций развития коллапса доступно в коллекции Станнингтона.У одного пациента, 2/1946, в течение двух лет было сделано большое количество рентгенограмм, которые демонстрируют изменения в легком после поступления и через прогрессирующие стадии коллапса легкого.
Пациентка 2/1946 была женщиной в возрасте 15 лет, когда она была госпитализирована в Станнингтон 21 июня 1945 года с легочным туберкулезом 3 стадии, после чего ее мокрота также оказалась положительной на туберкулез. Отчет о рентгеновском исследовании перед поступлением:
.
«В правом легком видно несколько активных очагов, которые начинают сливаться.Обширная инфильтрация в верхней зоне и подозрительные пятна в средней зоне. Небольшое кальцинированное помутнение в правой нижней зоне. Левое легкое показывает инфильтрацию в средней зоне. Верхняя зона и вершина четкие. Ранние активные очаги заметны в обоих легких на пораженных участках ».
Рис. 1 был первым рентгеновским снимком, сделанным после госпитализации 25 июня 1945 г., на три недели позже, чем тот, о котором сообщалось выше. Наблюдения на этой рентгеновской заметке:
«Рассеянные очаги в правой верхней зоне.Одна определенная полость. Повышенная маркировка бронхов на обоих основаниях. ’
Рисунок 1 — HOSP / STAN / 7/1/2 / 1057_22
25 июня 1945 г. Рисунок 2 — HOSP / STAN / 7/1/2 / 1057_18
31 августа 1945 г.
Было быстро решено, что искусственный пневмоторакс следует индуцировать на правой стороне, и это произошло 16 августа 1945 года.Рисунок 2, сделанный позже в том же месяце, показывает первые результаты искусственного пневмоторакса. Черная область вдоль боковой стороны правого легкого свидетельствует о том, что воздух был введен и легкое начало сжиматься.
Коллапс продолжался вплоть до 1947 года, и в течение этого периода ей приходилось подливать воздух каждые две недели. В течение первых трех месяцев она получала 200-300 куб.На рисунках 3-6 показано развитие искусственного пневмоторакса по мере того, как вводится больше воздуха, и легкое продолжает коллапсировать. Со временем мы видим, что полость в правой средней зоне схлопывается и закрывается, что является одной из основных целей лечения. В начале июня 1946 года была проведена операция по разделению спаек между легким и грудной стенкой, что позволило коллапсу развиваться дальше. Она была выписана в июне 1947 года, ее состояние улучшилось.
Рисунок 3 — HOSP / STAN / 7/1/2 / 1057_23
17 января 1946 г. Рисунок 4 — HOSP / STAN / 7/1/2 / 1057_09
18 июня 1946 г.
Рисунок 5 — HOSP / STAN / 7/1/2 / 1057_10
2 сентября 1946 г. Рисунок 6 — HOSP / STAN / 7/1/2 / 1057_27
15 апреля 1947 г.
Произошла ошибка при настройке вашего пользовательского файла cookie
Произошла ошибка при настройке вашего пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности.Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г.,
браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере. - Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie
потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт
не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к
остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Характеристика не связанной с искусственным пневмотораксом лимфомы, связанной с пиотораксом
Лимфома, связанная с пиотораксом (PAL), — редкое заболевание, развивающееся в результате длительного воспаления плевральной полости. Большинство зарегистрированных случаев PAL имеют в анамнезе искусственный пневмоторакс. Однако клинические особенности искусственного пневмоторакса, не связанного с ПАЛ, остаются в значительной степени неизвестными. Здесь мы сообщили о двух случаях PAL, диагностированных в нашем центре за последние десять лет. Один случай развился от бессимптомного пиоторакса после пневмонэктомии с латентным периодом 28 лет, в то время как другой случай показал относительно короткий латентный период в один год.Затем мы изучили литературу по PAL, не связанному с искусственным пневмотораксом, выполнив поиск в PubMed и Google Scholar за 2007 год. Всего было обнаружено девять случаев PAL, не связанных с искусственным пневмотораксом, преимущественно у пожилых мужчин со средним возрастом 76 лет (от 51 до 88). . В большинстве случаев была диагностирована диффузная крупноклеточная B-клеточная лимфома (DLBCL) ( n, = 8, 88,9%), и имелись доказательства инфекции вируса Эпштейна-Барра (EBV) ( n = 6, 66,7%) или туберкулезного плеврита ( n = 5, 55.6%). Примечательно, что четыре случая (44,4%) имели короткие интервалы (не более двух лет) между плевритом и PAL. Что касается общей выживаемости, одна треть случаев выжила более чем через 5 лет после постановки диагноза PAL. В заключение следует отметить, что признаки искусственного пневмоторакса, не связанного с PAL, сравнимы с классическим типом PAL, за исключением некоторых пациентов с непродолжительным плевритом, и их необходимо идентифицировать. Рекомендации по лечению DLBCL рекомендуются для управления PAL.
1. Введение
Пиоторакс-ассоциированная лимфома (PAL) — это редкий, но особый тип неходжкинской лимфомы [1–4].Диагноз PAL может быть установлен после того, как клетки лимфомы были обнаружены в давно воспалительной плевральной полости, такой как хронический пиоторакс [4–6]. В недавней классификации ВОЗ PAL определяется как прототип диффузной крупноклеточной B-клеточной лимфомы, связанной с хроническим воспалением (DLBCL-CI), что свидетельствует о тесной связи с инфекцией вируса Эпштейна-Барра (EBV) [7–11]. Большинство случаев PAL относится к B-клеточному происхождению, в то время как другие демонстрируют T-клеточный или двойной иммунофенотип B- и T-клеток [12–14]. В 1987 г. японские исследователи впервые сообщили о трех случаях В-клеточной лимфомы плевры, имевших в анамнезе искусственный пневмоторакс для лечения туберкулезного плеврита [15].С тех пор было опубликовано несколько случаев PAL в Японии, но мало случаев из других азиатских или западных стран [2–4, 14]. Заболеваемость PAL, вероятно, недооценивается, особенно в регионах, где высока распространенность легочного туберкулеза или инфекции EBV.
Однако искусственный пневмоторакс вышел из употребления из-за заметного прогресса в борьбе с туберкулезом во всем мире [16]. В последнее время в некоторых случаях PAL наблюдается относительно короткий промежуток времени между плевритом и PAL, а не очень длинный интервал, который обычно наблюдался в прошлом [17–20].Учитывая чрезвычайно низкую частоту этого заболевания, клинические характеристики и лечение искусственного пневмоторакса, не связанного с БАЛ, остаются в значительной степени неизвестными.
В настоящем исследовании мы сначала сообщили о двух случаях PAL из нашего центра, а затем обобщили литературу о случаях PAL без искусственного пневмоторакса в анамнезе. Обсуждались этиология, клинические особенности, дифференциальный диагноз и терапевтические возможности PAL. Мы также предоставили некоторые клинические рекомендации для клинической практики PAL.
2. Пациенты и методы
2.1. Диагностические критерии PAL
PAL был определен как лимфома, развивающаяся в плевральной полости с хроническим воспалением [9]. Диагноз PAL был установлен путем патологического исследования образцов биопсии, полученных из поражений в плевральной полости, как и в предыдущих сообщениях [3, 4].
2.2. Отбор пациентов и обзор медицинских записей
Мы рассмотрели четыре возможных случая PAL, выполнив поиск в библиотеке образцов патологоанатомов отделения патологии Шанхайского онкологического центра Фуданьского университета (FUSCC) с 2010 по 2019 год.После тщательного изучения истории болезни два пациента соответствовали диагностическим критериям PAL и оба лечились в отделении медицинской онкологии FUSCC. Клинические, лабораторные и патологические данные были собраны из институциональной системы электронных медицинских карт. Поскольку существует два ретроспективных исследования [3, 4], которые уже полностью изучали клинико-патологические особенности БЛА, связанного с искусственным пневмотораксом, до 2007 г. с большой группой пациентов, мы сосредоточились на случаях БАЛ, не связанного с искусственным пневмотораксом, с 2007 г. по настоящее время.Семь случаев PAL без искусственного пневмоторакса или терапии коллапса в анамнезе были получены через PubMed и Google Scholar путем поиска по ключевым словам, включая пиоторакс, плевральную лимфому, туберкулез, вирус Эпштейна-Барра и / или ритуксимаб. Клинические характеристики семи опубликованных PAL и двух случаев из настоящего исследования были обобщены в таблице 1. Международный прогностический индекс (IPI) оценивался, как описано ранее [23]. Инфекция EBV была определена как обнаруживаемая ДНК EBV или положительные антитела в сыворотке, или как кодируемая EBV малая РНК- (EBER-) 1/2 в опухолевых клетках [24].
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Примечание. n.a .: не доступен .; ЛТ: лучевая терапия; DCBCL: диффузная В-крупноклеточная лимфома; EBV: вирус Эпштейна-Барра; лет: лет; КТ: химиотерапия; и GCB: зародышевый центр, подобный В-клеткам. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
3. Результаты
3.1. Два отчета о болезни PAL
Пациент 1 был 51-летним мужчиной, у которого в течение одного месяца в феврале 2019 года в анамнезе были лихорадка, ночная потливость, боль и опухоль в левой верхней части грудной клетки.Он ранее перенес левую пневмонэктомию по поводу эмфизематозных булл в возрасте 23 лет. Компьютерная томография (КТ) перед поступлением показала резекцию левого легкого, компенсаторную гиперинфляцию правого легкого и образование на левой грудной стенке. Позитронно-эмиссионная томография (ПЭТ) показала повышенное накопление фтордезоксиглюкозы (ФДГ) в левой грудной стенке и левом подмышечном и грудном лимфатическом узле аорты (рис. 1 (а)). В марте 2019 года пациент был переведен в нашу больницу. Иммуногистохимия внутригрудной биопсии показала, что опухолевые клетки были положительными по CD20, CD30, c-Myc, BCL-2, Mum-1 и PD-L1, но отрицательными по CD3, CD5, CD10, BCL-6, PD-1 и циклин D1, соответствующий патологическому диагнозу диффузной крупноклеточной В-клеточной лимфомы (DLBCL) (рис. 2 (а)).Индекс Ki-67 опухолевых клеток был высоким (80–90%). Гибридизация in situ с использованием зонда EBER-1 действительно выявила положительные сигналы в ядре опухолевых клеток. Титр EBV в сыворотке крови составил 27200 копий / мл. Уровень сывороточной лактатдегидрогеназы (ЛДГ) составлял 604 Ед / л. Таким образом, был установлен диагноз DLBCL, ассоциированного с пиотораксом II стадии, с двумя баллами по шкале IPI. Однако после одного цикла химиотерапии R-CHOP-21 (ритуксимаб, циклофосфамид, доксорубицин, винкристин и преднизолон 21-дневного цикла) наблюдалось несколько тяжелых побочных эффектов (степень IV, фебрильная нейтропения и тромбоцитопения), и После второго цикла R-CHOP и далее потребовалось снижение доз химиотерапии на 20%.ПЭТ-КТ показала частичный метаболический ответ после 6 циклов лечения (рис. 1 (b)) с кистозным образованием на левой грудной стенке. Из кистозной массы аспирировали 200 мл коричневой жидкости с количеством лейкоцитов 10823/ мк л, количеством тромбоцитов 30000/ мк мкл, ЛДГ 2106 МЕ / л и несколькими атипичными клетками и фагоцитарными клетками. Титр EBV в сыворотке снизился до 3050 копий / мл. После многопрофильного обсуждения он получил лучевую терапию с общей дозой 39,6 Гр за 23 фракции на локальный участок опухоли левой груди в конце февраля 2020 года.Однако после лучевой терапии на груди осталось пальпируемое кистозное уплотнение.
Пациент 2, 57-летний мужчина, обратился в нашу больницу с историей боли в левой груди, лихорадки и ночного потоотделения в течение 1 месяца в июле 2010 года. Ранее ему был поставлен диагноз: пиоторакс и легочная болезнь. tuberculosis один и два года назад соответственно. Он также подвергся воздействию ядерной радиации во время службы в армии в возрасте 27 лет. ПЭТ-КТ перед госпитализацией показали множественные узелки с высоким уровнем поглощения ФДГ в двусторонней плевре.КТ грудной клетки после поступления выявила тень в левой нижней доле и заднем средостении, включая грудную стенку и плевру, с правым плевральным выпотом, ателектазом и увеличенными лимфатическими узлами (рис. 1 (c)). Иммуногистохимический анализ образцов биопсии левой плевры предположил DLBCL (рис. 2 (b)), где опухолевые клетки были положительными на CD20, PAX5 и BCL-2, но отрицательными на CD10, BCL-6, Mum-1 и LMP-1. . Скорость распространения (индекс Ki-67) была высокой (80–90%). Уровень сывороточного ЛДГ в норме.Окончательный диагноз был поставлен как связанный с пиотораксом DLBCL IV стадии с двумя баллами по шкале IPI. В августе 2010 года был начат курс лечения R-CEOP-21 (ритуксимаб, циклофосфамид, эпирубицин, винкристин и преднизолон 21-дневного цикла). Полный ответ был достигнут после четырех курсов химиотерапии (рис. 1 (d)). Однако пациент не хотел продолжать иммунохимиотерапию и вместо этого перешел на традиционную китайскую медицину. В июле 2012 года КТ грудной клетки показала множественные новые поражения в правом легком и плевральной полости, что подтверждает диагноз рецидива DLBCL.Пациент получил режим R-ESHAP (ритуксимаб, этопозид, метилпреднизолон, цитарабин и цисплатин) в качестве терапии спасения со снижением доз на 75%. Несмотря на то, что после трех циклов болезнь снова достигла полной ремиссии, пациент не имел права на трансплантацию стволовых клеток из-за сердечной дисфункции. Однако в январе 2014 года болезнь снова прогрессировала. В качестве лечения третьей линии был выбран режим R-GemOx (ритуксимаб, гемцитабин и оксалиплатин). Полный ответ наблюдался в конце четырех курсов химиотерапии.При следующем начале прогрессирования заболевания (рис. 1 (e)) мы назначили схему R2 (ритуксимаб и леналидомид) в качестве лечения четвертой линии. К сожалению, в мае 2016 г. во время поддерживающего лечения леналидомидом пациент умер от внезапного сердечного приступа.
3.2. Клинические характеристики не связанного с искусственным пневмотораксом PAL
Для дальнейшего изучения клинических особенностей PAL, не связанного с искусственным пневмотораксом, мы рассмотрели семь случаев PAL, выбранных из опубликованных статей (рис. 3).Результаты объединенного анализа девяти случаев PAL (включая два случая из нашего центра) показаны в таблице 1. Было семь мужчин и две женщины, а средний возраст составлял 76 лет (диапазон: 51–88). Пять пациентов (55,6%) имели в анамнезе туберкулез легких. Средний интервал между диагнозом плеврит и PAL составлял 27 лет (диапазон: 0–33). Интересно, что четыре случая (44,4%) имели короткие интервалы (менее или равные двум годам). Большинство пациентов ( n = 8, 88,9%) демонстрировали типичный гистологический иммунофенотип DLBCL, за исключением одного случая с двойным положительным результатом на CD3 и CD20 в рецидивирующем поражении.Шесть пациентов (66,7%) имели признаки ВЭБ-инфекции. Кроме того, в шести случаях были приняты предварительные схемы химиотерапии на основе CHOP, в четырех из которых был использован дополнительный ритуксимаб. Что касается выживаемости, одна треть случаев выжила более чем через 5 лет после первоначального диагноза PAL.
4. Обсуждение
В текущем исследовании мы представили два случая PAL вместе с семью опубликованными случаями из литературы, которые не были связаны с искусственным пневмотораксом. Семь из девяти пациентов были мужчинами, а средний возраст составлял 76 лет.У большинства пациентов (8/9) был диагностирован DLBCL. Туберкулез остается наиболее частым предрасполагающим фактором для PAL, причем 55,6% случаев здесь связаны с туберкулезом. Кроме того, PAL может развиться из любого типа эмпиемы, включая посттравматическую эмпиему [8], неспецифический плеврит [22] и пневмонэктомию [20, 25].
Клинические особенности случаев PAL в этом исследовании были сравнимы с PAL, связанным с искусственным пневмотораксом, за исключением некоторых случаев с относительно коротким анамнезом плеврита.Продолжительность интервала между искусственным пневмотораксом или плевритом и PAL обычно составляет несколько десятков лет [3, 4]. Пять пациентов в этом исследовании имели типичную длительную продолжительность от пиоторакса до БАЛ, в среднем 30 лет, в то время как у других четырех пациентов были короткие интервалы менее двух лет. Механизм подострого начала БАЛА неизвестен. Для исходной клетки, как определено алгоритмом Ханса, подтип, подобный В-клеткам негерминального центра (не GCB), более распространен в PAL с подтипом DLBCL, который поддерживался двумя настоящими случаями и описанным случаем. Автор Wang et al.[19]. Кроме того, с помощью количественного анализа полимеразной цепной реакции (ПЦР) PAL показали повышенную экспрессию активированных B-клеточных сигнатурных генов [26]. Кроме того, секвенирование гена вариабельной тяжелой цепи иммуноглобулина ( IgV H ) в клеточных линиях и клинических образцах показало, что клетки PAL происходят из В-клеток пост зародышевого центра [27].
Было высказано предположение, что инфекция EBV может способствовать развитию PAL [3]. Фактически, как и другие, мы обнаружили, что около 70% случаев PAL, не связанных с искусственным пневмотораксом, имеют доказательства EBV-инфекции [3].Однако механизмы, лежащие в основе, которые приводят хроническое воспаление в явное состояние, все еще остаются неуловимыми. Что касается геномных ландшафтов, повторяющиеся TP53 , мутации телеангиэктазии Ataxia (ATM) и RAD3-связанные (ATR) мутации вместе с инактивацией p16 INK4a / Rb могут вызвать нестабильность генома и, наконец, привести к нестабильности генома. до злокачественной трансформации [28, 29]. Кроме того, амплификация MYC произошла в 80% случаев PAL [30], что указывает на то, что PAL является рефрактерным заболеванием.Более того, иммуносупрессивное микроокружение опухоли с тоннами интерлейкина 6 (IL-6), IL-10, микроРНК, кодируемых EBV, и хемокинового рецептора 4 с мотивом CC (CCR-4) + регуляторных Т-клеток (Treg) может способствовать лимфоме. выживаемость клеток у иммунокомпетентных лиц [10, 31]. Интересно, что вирус EB может индуцировать высокий уровень экспрессии лиганда 1 запрограммированной гибели клеток 1 (PD-L1) в клетках лимфомы B, что также может быть связано с иммуносупрессией опухоли по оси PD-1 / PD-L1 [24]. Важно отметить, что туберкулез [32] и другие хронические воспалительные заболевания [33] могут вызывать воспаление хелперных клеток T (Th) 17 и Th2 и низкий ответ антиген-специфичных Т-клеток в легочном и лимфоидном компартментах.Тем не менее, механизм EBV-отрицательного PAL остается неясным.
Дифференциальный диагноз необходимо проводить между PAL и первичной выпотной лимфомой (PEL), потому что оба проявляются плевральным выпотом [6, 34]. PAL обычно проявляется относительно локализованной опухолевой массой, в то время как у пациентов с PEL обычно наблюдается выпот при отсутствии лимфаденопатии или органегалии. PEL обычно поражает людей с ослабленным иммунитетом, инфицированных вирусом иммунодефицита человека (ВИЧ), в то время как PAL — нет [35].Кроме того, вирус герпеса человека типа 8 (HHV-8) обычно положителен на PEL, но отрицателен на PAL. Однако коинфекция EBV и HHV-8 наблюдалась и в случаях PAL [36, 37], что указывает на возможные патогенные связи между PAL и PEL [38]. Ограничением этого исследования является отсутствие тестирования на HHV-8 в двух случаях из нашего центра, хотя клинические и патологические особенности подтверждали диагноз PAL.
Из-за ограниченного числа изученных случаев и отсутствия рандомизированных клинических испытаний оптимальные терапевтические стратегии для PAL остаются в значительной степени нераскрытыми, а рекомендации текущих руководств в первую очередь зависят от лечения DLBCL.Иммунохимиотерапия, включающая ритуксимаб и схему на основе CHOP, рекомендуется для лечения первой линии PAL. Учитывая преклонный возраст и плохую работоспособность большинства пациентов, обычно требуется снижение дозы, что может еще больше повлиять на эффективность лечения. Кроме того, ВЭБ-положительный PAL показал меньшую лекарственную реакцию и более неблагоприятные исходы [39]. Для пациентов с рецидивом или рефрактерным PAL рекомендуется агрессивная химиотерапия спасения с последующей трансплантацией аутологичных стволовых клеток; однако это может не подходить для пожилых или слабых пациентов.Таким образом, тогда можно рассмотреть менее агрессивные схемы, например, GDP (гемцитабин, дексаметазон и цисплатин) плюс ритуксимаб. Кроме того, леналидомид утвержден как эффективный и толерантный вариант лечения, особенно для DLBCL В-клеток с негерминальным центром (не GCB), поскольку он действует как иммуномодуляторы [40, 41]. Леналидомид в сочетании с ритуксимабом (R2) показал синергетический эффект с 28–41,2% общей частотой ответа (ЧОО) при R / R DLBCL [42].
В рандомизированном исследовании фазы II, сравнивающем полатузумаб ведотин (Pola) [43], конъюгат анти-CD79b-антитело и лекарственное средство, в комбинации с бендамустином (B) и ритуксимабом (R) по сравнению с BR для R / R DLBCL, общие показатели ответа были 45% и 17.5%, а процент полных ответов — 40% и 15% соответственно. Средняя общая выживаемость составила 11,8 месяцев в группе Pola-BR и 4,7 месяца в группе BR. Профиль токсичности Pola-BR был приемлемым. Таким образом, режим Pola-BR был одобрен FDA для лечения R / R DLBCL после как минимум двух предшествующих терапий. Эффективность ингибиторов иммунных контрольных точек, моноклональных антител против PD-1 или PD-L1, также оценивалась для DLBCL. Из-за низкой экспрессии PD-L1 в опухолевых клетках DLBCL лечение ниволумабом [44] (моноклональное антитело против PD-1) приводило только к 10% ответу на R / R DLBCL.Тем не менее, ингибиторы иммунных контрольных точек [45] могут быть многообещающим подходом для EBV-положительного DLBCL, а также для PAL.
5. Выводы
В заключение, результаты этого исследования показывают, что клинические характеристики пациентов с PAL сопоставимы с PAL, связанным с искусственным пневмотораксом, и длительный хронический пиоторакс, сопровождающийся EBV-инфекцией, способствует развитию PAL. Этиология PAL с непродолжительным плевритом неизвестна, поэтому необходимы дополнительные исследования.Необходимо уделять внимание точному диагнозу этой редкой лимфомы, и необходимо приложить усилия для изучения более эффективных и хорошо переносимых терапевтических режимов, таких как ингибиторы иммунных контрольных точек и химерный антигенный рецептор T (CAR-T) клетка. терапия.
5.1. Клинические рекомендации
(i) Диагноз пиоторакс-ассоциированной лимфомы (PAL) следует рассматривать, когда лимфома развивается в плевральной полости по результатам визуализации (например, внелегочные плевральные образования), обнаруживаемым новообразованиям и / или лимфаденопатии по результатам физикального обследования, и одному или другие из следующих симптомов: боль в груди и / или спине, лихорадка, ночная потливость или продуктивный кашель. (ii) Пациенты с PAL должны быть обследованы на наличие сопутствующих воспалительных состояний, таких как искусственный пневмоторакс, туберкулез или туберкулезный плеврит, посттравматическая эмпиема, пневмонэктомия и неспецифический плеврит (iii) CD30, лиганд 1 запрограммированной гибели клеток 1 (PD-L1), вирус Эпштейна-Барра (EBV), нагрузка ДНК EBV и вирус герпеса человека 8 типа (HHV-8) (срез крови или парафина) ) следует тестировать у пациентов с клиническим диагнозом PAL (iv) Иммунохимиотерапия, содержащая ритуксимаб, рекомендуется для лечения первой линии CD20-положительного PAL (v) Лучевая терапия должна быть назначена пациентам с PAL для остаточной опухоли после химиотерапии первой линии (vi) Ингибиторы иммунных контрольных точек, иммуномодуляторы или химерные антигенные рецепторы T (CAR-T) клеточная терапия может быть рассмотрена для пациентов с рецидивом или рефрактерным PAL
Доступность данных
Данные совместное использование не применимо к этой статье, так как никакие наборы данных не были созданы или проанализированы в ходе текущего исследования.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Благодарности
Авторы благодарят доктора Фанг-Тянь Ву за языковое редактирование рукописи и доктора Сяо-Ханг Лю за его поддержку в сборе изображений. Это исследование было поддержано грантом Национального фонда естественных наук Китая (№ 81802362) и Главного национального проекта науки и технологий (№ 2017ZX09304021).
Что такое ятрогенный пневмоторакс?
Автор
Брайан Дж. Дейли, MD, MBA, FACS, FCCP, CNSC Профессор и программный директор, Департамент хирургии, руководитель, Отделение травм и критических состояний, Медицинский научный центр Университета Теннесси, Медицинский колледж
Брайан Дж. Дейли, доктор медицинских наук , MBA, FACS, FCCP, CNSC является членом следующих медицинских обществ: Американская ассоциация хирургии травм, Восточная ассоциация хирургии травм, Южная хирургическая ассоциация, Американский колледж грудных врачей, Американский колледж хирургов, American Medical Ассоциация, Ассоциация академической хирургии, Ассоциация хирургического образования, Шоковое общество, Общество реаниматологии, Юго-Восточный хирургический конгресс, Медицинская ассоциация Теннесси
Раскрытие: Ничего не раскрывать.
Соавтор (ы)
Шабир Бхимджи, доктор медицины, доктор медицины Кардиоторакальный и сосудистый хирург, Больницы Саудовской Аравии и Ближнего Востока
Шабир Бхимджи, доктор медицины, доктор философии является членом следующих медицинских обществ: Американское онкологическое общество, Американский колледж грудных врачей, Американская ассоциация легких , Техасская медицинская ассоциация
Раскрытие информации: раскрывать нечего.
Ребекка Баском, доктор медицины, магистр здравоохранения Профессор медицины, отделение медицины, отделение легочной медицины, аллергии и реанимации, Медицинский колледж штата Пенсильвания, Медицинский центр Милтона С. Херши; Выпускник факультета Медицинского колледжа Государственного университета Пенсильвании и Института естественных наук им. Хака
Ребекка Баском, доктор медицины, магистр здравоохранения, является членом следующих медицинских обществ: Американское торакальное общество
Раскрытие информации: не подлежит разглашению.
Майкл Дж. Беннингхофф, DO, MS Лечащий врач отделения легочной медицины и реанимации, Медицинский центр Кристиана
Майкл Дж. Беннингхофф, DO, MS является членом следующих медицинских обществ: Американский колледж грудных врачей, Американский колледж врачей , Американская остеопатическая ассоциация, Американское торакальное общество, Общество интенсивной терапии
Раскрытие: Ничего не раскрывать.
Шоаиб Алам, доктор медицины Штатный врач отделения легочной и сосудистой медицины, Национальный институт сердца, легких и крови, Национальные институты здравоохранения
Шоаиб Алам, доктор медицины, является членом следующих медицинских обществ: Американского колледжа грудных врачей, США Торакальное общество, Общество интенсивной терапии, Международное общество магнитного резонанса в медицине, Европейское респираторное общество, Торакальное общество Пенсильвании
Раскрытие: Ничего не раскрывать.
Главный редактор
Мэри С. Манчини, доктор медицины, доктор медицинских наук, MMM Главный хирург и директор кардиоторакальной хирургии, Кристус Хайленд
Мэри К. Манчини, доктор медицинских наук, доктор медицинских наук, MMM является членом следующих медицинских обществ: Американской ассоциации торакальной хирургии , Американский колледж хирургов, Американская хирургическая ассоциация, Фи Бета Каппа, Общество торакальных хирургов
Раскрытие информации: нечего раскрывать.
Благодарности
Эрик Д. Бартон, доктор медицины, MS Заместитель директора, доцент, кафедра хирургии, отделение неотложной медицины, Центр медицинских наук Университета Юты
Эрик Д Бартон, доктор медицины, магистр медицины, является членом следующих медицинских обществ: Американского колледжа врачей скорой помощи, Американского колледжа спортивной медицины, Американской медицинской ассоциации и Общества академической неотложной медицины
Раскрытие: Ничего не раскрывать.
Марк Д. Бассон, доктор медицины, доктор философии, магистр делового администрирования, FACS Профессор, заведующий кафедрой хирургии, заместитель декана по развитию исследовательского факультета, Колледж медицины человека Мичиганского государственного университета
Марк Д. Бассон, доктор медицины, доктор философии, магистр делового администрирования, FACS является членом следующих медицинских обществ: Alpha Omega Alpha, Американского колледжа хирургов, Американской гастроэнтерологической ассоциации, Phi Beta Kappa и Sigma Xi
.
Раскрытие: Ничего не раскрывать.
H Скотт Бьерке, доктор медицины, FACS Доцент кафедры хирургии Медицинской школы Университета Миссури в Канзас-Сити; Медицинский директор травматологической службы Исследовательского медицинского центра; Клинический профессор кафедры хирургии Университета медицины и биологических наук Канзас-Сити
H Скотт Бьерке, доктор медицины, FACS является членом следующих медицинских обществ: Американской ассоциации истории медицины, Американской ассоциации хирургии травм, Американского колледжа хирургов, Ассоциации академической хирургии, Восточной ассоциации хирургии травм. , Хирургическая ассоциация Среднего Запада, Национальная ассоциация врачей скорой медицинской помощи, Пан-Тихоокеанская хирургическая ассоциация, Королевское медицинское общество, Юго-западный хирургический конгресс и Медицинское общество дикой природы
Раскрытие: Ничего не раскрывать.
Пол Блэкберн, DO, FACOEP, FACEP Лечащий врач, отделение неотложной медицины, Медицинский центр Марикопа
Пол Блэкберн, DO, FACOEP, FACEP является членом следующих медицинских обществ: Американского колледжа врачей неотложной помощи, Американского колледжа врачей неотложной помощи остеопатии, Американской медицинской ассоциации и Медицинской ассоциации Аризоны
Раскрытие: Ничего не раскрывать.
Джеффри Гленн Боуман, доктор медицины, MS Консультант, Highfield MRI
Раскрытие: Ничего не раскрывать.
Эндрю К. Чанг, доктор медицины Доцент кафедры неотложной медицины, Медицинский колледж Альберта Эйнштейна, Медицинский центр Монтефиоре
Эндрю К. Чанг, доктор медицины, является членом следующих медицинских обществ: Американской академии неотложной медицины, Американской академии неврологии, Американского колледжа врачей неотложной помощи и Общества академической неотложной медицины
Раскрытие: Ничего не раскрывать.
Джон Гейбель, доктор медицинских наук, магистр медицины Заместитель председателя и профессор отделения хирургии отделения желудочно-кишечной медицины и отделения клеточной и молекулярной физиологии Медицинской школы Йельского университета; Директор хирургического отделения хирургического отделения больницы Йель-Нью-Хейвен
Джон Гейбель, доктор медицинских наук, магистр медицины, является членом следующих медицинских обществ: Американской гастроэнтерологической ассоциации, Американского физиологического общества, Американского общества нефрологов, Ассоциации академической хирургии, Международного общества нефрологов, Нью-Йоркской академии наук и Общества исследователей. Хирургия пищеварительного тракта
Раскрытие информации: AMGEN Royalty Consulting; Членство в Совете по интересам ARdelyx
Tunc Iyriboz, MD Начальник отдела управления клиническими изображениями, доцент кафедры радиологии, Медицинский центр Херши, Государственный университет Пенсильвании
Tunc Iyriboz, MD является членом следующих медицинских обществ: Американского колледжа радиологии, Американской медицинской ассоциации и Радиологического общества Северной Америки
Раскрытие: Ничего не раскрывать.
Сима Джайн Медицинский колледж Государственного университета Пенсильвании
Раскрытие: Ничего не раскрывать.
Рик Кулкарни, MD Лечащий врач, Отделение неотложной медицины, Кембриджский альянс здравоохранения, Отделение неотложной медицины, Гарвардская медицинская школа
Рик Кулкарни, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha, Американская академия неотложной медицины, Американский колледж врачей неотложной помощи, Американская медицинская ассоциация, Американская ассоциация медицинской информатики, Phi Beta Kappa и Общество академической неотложной медицины
.
Раскрытие информации: WebMD Salary Employment
Эрик Л. Легом, доктор медицины Начальник отделения неотложной медицины, Больничный центр округа Кингс; Доцент кафедры неотложной медицины Нью-Йоркского медицинского колледжа
Эрик Л. Легом, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha, Американской академии неотложной медицины, Американского колледжа врачей неотложной помощи, Совета директоров ординатуры неотложной медицины и Общества академической неотложной медицины
Раскрытие: Ничего не раскрывать.
Пинаки Мукхерджи, доктор медицины Доцент, лечащий врач, отделение неотложной медицины, Медицинский центр Монтефиоре
Пинаки Мукхерджи, доктор медицины, является членом следующих медицинских обществ: Американский колледж врачей скорой помощи
Раскрытие: Ничего не раскрывать.
Роберт О’Коннор, доктор медицины, магистр здравоохранения Профессор и заведующий кафедрой неотложной медицины, Система здравоохранения Университета Вирджинии
Роберт О’Коннор, доктор медицины, магистр здравоохранения, является членом следующих медицинских обществ: Американской академии неотложной медицины, Американского колледжа врачей неотложной помощи, Американского колледжа врачей, Американской кардиологической ассоциации, Американской медицинской ассоциации, Медицинского общества штата Делавэр, Национальная ассоциация врачей скорой медицинской помощи, Общество академической неотложной медицины и Общество медицины дикой природы
Раскрытие: Ничего не раскрывать.
Бенсон Б. Роу, доктор медицины Почетный руководитель отделения кардиоторакальной хирургии, почетный профессор отделения хирургии Медицинского центра Калифорнийского университета в Сан-Франциско
Бенсон Б. Роу, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha, Американская ассоциация торакальной хирургии, Американский колледж кардиологии, Американский колледж хирургов, Американская кардиологическая ассоциация, Американская медицинская ассоциация, Американское общество искусственных внутренних органов, Американская хирургическая ассоциация, Калифорнийская медицинская ассоциация, Общество сосудистой хирургии, Общество торакальных хирургов и Общество университетских хирургов
Раскрытие: Ничего не раскрывать.
Джозеф А. Саломон III, доктор медицины Адъюнкт-профессор и обслуживающий персонал, Медицинские центры Трумэна, Медицинская школа Университета Миссури в Канзас-Сити; Медицинский директор EMS, Канзас-Сити, Миссури,
Джозеф А. Саломон III, доктор медицины, является членом следующих медицинских обществ: Американской академии неотложной медицины, Национальной ассоциации врачей скорой помощи и Общества академической неотложной медицины
Раскрытие: Ничего не раскрывать.
Daniel S. Schwartz, MD, FACS Ассистент клинического профессора кардиоторакальной хирургии, Медицинская школа Mount Sinai; Заведующий отделением торакальной хирургии больницы Хантингтон
Дэниел С. Шварц, доктор медицины, FACS является членом следующих медицинских обществ: Американского колледжа грудных врачей, Американского колледжа хирургов, Общества торакальных хирургов и Западной ассоциации торакальных хирургов
.
Раскрытие: Ничего не раскрывать.
Роберт Л. Шеридан, доктор медицины Заместитель начальника штаба, начальник ожоговой хирургии, Больница Шрайнерс Бернс; Доцент кафедры хирургии отделения травм и ожогов Массачусетской больницы общего профиля и Гарвардской медицинской школы
Роберт Л. Шеридан, доктор медицины, является членом следующих медицинских обществ: Американской академии педиатрии, Американской ассоциации хирургии травм, Американской ожоговой ассоциации и Американского колледжа хирургов
.
Раскрытие: Ничего не раскрывать.
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: Medscape Salary Employment
Милош Тукакович, доктор медицины Научный сотрудник, Отделение внутренней медицины, Отделения болезней легких, Аллергии и реанимации, Медицинский центр Милтона С. Херши, Государственный медицинский колледж Пенсильвании,
Милош Тукакович, доктор медицины, является членом следующих медицинских обществ: Американского колледжа врачей и Американской медицинской ассоциации
.
Раскрытие: Ничего не раскрывать.
Прикладные науки | Бесплатный полнотекстовый | Физическое лекарство от туберкулеза: Карло Форланини и изобретение терапевтического пневмоторакса
1. Annus Mirabilis
Иногда кажется, что в определенные моменты истории сходятся, определяя радикальные изменения в научной мысли и практике. 1882 год, несомненно, был одним из таких в истории инфекционных болезней. 24 марта того же года Роберт Кох объявил о выделении и идентификации Mycobacterium tuberculosis как возбудителя туберкулеза.Заседание Берлинского физиологического общества, в ходе которого немецкий врач сделал доклад об открытии этого нового микроорганизма, было одним из самых драматических моментов в истории медицины: наконец, неуловимость одного из главных Бичи -х годов нашли единственное этиологическое объяснение. Пауль Эрлих (которому в 1908 году будет присуждена Нобелевская премия по медицине), присутствовавший на конференции, всегда вспоминал тот вечер как «самый важный научный опыт в моей жизни» [1].Против всех тех, кто все еще отрицал заразную природу туберкулеза, ссылаясь на конституциональные, дегенеративные, пищевые или токсические объяснения, Кох выдвинул свои неопровержимые доказательства. Когда через несколько недель работа была опубликована, она быстро стала источником методологического вдохновения для новых микробиологических исследований. 1882 год также стал вехой в истории туберкулеза для второго важного вклада — публикации революционного терапевтического предложения для лечения туберкулеза. лечение легочного туберкулеза, которое имело большое значение до открытия метода лечения болезни стрептомицином: «терапевтический» или «искусственный пневмоторакс», задуманный итальянским врачом Карло Форланини [2,3,4,5] на рис. 1.Сформулированная сначала только как теоретическая гипотеза (один из немногих случаев в медицине, где публичное гипотетическое предсказание предшествует практической реализации), она впоследствии стала в руках ее сторонников в первой половине двадцатого века: изобретение, обычно применяемое для лечения многих избранных случаев туберкулеза, болезни, вызывающей истощение, вызванной туберкулезом легких. Этому же способу суждено было быть изображено крупным литературным деятелем. В романе Томаса Манна «Волшебная гора», действие которого происходит в годы, непосредственно предшествующие Первой мировой войне, группа пациентов, прошедших это лечение, которое в то время было основной эффективной прямой терапией, считает себя частью особого клуба.По словам Манна: «Они сформировали группу, потому что, конечно, такая вещь, как пневмоторакс, объединяет людей. Они называют себя «Клубом полулегких» [6,7]. Роман шотландского писателя-врача Арчибальда Кронина «Цитадель» также посвящает, с описательной точки зрения, важное и точное место лечению искусственного пневмоторакса.
Лекарство оставалось основным до открытия стрептомицина, первого эффективного антибиотика для лечения туберкулезной инфекции, представленного в 1943 году микробиологами Селманом Абрахамом Ваксманом, Альбертом Шацем и Элизабет Бьюги.Однако пневмоторакс не исчез сразу из терапевтических возможностей и продолжал использоваться до 1970-х годов, в тех случаях, когда наличие больших полостей легких делало пациентов легко восприимчивыми к застою инфекционных процессов.
2. Путь к изобретению
Карло Форланини, родившийся в Милане 11 июня 1847 года, был сыном врача и с детства дышал медициной. Туберкулез также присутствовал в начале его жизни, потому что его мать умерла от легочного туберкулеза.После окончания средней школы Форланини поступил на медицинский факультет Университета Павии в 1864 году в качестве ученика престижного колледжа Борромео. Это было время большого научного и политического энтузиазма, потому что Университет Павии был в авангарде применения новых теорий болезней, основанных на книге Рудольфа Вирхова «Die Cellularpathologie», и в то же время молодые студенты были в восторге от этого революционные движения во главе с Джузеппе Гарибальди, который через несколько лет привел бы к объединению Италии.В 1866 году Форланини был добровольным борцом в рядах Гарибальди в битвах при Монте Суелло и Беззекке. Вернувшись в Павию, он опубликовал свою первую научную работу в 1868 году и связал себя братской дружбой с Камилло Гольджи, который был в начале своей звездной научной карьеры [8]. В 1870 году он получил медицинское образование под руководством офтальмолога Антонио Куаглино; На следующий год Форланини работал в отделении хронических болезней больницы Маджоре в Милане.Тем временем он начал проявлять большой интерес к изучению заболеваний легких, начав изобретать устройства, которые могли бы улучшить вентиляцию легких. В этих усилиях он нашел помощь своего младшего брата Энрико, талантливого инженера, который был одним из пионеров воздушных полетов (в его честь назван аэропорт Милана Линате 1937 года). В 1875 году Карло Форланини основал Общество пневмотерапии и Миланский институт пневматики, а с 1881 года он также был главным врачом по кожным заболеваниям. Тем временем он начал серию попыток лечения туберкулеза и заболеваний легких с помощью принудительных дыхательных движений и аэротерапии для увеличения кровотока и притока воздуха в легкие.При научном сотрудничестве своего брата Энрико он также построил некоторые из первых барокамер, показанных на рис. 2.
Он наблюдал некоторые положительные результаты в лечении эмфиземы легких, а также небольшое улучшение при туберкулезе. Вскоре, однако, Форланини начал разрабатывать противоположные терапевтические соображения по поводу туберкулеза легких. Это был не дыхательный акт, приносящий пользу больному легкому, а отдых. Фактически, поражение легочной ткани, как и в случае туберкулеза, могло ухудшиться по мере его движения вплоть до образования и последующего развития полостей, которые затем постоянно увеличивались во время каждого респираторного акта.Исходя из этого соображения, он был убежден, что надлежащая терапия для остановки и блокирования развития легочной болезни заключается в том, чтобы привести легкие в состояние покоя через их искусственный коллапс. Фактически, уже были случайные предыдущие наблюдения, которые коррелировали блокировку движения легкого из-за спонтанного пневмоторакса с улучшением там туберкулезного процесса.
В 1822 году британский врач Джеймс Карсон после нескольких экспериментов на крысах также предпринял попытки вылечить туберкулез легких, вызвав пневмоторакс у людей, но эта попытка не увенчалась успехом [9].Однако другие врачи, такие как французские врачи Эмиль Туссен в 1880 году и Ипполит Эрард в 1881 году, сообщили об улучшении туберкулезного процесса легких после коллапса легкого после спонтанного пневмоторакса или гидропневмоторакса [4,10,11]. Исследования Форланини механизма развития туберкулезного процесса в легких и внимательное изучение предыдущих исследований, в частности наблюдений Туссена, натолкнули его на мысль о четко сформулированном терапевтическом предложении: заставить газ проникнуть в плевральную полость (межплевральное пространство), вызывая коллапс легкого внизу.В июле 1882 года Форланини предложил свой метод [10], который он применил только в 1888 году, когда впервые применил искусственный пневмоторакс. Два года спустя в статье двух его сотрудников мы находим первое упоминание о четырех пациентах, пролеченных этим методом [12]. Огромная заслуга Форланини заключалась в том, чтобы предложить технологию, с помощью которой можно было бы успокоить коллапс легкого, обеспечить дренирование и облитерацию туберкулезной полости, а затем рубцевание лежащих в основе поражений. Улучшение состояния пациента стало не только местным, но и общим, поскольку механическое сужение легких при искусственном пневмотораксе уменьшило воспалительный источник заболевания в легких и, возможно, могло улучшить общую иммунную реакцию организма на патологический процесс.Также было предложено, чтобы метод уменьшал абсорбцию токсических факторов, выделяемых туберкулезным поражением. Форланини наблюдал уменьшение и исчезновение кашля; уменьшение и исчезновение мокроты; падение температуры и потливость; и исчезновение астении. Пациент впал в эйфорию, повысился уровень питания, наблюдалось уменьшение или исчезновение токсико-инфекционного состояния. Форланини также отметил благоприятное воздействие на другое легкое, если оно поражено туберкулезом, как следствие общего улучшения [13].Наконец, он утверждал, что существует также косвенный терапевтический эффект на начальный туберкулез гортани и кишечника. Чтобы разработать соответствующую технику для повторной инъекции небольшого количества газа в плевральную полость (200–250 мл) через большую иглу для подкожных инъекций, он попросил помощи и совета у своего брата Энрико. Таким образом, медицинский опыт сочетается с технологическими навыками творческого инженера, и в результате получился новый аппарат. Сначала Форланини сделал несколько попыток с атмосферным воздухом, но затем он понял, что кислородная составляющая этого газа поглощается слишком быстро, и поэтому переключился на азот [14,15].Таким образом, легкое было иммобилизовано на более длительный срок. Для проведения пневмоторакса Форланини использовал два аппарата: одно для производства азота, второе для введения под давлением (контролируемого манометром) газа в интраплевральное пространство. Производство азота в первом аппарате происходило в результате химической реакции с помощью пирогалловой кислоты, которая сильно поглощает кислород воздуха. Затем азот переносили во второй аппарат, подключенный к игле, которую очень медленно вводили в предварительно выбранное межреберное пространство на рисунке 3.Проведя предварительные эксперименты на животных и трупах, Форланини пришел к выводу, что после перфорации париетальной плевры, как только кончик иглы касается висцеральной плевры, подлежащая эластическая ткань втягивается, увлекая за собой висцеральную плевру, в то время как газ попал в интраплевральное пространство. Таким образом, если введение было медленным, висцеральная плевра и нижележащее легкое не прокалывались. Форланини обычно начинал лечение с введения около 200 куб. См, но не более 400 куб. См (во избежание риска подкожной эмфиземы, т.е.е., попадание газа в ткани грудной стенки) или менее 100 куб. [14]. Через несколько дней снова вводили азот, чтобы добиться полного коллапса легких. Затем пневмоторакс повторялся каждые 15–20 дней и продолжался в течение многих месяцев, обычно до двух лет и более.
3. Успех и трудности
В 1884 году Форланини начал свою университетскую карьеру в Туринском университете и получил должность экстраординарного профессора «Clinica medica preparatoria» (подготовительная медицинская клиника).Вскоре после этого он достиг пика своей университетской карьеры, став профессором специальной медицинской патологии. Среди учеников Форланини в Туринском университете самым важным был Сципионе Рива Роччи, который под руководством мастера разработал тонометр с пневматической манжетой, который вскоре стал всемирным символом практической медицины. В 1898 году Форланини вернулся в Павию, сначала для временного преподавания специальной медицинской демонстративной патологии, а с 1900 года на престижной должности профессора медицинской клиники.Здесь вокруг него собралась школа талантливых врачей, таких как Рива Роччи, который переехал в Павию из Турина, Умберто Карпи де Ресмини и Эудженио Морелли [5]. Между тем, Форланини сообщил о своей операции на Рисунке 4 в отчете от 2 апреля 1894 года. на одиннадцатом международном медицинском конгрессе в Риме [16], а в следующем году — с лекцией на итальянском конгрессе внутренней медицины [17]. Однако реакция медицинского сообщества была не очень живой, и искусственный пневмоторакс также встретил возражения и возражения.С распространением операции и ее применением врачами, не очень хорошо знавшими метод и использовавшими неадекватные критерии отбора пациентов-кандидатов, количество серьезных и даже фатальных осложнений значительно увеличилось [18]. И это несмотря на то, что безопасность метода неуклонно повышалась в первые десятилетия нового века. Среди осложнений, описанных и обсужденных Форланини, были эмпиема, эмфизема и церебральная эмболия, особенно газовая.Еще одним осложнением была плевральная эклампсия, то есть обморок, симптомы которого Форланини описал следующим образом: «Пациент внезапно падает на кровать, теряет сознание, склонив голову набок или назад; глаз широко открыт, луковицы зафиксированы спереди или повернуты вверх или в одну сторону; зрачок максимальной амплитуды, жесткий; лицо крайне бледное, иногда синюшное, холодное, с синеватыми прожилками на шее, груди, конечностях; стиснутые зубы; жесткость туловища и конечностей; одышка и незаметный ритм пульса, короче говоря, впечатляющий синдром из-за реального бессилия симптомов, из-за внезапности, из-за мысли, что авария следует за операционным действием и может быть фатальной »[14].Более того, искусственный пневмоторакс иногда оказывался неэффективным из-за спаек плевры, предотвращавших коллапс легкого. Чтобы преодолеть эти трудности, шведский врач Ганс Христиан Якобей ввел разделение эндоплевральных спаек с помощью торакоскопа и прижигания [19]. Также были разработаны некоторые альтернативные искусственному пневмотораксу методы лечения туберкулеза легких. Попытка привести легкие в состояние покоя для ограничения экскурсий диафрагмы была предпринята в 1913 году Эрнстом Зауэрбрухом, который ввел френикотомию [20].В годы, предшествовавшие Первой мировой войне, были заложены основы хирургии туберкулеза легких. Уже в 1891 году Теодор Туффье удалил верхушку легкого в случае кавитированного туберкулеза; в 1893 году Дэвид Лоусон ввел пневмонэктомию; а два года спустя Уильям Мейсуэн удалил левое легкое по поводу туберкулеза (в 1940 году пациент был еще жив). В 1908 году Людольф Брауэр опубликовал первую радикальную торакопластику, и в последующие двадцать лет хирургия легких при туберкулезе легких непрерывно развивалась [21,22,23,24].Однако искусственный пневмоторакс оставался первым выбором, когда нужно было рассмотреть возможность вмешательства для лечения болезни.
4. Споры и распространение
Плохой сюрприз застал Форланини, когда в 1906 году он прочитал статью Людольфа Брауэра из Марбурга, опубликованную в авторитетном немецком журнале, в которой изобретение метода приписывалось важному американскому хирургу Джону Бенджамину. Мерфи [25]. Последний разработал версию операции, предположительно, не зная о работе итальянца, и описал ее в 1898 году на собрании Американской медицинской ассоциации [26,27,28].Мерфи был первым, кто применил новую рентгеновскую технологию (Вильгельм Рентген открыл рентген в 1895 году) для контроля результатов лечения пневмоторакса. Форланини немедленно отреагировал на статью Брауэра и опубликовал в другом авторитетном немецком журнале результаты, полученные им в 25 случаях туберкулеза легких, также заявив о приоритете изобретения [29]. Более того, он критиковал методы лечения Мерфи, поскольку они включали разрез кожи и грудных мышц (а не ни одного прокола, как он), а также большое количество азота, введенное американским хирургом (1000–3000 мл), что привело к к чрезмерному сдавлению легкого.Статья Форланини способствовала распространению его изобретения в немецком медицинском мире и, следовательно, в трансальпийской Европе. С этого момента Форланини продвигал этот метод, также проводя конференции для врачей. В 1906–1907 годах произошло технологическое развитие, сделавшее устройство более применимым, когда Кристиан Сугман из санатория Вейлефьорд в Дании усовершенствовал его, вставив в инструмент для пневмоторакса датчик давления воды, который позволил точно контролировать вводимый газ. .Более того, в 1912 году Маурицио Асколи предложил терапию частичного коллапса, которая позволила двустороннему пневмотораксу лечить случаи вовлечения двух легких в патологический процесс. В апреле 1912 года Форланини провел в Риме памятную лекцию под названием «Искусственный пневмоторакс в лечении заболеваний». туберкулез легких »на седьмом международном конгрессе по туберкулезу [30]. Презентация вызвала бурные овации, и после тридцати лет исследований пневмоторакса Форланини, наконец, получил полное международное признание.В Англии этот метод не применялся до 1911 г .; впоследствии он добился значительных успехов. В 1917 году доктор Клайв Ривьер написал в своем учебнике «Лечение пневмоторакса от туберкулеза легких»: «Никогда еще не приходил более обнадеживающий солнечный луч, чтобы осветить темные царства болезней, чем тот, который появился на пути чахоточного человека благодаря открытию чахотки. искусственный пневмоторакс »[31]. Ривьер подтвердил это суждение десятью годами позже в «Британском журнале туберкулеза» [32].Другие британские врачи выразили в целом положительное мнение о лечении [33,34,35,36,37,38,39,40,41,42,43,44,45,46,47], которое также применялось к детям [ 48]. Об уровне его популяризации свидетельствует и тот факт, что один из важных эпизодов романа шотландского писателя Арчибальда Джозефа Кронина «Цитадель» (1937) касается именно описания операции искусственного пневмоторакса. Однако распространение метода после 1912 г. достигло всех европейских стран, а с некоторой задержкой — и США.В Императорской России лечебный пневмоторакс уже использовал в 1910 году Аркадий Н. Рубель, который двумя годами позже опубликовал первую монографию по этой теме, пополнив свои знания в стране [18,49]. В 1930-х годах в сталинской России применение этого метода приобрело политический оттенок. Лечение считалось «аристократической терапией», а значит, контрреволюционным, и, в конце концов, устройство пневмоторакса было атаковано пропагандой как «машина для убийства». Один из ведущих российских врачей, пропагандирующих терапию пневмоторакса, Вольф С.Холцман, директор Московского областного туберкулезного института, был арестован в 1939 году во время сталинских чисток, а через два года казнен.
5. Битва и война
В 1912 году, добившись успеха на Седьмом международном конгрессе в Риме, Форланини стал всемирно известным ученым. В том же году он был впервые предложен на присуждение Нобелевской премии по медицине, и в последующие годы Форланини безуспешно номинировался на эту премию по крайней мере двадцать раз.Его друг и коллега-профессор Университета Павии, Камилло Гольджи (лауреат Нобелевской премии за 1906 г.), трижды предлагал ему, мотивируя это тем, что изобретение пневмоторакса принесло «большую пользу человечеству». кандидатские заслуги с волей Альфреда Нобеля. Однако Нобелевская премия не была присуждена в годы Первой мировой войны между 1915 и 1918 годами, и именно в этом году Форланини умер. Таким образом, итальянский врач имел возможность выиграть премию только в течение трех лет с 1912 по 1914 год.Однако были некоторые причины, подробно проанализированные Ханссоном и Полянски [18], которые, вероятно, помешали ему получить награду в этот короткий период времени. Фактически, все номинации исходили от итальянских ученых; метод еще не достиг стандартов безопасности, которые он получит несколько лет спустя; Были и другие альтернативные хирургические операции, менее успешные, но использовавшиеся при лечении туберкулеза легких. В 1913 году Форланини был назначен сенатором королевства и членом совета народного образования (см. рис. 5).В годы Первой мировой войны его здоровье постепенно ухудшалось. Однако он был рад видеть, что его изобретение широко используется в клиниках по всему миру. Форланини умер в Нерви, на Лигурийской Ривьере, 25 мая 1918 года. Сразу после своей смерти Гольджи опубликовал очень проникновенный некролог [50]. Этот великий врач выиграл битву с туберкулезом, первую из серии, которая будет продолжаться вместе с другими главными героями. . Его изобретение не исчезло полностью из медицинской практики и до сих пор используется в особых случаях, например, при преторакоскопическом искусственном пневмотораксе [51], что могло бы обрадовать Форланини.Однако, к сожалению, война с туберкулезом все еще продолжается, и окончательная победа еще не достигнута.
Эффективность искусственного пневмоторакса при двухлегочной вентиляции при видеоассистированной торакоскопической хирургии рака пищевода
Ферлей Дж., Сурджоматарам I, Эрвик М., Дикшит Р., Эзер С., Матерс С., Ребело М., Паркин Д., Форман Д. (2013) Bray F (2015) GLOBOCAN 2012 v1.0, заболеваемость раком и смертность во всем мире: IARC CancerBase no. 11. Международное агентство по изучению рака, Лион
Google ученый
Durkin C, Schisler T, Lohser J (2017) Современные тенденции в анестезии при эзофагэктомии. Curr Opin Anaesthesiol 30: 30–35
PubMed
Google ученый
Cuschieri A (1993) Эндоскопическая субтотальная эзофагэктомия при раке с использованием правого торакоскопического доступа. Surg Oncol 2 (Приложение 1): 3–11
Артикул
PubMed
Google ученый
Nomura S, Tsujimoto H, Aosasa S, Saitoh D, Hase K, Ono S, Yamamoto J, Ueno H (2018) Влияние уровней ангиотензинпревращающего фермента 2 на послеоперационную пневмонию после эзофагэктомии.J Surg Res 224: 200–206
CAS
Статья
PubMed
Google ученый
Tsujimoto H, Takahata R, Nomura S, Yaguchi Y, Kumano I, Matsumoto Y, Yoshida K, Horiguchi H, Hiraki S, Ono S, Yamamoto J, Hase K (2012) Видео-ассистированная торакоскопическая хирургия для Рак пищевода ослабляет послеоперационные системные реакции и легочные осложнения. Хирургия 151: 667–673
Статья
PubMed
Google ученый
Luketich JD, Pennathur A, Franchetti Y, Catalano PJ, Swanson S, Sugarbaker DJ, De Hoyos A, Maddaus MA, Nguyen NT, Benson AB, Fernando HC (2015) Минимально инвазивная эзофагэктомия: результаты проспективного многоцентрового исследования II фазы. исследование восточной кооперативной онкологической группы (E2202). Ann Surg 261: 702–707
Статья
PubMed
PubMed Central
Google ученый
Liu Z, Liu X, Huang Y, Zhao J (2016) Стратегии интраоперационной искусственной вентиляции легких у пациентов, которым выполняется вентиляция одним легким: метаанализ.SpringerPlus 5: 1251
Артикул
PubMed
PubMed Central
Google ученый
Blank RS, Colquhoun DA, Durieux ME, Kozower BD, McMurry TL, Bender SP, Naik BI (2016) Управление однолегочной вентиляцией: влияние дыхательного объема на осложнения после торакальной хирургии. Анестезиология 124: 1286–1295
Статья
PubMed
Google ученый
Lohser J, Slinger P (2015) Повреждение легкого после вентиляции одного легкого: обзор патофизиологических механизмов, влияющих на вентилируемое и разрушенное легкое.Anesth Analg 121: 302–318
Статья
PubMed
Google ученый
Palanivelu C, Prakash A, Senthilkumar R, Senthilnathan P, Parthasarathi R, Rajan PS, Venkatachlam S (2006) Минимально инвазивная эзофагэктомия: торакоскопическая мобилизация пищевода и средостенная лимфаденэктомия — опыт 130 пациентов с предэктомией средостения. J Am Coll Surg 203: 7–16
Статья
PubMed
Google ученый
Zhang R, Liu S, Sun H, Liu X, Wang Z, Qin J, Hua X, Li Y (2014) Применение однопросветной анестезии эндотрахеальной трубки с искусственным пневмотораксом при тораколапароскопической эзофагэктомии. Interact Cardiovasc Thorac Surg 19: 308–310
Статья
PubMed
Google ученый
Cai L, Li Y, Sun L, Yang XW, Wang WB, Feng F, Xu GH, Guo M, Lian X, Zhang HW (2017) Лучшие периоперационные результаты при торакоскопической эзофагэктомии с двухлегочной вентиляцией в положении полулежа.J Thorac Dis 9: 117–122
Статья
PubMed
PubMed Central
Google ученый
Lin M, Shen Y, Wang H, Fang Y, Qian C, Xu S, Ge D, Feng M, Tan L, Wang Q (2018) Сравнение вентиляции двух легких с CO 2 искусственного пневмоторакс и вентиляция одного легкого во время торакальной фазы малоинвазивной эзофагэктомии. J Thorac Dis 10: 1912–1918
Статья
PubMed
PubMed Central
Google ученый
Zhang BJ, Tian HT, Li HO, Meng J (2018) Влияние режима однолегочной вентиляции на функцию легких у пожилых пациентов, перенесших операцию по поводу рака пищевода. Лекарство 97: e9500
Артикул
PubMed
PubMed Central
Google ученый
Собин LH, Gospodarowicz MK, Wittekind C (2011) TNM-классификация злокачественных опухолей. Уайли, Нью-Йорк
Google ученый
Saikawa D, Okushiba S, Kawata M, Okubo T, Kitashiro S, Kawarada Y, Suzuki Y, Kato H (2014) Эффективность и безопасность искусственного пневмоторакса при двухлегочной вентиляции при торакоскопической эзофагэктомии при раке пищевода в положении лежа. Gen Thorac Cardiovasc Surg 62: 163–170
Статья
PubMed
Google ученый
Искусственный интеллект, считывающий рентгеновские снимки грудной клетки, одобрен FDA
Рентген грудной клетки, показывающий коллапс легкого или пневмоторакс. Изображение любезно предоставлено Рэйчел Каллкут, доктором медицины.
Новая технология на основе искусственного интеллекта может вскоре помочь сократить задержки в диагностике коллапса легкого или пневмоторакса, серьезного заболевания, которое можно быстро вылечить.
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США одобрило новый алгоритм искусственного интеллекта (AI), который работает с портативными рентгеновскими лучами для быстрого выявления коллапса легких. Технология была разработана исследователями GE Healthcare и Калифорнийского университета в Сан-Франциско.
Пневмоторакс возникает, когда воздух попадает в грудную полость, сдавливает легкие и вызывает частичный или полный коллапс. Десятки тысяч американцев ежегодно страдают пневмотораксом, часто из-за травм, хотя другие состояния также могут привести к коллапсу легкого.
«Это потенциально опасное для жизни открытие, при котором время до постановки диагноза является обязательным для оптимизации результата. В клиническом сценарии с высокой интенсивностью пневмоторакс может быть изначально не замечен врачами », — сказала Рэйчел Каллкут, доктор медицины, доцент хирургии в UCSF и хирург-травматолог в больнице общего профиля Цукерберга в Сан-Франциско.
Добавьте к этому большой объем изображений, которые рентгенологу поручено просмотреть, тот факт, что в некоторых медицинских центрах может не быть круглосуточного дежурного радиолога, а диагностика пневмоторакса может быть отложена на многие часы.
В случае заражения пневмоторакс можно лечить, вставив трубку для удаления просочившегося воздуха, но при отсутствии лечения пневмоторакс может привести к серьезному затруднению дыхания и даже к смерти.
Callcut, который также является директором по науке о данных в Центре инноваций в области цифрового здравоохранения (CDHI) в UCSF, руководил разработкой нового инструмента скрининга AI, известного как Critical Care Suite, который лицензируется UCSF Innovation Venture на GE Healthcare.Когда больной пациент поступает в отделение неотложной помощи, переносной рентгеновский снимок, встроенный в новый ИИ, может быть доставлен к его постели. Рентген грудной клетки немедленно отправляется рентгенологу, и если ИИ обнаруживает пневмоторакс, изображение перемещается в начало очереди для просмотра. Портативный рентгеновский аппарат также может отображать предупреждение, которое может помочь лечащим врачам, лечащим пациента, принимать более срочные решения.
Рэйчел Каллкут, доктор медицины, хирург-травматолог, руководила разработкой нового инструмента для скрининга искусственного интеллекта на пневмоторакс.
«Что делает Critical Care Suite особенным, так это то, что мы нацелены на решение опасных для жизни проблем, и он способен работать на месте оказания помощи», — сказал Каллкут. Она добавила, что больницам будет относительно легко внедрить эту технологию, поскольку она не требует новой дорогостоящей инфраструктуры.
Для разработки ИИ команда исследователей UCSF из CDHI и отделения радиологии, в том числе Джон Монган, доктор медицинских наук, и Эндрю Тейлор, доктор медицинских наук, обучили алгоритм с тысячами рентгеновских снимков, которые были обезличены и классифицируется как имеющий или не имеющий пневмоторакс.Затем ИИ был проверен на тысячах других рентгеновских снимков, достигнув точности, превышающей 96 процентов. В сотрудничестве с GE Healthcare исследовательская группа также проверила алгоритм на дополнительных рентгеновских снимках со всего мира и от различных пациентов и медицинских учреждений.
Скрининг пневмоторакса — первое из четырех клинических приложений ИИ, которые команда CDHI разрабатывает для Critical Care Suite.
GE Healthcare получила одобрение 510 (k) от FDA для Critical Care Suite, что означает, что теперь его можно использовать в клинической среде.Новый инструмент скрининга может иметь большое значение для пациентов, особенно в условиях ограниченных ресурсов.
«Я думаю об этом как о дополнительной проверке безопасности, которая может повысить эффективность лечения, чтобы быстрее поставить диагноз и оказать помощь пациентам, а также снизить риск игнорирования пневмоторакса».