Повышенное образование тромбина – потенциальный маркер неблагоприятных исходов беременности » Библиотека врача
Цель исследования. Оценить эффективность теста генерации тромбина (ТГТ) в определении высокого тромбогенного риска у беременных женщин.
Материал и методы. В работу были включены 30 небеременных здоровых женщин (группа контроля) и обследованы 32 беременные женщины в 3-м триместре. Из них 22 женщины с осложненным течением беременности составили исследуемую группу, 10 женщин вошли в группу сравнения. По итогам родоразрешения пациентки из исследуемой группы были поделены на подгруппу с благоприятным исходом беременности (n=15) и подгруппу с неблагоприятным исходом (n=7). Исследование состояния системы гемостаза проводилось с помощью стандартных коагулологических тестов, а также с помощью интегрального теста – ТГТ.
Результаты. Показано статистически значимое увеличение параметра ТГТ: эндогенного тромбинового потенциала (ЭТП) у беременных женщин по сравнению с небеременными (2300±400 и 1700±400 соответственно, р
Одной из актуальных проблем современной медицины является риск возникновения тромбозов у женщин во время беременности. Это связано с тем, что беременность сопровождается усилением коагуляционных свойств крови, необходимым для снижения кровопотери в родах. Изменения в свертывающей системе при физиологически протекающей беременности связаны с повышенным синтезом фибриногена и других факторов свертывания в сочетании со снижением уровня естественных ингибиторов свертывания крови, а также с подавлением фибринолиза [1, 2]. Эти изменения в гемостатической системе действуют как физиологическая «система безопасности», но могут быть причиной осложнений, как у матери, так и у плода [2–4]. Такими осложнениями могут быть венозная недостаточность, преэклампсия, отслойка плаценты, ограничение роста плода, поздний и повторный ранний выкидыш, внутриутробная смерть и мертворождение. В обзоре S.A. Mastrolia и соавт. [2] показана связь между тромбозами и осложнениями беременности. Риски выше у женщин с приобретенной или наследственной тромбофилией. В работе В.О. Бицадзе и соавт. [1] говорится о наличии этиопатогенетической связи между тромбофилией и акушерскими осложнениями и о высокой эффективности антикоагулянтной профилактики при условии ее раннего начала.
Это связано с тем, что беременность сопровождается усилением коагуляционных свойств крови, необходимым для снижения кровопотери в родах. Изменения в свертывающей системе при физиологически протекающей беременности связаны с повышенным синтезом фибриногена и других факторов свертывания в сочетании со снижением уровня естественных ингибиторов свертывания крови, а также с подавлением фибринолиза [1, 2]. Эти изменения в гемостатической системе действуют как физиологическая «система безопасности», но могут быть причиной осложнений, как у матери, так и у плода [2–4]. Такими осложнениями могут быть венозная недостаточность, преэклампсия, отслойка плаценты, ограничение роста плода, поздний и повторный ранний выкидыш, внутриутробная смерть и мертворождение. В обзоре S.A. Mastrolia и соавт. [2] показана связь между тромбозами и осложнениями беременности. Риски выше у женщин с приобретенной или наследственной тромбофилией. В работе В.О. Бицадзе и соавт. [1] говорится о наличии этиопатогенетической связи между тромбофилией и акушерскими осложнениями и о высокой эффективности антикоагулянтной профилактики при условии ее раннего начала.
Однако в настоящее время решение о назначении антикоагулянтной терапии беременным женщинам принимается лишь на основании факторов риска, то есть наличия собственного или семейного тромботического анамнеза, при выявлении той или иной тромбофилии (мутации фактора V Лейден, мутации протромбина, дефицита антитромбина, носительства антифосфолипидных антител и др.). Эти показания для назначения антикоагулянтов не всегда могут быть верны, поскольку они не основываются на точных лабораторных данных, фиксирующих гиперкоагуляционное состояние крови пациентов. Соответственно, использование этих показаний может привести как к неоправданно широкому применению антикоагулянтов во время беременности, так и наоборот, к недооценке риска и не использованию антикоагулянтной терапии в тех случаях, когда это необходимо.
Для исследования состояния системы гемостаза, как правило, применяют стандартные коагулологические тесты (активированное частичное тромбопластиновое время, тромбиновое время, протромбиновый индекс по Квику и др. ). Однако эти тесты свертывания крови имеют недостаточную прогностическую значимость и их сложно использовать для оценки риска тромбоза. Специфические молекулярные маркеры, отражающие процесс свертывания (D-димеры, фибринопептид, тромбин-антитромбиновый комплекс), могут выявить отклонения от референтного интервала, но не позволяют судить о наличии дисбаланса в системе коагуляции в целом, так как изменения отдельных компонентов свертывающей системы могут быть нивелированы в организме включением компенсаторных механизмов. Возможным решением является использование интегральных тестов, которые могут показать состояние системы гемостаза в целом [5, 6]. Тест генерации (ТГТ) – один из наиболее разработанных и изученных интегральных тестов гемостаза за рубежом. К сожалению, в России этот тест пока применяется редко.
). Однако эти тесты свертывания крови имеют недостаточную прогностическую значимость и их сложно использовать для оценки риска тромбоза. Специфические молекулярные маркеры, отражающие процесс свертывания (D-димеры, фибринопептид, тромбин-антитромбиновый комплекс), могут выявить отклонения от референтного интервала, но не позволяют судить о наличии дисбаланса в системе коагуляции в целом, так как изменения отдельных компонентов свертывающей системы могут быть нивелированы в организме включением компенсаторных механизмов. Возможным решением является использование интегральных тестов, которые могут показать состояние системы гемостаза в целом [5, 6]. Тест генерации (ТГТ) – один из наиболее разработанных и изученных интегральных тестов гемостаза за рубежом. К сожалению, в России этот тест пока применяется редко.
В ряде работ [7–9] сообщается о применении ТГТ для обследования женщин во время беременности, в том числе и для определения эффективности антикоагулянтной терапии [9].
Целью настоящего исследования было оценить эффективность ТГТ в определении высокого тромбогенного риска у беременных женщин, нуждающихся в назначении антикоагулянтной терапии для улучшения исходов беременности.
Материал и методы исследования
Исследование проводилось в соответствии с национальными и локальными законами о проведении исследований с участием животных и человека. Все пациенты включались в исследование после подписания информированного согласия, составленного в соответствии с принципами, изложенными в Хельсинской декларации. Представленное исследование было одобрено локальным этическим комитетом.
В работу были включены 30 небеременных здоровых женщин (группа контроля) и 32 беременные женщины. Все беременные были разделены на исследуемую группу (22 беременные) и группу сравнения (10 беременных). В исследуемую группу вошли пациентки с осложненным течением беременности, наличием факторов тромбогенности и сопутствующими патологиями (венозная недостаточность, плацентарная недостаточность, тромбофилия, преэклампсия) на …
1. Бицадзе В.О., Макацария А.Д., Хизроева Д.Х., Макацария Н.А., Яшенина Е.В., Казакова Л.А. Тромбофилия как важнейшее звено патогенеза осложнений беременности. Практическая медицина. 2012; 9: 24-31.
Практическая медицина. 2012; 9: 24-31.
2. Mastrolia S.A., Mazor M., Loverro G., Klaitman V., Erez O. Placental vascular pathology and increased thrombin generation as mechanisms of disease in obstetrical syndromes. PeerJ. 2014; 2: e653.
3. Simcox L.E., Ormesher L., Tower C., Greer I.A. Thrombophilia and pregnancy complications. Int. J. Mol. Sci. 2015; 16(12): 28418-28.
4. Bates S.M. Preventing thrombophilia-related complications of pregnancy: an update. Expert Rev. Hematol. 2013; 6(3): 287-300.
5. Липец Е.Н., Атауллаханов Ф.И., Пантелеев М.А. Интегральные лабораторные тесты гемостаза в диагностике гиперкоагуляции и оценке риска тромбоза. Онкогематология. 2015; 10(3): 73-91.
6. Othman M., Falcón B.J., Kadir R. Global hemostasis in pregnancy: are we using thromboelastography to its full potential? Semin. Thromb. Hemost. 2010; 36(7): 738-46.
7. Момот А.П., Молчанова И.В., Семенова Н.А., Романов В.В., Сердюк Г.В., Белозеров Д.Е., Трухина Д.А. , Кудинова И.Ю., Максимова Н.В. Динамика показателей системы гемостаза у женщин при вынашивании беременности и после родов. Лабораторная служба. 2015; 4(2): 3-11.
, Кудинова И.Ю., Максимова Н.В. Динамика показателей системы гемостаза у женщин при вынашивании беременности и после родов. Лабораторная служба. 2015; 4(2): 3-11.
8. Patel J.P., Patel R.K., Roberts L.N., Marsh M.S., Green B., Davies J.G., Arya R. Changes in thrombin generation and D-dimer concentrations in women injecting enoxaparin during pregnancy and the puerperium. BMC Pregnancy Childbirth. 2014; 14: 384.
9. Николаева А.Е., Кутуева Ф.Р., Кайка И.А., Папаян Л.П., Капустин С.И., Наместников Ю.А., Силина Н.Н. Клиническое значение ретрохориальной гематомы у беременных, имеющих факторы риска по возникновению репродуктивных потерь. Опыт ведения в условиях женской консультации. Акушерство и гинекология. 2011; 5: 94-8.
10. Hemker H.C., Giesen P., AlDieri R., Regnault V., de Smed E, Wagenvoord R. et al. The calibrated automated thrombogram (CAT): a universal routine test for hyper- and hypocoagulability. Pathophysiol. Haemost. Thromb. 2002; 32(5-6): 249-53.
11. Gribkova I.V., Lipets E.N., Rekhtina I.G., Bernakevich A.I., Ayusheev D.B., Ovsepyan R.A. et al. The modification of the thrombin generation test for the clinical assessment of dabigatran etexilate efficiency. Sci. Rep. 2016;6: 29242.
Gribkova I.V., Lipets E.N., Rekhtina I.G., Bernakevich A.I., Ayusheev D.B., Ovsepyan R.A. et al. The modification of the thrombin generation test for the clinical assessment of dabigatran etexilate efficiency. Sci. Rep. 2016;6: 29242.
12. McLean K.C., Bernstein I.M., Brummel-Ziedins K.E. Tissue factor-dependent thrombin generation across pregnancy. Am. J. Obstet. Gynecol. 2012; 207(2): 135. e1-6.
13. Erez O., Romero R., Vaisbuch E., Kusanovic J.P., Mazaki-Tovi S., Chaiworapongsa T. et al. The pattern and magnitude of “in vivo thrombin generation” differ in women with preeclampsia and in those with SGA fetuses without preeclampsia. J. Matern. Fetal Neonatal Med. 2018; 31(13): 1671-80.
14. Rosenkranz A., Hiden M., Leschnik B., Weiss E.C., Schlembach D., Lang U. et al. Calibrated automated thrombin generation in normal uncomplicated pregnancy. Thromb. Haemost. 2008; 99(2): 331-7.
15. Kovac M.K., Lalic-Cosic S.Z., Dmitrovic J.M., Djordjevic V.J., Radojkovic D. P. Thrombin generation, D-dimer and protein S in uncomplicated pregnancy. Clin. Chem. Lab. Med. 2015; 53(12): 1975-9.
P. Thrombin generation, D-dimer and protein S in uncomplicated pregnancy. Clin. Chem. Lab. Med. 2015; 53(12): 1975-9.
16. Joly B., Barbay V., Borg J.Y., Le Cam-Duchez V. Comparison of markers of coagulation activation and thrombin generation test in uncomplicated pregnancies. Thromb. Res. 2013; 132(3): 386-91.
17. Bagot C.N., Leishman E., Onyiaodike C.C., Jordan F., Freeman D.J. Normal pregnancy is associated with an increase in thrombin generation from the very early stages of the first trimester. Thromb. Res. 2017; 157: 49-54.
18. Efthymiou M., Lawrie A.S., Mackie I., Arachchillage D., Lane P.J., Machin S. et al. Thrombin generation and factor X assays for the assessment of warfarin anticoagulation in thrombotic antiphospholipid syndrome. Thromb. Res. 2015; 135(6): 1191-7.
19. Vidaeff A.C., Mongan M., Ramin S.M., Saade G., Sangi-Haghpeykar H. Is thrombin activation predictive of subsequent preterm delivery? Am. J. Obstet. Gynecol. 2013; 208: 306. e1-7.
20. Chowdary P., Adamidou D., Riddell A., Aghighi S., Griffioen A., Priest P. et al. Thrombin generation assay identifies individual variability in responses to low molecular weight heparin in pregnancy: implications for anticoagulant monitoring. Br. J. Haematol. 2015; 168(5): 719-27.
Chowdary P., Adamidou D., Riddell A., Aghighi S., Griffioen A., Priest P. et al. Thrombin generation assay identifies individual variability in responses to low molecular weight heparin in pregnancy: implications for anticoagulant monitoring. Br. J. Haematol. 2015; 168(5): 719-27.
21. Bennett S.A., Bagot C.N., Appiah A., Johns J., Ross J., Roberts L.N. et al. Women with unexplained recurrent pregnancy loss do not have evidence of an underlying prothrombotic state: experience with calibrated automated thrombography and rotational thromboelastometry. Thromb. Res. 2014; 133(5): 892-9.
Поступила 16.11.2017
Принята в печать 22.12.2017
Грибкова Ирина Владимировна, к.б.н., ведущий научный сотрудник научно-клинического отдела ГБУ г. Москвы Центр клинических исследований и оценки медицинских технологий Департамента здравоохранения города Москвы.
Адрес: 121096, Россия, Москва, ул. Минская, д. 12, корп. 2. Телефон: 8 (499) 144-00-30. E-mail: [email protected]
Королева Наталья Сергеевна, аспирант кафедры акушерства и гинекологии № 1 ФГАОУ ВО 1-й МГМУ им. И.М. Сеченова Минздрава России (Сеченовский университет). Адрес: 119991, Россия, Москва, ул. Большая Пироговская, д. 2, стр. 4. Телефон: 8 (916) 186-73-37. E-mail: [email protected]
И.М. Сеченова Минздрава России (Сеченовский университет). Адрес: 119991, Россия, Москва, ул. Большая Пироговская, д. 2, стр. 4. Телефон: 8 (916) 186-73-37. E-mail: [email protected]
Давыдовская М.В., д.м.н., зам. директора по научной работе ГБУ г. Москвы Центр клинических исследований и оценки медицинских технологий Департамента здравоохранения города Москвы; профессор кафедры неврологии, нейрохирургии и медицинской генетики ФБОУ РНИМУ им. Н.И. Пирогова Минздрава России.
Адрес: 117997, Россия, Москва, ул. Островитянова, д. 1. Телефон: 8 (499) 144-00-30. E-mail: [email protected]
Мурашко Андрей Владимирович, д.м.н., профессор кафедры акушерства и гинекологии №1 ФГАОУ ВО 1-й МГМУ им. И.М. Сеченова Минздрава России
(Сеченовский университет). Адрес: 119991, Россия, Москва, ул. Большая Пироговская, д. 2, стр. 4. Телефон: 8 (963) 782-02-45. E-mail: [email protected]
Для цитирования: Грибкова И.В., Королева Н.С., Давыдовская М.В., Мурашко А.В. Повышенное образование тромбина – потенциальный маркер неблагоприятных исходов беременности. Акушерство и гинекология. 2018; 8: 92-7.
Акушерство и гинекология. 2018; 8: 92-7.
https://dx.doi.org/10.18565/aig.2018.8.92-97
Гематология и трансфузиология №2 2010 стр. 32
Гематология и трансфузиология №2 2010
Ю. А.
Наместников
ФГУ «Российский научно-исследовательский институт гематологии и
трансфузиологии» Федерального медико-биологического агентства,
Санкт-Петербург
Для корреспонденции:
Наместников Юрий Андреевич, аспирант лаб. свертывания крови, ФГУ
«Российский научно-исследовательский институт гематологии и трансфузиологии»
Федерального медико-биологического агентства.
Адрес: 191024, Санкт-Петербург, 2-я Советская ул., д. 16.
Телефон: 8 (812) 717-35-82.
E-mail: [email protected]
ТЕСТ ГЕНЕРАЦИИ ТРОМБИНА — ИНТЕГРАЛЬНЫЙ ПОКАЗАТЕЛЬ СОСТОЯНИЯ СИСТЕМЫ
СВЕРТЫВАНИЯ КРОВИ
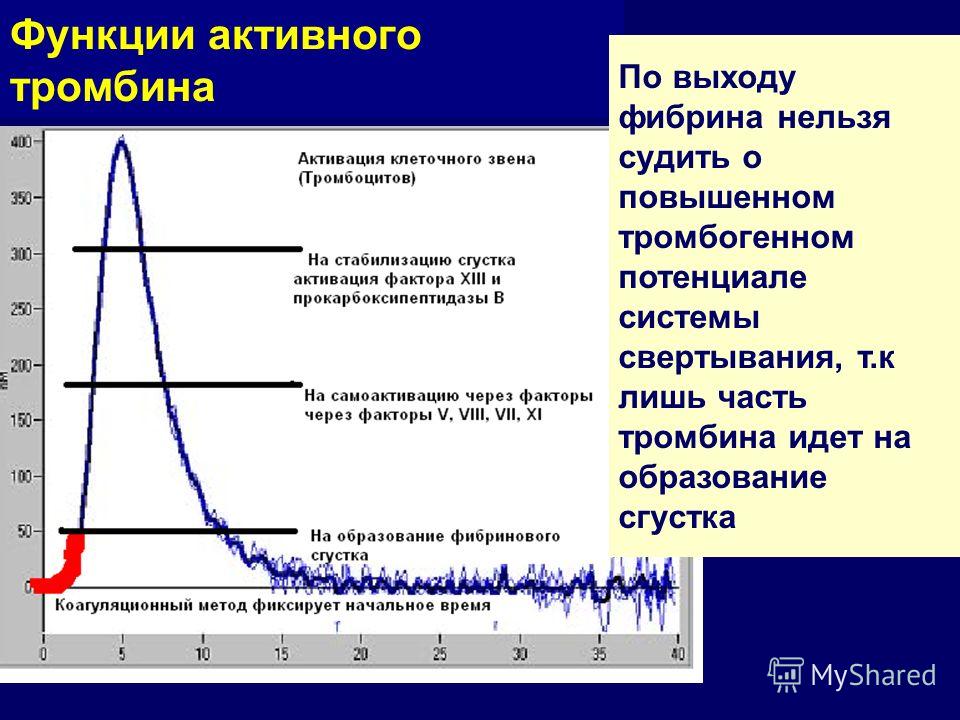
В обзоре литературы представлены данные о диагностической значимости теста
генерации тромбина. Показатели теста характеризуют скорость и интенсивность
образования тромбина — ключевого энзима гемостаза, которые могут быть
использованы для объективной оценки состояний гипо- или гиперкоагуляции.
Ключевые слова:
генерация тромбина, эндогенный тромбиновый потенциал,
калиброванная автоматизированная тромбограмма
ЛИТЕРАТУРА
1. Hemker H. C., Beguin S. Thrombin generation in plasma: its
assessment via the endogenous thrombin potential. Thromb. Haemost. 1995;
74(5): 134—138.
2. Baglin T.
The measurement and application of thrombin generation. Br. J. Haematol.
2005; 130: 653—661.
3. Macfarlane
R. G., Biggs R. A thrombin generation test: the application in
haemophilia and thrombocytopenia. J. Clin. Pathol. 1953; 6: 3—8.
4. Hemker H. C.,
Giesen P. L., Ramjee M. et al. The thrombogram: monitoring thrombin
generation in platelet-rich plasma. Thromb. Haemost. 2000; 83(4): 589—591.
5. Hemker H. C.,
Wielders S., Kessels H. et al. Continuous registration of thrombin
generation in plasma, its use for the determination of the thrombin
potential. Thromb. Haemost. 1993; 70(4): 617—624.
Thromb. Haemost. 1993; 70(4): 617—624.
6. Hemker H. C.,
Giesen P., Al Dieri R. et al. Calibrated automated thrombin generation
measurement in clotting plasma. Pathophysiol. Haemost. Thromb. 2003; 33:
4—15.
7. De Smedt E.,
Al Dieri R., Spronk H. M. et al. The technique of measuring thrombin
generation with fluorogenic substrates: 1. Necessity of adequate
calibration. Thromb. Haemost. 2008; 100(2): 343—349.
8. Baglin T.
The measurement and application of thrombin generation. Br. J. Haematol.
2005; 130: 653—661.
9. Van Veen
J. J., Gatt A., Makris M. Thrombin generation testing in routine
clinical practice: are we there yet? Br. J. Haematol. 2008; 142(6): 889—903.
10. Gerotziafas
G. T., Depasse F., Busson J. et al. Towards a standardization of
thrombin generation assessment: the influence of tissue factor, platelets
and phospholipids concentration on the normal values of
thrombogram—thrombinoscope assay. Thromb. J. 2005; 3: 16.
Thromb. J. 2005; 3: 16.
11. Dargaud Y.,
Luddington R., Gray E. et al. Effect of standardization and
normalization on imprecision of calibrated automated thrombography: an
international multicentre study. Br. J. Haematol. 2007; 139(2): 303—309.
12. Нemker H. C.,
Willems G. M., Beguin S. A computer assisted method to obtain the
prothrombin activation velocity in whole plasma independent of thrombin
decay processes. Thromb. Haemost. 1986; 56(1): 9—17.
13. Garcia-Hejl
C., Vest P., Renard C. et al. Reliability of thrombin generation assay
on frozen-thawed platelet-rich plasma: a reply. Clin. Chem. 2006; 11: 52.
14. Regnault V.,
Beguin S., Lecompte T. Calibrated automated thrombin generation in
frozen-thawed platelet-rich plasma to detect hypercoagulability.
Pathophysiol. Haemost. Thromb. 2003; 33: 25—31.
15. Bidot L., Jy
W., Bidot C. Jr. et al. Microparticle-mediated thrombin generation
Jr. et al. Microparticle-mediated thrombin generation
assay: increased activity in patients with recurrent thrombosis. J. Thromb.
Haemost. 2008; 6(6): 913—919.
16. Duchemin J.,
Pan-Petesch B., Arnaud B. et al. Influence of coagulation factors and
tissue factor concentration on the thrombin generation test in plasma.
Thromb. Haemost. 2008; 99(4): 767—773.
17.
Giansily-Blaizot M., Al Dieri R., Schved J. F. Thrombin generation
measurement in factor VII-depleted plasmas compared to inherited factor
VII-deficient plasmas. Pathophysiol. Haemost. Thromb. 2003; 33: 38—44.
18. Dargaud Y.,
Trzeciak M. C., Bordet J. C. et al. Use of calibrated automated
thrombinography +/- thrombomodulin to recognize the prothrombotic phenotype.
Thromb. Haemost. 2006; 96(5): 562—567.
19. Tripodi A.,
Martinelli I., Chantarangkul V. et al. The endogenous thrombin potential
and the risk of venous thromboembolism. Thromb. Res. 2007; 121: 353—359.
Thromb. Res. 2007; 121: 353—359.
20. Liesøl S.,
Sandset P. M., Mowinckel M. C., Wisløff F. Activated protein C
resistance determined with a thrombin generation-based test is associated
with thrombotic events in patients with lupus anticoagulants. J. Thromb.
Haemost. 2007; 5(11): 2204— 2210.
21. Tchaikovski
S., Huib A. A., van Vliet M. et al. Effect of oral contraceptives on
thrombin generation measured via calibrated automated thrombography. Thromb.
Haemost. 2007; 98(6): 1350—1356.
22. Häzard N.,
Bouaziz-Borgi L., Remy M. G., Nguyen P. Utility of thrombin-generation
assay in the screening of factor V G1691A (Leiden) and prothrombin G20210A
mutations and protein S deficiency. Clin. Chem. 2006; 52(4): 665—670.
23. Regnault V.,
Beguin S., Wahl D. et al. Thrombinography shows acquired resistance to
activated protein C in patients with lupus anticoagulants. Thromb. Haemost.
Thromb. Haemost.
2003; 89(2): 208—212.
24. Eilertsen
A. L., Liestol S., Mowinckel M. C. et al. Differential impact of
conventional and low-dose oral hormone therapy (HT), tibolone and raloxifene
on functionality of the activated protein C system. Thromb. Haemost. 2007;
97(6): 938—943.
25. Lecompte T.,
Wahl D., Perret-Guillaume C. et al. Hypercoagulability resulting from
opposite effects of lupus anticoagulants is associated strongly with
thrombotic risk. Haematologica 2007; 92: 714—715.
26. Besser M.,
Baglin C., Luddington R. et al. High rate of unprovoked recurrent venous
thrombosis is associated with high thrombin-generating potential in a
prospective cohort study. J. Thromb. Haemost. 2008; 6(10): 1720—1725.
27. Chantarangkul
V., Clerici M., Bressi C. et al. Thrombin generation assessed as
endogenous thrombin potential in patients with hyper- or hypo-coagulability.
Haematologica 2003; 88: 547— 554.
28.
Beltran-Miranda C. P., Khan A., Jaloma-Cruz A. R. et al. Thrombin
generation and phenotypic correlation in haemophilia A. Haemophilia 2005;
11: 326—334.
29. Dargaud Y.,
Beguin S., Lienhart A. et al. Evaluation of thrombin generating capacity
in plasma from patients with haemophilia A and B. Thromb. Haemost. 2005;
93(3): 475—480.
30. Siegemund T.,
Petros S., Siegemund A. et al. Thrombin generation in severe haemophilia
A and B: the endogenous thrombin potential in platelet-rich plasma. Thromb.
Haemost. 2003; 90(5): 781—786.
31. Varadi K.,
Negrier C., Berntorp E. et al. Monitoring the bioavailability of FEIBA
with a thrombin generation assay. J. Thromb. Haemost. 2003; 1(11):
2374—2380.
32. Kjalke M.,
Ezban M., Monroe D. M. et al. High-dose factor VIIa increases initial
thrombin generation and mediates faster platelet activation in
thrombocytopenia-like conditions in a cell-based model system. Br. J.
Br. J.
Haematol. 2001; 114(1): 114—120.
33. Gerotziafas
G. T., Depasse F., Chakroun T. et al. Recombinant factor VIIa partially
reverses the inhibitory effect of fondaparinux on thrombin generation after
tissue factor activation in platelet rich plasma and whole blood. Thromb.
Haemost. 2004; 91(3): 531—537.
34. Allen G. A.,
Hoffman M., Roberts H. R. et al. Manipulation of prothrombin
concentration improves response to high-dose factor VIIa in a cell-based
model of haemophilia. Br. J. Haematol. 2006; 134: 314—319.
35. Rugeri L.,
Beguin S., Hemker H. C. et al. Thrombin-generating capacity in patients
with von Willebrand’s disease. Haematologica 2007; 92: 1639—1646.
36. Reverter
J. C., Beguin S., Kessels H. et al. Inhibition of platelet-mediated,
tissue factor-induced thrombin generation by the mouse/human chimeric 7E3
antibody. Potential implications for the effect of c7E3 Fab treatment on
acute thrombosis and «clinical restenosis». J. Clin. Invest. 1996; 98(3):
J. Clin. Invest. 1996; 98(3):
863—874.
37. Beguin S.,
Keularts I., Al Dieri R. et al. Fibrin polymerization is crucial for
thrombin generation in platelet-rich plasma in a VWF-GPIb-dependent process,
defective in Bernard-Soulier syndrome. J. Thromb. Haemost. 2004; 2(1):
170—176.
38. Cauwenberghs
S., Feijge M. A., Theunissen E. et al. Novel methodology for assessment
of prophylactic platelet transfusion therapy by measuring increased thrombus
formation and thrombin generation. Br. J. Haematol. 2007; 136: 480—490.
39. Tripodi A.,
Primignani M., Chantarangkul V. et al. Thrombin generation in patients
with cirrhosis: the role of platelets. Hepatology 2006; 44: 440—445.
40. Collins
P. W., Macchiavello L. I., Lewis S. J. et al. Global tests of
haemostasis in critically ill patients with severe sepsis syndrome compared
to controls. Br. J. Haematol. 2006; 135: 220— 227.
41. Altman R.,
Scazziota A., Herrera L., González C. Relationship between thrombin
generation and international normalized ratio in patients receiving oral
vitamin K antagonist therapy. J. Thromb. Haemost. 2007; 5(7): 1552—1569.
42. Jackson
C. M., Esnouf M. P., Lindahl T. L. A critical evaluation of the
prothrombin time for monitoring oral anticoagulant therapy. Pathophysiol.
Haemost. Thromb. 2003; 33: 43—51.
43. Gatt A., van
Veen J. J., Bowyer A. et al. Significant variation in thrombin
generation potential in «adequately» anticoagulated patients. XXI-st
Сongress of the international society on haemostasis and thrombosis 2007,
Geneva, Switzerland, P-M-097.
44. Al Dieri R.,
Alban S., Béguin S. et al. Thrombin generation for the control of
heparin treatment, comparison with the activated partial thromboplastin
time. J. Thromb. Haemost. 2004; 2(8): 1395—1401.
45. Al Dieri R.,
Alban S., Béguin S., Hemker H. C. Fixed dosage of low-molecular-weight
heparins causes large individual variation in coagulability, only partly
correlated to body weight. J. Thromb. Haemost. 2006; 4(1): 83—89.
46. Gerotziafas
G. T., Petropoulou A. D., Verdy E. et al. Effect of the anti-factor Xa
and anti-factor IIa activities of low-molecular-weight heparins upon the
phases of thrombin generation. J. Thromb. Haemost. 2007; 5(5): 955—962.
47. Stief T. W.
Inhibition of thrombin generation in recalcified plasma. Blood Coagul.
Fibrinolyt. 2007; 18: 751—760.
48. Altman R.,
Scazziota A., Santoro S. et al. Abciximab does not inhibit the increase
of thrombin generation produced in platelet-rich plasma in vitro by sodium
arachidonate or tissue factor. Clin. Appl. Thromb. Hemost. 2005; 11:
271—277.
49. Altman R.,
Scazziota A. , De Lourdes Herrera M. et al. Recombinant factor VIIa
, De Lourdes Herrera M. et al. Recombinant factor VIIa
reverses the inhibitory effect of aspirin or aspirin plus clopidogrel on in
vitro thrombin generation. J. Thromb. Haemost. 2006; 4(9): 2022—2027.
50. Baglin T.,
Luddington R., Brown K. et al. Incidence of recurrent venous
thromboembolism in relation to clinical and thrombophilic risk factors:
prospective cohort study. Lancet 2003; 362: 523—526.
51. Christiansen
S. C., Cannegieter S. C., Koster T. et al. Thrombophilia, clinical
factors, and recurrent venous thrombotic events. J. A. M. A. 2005; 293:
2352—2361.
52. Legnani C.,
Mattarozzi S., Cini M. et al. Abnormally short activated partial
thromboplastin time values are associated with increased risk of recurrence
of venous thromboembolism after oral anticoagulation withdrawal. Br. J.
Haematol. 2006; 134: 227— 232.
53. Eichinger S.,
Minar E., Bialonezyk C. et al. D-dimer levels and risk of recurrent
et al. D-dimer levels and risk of recurrent
venous thromboembolism. J. A. M. A. 2003; 290: 1071—1074.
54. Palareti G.,
Cosmi B., Legnani C. et al. D-dimer testing to determine the duration of
anticoagulation therapy. N. Engl. J. Med. 2006; 355(17): 1780—1789.
55. Baglin T.,
Palmer C. R., Luddington R., Baglin C. Unprovoked recurrent venous
thrombosis: prediction by D-dimer and clinical risk factors. J. Thromb.
Haemost. 2008; 6(4): 577—582.
56. Bruinstroop
E., Klok F. A., Van de Ree M. A. et al. Elevated D-dimer levels predict
recurrence in patients with idiopathic venous thromboembolism: a
meta-analysis. J. Thromb. Haemost. 2009; 7(4): 611—618.
57. Кречетова
А. В., Синауридзе Е. И., Васильев С. А. и др. Активация свертывания
крови в первые сутки сепсиса. Материалы конференции «Клиническая
гемостазиология и гемореология в сердечно-сосудистой хирургии», Москва;
2009: 258—259.
58. Синауридзе
Е. И., Горбатенко А. С., Грибкова И. В. и др. Гиперкоагуляция, вызванная
разбавлением плазмы искусственными плазмозамещающими растворами. Технологии
живых систем 2008; 5(1): 3—14.
Прогностическое значение отдельных маркеров гиперкоагуляции при сепсисе |
В.В. Осовских1, М.С. Васильева2, А.Е. Баутин2, Л.Н. Киселева1
1 ФГБУ Российский научный центр радиологии и хирургических технологий им. А.М. Гранова, Санкт-Петербург, Россия
2 ФГБУ Национальный медицинский исследовательский центр им. В.А. Алмазова, Санкт-Петербург, Россия
Для корреспонденции: Осовских Виктор Васильевич — канд. мед. наук, врач отделения анестезии и реанимации клиники РНЦРХТ им. А.М. Гранова, Санкт-Петербург, Россия; e-mail: [email protected]
Для цитирования: В.В. Осовских, М.С. Васильева, А.Е. Баутин, Л.Н. Киселева. Прогностическое значение отдельных маркеров гиперкоагуляции при сепсисе. Вестник интенсивной терапии им. А.И. Салтанова. 2020;3:66–73. DOI: 10.21320/1818-474X-2020-3-66-73
Вестник интенсивной терапии им. А.И. Салтанова. 2020;3:66–73. DOI: 10.21320/1818-474X-2020-3-66-73
Реферат
Актуальность. Сепсис является гетерогенным синдромом, вызванным разбалансированным ответом организма-хозяина на инфекцию, приводящим к органной дисфункции. Развивающаяся при этом коагулопатия имеет различную степень выраженности, а частота развития явного синдрома диссеминированного внутрисосудистого свертывания крови (ДВС), в зависимости от критериев диагностики, варьирует от 30 до 60 %. Хотя диагностика явного ДВС не вызывает трудностей, выявление предшествующей ему стадии гиперкоагуляции представляет проблему, поскольку не выявляется доступными скрининговыми тестами коагуляции. Отсутствие ранней диагностики препятствует развитию превентивной терапии ДВС.
Цель исследования. Оценить частоту выявления отдельных маркеров гиперкоагуляции у септических пациентов с гиперкоагуляционным паттерном тромбоэластометрии (ТЭМ) и их связь с исходом заболевания.
Материалы и методы. При скрининге пациентов с сепсисом с помощью ТЭМ были выявлены 85 пациентов с гиперкоагуляцией. Из образцов плазмы был выполнен тест генерации тромбина с добавлением тромбомодулина, были определены скрининговые показатели коагуляции, уровни физиологических антикоагулянтов, а также отдельные маркеры гиперкоагуляции. В дальнейшем были выделены группы выживших и умерших.
Результаты. В группу выживших включено 62 пациента, умерших — 19. В тесте генерации тромбина гиперкоагуляция была выявлена только в 7 случаях. Группы выживших и умерших достоверно не различались по степени снижения эндогенного тромбинового потенциала: 20 (10–25) % и 14 (10–31) % соответственно, и пиковой концентрации тромбина: 8 (2,9–16) % и 7 (3–18) % соответственно. Группы выживших и умерших достоверно различались: протеин С 79,5 ± 28 % и 64,9 ± 25 %, фактор VIII 226,4 ± 66 % и 276,6 ± 94 %, фактор фон Виллебранда 269 ± 129 % и 435 ± 181 %, антитромбин 82 (60–94) % и 65 (41–80) % и D-димер 2157 (1341–3964) мкг/л и 3253 (1911–6914) мкг/л соответственно.
Заключение. Пациенты с сепсисом, имеющие признаки гиперкоагуляции по критериям ТЭМ, имеют различные сочетания маркеров тромбофилии. Локальные скрининговые коагуляционные тесты не оказывают влияния на прогноз. Низкий уровень протеина С и антитромбина, а также высокий уровень фактора VIII, фактора фон Виллебранда, D-димера имеют умеренное прогностическое значение и потенциально могут повлиять на тактику терапии.
Ключевые слова: сепсис, тромбофилия, тромбоэластография, тромбин, тромбомодулин, диссеминированное внутрисосудистое свертывание
Поступила: 15.03.2020
Принята к печати: 02.09.2020
Читать статью в PDF
Введение
Сепсис является гетерогенным синдромом, вызванным разбалансированным ответом организма-хозяина на инфекцию, приводящим к органной дисфункции [1]. Патогенез коагулопатии, развивающейся на фоне сепсиса, включает несколько механизмов.
Снижение уровня антитромбина выявляется у половины пациентов с сепсисом, а дефицит протеина C — у подавляющего большинства. В физиологических условиях антитромбин ингибирует тромбин и другие факторы свертывания (VII, IX, X и XI), а протеин С, активированный комплексом тромбин–тромбомодулин на поверхности эндотелиоцитов, инактивирует факторы Vа и VIIIа, разрывая петли положительной обратной связи и выступая естественным антикоагулянтом. Состояние повышенной прокоагулянтной активности и нарушенного фибринолиза приводит к образованию фибриновых сгустков в микроциркуляторном русле и, как следствие, органной недостаточности [2, 3]. Коагулопатия имеет различную степень выраженности, при этом частота
В физиологических условиях антитромбин ингибирует тромбин и другие факторы свертывания (VII, IX, X и XI), а протеин С, активированный комплексом тромбин–тромбомодулин на поверхности эндотелиоцитов, инактивирует факторы Vа и VIIIа, разрывая петли положительной обратной связи и выступая естественным антикоагулянтом. Состояние повышенной прокоагулянтной активности и нарушенного фибринолиза приводит к образованию фибриновых сгустков в микроциркуляторном русле и, как следствие, органной недостаточности [2, 3]. Коагулопатия имеет различную степень выраженности, при этом частота
Принцип испытания
Тромбодинамика Принцип теста
Тромбодинамика — это как качественная, так и количественная оценка состояния свертывания образца плазмы крови посредством измерения и анализа пространственно-временной динамики роста фибринового сгустка в гетерогенной системе in vitro .
Метод тромбодинамики направлен на имитацию in vitro физиологических и патофизиологических процессов, которые происходят in vivo во время образования гемостатической пробки или тромбоза. Процесс коагуляции в тромбодинамике начинается с локальной поверхности, на которой иммобилизован тканевой фактор, имитирующий повреждение стенки кровеносного сосуда.
Процесс коагуляции в тромбодинамике начинается с локальной поверхности, на которой иммобилизован тканевой фактор, имитирующий повреждение стенки кровеносного сосуда.
В отличие от других стандартных тестов на коагуляцию, в тромбодинамическом анализе процесс роста фибринового сгустка развивается в пространстве и времени, а не только во времени. Фибриновый сгусток начинает формироваться, расти с поверхности, несущей тканевой фактор, но затем распространяется в объеме образца плазмы без взаимодействия с поверхностью, несущей тканевой фактор.
Метод тромбодинамики включен в систему анализатора тромбодинамики Т-2. Предварительно подготовленные образцы плазмы крови помещаются в каналы специальной измерительной кюветы. Затем в кювету погружается специальная активирующая вставка. Торцы активирующей вставки покрыты специальным покрытием, содержащим тканевый фактор (ТФ) — основной физиологический активатор коагуляции. Торец активирующей вставки имитирует поврежденную поверхность кровеносного сосуда:
Полученная серия фотографий показывает, как форма, размер и плотность фибринового сгустка меняются с течением времени.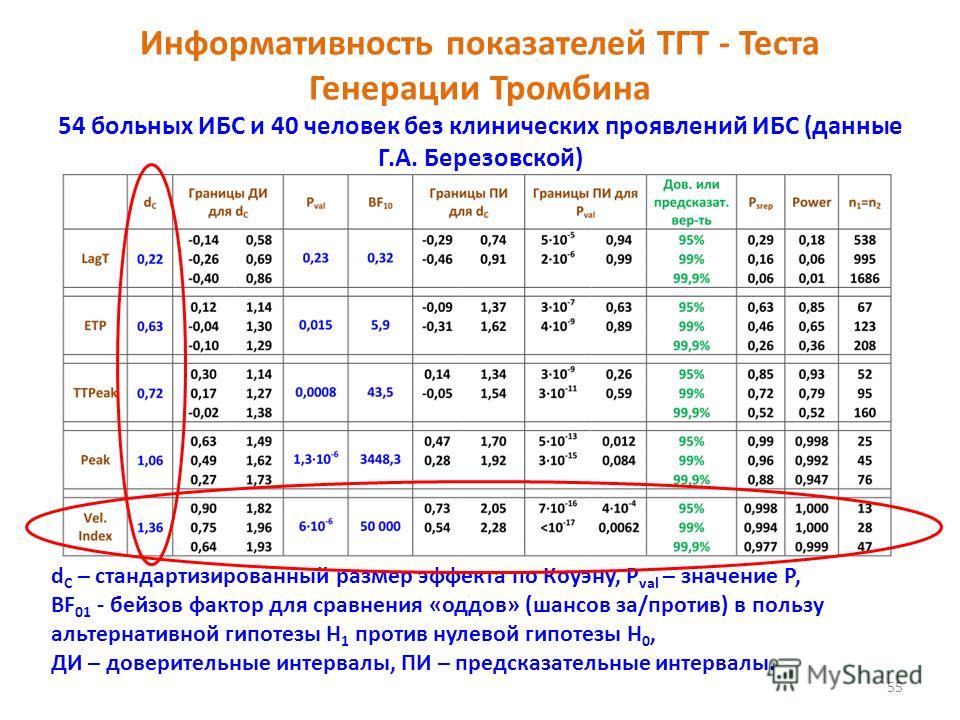 На основе записанных фотографий программное обеспечение Thrombodynamics Analytical рассчитывает численные параметры пространственно-временной динамики образования фибринового сгустка (Thrombodynamics parameters) . Как только образец плазмы крови входит в контакт с ТФ, начинается процесс коагуляции и начинается образование фибринового сгустка. растет от торца активирующей вставки в объем образца плазмы. Процесс образования фибринового сгустка регистрируется анализатором тромбодинамики Т-2 в режиме покадровой видеомикроскопии методом темнопольного светорассеяния.Цифровая камера анализатора Т-2 делает серию фотографий рассеяния света от кюветы.
На основе записанных фотографий программное обеспечение Thrombodynamics Analytical рассчитывает численные параметры пространственно-временной динамики образования фибринового сгустка (Thrombodynamics parameters) . Как только образец плазмы крови входит в контакт с ТФ, начинается процесс коагуляции и начинается образование фибринового сгустка. растет от торца активирующей вставки в объем образца плазмы. Процесс образования фибринового сгустка регистрируется анализатором тромбодинамики Т-2 в режиме покадровой видеомикроскопии методом темнопольного светорассеяния.Цифровая камера анализатора Т-2 делает серию фотографий рассеяния света от кюветы.
Принцип теста Thrombodynamics-4D
Thrombodynamics-4D assay — это новое поколение анализа тромбодинамики, доступное только для модели T2-T системы анализатора тромбодинамики. Помимо регистрации роста фибринового сгустка от иммобилизованного активатора коагуляции, Thrombodynamics-4D одновременно позволяет регистрировать пространственно-временную динамику тромбина, основного фермента каскада коагуляции. Регистрация образования тромбина основана на принципе флуоресцентной микроскопии. Флуорогенный субстрат для тромбина добавляется к образцу плазмы. Флуорогенный субстрат представляет собой молекулу 7-амино-4-метилкумарина (AMC), связанную с короткой аминокислотной последовательностью, которая необходима для распознавания субстрата тромбином. Связанные с подложкой, AMC не влияют на оптические свойства плазмы. В результате расщепления субстрата тромбином свободный AMC появляется в плазме и может флуоресцировать. Скорость образования AMC в каждой точке пропорциональна локальной концентрации тромбина.На основе записанных фотографий флуоресценции AMC программное обеспечение Thrombodynamics Analytical рассчитывает численные параметры пространственно-временной динамики образования тромбина (параметры thrombodynamics-4D).
Регистрация образования тромбина основана на принципе флуоресцентной микроскопии. Флуорогенный субстрат для тромбина добавляется к образцу плазмы. Флуорогенный субстрат представляет собой молекулу 7-амино-4-метилкумарина (AMC), связанную с короткой аминокислотной последовательностью, которая необходима для распознавания субстрата тромбином. Связанные с подложкой, AMC не влияют на оптические свойства плазмы. В результате расщепления субстрата тромбином свободный AMC появляется в плазме и может флуоресцировать. Скорость образования AMC в каждой точке пропорциональна локальной концентрации тромбина.На основе записанных фотографий флуоресценции AMC программное обеспечение Thrombodynamics Analytical рассчитывает численные параметры пространственно-временной динамики образования тромбина (параметры thrombodynamics-4D).
Каскад генерации тромбина — Siemens Healthineers Türkiye
Турция
Меню
Навигация
- Урун ве Хизметлер
НазадУрун ве Хизметлер
- Tıbbi Görüntüleme
НазадTıbbi Görüntüleme
- Анджиографи
- Bilgisayarlı Tomografi
- Floroskopi Ekipmanı
- Радясён Тедависи
- Manyetik Rezonans Görüntüleme
- Мамографи
- C-kol sistemleri
- Moleküler Görüntüleme
- Radyografi Sistemleri
- Восстановленные системы
- Роботик Рентген
- Ультрасон Чихазлары
- Юролоджи Экипмани
- Opsiyonlar ve Yükseltmeler
- Doğru Doz Bilgilendirme Merkezi
- Sağlık Yöneticileriyle İşbirliği
- Цифровая трансформация радиологии
- Развитие жизненного цикла активов
- Сессия по планированию активов
- Laboratuvar Diagnostiği
НазадLaboratuvar Diagnostiği
- Ателлика Урун Айлези
- Sistemlere Göre Test Menüleri
- Hastalıklara Göre Test Menüleri
- Лаборатувар Отомасёну
- Клиника Kimya Sistemleri
- Kötü Amaçlı Madde Kullanımı Testleri
- Hematoloji
- Гемостаз
- Иммуноанализ
- Enfeksiyon Hastalıkları Testleri
- Entegre Immunoassay ve Klinik Kimya Sistemleri
- Plazma Proteinleri
- Идрар Анализи
- Moleküler Diagnostik
- Siemens Sağlık Laboratuvarı
- Научные и клинические публикации
- Отвечая на призыв к борьбе с пандемией коронавируса
- Terapi Sistemleri
НазадTerapi Sistemleri
- Лучевая терапия
- Sağlık Bilgi Teknolojileri ve Altyapısı
НазадSağlık Bilgi Teknolojileri ve Altyapısı
- Портфель решений электронного здравоохранения
- Görüntüleme Yazılımları ve BT
- Диагностик БТ
- Аксесуарлар, OEM ve Elektronik
НазадАксесуарлар, OEM ve Elektronik
- Tıbbi Görüntüleme Aksesuar özümleri
- OEM продукты
- Медикал Электроник
- İşitme Cihazları
- Eğitim ve Öretim
НазадEğitim ve Öretim
- Медицинское образование — ключ к успеху
- Laboratuvar Diagnostiği Eğitimi
- PEPconnect
- Клинические специальные образовательные ресурсы
- Серия веб-семинаров «Здоровая мать / здоровый ребенок»
- Siemens Sağlık Akademi
- Müşteri Hizmetleri
НазадMüşteri Hizmetleri
- Bakım Onarım Anlaşmaları
- Taşıma ve Montaj Hizmetleri
- Эгитим Хизметлери
- Сервис Операсьон Меркези
- Йедек Парса Сатыш Хизметлери
- Kurumsal Hizmetler ve veözümler
НазадKurumsal Hizmetler ve veözümler
- Курумсал Департман Хизметлери
- Kurumsal Servisler ve özümlerin Faydaları
- Йонетилен Экипман Сервислери (МЧС)
- Siemens Entegre Servis Yönetimi
- Tıbbi Görüntüleme
- Klinik Uzmanlık ve Hastalıklar
НазадKlinik Uzmanlık ve Hastalıklar
- Nöroloji
НазадNöroloji
- Nörolojik Prosedürler
- Нёролоджик Бозуклуклар
- Onkoloji
НазадOnkoloji
- Kanser türleri
- Onkolojide Laboratuvar Diagnostiği
- Girişimsel Onkoloji Prosedürleri
- Визуализация в онкологии
- TRUS Destekli Prostat Biyopsisi için Sanal MR / Ultrason Rehberliği
- Onkolojide Klinik Referans Noktaları
- Сименс, 2016 ASCO Toplantısı’nda
- Cerrahi
НазадCerrahi
- Cerrahi Disiplinler
- Серрахи Урун Портфёю
- Hibrit Ameliyathaneyi Deneyimleyin — 360 ° Tur
- Тыбби Билги Кёшеси
- Cerrahi Konferansları
- Кадын Саглыги
НазадКадын Саглыги
- Kadın Sağlıına Yönelik Laboratuvar Diagnostii Çözümleri
- Kadın Sağlığı için Görüntüleme özümleri
- Daha yakından bakın.
 Ультразвуковой мамографический мем görüntüleme.
Ультразвуковой мамографический мем görüntüleme.
- Алерджи
НазадАлерджи
- Алерджи Хасталары Ичин
- Laborantlar için Bilgiler
- Хекимлер ичин Билджилер
- Eğitim ve Etkinlikler
- Микки ве Дев Качу
- Анеми
НазадАнеми
- Anemi Test Menüsü
- Анеми Тестлеринин Клиника Онеми
- Анеми Тюрлери
- Эк Кайнаклар
- ADVIA Centaur Active-B12 Testi Hizmetinizde!
- Отоиммюн Хасталыклар
НазадОтоиммюн Хасталыклар
- Роматоидный Артирит
- Otoimmün Test Portföyü
- Otoimmün Testlerin Klinik Önemi
- Бильгилендир
- Nöroloji
MedCrave онлайн
|
.

 Ультразвуковой мамографический мем görüntüleme.
Ультразвуковой мамографический мем görüntüleme.