- Новости
- Здоровье
- Семья и дети
- Питание и диеты
- Красота и мода
- Отношения
- Спорт
- О портале
Здоровье
- Диагностика
- Компьютерная томография
- МРТ диагностика
- Медицинские манипуляции
- Обследование организма
- Эндоскопия (эндоскопические исследования)
- Радионуклидная диагностика
- Рентген (рентгенологические исследования)
- Ультразвуковая диагностика (УЗИ)
- Лечение
- Операции
- Врачебные специальности
- Лечение болезней
- Обзор лекарственных средств
- Нетрадиционная медицина
- Стволовые клетки
- Физиотерапия
- Переливание крови
- Трансплантация
- Болезни
- Беременность, роды и послеродовой период
- Синдромы
- Хирургические болезни
- Болезни зубов (стоматология)
- Болезни молочных желез (маммология)
- Болезни суставов, мышц и соединительной ткани (ревматология)
- Рак (онкология)
- Болезни иммунной системы (иммунология)
- Болезни крови (гематология)
- Болезни сердца и сосудов (кардиология)
- Психическое здоровье (психиатрия)
- Травмы и отравления
- Болезни кожи и подкожной клетчатки (дерматология)
- Болезни легких, бронхов и плевры (пульмонология)
- Болезни уха, горла и носа (отоларингология)
- Болезни эндокринной системы и нарушения обмена веществ (эндокринология)
- Инфекции, передающиеся преимущественно половым путем (венерические болезни)
- Гинекологические болезни (гинекология)
- Болезни глаз (офтальмология)
- Болезни детей (педиатрия)
- Болезни печени и желчных путей
- Болезни прямой кишки и анальной области
- Болезни нервной системы (неврология)
- Болезни желудочно-кишечного тракта (гастроэнтерология)
- Инфекционные и паразитарные болезни
- Болезни мочеполовой системы
- Анализы
- Анализы на гормоны
- Гематологические исследования
- Генетические исследования
- Определение наркотиков
- Пренатальная диагностика
- ПЦР (Полимеразная цепная реакция, ПЦР-диагностика)
- Серологические исследования
- Токсикологические исследования
- Онкомаркеры
- Диагностика аутоиммунных заболеваний
- Иммунитет
- Исследование системы
Нарушение солевого обмена — причины появления симптома, способы лечения
Показать содержание
- Общие сведения
- Причины нарушения солевого обмена
- Гиперкалиемия
- Гиперкальцемия
Общие сведения
Водно-солевой обмен это совокупность процессов поступления воды и солей (электролитов) в организм, их всасывания, распределение во внутренних средах и выделение из организма. Суточное потребление человеком воды составляет около 2,5 л, из них около 1 л он получает с пищей. В организме человека 2/3 общего количества воды приходится на внутриклеточную жидкость и 1/3 — на внеклеточную. Часть внеклеточной воды находится в сосудистом русле (около 5% от массы тела), большая же часть внеклеточной воды находится вне сосудистого русла, это межуточная (интерстициальная), или тканевая, жидкость (около 15% от массы тела).
Кроме того, различают свободную воду, воду, удерживаемую коллоидами в виде так называемой воды набухания, т.е. связанную воду, и конституционную (внутримолекулярную) воду, входящую в состав молекул белков, жиров и углеводов и освобождающуюся при их окислении. Разные ткани характеризуются различным соотношением свободной, связанной и конституционной воды. За сутки почками выводится 1-1,4 л воды, кишечником — около 0,2 л; с потом и испарением через кожу человек теряет около 0,5 л, с выдыхаемым воздухом — около 0,4 л.
Системы регуляции водно-солевого обмена обеспечивают поддержание общей концентрации электролитов (натрия, калия, кальция, магния) и ионного состава внутриклеточной и внеклеточной жидкости на одном и том же уровне. В плазме крови человека концентрация ионов поддерживается с высокой степенью постоянства и составляет (в ммоль/л): натрия – 130-156, калия — 3,4-5,3, кальция — 2,3-2,75 (в т.ч. ионизированного, не связанного с белками — 1,13), магния — 0,7-1,2, хлора – 97-108.
По сравнению с плазмой крови и межклеточной жидкостью клетки отличаются более высоким содержанием ионов калия, магния, фосфатов и низкой концентрацией ионов натрия, кальция, хлора и ионов бикарбоната. Различия в солевом составе плазмы крови и тканевой жидкости обусловлены низкой проницаемостью капиллярной стенки для белков.
Точная регуляция водно-солевого обмена у здорового человека позволяет поддерживать не только постоянный состав, но и постоянный объем жидкостей тела, сохраняя практически одну и ту же концентрацию осмотически активных веществ и кислотно-щелочное равновесие.
Регуляция водно-солевого обмена осуществляется при участии нескольких физиологических систем. Сигналы, поступающие от специальных неточных рецепторов, реагирующих на изменение концентрации осмотически активных веществ, ионов и объема жидкости передаются в ЦНС, после чего выделение из организма воды и солей и их потребление организмом меняется соответствующим образом.
При увеличении концентрации электролитов и уменьшении объема циркулирующей жидкости (гиповолемии) появляется чувство жажды, а при увеличении объема циркулирующей жидкости (гиперволемии) оно уменьшается. Увеличение объема циркулирующей жидкости за счет повышенного содержания воды в крови (гидремия) может быть компенсаторным, возникающим после массивной кровопотери.
Гидремия представляет собой один из механизмов восстановления соответствия объема циркулирующей жидкости емкости сосудистого русла. Патологическая гидремия является следствием нарушения водно-солевого обмена, например при почечной недостаточности и др.
У здорового человека может развиться кратковременная физиологическая гидремия после приема больших количеств жидкости. Выведение воды и ионов электролитов почками контролируется нервной системой и рядом гормонов. В регуляции водно-солевого обмена участвуют и вырабатываемые в почке физиологически активные вещества — производные витамина D3, ренин, кинины и др.
Содержание натрия и организме регулируется в основном почками под контролем ЦНС через специфические натриорецепторы. реагирующие на изменение содержания натрия в жидкостях тела, а также волюморецепторы и осморецепторы, реагирующие на изменение объема циркулирующей жидкости и осмотического давления внеклеточной жидкости соответственно. Натриевый баланс в организме контролируется и ренин-ангиотензинной системой, альдостероном, натрийуретическими факторами.
При уменьшении содержания воды в организме и повышении осмотического давления крови усиливается секреция вазопрессина (антидиуретического гормона), который вызывает увеличение обратною всасывания воды в почечных канальцах. Увеличение задержки натрия почками вызывает альдостерон, а усиление выведения натрия: натрийуретические гормоны, или натрийуретические факторы. К ним относятся атриопептиды, синтезирующиеся в предсердиях и обладающие диуретическим, натрийуретическим действием, а также некоторые простагландины.
Причины нарушения солевого обмена
Причины нарушений могут быть разными, чаще всего негативно влияют на солевой обмен следующие факторы:
-
Малоподвижный образ жизни;
-
гормональная перестройка;
-
избыточное питание;
-
обильное употребление мясных, острых блюд и бобовых;
-
злоупотребление спиртными напитками;
-
курение;
-
переохлаждение организма.
Основное проявление нарушения солевого обмена это заболевания суставов: ограничение подвижности, в них, хруст и треск, боль в покое и при движениях, деформация, костные разрастания.
-
Нарушения водно-солевого обмена проявляются:
-
Накоплением жидкости в организме;
-
появлением отеков/дефицитом жидкости;
-
понижением/повышением осмотического давления крови;
-
нарушением электролитного баланса;
-
уменьшением/увеличением концентрации отдельных ионов;
-
изменением кислотно-щелочного состояния.
Знание патологических состояний, при которых меняется ионный состав плазмы крови или концентрация в ней отдельных ионов, важно для дифференциальной диагностики различных заболеваний.
Дефицит воды и ионов электролитов, в основном ионов Na+, К+ и Cl-, возникает при потере организмом жидкостей, содержащих электролиты. Отрицательный баланс натрия развивается при его выведении, превышающем поступление, в течение длительного времени. Потеря натрия, приводящая к патологии, может быть экстраренальной и ренальной.
Экстраренальная потеря натрия происходит главным образом через желудочно-кишечный тракт при следующих проявлениях:
Большая часть желудочно-кишечных соков почти изотонична плазме крови, поэтому если возмещение жидкости, потерянной через желудочно-кишечный тракт, проводится правильно, изменения осмоляльности внеклеточной жидкости обычно не наблюдаются. Однако если жидкость, теряемая при рвоте или поносе, возмещается изотоническим раствором глюкозы, развивается гипотоническое состояние и в качестве сопутствующего явления, уменьшение концентрации ионов К+ во внутриклеточной жидкости.
Наиболее часто потеря натрия через кожу происходит при ожогах. Потеря воды в этом случае относительно выше, чем потеря натрия, что приводит к развитию гетеросмоляльности внеклеточной и внутриклеточной жидкостей с последующим уменьшением их объемов. Почки способны экскретировать больше натрия, чем это необходимо для поддержания постоянства водно-солевого обмена, при нарушении механизмов регуляции реабсорбции натрия в почечных канальцах или при угнетении транспорта натрия в клетки почечных канальцев.
Значительная ренальная потеря натрия при здоровых почках может происходить при увеличении диуреза эндогенного или экзогенного происхождения, в т.ч. при недостаточном синтезе минералокортикоидов надпочечниками или введении диуретиков. При нарушении функции почек (например, при хронической почечной недостаточности) потеря натрия организмом происходит в основном вследствие нарушения его реабсорбции в почечных канальцах. Наиболее важными признаками дефицита натрия являются циркуляторные расстройства.
Дефицит воды с относительно небольшой потерей электролитов возникает за счет усиленного потоотделения при перегревании организма или при тяжелой физической работе. Вода теряется при длительной гипервентиляции легких, после приема мочегонных средств, не обладающих салуретическим эффектом.
Восстановление количества воды и изотоничности жидкости при патологическом обезвоживании организма достигается употреблением большого колличества питьевой воды или внутривенным введением изотонического раствора хлорида натрия и глюкозы. Потерю воды и натрия при повышенном потоотделении возмещают питьем подсоленной (0,5% раствор хлорида натрия) воды.
Избыток воды и электролитов проявляется в виде отеков. К основным причинам их возникновения относится избыток натрия во внутрисосудистом и интерстициальном пространствах, чаще при заболеваниях почек, хронической печеночной недостаточности, повышении проницаемости сосудистых стенок. При сердечной недостаточности избыток натрия в организме может превосходить избыток воды. Нарушенный водно-электролитный баланс восстанавливают ограничением натрия в диете и назначением натрийуретических мочегонных средств.
Избыток воды в организме с относительным дефицитом электролитов (так называемое водное отравление, или водная интоксикация, гипоосмолярная гипергидрия) образуется при введении в организм большого количества пресной воды или раствора глюкозы при недостаточном выделении жидкости; избыточное количество воды может поступить в организм также в виде гипоосмотической жидкости при проведении гемодиализа.
При водном отравлении развивается гипонатриемия, гипокалиемия, нарастает объем внеклеточной жидкости. Клинически это проявляется тошнотой и рвотой, усиливающейся после питья пресной воды, причем рвота не приносит облегчения; видимые слизистые оболочки у больных повышенно влажные. Оводнение клеточных структур мозга проявляется сонливостью, головной болью, подергиванием мышц, судорогами. В тяжелых случаях водного отравления развиваются отек легких, асцит, гидроторакс. Водную интоксикацию можно устранить внутривенным введением гипертонического раствора хлорида натрия и резким ограничением потребления воды.
Дефицит калия является в основном следствием его недостаточного поступления с пищей и потери при рвоте, длительных промываниях желудка, профузных поносах. Потеря калия при заболеваниях желудочно-кишечного тракта, таких как:
-
Опухоли пищевода;
-
опухоль желудка;
-
кишечная непроходимость;
-
свищи.
Связана в значительной степени с развивающейся при этих заболеваниях гипохлоремией, при которой резко возрастает общее количество калия, выделяемого с мочой. Значительные количества калия теряют больные, страдающие повторными кровотечениями любой этиологии.
Дефицит калия возникает у больных, продолжительно леченных кортикостероидами, сердечными гликозидами, мочегонными и слабительными средствами. Велики потери калия при операциях на желудке и тонкой кишке.
В послеоперационном периоде гипокалиемию чаще отмечают при вливании изотонического раствора хлорида натрия, т.к. ионы Na+ являются антагонистами ионов К+. Резко увеличивается выход ионов К+ из клеток во внеклеточную жидкость с последующим выведением их через почки при усиленном распаде белков; существенный дефицит калия развивается при болезнях и патологических состояниях, сопровождающихся нарушением трофики тканей и кахексией (обширные ожоги, перитонит, эмпиема, злокачественные опухоли). Дефицит калия в организме не имеет специфических клинических признаков.
Гипокалиемия сопровождается следующими симптомами:
-
сонливость;
-
апатия;
-
нарушения нервной и мышечной возбудимости;
-
снижение мышечной силы и рефлексов;
-
гипотония поперечно-полосатых и гладких мышц (атония кишечника, мочевого пузыря).
Важно оценить степень снижения содержания калия в тканях и клетках путем определения его количества в материале, полученном при биопсии мышцы, определения концентрации калия в эритроцитах, уровня экскреции его с суточной мочой, т.к. гипокалиемия не отражает всей степени дефицита калия в организме.Гипокалиемия имеет относительно четкие проявления на ЭКГ (снижение интервала Q-Т, удлинение отрезка Q-Т и зубца Т, уплощение зубца Т).
Гиперкалиемия
Дефицит калия возмещают введением в рацион продуктов, богатых калием. Это могут быть следующие продукты:
При недостаточности обогащенной калием диеты калий назначают внутрь в виде хлорида калия, панангина (аспаркама), внутривенных вливаний препаратов калия (при отсутствии анурии или олигурии). При быстрой потере калия его возмещение следует проводить в темпе, близком к темпу выведения ионов К+ из организма. Основные симптомы передозировки калия: артериальная гипотензия на фоне брадикардии, повышение и заострение зубца Т на ЭКГ, экстрасистолия. В этих случаях прекращают введение препаратов калия и назначают препараты кальция — физиологического антагониста калия, мочегонные средства, жидкость.
Гиперкалиемия развивается при нарушении выделения калия почками (например, при анурии любого генеза), выраженном гиперкортицизме, после адреналэктомии, при травматическом токсикозе, обширных ожогах кожи и других тканей, массивном гемолизе (в т.ч. после массивных переливаний крови), а также при усиленном распаде белков, например при гипоксии, кетоацидотической коме, при сахарном диабете и др. Клинически гиперкалиемия, особенно при ее быстром развитии, что имеет большое значение, проявляется характерным синдромом, хотя выраженность отдельных признаков зависит от генеза гиперкалиемии и тяжести основного заболевания.
Отмечаются следующие симптомы:
-
Сонливость;
-
спутанность сознания;
-
боль в мышцах конечностей;
-
боли в животе;
-
характерная боль языка.
Наблюдают вялые мышечные параличи, в т.ч. парез гладких мышц кишечника, снижение АД, брадикардию, расстройства проводимости и ритма сердца, сердечные тоны приглушены. В фазе диастолы может наступить остановка сердца. Лечение гиперкалиемии состоит в диете с ограничением продуктов, богатых калием, и внутривенном введении бикарбоната натрия; показано внутривенное введение 20% или 40% раствора глюкозы с одновременным введением инсулина и препаратов кальция. Наиболее эффективен при гиперкалиемии гемодиализ.
Натрий является основным катионом плазмы и экстрацеллю-лярной жидкости и в значительной степени определяет их осмотическое давление. Он выделяется в основном с мочой. Реабсорбцию натрия в дистальных канальцах почек усиливает альдостерон. Истинная гипонатриемия наблюдается при заболевании почек и передозироке диуретиков, а также при:
В этих случаях выявляется также недостаток натрия в тканях и тканевой жидкости.
Иное положение наблюдается у больных при развитии асцита, до лечения натрийуретиками. В подобных случаях гипонатриемия не отражает истинного баланса натрия, поскольку он в больших количествах накапливается в тканевой жидкости.
Введение таким больным внутривенно больших количеств натрия опасно из-за возможности развития отека легких. Успешное лечение асцита нередко приводит к исчезновению гипонатриемии у этих больных.
Гипонатриемия наблюдается у ряда больных острым алкогольным гепатитом, существенно реже — у больных острым вирусным гепатитом. В терминальной стадии заболеваний печени гипонатриемия наблюдается часто. Существенное снижение концентраций натрия в тканевой жидкости может вызывать серьезные повреждения гепатоцитов.
Калий играет важную роль в обменных процессах. Содержание калия в сыворотке крови регулируется преимущественно гормонами. Гипокалиемия нередко наблюдается при далеко зашедшем циррозе, а также при злокачественных опухолях печени. Выраженная гипокалиемия способствует развитию энцефалопатии у больных с тяжелым поражением печени. Эту форму энцефалопатии называли фальшивой комой Калька.
Гиперкальцемия
Кальций играет важную роль в обмене костной и соедини тельной ткани. Гиперкальциемия наблюдается при ряде заболеваний печени, протекающих с желтухой. Выраженные нарушения кальциевого обмена, приводящие к остеопорозу, выявляются при первичных и вторичных билиарных циррозах печени. Гипокальциемия наблюдается при молниеносном вирусном гепатите, особенно в случаях сопуствующего панкреатита и гипоальбуминемии.
Гипомагнезиемия встречается при тяжелых хронических (особенно алкогольных) заболеваниях печени и может способствовать развитию энцефалопатии. Наряду с этим отмечено, что очистительные клизмы с сульфатом магнезии у некоторых больных с печеночной энцефалопатией вызывали развитие гипермагнезиемии.
Нарушение водно-солевого обмена — причины появления симптома, способы лечения
Показать содержание
- Общие сведения
- Нарушение водно-солевого обмена
- Лечение и профилактика
Общие сведения
Человек состоит из воды в среднем на 70%. С возрастом этот процент немного уменьшается. У пожилых людей эта цифра составляет всего 55%. Сбалансированное поступление и выделение жидкостей в организме человека указывает на полноценный внутренний обмен. Суточная потребность в жидкости приблизительно 2, 5 л. Примерно половина жидкости поступает в организм вместе с едой. «Отработанная жидкость» выводиться из организма через почки.
Нарушение водно-солевого обмена
Нарушение водно-солевого обмена может быть связано с гипогидратацией. Нарушения с поступлением воды в организм приводит к даному заболеванию. Также может быть связано с потерей воды организмом. В запущенных случаях переростает в эксикоз. Он означает сильное обезвоживание организма.
Стабильная концентрация солей в организме, а также ее правильная регуляция является очень важной для правильной работы всего организма, как слаженной системы. Если природная система регуляциии дает сбой — это приводит к проблемам в других органах организма. Обмен жидкостей также способно поддерживать кислотно-щелочный баланс. Важную роль также играет содержание натрия в организме. Регуляция происходит при участии ЦНС (центральная нервная система). Обмен ионов натрия и калия отвечает за процессы возбуждения и торможения. Также очень важная роль принадлежит ионам хлора, работа которых зависит от обмена воды в организме, так как выводятся вместе с мочой.
Причины нарушения водно-солевого обмена:
- малоподвижный образ жизни;
- обильное употребление в пищу мяса, бобовых, острых блюд;
- переедание;
- курение и алкоголь;
- гормональная перестройка организма.
Кровопотери, которые означают уменьшение объема циркулируемой в органах крови, приводит к увеличению жидкостей в организме. Именно так действует регуляторный механизм копенсации. Помимо этого, к увеличению колличеству воды в организме приводит почечная недостаточность (поскольку почки помагают выводить жидкость из организма).
Переизбыток жидкостей в теле может вызвать физиологическую гидремию, но, как правило, влкючается механиз регуляции и излишняя жидкость выводиться. Также следует отметить, что употребление излишнего колличества жидкости также может вызвать физиологическую гидремию.
Сильная рвота, обильное потоотделение и уменьшение отеков также приводит к уменьшению жидкости в организме. Это приводит к потере ионов хлора и натрия. Стоит исключить самолечение мочегонными препаратами. Дело в том, что они оказывают существенное влияние на обмен жидкостей в организме.
Возможные причины повышенной концентрации хлора в организме:
- почечнокаменная болезнь;
- синдром гипервентеляции легких;
- чрезмерное употребление соли;
- гломерулонефрит.
Возможные причины повышенной концентрации натрия в организме:
- сердечная недостаточность;
- почечная патология;
- нарушения проницаемости сосудов.
Возможные причины повышенной концентрации калия в организме:
- сахарный диабет;
- травматический токсикоз;
- гемолиз эритроцитов.
Также при болезнях почек и нарушении их функционирования (выведение калия из организма) может возникать такое заболевание, как гиперкалиемия. Риск возникновения заболевания увеличивается при высокой концентрации калия в плазме (от 5 ммоль/л). Симптомы заболевания обычно проявляются болями в мышцах и сильной сонливостью. Также может проявляться пониженное давление, нарушение ритма сердца и паралич мышц кишечника и мочевого пузыря.
Симптомы нарушения водно-солевого обмена
При чрезмерной концентрации солей в организме у больного возникает сильное чувство жажды. Отеки или обезвоживание — одни из важнейших факторов нарушения обмена. Также следует следить за следующими показателями:
- изменение осмотического давления крови;
- изменения концентрации электролитов;
- кислотно-щелочный баланс организма.
Отеки указывают на переизбыток жидкостей в организме. Также могут наблюдаться сопутствующие симптомы: сонливость, головная боль, судороги. В целом, отеки довольно часто возникают при нарушениях обменных процессов в организме. Выделяют несколько факторов их развития:
- Онкотический. Развитие отеков в результате понижения давления крови. Важную роль в этом процессе играет снижение уровня белка. Кислородное голодание также возникает из-за некоторых заболеваний почек. Нарушения синтеза альбуминов также может привести к возникновению отеков.
- Осмотический. Связан с понижением давления в крови или наоборот — его повышение в межклеточой жидкости.
- Гиперосмия тканей. Может возникнуть, как следствие нарушений микроциркуляции. Отеки развиваются в очаге воспаления.
- Мембраногенный. В следствии возростания проницаемости сосудистой стенки формируется отек.
Лечение и профилактика
Лечением нарушений водно-солевого баланса может заниматься (в зависимости от причин заболевания) анестезиолог, терапевт и реанимолог. В большинстве случаев пациенту назначают специальную диету, ограничивают или исключают потребление определенных продуктов. Также пациентам назначают специальную лечебную гимнастику.
Также важно знать о профилактике заболевания. Очень важно соблюдать рациональную систему питания, избегать переедания, злоупотребления алкоголем. Важно вести активный образ жизни. Рекомендуем несколько профилактических упражнений:
Упражнение 1
Исходное положение — ноги согнуты в коленях, руки опущены. Поднять руки через стороны вверх — вдох, опустить — выдох. Повторить упражнение 3-4 раза в медленном темпе.
Упражнение 2
Руки согнуть, кисти к плечам. Круговые движения в плечевых суставах (с участием лопаток и ключиц) по и против часовой стрелки. По 6-8 раз в каждую сторону. Темп медленный, дыхание свободное.
Упражнение 3
Руки на поясе, голова опущена, подбородок касается груди. Поднять голову назад и вверх — вдох; вернуться в исходное положение — выдох. Упражнение выполнять безостановочно. Повторить 3-4 раза. Темп медленный.
Упражнение 4
Исходное положение — руки вверху, голова отклонена назад. Повернуть туловище направо, наклониться вниз, опустить руки, стараясь пальцами коснуться пола; вернуться в исходное положение. То же с поворотом налево. При наклоне подбородок поднят вверх. Упражнение повторить 5-7 раз в медленном темпе.
Упражнение 5
Сесть на стул, руки опущены. Сжимая и разжимая пальцы, выполнять движения в плечевых суставах наружу и внутрь; затем поднять руки вверх и опустить. Повторить упражнние 6-7 раз.
Упражнение 6
Исходное положение — упор лёжа. Выполнить отжимания от пола, выпрямляя и сгибая руки в локтях. Во время выполнения упражнения голову приподнять. Повторить в медленном темпе до 7 раз.
Упражнение 7
Опустить руки вдоль туловища. Поднимать и опускать руки перед собой одновременно сжимая пальцы в кулаки и разжимая. В медленном темпе повторить 4-6 раз. Дыхание свободное.
Так же очень полезна для профилактики нарушений водно-солевого обмена спортивная ходьба.
Нарушение водно-солевого баланса – симптомы и клинические проявления
Войти
Поиск
Найти
Главная
- Кулинария
- Бульоны и супы
- Горячие блюда
- Десерты
- Закуски
- Консервация
- Напитки
- Продукты питания
- Салаты
- Здоровье
- Медицина
- Ангиология
- Гастроэнтерология
- Гематология
- Гинекология
- Дерматология
- Инфекционные болезни
- Кардиология
- Лечебные диеты
- Неврология
- Нетрадиционная медицина
- Онкология
- Отоларингология
- Офтальмология
- Педиатрия
- Проктология
- Пульмонология
- Ревматология
- Стоматология
- Токсикология и Наркология
- Травматология
- Урология
- Фармакология
- Эндокринология
- Красота
- Женские прически
- Косметическая продукция
- Косметология
- Макияж
- Массаж и СПА
- Похудение
- Спорт и фитнес
- Уход за волосами
- Уход за кожей
- Уход за лицом
- Уход за ногтями
- Уход за телом
- Мода и стиль
- Аксессуары
- Женская одежда
- Модные тенденции
- Мужская одежда
- Обувь
- Шоппинг
- Ювелирные украшения
Водно-солевой обмен — нарушение и регуляция
Организм человека на 70% состоит из воды, большая часть которой располагается в клетках. Так как в жидких средах организма растворено множество различных электролитов, то водный и солевой обмены находятся в такой близкой взаимосвязи, что разделять их бессмысленно. Водно-солевой обмен включает в себя поступление, распределение, всасывание и выделение растворенных в жидкости минералов.
Вода поступает из внешней среды с напитками и едой (около 2 литров в сутки), а также образуется при метаболизме жиров, белков и углеводов (около полулитра в сутки). Минеральные вещества, необходимые для нормальной работы органов и систем включают натрий, калий, кальций, магний, хлор и фосфаты. Выделяется жидкость с растворенными в ней солями в основном через почки (1,5 литра), легкие (пол-литра), кишечник (0,2 литра) и кожу (пол-литра).
Регуляция водно-солевого обмена
Регуляция водно-солевого обмена
Основной способ регуляции водно-солевого обмена направлен на поддержание постоянства внутренней среды организма, или гомеостаза. Происходит она нейро-гуморальным путем, то есть в ответ на возбуждение определенных рецепторов нервной системы, выделяются гормоны, которые уменьшают или увеличивают выведение жидкости из организма.
Существует несколько типов рецепторов, участвующих в регуляции:
- Волюморецепторы, реагирующие на изменение внутрисосудистого объема;
- Осмотрецепторы, воспринимающие информацию об осмотическом давлении;
- Натриорецепторы, определяющие концентрацию натрия в средах организма.
Нервный импульс от воспринимающих центров передается в гипофиз и гипоталамус, расположенные в головном мозге. В ответ на это синтезируется и выделяется несколько видов гормонов:
- Антидиуретический гормон (вазопрессин), синтезируемый в нейронах гипоталамуса в ответ на повышение концентрации ионов натрия и увеличение осмотического давления внеклеточной жидкости. АДГ воздействует на собирательные трубочки и дистальные канальцы почек. При его отсутствии моча не концентрируется и в сутки ее может выделяться до 20 литров. Другой мишенью действия АДГ является гладкомышечная мускулатура. При высоких концентрациях происходит спазм сосудов и повышение давления.
- Альдостерон – самый активный минералокортикоид, образуется в коре надпочечников. Синтез и секреция стимулируются низкой концентрацией натрия и высокой калия. Альдостерон вызывает синтез транспортных белков натрия и калия. Благодаря этим переносчикам излишки калия удаляются с мочой, а ионы натрия задерживаются за счет реабсорбции в каналах нефронов.
- Предсердный натрийуретический фактор, на синтез которого влияет повышение артериального давления, осмолярности крови, частоты сердечных сокращений, уровня катехоламинов. ПНФ приводит к повышению почечного кровотока, увеличению скорости фильтрации и выведения натрия. Этот гормон снижает давление, так как вызывает расширение периферических артерий.
- Паратиреоидный гормон, отвечающий за метаболизм кальция и вырабатываемый околощитовидными железами. Стимулом для секреции является снижение концентрации кальция в крови. Он приводит к увеличению абсорбции калия почками и кишечником и выведению фосфатов.
Нарушения водно-солевого обмена
Нарушения водно-солевого обмена
Нарушения водно-солевого обмена вызывают задержку жидкости и появление отеков, либо обезвоживание. Основные причины включают:
- Гормональные нарушения, приводящие к нарушению работы почек;
- Недостаточное или избыточное поступление воды и минеральных веществ;
- Внепочечные потери жидкости.
Гормональные нарушения связаны с недостаточным или избыточным синтезом пептидов, участвующих в регуляции водно-солевого обмена.
- Несахарный диабет возникает при недостатке антидиуретического гормона, а также при различных нарушениях в системе передачи сигнала. При этом происходит неконтролируемое выделение мочи, быстро развивается дегидратация.
- Гиперальдостеронизм, возникающий при опухолях надпочечников, приводит к задержке натрия и жидкости и повышенному выведению калия, магния и протонов. Основные проявления – гипертензия, отеки, мышечная слабость.
К внепочечным потерям относят рвоту, понос, кровотечение. При ожоговой болезни и высокой температуре с поверхности тела испаряется большое количество жидкости, содержащей незначительные количества натрия. При гипервентиляции, возникающей в ответ на различные патологические состояния, потеря воды достигает двух литров. После приема мочегонных появляется дефицит воды и калия.
В результате нарушения водно-электролитного обмена может развиться:
- Дегидратация и гипергидратация, которые различаются в зависимости от осмолярности;
- Гипонатриемия и гипернатриемия;
- Избыток и дефицит калия;
- Нарушение всасывания и выведения магния и кальция.
Для диагностики нарушений водно-солевого обмена используют лабораторные методы, данные осмотра и анамнеза. В ряде случаев необходим анализ мочи.
Лечение водно-электролитных нарушений направлено на устранение жизнеугрожающих состояний, восстановление и поддержание гомеостаза.
Водно-солевой обмен включает в себя процесс поступления, перераспределения и выведения растворенных в жидкости электролитов. К основным ионам, содержащимся в организме, относятся натрий, калий, магний, кальций. Они присутствуют в виде хлоридов или фосфатов. Вода распределена между внутриклеточным пространством, плазмой крови и трансцеллюлярной жидкостью (спинномозговая, глазная и т.д.). Регуляция водно-электролитного обмена нейро-эндокринная и заключается в выработке определенных гормонов в ответ на раздражение периферических рецепторов. При различных нарушениях развивается гипергидратация и дегидратация, дефицит и избыток любых ионов. В тяжелых случаях коррекция нарушений проводится в стационаре.
что это такое, симптомы, лечение, причины, признаки
Нарушения водно-солевого баланса.
.
Причины нарушения водно-солевого баланса
Избыток воды за счет снижения осмолярности плазмы (рецепторы в печени и головном мозге) и увеличения ОЦК (рецепторы растяжения в правом предсердии) обычно ингибирует выброс АДГ и тем самым активирует диурез. АД, повышенное из-за гиперволемии, угнетает ренин-ангиотензин-альдостероновую систему. Одновременно стимулируется выброс натрийуретических факторов. Результат этого — натрийурия, которая с некоторым промедлением вызывает коррекцию объема и осмолярности плазмы. Избыток NaCl приводит к гиперосмолярности. Это, в свою очередь, увеличивает выброс АДГ и таким образом останавливает диурез и восстанавливает нормальную осмолярность.
Избыток воды и/или NaCl наблюдается, например, когда человек выпивает раствор с осмолярностью большей, чем максимальная осмолярность мочи (например, люди, пьющие морскую воду при кораблекрушении). Нарушение функции почек (СКФ+) также сопровождается уменьшением выведения воды и NaCl. Бесконтрольная инфузия изотонического раствора NaCl в таком состояние может привести к избытку NaCl и воды, в то время как инфузия изотонического раствора глюкозы ведет к накоплению избыточного количества воды, которая остается в организме после усвоения глюкозы. При чрезмерной выработке АДГ или минералокортикоидов (например, гормонпродуцирующей опухолью), даже если функция почек не нарушена, возникает избыток воды и NaCl. Если фильтрационное равновесие в периферической сосудистой сети нарушается, наблюдаются отеки. Это обусловливает уменьшению объема плазмы, что останавливает выделение натрийуретических факторов (предсердный натрийуретический фактор, уабаин) и стимулирует выработку АДГ, ренина, ангиотензина и альдостерона. Тогда задержка NaCl почками приводит к восстановлению объема плазмы и тем самым увеличению объема внеклеточной жидкости.
Недостаток воды и NaCl может быть результатом внешней потери жидкости, как в случае, например, после обильного потоотделения (лихорадка, жара), рвоты, диареи, потери крови, ожогов, осмотического диуреза (например, глюкозурия), назначения диуретиков, гипоальдостеронизма или развития состояния почки, теряющей соль. Почечная потеря воды может быть обусловлена дефицитом АДГ (центральный несахарный диабет) или нечувствительностью почек к воздействию АДГ (почечный несахарный диабет). Даже когда Внешний баланс сохранен, могут возникать опасные «внутренние потери», такие как перемещение объема плазмы в просвет кишки (при непроходимости кишечника), в брюшную полость (асцит) или периферические мягкие ткани (отек).
Избыток воды (гипергидратация) обязательно приводит к увеличению одного жидкостного пространства (компартмента) организма. Если одновременно с гипергидратацией наблюдается избыток NaCl (изотоническая или гипертоническая гипергидратация), растет внеклеточное пространство. При гипертонической гипергидратации внеклеточное пространство частично увеличивается за счет осмотического выхода воды из клеток. Если содержание NaCl в норме или понижено (гипотоническая гипергидратация), тогда преимущественно растет внутриклеточное пространство.
При нехватке воды (дегидратация) внеклеточное пространство уменьшается, особенно когда одновременно недостает и NaCl (изотоническая или гипотоническая дегидратация). При изолированном недостатке воды внутриклеточное пространство уменьшается (гипертоническая дегидратация), в то время как при изолированном недостатке NaCl — увеличивается (гипотоническая дегидратация).
Любое уменьшение внеклеточного пространства особенно опасно вследствие сокращения объема плазмы (гиповолемия). Признаками этого служат снижение центрального венозного давления, тахикардия и слабость. При падении АД нарушается функция почек, а выброс АДГ и альдостерона приводит к олигурии (опасность мочекаменной болезни). Увеличение внеклеточного объема, наоборот, ведет к росту АД, когда часть объема сохраняется в сосудистом пространстве. С другой стороны, внутрисосудистое разбавление белков стимулирует фильтрацию в периферических капиллярах и образование отеков, в наихудшем случае — отека легких.
Увеличение внутриклеточного объема чревато развитием отека головного мозга. Уменьшение внутриклеточного объема также приводит к нарушениям, главным образом ЦНС, которые могут прогрессировать до потери сознания и даже смерти.
Водно-солевой обмен человека: функции, нарушение и регуляция
Нормальная работа человеческого организма — это чрезвычайно сложный комплекс процессов, одним из которых является водно-солевой обмен. Когда он находится в нормальном состоянии, человек не спешит поправлять собственное здоровье, но как только появляются действительно заметные отклонения, многие сразу же пробуют применять разные меры. Чтобы этого избежать, лучше заранее понять, что такое водно-солевой обмен, и по какой причине так важно поддерживать его в нормальном состоянии.Также в этой статье мы рассмотрим основные нарушения и способы их устранения.
Что это?
Водно-солевой обмен — это совокупность других поступлений в организм электролитов и жидкостей, а также основных особенностей их ассимиляции и дальнейшего распределения во внутренних тканях, органах, средах, а также всех возможных процессов их удаления из организма. тело человека.
То, что сами по себе люди более чем наполовину состоят из воды, каждый знает с детства, и довольно интересно, что общее количество жидкости в нашем организме изменяется и определяется довольно большим количеством факторов, в том числе возрастом. , общая жировая масса и количество этих электролитов.Если новорожденный состоит из воды примерно на 77%, то взрослый мужчина составляет только 61%, а женщины — всего 54%. Столь низкое содержание воды в организме женщин связано с тем, что у них несколько иной водно-солевой обмен, а также имеется довольно большое количество жировых клеток.
Основные характеристики
Общее количество жидкости в организме человека устанавливается примерно следующим образом:
- Примерно 65% приходится на внутриклеточную жидкость, а также связано с фосфатом и калием, которые являются анионами и катионами, соответственно. .
- Примерно 35% — это внеклеточная жидкость, которая в основном находится в сосудистом русле и представляет собой тканевую и интерстициальную жидкость.
Среди прочего, стоит отметить, что вода в организме человека находится в свободном состоянии, постоянно удерживается коллоидами или принимает непосредственное участие в образовании и распаде молекул белков, жиров и углеводов. В разных тканях разное соотношение связанной, свободной и основной воды, что также напрямую влияет на регуляцию водно-солевого обмена.
По сравнению с плазмой крови, а также особой межклеточной жидкостью, ткань характеризуется наличием достаточно большого количества ионов магния, калия и фосфата, а также не такой большой концентрацией кальция, натрия, хлора и специальных бикарбонат-ионы. Это различие связано с тем, что стенка капилляров для белков имеет довольно низкую проницаемость.
Правильная регуляция водно-солевого обмена у здоровых людей обеспечивает не только поддержание постоянного состава, но и необходимого объема жидкостей организма, поддержание кислотно-щелочного баланса, а также практически идентичную концентрацию необходимых осмотически активных веществ. .
Положение
Необходимо правильно понимать, как работает водно-солевой обмен. Функции регуляции выполняют несколько физиологических систем. Во-первых, специализированные рецепторы реагируют на всевозможные изменения концентрации осмотически активных веществ, ионов, электролитов, а также количества присутствующей жидкости. В дальнейшем сигналы отправляются в центральную нервную систему человека, и только тогда организм начинает изменять потребление воды, а также выделение ее и необходимых солей, и, таким образом, водно-солевой обмен. система регулируется.
Выведение ионов, воды и электролитов почками под непосредственным контролем нервной системы и ряда гормонов. В процессе регуляции водно-солевого обмена также участвуют физиологически активные вещества, вырабатываемые в почках. Общее содержание натрия в организме постоянно регулируется, главным образом, почками под контролем центральной нервной системы через специализированные акцепторы натрия, которые постоянно реагируют на возникновение любых изменений содержания натрия в жидкостях организма, а также осморецепторы и объемные рецепторы, которые непрерывно анализируют осмотическое давление внеклеточной среды, а также объем циркулирующей жидкости.
За регулирование обмена калия в организме человека отвечает центральная нервная система, которая использует различные гормоны водно-солевого обмена, а также все виды кортикостероидов, включая инсулин и альдостерон.
Регуляция обмена хлора напрямую зависит от качества почек, и из организма его ионы выводятся в большинстве случаев вместе с мочой. Общее количество выведенного хлорида натрия напрямую зависит от используемого рациона человека, активности реабсорбции натрия, кислотно-щелочного баланса, состояния трубчатого аппарата почек, а также массы других элементов.Обмен хлоридов напрямую связан с обменом воды, поэтому на регулирование водно-солевого обмена в организме влияет множество других факторов нормального функционирования различных систем.
Что такое норма?
Огромное количество различных физиологических процессов, происходящих в нашем организме, напрямую зависит от общего количества солей и жидкостей. На данный момент известно, что для предотвращения нарушения водно-солевого обмена человеку следует в сутки выпивать около 30 мл воды на килограмм массы тела.Этого количества вполне достаточно, чтобы обеспечить наш организм нужным количеством минералов. В этом случае вода будет заливаться в различные клетки, сосуды, ткани и суставы, а также растворять и впоследствии вымывать всевозможные продукты жизнедеятельности. В большинстве случаев среднее количество воды, потребляемой человеком в течение дня, составляет почти не более двух с половиной литров, и такой объем часто составляет примерно так:
- до 1 литра мы получаем с пищей;
- до 1.5 литров — за счет питьевой простой воды;
- 0,3-0,4 литра — образование окислительной воды.
Регуляция водно-солевого обмена в организме напрямую зависит от баланса между количеством его поступления, а также выделением за определенный период времени. Если в течение дня в организм необходимо получить около 2,5 литров,
описание, нарушение, восстановление и рекомендации
Чтобы наш организм функционировал нормально, задействован сложный набор внутренних процессов.К одной из них относится поддержание нормального водно-солевого обмена. Когда он в порядке, у человека нет проблем со здоровьем, но его нарушение приводит к сложным и заметным отклонениям. Так что же такое водно-солевой баланс? Нарушение, его симптомы также будут рассмотрены.
общие сведения
Водно-солевым балансом считаются взаимодействующие между собой процессы поступления воды и солей в организм, их усвоения и распределения во внутренних органах и тканях, а также способы их удаления.
Всем известно, что человек более чем наполовину состоит из воды, количество которой в организме может быть разным. Это зависит от многих факторов, например, веса жира и возраста. Новорожденный на 77% состоит из воды, у взрослых мужчин этот показатель составляет 61%, а у женщин — 54%. Такое небольшое количество жидкости в женском организме связано с наличием большого количества жировых клеток. К старости такой показатель становится еще ниже.
Как вода распределяется в организме человека?
Распределение жидкости следующее:
- 2/3 от общего количества приходится на внутриклеточную жидкость;
- 1/3 от общего количества представлена внеклеточной жидкостью.
В организме человека вода находится в свободном состоянии, удерживается коллоидами или участвует в образовании и разложении молекул жиров, белков и углеводов.
По сравнению с межклеточной жидкостью и плазмокровью тканевая жидкость в клетках характеризуется более высокой концентрацией ионов магния, калия и фосфата и низким содержанием ионов хлора, натрия, кальция и ионов бикарбоната. Это различие объясняется тем, что стенка капилляров для белков имеет низкую проницаемость.Нормальный водно-солевой баланс у здорового человека помогает поддерживать не только стойкий состав, но и объем жидкости.
Регулирование водного баланса в почках и мочевыводящей системе
Почки необходимы для поддержания постоянного процесса
Как соль может повлиять на кровяное давление, сердце и почки — Основы здоровья от клиники Кливленда
Когда вы думаете об артериальном давлении, ваши почки могут не прийти в голову.
Клиника Кливленда — некоммерческий академический медицинский центр.Реклама на нашем сайте помогает поддерживать нашу миссию. Мы не поддерживаем продукты или услуги, не принадлежащие Cleveland Clinic. Политика
Но когда эти бобовидные органы получают повреждения или выходят из равновесия — возможно, из-за чрезмерного употребления соли — и ваше кровяное давление, и ваше сердце могут почувствовать последствия.
Ваши почки фильтруют более 120 литров крови каждый день. Они выводят токсины и нежелательную жидкость из клеток по всему телу, а затем отправляют их в мочевой пузырь.
Избыточное потребление соли может затруднить выведение почками жидкости, которая затем накапливается в организме и повышает кровяное давление.
Цикл повреждений: как влияет ваше сердце
Со временем чрезмерное потребление соли может привести к повышению артериального давления (гипертонии), которое приводит к сужению и жесткости кровеносных сосудов. Снижается приток крови и кислорода к ключевым органам. Таким образом, сердце изо всех сил пытается перекачивать кровь по всему телу, что еще больше увеличивает кровяное давление.
«Повышенное кровяное давление, особенно в течение длительного периода времени, создает невероятную нагрузку на сердце», — говорит кардиолог Люк Лаффин, доктор медицины. Это может увеличить левую насосную камеру сердца и ослабить сердечную мышцу (сердечная недостаточность).
Неконтролируемая гипертония также может повредить стенки артерий, которые начинают накапливать жир, что приводит к сердечным заболеваниям и, возможно, сердечному приступу или инсульту.
«Лучший способ предотвратить сердечный приступ — это предотвратить повреждение артерий», — сказал д-р.- говорит Лаффин.
Как гипертония влияет на почки
Эффект курицы или яйца можно наблюдать при высоком кровяном давлении и заболевании почек. Гипертония оказывает дополнительное давление на фильтрующие элементы почек, что может привести к образованию рубцов. Это ухудшает способность почек регулировать жидкость, что увеличивает кровяное давление.
«Если этот цикл не остановить, это может привести к заболеванию почек и почечной недостаточности», — говорит специалист по гипертонии Джордж Томас, доктор медицины, который является директором Центра нарушений артериального давления в отделении нефрологии и гипертонии.
«Высокое кровяное давление и неконтролируемый диабет — самые частые причины заболеваний почек».
К сожалению, подавляющее большинство людей с заболеванием почек не осознают, что у них оно есть. Признаки и симптомы могут быть связаны с другими состояниями и обычно появляются, когда почки уже начали отказывать. Вот симптомы, на которые следует обратить внимание:
- Необычная усталость.
- Проблемы со сном.
- Кожный зуд.
- Уменьшение мочеиспускания.
- Кровь или пена в моче.
- Отек лодыжек, стоп или вокруг глаз.
- Отсутствие аппетита, тошнота или рвота.
- Мышечные судороги.
- Путаница.
- Аномальный вкус.
Если вы испытываете какие-либо из этих симптомов — особенно если вы подвержены риску заболевания почек из-за того, что вам больше 60 лет, у вас высокое кровяное давление, диабет или семейная история почечной недостаточности, — поговорите со своим врачом об этом. здоровье почек и потребление соли.
Вопрос о солевой чувствительности
Соль по-разному действует на людей. «Некоторые люди могут потреблять натрий, не влияя на их кровяное давление», — говорит доктор Томас. «Но для других, кто« чувствителен к соли », даже небольшое увеличение потребления натрия наносит ущерб способности почек регулировать жидкость и повышает кровяное давление».
Чувствительность к соли наиболее распространена среди людей среднего и пожилого возраста, с избыточным весом или ожирением, а также среди афроамериканцев. С возрастом он также становится более распространенным.
Изменения в образе жизни могут помочь
Одна из первых вещей, которые порекомендует ваш врач, — это изменить свой образ жизни с помощью:
- Соблюдайте диету с низким содержанием натрия (Американская кардиологическая ассоциация рекомендует не более 1500 мг в день для большинства взрослых), особенно если вы из группы риска.
- Ограничение алкоголя.
- Регулярно тренируюсь.
- Поддержание здорового веса.
Даже при ограничении потребления соли и изменении образа жизни артериальное давление может оставаться повышенным.Примечания Лаффина. Помимо изменения образа жизни, лекарства часто также необходимы для снижения артериального давления. Примеры лекарств:
- Мочегонные средства, или пилюли с водой, которые усиливают мочеиспускание и помогают отвести лишнюю жидкость.
- Ингибиторы ангиотензинпревращающего фермента (АПФ) или блокаторы рецепторов ангиотензина II (БРА), которые помогают расслабить кровеносные сосуды.
Помимо того, что вы побуждаете держать гипертонию и диабет под контролем, ваш врач может ежегодно проверять вас на заболевание почек.
Работа с вашим врачом, чтобы убедиться, что потребление соли не повышает кровяное давление и не влияет на сердце и почки, может иметь серьезные последствия для вашего здоровья и долголетия.
Электролитный дисбаланс: симптомы, причины и лечение
Электролитный дисбаланс может возникнуть, если в организме слишком много или слишком мало воды.
Электролиты — это минералы в крови, тканях и других частях тела. Их название связано с тем, что у них есть электрический заряд.
Ниже вы узнаете, как может ощущаться электролитный дисбаланс, на что обращать внимание и когда обращаться за медицинской помощью.
Поделиться на PinterestПотребление напитка для регидратации может помочь восстановить баланс электролитов в организме.
Электролиты — это минералы, и они нужны организму для:
- баланса уровня воды
- перемещения питательных веществ в клетки
- удаления продуктов жизнедеятельности
- позволяют нервам посылать сигналы
- позволяют мышцам нормально расслабляться и сокращаться
- поддерживать Работа мозга и сердца
Люди получают электролиты из продуктов питания и напитков.Почки и печень помогают поддерживать баланс электролитов.
Если человек ест разнообразную пищу и пьет достаточно жидкости, уровень электролитов обычно остается на нужном уровне.
Примеры электролитов в организме человека включают:
- натрий
- калий
- кальций
- магний
- фосфат
- хлорид
- бикарбонат
Когда уровни электролитов становятся слишком высокими или низкими, это электролит дисбаланс.Это не болезнь, но это признак другой проблемы в организме.
Нарушение баланса электролитов может произойти, если человек обезвожен или в его теле слишком много воды.
Наиболее частыми причинами электролитного дисбаланса являются:
- рвота
- диарея
- недостаточное потребление жидкости
- недостаточное питание
- чрезмерное потоотделение
- определенные лекарства, такие как слабительные и мочегонные средства
- расстройства пищевого поведения
- Проблемы с печенью или почками
- Лечение рака
- Застойная сердечная недостаточность
Организм по-разному реагирует на электролитный дисбаланс.Эффекты могут зависеть от того, какие уровни электролитов несбалансированы, насколько серьезна проблема и есть ли у человека другие заболевания.
В одном исследовании были изучены данные 996 пациентов, получивших неотложную помощь по поводу электролитного дисбаланса.
Исследователи сообщают, что наиболее частыми симптомами были:
- лихорадка
- одышка
- спутанность сознания
- отек или вздутие живота
- учащенное сердцебиение
- нерегулярное сердцебиение
Другие симптомы могут включать:
- раздражительность
- усталость
- онемение
- покалывание
- мышечная слабость
- подергивание
- спазмы
- быстрые изменения артериального давления
- судороги
Дети имеют более высокий риск обезвоживания, чем взрослые, из-за их меньшего размера и быстрее метаболизм жидкостей и электролитов.
Если ребенок заболеет с сильной рвотой или диареей, у него может развиться электролитный дисбаланс, требующий медицинской помощи.
Ребенок с основным заболеванием, таким как болезнь щитовидной железы, сердца или почек, может иметь более высокий риск электролитного дисбаланса.
Если у ребенка есть риск обезвоживания или электролитного дисбаланса, немедленно обратитесь за медицинской помощью.
Исследования показали, что пожилые люди могут быть более подвержены обезвоживанию и электролитному дисбалансу, чем молодые люди.
Для этого есть много причин, в том числе:
- С возрастом почки могут потерять часть своих функций.
- Пожилые люди могут принимать несколько лекарств, например диуретики, которые могут изменять уровень электролитов.
- Они могут не получать достаточно еды или питья из-за инвалидности, отсутствия аппетита или жажды или из-за того, что у них нет постоянного доступа к еде и питью.
Опекуны и близкие должны внимательно следить за пожилыми людьми на предмет признаков обезвоживания.Возможно, им потребуется помочь убедиться, что человек ест и пьет достаточно.
Признаки обезвоживания у пожилых людей могут включать:
- сухость во рту, включая губы и язык
- запавшие глаза
- кожа, которая кажется сухой и менее упругой или эластичной
- сонливость
- спутанность сознания или дезориентация
- головокружение
- низкое кровяное давление
Если человек заболел коротким приступом рвоты или диареи или сильно потел, питьевая вода или раствор электролита, отпускаемый без рецепта, могут помочь восстановить баланс электролитов.
Многие напитки для пероральной регидратации доступны в магазинах, и их может быть достаточно, если у человека имеется легкий дисбаланс без серьезных симптомов.
У некоторых людей электролитный дисбаланс возникает из-за состояния здоровья, например болезни почек или сердца. В этом случае человек может исправить дисбаланс дома в течение нескольких дней или недель. Однако врач должен контролировать этот процесс, чтобы быть уверенным, что человек получает правильное количество.
Прием высоких уровней электролитов без консультации врача может создать еще один дисбаланс и привести к осложнениям со здоровьем.Кроме того, некоторым людям требуется дополнительное лечение для решения основной проблемы.
Если у человека более тяжелое заболевание почек, ему может потребоваться диализ для исправления электролитного дисбаланса.
Нарушение баланса электролитов может быть опасным. Если дисбаланс серьезный, человеку может потребоваться ввести электролиты через внутривенную или внутривенную линию в больнице.
Если человек считает, что у него может быть умеренное обезвоживание, он может попробовать напиток для регидратации, чтобы восстановить баланс электролитов.
Однако будьте осторожны с использованием спортивных напитков для этой цели. Некоторые эксперты считают, что спортивные напитки содержат слишком много сахара и слишком мало натрия, чтобы исправить дисбаланс.
Однако некоторые исследования показали, что спортивные напитки и растворы для пероральной регидратации дают аналогичные результаты у людей, которые тренировались в жаркую погоду.
Всемирная организация здравоохранения (ВОЗ) рекомендует готовить раствор для пероральной регидратации дома, а не покупать готовый напиток.
Рецепт включает в себя смешивание 1 литра воды с 1 чайной ложкой соли и 2 столовыми ложками сахара.Человек может использовать этот рецепт вместо купленного в магазине раствора электролита.
Поскольку дисбаланс электролитов может быть опасным для жизни, не пробуйте домашние средства, если у человека есть серьезные симптомы или какие-либо сопутствующие заболевания.
Младенцы, маленькие дети и пожилые люди также могут иметь более высокий риск серьезных осложнений. В таких случаях всегда консультируйтесь с врачом.
Здоровые взрослые с умеренным обезвоживанием могут обнаружить, что питье раствора для регидратации помогает им пополнить свои электролиты.
Если дисбаланс вызван состоянием здоровья, обратитесь к врачу.
Пожилые люди, младенцы и дети должны получать профессиональную помощь, если у них есть какие-либо симптомы электролитного дисбаланса или обезвоживания.
Промывание соленой водой: эффективность, риски и рецепты
Некоторые считают, что промывание соленой водой может облегчить запор, уменьшить вздутие живота или очистить толстую кишку. Промывание соленой водой становится все более популярным, но отзывы неоднозначны, и это домашнее средство может представлять опасность для здоровья.
Согласно некоторым источникам, промывание соленой водой может помочь с потерей веса, снятием задержки жидкости или улучшением пищеварения. С другой стороны, организм может очищаться без помощи приливов и смываний.
Перед тем, как начать какой-либо метод детоксикации, важно поговорить с врачом, чтобы узнать, подходит ли промывание соленой водой. Смыв соленой водой может быть опасен для людей с уже имеющимися заболеваниями.
Поделиться на PinterestПобочные эффекты промывки соленой водой могут включать тошноту и рвоту.
Изображение предоставлено: Poyraz 72, 2015
Промывание соленой водой используется для лечения запоров, вздутия живота и для детоксикации толстой кишки во время голодания на соке или аналогичной программы очищения.
Сторонники утверждают, что во время программ детоксикации, таких как приготовление сока, токсины попадают в толстую кишку и требуют удаления, что можно сделать с помощью промывки соленой водой.
Сторонники очищения толстой кишки связывают хронические медицинские проблемы с токсинами толстой кишки и поэтому рекомендуют очищение толстой кишки для повышения иммунной функции и уровня энергии.
Промывка соленой водой, предположительно, помогает толстой кишке вывести из организма старые фекалии и токсины, и в целом считается, что она безопасна.
Тем не менее, в медицинском сообществе есть некоторые, кто предостерегает от этой практики.
Есть некоторые побочные эффекты, которые могут быть серьезными, несмотря на то, что многие сторонники промывки соленой водой сообщают, что риски минимальны.
Общие побочные эффекты включают такие симптомы, как тошнота, рвота и слабость.
Потенциал обезвоживания и электролитного дисбаланса может привести к серьезным симптомам, в том числе:
- мышечные спазмы
- слабость
- подергивания
- онемение
- спутанность сознания
- чувство вялости
- судороги
- судороги
- сердце проблемы, включая изменения артериального давления и сердцебиения
Промывание соленой водой — не лучший вариант для всех, и обязательно поговорить с врачом перед тем, как начинать промывку соленой водой.Опять же, стоит помнить, что тело может очищаться и смываться без дополнительной помощи.
Людям с высоким кровяным давлением, проблемами пищеварения, заболеваниями почек или сердца или другими серьезными заболеваниями может быть рекомендовано избегать промывания солевым раствором и очищения толстой кишки.
Очищающие средства с соленой водой нельзя использовать беременным, кормящим женщинам или детям.
Существует ограниченное количество научных доказательств в пользу использования промывок солевым раствором.
Тем не менее, в Интернете есть много личного опыта, касающегося использования этого очищающего средства.Но в этой области необходимы дальнейшие исследования, чтобы определить эффективность и безопасность очищения толстой кишки.
Рецепт промывки обычной соленой водой включает смешивание не йодированной соли с водой путем:
- добавления 1-2 чайных ложек неионизированной соли, предпочтительно морской соли или розовой гималайской морской соли, в 1 литр воды и перемешивание до растворенный
- пить смесь в течение примерно 5 минут
Промывание соленой водой часто проводится натощак, например, первым делом утром, чтобы вызвать несколько дефекаций в течение дня.
Если человек пробует это средство, он должен удостовериться, что поблизости есть ванная в течение большей части дня.
Следует проявлять осторожность при рассмотрении возможности очищения толстой кишки слабительными средствами, таблетками, чаями и другими травяными добавками. Обычно они не регулируются Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) и не имеют существенных исследований в поддержку их использования.
Некоторые могут фактически мешать приему определенных лекарств или вызывать у некоторых людей серьезные побочные эффекты.
Альтернативы очищению соленой водой для поддержания здоровья толстой кишки, почек и печени могут включать:
- употребление диеты с высоким содержанием клетчатки, которая включает цельнозерновые, фрукты, овощи и бобовые
- прием пищевых добавок с клетчаткой для уменьшения запоров
- предотвращение обезвоживания путем питья большого количества воды в течение дня
- ограничение потребления алкоголя
- отказ от курения
- регулярные упражнения
- поддержание здорового веса тела для вашего типа телосложения
Промывание соленой водой становится все более популярным для облегчения симптомов запора и вздутия живота или то, что некоторые называют «токсичными» физическими симптомами.Однако крайне важно помнить, что в этой области необходимы дополнительные исследования для определения безопасности, эффективности и воздействия на организм.
Похоже, что в большинстве случаев промывки соленой водой относительно безопасны, но это верно не для всех. Тем, у кого высокое кровяное давление, проблемы с пищеварением, болезни почек или сердца, следует избегать промывания солевым раствором и очищения толстой кишки.
Перед тем, как пытаться очистить толстую кишку, пациенты должны обсудить со своим врачом безопасность в каждом случае.
Задержка воды (задержка жидкости): причины, симптомы и лечение
Задержка воды или жидкости возникает, когда существует проблема с одним или несколькими механизмами организма для поддержания уровня жидкости. Основные симптомы — отек и дискомфорт.
Система кровообращения, почки, лимфатическая система, гормональные факторы и другие системы организма — все это помогает поддерживать здоровый уровень жидкости. Однако, если проблема возникает с одной или несколькими из этих систем, может возникнуть задержка жидкости, также известная как отек.
Отек может поражать любую область тела. Это происходит по разным причинам.
В этой статье будут рассмотрены некоторые причины и симптомы задержки воды, а также способы их лечения.
Поделиться на Pinterest У человека с задержкой жидкости может наблюдаться скованность суставов, изменение цвета кожи и отек.
Симптомы задержки жидкости будут зависеть от пораженной области. Общие области включают голени, руки, живот и грудь.
В конечностях, ступнях и руках симптомы включают:
- отек
- изменение цвета кожи
- блестящая или опухшая кожа
- участки кожи, которые остаются вдавленными при нажатии пальцем, известные как точечный отек
- боли и болезненность в конечностях fu
- скованность в суставах
- прибавка в весе
Задержка жидкости также может влиять на следующие области:
Головной мозг
Также известная как гидроцефалия, задержка жидкости в головном мозге может вызывать симптомы, включая рвоту , помутнение зрения, головная боль и трудности с равновесием.Это может быть опасно для жизни.
Легкие
Избыток жидкости в легких или отек легких может указывать на серьезную проблему с сердцем или дыхательной системой. Симптомы включают затрудненное дыхание, кашель, боль в груди и слабость, поскольку это может повлиять на способность легких поставлять кислород в организм.
Многие отеки проходят без лечения.
Если есть основное заболевание, врач сосредоточит внимание на его лечении.
Диуретики — один из вариантов лечения.Они помогают почкам выводить жидкость из организма. Однако это обычно краткосрочный вариант, так как они могут вызывать побочные эффекты, такие как обезвоживание, повышенная задержка воды и повреждение почек.
Человеческое тело использует сложную систему для регулирования уровня воды. Гормональные факторы, сердечно-сосудистая система, мочевыводящая система, печень и почки — все это играет роль. Если есть проблема с какой-либо из этих частей, организм не может вытеснять жидкость должным образом.
В разделах ниже более подробно обсуждаются потенциальные причины задержки жидкости.
Повреждение капилляров
Капилляры — это крошечные кровеносные сосуды, играющие ключевую роль в управлении балансом жидкости в организме. Некоторые лекарства, например, от высокого кровяного давления, могут вызвать повреждение капилляров.
Капилляры доставляют жидкость к окружающим тканям. Эта жидкость, называемая интерстициальной жидкостью, снабжает клетки питательными веществами и кислородом. После доставки питательных веществ жидкость возвращается в капилляры.
При повреждении капилляров может возникнуть отек.Возможные проблемы включают изменения давления внутри капилляров и чрезмерную утечку стенок капилляров.
Если эти проблемы действительно возникают, слишком много жидкости может покинуть капилляры и попасть в промежутки между ячейками. Если капилляры не могут реабсорбировать жидкость, она останется в тканях, вызывая отек и задержку воды.
Некоторые люди испытывают этот тип отеков из-за редкого состояния, известного как синдром протекающих капилляров.
Застойная сердечная недостаточность
Насосное действие сердца помогает поддерживать нормальное давление в кровеносных сосудах.Если сердце человека перестает работать эффективно, его кровяное давление изменится. Из-за этого может возникнуть задержка жидкости.
Возможны отеки ног, ступней и лодыжек, а также жидкость в легких, что может вызвать длительный кашель или затрудненное дыхание.
Со временем застойная сердечная недостаточность может привести к проблемам с дыханием и нагрузке на сердце. Следовательно, это может быть опасно для жизни.
Лимфатическая система
Лимфатическая система переносит лимфу по телу.Лимфа — это жидкость, содержащая лейкоциты. Это помогает иммунной системе защитить организм от инфекции. Поскольку лимфатическая система доставляет и реабсорбирует лимфатическую жидкость, она также помогает организму поддерживать баланс жидкости.
Если проблема препятствует нормальной работе лимфатической системы, жидкость может начать накапливаться вокруг тканей. Это может вызвать отек различных частей тела, включая живот, лодыжки, ноги и ступни.
Рак, инфекции и закупорка могут вызвать проблемы с этой системой.
Что вызывает отек лодыжек? Узнайте больше здесь.
Почки
Почки фильтруют кровь и помогают поддерживать уровень жидкости в организме.
Отходы, жидкости и другие вещества попадают в крошечные канальцы в почках, которые действуют как фильтр. Кровоток реабсорбирует все, что организм может повторно использовать, и удаляет отходы с мочой.
Если почки не работают должным образом, они не могут удалять отходы, включая жидкости и натрий. Таким образом, жидкость останется в теле.
Например, люди с хроническим заболеванием почек могут заметить отеки в нижних конечностях, руках или лице.
Беременность
Во время беременности в организме содержится больше воды, чем обычно, и это может привести к отеку нижних конечностей, особенно в жаркую погоду или после длительного стояния.
Гормональные изменения и лишний вес в брюшной полости также могут способствовать.
Обычно это не опасно и обычно разрешается после доставки.
Однако, если опухоль внезапно усиливается, это может быть признаком преэклампсии. Это вид повышенного артериального давления, который может нанести вред как матери, так и плоду.
Всем, кто испытывает головную боль, рвоту, боль под ребрами или проблемы со зрением наряду с увеличенным отеком во время беременности, следует немедленно обратиться за медицинской помощью.
Отсутствие физической активности
У людей с ограниченными физическими возможностями или сидячим образом жизни могут развиться отеки в нижних конечностях.Недостаточное использование может привести к потере силы насоса икроножных мышц.
Это может помочь:
- держать ступни поднятыми
- носить компрессионные чулки
- выполнять упражнения, такие как подъем и опускание стоп или вращение лодыжек
ожирение
Люди с ожирением могут испытывать отеки из-за лишний вес они несут. Ожирение также увеличивает риск высокого кровяного давления, болезней почек и сердца, которые могут привести к отеку.
Ожирение также увеличивает риск метаболического синдрома, который включает диабет 2 типа, высокое кровяное давление и другие проблемы со здоровьем.
Недоедание
Альбумин — это белок, который помогает организму человека управлять жидкостями. Когда у человека наблюдается серьезный дефицит белка, его организму может быть труднее переместить интерстициальную жидкость обратно в капилляры.
Когда человек сильно истощается, у него может развиться квашиоркор. Симптомы включают потерю мышечной массы и увеличение живота.Это связано с задержкой жидкости в тканях тела.
Что такое недоедание и кто подвержен риску? Узнайте больше здесь.
Инфекции и аллергии
Роль иммунной системы заключается в защите организма от болезней и инфекций. Когда иммунная система обнаруживает нежелательного захватчика, такого как бактерии или аллерген, она начинает атаку. Воспаление — часть этого процесса.
Когда возникает воспаление, организм выделяет гистамин. Гистамин вызывает расширение промежутков между клетками стенок капилляров.Это делается для того, чтобы белые кровяные тельца, борющиеся с инфекцией, достигли места воспаления.
Однако он также может позволить жидкости просачиваться из капилляров в окружающие ткани. Отек, который возникает в результате этого, обычно кратковременный.
У людей с длительным воспалением может наблюдаться задержка воды.
Лекарства
Некоторые лекарства также могут вызывать задержку воды.
К ним относятся:
- блокаторы кальциевых каналов
- нестероидные противовоспалительные препараты
- габапентин
- некоторые гормональные препараты, в том числе некоторые противозачаточные таблетки
- преднизон, который является кортикостероидом
- некоторые лекарства от диабета
Все, кто у вас есть опасения по поводу отека при приеме лекарства, следует поговорить со своим врачом.Они могут изменить дозировку или предложить альтернативу.
Отек может развиться, когда человек принимает противозачаточные таблетки. Какие еще побочные эффекты могут возникнуть? Узнай здесь.
Гормональные нарушения
Гормональный дисбаланс может привести к задержке жидкости следующими способами:
Менструация : Изменения гормонального баланса могут привести к скоплению жидкости перед менструацией. В результате у человека может возникнуть вздутие живота и болезненность груди.
Проблемы с щитовидной железой : щитовидная железа выделяет гормоны, которые играют роль в регулировании уровня жидкости.Поэтому люди с заболеванием, поражающим щитовидную железу, могут испытывать задержку воды.
Синдром Кушинга : Это заболевание заставляет надпочечники вырабатывать слишком много стероидных гормонов, что приводит к отекам ног.
Зависимый отек возникает, когда жидкость скапливается в нижней части тела.


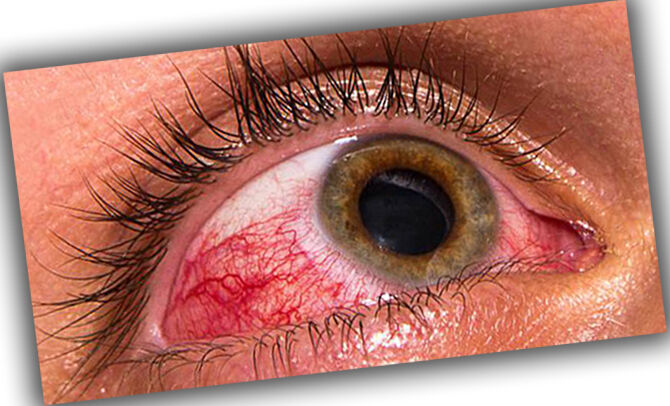




 Гемолитические анемии представляют собой совокупность как врожденных, так и приобретенных заболеваний, которые характеризуются разрушением эритроцитов внутри клеток или внутри сосудов. Аутоиммунные гемолитические анемии (сокращенно АГА) – наиболее часто встречающаяся разновидность гемолитических анемий.
Гемолитические анемии представляют собой совокупность как врожденных, так и приобретенных заболеваний, которые характеризуются разрушением эритроцитов внутри клеток или внутри сосудов. Аутоиммунные гемолитические анемии (сокращенно АГА) – наиболее часто встречающаяся разновидность гемолитических анемий. Тактика лечения аутоиммунной гемолитической анемии при остром течении заболевания или обострении хронического процесса в обязательном порядке включает гормонотерапию. Среднюю суточную дозу преднизолона 60-80 мг делят на три приема в соотношении 3:2:1. В случае неэффективности лечения она может быть увеличена до 150 мг и выше, а по мере улучшения состояния больного – постепенно снижается (на 2,5-5 мг в сутки с целью избежать рецидивов) сначала до половины начальной дозировки и далее вплоть до полной отмены препарата.
Тактика лечения аутоиммунной гемолитической анемии при остром течении заболевания или обострении хронического процесса в обязательном порядке включает гормонотерапию. Среднюю суточную дозу преднизолона 60-80 мг делят на три приема в соотношении 3:2:1. В случае неэффективности лечения она может быть увеличена до 150 мг и выше, а по мере улучшения состояния больного – постепенно снижается (на 2,5-5 мг в сутки с целью избежать рецидивов) сначала до половины начальной дозировки и далее вплоть до полной отмены препарата.









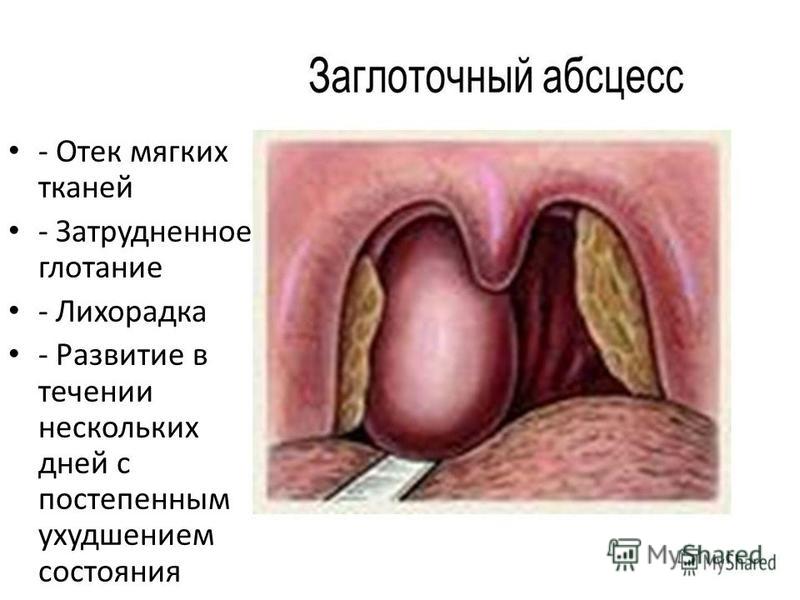
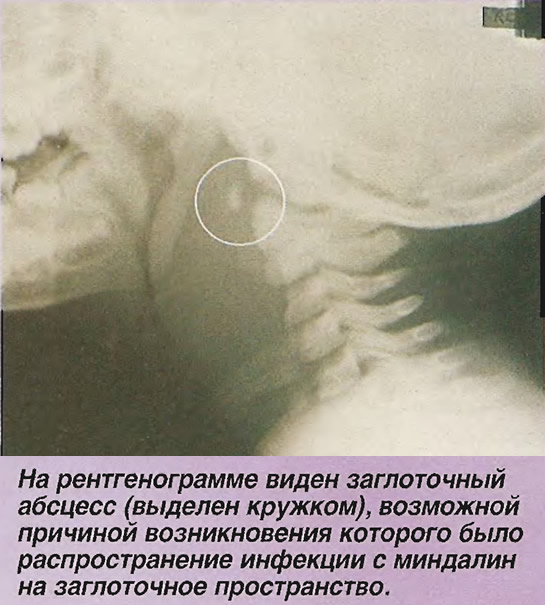
 Это может произойти в случае интубации трахеи, проглатывания инородного тела больших размеров или с острыми краями. Нередки случаи, когда симптомы заглоточного абсцесса проявлялись после проведения диагностики, к примеру, после введения эндоскопа в ротовую полость с целью изучения состояния органов пищеварительного тракта;
Это может произойти в случае интубации трахеи, проглатывания инородного тела больших размеров или с острыми краями. Нередки случаи, когда симптомы заглоточного абсцесса проявлялись после проведения диагностики, к примеру, после введения эндоскопа в ротовую полость с целью изучения состояния органов пищеварительного тракта; У детей симптоматика выражена более ярко, чем у взрослых людей. Важно при первых симптомах сразу посетить врача и провести лечение, чтобы избежать прогрессирования различных осложнений.
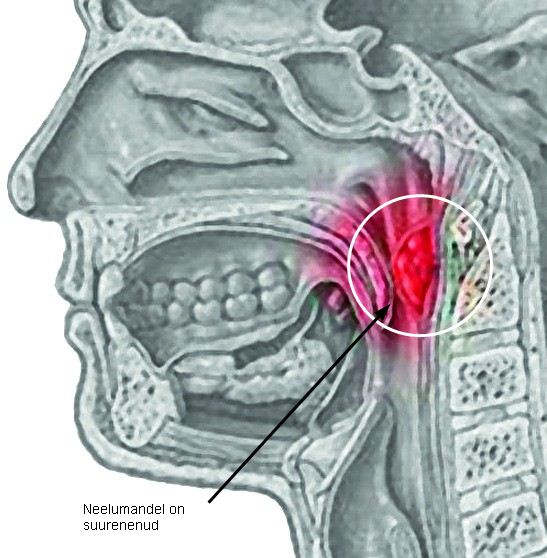
У детей симптоматика выражена более ярко, чем у взрослых людей. Важно при первых симптомах сразу посетить врача и провести лечение, чтобы избежать прогрессирования различных осложнений.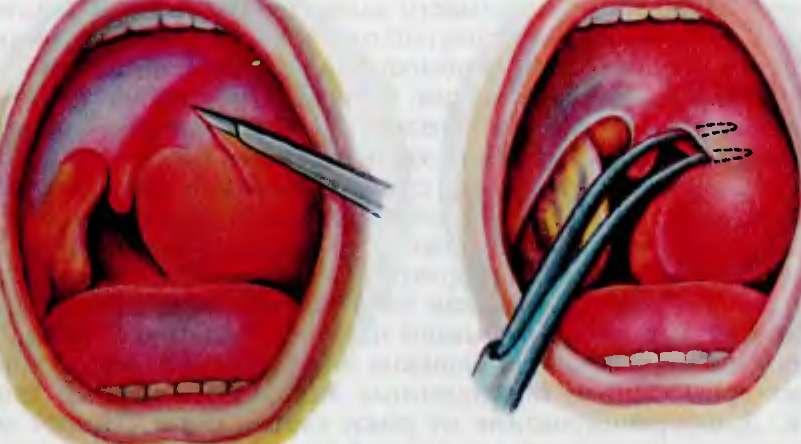 Если гнойное образование локализовано в ротовой части глотки, то у пациента отмечаются хрипы во время дыхательного процесса и нарушение функции глотания. При прогрессировании абсцесса в верхнем отделе отмечается гнусавость и проблемы с носовым дыханием.
Если гнойное образование локализовано в ротовой части глотки, то у пациента отмечаются хрипы во время дыхательного процесса и нарушение функции глотания. При прогрессировании абсцесса в верхнем отделе отмечается гнусавость и проблемы с носовым дыханием.
 Ведь бездействие грозит осложнениями: проблемами с дыханием, сепсисом, тромбозом, токсическим шоком и даже летальным исходом. Редакция UltraSmile.ru желает вам здоровья, а чтобы вы не оставили это опасное явление без внимания, постараемся рассказать все, что с ним связано.
Ведь бездействие грозит осложнениями: проблемами с дыханием, сепсисом, тромбозом, токсическим шоком и даже летальным исходом. Редакция UltraSmile.ru желает вам здоровья, а чтобы вы не оставили это опасное явление без внимания, постараемся рассказать все, что с ним связано. Она бывает настолько сильной, что невозможно даже без дискомфорта кушать пищу, особенно горячую, или глотать слюну. В жевательных мышцах происходит спазм и рот практически невозможно открыть без усилий,
Она бывает настолько сильной, что невозможно даже без дискомфорта кушать пищу, особенно горячую, или глотать слюну. В жевательных мышцах происходит спазм и рот практически невозможно открыть без усилий, Основных – всего пять.
Основных – всего пять.
 Когда увезли на скорой и вскрыли эту бяку, мне объяснили, что это абсцесс. Потом и уколы ставили с иммуноглобулином, у меня стафилококковый был. Хорошо болячка не заразная, как мне сказали, а то боялась, что мой ребенок тоже пострадает».
Когда увезли на скорой и вскрыли эту бяку, мне объяснили, что это абсцесс. Потом и уколы ставили с иммуноглобулином, у меня стафилококковый был. Хорошо болячка не заразная, как мне сказали, а то боялась, что мой ребенок тоже пострадает».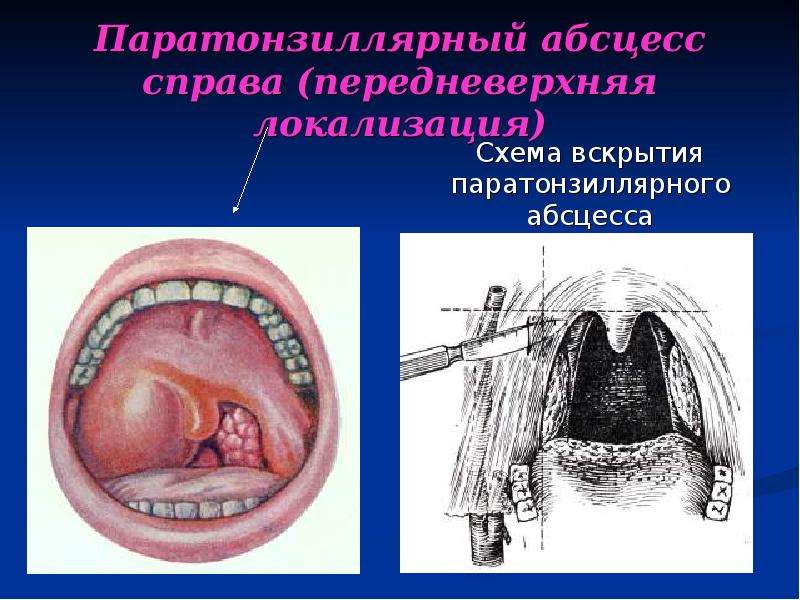 После на ранку накладывается резиновый дренаж, который защищает ее и предотвращает повторное скопление гноя.
После на ранку накладывается резиновый дренаж, который защищает ее и предотвращает повторное скопление гноя. Полоскания способствуют скорейшему заживлению раны: настои шалфея, ромашки или обычный солевой раствор в концентрации одна столовая ложка соли на 100 мл. теплой воды – полоскать горло 3-5 раз в сутки.
Полоскания способствуют скорейшему заживлению раны: настои шалфея, ромашки или обычный солевой раствор в концентрации одна столовая ложка соли на 100 мл. теплой воды – полоскать горло 3-5 раз в сутки. ..
.. В
В
 В
В
 Мы использовали коды CPT для разреза и дренирования абсцесса шеи, 21501 (разрез и дренаж, глубокий абсцесс или гематома, мягкие ткани шеи или грудной клетки), 42720 (разрез и дренаж абсцесса, заглоточный или парафарингеальный и интраоральный доступ) и 42725 ( разрез и дренаж абсцесса; заглоточный или парафарингеальный и наружный доступ), а также коды МКБ-9 для целлюлита и абсцесса шеи (682.1) и заглоточного абсцесса (478.24) для определения популяции пациентов. Существует много причин икоты, включая вздутие желудка, аэрофагия, вентрикулоперитонеальные шунты, гидроцефалия, рассеянный склероз, инсульты, эпидуральные или субдуральные гематомы, диффузное повреждение аксонов, церебральные ушибы, энцефалит, менингит, абсцессы головного мозга, нейросифилис, ларингит, фарингит, раздражение перепончатой оболочки среднего отдела глотки, абсцессы барабанной перепонки , эзофагит, бронхит, пневмония, инфаркт миокарда, перикардит, аневризмы аорты, перикардит, потеря места d провода кардиостимулятора, непроходимость тонкой кишки, перигепатит, поддиафрагмальный абсцесс, зоб, опухоль или киста шеи, барбитураты, стероиды, метилдопа и электролитные нарушения [1-4].Этот конкретный организм вызывает болезненную боль в горле («стрептококковое горло»), которая может длиться от трех до пяти дней, а также может вызывать долгосрочные осложнения, такие как ревматическая болезнь сердца, заглоточный абсцесс и постстрептококковый гломерулонефрит (заболевание почек). воспалительная реакция мускулатуры будет раздражать окружающие структуры, что приводит к симптоматике пациента, включая снижение подвижности шеи, боль в шее и одинофагию, которые в конечном итоге можно спутать с диагнозом заглоточного абсцесса или менингита (4).
Мы использовали коды CPT для разреза и дренирования абсцесса шеи, 21501 (разрез и дренаж, глубокий абсцесс или гематома, мягкие ткани шеи или грудной клетки), 42720 (разрез и дренаж абсцесса, заглоточный или парафарингеальный и интраоральный доступ) и 42725 ( разрез и дренаж абсцесса; заглоточный или парафарингеальный и наружный доступ), а также коды МКБ-9 для целлюлита и абсцесса шеи (682.1) и заглоточного абсцесса (478.24) для определения популяции пациентов. Существует много причин икоты, включая вздутие желудка, аэрофагия, вентрикулоперитонеальные шунты, гидроцефалия, рассеянный склероз, инсульты, эпидуральные или субдуральные гематомы, диффузное повреждение аксонов, церебральные ушибы, энцефалит, менингит, абсцессы головного мозга, нейросифилис, ларингит, фарингит, раздражение перепончатой оболочки среднего отдела глотки, абсцессы барабанной перепонки , эзофагит, бронхит, пневмония, инфаркт миокарда, перикардит, аневризмы аорты, перикардит, потеря места d провода кардиостимулятора, непроходимость тонкой кишки, перигепатит, поддиафрагмальный абсцесс, зоб, опухоль или киста шеи, барбитураты, стероиды, метилдопа и электролитные нарушения [1-4].Этот конкретный организм вызывает болезненную боль в горле («стрептококковое горло»), которая может длиться от трех до пяти дней, а также может вызывать долгосрочные осложнения, такие как ревматическая болезнь сердца, заглоточный абсцесс и постстрептококковый гломерулонефрит (заболевание почек). воспалительная реакция мускулатуры будет раздражать окружающие структуры, что приводит к симптоматике пациента, включая снижение подвижности шеи, боль в шее и одинофагию, которые в конечном итоге можно спутать с диагнозом заглоточного абсцесса или менингита (4).


 Данный синдром вызван рядом патологических отклонений. При таком состоянии костная ткань разрастается и повреждает окружающую клетчатку. Нарост находится в плантарной части пяточной кости. Размеры могут быть различны, а форма напоминает шпору, клюв или шип.
Данный синдром вызван рядом патологических отклонений. При таком состоянии костная ткань разрастается и повреждает окружающую клетчатку. Нарост находится в плантарной части пяточной кости. Размеры могут быть различны, а форма напоминает шпору, клюв или шип.

 Это абсолютно разные заболевания, которые находятся на разной части пятки, и лечение протекает по-разному. На основе рентгеновского фото врач определит стадию заболевания синдрома пяточной шпоры. На первой стадии присуща округлая форма. На второй стадии шпора меняет форму и увеличивается в размерах. В запущенной форме становится размером 12 мм и напоминает птичий клюв.
Это абсолютно разные заболевания, которые находятся на разной части пятки, и лечение протекает по-разному. На основе рентгеновского фото врач определит стадию заболевания синдрома пяточной шпоры. На первой стадии присуща округлая форма. На второй стадии шпора меняет форму и увеличивается в размерах. В запущенной форме становится размером 12 мм и напоминает птичий клюв.
 Согревающее действие улучшит кровообращение и наладит теплообмен. Самыми распространенными являются: Вольтарен, Хондроксид, Дексаметазон, Индометацин.
Согревающее действие улучшит кровообращение и наладит теплообмен. Самыми распространенными являются: Вольтарен, Хондроксид, Дексаметазон, Индометацин.

 Из-за этого могут развиться сопровождающиеся болевым синдромом патологии — трещины пяточной кости, ушибы, растяжения голеностопных связок и ахиллового сухожилия, пяточные шпоры и бурситы.
Из-за этого могут развиться сопровождающиеся болевым синдромом патологии — трещины пяточной кости, ушибы, растяжения голеностопных связок и ахиллового сухожилия, пяточные шпоры и бурситы. Поражение сосудов вызывает боль при ушибах, диабетической ангиопатии, остеомиелите и туберкулезе пяточной кости.
Поражение сосудов вызывает боль при ушибах, диабетической ангиопатии, остеомиелите и туберкулезе пяточной кости.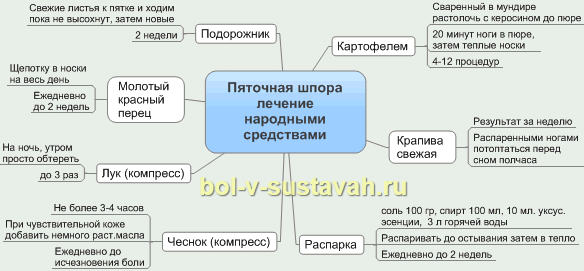 Врач подробно расспрашивает о жалобах, уточняя их характер, тип и локализацию боли, проводит осмотр больной области. Если есть необходимость, назначает ряд лабораторных тестов и инструментальных обследований. К ним относятся:
Врач подробно расспрашивает о жалобах, уточняя их характер, тип и локализацию боли, проводит осмотр больной области. Если есть необходимость, назначает ряд лабораторных тестов и инструментальных обследований. К ним относятся:
 В ходе операции иссекают омертвевшие ткани пяточной кости и дезинфицируют образовавшиеся внутри нее полости.
В ходе операции иссекают омертвевшие ткани пяточной кости и дезинфицируют образовавшиеся внутри нее полости. Так, у пациентов, страдающих плоскостопие очень часто выявляется пяточная шпора. В результате развития хронического воспалительного процесса в подошвенной̆ фасции, происходит отложение солей кальция. Основными пусковыми процессами являются:
Так, у пациентов, страдающих плоскостопие очень часто выявляется пяточная шпора. В результате развития хронического воспалительного процесса в подошвенной̆ фасции, происходит отложение солей кальция. Основными пусковыми процессами являются:


 Некоторые авторы указывают, что те или иные признаки можно выявить у 30% людей в возрасте старше 40 лет, однако боли, которые доставляют дискомфорт, будут беспокоить далеко не всех. В большинстве случаев (60-70%) с болями в пятках в медицинские учреждения обращаются женщины.
Некоторые авторы указывают, что те или иные признаки можно выявить у 30% людей в возрасте старше 40 лет, однако боли, которые доставляют дискомфорт, будут беспокоить далеко не всех. В большинстве случаев (60-70%) с болями в пятках в медицинские учреждения обращаются женщины. Воспаление распространяется на мышцы и слизистую сумку, находящуюся под пяточным бугром, ухудшается циркуляция крови и лимфы, нарушаются процессы восстановления. В результате в зоне воспаления около бугра пяточной кости откладываются соли кальция, ткани уплотняются, становятся ригидными, плотными, ещё больше нарушается их кровоснабжение, следовательно, и питание, развиваются дегенеративные изменения апоневроза.
Воспаление распространяется на мышцы и слизистую сумку, находящуюся под пяточным бугром, ухудшается циркуляция крови и лимфы, нарушаются процессы восстановления. В результате в зоне воспаления около бугра пяточной кости откладываются соли кальция, ткани уплотняются, становятся ригидными, плотными, ещё больше нарушается их кровоснабжение, следовательно, и питание, развиваются дегенеративные изменения апоневроза. Но пяточная шпора может быть связана с периодической или хронической болью — особенно при ходьбе, беге трусцой или беге — если воспаление развивается в месте образования шпоры. Как правило, причиной боли является не сама пяточная шпора, а связанное с ней повреждение мягких тканей.
Но пяточная шпора может быть связана с периодической или хронической болью — особенно при ходьбе, беге трусцой или беге — если воспаление развивается в месте образования шпоры. Как правило, причиной боли является не сама пяточная шпора, а связанное с ней повреждение мягких тканей. Хирургические методы включают:
Хирургические методы включают: Медицинский осмотр и другие диагностические изображения также могут использоваться для правильной диагностики основной причины легкой или сильной боли в пятке пациента. Однако важно отметить, что не все пяточные шпоры вызывают дискомфорт или боль. Фактически, по данным Американской академии хирургов-ортопедов, только около 5 процентов людей со шпорами пяточной кости будут испытывать боль в ногах.
Медицинский осмотр и другие диагностические изображения также могут использоваться для правильной диагностики основной причины легкой или сильной боли в пятке пациента. Однако важно отметить, что не все пяточные шпоры вызывают дискомфорт или боль. Фактически, по данным Американской академии хирургов-ортопедов, только около 5 процентов людей со шпорами пяточной кости будут испытывать боль в ногах.
 Подошвенный фасциит — это воспаление связки подошвенной фасции, которая проходит вдоль нижней части стопы, что может привести к развитию костных наростов вдоль пятки. Боль, связанная с этим типом пяточной шпоры, часто связана с самой воспаленной связкой. В этом случае врач может порекомендовать процедуру, известную как освобождение подошвенной фасции. Во время операции по освобождению подошвенной фасции хирург удаляет часть связки, чтобы уменьшить воспаление и боль.Эта процедура может быть эндоскопической или открытой. Эндоскопическая процедура будет включать меньшие разрезы и более короткое время восстановления, чем открытая процедура. Ваш врач порекомендует одну из этих процедур в зависимости от вашего конкретного состояния. В некоторых случаях может потребоваться удаление пяточной шпоры, хотя операция по удалению пяточной шпоры встречается реже, чем ранее упомянутые стратегии. Как правило, врач порекомендует удалить шпору пяточной кости только после того, как предыдущие варианты лечения пяточной шпоры не помогли облегчить симптомы.Во время операции по удалению пяточной шпоры хирург удалит отложения кальция вдоль пятки. Эта процедура также может быть открытой или эндоскопической, и, как и высвобождение подошвенной фасции, она будет варьироваться в зависимости от конкретного случая.
Подошвенный фасциит — это воспаление связки подошвенной фасции, которая проходит вдоль нижней части стопы, что может привести к развитию костных наростов вдоль пятки. Боль, связанная с этим типом пяточной шпоры, часто связана с самой воспаленной связкой. В этом случае врач может порекомендовать процедуру, известную как освобождение подошвенной фасции. Во время операции по освобождению подошвенной фасции хирург удаляет часть связки, чтобы уменьшить воспаление и боль.Эта процедура может быть эндоскопической или открытой. Эндоскопическая процедура будет включать меньшие разрезы и более короткое время восстановления, чем открытая процедура. Ваш врач порекомендует одну из этих процедур в зависимости от вашего конкретного состояния. В некоторых случаях может потребоваться удаление пяточной шпоры, хотя операция по удалению пяточной шпоры встречается реже, чем ранее упомянутые стратегии. Как правило, врач порекомендует удалить шпору пяточной кости только после того, как предыдущие варианты лечения пяточной шпоры не помогли облегчить симптомы.Во время операции по удалению пяточной шпоры хирург удалит отложения кальция вдоль пятки. Эта процедура также может быть открытой или эндоскопической, и, как и высвобождение подошвенной фасции, она будет варьироваться в зависимости от конкретного случая.
 Отросток пяточной шпоры простирается от нижней части пятки к своду (середине стопы). Эта область стопы называется подошвенной фасцией.
Отросток пяточной шпоры простирается от нижней части пятки к своду (середине стопы). Эта область стопы называется подошвенной фасцией.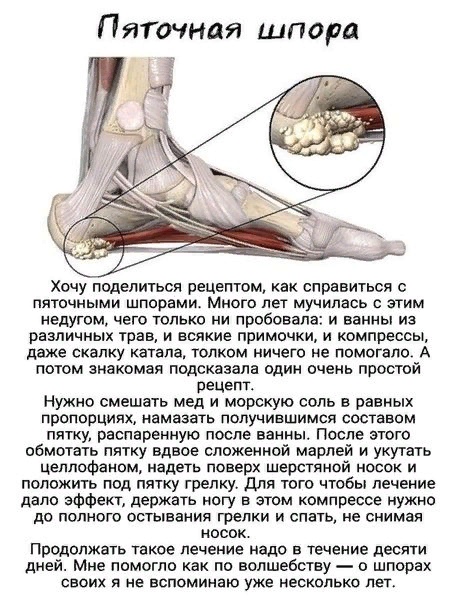



 Однако некоторые цифры показывают, что пяточные шпоры вызывают боль только в 5% случаев. Если кто-то испытывает боль в пятке, это может быть другая причина.
Однако некоторые цифры показывают, что пяточные шпоры вызывают боль только в 5% случаев. Если кто-то испытывает боль в пятке, это может быть другая причина. Человеку с подошвенным фасциитом может потребоваться временно уменьшить или прекратить такие занятия, как бег или аэробика.
Человеку с подошвенным фасциитом может потребоваться временно уменьшить или прекратить такие занятия, как бег или аэробика. AAOS рекомендует выполнять следующие упражнения в течение 4–6 недель под наблюдением врача.
AAOS рекомендует выполнять следующие упражнения в течение 4–6 недель под наблюдением врача. Неоднократный разрыв или повреждение мембраны, покрывающей пяточную кость, со временем приводит к накоплению твердых отложений кальция.
Неоднократный разрыв или повреждение мембраны, покрывающей пяточную кость, со временем приводит к накоплению твердых отложений кальция.


 Инфекция поражает не только дыхательные пути, но и многие другие органы, поскольку возбудитель может проникнуть в организм разными путями. Стоит учитывать, что источник инфекции весьма заразный, поэтому требуется принимать меры еще до заражения.
Инфекция поражает не только дыхательные пути, но и многие другие органы, поскольку возбудитель может проникнуть в организм разными путями. Стоит учитывать, что источник инфекции весьма заразный, поэтому требуется принимать меры еще до заражения. Кроме того, по этим причинам выделение крови при кашле может наблюдаться не только у людей с туберкулезом, но и при любом другом заболевании органов дыхания.
Кроме того, по этим причинам выделение крови при кашле может наблюдаться не только у людей с туберкулезом, но и при любом другом заболевании органов дыхания. При неблагоприятных факторах сосуд может быть поврежден, из-за чего кровь начинает попадать в бронхи. От величины сосуда зависит количество крови, иногда слишком крупный поврежденный сосуд заполняет бронхи и трахеи до такого состояния, что пациент не может спокойно дышать. Это может вызвать смерть от удушья, поэтому больному требуется срочная медицинская помощь.
При неблагоприятных факторах сосуд может быть поврежден, из-за чего кровь начинает попадать в бронхи. От величины сосуда зависит количество крови, иногда слишком крупный поврежденный сосуд заполняет бронхи и трахеи до такого состояния, что пациент не может спокойно дышать. Это может вызвать смерть от удушья, поэтому больному требуется срочная медицинская помощь. Наличие большого объема крови в органах дыхания препятствует нормальному дыханию, если не остановить вовремя кровотечение, больной может задохнуться.
Наличие большого объема крови в органах дыхания препятствует нормальному дыханию, если не остановить вовремя кровотечение, больной может задохнуться. После осмотра врач определит причины недуга и назначит соответствующее лечение.
После осмотра врач определит причины недуга и назначит соответствующее лечение.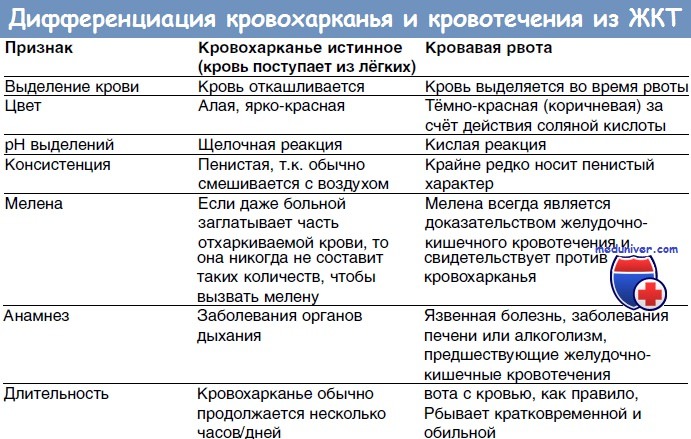



 В зависимости от состояния инфицированного, врач принимает решение, проводить операцию во время кровотечения или дождаться его остановки.
В зависимости от состояния инфицированного, врач принимает решение, проводить операцию во время кровотечения или дождаться его остановки. Стресс, нервные заболевания и физическое перенапряжение нужно старательно избегать.
Стресс, нервные заболевания и физическое перенапряжение нужно старательно избегать. Перечислим основные причины кровохарканья:
Перечислим основные причины кровохарканья: Помимо этого будут присутствовать жалобы на повышенную температуру, потливость, потерю веса, слабость, быструю утомляемость и кашель.
Помимо этого будут присутствовать жалобы на повышенную температуру, потливость, потерю веса, слабость, быструю утомляемость и кашель.

 Прогрессирование сердечной недостаточности и застоя в лёгких приводят к рецидиву кровохарканья. Специфическая терапия с применением кадиотоников, диуретиков и других лекарственных препаратов заметно улучшает состояние пациентов и прекращает выделение крови из дыхательных путей.
Прогрессирование сердечной недостаточности и застоя в лёгких приводят к рецидиву кровохарканья. Специфическая терапия с применением кадиотоников, диуретиков и других лекарственных препаратов заметно улучшает состояние пациентов и прекращает выделение крови из дыхательных путей.

 Наибольшую опасность представляют лекарственные средства из группы транквилизаторов. Они обладают миорелаксирующими эффектами (расслабляют мышцы, снимают напряжение), в том числе и на диафрагму.
Наибольшую опасность представляют лекарственные средства из группы транквилизаторов. Они обладают миорелаксирующими эффектами (расслабляют мышцы, снимают напряжение), в том числе и на диафрагму. Кроме того, в случае установления факта, что пациент болеет любой из форм туберкулёза, его переводят в специализированное противотуберкулёзное учреждение.
Кроме того, в случае установления факта, что пациент болеет любой из форм туберкулёза, его переводят в специализированное противотуберкулёзное учреждение. Могут применять Аминокапроновую или Транексамовую кислоты.
Могут применять Аминокапроновую или Транексамовую кислоты. Иногда при срочной бронхоскопии удается тампонировать кровоточащий сосуд специальной кровоостанавливающей (гемостатической) губкой. В ряде случаев встает вопрос о срочном хирургическом вмешательстве. При легочном кровотечении иногда производят переливание крови. Необходимо постоянно находиться у постели больного до полного прекращения кровотечения, контролируя пульс и измеряя давление. Ухаживая за больным с кровохарканьем, необходимо помнить, что банки, горчичники, грелки на грудную клетку противопоказаны. Пищу больному давать в холодном виде, полужидкую, легкоусвояемую, содержащую витамины. Одним из симптомов заболевания органов дыхания являются боли в грудной клетке, обычно они бывают при плеврите. При появлении болей в грудной клетке необходимо: помочь больному выбрать удобное положение, хорошо укрыть его, по назначению врача поставить банки, горчичники, если боли не уменьшаются в результате отвлекающей терапии – дать обезболивающие препараты. Заболевания органов дыхания очень часто сопровождаются лихорадкой и ознобом.
Иногда при срочной бронхоскопии удается тампонировать кровоточащий сосуд специальной кровоостанавливающей (гемостатической) губкой. В ряде случаев встает вопрос о срочном хирургическом вмешательстве. При легочном кровотечении иногда производят переливание крови. Необходимо постоянно находиться у постели больного до полного прекращения кровотечения, контролируя пульс и измеряя давление. Ухаживая за больным с кровохарканьем, необходимо помнить, что банки, горчичники, грелки на грудную клетку противопоказаны. Пищу больному давать в холодном виде, полужидкую, легкоусвояемую, содержащую витамины. Одним из симптомов заболевания органов дыхания являются боли в грудной клетке, обычно они бывают при плеврите. При появлении болей в грудной клетке необходимо: помочь больному выбрать удобное положение, хорошо укрыть его, по назначению врача поставить банки, горчичники, если боли не уменьшаются в результате отвлекающей терапии – дать обезболивающие препараты. Заболевания органов дыхания очень часто сопровождаются лихорадкой и ознобом. При повышении температуры, сопровождающейся ознобом, медсестра должна хорошо укрыть больного, положить теплые грелки к ногам, напоить его крепким чаем. Необходимо наблюдать за пульсом, артериальным давлением, чтобы своевременно предупредить развитие острой сосудистой и сердечной недостаточности. Работа среднего персонала в пульмонологическом отделении отличается определенной спецификой. Для профилактики вспышек внутрибольничных инфекций медсестра должна проводить ряд санитарно-гигиенических мероприятий:
При повышении температуры, сопровождающейся ознобом, медсестра должна хорошо укрыть больного, положить теплые грелки к ногам, напоить его крепким чаем. Необходимо наблюдать за пульсом, артериальным давлением, чтобы своевременно предупредить развитие острой сосудистой и сердечной недостаточности. Работа среднего персонала в пульмонологическом отделении отличается определенной спецификой. Для профилактики вспышек внутрибольничных инфекций медсестра должна проводить ряд санитарно-гигиенических мероприятий:
 В ряде случаев при подозрении на туберкулез производится посев мокроты на специальные среды. Для выявления возбудителей воспалительных заболеваний дыхательной системы и их чувствительности к антибиотикам мокроту берут в специальную чашку Петри, заполненную соответствующей питательной средой – кровяным агаром, сахарным бульоном и др. При взятии мокроты на атипичные клетки (опухолевые) мокроту сразу необходимо сразу отправить в лабораторию, т. к. эти клетки быстро разрушаются.
В ряде случаев при подозрении на туберкулез производится посев мокроты на специальные среды. Для выявления возбудителей воспалительных заболеваний дыхательной системы и их чувствительности к антибиотикам мокроту берут в специальную чашку Петри, заполненную соответствующей питательной средой – кровяным агаром, сахарным бульоном и др. При взятии мокроты на атипичные клетки (опухолевые) мокроту сразу необходимо сразу отправить в лабораторию, т. к. эти клетки быстро разрушаются.
 Количество дыханий в 1 мин (частота дыхания) у взрослого здорового человека колеблется от 16 до 20. Подсчет числа дыханий производится по движению грудной или брюшной стенки незаметно для больного.
Количество дыханий в 1 мин (частота дыхания) у взрослого здорового человека колеблется от 16 до 20. Подсчет числа дыханий производится по движению грудной или брюшной стенки незаметно для больного.







 Этиология болезни Бехчета не установлена. Существует несколько предположений возникновения заболевания. Это влияние токсических веществ, вирусные инфекции, генная предрасположенность.
Этиология болезни Бехчета не установлена. Существует несколько предположений возникновения заболевания. Это влияние токсических веществ, вирусные инфекции, генная предрасположенность. Главная сложность диагностики болезни Бехчета находится в том, что ее клиническое течение чрезвычайно изменчиво.
Главная сложность диагностики болезни Бехчета находится в том, что ее клиническое течение чрезвычайно изменчиво. Риск осложнений при патологии зависит от самочувствия человека, выраженности недуга и прочих обстоятельств. В одном случае синдром незаметен, в то время как в другом наступает смерть.
Риск осложнений при патологии зависит от самочувствия человека, выраженности недуга и прочих обстоятельств. В одном случае синдром незаметен, в то время как в другом наступает смерть.

 При распространении заболевания на внутренние органы понадобится сделать МРТ, УЗИ и компьютерную томографию.
При распространении заболевания на внутренние органы понадобится сделать МРТ, УЗИ и компьютерную томографию. При тяжелом течении заболевания прописывается лечение болезни Бехчета с более агрессивными препаратами:
При тяжелом течении заболевания прописывается лечение болезни Бехчета с более агрессивными препаратами: Чаще всего на начальной стадии отмечаются артралгии, глазные патологии и слизисто-кожные нарушения.
Чаще всего на начальной стадии отмечаются артралгии, глазные патологии и слизисто-кожные нарушения.